Изобретение относится к области органической химии, а именно к области получения производных 1,2-дигидропиридин-3-карбонитрилов, конкретно, 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов общей формулы (1)
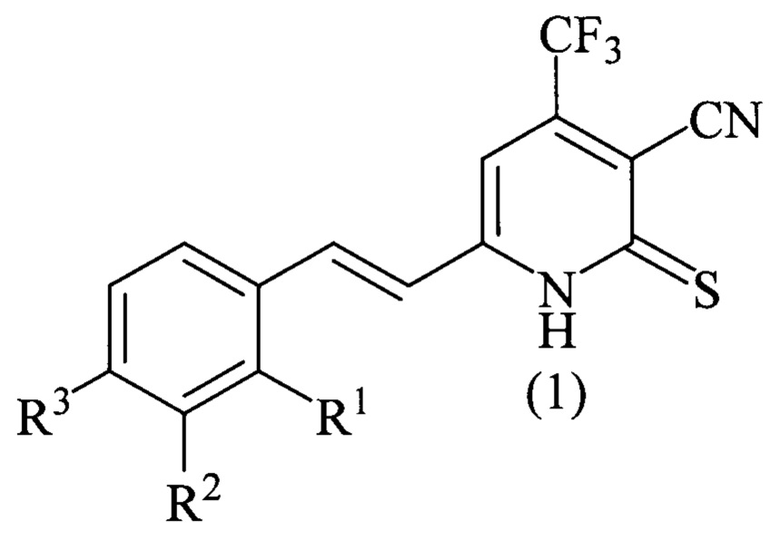
где R1=Н, R2=Н, R3=Н; R1=Н, R2=Н, R3=ОН, которые могут найти применение в фотовольтаике, молекулярной электронике, нелинейной оптике, фоторефрактивных устройствах, лазерной и сенсорной технике, а также в синтезе соединений с противоопухолевыми, противомикробными и противовирусными свойствами.
Известен способ получения 6-арил-3-цианопиридин-2-(1H)-тионов, заключающийся во взаимодействии ароматического кетона с цианотиоацетамидом в среде диметилформамида и диметилацетамида в течение 24 часов с дальнейшей нейтрализацией [Ren-Lin Zheng, Xiu-Xiu Zeng, Hai-Yun He, Jun He, Sheng-Yong Yang, Luo-Ting Yu, Li Yang. Facile Synthesis of 6-Aryl-3-cyanopyridine-2-(1H)-thiones from Aryl Ketones / Synthetic Communications, 2012, 42 (10), 1521-1531. doi: 10.1080/00397911.2010.541964]. Недостатками данного метода являются длительность процесса и невозможность получить трифторметилзамещенные производные.
Авторы [Shestopalov A.M., Rodinovskaya L.A., Zubarev A.A., Nesterov V.N., Ugrak B.I., Dutova T.Y. Synthesis and domino reactions of polymethylene-3-cyanopyridine-2(1H)-thiones / Journal of Heterocyclic Chemistry, 2019, 57 (2), 913-922. doi:10.1002/jhet.3836] описывают трехкомпонентный способ получения 3-цианопиридин-2(1H)-тионов при взаимодействии циклического кетона, ароматического альдегида и цианотиоацетамида в среде этанола в присутствии морфолина. Недостатком данного способа является невозможность получить трифторметилзамещенные производные.
В работе [Chunikhin K.S., Rodinovskaya L.A., Shestopalov A.M. Synthesis of 6-substituted 3-cyano-5-nitropyridine-2(1H)-thiones / Russian Chemical Bulletin, 2003, 52, 447-450. Doi: 10.1023/A:1023483521652] описан способ получения 3-циано-5-нитропиридин-2(1Н)-тионов при взаимодействии замещенных 2-нитро-3-фениламинопроп-2-ен-1-онов с цианотиоацетамидом в щелочной среде. Недостатками данного метода являются труднодоступность исходного реагента, невозможность получить трифторметилзамещенные производные и низкие выходы продуктов.
Наиболее близким к заявленному является способ получения 6-(4-(диметиламино)стирил)-2-оксо-4-(трифторметил)-1,2-дигидропиридин-3-карбонитрила взаимодействием 4-диметиламинобензальдегида и 6-метил-2-оксо-4-(трифторметил)-1,2-дигидропиридин-3-карбонитрила в среде 1,4-диоксана в присутствии пирролидина при 100°С в течение 32 часов [Sorokin S.P., Ievlev M.Yu., Ershov O.V. 2-Pyridone-based stilbazoles containing cyano and trifluoromethyl acceptors: Synthesis and fluorescence properties in solutions and in solid state / Dyes and Pigments, 2023, 219. doi: 10.1016/j.dyepig.2023.111581.]. Недостатками данного способа являются длительность метода и невозможность получить 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилы.
Задачей данного изобретения является разработка способа получения 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов, которые могут найти применение в фотовольтаике, молекулярной электронике, нелинейной оптике, фоторефрактивных устройствах, лазерной и сенсорной технике, а также в синтезе соединений с противоопухолевыми, противомикробными и противовирусными свойствами.
Техническим результатом является разработка способа получения ранее неописанных в литературе 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов с выходом 69-75%.
Технический результат достигается тем, что способ получения 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов общей формулы (1)
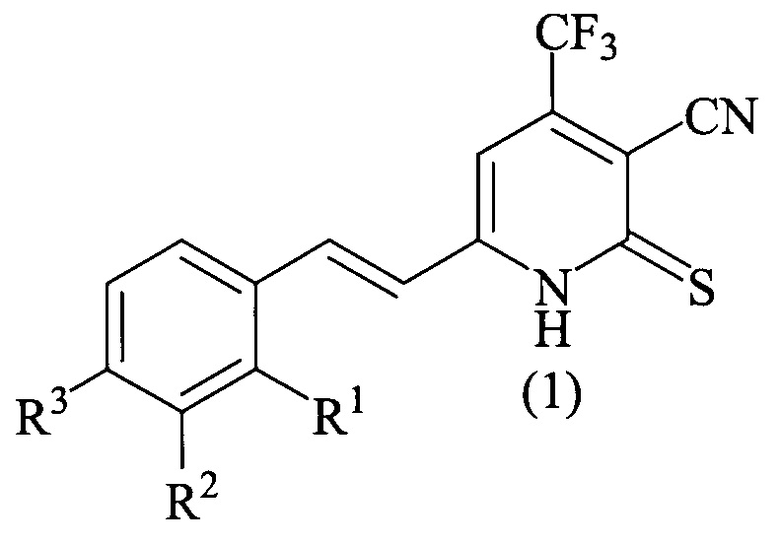
где R1=Н, R2=Н, R3=Н; R1=Н, R2=Н, R3=ОН, согласно изобретению, включает взаимодействие 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила с бензальдегидом с заместителями R1, R2 и R3 в бензольном кольце, как это определено выше, в среде 1,4-диоксана в присутствии пирролидина при температуре 70-80°С в течение 10-12 часов, разбавление реакционной массы водой, подкисление разбавленной соляной кислотой, фильтрование осадка.
Сопоставительный анализ заявляемого решения с известными показывает, что в разработанном способе получения за счет использования 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила в качестве реагента достигается возможность получения 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов и снижается длительность синтеза.
Сущность изобретения заключается в описанном способе получения: эквимолярные количества 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила, бензальдегидом с заместителями R1, R2 и R3 в бензольном кольце, как это определено выше и пирролидина растворяют в 1,4-диоксане, перемешивают при температуре 70-80°С в течение 10-12 часов, разбавляют реакционную массу водой, подкисляют разбавленной соляной кислотой, образовавшийся осадок фильтруют.
Ниже приведены примеры осуществления изобретения.
Пример 1. Способ получения 6-стирил-2-тиоксо-4-(трифторметил)-1,2-дигидропиридин-3-карбонитрила. К 0,1 моль бензальдегида в 10 мл 1,4-диоксана добавляют 0,1 моль 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила и 0,1 моль пирролидина. Полученную смесь оставляют на магнитной мешалке при температуре 70-80°С в течение 10-12 часов. Далее реакционную массу разбавляют водой, подкисляют разбавленной соляной кислотой, образовавшийся осадок фильтруют. Выход 75%. Кристаллы красного цвета. Т. пл. 173°С (разл.). 1Н ЯМР (500.13 МГц, DMCO-d6, δ, м.д. J, Гц): 7.33 (д, J=16.4, 1H, СН=СН), 7.46-7.53 (м, 3Н, С6Н5), 7.62-7.68 (м, 3Н, Ру-Н, С6Н5), 8.14 (д, У=16.4, 1Н, СН=СН), 14.64 (уш.с, 1Н, NH). 1Н ЯМР (500.13 МГц, CF3COOD, δ, м.д. J, Гц): 8.34 (д, J=16.0, Ш, СН=СН), 8.52-8.64 (м, 3Н, С6Н5), 8.70-8.81 (м, 3Н, Ру-Н, С6Н5), 9.08 (д, J=16.1, 1Н, СН=СН. 19F ЯМР (150.90 МГц, DMCO-d6, δ, м.д.): δ 62.99. Масс-спектр, m/z (Iотн, %): 305 [М]+ (100).
Пример 2. Способ получения 6-(4-гидроксистирил)-2-тиоксо-4-(трифторметил)-1,2-дигидропиридин-3-карбонитрила. Способ осуществляют аналогично способу 1, отличающийся тем, что вместо бензальдегида используют 4-гидроксибензальдегид. Выход продукта: 69%. Осадок темного красного цвета. Т. пл. 196°С (разл.). 1Н ЯМР (500.13 МГц, DMCO-d6, δ, м.д. J, Гц): 6.89 (д, J=8.6, 2Н, С6Н4), 7.11 (д, J=16.3, 1H, СН=СН), 7.51 (д, J=8.6, 2Н, С6Н4), 7.59 (с, 1Н, Ру-Н), 8.07 (д, J=16.3, 1H, СН=СН), 10.28 (с, 1Н, ОН), 14.43 (уш.с, 1H, NH). 19F ЯМР (150.90 МГц, DMCO-d6, δ, м.д.): δ 63.9. Масс-спектр, m/z (Iотн, %): 322 [М]+ (100).
Таким образом, предлагаемый способ позволяет получить 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилы, которые могут найти применение в фотовольтаике, молекулярной электронике, нелинейной оптике, фоторефрактивных устройствах, лазерной и сенсорной технике, а также в синтезе соединений с противоопухолевыми, противомикробными и противовирусными свойствами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-АРИЛ-2-ОКСО-2Н-ХРОМЕН-3-КАРБОНИТРИЛОВ | 2015 |
|
RU2577524C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АМИНО-8-ГИДРОКСИ-1,6-ДИОКСО-2,7-ДИАЗАСПИРО[4.4]НОН-3-ЕН-4-КАРБОНИТРИЛОВ | 2012 |
|
RU2495040C1 |
| Способ получения 6-амино-4-арил-2-тиоксо-1,2-дигидропиридин-3,5-дикарбонитрилов | 2022 |
|
RU2792625C1 |
| Способ получения аммонийных солей 3-амино-8-гидрокси-1,6-диоксо-4-циано-2,7-диазаспиро[4.4]нон-3-ен-2-идов | 2016 |
|
RU2631856C1 |
| CПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,2,3,6-ТЕТРАГИДРОПИРРОЛО[1,2-d][1,4]ДИАЗОЦИНОВ | 2008 |
|
RU2378279C1 |
| Производные 1,4-диоксида хиноксалин-2-карбонитрила, ингибирующие рост опухолевых клеток | 2016 |
|
RU2640304C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗОТИАЗИНОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2006 |
|
RU2395508C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1-АЦИЛ-4-ФЕНИЛСУЛЬФОНИЛПРОЛИНАМИДА И НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2012 |
|
RU2615997C2 |
| ПРОИЗВОДНЫЕ ИНДОЛИН-2-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2013 |
|
RU2627706C2 |
| Спироконденсированные производные 2,3-дигидроиндола, их применение в офтальмологии | 2017 |
|
RU2712039C2 |
Изобретение относится к области органической химии, конкретно к получению 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов общей формулы (1), где R1=Н, R2=Н, R3=Н или R1=Н, R2=Н, R3=ОН, которые могут найти применение в фотовольтаике, молекулярной электронике, нелинейной оптике, фоторефрактивных устройствах, лазерной и сенсорной технике, а также в синтезе соединений с противоопухолевыми, противомикробными и противовирусными свойствами. Способ включает взаимодействие 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила с бензальдегидом или 4-гидроксибензальдегидом в среде 1,4-диоксана в присутствии пирролидина при температуре 70-80°С в течение 10-12 часов, разбавление реакционной массы водой, подкисление разбавленной соляной кислотой и фильтрование осадка. Технический результат - обеспечение методом получения целевых продуктов с выходом 69-75%. 2 пр.
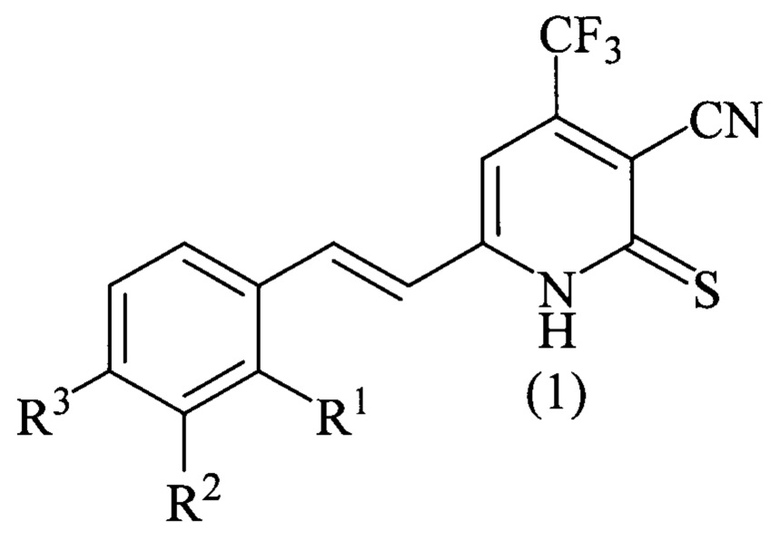
Способ получения 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов общей формулы (1)
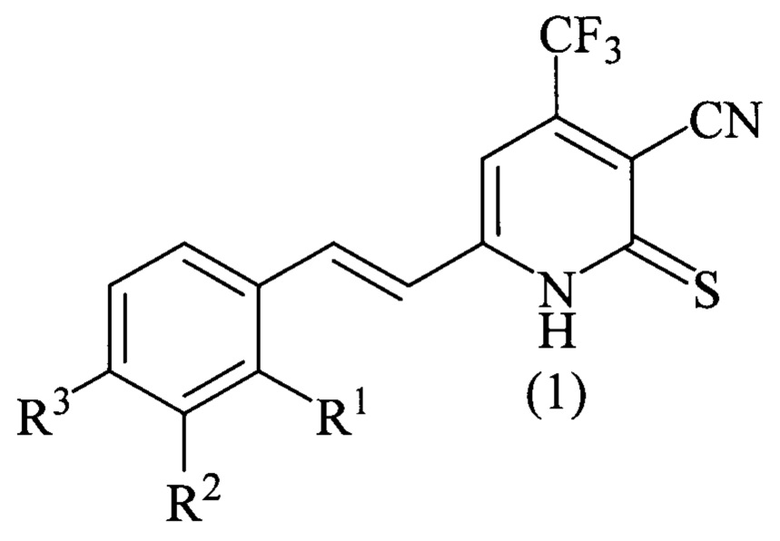
где R1=Н, R2=Н, R3=Н; R1=Н, R2=Н, R3=ОН, включающий взаимодействие 6-метил-2-тиоксо-4-трифторметил-1,2-дигидропиридин-3-карбонитрила с бензальдегидом с заместителями R1, R2 и R3 в бензольном кольце, как это определено выше, в среде 1,4-диоксана в присутствии пирролидина при температуре 70-80°С в течение 10-12 часов, разбавление реакционной массы водой, подкисление разбавленной соляной кислотой, фильтрование осадка.
| Дмитриев В.С | |||
| и др | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Sorokin S.P | |||
| et al., 2-Pyridone-based stilbazoles containing cyano and trifluoromethyl acceptors: Synthesis and fluorescence properties in | |||
Авторы
Даты
2024-10-04—Публикация
2023-11-23—Подача