Область техники, к которой относится изобретение
Изобретение относится к ветеринарной фармации, в частности, к препаратам для лечения и профилактики неврологических патологий у животных и может быть использовано в ветеринарии и животноводстве для лечения и профилактики заболеваний нервной системы у животных.
Уровень техники
Известна лекарственная композиция цитопротекторного действия и способ ее получения, которая представляет собой лекарственную композицию цитопротекторного действия в виде водного раствора, содержащую инозин, никотинамид, рибофлавина мононуклеотид натрия, янтарную кислоту и биологически активное соединение. При этом в качестве биологически активного соединения она содержит димеглюмина сукцинат формулы [HOCH2(CHOH)4CH2NH2CH3]+2[OOC(CH2)2COO]2-, при следующем соотношении компонентов, мас. %: димеглюмина сукцинат 38,76-47,37; инозин 1,80-2,20; никотинамид 0,90-1,10; Рибофлавина мононуклеотид натрия 0,18-0,22; янтарная кислота 0,01-0,62; вода для инъекций до 100. Изобретение обеспечивает получение композиции, обладающей высокой биологической активностью, безопасностью и стабильностью. (См. пат. RU № 2651047, кл. A61K 9/08, A61K 31/205, A61K 31/7052, А61К 31/525, А61К 31/455, A61P 39/00, опубл. 18.04.2018 г.).
Недостатком данного изобретения является отсутствие в составе компонентов, которые могли бы обеспечить достижение достаточного антиоксидантного и антигипоксантного эффектов.
Известно ноотропное средство "Ноотобрил" в форме раствора для инъекций, содержащее активное вещество - пирацетам и вспомогательные вещества - натрия ацетат, кислоту уксусную и воду для инъекций при следующем соотношении, мас. %: пирацетам 15-25; натрия ацетат 0,08-0,11; кислота уксусная до рН 5,8; вода для инъекций остальное. Препарат благодаря качественному и количественному подбору ингредиентов стабилен при хранении, что обеспечивает постоянный терапевтический эффект при соответствующем назначении. (См. пат. RU № 2453314, кл. A61K 31/4015, A61K 9/08, A61Р 25/00, опубл. 27.02.2004 г.).
Недостатком данной композиции является отсутствие антиоксидантного и антигипоксантного эффектов, недостаточное нейропротекторное действие.
Известен комбинированный препарат для парентерального введения, содержащий гидрохлорид или сукцинат метилэтилпиридинола и рибофлавин, содержащий фармацевтически приемлемую соль метилэтилпиридинола, который дополнительно содержит рибофлавин и имеет состав, г/100 мл: гидрохлорид или сукцинат метилэтилпиридинола 1,0-5,0; рибофлавин 0,002-0,05; вода для инъекций до 100 мл. Препарат, в частности, способен оказывать благотворное влияние при заболеваниях печени. (См. пат. RU № 2566725, кл. A61K 31/4412, A61K 31/525, опубл. 27.10.2015 г.).
Недостатком данного препарата является недостаточные церебропротекторный и нейротрофический эффекты.
Наиболее близкой по технической сущности и достигаемому положительному эффекту и принятая авторами за прототип является фармацевтическая композиция в форме раствора для инъекций этилметилгидроксипиридина сукцината и пиридоксина, способ ее получения и способ лечения, содержащая компоненты в следующем соотношении, мас. %: этилметилгидроксипиридина сукцинат 2,5-10; пиридоксин или его фармацевтически приемлемая соль 0,25-5; кислота янтарная 0,5-3; повидон (пласдон С-15 или коллидон 17 PF) 0,5-3,5; этилендиаминотетрауксусной кислоты динатриевая соль (трилон Б) 0,005-0,2; вода для инъекций до 100. Ей характерны высокая стабильность, удобство в применении и высокая терапевтическая эффективность при профилактике и лечении заболеваний сердечно-сосудистой и/или нервной системы, а также артериальной гипертензии. (См. пат. RU № 2383331, кл. A61K 9/08, A61K 31/194, A61К 31/4415, А61К 31/44, А61К 47/18, А61К 47/30, А61Р 7/00, А61Р 9/00, А61Р 25/28, опубл. 10.03.2010 г.).
Недостатком данной композиции является недостаточные нейропротекторный, церебропротекторный и нейротрофический эффекты.
Краткое описание чертежей и иных материалов
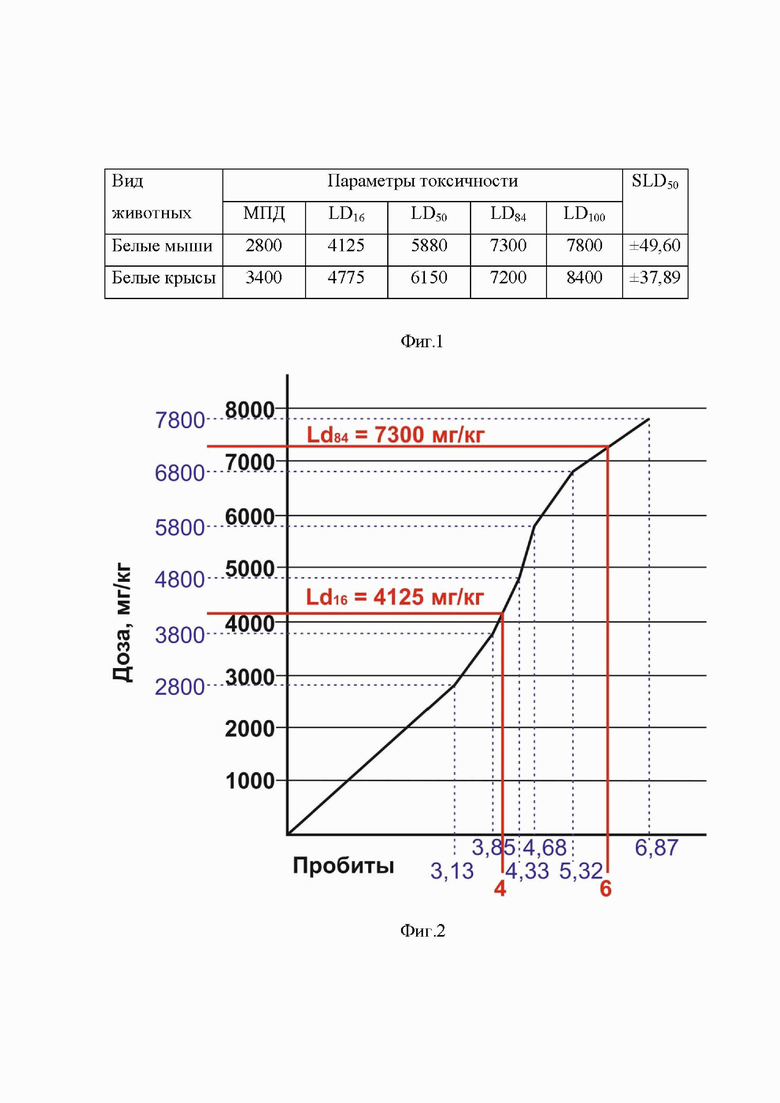
На фиг. 1 дан антиоксидантный препарат для лечения и профилактики неврологических патологий у животных. Параметры острой токсичности антиоксидантного препарата для лечения и профилактики неврологических патологий у животных
На фиг. 2, тоже, графическое изображение острой токсичности для белых мышей антиоксидантного препарата для лечения и профилактики неврологических патологий у животных
На фиг. 3, тоже, графическое изображение острой токсичности для белых лабораторных крыс антиоксидантного препарата для лечения и профилактики неврологических патологий у животных
На фиг. 4, тоже, гематологические показатели собак, которым проводили консервативное лечение грыжи межпозвоночного диска
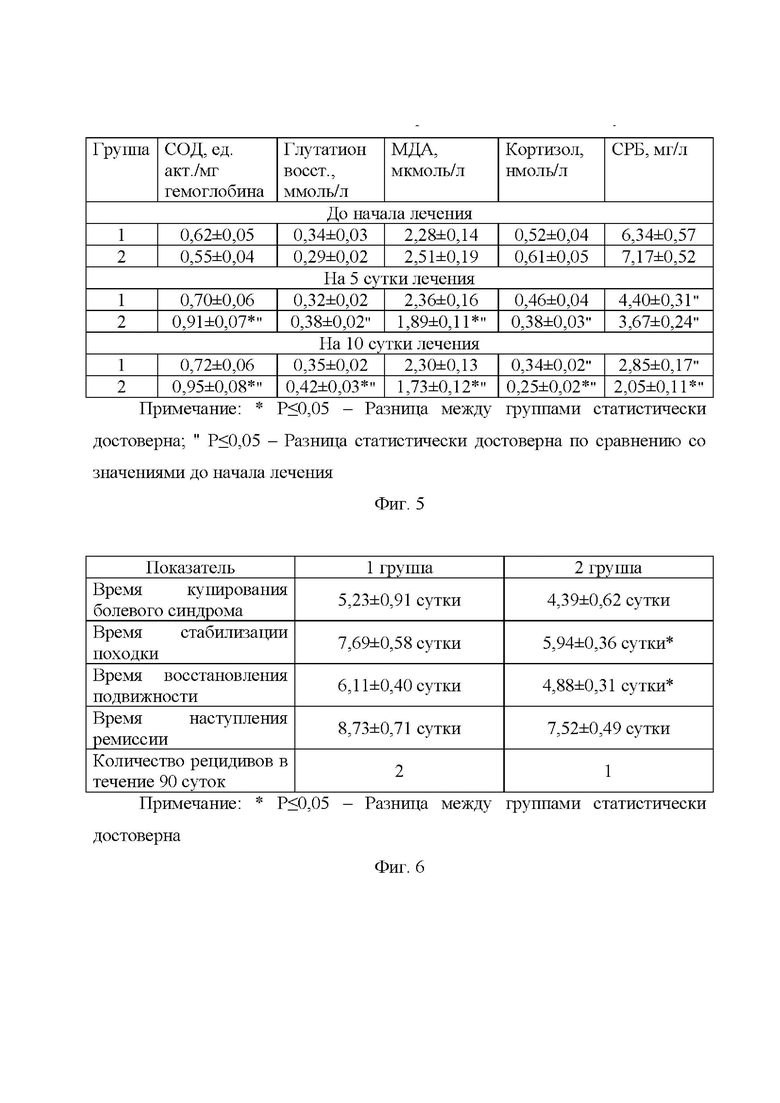
На фиг. 5, тоже, биохимические показатели крови собак, которым проводили консервативное лечение грыжи межпозвоночного диска
На фиг. 6, тоже, показатели, характеризующие клинический статус собак, которым проводили консервативное лечение грыжи межпозвоночного диска
Раскрытие изобретения
Задачей изобретения является разработка антиоксидантного препарата для лечения и профилактики неврологических патологий у животных, обладающего выраженным антиоксидантным и нейропротекторным действием, низкой токсичностью, церебропротекторным и нейротрофическим эффектом, стабильностью лекарственной формы, высокой эффективностью в профилактике и лечении заболеваний нервной системы у животных; удобством введения и дозировки.
Технический результат, который может быть достигнут с помощью предлагаемого изобретения, сводится к выраженному антиоксидантному, антигипоксантному, церебропротекторному и нейротрофическому действию, низкой токсичности и высокой эффективности в профилактике и лечении неврологических заболеваний у животных, стабильности лекарственной формы, удобству введения и дозировки.
Технический результат достигается с помощью антиоксидантного препарата для лечения и профилактики неврологических патологий у животных, включающего производное 3-оксипиридина, пиридоксина гидрохлорид и воду для инъекций, при этом дополнительно содержит 2-оксо-1-пирролидинацетамид, рибофлавина мононуклеотид и поливинилпирролидон, а в качестве производного 3-оксипиридина используют метилэтилпиридинола гидрохлорид, при следующем соотношении компонентов в мас.%:
Общим с заявленным препаратом является наличие в составе антиоксидантной субстанции из числа производных 3-оксипиридина и пиридоксина. Отличием от ближайшего аналога, заявляемого антиоксидантного препарата для лечения и профилактики неврологических патологий у животных является использование в качестве действующего вещества из числа производных 3-оксипиридина метилэтилпиридинола гидрохлорида и присутствие дополнительно 2-оксо-1-пирролидинацетамида, рибофлавина мононуклеотида и поливинилпирролидона, что позволяет достигать более выраженных антиоксидантного, антигипоксантного, нейропротекторного, церебропротекторного и нейротрофического эффектов и дает возможность проводить более эффективно лечение и профилактику неврологических заболеваний у животных.
Заявляемый антиоксидантный препарат для лечения и профилактики неврологических патологий у животных представляет собой водный прозрачный раствор с желтовато-оранжевым оттенком, со специфическим запахом, обладающий выраженными антиоксидантным, антигипоксантным, нейропротекторным, церебропротекторным и нейротрофическим эффектами, малотоксичен, удобен в применении и дозировании.
Число неврологических пациентов в ветеринарной практике постоянно растет. Это обусловлено увеличением числа травматических повреждений у животных (переломы, спондилолистезы), проявлением таких патологий, как остеохондрозы, опухоли спинного мозга и позвоночного столба (продолжительность жизни домашних питомцев в крупных мегаполисах увеличивается благодаря в т.ч. использованию в их кормлении готовых рационов), а также тесным имбридингом при разведении, что увеличивает долю генетических аномалий позвоночного столба (См. Козлов Н.А., Грядунова Ф.А. // Вестник Алтайского государственного аграрного университета. - 2021. - №11 (205). - С. 70-76.). Этим обусловлена необходимость разработки современных лекарственных средств ветеринарного назначения для лечения неврологических патологий животных.
Свободнорадикальное окисление является универсальным патофизиологическим феноменом при многих патологических состояниях, обязательной и существенной составляющей механизмов возрастных изменений организма и повреждающего действия хронического стресса, сосудистой и нейродегенеративной патологии мозга. Велика роль свободных радикалов в развитии апоптоза нейронов. Повышенная продукция свободных радикалов является одной из существенных причин длительного спазма церебральных сосудов, прогрессирования постишемического отека и дегенерации нейронов за счет нарушения целостности мембран. В последнее время оксидативный стресс рассматривается как один из ведущих факторов патогенеза нейродегенеративной патологии (См. Бурчинский С.Г. // Неврология и нейрохирургия. Восточная Европа. - 2017. - Т. 7. - №1. - С. 102-111.).
Большинство патологических процессов, протекающих непосредственно в мозге или затрагивающих его, сопровождаются ишемией мозга. Неуправляемая и некомпенсированная активация процессов перекисного окисления липидов, истощение эндогенных антиоксидантов и нарушение регуляторных механизмов антирадикальной защиты рассматриваются как ключевые звенья повреждения нейронов. Быстрое и своевременное устранение этих факторов является наиболее актуальной проблемой современной неврологии. Естественным выходом из этой ситуации может стать использование антиоксидантных соединений, способных понижать уровень свободных радикалов в тканях (См. Верещагин Н.В., Танашян М.М., Федорова Т.Н., Смирнова И.Н. // Атмосфера. Нервные болезни. - 2004. - №3. - С. 8-12.).
Метилэтилпиридинол - относительно новый антиоксидант, производное 3-оксипиридина. Антиокислительные свойства соединения обусловлены перехватом свободных радикалов за счет наличия экранированного алкильными радикалами фенольного гидроксила. Метилэтилпиридинол ингибирует свободнорадикальное окисление, взаимодействуя с активными формами кислорода, тормозит агрегацию тромбоцитов и нейтрофилов, полимеризацию фибрина, переход фибрина-мономера в фибрин-полимер, ингибирует фосфодиэстеразу циклических нуклеотидов, увеличивает содержание циклического аденозинмонофосфата и циклического гуанозинмонофосфата в клетках (См. Брюханов В.М., Мирошниченко А.Г. // Бюллетень сибирской медицины. - 2016. - Т. 15. - №4. - С. 11-19.).
Имеются данные, которые указывают на эффективность данного соединения в некоторых областях медицины, например в хирургии. Одним из путей, направленных на борьбу с гипоксией, является применение фармакологических препаратов - антигипоксантов. Было доказано, что применение метилэтилпиридинола гидрохлорида (эмоксипина) позволяет добиваться лучших результатов лечения огнестрельных ранений конечности по сравнению с другими лекарственными средствами из данной группы. Имеются сведения о том, что эмоксипин обладает более выраженным лечебным эффектом по сравнению с мексидолом при лечении огнестрельных ранений конечности. При этом отмечено, что внутримышечное введение метилэтилпиридинола гидрохлорида оказывает более выраженный лечебный эффект при травматических повреждениях мышц конечности по сравнению с внутрибрюшинным введением (См. Трухан А.П., Терешко Д.Г., Летковская Т.А. // Новости хирургии. - 2020. - Т. 28. - №5. - С. 491-497.).
Пирацетамоподобные препараты модулируют процессы возбуждения и/или торможения медиаторов, нейрогормонов и/или постсинаптических сигналов. Имеются сведения о том, что пирацетам играет важную роль в энергетическом метаболизме, в том числе в увеличении оксигенации головного мозга и проницаемости клеточных и митохондриальных мембран для посредников цикла Кребса, в увеличении синтеза цитохрома b5 (См. Сычев Д.А., Герасимова К.В., Отделенов В.А. // Русский Медицинский Журнал «РМЖ». - 2011. - Т. 19. - №15. - С. 957-962.).
Есть данные о том, что у пирацетама (2-оксо-1-пирролидинацетамид) выделяют следующие эффекты: восстановление текучести клеточной мембраны нейронов - важного свойства липидно-белковой оболочки клетки, обеспечивающего процессы трансмембранного транспорта и работу рецепторов; влияние на нейротрансмиссию (холинергическую, серотонинергическую, норадренергическую и глутаматергическую нейротрансмиттерные системы); нейропротекторный эффект; воздействие на нейропластичность, под которой понимается способность нервной системы к адаптации посредством модификации имеющихся или построения новых нейронных связей и синапсов; влияние на энергетический обмен в клетке; воздействие на сосудистые механизмы, такие как уменьшение адгезии эритроцитов к эндотелию стенки сосудов (См. Титова Н.В. // Медицинский совет. - 2017. - №10. - С. 102-109.).
Также, есть свидетельства того, что пирацетаму присущи такие фармакологические эффекты, как повышение устойчивости мозга к различным вредным воздействиям (гипоксия, интоксикации, понижение или повышение температуры и т. д.); коррекция нарушений функций центральной нервной системы и неврологических дефицитов, возникающих при старении и у молодых животных, родившихся от самок, подвергшихся вредным воздействиям; улучшение специфических гемореологических показателей и нормализация нарушенного мозгового кровообращения при отсутствии прямого влияния на сосуды (См. Востриков В.В. // Обзоры по клинической фармакологии и лекарственной терапии. - 2017. - Т. 15. - №1. - С. 14-25.).
Витамин В6 (2-метил-3-окси-4,5-ди-(оксиметил)-пиридин) представляет собой вещество, имеющее три различные пространственные формы организации молекулы, получившие название витамеры витамина В6 - пиридоксол (пиридоксин), пиридоксаль, пиридоксамин. Пиридоксин поддерживает, активизирует и ускоряет превращения дофамина в норадреналин, глютаминовой и аспарагиновой кислоты - в янтарную кислоту, которая существенно повышает энергетические обменные процессы в клетках. В ходе реакции дезаминирования происходит образование ацетилкоэнзима А, который является ключевым веществом цикла Кребса. Пиридоксальфосфат обеспечивает протекание реакций цикла Кребса и синтеза универсальной энергетической молекулы АТФ (аденозинтрифосфорной кислоты). В ходе реакций декарбоксилирования происходит образование гамма-аминомасляной кислоты из глютаминовой кислоты и серотонина - из триптофана, которые являются основными тормозными медиаторами в центральной нервной системе, под действием которых происходит процесс торможения и подавления возбуждения. Реакция декарбоксилирования, в ходе которой образуются гамма-аминомасляная кислота и серотонин, регулируется и запускается витамином В6. Поэтому при дефиците пиридоксина появляются признаки чрезмерного возбуждения центральной нервной системы (См. Мохирева Л.В., Каторгин Н.А., Шаркова Т.И. // Туберкулез и социально-значимые заболевания. - 2017. - №1. - С. 14-18.).
Дефицит пиридоксина приводит к возникновению дистальной симметричной, преимущественно сенсорной полиневропатии, проявляющейся ощущением онемения и парестезиями в виде «покалывания иголками». Пиридоксин оказывает положительное влияние на различные варианты эпилепсии. Наиболее известна пиридоксин-зависимая эпилепсия, которая относится к редким наследственным, передающихся аутосомно-рецессивным путем, формам эпилепсий (См. Строков И.А., Ахмеджанова Л.Т., Солоха О.А. // Русский Медицинский Журнал «РМЖ». - 2009. - Т. 17. - №11. - С. 776-783.).
Витамины группы В часто называют нейротрофическими. Оказывают витамины действие и на сосудистую систему, так как комбинация различных витамеров пиридоксина угнетает агрегацию тромбоцитов, реализуя свой эффект опосредованно через активацию рецепторов к простагландину Е. Для того чтобы быстро достичь высокой концентрации витаминов в крови и цитоплазме клеток, применяется парентеральное введение в больших дозах водорастворимых форм витаминов группы В, так как в этом случае их эффективность повышается (См. Строков И.А. // Русский Медицинский Журнал «РМЖ». - 2010. - Т. 18. - №25. - С. 1509-1513.).
В норме концентрация пиридоксина (витамина В6) в головном мозге примерно в 100 раз выше, чем в крови. С недостатком витамина В6 связывают различные метаболические и морфологические нарушения, такие как уменьшение ветвления дендритов, снижение количества синапсов и миелинизированных аксонов. Эти процессы имеют клинические проявления в виде нарушения поведения, развития эпилептических приступов и формирования двигательных расстройств (См. Бельская Г.Н., Лузанова Е.И., Сергиенко Д.А., Степанова С.Б., Макарова Л.Д. // Медицинский совет. - 2016. - №19. - С. 44-47.).
Витамин В2 (рибофлавин) имеет решающее значение для синтеза, превращения и рециркуляции других витаминов группы В - ниацина, фолата и витамина В6, а также для синтеза всех гемовых белков (включая гемоглобин), синтазы оксида азота, ферментов Р450 и белков, участвующих в переносе электронов и кислорода. Превращение пиридоксина в его коферментую форму, пиридоксаль-5'-фосфат (ПАЛФ), происходит под действием флавинмононуклеотид-зависимого фермента пиридоксин5'-фосфатоксидазы. Недостаточная обеспеченность организма витамином В2 приводит к снижению активности его и соответственно уменьшению образования активных коферментных форм витамина В6, то есть возникновению вторичного функционального дефицита витамина В6, причиной которого является недостаток витамина В2. Отмечается, что связь между рибофлавином и пиридоксином имеет клиническую значимость (См. Коденцова В.М., Леоненко С.Н., Рисник Д.В. // Вопросы диетологии. - 2020. - Т. 10. - №2. - С. 23-34.).
В организме рибофлавин превращается в коферментные формы -флавинмононуклеотид и флавинадениндинуклеотид, которые входят в состав ферментов из группы оксидаз и редуктаз, образуя редокс-системы дыхательных цепей и обеспечивает тканевое дыхание. Он необходим для синтеза катехоламинов, так как входит в состав фенилаланин-гидроксилазы и обеспечивает синтез L-ДОФА - предшественника дофамина и норадреналина в центральной нервной системе и надпочечниках. Витамин В2 стимулирует синтез эритропоэтина - основного стимулятора эритропоэза, входит в состав моноаминооксидаз (обеспечивают разрушение катехоламинов) и ксантиноксидазы (обеспечивает разрушение пуринов и синтез мочевой кислоты) (См. Хапалюк А.В. // Лечебное дело: научно-практический терапевтический журнал. - 2023. - №1 (84). - С. 58-74.).
Поливинилпирролидон полимерное производное пирролидона - белый или слегка желтоватый порошок со слабым специфическим запахом, гигроскопичен. Легко растворим в воде, этиловом спирте, хлороформе и большинстве органических растворителей, практически не растворим в эфире, алифатических и циклических углеводородах. Он широко применяется в медицине, во-первых как мощное дезинтоксикационное средство для лечения ряда патологических процессов, сопровождающихся интоксикацией организма, во-вторых, как плазмозаменитель - в виде иньекционных растворов, в-третьих, его высокомолекулярные фракции служат пролонгатором действия других лекарственных веществ (См. Краснюк (мл.) И.И., Беляцкая А.В., Краснюк И.И., Степанова О.И., Овсянникова Л.В., Грих В.В., Алленова Т.М., Одинцова Е.Б. // Фармация. - 2016. - Т. 65. - №6. - С. 7-11.).
Поливинилпирролидон обладает антитоксическим эффектом, заключающимся в связывании токсинов и их выведении из организма, способствует улучшению микроциркуляции в капиллярах и ликвидации стаза эритроцитов (См. Фрисс С.А. // Медицинская экспертиза и право. - 2011. - № 6. - С. 9-11.).
Сущность получения антиоксидантного препарата для лечения и профилактики неврологических патологий у животных заключается в следующем: исходные вещества в мас. %, а именно производное 3-оксипиридина, в качестве которого используют метилэтилпиридинола гидрохлорид - 0,8-1,2; 2-оксо-1-пирролидинацетамид - 7,0-11,0; пиридоксина гидрохлорид - 0,24-0,32; рибофлавина мононуклеотид - 0,018-0,038; поливинилпирролидон - 2,5-4,5; вода для инъекций - остальное смешивают в асептических условиях и упаковывают.
Осуществление изобретения
Примеры конкретного выполнения получения и испытания антиоксидантного препарата для лечения и профилактики неврологических патологий у животных.
Пример 1.
Антиоксидантный препарат для лечения и профилактики неврологических патологий у животных готовят путем смешения компонентов в асептических условиях и растворения в воде для инъекций при следующем соотношении компонентов в мас. %:
Данный препарат вводили внутримышечно белым лабораторным крысам (опытная группа), у которых было экспериментально смоделировано нейротоксическое повреждение мозга путем однократного внутрибрюшинного введения раствора хлорида триметилолова в дозе из расчета 7,5 мг действующего вещества на кг массы тела. Эксперимент проводили в сравнительном аспекте по отношению к группе белых лабораторных крыс (контрольная группа), которым аналогично вводили раствор хлорида триметилолова. Наблюдение за животными производили на протяжении четырнадцати суток. Установлено, что уменьшение массы тела крыс в опытной группе было в среднем на 26,1% меньше по сравнению с контрольной группой. У животных из опытной группы восстанавливались раньше на 41,3±4,26 часов нормальная двигательная активность, на 47,1±2,79 часов - нормальный аппетит, на 42,8±3,15 часов - нормальная реакция на внешние раздражители, а также быстрее исчезали на 56,9±5,30 часов видимая тревожность, на 2,7±0,43 часов - тремор, на 6,9±1,09 часов - периодические непроизвольные движения. Анализ результатов биохимического исследования крови, полученной от белых лабораторных крыс на восьмые сутки проводимого эксперимента, показал следующее: в опытной группе уровень восстановленного глутатиона составил 0,27±0,03 ммоль/л, активность супероксиддисмутазы - 0,43±0,03 ед. акт./мг гемоглобина, что на 28,6% и 43,3% больше, чем контрольной группе соответственно, а концентрация малонового диальдегида составила 2,37±0,19 мкмоль/л, С-реактивного белка - 7,65±0,51 мг/л, что на 19,4% и 5,6% меньше, чем контрольной группе соответственно.
Пример 2.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
После применения полученного препарата белым лабораторным крысам установлено, что уменьшение массы тела крыс в опытной группе было в среднем на 34,7% меньше по сравнению с контрольной группой. У животных из опытной группы восстанавливались раньше на 52,1±3,92 часов нормальная двигательная активность, на 54,4±3,15 часов - нормальный аппетит, на 46,8±2,93 часов - нормальная реакция на внешние раздражители, а также быстрее исчезали на 59,6±4,46 часов видимая тревожность, на 3,1±0,37 часов - тремор, на 9,6±0,91 часов - периодические непроизвольные движения. Анализ результатов биохимического исследования крови, полученной от белых лабораторных крыс на восьмые сутки проводимого эксперимента, показал следующее: в опытной группе уровень восстановленного глутатиона составил 0,29±0,03 ммоль/л, активность супероксиддисмутазы - 0,48±0,04 ед. акт./мг гемоглобина, что на 38,1% и 60,0% больше, чем контрольной группе соответственно, а концентрация малонового диальдегида составила 2,10±0,14 мкмоль/л, С-реактивного белка - 6,22±0,40 мг/л, что на 28,6% и 23,4% меньше, чем контрольной группе соответственно.
Пример 3.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
После применения полученного препарата белым лабораторным крысам установлено, что уменьшение массы тела крыс в опытной группе было в среднем на 42,3% меньше по сравнению с контрольной группой. У животных из опытной группы восстанавливались раньше на 59,4±5,13 часов нормальная двигательная активность, на 62,2±4,38 часов - нормальный аппетит, на 51,3±4,67 часов - нормальная реакция на внешние раздражители, а также быстрее исчезали на 66,1±5,28 часов видимая тревожность, на 3,7±0,29 часов - тремор, на 10,4±1,09 часов - периодические непроизвольные движения. Анализ результатов биохимического исследования крови, полученной от белых лабораторных крыс на восьмые сутки проводимого эксперимента, показал следующее: в опытной группе уровень восстановленного глутатиона составил 0,33±0,02 ммоль/л, активность супероксиддисмутазы - 0,56±0,04 ед. акт./мг гемоглобина, что на 57,1% и 86,6% больше, чем контрольной группе соответственно, а концентрация малонового диальдегида составила 1,97±0,16 мкмоль/л, С-реактивного белка - 5,57±0,34 мг/л, что на 33% и 31,4% меньше, чем контрольной группе соответственно.
Пример 4.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
После применения полученного препарата белым лабораторным крысам установлено, что уменьшение массы тела крыс в опытной группе было в среднем на 39,1% меньше по сравнению с контрольной группой. У животных из опытной группы восстанавливались раньше на 56,6±4,89 часов нормальная двигательная активность, на 58,3±4,71 часов - нормальный аппетит, на 50,2±3,93 часов - нормальная реакция на внешние раздражители, а также быстрее исчезали на 64,1±6,04 часов видимая тревожность, на 3,5±0,41 часов - тремор, на 9,9±0,78 часов - периодические непроизвольные движения. Анализ результатов биохимического исследования крови, полученной от белых лабораторных крыс на восьмые сутки проводимого эксперимента, показал следующее: в опытной группе уровень восстановленного глутатиона составил 0,32±0,02 ммоль/л, активность супероксиддисмутазы - 0,53±0,05 ед. акт./мг гемоглобина, что на 52,4% и 76,7% больше, чем контрольной группе соответственно, а концентрация малонового диальдегида составила 1,95±0,18 мкмоль/л, С-реактивного белка - 5,84±0,37 мг/л, что на 33,7% и 28,1% меньше, чем контрольной группе соответственно.
Пример 5.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
После применения полученного препарата белым лабораторным крысам установлено, что уменьшение массы тела крыс в опытной группе было в среднем на 36,5% меньше по сравнению с контрольной группой. У животных из опытной группы восстанавливались раньше на 54,3±3,77 часов нормальная двигательная активность, на 55,7±4,32 часов - нормальный аппетит, на 50,2±3,93 часов - нормальная реакция на внешние раздражители, а также быстрее исчезали на 62,4±5,40 часов видимая тревожность, на 3,2±0,36 часов - тремор, на 9,7±0,63 часов - периодические непроизвольные движения. Анализ результатов биохимического исследования крови, полученной от белых лабораторных крыс на восьмые сутки проводимого эксперимента, показал следующее: в опытной группе уровень восстановленного глутатиона составил 0,30±0,03 ммоль/л, активность супероксиддисмутазы - 0,50±0,04 ед. акт./мг гемоглобина, что на 42,8% и 66,6% больше, чем контрольной группе соответственно, а концентрация малонового диальдегида составила 2,06±0,21 мкмоль/л, С-реактивного белка - 6,13±0,51 мг/л, что на 29,9% и 24,5% меньше, чем контрольной группе соответственно.
Таким образом, наиболее оптимальными являются примеры 2, 3, 4, поскольку, в результате применения антиоксидантного препарата для лечения и профилактики неврологических патологий у животных в соответствии с ними, получают больший положительный эффект, заключающийся в уменьшении потери массы тела на 34,7 - 42,3%, времени проявления видимой тревожности - на 59,6 - 6,61 часов, наличия непроизвольных движений - на 9,6 - 10,4 часов и тремора - на 3,1 - 3,7 часов, более быстром восстановлении двигательной активности на 52,1 - 59,4 часов, аппетита - на 54,4 - 62,2 часов, реакции на внешние раздражители - на 46,8 - 51,3 часов по сравнению с контрольной группой, соответственно. При осуществлении этих примеров отмечено, что у белых лабораторных крыс из опытной группы по сравнению с белыми лабораторными крысами из контрольной группы увеличивался уровень восстановленного глутатиона на 38,1 - 57,1% и супероксиддисмутазы - на 60,0 - 86,6%, а также снижалась концентрация малонового диальдегида на 28,6 - 33,7%, и С-реактивного белка - на 23,4 - 31,4%..
Пример 6.
Для проведения оценки антиоксидантного препарата для лечения и профилактики неврологических патологий у животных на острую токсичность берут следующее соотношение компонентов в мас. %:
Исследования по изучению острой токсичности антиоксидантного препарата для лечения и профилактики неврологических патологий у животных проводят на белых лабораторных мышах и лабораторных крысах при однократном внутрижелудочном введении, что позволяет определить летальные дозы, классифицировать препарат по ГОСТ 12.1.007-76 и отнести его к 4 классу опасности «Вещества малоопасные» (фиг. 1,2,3).
Пример 7.
Эффективность антиоксидантного препарата для лечения и профилактики неврологических патологий у животных изучают на собаках согласно примера 3, являющимся наиболее эффективным, который включает следующее соотношение компонентов в мас. %: производное 3-оксипиридина, в качестве которого используют метилэтилпиридинола гидрохлорид - 1,0; 2-оксо-1-пирролидинацетамид - 9,0; пиридоксина гидрохлорид - 0,28; рибофлавина мононуклеотид - 0,028; поливинилпирролидон - 3,5; вода для инъекций - остальное.
Суть эксперимента заключается в том, что используют две группы разнополых собак возрастом 7-12 лет распределенных с учетом принципа аналогов с установленным диагнозом грыжа межпозвоночного диска в поясничном отделе в период обострения, по шесть особей в каждой. Первая группа животных выступает в качестве контроля и им применяется стандартная схема лечения, включающая пероральное введение препарата «Превикокс» (Boehringer Ingelheim, Франция) в дозе 1 таблетка на 10 кг массы тела (5,7 мг/кг) один раз в стуки на протяжении десяти дней и препарата «Фамотидин» (АО ФП «Оболенское», Россия) с кормом в дозе 1/4 таблетки на 10 кг массы тела (0,5 мг/кг) два раза в сутки на протяжении десяти дней. Во второй группе лечение проводят аналогично контроля, но дополнительно вводят внутримышечно антиоксидантный препарат для лечения и профилактики неврологических патологий у животных в дозе 1 мл на 2 кг массы тела (51,5 мг/кг) один раз в стуки на протяжении десяти дней. Ежедневно регистрируют клинические показатели у больных собак, а также получают кровь для лабораторного исследования на момент начала лечения, на пятые и десятые сутки лечения, при котором определяют гематологические и биохимические показатели.
При анализе результатов гематологического исследования (фиг. 4) установлено, что количество эритроцитов в крови собак до начала лечения было близко к нижним границам физиологической нормы. За время проведения эксперимента данный показатель увеличился в первой группе на 13,1%, а во второй - достоверно увеличился на 23,3% соответственно, но при этом различия между группами не носили статистически достоверного характера на протяжении всего периода наблюдения. Количество лейкоцитов в крови в начале опыта было в пределах референсных значений. Примененные схемы лечения способствовали снижению количества данных клеток у собак к десятым суткам проводимого эксперимента: в первой группе на 38,4%, во второй группе - на 33,6%, что определило оптимизацию данного параметра. При этом статистически недостоверная разница между группами, при которой в опытной группе уровень белых клеток крови был ниже, чем в контрольной, на пятые сутки составляла 16,7%, на десятые сутки - 11,9%. Уровень гемоглобина перед началом терапии в обеих группах был близок к средним справочным показателям в норме для данного вида животных, а в процессе лечения возрос в первой группе на 6,9%, во второй - на 20,3% соответственно.
Скорость оседания эритроцитов (СОЭ) у больных животных до начала лечения в первой группе составляла 3,62 мм/час, а во второй - 2,98 мм/час. Назначенное лечение привело к статистически достоверному снижению этого маркера к десятым суткам в первой группе на 43,1%, во второй группе - на 40,6%. При этом, к пятым и десятым суткам лечения во второй группе данный показатель был ниже на 15,1% и 14,1% по сравнению с первой группой соответственно. Снижение СОЭ, как и уменьшение количества лейкоцитов, мы связываем с воздействием нестероидного противовоспалительного средства, входящего в схему лечения. А наиболее оптимальные значения в опытной группе по сравнению с контрольной связаны с воздействием антиоксидантного препарата для лечения и профилактики неврологических патологий у животных.
С учетом данных, полученных при проведении биохимического исследования крови собак (фиг. 5), можно отметить, что активность одного из ключевых ферментов, характеризующих функциональное состояние системы антиоксидантной защиты организма - супероксиддисмутазы (СОД), до начала лечения была на низком уровне. В первой группе за весь период наблюдения уровень активности этого энзима возрос на 16,1%. В то время, как во второй группе, вследствие применения антиоксидантного препарата для лечения и профилактики неврологических патологий у животных, данный показатель к пятым суткам достоверно увеличился относительно изначальных значений на 65,4%, а к десятым - на 72,7%. Этим обусловлена статистически достоверная разница между опытной и контрольной группой, которая фиксировалась во время эксперимента на уровне 30,0-31,9%.
Уровень восстановленного глутатиона в крови собак до начала лечения составлял в первой группе 0,34 ммоль/л, во второй группе - 0,29 ммоль/л. Использование антиоксидантного препарата для лечения и профилактики неврологических патологий у животных во второй группе привело к статистически достоверному увеличению этого показателя за пять суток на 31,0%, за десять суток - на 44,8%, по сравнению с первоначальными значениями, что определило статистически достоверную разницу между опытной и контрольной группой к моменту завершения наблюдения. За анализируемый временной промежуток содержание восстановленного глутатиона в первой группе практически не изменился.
Концентрация малонового диальдегида (МДА) в крови собак до начала лечения значительно превышала физиологический уровень. У собак, которым применяли стандартную схему лечения, значимых изменений по данному параметру не отмечено. При этом, у животных, которым дополнительно вводили антиоксидантный препарат для лечения и профилактики неврологических патологий у животных, к пятым суткам снижение концентрации МДА относительно данных, установленных до начала лечения, было статистически достоверно и составляло 24,7%, а к десятым суткам - 31,1%.
Уровень кортизола в крови собак перед началом лечения был повышен. В обеих группах к моменту завершения наблюдения отмечено значительное уменьшение данного гормона. Так, в первой группе оно составило 34,6%, а во второй - 59,0%, чем была обусловлена статистически достоверная разница между ними. С-реактивный белок (СРБ) был повышен в крови собак до начала терапии. Его уровень снизился до нормативных показателей у всех животных уже к пятым суткам лечения. При этом, общее снижение в первой группе составило 55,0%, а во второй - 71,4% соответственно.
Результаты клинического наблюдения во время лечения собак и после его завершения (фиг. 6) указывают на высокую эффективность примененных схем консервативной терапии в обеих группах, но при этом их анализ дает основание говорить о более положительном достигнутом эффекте во второй группе. Это подтверждается тем, что у животных из опытной группы в среднем на 0,84 суток (16,1%) быстрее купировался болевой синдром, на 1,78 суток (22,7%) статистически достоверно быстрее стабилизировалась походка, на 1,23 сутки (20,1%) статистически достоверно быстрее восстанавливалась подвижность и на 1,21 сутки (13,8%) быстрее наступала ремиссия. Также установлено, что по истечении девяносто суток после завершения консервативного лечения у собак из первой группы зафиксировано два рецидива, а у животных из второй группы - один рецидив, соответственно.
В результате проведенного исследования установлено, что обострение течения заболевания при межпозвоночных грыжах в поясничном отделе у собак протекает на фоне значительной индукции процессов перекисного окисления липидов, снижения активности системы антиоксидантной защиты организма, незначительного уменьшения эритропоэза и умеренной воспалительной реакции, повышения уровня кортизола в крови, а клинически проявляется выраженным болевым синдромом, нарушением двигательной активности и походки. Применение при данном заболевании в комплексе со средствами патогенетической консервативной терапии антиоксидантного препарата для лечения и профилактики неврологических патологий у животных позволяет добиваться более выраженного терапевтического эффекта по сравнению со стандартной схемой лечения.
Преимущества предлагаемого антиоксидантного препарата для лечения и профилактики неврологических патологий у животных в том, что он содержит в комплексе производное 3-оксипиридина, в качестве которого используют метилэтилпиридинола гидрохлорид, 2-оксо-1-пирролидинацетамид, пиридоксина гидрохлорид, рибофлавина мононуклеотид, поливинилпирролидон и воду для инъекций, что значительно повышает его эффективность, а стабильный водный раствор и концентрация действующего вещества в нем, делает его удобным в дозировании и применении животным.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие технические преимущества:
- повышенный антиоксидантный эффект;
- повышенный антигипоксантный эффект;
- наличие церебропротекторного эффекта;
- наличие нейротрофического эффекта;
- комплексное действие;
- повышение терапевтической эффективности;
- снижение токсичности;
- стабильность лекарственной формы;
- удобство введения и дозирования.

Изобретение относится к ветеринарной фармации, в частности к препаратам для лечения и профилактики неврологических патологий у животных. Антиоксидантный препарат для лечения и профилактики неврологических патологий у животных включает компоненты в следующем соотношении, мас.%: производное 3-оксипиридина, в качестве которого используют метилэтилпиридинола гидрохлорид 0,8-1,2, 2-оксо-1-пирролидинацетамид 7,0-11,0, пиридоксина гидрохлорид 0,24-0,32, рибофлавина мононуклеотид 0,018-0,038, поливинилпирролидон 2,5-4,5, вода для инъекций - остальное. Предлагаемый антиоксидантный препарат для лечения и профилактики неврологических патологий у животных имеет выраженное антиоксидантное, антигипоксантное, церебропротекторное и нейротрофическое действие, низкую токсичность и высокую эффективность в профилактике и лечении неврологических заболеваний у животных, стабильность лекарственной формы, удобство введения и дозировки. 6 ил., 7 пр.
Антиоксидантный препарат для лечения и профилактики неврологических патологий у животных, включающий производное 3-оксипиридина, пиридоксина гидрохлорид и воду для инъекций, отличающийся тем, что дополнительно содержит 2-оксо-1-пирролидинацетамид, рибофлавина мононуклеотид и поливинилпирролидон, а в качестве производного 3-оксипиридина используют метилэтилпиридинола гидрохлорид при следующем соотношении компонентов в мас.%:
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТА И ПИРИДОКСИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2383331C1 |
| СОСТАВ И СПОСОБ ПОЛУЧЕНИЯ ИНФУЗИОННОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ НА ОСНОВЕ МЕТИЛЭТИЛПИРИДИНОЛА | 2011 |
|
RU2455003C1 |
| КОМБИНАЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ, ЛИПИДРЕГУЛИРУЮЩЕЙ И ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2453314C1 |
| КОМБИНИРОВАННЫЙ ПРЕПАРАТ ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ, СОДЕРЖАЩИЙ ГИДРОХЛОРИД ИЛИ СУКЦИНАТ МЕТИЛЭТИЛПИРИДИНОЛА И РИБОФЛАВИН | 2014 |
|
RU2566725C1 |
| US 20080254017 A1, 16.10.2008 | |||
| US 20210330611 A1, 28.10.2021. | |||
Авторы
Даты
2024-02-19—Публикация
2023-09-12—Подача