Изобретение относится к медицине, а именно к челюстно-лицевой хирургии, и может быть использовано при лечении венозных, капиллярно-венозных, артерио-венозных мальформаций и гиперплазии кровеносных сосудов (т.н. младенческая гемангиома) в стадии резидуальных проявлений в области головы или шеи. Вопросы лечения поражений кровеносных сосудов у детей в области головы или шеи (таких как венозные, капиллярно-венозные, артерио-венозные мальформаций, гиперплазии кровеносных сосудов (т.н. младенческая гемангиома)), до настоящего времени актуальны во всем мире, так как ни один из существующих методов, в том числе хирургический, не может полностью устранить клинические проявления и достичь стабильных результатов. До недавнего времени хирургическое иссечение являлось основным методом лечения патологических сосудистых образований в челюстно-лицевой области у детей. Заявленный способ лечения позволяет повысить эффективность хирургического лечения.
Известен способ деструкции сосудистых мальформаций путем радиочастотной абляции аппаратом «Cool-tip RF Ablation System».
Способ осуществляется за счет радиочастотной абляции субстрата сосудистой мальформаций игольчатым электродом под ультразвуковым контролем в течение 3-15 с из одного прокола в нескольких направлениях или из нескольких вколов до достижения сопротивления коагулированных тканей 350-600 Ом. (Рогинский В.В., Овчинников И.А., Надточий. А.Г. 2011 г., патент РФ №2476249).
Недостатком данного метода является большой риск возникновения некроза как патологических, так и окружающих здоровых тканей за счет термического ожога, а также возникновения аррозивного кровотечения в послеоперационном периоде из пораженных тканей в области хирургического вмешательства вследствие некроза.
Известен способ лечения объемных сосудистых и нейропластических образований методом электрокоагуляции. На патологически измененную ткань инвазивно воздействуют источником электрического тока с помощью активного электрода. Время воздействия 1-3 сек., температура 60-70 С. При этом происходит коагуляция патологически измененных тканей (Федореев Г.А. Гемангиомы кожи у детей. Л. 1971, с. 99-103).
Недостатками данного способа являются небольшие объемы коагуляции патологически измененных тканей под активным электродом, так как воздействию подвергаются лишь те участки ткани, которые непосредственно прилегают к активному электроду, вследствие чего необходимо многократно выполнять прокол пораженной области, что нежелательно в силу выраженной васкуляризации данных поражений. Кроме того, активный электрод в процессе воздействия подвергается обугливанию, что так же приводит к обугливанию близлежащих тканей. Также недостатком является длительность воздействия, что сказывается на времени нахождения пациента в состоянии наркоза, увеличивается расход медикаментозных средств. Помимо этого, происходит включение пациента в электрическую сеть и возможно появление тяжелых ожогов в области нейтрального электрода.
Наиболее близким к предложенному способу является способ лечения объемных сосудистых и нейропластических образований (Голубева С.Н. Интерстициальная лазерная коагуляция в комплексном лечении пациентов с аномалиями сосудистого и нейропластического генезов в области головы и шеи. Дисс. канд. мед. наук 2012 г., Патент РФ №2484786 (Способ лечения объемных сосудистых и нейропластических образований) Неробеев А.И., Надточий А.Г., Голубева С.Н.
Способ осуществляется за счет коагуляции с использованием инвазивного воздействия путем вкола в патологически измененную ткань световода неодимового лазера с длинной волны 1064 мкм, что приводит к рубцеванию и замещению фиброзной тканью. Коагуляцию осуществляют при мощности 18-25 Вт, частоте импульсов 50 Гц, температура кожного покрова 55-60°С, с последующим выводом продуктов распада с помощью дренажа. Способ позволяет проводить закрытые хирургические операции, предотвратить токсические осложнения, исключить грубые косметические повреждения.
Недостатком данного способа является возможный некроз кожного покрова в области воздействия, необходим контроль с использованием инфракрасного термометра Fluke 63, который позволяет измерять температуру кожного контроля над областью лазерного воздействия, для успешного выполнения коагуляции необходимо ее проводить из нескольких вколов, что не всегда выполнимо на лице у ребенка, учитывая небольшие площади кожного покрова, после проведения коагуляции патологических тканей необходимо дренирование раны через дополнительные разрезы, отсутствие прогнозированиялечения при обширных поражениях.
Техническим результатом данного изобретения является повышение функционального и эстетического эффектов и снижение травматичности способа. Поставленный технический результат достигается тем, что в способе лечения детей с поражениями кровеносных сосудов головы или шеи с использованием лазерной коагуляции, отличительной особенностью является то, что для концентрации эффекта открытым способом инвазивное воздействие на патологически измененную тканей осуществляется контактным или бесконтактным путем световода гольмиевого лазера с длиной волны 2100 нм и коагуляцией при мощности 2.5-20 Вт, частоте импульсов 15 Гц до повышения эхогенности в области воздействия и видимой коагуляции.
Способ осуществляется следующим образом.
Перед началом хирургического вмешательства оценивается объем и границы поражения путем анализа инструментальных исследований (УЗИ с допплеровским картированием, МРТ мягких тканей лица и шеи), на основании визуального и мануального осмотра, проведения функциональных проб (определение наличия и выраженности симптома наполнения и нагрузки).
Далее в условиях эндотрахеального наркоза проводится разрез с использованием скальпеля в зоне патологического очага, кожный или слизистый лоскут мобилизуется, патологические ткани удаляются полностью или частично с использованием ножниц, с последующей коррекцией оперируемой анатомической области лица или шеи, далее контактным или бесконтактым путем (поверхностное воздействие) проводится лазерная коагуляции остаточных патологических тканей с сосудами с использованием оптического волокна, диаметром кварцевой жилы 200 мкм, 365 мкм, 550 мкм. Если проводится контактное воздействие, то оптическое волокно вводится в патологические ткани на глубину до 1.5-2 см и проводится коагуляция, если проводится бесконтактное воздействие, то оптическое волокно располагается на расстоянии от патологической ткани на 0.5 мм и проводится коагуляция. Параметры воздействия прилазерной коагуляции составляют 15 Гц и мощность 2.5-20 Вт, в зависимости от объема и локализации патологических тканей. Процесс коагуляции сопровождается появлением зоны повышенной эхогенности у дистального конца кварцевой жилы, что визуально контролируется глазом и на экране ультразвукового аппарата. Диаметр этой зоны зависит от мощности выходной энергии и длительности экспозиции в данной точке.
В зависимости от оставшегося объема поражения после иссечения тканей и локализации патологического очага, лазерная коагуляция проводится контактным или бесконтактным способами.
Использование заявляемого способа позволяет достичь таких лечебных результатов как: проводить удаление патологических тканей с питающими сосудами в зоне очага в полном объеме за один этап, проводить совместно с удалением очага поражения коррекцию анатомической области с эстетическим результатом, полностью исключить осложнения в виде некроза кожных покровов в области воздействия.
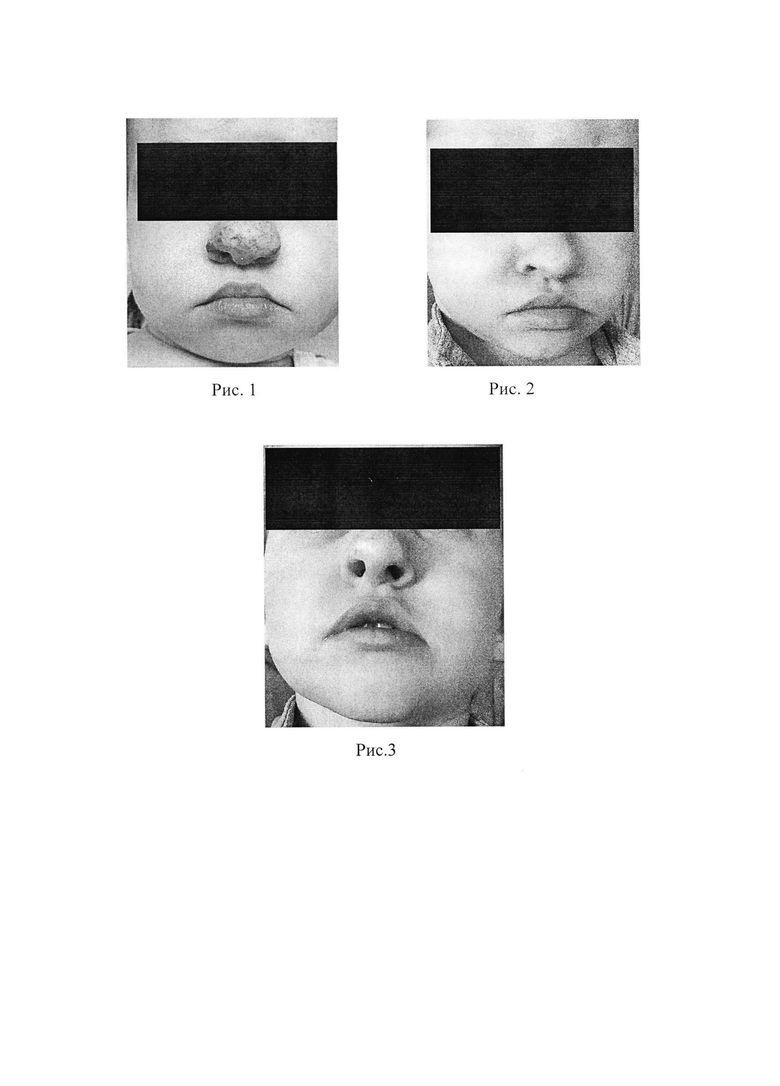
Пример 1. (Рис. 1-3)
Пациент Р., 2 года, находился на стационарном лечении в отделении хирургического лечения аномалий черепно-челюстно-лицевой области ФГБУ НМИЦ «ЦНИИСиЧЛХ» Минздрава России с диагнозом: Гиперплазия кровеносных сосудов (т.н. младенческая гемангиома) стадия резидуальных проявлений в области кончика носа».
Из анамнеза: красное пятно на коже кончике носа появилось через 1 неделю после рождения. С ростом ребенка пятно становилось ярко-красным, появился объем мягких тканей, изъязвления на коже в области кончика носа. С 2х месяцев до 1 года ребенок получал лечение бета-блокатором (Анаприлин), с положительной динамикой, окраска пятна стала бледно-розовой, но объем тканей не уменьшился в области кончика носа. С 1 года проводилось несколько сеансов склеротерапии раствором этоксисклерол, эффекта от лечения не было, объем тканей не изменился, форма кончика носа оставалась с избытком тканей, крыльные хрящи носа деформированы за счет давления избытка тканей на хрящи носа.
При внешнем осмотре пациента конфигурация лица и пропорции не нарушены. Отмечается увеличенный в размерах кончик носа за счет подкожного объемного сосудистого патологического образования, размерами до 1.5×1.5 см. Кожа над образованием в области кончика носа с множественными расширенными сосудами (остаточные телеангиэктазии), в центре кожа с участками побеления и мелкими рубцами. При пальпации мягких тканей в области кончика носа отмечается мягко-эластичной консистенции избыток тканей, пальпируется диастаз крыльных хрящей носа. Симптомы нагрузки и наполнения отрицательные. Носовые ходы суженные за счет деформации крыльных хрящей носа. Мимические пробы выполняет в полном объеме с двух сторон. Открывание рта в полном объеме, безболезненно. Слизистая оболочка полости рта бледно-розового цвета, умеренно увлажнена.
В стационаре, после клинико-лабораторного обследования и консультации смежных специалистов проведена хирургическая операция по предложенной методике.
В рамках предоперационного планирования операции было выполнено УЗИ с допплеровским картированием с целью определения глубины поражения, наличия кровотока и расположение крыльных хрящей носа.
Протокол операции: в условиях операционной, под комбинированным эндотрахеальным наркозом, выполнена антисептическая обработка лица, шеи и полости рта.
Выполнен разрез с использованием скальпеля в области колумеллы, ниже зоны патологического очага, кожный лоскут мобилизован вверх, объем патологических тканей удален в полном объеме с использованием ножниц, проведена коррекцией кончика носа, далее бесконтактым путем проведена лазерная коагуляции остаточных патологических тканей с сосудами, без воздействия на хрящи носа с использованием оптического волокна, диаметром кварцевой жилы 200 мкм. Оптическое волокно располагается на расстоянии от патологической ткани с сосудами на 0.5 мм и проводится коагуляция. Параметры воздействия при лазерной коагуляции составляют 15 Гц и мощность 2.5 Вт. Процесс коагуляции сопровождается появлением зоны повышенной эхогенности у дистального конца кварцевой жилы, что визуально контролируется глазом и на экране ультразвукового аппарата. Крыльные хрящи носа сшиваются между собой нитью Лавсан 5/0 в правильное анатомическое положение. Кожный лоскут укладывается на место, избытки кожи иссекаются и накладываются швы на кожу Prolen 6/0. На кончик носа накладываются прошивные швы Prolen 4/0в количестве 2х штук. На кожу кончика носа накладывается пластырная повязка.
В послеоперационном периоде проведена антибактериальная, противовоспалительная, десенсибилизирующая, обезболивающая терапии и ежедневные перевязки. Швы удалены на 8-е сутки. Кожа кончика носа без признаков воспаления и участков некроза. При пальпации отмечалось уплотнение мягких тканей послеоперационной области в сравнении с дооперационным состоянием. На 10-е сутки после операции и снятия швов отмечалось значительное уменьшение отека и объема патологических тканей. При проведении контроля УЗИ через 1 месяц в зоне оперативного вмешательства определяется фиброзная ткань и правильное расположение крыльных хрящей носа. При пальпации кончика носа постоперационные ткани плотные, кожа нормальной окраски и текстуры. Через 3 месяца после операции при контрольном УЗИ визуализируется фиброзно-соединительная ткань в области кончика носа.
В результате операции было выполнено полное иссечение избытка патологической ткани с питающими сосудами в дополнении с использованием лазерной коагуляции. Используя предложенную методику, удалось достигнуть функционального и эстетического результатов, уменьшения объема кончика носа, полностью за одну операции удалить все патологические ткани без повреждения кожных покровов, провести коррекцию крыльных хрящей носа с установкой их в правильное анатомическое положение.
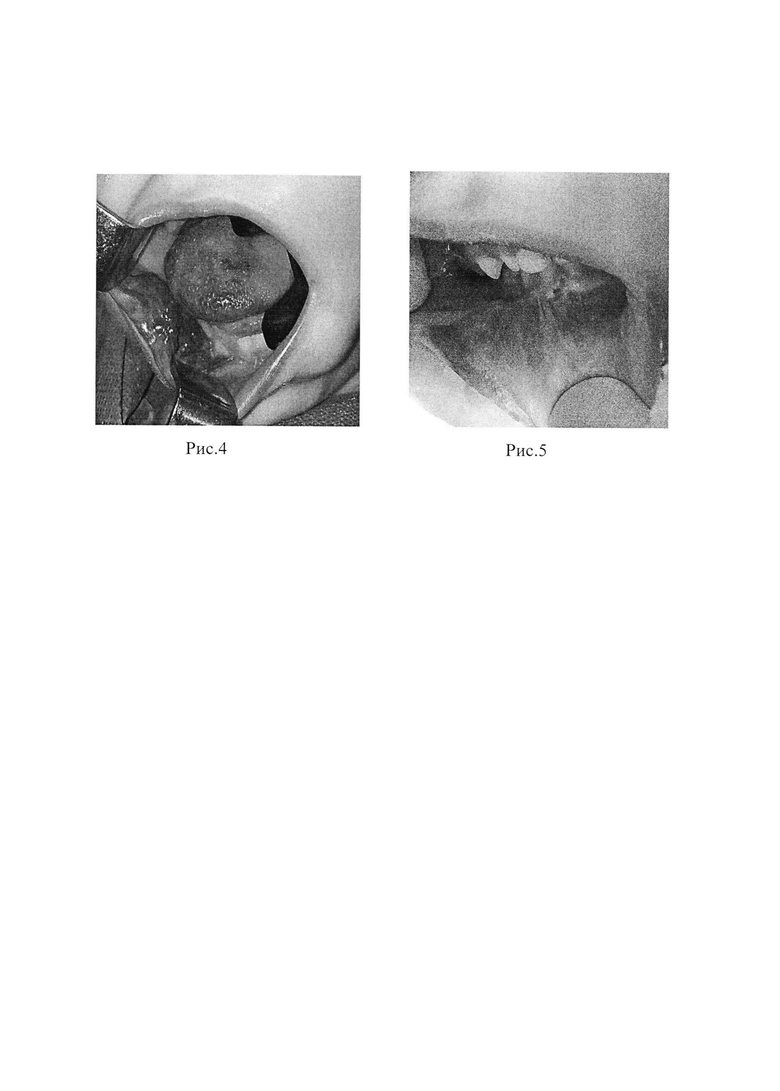
Пример 2. (Рис. 4-5)
Пациент С., 1 год, находился на стационарном лечении в отделении хирургического лечения аномалий черепно-челюстно-лицевой области ФГБУ НМИЦ «ЦНИИСиЧЛХ» Минздрава России с диагнозом: Обширная венозная мальформация правой щечной, околоушно-жевательной областей, угла рта, нижней губы справа, дна полости рта и языка справа»
Из анамнеза: заболевание врожденное, ранее оперативных вмешательств не проводилось.
При внешнем осмотре пациента отмечается выраженная асимметрия лица за счет увеличения объема мягких тканей правой половины лица, (околоушно-жевательная, щечная области), с переходом на угол рта, нижнюю губу справа, с переходом на слизистую оболочку нижней губы, щеки и альвеолярного отростка справа. Мягкие ткани в перечисленных областях «выстоят» над окружающими на 1-1.5 см, кожа в околоушно-жевательной области синюшного цвета. При пальпации патологические ткани мягко-эластичной консистенции, безболезненные, симптом наполнения и нагрузки резко положительные, патологической пульсации не определяется. Мимические пробы выполняет в полном объеме с обеих сторон. Осмотр полости рта: прикус временный. Слизистая оболочка в щечной области, с переходом на угол рта, нижнюю губу и альвеолярный отросток справа синюшно-багрового цвета, имеет бугристую поверхность, выраженно увеличена в объеме. При пальпации патологические ткани мягко-эластичной консистенции, безболезненные, симптом наполнения и нагрузки резко положительные, патологической пульсации не определяется. Правая половина языка синюшного цвета, язык увеличен справа на 1.5 см, симптом наполнения и нагрузки резко положительные.
В рамках предоперационного планирования операции было выполнено УЗИ с допплеровским картированием, МРТ мягких тканей лица и шеи, с целью определения глубины, распространенности поражения и наличия кровотока.
В стационаре, после клинико-лабораторного обследования и консультации смежных специалистов проведена хирургическая операция по предложенной методике.
Протокол операции: в условиях операционной, под комбинированным эндотрахеальным наркозом, выполнена антисептическая обработка лица, шеи и полости рта.
Выполнен разрез с использованием скальпеля в области слизистой оболочки щеки, с переходом на правую половину нижней губы, над зоной патологического очага, края раны мобилизованы, объем патологических тканей частично удален с использованием тупоконечных ножниц, далее контактным путем проведена лазерная коагуляции остаточных патологических тканей и сосудов, с использованием оптического волокна диаметром кварцевой жилы 550 мкм, оптическое волокно вводится в патологические ткани на глубину до 1,5 см и проводится коагуляция, Параметры воздействия при лазерной коагуляции составляют 15 Гц и мощность 20 Вт. Процесс коагуляции сопровождается появлением зоны повышенной эхогенности у дистального конца кварцевой жилы, что визуально контролируется глазом и на экране ультразвукового аппарата. Края раны укладывается на место, избытки слизистой оболочки иссекаются и накладываются рассасывающиеся швы Viclyl 4/0 на слизистую оболочку щечной области и нижней губы. На кожу щечной области, с переходом на подбородочную область накладывают пластырную силиконовую повязку.
В послеоперационном периоде проведена антибактериальная, противовоспалительная, десенсибилизирующая, обезболивающая терапии и ежедневные перевязки. Швы на слизистой оболочке щеки удалены на 12-е сутки. Кожа щечной области, угла рта, нижней губы без признаков воспаления и участков некроза. При пальпации отмечалось уплотнение мягких тканей послеоперационной области в сравнении с дооперационным состоянием. На 12-е сутки после операции и снятия швов отмечалось значительное уменьшение отека и объема патологических тканей. При проведении контроля УЗИ через 1 месяц в зоне оперативного вмешательства определяется фиброзная ткань. При пальпации постоперационные ткани плотные, кожа нормальной окраски и текстуры. Через 3 месяца после операции при контрольном УЗИ визуализируется фиброзно-соединительная ткань в области щеки, нижней губы справа. Слизистая оболочка щеки и нижней губы бледно-розового цвета.
В результате операции была выполнена частичная деструкция венозной мальформаций правых щечной, околоушно-жевательнойобластей, в области нижней губы. Используя предложенную методику, удалось достигнуть частичного разобщения патологического кровотока, ишемизации патологических тканей и уплотнения патологических тканей. Далее пациенту планируется еще несколько этапов операций по предложенной методике для достижения оптимального результата.
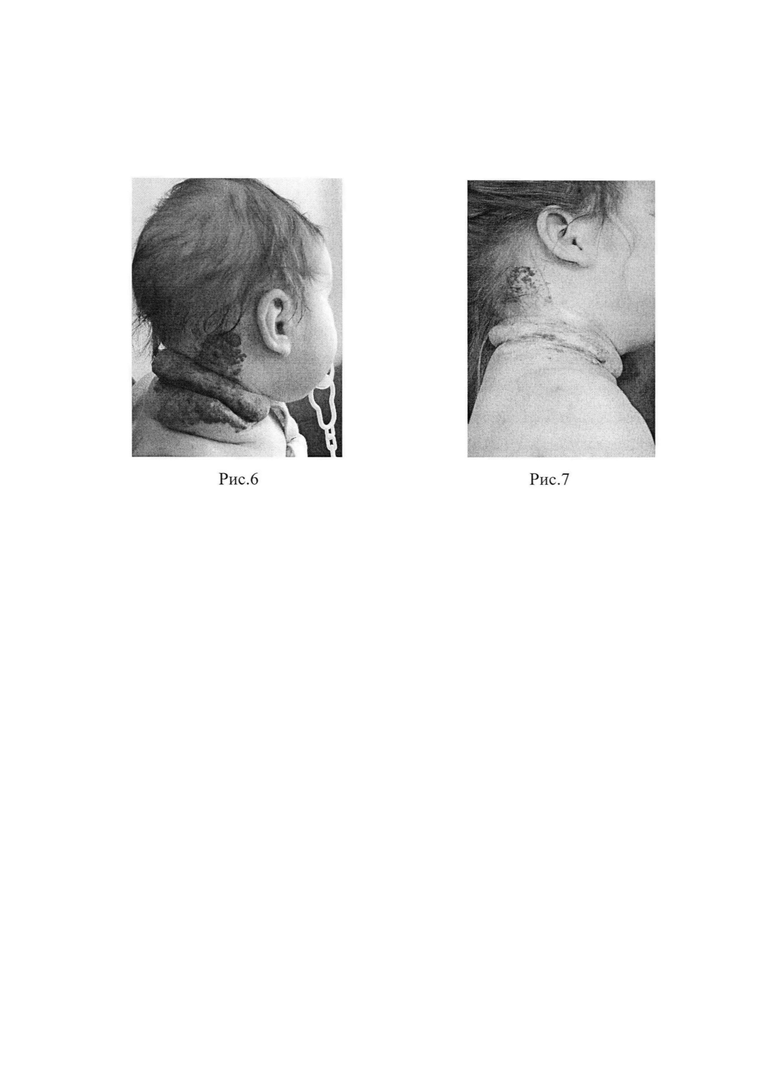
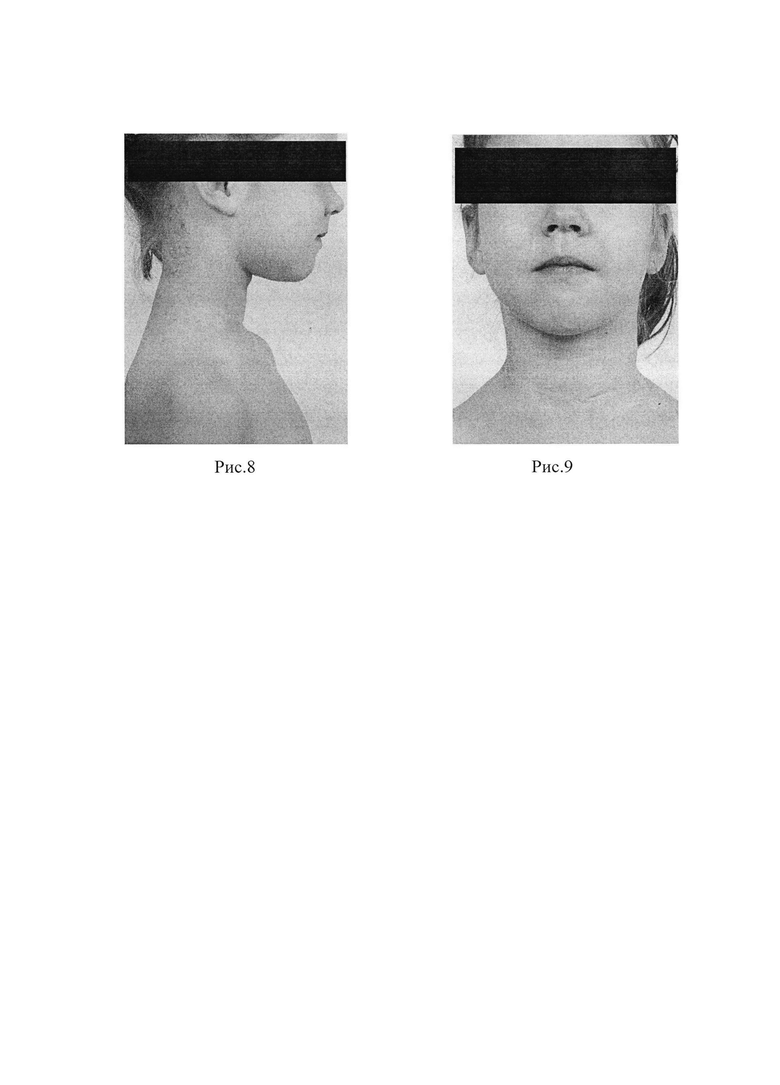
Пример 3. (Рис. 6-9)
Пациентка С., 2 год 5 мес., находилась на стационарном лечении в отделении хирургического лечения аномалий черепно-челюстно-лицевой области ФГБУ НМИЦ «ЦНИИС и ЧЛХ» Минздрава России с диагнозом: Гиперплазия кровеносных сосудов (т.н. младенческая гемангиома) стадия резидуальных проявлений в области задней, боковой, передней поверхностей шеи.
Из анамнеза: красное пятно на коже в области шеи справа появилось через 1.5 недели после рождения. С ростом ребенка пятно становилось ярко-красным, отмечался быстрый рост патологического образования, появился объем мягких тканей в передней, боковой, задней поверхности шеи. С 3-х месяцев до 1 года ребенок получал лечение бета-блокатором (Пропранолол), с положительной динамикой, окраска пятна стала бледно-розовой, но объем тканей не уменьшился в области шеи справа. В 1 год 8 месяцев проводилось оперативное лечение в объеме - частичное удаление патологических тканей в области шеи справа с закрытием дефекта местными тканями.
При внешнем осмотре пациентки конфигурация лица и пропорции не нарушены. Отмечается увеличенный в размерах передний, боковой, задний отдел шеи за счет подкожного объемного сосудистого патологического образования, размерами 15×4×2 см. Кожа над образованием в области шеи справа с множественными расширенными сосудами (остаточные телеангиэктазии), в центре кожа с участками побеления и послеоперационным линейным рубцом. При пальпации мягких тканей в области шеи справа отмечается мягко-эластичной консистенции избыток тканей, собирающийся в складку. Симптомы нагрузки и наполнения отрицательные. Мимические пробы выполняет в полном объеме с двух сторон. Открывание рта в полном объеме, безболезненно. Слизистая оболочка полости рта бледно-розового цвета, умеренно увлажнена.
В рамках предоперационного планирования операции было выполнено УЗИ с допплеровским картированием, МРТ мягких тканей лица и шеи, с целью определения глубины, распространенности поражения и наличия кровотока.
В стационаре, после клинико-лабораторного обследования и консультации смежных специалистов проведена хирургическая операция по предложенной методике.
Протокол операции: в условиях операционной, под комбинированным эндотрахеальным наркозом, выполнена антисептическая обработка лица, шеи и полости рта.
Выполнены два сходящихся разреза с использованием скальпеля в области передней, боковой, задней поверхностей шеи, над зоной патологического очага, края раны мобилизованы, объем патологических тканей полностью удален с использованием тупоконечных ножниц, далее бесконтактным путем проведена лазерная коагуляции остаточных патологических тканей и сосудов, с использованием оптического волокна диаметром кварцевой жилы 365 мкм, оптическое волокно располагается на расстоянии от патологической ткани с сосудами на 0.5 мм и проводится коагуляция. Параметры воздействия при лазерной коагуляции составляют 15 Гц и мощность 15 Вт. Процесс коагуляции сопровождается появлением зоны повышенной эхогенности у дистального конца кварцевой жилы, что визуально контролируется глазом и на экране ультразвукового аппарата. Края раны укладывается на место, избытки кожи иссекаются и накладываются нерассасывающиеся швы Prolen 5/0 на кожу шеи справа. На область шеи накладывают полуспиртовую бинтовую повязку.
В послеоперационном периоде проведена антибактериальная, противовоспалительная, десенсибилизирующая, обезболивающая терапии и ежедневные перевязки. Швы на шее удалены на 13-е сутки. Кожа в области шеи справа без признаков воспаления и участков некроза. При пальпации отмечалось уплотнение мягких тканей послеоперационной области в сравнении с дооперационным состоянием. На 13-е сутки после операции и снятия швов отмечалось значительное уменьшение отека и объема патологических тканей. При проведении контроля УЗИ через 1 месяц в зоне оперативного вмешательства определяется фиброзная ткань. При пальпации постоперационные ткани плотные, кожа нормальной окраски и текстуры. Через 3 месяца после операции при контрольном УЗИ визуализируется фиброзно-соединительная ткань в области шеи справа. Кожа в области шеи справа бледно-розового цвета.
В результате операции было выполнено полное иссечение избытка патологической ткани с питающими сосудами в дополнении с использованием лазерной коагуляции. Используя предложенную методику, удалось достигнуть функционального и эстетического результатов, уменьшения объема тканей в области передней, боковой, задней поверхностей шеи справа, полностью за одну операции удалить все патологические ткани без повреждения кожных покровов, провести коррекцию мягких тканей шеи справа в правильное анатомическое положение.
Предлагаемый способ имеет ряд преимуществ, таких как:
- может быть эффективно использован в лазерной хирургии при лечении объемных сосудистых образований, таких как гиперплазия кровеносных сосудов (т.н. младенческая гемангиома), различные сосудистые мальформаций;
- метод позволяет достичь полного удаления патологического очага с сосудами при комбинированном методе: хирургический с лазерной коагуляцией, с последующей коррекцией анатомической области лица или шеи, что обуславливает высокий функциональный и эстетический результат;
- проведение бесконтактного воздействия при проведении лазерной коагуляции позволяет избежать осложнений, таких как ожог кожи или хрящей.
- проведение бесконтактного воздействия при проведении лазерной коагуляции проводится под контролем глаз хирурга, что позволяет проводит манипуляцию с точностью в заданном направлении.
- наличие ультразвукового визуального контроля позволяет эффективно проводить процесс коагуляции патологических тканей;
- возможность уменьшения количества этапов лечения;
- отсутствие необходимости проведения гемотрансфузии, что является профилактикой инфицирования ВИЧ и гепатитами В, С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения детей с капиллярными мальформациями в области лица с использованием комбинированного метода | 2022 |
|
RU2814408C1 |
| Способ деструкции венозных и лимфовенозных мальформаций путем прошивания, склерозирования и компрессии | 2021 |
|
RU2780546C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РИНОФИМЫ | 2012 |
|
RU2492834C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВРОЖДЕННЫХ РАСЩЕЛИН ВЕРХНЕЙ ГУБЫ (ВАРИАНТЫ) | 2010 |
|
RU2440042C1 |
| Способ лечения детей с пороками развития челюстно-лицевой области после хейлоуранопластики | 2017 |
|
RU2704915C2 |
| Способ одномоментной двусторонней хейлоринопластики при асимметричной двусторонней расщелине верхней губы | 2019 |
|
RU2710857C1 |
| Способ реконструкции дефекта крыла носа у детей | 2024 |
|
RU2835126C1 |
| Способ удаления артериовенозной мальформации нижней челюсти | 2023 |
|
RU2812016C1 |
| Способ формирования кончика носа при односторонней расщелине верхней губы | 2022 |
|
RU2831769C2 |
| СПОСОБ ФОРМИРОВАНИЯ НАРУЖНОГО НОСОВОГО КЛАПАНА У ДЕТЕЙ ПОСЛЕ ХЕЙЛОУРАНОПЛАСТИКИ | 2016 |
|
RU2632783C1 |
Изобретение относится к медицине, а именно к педиатрии и хирургии, и может быть использовано для лечения сосудистых мальформаций и гиперплазии кровеносных сосудов у детей. Проводят удаление патологической ткани, после чего производят лазерную коагуляцию остаточных патологических тканей с сосудами, при помощи оптического волокна гольмиевого лазера с длиной волны 2100 нм, диаметром кварцевой жилы 200 мкм, 365 мкм, 550 мкм. Способ позволяет снизить травматичность, повысить функциональный и эстетический эффект, достичь полного удаления патологического очага с сосудами за счет комбинации хирургических и лазерных методов воздействия на патологические ткани. 2 з.п. ф-лы, 9 ил., 3 пр.
1. Способ лечения сосудистых мальформаций и гиперплазии кровеносных сосудов у детей с использованием лазерной коагуляции, включающий определение объема поражения путем визуального и мануального осмотра, отличающийся тем, что далее под эндотрахеальным наркозом в зоне патологического очага проводят разрез с использованием скальпеля, мобилизируют кожный или слизистый лоскут и с использованием ножниц удаляют патологические ткани, далее контактным или бесконтактным путём проводят лазерную коагуляцию, остаточных патологических тканей с использованием оптического волокна гольмиевого лазера с длиной волны 2100 нм, диаметром кварцевой жилы 200 мкм или 365 мкм или 550 мкм, с мощностью 2,5-20 Вт и частотой импульсов 15 Гц, появление зоны повышенной эхогенности у дистального конца кварцевой жилы контролируют визуально и на экране ультразвукового аппарата.
2. Способ по п.1, отличающийся тем, что при проведении контактного воздействия оптическое волокно вводят в патологические ткани на глубину до 2 см.
3. Способ по п.1, отличающийся тем, что при проведении бесконтактного воздействия оптическое волокно располагают на расстоянии 0.5 мм от патологической ткани.
| ГАВЕЛЯ Е.Ю | |||
| Комплексное лечение детей с различными поражениями кровеносных сосудов головы и шеи | |||
| Стоматология | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| Т | |||
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| С | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Способ удаления поверхностной мелкокистозной формы лимфатической или лимфовенозной мальформации языка | 2017 |
|
RU2676832C2 |
| Способ склеротерапии микропенной артерио-венозных мальформаций челюстно-лицевой области пациента под ультразвуковым контролем | 2018 |
|
RU2693344C1 |
| ПЕТУХОВ А.В | |||
| Способ удаления поверхностной мелкокистозной формы лимфатической или лимфовенозной мальформации языка у детей | |||
| Голова и шея | |||
| Российское | |||
Авторы
Даты
2024-02-28—Публикация
2022-12-16—Подача