ОБЛАСТЬ ТЕХНИКИ
[0001]
Настоящее изобретение относится к ионному проводнику, содержащему высокотемпературную фазу LiCB9H10, и к способу его получения.
УРОВЕНЬ ТЕХНИКИ
[0002]
За последнее время спрос на литиево-ионные перезаряжаемые аккумуляторы вырос в различных областях, включая переносные информационные терминалы, переносное электронное оборудование, электрические транспортные средства, гибридные электрические транспортные средства и стационарные системы накопления энергии. Однако в настоящее время в качестве электролитического раствора в литиево-ионные перезаряжаемых аккумуляторах используют горючий органический растворитель, и необходим прочный внешний корпус для предотвращения утечки органического растворителя. Кроме того, например, в случае портативных персональных компьютеров необходимо использовать предохраняющую конструкцию на случай возможной утечки органического растворителя. Таким образом, существует ограничение в отношении конструкций устройств.
[0003]
Кроме того, диапазон их применения расширен до подвижных объектов, таких как транспортные средства и воздушные летательные аппараты, а для стационарных литиево-ионных перезаряжаемых аккумуляторов необходима высокая емкость. В таких обстоятельствах важно уделять больше внимания безопасности, чем раньше, и все усилия сконцентрированы на разработке полностью твердотельных литиево-ионных перезаряжаемых аккумуляторов, в которых нет никаких токсичных веществ, таких как органические растворители.
Например, изучено применение оксидов, фосфатных соединений, органических полимеров, сульфидов, комплексных гидридов или т.п. в качестве твердого электролита в полностью твердотельных литиево-ионных перезаряжаемых аккумуляторах.
[0004]
Полностью твердотельные аккумуляторы упрощенно классифицируют на аккумуляторы тонкопленочного типа и объемного типа. В случае тонкопленочного типа связывание на границе раздела в идеале формируют с применением способа получения пленки в газовой фазе, но слой электрода является тонким (несколько мкм), площадь поверхности электрода является небольшой, количество энергии, которое может накапливаться в ячейке, является малым, а затраты высоки. Таким образом, они непригодны в качестве аккумуляторов для крупных устройств для накопления энергии или электрических транспортных средств, где необходимо накапливать большое количество энергии. В то же время в случае объемного типа толщину слоя электрода можно доводить до значения от нескольких десятков мкм до 100 мкм, и может быть получен полностью твердотельный аккумулятор с высокой плотностью энергии.
[0005]
Среди твердых электролитов выделяют сульфидные и комплексные гидриды, которые имеют такие характеристики, что они обладают высокой ионной проводимостью и являются относительно мягкими, и, следовательно, из них легко формировать границу раздела между твердыми элементами. По этой причине изучено их применение для полностью твердотельных аккумуляторов объемного типа (патентные документы 1 и 2).
[0006]
Однако обычные сульфидные твердые электролиты имеют такие характеристики, что они взаимодействуют с водой, и существуют проблемы образования сероводорода из сульфида и снижения ионной проводимости после их взаимодействия с водой. В то же время комплексные гидридные твердые электролиты обычно имеют несколько более низкую ионную проводимость, чем сульфидные твердые электролиты, и желательно улучшить их ионную проводимость.
[0007]
В непатентном документе 1 описан твердый электролит, имеющий высокую ионную проводимость, который описан как электролит «на основе карборана» (6,7 мСм/см, 25 °С), и в данном случае использован способ механического измельчения. Способ механического измельчения проблематичен для массового производства, и необходим способ промышленного синтеза с применением раствора. В то же время в непатентном документе 2 описан способ получения полностью твердотельного аккумулятора с превосходной производительностью, в котором раствор твердого электролита, в котором в качестве твердого электролита растворено боргидридное соединение, наносят на поверхность слоя положительного электрода и на поверхность слоя отрицательного электрода, которые будут обращены друг к другу в электроде, а затем удаляют растворитель и соединяют поверхности друг с другом с последующим прессованием при низком давлении.
[0008]
В непатентном документе 3 описан синтез твердого электролита с высокой ионной проводимостью, который назван электролитом «на основе карборана» (5 мСм/см при 35 °С), с применением водного растворителя, но он содержит не только высокотемпературную фазу LiCB9H10, но и фазу диплоэдров из LiCB9H10 и LiCB11H12. Кроме того, желательно дополнительно улучшить ионную проводимость.
ДОКУМЕНТЫ ИЗВЕСТНОГО УРОВНЯ ТЕХНИКИ
ПАТЕНТНЫЕ ДОКУМЕНТЫ
[0009]
Патентный документ 1: Японский патент № 6246816
Патентный документ 2: WO2017/126416
НЕПАТЕНТНЫЕ ДОКУМЕНТЫ
[0010]
Непатентный документ 1: Nature Communications, том 10, номер статьи: 1081 (2019)
Непатентный документ 2: 59-й Симпозиум Battery Symposium в Японии, 3BO4 Development of all-solid-state lithium battery using hydride-based solid electrolyte and battery characteristics thereof («Разработка полностью твердотельного литиевого аккумулятора с использованием твердого электролита на основе гидрида и его характеристики»)
Непатентный документ 3: ACS Energy Lett. 2016, 1, 659-664
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
ПРОБЛЕМЫ, РЕШАЕМЫЕ НАСТОЯЩИМ ИЗОБРЕТЕНИЕМ
[0011]
Задача настоящего изобретения заключается в обеспечении ионного проводника с превосходными различными характеристиками, включая ионную проводимость, и способа его получения.
СПОСОБЫ РЕШЕНИЯ ПРОБЛЕМ
[0012]
Авторами настоящего изобретения проведены активные исследования для решения вышеописанных проблем и обнаружено, что указанные проблемы могут быть решены с помощью ионного проводника, полученного с применением однородного раствора, полученного смешиванием в растворителе LiCB9H10 и LiCB11H12 друг с другом в определенном молярном соотношении. В частности, настоящее изобретение описано ниже.
<1> Способ получения ионного проводника, содержащего LiCB9H10 и LiCB11H12, включающий:
этап получения раствора для смешивания в растворителе LiCB9H10 и LiCB11H12 друг с другом в молярном соотношении LiCB9H10/LiCB11H12 от 1,1 до 20 с получением однородного раствора;
этап сушки для удаления растворителя из полученного однородного раствора с получением предшественника и
этап термической обработки для термической обработки предшественника с получением ионного проводника.
<2> Способ по п. <1>, согласно которому растворитель на этапе получения раствора представляет собой по меньшей мере одно, выбранное из группы, состоящей из воды, тетрагидрофурана, ацетонитрила, ацетона, этилацетата, метилацетата, толуола, метиленхлорида и хлороформа.
<3> Способ по п. <1>, согласно которому растворитель на этапе получения раствора состоит из воды.
<4> Способ по любому из пп. <1> - <3>, согласно которому время перемешивания и смешивания на этапе получения раствора составляет от 5 минут до 48 часов.
<5> Способ по любому из пп. <1> - <4>, согласно которому молярное соотношение между LiCB9H10 и LiCB11H12 (LiCB9H10/LiCB11H12) на этапе получения раствора составляет от 1,5 до 9.
<6> Способ по любому из пп. <1> - <5>, согласно которому температура на этапе сушки составляет от 50 до 260 °C.
<7> Способ по любому из пп. <1> - <6>, согласно которому время сушки на этапе сушки составляет от 1 до 24 часов.
<8> Способ по любому из пп. <1> - <7>, согласно которому температура на этапе термической обработки составляет от 150 до 260°С.
<9> Способ по любому из пп. <1> - <8>, согласно которому время нагревания на этапе термической обработки составляет от 1 до 24 часов.
<10> Способ по любому из пп. <1> - <9>, согласно которому полученный ионный проводник имеет однофазную кристаллическую структуру высокотемпературной фазы LiCB9H10.
<11> Способ по любому из пп. <1> - <10>, согласно которому полученный ионный проводник имеет пики рентгеновской дифракции при по меньшей мере 2θ=14,9±0,3 град, 16,4±0,3 град и 17,1±0,5 град на профиле рентгеновской дифракции при 25°С, и при этом отношение интенсивностей (B/A), рассчитанное в соответствии с выражениями: A=(интенсивность рентгеновской дифракции при 16,4±0,3 град)-(интенсивность рентгеновской дифракции при 20 град) и B=(интенсивность рентгеновской дифракции при 17,1±0,5 град)-(интенсивность рентгеновской дифракции при 20 град), составляет от 1,0 до 20.
<12> Способ по любому из пп. <1> - <11>, согласно которому полученный ионный проводник имеет ионную проводимость от 1,0 до 10 мСм/см при 25°C.
<13> Ионный проводник, полученный способом по любому из пп. <1> - <12>.
<14> Электрод, полученный с применением ионного проводника по п. <13>.
<15> Полностью твердотельный аккумулятор, полученный с применением ионного проводника по п. <13>.
ПОЛЕЗНЫЙ ЭФФЕКТ ИЗОБРЕТЕНИЯ
[0013]
В соответствии с настоящим изобретением, может быть обеспечен ионный проводник с превосходными различными характеристиками, включая ионную проводимость, и способ его получения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0014]
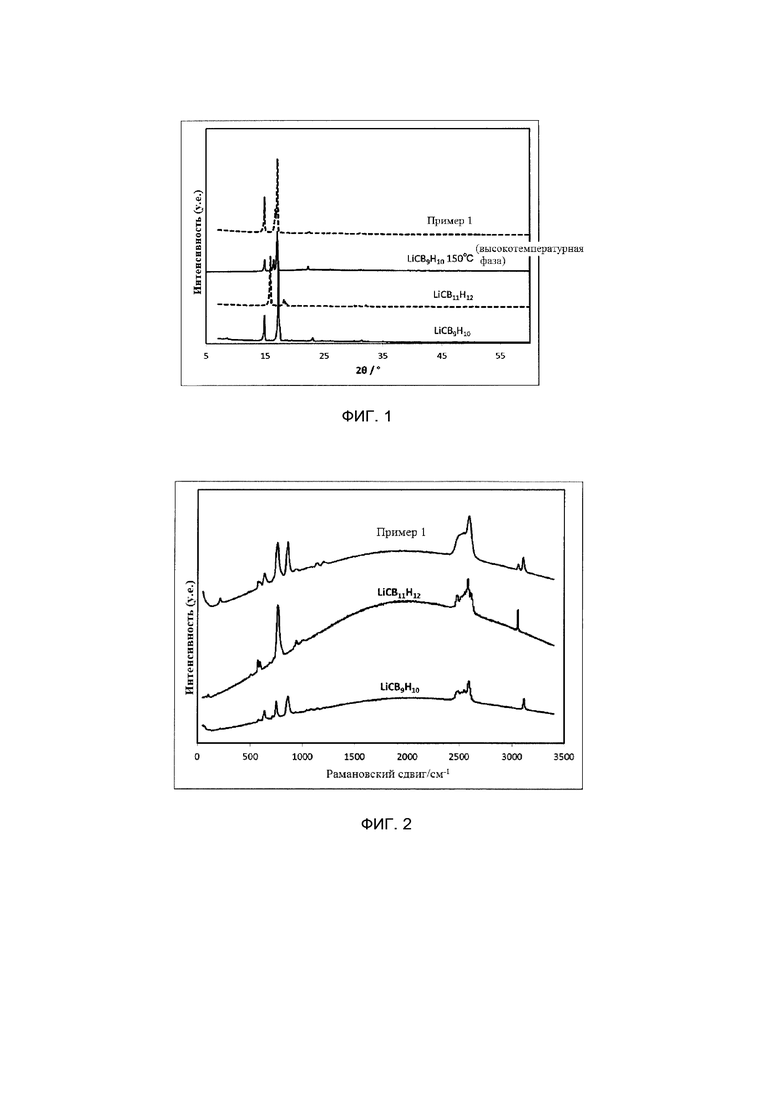
На фиг. 1 представлены пики рентгеновской дифракции порошка ионного проводника, полученного в примере 1.
На фиг. 2 представлен спектр Рамана ионного проводника, полученного в примере 1.
На фиг. 3 представлены результаты измерения ионной проводимости ионного проводника, полученного в примере 1.
На фиг. 4 представлены результаты измерения дифференциального термического анализа (ДТА), полученные в примере 1.
ВАРИАНТЫ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[0015]
Далее описаны варианты реализации настоящего изобретения. Следует отметить, что материалы, составы и т.д., описанные ниже, не ограничивают настоящее изобретение, и могут быть различным образом модифицированы в пределах сущности настоящего изобретения.
[0016]
1. Ионный проводник
В соответствии с одним вариантом реализации настоящего изобретения, предложен ионный проводник, содержащий литий (Li), углерод (C), бор (B) и водород (H). В одном варианте реализации предложенный ионный проводник предпочтительно содержит высокотемпературную фазу LiCB9H10 (фазу, имеющую высокую ионную проводимость) в виде кристалла, и более предпочтительно предложенный ионный проводник содержит высокотемпературную фазу LiCB9H10 (фазу, имеющую высокую ионную проводимость) в виде кристалла и состоит из LiCB9H10 и LiCB11H12.
[0017]
При рамановской спектроскопии ионный проводник согласно настоящему изобретению предпочтительно имеет пики, соответственно, при 749 см-1 (±5 см-1), который относится к LiCB9H10, и при 763 см-1 (±5 см-1), который относится к LiCB11H12. Ионный проводник может иметь пики в других областях, но пики, демонстрирующие его соответствующие характеристики, являются такими, как описано выше.
[0018]
Ионный проводник согласно настоящему изобретению предпочтительно содержит высокотемпературную фазу LiCB9H10 в виде кристалла. LiCB9H10 имеет высокотемпературную фазу и низкотемпературную фазу, которые зависят от его кристаллического состояния. Высокотемпературная фаза при высокой температуре (например, от примерно 75 до 150°С) имеет высокую ионную проводимость, но при примерно комнатной температуре (например, от примерно 20 до 65°С) она становится низкотемпературной фазой, и ионная проводимость уменьшается.
Ионный проводник согласно настоящему изобретению предпочтительно имеет пики рентгеновской дифракции на основе высокотемпературной фазы LiCB 9H10 при по меньшей мере 2θ=14,9±0,3 град., 16,4±0,3 град. и 17,1±0,5 град. в рентгеновской дифракции при 25°C. Более предпочтительно, отношение интенсивностей (B/A), рассчитанное в соответствии с выражениями: A=(интенсивность рентгеновской дифракции при 16,4±0,3 град)-(интенсивность рентгеновской дифракции при 20 град) и B=(интенсивность рентгеновской дифракции при 17,1±0,5 град)-(интенсивность рентгеновской дифракции при 20 град), предпочтительно составляет от 1,0 до 20, более предпочтительно от 1,0 до 15, и особенно предпочтительно от 1,0 до 10. Когда отношение интенсивностей (B/A) составляет от 1,0 до 20, температуру фазового перехода уменьшают путем твердого растворения LiCB11H12 в высокотемпературной фазе LiCB9H10, и состояние, в котором обеспечивается высокая ионная проводимость, может поддерживаться даже при почти комнатной температуре. Образование твердого раствора происходит при молярном соотношении LiCB9H10/LiCB11H12 1,1 или более. Предпочтительно, отношение LiCB9H10/LiCB11H12 составляет от 1,1 до 20, более предпочтительно от 1,25 до 10, и особенно предпочтительно от 1,5 до 9. В вышеописанном диапазоне значение ионной проводимости является высоким.
Следует отметить, что требуемый эффект достигается, даже если ионный проводник согласно настоящему изобретению содержит пики рентгеновской дифракции, отличные от вышеуказанных пиков.
Кроме того, ионный проводник согласно настоящему изобретению может содержать компоненты, отличные от лития (Li), углерода (С), бора (B) и водорода (H). Примеры других компонентов включают в себя кислород (O), азот (N), серу (S), фтор (F), хлор (Cl), бром (Br), йод (I), кремний (Si), германий (Ge), фосфор (P), щелочные металлы и щелочноземельные металлы.
[0019]
Вышеописанный ионный проводник является мягким, и из него можно формовать слой электрода и слой твердого электролита методом холодного прессования. Кроме того, слой электрода и слой твердого электролита, полученные таким образом, обладают повышенной прочностью по сравнению со случаем использования большого количества сульфидного твердого электролита или оксидного твердого электролита. Соответственно, при использовании ионного проводника согласно настоящему изобретению может быть получен слой электрода и слой твердого электролита, которые обладают превосходной формуемостью и стойкостью к разрушению (растрескивание маловероятно). Кроме того, поскольку ионный проводник согласно настоящему изобретению имеет низкую плотность, то может быть получен относительно легкий слой электрода и слой твердого электролита. Это является предпочтительным, поскольку таким образом может быть снижена общая масса аккумулятора. Кроме того, если ионный проводник согласно настоящему изобретению использован в слое твердого электролита, то может быть снижено сопротивление переходного слоя между ним и слоем электролита.
Кроме того, вышеописанный ионный проводник не разлагается даже при приведении его в контакт с влагой или кислородом, и не образуются опасные токсичные газы.
[0020]
Ионный проводник согласно настоящему изобретению имеет ионную проводимость при 25°С, которая предпочтительно составляет от 1,0 до 10 мСм/см, и более предпочтительно от 2,0 до 10 мСм/см.
[0021]
2. Способ получения ионного проводника
В соответствии с другим вариантом реализации настоящего изобретения, предложен способ получения ионного проводника, содержащего LiCB9H10 и LiCB11H12, включающий: этап получения раствора для смешивания в растворителе LiCB9H10 и LiCB11H12 друг с другом в молярном соотношении от 1,1 до 20 с получением однородного раствора; этап сушки для удаления из однородного раствора растворителя с получением предшественника; и этап термической обработки для термической обработки предшественника с получением ионного проводника.
В контексте настоящего изобретения «однородный раствор» определяют как раствор, который содержит по меньшей мере литий (Li), углерод (C), бор (B) и водород (H) в растворителе, причем в осадок не выпадает нерастворенное вещество, и при этом сырьевые материалы находятся в таком состоянии, что они растворены в растворителе.
[0022]
В качестве сырьевых материалов LiCB9H10 и LiCB11H12 можно использовать обычные продукты, доступные в продаже. Кроме того, их чистота предпочтительно составляет 95% или более, и более предпочтительно 98% или более. Требуемый кристалл можно без труда получить при использовании соединений, имеющих чистоту в вышеуказанном диапазоне.
[0023]
В отношении соотношения смешивания LiCB9H10 и LiCB11H12, молярное отношение LiCB9H10/LiCB11H12 должно составлять 1,1 или более. Предпочтительно, отношение LiCB9H10/LiCB11H12 составляет от 1,1 до 20, более предпочтительно от 1,25 до 10, и особенно предпочтительно от 1,5 до 9. Как описано выше, в вышеуказанном диапазоне значение ионной проводимости является особенно высоким.
[0024]
LiCB9H10 и LiCB11H12 можно смешивать друг с другом в однородном растворителе в определенной атмосфере.
[0025]
В отношении способа смешивания, его можно осуществлять в растворителе. Растворитель не имеет специального ограничения, и его примеры включают воду, растворитель на основе нитрила, такой как ацетонитрил, растворитель на основе простого эфира, такой как тетрагидрофуран и диэтиловый эфир, N,N-диметилформамид, N,N-диметилацетамид, растворитель на основе спирта, такой как метанол и этанол, ацетон, этилацетат, метилацетат, толуол, метиленхлорид и хлороформ. Среди указанных растворителей с точки зрения безопасности особенно предпочтительной является вода.
[0026]
Время смешивания в растворителе варьируется в зависимости от способа смешивания, но в случае перемешивания и смешивания в растворителе время смешивания предпочтительно составляет от 5 минут до 48 часов, и более предпочтительно от 5 минут до 1 часа.
[0027]
Давление на этапе получения раствора обычно составляет от 0,1 Па до 2 МПа абсолютного давления. Предпочтительно, давление составляет от 101 кПа до 1 МПа.
Этап получения раствора предпочтительно осуществляют в атмосфере инертного газа или в достаточно сухой атмосфере. Инертный газ не имеет специального ограничения, но особенно предпочтительным является аргон.
[0028]
Температура сушки растворителя на этапе сушки обычно составляет от 50 до 300°С, предпочтительно от 50 до 260°С, и более предпочтительно от 150 до 220°С.
Время сушки растворителя на этапе сушки незначительно варьируется в зависимости от типа растворителя и температуры сушки, но растворитель может быть в достаточной степени удален высушиванием в течение от 1 до 24 часов. Более предпочтительно, время сушки растворителя составляет от 10 до 14 часов. Следует отметить, что при удалении растворителя при пониженном давлении, как в случае вакуумной сушки, и посредством пропускания потока инертного газа, такого как азот и аргон, в котором содержание влаги является достаточно низким, температура при указанном времени удаления органического растворителя может быть снижена, а необходимое время может быть сокращено. Следует отметить, что этап термической обработки в качестве последующего этапа и этап сушки можно осуществлять одновременно.
[0029]
Состояние после сброса давления на этапе сушки растворителя обычно составляет 10-1 Па или менее, и предпочтительно 5×10-4 Па или менее.
[0030]
На этапе термической обработки предшественник, полученный на этапе сушки, подвергают термической обработке с получением ионного проводника.
Температура сушки предпочтительно составляет от 150 до 260°С, и более предпочтительно от 180 до 220°С. Если температура ниже вышеуказанного диапазона, то требуемые кристаллы образуются с трудом, а если температура выше указанного диапазона, то могут образовываться другие кристаллы, отличные от требуемых кристаллов.
[0031]
Время нагревания несколько варьируется в зависимости от температуры нагревания, но обычно кристаллизация может протекать в достаточной степени, если время нагревания составляет от 1 до 24 часов. Не является предпочтительным проведение нагревания при высокой температуре в течение продолжительного периода времени, превышающего вышеописанный диапазон, поскольку существует риск изменения качества ионного проводника. Более предпочтительно, время нагревания составляет от 10 до 14 часов.
Нагревание можно осуществлять при давлении, составляющем от вакуумного давления до 1 МПа, или в атмосфере инертного газа, но предпочтительно его осуществляют под вакуумом. В качестве инертного газа можно использовать азот, гелий, аргон или т.п., и среди них предпочтительным является аргон. Согласно настоящему изобретению, термическую обработку можно осуществлять, например, в атмосфере аргона при 1 МПа, а не под вакуумом. Предпочтительно, содержание кислорода и влаги является низким.
[0032]
При рамановской спектроскопии ионный проводник, полученный способом получения согласно настоящему изобретению, предпочтительно имеет пики, соответственно, при 749 см-1 (±5 см-1), который относится к LiCB9H10, и при 763 см-1 (±5 см-1), который относится к LiCB11H12. Кроме того, ионный проводник имеет пики рентгеновской дифракции, которые относятся к высокотемпературной фазе LiCB9H10, при по меньшей мере 2θ=14,9±0,3 град, 16,4±0,3 град и 17,1±0,5 град на профиле рентгеновской дифракции при 25°С, и при этом отношение интенсивностей (B/A), рассчитанное в соответствии с выражениями: A=(интенсивность рентгеновской дифракции при 16,4±0,3 град)-(интенсивность рентгеновской дифракции при 20 град) и B=(интенсивность рентгеновской дифракции при 17,1±0,5 град)-(интенсивность рентгеновской дифракции при 20 град), предпочтительно составляет от 1 до 20, более предпочтительно от 1,0 до 15, и особенно предпочтительно от 1,0 до 10.
[0033]
3. Полностью твердотельный аккумулятор
Ионный проводник согласно настоящему изобретению можно использовать в качестве твердого электролита для полностью твердотельных аккумуляторов. Соответственно, в соответствии с одним вариантом реализации настоящего изобретения предложен твердый электролит для полностью твердотельных аккумуляторов, содержащий вышеописанный ионный проводник. Кроме того, в соответствии с другим вариантом реализации настоящего изобретения, предложен полностью твердотельный аккумулятор, который получен с применением вышеописанного твердого электролита для полностью твердотельных аккумуляторов.
[0034]
В данном описании полностью твердотельный аккумулятор представляет собой полностью твердотельный аккумулятор, в котором электрическую проводимость обеспечивают ионы лития, и, в частности, полностью твердотельный литиево-ионный перезаряжаемый аккумулятор. Полностью твердотельный аккумулятор имеет структуру, в которой слой твердого электролита расположен между слоем положительного электрода и слоем отрицательного электрода. Ионный проводник согласно настоящему изобретению может содержаться в качестве твердого электролита в по меньшей мере одном из слоя положительного электрода, слоя отрицательного электрода и слоя твердого электролита. При использовании в слое электрода, применение в слое отрицательного электрода является более предпочтительным, по сравнению с применением в слое положительного электрода. Это обусловлено менее вероятным протеканием побочных реакций в слое отрицательного электрода, по сравнению со слоем положительного электрода. Если ионный проводник согласно настоящему изобретению содержится в слое положительного электрода или в слое отрицательного электрода, то ионный проводник используют в комбинации с общеизвестным активным материалом положительного электрода или активным материалом отрицательного электрода для литиево-ионных перезаряжаемых аккумуляторов. В качестве слоя отрицательного электрода предпочтительно используют объемный тип, в котором активный материал и твердый электролит смешаны друг с другом, поскольку емкость на один элемент больше.
[0035]
Полностью твердотельный аккумулятор получают посредством формования и послойного нанесения вышеописанных слоев, и способ формования и способ послойного нанесения соответствующих слоев не имеют специального ограничения. Их примеры включают: способ, в котором твердый электролит и/или активный материал электрода диспергируют в растворителе с получением взвесеподобной смеси, которую наносят с помощью ножевого устройства, методом центрифугирования или подобным методом и подвергают вальцеванию с получением пленки; газофазный способ, в котором формование пленки и послойное нанесение осуществляют методом вакуумного осаждения, методом ионного осаждения, методом напыления, методом лазерного выжигания или т.п.; и способ прессования, в котором горячим прессованием или холодным прессованием (без нагревания) получают порошок и осуществляют послойное нанесение. Поскольку ионный проводник согласно настоящему изобретению является относительно мягким, он особенно предпочтителен для получения аккумулятора посредством формования прессованием и послойным нанесением. Кроме того, можно использовать также способ, в котором: заранее получают электродный слой, содержащий активный материал, агент для усиления проводимости и связующее вещество; в который вводят поток раствора, полученного растворением твердого электролита в растворителе, или суспензии, полученной диспергированием твердого электролита в растворителе; и после этого удаляют растворитель, обеспечивая тем самым внедрение твердого электролита в электродный слой.
[0036]
В отношении атмосферы для получения полностью твердотельного аккумулятора, описанное получение предпочтительно осуществляют в инертном газе с контролируемым содержанием влаги или в сухом помещении. В отношении контролирования содержания влаги, температура точки росы составляет от -10°С до -100°С, более предпочтительно от -20°С до -80°С, и особенно предпочтительно от -30°С до -75°С. Это необходимо для предотвращения снижения ионной проводимости вследствие образования гидрата, несмотря на то, что скорость гидролиза ионного проводника согласно настоящему изобретению является очень низкой.
ПРИМЕРЫ
[0037]
Далее настоящее изобретение более подробно описано с помощью примеров, но содержание настоящего изобретения не ограничено ими.
[0038]
<Получение ионного проводника>
(Пример 1)
В перчаточном боксе в атмосфере аргона взвешивали 240 мг LiCB9H10 (производства компании Katchem) и 122,2 мг LiCB11H12 (производства компании Katchem), так что молярное отношение LiCB9H10:LiCB11H12 составляло 7:3. Затем к предварительно взвешенному и смешанному порошку LiCB9H10 и LiCB11H12 добавляли 10 мл чистой воды (вода, реагент, Alfa Aesar) для его растворения и перемешивали в течение 30 минут с помощью мешалки. С помощью печи в форме стеклянной трубки сушили полученный однородный раствор при пониженном давлении, составляющем 0,1 Па или менее, при 150°С в течение 12 часов для удаления чистой воды с получением сухого белого порошка (предшественника). Полученный белый порошок растирали в ступке в течение 15 минут и гранулировали 50 мг порошка при 240 МПа, и подвергали термической обработке в вакууме при 200 °С в течение 12 часов с помощью турбонасоса. Полученный ионный проводник подвергали измерению импенданса по переменному току для измерения ионной проводимости. Записывали профиль рентгеновской дифракции, и было установлено, что высокотемпературная фаза LiCB9H10 в полученном ионном проводнике была стабилизирована. При измерении ДТА не наблюдали фазовый переход. Спектр Рамана был таким же, как для продукта, полученного посредством синтеза с измельчением.
[0039]
(Сравнительный пример 1)
Ионный проводник получали таким же образом, как в примере 1, за исключением того, что сырьевые материалы использовали в молярном соотношении LiCB9H10:LiCB11H12 5:5.
[0040]
<Измерение рентгеновской дифракции>
Порошок ионного проводника, полученный в примере 1, подвергали измерению рентгеновской дифракции (X‘pert Pro производства компании PANalytical, CuKα: λ=1,5405  ) в атмосфере аргона при комнатной температуре (25°C), используя капилляр из линдемановского стекла (внешний диаметр: 0,5 мм, толщина: 0,01 мм). Полученные пики рентгеновской дифракции представлены на фиг. 1. Для сравнения, на фиг. 1 показаны также пики рентгеновской дифракции LiCB9H10 и LiCB11H12 в качестве сырьевых материалов и LiCB9H10 (высокотемпературной фазы при 150°C).
) в атмосфере аргона при комнатной температуре (25°C), используя капилляр из линдемановского стекла (внешний диаметр: 0,5 мм, толщина: 0,01 мм). Полученные пики рентгеновской дифракции представлены на фиг. 1. Для сравнения, на фиг. 1 показаны также пики рентгеновской дифракции LiCB9H10 и LiCB11H12 в качестве сырьевых материалов и LiCB9H10 (высокотемпературной фазы при 150°C).
В примере 1 пики рентгеновской дифракции наблюдали при по меньшей мере 2θ=14,9±0,3 град, 16,4±0,3 град и 17,1±0,5 град. Кроме того, интенсивности пиков в положениях 16,44 град и 17,07 град, которые представляют собой положения пиков высокотемпературной фазы LiCB9H10, рассматривали как A и B, соответственно. Следует отметить, что значение 2θ=20 град рассматривали как исходное значение, и соответствующие интенсивности рассчитывали в соответствии с выражениями: A=(интенсивность рентгеновской дифракции при 16,44 град)-(интенсивность рентгеновской дифракции при 20 град) и B=(интенсивность рентгеновской дифракции при 17,07 град)-(интенсивность рентгеновской дифракции при 20 град).
Следует понимать, что ионный проводник из примера 1 представляет собой твердый раствор, поскольку положения его пиков соответствуют положениям пиков высокотемпературной фазы LiCB9H10.
[0041]
<Рамановская спектроскопия>
(1) Получение образца
Образец для измерения получали, используя воздухонепроницаемый контейнер с кварцевым стеклом (Ф:60 мм, толщина: 1 мм) в верхней части в качестве оптического окна. В перчаточном боксе в атмосфере аргона в образце оставляли жидкость в таком состоянии, что она контактировала с кварцевым стеклом, затем закрывали контейнер и убирали из перчаточного бокса, и проводили рамановскую спектроскопию.
(2) Условия измерения
Используя лазерный рамановский спектрометр NRS-5100 (производства компании JASCO Corporation), проводили измерение при длине волны возбуждения 532,15 нм в течение времени экспозиции 5 секунд. Полученные спектры Рамана представлены на фиг. 2.
LiCB9H10 имеет пик при 749 см-1, а LiCB11H12 имеет пик при 763 см-1. Следует отметить, что величина смещения частоты вследствие рамановского рассеяния обусловлена связыванием и практически не зависит от состояния кристалла. Понятно, что в примере 1 пик при 763 см-1 является плечом пика при 749 см-1.
[0042]
<Измерение ионной проводимости>
В перчаточной камере в атмосфере аргона каждый ионный проводник, полученный в примере 1, а также LiCB9H10 и LiCB11H12 в качестве сырьевых материалов подвергали одноосному формованию (240 МПа) с получением диска, имеющего толщину примерно 1 мм и ϕ 8 мм. Импенданс по переменному току измеряли двухполюсным методом, используя литиевый электрод, при этом температуру повышали/понижали с интервалами по 10 °С в температурном диапазоне от комнатной температуры до 150°С или 80°С (HIOKI 3532-80, химический импедометр), и рассчитывали ионную проводимость. Частотный диапазон, использованный для измерения, составлял от 4 Гц до 1 МГц, а амплитуда составляла 100 мВ.
[0043]
Результаты измерения ионной проводимости представлены на фиг. 3. Кроме того, ионная проводимость и энергия активации при комнатной температуре (25°С) представлены в таблице 1. Следует отметить, что в примере 1 не наблюдали явление резкого снижения ионной проводимости при низких температурах, которое наблюдали для LiCB9H10 и LiCB11H12 в качестве сырьевых материалов. Кроме того, в таблице 1 представлена ионная проводимость ионного проводника, полученного в сравнительном примере 1.
[0044]
[0045]
<Дифференциальное измерение калорий ДТА>
Порошок ионного проводника, полученный в примере 1, подвергали дифференциальной калориметрии методом ДТА в атмосфере аргона при скорости повышения/понижения температуры 5°С в температурном диапазоне от комнатной температуры до 200°С, используя прибор для дифференциального калориметрического измерения ДТА (система Rigaku Thermo Plus TG-8120). Следует отметить, что в примере 1 не наблюдали фазовый переход, наблюдаемый для LiCB9H10 и LiCB11H12 в качестве сырьевых материалов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИОННЫЙ ПРОВОДНИК, СОДЕРЖАЩИЙ ВЫСОКОТЕМПЕРАТУРНУЮ ФАЗУ LiCBH, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ТВЕРДЫЙ ЭЛЕКТРОЛИТ ДЛЯ ПОЛНОСТЬЮ ТВЕРДОТЕЛЬНЫХ АККУМУЛЯТОРОВ, СОДЕРЖАЩИЙ УКАЗАННЫЙ ИОННЫЙ ПРОВОДНИК | 2019 |
|
RU2795829C2 |
| ИОННЫЙ ПРОВОДНИК, СОДЕРЖАЩИЙ LiBH И LiBH, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ТВЕРДЫЙ ЭЛЕКТРОЛИТ ДЛЯ ПОЛНОСТЬЮ ТВЕРДОТЕЛЬНЫХ АККУМУЛЯТОРОВ, СОДЕРЖАЩИЙ УКАЗАННЫЙ ИОННЫЙ ПРОВОДНИК | 2019 |
|
RU2772865C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИОННОГО ПРОВОДНИКА | 2017 |
|
RU2714498C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОГО ЭЛЕКТРОЛИТА, СОДЕРЖАЩЕГО LiPS | 2018 |
|
RU2751545C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОГО ЭЛЕКТРОЛИТА НА ОСНОВЕ LGPS | 2018 |
|
RU2754868C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОГО ЭЛЕКТРОЛИТА НА ОСНОВЕ LGPS | 2018 |
|
RU2766576C2 |
| ИОННЫЙ ПРОВОДНИК И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2015 |
|
RU2690293C2 |
| ТВЕРДЫЙ ЭЛЕКТРОЛИТ НА ОСНОВЕ LGPS И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2787019C2 |
| ТВЕРДОТЕЛЬНАЯ БАТАРЕЯ | 2014 |
|
RU2665046C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДНОГО ТВЕРДОГО ЭЛЕКТРОЛИТА | 2020 |
|
RU2804507C2 |
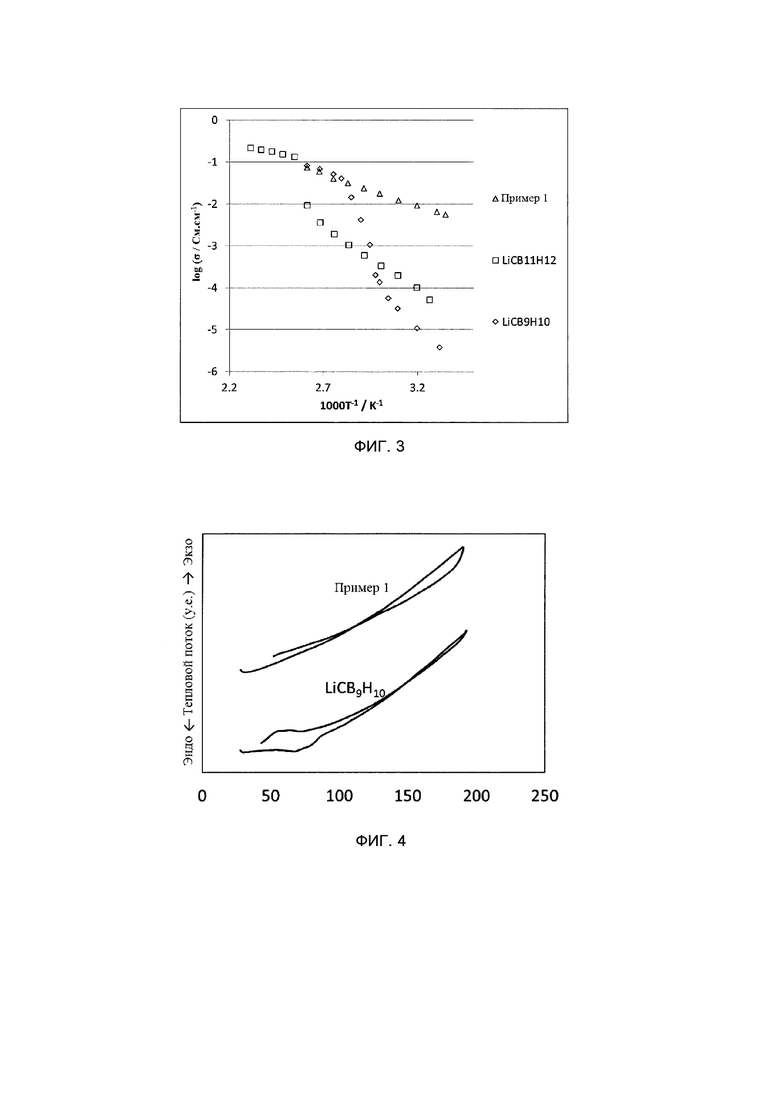
Группа изобретений относится к ионному проводнику, содержащему высокотемпературную фазу LiCB9H10, и к способу его получения. Способ получения ионного проводника, содержащего LiCB9H10 и LiCB11H12, включает: этап получения раствора, на котором получают однородный раствор посредством смешивания в растворителе LiCB9H10 и LiCB11H12 в молярном соотношении LiCB9H10/LiCB11H12 от 1,1 до 20; этап сушки, на котором получают предшественник посредством удаления растворителя из полученного однородного раствора; и этап термической обработки, на котором получают ионный проводник посредством термической обработки предшественника. Техническим результатом является обеспечение ионного проводника с превосходными характеристиками, включая ионную проводимость. 4 н. и 11 з.п. ф-лы, 4 ил., 1 пр., 1 табл.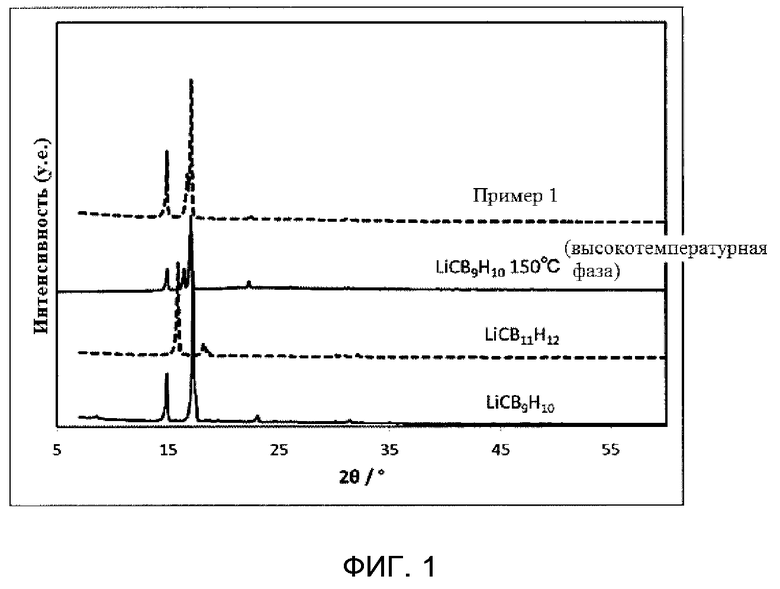
1. Способ получения ионного проводника, содержащего LiCB9H10 и LiCB11H12, включающий:
этап получения раствора для смешивания в растворителе LiCB9H10 и LiCB11H12 друг с другом в молярном соотношении LiCB9H10/LiCB11H12 от 1,1 до 20 с получением однородного раствора;
этап сушки для удаления растворителя из полученного однородного раствора с получением предшественника и
этап термической обработки для термической обработки предшественника с получением ионного проводника.
2. Способ по п. 1, согласно которому растворитель на этапе получения раствора представляет собой по меньшей мере одно, выбранное из группы, состоящей из воды, тетрагидрофурана, ацетонитрила, ацетона, этилацетата, метилацетата, толуола, метиленхлорида и хлороформа.
3. Способ по п. 1, согласно которому растворитель на этапе получения раствора состоит из воды.
4. Способ по любому из пп. 1-3, согласно которому время перемешивания и смешивания на этапе получения раствора составляет от 5 минут до 48 часов.
5. Способ по любому из пп. 1-4, согласно которому молярное соотношение между LiCB9H10 и LiCB11H12 (LiCB9H10/LiCB11H12) на этапе получения раствора составляет от 1,5 до 9.
6. Способ по любому из пп. 1-5, согласно которому температура на этапе сушки составляет от 50 до 260°С.
7. Способ по любому из пп. 1-6, согласно которому время сушки на этапе сушки составляет от 1 до 24 часов.
8. Способ по любому из пп. 1-7, согласно которому температура на этапе термической обработки составляет от 150 до 260°С.
9. Способ по любому из пп. 1-8, согласно которому время нагревания на этапе термической обработки составляет от 1 до 24 часов.
10. Способ по любому из пп. 1-9, согласно которому полученный ионный проводник имеет однофазную кристаллическую структуру высокотемпературной фазы LiCB9H10.
11. Способ по любому из пп. 1-10, согласно которому полученный ионный проводник имеет пики рентгеновской дифракции при по меньшей мере 2θ=14,9±0,3 град, 16,4±0,3 град и 17,1±0,5 град на профиле рентгеновской дифракции при 25°С, и при этом отношение интенсивностей (B/A), рассчитанное в соответствии с выражениями: A=(интенсивность рентгеновской дифракции при 16,4±0,3 град)-(интенсивность рентгеновской дифракции при 20 град) и B=(интенсивность рентгеновской дифракции при 17,1±0,5 град)-(интенсивность рентгеновской дифракции при 20 град), составляет от 1,0 до 20.
12. Способ по любому из пп. 1-11, согласно которому полученный ионный проводник имеет ионную проводимость от 1,0 до 10 мСм/см при 25°C.
13. Ионный проводник, полученный способом по любому из пп. 1-12.
14. Электрод, полученный с применением ионного проводника по п. 13.
15. Полностью твердотельный аккумулятор, полученный с применением ионного проводника по п. 13.
| US 10038192 B2, 31.07.2018 | |||
| US 20160372786 A1, 22.12.2016 | |||
| WO 2019078130 A1, 25.04.2019 | |||
| WO 2018139629 A1, 02.08.2018 | |||
| WO 2009139382 A1, 19.11.2009 | |||
| ИОННЫЙ ПРОВОДНИК И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2015 |
|
RU2690293C2 |
Авторы
Даты
2024-03-05—Публикация
2021-02-08—Подача