ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к нуклеиновой кислоте, фармацевтической композиции и конъюгату миРНК, способным ингибировать экспрессию гена белка комплемента 5 (C5). Настоящее изобретение также относится к способу получения и применению указанных конъюгата нуклеиновой кислоты, фармацевтической композиции и конъюгата миРНК.
УРОВЕНЬ ТЕХНИКИ
Миастения гравис (МГ) - это приобретенное аутоиммунное заболевание, главным образом опосредованное антителом к ацетилхолиновому рецептору (AchR-Ab), зависимостью от клеточного иммунитета и вовлечением комплементов, и связанное с ацетилхолиновым рецептором (AChR) на постсинаптической мембране нервно-мышечного синапса.
Белок комплемента (C5) является одной из ключевых мишеней для лечения миастении гравис. При участии комплементов AchR-Ab объединяется с AchR, что приводит к разрушению большого количества AchR посредством комплемент-опосредованного лизиса клеточной мембраны, что приводит к мышечной слабости из-за нарушения передачи сигнала ацетилхолином в постсинаптической мембране. Исследования показали, что путем специфичного связывания лекарственных средств с белком комплемента C5 можно предотвратить расщепление C5 на C5a и C5b, предотвращая таким образом образование мембраноатакующего комплекса, блокируя повреждение нервно-мышечного синапса мембраноатакующим комплексом и последующее продуцирование провоспалительных факторов, тем самым обеспечивая иммуносупрессивный эффект и лечение миастении гравис.
Малая интерферирующая РНК (миРНК), основанная на механизме РНК-интерференции (РНКи), может ингибировать или блокировать экспрессию представляющих интерес генов-мишеней сиквенс-специфичным образом, обеспечивая тем самым достижение цели лечения заболеваний. Если удастся обеспечить ингибирование экспрессии C5 для блокирования продукции белков комплемента, поддержания нормальных иммунных функций и ингибирования патологического иммунного ответа на уровне мРНК, это, несомненно, будет представляться самым совершенным вариантом лечения.
Ключом к разработке лекарственных средств на основе миРНК для ингибирования экспрессии гена C5 и лечения миастении гравис является поиск подходящей миРНК и ее модифицирование, а также эффективная система ее доставки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения неожиданно обнаружили, что конъюгат миРНК согласно настоящему изобретению может специфично ингибировать экспрессию гена C5, специфично нацеливаться на печень, ингибировать экспрессию гена C5 в печени и осуществлять лечение или предупреждение миастении гравис. Кроме того, авторы изобретения также разработали обладающую высокой активностью миРНК и фармацевтическую композицию.
В некоторых вариантах осуществления настоящего изобретения предложен конъюгат миРНК, имеющий структуру, представленную Формулой (308):
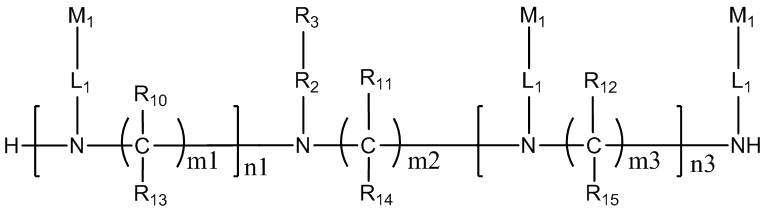
Формула (308),
где: n1 представляет собой целое число от 1 до 3, а n3 представляет собой целое число от 0 до 4; каждый из m1, m2 и m3 независимо представляет собой целое число от 2 до 10; каждый из R10, R11, R12, R13, R14 или R15 независимо представляет собой H или выбран из группы, состоящей из C1-C10 алкила, C1-C10 галогеналкила и C1-C10 алкокси;
R3 представляет собой группу, имеющую структуру, представленную Формулой A59:
 (A59),
(A59),
где E1 представляет собой OH, SH или BH2; и
Nu представляет собой миРНК; указанная миРНК содержит смысловую цепь и антисмысловую цепь, каждый нуклеотид в указанной миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, а антисмысловая цепь содержит нуклеотидную последовательность II; нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область; и нуклеотидная последовательность I и нуклеотидная последовательность II выбраны из группы последовательностей согласно следующим i) - vi):
i) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 1, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 2, и отличается от нее не более чем по трем нуклеотидам:
5’-CUUCAUUCAUACAGACAAZ1-3’ (SEQ ID NO: 1);
5’-Z2UUGUCUGUAUGAAUGAAG-3’ (SEQ ID NO: 2),
где Z1 представляет собой A, Z2 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z3 в сайте, соответствующем Z1, нуклеотидная последовательность II содержит нуклеотид Z4 в сайте, соответствующем Z2, и Z4 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
ii) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 61, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 62, и отличается от нее не более чем по трем нуклеотидам:
5’-CUACAGUUUAGAAGAUUUZ5-3’ (SEQ ID NO: 61);
5’-Z6AAAUCUUCUAAACUGUAG-3’ (SEQ ID NO: 62),
где Z5 представляет собой A, Z6 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z7 в сайте, соответствующем Z5, нуклеотидная последовательность II содержит нуклеотид Z8 в сайте, соответствующем Z6, и Z8 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
iii) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 121, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 122, и отличается от нее не более чем по трем нуклеотидам:
5’-GGAAGGUUACCGAGCAAUZ9-3’ (SEQ ID NO: 121);
5’-Z10AUUGCUCGGUAACCUUCC-3’ (SEQ ID NO: 122),
где Z9 представляет собой A, Z10 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z11 в сайте, соответствующем Z9, нуклеотидная последовательность II содержит нуклеотид Z12 в сайте, соответствующем Z10, и Z12 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
iv) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 181, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 182, и отличается от нее не более чем по трем нуклеотидам:
5’-AGAACAGACAGCAGAAUUZ13-3’ (SEQ ID NO: 181);
5’-Z14AAUUCUGCUGUCUGUUCU-3’ (SEQ ID NO: 182),
где Z13 представляет собой A, Z14 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z15 в сайте, соответствующем Z13, нуклеотидная последовательность II содержит нуклеотид Z16 в сайте, соответствующем Z14, и Z16 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
v) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 241, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 242, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAAGAAGAACGCUGCAAZ17-3’ (SEQ ID NO: 241);
5’-Z18UUGCAGCGUUCUUCUUGG-3’ (SEQ ID NO: 242),
где Z17 представляет собой A, Z18 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z19 в сайте, соответствующем Z17, нуклеотидная последовательность II содержит нуклеотид Z20 в сайте, соответствующем Z18, и Z20 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; и
vi) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 301, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 302, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAGUAAGCAAGCCAGAAZ21-3’ (SEQ ID NO: 301);
5’-Z22UUCUGGCUUGCUUACUGG-3’ (SEQ ID NO: 302),
где Z21 представляет собой A, Z22 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z23 в сайте, соответствующем Z21, нуклеотидная последовательность II содержит нуклеотид Z24 в сайте, соответствующем Z22, и Z24 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
R2 представляет собой линейный алкилен длиной от 1 до 20 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10 арилена, C3-C18 гетероциклилена и C5-C10 гетероарилена, и где R2 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10 арила, C5-C10 гетероарила, C1-C10 галогеналкила, -OC1-C10 алкила, -OC1-C10 алкилфенила, -C1-C10 алкил-OH, -OC1-C10 галогеналкила, -SC1-C10 алкила, -SC1-C10 алкилфенила, -C1-C10 алкил-SH, -SC1-C10 галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10 алкилфенила), -NH(C1-C10 алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10 алкилфенила, -C(O)C1-C10 галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10 галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10 галогеналкила);
каждый L1 независимо представляет собой линейный алкилен длиной от 1 до 70 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10 арилена, C3-C18 гетероциклилена и C5-C10 гетероарилена; и где L1 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10 арила, C5-C10 гетероарила, C1-C10 галогеналкила, -OC1-C10 алкила, -OC1-C10 алкилфенила, -C1-C10 алкил-OH, -OC1-C10 галогеналкила, -SC1-C10 алкила, -SC1-C10 алкилфенила, -C1-C10 алкил-SH, -SC1-C10 галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10 алкилфенила), -NH(C1-C10 алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10 алкилфенила, -C(O)C1-C10 галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10 галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10 галогеналкила); и
 обозначает сайт ковалентного присоединения группы; и M1 представляет собой нацеливающую группу.
обозначает сайт ковалентного присоединения группы; и M1 представляет собой нацеливающую группу.
В некоторых вариантах осуществления настоящего изобретения предложена миРНК, способная ингибировать экспрессию гена C5, где указанная миРНК содержит смысловую цепь и антисмысловую цепь, и каждый нуклеотид в смысловой цепи и антисмысловой цепи независимо представляет собой модифицированный фтором нуклеотид или нуклеотид с отличной от фтора модификацией; смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, модифицированные фтором нуклеотиды расположены в нуклеотидной последовательности I и нуклеотидной последовательности II, и, в направлении от 5’-конца к 3’-концу, нуклеотиды в положениях 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией; в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией, и нуклеотидная последовательность I и нуклеотидная последовательность II выбраны из одной из вышеперечисленных i) - vi).
В некоторых вариантах осуществления настоящего изобретения предложена фармацевтическая композиция, содержащая вышеупомянутую миРНК согласно настоящему изобретению и фармацевтически приемлемый носитель.
В некоторых вариантах осуществления настоящего изобретения предложен конъюгат миРНК, содержащий вышеупомянутую миРНК согласно настоящему изобретению и конъюгирующую группу, связанную путем конъюгации с указанной миРНК.
В некоторых вариантах осуществления настоящего изобретения предложено применение миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению для производства лекарственного средства для лечения и/или предупреждения миастении гравис.
В некоторых вариантах осуществления настоящего изобретения предложен способ лечения и/или предупреждения миастении гравис, включающий введение эффективного количества миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению субъекту, страдающему от миастении гравис.
В некоторых вариантах осуществления настоящего изобретения предложен способ ингибирования экспрессии гена C5 в гепатоците, включающий приведение эффективного количества миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению в контакт с указанным гепатоцитом.
В некоторых вариантах осуществления настоящего изобретения предложен набор, содержащий миРНК, и/или фармацевтическую композицию, и/или конъюгат миРНК согласно настоящему изобретению.
Положительные эффекты
В некоторых вариантах осуществления миРНК, фармацевтическая композиция и конъюгат миРНК согласно настоящему изобретению имеют лучшую стабильность, более высокую ингибирующую активность в отношении мРНК C5 и более низкое нецелевое действие, и/или могут в значительной степени лечить или облегчать симптомы миастении гравис.
В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют превосходную ингибирующую активность в отношении мРНК-мишени в экспериментах на клетках in vitro. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования мРНК-мишени в гепатоците, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению проявляет более высокую ингибирующую активность в клетках HepG2, и IC50 в отношении мРНК C5 составляет от 1,494 нМ до 9,688 нМ. В некоторых вариантах осуществления конъюгат миРНК согласно настоящему изобретению с флуоресцентной меткой подкожно инъецируют мышам C57 для проведения флуоресцентной визуализации в режиме реального времени на мышах и наблюдения за распределением флуоресценции по органам. Через 48 часов мышей умерщвляют для диссекции органов, и обнаруживается, что почти все конъюгаты миРНК скопились в печени, что указывает на то, что конъюгат миРНК согласно настоящему изобретению может эффективно и специфично доставлять миРНК в печень, что указывает на то, что конъюгат может специфично ингибировать экспрессию мРНК-мишени в печени.
В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению могут проявлять более высокую стабильность и/или более высокую активность in vivo. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования мРНК-мишени, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%, in vivo. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования экспрессии мРНК C5, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%, in vivo. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования экспрессии мРНК C5 в печени, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%, in vivo. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования экспрессии мРНК C5 в печени модельных животных, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%, in vivo. В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению проявляют процент ингибирования экспрессии мРНК C5 в печени у людей, равный по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 95%, in vivo.
В некоторых вариантах осуществления миРНК, фармацевтическая композиция или конъюгат миРНК согласно настоящему изобретению не проявляют существенного нецелевого действия. Нецелевое действие может представлять собой, например, ингибирование нормальной экспрессии гена, который не является геном-мишенью. Оно считается несущественным, если связывание/ингибирование экспрессии нецелевого гена находится на уровне ниже 50%, 40%, 30%, 20% или 10% от целевого действия.
Отсюда следует, что миРНК, фармацевтическая композиция и конъюгат миРНК согласно настоящему изобретению могут ингибировать экспрессию мРНК C5, эффективно лечат и/или предупреждают симптомы миастении гравис и имеют хорошие перспективы применения.
Другие особенности и преимущества настоящего изобретения будут подробно описаны в приведенном ниже разделе подробного описания изобретения.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
ФИГ. 1A-1H представляют собой кривые «доза-эффект», аппроксимированные на основании относительных уровней экспрессии мРНК C5 в клетках HepG2 после трансфекции различных конъюгатов 1-8.
ФИГ. 2A представляет собой фотографию флуоресцентной визуализации различных органов у мышей C57 через 48 часов после введения 5 мл/кг 1 × PBS, 3 мг/кг Cy5-миРНК 1 или 3 мг/кг Cy5-конъюгата 1.
ФИГ. 2B представляет собой фотографию флуоресцентной визуализации различных органов у мышей C57 через 48 часов после введения 5 мл/кг 1 × PBS, 3 мг/кг Cy5-миРНК 2 или 3 мг/кг Cy5-конъюгата 2.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Конкретные варианты осуществления настоящего изобретения подробно описаны ниже. Следует иметь в виду, что конкретные варианты осуществления, описанные в настоящем документе, служат только для иллюстрации и пояснения настоящего изобретения и не служат для ограничения настоящего изобретения в каком-либо отношении.
В настоящем изобретении мРНК C5 относится к мРНК с последовательностью, представленной под регистрационным номером в Genbank M57729.1. Кроме того, если не указано иное, термин «ген-мишень», используемый в настоящем изобретении, относится к гену, способному транскрибировать вышеуказанную мРНК C5, а термин «мРНК-мишень» относится к вышеуказанной мРНК C5.
Определения
В контексте настоящего изобретения, если не указано иное, заглавные буквы C, G, U и A обозначают основания в составе нуклеотидов; строчная буква m обозначает, что нуклеотид, расположенный слева от буквы m, представляет собой метокси-модифицированный нуклеотид; строчная буква f обозначает, что нуклеотид, расположенный слева от буквы f, представляет собой модифицированный фтором нуклеотид; строчная буква s обозначает, что два нуклеотида, расположенные слева и справа от буквы s, соединены тиофосфатом; P1 обозначает, что нуклеотид, расположенный справа от P1, представляет собой нуклеотид с 5’-фосфатной группой или нуклеотид, модифицированный аналогом 5’-фосфатной группы, комбинация букв VP обозначает, что нуклеотид, расположенный справа от комбинации букв VP, представляет собой модифицированный винилфосфатом нуклеотид, комбинация букв Ps обозначает, что нуклеотид, расположенный справа от комбинации букв Ps, представляет собой модифицированный тиофосфатом нуклеотид, а заглавная буква P обозначает, что нуклеотид, расположенный справа от буквы P, представляет собой нуклеотид с 5’-фосфатной группой.
В контексте настоящего изобретения «модифицированный фтором нуклеотид» относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида фтором, а термин «нуклеотид с отличной от фтора модификацией» относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида группой, отличной от фтора, или к аналогу нуклеотида. «Аналог нуклеотида» относится к группе, которая может заменять нуклеотид в нуклеиновой кислоте, при этом она структурно отличается от аденинового рибонуклеотида, гуанинового рибонуклеотида, цитозинового рибонуклеотида, урацилового рибонуклеотида или тимидинового дезоксирибонуклеотида, например, представляет собой изонуклеотид, нуклеотид мостиковой нуклеиновой кислоты (BNA) или ациклический нуклеотид. «Метокси-модифицированный нуклеотид» относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы метоксигруппой.
В контексте настоящего изобретения выражения «комплементарный» и «обратно комплементарный» могут использоваться взаимозаменяемо и имеют общеизвестное в данной области техники значение, а именно, основания в одной цепи комплементарно спарены с основаниями в другой цепи двухцепочечной молекулы нуклеиновой кислоты. В ДНК пуриновое основание аденин (A) всегда спарено с пиримидиновым основанием тимином (T) (или урацилом (U) в РНК); и пуриновое основание гуанин (G) всегда спарено с пиримидиновым основанием цитозином (C). Каждая пара оснований содержит пурин и пиримидин. Если аденины в одной цепи всегда спарены с тиминами (или урацилами) в другой цепи, а гуанины всегда спарены с цитозинами, эти две цепи считаются комплементарными друг другу; и последовательность цепи может быть выведена из последовательности ее комплементарной цепи. Соответственно, «ошибочное спаривание» означает, что в двухцепочечной нуклеиновой кислоте основания в соответствующих сайтах не представлены в виде комплементарно спаренных.
В контексте настоящего изобретения, если не указано иное, «преимущественно обратно комплементарный» означает, что между двумя нуклеотидными последовательностями присутствует не более 3 ошибочно спаренных оснований. «По существу обратно комплементарный» означает, что между двумя нуклеотидными последовательностями присутствует не более 1 ошибочно спаренного основания. «Полностью комплементарный» означает, что между двумя нуклеотидными последовательностями отсутствуют ошибочно спаренные основания.
В контексте настоящего изобретения, если нуклеотидная последовательность имеет «различие по нуклеотидам» от другой нуклеотидной последовательности, нуклеотидные основания в одном и том же положении в них изменены. Например, если нуклеотидное основание во второй последовательности представляет собой A, а нуклеотидное основание в том же положении в первой последовательности представляет собой U, C, G или T, эти две нуклеотидные последовательности считаются имеющими различие по нуклеотиду в этом положении. В некоторых вариантах осуществления, если нуклеотид в каком-либо положении заменен лишенным азотистого основания нуклеотидом или аналогом нуклеотида, также считается, что в этом положении имеется различие по нуклеотиду.
В контексте настоящего изобретения, в частности, в описании способа получения миРНК, композиции, содержащей миРНК, или конъюгата миРНК согласно настоящему изобретению, если не указано иное, нуклеозидный мономер относится, в соответствии с видом и последовательностью нуклеотидов в миРНК или конъюгате миРНК, которые необходимо получить, к немодифицированным или модифицированным рибонуклеозидным амидофосфитам, применяемым в твердофазном амидофосфитном синтезе (РНК-амидофосфиты в других местах также называются нуклеозидными амидофосфитами). Твердофазный амидофосфитный синтез представляет собой метод, хорошо известный специалистам в данной области техники и используемый в синтезе РНК. Нуклеозидные мономеры, используемые в настоящем изобретении, могут быть доступны на рынке.
В контексте настоящего изобретения, если не указано иное, «конъюгирование» относится к двум или более химическим фрагментам, каждый из которых имеет определенную функцию, соединенным друг с другом посредством ковалентной связи. Соответственно, «конъюгат» относится к соединению, образованному ковалентным связыванием отдельных химических фрагментов. Кроме того, «конъюгат миРНК» представляет собой соединение, образованное ковалентным связыванием одного или более химических фрагментов с определенными функциями с миРНК. Далее в настоящем документе конъюгат миРНК согласно настоящему изобретению иногда сокращенно называется «конъюгатом». Конъюгат миРНК следует понимать в соответствии с контекстом как общий термин для множества конъюгатов миРНК или конъюгатов миРНК, представленных в определенных химических формулах. В контексте настоящего изобретения термин «конъюгирующая молекула» следует понимать как конкретное соединение, которое может быть конъюгировано с миРНК посредством реакций с получением в конечном итоге конъюгата миРНК согласно настоящему изобретению.
Применительно к настоящему изобретению термин «необязательный» или «необязательно» означает, что описанное далее событие или условие может происходить или может не происходить, и что описание включает случаи, когда событие или условие может происходить или может не происходить. Например, термин «необязательно замещенный» «алкил» включает как «алкил», так и «замещенный алкил», как определено ниже. Специалистам в данной области техники будет ясно, в отношении любой группы, содержащей один или более заместителей, что такие группы не подразумевают введения какого-либо замещения или типа замещения, которые являются стерически невыгодными, синтетически неосуществимыми и/или нестабильными по своей природе.
Применительно к настоящему изобретению «алкил» относится к линейной цепи и разветвленной цепи, имеющей указанное количество атомов углерода, обычно от 1 до 20 атомов углерода, например, от 1 до 10 атомов углерода, например, от 1 до 8 или от 1 до 6 атомов углерода. Например, C1-C6 алкил включает алкил как с линейной, так и с разветвленный цепью, имеющий от 1 до 6 атомов углерода. При обозначении алкильного остатка, имеющего определенное количество атомов углерода, подразумевается включение всех форм с разветвленной цепью и линейной цепью, имеющих это количество атомов углерода; таким образом, например, под «бутилом» подразумевается н-бутил, втор-бутил, изобутил и трет-бутил; а под «пропилом» подразумевается н-пропил и изопропил. Алкилен представляет собой разновидность алкила, относящуюся к тем же остаткам, что и алкил, но имеющую два положения присоединения.
Применительно к настоящему изобретению «алкенил» относится к ненасыщенному разветвленному или линейному алкилу, имеющему по меньшей мере одну двойную связь углерод-углерод, образованную путем соответствующего удаления одной молекулы водорода от двух соседних атомов углерода исходного алкила. Группа может иметь цис- или транс-конфигурацию двойной связи. Типичные алкенильные группы включают, не ограничиваясь перечисленным, этенил; пропенилы, такие как проп-1-ен-1-ил, проп-1-ен-2-ил, проп-2-ен-1-ил (аллил) и проп-2-ен-2-ил; и бутенилы, такие как бут-1-ен-1-ил, бут-1-ен-2-ил, 2-метилпроп-1-ен-1-ил, бут-2-ен-1-ил, бут-2-ен-2-ил, бута-1,3-диен-1-ил, бута-1,3-диен-2-ил и тому подобное. В отдельных вариантах осуществления алкенильная группа имеет от 2 до 20 атомов углерода, а в других вариантах осуществления от 2 до 10, от 2 до 8 или от 2 до 6 атомов углерода. Алкенилен представляет собой разновидность алкенила, относящуюся к тем же остаткам, что и алкенил, но имеющую два положения присоединения.
Применительно к настоящему изобретению «алкинил» относится к ненасыщенному разветвленному или линейному алкилу, имеющему по меньшей мере одну тройную связь углерод-углерод, образованную путем соответствующего удаления двух молекул водорода от двух соседних атомов углерода исходного алкила. Типичные алкинильные группы включают, не ограничиваясь перечисленным, этинил; пропинилы, такие как проп-1-ин-1-ил и проп-2-ин-1-ил; и бутинилы, такие как бут-1-ин-1-ил, бут-1-ин-3-ил, бут-3-ин-1-ил и тому подобное. В отдельных вариантах осуществления алкинильная группа имеет от 2 до 20 атомов углерода, а в других вариантах осуществления от 2 до 10, от 2 до 8 или от 2 до 6 атомов углерода. Алкинилен представляет собой разновидность алкинила, относящуюся к тем же остаткам, что и алкинил, но имеющую два положения присоединения.
Применительно к настоящему изобретению «алкокси» относится к алкильной группе с указанным количеством атомов углерода, присоединяемой посредством кислородного мостика, такой как метокси, этокси, пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, пентилокси, 2-пентилокси, изопентилокси, неопентилокси, гексилокси, 2-гексилокси, 3-гексилокси, 3-метилпентилокси и тому подобное. Алкокси обычно имеет от 1 до 10, от 1 до 8, от 1 до 6 или от 1 до 4 атомов углерода, присоединенных посредством кислородного мостика.
Применительно к настоящему изобретению «арил» относится к группе, получаемой из ароматической моноциклической или полициклической углеводородной кольцевой системы путем удаления атома водорода от атома углерода кольца. Ароматическая моноциклическая или полициклическая углеводородная кольцевая система содержит только водород и от 6 до 18 атомов углерода, причем по меньшей мере одно кольцо в кольцевой системе является полностью ненасыщенным, т. е. содержит циклическую делокализованную (4n+2)π-электронную систему в соответствии с теорией Хюккеля. Арильные группы включают, не ограничиваясь перечисленным, фенил, флуоренил, нафтил и тому подобное. Арилен представляет собой разновидность арила, относящуюся к тем же остаткам, что и арил, но имеющую два положения присоединения.
Применительно к настоящему изобретению «галогеновый заместитель» или «галоген» относится к фтору, хлору, брому и иоду, а термин «галоген» включает фтор, хлор, бром или иод.
Применительно к настоящему изобретению «галогеналкил» относится к алкилу, как определено выше, в котором указанное количество атомов углерода замещено одним или более атомами галогена, вплоть до максимально допустимого количества атомов галогена. Примеры галогеналкила включают, не ограничиваясь перечисленным, трифторметил, дифторметил, 2-фторэтил и пентафторэтил.
«Гетероциклил» относится к стабильному 3-18-членному неароматическому кольцевому радикалу, содержащему 2-12 атомов углерода и 1-6 гетероатомов, выбранных из азота, кислорода или серы. Если в описании не указано иное, гетероциклил представляет собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, которая может содержать конденсированные или мостиковые кольцевые системы. Гетероатомы в гетероциклиле необязательно могут быть окислены. Один или более атомов азота, если они присутствуют, необязательно являются кватернизированными. Гетероциклил является частично или полностью насыщенным. Гетероциклил может быть соединен с остальной частью молекулы через любой атом кольца. Примеры такого гетероциклила включают, не ограничиваясь перечисленным, диоксанил, тиенил[1,3]дисульфонил, декагидроизохинолил, имидазолинил, имидазолидинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, 2-оксапиперазинил, 2-оксапиперидинил, 2-оксапирролидинил, оксазолидинил, пиперидинил, пиперазинил, 4-пиперидонил, пирролидинил, пиразолидинил, хинуклидинил, тиазолидинил, тетрагидрофурил, тритианил, тетрагидропиранил, тиоморфолинил, тиаморфолинил, 1-оксотиоморфолинил и 1,1-диоксотиоморфолинил.
«Гетероарил» относится к группе, происходящей из 3-18-членного ароматического кольцевого радикала, содержащего от 2 до 17 атомов углерода и от 1 до 6 гетероатомов, выбранных из азота, кислорода и серы. Применительно к настоящему изобретению гетероарил может представлять собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, причем по меньшей мере одно кольцо в кольцевой системе является полностью ненасыщенным, т. е. содержит циклическую делокализованную (4n+2)π-электронную систему в соответствии с теорией Хюккеля. Гетероарил включает конденсированные или мостиковые кольцевые системы. Гетероатомы в гетероариле необязательно окислены. Один или более атомов азота, если они присутствуют, необязательно являются кватернизированными. Гетероарил может быть соединен с остальной частью молекулы через любой атом кольца. Примеры таких гетероарилов включают, не ограничиваясь перечисленным, азепинил, акридинил, бензимидазолил, бензиндолил, 1,3-бензодиоксазолил, бензофуранил, бензоксазолил, бензо[d]тиазолил, бензотиадиазолил, бензо[b][1,4]диоксепинил, бензо[b][1,4]оксазинил, 1,4-бензодиоксанил, бензонафтофуранил, бензоксазолил, бензодиоксолил, бензопиранил, бензопиранонил, бензофуранил, бензофуранонил, бензотиенил, бензотиено[3,2-d]пиримидинил, бензотриазолил, бензо[4,6]имидазо[1,2-а]пиридинил, карбазолил, циннолинил, циклопента[d]пиримидинил, 6,7-дигидро-5Н-циклопента[4,5]-тиено[2,3-d]пиримидинил, 5,6-дигидробензо[h]хиназолинил, 5,6-дигидробензо[h]циннолинил, 6,7-дигидро-5H-бензо[6,7]циклогепта[1,2-c]пиридазинил, дибензофуранил, дибензотиенил, фуранил, фуранонил, фуро[3,2-c]пиридинил, 5,6,7,8,9,10-гексагидроциклоокта[d]пиримидинил, 5,6,7,8,9,10-гексагидроциклоокта[d]пиридазинил, 5,6,7,8,9,10-гексагидроциклоокта[d]пиридинил, изотиазолил, имидазолил, индазолил, индолил, изоиндолил, индолинил, изоиндолинил, изохинолил, индолизинил, изоксазолил, 5,8-метан-5,6,7,8-тетрагидрохиназолинил, нафтиридинил, 1,6-нафтиридинонил, оксадиазолил, 2-оксоазепинил, оксазолил, оксиранил, 5,6,6a,7,8,9,10,10a-октагидробензо[h]хиназолинил, 1-фенил-1H-пирролил, феназинил, фенотиазинил, феноксазинил, фталазинил, птеридинил, пуринил, пирролил, пиразолил, пиразоло[3,4-d]пиримидинил, пиридинил, пиридо[3,2-d]пиримидинил, пиридо[3,4-d]пиримидинил, пиразинил, пиримидинил, пиридазинил, хиназолинил, хиноксалинил, хинолинил, тетрагидрохинолинил, 5,6,7,8-тетрагидрохиназолинил, 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]пиримидинил, 6,7,8,9-тетрагидро-5H-циклогепта[4,5]тиено[2,3-d]пиримидинил, 5,6,7,8-тетрагидропиридо[4,5-c]пиридазинил, тиазолил, тиадиазолил, триазолил, тетразолил, триазинил, тиено[2,3-d]пиримидинил, тиено[3,2-d]пиримидинил, тиено[2,3-c]придинил и тиофенил/тиенил.
В настоящем изобретении могут быть использованы различные гидроксизащитные группы. Как правило, защитные группы делают химические функциональные группы инертными к определенным условиям реакции и могут быть присоединены к таким функциональным группам в молекуле и удалены из них без значительного повреждения остальной части молекулы. Иллюстративные гидроксизащитные группы раскрыты в источнике Tetrahedron 1992, 48, 2223-2311 за авт. Beaucage, et al., а также в источнике Greene and Wuts, Protective Groups in Organic Synthesis, Chapter 2, 2d ed, John Wiley & Sons, New York, 1991, каждый из которых включен в настоящий документ посредством ссылки в полном объеме. В некоторых вариантах осуществления защитная группа стабильна в основных условиях, но может быть удалена в кислых условиях. В некоторых вариантах осуществления неисключающие примеры гидроксизащитных групп, применяемых в настоящем документе, включают диметокситритил (DMT), монометокситритил, 9-фенилксантен-9-ил (Pixyl) или 9-(п-метоксифенил)ксантен-9-ил (Mox). В некоторых вариантах осуществления неисключающие примеры гидроксизащитных групп, применяемых в настоящем документе, включают Tr (тритил), MMTr (4-метокситритил), DMTr (4,4'-диметокситритил) и TMTr (4,4',4"-триметокситритил).
Применительно к настоящему изобретению термин «субъект» относится к любому животному, например, млекопитающему или сумчатому. Субъект согласно настоящему изобретению включает, не ограничиваясь перечисленным, человека, примата, отличного от человека (например, макака-резуса или другие виды макак), мышь, свинью, лошадь, осла, корову, овцу, крысу и любые виды домашней птицы.
Применительно к настоящему изобретению «лечение» относится к способу получения благоприятного или желаемого результата, включая, не ограничиваясь перечисленным, терапевтический эффект. «Терапевтический эффект» означает устранение или улучшение потенциального расстройства, подлежащего лечению. Более того, терапевтический эффект достигается путем устранения или ослабления одного или более физиологических симптомов, ассоциированных с потенциальным расстройством, так, что у субъекта наблюдается улучшение, несмотря на то, что субъект все еще может быть поражен потенциальным расстройством.
Применительно к настоящему изобретению «предупреждение» относится к способу получения благоприятного или целевого результата, включая, не ограничиваясь перечисленным, профилактический эффект. Для достижения «профилактического эффекта» конъюгат миРНК или композиция могут быть введены субъекту, подверженному риску развития конкретного заболевания, или субъекту, сообщающему об одном или более физиологических симптомах заболевания, даже это заболевание еще не было диагностировано.
миРНК
В одном аспекте настоящее изобретение относится к шести типам миРНК, способных ингибировать экспрессию гена C5.
миРНК согласно настоящему изобретению содержит нуклеотиды в качестве основных структурных единиц. Специалистам в данной области техники хорошо известно, что нуклеотид содержит фосфатную группу, рибозную группу и основание. Подробные иллюстрации, относящиеся к таким группам, в настоящем документе не представлены.
миРНК согласно настоящему изобретению содержит смысловую цепь и антисмысловую цепь, причем длины смысловой цепи и антисмысловой цепи являются одинаковыми или различными, длина смысловой цепи составляет 19-23 нуклеотида, а длина антисмысловой цепи составляет 19-26 нуклеотидов. Таким образом, отношение длины смысловой цепи к длине антисмысловой цепи миРНК согласно настоящему изобретению может составлять 19/19, 19/20, 19/21, 19/22, 19/23, 19/24, 19/25, 19/26, 20/20, 20/21, 20/22, 20/23, 20/24, 20/25, 20/26, 21/20, 21/21, 21/22, 21/23, 21/24, 21/25, 21/26, 22/20, 22/21, 22/22, 22/23, 22/24, 22/25, 22/26, 23/20, 23/21, 23/22, 23/23, 23/24, 23/25 или 23/26. В некоторых вариантах осуществления отношение длины смысловой цепи к длине антисмысловой цепи миРНК составляет 19/21, 21/23 или 23/25.
Первая миРНК
Согласно настоящему изобретению миРНК может представлять собой первую миРНК.
Первая миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид в первой миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 1, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 2, и отличается от нее не более чем по трем нуклеотидам:
5’-CUUCAUUCAUACAGACAAZ1-3’ (SEQ ID NO: 1);
5’-Z2UUGUCUGUAUGAAUGAAG-3’ (SEQ ID NO: 2),
где Z1 представляет собой A, Z2 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z3 в сайте, соответствующем Z1, нуклеотидная последовательность II содержит нуклеотид Z4 в сайте, соответствующем Z2, и Z4 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В данном контексте термин «соответствующий сайт» означает нахождение в одном и том же сайте в нуклеотидной последовательности при отсчете с одного и того же конца нуклеотидной последовательности. Например, первый нуклеотид на 3’-конце нуклеотидной последовательности I представляет собой нуклеотид в сайте, соответствующем первому нуклеотиду на 3’-конце SEQ ID NO: 1.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 1, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 2, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 2, включает различие в сайте Z4, и Z4 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z4, и Z4 выбран из A, C или G. В некоторых вариантах осуществления Z3 представляет собой нуклеотид, комплементарный Z4. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II. «Преимущественно обратно комплементарный» означает наличие не более чем трех ошибочно спаренных основания между двумя нуклеотидными последовательностями; «по существу обратно комплементарный» означает наличие не более чем одного ошибочно спаренного основания между двумя нуклеотидными последовательностями; и «полностью обратно комплементарный» означает отсутствие ошибочно спаренного основания между двумя нуклеотидными последовательностями.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 3, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 4:
5’-CUUCAUUCAUACAGACAAZ3-3’ (SEQ ID NO: 3);
5’-Z4UUGUCUGUAUGAAUGAAG-3’ (SEQ ID NO: 4),
где Z4 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z3 выбран из A, U, G или C; и Z4 представляет собой нуклеотид, комплементарный Z3; и в некоторых вариантах осуществления Z3 представляет собой A, а Z4 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. В некоторых вариантах осуществления нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 1, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой U, а основание нуклеотидной последовательности IV представляет собой A; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CU, а состав оснований нуклеотидной последовательности IV представляет собой AG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UCU, а состав оснований нуклеотидной последовательности IV представляет собой AGA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UUCU, а состав оснований нуклеотидной последовательности IV представляет собой AGAA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CU, а состав оснований нуклеотидной последовательности IV представляет собой AG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Вторая миРНК
Согласно настоящему изобретению миРНК может представлять собой вторую миРНК.
Вторая миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид во второй миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 61, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 62, и отличается от нее не более чем по трем нуклеотидам:
5’-CUACAGUUUAGAAGAUUUZ5-3’ (SEQ ID NO: 61);
5’-Z6AAAUCUUCUAAACUGUAG-3’ (SEQ ID NO: 62),
где Z5 представляет собой A, Z6 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z7 в сайте, соответствующем Z5, нуклеотидная последовательность II содержит нуклеотид Z8 в сайте, соответствующем Z6, и Z8 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 61, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 62, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 62, включает различие в сайте Z8, и Z8 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z8, и Z8 выбран из A, C или G. В некоторых вариантах осуществления Z7 представляет собой нуклеотид, комплементарный Z8. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 63, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 64:
5’-CUACAGUUUAGAAGAUUUZ7-3’ (SEQ ID NO: 63);
5’-Z8AAAUCUUCUAAACUGUAG-3’ (SEQ ID NO: 64),
где Z8 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z7 выбран из A, U, G или C; и Z8 представляет собой нуклеотид, комплементарный Z7; и в некоторых вариантах осуществления Z7 представляет собой A, а Z8 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. Нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 61, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой A, а основание нуклеотидной последовательности IV представляет собой U; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA, и состав оснований нуклеотидной последовательности IV представляет собой UA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AUA, а состав оснований нуклеотидной последовательности IV представляет собой UAU; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAUA, а состав оснований нуклеотидной последовательности IV представляет собой UAUG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA, и состав оснований нуклеотидной последовательности IV представляет собой UA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Третья миРНК
Согласно настоящему изобретению миРНК может представлять собой третью миРНК.
Третья миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид в третьей миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 121, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 122, и отличается от нее не более чем по трем нуклеотидам:
5’-GGAAGGUUACCGAGCAAUZ9-3’ (SEQ ID NO: 121);
5’-Z10AUUGCUCGGUAACCUUCC-3’ (SEQ ID NO: 122),
где Z9 представляет собой A, Z10 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z11 в сайте, соответствующем Z9, нуклеотидная последовательность II содержит нуклеотид Z12 в сайте, соответствующем Z10, и Z12 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 121, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 122, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 122, включает различие в сайте Z12, и Z12 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z12, и Z12 выбран из A, C или G. В некоторых вариантах осуществления Z11 представляет собой нуклеотид, комплементарный Z12. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 123, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 124:
5’-GGAAGGUUACCGAGCAAUZ11-3’ (SEQ ID NO: 123);
5’-Z12AUUGCUCGGUAACCUUCC-3’ (SEQ ID NO: 124),
где Z12 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z11 выбран из A, U, G или C; и Z12 представляет собой нуклеотид, комплементарный Z11; и в некоторых вариантах осуществления Z11 представляет собой A, а Z12 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. Нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 121, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой G, а основание нуклеотидной последовательности IV представляет собой C; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AG, а состав оснований нуклеотидной последовательности IV представляет собой CU; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAG, а состав оснований нуклеотидной последовательности IV представляет собой CUG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CCAG, а состав оснований нуклеотидной последовательности IV представляет собой CUGG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AG, а состав оснований нуклеотидной последовательности IV представляет собой CU; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Четвертая миРНК
Согласно настоящему изобретению миРНК может представлять собой четвертую миРНК.
Четвертая миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид в четвертой миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 181, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 182, и отличается от нее не более чем по трем нуклеотидам:
5’-AGAACAGACAGCAGAAUUZ13-3’ (SEQ ID NO: 181);
5’-Z14AAUUCUGCUGUCUGUUCU-3’ (SEQ ID NO: 182),
где Z13 представляет собой A, Z14 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z15 в сайте, соответствующем Z13, нуклеотидная последовательность II содержит нуклеотид Z16 в сайте, соответствующем Z14, и Z16 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 181, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 182, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 182, включает различие в сайте Z16, и Z16 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z16, и Z16 выбран из A, C или G. В некоторых вариантах осуществления Z15 представляет собой нуклеотид, комплементарный Z16. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 183, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 184:
5’-AGAACAGACAGCAGAAUUZ15-3’ (SEQ ID NO: 183);
5’-Z16AAUUCUGCUGUCUGUUCU-3’ (SEQ ID NO: 184),
где Z16 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z15 выбран из A, U, G или C; и Z16 представляет собой нуклеотид, комплементарный Z15; и в некоторых вариантах осуществления Z15 представляет собой A, а Z16 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. Нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 181, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой G, а основание нуклеотидной последовательности IV представляет собой C; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG, а состав оснований нуклеотидной последовательности IV представляет собой CC; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AGG, а состав оснований нуклеотидной последовательности IV представляет собой CCU; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAGG, а состав оснований нуклеотидной последовательности IV представляет собой CCUG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG, а состав оснований нуклеотидной последовательности IV представляет собой CC; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Пятая миРНК
Согласно настоящему изобретению миРНК может представлять собой пятую миРНК.
Пятая миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид в пятой миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 241, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 242, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAAGAAGAACGCUGCAAZ17-3’ (SEQ ID NO: 241);
5’-Z18UUGCAGCGUUCUUCUUGG-3’ (SEQ ID NO: 242),
где Z17 представляет собой A, Z18 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z19 в сайте, соответствующем Z17, нуклеотидная последовательность II содержит нуклеотид Z20 в сайте, соответствующем Z18, и Z20 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 241, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 242, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 242, включает различие в сайте Z20, и Z20 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z20, и Z20 выбран из A, C или G. В некоторых вариантах осуществления Z19 представляет собой нуклеотид, комплементарный Z20. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 243, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 244:
5’-CCAAGAAGAACGCUGCAAZ19-3’ (SEQ ID NO: 243);
5’-Z20UUGCAGCGUUCUUCUUGG-3’ (SEQ ID NO: 244),
где Z20 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z19 выбран из A, U, G или C; и Z20 представляет собой нуклеотид, комплементарный Z19; и в некоторых вариантах осуществления Z19 представляет собой A, а Z20 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. Нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 241, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой G, а основание нуклеотидной последовательности IV представляет собой C; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG, а состав оснований нуклеотидной последовательности IV представляет собой CC; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AGG, а состав оснований нуклеотидной последовательности IV представляет собой CCU; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAGG, а состав оснований нуклеотидной последовательности IV представляет собой CCUG; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG, а состав оснований нуклеотидной последовательности IV представляет собой CC; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Шестая миРНК
Согласно настоящему изобретению миРНК может представлять собой шестую миРНК.
Шестая миРНК содержит смысловую цепь и антисмысловую цепь. Каждый нуклеотид в шестой миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, антисмысловая цепь содержит нуклеотидную последовательность II, и нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область, где нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 301, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 302, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAGUAAGCAAGCCAGAAZ21-3’ (SEQ ID NO: 301);
5’-Z22UUCUGGCUUGCUUACUGG-3’ (SEQ ID NO: 302),
где Z21 представляет собой A, Z22 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z23 в сайте, соответствующем Z21, нуклеотидная последовательность II содержит нуклеотид Z24 в сайте, соответствующем Z22, и Z24 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи.
В некоторых вариантах осуществления смысловая цепь содержит исключительно нуклеотидную последовательность I, а антисмысловая цепь содержит исключительно нуклеотидную последовательность II.
В некоторых вариантах осуществления нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 301, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 302, не более чем по одному нуклеотиду.
В некоторых вариантах осуществления различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 302, включает различие в сайте Z24, и Z24 выбран из A, C или G. В некоторых вариантах осуществления различие по нуклеотиду представляет собой различие в сайте Z24, и Z24 выбран из A, C или G. В некоторых вариантах осуществления Z23 представляет собой нуклеотид, комплементарный Z24. миРНК, имеющие вышеуказанное различие по нуклеотиду, обладают более высокой способностью миРНК ингибировать мРНК-мишень, и эти миРНК также включены в объем настоящего изобретения.
В некоторых вариантах осуществления нуклеотидная последовательность I является преимущественно обратно комплементарной, по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности II.
В некоторых вариантах осуществления нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 303, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 304:
5’-CCAGUAAGCAAGCCAGAAZ23-3’ (SEQ ID NO: 303);
5’-Z24UUCUGGCUUGCUUACUGG-3’ (SEQ ID NO: 304),
где Z24 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z23 выбран из A, U, G или C; и Z24 представляет собой нуклеотид, комплементарный Z23; и в некоторых вариантах осуществления Z23 представляет собой A, а Z24 представляет собой U.
В некоторых вариантах осуществления смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, и каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида; нуклеотидная последовательность III имеет ту же длину и по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности IV; нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, а нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II. Нуклеотидная последовательность IV по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, и нуклеотидная последовательность II относится к нуклеотидной последовательности, примыкающей к 5’-концу нуклеотидной последовательности, представленной SEQ ID NO: 301, в мРНК-мишени, и имеющей ту же длину, что и нуклеотидная последовательность IV.
В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV обе имеют длину в один нуклеотид. Основание нуклеотидной последовательности III представляет собой A, а основание нуклеотидной последовательности IV представляет собой U; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 20/20; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA, и состав оснований нуклеотидной последовательности IV представляет собой UA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UUA, а состав оснований нуклеотидной последовательности IV представляет собой UAA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 22/22; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GUUA, а состав оснований нуклеотидной последовательности IV представляет собой UAAC; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 23/23. В некоторых вариантах осуществления нуклеотидная последовательность III и нуклеотидная последовательность IV имеют длину два нуклеотида, и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA, и состав оснований нуклеотидной последовательности IV представляет собой UA; в этом случае отношение длины смысловой цепи к длине антисмысловой цепи составляет 21/21.
В некоторых вариантах осуществления нуклеотидная последовательность III полностью обратно комплементарна нуклеотидной последовательности IV. Таким образом, если известно основание(ия) нуклеотидной последовательности III, то основание(ия) нуклеотидной последовательности IV также может быть определено.
Выступающие концы и модификация миРНК
Следующее описание нуклеотидной последовательности V, последовательности нуклеиновой кислоты, нуклеотидной модификации в миРНК и модифицированной последовательности применимо к любой из миРНК с первой по шестую. То есть, если не указано иное, следующее описание миРНК следует рассматривать как описывающее первую миРНК, вторую миРНК, третью миРНК, четвертую миРНК, пятую миРНК и шестую миРНК поочередно. Например, если конкретная миРНК не указана, «миРНК дополнительно содержит нуклеотидную последовательность V» означает «первая миРНК, вторая миРНК, третья миРНК, четвертая миРНК, пятая миРНК или шестая миРНК дополнительно содержит нуклеотидную последовательность V».
В некоторых вариантах осуществления смысловая цепь и антисмысловая цепь имеют разную длину. Нуклеотидная последовательность II дополнительно содержит нуклеотидную последовательность V, которая имеет длину 1-3 нуклеотида и связана с 3’-концом антисмысловой цепи с образованием 3’-выступающего конца антисмысловой цепи. Таким образом, отношение длины смысловой цепи к длине антисмысловой цепи в миРНК согласно настоящему изобретению может составлять 19/20, 19/21, 19/22, 20/21, 20/22, 20/23, 21/22, 21/23, 21/24, 22/23, 22/24, 22/25, 23/24, 23/25 или 23/26. В некоторых вариантах осуществления нуклеотидная последовательность V имеет длину 2 нуклеотида. Таким образом, отношение длины смысловой цепи к длине антисмысловой цепи в миРНК согласно настоящему изобретению может составлять 19/21, 21/23 или 23/25.
Каждый нуклеотид в нуклеотидной последовательности V может представлять собой любой нуклеотид. Для упрощения синтеза и снижения затрат на его проведение нуклеотидная последовательность V представляет собой 2 тимидиновых дезоксирибонуклеотида подряд (dTdT) или 2 урациловых рибонуклеотида подряд (UU); или, для улучшения аффинности антисмысловой цепи миРНК к мРНК-мишени, нуклеотидная последовательность V комплементарна нуклеотидам в соответствующем сайте мРНК-мишени. Следовательно, в некоторых вариантах осуществления отношение длины смысловой цепи к длине антисмысловой цепи миРНК согласно настоящему изобретению составляет 19/21 или 21/23. В этом случае миРНК согласно настоящему изобретению обладает лучшей сайленсинговой активностью в отношении мРНК.
Нуклеотид в соответствующем сайте мРНК-мишени относится к нуклеотиду или нуклеотидной последовательности, примыкающей к нуклеотидной последовательности III мРНК-мишени с 5’-конца. Нуклеотидная последовательность III по существу обратно комплементарна или полностью обратно комплементарна нуклеотидной последовательности II, или представляет собой нуклеотидную последовательность, по существу обратно комплементарную или полностью обратно комплементарную нуклеотидной последовательности, образованной нуклеотидной последовательностью II и нуклеотидной последовательностью IV.
В некоторых вариантах осуществления для первой миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 5, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 6:
5’-CUUCAUUCAUACAGACAAZ3-3’ (SEQ ID NO: 5);
5’-Z4UUGUCUGUAUGAAUGAAGAG-3’ (SEQ ID NO: 6);
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 7, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 8:
5’-CUCUUCAUUCAUACAGACAAZ3-3’ (SEQ ID NO: 7);
5’-Z4UUGUCUGUAUGAAUGAAGAGAA-3’ (SEQ ID NO: 8);
где Z4 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z3 выбран из A, U, G или C; и Z4 представляет собой нуклеотид, комплементарный Z3.
В некоторых вариантах осуществления для миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 65, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 66:
5’-CUACAGUUUAGAAGAUUUZ7-3’ (SEQ ID NO: 65);
5’-Z8AAAUCUUCUAAACUGUAGUA-3’ (SEQ ID NO: 66),
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 67, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 68:
5’-UACUACAGUUUAGAAGAUUUZ7-3’ (SEQ ID NO: 67);
5’-Z8AAAUCUUCUAAACUGUAGUAUG-3’ (SEQ ID NO: 68),
где Z8 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z7 выбран из A, U, G или C; и Z8 представляет собой нуклеотид, комплементарный Z7.
В некоторых вариантах осуществления для третьей миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 125, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 126:
5’-GGAAGGUUACCGAGCAAUZ11-3’ (SEQ ID NO: 125);
5’-Z12AUUGCUCGGUAACCUUCCCU-3’ (SEQ ID NO: 126),
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 127, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 128:
5’-AGGGAAGGUUACCGAGCAAUZ11-3’ (SEQ ID NO: 127);
5’-Z12AUUGCUCGGUAACCUUCCCUGG-3’ (SEQ ID NO: 128),
где Z12 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z11 выбран из A, U, G или C; и Z12 представляет собой нуклеотид, комплементарный Z11.
В некоторых вариантах осуществления для четвертой миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 185, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 186:
5’-AGAACAGACAGCAGAAUUZ15-3’ (SEQ ID NO: 185);
5’-Z16AAUUCUGCUGUCUGUUCUCC-3’ (SEQ ID NO: 186),
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 187, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 188:
5’-GGAGAACAGACAGCAGAAUUZ15-3’ (SEQ ID NO: 187);
5’-Z16AAUUCUGCUGUCUGUUCUCCUG-3’ (SEQ ID NO: 188),
где Z16 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z15 выбран из A, U, G или C; и Z16 представляет собой нуклеотид, комплементарный Z15.
В некоторых вариантах осуществления для пятой миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 245, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 246:
5’-CCAAGAAGAACGCUGCAAZ19-3’ (SEQ ID NO: 245);
5’-Z20UUGCAGCGUUCUUCUUGGCC-3’ (SEQ ID NO: 246),
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 247, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 248:
5’-GGCCAAGAAGAACGCUGCAAZ19-3’ (SEQ ID NO: 247);
5’-Z20UUGCAGCGUUCUUCUUGGCCUG-3’ (SEQ ID NO: 248),
где Z20 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z19 выбран из A, U, G или C; и Z20 представляет собой нуклеотид, комплементарный Z19.
В некоторых вариантах осуществления для шестой миРНК смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 305, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 306:
5’-CCAGUAAGCAAGCCAGAAZ23-3’ (SEQ ID NO: 305);
5’-Z24UUCUGGCUUGCUUACUGGUA-3’ (SEQ ID NO: 306),
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 307, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 308:
5’-UACCAGUAAGCAAGCCAGAAZ23-3’ (SEQ ID NO: 307);
5’-Z24UUCUGGCUUGCUUACUGGUAAC-3’ (SEQ ID NO: 308),
где Z24 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; Z23 выбран из A, U, G или C; и Z24 представляет собой нуклеотид, комплементарный Z23.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой siC5a1, siC5a2, siC5b1, siC5b2, siC5c1, siC5c2, siC5d1, siC5d2, siC5e1, siC5e2, siC5f1 или siC5f2, перечисленные в таблицах 1a-1f.
Как описано выше, каждый из нуклеотидов в миРНК согласно настоящему изобретению независимо представляет собой модифицированные или немодифицированные нуклеотиды. В некоторых вариантах осуществления нуклеотиды в миРНК согласно настоящему изобретению представляют собой немодифицированные нуклеотиды. В некоторых вариантах осуществления некоторые или все нуклеотиды в миРНК согласно настоящему изобретению представляют собой модифицированные нуклеотиды. Такие модификации на нуклеотидах не будут вызывать значительного уменьшения или потери функции миРНК согласно настоящему изобретению в отношении ингибирования экспрессии генов C5.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению содержит по меньшей мере один модифицированный нуклеотид. В контексте настоящего изобретения термин «модифицированный нуклеотид», применяемый в настоящем документе, относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида другими группами, аналогу нуклеотида или нуклеотиду с модифицированным основанием. Такие модифицированные нуклеотиды не будут вызывать значительного уменьшения или потери функции миРНК в отношении ингибирования экспрессии генов. Например, могут быть выбраны модифицированные нуклеотиды, раскрытые в источнике Chemically Modified siRNA: tools and applications. Drug Discov Today, 2008.13(19-20): 842-55 за авт. J.K. Watts, G. F. Deleavey и M. J.Damha.
В некоторых вариантах осуществления по меньшей мере один нуклеотид в смысловой цепи или антисмысловой цепи миРНК согласно настоящему изобретению представляет собой модифицированный нуклеотид, и/или по меньшей мере один фосфат представляет собой фосфатную группу с модифицированной группой. Другими словами, по меньшей мере часть фосфатной группы и/или рибозной группы в фосфатно-рибозном остове по меньшей мере одной одиночной цепи в смысловой цепи и антисмысловой цепи представляет собой фосфатную группу с модифицированной группой и/или рибозную группу с модифицированной группой.
В некоторых вариантах осуществления все нуклеотиды в смысловой цепи и/или антисмысловой цепи представляют собой модифицированные нуклеотиды. В некоторых вариантах осуществления каждый нуклеотид в смысловой цепи и антисмысловой цепи миРНК согласно настоящему изобретению независимо представляет собой модифицированный фтором нуклеотид или нуклеотид с отличной от фтора модификацией.
Авторы настоящего изобретения неожиданно обнаружили, что миРНК согласно настоящему изобретению обладает высокой степенью равновесия между стабильностью в сыворотке и эффективностью сайленсинга генов в экспериментах на животных.
В некоторых вариантах осуществления модифицированные фтором нуклеотиды расположены в нуклеотидной последовательности I и нуклеотидной последовательности II; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 нуклеотидной последовательности I представляют собой модифицированные фтором нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности ii представляют собой модифицированные фтором нуклеотиды.
В некоторых вариантах осуществления модифицированные фтором нуклеотиды расположены в нуклеотидной последовательности I и нуклеотидной последовательности II; в нуклеотидной последовательности I присутствует не более 5 модифицированных фтором нуклеотидов, и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 в нуклеотидной последовательности I представляют собой модифицированные фтором нуклеотиды; в нуклеотидной последовательности II присутствует не более 7 модифицированных фтором нуклеотидов, и нуклеотиды в положениях 2, 6, 14 и 16 в нуклеотидной последовательности II представляют собой модифицированные фтором нуклеотиды.
В некоторых вариантах осуществления в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 или 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 или 2, 6, 8, 9, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией.
В контексте настоящего изобретения термин «модифицированный фтором нуклеотид» относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида фтором, который имеет структуру, представленную Формулой (7). «Нуклеотид с отличной от фтора модификацией» относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида группой, отличной от фтора, или аналогу нуклеотида. В некоторых вариантах осуществления каждый нуклеотид с отличной от фтора модификацией независимо выбран из нуклеотида, образованного путем замещения 2’-гидроксигруппы рибозной группы нуклеотида группой, отличной от фтора, или аналога нуклеотида.
Эти нуклеотиды, образованные путем замещения 2’-гидроксигруппы рибозной группы группой, отличной от фтора, хорошо известны специалистам в данной области техники, и эти нуклеотиды могут быть выбраны из одного из 2’-алкокси-модифицированного нуклеотида, 2’-замещенный алкокси-модифицированного нуклеотида, 2’-алкил-модифицированного нуклеотида, 2’-замещенный алкил-модифицированного нуклеотида, 2’-амино-модифицированного нуклеотида, 2’-замещенный амино-модифицированного нуклеотида и 2’-дезоксинуклеотида.
В некоторых вариантах осуществления 2’-алкокси-модифицированный нуклеотид представляет собой 2’-метокси-модифицированный нуклеотид (2’-OMe), представленный Формулой (8). В некоторых вариантах осуществления 2’-замещенный алкокси-модифицированный нуклеотид представляет собой, например, 2’-O-метоксиэтокси-модифицированный нуклеотид (2’-MOE), представленный Формулой (9). В некоторых вариантах осуществления 2’-амино-модифицированный нуклеотид (2’-NH2) соответствует представленному Формулой (10). В некоторых вариантах осуществления 2’-дезоксинуклеотид (ДНК) соответствует представленному Формулой (11):
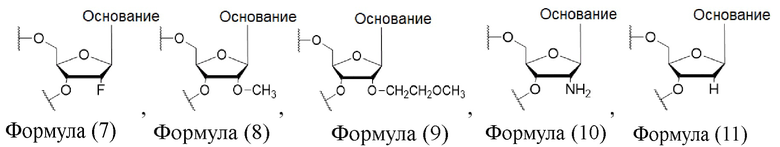
Аналог нуклеотида относится к группе, которая может заменять нуклеотид в нуклеиновой кислоте и при этом структурно отличается от аденинового рибонуклеотида, гуанинового рибонуклеотида, цитозинового рибонуклеотида, урацилового рибонуклеотида или тимидинового дезоксирибонуклеотида. В некоторых вариантах осуществления аналог нуклеотида может представлять собой изонуклеотид, мостиковую нуклеиновую кислоту или ациклический нуклеотид.
Мостиковая нуклеиновая кислота (BNA) представляет собой нуклеотид, который пространственно ограничен или недоступен. BNA может содержать структуру 5-членного кольца, 6-членного кольца или 7-членного кольца, связанного мостиком, имеющую выступ сахара в «фиксированной» C3’-эндоконформации. Мостик, как правило, встроен в 2’- и 4'-положения рибозы, образуя 2’,4'-BNA нуклеотид. В некоторых вариантах осуществления BNA может представлять собой LNA, ENA и cET BNA, где LNA соответствует представленной Формулой (12), ENA соответствует представленной Формулой (13), и cET BNA соответствует представленной Формулой (14):

Ациклический нуклеотид представляет собой нуклеотид, в котором рибозное кольцо открыто. В некоторых вариантах осуществления ациклический нуклеотид может представлять собой незаблокированную нуклеиновую кислоту (UNA) или гликолевую нуклеиновую кислоту (GNA), где UNA соответствует представленной Формулой (15), а GNA соответствует представленной Формулой (16):
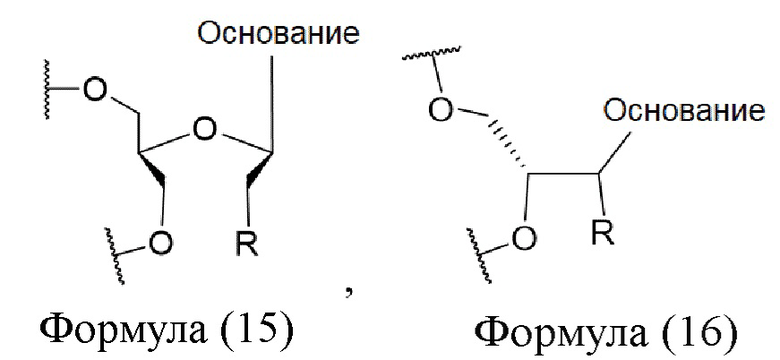
В Формуле (15) и Формуле (16) R выбран из H, OH или алкокси (O-алкила).
Изонуклеотид представляет собой соединение, образованное при изменении положения основания на рибозном кольце в нуклеотиде. В некоторых вариантах осуществления изонуклеотид может представлять собой соединение, в котором основание перемещено из положения-1' в положение-2’ или положение-3’ на рибозном кольце, как представлено Формулами (17) или (18):
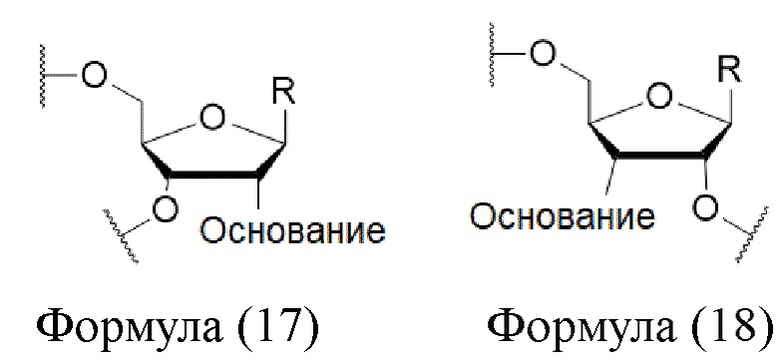
В соединениях, представленных Формулой (17) и Формулой (18) выше, Основание представляет собой основание, такое как A, U, G, C или T; и R выбран из H, OH, F или группы, отличной от фтора, описанной выше.
В некоторых вариантах осуществления аналог нуклеотида выбран из одного из изонуклеотида, LNA, ENA, cET, UNA и GNA. В некоторых вариантах осуществления каждый нуклеотид с отличной от фтора модификацией представляет собой метокси-модифицированный нуклеотид. В контексте настоящего изобретения метокси-модифицированный нуклеотид относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы метоксигруппой.
В контексте настоящего изобретения термины «модифицированный фтором нуклеотид», «2’-фтор-модифицированный нуклеотид», «нуклеотид, в котором 2’-гидроксигруппа рибозной группы замещена фтором» и «2’-фторрибозил» имеют одинаковое значение и относятся к соединению, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида фтором, имеющему структуру, представленную Формулой (7). Термины «метокси-модифицированный нуклеотид», «2’-метокси-модифицированный нуклеотид», «нуклеотид, в котором 2’-гидроксигруппа рибозной группы замещена метокси» и «2’-метоксирибозил» имеют одинаковое значение и относятся к соединению, образованному путем замещения 2’-гидроксигруппы рибозной группы нуклеотида метоксигруппой, имеющему структуру, представленную Формулой (8).
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой миРНК со следующими модификациями: в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 или 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи представляют собой метокси-модифицированные нуклеотиды; и нуклеотиды в положениях 2, 6, 14 и 16 или 2, 6, 8, 9, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи представляют собой метокси-модифицированные нуклеотиды.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой миРНК со следующими модификациями: в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 8, 9, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды;
или в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды;
или в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой любую из siC5a1-M1, siC5a1-M2, siC5a1-M3, siC5a2-M1, siC5a2-M2, siC5a2-M3, siC5b1-M1, siC5b1-M2, siC5b1-M3, siC5b2-M1, siC5b2-M2, siC5b2-M3, siC5c1-M1, siC5c1-M2, siC5c1-M3, siC5c2-M1, siC5c2-M2, siC5c2-M3, siC5d1-M1, siC5d1-M2, siC5d1-M3, siC5d2-M1, siC5d2-M2, siC5d2-M3, siC5e1-M1, siC5e1-M2, siC5e1-M3, siC5e2-M1, siC5e2-M2, siC5e2-M3, siC5f1-M1, siC5f1-M2, siC5f1-M3, siC5f2-M1, siC5f2-M2 или siC5f2-M3, перечисленных в таблицах 1a-1f.
миРНК с вышеуказанными модификациями не только могут быть получены с более низкими затратами, но также снижают склонность рибонуклеаз в крови расщеплять нуклеиновую кислоту, повышая тем самым стабильность нуклеиновой кислоты и обеспечивая более высокую устойчивость нуклеиновой кислоты к нуклеазному гидролизу.
В некоторых вариантах осуществления по меньшей мере часть фосфатной группы в фосфатно-рибозном остове по меньшей мере одной одиночной цепи в смысловой цепи и антисмысловой цепи миРНК согласно настоящему изобретению представляет собой фосфатную группу с модифицированной группой. В некоторых вариантах осуществления фосфатная группа с модифицированной группой представляет собой тиофосфатную группу, образованную путем замещения по меньшей мере одного атома кислорода в фосфодиэфирной связи в фосфатной группе атомом серы; и в некоторых вариантах осуществления фосфатная группа с модифицированной группой представляет собой тиофосфатную группу, имеющую структуру, представленную Формулой (1):
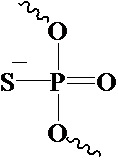 Формула (1).
Формула (1).
Эта модификация может стабилизировать двухцепочечную структуру миРНК, тем самым сохраняя высокую специфичность и высокую аффинность спаривания оснований.
В некоторых вариантах осуществления в миРНК согласно настоящему изобретению тиофосфатная связь присутствует в по меньшей мере одном из следующих положений: положение между первым нуклеотидом и вторым нуклеотидом на любом конце смысловой цепи или антисмысловой цепи; положение между вторым и третьим нуклеотидами на любом конце смысловой цепи или антисмысловой цепи; или любой их комбинации. В некоторых вариантах осуществления тиофосфатная связь присутствует во всех вышеуказанных положениях, за исключением 5’-конца смысловой цепи. В некоторых вариантах осуществления тиофосфатная связь присутствует во всех вышеуказанных положениях, за исключением 3’-конца смысловой цепи. В некоторых вариантах осуществления тиофосфатная связь присутствует в по меньшей мере одном из следующих положений:
положение между первым нуклеотидом и вторым нуклеотидом на 5’-конце смысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 5’-конце смысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 3’-конце смысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 3’-конце смысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 5’-конце антисмысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 5’-конце антисмысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 3’-конце антисмысловой цепи; и
положение между вторым нуклеотидом и третьим нуклеотидом на 3’-конце антисмысловой цепи.
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой любую из siC5a1-M1S, siC5a1-M2S, siC5a1-M3S, siC5a2-M1S, siC5a2-M2S, siC5a2-M3S, siC5b1-M1S, siC5b1-M2S, siC5b1-M3S, siC5b2-M1S, siC5b2-M2S, siC5b2-M3S, siC5c1-M1S, siC5c1-M2S, siC5c1-M3S, siC5c2-M1S, siC5c2-M2S, siC5c2-M3S, siC5d1-M1S, siC5d1-M2S, siC5d1-M3S, siC5d2-M1S, siC5d2-M2S, siC5d2-M3S, siC5e1-M1S, siC5e1-M2S, siC5e1-M3S, siC5e2-M1S, siC5e2-M2S, siC5e2-M3S, siC5f1-M1S, siC5f1-M2S, siC5f1-M3S, siC5f2-M1S, siC5f2-M2S или siC5f2-M3S, перечисленных в таблицах 1a-1f.
В некоторых вариантах осуществления 5’-концевой нуклеотид в антисмысловой цепи миРНК представляет собой нуклеотид с 5’-фосфатной группой или нуклеотид, модифицированный аналогом 5’-фосфатной группы.
Обычные типы нуклеотидов с 5’-фосфатной группой или нуклеотидов, модифицированных аналогом 5’-фосфатной группы, хорошо известны специалистам в данной области техники; например, нуклеотиды с 5’-фосфатной группой могут иметь следующую структуру:
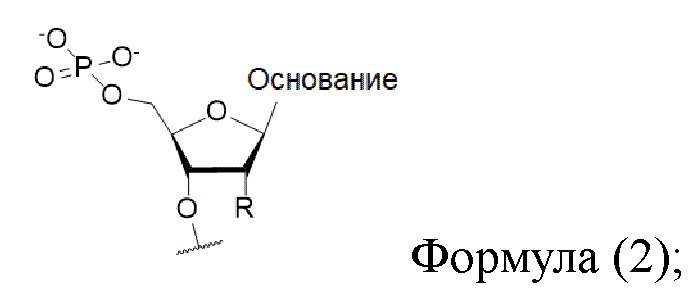
В качестве еще одного примера, в источнике The chemical evolution of oligonucleotide therapies of clinical utility. Nature Biotechnology, 2017, 35(3): 238-48 за авт. Anastasia Khvorova и Jonathan K. Watts, раскрыты следующие четыре нуклеотида, модифицированные аналогом 5’-фосфатной группы:
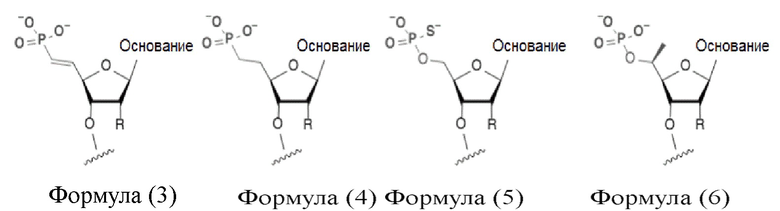
где R выбран из H, OH, метокси или F; и Основание представляет собой основание, выбранное из A, U, C, G или T.
В некоторых вариантах осуществления нуклеотид с 5’-фосфатной группой представляет собой нуклеотид с 5’-фосфатной модификацией, представленный Формулой (2); нуклеотид, модифицированный аналогом 5’-фосфатной группы, представляет собой нуклеотид с 5’-(E)-винилфосфонатной (E-VP) модификацией, представленный Формулой (3), или модифицированный тиофосфатом нуклеотид, представленный Формулой (5).
В некоторых вариантах осуществления миРНК согласно настоящему изобретению представляет собой любую из siC5a1-M1P1, siC5a1-M2P1, siC5a1-M3P1, siC5a2-M1P1, siC5a2-M2P1, siC5a2-M3P1, siC5b1-M1P1, siC5b1-M2P1, siC5b1-M3P1, siC5b2-M1P1, siC5b2-M2P1, siC5b2-M3P1, siC5c1-M1P1, siC5c1-M2P1, siC5c1-M3P1, siC5c2-M1P1, siC5c2-M2P1, siC5c2-M3P1, siC5d1-M1P1, siC5d1-M2P1, siC5d1-M3P1, siC5d2-M1P1, siC5d2-M2P1, siC5d2-M3P1, siC5e1-M1P1, siC5e1-M2P1, siC5e1-M3P1, siC5e2-M1P1, siC5e2-M2P1, siC5e2-M3P1, siC5f1-M1P1, siC5f1-M2P1, siC5f1-M3P1, siC5f2-M1P1, siC5f2-M2P1, siC5f2-M3P1, siC5a1-M1SP1, siC5a1-M2SP1, siC5a1-M3SP1, siC5a2-M1SP1, siC5a2-M2SP1, siC5a2-M3SP1, siC5b1-M1SP1, siC5b1-M2SP1, siC5b1-M3SP1, siC5b2-M1SP1, siC5b2-M2SP1, siC5b2-M3SP1, siC5c1-M1SP1, siC5c1-M2SP1, siC5c1-M3SP1, siC5c2-M1SP1, siC5c2-M2SP1, siC5c2-M3SP1, siC5d1-M1SP1, siC5d1-M2SP1, siC5d1-M3SP1, siC5d2-M1SP1, siC5d2-M2SP1, siC5d2-M3SP1, siC5e1-M1SP1, siC5e1-M2SP1, siC5e1-M3SP1, siC5e2-M1SP1, siC5e2-M2SP1, siC5e2-M3SP1, siC5f1-M1SP1, siC5f1-M2SP1, siC5f1-M3SP1, siC5f2-M1SP1, siC5f2-M2SP1 или siC5f2-M3SP1, перечисленных в таблицах 1a-1f.
Авторы настоящего изобретения неожиданно обнаружили, что миРНК согласно настоящему изобретению обладает значительно повышенной стабильностью в плазме и лизосомах и обладает более высокой ингибирующей активностью в отношении мРНК-мишени.
миРНК согласно настоящему изобретению может быть получена с помощью обычных способов получения миРНК в данной области техники (например, с помощью способов твердофазного синтеза и жидкофазного синтеза). Для твердофазного синтеза уже доступны коммерческие услуги по изготовлению на заказ. Модифицированные нуклеотиды могут быть введены в миРНК согласно настоящему изобретению с применением нуклеотидного мономера, имеющего соответствующую модификацию, где способы получения нуклеотидного мономера, имеющего соответствующую модификацию, и способы введения модифицированного нуклеотида в миРНК также хорошо известны специалистам в данной области техники. Модифицированные нуклеотидные группы могут быть введены в миРНК согласно настоящему изобретению с применением нуклеотидного мономера, имеющего соответствующую модификацию, где способы получения нуклеотидного мономера, имеющего соответствующую модификацию, и способы введения модифицированного нуклеотида в миРНК также хорошо известны специалистам в данной области техники.
Фармацевтическая композиция
Согласно настоящему изобретению предложена фармацевтическая композиция, содержащая миРНК, описанную выше, в качестве активного ингредиента и фармацевтически приемлемый носитель.
Фармацевтически приемлемый носитель может представлять собой носитель, обычно применяемый в области введения миРНК, например, не ограничиваясь перечисленным, одно или более из магнитных наночастиц (таких как наночастицы на основе Fe3O4 или Fe2O3), углеродных нанотрубок, мезопористого кремния, наночастиц фосфата кальция, полиэтиленимина (PEI), дендримера полиамидоамина (PAMAM), поли(L-лизина) (PLL), хитозана, 1,2-диолеоил-3-триметиламмоний-пропана (DOTAP), сополимера D,L-молочной и гликолевой кислот (PLGA), поли(2-аминоэтилэтиленфосфата) (PPEEA), поли(2-диметиламиноэтилметакрилата) (PDMAEMA) и их производных.
Нет никаких особых требований к содержанию миРНК и фармацевтически приемлемого носителя в фармацевтической композиции, и оно может представлять собой обычное содержание каждого компонента. В некоторых вариантах осуществления массовое отношение миРНК к фармацевтически приемлемому носителю составляет 1:(1-500), а в некоторых вариантах осуществления вышеуказанное массовое отношение составляет 1:(1-50).
В некоторых вариантах осуществления фармацевтическая композиция также может содержать другие фармацевтически приемлемые вспомогательные вещества, которые могут представлять собой один или более из различных общепринятых в данной области техники составов или соединений. Например, другие фармацевтически приемлемые вспомогательные вещества могут содержать по меньшей мере один из pH-буферного раствора, защитного агента и регулятора осмотического давления.
pH-буферный раствор может представлять собой буферный раствор гидрохлорида трис(гидроксиметил)аминометана с pH = 7,5-8,5, и/или фосфатный буферный раствор с pH = 5,5-8,5, предпочтительно фосфатный буферный раствор с pH = 5,5-8,5.
Защитный агент может представлять собой по меньшей мере один из инозита, сорбита, сахарозы, трегалозы, маннозы, мальтозы, лактозы и глюкозы. Содержание защитного агента может составлять от 0,01 мас.% до 30 мас.% от общей массы фармацевтической композиции.
Регулятор осмотического давления может представлять собой хлорид натрия и/или хлорид калия. Содержание регулятора осмотического давления обеспечивает осмотическое давление фармацевтической композиции на уровне 200-700 миллиосмоль/кг (мОсм/кг). В зависимости от целевого осмотического давления специалисты в данной области техники могут легко определить содержание регулятора осмотического давления.
В некоторых вариантах осуществления фармацевтическая композиция может представлять собой жидкий состав, например, раствор для инъекций; или лиофилизированный порошок для инъекций, который смешивают с жидким вспомогательным веществом для получения жидкого состава при введении. Жидкий состав может быть введен, не ограничиваясь перечисленным, путем подкожной, внутримышечной или внутривенной инъекции, а также может быть введен, не ограничиваясь перечисленным, в легкие путем распыления или другие органы (такие как печень) через легкие путем распыления. В некоторых вариантах осуществления фармацевтическую композицию вводят путем внутривенной инъекции.
В некоторых вариантах осуществления фармацевтическая композиция может находиться в форме липосомного препарата. В некоторых вариантах осуществления фармацевтически приемлемый носитель, применяемый в липосомном препарате, содержит аминосодержащее соединение для трансфекции (далее в настоящем документе также называемое органическим амином), вспомогательный липид и/или пегилированный липид. Органический амин, вспомогательный липид и пегилированный липид могут быть выбраны, соответственно, из одного или более из аминосодержащих соединений для трансфекции или их фармацевтически приемлемых солей или производных, вспомогательных липидов и пегилированных липидов, описанных в источнике CN103380113A (включенном в настоящий документ посредством ссылки в полном объеме).
В некоторых вариантах осуществления органический амин может представлять собой соединение, представленное Формулой (201), описанное в источнике CN103380113A, или его фармацевтически приемлемую соль:
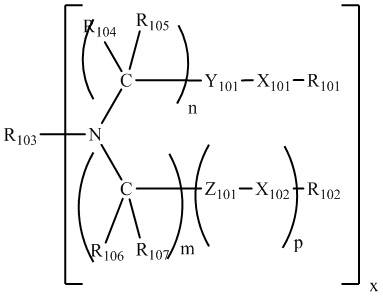 Формула (201),
Формула (201),
где:
X101 или X102 независимо выбран из O, S, N-A или C-A, где A представляет собой водород или C1-C20 углеводородную цепь;
Y101 или Z101 независимо выбран из C=O, C=S, S=O, CH-OH или SO2;
R101, R102, R103, R104, R105, R106 или R107 независимо выбран из водорода; циклической или алифатической, замещенной или незамещенной, разветвленной или линейной алифатической группы; циклической или алифатической, замещенной или незамещенной, разветвленной или линейной гетероалифатической группы; замещенной или незамещенной, разветвленной или линейной ацильной группы; замещенного или незамещенного, разветвленного или линейного арила или замещенного или незамещенного, разветвленного или линейного гетероарила;
x представляет собой целое число от 1 до 10;
n представляет собой целое число от 1 до 3, m представляет собой целое число от 0 до 20, и p равно 0 или 1, где, если m и p оба равны 0, то R102 представляет собой водород, и
если по меньшей мере один из n или m равен 2, то R103 и азот в Формуле (201) образуют структуру, представленную Формулой (202) или (203):

где g, e или f независимо представляет собой целое число от 1 до 6, «HCC» представляет собой углеводородную цепь, и каждый *N представляет собой атом азота, показанный в Формуле (201).
В некоторых вариантах осуществления R103 представляет собой полиамин. В других вариантах осуществления R103 представляет собой кеталь. В некоторых вариантах осуществления каждый из R101 и R102 в Формуле (201) независимо представляет собой любой замещенный или незамещенный, разветвленный или линейный алкил или алкенил, где указанный алкил или алкенил имеет от 3 до приблизительно 20 атомов углерода (например, от 8 до приблизительно 18 атомов углерода) и от 0 до 4 двойных связей (например, от 0 до 2 двойных связей).
В некоторых вариантах осуществления, если каждый из n и m независимо равен от 1 до 3, R103 может быть представлен любой из следующих Формул (204)-(213):

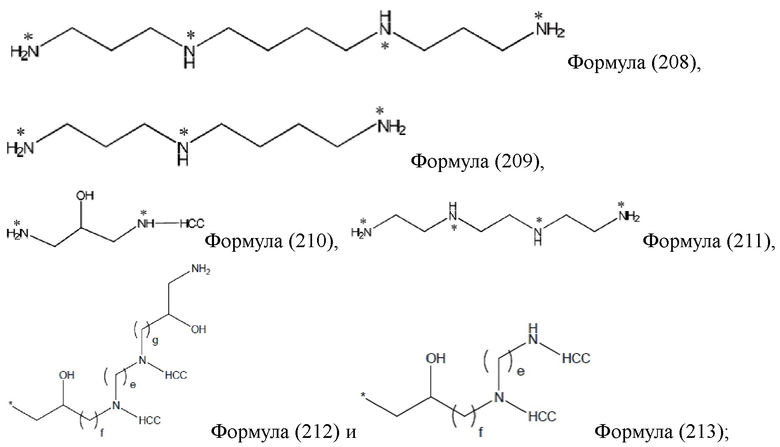
где в Формуле (204) - Формуле (213) каждый из g, e и f независимо представляет собой целое число от 1 до 6; каждый «HCC» представляет собой углеводородную цепь, и каждая * обозначает потенциальную точку присоединения R103 к атому азота в Формуле (201), где каждый H в любом отмеченном * положении может быть замещен, чтобы осуществить присоединение к атому азота в Формуле (201).
Соединение, представленное в (201), может быть получено, как описано в источнике CN103380113A.
В некоторых вариантах осуществления органический амин может представлять собой органический амин, представленный Формулой (214), и/или органический амин, представленный Формулой (215):
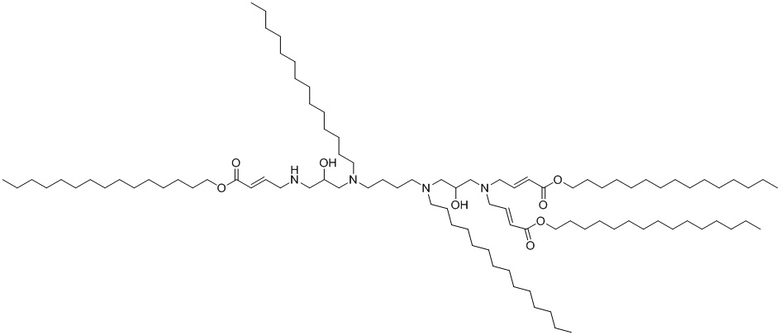 Формула (214),
Формула (214),
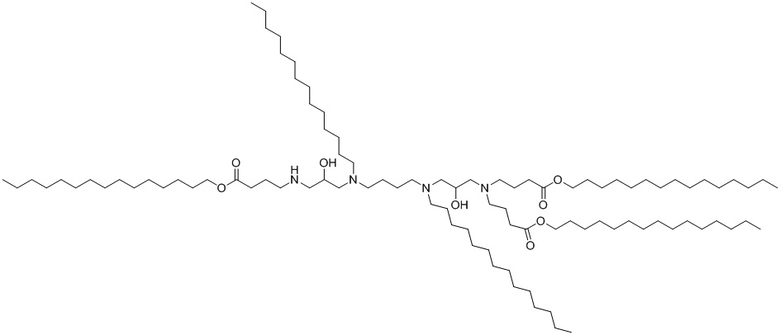 Формула (215).
Формула (215).
Вспомогательный липид представляет собой холестерин, аналог холестерина и/или производное холестерина.
Пегилированный липид представляет собой 1,2-дипальмитоил-sn-глицеро-3-фосфатидилэтаноламин-N-[метокси(полиэтиленгликоль)]-2000.
В некоторых вариантах осуществления молярное отношение между органическим амином, вспомогательным липидом и пегилированным липидом в фармацевтической композиции составляет (19,7-80): (19,7-80): (0,3-50); например, молярное отношение может составлять (50-70): (20-40): (3-20).
В некоторых вариантах осуществления фармацевтические композиции, образованные миРНК согласно настоящему изобретению и вышеуказанным аминосодержащим агентом для трансфекции, имеют средний диаметр от приблизительно 30 нм до приблизительно 200 нм, как правило, от приблизительно 40 нм до приблизительно 135 нм, и чаще средний диаметр липосомных частиц составляет от приблизительно 50 нм до приблизительно 120 нм, от приблизительно 50 нм до приблизительно 100 нм, от приблизительно 60 нм до приблизительно 90 нм или от приблизительно 70 нм до приблизительно 90 нм, например, средний диаметр липосомных частиц составляет приблизительно 30, 40, 50, 60, 70, 75, 80, 85, 90, 100, 110, 120, 130, 140, 150 или 160 нм.
В некоторых вариантах осуществления в фармацевтической композиции, образованной миРНК согласно настоящему изобретению и вышеуказанным аминосодержащим агентом для трансфекции, массовое отношение (отношение масса/масса) миРНК к общему количеству липидов (например, органического амина, вспомогательного липида и/или пегилированного липида) варьируется от приблизительно 1:1 до приблизительно 1:50, от приблизительно 1:1 до приблизительно 1:30, от приблизительно 1:3 до приблизительно 1:20, от приблизительно 1:4 до приблизительно 1:18, от приблизительно 1:5 до приблизительно 1:17, от приблизительно 1:5 до приблизительно 1:15, от приблизительно 1:5 до приблизительно 1:12, от приблизительно 1:6 до приблизительно 1:12, или от приблизительно 1:6 до приблизительно 1:10. Например, массовое отношение миРНК согласно настоящему изобретению к общему количеству липидов составляет приблизительно 1:5, 1:6, 1:7, 1:8, 1:9, 1:10, 1:11, 1:12, 1:13, 1:14, 1:15, 1:16, 1:17 или 1:18.
В некоторых вариантах осуществления каждый компонент в фармацевтической композиции при ее реализации на рынке может быть предоставлен отдельно, и композиция может применяться в форме жидкого состава. В некоторых вариантах осуществления фармацевтическая композиция, образованная миРНК согласно настоящему изобретению и вышеуказанным фармацевтически приемлемым носителем, может быть получена с помощью различных известных способов, за исключением замены существующей миРНК с помощью миРНК согласно настоящему изобретению. В некоторых вариантах осуществления фармацевтическая композиция может быть получена в соответствии со следующим способом.
Органические амины, вспомогательные липиды и пегилированные липиды суспендируют в спирте в молярном отношении, описанном выше, и смешивают до однородности с получением раствора липидов; и спирт применяют в таком количестве, чтобы полученный раствор липидов имел общую массовую концентрацию от 2 до 25 мг/мл, например, от 8 до 18 мг/мл. Спирт представляет собой фармацевтически приемлемый спирт, такой как спирт, который находится в жидкой форме при приблизительно комнатной температуре, например, один или более из этанола, пропиленгликоля, бензилового спирта, глицерина, ПЭГ 200, ПЭГ 300, ПЭГ 400 и, например, этанол.
миРНК согласно настоящему изобретению растворяют в забуференном солевом растворе для получения водного раствора миРНК. Забуференный солевой раствор имеет концентрацию 0,05-0,5 М, например, 0,1-0,2 М. pH забуференного солевого раствора доводят до 4,0-5,5, например, 5,0-5,2. Забуференный солевой раствор применяют в таком количестве, чтобы миРНК присутствовала в концентрации менее 0,6 мг/мл, например, 0,2-0,4 мг/мл. Буферная соль может представлять собой одну или более из группы, состоящей из растворимого ацетата и растворимого цитрата, таких как ацетат натрия и/или ацетат калия.
Раствор липидов и водный раствор миРНК смешивают. Продукт, полученный после смешивания, инкубируют при температуре 40-60°C в течение по меньшей мере 2 минут (например, 5-30 минут) с получением инкубированного препарата на липидной основе. Объемное отношение раствора липидов к водному раствору миРНК составляет 1:(2-5).
Инкубированный липосомный препарат концентрируют или разбавляют, очищают для удаления примесей, а затем стерилизуют с получением фармацевтической композиции согласно настоящему изобретению, имеющей следующие физико-химические параметры: pH 6,5-8, процент инкапсуляции более 80%, размер частиц 40-200 нм, коэффициент полидисперсности менее 0,30 и осмотическое давление 250-400 мОсм/кг; например, физико-химические параметры могут быть следующими: pH 7,2-7,6, процент инкапсуляции более 90%, размер частиц 60-100 нм, коэффициент полидисперсности менее 0,20 и осмотическое давление 300-400 мОсм/кг.
Стадия концентрирования или разбавления может быть проведена до, после или одновременно со стадией удаления примесей. Способ удаления примесей может представлять собой любой из различных существующих способов, таких как ультрафильтрация с применением колонки с полыми волокнами на 100 кДа и фосфатного буферного раствора (PBS) при pH = 7,4 в качестве заменяемого раствора для ультрафильтрации, и системы с тангенциальным потоком. Способ стерилизации может представлять собой любой из различных существующих способов, таких как стерилизующая фильтрация на фильтре с размером пор 0,22 мкм.
Конъюгат миРНК
Настоящее изобретение относится к конъюгату миРНК, содержащему вышеуказанную миРНК и конъюгирующую группу, связанную путем конъюгации с указанной миРНК.
Конъюгирующая группа, как правило, содержит по меньшей мере одну фармацевтически приемлемую нацеливающую группу и необязательный линкер. Кроме того, миРНК, линкер и нацеливающая группа соединены последовательно. В некоторых вариантах осуществления присутствует 1-6 нацеливающих групп. В некоторых вариантах осуществления присутствует 2-4 нацеливающие группы. Молекула миРНК может быть нековалентно или ковалентно конъюгирована с конъюгирующей группой, например, молекула миРНК может быть ковалентно конъюгирована с конъюгирующей группой. Сайт конъюгации миРНК и конъюгирующей группы может быть расположен на 3’-конце или 5’-конце смысловой цепи миРНК, или на 5’-конце антисмысловой цепи, или во внутренней последовательности миРНК. В некоторых вариантах осуществления сайт конъюгации миРНК и конъюгирующей группы расположен на 3’-конце смысловой цепи миРНК.
В некоторых вариантах осуществления конъюгирующая группа связана с фосфатной группой, 2’-гидрокси или основанием нуклеотида. В некоторых вариантах осуществления конъюгирующая группа может быть связана с 3’-гидрокси, когда нуклеотиды связаны посредством 2’-5’-фосфодиэфирной связи. Если конъюгирующая группа связана с концом миРНК, конъюгирующая группа, как правило, связана с фосфатной группой нуклеотида; если конъюгирующая группа связана с внутренней последовательностью миРНК, конъюгирующая группа, как правило, связана с рибозным кольцом или основанием. Конкретные варианты связывания приведены в источнике siRNA conjugates carrying sequentially assembled trivalent N-acetylgalactosamine linked through nucleosides elicit robust gene silencing in vivo in hepatocytes. ACS Chemical biology, 2015,10(5):1181-7, за авт. Muthiah Manoharan et.al.
В некоторых вариантах осуществления миРНК и конъюгирующая группа могут быть связаны посредством кислото-неустойчивой или восстанавливаемой химической связи, и эти химические связи могут быть разрушены в кислой среде эндосом клетки, приводя миРНК в свободное состояние. Для вариантов неразрушаемой конъюгации конъюгирующая группа может быть связана со смысловой цепью миРНК, что сводит к минимуму влияние конъюгации на активность миРНК.
В некоторых вариантах осуществления фармацевтически приемлемая нацеливающая группа может представлять собой обычно используемый в области введения миРНК лиганд, например, различные лиганды, описанные в источнике WO2009082607A2, включенном в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах осуществления фармацевтически приемлемая нацеливающая группа может быть выбрана из одного или более из лигандов, образованных следующими нацеливающими молекулами или их производными: липофильные молекулы, такие как холестерин, желчные кислоты, витамины (такие как витамин Е), молекулы липидов с разной длиной цепи; полимеры, такие как полиэтиленгликоль; полипептиды, такие как проникающий пептид; аптамеры; антитела; квантовые точки; сахариды, такие как лактоза, полилактоза, манноза, галактоза и N-ацетилгалактозамин (GalNAc); фолат; и лиганды рецепторов, экспрессируемые в паренхимных клетках печени, такие как асиалогликопротеин, асиало-сахарный остаток, липопротеины (такие как липопротеин высокой плотности, липопротеин низкой плотности), глюкагон, нейромедиаторы (такие как адреналин), факторы роста, трансферрин и тому подобное.
В некоторых вариантах осуществления каждый лиганд независимо представляет собой лиганд, способный связываться с поверхностным клеточным рецептором. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой лиганд, способный связываться с поверхностным рецептором гепатоцита. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой лиганд, способный связываться с поверхностным рецептором клетки млекопитающего. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой лиганд, способный связываться с поверхностным рецептором клетки человека. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой лиганд, способный связываться с асиалогликопротеиновым рецептором (ASGPR) на поверхности гепатоцита. Типы этих лигандов хорошо известны специалистам в данной области техники, и они, как правило, выполняют функцию связывания с определенными рецепторами на поверхности клетки-мишени, опосредуя доставку миРНК, связанной с лигандом, в клетку-мишень.
В некоторых вариантах осуществления фармацевтически приемлемая нацеливающая группа может представлять собой любой лиганд, который связывается с асиалогликопротеиновыми рецепторами (ASGPR) на поверхности гепатоцитов млекопитающего. В одном варианте осуществления каждый лиганд независимо представляет собой асиалогликопротеин, такой как асиалоорозомукоид (ASOR) или асиалофетуин (ASF). В некоторых вариантах осуществления лиганд представляет собой сахарид или производное сахарида.
В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой сахарид. В некоторых вариантах осуществления каждый лиганд представляет собой сахарид. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой моносахарид, полисахарид, модифицированный моносахарид, модифицированный полисахарид или производное сахарида. В некоторых вариантах осуществления по меньшей мере один лиганд может представлять собой моносахарид, дисахарид или трисахарид. В некоторых вариантах осуществления по меньшей мере один лиганд представляет собой модифицированный сахарид. В некоторых вариантах осуществления каждый лиганд представляет собой модифицированный сахарид. В некоторых вариантах осуществления каждый лиганд независимо выбран из группы, состоящей из полисахаридов, модифицированных полисахаридов, моносахаридов, модифицированных моносахаридов, производных полисахаридов или производных моносахаридов. В некоторых вариантах осуществления каждый лиганд или по меньшей мере один лиганд выбран из группы, состоящей из следующих сахаридов: глюкозы и ее производного, маннозы и ее производного, галактозы и ее производного, ксилозы и ее производного, рибозы и ее производного, фукозы и ее производного, лактозы и ее производного, мальтозы и ее производного, арабинозы и ее производного, фруктозы и ее производного, и сиаловой кислоты.
В некоторых вариантах осуществления каждый лиганд может быть независимо выбран из одного из следующих: D-маннопираноза, L-маннопираноза, D-арабиноза, D-ксилофураноза, L-ксилофураноза, D-глюкоза, L-глюкоза, D-галактоза, L-галактоза, α-D-маннофураноза, β-D-маннофураноза, α-D-маннопираноза, β-D-маннопираноза, α-D-глюкопираноза, β-D-глюкопираноза, α-D-глюкофураноза, β-D-глюкофураноза, α-D-фруктофураноза, α-D-фруктопираноза, α-D-галактопираноза, β-D-галактопираноза, α-D-галактофураноза, β-D-галактофураноза, глюкозамин, сиаловая кислота, галактозамин, N-ацетилгалактозамин, N-трифторацетилгалактозамин, N-пропионилгалактозамин, N-н-бутирилгалактозамин, N-изобутирилгалактозамин, 2-амино-3-O-[(R)-1-карбоксиэтил]-2-дезокси-β-D-глюкопираноза, 2-дезокси-2-метиламино-L-глюкопираноза, 4,6-дидезокси-4-формамидо-2,3-ди-O-метил-D-маннопираноза, 2-дезокси-2-сульфоамино-D-глюкопираноза, N-гликолил-α-нейраминовая кислота, 5-тио-β-D-глюкофураноза, метил-2,3,4-трис-O-ацетил-1-тио-6-O-тритил-α-D-глюкофураноза, 4-тио-β-D-галактопираноза, этил-3,4,6,7-тетра-O-ацетил-2-дезокси-1,5-дитио-α-D-глюкогептопиранозид, 2,5-ангидро-D-аллононитрил, рибоза, D-рибоза, D-4-тиорибоза, L-рибоза или L-4-тиорибоза. Другие подборки лигандов можно найти, например, в источнике CN105378082A, включенном в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах осуществления фармацевтически приемлемая нацеливающая группа в конъюгате миРНК может представлять собой галактозу или N-ацетилгалактозамин, где молекулы галактозы или N-ацетилгалактозамина могут быть одновалентными, двухвалентными, трехвалентными и четырехвалентными. Следует иметь в виду, что термины «одновалентный», «двухвалентный», «трехвалентный» и «четырехвалентный», описанные в настоящем документе, соответственно означают, что молярное отношение молекулы миРНК к молекуле галактозы или N-ацетилгалактозамина в конъюгате миРНК составляет 1:1, 1:2, 1:3 или 1:4, где конъюгат миРНК образован из молекулы миРНК и конъюгирующей группы, содержащей галактозу или N-ацетилгалактозамин в качестве нацеливающей группы. В некоторых вариантах осуществления фармацевтически приемлемая нацеливающая группа представляет собой N-ацетилгалактозамин. В некоторых вариантах осуществления, когда миРНК согласно настоящему изобретению конъюгирована с конъюгирующей группой, содержащей N-ацетилгалактозамин, молекула N-ацетилгалактозамина является трехвалентной или четырехвалентной. В некоторых вариантах осуществления, когда миРНК согласно настоящему изобретению конъюгирована с конъюгирующей группой, содержащей N-ацетилгалактозамин, молекула N-ацетилгалактозамина является трехвалентной.
Нацеливающая группа может быть связана с молекулой миРНК посредством подходящего линкера, и указанный подходящий линкер может быть выбран специалистами в данной области техники в соответствии с конкретным типом нацеливающей группы. Типы этих линкеров и нацеливающих групп, а также методы связывания с миРНК можно найти в источнике WO2015006740A2, включенном в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах осуществления, когда нацеливающая группа представляет собой N-ацетилгалактозамин, подходящий линкер может представлять собой структуру, представленную Формулой (301):
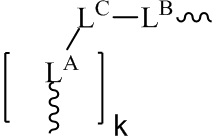 Формула (301),
Формула (301),
где
k представляет собой целое число от 1 до 3; и
LA представляет собой фрагмент цепи, содержащий амидную связь, имеющий структуру, представленную Формулой (302), причем каждый LA соответствующим образом связан с нацеливающей группой и фрагментом LC посредством простой эфирной связи на двух его концах:
 Формула (302);
Формула (302);
LB представляет собой фрагмент цепи, содержащий N-ацилпирролидин, имеющий структуру, представленную Формулой (303), причем фрагмент цепи содержит карбонил на одном его конце и связан с фрагментом LC посредством амидной связи, и содержит оксигруппу на другом его конце и связан с миРНК посредством фосфоэфирной связи:
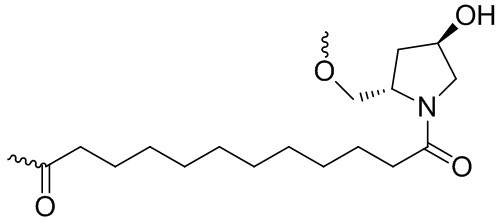 Формула (303);
Формула (303);
LC представляет собой двух-четырехвалентную связывающую группу на основе гидроксиметиламинометана, дигидроксиметиламинометана или тригидроксиметиламинометана, причем LC связан с каждым из фрагментов LA посредством простой эфирной связи через атом кислорода и связан с фрагментом LB посредством амидной связи через атом азота.
В некоторых вариантах осуществления, когда n=3 и LC представляет собой четырехвалентную связывающую группу на основе тригидроксиметиламинометана, конъюгат миРНК, образованный путем связывания молекулы N-ацетилгалактозамина с молекулой миРНК с помощью -(LA)3-тригидроксиметиламинометан-LB- в качестве линкера, имеет структуру, представленную Формулой (304):
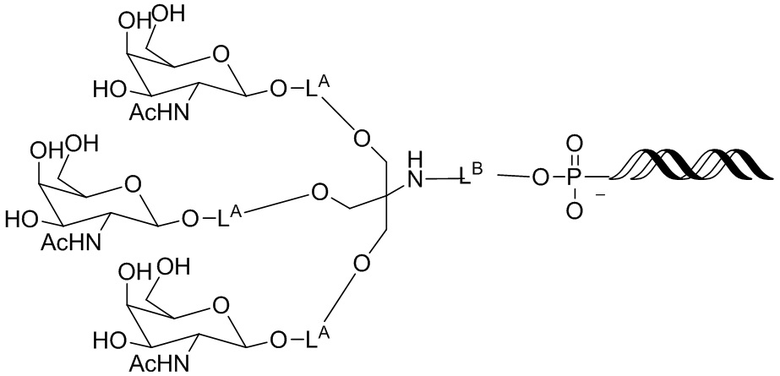 Формула (304),
Формула (304),
где структура двойной спирали представляет собой миРНК.
Аналогичным образом, сайт конъюгации миРНК и конъюгирующей группы может быть расположен на 3’-конце или 5’-конце смысловой цепи миРНК, или на 5’-конце антисмысловой цепи, или во внутренней последовательности миРНК.
В некоторых вариантах осуществления 3’-конец смысловой цепи миРНК согласно настоящему изобретению ковалентно конъюгирован с тремя молекулами N-ацетилгалактозамина (GalNAc) с помощью линкера -(LA)3-тригидроксиметиламинометан-LB- с получением конъюгата миРНК, в котором молярное отношение молекулы миРНК к молекуле GaINAc составляет 1:3, который далее в настоящем документе также может называться (GaINAc)3-миРНК), и конъюгат миРНК имеет структуру, представленную Формулой (305):
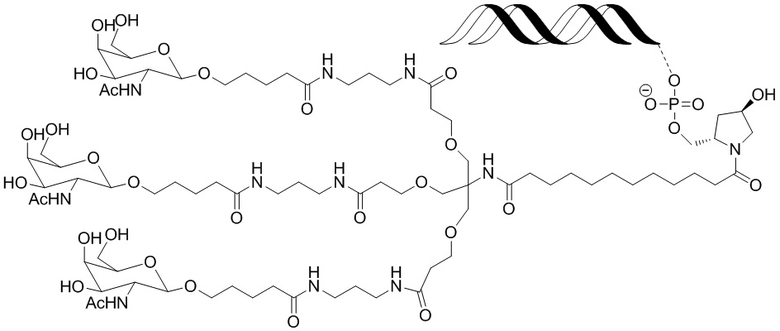 Формула (305),
Формула (305),
где структура двойной спирали представляет собой миРНК; и линкер связан с 3’-концом смысловой цепи миРНК.
В некоторых вариантах осуществления, когда нацеливающая группа представляет собой N-ацетилгалактозамин, подходящий линкер может представлять собой структуру, представленную Формулой (306):
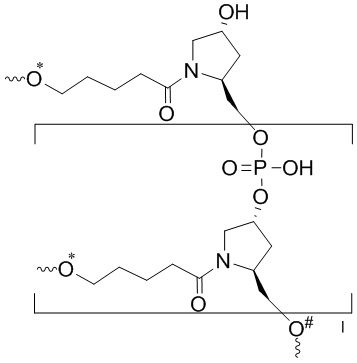 , Формула (306),
, Формула (306),
где
l представляет собой целое число от 0 до 3;
* обозначает сайт, связанный с нацеливающей группой посредством простой эфирной связи на линкере; и
# обозначает сайт, связанный с миРНК посредством фосфоэфирной связи на линкере.
В некоторых вариантах осуществления, когда l=2, конъюгат миРНК имеет структуру, представленную Формулой (307):
 Формула (307),
Формула (307),
где структура двойной спирали представляет собой миРНК; и линкер связан с 3’-концом смысловой цепи миРНК.
Вышеуказанные конъюгаты могут быть синтезированы в соответствии со способами, подробно описанными в уровне техники. Например, в источнике WO2015006740A2 подробно описан способ получения различных конъюгатов. Конъюгат миРНК согласно настоящему изобретению может быть получен способами, хорошо известными специалистам в данной области техники. В качестве еще одного примера в источнике WO2014025805A1 описан способ получения конъюгата, имеющего структуру, представленную Формулой (305). Rajeev et al. описывают способ получения конъюгата, имеющего структуру, представленную Формулой (307), в ChemBioChem 2015, 16, 903-908.
В некоторых вариантах осуществления конъюгат миРНК имеет структуру, представленную Формулой (308):

Формула (308),
где:
n1 представляет собой целое число от 1 до 3, а n3 представляет собой целое число от 0 до 4;
каждый из m1, m2 и m3 независимо представляет собой целое число от 2 до 10;
каждый из R10, R11, R12, R13, R14 или R15 независимо представляет собой H или выбран из группы, состоящей из C1-C10 алкила, C1-C10 галогеналкила и C1-C10 алкокси; и
R3 представляет собой группу, имеющую структуру, представленную Формулой A59:

(A59),
где E1 представляет собой OH, SH или BH2, а Nu представляет собой миРНК согласно настоящему изобретению;
R2 представляет собой линейный алкилен длиной от 1 до 20 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10 арилена, C3-C18 гетероциклилена и C5-C10 гетероарилена, и где R2 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10 арила, C5-C10 гетероарила, C1-C10 галогеналкила, -OC1-C10 алкила, -OC1-C10 алкилфенила, -C1-C10 алкил-OH, -OC1-C10 галогеналкила, -SC1-C10 алкила, -SC1-C10 алкилфенила, -C1-C10 алкил-SH, -SC1-C10 галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10 алкилфенила), -NH(C1-C10 алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10 алкилфенила, -C(O)C1-C10 галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10 галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10 галогеналкила); и
каждый L1 независимо представляет собой линейный алкилен длиной от 1 до 70 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10 арилена, C3-C18 гетероциклилена и C5-C10 гетероарилена; и где L1 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10 арила, C5-C10 гетероарила, C1-C10 галогеналкила, -OC1-C10 алкила, -OC1-C10 алкилфенила, -C1-C10 алкил-OH, -OC1-C10 галогеналкила, -SC1-C10 алкила, -SC1-C10 алкилфенила, -C1-C10 алкил-SH, -SC1-C10 галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10 алкилфенила), -NH(C1-C10 алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10 алкилфенила, -C(O)C1-C10 галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10 галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10 галогеналкила).
В некоторых вариантах осуществления L1 может быть выбран из группы, состоящей из групп (A1)-(A26) и любой их комбинации, где структуры и определения (A1)-(A26) представляют собой следующие:
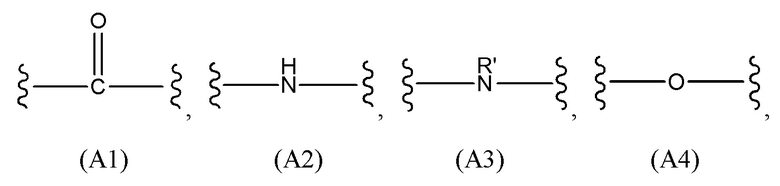
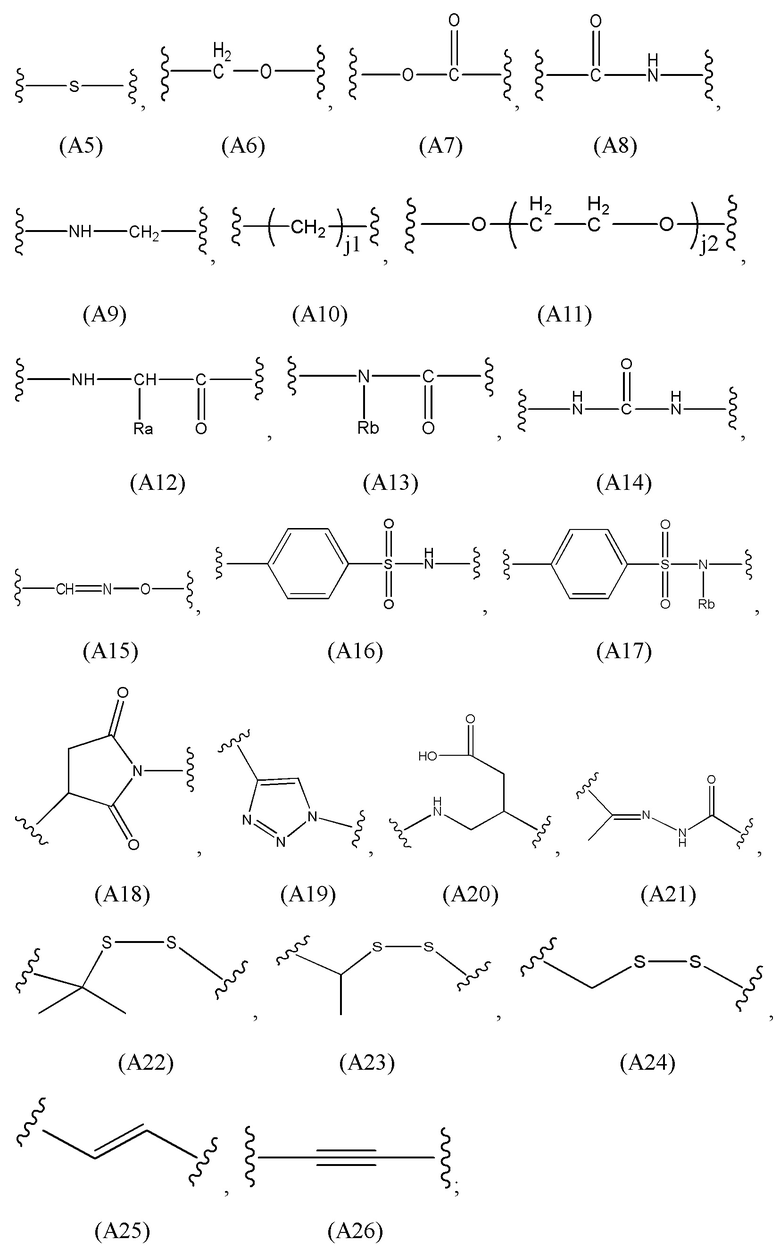
где каждый j1 независимо представляет собой целое число от 1 до 20; и каждый j2 независимо представляет собой целое число от 1 до 20;
каждый R' независимо представляет собой C1-C10 алкил; и
каждый Ra независимо выбран из группы, состоящей из групп (A27)-(A45) и любых комбинаций их соединений:
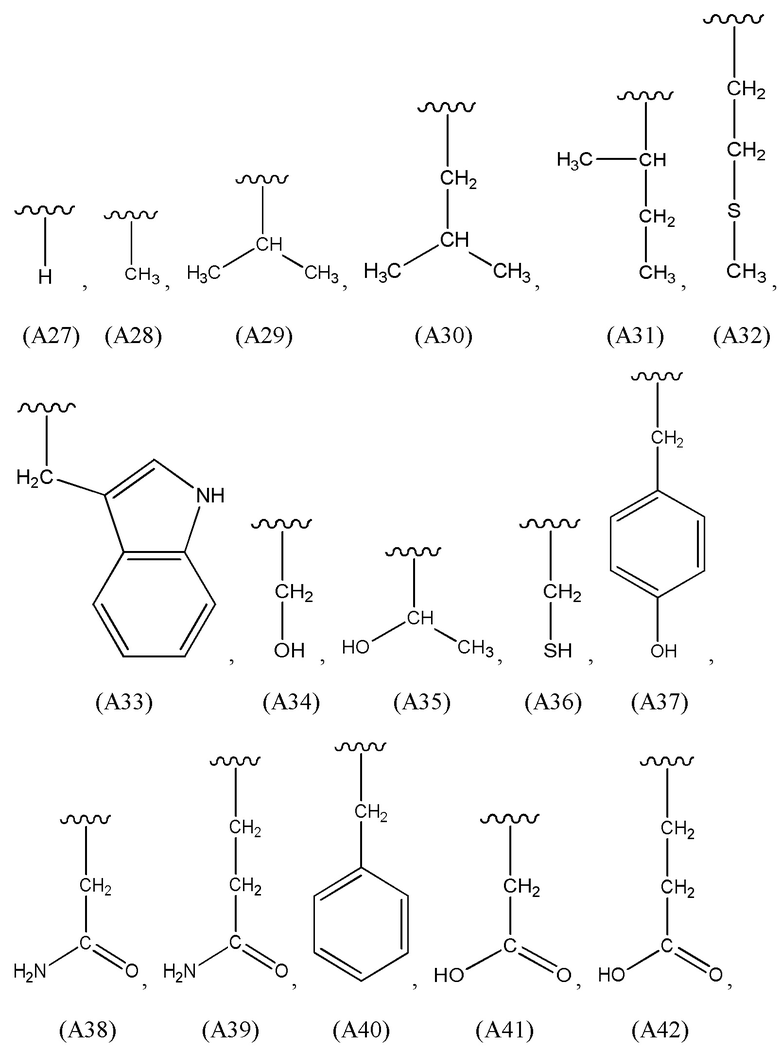

каждый Rb независимо представляет собой C1-C10 алкил; и  обозначает сайт ковалентного присоединения группы.
обозначает сайт ковалентного присоединения группы.
Специалистам в данной области техники будет ясно, что, несмотря на то, что для удобства L1 определен как линейный алкилен, он может не представлять собой линейную группу или может называться по-другому, например, амином или алкенилом, полученным посредством вышеуказанной замены и/или замещения. Для целей настоящего изобретения длина L1 представляет собой количество атомов в цепи, соединяющей две точки присоединения. Для этой цели кольцо, получаемое путем замены атома углерода линейного алкилена, такого как гетероциклилен или гетероарилен, считается за один атом.
M1 представляет собой нацеливающую группу, определения и варианты которой аналогичны описанным выше. В некоторых вариантах осуществления каждая M1 независимо выбрана из одного из лигандов, обладающих аффинностью к асиалогликопротеиновому рецептору на поверхности гепатоцитов млекопитающего.
Когда M1 представляет собой лиганд, обладающий аффинностью к асиалогликопротеиновому рецептору на поверхности гепатоцитов млекопитающего, в некоторых вариантах осуществления n1 может представлять собой целое число от 1 до 3, а n3 может представлять собой целое число от 0 до 4, чтобы количество нацеливающих групп M1 в конъюгате миРНК могло составлять по меньшей мере 2. В некоторых вариантах осуществления n1+n3≥2, так что количество нацеливающих групп M1 в конъюгате может составлять по меньшей мере 3, обеспечивая тем самым более легкое связывание нацеливающей группы M1 с асиалогликопротеиновым рецептором на поверхности гепатоцитов, что может облегчать эндоцитоз конъюгата миРНК в клетки. Эксперименты показали, что, когда количество нацеливающих групп M1 превышает 3, легкость связывания нацеливающей группы M1 с асиалогликопротеиновым рецептором на поверхности гепатоцитов существенно не увеличивается. Таким образом, с учетом различных аспектов, таких как удобство синтеза, структура/затраты на проведение способа и эффективность доставки, в некоторых вариантах осуществления n1 представляет собой целое число от 1 до 2, n3 представляет собой целое число от 0 до 1, и n1+n3=2-3.
В некоторых вариантах осуществления, когда каждый из m1, m2 или m3 независимо выбран из целого числа от 2 до 10, взаимные пространственные расположения множества нацеливающих групп M1 могут быть подходящими для связывания нацеливающих групп M1 с асиалогликопротеиновым рецептором на поверхности гепатоцитов. Для того, чтобы конъюгат миРНК согласно настоящему изобретению имел более простую структуру, более простой синтез и/или сниженную стоимость, в некоторых вариантах осуществления m1, m2 или m3 независимо представляет собой целое число от 2 до 5, и в некоторых вариантах осуществления m1=m2=m3.
Специалистам в данной области техники будет ясно, что, когда каждый из R10, R11, R12, R13, R14 или R15 независимо выбран из H, C1-C10 алкила, C1-C10 галогеналкила и C1-C10 алкокси, они не изменяют свойства конъюгата миРНК согласно настоящему изобретению и все способны достичь цели настоящего изобретения. В некоторых вариантах осуществления каждый из R10, R11, R12, R13, R14 или R15 независимо выбран из H, метила или этила. В некоторых вариантах осуществления все из R10, R11, R12, R13, R14 и R15 представляют собой H.
R3 представляет собой группу, имеющую структуру, представленную Формулой A59, где E1 представляет собой OH, SH или BH2, и при доступности исходных веществ в некоторых вариантах осуществления E1 представляет собой OH или SH.
R2 выбирают таким образом, чтобы обеспечить связь между группой, представленной Формулой A59, и атомом N на азотсодержащем остове. В контексте настоящего изобретения «азотсодержащий остов» относится к цепочечной структуре, в которой атомы углерода, присоединенные к R10, R11, R12, R13, R14 и R15, и атомы N связаны друг с другом. Следовательно, R2 может представлять собой любую связывающую группу, способную присоединять группу, представленную Формулой A59, к атому N на азотсодержащем остове с помощью подходящих средств. В некоторых вариантах осуществления, в случае, если конъюгат миРНК, представленный Формулой (308), согласно настоящему изобретению, получают с помощью процесса твердофазного синтеза, группа R2 должна иметь как сайт связывания с атомом N на азотсодержащем остове, так и сайт связывания с атомом P в R3. В некоторых вариантах осуществления в R2 сайт связывания с атомом N на азотсодержащем остове образует амидную связь с атомом N, а сайт связывания с атомом P в R3 образует фосфоэфирную связь с атомом P. В некоторых вариантах осуществления R2 может представлять собой B5, B6, B5' или B6':
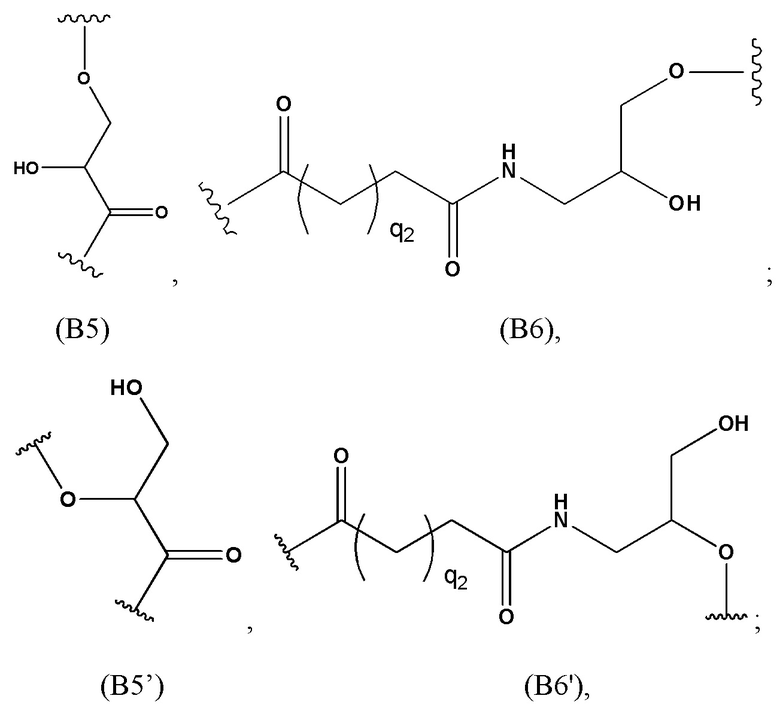
где  обозначает сайт ковалентного присоединения группы; и
обозначает сайт ковалентного присоединения группы; и
диапазон значений q2 может представлять собой целое число от 1 до 10; и в некоторых вариантах осуществления q2 представляет собой целое число от 1 до 5.
L1 используется для связывания нацеливающей группы M1 с атомом N на азотсодержащем остове, что наделяют конъюгат миРНК, представленный Формулой (308), функцией нацеливания на печень. В некоторых вариантах осуществления L1 выбран из комбинаций соединений одной или более из групп, представленных Формулами A1-A26. В некоторых вариантах осуществления L1 выбран из комбинаций соединений одной или более из A1, A4, A5, A6, A8, A10, A11 и A13. В некоторых вариантах осуществления L1 выбран из комбинаций соединений по меньшей мере двух из A1, A4, A8, A10 и A11. В некоторых вариантах осуществления L1 выбран из комбинаций соединений по меньшей мере двух из A1, A8 и A10.
В некоторых вариантах осуществления длина L1 может составлять 3-25 атомов, 3-20 атомов, 4-15 атомов или 5-12 атомов. В некоторых вариантах осуществления длина L1 составляет 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60 атомов.
В некоторых вариантах осуществления j1 представляет собой целое число от 2 до 10, и в некоторых вариантах осуществления j1 представляет собой целое число от 3 до 5. В некоторых вариантах осуществления j2 представляет собой целое число от 2 до 10, и в некоторых вариантах осуществления j2 представляет собой целое число от 3 до 5. R' представляет собой C1-C4 алкил, и в некоторых вариантах осуществления R' представляет собой один из метила, этила и изопропила. Ra представляет собой одну из A27, A28, A29, A30 и A31, и в некоторых вариантах осуществления Ra представляет собой A27 или A28. Rb представляет собой C1-C5 алкил, и в некоторых вариантах осуществления Rb представляет собой один из метила, этила, изопропила и бутила. В некоторых вариантах осуществления j1, j2, R', Ra и Rb Формул A1-A26 выбраны соответствующим образом, чтобы обеспечить связывание между нацеливающей группой M1 и атомом N на азотсодержащем остове, а также чтобы создать взаимное пространственное расположение нацеливающих групп M1, более подходящее для связывания нацеливающей группы M1 с асиалогликопротеиновым рецептором на поверхности гепатоцитов.
В некоторых вариантах осуществления конъюгат миРНК имеет структуру, представленную Формулой (403), (404), (405), (406), (407), (408), (409), (410), (411), (412), (413), (414), (415), (416), (417), (418), (419), (420), (421) или (422):
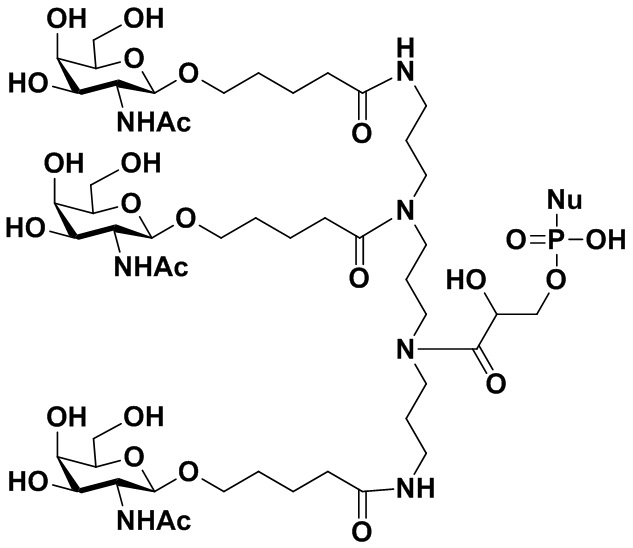
Формула (403)

Формула (404)

Формула (405)

Формула (406)
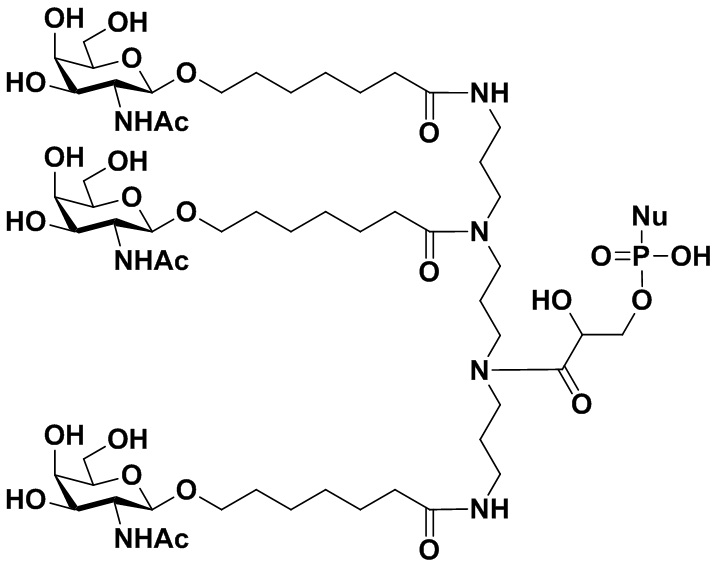
Формула (407)

Формула (408)

Формула (409)
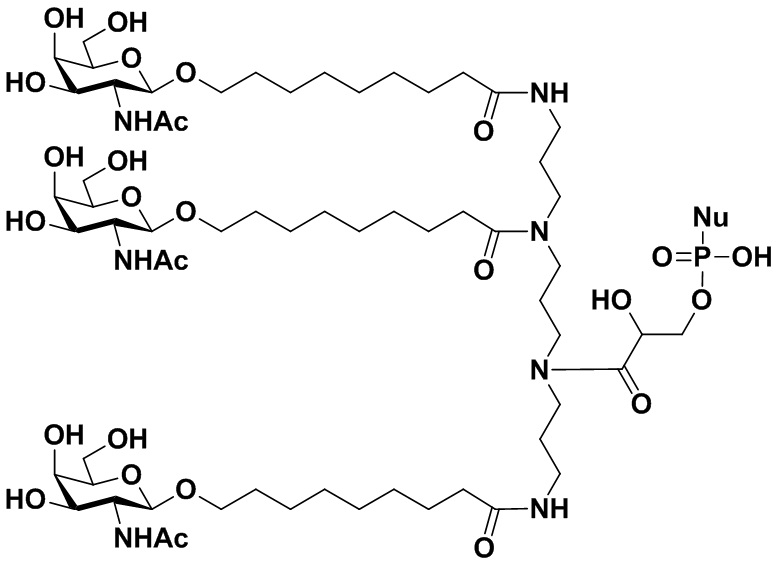
Формула (410)

Формула (411)
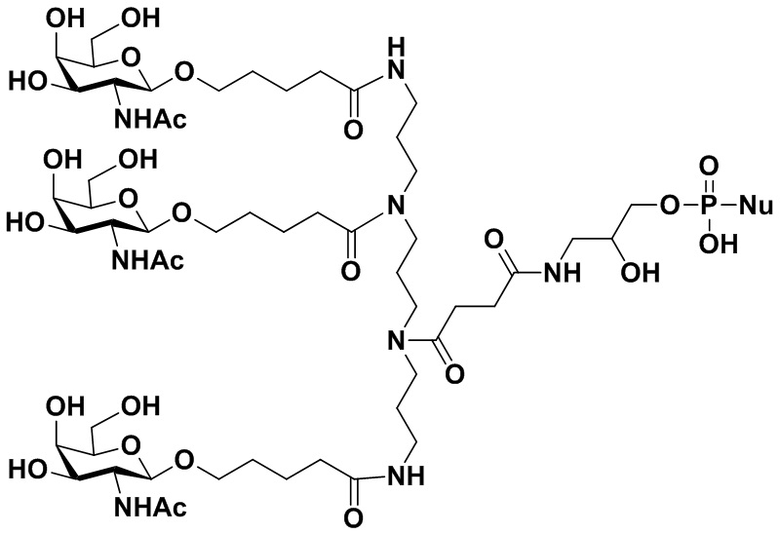
Формула (412)
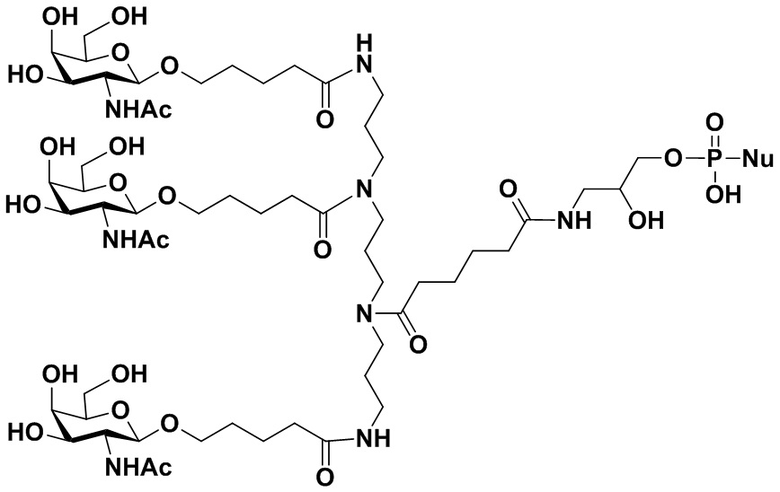
Формула (413)
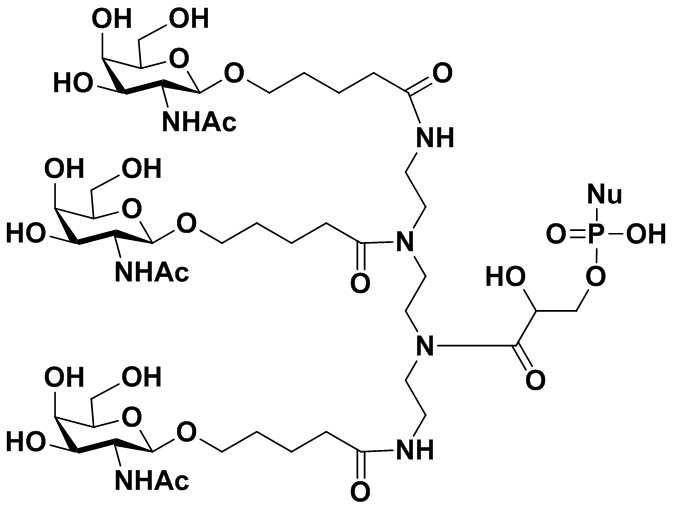
Формула (414)
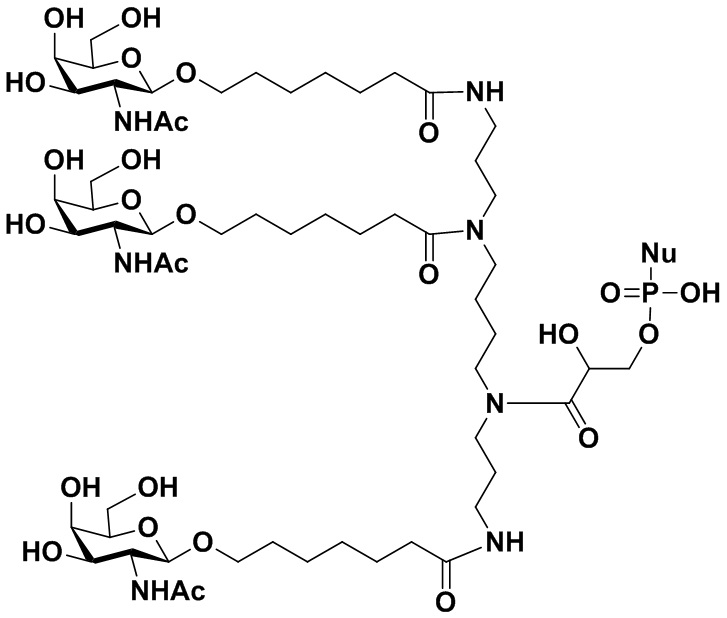
Формула (415)
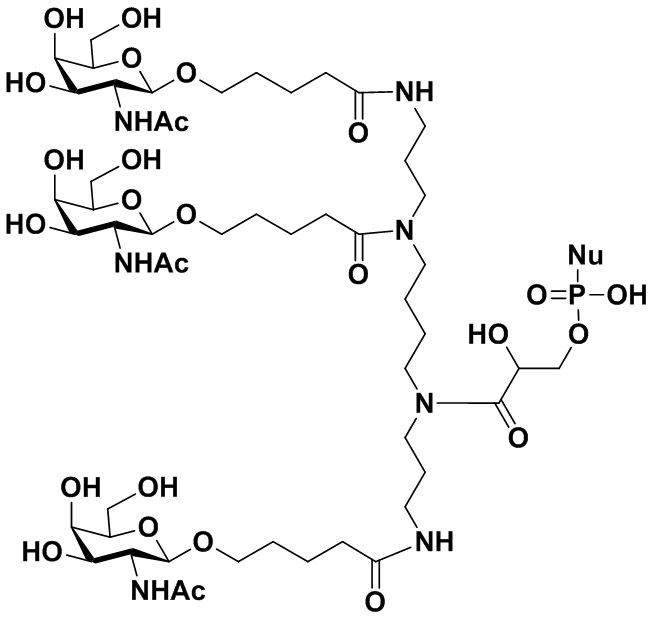
Формула (416)
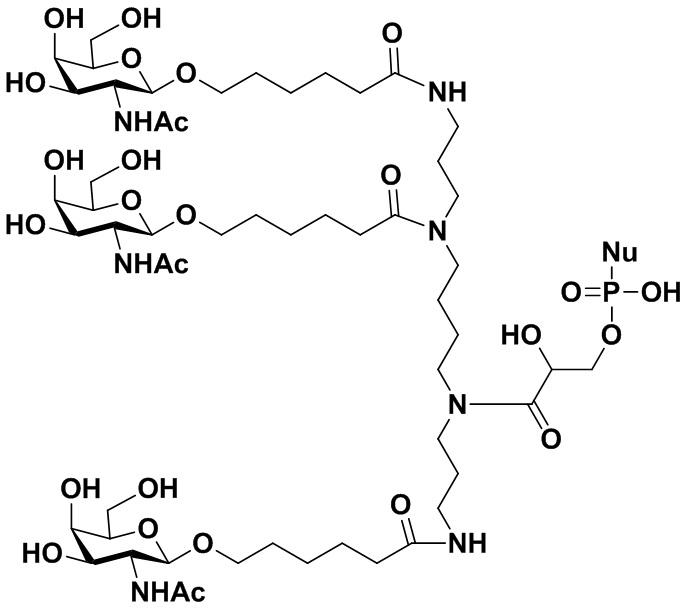
Формула (417)

Формула (418)
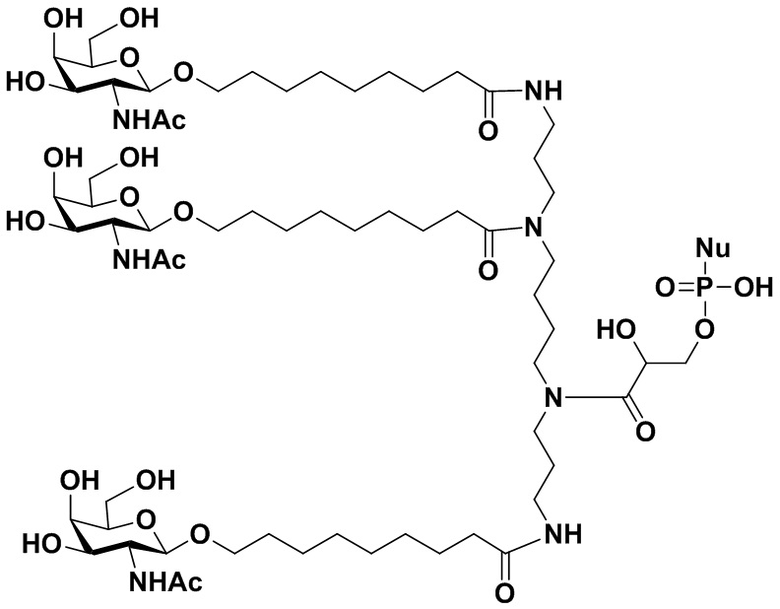
Формула (419)
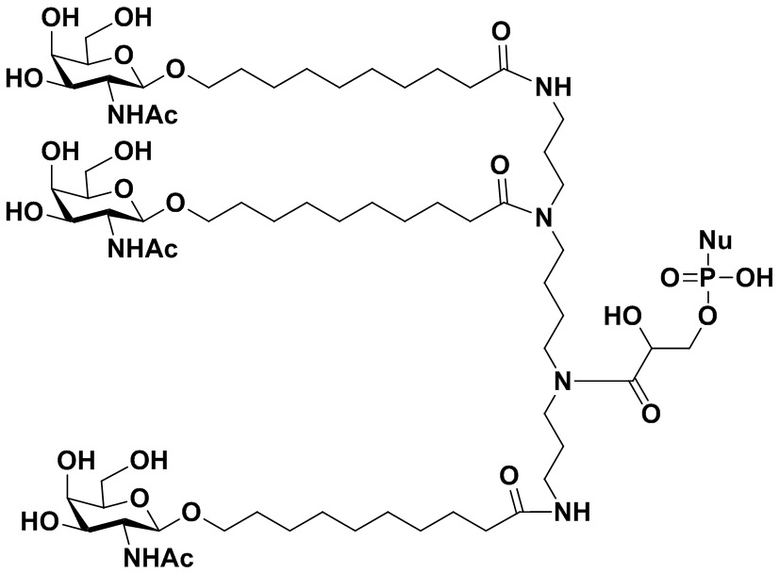
Формула (420)
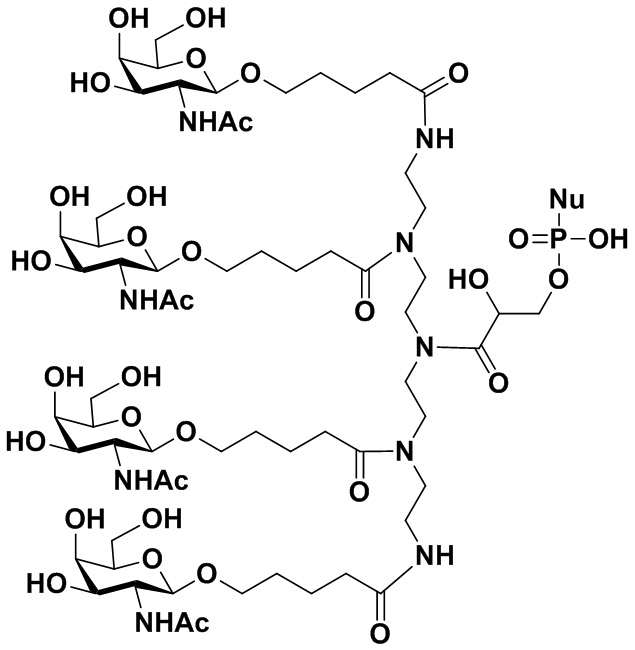
Формула (421)

Формула (422).
В некоторых вариантах осуществления атом P в Формуле A59 может быть связан с любым возможным положением в последовательности миРНК, например, атом P в Формуле A59 может быть связан с любым нуклеотидом в смысловой цепи или антисмысловой цепи миРНК. В некоторых вариантах осуществления атом P в Формуле A59 связан с любым нуклеотидом в смысловой цепи миРНК. В некоторых вариантах осуществления атом P в Формуле A59 связан с концом смысловой цепи или антисмысловой цепи миРНК. В некоторых вариантах осуществления атом P в Формуле A59 связан с концом смысловой цепи миРНК. Конец относится к первым 4 нуклеотидам, отсчитанным от одного конца смысловой цепи или антисмысловой цепи. В некоторых вариантах осуществления атом P в Формуле A59 связан с концом смысловой цепи или антисмысловой цепи миРНК. В некоторых вариантах осуществления атом P в Формуле A59 связан с 3’-концом смысловой цепи миРНК. В случае, если атом P в Формуле A59 связан с вышеуказанным положением в смысловой цепи миРНК, после проникновения в клетки конъюгат миРНК, представленный Формулой (308), может высвобождать отдельную антисмысловую цепь миРНК во время расплетания, тем самым блокируя трансляцию мРНК C5 в белок и ингибируя экспрессию гена белка комплемента C5.
В некоторых вариантах осуществления атом P в Формуле A59 может быть связан с любым возможным положением нуклеотида в миРНК, например, с положением 5’, 2’ или 3’, или с основанием нуклеотида. В некоторых вариантах осуществления атом P в Формуле A59 может быть связан с положением 2’, 3’ или 5’ нуклеотида в миРНК путем образования фосфодиэфирной связи. В некоторых вариантах осуществления атом P в Формуле A59 связан с атомом кислорода, образованным в результате депротонирования 3’-гидроксигруппы нуклеотида на 3’-конце смысловой цепи миРНК (в это время атом P в Формуле A59 также может рассматриваться как атом P в фосфатной группе, содержащейся в миРНК), или атом P в Формуле A59 связан с нуклеотидом путем замещения атома водорода в 2’-гидроксигруппе нуклеотида смысловой цепи миРНК, или атом P в Формуле A59 связан с нуклеотидом путем замещения водорода в 5’-гидроксигруппе нуклеотида на 5’-конце смысловой цепи миРНК.
Авторы настоящего изобретения неожиданно обнаружили, что конъюгат миРНК согласно настоящему изобретению обладает значительно улучшенной стабильностью в плазме и низким нецелевым действием, а также демонстрируют более высокую сайленсинговую активность в отношении мРНК C5. В некоторых вариантах осуществления миРНК согласно настоящему изобретению может представлять собой одну из миРНК, представленных в таблицах 1a-1f. Конъюгаты миРНК, содержащие эти миРНК, демонстрируют более высокую сайленсинговую активность в отношении мРНК C5.
Таблица 1a. Последовательность первой миРНК согласно настоящему изобретению
Таблица 1b. Последовательность второй миРНК согласно настоящему изобретению
Таблица 1c. Последовательность третьей миРНК согласно настоящему изобретению
Таблица 1d. Последовательность четвертой миРНК согласно настоящему изобретению
Таблица 1e. Последовательность пятой миРНК согласно настоящему изобретению
Таблица 1f. Последовательность шестой миРНК согласно настоящему изобретению
В миРНК или конъюгате миРНК согласно настоящему изобретению каждая пара соседних нуклеотидов связана фосфодиэфирной связью или тиофосфатной связью. Немостиковый атом кислорода или атом серы в фосфодиэфирной связи или тиофосфатной связи заряжен отрицательно и может присутствовать в форме гидроксигруппы или сульфгидрильной группы. Кроме того, ион водорода в гидроксигруппе или сульфгидрильной группе может быть частично или полностью замещен катионом. Катион может представлять собой любой катион, такой как катион металла, ион аммония NH4+ или катион органического аммония. Чтобы повысить растворимость, в некоторых вариантах осуществления катион выбран из одного или более из иона щелочного металла, катиона аммония, образованного третичным амином, и катиона четвертичного аммония. Ион щелочного металла может представлять собой K+ и/или Na+, а катион, образованный третичным амином, может представлять собой ион аммония, образованный триэтиламином, и/или ион аммония, образованный N,N-диизопропилэтиламином. Таким образом, миРНК или конъюгат миРНК согласно настоящему изобретению может по меньшей мере частично присутствовать в форме соли. В одном из вариантов осуществления немостиковый атом кислорода или атом серы в фосфодиэфирной связи или тиофосфатной связи по меньшей мере частично связывается с ионом натрия, и, таким образом, миРНК или конъюгат миРНК согласно настоящему изобретению присутствует или частично присутствует в форме натриевой соли.
Специалистам в данной области техники хорошо известно, что модифицированная нуклеотидная группа может быть введена в миРНК согласно настоящему изобретению с помощью нуклеозидного мономера, имеющего соответствующую модификацию. Способы получения нуклеозидного мономера, имеющего соответствующую модификацию, и способы введения модифицированной нуклеотидной группы в миРНК также хорошо известны специалистам в данной области техники. Все модифицированные нуклеозидные мономеры могут быть доступны на рынке или получены с помощью известных способов.
Получение конъюгата миРНК, представленного Формулой (308)
Конъюгат миРНК, представленный Формулой (308), может быть получен с помощью любых подходящих путей синтеза.
В некоторых вариантах осуществления конъюгат миРНК, представленный Формулой (308), может быть получен с помощью следующего способа. Способ включает: последовательное связывание нуклеозидных мономеров в направлении от 3’ к 5’ в соответствии с типами и последовательностями нуклеотидов в смысловой цепи и антисмысловой цепи, соответственно, в условиях твердофазного амидофосфитного синтеза, где стадия связывания каждого нуклеозидного мономера включает четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления или сульфуризации; выделение смысловой цепи и антисмысловой цепи миРНК; и отжиг; где миРНК представляет собой миРНК согласно настоящему изобретению, упомянутую выше.
Кроме того, способ дополнительно включает: приведение соединения, представленного Формулой (321), в контакт с нуклеозидным мономером или нуклеотидной последовательностью, связанной с твердофазной подложкой, в условиях реакции сочетания и в присутствии агента реакции сочетания, обеспечивая связывание соединения, представленного Формулой (321), с нуклеотидной последовательностью посредством реакции сочетания. Далее в настоящем документе соединение, представленное Формулой (321), также называется конъюгирующей молекулой.

Формула (321),
где:
R4 представляет собой группу, способную связываться с миРНК, представленной Nu в соединении, представленном Формулой (308). В некоторых вариантах осуществления R4 представляет собой группу, способную связываться с миРНК, представленной Nu, посредством ковалентной связи. В некоторых вариантах осуществления R4 представляет собой группу, способную конъюгироваться с любой функциональной группой миРНК, представленной Nu, посредством фосфодиэфирной связи в ходе реакции;
каждый S1 независимо представляет собой M1, которая представляет собой группу, образованную замещением всех активных гидроксигрупп группой YCOO-, где каждый Y независимо выбран из одного из метила, трифторметила, дифторметила, монофторметила, трихлорметила, дихлорметила, монохлорметила, этила, н-пропила, изопропила, фенила, галогенфенила и алкилфенила. В некоторых вариантах осуществления Y представляет собой метил.
Определения и варианты n1, n3, m1, m2, m3, R10, R11, R12, R13, R14, R15, L1 и M1 соответственно представляют собой такие, как описано выше.
R4 выбирают таким образом, чтобы обеспечить связывание с атомом N на азотсодержащем остове и обеспечить подходящий реакционный сайт для синтеза конъюгата миРНК, представленного Формулой (308). В некоторых вариантах осуществления R4 содержит связывающую группу R 2 или защищенную связывающую группу R2 и может образовывать функциональную группу, представленную Формулой (A59), с миРНК посредством реакции.
В некоторых вариантах осуществления R4 содержит первую функциональную группу, которая может реагировать с группой на миРНК или нуклеозидном мономере, представленном Nu, с образованием фосфитного эфира, и вторую функциональную группу, которая может образовывать ковалентную связь с гидроксигруппой или аминогруппой или содержит твердофазную подложку, связанную посредством ковалентной связи. В некоторых вариантах осуществления первая функциональная группа представляет собой амидофосфит, гидроксигруппу или защищенную гидроксигруппу. В некоторых вариантах осуществления вторая функциональная группа представляет собой амидофосфит, карбоксил или карбоксилат. В некоторых вариантах осуществления вторая функциональная группа представляет собой твердофазную подложку, связанную с остальной частью молекулы посредством ковалентной связи, образованной гидроксигруппой или аминогруппой. В некоторых вариантах осуществления твердофазная подложка связана посредством фосфоэфирной связи, карбоксиэфирной связи или амидной связи. В некоторых вариантах осуществления твердофазная подложка представляет собой смолу.
В некоторых вариантах осуществления первая функциональная группа содержит гидроксигруппу, -ORk или группу, представленную Формулой (C3); а вторая функциональная группа содержит группу, представленную Формулой (C1), (C2), (C3), (C1') или (C3’):
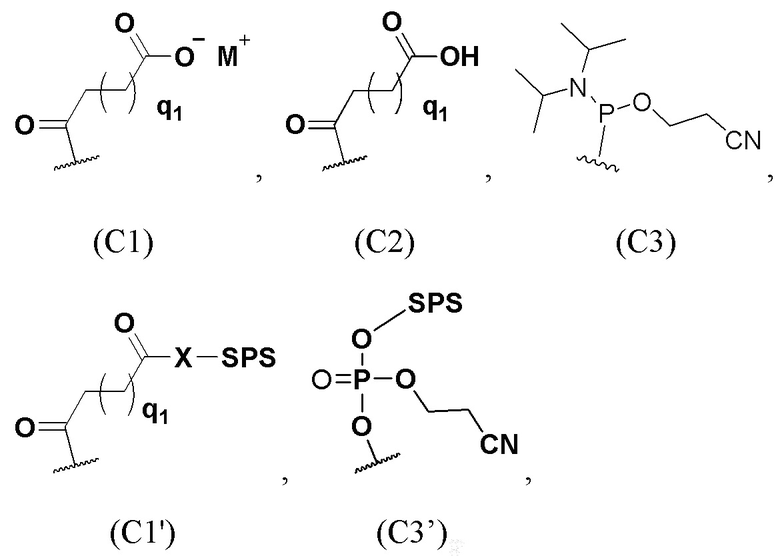
где q1 представляет собой целое число от 1 до 4, X представляет собой O или NH, M+ представляет собой катион, Rk представляет собой гидроксизащитную группу, ТФП представляет собой твердофазную подложку, и  обозначает сайт ковалентного присоединения группы.
обозначает сайт ковалентного присоединения группы.
В некоторых вариантах осуществления первая функциональная группа содержит амидофосфитную группу, представленную Формулой (C3). Амидофосфитная группа может образовывать фосфитный эфир с гидроксигруппой в любом положении на нуклеотиде, такой как 2’- или 3’ -гидроксигруппа, посредством реакции сочетания, а фосфитный эфир может образовывать фосфодиэфирную связь или тиофосфатную связь, представленную Формулой (A59), посредством окисления или сульфуризации, чтобы конъюгировать конъюгирующую молекулу с миРНК. В этом случае, даже если вторая функциональная группа не существует, соединение, представленное Формулой (321), по-прежнему может быть конъюгировано с нуклеотидом, не влияя на получение конъюгата миРНК, представленного Формулой (308). В таких обстоятельствах после получения смысловой цепи или антисмысловой цепи миРНК с помощью такого способа, как твердофазный амидофосфитный синтез, соединение, представленное Формулой (321), подвергают взаимодействию с гидроксигруппой на концевом нуклеотиде нуклеотидной последовательности, и обеспечивают образование фосфодиэфирной связи или тиофосфатной связи в результате последующего процесса окисления или сульфуризации, что приводит к конъюгации соединения, представленного Формулой (321), с миРНК.
В некоторых вариантах осуществления первая функциональная группа содержит защищенную гидроксигруппу. В некоторых вариантах осуществления вторая функциональная группа содержит группу, которая может реагировать с твердофазной подложкой с получением конъюгирующей молекулы, содержащей твердофазную подложку. В некоторых вариантах осуществления вторая функциональная группа содержит карбоксил, карбоксилат или амидофосфит, как представлено Формулой (C1), (C2) или (C3). Когда вторая функциональная группа содержит карбоксил или карбоксилат, соединение, представленное Формулой (321), реагирует с гидроксигруппой или аминогруппой на твердофазной подложке, такой как смола, посредством реакции этерификации или амидирования, с образованием конъюгирующей молекулы, содержащей твердофазную подложку, связанную посредством карбоксиэфирной связи. Когда вторая функциональная группа содержит амидофосфитную функциональную группу, соединение, представленное Формулой (321), может быть связано с гидроксигруппой на универсальной твердофазной подложке, такой как смола, и образовать путем окисления конъюгирующую молекулу, содержащую твердофазную подложку, связанную посредством фосфодиэфирной связи. Затем, начиная с выше указанного продукта, связанного с твердофазной подложкой, последовательно связывают нуклеозидные мономеры с помощью способа твердофазного амидофосфитного синтеза с получением таким образом смысловой цепи или антисмысловой цепи миРНК, связанной с конъюгирующей группой. Во время твердофазного амидофосфитного синтеза снимают защиту с первой функциональной группы, а затем подвергают ее реакции сочетания с амидофосфитной группой на нуклеозидном мономере в условиях реакции сочетания.
В некоторых вариантах осуществления первая функциональная группа содержит гидроксигруппу или защищенную гидроксигруппу; а вторая функциональная группа содержит твердофазную подложку, связанную посредством карбоксиэфирной связи, твердофазную подложку, связанную посредством амидной связи, или твердофазную подложку, связанную посредством фосфоэфирной связи, как представлено Формулой (C1') или (C3’). В этом случае, начиная с соединения, представленного Формулой (321), вместо твердофазной подложки последовательно связывают нуклеозидные мономеры с помощью твердофазного амидофосфитного синтеза с получением таким образом смысловой цепи или антисмысловой цепи миРНК, связанной с конъюгирующей группой.
В некоторых вариантах осуществления карбоксилат может быть обозначен в виде -COO-M+, где M+ представляет собой катион, такой как один из катиона металла, катиона аммония NH4+ и катиона органического аммония. В одном из вариантов осуществления ион металла может представлять собой ион щелочного металла, такой как K+ или Na+. Чтобы повысить растворимость и облегчить протекание реакции, в некоторых вариантах осуществления ион органического аммония представляет собой катион аммония, образованный третичным амином, или катион четвертичного аммония, такой как ион аммония, образованный триэтиламином, или ион аммония, образованный N,N-диизопропилэтиламином. В некоторых вариантах осуществления карбоксилат представляет собой карбоксилат триэтиламина или карбоксилат N,N-диизопропилэтиламина.
В некоторых вариантах осуществления R4 содержит структуру, представленную Формулой (B9), (B10), (B9'), (B10'), (B11), (B12), (B11') или (B12’):
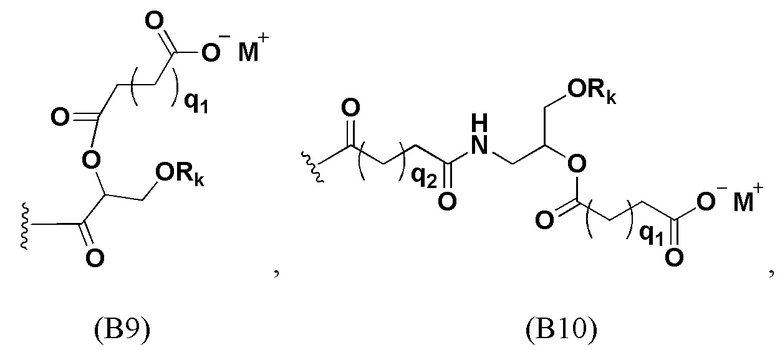
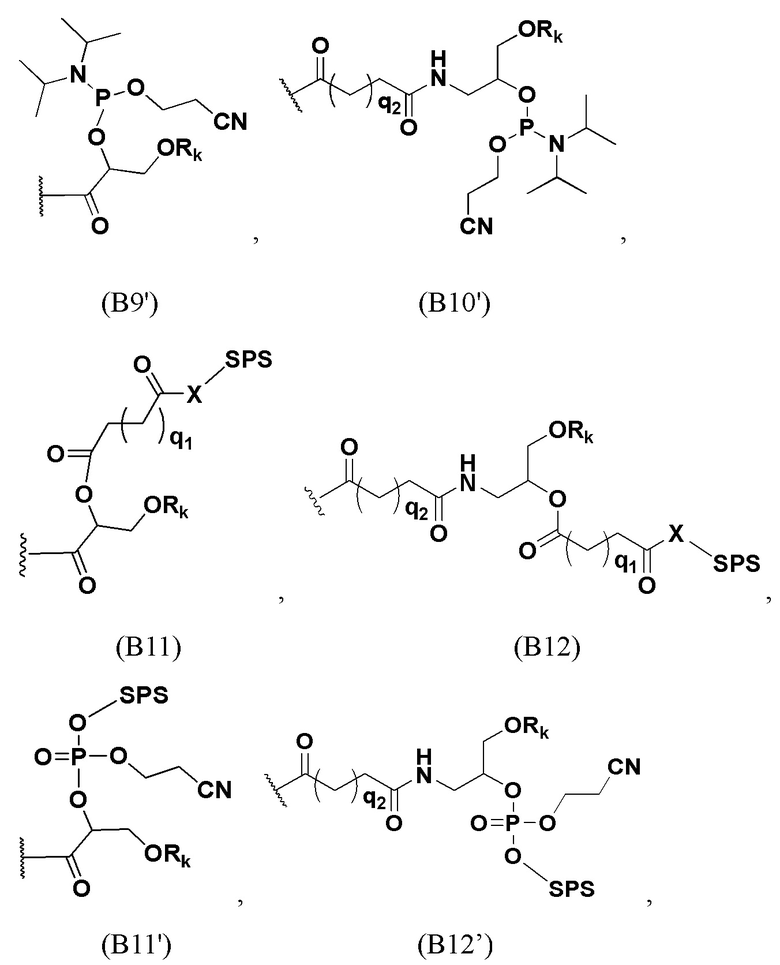
где q1 представляет собой целое число от 1 до 4, q2 представляет собой целое число от 1 до 10, X представляет собой O или NH, M+ представляет собой катион, Rk представляет собой гидроксизащитную группу, ТФП представляет собой твердофазную подложку, и  обозначает сайт ковалентного присоединения группы. В некоторых вариантах осуществления q1 равно 1 или 2. В некоторых вариантах осуществления q2 представляет собой целое число от 1 до 5. В некоторых вариантах осуществления R4 содержит структуру, представленную Формулой (B9) или (B10). В некоторых вариантах осуществления R4 содержит структуру, представленную Формулой (B11) или (B12).
обозначает сайт ковалентного присоединения группы. В некоторых вариантах осуществления q1 равно 1 или 2. В некоторых вариантах осуществления q2 представляет собой целое число от 1 до 5. В некоторых вариантах осуществления R4 содержит структуру, представленную Формулой (B9) или (B10). В некоторых вариантах осуществления R4 содержит структуру, представленную Формулой (B11) или (B12).
В некоторых вариантах осуществления Rk представляет собой один или более из Tr (тритил), MMTr (4-метокситритил), DMTr (4,4'-диметокситритил) и TMTr (4,4',4"-триметокситритил). В некоторых вариантах осуществления Rk может представлять собой DMTr, т. е. 4,4'-диметокситритил.
Определение L1 соответствует описанному выше.
В некоторых вариантах осуществления L1 используется для связывания нацеливающей группы M1 с атомом N на азотсодержащем остове, что наделяют конъюгат миРНК, представленный Формулой (308), функцией нацеливания на печень. В некоторых вариантах осуществления L1 содержит любую из Формул (A1) - (A26) или их комбинацию.
В соответствии с приведенным выше описанием, специалисты в данной области техники без труда поймут, что по сравнению со способами твердофазного амидофосфитного синтеза, хорошо известными в данной области техники, конъюгат миРНК, в котором конъюгирующая молекула связана с любым возможным положением нуклеотидной последовательности, может быть получен с помощью вышеуказанной первой функциональной группы и необязательной второй функциональной группы. Например, конъюгирующая молекула связана с концом нуклеотидной последовательности или с обоими концами нуклеотидной последовательности. Соответственно, если не указано иное, в следующем описании применительно к получению конъюгата миРНК и/или конъюгирующей молекулы при упоминании таких реакций, как «снятие защиты», «сочетание», «кэпирование», «окисление», «сульфуризация», подразумевается, что к этим реакциям также будут применимы условия реакции и агенты, используемые в хорошо известных в данной области техники способах твердофазного амидофосфитного синтеза нуклеиновых кислот. Примеры условий реакции и агентов будут подробно описаны ниже.
В некоторых вариантах осуществления каждый S1 независимо представляет собой M1. В некоторых вариантах осуществления каждый S1 независимо представляет собой группу, образованную в результате защиты по меньшей мере одной активной гидроксигруппы в M1 гидроксизащитными группами. В некоторых вариантах осуществления каждый S1 независимо представляет собой группу, образованную в результате защиты всех активных гидроксигрупп в M1 гидроксизащитными группами. В некоторых вариантах осуществления любая гидроксизащитная группа, известная специалистам в данной области техники, может быть ипользована для защиты активной гидроксигруппы в M1. В некоторых вариантах осуществления защищенная гидроксигруппа обозначена формулой YCOO-, где каждый Y независимо выбран из группы, состоящей из C1-C10 алкила и C6-C10 арила, где C1-C10 алкил и C6-C10 арил необязательно замещены одним или более заместителями, выбранными из группы, состоящей из галогена и C1-C6 алкила. В некоторых вариантах осуществления каждый Y независимо выбран из группы, состоящей из метила, трифторметила, дифторметила, монофторметила, трихлорметила, дихлорметила, монохлорметила, этила, н-пропила, изопропила, фенила, галогенфенила и C1-C6 алкилфенила.
В некоторых вариантах осуществления каждый S1 независимо выбран из группы, состоящей из Формул A46-A54:
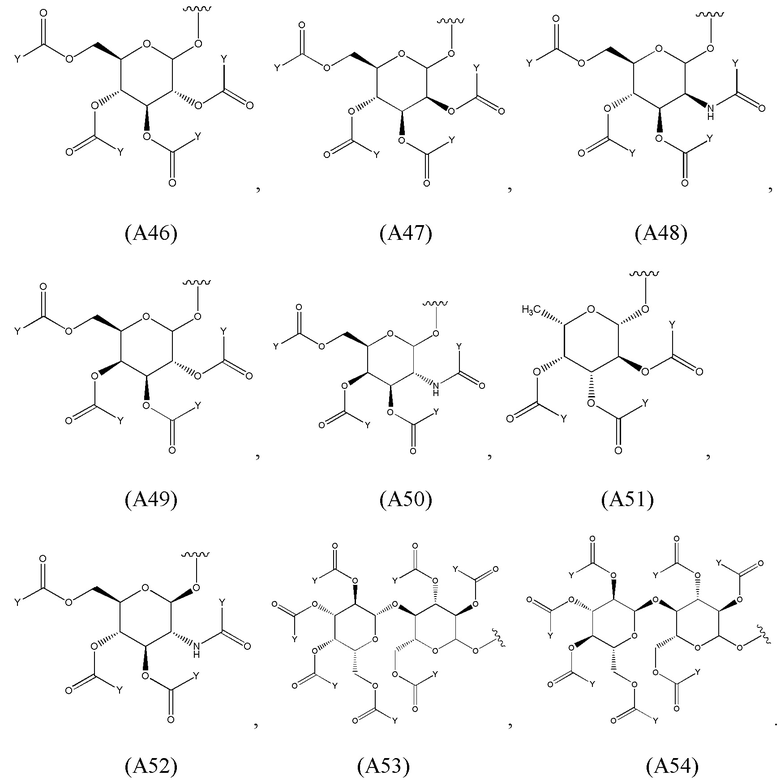
В некоторых вариантах осуществления S1 представляет собой Формулу A49 или A50.
В некоторых вариантах осуществления каждый Y независимо выбран из одного из метила, трифторметила, дифторметила, монофторметила, трихлорметила, дихлорметила, монохлорметила, этила, н-пропила, изопропила, фенила, галогенфенила и алкилфенила. В некоторых вариантах осуществления Y представляет собой метил.
Как упоминалось ранее, способ получения конъюгата миРНК, представленного Формулой (308), дополнительно включает следующие стадии: синтез другой цепи миРНК (например, когда смысловая цепь миРНК, связанная с конъюгирующей молекулой, синтезирована на вышеуказанной стадии, способ дополнительно включает синтез антисмысловой цепи миРНК методом твердофазного синтеза, и наоборот); выделение смысловой цепи и антисмысловой цепи; и отжиг. В частности, на стадии выделения твердофазную подложку, связанную с нуклеотидной последовательностью и/или конъюгируемой молекулой, отщепляют, и в это же время удаляют необходимую защитную группу (в этом случае каждая группа S1 в соединении, представленном Формулой (321), превращается в соответствующую нацеливающую группу M1), с получением смысловой цепи (или антисмысловой цепи) миРНК, связанной с конъюгирующей молекулой, и соответствующей антисмысловой цепи (или смысловой цепи). Смысловую цепь и антисмысловую цепь отжигают с образованием двухцепочечной структуры РНК, с получением таким образом конъюгата миРНК, представленного Формулой (308).
В некоторых вариантах осуществления способ получения конъюгата миРНК, представленного Формулой (308), дополнительно включает следующие стадии: приведение соединения, представленного Формулой (321), в контакт с первым нуклеозидным мономером на 3’-конце смысловой цепи или антисмысловой цепи в условиях реакции сочетания в присутствии агента реакции сочетания, тем самым связывая соединение, представленное Формулой (321), с первым нуклеотидом в последовательности; последовательное связывание нуклеозидных мономеров в направлении от 3’ к 5’ для синтеза смысловой цепи или антисмысловой цепи миРНК в соответствии с желаемым типом нуклеотидов и последовательностью смысловой цепи или антисмысловой цепи, в условиях твердофазного амидофосфитного синтеза; где соединение, представленное Формулой (321), представляет собой соединение, в котором R4 содержит первую функциональную группу и вторую функциональную группу, первая функциональная группа содержит защищенную гидроксигруппу, а вторая функциональная группа содержит группу, представленную Формулой (C1') или (C3’), и с соединения, представленного Формулой (321), снимают защиту перед связыванием с первым нуклеозидным мономером; и связывание каждого нуклеозидного мономера включает четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления или сульфуризации, с получением таким образом смысловой цепи или антисмысловой цепи нуклеиновой кислоты, связанной с конъюгирующей молекулой; последовательное связывание нуклеозидных мономеров в направлении от 3’ к 5’ для синтеза смысловой цепи или антисмысловой цепи нуклеиновой кислоты в соответствии с типом нуклеотидов и последовательностью смысловой цепи или антисмысловой цепи, в условиях твердофазного амидофосфитного синтеза; где связывание каждого нуклеозидного мономера включает четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления или сульфуризации; удаление защитных групп и отщепление твердофазной подложки; выделение и очистка с получением смысловой цепи и антисмысловой цепи; и отжиг.
В некоторых вариантах осуществления способ получения конъюгата миРНК, представленного Формулой (308), дополнительно включает следующие стадии: последовательное связывание нуклеозидных мономеров в направлении от 3’ к 5’ для синтеза смысловой цепи или антисмысловой цепи в соответствии с типом нуклеотидов и последовательностью смысловой цепи или антисмысловой цепи в двухцепочечной миРНК; где связывание каждого нуклеозидного мономера включает четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления или сульфуризации, с получением таким образом смысловой цепи, связанной с твердофазной подложкой, и антисмысловой цепи, связанной с твердофазной подложкой; приведение соединения, представленного Формулой (321), в контакт со смысловой цепью, связанной с твердофазной подложкой, или антисмысловой цепью, связанной с твердофазной подложкой, в условиях реакции сочетания в присутствии агента реакции сочетания, тем самым связывая соединение, представленное Формулой (321), со смысловой цепью или антисмысловой цепью; где соединение, представленное Формулой (321), представляет собой соединение, в котором R4 содержит амидофосфитную группу в качестве первой функциональной группы; удаление защитных групп и отщепление твердофазной подложки; соответственно выделение и очистка с получением смысловой цепи или антисмысловой цепи миРНК; и отжиг; где смысловая цепь или антисмысловая цепь миРНК связана с конъюгирующей молекулой.
В некоторых вариантах осуществления атом P в Формуле A59 связан с 3’-концом смысловой цепи миРНК, и способ получения конъюгата миРНК, представленного Формулой (308), включает:
(1) удаление гидроксизащитной группы Rk из соединения, представленного Формулой (321) (где соединение, представленное Формулой (321), представляет собой соединение, в котором R4 содержит первую функциональную группу и вторую функциональную группу, первая функциональная группа содержит защищенную гидроксигруппу ORk, а вторая функциональная группа содержит структуру, представленную Формулой (C1') или (C3’)); и приведение продукта со снятой защитой в контакт с нуклеозидным мономером с получением нуклеозидного мономера, связанного с твердофазной подложкой через конъюгирующую молекулу в условиях реакции сочетания в присутствии агента реакции сочетания;
(2) синтезирование, начиная с нуклеозидного мономера, связанного с твердофазной подложкой через конъюгирующую молекулу, смысловой цепи миРНК в направлении от 3’ к 5’ с помощью твердофазного амидофосфитного синтеза;
(3) синтезирование антисмысловой цепи миРНК методом твердофазного амидофосфитного синтеза; и
(4) выделение смысловой цепи и антисмысловой цепи миРНК и их отжиг с получением конъюгата миРНК, представленного Формулой (308).
На стадии (1) способ удаления защитной группы Rk из соединения, представленного Формулой (321), включает приведение соединения, представленного Формулой (321), в контакт с агентом для снятия защиты в условиях снятия защиты. Условия снятия защиты включают температуру 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 30-300 секунд, и в некоторых вариантах осуществления 50-150 секунд. Агент для снятия защиты может быть выбран из одной или более из трифторуксусной кислоты, трихлоруксусной кислоты, дихлоруксусной кислоты и монохлоруксусной кислоты, и в некоторых вариантах осуществления агент для снятия защиты представляет собой дихлоруксусную кислоту. Молярное отношение агента для снятия защиты к соединению, представленному Формулой (321), может составлять от 10:1 до 1000:1, и в некоторых вариантах осуществления от 50:1 до 500:1.
Условия реакции сочетания и агент реакции сочетания могут представлять собой любые условия и агенты, подходящие для вышеуказанной реакции сочетания. В некоторых вариантах осуществления могут быть использованы те же условия и агент, что и в реакции сочетания в методе твердофазного синтеза.
В некоторых вариантах осуществления условия реакции сочетания включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C. Молярное отношение соединения, представленного Формулой (321), к нуклеозидному мономеру может составлять от 1:1 до 1:50, и в некоторых вариантах осуществления от 1:2 до 1:5. Молярное отношение соединения, представленного Формулой (321) к агенту реакции сочетания может составлять от 1:1 до 1:50, и в некоторых вариантах осуществления от 1:3 до 1:10. Продолжительность проведения реакции может составлять 200-3000 секунд, и в некоторых вариантах осуществления 500-1500 секунд. Агент реакции сочетания может быть выбран из одного или более из 1H-тетразола, 5-этилтио-1H-тетразола и 5-бензилтио-1H-тетразола, и в некоторых вариантах осуществления представляет собой 5-этилтио-1H-тетразол. Органический растворитель может быть выбран из одного или более из безводного ацетонитрила, безводного ДМФА и безводного дихлорметана, и в некоторых вариантах осуществления представляет собой безводный ацетонитрил. Количество органического растворителя может составлять 3-50 л/моль, и в некоторых вариантах осуществления 5-20 л/моль, относительно соединения, представленного Формулой (321).
На стадии (2) смысловую цепь SS конъюгата миРНК синтезируют в направлении от 3’ к 5’ методом твердофазного амидофосфитного синтеза нуклеиновых кислот, начиная с нуклеозидного мономера, связанного с твердофазной подложкой через конъюгирующую молекулу, полученного на вышеуказанных стадиях. В этом случае конъюгирующая молекула связана с 3’-концом полученной смысловой цепи.
Другие условия твердофазного синтеза на стадиях (2) и (3), включающие условия снятия защиты с нуклеозидного мономера, тип и количество агента для снятия защиты, условия реакции сочетания, тип и количество агента реакции сочетания, условия реакции кэпирования, тип и количество кэпирующего агента, условия реакции окисления, тип и количество окисляющего агента, условия реакции сульфуризации и тип и количество агента для сульфуризации, включают использование агентов, количеств и условий, общепринятых в данной области техники.
Например, в некоторых вариантах осуществления для твердофазного синтеза на стадиях (2) и (3) могут быть использованы следующие условия:
Условия снятия защиты для нуклеозидного мономера включают температуру 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 30-300 секунд, и в некоторых вариантах осуществления 50-150 секунд. Агент для снятия защиты может быть выбран из одной или более из трифторуксусной кислоты, трихлоруксусной кислоты, дихлоруксусной кислоты и монохлоруксусной кислоты, и в некоторых вариантах осуществления агент для снятия защиты представляет собой дихлоруксусную кислоту. Молярное отношение агента для снятия защиты к 4,4'-диметокситритильной защитной группе на твердофазной подложке составляет от 2:1 до 100:1, и в некоторых вариантах осуществления от 3:1 до 50:1.
Условия реакции сочетания включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C. Молярное отношение последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, к нуклеозидному мономеру составляет от 1:1 до 1:50, и в некоторых вариантах осуществления от 1:5 до 1:15. Молярное отношение последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, к агенту реакции сочетания составляет от 1:1 до 1:100, и в некоторых вариантах осуществления от 1:50 до 1:80. Продолжительность проведения реакции и агент реакции сочетания могут быть выбраны так же, как указано выше.
Условия реакции кэпирования включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 5-500 секунд, и в некоторых вариантах осуществления 10-100 секунд. Кэпирующий агент может быть выбран так же, как указано выше. Молярное отношение общего количества кэпирующего агента к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, может составлять от 1:100 до 100:1, и в некоторых вариантах осуществления составляет от 1:10 до 10:1. В случае, когда в качестве кэпирующего агента используют эквимолярные количества уксусного ангидрида и N-метилимидазола, молярное отношение уксусного ангидрида к N-метилимидазолу и последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, может составлять от 1:1:10 до 10:10:1, и в некоторых вариантах осуществления составляет от 1:1:2 до 2:2:1.
Условия реакции окисления включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 1-100 секунд, и в некоторых вариантах осуществления 5-50 секунд. В некоторых вариантах осуществления окисляющий агент представляет собой иод (в некоторых вариантах осуществления обеспечиваемый в виде иодной воды). Молярное отношение окисляющего агента к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой на стадии сочетания, может составлять от 1:1 до 100:1, и в некоторых вариантах осуществления составляет от 5:1 до 50:1. В некоторых вариантах осуществления реакцию окисления проводят в смешанном растворителе, в котором отношение тетрагидрофуран:вода:пиридин составляет от 3:1:1 до 1:1:3. Условия реакции сульфуризации включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 50-2000 секунд, и в некоторых вариантах осуществления 100-1000 секунд. В некоторых вариантах осуществления агент для сульфуризации представляет собой гидрид ксантана. Молярное отношение агента для сульфуризации к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой на стадии сочетания, составляет от 10:1 до 1000:1, и в некоторых вариантах осуществления составляет от 10:1 до 500:1. В некоторых вариантах осуществления реакцию сульфуризации проводят в смешанном растворителе, в котором отношение ацетонитрил:пиридин составляет от 1:3 до 3:1.
Способ дополнительно включает выделение смысловой цепи и антисмысловой цепи миРНК после связывания всех нуклеозидных мономеров и перед отжигом. Способы выделения хорошо известны специалистам в данной области техники и обычно включают отщепление синтезированной нуклеотидной последовательности от твердофазной подложки, удаление защитных групп на основаниях, фосфатных группах и лигандах, очистку и обессоливание.
Для отщепления синтезированной нуклеотидной последовательности от твердофазной подложки и удаления защитных групп на основаниях, фосфатных группах и лигандах могут быть использованы общепринятые способы отщепления и снятия защиты при синтезе миРНК. Например, приведение полученной нуклеотидной последовательности, связанной с твердофазной подложкой, в контакт с крепким водным раствором аммиака; во время снятия защиты защитная группа YCOO- на группах A46-A54 превращается в гидроксигруппу, и, таким образом, группы S1 превращаются в соответствующую группу M1, с получением конъюгата, представленного Формулой (308); где крепкий водный раствор аммиака может представлять собой водный раствор аммиака концентрацией 25-30 мас.%. Количество крепкого водного раствора аммиака может составлять от 0,2 мл/мкмоль до 0,8 мл/мкмоль относительно целевой миРНК.
Когда на синтезированной нуклеотидной последовательности имеется по меньшей мере одна защитная группа 2’-TBDMS, способ дополнительно включает приведение нуклеотидной последовательности, снятой с твердофазной подложки, в контакт с тригидрофторидом триэтиламина для снятия 2’-TBDMS-защиты. В этом случае полученная целевая последовательность миРНК содержит соответствующий нуклеозид, имеющий свободную 2’-гидроксигруппу. Количество чистого тригидрофторида триэтиламина составляет от 0,4 мл/мкмоль до 1,0 мл/мкмоль относительно целевой последовательности миРНК. Таким образом может быть получен конъюгат миРНК, представленный Формулой (308).
Способы очистки и обессоливания хорошо известны специалистам в данной области техники. Например, очистка нуклеиновой кислоты может быть проведена с помощью колонки для очистки методом препаративной ионообменной хроматографии с градиентным элюированием NaBr или NaCl; после сбора и объединения продукта может быть проведено обессоливание с помощью колонки для очистки методом обращенно-фазовой хроматографии.
Немостиковый атом кислорода или атом серы в фосфодиэфирной связи или тиофосфатной связи между нуклеотидами в полученном конъюгате миРНК, представленном Формулой (308), по существу связывается с ионом натрия, и конъюгат миРНК, представленный Формулой (308), по существу присутствует в форме натриевой соли. Могут быть использованы хорошо известные методы ионного обмена, в которых ион натрия может быть заменен ионом водорода и/или другими катионами, обеспечивая другие формы конъюгатов миРНК, представленных Формулой (308). Катионы представляют собой описанные выше.
Во время синтеза чистоту и молекулярную массу последовательности нуклеиновой кислоты можно определить в любое время. Для лучшего контроля качества синтеза такие способы определения хорошо известны специалистам в данной области техники. Например, чистоту нуклеиновой кислоты можно определить с помощью ионообменной хроматографии, а молекулярную массу можно определить с помощью жидкостной хроматографии с масс-спектрометрией (ЖХ-МС).
Способы отжига также хорошо известны специалистам в данной области техники. Например, синтезированная смысловая цепь (SS-цепь) и антисмысловая цепь (AS-цепь) могут быть просто смешаны в воде для инъекций в эквимолярном соотношении, нагреты до 70-95°C, а затем охлаждены при комнатной температуре с образованием двухцепочечной структуры посредством водородных связей. Таким образом может быть получен конъюгат миРНК, представленный Формулой (308).
После получения конъюгата в некоторых вариантах осуществления синтезированный таким образом конъюгат миРНК, представленный Формулой (308), также может быть охарактеризован с помощью таких средств, как определение молекулярной массы, такими методами, как жидкостная хроматография с масс-спектрометрией, чтобы подтвердить, что синтезированный конъюгат миРНК представляет собой целевой разработанный конъюгат миРНК, представленный Формулой (308), и последовательность синтезированной миРНК представляет собой последовательность миРНК, которую требовалось синтезировать, например, представляет собой одну из последовательностей, перечисленных в таблицах 1a-1f.
Соединение, представленное Формулой (321), может быть получено с помощью следующего способа, включающего: приведение соединения, представленного Формулой (313), в контакт с циклическим ангидридом в органическом растворителе в условиях реакции этерификации в присутствии основания и катализатора этерификации; и выделение соединения, представленного Формулой (321), с помощью ионного обмена:
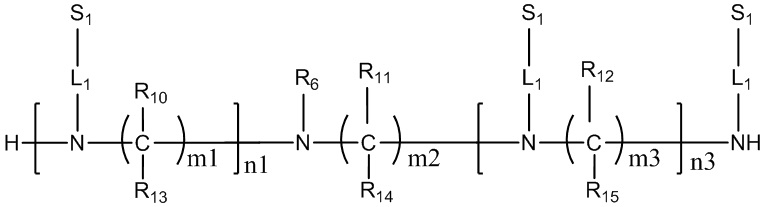
Формула (313),
где определения и варианты n1, n3, m1, m2, m3, R10, R11, R12, R13, R14, R15, L1 и S1 соответственно представляют собой такие, как описано выше;
R6 представляет собой группу, обеспечивающую R4 Формулы (321). В некоторых вариантах осуществления R6 содержит структуру, представленную Формулой (A61):
 ,
,
(A61),
где Ri представляет собой любую группу, способную связываться с атомом N на азотсодержащем остове, связываться с RkO и связываться со свободной гидроксигруппой; и Rk представляет собой гидроксизащитную группу. В этом случае получают соединение, представленное Формулой (321), где R4 содержит первую функциональную группу в виде гидроксизащитной группы и вторую функциональную группу, содержащую группу, представленную Формулой (C1) или (C2).
Условия реакции этерификации включают температуру реакции 0-100°C и продолжительность проведения реакции 8-48 часов. В некоторых вариантах осуществления условия реакции этерификации включают температуру реакции 10-40°C и продолжительность проведения реакции 20-30 часов.
В некоторых вариантах осуществления органический растворитель включает один или более из эпоксидного растворителя, простого эфирного растворителя, галогеналканового растворителя, диметилсульфоксида, N,N-диметилформамида и N,N-диизопропилэтиламина. В некоторых вариантах осуществления эпоксидный растворитель представляет собой диоксан и/или тетрагидрофуран, простой эфирный растворитель представляет собой диэтиловый эфир и/или метил-трет-бутиловый эфир, и галогеналкановый растворитель представляет собой один или более из дихлорметана, трихлорметана и 1,2-дихлорэтана. В некоторых вариантах осуществления органический растворитель представляет собой дихлорметан. Количество органического растворителя составляет 3-50 л/моль, и в некоторых вариантах осуществления 5-20 л/моль, относительно соединения, представленного Формулой (313).
В некоторых вариантах осуществления циклический ангидрид представляет собой один из янтарного ангидрида, глутарового ангидрида, адипинового ангидрида или пимелинового ангидрида, и в некоторых вариантах осуществления циклический ангидрид представляет собой янтарный ангидрид. Молярное отношение циклического ангидрида к соединению, представленному Формулой (313), составляет от 1:1 до 10:1, и в некоторых вариантах осуществления от 2:1 до 5:1.
Катализатор этерификации может представлять собой любой катализатор, способный катализировать этерификацию, например, катализатор может представлять собой 4-диметиламинопиридин. Молярное отношение катализатора к соединению, представленному Формулой (313), составляет от 1:1 до 10:1, и в некоторых вариантах осуществления от 2:1 до 5:1.
В некоторых вариантах осуществления основание может представлять собой любое неорганическое основание, органическое основание или их комбинацию. Учитывая растворимость и стабильность продукта, основание может представлять собой, например, третичный амин. В некоторых вариантах осуществления третичный амин представляет собой триэтиламин или N,N-диизопропилэтиламин. Молярное отношение третичного амина к соединению, представленному Формулой (313), составляет от 1:1 до 20:1, и в некоторых вариантах осуществления от 3:1 до 10:1.
Ионный обмен выполняет функцию превращения соединения, представленного Формулой (321), в целевую форму карбоновой кислоты или соли карбоновой кислоты, и способы ионного обмена хорошо известны специалистам в данной области техники. Вышеуказанная конъюгирующая молекула, в которой катион представляет собой M+, может быть получена с использованием подходящего ионообменного раствора и условий ионного обмена, которые не описаны подробно в настоящем документе. В некоторых вариантах осуществления в реакции ионного обмена используют раствор фосфата триэтиламина, и концентрация раствора фосфата триэтиламина составляет 0,2-0,8 М. В некоторых вариантах осуществления концентрация раствора фосфата триэтиламина составляет 0,4-0,6 М. В некоторых вариантах осуществления количество раствора фосфата триэтиламина составляет 3-6 л/моль, и в дополнительном варианте осуществления 4-5 л/моль, относительно соединения, представленного Формулой (313).
Соединение, представленное Формулой (321), может быть выделено из реакционной смеси с помощью любых подходящих способов выделения. В некоторых вариантах осуществления соединение, представленное Формулой (321), может быть выделено посредством удаления растворителя выпариванием с последующей хроматографией, например, с использованием следующих двух условий хроматографирования для выделения: (1) нормально-фазовая очистка силикагелевым фильтром с размером зерен 200-300 меш и градиентное элюирование 1 мас.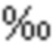 триэтиламина в смеси дихлорметан:метанол в соотношении от 100:18 до 100:20; или (2) обращенно-фазовая очистка с наполнителем с обращенной фазой C18 и C8 и градиентное элюирование смесью метанол:ацетонитрил в соотношении от 0,1:1 до 1:0,1. В некоторых вариантах осуществления растворитель может быть сразу же удален с получением неочищенного продукта соединения, представленного Формулой (321), который может быть сразу использован в последующих реакциях.
триэтиламина в смеси дихлорметан:метанол в соотношении от 100:18 до 100:20; или (2) обращенно-фазовая очистка с наполнителем с обращенной фазой C18 и C8 и градиентное элюирование смесью метанол:ацетонитрил в соотношении от 0,1:1 до 1:0,1. В некоторых вариантах осуществления растворитель может быть сразу же удален с получением неочищенного продукта соединения, представленного Формулой (321), который может быть сразу использован в последующих реакциях.
В некоторых вариантах осуществления способ получения соединения, представленного Формулой (321), дополнительно включает: приведение продукта, полученного в результате вышеуказанной реакции ионного обмена, в контакт с твердофазной подложкой, содержащей аминогруппы или гидроксигруппы в органическом растворителе, в условиях реакции конденсации в присутствии конденсирующего агента, катализатора конденсации и третичного амина. В этом случае получают соединение, представленное Формулой (321), где R4 содержит первую функциональную группу, содержащую гидроксизащитную группу, и вторую функциональную группу, имеющую структуру, представленную Формулой (C1').
Твердофазная подложка представляет собой один из носителей, применяемых в твердофазном синтезе миРНК, некоторые из которых хорошо известны специалистам в данной области техники. Например, твердофазная подложка может быть выбрана из твердофазных подложек, содержащих активную функциональную гидроксигруппу или аминогруппу. В некоторых вариантах осуществления твердофазная подложка представляет собой аминосмолу или гидроксисмолу. В некоторых вариантах осуществления аминосмола или гидроксисмола имеет следующие параметры: размер частиц 100-400 меш и удельное содержание аминогрупп или гидроксигрупп 0,2-0,5 ммоль/г. Отношение соединения, представленного Формулой (321), к твердофазной подложке составляет 10-400 мкмоль соединения на грамм твердофазной подложки (мкмоль/г). В некоторых вариантах осуществления отношение соединения Формулы (321) к твердофазной подложке составляет 50-200 мкмоль/г.
Органический растворитель может представлять собой любой подходящий растворитель или смешанные растворители, известные специалистам в данной области техники. В некоторых вариантах осуществления органический растворитель включает один или более из ацетонитрила, эпоксидного растворителя, простого эфирного растворителя, галогеналканового растворителя, диметилсульфоксида, N,N-диметилформамида и N,N-диизопропилэтиламина. В некоторых вариантах осуществления эпоксидный растворитель представляет собой диоксан и/или тетрагидрофуран, простой эфирный растворитель представляет собой диэтиловый эфир и/или метил-трет-бутиловый эфир, и галогеналкановый растворитель представляет собой один или более из дихлорметана, трихлорметана и 1,2-дихлорэтана. В некоторых вариантах осуществления органический растворитель представляет собой ацетонитрил. Количество органического растворителя может составлять 20-200 л/моль, и в некоторых вариантах осуществления 50-100 л/моль, относительно соединения, представленного Формулой (321).
В некоторых вариантах осуществления конденсирующий агент может представлять собой бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат (PyBop), 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он (DEPBT) и/или O-бензотриазол-1-ил-тетраметилурония гексафторфосфат. В некоторых вариантах осуществления конденсирующий агент представляет собой O-бензотриазол-1-ил-тетраметилурония гексафторфосфат. Молярное отношение конденсирующего агента к соединению, представленному Формулой (321), составляет от 1:1 до 20:1, и в некоторых вариантах осуществления от 1:1 до 5:1.
В некоторых вариантах осуществления третичный амин представляет собой триэтиламин и/или N,N-диизопропилэтиламин, и в некоторых вариантах осуществления N,N-диизопропилэтиламин. Молярное отношение третичного амина к соединению, представленному Формулой (321), составляет от 1:1 до 20:1, и в некоторых вариантах осуществления от 1:1 до 5:1.
В некоторых вариантах осуществления способ получения соединения, представленного Формулой (321), дополнительно включает: приведение полученного продукта конденсации в контакт с кэпирующим агентом и катализатором ацилирования в органическом растворителе в условии реакции кэпирования и выделение соединения, представленного Формулой (321). Реакция кэпирования используется для удаления любых активных функциональных групп, полностью не вступающих в реакцию, чтобы избежать образования побочных продуктов в последующих реакциях. Условия реакции кэпирования включают температуру реакции 0-50°C, и в некоторых вариантах осуществления 15-35°C, и продолжительность проведения реакции 1-10 часов, и в некоторых вариантах осуществления 3-6 часов. Кэпирующий агент может представлять собой кэпирующий агент, применяемый в твердофазном синтезе миРНК, и кэпирующий агент, применяемый в твердофазном синтезе миРНК, хорошо известен специалистам в данной области техники.
В некоторых вариантах осуществления кэпирующий агент состоит из кэпирующего агента 1 (cap1) и кэпирующего агента 2 (cap2). Cap1 представляет собой N-метилимидазол, и в некоторых вариантах осуществления обеспечивают в виде смешанного раствора N-метилимидазола в пиридине/ацетонитриле, где объемное отношение пиридина к ацетонитрилу составляет от 1:10 до 1:1, и в некоторых вариантах осуществления от 1:3 до 1:1. В некоторых вариантах осуществления отношение общего объема пиридина и ацетонитрила к объему N-метилимидазола составляет от 1:1 до 10:1, и в некоторых вариантах осуществления от 3:1 до 7:1. Кэпирующий агент 2 представляет собой уксусный ангидрид. В некоторых вариантах осуществления кэпирующий агент 2 обеспечивают в виде раствора уксусного ангидрида в ацетонитриле, где объемное отношение уксусного ангидрида к ацетонитрилу составляет от 1:1 до 1:10, и в некоторых вариантах осуществления от 1:2 до 1:6.
В некоторых вариантах осуществления отношение объема смешанного раствора N-метилимидазола в пиридине/ацетонитриле к массе соединения, представленного Формулой (321), составляет от 5 мл/г до 50 мл/г, и в некоторых вариантах осуществления от 15 мл/г до 30 мл/г. Отношение объема раствора уксусного ангидрида в ацетонитриле к массе соединения, представленного Формулой (321), составляет от 0,5 мл/г до 10 мл/г, и в некоторых вариантах осуществления от 1 мл/г до 5 мл/г.
В некоторых вариантах осуществления кэпирующий агент содержит эквимолярные количества уксусного ангидрида и N-метилимидазола. В некоторых вариантах осуществления органический растворитель включает один или более из ацетонитрила, эпоксидного растворителя, простого эфирного растворителя, галогеналканового растворителя, диметилсульфоксида, N,N-диметилформамида и N,N-диизопропилэтиламина. В некоторых вариантах осуществления органический растворитель представляет собой ацетонитрил. Количество органического растворителя может составлять 10-50 л/моль, и в некоторых вариантах осуществления 5-30 л/моль, относительно соединения, представленного Формулой (321).
В некоторых вариантах осуществления катализатор ацилирования может быть выбран из любого катализатора, который может быть использован для конденсации путем этерификации или амидной конденсации, такого как щелочные гетероциклические соединения. В некоторых вариантах осуществления катализатор ацилирования представляет собой 4-диметиламинопиридин. Массовое отношение катализатора к соединению, представленному Формулой (321), может составлять от 0,001:1 до 1:1, и в некоторых вариантах осуществления от 0,01:1 до 0,1:1.
В некоторых вариантах осуществления соединение, представленное Формулой (321), может быть выделено из реакционной смеси с помощью любых подходящих способов выделения. В некоторых вариантах осуществления соединение, представленное Формулой (321), может быть получено путем тщательной промывки органическим растворителем и фильтрации для удаления непрореагировавших реагентов, избытка кэпирующего агента и других примесей, где органический растворитель выбран из ацетонитрила, дихлорметана или метанола. В некоторых вариантах осуществления органический растворитель представляет собой ацетонитрил.
В некоторых вариантах осуществления получение конъюгирующей молекулы, представленной Формулой (321), включает приведение соединения, представленного Формулой (313), в контакт с диамидофосфитом в органическом растворителе в условиях реакции сочетания в присутствии агента реакции сочетания, и выделение соединения, представленного Формулой (321). В этом случае получают соединение, представленное Формулой (321), где R4 содержит первую функциональную группу, содержащую гидроксизащитную группу, и вторую функциональную группу, имеющую структуру, представленную Формулой (C3).
В некоторых вариантах осуществления условия реакция сочетания включают температуру реакции 0-50°C, например, 15-35°C. Молярное отношение соединения, представленного Формулой (313), к диамидофосфиту может составлять от 1:1 до 1:50, например, от 1:5 до 1:15.Молярное отношение соединения, представленного Формулой (313), к агенту реакции сочетания может составлять от 1:1 до 1:100, например, от 1:50 до 80. Продолжительность проведения реакции может составлять 200-3000 секунд, например, 500-1500 секунд. Диамидофосфит может представлять собой, например, бис(диизопропиламино)(2-цианоэтокси)фосфин, который может быть доступен на рынке или синтезирован в соответствии со способами, хорошо известными в данной области техники. Агент реакции сочетания выбран из одного или более из 1H-тетразола, 5-этилтио-1H-тетразола и 5-бензилтио-1H-тетразола, например, 5-этилтио-1H-тетразола. Реакция сочетания может проводиться в органическом растворителе, и органический растворитель выбран из одного или более из безводного ацетонитрила, безводного ДМФА (диметилформамид) и безводного дихлорметана, например, безводного ацетонитрила. Количество органического растворителя может составлять 3-50 л/моль, например, 5-20 л/моль, относительно соединения, представленного Формулой (313). При проведении реакции сочетания гидроксигруппа в соединении, представленном Формулой (313), реагирует с диамидофосфитом с образованием амидофосфитной группы. В некоторых вариантах осуществления растворитель может быть сразу же удален с получением неочищенного продукта соединения, представленного Формулой (321), который может быть сразу использован в последующих реакциях.
В некоторых вариантах осуществления способ получения соединения, представленного Формулой (321), дополнительно включает: приведение выделенного продукта в контакт с твердофазной подложкой, содержащей гидроксигруппы, в органическом растворителе в условиях реакции сочетания в присутствии агента реакции сочетания с последующим кэпированием, окислением и выделением, с получением соединения, представленного Формулой (321). В этом случае получают соединение, представленное Формулой (321), где R4 содержит первую функциональную группу, содержащую гидроксизащитную группу, и вторую функциональную группу, имеющую структуру, представленную Формулой (C3’).
В некоторых вариантах осуществления твердофазная подложка представляет собой хорошо известную твердофазную подложку в области твердофазного синтеза нуклеиновых кислот, такую как доступная на рынке незащищенная универсальная твердофазная подложка (подложка для синтеза олигонуклеотидов NittoPhase®HL UnyLinker™ 300, Kinovate Life Sciences, представленная Формулой B80):

(B80).
Реакция снятия защиты хорошо известна в данной области техники. В некоторых вариантах осуществления условия снятия защиты включают температуру 0-50°C, например, 15-35°C, и продолжительность проведения реакции 30-300 секунд, например, 50-150 секунд. Агент для снятия защиты может быть выбран из одной или более из трифторуксусной кислоты, трихлоруксусной кислоты, дихлоруксусной кислоты и монохлоруксусной кислоты. В некоторых вариантах осуществления агент для снятия защиты представляет собой дихлоруксусную кислоту. Молярное отношение агента для снятия защиты к защитной группе -DMTr (4,4'-диметокситритил) на твердофазной подложке может составлять от 2:1 до 100:1, например, от 3:1 до 50:1. С помощью такого снятия защиты на поверхности твердофазной подложки получают реакционноспособные гидроксигруппы для облегчения последующей реакции сочетания.
Условия реакции сочетания и агент реакции сочетания могут быть выбраны, как указано выше. При проведении реакции сочетания свободные гидроксигруппы, образованные в реакции снятия защиты, реагируют с амидофосфитными группами с образованием фосфитной эфирной связи.
В некоторых вариантах осуществления условия реакции кэпирования включают температуру реакции 0-50°C, например, 15-35°C, и продолжительность проведения реакции 5-500 секунд, например, 10-100 секунд. Реакцию кэпирования проводят в присутствии кэпирующего агента. Кэпирующий агент и его количество выбирают, как указано выше.
Условия реакции окисления могут включать температуру 0-50°C, например, 15-35°C, и продолжительность проведения реакции 1-100 секунд, например, 5-50 секунд. Окисляющий агент может представлять собой, например, иод (в некоторых вариантах осуществления обеспечиваемый в виде иодной воды). В некоторых вариантах осуществления молярное отношение окисляющего агента к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, составляет от 1:1 до 100:1, например, от 5:1 до 50:1. В некоторых вариантах осуществления реакцию окисления проводят в смешанном растворителе, в котором отношение тетрагидрофуран:вода:пиридин составляет от 3:1:1 до 1:1:3.
В некоторых вариантах осуществления R6 представляет собой группу, представленную Формулой B7 или B8:
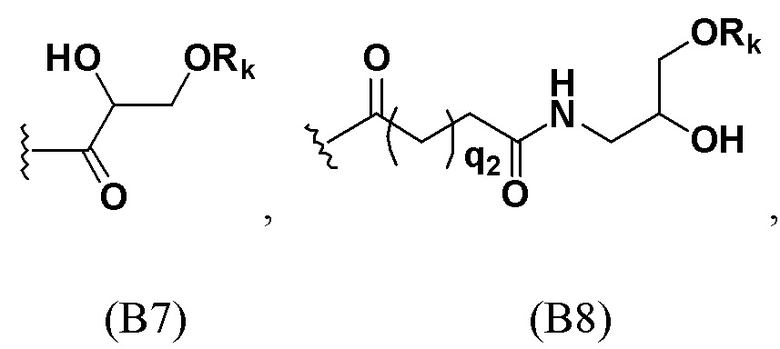
где определения q2 и Rk соответствуют описанным выше.
В этом случае соединение, представленное Формулой (313), может быть получено с помощью следующего способа: приведение соединения, представленного Формулой (314), в контакт с соединением, представленным Формулой (A-1), или соединением, представленным Формулой (A-2), в органическом растворителе в условиях реакции амидирования в присутствии агента для амидной конденсации и третичного амина, и выделение:
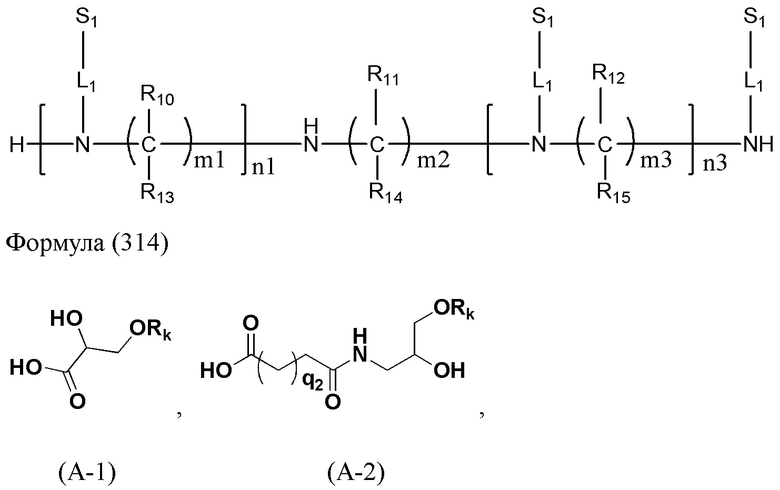
где определения и варианты n1, n3, m1, m2, m3, R10, R11, R12, R13, R14, R15, L1, S1, q2 и Rk соответственно представляют собой такие, как описано выше.
Условия реакции амидирования могут включать температуру реакции 0-100°C и продолжительность проведения реакции 1-48 часов. В некоторых вариантах осуществления условия реакции амидирования включают температуру реакции 10-40°C и продолжительность проведения реакции 2-16 часов.
В некоторых вариантах осуществления органический растворитель представляет собой один или более из спиртового растворителя, эпоксидного растворителя, простого эфирного растворителя, галогеналканового растворителя, диметилсульфоксида, N,N-диметилформамида и N,N-диизопропилэтиламина. В некоторых вариантах осуществления спиртовой растворитель представляет собой один или более из метанола, этанола и пропанола, и в некоторых вариантах осуществления представляет собой этанол. В некоторых вариантах осуществления эпоксидный растворитель представляет собой диоксан и/или тетрагидрофуран. В некоторых вариантах осуществления простой эфирный растворитель представляет собой диэтиловый эфир и/или метил-трет-бутиловый эфир. В некоторых вариантах осуществления галогеналкановый растворитель представляет собой один или более из дихлорметана, трихлорметана и 1,2-дихлорэтана. В некоторых вариантах осуществления органический растворитель представляет собой дихлорметан. Количество органического растворителя составляет 3-50 л/моль, и в дополнительных вариантах осуществления 3-20 л/моль, относительно соединения, представленного Формулой (314).
В некоторых вариантах осуществления агент для амидной конденсации представляет собой бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат, 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он, 4-(4,6-диметокситриазин-2-ил)-4-метилморфолина гидрохлорид, 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин (EEDQ) или O-бензотриазол-1-ил-тетраметилурония гексафторфосфат, и в дополнительных вариантах осуществления представляет собой 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он. Молярное отношение агента для амидной конденсации к соединению, представленному Формулой (314), может составлять от 1:1 до 10:1, и в некоторых вариантах осуществления от 2,5:1 до 5:1.
В некоторых вариантах осуществления третичный амин представляет собой триэтиламин и/или N,N-диизопропилэтиламин, и в дополнительных вариантах осуществления N,N-диизопропилэтиламин. Молярное отношение третичного амина к соединению, представленному Формулой (314), составляет от 3:1 до 20:1, и в некоторых вариантах осуществления от 5:1 до 10:1.
Соединения, представленные Формулой (A-1) и Формулой (A-2), могут быть получены с помощью любых подходящих способов. Например, когда Rk представляет собой группу DMTr, соединение, представленное Формулой (A-1), может быть получено путем взаимодействия с DMTrCl глицерата кальция. Аналогичным образом, соединение, представленное Формулой (A-2), может быть получено путем приведения 3-амино-1,2-пропандиола в контакт с циклическим ангидридом и последующим взаимодействием с DMTrCl, где циклический ангидрид может содержать 4-13 атомов углерода, и в некоторых вариантах осуществления 4-8 атомов углерода. Специалисты в данной области техники без труда поймут, что выбираемые циклические ангидриды соответствуют различным значениям q2 в соединении, представленном Формулой (A-2). Например, если циклический ангидрид представляет собой янтарный ангидрид, q2=1; если циклический ангидрид представляет собой глутаровый ангидрид, q2=2, и так далее.
В некоторых вариантах осуществления соединение, представленное Формулой (313), также может быть получено путем последовательного взаимодействия соединения, представленного Формулой (314), с циклическим ангидридом, 3-амино-1,2-пропандиолом и DMTrCl. Специалисты в данной области техники без труда поймут, что эти варианты не будут влиять на структуру и функцию соединения, представленного Формулой (313), и эти варианты могут быть легко осуществлены специалистами в данной области техники на основе вышеуказанных способов.
Аналогичным образом, соединение, представленное Формулой (313), может быть выделено из реакционной смеси с помощью любых подходящих способов выделения. В некоторых вариантах осуществления соединение, представленное Формулой (313), может быть выделено посредством удаления растворителя выпариванием с последующей хроматографией, например, с использованием следующих двух условий хроматографирования для выделения: (1) нормально-фазовая очистка силикагелевым фильтром с размером частиц 200-300 меш и градиентное элюирование смесью петролейный эфир:этилацетат:дихлорметан:N,N-диметилформамид в соотношении от 1:1:1:0,5 до 1:1:1:0,6; и (2) обращенно-фазовая очистка с наполнителями с обращенной фазой C18 и C8 и градиентное элюирование смесью метанол:ацетонитрил в соотношении от 0,1:1 до 1:0,1. В некоторых вариантах осуществления растворитель может быть сразу же удален с получением неочищенного продукта соединения, представленного Формулой (313), который может быть сразу использован в последующих реакциях.
В некоторых вариантах осуществления соединение, представленное Формулой (314), может быть получено с помощью следующего способа, включающего: приведение соединения, представленного Формулой (320), в контакт с соединением, представленным Формулой (316), в органическом растворителе в условиях реакции конденсации в присутствии агента для амидной конденсации и третичного амина, и выделение:

Формула (316)
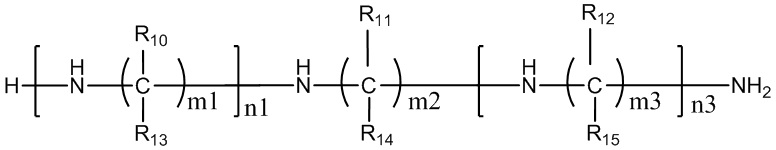
Формула (320),
где определения и варианты n1, n3, m1, m2, m3, R10, R11, R12, R13, R14 и R15 соответственно представляют собой такие, как описано выше.
Соединение, представленное Формулой (316), может представлять собой такое, как описано в источнике J. Am. Chem. Soc. 2014, 136, 16958-16961, или соединение, представленное Формулой (316), может быть получено специалистами в данной области техники с помощью различных способов. Например, некоторые соединения, представленные Формулой (316), могут быть получены в соответствии со способами, раскрытыми в примере 1 патента США № 8106022 B2, включенного в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах осуществления условия реакции конденсации включают температуру реакции 0-100°C и продолжительность проведения реакции 0,1-24 часа. В некоторых вариантах осуществления условия реакции конденсации включают температуру реакции 10-40°C и продолжительность проведения реакции 0,5-16 часов.
Учитывая структуру целевого соединения, представленного Формулой (314), молярное отношение соединения, представленного Формулой (316), к соединению, представленному Формулой (320), следует определять, основываясь на сумме n1 и n3 в Формуле (320). В некоторых вариантах осуществления, например, когда n1+n3=3, для обеспечения полноты протекания реакции и отсутствия избытка, молярное отношение соединения, представленного Формулой (316), к соединению, представленному Формулой (320), может составлять от 3:1 до 3,5:1, и в некоторых вариантах осуществления составляет от 3,01:1 до 3,15:1.
В некоторых вариантах осуществления органический растворитель представляет собой один или более из ацетонитрила, эпоксидного растворителя, простого эфирного растворителя, галогеналканового растворителя, диметилсульфоксида, N,N-диметилформамида и N,N-диизопропилэтиламина. В некоторых вариантах осуществления эпоксидный растворитель представляет собой диоксан и/или тетрагидрофуран. В некоторых вариантах осуществления простой эфирный растворитель представляет собой диэтиловый эфир и/или метил-трет-бутиловый эфир. В некоторых вариантах осуществления галогеналкановый растворитель представляет собой один или более из дихлорметана, трихлорметана и 1,2-дихлорэтана. В некоторых вариантах осуществления органический растворитель представляет собой ацетонитрил. Количество органического растворителя составляет 3-50 л/моль, и в некоторых вариантах осуществления 5-20 л/моль, относительно соединения, представленного Формулой (320).
В некоторых вариантах осуществления агент для амидной конденсации представляет собой бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат, 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он (DEPBT), O-бензотриазол-1-ил-тетраметилурония гексафторфосфат, 4-(4,6-диметокситриазин-2-ил)-4-метилморфолина гидрохлорид или 1-гидроксибензотриазол, и в дополнительных вариантах осуществления представляет собой смесь бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфата и 1-гидроксибензотриазола, где бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат (PyBop) и 1-гидроксибензотриазол содержатся в эквимолярных количествах. Молярное отношение общего количества агента для амидной конденсации к соединению, представленному Формулой (316), может составлять от 1:1 до 3:1, и в некоторых вариантах осуществления составляет от 1,05:1 до 1,5:1.
Третичный амин может представлять собой N-метилморфолин, триэтиламин или N,N-диизопропилэтиламин, и в некоторых вариантах осуществления N-метилморфолин. Молярное отношение третичного амина к соединению, представленному Формулой (316), может составлять от 2:1 до 10:1, и в некоторых вариантах осуществления составляет от 2:1 до 5:1.
Аналогичным образом, соединение, представленное Формулой (314), может быть выделено из реакционной смеси с помощью любых подходящих способов выделения. В некоторых вариантах осуществления соединение, представленное Формулой (314), выделяют посредством удаления растворителя выпариванием с последующей хроматографией, например, с использованием следующих двух условий хроматографирования для выделения: (1) нормально-фазовая очистка силикагелевым фильтром с размером зерен 200-300 меш и градиентное элюирование смесью дихлорметан:метанол в соотношении от 100:5 до 100:7; и (2) обращенно-фазовая очистка с наполнителями с обращенной фазой C18 и C8 и градиентное элюирование смесью метанол:ацетонитрил в соотношении от 0,1:1 до 1:0,1. В некоторых вариантах осуществления растворитель сразу же удаляют с получением неочищенного продукта соединения, представленного Формулой (314), который может быть сразу использован в последующих реакциях.
Соединение, представленное Формулой (320), может быть доступно на рынке или получено специалистами в данной области техники с помощью известных способов. Например, в случае, если m1=m2=m3=3, n1=1, n3=2, и R10, R11, R12, R13, R14 и R15 все представляют собой H, соединение, представленное Формулой (320), доступно на рынке от Alfa Aesar Inc.
Конъюгат миРНК согласно настоящему изобретению также может быть применен в комбинации с другими фармацевтически приемлемыми вспомогательными веществами, которые могут представлять собой один или более из различных общепринятых в данной области техники составов или соединений. Подробная информация содержится в приведенном выше описании фармацевтических композиций согласно настоящему изобретению.
Применение миРНК, фармацевтической композиции и конъюгата миРНК согласно настоящему изобретению
В некоторых вариантах осуществления настоящего изобретения предложено применение миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению для производства лекарственного средства для лечения и/или предупреждения миастении гравис.
Согласно некоторым вариантам осуществления настоящего изобретения предложен способ предупреждения и/или лечения миастении гравис, включающий введение эффективного количества миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению нуждающемуся субъекту.
Цель предупреждения и/или лечения миастении гравис может быть достигнута на основе механизма РНК-интерференции путем введения активных ингредиентов миРНК согласно настоящему изобретению нуждающемуся субъекту. Таким образом, миРНК, и/или фармацевтическая композиция, и/или конъюгат миРНК согласно настоящему изобретению могут применяться для предупреждения и/или лечения миастении гравис или для производства лекарственного средства для предупреждения и/или лечения миастении гравис.
Применительно к настоящему изобретению термин «введение/вводить» относится к доставке миРНК, фармацевтической композиции и/или конъюгата миРНК согласно настоящему изобретению в организм субъекта с помощью способа или пути, который по меньшей мере частично локализует миРНК, фармацевтическую композицию и/или конъюгат миРНК согласно настоящему изобретению в желаемом месте для получения желаемого эффекта. Подходящие пути введения для способов согласно настоящему изобретению включают местное введение и системное введение. Как правило, местное введение приводит к доставке большего количества конъюгата миРНК в определенное место по сравнению с системным кровотоком субъекта, тогда как системное введение приводит к доставке миРНК, фармацевтической композиции и/или конъюгата миРНК согласно настоящему изобретению по существу в системный кровоток субъекта. Принимая во внимание, что согласно настоящему изобретению могут быть предложены средства для предупреждения и/или лечения миастении гравис, в некоторых вариантах осуществления применяется способ введения, способный доставлять лекарственные средства в печень.
Введение субъекту может быть осуществлено с помощью любых подходящих путей, известных в данной области техники, включая, не ограничиваясь перечисленным, пероральный или парентеральный путь, такой как внутривенное введение, внутримышечное введение, подкожное введение, трансдермальное введение, внутритрахеальное введение (аэрозоль), ингаляционное введение, интраназальное введение, ректальное введение и местное введение (включая трансбуккальное введение и сублингвальное введение). Частота введения может составлять один или более раз в сутки, еженедельно, один раз в две недели, один раз в три недели, ежемесячно, один раз в два месяца, один раз в три месяца, один раз в полгода или ежегодно.
Доза миРНК, фармацевтической композиции или конъюгата второй миРНК согласно настоящему изобретению может представлять собой обычную дозу в данной области техники, и доза может быть определена в соответствии с различными параметрами, в частности, возрастом, массой тела и полом субъекта. Токсичность и эффективность могут быть измерены в клеточных культурах или на подопытных животных с помощью стандартных фармацевтических процедур, например, путем определения LD50 (летальная доза, вызывающая гибель 50% популяции), ED50 (доза, которая при количественном ответе может вызвать 50% от максимальной интенсивности ответа, и при качественном ответе обеспечивает положительный ответ у 50% подопытных субъектов) или IC50 (концентрация ингибитора/лекарственного средства, необходимая для подавления количественной реакции наполовину). Диапазон доз для человека может быть получен на основании данных, полученных из анализа на клеточной культуре и исследований на животных.
При введении миРНК, фармацевтической композиции или конъюгата миРНК согласно настоящему изобретению, например, самцам или самкам мышей C57BL/6J в возрасте 6-12 недель и с массой тела 18-25 г, и вычислении на основании количества миРНК: (i) для конъюгата миРНК дозировка содержащейся в нем миРНК может составлять 0,001-100 мг/кг массы тела, и в дополнительных вариантах осуществления составляет 0,01-50 мг/кг массы тела, и в некоторых вариантах осуществления составляет 0,05-20 мг/кг массы тела, в некоторых других вариантах осуществления составляет 0,1-15 мг/кг массы тела, и в некоторых других вариантах осуществления настоящего изобретения составляет 0,1-10 мг/кг массы тела; и (ii) для фармацевтической композиции, состоящей из миРНК и фармацевтически приемлемого носителя, дозировка содержащейся в ней миРНК может составлять 0,001-50 мг/кг массы тела, в некоторых вариантах осуществления составляет 0,01-10 мг/кг массы тела, в некоторых вариантах осуществления составляет 0,05-5 мг/кг массы тела, и в некоторых вариантах осуществления составляет 0,1-3 мг/кг массы тела.
В некоторых вариантах осуществления настоящего изобретения предложен способ ингибирования экспрессии гена C5 в гепатоците. Указанный способ включает приведение эффективного количества миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению в контакт с указанным гепатоцитом, введение миРНК, и/или фармацевтической композиции, и/или конъюгата миРНК согласно настоящему изобретению в указанный гепатоцит и достижение цели ингибирования экспрессии гена C5 в указанном гепатоците посредством механизма РНК-интерференции. Гепатоцит может быть выбран из SMMC-7721, HepG2, Huh7 и других линий клеток гепатомы или выделенных первичных гепатоцитов. В некоторых вариантах осуществления клетки представляют собой клетки гепатомы HepG2.
При ингибировании экспрессии C5 в клетке с помощью способа согласно настоящему изобретению количество миРНК в предложенных модифицированной миРНК, фармацевтической композиции и/или конъюгате миРНК, как правило, представляет собой количество, достаточное для снижения экспрессии гена-мишени и достижения внеклеточной концентрации от 1 пМ до 1 мкМ, или от 0,01 нМ до 100 нМ, или от 0,05 нМ до 50 нМ, или от 0,05 нМ до приблизительно 5 нМ на поверхности клетки-мишени. Количество, требуемое для достижения этой локальной концентрации, будет варьировать в зависимости от различных факторов, включая способ доставки, место доставки, количество клеточных слоев между местом доставки и клетками- или тканями-мишенями, путь доставки (местный или системный) и т. д. Концентрация в месте доставки может быть значительно выше, чем концентрация на поверхности клеток- или тканей-мишеней.
Набор
Согласно настоящему изобретению предложен набор, содержащий эффективное количество по меньшей мере одного из модифицированной миРНК, фармацевтической композиции и конъюгата миРНК согласно настоящему изобретению.
В некоторых вариантах осуществления в наборе, раскрытом в настоящем документе, может предоставляться модифицированная миРНК в одном контейнере. В некоторых вариантах осуществления набор согласно настоящему изобретению может содержать контейнер, в котором предоставляются фармацевтически приемлемые вспомогательные вещества. В некоторых вариантах осуществления указанный набор может дополнительно содержать дополнительные ингредиенты, такие как стабилизаторы или консерванты. В некоторых вариантах осуществления набор согласно настоящему изобретению может содержать по меньшей мере один дополнительный терапевтический агент в контейнере, отличном от контейнера, в котором предоставляется модифицированная миРНК согласно настоящему изобретению. В некоторых вариантах осуществления набор может содержать инструкцию по смешиванию модифицированной миРНК с фармацевтически приемлемым носителем и/или адъювантами или другими ингредиентами (если таковые имеются).
В наборе согласно настоящему изобретению модифицированная миРНК и фармацевтически приемлемый носитель и/или адъюванты, а также модифицированная миРНК, фармацевтическая композиция и/или конъюгат миРНК, и/или фармацевтически приемлемые адъюванты могут предоставляться в любой форме, например, в жидкой форме, сухой форме или лиофилизированной форме. В некоторых вариантах осуществления модифицированная миРНК и фармацевтически приемлемый носитель и/или адъюванты, а также фармацевтическая композиция и/или конъюгат миРНК и необязательные фармацевтически приемлемые адъюванты являются по существу чистыми и/или стерильными. В некоторых вариантах осуществления в наборе согласно настоящему изобретению может быть предоставлена стерильная вода.
Далее в настоящем документе настоящее изобретение будет дополнительно описано с помощью примеров, но не ограничивается ими ни в каком отношении.
Примеры
Если не указано иное, все агенты и культуральные среды, использованные в следующих примерах, доступны на рынке, и все применяемые процедуры, такие как электрофорез нуклеиновых кислот и ПЦР в реальном времени, проведены в соответствии с методами, описанными в источнике Molecular Cloning (Cold Spring Harbor Laboratory Press (1989)).
Lipofectamine™ 2000 (Invitrogen) использовали в качестве реагента для трансфекции при трансфекции клеток миРНК и конъюгатом миРНК к гену C5, синтезированными в настоящем изобретении, или миРНК и конъюгатом миРНК в качестве отрицательного контроля, и конкретный процесс соответствует инструкциям, предоставленным производителем.
Если не указано иное, все отношения реагентов, приведенные ниже, рассчитаны как отношения по объему (об./об.).
Все экспериментальные данные выражены как 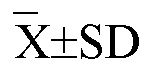 , и анализ данных осуществлен с помощью программного обеспечения для статистического анализа Graphpad prism 5.0.
, и анализ данных осуществлен с помощью программного обеспечения для статистического анализа Graphpad prism 5.0.
Пример получения 1. Получение конъюгата 1
В этом примере получения синтезировали конъюгат 1 (т. е. L10-siC5a1M1SP). Конъюгированная миРНК в конъюгате имеет последовательности смысловой цепи и антисмысловой цепи, соответствующие конъюгату 1 из таблицы 3.
(1-1) Синтез соединения L-10
Соединение L-10 синтезировали в соответствии со следующим способом:
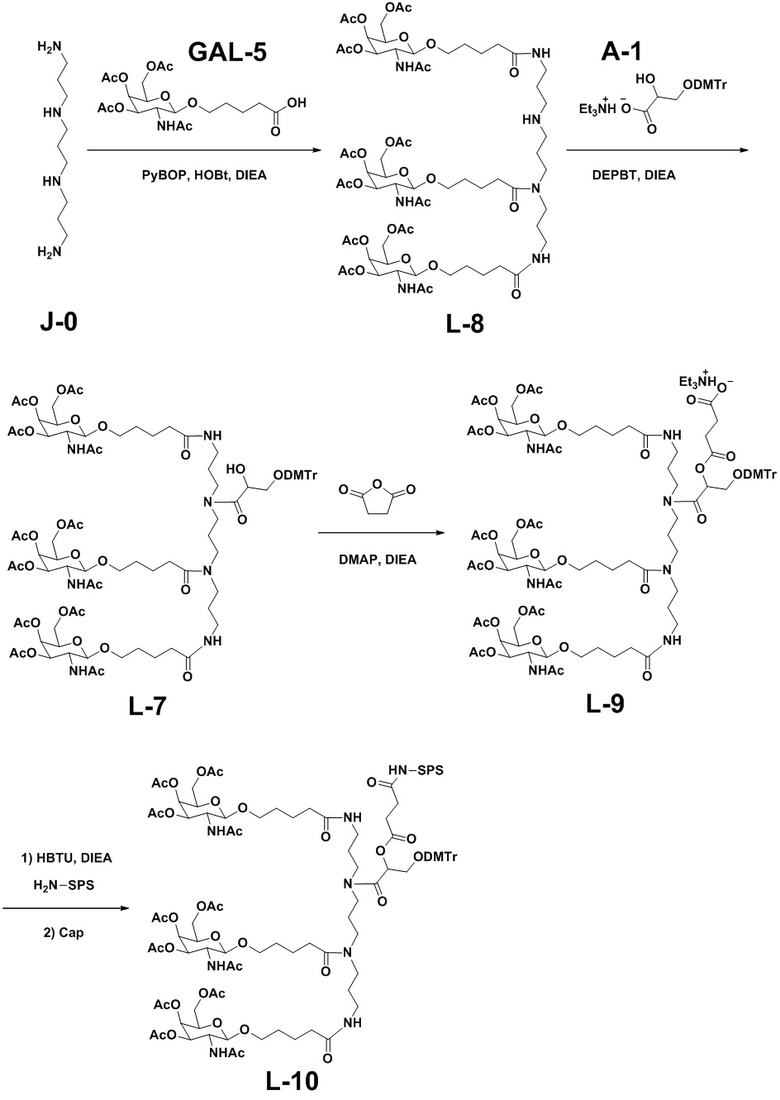
(1-1-1) Синтез GAL-5 (концевой конъюгирующей молекулы)
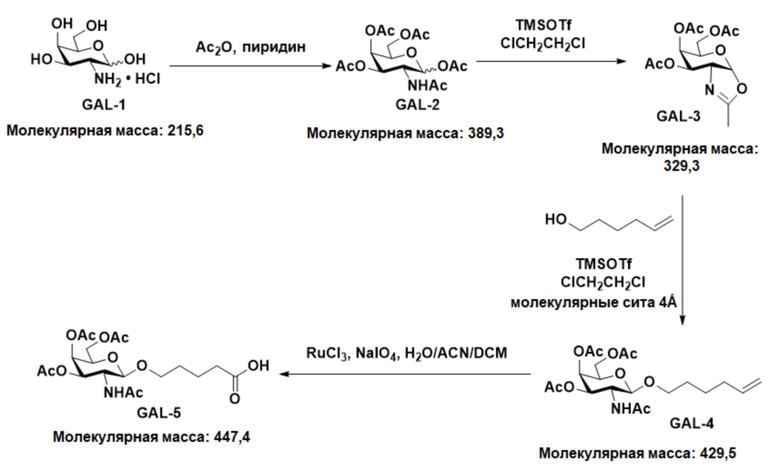
(1-1-1a) Синтез GAL-2
100,0 г GAL-1 (гидрохлорида N-ацетил-D-галактозамина, № CAS 1772-03-8, приобретен у Ningbo Hongxiang Bio-Chem Co., Ltd., 463,8 ммоль) растворяли в 1000 мл безводного пиридина, к которому добавляли 540 мл уксусного ангидрида (приобретен у Enox Inc., 5565,6 ммоль) на бане с ледяной водой для проведения взаимодействия при перемешивании при комнатной температуре в течение 1,5 часов. Полученный реакционный раствор выливали в 10 л ледяной воды и подвергали вакуумной фильтрации при пониженном давлении. Остаток промывали 2 л ледяной воды, а затем добавляли смешанный растворитель ацетонитрил/толуол (отношение об./об. = 1:1) до полного растворения. Растворитель удаляли с помощью выпаривания с получением 130,0 г продукта GAL-2 в виде белого твердого вещества.
(1-1-1b) Синтез GAL-3
GAL-2 (35,1 г, 90,0 ммоль), полученный на стадии (1-1-1a), растворяли в 213 мл безводного 1,2-дихлорэтана, к которому добавляли 24,0 г триметилсилилтрифторметансульфоната (TMSOTf, № CAS 27607-77-8, приобретен у Macklin Inc., 108,0 ммоль) на бане с ледяной водой и в защитной атмосфере азота для проведения взаимодействия при комнатной температуре в течение ночи.
К реакционному раствору добавляли 400 мл дихлорметана для разбавления, фильтровали через диатомит, а затем добавляли 1 л насыщенного водного раствора бикарбоната натрия и перемешивали до однородности. Выделяли органическую фазу. Оставшуюся водную фазу дважды экстрагировали, каждый раз с помощью 300 мл дихлорэтана, и все органические фазы объединяли и промывали с помощью 300 мл насыщенного водного раствора бикарбоната натрия и 300 мл насыщенного рассола, соответственно. Органическую фазу, полученную в результате промывки, выделяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении с получением 26,9 г продукта GAL-3 в виде светло-желтого вязкого сиропа.
(1-1-1c) Синтез GAL-4
GAL-3 (26,9 г, 81,7 ммоль), полученный на стадии (1-1-1b), растворяли в 136 мл безводного 1,2-дихлорэтана, добавляли 30 г порошка сухих молекулярных сит 4 , а затем 9,0 г 5-гексен-1-ола (№ CAS 821-41-0, приобретен у Adamas-beta Inc., 89,9 ммоль), и перемешивали при комнатной температуре в течение 30 минут. Добавляли 9,08 мл TMSOTf (40,9 ммоль) на ледяной бане и в защитной атмосфере азота для проведения взаимодействия при перемешивании при комнатной температуре в течение ночи. Порошок молекулярных сит 4
, а затем 9,0 г 5-гексен-1-ола (№ CAS 821-41-0, приобретен у Adamas-beta Inc., 89,9 ммоль), и перемешивали при комнатной температуре в течение 30 минут. Добавляли 9,08 мл TMSOTf (40,9 ммоль) на ледяной бане и в защитной атмосфере азота для проведения взаимодействия при перемешивании при комнатной температуре в течение ночи. Порошок молекулярных сит 4 удаляли с помощью фильтрации. К фильтрату добавляли 300 мл дихлорэтана для разбавления, фильтровали через диатомит, а затем добавляли 500 мл насыщенного водного раствора бикарбоната натрия и перемешивали в течение 10 минут для промывки. Выделяли органическую фазу. Водную фазу однократно экстрагировали с помощью 300 мл дихлорэтана. Все органические фазы объединяли и промывали с помощью 300 мл насыщенного водного раствора бикарбоната натрия и 300 мл насыщенного рассола, соответственно. Органическую фазу, полученную в результате промывки, выделяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении с получением 41,3 г продукта GAL-4 в виде желтого сиропа, который сразу использовали в следующей реакции окисления без очистки.
удаляли с помощью фильтрации. К фильтрату добавляли 300 мл дихлорэтана для разбавления, фильтровали через диатомит, а затем добавляли 500 мл насыщенного водного раствора бикарбоната натрия и перемешивали в течение 10 минут для промывки. Выделяли органическую фазу. Водную фазу однократно экстрагировали с помощью 300 мл дихлорэтана. Все органические фазы объединяли и промывали с помощью 300 мл насыщенного водного раствора бикарбоната натрия и 300 мл насыщенного рассола, соответственно. Органическую фазу, полученную в результате промывки, выделяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении с получением 41,3 г продукта GAL-4 в виде желтого сиропа, который сразу использовали в следующей реакции окисления без очистки.
(1-1-1d) Синтез GAL-5
GAL-4 (14,9 г, 34,7 ммоль), полученный в соответствии со способом, описанным на стадии (1-1 1c), растворяли в смешанном растворителе из 77 мл дихлорметана и 77 мл ацетонитрила, добавляли 103 мл деионизированной воды и 29,7 г периодата натрия (№ CAS 7790-28-5, приобретен у Aladdin Inc., 138,8 ммоль), соответственно, и перемешивали на ледяной бане в течение 10 минут. Добавляли трихлорид рутения (№ CAS 14898-67-0, приобретен у Energy Chemical, 238 мг, 1,145 ммоль) для проведения взаимодействия при комнатной температуре в течение ночи. Полученный реакционный раствор разбавляли путем добавления 300 мл воды при перемешивании и доводили до pH приблизительно 7,5, добавляя насыщенный бикарбонат натрия. Органическую фазу выделяли и отбрасывали. Водную фазу трижды экстрагировали, каждый раз с помощью 200 мл дихлорметана, и отбрасывали органическую фазу, полученную в результате экстракции. Водную фазу, полученную в результате экстракции, доводили до pH, равного приблизительно 3, с помощью порошка лимонной кислоты, трижды экстрагировали, каждый раз с помощью 200 мл дихлорметана, и полученные органические фазы объединяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении с получением 6,85 г продукта GAL-5 в виде белого пенистого твердого вещества. 1H ЯМР (400 МГц, ДМСО) δ 12,01 (br, 1H), 7,83 (d, J = 9,2 Гц, 1H), 5,21 (d, J = 3,2 Гц, 1H), 4,96 (dd, J = 11,2, 3,2 Гц, 1H), 4,49 (d, J = 8,4 Гц, 1H), 4,07 - 3,95 (m, 3H), 3,92 - 3,85 (m, 1H), 3,74 - 3,67 (m, 1H), 3,48 - 3,39 (m, 1H), 2,20 (t, J = 6,8 Гц, 2H), 2,11 (s, 3H), 2,00 (s, 3H), 1,90 (s, 3H), 1,77 (s, 3H), 1,55 - 1,45 (m, 4H).
(1-1-2) Синтез L-8:
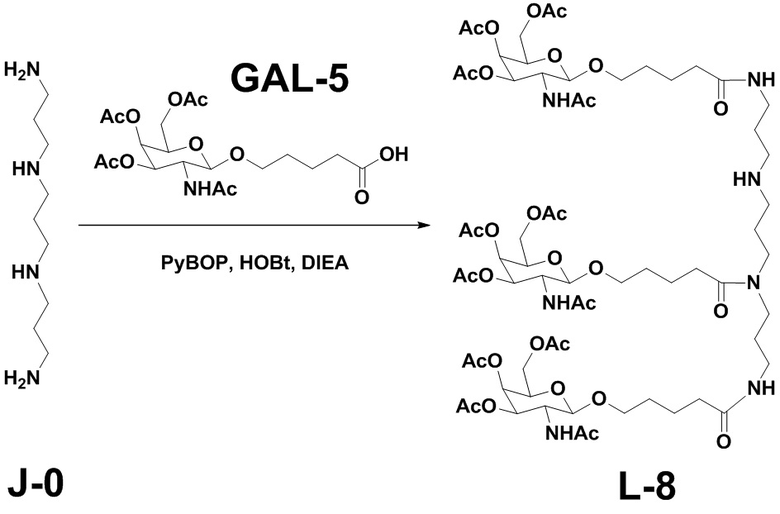
J-0 (9,886 г, 52,5 ммоль, приобретен у AlfaAesar) и GAL-5 (72,819 г, 162,75 ммоль, получен путем объединения продуктов нескольких партий), полученный на стадии (1-1-1), растворяли в 525 мл дихлорметана, добавляли диизопропилэтиламин (DIEA, 44,782 г, 346,50 ммоль), бензотриазол-1-ил-окситрипирролидинофосфония гексафторфосфат (PyBop, 90,158 г, 173,25 ммоль) и гидроксибензотриазол (HOBt, 23,410 г, 173,25 ммоль) для проведения взаимодействия при комнатной температуре в течение 4 часов, а затем добавляли 20 мл насыщенного бикарбоната натрия и 200 мл насыщенного рассола для промывки. Водную фазу дважды экстрагировали, каждый раз с помощью 100 мл дихлорметана, и полученные органические фазы объединяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении с получением неочищенного продукта. Неочищенный продукт очищали с помощью нормально-фазовой колонки с силикагелем (200-300 меш). В колонку вносили 10 мас.% триэтиламина для нейтрализации кислотности силикагеля, уравновешивали 1 мас.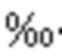 триэтиламина и элюировали в режиме градиентного элюирования смесью дихлорметан:метанол в соотношении от 100:30 до 100:40. Собирали элюат и удаляли растворитель с помощью выпаривания при пониженном давлении с получением 38,8 г чистого продукта L-8. 1H ЯМР (400 МГц, ДМСО) δ 7,84 (d, J = 9,0 Гц, 3H), 7,27 - 7,23 (m, 1H), 7,13 - 7,18 (m, 1H), 5,22 (d, J = 3,1 Гц, 3H), 4,97 (dd, J = 11,3, 3,1 Гц, 3H), 4,48 (d, J = 8,4 Гц, 3H), 4,09 - 3,98 (m, 9H), 3,88 (dd, J = 19,3, 9,3 Гц, 3H), 3,75 - 3,66 (m, 3H), 3,44 - 3,38 (m, 3H), 3,17 - 3,30 (m, 4H), 3,10 - 2,97 (m, 4H), 2,35 - 2,20 (m, 6H), 2,15 - 2,08 (m, 9H), 2,07 - 1,98 (m, 13H), 1,94 - 1,87 (m, 9H), 1,81 - 1,74 (m, 9H), 1,65 - 1,42 (m, 18H). МС m/z: C85H119N7O30, [M+H]+, рассчитано: 1477,59, измерено: 1477,23.
триэтиламина и элюировали в режиме градиентного элюирования смесью дихлорметан:метанол в соотношении от 100:30 до 100:40. Собирали элюат и удаляли растворитель с помощью выпаривания при пониженном давлении с получением 38,8 г чистого продукта L-8. 1H ЯМР (400 МГц, ДМСО) δ 7,84 (d, J = 9,0 Гц, 3H), 7,27 - 7,23 (m, 1H), 7,13 - 7,18 (m, 1H), 5,22 (d, J = 3,1 Гц, 3H), 4,97 (dd, J = 11,3, 3,1 Гц, 3H), 4,48 (d, J = 8,4 Гц, 3H), 4,09 - 3,98 (m, 9H), 3,88 (dd, J = 19,3, 9,3 Гц, 3H), 3,75 - 3,66 (m, 3H), 3,44 - 3,38 (m, 3H), 3,17 - 3,30 (m, 4H), 3,10 - 2,97 (m, 4H), 2,35 - 2,20 (m, 6H), 2,15 - 2,08 (m, 9H), 2,07 - 1,98 (m, 13H), 1,94 - 1,87 (m, 9H), 1,81 - 1,74 (m, 9H), 1,65 - 1,42 (m, 18H). МС m/z: C85H119N7O30, [M+H]+, рассчитано: 1477,59, измерено: 1477,23.
(1-1-3a) Синтез A-1

DMTrCl (хлорид 4,4'-диметокситритила, 101,65 г, 300 ммоль) растворяли в 1000 мл безводного пиридина и добавляли гидрат DL-глицерата кальция (28,63 г, 100 ммоль) для проведения взаимодействия при 45°C в течение 20 часов. Реакционный раствор фильтровали. Остаток промывали с помощью 200 мл DCM и концентрировали фильтрат досуха при пониженном давлении. Остаток повторно растворяли в 500 мл дихлорметана и дважды промывали, каждый раз с помощью 200 мл 0,5 М фосфата триэтиламина (pH=7-8). Выделенную водную фазу дважды экстрагировали, каждый раз с помощью 200 мл дихлорметана. Все органические фазы объединяли, сушили с помощью безводного сульфата натрия и фильтровали. Растворитель удаляли с помощью выпаривания при пониженном давлении, и остаток очищали с помощью нормально-фазовой колонки с силикагелем (200-300 меш), которую элюировали в режиме градиентного элюирования смесью петролейный эфир:этилацетат:дихлорметан:метанол в соотношении от 1:1:1:0,35 до 1:1:1:0,55. Собирали элюат и удаляли растворитель с помощью выпаривания при пониженном давлении. Остаток повторно растворяли в 600 мл дихлорметана и однократно промывали с помощью 200 мл 0,5 М фосфата триэтиламина. Выделенную водную фазу однократно экстрагировали с помощью 200 мл дихлорметана. Все органические фазы объединяли, сушили с помощью безводного сульфата натрия и фильтровали. Растворитель удаляли с помощью выпаривания при пониженном давлении и в течение ночи при пониженном давлении, создаваемом вакуумным масляным насосом, с получением 50,7 г продукта A-1 в виде белого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ 7,46 (ddd, J = 6,5, 2,3, 1,1 Гц, 1H), 7,40 - 7,28 (m, 7H), 6,89 - 6,81 (m, 4H), 4,84 (d, J = 5,0 Гц, 1H), 4,36 - 4,24 (m, 1H), 4,29 (s, 6H), 3,92 (dd, J = 12,4, 7,0 Гц, 1H), 3,67 (dd, J = 12,3, 7,0 Гц, 1H), 2,52 (q, J = 6,3 Гц, 6H), 1,03 (t, J = 6,3 Гц, 9H). МС m/z: C24H23O6, [M-H]-, рассчитано: 407,15, измерено: 406,92.
(1-1-3b) Синтез L-7

L-8 (40 г, 27,09 ммоль, получен путем объединения продуктов нескольких партий), полученный на стадии (1-1-2), и A-1 (41,418 г, 81,27 ммоль), полученный на стадии (1-1-3a), смешивали и растворяли в 271 мл дихлорметана, добавляли 3-(диэтоксифосфорилокси)-1,2,3-бензотриазин-4(3H)-он (DEPBT, 24,318 г, 81,37 ммоль), а затем добавляли диизопропилэтиламин (21,007 г, 162,54 ммоль) для проведения взаимодействия при перемешивании при 25°C в течение 1,5 часов. Органическую фазу промывали с помощью 800 мл насыщенного раствора бикарбоната натрия. Выделенную водную фазу трижды экстрагировали, каждый раз с помощью 50 мл дихлорметана. Органическую фазу промывали с помощью 150 мл насыщенного рассола, а водную фазу однократно экстрагировали с помощью 50 мл дихлорметана. Полученные органические фазы объединяли и сушили с помощью безводного сульфата натрия. Растворитель удаляли с помощью выпаривания при пониженном давлении, а остаток сушили во вспененном состоянии с помощью вакуумного масляного насоса в течение ночи с получением неочищенного продукта. Неочищенный продукт подвергали очистке на колонке. Колонку заполняли 2 кг силикагеля с нормальной фазой (200-300 меш), добавляли 200 мл триэтиламина для нейтрализации кислотности силикагеля, уравновешивали петролейным эфиром, содержащим 1 мас.% триэтиламина, и элюировали в режиме градиентного элюирования смесью петролейный эфир:этилацетат:дихлорметан:N,N-диметилформамид в соотношении от 1:1:1:0,5 до 1:1:1:0,6. Собирали элюат и удаляли растворитель с помощью выпаривания при пониженном давлении с получением 40,4 г чистого продукта L-7. 1H ЯМР (400 МГц, ДМСО) δ 7,90 - 7,78 (m, 4H), 7,75 - 7,64 (m, 1H), 7,38 - 7,18 (m, 9H), 6,91 - 6,83 (m, 4H), 5,25 - 5,10 (m, 4H), 4,97 (dd, J = 11,2, 3,2 Гц, 3H), 4,48 - 4,30 (m, 4H), 4,02 (s, 9H), 3,93 - 3,84 (m, 3H), 3,76 - 3,66 (m, 9H), 3,45 - 3,35 (m, 3H), 3,24 - 2,98 (m, 10H), 2,30 - 2,20 (m, 2H), 2,11 - 1,88 (m, 31H), 1,80 - 1,40 (m, 28H). МС m/z: C90H128N7O35, [M-DMTr]+, рассчитано: 1564,65, измерено: 1564,88.
(1-1-4) Синтез L-9

L-7 (40 г, 21,4247 ммоль), полученный на стадии (1-1-3b), янтарный ангидрид (4,288 г, 42,8494 ммоль) и 4-диметиламинопиридин (DMAP, 5,235 г, 42,8494 ммоль) смешивали и растворяли в 215 мл дихлорметана, затем добавляли диизопропилэтиламин (DIPEA, 13,845 г, 107,1235 ммоль) и перемешивали при 25°C в течение 24 часов. Реакционный раствор промывали с помощью 800 мл 0,5 М фосфата триэтиламина. Водную фазу трижды экстрагировали, каждый раз с помощью 5 мл дихлорметана. Все органические фазы объединяли и выпаривали растворитель при пониженном давлении с получением неочищенного продукта. Неочищенный продукт подвергали очистке на колонке. Колонку заполняли 1 кг силикагеля с нормальной фазой (200-300 меш), добавляли 1 мас.% триэтиламина для нейтрализации кислотности силикагеля, уравновешивали дихлорметаном и элюировали в режиме градиентного элюирования смесью дихлорметан (содержащий 1 мас.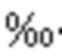 триэтиламина):метанол в соотношении от 100:18 до 100:20. Собирали элюат и выпаривали растворитель при пониженном давлении с получением 31,0 г чистого продукта конъюгирующей молекулы L-9. 1H ЯМР (400 МГц, ДМСО) δ 8,58 (d, J = 4,2 Гц, 1H), 7,94 - 7,82 (m, 3H), 7,41 - 7,29 (m, 5H), 7,22 (d, J = 8,1 Гц, 5H), 6,89 (d, J = 8,3 Гц, 4H), 5,49 - 5,37 (m, 1H), 5,21 (d, J = 3,0 Гц, 3H), 4,97 (d, J = 11,1 Гц, 3H), 4,49 (d, J = 8,2 Гц, 3H), 4,02 (s, 9H), 3,88 (dd, J = 19,4, 9,4 Гц, 3H), 3,77 - 3,65 (m, 9H), 3,50 - 3,39 (m, 6H), 3,11 - 2,90 (m, 5H), 2,61 - 2,54 (m, 4H), 2,47 - 2,41 (m, 2H), 2,26 - 2,17 (m, 2H), 2,15 - 1,95 (m, 22H), 1,92 - 1,84 (m, 9H), 1,80 - 1,70 (m, 10H), 1,65 - 1,35 (m, 17H), 1,31 - 1,19 (m, 4H), 0,96 (t, J = 7,1 Гц, 9H). МС m/z: C94H132N7O38, [M-DMTr]+, рассчитано: 1664,72, измерено: 1665,03.
триэтиламина):метанол в соотношении от 100:18 до 100:20. Собирали элюат и выпаривали растворитель при пониженном давлении с получением 31,0 г чистого продукта конъюгирующей молекулы L-9. 1H ЯМР (400 МГц, ДМСО) δ 8,58 (d, J = 4,2 Гц, 1H), 7,94 - 7,82 (m, 3H), 7,41 - 7,29 (m, 5H), 7,22 (d, J = 8,1 Гц, 5H), 6,89 (d, J = 8,3 Гц, 4H), 5,49 - 5,37 (m, 1H), 5,21 (d, J = 3,0 Гц, 3H), 4,97 (d, J = 11,1 Гц, 3H), 4,49 (d, J = 8,2 Гц, 3H), 4,02 (s, 9H), 3,88 (dd, J = 19,4, 9,4 Гц, 3H), 3,77 - 3,65 (m, 9H), 3,50 - 3,39 (m, 6H), 3,11 - 2,90 (m, 5H), 2,61 - 2,54 (m, 4H), 2,47 - 2,41 (m, 2H), 2,26 - 2,17 (m, 2H), 2,15 - 1,95 (m, 22H), 1,92 - 1,84 (m, 9H), 1,80 - 1,70 (m, 10H), 1,65 - 1,35 (m, 17H), 1,31 - 1,19 (m, 4H), 0,96 (t, J = 7,1 Гц, 9H). МС m/z: C94H132N7O38, [M-DMTr]+, рассчитано: 1664,72, измерено: 1665,03.
(1-1-5) Синтез соединения L-10:

На этой стадии получали соединение L-10 путем связывания конъюгирующей молекулы L-9 с твердофазной подложкой.
Конъюгирующую молекулу L-9 (22,751 г, 11 ммоль), полученную на стадии (1-1-4), O-бензотриазол-1-ил-тетраметилурония гексафторфосфат (HBTU, 6,257 г, 16,5 ммоль) и диизопропилэтиламин (DIEA, 2,843 г, 22 ммоль) смешивали, растворяли в 900 мл ацетонитрила и перемешивали при комнатной температуре в течение 5 минут. К реакционному раствору добавляли аминометиловую смолу (88 г, 100-200 меш, содержание аминогрупп: 400 мкмоль/г, приобретена у Tianjin Nankai HECHENG S&T Co., Ltd.). Реакцию проводили на шейкере при 25°C и 150 об/мин в течение 18 часов с последующей фильтрацией. Остаток дважды промывали, каждый раз с помощью 300 мл DCM, и трижды промывали, каждый раз с помощью 300 мл ацетонитрила, и сушили в течение 18 часов с помощью вакуумного масляного насоса. Затем проводили реакцию кэпирования путем добавления исходных веществ (CapA, CapB, 4-диметиламинопиридина (DMAP) и ацетонитрила) в соответствии с соотношением, приведенным в таблице 2. Реакцию проводили на шейкере при 25°C и 150 об/мин в течение 5 часов. Реакционный раствор фильтровали. Остаток трижды промывали, каждый раз с помощью 300 мл ацетонитрила, растворитель выпаривали досуха и сушили смесь в течение ночи при пониженном давлении с помощью вакуумного масляного насоса с получением 102 г соединения L-10 (т. е. конъюгирующей молекулы L-9, связанной с твердофазной подложкой), с содержанием 90,8 мкмоль/г.
Таблица 2. Соотношение исходных веществ в реакции кэпирования
В приведенной выше таблице CapA и CapB представляют собой растворы кэпирующих агентов. CapA представляет собой 20 об.% раствор N-метилимидазола в смеси пиридин/ацетонитрил, где объемное отношение пиридина к ацетонитрилу составляет 3:5. CapB представляет собой 20 об.% раствор уксусного ангидрида в ацетонитриле.
(1-2) Синтез смысловой цепи конъюгата 1
Нуклеозидные мономеры последовательно связывали в направлении от 3’ к 5’ в соответствии с последовательностью расположения нуклеотидов в смысловой цепи методом твердофазного фосфоамидитного синтеза, циклы начинали с соединения L-10, полученного на вышеописанной стадии, для синтеза смысловой цепи SS конъюгата 1 из таблицы 3. Связывание каждого нуклеозидного мономера включало четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления или сульфуризации. Когда два нуклеотида были связаны посредством фосфоэфира, четырехстадийную реакцию снятия защиты, сочетания, кэпирования и окисления проводили во время связывания следующего нуклеозидного мономера. Когда два нуклеотида были связаны посредством тиофосфата, четырехстадийную реакцию снятия защиты, сочетания, кэпирования и сульфуризации проводили во время связывания следующего нуклеозидного мономера. Условия синтеза были заданы следующим образом.
Нуклеозидные мономеры были предоставлены в 0,1 М растворе ацетонитрила. Условия реакции снятия защиты были идентичными на всех стадиях, т. е. температура 25°C, продолжительность проведения реакции 70 секунд, раствор дихлоруксусной кислоты в дихлорметане (3% об./об.) в качестве агента для снятия защиты и молярное отношение дихлоруксусной кислоты к 4,4'-диметокситритильной защитной группе на твердофазной подложке, равное 5:1.
Условия реакции сочетания были идентичными на всех стадиях и включали температуру 25°C, молярное отношение последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, к нуклеозидным мономерам, равное 1:10, молярное отношение последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, к агенту реакции сочетания, равное 1:65, продолжительность проведения реакции 600 секунд и 0,5 М раствор 5-этилтио-1H-тетразола (ETT) в ацетонитриле в качестве агента реакции сочетания.
Условия реакции кэпирования были идентичными на всех стадиях и включали температуру 25°C и продолжительность проведения реакции 15 секунд. Кэпирующий агент представлял собой смешанный раствор Cap A и Cap B в молярном отношении 1:1, и молярное отношение кэпирующего агента к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой, составляло 1:1:1 (ангидрид:N-метилимидазол:последовательность нуклеиновой кислоты, связанная с твердофазной подложкой).
Условия реакции окисления были идентичными на всех стадиях и включали температуру 25°C, продолжительность проведения реакции 15 секунд и 0,05 М иодную воду в качестве окисляющего агента. Молярное отношение иода к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой на стадии сочетания, составляло 30:1. Реакцию проводили в смешанном растворителе, в котором отношение тетрагидрофуран:вода:пиридин составляло 3:1:1.
Условия реакции сульфуризации были идентичными на всех стадиях и включали температуру 25°C, продолжительность проведения реакции 300 секунд и гидрид ксантана в качестве агента для сульфуризации. Молярное отношение агента для сульфуризации к последовательности нуклеиновой кислоты, связанной с твердофазной подложкой на стадии сочетания, составляло 120:1. Реакцию проводили в смешанном растворителе, в котором отношение ацетонитрил: пиридин составляло 1:1.
После связывания последнего нуклеозидного мономера последовательность нуклеиновой кислоты, связанную с твердофазной подложкой, отщепляли, снимали защиту, очищали и обессоливали, а затем лиофилизировали с получением смысловой цепи, где
условия отщепления и снятия защиты были следующими: добавление синтезированной нуклеотидной последовательности, связанной с подложкой, в 25 мас.% водный раствор аммиака для проведения взаимодействия в течение 16 часов при 55°C, где количество водного раствора аммиака составляло 0,5 мл/мкмоль; фильтрация для удаления подложки и концентрирование супернатанта в вакууме досуха.
Условия очистки и обессоливания были следующими: очистка нуклеиновой кислоты с помощью колонки для препаративной ионообменной хроматографии (Source 15Q) с градиентным элюированием NaCl. В частности, элюент A: 20 мМ фосфат натрия (pH = 8,1), растворитель: вода/ацетонитрил = 9:1 (об./об.); элюент B: 1,5 М хлорид натрия, 20 мМ фосфат натрия (pH = 8,1), растворитель: вода/ацетонитрил = 9:1 (об./об.); градиент элюирования: элюент A:элюент B = от 100:0 до 50:50. Элюат собирали, объединяли и обессоливали, используя колонку для очистки методом обращенно-фазовой хроматографии. Конкретные условия включали использование колонки с Sephadex (наполнитель: Sephadex-G25) для обессоливания и деионизированной воды для элюирования.
Метод обнаружения представлял собой следующий: определение чистоты вышеописанной смысловой цепи методом ионообменной хроматографии (ИОХ-ВЭЖХ); и анализ молекулярной массы методом жидкостной хроматографии с масс-спектрометрией (ЖХ-МС). Измеренное значение соответствовало рассчитанному значению, что свидетельствует о синтезировании смысловой цепи SS, конъюгированной с конъюгирующей молекулой L-9 на 3’-конце.
(1-3) Синтез антисмысловой цепи конъюгата 1
Антисмысловую цепь AS конъюгата 1 из таблицы 3 синтезировали, начиная циклы с использованием универсальной твердофазной подложки (твердофазные подложки NittoPhase®HL, загруженные UnyLinker™, Kinovate Life Sciences Inc.) в соответствии с методом твердофазного амидофосфитного синтеза. В методе твердофазного синтеза использовали те же условия проведения реакций снятия защиты, сочетания, кэпирования, окисления или сульфуризации, и те же условия отщепления и снятия защиты, очистки и обессоливания, как при синтезе смысловой цепи. Отличие заключалось в том, что антисмысловая цепь содержала 5’-фосфорную кислоту на первом нуклеотиде с 5’-конца. Поэтому в процессе получения антисмысловой цепи в соответствии с методом твердофазного амидофосфитного синтеза после связывания последнего нуклеозидного мономера антисмысловой цепи мономер CPR-I (Suzhou GenePharma, арт. № кат. № 13-2601-XX) был связан с 5’-концом антисмысловой цепи с образованием 5’-фосфоэфирной модификации посредством четырех стадий снятия защиты, сочетания, кэпирования и окисления.

(CPR-I)
Для этого связывания использовали те же условия проведения реакций снятия защиты, сочетания, кэпирования и окисления, и те же условия отщепления и снятия защиты, очистки и обессоливания, как при синтезе смысловой цепи. Остаток лиофилизировали с получением в результате антисмысловой цепи. Чистоту антисмысловой цепи определяли методом ионообменной хроматографии (ИОХ-ВЭЖХ), а молекулярную массу анализировали методом жидкостной хроматографии с масс-спектрометрией (ЖХ-МС). Измеренное значение соответствовало рассчитанному значению, что свидетельствует о синтезировании антисмысловой цепи AS, имеющей целевую последовательность.
(1-4) Синтез конъюгата 1
Смысловую цепь и антисмысловую цепь соответственно растворяли в воде для инъекций с получением раствора 40 мг/мл, смешивали в эквимолярном соотношении, нагревали при 50°C в течение 15 минут, а затем охлаждали при комнатной температуре, в результате чего получали отожженный продукт, а затем лиофилизировали с получением лиофилизированного порошка. Конъюгат разбавляли до концентрации 0,2 мг/мл сверхчистой водой (приготовленной с помощью установки для получения сверхчистой воды Milli-Q, с удельным сопротивлением 18,2 МОм*см (25°C)). Молекулярную массу измеряли методом жидкостной хроматографии с масс-спектрометрией (ЖХ-МС, прибор приобретен у Waters Corp., модель: LCT Premier). Поскольку измеренное значение соответствовало рассчитанному значению, было подтверждено, что синтезированный конъюгат 1 представлял собой целевую разработанную последовательность двухцепочечной нуклеиновой кислоты с конъюгирующей молекулой L-9. Структура конъюгата 1 соответсвовала представленной в Формуле (403), последовательность конъюгированной миРНК соответствует последовательности конъюгата 1 (т. е. L10-siC5a1M1SP), как показано в таблице 3.
Пример получения 2. Получение конъюгатов 2-8
Конъюгаты 2-6, представленные в таблице 3, синтезировали тем же способом, как в Примере получения 1, и определяли молекулярные массы. Отличие заключалось в том, что последовательности смысловых цепей и антисмысловых цепей, использованные в синтезе, представляли собой последовательности, представленные в таблице 3, соответствующие смысловым цепям и антисмысловым цепям конъюгированных миРНК в конъюгате 2, конъюгате 3, конъюгате 4, конъюгате 5 или конъюгате 6, соответственно, и в результате получили конъюгаты 2-6, соответственно.
Конъюгаты 7-8, представленные в таблице 3, синтезировали тем же способом, как в Примере получения 1, и определяли молекулярные массы. Отличие заключалось в том, что последовательности смысловых цепей и антисмысловых цепей, использованные в синтезе, представляли собой последовательности, представленные в таблице 3, соответствующие смысловым цепям и антисмысловым цепям конъюгированных миРНК в конъюгате 7 или конъюгате 8, соответственно, при этом антисмысловые цепи конъюгата 7 и конъюгата 8 не имеют 5’-фосфорной кислоты на первых нуклеотидах с их 5’-концов по сравнению с антисмысловой цепью конъюгата 1. Следовательно, в процессе получения антисмысловых цепей в соответствии с методом твердофазного амидофосфитного синтеза нет необходимости связывать мономер CPR-I после связывания последнего нуклеозидного мономера антисмысловой цепи, с получением конъюгатов 7-8, соответственно.
В таблице 3 перечислены номера конъюгатов и составы последовательностей миРНК.
Таблица 3. Конъюгаты миРНК
Пример получения 3. Синтез последовательности миРНК
миРНК 1, представленную в таблице 4a, синтезировали тем же способом, как в Примере получения 1, с тем отличием, что:
1) для смысловой цепи циклы начинали с использованием универсальной твердофазной подложки (твердофазные подложки NittoPhase®HL, загруженные UnyLinker™, Kinovate Life Sciences Inc.); и
2) для антисмысловой цепи, по сравнению с последовательностью антисмысловой цепи миРНК, конъюгированной в конъюгате 1, первый нуклеотид на 5’-конце миРНК 1 не содержал 5’-фосфорную кислоту. Следовательно, в процессе получения антисмысловых цепей в соответствии с методом твердофазного амидофосфитного синтеза не было необходимости связывать мономер CPR-I после связывания последнего нуклеозидного мономера антисмысловой цепи.
Таким образом была получена миРНК 1.
миРНК 2-6 синтезировали тем же способом, что и миРНК 1, с тем отличием, что последовательности смысловых цепей и антисмысловых цепей миРНК, используемых в синтезе, представляли собой последовательности, представленные в таблице 4, соответствующие смысловым цепям и антисмысловым цепям миРНК 2, миРНК 3, миРНК 4, миРНК 5 или миРНК 6, соответственно, и в результате получили миРНК 2-6, соответственно.
В таблице 4a перечислены номера миРНК и составы последовательностей миРНК.
Таблица 4a. Последовательности миРНК
Пример получения 4. Синтез конъюгатов Cy5-меченых миРНК и Cy5-меченых миРНК
(4-1) Синтез Cy5-конъюгата 1 и Cy5-конъюгата 2
Cy5-конъюгат 1, представленный в таблице 4b, синтезировали тем же способом, как в Примере получения 1, и определяли молекулярную массу. Отличие заключалось в том, что последовательности смысловой цепи и антисмысловой цепи, использованные в синтезе, представляли собой последовательности, представленные в таблице 4b, соответствующие смысловой цепи и антисмысловой цепи миРНК, конъюгированной в Cy5-конъюгате 1, при этом (1): флуоресцентная группа Cy5 была ковалентно связана с 5’-концом смысловой цепи миРНК, конъюгированной в Cy5-конъюгате 1. Следовательно, в процессе получения смысловой цепи в соответствии с методом твердофазного амидофосфитного синтеза, описанным на стадии (1-2) Примера получения 1, после связывания последнего нуклеозидного мономера смысловой цепи необходимо было связать мономер амидофосфитного производного Cy5 (приобретен у Shanghai HonGene Biotech, арт. № OP-057) с 5’-концом смысловой цепи посредством четырехстадийной реакции снятия защиты, сочетания, кэпирования и окисления; и (2) первый нуклеотид на 5’-конце миРНК, конъюгированной в Cy5-конъюгате 1, не содержал 5’-фосфорной кислоты; следовательно, в процессе получения антисмысловых цепей в соответствии с методом твердофазного амидофосфитного синтеза, описанным на стадии (1-3) Примера получения 1, не было необходимости связывать мономер CPR-I после связывания последнего нуклеозидного мономера антисмысловой цепи.
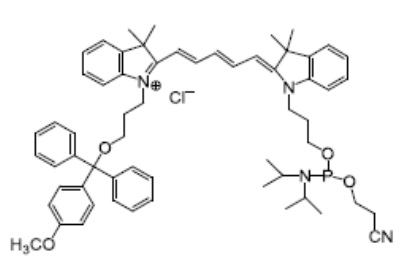
(мономер амидофосфитного производного Cy5)
В процессе связывания мономера амидофосфитного производного Cy5 с 5’-концом смысловой цепи использовали те же условия проведения реакций снятия защиты, сочетания, кэпирования и окисления, как описано для синтеза смысловой цепи на стадии (1-2) Примера получения 1, и отличия заключались в том, что: 1) продолжительность проведения реакции снятия защиты была увеличена до 300 секунд; и 2) продолжительность проведения реакции сочетания Cy5 была увеличена до 900 секунд.
Затем, условия отщепления и снятия защиты со смысловой цепи были следующими: добавление синтезированной нуклеотидной последовательности, связанной с подложкой, в раствор AMA (смешанный раствор 40 мас.% водного раствора метиламина и 25 мас.% водного раствора аммиака в объемном отношении 1:1), где количество раствора AMA составляло 0,5 мл/мкмоль, проведение взаимодействия в течение 2 часов на водяной бане при 25°C, удаление оставшейся подложки фильтрацией и концентрирование супернатанта досуха в вакууме. Условия очистки и обессоливания смысловой цепи были такими же, как при синтезе смысловой цепи на стадии (1-2) в Примере получения 1. Затем остаток лиофилизировали с получением смысловой цепи Cy5-конъюгата 1.
Таким образом, был получен Cy5-конъюгат 1, и флуоресцентная группа Cy5 была ковалентно связана с 5’-концом смысловой цепи миРНК в составе конъюгата миРНК, которая имела последовательности смысловой цепи и антисмысловой цепи, представленные в таблице 4b, соответствующие Cy5-конъюгату 1.
Cy5-конъюгат 2 получали тем же способом, что и Cy5-конъюгат 1, и определяли молекулярную массу. Отличие заключалось в том, что последовательности смысловых цепей и антисмысловых цепей, использованные в синтезе, представляли собой последовательности, представленные в таблице 4b, соответствующие смысловой цепи и антисмысловой цепи миРНК, конъюгированных в Cy5-конъюгате 2, соответственно, и в результате получили Cy5-конъюгат 2.
(4-2) Синтез Cy5-миРНК 1 и Cy5-миРНК 2
Cy5-миРНК 1 получали тем же способом, что и Cy5-конъюгат 1, и определяли молекулярную массу. Отличие заключалось в том, что циклы начинали с использованием универсальной твердофазной подложки (твердофазные подложки NittoPhase®HL, загруженные UnyLinker™, Kinovate Life Sciences Inc.), и в результате получили Cy5-миРНК 1.
Cy5-миРНК 2 получали тем же способом, что и Cy5-миРНК 1, и определяли молекулярную массу. Отличие заключалось в том, что последовательности смысловых цепей и антисмысловых цепей, использованные в синтезе, представляли собой последовательности, представленные в таблице 4b, соответствующие смысловой цепи и антисмысловой цепи Cy5-миРНК, соответственно, и в результате получили Cy5-миРНК 2.
В таблице 4b перечислены номера и последовательности миРНК Cy5-конъюгата 1, Cy5-конъюгата 2, Cy5-миРНК 1 и Cy5-миРНК 2.
Таблица 4b. Последовательности миРНК в конъюгатах Cy5-меченых миРНК и Cy5-меченых миРНК
Экспериментальный пример 1. Определение IC50 конъюгата миРНК в отношении мРНК C5 в клетках HepG2
Клетки HepG2 (приобретенные у Nanjing COBIOER Biotechnology Co., Ltd.) культивировали в полной среде H-DMEM (от компании HyClone), содержащей 10% фетальной бычьей сыворотки (FBS, от компании RMBIO) и 0,2 об.% пенициллин-стрептомицина (от компании HyClone), при 37°C в инкубаторе, содержащем 5% CO2/95% воздуха.
Клетки HepG2 высевали в 24-луночный планшет из расчета 7x104 клеток/лунка. Через 16 часов, когда конфлюэнтность клеток достигла 70-80%, из культуральных лунок аспирировали полную среду H-DMEM и добавляли в каждую лунку 500 мкл среды Opti-MEM (от компании GIBCO) для продолжения культивирования в течение 1,5 часов.
Из каждого из конъюгата 1, конъюгата 2, конъюгата 3, конъюгата 4, конъюгата 5, конъюгата 6, конъюгата 7 и конъюгата 8 готовили рабочие растворы конъюгата с 7 различными концентрациями, включавшими 20 мкМ, 5 мкМ, 1,25 мкМ, 0,313 мкМ, 0,0781 мкМ, 0,0195 мкМ и 0,0049 мкМ (в пересчете на миРНК), в обработанной ДЭПК (диэтилпирокарбонатом) воде, соответственно.
Для каждого конъюгата готовили раствор A1-A7, и каждый раствор содержал 3 мкл рабочего раствора конъюгата с 7 концентрациями, как показано выше, и 50 мкл среды Opti-MEM.
Отдельно готовили раствор B для каждого конъюгата, и каждый раствор B содержал 1 мкл Lipofectamine™ 2000 и 50 мкл среды Opti-MEM.
Для каждого конъюгата последовательно смешивали одну порцию раствора B с одной порцией раствора A1-A7, а затем инкубировали в течение 20 минут при комнатной температуре для получения трансфекционных комплексов X1-X7. Для каждого трансфекционного комплекса готовили две порции.
Одну порцию раствора B смешивали с 50 мкл среды Opti-MEM и инкубировали в течение 20 минут при комнатной температуре для получения трансфекционного комплекса X8. Готовили четыре порции трансфекционного комплекса.
Трансфекционные комплексы X1-X7, соответствующие каждому из конъюгатов, добавляли в вышеуказанные культуральные лунки для культивирования клеток HepG2 из расчета 100 мкл/лунка и равномерно перемешивали с получением трансфекционных смесей с конечными концентрациями (в пересчете на миРНК) 100 нМ, 25 нМ, 6,25 нМ, 1,56 нМ, 0,391 нМ, 0,098 нМ и 0,024 нМ, соответственно. Два трансфекционных комплекса X1-X7 с одинаковой концентрацией добавляли в две разные культуральные лунки для получения трансфекционных смесей, содержащих конъюгаты, которые были помечены как тестовые группы 1-7.
В остальные четыре культуральные лунки добавляли одну порцию трансфекционного комплекса X8 из расчета 100 мкл/лунка для получения трансфекционной смеси без конъюгата, которая была помечена как контрольная группа.
После инкубации трансфекционной смеси, содержащей конъюгат, и трансфекционной смеси без конъюгата с клетками в культуральных лунках в течение 4 часов в каждую лунку вносили добавку 1 мл полной среды H-DMEM, содержащей 20% FBS. 24-луночный планшет помещали в инкубатор, содержащий 5% CO2/95% воздуха, на 24 часа.
Затем использовали RNAVzol (приобретен у Vigorous Biotechnology Beijing Co., Ltd., арт. № N002) для выделения тотальной РНК из клеток в каждой лунке в соответствии с этапами процесса выделения тотальной РНК в инструкции по применению.
В качестве матрицы для обратной транскрипции для клеток в каждой лунке брали 1 мкг тотальной РНК и использовали реагенты из набора для проведения обратной транскрипции Goldenstar™ RT6 cDNA Synthesis Kit (приобретен у Beijing Tsingke Biotechnology Co., Ltd., арт. № TSK301M), в котором в качестве праймера был выбран Goldenstar™ Oligo (dT)17, и готовили 20 мкл реакционной системы для обратной транскрипции в соответствии с этапами процесса проведения обратной транскрипции в инструкции к набору, для ревертирования тотальной РНК клеток из каждой лунки. Условия проведения реакции обратной транскрипции были следующими: реакционную систему для обратной транскрипции инкубировали при 50°C в течение 50 минут, затем инкубировали при 85°C в течение 5 минут и, наконец, инкубировали при 4°C в течение 30 секунд. После проведения реакции в реакционную систему для обратной транскрипции добавляли 80 мкл обработанной ДЭПК воды для получения раствора, содержащего кДНК.
Для каждой реакционной системы для обратной транскрипции в качестве матрицы для кПЦР брали 5 мкл раствора, содержащего кДНК, и готовили 20 мкл реакционной системы для кПЦР, используя реагент из набора NovoStart® SYBR qPCR SuperMix Plus (приобретен у Novoprotein Science and Technology Co., Ltd., арт. № E096-01B), где последовательности ПЦР-праймеров для амплификации гена-мишени C5 и гена GAPDH внутреннего контроля представлены в таблице 5, и конечная концентрация каждого праймера составляла 0,25 мкМ. Реакционную систему для кПЦР помещали на прибор для проведения ПЦР в реальном времени StepOnePlus от ABI и проводили трехэтапный процесс амплификации. Процедура амплификации включала предварительную денатурацию при 95°С в течение 10 минут, затем денатурацию при 95°С в течение 30 секунд, отжиг при 60°С в течение 30 секунд и элонгацию при 72°С в течение 30 секунд. После 40-кратного повторения вышеуказанных процессов денатурации, отжига и элонгации был получен продукт W, содержащий амплифицированный ген-мишень C5 и ген GAPDH внутреннего контроля. Затем продукт W поочередно инкубировали при 95°C в течение 15 секунд, 60°C в течение 1 минуты и 95°C в течение 15 секунд. Кривые плавления гена-мишени C5 и гена GAPDH внутреннего контроля в продукте W регистрировали с помощью количественной ПЦР в реальном времени с флуоресцентным детектированием, и получали значения Ct (пороговое число циклов) для гена-мишени C5 и гена GAPDH внутреннего контроля.
Таблица 5. Последовательности праймеров для определения
(SEQ ID NO: 387)
(SEQ ID NO: 388)
Сравнительный метод оценки Ct (ΔΔCt) использовали для относительной количественной оценки экспрессии гена-мишени C5 в каждой тестовой группе и контрольной группе. Метод расчета был следующим:
ΔCt (тестовая группа) = Ct (ген-мишень тестовой группы) - Ct (ген внутреннего контроля тестовой группы)
ΔCt (контрольная группа) = Ct (ген-мишень контрольной группы) - Ct (ген внутреннего контроля контрольной группы)
ΔΔCt (тестовая группа) = ΔCt (тестовая группа) - ΔCt (контрольная группа)
ΔΔCt (контрольная группа) = ΔCt (контрольная группа) - ΔCt (среднее значение контрольной группы)
где ΔCt (среднее значение контрольной группы) представляло собой среднее арифметическое значение ΔCt (контрольной группы) каждой из четырех культуральных лунок контрольной группы. Таким образом, каждая культуральная лунка каждой тестовой группы соответствовала одной ΔΔCt (тестовая группа), и каждая культуральная лунка контрольной группы соответствовала одной ΔΔCt (контрольная группа).
Уровень экспрессии мРНК C5 в тестовой группе нормировали относительно контрольной группы, где уровень экспрессии мРНК C5 в контрольной группе был принят за 100%.
Относительный уровень экспрессии мРНК C5 в тестовой группе = 2^ (-ΔΔCt (тестовая группа)) × 100%.
На основании относительного уровня экспрессии мРНК C5 в клетках HepG2, трансфицированных разными конъюгатами (конъюгаты 1-8), были получены кривые «доза-эффект» для конъюгатов 1-8, как показано на ФИГ. 1A-1H, путем аппроксимации трехпараметрической моделью «log(inhibitor) vs. response» с помощью программного обеспечения Graphpad 5.0, где логарифм (lg нМ) конечной концентрации конъюгата миРНК откладывали по оси абсцисс, а относительный уровень экспрессии (%) мРНК C5 откладывали по оси ординат, и каждая точка представляла собой среднее значение относительного уровня экспрессии мРНК C5 в двух культуральных лунках тестовой группы по сравнению с контрольной группой.
IC50 каждого конъюгата в отношении мРНК C5 рассчитывали на основании функции, соответствующей аппроксимированной кривой «доза-эффект», где функция представляла собой следующую:
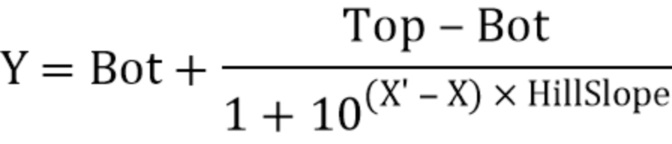
где:
Y представляет собой относительный уровень экспрессии мРНК C5 тестовой группы,
X представляет собой логарифм конечной концентрации конъюгата миРНК,
Bot представляет собой значение Y в нижней области плато,
Top представляет собой значение Y в верхней области плато, и
X' представляет собой значение X, при котором Y представляет собой медианное значение между низом и верхом асимптоты, а HillSlope (угловой коэффициент Хилла) представляет собой наклон кривой при X', который в данном случае определен как -1.
На основе кривой «доза-эффект» и соответствующей функции было определено соответствующее значение X50, когда Y=50%, и было рассчитано значение IC50 каждого конъюгата, составившее 10^X50 (нМ).
Значение IC50 в отношении мРНК C5 и значение R2 аппроксимированной кривой для каждого конъюгата обобщенно представлены в таблице 6.
Таблица 6. Значение IC50 в отношении мРНК C5 и значение R2 аппроксимированной кривой «доза-эффект» для конъюгата миРНК
Из результатов на ФИГ. 1A-1H и в таблице 6 выше можно видеть, что конъюгат миРНК согласно настоящему изобретению обладает высокой ингибирующей активностью в клетках гепатомы HepG2 in vitro, и IC50 составляет от 1,494 нМ до 9,688 нМ.
Экспериментальный пример 2. Распределение конъюгатов миРНК по различным органам мышей C57
Использовали 1 × раствор PBS для растворения соответственно Cy5-миРНК 1, Cy5-конъюгата 1, Cy5-миРНК 2 или Cy5-конъюгата 2 с получением раствора 0,6 мг/мл (в пересчете на миРНК).
Десять самок мышей C57BL/6J возрастом 6-7 недель (приобретенных у Beijing Charles River Laboratory Animal Technology Co., Ltd., для краткости называемых мышами C57) случайным образом разделяли на группы, по две мыши в каждой группе, и подкожно вводили им соответственно 1 × PBS и раствор Cy5-миРНК 1, Cy5-конъюгата 1, Cy5-миРНК 2 или Cy5-конъюгата 2, полученный выше. Вводимые дозы для всех животных рассчитывали в соответствии с их массой тела, а объем введения составлял 5 мл/кг массы тела. В пересчете на миРНК вводимая доза для каждого животного составляла 3 мг/кг массы тела.
Через 2 часа, 6 часов, 24 часа и 48 часов после введения мышей каждой группы помещали в систему оптической визуализации in vivo IVIS Lumina Series III для мелких животных. Мышам проводили ингаляционную анестезию изофлураном и под воздействием анестезии помещали их для визуализации in vivo животом вверх в систему оптической визуализации in vivo для мелких животных для динамического обнаружения сигналов флуоресценции Cy5 и отслеживания распределения Cy5-меченых миРНК или Cy5-меченых конъюгатов у живых животных. Только мыши, которым вводили Cy5-меченые конъюгаты, имели значительно повышенные флуоресцентные сигналы в области их печени, а мыши, которым вводили Cy5-меченые миРНК или 1 × PBS, не имели какого-либо флуоресцентного сигнала в области их печени.
Через 48 часов всех мышей умерщвляли, и извлекали пять органов каждой мыши, включая сердце, легкие, печень, селезенку и почки, для флуоресцентной визуализации в IVIS Lumina Series III. Из каждой группы мышей выбирали одно животное и располагали его вышеупомянутые пять органов поочередно в продольном направлении. Органы мышей, которым вводили 1 × PBS, или Cy5-миРНК 1, или Cy5-конъюгат 1, фотографировали в одном и том же поле зрения, и результаты показаны на ФИГ. 2A. Органы мышей, которым вводили 1 × PBS и Cy5-миРНК 2 или Cy5-конъюгат 2, фотографировали в одном и том же поле зрения, и результаты показаны на ФИГ. 2B.
Из ФИГ. 2A-2B можно видеть, что только Cy5-конъюгат 1 и Cy5-конъюгат 2 способны накапливаться в большом количестве в печени, и Cy5-конъюгат 1 и Cy5-конъюгат 2 в небольшом количестве накоплены в почке, но не накоплены в других органах, что свидетельствует о том, что конъюгат согласно настоящему изобретению способен эффективную доставлять миРНК непосредственно в печень. Кроме того, в сочетании с результатами на ФИГ. 1G (демонстрирующими, что конъюгат 7 обладает более высокой ингибирующей активностью in vitro) и ФИГ. 1F (демонстрирующими, что конъюгат 6 обладает более высокой ингибирующей активностью in vitro), это говорит о том, что конъюгат согласно настоящему изобретению способен специфично ингибировать экспрессию гена-мишени в печени.
Некоторые варианты осуществления настоящего изобретения подробно описаны выше, но настоящее изобретение не ограничено конкретными подробностями вышеописанных вариантов осуществления. Различные простые изменения технического решения согласно настоящему изобретению могут быть сделаны в пределах объема технической концепции настоящего изобретения, и эти простые изменения находятся в пределах объема настоящего изобретения.
Кроме того, следует отметить, что все конкретные технические признаки, описанные в приведенных выше вариантах осуществления, могут комбинироваться любым подходящим образом, при условии, что это не приводит к противоречию. Чтобы избежать ненужного повторения, различные возможные варианты комбинирования дополнительно не будут описаны в настоящем описании.
Кроме того, различные варианты осуществления настоящего изобретения также могут быть реализованы в любой комбинации, при условии, что они не вступают в противоречие с сущностью настоящего изобретения, и такие комбинации также следует рассматривать как часть раскрытия настоящего изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SUZHOU RIBO LIFE SCIENCE CO., LTD.
<120> НУКЛЕИНОВАЯ КИСЛОТА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И КОНЪЮГАТ,
СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ
<130> DSP1V211765ZX
<150> CN201910440575.8
<151> 2019-05-24
<160> 388
<170> PatentIn версии 3.5
<210> 1
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<222> (19)..(19)
<221> misc_feature
<223> n представляет собой Z1, и Z1 представляет собой A
<400> 1
cuucauucau acagacaan
19
<210> 2
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z2, и Z2 представляет собой U
<400> 2
nuugucugua ugaaugaag
19
<210> 3
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z3, и Z3 выбран из A, U, G или C
<400> 3
cuucauucau acagacaan
19
<210> 4
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z4, Z4 представляет собой нуклеотид,
комплементарный Z3, и Z3 выбран из A, U, G или C
<400> 4
nuugucugua ugaaugaag
19
<210> 5
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z3, и Z3 выбран из A, U, G или C
<400> 5
cuucauucau acagacaan
19
<210> 6
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z4, Z4 представляет собой нуклеотид,
комплементарный Z3, и Z3 выбран из A, U, G или C
<400> 6
nuugucugua ugaaugaaga g
21
<210> 7
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z3, и Z3 выбран из A, U, G или C
<400> 7
uucuucauuc auacagacaa n
21
<210> 8
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<222> (1)..(1)
<221> misc_feature
<223> n представляет собой Z4, Z4 представляет собой нуклеотид,
комплементарный Z3, и Z3 выбран из A, U, G или C
<400> 8
nuugucugua ugaaugaaga gaa
23
<210> 9
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 9
cuucauucau acagacaaa
19
<210> 10
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 10
uuugucugua ugaaugaaga g
21
<210> 11
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 11
cucuucauuc auacagacaa a
21
<210> 12
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 12
uuugucugua ugaaugaaga gaa
23
<210> 13
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 13
cuucauucau acagacaaa
19
<210> 14
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 14
uuugucugua ugaaugaaga g
21
<210> 15
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 15
cuucauucau acagacaaa
19
<210> 16
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 16
uuugucugua ugaaugaaga g
21
<210> 17
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 17
cuucauucau acagacaaa
19
<210> 18
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 18
uuugucugua ugaaugaaga g
21
<210> 19
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 19
cucuucauuc auacagacaa a
21
<210> 20
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 20
uuugucugua ugaaugaaga gaa
23
<210> 21
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 21
cucuucauuc auacagacaa a
21
<210> 22
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 22
uuugucugua ugaaugaaga gaa
23
<210> 23
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 23
cucuucauuc auacagacaa a
21
<210> 24
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 24
uuugucugua ugaaugaaga gaa
23
<210> 25
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 25
cuucauucau acagacaaa
19
<210> 26
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 26
uuugucugua ugaaugaaga g
21
<210> 27
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 27
cuucauucau acagacaaa
19
<210> 28
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 28
uuugucugua ugaaugaaga g
21
<210> 29
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 29
cuucauucau acagacaaa
19
<210> 30
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 30
uuugucugua ugaaugaaga g
21
<210> 31
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 31
cucuucauuc auacagacaa a
21
<210> 32
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 32
uuugucugua ugaaugaaga gaa
23
<210> 33
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 33
cucuucauuc auacagacaa a
21
<210> 34
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 34
uuugucugua ugaaugaaga gaa
23
<210> 35
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 35
cucuucauuc auacagacaa a
21
<210> 36
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 36
uuugucugua ugaaugaaga gaa
23
<210> 37
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 37
cuucauucau acagacaaa
19
<210> 38
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 38
uuugucugua ugaaugaaga g
21
<210> 39
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 39
cuucauucau acagacaaa
19
<210> 40
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 40
uuugucugua ugaaugaaga g
21
<210> 41
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 41
cuucauucau acagacaaa
19
<210> 42
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 42
uuugucugua ugaaugaaga g
21
<210> 43
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 43
cucuucauuc auacagacaa a
21
<210> 44
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 44
uuugucugua ugaaugaaga gaa
23
<210> 45
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 45
cucuucauuc auacagacaa a
21
<210> 46
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 46
uuugucugua ugaaugaaga gaa
23
<210> 47
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 47
cucuucauuc auacagacaa a
21
<210> 48
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 48
uuugucugua ugaaugaaga gaa
23
<210> 49
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 49
cuucauucau acagacaaa
19
<210> 50
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 50
uuugucugua ugaaugaaga g
21
<210> 51
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 51
cuucauucau acagacaaa
19
<210> 52
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 52
uuugucugua ugaaugaaga g
21
<210> 53
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 53
cuucauucau acagacaaa
19
<210> 54
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 54
uuugucugua ugaaugaaga g
21
<210> 55
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 55
cucuucauuc auacagacaa a
21
<210> 56
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 56
uuugucugua ugaaugaaga gaa
23
<210> 57
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 57
cucuucauuc auacagacaa a
21
<210> 58
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 58
uuugucugua ugaaugaaga gaa
23
<210> 59
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 59
cucuucauuc auacagacaa a
21
<210> 60
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 60
uuugucugua ugaaugaaga gaa
23
<210> 61
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> N представляет собой Z5, и Z5 представляет собой A
<400> 61
cuacaguuua gaagauuun
19
<210> 62
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z6, и Z6 представляет собой U
<400> 62
naaaucuucu aaacuguag
19
<210> 63
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z7, и Z7 выбран из A, U, G или C
<400> 63
cuacaguuua gaagauuun
19
<210> 64
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z8, Z8 представляет собой нуклеотид,
комплементарный Z8, и Z7 выбран из A, U, G или C
<400> 64
naaaucuucu aaacuguag
19
<210> 65
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z7, и Z7 выбран из A, U, G или C
<400> 65
cuacaguuua gaagauuun
19
<210> 66
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z8, Z8 представляет собой нуклеотид,
комплементарный Z8, и Z7 выбран из A, U, G или C
<400> 66
naaaucuucu aaacuguagu a
21
<210> 67
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z7, и Z7 выбран из A, U, G или C
<400> 67
uacuacaguu uagaagauuu n
21
<210> 68
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z8, Z8 представляет собой нуклеотид,
комплементарный Z8, и Z7 выбран из A, U, G или C
<400> 68
naaaucuucu aaacuguagu aug
23
<210> 69
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 69
cuacaguuua gaagauuua
19
<210> 70
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 70
uaaaucuucu aaacuguagu a
21
<210> 71
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 71
uacuacaguu uagaagauuu a
21
<210> 72
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 72
uaaaucuucu aaacuguagu aug
23
<210> 73
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 73
cuacaguuua gaagauuua
19
<210> 74
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 74
uaaaucuucu aaacuguagu a
21
<210> 75
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 75
cuacaguuua gaagauuua
19
<210> 76
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 76
uaaaucuucu aaacuguagu a
21
<210> 77
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 77
cuacaguuua gaagauuua
19
<210> 78
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 78
uaaaucuucu aaacuguagu a
21
<210> 79
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 79
uacuacaguu uagaagauuu a
21
<210> 80
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 80
uaaaucuucu aaacuguagu aug
23
<210> 81
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 81
uacuacaguu uagaagauuu a
21
<210> 82
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 82
uaaaucuucu aaacuguagu aug
23
<210> 83
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 83
uacuacaguu uagaagauuu a
21
<210> 84
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 84
uaaaucuucu aaacuguagu aug
23
<210> 85
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 85
cuacaguuua gaagauuua
19
<210> 86
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 86
uaaaucuucu aaacuguagu a
21
<210> 87
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 87
cuacaguuua gaagauuua
19
<210> 88
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 88
uaaaucuucu aaacuguagu a
21
<210> 89
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 89
cuacaguuua gaagauuua
19
<210> 90
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 90
uaaaucuucu aaacuguagu a
21
<210> 91
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 91
uacuacaguu uagaagauuu a
21
<210> 92
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 92
uaaaucuucu aaacuguagu aug
23
<210> 93
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 93
uacuacaguu uagaagauuu a
21
<210> 94
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 94
uaaaucuucu aaacuguagu aug
23
<210> 95
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 95
uacuacaguu uagaagauuu a
21
<210> 96
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 96
uaaaucuucu aaacuguagu aug
23
<210> 97
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 97
cuacaguuua gaagauuua
19
<210> 98
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 98
uaaaucuucu aaacuguagu a
21
<210> 99
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 99
cuacaguuua gaagauuua
19
<210> 100
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 100
uaaaucuucu aaacuguagu a
21
<210> 101
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 101
cuacaguuua gaagauuua
19
<210> 102
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 102
uaaaucuucu aaacuguagu a
21
<210> 103
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 103
uacuacaguu uagaagauuu a
21
<210> 104
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 104
uaaaucuucu aaacuguagu aug
23
<210> 105
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 105
uacuacaguu uagaagauuu a
21
<210> 106
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 106
uaaaucuucu aaacuguagu aug
23
<210> 107
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 107
uacuacaguu uagaagauuu a
21
<210> 108
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 108
uaaaucuucu aaacuguagu aug
23
<210> 109
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 109
cuacaguuua gaagauuua
19
<210> 110
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 110
uaaaucuucu aaacuguagu a
21
<210> 111
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 111
cuacaguuua gaagauuua
19
<210> 112
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 112
uaaaucuucu aaacuguagu a
21
<210> 113
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 113
cuacaguuua gaagauuua
19
<210> 114
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 114
uaaaucuucu aaacuguagu a
21
<210> 115
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 115
uacuacaguu uagaagauuu a
21
<210> 116
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 116
uaaaucuucu aaacuguagu aug
23
<210> 117
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 117
uacuacaguu uagaagauuu a
21
<210> 118
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 118
uaaaucuucu aaacuguagu aug
23
<210> 119
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 119
uacuacaguu uagaagauuu a
21
<210> 120
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 120
uaaaucuucu aaacuguagu aug
23
<210> 121
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z9, и Z9 представляет собой A
<400> 121
ggaagguuac cgagcaaun
19
<210> 122
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z10, и Z10 представляет собой U
<400> 122
nauugcucgg uaaccuucc
19
<210> 123
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z11, и Z11 выбран из A, U, G или C
<400> 123
ggaagguuac cgagcaaun
19
<210> 124
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z12, Z12 представляет собой нуклеотид,
комплементарный Z11, и Z11 выбран из A, U, G или C
<400> 124
nauugcucgg uaaccuucc
19
<210> 125
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z11, и Z11 выбран из A, U, G или C
<400> 125
ggaagguuac cgagcaaun
19
<210> 126
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z12, Z12 представляет собой нуклеотид,
комплементарный Z11, и Z11 выбран из A, U, G или C
<400> 126
nauugcucgg uaaccuuccc u
21
<210> 127
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z11, и Z11 выбран из A, U, G или C
<400> 127
agggaagguu accgagcaau n
21
<210> 128
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z12, Z12 представляет собой нуклеотид,
комплементарный Z11, и Z11 выбран из A, U, G или C
<400> 128
nauugcucgg uaaccuuccc ugg
23
<210> 129
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 129
ggaagguuac cgagcaaua
19
<210> 130
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 130
uauugcucgg uaaccuuccc u
21
<210> 131
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 131
agggaagguu accgagcaau a
21
<210> 132
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 132
uauugcucgg uaaccuuccc ugg
23
<210> 133
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 133
ggaagguuac cgagcaaua
19
<210> 134
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 134
uauugcucgg uaaccuuccc u
21
<210> 135
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 135
ggaagguuac cgagcaaua
19
<210> 136
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 136
uauugcucgg uaaccuuccc u
21
<210> 137
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 137
ggaagguuac cgagcaaua
19
<210> 138
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 138
uauugcucgg uaaccuuccc u
21
<210> 139
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 139
agggaagguu accgagcaau a
21
<210> 140
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 140
uauugcucgg uaaccuuccc ugg
23
<210> 141
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 141
agggaagguu accgagcaau a
21
<210> 142
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 142
uauugcucgg uaaccuuccc ugg
23
<210> 143
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 143
agggaagguu accgagcaau a
21
<210> 144
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 144
uauugcucgg uaaccuuccc ugg
23
<210> 145
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 145
ggaagguuac cgagcaaua
19
<210> 146
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 146
uauugcucgg uaaccuuccc u
21
<210> 147
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 147
ggaagguuac cgagcaaua
19
<210> 148
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 148
uauugcucgg uaaccuuccc u
21
<210> 149
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 149
ggaagguuac cgagcaaua
19
<210> 150
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 150
uauugcucgg uaaccuuccc u
21
<210> 151
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 151
agggaagguu accgagcaau a
21
<210> 152
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 152
uauugcucgg uaaccuuccc ugg
23
<210> 153
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 153
agggaagguu accgagcaau a
21
<210> 154
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 154
uauugcucgg uaaccuuccc ugg
23
<210> 155
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 155
agggaagguu accgagcaau a
21
<210> 156
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 156
uauugcucgg uaaccuuccc ugg
23
<210> 157
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 157
ggaagguuac cgagcaaua
19
<210> 158
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 158
uauugcucgg uaaccuuccc u
21
<210> 159
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 159
ggaagguuac cgagcaaua
19
<210> 160
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 160
uauugcucgg uaaccuuccc u
21
<210> 161
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 161
ggaagguuac cgagcaaua
19
<210> 162
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 162
uauugcucgg uaaccuuccc u
21
<210> 163
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 163
agggaagguu accgagcaau a
21
<210> 164
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 164
uauugcucgg uaaccuuccc ugg
23
<210> 165
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 165
agggaagguu accgagcaau a
21
<210> 166
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 166
uauugcucgg uaaccuuccc ugg
23
<210> 167
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 167
agggaagguu accgagcaau a
21
<210> 168
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 168
uauugcucgg uaaccuuccc ugg
23
<210> 169
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 169
ggaagguuac cgagcaaua
19
<210> 170
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 170
uauugcucgg uaaccuuccc u
21
<210> 171
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 171
ggaagguuac cgagcaaua
19
<210> 172
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 172
uauugcucgg uaaccuuccc u
21
<210> 173
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 173
ggaagguuac cgagcaaua
19
<210> 174
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 174
uauugcucgg uaaccuuccc u
21
<210> 175
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 175
agggaagguu accgagcaau a
21
<210> 176
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 176
uauugcucgg uaaccuuccc ugg
23
<210> 177
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 177
agggaagguu accgagcaau a
21
<210> 178
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 178
uauugcucgg uaaccuuccc ugg
23
<210> 179
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 179
agggaagguu accgagcaau a
21
<210> 180
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 180
uauugcucgg uaaccuuccc ugg
23
<210> 181
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> N представляет собой Z13, и Z13 представляет собой A
<400> 181
agaacagaca gcagaauun
19
<210> 182
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z14, и Z14 представляет собой U
<400> 182
naauucugcu gucuguucu
19
<210> 183
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z15, и Z15 выбран из A, U, G или C
<400> 183
agaacagaca gcagaauun
19
<210> 184
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z16, Z16 представляет собой нуклеотид,
комплементарный Z15, и Z15 выбран из A, U, G или C
<400> 184
naauucugcu gucuguucu
19
<210> 185
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z15, и Z15 выбран из A, U, G или C
<400> 185
agaacagaca gcagaauun
19
<210> 186
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z16, Z16 представляет собой нуклеотид,
комплементарный Z15, и Z15 выбран из A, U, G или C
<400> 186
naauucugcu gucuguucuc c
21
<210> 187
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z15, и Z15 выбран из A, U, G или C
<400> 187
ggagaacaga cagcagaauu n
21
<210> 188
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> N представляет собой Z16, Z16 представляет собой нуклеотид,
комплементарный Z15, и Z15 выбран из A, U, G или C
<400> 188
naauucugcu gucuguucuc cug
23
<210> 189
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 189
agaacagaca gcagaauua
19
<210> 190
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 190
uaauucugcu gucuguucuc c
21
<210> 191
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 191
ggagaacaga cagcagaauu a
21
<210> 192
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 192
uaauucugcu gucuguucuc cug
23
<210> 193
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 193
agaacagaca gcagaauua
19
<210> 194
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 194
uaauucugcu gucuguucuc c
21
<210> 195
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 195
agaacagaca gcagaauua
19
<210> 196
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 196
uaauucugcu gucuguucuc c
21
<210> 197
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 197
agaacagaca gcagaauua
19
<210> 198
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 198
uaauucugcu gucuguucuc c
21
<210> 199
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 199
ggagaacaga cagcagaauu a
21
<210> 200
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 200
uaauucugcu gucuguucuc cug
23
<210> 201
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 201
ggagaacaga cagcagaauu a
21
<210> 202
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 202
uaauucugcu gucuguucuc cug
23
<210> 203
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 203
ggagaacaga cagcagaauu a
21
<210> 204
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 204
uaauucugcu gucuguucuc cug
23
<210> 205
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 205
agaacagaca gcagaauua
19
<210> 206
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 206
uaauucugcu gucuguucuc c
21
<210> 207
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 207
agaacagaca gcagaauua
19
<210> 208
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 208
uaauucugcu gucuguucuc c
21
<210> 209
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 209
agaacagaca gcagaauua
19
<210> 210
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 210
uaauucugcu gucuguucuc c
21
<210> 211
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 211
ggagaacaga cagcagaauu a
21
<210> 212
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 212
uaauucugcu gucuguucuc cug
23
<210> 213
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 213
ggagaacaga cagcagaauu a
21
<210> 214
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 214
uaauucugcu gucuguucuc cug
23
<210> 215
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 215
ggagaacaga cagcagaauu a
21
<210> 216
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 216
uaauucugcu gucuguucuc cug
23
<210> 217
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 217
agaacagaca gcagaauua
19
<210> 218
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 218
uaauucugcu gucuguucuc c
21
<210> 219
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 219
agaacagaca gcagaauua
19
<210> 220
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 220
uaauucugcu gucuguucuc c
21
<210> 221
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 221
agaacagaca gcagaauua
19
<210> 222
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 222
uaauucugcu gucuguucuc c
21
<210> 223
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 223
ggagaacaga cagcagaauu a
21
<210> 224
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 224
uaauucugcu gucuguucuc cug
23
<210> 225
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 225
ggagaacaga cagcagaauu a
21
<210> 226
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 226
uaauucugcu gucuguucuc cug
23
<210> 227
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 227
ggagaacaga cagcagaauu a
21
<210> 228
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 228
uaauucugcu gucuguucuc cug
23
<210> 229
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 229
agaacagaca gcagaauua
19
<210> 230
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 230
uaauucugcu gucuguucuc c
21
<210> 231
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 231
agaacagaca gcagaauua
19
<210> 232
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 232
uaauucugcu gucuguucuc c
21
<210> 233
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 233
agaacagaca gcagaauua
19
<210> 234
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 234
uaauucugcu gucuguucuc c
21
<210> 235
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 235
ggagaacaga cagcagaauu a
21
<210> 236
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 236
uaauucugcu gucuguucuc cug
23
<210> 237
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 237
ggagaacaga cagcagaauu a
21
<210> 238
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 238
uaauucugcu gucuguucuc cug
23
<210> 239
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 239
ggagaacaga cagcagaauu a
21
<210> 240
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 240
uaauucugcu gucuguucuc cug
23
<210> 241
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z17, и Z17 представляет собой A
<400> 241
ccaagaagaa cgcugcaan
19
<210> 242
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z18, и Z18 представляет собой U
<400> 242
nuugcagcgu ucuucuugg
19
<210> 243
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z19, и Z19 выбран из A, U, G или C
<400> 243
ccaagaagaa cgcugcaan
19
<210> 244
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z20, Z20 представляет собой нуклеотид,
комплементарный Z19, и Z19 выбран из A, U, G или C
<400> 244
nuugcagcgu ucuucuugg
19
<210> 245
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z19, и Z19 выбран из A, U, G или C
<400> 245
ccaagaagaa cgcugcaan
19
<210> 246
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z20, Z20 представляет собой нуклеотид,
комплементарный Z19, и Z19 выбран из A, U, G или C
<400> 246
nuugcagcgu ucuucuuggc c
21
<210> 247
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z19, и Z19 выбран из A, U, G или C
<400> 247
ggccaagaag aacgcugcaa n
21
<210> 248
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z20, Z20 представляет собой нуклеотид,
комплементарный Z19, и Z19 выбран из A, U, G или C
<400> 248
nuugcagcgu ucuucuuggc cug
23
<210> 249
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 249
ccaagaagaa cgcugcaaa
19
<210> 250
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 250
uuugcagcgu ucuucuuggc c
21
<210> 251
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 251
ggccaagaag aacgcugcaa a
21
<210> 252
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 252
uuugcagcgu ucuucuuggc cug
23
<210> 253
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 253
ccaagaagaa cgcugcaaa
19
<210> 254
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 254
uuugcagcgu ucuucuuggc c
21
<210> 255
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 255
ccaagaagaa cgcugcaaa
19
<210> 256
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 256
uuugcagcgu ucuucuuggc c
21
<210> 257
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 257
ccaagaagaa cgcugcaaa
19
<210> 258
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 258
uuugcagcgu ucuucuuggc c
21
<210> 259
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 259
ggccaagaag aacgcugcaa a
21
<210> 260
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 260
uuugcagcgu ucuucuuggc cug
23
<210> 261
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 261
ggccaagaag aacgcugcaa a
21
<210> 262
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 262
uuugcagcgu ucuucuuggc cug
23
<210> 263
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 263
ggccaagaag aacgcugcaa a
21
<210> 264
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 264
uuugcagcgu ucuucuuggc cug
23
<210> 265
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 265
ccaagaagaa cgcugcaaa
19
<210> 266
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 266
uuugcagcgu ucuucuuggc c
21
<210> 267
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 267
ccaagaagaa cgcugcaaa
19
<210> 268
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 268
uuugcagcgu ucuucuuggc c
21
<210> 269
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 269
ccaagaagaa cgcugcaaa
19
<210> 270
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 270
uuugcagcgu ucuucuuggc c
21
<210> 271
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 271
ggccaagaag aacgcugcaa a
21
<210> 272
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 272
uuugcagcgu ucuucuuggc cug
23
<210> 273
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 273
ggccaagaag aacgcugcaa a
21
<210> 274
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 274
uuugcagcgu ucuucuuggc cug
23
<210> 275
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 275
ggccaagaag aacgcugcaa a
21
<210> 276
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 276
uuugcagcgu ucuucuuggc cug
23
<210> 277
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 277
ccaagaagaa cgcugcaaa
19
<210> 278
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 278
uuugcagcgu ucuucuuggc c
21
<210> 279
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 279
ccaagaagaa cgcugcaaa
19
<210> 280
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 280
uuugcagcgu ucuucuuggc c
21
<210> 281
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 281
ccaagaagaa cgcugcaaa
19
<210> 282
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 282
uuugcagcgu ucuucuuggc c
21
<210> 283
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 283
ggccaagaag aacgcugcaa a
21
<210> 284
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 284
uuugcagcgu ucuucuuggc cug
23
<210> 285
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 285
ggccaagaag aacgcugcaa a
21
<210> 286
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 286
uuugcagcgu ucuucuuggc cug
23
<210> 287
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 287
ggccaagaag aacgcugcaa a
21
<210> 288
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 288
uuugcagcgu ucuucuuggc cug
23
<210> 289
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 289
ccaagaagaa cgcugcaaa
19
<210> 290
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 290
uuugcagcgu ucuucuuggc c
21
<210> 291
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 291
ccaagaagaa cgcugcaaa
19
<210> 292
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 292
uuugcagcgu ucuucuuggc c
21
<210> 293
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 293
ccaagaagaa cgcugcaaa
19
<210> 294
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 294
uuugcagcgu ucuucuuggc c
21
<210> 295
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 295
ggccaagaag aacgcugcaa a
21
<210> 296
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 296
uuugcagcgu ucuucuuggc cug
23
<210> 297
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 297
ggccaagaag aacgcugcaa a
21
<210> 298
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 298
uuugcagcgu ucuucuuggc cug
23
<210> 299
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 299
ggccaagaag aacgcugcaa a
21
<210> 300
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 300
uuugcagcgu ucuucuuggc cug
23
<210> 301
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z21, и Z21 представляет собой A
<400> 301
ccaguaagca agccagaan
19
<210> 302
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z22, и Z22 представляет собой U
<400> 302
nuucuggcuu gcuuacugg
19
<210> 303
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z23, и Z23 выбран из A, U, G или C
<400> 303
ccaguaagca agccagaan
19
<210> 304
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z24, Z24 представляет собой нуклеотид,
комплементарный Z23, и Z23 выбран из A, U, G или C
<400> 304
nuucuggcuu gcuuacugg
19
<210> 305
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (19)..(19)
<223> n представляет собой Z23, и Z23 выбран из A, U, G или C
<400> 305
ccaguaagca agccagaan
19
<210> 306
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z24, Z24 представляет собой нуклеотид,
комплементарный Z23, и Z23 выбран из A, U, G или C
<400> 306
nuucuggcuu gcuuacuggu a
21
<210> 307
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (21)..(21)
<223> n представляет собой Z23, и Z23 выбран из A, U, G или C
<400> 307
uaccaguaag caagccagaa n
21
<210> 308
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<220>
<221> misc_feature
<222> (1)..(1)
<223> n представляет собой Z24, Z24 представляет собой нуклеотид,
комплементарный Z23, и Z23 выбран из A, U, G или C
<400> 308
nuucuggcuu gcuuacuggu aac
23
<210> 309
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 309
ccaguaagca agccagaaa
19
<210> 310
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 310
uuucuggcuu gcuuacuggu a
21
<210> 311
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 311
uaccaguaag caagccagaa a
21
<210> 312
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 312
uuucuggcuu gcuuacuggu aac
23
<210> 313
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 313
ccaguaagca agccagaaa
19
<210> 314
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 314
uuucuggcuu gcuuacuggu a
21
<210> 315
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 315
ccaguaagca agccagaaa
19
<210> 316
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 316
uuucuggcuu gcuuacuggu a
21
<210> 317
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 317
ccaguaagca agccagaaa
19
<210> 318
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 318
uuucuggcuu gcuuacuggu a
21
<210> 319
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 319
uaccaguaag caagccagaa a
21
<210> 320
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 320
uuucuggcuu gcuuacuggu aac
23
<210> 321
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 321
uaccaguaag caagccagaa a
21
<210> 322
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 322
uuucuggcuu gcuuacuggu aac
23
<210> 323
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 323
uaccaguaag caagccagaa a
21
<210> 324
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 324
uuucuggcuu gcuuacuggu aac
23
<210> 325
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 325
ccaguaagca agccagaaa
19
<210> 326
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 326
uuucuggcuu gcuuacuggu a
21
<210> 327
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 327
ccaguaagca agccagaaa
19
<210> 328
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 328
uuucuggcuu gcuuacuggu a
21
<210> 329
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 329
ccaguaagca agccagaaa
19
<210> 330
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 330
uuucuggcuu gcuuacuggu a
21
<210> 331
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 331
uaccaguaag caagccagaa a
21
<210> 332
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 332
uuucuggcuu gcuuacuggu aac
23
<210> 333
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 333
uaccaguaag caagccagaa a
21
<210> 334
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 334
uuucuggcuu gcuuacuggu aac
23
<210> 335
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 335
uaccaguaag caagccagaa a
21
<210> 336
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 336
uuucuggcuu gcuuacuggu aac
23
<210> 337
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 337
ccaguaagca agccagaaa
19
<210> 338
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 338
uuucuggcuu gcuuacuggu a
21
<210> 339
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 339
ccaguaagca agccagaaa
19
<210> 340
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 340
uuucuggcuu gcuuacuggu a
21
<210> 341
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 341
ccaguaagca agccagaaa
19
<210> 342
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 342
uuucuggcuu gcuuacuggu a
21
<210> 343
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 343
uaccaguaag caagccagaa a
21
<210> 344
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 344
uuucuggcuu gcuuacuggu aac
23
<210> 345
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 345
uaccaguaag caagccagaa a
21
<210> 346
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 346
uuucuggcuu gcuuacuggu aac
23
<210> 347
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 347
uaccaguaag caagccagaa a
21
<210> 348
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 348
uuucuggcuu gcuuacuggu aac
23
<210> 349
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 349
ccaguaagca agccagaaa
19
<210> 350
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 350
uuucuggcuu gcuuacuggu a
21
<210> 351
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 351
ccaguaagca agccagaaa
19
<210> 352
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 352
uuucuggcuu gcuuacuggu a
21
<210> 353
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 353
ccaguaagca agccagaaa
19
<210> 354
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 354
uuucuggcuu gcuuacuggu a
21
<210> 355
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 355
uaccaguaag caagccagaa a
21
<210> 356
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 356
uuucuggcuu gcuuacuggu aac
23
<210> 357
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 357
uaccaguaag caagccagaa a
21
<210> 358
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 358
uuucuggcuu gcuuacuggu aac
23
<210> 359
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 359
uaccaguaag caagccagaa a
21
<210> 360
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 360
uuucuggcuu gcuuacuggu aac
23
<210> 361
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 361
cuucauucau acagacaaa
19
<210> 362
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 362
uuugucugua ugaaugaaga g
21
<210> 363
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 363
cuacaguuua gaagauuua
19
<210> 364
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 364
uaaaucuucu aaacuguagu a
21
<210> 365
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 365
ggaagguuac cgagcaaua
19
<210> 366
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 366
uauugcucgg uaaccuuccc u
21
<210> 367
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 367
agaacagaca gcagaauua
19
<210> 368
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 368
uaauucugcu gucuguucuc c
21
<210> 369
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 369
ccaagaagaa cgcugcaaa
19
<210> 370
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 370
uuugcagcgu ucuucuuggc c
21
<210> 371
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 371
ccaguaagca agccagaaa
19
<210> 372
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 372
uuucuggcuu gcuuacuggu a
21
<210> 373
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 373
cuucauucau acagacaaa
19
<210> 374
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 374
uuugucugua ugaaugaaga g
21
<210> 375
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 375
cuacaguuua gaagauuua
19
<210> 376
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 376
uaaaucuucu aaacuguagu a
21
<210> 377
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 377
ggaagguuac cgagcaaua
19
<210> 378
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 378
uauugcucgg uaaccuuccc u
21
<210> 379
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 379
agaacagaca gcagaauua
19
<210> 380
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 380
uaauucugcu gucuguucuc c
21
<210> 381
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 381
ccaagaagaa cgcugcaaa
19
<210> 382
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 382
uuugcagcgu ucuucuuggc c
21
<210> 383
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 383
ccaguaagca agccagaaa
19
<210> 384
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 384
uuucuggcuu gcuuacuggu a
21
<210> 385
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 385
atcaggccag ggaaggttac
20
<210> 386
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 386
tcgggatgaa ggaaccatgt
20
<210> 387
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 387
ggtcggagtc aacggattt
19
<210> 388
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 388
ccagcatcgc cccacttga
19
<---
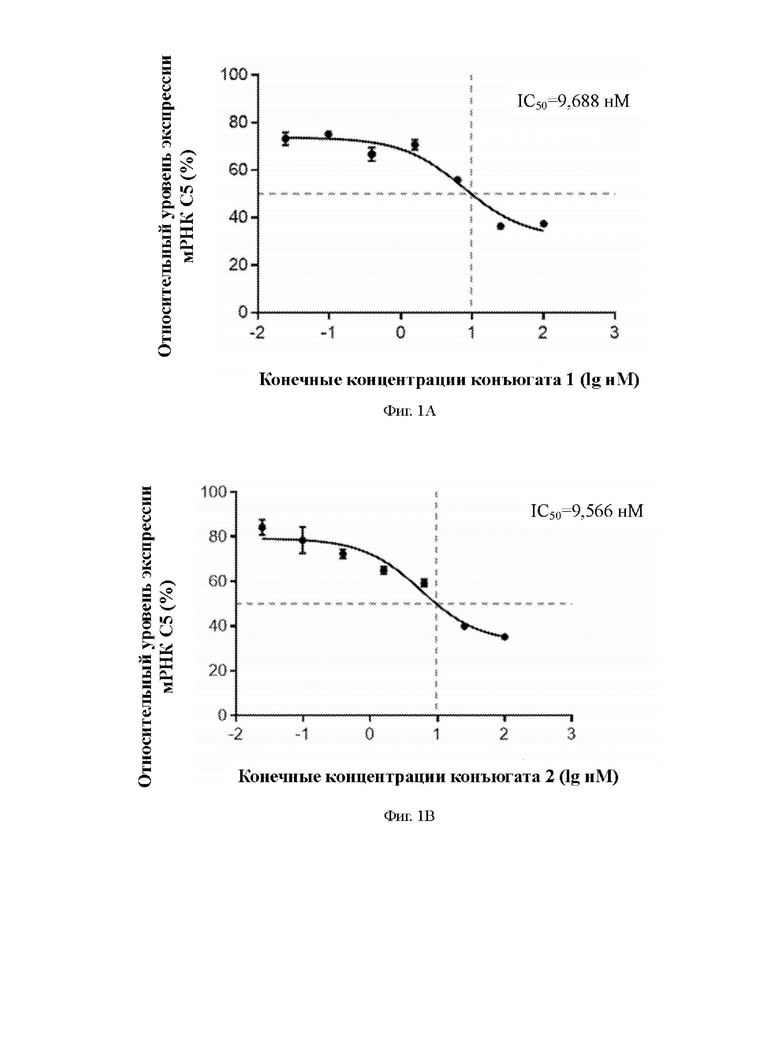





Предложен конъюгат миРНК, имеющий структуру, представленную Формулой (308), где L1, M1, R2, R3, R10-R15, m1-m3, n1-n3 определены в формуле изобретения, и в котором миРНК способна ингибировать экспрессию гена белка комплемента 5 (C5), где каждый нуклеотид в миРНК представляет собой независимый модифицированный или немодифицированный нуклеотид. siRNA содержит смысловую цепь и антисмысловую цепь. Смысловая цепь содержит нуклеотидную последовательность I, а нуклеотидная последовательность I имеет такую же длину и не более чем на три нуклеотидных отличия от нуклеотидной последовательности, показанной в SEQ ID NO: 1. Антисмысловая цепь содержит нуклеотидную последовательность II, а нуклеотидная последовательность II имеет ту же длину и не более чем на три нуклеотидных отличия от нуклеотидной последовательности, показанной в SEQ ID NO: 2. Также предложено применение конъюгата миРНК для производства лекарственного средства для лечения и/или предупреждения миастении гравис и способ ингибирования экспрессии гена C5 в гепатоците. 3 н. и 21 з.п. ф-лы, 2 ил., 6 табл., 4 пр.
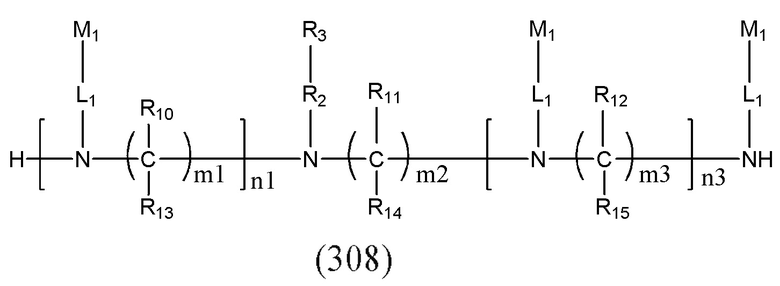
1. Конъюгат миРНК, имеющий структуру, представленную Формулой (308)

где n1 представляет собой целое число от 1 до 3, а n3 представляет собой целое число от 0 до 4; каждый из m1, m2 и m3 независимо представляет собой целое число от 2 до 10; каждый из R10, R11, R12, R13, R14 или R15 независимо выбран из H, метила и этила;
R3 представляет собой группу, имеющую структуру, представленную Формулой A59
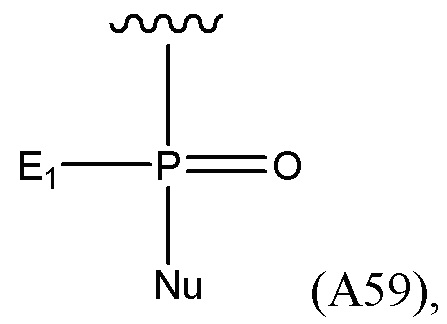
где E1 представляет собой OH, SH или BH2; и
Nu представляет собой миРНК; указанная миРНК содержит смысловую цепь и антисмысловую цепь, каждый нуклеотид в указанной миРНК независимо представляет собой модифицированный или немодифицированный нуклеотид, где смысловая цепь содержит нуклеотидную последовательность I, а антисмысловая цепь содержит нуклеотидную последовательность II; нуклеотидная последовательность I и нуклеотидная последовательность II по меньшей мере частично обратно комплементарны, образуя двухцепочечную область; и нуклеотидная последовательность I и нуклеотидная последовательность II выбраны из группы последовательностей согласно следующим i) - vi):
i) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 1, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 2, и отличается от нее не более чем по трем нуклеотидам:
5’-CUUCAUUCAUACAGACAAZ1-3’ (SEQ ID NO: 1);
5’-Z2UUGUCUGUAUGAAUGAAG-3’ (SEQ ID NO: 2),
где Z1 представляет собой A, Z2 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z3 в сайте, соответствующем Z1, нуклеотидная последовательность II содержит нуклеотид Z4 в сайте, соответствующем Z2, и Z4 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
ii) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 61, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 62, и отличается от нее не более чем по трем нуклеотидам:
5’-CUACAGUUUAGAAGAUUUZ5-3’ (SEQ ID NO: 61);
5’-Z6AAAUCUUCUAAACUGUAG-3’ (SEQ ID NO: 62),
где Z5 представляет собой A, Z6 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z7 в сайте, соответствующем Z5, нуклеотидная последовательность II содержит нуклеотид Z8 в сайте, соответствующем Z6, и Z8 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
iii) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 121, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 122, и отличается от нее не более чем по трем нуклеотидам:
5’-GGAAGGUUACCGAGCAAUZ9-3’ (SEQ ID NO: 121);
5’-Z10AUUGCUCGGUAACCUUCC-3’ (SEQ ID NO: 122),
где Z9 представляет собой A, Z10 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z11 в сайте, соответствующем Z9, нуклеотидная последовательность II содержит нуклеотид Z12 в сайте, соответствующем Z10, и Z12 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
iv) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 181, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 182, и отличается от нее не более чем по трем нуклеотидам:
5’-AGAACAGACAGCAGAAUUZ13-3’ (SEQ ID NO: 181);
5’-Z14AAUUCUGCUGUCUGUUCU-3’ (SEQ ID NO: 182),
где Z13 представляет собой A, Z14 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z15 в сайте, соответствующем Z13, нуклеотидная последовательность II содержит нуклеотид Z16 в сайте, соответствующем Z14, и Z16 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
v) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 241, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 242, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAAGAAGAACGCUGCAAZ17-3’ (SEQ ID NO: 241);
5’-Z18UUGCAGCGUUCUUCUUGG-3’ (SEQ ID NO: 242),
где Z17 представляет собой A, Z18 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z19 в сайте, соответствующем Z17, нуклеотидная последовательность II содержит нуклеотид Z20 в сайте, соответствующем Z18, и Z20 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи; и
vi) нуклеотидная последовательность I имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 301, и отличается от нее не более чем по трем нуклеотидам; и нуклеотидная последовательность II имеет ту же длину, что и нуклеотидная последовательность, представленная в SEQ ID NO: 302, и отличается от нее не более чем по трем нуклеотидам:
5’-CCAGUAAGCAAGCCAGAAZ21-3’ (SEQ ID NO: 301);
5’-Z22UUCUGGCUUGCUUACUGG-3’ (SEQ ID NO: 302),
где Z21 представляет собой A, Z22 представляет собой U, нуклеотидная последовательность I содержит нуклеотид Z23 в сайте, соответствующем Z21, нуклеотидная последовательность II содержит нуклеотид Z24 в сайте, соответствующем Z22, и Z24 представляет собой первый нуклеотид с 5’-конца антисмысловой цепи;
R2 представляет собой линейный алкилен длиной от 1 до 20 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10 арилена, C3-C18 гетероциклилена и C5-C10 гетероарилена, и где R2 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10арила, C5-C10гетероарила, C1-C10галогеналкила, -OC1-C10 алкила, -OC1-C10алкилфенила, -C1-C10 алкил-OH, -OC1-C10галогеналкила, -SC1-C10 алкила, -SC1-C10алкилфенила, -C1-C10 алкил-SH, -SC1-C10галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10алкилфенила), -NH(C1-C10алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10алкилфенила, -C(O)C1-C10галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10галогеналкила);
каждый L1 независимо представляет собой линейный алкилен длиной от 1 до 70 атомов углерода, где один или более атомов углерода необязательно замещены любым одним или более из группы, состоящей из: C(O), NH, O, S, CH=N, S(O)2, C2-C10 алкенилена, C2-C10 алкинилена, C6-C10арилена, C3-C18гетероциклилена и C5-C10 гетероарилена; и где L1 необязательно замещен любым одним или более из группы, состоящей из: C1-C10 алкила, C6-C10арила, C5-C10гетероарила, C1-C10галогеналкила, -OC1-C10 алкила, -OC1-C10алкилфенила, -C1-C10 алкил-OH, -OC1-C10галогеналкила, -SC1-C10 алкила, -SC1-C10алкилфенила, -C1-C10 алкил-SH, -SC1-C10галогеналкила, галогенового заместителя, -OH, -SH, -NH2, -C1-C10 алкил-NH2, -N(C1-C10 алкил)(C1-C10 алкила), -NH(C1-C10 алкила), -N(C1-C10 алкил)(C1-C10алкилфенила), -NH(C1-C10алкилфенила), циано, нитро, -CO2H, -C(O)O(C1-C10 алкила), -CON(C1-C10 алкил)(C1-C10 алкила), -CONH(C1-C10 алкила), -CONH2, -NHC(O)(C1-C10 алкила), -NHC(O)(фенила), -N(C1-C10 алкил)C(O)(C1-C10 алкила), -N(C1-C10 алкил)C(O)(фенила), -C(O)C1-C10 алкила, -C(O)C1-C10алкилфенила, -C(O)C1-C10галогеналкила, -OC(O)C1-C10 алкила, -SO2(C1-C10 алкила), -SO2(фенила), -SO2(C1-C10галогеналкила), -SO2NH2, -SO2NH(C1-C10 алкила), -SO2NH(фенила), -NHSO2(C1-C10 алкила), -NHSO2(фенила) и -NHSO2(C1-C10галогеналкила), и L1 представляет собой комбинацию соединений по меньшей мере двух групп A1, A4, A8, A10 и A11:
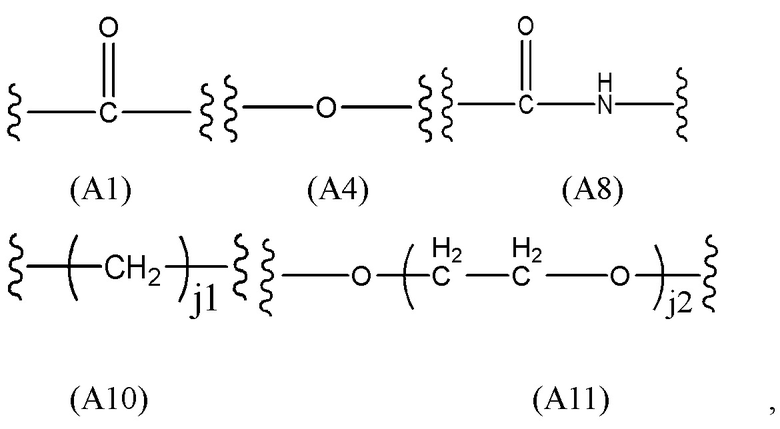
где каждый j1 независимо представляет собой целое число от 1 до 20; и каждый j2 независимо представляет собой целое число от 1 до 20; и
 обозначает сайт ковалентного присоединения группы; и
обозначает сайт ковалентного присоединения группы; и
M1 представляет собой нацеливающую группу, где каждая нацеливающая группа независимо представляет собой лиганд, который связывается с асиалогликопротеиновым рецептором на поверхности гепатоцита млекопитающего.
2. Конъюгат миРНК по п. 1, где длина L1 составляет 3-25 атомов;
или длина L1 составляет 4-15 атомов.
3. Конъюгат миРНК по п. 1 или 2, где каждый из m1, m2 и m3 независимо представляет собой целое число от 2 до 5 и/или m1=m2=m3.
4. Конъюгат миРНК по любому из пп. 1-3, где каждая нацеливающая группа независимо представляет собой асиалогликопротеин или сахарид;
или каждая нацеливающая группа независимо выбрана из одной из следующих: D-маннопираноза, L-маннопираноза, D-арабиноза, D-ксилофураноза, L-ксилофураноза, D-глюкоза, L-глюкоза, D-галактоза, L-галактоза, α-D-маннофураноза, β-D-маннофураноза, α-D-маннопираноза, β-D-маннопираноза, α-D-глюкопираноза, β-D-глюкопираноза, α-D-глюкофураноза, β-D-глюкофураноза, α-D-фруктофураноза, α-D-фруктопираноза, α-D-галактопираноза, β-D-галактопираноза, α-D-галактофураноза, β-D-галактофураноза, глюкозамин, сиаловая кислота, галактозамин, N-ацетилгалактозамин, N-трифторацетилгалактозамин, N-пропионилгалактозамин, N-н-бутирилгалактозамин, N-изобутирилгалактозамин, 2-амино-3-O-[(R)-1-карбоксиэтил]-2-дезокси-β-D-глюкопираноза, 2-дезокси-2-метиламино-L-глюкопираноза, 4,6-дидезокси-4-формамидо-2,3-ди-O-метил-D-маннопираноза, 2-дезокси-2-сульфоамино-D-глюкопираноза, N-гликолил-α-нейраминовая кислота, 5-тио-β-D-глюкофураноза, метил-2,3,4-трис-O-ацетил-1-тио-6-O-тритил-α-D-глюкофураноза, 4-тио-β-D-галактопираноза, этил-3,4,6,7-тетра-O-ацетил-2-дезокси-1,5-дитио-α-D-глюкогептопиранозид, 2,5-ангидро-D-аллононитрил, рибоза, D-рибоза, D-4-тиорибоза, L-рибоза и L-4-тиорибоза;
или по меньшей мере одна или каждая нацеливающая группа представляет собой галактозу или N-ацетилгалактозамин.
5. Конъюгат миРНК по любому из пп. 1-4, где R2 содержит как сайт связывания с атомом N на азотсодержащем остове, так и сайт связывания с атомом P в R3;
или в R2 сайт связывания с атомом N на азотсодержащем остове образует амидную связь с атомом N, а сайт связывания с атомом P в R3 образует фосфоэфирную связь с атомом P;
или R2 выбран из групп, представленных Формулами (B5), (B6), (B5') или (B6'):

где  обозначает сайт ковалентного присоединения группы; и
обозначает сайт ковалентного присоединения группы; и
q2 представляет собой целое число от 1 до 10.
6. Конъюгат миРНК по любому из пп. 1-5, имеющий структуру, представленную Формулами (403), (404), (405), (406), (407), (408), (409), (410), (411), (412), (413), (414), (415), (416), (417), (418), (419), (420), (421) или (422):
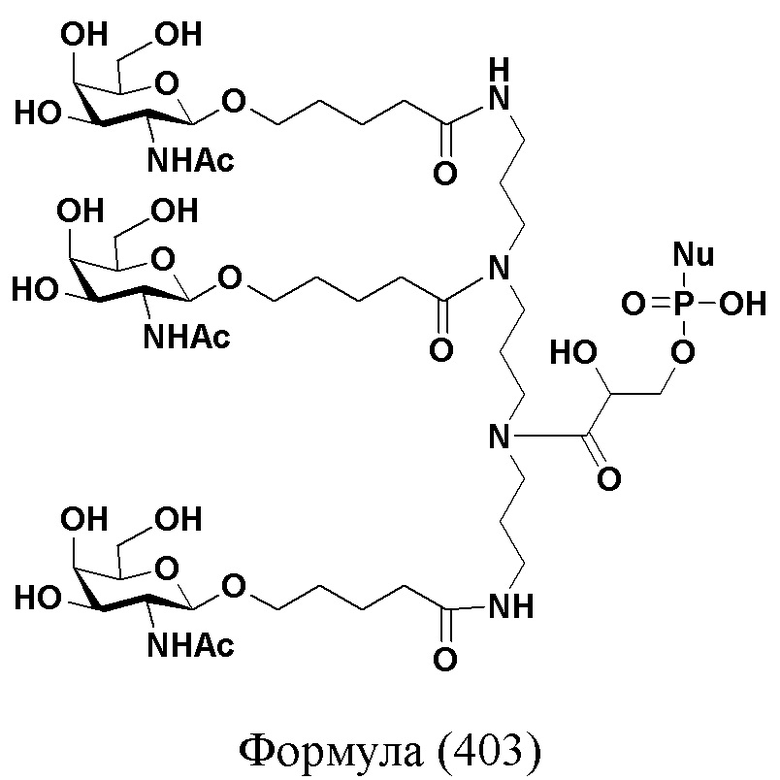
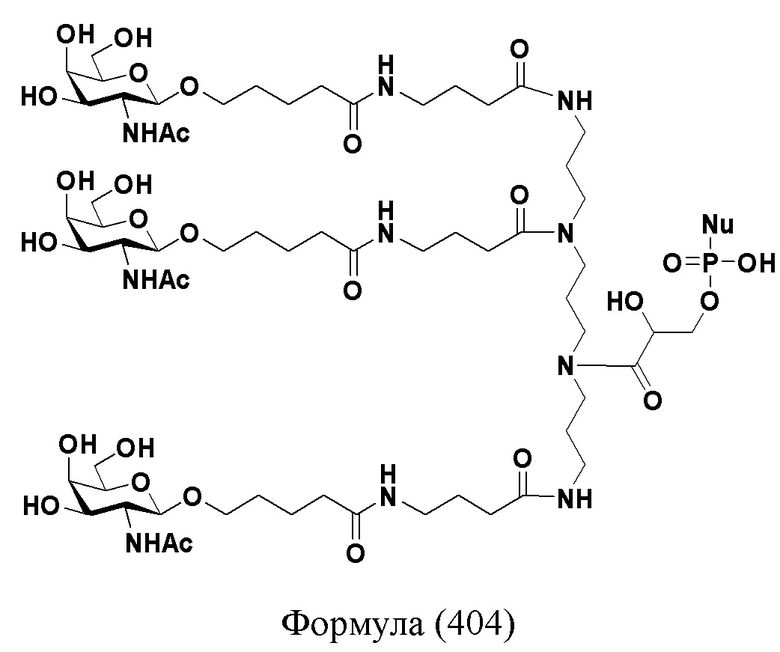



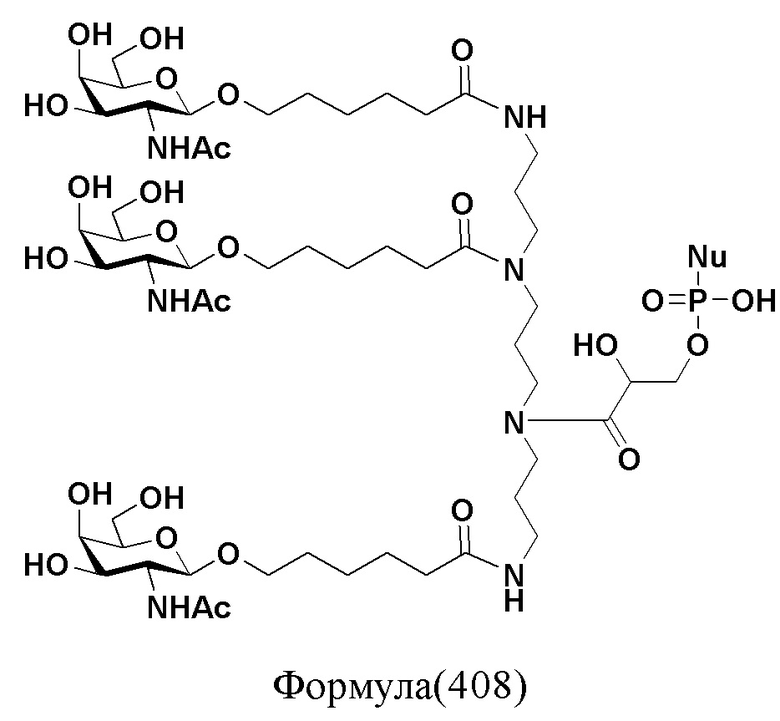
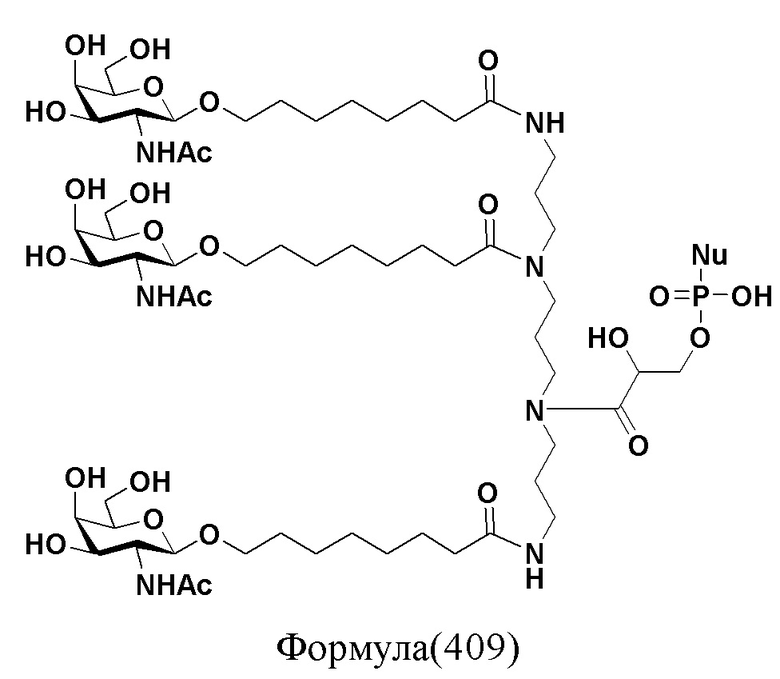



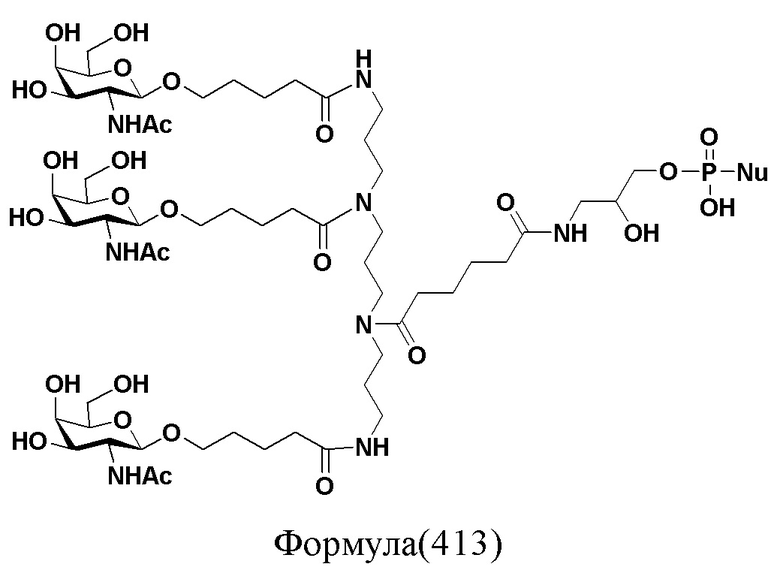

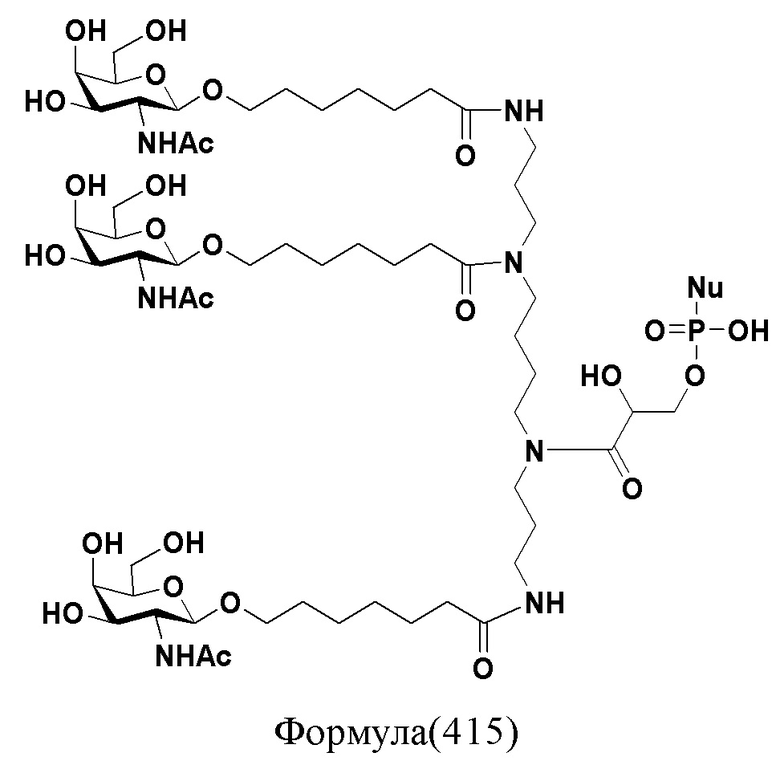

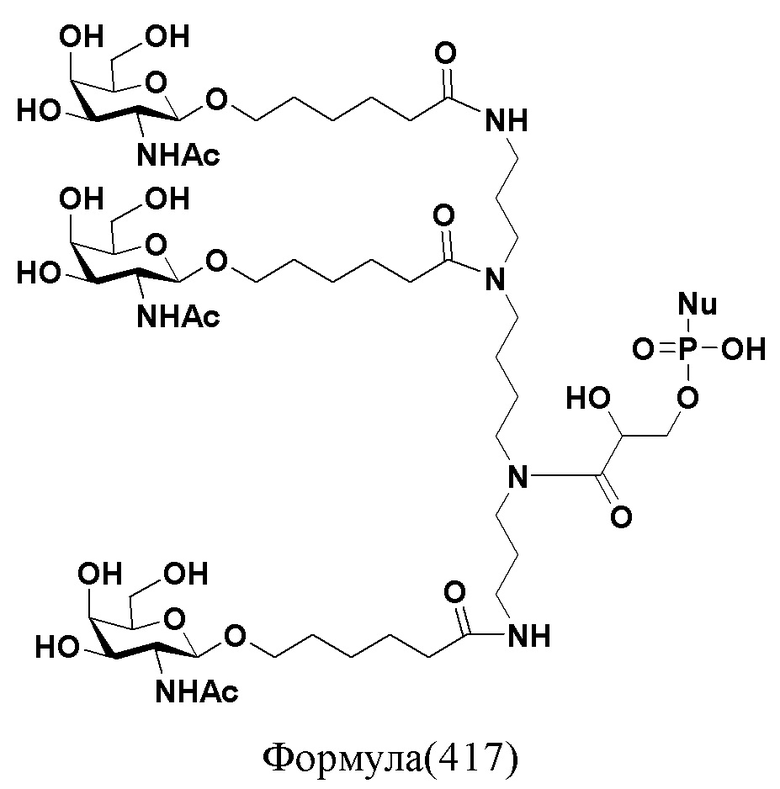

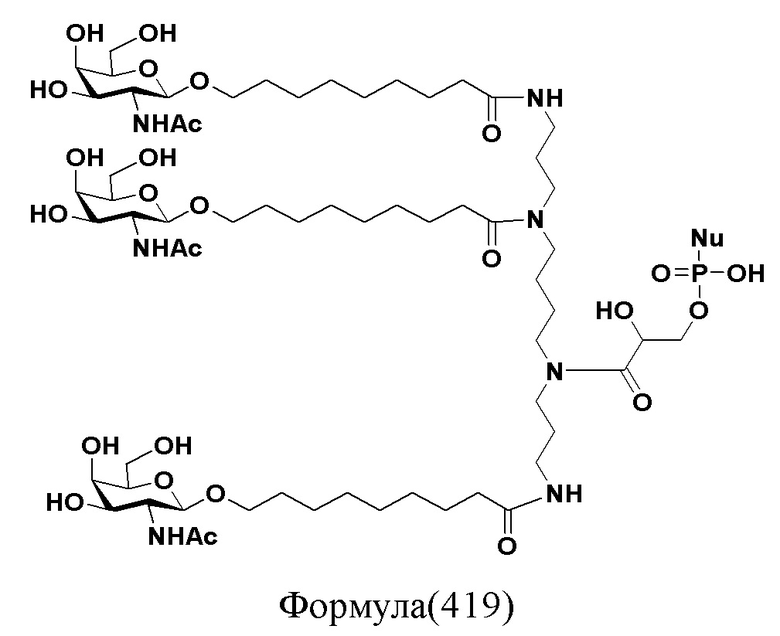
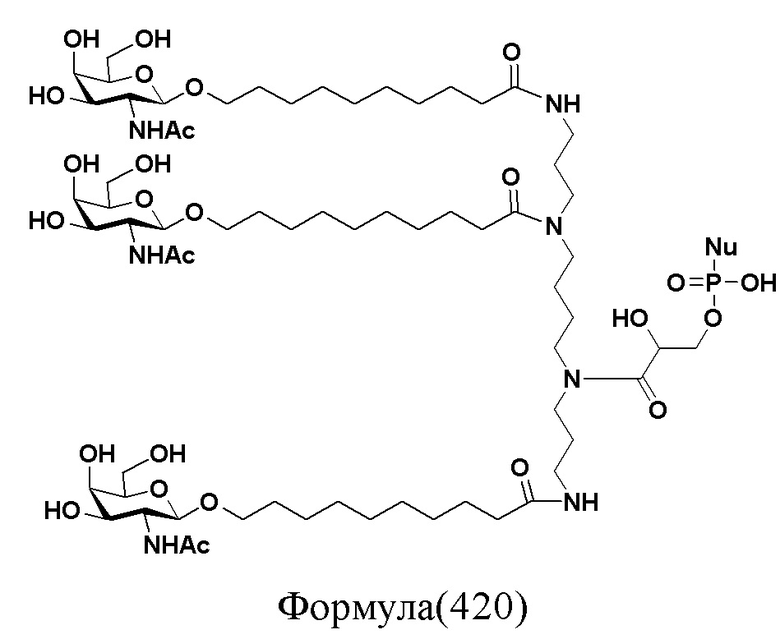


7. Конъюгат миРНК по любому из пп. 1-6, где атом P в Формуле A59 связан с концевой областью смысловой цепи или антисмысловой цепи миРНК и концевая область относится к первым четырем нуклеотидам, расположенным ближе всего к любому из концов смысловой цепи или антисмысловой цепи;
или атом P в Формуле A59 связан с концом смысловой цепи или антисмысловой цепи миРНК; или атом P в Формуле A59 связан с 3’-концом смысловой цепи миРНК;
или атом P в Формуле A59 связан с положением 2’, 3’ или 5’ нуклеотида в миРНК фосфодиэфирной связью.
8. Конъюгат миРНК по п. 1, где
i) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 1, не более чем по одному нуклеотиду; и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 2, не более чем по одному нуклеотиду; или
ii) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 61, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 62, не более чем по одному нуклеотиду; или
iii) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 121, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 122, не более чем по одному нуклеотиду; или
iv) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 181, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 182, не более чем по одному нуклеотиду; или
v) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 241, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 242, не более чем по одному нуклеотиду; или
vi) нуклеотидная последовательность I отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 301, не более чем по одному нуклеотиду, и/или нуклеотидная последовательность II отличается от нуклеотидной последовательности, представленной в SEQ ID NO: 302, не более чем по одному нуклеотиду.
9. Конъюгат миРНК по п. 1 или 8, где
i) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 2, включает различие в сайте Z4, и Z4 выбран из A, C или G; или
ii) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 62, включает различие в сайте Z8, и Z8 выбран из A, C или G; или
iii) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 122, включает различие в сайте Z12, и Z12 выбран из A, C или G; или
iv) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 182, включает различие в сайте Z16, и Z16 выбран из A, C или G; или
v) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 242, включает различие в сайте Z20, и Z20 выбран из A, C или G; или
vi) различие по нуклеотиду между нуклеотидной последовательностью II и нуклеотидной последовательностью, представленной в SEQ ID NO: 302, включает различие в сайте Z24, и Z24 выбран из A, C или G,
где Z3 представляет собой нуклеотид, комплементарный Z4; или Z7 представляет собой нуклеотид, комплементарный Z8; или Z11 представляет собой нуклеотид, комплементарный Z12; или Z15 представляет собой нуклеотид, комплементарный Z16; или Z19 представляет собой нуклеотид, комплементарный Z20; или Z23 представляет собой нуклеотид, комплементарный Z24.
10. Конъюгат миРНК по п. 8 или 9, где смысловая цепь дополнительно содержит нуклеотидную последовательность III, антисмысловая цепь дополнительно содержит нуклеотидную последовательность IV, каждая из нуклеотидной последовательности III и нуклеотидной последовательности IV независимо имеет длину 1-4 нуклеотида, нуклеотидная последовательность III связана с 5’-концом нуклеотидной последовательности I, нуклеотидная последовательность IV связана с 3’-концом нуклеотидной последовательности II и нуклеотидная последовательность III имеет ту же длину и является по существу обратно комплементарной или полностью обратно комплементарной нуклеотидной последовательности IV; по существу обратно комплементарный относится к не более чем одному ошибочно спаренному основанию между двумя нуклеотидными последовательностями; и полностью обратно комплементарный относится к отсутствию ошибочного спаривания между двумя нуклеотидными последовательностями.
11. Конъюгат миРНК по п. 10, где
i) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 3, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 4; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид, и основание нуклеотидной последовательности III представляет собой U; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CU; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UCU; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UUCU; или
ii) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 63, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 64; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид и основание нуклеотидной последовательности III представляет собой A; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AUA; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAUA; или
iii) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 123, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 124; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид и основание нуклеотидной последовательности III представляет собой G; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AG; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAG; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CCAG; или
iv) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 183, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 184; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид и основание нуклеотидной последовательности III представляет собой G; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AGG; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAGG; или
v) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 243, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 244; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид и основание нуклеотидной последовательности III представляет собой G; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GG; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой AGG; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой CAGG; или
vi) нуклеотидная последовательность I представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 303, а нуклеотидная последовательность II представляет собой нуклеотидную последовательность, представленную в SEQ ID NO: 304; и нуклеотидные последовательности III и IV обе имеют длину в один нуклеотид и основание нуклеотидной последовательности III представляет собой A; или нуклеотидные последовательности III и IV обе имеют длину два нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UA; или нуклеотидные последовательности III и IV обе имеют длину три нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой UUA; или нуклеотидные последовательности III и IV обе имеют длину четыре нуклеотида и в направлении от 5’-конца к 3’-концу состав оснований нуклеотидной последовательности III представляет собой GUUA.
12. Конъюгат миРНК по любому из пп. 1-11, где антисмысловая цепь дополнительно содержит нуклеотидную последовательность V, причем нуклеотидная последовательность V имеет длину 1-3 нуклеотида и связана с 3’-концом антисмысловой цепи с образованием 3’-выступающего конца антисмысловой цепи; или нуклеотидная последовательность V имеет длину 2 нуклеотида; или нуклеотидная последовательность V представляет собой два тимидиновых дезоксирибонуклеотида подряд или два уридиновых рибонуклеотида подряд; или нуклеотидная последовательность V комплементарна нуклеотидам в соответствующем сайте мРНК-мишени.
13. Конъюгат миРНК по любому из пп. 1-12, где
смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 5, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 6; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 7, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 8;
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 65, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 66; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 67, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 68;
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 125, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 126; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 127, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 128;
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 185, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 186; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 187, а антисмысловая цепь содержит нуклеотидную последовательность, представленную в SEQ ID NO: 188;
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 245, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 246; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 247, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 248;
или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 305, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 306; или смысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 307, а антисмысловая цепь миРНК содержит нуклеотидную последовательность, представленную в SEQ ID NO: 308.
14. Конъюгат миРНК по любому из пп. 8-13, где миРНК имеет нуклеотидную последовательность, представленную в siC5a1, siC5a2, siC5b1, siC5b2, siC5c1, siC5c2, siC5d1, siC5d2, siC5e1, siC5e2, siC5f1 или siC5f2:
siC5a1:
5'-CUUCAUUCAUACAGACAAA-3' (SEQ ID NO: 9)
5'-UUUGUCUGUAUGAAUGAAGAG-3' (SEQ ID NO: 10)
siC5a2:
5'-CUCUUCAUUCAUACAGACAAA-3' (SEQ ID NO: 11)
5'-UUUGUCUGUAUGAAUGAAGAGAA-3' (SEQ ID NO: 12)
siC5b1:
5'-CUACAGUUUAGAAGAUUUA-3' (SEQ ID NO: 69)
5'-UAAAUCUUCUAAACUGUAGUA-3' (SEQ ID NO: 70)
siC5b2:
5'-UACUACAGUUUAGAAGAUUUA-3' (SEQ ID NO: 71)
5'-UAAAUCUUCUAAACUGUAGUAUG-3' (SEQ ID NO: 72)
siC5c1:
5'-GGAAGGUUACCGAGCAAUA-3' (SEQ ID NO: 129)
5'-UAUUGCUCGGUAACCUUCCCU-3' (SEQ ID NO: 130)
siC5c2:
5'-AGGGAAGGUUACCGAGCAAUA-3' (SEQ ID NO: 131)
5'-UAUUGCUCGGUAACCUUCCCUGG-3' (SEQ ID NO: 132)
siC5d1:
5'-AGAACAGACAGCAGAAUUA-3' (SEQ ID NO: 189)
5'-UAAUUCUGCUGUCUGUUCUCC-3' (SEQ ID NO: 190)
siC5d2:
5'-GGAGAACAGACAGCAGAAUUA-3' (SEQ ID NO: 191)
5'-UAAUUCUGCUGUCUGUUCUCCUG-3' (SEQ ID NO: 192)
siC5e1:
5'-CCAAGAAGAACGCUGCAAA-3' (SEQ ID NO: 249)
5'-UUUGCAGCGUUCUUCUUGGCC-3' (SEQ ID NO: 250)
siC5e2:
5'-GGCCAAGAAGAACGCUGCAAA-3' (SEQ ID NO: 251)
5'-UUUGCAGCGUUCUUCUUGGCCUG-3' (SEQ ID NO: 252)
siC5f1:
5'-CCAGUAAGCAAGCCAGAAA-3' (SEQ ID NO: 309)
5'-UUUCUGGCUUGCUUACUGGUA-3' (SEQ ID NO: 310)
siC5f2:
5'-UACCAGUAAGCAAGCCAGAAA-3' (SEQ ID NO: 311)
5'-UUUCUGGCUUGCUUACUGGUAAC-3' (SEQ ID NO: 312).
15. Конъюгат миРНК по п. 1, где каждый нуклеотид в смысловой цепи и антисмысловой цепи независимо представляет собой модифицированный фтором нуклеотид или нуклеотид с отличной от фтора модификацией;
или модифицированные фтором нуклеотиды расположены в нуклеотидной последовательности I и нуклеотидной последовательности II; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 нуклеотидной последовательности I представляют собой модифицированные фтором нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II представляют собой модифицированные фтором нуклеотиды;
или в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 или 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 или 2, 6, 8, 9, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи представляют собой нуклеотиды с отличной от фтора модификацией.
16. Конъюгат миРНК по п. 15, где каждый нуклеотид с отличной от фтора модификацией независимо выбран из нуклеотида, образованного путем замещения 2’-гидроксигруппы рибозной группы нуклеотида группой, отличной от фтора, или аналога нуклеотида;
или нуклеотид, образованный путем замещения 2’-гидроксигруппы рибозной группы нуклеотида группой, отличной от фтора, выбран из одного из 2’-алкокси-модифицированного нуклеотида, 2’-замещенный алкокси-модифицированного нуклеотида, 2’-алкил-модифицированного нуклеотида, 2’-замещенный алкил-модифицированного нуклеотида, 2’-амино-модифицированного нуклеотида, 2’-замещенный амино-модифицированного нуклеотида и 2’-дезоксинуклеотида; и аналог нуклеотида выбран из одного из изонуклеотида, LNA, ENA, cET, UNA и GNA;
или каждый нуклеотид с отличной от фтора модификацией представляет собой метокси-модифицированный нуклеотид и метокси-модифицированный нуклеотид относится к нуклеотиду, образованному путем замещения 2’-гидроксигруппы рибозной группы метоксигруппой.
17. Конъюгат миРНК по п. 15 или 16, где в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 8, 9, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды;
или в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 5, 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды;
или в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 7, 8 и 9 нуклеотидной последовательности I в смысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в смысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды; и в направлении от 5’-конца к 3’-концу нуклеотиды в положениях 2, 6, 14 и 16 нуклеотидной последовательности II в антисмысловой цепи миРНК представляют собой модифицированные фтором нуклеотиды, а нуклеотиды в остальных положениях в антисмысловой цепи миРНК представляют собой метокси-модифицированные нуклеотиды.
18. Конъюгат миРНК по любому из пп. 1-17, где миРНК представляет собой любую из siC5a1-M1, siC5a2-M1, siC5a1-M2, siC5a2-M2, siC5a1-M3, siC5a2-M3, siC5b1-M1, siC5b2-M1, siC5b1-M2, siC5b2-M2, siC5b1-M3, siC5b2-M3, siC5c1-M1, siC5c2-M1, siC5c1-M2, siC5c2-M2, siC5c1-M3, siC5c2-M3, siC5d1-M1, siC5d2-M1, siC5d1-M2, siC5d2-M2, siC5d1-M3, siC5d2-M3, siC5e1-M1, siC5e2-M1, siC5e1-M2, siC5e2-M2, siC5e1-M3, siC5e2-M3, siC5f1-M1, siC5f2-M1, siC5f1-M2, siC5f2-M2, siC5f1-M3 или siC5f2-M3:
siC5a1-M1:
5'-CmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 13)
5'-UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGm-3' (SEQ ID NO: 14)
siC5a2-M1:
5'-CmUmCmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 19)
5'-UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 20)
siC5a1-M2:
5'-CmsUmsUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 27)
5'-UmsUfsUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 28)
siC5a2-M2:
5'-CmUmCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 21)
5'-UmUfUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 22)
siC5a1-M3:
5'-CmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 17)
5'-UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGm-3' (SEQ ID NO: 18)
siC5a2-M3:
5'-CmUmCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 23)
5'-UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 24)
siC5b1-M1:
5'-CmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 73)
5'-UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 74)
siC5b2-M1:
5'-UmAmCmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 79)
5'-UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 80)
siC5b1-M2:
5'-CmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 75)
5'-UmAfAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 76)
siC5b2-M2:
5'-UmAmCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 81)
5'-UmAfAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 82)
siC5b1-M3:
5'-CmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 77)
5'-UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 78)
siC5b2-M3:
5'-UmAmCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 83)
5'-UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 84)
siC5c1-M1:
5'-GmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 133)
5'-UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 134)
siC5c2-M1:
5'-AmGmGmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 139)
5'-UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 140)
siC5c1-M2:
5'-GmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 135)
5'-UmAfUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 136)
siC5c2-M2:
5'-AmGmGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 141)
5'-UmAfUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 142)
siC5c1-M3:
5'-GmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 137)
5'-UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 138)
siC5c2-M3:
5'-AmGmGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 143)
5'-UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 144)
siC5d1-M1:
5'-AmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 193)
5'-UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 194)
siC5d2-M1:
5'-GmGmAmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 199)
5'-UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 200)
siC5d1-M2:
5'-AmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 195)
5'-UmAfAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 196)
siC5d2-M2:
5'-GmGmAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 201)
5'-UmAfAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 202)
siC5d1-M3:
5'-AmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 197)
5'-UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 198)
siC5d2-M3:
5'-GmGmAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 203)
5'-UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 204)
siC5e1-M1:
5'-CmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 253)
5'-UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 254)
siC5e2-M1:
5'-GmGmCmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 259)
5'-UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 260)
siC5e1-M2:
5'-CmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 255)
5'-UmUfUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 256)
siC5e2-M2:
5'-GmGmCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 261)
5'-UmUfUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 262)
siC5e1-M3:
5'-CmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 257)
5'-UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 258)
siC5e2-M3:
5'-GmGmCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 263)
5'-UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 264)
siC5f1-M1:
5'-CmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 313)
5'-UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 314)
siC5f2-M1:
5'-UmAmCmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 319)
5'-UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 320)
siC5f1-M2:
5'-CmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 315)
5'-UmUfUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 316)
siC5f2-M2:
5'-UmAmCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 321)
5'-UmUfUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 322)
siC5f1-M3:
5'-CmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 317)
5'-UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 318)
siC5f2-M3:
5'-UmAmCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 323)
5'-UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 324).
19. Конъюгат миРНК по п. 1, где в миРНК по меньшей мере одна фосфатная группа представляет собой тиофосфатную группу и указанная тиофосфатная связь присутствует в по меньшей мере одном из следующих положений:
положение между первым нуклеотидом и вторым нуклеотидом на 5’-конце смысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 5’-конце смысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 3’-конце смысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 3’-конце смысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 5’-конце антисмысловой цепи;
положение между вторым нуклеотидом и третьим нуклеотидом на 5’-конце антисмысловой цепи;
положение между первым нуклеотидом и вторым нуклеотидом на 3’-конце антисмысловой цепи; и
положение между вторым нуклеотидом и третьим нуклеотидом на 3’-конце антисмысловой цепи.
20. Конъюгат миРНК по любому из пп. 1-19, где миРНК представляет собой любую из siC5a1-M1S, siC5a2-M1S, siC5a1-M2S, siC5a2-M2S, siC5a1-M3S, siC5a2-M3S, siC5b1-M1S, siC5b2-M1S, siC5b1-M2S, siC5b2-M2S, siC5b1-M3S, siC5b2-M3S, siC5c1-M1S, siC5c2-M1S, siC5c1-M2S, siC5c2-M2S, siC5c1-M3S, siC5c2-M3S, siC5d1-M1S, siC5d2-M1S, siC5d1-M2S, siC5d2-M2S, siC5d1-M3S, siC5d2-M3S, siC5e1-M1S, siC5e2-M1S, siC5e1-M2S, siC5e2-M2S, siC5e1-M3S, siC5e2-M3S, siC5f1-M1S, siC5f2-M1S, siC5f1-M2S, siC5f2-M2S, siC5f1-M3S или iC5f2-M3S:
siC5a1-M1S:
5'-CmsUmsUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 25)
5'-UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 26)
siC5a2-M1S:
5'-CmsUmsCmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 31)
5'-UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 32)
siC5a1-M2S:
5'-CmsUmsUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 27)
5'-UmsUfsUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 28)
siC5a2-M2S:
5'-CmsUmsCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 33)
5'-UmsUfsUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 34)
siC5a1-M3S:
5'-CmsUmsUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 29)
5'-UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 30)
siC5a2-M3S:
5'-CmsUmsCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 35)
5'-UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 36)
siC5b1-M1S:
5'-CmsUmsAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 85)
5'-UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 86)
siC5b2-M1S:
5'-UmsAmsCmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 91)
5'-UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 92)
siC5b1-M2S:
5'-CmsUmsAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 87)
5'-UmsAfsAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 88)
siC5b2-M2S:
5'-UmsAmsCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 93)
5'-UmsAfsAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 94)
siC5b1-M3S:
5'-CmsUmsAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 89)
5'-UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 90)
siC5b2-M3S:
5'-UmsAmsCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 95)
5'-UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 96)
siC5c1-M1S:
5'-GmsGmsAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 145)
5'-UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 146)
siC5c2-M1S:
5'-AmsGmsGmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 151)
5'-UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 152)
siC5c1-M2S:
5'-GmsGmsAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 147)
5'-UmsAfsUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 148)
siC5c2-M2S:
5'-AmsGmsGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 153)
5'-UmsAfsUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 154)
siC5c1-M3S:
5'-GmsGmsAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 149)
5'-UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 150)
siC5c2-M3S:
5'-AmsGmsGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 155)
5'-UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 156)
siC5d1-M1S:
5'-AmsGmsAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 205)
5'-UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 206)
siC5d2-M1S:
5'-GmsGmsAmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 211)
5'-UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 212)
siC5d1-M2S:
5'-AmsGmsAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 207)
5'-UmsAfsAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 208)
siC5d2-M2S:
5'-GmsGmsAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 213)
5'-UmsAfsAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 214)
siC5d1-M3S:
5'-AmsGmsAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 209)
5'-UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 210)
siC5d2-M3S:
5'-GmsGmsAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 215)
5'-UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 216)
siC5e1-M1S:
5'-CmsCmsAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 265)
5'-UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 266)
siC5e2-M1S:
5'-GmsGmsCmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 271)
5'-UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 272)
siC5e1-M2S:
5'-CmsCmsAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 267)
5'-UmsUfsUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 268)
siC5e2-M2S:
5'-GmsGmsCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 273)
5'-UmsUfsUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 274)
siC5e1-M3S:
5'-CmsCmsAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 269)
5'-UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 270)
siC5e2-M3S:
5'-GmsGmsCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 275)
5'-UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 276)
siC5f1-M1S:
5'-CmsCmsAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 325)
5'-UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 326)
siC5f2-M1S:
5'-UmsAmsCmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 331)
5'-UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 332)
siC5f1-M2S:
5'-CmsCmsAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 327)
5'-UmsUfsUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 328)
siC5f2-M2S:
5'-UmsAmsCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 333)
5'-UmsUfsUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 334)
siC5f1-M3S:
5'-CmsCmsAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 329)
5'-UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 330)
siC5f2-M3S:
5'-UmsAmsCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 335)
5'-UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 336).
21. Конъюгат миРНК по любому из пп. 1-20, где 5’-концевой нуклеотид в антисмысловой цепи миРНК представляет собой нуклеотид с 5’-фосфатной группой или нуклеотид, модифицированный аналогом 5’-фосфатной группы;
или нуклеотид с 5’-фосфатной группой представляет собой нуклеотид, представленный Формулой (2); и нуклеотид, модифицированный аналогом 5’-фосфатной группы, выбран из нуклеотида, представленного любой из Формул (3)-(6):
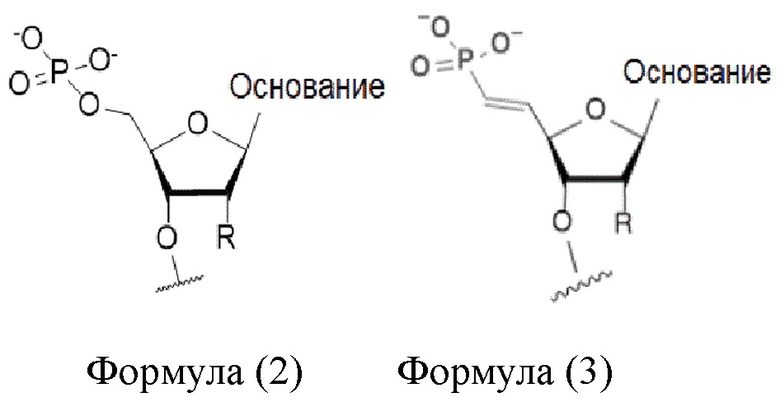

где R выбран из H, OH, метокси или F; и Основание представляет собой основание, выбранное из A, U, C, G или T.
22. Конъюгат миРНК по любому из пп. 1-21, где миРНК представляет собой любую из siC5a1-M1P1, siC5a1-M2P1, siC5a1-M3P1, siC5a2-M1P1, siC5a2-M2P1, siC5a2-M3P1, siC5a1-M1SP1, siC5a1-M2SP1, siC5a1-M3SP1, siC5a2-M1SP1, siC5a2-M2SP1, siC5a2-M3SP1, siC5b1-M1P1, siC5b1-M2P1, siC5b1-M3P1, siC5b2-M1P1, siC5b2-M2P1, siC5b2-M3P1, siC5b1-M1SP1, siC5b1-M2SP1, siC5b1-M3SP1, siC5b2-M1SP1, siC5b2-M2SP1, siC5b2-M3SP1, siC5c1-M1P1, siC5c1-M2P1, siC5c1-M3P1, siC5c2-M1P1, siC5c2-M2P1, siC5c2-M3P1, siC5c1-M1SP1, siC5c1-M2SP1, siC5c1-M3SP1, siC5c2-M1SP1, siC5c2-M2SP1, siC5c2-M3SP1, siC5d1-M1P1, siC5d1-M2P1, siC5d1-M3P1, siC5d2-M1P1, siC5d2-M2P1, siC5d2-M3P1, siC5d1-M1SP1, siC5d1-M2SP1, siC5d1-M3SP1, siC5d2-M1SP1, siC5d2-M2SP1, siC5d2-M3SP1, siC5e1-M1P1, siC5e1-M2P1, siC5e1-M3P1, siC5e2-M1P1, siC5e2-M2P1, siC5e2-M3P1, siC5e1-M1SP1, siC5e1-M2SP1, siC5e1-M3SP1, siC5e2-M1SP1, siC5e2-M2SP1, siC5e2-M3SP1, siC5f1-M1P1, siC5f1-M2P1, siC5f1-M3P1, siC5f2-M1P1, siC5f2-M2P1, siC5f2-M3P1, siC5f1-M1SP1, siC5f1-M2SP1, siC5f1-M3SP1, siC5f2-M1SP1, siC5f2-M2SP1 или siC5f2-M3SP1:
siC5a1-M1P1:
5'-CmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 37)
5'-P1UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGm-3' (SEQ ID NO: 38)
siC5a1-M2P1:
5'-CmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 39)
5'-P1UmUfUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmAmGm-3' (SEQ ID NO: 40)
siC5a1-M3P1:
5'-CmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 41)
5'-P1UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGm-3' (SEQ ID NO: 42)
siC5a2-M1P1:
5'-CmUmCmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 43)
5'-P1UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 44)
siC5a2-M2P1:
5'-CmUmCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 45)
5'-P1UmUfUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 46)
siC5a2-M3P1:
5'-CmUmCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 47)
5'-P1UmUfUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmAmAm-3' (SEQ ID NO: 48)
siC5a1-M1SP1:
5'-CmsUmsUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 49)
5'-P1UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 50)
siC5a1-M2SP1:
5'-CmsUmsUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 51)
5'-P1UmsUfsUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 52)
siC5a1-M3SP1:
5'-CmsUmsUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 53)
5'-P1UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmsAmsGm-3' (SEQ ID NO: 54)
siC5a2-M1SP1:
5'-CmsUmsCmUmUmCmAmUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 55)
5'-P1UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 56)
siC5a2-M2SP1:
5'-CmsUmsCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 57)
5'-P1UmsUfsUmGmUmCfUmGfUfAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 58)
siC5a2-M3SP1:
5'-CmsUmsCmUmUmCmAfUmUfCfAfUmAmCmAmGmAmCmAmAmAm-3' (SEQ ID NO: 59)
5'-P1UmsUfsUmGmUmCfUmGmUmAmUmGmAmAfUmGfAmAmGmAmGmsAmsAm-3' (SEQ ID NO: 60)
siC5b1-M1P1:
5'-CmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 97)
5'-P1UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 98)
siC5b1-M2P1:
5'-CmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 99)
5'-P1UmAfAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 100)
siC5b1-M3P1:
5'-CmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 101)
5'-P1UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAm-3' (SEQ ID NO: 102)
siC5b2-M1P1:
5'-UmAmCmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 103)
5'-P1UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 104)
siC5b2-M2P1:
5'-UmAmCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 105)
5'-P1UmAfAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 106)
siC5b2-M3P1:
5'-UmAmCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 107)
5'-P1UmAfAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmUmGm-3' (SEQ ID NO: 108)
siC5b1-M1SP1:
5'-CmsUmsAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 109)
5'-P1UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 110)
siC5b1-M2SP1:
5'-CmsUmsAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 111)
5'-P1UmsAfsAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 112)
siC5b1-M3SP1:
5'-CmsUmsAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 113)
5'-P1UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmsUmsAm-3' (SEQ ID NO: 114)
siC5b2-M1SP1:
5'-UmsAmsCmUmAmCmAmGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 115)
5'-P1UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 116)
siC5b2-M2SP1:
5'-UmsAmsCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 117)
5'-P1UmsAfsAmAmUmCfUmUfCfUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 118)
siC5b2-M3SP1:
5'-UmsAmsCmUmAmCmAfGmUfUfUfAmGmAmAmGmAmUmUmUmAm-3' (SEQ ID NO: 119)
5'-P1UmsAfsAmAmUmCfUmUmCmUmAmAmAmCfUmGfUmAmGmUmAmsUmsGm-3' (SEQ ID NO: 120)
siC5c1-M1P1:
5'-GmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 157)
5'-P1UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 158)
siC5c1-M2P1:
5'-GmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 159)
5'-P1UmAfUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 160)
siC5c1-M3P1:
5'-GmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 161)
5'-P1UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUm-3' (SEQ ID NO: 162)
siC5c2-M1P1:
5'-AmGmGmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 163)
5'-P1UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 164)
siC5c2-M2P1:
5'-AmGmGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 165)
5'-P1UmAfUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 166)
siC5c2-M3P1:
5'-AmGmGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 167)
5'-P1UmAfUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmGmGm-3' (SEQ ID NO: 168)
siC5c1-M1SP1:
5'-GmsGmsAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 169)
5'-P1UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 170)
siC5c1-M2SP1:
5'-GmsGmsAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 171)
5'-P1UmsAfsUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 172)
siC5c1-M3SP1:
5'-GmsGmsAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 173)
5'-P1UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmsCmsUm-3' (SEQ ID NO: 174)
siC5c2-M1SP1:
5'-AmsGmsGmGmAmAmGmGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 175)
5'-P1UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 176)
siC5c2-M2SP1:
5'-AmsGmsGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 177)
5'-P1UmsAfsUmUmGmCfUmCfGfGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 178)
siC5c2-M3SP1:
5'-AmsGmsGmGmAmAmGfGmUfUfAfCmCmGmAmGmCmAmAmUmAm-3' (SEQ ID NO: 179)
5'-P1UmsAfsUmUmGmCfUmCmGmGmUmAmAmCfCmUfUmCmCmCmUmsGmsGm-3' (SEQ ID NO: 180)
siC5d1-M1P1:
5'-AmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 217)
5'-P1UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 218)
siC5d1-M2P1:
5'-AmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 219)
5'-P1UmAfAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 220)
siC5d1-M3P1:
5'-AmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 221)
5'-P1UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCm-3' (SEQ ID NO: 222)
siC5d2-M1P1:
5'-GmGmAmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 223)
5'-P1UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 224)
siC5d2-M2P1:
5'-GmGmAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 225)
5'-P1UmAfAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 226)
siC5d2-M3P1:
5'-GmGmAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 227)
5'-P1UmAfAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmUmGm-3' (SEQ ID NO: 228)
siC5d1-M1SP1:
5'-AmsGmsAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 229)
5'-P1UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 230)
siC5d1-M2SP1:
5'-AmsGmsAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 231)
5'-P1UmsAfsAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 232)
siC5d1-M3SP1:
5'-AmsGmsAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 233)
5'-P1UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmsCmsCm-3' (SEQ ID NO: 234)
siC5d2-M1SP1:
5'-GmsGmsAmGmAmAmCmAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 235)
5'-P1UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 236)
siC5d2-M2SP1:
5'-GmsGmsAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 237)
5'-P1UmsAfsAmUmUmCfUmGfCfUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 238)
siC5d2-M3SP1:
5'-GmsGmsAmGmAmAmCfAmGfAfCfAmGmCmAmGmAmAmUmUmAm-3' (SEQ ID NO: 239)
5'-P1UmsAfsAmUmUmCfUmGmCmUmGmUmCmUfGmUfUmCmUmCmCmsUmsGm-3' (SEQ ID NO: 240)
siC5e1-M1P1:
5'-CmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 277)
5'-P1UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 278)
siC5e1-M2P1:
5'-CmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 279)
5'-P1UmUfUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 280)
siC5e1-M3P1:
5'-CmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 281)
5'-P1UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCm-3' (SEQ ID NO: 282)
siC5e2-M1P1:
5'-GmGmCmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 283)
5'-P1UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 284)
siC5e2-M2P1:
5'-GmGmCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 285)
5'-P1UmUfUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 286)
siC5e2-M3P1:
5'-GmGmCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 287)
5'-P1UmUfUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmUmGm-3' (SEQ ID NO: 288)
siC5e1-M1SP1:
5'-CmsCmsAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 289)
5'-P1UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 290)
siC5e1-M2SP1:
5'-CmsCmsAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 291)
5'-P1UmsUfsUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 292)
siC5e1-M3SP1:
5'-CmsCmsAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 293)
5'-P1UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmsCmsCm-3' (SEQ ID NO: 294)
siC5e2-M1SP1:
5'-GmsGmsCmCmAmAmGmAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 295)
5'-P1UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 296)
siC5e2-M2SP1:
5'-GmsGmsCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 297)
5'-P1UmsUfsUmGmCmAfGmCfGfUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 298)
siC5e2-M3SP1:
5'-GmsGmsCmCmAmAmGfAmAfGfAfAmCmGmCmUmGmCmAmAmAm-3' (SEQ ID NO: 299)
5'-P1UmsUfsUmGmCmAfGmCmGmUmUmCmUmUfCmUfUmGmGmCmCmsUmsGm-3' (SEQ ID NO: 300)
siC5f1-M1P1:
5'-CmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 337)
5'-P1UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 338)
siC5f1-M2P1:
5'-CmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 339)
5'-P1UmUfUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 340)
siC5f1-M3P1:
5'-CmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 341)
5'-P1UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAm-3' (SEQ ID NO: 342)
siC5f2-M1P1:
5'-UmAmCmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 343)
5'-P1UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 344)
siC5f2-M2P1:
5'-UmAmCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 345)
5'-P1UmUfUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 346)
siC5f2-M3P1:
5'-UmAmCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 347)
5'-P1UmUfUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmAmCm-3' (SEQ ID NO: 348)
siC5f1-M1SP1:
5'-CmsCmsAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 349)
5'-P1UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 350)
siC5f1-M2SP1:
5'-CmsCmsAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 351)
5'-P1UmsUfsUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 352)
siC5f1-M3SP1:
5'-CmsCmsAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 353)
5'-P1UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmsUmsAm-3' (SEQ ID NO: 354)
siC5f2-M1SP1:
5'-UmsAmsCmCmAmGmUmAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 355)
5'-P1UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 356)
siC5f2-M2SP1:
5'-UmsAmsCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 357)
5'-P1UmsUfsUmCmUmGfGmCfUfUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 358)
siC5f2-M3SP1:
5'-UmsAmsCmCmAmGmUfAmAfGfCfAmAmGmCmCmAmGmAmAmAm-3' (SEQ ID NO: 359)
5'-P1UmsUfsUmCmUmGfGmCmUmUmGmCmUmUfAmCfUmGmGmUmAmsAmsCm-3' (SEQ ID NO: 360).
23. Применение конъюгата миРНК по любому из пп. 1-22 для производства лекарственного средства для лечения и/или предупреждения миастении гравис.
24. Способ ингибирования экспрессии гена C5 в гепатоците, включающий приведение эффективного количества конъюгата миРНК по любому из пп. 1-22 в контакт с указанным гепатоцитом.
| EA 201591707 A1, 31.03.2016 | |||
| WO 2016201301 A1, 15.12.2016 | |||
| WO 2018013525 A1, 18.01.2018 | |||
| WO 2017178656 A1, 19.10.2017. |
Авторы
Даты
2024-04-08—Публикация
2020-05-21—Подача