Область техники
Настоящее изобретение касается пиридазинового соединения и гербицида, содержащего это соединение в качестве действующего вещества.
В настоящей заявке испрашивается приоритет по заявке на патент Японии № 2019-174532, поданной в Японии 25 сентября 2019 г., содержание которой включено в настоящий текст посредством ссылки.
Уровень техники
При возделывании сельскохозяйственных и плодоовощных культур для борьбы с сорняками могут применяться гербициды. К настоящему моменту различные соединения были предложены в качестве действующих веществ для гербицидов.
Например, в Патентом документе 1 раскрыто пиридазиновое соединение, представленное формулой (A), и подобные ему.
[Хим. 1]
 … (А)
… (А)
Документы уровня техники
Патентный документ
Патентный документ 1. WO2013/050421.
Краткое описание сути изобретения
Задачи, на решение которых направлено настоящее изобретение
От гербицидов требуется не только прекрасная эффективность в борьбе с сорняками, но также уменьшенная фитотоксичность по отношению к культурным растениям, пониженная вероятность накопления в окружающей среде, кроме того, они не должны загрязнять окружающую среду.
Целью настоящего изобретения является разработка нового пиридазинового соединения, которое может применяться в качестве действующего вещества в гербицидах, которое обладает надежной эффективностью в борьбе с сорняками даже в низкой дозировке, обладает сниженной фитотоксичностью по отношению к культурным растениям и безопасно для окружающей среды; а также разработка соответствующего гербицида.
Результатом интенсивных исследований, направленных на решение описанной выше задачи, стало настоящее изобретение, включающее описанные ниже аспекты.
[1] Соединение, имеющее формулу (I), или его соль.
[Хим. 2]
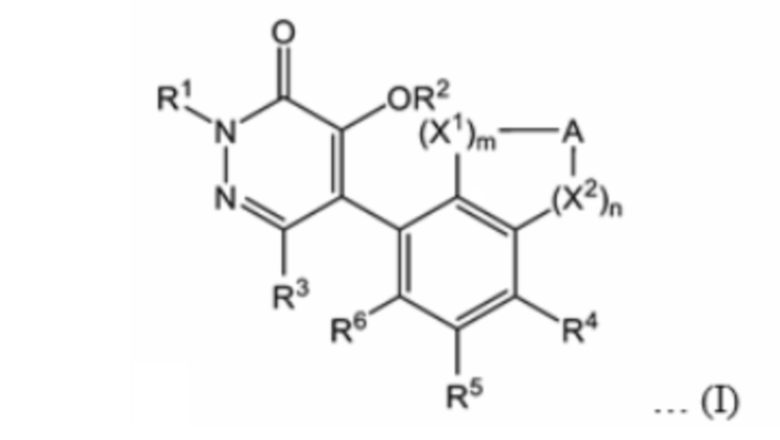
В формуле (I)
R1 представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу,
R2 представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, группу Ra-CO-, группу RaO-CO-, группу RaNH-CO-, группу Ra2N-CO-, группу Ra-SO2-, группу Ra-CO-O-CRb2-, или группу RaO-CO-O-CRb2-,
каждый Ra независимо представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, замещенную или незамещенную C3 - C6 циклоалкильную группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу, или замещенную или незамещенную 5-6-членную гетероциклильную группу,
каждый Rb независимо представляет собой атом водорода или замещенную или незамещенную C1 - C6 алкильную группу,
R3 представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу,
R4 представляет собой галоген, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C1 - C6 алкокси-группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу, замещенную или незамещенную 5-6-членную гетероарильную группу или циано-группу,
R5 представляет собой атом водорода или галоген,
R6 представляет собой атом водорода или галоген,
A представляет собой замещенную или незамещенную C1 - C4 алкиленовую группу, замещенную или незамещенную C2 - C3 алкениленовую группу, или замещенную или незамещенную C1 - C2 алкиленокси C1 - C2 алкиленовую группу,
X1 представляет собой атом кислорода или сульфонильную группу,
X2 представляет собой атом кислорода, сульфенильную группу, сульфинильную группу, сульфонильную группу, группу -S(=NRc)- или группу -S(=O)(=NRc)-,
каждый Rc независимо представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу или циано-группу,
m равен 0 или 1, n равен 0 или 1, и
сумма m и n равна 1 или 2, и когда A представляет собой замещенную или незамещенную метиленовую группу, сумма m и n равна 2.
[2] Гербицид, содержащий по меньшей мере один представитель, выбранный из группы, состоящей из соединений по п. [1] и их солей, в качестве действующего вещества.
[3] Способ борьбы с однодольными и/или двудольными сорняками культурных растений, включающий стадию нанесения соединения по п. [1] или его соли или гербицида, содержащего указанное выше соединение, на указанные выше сорняки и/или указанные выше растения и/или место их произрастания.
Эффект, обеспечиваемый изобретением
Пиридазиновые соединения по настоящему изобретению обладают надежной эффективностью в борьбе с сорняками даже в низкой дозировке, обладают пониженной фитотоксичностью по отношению к культурным растениям и безопасно для окружающей среды. Поэтому пиридазиновые соединения по настоящему изобретению можно применять в качестве действующего вещества в гербицидах. Гербициды по настоящему изобретению можно безопасно использовать для борьбы с сорняками при выращивании сельскохозяйственных и плодовоовощных культур.
Варианты осуществления изобретения
Пиридазиновое соединение по настоящему изобретению (далее по тексту для простоты в некоторых случаях может именоваться “соединение по настоящему изобретению”) представляет собой соединение, имеющее формулу (I) ((в некоторых случаях именуется “соединение (I)”) или соль соединения (I). Соединение (I) включает также гидраты, различные типы сольватов, полиморфы кристаллических форм и т.п. Соединение (I) может иметь стереоизомеры и таутомеры при наличии асимметрических атомов углерода, двойных связей и т.п. Все такие изомеры и их смеси входят в объем настоящего изобретения.
Термин “незамещенный” при использовании в настоящем тексте означает только группу, которая является ядром. Когда упоминается только название группы, которая является ядром, без приставки “замещенный”, это автоматически означает “незамещенный”, если не указано иное.
С другой стороны, термин “замещенный” означает, что один из атомов водорода в группе, являющейся ядром, замещен на группу, имеющую такую же структуру, как у ядра, или другую структуру. Таким образом, “заместитель” – это другая группа, связанная с группой, являющейся ядром. Число заместителей может составлять один, два или больше. Если присутствуют два или больше заместителей, то они могут быть одинаковыми или разными.
Такие термины как “C1 - C6” означают, что число атомов углерода в группе, которая является материнским ядром, составляет от 1 до 6 и т.п. Это число атомов углерода не включает атомы углерода, присутствующие в заместителе. Например, бутильная группа, содержащая в качестве заместителя этокси-группу, классифицируется как C2 алкокси C4 алкильная группа.
“Заместитель” не ограничивается каким-либо особым образом, при условии, что он является химически устойчивым и обеспечивает эффект настоящего изобретения.
Частные примеры групп, которые могут являться “заместителем”, включают группы, перечисленные ниже.
C1 - C6 алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изо-пропильная группа, н-бутильная группа, втор-бутильная группа, изо-бутильная группа, трет-бутильная группа, н-пентильная группа и н-гексильная группа;
C2 - C6 алкенильные группы, такие как винильная группа, 1-пропенильная группа, 2-пропенильная группа (аллильная группа), 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа, 1-метил-2-пропенильная группа и 2-метил-2-пропенильная группа;
C2 - C6 алкинильные группы, такие как этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа, 3-бутинильная группа и 1-метил-2-пропинильная группа;
C3 - C6 циклоалкильные группы, такие как циклопропильная группа, циклобутильная группа, циклопентильная группа и циклогексильная группа;
фенильная группа, нафтильная группа;
фенил C1 - C6 алкильные группы, такие как бензильная группа и фенетильная группа;
3-6-членные гетероциклильные группы;
3-6-членные гетероциклил C1 - C6 алкильные группы;
гидроксильная группа;
C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа;
C2 - C6 алкенилокси-группы, такие как винилокси-группа, аллилокси-группа, пропенилокси-группа и бутенилокси-группа;
C2 - C6 алкинилокси-группы, такие как этинилокси-группа и пропаргилокси-группа;
фенокси-группа, нафтокси-группа;
фенил C1 - 6 алкокси-группы, такие как бензилокси-группа и фенетилокси-группа;
5-6-членные гетероарилокси группы, такие как тиазолилокси-группа и пиридилокси-группа;
5-6-членный гетероарил C1 - C6 алкилокси-группы, такие как тиазолилметилокси-группа и пиридилметилокси-группа;
формильная группа;
C1 - C6 алкилкарбонильные группы, такие как ацетильная группа и пропионильная группа;
формилокси-группа;
C1 - C6 алкилкарбонилокси группы, такие как ацетилокси-группа и пропионилокси-группа;
бензоильные группы;
C1 - C6 алкоксикарбонильные группы, такие как метоксикарбонильная группа, этоксикарбонильная группа, н-пропоксикарбонильная группа, изо-пропоксикарбонильная группа, н-бутоксикарбонильная группа и трет-бутоксикарбонильная группа;
C1 - C6 алкоксикарбонилокси-группы, такие как метоксикарбонилокси-группа, этоксикарбонилокси-группа, н-пропоксикарбонилокси-группа, изо-пропоксикарбонилокси-группа, н-бутоксикарбонилокси-группа и трет-бутоксикарбонилокси-группа;
карбоксильная группа;
галогены, такие как атом фтора, атом хлора, атом брома и атом иода;
C1 - C6 галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа, 2,2,2-трифторэтильная группа и 1-фтор-н-бутильная группа;
C2 - C6 галогеналкенильные группы, такие как 2-хлор-1-пропенильная группа и 2-фтор-1-бутенильная группа;
C2 - C6 галогеналкинильные группы, такие как 4,4-дихлор-1-бутинильная группа, 4-фтор-1-пентинильная группа и 5-бром-2-пентинильная группа;
C1 - C6 галогеналкокси-группы, такие как трифторметокси-группа, 2,2,2-трифторэтокси-группа и 2,3-дихлорбутокси-группа;
C2 - C6 галогеналкенилокси-группы, такие как 2-хлорпропенилокси-группа и 3-бромбутенилокси-группа;
C1 - C6 галогеналкилкарбонильные группы, такие как хлорацетильная группа, трифторацетильная группа и трихлорацетильная группа;
амино-группа;
C1 - C6 алкил-замещенные амино-группы, такие как метиламино-группа, диметиламино-группа и диэтиламино-группа;
анилино-группа, нафтиламино-группа;
фенил C1 - C6 алкиламино-группы, такие как бензиламино-группа и фенетиламино-группа;
формиламино-группа;
C1 - C6 алкилкарбониламино-группы, такие как ацетиламино-группа, пропаноиламино-группа, бутириламино-группа и изо-пропилкарбониламино-группа;
C1 - C6 алкоксикарбониламино-группы, такие как метоксикарбониламино-группа, этоксикарбониламино-группа, н-пропоксикарбониламино-группа и изо-пропоксикарбониламино-группа;
замещенные или незамещенные аминокарбонильные группы, такие как аминокарбонильной группа, диметиламинокарбонильной группа, фениламинокарбонильной группа и N-фенил-N-метиламинокарбонильной группа,
имино C1 - C6 алкильные группы, такие как иминометильная группа, (1-имино)этильная группа и (1-имино)-н-пропильная группа;
замещенные или незамещенные имино C1 - C6 алкильные группы, такие как N-гидрокси-иминометильная группа, (1-(N-гидрокси)-имино) этильная группа, (1-(N-гидрокси)-имино) пропильная группа, N-метокси-иминометильная группа и 1-(N-метокси)-имино) этильная группа;
аминокарбонильная группа;
C1 - C6 алкил-замещенные аминокарбонилокси-группы, такие как этиламинокарбонилокси-группа и диметиламинокарбонилокси-группа;
меркапто-группа;
C1 - C6 алкилтио-группы, такие как метилтио-группа, этилтио-группа, н-пропилтио-группа, изо-пропилтио-группа, н-бутилтио-группа изо-бутилтио-группа, втор-бутилтио-группа и трет-бутилтио-группа;
C1 - C6 галогеналкилтио-группы, такие как трифторметилтио-группа и 2,2,2-трифторэтилтио-группа;
фенилтио-группа;
5-6-членные гетероарилтио-группы, такие как тиазолилтио-группа и пиридилтио-группа;
C1 - C6 алкилсульфинильные группы, такие как метилсульфинильная группа, этилсульфинильная группа и трет-бутилсульфинильная группа;
C1 - C6 галогеналкилсульфинильные группы, такие как трифторметилсульфинильная группа и 2,2,2-трифторэтилсульфинильная группа;
фенилсульфинильная группа;
5-6-членные гетероарилсульфинильные группы, такие как тиазолилсульфинильная группа и пиридилсульфинильная группа;
C1 - C6 алкилсульфонильные группы, такие как метилсульфонильная группа, этилсульфонильная группа и трет-бутилсульфонильная группа;
C1 - C6 галогеналкилсульфонильные группы, такие как трифторметилсульфонильная группа и 2,2,2-трифторэтилсульфонильная группа;
фенилсульфонильная группа;
5-6-членные гетероарилсульфонильные группы, такие как тиазолилсульфонильная группа и пиридилсульфонильная группа;
C1 - C6 алкилсульфонилокси-группы, такие как метилсульфонилокси-группа, этилсульфонилокси-группа и трет-бутилсульфонилокси-группа;
C1 - C6 галогеналкилсульфонилокси-группы, такие как трифторметилсульфонилокси-группа и 2,2,2-трифторэтилсульфонилокси-группа;
три (C1 - C6 алкил)-замещенные силильные группы, такие как триметилсилильная группа, триэтилсилильная группа и трет-бутилдиметилсилильная группа;
трифенилсилильная группа;
пентафторсульфанильная группа;
циано-группа; и нитро-группа.
Кроме того, в этих “заместителях” любой атом водорода в любом из перечисленных выше заместителей может быть замещен группой, имеющей другую структуру. Примеры “заместителей” в этом случае включают C1 - C6 алкильные группы, C1 - C6 галогеналкильные группы, C1 - C6 алкокси-группы, C1 - C6 галогеналкокси-группы, галогены, циано-группу и нитро-группу.
Кроме того, описанная выше “3-6-членная гетероциклильная группа” представляет собой 3-членное кольцо, 4-членное кольцо, 5-членное кольцо или 6-членное кольцо, содержащее 1-4 гетероатомов, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы, в качестве атомов-членов кольца. Гетероциклильная группа может быть моноциклической или полициклической. Если полициклическая гетероциклильная группа включает по меньшей мере одно гетероциклическое кольцо, остальные кольца могут представлять собой насыщенное алициклическое кольцо, ненасыщенное алициклическое кольцо или ароматическое кольцо. Примеры “3-6-членной гетероциклильной группы” включают 3-6-членную насыщенную гетероциклильную группу, 5-6-членную гетероарильную группу и 5-6-членную ненасыщенную гетероциклильную группу, и т.п.
Примеры 3-6-членной насыщенной гетероциклильной группы включают следующие: азиридинильная группа, эпокси-группа, азетидинильная группа, пирролидинильная группа, тетрагидрофуранильная группа, диоксоланильная группа, тетрагидропиранильная группа, пиперидильная группа, пиперазинильная группа, морфолинильная группа, диоксанильная группа и т.п.
Примеры 5-6-членной ненасыщенной гетероциклильной группы включают следующие: пирролинильная группа, дигидрофуранильная группа, имидазолинильная группа, пиразолинильная группа, оксазолинильная группа, изооксазолинильная группа, тиазолинильная группа, изотиазолинильная группа, дигидропиранильная группа, дигидрооксадиинильная группа, и т.п.
Примеры 5-членной гетероарильной группы включают следующие: пирролильная группа, фурильная группа, тиенильная группа, имидазолильная группа, пиразолильная группа, оксазолильная группа, изоксазолильная группа, тиазолильная группа, изотиазолильная группа, триазолильная группа, оксадиазолильная группа, тиадиазолильная группа и тетразолильная группа, и т.п.
Примеры 6-членной гетероарильной группы включают следующие: пиридильная группа, пиразинильная группа, пиримидинильная группа, пиридазинильная группа, триазинильная группа и т.п.
R1
R1 представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу.
“C1 - C6 алкильная группа” в качестве R1 может быть линейной или разветвленной. Примеры “C1 - C6 алкильной группы” включают следующие: метильная группа, этильная группа, н-пропильная группа, н-бутильная группа, н-пентильная группа, н-гексильная группа, изо-пропильная группа, изо-бутильная группа, втор-бутильная группа, трет-бутильная группа, изо-пентильная группа, неопентильная группа, 2-метилбутильная группа и изо-гексильная группа.
Примеры “C2 - C6 алкенильной группы” в качестве R1 включают следующие: винильная группа, 1-пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа, 1-метил-2-пропенильная группа, 2-метил-2-пропенильная группа, 1-пентенильная группа, 2-пентенильная группа, 3-пентенильная группа, 4-пентенильная группа, 1-метил-2-бутенильная группа, 2-метил-2-бутенильная группа, 1-гексенильная группа, 2-гексенильная группа, 3-гексенильная группа, 4-гексенильная группа и 5-гексенильная группа.
Примеры “C2 - C6 алкинильной группы” в качестве R1 включают следующие: этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа, 3-бутинильная группа, 1-метил-2-пропинильная группа, 2-метил-3-бутинильная группа, 1-пентинильная группа, 2-пентинильная группа, 3-пентинильная группа, 4-пентинильная группа, 1-метил-2-бутинильная группа, 2-метил-3-пентинильная группа, 1-гексинильная группа и 1,1-диметил-2-бутинильная группа.
Примеры предпочтительных заместителей в “C1 - C6 алкильной группе”, “C2 - C6 алкенильной группе” и “C2 - C6 алкинильной группе” в качестве R1 включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; фенильную группу, нафтильную группу; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную фенильную группу, такую как 4-хлорфенильная группа, 4-трифторметилфенильная группа, 4-трифторметоксифенильная группа; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную нафтильную группу; и циано-группу.
Примеры “C3 - C6 циклоалкильной группы” в качестве R1 включают следующие: циклопропильная группа, циклобутильная группа, циклопентильная группа и циклогексильная группа.
Примеры предпочтительных заместителей в “C3 - C8 циклоалкильной группе” в качестве R1 включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; C1 - C6 алкильную группу, такую как метильная группа, этильная группа, н-пропильная группа, изо-пропильная группа, н-бутильная группа, втор-бутильная группа, изо-бутильная группа, трет-бутильная группа, н-пентильная группа и н-гексильная группа; C1 - C6 галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа и 1-фтор-н-бутильная группа; гидроксильную группу; C1 - C6 алкокси-группу, такую как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группу, такую как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; и циано-группу.
В настоящем изобретении R1 предпочтительно представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу.
Заместитель в C1 - C6 алкильной группе предпочтительно представляет собой галоген или C1 - C6 алкокси-группу.
R2
R2 представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, группу Ra-CO-, группу RaO-CO-, группу RaNH-CO-, группу Ra2N-CO-, группу Ra-SO2-, группу Ra-CO-O-CRb2-, или группу RaO-CO-O-CRb2-.
Частные примеры замещенной или незамещенной C1 - C6 алкильной группы, замещенной или незамещенной C2 - C6 алкенильной группы или замещенной или незамещенной C2 - C6 алкинильной группы в качестве R2 включают те же, которые были приведены в качестве примера для R1.
Каждый Ra в “группе Ra-CO-”, “группе RaNH-CO-”, “группе Ra2N-CO-”, “группе Ra-SO2-“, “группе Ra-CO-O-CRb2-” и “группе RaO-CO-O-CRb2-” в качестве R2 независимо представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, замещенную или незамещенную C3 - C6 циклоалкильную группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу, или замещенную или незамещенную 5-6-членную гетероциклильную группу.
Примеры “C1 - C6 алкильной группы” в качестве Ra включают следующие: метильная группа, этильная группа, н-пропильная группа, н-бутильная группа, н-пентильная группа, н-гексильная группа, изо-пропильная группа, изо-бутильная группа, втор-бутильная группа, трет-бутильная группа, изо-пентильная группа, неопентильная группа, 2-метилбутильная группа, изо-гексильная группа и т.п.
Примеры “C2 - C6 алкенильной группы” в качестве Ra включают следующие: винильная группа, 1-пропенильная группа и т.п.
Примеры “C2 - C6 алкинильной группы” в качестве Ra включают следующие: этинильная группа, 1-пропинильная группа и т.п.
Примеры предпочтительных заместителей в “C1 - C6 алкильной группе”, “C2 - C6 алкенильной группе” и “C2 - C6 алкинильной группе” в качестве Ra включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; C3 - C6 циклоалкильные группы, такие как циклопропильная группа, циклобутильная группа, циклопентильная группа и циклогексильная группа; фенильную группу, нафтильную группу; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную фенильную группу, такую как 4-хлорфенильная группа, 4-трифторметилфенильная группа, 4-трифторметоксифенильная группа; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную нафтильную группу; и циано-группу.
Примеры “C3 - C6 циклоалкильной группы” в качестве Ra включают следующие: циклопропильная группа, циклобутильная группа, циклопентильная группа, циклогексильная группа и т.п.
“5-6-членная гетероциклильная группа” в качестве Ra представляет собой 5-членное кольцо или 6-членное кольцо, содержащее в кольце 1, 2, 3 или 4 гетероатомов, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. В случае наличия 2 или больше гетероатомов, они могут быть одинаковыми или разными. Примеры “5-6-членной гетероциклильной группы” включают 5-6-членную насыщенную гетероциклильную группу, 5-6-членную гетероарильную группу, 5-6-членную ненасыщенную гетероциклильную группу и т.п.
Примеры 5-6-членной насыщенной гетероциклильной группы включают следующие: пирролидинильная группа, тетрагидрофуранильная группа, диоксоланильная группа, тетрагидропиранильная группа, пиперидинильная группа, пиперазинильная группа, морфолинильная группа, диоксанильная группа и т.п.
Примеры 5-6-членной ненасыщенной гетероциклильной группы включают следующие: пирролинильная группа, дигидрофуранильная группа, имидазолинильная группа, пиразолинильная группа, оксазолинильная группа, изоксазолинильная группа, тиазолидинильная группа, изотиазолидинильная группа и т.п.
Примеры 6-членной ненасыщенной гетероциклильной группы включают следующие: дигидропиранильная группа, дигидрооксадиинильная группа и т.п.
Примеры 5-членной гетероарильной группы включают следующие: пирролильная группа, фурильная группа, тиенильная группа, имидазолильная группа, пиразолильная группа, оксазолильная группа, изоксазолильная группа, тиазолильная группа, изотиазолильная группа, триазолильная группа, оксадиазолильная группа, тиадиазолильная группа, тетразолильная группа и т.п.
Примеры 6-членной гетероарильной группы включают следующие: пиридильная группа, пиразинильная группа, пиримидинильная группа, пиридазинильная группа, триазинильная группа и т.п.
Примеры предпочтительных заместителей в “C3 - C6 циклоалкильной группе”, “фенильной группе”, “нафтильной группе” или “5-6-членной гетероциклильной группе” в качестве Ra включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; C1 - C6 алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изо-пропильная группа, н-бутильная группа, втор-бутильная группа, изо-бутильная группа, трет-бутильная группа, н-пентильная группа и н-гексильная группа; C1 - C6 галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа и 1-фтор-н-бутильная группа; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; фенильную группу, нафтильную группу; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную фенильную группу, такую как 4-хлорфенильная группа, 4-трифторметилфенильная группа или 4-трифторметоксифенильная группа; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную нафтильную группу; и циано-группу.
Примеры “группы Ra-CO-” в качестве R2 включают ацетильную группу и т.п.
Примеры “группы RaO-CO-” в качестве R2 включают метоксикарбонильную группу, этоксикарбонильную группу и т.п.
Примеры “группы RaNH-CO-” в качестве R2 включают N-метиламинокарбонильную группу, N-(изо-пропил)аминокарбонильную группу и т.п.
Примеры “группы Ra2N-CO-” в качестве R2 включают N,N-диметиламинокарбонильную группу, N-(изо-пропил)-N-метиламинокарбонильную группу и т.п.
Примеры “группы Ra-SO2-” в качестве R2 включают метансульфонильную группу и т.п.
В “группе Ra-CO-O-CRb2-” или “группе RaO-CO-O-CRb2-” в качестве R2, каждый Rb независимо представляет собой атом водорода или замещенную или незамещенную C1 - C6 алкильную группу.
Примеры “C1 - C6 алкильной группы в качестве Rb включают те же, которые перечислены для Ra. Кроме того, примеры заместителей в “C1 - C6 алкильной группе” в качестве Rb, включают те же, которые перечислены для Ra.
Примеры “группы Ra-CO-O-CRb2-” в качестве R2 включают следующие: ацетоксиметильная группа, изопропилкарбонилоксиметильная группа, 1-ацетоксиэтильная группа, 1-изопропилкарбонилоксиэтильная группа и т.п.
Примеры “группы RaO-CO-O-CRb2-” в качестве R2 включают следующие: метоксикарбонилоксиметильная группа, изопропилоксикарбонилоксиметильная группа, 1-(метилоксикарбонилокси)этильная группа, 1-(изопропилоксикарбонилокси)этильная группа и т.п.
В настоящем изобретении R2 предпочтительно представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, группу Ra-CO-, группу RaO-CO-, группу Ra-SO2-, группу Ra-CO-O-CRb2- или группу RaO-CO-O-CRb2-.
Ra предпочтительно представляет собой замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную фенильную группу, или замещенную или незамещенную 5-6-членную гетероциклильную группу.
Rb предпочтительно представляет собой атом водорода, или замещенную или незамещенную C1 - C6 алкильную группу.
Примеры предпочтительных заместителей в “C1 - C6 алкильной группе” в качестве R2 включают галоген, C1 - C6 алкокси-группу, C1 - C6 галогеналкокси-группу, фенильную группу; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную фенильную группу; или циано-группу. Особенно предпочтительными являются C1 - C6 алкокси-группа, фенильная группа; или галоген-замещенная, C1 - C6 галогеналкил-замещенная или C1 - C6 галогеналкокси-замещенная фенильная группа.
R3
R3 представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C2 - C6 алкенильную группу, замещенную или незамещенную C2 - C6 алкинильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу.
Примеры замещенной или незамещенной C1 - C6 алкильной группы, замещенной или незамещенной C2 - C6 алкенильной группы, замещенной или незамещенной C2 - C6 алкинильной группы, или замещенной или незамещенной C3 - C6 циклоалкильной группы в качестве R3 включают те же, которые перечислены для R1.
В настоящем изобретении R3 предпочтительно представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, или замещенную или незамещенную C3 - C6 циклоалкильную группу.
Заместитель в C1 - C6 алкильной группе предпочтительно представляет собой галоген.
Заместитель в C3 - C6 циклоалкильной группе предпочтительно представляет собой галоген или C1 - C6 алкильную группу.
R4
R4 представляет собой галоген, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C1 - C6 алкокси-группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу, замещенную или незамещенную 5-6-членную гетероарильную группу или циано-группу.
Примеры “галогена” в качестве R4 включают фтор, хлор, бром, иод и т.п.
“C1 - C6 алкильная группа” в качестве R4 может быть линейной или разветвленной. Примеры “C1 - C6 алкильной группы” в качестве R4 включают следующие: метильная группа, этильная группа, н-пропильная группа, н-бутильная группа, н-пентильная группа, н-гексильная группа, изо-пропильная группа, изо-бутильная группа, втор-бутильная группа, трет-бутильная группа, изо-пентильная группа, неопентильная группа, 2-метилбутильная группа, изо-гексильная группа и т.п.
Примеры “C1 - C6 алкокси-группы” в качестве R4 включают следующие: метокси-группа, этокси-группа, н-пропокси-группа, н-бутокси-группа, н-пентилокси-группа, н-гексилокси-группа, изо-пропокси-группа, изо-бутокси-группа, втор-бутокси-группа, трет-бутокси-группа, изо-гексилокси-группа и т.п.
Примеры предпочтительных заместителей в “C1 - C6 алкильной группе” или “C1 - C6 алкокси-группе” в качестве R4 включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; фенильную группу, нафтильную группу; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную фенильную группу, такую как 4-хлорфенильная группа, 4-трифторметилфенильная группа, 4-трифторметоксифенильная группа; галоген-замещенную, C1 - C6 галогеналкил-замещенную или C1 - C6 галогеналкокси-замещенную нафтильную группу; и циано-группу.
“5-6-членная гетероарильная группа” в качестве R4 представляет собой 5-членное ароматическое кольцо или 6-членное ароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатомов, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. Когда присутствует два или больше гетероатомов, они могут быть одинаковыми или разными.
Примеры 5-членной гетероарильной группы включают следующие: пирролильная группа, фурильная группа, тиенильная группа, имидазолильная группа, пиразолильная группа, оксазолильная группа, изоксазолильная группа, тиазолильная группа, изотиазолильная группа, триазолильная группа, оксадиазолильная группа, тиадиазолильная группа, тетразолильная группа и т.п.
Примеры 6-членной гетероарильной группы включают следующие: пиридильная группа, пиразинильная группа, пиримидинильная группа, пиридазинильная группа, триазинильная группа и т.п.
Примеры предпочтительных заместителей в “фенильной группе”, “нафтильной группе” или “5-6-членной гетероарильной группе” в качестве R4 включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; C1 - C6 алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изо-пропильная группа, н-бутильная группа, втор-бутильная группа, изо-бутильная группа, трет-бутильная группа, н-пентильная группа и н-гексильная группа; C1 - C6 галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа и 1-фтор-н-бутильная группа; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; и циано-группу.
В настоящем изобретении R4 предпочтительно представляет собой галоген, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную C1 - C6 алкокси-группу или циано-группу.
Заместитель в C1 - C6 алкильной группе или C1 - C6 алкокси-группе предпочтительно представляет собой галоген.
R5, R6
R5 представляет собой атом водорода или галоген.
R6 представляет собой атом водорода или галоген. R6 предпочтительно представляет собой атом водорода.
A
A представляет собой замещенную или незамещенную C1 - C4 алкиленовую группу, замещенную или незамещенную C2 - C3 алкениленовую группу, или замещенную или незамещенную C1 - C2 алкиленокси C1 - C2 алкиленовую группу.
Примеры “C1 - C4 алкиленовой группы” включают метиленовую группу, диметиленовую группу, триметиленовую группу, тетраметиленовую группу и т.п.
Примеры “C2 - C3 алкениленовой группы” включают виниленовую группу (-CH=CH-), пропениленовую группу (-CH=CH-CH2- или -CH2-CH=CH-) и т.п.
Примеры “C1 - C2 алкиленокси C1 - C2 алкиленовой группы” включают метиленоксиметиленовую группу (-CH2-O-CH2-), метиленоксидиметиленовую группу (-CH2-O-CH2CH2-), диметиленоксиметиленовую группу (-CH2CH2-O-CH2-), диметиленоксидиметиленовую группу (-CH2CH2-O-CH2CH2-) и т.п.
Примеры заместителей в “C1 - C4 алкиленовой группе”, “C2 - C3 алкениленовой группе” или “C1 - C2 алкиленокси C1 - C2 алкиленовой группе” включают галогены, такие как атом фтора, атом хлора, атом брома и атом иода; C1 - C6 алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изо-пропильная группа, н-бутильная группа, втор-бутильная группа, изо-бутильная группа и трет-бутильная группа; C1 - C6 галогеналкильные группы, такие как хлорметильная группа, хлорэтильная группа, трифторметильная группа, 1,2-дихлор-н-пропильная группа и 1-фтор-н-бутильная группа; гидроксильную группу; C1 - C6 алкокси-группы, такие как метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, втор-бутокси-группа, изо-бутокси-группа и трет-бутокси-группа; C1 - C6 галогеналкокси-группы, такие как 2-хлор-н-пропокси-группа, 2,3-дихлорбутокси-группа и трифторметокси-группа; C1 - C6 алкокси C1 - C6 алкильные группы, такие как метоксиметильная группа; фенильная группа, нафтильная группа; галоген-замещенные, C1 - C6 галогеналкил-замещенные или C1 - C6 галогеналкокси-замещенные фенильные группы, такие как 4-хлорфенильная группа, 4-трифторметилфенильная группа и 4-трифторметоксифенильная группа; галоген-замещенные, C1 - C6 галогеналкил-замещенные или C1 - C6 галогеналкокси-замещенные нафтильные группы; и циано-группу.
В настоящем изобретении, A предпочтительно представляет собой замещенную или незамещенную C1 - C4 алкиленовую группу.
Предпочтительные примеры заместителей в C1 - C4 алкиленовой группе включают C1 - C6 алкильную группу или галоген.
X1, X2, Rc, m и n
X1 представляет собой атом кислорода или сульфонильную группу.
X2 представляет собой атом кислорода, сульфенильную группу, сульфинильную группу, сульфонильную группу, группу -S(=NRc)- или группу -S(=O)(=NRc)-.
Каждый Rc независимо представляет собой атом водорода, замещенную или незамещенную C1 - C6 алкильную группу, замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу или циано-группу. Примерами “C1 - C6 алкильной группы” в качестве Rc являются те же, которые перечислены для Ra.
m равен 0 или 1, и n равен 0 или 1. Сумма m и n равна 1 или 2. Когда A представляет собой замещенную или незамещенную метиленовую группу, сумма m и n равна 2.
В настоящем изобретении X1 предпочтительно представляет собой атом кислорода или сульфонильную группу, и X2 предпочтительно представляет собой атом кислорода, сульфенильную группу или сульфонильную группу.
В настоящем изобретении предпочтительным является соединение, имеющее формулу (I-2), в котором A представляет собой триметиленовую группу, m равно 0, и n равно 1.
[Хим. 3]
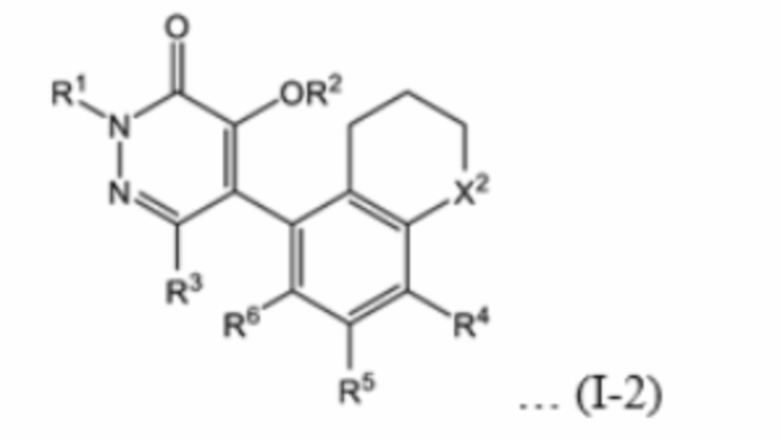
В формуле (I-2) X2 и R1 - R6 имеют те же определения, как в формуле (I).
В настоящем изобретении предпочтительным является соединение, имеющее формулу (I-1), в котором A представляет собой триметиленовую группу, R5 и R6 представляют собой атом водорода, m равно 0, и n равно 1.
[Хим. 4]
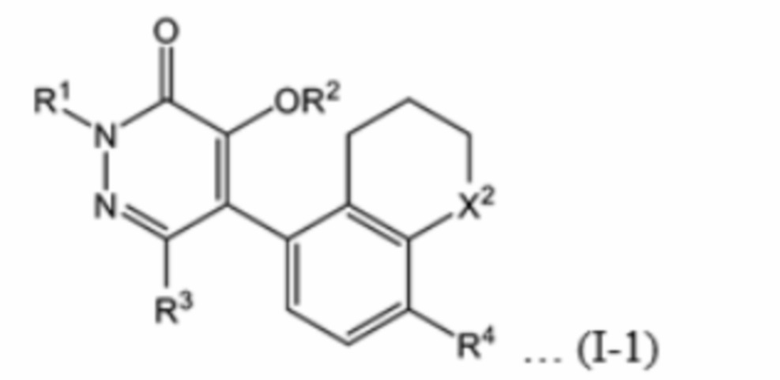
В формуле (I-1) X2 и R1 - R4 имеют те же определения, как в формуле (I).
Соль
Примеры солей соединения (I) включают соль щелочного металла, такого как литий, натрий или калий; соль щелочно-земельного металла, такого как кальций или магний; соль переходного металла, такого как железо или медь; соль аммония; соль органического основания, такого как триэтиламин, трибутиламин, пиридин или гидразин; и т.п.
Структуру соединения (I) или соли соединения (I) можно определить методами ЯМР-спектроскопии, ИК-спектроскопии, масс-спектрометрии и т.п.
Соединение (I) не ограничено способом его получения. Кроме того, соль соединения (I) можно получить известным способом из соединения (I). Соединение (I) можно получить способом, описанным в Примерах и т.п., например, с использованием соединения, полученного способом, описанным в Патентном документе 1, в качестве промежуточного продукта.
Схема реакции 1
Например, соединение (I), в котором R2 отличен от низшей алкильной группы или атома водорода (соединение формулы (I-a)), можно получить из соединения формулы (I-b), как показано на приведенной ниже схеме реакции 1. Соединение формулы (I-b) представляет собой соединение из числа соединений общей формулы (I), в котором R2 представляет собой атом водорода. Символы в формуле (I-a) и формуле (I-b) имеют те же значения, какие указаны для формулы (I). Xa в формуле (2) представляет собой галоген, такой как хлор или бром. R2a в формуле (2) представляет собой R2, отличающийся от низшей алкильной группы или атома водорода.
[Хим. 5]
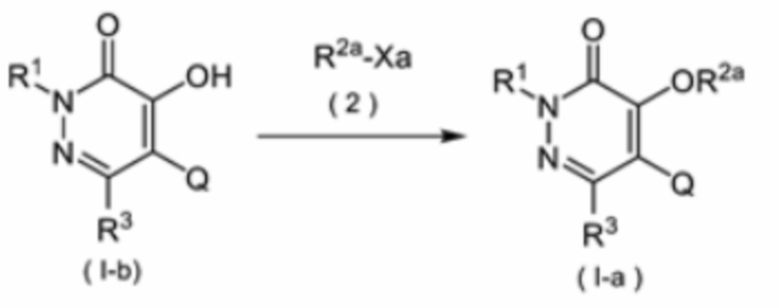
Соединение формулы (I-a) можно получить реакцией соединения формулы (I-b) с соединением формулы (2) в присутствии подходящего основания (например, неорганического основания, такого как карбонат калия).
Схема реакции 2
Соединение формулы (I-b) можно получить из соединения формулы (I-c) как показано на приведенной ниже схеме реакции 2. Символы в формуле (I-c) и формуле (I-b) имеют те же значения, какие указаны в формуле (I). R2a представляет собой низшую алкильную группу, такую как метильная группа. Далее по тексту R2a имеет такое же значение.
[Хим. 6]
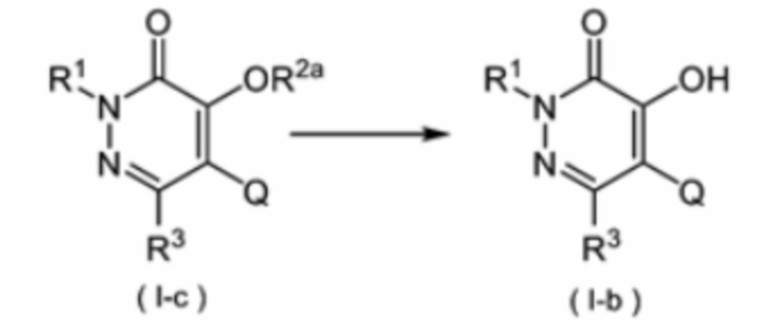
Соединение формулы (I-b) можно получить нагреванием соединения формулы (I-c) совместно с морфолином.
Схема реакции 3
Соединение формулы (I-c) можно получить конденсацией соединения формулы (4) и соединения формулы (5), как показано на приведенной ниже схеме реакции 3.
Символы в формуле (4) имеют те же значения, какие указаны в формуле (I). Ry представляет собой низшую алкильную группу, такую как метильная группа или этильная группа. Кроме того, Ry может быть соединен с другим Ry, образуя 1,3,2-диоксаборолановое кольцо. Q в формуле (5) означает фрагмент бензольного кольца, содержащий заместитель R4 в формуле (I). Xb представляет собой галоген.
[Хим. 7]
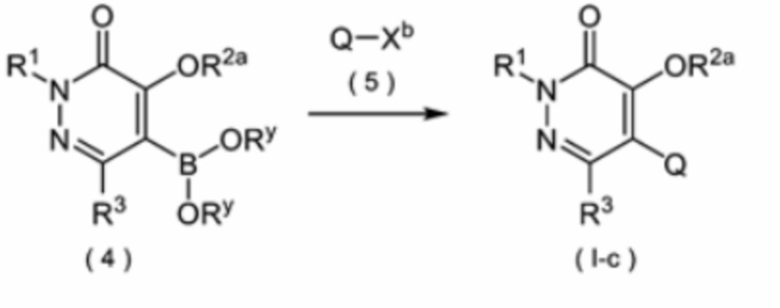
Соединение формулы (I-c) можно получить реакцией соединения формулы (4) с соединением формулы (5) в присутствии подходящего основания (например, неорганического основания, такого как фосфат калия или фторид цезия), металлического катализатора (например, палладиевого катализатора, такого как Pd(OAc)2), и, необязательно, лиганда (например, фосфинового лиганда).
Металлический катализатор и лиганд можно добавлять в виде предварительного сформированного комплекса (например, палладий/фосфиновый комплекс, такой как бис(трифенилфосфин)палладий или аддукт [1,1-бис(дифенилфосфино)ферроцен] палладий дихлорида с дихлорметаном).
Схема реакции 4
Соединение формулы (4) можно получить из соединения формулы (6), как показано на приведенной ниже схеме реакции 4. Символы в формуле (6) имеют те же значения, какие указаны в формуле (I).
[Хим. 8]
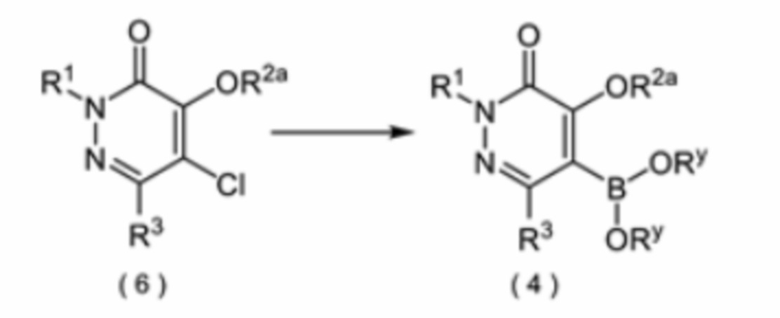
Соединение формулы (4) можно получить реакцией соединения формулы (6) с бороновой кислотой или эфиром бороновой кислоты, таким как бис(пинаколато)диборон, в присутствии подходящего основания (например, неорганического основания, такого как фосфат калия или фторид цезия), металлического катализатора (например, палладиевого катализатора, такого как Pd2(dba)3 или Pd(OAc)2 и, необязательно, лиганда (например, фосфинового лиганда).
Металлический катализатор и лиганд можно добавлять в виде предварительного сформированного комплекса (например, палладий/фосфиновый комплекс, такой как бис(трифенилфосфин)палладий дихлорид или аддукт [1,1-бис(дифенилфосфино) ферроцен]палладий дихлорида с дихлорметаном).
(Схема реакции 5)
Соединение формулы (6) можно получить из соединения формулы (7), как показано на приведенной ниже схеме 5.
[Хим. 9]
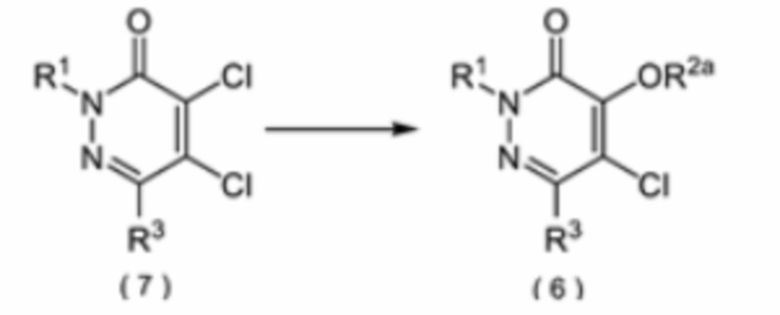
Соединение формулы (6) можно получить реакцией соединения формулы (7) с подходящим алкоксидом металла, таким как метоксид натрия.
Соединение формулы (7) можно получить известным способом.
Схема реакции 3A
Соединение формулы (I-c) можно получить конденсацией соединения формулы (6) и соединения формулы (8), как показано на приведенной ниже схеме 3A.
Q в формуле (8) означает бензольное кольцо, содержащее заместитель R4 в формуле (I). Xb представляет собой галоген. Ry представляет собой низшую алкильную группу, такую как метильная группа или этильная группа. Кроме того, Ry может быть соединен с другим Ry с формированием 1,3,2-диоксабороланового кольца.
[Хим. 10]
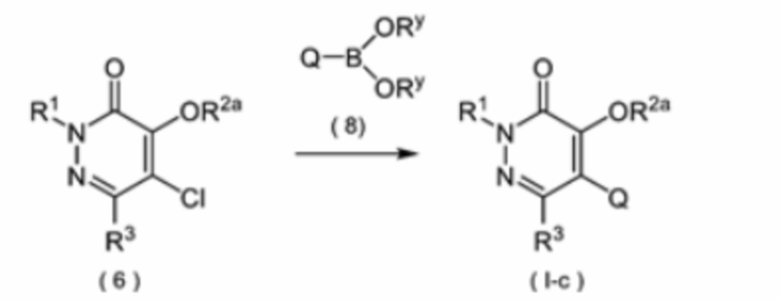
Соединение формулы (I-c) можно получить реакцией соединения формулы (6) с соединением формулы (8) в присутствии подходящего основания (например, неорганического основания, такого как фосфат калия или фторид цезия), металлического катализатора (например, палладиевого катализатора, такого как Pd(OAc)2), и, необязательно, лиганда (например, фосфинового лиганда).
Металлический катализатор и лиганд можно добавлять в виде предварительного сформированного комплекса (например, палладий/фосфиновый комплекс, такой как бис(трифенилфосфин)палладий дихлорид или аддукт [1,1-бис(дифенилфосфино) ферроцен]палладий дихлорида с дихлорметаном).
Соединение по настоящему изобретению демонстрирует высокую гербицидную активность как при обработке почвы, так и при обработке листвы (всходов), в условиях пастбищно-выпасного хозяйства на холмах.
Соединения по настоящему изобретению эффективны против различных сорняков полей и могут демонстрировать селективность к культурам, таким как кукуруза и пшеница.
Гербицид по настоящему изобретению содержит по меньшей мере одно из группы, состоящей из соединения (I) и соли соединения (I), в качестве действующего вещества.
Таким образом, один аспект настоящего изобретения представляет собой гербицид, содержащий по меньшей мере одно из группы, состоящей из соединения (I) и его соли, в качестве действующего вещества.
Гербицид по настоящему изобретению демонстрирует высокую гербицидную активность как при обработке почвы, так и при обработке листвы (всходов), в условиях пастбищно-выпасного хозяйства на холмах.
Кроме того, гербицид по настоящему изобретению оказывает прекрасное гербицидное действие на сорняки затопляемых полей, такие как Echinochloa spp., Cyperus difforis, Sagittaria trifolia и Schoenoplectiella hotarui, и может демонстрировать селективность к рису.
Кроме того, гербицид по настоящему изобретению можно также применять для борьбы с сорняками в таких местах, как фруктовые сады, лужайки, дорожки и незанятые пространства.
Полезные растения, для которых можно применять гербицид по настоящему изобретению, включают сельскохозяйственные культуры, такие как ячмень и пшеница, хлопок, рапс, подсолнечник, кукурузу, рис, сою, сахарную свеклу, сахарный тростник и газонные травы.
Сельскохозяйственные культуры могут также включать деревья, такие как фруктовые деревья, пальмы, кокосовые пальмы или другие орехи, а также включают виноград, фруктовые кустарники, плодовые растения и овощи.
Примеры сорняков на незатопляемых полях, с которыми может осуществляться борьба, включают следующие сорняки.
(A) Однодольные сорняки
(1) Сорняки из семейства Cyperaceae
Сорняки из рода Cyperus, такие как Cyperus esculentus, Cyperus iria, Cyperus microiria и Cyperus rotundus.
(2) Сорняки из семейства Poaceae
Сорняки из рода Alopecurus, такие как Alopecurus aequalis и Alopecurus myosuroides;
Сорняки из рода Apera, такие как Apera spica-venti;
Сорняки из рода Avena, такие как Avena sativa;
Сорняки из рода Bromus, такие как Bromus japonicus и Bromus sterilis;
Сорняки из рода Digitaria, такие как Digitaria ciliaris и Digitaria sanguinalis;
Сорняки из рода Echinochloa, такие как Echinochloa crus-galli;
Сорняки из рода Eleusine, такие как Eleusine indica;
Сорняки из рода Lolium, такие как Lolium multiflorum Lam.;
Сорняки из рода Panicum, такие как Panicum dichotomiflorum;
Сорняки из рода Poa, такие как Poa annua;
Сорняки из рода Setaria, такие как Setaria faberi, Setaria pumila и Setaria viridis;
Сорняки из рода Sorghum, такие как Sorghum bicolor; и
Сорняки из рода Urochloa, такие как Urochloa platyphylla.
(B) Двудольные сорняки
(1) Сорняки из семейства Amaranthaceae
Сорняки из рода Amaranthus, такие как Amaranthus blitum, Amaranthus palmeri, Amaranthus retroflexus и Amaranthus rudis;
Сорняки из рода Chenopodium, такие как Chenopodium album;
Сорняки из рода Bassia, такие как Bassia scoparia.
(2) Сорняки из семейства Asteraceae
Сорняки из рода Ambrosia, такие как Ambrosia artemisiifolia и Ambrosia trifida;
Сорняки из рода Conyza, такие как Conyza canadensis и Conyza sumatrensis;
Сорняки из рода Erigeron, такие как Erigeron annuus;
Сорняки из рода Matricaria, такие как Matricaria inodora и Matricaria recutita;
Сорняки из рода Xanthium, такие как Xanthium occidentale.
(3) Сорняки из семейства Caryophyllaceae
Сорняки из рода Sagina, такие как Sagina japonica;
Сорняки из рода Stellaria, такие как Stellaria media.
(4) Сорняки из семейства Convolvulaceae
Сорняки из рода Calystegia, такие как Calystegia japonica;
Сорняки из рода Ipomoea, такие как Ipomoea coccinea, Ipomoea hederacea, Ipomoea lacunosa и Ipomoea triloba.
(5) Сорняки из семейства Lamiaceae
Сорняки из рода Lamium, такие как Lamium album var. barbatum, Lamium amplexicaule и Lamium purpureum.
(6) Сорняки из семейства Malvaceae
Сорняки из рода Abutilon, такие как Abutilon theophrasti;
Сорняки из рода Sida, такие как Sida spinosa.
(7) Сорняки из семейства Plantaginaceae
Сорняки из рода Veronica, такие как Veronica persica.
(8) Сорняки из семейства Polygonaceae
Сорняки из рода Fallopia, такие как Fallopia convolvulus.
Сорняки из рода Persicaria, такие как Persicaria lapathifolia и Persicaria longiseta.
(9) Сорняки из семейства Rubiaceae
Сорняки из рода Galium, такие как Galium spurium var. echinospermon.
Примеры сорняков на затопляемых полях, с которыми может осуществляться борьба, включают следующие сорняки.
(A) Однодольные сорняки
(1) Сорняки из семейства Alismataceae
Сорняки из рода Sagittaria, такие как Sagittaria pygmaea Miq. и Sagittaria trifolia.
(2) Сорняки из семейства Cyperaceae
Сорняки из рода Cyperus, такие как Cyperus serotinus и Cyperus difforis;
Сорняки из рода Eleocharis, такие как Eleocharis kuroguwai Ohwi;
Сорняки из рода Schoenoplectiella, такие как Schoenoplectiella hotarui и Schoenoplectiella juncoides Roxb.
Сорняки из рода Scirpus, такие как Scirpus maritimus (Scirpus martimus) и Scirpus nipponicus.
(3) Сорняки из семейства Poaceae
Сорняки из рода Echinochloa, такие как Echinochloa oryzoides и Echinochloa crus-galli;
Сорняки из рода Leersia, такие как Leersia japonica;
Сорняки из рода Paspalum, такие как Paspalum distichum.
(4) Сорняки из семейства Pontederiaceae
Сорняки из рода Monochoria, такие как Monochoria korsakowii и Monochoria vaginalis var. plantaginea.
(B) Двудольные сорняки
(1) Сорняки из семейства Apiaceae
Сорняки из рода Oenanthe, такие как Oenanthe javanica.
(2) Сорняки из семейства Elatinaceae
Сорняки из рода Elatine, такие как Elatine triandra.
(3) Сорняки из семейства Linderniaceae
Сорняки из рода Lindernia, такие как Lindernia dubia subsp. major, Lindernia dubia subsp. dubia и Lindernia procumbens.
(4) Сорняки из семейства Lythraceae
Сорняки из рода Rotala, такие как Rotala indica var. uliginosa.
Кроме того, настоящее изобретение касается способа борьбы с однодольными и/или двудольными сорняками культурных растений, включающего стадию нанесения соединения (I) или его соли, или гербицида, содержащего соединение (I), на сорняки и/или указанные выше растения и/или их локусы.
Применение способа по настоящему изобретению позволяет селективно бороться с сорняками даже в локусах, где находятся культурные растения и/или сорняки.
Кроме того, с сорняками можно бороться даже в локусах, где будут выращиваться культурные растения, а не в локусах, где уже выращиваются культурные растения. Нанесение гербицида можно в целом осуществлять такими способами, как опрыскивание, посыпание порошком, капельное орошение, орошение, смешивание, в соответствии с готовой формой гербицида.
Гербицид по настоящему изобретению может состоять только из соединения по настоящему изобретению, или он может иметь вид дозированной формы, адаптированной для сельскохозяйственных химикатов, например, смачиваемый порошок, гранулы, порошок, концентрат эмульсии, водорастворимый порошок, суспензия, текучий состав и т.п.
В составе можно использовать известный носитель или добавку.
Один аспект настоящего изобретения представляет собой гербицид, содержащий агрохимически приемлемый твердый носитель и/или жидкий носитель.
Для твердых дозированных форм можно применять порошки растительного происхождения, такие как соевая мука и пшеничная мука, мелкие минеральные порошки, такие как диатомовая земля, апатит, гипс, тальк, бентонит, пирофиллит и глина, и твердые носители, представляющие собой органические и неорганические соединения, такие как бензоат натрия, мочевина и мирабилит.
Для жидких дозированных форм можно применять нефтяные фракции, такие как керосин, ксилол и сольвент нафта, и жидкие носители, такие как циклогексан, циклогексанон, диметилформамид, тиметилсульфоксид, спирт, ацетон, трихлорэтилен, метилизобутилкетон, минеральное масло, растительное масло и вода.
При необходимости в составе можно применять поверхностно-активное вещество. Примеры поверхностно-активного вещества включают неионные поверхностно-активные вещества, такие как алкилфениловые эфиры, к которым присоединен полиоксиэтилен, алкиловые эфиры, к которым присоединен полиоксиэтилен, эфиры высших жирных кислот, к которым присоединен полиоксиэтилен, сорбитановые эфиры высших жирных кислот, к которым присоединен полиоксиэтилен, и тристирилфениловые эфиры, к которым присоединен полиоксиэтилен, соли эфиров серной кислоты с алкилфениловыми эфирами, к которым присоединен полиоксиэтилен, алкилнафталин сульфонат, поликарбоксилат, лигнин сульфонат, конденсаты формальдегида с алкилнафталин сульфонатом и сополимеры изобутилен-малеиновый ангидрид.
В гербициде по настоящему изобретению концентрацию действующего вещества можно устанавливать в соответствии с выбранной дозированной формой. Например, концентрация действующего вещества в смачиваемом порошке предпочтительно находится в диапазоне от 5 до 90% по весу, и более предпочтительно – в диапазоне от 10 до 85% по весу. Концентрация действующего вещества в концентрате эмульсии предпочтительно находится в диапазоне от 3 до 70% по весу, и более предпочтительно – в диапазоне от 5 до 60% по весу. Концентрация действующего вещества в гранулах предпочтительно находится в диапазоне от 0.01 до 50% по весу, и более предпочтительно – в диапазоне от 0.05 до 40% по весу.
Смачиваемый порошок или концентрат эмульсии, получаемый таким образом, можно использовать в виде суспензии или эмульсии, разбавляя водой до определенной концентрации, а гранулы можно распылять непосредственно или смешивать с землей до или после прорастания сорняков. Когда гербицид по настоящему изобретению используется на сельскохозяйственных угодьях, может применяться 0.1 г или больше действующего вещества на гектар.
Кроме того, гербицид по настоящему изобретению можно также применять, смешивая с известным фунгицидом, активным компонентом фунгицида, инсектицидом, активным компонентом инсектицида, акарицидом, активным компонентом акарицида, гербицидом, активным компонентом гербицида, регулятором роста растений, удобрением, веществом для уменьшения фитотоксичности (антидотом) и т.п. В частности, можно уменьшать количество применяемого вещества путем использования его в комбинации с гербицидом. Кроме того, помимо снижения трудозатрат, еще более сильный эффект можно ожидать благодаря синергетическому действию смесевых составов. В этом случае возможны комбинации с множеством известных гербицидов.
Таким образом, одним аспектом настоящего изобретения является гербицид, содержащий один или больше дополнительных гербицидно активных ингредиентов.
Кроме того, одним аспектом настоящего изобретения является гербицид, содержащий один или больше дополнительных антидотов.
Другие гербицидно активные ингредиенты для применения в настоящем изобретении не ограничены каким-либо специальным образом, и их примеры включают перечисленные ниже.
(a) Ингредиенты на основе эфиров арилоксифеноксипропионовой кислоты, такие как клодинафоп-пропаргил, цигалофоп-бутил, диклофоп-метил, феноксапроп-P-этил, флуазифоп-P, флуазифоп-P-бутил, галоксифоп-метил, пирифеноп-натрий, пропаквизафоп, квизалофоп-P-этил и метамифоп; циклогександионовые ингредиенты, такие как аллоксидим, бутроксидим, клетодим, циклоксидим, профоксидим, этоксидим, тепралоксидим и тралкоксидим; фенилпиразолиновые ингредиенты, такие как пиноксаден; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования ацетил КоА карбоксилазы растений.
(b) Ингредиенты на основе сульфонилмочевины, такие как амидосульфурон, азимсульфурон, бенсульфурон-метил, хлоримурон-этил, хлорсульфурон, циносульфурон, циклосульфамурон, этаметсульфурон-метил, этоксисульфурон, флазасульфурон, флупирсульфурон, форамсульфурон, галосульфурон-метил, имазосульфурон, иодсульфурон-метил, мезосульфурон, мезосульфурон-метил, метсульфурон-метил, никосульфурон, оксасульфурон, примисульфурон, просульфурон, пиразосульфурон-этил, римсульфурон, сульфометурон-метил, сульфосульфурон, тифенсульфурон-метил, триасульфурон, трибенурон-метил, трифоксисульфурон, трифлусульфурон-метил, тритосульфурон, ортосульфамурон, пропирисульфурон, флуцетосульфурон, метазосульфурон, метиопирсульфурон, моносульфурон-метил, ортосульфурон и иофенсульфурон; имизаолиноновые ингредиенты, такие как имазапик, имазаметабенз, имазамокс-аммоний, имазапир, имазаквин и имазэтапир; триазолопиримидин сульфонамидные ингредиенты, такие как клорансулам-метил, диклосулам, флорасулам, флуметсулам, метосулам, пенокссулам, пирокссулам и метосульфам; пиримидинил(тио)бензоатные ингредиенты, такие как биспирибак-натрий, пирибензоксим, пирифталид, пиритиобак-натрий, пириминобак-метил и пиримисульфан; сульфониламино карбонил триазолиноновые ингредиенты, такие как флукарбазон, пропоксикарбазон и тиенкарбазон-метил; сульфонанилидовые ингредиенты, такие как триафамон; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования ацетолактат синтазы (ALS) (синтетаза ацетoгидрокси кислот (AHAS)) растений.
(c) Триазиновые ингредиенты, такие как аметрин, атразин, цианазин, десметрин, диметаметрин, прометон, прометрин, пропазиновые ингредиенты (пропазин), CAT (симазин), симетрин, тербуметон, тербутилазин, тербутрин, триэтазин, атратон и цибутрин; триазиноновые ингредиенты, такие как гексазинон, метамитрон и метрибузин; тризолиноновые ингредиенты, такие как амикарбазон; урацильные ингредиенты, такие как бромацил, ленацил и тербацил; пиридазиноновые ингредиенты, такие как PAC (хлоридазон); карбаматные ингредиенты, такие как десмедифам, фенмедифам и swep; ингредиенты на основе мочевины, такие как хлорбромурон, хлортолурон, хлорксурон, димефурон, DCMU (диурон), этидимурон, фенурон, флуометурон, изопротурон, изоурон, линурон, метабензтиазурон, метобромурон, метоксурон, монолинурон, небурон, сидурон, тубутиурон, метобензурон и карбутилат; амидные ингредиенты, такие как DCPA (пропанил) и CMMP (пентанохлор); анилидные ингредиенты, такие как ципромид; нитрильные ингредиенты, такие как бромфеноксим, бромксинил и иоксинил; бензотидиазиноновые ингредиенты, такие как бентазон; фенилпиридазиновые ингредиенты, такие как пиридат и пиридафол; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования фотосинтеза у растений, такие как метазол.
(d) Бипиридилиевые ингредиенты, такие как дикват и паракват; и другие ингредиенты, которые в растениях превращаются в свободные радикалы и генерируют активный кислород, что дает быстрое гербицидное действие.
(e) Ингредиенты на основе дифенилового эфира, такие как ацифлуофен-натрий, бифенокс, хлометоксинил (хлометоксифен), фторгликофен, фомесафен, галосафен, лактофен, оксифлуорфен, нитрофен и этоксифен-этил; фенилпиразольные ингредиенты, такие как флуазолат и пирафлуфен-этил; N-фенилфталимидные ингредиенты, такие как цинидон-этил, флумиоксазин, флумиклорак-пентил и хлорфталим; тиадиазольные ингредиенты, такие как флутиацет-метил и тидиазимин; оксазиазольные ингредиенты, такие как оксадиазон и оксадиаргил; триазолиноновые ингредиенты, такие как азафенидин, карфентразон-этил, сульфентразон и бенкарбазон; оксазолидиндионовые ингредиенты, такие как пентоксазон; пиримидиндионовые ингредиенты, такие как бензфендизон и бутафенацил; сульфониламидные ингредиенты, такие как сафлуфенацил; пиридазиновые ингредиенты, такие как флуфенпир-этил; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования биосинтеза хлорофилла у растений и аномального накопления светочувствительных пероксидных веществ в тканях растений, такие как пирахлонил, профлуазол, тиафенацил и трифлудимоксазин.
(f) Пиридазиновые ингредиенты, такие как норфлуразон и метфлуразон; пиридинкарбоксамидные ингредиенты, такие как дифлуфеникан и пиколинафен; трикетоновые ингредиенты, такие как мезотрион, сулкотрион, тефурилтрион, темботрион, бициклопирон и фенквинотрион; изоксазольные ингредиенты, такие как изоксахлортол и изоксафлутол; пиразольные ингредиенты, такие как бензофенап, пиразолинат, пиразоксифен, топрамезон, пирасульфотол и толпиралат; триазольные ингредиенты, такие как ATA (амитрол); изооксазолидиноновые ингредиенты, такие как кломазон; ингредиенты на основе дифенилового эфира, такие как аклонифен; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования биосинтеза пигментов у растений, таких как каротеноиды, отличающиеся отбеливающим действием, такие как бефлубутамид, флуридон, флурохлоридон, флуртамон, бензобициклон, метоксифенон и кетоспирадокс.
(g) Глициновые ингредиенты, такие как глифосат, глифосат-аммоний, глифосат-изопропиламин и глифосат тримезиум (сульфосат); и другие ингредиенты, ингибирующие EPSP синтетазу.
(h) Ингредиенты на основе фосфиновой кислоты, ингибирующие глутамин синтетазу, такие как глуфосинат, глуфосинат-аммоний и биалафос (биланафос), и
другие ингредиенты, проявляющие гербицидную активность путем ингибирования биосинтеза аминокислот у растений.
(i) Карбаматные ингредиенты, такие как aсулам; и другие ингредиенты, ингибирующие DHP (дигидроптероат) синтетазу
(j) Ингредиенты на основе динитроанилина, такие как бентродин (бенфлуралин), бутралин, динитрамин, эталфлуралин, оризалин, пендиметалин, трифлуралин, нитралин и продиамин; фосфорамидатные ингредиенты, такие как амипрофос-метил и бутамифос; пиридиновые ингредиенты, такие как дитиопир и тиазопир; бензамидные ингредиенты, такие как пропизамид и тебутам; ингредиенты на основе бензойной кислоты, такие как хлортал и TCTP (хлортал-диметил); карбаматные ингредиенты, такие как IPC (хлорпрофам), профам, карбетамид и барбан; арилаланиновые ингредиенты, такие как флампроп-M и флампроп-M-изопропил; хлорацетамидные ингредиенты, такие как ацетохлор, алахлор, бутахлор, диметахлор, диметенамид, диметенамид-P, метазахлор, метолахлор, S-метолахлор, петоксамид, претилахлор, пропахлор, пропизохлор и тенилхлор; ацетамидные ингредиенты, такие как дифенамид, напропамид и напроанилид; оксиацетамидные ингредиенты, такие как флуфенацет и мефенацет; тетразолиновые ингредиенты, такие как фентразамид; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования полимеризации микротрубочек, образования микротрубочек и деления клеток у растений, или путем ингибирования биосинтеза очень длинноцепочечных жирных кислот (VLCFA), такие как анилофос, инданофан, кафенстрол, пиперофос, метиозолин, феноксасульфон, пироксасульфон и ипфенкарбазон.
(k) Нитрильные ингредиенты, такие как DBN (диклобенил) и DCBN (хлортиамид); бензамидные ингредиенты, такие как изоксабен; триазолокарбоксамидные ингредиенты, такие как флупоксам; ингредиенты на основе хинолинкарбоновой кислоты, такие как хинклорак; и другие ингредиенты, проявляющие гербицидную активность путем ингибирования синтеза клеточной стенки (целлюлозы), такие как триазифлам и индазифлам.
(l) Динитрофенольные ингредиенты, такие как DNOC, DNBP (диносеб) и динотерб; и другие ингредиенты, проявляющие гербицидную активность путем расцепления (разрушение мембраны).
(m) Тиокарбаматные ингредиенты, такие как бутилат, гексилтиокарбам (циклоат), димепиперат, EPTC, эспрокарб, молинат, орбенкарб, пебулат, просульфокарб, бентиокарб (тиобенкарб), тиокарбазил, триаллат, вернолат и диаллат; фосфодитиоатные ингредиенты, такие как SAP (бенсулид); бензофурановые ингредиенты, такие как бенфуресат и этофумесат; ингредиенты на основе хлоругольной кислоты, такие как TCA, DPA (далапон) и тетрапион (флупропранат); и другие ингредиенты, проявляющие гербицидную активность путем ингибирования биосинтеза липидов у растений.
(n) Ингредиенты на основе феноксикарбоновых кислот, такие как кломепроп, 2,4-PA (2,4-D), 2,4-DB, дихлорпроп, MCPA, MCPB и MCPP (мекопроп); ингредиенты на основе бензойной кислоты, такие как хлорамфен, MDBA (дикамба) и TCBA (2,3,6-TBA); ингредиенты на основе пиридинкарбоновой кислоты, такие как клопиралид, аминопиралид, флуроксипир, пиклорам, триклопир и галауксифен; ингредиенты на основе хинолинкарбоновой кислоты, такие как хиклорак и хинмерак; ингредиенты на основе фталамат семикарбазона, такие как NPA (напталам) и дифлуфензопир; и другие ингредиенты, проявляющие гербицидную активность путем нарушения работы гормонов у растений, такие как беназолин, дифлуфензопир, флуроксипир, хлорфлуренол, аминоциклопирахлор и DAS534.
(o) Ингредиенты на основе ариламинопропионовой кислоты, такие как флампроп-изопропил; пиразолиевые ингредиенты, такие как дифензокват; ингредиенты на основе мышьякорганических соединений, такие как DSMA и MSMA; и другие гербициды, такие как бромбутид, хлорфлуренол, цинметилин, кумилурон, дазомет, даимурон, метил-димрон, этобензанид, фосамин, оксацикломефон, олеиновая кислота, пеларгоновая кислота, пирубутикарб, эндоталл, хлорат натрия, метам, хинокламин, циклопириморат, тридифан и клацифос.
Примеры веществ, уменьшающих фитотоксичность (антидоты), которые можно применять по настоящему изобретению, включают беноксакор, клоквинтоцет, клоквинтоцет-мексил, циометринил, ципросульфамид, дихлормид, дициклонон, диэтолат, фенхлоразол, фенхлоразол-этил, фенклорим, флуразол, флуксофеним, фурилазол, изоксадифен, изоксадифен-этил, мефенпир, мефенпир-диэтил, мефенат, нафталевый ангидрид и оксабетринил.
Примеры
Примеры составов
Ниже описаны некоторые примеры составов гербицидов по настоящему изобретению; но соединения по настоящему изобретению (действующее вещество), добавки и соотношения не ограничиваются только этими примерами и могут варьироваться в широких пределах. Термин “часть” в примерах составов означает “часть по весу”.
Пример состава 1
Смачиваемый порошок
Перечисленные выше компоненты тщательно перемешивали и затем измельчали до получения тонкого смачиваемого порошка, содержащего 20% действующего вещества.
Пример состава 2
Концентрат эмульсии
Перечисленные выше компоненты перемешивали и растворяли, получая эмульсию, содержащую 20% действующего вещества.
Пример состава 3
Гранулы
Перечисленные выше компоненты тщательно перемешивали и затем измельчали до получения тонкого порошка. Полученный продукт затем гранулировали с получением гранул, имеющих диаметр от 0.5 до 1.0 мм и содержащих 5% действующего вещества.
Далее описаны примеры синтезов. Однако следует понимать. Что настоящее изобретение не ограничивается описанными ниже Примерами.
Пример 1
Синтез 5-(1,1-диоксидо-8-(трифторметил)тиохроман-5-ил)-4-метокси-2-метилпиридазин-3(2H)-она (Соединение № A-1)
Стадия 1
Синтез 3-(6-бром-2-фтор-3-(трифторметил)фенил)пропионовой кислоты
[Хим. 11]
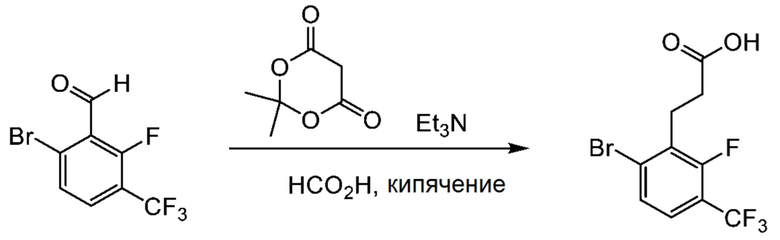
Муравьиную кислоту (58.2 г), триэтиламин (18.3 г), 6-бром-2-фтор-3-(трифторметил)бензальдегид (48.7 г) и кислоту Мельдрума (26.0 г) последовательно помещали при 0°C в четырехгорлую колбу объемом 500 мл. Затем смесь кипятили 4 часа.
В полученный раствор добавляли соляную кислоту, и выпавший в осадок твердый продукт отделяли фильтрованием. Полученный твердый продукт сушили. После этого получали 53.8 г целевого соединения.
Стадия 2
Синтез 3-(6-бром-2-фтор-3-(трифторметил) фенил)пропан-1-ола
[Хим. 12]
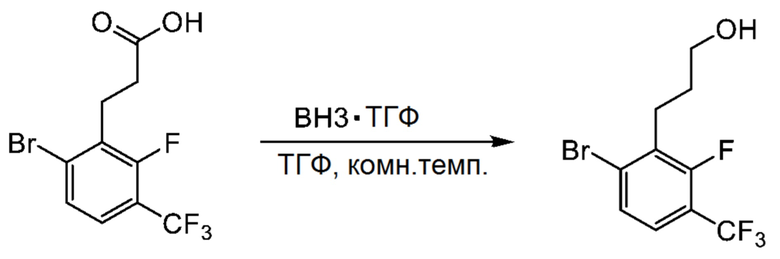
3-(6-Бром-2-фтор-3-(трифторметил)фенил)пропионовую кислоту (30 г) растворяли в тетрагидрофуране (191 мл), и полученный раствор перемешивали при 0°C. Добавляли комплекс боран-тетрагидрофуран (0.9 M, 127 мл), и полученную смесь перемешивали 1 час при комнатной температуре.
Полученный раствор выливали в соляную кислоту, и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Было получено 28.9 г целевого соединения.
Стадия 3
Синтез 1-бром-2-(3-хлорпропил)-3-фтор-4-(трифторметил)бензола
[Хим. 13]
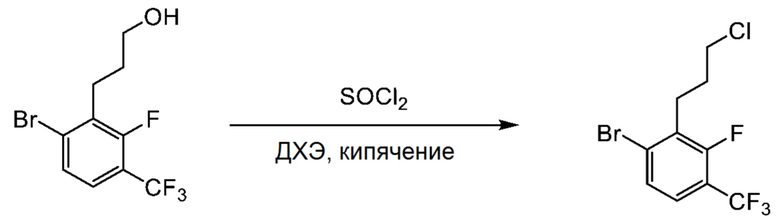
3-(6-Бром-2-фтор-3-(трифторметил)фенил)пропан-1-ол (15.3 г) растворяли в дихлорэтане (102 мл), и раствор перемешивали при комнатной температуре. Добавляли тионилхлорид (9.1 г) и N,N-диметилформамид (0.2 г), и смесь кипятили в течение 2 часов.
Полученный раствор упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Получали 16.4 г целевого соединения.
Стадия 4
Синтез 5-бром-8-(трифторметил)тиохромана
[Хим. 14]
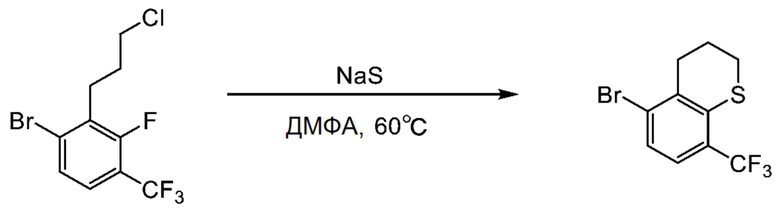
1-Бром-2-(3-хлорпропил)-3-фтор-4-(трифторметил)бензол (14.4 г) растворяли в N,N-диметилформамиде (158 мл), и раствор перемешивали при комнатной температуре. Добавляли сульфид натрия (4.2 г), и смесь нагревали при 60°C в течение ночи до кипения.
Полученный раствор выливали в воду, и затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Получали 6.8 г целевого соединения.
Стадия 5
Синтез 5-бром-8-(трифторметил)тиохроман 1,1-диоксида
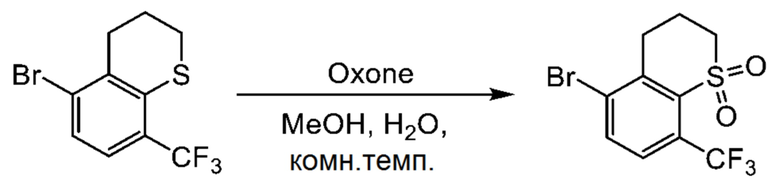
5-Бром-8-(трифторметил)тиохроман (2.0 г) растворяли в 27 мл метанола и 7 мл воды, и раствор перемешивали при комнатной температуре. Добавляли оксон (8.3 г), и смесь перемешивали 48 часов при комнатной температуре.
Полученный раствор фильтровали. Фильтрат упаривали при пониженном давлении. Добавляли воду, и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Получали 2.0 г целевого соединения.
Стадия 6
Синтез 5-(1,1-диоксидо-8-(трифторметил) тиохроман-5-ил)-4-метокси-2-метилпиридазин-3(2H)-она (Соединение № A-1)
[Хим. 16]
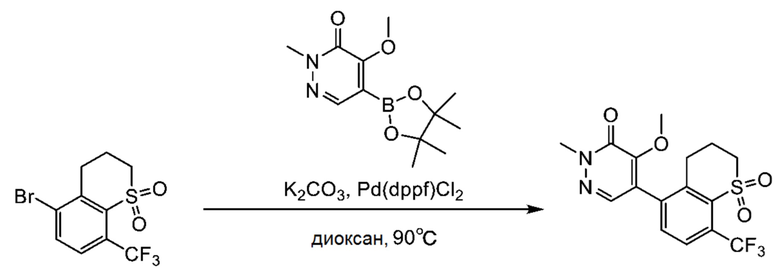
5-Бром-8-(трифторметил)тиохроман 1,1-диоксид (0.36 г) растворяли в диоксане (10 мл), и раствор перемешивали при комнатной температуре. 4-Метокси-2-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил) пиридазин-3(2H)-он (0.27 г), карбонат калия (0.41 г), и аддукт [1,1’-бис(дифенилфосфино)ферроцен]палладий (II) дихлорида с дихлорметаном (0.04 г). Смесь перемешивали в течение ночи при 90°C.
Полученный раствор фильтровали. Фильтрат упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Было получено 0.22 г целевого соединения.
Соединение A-1: 1H-ЯМР (400 МГц, CDCl3): δ 2.40 - 2.48 (м, 2H), 2.72 - 2.80 (м, 1H), 2.86 - 2.95 (м, 1H), 3.40 (т, 2H), 3.83 (с, 3H), 4.12 (с, 3H), 7.41 (д, 1H), 7.44 (с, 1H), 7.84 (д, 1H).
Пример 2
Синтез 5-(1,1-диоксидо-8-(трифторметил) тиохроман-5-ил)-4-гидрокси-2-метилпиридазин-3(2H)-он (Соединение № A-2)
[Хим. 17]
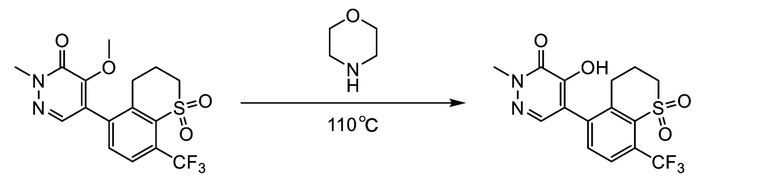
5-(1,1-Диоксидо-8-(трифторметил) тиохроман-5-ил)-4-метокси-2-метилпиридазин-3(2H)-он (0.39 г) растворяли в морфолине (2 мл). Раствор кипятили при 110°C в течение 1 часа.
Полученный раствор выливали в соляную кислоту, и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат упаривали при пониженном давлении. Получали 0.31 г целевого продукта.
Пример 3
Синтез 1-((5-(1,1-диоксидо-8-(трифторметил) тиохроман-5-ил)-2-метил-3-оксо-2,3-дигидропиридазин-4-ил) окси)этилметил карбоната (Соединение № A-3)
[Хим. 18]
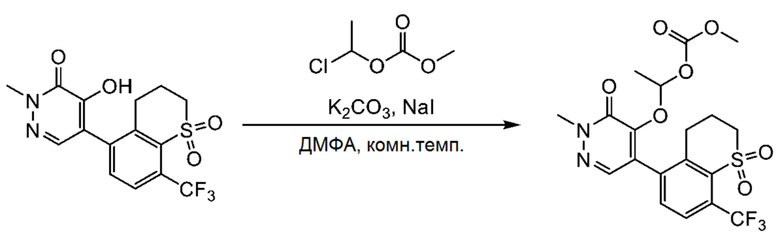
5-(1,1-диоксидо-8-(трифторметил) тиохроман-5-ил)-4-гидрокси-2-метилпиридазин-3(2H)-он (0.10 г) растворяли в N,N-диметилформамиде (1 мл), и раствор перемешивали при комнатной температуре. Последовательно добавляли карбонат калия (0.06 г), 1-хлорэтил метилкарбонат (0.06 г) и иодид натрия (0.01 г), и смесь перемешивали 3 часа при комнатной температуре.
Полученный раствор упаривали при пониженном давлении. Остаток от упаривания очищали методом колоночной хроматографии на силикагеле. Получали 0.11 г целевого соединения.
Примеры соединений по настоящему изобретению, полученных методами, аналогичными описанным выше в Примерах синтезов, приведены в таблице 1. В таблице 1 указаны заместители в соединениях, имеющих формулу (I-1). Кроме того, приведены физические параметры в виде температуры плавления. В таблице Me означает метильную группу, iPr означает изо-пропильную группу, cPr означает циклопропильную группу, и Ph означает фенильную группу. Такие же обозначения применяются в таблице 2.
[Хим. 19]
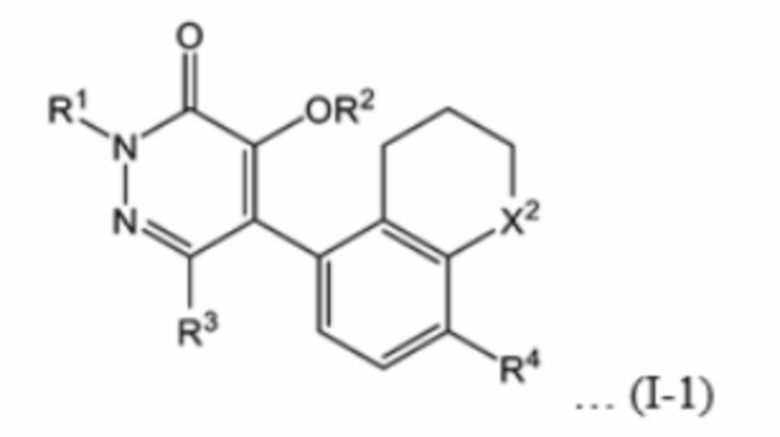
Таблица 1
Кроме того, примеры соединений по настоящему изобретению, полученных методами, аналогичными описанным выше в Примерах синтезов, приведены в таблице 2.
Таблица 2
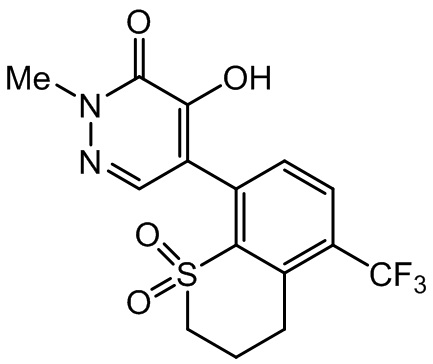
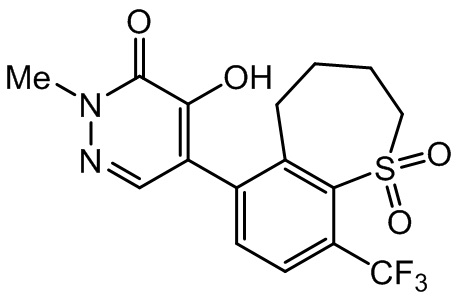
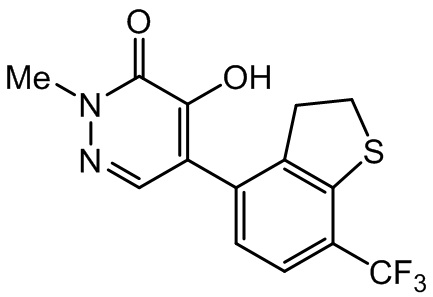
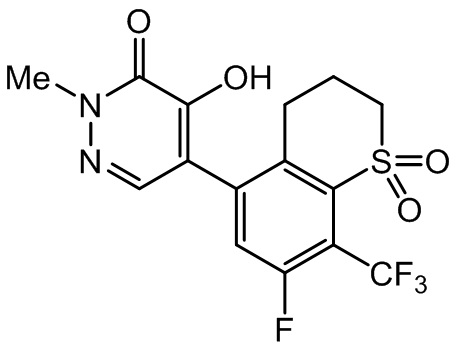
Из числа соединений, перечисленных в таблицах 1 и 2, соединения с символом * в ячейке, касающейся физических свойств, находились в аморфном состоянии или в виде вязкого масла. Ниже приведены данные 1H-ЯМР анализа.
Соединение A-4: 1H-ЯМР (400 МГц, ДМСО-d6): δ 2.20 - 2.26 (м, 2H), 2.78 -2.79 (м, 2H), 3.68 - 3.72 (м, 5H), 7.65 (д, 1H), 7.70 (с, 1H), 8.07 (д, 1H).
Соединение A-7: 1H-ЯМР (400 МГц, CDCl3): δ 2.25 (с, 3H), 2.46 - 2.52 (м, 2H), 2.90 - 2.96 (м, 2H), 3.40 - 3.43 (м, 2H), 3.91 (с, 3H), 4.06 (с, 3H), 6.63 (с, 1H), 7.51 (д, 1H), 7.64 (с, 1H), 7.86 (д, 1H).
Соединение A-18: 1H-ЯМР (400 МГц, CDCl3): δ 2.05 - 2.17 (м, 2H), 2.64 (м, 2H), 3.06 - 3.08 (м, 2H), 3.88 (с, 3H), 6.87 (д, 1H), 7.28 (д, 1H), 7.61 (с, 1H).
Соединение B-1: 1H-ЯМР (400 МГц, ДМСО-d6): δ 2.30 - 2.36 (м, 2H), 3.16 -3.19 (м, 2H), 3.50 - 3.58 (м, 2H), 3.70 (с, 3H), 7.47 (д, 1H), 7.62 (с, 1H), 8.01 (д, 1H).
Соединение B-4: 1H-ЯМР (400 МГц, ДМСО-d6): δ 2.21 - 2.28 (м, 2H), 2.76 -2.81 (м, 2H), 3.54 - 3.56 (м, 2H), 3.72 (с, 3H), 7.77 (д, 1H).
Оценка гербицидного действия
В описанных ниже Примерах тестов продемонстрировано, что соединения по настоящему изобретению могут применяться в качестве действующего вещества в гербицидах.
Пример теста 1
(1) Получение концентрата эмульсии для теста
Концентрат эмульсии получали смешиванием и растворением ПОЭ аллил фенилового эфира (4.1 вес.частей), ПОЭ-ПОП гликоля (1 вес.часть), ПОЭ сорбитан лаурата (0.8 вес.частей), глицерина (2.6 вес.частей), диметилформамида (65.9 вес.частей), N-метилпирролидона (5.1 вес.частей), циклогексанона (15.4 вес.частей) и ароматического углеводорода (5.1 вес.частей). Соединение по настоящему изобретению (4 мг) растворяли в полученном концентрате эмульсии (100 мкМ), получая концентрат эмульсии для тестирования. ПОА означает “полиоксиалкилен”, ПОЭ означает “полиоксиэтилен”, и ПОП означает “полиоксипропилен”.
(2) Обработка всходов опрыскиванием
Семена Avena sativa, Matricaria chamomilla, Setaria faberi, Digitaria ciliaris, Abutilon theophrasti и Amaranthus retroflexus помещали на слой почвы в горшке площадью 150 см2 и затем слегка присыпали почвой. Затем горшки выдерживали в теплице для прорастания растений. Когда каждое из растений дало всходы высотой от 2 до 4 см, описанный выше концентрат эмульсии разводили водой до указанного количества действующего вещества и затем опрыскивали всходы через небольшой спреер в норме расхода 250 л воды на гектар.
(3) Оценка
Через три недели после обработки определяли вес всходов для каждого сорняка в необработанном горшке и в обработанном горшке. Коэффициент гербицидного действия вычисляли по приведенной ниже формуле.
(4) Вычисление коэффициента гербицидного действия
Коэффициент гербицидного действия (%) = [(Вес всходов живого растения в необработанном горшке – Вес всходов живого растения в обработанном горшке) / (Вес всходов живого растения в необработанном горшке)] × 100
(a) Avena sativa
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 3, распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 100% гербицидную активность в отношении Avena sativa.
Таблица 3
(b) Matricaria chamomilla
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 4, распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 80% или больше гербицидную активность в отношении Matricaria chamomilla.
Таблица 4
(c) Setaria faberi
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 5 распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 100% гербицидную активность в отношении Setaria faberi.
Таблица 5
(d) Digitaria ciliaris
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 6, распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 100% гербицидную активность в отношении Digitaria ciliaris.
Таблица 6
(e) Abutilon theophrasti
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 7, распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 80% или больше гербицидную активность в отношении Abutilon theophrasti.
Таблица 7
(f) Amaranthus retroflexus
Разведенный концентрат эмульсии каждого из соединений, перечисленных в таблице 8, распрыскивали в дозировке 250 грамм соединения на гектар. В результате все соединения продемонстрировали 100% гербицидную активность в отношении Amaranthus retroflexus.
Таблица 8
Пример теста 2
Тесты опрыскивания всходов
(1) Получение концентрата эмульсии для теста
Концентрат эмульсии для тестирования получали таким же образом, как описано в Примере теста 1.
(2) Обработка всходов опрыскиванием
Семена Lolium multiflorum, Digitaria ciliaris и кормовой Zea mays помещали на слой почвы в горшке площадью 150 см2 и затем слегка присыпали почвой. Затем горшки выдерживали в теплице для прорастания растений. Когда Lolium multiflorum и Digitaria ciliaris дали всходы высотой от 2 до 4 см, и кормовая Zea mays дала всходы высотой от 20 до 30 см, описанный выше концентрат эмульсии разводили водой до указанного количества действующего вещества и затем опрыскивали всходы через небольшой спреер в норме расхода 250 л воды на гектар.
(3) Оценка
Через четыре недели после обработки определяли вес всходов живого растения в необработанном горшке и в обработанном горшке для Lolium multiflorum, Digitaria ciliaris и кормовой Zea mays. Коэффициент гербицидного действия вычисляли по приведенной ниже формуле.
(4) Вычисление коэффициента гербицидного действия
Коэффициент гербицидного действия (%) = [(Вес всходов живого растения в необработанном горшке – Вес всходов живого растения в обработанном горшке) / (Вес всходов живого растения в необработанном горшке)] × 100
Разведенный концентрат эмульсии соединения A-2 распрыскивали в дозировке 63 грамм соединения на гектар.
Кроме того, для соединения (A), описанного в Патентом документе 1, проводили аналогичные опыты по описанной выше методике.
[Хим. 20]
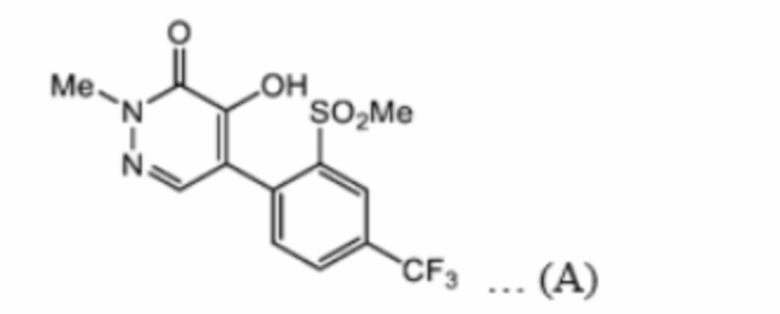
Коэффициент гербицидного действия для каждого из соединений приведен в таблице 9.
Таблица 9
multiflorum
Пример теста 3
(1) Получение концентрата эмульсии для теста
Концентрат эмульсии для тестирования получали таким же образом, как описано в Примере теста 1.
(2) Обработка всходов опрыскиванием
Семена кормовой Zea mays, Alopecurus myosuroides, Lolium multiflorum, Avena sativa, Digitaria ciliaris, Setaria faberi, Abutilon theophrasti и Amaranthus retroflexus помещали на слой почвы в горшке площадью 150 см2 и затем слегка присыпали почвой. Затем горшки выдерживали в теплице для прорастания растений. Когда Alopecurus myosuroides, Lolium multiflorum, Avena sativa, Digitaria ciliaris, Setaria faberi, Abutilon theophrasti и Amaranthus retroflexus дали всходы высотой от 2 до 4 см, и кормовая Zea mays дала всходы высотой от 20 до 30 см, описанный выше концентрат эмульсии разводили водой до указанного количества действующего вещества и затем опрыскивали всходы через небольшой спреер в норме расхода 250 л воды на гектар.
(3) Оценка
Через три недели после обработки определяли вес всходов живого растения в необработанном горшке и в обработанном горшке для каждого растения. Коэффициент гербицидного действия вычисляли по приведенной ниже формуле.
(4) Вычисление коэффициента гербицидного действия
Коэффициент гербицидного действия (%) = [(Вес всходов живого растения в необработанном горшке – Вес всходов живого растения в обработанном горшке) / (Вес всходов живого растения в необработанном горшке)] × 100
Разведенный концентрат эмульсии соединения A-2 распрыскивали в дозировке 250 г или 63 грамм соединения на гектар.
Кроме того, для соединения (A), описанного в Патентом документе 1, проводили аналогичные опыты по описанной выше методике.
Коэффициент гербицидного действия для каждого из соединений приведен в таблице 10. В таблице 10, “г ДВ” означает граммы (г) действующего вещества (ДВ).
Таблица 10
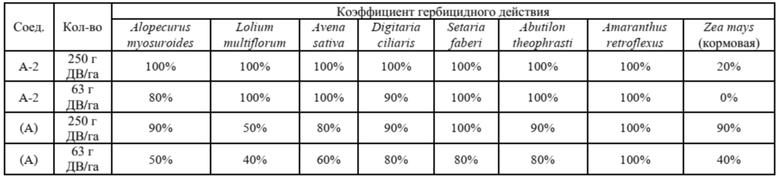
Результаты, приведенные выше в таблице 9 и таблице 10, ясно показывают, что соединение по настоящему изобретению оказывает более сильное гербицидное действие при обработке всходов даже в низкой дозировке, по сравнению с соединением, описанным в Патентном документе 1. С другой стороны, соединение по настоящему изобретению не оказывает гербицидного действия на кормовую Zea mays, и это показывает, что соединение по настоящему изобретению более безопасно для культурных растений.
Промышленная применимость
Пиридазиновые соединения по настоящему изобретению демонстрируют надежную эффективность в борьбе с сорняками даже в низкой дозировке, обладают уменьшенной фитотоксичностью по отношению к культурным растениям и безопасны для окружающей среды. Поэтому пиридазиновые соединения по настоящему изобретению могут применяться в качестве действующего вещества в гербицидах. Гербициды по настоящему изобретению можно безопасно использовать для борьбы с сорняками при выращивании сельскохозяйственных и плодовоовощных культур.
| название | год | авторы | номер документа |
|---|---|---|---|
| 7-ОКСА-3,4-ДИАЗАБИЦИКЛО[4.1.0]ГЕПТ-4-ЕН-2-ОНОВОЕ СОЕДИНЕНИЕ И ГЕРБИЦИД | 2020 |
|
RU2818255C2 |
| СРЕДСТВО ДЛЯ ЗАЩИТЫ КУЛЬТУРНЫХ РАСТЕНИЙ ОТ ФИТОТОКСИЧЕСКОГО ПОБОЧНОГО ДЕЙСТВИЯ ГЕРБИЦИДОВ, N-АЦИЛСУЛЬФОНАМИДЫ | 1997 |
|
RU2182423C2 |
| ИЗОКСАЗОЛИНОВЫЕ ПРОИЗВОДНЫЕ И ГЕРБИЦИДЫ, СОДЕРЖАЩИЕ ИХ В КАЧЕСТВЕ АКТИВНЫХ ИНГРЕДИЕНТОВ | 2000 |
|
RU2237664C2 |
| СОЕДИНЕНИЕ НА ОСНОВЕ ЗАМЕЩЕННОГО ТИАЗОЛЬНОГО АРОМАТИЧЕСКОГО КОЛЬЦА И СПОСОБ ЕГО ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2830426C1 |
| ПРОИЗВОДНЫЕ АМИДОВ ПИРАЗОЛГЛИКОЛЕВОЙ КИСЛОТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1992 |
|
RU2090560C1 |
| ЗАМЕЩЕННОЕ АРОМАТИЧЕСКОЕ СОЕДИНЕНИЕ С КОНДЕНСИРОВАННЫМ КОЛЬЦОМ, СПОСОБ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2828176C1 |
| АРИЛОКСИПИРИМИДИНИЛОВЫЕ ЭФИРЫ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2016 |
|
RU2745802C2 |
| ЗАМЕЩЕННОЕ ПРОИЗВОДНОЕ ПИРИМИДИНИЛФОРМИЛОКСИМА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЕГО ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2018 |
|
RU2777594C2 |
| 2,6-ДИОКСО-3,6-ДИГИДРОПИРИМИДИН, СЕЛЬСКОХОЗЯЙСТВЕННЫЙ И САДОВОДЧЕСКИЙ БАКТЕРИЦИД, НЕМАТОЦИД И МЕДИЦИНСКОЕ И ВЕТЕРИНАРНОЕ ФУНГИЦИДНОЕ СРЕДСТВО | 2020 |
|
RU2837454C1 |
| ПРОИЗВОДНЫЕ СУЛЬФАМИДОСУЛЬФОНИЛМОЧЕВИНЫ И СЕЛЕКТИВНАЯ ГЕРБЕЦИДНАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2088583C1 |
Изобретение относится к новому пиридазиновому соединению формулы (I). В формуле (I) R1 представляет собой замещенную или незамещенную C1-C6 алкильную группу, незамещенную C2-C6 алкенильную группу или незамещенную C3-C6 циклоалкильную группу, где заместитель в C1-C6 алкильной группе представляет собой галоген или C1-C6 алкокси-группу, R2 представляет собой атом водорода, замещенную или незамещенную C1-C6 алкильную группу, группу Ra-CO-, группу RaO-CO-, группу Ra-SO2-, группу Ra-CO-O-CRb2- или группу RaO-CO-O-CRb2-, где заместитель в C1-C6 алкильной группе представляет собой C1-C6 алкокси-группу, каждый Ra независимо представляет собой незамещенную C1-C6 алкильную группу, замещенную или незамещенную фенильную группу или замещенную или незамещенную пиразолильную группу, где заместитель в фенильной группе или пиразолильной группе представляет собой C1-C6 алкильную группу, каждый Rb независимо представляет собой атом водорода или незамещенную C1-C6 алкильную группу, R3 представляет собой атом водорода, незамещенную C1-C6 алкильную группу или незамещенную C3-C6 циклоалкильную группу, R4 представляет собой галоген, замещенную или незамещенную C1-C6 алкильную группу, замещенную или незамещенную C1-C6 алкокси-группу или циано-группу, где заместитель в C1-C6 алкильной группе или C1-C6 алкокси-группе представляет собой галоген, R5 представляет собой атом водорода или галоген и R6 представляет собой атом водорода, A представляет собой незамещенную C1-C4 алкиленовую группу, X1 представляет собой сульфонильную группу, X2 представляет собой сульфенильную группу или сульфонильную группу, m равен 0 или 1, n равен 0 или 1, и сумма m и n равна 1 или 2, и, когда A представляет собой незамещенную метиленовую группу, сумма m и n равна 2. Также предложены гербицид, содержащий по меньшей мере один представитель, выбранный из группы, состоящей из соединения формулы (I) и его соли, в качестве действующего вещества, и способ борьбы с однодольными и/или двудольными сорняками среди культурных растений. Предложенное пиридазиновое соединение может применяться в качестве действующего вещества в гербицидах, обладает надежной эффективностью в борьбе с сорняками даже в низкой дозировке, сниженной фитотоксичностью по отношению к культурным растениям и безопасно для окружающей среды. 3 н.п. ф-лы, 10 табл., 9 пр.
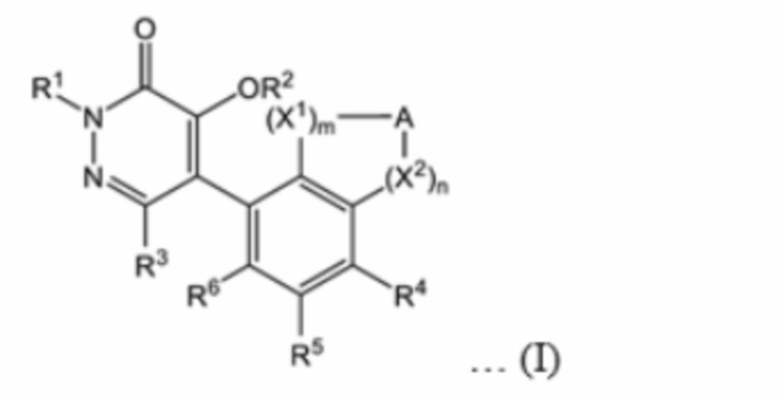
1. Соединение, имеющее формулу (I)
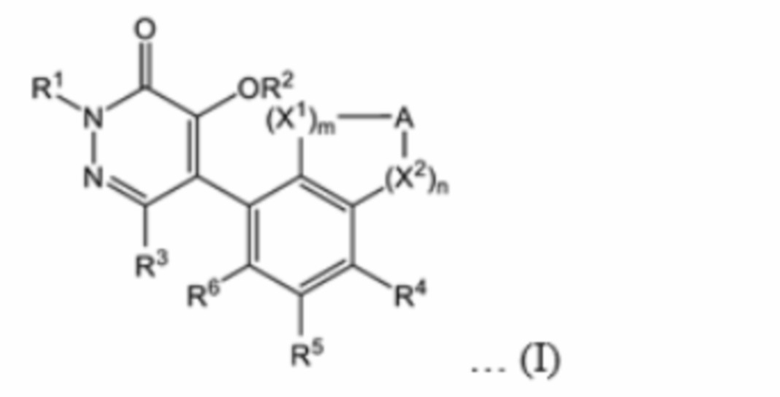
в формуле (I)
R1 представляет собой замещенную или незамещенную C1-C6 алкильную группу, незамещенную C2-C6 алкенильную группу или незамещенную C3-C6 циклоалкильную группу, где заместитель в C1-C6 алкильной группе представляет собой галоген или C1-C6 алкокси-группу,
R2 представляет собой атом водорода, замещенную или незамещенную C1-C6 алкильную группу, группу Ra-CO-, группу RaO-CO-, группу Ra-SO2-, группу Ra-CO-O-CRb2- или группу RaO-CO-O-CRb2-, где заместитель в C1-C6 алкильной группе представляет собой C1-C6 алкокси-группу,
каждый Ra независимо представляет собой незамещенную C1-C6 алкильную группу, замещенную или незамещенную фенильную группу или замещенную или незамещенную пиразолильную группу, где заместитель в фенильной группе или пиразолильной группе представляет собой C1-C6 алкильную группу,
каждый Rb независимо представляет собой атом водорода или незамещенную C1-C6 алкильную группу,
R3 представляет собой атом водорода, незамещенную C1-C6 алкильную группу или незамещенную C3-C6 циклоалкильную группу,
R4 представляет собой галоген, замещенную или незамещенную C1-C6 алкильную группу, замещенную или незамещенную C1-C6 алкокси-группу или циано-группу, где заместитель в C1-C6 алкильной группе или C1-C6 алкокси-группе представляет собой галоген,
R5 представляет собой атом водорода или галоген, и
R6 представляет собой атом водорода,
A представляет собой незамещенную C1-C4 алкиленовую группу,
X1 представляет собой сульфонильную группу,
X2 представляет собой сульфенильную группу или сульфонильную группу,
m равен 0 или 1, n равен 0 или 1, и
сумма m и n равна 1 или 2, и, когда A представляет собой незамещенную метиленовую группу, сумма m и n равна 2.
2. Гербицид, содержащий по меньшей мере один представитель, выбранный из группы, состоящей из соединения по п. 1 и его соли, в качестве действующего вещества.
3. Способ борьбы с однодольными и/или двудольными сорняками среди культурных растений, включающий стадию нанесения соединения по п. 1 или его соли, или гербицида, содержащего указанное соединение, на сорняки и/или культурные растения, и/или их локусы.
| EA 201400396 A1, 29.08.2014 | |||
| US 5723411 A, 03.03.1998 | |||
| WO 2017074992 A1, 04.05.2017 | |||
| WO 2017074988 А1, 04.05.2017 | |||
| EA 201692186 A1, 28.04.2017 | |||
| JP 2004043397 A, 12.02.2004. |
Авторы
Даты
2024-04-09—Публикация
2020-09-23—Подача