Область техники
Изобретение относится к области пестицидной технологии, и в частности, к типу замещенного ароматического соединения с конденсированным кольцом, способу получения, гербицидной композиции и ее применению.
Уровень техники
Борьба с сорняками является одним из важнейших звеньев в процессе достижения высокой эффективности сельского хозяйства. На рынке доступны различные гербициды, например, патенты WO00/50409 и т.д. описывают использование соединения общей формулы 1-арил-4-тиотриазин в качестве гербицида; CN105753853A описывает изоксазолин-содержащее соединение урацила и его применение в качестве гербицида. Однако гербицидные свойства этих известных соединений против вредных растений и их селективность в отношении сельскохозяйственных культур не являются полностью удовлетворительными. И ученым по-прежнему необходимо постоянно проводить исследования и разрабатывать новые гербициды с высокой эффективностью, безопасностью, экономичностью и различными способами действия из-за таких проблем, как растущий рынок, устойчивость сорняков, срок службы и экономичность пестицидов, а также растущее беспокойство людей по вопросам охраны окружающей среды.
Сущность изобретения
В настоящем изобретении представлен тип замещенного ароматического соединения с конденсированным кольцом, способ получения, гербицидная композиция и ее применение. Соединение обладает превосходной гербицидной активностью против злаковых сорняков, широколиственных сорняков и т.д., даже при низких нормах расхода, и имеет высокую селективность для сельскохозяйственных культур.
Техническое решение, принятое в соответствии с изобретением, заключается в следующем:
Замещенное ароматическое соединение с конденсированным кольцом, представленное общей формулой I:
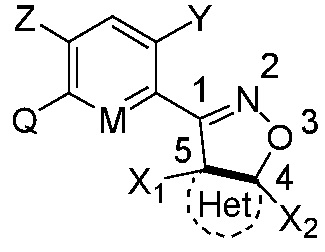
I
где
Q является  ,
,
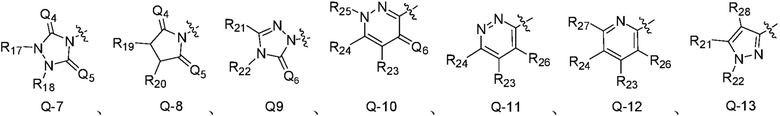 ,
,
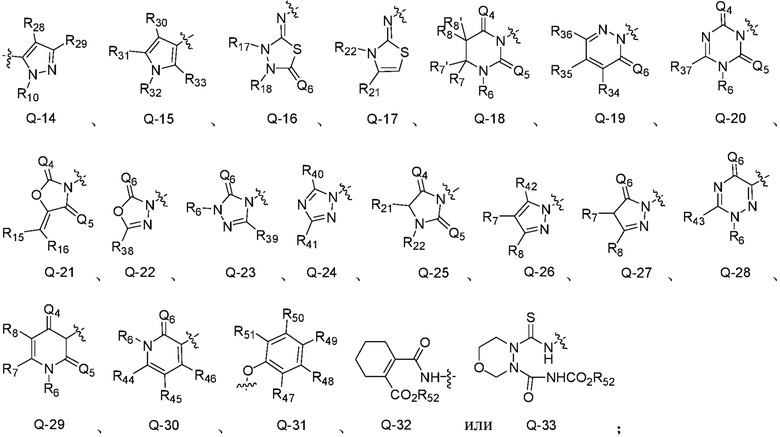
Y является галогеном, галоалкилом, циано, нитро или амино;
Z является H, галогеном или гидрокси;
M является CH или N;
Q1, Q2, Q3, Q4, Q5, Q6 каждый независимо является O или S;
Het является циклической структурой, связанной посредством двух атомов углерода в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3~8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом, содержащим 1, 2 или 3 гетероатома, выбранных из O, S, N, NH, CO, SO2 или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо не замещено или замещено, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -SOR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(CO)OR14;
X1, X2 каждый независимо является H, галогеном, нитро, циано, тиоциано, гидрокси, меркапто, сульфо, формилом, галоформилом, азидо, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, -PO(OR’)2, -OR”, -(CO)R”, -SR”, -(SO)R”, -(SO2)R”, -Si(R”)3, -O(CO)R”, -O-(SO2)R”, -S(CO)R”, -(SO2)OR”, -O(CO)OR”, -(CO)(CO)OR”, 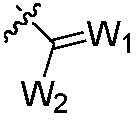 , -CR’=N-OH, -CR’=N-O-R”, гетероциклилом, гетероциклилалкилом, арилом, арилалкилом, амино, аминоалкилом, аминокарбонилалкилом, аминокарбонилоксиалкилом, аминотиокарбонилоксиалкилом, аминосульфонилом или аминосульфонилоксиалкилом, где
, -CR’=N-OH, -CR’=N-O-R”, гетероциклилом, гетероциклилалкилом, арилом, арилалкилом, амино, аминоалкилом, аминокарбонилалкилом, аминокарбонилоксиалкилом, аминотиокарбонилоксиалкилом, аминосульфонилом или аминосульфонилоксиалкилом, где
группы «алкил», «алкенил» и «алкинил» каждая независимо не замещена или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, гидрокси, меркапто, карбоксила, -OR’’, -(CO)R’’, -SR’’, -(SO2)R’’, -O(CO)H, -O(CO)R’’, -O-(SO2)R’’, -(CO)OR’’, -O(CO)OR’’, -O(CO)(CO)OH, -O(CO)(CO)OR’’, -O-алкил-(CO)OH или -O-алкил-(CO)OR’’,
группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «гетероциклил», «гетероциклилалкил», «арил» и «арилалкил» каждая независимо не замещена или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо,
группы «амино», «аминоалкил», «аминокарбонилалкил», «аминокарбонилоксиалкил», «аминотиокарбонилоксиалкил», «аминосульфонил» и «аминосульфонилокси алкил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -алкил-(CO)OR11, -(SO2)R11, -(SO2)OR11, -алкил-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2;
R’ независимо является H, галогеном, алкокси, алкоксиалкилом, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, арилом, арилалкилом, гетероциклилом или гетероциклилалкилом; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена галогеном; группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «арил», «арилалкил», «гетероциклил» и «гетероциклилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R’’ независимо является алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, арилом, арилалкилом, арилалкенилом, гетероциклилом, гетероциклилалкилом или гетероциклилалкенилом; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, триалкилсилила, -OR13, -SR13, -O(CO)R13, -(CO)R13, -(CO)OR13 или -O(CO)OR13; группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «арил», «арилалкил», «арилалкенил», «гетероциклил», «гетероциклилалкил» и «гетероциклилалкенил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
W1 является O, S, NH или N-алкил;
W2 является OW3, SW3 или N(W3)2;
W3 независимо является H, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкенилом, гетероциклилом, арилом, 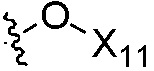 ,
, 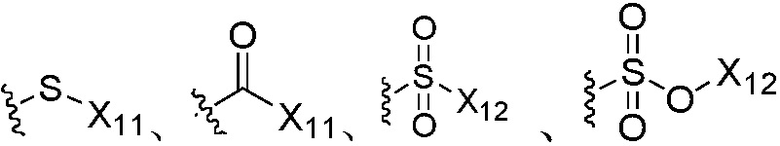 ,
, 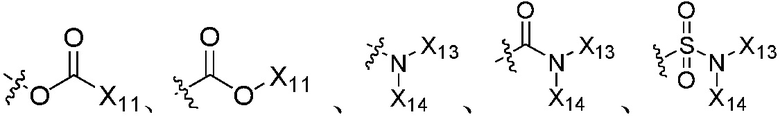 ,
, 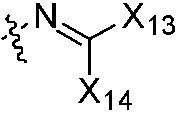 или
или 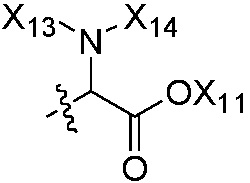 ; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, циклоалкила, триалкилсилила, циклоалкенила, гетероциклила, арила,
; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, циклоалкила, триалкилсилила, циклоалкенила, гетероциклила, арила, 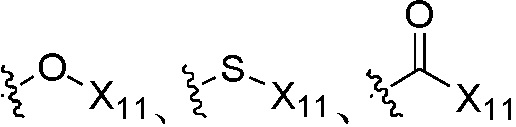 ,
, 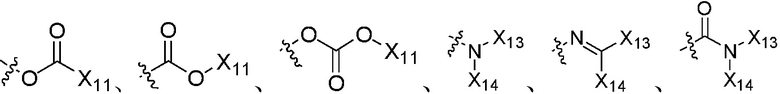 или
или 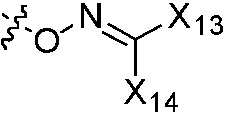 ; группы «циклоалкил», «циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
; группы «циклоалкил», «циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или N(W3)2 является незамещенным или замещенным гетероциклом с атомом азота в 1-положении;
X11 независимо является H, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, гетероциклилом, гетероциклилалкилом, арилом или арилалкилом; где группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «гетероциклил», «гетероциклилалкил», «арил» и «арилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X12 независимо является алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, гетероциклилом, гетероциклилалкилом, арилом или арилалкилом; где группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «гетероциклил», «гетероциклилалкил», «арил» и «арилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X13, X14 каждый независимо является H, галогеном, циано, алкокси, алкоксиалкилом, алкил карбонилом, алкокси карбонилом, алкил сульфонилом, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, арилом, арилалкилом, гетероциклилом или гетероциклилалкилом, или группа CX13X14, взятые вместе, образуют не замещенную или замещенную циклическую структуру, или группа NX13X14, взятые вместе, образуют не замещенный или замещенный гетероциклил с атомом азота в 1-положении; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена галогеном; группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «арил», «арилалкил», «гетероциклил» и «гетероциклилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является H, циано, алкилом, алкенилом, алкинилом, формилалкилом, цианоалкилом, амино, аминоалкилом, аминокарбонилом, аминокарбонилалкилом, аминосульфонилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, гетероциклилом, гетероциклилалкилом, арилом, арилалкилом, R4R5N-(CO)-NR3-, 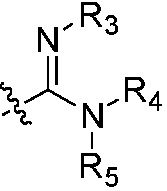 , R3-S(O)m-(алкил)n-, R3-O-(алкилом)n-, R3-(CO)-(алкилом)n-, R3-O-(алкил)n-(CO)-, R3-(CO)-O-(алкилом)n-, R3-S-(CO)-(алкилом)n-, R3-O-(CO)-алкилом- или R3-O-(CO)-O-алкилом-, где
, R3-S(O)m-(алкил)n-, R3-O-(алкилом)n-, R3-(CO)-(алкилом)n-, R3-O-(алкил)n-(CO)-, R3-(CO)-O-(алкилом)n-, R3-S-(CO)-(алкилом)n-, R3-O-(CO)-алкилом- или R3-O-(CO)-O-алкилом-, где
группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена галогеном,
группы «амино», «аминоалкил», «аминокарбонил», «аминокарбонилалкил» и «аминосульфонил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -алкил-(CO)OR11, -(SO2)R11, -(SO2)OR11, -алкил-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2,
группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «гетероциклил», «гетероциклилалкил», «арил» и «арилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или R17, R18, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH2OCH2-, который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, алкила или галоалкила;
R3, R4, R5 каждый независимо является H, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, гетероциклилом, гетероциклилалкилом, арилом или арилалкилом; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена галогеном; группы «циклоалкил», «циклоалкилалкил», «циклоалкенил», «циклоалкенилалкил», «гетероциклил», «гетероциклилалкил», «арил» и «арилалкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, галоалкила, галоалкенила, галоалкинила, галоциклоалкила, алкил-замещенного циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-алкил-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R7, R8, R7’, R8’, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R34, R35, R36, R37, R38, R39, R40, R41, R42, R43, R44, R45, R46, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, меркапто, формилом, гидроксиалкилом, нитро, циано, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, -OR11, -SR11, -(SO)R11, -(SO2)R11, -(SO2)OR11, -O(SO2)R11, -N(R12)2, фенилом или бензилом, где
группы «алкил», «алкенил», «алкинил», «циклоалкил», «циклоалкилалкил», «циклоалкенил» и «циклоалкенилалкил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, алкила, галоалкила, алкокси карбонила, алкилтио, алкилсульфонила, алкокси или галоалкокси;
или R7, R8, взятые вместе образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, алкила или галоалкила;
или R19, R20, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, алкила или галоалкила;
или R21, R22, взятые вместе образуют -CH2CH2CH2-, -CH2OCH2CH2- или -CH2CH2CH2CH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, алкила или галоалкила;
R11 независимо является алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом, циклоалкенилалкилом, фенилом или бензилом; где группы «алкил», «алкенил» и «алкинил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, алкила, галоалкила, алкокси карбонила, алкилтио, алкилсульфонила, алкокси или галоалкокси;
R12 независимо является H, алкилом, алкенилом, алкинилом, алкокси, алкил сульфонилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом или циклоалкенилалкилом, или группа N(R12)2 в -(CO)N(R12)2 или -(SO2)N(R12)2 независимо является незамещенным или замещенным гетероциклом с атомом азота в 1-положении;
R13 независимо является алкилом, алкенилом, алкинилом, циклоалкилом, фенилом или фенилом, замещенным, по меньшей мере, одной группой, выбранной из: галогена, циано, нитро, алкила, галоалкила, алкокси, галоалкокси, алкоксикарбонила, алкилтио, алкилсульфонила или фенокси, замещенным, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, алкила, галоалкила, алкокси или галоалкокси;
R14 независимо является H, алкилом, галоалкилом, фенилом или фенилом, замещенным, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, алкила, галоалкила, алкоксикарбонила, алкилтио, алкилсульфонила, алкокси или галоалкокси;
R15, R16, R52 каждый независимо является H, галогеном, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкилалкилом, циклоалкенилом или циклоалкенилалкилом, где группы «алкил», «алкенил», «алкинил», «циклоалкил», «циклоалкилалкил», «циклоалкенил» и «циклоалкенилалкил» каждая независимо является незамещенной или замещена галогеном;
m является 0, 1 или 2; n независимо является 0 или 1.
Предпочтительно, Y является галогеном, гало C1-C8 алкилом, циано, нитро или амино;
Het является циклической структурой, которая имеет два общих атома в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3~8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом содержащим 1, 2 или 3 гетероатома, выбранных из O, S, N, NH, CO, SO2 или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо не замещено или замещено, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -SOR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(CO)OR14;
X1, X2 каждый независимо является H, галогеном, нитро, циано, тиоциано, гидрокси, меркапто, сульфо, формилом, галоформилом, азидо, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, -PO(OR’)2, -OR’’, -(CO)R’’, -SR’’, -(SO)R’’, -(SO2)R’’, -Si(R’’)3, -O(CO)R’’, -O-(SO2)R’’, -S(CO)R’’, -(SO2)OR’’, -O(CO)OR’’, -(CO)(CO)OR’’, 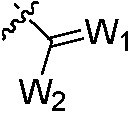 , -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C8 алкилом, арилом, арил C1-C8 алкилом, амино, амино C1-C8 алкилом, аминокарбонил C1-C8 алкилом, аминокарбонилокси C1-C8 алкилом, аминотиокарбонилокси C1-C8 алкилом, аминосульфонилом или аминосульфонилокси C1-C8 алкилом, где
, -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C8 алкилом, арилом, арил C1-C8 алкилом, амино, амино C1-C8 алкилом, аминокарбонил C1-C8 алкилом, аминокарбонилокси C1-C8 алкилом, аминотиокарбонилокси C1-C8 алкилом, аминосульфонилом или аминосульфонилокси C1-C8 алкилом, где
группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, гидрокси, меркапто, карбоксила, -OR’’, -(CO)R’’, -SR’’, -(SO2)R’’, -O(CO)H, -O(CO)R’’, -O-(SO2)R’’, -(CO)OR’’, -O(CO)OR’’, -O(CO)(CO)OH, -O(CO)(CO)OR’’, -O-(C1-C8 алкил)-(CO)OH или -O-(C1-C8 алкил)-(CO)OR’’,
группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «гетероциклил», «гетероциклил C1-C8 алкил», «арил» и «арил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо,
группы «амино», «амино C1-C8 алкил», «аминокарбонил C1-C8 алкил», «аминокарбонилокси C1-C8 алкил», «аминотиокарбонилокси C1-C8 алкил», «аминосульфонил» и «аминосульфонилокси C1-C8 алкил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -(C1-C8 алкил)-(CO)OR11, -(SO2)R11, -(SO2)OR11, -(C1-C8 алкил)-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2;
R’ независимо является H, галогеном, C1-C8 алкокси, C1-C8 алкокси C1-C8 алкилом, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, арилом, арил C1-C8 алкилом, гетероциклилом или гетероциклил C1-C8 алкилом, где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «арил», «арил C1-C8 алкил», «гетероциклил» и «гетероциклил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R’’ независимо является C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, арилом, арил C1-C8 алкилом, арил C2-C8 алкенилом, гетероциклилом, гетероциклил C1-C8 алкилом или гетероциклил C2-C8 алкенилом; где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, три C1-C8 алкилсилила, -OR13, -SR13, -O(CO)R13, -(CO)R13, -(CO)OR13 или -O(CO)OR13; группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «арил», «арил C1-C8 алкил», «арил C2-C8 алкенил», «гетероциклил», «гетероциклил C1-C8 алкил» и «гетероциклил C2-C8 алкенил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
W1 является O, S, NH или N-(C1-C8 алкилом);
W3 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкенилом, гетероциклилом, арилом, 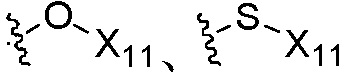 ,
, 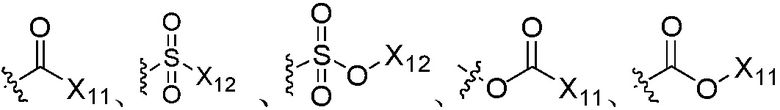 ,
, 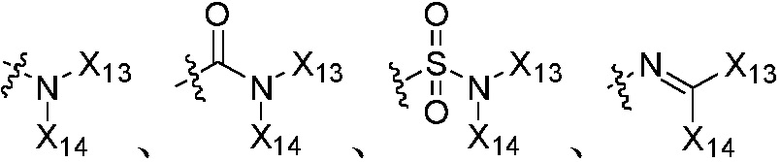 или
или 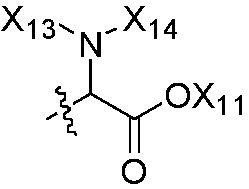 , где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C3-C8 циклоалкила, три C1-C8 алкилсилила, C3-C8 циклоалкенила, гетероциклила, арила,
, где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C3-C8 циклоалкила, три C1-C8 алкилсилила, C3-C8 циклоалкенила, гетероциклила, арила, 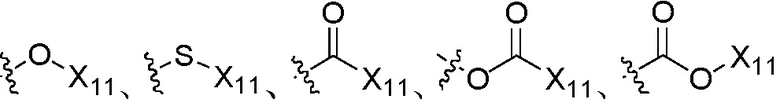 ,
, 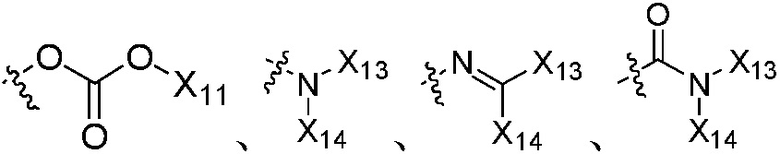 или
или 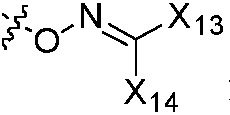 ; группы «C3-C8 циклоалкил», «C3-C8 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
; группы «C3-C8 циклоалкил», «C3-C8 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или N(W3)2 является 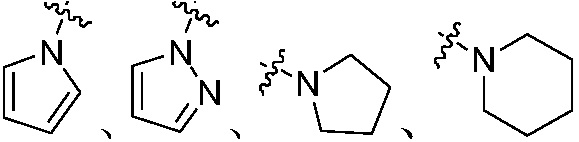 или
или 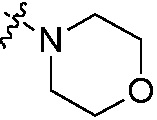 , который не замещен или замещен, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
, который не замещен или замещен, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
X11 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, гетероциклилом, гетероциклил C1-C8 алкилом, арилом или арил C1-C8 алкилом; где группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «гетероциклил», «гетероциклил C1-C8 алкил», «арил» и «арил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X12 независимо является C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, гетероциклилом, гетероциклил C1-C8 алкилом, арилом или арил C1-C8 алкилом; где группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «гетероциклил», «гетероциклил C1-C8 алкил», «арил» и «арил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X13, X14 каждый независимо является H, галогеном, циано, C1-C8 алкокси, C1-C8 алкокси C1-C8 алкилом, C1-C8 алкилкарбонилом, C1-C8 алкоксикарбонилом, C1-C8 алкилсульфонилом, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, арилом, арил C1-C8 алкилом, гетероциклилом или гетероциклил C1-C8 алкилом, или группа CX13X14, взятые вместе образуют 5~8-членный карбоциклил или гетероциклил, содержащий кислород, серу или азот, или группа NX13X14, взятые вместе образуют 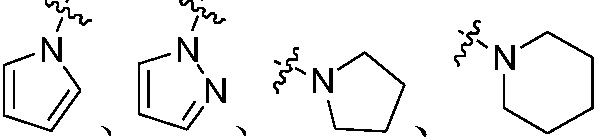 или
или 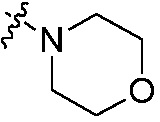 ; где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «арил», «арил C1-C8 алкил», «гетероциклил» и «гетероциклил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный карбоциклил или гетероциклил, содержащий кислород, серу или азот» не замещены или замещены, по меньшей мере, одной группой, выбранной из C1-C8 алкила, C1-C8 алкоксикарбонила или бензила, или вместе с арилом или гетероциклилом образуют конденсированное кольцо; группы «
; где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «арил», «арил C1-C8 алкил», «гетероциклил» и «гетероциклил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный карбоциклил или гетероциклил, содержащий кислород, серу или азот» не замещены или замещены, по меньшей мере, одной группой, выбранной из C1-C8 алкила, C1-C8 алкоксикарбонила или бензила, или вместе с арилом или гетероциклилом образуют конденсированное кольцо; группы « 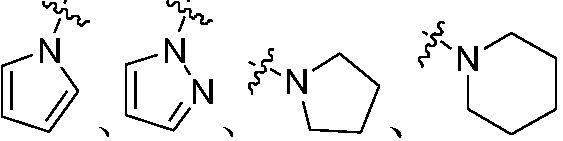 или
или 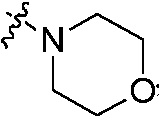 » не замещены или замещены, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
» не замещены или замещены, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является H, циано, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, формил C1-C8 алкилом, циано C1-C8 алкилом, амино, амино C1-C8 алкилом, аминокарбонилом, аминокарбонил C1-C8 алкилом, аминосульфонилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, гетероциклилом, гетероциклил C1-C8 алкилом, арилом, арил C1-C8 алкилом, R4R5N-(CO)-NR3-, 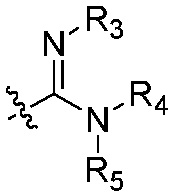 , R3-S(O)m-(C1-C8 алкилом)n-, R3-O-(C1-C8 алкилом)n-, R3-(CO)-(C1-C8 алкилом)n-, R3-O-(C1-C8 алкил)n-(CO)-, R3-(CO)-O-(C1-C8 алкилом)n-, R3-S-(CO)-(C1-C8 алкилом)n-, R3-O-(CO)-(C1-C8 алкилом)- или R3-O-(CO)-O-(C1-C8 алкилом)-, где
, R3-S(O)m-(C1-C8 алкилом)n-, R3-O-(C1-C8 алкилом)n-, R3-(CO)-(C1-C8 алкилом)n-, R3-O-(C1-C8 алкил)n-(CO)-, R3-(CO)-O-(C1-C8 алкилом)n-, R3-S-(CO)-(C1-C8 алкилом)n-, R3-O-(CO)-(C1-C8 алкилом)- или R3-O-(CO)-O-(C1-C8 алкилом)-, где
группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном,
группы «амино», «амино C1-C8 алкил», «аминокарбонил», «аминокарбонил C1-C8 алкил» и «аминосульфонил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -(C1-C8 алкил)-(CO)OR11, -(SO2)R11, -(SO2)OR11, -(C1-C8 алкил)-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2,
группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «гетероциклил», «гетероциклил C1-C8 алкил», «арил» и «арил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или R17, R18, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH2OCH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C8 алкила или гало C1-C8 алкила;
R3, R4, R5 каждый независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, гетероциклилом, гетероциклил C1-C8 алкилом, арилом или арил C1-C8 алкилом, где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном, группы «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил», «C3-C8 циклоалкенил C1-C8 алкил», «гетероциклил», «гетероциклил C1-C8 алкил», «арил» и «арил C1-C8 алкил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из оксо, галогена, циано, нитро, C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, гало C1-C8 алкила, гало C2-C8 алкенила, гало C2-C8 алкинила, гало C3-C8 циклоалкила, C1-C8 алкил-замещенного C3-C8 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C8 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R7, R8, R7’, R8’, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R34, R35, R36, R37, R38, R39, R40, R41, R42, R43, R44, R45, R46, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, меркапто, формилом, гидрокси C1-C8 алкилом, нитро, циано, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, -OR11, -SR11, -(SO)R11, -(SO2)R11, -(SO2)OR11, -O(SO2)R11, -N(R12)2, фенилом или бензилом, где
группы «C1-C8 алкил», «C2-C8 алкенил», «C2-C8 алкинил», «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил» и «C3-C8 циклоалкенил C1-C8 алкил» каждая независимо является незамещенной или замещена галогеном, группы «фенил» и «бензил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C8 алкила, гало C1-C8 алкила, C1-C8 алкоксикарбонила, C1-C8 алкилтио, C1-C8 алкилсульфонила, C1-C8 алкокси или гало C1-C8 алкокси;
или R7, R8, взятые вместе образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C8 алкила или гало C1-C8 алкила;
или R19, R20, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C8 алкила или гало C1-C8 алкила;
или R21, R22, взятые вместе образуют -CH2CH2CH2-, -CH2OCH2CH2- или -CH2CH2CH2CH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C8 алкила или гало C1-C8 алкила;
R11 независимо является C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом, C3-C8 циклоалкенил C1-C8 алкилом, фенилом или бензилом; где группы «C1-C8 алкил», «C2-C8 алкенил» и «C2-C8 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C8 алкила, гало C1-C8 алкила, C1-C8 алкоксикарбонила, C1-C8 алкилтио, C1-C8 алкилсульфонила, C1-C8 алкокси или гало C1-C8 алкокси;
R12 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C1-C8 алкокси, C1-C8 алкилсульфонилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом или C3-C8 циклоалкенил C1-C8 алкилом, или группа N(R12)2 в -(CO)N(R12)2 или -(SO2)N(R12)2 независимо является 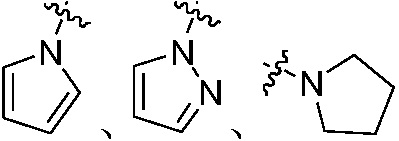 ,
, 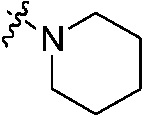 или
или 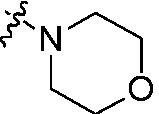 , который не замещен или замещен, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
, который не замещен или замещен, по меньшей мере, одной группой, выбранной из оксо, C1-C8 алкила или C1-C8 алкоксикарбонила;
R13 независимо является C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, фенилом или фенилом, замещенным, по меньшей мере, одной группой, выбранной из: галогена, циано, нитро, C1-C8 алкила, гало C1-C8 алкила, C1-C8 алкокси, гало C1-C8 алкокси, C1-C8 алкоксикарбонила, C1-C8 алкилтио, C1-C8 алкилсульфонила или фенокси, замещенного, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C8 алкила, гало C1-C8 алкила, C1-C8 алкокси или гало C1-C8 алкокси;
R14 независимо является H, C1-C8 алкилом, гало C1-C8 алкилом, фенилом или фенилом, замещенным, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C8 алкила, гало C1-C8 алкила, C1-C8 алкоксикарбонила, C1-C8 алкилтио, C1-C8 алкилсульфонила, C1-C8 алкокси или гало C1-C8 алкокси;
R15, R16, R52 каждый независимо является H, галогеном, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, C3-C8 циклоалкил C1-C8 алкилом, C3-C8 циклоалкенилом или C3-C8 циклоалкенил C1-C8 алкилом, где группы «C1-C8 алкил», «C2-C8 алкенил», «C2-C8 алкинил», «C3-C8 циклоалкил», «C3-C8 циклоалкил C1-C8 алкил», «C3-C8 циклоалкенил» и «C3-C8 циклоалкенил C1-C8 алкил» каждая независимо является незамещенной или замещена галогеном.
Более предпочтительно, Y является галогеном, гало C1-C6 алкилом, циано, нитро или амино;
Het является циклической структурой, которая имеет два общих атома в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3~8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом содержащим 1, 2 или 3 гетероатома, выбранных из O, S, N, NH, CO, SO2 или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо не замещено или замещено, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -SOR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(CO)OR14;
X1, X2 каждый независимо является H, галогеном, нитро, циано, тиоциано, гидрокси, меркапто, сульфо, формилом, галоформилом, азидо, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, -PO(OR’)2, -OR’’, -(CO)R’’, -SR’’, -(SO)R’’, -(SO2)R’’, -Si(R’’)3, -O(CO)R’’, -O-(SO2)R’’, -S(CO)R’’, -(SO2)OR’’, -O(CO)OR’’, -(CO)(CO)OR’’, 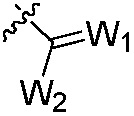 , -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C6 алкилом, арилом, арил C1-C6 алкилом, амино, амино C1-C6 алкилом, аминокарбонил C1-C6 алкилом, аминокарбонилокси C1-C6 алкилом, аминотиокарбонилокси C1-C6 алкилом, аминосульфонилом или аминосульфонилокси C1-C6 алкилом, где
, -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C6 алкилом, арилом, арил C1-C6 алкилом, амино, амино C1-C6 алкилом, аминокарбонил C1-C6 алкилом, аминокарбонилокси C1-C6 алкилом, аминотиокарбонилокси C1-C6 алкилом, аминосульфонилом или аминосульфонилокси C1-C6 алкилом, где
группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, гидрокси, меркапто, карбоксила, -OR’’, -(CO)R’’, -SR’’, -(SO2)R’’, -O(CO)H, -O(CO)R’’, -O-(SO2)R’’, -(CO)OR’’, -O(CO)OR’’, -O(CO)(CO)OH, -O(CO)(CO)OR’’, -O-(C1-C6 алкил)-(CO)OH или -O-(C1-C6 алкил)-(CO)OR’’,
группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «гетероциклил», «гетероциклил C1-C6 алкил», «арил» и «арил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо,
группы «амино», «амино C1-C6 алкил», «аминокарбонил C1-C6 алкил», «аминокарбонилокси C1-C6 алкил», «аминотиокарбонилокси C1-C6 алкил», «аминосульфонил» и «аминосульфонилокси C1-C6 алкил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -(C1-C6 алкил)-(CO)OR11, -(SO2)R11, -(SO2)OR11, -(C1-C6 алкил)-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2;
R’ независимо является H, галогеном, C1-C6 алкокси, C1-C6 алкокси C1-C6 алкилом, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, арилом, арил C1-C6 алкилом, гетероциклилом или гетероциклил C1-C6 алкилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «арил», «арил C1-C6 алкил», «гетероциклил» и «гетероциклил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R’’ независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, арилом, арил C1-C6 алкилом, арил C2-C6 алкенилом, гетероциклилом, гетероциклил C1-C6 алкилом или гетероциклил C2-C6 алкенилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, три C1-C6 алкилсилила, -OR13, -SR13, -O(CO)R13, -(CO)R13, -(CO)OR13 или -O(CO)OR13; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «арил», «арил C1-C6 алкил», «арил C2-C6 алкенил», «гетероциклил», «гетероциклил C1-C6 алкил» и «гетероциклил C2-C6 алкенил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
W1 является O, S, NH или N-(C1-C6 алкилом);
W3 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкенилом, гетероциклилом, арилом, 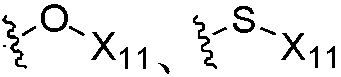 ,
, 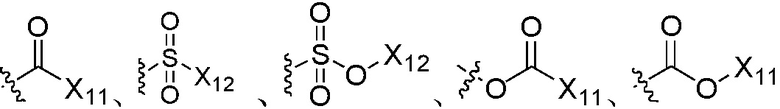 ,
, 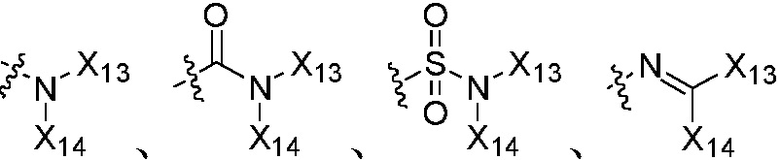 или
или 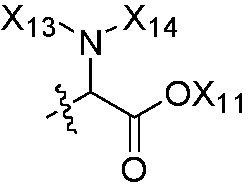 , где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C3-C6 циклоалкила, три C1-C6 алкилсилила, C3-C6 циклоалкенила, гетероциклила, арила,
, где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C3-C6 циклоалкила, три C1-C6 алкилсилила, C3-C6 циклоалкенила, гетероциклила, арила, 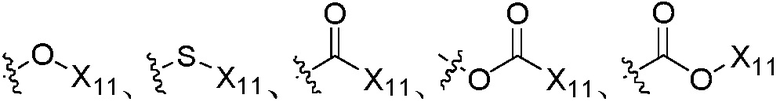 ,
, 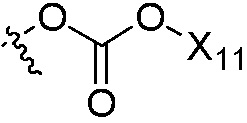 ,
, 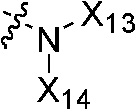 ,
,  или
или 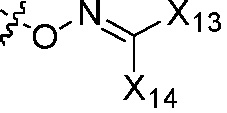 ; группы «C3-C6 циклоалкил», «C3-C6 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
; группы «C3-C6 циклоалкил», «C3-C6 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или N(W3)2 является 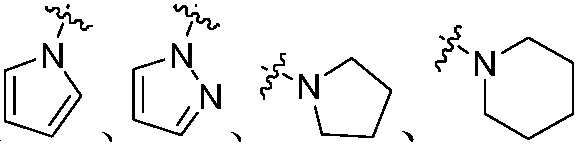 или
или 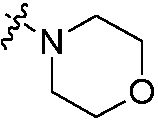 , который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
, который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
X11 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, гетероциклилом, гетероциклил C1-C6 алкилом, арилом или арил C1-C6 алкилом, где группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «гетероциклил», «гетероциклил C1-C6 алкил», «арил» и «арил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X12 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, гетероциклилом, гетероциклил C1-C6 алкилом, арилом или арил C1-C6 алкилом; где группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «гетероциклил», «гетероциклил C1-C6 алкил», «арил» и «арил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X13, X14 каждый независимо является H, галогеном, циано, C1-C6 алкокси, C1-C6 алкокси C1-C6 алкилом, C1-C6 алкилкарбонилом, C1-C6 алкоксикарбонилом, C1-C6 алкилсульфонилом, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, арилом, арил C1-C6 алкилом, гетероциклилом или гетероциклил C1-C6 алкилом, или группа CX13X14, взятые вместе образуют 5~8-членный насыщенный карбоциклил, 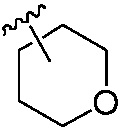 или
или 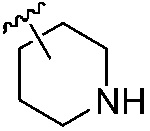 , или группа NX13X14, взятые вместе образуют
, или группа NX13X14, взятые вместе образуют 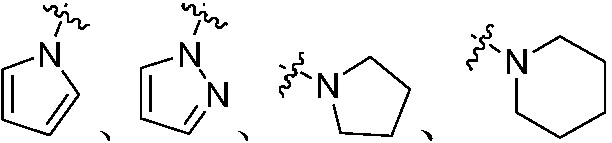 или
или 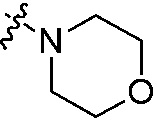 ; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «арил», «арил C1-C6 алкил», «гетероциклил» и «гетероциклил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный насыщенный карбоциклил,
; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «арил», «арил C1-C6 алкил», «гетероциклил» и «гетероциклил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный насыщенный карбоциклил,  или
или  » не замещены или замещены 1, 2 или 3 группами, выбранными из C1-C6 алкила, C1-C6 алкоксикарбонила или бензила, или вместе с арилом или гетероциклилом образуют конденсированное кольцо; группы «
» не замещены или замещены 1, 2 или 3 группами, выбранными из C1-C6 алкила, C1-C6 алкоксикарбонила или бензила, или вместе с арилом или гетероциклилом образуют конденсированное кольцо; группы « 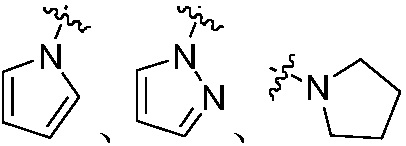 ,
, 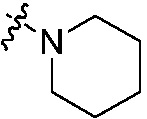 или
или  » не замещены или замещены 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
» не замещены или замещены 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является H, циано, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, формил C1-C6 алкилом, циано C1-C6 алкилом, амино, амино C1-C6 алкилом, аминокарбонилом, аминокарбонил C1-C6 алкилом, аминосульфонилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, гетероциклилом, гетероциклил C1-C6 алкилом, арилом, арил C1-C6 алкилом, R4R5N-(CO)-NR3-, 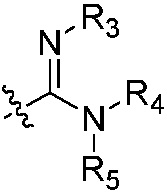 , R3-S(O)m-(C1-C6 алкилом)n-, R3-O-(C1-C6 алкилом)n-, R3-(CO)-(C1-C6 алкилом)n-, R3-O-(C1-C6 алкил)n-(CO)-, R3-(CO)-O-(C1-C6 алкилом)n-, R3-S-(CO)-(C1-C6 алкилом)n-, R3-O-(CO)-(C1-C6 алкилом)- или R3-O-(CO)-O-(C1-C6 алкилом)-, где
, R3-S(O)m-(C1-C6 алкилом)n-, R3-O-(C1-C6 алкилом)n-, R3-(CO)-(C1-C6 алкилом)n-, R3-O-(C1-C6 алкил)n-(CO)-, R3-(CO)-O-(C1-C6 алкилом)n-, R3-S-(CO)-(C1-C6 алкилом)n-, R3-O-(CO)-(C1-C6 алкилом)- или R3-O-(CO)-O-(C1-C6 алкилом)-, где
группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном,
группы «амино», «амино C1-C6 алкил», «аминокарбонил», «аминокарбонил C1-C6 алкил» и «аминосульфонил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -(C1-C6 алкил)-(CO)OR11, -(SO2)R11, -(SO2)OR11, -(C1-C6 алкил)-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2,
группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «гетероциклил», «гетероциклил C1-C6 алкил», «арил» и «арил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или R17, R18, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH2OCH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C6 алкила или гало C1-C6 алкила;
R3, R4, R5 каждый независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, гетероциклилом, гетероциклил C1-C6 алкилом, арилом или арил C1-C6 алкилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C6 алкил», «гетероциклил», «гетероциклил C1-C6 алкил», «арил» и «арил C1-C6 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C6 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R7, R8, R7’, R8’, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R34, R35, R36, R37, R38, R39, R40, R41, R42, R43, R44, R45, R46, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, меркапто, формилом, гидрокси C1-C6 алкилом, нитро, циано, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, -OR11, -SR11, -(SO)R11, -(SO2)R11, -(SO2)OR11, -O(SO2)R11, -N(R12)2, фенилом или бензилом, где
группы «C1-C6 алкил», «C2-C6 алкенил», «C2-C6 алкинил», «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил» и «C3-C6 циклоалкенил C1-C6 алкил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена, по меньшей мере, одной группой, выбранной из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила, C1-C6 алкокси или гало C1-C6 алкокси;
или R7, R8, взятые вместе образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C6 алкила или гало C1-C6 алкила;
или R19, R20, взятые вместе образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C6 алкила или гало C1-C6 алкила;
или R21, R22, взятые вместе образуют -CH2CH2CH2-, -CH2OCH2CH2- или -CH2CH2CH2CH2- который не замещен или замещен, по меньшей мере, одной группой, выбранной из галогена, C1-C6 алкила или гало C1-C6 алкила;
R11 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C6 алкилом, фенилом или бензилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила, C1-C6 алкокси или гало C1-C6 алкокси;
R12 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C1-C6 алкокси, C1-C6 алкилсульфонилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом или C3-C6 циклоалкенил C1-C6 алкилом, или группа N(R12)2 в -(CO)N(R12)2 или -(SO2)N(R12)2 независимо является  или
или  , который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
, который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
R13 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, фенилом или фенилом, замещенным 1, 2 или 3 группами, выбранными из: галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкокси, гало C1-C6 алкокси, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила или фенокси, замещенного 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкокси или гало C1-C6 алкокси;
R14 независимо является H, C1-C6 алкилом, гало C1-C6 алкилом, фенилом или фенилом, замещенным 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила, C1-C6 алкокси или гало C1-C6 алкокси;
R15, R16, R52 каждый независимо является H, галогеном, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C6 алкилом, C3-C6 циклоалкенилом или C3-C6 циклоалкенил C1-C6 алкилом, где группы «C1-C6 алкил», «C2-C6 алкенил», «C2-C6 алкинил», «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C6 алкил», «C3-C6 циклоалкенил» и «C3-C6 циклоалкенил C1-C6 алкил» каждая независимо является незамещенной или замещена галогеном.
Также предпочтительно, X1, X2 каждый независимо является H, галогеном, нитро, циано, тиоциано, гидрокси, меркапто, сульфо, формилом, галоформилом, азидо, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, -PO(OR’)2, -OR’’, -(CO)R’’, -SR’’, -(SO)R’’, -(SO2)R’’, -Si(R’’)3, -O(CO)R’’, -O-(SO2)R’’, -S(CO)R’’, -(SO2)OR’’, -O(CO)OR’’, -(CO)(CO)OR’’, 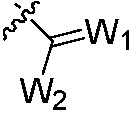 , -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C3 алкилом, арилом, арил C1-C3 алкилом, амино, амино C1-C3 алкилом, аминокарбонил C1-C3 алкилом, аминокарбонилокси C1-C3 алкилом, аминотиокарбонилокси C1-C3 алкилом, аминосульфонилом или аминосульфонилокси C1-C3 алкилом, где
, -CR’=N-OH, -CR’=N-O-R’’, гетероциклилом, гетероциклил C1-C3 алкилом, арилом, арил C1-C3 алкилом, амино, амино C1-C3 алкилом, аминокарбонил C1-C3 алкилом, аминокарбонилокси C1-C3 алкилом, аминотиокарбонилокси C1-C3 алкилом, аминосульфонилом или аминосульфонилокси C1-C3 алкилом, где
группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, гидрокси, меркапто, карбоксила, -OR’’, -(CO)R’’, -SR’’, -(SO2)R’’, -O(CO)H, -O(CO)R’’, -O-(SO2)R’’, -(CO)OR’’, -O(CO)OR’’, -O(CO)(CO)OH, -O(CO)(CO)OR’’, -O-(C1-C3 алкил)-(CO)OH или -O-(C1-C3 алкил)-(CO)OR’’,
группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «гетероциклил», «гетероциклил C1-C3 алкил», «арил» и «арил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо,
группы «амино», «амино C1-C3 алкил», «аминокарбонил C1-C3 алкил», «аминокарбонилокси C1-C3 алкил», «аминотиокарбонилокси C1-C3 алкил», «аминосульфонил» и «аминосульфонилокси C1-C3 алкил» каждая независимо является незамещенной или замещена одной или двумя группами, выбранными из -R11, -OR11, -(CO)R11, -(CO)OR11, -(C1-C3 алкил)-(CO)OR11, -(SO2)R11, -(SO2)OR11, -(C1-C3 алкил)-(SO2)R11, -(CO)N(R12)2 или -(SO2)N(R12)2;
R’ независимо является H, галогеном, C1-C6 алкокси, C1-C6 алкокси C1-C3 алкилом, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, арилом, арил C1-C3 алкилом, гетероциклилом или гетероциклил C1-C3 алкилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «арил», «арил C1-C3 алкил», «гетероциклил» и «гетероциклил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
R’’ независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, арилом, арил C1-C3 алкилом, арил C2-C3 алкенилом, гетероциклилом, гетероциклил C1-C3 алкилом или гетероциклил C2-C3 алкенилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, три C1-C6 алкилсилила, -OR13, -SR13, -O(CO)R13, -(CO)R13, -(CO)OR13 или -O(CO)OR13; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «арил», «арил C1-C3 алкил», «арил C2-C3алкенил», «гетероциклил», «гетероциклил C1-C3 алкил» и «гетероциклил C2-C3 алкенил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
W3 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкенилом, гетероциклилом, арилом, 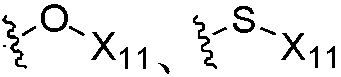 ,
, 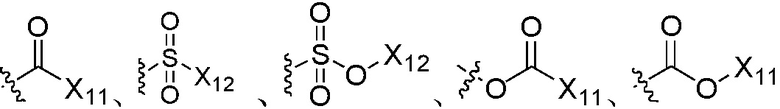 ,
,  или
или  ; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C3-C6 циклоалкила, три C1-C6 алкилсилила, C3-C6 циклоалкенила, гетероциклила, арила,
; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C3-C6 циклоалкила, три C1-C6 алкилсилила, C3-C6 циклоалкенила, гетероциклила, арила, 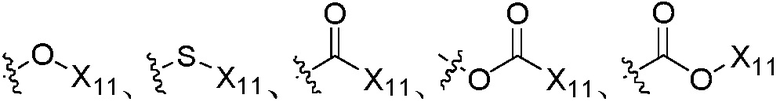 ,
,  ,
, 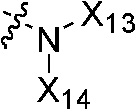 ,
,  или
или  ; группы «C3-C6 циклоалкил», «C3-C6 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
; группы «C3-C6 циклоалкил», «C3-C6 циклоалкенил», «гетероциклил» и «арил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
или N(W3)2 является 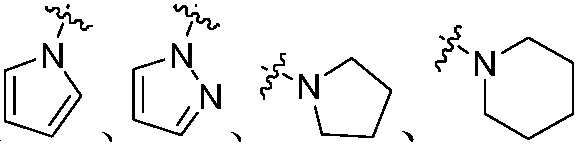 или
или  , который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
, который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
X11 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, гетероциклилом, гетероциклил C1-C3 алкилом, арилом или арил C1-C3 алкилом; где группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «гетероциклил», «гетероциклил C1-C3 алкил», «арил» и «арил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X12 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, гетероциклилом, гетероциклил C1-C3 алкилом, арилом или арил C1-C3 алкилом; где группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «гетероциклил», «гетероциклил C1-C3 алкил», «арил» и «арил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо;
X13, X14 каждый независимо является H, галогеном, циано, C1-C6 алкокси, C1-C6 алкокси C1-C3 алкилом, C1-C6 алкилкарбонилом, C1-C6 алкоксикарбонилом, C1-C6 алкилсульфонилом, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, арилом, арил C1-C3 алкилом, гетероциклилом или гетероциклил C1-C3 алкилом, или группа CX13X14, взятые вместе образуют 5~8-членный насыщенный карбоциклил,  или
или  , или группа NX13X14, взятые вместе образуют
, или группа NX13X14, взятые вместе образуют  или
или  ; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «арил», «арил C1-C3 алкил», «гетероциклил» и «гетероциклил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный насыщенный карбоциклил,
; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «C3-C6 циклоалкил», «C3-C6 циклоалкил C1-C3 алкил», «C3-C6 циклоалкенил», «C3-C6 циклоалкенил C1-C3 алкил», «арил», «арил C1-C3 алкил», «гетероциклил» и «гетероциклил C1-C3 алкил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из оксо, галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14, или два соседних атома углерода на кольце вместе с не замещенным или галоген-замещенным -OCH2CH2- или -OCH2O- образуют конденсированное кольцо; группы «5~8-членный насыщенный карбоциклил,  или
или  » не замещены или замещены 1, 2 или 3 группами, выбранными из C1-C6 алкил, C1-C6 алкоксикарбонил или бензил, или вместе с фенилом или тиенилом образуют конденсированное кольцо; группы «
» не замещены или замещены 1, 2 или 3 группами, выбранными из C1-C6 алкил, C1-C6 алкоксикарбонил или бензил, или вместе с фенилом или тиенилом образуют конденсированное кольцо; группы «  ,
,  или
или  » не замещены или замещены 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
» не замещены или замещены 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
R11 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом, C3-C6 циклоалкенил C1-C3 алкилом, фенилом, бензилом; где группы «C1-C6 алкил», «C2-C6 алкенил» и «C2-C6 алкинил» каждая независимо является незамещенной или замещена галогеном; группы «фенил» и «бензил» каждая независимо является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила, C1-C6 алкокси или гало C1-C6 алкокси;
R12 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C1-C6 алкокси, C1-C6 алкилсульфонилом, C3-C6 циклоалкилом, C3-C6 циклоалкил C1-C3 алкилом, C3-C6 циклоалкенилом или C3-C6 циклоалкенил C1-C3 алкилом, или группа N(R12)2 в -(CO)N(R12)2 или -(SO2)N(R12)2 независимо является  или
или  , который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
, который не замещен или замещен 1, 2 или 3 группами, выбранными из оксо, C1-C6 алкила или C1-C6 алкоксикарбонила;
R13 независимо является C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C3-C6 циклоалкилом, фенилом или фенилом, замещенным 1, 2 или 3 группами, выбранными из: галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкокси, гало C1-C6 алкокси, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила или фенокси, замещенного 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкокси или гало C1-C6 алкокси;
R14 независимо является H, C1-C6 алкилом, гало C1-C6 алкилом, фенилом или фенилом, замещенным 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, гало C1-C6 алкила, C1-C6 алкоксикарбонила, C1-C6 алкилтио, C1-C6 алкилсульфонила, C1-C6 алкокси или гало C1-C6 алкокси.
Более предпочтительно, Het является 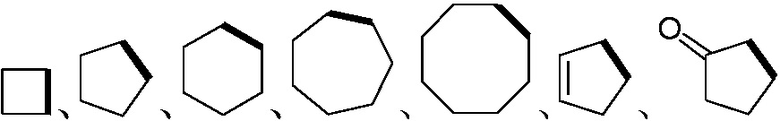 ,
,  ,
, 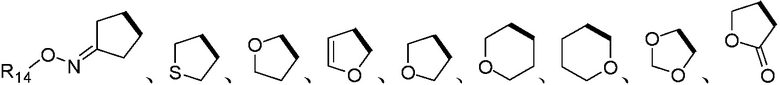 ,
, 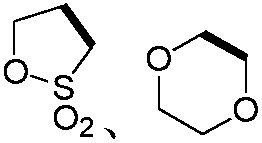 или
или 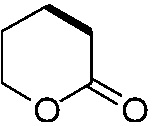 (где жирная химическая связь соответствует жирной химической связи в общей формуле, и атомы углерода на концах жирной химической связи соответственно соответствуют C4 и C5 в общей формуле без определенного порядка; например, когда Het является
(где жирная химическая связь соответствует жирной химической связи в общей формуле, и атомы углерода на концах жирной химической связи соответственно соответствуют C4 и C5 в общей формуле без определенного порядка; например, когда Het является 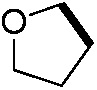 , общая формула является
, общая формула является 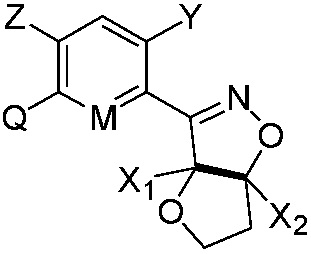 или
или  ); за исключением 4- и 5-положений, которые соответственно замещены X2 или X1 в общей формуле I, другие положения на Het каждое независимо не замещено или замещено 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -SOR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14.
); за исключением 4- и 5-положений, которые соответственно замещены X2 или X1 в общей формуле I, другие положения на Het каждое независимо не замещено или замещено 1, 2 или 3 группами, выбранными из галогена, циано, нитро, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, гало C1-C6 алкила, гало C2-C6 алкенила, гало C2-C6 алкинила, гало C3-C6 циклоалкила, C1-C6 алкил-замещенного C3-C6 циклоалкила, -OR14, -SR14, -SOR14, -(CO)OR14, -(SO2)R14, -N(R14)2 или -O-(C1-C3 алкил)-(CO)OR14.
Также предпочтительно, Q является
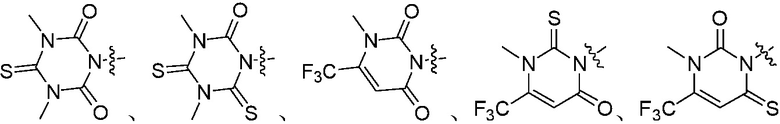 ,
,
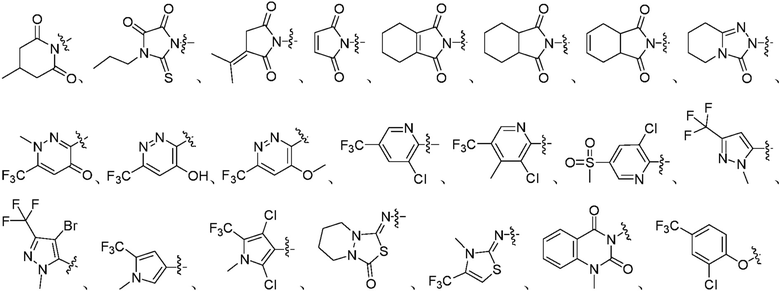 или
или 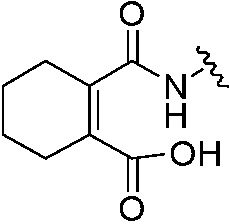 .
.
В определении соединения, представленного приведенной выше формулой и всеми нижеследующими структурными формулами, используемые технические термины, используемые отдельно или в составе слова, представляют следующие заместители: алкил, содержащий более двух атомов углерода, может быть линейным или разветвленным. Например, алкил в сложном слове «-алкил-(CO)OR11» может быть -CH2-, -CH2CH2-, -CH(CH3)-, -C(CH3)2- и т.п. Алкилом является, например, C1 алкил: метил; C2 алкил: этил; C3 алкил: пропил, такой как н-пропил или изопропил; C4 алкил: бутил, такой как н-бутил, изобутил, трет-бутил или 2-бутил; C5 алкил: пентил, такой как н-пентил; C6 алкил: гексил, такой как н-гексил, изогексил и 1,3-диметилбутил. Аналогично, алкенилом является, например, винил, аллил, 1-метилпроп-2-ен-1-ил, 2-метилпроп-2-ен-1-ил, бут-2-ен-1-ил, бутил-3-ен-1-ил, 1-метилбут-3-ен-1-ил и 1-метилбут-2-ен-1-ил. Алкинилом является, например, этинил, пропаргил, бут-2-ин-1-ил, бут-3-ин-1-ил, 1-метилбут-3-ин-1-ил. Множественная связь может быть размещена в любом положении каждой ненасыщенной группы. Циклоалкилом является карбоциклическая насыщенная кольцевая систему, содержащую, например, от трех до шести атомов углерода, такая как циклопропил, циклобутил, циклопентил или циклогексил. Подобным образом, циклоалкенилом является моноциклоалкенил, имеющий, например, от трех до шести углеродных членов в кольце, такой как циклопропенил, циклобутенил, циклопентенил и циклогексенил, где двойная связь может находиться в любом положении. Галогеном является фтор, хлор, бром или йод.
Если не указано иначе, «арил» в настоящем изобретении включает, но не ограничен ими, фенил, нафтил, 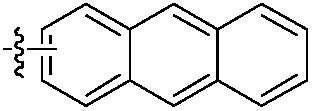 , или
, или 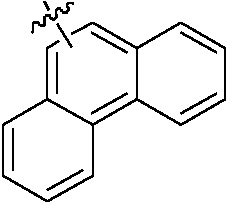 ; «гетероциклил» не только включает, но не ограничен ими, насыщенную или ненасыщенную не ароматическую циклическую группу
; «гетероциклил» не только включает, но не ограничен ими, насыщенную или ненасыщенную не ароматическую циклическую группу 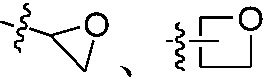 ,
,  ,
, 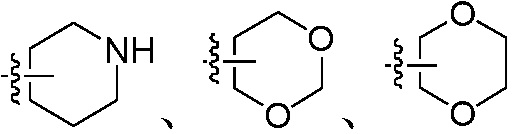 ,
, 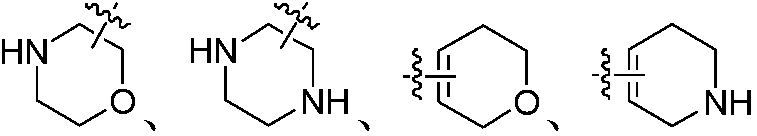 или
или 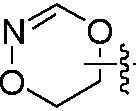 , и т.д., но также включает, но не ограничен ими, «гетероарил», который является ароматической циклической группой, имеющей, например, 3-6 атомов в кольце, и которая также может быть конденсирована с бензо кольцом, и 1-4 (например, 1, 2, 3 или 4) гетероатома кольца выбраны из группы, состоящей из кислорода, азота и серы. Например,
, и т.д., но также включает, но не ограничен ими, «гетероарил», который является ароматической циклической группой, имеющей, например, 3-6 атомов в кольце, и которая также может быть конденсирована с бензо кольцом, и 1-4 (например, 1, 2, 3 или 4) гетероатома кольца выбраны из группы, состоящей из кислорода, азота и серы. Например,
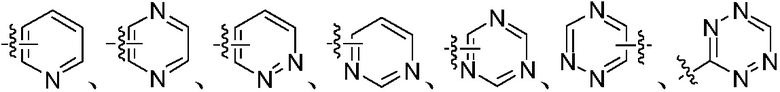 ,
,
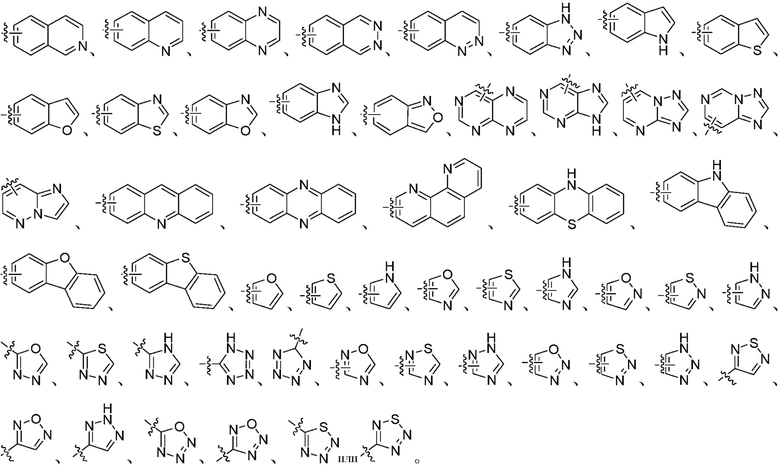
Если группа замещена группой, это следует понимать как означающее, что группа замещена одной или несколькими группами, которые являются одинаковыми или разными группами, выбранными из упомянутых групп. Кроме того, одинаковые или разные символы замещения, содержащиеся в одинаковых или разных заместителях, выбирают независимо и они могут быть одинаковыми или разными. Это также применимо к кольцевым системам, образованным различными атомами и единицами. Между тем, объем формулы изобретения исключает те соединения, которые химически нестабильны в стандартных условиях, известных специалистам в данной области техники.
Кроме того, если не указано иное, термин «замещенный, по меньшей мере, одной группой» в настоящем документе относится к замещению 1, 2, 3, 4 или 5 группами; группа (включая гетероциклил, арил и т. д.) без указания места связывания может быть присоединена в любом месте, включая место C или N; если он замещен, заместитель может быть замещен в любом месте, если он соответствует теории валентной связи. Например, если гетероарил 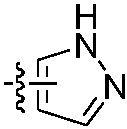 замещен одним метилом, он может быть
замещен одним метилом, он может быть 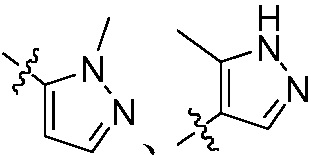 ,
, 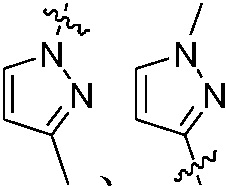 , и т.д.
, и т.д.
В зависимости от свойства заместителей и способа их связывания, соединение формулы I и его производные могут существовать в виде стереоизомера. Стереоизомер может быть получен из смесей, полученных при получении обычными способами разделения, например хроматографическим разделением. Стереоизомер также может быть получен селективно, с использованием стереоселективных реакций и с использованием оптически активных исходных материалов и/или вспомогательных веществ. Настоящее изобретение также относится ко всем стереоизомерам и их смесям, которые включены в общую формулу I, но конкретно не определены.
Соединение, представленное общей формулой I по настоящему изобретению, может быть получено стандартными способами органической химии, например, способом получения замещенного ароматического соединения с конденсированным кольцом, включающим стадию:
превращения соединения, представленного общей формулой II
converting a compound представленное общей формулой II 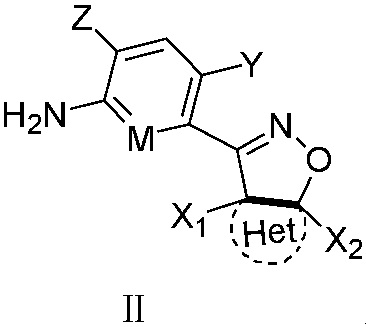 в соединение, представленное общей формулой I; способ зависит от природы группы Q. Эти способы конкретно описаны в патентах US5679791, WO2012/041789, WO2019/101551, WO00/50409, CN105753853A и подобных.
в соединение, представленное общей формулой I; способ зависит от природы группы Q. Эти способы конкретно описаны в патентах US5679791, WO2012/041789, WO2019/101551, WO00/50409, CN105753853A и подобных.
Альтернативно, соединение, представленное общей формулой I, может быть получено реакцией циклизации соединения, представленного общей формулой IV, и соединения, представленного общей формулой V. Предпочтительно, реакцию проводят в присутствии растворителя и основания. Способ, в котором применяют соединение, представленное общей формулой IV, конкретно описан в патенте WO1999/055693 и подобных.
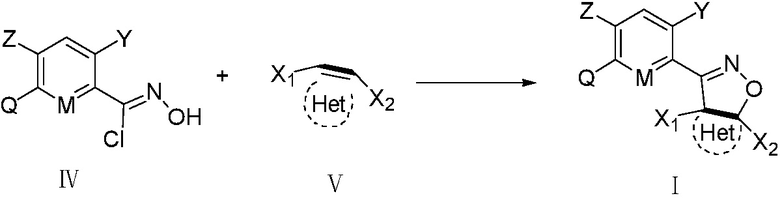
Например, если Q является 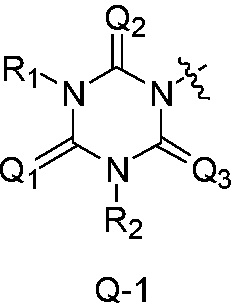 , (1) взаимодействие соединения, представленного общей формулой II, с
, (1) взаимодействие соединения, представленного общей формулой II, с 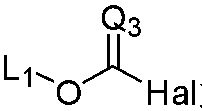 , с получением соединения, представленного общей формулой II-1, и затем циклизация с соединением, представленным общей формулой III-1, с получением соединения, представленного общей формулой I-1, где уравнение химической реакции показано следующим образом:
, с получением соединения, представленного общей формулой II-1, и затем циклизация с соединением, представленным общей формулой III-1, с получением соединения, представленного общей формулой I-1, где уравнение химической реакции показано следующим образом:
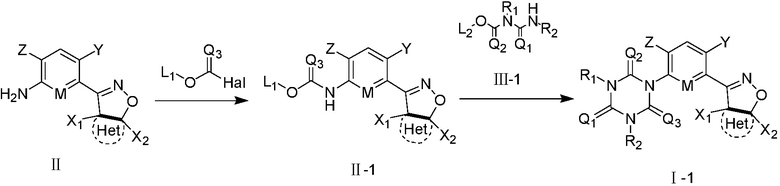
(2) взаимодействие соединения, представленного общей формулой II, с 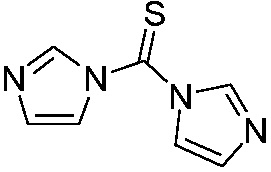 , с получением соединения, представленного общей формулой II-2, и затем взаимодействие с соединением, представленным общей формулой III-1, с получением соединения, представленного общей формулой I-2; где уравнение химической реакции показано следующим образом:
, с получением соединения, представленного общей формулой II-2, и затем взаимодействие с соединением, представленным общей формулой III-1, с получением соединения, представленного общей формулой I-2; где уравнение химической реакции показано следующим образом:
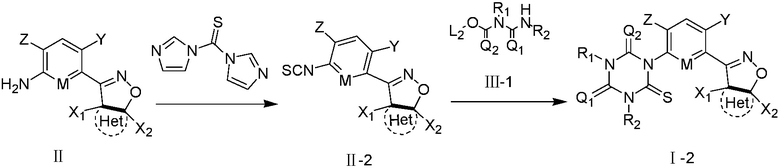
если Q является 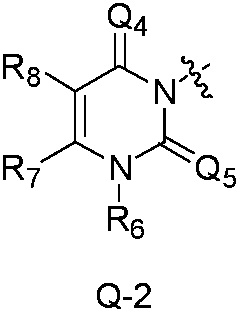 , (3) взаимодействие соединения, представленного общей формулой II, с соединением, представленным общей формулой III-2, с получением соединения, представленного общей формулой I-3; где уравнение химической реакции показано следующим образом:
, (3) взаимодействие соединения, представленного общей формулой II, с соединением, представленным общей формулой III-2, с получением соединения, представленного общей формулой I-3; где уравнение химической реакции показано следующим образом:
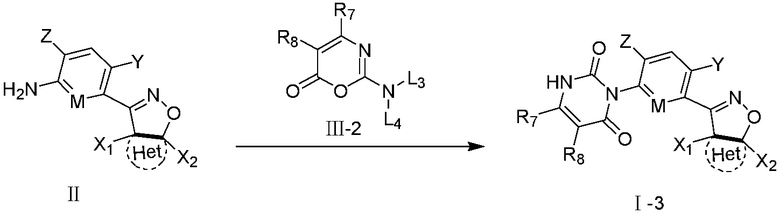
(4) взаимодействие соединения, представленного общей формулой II, с 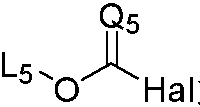 , с получением соединения, представленного общей формулой II-3, и затем циклизация с соединением, представленным общей формулой III-3, с получением соединения, представленного общей формулой I-4, где уравнение химической реакции показано следующим образом:
, с получением соединения, представленного общей формулой II-3, и затем циклизация с соединением, представленным общей формулой III-3, с получением соединения, представленного общей формулой I-4, где уравнение химической реакции показано следующим образом:
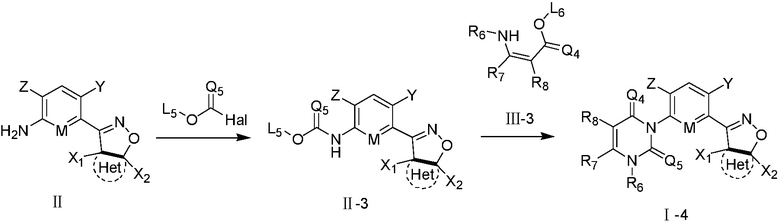
(5) взаимодействие соединения, представленного общей формулой II, с 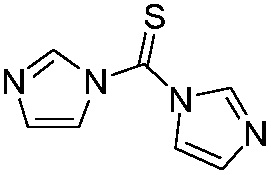 , с получением соединения, представленного общей формулой II-2, и затем взаимодействие с соединением, представленным общей формулой III-4, с получением соединения, представленного общей формулой I-5; где уравнение химической реакции показано следующим образом:
, с получением соединения, представленного общей формулой II-2, и затем взаимодействие с соединением, представленным общей формулой III-4, с получением соединения, представленного общей формулой I-5; где уравнение химической реакции показано следующим образом:
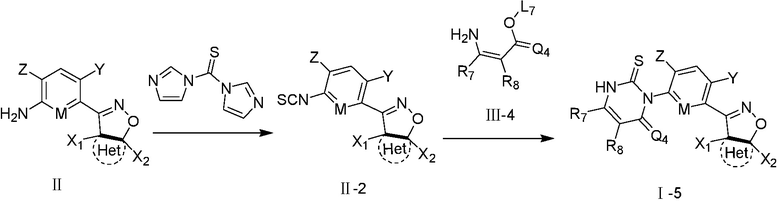
Альтернативно, (6) соединение, представленное общей формулой I-6, подвергают реакции замещения с R6’-Hal с получением соединения, представленного общей формулой I-7; где уравнение химической реакции показано следующим образом:
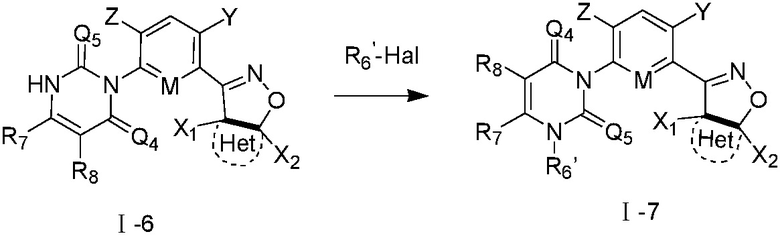
где L1, L2, L3, L4, L5, L6 и L7 каждый независимо является C1-C6 алкилом или арилом, предпочтительно, метилом, этилом или фенилом; Hal независимо является галогеном, предпочтительно, хлором, йодом; R6’ является группой, за исключением H, представленной R6; другие заместители R1, R2, R6, R7, R8, 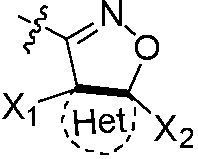 , Q1, Q2, Q3, Q4, Q5, Y, Z и M такие, как определены выше.
, Q1, Q2, Q3, Q4, Q5, Y, Z и M такие, как определены выше.
Предпочтительно, первую стадию на стадии (1) и первую стадию на стадии (4) обе проводят в присутствии растворителя
Предпочтительно, вторую стадию на стадии (1), вторую стадию на стадиях (2) и (4) и стадиях (5) и (6) проводят в присутствии основания и растворителя.
Предпочтительно, стадию (3) проводят в присутствии кислоты.
Основанием является, по меньшей мере, одно, выбранное из неорганических оснований (таких как K2CO3, Na2CO3, Cs2CO3, NaHCO3, KF, CsF, KOAc, AcONa, K3PO4, t-BuONa, EtONa, NaOH, KOH, NaOMe и подобные) или органических оснований (таких как пиразол, триэтиламин, ДИЭА и подобные).
Растворителем является, по меньшей мере, один, выбранный из ДМФ, ДМА, метанола, этанола, ацетонитрила, дихлорэтана, ДМСО, диоксана, дихлорметана, толуола или этилацетата.
Кислоту выбирают из уксусной кислоты, хлористоводородной кислоты или серной кислоты.
Кроме того, если, по меньшей мере, один из заместителей Q1, Q2, Q3 в Q ( 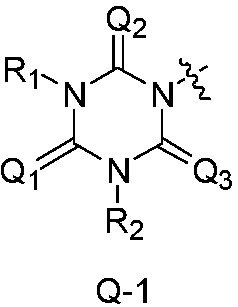 или
или 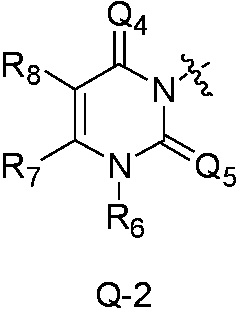 ) является S, или когда, по меньшей мере, один из Q4 и Q5 является S, он также может быть получен с применением соответствующего соединения, где Q является
) является S, или когда, по меньшей мере, один из Q4 и Q5 является S, он также может быть получен с применением соответствующего соединения, где Q является 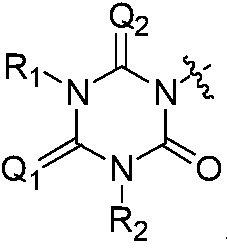 или
или 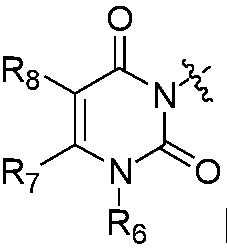 , в качестве исходного соединения, через обычную реакцию серного замещения в присутствии реагента Ловессона (
, в качестве исходного соединения, через обычную реакцию серного замещения в присутствии реагента Ловессона ( 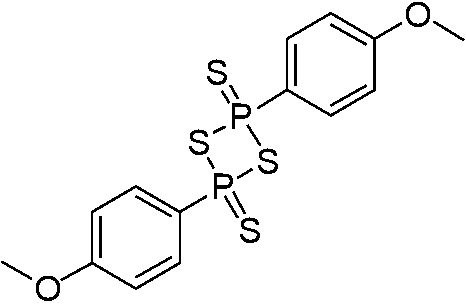 ) или пентасульфида фосфона.
) или пентасульфида фосфона.
Гербицидная композиция, содержащая гербицидно эффективную дозу, по меньшей мере, одного из замещенного ароматического соединения с конденсированным кольцом; предпочтительно, гербицидная композиция также содержит вспомогательное средство для препарата.
Способ борьбы с сорняками, который включает нанесение гербицидно эффективной дозы, по меньшей мере, одного из замещенного ароматического соединения с конденсированным кольцом или гербицидной композиции на растение или на участок с сорняком.
Использование, по меньшей мере, одного из замещенного ароматического соединения с конденсированным кольцом или гербицидной композиции, как описано выше, для борьбы с сорняками, предпочтительно, где замещенное ароматическое соединение с конденсированным кольцом, используют для профилактики и/или борьбы с сорняками в полезной культуре, где полезной культурой является трансгенная культура или культура, обработанная методом редактирования генов.
Соединения формулы I по изобретению обладают выдающейся гербицидной активностью против широкого спектра экономически важных однодольных и двудольных вредных растений. Активные соединения также эффективно действуют на многолетние сорняки, которые дают побеги из корневищ, корневых побегов или других органов многолетников, и с которыми трудно бороться. В этом контексте, как правило, не имеет значения, применяются ли вещества до посева, до появления всходов или после появления всходов. В частности, можно упомянуть примеры некоторых представителей однодольных и двудольных сорняков, с которыми можно бороться с помощью соединений по изобретению, без ограничения определенными видами. Примерами сорняков, на которые эффективно действуют активные соединения, являются, среди прочих, однодольные, Avena, Lolium, Alopecurus, Phalaris, Echinochloa, Digitaria, Setaria, а также виды Cyperus из однолетнего сектора и из числа многолетних видов Agropyron, Cynodon, Imperata и Sorghum, а также многолетние виды Cyperus.
В случае двудольных сорняков, спектр действия распространяется на такие виды, как, например, Galium, Viola, Veronica, Lamium, Stellaria, Amaranthus, Sinapis, Ipomoea, Sida, Matricaria и Abutilon из однолетних растений, и Convolvulus, Cirsium, Rumex и Artemisia в случае многолетних сорняков. Активные соединения по изобретению также обеспечивают превосходный контроль над вредными растениями, которые встречаются в определенных условиях выращивания риса, такими как, например, Echinochloa, Sagittaria, Alisma, Eleocharis, Scirpus и Cyperus. Если соединения по изобретению наносят на поверхность почвы до прорастания, то прорастание сорняков либо полностью предотвращается, либо сорняки растут до тех пор, пока не достигнут стадии семядолей, но затем их рост прекращается, и, в конечном итоге, по прошествии трех-четырех недель они полностью умирают. В частности, соединения по изобретению проявляют превосходную активность против Apera spica venti, Chenopodium album, Lamium purpureum, Polygonum convulvulus, Stellaria media, Veronica hederifolia, Veronica persica, Viola tricolor и против видов Amaranthus, Galium и Kochia.
Хотя соединения по изобретению обладают превосходной гербицидной активностью против однодольных и двудольных сорняков, культурные растения экономически важных культур, таких как, например, пшеница, ячмень, рожь, рис, кукуруза, сахарная свекла, хлопок и соя, совсем не повреждаются, или только в незначительной степени. В частности, они обладают отличной совместимостью с зерновыми культурами, такими как пшеница, ячмень и кукуруза, в частности, пшеница. По этим причинам, настоящие соединения очень подходят для селективного контроля нежелательного роста растений в насаждениях для использования в сельском хозяйстве или в посадках декоративных растений.
Благодаря своим гербицидным свойствам, эти активные соединения также могут применяться для борьбы с вредными растениями в культурах известных или все еще разрабатываемых с помощью генной инженерии растений. Трансгенные растения обычно имеют особенно полезные свойства, например устойчивость к определенным пестицидам, в частности определенным гербицидам, устойчивость к болезням растений или организмам, вызывающим заболевания растений, таким как определенные насекомые или микроорганизмы, такие как грибы, бактерии или вирусы. Другие особые свойства относятся, например, к количеству, качеству, стабильности при хранении, составу и конкретным ингредиентам собранного продукта. Таким образом, известны трансгенные растения, имеющие повышенное содержание крахмала или измененное качество крахмала, или растения, имеющие другой состав жирных кислот в собранном продукте.
Применение соединений формулы I по изобретению или их солей в экономически важных трансгенных культурах полезных и декоративных растений, например зерновых, таких как пшеница, ячмень, рожь, овес, просо, рис, маниока и кукуруза, или также в посевах сахарной свеклы, хлопка, сои, рапса, картофеля, томатов, гороха и других видов овощей, является предпочтительным. Соединения формулы I предпочтительно могут применяться в качестве гербицидов в культурах полезных растений, которые устойчивы или которые были сделаны устойчивыми с помощью генной инженерии, к фитотоксическим эффектам гербицидов.
Обычные способы получения новых растений, которые имеют модифицированные свойства по сравнению с известными растениями, включают, например, традиционные способы селекции и создание мутантов. Альтернативно, новые растения с модифицированными свойствами могут быть созданы с помощью способов генной инженерии (см., например, EP-A 0 221 044, EP-A 0 131 624). Например, было описано несколько случаев:
- генно-инженерные изменения сельскохозяйственных культур с целью модификации крахмала, синтезированного в растениях (например, WO 92/11376, WO 92/14827, WO 91/19806),
- трансгенные культурные растения, устойчивые к определенным гербицидам глуфосинатного (см., например, EP-A 0 242 236, EP-A 0 242 246) или глифосатного типа (WO 92/00377), или сульфонилмочевинного типа (EP-A 0 257 993, патент США № 5013659A),
- трансгенные культурные растения, например хлопок, обладающие способностью продуцировать токсины Bacillus thuringiensis (токсины Bt), которые придают растениям устойчивость к определенным вредителям (EP-A 0 142 924, EP-A 0 193 259),
- трансгенные культурные растения с модифицированным составом жирных кислот (WO 91/13972).
В принципе известны многочисленные методы молекулярной биологии, позволяющие получать новые трансгенные растения с модифицированными свойствами; см., например, Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.; или Winnacker "Gene und Klone" [Genes and Clones], VCH Weinheim, 2nd edition 1996, или Christou, "Trends in Plant Science" 1 (1996) 423-431). Для осуществления таких манипуляций генной инженерии можно ввести молекулы нуклеиновой кислоты в плазмиды, которые позволяют мутагенез или изменение последовательности через рекомбинацию последовательностей ДНК. Используя вышеупомянутые стандартные процессы, можно, например, обменивать основания, удалять частичные последовательности или добавлять природные или синтетические последовательности. Чтобы связать фрагменты ДНК друг с другом, к фрагментам можно присоединить адаптеры или линкеры.
Клетки растений, обладающие пониженной активностью генного продукта, могут быть получены, например, экспрессией, по меньшей мере, одной подходящей антисмысловой РНК, смысловой РНК для достижения эффекта косупрессии, или экспрессии, по меньшей мере, одного соответствующим образом сконструированного рибозима, который специфически расщепляет транскрипты вышеупомянутого генного продукта.
С этой целью можно использовать обе молекулы ДНК, которые содержат всю кодирующую последовательность генного продукта, включая любые фланкирующие последовательности, которые могут присутствовать, и молекулы ДНК, которые включают только части кодирующей последовательности, при этом необходимо, чтобы эти части были достаточно длинными, чтобы вызвать антисмысловой эффект в клетках. Также возможно использовать последовательности ДНК, которые имеют высокую степень гомологии с кодирующими последовательностями генного продукта, но которые не полностью идентичны.
При экспрессии молекул нуклеиновой кислоты в растениях, синтезированный белок может быть локализован в любом желаемом компартменте клеток растения. Однако для достижения локализации в определенном компартменте, например, возможно связать кодирующую область с последовательностями ДНК, которые обеспечивают локализацию в определенном компартменте. Такие последовательности известны специалисту в данной области техники (см., например, Braun et al., EMBO J. 11 (1992), 3219-3227; Wolter et al., Proc. Natl. Acad. Sci. USA 85 (1988), 846-850; Sonnewald et al., Plant J. 1 (1991), 95-106).
Трансгенные клетки растений могут быть регенерированы до целых растений с использованием известных методик. Трансгенные растения в принципе могут быть растениями любых желаемых видов растений, т.е. как однодольных, так и двудольных растений. Таким способом возможно получение трансгенных растений, которые имеют модифицированные свойства, сверхэкспрессией, подавлением или ингибированием гомологичных (=природных) генов или последовательностей генов, или экспрессией гетерологичных (=чужеродных) генов или последовательностей генов.
При использовании активных соединений по изобретению в трансгенных культурах, помимо действия против вредных растений, которое можно наблюдать у других культур, часто возникают эффекты, специфичные для применения в соответствующей трансгенной культуре, например, модифицированный или специфически расширенный спектр сорняков, с которыми можно бороться, измененные нормы расхода, которые могут применяться для нанесения, предпочтительно, хорошая сочетаемость с гербицидами, к которым устойчивы трансгенные культуры, и влияние на рост и урожай трансгенных сельскохозяйственных культур. Таким образом, изобретение также представляет использование соединений по изобретению в качестве гербицидов для борьбы с вредными растениями в трансгенных сельскохозяйственных культурах.
Кроме того, вещества согласно изобретению обладают выдающимися свойствами регулирования роста сельскохозяйственных культур. Они участвуют в метаболизме растений регулирующим образом, и поэтому могут применяться для таргетного контроля компонентов растений и для облегчения сбора урожая, например, провоцируя высыхание и задержку роста. Кроме того, они также подходят для общего регулирования и ингибирования нежелательного вегетативного роста, не уничтожая при этом растения. Подавление вегетативного роста играет важную роль во многих однодольных и двудольных культурах, поскольку таким образом можно уменьшить или полностью предотвратить полегание.
Соединения по изобретению могут применяться в обычных составах в форме смачиваемых порошков, эмульгируемых концентратов, распыляемых растворов, дустов или гранул. Таким образом, изобретение также представляет гербицидные композиции, содержащие соединения формулы I. Соединения формулы I могут быть составлены различными способами в зависимости от преобладающих биологических и/или химико-физических параметров. Примеры подходящих вариантов составов включают: смачиваемые порошки (WP), водорастворимые порошки (SP), водорастворимые концентраты, эмульгируемые концентраты (EC), эмульсии (EW), такие как масло в воде и вода в масле. эмульсии, распыляемые растворы, концентраты суспензий (SC), масляные дисперсии (OD), дисперсии на масляной или водной основе, маслосмешиваемые растворы, дусты (DP), капсульные суспензии (CS), протравливающие композиции, гранулы для рассыпания и внесения в почву, гранулы (GR) в виде микрогранул, гранулы для распыления, гранулы для покрытия и адсорбционные гранулы, вододиспергируемые гранулы (WG), водорастворимые гранулы (SG), составы ULV, микрокапсулы и воски. Эти индивидуальные типы составов в принципе известны и описаны, например, в Winnacker-Küchler, "Chemische Technologie" [Chemical Technology], Volume 7, C. Hauser Verlag Munich, 4th. Edition 1986; Wade van Valkenburg, "Pesticide Formulations", Marcel Dekker, N.Y., 1973; K. Martens, "Spray Drying" Handbook, 3rd Ed. 1979, G. Goodwin Ltd. London.
Необходимые вспомогательные вещества для составов, такие как инертные материалы, поверхностно-активные вещества, растворители и другие добавки, также известны и описаны, например, в Watkins, "Handbook of Insecticide Dust Diluents and Carriers", 2nd Ed., Darland Books, Caldwell N.J., H. v. Olphen, "Introduction to Clay Colloid Chemistry"; 2nd Ed., J. Wiley & Sons, N.Y.; C. Marsden, "Solvents Guide"; 2nd Ed., Interscience, N.Y. 1963; McCutcheon's "Detergents and Emulsifiers Annual", MC Publ. Corp., Ridgewood N.J.; Sisley and Wood, "Encyclopedia of Surface Active Agents", Chem. Publ. Co. Inc., N.Y. 1964; Schönfeldt, "Grenzflüchenaktive Äthylenoxidaddkte" [Surface-active ethylene oxide adducts], Wiss. Verlagagesell. Stuttgart 1976; Winnacker-Küchler, "Chemische Technologie" [Chemical Technology], Volume 7, C. Hauser Verlag Munich, 4th Edition 1986.
Смачиваемые порошки представляют собой препараты, которые равномерно диспергируются в воде и которые содержат, помимо активного соединения, а также разбавителя или инертного вещества, поверхностно-активные вещества ионного и/или не ионного типа (смачивающие агенты, диспергаторы), например, полиэтоксилированные алкилфенолы, полиэтоксилированные жирные спирты, полиэтоксилированные жирные амины, сульфаты полигликолевых эфиров жирных спиртов, алкансульфонаты, алкилбензолсульфонаты, лигнинсульфонат натрия, 2,2'-динафтилметан-6,6'-дисульфонат натрия, дибутиинафталинсульфонат натрия или олеоилметилтауринат натрия. Для приготовления смачиваемых порошков гербицидно активные соединения тонко измельчают, например, в обычном оборудовании, таком как молотковые мельницы, веерные мельницы и воздушно-струйные мельницы, и смешивают одновременно или последовательно со вспомогательными веществами состава.
Эмульгируемые концентраты получают растворением активного соединения в органическом растворителе, например бутаноле, циклогексаноне, диметилформамиде, ксилоле или других относительно высококипящих ароматических соединениях или углеводородах или смесях растворителей, с добавлением одного или нескольких поверхностно-активных веществ ионного и/или неионного типа (эмульгаторов). Примерами эмульгаторов, которые могут быть использованы, являются алкиларилсульфонаты кальция, такие как додецилбензолсульфонат Са, или неионные эмульгаторы, такие как полигликолевые эфиры жирной кислоты, простые алкиларилполигликолевые эфиры, простые полигликолевые эфиры жирных спиртов, продукты конденсации пропиленоксида-этиленоксида, сложные эфиры сорбитана, например, сложные эфиры сорбитана и жирной кислоты или сложные эфиры полиоксиэтиленсорбитана, например, сложные эфиры полиоксиэтиленсорбитана и жирной кислоты.
Дуст получают измельчением активного соединения с мелкодисперсными твердыми веществами, например тальком, природными глинами, такими как каолин, бентонит и пирофиллит, или диатомовой землей. Концентраты суспензий могут быть на водной или масляной основе. Их можно приготовить, например, путем мокрого измельчения с использованием обычных коммерческих бисерных мельниц с или без добавления поверхностно-активных веществ, как уже упоминалось выше, например, в случае других типов составов.
Эмульсии, например эмульсии масло-в-воде (EW), могут быть приготовлены, например, с помощью мешалок, коллоидных мельниц и/или статических смесителей с использованием водных органических растворителей и, при желании, поверхностно-активных веществ, как уже упоминалось выше, например, в случае других типов составов.
Гранулы могут быть получены либо распылением активного соединения на адсорбционный гранулированный инертный материал, либо нанесением концентратов активного соединения на поверхность носителей, таких как песок, каолиниты или гранулированный инертный материал, с помощью адгезионных связующих агентов, например поливинилового спирта, полиакрилата натрия или других минеральных масел. Подходящие активные соединения можно также гранулировать обычным для получения гранул удобрений способом, если желательно, в виде смеси с удобрениями. Диспергируемые в воде гранулы обычно получают обычными способами, такими как сушка распылением, гранулирование в псевдоожиженном слое, гранулирование на дисках, смешивание с использованием высокоскоростных смесителей и экструзия без твердого инертного материала.
Способы получения гранул на диске, в псевдоожиженном слое, экструдере и распылением см., например, в "Spray-Drying Handbook" 3rd ed. 1979, G. Goodwin Ltd., London; J. E. Browning, "Agglomeration", Chemical and Engineering 1967, страницы 147 и далее; "Perry's Chemical Engineer's Handbook", 5th Ed., McGraw-Hill, New York 1973, pp. 8-57. Для получения дополнительной информации о составлении средств защиты растений см., например, G. C. Klingman, "Weed Control as a Science", John Wiley and Sons Inc., New York, 1961, страницы 81-96 и J. D. Freyer, S. A. Evans, "Weed Control Handbook", 5th Ed., Blackwell Scientific Publications, Oxford, 1968, страницы 101-103.
Агрохимические составы обычно содержат от 0,1 до 99% массовых, в частности от 0,1 до 95% массовых, активного соединения формулы I. В смачиваемых порошках концентрация активного соединения составляет, например, от примерно 10 до 99% массовых, остаток до 100% массовых состоит из обычных компонентов состава. В эмульгируемых концентратах, концентрация активного соединения может составлять от примерно 1 до 90%, предпочтительно от 5 до 80% массовых. Составы в виде дустов содержат от 1 до 30% массовых активного соединения, чаще всего от 5 до 20% массовых активного соединения, в то время как распыляемые растворы содержат примерно от 0,05 до 80%, предпочтительно от 2 до 50% массовых активного соединения. В случае вододиспергируемых гранул, содержание активного соединения частично зависит от того, находится ли активное соединение в жидкой или твердой форме, и от используемых вспомогательных веществ для гранулирования, наполнителей и т.д. В вододиспергируемых гранулах содержание активного соединения, например, составляет от 1 до 95% массовых, предпочтительно от 10 до 80% массовых.
Кроме того, составы активного соединения могут включать вещества, повышающие клейкость, смачивающие агенты, диспергаторы, эмульгаторы, пенетранты, консерванты, антифризы, растворители, наполнители, носители, красители, пеногасители, ингибиторы испарения и регуляторы pH и вязкости, которые являются обычными в каждом случае.
На основе этих составов также можно получать комбинации с другими пестицидно активными веществами, например, инсектицидами, акарицидами, гербицидами и фунгицидами, а также с антидотами, удобрениями и/или регуляторами роста, например, в виде готовой смеси или баковой смеси.
Подходящие активные соединения, которые можно комбинировать с активными соединениями по изобретению в смешанных составах или в баковой смеси, включают, например, известные активные соединения, как описано в World Herbicide New Product Technology Handbook, China Agricultural Science and Farming Techniques Press, 2010.9 и в цитируемой там литературе. Например, следующие активные соединения могут быть упомянуты в качестве гербицидов, которые можно комбинировать с соединениями формулы I (примечание: соединения имеют либо «общее название» в соответствии с International Organization for Standardization (ISO), либо химические названия, если необходимо, вместе с обычным кодовым номером): ацетохлор, бутахлор, алахлор, пропизохлор, метолахлор, s-метолахлор, претилахлор, пропахлор, этахлор, напропамид, R-левовращающийся напропамид, пропанил, мефенацет, дифенамид, дифлуфеникан, этапрохлор, бефлубутамид, бромбутид, диметенамид, диметенамид-P, этобензанид, флуфенацет, тенилхлор, метазахлор, изоксабен, флампроп-M-метил, флампроп-M-пропил, аллидохлор, петоксамид, хлоранокрил, ципразин, мефлуидид, моналид, делахлор, принахлор, тербухлор, ксилахлор, диметахлор, цисанилид, тримексахлор, кломепроп, пропизамид, пентанохлор, карбетамид, бензоилпроп-этил, ципразол, бутенахлор, тебутам, бензипрам, могртон, дихлофлуанид, напроанилид, диэтатил-этил, напталам, флуфенацет, EL-177, бензадокс, хлортиамид, хлорофталимид, изокарбамид, пиколинафен, атразин, симазин, прометрин, цианатрин, симетрин, аметрин, пропазин, дипропетрин, dipropetryn, SSH-108, тербутрин, тербутилазин, триазифлам, ципразин, проглиназин, триэтазин, прометон, симетон, азипротрин, десметрин, диметаметрин, проциазин, мезопразин, себутилазин, секбуметон, тербуметон, метопротрин, цианатрин, ипазин, хлоразин, атратон, пендиметалин, эглиназин, циануровую кислоту, индазифлам, хлорсульфурон, метсульфурон-метил, бенсульфурон метил, хлоримурон-этил, трибенурон-метил, тифенсульфурон-метил, пиразосульфурон-этил, мезосульфурон, йодосульфурон-метил натрия, форамсульфурон, циносульфурон, триасульфурон, сульфометурон метил, никосульфурон, этаметсульфурон-метил, амидосульфурон, этоксисульфурон, циклосульфамурон, римсульфурон, азимсульфурон, флазасульфурон, моносульфурон, моносульфурон-сложный эфир, флукарбазон-натрий, флупирсульфурон-метил, галосульфурон-метил, оксасульфурон, имазосульфурон, примисульфурон, пропоксикарбазон, просульфурон, сульфосульфурон, трифлоксисульфурон, трифлусульфурон-метил, тритосульфурон, метсульфуронметил натрия, флуцетосульфурон, HNPC-C, ортосульфамурон, пропирисульфурон, метазосульфурон, ацифлуорфен, фомесафен, лактофен, флуорогликофен, оксифлуорфен, хлорнитрофен, аклонифен, этоксифен-этил, бифенокс, нитрофлуорфен, хлометоксифен, флуородифен, флуоронитрофен, фурилоксифен, нитрофен, TOPE, DMNP, PPG1013, AKH-7088, галозафен, хлортолурон, изопротурон, линурон, диурон, флуометурон, бензтиазурон, метабензтиазурон, кумилурон, этидимурон, изоурон, тебутиурон, бутурон, хлорбромурон, метилдимрон, фенобензурон, SK-85, метобромурон, метоксурон, афезин, монурон, сидурон, фенурон, флуотиурон, небурон, хлороксурон, норурон, изонорурон, 3-циклооктил-1, триазфлурон, тебутиурон, дифеноксурон, парафлурон, метиламин трибунил, карбутилат, триметурон, димефурон, монисурон, анисурон, метиурон, хлоретурон, тетрафлурон, фенмедифам, фенмедифам-этил, десмедифам, асулам, тербукарб, барбан, профам, хлорпрофам, роумат, свеп, хлорбуфам, карбоксазол, хлорпрокарб, фенасулам, BCPC, CPPC, карбасулам, бутилат, бентиокарб, вернолат, молинат, триаллат, димепиперат, эспрокарб, пирибутикарб, циклоат, авадекс, EPTC, этиолат, орбенкарб, пебулат, просульфокарб, тиокарбазил, CDEC, димексано, изополинат, метобенкарб, 2,4-D бутиловый эфир, MCPA-Na, 2,4-D изооктиловый эфир, MCPA изооктиловый эфир, 2,4-D натриевая соль, 2,4-D диметиламиновая соль, MCPA-тиоэтил, MCPA, 2,4-D пропионовая кислота, соль 2,4-D пропионовой кислоты с высоким содержанием, 2,4-D масляная кислота, MCPA пропионовая кислота, MCPA соль пропионовой кислоты, MCPA масляная кислота, 2,4,5-D, 2,4,5-D пропионовая кислота, 2,4,5-D масляная кислота, MCPA аминовая соль, дикамба, эрбон, хлорфенак, саисон, TBA, хлорамбен, метокси-TBA, диклофоп-метил, флуазифоп-бутил, флуазифоп-п-бутил, галоксифоп-метил, галоксифоп-P, хизалофоп-этил, хизалофоп-п-этил, феноксапроп-этил, феноксапроп-п-этил, пропаквизафоп, цигалофоп-бутил, метамифоп, клодинафоп-пропаргил, фентиапроп-этил, хлороазифоп-пропинил, поппенат-метил, трифопсим, изоксапирифоп, паракват, дикват, оризалин, эталфлуралин, изопропалин, нитралин, профлуралин, продинамин, бенфлуралин, флухлоралин, динитамина, дипропалин, хлорнидин, металпропалин, динопроп, глифосат, анилофос, глуфосинат аммония, амипрофос-метил, сульфосат, пиперофос, биалафос-натрий, бенсулид, бутамифос, фокарб, 2,4-DEP, H-9201, зитрон, имазапир, имазетапир, имазаквин, имазамокс, аммониевая соль имазамокса, имазапик, имазаметабенз-метил, флуроксипир, изооктиловый эфир флуроксипира, клопиралид, пиклорам, трихлопир, дитиопир, галооксидин, 3,5,6-трихлор-2-пиридинол, тиазопир, флуридон, аминопиралид, дифлуфензопир, триклопир-бутотил, клиодинат, сетоксидим, клетодим, циклоксидим, аллоксидим, клефоксидим, бутроксидим, тралкоксидим, тепралоксидим, бутидазол, метрибузин, гексазинон, метамитрон, этиозин, аметридион, амибузин, бромоксинил, бромоксинила октаноат, иоксинила октаноат, иоксинил, дихлобенил, дифенатрил, пираклонил, хлороксинил, йодобонил, флуметсулам, флорасулам, пеноксулам, метосулам, клорансулам-метил, диклосулам, пироксулам, бензофуресат, биспирибак-натрий, пирибензоксим, пирифталид, пириминобак-метил, пиритиобак-натрий, бензобицилон, мезотрион, сулкотрион, темботрион, тефурилтрион, бициклопирон, кетодпирадокс, изоксафлутол, кломазон, феноксасульфон, метиозолин, флуазолат, пирафлуфен-этил, пиразолинат, дифензокват, пиразоксифен, бензофенап, нипираклофен, пирасульфотол, топрамезон, пироксасульфон, кафенстрол, флупоксам, аминотриазол, аминокарбазон, азафенидин, карфентразон-этил, сульфентразон, бенкарбазон, бензфендизон, бутафенацил, бромацил, изоцил, ленацил, тербацил, флупропацил, цинидон-этил, флумиклорак-пентил, флумиоксазин, пропизамид, MK-129, флумезин, пентахлорфенол, диносеб, динотерб, динотерба ацетат, диносам, DNOC, хлорнитрофен, медиотерба ацетат, динофенат, оксадиаргил, оксадиазон, пентоксазон, флуфенацет, флутиацет-метил, фентразамид, флуфенпир-этил, пиразон, бромпиразон, метфлуразон, кусакира, димидазон, оксапиразон, норфлуразон, пиридафол, хинклорак, хинмерак, бентазон, пиридат, оксазикломефон, беназолин, кломазон, цинметилин, ZJ0702, пирибпмбенз-пропил, инданофан, хлорат натрия, далапон, трихлоруксусная кислота, монохлоруксусная кислота, гексахлорацетон, флупропанат, циперкват, бромфеноксим, эпроназ, метазол, флуртамон, бенфуресат, этофумесат, тиохлорим, хлортал, флуорохлоридон, таврон, акролеин, бентранил, сафлуфенацил, клацифос, хлоропон, алорак, диэтамкват, этнипромид, ипримидам, ипфенкарбазон, тиенкарбазон-метил, пиримисульфан, хлорфлуразол, трипропиндан, сульгликапин, просульфалин, камбендихлор, аминоциклопирахлор, родетанил, беноксакор, фенклорим, флуразол, фенхлоразол-этил, клоквинтоцет-мексил, оксабетринил, MG/91, циометринил, DKA-24, мефенпир-диэтил, фурилазол, флуксофеним, изоксадифен-этил, дихлормид, галауксифен-метил, DOW флорпирауксифен, UBH-509, D489, LS 82-556, KPP-300, NC-324, NC-330, KH-218, DPX-N8189, SC-0744, DOWCO535, DK-8910, V-53482, PP-600, MBH-001, KIH-9201, ET-751, KIH-6127 и KIH-2023.
Для использования составы, которые присутствуют в коммерчески доступной форме, при необходимости разбавляют обычным способом, например, используя воду в случае смачиваемых порошков, эмульгируемых концентратов, дисперсий и диспергируемых в воде гранул. Продукты в форме дустов, гранул для обработки почвы или разбрызгивания и распыляемые растворы обычно не разбавляют другими инертными веществами перед использованием. Требуемая норма расхода соединений формулы I зависит от внешних условий, таких как температура, влажность, природа используемого гербицида и подобные. Она может варьироваться в широких пределах, например от 0,001 до 1,0 кг а. и./га или более активного вещества, но обычно составляет от 0,005 до 750 г а. и./га, особенно между 0,005 и 250 г а. и./га.
Конкретный способ осуществления изобретения
Следующие ниже варианты осуществления используют для подробной иллюстрации настоящего изобретения и они не должны рассматриваться как ограничение настоящего изобретения. Объем изобретения поясняется формулой изобретения.
Принимая во внимание экономичность и разнообразие соединения, мы предпочтительно синтезировали несколько соединений, часть которых перечислена в следующей таблице 1. Структура и информация о конкретном соединении показаны в таблице 1. Соединения в таблице 1 перечислены для дальнейшего объяснения настоящего изобретения, а не для его ограничения. Объект настоящего изобретения не должен интерпретироваться специалистами в данной области техники как ограниченный следующими соединениями.
Таблица 1: Структуры и 1H ЯМР данные соединений
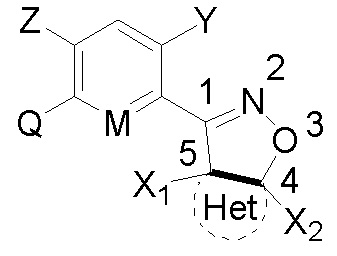
I
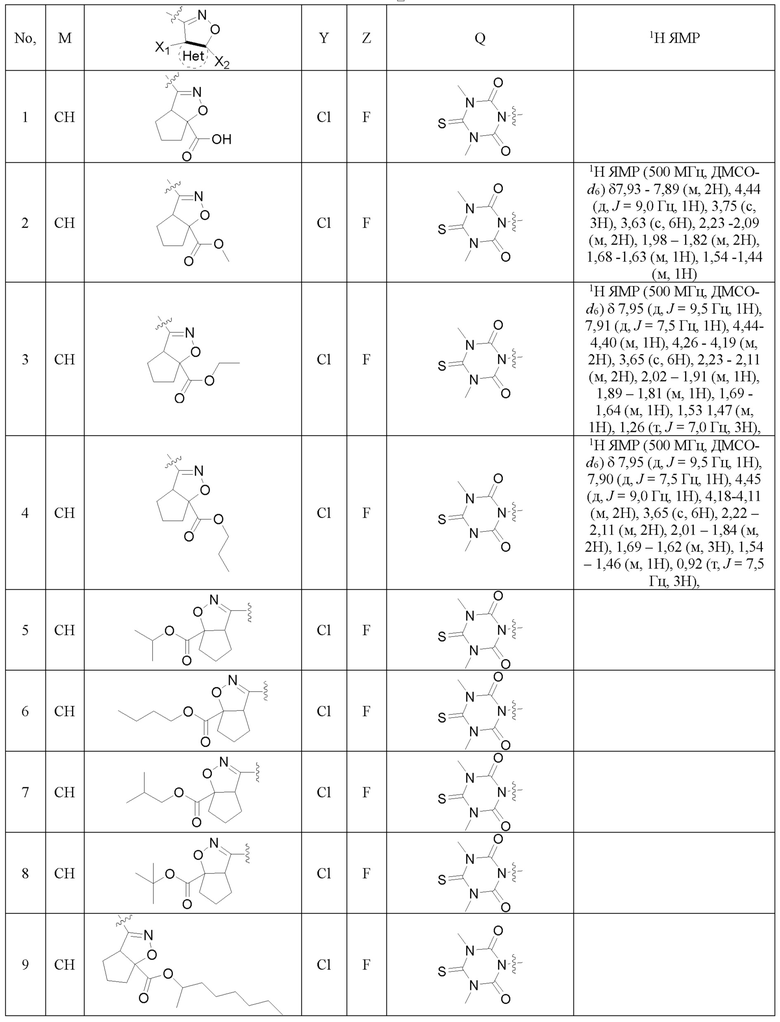
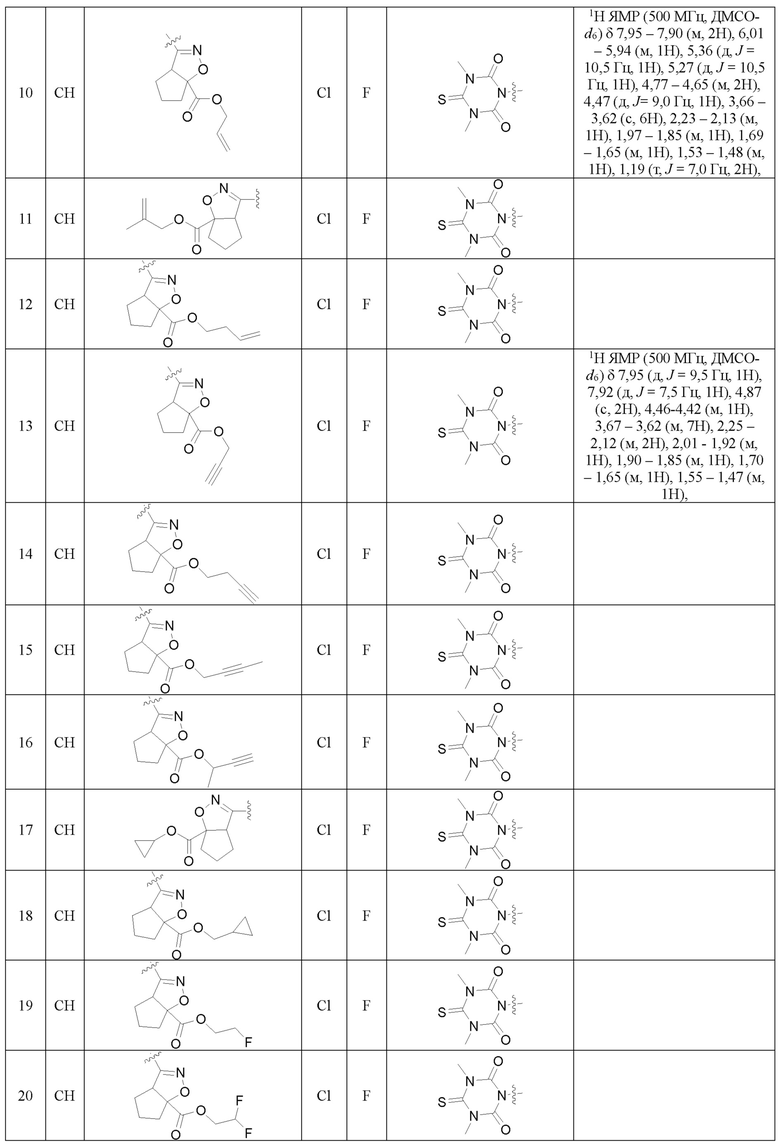
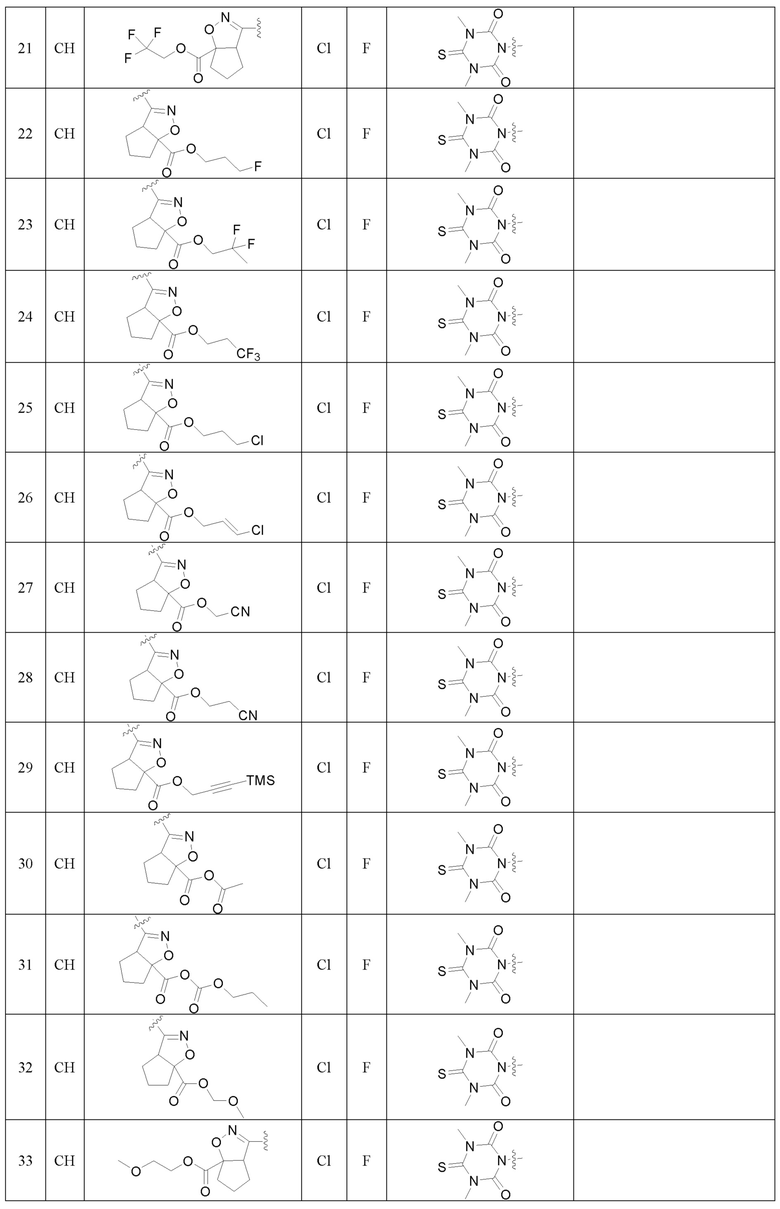
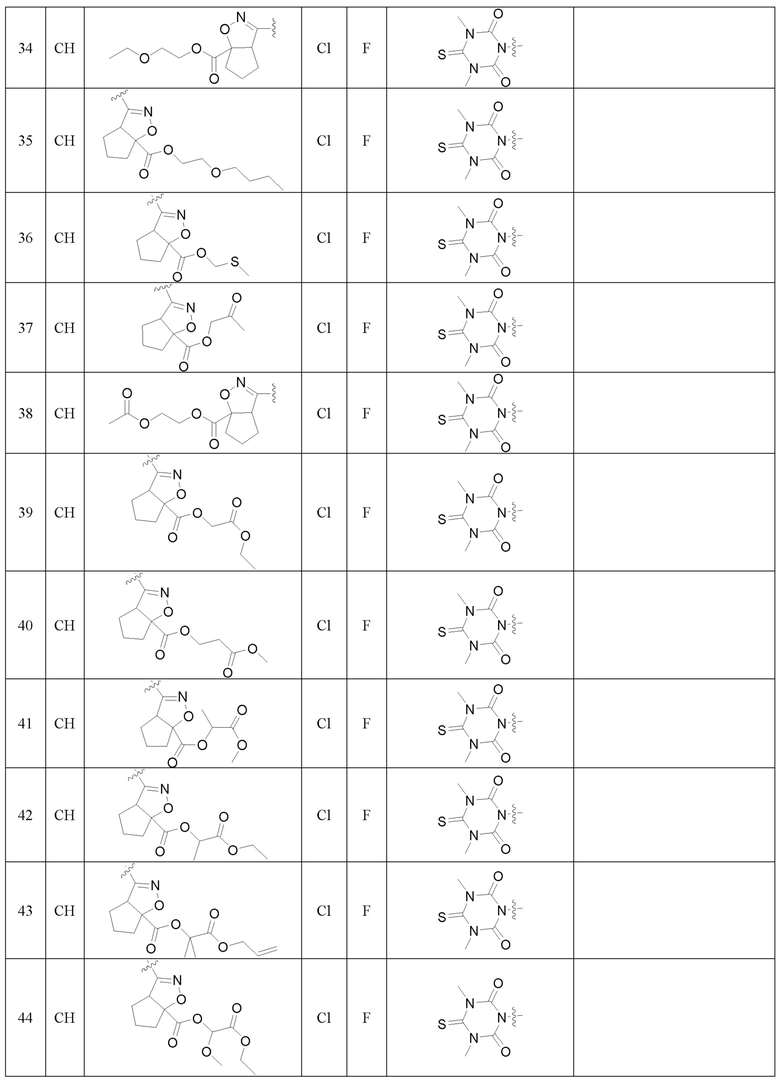
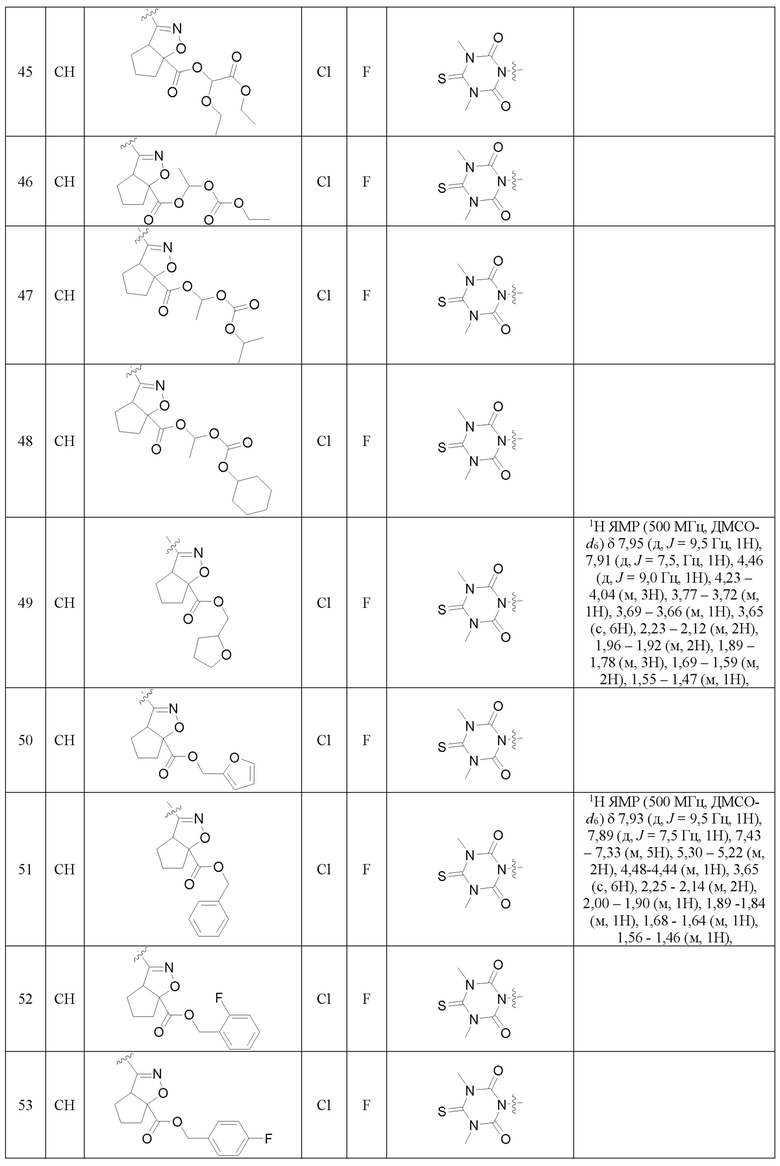
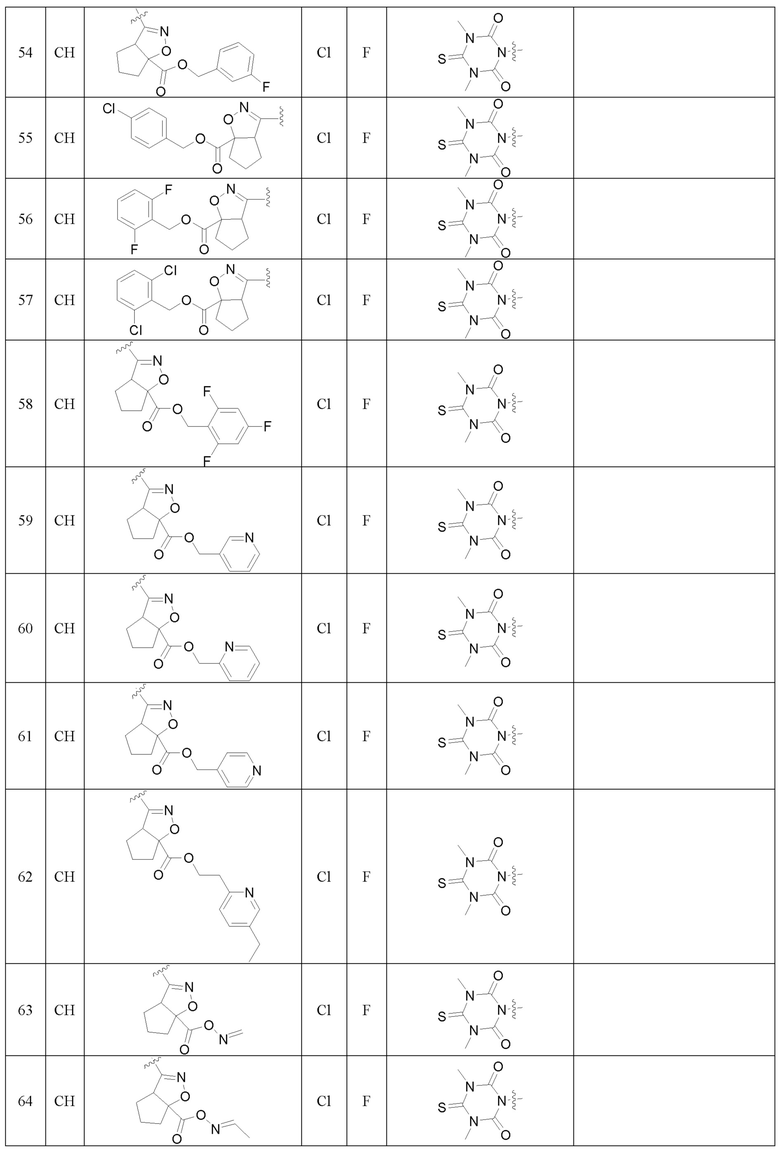
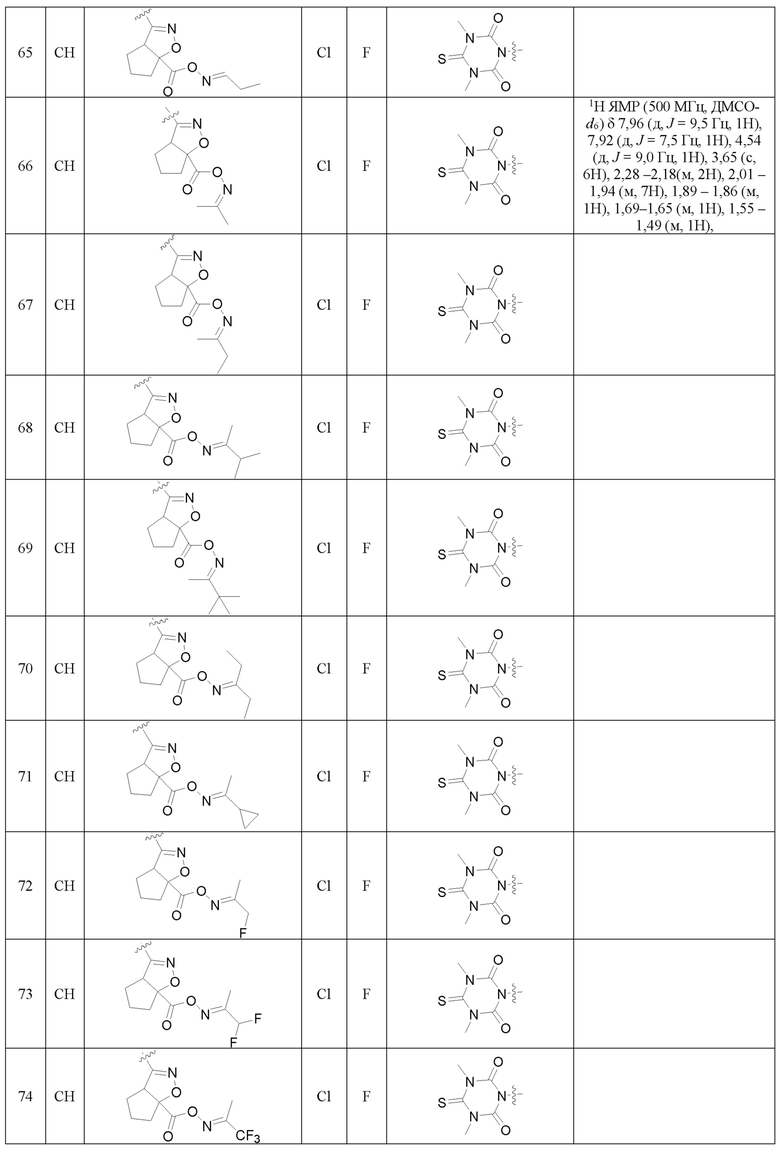
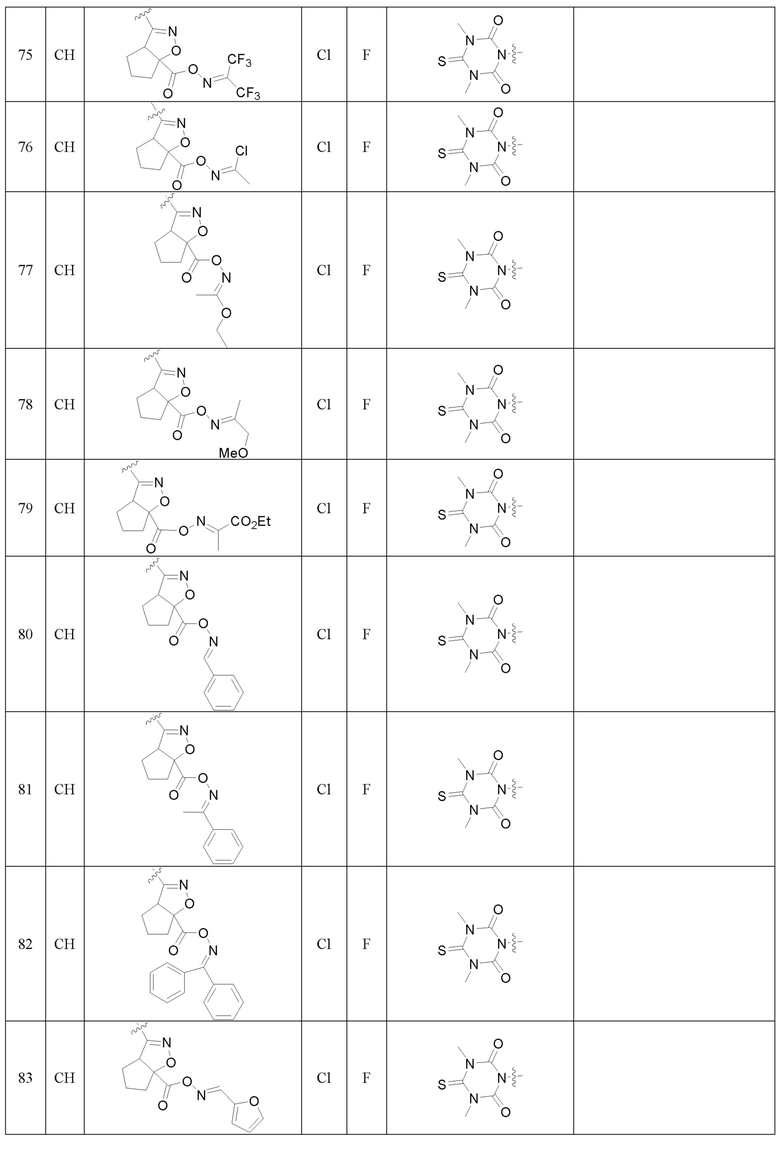
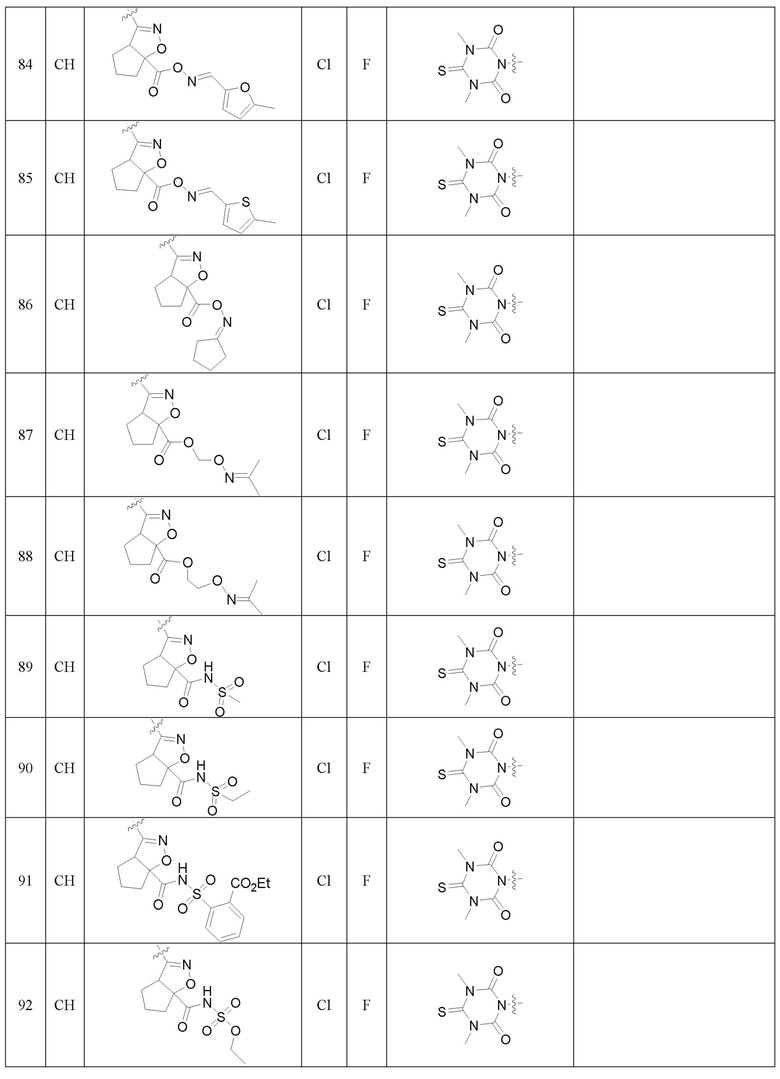
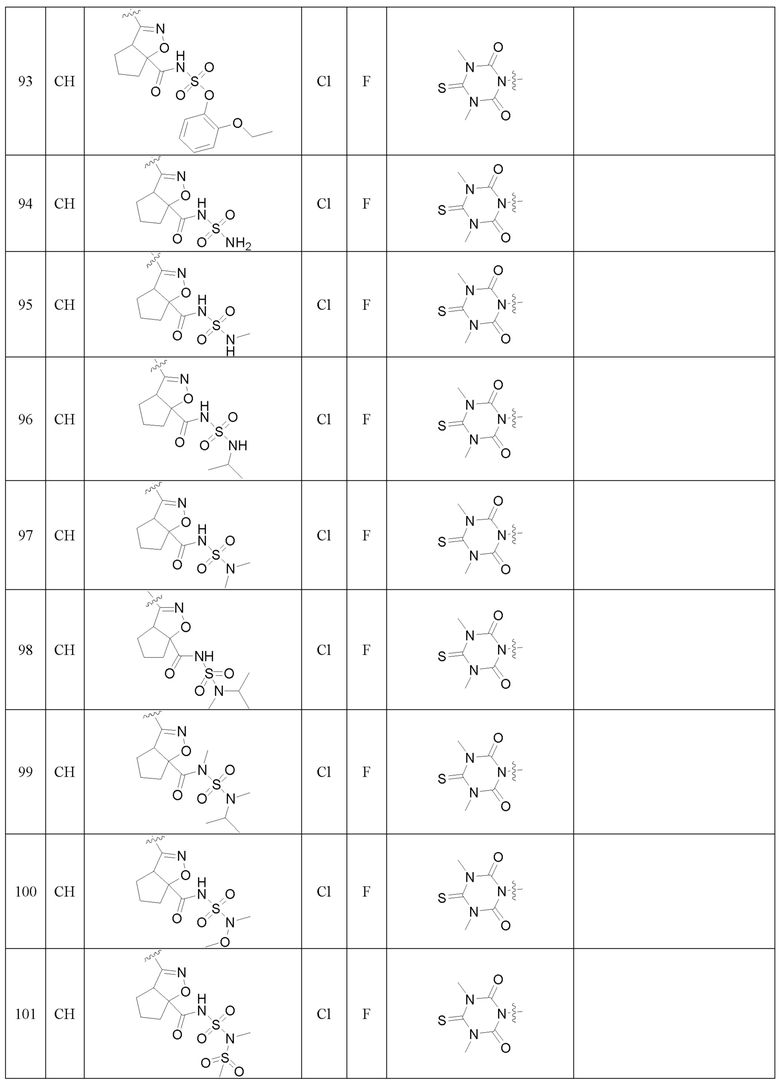
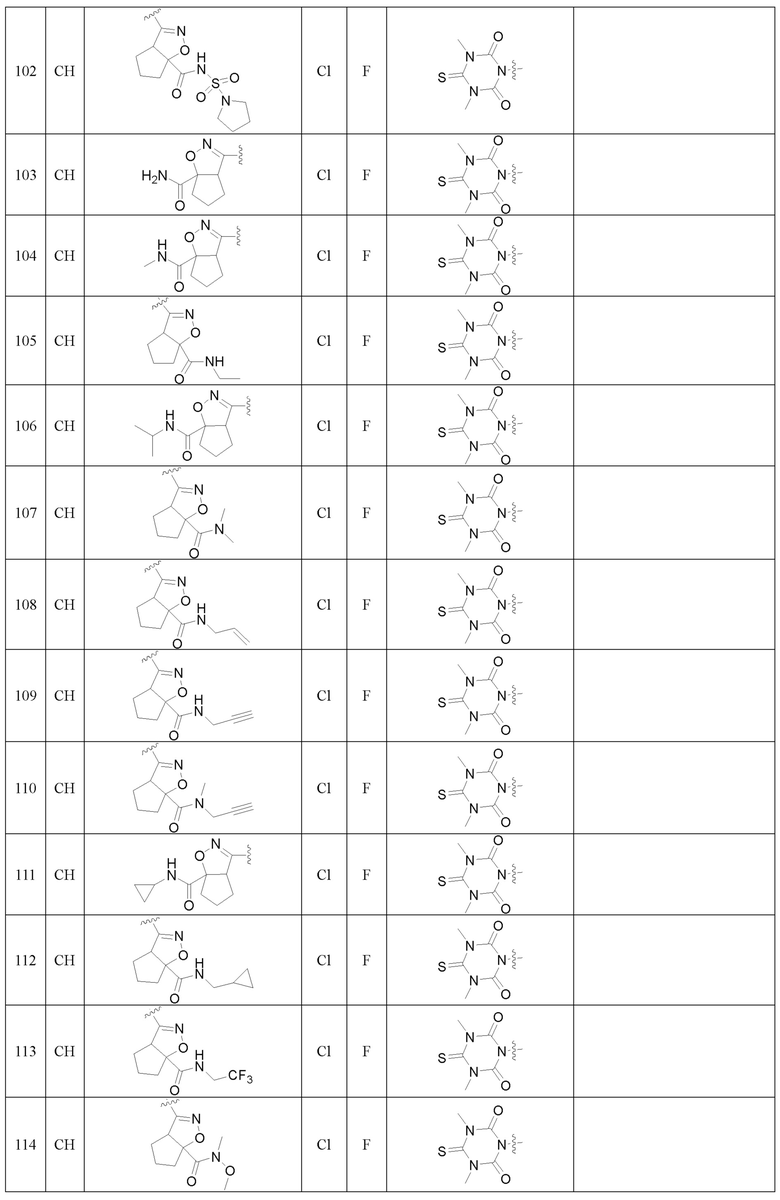
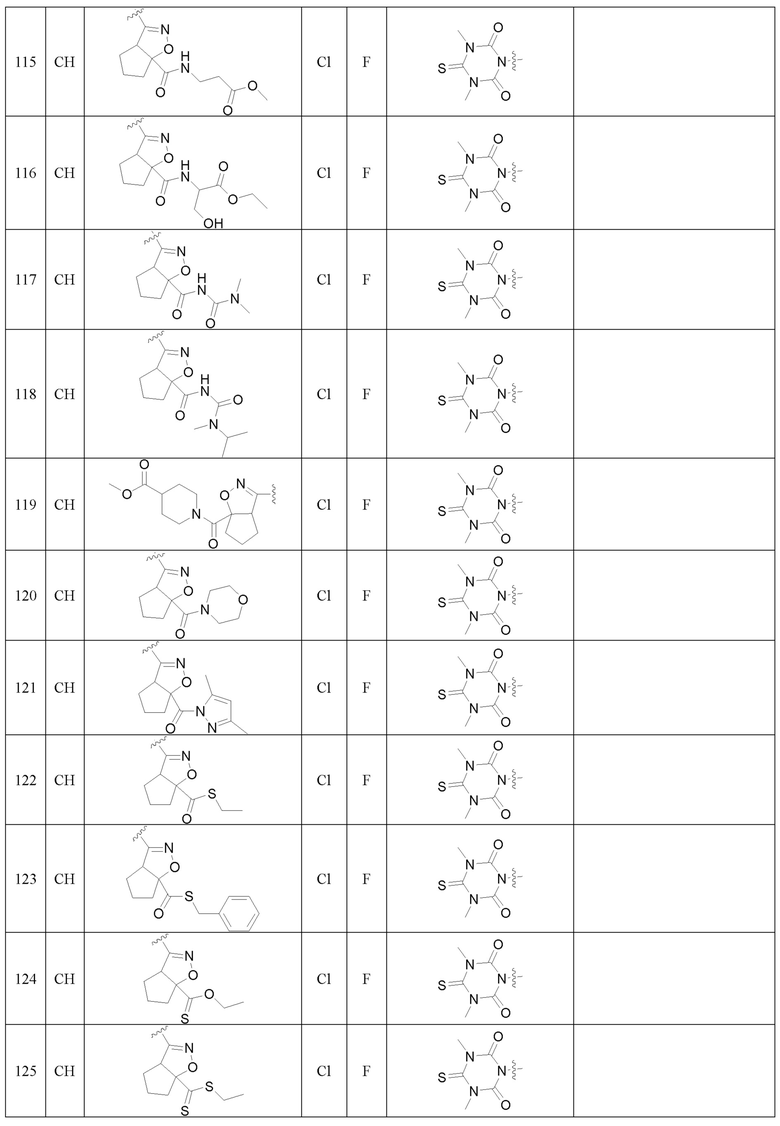
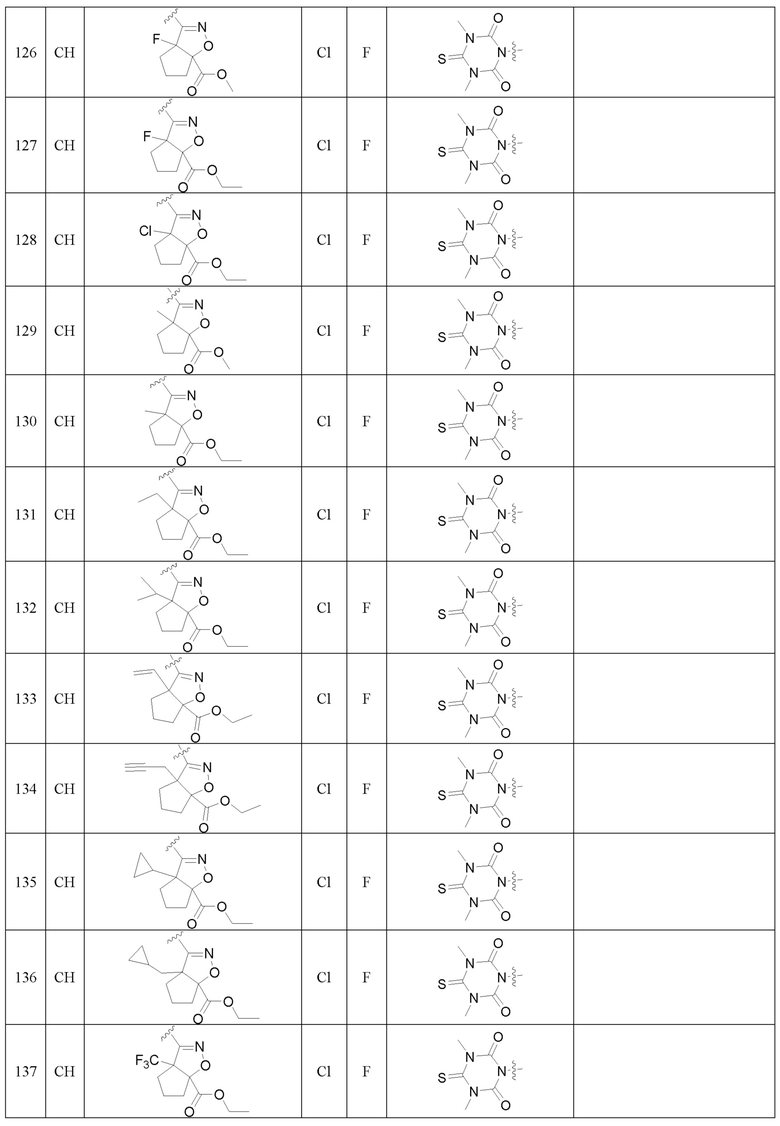
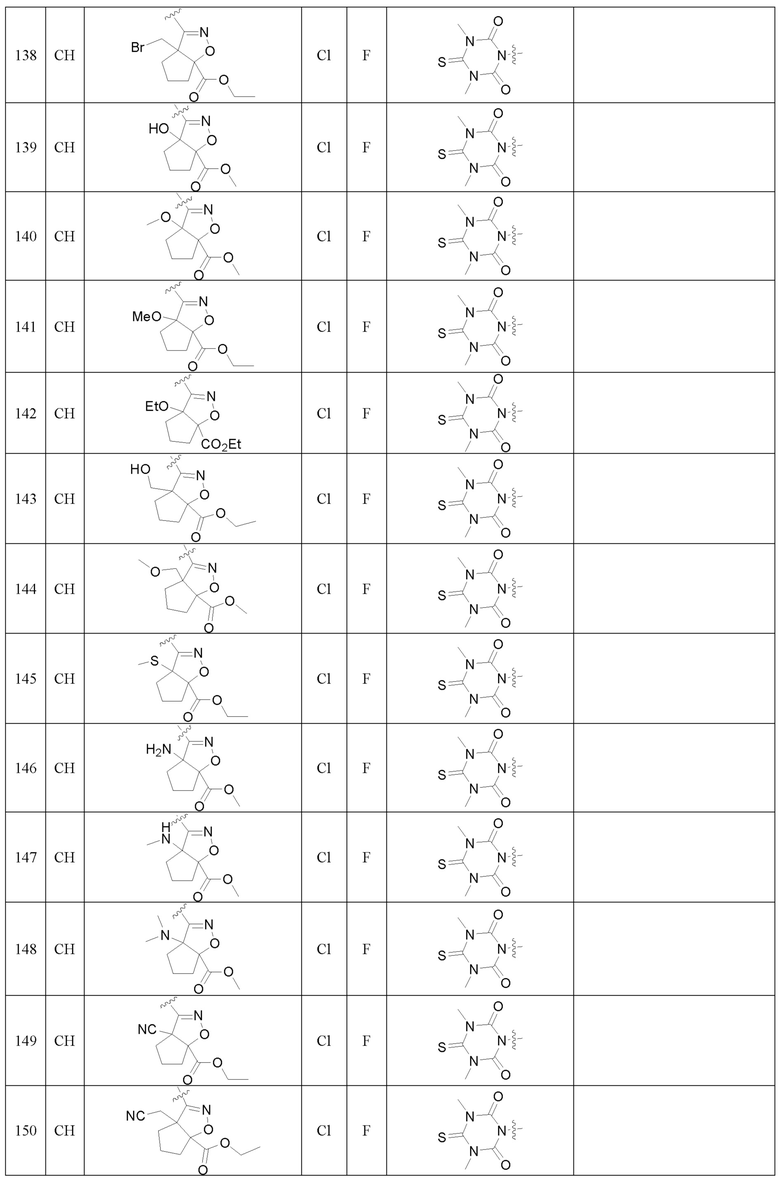
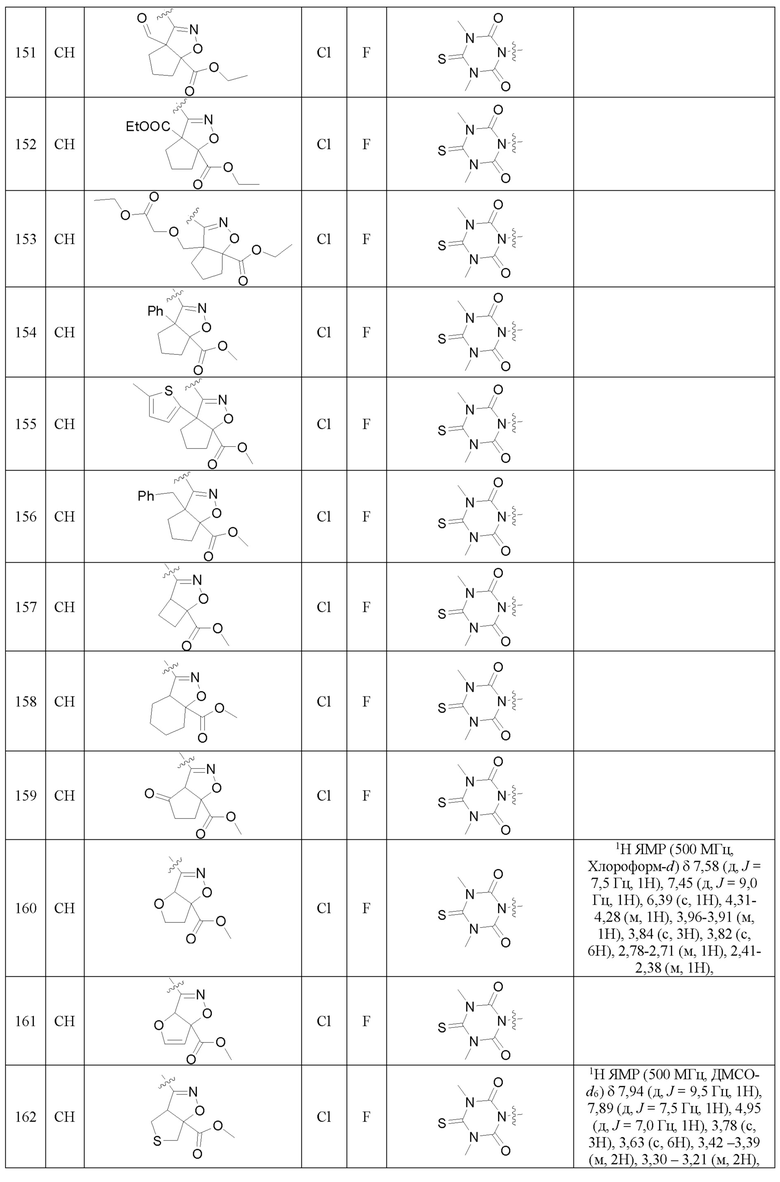
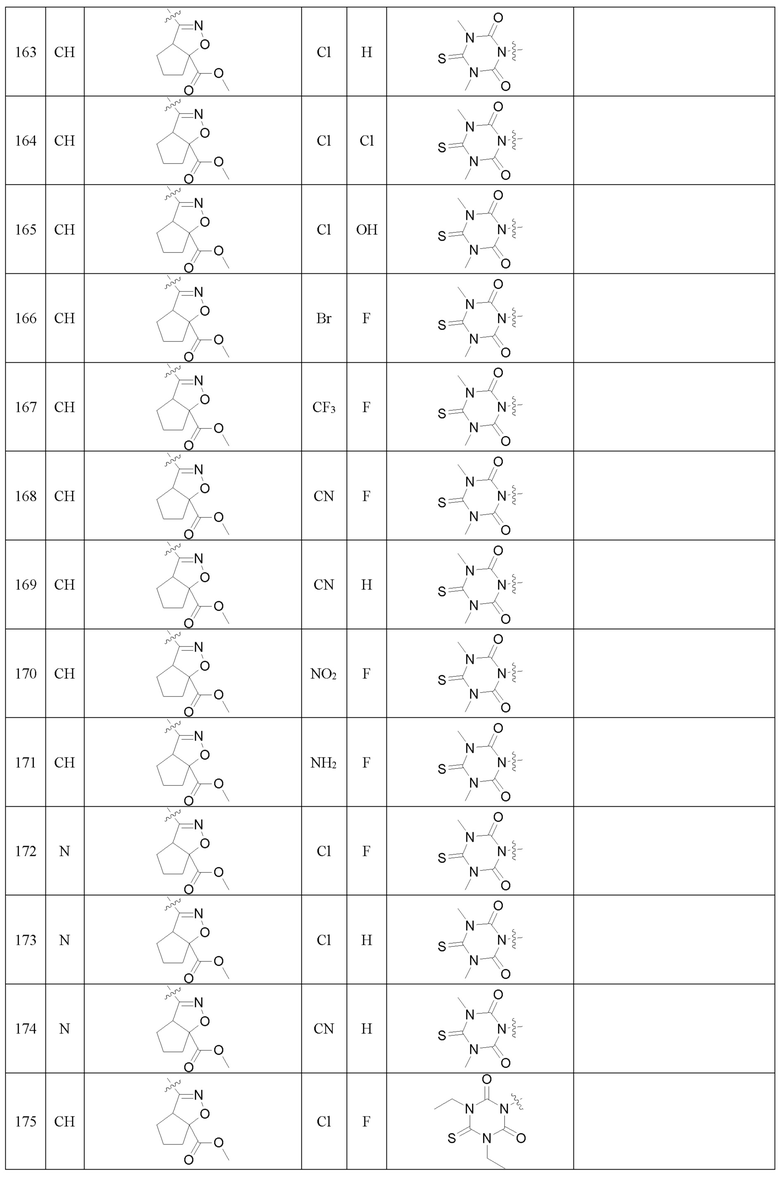
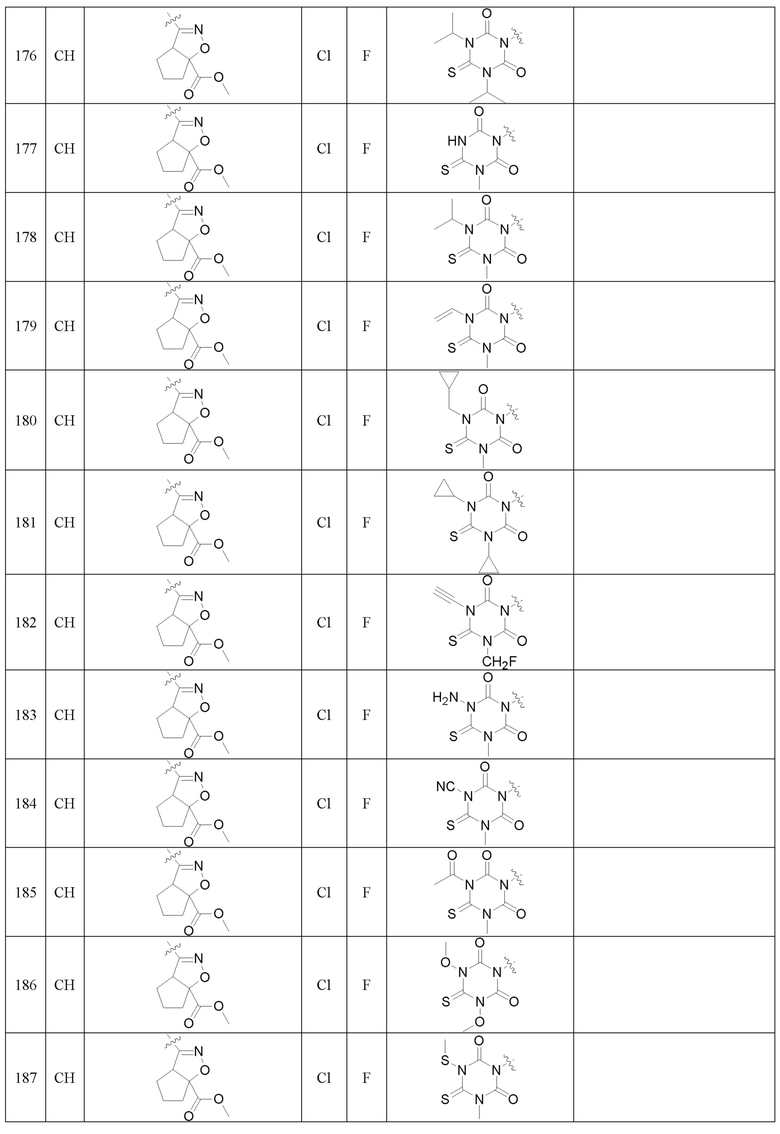
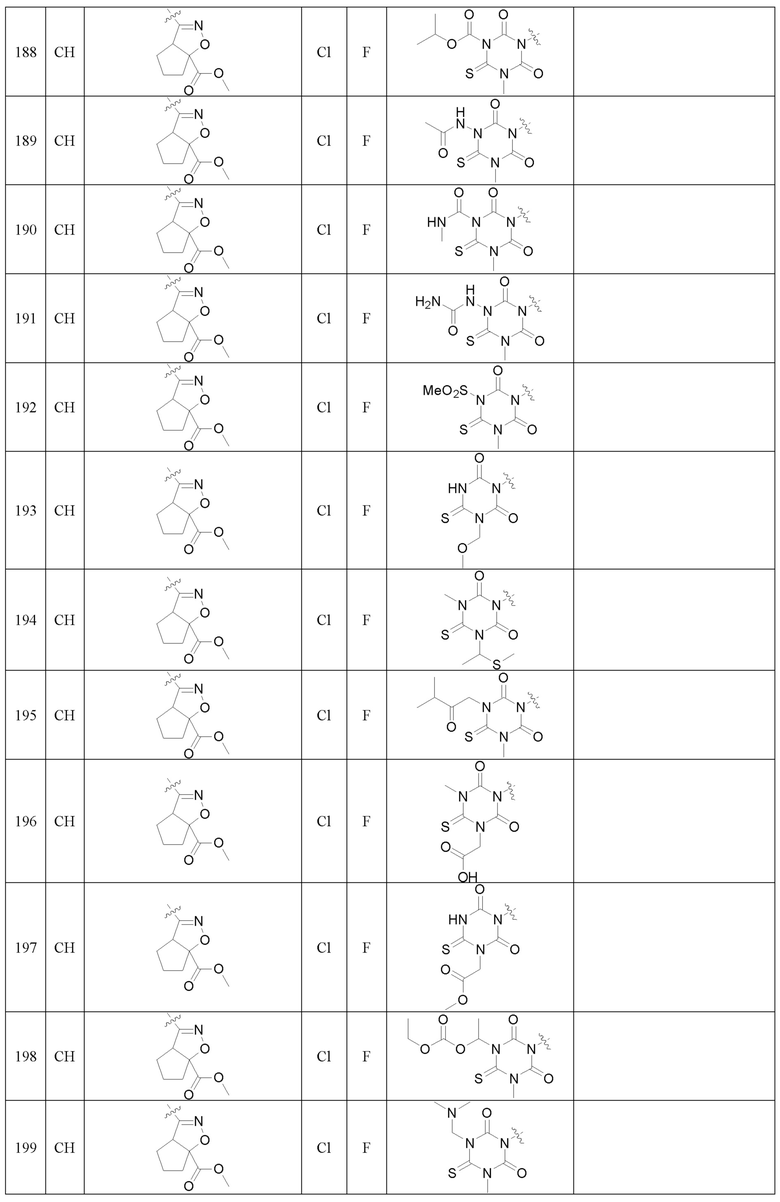
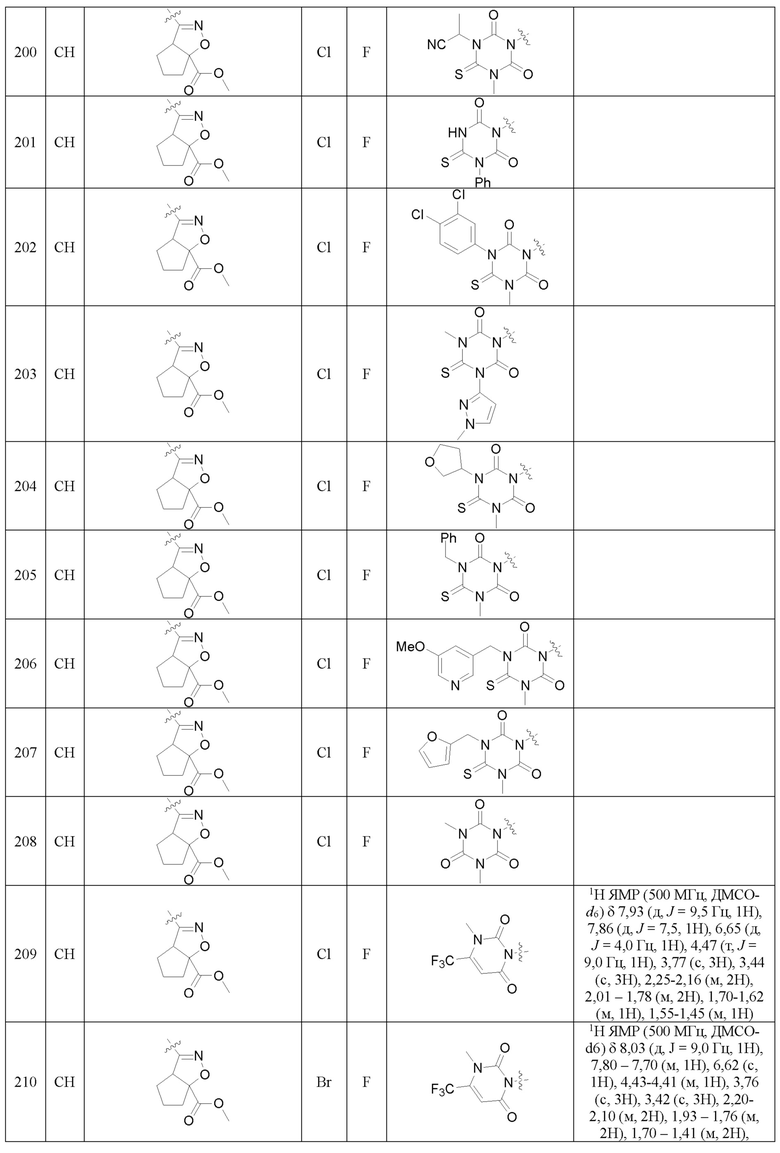
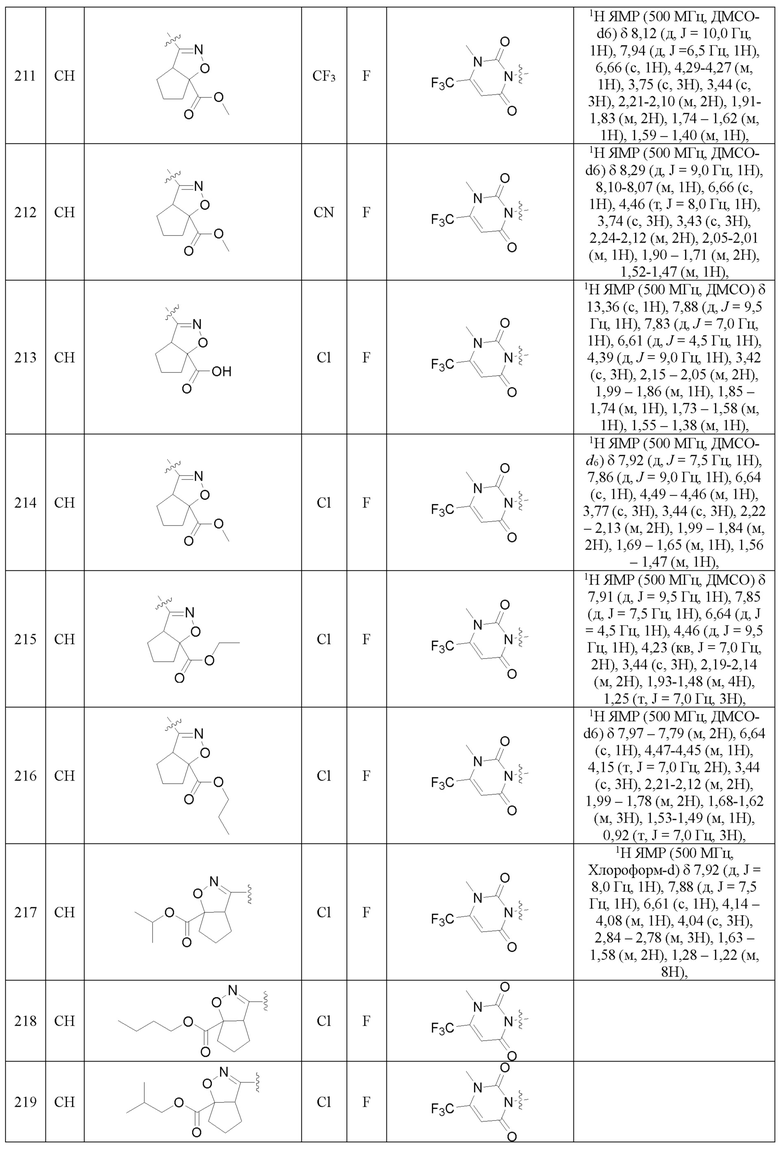
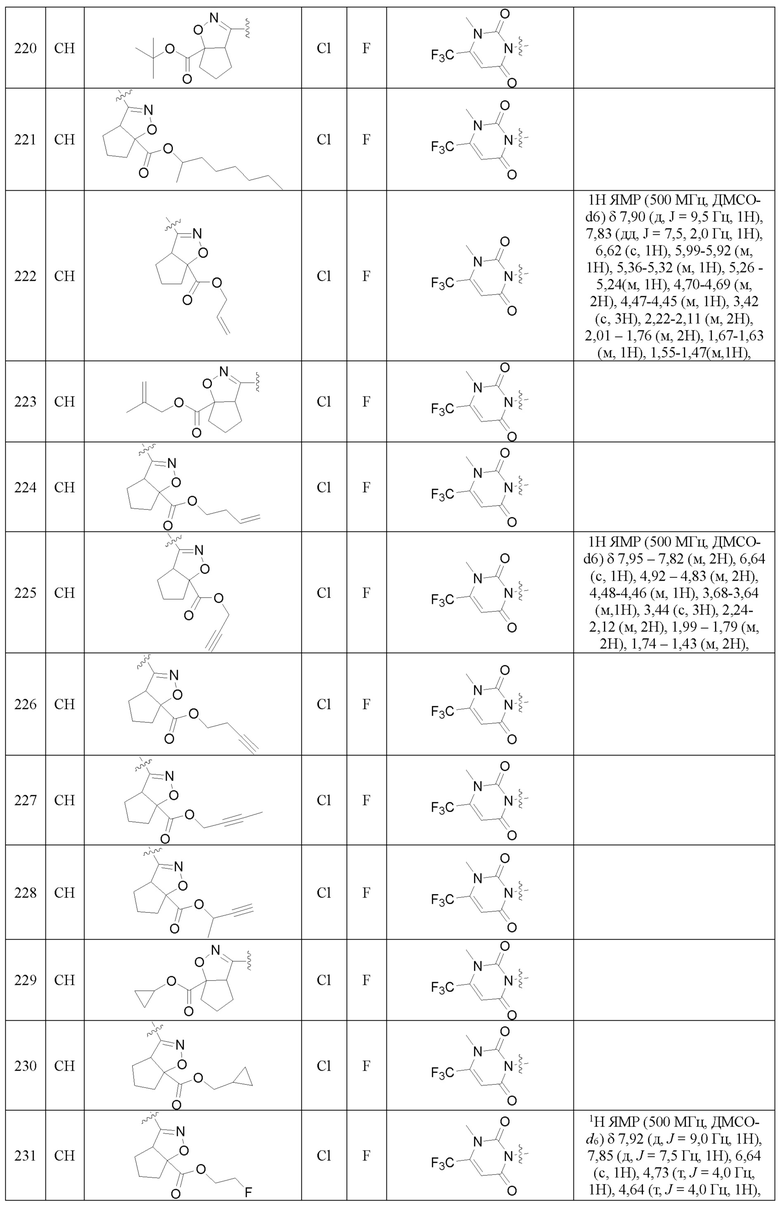
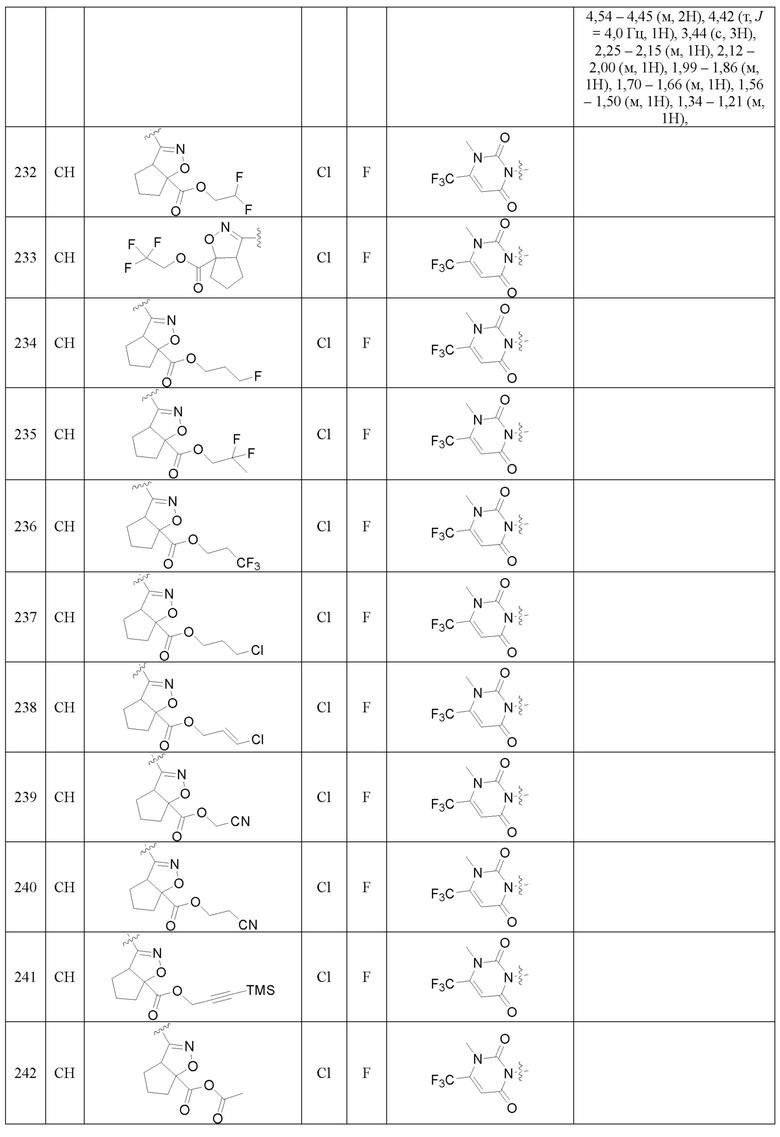
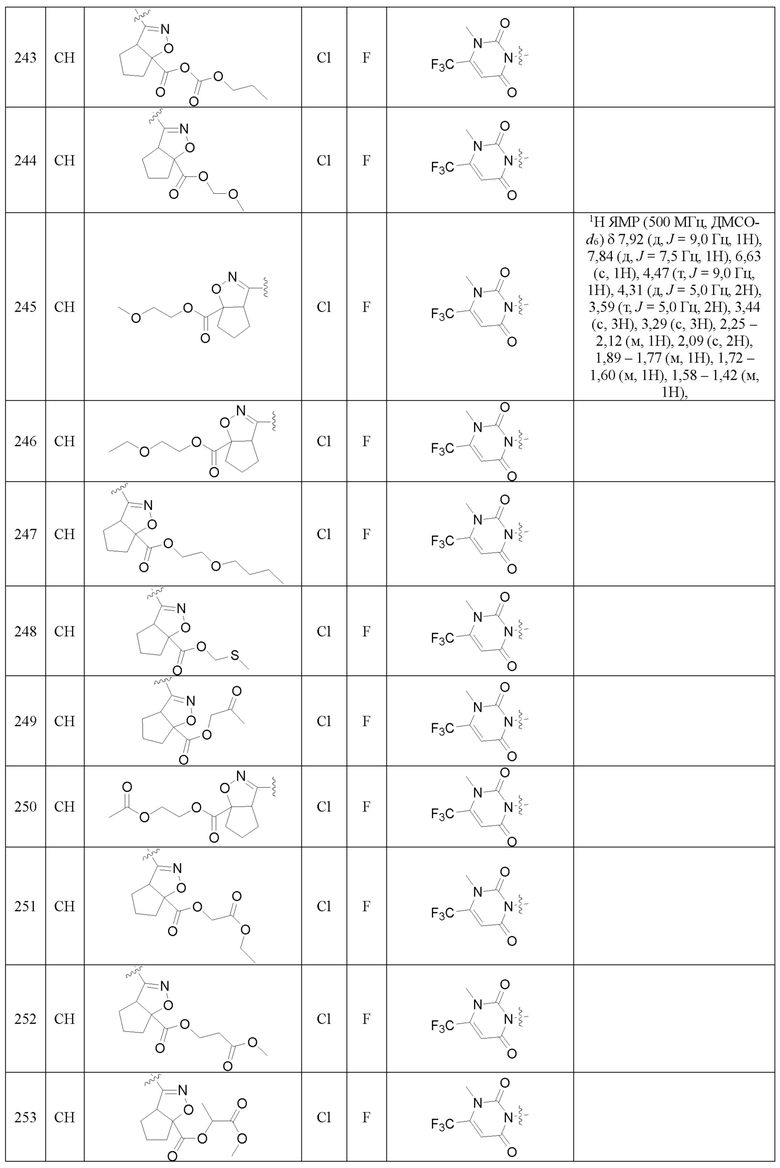
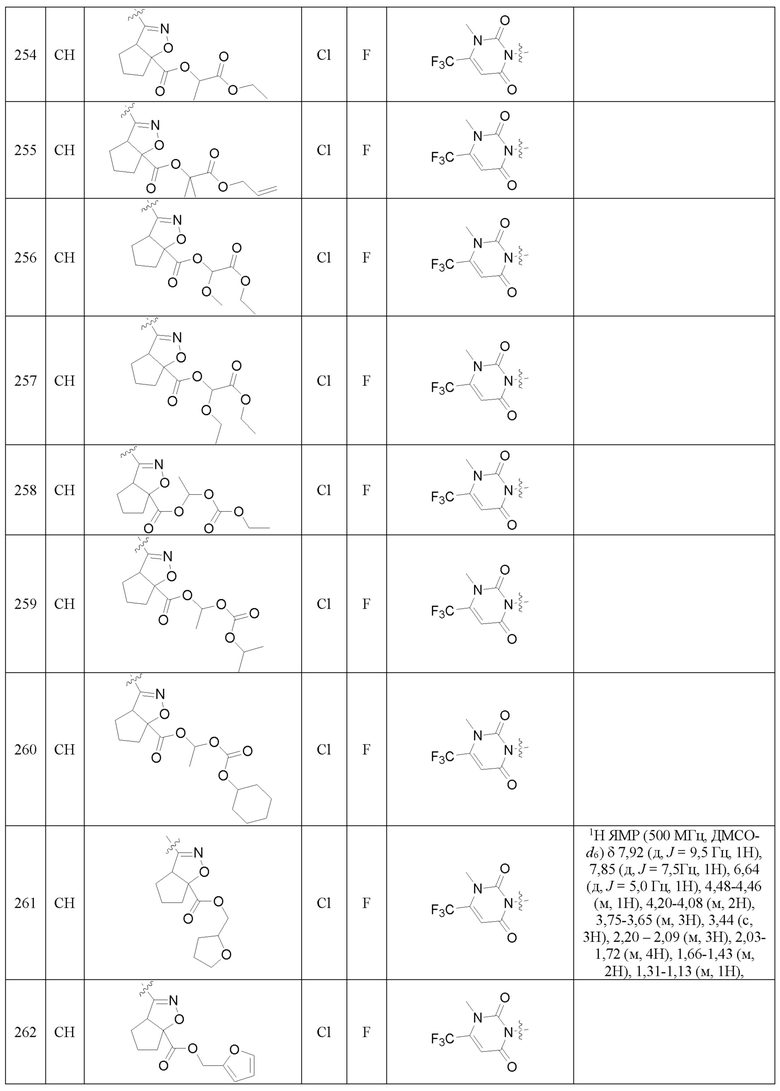
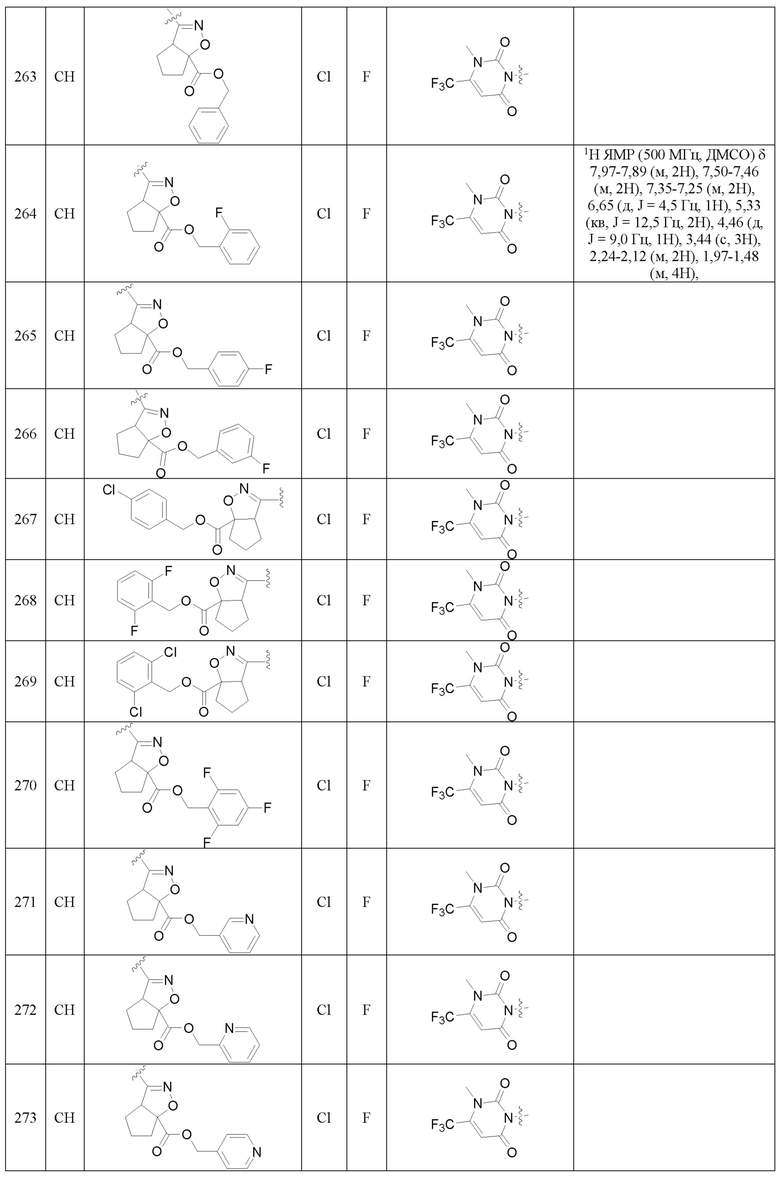
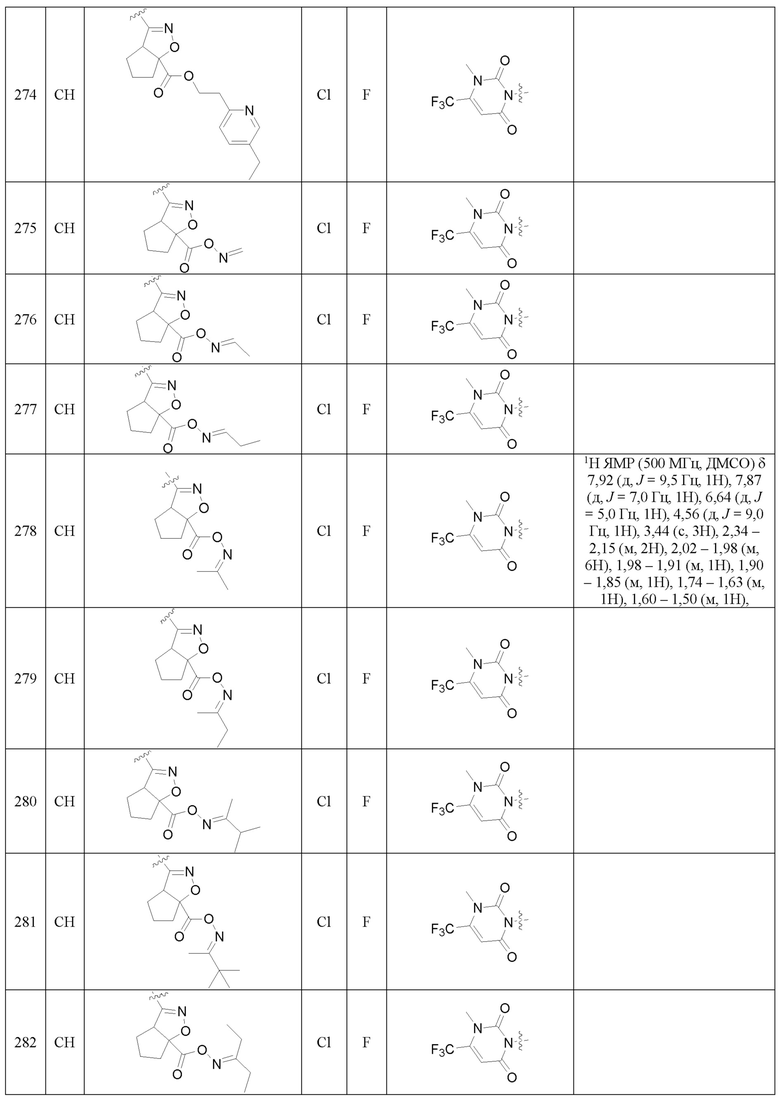
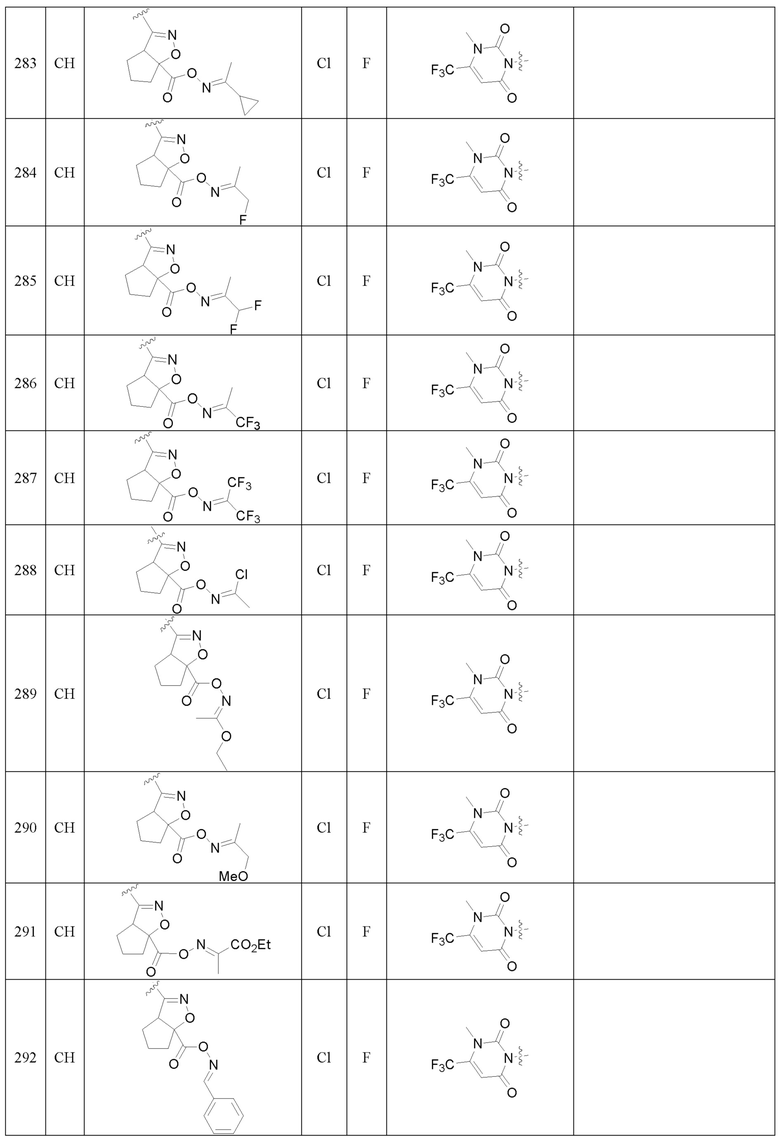
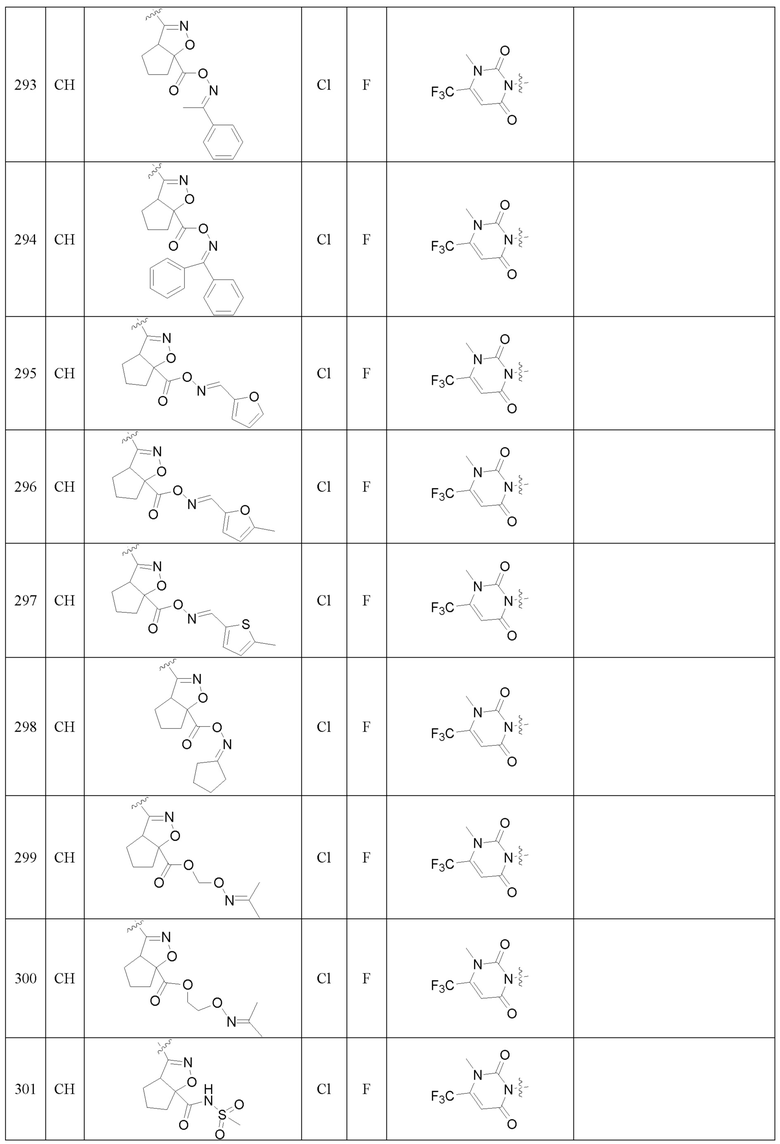
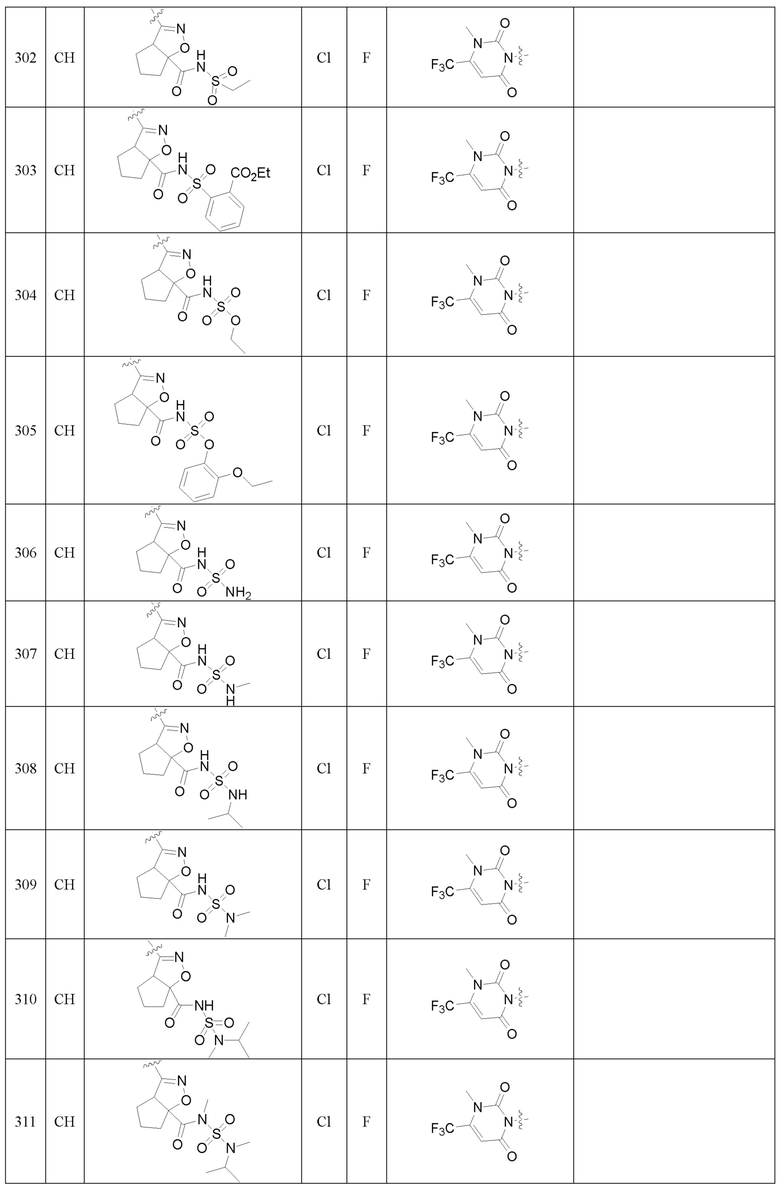
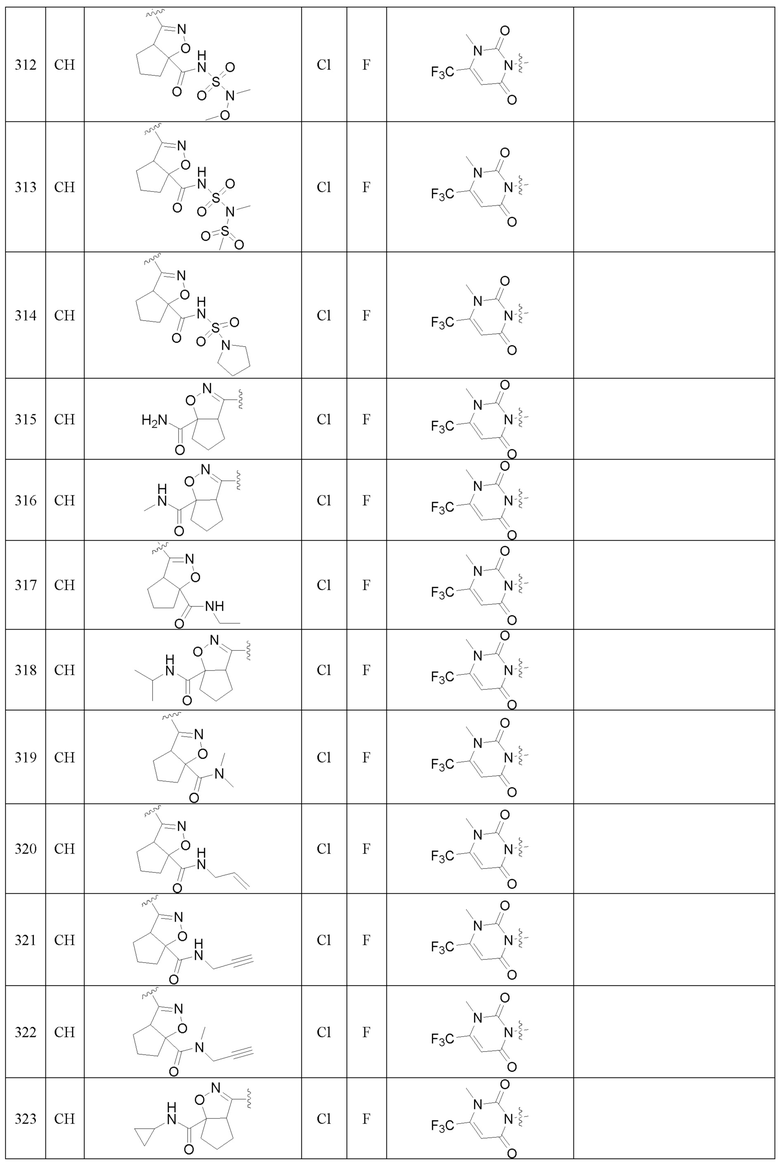
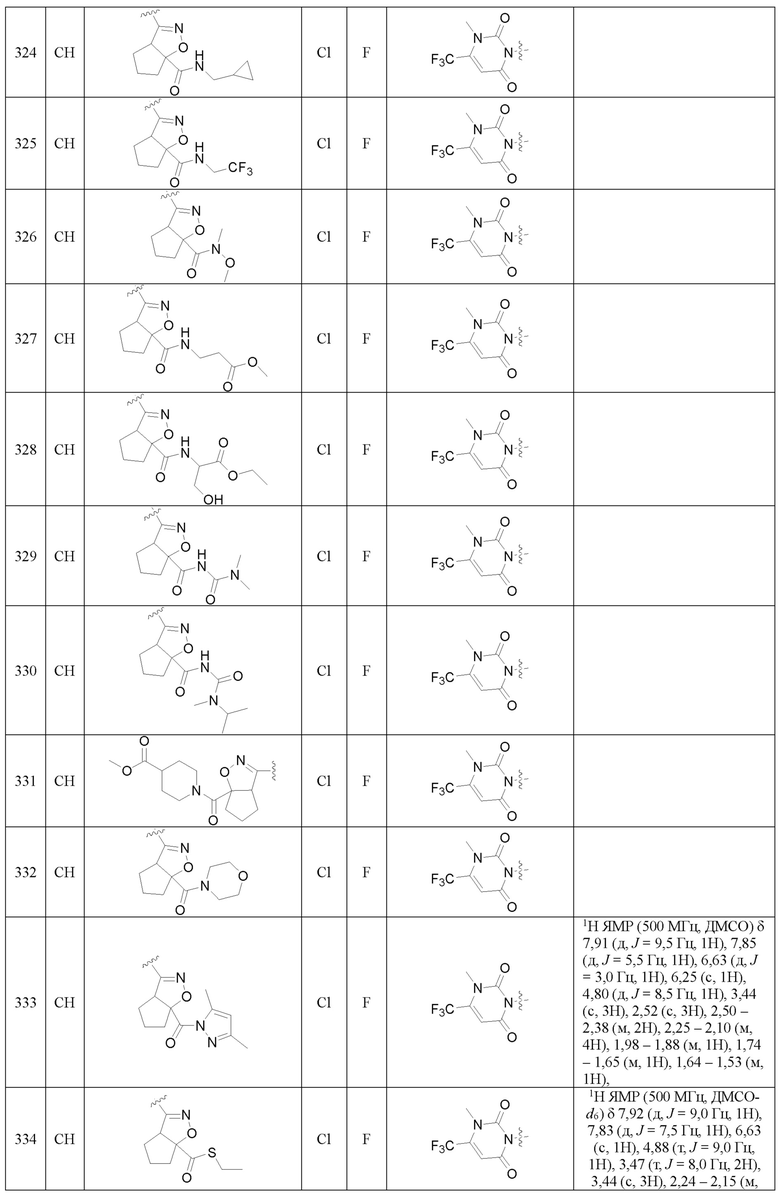
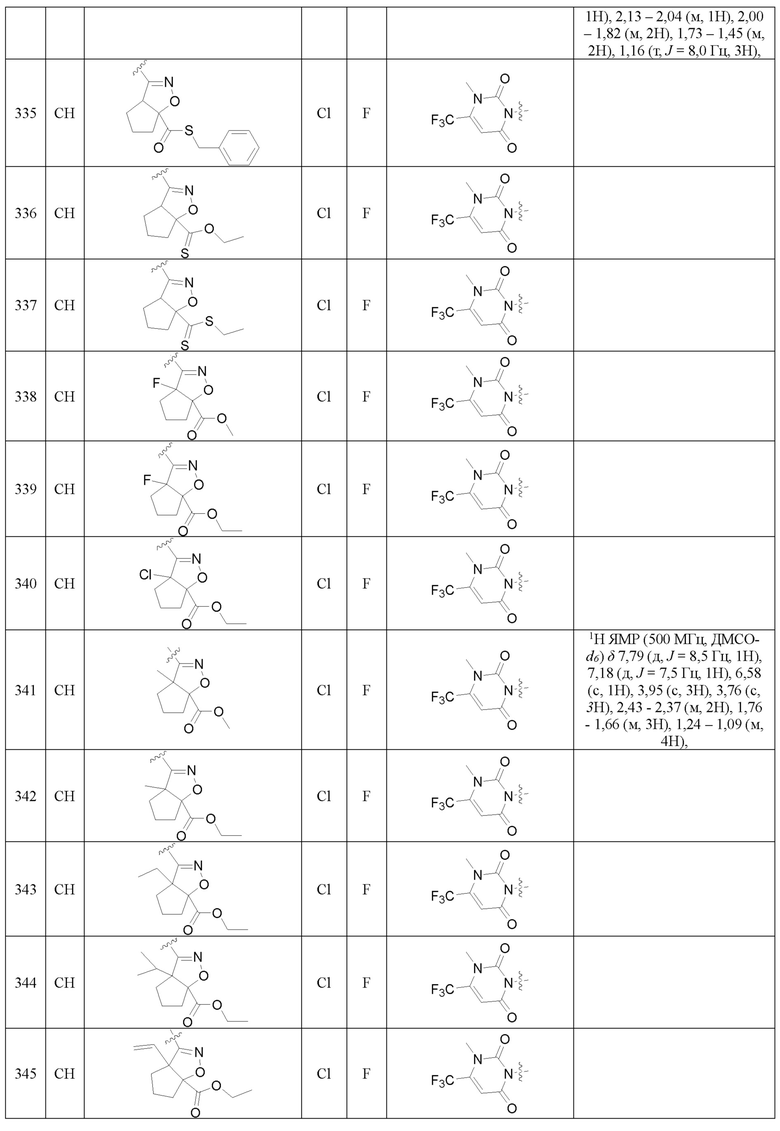
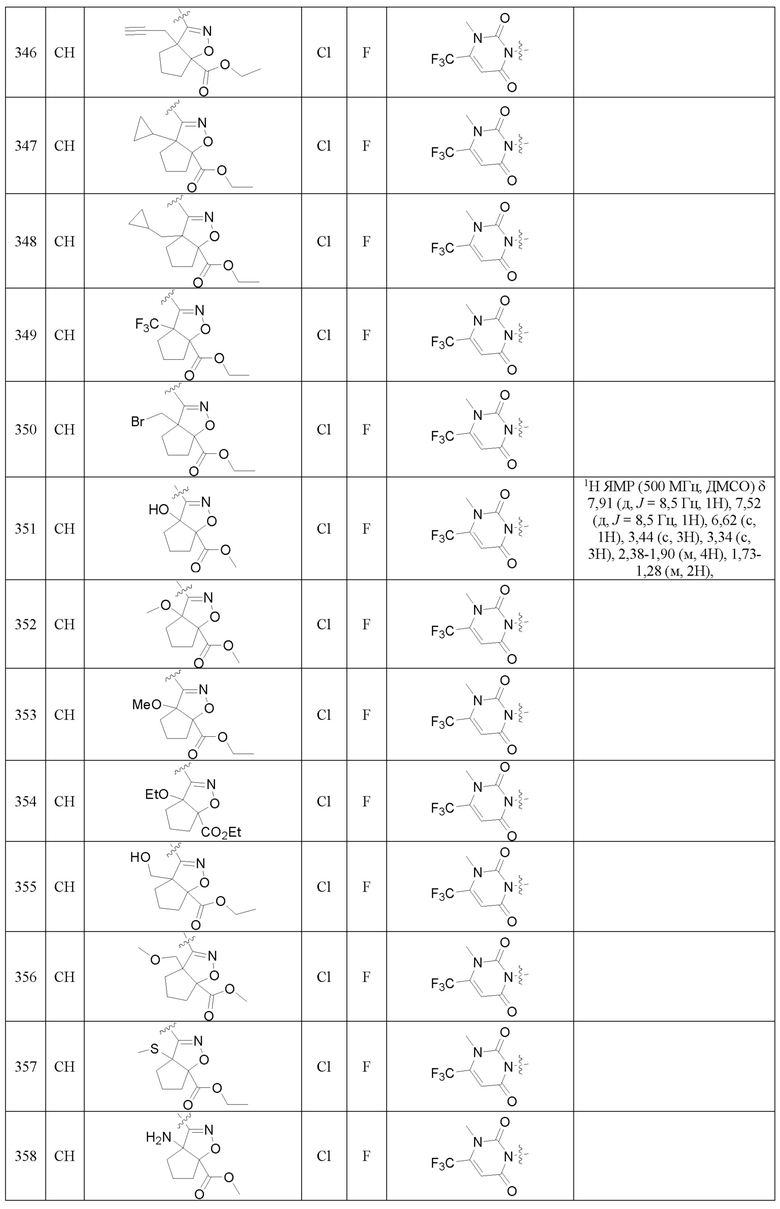
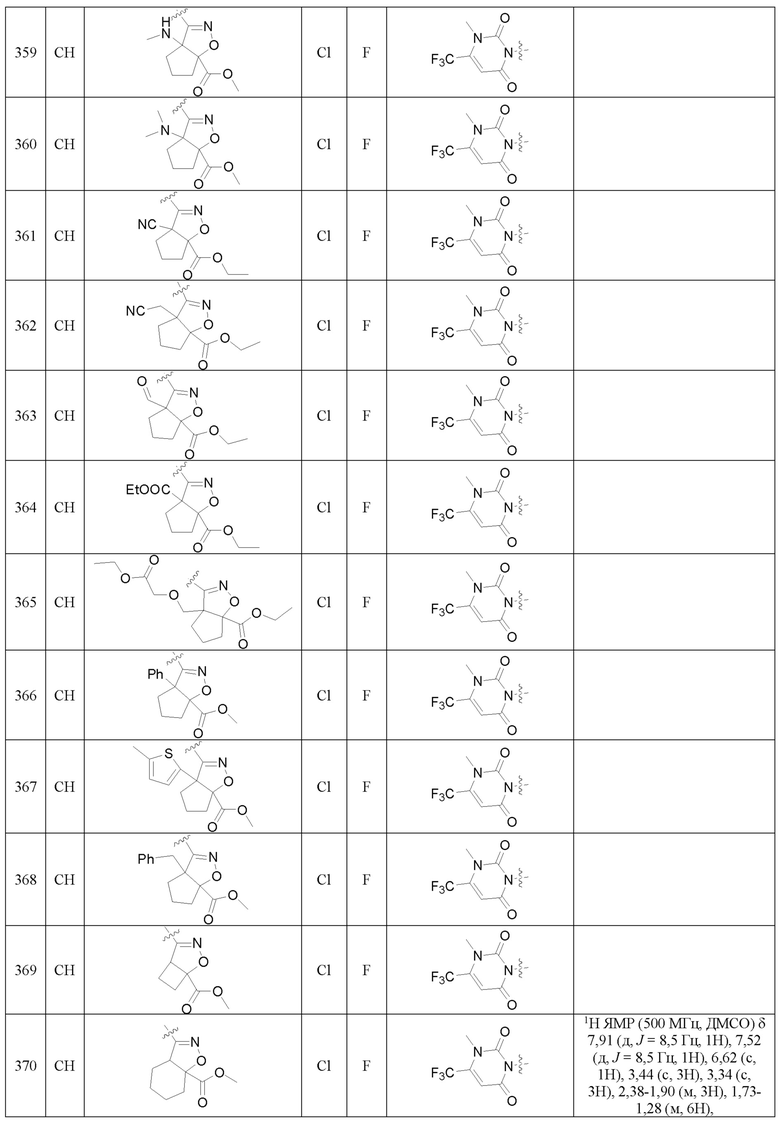
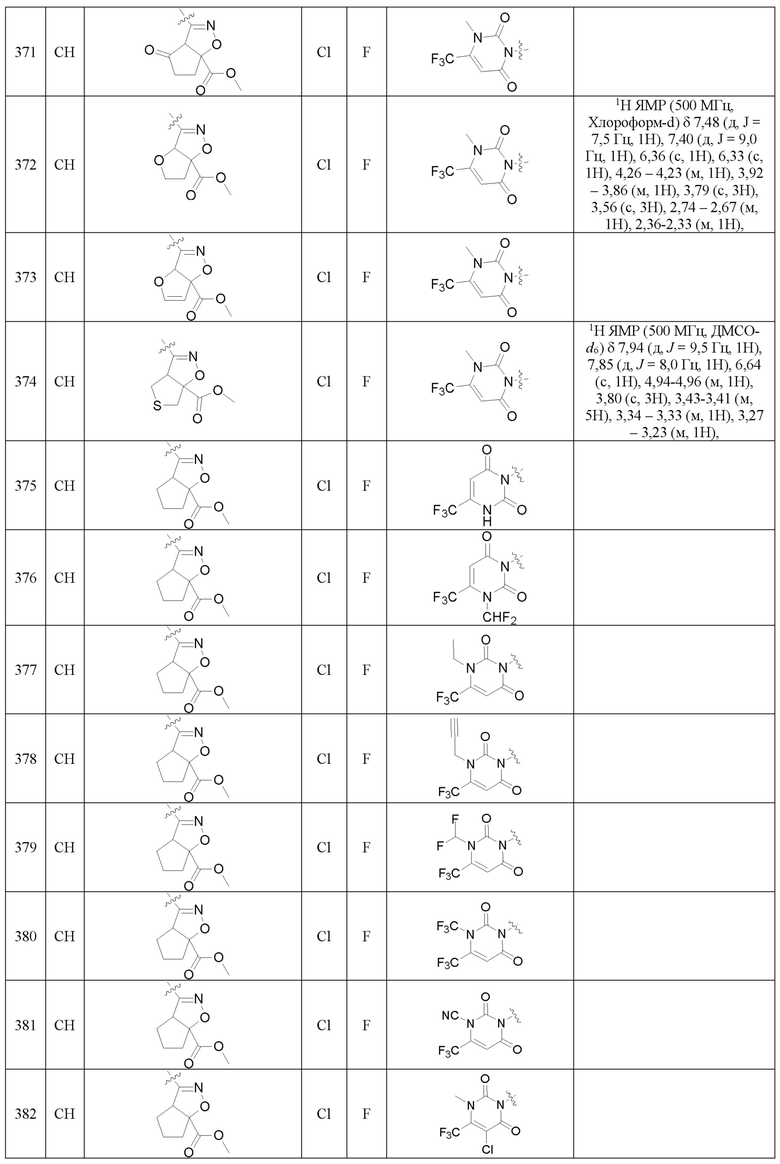
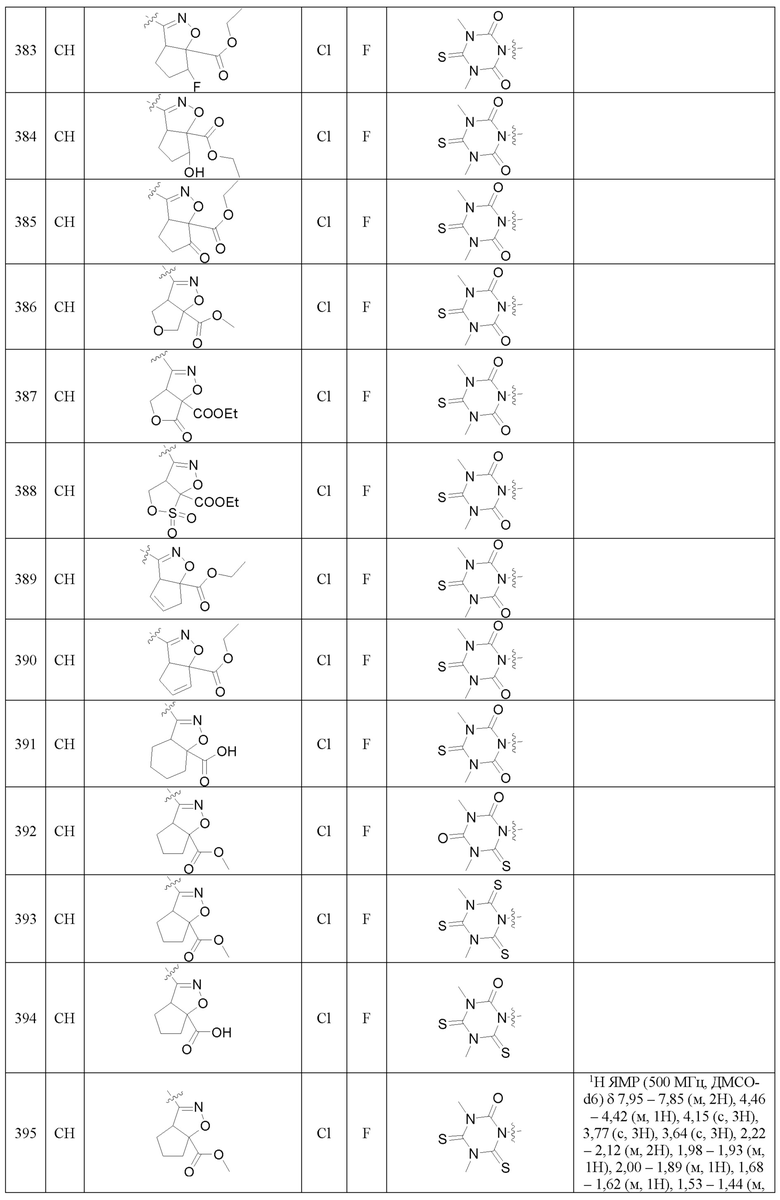
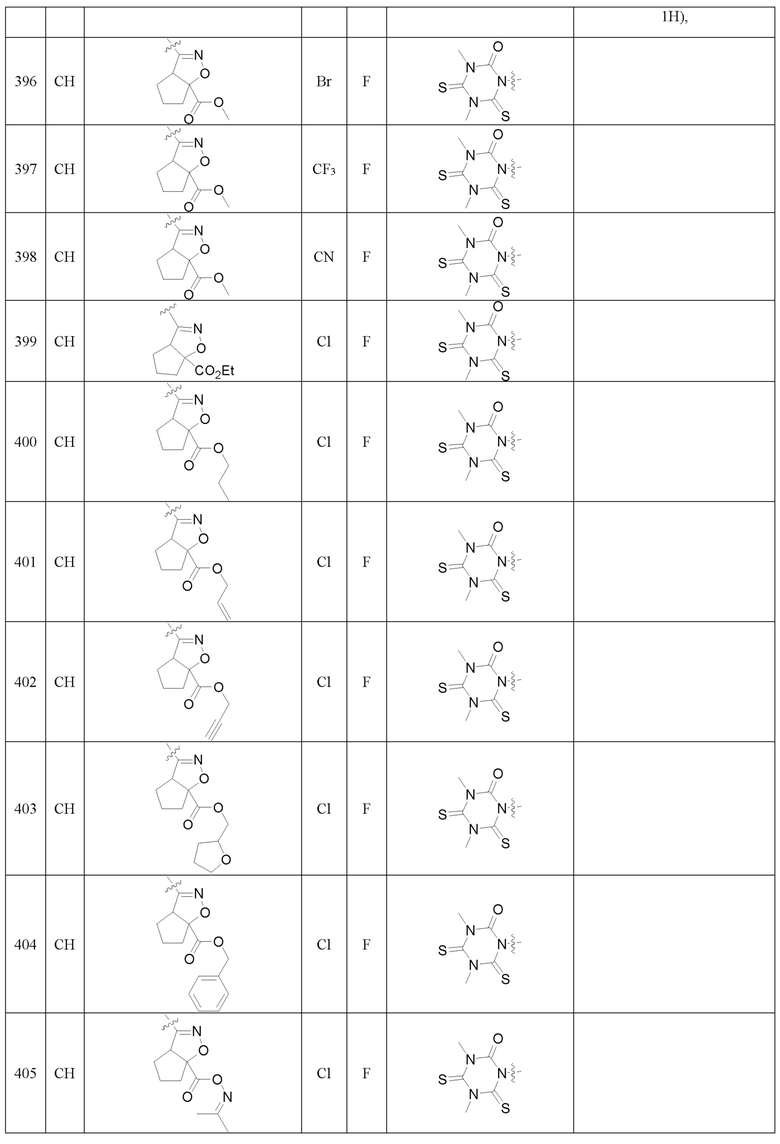
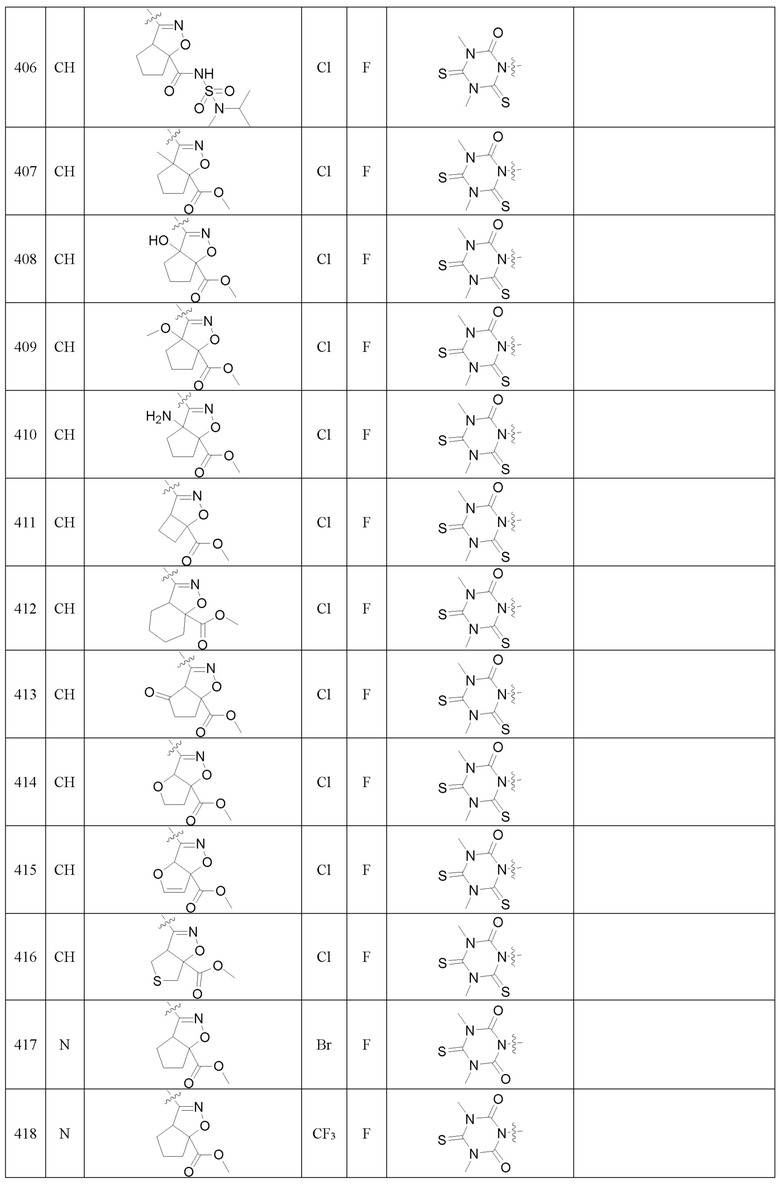
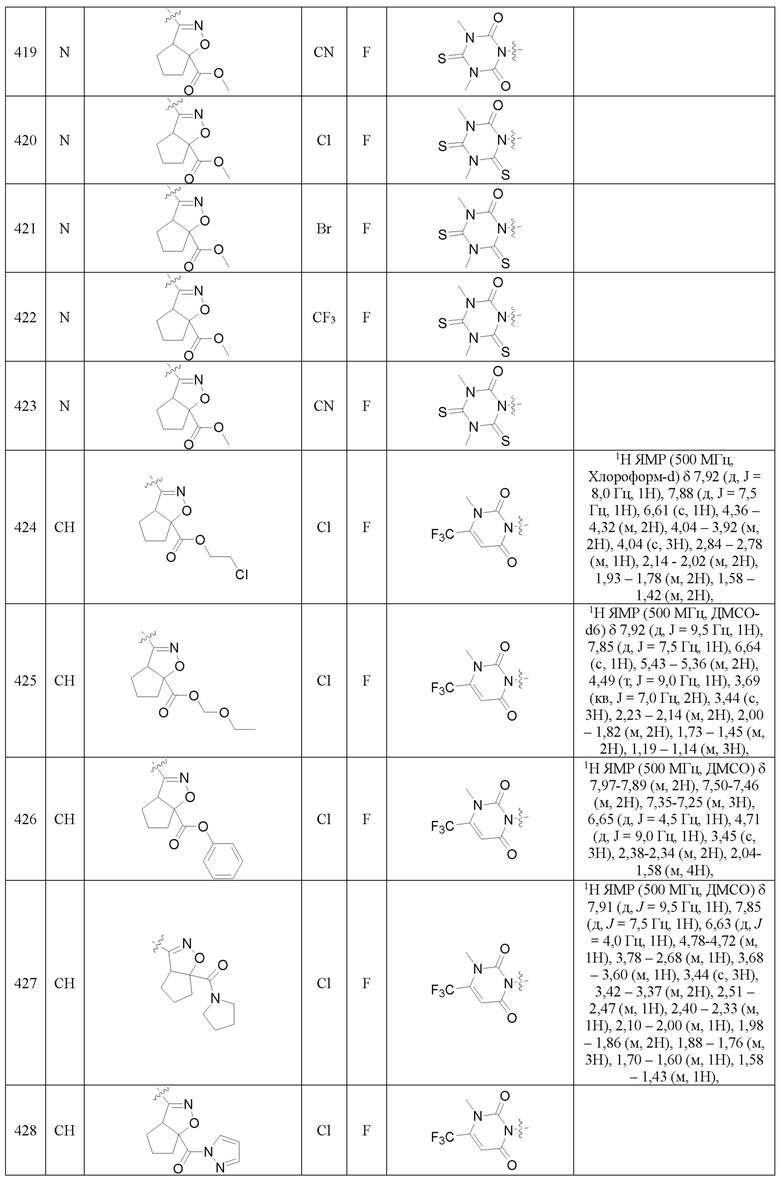
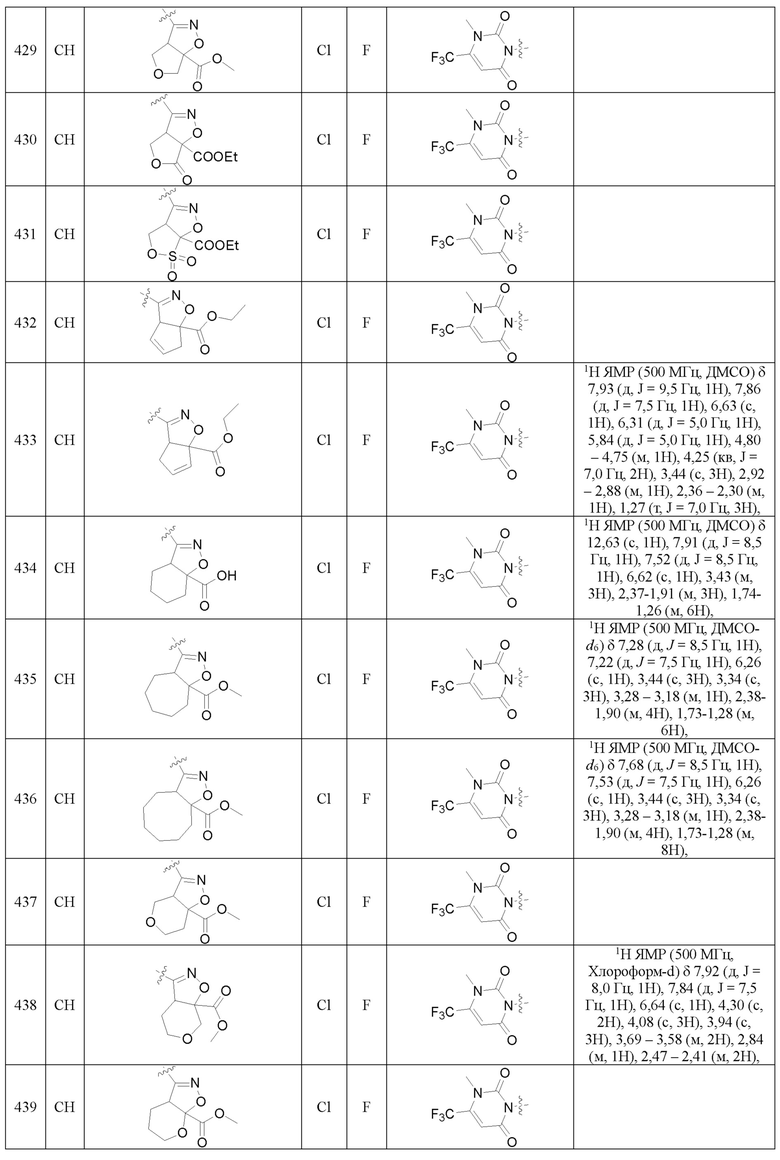
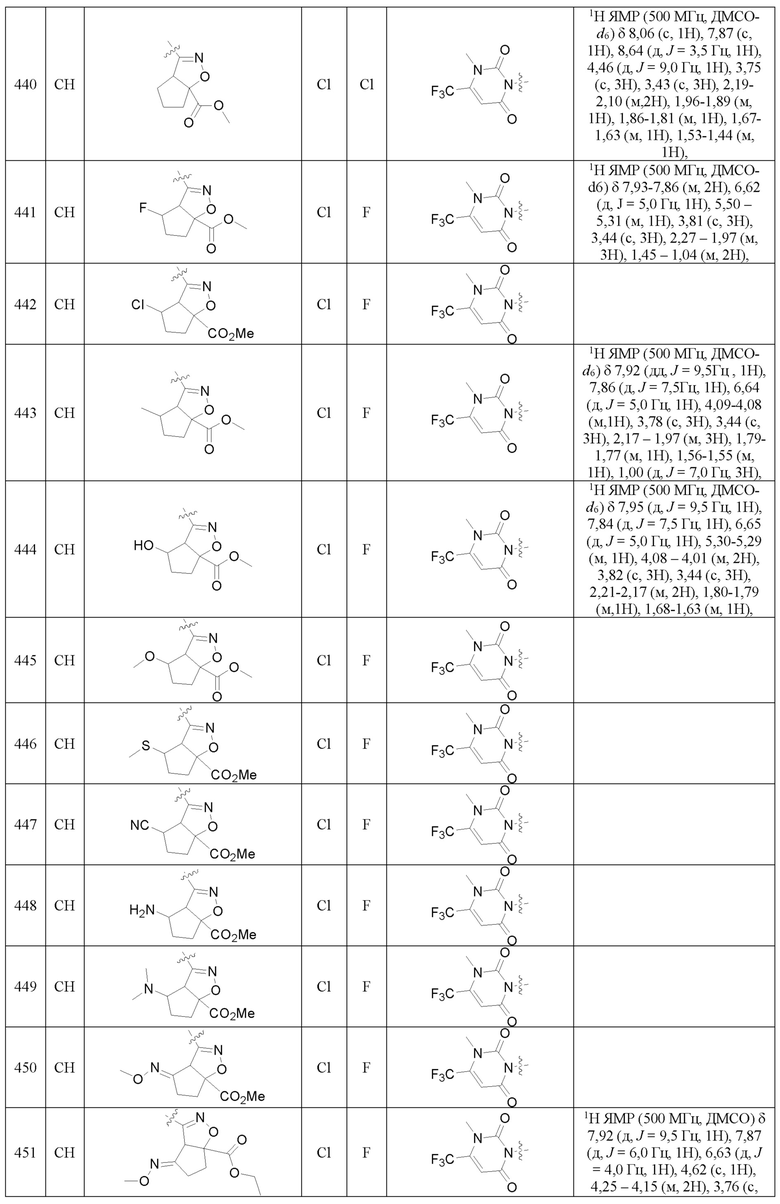
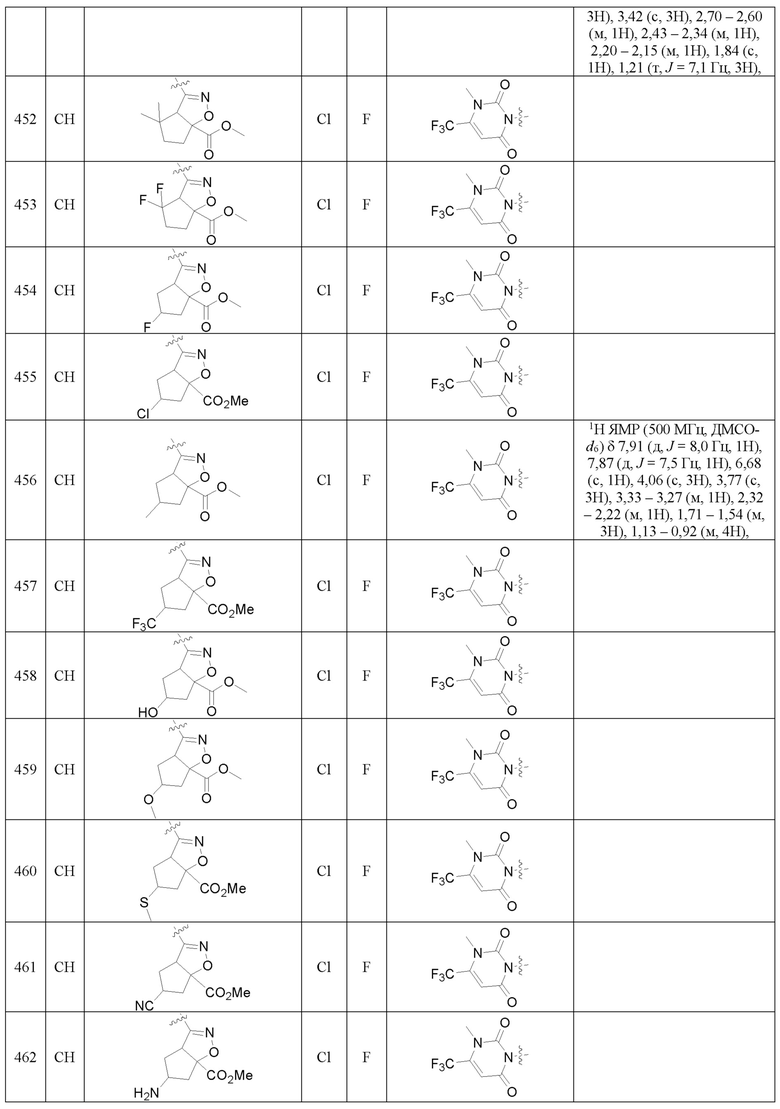
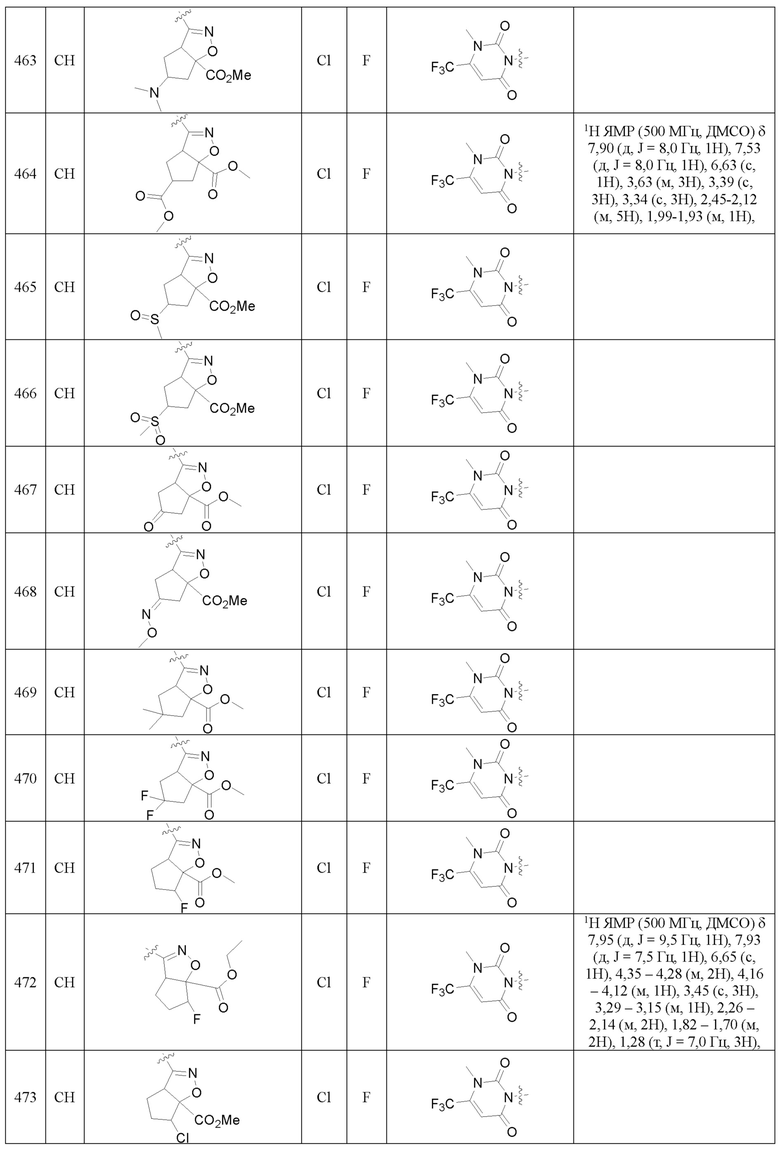
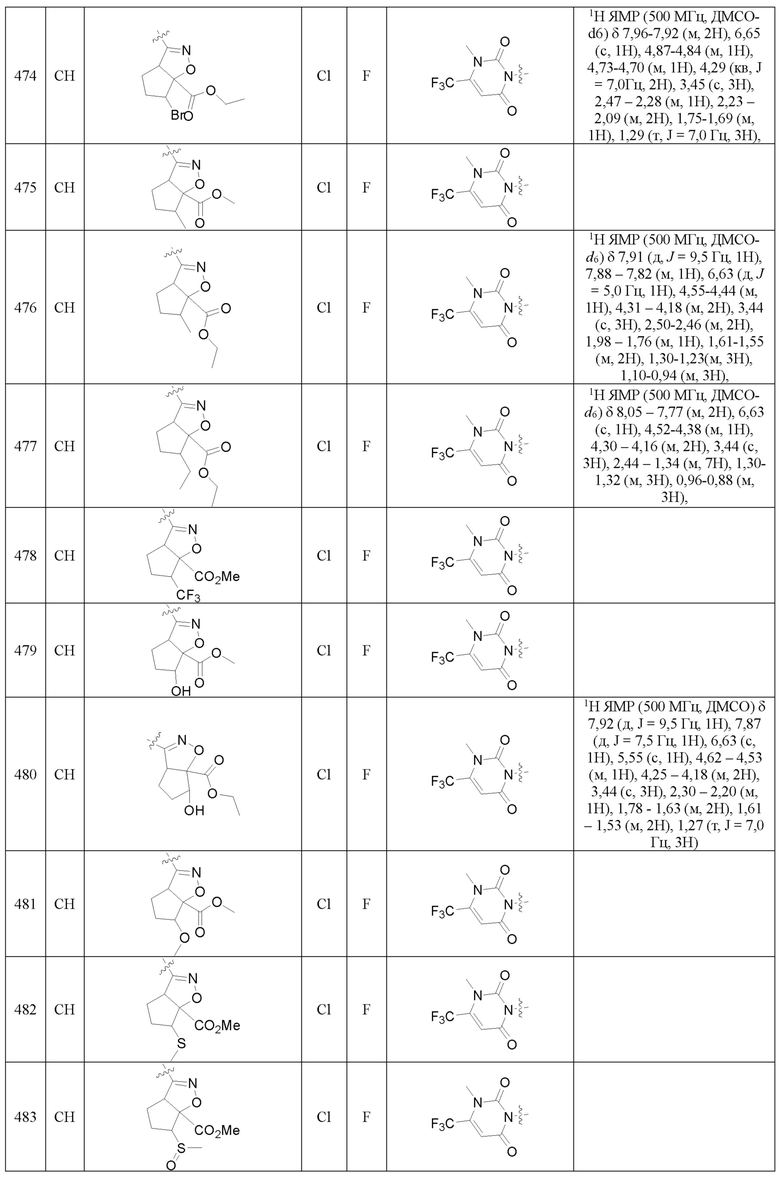
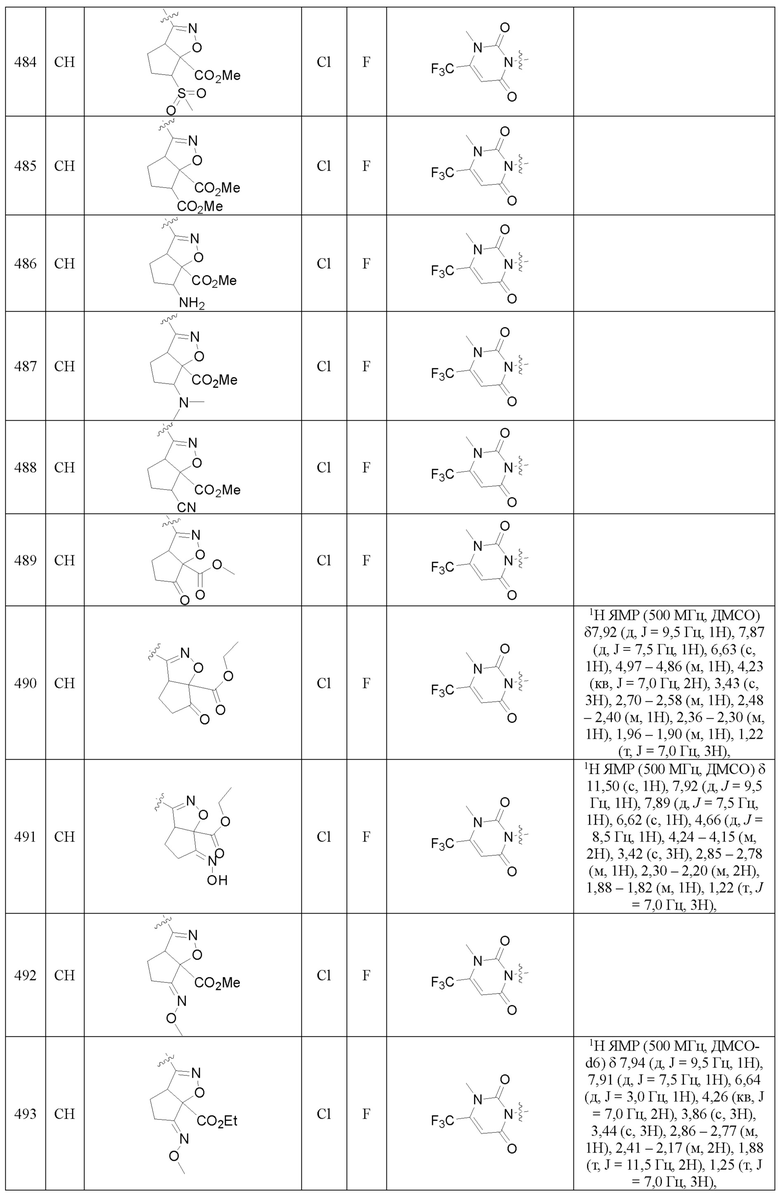

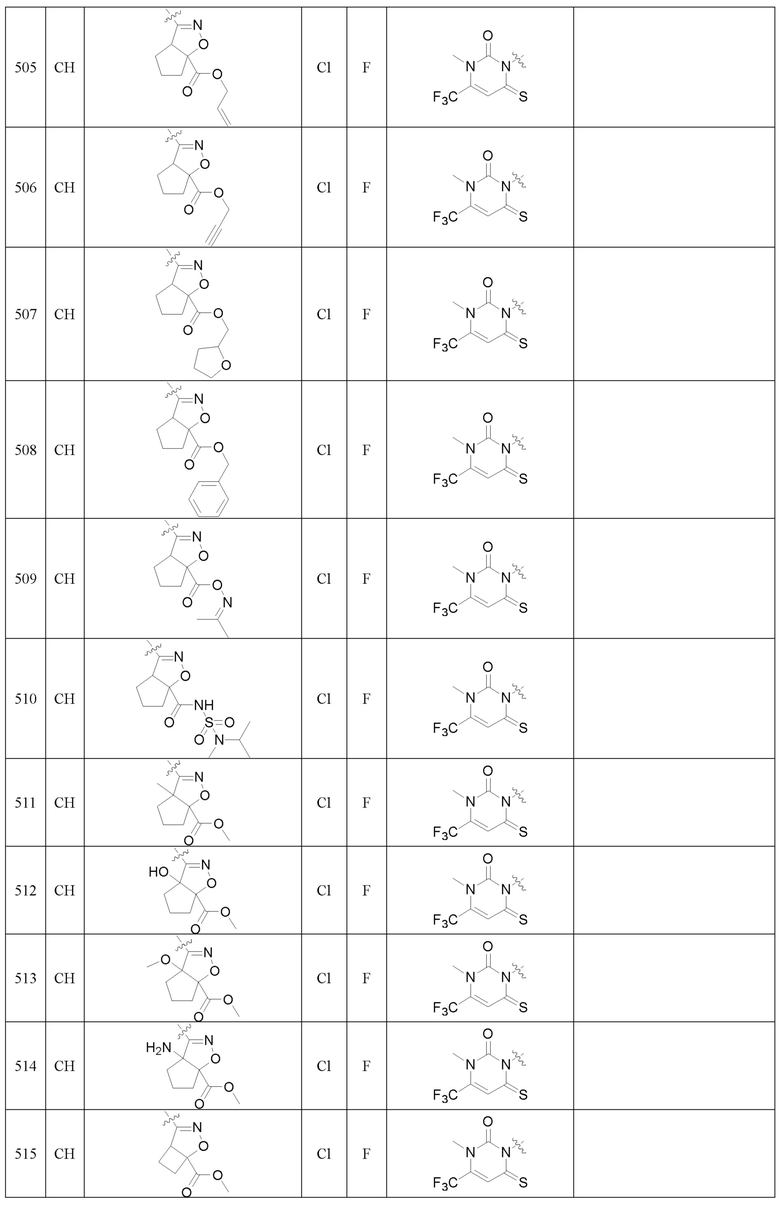
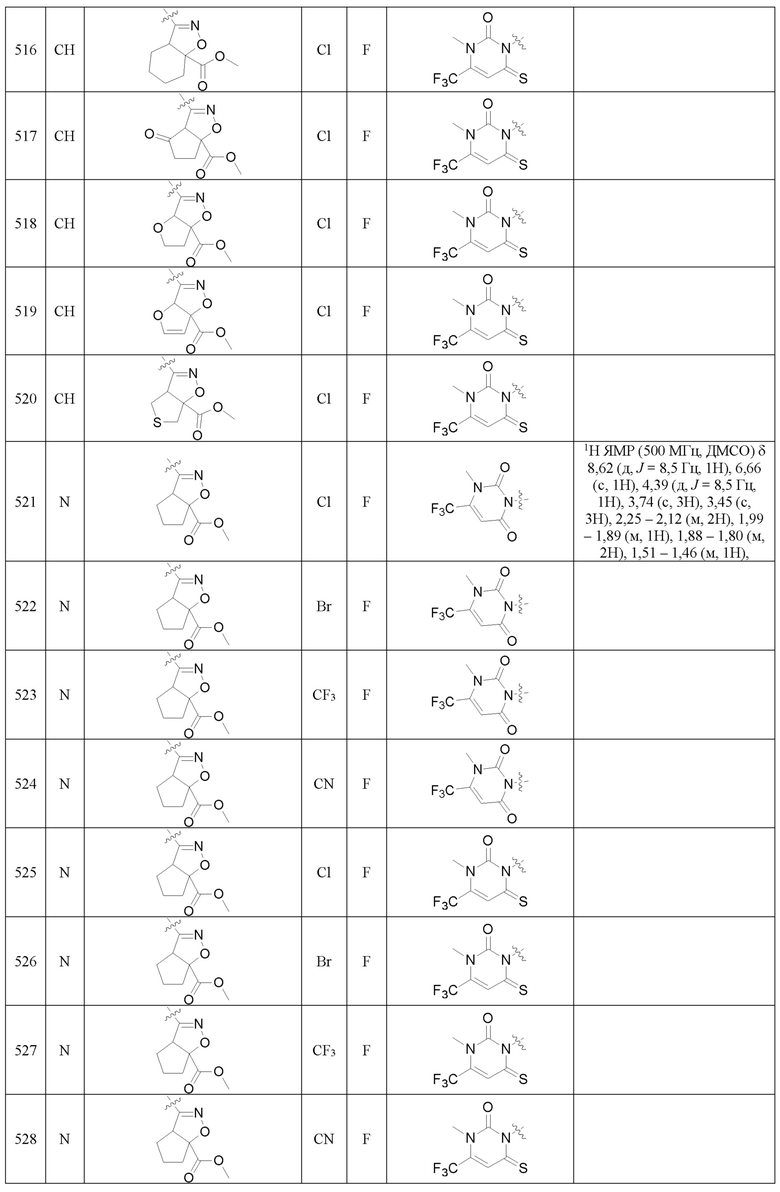
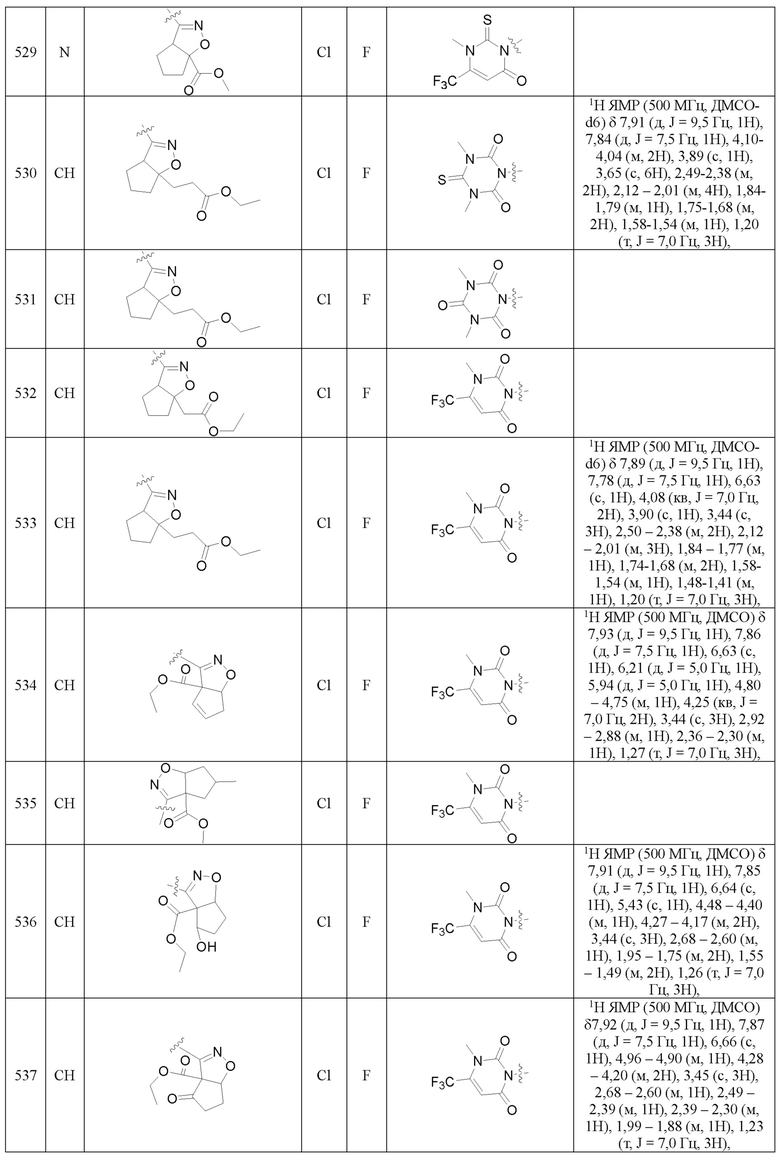
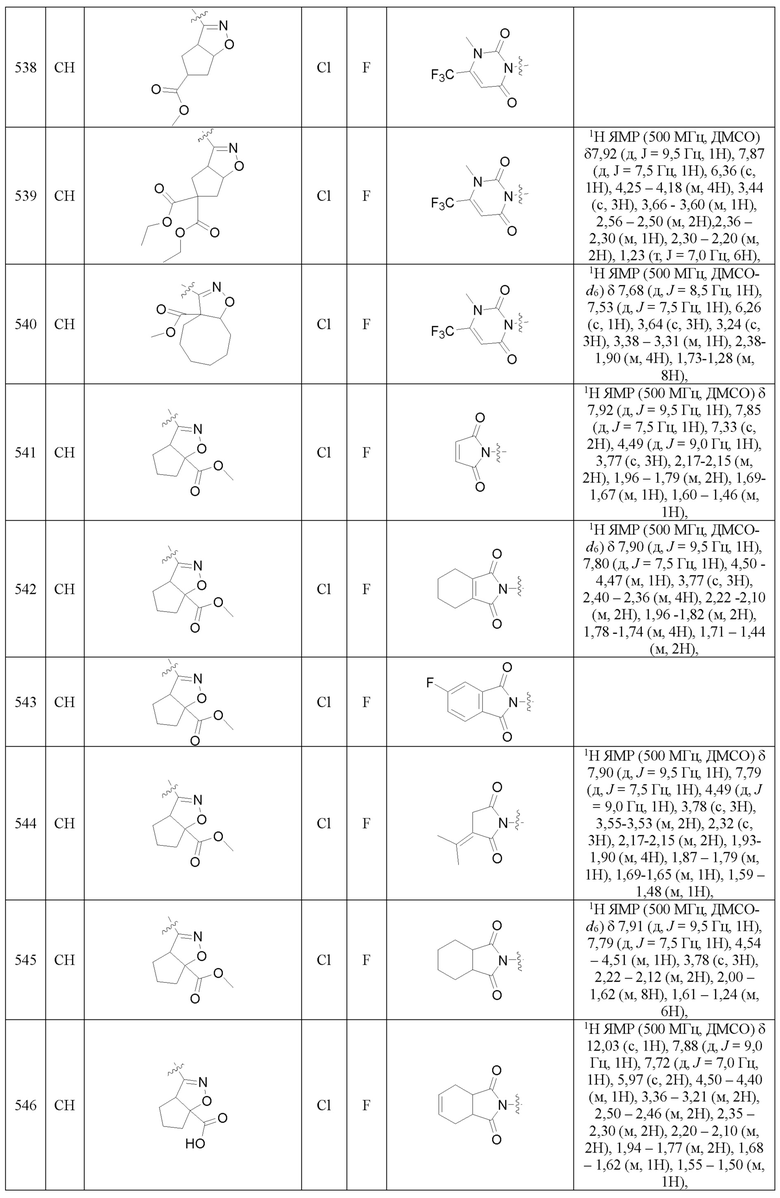
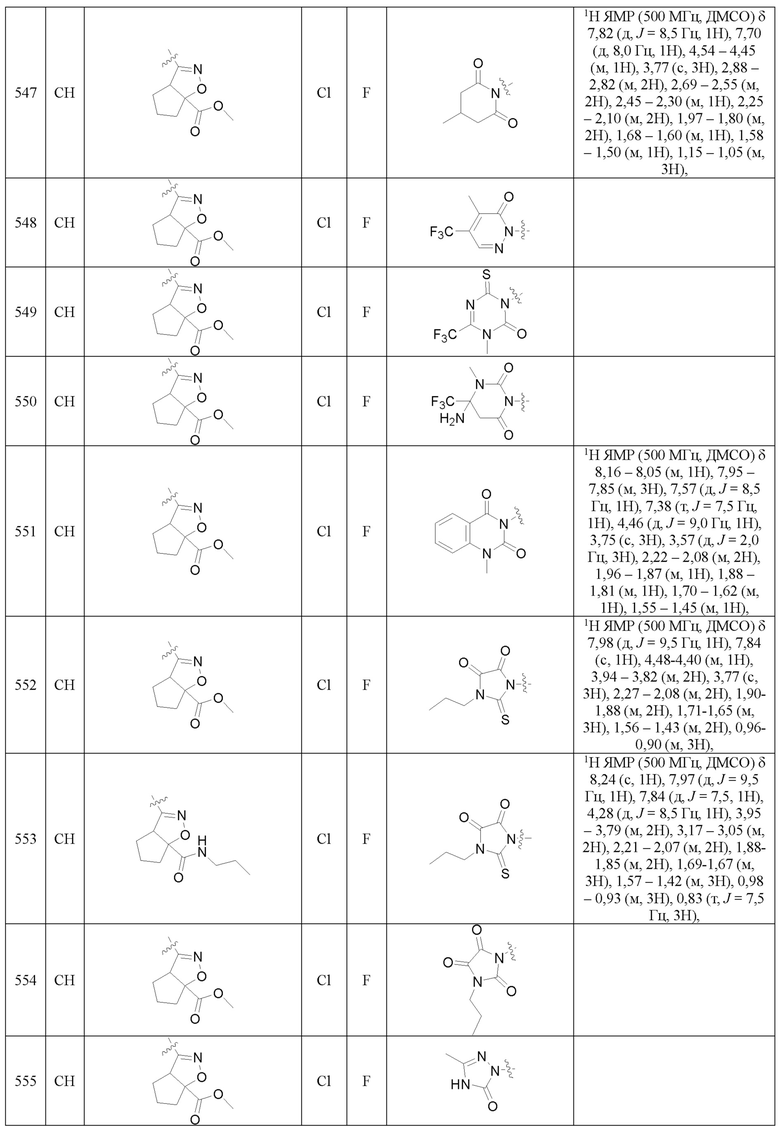
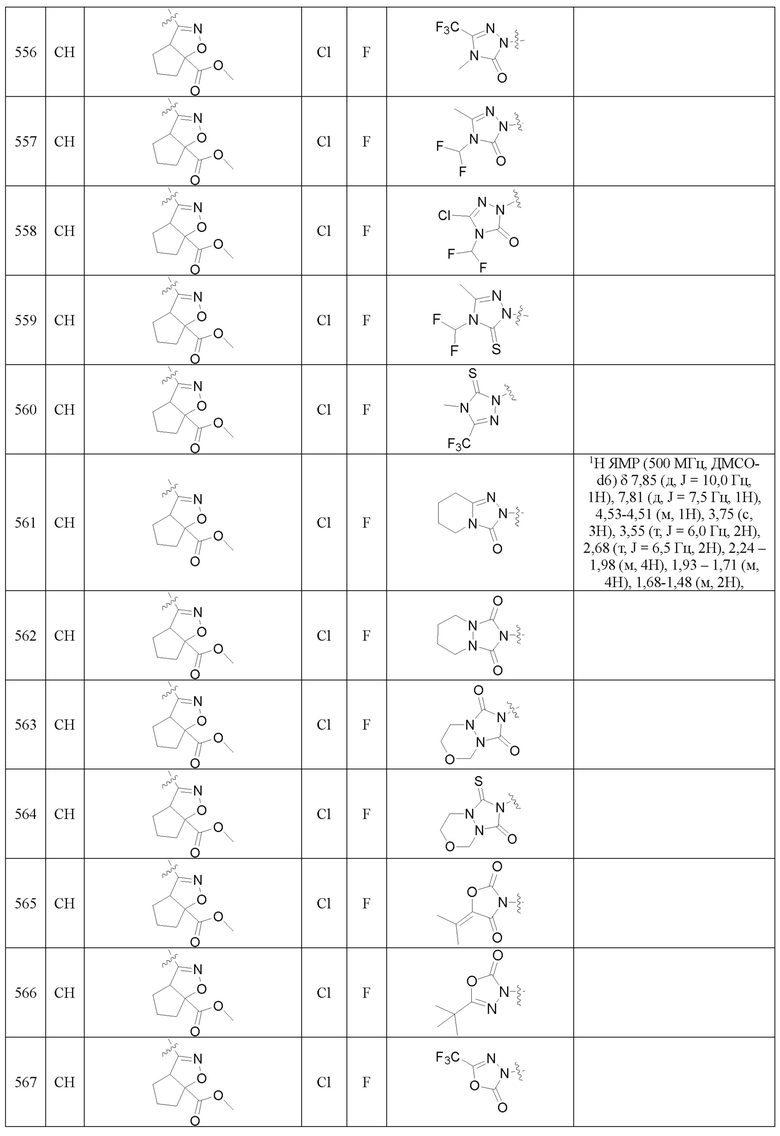
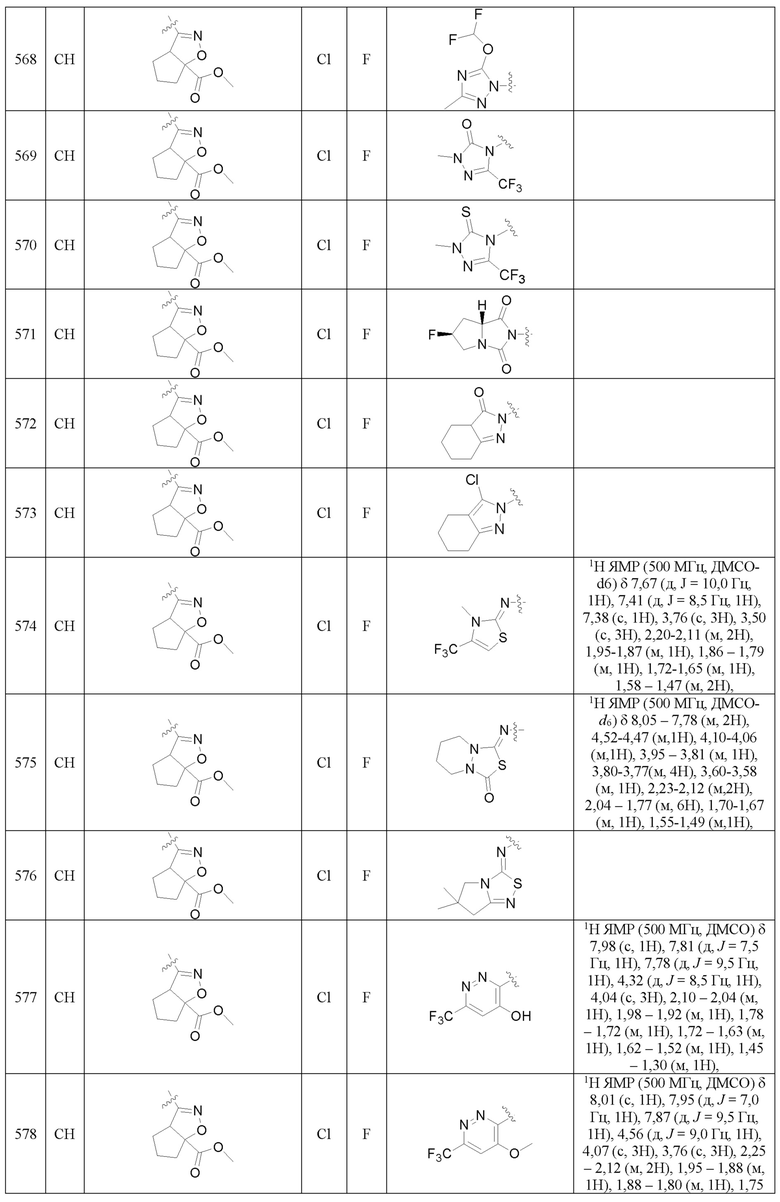
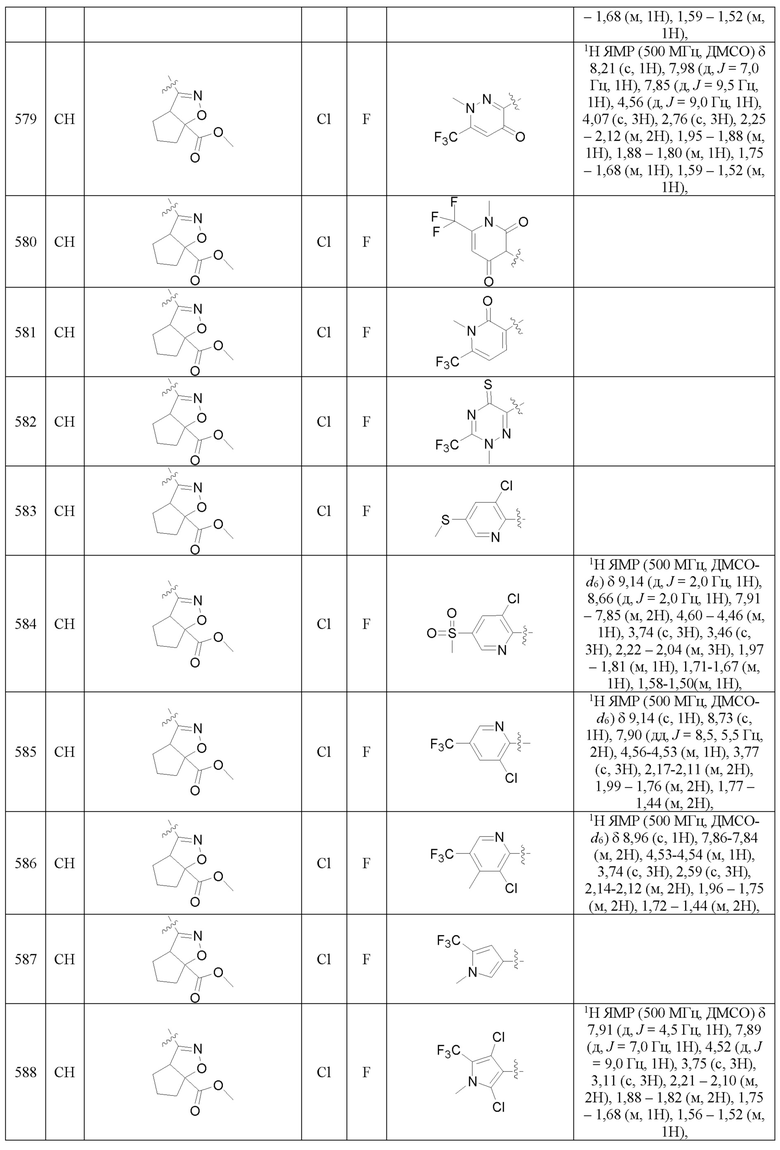
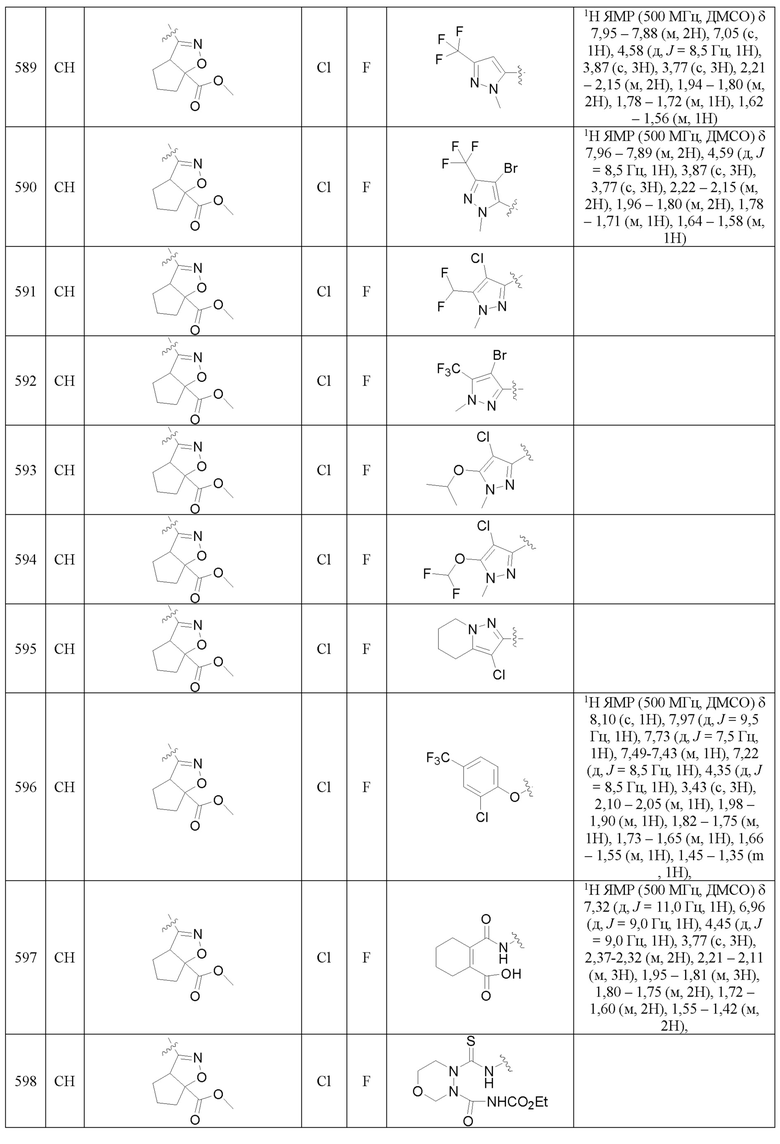
Способ получения соединения изобретения будет подробно объяснен в следующей программе и варианте осуществления. Материал коммерчески доступен или получен известным способом, описанным в литературе, или указанным в пути синтеза. Специалисты в данной области техники должны понимать, что соединение по настоящему изобретению также можно синтезировать другим путем синтеза. Хотя подробный материал и условия реакции в пути синтеза объясняются в следующем тексте, его все же легко заменить другим аналогичным материалом и условиями. Изомер соединения, например, полученный с помощью варианта способа получения настоящего изобретения, включен в объем настоящего изобретения. Кроме того, следующий способ получения может быть дополнительно модифицирован в соответствии с описанием настоящего изобретения с использованием обычного химического способа, известного специалистам в данной области техники, например, защитой подходящей группы в процессе реакции и т. д.
Следующий способ применения может быть использован для лучшего понимания способа получения по настоящему изобретению. Конкретный материал, класс и состояние были определены как дальнейшее объяснение настоящего изобретения, а не как ограничение его разумного объема. Реагенты для следующего синтеза соединения, представленного в таблице, могут быть либо приобретены у коммерческих поставщиков, либо легко получены специалистами в данной области техники.
Примеры типовых соединений представлены ниже, способы синтеза других соединений аналогичны и не будут здесь подробно описываться.
1. Синтез соединения 2
(1) Соединение 2-0 (20 г, 91,5 ммоль, 1,0 экв.) добавляют к 150 мл ДМФ, и затем NCS (13,4 г, 100,7 ммоль, 1,1 экв.) медленно добавляют к реакционному раствору при 35°C. После завершения добавления, реакционный раствор перемешивают при 35°C в течение 1,5 часов. Исходные материалы практически полностью прореагировали, по данным ЖХМС. Реакционный раствор выливают в 100 мл HCl (1 M) и затем экстрагируют дихлорметаном. Органическую фазу промывают насыщенным раствором соли (100 мл×3), и затем концентрируют с получением неочищенного продукта соединения 2-1 (26 г, неочищенный продукт) (желтое масло). Неочищенный продукт используют на следующей стадии без дальнейшей очистки.
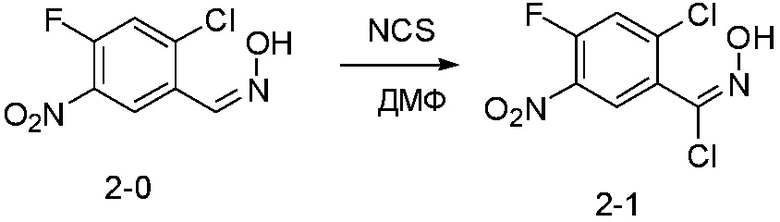
(2) Соединение 2-1 (1 г) и Et3N (600 мг, 6,0 ммоль, 1,5 экв.) добавляют к 10 мл ДХМ, и затем соединение a (605 мг, 4,8 ммоль, 1,2 экв.) добавляют к реакционному раствору при 0°C. Реакционный раствор медленно нагревают до 20°C, и подвергают взаимодействию в течение 16 часов. Продукт определяют ЖХМС. 10 мл воды добавляют к реакционному раствору, и затем реакционный раствор экстрагируют дихлорметаном (10 мл×3). Органическую фазу сушат с безводным сульфатом натрия и затем концентрируют. Полученный неочищенный продукт выделяют и очищают колоночной хроматографией с получением соединения 2-2 (400 мг, 1,2 ммоль, выход: 30%).
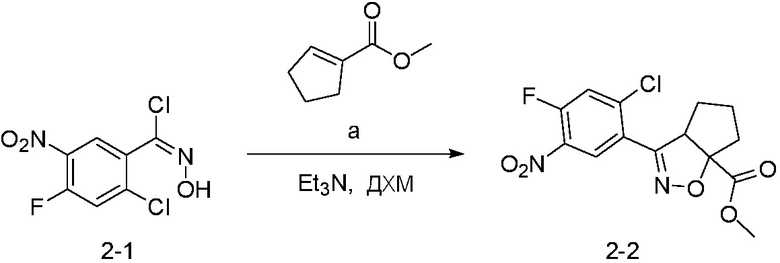
(3) Соединение 2-2 (400 мг, 1,2 ммоль, 1,0 экв.), порошок Fe (202 мг, 3,6 ммоль, 3 экв.), NH4Cl (127 мг, 2,4 ммоль, 2 экв.) и воду (1 мл) добавляют к 5 мл EtOH последовательно. Затем, реакционный раствор подвергают взаимодействию при 80°C в течение 2 часов. ЖХМС показала, что пики исходного сырья в ЖХМС хроматограмме исчезли, и основной пик в хроматограмме принадлежит продукту. После охлаждения, реакционный раствор фильтруют с целитом и затем концентрируют удалением этанола. Воду (10 мл) добавляют к реакционному раствору. Реакционный раствор экстрагируют этилацетатом и затем концентрируют с получением черного неочищенного продукта. Неочищенный продукт выделяют и очищают колоночной хроматографией с получением соединения 2-3 (300 мг, 0,96 ммоль, выход: 80%).
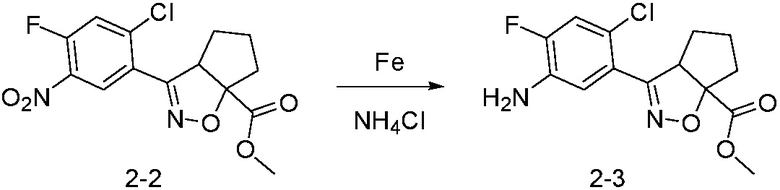
(4) Соединение 2-3 (0,3 г, 0,96 ммоль, 1,0 экв.) и соединение b (165 мг, 1,06 ммоль, 1,1 экв.) растворяют в 5 мл диоксана. Реакционный раствор нагревают при 110°C в течение 30 минут. ЖХМС показала, что реакция исходного материала в основном завершена, и основной пик ЖХМС хроматограммы принадлежит продукту. Реакционный раствор концентрируют удалением растворителя. Полученный неочищенный продукт выделяют колоночной хроматографией с получением соединения 2-4 (0,4 г, 0,92 ммоль, выход: 96%).
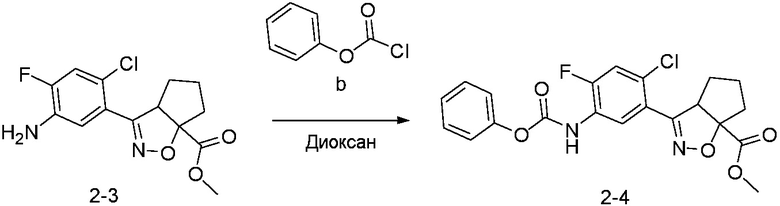
(5) Соединение c (217 мг, 0,97 ммоль, 1,05 экв.) и AcONa (38 мг, 0,46 ммоль, 0,5 экв.) добавляют к 3 мл ДМФ, и затем соединение 2-4 (0,4 г, 0,92 ммоль, 1,0 экв.) медленно добавляют к реакционному раствору при 60°C, затем подвергают взаимодействию при 60°C в течение 10 минут. Продукт определяют ЖХМС. Воду (10 мл) добавляют к реакционному раствору, и затем реакционный раствор экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли (20 мл х 1), и затем концентрируют. Полученный неочищенный продукт выделяют колоночной хроматографией с получением соединения 2 (0,3 г, 0,64 ммоль, выход: 70%).
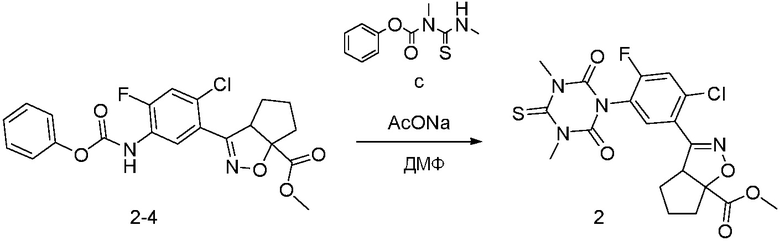
2. Синтез соединения 49
В 50 мл бутылку в форме баклажана, соединение 2 (1,0 экв., 100 мг) растворяют в соединении 49-1 (5V), к которому добавляют тетраизопропил титанат (20% моль). Реакционный раствор подвергают взаимодействию при 80°C в течение 1-2 часов. ЖХМС показала, что пики исходных материалов в ЖХМС хроматограмме исчезли, и основной пик в хроматограмме принадлежит продукту. Реакционный раствор смешивают непосредственно с силикагелем. Неочищенный продукт выделяют и очищают колоночной хроматографией с получением соединения 49 (31 мг, выход: 22%) (светло-желтое твердое вещество).
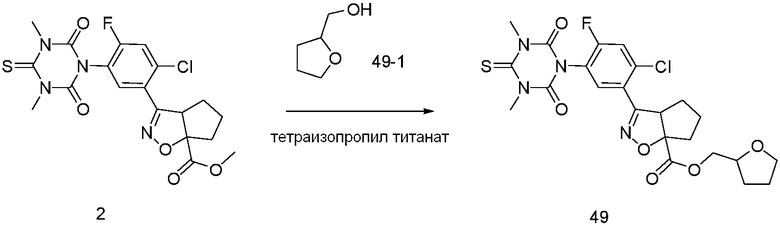
3. Синтез соединения 209
(1) Соединение 2-3 (1,0 экв.) и исходное соединение 210-7 (1,0 экв.) добавляют к 10V уксусной кислоты. Реакционный раствор подвергают взаимодействию при 125°C в течение 1 часа, с последующим роторным испарением для удаления карбоновой кислоты. Полученный продукт применяют на следующей стадии без дальнейшей очистки.
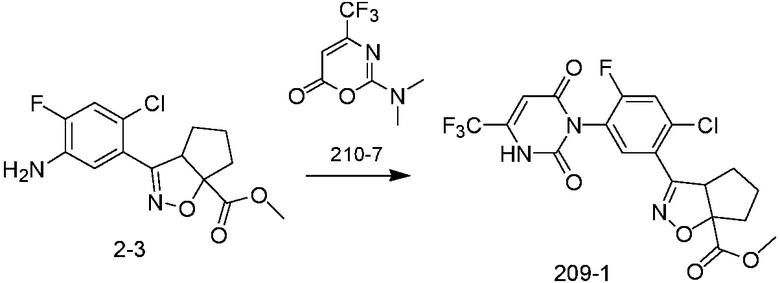
(2) Соединение 209-1 (1,0 экв.), метилйодид (4,0 экв.) и K2CO3 (2,0 экв.) добавляют к 5V ДМФ последовательно. Затем, реакционный раствор подвергают взаимодействию при 25-30°C в течение 16 часов, реакция завершается по данным ЖХМС. Воду добавляют к реакционному раствору, и затем реакционный раствор экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли, и затем выделяют колоночной хроматографией с получением соединения 209 (выход: 30%).
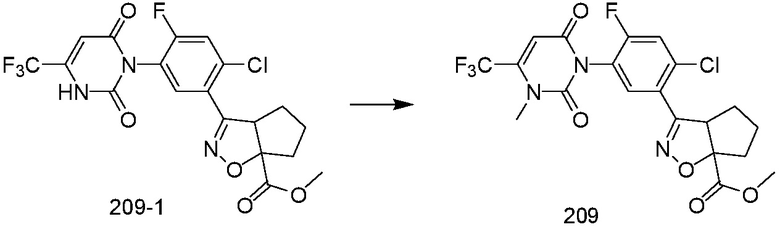
4. Синтез соединений 210 и 212
(1) При 0°C, дымящую азотную кислоту (18,62 г, 0,296 моль, 3 экв.) постепенно добавляют к концентрированной серной кислоте (87 г, 0,887 моль, 9 экв.). После завершения добавления, при 0°C, соединение 210-1 (20 г, 98,52 ммоль, 1 экв.) добавляют к полученному выше раствору партиями. Затем, реакционный раствор подвергают взаимодействию при 0°C в течение 8 часов. Как определено ЖХМС, остается небольшое количество исходных материалов, и появляется один новый основной пик. Реакционный раствор медленно добавляют к смеси льда и воды, и экстрагируют этилацетатом. Органическую фазу промывают насыщенным бикарбонатом натрия пока он не станет слабощелочным, сушат над безводным сульфатом натрия, концентрируют, и затем соединение 210-2 выделяют колоночной хроматографией (16 г, выход: 65%).
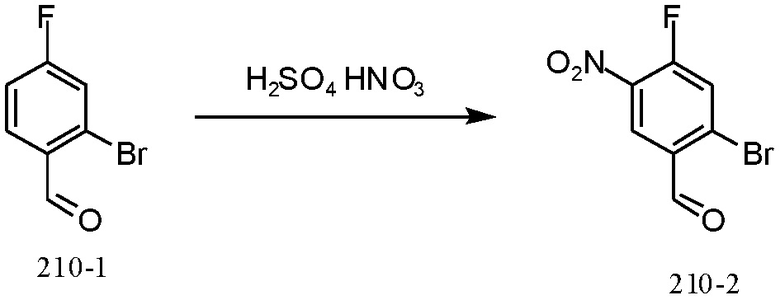
(2) Соединение 210-2 (16 г, 64,5 ммоль, 1,0 экв.) добавляют к 160 мл EtOH, и затем водный раствор (20 мл), содержащий NH2OHHCl (4,93 г, 70,97 ммоль, 1,1 экв.), по каплям добавляют к реакционному раствору при 0°C. После завершения добавления, реакционный раствор перемешивают при 0°C в течение 3 часов. ЖХМС показала, что исходные материалы практически израсходованы, и новый основной пик появился на ЖХМС хроматограмме. Реакционный раствор концентрируют для удаления большей части этанола и затем выливают в 100 мл воды для осаждения твердого вещества. После фильтрации, фильтровальную лепешку промывают водой и сушат с получением соединения 210-3 (15 г, выход: 88%).

(3) Соединение 210-3 (10 г, 38,02 ммоль, 1,0 экв.) добавляют к 150 мл ДМФ, и затем NCS (5,58 г, 41,82 ммоль, 1,1 экв.) медленно добавляют к реакционному раствору при 35°C. После завершения добавления, реакционный раствор перемешивают при 35°C в течение 2 часов. Реакция исходных материалов в основном завершена, как определено ЖХМС. Реакционный раствор выливают в 100 мл воды и экстрагируют дихлорметаном. Органическую фазу промывают насыщенным раствором соли (100 мл х 3), и затем концентрируют с получением неочищенного продукта соединения 210-4 (11 г, выход: 97%). Неочищенный продукт используют на следующей стадии без дальнейшей очистки.
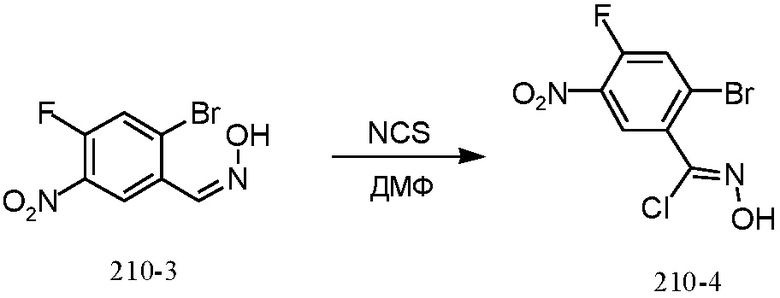
(4) Соединение 210-4 (11 г, 36,98 ммоль, 1,0 экв.) и Et3N (5,61 г, 55,47 ммоль, 1,5 экв.) добавляют к 200 мл ДХМ, и затем соединение a (5,13 г, 40,68 ммоль, 1,1 экв.) добавляют к реакционному раствору при 0°C. Реакционный раствор подвергают взаимодействию при 0°C в течение 1 часа, и затем медленно нагревают до комнатной температуры, и подвергают взаимодействию при комнатной температуре в течение ночи. Образуется продукт, как определено ЖХМС. 100 мл воды добавляют к реакционному раствору, и затем реакционный раствор экстрагируют дихлорметаном (100 мл х 3). Органическую фазу сушат над безводным сульфатом натрия и затем концентрируют. Полученный неочищенный продукт очищают колоночной хроматографией с получением соединения 210-5 (4,7 г, выход: 32%).

(5) Соединение 210-5 (4,7 г, 12,14 ммоль, 1,0 экв.), порошок Fe (2,03 г, 36,42 ммоль, 3 экв.), NH4Cl (1,95 г, 36,42 ммоль, 3 экв.) и воду (50 мл) добавляют к 200 мл EtOH последовательно. Затем, реакционный раствор подвергают взаимодействию при 80°C в течение 1 часа. ЖХМС показала, что исходные материалы израсходованы, и основной пик на ЖХМС хроматограмме принадлежит продукту. Реакционный раствор фильтруют с целитом и затем концентрируют для удаления этанола. Воду (100 мл) добавляют к реакционному раствору, и затем реакционный раствор экстрагируют этилацетатом. Органическую фазу концентрируют с получением соединения 210-6 (4,2 г, выход: 96%).
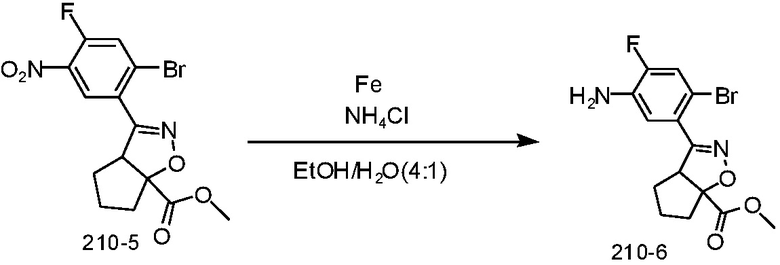
(6) Соединение 210-6 (4,25 г, 11,9 ммоль, 1,0 экв.) и соединение 210-7 (2,48 г, 11,9 ммоль, 1,0 экв.) добавляют к 50 мл уксусной кислоты. Реакционный раствор подвергают взаимодействию при 125°C в течение 0,5-1 часа. ЖХМС показала что реакция исходного материала в основном завершена, и основной пик ЖХМС хроматограммы принадлежит продукту. Реакционный раствор концентрируют для удаления растворителя с получением неочищенного продукта соединения 210-8 (9 г).
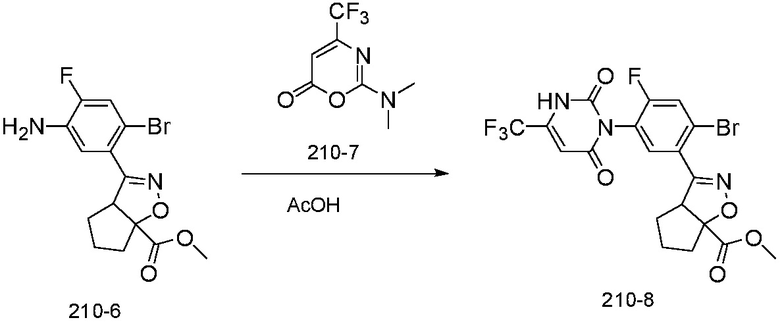
(7) Соединение 210-8 (9 г, 17,30 ммоль, 1,0 экв.) и K2CO3(7,17 г, 51,9 ммоль, 3 экв.) добавляют к 100 мл ДМФ последовательно, туда добавляют по каплям метилйодид (7,37 г, 51,9 ммоль, 3 экв.) при комнатной температуре. Затем, реакционный раствор подвергают взаимодействию при 35°C в течение 3 часов. Молекулярную массу продукта определяют ЖХМС, и пики исходных материалов на ЖХМС хроматограмме почти исчезли. Реакционный раствор экстрагируют этилацетат и водой. Органическую фазу промывают три раза насыщенным водным раствором хлорида натрия, сушат и концентрируют, и очищают колоночной хроматографией с получением соединения 210 (2 г, красное твердое вещество).
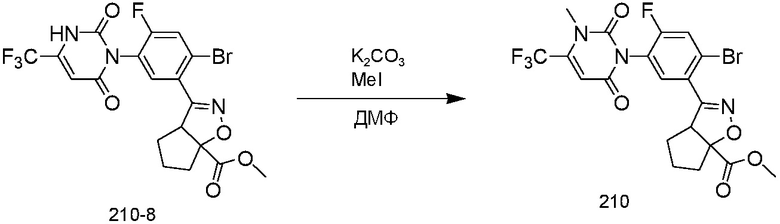
(8) 10 мл ДМФ, соединение 210 (0,5 г, 0,3935 ммоль, 1,0 экв.), CuCN (167,6 мг, 1,87 ммоль, 2 экв.) последовательно добавляют в микроволновую пробирку, содержащую 20 мл ДМФ, и под защитой N2, реакцию проводят с микроволнами при 150°C в течение 1 часа. Реакция исходных материалов в основном завершена, как определено ЖХМС, и основные пики в ЖХМС хроматограмме принадлежит продукту. Реакционный раствор экстрагируют этилацетатом и водой. Органическую фазу промывают три раза насыщенным водным раствором хлорида натрия, сушат и концентрируют, и очищают колоночной хроматографией с получением соединения 212 (0,1 г, выход: 22%).
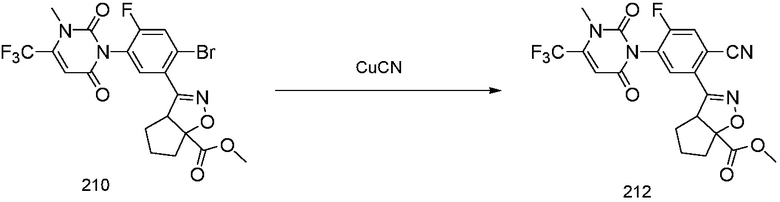
5. Синтез соединения 372
(1) Соединение 2-1 (1,0 экв.) и дихлорметан в качестве растворителя (10 V) загружают в 50 мл бутылку, к которой добавляют по каплям триэтиламин (1,5 экв.), и затем добавляют соединение 372-1 (1,1 экв.) в условиях бани с ледяной водой. Полученный раствор нагревают до комнатной температуры, и подвергают взаимодействию при перемешивании в течение ночи. После завершения реакции, реакционный раствор промывают водой. Органическую фазу собирают, смешивают с силикагелем и отправляют на разделение (ДХМ:MeOH), с получением соединения 372-2, выход: 42%.
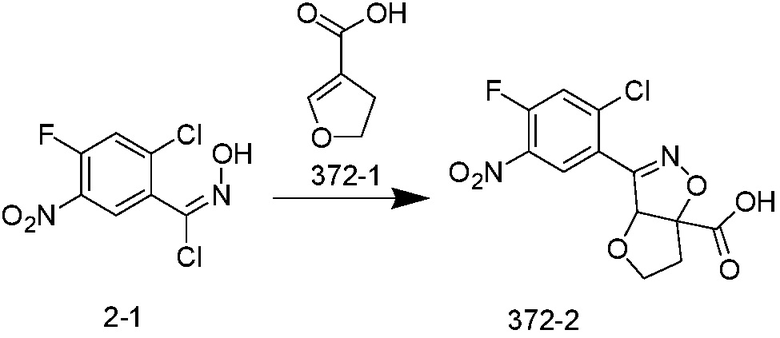
(2) Соединение 372-2 (1,0 экв.), полученное на предыдущей стадии, дихлорметан в качестве растворителя (5V) и ДМФ (10% моль) в каталитическом количестве загружают в 50 мл бутылку, в которую добавляют по каплям тионилхлорид (2,0 экв.) в условиях водяной бани. После завершения добавления, реакционный раствор нагревают до кипения с обратным холодильником в течение 2 ч. После завершения реакции, растворитель и избыток тионилхлорида удаляют при пониженном давлении. Остаток растворяют в дихлорметане (5V), к которому добавляют по каплям метанол (10,0 экв.), затем нагревают до кипения с обратным холодильником. После завершения реакции, растворитель и метанол удаляют при пониженном давлении. Остаток растворяют в этилацетате и промывают насыщенным раствором соли. Органическую фазу собирают, смешивают с силикагелем и отправляют на разделение, с получением соединения 372-3, (выход: 85%).
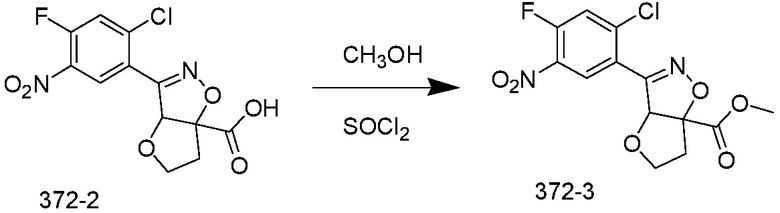
(3) Соединение 372-3, полученное на предыдущей стадии, этанол и воду (5:1) в качестве растворителя, порошок Fe (3,0 экв.), и хлорид аммония (2,0 экв.) загружают в 50 мл бутылку. Реакционный раствор нагревают до 80°C и подвергают взаимодействию при перемешивании в течение 1 ч. После завершения реакции, реакционный раствор фильтруют с целитом, и фильтрат собирают и концентрируют роторным испарением. Остаток растворяют в этилацетате и промывают насыщенным раствором соли. Органическую фазу собирают, сушат и концентрируют роторным испарением, с получением соединения 372-4, (выход: 40%).
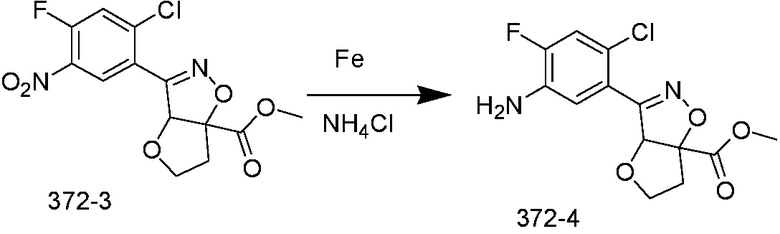
(4) Соединение 372-4, полученное на предыдущей стадии, уксусную кислоту (10 об.) в качестве растворителя, и соединение циклического лактона 210-7 (1,1 экв.) загружают в 50 мл бутылку. Полученный раствор нагревают до 125°C для проведения реакции в течение 0,5 часов. После завершения реакции, растворитель удаляют роторным испарением при пониженном давлении, и остаток растворяют в ДМФ и откладывают для дальнейшего применения.
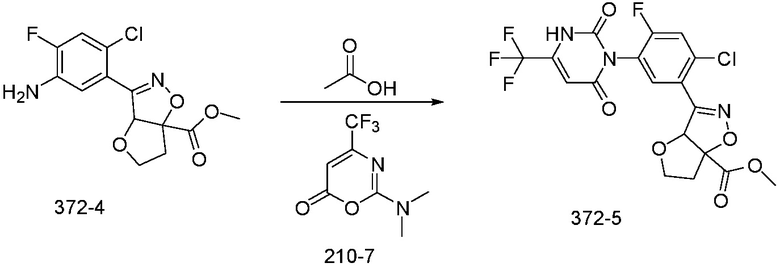
(5) Метилйодид (3,0 экв.) и безводный карбонат калия (5,0 экв.) добавляют непосредственно в реакционную бутылку с предыдущей стадии. Затем реакционный раствор подвергают взаимодействию при 30°C в течение ночи. После завершения реакции, воду добавляют к реакционному раствору для разбавления, и затем реакционный раствор экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли, собирают, смешивают с силикагелем и отправляют на разделение, с получением соединения 372, (выход: 32%).
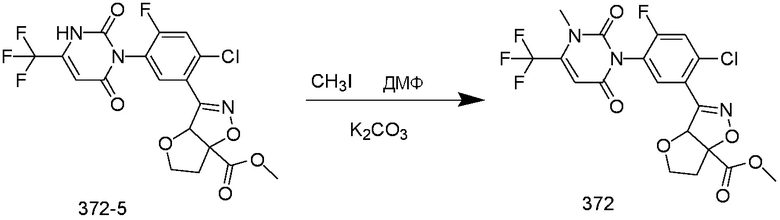
6. Синтез соединения 521
Со ссылкой на способ со стадий (2) и (3) пункта 4, описанного выше, соединение 521-1 получают из 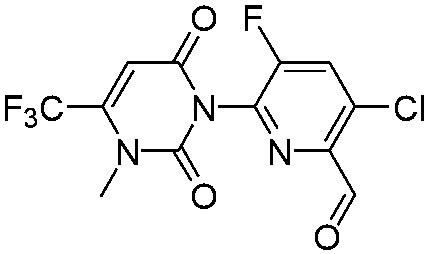 , и затем соединение 521-1 (0,4 г, 1 ммоль, 1,0 экв.), соединение a (0,126 г, 1 ммоль, 1,0 экв.) и ТЭА (0,202 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл ДХМ. Затем полученный раствор подвергают взаимодействию при комнатной температуре при перемешивании в течение 2 часов. Завершение реакции определяют с применением ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением соединения 521 (0,245 г, выход: 50%) (белое масло).
, и затем соединение 521-1 (0,4 г, 1 ммоль, 1,0 экв.), соединение a (0,126 г, 1 ммоль, 1,0 экв.) и ТЭА (0,202 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл ДХМ. Затем полученный раствор подвергают взаимодействию при комнатной температуре при перемешивании в течение 2 часов. Завершение реакции определяют с применением ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением соединения 521 (0,245 г, выход: 50%) (белое масло).
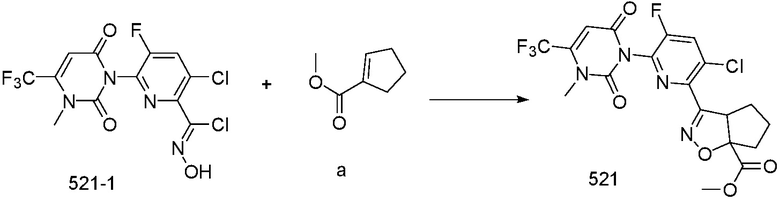
7. Синтез соединения 533
(1) Йодид триметилсеры (4 экв.) и ТГФ в качестве растворителя (10 об.) загружают в 100 мл трехгорлую колбу, температуру снижают до -20°C, и затем, под защитой азота по каплям добавляют н-бутиллитий (3,3 экв.). После завершения добавления, реакционный раствор перемешивают в условиях теплоизоляции в течение 30 мин, затем туда добавляют по каплям раствор 1,2-эпоксициклопентана (соединение 533-1) в ТГФ. После завершения добавления, реакционный раствор медленно нагревают до комнатной температуры в течение 1 ч, и перемешивают при комнатной температуре в течение 2 ч. После завершения реакции, реакционный раствор гасят водой и затем экстрагируют этиловым эфиром. Органическую фазу собирают, промывают насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют, и концентрируют до примерно 10 мл, и откладывают для дальнейшего применения.
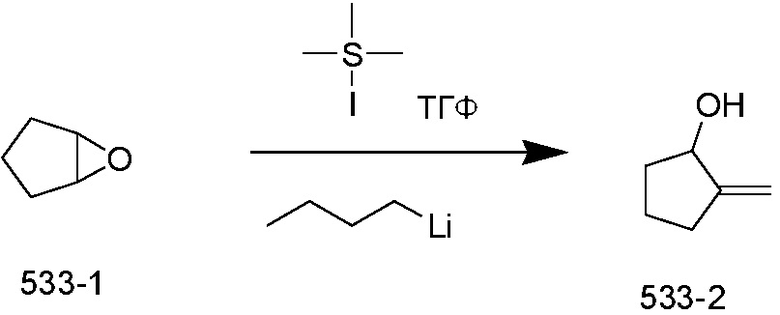
(2) Триэтилортоацетат (5,38 экв.) и пропионовую кислоту (0,26 экв.) загружают в колбу с предыдущей стадии, затем нагревают до 145°C. Реакционный раствор подвергают взаимодействию в открытых условиях для выпаривания образовавшегося этанола. Затем этанол удаляют, реакционный раствор хранят при 145°C и подвергают взаимодействию при перемешивании в течение 1 ч. После завершения реакции, реакционный раствор охлаждают до комнатной температуры, разбавляют добавлением этилового эфира, и затем подвергают взаимодействию с 1M KHSO4 (30 мл) при перемешивании в течение ночи. Органическую фазу выделяют, и водную фазу экстрагируют этиловым эфиром. Органические фазы объединяют, промывают насыщенным бикарбонатом натрия, собирают, сушат над безводным сульфатом натрия и выпаривают на роторном испарителе, с получением соединения 533-3. Полученный продукт применяют на следующей стадии без дальнейшей очистки.
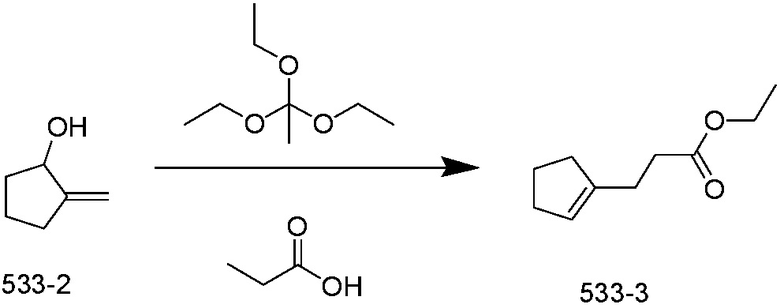
(3) Соединение 2-1 (1,0 экв.) и дихлорметан в качестве растворителя (5 об.) загружают в 50 мл бутылку. В условиях бани с ледяной водой, триэтиламин (2 экв.) и затем 533-3 (1,2 экв.) добавляют по каплям. Полученный раствор нагревают до комнатной температуры, и подвергают взаимодействию при перемешивании в течение ночи. После завершения реакции, реакционный раствор промывают водой. Органическую фазу собирают, смешивают с силикагелем и отправляют на разделение, с получением соединения 533-4.
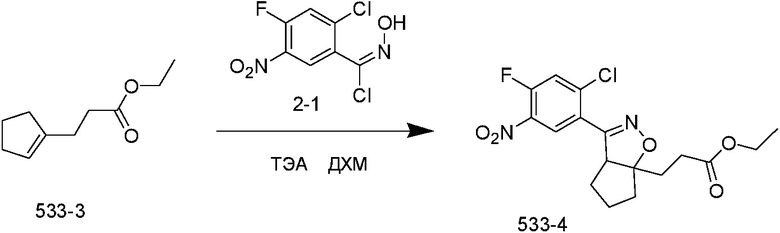
(4) Соединение 533-4 (1,0 экв.), полученное на предыдущей стадии, смешанный растворитель этанола и воды (5:1), порошок Fe (3 экв.) и хлорид аммония (2 экв.) загружают в 50 мл бутылку. Полученный раствор нагревают до 80°C и подвергают взаимодействию при перемешивании в течение 1 ч. После завершения реакции, реакционный раствор фильтруют с целитом, и фильтрат собирают и выпаривают на роторном испарителе. Остаток растворяют с этилацетатом и промывают насыщенным раствором соли. Органическую фазу собирают, сушат и выпаривают на роторном испарителе, с получением соединения 533-5.
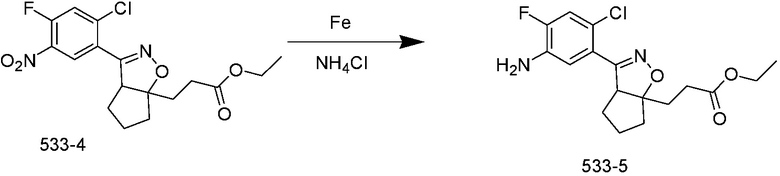
(5) Соединение 533-5 (1,0 экв.), полученное на предыдущей стадии, уксусную кислоту в качестве растворителя (10 об.) и соединение 210-7 (1,1 экв.) загружают в 50 мл бутылку. Полученный раствор нагревают до 125°C для проведения реакции в течение 0,5 часов. После завершения реакции, реакционный раствор выпаривают на роторном испарителе при пониженном давлении для удаления растворителя. Остаток растворяют в ДМФ и откладывают для дальнейшего применения.
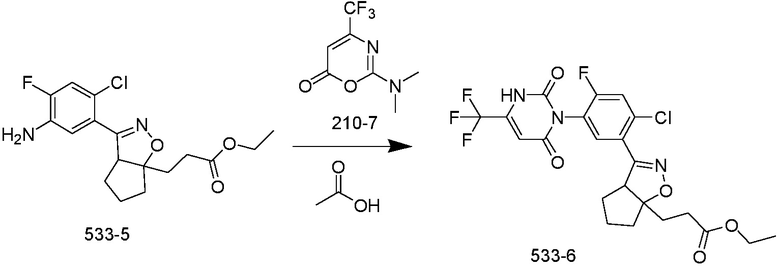
(6) Метилйодид (3,0 экв.) и безводный карбонат калия (5 экв.) прямо добавляют в колбу с предыдущей стадии. Затем реакционный раствор подвергают взаимодействию при 30°C в течение ночи. После завершения реакции, в реакционный раствор добавляют воду для разбавления и экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли, собирают, смешивают с силикагелем и отправляют на разделение, с получением соединения 533.
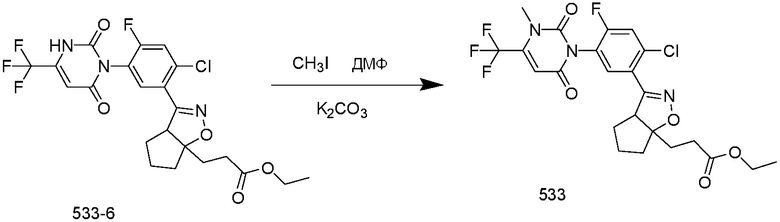
8. Синтез соединений 541 и 544
(1) Соединения 2-3 и 541-1 (2,0 экв.) добавляют к 20 мл уксусной кислоты. Реакционный раствор подвергают взаимодействию при 125°C в течение 15 часов. ЖХМС показала что реакция исходного материала в основном завершена, и основной пик на ЖХМС хроматограмме принадлежит продукту. Реакционный раствор концентрируют для удаления растворителя. Полученный неочищенный продукт отделяют колоночной хроматографией с получением соединения 541 (выход: 54%).
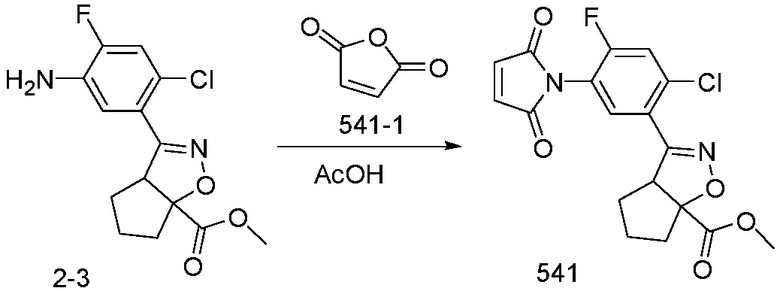
(2) Соединение 541, нитроизопропан (1,5 экв.) и ТЭА (1,5 экв.) добавляют к 20 мл ДХМ. Затем полученный раствор подвергают взаимодействию при комнатной температуре в течение 10 минут. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Полученный неочищенный продукт смешивают непосредственно с силикагелем, и очищают колоночной хроматографией с получением соединения 544 (желтое твердое вещество), выход 56%.
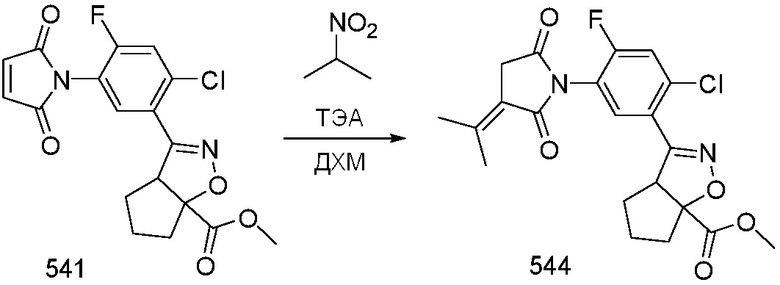
9. Синтез соединения 545
Соединение 2-3 (1,0 экв.), соединение 545-1 (2,0 экв.) и ледяную уксусную кислоту загружают в одногорлую колбу. Реакционный раствор нагревают до 125°C, и перемешивают в течение 3 часов. ЖХМС показала что реакция исходного материала в основном завершена. Реакционный раствор выпаривают на роторном испарителе для удаления растворителя. Остаток растворяют с этилацетатом, смешивают с силикагелем, и очищают колоночной хроматографией с получением соединения 545 (выход 62%).
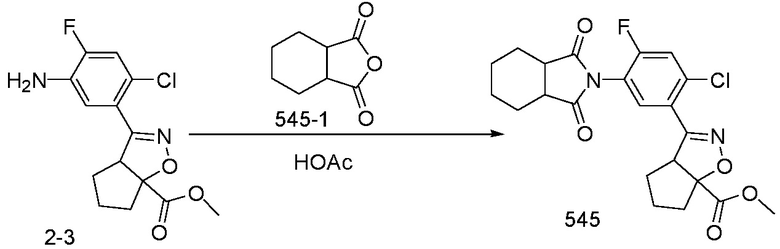
10. Синтез соединения 547
Соединение 547-1 (0,128 г, 1 ммоль, 1,0 экв.) и соединение 2-3 (0,312 г, 1 ммоль, 1,0 экв.) добавляют к 10 мл уксусной кислоты. Затем реакционный раствор перемешивают при 120°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением соединения 547. (0,11 г, выход: 26%) (белое масло).
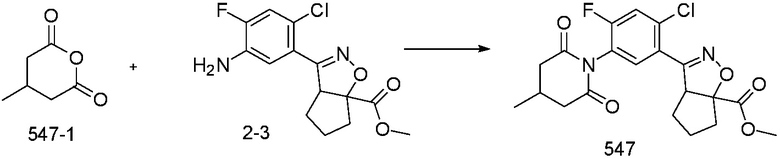
11. Синтез соединения 551
Соединение 2-3 (0,312 г, 1 ммоль, 1,0 экв.), соединение 551-1 (0,165 г, 1 ммоль, 1,0 экв.), ТЭА (0,202 г, 2 ммоль, 2,0 экв.) и КДИ (0,162 г, 1 ммоль, 1,0 экв.) добавляют к 10 мл ацетонитрила. Затем, реакционный раствор перемешивают при 60°C в течение 1 часа. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением соединения 551, 0,11 г (26% выход) (белое твердое вещество).
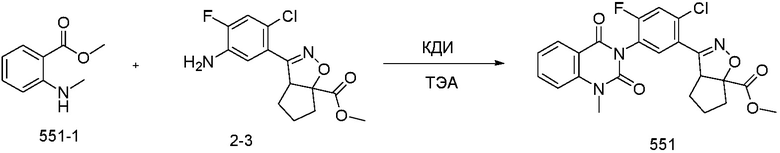
12. Синтез соединения 552
(1) Соединение 2-3 (260 мг), Et3N (3 экв.) и S-КДИ ( 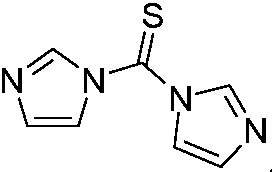 , 3,0 экв.) добавляют к 20 мл ДХМ. Затем, реакционный раствор подвергают взаимодействию при комнатной температуре в течение ночи. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Полученный неочищенный продукт смешивают непосредственно с силикагелем, и очищают колоночной хроматографией с получением соединения 552-1 (выход: 65%) (желтое твердое вещество).
, 3,0 экв.) добавляют к 20 мл ДХМ. Затем, реакционный раствор подвергают взаимодействию при комнатной температуре в течение ночи. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Полученный неочищенный продукт смешивают непосредственно с силикагелем, и очищают колоночной хроматографией с получением соединения 552-1 (выход: 65%) (желтое твердое вещество).
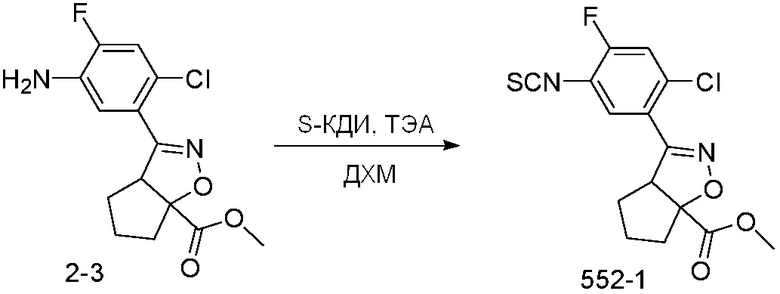
(2) Соединение 552-1, Et3N (3 экв.) и пропиламин (3 экв.) добавляют к 20 мл ДХМ. Затем, полученный раствор подвергают взаимодействию при комнатной температуре в течение 3 часов. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Полученный неочищенный продукт смешивают непосредственно с силикагелем, и очищают колоночной хроматографией с получением соединения 552-2 (желтое твердое вещество); выход: 52%.

(3) Соединение 552-2, карбонат калия (3 экв.) и оксалилхлорид (1,1 экв.) добавляют к 20 мл ДМФ. Полученный раствор сначала подвергают взаимодействию в условиях ледяной бани на полчаса, и затем нагревают до 50°C для продолжения реакции в течение 1 часа. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Реакционный раствор промывают водой, и экстрагируют этилацетатом. Органическую фазу смешивают с силикагелем, и очищают колоночной хроматографией с получением соединения 552 (желтое твердое вещество); выход: 38%.
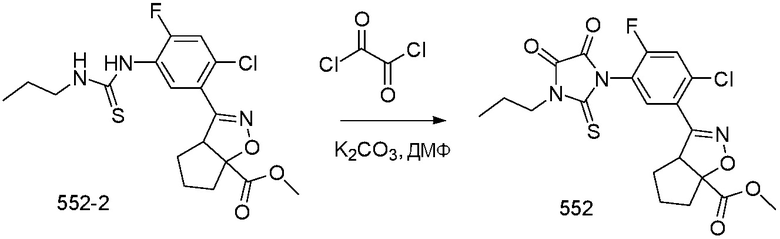
13. Синтез соединения 553
Соединение 552 и пропиламин (10 экв.) добавляют к 20 мл ДХМ. Затем, полученный раствор подвергают взаимодействию при комнатной температуре в течение 3 часов. ЖХМС показала что пики исходных материалов в ЖХМС хроматограмме исчезли. Полученный неочищенный продукт смешивают непосредственно с силикагелем, и очищают колоночной хроматографией с получением соединения 553 (желтое твердое вещество); выход: 72%.
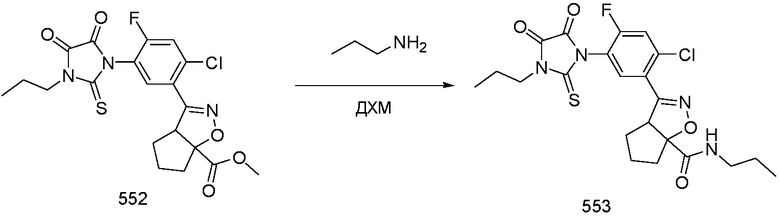
14. Синтез соединения 561
(1) Порошок активированного угля (0,25 г) добавляют к соединению 561-2 (3,10 мл, 25,7 ммоль) при перемешивании при -20°C (охлаждают на бане сухой лед/изопропанол) в условиях азотной защиты. Соединение 561-1 (2,55 г, 25,7 ммоль) растворяют в этилацетате (25 мл) и медленно добавляют по каплям в реакционную систему, сохраняя температуру ниже 0°C. Реакционный раствор подвергают взаимодействию при комнатной температуре в течение ночи. ТСХ показывает (перманганат калия для проявления цвета), что реакция исходных материалов почти завершена. Реакционный раствор фильтруют для удаления осадка и активированного угля, и фильтровальную лепешку промывают этилацетатом. Фильтрат сушат под вакуумом при 40°C с получением неочищенного продукта соединения 561-3 (1,8 г). Соединение 561-3 представляет собой желтое мутное масло.
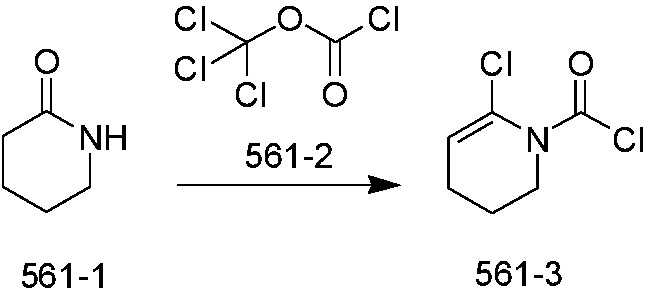
(2) Соединение 2-3 (1,5 г, 4,8 ммоль) растворяют в концентрированной хлористоводородной кислоте (15 мл). Раствор охлаждают до -5°C, туда медленно добавляют по каплям водный раствор NaNO2 (397 мг, 5,76 ммоль), затем подвергают взаимодействию при -5°C в течение 1 часа. Двухлористое олово (2,27 г, 11,99 ммоль) растворяют в концентрированной хлористоводородной кислоте (5 мл), и медленно добавляют по каплям к реакционной системе, затем подвергают взаимодействию при 0°C в течение 1~2 часов. ЖХМС показала, что реакция исходных материалов почти завершена, и образуется продукт в количестве ~75%. 10 г целита добавляют к реакционной системе при энергичном перемешивании. pH реакционной системы доводят до примерно 8~9 с 10% NaOH водным раствором при 0°C, затем экстрагируют дважды дихлорметаном. Органическую фазу сушат и затем концентрируют с получением неочищенного продукта соединения 561-4 (1,2 г).
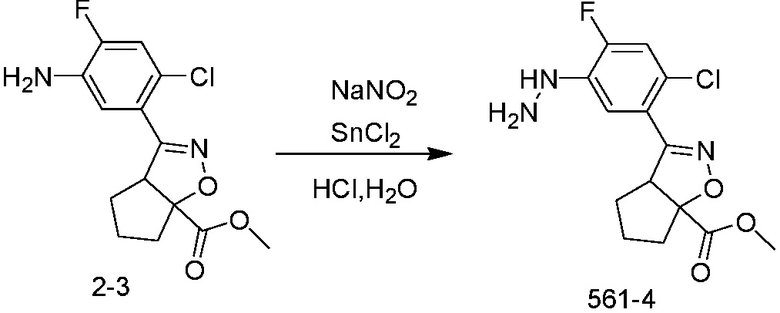
(3) Соединение 561-4 (1,2 г, 3,66 ммоль) растворяют с безводным дихлорметаном (50 мл) и загружают в 100 мл одногорлую колбу, туда добавляют по каплям муравьиную кислоту (185 мг, 4,03 ммоль) при комнатной температуре. Полученный раствор подвергают взаимодействию при комнатной температуре в течение ночи. ЖХМС показала, что реакция исходных материалов завершена, и основной пик ЖХМС хроматограммы принадлежит продукту. Реакционный раствор концентрируют при 40°C с получением неочищенного продукта соединения 561-5 (0,8 г).
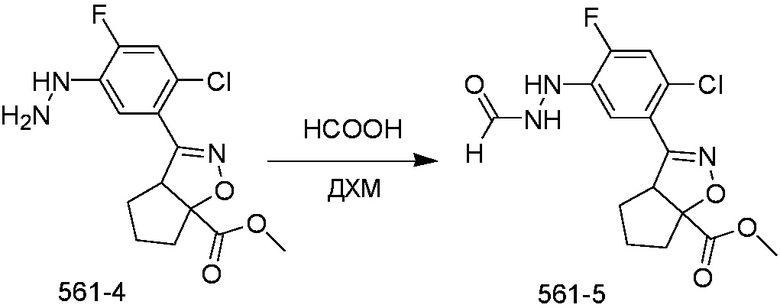
(4) Соединение 561-5 (0,75 г, 2,11 ммоль) растворяют с безводным ацетонитрилом (30 мл) и загружают в 100 мл одногорлую колбу. Раствор охлаждают до 0°C, к которому добавляют по каплям раствор соединения 561-3 (417 мг, 2,32 ммоль) в ацетонитриле (10 мл). При сохранении температуры ниже 10°C, по каплям добавляют триэтиламин (87 мг, 2,16 ммоль). Полученный раствор подвергают взаимодействию при 0°C в течение 30 мин, и затем нагревают до 50°C для продолжения реакции в течение 6~7 часов. ЖХМС показала, что реакция исходных материалов завершена и образовалась промежуточная соль. 6N HCl (3,16 мл, 18,97 ммоль) по каплям добавляют в реакционную систему, и затем реакцию продолжают при 50°C в течение 1 часа. ЖХМС показала, что образуется продукт. Реакционный раствор концентрируют и очищают колоночной хроматографией с обращенной фазой с получением чистого продукта соединения 561 (27 мг, выход 3%).
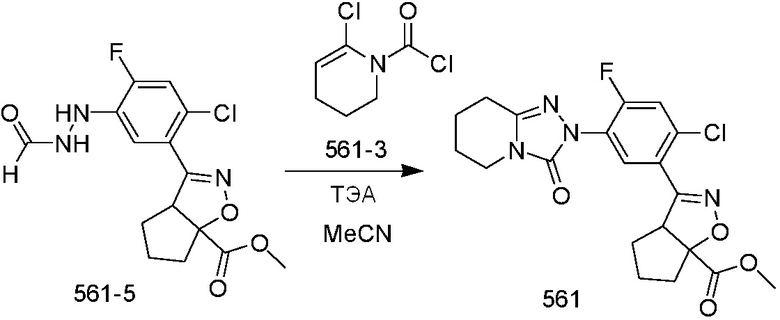
15. Синтез соединения 574
(1) Соединение 552-1 (0,3 г, 0,85 ммоль, 1,0 экв.), MeNH2HCl (0,11 г, 1,7 ммоль, 2,0 экв.) и ТЭА (0,34 г, 3,4 ммоль, 4,0 экв.) добавляют к 10 мл ДХМ. Затем, реакционный раствор перемешивают при комнатной температуре в течение 3 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 574-1 (0,25 г, выход: 76%) (белое масло).
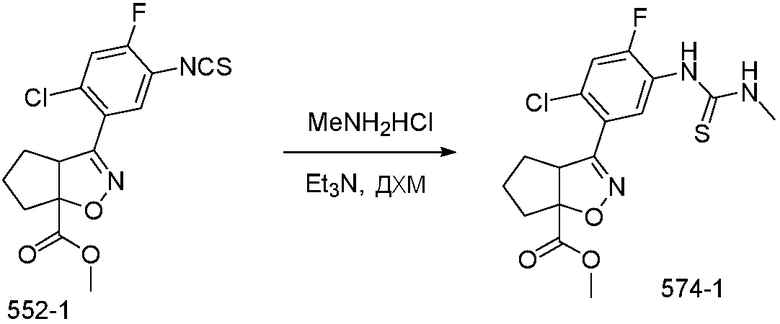
(2) Соединение 574-1 (0,25 г, 0,65 ммоль, 1,0 экв.), соединение 574-2 (0,14 г, 0,71 ммоль, 1,1 экв.) и ТЭА (0,08 г, 0,78 ммоль, 1,2 экв.) добавляют к 10 мл толуола. Затем реакционный раствор перемешивают при 100°C в течение 8 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением соединения 574 (0,03 г, выход: 10%) (белое твердое вещество).
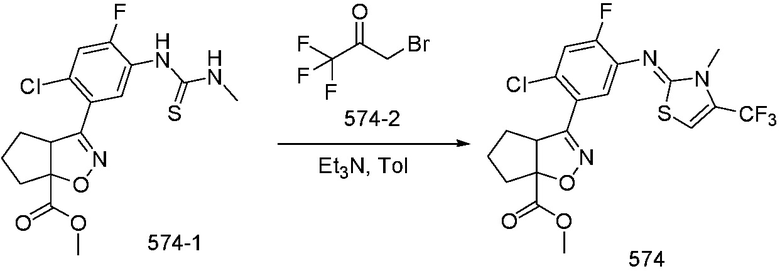
16. Синтез соединения 575
Соединение 552-1 (1,0 экв.) и гидрохлорид гексагидропиридазина (1,1 экв.) и триэтиламин (3,0 экв.) растворяют в ДХМ (10 об.), затем подвергают взаимодействию при комнатной температуре в течение 1 часа. После завершения технологического контроля, добавляют КДИ (1,5 экв.). Реакционный раствор нагревают до 45°C для продолжения реакции в течение ночи, и во время технологического контроля образуется продукт. Полученный неочищенный продукт смешивают с силикагелем и очищают колоночной хроматографией с получением соединения 575 (выход 38%).
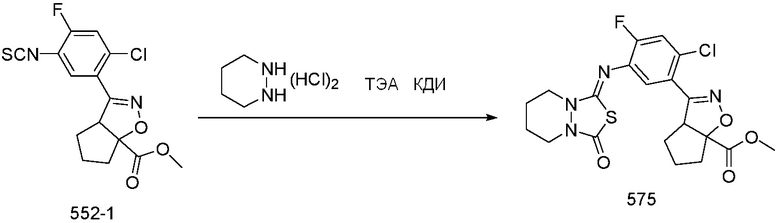
17. Синтез соединений 577, 578 и 579
(1) Соединение 2-3 (0,312 г, 1 ммоль, 1,0 экв.) и NaNO2 (0,14 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл водного раствора HBr, и CuBr (0,284 г, 2 ммоль, 2,0 экв.) добавляют при 0°C. Затем, реакционный раствор перемешивают при комнатной температуре в течение 2 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли, выпаривают досуха и очищают колоночной хроматографией с получением соединения 578-1 в качестве промежуточного соединения (0,3 г, выход: 85%) (желтое твердое вещество).
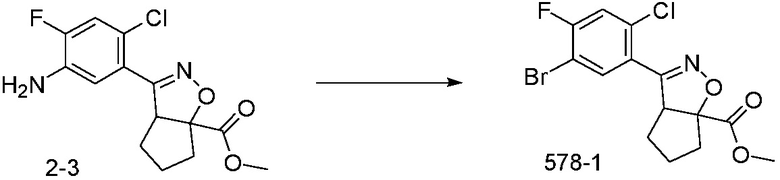
(2) Соединение 578-1 (0,376 г, 1 ммоль, 1,0 экв.), соединение 578-2 (0,254 г, 1 ммоль, 1,0 экв.) и KOAc (0,2 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл диоксана, и Pd(dppf)Cl2 (0,1 г, 0,1 ммоль, 0,1 экв.) добавляют в условиях азотной защиты. Затем, реакционный раствор перемешивают при 80°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 578-3 в качестве промежуточного соединения (0,17 г, выход: 50%) (белое масло).

(3) Соединение 578-4 растворяют в диоксане, который имеет объем в 12 раз больше соединения 578-4, туда медленно добавляют по каплям раствор метоксида натрия (1,5 экв., 30%), затем нагревают до 100°C и подвергают взаимодействию в течение 16 часов. После завершения технологического контроля реакционный раствор охлаждают и фильтруют под вакуумом. Твердое вещество растворяют с 1M раствором хлористоводородной кислоты. Жидкую фазу концентрируют и затем растворяют с 1M раствором хлористоводородной кислоты. Два раствора объединяют и экстрагируют этилацетатом до тех пор, пока в водной фазе не останется продукта. Органическую фазу концентрируют с получением твердого вещества, которое затем измельчают и очищают петролейным эфиром:этилацетатом=10:1, фильтруют, и сушат с получением соединения 578-5.
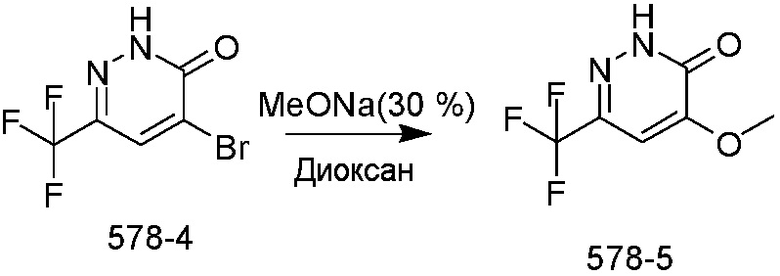
(4) Соединение 578-5 добавляют к ДХЭ, который имеет объем в 10 раз больше соединения 578-5, туда затем добавляют оксихлорид фосфора (3,0 экв.) и каталитическое количество ДМФ (5%), затем нагревают до 100°C и оставляют взаимодействовать в течение 16 часов. После технологического контроля, реакционный раствор охлаждают, и концентрируют для удаления избытка оксихлорида фосфора. После добавления воды для гашения реакции, pH реакционного раствора доводят до 8-9 карбонатом калия. Реакционный раствор экстрагируют дихлорметаном. Органическую фазу концентрируют, смешивают с силикагелем, и очищают колоночной хроматографией с получением соединения 578-6.
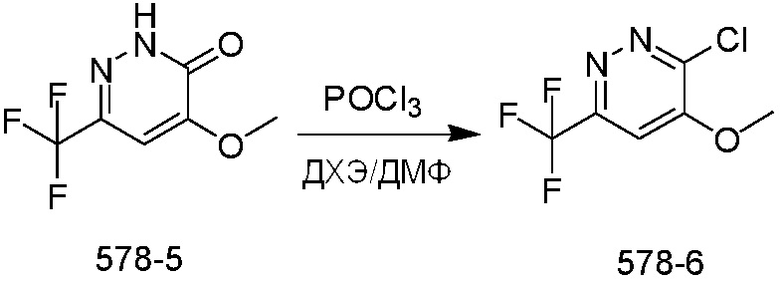
(5) Воду (1 мл), соединение 578-6 (0,212 г, 1 ммоль, 1,0 экв.), соединение 578-3 (0,341 г, 1 ммоль, 1,0 экв.) и Cs2CO3 (0,652 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл диоксана, и Pd(dppf)Cl2 (0,1 г, 0,1 ммоль, 0,1 экв.) добавляют в условиях азотной защиты. Затем реакционный раствор перемешивают при 100°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 578 (0,24 г, выход: 50%) (белое масло).
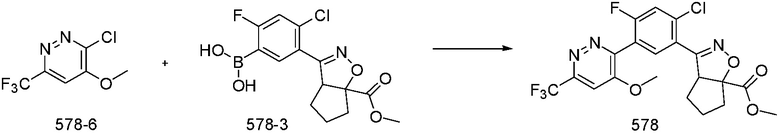
(6) Соединение 578 (0,473 г, 1 ммоль, 1,0 экв.) и KOAc (0,2 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл ДМСО. Затем реакционный раствор перемешивают при 120°C в течение 2 часов. ЖХМС тест показал завершение реакции. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 577 (0,23 г, 51% выход) (белое масло).
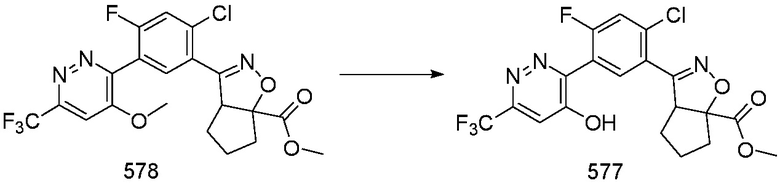
(7) Соединение 577 (0,459 г, 1 ммоль, 1,0 экв.), K2CO3 (0,276 г, 2 ммоль, 2,0 экв.), IME (0,286 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл ДМФ. Затем, реакционный раствор перемешивают при комнатной температуре в течение 2 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 579 (0,12 г, выход: 25%) (белое масло).
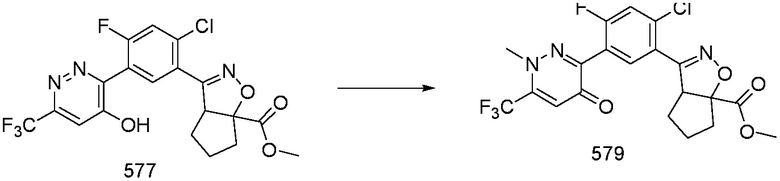
18. Синтез соединений 587 и 588
(1) Соединение 587-1 (0,1 г, 1 ммоль, 1,0 экв.), соединение 578-1 (0,376 г, 1 ммоль, 1,0 экв.) и ТЭА (0,202 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл диоксана. Pd(pph3)4 (0,1 г, 0,1 ммоль, 0,1 экв.) и CuI (0,019 г, 0,1 ммоль, 0,1 экв.) добавляют в условиях азотной защиты. Затем реакционный раствор перемешивают при 100°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением продукта 0,19 г (выход: 49%) (желтое твердое вещество).
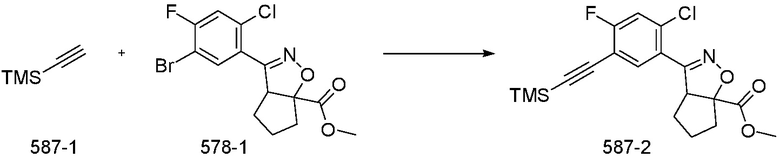
(2) Соединение 587-2 (0,394 г, 1 ммоль, 1,0 экв.) и K2CO3 (0,138 г, 1 ммоль, 1,0 экв.) добавляют к 10 мл ТГФ. Затем реакционный раствор перемешивают при комнатной температуре в течение 2 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением продукта 0,2 г (выход: 62%) (белое масло).
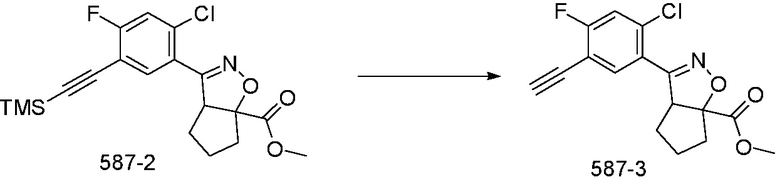
(3) Соединение 587-3 (0,321 г, 1 ммоль, 1,0 экв.), саркозин (0,2 г, 2 ммоль, 2,0 экв.) и (CF3CO)2O (0,218 г, 1 ммоль, 1,0 экв.) добавляют к 10 мл Ac2O. Затем реакционный раствор перемешивают при 120°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением продукта 0,22 г (выход: 51%) (белое масло).
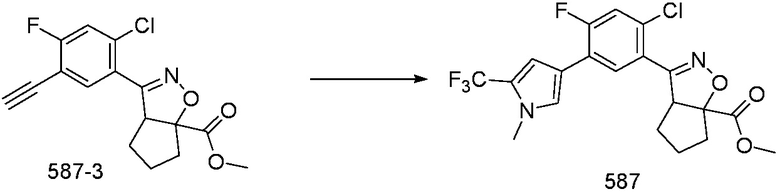
(4) Соединение 587 (0,44 г, 1 ммоль, 1,0 экв.) и NCS (0,27 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл ДМФ. Затем, реакционный раствор перемешивают при 60°C в течение 2 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением продукта 0,1 г (выход: 20%) (белое масло).
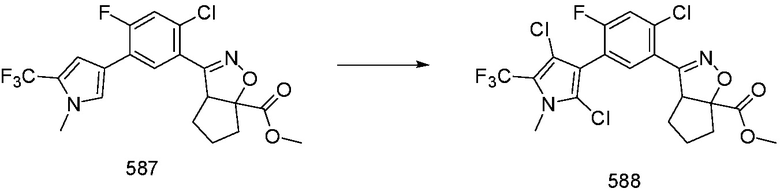
19. Синтез соединений 589 и 590
(1) Воду (1 мл), соединение 589-1 (0,228 г, 1 ммоль, 1,0 экв.), соединение 578-3 (0,341 г, 1 ммоль, 1,0 экв.) и Cs2CO3 (0,652 г, 2 ммоль, 2,0 экв.) добавляют к 10 мл диоксана, и Pd(dppf)Cl2 (0,1 г, 0,1 ммоль, 0,1 экв.) добавляют в условиях азотной защиты. Затем, реакционный раствор перемешивают при 100°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют, и очищают колоночной хроматографией с получением продукта 0,11 г (выход: 25%) (белое твердое вещество).
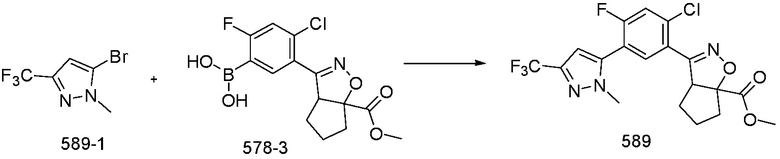
(2) Соединение 589 (0,44 г, 1 ммоль, 1,0 экв.) и NBS (0,178 г, 1 ммоль, 1,0 экв.) добавляют к 10 мл ДМФ. Затем, реакционный раствор перемешивают при 80°C в течение 12 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением продукта 0,1 г (выход: 19%) (белое твердое вещество).
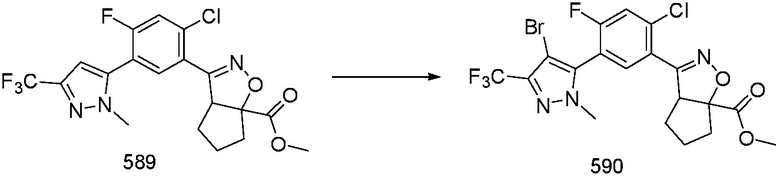
20. Синтез соединения 596
Соединение 596-1 (0,196 г, 1 ммоль, 1,0 экв.), соединение 578-1 (0,375 г, 1 ммоль, 1,0 экв.), K2CO3 (0,276 г, 2 ммоль, 2,0 экв.) и Cu2O (0,028 г, 0,2 ммоль, 0,2 экв.) добавляют к 10 мл ДМФ. Затем, реакционный раствор перемешивают при 140°C в течение 2 часов. Завершение реакции определяют ЖХМС. Реакционный раствор концентрируют и очищают колоночной хроматографией с получением соединения 596 (0,1 г, выход: 21%) (белое масло).
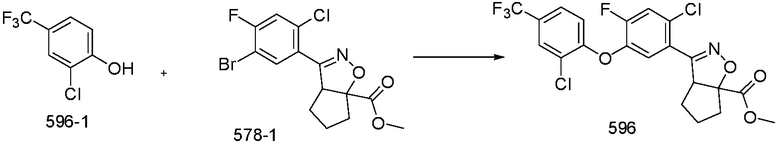
Оценка биологической активности:
Критерии уровня активности относительно повреждения растений (т.е. степени контроля роста) следующие:
Уровень 5: степень контроля роста примерно 85%;
Уровень 4: степень контроля роста больше или равна 60% и меньше 85%;
Уровень 3: степень контроля роста больше или равна 40% и меньше 60%;
Уровень 2: степень контроля роста больше или равна 20% и меньше 40%;
Уровень 1: степень контроля роста больше или равна 5% и меньше 20%;
Уровень 0: степень контроля роста меньше 5%.
Вышеуказанные степени контроля роста являются степенями контроля сырого веса.
Эксперимент по прополке в послевсходовый период:
Семена однодольных и двудольных сорняков (Descurainia sophia, Capsella bursa-pastoris, Abutilon theophrasti, Galium aparine, Stellaria media, Lithospermum arvense, Rorippa indica, Alopecurus aequalis, Alopecurus japonicus, Eleusine indica, Beckmannia syzigachne, Sclerochloa dura, Phleum paniculatum, Veronica didyma Tenore, Bromus japonicus, Aegilops tauschii, Phalaris arundinacea, Amaranthus retroflexus, Chenopodiaceae, Commelina communis, Sonchus arvensis, convolvulus arvensis, Cirsium setosum, Solanum nigrum, Acalypha australis, Digitaria sanguinalis, Echinochloa crusgalli, Setaria viridis, Setaria glauca, Leptochloa chinensis, Monochoria vaginalis, Sagittaria trifolia, Scirpus juncoides, Cyperus rotundus, Cyperus iria, Cyperus difformis, Fimbristylis, Portulaca oleracea, Xanthium sibiricum, Pharbitis nil, Conyza japonica, и т.д.) и семена основных сельскохозяйственных культур (пшеница, кукуруза, рис, соя, хлопок, масличный рапс, просо, сорго, картофель, кунжут, клещевина и т.д.) помещают в пластиковые горшки, наполненные почвой, затем покрывают слоем почвы толщиной 0,5-2 см, позволяют расти в хорошей тепличной среде. Через 2 недели после посева, тестируемые растения обрабатывают на стадии 2-3 листьев. Тестируемые соединения по настоящему изобретению соответственно растворяют в ацетоне, затем добавляют Tween 80 и 1,5 литра/га эмульгируемого концентрата метилолеата в качестве синергиста, разводят определенным количеством воды с получением раствора с определенной концентрацией, и опрыскивают растения с помощью скруббера с разбрызгивающим устройством. После нанесения, растения культивируют в течение 3 недель в теплице, и затем подсчитывают экспериментальные результаты прополки. Дозы используемых соединений составляют 500, 250, 125, 60, 15, 7,5 г а.и./га, и средние значения получают путем трехкратного повторения. Типовые данные перечислены в таблице 2-3.
Таблица 2. Результаты прополки в послевсходовый период
Примечание: N означает отсутствие данных.
Таблица 3. Контрольные результаты тестирования прополки в послевсходовый период
Примечание: контрольное соединение A: 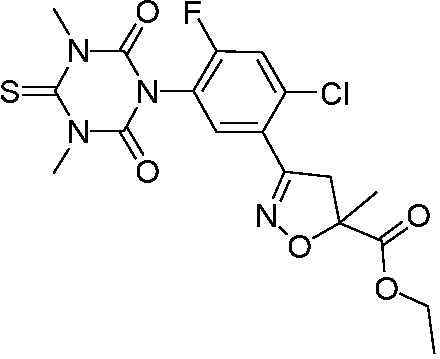 ; контрольное соединение B:
; контрольное соединение B: 
Эксперимент по прополке в довсходовый период:
Семена однодольных и двудольных сорняков и основных сельскохозяйственных культур (например, пшеницы, кукурузы, риса, сои, хлопка, масличного рапса, проса и сорго) помещают в пластиковый горшок, заполненный почвой, и засыпают почвой на 0,5-2 см. Тестируемые соединения по настоящему изобретению растворяют с ацетоном, затем добавляют tween 80, разводят определенным количеством воды для достижения определенной концентрации и распыляют сразу после посева. Полученные семена инкубируют в теплице 4 недели после опрыскивания и наблюдают результаты тестирования. Отмечают, что гербицид в основном имеет превосходный эффект при норме расходе 250 г а.и./га, особенно в отношении сорняков, таких как Echinochloa crusgalli, Digitaria sanguinalis и Abutilon theophrasti и т. д. и многие соединения имеют хорошую селективность для кукурузы, пшеницы, риса и сои и т.д.
Эксперименты с основными сорняками на пшеничных и рисовых полях показали, что соединения по настоящему изобретению обычно обладают хорошей эффективностью в борьбе с сорняками. Прежде всего, следует отметить, что соединения по настоящему изобретению обладают чрезвычайно высокой активностью в отношении широколистных сорняков и сорняков cyperaceae, устойчивых к ингибитору ALS, таких как Sagittaria trifolia, Scirpus juncoides, Cyperus difformis, Descurainia sophia, Capsella bursa-pastoris, Lithospermum arvense, Galium aparine, и Cyperus rotundus и т. д. и имеют отличную коммерческую ценность.
Оценка безопасности пересаженного риса и оценка эффекта борьбы с сорняками на рисовом поле:
Почву рисового поля засыпают в горшок размером 1/1000000 га. Семена Echinochloa crusgalli, Scirpus juncoides, и Bidens tripartita L. высевают и аккуратно засыпают почвой, затем оставляют выстаиваться в теплице в 0,5-1 см воды. Клубень Sagittaria trifolia высаживают на следующий день или через 2 дня. Затем его хранят в 3-4 см воды. Сорняки обрабатывают капельным способом водными разбавителями WP или SC, приготовленными в соответствии с обычным способом получения соединений по настоящему изобретению, с помощью пипетки, гомогенно, для достижения указанного эффективного количества, когда Echinochloa crusgalli, Scirpus juncoides, и Bidens tripartita L. достигают стадии 0,5 листа и Sagittaria trifolia достигает стадии первичного листа.
Дополнительно, почву рисового поля засыпают в горшок размером 1/1000000 га, выравнивают для сохранения запасов воды на глубине 3-4 см. На следующий день рис в стадии 3 листа (рис японский) пересаживают на глубину 3 см. Соединение по настоящему изобретению наносят таким же образом через 5 дней после пересадки.
Способность к плодоношению Echinochloa crusgalli, Scirpus juncoides, Bidens tripartita L. и Sagittaria trifolia через 14 дней после обработки соединением по изобретению и способность к плодоношению риса через 21 день после обработки соединением по изобретению, соответственно, оценивают невооруженным глазом. Оценивают эффект борьбы с сорняками с помощью вышеуказанного стандартного уровня активности. Многие соединения демонстрируют отличную активность и селективность.
Примечание: семена Echinochloa crusgalli, Scirpus juncoides, Bidens tripartita L. и Sagittaria trifolia собирают в провинции Хэйлунцзян в Китае. Тесты показывают, что сорняки устойчивы к обычным дозам пиразосульфурона-этила.
В то же время после нескольких тестов обнаружено, что соединения и композиции по настоящему изобретению обладают хорошей селективностью в отношении многих злаковых трав, таких как цойсия японская, бермудская трава, овсяница высокорослая, мятлик, плевел и морской паспалум и т. д., и способны контролировать много важных злаковых и широколиственных сорняков. Соединения также демонстрируют превосходную селективность и коммерческую ценность в тестах на сахарном тростнике, сое, хлопке, масличном подсолнечнике, картофеле, фруктах и овощах при различных способах нанесения гербицидов.
Изобретение относится к замещенному ароматическому соединению с конденсированным кольцом, представленному общей формулой I, которое может найти применение в качестве гербицида для борьбы с сорняками. В формуле I Q является Q-1-Q-6, Q-8-Q-12, Q-14-Q-17, Q-31 или Q-32, Y является галогеном, галоC1-C8 алкилом или циано; Z является галогеном; M является CH или N; Q1, Q2, Q3, Q4, Q5, Q6 каждый независимо является O или S; Het является циклической структурой, связанной посредством двух атомов углерода в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3-8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом, содержащим 1 гетероатом, выбранный из O, S, CO или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо не замещено или замещено по меньшей мере одной группой, выбранной из галогена, С1-С8 алкила, -OR14 или -(CO)OR14; X1, X2 каждый независимо является H, гидрокси, C1-C8 алкилом, -(CO)R’’ или 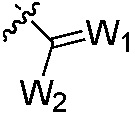 , где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из -(CO)OR’’; R’’ независимо является C1-C8 алкилом, насыщенным или ненасыщенным 5-членным гетероциклилом, содержащим 1 или 2 гетероатома, выбранных из N, где группа гетероциклил является незамещенной или замещена по меньшей мере одной группой, выбранной из C1-C8 алкила; W1 является O; W2 является OW3, SW3 или N(W3)2; W3 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, С6 арилом или
, где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из -(CO)OR’’; R’’ независимо является C1-C8 алкилом, насыщенным или ненасыщенным 5-членным гетероциклилом, содержащим 1 или 2 гетероатома, выбранных из N, где группа гетероциклил является незамещенной или замещена по меньшей мере одной группой, выбранной из C1-C8 алкила; W1 является O; W2 является OW3, SW3 или N(W3)2; W3 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, С6 арилом или 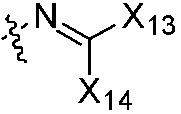 ; где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена, насыщенного 5-членного гетероциклила, содержащего 1 гетероатом, выбранный из О, С6 арила или
; где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена, насыщенного 5-членного гетероциклила, содержащего 1 гетероатом, выбранный из О, С6 арила или 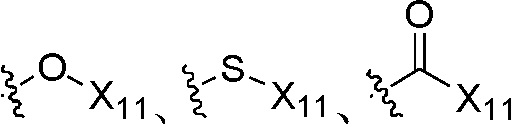 , где группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена; X11 независимо является С1-С8 алкилом; X13, X14 каждый независимо является С1-С8 алкилом; R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является С1-С8 алкилом; или R17, R18, взятые вместе, образуют -CH2CH2CH2CH2-; R7, R8, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, С1-С8 алкилом, -OR11 или -(SO2)R11, где группа С1-С8 алкил является незамещенной или замещена галогеном; или R7, R8, взятые вместе, образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH-; или R19, R20, взятые вместе, образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2-; или R21, R22, взятые вместе, образуют -CH2CH2CH2- или -CH2CH2CH2CH2-; R11 независимо является С1-С8 алкилом; R14 независимо является H или С1-С8 алкилом; R15, R16, R52 каждый независимо является H или С1-С8 алкилом. Изобретение относится также к способу получения указанного соединения, к способу борьбы с сорняками с его использованием и его применению для борьбы с сорняками. 4 н. и 9 з.п. ф-лы, 3 табл., 91 пр.
, где группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена; X11 независимо является С1-С8 алкилом; X13, X14 каждый независимо является С1-С8 алкилом; R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является С1-С8 алкилом; или R17, R18, взятые вместе, образуют -CH2CH2CH2CH2-; R7, R8, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, С1-С8 алкилом, -OR11 или -(SO2)R11, где группа С1-С8 алкил является незамещенной или замещена галогеном; или R7, R8, взятые вместе, образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH-; или R19, R20, взятые вместе, образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2-; или R21, R22, взятые вместе, образуют -CH2CH2CH2- или -CH2CH2CH2CH2-; R11 независимо является С1-С8 алкилом; R14 независимо является H или С1-С8 алкилом; R15, R16, R52 каждый независимо является H или С1-С8 алкилом. Изобретение относится также к способу получения указанного соединения, к способу борьбы с сорняками с его использованием и его применению для борьбы с сорняками. 4 н. и 9 з.п. ф-лы, 3 табл., 91 пр.
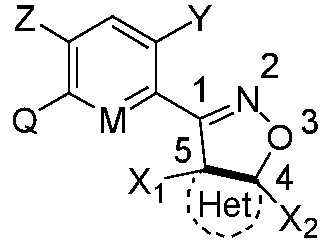 I
I
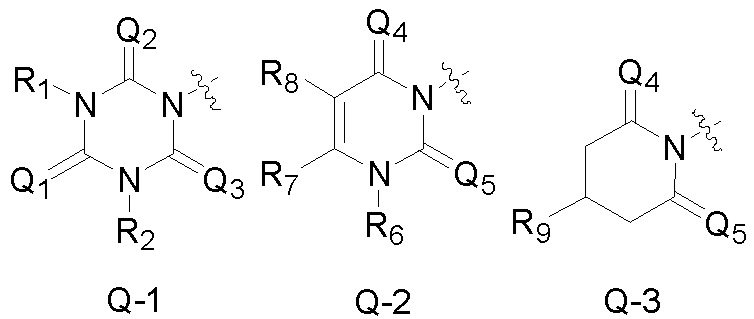
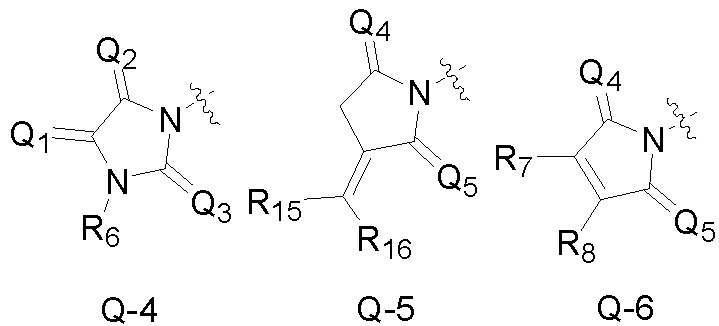
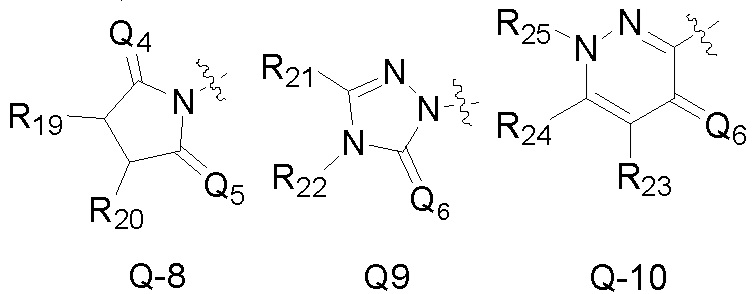
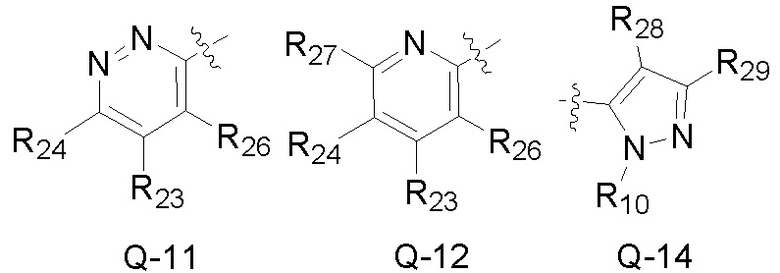
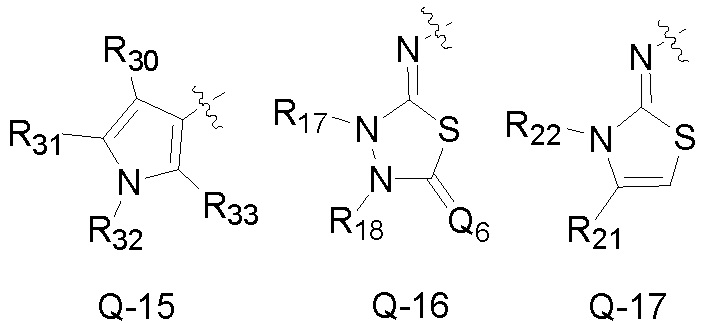
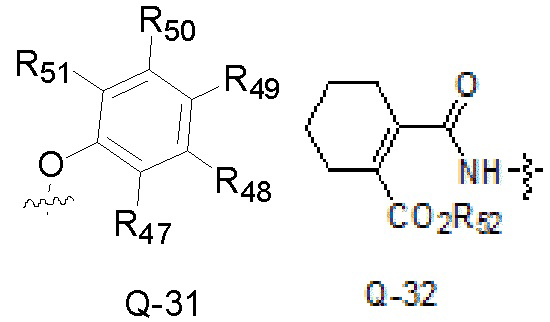
1. Замещенное ароматическое соединение с конденсированным кольцом, представленное общей формулой I
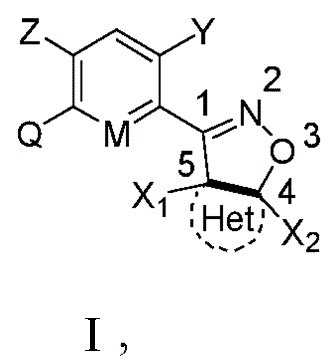
где Q является
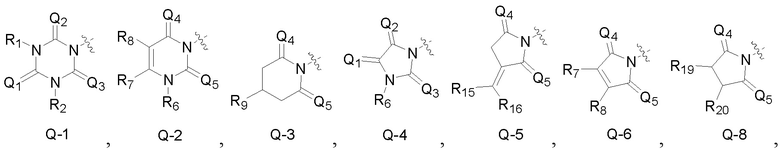
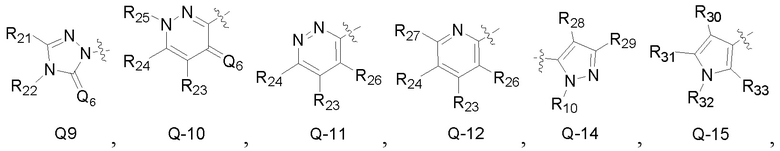
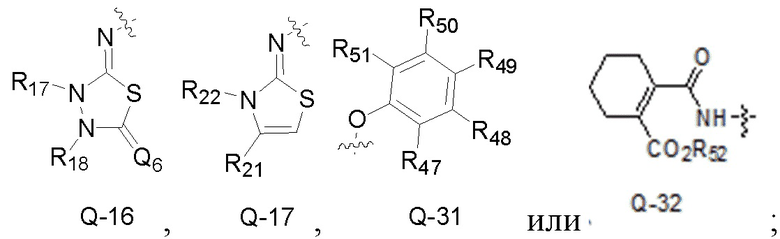
Y является галогеном, галоC1-C8 алкилом или циано;
Z является галогеном;
M является CH или N;
Q1, Q2, Q3, Q4, Q5, Q6 каждый независимо является O или S;
Het является циклической структурой, связанной посредством двух атомов углерода в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3-8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом, содержащим 1 гетероатом, выбранный из O, S, CO или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо не замещено или замещено по меньшей мере одной группой, выбранной из галогена, С1-С8 алкила, -OR14 или -(CO)OR14;
X1, X2 каждый независимо является H, гидрокси, C1-C8 алкилом, -(CO)R’’ или 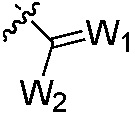 , где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из -(CO)OR’’;
, где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из -(CO)OR’’;
R’’ независимо является C1-C8 алкилом, насыщенным или ненасыщенным 5-членным гетероциклилом, содержащим 1 или 2 гетероатома, выбранных из N, где группа гетероциклил является незамещенной или замещена по меньшей мере одной группой, выбранной из C1-C8 алкила;
W1 является O;
W2 является OW3, SW3 или N(W3)2;
W3 независимо является H, C1-C8 алкилом, C2-C8 алкенилом, C2-C8 алкинилом, С6 арилом или 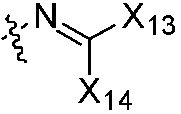 ; где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена, насыщенного 5-членного гетероциклила, содержащего 1 гетероатом, выбранный из О, С6 арила или
; где группа C1-C8 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена, насыщенного 5-членного гетероциклила, содержащего 1 гетероатом, выбранный из О, С6 арила или 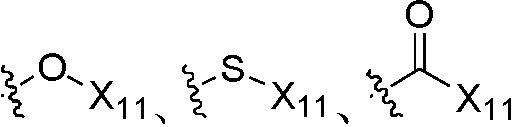 , где группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена;
, где группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена;
X11 независимо является С1-С8 алкилом;
X13, X14 каждый независимо является С1-С8 алкилом;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является С1-С8 алкилом;
или R17, R18, взятые вместе, образуют -CH2CH2CH2CH2-;
R7, R8, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, С1-С8 алкилом, -OR11 или -(SO2)R11, где группа С1-С8 алкил является незамещенной или замещена галогеном;
или R7, R8, взятые вместе, образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH-;
или R19, R20, взятые вместе, образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2-;
или R21, R22, взятые вместе, образуют -CH2CH2CH2- или -CH2CH2CH2CH2-;
R11 независимо является С1-С8 алкилом;
R14 независимо является H или С1-С8 алкилом;
R15, R16, R52 каждый независимо является H или С1-С8 алкилом.
2. Замещенное ароматическое соединение с конденсированным кольцом по п. 1, отличающееся тем, что
Y является галогеном, галоC1-C6 алкилом или циано;
Het является циклической структурой, которая связана посредством двух атомов углерода в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3-8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным гетероциклилом, содержащим 1 гетероатом, выбранный из O, S, CO или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо является незамещенным или замещено по меньшей мере одной группой, выбранной из галогена, C1-C6 алкила, -OR14 или -(CO)OR14;
X1, X2 каждый независимо является H, гидрокси, C1-C6 алкилом, -(CO)R’’ или 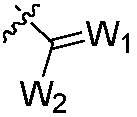 , где
, где
группы C1-C6 алкил независимо являются незамещенными или замещены по меньшей мере одной группой, выбранной из -(CO)OR’’,
R’’ независимо является C1-C6 алкилом или насыщенным или ненасыщенным 5-членным гетероциклилом, содержащим 1 или 2 гетероатома, выбранных из N, группа гетероциклил является незамещенной или замещена по меньшей мере одной группой, выбранной из С1-С6 алкила;
W1 является O;
W3 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, С6 арилом или  ,
,
где группа C1-C6 алкил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена, насыщенного 5-членного гетероциклила, содержащего 1 гетероатом, выбранный из О, С6 арила или 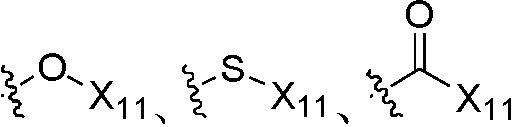 , группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена;
, группа С6 арил является незамещенной или замещена по меньшей мере одной группой, выбранной из галогена;
X11 независимо является C1-C6 алкилом;
X13, X14 каждый независимо является C1-C6 алкилом;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является C1-C6 алкилом;
или R17, R18, взятые вместе, образуют -CH2CH2CH2CH2-;
R7, R8, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, C1-C6 алкилом, -OR11, -(SO2)R11, где
группа C1-C6 алкил является незамещенной или замещена галогеном;
или R7, R8, взятые вместе, образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH-;
или R19, R20, взятые вместе, образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2-;
или R21, R22, взятые вместе, образуют -CH2CH2CH2- или -CH2CH2CH2CH2-;
R11 независимо является C1-C6 алкилом;
R14 независимо является H или C1-C6 алкилом;
R15, R16, R52 каждый независимо является H или C1-C6 алкилом.
3. Замещенное ароматическое соединение с конденсированным кольцом по п. 2, отличающееся тем, что
Het является
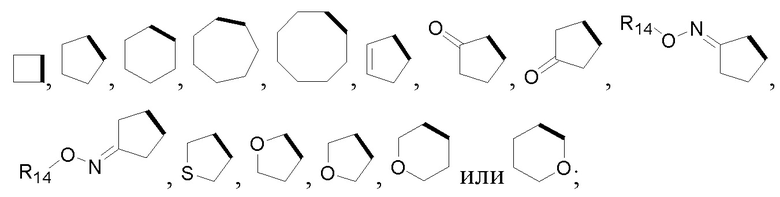
за исключением 4- и 5-положений, которые соответственно замещены X2 или X1 в общей формуле I, другие положения на Het каждое независимо является незамещенным или замещено 1, 2 или 3 группами, выбранными из галогена, С1-С6 алкила, -OR14 или -(CO)OR14.
4. Замещенное ароматическое соединение с конденсированным кольцом по п. 2, отличающееся тем, что
Het является циклической структурой, связанной посредством двух атомов углерода в 4- и 5-положениях с изоксазолиновым кольцом с образованием конденсированного кольца; циклическая структура является 3-8-членным насыщенным или ненасыщенным карбоциклилом или насыщенным или ненасыщенным гетероциклилом, содержащим 1 гетероатом, выбранный из O, S, СО или C=N-O-R14; за исключением 4- и 5-положений, которые соответственно замещены X2 или X1, другие положения на Het каждое независимо является незамещенным или замещено по меньшей мере одной группой, выбранной из галогена, C1-C6 алкила, -OR14 или -(CO)OR14;
W1 является O;
R1, R2, R6, R10, R17, R18, R22, R25, R32 каждый независимо является C1-C6 алкилом;
или R17, R18, взятые вместе, образуют -CH2CH2CH2CH2-;
R7, R8, R9, R19, R20, R21, R23, R24, R26, R27, R28, R29, R30, R31, R33, R47, R48, R49, R50, R51 каждый независимо является H, галогеном, гидрокси, C1-C6 алкилом, -OR11, -(SO2)R11, где
группа C1-C6 алкил является незамещенной или замещена галогеном;
или R7, R8, взятые вместе, образуют -CH2CH2CH2CH2- или -CH=CH-CH=CH-;
или R19, R20, взятые вместе, образуют -CH2CH2CH2CH2- или -CH2CH=CHCH2-;
или R21, R22, взятые вместе, образуют -CH2CH2CH2CH2-;
R15, R16, R52 каждый независимо является H, C1-C6 алкилом.
5. Замещенное ароматическое соединение с конденсированным кольцом по п. 4, отличающееся тем, что
Het является
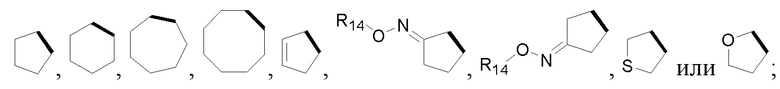
за исключением 4- и 5-положений, которые соответственно замещены X2 или X1 в общей формуле I, другие положения на Het каждое независимо является незамещенным или замещено 1, 2 или 3 группами, выбранными из галогена, С1-С6 алкила, -OR14 или -(CO)OR14.
6. Замещенное ароматическое соединение с конденсированным кольцом по любому из пп. 1-5, отличающееся тем, что
X1 является H, гидрокси или 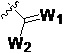 , X2 является H,
, X2 является H,  или C1-C6 алкилом, который замещен 1, 2 или 3 группами, выбранными из -(CO)OR’’;
или C1-C6 алкилом, который замещен 1, 2 или 3 группами, выбранными из -(CO)OR’’;
R’’ независимо является C1-C6 алкилом;
W3 независимо является H, C1-C6 алкилом, C2-C6 алкенилом, C2-C6 алкинилом, C6 арилом или 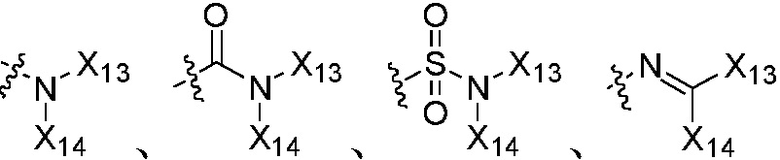 ; где группа C1-C6 алкил является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена;
; где группа C1-C6 алкил является незамещенной или замещена 1, 2 или 3 группами, выбранными из галогена;
X11 независимо является C1-C6 алкилом;
X13, X14 каждый независимо является C1-C6 алкилом;
R11 независимо является C1-C6 алкилом;
R14 независимо является H, C1-C6 алкилом.
7. Замещенное ароматическое соединение с конденсированным кольцом по п. 6, отличающееся тем, что
Q является
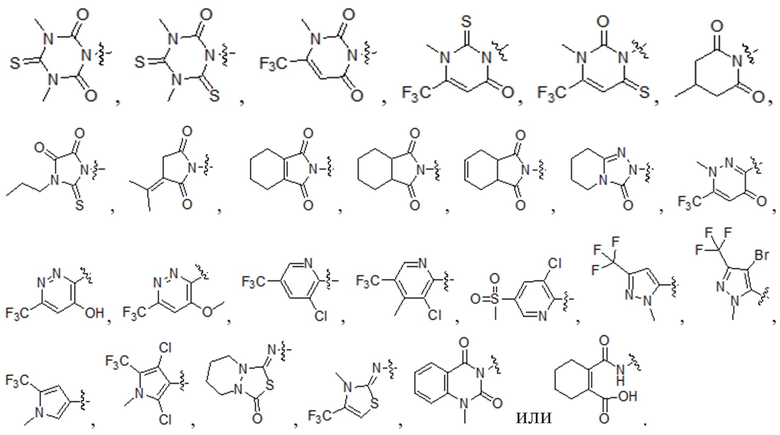
8. Замещенное ароматическое соединение с конденсированным кольцом по п. 7, отличающееся тем, что
Q является 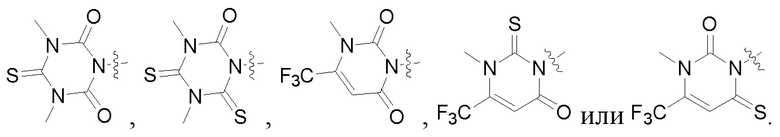
9. Замещенное ароматическое соединение с конденсированным кольцом по п. 1, отличающееся тем, что соединение выбрано из следующих соединений:
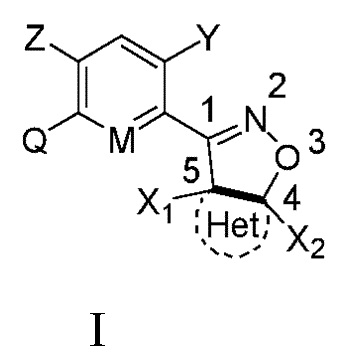
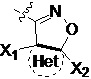
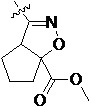
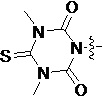
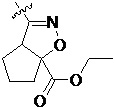

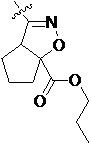

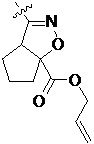

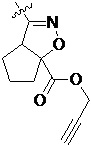

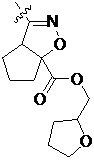

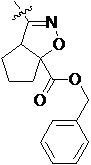

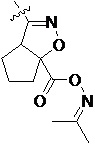

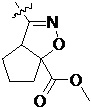







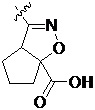







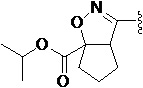





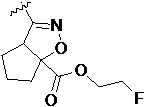

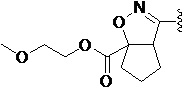



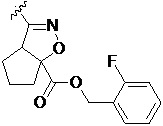



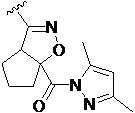

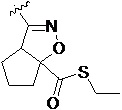

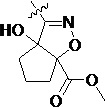

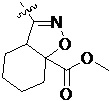

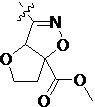

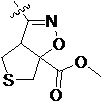


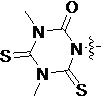


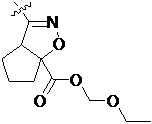

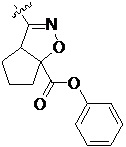

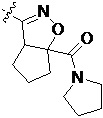

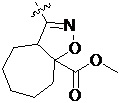

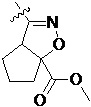

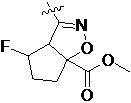

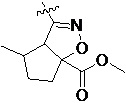

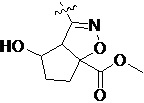





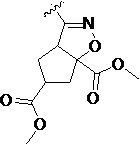

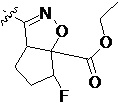

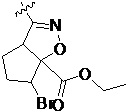

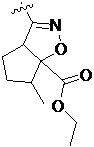

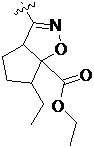

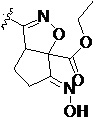


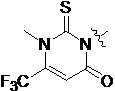

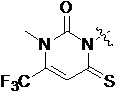


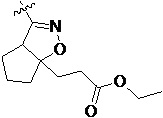



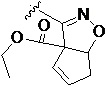

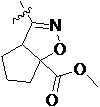


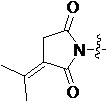

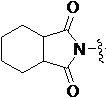
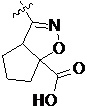
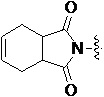



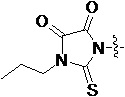
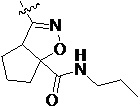
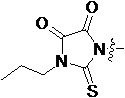

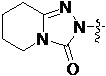

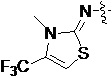

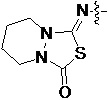

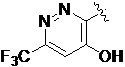

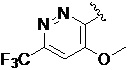

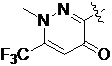

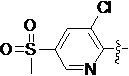

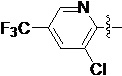

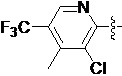

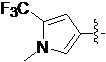

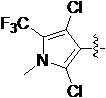

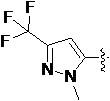



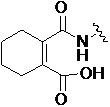
10. Способ получения замещенного ароматического соединения с конденсированным кольцом по любому из пп. 1-9, который включает следующую стадию:
превращение соединения, представленного общей формулой II
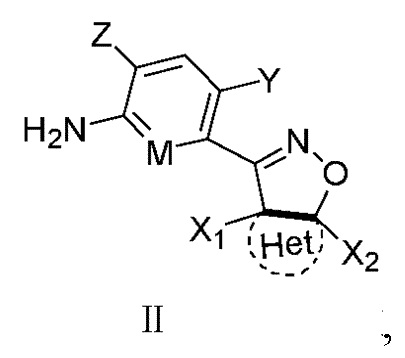
в соединение, представленное общей формулой I; заместители X1, X2, Het, Q, Y, Z и M такие, как определены в пп. 1-9.
11. Способ борьбы с сорняками, который включает нанесение гербицидно эффективной дозы по меньшей мере одного из замещенного ароматического соединения с конденсированным кольцом по любому из пп. 1-9 на растение или площадь с сорняками.
12. Применение по меньшей мере одного из замещенных ароматических соединений с конденсированным кольцом по любому из пп. 1-9 для борьбы с сорняками.
13. Применение по п. 12, где замещенное ароматическое соединение с конденсированным кольцом применяется для профилактики и/или борьбы с сорняками в полезной культуре, где полезной культурой является трансгенная культура или культура, обработанная способом генной инженерии.
| Устройство для подогревания цилиндров и золотниковых коробок паровоза продуктами горения | 1927 |
|
SU13111A1 |
| CN 109864067 A, 11.06.2019 | |||
| CN 109293640 A, 01.02.2019 | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| JP 2001288175 A, 16.10.2001 | |||
| ПРОИЗВОДНОЕ ИЗОКСАЗОЛИНА И ГЕРБИЦИД, СОДЕРЖАЩИЙ ЕГО В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2002 |
|
RU2286989C2 |
Авторы
Даты
2024-10-07—Публикация
2021-01-12—Подача