ОБЛАСТЬ ТЕХНИКИ
[1] Настоящее изобретение относится к способу получения водного раствора, содержащего никель, кобальт и марганец. Более конкретно, настоящее изобретение относится к способу получения водного раствора, содержащего никель, кобальт и марганец, который позволяет восстанавливать никель, кобальт и марганец из сырья и использовать их для изготовления катодно-активного материала литий-ионной вторичной батареи.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[2] Ценные металлы, такие как никель, кобальт и марганец, восстанавливают в основном посредством способа экстракции растворителем после растворения сырья, такого как низкосортная руда или т.п., в кислоте. Способ экстракции растворителем использует принцип, при котором ионы металлов экстрагируются из водного раствора с помощью органического растворителя. Поскольку органический растворитель, используемый в способе экстракции растворителем, подвержен риску возгорания и взрыва, он обладает меньшей рабочей стабильностью. Кроме того, поскольку органический растворитель является дорогостоящим, для повышения эффективности восстановления ценных металлов посредством способа экстракции растворителем затраты возрастают. Кроме того, поскольку в способе экстракции растворителем используется процесс экстракции растворителем, процесс очистки и процесс отделения, если определенные компоненты разделяются с помощью способа экстракции растворителем, требуется ряд этапов процесса, соответствующих конкретным компонентам. Это усложняет проведение работы.
[3] Тем временем осуществляется процесс выщелачивания, в ходе которого сырье вступает в реакцию с кислотой для восстановления ценных металлов. В процессе выщелачивания обычно используется способ выщелачивания при атмосферном давлении. Тем не менее, если концентрат выщелачивается с использованием способа выщелачивания при атмосферном давлении, то для повышения эффективности выщелачивания необходимо продолжать реакцию в течение 30 часов или больше, что приводит к снижению эффективности производства. Кроме того, железо (Fe), являющееся примесью, выщелачивается вместе с ним с помощью способа выщелачивания при атмосферном давлении. Таким образом, способ выщелачивания при атмосферном давлении не подходит для селективного выщелачивания.
[4] Магний (Mg), который является примесью, содержащейся в сырье, удаляется с помощью средства для удаления, такого как фторид натрия (NaF) или т.п. Тем не менее, если все количество магния удаляется с помощью средства для удаления, то из-за использования средства для удаления образуется большое количество остатка примесей, что приводит к увеличению затрат на отходы. При увеличении количества средства для удаления возникают дополнительные расходы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[5] Настоящее изобретение предусматривает варианты осуществления методики, позволяющей восстанавливать ценные металлы, такие как никель, кобальт и марганец, из сырья посредством процесса выщелачивания под давлением, процесса удаления примесей и процесса осаждения целевого вещества, тем самым снижая количество используемого растворителя для экстракции с целью обеспечения стабильной рабочей среды, повышения производительности и снижения себестоимости производства.
[6] В соответствии с одним вариантом осуществления способ получения водного раствора, содержащего никель, кобальт и марганец, может включать: процесс выщелачивания, включающий процесс выщелачивания под давлением, заключающийся в выщелачивании сырья с образованием продукта выщелачивания, содержащего никель, кобальт, марганец и примеси; процесс удаления примесей, заключающийся в удалении примесей из продукта выщелачивания; процесс осаждения целевого вещества, заключающийся в осаждении осадка смешанного гидроксида, содержащего никель, кобальт и марганец, путем введения нейтрализующего средства в фильтрат, из которого примеси удаляют; и процесс растворения, заключающийся в растворении осадка смешанного гидроксида в кислоте, где процесс выщелачивания под давлением включает процесс выщелачивания под давлением первой ступени и процесс выщелачивания под давлением второй ступени, заключающийся в выщелачивании под давлением остатка процесса выщелачивания под давлением первой ступени с кислотностью выше, чем кислотность в процессе выщелачивания под давлением первой ступени, и процесс удаления примесей включает процесс экстракции растворителем первой ступени, заключающийся в селективной экстракции цинка из примесей путем введения первого растворителя-экстрагента, и процесс экстракции растворителем второй ступени, заключающийся в селективной экстракции магния из примесей путем введения второго растворителя-экстрагента.
[7] В одном варианте осуществления настоящего изобретения фильтрат после процесса выщелачивания под давлением второй ступени может быть направлен в процесс выщелачивания под давлением первой ступени.
[8] В одном варианте осуществления настоящего изобретения процесс выщелачивания под давлением может быть проведен при температуре в диапазоне от 150 до 250 градусов C и при давлении в диапазоне от 8 до 43 бар изб.
[9] В одном варианте осуществления настоящего изобретения фильтрат после процесса выщелачивания под давлением первой ступени может обладать кислотностью 10 г/л или меньше, а фильтрат после процесса выщелачивания под давлением второй ступени может обладать кислотностью 50 г/л или больше.
[10] В одном варианте осуществления настоящего изобретения в процессе выщелачивания под давлением кислород может быть введен в устройство под давлением для создания давления в диапазоне от 2 до 8 бар изб.
[11] В одном варианте осуществления настоящего изобретения процесс выщелачивания может дополнительно включать процесс нейтрализации, заключающийся в регулировании pH путем введения осадка смешанного гидроксида.
[12] В одном варианте осуществления настоящего изобретения железо в фильтрате после процесса нейтрализации может быть осаждено в форме соединения, представляющего собой оксид железа.
[13] В одном варианте осуществления настоящего изобретения в процессе нейтрализации pH можно контролировать на уровне 2,5-4,0, при этом концентрация железа может быть 100 мг/л или меньше.
[14] В одном варианте осуществления настоящего изобретения остаток, осажденный в процессе нейтрализации, может быть введен в процесс выщелачивания под давлением первой ступени.
[15] В одном варианте осуществления настоящего изобретения каждый из первого растворителя-экстрагента и второго растворителя-экстрагента может представлять собой D2EHPA (ди-(2-этилгексил)фосфорную кислоту).
[16] В одном варианте осуществления настоящего изобретения процесс удаления примесей может дополнительно включать процесс удаления меди, процесс удаления алюминия и процесс удаления магния.
[17] В одном варианте осуществления настоящего изобретения процесс удаления меди может включать процесс осаждения меди путем введения гидросульфида натрия (NaSH), а процесс удаления алюминия может включать процесс осаждения алюминия путем введения гидроксида натрия (NaOH).
[18] В одном варианте осуществления настоящего изобретения процесс удаления магния может включать процесс дополнительного удаления магния путем введения фторида натрия (NaF) после процесса экстракции растворителем второй ступени.
[19] В одном варианте осуществления настоящего изобретения фторид натрия может быть введен в количестве 1,4 эквивалента (экв.) или больше.
[20] В одном варианте осуществления настоящего изобретения в процессе осаждения целевого вещества pH можно контролировать на уровне 9,0-10,0 путем введения нейтрализующего средства.
[21] В одном варианте осуществления настоящего изобретения способ может дополнительно включать: процесс подготовки сырья, заключающийся в подготовке сырья перед процессом выщелачивания, где процесс подготовки сырья может включать процесс обжига, заключающийся в образовании окисленной никелевой руды из сульфидной никелевой руды.
[22] В одном варианте осуществления настоящего изобретения серная кислота может быть получена с использованием диоксида серы, полученного в процессе обжига, и может быть использована в виде раствора, вводимого в процесс выщелачивания.
[23] В соответствии с различными вариантами осуществления настоящего изобретения можно уменьшить количество используемого дорогостоящего органического растворителя, подверженного риску взрыва и возгорания, тем самым улучшая рабочую стабильность и производительность, а также снижая себестоимость производства.
[24] В соответствии с различными вариантами осуществления настоящего изобретения можно эффективно проводить процесс очистки для отделения примесей при уменьшении используемого количества органического растворителя, тем самым улучшая рабочую стабильность и производительность.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[25] На фиг. 1 показан вид, на котором проиллюстрирован процесс обжига и процесс выщелачивания для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения.
[26] На фиг. 2 показан вид, на котором проиллюстрирован процесс удаления примесей и процесс осаждения целевого вещества для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения.
[27] На фиг. 3 показан вид, на котором проиллюстрирован процесс растворения и последний процесс удаления примесей для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ
[28] Варианты осуществления настоящего изобретения проиллюстрированы для описания технической сущности настоящего изобретения. Объем формулы изобретения согласно настоящему изобретению не ограничивается вариантами осуществления, описанными ниже, или подробными описаниями этих вариантов осуществления.
[29] Далее настоящее изобретение будет описано со ссылкой на графические материалы.
[30] На фиг. 1 показан вид, на котором проиллюстрирован процесс обжига (S10) и процесс выщелачивания (S20) для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения. На фиг. 2 показан вид, на котором проиллюстрирован процесс удаления примесей (S30) и процесс осаждения целевого вещества (S40) для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения. На фиг. 3 показан вид, на котором проиллюстрирован процесс растворения (S50) и последний процесс удаления примесей (S60) для получения водного раствора, содержащего никель, кобальт и марганец, в соответствии с вариантом осуществления настоящего изобретения.
[31] Как показано на фиг. 1-3, предусмотрен способ, в котором водный раствор, содержащий никель, кобальт и марганец, который может быть использован для изготовления катодно-активного материала литий-ионной вторичной батареи, получают из концентрата (сульфидной никелевой руды) посредством серии процессов. Согласно этому способу возможно улучшить рабочую стабильность и производительность, а также снизить себестоимость производства. Далее соответствующие процессы будут описаны подробно со ссылкой на графические материалы.
[32] Как показано сначала на фиг. 1, может быть выполнен процесс обжига (S10) для превращения концентрата (сульфидной никелевой руды) в обожженную руду (окисленную никелевую руду) и процесс выщелачивания (S20) для выщелачивания ценного металла путем растворения обожженной руды в кислоте.
[33] Процесс обжига (S10)
[34] Процесс обжига (S10) представляет собой процесс превращения сульфидной никелевой руды в оксид с использованием тепла и кислорода, в результате чего образуется окисленная никелевая руда. Процесс обжига (S10) можно осуществлять при температуре 600 градусов C или выше, предпочтительно 700 градусов C или выше.
[37] Если сульфидную никелевую руду выщелачивают в раствор серной кислоты, образуется сульфид водорода (H2S), который является токсичным веществом, как представлено в формуле реакции 1 ниже. Тем не менее, если окисленную никелевую руду выщелачивают в раствор серной кислоты, образуется вода (H2O), как представлено в формуле реакции 2 ниже. Таким образом, если сульфидную никелевую руду превращают в окисленную никелевую руду с помощью процесса обжига (S10), а затем окисленную никелевую руду подвергают процессу выщелачивания (S20), то возможно уменьшить образование токсичного вещества. Кроме того, поскольку свободная энергия Гиббса (ΔG) формулы реакции 1 составляет -8,4 ккал, а свободная энергия Гиббса (ΔG) формулы реакции 2 составляет -22 ккал, формула реакции 2 является термодинамически более стабильной, чем формула реакции 1.
[36] [Формула реакции 1]
[37] NiS + H2SO4 = NiSO4 + H2S
[38] [Формула реакции 2]
[39] NiO + H2SO4 = NiSO4 + H2O
[40] В одном варианте осуществления в процессе обжига (S10) диоксид серы (SO2) может быть получен из сульфидной никелевой руды. После окисления диоксида серы в триоксид серы (SO3) триоксид серы растворяют в воде с получением серной кислоты (H2SO4). Поскольку полученная серная кислота может быть использована в виде раствора, вводимого в процесс выщелачивания (S20), то возможно снижение себестоимости производства.
[41] В одном варианте осуществления процесс обжига (S10) может быть пропущен, а сульфидная никелевая руда может быть непосредственно введена в процесс выщелачивания (S20).
[42] Процесс выщелачивания (S20)
[43] Процесс выщелачивания (S20) представляет собой процесс образования продукта выщелачивания путем растворения обожженной руды, полученной в процессе обжига (S10), в кислом растворе, содержащем серную кислоту или т.п. Процесс выщелачивания (S20) может включать процесс выщелачивания под давлением и процесс нейтрализации (S26). Процесс выщелачивания под давлением представляет собой процесс, в котором ценный металл выщелачивают под давлением путем получения кислого раствора в устройстве под давлением и введения сырья и кислорода в устройство под давлением. Сырьем, используемым в данном случае, может быть окисленная никелевая руда или сульфидная никелевая руда.
[44] В одном варианте осуществления в процессе выщелачивания под давлением может использоваться двухступенчатый способ выщелачивания. Процесс выщелачивания под давлением может представлять собой процесс нагревания и выщелачивания под высоким давлением. Например, процесс выщелачивания под давлением может включать процесс выщелачивания под давлением первой ступени (S22) и процесс выщелачивания под давлением второй ступени (S24). Процесс выщелачивания под давлением первой ступени (S22) и процесс выщелачивания под давлением второй ступени (S24) могут быть выполнены в устройстве под давлением, состоящем из элементов для двух ступеней, или могут быть выполнены в одном устройстве под давлением при изменении только условий процесса (например, температуры, давления или кислотности). Каждый процесс выщелачивания под давлением первой ступени (S22) и процесс выщелачивания под давлением второй ступени (S24) может быть выполнен путем введения кислорода в устройство под давлением.
[45] Ценные металлы могут быть выщелочены из сырья в процессе выщелачивания под давлением первой ступени (S22). Например, ценные металлы, такие как никель, кобальт и марганец в сырье, могут быть выщелочены. Кроме того, такие элементы, как железо, медь, алюминий, цинк или магний в сырье, также могут быть выщелочены. Процесс выщелачивания под давлением первой ступени (S22) может быть выполнен при температуре в диапазоне от 150 до 250 градусов C и при давлении в диапазоне от 8 до 43 бар изб. При указанных выше условиях давления естественное давление пара в зависимости от температуры может находиться в диапазоне от 3 до 38 бар изб. Давление введения кислорода при вышеуказанном условии давления может быть в диапазоне от 2 до 8 бар изб., предпочтительно от 4 до 6 бар изб. В одном варианте осуществления давление введения кислорода при вышеуказанном условии давления может составлять 5 бар изб. Если давление введения кислорода меньше указанного выше диапазона, скорость выщелачивания ценных металлов может снизиться.
[46] Регулируя кислотность фильтрата до 10 г/л или меньше в процессе выщелачивания под давлением первой ступени (S22) является возможным предотвратить чрезмерное выщелачивание железа (Fe), которое является примесью, содержащейся в сырье. Таким образом, дополнительный процесс удаления железа на последнем этапе может не потребоваться. Например, в процессе выщелачивания под давлением первой ступени (S22) концентрация железа (Fe) в растворе может быть в диапазоне от 1 до 3 г/л. В процессе выщелачивания под давлением первой ступени (S22) фильтрат может быть введен в процесс нейтрализации (S26), а остаток может быть впоследствии обработан в процессе выщелачивания под давлением второй ступени (S24). Поскольку процесс выщелачивания под давлением первой ступени (S22) представляет собой процесс снижения кислотности раствора перед процессом нейтрализации (S26), количество нейтрализующего средства, вводимого в процессе нейтрализации (S26), может быть уменьшено.
[47] В процессе выщелачивания под давлением второй ступени (S24) выщелачивание выщелоченного остатка, осажденного в процессе выщелачивания под давлением первой ступени (S22), может проводиться при температуре в диапазоне от 150 до 250 градусов C и давлении в диапазоне от 8 до 43 бар изб. Естественное давление пара и давление введения кислорода в процессе выщелачивания под давлением второй ступени (S24) могут быть такими же, как естественное давление пара и давление введения кислорода в процессе выщелачивания под давлением первой ступени (S22) соответственно.
[48] Кислотность фильтрата в процессе выщелачивания под давлением второй ступени (S24) может быть выше, чем кислотность фильтрата в процессе выщелачивания под давлением первой ступени (S22). Например, степень выщелачивания под давлением может быть увеличена путем регулирования кислотности фильтрата до 50 г/л или больше в процессе выщелачивания под давлением второй ступени (S24). Соответственно, все ценные металлы, содержащиеся в сырье, могут быть выщелочены. Например, никель, кобальт, марганец, железо, медь, алюминий, цинк и магний, содержащиеся в сырье, могут быть выщелочены полностью.
[49] Кроме того, поскольку степень выщелачивания железа увеличивается вследствие повышения кислотности в процессе выщелачивания под давлением второй ступени (S24), концентрация железа (Fe) в растворе увеличивается приблизительно до 5 г/л. Тем не менее, железный компонент можно селективно отделить или осадить, установив кислотность на уровне 50 г/л или выше. В этом случае железо (Fe) осаждается в форме соединения, представляющего собой оксид железа, и удаляется в виде остатка. Например, в кислой атмосфере процесса выщелачивания под давлением второй ступени (S24) в качестве окислителя используется кислород. Железо в растворе окисляется из Fe2+ до Fe3+ и осаждается в форме ярозита или оксида железа.
[50] В одном варианте осуществления фильтрат, образованный в процессе выщелачивания под давлением второй ступени (S24), может быть повторно введен в процесс выщелачивания под давлением первой ступени (S22), как показано на фиг. 1. В этом случае раствор, обладающий кислотностью, пониженной в процессе выщелачивания под давлением первой ступени (S22), направляется в процесс нейтрализации (S26). Таким образом, возможно уменьшить количество вводимого осадка смешанного гидроксида (MHP), который представляет собой нейтрализующее средство, в процессе нейтрализации (S26), тем самым снижая стоимость процесса.
[51] В случае обычно используемого способа выщелачивания при атмосферном давлении время реакции должно длиться 18 часов или дольше, чтобы увеличить степень выщелачивания ценных металлов. В этом случае возникают дополнительные расходы вследствие более широкого использования топлива и пара, а производительность оказывается низкой, поскольку количество перерабатываемого сырья в день является небольшим. Кроме того, при использовании способа выщелачивания под атмосферным давлением железный компонент также выщелачивается, что требует дополнительного процесса удаления железного компонента на более позднем этапе. Тем не менее, в соответствии с вариантом осуществления настоящего изобретения, эффективность выщелачивания ценных металлов может быть улучшена посредством применения двухступенчатого способа выщелачивания под давлением, а последующий процесс (например, дополнительный процесс удаления железа) может быть опущен за счет селективного осаждения железного компонента. Таким образом, возможно снизить себестоимость производства и повысить производительность.
[52] В одном варианте осуществления устройство под давлением может представлять собой установку для автоклавирования. Сырье может быть введено в установку для автоклавирования через ее входное отверстие, а продукт выщелачивания под давлением после реакции может быть выведен наружу установки для автоклавирования через выпускное отверстие. Продукт выщелачивания под давлением может быть направлен в процесс нейтрализации (S26).
[53] В одном варианте осуществления плотность твердого сырья, вводимого в устройство под давлением, может быть 200 г/л или больше. Например, плотность твердого сырья может быть в диапазоне от 200 до 300 г/л. В это время плотность твердого вещества определяется как отношение массы сырья, введенного в устройство под давлением, к объему раствора кислоты, ранее введенного в устройство под давлением. Другими словами, плотность твердого вещества может представлять собой отношение массы введенного сырья к единице растворителя, а также может представлять собой массу сырья на 1 л растворителя.
[54] Осадок смешанного гидроксида (MHP) и кислород могут быть введены в процессе нейтрализации (S26) для регулирования pH продукта выщелачивания под давлением. Осадок смешанного гидроксида (MHP) может быть получен в процессе осаждения целевого вещества (S40), который будет описан позже. В процессе нейтрализации (S26) железо может осаждаться в форме оксида железа. В процессе нейтрализации (S26) pH можно контролировать на уровне 2,5-4,0, и концентрацию железа (Fe) в фильтрате можно контролировать на уровне 100 мг/л или меньше. Процесс нейтрализации (S26) можно осуществлять при температуре 70-90 градусов C в течение 3 часов или больше. Если в процессе нейтрализации (S26) pH меньше 2,5, степень осаждения железа снижается, а количество вводимого осадка смешанного гидроксида (MHP) для повышения pH увеличивается, что может привести к увеличению стоимости процесса.
[55] Поскольку кислота продукта выщелачивания под давлением и осадок смешанного гидроксида (MHP) обладают превосходной реакционной способностью, процесс нейтрализации (S26) может быть проведен за короткое время реакции и при низкой температуре реакции, даже если используется способ выщелачивания под атмосферным давлением.
[56] Поскольку остаток, осажденный в процессе нейтрализации (S26), обладает высоким содержанием ценных металлов, таких как никель, кобальт и марганец, как показано на фиг. 1, остаток может быть повторно введен в устройство под давлением, используемое в процессе выщелачивания под давлением первой ступени (S22). Это позволяет снизить степень потери ценных металлов. Кроме того, поскольку продукт выщелачивания, pH которого слегка повышается в результате процесса нейтрализации (S26), направляется в последующий процесс, возможно уменьшить количество вводимого дополнительного материала для контроля pH в последующем процессе. Продукт выщелачивания, который представляет собой фильтрат, полученный в процессе нейтрализации (S26), направляется в процесс удаления примесей (S30).
[57] Ссылаясь на фиг. 2, может быть проведен процесс удаления примесей (S30) для удаления примесей из продукта выщелачивания и процесс осаждения целевого вещества (S40) для осаждения осадка смешанного гидроксида (MHP).
[58] Процесс удаления примесей (S30)
[59] Процесс удаления примесей (S30) представляет собой процесс удаления примесей, отличных от ценных металлов, из продукта выщелачивания. Процесс удаления примесей (S30) может быть выполнен с помощью нескольких процессов. Например, процесс удаления примесей (S30) может включать по меньшей мере одно из процесса удаления меди (S31), процесса удаления алюминия (S32), процесса экстракции цинка (S33), процесса экстракции магния (S34) и процесса удаления магния (S35), которые выполняются последовательно. Тем не менее, порядок различных процессов процесса удаления примесей (S30) может варьироваться в соответствии с вариантами осуществления и не ограничивается порядком, показанным на графических материалах.
[60] Процесс удаления меди (S31) представляет собой процесс удаления меди (Cu) из раствора путем введения в раствор гидросульфида натрия (NaSH). Медь может быть осаждена в виде соединения сульфида меди (CuS) в результате реакции, представленной формулой реакции 3. После процесса удаления меди (S31) фильтрат может быть направлен в процесс удаления алюминия (S32). Сульфид меди (CuS) может осаждаться при pH выше 1,0. Для этого в процессе удаления меди (S31) pH раствора может поддерживаться при 1,0-2,5. В одном варианте осуществления pH раствора в процессе удаления меди (S31) может поддерживаться при 2,0-2,5. Если pH раствора меньше 1,0 или меньше 2,0, то трудно удалить медь из раствора при 20 мг/л или меньше. Если pH раствора больше 2,5, растворимость никеля в серной кислоте может снизиться и может произойти потеря никеля. В соответствии с вариантом осуществления, если рН раствора поддерживается при 2,5 в процессе удаления меди (S31), потеря никеля может быть минимизирована при удалении меди из раствора до 20 мг/л или меньше.
[61] В одном варианте осуществления гидросульфид натрия (NaSH) можно вводить медленно, чтобы рН раствора не менялся быстро. Например, гидросульфид натрия (NaSH) может быть добавлен в течение 1-2 часов при перемешивании продукта выщелачивания. Соответственно, можно предотвратить увеличение степени потери никеля вследствие быстрого повышения pH раствора в некоторых областях.
[62] В одном варианте осуществления гидросульфид натрия (NaSH) может быть введен в количестве от 1,0 эквивалента (экв.) до 1,5 эквивалента (экв.). Если вводимое количество гидросульфида натрия (NaSH) составляет менее 1,0 эквивалента (экв.), то трудно обеспечить достаточное удаление меди из раствора, поскольку степень удаления меди составляет 98% или меньше. Если вводимое количество гидросульфида натрия (NaSH) превышает 1,5 эквивалента (экв.), степень удаления никеля снижается, поскольку степень удаления никеля составляет 4% или больше. Это не подходит для способа получения материалов для вторичных батарей. В соответствии с вариантом осуществления, если количество вводимого гидросульфида натрия (NaSH) составляет 1,4 эквивалента (экв.) в процессе удаления меди (S31), потеря никеля может быть минимизирована при удалении меди из раствора до 20 мг/л или меньше
[63] При проведении процесса удаления меди (S31) в течение 3 часов или больше при температуре реакции в диапазоне от 60 до 80 градусов C можно снизить осаждение никеля в фильтрате и отделить только медь путем селективного осаждения. Гидросульфид натрия может представлять собой продукт с концентрацией от 30 до 70 вес. %.
[64] [Формула реакции 3]
[65] 2CuSO4 + 2NaSH = 2CuS + Na2SO4 +H2SO4
[66] Процесс удаления алюминия (S32) представляет собой процесс удаления алюминия (Al) из раствора путем введения в раствор гидроксида натрия (NaOH). Алюминий может быть осажден в виде соединения гидроксида алюминия (Al(OH)3) в результате реакции, представленной формулой реакции 4 ниже. После процесса удаления алюминия (S32) фильтрат может быть направлен в процесс экстракции цинка (S33). Если pH составляет 6,0 или больше, никель (Ni) в растворе осаждается в виде соединения гидроксида никеля (Ni(OH)2), что приводит к увеличению степени потери никеля. Таким образом, в процессе удаления алюминия (S32) pH раствора может поддерживаться на уровне 6,0 или меньше, предпочтительно 4,0 или меньше. При проведении процесса удаления алюминия (S32) в течение 8 часов или меньше при температуре реакции в диапазоне от 80 до 90 градусов C можно снизить осаждение алюминия в фильтрате и отделить только медь путем селективного осаждения. Концентрация вводимого гидроксида натрия (NaOH) может быть в диапазоне от 100 г/л до 150 г/л. Если концентрация вводимого гидроксида натрия (NaOH) составляет 100 г/л или меньше, то увеличение количества раствора снижает эффективность процесса, а увеличение количества раствора во всем процессе приводит к увеличению размера установки. В этом случае возрастают начальные капиталовложения, что не является предпочтительным с точки зрения эффективности и экономичности процесса.
[67] [Формула реакции 4]
[68] Al2(SO4)3 + 6NaOH = 2Al(OH)3 + 3Na2SO4
[69] Процесс экстракции цинка (S33), который представляет собой процесс экстракции растворителем первой ступени, представляет собой процесс введения D2EHPA (ди-(2-этилгексил)фосфорной кислоты) в качестве средства для экстракции растворителем при pH 2,0. Процесс экстракции магния (S34), который представляет собой процесс экстракции растворителем второй ступени, представляет собой процесс введения растворителя-экстрагента (D2EHPA) при pH 3,5. Водный раствор, полученный в процессе экстракции растворителем первой ступени, может быть введен в процесс экстракции растворителем второй ступени. Цинк и магний могут быть селективно экстрагированы с помощью органического растворителя посредством реакции, представленной формулой реакции 5 ниже. Каждый процесс экстракции цинка (S33) и процесс экстракции магния (S34) можно проводить при температуре в диапазоне от 30 до 50 градусов C в течение 20 минут или больше.
[70] В процессе экстракции растворителем первой ступени цинк экстрагируется полностью, а марганец экстрагируется на приблизительно 63%. Водный раствор, полученный в процессе экстракции растворителем первой ступени, вводят в процесс экстракции растворителем второй ступени. В процессе экстракции растворителем второй ступени экстрагируется 40% магния или больше и 90% марганца или больше. Водный раствор, полученный в процессе экстракции растворителем второй ступени, содержит никель, кобальт и магний, а также содержит незначительное количество марганца.
[71] Предпочтительный диапазон pH для экстракции цинка в процессе экстракции растворителем первой ступени может составлять от 1,5 до 2,5. Предпочтительный диапазон pH для экстракции магния в процессе экстракции растворителем второй ступени может составлять от 3,0 до 4,0. Если pH меньше 3,0 в процессе экстракции растворителем второй ступени, степень экстракции магния снижается. Таким образом, количество фторида натрия (NaF), добавленного для дополнительного удаления магния в последующем процессе, может увеличиться. Если pH больше 4,0 в процессе экстракции растворителем второй ступени, степень экстракции никеля и кобальта может увеличиваться, и степень потери никеля и кобальта может увеличиваться.
[72] [Формула реакции 5]
[73] 2HR(орг.) + MeSO4(водн.) = MeR2(орг.) + H2SO4(водн.) (Me = Zn или Mg, R = органический растворитель)
[74] Процесс очистки и процесс отделения могут быть последовательно выполнены с первым органическим растворителем после проведения экстракции в процессе экстракции растворителем первой ступени.
[75] В процессе очистки никель и кобальт могут быть восстановлены путем введения цинкового продукта выщелачивания. Цинковый продукт выщелачивания может представлять собой раствор, полученный в процессе плавления цинка. Например, цинковый продукт выщелачивания может представлять собой раствор, полученный путем выщелачивания обожженной руды в серной кислоте в процессе плавления цинка. Поскольку цинк является более реакционноспособным с D2EHPA, чем никель, кобальт, магний, медь и марганец, процесс очистки может обеспечить восстановление никеля и кобальта в водном растворе. Водный раствор, содержащий никель и кобальт, восстановленные таким образом, может быть введен в устройство под давлением, в котором проводится процесс выщелачивания (S20), например, процесс выщелачивания под давлением первой ступени (S22). Таким образом, степень потери никеля и кобальта может быть снижена. Восстановленный таким образом водный раствор может также содержать магний, медь и марганец.
[76] В процессе отделения серную кислоту вводят для отделения цинка от D2EHPA в первом органическом растворителе. Регенерированный и восстановленный D2EHPA может быть снова использован в процессах экстракции растворителем первой ступени и второй ступени. Соответственно, возможна вторичная переработка D2EHPA, за счет чего снижается стоимость процесса. Процесс отделения представляет собой процесс, в котором ионы водорода загружаются в органический растворитель путем реакции серной кислоты с загруженным первым органическим растворителем, а цинк, который является загруженной примесью, восстанавливается в водный раствор.
[77] Процесс отделения может быть выполнен со вторым органическим растворителем после проведения экстракции в процессе экстракции растворителем второй ступени. Процесс отделения для второго органического растворителя может включать этап разделения никеля в водном растворе и D2EHPA во втором органическом растворителе путем введения серной кислоты и этап выщелачивания никеля в водном растворе с помощью процесса селективного осаждения никеля. Процесс селективного выщелачивания никеля может представлять собой процесс осаждения никеля в форме гидроксида никеля (Ni(OH)2) путем введения нейтрализующего средства и повышения pH до 7,5. Остаток после процесса селективного выщелачивания никеля может быть введен в процесс выщелачивания (S20). Таким образом, степень потери никеля может быть снижена.
[78] В одном варианте осуществления, если процесс экстракции растворителем проводится только на одном этапе, цинк, магний и небольшое количество никеля распределяются в растворе для отделения. При проведении процесса селективного выщелачивания никеля цинк и никель осаждаются вместе. Соответственно, цинк продолжает накапливаться, если отдельно не осуществляется процесс селективного удаления цинка, что затрудняет эффективное восстановление никеля. Другими словами, цинк и магний могут быть селективно удалены, если процесс экстракции растворителем проводится в два этапа, а не в один. Это делает возможным повышение эффективности восстановления никеля.
[79] В одном варианте осуществления отношение органического растворителя (O) к водному раствору (A) можно контролировать в зависимости от концентрации компонента, экстрагируемого из раствора. Например, отношение (O:A) органического растворителя (O) к водному раствору (A) может быть в диапазоне от 0,5:1 до 2:1. Например, отношение O:A может составлять 1:1. В этом случае концентрация цинка в растворе может быть снижена до 2 мг/л.
[80] В одном варианте осуществления в процессе экстракции растворителем второй ступени цинк может быть селективно отделен или экстрагирован, и 40% или больше магния может быть селективно отделено или экстрагировано. В процессе экстракции растворителем второй ступени 90% или больше марганца может быть селективно отделено или экстрагировано.
[81] В одном варианте осуществления D2EHPA может находиться в концентрации от 30 до 40 вес. %, а остальные от 60 до 70 вес. % могут представлять собой керосин, например, Escaid 110. Если концентрация D2EHPA больше 40 вес. %, текучесть раствора снижается вследствие высокой вязкости органического растворителя. Это может затруднить расположение труб, подачу водного раствора и перемешивание водного раствора.
[82] Процесс удаления магния (S35) может быть выполнен для дополнительного удаления магния, оставшегося в растворе после процесса экстракции магния (S34). После процесса удаления магния (S35) фильтрат может быть направлен в процесс осаждения целевого вещества (S40). Приблизительно половина магния, присутствующего в водном растворе, удаляется в предыдущем процессе экстракции магния (S34), а оставшийся магний необходимо удалить с помощью дополнительного процесса. Например, процесс удаления магния (S35) представляет собой процесс удаления магния, оставшегося в растворе, путем введения в раствор фторида натрия (NaF). В процессе удаления магния (S35) карбонат натрия (Na2CO3) может быть введен для повышения pH. Магний может быть осажден в виде фторида магния в результате реакции, представленной формулой реакции 6. В процессе удаления магния (S35) магний в растворе может быть удален до 2 мг/л. В процессе удаления магния (S35) pH раствора можно контролировать на уровне 5,2-6,2. При проведении процесса удаления магния (S35) в течение 3 часов или больше при температуре реакции в диапазоне от 50 до 70 градусов C можно снизить осаждение никеля в фильтрате и отделить только магний путем селективного осаждения.
[83] [Формула реакции 6]
[84] MgSO4 + 2NaF = MgF2 + Na2SO4
[85] В одном варианте осуществления фторид натрия может быть введен в количестве 1,4 эквивалента (экв.) или больше. В соответствии с вариантом осуществления, если фторид натрия вводится в количестве 1 эквивалента (экв.), то трудно удалить магний до уровня 2 мг/л или меньше. Тем не менее, при введении 1,4 эквивалента (экв.) фторида натрия, магний может быть удален до уровня 2 мг/л или меньше. То есть, при отсутствии процесса экстракции растворителем второй ступени для удаления всего количества магния необходимо по меньшей мере 2,0 эквивалента (экв.) фторида натрия. В соответствии с вариантом осуществления 1,4 эквивалента (экв.) фторида натрия вводят для снижения содержания магния в растворе до 1,7 мг/л. В одном варианте осуществления количество вводимого фторида натрия в процессе удаления магния (S35) может быть в диапазоне от 1,0 эквивалента (экв.) до 1,5 эквивалента (экв.), что меньше 2,0 эквивалента (экв.).
[86] Процесс осаждения целевого вещества (S40)
[87] В процессе осаждения целевого вещества (S40) карбонат натрия (Na2CO3) может быть введен в фильтрат в качестве нейтрализующего средства после процесса удаления примесей (S30). После удаления примесей никель, кобальт и марганец осаждаются в виде осадка смешанного гидроксида в процессе осаждения целевого вещества (S40). Таким образом, нет необходимости использовать растворитель-экстрагент, используемый в других случаях для селективного экстракции никеля, кобальта и марганца. Никель, кобальт и марганец могут быть осаждены в виде осадка смешанного гидроксида в результате реакции, представленной формулой реакции 7 ниже. Процесс осаждения целевого вещества (S40) можно проводить в течение 4 часов или больше при pH в диапазоне от 9,0 до 10,0 и температуре в диапазоне от 80 до 90 градусов C.
[88] Поскольку никель, кобальт и марганец могут быть восстановлены с помощью процесса осаждения целевого вещества (S40), это позволяет сократить использование дорогостоящих органических растворителей, которые подвержены риску взрыва и возгорания. Таким образом, возможно улучшить рабочую стабильность и производительность, а также снизить себестоимость производства.
[89] [Формула реакции 7]
[90] 3MeSO4 + 3Na2CO3 + 2H2O = MeCO3⋅2Me(OH)2 + 3Na2SO4 + 3CO2 (Me = Ni, Co или Mn)
[91] Поскольку небольшое количество натрия (Na) присутствует в осадке смешанного гидроксида, натрий (Na) может быть удален с помощью процесса двухступенчатой промывки с использованием чистой воды в последующем процессе. Поскольку фильтрат, образующийся в процессе двухступенчатой промывки, повторно используется для производства карбоната натрия (Na2CO3) в качестве нейтрализующего средства, это позволяет снизить себестоимость производства.
[92] Ссылаясь на фиг. 3, может быть выполнен процесс растворения (S50) для растворения осадка смешанного гидроксида (MHP) в кислоте и последний процесс удаления примесей (S60) для удаления следового количества примесей.
[93] Процесс растворения (S50)
[94] В процессе растворения (S50) осадок смешанного гидроксида (MHP) может быть введен в раствор, полученный путем смешивания серной кислоты с чистой водой при кислотности от 150 до 200 г/л. Никель, кобальт, марганец и следовое количество примесей, содержащихся в осадке смешанного гидроксида, могут быть растворены в водном растворе серной кислоты. Водный раствор серной кислоты и осадок смешанного гидроксида (MHP) подвергают реакции до тех пор, пока pH не достигнет 2,0. В одном варианте осуществления пероксид водорода (H2O2) может быть введен для улучшения степени растворения в процессе растворения (S50). В процессе растворения (S50) реакцию можно проводить в течение 4 часов или больше при pH в диапазоне от 1,0 до 3,0 и температуре в диапазоне от 50 до 70 градусов C.
[95] Последний процесс удаления примесей (S60)
[96] Фильтрат после процесса растворения (S50) представляет собой высококачественный водный раствор никеля, кобальта и марганца, но содержит следовое количество примесей в диапазоне от 1 до 20 мг/л. Таким образом, для удаления примесей может быть дополнительно выполнен последний процесс удаления примесей (S60), отличный от первого процесса удаления примесей (S30). Например, последний процесс удаления примесей (S60) может включать процесс удаления меди (S62) и процесс удаления алюминия/железа (S64). Процесс удаления меди (S62) представляет собой процесс введения гидросульфида натрия (NaSH) при pH 2,0. Процесс удаления алюминия/железа (S64) представляет собой процесс введения гидроксида натрия (NaOH) при pH 5,0. В одном варианте осуществления кремний (Si) в растворе также может быть удален путем введения гидроксида натрия. Может быть получен водный раствор, содержащий никель, кобальт и марганец, из которого окончательно удалены примеси с помощью последнего процесса удаления примесей (S60). Водный раствор, содержащий никель, кобальт и марганец, полученный таким образом, может быть использован в предшествующем процессе для получения катодного активного материала для вторичной батареи.
[97] Экспериментальный пример
[98] (1) Качество концентрата никеля, используемого в экспериментах
[99] [Таблица 1]

[100] (2) Сравнение степеней выщелачивания сульфида никеля и оксида никеля в атмосферных условиях
[101] Для сравнения степеней выщелачивания сульфида никеля и оксида никеля в условиях атмосферного давления проводили процесс обжига путем смешивания концентратов A-D из таблицы 1. Результаты выщелачивания сульфида никеля и оксида никеля в растворе серной кислоты приведены в таблице 2 и таблице 3. В таблице 2 показаны степени выщелачивания (%) при начальной кислотности 150 г/л, в таблице 3 показаны степени выщелачивания (%) при начальной кислотности 200 г/л.
[102] Время реакции составляло 18 часов, температуру поддерживали при 95-98 градусах С, а истинную твердого вводимого концентрата поддерживали при 150 г/л.
[103] Поскольку концентрат E в таблице 1 характеризуется содержанием серы (S) 11,2%, то выполнять процесс обжига затруднительно. Даже если процесс обжига будет выполнен, то трудно получить дополнительный материал, пригодный для производства серной кислоты, в отличие от концентратов A-D. Таким образом, концентрат E не подходит для данного эксперимента.
[104] Кроме того, также сравнивали эффективность реакции в зависимости от введения кислорода во время выщелачивания. В примерах эксперимента, приведенных ниже, начальная кислотность может соответствовать кислотности процесса выщелачивания под давлением первой ступени (S22) в одном варианте осуществления настоящего изобретения. Ссылаясь на примеры экспериментов, приведенные в таблице 2 и таблице 3, даже при дальнейшем увеличении начальной кислотности в условиях атмосферного давления трудно дополнительно улучшить степень выщелачивания по сравнению со степенью выщелачивания в условиях под давлением (см. таблицу 4, таблицу 5 и таблицу 6 ниже).
[105] [Таблица 2]

[106] [Таблица 3]

[107] (3) Сравнение степеней выщелачивания сульфида никеля и оксида никеля в условиях под давлением
[108] В таблице 4 приведены результаты сравнения степеней выщелачивания при введении сульфида никеля и оксида никеля в установку для автоклавирования в условиях повышенного давления. Время реакции составляло 3 часа, температура составляла 200 градусов С, а плотность твердого вводимого концентрата поддерживали при 150 г/л. Начальная кислотность составляла 200 г/л. Кроме того, также сравнивали эффективность реакции в зависимости от введения кислорода во время выщелачивания.
[109] Ссылаясь на примеры экспериментов, показанные в таблице 4, при введении окисленной никелевой руды степень выщелачивания железа значительно снижалась при введении кислорода по сравнению с отсутствием его введения. При введении кислорода железо осаждается в форме ярозита и оксида железа в условиях давления при высоких температурах. Таким образом, подтверждается, что степень выщелачивания железа низкая, поскольку железо не выщелачивается в раствор.
[110] [Таблица 4]

[111] (4) Сравнение степеней выщелачивания в зависимости от начальной кислотности, давления и температуры в условиях давления
[112] В таблице 5 и таблице 6 показаны результаты выщелачивания с использованием оксида никеля в условиях давления при изменении начальной кислотности, давления и температуры. В таблице 5 приведены степени выщелачивания в зависимости от начальной кислотности при температуре 220 градусов C и давлении 22 бар изб. + 5 бар изб. (O2). В таблице 6 приведены степени выщелачивания в зависимости от начальной кислотности при температуре 240 градусов C и давлении 32 бар изб. + 5 бар изб. (O2). Кислород вводили в устройство под давлением при давлении введения 5 бар изб. Кислотность готового раствора контролировали на уровне 50-60 г/л.
[113] Ссылаясь на примеры экспериментов, приведенные в таблице 5 и таблице 6, результат сравнения степеней выщелачивания в зависимости от начальной кислотности при различных условиях давления показывал, что степень выщелачивания каждого компонента увеличивается по мере повышения давления. Если начальная кислотность выше, степень выщелачивания железа увеличивалась вместе со степенями выщелачивания никеля, кобальта и т.п. Таким образом, на последнем этапе может потребоваться отдельный процесс для удаления железа. Соответственно, необходимо соответствующим образом регулировать начальную кислотность.
[114] [Таблица 5]
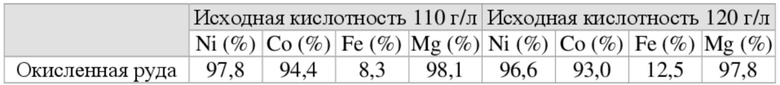
[115] [Таблица 6]

[116] (5) Сравнение эффективности реакции в зависимости от типа нейтрализующего средства, введенного в процесс нейтрализации
[117] В таблице 7 и таблице 8 показаны результаты проведения нейтрального выщелачивания, которое представляет собой процесс нейтрализации, при введении кислорода при 60 нл/час при температуре 85 градусов С. В таблице 7 представлены степени выщелачивания и кислотность в зависимости от времени реакции при использовании окисленной никелевой руды в качестве нейтрализующего средства. В таблице 8 показаны степени выщелачивания и кислотность в зависимости от времени реакции при использовании осадка смешанного гидроксида в качестве нейтрализующего средства. В качестве нейтрализующего средства использовали окисленную никелевую руду или осадок смешанного гидроксида (MHP). Соответствие нейтрализующего средства проверяли путем измерения кислотности и pH фильтрата.
[118] Ссылаясь на примеры экспериментов, приведенные в таблице 7 и таблице 8, можно сделать более коротким время процесса нейтрализации и более эффективно удалять железо при использовании осадка смешанного гидроксида (MHP) в качестве нейтрализующего средства, чем при использовании окисленной никелевой руды в качестве нейтрализующего средства.
[119] В таблице 8, если степень выщелачивания железа характеризуется отрицательным значением, это означает, что железо осаждается.
[120] [Таблица 7]

[121] [Таблица 8]

[122] (6) Степень удаления (%) никеля, кобальта и меди в зависимости от эквивалента (экв.) введения гидросульфида натрия (NaSH)
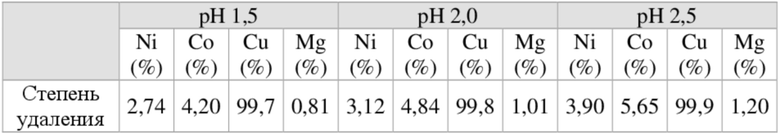
[123] В таблице 9 показаны результаты сравнения степеней удаления меди при введении гидросульфида натрия (NaSH) в количестве 1,2 экв., 1,3 экв. и 1,5 экв. в зависимости от концентрации меди в растворе с целью определения оптимальных условий для введения количества гидросульфида натрия (NaSH). Кроме того, в таблице 10 приведены результаты сравнения степеней удаления меди и степеней потери никеля в зависимости от pH. В таблице 9 показаны степени удаления (%) никеля, кобальта и меди в зависимости от эквивалента введения (экв.) гидросульфида натрия (NaSH). В таблице 10 приведены степени удаления (%) никеля, кобальта, меди и магния из раствора в зависимости от pH. Реакцию проводили при 70 градусах C в течение 3 часов.
[124] Ссылаясь на примеры экспериментов, показанные в таблице 9 и таблице 10, можно увидеть, что степень удаления меди увеличивается по мере увеличения количества вводимого гидросульфида натрия (NaSH) и рН. В соответствии с вариантом осуществления, если количество вводимого гидросульфида натрия (NaSH) установлено на 1,4 эквивалента (экв.) при pH 2,5, потеря никеля может быть минимизирована при удалении меди в растворе до 20 мг/л или меньше.
[125] [Таблица 9]

[126] [Таблица 10]
[127] (7) Сравнение оптимального pH в способе экстракции цинка с использованием D2EHPA
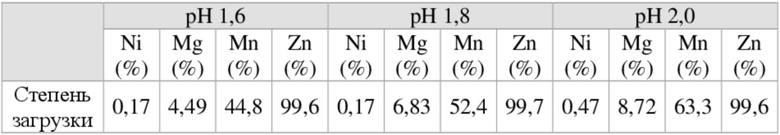
[128] В таблице 11 приведены результаты сравнения степеней удаления примесей при рН 1,6, 1,8 и 2,0. Реакцию проводили при 40 градусах C в течение 20 минут. После перемешивания органического растворителя и водного раствора смесь выдерживали без перемешивания в течение 20 минут для отделения водного раствора и сравнивали степень загрузки примесей в раствор.
[129] Ссылаясь на примеры экспериментов, показанные в таблице 11, при введении D2EHPA степень загрузки цинка составляла 99,6% или больше в диапазоне рН от 1,6 до 2,0. В соответствии с вариантом осуществления, если отношение органического растворителя (O) к водному раствору (A) составляет 1:1 при условии pH 2,0, цинк в растворе может быть удален до 2 мг/л.
[130] [Таблица 11]
[131] (8) Сравнение оптимального pH в способе экстракции магния с использованием D2EHPA
[132] В таблице 12 приведены результаты сравнения степеней удаления примесей при рН 3,0, 3,5 и 3,8. Реакцию проводили при 40 градусах C в течение 20 минут. После перемешивания органического растворителя и водного раствора смесь выдерживали без перемешивания в течение 20 минут для отделения водного раствора и сравнивали степень загрузки примесей в раствор.
[133] Ссылаясь на примеры экспериментов, показанные в таблице 12, при введении D2EHPA степень загрузки магния составляла 40% или больше в диапазоне рН от 3,0 до 3,8.
[134] [Таблица 12]

[135] (9) Степень удаления примесей (%) в зависимости от количества вводимого фторида натрия (NaF)
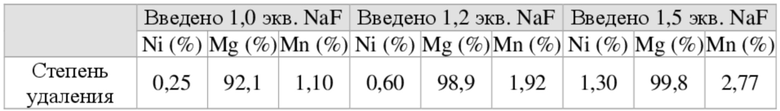
[136] Для определения оптимального количества вводимого фторида натрия (NaF) сравнивали степени удаления компонентов в зависимости от количества вводимого фторида натрия по отношению к магнию. В таблице 13 представлены результаты. Реакцию проводили в течение 3 часов при pH 5,2 и температуре 60 градусов C.
[137] Ссылаясь на примеры экспериментов, показанные в таблице 13, можно увидеть, что оптимальное количество вводимого фторида натрия (NaF) составляло 1,5 эквивалента (экв.).
[138] [Таблица 13]
[139] (10) Степень удаления компонентов (%) в зависимости от pH при введении 1,5 эквивалента (экв.) фторида натрия (NaF)
[140] Для определения оптимального рН фторида натрия проводили сравнение степени удаления компонентов в зависимости от рН раствора. В таблице 14 представлены результаты. Реакцию проводили в течение 3 часов при pH 4,2, 5,2 и 6,2 и температуре 60 градусов C.
[141] Ссылаясь на примеры экспериментов, показанные в таблице 14, можно увидеть, что оптимальный pH находится в диапазоне от 5,2 до 6,2 при введении 1,5 эквивалента (экв.) фторида натрия (NaF).
[142] [Таблица 14]

[143] Хотя варианты осуществления настоящего изобретения были описаны со ссылкой на сопровождающие графические материалы, специалистам в данной области техники, к которой относится настоящее изобретение, будет понятно, что варианты осуществления могут быть реализованы в других конкретных формах без изменения технической сущности или существенных признаков настоящего изобретения.
[144] Следовательно, следует понимать, что варианты осуществления, описанные выше, являются иллюстративными, а не ограничивающими, во всех отношениях. Объем настоящего изобретения определяется формулой изобретения, а не подробным описанием. Следует понимать, что все изменения или модифицированные формы, вытекающие из сути и объема формулы изобретения и ее эквивалентных понятий, включены в объем настоящего изобретения.



Изобретение относится к способу получения водного раствора, содержащего никель, кобальт и марганец, который позволяет восстанавливать никель, кобальт и марганец из сырья и использовать их для изготовления катодно-активного материала литий-ионной вторичной батареи. Способ позволяет восстанавливать ценные металлы, такие как никель, кобальт и марганец, из сырья посредством процесса выщелачивания под давлением, процесса удаления примесей и процесса осаждения целевого вещества, тем самым снижая количество используемого растворителя для экстракции. Техническим результатом является обеспечение стабильной рабочей среды, повышение производительности и снижение себестоимости производства. 16 з.п. ф-лы, 3 ил., 14 табл. 
1. Способ получения водного раствора, содержащего никель, кобальт и марганец, включающий:
процесс выщелачивания, включающий процесс выщелачивания под давлением, заключающийся в выщелачивании сырья с образованием продукта выщелачивания, содержащего никель, кобальт, марганец и примеси;
процесс удаления примесей, заключающийся в удалении примесей из продукта выщелачивания;
процесс осаждения целевого вещества, заключающийся в осаждении осадка смешанного гидроксида, содержащего никель, кобальт и марганец, путем введения нейтрализующего средства в фильтрат, из которого удалены примеси; и
процесс растворения, заключающийся в растворении осадка смешанного гидроксида в кислоте,
где процесс выщелачивания под давлением включает процесс выщелачивания под давлением первой ступени и процесс выщелачивания под давлением второй ступени, заключающийся в выщелачивании под давлением остатка после процесса выщелачивания под давлением первой ступени с кислотностью выше, чем кислотность в процессе выщелачивания под давлением первой ступени, и
процесс удаления примесей, включающий процесс экстракции растворителем первой ступени, заключающийся в селективной экстракции цинка из примесей путем введения первого растворителя-экстрагента, и процесс экстракции растворителем второй ступени, заключающийся в селективной экстракции магния из примесей путем введения второго растворителя-экстрагента.
2. Способ по п. 1, где фильтрат после процесса выщелачивания под давлением второй ступени направляют в процесс выщелачивания под давлением первой ступени.
3. Способ по п. 1, где процесс выщелачивания под давлением проводят при температуре в диапазоне от 150 до 250°C и при давлении в диапазоне от 8 до 43 бар изб.
4. Способ по п. 1, где фильтрат после процесса выщелачивания под давлением первой ступени обладает кислотностью 10 г/л или меньше, и
фильтрат после процесса выщелачивания под давлением второй ступени обладает кислотностью 50 г/л или больше.
5. Способ по п. 1, где в процессе выщелачивания под давлением кислород вводят в устройство под давлением для создания давления в диапазоне от 2 до 8 бар изб.
6. Способ по любому из пп. 1-5, где процесс выщелачивания дополнительно включает процесс нейтрализации, заключающийся в регулировании pH путем введения осадка смешанного гидроксида.
7. Способ по п. 6, где железо в фильтрате после процесса нейтрализации осаждают в форме соединения, представляющего собой оксид железа.
8. Способ по п. 6, где в процессе нейтрализации pH контролируют на уровне 2,5-4,0, при этом концентрация железа составляет 100 мг/л или меньше.
9. Способ по п. 6, где остаток, осажденный в процессе нейтрализации, вводят в процесс выщелачивания под давлением первой ступени.
10. Способ по п. 1, где каждый из первого растворителя-экстрагента и второго растворителя-экстрагента представляет собой D2EHPA (ди-(2-этилгексил)фосфорную кислоту).
11. Способ по п. 1, где процесс удаления примесей дополнительно включает процесс удаления меди, процесс удаления алюминия и процесс удаления магния.
12. Способ по п. 11, где процесс удаления меди включает процесс осаждения меди путем введения гидросульфида натрия (NaSH), и
процесс удаления алюминия включает процесс осаждения алюминия путем введения гидроксида натрия (NaOH).
13. Способ по п. 11, где процесс удаления магния включает процесс дополнительного удаления магния путем введения фторида натрия (NaF) после процесса экстракции растворителем второй ступени.
14. Способ по п. 13, где фторид натрия вводят в количестве 1,4 эквивалента (экв.) или больше.
15. Способ по п. 1, где в процессе осаждения целевого вещества pH контролируют на уровне 9,0-10,0 путем введения нейтрализующего средства.
16. Способ по п. 1, дополнительно включающий
процесс подготовки сырья, заключающийся в подготовке сырья перед процессом выщелачивания,
где процесс подготовки сырья включает процесс обжига, заключающийся в образовании окисленной никелевой руды из сульфидной никелевой руды.
17. Способ по п. 16, где серную кислоту получают с использованием диоксида серы, полученного в процессе обжига, и используют в виде раствора, вводимого в процесс выщелачивания.
| Устройство для прерывания программ | 1986 |
|
SU1336003A1 |
| CN106848474 B, 09.07.2021 | |||
| KR102154599 B1, 10.09.2020 | |||
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ, СОДЕРЖАЩИХ НИКЕЛЬ ИЛИ КОБАЛЬТ | 2017 |
|
RU2726618C1 |
| JP2008013387 A, 24.01.2008 | |||
| СПОСОБ ИЗВЛЕЧЕНИЯ НИКЕЛЯ И КОБАЛЬТА ИЗ СИЛИКАТНЫХ НИКЕЛЬ-КОБАЛЬТОВЫХ РУД | 2011 |
|
RU2465449C1 |
Авторы
Даты
2024-04-10—Публикация
2024-01-11—Подача