Предлагаемое изобретение относится к медицине и вирусологии и может быть применено в лабораторной диагностике для обнаружения всех подтипов вируса гриппа А и В, а также для выявления специфических антител к этим вирусам с помощью тест-системы, основанной на сиалированных полимерных микросферах, в реакциях латекс-агглютинации и торможения латекс-агглютинации.
Известно, что многие вирусы обладают гемагглютинирующими свойствами, например вирусы гриппа, арбовирусы, парагриппа, осповакцины, краснухи и других [1]. Рутинные классические способы на основе реакции гемагглютинации (РГА) и реакции торможения гемагглютинации (РТГА) являются золотым стандартом для детекции всех типов вируса гриппа и нейтрализующих антител к этим вирусам. Обе реакции основаны на способности поверхностного гликопротеина гемагглютинина вируса гриппа взаимодействовать с сиаловыми остатками, расположенными на мембранных белках эритроцитов крови млекопитающих и птиц. Взаимодействие вируса с эритроцитами приводит к их агглютинации, что можно наблюдать по изменению свойств сформированного осадка этих клеток: в отсутствии такого взаимодействия происходит накопление осадка в центре U-образной или V-образной лунки планшета, а при взаимодействии вируса осадок распределяется по всей поверхности дна лунки. В случае РГА к эритроцитам добавляется только суспензия вируса, в случае РТГА к эритроцитам добавляется суспензия вируса в смеси с антителами, которые могут предотвращать взаимодействие вируса с эритроцитами [2].
Недостатком РГА и РТГА является необходимость использования эритроцитов кур, морской свинки, лошади, человека или др., то есть требуется наличие доноров крови. Более того, приготовленная суспензия эритроцитов сохраняется в рабочем состоянии достаточно ограниченное время - в течение нескольких суток. Для РТГА существуют коммерчески доступные препараты инактивированных вирусов, позволяющие выявлять специфические антитела. Например, такие препараты выпускаются ООО «Предприятие по производству диагностических препаратов» (Санкт-Петербург, Россия).
В настоящее время известны тест-системы для выявления различных патогенов помощью реакции латекс-агглютинации (РЛА). Например, такие тест-системы созданы для детекции патогенных штаммов E.coli [3], возбудителя мелиоидоза [4] и менингита [5], возбудителей лептоспироза [6], легионелл [7] и других патогенов. В них используют полимерные микросферы, конъюгированные со специфическими антителами к определенному патогену. Агглютинация таких микросфер в присутствии патогена происходит за счет специфической реакции «антиген-антитело».
Прототипом предлагаемого изобретения может служить тест-система на основе полимерных микросфер, а именно: полистироловых частиц с иммобилизованными на их поверхности специфическими антителами, для выявления штаммов вируса гриппа А, содержащих гемагглютинин пятого подтипа (Н5) [8]. Недостатком этой, основанной на использовании полимерных микросфер тест-системы, является невозможность ее использования для выявления других подтипов вируса гриппа в силу специфического взаимодействия иммобилизованных антител только с одним подтипом гемагглютинина.
Реакция торможения латекс-агглютинации (РТЛА) используется в коммерчески доступном тесте для выявления хорионического гонадотропина в моче. В нем присутствуют два компонента: полимерные микросферы с иммобилизованным хорионическим гонадотропином и специфические антитела к этому гормону. При наличии свободного гормона в исследуемом материале происходит взаимодействие антител с ним, что приводит к отсутствию агрегации микросфер [9]. Для вирусов гриппа тест-системы на основе реакции торможения латекс-агглютинации неизвестны.
В настоящее время неизвестно ни одной стабильной универсальной тест-системы, позволяющей выявлять все подтипы вируса гриппа А и В с помощью латекс-агглютинации или антител к ним в реакции торможения латекс-агглютинации.
Сущность предлагаемого ИЗО
Настоящее изобретение, в отличие от предшествующих разработок, основанных иммобилизации на микросферах специфических антител, заключается в разработке способа создания нового реагента для выявления латекс-агглютинирующей активности всех подтипов вирусов гриппа А и В, способа детекции всех подтипов вирусов гриппа А и В с помощью латекс-агглютинирующей активности, а также способа детекции специфических антител к любым подтипам вирусов гриппа А и В с помощью реакции торможения латекс-агглютинации и создании тест-системы для выявления всех подтипов вирусов гриппа А и В в РЛА и антител к этим вирусам в РТЛА.
Технический результат
Настоящая разработка решает задачу выявления всех подтипов вирусов гриппа А и В, а также специфических антител к ним с помощью чувствительной диагностической системы, основанной на агглютинации полимерных сиалированных микросфер и обладающей стабильностью при длительном хранении (не менее полугода). Изобретение основано на иммобилизации белка, содержащего сиаловые остатки, на полимерных микросферах, что позволяет выявлять все типы и подтипы вирусов гриппа А и В, а также нейтрализующие антитела к ним.
В предлагаемой разработке полимерные сиалированные микросферы - это частицы сферической формы размером 0,1 - 10 мкм, состоящие из аморфного полимера, в частности - полистирола, несущие на своей поверхности сиалированный гликопротеин.
Краткое описание чертежей
На фиг. 1 представлены результаты латекс-агглютинации:
А - отсутствие агглютинации, т.е. агрегации сиалированных полимерных микросфер, после инкубации с незараженной аллантоисной жидкостью, взятой в качестве контроля;
Б - агрегация сиалированных полимерных микросфер после инкубации суспензии вируса гриппа А в аллантоисной жидкости.
Далее приводятся примеры. Однако эти примеры не должны рассматриваться как некое ограничение объема настоящего изобретения во всех отношениях.
Пример 1. Способ получения полимерных сиалированных микросфер
Для изготовления таких микросфер были выбраны полистирольные микросферы диаметром 1,5 мкм концентрацией 5,2×1010 частиц на 1,0 мл и сиалированный гликопротеин, например - фетуин из эмбриональной сыворотки крупного рогатого скота. Связывание сиалированного гликопротеина с микросферами проводили по следующему протоколу:
1. Полистироловые микросферы промывали фосфатно-солевым буфером (ФСБ) (рН 7,2 - 7,6) не менее двух раз с помощью центрифугирования суспензии микросфер на скорости 10 000 g в течение одной минуты, затем супернатант удаляли и осадок ресуспендировали в ФСБ.
2. Готовили 1% раствор сиалированного гликопротеина, например фетуина, на ФСБ.
3. К полученному осадку микросфер добавляли 1% раствор этого белка, приготовленного на ФСБ из расчета 1,0 мл раствора белка на 1,0×109 полистирольных микросфер и инкубировали при комнатной температуре при постоянном перемешивании 1 час.
4. Далее полученные полистирольные сиалированные микросферы осаждали на скорости 10 000g в течение одной минуты, не менее двух раз промывали и ресуспендировали в ФСБ в концентрации на 1,0×108 частиц на 1,0 мл.
5. Для предотвращения бактериальной контаминации в суспензию полистирольных сиалированных микросфер добавляли бактерицидный агент, например тиомерсал до концентрации 0,005%. Суспензию хранили при температуре +4°С. Стабильность этой суспензии сохранялась не менее полугода и ее бактериальная контаминация не выявлена.
Пример 2. Исследование агглютинирующей активности вирусов гриппа с помощью предлагаемой реакции латекс-агглютинации
Проведение РЛА проводили по следующему протоколу:
10,0 мкл суспензии полистирольных сиалированных микросфер, полученных в Примере 1, смешивали с 10,0 мкл суспензии тестируемого вируссодержащего материала и инкубировали при +4°С в течение 50 мин в микропробирке. Затем добавляли равный объем 6% раствора параформальдегида, приготовленного на ФСБ, и инкубировали 10 мин при комнатной температуре.
Агглютинацию, то есть агрегацию индивидуальных полистирольных сиалированных микросфер, анализировали с помощью световой микроскопии, например фазово-контрастной микроскопии с помощью инвертированного микроскопа. Для этого использовали один из двух вариантов изготовления микроскопических препаратов:
1) 4,0 мкл суспензии агрегированных латексных частиц наносили на предметное стекло и накрывали покровным стеклом; или
2) к объему 20,0 мкл суспензии добавляли 30,0 мкл ФСБ и переносили смесь в лунку плоскодонного 96-луночного планшета, например планшета фирмы «Costar» (США).
Результат латекс-агглютинации оценивали как наличие или отсутствие агглютинации сиалированных полимерных микросфер (фиг. 1).
Результат латекс-агглютинации оценивают либо качественно: как наличие или отсутствие агрегации, либо количественно: как долю сиалированных микросфер в препарате, находящихся в агрегированном состоянии.
Пример 3. Исследование вирусов гриппа с помощью реакции гемагглютинации
В тесте использованы 12 вирусов гриппа А разных подтипов гемагглютинина и два вируса гриппа В различных эволюционных линий («ямагатской» и «викторианской»). Исследование проводили стандартным методом с использованием куриных эритроцитов. В качестве контролей были использованы ФСБ (контроль 1) и аллантоисная жидкость из незараженного эмбриона (контроль 2). Результаты представлены в Таблице 1 как максимальное разведение суспензии вируса, при котором детектирована агглютинация эритроцитов.
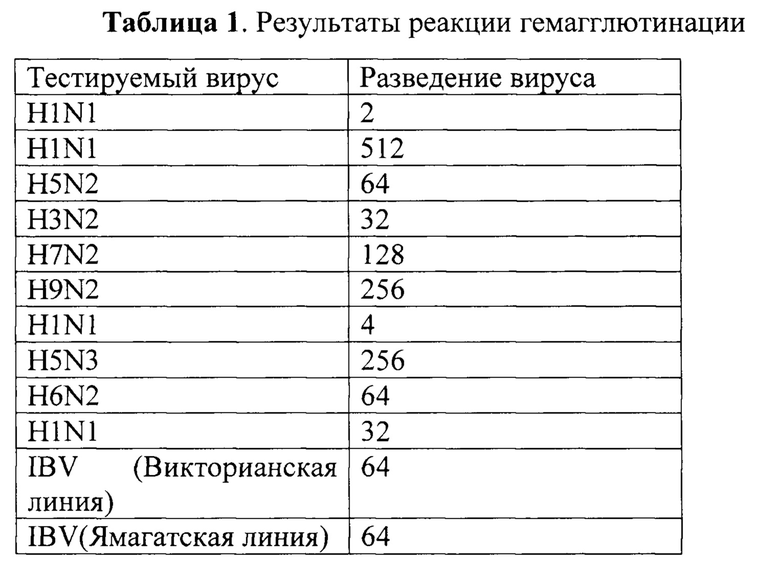
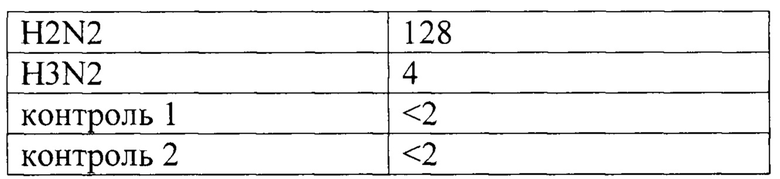
Из таблицы видно, что все протестированные вирусы вызывают агглютинацию эритроцитов, при этом в контроле агглютинация отсутствует.
Пример 4. Исследование вирусов гриппа с помощью реакции латекс-агглютинации
С помощью полистирольных сиалированных микросфер, полученных в Примере 1 и способом, описанным в Примере 2, проведена реакция латекс-агглютинации с вирусами, указанными в Примере 3. В качестве контролей были использованы ФСБ (контроль 1) и аллантоисная жидкость из незараженного эмбриона (контроль 2). Результаты представлены в Таблице 2 как максимальное разведение суспензии вируса, при котором детектирована латекс-агглютинация.

Из таблицы видно, что все протестированные вирусы вызывают агглютинацию полистирольных сиалированных микросфер, при этом в контроле агглютинация отсутствует.
Пример 5. Сравнительное исследование результатов, полученных в реакции гемагглютинации и реакции латекс-агглютинации
Результаты, полученные в Примере 3 и Примере 4, сведены в таблицу 3. Статистическое исследование результатов проводили с помощью программы Statistica 12. Анализ показал, что значения разведений вирусов, полученные в РГА и РЛА, достоверно коррелировали (р<0,05) между собой с очень высоким коэффициентом корреляции (R=0,94).
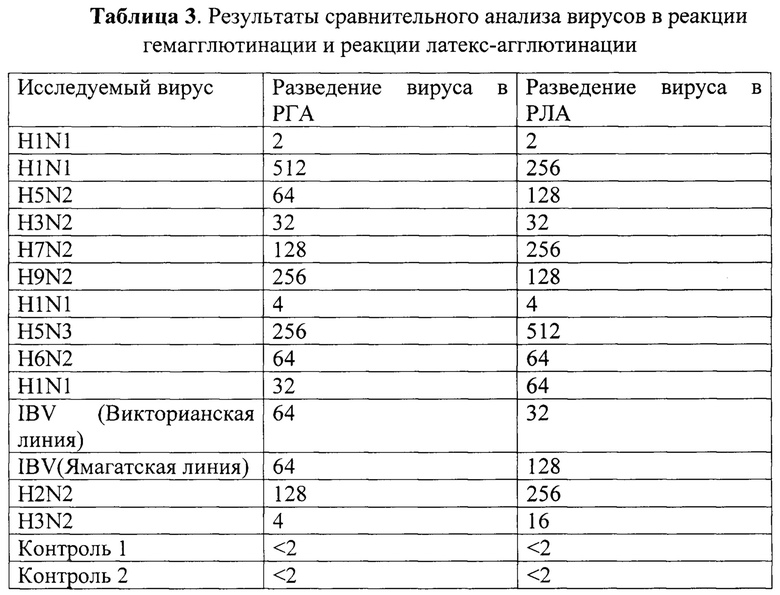
Из таблицы видно, что результаты РЛА и РГА очень близки, разница для всех исследованных вирусов не превышала одно разведение. Таким образом, РЛА адекватный метод и может заменять метод РГА в исследованиях.
Пример 6. Реакция торможения гемагглютинации
С этой целью были получены иммунные сыворотки к пяти вариантам вируса гриппа А подтипа H7N2. Для этого белые беспородные мыши были иммунизированы исходным вирусом A/Chicken/NJ/294598 - 12/2004-МА (H7N2), либо одним из его четырех мутантов, содержащих аминокислотные замены в гемагглютинине. Для полученных пяти сывороток (обозначенных как сыворотка №1 - №5) была проверена нейтрализующая активность против всех пяти использованных для вакцинации вариантов вируса (обозначенных как вирус №1 - №5) стандартным методом торможения гемагглютинации (РТГА) с помощью куриных эритроцитов.
Результаты РТГА представлены в Таблице 4 как максимальные разведения сывороток, при которых детектировано торможение гемагглютинации для каждого из исследованных вирусов.
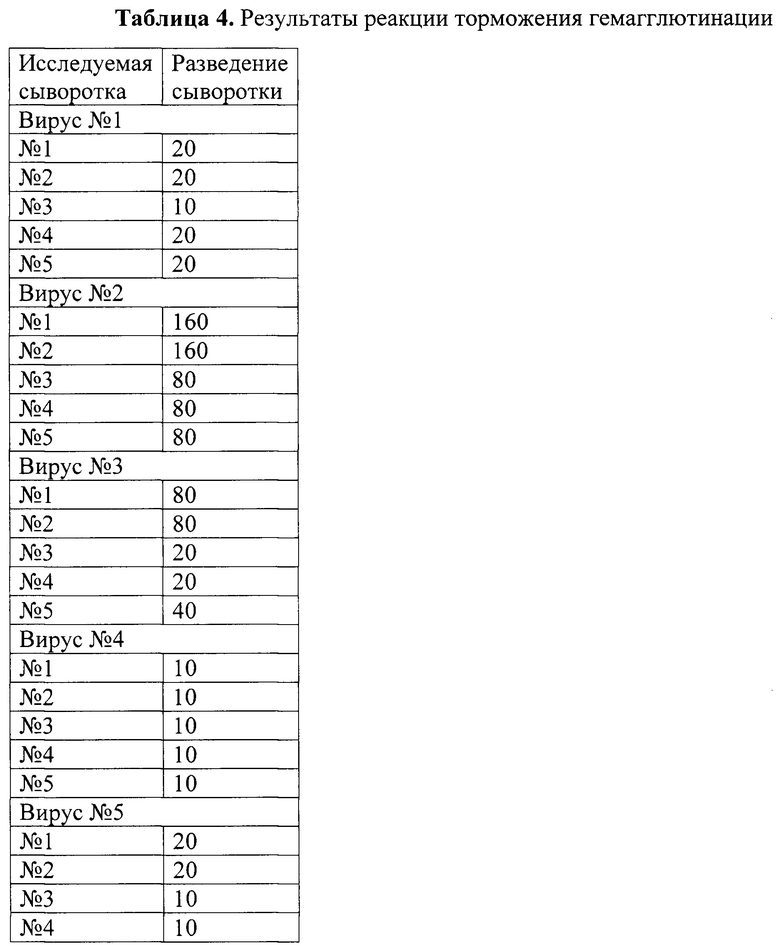
Из таблицы видно, что все протестированные сыворотки предотвращают агглютинацию эритроцитов исследованными вирусами.
Пример 7. Реакция торможения латекс-агглютинации
С помощью полистирольных сиалированных микросфер, полученных в Примере 1, и способом, описанным в Примере 2, исследована нейтрализующая активность мышиных поликлональных сывороток, полученных в Примере 6, в отношении пяти вирусов подтипа H7N2, указанных в Примере 6. Результаты реакции торможения латекс-агглютинации (РЛГА) представлены в Таблице 5 как максимальные разведения сывороток, при которых детектировано торможение агглютинации для каждого из исследованных вирусов.
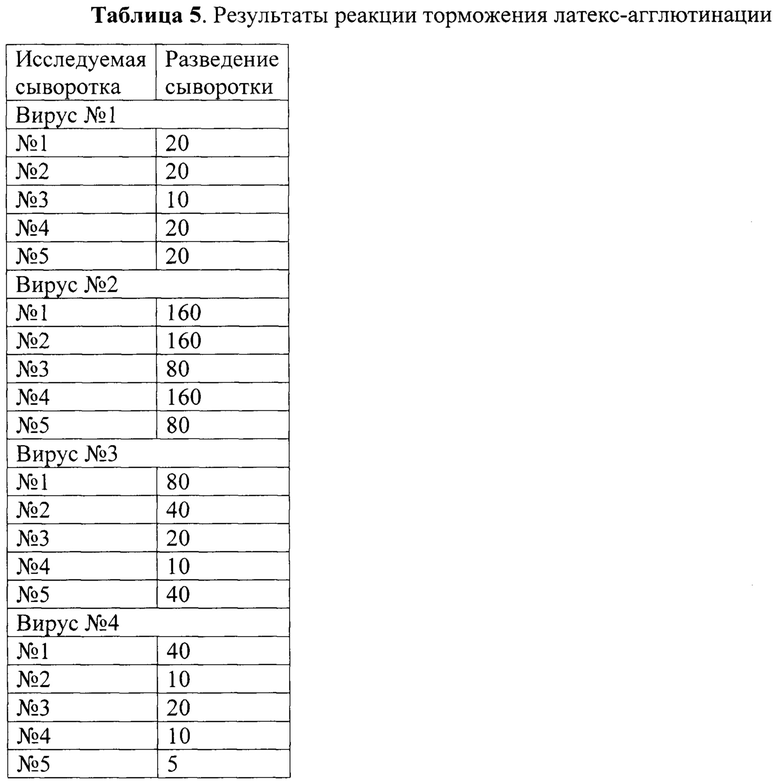

Из таблицы видно, что все протестированные сыворотки предотвращают агглютинацию сиалированных полимерных микросфер исследованными вирусами.
Пример 8. Сравнительное исследование результатов, полученных в реакции РТГА и РТЛА
Результаты, полученные в Примерах 6 и 7, сведены в Таблицу 6. Статистическое исследование результатов проводили с помощью программы Statistica 12. Анализ показал, что значения, полученные в РТГА и РТЛА, достоверно коррелировали (р<0,05) с высоким коэффициентом корреляции (R=0,74).
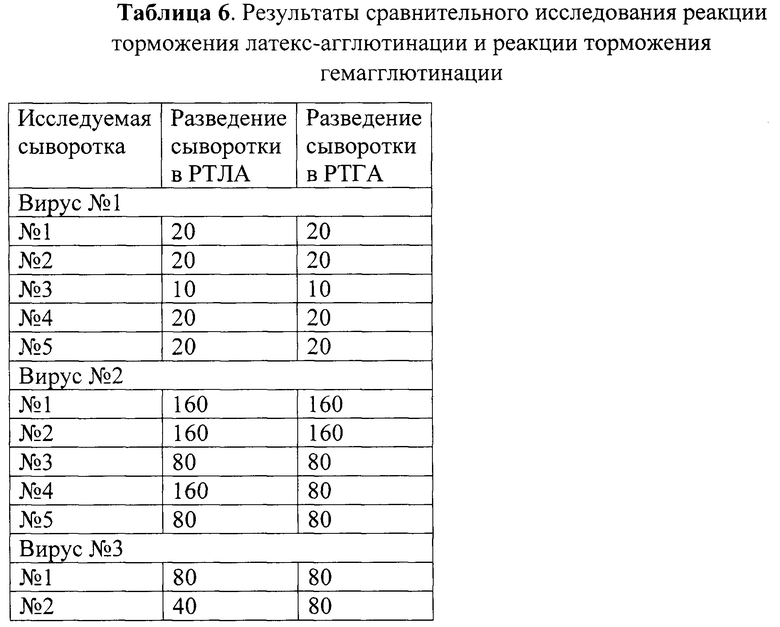
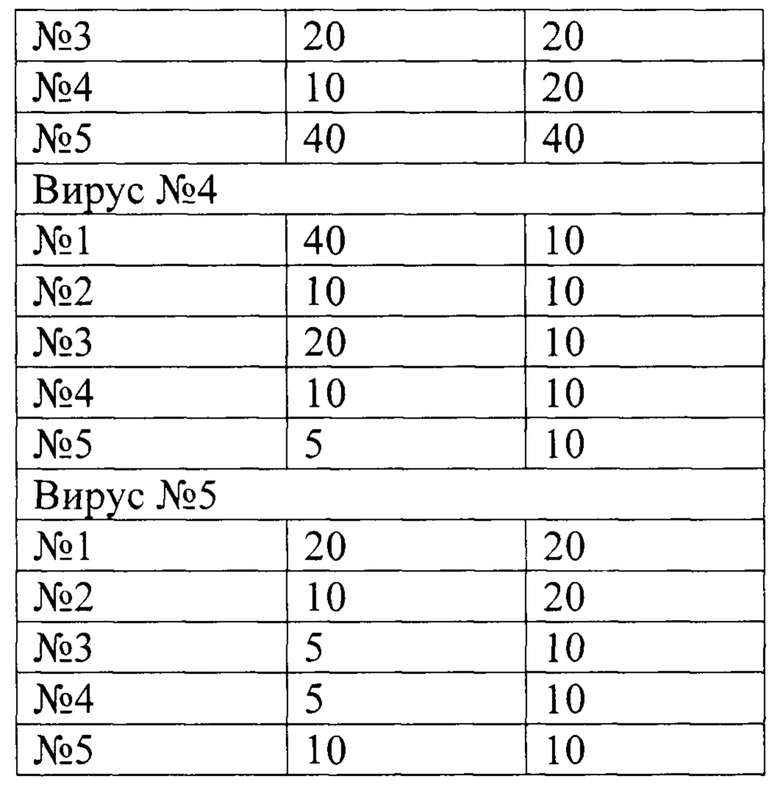
Из таблицы видно, что результаты РТЛА и РТГА близки, разница для всех исследованных сывороток не превышала два разведения. Таким образом, РТЛА - адекватный метод детекции нейтрализующей активности антител, по чувствительности не уступает РТГА, и может заменять метод РТГА в исследованиях.
Таким образом, предлагаемый способ детекции, основанный на агглютинации полимерных сиалированных микросфер при взаимодействии с исследуемым вирусом, является универсальным и адекватным способом для выявления агглютинирующей активности всех подтипов вирусов гриппа А и В. Реакция латекс-агглютинации и реакция торможения латекс-агглютинации с использованием предлагаемых микросфер может заменять или дополнять реакцию гемагглютинации и реакцию торможения гемагглютинации в лабораторной практике. Предлагаемые способы будут менее ресурсозатратными по сравнению с рутинными. В частности, они не требуют использования эритроцитов животных. Созданная тест-система на их основе стабильна и сохраняет все необходимые свойства без изменений при хранении на протяжении, по крайней мере полгода, что позволяет производить такой диагностикум в промышленном масштабе.
Список литературы
1. Дерябин П.Г., Бутенко A.M., Бурцева Е.И. Реакция гемагглютинации и торможения гемагглютинации / Под ред. академика РАН Д.К. Львова // Руководство по вирусологии: Вирусы и вирусные инфекции человека и животных. Москва: Медицинское информационное агентство, 2013. Стр. 426-430
2. Palmer D.F., Dowdle W.R., Coleman M.T. and Schild G.C. (1975): Advanced laboratory techniques for influenza diagnosis. U.S. Department of Health, Education, and Welfare, immunology series no. 6. Centers for Disease Control, Atlanta, GA.
3. Hajra T.K., Bag P.K., Das S.C., Mukherjee S., Khan A., Ramamurthy T. Development of a simple latex agglutination assay for detection of shiga toxin-producing Escherichia coli (STEC) by using polyclonal antibody against STEC. Clin Vaccine Immunol. 2007;14(5):600-604. doi:10.1128/CVI.00342-06D. M. Frolov, Т.V. Senina, Т.V. Zamarina, N.
4. P. Khrapova, Application of Latex-Agglutination for Rapid Detection of Pathogenic Burkholderia. Problems of Particularly Dangerous Infections. 2019 (3). doi.org/10.21055/0370-1069-2019-3-106-110
5. Poplin V., Boulware D.R., Bahr N.C. Methods for rapid diagnosis of meningitis etiology in adults. Biomark Med. 2020;14(6):459-479. doi:10.2217/bmm-2019-0333
6. Патент RU 2177617 СПОСОБ ПРИГОТОВЛЕНИЯ ЛЕПТОСПИРОЗНОГО ДИАГНОСТИКУМА ДЛЯ ПОСТАНОВКИ РЕАКЦИИ ЛАТЕКС-АГГЛЮТИНАЦИИ
7. Sedgwick А.K., Tilton R.C. Identification of Legionella pneumophila by latex agglutination. J Clin Microbiol. 1983 Feb;17(2):365-8. doi:10.1128/jcm.17.2.365-368.1983.
8. Chen J., Jin M., Yu Z. et al. A Latex Agglutination Test for the Rapid Detection of Avian Influenza Virus Subtype H5N1 and its Clinical Application. Journal of Veterinary Diagnostic Investigation. 2007;19(2):155-160. doi:10.1177/104063870701900203
9. Lim P.L., Choy W.F. An improved latex agglutination-inhibition test for the detection of human chorionic gonadotropin in urine. J Immunol Methods. 1989 Feb 8;117(1):137-9. doi:10.1016/0022-1759(89)90128-2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНОГО ДИАГНОСТИКУМА ДЛЯ ПОСТАНОВКИ РЕАКЦИИ ЛАТЕКС-АГГЛЮТИНАЦИИ | 2004 |
|
RU2270449C1 |
| Диагностический набор для выявления антител к вирусу гриппа птиц и идентификации подтипа гемагглютинирующего вирусного агента в реакции торможения гемагглютинации | 2023 |
|
RU2815532C1 |
| СПОСОБ ПОСТАНОВКИ РЕАКЦИИ ЛАТЕКСНОЙ АГГЛЮТИНАЦИИ | 2001 |
|
RU2198407C2 |
| Диагностический набор для выявления антител к вирусу гриппа птиц подтипа Н9 в реакции торможения гемагглютинации | 2020 |
|
RU2738900C1 |
| Способ получения бруцеллезного полистирольного латексного диагностикума | 2022 |
|
RU2798124C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНЫХ АНТИГЕННЫХ ДИАГНОСТИКУМОВ ДЛЯ ВЫЯВЛЕНИЯ АНТИТЕЛ ПРОТИВ ВОЗБУДИТЕЛЕЙ БРУЦЕЛЛЕЗА, ТУЛЯРЕМИИ | 2021 |
|
RU2777803C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЛЕПТОСПИРОЗНОГО ДИАГНОСТИКУМА ДЛЯ ПОСТАНОВКИ РЕАКЦИИ ЛАТЕКС-АГГЛЮТИНАЦИИ | 2000 |
|
RU2177617C1 |
| СПОСОБ ЭКСПРЕСС-ДИАГНОСТИКИ ТУБЕРКУЛЕЗА НА ОСНОВЕ РЕАКЦИИ ЛАТЕКС-АГГЛЮТИНАЦИИ | 1998 |
|
RU2130615C1 |
| ДИАГНОСТИЧЕСКАЯ ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ВИРУСА ГРИППА ПТИЦ А/Н5N1 | 2006 |
|
RU2339694C2 |
| РЕАССОРТАНТНЫЙ ШТАММ ВИРУСА ГРИППА RN9/13-HUMAN A(H6N9) ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К НЕЙРАМИНИДАЗЕ ПРИ ГРИППОЗНОЙ ИНФЕКЦИИ И ВАКЦИНАЦИИ | 2014 |
|
RU2587629C1 |

Изобретение относится к медицине и вирусологии. Описана тест-система для детекции подтипов вирусов гриппа А и В в реакции латекс-агглютинации или для детекции специфических антител к этим подтипам вирусов гриппа в реакции торможения латекс-агглютинации. Тест-система включает сиалированные полимерные микросферы, созданные путем адсорбции сиалированного гликопротеина поверхности полистирольных микросфер, которые промывают фосфатно-солевым буфером рН 7,4, центрифугируя в течение 30 с на скорости 10000g, затем к полученному осадку промытых микросфер добавляют 1% раствор сиалированного гликопротеина на фосфатно-солевом буфере, до конечной концентрации 1,0 х109 полистирольных микросфер на 1,0 мл раствора, затем эти микросферы инкубируют в растворе сиалированного гликопротеина в течение 1 ч при постоянном перемешивании при комнатной температуре и осаждают центрифугированием в течение 30 с на скорости 10000g, далее промывают фосфатно-солевым буфером и ресуспендируют в фосфатно-солевом буфере с конечной концентрацией 1,0 х108 сиалированных микросфер на 1,0 мл, для стабилизации полученной суспензии в нее добавляют бактерицидный агент и хранят при температуре +4°С. Изобретение отличается от предшествующих разработок, основанных на иммобилизации на микросферах специфических антител тем, что в ней используют новый реагент для выявления латекс-агглютинирующей активности любых подтипов вирусов гриппа А и В. Также описан способ детекции в реакции латекс-агглютинации подтипов вирусов гриппа А и В с помощью тест-системы, заключающийся в смешивании 10,0 мкл суспензии вируса с 1,0 х106 сиалированными полимерными микросферами и инкубации полученной смеси 50 мин при температуре +4°С, в которую затем добавляют равный объем 6% раствора параформальдегида, приготовленного на фосфатно-солевом буфере, смесь фиксируют при комнатной температуре 10 мин и анализируют фиксированный материал методом световой микроскопии. Изобретение расширяет арсенал средств лабораторной диагностики для обнаружения любых подтипов вируса гриппа А и В. 3 н. и 2 з.п. ф-лы, 1 ил., 6 табл., 5 пр.
1. Тест-система для детекции подтипов вирусов гриппа А и В в реакции латекс-агглютинации или для детекции специфических антител к этим подтипам вирусов А и В в реакции торможения латекс-агглютинации, главный компонент которой - сиалированные полимерные микросферы, созданные путем адсорбции сиалированного гликопротеина поверхности полистирольных микросфер, которые промывают фосфатно-солевым буфером рН 7,4, центрифугируя в течение 30 с на скорости 10000g, затем к полученному осадку промытых микросфер добавляют 1% раствор сиалированного гликопротеина на фосфатно-солевом буфере, до конечной концентрации 1,0×109 полистирольных микросфер на 1,0 мл раствора, затем эти микросферы инкубируют в растворе сиалированного гликопротеина в течение 1 ч при постоянном перемешивании при комнатной температуре и осаждают центрифугированием в течение 30 с на скорости 10000g, далее промывают фосфатно-солевым буфером и ресуспендируют в фосфатно-солевом буфере с конечной концентрацией 1,0×108 сиалированных микросфер на 1,0 мл, для стабилизации полученной суспензии в нее добавляют бактерицидный агент и хранят при температуре +4°С.
2. Тест-система по п. 1, в которой в качестве сиалированного гликопротеина, предназначенного для создания сиалированных полимерных микросфер, используют фетуин.
3. Тест-система по пп. 1, 2, в которой для главного компонента в качестве бактерицидного агента используют тиомерсал, добавляемый до конечной концентрации 0,005%.
4. Способ детекции в реакции латекс-агглютинации подтипов вирусов гриппа А и В с помощью тест-системы по пп. 1-3, заключающийся в смешивании 10,0 мкл суспензии вируса с 1,0 ×106 сиалированными полимерными микросферами и инкубации полученной смеси 50 мин при температуре +4°С, в которую затем добавляют равный объем 6% раствора параформальдегида, приготовленного на фосфатно-солевом буфере, смесь фиксируют при комнатной температуре 10 мин и анализируют фиксированный материал методом световой микроскопии.
5. Применение тест-системы по пп. 1-3 для детекции подтипов вируса гриппа А и В.
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНОГО ДИАГНОСТИКУМА ДЛЯ ПОСТАНОВКИ РЕАКЦИИ ЛАТЕКС-АГГЛЮТИНАЦИИ | 2004 |
|
RU2270449C1 |
| Тест-система на основе конъюгатов "полимерная микросфера-тиреоглобулин" для экспресс-диагностики аутоиммунных заболеваний щитовидной железы | 2017 |
|
RU2657834C1 |
| WO 2011117848 A1, 29.09.2011. | |||
Авторы
Даты
2024-04-12—Публикация
2022-07-25—Подача