Область техники, к которой относится изобретение
Настоящая заявка относится к области генетики, генной терапии и молекулярной биологии. Более конкретно, настоящее изобретение относится к нуклеиновой кислоте, которая кодирует слитый белок на основе FVIII-BDD (фактор свертывания крови VIII с делетированным В доменом) и гетерологичного сигнального пептида, экспрессионной кассете и вектору на ее основе, клетке-хозяину для получения слитого белка на основе FVIII-BDD и гетерологичного сигнального пептида, а также к различным применениям вышеуказанного вектора.
Уровень техники
Гемофилия - это рецессивное, Х-сцепленное, врожденное нарушение, ведущее к дефициту одного из белков, участвующих во вторичном гемостазе. Гемофилия А, или классическая гемофилия, - наиболее распространенная форма гемофилии; встречается у 1 из 5000 новорожденных мальчиков (Report on the annual global survey 2019, WFH https://www.wfh.org/en/our-work-research-data/annual-global-survey) и обусловлена дефицитом белка фактора свертывания VIII. Согласно данным Всероссийского общества гемофилии, в России насчитывается более 6,5 тыс.пациентов с гемофилией A (Report on the annual global survey 2019, WFH).
Фактор свертывания VIII (FVIII) - это белок размером 280 кДа, который секретируется в кровь преимущественно из синусоидальных эпителиальных клеток печени (Fahs SA, Hille МТ, Shi Q, Weiler H, Montgomery RR. A conditional knockout mouse model reveals endothelial cells as the principal and possibly exclusive source of plasma factor VIII/ Blood. 2014 Jun 12;123(24):3706-13. doi: 10.1182/blood-2014-02-555151. Epub 2014 Apr 4. PMID: 24705491 и Everett LA, Cleuren AC, Khoriaty RN, Ginsburg D. Murine coagulation factor VIII is synthesized in endothelial cells/ Blood. 2014 Jun 12;123(24):3697-705. doi: 10.1182/blood-2014-02-554501. Epub 2014 Apr 9. PMID: 24719406). Активированный FVIII циркулирует в организме в виде гетеродимера, состоящего из тяжелой (домены A1, А2, В) и легкой (домены A3, C1, С3) цепей, связанных друг с другом за счет нековалентных металл-зависимых взаимодействий. В результате процессинга FVIII в активированной форме белка присутствуют только домены А1-А3, C1, С2. Этот факт способствовал созданию рекомбинантного FVIII с удаленным В доменом (FVIII-BDD), который не уступает по своей активности полноразмерному FVIII (Pittman DD, Alderman EM, Tomkinson KN, Wang JH, Giles AR, Kaufman RJ. Biochemical, immunological, and in vivo functional characterization of B-domain-deleted factor VIII/ Blood. 1993 Jun 1; 81(11):2925-35. PMID: 8499631). В отличии от других белков каскада свертывания крови, которые преимущественно относятся к протеазам, FVIII - гликопротеин. Однако он играет критичную роль в формировании теназного комплекса, который необходим для образования активированного фактора свертывания X (FXa), первого члена окончательного общего пути коагуляции, что в итоге приводит к образованию сшитого фибрина.
Более чем в половине случаев к тяжелой форме гемофилии А приводят инверсии в 1 или 22 интроне гена FVIII (Habart D, Kalabova D, Novotny M, Vorlova Z. Thirty-four novel mutations detected in factor VIII gene by multiplex CSGE: modeling of 13 novel amino acid substitutions/J ThrombHaemost. 2003 Apr; 1(4):773-81. doi: 10.1046/j.l538-7836.2003.00149.x. PMID: 1287141). В других случаях нарушения в последовательности FVIII связаны с различными мутациями, в том числе антисмысловыми мутациями, сдвигами рамки считывания, мутациями в сплайсинг-сайтах, делециями и инсерциями.
Склонность к кровотечениям при гемофилии А взаимосвязана с определяемой активностью FVIII и классифицируется как легкая (0,05-0,40 ME/мл), умеренная (0,01-0,05 ME/мл) или тяжелая (<0,01 ME/мл). Пациенты с легкой формой гемофилии, как правило, испытывают аномальное кровотечение только в связи с оперативным вмешательством или полученными травмами. Напротив, у пациентов с умеренной формой гемофилии наблюдаются длительные реакции кровотечения на относительно незначительные травмы, а у пациентов с тяжелой формой заболевания часто возникают спонтанные кровотечения. Тяжелая форма гемофилии А проявляется спонтанными гемартрозом, гематомами мягких тканей, забрюшинными кровотечениями, внутримозговыми кровоизлияниями и отсроченными послеоперационными кровотечениями. Со временем осложнения от рецидивирующего гемартроза и гематом мягких тканей включают тяжелую артропатию, контрактуры суставов и псевдоопухоли, приводящие к хроническим заболеваниям. Доля пациентов с легкой, средней и тяжелой формами гемофилии А точно не установлена, но, согласно последним эпидемиологическим исследованиям, предполагается, что примерно 60% пациентов с гемофилией А имеют тяжелую форму (Report on the annual global survey 2019, WFH).
На сегодняшний день стандартная схема лечения пациентов, страдающих гемофилией А, заключается в пожизненной заместительной терапии в виде инъекций рекомбинантного FVIII (Report on the annual global survey 2019, WFH). Несмотря на успех терапии гемофилии, существуют серьезные проблемы подобного подхода. Профилактическая заместительная терапия гемофилии А предполагает внутривенные инъекции рекомбинантного FVIII каждые три дня в течение всей жизни пациента с тяжелой формой заболевания. Подобный формат лечения является очень дорогостоящим и не гарантирует отсутствия осложнений, связанных в первую очередь с гемартрозом. В некоторых случаях у пациентов вырабатываются ингибирующие антитела. Ингибиторные формы гемофилии А чаще наблюдаются у пациентов с тяжелой формой заболевания и требуют применения альтернативных подходов к лечению и профилактике заболевания (Eckhardt CL, van der Bom JG, van der Naald M, Peters M, Kamphuisen PW, Fijnvandraat K. Surgery and inhibitor development in hemophilia A: a systematic review/ J Thromb Haemost. 2011 Oct; 9(10): 1948-58. doi: 10.1111/j.1538-7836.2011.04467.x. PMID: 21838755).
Генная терапия гемофилии А посредством вирусных (экспрессионных) векторов на основе аденоассоциированных вирусов (AAV), кодирующих ген FVIII, показала впечатляющие результаты в серии доклинических и клинических исследований (Bunting S, Zhang L, Xie L, Bullens S, Mahimkar R, Fong S, Sandza K, Harmon D, Yates B, Handyside B, Sihn CR, Galicia N, Tsuruda L, O'Neill CA, Bagri A, Colosi P, Long S, Vehar G, Carter B. Gene Therapy with BMN 270 Results in Therapeutic Levels of FVIII in Mice and Primates and Normalization of Bleeding in Hemophilic Mice/ Mol Ther. 2018 Feb 7;26(2):496-509. doi: 10.1016/j.ymthe.2017.12.009. Epub 2017 Dec 14.PMID: 29292164 и Peyvandi F, Garagiola I. Clinical advances in gene therapy updates on clinical trials of gene therapy in haemophilia/ Haemophilia. 2019 Sep; 25(5):738-746. doi: 10.1111/hae.13816. Epub 2019 Jul 8.PMID: 31282050). В отличие от традиционных подходов к лечению гемофилии, генная терапия с использованием AAV позволяет поддерживать уровень экспрессии привнесенного FVIII на достаточном уровне в течение нескольких лет после однократного введения препарата пациентам (Long BR, Veron Р, Kuranda К, Hardet R, Mitchell N, Hayes GM, Wong WY, Lau K, Li M, Hock MB, Zoog SJ, Vettermann C, Mingozzi F, Schweighardt B. Early Phase Clinical Immunogenicity of Valoctocogene Roxaparvovec, an AAV5-Mediated Gene Therapy for Hemophilia A/ Mol Ther. 2021 Feb 3; 29(2):597-610. doi: 10.1016/j.ymthe.2020.12.008. Epub 2020 Dec 10. PMID: 33309883).
На данный момент, в мире нет ни одного зарегистрированного генотерапевтического препарата для лечения гемофилии А.
Таким образом, является актуальным разработка генотерапевтического препарата для лечения гемофилии А, а также решений, которые позволят улучшить эффективность генотерапевтического препарата для лечения гемофилии А.
Раскрытие сущности изобретения
Авторы изобретения неожиданно обнаружили, что использование нуклеиновой кислоты, кодирующей
1) слитый белок на основе FVIII-BDD и сигнального пептида FIX (СП-FIX), который имеет аминокислотную последовательность SEQ ID NO: 7 или
2) слитый белок на основе FVIII-BDD и сигнального пептида Карра цепи иммуноглобулина G (СП-IgGK), который имеет аминокислотную последовательность SEQ ID NO: 8 или
3) слитый белок на основе FVIII-BDD и сигнального пептида Lactalbumin (СП-Lactalbumin), который имеет аминокислотную последовательность SEQ ID NO: 9,
приводит к увеличению уровня продукции и активности белка FVIII-BDD по сравнению с использованием нуклеиновой кислоты, кодирующей белок FVIII-BDD с природным сигнальным пептидом FVIII (дикий тип).
Определения и общие методы
Если иное не определено в настоящем документе, научные и технические термины, используемые в связи с настоящим изобретением, будут иметь значения, которые обычно понятны специалистам в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
Определения «встречающийся в природе», «нативный» или «дикого типа» используют для описания объекта, который можно обнаружить в природе как отличающийся от получаемого искусственно. Например, белок или нуклеотидная последовательность, присутствующие в организме, в том числе в составе вируса, которые можно изолировать из источника в природе, и которые не модифицированы умышленно специалистом в лаборатории, являются встречающимися в природе.
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «включать» и «содержать» или их вариации, такие как «включает», «включающий», «содержит» или «содержащий», следует понимать как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых.
Белок (Пептид)
В настоящем описании термины «пептид», «полипептид» и «белок» используют взаимозаменяемо, и они относятся к соединению, состоящему из аминокислотных остатков, ковалентно связанных пептидными связями. Полипептиды включают природные пептиды, рекомбинантные пептиды, синтетические пептиды или их комбинацию.
Молекулы нуклеиновых кислот
Термины «нуклеиновая кислота», «нуклеиновая последовательность» или «нуклеиновокислотная последовательность», «полинуклеотид», «олигонуклеотид», «полинуклеотидная последовательность» и «нуклеотидная последовательность», которые используются равнозначно в данном описании, обозначают четкую последовательность нуклеотидов, модифицированных или не модифицированных, определяющую фрагмент или участок нуклеиновой кислоты, содержащую или не содержащую неприродные нуклеотиды и являющуюся либо двухцепочечной ДНК или РНК, либо одноцепочечной ДНК или РНК, либо продуктами транскрипции указанных ДНК.
Как применяют в настоящем описании, полинуклеотиды включают, в качестве неограничивающих примеров, все последовательности нуклеиновой кислоты, получаемые любыми способами, доступными в этой области, включая, в качестве неограничивающих примеров, рекомбинантные способы, т.е. клонирование последовательностей нуклеиновой кислоты из рекомбинантной библиотеки или генома клетки, использование обычной технологии клонирования и ПЦР и т.п., и способами синтеза.
Здесь также следует упомянуть, что данное изобретение не относится к нуклеотидным последовательностям в их природной хромосомной среде, т.е. в природном состоянии. Последовательности данного изобретения были выделены и/или очищены, т.е. были взяты прямо или косвенно, например, путем копирования, при этом их среда была по меньшей мере частично модифицирована. Таким образом, также здесь следует подразумевать изолированные нуклеиновые кислоты, полученные путем генетической рекомбинации, например, с помощью принимающих клеток (клеток-хозяев), или полученные путем химического синтеза.
Термин нуклеотидная последовательность охватывает его комплемент, если не указано иное. Таким образом, нуклеиновую кислоту, имеющую определенную последовательность следует понимать как охватывающие ее комплементарную цепь с ее комплементарной последовательностью.
Вектор
Термин «вектор» при использовании в настоящем документе означает молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она соединена. Кроме того, термин «вектор» в данном настоящем документе означает рекомбинантную вирусную частицу, способную транспортировать нуклеиновую кислоту.
Как применяют в настоящем описании, термин «экспрессия» определяют как транскрипцию и/или трансляцию конкретной нуклеотидной последовательности, запускаемую ее промотором.
Применение
«Генная терапия» представляет собой вставку генов в клетки и/или ткани субъекта для лечения заболевания, обычно, наследственных заболеваний, при этом дефектный мутантный аллель заменяется или дополняется функциональным аллелем.
«Лечить», «лечение» и «терапия» относятся к методу смягчения или устранения биологического расстройства и/или по меньшей мере одного из сопутствующих ему симптомов.
Термин «субъект», «пациент», «индивидуум» и т.п. используют в настоящем описании взаимозаменяемо, и они относятся к любому животному, которое поддается воздействию способами, представленными в настоящем описании. В конкретных неограничивающих вариантах осуществления субъект, пациент или индивидуум является человеком. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
«Терапевтически эффективным количеством» или «эффективным количеством» считается количество вводимого терапевтического агента, которое избавит в определенной степени от одного или нескольких симптомов заболевания, по поводу которого проводится лечение.
Подробное описание изобретения
Нуклеиновая кислота
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, которая кодирует слитый белок на основе FVIII-BDD (фактор свертывания крови VIII с делетированным В доменом) и гетерологичного сигнального пептида, который включает аминокислотную последовательность, выбранную из SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9.
«Выделенная» молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, которая идентифицирована и отделена от по меньшей мере одной молекулы нуклеиновой кислоты-примеси. Выделенная молекула нуклеиновой кислоты отличается от той формы или набора, в которых она находится в естественных условиях. Таким образом, выделенная молекула нуклеиновой кислоты отличается от молекулы нуклеиновой кислоты, существующей в клетках в естественных условиях.
Сигнальный пептид обеспечивает транспорт белка интереса внутри клетки до целевых органелл или способствует секреции белка интереса в межклеточное пространство.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнального пептида FIX с аминокислотной последовательностью SEQ ID NO: 2.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнального пептида Карра цепи иммуноглобулина G с аминокислотной последовательностью SEQ ID NO: 3.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнального пептида Lactalbumin с аминокислотной последовательностью SEQ ID NO: 4.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида, который имеет аминокислотную последовательность SEQ ID NO: 7. Данный слитый белок с аминокислотной последовательностью SEQ ID NO: 7 включает FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнальный пептид FIX с аминокислотной последовательностью SEQ ID NO: 2.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида, который имеет аминокислотную последовательность SEQ ID NO: 8. Данный слитый белок с аминокислотной последовательностью SEQ ID NO: 8 включает FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнальный пептид Карра цепи иммуноглобулина G с аминокислотной последовательностью SEQ ID NO: 3.
В некоторых вариантах выделенная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида, который имеет аминокислотную последовательность SEQ ID NO: 9. Данный слитый белок с аминокислотной последовательностью SEQ ID NO: 9 включает FVIII-BDD с аминокислотной последовательностью SEQ ID NO: 5 и сигнальный пептид Lactalbumin с аминокислотной последовательностью SEQ ID NO: 4.
В некоторых вариантах выделенная нуклеиновая кислота представляет собой нуклеотидную последовательность SEQ ID NO: 11. Данная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7.
В некоторых вариантах выделенная нуклеиновая кислота представляет собой нуклеотидную последовательность SEQ ID NO: 12. Данная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и сигнального пептида Карра цепи иммуноглобулина G, который имеет аминокислотную последовательность SEQ ID NO: 8.
В некоторых вариантах выделенная нуклеиновая кислота представляет собой нуклеотидную последовательность SEQ ID NO: 13. Данная нуклеиновая кислота кодирует слитый белок на основе FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9.
Экспрессионная кассета. Экспрессионный вектор.
В одном из аспектов настоящее изобретение относится к экспрессионной кассете, которая включает вышеуказанную нуклеиновую кислоту, которая кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида.
Термин «кассета, которая экспрессирует» или «экспрессионная кассета» при использовании в данном документе, в частности, относится к фрагменту ДНК, который способен в соответствующей обстановке запускать экспрессию полинуклеотида, кодирующего представляющий интерес полипептид, последовательность которого включена в указанную экспрессионную кассету. При введении в клетку-хозяина экспрессионная кассета помимо прочего способна задействовать клеточные механизмы для транскрипции полинуклеотида, кодирующего представляющий интерес полипептид, в РНК, которая затем обычно дополнительно процессируется и, наконец, транслируется в представляющий интерес полипептид. Экспрессионная кассета может содержаться в экспрессионном векторе.
Экспрессионная кассета по настоящему изобретению содержит в качестве элемента промотор. Термин «промотор», используемый в настоящем документе, в частности, относится к элементу ДНК, который способствует транскрипции полинуклеотида, с которым функционально связан промотор. Промотор может также составлять часть элемента «промотор/энхансер». Хотя физические границы между элементами «промотор» и «энхансер» не всегда ясны, термин «промотор» обычно относится к месту на молекуле нуклеиновой кислоты, с которым связывается РНК-полимераза и/или связанные с ней факторы, и с которого инициируется транскрипция. Энхансеры усиливают активность промотора во времени, а также пространственно. В данной области известно множество промоторов, которые транскрипционно активны в широком диапазоне типов клеток. Промоторы могут быть разделены на два класса: на тех, которые функционируют конститутивно, и тех, которые регулируются индукцией или снятием репрессии. Для экспрессии белка пригодны оба класса. Промоторы, которые используются для продукции высокого уровня полипептидов в эукариотических клетках и, в частности, в клетках млекопитающих, должны быть сильными и, предпочтительно, должны быть активными в широком диапазоне типов клеток. Сильные конститутивные промоторы, которые способны запускать экспрессию во многих типах клеток, хорошо известны в данной области и, поэтому, нет необходимости в их подробном описании в данном документе.
Согласно одному варианту осуществления изобретения промотор HLP используется в экспрессионной кассете по настоящему изобретению.
В некоторых вариантах экспрессионная кассета включает следующие элементы в направлении от 5'-конца к 3'-концу:
левый (первый) ITR (инвертированные концевые повторы);
промотор;
любая из вышеуказанных нуклеиновых кислот, которая кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида;
сигнал полиаденилирования;
правый (второй) ITR.
Вышеуказанные структурные элементы экспрессионной кассеты являются функционально связанными между собой.
В контексте настоящего описания термин «функционально связанный» относится к связи полинуклеотидных (или полипептидных) элементов в функциональную связь. Нуклеиновая кислота является «функционально связанной», если она находится в условиях функциональной связи с другой последовательностью нуклеиновой кислоты. Например, регуляторная последовательность транскрипции функционально связана с кодирующей последовательностью, если она влияет на транскрипцию указанной кодирующей последовательности. Термин «функционально связанный» означает, что связанные последовательности ДНК являются, как правило, непрерывными, и при необходимости соединения двух участков, кодирующих белок, являются также непрерывными и находятся в рамке считывания.
В некоторых вариантах экспрессионная кассета включает левый (первый) ITR с нуклеотидной последовательностью SEQ ID NO: 14.
В некоторых вариантах экспрессионная кассета включает промотор HLP с нуклеотидной последовательностью SEQ ID NO: 15.
В некоторых вариантах экспрессионная кассета включает сигнал полиаденилирования с нуклеотидной последовательностью SEQ ID NO: 16.
В некоторых вариантах экспрессионная кассета включает правый (второй) ITR с нуклеотидной последовательностью SEQ ID NO: 17.
В некоторых вариантах экспрессионная кассета включает следующие элементы в направлении от 5'-конца к 3'-концу:
левый (первый) ITR (инвертированные концевые повторы) с нуклеотидной последовательностью SEQ ID NO: 14;
промотор с нуклеотидной последовательностью SEQ ID NO: 15;
любая из вышеуказанных нуклеиновых кислот, которая кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида;
сигнал полиаденилирования с нуклеотидной последовательностью SEQ ID NO: 16;
правый (второй) ITR с нуклеотидной последовательностью SEQ ID NO: 17.
В одном из аспектов настоящее изобретение относится к экспрессионному вектору, который включает любую из вышеуказанных нуклеиновых кислот, которая кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида, или любую из вышеуказанных экспрессионных кассет.
В некоторых вариантах осуществления изобретения вектор представляет собой плазмиду, т.е. кольцевую двухцепочечную часть ДНК, в которую могут быть вставлены дополнительные сегменты ДНК.
В некоторых вариантах осуществления изобретения вектор представляет собой вирусный (экспрессионный) вектор, в котором дополнительные сегменты ДНК могут быть вставлены в вирусный геном.
В некоторых вариантах осуществления изобретения векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальный сайт инициации репликации и эписомные векторы). В других вариантах осуществления изобретения векторы (например, неэписомальные векторы) могут быть интегрированы в геном клетки-хозяина при введении в клетку-хозяина, и таким образом реплицируются вместе с геном хозяина. Более того, некоторые векторы способны направлять экспрессию генов, с которыми они функционально соединены. Такие векторы упоминаются в данном документе как «рекомбинантные экспрессирующие векторы» (или просто «экспрессирующие векторы» («вектор экспрессии» или «экспрессионный вектор»)).
Экспрессионные векторы включают плазмиды, ретровирусы, аденовирусы, аденоассоциированные вирусы (AAV), вирусы растений, такие как вирус мозаики цветной капусты, вирусы табачной мозаики, космиды, YAC, EBV и тому подобное. Молекулы ДНК могут быть вставлены в вектор таким образом, что последовательности, контролирующие транскрипцию и трансляцию в векторе, выполняют предусмотренную функцию регуляции транскрипции и трансляции ДНК. Экспрессионный вектор и последовательности контроля экспрессии могут быть выбраны таким образом, чтобы быть совместимыми с используемой экспрессирующей клеткой-хозяином. Молекулы ДНК могут быть введены в экспрессионный вектор стандартными способами (например, лигированием комплементарных сайтов рестрикции или лигированием тупых концов, если сайты рестрикции отсутствуют).
В некоторых вариантах экспрессионный вектор представляет собой рекомбинантный аденоассоциированный вирус (AAV).
В некоторых вариантах AAV выбирают из группы, включающей следующие серотипы AAV: AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10 AAV11, AAV12, AAV13, AAV14, AAV15, AAV16, rAAV.rh8, rAAV.rhlO, rAAV.rh20, rAAV.rh39, rAAV.Rh74, rAAV.RHM4-1, AAV.hu37, rAAV.Anc80, rAAV.Anc80L65, rAAV.7m8, rAAV.PHP.B, rAAV2.5, rAAV2tYF, rAAV3B, rAAV.LK03, AAV.HSC1, AAV.HSC2, AAV.HSC3, AAV.HSC4, AAV.HSC5, AAV.HSC6, AAV.HSC7, AAV.HSC8, AAV.HSC9, AAV.HSC10, AAV.HSC11, AAV.HSC12, AAV.HSC13, AAV.HSC14, AAV.HSC15 или AAV.HSC16.
В некоторых вариантах осуществления изобретения вектор или кассета может включать последовательность контроля экспрессии. Термин «последовательность контроля экспрессии», используемый в данном описании, означает полинуклеотидные последовательности, которые необходимы для воздействия на экспрессию и процессинг кодирующих последовательностей, к которым они вставлены. Специалистам в этой области будет понятно, что дизайн экспрессионного вектора или кассеты, включая выбор последовательностей контроля экспрессии, может зависеть от таких факторов, как выбор типа клетки-хозяина для трансформации, требуемый уровень экспрессии белка, и т.д. Последовательности контроля экспрессии включают соответствующие последовательности инициации транскрипции, терминации, промотора и энхансера; эффективные сигналы процессинга РНК, такие как сплайсинг и сигналы полиаденилирования; последовательности, которые стабилизируют цитоплазматическую мРНК; последовательности, которые повышают эффективность трансляции (т.е. консенсусная последовательность Козака); последовательности, которые повышают стабильность белка; и, при желании, последовательности, которые усиливают секрецию белка. Характер таких контролирующих последовательностей различается в зависимости от организма-хозяина; в прокариотах такие контролирующие последовательности, как правило, включают промотор, сайт связывания рибосомы, а также последовательности терминации транскрипции; в эукариотах, как правило, такие контролирующие последовательности включают промоторы и последовательности терминации транскрипции. Предпочтительные последовательности контроля экспрессии для экспрессирующей клетки-хозяина млекопитающего включают вирусные элементы обеспечивающие высокий уровень экспрессии белков в клетках млекопитающих, таких как промоторы и/или энхансеры, полученные из ретровирусной LTR, цитомегаловируса (CMV) (например, CMV промотора/энхансера), обезьяньего вируса 40 (SV40) (например, SV40 промотора/энхансера), аденовируса, (например, большого позднего промотора аденовируса (AdMLP)), вирус полиомы, а также сильных промоторов млекопитающих, таких как TTR промотор, промотор нативных иммуноглобулинов, промотор актина, а также промотор HLP (hybrid liver-speciHc promotor). Последовательности контроля экспрессии включают, как минимум, все компоненты, наличие которых имеет важное значение для экспрессии и процессинга.
В дополнение к вышеуказанным генам и последовательностям контроля экспрессии, рекомбинантные векторы экспрессии изобретения могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, точки начала репликации) и гены селектируемого маркера. Ген селектируемого маркера облегчает селекцию клеток-хозяев, в которые был введен вектор или кассету.
В одном из вариантов настоящего изобретения экспрессионный вектор относится к вектору, содержащему одну или несколько интересующих полинуклеотидных последовательностей, интересующих генов или трансгенов, которые фланкированы парвовирусными или инвертированными концевыми повторяющимися последовательностями (ITR).
Ни кассета, ни вектор по изобретению не содержит нуклеотидные последовательности генов, кодирующих неструктурные белки (Rep) и структурные белки (Сар) аденоассоциированного вируса.
Клетка-хозяин
В одном из аспектов настоящее изобретение относится к клетке-хозяину для получения слитого белка на основе FVIII-BDD и гетерологичного сигнального пептида или для получения любого из вышеуказанных экспрессионных векторов, которая содержит любую из вышеуказанных нуклеиновых кислот, которая кодирует слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида.
Термин «клетка-хозяин» при использовании в данном документе означает клетку, в которую введен рекомбинантный экспрессионный вектор или кассету по изобретению. Настоящее изобретение относится к клеткам-хозяевам, которые могут включать, например, вектор в соответствии с настоящим изобретением, описанным выше. Следует понимать, что «клетка-хозяин» означают не только конкретную заявленную клетку, но также и потомство такой клетки. Поскольку модификации могут проходить в последующих поколениях вследствие мутации или воздействий окружающей среды, такое потомство не может, на самом деле, быть идентичным родительской клетке, но такие клетки по-прежнему включены в объем термина «клетка-хозяин» при использовании в настоящем документе.
Экспрессионные векторы или кассеты по изобретению могут быть использованы для трансфекции клетки млекопитающего, клетки растения, бактериальной или дрожжевой клетки-хозяина. Трансфекция может происходить любым известным способом для введения полинуклеотидов в клетку хозяина. Способы введения гетерологичных полинуклеотидов в клетки млекопитающих хорошо известны в данной области и включают декстран опосредованную трансфекцию, трансфекцию комплексом нуклеиновой кислоты и позитивно заряженного полимера, трансфекцию преципитатом нуклеиновой кислоты и фосфата кальция, полибрен опосредованную трансфекцию, слияние протопластов, трансфекцию инкапсулированными в липосомы полинуклеотидами и прямую микроинъекцию ДНК в ядра. В дополнение молекулы нуклеиновых кислот могут быть введены в клетки млекопитающих вирусными (экспрессионными) векторами.
Клеточные линии млекопитающих, используемые в качестве хозяев для трансформации, хорошо известны в данной области и включают множество иммортализованных доступных клеточных линий. К ним относятся, например, клетки яичников китайского хомячка (СНО), NS0 клетки, клетки SP2, HEK-293Т клетки, 293 Фристайл клетки (Invitrogen), NIH-3T3 клетки, клетки HeLa, клетки почек хомячка (BHK), клетки почек африканских зеленых мартышек (COS), клетки гепатоцеллюлярной карциномы человека (например, Hep G2), А549 клетки, SK-HEP1, HUH7, Hep-RG и ряд других клеточных линий. Клеточные линии выбираются путем определения, какие клеточные линии имеют высокие уровни экспрессии и обеспечивают необходимые характеристики продуцируемого белка. Другими клеточными линиями, которые могут быть использованы, являются клеточные линии насекомых, такие как Sf9 или Sf21 клетки. Когда векторы рекомбинантной экспрессии по изобретению вводятся в клетки-хозяева млекопитающих слитый белок продуцируется путем культивирования клеток-хозяев в течение времени, достаточного для экспрессии слитого белка в клетках-хозяевах или, предпочтительнее, выделения слитого белка в питательную среду, в которой выращиваются клетки-хозяева. Слитый белок может быть выделен из питательной среды с использованием стандартных методов очистки белка. Клетки-хозяева растений, например, включают Nicotiana, Arabidopsis, ряску, кукурузу, пшеницу, картофель и т.д. Клетки бактерий хозяина включают виды Escherichia и Streptomyces. Дрожжевые клетки-хозяева включают Schizosaccharomyces pombe, Saccharomyces cerevisiae и Pichia pastoris.
Вышеуказанная клетка-хозяин не относится к клетке-хозяину, полученной с использованием человеческих эмбрионов.
Вышеуказанная клетка-хозяин не относится к клетке-хозяину, полученной с модификации генетической целостности клеток зародышевой линии человека.
Фармацевтическая композиция
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для доставки гена FVIII-BDD в целевые клетки, который включает любой из вышеуказанных экспрессионных векторов или кассет.
В некоторых вариантах фармацевтическая композиция для доставки гена FVIII-BDD в целевые клетки включает любой из вышеуказанных экспрессионных векторов или кассет в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами.
Действующее вещество в вышеуказанной композиции находится в эффективном количестве, например, в биологически эффективном количестве.
«Фармацевтическая композиция» обозначает композицию, включающую в себя любой из вышеуказанных экспрессионных векторов по изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых эксипиентов, наполнителей, растворителей, разбавителей, носителей, вспомогательных средств, распределяющих средств или средств доставки.
Фармацевтические композиции по настоящему изобретению и способы их изготовления будут бесспорно очевидными для специалистов в этой области. Производство фармацевтических композиций предпочтительно должно соответствовать требованиям GMP (надлежащей производственной практики).
В некоторых вариантах осуществления фармацевтической композиции она может включать буферную композицию, тонические агенты (осмолитик или осмотический агент), стабилизаторы и/или солюбилизаторы.
«Фармацевтически приемлемым» считается материал, который не имеет биологических или других противопоказаний, например, материал можно вводить субъекту без каких-либо нежелательных биологических эффектов. Таким образом, такие фармацевтические композиции можно использовать, например, для трансфекции клетки ех vivo или для введения in vivo любого из вышеуказанных экспрессионных векторов по изобретению непосредственно субъекту.
Термин «эксципиент» или «вспомогательное вещество» используется в данном документе для описания любого компонента, отличающегося от ранее описанных по данному изобретению. Это вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств.
Фармацевтическая композиция по изобретению является стабильной.
Фармацевтическая композиция является «стабильной», если активный агент сохраняет свою физическую стабильность и/или химическую стабильность и/или биологическую активность в течение заявленного срока годности при температуре хранения, например, при 2-8°С. Предпочтительно, чтобы активный агент сохранял и физическую, и химическую стабильность, а также биологическую активность. Период хранения выбирается на основании результатов исследования стабильности при ускоренном и естественном хранении.
В некоторых вариантах фармацевтическая композиция представляет собой раствор для внутривенного введения.
В некоторых вариантах фармацевтическая композиция представляет собой концентрат для приготовления раствора для внутривенного введения.
Применение
В одном из аспектов настоящее изобретение относится к применению любого из вышеуказанных экспрессионных кассет или векторов или вышеуказанной композиции для доставки гена FVIII-BDD в целевые клетки.
В одном из аспектов настоящее изобретение относится к применению любого из вышеуказанных экспрессионных кассет или векторов или вышеуказанной композиции для обеспечения белком FVIII-BDD субъекта, который имеет гемофилию А и/или не имеет функциональных копий гена FVIII.
Под отсутствием функциональных копий гена FVIII подразумеваются инактивирующие мутации или делеции во всех копиях гена FVIII в геноме, которые приводят к потере или дефекту функции гена FVIII.
В одном из аспектов настоящее изобретение относится к способу обеспечения белком FVIII-BDD субъекта с гемофилией А, который включает введение терапевтически эффективного количества любого из вышеуказанных экспрессионных векторов или вышеуказанной композиции в клетки субъекта, нуждающегося в этом.
В одном из аспектов настоящее изобретение относится к способу доставки гена FVIII-BDD в целевые клетки субъекта с гемофилией А, который включает введение любого из вышеуказанных экспрессионных векторов или вышеуказанной композиции в клетки субъекта.
Под субъектом, нуждающимся в доставке гена FVIII-BDD в целевые клетки, или субъектом, нуждающимся в обеспечении белком FVIII-BDD, подразумевается субъект, который имеет гемофилию А, или субъект, который имеет дефицит фактора свертывания крови FVIII, или субъект, который имеет инактивирующие мутации или делеции в гене FVIII, которые приводят к потере или дефекту функции гена FVIII.
В одном из аспектов настоящее изобретение относится к применению любого из вышеуказанных экспрессионных векторов или вышеуказанной композиции для лечения гемофилии А у субъекта, который имеет гемофилию А.
В одном из аспектов настоящее изобретение относится к способу лечения гемофилии А у субъекта, который включает ведение терапевтически эффективного количества любого из вышеуказанных экспрессионных векторов или вышеуказанной композиции субъекту, который имеет гемофилию А.
В некоторых вариантах гемофилия А представляет собой тяжелую форму гемофилии А (активность фактора VIII <1%) или среднетяжелую форму гемофилии А (активность фактора VIII 1-5%).
Примеры способов введения включают в себя местное применение, интраназальное, ингаляционное, чрезслизистое, трансдермальное, энтеральное (например, пероральное, ректальное), парентеральное (например, внутривенное, подкожное, внутрикожное, внутримышечное) введения, а также инъекции непосредственно в ткань или в орган.
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов или вышеуказанная композиция вводится субъекту как внутривенная инфузия.
Любой из вышеуказанных экспрессионных векторов вводят в организм в эффективном количестве. Любой из вышеуказанных экспрессионных векторов предпочтительно вводят в организм в биологически эффективном количестве. «Биологически эффективное» количество экспрессионного вектора представляет собой количество, которое достаточно, чтобы вызвать трансдукцию клеток и экспрессию последовательности нуклеиновой кислоты в клетке. Если экспрессионный вектор вводят в клетку in vivo, «биологически эффективное» количество экспрессионного вектора представляет собой количество, которое достаточно, чтобы вызвать трансдукцию клеток-мишеней и экспрессию последовательности нуклеиновой кислоты в клетке-мишени.
Дозировки любого из вышеуказанных экспрессионных векторов по данному изобретению будут зависеть от способа введения конкретного вектора, и их можно определять рутинными способами.
Клетка для введения любого из вышеуказанных экспрессионных кассет или векторов по данному изобретению может быть клеткой любого типа, включая в себя без ограничения, эпителиальные клетки (например, эпителиальные клетки кожи, дыхательных путей и кишечника), печеночные клетки, мышечные клетки, клетки селезенки, фибробласты, эндотелиальные клетки и тому подобное.
Любой из вышеуказанных экспрессионных кассет или векторов по данному изобретению не используется для модификации генетической целостности клеток зародышевой линии человека.
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе применяют в формате монотерапии.
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе применяют в комбинации с заместительной терапией концентратами факторов свертывания, десмопрессином и/или ингибиторами фибринолиза.
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе применяют в комбинации с моноклональным антителом (например, эмицизумаб).
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе применяют в комбинации с препаратами на базе технологии РНК-интерференции (например, фитусиран).
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе вводят субъекту однократно.
В некоторых вариантах применения любой из вышеуказанных экспрессионных векторов по данному изобретению, а также препарат на его основе вводят субъекту многократно.
Краткое описание чертежей
Фигура 1 представляет собой график, который показывает увеличение уровня продукции белка FVIII-BDD в культуральную жидкость после трансфекции нуклеиновыми кислотами, кодирующими слитый белок на основе FVIII-BDD (фактор свертывания крови VIII с делетированным В доменом) и одного из гетерологичных сигнальных пептидов, по сравнению с нуклеиновой кислотой, кодирующей FVIII-BDD с сигнальным пептидом FVIII дикого типа.
1 - уровень белка FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и природного сигнального пептида FVIII, который имеет аминокислотную последовательность SEQ ID NO: 6 (СП-FVIII-FVIII-BDD).
2 - уровень белка FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7 (СП-FIX-FVIII-BDD).
3 - уровень белка FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9 (СП-Lactalbumin-FVIII-BDD).
4 - уровень белка FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Карра цепь иммуноглобулина G, который имеет аминокислотную последовательность SEQ ID NO: 8 (СП-IgGK-FVIII-BDD).
Фигура 2 представляет собой график, который показывает увеличение уровня активности белка FVIII-BDD в культуральной жидкости после трансфекции нуклеиновыми кислотами, кодирующими слитый белок на основе FVIII-BDD (фактор свертывания крови VIII с делетированным В доменом) и одного из гетерологичных сигнальных пептидов, по сравнению с нуклеиновой кислотой, кодирующей FVIII-BDD с сигнальным пептидом FVIII дикого типа.
1 - уровень активности FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и природного сигнального пептида FVIII, который имеет аминокислотную последовательность SEQ ID NO: 6 (СП-FVIII-FVIII-BDD).
2 - уровень активности FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7 (СП-FIX-FVIII-BDD).
3 - уровень активности FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9 (СП-Lactalbumin-FVIII-BDD).
4 - уровень активности FVIII-BDD после трансфекции клеток нуклеиновой кислотой, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Карра цепь иммуноглобулина G, который имеет аминокислотную последовательность SEQ ID NO: 8 (СП-IgGK-FVIII-BDD).
Фигура 3 представляет собой график, который показывает увеличение уровня продукции белка FVIII-BDD при доставке in vitro нуклеиновых кислот в виде экспрессионного вектора на основе rAAV, содержащего нуклеиновую кислоту, кодирующую слитый белок на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, по сравнению с экспрессионным вектором на основе rAAV, содержащим нуклеиновую кислоту, кодирующую FVIII-BDD с сигнальным пептидом FVIII дикого типа.
1 - уровень белка FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе человеческого FVIII-BDD и природного сигнального пептида FVIII, который имеет аминокислотную последовательность SEQ ID NO: 6 (СП-FVIII-FVIII-BDD).
2 - уровень белка FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7 (СП-FIX-FVIII-BDD).
3 - уровень белка FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9 (СП-Lactalbumin FVIII-BDD).
Фигура 4 представляет собой график, который показывает увеличение уровня активности белка FVIII-BDD при доставке in vitro нуклеиновых кислот в виде экспрессионного вектора на основе rAAV, содержащего нуклеиновую кислоту, кодирующую слитый белок на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, по сравнению с экспрессионным вектором на основе rAAV, содержащим нуклеиновую кислоту, кодирующую FVIII-BDD с сигнальным пептидом FVIII дикого типа.
1 - уровень активности FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе человеческого FVIII-BDD и природного сигнального пептида FVIII, который имеет аминокислотную последовательность SEQ ID NO: 6 (СП-FVIII-FVIII-BDD).
2 - уровень активности FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7 (СП-FIX-FVIII-BDD).
3 - уровень активности FVIII-BDD после трансдукции клеток экспрессионными векторами, содержащими нуклеиновую кислоту, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9 (СП-Lactalbumin FVIII-BDD).
Фигура 5 представляет собой график, который показывает увеличение уровня белка FVIII-BDD при доставке нуклеиновой кислоты, кодирующей слитый белок на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, in vivo мышам линии B6.129S-F8tm1Smoc (HemA) в виде экспрессионного вектора на основе rAAV.
1 - уровень белка FVIII-BDD в плазме крови животных после инъекции контрольный раствор без AAV (негативный контроль).
2 - уровень белка FVIII-BDD в плазме крови животных после инъекции экспрессионного вектора, содержащего нуклеиновую кислоту, которая кодирует слитый белок на основе FVIII-BDD и сигнального пептида FIX, который имеет аминокислотную последовательность SEQ ID NO: 7 (СП-FIX-FVIII-BDD).
3 - уровень белка FVIII-BDD в плазме крови животных после инъекции экспрессионного вектора, содержащего нуклеиновую кислоту, которая кодирует слитый белок на основе человеческого FVIII-BDD и сигнального пептида Lactalbumin, который имеет аминокислотную последовательность SEQ ID NO: 9 (СП-Lactalbumin FVIII-BDD).
Примеры
Для наилучшего понимания изобретения приводятся следующие примеры. Эти примеры приведены только в иллюстративных целях и не должны толковаться как ограничивающие сферу применения изобретения в любой форме.
Все публикации, патенты и патентные заявки, указанные в этой спецификации включены в данный документ путем отсылки. Хотя вышеупомянутое изобретение было довольно подробно описано путем иллюстрации и примера в целях исключения двусмысленного толкования, специалистам в данной области на основе идей, раскрытых в данном изобретении, будет вполне понятно, что могут быть внесены определенные изменения и модификации без отклонения от сущности и объема прилагаемых вариантов осуществления изобретения.
Материалы и общие методы
Методы рекомбинантной ДНК
Для манипуляций с ДНК использовали стандартные методы, описанные у Sambrook J. и др., Molecular cloning: A laboratory manual; Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 1989. Реагенты для молекулярной биологии использовали согласно инструкциям производителей. Вкратце, плазмидную ДНК нарабатывали для дальнейших манипуляций в клетках Е. coli, выращиваемых под селективным давлением с антибиотиками для того, чтобы плазмиды не терялись в клеточной популяции. Плазмидную ДНК выделяли из клеток коммерческими наборами, измеряли концентрацию и использовали для клонирования с помощью обработки эндонуклеазами рестрикции или методами ПЦР-амплификации. Фрагменты ДНК лигировали между собой с помощью лигаз и трансформировали в бактериальные клетки для отбора клонов и дальнейших наработок. Все полученные генетические конструкции подтверждали по паттернам рестрикции и полным секвенированием по Сэнгеру.
Синтез генов
Требуемые сегменты генов получали из олигонуклеотидов, созданных путем химического синтеза. Генные фрагменты длиной от 300 до 1000 п.н., которые фланкированы уникальными сайтами рестрикции, собирали путем ренатурации олигонуклеотидов друг на друге с последующей ПЦР-амплификацией с крайних праймеров. В результате получали смесь фрагментов, включая нужный. Фрагменты клонировали по сайтам рестрикции в промежуточные векторы, после чего последовательности ДНК субклонированных фрагментов подтверждали путем секвенирования ДНК.
Определение последовательностей ДНК
Последовательности ДНК определяли путем секвенирования по Сэнгеру. Анализ последовательностей ДНК и белков и обработку данных о последовательностях осуществляли в программе SnapGene 4.2 и выше для создания, картирования, анализа, аннотирования и иллюстрации последовательностей.
Культивирование клеточных культур
В экспериментах были использованы клеточные линии HEK293 (Human Embryonic Kidney clone 293), HUH7 (human hepatocellular carcinoma cell lines) и HepG2 (human hepatocellular carcinoma cell lines). Суспензионные клетки HEK293, используемые для наработки AAV, культивировались в стандартных условиях при 37°С и 5% CO2, на полной питательной среде без FBS и антибиотика. Адгезионные клетки HUH7 и HepG2, используемые для проверки эффективности препаратов AAV, культивировались в стандартных условиях при 37°С и 5% СО2, на полной питательной среде DMEM добавлением 10% FBS, антибиотика/антимикотика. Пересев клеток HUH7 и HepG2 осуществлялся при достижении 80-90% конфлюентности. Для диссоциации клеточного монослоя использовался TrypLE Select enzyme (10х). Жизнеспособность клеток оценивалась с помощью окраски Trypan Blue и одноразовых камер для подсчета клеток с помощью автоматического счетчика Countess II.
Трансфекции клеточных культур
Для оценки функциональности новых вариантов слитых белков при трансфекции использовались плазмиды, содержащие экспрессионную кассету для экспрессии различных вариантов трансгенов hFVIII-BDD. Клеточную линию HepG2 заранее засевали в лунки 12-луночных планшетов с плотностью 10000 кл/см2. Через сутки вносились плазмиды в одинаковой копийности в составе комплекса с Lipofectamine 3000. На 7 день после трансфекции определяли содержание белка FVIII-BDD и его активность в культуральной жидкости методом ИФА и хромогенного теста. Работы по оценке уровня и активности белка FVIII-BDD в культуральной жидкости проводились в 6 независимых экспериментах. Для негативного контроля были использованы интактные клетки HepG2.
Сборка и очистка экспрессионных векторов на основе AAV
Для сборки экспрессионных векторов на основе AAV, содержащих кодон-оптимизированные варианты гена FVIII-BDD, использовали клетки-продуценты HEK293, которые трансфецировали 3-мя плазмидами:
1) плазмиды, содержащие экспрессионную кассету AAV для экспрессии различных вариантов трансгенов hFVIII-BDD;
2) плазмида для экспрессии гена Сар серотипа AAV6 и гена Rep серотипа AAV2. Каждый ген с помощью альтернативных рамок считывания кодирует несколько белковых продуктов;
3) плазмида для экспрессии генов аденовируса Ad2, необходимых для сборки и упаковки капсидов AAV.
Через 72 часа клетки лизировали и проводили очистку и концентрирование частиц с помощью методов фильтрации, хроматографии и ультрацентрифугирования. Титр частиц определяли с помощью количественной ПЦР с праймерами и пробой, специфичными к участку рекомбинантного вирусного генома, и выражали в виде количества копий вирусных геномов на 1 мл.
Трансдукция клеточных культур
Клеточную линию HUH7 заранее засевали в лунки 12-луночных планшетов с плотностью 10000 кл/см2. После прикрепления клеток к адгезивной подложке, вносились препараты AAV при MOI 500000 вг/кл. На 7 день после трансдукции определяли содержание белка FVIII-BDD и его активность в культуральной жидкости методом ИФА и хромогенным тестом. Работы по оценке уровня и активности белка FVIII-BDD в культуральной жидкости проводились в 6 независимых экспериментах. Для негативного контроля были использованы интактные клетки.
Определение количества белка фактора свертывания крови VIII BDD методом ИФА
Оценка содержания белка фактора свертывания крови VIII-BDD в культуральной жидкости после трансфекции клеток линии HepG2 и трансдукции клеток линии HUH7, а также после инъекции животным (мыши) в плазме крови целевыми кандидатами проводилась «сэндвич»-методом неконкурентного твердофазного иммуноферментного анализа (ИФА). Вкратце, разведенные в буфере для разведений образцы, вносились в лунки 96-луночного планшета, сенсибилизированные первичными специфическими к фактору свертывания крови VIII-BDD антителами. В этот же планшет вносились стандарты для построения калибровочной кривой, контроли. Планшет инкубировался 1 час при температуре 37°С. Производили отмывку лунок планшета отмывочным буфером перед внесением биотинилированных антител, раствора конъюгата стрептавидин-пероксидазы и ТМВ. Вносился раствор со специфическими биотинилированными детектирующими антителами к фактору VIII-BDD и планшет инкубировался 30 минут при температуре 37°С. Далее к образовавшемуся комплексу добавлялся раствор конъюгата стрептавидин-пероксидазы и планшет инкубировался 30 минут при температуре 37°С. Для визуализации ферментативной реакции вносился раствор ТМВ. По достижении нужной степени интенсивности окрашивания во все лунки добавляется стоп-раствор для остановки реакции. Далее измерялась оптическая плотность растворов в лунках планшета. Концентрация фактора свертывания крови VIII-BDD в исследуемых образцах определялась по калибровочной кривой с учетом предварительного разведения образцов.
Определение уровня активности белка фактора свертывания крови VIII BDD методом ИФА
Оценка активности белка фактора свертывания крови VIII в культуральной жидкости после трансфекции клеток линии HepG2 и трансдукции клеток линии HUH7 целевыми кандидатами проводилась при помощи хромогенного теста. Суть теста заключается в том, что в присутствии ионов кальция, фосфолипидов и фактора IXa фактор X переходит в активированную форму Ха, фактор VIII действует как кофактор в этой реакции, и скорость активации фактора X линейно связана с количество фактора VIII. Вкратце, разведенные в буфере для разведений образцы культуральной жидкости, стандарты для построения калибровочной кривой и контроли вносились в лунки 96-луночного планшета. Планшет инкубировался 3 минуты при температуре 37°С. Во все лунки планшета вносили раствор Factor reagent, содержащий фактор IXa, фактор X, тромбин, CaCl2 и фосфолипиды. Планшет инкубировался 4 минуты при температуре 37°С. Во все лунки планшета вносили раствор хромогенного субстрата S-2765+I-2581. Планшет инкубировался 7 минут при температуре 37°С. По достижению нужной степени интенсивности окрашивания во все лунки добавляли 20% раствор уксусной кислоты для остановки реакции. Далее измерялась оптическая плотность растворов в лунках планшета. Активность фактора свертывания крови VIII в исследуемых образцах определялась по калибровочной кривой с учетом предварительного разведения образцов.
Проведение in vivo исследования на лабораторных животных
Для экспериментов были использованы мыши линии B6.129S-F8tm1Smoc (HemA), дефицитные по FVIII (самцы возрастом 6-8 недель). Препараты вводили животным однократно путем внутривенного введения в хвостовую вену. Группе животных отрицательного контроля вводился буферный раствор, не содержащий AAV. Отбор плазмы крови производился в день инъекции до введения препаратов, далее - на 14 и 56 дни после введения экспрессионных векторов.
Статистический анализ данных
Результаты представлены в виде среднего значения±стандартное отклонение (SD), для сравнения результатов эксперимента использовали однофакторный дисперсионный анализ с поправкой на множественные попарные сравнения по методу Даннета (One-way ANOVA), и они были определены как статистически значимые.
Пример 1
С целью повышения уровня секреции белка FVIII-BDD (фактор свертывания крови VIII с делетированным В доменом) последовательность SEQ ID NO: 6 (СП-FVIII-FVIII-BDD) была модифицирована путем замены последовательности сигнального пептида FVIII дикого типа на сигнальный пептид, соответствующий аминокислотной последовательности, указанной в SEQ ID NO: 2 (СП-FIX) или SEQ ID NO: 3 (СП-IgGK) или SEQ ID NO: 4 (СП-Lactalbumin), что привело к получению слитых белков, соответствующих аминокислотным последовательностям SEQ ID NO: 7 (СП-FIX-FVIII-BDD), SEQ ID NO: 8 (СП-IgGK-FVIII-BDD) и SEQ ID NO: 9 (СП-LactalbuminFVIII-BDD).
Полученные нами нуклеиновые кислоты, кодирующие слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, были проверены при трансфекции клеток линии in vitro в составе экспрессионной кассеты, состоящей из левого (первого) ITR (инвертированные концевые повторы), соответствующего последовательности SEQ ID NO: 14, промотора HLP (SEQ ID NO: 15), гена интереса, сигнала полиаденилирования (SEQ ID NO: 16), правого (второго) ITR (SEQ ID NO: 17), где геном интереса является одна из последовательностей SEQ ID NO: 10-13. В качестве контроля использовалась нуклеиновая кислота, которая кодирует белок человеческого FVIII-BDD, включая природный сигнальный пептид FVIII-BDD, соответствующая последовательности SEQ ID NO 10 (СП-FVIII-FVIII-BDD).
Использование всех нуклеиновых кислот SEQ ID NO: 11-13, кодирующих слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов с последовательностями SEQ ID NO: 7-9, привело к увеличению уровня продукции (Фигура 1) и активности (Фигура 2) белка FVIII-BDD по сравнению с использованием нуклеиновой кислоты SEQ ID NO: 10, кодирующей белок FVIII-BDD с природным сигнальным пептидом SEQ ID NO: 6 (СП-FVIII-FVIII-BDD). При этом неожиданное увеличение уровня продукции белка FVIII-BDD в полученной после трансфекции культуральной жидкости по сравнению с использованием нуклеиновой кислоты SEQ ID NO: 10 (СП-FVIII-FVIII-BDD) в 4,3 раза показала последовательность SEQ ID NO: 11 (СП-FIX-FVIII-BDD), в 1,3 раза показала последовательность SEQ ID NO: 12 (СП-IgGK-FVIII-BDD), и в 4,9 раз показала последовательность SEQ ID NO: 13 (СП-LactalbuminFVIII-BDD). Аналогичные данные наблюдались по активности FVIII-BDD в полученной после трансфекции культуральной жидкости: наблюдалось неожиданное увеличение при сравнении нуклеиновой кислоты SEQ ID NO: 10 (СП-FVIII-FVIII-BDD) с нуклеиновыми кислотами SEQ ID NO: 11 (СП-FIX-FVIII-BDD) (увеличение в 8,6 раз), с SEQ ID NO: 12 (СП-IgGK-FVIII-BDD) (увеличение в 1,9 раз) и с SEQ ID NO: 13 (СП-LactalbuminFVIII-BDD) (увеличение в 7,2 раза). Наблюдаемое соответствие между результатами по продукции и активности белка FVIII-BDD говорит о том, что замена природного сигнального пептида FVIII-BDD на сигнальный пептид, соответствующий аминокислотной последовательности указанной в SEQ ID NO: 2 (СП-FIX), или SEQ ID NO: 3 (СП-IgGK), или SEQ ID NO: 4 (СП-Lactalbumin) приводит к значительному увеличению продукции и активности белка FVIII-BDD, но при этом не влияет на функциональность белка FVIII-BDD.
Таким образом, полученные нами нуклеиновые кислоты, кодирующие слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, способны приводить к экспрессии белка FVIII-BDD in vitro в клетке-хозяине и обладают высоким потенциалом для получения рекомбинантного белка FVIII-BDD в клетках-продуцентах для терапии Гемофилии А.
Пример 2
Были получены экспрессионные векторы на основе rAAV, содержащие нуклеиновые кислоты SEQ ID NO: 11-13, которые кодируют слитые белки на основе FVIII-BDD и гетерологичные сигнальные пептиды, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7-9. Указанные экспрессионные вектора были проверены при трансдукции клеток линии HUH7 in vitro. В качестве контроля использовался экспрессионные вектор на основе rAAV, содержащий нуклеиновую кислоту SEQ ID NO: 10, которая кодирует белок человеческого FVIII-BDD, включая природный сигнальный пептид FVIII, соответствующая последовательности SEQ ID NO: 6 (СП-FVIII-FVIII-BDD).
Использование экспрессионных векторов, содержащих нуклеиновые кислоты SEQ ID NO: 11-13, привело к увеличению уровня продукции (Фигура 3) и активности (Фигура 4) белка FVIII-BDD по сравнению с использованием экспрессионного вектора, содержащего нуклеиновую кислоту SEQ ID NO: 10 (СП-FVIII-FVIII-BDD). При этом неожиданное увеличение уровня продукции белка FVIII-BDD в полученной после трансдукции культуральной жидкости по сравнению с использованием экспрессионного вектора с нуклеиновой кислотой SEQ ID NO: 10 (СП-FVIII-FVIII-BDD) в 2,7 раза показал экспрессионный вектор с последовательностью SEQ ID NO: 11 (СП-FIX-FVIII-BDD), в 2,4 раза показал экспрессионный вектор с последовательностью SEQ ID NO: 13 (СП-Lactalbumin-FVIII-BDD). Аналогичные данные наблюдались по активности FVIII-BDD в полученной после трансдукции культуральной жидкости. Наблюдалось неожиданное увеличение при сравнении экспрессионного вектора с нуклеиновой кислотой SEQ ID NO: 10 (СП-FVIII-FVIII-BDD) с экспрессионными векторами с нуклеиновыми кислотами SEQ ID NO: 11 (СП-FIX-FVIII-BDD) (увеличение в 3,9 раза) и с SEQ ID NO: 13 (СП-Lactalbumin-FVIII-BDD) (увеличение в 3,5 раза). Полученные результаты находятся в соответствии с данными, полученными при трансфекции клеток линии HepG2.
Таким образом, разработанные экспрессионные вектора на основе rAAV, кодирующие слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, способны приводить к экспрессии белка FVIII-BDD; in vitro.
Пример 3
Для проведения in vivo исследований экспрессионных векторов на основе rAAV, содержащих нуклеиновую кислоту, выбранную из SEQ ID NO: 11 или SEQ ID NO: 13, которые кодируют слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7 или SEQ ID NO: 9, были использованы лабораторные мыши линии В6.129S-F8tm1Smoc (HemA), дефицитные по FVIII. В исследовании использовали дозу rAAV препаратов равную 6×1013 вг/кг. В качестве негативного контроля был использованы контрольный раствор без AAV. Препараты вводили животным однократно путем внутривенного гидродинамического введения в хвостовую вену. Отбор плазмы крови производился в день инъекции до введения препаратов, далее - на 14 и 56 дни после введения препаратов. В образцах плазмы крови определяли уровень белка фактора свертывания крови VIII-BDD методом ИФА, как было описано выше.
В результате проведенных in vivo исследований (Фигура 5) было показано, что в случае использования обоих экспрессионных векторов на основе rAAV, содержащих нуклеиновую кислоту, выбранную из SEQ ID NO: 11 или SEQ ID NO: 13, наблюдается достоверное увеличение количества фактора VIII-BDD в плазме крови животных на 14 и на 56 дни (Фигура 5). В случае использования экспрессионного вектора, содержащего нуклеиновую кислоту SEQ ID NO: 11, в плазме крови животных на 14 и 56 дни после инъекции наблюдалась экспрессия FVIII-BDD на уровне 296 и 504 нг/мл, соответственно. В случае использования экспрессионного вектора, содержащего нуклеиновую кислоту SEQ ID NO: 13, в плазме крови животных на 14 и 56 дни после инъекции наблюдалась экспрессия FVIII-BDD на уровне 270 и 381 нг/мл, соответственно.
Таким образом, разработанные экспрессионные вектора на основе rAAV, содержащие нуклеиновую кислоту, выбранную из SEQ ID NO: 11 или SEQ ID NO: 13, которые кодируют слитые белки на основе FVIII-BDD и одного из гетерологичных сигнальных пептидов, которые включают аминокислотную последовательность, выбранную из SEQ ID NO: 7 или SEQ ID NO: 9, способны приводить к экспрессии белка FVIII-BDD in vivo и обладают высоким потенциалом для генной терапии Гемофилии А.
--->
Перечень последовательностей
<110> АО "БИОКАД"
<120> Выделенная нуклеиновая кислота, которая кодирует слитый белок на основе
FVIII-BDD и гетерологичного сигнального пептида, и ее применение
<160> 17
<170> BiSSAP 1.3.6
<210> 1
<211> 19
<212> PRT
<213> Природная последовательность
<220>
<223> сигнальный пептид FVIII
<400> 1
Met Gln Ile Glu Leu Ser Thr Cys Phe Phe Leu Cys Leu Leu Arg Phe
1 5 10 15
Cys Phe Ser
<210> 2
<211> 28
<212> PRT
<213> Природная последовательность
<220>
<223> сигнальный пептид FIX
<400> 2
Met Gln Arg Val Asn Met Ile Met Ala Glu Ser Pro Gly Leu Ile Thr
1 5 10 15
Ile Cys Leu Leu Gly Tyr Leu Leu Ser Ala Glu Cys
20 25
<210> 3
<211> 20
<212> PRT
<213> Природная последовательность
<220>
<223> сигнальный пептид Kappa цепи иммуноглобулина G
<400> 3
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 4
<211> 19
<212> PRT
<213> Природная последовательность
<220>
<223> сигнальный пептид Lactalbumin
<400> 4
Met Met Ser Phe Val Ser Leu Leu Leu Val Gly Ile Leu Phe His Ala
1 5 10 15
Thr Gln Ala
<210> 5
<211> 1438
<212> PRT
<213> Искусственная последовательность
<220>
<223> белок FVIII-BDD (фактор свёртывания крови VIII c делетированным B
доменом)
<400> 5
Ala Thr Arg Arg Tyr Tyr Leu Gly Ala Val Glu Leu Ser Trp Asp Tyr
1 5 10 15
Met Gln Ser Asp Leu Gly Glu Leu Pro Val Asp Ala Arg Phe Pro Pro
20 25 30
Arg Val Pro Lys Ser Phe Pro Phe Asn Thr Ser Val Val Tyr Lys Lys
35 40 45
Thr Leu Phe Val Glu Phe Thr Asp His Leu Phe Asn Ile Ala Lys Pro
50 55 60
Arg Pro Pro Trp Met Gly Leu Leu Gly Pro Thr Ile Gln Ala Glu Val
65 70 75 80
Tyr Asp Thr Val Val Ile Thr Leu Lys Asn Met Ala Ser His Pro Val
85 90 95
Ser Leu His Ala Val Gly Val Ser Tyr Trp Lys Ala Ser Glu Gly Ala
100 105 110
Glu Tyr Asp Asp Gln Thr Ser Gln Arg Glu Lys Glu Asp Asp Lys Val
115 120 125
Phe Pro Gly Gly Ser His Thr Tyr Val Trp Gln Val Leu Lys Glu Asn
130 135 140
Gly Pro Met Ala Ser Asp Pro Leu Cys Leu Thr Tyr Ser Tyr Leu Ser
145 150 155 160
His Val Asp Leu Val Lys Asp Leu Asn Ser Gly Leu Ile Gly Ala Leu
165 170 175
Leu Val Cys Arg Glu Gly Ser Leu Ala Lys Glu Lys Thr Gln Thr Leu
180 185 190
His Lys Phe Ile Leu Leu Phe Ala Val Phe Asp Glu Gly Lys Ser Trp
195 200 205
His Ser Glu Thr Lys Asn Ser Leu Met Gln Asp Arg Asp Ala Ala Ser
210 215 220
Ala Arg Ala Trp Pro Lys Met His Thr Val Asn Gly Tyr Val Asn Arg
225 230 235 240
Ser Leu Pro Gly Leu Ile Gly Cys His Arg Lys Ser Val Tyr Trp His
245 250 255
Val Ile Gly Met Gly Thr Thr Pro Glu Val His Ser Ile Phe Leu Glu
260 265 270
Gly His Thr Phe Leu Val Arg Asn His Arg Gln Ala Ser Leu Glu Ile
275 280 285
Ser Pro Ile Thr Phe Leu Thr Ala Gln Thr Leu Leu Met Asp Leu Gly
290 295 300
Gln Phe Leu Leu Phe Cys His Ile Ser Ser His Gln His Asp Gly Met
305 310 315 320
Glu Ala Tyr Val Lys Val Asp Ser Cys Pro Glu Glu Pro Gln Leu Arg
325 330 335
Met Lys Asn Asn Glu Glu Ala Glu Asp Tyr Asp Asp Asp Leu Thr Asp
340 345 350
Ser Glu Met Asp Val Val Arg Phe Asp Asp Asp Asn Ser Pro Ser Phe
355 360 365
Ile Gln Ile Arg Ser Val Ala Lys Lys His Pro Lys Thr Trp Val His
370 375 380
Tyr Ile Ala Ala Glu Glu Glu Asp Trp Asp Tyr Ala Pro Leu Val Leu
385 390 395 400
Ala Pro Asp Asp Arg Ser Tyr Lys Ser Gln Tyr Leu Asn Asn Gly Pro
405 410 415
Gln Arg Ile Gly Arg Lys Tyr Lys Lys Val Arg Phe Met Ala Tyr Thr
420 425 430
Asp Glu Thr Phe Lys Thr Arg Glu Ala Ile Gln His Glu Ser Gly Ile
435 440 445
Leu Gly Pro Leu Leu Tyr Gly Glu Val Gly Asp Thr Leu Leu Ile Ile
450 455 460
Phe Lys Asn Gln Ala Ser Arg Pro Tyr Asn Ile Tyr Pro His Gly Ile
465 470 475 480
Thr Asp Val Arg Pro Leu Tyr Ser Arg Arg Leu Pro Lys Gly Val Lys
485 490 495
His Leu Lys Asp Phe Pro Ile Leu Pro Gly Glu Ile Phe Lys Tyr Lys
500 505 510
Trp Thr Val Thr Val Glu Asp Gly Pro Thr Lys Ser Asp Pro Arg Cys
515 520 525
Leu Thr Arg Tyr Tyr Ser Ser Phe Val Asn Met Glu Arg Asp Leu Ala
530 535 540
Ser Gly Leu Ile Gly Pro Leu Leu Ile Cys Tyr Lys Glu Ser Val Asp
545 550 555 560
Gln Arg Gly Asn Gln Ile Met Ser Asp Lys Arg Asn Val Ile Leu Phe
565 570 575
Ser Val Phe Asp Glu Asn Arg Ser Trp Tyr Leu Thr Glu Asn Ile Gln
580 585 590
Arg Phe Leu Pro Asn Pro Ala Gly Val Gln Leu Glu Asp Pro Glu Phe
595 600 605
Gln Ala Ser Asn Ile Met His Ser Ile Asn Gly Tyr Val Phe Asp Ser
610 615 620
Leu Gln Leu Ser Val Cys Leu His Glu Val Ala Tyr Trp Tyr Ile Leu
625 630 635 640
Ser Ile Gly Ala Gln Thr Asp Phe Leu Ser Val Phe Phe Ser Gly Tyr
645 650 655
Thr Phe Lys His Lys Met Val Tyr Glu Asp Thr Leu Thr Leu Phe Pro
660 665 670
Phe Ser Gly Glu Thr Val Phe Met Ser Met Glu Asn Pro Gly Leu Trp
675 680 685
Ile Leu Gly Cys His Asn Ser Asp Phe Arg Asn Arg Gly Met Thr Ala
690 695 700
Leu Leu Lys Val Ser Ser Cys Asp Lys Asn Thr Gly Asp Tyr Tyr Glu
705 710 715 720
Asp Ser Tyr Glu Asp Ile Ser Ala Tyr Leu Leu Ser Lys Asn Asn Ala
725 730 735
Ile Glu Pro Arg Ser Phe Ser Gln Asn Pro Pro Val Leu Lys Arg His
740 745 750
Gln Arg Glu Ile Thr Arg Thr Thr Leu Gln Ser Asp Gln Glu Glu Ile
755 760 765
Asp Tyr Asp Asp Thr Ile Ser Val Glu Met Lys Lys Glu Asp Phe Asp
770 775 780
Ile Tyr Asp Glu Asp Glu Asn Gln Ser Pro Arg Ser Phe Gln Lys Lys
785 790 795 800
Thr Arg His Tyr Phe Ile Ala Ala Val Glu Arg Leu Trp Asp Tyr Gly
805 810 815
Met Ser Ser Ser Pro His Val Leu Arg Asn Arg Ala Gln Ser Gly Ser
820 825 830
Val Pro Gln Phe Lys Lys Val Val Phe Gln Glu Phe Thr Asp Gly Ser
835 840 845
Phe Thr Gln Pro Leu Tyr Arg Gly Glu Leu Asn Glu His Leu Gly Leu
850 855 860
Leu Gly Pro Tyr Ile Arg Ala Glu Val Glu Asp Asn Ile Met Val Thr
865 870 875 880
Phe Arg Asn Gln Ala Ser Arg Pro Tyr Ser Phe Tyr Ser Ser Leu Ile
885 890 895
Ser Tyr Glu Glu Asp Gln Arg Gln Gly Ala Glu Pro Arg Lys Asn Phe
900 905 910
Val Lys Pro Asn Glu Thr Lys Thr Tyr Phe Trp Lys Val Gln His His
915 920 925
Met Ala Pro Thr Lys Asp Glu Phe Asp Cys Lys Ala Trp Ala Tyr Phe
930 935 940
Ser Asp Val Asp Leu Glu Lys Asp Val His Ser Gly Leu Ile Gly Pro
945 950 955 960
Leu Leu Val Cys His Thr Asn Thr Leu Asn Pro Ala His Gly Arg Gln
965 970 975
Val Thr Val Gln Glu Phe Ala Leu Phe Phe Thr Ile Phe Asp Glu Thr
980 985 990
Lys Ser Trp Tyr Phe Thr Glu Asn Met Glu Arg Asn Cys Arg Ala Pro
995 1000 1005
Cys Asn Ile Gln Met Glu Asp Pro Thr Phe Lys Glu Asn Tyr Arg Phe
1010 1015 1020
His Ala Ile Asn Gly Tyr Ile Met Asp Thr Leu Pro Gly Leu Val Met
1025 1030 1035 1040
Ala Gln Asp Gln Arg Ile Arg Trp Tyr Leu Leu Ser Met Gly Ser Asn
1045 1050 1055
Glu Asn Ile His Ser Ile His Phe Ser Gly His Val Phe Thr Val Arg
1060 1065 1070
Lys Lys Glu Glu Tyr Lys Met Ala Leu Tyr Asn Leu Tyr Pro Gly Val
1075 1080 1085
Phe Glu Thr Val Glu Met Leu Pro Ser Lys Ala Gly Ile Trp Arg Val
1090 1095 1100
Glu Cys Leu Ile Gly Glu His Leu His Ala Gly Met Ser Thr Leu Phe
1105 1110 1115 1120
Leu Val Tyr Ser Asn Lys Cys Gln Thr Pro Leu Gly Met Ala Ser Gly
1125 1130 1135
His Ile Arg Asp Phe Gln Ile Thr Ala Ser Gly Gln Tyr Gly Gln Trp
1140 1145 1150
Ala Pro Lys Leu Ala Arg Leu His Tyr Ser Gly Ser Ile Asn Ala Trp
1155 1160 1165
Ser Thr Lys Glu Pro Phe Ser Trp Ile Lys Val Asp Leu Leu Ala Pro
1170 1175 1180
Met Ile Ile His Gly Ile Lys Thr Gln Gly Ala Arg Gln Lys Phe Ser
1185 1190 1195 1200
Ser Leu Tyr Ile Ser Gln Phe Ile Ile Met Tyr Ser Leu Asp Gly Lys
1205 1210 1215
Lys Trp Gln Thr Tyr Arg Gly Asn Ser Thr Gly Thr Leu Met Val Phe
1220 1225 1230
Phe Gly Asn Val Asp Ser Ser Gly Ile Lys His Asn Ile Phe Asn Pro
1235 1240 1245
Pro Ile Ile Ala Arg Tyr Ile Arg Leu His Pro Thr His Tyr Ser Ile
1250 1255 1260
Arg Ser Thr Leu Arg Met Glu Leu Met Gly Cys Asp Leu Asn Ser Cys
1265 1270 1275 1280
Ser Met Pro Leu Gly Met Glu Ser Lys Ala Ile Ser Asp Ala Gln Ile
1285 1290 1295
Thr Ala Ser Ser Tyr Phe Thr Asn Met Phe Ala Thr Trp Ser Pro Ser
1300 1305 1310
Lys Ala Arg Leu His Leu Gln Gly Arg Ser Asn Ala Trp Arg Pro Gln
1315 1320 1325
Val Asn Asn Pro Lys Glu Trp Leu Gln Val Asp Phe Gln Lys Thr Met
1330 1335 1340
Lys Val Thr Gly Val Thr Thr Gln Gly Val Lys Ser Leu Leu Thr Ser
1345 1350 1355 1360
Met Tyr Val Lys Glu Phe Leu Ile Ser Ser Ser Gln Asp Gly His Gln
1365 1370 1375
Trp Thr Leu Phe Phe Gln Asn Gly Lys Val Lys Val Phe Gln Gly Asn
1380 1385 1390
Gln Asp Ser Phe Thr Pro Val Val Asn Ser Leu Asp Pro Pro Leu Leu
1395 1400 1405
Thr Arg Tyr Leu Arg Ile His Pro Gln Ser Trp Val His Gln Ile Ala
1410 1415 1420
Leu Arg Met Glu Val Leu Gly Cys Glu Ala Gln Asp Leu Tyr
1425 1430 1435
<210> 6
<211> 1457
<212> PRT
<213> Искусственная последовательность
<220>
<223> белок FVIII-BDD с сигнальным дикого типа (СП-FVIII-FVIII-BDD)
<400> 6
Met Gln Ile Glu Leu Ser Thr Cys Phe Phe Leu Cys Leu Leu Arg Phe
1 5 10 15
Cys Phe Ser Ala Thr Arg Arg Tyr Tyr Leu Gly Ala Val Glu Leu Ser
20 25 30
Trp Asp Tyr Met Gln Ser Asp Leu Gly Glu Leu Pro Val Asp Ala Arg
35 40 45
Phe Pro Pro Arg Val Pro Lys Ser Phe Pro Phe Asn Thr Ser Val Val
50 55 60
Tyr Lys Lys Thr Leu Phe Val Glu Phe Thr Asp His Leu Phe Asn Ile
65 70 75 80
Ala Lys Pro Arg Pro Pro Trp Met Gly Leu Leu Gly Pro Thr Ile Gln
85 90 95
Ala Glu Val Tyr Asp Thr Val Val Ile Thr Leu Lys Asn Met Ala Ser
100 105 110
His Pro Val Ser Leu His Ala Val Gly Val Ser Tyr Trp Lys Ala Ser
115 120 125
Glu Gly Ala Glu Tyr Asp Asp Gln Thr Ser Gln Arg Glu Lys Glu Asp
130 135 140
Asp Lys Val Phe Pro Gly Gly Ser His Thr Tyr Val Trp Gln Val Leu
145 150 155 160
Lys Glu Asn Gly Pro Met Ala Ser Asp Pro Leu Cys Leu Thr Tyr Ser
165 170 175
Tyr Leu Ser His Val Asp Leu Val Lys Asp Leu Asn Ser Gly Leu Ile
180 185 190
Gly Ala Leu Leu Val Cys Arg Glu Gly Ser Leu Ala Lys Glu Lys Thr
195 200 205
Gln Thr Leu His Lys Phe Ile Leu Leu Phe Ala Val Phe Asp Glu Gly
210 215 220
Lys Ser Trp His Ser Glu Thr Lys Asn Ser Leu Met Gln Asp Arg Asp
225 230 235 240
Ala Ala Ser Ala Arg Ala Trp Pro Lys Met His Thr Val Asn Gly Tyr
245 250 255
Val Asn Arg Ser Leu Pro Gly Leu Ile Gly Cys His Arg Lys Ser Val
260 265 270
Tyr Trp His Val Ile Gly Met Gly Thr Thr Pro Glu Val His Ser Ile
275 280 285
Phe Leu Glu Gly His Thr Phe Leu Val Arg Asn His Arg Gln Ala Ser
290 295 300
Leu Glu Ile Ser Pro Ile Thr Phe Leu Thr Ala Gln Thr Leu Leu Met
305 310 315 320
Asp Leu Gly Gln Phe Leu Leu Phe Cys His Ile Ser Ser His Gln His
325 330 335
Asp Gly Met Glu Ala Tyr Val Lys Val Asp Ser Cys Pro Glu Glu Pro
340 345 350
Gln Leu Arg Met Lys Asn Asn Glu Glu Ala Glu Asp Tyr Asp Asp Asp
355 360 365
Leu Thr Asp Ser Glu Met Asp Val Val Arg Phe Asp Asp Asp Asn Ser
370 375 380
Pro Ser Phe Ile Gln Ile Arg Ser Val Ala Lys Lys His Pro Lys Thr
385 390 395 400
Trp Val His Tyr Ile Ala Ala Glu Glu Glu Asp Trp Asp Tyr Ala Pro
405 410 415
Leu Val Leu Ala Pro Asp Asp Arg Ser Tyr Lys Ser Gln Tyr Leu Asn
420 425 430
Asn Gly Pro Gln Arg Ile Gly Arg Lys Tyr Lys Lys Val Arg Phe Met
435 440 445
Ala Tyr Thr Asp Glu Thr Phe Lys Thr Arg Glu Ala Ile Gln His Glu
450 455 460
Ser Gly Ile Leu Gly Pro Leu Leu Tyr Gly Glu Val Gly Asp Thr Leu
465 470 475 480
Leu Ile Ile Phe Lys Asn Gln Ala Ser Arg Pro Tyr Asn Ile Tyr Pro
485 490 495
His Gly Ile Thr Asp Val Arg Pro Leu Tyr Ser Arg Arg Leu Pro Lys
500 505 510
Gly Val Lys His Leu Lys Asp Phe Pro Ile Leu Pro Gly Glu Ile Phe
515 520 525
Lys Tyr Lys Trp Thr Val Thr Val Glu Asp Gly Pro Thr Lys Ser Asp
530 535 540
Pro Arg Cys Leu Thr Arg Tyr Tyr Ser Ser Phe Val Asn Met Glu Arg
545 550 555 560
Asp Leu Ala Ser Gly Leu Ile Gly Pro Leu Leu Ile Cys Tyr Lys Glu
565 570 575
Ser Val Asp Gln Arg Gly Asn Gln Ile Met Ser Asp Lys Arg Asn Val
580 585 590
Ile Leu Phe Ser Val Phe Asp Glu Asn Arg Ser Trp Tyr Leu Thr Glu
595 600 605
Asn Ile Gln Arg Phe Leu Pro Asn Pro Ala Gly Val Gln Leu Glu Asp
610 615 620
Pro Glu Phe Gln Ala Ser Asn Ile Met His Ser Ile Asn Gly Tyr Val
625 630 635 640
Phe Asp Ser Leu Gln Leu Ser Val Cys Leu His Glu Val Ala Tyr Trp
645 650 655
Tyr Ile Leu Ser Ile Gly Ala Gln Thr Asp Phe Leu Ser Val Phe Phe
660 665 670
Ser Gly Tyr Thr Phe Lys His Lys Met Val Tyr Glu Asp Thr Leu Thr
675 680 685
Leu Phe Pro Phe Ser Gly Glu Thr Val Phe Met Ser Met Glu Asn Pro
690 695 700
Gly Leu Trp Ile Leu Gly Cys His Asn Ser Asp Phe Arg Asn Arg Gly
705 710 715 720
Met Thr Ala Leu Leu Lys Val Ser Ser Cys Asp Lys Asn Thr Gly Asp
725 730 735
Tyr Tyr Glu Asp Ser Tyr Glu Asp Ile Ser Ala Tyr Leu Leu Ser Lys
740 745 750
Asn Asn Ala Ile Glu Pro Arg Ser Phe Ser Gln Asn Pro Pro Val Leu
755 760 765
Lys Arg His Gln Arg Glu Ile Thr Arg Thr Thr Leu Gln Ser Asp Gln
770 775 780
Glu Glu Ile Asp Tyr Asp Asp Thr Ile Ser Val Glu Met Lys Lys Glu
785 790 795 800
Asp Phe Asp Ile Tyr Asp Glu Asp Glu Asn Gln Ser Pro Arg Ser Phe
805 810 815
Gln Lys Lys Thr Arg His Tyr Phe Ile Ala Ala Val Glu Arg Leu Trp
820 825 830
Asp Tyr Gly Met Ser Ser Ser Pro His Val Leu Arg Asn Arg Ala Gln
835 840 845
Ser Gly Ser Val Pro Gln Phe Lys Lys Val Val Phe Gln Glu Phe Thr
850 855 860
Asp Gly Ser Phe Thr Gln Pro Leu Tyr Arg Gly Glu Leu Asn Glu His
865 870 875 880
Leu Gly Leu Leu Gly Pro Tyr Ile Arg Ala Glu Val Glu Asp Asn Ile
885 890 895
Met Val Thr Phe Arg Asn Gln Ala Ser Arg Pro Tyr Ser Phe Tyr Ser
900 905 910
Ser Leu Ile Ser Tyr Glu Glu Asp Gln Arg Gln Gly Ala Glu Pro Arg
915 920 925
Lys Asn Phe Val Lys Pro Asn Glu Thr Lys Thr Tyr Phe Trp Lys Val
930 935 940
Gln His His Met Ala Pro Thr Lys Asp Glu Phe Asp Cys Lys Ala Trp
945 950 955 960
Ala Tyr Phe Ser Asp Val Asp Leu Glu Lys Asp Val His Ser Gly Leu
965 970 975
Ile Gly Pro Leu Leu Val Cys His Thr Asn Thr Leu Asn Pro Ala His
980 985 990
Gly Arg Gln Val Thr Val Gln Glu Phe Ala Leu Phe Phe Thr Ile Phe
995 1000 1005
Asp Glu Thr Lys Ser Trp Tyr Phe Thr Glu Asn Met Glu Arg Asn Cys
1010 1015 1020
Arg Ala Pro Cys Asn Ile Gln Met Glu Asp Pro Thr Phe Lys Glu Asn
1025 1030 1035 1040
Tyr Arg Phe His Ala Ile Asn Gly Tyr Ile Met Asp Thr Leu Pro Gly
1045 1050 1055
Leu Val Met Ala Gln Asp Gln Arg Ile Arg Trp Tyr Leu Leu Ser Met
1060 1065 1070
Gly Ser Asn Glu Asn Ile His Ser Ile His Phe Ser Gly His Val Phe
1075 1080 1085
Thr Val Arg Lys Lys Glu Glu Tyr Lys Met Ala Leu Tyr Asn Leu Tyr
1090 1095 1100
Pro Gly Val Phe Glu Thr Val Glu Met Leu Pro Ser Lys Ala Gly Ile
1105 1110 1115 1120
Trp Arg Val Glu Cys Leu Ile Gly Glu His Leu His Ala Gly Met Ser
1125 1130 1135
Thr Leu Phe Leu Val Tyr Ser Asn Lys Cys Gln Thr Pro Leu Gly Met
1140 1145 1150
Ala Ser Gly His Ile Arg Asp Phe Gln Ile Thr Ala Ser Gly Gln Tyr
1155 1160 1165
Gly Gln Trp Ala Pro Lys Leu Ala Arg Leu His Tyr Ser Gly Ser Ile
1170 1175 1180
Asn Ala Trp Ser Thr Lys Glu Pro Phe Ser Trp Ile Lys Val Asp Leu
1185 1190 1195 1200
Leu Ala Pro Met Ile Ile His Gly Ile Lys Thr Gln Gly Ala Arg Gln
1205 1210 1215
Lys Phe Ser Ser Leu Tyr Ile Ser Gln Phe Ile Ile Met Tyr Ser Leu
1220 1225 1230
Asp Gly Lys Lys Trp Gln Thr Tyr Arg Gly Asn Ser Thr Gly Thr Leu
1235 1240 1245
Met Val Phe Phe Gly Asn Val Asp Ser Ser Gly Ile Lys His Asn Ile
1250 1255 1260
Phe Asn Pro Pro Ile Ile Ala Arg Tyr Ile Arg Leu His Pro Thr His
1265 1270 1275 1280
Tyr Ser Ile Arg Ser Thr Leu Arg Met Glu Leu Met Gly Cys Asp Leu
1285 1290 1295
Asn Ser Cys Ser Met Pro Leu Gly Met Glu Ser Lys Ala Ile Ser Asp
1300 1305 1310
Ala Gln Ile Thr Ala Ser Ser Tyr Phe Thr Asn Met Phe Ala Thr Trp
1315 1320 1325
Ser Pro Ser Lys Ala Arg Leu His Leu Gln Gly Arg Ser Asn Ala Trp
1330 1335 1340
Arg Pro Gln Val Asn Asn Pro Lys Glu Trp Leu Gln Val Asp Phe Gln
1345 1350 1355 1360
Lys Thr Met Lys Val Thr Gly Val Thr Thr Gln Gly Val Lys Ser Leu
1365 1370 1375
Leu Thr Ser Met Tyr Val Lys Glu Phe Leu Ile Ser Ser Ser Gln Asp
1380 1385 1390
Gly His Gln Trp Thr Leu Phe Phe Gln Asn Gly Lys Val Lys Val Phe
1395 1400 1405
Gln Gly Asn Gln Asp Ser Phe Thr Pro Val Val Asn Ser Leu Asp Pro
1410 1415 1420
Pro Leu Leu Thr Arg Tyr Leu Arg Ile His Pro Gln Ser Trp Val His
1425 1430 1435 1440
Gln Ile Ala Leu Arg Met Glu Val Leu Gly Cys Glu Ala Gln Asp Leu
1445 1450 1455
Tyr
<210> 7
<211> 1466
<212> PRT
<213> Искусственная последовательность
<220>
<223> слитый белок на основе человеческого FVIII-BDD и сигнального
пептида FIX (СП-FIX-FVIII-BDD)
<400> 7
Met Gln Arg Val Asn Met Ile Met Ala Glu Ser Pro Gly Leu Ile Thr
1 5 10 15
Ile Cys Leu Leu Gly Tyr Leu Leu Ser Ala Glu Cys Ala Thr Arg Arg
20 25 30
Tyr Tyr Leu Gly Ala Val Glu Leu Ser Trp Asp Tyr Met Gln Ser Asp
35 40 45
Leu Gly Glu Leu Pro Val Asp Ala Arg Phe Pro Pro Arg Val Pro Lys
50 55 60
Ser Phe Pro Phe Asn Thr Ser Val Val Tyr Lys Lys Thr Leu Phe Val
65 70 75 80
Glu Phe Thr Asp His Leu Phe Asn Ile Ala Lys Pro Arg Pro Pro Trp
85 90 95
Met Gly Leu Leu Gly Pro Thr Ile Gln Ala Glu Val Tyr Asp Thr Val
100 105 110
Val Ile Thr Leu Lys Asn Met Ala Ser His Pro Val Ser Leu His Ala
115 120 125
Val Gly Val Ser Tyr Trp Lys Ala Ser Glu Gly Ala Glu Tyr Asp Asp
130 135 140
Gln Thr Ser Gln Arg Glu Lys Glu Asp Asp Lys Val Phe Pro Gly Gly
145 150 155 160
Ser His Thr Tyr Val Trp Gln Val Leu Lys Glu Asn Gly Pro Met Ala
165 170 175
Ser Asp Pro Leu Cys Leu Thr Tyr Ser Tyr Leu Ser His Val Asp Leu
180 185 190
Val Lys Asp Leu Asn Ser Gly Leu Ile Gly Ala Leu Leu Val Cys Arg
195 200 205
Glu Gly Ser Leu Ala Lys Glu Lys Thr Gln Thr Leu His Lys Phe Ile
210 215 220
Leu Leu Phe Ala Val Phe Asp Glu Gly Lys Ser Trp His Ser Glu Thr
225 230 235 240
Lys Asn Ser Leu Met Gln Asp Arg Asp Ala Ala Ser Ala Arg Ala Trp
245 250 255
Pro Lys Met His Thr Val Asn Gly Tyr Val Asn Arg Ser Leu Pro Gly
260 265 270
Leu Ile Gly Cys His Arg Lys Ser Val Tyr Trp His Val Ile Gly Met
275 280 285
Gly Thr Thr Pro Glu Val His Ser Ile Phe Leu Glu Gly His Thr Phe
290 295 300
Leu Val Arg Asn His Arg Gln Ala Ser Leu Glu Ile Ser Pro Ile Thr
305 310 315 320
Phe Leu Thr Ala Gln Thr Leu Leu Met Asp Leu Gly Gln Phe Leu Leu
325 330 335
Phe Cys His Ile Ser Ser His Gln His Asp Gly Met Glu Ala Tyr Val
340 345 350
Lys Val Asp Ser Cys Pro Glu Glu Pro Gln Leu Arg Met Lys Asn Asn
355 360 365
Glu Glu Ala Glu Asp Tyr Asp Asp Asp Leu Thr Asp Ser Glu Met Asp
370 375 380
Val Val Arg Phe Asp Asp Asp Asn Ser Pro Ser Phe Ile Gln Ile Arg
385 390 395 400
Ser Val Ala Lys Lys His Pro Lys Thr Trp Val His Tyr Ile Ala Ala
405 410 415
Glu Glu Glu Asp Trp Asp Tyr Ala Pro Leu Val Leu Ala Pro Asp Asp
420 425 430
Arg Ser Tyr Lys Ser Gln Tyr Leu Asn Asn Gly Pro Gln Arg Ile Gly
435 440 445
Arg Lys Tyr Lys Lys Val Arg Phe Met Ala Tyr Thr Asp Glu Thr Phe
450 455 460
Lys Thr Arg Glu Ala Ile Gln His Glu Ser Gly Ile Leu Gly Pro Leu
465 470 475 480
Leu Tyr Gly Glu Val Gly Asp Thr Leu Leu Ile Ile Phe Lys Asn Gln
485 490 495
Ala Ser Arg Pro Tyr Asn Ile Tyr Pro His Gly Ile Thr Asp Val Arg
500 505 510
Pro Leu Tyr Ser Arg Arg Leu Pro Lys Gly Val Lys His Leu Lys Asp
515 520 525
Phe Pro Ile Leu Pro Gly Glu Ile Phe Lys Tyr Lys Trp Thr Val Thr
530 535 540
Val Glu Asp Gly Pro Thr Lys Ser Asp Pro Arg Cys Leu Thr Arg Tyr
545 550 555 560
Tyr Ser Ser Phe Val Asn Met Glu Arg Asp Leu Ala Ser Gly Leu Ile
565 570 575
Gly Pro Leu Leu Ile Cys Tyr Lys Glu Ser Val Asp Gln Arg Gly Asn
580 585 590
Gln Ile Met Ser Asp Lys Arg Asn Val Ile Leu Phe Ser Val Phe Asp
595 600 605
Glu Asn Arg Ser Trp Tyr Leu Thr Glu Asn Ile Gln Arg Phe Leu Pro
610 615 620
Asn Pro Ala Gly Val Gln Leu Glu Asp Pro Glu Phe Gln Ala Ser Asn
625 630 635 640
Ile Met His Ser Ile Asn Gly Tyr Val Phe Asp Ser Leu Gln Leu Ser
645 650 655
Val Cys Leu His Glu Val Ala Tyr Trp Tyr Ile Leu Ser Ile Gly Ala
660 665 670
Gln Thr Asp Phe Leu Ser Val Phe Phe Ser Gly Tyr Thr Phe Lys His
675 680 685
Lys Met Val Tyr Glu Asp Thr Leu Thr Leu Phe Pro Phe Ser Gly Glu
690 695 700
Thr Val Phe Met Ser Met Glu Asn Pro Gly Leu Trp Ile Leu Gly Cys
705 710 715 720
His Asn Ser Asp Phe Arg Asn Arg Gly Met Thr Ala Leu Leu Lys Val
725 730 735
Ser Ser Cys Asp Lys Asn Thr Gly Asp Tyr Tyr Glu Asp Ser Tyr Glu
740 745 750
Asp Ile Ser Ala Tyr Leu Leu Ser Lys Asn Asn Ala Ile Glu Pro Arg
755 760 765
Ser Phe Ser Gln Asn Pro Pro Val Leu Lys Arg His Gln Arg Glu Ile
770 775 780
Thr Arg Thr Thr Leu Gln Ser Asp Gln Glu Glu Ile Asp Tyr Asp Asp
785 790 795 800
Thr Ile Ser Val Glu Met Lys Lys Glu Asp Phe Asp Ile Tyr Asp Glu
805 810 815
Asp Glu Asn Gln Ser Pro Arg Ser Phe Gln Lys Lys Thr Arg His Tyr
820 825 830
Phe Ile Ala Ala Val Glu Arg Leu Trp Asp Tyr Gly Met Ser Ser Ser
835 840 845
Pro His Val Leu Arg Asn Arg Ala Gln Ser Gly Ser Val Pro Gln Phe
850 855 860
Lys Lys Val Val Phe Gln Glu Phe Thr Asp Gly Ser Phe Thr Gln Pro
865 870 875 880
Leu Tyr Arg Gly Glu Leu Asn Glu His Leu Gly Leu Leu Gly Pro Tyr
885 890 895
Ile Arg Ala Glu Val Glu Asp Asn Ile Met Val Thr Phe Arg Asn Gln
900 905 910
Ala Ser Arg Pro Tyr Ser Phe Tyr Ser Ser Leu Ile Ser Tyr Glu Glu
915 920 925
Asp Gln Arg Gln Gly Ala Glu Pro Arg Lys Asn Phe Val Lys Pro Asn
930 935 940
Glu Thr Lys Thr Tyr Phe Trp Lys Val Gln His His Met Ala Pro Thr
945 950 955 960
Lys Asp Glu Phe Asp Cys Lys Ala Trp Ala Tyr Phe Ser Asp Val Asp
965 970 975
Leu Glu Lys Asp Val His Ser Gly Leu Ile Gly Pro Leu Leu Val Cys
980 985 990
His Thr Asn Thr Leu Asn Pro Ala His Gly Arg Gln Val Thr Val Gln
995 1000 1005
Glu Phe Ala Leu Phe Phe Thr Ile Phe Asp Glu Thr Lys Ser Trp Tyr
1010 1015 1020
Phe Thr Glu Asn Met Glu Arg Asn Cys Arg Ala Pro Cys Asn Ile Gln
1025 1030 1035 1040
Met Glu Asp Pro Thr Phe Lys Glu Asn Tyr Arg Phe His Ala Ile Asn
1045 1050 1055
Gly Tyr Ile Met Asp Thr Leu Pro Gly Leu Val Met Ala Gln Asp Gln
1060 1065 1070
Arg Ile Arg Trp Tyr Leu Leu Ser Met Gly Ser Asn Glu Asn Ile His
1075 1080 1085
Ser Ile His Phe Ser Gly His Val Phe Thr Val Arg Lys Lys Glu Glu
1090 1095 1100
Tyr Lys Met Ala Leu Tyr Asn Leu Tyr Pro Gly Val Phe Glu Thr Val
1105 1110 1115 1120
Glu Met Leu Pro Ser Lys Ala Gly Ile Trp Arg Val Glu Cys Leu Ile
1125 1130 1135
Gly Glu His Leu His Ala Gly Met Ser Thr Leu Phe Leu Val Tyr Ser
1140 1145 1150
Asn Lys Cys Gln Thr Pro Leu Gly Met Ala Ser Gly His Ile Arg Asp
1155 1160 1165
Phe Gln Ile Thr Ala Ser Gly Gln Tyr Gly Gln Trp Ala Pro Lys Leu
1170 1175 1180
Ala Arg Leu His Tyr Ser Gly Ser Ile Asn Ala Trp Ser Thr Lys Glu
1185 1190 1195 1200
Pro Phe Ser Trp Ile Lys Val Asp Leu Leu Ala Pro Met Ile Ile His
1205 1210 1215
Gly Ile Lys Thr Gln Gly Ala Arg Gln Lys Phe Ser Ser Leu Tyr Ile
1220 1225 1230
Ser Gln Phe Ile Ile Met Tyr Ser Leu Asp Gly Lys Lys Trp Gln Thr
1235 1240 1245
Tyr Arg Gly Asn Ser Thr Gly Thr Leu Met Val Phe Phe Gly Asn Val
1250 1255 1260
Asp Ser Ser Gly Ile Lys His Asn Ile Phe Asn Pro Pro Ile Ile Ala
1265 1270 1275 1280
Arg Tyr Ile Arg Leu His Pro Thr His Tyr Ser Ile Arg Ser Thr Leu
1285 1290 1295
Arg Met Glu Leu Met Gly Cys Asp Leu Asn Ser Cys Ser Met Pro Leu
1300 1305 1310
Gly Met Glu Ser Lys Ala Ile Ser Asp Ala Gln Ile Thr Ala Ser Ser
1315 1320 1325
Tyr Phe Thr Asn Met Phe Ala Thr Trp Ser Pro Ser Lys Ala Arg Leu
1330 1335 1340
His Leu Gln Gly Arg Ser Asn Ala Trp Arg Pro Gln Val Asn Asn Pro
1345 1350 1355 1360
Lys Glu Trp Leu Gln Val Asp Phe Gln Lys Thr Met Lys Val Thr Gly
1365 1370 1375
Val Thr Thr Gln Gly Val Lys Ser Leu Leu Thr Ser Met Tyr Val Lys
1380 1385 1390
Glu Phe Leu Ile Ser Ser Ser Gln Asp Gly His Gln Trp Thr Leu Phe
1395 1400 1405
Phe Gln Asn Gly Lys Val Lys Val Phe Gln Gly Asn Gln Asp Ser Phe
1410 1415 1420
Thr Pro Val Val Asn Ser Leu Asp Pro Pro Leu Leu Thr Arg Tyr Leu
1425 1430 1435 1440
Arg Ile His Pro Gln Ser Trp Val His Gln Ile Ala Leu Arg Met Glu
1445 1450 1455
Val Leu Gly Cys Glu Ala Gln Asp Leu Tyr
1460 1465
<210> 8
<211> 1458
<212> PRT
<213> Искусственная последовательность
<220>
<223> слитый белок на основе человеческого FVIII-BDD и сигнального
пептида Kappa цепь иммуноглобулина G (СП-IgGK-FVIII-BDD)
<400> 8
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Ala Thr Arg Arg Tyr Tyr Leu Gly Ala Val Glu Leu
20 25 30
Ser Trp Asp Tyr Met Gln Ser Asp Leu Gly Glu Leu Pro Val Asp Ala
35 40 45
Arg Phe Pro Pro Arg Val Pro Lys Ser Phe Pro Phe Asn Thr Ser Val
50 55 60
Val Tyr Lys Lys Thr Leu Phe Val Glu Phe Thr Asp His Leu Phe Asn
65 70 75 80
Ile Ala Lys Pro Arg Pro Pro Trp Met Gly Leu Leu Gly Pro Thr Ile
85 90 95
Gln Ala Glu Val Tyr Asp Thr Val Val Ile Thr Leu Lys Asn Met Ala
100 105 110
Ser His Pro Val Ser Leu His Ala Val Gly Val Ser Tyr Trp Lys Ala
115 120 125
Ser Glu Gly Ala Glu Tyr Asp Asp Gln Thr Ser Gln Arg Glu Lys Glu
130 135 140
Asp Asp Lys Val Phe Pro Gly Gly Ser His Thr Tyr Val Trp Gln Val
145 150 155 160
Leu Lys Glu Asn Gly Pro Met Ala Ser Asp Pro Leu Cys Leu Thr Tyr
165 170 175
Ser Tyr Leu Ser His Val Asp Leu Val Lys Asp Leu Asn Ser Gly Leu
180 185 190
Ile Gly Ala Leu Leu Val Cys Arg Glu Gly Ser Leu Ala Lys Glu Lys
195 200 205
Thr Gln Thr Leu His Lys Phe Ile Leu Leu Phe Ala Val Phe Asp Glu
210 215 220
Gly Lys Ser Trp His Ser Glu Thr Lys Asn Ser Leu Met Gln Asp Arg
225 230 235 240
Asp Ala Ala Ser Ala Arg Ala Trp Pro Lys Met His Thr Val Asn Gly
245 250 255
Tyr Val Asn Arg Ser Leu Pro Gly Leu Ile Gly Cys His Arg Lys Ser
260 265 270
Val Tyr Trp His Val Ile Gly Met Gly Thr Thr Pro Glu Val His Ser
275 280 285
Ile Phe Leu Glu Gly His Thr Phe Leu Val Arg Asn His Arg Gln Ala
290 295 300
Ser Leu Glu Ile Ser Pro Ile Thr Phe Leu Thr Ala Gln Thr Leu Leu
305 310 315 320
Met Asp Leu Gly Gln Phe Leu Leu Phe Cys His Ile Ser Ser His Gln
325 330 335
His Asp Gly Met Glu Ala Tyr Val Lys Val Asp Ser Cys Pro Glu Glu
340 345 350
Pro Gln Leu Arg Met Lys Asn Asn Glu Glu Ala Glu Asp Tyr Asp Asp
355 360 365
Asp Leu Thr Asp Ser Glu Met Asp Val Val Arg Phe Asp Asp Asp Asn
370 375 380
Ser Pro Ser Phe Ile Gln Ile Arg Ser Val Ala Lys Lys His Pro Lys
385 390 395 400
Thr Trp Val His Tyr Ile Ala Ala Glu Glu Glu Asp Trp Asp Tyr Ala
405 410 415
Pro Leu Val Leu Ala Pro Asp Asp Arg Ser Tyr Lys Ser Gln Tyr Leu
420 425 430
Asn Asn Gly Pro Gln Arg Ile Gly Arg Lys Tyr Lys Lys Val Arg Phe
435 440 445
Met Ala Tyr Thr Asp Glu Thr Phe Lys Thr Arg Glu Ala Ile Gln His
450 455 460
Glu Ser Gly Ile Leu Gly Pro Leu Leu Tyr Gly Glu Val Gly Asp Thr
465 470 475 480
Leu Leu Ile Ile Phe Lys Asn Gln Ala Ser Arg Pro Tyr Asn Ile Tyr
485 490 495
Pro His Gly Ile Thr Asp Val Arg Pro Leu Tyr Ser Arg Arg Leu Pro
500 505 510
Lys Gly Val Lys His Leu Lys Asp Phe Pro Ile Leu Pro Gly Glu Ile
515 520 525
Phe Lys Tyr Lys Trp Thr Val Thr Val Glu Asp Gly Pro Thr Lys Ser
530 535 540
Asp Pro Arg Cys Leu Thr Arg Tyr Tyr Ser Ser Phe Val Asn Met Glu
545 550 555 560
Arg Asp Leu Ala Ser Gly Leu Ile Gly Pro Leu Leu Ile Cys Tyr Lys
565 570 575
Glu Ser Val Asp Gln Arg Gly Asn Gln Ile Met Ser Asp Lys Arg Asn
580 585 590
Val Ile Leu Phe Ser Val Phe Asp Glu Asn Arg Ser Trp Tyr Leu Thr
595 600 605
Glu Asn Ile Gln Arg Phe Leu Pro Asn Pro Ala Gly Val Gln Leu Glu
610 615 620
Asp Pro Glu Phe Gln Ala Ser Asn Ile Met His Ser Ile Asn Gly Tyr
625 630 635 640
Val Phe Asp Ser Leu Gln Leu Ser Val Cys Leu His Glu Val Ala Tyr
645 650 655
Trp Tyr Ile Leu Ser Ile Gly Ala Gln Thr Asp Phe Leu Ser Val Phe
660 665 670
Phe Ser Gly Tyr Thr Phe Lys His Lys Met Val Tyr Glu Asp Thr Leu
675 680 685
Thr Leu Phe Pro Phe Ser Gly Glu Thr Val Phe Met Ser Met Glu Asn
690 695 700
Pro Gly Leu Trp Ile Leu Gly Cys His Asn Ser Asp Phe Arg Asn Arg
705 710 715 720
Gly Met Thr Ala Leu Leu Lys Val Ser Ser Cys Asp Lys Asn Thr Gly
725 730 735
Asp Tyr Tyr Glu Asp Ser Tyr Glu Asp Ile Ser Ala Tyr Leu Leu Ser
740 745 750
Lys Asn Asn Ala Ile Glu Pro Arg Ser Phe Ser Gln Asn Pro Pro Val
755 760 765
Leu Lys Arg His Gln Arg Glu Ile Thr Arg Thr Thr Leu Gln Ser Asp
770 775 780
Gln Glu Glu Ile Asp Tyr Asp Asp Thr Ile Ser Val Glu Met Lys Lys
785 790 795 800
Glu Asp Phe Asp Ile Tyr Asp Glu Asp Glu Asn Gln Ser Pro Arg Ser
805 810 815
Phe Gln Lys Lys Thr Arg His Tyr Phe Ile Ala Ala Val Glu Arg Leu
820 825 830
Trp Asp Tyr Gly Met Ser Ser Ser Pro His Val Leu Arg Asn Arg Ala
835 840 845
Gln Ser Gly Ser Val Pro Gln Phe Lys Lys Val Val Phe Gln Glu Phe
850 855 860
Thr Asp Gly Ser Phe Thr Gln Pro Leu Tyr Arg Gly Glu Leu Asn Glu
865 870 875 880
His Leu Gly Leu Leu Gly Pro Tyr Ile Arg Ala Glu Val Glu Asp Asn
885 890 895
Ile Met Val Thr Phe Arg Asn Gln Ala Ser Arg Pro Tyr Ser Phe Tyr
900 905 910
Ser Ser Leu Ile Ser Tyr Glu Glu Asp Gln Arg Gln Gly Ala Glu Pro
915 920 925
Arg Lys Asn Phe Val Lys Pro Asn Glu Thr Lys Thr Tyr Phe Trp Lys
930 935 940
Val Gln His His Met Ala Pro Thr Lys Asp Glu Phe Asp Cys Lys Ala
945 950 955 960
Trp Ala Tyr Phe Ser Asp Val Asp Leu Glu Lys Asp Val His Ser Gly
965 970 975
Leu Ile Gly Pro Leu Leu Val Cys His Thr Asn Thr Leu Asn Pro Ala
980 985 990
His Gly Arg Gln Val Thr Val Gln Glu Phe Ala Leu Phe Phe Thr Ile
995 1000 1005
Phe Asp Glu Thr Lys Ser Trp Tyr Phe Thr Glu Asn Met Glu Arg Asn
1010 1015 1020
Cys Arg Ala Pro Cys Asn Ile Gln Met Glu Asp Pro Thr Phe Lys Glu
1025 1030 1035 1040
Asn Tyr Arg Phe His Ala Ile Asn Gly Tyr Ile Met Asp Thr Leu Pro
1045 1050 1055
Gly Leu Val Met Ala Gln Asp Gln Arg Ile Arg Trp Tyr Leu Leu Ser
1060 1065 1070
Met Gly Ser Asn Glu Asn Ile His Ser Ile His Phe Ser Gly His Val
1075 1080 1085
Phe Thr Val Arg Lys Lys Glu Glu Tyr Lys Met Ala Leu Tyr Asn Leu
1090 1095 1100
Tyr Pro Gly Val Phe Glu Thr Val Glu Met Leu Pro Ser Lys Ala Gly
1105 1110 1115 1120
Ile Trp Arg Val Glu Cys Leu Ile Gly Glu His Leu His Ala Gly Met
1125 1130 1135
Ser Thr Leu Phe Leu Val Tyr Ser Asn Lys Cys Gln Thr Pro Leu Gly
1140 1145 1150
Met Ala Ser Gly His Ile Arg Asp Phe Gln Ile Thr Ala Ser Gly Gln
1155 1160 1165
Tyr Gly Gln Trp Ala Pro Lys Leu Ala Arg Leu His Tyr Ser Gly Ser
1170 1175 1180
Ile Asn Ala Trp Ser Thr Lys Glu Pro Phe Ser Trp Ile Lys Val Asp
1185 1190 1195 1200
Leu Leu Ala Pro Met Ile Ile His Gly Ile Lys Thr Gln Gly Ala Arg
1205 1210 1215
Gln Lys Phe Ser Ser Leu Tyr Ile Ser Gln Phe Ile Ile Met Tyr Ser
1220 1225 1230
Leu Asp Gly Lys Lys Trp Gln Thr Tyr Arg Gly Asn Ser Thr Gly Thr
1235 1240 1245
Leu Met Val Phe Phe Gly Asn Val Asp Ser Ser Gly Ile Lys His Asn
1250 1255 1260
Ile Phe Asn Pro Pro Ile Ile Ala Arg Tyr Ile Arg Leu His Pro Thr
1265 1270 1275 1280
His Tyr Ser Ile Arg Ser Thr Leu Arg Met Glu Leu Met Gly Cys Asp
1285 1290 1295
Leu Asn Ser Cys Ser Met Pro Leu Gly Met Glu Ser Lys Ala Ile Ser
1300 1305 1310
Asp Ala Gln Ile Thr Ala Ser Ser Tyr Phe Thr Asn Met Phe Ala Thr
1315 1320 1325
Trp Ser Pro Ser Lys Ala Arg Leu His Leu Gln Gly Arg Ser Asn Ala
1330 1335 1340
Trp Arg Pro Gln Val Asn Asn Pro Lys Glu Trp Leu Gln Val Asp Phe
1345 1350 1355 1360
Gln Lys Thr Met Lys Val Thr Gly Val Thr Thr Gln Gly Val Lys Ser
1365 1370 1375
Leu Leu Thr Ser Met Tyr Val Lys Glu Phe Leu Ile Ser Ser Ser Gln
1380 1385 1390
Asp Gly His Gln Trp Thr Leu Phe Phe Gln Asn Gly Lys Val Lys Val
1395 1400 1405
Phe Gln Gly Asn Gln Asp Ser Phe Thr Pro Val Val Asn Ser Leu Asp
1410 1415 1420
Pro Pro Leu Leu Thr Arg Tyr Leu Arg Ile His Pro Gln Ser Trp Val
1425 1430 1435 1440
His Gln Ile Ala Leu Arg Met Glu Val Leu Gly Cys Glu Ala Gln Asp
1445 1450 1455
Leu Tyr
<210> 9
<211> 1457
<212> PRT
<213> Искусственная последовательность
<220>
<223> слитый белок на основе человеческого FVIII-BDD и сигнального
пептида Lactalbumin (СП-Lactalbumin-FVIII-BDD)
<400> 9
Met Met Ser Phe Val Ser Leu Leu Leu Val Gly Ile Leu Phe His Ala
1 5 10 15
Thr Gln Ala Ala Thr Arg Arg Tyr Tyr Leu Gly Ala Val Glu Leu Ser
20 25 30
Trp Asp Tyr Met Gln Ser Asp Leu Gly Glu Leu Pro Val Asp Ala Arg
35 40 45
Phe Pro Pro Arg Val Pro Lys Ser Phe Pro Phe Asn Thr Ser Val Val
50 55 60
Tyr Lys Lys Thr Leu Phe Val Glu Phe Thr Asp His Leu Phe Asn Ile
65 70 75 80
Ala Lys Pro Arg Pro Pro Trp Met Gly Leu Leu Gly Pro Thr Ile Gln
85 90 95
Ala Glu Val Tyr Asp Thr Val Val Ile Thr Leu Lys Asn Met Ala Ser
100 105 110
His Pro Val Ser Leu His Ala Val Gly Val Ser Tyr Trp Lys Ala Ser
115 120 125
Glu Gly Ala Glu Tyr Asp Asp Gln Thr Ser Gln Arg Glu Lys Glu Asp
130 135 140
Asp Lys Val Phe Pro Gly Gly Ser His Thr Tyr Val Trp Gln Val Leu
145 150 155 160
Lys Glu Asn Gly Pro Met Ala Ser Asp Pro Leu Cys Leu Thr Tyr Ser
165 170 175
Tyr Leu Ser His Val Asp Leu Val Lys Asp Leu Asn Ser Gly Leu Ile
180 185 190
Gly Ala Leu Leu Val Cys Arg Glu Gly Ser Leu Ala Lys Glu Lys Thr
195 200 205
Gln Thr Leu His Lys Phe Ile Leu Leu Phe Ala Val Phe Asp Glu Gly
210 215 220
Lys Ser Trp His Ser Glu Thr Lys Asn Ser Leu Met Gln Asp Arg Asp
225 230 235 240
Ala Ala Ser Ala Arg Ala Trp Pro Lys Met His Thr Val Asn Gly Tyr
245 250 255
Val Asn Arg Ser Leu Pro Gly Leu Ile Gly Cys His Arg Lys Ser Val
260 265 270
Tyr Trp His Val Ile Gly Met Gly Thr Thr Pro Glu Val His Ser Ile
275 280 285
Phe Leu Glu Gly His Thr Phe Leu Val Arg Asn His Arg Gln Ala Ser
290 295 300
Leu Glu Ile Ser Pro Ile Thr Phe Leu Thr Ala Gln Thr Leu Leu Met
305 310 315 320
Asp Leu Gly Gln Phe Leu Leu Phe Cys His Ile Ser Ser His Gln His
325 330 335
Asp Gly Met Glu Ala Tyr Val Lys Val Asp Ser Cys Pro Glu Glu Pro
340 345 350
Gln Leu Arg Met Lys Asn Asn Glu Glu Ala Glu Asp Tyr Asp Asp Asp
355 360 365
Leu Thr Asp Ser Glu Met Asp Val Val Arg Phe Asp Asp Asp Asn Ser
370 375 380
Pro Ser Phe Ile Gln Ile Arg Ser Val Ala Lys Lys His Pro Lys Thr
385 390 395 400
Trp Val His Tyr Ile Ala Ala Glu Glu Glu Asp Trp Asp Tyr Ala Pro
405 410 415
Leu Val Leu Ala Pro Asp Asp Arg Ser Tyr Lys Ser Gln Tyr Leu Asn
420 425 430
Asn Gly Pro Gln Arg Ile Gly Arg Lys Tyr Lys Lys Val Arg Phe Met
435 440 445
Ala Tyr Thr Asp Glu Thr Phe Lys Thr Arg Glu Ala Ile Gln His Glu
450 455 460
Ser Gly Ile Leu Gly Pro Leu Leu Tyr Gly Glu Val Gly Asp Thr Leu
465 470 475 480
Leu Ile Ile Phe Lys Asn Gln Ala Ser Arg Pro Tyr Asn Ile Tyr Pro
485 490 495
His Gly Ile Thr Asp Val Arg Pro Leu Tyr Ser Arg Arg Leu Pro Lys
500 505 510
Gly Val Lys His Leu Lys Asp Phe Pro Ile Leu Pro Gly Glu Ile Phe
515 520 525
Lys Tyr Lys Trp Thr Val Thr Val Glu Asp Gly Pro Thr Lys Ser Asp
530 535 540
Pro Arg Cys Leu Thr Arg Tyr Tyr Ser Ser Phe Val Asn Met Glu Arg
545 550 555 560
Asp Leu Ala Ser Gly Leu Ile Gly Pro Leu Leu Ile Cys Tyr Lys Glu
565 570 575
Ser Val Asp Gln Arg Gly Asn Gln Ile Met Ser Asp Lys Arg Asn Val
580 585 590
Ile Leu Phe Ser Val Phe Asp Glu Asn Arg Ser Trp Tyr Leu Thr Glu
595 600 605
Asn Ile Gln Arg Phe Leu Pro Asn Pro Ala Gly Val Gln Leu Glu Asp
610 615 620
Pro Glu Phe Gln Ala Ser Asn Ile Met His Ser Ile Asn Gly Tyr Val
625 630 635 640
Phe Asp Ser Leu Gln Leu Ser Val Cys Leu His Glu Val Ala Tyr Trp
645 650 655
Tyr Ile Leu Ser Ile Gly Ala Gln Thr Asp Phe Leu Ser Val Phe Phe
660 665 670
Ser Gly Tyr Thr Phe Lys His Lys Met Val Tyr Glu Asp Thr Leu Thr
675 680 685
Leu Phe Pro Phe Ser Gly Glu Thr Val Phe Met Ser Met Glu Asn Pro
690 695 700
Gly Leu Trp Ile Leu Gly Cys His Asn Ser Asp Phe Arg Asn Arg Gly
705 710 715 720
Met Thr Ala Leu Leu Lys Val Ser Ser Cys Asp Lys Asn Thr Gly Asp
725 730 735
Tyr Tyr Glu Asp Ser Tyr Glu Asp Ile Ser Ala Tyr Leu Leu Ser Lys
740 745 750
Asn Asn Ala Ile Glu Pro Arg Ser Phe Ser Gln Asn Pro Pro Val Leu
755 760 765
Lys Arg His Gln Arg Glu Ile Thr Arg Thr Thr Leu Gln Ser Asp Gln
770 775 780
Glu Glu Ile Asp Tyr Asp Asp Thr Ile Ser Val Glu Met Lys Lys Glu
785 790 795 800
Asp Phe Asp Ile Tyr Asp Glu Asp Glu Asn Gln Ser Pro Arg Ser Phe
805 810 815
Gln Lys Lys Thr Arg His Tyr Phe Ile Ala Ala Val Glu Arg Leu Trp
820 825 830
Asp Tyr Gly Met Ser Ser Ser Pro His Val Leu Arg Asn Arg Ala Gln
835 840 845
Ser Gly Ser Val Pro Gln Phe Lys Lys Val Val Phe Gln Glu Phe Thr
850 855 860
Asp Gly Ser Phe Thr Gln Pro Leu Tyr Arg Gly Glu Leu Asn Glu His
865 870 875 880
Leu Gly Leu Leu Gly Pro Tyr Ile Arg Ala Glu Val Glu Asp Asn Ile
885 890 895
Met Val Thr Phe Arg Asn Gln Ala Ser Arg Pro Tyr Ser Phe Tyr Ser
900 905 910
Ser Leu Ile Ser Tyr Glu Glu Asp Gln Arg Gln Gly Ala Glu Pro Arg
915 920 925
Lys Asn Phe Val Lys Pro Asn Glu Thr Lys Thr Tyr Phe Trp Lys Val
930 935 940
Gln His His Met Ala Pro Thr Lys Asp Glu Phe Asp Cys Lys Ala Trp
945 950 955 960
Ala Tyr Phe Ser Asp Val Asp Leu Glu Lys Asp Val His Ser Gly Leu
965 970 975
Ile Gly Pro Leu Leu Val Cys His Thr Asn Thr Leu Asn Pro Ala His
980 985 990
Gly Arg Gln Val Thr Val Gln Glu Phe Ala Leu Phe Phe Thr Ile Phe
995 1000 1005
Asp Glu Thr Lys Ser Trp Tyr Phe Thr Glu Asn Met Glu Arg Asn Cys
1010 1015 1020
Arg Ala Pro Cys Asn Ile Gln Met Glu Asp Pro Thr Phe Lys Glu Asn
1025 1030 1035 1040
Tyr Arg Phe His Ala Ile Asn Gly Tyr Ile Met Asp Thr Leu Pro Gly
1045 1050 1055
Leu Val Met Ala Gln Asp Gln Arg Ile Arg Trp Tyr Leu Leu Ser Met
1060 1065 1070
Gly Ser Asn Glu Asn Ile His Ser Ile His Phe Ser Gly His Val Phe
1075 1080 1085
Thr Val Arg Lys Lys Glu Glu Tyr Lys Met Ala Leu Tyr Asn Leu Tyr
1090 1095 1100
Pro Gly Val Phe Glu Thr Val Glu Met Leu Pro Ser Lys Ala Gly Ile
1105 1110 1115 1120
Trp Arg Val Glu Cys Leu Ile Gly Glu His Leu His Ala Gly Met Ser
1125 1130 1135
Thr Leu Phe Leu Val Tyr Ser Asn Lys Cys Gln Thr Pro Leu Gly Met
1140 1145 1150
Ala Ser Gly His Ile Arg Asp Phe Gln Ile Thr Ala Ser Gly Gln Tyr
1155 1160 1165
Gly Gln Trp Ala Pro Lys Leu Ala Arg Leu His Tyr Ser Gly Ser Ile
1170 1175 1180
Asn Ala Trp Ser Thr Lys Glu Pro Phe Ser Trp Ile Lys Val Asp Leu
1185 1190 1195 1200
Leu Ala Pro Met Ile Ile His Gly Ile Lys Thr Gln Gly Ala Arg Gln
1205 1210 1215
Lys Phe Ser Ser Leu Tyr Ile Ser Gln Phe Ile Ile Met Tyr Ser Leu
1220 1225 1230
Asp Gly Lys Lys Trp Gln Thr Tyr Arg Gly Asn Ser Thr Gly Thr Leu
1235 1240 1245
Met Val Phe Phe Gly Asn Val Asp Ser Ser Gly Ile Lys His Asn Ile
1250 1255 1260
Phe Asn Pro Pro Ile Ile Ala Arg Tyr Ile Arg Leu His Pro Thr His
1265 1270 1275 1280
Tyr Ser Ile Arg Ser Thr Leu Arg Met Glu Leu Met Gly Cys Asp Leu
1285 1290 1295
Asn Ser Cys Ser Met Pro Leu Gly Met Glu Ser Lys Ala Ile Ser Asp
1300 1305 1310
Ala Gln Ile Thr Ala Ser Ser Tyr Phe Thr Asn Met Phe Ala Thr Trp
1315 1320 1325
Ser Pro Ser Lys Ala Arg Leu His Leu Gln Gly Arg Ser Asn Ala Trp
1330 1335 1340
Arg Pro Gln Val Asn Asn Pro Lys Glu Trp Leu Gln Val Asp Phe Gln
1345 1350 1355 1360
Lys Thr Met Lys Val Thr Gly Val Thr Thr Gln Gly Val Lys Ser Leu
1365 1370 1375
Leu Thr Ser Met Tyr Val Lys Glu Phe Leu Ile Ser Ser Ser Gln Asp
1380 1385 1390
Gly His Gln Trp Thr Leu Phe Phe Gln Asn Gly Lys Val Lys Val Phe
1395 1400 1405
Gln Gly Asn Gln Asp Ser Phe Thr Pro Val Val Asn Ser Leu Asp Pro
1410 1415 1420
Pro Leu Leu Thr Arg Tyr Leu Arg Ile His Pro Gln Ser Trp Val His
1425 1430 1435 1440
Gln Ile Ala Leu Arg Met Glu Val Leu Gly Cys Glu Ala Gln Asp Leu
1445 1450 1455
Tyr
<210> 10
<211> 4374
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует белок FVIII-BDD с
сигнальным дикого типа (СП-FVIII-FVIII-BDD)
<400> 10
atgcaaatag agctctccac ctgcttcttt ctgtgccttt tgcgattctg ctttagtgcc 60
accagaagat actacctggg tgcagtggaa ctgtcatggg actatatgca aagtgatctc 120
ggtgagctgc ctgtggacgc aagatttcct cctagagtgc caaaatcttt tccattcaac 180
acctcagtcg tgtacaaaaa gactctgttt gtagaattca cggatcacct tttcaacatc 240
gctaagccaa ggccaccctg gatgggtctg ctaggtccta ccatccaggc tgaggtttat 300
gatacagtgg tcattacact taagaacatg gcttcccatc ctgtcagtct tcatgctgtt 360
ggtgtatcct actggaaagc ttctgaggga gctgaatatg atgatcagac cagtcaaagg 420
gagaaagaag atgataaagt cttccctggt ggaagccata catatgtctg gcaggtcctg 480
aaagagaatg gtccaatggc ctctgaccca ctgtgcctta cctactcata tctttctcat 540
gtggacctgg taaaagactt gaattcaggc ctcattggag ccctactagt atgtagagaa 600
gggagtctgg ccaaggaaaa gacacagacc ttgcacaaat ttatactact ttttgctgta 660
tttgatgaag ggaaaagttg gcactcagaa acaaagaact ccttgatgca ggatagggat 720
gctgcatctg ctcgggcctg gcctaaaatg cacacagtca atggttatgt aaacaggtct 780
ctgccaggtc tgattggatg ccacaggaaa tcagtctatt ggcatgtgat tggaatgggc 840
accactcctg aagtgcactc aatattcctc gaaggtcaca catttcttgt gaggaaccat 900
cgccaggcgt ccttggaaat ctcgccaata actttcctta ctgctcaaac actcttgatg 960
gaccttggac agtttctact gttttgtcat atctcttccc accaacatga tggcatggaa 1020
gcttatgtca aagtagacag ctgtccagag gaaccccaac tacgaatgaa aaataatgaa 1080
gaagcggaag actatgatga tgatcttact gattctgaaa tggatgtggt caggtttgat 1140
gatgacaact ctccttcctt tatccaaatt cgctcagttg ccaagaagca tcctaaaact 1200
tgggtacatt acattgctgc tgaagaggag gactgggact atgctccctt agtcctcgcc 1260
cccgatgaca gaagttataa aagtcaatat ttgaacaatg gccctcagcg gattggtagg 1320
aagtacaaaa aagtccgatt tatggcatac acagatgaaa cctttaagac tcgtgaagct 1380
attcagcatg aatcaggaat cttgggacct ttactttatg gggaagttgg agacacactg 1440
ttgattatat ttaagaatca agcaagcaga ccatataaca tctaccctca cggaatcact 1500
gatgtccgtc ctttgtattc aaggagatta ccaaaaggtg taaaacattt gaaggatttt 1560
ccaattctgc caggagaaat attcaaatat aaatggacag tgactgtaga agatgggcca 1620
actaaatcag atcctcggtg cctgacccgc tattactcta gtttcgttaa tatggagaga 1680
gatctagctt caggactcat tggccctctc ctcatctgct acaaagaatc tgtagatcaa 1740
agaggaaacc agataatgtc agacaagagg aatgtcatcc tgttttctgt atttgatgag 1800
aaccgaagct ggtacctcac agagaatata caacgctttc tccccaatcc agctggagtg 1860
cagcttgagg atccagagtt ccaagcctcc aacatcatgc acagcatcaa tggctatgtt 1920
tttgatagtt tgcagttgtc agtttgtttg catgaggtgg catactggta cattctaagc 1980
attggagcac agactgactt cctttctgtc ttcttctctg gatatacctt caaacacaaa 2040
atggtctatg aagacacact caccctattc ccattctcag gagaaactgt cttcatgtcg 2100
atggaaaacc caggtctatg gattctgggg tgccacaact cagactttcg gaacagaggc 2160
atgaccgcct tactgaaggt ttctagttgt gacaagaaca ctggtgatta ttacgaggac 2220
agttatgaag atatttcagc atacttgctg agtaaaaaca atgccattga accaagaagc 2280
ttctctcaaa acccaccagt cttgaaacgc catcaacggg aaataactcg tactactctt 2340
cagtcagatc aagaggaaat tgactatgat gataccatat cagttgaaat gaagaaggaa 2400
gattttgaca tttatgatga ggatgaaaat cagagccccc gcagctttca aaagaaaaca 2460
cgacactatt ttattgctgc agtggagagg ctctgggatt atgggatgag tagctcccca 2520
catgttctaa gaaacagggc tcagagtggc agtgtccctc agttcaagaa agttgttttc 2580
caggaattta ctgatggctc ctttactcag cccttatacc gtggagaact aaatgaacat 2640
ttgggactcc tggggccata tataagagca gaagttgaag ataatatcat ggtaactttc 2700
agaaatcagg cctctcgtcc ctattccttc tattctagcc ttatttctta tgaggaagat 2760
cagaggcaag gagcagaacc tagaaaaaac tttgtcaagc ctaatgaaac caaaacttac 2820
ttttggaaag tgcaacatca tatggcaccc actaaagatg agtttgactg caaagcctgg 2880
gcttatttct ctgatgttga cctggaaaaa gatgtgcact caggcctgat tggacccctt 2940
ctggtctgcc acactaacac actgaaccct gctcatggga gacaagtgac agtacaggaa 3000
tttgctctgt ttttcaccat ctttgatgag accaaaagct ggtacttcac tgaaaatatg 3060
gaaagaaact gcagggctcc ctgcaatatc cagatggaag atcccacttt taaagagaat 3120
tatcgcttcc atgcaatcaa tggctacata atggatacac tacctggctt agtaatggct 3180
caggatcaaa ggattcgatg gtatctgctc agcatgggca gcaatgaaaa catccattct 3240
attcatttca gtggacatgt gttcactgta cgaaaaaaag aggagtataa aatggcactg 3300
tacaatctct atccaggtgt ttttgagaca gtggaaatgt taccatccaa agctggaatt 3360
tggcgggtgg aatgccttat tggcgagcat ctacatgctg ggatgagcac actttttctg 3420
gtgtacagca ataagtgtca gactcccctg ggaatggctt ctggacacat tagagatttt 3480
cagattacag cttcaggaca atatggacag tgggccccaa agctggccag acttcattat 3540
tccggatcaa tcaatgcctg gagcaccaag gagccctttt cttggatcaa ggtggatctg 3600
ttggcaccaa tgattattca cggcatcaag acccagggtg cccgtcagaa gttctccagc 3660
ctctacatct ctcagtttat catcatgtat agtcttgatg ggaagaagtg gcagacttat 3720
cgaggaaatt ccactggaac cttaatggtc ttctttggca atgtggattc atctgggata 3780
aaacacaata tttttaaccc tccaattatt gctcgataca tccgtttgca cccaactcat 3840
tatagcattc gcagcactct tcgcatggag ttgatgggct gtgatttaaa tagttgcagc 3900
atgccattgg gaatggagag taaagcaata tcagatgcac agattactgc ttcatcctac 3960
tttaccaata tgtttgccac ctggtctcct tcaaaagctc gacttcacct ccaagggagg 4020
agtaatgcct ggagacctca ggtgaataat ccaaaagagt ggctgcaagt ggacttccag 4080
aagacaatga aagtcacagg agtaactact cagggagtaa aatctctgct taccagcatg 4140
tatgtgaagg agttcctcat ctccagcagt caagatggcc atcagtggac tctctttttt 4200
cagaatggca aagtaaaggt ttttcaggga aatcaagact ccttcacacc tgtggtgaac 4260
tctctagacc caccgttact gactcgctac cttcgaattc acccccagag ttgggtgcac 4320
cagattgccc tgaggatgga ggttctgggc tgcgaggcac aggacctcta ctga 4374
<210> 11
<211> 4401
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует слитый белок на основе
человеческого FVIII-BDD и сигнального пептида FIX
(СП-FIX-FVIII-BDD)
<400> 11
atgcagcgcg tgaacatgat catggcagaa tcaccaggcc tcatcaccat ctgcctttta 60
ggatatctac tcagtgctga atgtgccacc agaagatact acctgggtgc agtggaactg 120
tcatgggact atatgcaaag tgatctcggt gagctgcctg tggacgcaag atttcctcct 180
agagtgccaa aatcttttcc attcaacacc tcagtcgtgt acaaaaagac tctgtttgta 240
gaattcacgg atcacctttt caacatcgct aagccaaggc caccctggat gggtctgcta 300
ggtcctacca tccaggctga ggtttatgat acagtggtca ttacacttaa gaacatggct 360
tcccatcctg tcagtcttca tgctgttggt gtatcctact ggaaagcttc tgagggagct 420
gaatatgatg atcagaccag tcaaagggag aaagaagatg ataaagtctt ccctggtgga 480
agccatacat atgtctggca ggtcctgaaa gagaatggtc caatggcctc tgacccactg 540
tgccttacct actcatatct ttctcatgtg gacctggtaa aagacttgaa ttcaggcctc 600
attggagccc tactagtatg tagagaaggg agtctggcca aggaaaagac acagaccttg 660
cacaaattta tactactttt tgctgtattt gatgaaggga aaagttggca ctcagaaaca 720
aagaactcct tgatgcagga tagggatgct gcatctgctc gggcctggcc taaaatgcac 780
acagtcaatg gttatgtaaa caggtctctg ccaggtctga ttggatgcca caggaaatca 840
gtctattggc atgtgattgg aatgggcacc actcctgaag tgcactcaat attcctcgaa 900
ggtcacacat ttcttgtgag gaaccatcgc caggcgtcct tggaaatctc gccaataact 960
ttccttactg ctcaaacact cttgatggac cttggacagt ttctactgtt ttgtcatatc 1020
tcttcccacc aacatgatgg catggaagct tatgtcaaag tagacagctg tccagaggaa 1080
ccccaactac gaatgaaaaa taatgaagaa gcggaagact atgatgatga tcttactgat 1140
tctgaaatgg atgtggtcag gtttgatgat gacaactctc cttcctttat ccaaattcgc 1200
tcagttgcca agaagcatcc taaaacttgg gtacattaca ttgctgctga agaggaggac 1260
tgggactatg ctcccttagt cctcgccccc gatgacagaa gttataaaag tcaatatttg 1320
aacaatggcc ctcagcggat tggtaggaag tacaaaaaag tccgatttat ggcatacaca 1380
gatgaaacct ttaagactcg tgaagctatt cagcatgaat caggaatctt gggaccttta 1440
ctttatgggg aagttggaga cacactgttg attatattta agaatcaagc aagcagacca 1500
tataacatct accctcacgg aatcactgat gtccgtcctt tgtattcaag gagattacca 1560
aaaggtgtaa aacatttgaa ggattttcca attctgccag gagaaatatt caaatataaa 1620
tggacagtga ctgtagaaga tgggccaact aaatcagatc ctcggtgcct gacccgctat 1680
tactctagtt tcgttaatat ggagagagat ctagcttcag gactcattgg ccctctcctc 1740
atctgctaca aagaatctgt agatcaaaga ggaaaccaga taatgtcaga caagaggaat 1800
gtcatcctgt tttctgtatt tgatgagaac cgaagctggt acctcacaga gaatatacaa 1860
cgctttctcc ccaatccagc tggagtgcag cttgaggatc cagagttcca agcctccaac 1920
atcatgcaca gcatcaatgg ctatgttttt gatagtttgc agttgtcagt ttgtttgcat 1980
gaggtggcat actggtacat tctaagcatt ggagcacaga ctgacttcct ttctgtcttc 2040
ttctctggat ataccttcaa acacaaaatg gtctatgaag acacactcac cctattccca 2100
ttctcaggag aaactgtctt catgtcgatg gaaaacccag gtctatggat tctggggtgc 2160
cacaactcag actttcggaa cagaggcatg accgccttac tgaaggtttc tagttgtgac 2220
aagaacactg gtgattatta cgaggacagt tatgaagata tttcagcata cttgctgagt 2280
aaaaacaatg ccattgaacc aagaagcttc tctcaaaacc caccagtctt gaaacgccat 2340
caacgggaaa taactcgtac tactcttcag tcagatcaag aggaaattga ctatgatgat 2400
accatatcag ttgaaatgaa gaaggaagat tttgacattt atgatgagga tgaaaatcag 2460
agcccccgca gctttcaaaa gaaaacacga cactatttta ttgctgcagt ggagaggctc 2520
tgggattatg ggatgagtag ctccccacat gttctaagaa acagggctca gagtggcagt 2580
gtccctcagt tcaagaaagt tgttttccag gaatttactg atggctcctt tactcagccc 2640
ttataccgtg gagaactaaa tgaacatttg ggactcctgg ggccatatat aagagcagaa 2700
gttgaagata atatcatggt aactttcaga aatcaggcct ctcgtcccta ttccttctat 2760
tctagcctta tttcttatga ggaagatcag aggcaaggag cagaacctag aaaaaacttt 2820
gtcaagccta atgaaaccaa aacttacttt tggaaagtgc aacatcatat ggcacccact 2880
aaagatgagt ttgactgcaa agcctgggct tatttctctg atgttgacct ggaaaaagat 2940
gtgcactcag gcctgattgg accccttctg gtctgccaca ctaacacact gaaccctgct 3000
catgggagac aagtgacagt acaggaattt gctctgtttt tcaccatctt tgatgagacc 3060
aaaagctggt acttcactga aaatatggaa agaaactgca gggctccctg caatatccag 3120
atggaagatc ccacttttaa agagaattat cgcttccatg caatcaatgg ctacataatg 3180
gatacactac ctggcttagt aatggctcag gatcaaagga ttcgatggta tctgctcagc 3240
atgggcagca atgaaaacat ccattctatt catttcagtg gacatgtgtt cactgtacga 3300
aaaaaagagg agtataaaat ggcactgtac aatctctatc caggtgtttt tgagacagtg 3360
gaaatgttac catccaaagc tggaatttgg cgggtggaat gccttattgg cgagcatcta 3420
catgctggga tgagcacact ttttctggtg tacagcaata agtgtcagac tcccctggga 3480
atggcttctg gacacattag agattttcag attacagctt caggacaata tggacagtgg 3540
gccccaaagc tggccagact tcattattcc ggatcaatca atgcctggag caccaaggag 3600
cccttttctt ggatcaaggt ggatctgttg gcaccaatga ttattcacgg catcaagacc 3660
cagggtgccc gtcagaagtt ctccagcctc tacatctctc agtttatcat catgtatagt 3720
cttgatggga agaagtggca gacttatcga ggaaattcca ctggaacctt aatggtcttc 3780
tttggcaatg tggattcatc tgggataaaa cacaatattt ttaaccctcc aattattgct 3840
cgatacatcc gtttgcaccc aactcattat agcattcgca gcactcttcg catggagttg 3900
atgggctgtg atttaaatag ttgcagcatg ccattgggaa tggagagtaa agcaatatca 3960
gatgcacaga ttactgcttc atcctacttt accaatatgt ttgccacctg gtctccttca 4020
aaagctcgac ttcacctcca agggaggagt aatgcctgga gacctcaggt gaataatcca 4080
aaagagtggc tgcaagtgga cttccagaag acaatgaaag tcacaggagt aactactcag 4140
ggagtaaaat ctctgcttac cagcatgtat gtgaaggagt tcctcatctc cagcagtcaa 4200
gatggccatc agtggactct cttttttcag aatggcaaag taaaggtttt tcagggaaat 4260
caagactcct tcacacctgt ggtgaactct ctagacccac cgttactgac tcgctacctt 4320
cgaattcacc cccagagttg ggtgcaccag attgccctga ggatggaggt tctgggctgc 4380
gaggcacagg acctctactg a 4401
<210> 12
<211> 4377
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая кодирует слитый белок на основе
человеческого FVIII-BDD и сигнального пептида Kappa цепь
иммуноглобулина G (СП-IgGK-FVIII-BDD)
<400> 12
atggagaccg acaccctgct gctgtgggtg ctgctgctgt gggtgcccgg gtcgaccggt 60
gccaccagaa gatactacct gggtgcagtg gaactgtcat gggactatat gcaaagtgat 120
ctcggtgagc tgcctgtgga cgcaagattt cctcctagag tgccaaaatc ttttccattc 180
aacacctcag tcgtgtacaa aaagactctg tttgtagaat tcacggatca ccttttcaac 240
atcgctaagc caaggccacc ctggatgggt ctgctaggtc ctaccatcca ggctgaggtt 300
tatgatacag tggtcattac acttaagaac atggcttccc atcctgtcag tcttcatgct 360
gttggtgtat cctactggaa agcttctgag ggagctgaat atgatgatca gaccagtcaa 420
agggagaaag aagatgataa agtcttccct ggtggaagcc atacatatgt ctggcaggtc 480
ctgaaagaga atggtccaat ggcctctgac ccactgtgcc ttacctactc atatctttct 540
catgtggacc tggtaaaaga cttgaattca ggcctcattg gagccctact agtatgtaga 600
gaagggagtc tggccaagga aaagacacag accttgcaca aatttatact actttttgct 660
gtatttgatg aagggaaaag ttggcactca gaaacaaaga actccttgat gcaggatagg 720
gatgctgcat ctgctcgggc ctggcctaaa atgcacacag tcaatggtta tgtaaacagg 780
tctctgccag gtctgattgg atgccacagg aaatcagtct attggcatgt gattggaatg 840
ggcaccactc ctgaagtgca ctcaatattc ctcgaaggtc acacatttct tgtgaggaac 900
catcgccagg cgtccttgga aatctcgcca ataactttcc ttactgctca aacactcttg 960
atggaccttg gacagtttct actgttttgt catatctctt cccaccaaca tgatggcatg 1020
gaagcttatg tcaaagtaga cagctgtcca gaggaacccc aactacgaat gaaaaataat 1080
gaagaagcgg aagactatga tgatgatctt actgattctg aaatggatgt ggtcaggttt 1140
gatgatgaca actctccttc ctttatccaa attcgctcag ttgccaagaa gcatcctaaa 1200
acttgggtac attacattgc tgctgaagag gaggactggg actatgctcc cttagtcctc 1260
gcccccgatg acagaagtta taaaagtcaa tatttgaaca atggccctca gcggattggt 1320
aggaagtaca aaaaagtccg atttatggca tacacagatg aaacctttaa gactcgtgaa 1380
gctattcagc atgaatcagg aatcttggga cctttacttt atggggaagt tggagacaca 1440
ctgttgatta tatttaagaa tcaagcaagc agaccatata acatctaccc tcacggaatc 1500
actgatgtcc gtcctttgta ttcaaggaga ttaccaaaag gtgtaaaaca tttgaaggat 1560
tttccaattc tgccaggaga aatattcaaa tataaatgga cagtgactgt agaagatggg 1620
ccaactaaat cagatcctcg gtgcctgacc cgctattact ctagtttcgt taatatggag 1680
agagatctag cttcaggact cattggccct ctcctcatct gctacaaaga atctgtagat 1740
caaagaggaa accagataat gtcagacaag aggaatgtca tcctgttttc tgtatttgat 1800
gagaaccgaa gctggtacct cacagagaat atacaacgct ttctccccaa tccagctgga 1860
gtgcagcttg aggatccaga gttccaagcc tccaacatca tgcacagcat caatggctat 1920
gtttttgata gtttgcagtt gtcagtttgt ttgcatgagg tggcatactg gtacattcta 1980
agcattggag cacagactga cttcctttct gtcttcttct ctggatatac cttcaaacac 2040
aaaatggtct atgaagacac actcacccta ttcccattct caggagaaac tgtcttcatg 2100
tcgatggaaa acccaggtct atggattctg gggtgccaca actcagactt tcggaacaga 2160
ggcatgaccg ccttactgaa ggtttctagt tgtgacaaga acactggtga ttattacgag 2220
gacagttatg aagatatttc agcatacttg ctgagtaaaa acaatgccat tgaaccaaga 2280
agcttctctc aaaacccacc agtcttgaaa cgccatcaac gggaaataac tcgtactact 2340
cttcagtcag atcaagagga aattgactat gatgatacca tatcagttga aatgaagaag 2400
gaagattttg acatttatga tgaggatgaa aatcagagcc cccgcagctt tcaaaagaaa 2460
acacgacact attttattgc tgcagtggag aggctctggg attatgggat gagtagctcc 2520
ccacatgttc taagaaacag ggctcagagt ggcagtgtcc ctcagttcaa gaaagttgtt 2580
ttccaggaat ttactgatgg ctcctttact cagcccttat accgtggaga actaaatgaa 2640
catttgggac tcctggggcc atatataaga gcagaagttg aagataatat catggtaact 2700
ttcagaaatc aggcctctcg tccctattcc ttctattcta gccttatttc ttatgaggaa 2760
gatcagaggc aaggagcaga acctagaaaa aactttgtca agcctaatga aaccaaaact 2820
tacttttgga aagtgcaaca tcatatggca cccactaaag atgagtttga ctgcaaagcc 2880
tgggcttatt tctctgatgt tgacctggaa aaagatgtgc actcaggcct gattggaccc 2940
cttctggtct gccacactaa cacactgaac cctgctcatg ggagacaagt gacagtacag 3000
gaatttgctc tgtttttcac catctttgat gagaccaaaa gctggtactt cactgaaaat 3060
atggaaagaa actgcagggc tccctgcaat atccagatgg aagatcccac ttttaaagag 3120
aattatcgct tccatgcaat caatggctac ataatggata cactacctgg cttagtaatg 3180
gctcaggatc aaaggattcg atggtatctg ctcagcatgg gcagcaatga aaacatccat 3240
tctattcatt tcagtggaca tgtgttcact gtacgaaaaa aagaggagta taaaatggca 3300
ctgtacaatc tctatccagg tgtttttgag acagtggaaa tgttaccatc caaagctgga 3360
atttggcggg tggaatgcct tattggcgag catctacatg ctgggatgag cacacttttt 3420
ctggtgtaca gcaataagtg tcagactccc ctgggaatgg cttctggaca cattagagat 3480
tttcagatta cagcttcagg acaatatgga cagtgggccc caaagctggc cagacttcat 3540
tattccggat caatcaatgc ctggagcacc aaggagccct tttcttggat caaggtggat 3600
ctgttggcac caatgattat tcacggcatc aagacccagg gtgcccgtca gaagttctcc 3660
agcctctaca tctctcagtt tatcatcatg tatagtcttg atgggaagaa gtggcagact 3720
tatcgaggaa attccactgg aaccttaatg gtcttctttg gcaatgtgga ttcatctggg 3780
ataaaacaca atatttttaa ccctccaatt attgctcgat acatccgttt gcacccaact 3840
cattatagca ttcgcagcac tcttcgcatg gagttgatgg gctgtgattt aaatagttgc 3900
agcatgccat tgggaatgga gagtaaagca atatcagatg cacagattac tgcttcatcc 3960
tactttacca atatgtttgc cacctggtct ccttcaaaag ctcgacttca cctccaaggg 4020
aggagtaatg cctggagacc tcaggtgaat aatccaaaag agtggctgca agtggacttc 4080
cagaagacaa tgaaagtcac aggagtaact actcagggag taaaatctct gcttaccagc 4140
atgtatgtga aggagttcct catctccagc agtcaagatg gccatcagtg gactctcttt 4200
tttcagaatg gcaaagtaaa ggtttttcag ggaaatcaag actccttcac acctgtggtg 4260
aactctctag acccaccgtt actgactcgc taccttcgaa ttcaccccca gagttgggtg 4320
caccagattg ccctgaggat ggaggttctg ggctgcgagg cacaggacct ctactga 4377
<210> 13
<211> 4374
<212> DNA
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, которая слитый белок на основе человеческого
FVIII-BDD и сигнального пептида Lactalbumin
(СП-Lactalbumin-¬FVIII-BDD)
<400> 13
atgatgtcct ttgtctctct gctcctggtt ggcatcctgt tccatgccac ccaggccgcc 60
accagaagat actacctggg tgcagtggaa ctgtcatggg actatatgca aagtgatctc 120
ggtgagctgc ctgtggacgc aagatttcct cctagagtgc caaaatcttt tccattcaac 180
acctcagtcg tgtacaaaaa gactctgttt gtagaattca cggatcacct tttcaacatc 240
gctaagccaa ggccaccctg gatgggtctg ctaggtccta ccatccaggc tgaggtttat 300
gatacagtgg tcattacact taagaacatg gcttcccatc ctgtcagtct tcatgctgtt 360
ggtgtatcct actggaaagc ttctgaggga gctgaatatg atgatcagac cagtcaaagg 420
gagaaagaag atgataaagt cttccctggt ggaagccata catatgtctg gcaggtcctg 480
aaagagaatg gtccaatggc ctctgaccca ctgtgcctta cctactcata tctttctcat 540
gtggacctgg taaaagactt gaattcaggc ctcattggag ccctactagt atgtagagaa 600
gggagtctgg ccaaggaaaa gacacagacc ttgcacaaat ttatactact ttttgctgta 660
tttgatgaag ggaaaagttg gcactcagaa acaaagaact ccttgatgca ggatagggat 720
gctgcatctg ctcgggcctg gcctaaaatg cacacagtca atggttatgt aaacaggtct 780
ctgccaggtc tgattggatg ccacaggaaa tcagtctatt ggcatgtgat tggaatgggc 840
accactcctg aagtgcactc aatattcctc gaaggtcaca catttcttgt gaggaaccat 900
cgccaggcgt ccttggaaat ctcgccaata actttcctta ctgctcaaac actcttgatg 960
gaccttggac agtttctact gttttgtcat atctcttccc accaacatga tggcatggaa 1020
gcttatgtca aagtagacag ctgtccagag gaaccccaac tacgaatgaa aaataatgaa 1080
gaagcggaag actatgatga tgatcttact gattctgaaa tggatgtggt caggtttgat 1140
gatgacaact ctccttcctt tatccaaatt cgctcagttg ccaagaagca tcctaaaact 1200
tgggtacatt acattgctgc tgaagaggag gactgggact atgctccctt agtcctcgcc 1260
cccgatgaca gaagttataa aagtcaatat ttgaacaatg gccctcagcg gattggtagg 1320
aagtacaaaa aagtccgatt tatggcatac acagatgaaa cctttaagac tcgtgaagct 1380
attcagcatg aatcaggaat cttgggacct ttactttatg gggaagttgg agacacactg 1440
ttgattatat ttaagaatca agcaagcaga ccatataaca tctaccctca cggaatcact 1500
gatgtccgtc ctttgtattc aaggagatta ccaaaaggtg taaaacattt gaaggatttt 1560
ccaattctgc caggagaaat attcaaatat aaatggacag tgactgtaga agatgggcca 1620
actaaatcag atcctcggtg cctgacccgc tattactcta gtttcgttaa tatggagaga 1680
gatctagctt caggactcat tggccctctc ctcatctgct acaaagaatc tgtagatcaa 1740
agaggaaacc agataatgtc agacaagagg aatgtcatcc tgttttctgt atttgatgag 1800
aaccgaagct ggtacctcac agagaatata caacgctttc tccccaatcc agctggagtg 1860
cagcttgagg atccagagtt ccaagcctcc aacatcatgc acagcatcaa tggctatgtt 1920
tttgatagtt tgcagttgtc agtttgtttg catgaggtgg catactggta cattctaagc 1980
attggagcac agactgactt cctttctgtc ttcttctctg gatatacctt caaacacaaa 2040
atggtctatg aagacacact caccctattc ccattctcag gagaaactgt cttcatgtcg 2100
atggaaaacc caggtctatg gattctgggg tgccacaact cagactttcg gaacagaggc 2160
atgaccgcct tactgaaggt ttctagttgt gacaagaaca ctggtgatta ttacgaggac 2220
agttatgaag atatttcagc atacttgctg agtaaaaaca atgccattga accaagaagc 2280
ttctctcaaa acccaccagt cttgaaacgc catcaacggg aaataactcg tactactctt 2340
cagtcagatc aagaggaaat tgactatgat gataccatat cagttgaaat gaagaaggaa 2400
gattttgaca tttatgatga ggatgaaaat cagagccccc gcagctttca aaagaaaaca 2460
cgacactatt ttattgctgc agtggagagg ctctgggatt atgggatgag tagctcccca 2520
catgttctaa gaaacagggc tcagagtggc agtgtccctc agttcaagaa agttgttttc 2580
caggaattta ctgatggctc ctttactcag cccttatacc gtggagaact aaatgaacat 2640
ttgggactcc tggggccata tataagagca gaagttgaag ataatatcat ggtaactttc 2700
agaaatcagg cctctcgtcc ctattccttc tattctagcc ttatttctta tgaggaagat 2760
cagaggcaag gagcagaacc tagaaaaaac tttgtcaagc ctaatgaaac caaaacttac 2820
ttttggaaag tgcaacatca tatggcaccc actaaagatg agtttgactg caaagcctgg 2880
gcttatttct ctgatgttga cctggaaaaa gatgtgcact caggcctgat tggacccctt 2940
ctggtctgcc acactaacac actgaaccct gctcatggga gacaagtgac agtacaggaa 3000
tttgctctgt ttttcaccat ctttgatgag accaaaagct ggtacttcac tgaaaatatg 3060
gaaagaaact gcagggctcc ctgcaatatc cagatggaag atcccacttt taaagagaat 3120
tatcgcttcc atgcaatcaa tggctacata atggatacac tacctggctt agtaatggct 3180
caggatcaaa ggattcgatg gtatctgctc agcatgggca gcaatgaaaa catccattct 3240
attcatttca gtggacatgt gttcactgta cgaaaaaaag aggagtataa aatggcactg 3300
tacaatctct atccaggtgt ttttgagaca gtggaaatgt taccatccaa agctggaatt 3360
tggcgggtgg aatgccttat tggcgagcat ctacatgctg ggatgagcac actttttctg 3420
gtgtacagca ataagtgtca gactcccctg ggaatggctt ctggacacat tagagatttt 3480
cagattacag cttcaggaca atatggacag tgggccccaa agctggccag acttcattat 3540
tccggatcaa tcaatgcctg gagcaccaag gagccctttt cttggatcaa ggtggatctg 3600
ttggcaccaa tgattattca cggcatcaag acccagggtg cccgtcagaa gttctccagc 3660
ctctacatct ctcagtttat catcatgtat agtcttgatg ggaagaagtg gcagacttat 3720
cgaggaaatt ccactggaac cttaatggtc ttctttggca atgtggattc atctgggata 3780
aaacacaata tttttaaccc tccaattatt gctcgataca tccgtttgca cccaactcat 3840
tatagcattc gcagcactct tcgcatggag ttgatgggct gtgatttaaa tagttgcagc 3900
atgccattgg gaatggagag taaagcaata tcagatgcac agattactgc ttcatcctac 3960
tttaccaata tgtttgccac ctggtctcct tcaaaagctc gacttcacct ccaagggagg 4020
agtaatgcct ggagacctca ggtgaataat ccaaaagagt ggctgcaagt ggacttccag 4080
aagacaatga aagtcacagg agtaactact cagggagtaa aatctctgct taccagcatg 4140
tatgtgaagg agttcctcat ctccagcagt caagatggcc atcagtggac tctctttttt 4200
cagaatggca aagtaaaggt ttttcaggga aatcaagact ccttcacacc tgtggtgaac 4260
tctctagacc caccgttact gactcgctac cttcgaattc acccccagag ttgggtgcac 4320
cagattgccc tgaggatgga ggttctgggc tgcgaggcac aggacctcta ctga 4374
<210> 14
<211> 130
<212> DNA
<213> Природная последовательность
<220>
<223> Левый (первый) ITR (инвертированные концевые повторы)
<400> 14
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact 120
aggggttcct 130
<210> 15
<211> 252
<212> DNA
<213> Искусственная последовательность
<220>
<223> Промотор HLP
<400> 15
tgtttgctgc ttgcaatgtt tgcccatttt agggtggaca caggacgctg tggtttctga 60
gccagggggc gactcagatc ccagccagtg gacttagccc ctgtttgctc ctccgataac 120
tggggtgacc ttggttaata ttcaccagca gcctcccccg ttgcccctct ggatccactg 180
cttaaatacg gacgaggaca gggccctgtc tcctcagctt caggcaccac cactgacctg 240
ggacagtgaa tc 252
<210> 16
<211> 60
<212> DNA
<213> Искусственная последовательность
<220>
<223> Сигнал полиаденилирования
<400> 16
cgcgaataaa agatctttat tttcattaga tctgtgtgtt ggttttttgt gtgatgcagc 60
<210> 17
<211> 141
<212> DNA
<213> Природная последовательность
<220>
<223> Правый ITR
<400> 17
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcggcctca gtgagcgagc 120
gagcgcgcag ctgcctgcag g 141
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Кодон-оптимизированная нуклеиновая кислота, которая кодирует белок фактора свёртывания крови VIII c делетированным B доменом, и ее применение | 2022 |
|
RU2808564C2 |
| МОЛЕКУЛЫ НУКЛЕИНОВОЙ КИСЛОТЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2819144C2 |
| ГЕННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕМОФИЛИИ A | 2017 |
|
RU2762257C2 |
| МОЛЕКУЛЫ НУКЛЕИНОВОЙ КИСЛОТЫ И ПУТИ ИХ ПРИМЕНЕНИЯ ДЛЯ НЕВИРУСНОЙ ГЕННОЙ ТЕРАПИИ | 2019 |
|
RU2834625C2 |
| СПОСОБЫ ГЕНОТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ГЕНА ФАКТОРА VIII (FVIII) | 2018 |
|
RU2808274C2 |
| АНТИТЕЛО, КОТОРОЕ ОБЛАДАЕТ СПОСОБНОСТЬЮ НЕЙТРАЛИЗОВАТЬ СУБСТАНЦИЮ, ОБЛАДАЮЩУЮ АКТИВНОСТЬЮ, АЛЬТЕРНАТИВНОЙ ФУНКЦИИ ФАКТОРА СВЕРТЫВАНИЯ VIII (FVIII) | 2015 |
|
RU2737145C2 |
| КОДИРУЮЩИЕ ФАКТОР VIII ВАРИАНТЫ С ПОНИЖЕННЫМ СОДЕРЖАНИЕМ CPG, КОМПОЗИЦИИ И СПОСОБЫ И ПРИМЕНЕНИЕ В ЛЕЧЕНИИ НАРУШЕНИЙ ГЕМОСТАЗА | 2016 |
|
RU2745506C2 |
| ПРИМЕНЕНИЕ ЛЕНТИВИРУСНЫХ ВЕКТОРОВ, ЭКСПРЕССИРУЮЩИХ ФАКТОР VIII | 2019 |
|
RU2803163C2 |
| ГЛИКОЗИЛИРОВАННЫЕ СЛИТЫЕ БЕЛКИ VWF С УЛУЧШЕННОЙ ФАРМАКОКИНЕТИКОЙ | 2017 |
|
RU2782212C2 |
| ПОЛИПЕПТИДЫ, МОДУЛИРУЮЩИЕ SIGLEC-ЗАВИСИМЫЕ ИММУННЫЕ ОТВЕТЫ | 2017 |
|
RU2776807C2 |
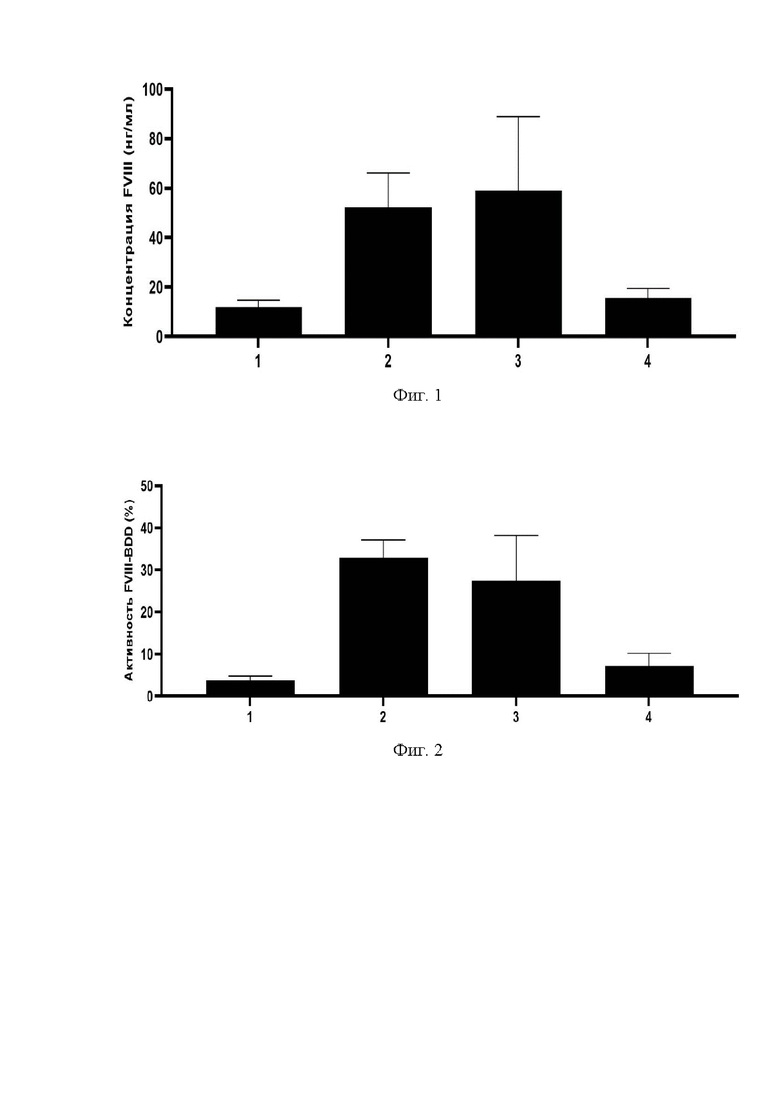
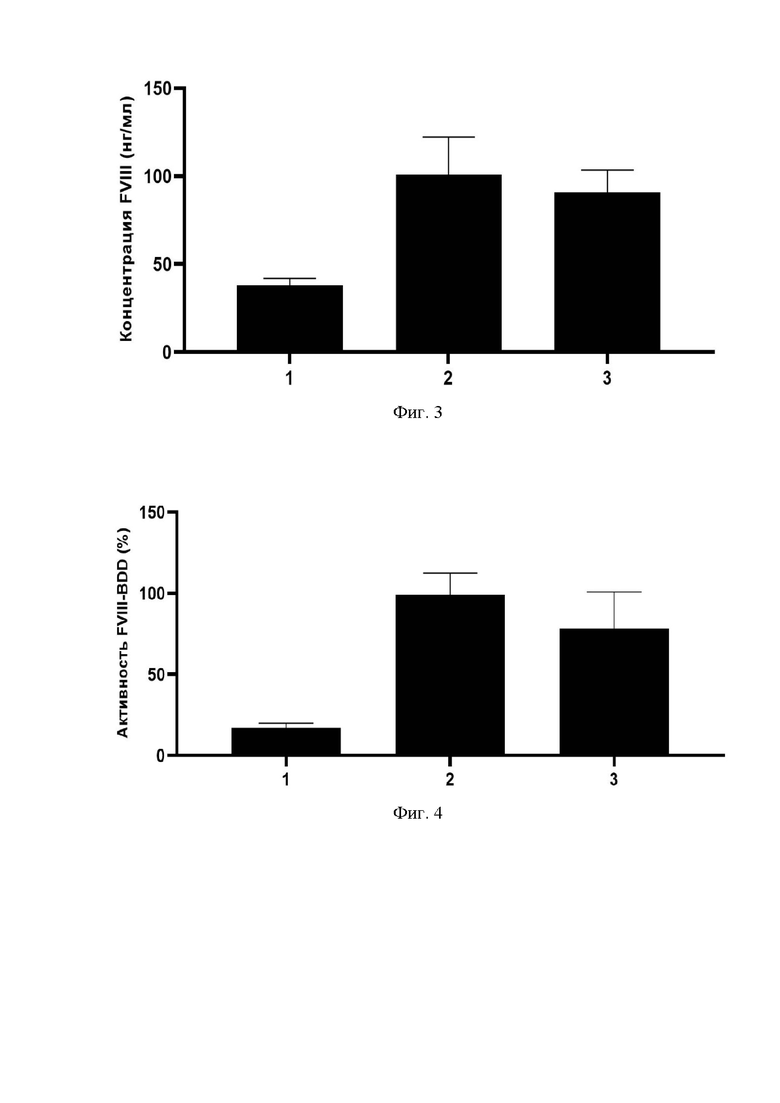
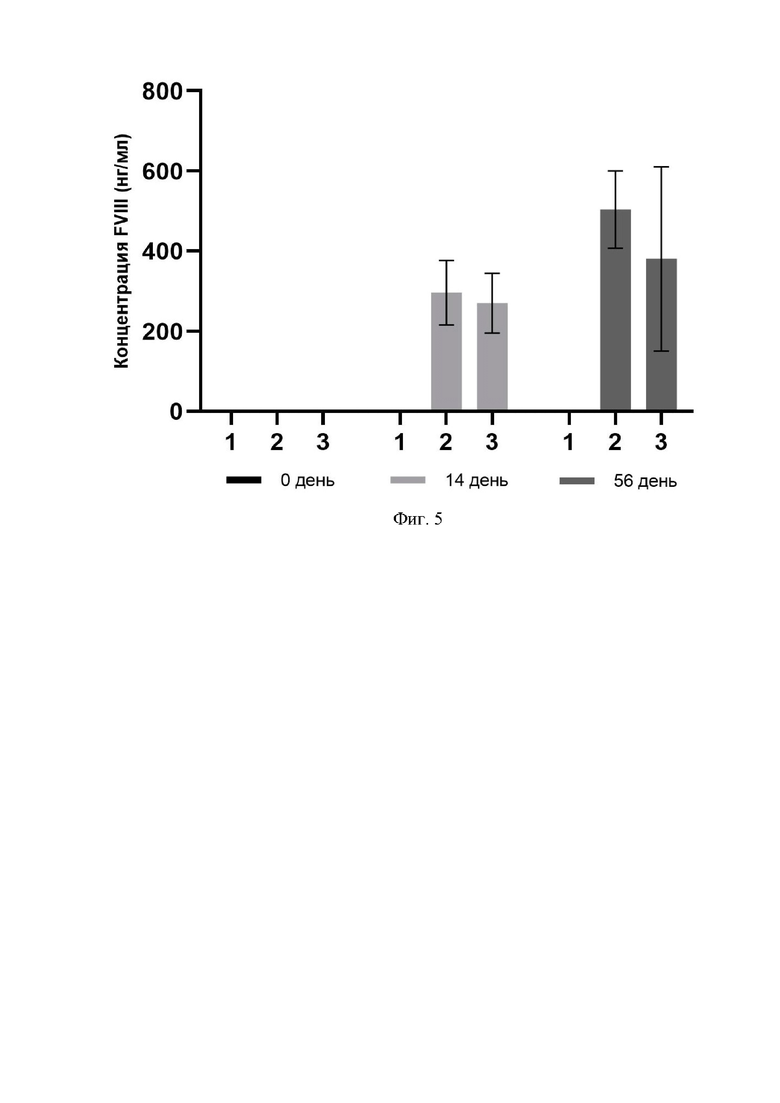
Изобретение относится к области биотехнологии, в частности к выделенной нуклеиновой кислоте, кодирующей слитый белок на основе FVIII-BDD (фактор свёртывания крови VIII c делетированным B доменом) и гетерологичного сигнального пептида, а также предлагается экспрессионная кассета, вектор и клетка, ее содержащие. Также раскрыта фармацевтическая композиция, содержащая вышеуказанный вектор или кассету. Изобретение эффективно для обеспечения белком FVIII-BDD субъекта с гемофилией А, а также для лечения гемофилии А у субъекта. 11 н. и 7 з.п. ф-лы, 5 ил., 3 пр.
1. Выделенная нуклеиновая кислота, которая кодирует слитый белок на основе FVIII-BDD (фактор свёртывания крови VIII c делетированным B доменом) и гетерологичного сигнального пептида, который включает аминокислотную последовательность, выбранную из SEQ ID NO: 7 или SEQ ID NO: 9.
2. Выделенная нуклеиновая кислота по п. 1, где слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида имеет аминокислотную последовательность SEQ ID NO: 7.
3. Выделенная нуклеиновая кислота по п. 1, где слитый белок на основе FVIII-BDD и гетерологичного сигнального пептида имеет аминокислотную последовательность SEQ ID NO: 9.
4. Выделенная нуклеиновая кислота по п. 2, которая представляет собой нуклеотидную последовательность SEQ ID NO: 11.
5. Выделенная нуклеиновая кислота по п. 3, которая представляет собой нуклеотидную последовательность SEQ ID NO: 13.
6. Экспрессионная кассета, которая включает нуклеиновую кислоту по любому из пп. 1-5.
7. Экспрессионная кассета по п. 6, включающая следующие элементы в направлении от 5'-конца к 3'-концу:
левый (первый) ITR (инвертированные концевые повторы);
промотор;
нуклеиновую кислоту по любому из пп. 1-5;
сигнал полиаденилирования;
правый (второй) ITR.
8. Экспрессионный вектор, который включает нуклеиновую кислоту по любому из пп. 1-5 или экспрессионную кассету по любому из пп. 6, 7.
9. Экспрессионный вектор по п. 8, где экспрессионный вектор представляет собой рекомбинантный аденоассоциированный вирус (AAV).
10. Экспрессионный вектор по п. 9, где AAV выбирают из группы, включающей следующие серотипы AAV: AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10 AAV11, AAV12, AAV13, AAV14, AAV15, AAV16, rAAV.rh8, rAAV.rhlO, rAAV.rh20, rAAV.rh39, rAAV.Rh74, rAAV.RHM4-l, AAV.hu37, rAAV.Anc80, rAAV.Anc80L65, rAAV.7m8, rAAV.PHP.B, rAAV2.5, rAAV2tYF, rAAV3B, rAAV.LK03, AAV.HSC1, AAV.HSC2, AAV.HSC3, AAV.HSC4, AAV.HSC5, AAV.HSC6, AAV.HSC7, AAV.HSC8, AAV.HSC9, AAV.HSC10, AAV.HSC11, AAV.HSC12, AAV.HSC13, AAV.HSC14, AAV.HSC15 или AAV.HSC16.
11. Клетка-хозяин для получения слитого белка на основе FVIII-BDD и гетерологичного сигнального пептида, содержащая нуклеиновую кислоту по любому из пп. 1-5.
12. Фармацевтическая композиция для доставки гена FVIII-BDD в целевые клетки, включающая экспрессионный вектор или кассету по любому из пп. 8-10 в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами.
13. Применение экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 для доставки гена FVIII-BDD в целевые клетки.
14. Применение экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 для обеспечения белком FVIII-BDD субъекта, который имеет гемофилию А и/или не имеет функциональных копий гена FVIII.
15. Способ обеспечения белком FVIII-BDD субъекта с гемофилией А, включающий введение терапевтически эффективного количества экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 в клетки субъекта, нуждающегося в этом.
16. Способ доставки гена FVIII-BDD в целевые клетки субъекта с гемофилией А, включающий введение экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 в клетки субъекта.
17. Применение экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 для лечения гемофилии А у субъекта, который имеет гемофилию А.
18. Способ лечения гемофилии А у субъекта, который включает введение терапевтически эффективного количества экспрессионного вектора по любому из пп. 8-10 или композиции по п. 12 субъекту, который имеет гемофилию А.
| WO 2021084276 A2, 06.05.2021 | |||
| WO 2021045541 A1, 11.03.2021 | |||
| WO 2017136358 A1, 10.08.2017 | |||
| JOSHUA I | |||
| SINER et al., Minimal modification in the factor VIII B-domain sequence ameliorates the murine hemophilia A phenotype, Blood, 2013, 121 (21), pp | |||
| ТЕПЛОВОЗ С НЕПОСРЕДСТВЕННОЙ ПЕРЕДАЧЕЙ ДВИЖЕНИЯ ОТ ДВИГАТЕЛЯ К ХОДОВЫМ ОСЯМ | 1925 |
|
SU4396A1 |
| Химерный улучшенный рекомбинантный фактор VIII | 2015 |
|
RU2647769C2 |
Авторы
Даты
2024-04-26—Публикация
2022-04-28—Подача