РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет по заявке EP № 18306840.2, поданной 24 декабря 2018 года, и заявке EP № 19305813.8, поданной 21 июня 2019 года, содержание которых включено в данный документ посредством ссылки для всех целей.
УРОВЕНЬ ТЕХНИКИ
[0001] Создание асимметрии в нативной структуре антитела является необходимым условием для создания мультиспецифических связывающих белков, имеющих две (например, биспецифические антитела) или более специфичностей связывания. Например, за счет разделения одной или более Fv путем размещения на разных асимметричных связывающих плечах или Fab можно получать биспецифическое антитело с возможностью связывания двух разных антигенов или эпитопов одновременно. Однако, несмотря на эти преимущества, самые разнообразные технологии получения мультиспецифических антител сталкиваются с технологическими и производственными проблемами вследствие неправильного спаривания различных асимметричных тяжелых и легких цепей. Например, многие из этих технологий сталкиваются с так называемой "проблемой легких цепей", при которой случайное спаривание двух различных легких цепей с тяжелыми цепями создает различные комбинации пар цепей, отличные от требуемой комбинации. В некоторых случаях "проблему легких цепей" можно обойти путем применения общей легкой цепи, которая позволяет связываться с обоими антигенами или эпитопами. Однако данный способ может быть невозможным в случае многих антител, поскольку данный формат требует образования антител de novo в трансгенных мышах. Более того, редкие антитела, такие как нейтрализующие антитела против ВИЧ широкого спектра действия, полученные от пациентов-людей, нельзя адаптировать к такому формату. Соответственно, остается потребность в альтернативных и творческих решениях проблемы неправильного спаривания.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение основано на обнаружении нового домена гетеродимеризации, названного "стабилизированный нокаутный домен", который можно использовать для образования "псевдо-Fab". Раскрытую в данном документе псевдо-Fab можно вводить в самые разнообразные связывающие белки и форматы связывания для обеспечения свойств мультиспецифического связывания. В определенных аспектах компонент псевдо-Fab может облегчать предпочтительное продуцирование, синтез или очистку требуемого мультиспецифического связывающего белка, сводя к минимуму или устраняя нежелательные неправильные спаривания цепей, которые обычно образуются при использовании традиционных форматов мультиспецифических связывающих белков. В одном аспекте настоящего изобретения предусмотрен связывающий белок, содержащий:
первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена;
где стабилизированный нокаутный домен содержит (3) одну или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном; и (4) одну или более сконструированных межцепочечных дисульфидных связей.
[0003] В одном аспекте настоящего изобретения предусмотрен связывающий белок, содержащий:
первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена;
где стабилизированный нокаутный домен содержит (3) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (4) одну или более сконструированных межцепочечных дисульфидных связей, которые придают псевдо-Fab повышенную термостабильность (Tm) по сравнению с эталонной молекулой Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
[0004] В некоторых вариантах осуществления связывающий белок представляет собой мультиспецифический связывающий белок, дополнительно содержащий:
по меньшей мере второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B.
[0005] В одном аспекте настоящего изобретения предусмотрен мультиспецифический связывающий белок, содержащий:
a) первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена;
b) первую Fab-часть, содержащую (3) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B; (4) первый домен CH1, спаренный с первым доменом CL; и
где стабилизированный нокаутный домен содержит (5) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (6) одну или более сконструированных межцепочечных дисульфидных связей; или в качестве альтернативы, где стабилизированный нокаутный домен содержит (5) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (6) одну или более сконструированных межцепочечных дисульфидных связей, которые придают псевдо-Fab повышенную термостабильность (Tm) по сравнению с эталонной молекулой Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
[0006] В другом аспекте настоящего изобретения предусмотрен мультиспецифический связывающий белок, содержащий:
a) первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием стабилизированного нокаутного домена, при условии, что первая псевдо-Fab-часть не содержит домен CH1, спаренный с доменом CL;
где стабилизированный нокаутный домен содержит (3) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (4) одну или более сконструированных межцепочечных дисульфидных связей; или в качестве альтернативы, где стабилизированный нокаутный домен содержит (3) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (4) одну или более сконструированных межцепочечных дисульфидных связей, которые придают псевдо-Fab повышенную термостабильность (Tm) по сравнению с эталонной молекулой Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX;
b) первую Fab-часть, содержащую (5) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B; (6) первый домен CH1, спаренный с первым доменом CL; и
c) линкерную часть, которая функционально связывает первую Fab-часть и первую псевдо-Fab-часть.
[0007] В другом аспекте настоящего изобретения предусмотрен мультиспецифический связывающий белок, содержащий:
a) первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена;
b) первую Fab-часть, содержащую (3) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B; (4) первый домен CH1, спаренный с первым доменом CL; и
где стабилизированный нокаутный домен содержит (5) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (6) одну или более сконструированных межцепочечных дисульфидных связей; или в качестве альтернативы, где стабилизированный нокаутный домен содержит (5) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (6) одну или более сконструированных межцепочечных дисульфидных связей, которые придают псевдо-Fab повышенную термостабильность (Tm) по сравнению с эталонной молекулой Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
c) линкерную часть, которая функционально связывает первую Fab-часть и первую псевдо-Fab-часть.
[0008] В некоторых вариантах осуществления линкерная часть находится на одной или более тяжелых цепях.
[0009] В некоторых вариантах осуществления мультиспецифический связывающий белок дополнительно содержит третий домен VL (VLc), спаренный с третьим доменом VH (VHc) с образованием третьего функционального антигенсвязывающего участка, который связывает целевой антиген C.
[0010] В некоторых вариантах осуществления мультиспецифический связывающий белок содержит независимо одну или две псевдо-Fab-части и одну или две Fab-части.
[0011] В некоторых вариантах осуществления линкерная часть представляет собой пептидный линкер. В некоторых вариантах осуществления пептидный линкер представляет собой линкер Gly-Ser, имеющий состав (Gly4Ser)n, где n составляет 1-10.
[0012] В некоторых вариантах осуществления домен гетеродимеризации содержит полноразмерное антитело IgG. В некоторых вариантах осуществления домен гетеродимеризации содержит домен Fc полноразмерного антитела IgG или его функциональный фрагмент.
[0013] В некоторых вариантах осуществления связывающий белок содержит отдельные белковые цепи и выбран из одной из следующих групп:
(a) VHa-CH1-L1-VHb-L2-VHX, и VLa-CL, и VLb-L3-VLX;
(b) VHa-L2-VHX-L1-VHb-CH1, и VLa-L3-VLX, и VLb-CL;
(c) VHa-CH1-L1-VHa-CH1, и VHb-L2-VHX-L3-VHb-L4-VHX, и две цепи VLb-L5-VLX и две цепи VLa-CL;
где цепи из (а) и (b) могут присутствовать один раз или дважды, и где L1, L2, L3, L4 и L5 представляют собой линкеры, которые независимо могут быть одинаковыми или разными.
[0014] В настоящем изобретении предусмотрено мультиспецифическое антитело, содержащее:
a) первую псевдо-Fab-часть, содержащую:
(1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого антигенсвязывающего участка, который связывает целевой антиген A;
(2) первый стабилизированный нокаутный домен VL (VLX), спаренный с первым стабилизированным нокаутным доменом VH (VHX) с образованием первого стабилизированного дисульфидом нокаутного (dsKO) домена;
(3) первый домен гетеродимеризации (HD1);
где первый домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном, и (ii) одну или более сконструированных межцепочечных дисульфидных связей; или в качестве альтернативы содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (ii) одну или более сконструированных межцепочечных дисульфидных связей, которые придают повышенную термостабильность (Tm) псевдо-Fab относительно эталонной молекулы Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX;
b) первую Fab-часть, содержащую:
(1) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(2) первый домен CH1, спаренный с первым доменом CL; и
(3) второй домен гетеродимеризации (HD2).
[0015] В некоторых вариантах осуществления первый домен гетеродимеризации (HD1) функционально связан с С-концом домена VHX псевдо-Fab-части.
[0016] В некоторых вариантах осуществления второй домен гетеродимеризации (HD2) функционально связан с С-концом первого домена CH1 первой Fab-части.
[0017] В некоторых вариантах осуществления первый и второй домены гетеродимеризации содержат первый и второй домены Fc.
[0018] В некоторых вариантах осуществления домены Fc содержат общую структуру шарнир-домен CH2-домен CH3.
[0019] В некоторых вариантах осуществления домены Fc содержат одну или более мутаций типа "выступ-во-впадину" (KIH).
[0020] В некоторых вариантах осуществления один из доменов Fc содержит первый домен CH3, содержащий одну или обе из мутаций S354C и T366W, а другой домен Fc содержит второй домен CH3, содержащий одну или обе из мутаций Y349C, T366S, L368A и Y407V.
[0021] В некоторых вариантах осуществления домены Fc содержат мутации H435R и/или Y436F.
[0022] В некоторых вариантах осуществления первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ia) N-VHa-L1-VHX-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIa) N-VLa-L2-VLX-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
[0023] В некоторых вариантах осуществления первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ib) N-VHX-L1-VHa-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIb) N-VLX-L2-VLa-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
[0024] В некоторых вариантах осуществления первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ic) N-VLa-L1-VHX-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIc) N-VHa-L2-VLX-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
[0025] В некоторых вариантах осуществления первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Id) N-VHX-L1-VLa-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IId) N-VLX-L2-VHa-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
[0026] В некоторых вариантах осуществления по меньшей мере два из целевого антигена A, целевого антигена B и целевого антигена C представляют собой разные целевые антигены.
[0027] В некоторых вариантах осуществления по меньшей мере один из целевых антигенов представляет собой лиганд рецептора клеточной поверхности, и по меньшей мере один из целевых антигенов представляет собой рецептор клеточной поверхности.
[0028] В некоторых вариантах осуществления антигенсвязывающие участки получены из разных антител.
[0029] В некоторых вариантах осуществления целевой антиген A, целевой антиген B и целевой антиген C представляют собой один и тот же целевой антиген.
[0030] В некоторых вариантах осуществления антигенсвязывающие участки связывают разные эпитопы на одном и том же целевом антигене.
[0031] В некоторых вариантах осуществления антигенсвязывающие участки связывают один и тот же эпитоп на одном и том же целевом антигене.
[0032] В некоторых вариантах осуществления антигенсвязывающие участки получены из одного антитела.
[0033] В некоторых вариантах осуществления температура плавления (Tm) псевдо-Fab-части на по меньшей мере 4 градуса Цельсия превышает таковую у эталонной молекулы Fab.
[0034] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH44C-VL100C.
[0035] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH105C-VL43C.
[0036] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в домене VHX псевдо-Fab-части.
[0037] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH3 домена VHX.
[0038] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH2 домена VHX.
[0039] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH1 домена VHX.
[0040] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в домене VLX псевдо-Fab-части.
[0041] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL3 домена VLX.
[0042] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL2 домена VLX.
[0043] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL1 домена VLX.
[0044] В некоторых вариантах осуществления домен VHX псевдо-Fab-части содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 77, SEQ ID NO: 78 и SEQ ID NO: 79.
[0045] В некоторых вариантах осуществления пара VLX/VHX выбрана из группы, состоящей из:
(i) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 77;
ii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 78; и
iii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 79.
[0046] В некоторых вариантах осуществления связывающий белок дополнительно содержит один или более дополнительных связывающих доменов, функционально связанных с N- или C-концом связывающего белка.
[0047] В некоторых вариантах осуществления один или более дополнительных связывающих доменов функционально связаны с N-концом первой или второй псевдо-Fab-части.
[0048] В некоторых вариантах осуществления один или более дополнительных связывающих доменов функционально связаны с N-концом первой или второй Fab-части.
[0049] В другом аспекте настоящего изобретения предусмотрен мультиспецифический связывающий белок, содержащий четыре полипептидные цепи, которые образуют по меньшей мере два антигенсвязывающих участка, где
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHb-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1 и L2 представляют собой аминокислотные линкеры, которые независимо могут быть одинаковыми или разными;
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0050] В другом аспекте настоящего изобретения предусмотрен антигенсвязывающий белок, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0051] В другом аспекте настоящего изобретения предусмотрен антигенсвязывающий белок, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0052] В другом аспекте настоящего изобретения предусмотрен антигенсвязывающий белок, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHa-L4-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L5-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4 и L5 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0053] В другом аспекте настоящего изобретения предусмотрен антигенсвязывающий белок, содержащий четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где:
(a) полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-L3-VLc-L4-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHc-L5-VHb-L6-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VLc представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VHc представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
VLX представляет собой первый стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой первый стабилизированный нокаутный вариабельный домен тяжелой цепи;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4, L5 и L6 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) третий домен VL (VLc) спарен с третьим доменом VH (VHc) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген C;
(4) полипептид формулы III и полипептид формулы IV образуют кроссоверную пару легкая цепь-тяжелая цепь (CODV);
(5) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0054] В другом аспекте настоящего изобретения предусмотрен антигенсвязывающий белок, содержащий четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где:
(a) полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-L3-VLc-L4-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHc-L5-VHb-L6-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VLc представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VHc представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
VLX представляет собой первый стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой первый стабилизированный нокаутный вариабельный домен тяжелой цепи;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4, L5 и L6 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) третий домен VL (VLc) спарен с третьим доменом VH (VHc) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген C;
(4) полипептид формулы III и полипептид формулы IV образуют кроссоверную пару легкая цепь-тяжелая цепь (CODV);
(5) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном относительно эталонной молекулы Fab; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[0055] В других аспектах некоторые варианты осуществления относятся ко всем связывающим белкам, описанным в данном документе, где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном по сравнению с доменами дикого типа, и (ii) одну или более сконструированных межцепочечных дисульфидных связей, которые придают повышенную термостабильность (Tm) псевдо-Fab относительно эталонной молекулы Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX. В этих вариантах осуществления связывание с целевым антигеном измеряют посредством методов, известных в данной области техники, таких как без ограничения поверхностный плазмонный резонанс, а термостабильность измеряют посредством методов, известных в данной области техники, таких как без ограничения дифференциальная сканирующая калориметрия.
[0056] В некоторых вариантах осуществления домены FC1 и FC2 содержат одну или более мутаций типа "выступ-во-впадину" (KIH), при этом мутации облегчают гетеродимеризацию домена Fc полипептидов.
[0057] В некоторых вариантах осуществления один из FC1 или FC2 содержит первый домен CH3, содержащий одну или обе из мутаций S354C и T366W, и другой из FC1 или FC2 содержит второй домен CH3, содержащий одну или обе из мутаций Y349C, T366S, L368A, и Y407V, при этом мутации облегчают гетеродимеризацию домена Fc.
[0058] В некоторых вариантах осуществления домены FC1 или FC2 содержат мутации H435R и/или Y436F.
[0059] В некоторых вариантах осуществления по меньшей мере два из целевого антигена A, целевого антигена B и целевого антигена C представляют собой разные целевые антигены.
[0060] В некоторых вариантах осуществления по меньшей мере один из целевых антигенов представляет собой лиганд рецептора клеточной поверхности, и по меньшей мере один из целевых антигенов представляет собой рецептор клеточной поверхности.
[0061] В некоторых вариантах осуществления антигенсвязывающие участки получены из разных антител.
[0062] В некоторых вариантах осуществления целевой антиген A, целевой антиген B и целевой антиген C представляют собой один и тот же целевой антиген.
[0063] В некоторых вариантах осуществления антигенсвязывающие участки связывают разные эпитопы на одном и том же целевом антигене.
[0064] В некоторых вариантах осуществления антигенсвязывающие участки связывают один и тот же эпитоп на одном и том же целевом антигене.
[0065] В некоторых вариантах осуществления антигенсвязывающие участки получены из одного антитела.
[0066] В некоторых вариантах осуществления температура плавления (Tm) псевдо-Fab-части на по меньшей мере 4 градуса Цельсия превышает таковую у эталонной молекулы Fab.
[0067] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH44C-VL100C.
[0068] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH105C-VL43C.
[0069] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в домене VHX псевдо-Fab-части.
[0070] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH3 домена VHX.
[0071] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH2 домена VHX.
[0072] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRH1 домена VHX.
[0073] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в домене VLX псевдо-Fab-части.
[0074] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL3 домена VLX.
[0075] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL2 домена VLX.
[0076] В некоторых вариантах осуществления по меньшей мере одна из одной или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном, присутствует в CDRL1 домена VLX.
[0077] В некоторых вариантах осуществления домен VHX псевдо-Fab-части содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 77, SEQ ID NO: 78 и SEQ ID NO: 79.
[0078] В некоторых вариантах осуществления пара VLX/VHX выбрана из группы, состоящей из:
(i) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 77;
ii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 78; и
iii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 79.
[0079] В другом аспекте настоящего изобретения предусмотрено применение стабилизированного нокаутного домена для снижения неправильного спаривания тяжелой цепи и легкой цепи в мультиспецифическом связывающем белке, где стабилизированный нокаутный домен содержит домены VHX и VLX, содержащие (3) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (4) одну или более сконструированных межцепочечных дисульфидных связей, которые придают повышенную термостабильность (Tm) псевдо-Fab относительно эталонной молекулы Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
[0080] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH44C-VL100C.
[0081] В некоторых вариантах осуществления сконструированная межцепочечная дисульфидная связь представляет собой VH105C-VL43C.
[0082] В некоторых вариантах осуществления домен VHX псевдо-Fab-части содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 77, SEQ ID NO: 78 и SEQ ID NO: 79.
[0083] В некоторых вариантах осуществления пара VLX/VHX выбрана из группы, состоящей из:
(i) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 77;
ii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 78; и
iii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 79.
[0084] В некоторых вариантах осуществления в псевдо-Fab отсутствуют домены CH1 и CL.
[0085] В некоторых вариантах осуществления предусмотрена выделенная молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую один или более связывающих белков. В некоторых вариантах осуществления предусмотрен набор выделенных молекул нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более связывающих белков.
[0086] В некоторых вариантах осуществления предусмотрен вектор экспрессии, содержащий молекулу нуклеиновой кислоты. В некоторых вариантах осуществления предусмотрен набор векторов экспрессии, содержащий набор молекул нуклеиновой кислоты.
[0087] В некоторых вариантах осуществления предусмотрена выделенная клетка-хозяин, содержащая молекулу нуклеиновой кислоты или вектор экспрессии. В некоторых вариантах осуществления предусмотрена выделенная клетка-хозяин, содержащая набор молекул нуклеиновой кислоты или набор векторов экспрессии.
[0088] В некоторых вариантах осуществления предусмотрен способ получения связывающего белка, включающий культивирование клетки-хозяина в условиях, при которых экспрессируется связывающий белок; и очистку связывающего белка из клетки-хозяина.
[0089] В некоторых вариантах осуществления предусмотрена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и терапевтически эффективное количество мультиспецифического связывающего белка. В некоторых вариантах осуществления предусмотрен мультиспецифический связывающий белок для применения в качестве лекарственного препарата.
[0090] В некоторых вариантах осуществления предусмотрен способ лечения нарушения, при котором активность антигена оказывает негативное воздействие, причем способ включает введение субъекту, нуждающемуся в этом, эффективного количества мультиспецифического связывающего белка.
[0091] Описанное выше краткое описание изобретения не является ограничивающим, и другие признаки и преимущества раскрытых композиций и способов будут очевидны из следующего подробного описания изобретения и из формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0092] SEQ ID NO: 1: последовательность вариабельной области легкой цепи трастузумаба.
[0093] SEQ ID NO: 2: последовательность вариабельной области тяжелой цепи трастузумаба.
[0094] SEQ ID NO: 3: последовательность вариабельной области тяжелой цепи варианта 1 ko-трастузумаба.
[0095] SEQ ID NO: 4: последовательность вариабельной области тяжелой цепи варианта 2 ko-трастузумаба.
[0096] SEQ ID NO: 5: последовательность вариабельной области тяжелой цепи варианта 3 ko-трастузумаба.
[0097] SEQ ID NO: 6: VL антитела к IL13-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[0098] SEQ ID NO: 7: VH антитела к IL13-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[0099] SEQ ID NO: 8: VL антитела к IL13-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00100] SEQ ID NO: 9: VH антитела к IL13-(G4S)2-VH антитела к Her2-(трастузумаб-G44C)-Fc huIgG1.
[00101] SEQ ID NO: 10: VL3 антитела к IL13-IGK.
[00102] SEQ ID NO: 11: VH2 антитела к IL13-IGHG1.
[00103] SEQ ID NO: 12: VL антитела к TNF-альфа-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[00104] SEQ ID NO: 13: VH антитела к TNF-альфа-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00105] SEQ ID NO: 14: VL антитела к TNF-альфа-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00106] SEQ ID NO: 15: VH антитела к TNF-альфа-(G4S)2-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00107] SEQ ID NO: 16: VL антитела к TNFa-huIGKC.
[00108] SEQ ID NO: 17: VH антитела к TNFa-huIgG1.
[00109] SEQ ID NO: 18: VL антитела к IL6R-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[00110] SEQ ID NO: 19: VH антитела к IL6R-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00111] SEQ ID NO: 20: VL антитела к IL6R-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00112] SEQ ID NO: 21: VH антитела к IL6R-(G4S)2-VH антитела к Her2-(трастузумаб-G44C)-Fc huIgG1.
[00113] SEQ ID NO: 22: VL антитела к IL6R-huIGKC.
[00114] SEQ ID NO: 23: VH антитела к IL6R-huIgG1.
[00115] SEQ ID NO: 24: VL антитела к CTLA4-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[00116] SEQ ID NO: 25: VH антитела к CTLA4-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00117] SEQ ID NO: 26: VL антитела к CTLA4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00118] SEQ ID NO: 27: VH антитела к CTLA4-(G4S)2-VH антитела к Her2-(трастузумаб-G44C)-Fc huIgG1.
[00119] SEQ ID NO: 28: VL антитела к CTLA4-huIGKC.
[00120] SEQ ID NO: 29: VH антитела к CTLA4-huIgG1.
[00121] SEQ ID NO: 30: VL антитела к PD1-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[00122] SEQ ID NO: 31: VH антитела к PD1-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00123] SEQ ID NO: 32: VL антитела к PD1-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00124] SEQ ID NO: 33: VH антитела к PD1-(G4S)2-VH антитела к Her2-(трастузумаб-G44C)-Fc huIgG1.
[00125] SEQ ID NO: 34: VL антитела к huPD-1-huIGKC.
[00126] SEQ ID NO: 35: VH антитела к huPD-1-huIgG1.
[00127] SEQ ID NO: 36: VL антитела к IL4-G4S-VL антитела к Her2 (трастузумаб-Q100C).
[00128] SEQ ID NO: 37: VH антитела к IL4-G4S-VH антитела к Her2 (трастузумаб-G44C)-Fc huIgG1.
[00129] SEQ ID NO: 38: VL антитела к IL4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00130] SEQ ID NO: 39: VH антитела к IL4-(G4S)2-VH антитела к Her2-(трастузумаб-G44C)-Fc huIgG1.
[00131] SEQ ID NO: 40: VL1 антитела к IL4-IGKC.
[00132] SEQ ID NO: 41: VH1 антитела к IL4-IgG1.
[00133] SEQ ID NO: 42: VL антитела к PD1-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00134] SEQ ID NO: 43: VH антитела к PD1-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1.
[00135] SEQ ID NO: 44: VL антитела к CTLA4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00136] SEQ ID NO: 45: VH антитела к CTLA4-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1.
[00137] SEQ ID NO: 46: VL антитела к IL4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00138] SEQ ID NO: 47: VH антитела к IL4-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1.
[00139] SEQ ID NO: 48: VL антитела к IL13-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00140] SEQ ID NO: 49: VH антитела к IL13-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-DKTHT-His6.
[00141] SEQ ID NO: 50: VL антитела к IL13-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00142] SEQ ID NO: 51: VH антитела к IL13-(G4S)2-VH антитела к Her2 (VH трастузумаба-вариант 1-G44C)-Fc huIgG1.
[00143] SEQ ID NO: 52: VL антитела к IL4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00144] SEQ ID NO: 53: VH антитела к IL4-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00145] SEQ ID NO: 54: антитело к PD1-huIGKC.
[00146] SEQ ID NO: 55: VH антитела к PD1-huIgG1 (впадина-RF).
[00147] SEQ ID NO: 56: VL антитела к IL13-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00148] SEQ ID NO: 57: VH антитела к IL13 -(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00149] SEQ ID NO: 58: VL антитела к PD1-huIGKC.
[00150] SEQ ID NO: 59: VH антитела к PD1-huIgG1 (впадина-RF).
[00151] SEQ ID NO: 60: VL антитела к PD1-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00152] SEQ ID NO: 61: VH антитела к PD1-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00153] SEQ ID NO: 62: VL антитела к IL13-huIGKC.
[00154] SEQ ID NO: 63: VH антитела к IL13-huIgG1 (впадина-RF).
[00155] SEQ ID NO: 64: VL антитела к CTLA4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00156] SEQ ID NO: 65: VH антитела к CTLA4-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00157] SEQ ID NO: 66: VL антитела к PD1-huIGKC.
[00158] SEQ ID NO: 67: VH антитела к PD1-huIgG1 (впадина-RF).
[00159] SEQ ID NO: 68: VL антитела к IL4-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00160] SEQ ID NO: 69: VH антитела к IL4-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00161] SEQ ID NO: 70: VL антитела к IL13-huIGKC.
[00162] SEQ ID NO: 71: VH антитела к IL13-huIgG1 (впадина-RF).
[00163] SEQ ID NO: 72: VL антитела к PD1-(G4S)2-VL антитела к Her2 (трастузумаб-Q100C).
[00164] SEQ ID NO: 73: VH антитела к PD1-(G4S)2-VH антитела к Her2 (трастузумаб-G44C-вариант 2)-Fc huIgG1 (выступ).
[00165] SEQ ID NO: 74: VL антитела к PD1-huIGKC.
[00166] SEQ ID NO: 75: VH антитела к PD1-huIgG1 (впадина-RF).
[00167] SEQ ID NO: 76: последовательность вариабельной области легкой цепи dsKO-трастузумаба.
[00168] SEQ ID NO: 77: последовательность вариабельной области тяжелой цепи dsKO-трастузумаба, вариант 1.
[00169] SEQ ID NO: 78: последовательность вариабельной области тяжелой цепи dsKO-трастузумаба, вариант 2.
[00170] SEQ ID NO: 79: последовательность вариабельной области тяжелой цепи dsKO-трастузумаба, вариант 3.
[00171] SEQ ID NO: 80: антитело к TCR α/β x антитело к CD123 дикого типа
[00172] SEQ ID NO: 81: антитело к TCR α/β x антитело к CD123-dsTrasKO2
[00173] SEQ ID NO: 82: антитело к TCR α/β-dsTrasKO2 x антитело к CD123
[00174] SEQ ID NO: 83: антитело к CD3ε x антитело к CD123 дикого типа
[00175] SEQ ID NO: 84: антитело к CD3ε x антитело к CD123-dsTrasKO2
[00176] SEQ ID NO: 85: антитело к CD3ε-dsTrasKO2 x антитело к CD123
[00177] SEQ ID NO: 86: антитело к CD3ε x антитело к CD123 дикого типа
[00178] SEQ ID NO: 87: антитело к CD3ε x антитело к CD123-dsTrasKO2
[00179] SEQ ID NO: 88: антитело к CD3ε-dsTrasKO2 x антитело к CD123
[00180] SEQ ID NO: 89: антитело к TCR α/β x антитело к TNP дикого типа - отрицательный контроль
[00181] SEQ ID NO: 90: антитело к TCR α/β x антитело к TNP-dsTrasKO2 - отрицательный контроль
[00182] SEQ ID NO: 91: антитело к TCR α/β-dsTrasKO2 x антитело к TNP - отрицательный контроль
[00183] SEQ ID NO: 92: антитело к TNP x антитело к CD123 дикого типа - отрицательный контроль
[00184] SEQ ID NO: 93: антитело к TNP x антитело к CD123-dsTrasKO2 - отрицательный контроль
[00185] SEQ ID NO: 94: антитело к TNP-dsTrasKO2 x антитело к CD123 - отрицательный контроль
[00186] SEQ ID NO: 95: антитело к CD3ε x антитело к TNP дикого типа - отрицательный контроль
[00187] SEQ ID NO: 96: антитело к CD3ε x антитело к TNP-dsTrasKO2 - отрицательный контроль
[00188] SEQ ID NO: 97: антитело к CD3ε-dsTrasKO2 x антитело к TNP - отрицательный контроль
[00189] SEQ ID NO: 98: антитело к CD3ε x антитело к TNP дикого типа - отрицательный контроль
[00190] SEQ ID NO: 99: антитело к CD3ε x антитело к TNP-dsTrasKO2 - отрицательный контроль
[00191] SEQ ID NO: 100: антитело к CD3ε-dsTrasKO2 x антитело к TNP - отрицательный контроль
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[00192] Вышеизложенные и другие признаки и преимущества настоящего изобретения будут в большей степени понятны из следующего подробного описания иллюстративных вариантов осуществления во взаимосвязи с прилагаемыми графическими материалами. Комплект материалов настоящего патента или заявки содержит как минимум один рисунок, выполненный в цвете. Копии публикации настоящего патента или патентной заявки с цветным(-ми) рисунком(-ами) будут предоставлены патентным ведомством по запросу и при оплате необходимого сбора.
[00193] На фиг. 1A - фиг. 1B схематически изображены димерные биспецифические тандемные молекулы, содержащие фрагменты псевдо-Fab с замещением пары CH1/CL на стабилизированный дисульфидом нокаутный домен (dsKO). Тандемная молекула (Fv-Fab x Fv-псевдо-Fab) изображена на фиг. 1A, а тандемная молекула (Fv-псевдо-Fab x Fv-Fab) изображена на фиг. 1B.
[00194] На фиг. 2 схематически изображена иллюстративная димерная биспецифическая молекула IgG ((Fv-псевдо-Fab) x (Fv-Fab) -Fc)). Стабилизированный дисульфидом нокаутный домен (dsKO) заменяет домены CH/CL одного Fab-плеча молекулы IgG. Пептидные линкеры (например, G4S или (G4S)2) связывают первый антигенсвязывающий участок (Fv) с доменом dsKO с образованием псевдо-Fab-части, которая связывает антиген-мишень A. Домен Fc-гетеродимеризации с мутациями типа "выступ-во-впадину" (KIH) или RF связывает псевдо-Fab-часть со вторым связывающим плечом Fab, которое связывает антиген-мишень B.
[00195] На фиг. 3A - фиг. 3C схематически изображена мономерная фракция конструкции антитела, содержащей замещение CH1/CL на VH/VL WT трастузумаба (фиг. 3A), по сравнению с конструкцией антитела, содержащей замену CH1/CL на стабилизированные дисульфидом нокаутные VH/VL трастузумаба ("dsTrastKO") (фиг. 3B), а также термостабильность обеих конструкций (фиг. 3C).
[00196] На фиг. 4 схематически изображена структура 1N8Z из PDB, на которой показано связывание трастузумаба с HER2. Отмечено расположение четырех инактивирующих мутаций, которые устраняют связывание с HER2 (R50, R59, Y33 и Y103).
[00197] На фиг. 5A - фиг. 5B графически изображены результаты экспериментов по связыванию, демонстрирующие, что варианты 1-3 с dsTrastuKO больше не связывают HER2.
[00198] На фиг. 6A - фиг. 6B изображены конструкции псевдо-IgG и псевдо-Fab, используемые в качестве определенных контролей в экспериментах.
[00199] На фиг. 7A - фиг. 7D изображены типичный биспецифический формат и результаты очистки в соответствии с определенными иллюстративными вариантами осуществления. На фиг. 7A показано расположение отдельных доменов в пределах каркаса IgG. Fv1 (антитело к IL4) слит с VL/VH dsTrasKO2 через линкер (G4S)2. Fv2 (антитело к IL13) сохраняет конфигурацию дикого типа. На фиг. 7B показаны восстановленная (одна легкая и одна тяжелая цепи) и окисленная форма антитела при проведении электрофореза в полиакриламидном геле с 4-12% бис/трис-MOPS-додецилсульфата натрия (SDS-PAGE). Чистота продукта показана на фиг. 7C при проведении аналитической эксклюзионной хроматографии. Целостность молекул подтверждали посредством анализа массы интактного вещества с использованием детектора Q-TOF сверхвысокого разрешения (UHD) Agilent 6540, оснащенного двойным ESI-интерфейсом Jet Stream, и LC-системы Agilent 1290/1260 Infinity (фиг. 7D).
[00200] На фиг. 8 показаны результаты анализов с помощью хроматографии гидрофобного взаимодействия (HIC), показывающие, что биспецифические конструкции с dsTrasKO2 характеризовались правильным спариванием и не содержали случайных разновидностей.
[00201] На фиг. 9 схематично изображена кристаллическая структура конструкции псевдо-Fab антитела к IL13-dsTrasKO2, имеющей ультраструктуру, показанную на фигуре 6A. Структуру определяли при 3,75Å. Структура показывает наложение доменов VH/VL антитела к IL13 у псевдо-Fab антитела к IL13 с TrasKO2 (светло-серый) и Fab антитела к IL13 (темно-серый).
[00202] На фиг. 10A-10B схематически изображены димерные биспецифические тандемные молекулы, содержащие фрагменты псевдо-Fab с замещением пары CH1/CL на стабилизированный дисульфидом нокаутный домен (dsKO). Тандемная молекула (Fv-Fab x Fv-псевдо-Fab)-IgG изображена на фиг. 10A, а тандемная молекула (Fv-псевдо-Fab x Fv-Fab)-IgG изображена на фиг. 10B.
[00203] На фиг. 11A-11B схематически изображены димерные биспецифические тандемные молекулы, содержащие фрагменты псевдо-Fab с замещением пары CH1/CL на стабилизированный дисульфидом нокаутный домен (dsKO). Молекула (((Fv-псевдо-Fab)[HC]-(Fv-псевдо-Fab)) x ((Fv-Fab)[HC]-(Fv-Fab)))-Fc с доменом Fc-гетеродимеризации, содержащим мутации типа "выступ-во-впадину" (KIH) и RF, изображена на фиг. 11A, а содержащим только мутации RF на фиг. 11B.
[00204] На фиг. 12A - фиг. 12D изображена типичная структура биспецифического тандемного IgG, в котором первый псевдо-Fab содержит домен Fv1 (характеризующийся специфичностью связывания с первым целевым антигеном A, т.е. GITR) и домен dsTrasKO, присоединенный к каждому домену Fv2 (характеризующемуся специфичностью связывания со вторым целевым антигеном B, т.е. Ox40) традиционного антитела IgG (погализумаб). На фиг. 12A показано расположение отдельных доменов в пределах каркаса IgG. Fv1 (антитело к GITR) слит с VL/VH dsTrasKO2 через линкер (G4S)2. Fv2 (антитело к Ox40) сохраняет конфигурацию дикого типа. Fv1-dsTrasKO2 слит с Fv2-Ck/CH1 через линкер (G4S)2. На фиг. 12B показаны восстановленная (две легкие и одна тяжелая цепи) и окисленная формы антитела при проведении электрофореза в полиакриламидном геле с 4-12% бис/трис-MOPS-додецилсульфата натрия (SDS-PAGE). Чистота продукта показана на фиг. 12C при проведении аналитической эксклюзионной хроматографии. Целостность молекул подтверждали посредством анализа массы интактного вещества с использованием детектора Q-TOF сверхвысокого разрешения (UHD) Agilent 6540, оснащенного двойным ESI-интерфейсом Jet Stream, и LC-системы Agilent 1290/1260 Infinity (фиг. 12D).
[00205] На фиг. 13A - фиг. 13D изображена типичная структура триспецифического CODV IgG, в котором первый псевдо-Fab содержит домен Fv3 (характеризующийся специфичностью связывания с первым целевым антигеном A, т.е. CD137) и домен dsTrasKO, образующий пару с плечом CODV (характеризующийся специфичностью связывания (Fv1) со вторым целевым антигеном B, т.е. Ox40, и специфичностью связывания (Fv2) с третьим целевым антигеном C, т.е. PD1). На фиг. 13A показано расположение отдельных доменов внутри каркаса CODV IgG. Fv1 (антитело к Ox40) и Fv2 (антитело к PD1) на плече CODV слиты с доменами лямбда-цепи и CH1 дикого типа. Fv3 (антитело к CD137) на плече Fab слит с VL/VH dsTrasKO2 через линкер (G4S)2. На фиг. 13B показаны восстановленная (две легкие и две тяжелые цепи) и окисленная форма CODV-антитела при проведении электрофореза в полиакриламидном геле с 4-12% бис/трис-MOPS-додецилсульфата натрия (SDS-PAGE). Чистота продукта показана на фиг. 13C при проведении аналитической эксклюзионной хроматографии. Целостность молекул подтверждали посредством анализа массы интактного вещества с использованием детектора Q-TOF сверхвысокого разрешения (UHD) Agilent 6540, оснащенного двойным ESI-интерфейсом Jet Stream, и LC-системы Agilent 1290/1260 Infinity (фиг. 13D).
[00206] На фиг. 14 изображена схема двухстадийного процесса очистки, используемого для обеспечения правильного спаривания легких цепей с биспецифическими нокаутными молекулами с dsTrasKO2.
[00207] На фиг. 15A - фиг. 15B изображены анализы цитотоксичности T-клеток человека всех типов против целевых клеток THP-1, инкубируемых совместно с биспецифическими антителами на основе антитела к CD3ε x антитела к CD123. На фиг. 15A представлены биспецифические антитела с ID номерами 33, 34 и 35 с отрицательными контролями 45 и 46. На фиг. 15B представлены биспецифические антитела с ID номерами 36, 37 и 38 с отрицательными контролями 47 и 48. Эффекторные Т-клетки и целевые клетки THP-1, меченные CFSE, высевали в соотношении эффектор-мишень 10:1 и инкубировали совместно с серийными разведениями соответствующих биспецифических молекул (10 нМ - 0 нМ) в течение 20 часов при 37°C. Мертвые клетки окрашивали с помощью 7-AAD и измеряли посредством проточной цитометрии. Цитотоксическую активность рассчитывали на основании процентной доли мертвых целевых клеток THP-1 (двойные положительные по 7-AAD/CFSE). Данные показаны в виде числа мертвых целевых клеток [%] в зависимости от концентрации биспецифических молекул [пМ] как среднее для двух репрезентативных здоровых доноров.
ПОДРОБНОЕ ОПИСАНИЕ
Определения
Чтобы настоящее изобретение можно было легче понимать, ниже определены выбранные термины.
[00208] Используемые в данном документе двадцать стандартных аминокислот и их аббревиатуры соответствуют общепринятой практике. Стереоизомеры (например, D-аминокислоты) двадцати стандартных аминокислот; неприродные аминокислоты, такие как a-двузамещенные аминокислоты, N-алкиламинокислоты, молочная кислота и другие нестандартные аминокислоты также могут быть подходящими компонентами полипептидных цепей связывающих белков по настоящему изобретению. Примеры нестандартных аминокислот включают 4-гидроксипролин, y-карбоксиглутамат, c-N, N,N-триметиллизин, c-N-ацетиллизин, O-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метилгистидин, 5-гидроксилизин, u-N-метиларгинин и другие подобные аминокислоты и иминокислоты (например, 4-гидроксипролин). В системе обозначений полипептидов, используемой в данном документе, левое направление представляет собой направление в сторону аминоконца, а правое направление представляет собой направление в сторону карбоксильного конца в соответствии со стандартной практикой и правилами. Встречающиеся в природе остатки можно разделить на классы на основании общих свойств боковой цепи (см. таблицу 1).
S-содержащая алифатическая
ароматическая
иминогруппа
Met
Phe, Trp
Pro
амидная
ароматическая
гидроксильная
сульфгидрильная
Asn, Gln
Tyr
Ser, Thr
Cys
Таблица 1.
Консервативные аминокислотные замены могут включать обмен представителя одного из этих классов на другого представителя того же класса. Консервативные аминокислотные замены могут охватывать не встречающиеся в природе аминокислотные остатки, которые обычно включаются за счет химического пептидного синтеза, а не за счет синтеза в биологических системах. Они включают пептидомиметики, а также другие обращенные или инвертированные формы аминокислотных остатков. Неконсервативные замены могут включать обмен представителя одного из этих классов на представителя другого класса.
[00209] Используемый в данном документе термин "мутация" или "мутированный" относится к изменению аминокислотной последовательности за счет делеции, вставки и/или замены одной или более аминокислот. Мутация вводится в заданную последовательность, например, аминокислотную последовательность пары VL1 и/или VH1, которая специфически распознает эпитоп 1. Термин "немутированная" относится к любой аминокислотной последовательности, проявляющей функциональные свойства, например, любой последовательности, все еще проявляющей связывающие свойства. Иллюстрацией этого является следующая ситуация. VH1/VL1 является мутированным, так что он не проявляет специфического связывания с эпитопом. Немутированная форма этого VH1/VL1 все еще проявляет специфическое связывание с эпитопом 1. Таким образом, каждый домен VH/VL антитела, связывающегося с любым эпитопом, подходит для осуществления мутации, чтобы служить в качестве каркасного белка по настоящему изобретению.
[00210] Используемый в данном документе термин "вариант" относится к аминокислотной последовательности, которая на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, из которой она была получена, например SEQ ID NO: 1 или SEQ ID NO: 2. Определение процентной идентичности между двумя последовательностями осуществляют с применением математического алгоритма по Karlin and Altschul, Proc. Natl. Acad. Sci. USA 90, 5873-5877, 1993. Такой алгоритм включен в программы BLASTN и BLASTP из Altschul et al. (1990) J. Mol. Biol. 215, 403-410. Чтобы получить выравнивания с гэпами для целей сравнения, используют BLAST с введением гэпов, описанный в Altschul et al. (1997) Nucleic Acids Res. 25, 3389-3402. При использовании программ BLAST и BLAST с введением гэпов в соответствующих программах применяют параметры по умолчанию. В качестве альтернативы вариант также можно определить как содержащий вплоть до 20, 15, 10, 5, 4, 3, 2 или 1 аминокислотной замены, в частности, консервативной аминокислотной замены. Консервативные замены хорошо известны в данной области техники (см., например, Creighton (1984) Proteins. W.H. Freeman and Company). Обзор физических и химических свойств аминокислот приведен в таблице 1 выше. В конкретном варианте осуществления консервативные замены представляют собой замены с использованием аминокислот, характеризующихся по меньшей мере одним общим свойством согласно таблице 1 (т.е. из колонки 1 и/или 2). Термин "вариант" также включает фрагменты. Фрагмент имеет N-концевую и/или C-концевую делецию, составляющую в общей сложности вплоть до 20, 15, 10, 5, 4, 3, 2 или 1 аминокислоты. В качестве дополнения или альтернативы вариант может быть модифицирован, например, с помощью N-концевых и/или C-концевых добавлений аминокислот, составляющих в общей сложности вплоть до 50, 40, 30, 20, 10, 5, 4, 3, 2 или 1 аминокислоты.
[00211] Используемый в данном документе термин "связывающий белок" или "связывающий полипептид" относится к полипептиду (например, антителу или его фрагменту), который содержит по меньшей мере один связывающий участок, который отвечает за селективное связывание с представляющим интерес целевым антигеном (например, антигеном человека). Иллюстративные связывающие участки включают без ограничения вариабельный домен антитела, лигандсвязывающий участок рецептора или рецепторсвязывающий участок лиганда. В определенных аспектах связывающие полипептиды содержат множественные (например, два, три, четыре или более) сайтов связывания. В некоторых аспектах связывающий белок не является терапевтическим ферментом.
[00212] Используемый в данном документе термин "Her2" или "HER2" относиться к рецептору эпидермального фактора роста человека 2 типа, который является представителем семейства рецепторов эпидермального фактора роста.
[00213] Используемый в данном документе термин "связывающий белок" относится к не встречающейся в природе, рекомбинантной или сконструированной молекуле, способной специфически связываться с по меньшей мере одним антигеном. В конкретном варианте осуществления связывающий белок содержит по меньшей мере одну пару VH/VL, которая специфически связывается с антигеном.
[00214] Получение биспецифического связывающего белка за счет совместной экспрессии двух легких и двух тяжелых цепей в одной клетке-хозяине может быть очень сложной задачей из-за низкого выхода требуемого биспецифического связывающего белка и сложности удаления контаминантов, представляющих собой близкородственные связывающие белки с неправильно спаренными цепями (Suresh et al., Proc. Natl. Acad. Sci. U.S.A.83, 7989-7993, 1986). Это связано с тем, что тяжелые цепи образуют гомодимеры, а также требуемые гетеродимеры, что в данном документе обозначается как "проблема спаривания тяжелых цепей". Кроме того, легкие цепи могут неправильно спариваться с неродственными тяжелыми цепями, что в данном документе обозначается как "проблема спаривания легких цепей". Следовательно, совместная экспрессия двух антител может привести к образованию вплоть до девяти нежелательных разновидностей в дополнение к требуемым биспецифическим связывающим белкам.
[00215] Используемый в данном документе термин "домен гетеродимеризации" относится к субъединице би- или мультиспецифического связывающего белка, которая облегчает, направляет или принудительно приводит к правильной сборке легких цепей и их родственных тяжелых цепей, что приводит к получению требуемого белка, при этом предотвращает неправильное спаривание соответствующих легких или тяжелых цепей.
[00216] Используемый в данном документе термин "гетеродимеризующийся Fc" или "функциональный фрагмент гетеродимеризирующегося Fc" относится к мутантной форме константного домена, например, CH2-CH3 или CH2-CH3-CH4, которая является мутированной относительно встречающейся в природе Fc-части, так что она больше не образует гомодимеры, а образует гетеродимер с соответствующим образом мутированной Fc-частью. Таким образом, термин относится к одной части из двух цепей, которые образуют гетеродимер. Некоторые из таких пар известны в данной области техники и включают, например, вариант типа "выступ-во-впадину" (KIH) или вариант EV-RWT.
[00217] Ridgeway и соавторы создали поверхность контакта CH3, которая способствует гетеродимерной сборке, путем замены небольших боковых цепей на поверхности контакта одного CH3 на более крупные, чтобы создать выступ, и замены крупных боковых цепей на другом домене CH3 на меньшие, чтобы образовалась впадина. Тестирование таких вариантов продемонстрировало преимущественную гетеродимеризацию. Эти исходные мутации типа "выступы-во-впадину" расширяли далее для идентификации с помощью фагового дисплея дополнительных подходящих комбинаций, которые использовали для создания биспецифических антител IgG при тестировании дополнительных замен, обеспечивающих образование дисульфидной связи. Варианты с мутациями типа "выступ-во-впадину" дополнительно описаны в патенте США № 5732168 и патенте США № 8216805, которые включены в данный документ посредством ссылки. Соответственно, в одном варианте осуществления домен CH3 в одном домене FC или домене гетеродимеризации содержит мутации Y349C, T366S, L368A и Y407V, и домен CH3 в другом домене FC или домене гетеродимеризации содержит мутации S354C и T366W (положение аминокислот указано со ссылкой на последовательность lgG1).
[00218] Используемый в данном документе термин "домен гомодимеризации" относится к домену, опосредующему гомодимеризацию двух подобных доменов, например, двух тяжелых цепей. В молекулах IgG спаривание тяжелых цепей опосредует последний домен константной области, т. е. CH3, который образует гомодимерные комплексы с высокой аффинностью (KD ~10 пМ). Дополнительные взаимодействия происходят в шарнирной области, которая отвечает за образование ковалентной связи между двумя тяжелыми цепями, которые образуются после сборки тяжелых цепей. Во взаимодействие в гомодимере CH3 вовлечены приблизительно 16 остатков на поверхности контакта CH3-CH3, как показано для γ1 CH3 человека, при этом пятно, образованное 6 остатками (T366, L368, F405, Y407 и K409), в центре поверхности контакта вносит большой вклад в стабильность. Домены гомодимеризации включают без ограничения области Fc и их варианты с модифицированной эффекторной функцией, и фрагменты любого из них, домены CH2 или их фрагменты, домены CH3 или их фрагменты, домены CH4 или фрагменты и т.п.
[00219] Встречающиеся в природе антитела обычно представляют собой тетрамер. Каждый такой тетрамер обычно состоит из двух идентичных пар полипептидных цепей, при этом каждая пара содержит одну полноразмерную "легкую" цепь (обычно имеющую молекулярную массу приблизительно 25 кДа) и одну полноразмерную "тяжелую" цепь (обычно имеющую молекулярную массу приблизительно 50-70 кДа). Используемые в данном документе термины "тяжелая цепь" и "легкая цепь" относятся к любому полипептиду иммуноглобулина, содержащему последовательность вариабельного домена, достаточную для придания специфичности в отношении целевого антигена. Аминоконцевая часть каждой легкой и тяжелой цепи обычно содержит вариабельный домен из приблизительно 100-110 аминокислот или больше, который обычно отвечает за распознавание антигена. Карбоксиконцевая часть каждой цепи обычно содержит константный домен, который отвечает за эффекторную функцию. Таким образом, во встречающемся в природе антителе полипептид полноразмерной тяжелой цепи иммуноглобулина IgG содержит вариабельный домен (VH) и три константных домена (CH1, CH2 и CH3), при этом домен VH находится на аминоконце полипептида, а домен CH3 находится на карбоксильном конце, а полипептид полноразмерной легкой цепи иммуноглобулина содержит вариабельный домен (VL) и константный домен (CL), при этом домен VL находится на аминоконце полипептида, а домен CL находится на карбоксильном конце.
[00220] Легкие цепи человека обычно классифицируют как легкие каппа- и лямбда-цепи, а тяжелые цепи человека обычно классифицируют как мю, дельта, гамма, альфа или эпсилон, и они определяют изотип антитела IgM, IgD, IgG, IgA и IgE соответственно. IgG имеет несколько подклассов, в том числе без ограничения IgG1, IgG2, IgG3 и IgG4. IgM имеет подклассы, в том числе без ограничения IgM1 и IgM2. IgA аналогичным образом подразделяют на подклассы, в том числе без ограничения IgA1 и IgA2. В пределах полноразмерных легких и тяжелых цепей вариабельные и константные домены обычно соединены с помощью "J"-области, состоящую из приблизительно 12 аминокислот или больше, при этом тяжелая цепь также содержит "D"-область, состоящую из приблизительно 10 аминокислот или больше. См., например, Fundamental Immunology (Paul, W., ed., Raven Press, 2nd ed., 1989), который включен посредством ссылки во всей своей полноте для всех целей. Вариабельные области каждой пары легкая/тяжелая цепь обычно образуют антигенсвязывающий участок. Вариабельные домены встречающихся в природе антител обычно характеризуются одинаковой общей структурой относительно консервативных каркасных областей (FR), соединенных с помощью трех гипервариабельных областей, также называемых определяющими комплементарность областями или CDR. CDR из двух цепей каждой пары обычно выровнены с помощью каркасных областей, что может обеспечивать связывание со специфическим эпитопом. От аминоконца к карбоксильному концу вариабельные домены как легкой, так и тяжелой цепей обычно содержат домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4.
[00221] Используемый в данном документе термин "совокупности CDR" обозначает группу из трех CDR, которые содержатся в одном вариабельном участке, способном связывать антиген. Точные границы этих CDR определяли по-разному в соответствии с различными системами. Система, описанная в Kabat (Kabat et al., SEQUENCES OF PROTEINS OF IMMUNOLOGICAL INTEREST (National Institutes of Health, Bethesda, MD (1987) и (1991)) не только обеспечивает однозначную систему нумерации остатков, применимую к любой вариабельной области антитела, но также обеспечивает точные границы остатков, определяющие три CDR. Эти CDR могут называться CDR в соответствии с Kabat. Chothia и соавторы (Chothia and Lesk, 1987, J. Affol. Biol. 196: 901-17; Chothia et al., 1989, Nature 342: 877-83) обнаружили, что определенные субфрагменты в пределах CDR в соответствии с Kabat принимают почти идентичные конформации пептидного каркаса, несмотря на наличие большого различия на уровне аминокислотной последовательности. Эти субфрагменты были обозначены как L1, L2 и L3 или H1, H2 и H3, где "L" и "H" обозначают области легкой цепи и тяжелой цепи соответственно. Эти области могут называться CDR в соответствии с Chothia, границы которых частично совпадают с CDR в соответствии с Kabat. Другие границы, определяющие CDR, которые частично совпадают с CDR в соответствии с Kabat, были описаны в Padlan, 1995, FASEB J. 9: 13339; MacCallum, 1996, J. Mol. Biol. 262(5): 732-45; и Lefranc, 2003, Dev. Comp. Immunol. 27: 55-77. Еще одни определения границ CDR могут не строго соответствовать одной из систем, приведенных в данном документе, но тем не менее будут совпадать с CDR в соответствии с Kabat, несмотря на то, что они могут быть укорочены или удлинены с учетом прогностических или экспериментальных выводов о том, что конкретные остатки или группы остатков или даже все CDR не влияют в значительной степени на связывание антигена. В способах, используемых в данном документе, могут применять CDR, определенные в соответствии с любой из этих систем, несмотря на то, что в определенных вариантах осуществления применяют CDR, определенные в соответствии с Kabat или Chothia. Идентификация прогнозируемых CDR с помощью аминокислотной последовательности хорошо известна в данной области техники, например, в Martin, A.C. "Protein sequence and structure analysis of antibody variable domains" в Antibody Engineering, Vol. 2. Kontermann R., Dikel S., eds. Springer-Verlag, Berlin, p. 33-51 (2010). Аминокислотную последовательность вариабельного домена тяжелой и/или легкой цепи можно также исследовать с целью идентификации последовательностей CDR с помощью других традиционных способов, например, путем сравнения с известными аминокислотными последовательностями других вариабельных областей тяжелой и легкой цепей для определения областей гипервариабельности последовательности. Пронумерованные последовательности можно выравнивать вручную или путем использования программы выравнивания, такой как одна из пакета программ CLUSTAL, как описано в Thompson, 1994, Nucleic Acids Res. 22: 4673-80. Молекулярные модели традиционно применяют для того, чтобы правильно определить каркасные области и области CDR, и таким образом скорректировать выравнивания, основанные на последовательности.
[00222] В некоторых вариантах осуществления определение CDR/FR в легкой или тяжелой цепи иммуноглобулина следует производить на основании определения по IMGT (Lefranc et al. Dev. Comp. Immunol., 2003, 27(1):55-77; www.imgt.org).
[00223] Используемый в данном документе термин "Fc" относится к молекуле, содержащей последовательность, не являющуюся антигенсвязывающим фрагментом, который получен в результате расщепления антитела или получен другими способами, которая находится в мономерной или мультимерной форме, и при этом она может содержать шарнирную область. Исходный иммуноглобулин, служащий источником нативного Fc, обычно происходит от человека и может представлять собой любой из иммуноглобулинов, хотя в иллюстративных вариантах осуществления применяются IgG1 и IgG2. Молекулы Fc составлены из мономерных полипептидов, которые могут быть связаны в димерные или мультимерные формы посредством ковалентной (т.е. дисульфидных связей) и нековалентной связи. Количество межмолекулярных дисульфидных связей между мономерными субъединицами нативных молекул Fc находится в диапазоне от 1 до 4 в зависимости от класса (например, IgG, IgA и IgE) или подкласса (например, IgG1, IgG2, IgG3, IgA1 и IgGA2). Одним примером Fc является димер с дисульфидной связью, полученный в результате расщепления IgG папаином. Используемый в данном документе термин "нативная Fc" является общим для мономерных, димерных и мультимерных форм.
[00224] F(ab)-фрагмент обычно содержит одну легкую цепь и домены VH и CH1 одной тяжелой цепи, где часть VH-CH1 тяжелой цепи F(ab)-фрагмента не может образовывать дисульфидную связь с полипептидом другой тяжелой цепи. Используемый в данном документе F(ab)-фрагмент также может содержать одну легкую цепь, содержащую два вариабельных домена, разделенных аминокислотным линкером, и одну тяжелую цепь, содержащую два вариабельных домена, разделенных аминокислотным линкером, и домен CH1.
[00225] F(ab')-фрагмент обычно содержит одну легкую цепь и часть одной тяжелой цепи, которая содержит большую часть константной области (между доменами CH1 и CH2), так что между двумя тяжелыми цепями может образовываться межцепочечная дисульфидная связь с образованием молекулы F(ab')2.
[00226] Используемый в данном документе термин "Tm" относится к температуре плавления связывающего белка, антигенсвязывающего белка, антитела, и она представляет собой параметр, критически важный для термостабильности антигенсвязывающих белков. Tm обычно относится к термостабильности Fv-фрагмента, то есть вариабельной области тяжелой и легкой цепи (VH/VL). Tm можно измерить с помощью дифференциальной сканирующей калориметрии (DSC).
[00227] В одном варианте осуществления настоящего изобретения предусмотрены связывающие белки, характеризующиеся биологической и иммунологической специфичностью в отношении одного-трех целевых антигенов. В другом варианте осуществления настоящего изобретения предусмотрены молекулы нуклеиновой кислоты, содержащие нуклеотидные последовательности, кодирующие полипептидные цепи, которые образуют такие связывающие белки. В другом варианте осуществления настоящего изобретения предусмотрены векторы экспрессии, содержащие молекулы нуклеиновой кислоты, содержащие нуклеотидные последовательности, кодирующие полипептидные цепи, которые образуют такие связывающие белки. В еще одном варианте осуществления настоящего изобретения предусмотрены клетки-хозяева, которые экспрессируют такие связывающие белки (т.е. содержащие молекулы нуклеиновой кислоты или векторы, кодирующие полипептидные цепи, которые образуют такие связывающие белки).
[00228] Используемый в данном документе термин "антиген", или "целевой антиген", или "антиген-мишень" относится к молекуле или части молекулы (например, эпитопу), которые могут связываться связывающим белком, и дополнительно их можно использовать у животного для получения антител, способных связываться с эпитопом такого антигена. Целевой антиген может иметь один или более эпитопов. С учетом того, что каждый целевой антиген распознается связывающим белком, связывающий белок способен конкурировать с интактным антителом, которое распознает целевой антиген.
[00229] Используемый в данном документе термин "эпитоп" или "целевой эпитоп" относится к любой детерминанте, например, полипептидной детерминанте, способную специфически связываться с иммуноглобулином или T-клеточным рецептором. Например, но никоим образом не ограничиваясь, целевой эпитоп A может быть первым эпитопом антигена, а целевой эпитоп B может быть вторым эпитопом антигена. В качестве альтернативы целевой эпитоп B может быть вторым эпитопом на втором антигене. В определенных вариантах осуществления эпитопные детерминанты включают химически активные поверхностные группы молекул, такие как аминокислоты, боковые цепи сахаров, фосфорильные группы или сульфонильные группы, и в определенных вариантах осуществления могут иметь специфические характеристики трехмерной структуры и/или специфические характеристики заряда. Эпитоп представляет собой область антигена, которая связывается антителом, или антигенсвязывающим фрагментом антитела, или связывающим белком. В определенных вариантах осуществления считается, что связывающий белок специфически связывает антиген, если он предпочтительно распознает свой целевой антиген в сложной смеси белков и/или макромолекул. В некоторых вариантах осуществления считается, что связывающий белок специфически связывает антиген, если равновесная константа диссоциации составляет <10-8 M, если равновесная константа диссоциации составляет <1-9 M или если константа диссоциации составляет <10-10 M.
[00230] Используемый в данном документе термин "линкер" относится к 0-100 смежным аминокислотным остаткам. Линкеры могут присутствовать или отсутствовать, являются одинаковыми или разными. Все линкеры могут иметь одинаковую аминокислотную последовательность или все они могут иметь разные аминокислотные последовательности.
[00231] В некоторых вариантах осуществления термин "линкер" относится к 1-15 смежным аминокислотным остаткам. Обычно линкер обеспечивает гибкость и пространственное разделение двух аминокислот или двух полипептидных доменов. Линкер можно вставлять между доменами VH, VL, CH и/или CL для обеспечения достаточной степени гибкости и подвижности у доменов легкой и тяжелой цепей в зависимости от формата молекулы, например, для складывания в кроссоверные иммуноглобулины с двойной вариабельной областью. Линкер обычно вставляют в переходную область между вариабельными доменами, между вариабельным и нокаутным доменом или между вариабельным и константным доменами соответственно на уровне аминокислотной последовательности. Переходную область между доменами можно идентифицировать, поскольку приблизительный размер доменов иммуноглобулина хорошо известен. Точное местоположение переходной области между доменами можно определить путем определения местоположения пептидных участков, которые не образуют элементов с вторичной структурой, таких как бета-слои или альфа-спирали, что показано с помощью экспериментальных данных или что можно определить с помощью методик моделирования или прогнозирования вторичной структуры. В некоторых иллюстративных вариантах осуществления линкер может быть вставлен между доменами Fab для создания антитела с тандемными Fab. В конкретных вариантах осуществления линкер может быть вставлен между N-концом домена VH первого Fab и С-концом домена CH1 второго Fab.
[00232] Природа и последовательность аминокислотных остатков в линкере может меняться в зависимости от типа элемента(-ов) вторичной структуры, которую необходимо достигнуть в линкере. Например, глицин, серин и аланин подходят для линкеров, характеризующихся максимальной гибкостью. Определенные комбинации глицина, пролина, треонина и серина применимы, если требуется более жесткий и удлиненный линкер. Любой аминокислотный остаток может рассматриваться в качестве линкера в комбинации с другими аминокислотными остатками для конструирования, при необходимости, более длинных пептидных линкеров в зависимости от требуемых свойств.
[00233] В некоторых вариантах осуществления линкер содержит: одиночный остаток глицина (Gly); диглициновый пептид (Gly-Gly); трипептид (Gly-Gly-Gly); пептид из четырех остатков глицина (Gly-Gly- Gly-Gly; SEQ ID NO: x); пептид из пяти остатков глицина (Gly-Gly-Gly-Gly-Gly; SEQ ID NO: x); пептид из шести остатков глицина (Gly-Gly-Gly-Gly-Gly-Gly; SEQ ID NO: x); пептид из семи остатков глицина (Gly-Gly-Gly-Gly-Gly-Gly-Gly; SEQ ID NO: x) и пептид из восьми остатков глицина (Gly-Gly-Gly-Gly-Gly-Gly-Gly-Gly; SEQ ID NO: x).
[00234] В некоторых вариантах осуществления линкер содержит небольшие аминокислоты, такие как Gly, Ala или Ser.
[00235] В некоторых вариантах осуществления линкер содержит Gly и Ser, или GS, GGS, GGGS или GGGGS. В некоторых вариантах осуществления линкер содержит (Gly-Gly-Gly-Gly-Ser)2 (т. е. (GGGGS)2). В некоторых вариантах осуществления линкер содержит (Gly-Gly-Gly-Gly-Ser)3 (т. е. (GGGGS)3).
[00236] В некоторых вариантах осуществления линкер содержит Gly-Gly- Gly-Gly-Ser (SEQ ID NO: x) пептид Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), пептид Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly- Gly-Ser (SEQ ID NO: x), и пептид Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO:x).
[00237] В некоторых вариантах осуществления линкер содержит одиночный остаток Ser; одиночный остаток Val; дипептид, выбранный из Arg-Thr, Gln-Pro, Ser-Ser, Thr-Lys и Ser-Leu; Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), Thr-Val-Ala-Ala-Pro (SEQ ID NO: x), Gln-Pro-Lys-Ala-Ala (SEQ ID NO: x), Gln-Arg- Ile-Glu-Gly (SEQ ID NO: x); Ala-Ser-Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), Arg-Thr- Val-Ala-Ala-Pro-Ser (SEQ ID NO: x), Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO:x), His-Ile-Asp-Ser-Pro-Asn-Lys (SEQ ID NO: x) и Asp-Lys-Thr-His-Thr (SEQ ID NO: x).
[00238] В некоторых вариантах осуществления два тандемных Fab связаны через линкер (Gly-Gly-Gly-Gly-Ser)2. В некоторых вариантах осуществления линкер между стабилизированным нокаутным доменом и парой VH/VL представляет собой линкер (Gly-Gly-Gly-Gly-Ser)2.
[00239] В некоторых вариантах осуществления имеется CODV-Fab-часть, где L1 и L2 находятся на легкой цепи, а L3 и L4 находятся на тяжелой цепи, длина L1 составляет 3-12 аминокислотных остатков, длина L2 составляет 3-14 аминокислотных остатков, длина L3 составляет 1-8 аминокислотных остатков, и длина L4 составляет 1-3 аминокислотных остатка. В некоторых вариантах осуществления длина L1 составляет 5-10 аминокислотных остатков, длина L2 составляет 5-8 аминокислотных остатков, длина L3 составляет 1-5 аминокислотных остатков, и длина L4 составляет 1-2 аминокислотных остатка. В некоторых вариантах осуществления длина L1 составляет 7 аминокислотных остатков, длина L2 составляет 5 аминокислотных остатков, длина L3 составляет 1 аминокислотный остаток, и длина L4 составляет 2 аминокислотных остатка. В некоторых вариантах осуществления длина L1 составляет 10 аминокислотных остатков, длина L2 составляет 10 аминокислотных остатков, длина L3 составляет 0 аминокислотных остатков, и длина L4 составляет 0 аминокислотных остатков. В некоторых вариантах осуществления длина каждого из L1, L2, L3 и L4 независимо выбрана из 0-15 аминокислот (например, составляет 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислот), где длина по меньшей мере двух из линкеров составляет 1-15 аминокислот (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислот). В некоторых вариантах осуществления L1, L2, L3 и L4 представляют собой Asp-Lys-Thr-His-Thr (SEQ ID NO: x). В некоторых вариантах осуществления линкер(-ы) содержит(-ат) последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x). В некоторых вариантах осуществления L1 содержит последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x). В некоторых вариантах осуществления L1 содержит последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x), L2 содержит последовательность Thr-Lys-Gly-Pro-Ser-Arg (SEQ ID NO: x), L3 содержит последовательность Ser, и L4 содержит последовательность Arg-Thr. В некоторых вариантах осуществления L3 содержит последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x). В некоторых вариантах осуществления L1 содержит последовательность Ser, L2 содержит последовательность Arg-Thr, L3 содержит последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x), и L4 содержит последовательность Thr-Lys-Gly-Pro-Ser-Arg (SEQ ID NO: x).
[00240] В некоторых вариантах осуществления каждый из L1, L2, L3 и L4 независимо содержит последовательность, выбранную из (Gly-Gly-Gly-Gly-Ser)n (где n составляет целое число от 0 до 5; SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Ser, Arg-Thr, Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x) и Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO: x). В некоторых вариантах осуществления L1 содержит последовательность Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x), L2 содержит последовательность Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), L3 содержит последовательность Ser, и L4 содержит последовательность Arg-Thr. В некоторых вариантах осуществления L1 содержит последовательность Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), L2 содержит последовательность Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), длина L3 составляет 0 аминокислот, и длина L4 составляет 0 аминокислот. В некоторых вариантах осуществления L1 содержит последовательность Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO: x), L2 содержит последовательность Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO: x), длина L3 составляет 0 аминокислот, и длина L4 составляет 0 аминокислот. В некоторых вариантах осуществления L1 содержит последовательность Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), длина L2 составляет 0 аминокислот, L3 содержит последовательность Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), и дина L4 составляет 0 аминокислот. В некоторых вариантах осуществления длина L1 и L2 составляет нуль аминокислот, и каждый из L3 и L4 содержит последовательность, независимо выбранную из (Gly-Gly-Gly-Gly-Ser)n (SEQ ID NO: x) (где n составляет целое число от 0 до 5; SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Ser, Arg-Thr, Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x) и Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO: x). В некоторых вариантах осуществления длина L3 и L4 составляет нуль аминокислот, и каждый из L1 и L2 содержит последовательность, независимо выбранную из (Gly-Gly-Gly-Gly-Ser)n (где n составляет целое число от 0 до 5; SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: x), Ser, Arg-Thr, Thr-Lys-Gly-Pro-Ser (SEQ ID NO: x), Gly-Gln-Pro-Lys-Ala-Ala-Pro (SEQ ID NO: x) и Gly-Gly-Ser-Gly-Ser-Ser-Gly-Ser-Gly-Gly (SEQ ID NO: x).
[00241] В некоторых вариантах осуществления линкер(-ы) содержит(-ат) последовательность, полученную из встречающейся в природе последовательности в участке соединения между вариабельным доменом антитела и константным доменом антитела (например, как описано в WO2012/135345). Например, в некоторых вариантах осуществления линкер содержит последовательность, встречающуюся в переходной области между эндогенными доменами VH и CH1 или между эндогенными доменами VL и CL (например, в каппа- или лямбда-цепи). В некоторых вариантах осуществления линкер содержит последовательность, встречающуюся в переходной области между эндогенными доменами VH и CH1 человека или между эндогенными доменами VL и CL человека (например, в каппа- или лямбда-цепи человека).
[00242] Вышеперечисленные примеры не предназначены для какого-либо ограничения объема настоящего изобретения, и линкеры, содержащие выбранные случайным образом аминокислоты, выбранные из группы, состоящей из валина, лейцина, изолейцина, серина, треонина, лизина, аргинина, гистидина, аспартата, глутамата, аспарагина, глутамина, глицина и пролина, подходят для использования в связывающих белках, описанных в данном документе. Дополнительные описания линкерных последовательностей см., например, в WO2012135345, WO2017/180913, включенных в данный документ посредством ссылки.
[00243] Используемый в данном документе термин "валентность" относится к количеству связывающих участков связывающего белка, эпитопа, антигенсвязывающего белка или антитела. Например, термин "моновалентный связывающий белок" относится к связывающему белку, который имеет один антигенсвязывающий участок. Термин "бивалентный связывающий белок" относится к связывающему белку, который имеет два связывающих участка. Термин "тривалентный связывающий белок" относится к связывающему белку, который имеет три связывающих участка. Термин "тетравалентный связывающий белок" относится к связывающему белку, который имеет четыре связывающих участка. В конкретных вариантах осуществления бивалентный связывающий белок может связываться с одним антигеном-мишенью. В других вариантах осуществления бивалентный связывающий белок может связываться с двумя разными антигенами-мишенями. В конкретных вариантах осуществления тривалентный связывающий белок может связываться с одним антигеном-мишенью, т.е. является моноспецифическим. В других вариантах осуществления тривалентный связывающий белок может связываться с двумя разными антигенами-мишенями, т.е. является биспецифическим. В других вариантах осуществления тривалентный связывающий белок может связываться с тремя разными антигенами-мишенями, т. е. является триспецифическим. В конкретных вариантах осуществления тетравалентный связывающий белок может связываться с одним антигеном-мишенью, т.е. является моноспецифическим. В других вариантах осуществления тетравалентный связывающий белок может связываться с двумя разными антигенами-мишенями, т.е. является биспецифическим. В других вариантах осуществления тетравалентный связывающий белок может связываться с тремя разными антигенами-мишенями, т.е. является триспецифическим. В других вариантах осуществления тетравалентный связывающий белок может связываться с четырьмя разными антигенами-мишенями, т.е. является тетраспецифическим.
[00244] Используемый в данном документе термин "специфичность" относится к количеству специфичностей связывания связывающего белка, эпитопа, антигенсвязывающего белка или антитела. Например, термин "моноспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с одним антигеном-мишенью. Термин "биспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с двумя различными антигенами-мишенями. Термин "триспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с тремя различными антигенами-мишенями. Термин "тетраспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с четырьмя различными антигенами-мишенями и т.д.
[00245] Используемый в данном документе термин "участок селективного распознавания" относится к модификации связывающего белка, обеспечивающей его селективное распознавание посредством связывания аффинного реагента с участком селективного распознавания. Примеры участка селективного распознавания включают связывающий участок для белка А в Fc-части иммуноглобулина.
[00246] Используемый в данном документе термин "аффинный реагент" относится к реагенту, который содержит лиганд, который иммобилизован на матрице и специфически связывается с поверхностными группами молекул, такими как аминокислоты или боковые цепи сахаров, и обычно имеет специфические характеристики трехмерной структуры, а также специфические характеристики заряда. Аффинные реагенты представляют собой инструменты в аффинной хроматографии, где очистка осуществляется за счет специфического взаимодействия между лигандом и продуктом. "Белок L", который является примером аффинного реагента, относится к рекомбинантному белку L, который иммобилизован на матрице с образованием лиганда, который характеризуется аффинностью в отношении подгруппы вариабельного домена легких каппа-цепей иммуноглобулина. Такие матрицы могут представлять собой смолы. Другим примером аффинного реагента является "KappaSelect", который относится к рекомбинантному полученному от верблюдовых одноцепочечному антителу размером 13 кДа, которое иммобилизовано на матрице с образованием лиганда, который характеризуется аффинностью в отношении константного домена легких каппа-цепей иммуноглобулина человека. Другим примером аффинного реагента является белок А. Белок А представляет собой поверхностный белок размером 42 кДа, изначально обнаруженный в клеточной стенке бактерий Staphylococcus aureus. С помощью кристаллографического анализа было показано, что первичный связывающий участок для белка A находится в области Fc, между доменами CH2 и CH3. Кроме того, было показано, что белок А связывает молекулы IgG человека, содержащие фрагменты F(ab')2 IgG из семейства генов VH3 человека. Белок A может связываться с сильной аффинностью с Fc-частью иммуноглобулина определенных видов.
[00247] Константу диссоциации (KD) связывающего белка можно определить, например, с помощью поверхностного плазмонного резонанса. В целом, в анализе поверхностного плазмонного резонанса измеряют связывающие взаимодействия между лигандом (целевым антигеном на биосенсорной матрице) и аналитом (связывающим белком в растворе) в режиме реального времени с помощью поверхностного плазмонного резонанса (SPR) с применением системы BIAcore (Pharmacia Biosensor; Пискатауэй, Нью-Джерси). Поверхностный плазмонный анализ можно также выполнять посредством иммобилизации аналита (связывающего белка на биосенсорной матрице) и представления лиганда (целевого антигена). Используемый в данном документе термин "KD" относится к константе диссоциации взаимодействия между конкретным связывающим белком и целевым антигеном.
[00248] Используемый в данном документе термин "специфически связывается" относится к способности связывающего белка или его антигенсвязывающего фрагмента связываться с антигеном, содержащим эпитоп, при Kd, составляющей по меньшей мере приблизительно 1×10-6 M, 1×10-7 M, 1×10-8 M, 1×10-9 M, 1×10-10 M, 1×10-11 M, 1×10-12 M или больше, и/или связываться с эпитопом с аффинностью, которая в по меньшей мере два раза превышает его аффинность в отношении неспецифического антигена. Определение аффинности связывания антигена со связывающим белком или антителом может быть выполнено с помощью поверхностного плазмонного резонанса (SPR) с использованием прибора BIAcore.
[00249] Используемый в данном документе термин "эталонная молекула Fab" относится к молекуле, которая идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX. "Эталонная молекула Fab" относится к молекуле, в которой вариабельные домены идентичны вариабельным доменам псевдо-Fab, и она имеет домены CH1 и CL. В молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
[00250] Используемый в данном документе термин "нуклеиновая кислота" относится к полимерным или олигомерным макромолекулам или крупным биомолекулам, необходимым для всех известных форм жизни. Нуклеиновые кислоты, которые включают ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота), состоят из мономеров, известных как нуклеотиды. Большинство встречающихся в природе молекул ДНК состоят из двух комплементарных биополимерных нитей, закрученных друг вокруг друга с образованием двойной спирали. Нить ДНК также известна как полинуклеотиды, состоящие из нуклеотидов. В состав каждого нуклеотида входит азотсодержащеее нуклеиновое основания, а также моносахаридный сахар, называемый дезоксирибозой или рибозой, и фосфатная группа. Встречающиеся в природе нуклеиновые основания включают гуанин (G), аденин (A), тимин (T), урацил (U) или цитозин (C). Нуклеотиды соединены друг с другом в цепь за счет ковалентных связей между сахаром одного нуклеотида и фосфатной группой следующего, что приводит к чередующемуся сахарофосфатному остову. Если сахар представляет собой дезоксирибозу, то полимер является ДНК. Если сахар представляет собой рибозу, то полимер является РНК. Обычно полинуклеотид образуется благодаря фосфодиэфирным связям между отдельными нуклеотидными мономерами.
[00251] Используемый в данном документе термин "полинуклеотид" относится к однонитевым или двухнитевым полимерам нуклеиновых кислот, имеющим длину по меньшей мере 10 нуклеотидов. Понятно, что нуклеотиды, составляющие полинуклеотид, могут быть рибонуклеотидами или дезоксирибонуклеотидами или модифицированной формой любого типа нуклеотида. Такие модификации включают модификации оснований, такие как бромуридин, модификации рибозы, такие как арабинозид и 2',3'-дидезоксирибоза, и модификации межнуклеотидных связей, такие как фосфотиоат, фосфодитиоат, фосфоселеноат, фосфодиселеноат, фосфоанилотиоат, фосфоаниладат и фосфоамидат. Конкретнее, термин "полинуклеотид" включает однонитевые и двухнитевые формы ДНК.
[00252] "Выделенный полинуклеотид" представляет собой полинуклеотид, имеющий геномное, кДНК- или синтетическое происхождение или характеризующийся некоторой их комбинацией, который: (1) не ассоциирован со всем полинуклеотидом, в котором выделенный полинуклеотид встречается в природе, или его частью, (2) связан с полинуклеотидом, с которым он не связан в природе, или (3) не встречается в природе в виде части более крупной последовательности.
[00253] "Выделенный полипептид" представляет собой такой полипептид, который: (1) не содержит по меньшей мере некоторых других полипептидов, с которыми он обычно встречается, (2) практически не содержит другие полипептиды из того же источника, например, от того же вида, (3) экспрессируется клеткой другого вида, (4) был отделен от по меньшей мере приблизительно 50 процентов полинуклеотидов, липидов, углеводов или других материалов, с которыми он связан в природе, (5) не связан (ковалентным или нековалентным взаимодействием) с частями полипептида, с которыми "выделенный полипептид" связан в природе, (6) функционально связан (ковалентным или нековалентным взаимодействием) с полипептидом, с которым он не связан в природе, или (7) не встречается в природе. Такой выделенный полипептид может кодироваться геномной ДНК, кДНК, мРНК или другой РНК синтетического происхождения или любой их комбинацией. В иллюстративных вариантах осуществления выделенный полипептид практически не содержит полипептиды или другие контаминанты, которые встречаются в его природном окружении, которые бы препятствовали его применению (терапевтическому, диагностическому, профилактическому, исследовательскому или иному).
[00254] Используемый в данном документе термин "вектор экспрессии", также называемый конструкцией экспрессии, обычно относится к плазмиде или вирусу, разработанным для экспрессии белка в клетках. Термин "вектор" относится к белку или полинуклеотиду или их смеси, которые можно вводить или вводят содержащиеся в них белки и/или нуклеиновые кислоты в клетку. Примеры векторов включают без ограничения плазмиды, космиды, фаги, вирусы или искусственные хромосомы. В частности, вектор используется для транспортировки представляющего интерес генного продукта, такого как, например, чужеродная или гетерологичная ДНК, в подходящую клетку-хозяина. Векторы могут содержать полинуклеотидные последовательности "репликона", который облегчает автономную репликацию вектора в клетке-хозяине. Чужеродную ДНК определяют как гетерологичную ДНК, которая представляет собой ДНК, не встречающуюся в природе в клетке-хозяине, которая, например, осуществляет репликацию молекулы вектора, кодирует селектируемый или поддающийся скринингу маркер или кодирует трансген. После попадания в клетку-хозяина вектор может реплицироваться независимо от хромосомной ДНК хозяина или одновременно с ней, и может образоваться несколько копий вектора и встроенной в него ДНК. Кроме того, вектор также может содержать необходимые элементы, которые обеспечивают транскрипцию встроенной ДНК в молекулу мРНК или иным образом обусловливают репликацию встроенной ДНК в множественные копии РНК. Векторы могут дополнительно содержать "последовательности контроля экспрессии", которые регулируют экспрессию представляющего интерес гена. Обычно последовательности контроля экспрессии представляют собой полипептиды или полинуклеотиды, такие как без ограничения промоторы, энхансеры, сайленсеры, инсуляторы или репрессоры. В векторе, содержащем более одного полинуклеотида, кодирующего один или более представляющих интерес генных продуктов, экспрессию можно контролировать вместе или по отдельности с помощью одной или более последовательностей контроля экспрессии. Более конкретно, каждый полинуклеотид, содержащийся в векторе, может находиться под контролем отдельной последовательности контроля экспрессии, или все полинуклеотиды, содержащиеся в векторе, могут находиться под контролем одной последовательности контроля экспрессии. Полинуклеотиды, содержащиеся в одном векторе, контролируемом одной последовательностью контроля экспрессии, могут образовывать открытую рамку считывания. Некоторые векторы экспрессии дополнительно содержат элементы последовательности, смежные со встроенной ДНК, которые увеличивают время полужизни экспрессированной мРНК и/или обеспечивают трансляцию мРНК в молекулу белка. Таким образом, можно быстро синтезировать множество молекул мРНК и полипептида, кодируемых встроенной ДНК.
[00255] Используемый в данном документе термин "клетка-хозяин" относится к клетке, в которую был введен рекомбинантный вектор экспрессии. Подразумевается, что рекомбинантная клетка-хозяин или клетка-хозяин относятся не только к конкретной рассматриваемой клетке, но также и потомству такой клетки. Поскольку в последующих поколениях могут возникать определенные модификации вследствие либо мутации, либо влияний окружающей среды, такое потомство в действительности может не быть идентичным родительской клетке, но такие клетки по-прежнему включены в объем термина "клетка-хозяин", используемого в данном документе. Для экспрессии связывающих белков в клетке-хозяине можно применять самые разнообразные системы экспрессии, в том числе системы экспрессии на основе бактерий, дрожжей, бакуловирусов и клеток млекопитающих (а также системы экспрессии на основе фагового дисплея). Примером подходящего бактериального вектора экспрессии является pUC19. Для рекомбинантной экспрессии связывающего белка клетку-хозяина трансформируют или трансфицируют одним или более рекомбинантными векторами экспрессии, несущими фрагменты ДНК, кодирующие полипептидные цепи связывающего белка, так что полипептидные цепи экспрессируются в клетке-хозяине и в иллюстративных вариантах осуществления секретируются в среду, в которой культивируются клетки-хозяева, при этом связывающий белок можно извлекать из данной среды.
[00256] Используемый в данном документе термин "фармацевтическая композиция" относится к соединению или композиции, способным индуцировать требуемый терапевтический эффект при правильном введении пациенту.
[00257] Используемый в данном документе термин "фармацевтически приемлемый носитель" или "физиологически приемлемый носитель" относится к одному или более веществам состава, подходящим для осуществления или улучшения доставки связывающего белка.
[00258] Термины "эффективное количество" и "терапевтически эффективное количество" при использовании в отношении фармацевтической композиции, содержащей один или более связывающих белков (например, антитела или их антигенсвязывающие фрагменты), относятся к количеству или дозировке, достаточным для получения требуемого терапевтического результата. Более конкретно, терапевтически эффективное количество представляет собой количество связывающего белка (например, антитела или его антигенсвязывающего фрагмента), достаточное для подавления в течение некоторого периода времени одного или более клинически определенных патологических процессов, ассоциированных с состоянием, подлежащим лечению. Эффективное количество может меняться в зависимости от конкретного антителоподобного связывающего белка, подлежащего применению, а также зависит от ряда факторов и состояний, связанных с пациентом, подлежащим лечению, и тяжестью нарушения. Например, если связывающий белок или мультиспецифический связывающий белок подлежат введению in vivo, в число таких учитываемых факторов будут входить такие факторы, как возраст, масса тела и состояние здоровья пациента, а также кривые зависимости "доза-эффект" и данные о токсичности, полученные в доклиническом исследовании на животных. Определение эффективного количества или терапевтически эффективного количества указанной фармацевтической композиции находится в пределах компетенции специалистов в данной области техники.
[00259] Используемый в данном документе термин "способ получения связывающего белка" относится к рекомбинантным способам экспрессии белка с использованием методик, хорошо известных в данной области техники.
КОМПОНЕНТЫ ПСЕВДО-FAB
[00260] В определенных вариантах осуществления связывающая молекула, описанная в данной документе, содержит по меньшей мере один компонент псевдо-Fab. Используемый в данном документе компонент "псевдо-Fab" является аналогичным компоненту Fab традиционного антитела в том, что он содержит функциональную антигенсвязывающую часть, образованную спариванием вариабельного домена легкой цепи (VL) с вариабельной областью тяжелой цепи (VH). Однако, если домены VL и VH традиционного Fab слиты или связаны непосредственно с константным доменом легкой цепи (CL) и константным доменом 1 тяжелой цепи (CH1) соответственно, компонент псевдо-Fab не содержит домены CH1 и CL. Вместо этого домены VL и VH псевдо-Fab функционально связаны со второй парой стабилизированных нокаутных доменов VL и VH (обозначенных в данном документе как VLX и VHX), которые образуют неактивную или нефункциональную связывающую часть (в данном случае "стабилизированную нокаутную" часть или домен), которая не способна специфически связываться с целевым антигеном (например, с любым целевым антигеном). В определенных вариантах осуществления компонент псевдо-Fab не способен связывать целевой антиген соответствующего компонента Fab, из которого он получен. Компонент псевдо-Fab не содержит домены CH и CL.
[00261] Хотя домены VLX и VHX псевдо-Fab не могут селективно связываться с целевым антигеном, они, тем не менее, предпочтительно ассоциируют друг с другом с образованием стабильного спаривания цепей. Следовательно, путем присоединения псевдо-Fab к одному или более дополнительным связывающим доменам отличающейся специфичности собственная стабильность спаривания цепей VLX/VHX у псевдо-Fab может управлять гетеродимеризацией цепей требуемой мультиспецифической связывающей молекулы.
[00262] Соответственно, псевдо-Fab по настоящему изобретению содержит или состоит из первой полипептидной цепи, имеющей структуру, представленную формулой:
VHa-L1-VHX или
VHb-L1-VHX,
и второй полипептидной цепи, имеющей структуру, представленную формулой:
VLa-L2-VLX или
VLb-L2-VLX,
где
VHX связывается с VLX с образованием нокаутного домена,
VH связывается с VL с образованием первого функционального антигенсвязывающего домена, и
L1 и L2 представляют собой линкеры, которые могут присутствовать или отсутствовать.
[00263] В определенных вариантах осуществления первая полипептидная цепь псевдо-Fab имеет структуру VH-L1-VHX, а вторая полипептидная цепь псевдо-Fab имеет структуру VL-L2-VLX.
[00264] В других вариантах осуществления первый полипептид псевдо-Fab имеет структуру VHX-L1-VH, а вторая полипептидная цепь имеет структуру VLX-L2-VL.
[00265] В некоторых вариантах осуществления связывающий белок содержит отдельные белковые цепи, выбранные из одной из следующих групп:
(a) VHa-CH1-L1-VHb-L2-VHX, и VLa-CL, и VLb-L3-VLX;
(b) VHa-L2-VHX-L1-VHb-CH1, и VLa-L3-VLX, и VLb-CL;
(c) VHa-CH1-L1-VHa-CH1, и VHb-L2-VHX-L3-VHb-L4-VHX, и две цепи VLb-L5-VLX, и две цепи VLa-CL;
где цепи (а) и (b) могут присутствовать один раз или дважды, и где L1, L2, L3, L4 и L5 представляют собой линкеры, которые независимо могут быть одинаковыми или разными.
(a) Нокаутные домены
[00266] "Нокаутный" домен псевдо-Fab может быть получен любым способом, который приводит к отмене или уменьшению аффинности связывания или специфичности нормального функционального антигенсвязывающего участка. В некоторых вариантах осуществления нокаутный домен псевдо-Fab стал неактивным или нефункциональным за счет одной или мутаций в одном или обоих доменах VLX и VHX нокаутного домена. В одном варианте осуществления нокаутная модификация представляет собой аминокислотную замену. В других вариантах осуществления нокаутная модификация представляет собой аминокислотную вставку или делецию. В другом варианте осуществления нокаутная модификация представляет собой комбинацию одной или более аминокислотных замен, аминокислотных вставок и аминокислотных делеций. В других вариантах осуществления нокаутный домен становится нефункциональным за счет ковалентной модификации, например, с помощью компонента, который препятствует способности вариабельного домена связывать целевой антиген.
[00267] В определенных вариантах осуществления нокаутная модификация устраняет связывание за счет создания отталкивания или разрушения комплексов стабилизированных антигенсвязывающих белков. В определенных вариантах осуществления нокаутная модификация может включать замещение остатка, который в норме образует контакт с целевым антигеном, аминокислотой, которая создает отталкивание заряд-заряд с целевым антигеном. В качестве дополнения или альтернативы можно вводить мутации, которые дестабилизируют комплексы pi-pi-взаимодействий.
[00268] В определенных вариантах осуществления нокаутная модификация представляет собой замену заряженной аминокислоты незаряженной аминокислотой. В других вариантах осуществления нокаутная модификация представляет собой замену незаряженной аминокислоты заряженной аминокислотой. В других вариантах осуществления нокаутная модификация представляет собой замену полярной аминокислоты неполярной аминокислотой. В других вариантах осуществления нокаутная модификация представляет собой замену заряженных аминокислот полярными и незаряженными аминокислотами, и полярных незаряженных аминокислот неполярными гидрофобными аминокислотами.
[00269] В определенных вариантах осуществления нокаутную модификацию вводят в положение аминокислоты, которая образует связывающее взаимодействие с антигеном. Например, нокаутная модификация может быть расположена на поверхности белка, где в норме происходит взаимодействие антиген-антитело. В определенных иллюстративных вариантах осуществления модификации могут быть введены в определяющие комплементарность области (CDR) одного или обоих доменов VLX или VHX.
[00270] В определенных вариантах осуществления нокаутная модификация представляет собой замену остатка в CDRH1 домена VHX. В другом варианте осуществления нокаутная модификация представляет собой замену остатка в CDRH2 домена VHX. В другом варианте осуществления нокаутная модификация представляет собой замену остатка в CDRH3 домена VHX.
[00271] В определенных вариантах осуществления нокаутная модификация представляет собой замену остатка в CDRL1 домена VLX. В другом варианте осуществления нокаутная модификация представляет собой замену остатка в CDRL2 домена VLX. В другом варианте осуществления нокаутная модификация представляет собой замену остатка в CDRL3 домена VLX.
[00272] В некоторых иллюстративных вариантах осуществления аргинин в CDR доменов VHX или VLX подвергнуты мутации в глутамат. В других вариантах осуществления один или более остатков тирозина в CDR домена VHX или VLX подвергнуты мутации в аланин.
[00273] В определенных вариантах осуществления модификация приводит к образованию нокаутного домена, который полностью лишен активности связывания целевого антигена, присущей функциональному ненокаутному (т.е. дикого типа) аналогу, из которого он получен. В качестве альтернативы функциональность связывания у нокаутного домена может быть существенно снижена по сравнению с его функциональным ненокаутным аналогом, хотя при этом сохраняется некоторый уровень детектируемого связывания.
[00274] Каркасы для создания нокаутных доменов можно получить, например, из Базы данных структуры белков (PDB). PDB представляет собой базу кристаллографических данных, содержащую данные по трехмерной структуре крупных биологических молекул, таких как белки и нуклеиновые кислоты. Нокаутные домены можно получать за счет введения специфических мутаций аминокислот, которые, как предполагается, вовлечены в связывание антигена, путем компьютерного моделирования антигенсвязывающего домена и родственного ему целевого антигена. Последующие исследования по связыванию можно проводить с использованием методов, известных в данной области техники, например, поверхностного плазмонного резонанса, и выявлять с высокой точностью, устранилась ли функция связывания и нарушено ли взаимодействие между связывающим доменом и его мишенью.
(b) Стабилизированные нокаутные домены
[00275] В определенных вариантах осуществления нокаутный домен представляет собой стабилизированный нокаутный домен, характеризующийся повышенной термостабильностью по сравнению с его аналогом дикого типа. Например, в определенных иллюстративных вариантах осуществления температура плавления (Tm) нокаутного домена находится в пределах по меньшей мере 0,25°C, по меньшей мере 0,5°C, по меньшей мере 0,75°C, по меньшей мере 1°C, по меньшей мере 2°C, по меньшей мере 3°C, по меньшей мере 4°C, по меньшей мере 5°C или по меньшей мере 10°C относительно аналога дикого типа, из которого он получен. В других иллюстративных вариантах осуществления Tm нокаутного домена увеличена по сравнению с его аналогом дикого типа. Например, Tm может быть увеличена на по меньшей мере 0,25°C, по меньшей мере 0,5°C, по меньшей мере 0,75°C, по меньшей мере 1°C, по меньшей мере 2°C, по меньшей мере 3°C, по меньшей мере 4°C, по меньшей мере 5°C или по меньшей мере 10°C по сравнению с аналогом дикого типа, из которого он получен. Термостабильность можно измерять с помощью дифференциальной сканирующей флуориметрии (DSF) или других биоаналитических методов, обычно используемых специалистами в данной области техники.
[00276] В определенных вариантах осуществления псевдо-Fab содержит сконструированную внутрицепочечную дисульфидную связь между доменами VHX или VLX нокаутного домена псевдо-Fab, которая придает повышенную стабильность. Обычно данная модификация представляет собой замену по меньшей мере одной аминокислоты домена VHX остатком цистеина (Cys) и по меньшей мере одной аминокислоты в домене VLX остатком Cys. Остатки Cys могут быть введены в положения доменов VHX и VLX, которые обеспечивают возможность образования дисульфидной связи после образования димера. В определенных вариантах осуществления для повышения стабильности между поверхностью контакта VH/VL мутации могут быть введены в поверхность контакта VH и VL. Специфические совокупности аминокислотных мутаций в домене VH и доменах VL могут улучшать стабильность благодаря введению ненативных остатков цистеина, которые образуют дисульфидные мостики.
[00277] Первая совокупность мутаций стабилизации дисульфидом может быть введена в аминокислотные остатки в доменах VH и VL. В иллюстративном варианте осуществления дисульфидная связь образована Cys в положении 44 домена VHX и Cys в положении 100 домена VLX. Данная совокупность мутаций стабилизации дисульфидом в качестве альтернативы может называться совокупностью мутаций "VH44C/VL100C". Первая совокупность мутаций стабилизации дисульфидом более подробно описана в Reiter et al. Nature Biotechnology. Vol. 14. Pp. 1239-1245. 1996, включенном в данном документе посредством ссылки для всех целей.
[00278] Вторая совокупность мутации стабилизации дисульфидом может быть введена в аминокислотные остатки в домене VH и VL. В иллюстративном варианте осуществления дисульфидная связь образована Cys в положении 105 домена VHX и Cys в положении 43 домена VLX. Вторая совокупность мутаций стабилизации дисульфидом в качестве альтернативы может называться совокупностью мутаций "VH105C/VL43C". Другие мутации стабилизации дисульфидом более подробно описаны в патенте США № 9527927, который включен в данном документе посредством ссылки для всех целей.
[00279] В некоторых вариантах осуществления домен VLX псевдо-Fab содержит вариант SEQ ID NO: 1 с по меньшей мере одной нокаутной модификацией. Например, домен VLX может содержать аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% или на 100% идентична аминокислотной последовательности под SEQ ID NO: 1, за исключением нокаутной модификации.
[00280] В некоторых вариантах осуществления домен VHX псевдо-Fab содержит вариант SEQ ID NO: 2 с по меньшей мере одной нокаутной модификацией. Например, домен VHX может содержать аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% или на 100% идентична аминокислотной последовательности под SEQ ID NO: 2, за исключением нокаутной модификации.
[00281] В одном варианте осуществления домен VLX псевдо-Fab содержит аминокислотную последовательность под SEQ ID NO: 76, и домен VHX псевдо-Fab содержит аминокислотную последовательность, выбранную из группы из SEQ ID NO: 77, SEQ ID NO: 78 и SEQ ID NO: 79.
МУЛЬТИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ ПОЛИПЕПТИДЫ, СОДЕРЖАЩИЕ ПСЕВДО-FAB
[00282] В других аспектах предусмотрены мультиспецифические связывающие белки, содержащие компонент псевдо-Fab, описанный в данном документе. В высшей степени модульная природа компонента псевдо-Fab позволяет осуществлять получение самых разнообразных мультиспецифических структур.
[00283] В определенных вариантах осуществления мультиспецифические связывающие белки по настоящему описанию содержат дополнительные специфичности связывания, присоединенные к N-концу и/или C-концу одной или обеих цепей компонента псевдо-Fab с образованием мультивалентного связывающего белка, содержащего псевдо-Fab.
[00284] В некоторых вариантах осуществления мультиспецифический связывающий белок содержит:
a) первую псевдо-Fab-часть, содержащую:
(1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого антигенсвязывающего участка, который связывает целевой антиген A;
(2) первый стабилизированный нокаутный домен VL (VLX), спаренный с первым стабилизированным нокаутным доменом VH (VHX) с образованием первого стабилизированного дисульфидом нокаутного домена (dsKO);
(3) первый домен гетеродимеризации (HD1);
где первый домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей;
b) первую Fab-часть, содержащую
(1) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(2) первый домен CH1, спаренный с первым доменом CL; и
(3) второй домен гетеродимеризации (HD2).
[00285] В некоторых вариантах осуществления первый и второй домены гетеродимеризации связывающего белка содержат первый и второй домены Fc. В некоторых вариантах осуществления домены Fc содержат общую структуру шарнир-домен CH2-домен CH3.
(a) Домены Fc-гетеродимеризации
[00286] В определенных вариантах осуществления мультиспецифические связывающие белки по настоящему описанию могут дополнительно содержать домен Fc-гетеродимеризации C1 или C2. В некоторых вариантах осуществления домен Fc-гетеродимеризации выбран из группы, состоящей из гетеродимеризующегося Fc или его фрагментов, в частности, варианта Fc-части с мутацией типа "выступ-во-впадину" (KIH) и его вариантов с модифицированной эффекторной функцией, или гетеродимеризующегося Fc или его фрагментов, в частности варианта Fc EV-RWT и его вариантов с модифицированной эффекторной функцией. В некоторых вариантах осуществления Fc содержит одну или более аминокислотных мутаций. Одной из возможностей является удаление участка селективного распознавания для первого аффинного реагента, например, за счет введения мутаций, выбранных из группы, состоящей из H435R, Y436F, и введения участка селективного распознавания для второго аффинного реагента. В качестве альтернативы может только вводиться участок селективного распознавания для второго аффинного реагента.
(b) Домены гомодимеризации
[00287] В определенных вариантах осуществления мультиспецифические связывающие белки по настоящему описанию могут дополнительно содержать домен гомодимеризации. В некоторых вариантах осуществления домен гомодимеризации выбран из группы, состоящей из области Fc и ее вариантов с модифицированной эффекторной функцией; одного или более доменов CH2, например, из IgG, IgE или IgM; одного или более доменов CH3, например, из IgG, IgA или IgD; и одного или более доменов CH4, например, из IgE или IgM..
Мультимерные связывающие белки, содержащие псевдо-Fab
(a) Симметричные тетравалентные конструкции
[00288] В другом варианте осуществления связывающий полипептид включает связывающий белок, содержащий псевдо-Fab, который содержит дополнительные полипептидные цепи, которые связываются с полипептидными цепями псевдо-Fab с образованием дополнительных связывающих доменов. Данные связывающие полипептиды, содержащие псевдо-Fab, дополнительно слиты с доменом Fc-гетеродимеризации с образованием одной половины традиционного Y-образного антитела.
[00289] В некоторых вариантах осуществления антигенсвязывающий белок содержит шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00290] Данные молекулы также могут называться "тандемная молекула (Fv-псевдо-Fab x Fv-Fab)" (см. фиг. 10B).
[00291] В некоторых вариантах осуществления антигенсвязывающий белок содержит шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00292] Данные молекулы также могут называться "тандемная молекула (Fv-Fab x Fv-псевдо-Fab-IgG)" (см. фиг. 10A).
(b) Асимметричные тетраспецифические молекулы
[00293] Димеризация связывающих полипептидов, где только один из них содержит псевдо-Fab, приводит к асимметричным конструкциям с дополнительными специфичностями. Данные связывающие полипептиды, содержащие псевдо-Fab, дополнительно слиты с доменом Fc-гетеродимеризации с образованием одной половины традиционного полноразмерного Y-образного антитела IgG.
[00294] В некоторых вариантах осуществления мультиспецифический связывающий белок содержит четыре полипептидные цепи, которые образуют по меньшей мере два антигенсвязывающих участка, где
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHb-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1 и L2 представляют собой аминокислотные линкеры, которые независимо могут быть одинаковыми или разными,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00295] Данные молекулы также могут называться димерными биспецифическими молекулами IgG (Fv-псевдо-Fab) x (Fv-Fab)-Fc (см.фиг. 2 и 7).
[00296] В другом варианте осуществления связывающий полипептид предусматривает связывающий белок, содержащий псевдо-Fab, который содержит дополнительные полипептидные цепи, которые связываются с полипептидными цепями псевдо-Fab с образованием дополнительных связывающих доменов. Данные связывающие полипептиды, содержащие псевдо-Fab, дополнительно слиты с доменом Fc-гетеродимеризации с образованием одной половины традиционного Y-образного антитела. Димеризация таких молекул приводит к конструкциям с дополнительными специфичностями.
[00297] В некоторых вариантах осуществления антигенсвязывающий белок содержит шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHa-L4-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L5-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4 и L5 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где домены dsKO содержат (i) одну или более инактивирующих мутаций, которые устраняют их связывание с целевым антигеном; (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00298] С-концевой домен гетеродимеризации может представлять собой традиционный домен Fc-гетеродимеризации с мутацией типа "выступ-во-впадину", традиционный домен Fc-RF-гетеродимеризации или их комбинации. Данные молекулы также могут называться "Fv-псевдо-Fab([HC]-(Fv-псевдо-Fab)) x ((Fv-Fab)[HC]-(Fv-Fab)))-Fc" (см. фиг. 11).
[00299] В некоторых вариантах осуществления антигенсвязывающий белок содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где:
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-L3-VLc-L4-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHc-L5-VHb-L6-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VLc представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VHc представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4, L5 и L6 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) третий домен VL (VLc) спарен с третьим доменом VH (VHc) с образованием третьего функционального антигенсвязывающего участка, который связывает целевой антиген C;
(4) полипептид формулы III и полипептид формулы IV образуют кроссоверную пару легкая цепь-тяжелая цепь (CODV);
(5) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного домена (dsKO2);
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00300] В некоторых вариантах осуществления антигенсвязывающий белок содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где:
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-L3-VLc-L4-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHc-L5-VHb-L6-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VLc представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VHc представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4, L5 и L6 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) третий домен VL (VLc) спарен с третьим доменом VH (VHc) с образованием третьего функционального антигенсвязывающего участка, который связывает целевой антиген C;
(4) полипептид формулы III и полипептид формулы IV образуют кроссоверную пару легкая цепь-тяжелая цепь (CODV);
(5) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного домена (dsKO2);
где домен dsKO содержит (i) одну или более инактивирующих мутаций, которые устраняют его связывание с целевым антигеном относительно эталонной молекулы Fab; и (ii) одну или более сконструированных межцепочечных дисульфидных связей.
[00301] Данные молекулы также могут называться "(CODV-Fab ) x (псевдо-Fab)-Fc" (см. фиг. 13).
[00302] В конкретных вариантах осуществления первого и второго аспектов настоящего изобретения связывающий белок содержит пару легкой цепи и тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 6 и 7; SEQ ID NO: 8 и 9; SEQ ID NO: 10 и 11; SEQ ID NO: 12 и 13; SEQ ID NO: 14 и 15; SEQ ID NO: 16 и 17; SEQ ID NO: 18 и 19; SEQ ID NO: 20 и 21; SEQ ID NO: 22 и 23; SEQ ID NO: 24 и 25; SEQ ID NO: 26 и 27; SEQ ID NO: 28 и 29; SEQ ID NO: 30 и 31; SEQ ID NO: 32 и 33; SEQ ID NO: 34 и 35; SEQ ID NO: 36 и 37; SEQ ID NO: 38 и 39; SEQ ID NO: 40 и 41; SEQ ID NO: 42 и 43; SEQ ID NO: 44 и 45; SEQ ID NO: 46 и 47 и SEQ ID NO: 48 и 49; SEQ ID NO: 50 и 51; SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55; SEQ ID NO: 56 и 57 и SEQ ID NO: 58 и 59; SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63; SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67; SEQ ID NO: 68 и 69 и SEQ ID NO: 70 и 71; SEQ ID NO: 72 и 73; и SEQ ID NO: 74 и 75.
[00303] В некоторых вариантах осуществления первый и второй CL независимо выбраны из группы, состоящий из константной области легкой каппа-цепи (CLκ) и константной области легкой лямбда-цепи (CLλ).
[00304] В некоторых вариантах осуществления каждый из HD1 и HD2 содержит область Fc и ее варианты с модифицированной эффекторной функцией; гетеродимеризирующуюся Fc-часть, в частности, вариант Fc-части с мутацией типа "выступ-во-впадину" (KIH) и ее варианты с модифицированной эффекторной функцией; один или более доменов CH2, например, из IgG, IgE или IgM, один или более доменов CH3, например, из IgG, IgA или IgD, или один или более доменов CH4, например, из IgE или IgM.
[00305] В некоторых вариантах осуществления один из доменов Fc содержит первый домен CH3, содержащий одну или обе из мутаций S354C и T366W, а другой домен Fc содержит второй домен CH3, содержащий одну или обе из мутаций Y349C, T366S, L368A и Y407V.
[00306] В одном варианте осуществления область Fc в HD1 или HD2 содержит одну или более аминокислотных мутаций, которые приводят к удалению участка селективного распознавания для второго аффинного реагента, например, выбранную из группы, состоящей из H435R или Y436F, или приводят к введению участка селективного распознавания для третьего аффинного реагента.
Таблица 2. Последовательности выбранных связывающих белков
SEQ ID NO:1
SEQ ID NO:2
SEQ ID NO: 3
SEQ ID NO: 4
SEQ ID NO: 5
(SEQ ID NO: 6)
(SEQ ID NO: 7)
(SEQ ID NO: 8)
(SEQ ID NO: 9)
(SEQ ID NO: 10)
(SEQ ID NO: 11)
(SEQ ID NO: 12)
(SEQ ID NO: 13)
(SEQ ID NO: 14)
(SEQ ID NO: 15)
(SEQ ID NO: 16)
(SEQ ID NO: 17)
(SEQ ID NO: 18)
(SEQ ID NO: 19)
(SEQ ID NO: 20)
(SEQ ID NO: 21)
(SEQ ID NO: 22)
(SEQ ID NO: 23)
(SEQ ID NO: 24)
(SEQ ID NO: 25)
(SEQ ID NO: 26)
(SEQ ID NO: 27)
(SEQ ID NO: 28)
(SEQ ID NO: 29
(SEQ ID NO: 30)
(SEQ ID NO: 31)
(SEQ ID NO: 32)
(SEQ ID NO: 33)
(SEQ ID NO: 34)
(SEQ ID NO: 35)
(SEQ ID NO: 36)
(SEQ ID NO: 37)
(SEQ ID NO: 38)
(SEQ ID NO: 39)
(SEQ ID NO: 40)
(SEQ ID NO: 41)
(SEQ ID NO: 42)
(SEQ ID NO: 43)
(SEQ ID NO: 44)
(SEQ ID NO: 45)
(SEQ ID NO: 46)
(SEQ ID NO: 47)
(SEQ ID NO: 48)
(SEQ ID NO: 49)
(SEQ ID NO: 50)
(SEQ ID NO: 51)
(SEQ ID NO: 52)
(SEQ ID NO: 53)
(SEQ ID NO: 54)
(SEQ ID NO: 55)
(SEQ ID NO: 56)
(SEQ ID NO: 57)
(SEQ ID NO: 58)
(SEQ ID NO: 59)
(SEQ ID NO: 60)
(SEQ ID NO: 61)
(SEQ ID NO: 62)
(SEQ ID NO: 63)
(SEQ ID NO: 64)
(SEQ ID NO: 65)
(SEQ ID NO: 66)
(SEQ ID NO: 67)
(SEQ ID NO: 68)
(SEQ ID NO: 69)
(SEQ ID NO: 70)
(SEQ ID NO: 71)
(SEQ ID NO: 72)
(SEQ ID NO: 73)
(SEQ ID NO: 74)
(SEQ ID NO: 75)
SEQ ID NO:76
SEQ ID NO: 77
SEQ ID NO: 78
SEQ ID NO: 79
Таблица 3. Последовательности биспецифических антител-активаторов Т-клеток
Последовательность
Последовательность
Последовательность
Последовательность
антитело к TCR α/β x антитело к CD123
дикий тип
SEQ ID NO: 80
антитело к TCR α/β x антитело к CD123-dsTrasKO2
SEQ ID NO: 81
антитело к TCR α/β-dsTrasKO2
x антитело к CD123
SEQ ID NO: 82
антитело к CD3ε x антитело к CD123
дикий тип
SEQ ID NO: 83
антитело к CD3ε x антитело к CD123-dsTrasKO2
SEQ ID NO: 84
антитело к CD3ε-dsTrasKO2 x антитело к CD123
SEQ ID NO: 85
антитело к CD3ε x антитело к CD123
дикий тип
SEQ ID NO: 86
антитело к CD3ε x антитело к CD123-dsTrasKO2
SEQ ID NO: 87
антитело к CD3ε-dsTrasKO2 x антитело к CD123
SEQ ID NO: 88
антитело к TCR α/β x антитело к TNP
отрицательный контроль
дикий тип
SEQ ID NO: 89
антитело к TCR α/β x антитело к TNP-dsTrasKO2
отрицательный контроль
SEQ ID NO: 90
антитело к TCR α/β-dsTrasKO2 x антитело к TNP
отрицательный контроль
SEQ ID NO: 91
антитело к TNP x антитело к CD123
отрицательный контроль
дикий тип
SEQ ID NO: 92
антитело к TNP x антитело к CD123-dsTrasKO2
отрицательный контроль
SEQ ID NO: 93
антитело к TNP-dsTrasKO2 x антитело к CD123
отрицательный контроль
SEQ ID NO: 94
антитело к CD3ε x антитело к TNP
отрицательный контроль
дикий тип
SEQ ID NO: 95
антитело к CD3ε x антитело к TNP-dsTrasKO2
отрицательный контроль
SEQ ID NO: 96
антитело к CD3ε-dsTrasKO2 x антитело к TNP
отрицательный контроль
SEQ ID NO: 97
антитело к CD3ε x антитело к TNP
отрицательный контроль
дикий тип
SEQ ID NO: 98
антитело к CD3ε x антитело к TNP-dsTrasKO2
отрицательный контроль
SEQ ID NO: 99
антитело к CD3ε-dsTrasKO2
x антитело к TNP
отрицательный контроль
SEQ ID NO: 100
(e) Нуклеиновые кислоты
[00307] В пятом аспекте настоящее изобретение относится к выделенной молекуле нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую псевдо-Fab, содержащий один или оба из связывающего белка и мультиспецифического связывающего белка по первому, второму или третьему аспекту настоящего изобретения.
[00308] Один аспект настоящего изобретения относится к полинуклеотиду, кодирующему связывающий белок по любому из первого - третьего аспектов настоящего изобретения.
[00309] Стандартные технологии рекомбинантной ДНК применяют для конструирования полинуклеотидов, которые кодируют полипептиды, образующие связывающие белки, встраивания этих полинуклеотидов в рекомбинантные векторы экспрессии и введения таких векторов в клетки-хозяева. См. например, Sambrook et al., 2001, MOLECULAR CLONING: A LABORATORY MANUAL (Cold Spring Harbor Laboratory Press, 3rd ed.). Ферментативные реакции и методики очистки можно проводить в соответствии со спецификациями производителей, которые обычно выполняют в данной области техники или как описано в данном документе. Если не предусмотрены конкретные определения, то терминология, используемая в контексте аналитической химии, химии органического синтеза и медицинской и фармацевтической химии, а также их лабораторные процедуры и методики, описанные в данном документе, являются общеизвестными и широко используемыми в данной области техники. Аналогично, традиционные методики можно применять при химических синтезах, химических анализах, фармацевтическом получении, составлении, доставке и лечении пациентов.
[00310] Другие аспекты настоящего изобретения относятся к выделенным молекулам нуклеиновой кислоты, содержащим нуклеотидную последовательность, кодирующую любой из связывающих белков, описанных в данном документе. В некоторых вариантах осуществления пятого аспекта настоящего изобретения выделенные молекулы нуклеиновой кислоты содержат последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99%, или 100% идентична нуклеиновой кислоте, кодирующей любой из связывающих белков, описанных в данном документе.
[00311] Определенные аспекты настоящего изобретения относятся к наборам полинуклеотидов. В некоторых вариантах осуществления один или более из полинуклеотидов представляют собой вектор (например, вектор экспрессии). Помимо прочего, наборы могут найти применение в получении одного или более связывающих белков, описанных в данном документе, например, домена гетеродимеризации, бивалентного, тривалентного, тетравалентного или мультивалентного связывающего белка по настоящему раскрытию.
[00312] В некоторых вариантах осуществления выделенная нуклеиновая кислота функционально связана с гетерологичным промотором для управления транскрипцией последовательности нуклеиновой кислоты, кодирующей связывающий белок. Промотор может относиться к последовательностям контроля нуклеиновой кислоты, которые управляют транскрипцией нуклеиновой кислоты. Первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты, если первая последовательность нуклеиновой кислоты находится в функциональной взаимосвязи со второй последовательностью нуклеиновой кислоты. Например, промотор функционально связан с кодирующей последовательностью связывающего белка, если промотор воздействует на транскрипцию или экспрессию кодирующей последовательности. Примеры промоторов могут включать без ограничения промоторы, полученные из геномов вирусов (таких как вирус полиомы, вирус оспы кур, аденовирус (такой как аденовирус 2), вирус папилломы крупного рогатого скота, вирус саркомы птиц, цитомегаловирус, ретровирус, вирус гепатита B, вирус обезьян 40 (SV40) и т. п.), гетерологичные промоторы эукариот (такие как промотор актина, промотор иммуноглобулина, промоторы белков теплового шока и т. п.), CAG-промотор (Niwa et al., Gene 108(2):193-9, 1991), промотор фосфоглицераткиназы (PGK), индуцируемый тетрациклином промотор (Masui et al., Nucleic Acids Res. 33:e43, 2005), lac-систему, trp-систему, tac-систему, trc-систему, основные операторные и промоторные области фага лямбда, промотор гена 3-фосфоглицераткиназы, промоторы гена кислой фосфатазы дрожжей и промотор гена альфа-факторов спаривания дрожжей. Полинуклеотиды, кодирующие связывающие белки по настоящему изобретению, могут находиться под контролем конститутивного промотора, индуцируемого промотора или любого другого подходящего промотора, описанного в данном документе, или другого подходящего промотора, который легко распознает специалист в данной области техники.
[00313] В некоторых вариантах осуществления выделенную нуклеиновую кислоту встраивают в вектор. В некоторых вариантах осуществления вектор представляет собой вектор экспрессии. Векторы экспрессии могут содержать одну или более регуляторных последовательностей, функционально связанных с полинуклеотидом, подлежащим экспрессии. Используемый в данном документе термин "регуляторная последовательность" включает промоторы, энхансеры и другие элементы контроля экспрессии (например, сигналы полиаденилирования). Примеры подходящих энхансеров могут включать без ограничения энхансерные последовательности из генов млекопитающих (таких как гены глобина, эластазы, альбумина, α-фетопротеина, инсулина и т. п.) и энхансерные последовательности из вируса эукариотических клеток (такие как энхансер SV40 на участке позднего начала репликации (100-270 п. о.), ранний промотор/энхансер цитомегаловируса, энхансер полиомы на участке позднего начала репликации, энхансеры аденовирусов и т. п.). Примеры подходящих векторов могут включать, например, плазмиды, космиды, эписомы, транспозоны и вирусные векторы (например, векторы на основе аденовируса, вируса коровьей оспы, вируса Синдбиса, вируса кори, вируса герпеса, лентивируса, ретровируса, аденоассоциированного вируса и т. д.). Векторы экспрессии можно применять для трансфекции клеток-хозяев, таких как, например, клетки бактерий, клетки дрожжей, клетки насекомых и клетки млекопитающих. Биологически функциональные векторы на основе ДНК вируса и плазмидной ДНК, способные экспрессироваться и реплицироваться в хозяине, известны в данной области техники и могут применяться для трансфекции любой клетки, представляющей интерес.
[00314] В шестом аспекте настоящее изобретение относится к вектору экспрессии, содержащему молекулу нуклеиновой кислоты по пятому аспекту настоящего изобретения.
[00315] Другие аспекты настоящего изобретения относятся к векторной системе, содержащей один или более векторов, кодирующих первую, вторую, третью и четвертую полипептидную цепь любого из связывающих белков, описанных в данном документе. В некоторых вариантах осуществления шестого аспекта настоящего изобретения векторная система содержит первый вектор, кодирующий первую полипептидную цепь связывающего белка, второй вектор, кодирующий вторую полипептидную цепь связывающего белка, третий вектор, кодирующий третью полипептидную цепь связывающего белка, и четвертый вектор, кодирующий четвертую полипептидную цепь связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и вторую полипептидные цепи связывающего белка, и второй вектор, кодирующий третью и четвертую полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и третью полипептидные цепи связывающего белка, и второй вектор, кодирующий вторую и четвертую полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и четвертую полипептидные цепи связывающего белка, и второй вектор, кодирующий вторую и третью полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую, вторую, третью и четвертую полипептидные цепи связывающего белка. Один или более векторов векторной системы могут представлять собой любые из векторов, описанных в данном документе. В некоторых вариантах осуществления один или более векторов представляют собой векторы экспрессии.
(f) Выделенные клетки-хозяева
[00316] В седьмом аспекте настоящее изобретение относится к выделенной клетке-хозяину, содержащей молекулу нуклеиновой кислоты по пятому аспекту настоящего изобретения или вектор экспрессии по шестому аспекту настоящего изобретения.
[00317] Другие аспекты настоящего изобретения относятся к выделенной клетке-хозяину, содержащей один или более выделенных полинуклеотидов, наборов полинуклеотидов, векторов и/или векторных систем, описанных в данном документе. В некоторых вариантах осуществления седьмого аспекта настоящего изобретения клетка-хозяин представляет собой клетку бактерии (например, клетку E. coli). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку E. coli DH5α. В некоторых вариантах осуществления клетка-хозяин представляет собой клетку дрожжей (например, клетку S. cerevisiae). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку насекомого. Примеры клеток-хозяев насекомого могут включать, например, клетки Drosophila (например, клетки S2), клетки Trichoplusia ni (например, клетки High Five™) и клетки Spodoptera frugiperda (например, клетки Sf21 или Sf9). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку млекопитающего. Примеры клеток-хозяев, представляющих собой клетки млекопитающих, могут включать, например, клетки почки эмбриона человека (например, клетки 293 или клетки 293, субклонированные для роста в суспензионной культуре), клетки Expi293TM, клетки CHO, клетки почки новорожденного хомячка (например, BHK, ATCC CCL 10), клетки Сертоли мыши (например, клетки TM4), клетки почки обезьяны (например, CV1 ATCC CCL 70), клетки почки африканской зеленой мартышки (например, VERO-76, ATCC CRL-1587), клетки карциномы шейки матки человека (например, HELA, ATCC CCL 2), клетки почки собаки (например, MDCK, ATCC CCL 34), клетки печени крысы линии Buffalo (например, BRL 3A, ATCC CRL 1442), клетки легкого человека (например, W138, ATCC CCL 75), клетки печени человека (например, Hep G2, HB 8065), клетки опухоли молочной железы мыши (например, MMT 060562, ATCC CCL51), клетки TRI, клетки MRC 5, клетки FS4, линию клеток гепатомы человека (например, Hep G2), клетки миеломы (например, клетки NS0 и Sp2/0) и т. п.
Способы получения
1. Способы экспрессии
[00318] Другие аспекты настоящего изобретения относятся к способу получения любого из связывающих белков, описанных в данном документе. В некоторых вариантах осуществления способ включает:
a) культивирование клетки-хозяина (например, любой из клеток-хозяев, описанных в данном документе), содержащей выделенную нуклеиновую кислоту, вектор и/или векторную систему (например, любое из выделенных нуклеиновых кислот, векторов и/или векторных систем, описанных в данном документе), в условиях, при которых клетка-хозяин экспрессирует связывающий белок; и
b) выделение связывающего белка из клетки-хозяина. Способы культивирования клеток-хозяев в условиях, обеспечивающих экспрессию белка, хорошо известны среднему специалисту в данной области техники. Способы выделения белков из культивируемых клеток-хозяев хорошо известны среднему специалисту в данной области техники, в том числе, например, с помощью аффинной хроматографии (например, двухстадийной аффинной хроматографии, включающей аффинную хроматографию на белке A с последующей эксклюзионной хроматографией).
2. Способы очистки
[00319] В четвертом аспекте настоящее изобретение относится к способу очистки мультиспецифического связывающего белка по третьему аспекту настоящего изобретения, включающему стадии:
(i) нанесения раствора, содержащего мультиспецифический связывающий белок, на первый, второй или третий аффинный реагент, который специфически связывается с участком распознавания мультиспецифического связывающего белка для первого, второго или третьего аффинного реагента; и
(ii) выделения либо мультиспецифического связывающего белка, который не связывается с первым, вторым или третьим аффинным реагентом, либо мультиспецифического связывающего белка, который связывается с первым или третьим аффинным реагентом,
где каждый из первого, второго и третьего аффинных реагентов связывается с отличающимся участком узнавания мультиспецифического связывающего белка.
[00320] В некоторых вариантах осуществления способ включает дополнительные стадии нанесения раствора, содержащего мультиспецифический связывающий белок, выделенный на стадии (ii), на первый, второй или третий аффинный реагент, где аффинный реагент отличается от аффинного реагента, используемого на стадии (i), выделения либо мультиспецифического связывающего белка, который не связывается с первым, вторым или третьим аффинным реагентом, либо мультиспецифического связывающего белка, который связывается с первым или третьим аффинным реагентом.
[00321] В некоторых вариантах осуществления первый аффинный реагент связывается с Cκ; второй аффинный реагент представляет собой белок А; и/или третий аффинный реагент представляет собой белок G.
[00322] В некоторых вариантах осуществления связывающий белок по настоящему изобретению очищают с помощью аффинной хроматографии на белке A, аффинной хроматографии легких каппа-цепей (например, с использованием смолы KappaSelect в соответствии с инструкциями производителя; GE Healthcare) и необязательно аффинной хроматографии легких лямбда-цепей (например, с использованием смолы LambdaFabSelect в соответствии с инструкциями производителя; GE Healthcare). В некоторых вариантах осуществления связывающий белок по настоящему изобретению очищают с помощью аффинной хроматографии на белке A, аффинной хроматографии легких лямбда-цепей (например, с использованием смолы LambdaFabSelect в соответствии с инструкциями производителя; GE Healthcare) и необязательно аффинной хроматографии легких каппа-цепей (например, с использованием смолы KappaSelect в соответствии с инструкциями производителя; GE Healthcare). В некоторых вариантах осуществления связывающий белок содержит две области Fc, каждая из которых содержит домен CH3, и только один из доменов CH3 содержит аминокислотные замены в положениях, соответствующих положениям 435 и 436 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой H435R и Y436F. В некоторых вариантах осуществления связывающий белок согласно настоящему изобретению последовательно очищают с помощью аффинной хроматографии на белке A, затем аффинной хроматографии легких каппа-цепей (например, с использованием смолы KappaSelect в соответствии с инструкциями производителя; GE Healthcare), затем необязательно аффинной хроматографии легких лямбда-цепей (например, с использованием смолы LambdaFabSelect в соответствии с инструкциями производителя; GE Healthcare). В некоторых вариантах осуществления связывающий белок по настоящему изобретению очищают с помощью аффинной хроматографии на белке A, затем аффинной хроматографии легких лямбда-цепей (например, с использованием смолы LambdaFabSelect в соответствии с инструкциями производителя; GE Healthcare), затем необязательно аффинной хроматографии легких каппа-цепей (например, с использованием смолы KappaSelect в соответствии с инструкциями производителя; GE Healthcare). Например, в некоторых вариантах осуществления связывающий белок приводят в контакт с белком A, элюируют от белка A в условиях, подходящих для выделения связывающего белка из связывающих белков, содержащих 0 или 2 домена CH3, содержащих аминокислотные замены H435R и Y436F, приводят в контакт со средой для аффинной хроматографии легких каппа-цепей (например, используемой со смолой KappaSelect; GE Healthcare) и элюируют из среды для аффинной хроматографии легких каппа-цепей в условиях, подходящих для выделения связывающего белка из связывающих белков, содержащих только домены CL лямбда-цепей (например, в соответствии с инструкциями производителя).
[00323] Условия, подходящие для элюирования от белка A, известны в данной области техники, в том числе без ограничения элюирование при ступенчатом градиенте pH 4,5-2,8. В некоторых вариантах осуществления для очистки белков используется белок A или вариант белка A. В некоторых вариантах осуществления белок A присоединен к подложке или смоле, например, в качестве части среды для хроматографии. В некоторых вариантах осуществления после элюирования из среды для аффинной хроматографии легких каппа-цепей связывающий белок приводят в контакт со средой для аффинной хроматографии легких лямбда-цепей (например, используемой со смолой LambdaFabSelect; GE Healthcare) и элюируют из среды для аффинной хроматографии легких лямбда-цепей в условиях, подходящих для выделения связывающего белка из связывающих белков, содержащих только домены CL каппа-цепей (например, в соответствии с инструкциями производителя). В некоторых вариантах осуществления связывающий белок по настоящему изобретению выявляют с помощью HIC-хроматографии. В некоторых вариантах осуществления связывающий белок содержит первую полипептидную цепь, которая содержит домен CL лямбда-цепи; домен CH3 второй полипептидной цепи, который содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W; домен CH3 третьей полипептидной цепи, который содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368, 407, 435 и 436 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A, Y407V, H435R и Y436F; и четвертую полипептидную цепь, которая содержит домен CL каппа-цепи. В некоторых вариантах осуществления связывающий белок продуцируется клеткой-хозяином. В некоторых вариантах осуществления связывающий белок очищают из среды для культивирования клеток или экстракта клеток-хозяев. В некоторых вариантах осуществления связывающие белки секретируются клеткой-хозяином или продуцируются клеткой-хозяином и экстрагируются из нее (например, перед приведением в контакт с белком A). В некоторых вариантах осуществления связывающий белок находится в среде для культивирования клеток или экстракте клеток-хозяев при приведении в контакт с белком A. В некоторых вариантах осуществления связывающий белок очищают от других связывающих белков, полипептидов и/или других клеточных компонентов.
[00324] В некоторых вариантах осуществления стабилизированный нокаутный домен используется для облегчения предпочтительного синтеза или очистки требуемого мультиспецифического связывающего белка, где стабилизированный нокаутный домен содержит (1) одну или более инактивирующих мутаций, которые устраняют связывание с целевым антигеном; и (2) одну или более сконструированных межцепочечных дисульфидных связей, которые придают повышенную термостабильность (Tm) по сравнению с эталонной молекулой Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
СОСТАВ/ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
[00325] В восьмом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель и терапевтически эффективное количество белка по любому из первого - третьего аспектов настоящего изобретения.
[00326] Терапевтические или фармацевтические композиции, содержащие связывающие белки, находятся в пределах объема настоящего изобретения. Некоторые варианты осуществления восьмого аспекта настоящего изобретения включают фармацевтические композиции, содержащие терапевтически эффективное количество любого из связывающих белков, описанных в данном документе, или конъюгат связывающего белка и лекарственного средства в смеси с фармацевтически или физиологически приемлемым средством для составления, выбранным в соответствии со способом введения.
[00327] Приемлемые вещества для составления обычно являются нетоксичными для реципиентов при используемых дозировках и концентрациях.
[00328] В некоторых вариантах осуществления фармацевтическая композиция может содержать вещества для составления, предназначенные для модификации, поддержания или сохранения, например, pH, осмолярности, вязкости, прозрачности, цвета, изотоничности, запаха, стерильности, стабильности, скорости растворения или высвобождения, всасывания или проникновения композиции. Подходящие вещества для составления включают без ограничения аминокислоты (такие как глицин, глутамин, аспарагин, аргинин или лизин), противомикробные вещества, антиоксиданты (такие как аскорбиновая кислота, сульфит натрия или гидросульфит натрия), буферы (такие как борат, бикарбонат, Tris-HCl, цитраты, фосфаты или другие органические кислоты), объемообразующие средства (такие как маннит или глицин), хелатирующие средства (такие как этилендиаминтетрауксусная кислота (EDTA)), комплексообразующие средства (такие как кофеин, поливинилпирролидон, бета-циклодекстрин или гидроксипропил-бета-циклодекстрин), наполнители, моносахариды, дисахариды и другие углеводы (такие как глюкоза, манноза или декстрины), белки (такие как сывороточный альбумин, желатин или иммуноглобулины), окрашивающие, вкусоароматические и разбавляющие средства, эмульгирующие средства, гидрофильные полимеры (такие как поливинилпирролидон), низкомолекулярные полипептиды, солеобразующие противоионы (такие как ион натрия), консерванты (такие как хлорид бензалкония, бензойная кислота, салициловая кислота, тимеросал, фенетиловый спирт, метилпарабен, пропилпарабен, хлоргексидин, сорбиновая кислота или пероксид водорода), растворители (такие как глицерин, пропиленгликоль или полиэтиленгликоль), сахароспирты (такие как маннит или сорбит), суспендирующие средства, поверхностно-активные или смачивающие средства (такие как плюроники; ПЭГ; сложные эфиры сорбитана; полисорбаты, такие как полисорбат 20 или полисорбат 80; тритон; трометамин; лецитин; холестерин или тилоксапол), средства, повышающие стабильность (такие как сахароза и сорбит), средства, улучшающие тоничность (такие как галогениды щелочных металлов, например, хлорид натрия или калия, или маннит, сорбит), среды-носители для доставки, разбавители, вспомогательные вещества и/или фармацевтические адъюванты (см., например, Remington's Pharmaceutical Sciences (18th Ed., A.R. Gennaro, ed., Mack Publishing Company 1990) и его последующие издания, которые включены в данный документ посредством ссылки для любой цели).
[00329] В некоторых вариантах осуществления оптимальную фармацевтическую композицию будет определять специалист в данной области техники в зависимости, например, от предполагаемого пути введения, формата доставки и требуемой дозировки. На такие композиции могут оказывать влияние физическое состояние, стабильность, скорость высвобождения in vivo и скорость выведения in vivo связывающего белка.
[00330] В некоторых вариантах осуществления основная среда-носитель или носитель в фармацевтической композиции по своей природе могут быть водными или неводными. Например, подходящей средой-носителем или носителем для инъекции может быть вода, физиологический солевой раствор или искусственная спинномозговая жидкость, возможно, с добавлением других веществ, общепринятых в случае композиций для парентерального введения. Нейтральный забуференный солевой раствор или солевой раствор, смешанный с сывороточным альбумином, представляют собой дополнительные иллюстративные среды-носители. Другие иллюстративные фармацевтические композиции содержат Tris-буфер со значением pH, составляющим приблизительно 7,0-8,5, или ацетатный буфер со значением pH, составляющим приблизительно 4,0-5,5, который может дополнительно включать сорбит или подходящий заменитель. В одном варианте осуществления настоящего изобретения композиции на основе связывающего белка могут быть приготовлены для хранения в форме лиофилизованного порошка или водного раствора путем смешивания выбранной композиции с требуемой степенью чистоты с необязательными средствами для составления. Кроме того, связывающий белок может быть составлен в форме лиофилизата с применением соответствующих вспомогательных веществ, таких как сахароза.
[00331] В некоторых вариантах осуществления фармацевтические композиции по настоящему изобретению могут предназначаться для парентеральной или подкожной доставки. В качестве альтернативы композиции могут предназначаться для ингаляции или для доставки через пищеварительный тракт, например перорально. Получение таких фармацевтически приемлемых композиций находится в пределах компетенции специалиста в данной области техники.
[00332] В некоторых вариантах осуществления компоненты состава присутствуют в концентрациях, которые являются приемлемыми для места введения. Например, буферы используют для поддержания значения pH композиции на физиологическом уровне или при немного меньшем значении pH, обычно в диапазоне значений pH от приблизительно 5 до приблизительно 8.
[00333] Если предусмотрено парентеральное введение, то терапевтические композиции, предназначенные для применения, могут быть в форме апирогенного приемлемого для парентерального введения водного раствора, содержащего требуемый связывающий белок в фармацевтически приемлемой среде. Особенно подходящей средой-носителем для парентеральной инъекции является стерильная дистиллированная вода, в которой связывающий белок составляют в виде стерильного изотонического раствора с подходящими консервантами. Еще один препарат может предусматривать состав на основе требуемой молекулы со средством, таким как инъецируемые микросферы, биоразлагаемые частицы, полимерные соединения (такие как полимолочная кислота или полигликолевая кислота), гранулы или липосомы, которое обеспечивает контролируемое или замедленное высвобождение продукта, который затем можно доставлять посредством депо-инъекции. Можно также использовать гиалуроновую кислоту, и она может оказывать эффект содействия длительному пребыванию в кровотоке. Другие подходящие средства для введения требуемой молекулы включают имплантируемые устройства для доставки лекарственных средств.
[00334] В одном варианте осуществления фармацевтическая композиция может быть составлена для ингаляции. Например, связывающий белок может быть составлен в виде сухого порошка для ингаляции. Растворы для ингаляций на основе связывающего белка можно также составлять с пропеллентом для аэрозольной доставки. В еще одном варианте осуществления растворы можно распылять.
[00335] Также предусматривается, что определенные составы можно вводить перорально. В одном варианте осуществления настоящего изобретения мультиспецифические связывающие белки, которые вводят таким способом, можно составлять с такими носителями, которые обычно используют при составлении твердых лекарственных форм, таких как таблетки и капсулы, или без них. Например, капсула может быть предназначена для высвобождения активной части состава в таком месте пищеварительного тракта, где биодоступность повышается до максимума, а распад до попадания в системный кровоток сводится к минимуму. Для облегчения всасывания связывающего белка можно включать дополнительные вещества. Также можно использовать разбавители, ароматизаторы, легкоплавкие воски, растительные масла, смазывающие вещества, суспендирующие средства, средства для улучшения распадаемости таблеток и связующие вещества.
[00336] Другая фармацевтическая композиция может включать эффективное количество мультиспецифических связывающих белков в смеси с нетоксичными вспомогательными веществами, которые подходят для изготовления таблеток. Путем растворения таблеток в стерильной воде или другой подходящей среде-носителе можно получить растворы в форме одноразовой дозы. Подходящие вспомогательные вещества включают без ограничения инертные разбавители, такие как карбонат кальция, карбонат или бикарбонат натрия, лактоза или фосфат кальция; или связывающие средства, такие как крахмал, желатин или аравийская камедь; или смазывающие средства, такие как стеарат магния, стеариновая кислота или тальк.
[00337] Специалистам в данной области техники будут очевидны дополнительные фармацевтические композиции по настоящему изобретению, в том числе составы, содержащие связывающие белки, в форме составов с замедленной или контролируемой доставкой. Методики составления целого ряда других средств с замедленной или контролируемой доставкой, таких как липосомные носители, биоразлагаемые микрочастицы или пористые гранулы и депо-инъекции, также известны специалистам в данной области техники. Дополнительные примеры препаратов с замедленным высвобождением включают полупроницаемые полимерные матрицы в форме изделий определенной формы, например, пленок или микрокапсул. Матрицы с замедленным высвобождением могут включать сложные полиэфиры, гидрогели, полилактиды, сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата, сополимеры 2-гидросиэтила и метакрилата, этиленвинилацетат или поли-D(-)-3-гидроксимасляную кислоту. Композиции с замедленным высвобождением также могут включать липосомы, которые можно получить любым из нескольких способов, известных в данной области техники.
[00338] В некоторых вариантах осуществления фармацевтические композиции, подлежащие применению для введения in vivo, обычно должны быть стерильными. Этого можно достичь путем фильтрации через стерильные фильтрационные мембраны. Если композиция является лиофилизированной, то стерилизацию с применением данного способа можно проводить либо до, либо после лиофилизации и восстановления. Композиция для парентерального введения может храниться в лиофилизированной форме или в форме раствора. Кроме того, композиции для парентерального введения, как правило, помещают в контейнер, имеющий стерильное входное отверстие, например, мешок с раствором для внутривенной инъекции или флакон с пробкой, которую можно проколоть иглой для подкожных инъекций.
[00339] После того как фармацевтическая композиция была составлена, ее можно хранить в стерильных флаконах в виде раствора, суспензии, геля, эмульсии, твердого вещества или в виде обезвоженного или лиофилизированного порошка. Такие составы можно хранить либо в готовой к применению форме, либо в форме (например, лиофилизированной), требующей восстановления перед введением.
[00340] Настоящее изобретение также охватывает наборы для получения формы для введения однократной дозы. Каждый из наборов может содержать как первый контейнер с высушенным мультиспецифическим связывающим белком, так и второй контейнер с водным составом. В объем настоящего изобретения также включены наборы, содержащие одно- и многокамерные предварительно заполненные шприцы (например, шприцы с жидкостью и шприцы с лиофилизатом).
[00341] Эффективное количество фармацевтической композиции на основе связывающего белка, подлежащей терапевтическому применению, будет зависеть, например, от терапевтического случая и целей. Специалисту в данной области техники будет понятно, что соответствующие уровни дозировок для лечения при этом будут меняться, отчасти в зависимости от доставляемой молекулы, показания, для которого будут применять связывающий белок, пути введения и размерных характеристик (массы тела, поверхности тела или размера органа) и состояния (возраста и общего состояния здоровья) пациента. Соответственно врач может подобрать дозировку и модифицировать путь введения для получения оптимального терапевтического эффекта.
[00342] Частота введения доз будет зависеть от фармакокинетических параметров связывающего белка в подлежащем применению составе. Обычно врач будет вводить композицию до тех пор, пока дозировка не достигнет такого уровня, при котором достигается требуемый эффект. Следовательно, композицию можно вводить в виде однократной дозы, в виде двух или более доз (которые могут содержать одинаковое или не одинаковое количество требуемой молекулы) в течение определенного периода времени или в виде непрерывной инфузии посредством имплантируемого устройства или катетера. Дополнительное уточнение подходящей дозировки выполняют стандартным способом средние специалисты в данной области техники, и это находится в рамках задач, которые они традиционно выполняют. Подходящие дозировки можно определять с помощью соответствующих данных доза-ответ.
[00343] Путь введения фармацевтической композиции соответствует известным способам, например, перорально; посредством инъекции с помощью внутривенного, внутрибрюшинного, внутримозгового (интрапаренхиматозного), интрацеребровентрикулярного, внутримышечного, внутриглазного, внутриартериального, интрапортального или внутриочагового путей; с помощью систем с замедленным высвобождением или с помощью имплантируемых устройств. При необходимости композиции можно вводить в виде болюсной инъекции или непрерывно путем инфузии или с помощью имплантируемого устройства.
[00344] В некоторых вариантах осуществления композицию также можно вводить местно посредством имплантации мембраны, губки или другого подходящего материала, в котором была абсорбирована или инкапсулирована требуемая молекула. Если применяют имплантируемое устройство, то устройство можно имплантировать в любую подходящую ткань или орган, и доставка требуемой молекулы может осуществляться путем диффузии, регулируемого по времени высвобождения болюса или непрерывного введения.
СПОСОБЫ ЛЕЧЕНИЯ/ПРИМЕНЕНИЯ
[00345] В девятом аспекте настоящее изобретение относится к способу лечения нарушения, при котором активность антигена оказывает негативное воздействие, причем способ включает введение субъекту, нуждающемуся в этом, эффективного количества связывающего белка по любому из первого - третьего аспектов настоящего изобретения. В некоторых вариантах осуществления предусмотрен мультиспецифический связывающий белок для применения в качестве лекарственного препарата.
[00346] Связывающие белки можно использовать в любом известном способе анализа, таком как анализы конкурентного связывания, прямые и непрямые сэндвич-анализы и анализы иммунопреципитации для выявления и количественного определения одного или более целевых антигенов. Связывающие белки будут связывать один или более целевых антигенов с аффинностью, которая соответствует используемому способу анализа.
[00347] Для диагностических применений в некоторых вариантах осуществления связывающие белки можно метить с помощью выявляемого компонента. Выявляемый компонент может представлять собой любой компонент, который способен непосредственно или опосредованно генерировать выявляемый сигнал. Например, выявляемый компонент может представлять собой радиоизотоп, такой как 3H, 14C, 32P, 35S, 125I, 99Tc, 111In или 67Ga; флуоресцентное или хемилюминесцентное соединение, такое как изотиоцианат флуоресцеина, родамин или люциферин; или фермент, такой как щелочная фосфатаза, β-галактозидаза или пероксидаза хрена.
[00348] Связывающие белки также применимы для визуализации in vivo. Связывающий белок, меченный выявляемым компонентом, можно вводить животному, например в кровоток, и определять присутствие и местоположение меченного антитела в организме хозяина. Связывающий белок можно метить любым компонентом, который можно выявить в организме животного будь-то с помощью ядерного магнитного резонанса, рентгенологического исследования или других способов выявления, известных в данной области техники.
[00349] Для клинических или исследовательских применений в некоторых вариантах осуществления связывающие белки могут быть конъюгированы с цитотоксическим средством. Для нацеливания цитотоксических полезных нагрузок на специфические опухолевые клетки были использованы разнообразные антитела, сопряженные с цитотоксическими средствами (т. е. конъюгаты антитела и лекарственного средства). Цитотоксические средства и линкеры, которые обеспечивают конъюгацию средства с антителом, известны в данной области техники; см., например, Parslow, A.C. et al. (2016) Biomedicines 4:14 и Kalim, M. et al. (2017) Drug Des. Devel. Ther. 11:2265-2276.
[00350] Настоящее изобретение также относится к набору, содержащему связывающий белок и другие реагенты, применимые для выявления уровней целевых антигенов в биологических образцах. Такие реагенты могут включать выявляемую метку, блокирующую сыворотку крови, образцы положительного и отрицательного контроля и реагенты для выявления. В некоторых вариантах осуществления набор содержит композицию, содержащую любой связывающий белок, полинуклеотид, вектор, векторную систему и/или клетку-хозяина, описанные в данном документе. В некоторых вариантах осуществления набор содержит контейнер и этикетку или листок-вкладыш, размещенные на контейнере или связанные с ним. Подходящие контейнеры включают, например, бутыли, флаконы, шприцы, пакеты с раствором для в/в инъекции и т. д. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластик. Контейнер содержит композицию, которая сама по себе или в комбинации с другой композицией является эффективной для лечения, предупреждения и/или диагностирования состояния, и он может иметь стерильное входное отверстие (например, контейнер может представлять собой пакет с раствором для внутривенной инъекции или флакон с пробкой, которую можно проколоть иглой для подкожных инъекций). В некоторых вариантах осуществления на этикетке или листке-вкладыше указано, что композиция применяется для предупреждения, диагностирования и/или лечения выбранного состояния. В качестве альтернативы или дополнения изделие или набор могут дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), фосфатно-солевой буферный раствор, раствор Рингера и раствор декстрозы. Они могут дополнительно включать другие вещества, необходимые с коммерческой точки зрения и с точки зрения потребителя, в том числе другие буферы, разбавители, наполнители, иглы и шприцы.
[00351] В некоторых вариантах осуществления связывающий белок по настоящему изобретению вводят пациенту, нуждающемуся в этом, для лечения или предупреждения рака. В некоторых вариантах осуществления настоящее изобретение относится к способу предупреждения и/или лечения пролиферативного заболевания или нарушения (например, рака). В некоторых вариантах осуществления способ включает введение пациенту терапевтически эффективного количества по меньшей мере одного из связывающих белков или фармацевтических композиций на его основе, описанных в данном документе. В некоторых вариантах осуществления пациентом является человек.
[00352] В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят в комбинации с одним или более средствами противораковой терапии (например, любым средством противораковой терапии, известным в данной области техники, таким как химиотерапевтическое средство или терапия). В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят до одного или более средств противораковой терапии. В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят одновременно с одним или более средствами противораковой терапии. В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят после одного или более средств антиретровирусной терапии.
ПРИМЕРЫ
[00353] Перед тем, как настоящее изобретение будет подробно описано ниже, следует понимать, что настоящее изобретение не ограничивается конкретной методикой, протоколами и реагентами, описанными в данном документе, поскольку они могут меняться. Также следует понимать, что терминология, используемая в данном документе, предназначена лишь для целей описания конкретных вариантов осуществления и не предполагает ограничения объема настоящего изобретения, который будет ограничиваться лишь прилагаемой формулой изобретения. Если не определено иное, то все технические и научные термины, используемые в данном документе, имеют такие же значения, которые обычно понятны специалисту в данной области техники. В конкретных вариантах осуществления термины, используемые в данном документе, определены, как описано в "A multilingual glossary of biotechnological terms: (IUPAC Recommendations)," Leuenberger, H.G.W, Nagel, B. и Kolb, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Базель, Швейцария). Если в данном документе не определено иное, научные и технические термины, используемые в данном документе, имеют значения, которое общеизвестно специалистами в данной области техники. В случае любой скрытой неясности определения, приведенные в данном документе, имеют приоритет над любым словарным или внешним определением. Если по контексту не требуется иное, термины в единственном числе будут включать формы множественного числа, а термины во множественном числе будут включать форму единственного числа. Применение "или" означает "и/или", если не указано иное. Применение термина "включающий", а также других форм, таких как "включает" и "включенный", не является ограничивающим. Если не указано иное, используемые в данном документе формы единственного числа включают ссылку на множественное число. Таким образом, например, ссылка на "белок" включает несколько белковых молекул.
[00354] Кроме того, в описанных в данном документе экспериментах, если не указано иное, применяются традиционные методики молекулярной и клеточной биологии и иммунологии в рамках компетенции специалистов в данной области техники. Такие методики хорошо известны опытному специалисту и в полном объеме объясняются в литературе. См., например, Ausubel, et al., ed., Current Protocols in Molecular Biology, John Wiley & Sons, Inc., NY, N.Y. (1987-2008), включая все приложения, Molecular Cloning: A Laboratory Manual (четвертое издание) под ред. MR Green и J. Sambrook и Harlow et al., Antibodies: A Laboratory Manual, раздел 14, Cold Spring Harbor Laboratory, Cold Spring Harbor (2013, 2-е издание).
[00355] На протяжении данного описания процитированы несколько документов. Каждый из документов, процитированных в данном документе (включая все патенты, заявки на патент, научные публикации, документация производителя, инструкции и т.п.), независимо от того, упомянут ли он выше или ниже, настоящим включен посредством ссылки во всей своей полноте. Ничто в данном документе не следует толковать как признание того, что настоящее изобретение не имеет оснований для противопоставления такому раскрытию на основании более раннего изобретения.
[00356] Далее будут описаны элементы настоящего изобретения. Эти элементы перечислены в специфических вариантах осуществления, однако следует понимать, что их можно комбинировать любым способом и в любом количестве для получения дополнительных вариантов осуществления. Различным образом описанные примеры и предпочтительные/конкретные варианты осуществления не должны истолковываться как ограничивающие настоящее изобретение только явно описанными вариантами осуществления. Следует понимать, что данное описание поддерживает и охватывает варианты осуществления, которые комбинируют явно описанные варианты осуществления с любым числом раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных элементов в данной заявке следует рассматривать как раскрытые с помощью описания настоящей заявки, если контекст не указывает на иное.
[00357] Как правило, терминология, используемая в контексте культивирования клеток и тканей, молекулярной биологии, иммунологии, микробиологии, генетики и химии и гибридизации белков и нуклеиновых кислот, описанная в данном документе, является хорошо известной и широко используемой в данной области техники. Предусмотренные в данном документе способы и методики обычно выполняют в соответствии с общепринятыми способами, хорошо известными из уровня техники и описанными в различных общих и более специфических литературных источниках, которые упоминаются и обсуждаются в настоящем описании, если не указано иное. Ферментативные реакции и методики очистки выполняют в соответствии с документацией производителя, как обычно осуществляется в данной области техники или как описано в данном документе. Терминология, используемая в контексте аналитической химии, химии органического синтеза и медицинской и фармацевтической химии, а также их лабораторные процедуры и методики, описанные в данном документе, являются общеизвестными и широко используемыми в данной области техники. Стандартные методики используют при химических синтезах, химических анализах, фармацевтическом получении, составлении и доставки, а также при лечении пациентов.
Пример 1. Идентификация подходящего замещающего каркаса
[00358] Связывающие белки, раскрытые в данном документе, содержат замещение одной пары CH1/CL на нокаутный домен VH/VL в различных форматах антител (см. фиг. 1, 2, 7, 10-13). Чтобы идентифицировать подходящий замещающий остов для замещения димера CH1/CL, исследовали введение дисульфидных мостиков в определенные пары VH/VL. Кроме того, исследовали возможность экспрессии и слияния с другой парой VH/VL.
[00359] Определили, что трастузумаб представляет собой подходящий замещающий остов для замены димера CH1/CL с целью решения проблемы правильного спаривания легких цепей.
Пример 2. Применение вариабельных доменов трастузумаба для замещения CH1/CL
[00360] Определили, что остатки цистеина в положениях VH44 и VL100 подходили для образования дисульфидной связи между VH/VL трастузумаба (называется в данном документе ds-трастузумаб), за счет чего происходит стабилизация гетеродимера. Чтобы определить его термостабильность, домены ds-трастузумаба инкубировали при концентрации 1 мг/мл в буфере D-PBS (GIBCO) в течение 14 дней при 40°C. Контрольные образцы с той же концентрацией хранили при -80°C и 4°C. После завершения стресс-теста образцы анализировали в отношении содержание агрегатов с помощью аналитической эксклюзионной хроматографии (SEC). Аналитическую SEC выполняли с использованием прибора BioSECcurity (PSS Polymer) с колонкой TSKgel SuperSW3000 (4,6 мм x 300 мм) и предколонкой для HPLC TSKgel SuperSW (Tosoh Bioscience) при 25°C. Анализ проводили при скорости потока 0,25 мл/мин с использованием 250 мМ NaCl, 100 мМ фосфата Na, pH 6,7, с выявлением при 280 нм и 260 нм. Статическое светорассеяние выявили при 436 нм. На колонку наносили 5 мкл образца белка (при концентрации 1 мг/мл). Оценку данных выполняли с использованием программного обеспечения WinGPC v8.1 (PSS Polymer). Для оценки молекулярной массы колонку для SEC калибровали с помощью стандартных белков в диапазоне молекулярной массы от 6,5 до 670 кДа.
[00361] Обнаружили, что остов ds-трастузумаба (с модификациями VH44/VL100 на цистеин) увеличил термостабильность на 4°C (см. фиг. 3A-C).
Пример 3. Исследование соединения с VH/VL в структуре псевдо-IgG
[00362] Создавали конструкции псевдо-IgG1, содержащие стабилизированный дисульфидной связью остов трастузумаба в качестве замещающего остова для CH1/CL. Остов ds-трастузумаба сливали с представляющей интерес VH/VL с помощью линкера G4S или (G4S)2 (см. фиг. 6).
Определение точек плавления (Tm)
[00363] Точки плавления (Tm) определяли с использованием дифференциальной сканирующей флуориметрии (DSF). Образцы разбавляли в буфере D-PBS (Invitrogen) до конечной концентрации 0,2 мкг/мкл, содержащей 4x концентрированный раствор красителя SYPRO-Orange (Invitrogen, 5000x исходный раствор в DMSO) в D-PBS, в белых полуокаймленных 96-луночных планшетах (BIORAD). Все измерения проводили в двух повторностях с применением прибора для ПЦР в режиме реального времени MyiQ2 (BIORAD). Кривые отрицательной первой производной (-d(RFU)/dT) для кривых плавления получали на программном обеспечении iQ5 v2.1 (BIORAD). Затем данные экспортировали в Excel для определения Tm и графического представления данных.
[00364] Последовательности шести антител экспрессировали в слиянии с ds-трастузумабом, и в таблице 4 ниже описан % мономеров после очистки с помощью белка A и температура плавления для каждого слитого белка, а также антитела псевдо-IgG без домена ds-трастузумаба. Уровень экспрессии был немного ниже по сравнению с уровнем WT-IgG, а показатель содержания мономеров был немного ниже относительно такового для WT-IgG.
Таблица 4. % мономеров и температура плавления слитых белков антитело псевдо-IgG1-ds-трастузумаб
(SEQ ID NO: 6 и 7)
(SEQ ID NO: 8 и 9)
(SEQ ID NO: 10 и 11)
(SEQ ID NO: 12 и 13)
(SEQ ID NO: 14 и 15)
(SEQ ID NO: 16 и 17)
(SEQ ID NO: 18 и 19)
(SEQ ID NO: 20 и 21)
(SEQ ID NO: 22 и 23)
(SEQ ID NO: 24 и 25)
(SEQ ID NO: 26 и 27
(SEQ ID NO: 28 и 29
(SEQ ID NO: 30 и 31)
(SEQ ID NO: 32 и 33)
(SEQ ID NO: 34 и 35)
(SEQ ID NO: 36 и 37)
(SEQ ID NO: 38 и 39)
(SEQ ID NO: 40 и 41)
Пример 4. Создание нокаутных вариантов ds-Tras (dsTrasKO)
[00365] Связывающую активность трастузумаба подвергали выключению за счет введения четырех ключевых точечных мутаций аминокислотных остатков в паратопную область антитела трастузумаба, чтобы воздействовать на способность связывания антитела с рецепторной тирозинпротеинкиназой erbB-2 (HER2). Трастузумаб моделировали на основе структуры 1N8Z из PDB, доступной в общедоступной базе данных PDB. В тяжелой цепи идентифицировали четыре положения, которые потенциально разрушали взаимодействие ds-трастузумаба с его антигеном. Положения включают оба аргинина R59 и R50, которые связывают глутамат и аспартат на HER2. Обращение зарядов путем мутирования аргинина в остатки глутамата должно приводить к отталкиванию HER2. Без привязки к научной теории, два других положения, тирозин Y33 и Y105, по-видимому, стабилизируют комплекс за счет Pi-Pi взаимодействия с фенилаланином. Без привязки к научной теории, мутирование в аланин должно разрушать данное взаимодействие. Кристаллографические данные из файла 1N8Z анализировали с помощью пакета BIOVIA Discovery Studio. Особое внимание уделяли существующей области контакта между антителом (fab трастузумаба) и его мишенью (домен белка HER2) (см. фиг. 4).
Анализ области контакта сокристалла 1N8Z
[00366] В ходе анализов области контакта антитела и мишени все нековалентные взаимодействия квалифицировали с использованием отслеживания взаимодействий, не являющихся связями, от BIOVIA Discovery Studio. Отрывок из полученной таблицы представлен в таблице 5. Для каждого взаимодействия в таблице 5 представлено расстояние между взаимодействующими атомами, природа типа взаимодействия и характеристики взаимодействующих атомов.
Таблица 5.
Отрывок результатов отслеживания взаимодействий, не являющихся связями, для файла 1N8Z. из PDB Цепи A, B и C соответствуют легкой цепи Fab трастузумаба, тяжелой цепи Fab трастузумаба и HER2 соответственно
[00367] На основании таблицы нековалентных взаимодействий, возникающие между fab трастузумаба и белком HER2, определенные взаимодействия выбирали для устранения, чтобы разрушить связывающие взаимодействия.
Предлагаемые комбинации мутаций для разрушения связывающих взаимодействий
[00368] На основе данных о взаимодействиях, не являющихся связями, выбрали следующие четыре мутации аминокислотных остатков, чтобы сохранить исходные последовательности трастузумаба.
Аргументация в пользу остатка аргинина 50 в тяжелой цепи трастузумаба
[00369] Данный остаток аргинина в антителе обеспечивает взаимодействия по типу солевого мостика с остатками глутамата 558 и аспартата 560 в HER2. Аргинин 50 мутировали в остаток глутамата, чтобы создать отталкивание остатков глутамата 558 и аспартата 560 в HER2.
Аргументация в пользу остатка аргинина 59 в тяжелой цепи трастузумаба
[00370] Данный остаток аргинина в антителе обеспечивает взаимодействия по типу солевого мостика с остатками глутамата 558 и аспартата 560 в HER2. Аргинин 59 мутировали в остаток глутамата, чтобы создать отталкивание остатков глутамата 558 и аспартата 560 в HER2.
Аргументация в пользу остатка аргинина 33 в тяжелой цепи тирозина
[00371] Данный остаток тирозина 33 в антителе обеспечивает Pi-взаимодействия с остатком фенилаланина 573 в HER2. Тирозин 33 мутировали в остаток аланина, чтобы разрушить данные Pi-взаимодействия, возникающие между антителом и его мишенью.
Аргументация в пользу остатка аргинина 105 в тяжелой цепи тирозина
[00372] Данный остаток тирозина 105 в антителе обеспечивает Pi-взаимодействия с остатком фенилаланина 573 в HER2. Тирозин 105 мутировали в остаток аланина, чтобы разрушить данные Pi-взаимодействия, возникающие между антителом и его мишенью.
[00373] Конкретные комбинации аминокислотных остатков, предложенные для мутирования, представлены в таблице 6. Данные комбинации привели к двум вариантам антитела трастузумаба.
Таблица 6. Нокаутные варианты трастузумаба (TrasKO)
(SEQ ID NO: 2)
(SEQ ID NO: 3)
(SEQ ID NO: 4)
(SEQ ID NO: 5)
Вариант 1 Fab содержит все четыре точечные мутации. Вариант 2 Fab с обращением двух положительно заряженных остатков в отрицательно заряженные остатки имеет зону отталкивания для белка HER2 в исходной связывающей области трастузумаба для HER2. Вариант 3 Fab с нарушением Pi-взаимодействий с фенилаланином 573 в HER2 индуцирует дестабилизацию комплекса трастузумаб-HER2. Обнаружили, что все три варианта dsTrasKO устраняют связывание с HER2 (см. фиг. 5A - фиг. 5B). Вариант 2 (dsTrasKO2) идентифицировали как лучший продуцент
Пример 5. Оценка dstrasko2 в качестве замещающего остова для CH1/CL
[00374] Варианты dsTrasKO оценивали в формате псевдо-IgG (моноспецифического) (см. фиг. 6A) и псевдо-Fab (см. фиг. 6B). Характеристики экспрессии и очистки у протестированных форматов псевдо-IgG и псевдо-Fab были аналогичны характеристикам исходного антитела (см. таблицу 7).
Таблица 7. Результаты по экспрессии и очистке антител псевдо-IgG с заменой домена CH1/CL на dsTrasKO2
(SEQ ID NO: 42 и 43)
(SEQ ID NO: 44 и 45)
(SEQ ID NO: 46 и 47)
(SEQ ID NO: 48 и 49)
(SEQ ID NO: 50 и 51)
Пример 6. Оценка биспецифических антител с нативной структурой с использованием dstrasko2 в качестве замещающего остова для CH1/CL
Домен dsTrasKO2 оценивали в качестве замещающего остова в биспецифическом антителе с нативной структурой IgG. В частности, синтезировали биспецифическую структуру антитело к IL4-dsTrasKO (вариант 2) x антитело к IL13-huIgG1 с RF-мутациями в Fc (см. фиг. 7).
[00375] i. Экспрессия биспецифических молекул с dsTrasKO2
[00376] Плазмиды экспрессии, кодирующие обе тяжелые цепи (dsTrasKO2-выступ и WT-впадина) и обе легкие цепи (dsTrasKO и WT-каппа/лямбда) соответствующих конструкций, размножали в E. coli DH5α. Плазмиды, применяемые для трансфекции, получали из E. coli с применением мега-набора EndoFree Plasmid от Qiagen
[00377] Клетки HEK 293-FS, выращиваемые в суспензионной культуре с бессывороточной средой F17 (Invitrogen), трансфицировали указанными плазмидами с легкой цепью (LC) и тяжелой цепью (HC) с использованием реагента для трансфекции на основе полиэтиленимина. После 7 дней культивирования при 37°C клетки удаляли с помощью центрифугирования, а супернатант пропускали через фильтр с размером пор 0,22 мкм для удаления частиц.
[00378] Для очистки антитело захватывали на колонке MabSelect SuRe (№ по кат.: 11-0034-93, GE Healthcare) и элюировали 0,1 М цитратным буфером, pH 3,0, и сразу же подвергали обессоливанию с использованием обессоливающей колонки HiPrep 26/10 (№ по кат.: 17-05087-02, GE Healthcare). Предполагаемые гомодимерные моноспецифические молекулы с dsTrasKO2 будут отсортировываться с использованием дополнительной стадии захвата на KappaSelect (элюирующий буфер 0,1 М глицина, pH 2,7) (см. фиг. 14). После заключительной очистки белка с помощью эксклюзионной хроматографии (SEC, проводимой, как описано в примере 2 выше) с использованием Superdex200 26/60 (GE) и конечной стадии концентрирования ультрафильтрацией, белок использовали для дальнейшего определения характеристик. Результаты очистки биспецифических конструкций с dsTrasKO2 см в таблице 8. Типичную биспецифическую структуру и результаты очистки см. на фиг. 7A - фиг. 7D.
Таблица 8. Выход при очистке биспецифических конструкций с dsTrasKO2
(SEQ ID NO: 68 и 69 и SEQ ID NO: 70 и 71)
(SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63)
(SEQ ID NO: 56 и 57 и SEQ ID NO: 58 и 59)
(SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55)
(SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67)
Оценка связывания антигена у биспецифических антител, содержащих замену пары CH1/CL на dsTrasKO2.
[00379] Поверхностный плазмонный резонанс (SPR) использовали для оценки связывания антигенов с антителом. Связывание антигенов с конструкциями антител измеряли с использованием поверхностного плазмонного резонанса (SPR) с помощью прибора BIAcore 3000 (GE Healthcare) с буфером HBS-EP (GE Healthcare). IL4 человека (IL004, Millipore) и IL13 человека (IL012, Millipore), HER2 человека (1129-ER, R&D Systems), TNFa человека (H8916, SIGMA Aldrich), CTLA4 человека (CT4-H5229, ACRO Biosystems), PD-1 человека (8986-PD, R&D Systems) и IL6Ra человека (227-SR/CF, R&D Systems) использовали в качестве антигенов. Захватывающее антитело к Fc человека (набор для захвата антител человека, GE Life Sciences) иммобилизовали посредством первичных аминогрупп (11000 RU) на чипе CM5 класса для исследований (GE Life Sciences) с использованием стандартных процедур. Захват лигандов выполнялся при скорости потока 10 мкл/мин со скорректированным значением RU, что привело к максимальному связыванию аналита, составляющему 30 RU. Тесты на связывание с HER2 выполняли путем захвата антигена с помощью антитела к Fc человека. Тестируемые конструкции антител использовали в качестве аналитов и вводили в концентрации 100 нМ в течение 240 секунд с временем диссоциации 300 секунд при скорости потока 30 мкл/мин. Измерения кинетики связывания выполняли с использованием захваченных антител при введении двукратных серийных разведений аналитов от 3 нМ до 100 нМ. Для IL4 и IL13 человека использовали серии разведений от 0,1 нМ до 3 нМ и от 0,8 нМ до 25 нМ соответственно. Поверхности чипа регенерировали с помощью 2-минутных введений регенерирующего буфера, входящего в набор для захвата. Сенсограммы дважды сопоставляли с холостой поверхностью чипа и холостыми буферными растворами HBS-EP. Анализ данных выполняли с использованием программного обеспечения BIAevaluation v4.1. Характеристики связывания mAb, псевдо-IgG и биспецифических молекул показаны в таблице 9 ниже.
Таблица 9. Кинетика связывания, определенная с помощью SPR: сравнение mAb, псевдо-IgG и биспецифических молекул
(SEQ ID NO: 40 и 41)
(SEQ ID NO: 46 и 47)
(SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55)
(SEQ ID NO: 10 и 11)
(SEQ ID NO: 48 и 49)
(SEQ ID NO: 56 и 57 и SEQ ID NO: 58 и 59)
(SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63)
(SEQ ID NO: 28 и 29)
(SEQ ID NO: 44 и 45)
(SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67)
(SEQ ID NO: 34 и 35)
(SEQ ID NO: 42 и 43)
(SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63)
(SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55)
(SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67)
[00380] Результаты SPR показали, что различные VH/VL, слитые с dsTrasKO2, сохраняют аффинности связывания с исходным антигеном, в том числе биспецифические антитела.
Анализ целостности белка
[00381] Целостность белка и возможное неправильное спаривание гетеродимерных конструкций анализировали посредством LC-масс-спектрометрии (LC-MS). Образцы белка подвергали дегликозилированию с использованием 12,5 мкг белка, разведенного до 0,5 мг/мл в буфере D-PBS, обработанном 0,5 мкл PNGaseF (без глицерина, New England Biolabs), при 37°C в течение 15 часов. Анализ LC-MS выполняли с использованием прибора 6540 UHD Accurate-Mass Q-TOF LC/MS (Agilent). Хроматографию с обращенной фазой (RP) проводили с использованием колонки Poroshell 300SB-C8 5 мкм, 75×0,5 мм (Agilent) с предколонкой Poroshell 300SB-C8, 5 мкм, 2,1×12,5 мм (Agilent) при скорости потока 180 мкл/мин. Элюентами были вода для LC, 0,1% муравьиной кислоты (A) и 90% ацетонитрила, 10% воды для LC, 0,1% муравьиной кислоты (B). 2 мкг белка вводили в колонку и элюировали с использованием линейного градиента от 0% до 100% B в течение 13 минут. Анализ данных проводили с использованием программного обеспечения MassHunter B.06 (Agilent). Молекулярные массы рассчитывали на основе аминокислотных последовательностей белков с использованием программного обеспечения GPMAW версии 9.13a2 (Lighthouse data). Показано, что белки слияния dsTrasKO2-антитело в основном были интактными и демонстрировали правильное спаривание гетеродимеров (см. таблицу 10 ниже).
Таблица 10. LC-MS результаты для белков слияния dsTrasKO2-антитело
(SEQ ID NO: 46 и 47)
(SEQ ID NO: 44 и 45)
(SEQ ID NO: 42 и 43)
(SEQ ID NO: 68 и 69 и SEQ ID NO: 70 и 71)
(SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63)
(SEQ ID NO: 56 и 57 и SEQ ID NO: 58 и 59)
(SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55)
(SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67)
(SEQ ID NO: 72 и 73 и SEQ ID NO: 74 и 75)
[00382] В дополнение к LC-MS анализу биспецифические образцы также анализировали посредством хроматографии гидрофобного взаимодействия (HIC) для выявления потенциальных неправильно спаренных или случайных разновидностей. Аналитическую HIC выполняли с использованием прибора для HPLC LC10 (Shimadzu) с колонкой TSKgel Ether-5PW 10 мкм, 2×75 мм (Tosoh Bioscience) при 25°C. Анализ проводили при скорости потока 0,1 мл/мин с выявлением при 280 нм. В колонку вносили 5 мкг неразбавленного образца белка. Градиентное элюирование составляло от 0 до 30 минут (от 0% до 100% B), с последующими 10 минутами 100% B и 15 минутами повторного уравновешивания. В состав буфера A входили 1,5 М сульфата аммония, 25 мМ фосфата натрия, pH 7,0. В состав буфера B входили 25 мМ фосфата натрия, pH 7,0. Оценку данных осуществляли с использованием программного обеспечения LabSolutions v5.85 (Shimadzu). Данные показали, что биспецифические образцы с dsTrasKO2 характеризовались гомогенным профилем HIC, что свидетельствует о том, что отсутствовали случайные разновидности и что биспецифические образцы характеризовались правильным спариванием (см. фиг. 8).
Термостабильность: сравнение псевдо-IgG и биспецифических молекул
[00383] Термостабильность образцов псевдо-IgG и биспецифических молекул с dsTrasKO2 оценивали, как описано выше в примере 2. Точки плавления (Tm) определяли с использованием дифференциальной сканирующей флуориметрии (DSF), как описано в примере 3. Для конструкций на основе dsTrasKO2 показана сниженная температура плавления по сравнению с исходным моноклональным IgG, и не выявлено никакого нарушения стабильности в анализе на термостабильность в течение 2 недель (40°C, 4°C и -80°C) (см. таблицу 11 ниже).
Таблица 11. Термостабильность конструкций dsTrasKO2-антитело.
(°C)
(SEQ ID NO: 40 и 41)
(SEQ ID NO: 46 и 47)
(SEQ ID NO: 52 и 53 и SEQ ID NO: 54 и 55)
(SEQ ID NO: 10 и 11)
(SEQ ID NO: 48 и 49)
(SEQ ID NO: 56 и 57 и SEQ ID NO: 58 и 59)
(SEQ ID NO: 28 и 29
(SEQ ID NO: 44 и 45)
(SEQ ID NO: 64 и 65 и SEQ ID NO: 66 и 67)
(SEQ ID NO: 34 и 35)
(SEQ ID NO: 42 и 43)
(SEQ ID NO: 60 и 61 и SEQ ID NO: 62 и 63)
Пример 7. Кристаллическая структура псевдо-fab к IL-13
[00384] Для исследований структуры выполняли кристаллизация dsTrasKO2-псевдо-Fab к IL13. Испытания по кристаллизации проводили в виде экспериментов с сидячей каплей в стандартных 96-луночных планшетах MRC на две капли с использованием соотношения белок : резервуарный раствор 1:1 и инкубировали при 20°C. Оба TrasKO2-CH1/CL и антитело к IL13-TrasKO2 подвергали скринингу в отношении успешных кристаллизаций в сравнении с рядом коммерчески доступных скринингов по типу разреженной матрицы. Капли для выполнения скрининга для TrasKO2-CH1/CL (исходная концентрация 15 мг/мл) и антитело к IL13-TrasKO2 (исходная концентрация 15,6 мг/мл) в 20 мМ HEPES, pH 7,5, 0,1 М хлорида натрия получали путем смешивания 100 нл раствора белка с 100 нл резервуарного раствора и уравновешивали в экспериментах по паровой диффузии сидячей капли с 80 мкл резервуарного раствора. Конечные кристаллы TrasKO2-CH1/CL, подходящие для сбора данных, и структурный раствор выращивали при 20°C с резервуарным раствором, состоящим из 0,1 М цитрата фосфата натрия, pH 4,2, 20% (вес./об.) полиэтиленгликоля 8000 и 0,2 М хлорида натрия. Кристаллы антитело к IL13-TrasKO2 качества, подходящего для дифракционного анализа, выращивали с резервуарным раствором, состоящим из 0,1 М CHES, pH 9,5, и 20% (вес./об.) полиэтиленгликоля 8000. Все кристаллы подвергали криозащите перед мгновенным охлаждением в жидком азоте путем добавления 25% (вес./об.) этиленгликоля (конечная концентрация).
Сбор данных и определение структуры
[00385] Дифракционные данные собирали на источнике синхронного излучения PSII в Swiss Light Source (SLS), Виллинген, Швейцария. Дифракционные данные обрабатывали с использованием комбинации XDS (Kabsch, 2010) и AIMLESS (Evans & Mushudov, 2013) в пакете программ CCP4 (Winn et al., 2011). TrasKO2-CH1/CL кристаллизовались в пространственной группе I23 с параметрами ячейки 153.23 Å, 153.23 Å, 153.23 Å, 90.00°, 90.00°, 90.00°, данные расширены до разрешения 3,70 Å. Кристаллы антитело к IL13-TrasKO2 принадлежали к пространственной группе P3221 с параметрами ячейки 145,37, 145,37, 52,06, 90,00, 90,00 120,00 и дифрагировали до 1,85 Å.
[00386] Структуры определяли путем молекулярной замены с использованием реализации Phaser в CCP4 (McCoy et al., 2007). В случае TrasKO2-CH1/CL в качестве моделей поиска использовали модифицированную версию домена VH-VL трастузумаба и домена CH1/CL из записи 1n8z в PDB. Молекулярную замену в молекуле антитело к IL13-TrasKO2 выполняли с помощью домена VH/VL антитела к IL13 из структуры Fab собственного антитела к IL13 от Sanofi и модифицированной версии домена VH/VL из 1n8z в качестве моделей фазирования. Атомарные модели строили путем итеративных раундов ручного построения и уточнения моделей с использованием Coot (Emsley et al., 2010) и Refine (Bricogne, 2017). R- и R-свободные факторы окончательных моделей составляют 19,2/23,2 для TrasKO2-CH1/CL и 21,0/31,2 для антитело к IL13-TrasKO2 (кристаллическую структуру см. на фиг. 9).
Пример 8. Оценка биспецифических антител с тандемной структурой с использованием dstrasko2 в качестве замещающего остова для CH1/CL
[00387] Домен dsTrasKO2 оценивали в качестве замещающего остова в структуре биспецифического тандемного IgG. В частности, синтезировали и тестировали тандемную IgG структуру антитело к GITR-dsTrasKO2 x антитело к OX40-каппа-huIgG1 (см. фиг. 10-12).
Экспрессия биспецифических тандемных молекул с dsTrasKO2
Плазмиды экспрессии, кодирующие тяжелую и обе легкие цепи (dsTrasKO и WT-каппа/лямбда) соответствующих конструкций, размножали в E. coli DH5a. Плазмиды, применяемые для трансфекции, получали из E. coli с применением мега-набора EndoFree Plasmid от Qiagen
Клетки HEK 293-FS, выращиваемые в суспензионной культуре с бессывороточной средой F17 (Invitrogen), трансфицировали указанными плазмидами с LC и HC с использованием реагента для трансфекции на основе полиэтиленимина. После 7 дней культивирования при 37°C клетки удаляли с помощью центрифугирования, а супернатант пропускали через фильтр с размером пор 0,22 мкм для удаления частиц.
Для очистки антитела осуществляли его захват на колонке MabSelect SuRe (№ по кат. 11-0034-93, GE Healthcare) и элюировали 0,1 М цитратным буфером, pH 3,0, и сразу же подвергали обессоливанию с использованием обессоливающей колонки HiPrep 26/10 (№ по кат.: 17-05087-02, GE Healthcare). Предполагаемые гомодимерные моноспецифические молекулы с dsTrasKO2 будут отсортировываться с использованием дополнительной стадии захвата на KappaSelect (элюирующий буфер 0,1 М глицина, pH 2,7) (см. фиг. 14). После заключительной очистки белка с помощью эксклюзионной хроматографии (SEC) с применением Superdex200 26/60 (GE) и конечной стадии концентрирования ультрафильтрацией белок применяли для дальнейшего определения характеристик.
Типичную биспецифическую структуру и результаты очистки см. на фиг. 12A - фиг. 12D.
Пример 9. Оценка триспецифических антител с CODV-структурой с использованием dstrasko2 в качестве замещающего остова для CH1/CL
[00388] Домен dsTrasKO2 оценивали в качестве замещающего остова в структуре с триспецифическими кроссоверными вариабельными доменами (CODV). В частности, синтезировали и тестировали конструкцию CODV-антитело к Ox40 x антитело к PD1] x антитело к CD137-dsTrasKO2-huIgG1-LALA-KIH-RF (см. фиг. 13).
Экспрессия триспецифических молекул с dsTrasKO2 CODV
Плазмиды экспрессии, кодирующие тяжелую и обе легкие цепи (dsTrasKO и WT), и плазмиды экспрессии, кодирующие обе тяжелые (CODV-выступ и dsTrasKO2-впадина) и обе легкие цепи (CODV и dsTrasKO) соответствующих конструкций, размножали в Е.coli DH5a. Плазмиды, применяемые для трансфекции, получали из E. coli с применением мега-набора EndoFree Plasmid от Qiagen
Клетки HEK 293-FS, выращиваемые в суспензионной культуре с бессывороточной средой F17 (Invitrogen), трансфицировали указанными плазмидами с LC и HC с использованием реагента для трансфекции на основе полиэтиленимина. После 7 дней культивирования при 37°C клетки удаляли с помощью центрифугирования, а супернатант пропускали через фильтр с размером пор 0,22 мкм для удаления частиц.
Для очистки антитела осуществляли его захват на колонке MabSelect SuRe (№ по кат. 11-0034-93, GE Healthcare) и элюировали 0,1 М цитратным буфером, pH 3,0, и сразу же подвергали обессоливанию с использованием обессоливающей колонки HiPrep 26/10 (№ по кат.: 17-05087-02, GE Healthcare). Далее образец очищали на катионообменной колонке MonoS (№ по кат.: 17-5169-01, GE Healthcare, градиент соли 0-1 М NaCl в буфере на основе 0,01 М L-гистидина, pH 6,0). После стадии концентрирования с помощью ультрафильтрации белок использовали для дальнейшего определения характеристик.
Типичную триспецифическую структуру и результаты очистки см. на фиг. 13A - фиг. 13D.
Пример 10. Оценка биспецифических антител-активаторов Т-клеток с использованием dstrasko2 в качестве замещающего остова для CH1/CL
Общие способы
Аналитическая эксклюзионная хроматография (SEC)
[00389] Аналитическую SEC выполняли с использованием прибора BioSECcurity (PSS Polymer) с колонкой AdvanceBio 300 (4,6 мм x 300 мм) и предколонкой AdvanceBio 300 (Agilent Technologies) при 25°C. Анализ проводили при скорости потока 0,5 мл/мин с использованием 2x концентрированного буфера D-PBS (Thermo Fisher Scientific) с выявлением при 280 нм. В колонку вносили 10 мкл образца белка (при концентрации 1 мг/мл). Оценку данных выполняли с использованием программного обеспечения WinGPC v8.1 (PSS Polymer). Для оценки молекулярной массы колонку SEC калибровали с помощью смеси калибровочных стандартов для белков (Agilent Technologies).
Аналитическая хроматография гидрофобного взаимодействия (HIC)
[00390] Аналитическую HIC выполняли на приборе для HPLC LC10 (Shimadzu) или на приборе для HPLC Vanquish (Thermo Fisher Scientific), оснащенном колонкой TSKgel бутил-NPR (2,5 мкм, 4,6×35 мм) (Tosoh Bioscience) при 25°C. Анализ проводили при скорости потока 1 мл/мин с выявлением при 280 нм. В колонку вносили 5 мкг неразбавленного образца белка. Градиентное элюирование проводили в условиях от 15% B до 85% B в течение 7 минут, затем в течение 1 минуты до 100% B, затем в течение 1 минуты до 15% B, а затем уравновешивание в течение 3 минут при 15% B. В состав буфер A входили 1,5 М сульфата аммония, 25 мМ фосфата натрия, pH 7,0. В состав буфера B входили 25 мМ фосфата натрия, pH 7,0. Оценку данных выполняли с использованием либо программного обеспечения LabSolutions v5.85 (Shimadzu), либо программного обеспечения Chromeleon 7 (Thermo Fisher Scientific).
nanoDSF
[00391] Температуру начала (Tonset) и точки плавления (Tm) денатурации белка определяли с использованием нано-дифференциальной сканирующей флуориметрии (nanoDSF). Образцы разбавляли в буфере для составления до конечной концентрации 0,5 мкг/мкл и загружали в капилляры для nanoDSF (Nanotemper Technologies) в двойных повторностях. Все измерения проводили с использованием устройства для nanoDSF Prometheus NT.plex (Nanotemper Technologies). Скорость нагрева составляла 1°C в минуту от 20°C до 95°C. Данные регистрировали с использованием программного обеспечения PR.ThermControl v2.3.1 (Nanotemper Technologies) и анализировали с использованием программного обеспечения PR.Stability Analysis v1.0.3 (Nanotemper Technologies).
Поверхностный плазмонный резонанс (SPR)
[00392] Связывание антигенов с конструкциями антител измеряли с использованием поверхностного плазмонного резонанса (SPR) с помощью прибора BIAcore 8K (GE Healthcare) с буфером HBS-EP (GE Healthcare). Для определения кинетики связывания и аффинности в качестве антигенов использовали слитые белки CD3εδ человека-Fc-His и CD123 человека-Fc-His (оба из собственного источника). Захватывающее антитело к His (набор для захвата His, GE Life Sciences) иммобилизовали посредством первичных аминогрупп (11000 RU) на чипе CM5 класса для исследований (GE Life Sciences) с использованием стандартных процедур. Антигены захватывались поверхностью чипа с захватывающим антителом к His при скорости потока 10 мкл/мин в течение 90 секунд для достижения уровня связывания антител от 10 до 30 RU. Антитела вводили в течение 240 секунд со скоростью 30 мкл/мин в серии двукратных разведений от 100 нМ до 3,1 нМ для определения аффинности с CD123 и от 400 нМ до 3,1 нМ или от 100 нМ до 3,1 нМ для определения аффинности связывания CD3. Диссоциацию измеряли при скорости 30 мкл/мин путем введения буфера HBS-EP+ в течение 1200 секунд. Поверхность чипа регенерировали путем введения регенерационного буфера (набор для захвата His, GE Life Sciences). Сенсограммы дважды сопоставляли с холостой поверхностью чипа и холостыми буферными растворами HBS-EP. Данные аппроксимировали с моделью связывания Ленгмюра 1:1 для определения констант кинетики и аффинности, ka, kd и KD, с использованием программного обеспечения для оценки Biacore 8K, v1.11.7442 (GE Healthcare).
[00393] Для оценки относительных уровней связывания (% Rmax) антител с CD3 и CD123 антитела захватывали с помощью аффинного захватывающего антитела к Fc на сенсорном чипе. В данном анализе использовали белки CD3εδ человека-FLAG-His (№ CT038-H2508H, Sino Biological) и CD123 человека (#301-R3/CF, R&D Systems). Захватывающее антитело к Fc человека (набор для захвата антител человека, GE Life Sciences) иммобилизовали посредством первичных аминогрупп (11000 RU) на чипе CM5 класса для исследований (GE Life Sciences) с использованием стандартных процедур. Захват антител выполняли при скорости потока 10 мкл/мин со скорректированным значением RU, что привело к максимальному связыванию аналита, составляющему 10-30 RU. Антигены использовали в качестве аналитов и вводили либо в концентрации 400 нМ и 100 нМ в случае CD3εδ-FLAG-His, либо в концентрации 100 нМ в случае CD123. Антигены вводили в течение 240 секунд с временем диссоциации 300 секунд при скорости потока 30 мкл/мин. Поверхности чипа регенерировали с помощью 2-минутных введений регенерирующего буфера, входящего в набор для захвата. Сенсограммы дважды сопоставляли с холостой поверхностью чипа и холостыми буферными растворами HBS-EP. Анализ данных и определение уровня связывания выполняли с использованием программного обеспечения для оценки Biacore 8K, v1.11.7442 (GE Healthcare). Значения % Rmax рассчитывали с использованием максимального уровня связывания, деленного на теоретическое значение Rmax. Теоретические значения Rmax рассчитывали на основе уровня захвата Rcapture, стехиометрии связывания N и молекулярной массы антитела Mw (Ab) и антигена Mw (Ag) с использованием формулы Rmax=Rcapture*N*(Mw (Ag)/Mw (Ab)).
Масс-спектрометрия
[00394] Целостность белка и возможное неправильное спаривание гетеродимерных конструкций анализировали посредством LC-масс-спектрометрии (LC-MS). Образцы белка подвергали дегликозилированию с использованием 12,5 мкг белка, разведенного до 0,17 мг/мл в воде класса для LC-MS (Thermo Scientific), обработанной 0,5 мкл PNGaseF (без глицерина, New England Biolabs), при 37°C в течение 16 часов. LC-MS анализ проводили с использованием масс-спектрометра Orbitrap Fusion Lumos Tribrid. Обращенно-фазовую (RP) хроматографию выполняли с использованием аналитической колонки для RP HPLC MabPac, размер частиц 4 мкм, 2,1×100 мм (Thermo Scientific) при скорости потока 300 мкл/мин. Элюентами были вода для LC, 0,1% муравьиной кислоты (A) и 90% ацетонитрила, 10% воды для LC, 0,1% муравьиной кислоты (B). Раствор с 2 мкг белка вводили в колонку и элюировали с использованием линейного градиента от 0% до 95% B в течение 12 минут. Анализ данных проводили с использованием программного обеспечения Expressionist 13.0.3 (Genedata). Молекулярные массы рассчитывали на основе аминокислотных последовательностей белков с использованием программного обеспечения GPMAW версии 10.32b1 (Lighthouse data).
Анализ цитотоксичности с использованием биспецифических молекул с TrasKO2
[00395] Проводили анализ биспецифических молекул с TrasKO2 в анализах цитотоксичности с использованием первичных Т-клеток человека. Мононуклеарные клетки периферической крови человека из крови здоровых доноров выделяли в пробирках Leucosep (Greiner Bio-One, № 227290) с использованием 15 мл Histopaque (Sigma-Aldrich, № 10771) и центрифугирования в течение 10 мин при 1000 x g. Выделенные PBMC дважды промывали в буфере для промывки autoMACS (Miltenyi Biotec, № 130-091-222), дополненном 5% исходным раствором BSA MACS (Miltenyi Biotec, № 130-091-370). Первичные Т-клетки человека выделяли из PBMC человека с помощью сепаратора MACSpro (Miltenyi Biotec) и набора для выделения T-клеток всех типов (Miltenyi Biotec, № 130-096-535) в соответствии с протоколами производителей. Выделенные Т-клетки человека ресуспендировали при концентрации 5×106 клеток/мл в среде RPMI GlutaMAX I (Gibco, № 72400), дополненной 10% FCS HI (Gibco, № 10082-147). Перед проведением анализа цитотоксичности целевые клетки THP-1 (ADCC TIB-202) окрашивали с помощью 1 мкМ CFSE (Invitrogen, № C1157) в течение 15 мин при 37°C. Клетки дважды промывали средой RPMI+ GlutaMAX I и центрифугировали при 400 x g в течение 5 мин. Целевые клетки THP-1 ресуспендировали при концентрации 5×105 клеток/мл в среде RPMI, дополненной 10% FCS HI. Меченные CFSE клетки THP-1 и T-клетки человека всех типов смешивали при соотношении эффектор/мишень 10:1 и высевали в общем объеме 100 мкл/лунка в 96-луночный аналитический планшет (Greiner BioOne, № 650185). Биспецифические молекулы с TrasKO2 добавляли в сериях по 11 разведений, начиная от 10 нМ - 0 нМ (разведение 1:6) в объеме 5 мкл/лунку к клеткам и инкубировали в течение 20 ч при 37°C и 5% CO2. После инкубации клетки окрашивали с помощью 5 мкг/мл 7-AAD (Invitrogen, № A1310) в течение 30 мин при 4°C. Для определения цитотоксичности мертвые целевые клетки измеряли путем гейтирования по клеткам THP-1, дважды положительным по CFSE/7-AAD, на проточном цитометре LSRII (BD), а значения EC50 определяли с использованием программного обеспечения Xlfit.
[00396] Домен dsTrasKO2 оценивали в качестве замещающего остова в структуре биспецифического антитела-активатора Т-клеток. Биспецифические активаторы Т-клеток создавали с использованием антитела к TCR α/β или одного из двух различных антител к CD3ε в качестве эффекторных плеч и антитела к CD123 в качестве нацеливающего плеча. Отрицательные контроли для обоих плеч создавали с использованием последовательностей антитела к TNP (антитело к тринитрофенолу). Биспецифические белки очищали посредством MabSelect Sure, затем KappaSelect и SEC. Биспецифические антитела экспрессировали либо в виде биспецифических IgG дикого типа (выявление встречающегося в природе неправильного спаривания), либо с заменой TrasKO2 на одном из плеч Fab (получали оба возможных сконструированных плеча Fab). Биофизические характеристики биспецифических антител описаны ниже в таблице 12.
Таблица 12. Определение биофизических характеристик конструкций антител-активаторов T-клеток с dsTrasKO2.
[% мономеров]
LC1+HC1 LC2+HC2,
[%]
LC1+HC1 LC1+HC2,
[%]
LC2+HC1 LC2+HC2,
[%]
x антитело к CD123
x антитело к TNP
[M]
(CD123)
[00397] В дополнение к вышеуказанному определению биофизических характеристик биспецифические проводили анализ молекул с TrasKO2 в клеточных анализах цитотоксичности. Как показано на фиг. 15А, все три биспецифических антитела со специфичностью антитело к CD3ε x антитело к CD123 продемонстрировали сопоставимую и устойчивую активность. Присутствие домена dsTrasKO2 в антителах с ID номерами 34 и 35 не оказывало негативного влияния на активность, при этом уменьшало неправильное спаривание цепей. В качестве отрицательных контролей использовали антитела с ID номерами 45 и 46, которые содержат последовательности антитела к TNP. Как показано на фиг. 15B, все три биспецифических антитела со специфичностью антитело к CD3ε x антитело к CD123, имеющие альтернативный связывающий домен для CD3ε, также продемонстрировали сравнимую и устойчивую активность. Присутствие домена dsTrasKO2 в антителах с ID номерами 37 и 38 не оказывало негативного влияния на активность, при этом уменьшало неправильное спаривание цепей. В качестве отрицательных контролей использовали антитела с ID номерами 47 и 48, которые содержат последовательности антитела к TNP.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SANOFI
<120> МУЛЬТИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ НА ОСНОВЕ ПСЕВДО-FAB
<130> 618078: SA9-240PC
<140> PCT/IB2019/061304
<141> 2019-12-23
<150> EP 19305813.8
<151> 2019-06-21
<150> EP 18306840.2
<151> 2018-12-24
<160> 206
<170> PatentIn версия 3.5
<210> 1
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 2
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 2
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 3
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 3
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Ala Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Ala Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 4
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 5
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 5
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Ala Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Ala Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 223
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 6
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 7
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 7
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Arg Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 8
<211> 228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 8
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
115 120 125
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
130 135 140
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys
145 150 155 160
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
165 170 175
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe
180 185 190
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
195 200 205
Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys
210 215 220
Val Glu Ile Lys
225
<210> 9
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 9
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 10
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 10
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 11
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 11
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 12
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 12
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Arg Tyr Asn Arg Ala Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
115 120 125
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
130 135 140
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
145 150 155 160
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
165 170 175
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
180 185 190
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
195 200 205
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215
<210> 13
<211> 472
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 13
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Trp Asn Ser Gly His Ile Asp Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ser Tyr Leu Ser Thr Ala Ser Ser Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Val
115 120 125
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
130 135 140
Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile
145 150 155 160
His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Arg
165 170 175
Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly
180 185 190
Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln
195 200 205
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg
210 215 220
Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro
245 250 255
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
260 265 270
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
275 280 285
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
290 295 300
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
305 310 315 320
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
325 330 335
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
340 345 350
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
355 360 365
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
370 375 380
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
385 390 395 400
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
405 410 415
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
420 425 430
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
435 440 445
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
450 455 460
Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 14
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Arg Tyr Asn Arg Ala Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 15
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 15
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Trp Asn Ser Gly His Ile Asp Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ser Tyr Leu Ser Thr Ala Ser Ser Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
370 375 380
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 16
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 16
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Arg Tyr Asn Arg Ala Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 17
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 17
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Trp Asn Ser Gly His Ile Asp Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ser Tyr Leu Ser Thr Ala Ser Ser Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 18
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
115 120 125
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
130 135 140
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
145 150 155 160
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
165 170 175
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
180 185 190
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
195 200 205
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215
<210> 19
<211> 470
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 19
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
His Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Met Leu Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ser Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
115 120 125
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
130 135 140
Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp
145 150 155 160
Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Arg Ile Tyr
165 170 175
Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe
180 185 190
Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn
195 200 205
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly
210 215 220
Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
225 230 235 240
Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
245 250 255
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
260 265 270
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
275 280 285
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
290 295 300
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
305 310 315 320
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
325 330 335
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
340 345 350
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
355 360 365
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
370 375 380
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
385 390 395 400
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
405 410 415
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
420 425 430
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
435 440 445
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
450 455 460
Leu Ser Leu Ser Pro Gly
465 470
<210> 20
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 20
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 21
<211> 475
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 21
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
His Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Met Leu Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ser Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
145 150 155 160
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp
165 170 175
Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser
180 185 190
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
225 230 235 240
Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro
245 250 255
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
260 265 270
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
275 280 285
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
290 295 300
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
305 310 315 320
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
325 330 335
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
340 345 350
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
355 360 365
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
370 375 380
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
385 390 395 400
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
405 410 415
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
420 425 430
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
435 440 445
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 22
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 23
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 23
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
His Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Met Leu Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ser Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 24
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 24
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
100 105 110
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
115 120 125
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr
130 135 140
Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
145 150 155 160
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
165 170 175
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
180 185 190
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro
195 200 205
Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 25
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 25
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Arg Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 26
<211> 225
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 26
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
100 105 110
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
115 120 125
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
130 135 140
Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys
145 150 155 160
Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val
165 170 175
Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr
180 185 190
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
195 200 205
His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile
210 215 220
Lys
225
<210> 27
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 27
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 28
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 28
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 29
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 29
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 30
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 30
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
115 120 125
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
130 135 140
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
145 150 155 160
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
165 170 175
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
180 185 190
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
195 200 205
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215
<210> 31
<211> 464
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 31
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
115 120 125
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
130 135 140
Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly
145 150 155 160
Lys Cys Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr
165 170 175
Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr
180 185 190
Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
195 200 205
Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala
210 215 220
Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys
225 230 235 240
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
245 250 255
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
260 265 270
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
275 280 285
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
290 295 300
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
305 310 315 320
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
325 330 335
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
340 345 350
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
355 360 365
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
370 375 380
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
385 390 395 400
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
405 410 415
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
420 425 430
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
435 440 445
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455 460
<210> 32
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 32
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 33
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 33
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Arg Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 34
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 34
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 35
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 35
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
340 345 350
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440
<210> 36
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 36
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
115 120 125
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
130 135 140
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
145 150 155 160
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
165 170 175
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
180 185 190
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
195 200 205
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215
<210> 37
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 37
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 38
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 38
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 39
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 39
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
130 135 140
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
145 150 155 160
Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys
165 170 175
Cys Leu Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg
180 185 190
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 40
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 40
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 41
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 41
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly
450
<210> 42
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 42
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 43
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 43
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 44
<211> 225
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 44
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
100 105 110
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
115 120 125
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
130 135 140
Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys
145 150 155 160
Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val
165 170 175
Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr
180 185 190
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
195 200 205
His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile
210 215 220
Lys
225
<210> 45
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 45
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 46
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 46
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 47
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 47
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
130 135 140
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
145 150 155 160
Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys
165 170 175
Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu
180 185 190
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 48
<211> 228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 48
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
115 120 125
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
130 135 140
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys
145 150 155 160
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
165 170 175
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe
180 185 190
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
195 200 205
Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys
210 215 220
Val Glu Ile Lys
225
<210> 49
<211> 259
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 49
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr His His His
245 250 255
His His His
<210> 50
<211> 228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 50
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
115 120 125
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
130 135 140
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys
145 150 155 160
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
165 170 175
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe
180 185 190
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
195 200 205
Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys
210 215 220
Val Glu Ile Lys
225
<210> 51
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 51
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Ala Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Ala Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 52
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 52
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 53
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 53
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
130 135 140
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
145 150 155 160
Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys
165 170 175
Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu
180 185 190
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 54
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 54
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 55
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 55
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp
340 345 350
Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440
<210> 56
<211> 228
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 56
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
115 120 125
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
130 135 140
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys
145 150 155 160
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
165 170 175
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe
180 185 190
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
195 200 205
Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys
210 215 220
Val Glu Ile Lys
225
<210> 57
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 57
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 58
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 58
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 59
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 59
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp
340 345 350
Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440
<210> 60
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 60
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 61
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 61
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 62
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 62
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 63
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 63
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys
355 360 365
Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 64
<211> 225
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 64
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
100 105 110
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
115 120 125
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
130 135 140
Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys
145 150 155 160
Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val
165 170 175
Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr
180 185 190
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
195 200 205
His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile
210 215 220
Lys
225
<210> 65
<211> 474
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 65
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
130 135 140
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
145 150 155 160
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
165 170 175
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
180 185 190
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470
<210> 66
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 66
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 67
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 67
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp
340 345 350
Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440
<210> 68
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Val Ser Val Gly
1 5 10 15
Asp Thr Ile Thr Leu Thr Cys His Ala Ser Gln Asn Ile Asp Val Trp
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Asn Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ala His Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 69
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 69
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile His Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Asp Pro Ser Asp Gly Glu Thr Arg Leu Asn Gln Arg Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Leu Lys Glu Tyr Gly Asn Tyr Asp Ser Phe Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
130 135 140
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
145 150 155 160
Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys
165 170 175
Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu
180 185 190
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 70
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 70
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Gln Ser Tyr Met His Trp Tyr Gln Gln Lys Ala Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Gln Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Asn Ala
85 90 95
Glu Asp Ser Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 71
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 71
Glu Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Gly Gly
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asp Ser
20 25 30
Ser Ile Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Arg Ile Asp Tyr Ala Asp Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Glu Met Thr Ser Leu Arg Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Gly Tyr Phe Pro Tyr Ala Met Asp Phe Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys
355 360 365
Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 72
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 72
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
130 135 140
Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
195 200 205
Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 73
<211> 469
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 73
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
115 120 125
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
130 135 140
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
145 150 155 160
Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro
165 170 175
Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
210 215 220
Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
225 230 235 240
Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
370 375 380
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly
465
<210> 74
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 74
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 75
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 75
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp
340 345 350
Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440
<210> 76
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 76
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
100 105
<210> 77
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 77
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Ala Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Ala Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 78
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 78
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 79
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 79
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Ala Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Ala Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 80
<211> 1331
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 80
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
210 215 220
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
225 230 235 240
Lys Phe Thr Ser Tyr Val Met His Trp Val Lys Gln Lys Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys
260 265 270
Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val His Tyr Cys Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe
305 310 315 320
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
325 330 335
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
340 345 350
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
355 360 365
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
370 375 380
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
385 390 395 400
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
405 410 415
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
420 425 430
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
435 440 445
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
450 455 460
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
465 470 475 480
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
485 490 495
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
500 505 510
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
515 520 525
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
530 535 540
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
545 550 555 560
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
565 570 575
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
580 585 590
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
595 600 605
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
610 615 620
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
625 630 635 640
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
645 650 655
Leu Ser Leu Ser Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu
660 665 670
Leu Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly
675 680 685
Tyr Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly
690 695 700
Lys Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr
705 710 715 720
Phe Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg
725 730 735
Ser Ser Ser Thr Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp
740 745 750
Ser Ala Val Tyr Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp
755 760 765
Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser
770 775 780
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
785 790 795 800
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
805 810 815
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
820 825 830
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
835 840 845
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
850 855 860
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
865 870 875 880
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
885 890 895
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
900 905 910
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
915 920 925
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
930 935 940
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
945 950 955 960
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
965 970 975
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
980 985 990
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
995 1000 1005
Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu
1010 1015 1020
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
1025 1030 1035
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
1040 1045 1050
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
1055 1060 1065
Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
1070 1075 1080
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
1085 1090 1095
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe
1100 1105 1110
Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu
1115 1120 1125
Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
1130 1135 1140
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly
1145 1150 1155
Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser
1160 1165 1170
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe
1175 1180 1185
Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr
1190 1195 1200
Tyr Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly
1205 1210 1215
Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
1220 1225 1230
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser
1235 1240 1245
Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val
1250 1255 1260
Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
1265 1270 1275
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
1280 1285 1290
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
1295 1300 1305
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
1310 1315 1320
Lys Ser Phe Asn Arg Gly Glu Cys
1325 1330
<210> 81
<211> 1368
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 81
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
210 215 220
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
225 230 235 240
Lys Phe Thr Ser Tyr Val Met His Trp Val Lys Gln Lys Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys
260 265 270
Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val His Tyr Cys Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe
305 310 315 320
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
325 330 335
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
340 345 350
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
355 360 365
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
370 375 380
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
385 390 395 400
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
405 410 415
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
420 425 430
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
435 440 445
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
450 455 460
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
465 470 475 480
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
485 490 495
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
500 505 510
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
515 520 525
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
530 535 540
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
545 550 555 560
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
565 570 575
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
580 585 590
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
595 600 605
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
610 615 620
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
625 630 635 640
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
645 650 655
Leu Ser Leu Ser Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu
660 665 670
Leu Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly
675 680 685
Tyr Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly
690 695 700
Lys Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr
705 710 715 720
Phe Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg
725 730 735
Ser Ser Ser Thr Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp
740 745 750
Ser Ala Val Tyr Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp
755 760 765
Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Gly Gly
770 775 780
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
785 790 795 800
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
805 810 815
Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala
820 825 830
Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly
835 840 845
Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala
850 855 860
Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala
865 870 875 880
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe
885 890 895
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
900 905 910
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
915 920 925
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
930 935 940
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
945 950 955 960
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
965 970 975
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
980 985 990
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
995 1000 1005
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
1010 1015 1020
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
1025 1030 1035
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
1040 1045 1050
Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp
1055 1060 1065
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
1070 1075 1080
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
1085 1090 1095
Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
1100 1105 1110
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
1115 1120 1125
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe Val Met Thr
1130 1135 1140
Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu Lys Val Thr
1145 1150 1155
Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln
1160 1165 1170
Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro
1175 1180 1185
Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro
1190 1195 1200
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
1205 1210 1215
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln
1220 1225 1230
Asn Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu
1235 1240 1245
Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
1250 1255 1260
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
1265 1270 1275
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
1280 1285 1290
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
1295 1300 1305
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe
1310 1315 1320
Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
1325 1330 1335
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
1340 1345 1350
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
1355 1360 1365
<210> 82
<211> 1368
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 82
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Glu
210 215 220
Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser
225 230 235 240
Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val
245 250 255
Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile Gly
260 265 270
Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys
275 280 285
Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr Met
290 295 300
Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys Ala
305 310 315 320
Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln Gly
325 330 335
Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly
340 345 350
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
355 360 365
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
370 375 380
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp
385 390 395 400
Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser
405 410 415
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
420 425 430
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
435 440 445
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
450 455 460
Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro
465 470 475 480
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
485 490 495
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
500 505 510
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
515 520 525
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
530 535 540
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
545 550 555 560
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
565 570 575
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
580 585 590
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
595 600 605
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
610 615 620
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
625 630 635 640
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
645 650 655
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
660 665 670
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
675 680 685
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln Leu Gln
690 695 700
Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys Met Ser
705 710 715 720
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val
725 730 735
Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro
740 745 750
Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr
755 760 765
Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu Asn Ser
770 775 780
Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser His Leu
785 790 795 800
Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
805 810 815
Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
820 825 830
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
835 840 845
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
850 855 860
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
865 870 875 880
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
885 890 895
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
900 905 910
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
915 920 925
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
930 935 940
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
945 950 955 960
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
965 970 975
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
980 985 990
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
995 1000 1005
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
1010 1015 1020
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
1025 1030 1035
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
1040 1045 1050
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
1055 1060 1065
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
1070 1075 1080
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
1085 1090 1095
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
1100 1105 1110
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
1115 1120 1125
Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu
1130 1135 1140
Ser Leu Ser Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser
1145 1150 1155
Leu Thr Val Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser
1160 1165 1170
Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr
1175 1180 1185
Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr
1190 1195 1200
Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly
1205 1210 1215
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln
1220 1225 1230
Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr
1235 1240 1245
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr
1250 1255 1260
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1265 1270 1275
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
1280 1285 1290
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
1295 1300 1305
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys
1310 1315 1320
Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
1325 1330 1335
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
1340 1345 1350
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1355 1360 1365
<210> 83
<211> 1330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 83
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu
210 215 220
Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr
225 230 235 240
Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn
260 265 270
Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp
305 310 315 320
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys
325 330 335
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
340 345 350
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
355 360 365
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
370 375 380
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
385 390 395 400
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
405 410 415
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
420 425 430
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
435 440 445
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
450 455 460
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
465 470 475 480
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
485 490 495
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
500 505 510
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
515 520 525
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
530 535 540
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
545 550 555 560
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
565 570 575
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
580 585 590
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
595 600 605
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
610 615 620
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
625 630 635 640
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
645 650 655
Ser Leu Ser Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
660 665 670
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
675 680 685
Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys
690 695 700
Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe
705 710 715 720
Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser
725 730 735
Ser Ser Thr Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser
740 745 750
Ala Val Tyr Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe
755 760 765
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
770 775 780
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
785 790 795 800
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
805 810 815
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
820 825 830
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
835 840 845
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
850 855 860
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
865 870 875 880
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
885 890 895
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
900 905 910
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
915 920 925
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
930 935 940
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
945 950 955 960
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
965 970 975
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
980 985 990
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
995 1000 1005
Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
1010 1015 1020
Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
1025 1030 1035
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
1040 1045 1050
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
1055 1060 1065
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
1070 1075 1080
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
1085 1090 1095
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe Val
1100 1105 1110
Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu Lys
1115 1120 1125
Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly
1130 1135 1140
Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
1145 1150 1155
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly
1160 1165 1170
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
1175 1180 1185
Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr
1190 1195 1200
Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
1205 1210 1215
Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1220 1225 1230
Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
1235 1240 1245
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln
1250 1255 1260
Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser
1265 1270 1275
Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
1280 1285 1290
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
1295 1300 1305
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
1310 1315 1320
Ser Phe Asn Arg Gly Glu Cys
1325 1330
<210> 84
<211> 1367
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 84
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu
210 215 220
Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr
225 230 235 240
Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn
260 265 270
Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp
305 310 315 320
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys
325 330 335
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
340 345 350
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
355 360 365
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
370 375 380
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
385 390 395 400
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
405 410 415
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
420 425 430
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
435 440 445
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
450 455 460
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
465 470 475 480
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
485 490 495
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
500 505 510
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
515 520 525
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
530 535 540
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
545 550 555 560
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
565 570 575
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
580 585 590
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
595 600 605
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
610 615 620
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
625 630 635 640
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
645 650 655
Ser Leu Ser Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
660 665 670
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
675 680 685
Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys
690 695 700
Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe
705 710 715 720
Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser
725 730 735
Ser Ser Thr Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser
740 745 750
Ala Val Tyr Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe
755 760 765
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly
770 775 780
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
785 790 795 800
Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser
805 810 815
Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro
820 825 830
Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr
835 840 845
Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp
850 855 860
Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
865 870 875 880
Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr
885 890 895
Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp
900 905 910
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
915 920 925
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
930 935 940
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
945 950 955 960
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
965 970 975
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
980 985 990
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
995 1000 1005
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
1010 1015 1020
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
1025 1030 1035
Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
1040 1045 1050
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile
1055 1060 1065
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
1070 1075 1080
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val
1085 1090 1095
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
1100 1105 1110
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr
1115 1120 1125
Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe Val Met Thr Gln
1130 1135 1140
Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu Lys Val Thr Met
1145 1150 1155
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys
1160 1165 1170
Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Lys
1175 1180 1185
Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
1190 1195 1200
Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
1205 1210 1215
Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
1220 1225 1230
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu
1235 1240 1245
Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
1250 1255 1260
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
1265 1270 1275
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val
1280 1285 1290
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
1295 1300 1305
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
1310 1315 1320
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
1325 1330 1335
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr
1340 1345 1350
Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
1355 1360 1365
<210> 85
<211> 1367
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 85
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Asp
210 215 220
Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala Ser
225 230 235 240
Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr Thr
245 250 255
Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly
260 265 270
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe Lys
275 280 285
Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr Met
290 295 300
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala
305 310 315 320
Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly Thr
325 330 335
Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
340 345 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
355 360 365
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
370 375 380
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
385 390 395 400
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
405 410 415
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
420 425 430
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
435 440 445
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
450 455 460
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
595 600 605
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln Leu Gln Gln
690 695 700
Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys
705 710 715 720
Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys Trp Val Lys
725 730 735
Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile Ile Pro Ser
740 745 750
Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu
755 760 765
Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu Asn Ser Leu
770 775 780
Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser His Leu Leu
785 790 795 800
Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
805 810 815
Ser Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
820 825 830
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
835 840 845
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
850 855 860
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
865 870 875 880
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
885 890 895
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
900 905 910
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
915 920 925
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
930 935 940
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
945 950 955 960
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
965 970 975
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
980 985 990
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
995 1000 1005
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
1010 1015 1020
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
1025 1030 1035
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro
1040 1045 1050
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys
1055 1060 1065
Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
1070 1075 1080
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
1085 1090 1095
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
1100 1105 1110
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
1115 1120 1125
Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser
1130 1135 1140
Leu Ser Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu
1145 1150 1155
Thr Val Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser Ser
1160 1165 1170
Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr Trp
1175 1180 1185
Tyr Leu Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp
1190 1195 1200
Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
1205 1210 1215
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala
1220 1225 1230
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr Pro
1235 1240 1245
Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val
1250 1255 1260
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
1265 1270 1275
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
1280 1285 1290
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
1295 1300 1305
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
1310 1315 1320
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp
1325 1330 1335
Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly
1340 1345 1350
Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1355 1360 1365
<210> 86
<211> 1338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 86
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Val Gln Leu Val
210 215 220
Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser
225 230 235 240
Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val
245 250 255
Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp
260 265 270
Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg
275 280 285
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met
290 295 300
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val
305 310 315 320
Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln
660 665 670
Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys
675 680 685
Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys
690 695 700
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile
705 710 715 720
Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys
725 730 735
Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu
740 745 750
Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser
755 760 765
His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
770 775 780
Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
785 790 795 800
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
805 810 815
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
820 825 830
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
835 840 845
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
850 855 860
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
865 870 875 880
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
885 890 895
Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val
900 905 910
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
915 920 925
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
930 935 940
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
945 950 955 960
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
965 970 975
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
980 985 990
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
995 1000 1005
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
1010 1015 1020
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
1025 1030 1035
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
1040 1045 1050
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
1055 1060 1065
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
1070 1075 1080
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
1085 1090 1095
Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu
1100 1105 1110
Ser Leu Ser Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser
1115 1120 1125
Leu Thr Val Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser
1130 1135 1140
Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr
1145 1150 1155
Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr
1160 1165 1170
Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly
1175 1180 1185
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln
1190 1195 1200
Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr
1205 1210 1215
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr
1220 1225 1230
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1235 1240 1245
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
1250 1255 1260
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
1265 1270 1275
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys
1280 1285 1290
Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
1295 1300 1305
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
1310 1315 1320
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1325 1330 1335
<210> 87
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 87
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Val Gln Leu Val
210 215 220
Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser
225 230 235 240
Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val
245 250 255
Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp
260 265 270
Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg
275 280 285
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met
290 295 300
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val
305 310 315 320
Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln
660 665 670
Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys
675 680 685
Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys
690 695 700
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile
705 710 715 720
Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys
725 730 735
Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu
740 745 750
Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser
755 760 765
His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
770 775 780
Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
785 790 795 800
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
805 810 815
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
820 825 830
Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala
835 840 845
Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys
850 855 860
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
865 870 875 880
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
885 890 895
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
900 905 910
Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys
915 920 925
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
930 935 940
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
945 950 955 960
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
965 970 975
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
980 985 990
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
995 1000 1005
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
1010 1015 1020
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
1025 1030 1035
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
1040 1045 1050
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
1055 1060 1065
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
1070 1075 1080
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
1085 1090 1095
Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
1100 1105 1110
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
1115 1120 1125
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
1130 1135 1140
Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val
1145 1150 1155
Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser
1160 1165 1170
Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu
1175 1180 1185
Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser
1190 1195 1200
Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
1205 1210 1215
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp
1220 1225 1230
Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr
1235 1240 1245
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
1250 1255 1260
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
1265 1270 1275
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
1280 1285 1290
Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro
1295 1300 1305
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
1310 1315 1320
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
1325 1330 1335
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
1340 1345 1350
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys
1355 1360 1365
Gly Thr Lys Val Glu Ile Lys
1370 1375
<210> 88
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 88
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
225 230 235 240
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
245 250 255
Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln Ala Pro Gly Lys
260 265 270
Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala
275 280 285
Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
290 295 300
Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
305 310 315 320
Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro
325 330 335
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
340 345 350
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
355 360 365
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
370 375 380
Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala
385 390 395 400
Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly
405 410 415
Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala
420 425 430
Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala
435 440 445
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe
450 455 460
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
465 470 475 480
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
485 490 495
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
500 505 510
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
515 520 525
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
530 535 540
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
545 550 555 560
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
565 570 575
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
580 585 590
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
595 600 605
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
610 615 620
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
625 630 635 640
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
645 650 655
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
660 665 670
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
675 680 685
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
690 695 700
Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro
705 710 715 720
Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
725 730 735
Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu
740 745 750
Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln
755 760 765
Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr
770 775 780
Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr
785 790 795 800
Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp
805 810 815
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro
820 825 830
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
835 840 845
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
850 855 860
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
865 870 875 880
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
885 890 895
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
900 905 910
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
915 920 925
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
930 935 940
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
945 950 955 960
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
965 970 975
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
980 985 990
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
995 1000 1005
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
1010 1015 1020
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
1025 1030 1035
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
1040 1045 1050
Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
1055 1060 1065
Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
1070 1075 1080
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
1085 1090 1095
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
1100 1105 1110
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
1115 1120 1125
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
1130 1135 1140
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe Val
1145 1150 1155
Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu Lys
1160 1165 1170
Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly
1175 1180 1185
Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
1190 1195 1200
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly
1205 1210 1215
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
1220 1225 1230
Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr
1235 1240 1245
Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
1250 1255 1260
Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1265 1270 1275
Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
1280 1285 1290
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln
1295 1300 1305
Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser
1310 1315 1320
Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
1325 1330 1335
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
1340 1345 1350
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
1355 1360 1365
Ser Phe Asn Arg Gly Glu Cys
1370 1375
<210> 89
<211> 1331
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 89
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
210 215 220
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
225 230 235 240
Lys Phe Thr Ser Tyr Val Met His Trp Val Lys Gln Lys Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys
260 265 270
Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val His Tyr Cys Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe
305 310 315 320
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
325 330 335
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
340 345 350
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
355 360 365
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
370 375 380
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
385 390 395 400
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
405 410 415
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
420 425 430
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
435 440 445
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
450 455 460
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
465 470 475 480
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
485 490 495
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
500 505 510
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
515 520 525
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
530 535 540
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
545 550 555 560
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
565 570 575
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
580 585 590
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
595 600 605
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
610 615 620
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
625 630 635 640
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
645 650 655
Leu Ser Leu Ser Pro Gly Gln Ile Gln Leu Val Gln Ser Gly Ser Glu
660 665 670
Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly
675 680 685
Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly
690 695 700
Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro
705 710 715 720
Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr
725 730 735
Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp
740 745 750
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp
755 760 765
Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Ala
770 775 780
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
785 790 795 800
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
805 810 815
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
820 825 830
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
835 840 845
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
850 855 860
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
865 870 875 880
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
885 890 895
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
900 905 910
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
915 920 925
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
930 935 940
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
945 950 955 960
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
965 970 975
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
980 985 990
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
995 1000 1005
Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu
1010 1015 1020
Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
1025 1030 1035
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
1040 1045 1050
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
1055 1060 1065
Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
1070 1075 1080
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
1085 1090 1095
His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp
1100 1105 1110
Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1115 1120 1125
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His
1130 1135 1140
Ser Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly
1145 1150 1155
Gln Ser Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser
1160 1165 1170
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
1175 1180 1185
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
1190 1195 1200
Tyr Cys Ser Gln Ser Thr His Val Pro Phe Thr Phe Gly Gln Gly
1205 1210 1215
Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
1220 1225 1230
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser
1235 1240 1245
Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val
1250 1255 1260
Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
1265 1270 1275
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
1280 1285 1290
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
1295 1300 1305
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
1310 1315 1320
Lys Ser Phe Asn Arg Gly Glu Cys
1325 1330
<210> 90
<211> 1368
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 90
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
210 215 220
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
225 230 235 240
Lys Phe Thr Ser Tyr Val Met His Trp Val Lys Gln Lys Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys
260 265 270
Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val His Tyr Cys Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe
305 310 315 320
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
325 330 335
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
340 345 350
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
355 360 365
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
370 375 380
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
385 390 395 400
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
405 410 415
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
420 425 430
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
435 440 445
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
450 455 460
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
465 470 475 480
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
485 490 495
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
500 505 510
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
515 520 525
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
530 535 540
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
545 550 555 560
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
565 570 575
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
580 585 590
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
595 600 605
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
610 615 620
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
625 630 635 640
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
645 650 655
Leu Ser Leu Ser Pro Gly Gln Ile Gln Leu Val Gln Ser Gly Ser Glu
660 665 670
Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly
675 680 685
Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly
690 695 700
Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro
705 710 715 720
Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr
725 730 735
Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp
740 745 750
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp
755 760 765
Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
770 775 780
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
785 790 795 800
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
805 810 815
Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln
820 825 830
Ala Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn
835 840 845
Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
850 855 860
Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg
865 870 875 880
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly
885 890 895
Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
900 905 910
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
915 920 925
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
930 935 940
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
945 950 955 960
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
965 970 975
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
980 985 990
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
995 1000 1005
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
1010 1015 1020
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
1025 1030 1035
Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
1040 1045 1050
Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser
1055 1060 1065
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
1070 1075 1080
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
1085 1090 1095
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
1100 1105 1110
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg
1115 1120 1125
Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Val Val Met
1130 1135 1140
Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala
1145 1150 1155
Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser Ile Gly
1160 1165 1170
Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro
1175 1180 1185
Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
1190 1195 1200
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys
1205 1210 1215
Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser
1220 1225 1230
Gln Ser Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu
1235 1240 1245
Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
1250 1255 1260
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
1265 1270 1275
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
1280 1285 1290
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
1295 1300 1305
Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe
1310 1315 1320
Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
1325 1330 1335
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
1340 1345 1350
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
1355 1360 1365
<210> 91
<211> 1368
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 91
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Glu
210 215 220
Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser
225 230 235 240
Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val
245 250 255
Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile Gly
260 265 270
Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys
275 280 285
Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr Met
290 295 300
Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys Ala
305 310 315 320
Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln Gly
325 330 335
Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly
340 345 350
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
355 360 365
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
370 375 380
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp
385 390 395 400
Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser
405 410 415
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
420 425 430
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
435 440 445
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
450 455 460
Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro
465 470 475 480
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
485 490 495
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
500 505 510
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
515 520 525
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
530 535 540
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
545 550 555 560
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
565 570 575
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
580 585 590
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
595 600 605
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
610 615 620
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
625 630 635 640
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
645 650 655
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
660 665 670
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
675 680 685
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Gln Ile Gln Leu Val
690 695 700
Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser
705 710 715 720
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val
725 730 735
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr
740 745 750
Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val
755 760 765
Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser
770 775 780
Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr
785 790 795 800
Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val
805 810 815
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
820 825 830
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
835 840 845
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
850 855 860
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
865 870 875 880
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
885 890 895
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
900 905 910
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
915 920 925
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
930 935 940
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
945 950 955 960
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
965 970 975
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
980 985 990
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
995 1000 1005
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
1010 1015 1020
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
1025 1030 1035
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
1040 1045 1050
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
1055 1060 1065
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
1070 1075 1080
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
1085 1090 1095
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
1100 1105 1110
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
1115 1120 1125
Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser
1130 1135 1140
Leu Ser Leu Ser Pro Gly Asp Val Val Met Thr Gln Ser Pro Leu
1145 1150 1155
Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Arg
1160 1165 1170
Ser Ser Gln Ser Leu Val His Ser Ile Gly Asn Thr Tyr Leu His
1175 1180 1185
Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Arg Leu Leu Ile Tyr
1190 1195 1200
Lys Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly
1205 1210 1215
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu
1220 1225 1230
Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val
1235 1240 1245
Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr
1250 1255 1260
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1265 1270 1275
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
1280 1285 1290
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
1295 1300 1305
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys
1310 1315 1320
Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
1325 1330 1335
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
1340 1345 1350
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1355 1360 1365
<210> 92
<211> 1338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 92
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Ile Gln Leu Val
210 215 220
Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser
225 230 235 240
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val
245 250 255
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr
260 265 270
Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val
275 280 285
Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser
290 295 300
Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr
305 310 315 320
Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln
660 665 670
Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys
675 680 685
Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys
690 695 700
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile
705 710 715 720
Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys
725 730 735
Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu
740 745 750
Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser
755 760 765
His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
770 775 780
Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
785 790 795 800
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
805 810 815
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
820 825 830
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
835 840 845
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
850 855 860
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
865 870 875 880
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
885 890 895
Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val
900 905 910
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
915 920 925
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
930 935 940
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
945 950 955 960
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
965 970 975
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
980 985 990
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
995 1000 1005
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
1010 1015 1020
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
1025 1030 1035
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
1040 1045 1050
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
1055 1060 1065
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
1070 1075 1080
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
1085 1090 1095
Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu
1100 1105 1110
Ser Leu Ser Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser
1115 1120 1125
Leu Thr Val Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser
1130 1135 1140
Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr
1145 1150 1155
Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr
1160 1165 1170
Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly
1175 1180 1185
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln
1190 1195 1200
Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr
1205 1210 1215
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr
1220 1225 1230
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1235 1240 1245
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
1250 1255 1260
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
1265 1270 1275
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys
1280 1285 1290
Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
1295 1300 1305
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
1310 1315 1320
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1325 1330 1335
<210> 93
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 93
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Ile Gln Leu Val
210 215 220
Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser
225 230 235 240
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val
245 250 255
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr
260 265 270
Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val
275 280 285
Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser
290 295 300
Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr
305 310 315 320
Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Glu Val Gln
660 665 670
Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys
675 680 685
Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys
690 695 700
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Asp Ile
705 710 715 720
Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe Lys Gly Lys
725 730 735
Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr Met His Leu
740 745 750
Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser
755 760 765
His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
770 775 780
Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
785 790 795 800
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
805 810 815
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr
820 825 830
Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val Ala
835 840 845
Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val Lys
850 855 860
Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu
865 870 875 880
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser
885 890 895
Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly
900 905 910
Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys
915 920 925
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
930 935 940
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
945 950 955 960
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
965 970 975
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
980 985 990
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
995 1000 1005
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
1010 1015 1020
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
1025 1030 1035
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
1040 1045 1050
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
1055 1060 1065
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
1070 1075 1080
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
1085 1090 1095
Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
1100 1105 1110
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
1115 1120 1125
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
1130 1135 1140
Pro Gly Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val
1145 1150 1155
Thr Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser
1160 1165 1170
Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu
1175 1180 1185
Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser
1190 1195 1200
Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
1205 1210 1215
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp
1220 1225 1230
Leu Ala Val Tyr Tyr Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr
1235 1240 1245
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
1250 1255 1260
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
1265 1270 1275
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
1280 1285 1290
Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro
1295 1300 1305
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
1310 1315 1320
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
1325 1330 1335
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
1340 1345 1350
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys
1355 1360 1365
Gly Thr Lys Val Glu Ile Lys
1370 1375
<210> 94
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 94
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu
225 230 235 240
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
245 250 255
Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln
260 265 270
Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys
275 280 285
Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser
290 295 300
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
305 310 315 320
Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr
325 330 335
Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly
340 345 350
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
355 360 365
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
370 375 380
Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala
385 390 395 400
Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly
405 410 415
Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala
420 425 430
Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala
435 440 445
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe
450 455 460
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
465 470 475 480
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
485 490 495
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
500 505 510
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
515 520 525
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
530 535 540
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
545 550 555 560
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
565 570 575
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
580 585 590
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
595 600 605
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
610 615 620
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
625 630 635 640
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
645 650 655
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
660 665 670
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
675 680 685
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
690 695 700
Pro Gly Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro
705 710 715 720
Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
725 730 735
Asp Tyr Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu
740 745 750
Trp Ile Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln
755 760 765
Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr
770 775 780
Ala Tyr Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr
785 790 795 800
Tyr Cys Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp
805 810 815
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro
820 825 830
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
835 840 845
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
850 855 860
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
865 870 875 880
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
885 890 895
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
900 905 910
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
915 920 925
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
930 935 940
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
945 950 955 960
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
965 970 975
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
980 985 990
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
995 1000 1005
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
1010 1015 1020
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
1025 1030 1035
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
1040 1045 1050
Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
1055 1060 1065
Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro
1070 1075 1080
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
1085 1090 1095
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
1100 1105 1110
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
1115 1120 1125
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
1130 1135 1140
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Phe Val
1145 1150 1155
Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly Glu Lys
1160 1165 1170
Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly
1175 1180 1185
Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
1190 1195 1200
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly
1205 1210 1215
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
1220 1225 1230
Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr
1235 1240 1245
Cys Gln Asn Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
1250 1255 1260
Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1265 1270 1275
Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
1280 1285 1290
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln
1295 1300 1305
Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser
1310 1315 1320
Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
1325 1330 1335
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
1340 1345 1350
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
1355 1360 1365
Ser Phe Asn Arg Gly Glu Cys
1370 1375
<210> 95
<211> 1330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 95
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu
210 215 220
Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr
225 230 235 240
Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn
260 265 270
Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp
305 310 315 320
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys
325 330 335
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
340 345 350
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
355 360 365
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
370 375 380
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
385 390 395 400
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
405 410 415
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
420 425 430
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
435 440 445
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
450 455 460
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
465 470 475 480
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
485 490 495
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
500 505 510
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
515 520 525
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
530 535 540
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
545 550 555 560
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
565 570 575
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
580 585 590
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
595 600 605
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
610 615 620
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
625 630 635 640
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
645 650 655
Ser Leu Ser Pro Gly Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu
660 665 670
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
675 680 685
Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln
690 695 700
Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys
705 710 715 720
Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser
725 730 735
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
740 745 750
Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr
755 760 765
Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser
770 775 780
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
785 790 795 800
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
805 810 815
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
820 825 830
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
835 840 845
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
850 855 860
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
865 870 875 880
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
885 890 895
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
900 905 910
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
915 920 925
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
930 935 940
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
945 950 955 960
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
965 970 975
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
980 985 990
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
995 1000 1005
Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu
1010 1015 1020
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
1025 1030 1035
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
1040 1045 1050
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
1055 1060 1065
Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
1070 1075 1080
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
1085 1090 1095
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Val
1100 1105 1110
Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln
1115 1120 1125
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
1130 1135 1140
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln
1145 1150 1155
Ser Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly
1160 1165 1170
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1175 1180 1185
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
1190 1195 1200
Cys Ser Gln Ser Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr
1205 1210 1215
Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1220 1225 1230
Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
1235 1240 1245
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln
1250 1255 1260
Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser
1265 1270 1275
Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
1280 1285 1290
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
1295 1300 1305
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
1310 1315 1320
Ser Phe Asn Arg Gly Glu Cys
1325 1330
<210> 96
<211> 1367
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 96
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu
210 215 220
Ala Arg Pro Gly Ala Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr
225 230 235 240
Thr Phe Thr Arg Tyr Thr Met His Trp Val Lys Gln Arg Pro Gly Gln
245 250 255
Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn
260 265 270
Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser
275 280 285
Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser
290 295 300
Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp
305 310 315 320
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys
325 330 335
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
340 345 350
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
355 360 365
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
370 375 380
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
385 390 395 400
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
405 410 415
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
420 425 430
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
435 440 445
Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
450 455 460
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
465 470 475 480
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
485 490 495
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
500 505 510
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
515 520 525
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
530 535 540
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
545 550 555 560
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn
565 570 575
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
580 585 590
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
595 600 605
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
610 615 620
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
625 630 635 640
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
645 650 655
Ser Leu Ser Pro Gly Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu
660 665 670
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
675 680 685
Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln
690 695 700
Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys
705 710 715 720
Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser
725 730 735
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
740 745 750
Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr
755 760 765
Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly
770 775 780
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
785 790 795 800
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
805 810 815
Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala
820 825 830
Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly
835 840 845
Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala
850 855 860
Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala
865 870 875 880
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe
885 890 895
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
900 905 910
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
915 920 925
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
930 935 940
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
945 950 955 960
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
965 970 975
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
980 985 990
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
995 1000 1005
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
1010 1015 1020
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
1025 1030 1035
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
1040 1045 1050
Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp
1055 1060 1065
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
1070 1075 1080
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
1085 1090 1095
Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
1100 1105 1110
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
1115 1120 1125
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Val Val Met Thr
1130 1135 1140
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser
1145 1150 1155
Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser Ile Gly Asn
1160 1165 1170
Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Arg
1175 1180 1185
Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro Asp
1190 1195 1200
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
1205 1210 1215
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln
1220 1225 1230
Ser Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu
1235 1240 1245
Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
1250 1255 1260
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
1265 1270 1275
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val
1280 1285 1290
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
1295 1300 1305
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser
1310 1315 1320
Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
1325 1330 1335
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr
1340 1345 1350
Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
1355 1360 1365
<210> 97
<211> 1367
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 97
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Asp
210 215 220
Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala Ser
225 230 235 240
Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr Thr
245 250 255
Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly
260 265 270
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe Lys
275 280 285
Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr Met
290 295 300
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala
305 310 315 320
Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly Thr
325 330 335
Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
340 345 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
355 360 365
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
370 375 380
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
385 390 395 400
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
405 410 415
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
420 425 430
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
435 440 445
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
450 455 460
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
595 600 605
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Gln Ile Gln Leu Val Gln
690 695 700
Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys
705 710 715 720
Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Arg
725 730 735
Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile Asn Thr Tyr
740 745 750
Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe
755 760 765
Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu
770 775 780
Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Ile Tyr Asp
785 790 795 800
Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr Leu Val Thr
805 810 815
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
820 825 830
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
835 840 845
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
850 855 860
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
865 870 875 880
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
885 890 895
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
900 905 910
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
915 920 925
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
930 935 940
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
945 950 955 960
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
965 970 975
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
980 985 990
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
995 1000 1005
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
1010 1015 1020
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
1025 1030 1035
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu
1040 1045 1050
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
1055 1060 1065
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
1070 1075 1080
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
1085 1090 1095
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
1100 1105 1110
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
1115 1120 1125
Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu
1130 1135 1140
Ser Leu Ser Pro Gly Asp Val Val Met Thr Gln Ser Pro Leu Ser
1145 1150 1155
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Arg Ser
1160 1165 1170
Ser Gln Ser Leu Val His Ser Ile Gly Asn Thr Tyr Leu His Trp
1175 1180 1185
Tyr Gln Gln Arg Pro Gly Gln Ser Pro Arg Leu Leu Ile Tyr Lys
1190 1195 1200
Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
1205 1210 1215
Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
1220 1225 1230
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro
1235 1240 1245
Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val
1250 1255 1260
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
1265 1270 1275
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
1280 1285 1290
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
1295 1300 1305
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
1310 1315 1320
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp
1325 1330 1335
Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly
1340 1345 1350
Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1355 1360 1365
<210> 98
<211> 1338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 98
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Val Gln Leu Val
210 215 220
Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser
225 230 235 240
Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val
245 250 255
Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp
260 265 270
Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg
275 280 285
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met
290 295 300
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val
305 310 315 320
Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Gln Ile Gln
660 665 670
Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys
675 680 685
Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn
690 695 700
Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile
705 710 715 720
Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg
725 730 735
Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile
740 745 750
Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly
755 760 765
Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr
770 775 780
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
785 790 795 800
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
805 810 815
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
820 825 830
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
835 840 845
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
850 855 860
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
865 870 875 880
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
885 890 895
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser
900 905 910
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
915 920 925
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
930 935 940
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
945 950 955 960
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
965 970 975
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
980 985 990
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
995 1000 1005
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
1010 1015 1020
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
1025 1030 1035
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
1040 1045 1050
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
1055 1060 1065
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
1070 1075 1080
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
1085 1090 1095
Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser
1100 1105 1110
Leu Ser Leu Ser Pro Gly Asp Val Val Met Thr Gln Ser Pro Leu
1115 1120 1125
Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Arg
1130 1135 1140
Ser Ser Gln Ser Leu Val His Ser Ile Gly Asn Thr Tyr Leu His
1145 1150 1155
Trp Tyr Gln Gln Arg Pro Gly Gln Ser Pro Arg Leu Leu Ile Tyr
1160 1165 1170
Lys Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly
1175 1180 1185
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu
1190 1195 1200
Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val
1205 1210 1215
Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr
1220 1225 1230
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1235 1240 1245
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
1250 1255 1260
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
1265 1270 1275
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys
1280 1285 1290
Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
1295 1300 1305
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
1310 1315 1320
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
1325 1330 1335
<210> 99
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 99
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gln Val Gln Leu Val
210 215 220
Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser
225 230 235 240
Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val
245 250 255
Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp
260 265 270
Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg
275 280 285
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met
290 295 300
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val
305 310 315 320
Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
325 330 335
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
340 345 350
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
355 360 365
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
370 375 380
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
385 390 395 400
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
405 410 415
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
420 425 430
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
435 440 445
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
450 455 460
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
465 470 475 480
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
485 490 495
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
500 505 510
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
515 520 525
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
530 535 540
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
545 550 555 560
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
565 570 575
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
580 585 590
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
595 600 605
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
610 615 620
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
625 630 635 640
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
645 650 655
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Gln Ile Gln
660 665 670
Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys
675 680 685
Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn
690 695 700
Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val Gly Trp Ile
705 710 715 720
Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe Thr Gly Arg
725 730 735
Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile
740 745 750
Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly
755 760 765
Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly Arg Gly Thr
770 775 780
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
785 790 795 800
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
805 810 815
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
820 825 830
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Val
835 840 845
Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser Val
850 855 860
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
865 870 875 880
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
885 890 895
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
900 905 910
Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro Pro
915 920 925
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
930 935 940
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
945 950 955 960
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
965 970 975
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
980 985 990
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
995 1000 1005
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
1010 1015 1020
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
1025 1030 1035
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
1040 1045 1050
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala
1055 1060 1065
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
1070 1075 1080
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
1085 1090 1095
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
1100 1105 1110
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
1115 1120 1125
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu
1130 1135 1140
Ser Pro Gly Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro
1145 1150 1155
Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln
1160 1165 1170
Ser Leu Val His Ser Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln
1175 1180 1185
Gln Arg Pro Gly Gln Ser Pro Arg Leu Leu Ile Tyr Lys Val Ser
1190 1195 1200
Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser
1205 1210 1215
Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
1220 1225 1230
Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Phe Thr
1235 1240 1245
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
1250 1255 1260
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
1265 1270 1275
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
1280 1285 1290
Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro
1295 1300 1305
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr
1310 1315 1320
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
1325 1330 1335
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
1340 1345 1350
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys
1355 1360 1365
Gly Thr Lys Val Glu Ile Lys
1370 1375
<210> 100
<211> 1375
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 100
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
225 230 235 240
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
245 250 255
Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln Ala Pro Gly Lys
260 265 270
Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala
275 280 285
Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
290 295 300
Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
305 310 315 320
Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro
325 330 335
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
340 345 350
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
355 360 365
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
370 375 380
Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala
385 390 395 400
Pro Gly Lys Cys Leu Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly
405 410 415
Tyr Thr Glu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala
420 425 430
Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala
435 440 445
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe
450 455 460
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
465 470 475 480
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
485 490 495
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
500 505 510
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
515 520 525
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
530 535 540
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
545 550 555 560
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
565 570 575
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
580 585 590
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
595 600 605
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
610 615 620
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
625 630 635 640
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
645 650 655
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
660 665 670
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
675 680 685
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
690 695 700
Pro Gly Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro
705 710 715 720
Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
725 730 735
Asn Tyr Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu
740 745 750
Trp Val Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln
755 760 765
Gly Phe Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr
770 775 780
Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr
785 790 795 800
Tyr Cys Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val
805 810 815
Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
820 825 830
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
835 840 845
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
850 855 860
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
865 870 875 880
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
885 890 895
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
900 905 910
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
915 920 925
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
930 935 940
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
945 950 955 960
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
965 970 975
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
980 985 990
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
995 1000 1005
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
1010 1015 1020
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
1025 1030 1035
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
1040 1045 1050
Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu
1055 1060 1065
Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
1070 1075 1080
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
1085 1090 1095
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
1100 1105 1110
Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
1115 1120 1125
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
1130 1135 1140
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Asp Val
1145 1150 1155
Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln
1160 1165 1170
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
1175 1180 1185
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln
1190 1195 1200
Ser Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly
1205 1210 1215
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1220 1225 1230
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
1235 1240 1245
Cys Ser Gln Ser Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr
1250 1255 1260
Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile
1265 1270 1275
Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
1280 1285 1290
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln
1295 1300 1305
Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser
1310 1315 1320
Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
1325 1330 1335
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
1340 1345 1350
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
1355 1360 1365
Ser Phe Asn Arg Gly Glu Cys
1370 1375
<210> 101
<211> 50
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> Сайт
<222> (1)..(50)
<223> /примечание="Эта последовательность может охватывать
1-10 повторяющихся звеньев "Gly Gly Gly Gly Ser"
<400> 101
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
35 40 45
Gly Ser
50
<210> 102
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 102
Gly Gly Gly Gly Ser
1 5
<210> 103
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 103
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 104
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 104
Gly Gly Gly Gly
1
<210> 105
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 105
Gly Gly Gly Gly Gly
1 5
<210> 106
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 106
Gly Gly Gly Gly Gly Gly
1 5
<210> 107
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 107
Gly Gly Gly Gly Gly Gly Gly
1 5
<210> 108
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 108
Gly Gly Gly Gly Gly Gly Gly Gly
1 5
<210> 109
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 109
Gly Gly Gly Ser
1
<210> 110
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 111
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 111
Gly Gly Ser Gly Ser Ser Gly Ser Gly Gly
1 5 10
<210> 112
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 112
Thr Lys Gly Pro Ser
1 5
<210> 113
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 113
Thr Val Ala Ala Pro
1 5
<210> 114
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 114
Gln Pro Lys Ala Ala
1 5
<210> 115
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 115
Gln Arg Ile Glu Gly
1 5
<210> 116
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 116
Ala Ser Thr Lys Gly Pro Ser
1 5
<210> 117
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 117
Arg Thr Val Ala Ala Pro Ser
1 5
<210> 118
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 118
Gly Gln Pro Lys Ala Ala Pro
1 5
<210> 119
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 119
His Ile Asp Ser Pro Asn Lys
1 5
<210> 120
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 120
Asp Lys Thr His Thr
1 5
<210> 121
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 121
Thr Lys Gly Pro Ser Arg
1 5
<210> 122
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> Сайт
<222> (1)..(25)
<223> /примечание="Эта последовательность может охватывать
0-5 повторяющихся звеньев "Gly Gly Gly Gly Ser"
<400> 122
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 123
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 123
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 124
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 124
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 125
<211> 223
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 125
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 126
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 126
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 127
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 127
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 128
<211> 223
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 128
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 129
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 129
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 130
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 130
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 131
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 131
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 132
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 132
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 133
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 133
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 134
<211> 223
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 134
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 135
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 135
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 136
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 136
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 137
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 137
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 138
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 138
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 139
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 139
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 140
<211> 223
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 140
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
115 120 125
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
130 135 140
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
145 150 155 160
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
165 170 175
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
180 185 190
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
195 200 205
Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys
210 215 220
<210> 141
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 141
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 142
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 142
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 143
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 143
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 144
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 144
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 145
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 145
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 146
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 146
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 147
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 147
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 148
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 148
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 149
<211> 475
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 149
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
145 150 155 160
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp
165 170 175
Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser
180 185 190
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
225 230 235 240
Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro
245 250 255
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
260 265 270
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
275 280 285
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
290 295 300
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
305 310 315 320
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
325 330 335
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
340 345 350
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
355 360 365
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
370 375 380
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
385 390 395 400
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
405 410 415
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
420 425 430
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
435 440 445
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 150
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 150
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 151
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 151
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 152
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 152
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
370 375 380
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 153
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 153
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 154
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 154
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 155
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический полипептид"
<400> 155
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 156
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 156
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 157
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 157
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 158
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 158
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
370 375 380
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 159
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 159
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 160
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 160
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 161
<211> 475
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 161
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
145 150 155 160
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp
165 170 175
Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp Ser
180 185 190
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
195 200 205
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly
225 230 235 240
Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys Pro
245 250 255
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
260 265 270
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
275 280 285
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
290 295 300
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
305 310 315 320
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
325 330 335
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
340 345 350
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
355 360 365
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
370 375 380
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
385 390 395 400
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
405 410 415
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
420 425 430
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
435 440 445
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 162
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 162
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 163
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 163
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 164
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 164
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
370 375 380
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 165
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 165
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 166
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 166
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 167
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 167
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 168
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 168
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 169
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 169
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 170
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 170
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 171
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 171
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 172
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 172
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 173
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 173
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 174
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 174
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 175
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 175
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
370 375 380
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 176
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 176
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 177
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 177
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 178
<211> 476
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 178
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
130 135 140
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys
145 150 155 160
Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu
165 170 175
Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala Asp
180 185 190
Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr
195 200 205
Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
210 215 220
Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 179
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 179
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Ile Pro Ser Asn Gly Ala Thr Phe Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Leu Leu Arg Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 180
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 180
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 181
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 181
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
370 375 380
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 182
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 182
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 183
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 183
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 184
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 184
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
145 150 155 160
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Cys Leu
165 170 175
Glu Trp Val Ala Glu Ile Tyr Pro Thr Asn Gly Tyr Thr Glu Tyr Ala
180 185 190
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
195 200 205
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
210 215 220
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
370 375 380
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475
<210> 185
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 185
Gln Ile Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Gly Pro Lys Tyr Ala Gln Gly Phe
50 55 60
Thr Gly Arg Phe Val Phe Ser Val Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ile Tyr Asp Gly Tyr His Trp Tyr Phe Asp Val Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 186
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 186
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 187
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 187
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
115 120 125
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
130 135 140
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
145 150 155 160
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
165 170 175
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
180 185 190
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
195 200 205
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly
210 215 220
Thr Lys Val Glu Ile Lys
225 230
<210> 188
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 188
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 189
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 189
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 190
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 190
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
115 120 125
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
130 135 140
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
145 150 155 160
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
165 170 175
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
180 185 190
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
195 200 205
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly
210 215 220
Thr Lys Val Glu Ile Lys
225 230
<210> 191
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 191
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 192
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 192
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 193
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 193
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
115 120 125
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
130 135 140
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
145 150 155 160
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
165 170 175
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
180 185 190
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
195 200 205
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly
210 215 220
Thr Lys Val Glu Ile Lys
225 230
<210> 194
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 194
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 195
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 195
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 196
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 196
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 197
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 197
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 198
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 198
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 199
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 199
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
115 120 125
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
130 135 140
Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln
145 150 155 160
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe
165 170 175
Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr
180 185 190
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
195 200 205
Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly
210 215 220
Thr Lys Val Glu Ile Lys
225 230
<210> 200
<211> 220
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 200
Asp Phe Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 201
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 201
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 202
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 202
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 203
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 203
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 204
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 204
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 205
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 205
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
115 120 125
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
130 135 140
Cys Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala Trp Tyr Gln Gln
145 150 155 160
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu
165 170 175
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp
180 185 190
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
195 200 205
Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro Thr Phe Gly Cys Gly Thr
210 215 220
Lys Val Glu Ile Lys
225
<210> 206
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 206
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| УЛУЧШЕННЫЕ АНТИГЕНСВЯЗЫВАЮЩИЕ РЕЦЕПТОРЫ | 2018 |
|
RU2825816C2 |
| БИСПЕЦИФИЧЕСКИЕ 2+1 КОНТОРСТЕЛА | 2018 |
|
RU2797305C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СОДЕРЖАЩИЕ АНТИ-FAP КЛОН 212 | 2019 |
|
RU2799429C2 |
| HER-2-НАПРАВЛЕННЫЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СОДЕРЖАЩИЕ 4-1BBL | 2019 |
|
RU2815451C2 |
| АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТСЯ С СОРТИЛИНОМ И ПОДАВЛЯЮТ СВЯЗЫВАНИЕ ПРОГРАНУЛИНА | 2016 |
|
RU2735639C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, СПЕЦИФИЧЕСКИ СВЯЗЫВАЮЩИЕСЯ С PD1 И LAG3 | 2018 |
|
RU2778805C2 |
| АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТСЯ С РАКОВЫМИ КЛЕТКАМИ И ОБЕСПЕЧИВАЮТ НАПРАВЛЕННЫЙ ПЕРЕНОС РАДИОНУКЛИДОВ К УКАЗАННЫМ КЛЕТКАМ | 2020 |
|
RU2833191C2 |
| АНТИТЕЛО-ПОДОБНЫЕ СВЯЗЫВАЮЩИЕ БЕЛКИ С ДВОЙНЫМИ ВАРИАБЕЛЬНЫМИ ОБЛАСТЯМИ, ИМЕЮЩИЕ ОРИЕНТАЦИЮ СВЯЗЫВАЮЩИХ ОБЛАСТЕЙ КРЕСТ-НАКРЕСТ | 2012 |
|
RU2823693C2 |





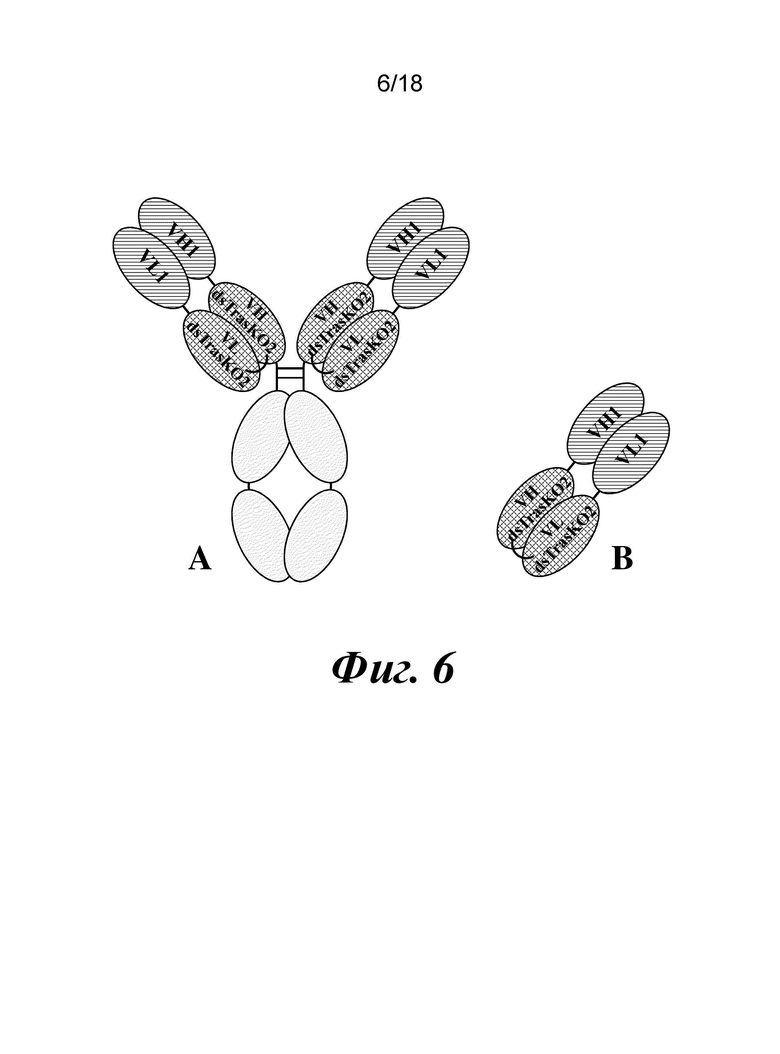




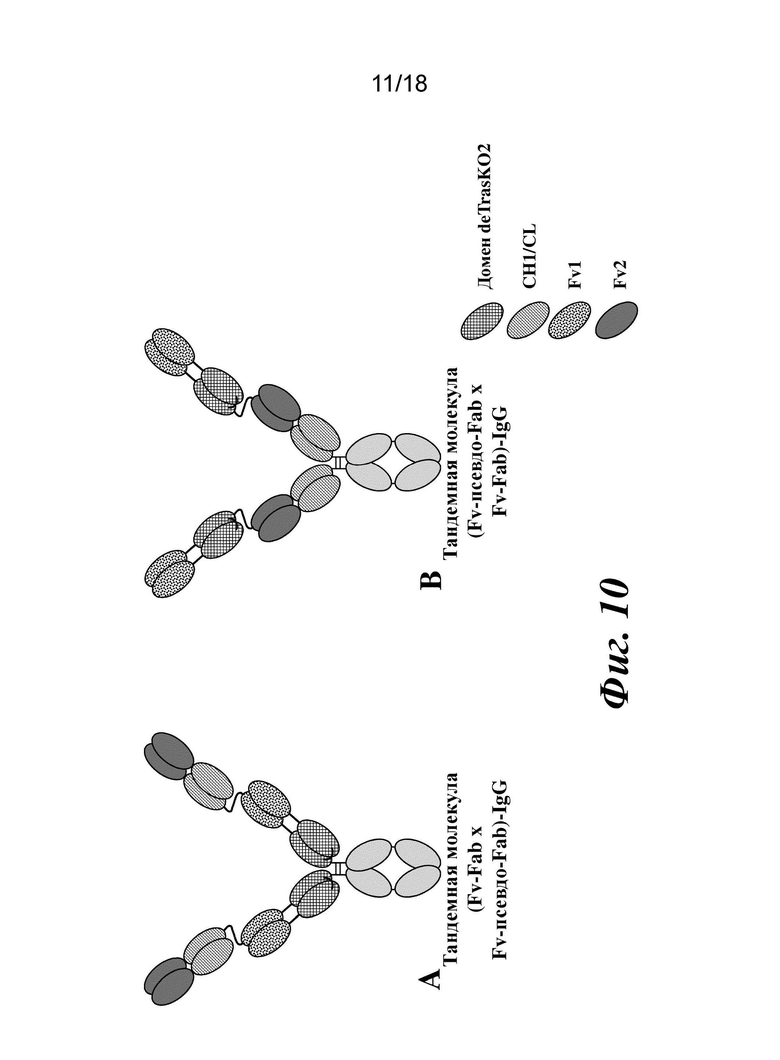







Группа изобретений относится к биотехнологии. Представлены: связывающие и мультиспецифические связывающие белки, которые связывают целевой антиген, где VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C и/или VLX содержит цистеиновую замену Q100C, способы их получения и применения. Также раскрыты молекулы нуклеиновых кислот, векторы экспрессии, клетки-хозяина и фармацевтические композиции их содержащие. Группа изобретений применяется для лечения нарушений, при которых активность антигена оказывает негативное воздействие на организм, в частности онкологических заболеваний. 22 н. и 21 з.п. ф-лы, 12 табл., 18 ил., 10 пр.
1. Связывающий белок, который связывает целевой антиген, содержащий:
по меньшей мере одну псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; и (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена; где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
2. Связывающий белок по п. 1, где связывающий белок содержит по меньшей мере второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B.
3. Мультиспецифический связывающий белок, который связывает целевой антиген, содержащий:
первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена; и
b) первую Fab-часть, содержащую (3) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B; (4) первый домен CH1, спаренный с первым доменом CL; и
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
4. Мультиспецифический связывающий белок, который связывает целевой антиген, содержащий:
первую псевдо-Fab-часть, содержащую (1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A; (2) первый стабилизированный нокаутный домен VH (VHX), спаренный с первым стабилизированным нокаутным доменом VL (VLX) с образованием первого стабилизированного нокаутного домена; и
b) первую Fab-часть, содержащую (3) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B; (4) первый домен CH1, спаренный с первым доменом CL; и
c) линкерную часть, которая функционально связывает первую Fab-часть и первую псевдо-Fab-часть,
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
5. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-4, где линкерная часть представляет собой пептидный линкер.
6. Связывающий белок или мультиспецифический связывающий белок по п. 5, где пептидный линкер представляет собой линкер Gly-Ser, имеющий состав (Gly4Ser)n, где n составляет 1-10.
7. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-6, где линкерная часть представляет собой домен гетеродимеризации.
8. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-7, содержащий независимо одну или две первые псевдо-Fab-части и одну или две первые Fab-части.
9. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-8, содержащий отдельные белковые цепи, выбранные из одной из следующих групп:
(a) VHa-CH1-L1-VHb-L2-VHX, и VLa-CL, и VLb-L3-VLX;
(b) VHa-L2-VHX-L1-VHb-CH1, и VLa-L3-VLX, и VLb-CL;
(c) VHa-CH1-L1-VHa-CH1, и VHb-L2-VHX-L3-VHb-L4-VHX, и две цепи VLb-L5-VLX, и две цепи VLa-CL;
где цепи из (а) и (b) могут присутствовать один раз или дважды, и где L1, L2, L3, L4 и L5 представляют собой линкеры, которые независимо могут быть одинаковыми или разными.
10. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-9, где первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ia) N-VHa-L1-VHX-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIa) N-VLa-L2-VLX-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
11. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-10, где первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ib) N-VHX-L1-VHa-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIb) N-VLX-L2-VLa-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
12. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-11, где первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Ic) N-VLa-L1-VHX-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IIc) N-VHa-L2-VLX-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
13. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-12, где первая псевдо-Fab-часть содержит первую полипептидную цепь, имеющую структуру, представленную формулой:
(Id) N-VHX-L1-VLa-C,
и вторую полипептидную цепь, имеющую структуру, представленную формулой:
(IId) N-VLX-L2-VHa-C,
где L1 и L2 представляют собой линкеры, которые независимо могут присутствовать или отсутствовать, и где N и C обозначают N- и C-терминальные концы соответственно.
14. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-13, дополнительно содержащий один или более дополнительных связывающих доменов, функционально связанных с N- или C-концом связывающего белка.
15. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-14, где один или более дополнительных связывающих доменов функционально связаны с N-концом первой или второй псевдо-Fab-части.
16. Мультиспецифический связывающий белок, который связывает целевой антиген, содержащий:
a) первую псевдо-Fab-часть, содержащую:
(1) первый домен VL (VLa), спаренный с первым доменом VH (VHa) с образованием первого антигенсвязывающего участка, который связывает целевой антиген A;
(2) первый стабилизированный нокаутный домен VL (VLX), спаренный с первым стабилизированным нокаутным доменом VH (VHX) с образованием первого стабилизированного дисульфидом нокаутного домена (dsKO);
(3) первый домен гетеродимеризации (HD1);
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C;
b) первую Fab-часть, содержащую
(1) второй домен VL (VLb), спаренный со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(2) первый домен CH1, спаренный с первым доменом CL; и
(3) второй домен гетеродимеризации (HD2).
17. Мультиспецифический связывающий белок по п. 16, где первый и второй домены гетеродимеризации содержат первый и второй домены Fc.
18. Мультиспецифический связывающий белок по п. 16 или 17, где домены Fc содержат общую структуру шарнир-домен CH2-домен CH3.
19. Мультиспецифический связывающий белок, который связывает целевой антиген, содержащий четыре полипептидные цепи, которые образуют по меньшей мере два антигенсвязывающих участка, где
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHb-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1 и L2 представляют собой аминокислотные линкеры, которые независимо могут быть одинаковыми или разными,
где
(1) первый домен VL (VLa) спарен с указанным первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен с указанным вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
20. Антигенсвязывающий белок, который связывает целевой антиген, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
21. Антигенсвязывающий белок, который связывает целевой антиген, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L3-VHa-L2-VHX-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2 и L3 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
22. Антигенсвязывающий белок, который связывает целевой антиген, содержащий шесть полипептидных цепей, которые образуют четыре антигенсвязывающих участка, где
(a) первый и второй полипептиды содержат структуру, представленную формулой:
VLa-L1-VLX [I] и [II],
(b) третий и четвертый полипептиды содержат структуру, представленную формулой:
VLb-CL [III] и [IV],
(c) пятый полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-L3-VHa-L4-VHX-FC1 [V],
(d) шестой полипептид содержит структуру, представленную формулой:
VHb-CH1-L5-VHb-CH1-FC2 [VI],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен тяжелой цепи иммуноглобулина;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4 и L5 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного (dsKO) домена;
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
23. Антигенсвязывающий белок, который связывает целевой антиген, содержащий четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где:
(a) первый полипептид содержит структуру, представленную формулой:
VLa-L1-VLX [I],
(b) второй полипептид содержит структуру, представленную формулой:
VHa-L2-VHX-FC1 [II],
(c) третий полипептид содержит структуру, представленную формулой:
VLb-L3-VLc-L4-CL [III],
(d) четвертый полипептид содержит структуру, представленную формулой:
VHc-L5-VHb-L6-CH1-FC2 [IV],
где
VLa представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VLb представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VLc представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VHa представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VHb представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VHc представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
VLX представляет собой стабилизированный нокаутный вариабельный домен легкой цепи;
VHX представляет собой стабилизированный нокаутный вариабельный домен тяжелой цепи;
FC1 и FC2 представляют собой домены Fc, содержащие шарнирный участок иммуноглобулина и константные домены тяжелой цепи иммуноглобулина CH2 и CH3; и
L1, L2, L3, L4, L5 и L6 представляют собой аминокислотные линкеры,
где
(1) первый домен VL (VLa) спарен с первым доменом VH (VHa) с образованием первого функционального антигенсвязывающего участка, который связывает целевой антиген A;
(2) второй домен VL (VLb) спарен со вторым доменом VH (VHb) с образованием второго функционального антигенсвязывающего участка, который связывает целевой антиген B;
(3) третий домен VL (VLc) спарен с третьим доменом VH (VHc) с образованием третьего функционального антигенсвязывающего участка, который связывает целевой антиген C;
(4) полипептид формулы III и полипептид формулы IV образуют кроссоверную пару легкая цепь-тяжелая цепь (CODV);
(5) стабилизированный нокаутный домен VL (VLX) спарен со стабилизированным нокаутным доменом VH (VHX) с образованием стабилизированного дисульфидом нокаутного домена (dsKO2);
где:
(i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или
(ii) VLX содержит цистеиновую замену Q100C.
24. Связывающий белок по любому из пп. 17-23, где домены Fc содержат одну или более мутаций типа "выступ-во-впадину" (KIH).
25. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-24, где температура плавления (Tm) псевдо-Fab-части на по меньшей мере 4 градуса Цельсия превышает таковую у эталонной молекулы Fab.
26. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-25, где по меньшей мере одна из одной или более сконструированных межцепочечных дисульфидных связей представляет собой VH44C-VL100C.
27. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-26, где целевой антиген A и целевой антиген B являются разными эпитопами одного и того же антигена.
28. Связывающий белок или мультиспецифический связывающий белок по любому из пп. 1-27, где пара VLX/VHX выбрана из группы, состоящей из:
(i) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 77;
ii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 78; и
iii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 79.
29. Применение стабилизированного нокаутного домена для снижения неправильного спаривания тяжелой цепи и легкой цепи в мультиспецифическом связывающем белке, где стабилизированный нокаутный домен содержит домены VHХ и VLX, где (i) VHX содержит одну или более инактивирующих мутаций Y33A, R50E, R59E и Y105A и/или цистеиновую замену G44C; и/или (ii) VLX содержит цистеиновую замену Q100C, которые придают повышенную термостабильность (Tm) псевдо-Fab относительно эталонной молекулы Fab, где эталонная молекула Fab идентична молекуле псевдо-Fab, за исключением того, что в эталонной молекуле псевдо-Fab домены CH1 и CL эталонной молекулы Fab заменены доменами VHX и VLX.
30. Применение по п. 29, где пара VLX/VHX выбрана из группы, состоящей из:
(i) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 77;
ii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 78; и
iii) VLX, содержащего аминокислотную последовательность под SEQ ID NO: 76, и
VHX, содержащего аминокислотную последовательность под SEQ ID NO: 79.
31. Выделенная молекула нуклеиновой кислоты, кодирующая связывающий белок по любому из пп. 1-28.
32. Выделенная молекула нуклеиновой кислоты, кодирующая мультиспецифический связывающий белок по любому из пп. 1-28.
33. Вектор экспрессии, содержащий молекулу нуклеиновой кислоты по п. 31.
34. Вектор экспрессии, содержащий молекулу нуклеиновой кислоты по п. 32.
35. Выделенная клетка-хозяин, экспрессирующая связывающий белок по любому из пп. 1-28, содержащая молекулу нуклеиновой кислоты по п. 31 или вектор экспрессии по п. 33.
36. Выделенная клетка-хозяин, экспрессирующая мультиспецифический связывающий белок по любому из пп. 1-28, содержащая молекулу нуклеиновой кислоты по п. 32 или вектор экспрессии по п. 34.
37. Способ получения связывающего белка по любому из пп. 1-28, включающий культивирование клетки-хозяина по п. 35 в условиях, при которых экспрессируется связывающий белок; и очистку связывающего белка из клетки-хозяина.
38. Способ получения мультиспецифического связывающего белка по любому из пп. 1-28, включающий культивирование клетки-хозяина по п. 36 в условиях, при которых экспрессируется мультиспецифический связывающий белок; и очистку мультиспецифического связывающего белка из клетки-хозяина.
39. Фармацевтическая композиция для лечения нарушения, при котором активность антигена оказывает негативное воздействие, содержащая фармацевтически приемлемый носитель и терапевтически эффективное количество связывающего белка по любому из пп. 1-28, где указанный связывающий белок связывает указанный антиген.
40. Фармацевтическая композиция для лечения нарушения, при котором активность антигена оказывает негативное воздействие, содержащая фармацевтически приемлемый носитель и терапевтически эффективное количество мультиспецифического связывающего белка по любому из пп. 1-28, где указанный мультиспецифический связывающий белок связывает указанный антиген.
41. Применение связывающего белка по любому из пп. 1-28 для лечения нарушения, при котором активность антигена оказывает негативное воздействие, где указанное применение включает введение субъекту, нуждающемуся в этом, эффективного количества указанного связывающего белка, где указанный связывающий белок связывает указанный антиген.
42. Применение мультиспецифического связывающего белка по любому из пп. 1-28 для лечения нарушения, при котором активность антигена оказывает негативное воздействие, где указанное применение включает введение субъекту, нуждающемуся в этом, эффективного количества указанного мультиспецифического связывающего белка, где указанный мультиспецифический связывающий белок связывает указанный антиген.
43. Применение по п. 41 или 42, где указанное нарушение представляет собой рак.
| WO 2011117653 A1, 29.09.2011 | |||
| SCHMIEDL A | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Насос | 1917 |
|
SU13A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| БУНКЕР С ПОДВИЖНЫМ ПЛОСКИМ ДНИЩЕМ | 0 |
|
SU177342A1 |
| ИНСТРУМЕНТ С ПРЕДЕЛЬНОЙ МУФТОЙ ДЛЯ ЗАТЯЖКИКРЕПЕЖА | 0 |
|
SU202781A1 |
| BRINKMANN U ED - ROLAND KONTERMANN AND STEFAN DÜBEL: "Antibody Engineering, | |||
Авторы
Даты
2024-05-31—Публикация
2019-12-23—Подача