Изобретение относится к органической химии и касается известной кристаллической модификации 3β-гидрокси-5-андростен-17-она (дегидроэпиандростерона, прастерона, ДГЕА) FIII, и способа ее получения, которая может быть использована в фармацевтической промышленности и медицине.
Данное соединение является андрогенным стероидным гормоном, активно участвующим в регуляции многочисленных важных функций в человеческом организме. По своему химическому строению ДГЕА аналогичен тестостерону и эстрогену, легко превращается в один из этих гормонов.
Выработка ДГЕА достигает максимума в период полового созревания и снижается по мере старения человека. Таким образом, многие возрастные болезни коррелируют с низким уровнем ДГЕА. Заместительная терапия физиологическими дозами ДГЕА при его эндогенном дефиците в том числе позволяет:
- предотвратить или облегчить развитие многих заболеваний, связанных со старением,
- нормализовать гормональный фон у мужчин и женщин,
- нормализовать содержание жира в мышцах,
- отодвинуть наступление менопаузы у женщин,
- повысить плотность костной ткани и предотвратить остеопороз,
- повысить синтез гормонов, определяющих сексуальную активность человека (эстроген и тестостерон),
- снизить риск возникновения сердечно-сосудистых заболеваний.
[Н.П. Гончаров, Г.В. Кация //Гормон здоровья и долголетия; М.: ООО Издательство «АДАМАНТ», 2012]
Известны четыре кристаллические модификации 3β-гидрокси-5-андростен-17-она, характеризующиеся рентгеноструктурными исследованиями - определенными параметрами кристаллических решеток:
- модификация FI; тип - моноклинная, а = 6,208(1) Å, b = 44,437(7) Å, с = 6,270(1) Å, β = 107,10(2)°, V=1653,21 Å3, ρвыч.=1,17 г/см3, Z = 4 C18H28O2, пространственная группа P21, файл ZOYMOP Кембриджской базы кристаллографических данных [M.R. Caira, J.K. Guillory, L-C. Chang //Crystal and molecular structures of three modification of androgen dehydroepiandrosterone (DHEA), J. Chem. Crystallogr., 1995, V. 25, pp.393 - 400],
- модификация FII; тип - орторомбическая, а = 6,6408(4) Å, b = 11,4423(11) Å, с = 22,085(2) Å, β = 90,00°, V = 1678,15 Å3 ρвыч. = 1,16 г/см3, Z = 4 C18H28O2, пространственная группа P212121, файл ZOYMOP01 Кембриджской базы кристаллографических данных [N.S. Bhacca, F.R. Fronczek, A.J. Sygula //Investigation of dehydroepiandrosterone. Part I: crystal structure of sublimed DHEA, Chem. Crystallogr., 1996, V. 26, pp. 483 - 487],
- модификация FIII: тип - моноклинная, а = 14.5339(18) Å, b = 10,3792(14) Å, с = 11,8253(14) Å, β = 111,559(18)°, V = 1659,1(4) Å3 ρвыч. = 1,155 г/см3, Z = 4 (2) C18H28O2, пространственная группа P21, файл ZOYMOP03 Кембриджской базы кристаллографических данных [V.V. Chernyshev, Yu.N. Morozov, I.S. Bushmarinov, A.A. Makoed, G.B. Sergeev //New Polymorph of Dehydroepiandrosterone (DHEA) obtained via cryomodification, Crystal Growth & Design, 2016, V. 16, pp. 1088 - 1095],
- модификация FVI: тип - моноклинная, а = 6,621 Å, b = 21,620 Å, с = 6,432 Å, β=107,81°, V = 840,431 Å3, ρвыч.=1,17 г/см3, Z = 2 C18H28O2 пространственная группа P21 файл ZOYMOP02 Кембриджской базы кристаллографических данных [G.P. Stahly, S. Bates, M.C.Andres, B.A.Cowans//Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from X-ray Powder Diffraction Data, Crystal Growth & Design, 2006, V. 6, pp. 925 - 932],
- модификация FVII: тип - моноклинная, а = 13.105(2) Å, b = 5,9034(18) Å, с = 10,829(2) Å, β = 97,64(2)°, V = 830,3(3) Å3 ρвыч. = 1,154 г/см3, Z = 2 C18H28O2, пространственная группа P21, файл ZOYMOP03 Кембриджской базы кристаллографических данных [Ю.Н. Морозов, А.Ю. Утехина, Г.Б. Сергеев, В.В. Чернышев, В.В. Чистяков, Н.П. Гончаров, В.М. Ржезников//Кристаллическая модификация 3β-гидрокси-5-андростен-17-она FVII и способ ее получения, Патент РФ № 2528990 от 23.03.2013, V.V. Chernyshev, Yu.N. Morozov, I.S. Bushmarinov, A.A. Makoed, G.B. Sergeev //New Polymorph of Dehydroepiandrosterone (DHEA) obtained via cryomodification, Crystal Growth & Design, 2016, V. 16, pp. 1088 - 1095].
Кристаллические модификации FI и FII 3β-гидрокси-5-андростен-17-она получают перекристаллизацией из органических растворителей: для получения модификации FI используют ацетон, этиловый эфир уксусной кислоты, изопропанол, ацетонитрил, для получения модификации FII используют диоксан, тетрагидрофуран, хлороформ и смесь хлороформа с тетрагидрофураном [L-C.Chang, M.R.Caira, J.K.Guillory //Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179], [G.P. Stahly, S. Bates, M.C. Andres, B.A. Cowans //Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from X-ray Powder Diffraction Data, Crystal Growth & Design, 2006, V. 6, pp. 925 - 932],
Кристаллическую модификацию FII можно также получить в сублимационно-десублимационном процессе [N.S. Bhacca, F.R. Fronczek, A.J. Sygula //Investigation of dehydroepiandrosterone. Part I: crystal structure of sublimed DHEA, Chem. Crystallogr., 1996, V. 26, pp. 483 - 487].
Кристаллическую модификацию FIII получали десольватацией кристаллогидрата или метанольного кристаллосольвата 3β-гидрокси-5-андростен-17-она при комнатной температуре путем выдерживания в вакууме [L-C. Chang, M.R. Caira, J.K. Guillory //Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179].
Кристаллическая модификация FVI в чистом виде зафиксирована только для одного образца 3β-гидрокси-5-андростен-17-она, условия кристаллизации которого неизвестны [G.P. Stahly, S. Bates, M.C.Andres, B.A.Cowans //Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from X-ray Powder Diffraction Data, Crystal Growth & Design, 2006, V. 6, pp. 925 - 932].
Кристаллическую модификацию FVII получали испарением исходной субстанции (в формах FI и FII) в вакууме в токе инертного газа и конденсацией на охлажденной поверхности [Ю.Н. Морозов, А.Ю. Утехина, Г.Б. Сергеев, В.В. Чернышев, В.В. Чистяков, Н.П. Гончаров, В.М. Ржезников//Кристаллическая модификация 3β-гидрокси-5-андростен-17-она FVII и способ ее получения, Патент РФ № 2528990 от 23.03.2013, V.V. Chernyshev, Yu.N. Morozov, I.S. Bushmarinov, A.A. Makoed, G.B. Sergeev //New Polymorph of Dehydroepiandrosterone (DHEA) obtained via cryomodification, Crystal Growth & Design, 2016, V. 16, pp. 1088 - 1095].
Кристаллические модификации FIV и FV 3β-гидрокси-5-андростен-17-она получены путем кристаллизации расплава и охарактеризованы только термомикроскопическими исследованиями [L-C. Chang, M.R. Caira, J.K. Guillory// Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V.84, pp.1169 - 1179], [G. P. Stahly, S. Bates, M.C. Andres, B.A. Cowans //Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from X-ray Powder Diffraction Data, Crystal Growth&Design, 2006, V. 6, No.4, pp.925 - 932].
Кристаллическая модификация FVIII образуется вместе с кристаллической модификацией FVII и проявляется на рентгенограммах в виде ограниченного числа уширенных линий, что не даёт возможности определения ее кристаллографических параметров V.V. Chernyshev, Yu.N. Morozov, I.S. Bushmarinov, A.A. Makoed, G.B. Sergeev //New Polymorph of Dehydroepiandrosterone (DHEA) obtained via cryomodification, Crystal Growth & Design, 2016, V. 16, pp. 1088 - 1095].
Кристаллические модификации FI, FII, FIII, FVII исследованы методом ИК-спектроскопии в области 4000-400 см-1, для них определены частоты характеристических полос поглощения. Кристаллические модификации FI, FII и FIII можно идентифицировать по положению полос валентных колебаний O-H (3600-3300 см-1), C=O (1750-1720 см-1) и C-O (1100-1000 см-1) связей, по характерным полосам валентных колебаний C-H (3100-2800 см-1) связей, имеются также характерные отличия в области «отпечатков пальцев» (1500-700 см-1). Кристаллическая модификация FI имеет дублетную полосу при 3501 и 3458 см-1 в области валентных колебаний O-H связи, полосу при 1729 см-1 в области валентных колебаний C=O связи, полосу при 1067 см-1 в области валентных колебаний C-O связи. Кристаллическая модификация FII имеет полосу при 3428 см-1 в области валентных колебаний O-H связи, полосу при 1728 см-1 в области валентных колебаний C=O связи, полосу при 1067 см-1 в области валентных колебаний C-O связи. Кристаллическая модификация FIII имеет дублетную полосу при 3413 и 3369 см-1 в области валентных колебаний O-H связи, дублетную полосу при 1740 и 1724 см-1 в области валентных колебаний C=O связи, дублетную полосу примерно при 1067 и 1057 см-1 в области валентных колебаний C-O связи [L-C. Chang, M.R. Caira, J.K. Guillory// Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179]. Кристаллическая модификация FVII имеет полосу при 3437 см-1 в области валентных колебаний O-H связи, полосу при 1740 см-1 в области валентных колебаний C=O связи, полосу при 1057 см-1 в области валентных колебаний C-O связи [Ю.Н. Морозов, А.Ю. Утехина, Г.Б. Сергеев, В.В. Чернышев, В.В. Чистяков, Н.П. Гончаров, В.М. Ржезников//Кристаллическая модификация 3β-гидрокси-5-андростен-17-она FVII и способ ее получения, Патент РФ № 2528990 от 23.03.2013].
В качестве исходного препарата 3β-гидрокси-5-андростен-17-она использовали фармакопейную субстанцию производства фирмы "Acros Organic" (Бельгия).
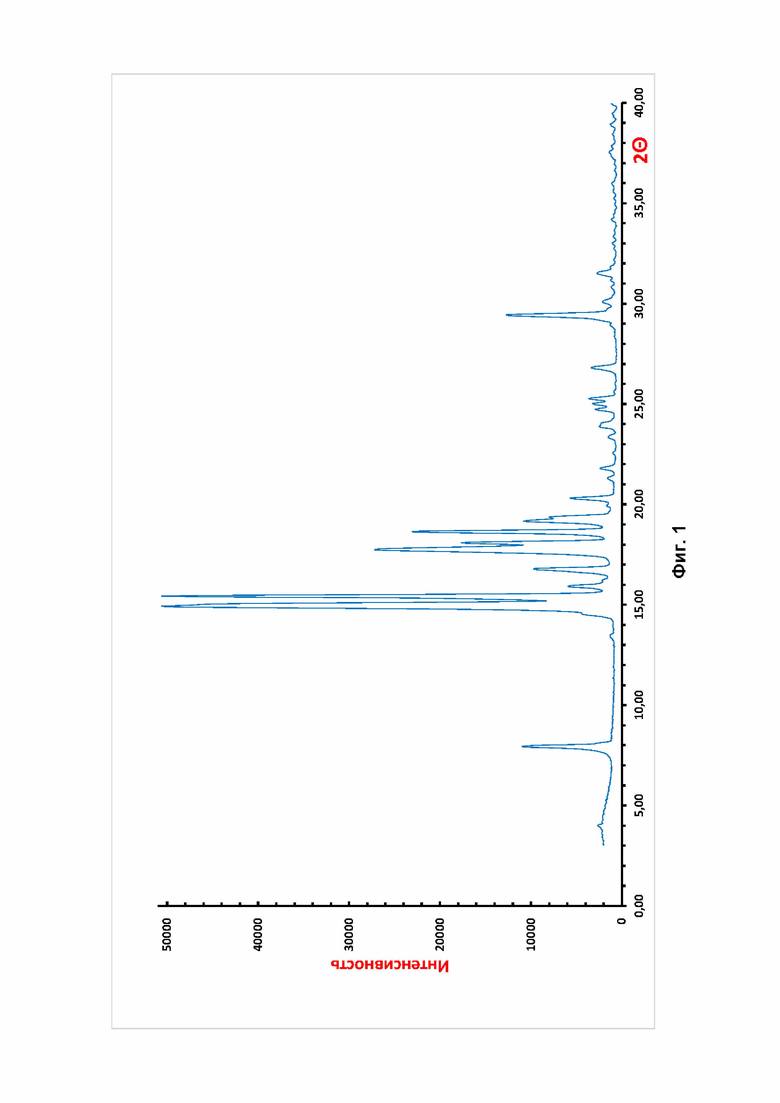
Известная фармакопейная субстанция 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) представляет собой порошок белого цвета, который практически не растворим в воде, плохо растворим в этаноле (95-96%), хорошо растворим в хлороформе, ацетоне, тетрагидрофуране, изопропаноле. Порошковая рентгенограмма препарата соответствует известной модификации FI; тип - моноклинная, а = 6,208(1) Å, b = 44,437(7) Å, с = 6,270(1) Å, β = 107,10(2)°, V = 1653,21 Å3, ρвыч. = 1,17 г/см3, Z = 4 C18H28O2, пространственная группа P21, файл ZOYMOP Кембриджской базы кристаллографических данных [M.R. Caira, J.K. Guillory, L-C. Chang //Crystal and molecular structures of three modification of androgen dehydroepiandrosterone (DHEA), J. Chem. Crystallogr., 1995, V. 25, pp.393 - 400] (Фиг.1, табл.1).
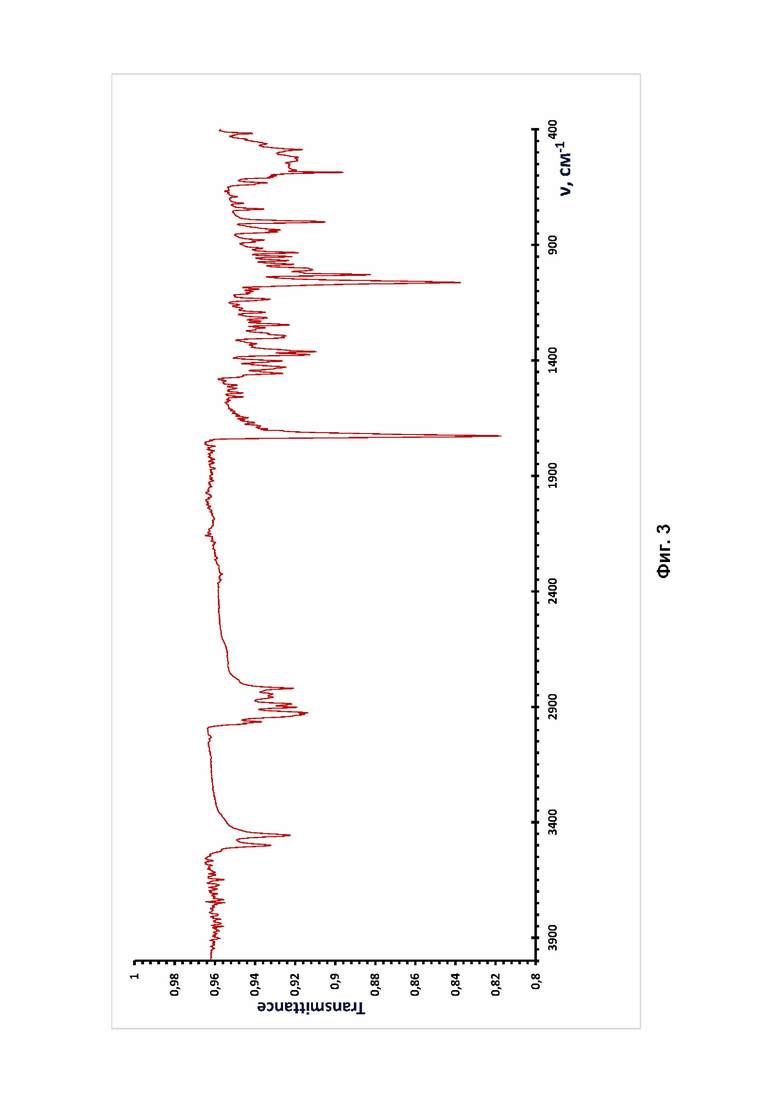
Зарегистрированные ИК-спектры фармакопейной субстанции 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) (Фиг. 2), полностью соответствуют спектрам кристаллической модификации FI 3β-гидрокси-5-андростен-17-она [L-C. Chang, M.R. Caira, J.K. Guillory // Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179].
Раскрытие изобретения.
Задачей настоящего изобретения разработка способа получения известной кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII.
Поставленная цель достигнута настоящим изобретением, а именно получением кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII, характеризующейся следующим набором межплоскостных расстояний (Ǻ) и соответствующих им интенсивностей:
13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5.
Кроме того, поставленная цель достигнута способом получения кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII, в котором исходную субстанцию 3β-гидрокси-5-андростен-17-она испаряют при температуре 60…150°C в вакууме 5 ÷ 5×10-4 Торр в токе закиси азота - N2O со скоростью потока от 1 до 20 мл/мин (2,5*10-3 ÷ 5,0*10-2 моль/час) и конденсируют на охлажденной до +0°C…-196°C поверхности.
Из патентной и научно-технической литературы известна кристаллическая модификация 3β-гидрокси-5-андростен-17-она FIII и способ ее получения. Кристаллическую модификацию FIII получали десольватацией кристаллогидрата или метанольного кристаллосольвата 3β-гидрокси-5-андростен-17-она при комнатной температуре путем выдерживания в вакууме [L-C. Chang, M.R. Caira, J.K. Guillory.// Solid State characterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179]. Однако, получение кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII путем десольватации метанольного кристаллосольвата исключает возможность её применения в медицинских целях. В образцах 3β-гидрокси-5-андростен-17-она, полученных путем десольватации кристаллогидрата, содержание кристаллической модификации FIII далеко от 100 % [G.P. Stahly, S. Bates, M.C.Andres, B.A.Cowans //Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from X-ray Powder Diffraction Data, Crystal Growth & Design, 2006, V. 6, pp. 925 - 932].
В связи с этим, задача получения фазово-чистой модификации 3β-гидрокси-5-андростен-17-она FIII, остается актуальной.
Заявляемая кристаллическая модификация 3β-гидрокси-5-андростен-17-она FIII может применяться в фармацевтической промышленности и медицине в качестве лечебно-профилактического средства многофункционального назначения.
Заявляемая кристаллическая модификация 3β-гидрокси-5-андростен-17-она FIII представляет собой легкий пушистый порошок белого цвета, который практически не растворим в воде, плохо растворим в этаноле (95 - 96%), хорошо растворим в хлороформе, ацетоне, тетрагидрофуране, изопропаноле.
Для идентификации полученного вещества был проведен комплекс физико-химических методов анализа.
Сходство заявляемой кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII с известной кристаллической модификацией FIII, заключается в сходстве наборов межплоскостных расстояний, соответствующих им интенсивностей, сходных значениях кристаллографических параметров кристаллических решеток и идентичных ИК-Фурье спектрах.
Для пояснения сущности заявляемого технического решения к описанию приложены следующие таблицы и чертежи:
Таблица 1. Межплоскостные расстояния (d, Å) и интенсивности рефлексов (Iотн., %) на рентгенограмме исходного препарата 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) и теоретической рентгенограмме кристаллической модификации FI 3β-гидрокси-5-андростен-17-она.
Таблица 2. Межплоскостные расстояния (d, Å) и интенсивности рефлексов (Iотн, %) на рентгенограмме кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII, полученной предлагаемым способом и теоретической рентгенограмме кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она.
Фиг. 1 Порошковая рентгенограмма исходного препарата 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия).
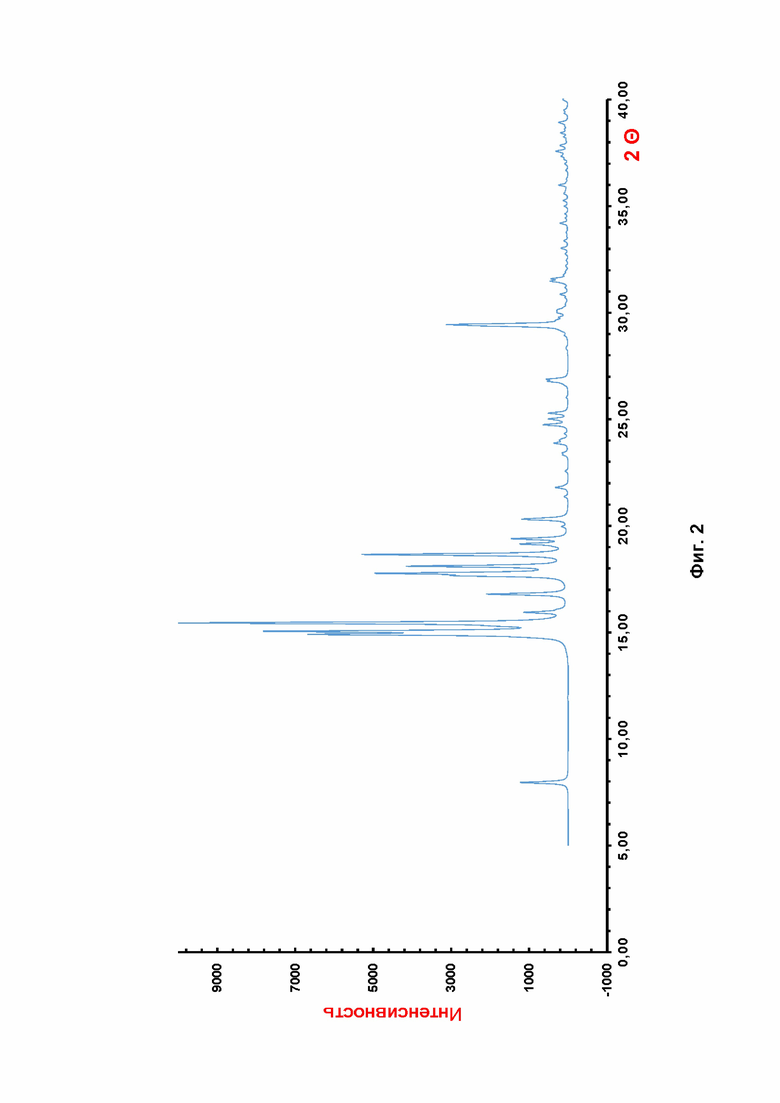
Фиг. 2 Теоретическая рентгенограмма кристаллической модификации FI 3β-гидрокси-5-андростен-17-она.
Фиг. 3 ИК-Фурье спектр исходного препарата 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия).
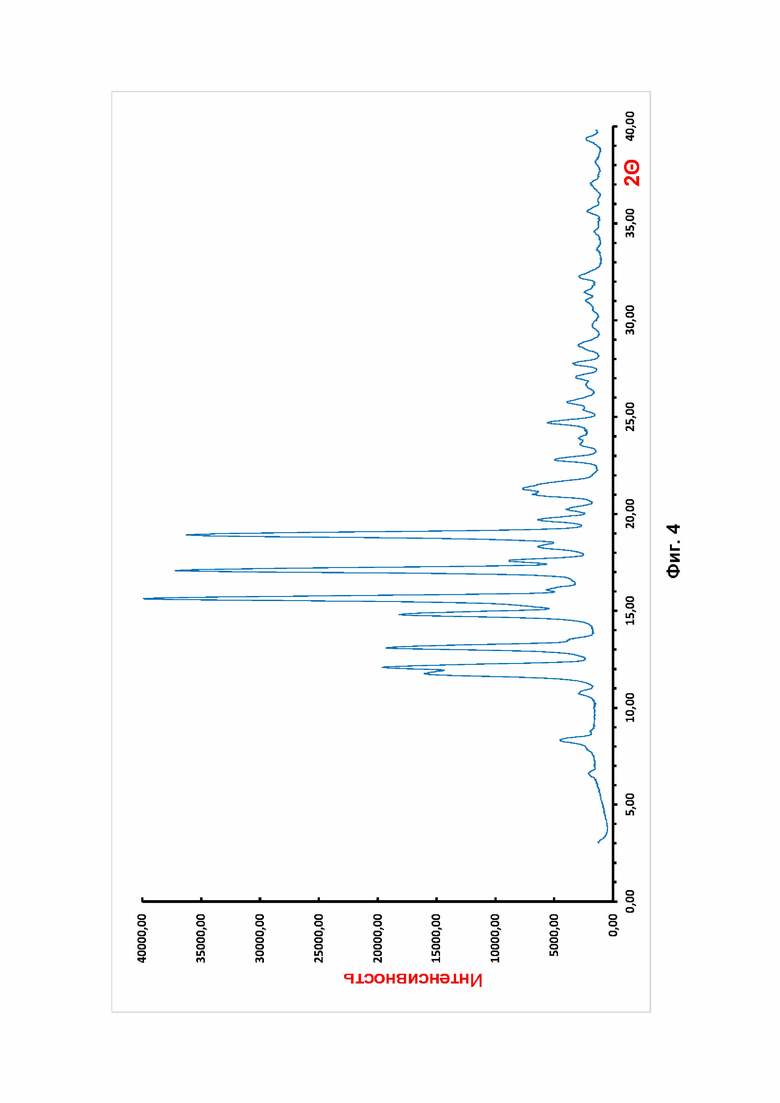
Фиг. 4 Порошковая рентгенограмма кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она, полученной предлагаемым способом.
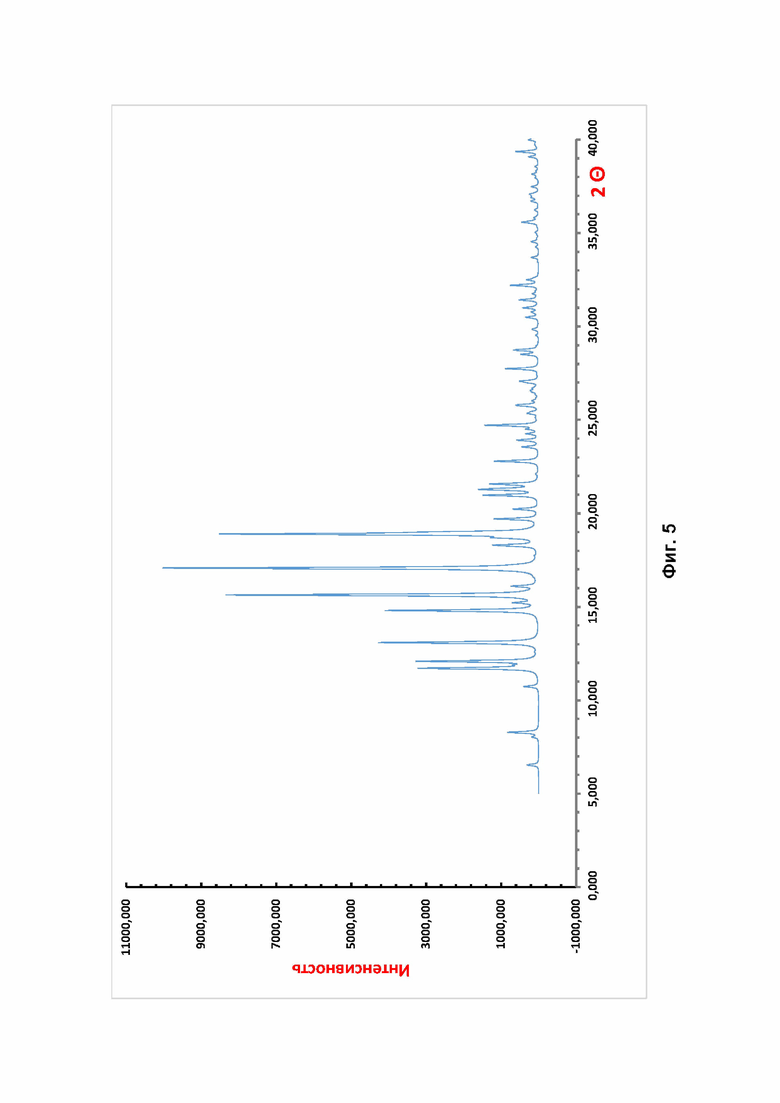
Фиг. 5 Теоретическая рентгенограмма кристаллической модификации FI 3β-гидрокси-5-андростен-17-она.
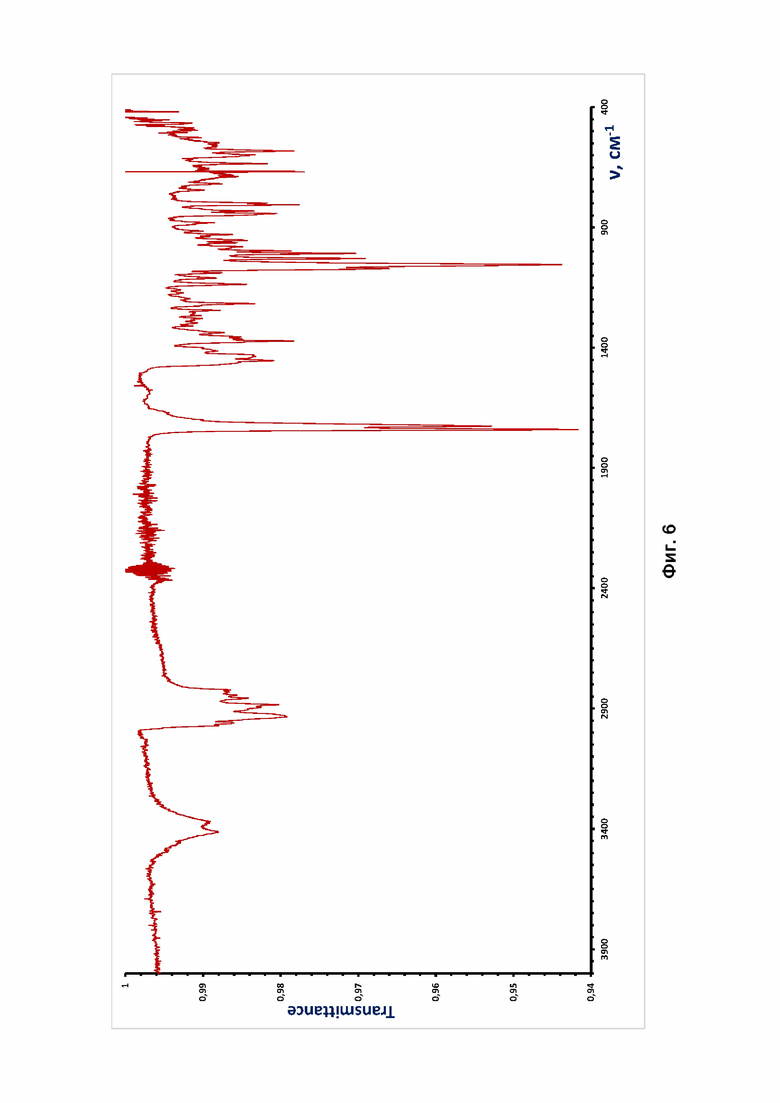
Фиг. 6 ИК-Фурье спектр кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она, полученной предлагаемым способом.
Для подтверждения того, что полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она, были проведены порошковый рентгеноструктурный (пРСА) анализ, ИК-Фурье ИК-Фурье спектроскопические исследования, определение размера частиц.
Порошковые дифракционные измерения образцов 3β-гидрокси-5-андростен-17-она проводили при следующих условиях: дифрактометр EMPYREAN (PANalytical), CuKα - излучение (λ=1,54059 Å), никелевый фильтр на первичном пучке, съемка на отражение в области углов 2-40° 2Θ, напряжение 45 кВ, ток 40 мА, линейный детектор X'celerator.
ИК-Фурье спектры исходной субстанции 3β-гидрокси-5-андростен-17-она и полученной из них кристаллической модификации FIII регистрировали на ИК-Фурье-спектрометре «Tenzor II» с НПВО приставкой A225/Q platinum ATR (производства компании Bruker (Германия). Для увеличения соотношения сигнал-шум производилось накопление и усреднение спектра по 32 сканированиям. Разрешение составляло 1 см-1.
Сравнение результатов порошкового рентгеноструктурного анализа (пРСА) исходного препарата 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) (Фиг. 1, Фиг. 3, табл. 1) и полученного из них вещества (Фиг.с4, Фиг. 6, табл. 2) свидетельствует о том, что оно является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она c параметрами кристаллической решетки: тип - моноклинная, а = 14.5339(18) Å, b = 10,3792(14) Å, с = 11,8253(14) Å, β = 111,559(18)°, V = 1659,1(4), Å3 ρвыч. = 1,155 г/см3, Z = 4 (2) C18H28O2, пространственная группа P21.
Сравнение полученных результатов с известными из литературы:
[L-C. Chang, M.R. Caira, J.K. Guillory //Solid State haracterization of Dehydroepiandrosterone, J. Pharm. Sci. 1995, V. 84, pp.1169 - 1179], [G. Patrick Stahly, Simon Bates, Mark C. Andres, and Brett A. Cowans. //Discovery of a New Polymorph of Dehydroepiandrosterone (Prasterone) and Solution of Its Crystal Structure from Xray Powder Diffraction Data, Crystal Growth&Design, 2006, V. 6, No. 4, pp. 925 - 932], свидетельствует о том, что полученное из исходных препаратов 3β-гидрокси-5-андростен-17-она (препарата фирмы "Acros Organic" (Бельгия) вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Проведенные эксперименты показали, что использование ИК-Фурье спектроскопии позволяет различать исходную субстанцию 3β-гидрокси-5-андростен-17-она и полученную из нее кристаллическую модификацию FIII (Фиг. 3, Фиг. 6). В частности, полоса валентных колебаний O-H связи лежит для кристаллической модификации FI при 3501 и 3458 см-1, а для кристаллической модификации FIII при 3413 и 3369 см-1; полоса валентных колебаний C=O связи лежит для кристаллической модификации FI при 1729 см-1, а для кристаллической модификации FIII при 1740 и 1724 см-1; полоса валентных колебаний C-O связи лежит для кристаллической модификации FI при 1067 см-1, а для кристаллической модификации FIII при 1067 и 1057 см-1.
Определение диаметра частиц исходного препарата 3β-гидрокси-5-андростен-17-она проводили по микрофотографиям, полученным на оптическом микроскопе "ERGAVAL" производства фирмы "Karl Ceiss" (Германия), определение диаметра частиц новой кристаллической модификации 3β-гидрокси-5-андростен-17-она FVII проводили на сканирующем электронном микроскопе JSM 6380 LA при увеличениях ×1000 - 20000. Оказалось, что диаметр частиц исходного препарата 3β-гидрокси-5-андростен-17-она равен 10 - 100 мкм, а полученной из него новой кристаллической модификации FVII - 0,05-1,5 мкм в зависимости от условий получения.
Таким образом, экспериментальные результаты порошкового рентгеноструктурного анализа, ИК-Фурье спектроскопии и определения среднего диаметра частиц однозначно свидетельствуют о том, что полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она. Она характеризуется:
- порошковой дифрактограммой, характеризующейся следующим набором межплоскостных расстояний (Ǻ) и соответствующих им интенсивностей:
13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5.
- параметрами кристаллической решетки: тип - моноклинная, а = 14.5339(18) Å, b = 10,3792(14) Å, с = 11,8253(14) Å, β = 111,559(18)°, V = 1659,1(4), Å3 ρвыч. = 1,155 г/см3, Z = 4 (2) C18H28O2, пространственная группа P21.
- ИК-Фурье спектрами в областях валентных колебаний O-H (3413 и 3369 см-1), C=O (1740 и 1724 см-1) и C-O (1067 и 1057 см-1) связей, области валентных колебаний C-H (3100 - 2800 см-1) связей, и в области «отпечатков пальцев» (1500-700 см-1),
- средним диаметром частиц 0,05 - 1,5 мкм.
Способ получения кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII заключается в том, что исходную субстанцию 3β-гидрокси-5-андростен-17-она испаряют при температуре 60 - 150°C (333 - 413 К) в вакууме 5÷5×10-4 Торр в токе закиси азота - N2O со скоростью потока от 1 до 20 мл/мин (2,5*10-3 ÷ 5,0*10-2 моль/час) и конденсируют на охлажденную до -196°C (77 К) - 0°С (273 К) поверхность.
Отличиями предложенного способа являются величины интервалов: температуры испарения исходной субстанции 3β-гидрокси-5-андростен-17-она, остаточного давления, использование в качестве газа - носителя закиси азота N2O с определенным интервалом скорости его подачи и температуры конденсации.
Использование в качестве газа - носителя инертного газа, отличного от закиси азота N2O (N2, Ar, He и др.), приводит к тому, что в основном образуются кристаллические модификации FVII и FVIII 3β-гидрокси-5-андростен-17-она, кристаллическую модификацию 3β-гидрокси-5-андростен-17-она FIII получить не удается.
При уменьшении температуры испарителя ниже 60°C (333 К) скорость сублимации становится пренебрежимо малой. Кристаллическую модификацию 3β-гидрокси-5-андростен-17-она FIII получить не удается. Увеличение температуры испарителя выше 150°C (423 К) приводит к плавлению исходной субстанции и выносу вещества в виде капель. При конденсации на холодную поверхность образуется в основном кристаллическая модификация FII 3β-гидрокси-5-андростен-17-она, кристаллическую модификацию 3β-гидрокси-5-андростен-17-она FIII получить не удается.
При увеличении остаточного давлении выше 5 Торр процесс сублимации замедляется настолько, что время эксперимента становится недопустимо большим. Уменьшение остаточного давления в реакторе ниже 5×10-4 Торр нецелесообразно из-за экономических и аппаратурных затруднений.
Уменьшение скорости подачи закиси азота N2O ниже 1 мл/мин (2,5*10-3 моль/час) приводит к замедлению процесса сублимации и, как следствие, к смене режима зародышеобразования с газофазного гомогенного на гетерогенный поверхностный. При конденсации на холодной поверхности в основном образуется кристаллическая модификация FII 3β-гидрокси-5-андростен-17-она, кристаллическую модификацию 3β-гидрокси-5-андростен-17-она FIII получить не удается. Увеличение скорости подачи закиси азота N2O выше 20 мл/мин (5,0*10-2 моль/час) приводит к образованию смеси кристаллических модификаций FIII, FVII и FVIII, кристаллическую модификацию FIII в чистом виде получить не удается.
Повышение температуры низкотемпературного конденсора выше 0°C (273 К) приводит к замедлению процессов зародышеобразования, в связи с чем вещество не осаждается на стенках реактора, в связи с чем выход продукта существенно уменьшается. Понижение температуры конденсации ниже -196°C (77 К) нецелесообразно из-за экономических и аппаратурных затруднений.
Возможность осуществления предлагаемого изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Осуществление изобретения
Пример 1. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм сублимировали в вакуумной установке при температуре 140°C (413 К), остаточном давлении 2×10-2 Торр, в потоке газообразного азота (N2), подающегося со скоростью 20 мл/мин (5*10-2 моль/час). Пары сконденсировали на охлажденной до - 196°C (77 К) поверхности. Выход продукта составил 87,3% масс. По данным пРСА полученное вещество содержит в основном кристаллическую модификацию FVII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FVII 3β-гидрокси-5-андростен-17-она FVII. По данным микроскопического анализа размер частиц полученного порошка 0,08 - 0,12 мкм. Полученные результаты свидетельствуют о том, что вещество не является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 2. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм сублимировали в вакуумной установке при температуре 140°C (413 К), остаточном давлении 2×10-2 Торр, в потоке газообразного аргона (Ar), подающегося со скоростью 20 мл/мин (5*10-2 моль/час). Пары сконденсировали на охлажденной до - 196°C (77 К) поверхности. Выход продукта составил 85,7% масс. По данным пРСА полученное вещество содержит в основном кристаллическую модификацию FVII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FVII 3β-гидрокси-5-андростен-17-она FVII. По данным микроскопического анализа размер частиц полученного порошка 0,07 - 0,13 мкм. Полученные результаты свидетельствуют о том, что вещество не является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 3. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм сублимировали в вакуумной установке при температуре 140°C (413 К), остаточном давлении 2×10-2 Торр, в потоке газообразного гелия (He), подающегося со скоростью 20 мл/мин (5*10-2 моль/час). Пары сконденсировали на охлажденной до - 196°C (77 К) поверхности. Выход продукта составил 83,5% масс. По данным пРСА полученное вещество содержит в основном кристаллическую модификацию FVII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FVII 3β-гидрокси-5-андростен-17-она FVII. По данным микроскопического анализа размер частиц полученного порошка 0,1 - 0,3 мкм. Полученные результаты свидетельствуют о том, что вещество не является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 4. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 0,5 Торр, в потоке закиси азота (N2O), подающегося со скоростью 20 мл/мин (1*10-4 моль/час). Пары сконденсировали на, поверхности с температурой -196 0°C (77 К). Выход продукта составил 94,7% масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 4). По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,1 - 0,15 мкм. Полученные результаты свидетельствуют о том, что вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 5. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 0,5 Торр, в потоке закиси азота (N2O), подающегося со скоростью 20 мл/мин (5,0*10-2 моль/час). Пары сконденсировали на, поверхности с температурой 0°C (273 К). Выход продукта составил 12,5 % масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 4). По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,5 - 1,5 мкм. Полученные результаты свидетельствуют о том, что вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 6. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 1*10-4 Торр, в потоке закиси азота (N2O), подающегося со скоростью 25 мл/мин (6,3*10-2 моль/час). Пары сконденсировали на, поверхности с температурой -196 0°C (77 К). Выход продукта составил 95,4% масс. По данным пРСА полученное вещество является смесью кристаллических модификаций FIII и FVII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок не характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,1 - 0,15 мкм. Полученные результаты свидетельствуют о том, что вещество не является чистой кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 7. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 60°C (333 К), остаточном давлении 1×10-4 Торр, в потоке в потоке закиси азота (N2O), подающегося со скоростью 10 мл/мин (2,5*10-2 моль/час. Пары сконденсировали на охлажденной до - 196°C (77 К) поверхности. Выход продукта составил 85,7% масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она (Фиг. 4). По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка 0,09 - 0,15 мкм.
Пример 8. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 1*10-4 Торр, в потоке закиси азота (N2O), подающегося со скоростью 1 мл/мин (2,5*10-3 моль/час). Пары сконденсировали на, поверхности с температурой -196 0°C (77 К). Выход продукта составил 67,8% масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она (Фиг. 4). По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,9 - 0,17 мкм. Полученные результаты свидетельствуют о том, что вещество не является чистой кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 9. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 1*10-4 Торр, в потоке закиси азота (N2O), подающегося со скоростью 0,5 мл/мин (1,3*10-3 моль/час). Пары сконденсировали на, поверхности с температурой -196 0°C (77 К). Выход продукта составил 48,2% масс. По данным пРСА полученное вещество является смесью кристаллических модификацией FII и FIII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, не присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,15 - 0,30 мкм. Полученные результаты свидетельствуют о том, что вещество не является чистой кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 10. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 160°C (333 К), остаточном давлении 1*10-4 Торр, в потоке закиси азота (N2O), подающегося со скоростью 5 мл/мин (1,3*10-2 моль/час). Пары сконденсировали на, поверхности с температурой -196 0°C (77 К). Выход продукта составил 89,2% масс. По данным пРСА полученное вещество является кристаллической модификацией FII 3β-гидрокси-5-андростен-17-она. По результатам ИК-спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FII 3β-гидрокси-5-андростен-17-она FVII. По данным микроскопического анализа размер частиц полученного порошка составляет 1 - 5 мкм. Полученные результаты свидетельствуют о том, что вещество не является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 11. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 5 Торр, в потоке закиси азота (N2O), подающегося со скоростью 10 мл/мин (2,5*10-2 моль/час). Пары сконденсировали на охлажденной до -196 °C (77 К) поверхности. Выход продукта составил 12,2 % масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она (Фиг. 4). По результатам ИК-Фурье спектроскопии полученный порошок характеризуется ИК-спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг.7). По данным микроскопического анализа размер частиц полученного порошка составляет 0,3 - 1,2 мкм. Полученные результаты свидетельствуют о том, что вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 12. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 5 Торр, в потоке закиси азота (N2O), подающегося со скоростью 10 мл/мин (2,5*10-2 моль/час). Пары сконденсировали на охлажденной до 10 °C (283 К) поверхности. Выход продукта составил 2,2 % масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она (Фиг. 4). По результатам ИК-Фурье спектроскопии полученный порошок характеризуется ИК-спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 7). По данным микроскопического анализа размер частиц полученного порошка составляет 3 - 10 мкм. Полученные результаты свидетельствуют о том, что вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Пример 13. 1,2 г 3β-гидрокси-5-андростен-17-она производства фирмы "Acros Organic" (Бельгия) с размером частиц более 10 мкм испарили в вакуумной установке при температуре 140°C (413 К), остаточном давлении 3*10-2 Торр, в потоке закиси азота (N2O), подающегося со скоростью 10 мл/мин (1,3*10-2 моль/час). Пары сконденсировали на, поверхности с температурой -78 0°C (195 К). Выход продукта составил 68,2% масс. По данным пРСА полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она (Фиг. 4). По результатам ИК-Фурье спектроскопии полученный порошок характеризуется ИК-Фурье спектром, присущим кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она FVII (Фиг. 6). По данным микроскопического анализа размер частиц полученного порошка составляет 0,3 - 0,8 мкм. Полученные результаты свидетельствуют о том, что вещество является чистой кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она.
Приведенные результаты свидетельствуют о том, что полученное вещество является кристаллической модификацией FIII 3β-гидрокси-5-андростен-17-она. Она характеризуется:
- порошковой дифрактограммой, характеризующейся набором межплоскостных расстояний (Ǻ) и соответствующих им интенсивностей:
- 13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5.
- параметрами кристаллической решетки: тип - моноклинная, а = 14.5339(18) Å, b = 10,3792(14) Å, с = 11,8253(14) Å, β = 111,559(18)°, V = 1659,1(4), Å3 ρвыч. = 1,155 г/см3, Z = 4 (2) C18H28O2, пространственная группа P21.
- ИК-Фурье спектрами в областях валентных колебаний O-H (3413 и 3369 см-1), C=O (1740 и 1724 см-1) и C-O (1067 и 1057 см-1) связей, области валентных колебаний C-H (3100 - 2800 см-1) связей, и в области «отпечатков пальцев» (1500-700 см-1),
- средним диаметром частиц 0,05 - 1,5 мкм.
Из вышеизложенного можно сделать вывод о том, что способ получения кристаллической модификации 3β-гидрокси-5-андростен-17-она FIII является новыми и удовлетворяет критериям «изобретательский уровень» и «промышленная применимость».
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ МОДИФИКАЦИЯ 3β-ГИДРОКСИ-5-АНДРОСТЕН-17-ОНА FVII И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2528990C1 |
| КРИСТАЛЛИЧЕСКАЯ БЕТА-МОДИФИКАЦИЯ 7-БРОМ-1,3-ДИГИДРО-5-(2-ХЛОРФЕНИЛ)-2Н-1,4-БЕНЗОДИАЗЕПИН-2-ОНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2430094C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3β-ГИДРОКСИ-17-(1Н-БЕНЗИМИДАЗОЛ-1-ИЛ)АНДРОСТА-5,16-ДИЕНА | 2017 |
|
RU2749134C1 |
| Средства на основе дегидроэпиандростерона, обладающие избирательной цитопротекторной, противовоспалительной, иммуномодулирующей активностями, и способы их получения | 2024 |
|
RU2837885C1 |
| АНДРОСТАНЫ | 1995 |
|
RU2160740C2 |
| СПОСОБ ПОЛУЧЕНИЯ 7-ЗАМЕЩЕННЫХ СТЕРОИДНЫХ СОЕДИНЕНИЙ, СОЕДИНЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ ЭПЛЕРЕНОНА, ПРОДУКТ | 2003 |
|
RU2289586C2 |
| Фосфорил замещенные 3-кето-андрост-4-ен-[16,17-d]пиридазины и способ их получения | 2023 |
|
RU2807870C1 |
| Композитный геттерный материал на основе цеолита и способ его получения | 2016 |
|
RU2651174C1 |
| Способ получения трис(8-гидроксихинолината) алюминия | 2024 |
|
RU2830365C1 |
| 7-КАРБОКСИЗАМЕЩЕННЫЕ СТЕРОИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ ЭПЛЕРЕНОНА | 2003 |
|
RU2304144C2 |
Изобретение относится к способу получения кристаллической модификации 3β-гидрокси-5-андростен-17-она (дегидроэпиандрастерона, прастерона, ДГЕА) FIII, которая может быть использована в медицине и фармацевтической промышленности. Кристаллическая модификация FIII 3β-гидрокси-5-андростен-17-она (дегидроэпиандростерона, прастерона, ДГЕА) характеризуется: (а) набором межплоскостных расстояний  и соответствующих им интенсивностей: 13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5, (б) типом кристаллической решетки - моноклинная, пространственная группа P21, а = 14.5339(18)
и соответствующих им интенсивностей: 13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5, (б) типом кристаллической решетки - моноклинная, пространственная группа P21, а = 14.5339(18) 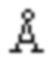 , b = 10,3792(14)
, b = 10,3792(14) 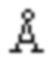 , с = 11,8253(14)
, с = 11,8253(14) 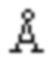 , β = 111,559(18)°, V = 1659,1(4)
, β = 111,559(18)°, V = 1659,1(4) 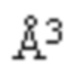 ρвыч = 1,155 г/см3, Z = 4 (2) C18H28O2, (с) ИК-Фурье спектрами в областях валентных колебаний O-H (3413 и 3369 см-1), C=O (1740 и 1724 см-1) и C-O (1067 и 1057 см-1) связей, области валентных колебаний C-H (3100-2800 см-1) связей, и в области «отпечатков пальцев» (1500-700 см-1). Способ получения кристаллической модификации 3β-гидрокси-5-андростен-17-она (дегидроэпиандрастерона, прастерона, ДГЕА) FIII характеризуется тем, что исходную субстанцию 3β-гидрокси-5-андростен-17-она испаряют при температуре 60-150°C в вакууме 5÷5×10-4 Торр в токе закиси азота - N2O со скоростью потока от 1 до 20 мл/мин (2,5*10-3 ÷ 5,0*10-2 моль/ч) и конденсируют на охлажденной до 0°C (273 К) - -196°C (77 К) поверхности. Технический результат – получение фазово-чистой модификации кристаллической формы FIII 3β-гидрокси-5-андростен-17-она (дегидроэпиандрастерона, прастерона, ДГЕА). 2 табл., 6 ил., 13 пр.
ρвыч = 1,155 г/см3, Z = 4 (2) C18H28O2, (с) ИК-Фурье спектрами в областях валентных колебаний O-H (3413 и 3369 см-1), C=O (1740 и 1724 см-1) и C-O (1067 и 1057 см-1) связей, области валентных колебаний C-H (3100-2800 см-1) связей, и в области «отпечатков пальцев» (1500-700 см-1). Способ получения кристаллической модификации 3β-гидрокси-5-андростен-17-она (дегидроэпиандрастерона, прастерона, ДГЕА) FIII характеризуется тем, что исходную субстанцию 3β-гидрокси-5-андростен-17-она испаряют при температуре 60-150°C в вакууме 5÷5×10-4 Торр в токе закиси азота - N2O со скоростью потока от 1 до 20 мл/мин (2,5*10-3 ÷ 5,0*10-2 моль/ч) и конденсируют на охлажденной до 0°C (273 К) - -196°C (77 К) поверхности. Технический результат – получение фазово-чистой модификации кристаллической формы FIII 3β-гидрокси-5-андростен-17-она (дегидроэпиандрастерона, прастерона, ДГЕА). 2 табл., 6 ил., 13 пр.
Способ получения кристаллической модификации FIII 3β-гидрокси-5-андростен-17-она (дегидроэпиандростерона, прастерона, ДГЕА), характеризующейся:
- набором межплоскостных расстояний 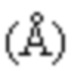 и соответствующих им интенсивностей:
и соответствующих им интенсивностей:
13,301 - 5,2; 10,568 - 11,1; 8,155 - 6,9; 7,487 - 39,4; 7,327 - 49,1; 6,748 - 47,9; 5,973 - 45,1; 5,669 - 100; 5,494 - 13,5; 5,190 - 93,3; 5,029 - 21,9; 4,834 - 15,7; 4,687 - 90,9; 4,512 - 15,5; 4,375 - 9,4; 4,217 - 16,4; 4,156 - 18,9; 3,895 - 12,3; 3,750 - 6,6; 3,708 - 7,0; 3,594 - 13,6; 3,500 - 6,2; 3,444 - 8,8; 3,328 - 5,6; 3,283 - 7,2; 3,207 - 8,1; 3,098 - 6,9; 2,987 - 4,2; 2,873 - 5,4; 2,834 - 5,5; 2,770 - 7,1; 2,652 - 3,4; 2,585 - 3,7; 2,517 - 5,6; 2,421 - 4,5; 2,347 - 3,3; 2,283 - 5,5,
типом кристаллической решетки - моноклинная, пространственная группа P21, а = 14.5339(18) 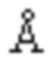 , b = 10,3792(14)
, b = 10,3792(14) 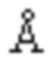 , с = 11,8253(14)
, с = 11,8253(14) 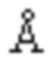 , β = 111,559(18)°, V = 1659,1(4)
, β = 111,559(18)°, V = 1659,1(4) 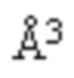 ρвыч = 1,155 г/см3, Z = 4 (2) C18H28O2,
ρвыч = 1,155 г/см3, Z = 4 (2) C18H28O2,
- ИК-Фурье спектрами в областях валентных колебаний O-H (3413 и 3369 см-1), C=O (1740 и 1724 см-1) и C-O (1067 и 1057 см-1) связей, области валентных колебаний C-H (3100 - 2800 см-1) связей, и в области «отпечатков пальцев» (1500-700 см-1),
отличающийся тем, что исходную субстанцию 3β-гидрокси-5-андростен-17-она испаряют при температуре 60-150°C в вакууме 5÷5×10-4 Торр в токе закиси азота - N2O со скоростью потока от 1 до 20 мл/мин (2,5*10-3 ÷ 5,0*10-2 моль/ч) и конденсируют на охлажденной до 0°C (273 К) - -196°C (77 К) поверхности.
| V.V | |||
| Chernyshev, Yu.N | |||
| Morozov, I.S | |||
| Bushmarinov, A.A | |||
| Makoed, G.B | |||
| Sergeev | |||
| New Polymorph of Dehydroepiandrosterone (DHEA) obtained via cryomodification | |||
| Crystal Growth & Design, 2016, V | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ РЕКЛАМ В ТРАМВАЙНЫХ ВАГОНАХ, АВТОБУСАХ И Т.П. | 1923 |
|
SU1088A1 |
| L-C | |||
| Chang, M.R | |||
| Caira, J.K | |||
| Guillory | |||
| Solid State characterization of Dehydroepiandrosterone, J | |||
| Pharm | |||
| Sci | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| Способ приготовления сернистого красителя защитного цвета | 1921 |
|
SU84A1 |
| RU | |||
Авторы
Даты
2024-06-07—Публикация
2022-11-22—Подача