Область изобретения
Настоящее изобретение относится к антителу или его фрагменту, содержащему по меньшей мере одну гетерологичную аминокислотную, последовательность, включенную вовнутрь по меньшей мере одного CDR участка указанного антитела или его фрагмента, где указанная по меньшей мере одна гетерологичная аминокислотная последовательность содержит N-терминальную линкерную последовательность (Ntls), предсердный натрийуретический пептид (ANP) и C-терминальную линкерную последовательность (Ctls). Необязательно, по меньшей мере часть указанного по меньшей мере одного CDR участка замещена указанной по меньшей мере одной гетерологичной аминокислотной последовательностью, включенной в него. По меньшей мере 12 аминокислотных остатков присутствуют между аминокислотным остатком HC (тяжелая цепь) res25 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1; аминокислотным остатком HC res51 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2; аминокислотным остатком HC res92 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3; аминокислотным остатком LC (легкой цепи) res26 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1; аминокислотным остатком LC res49 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или аминокислотным остатком LC res88 по Кэботу и первым аминокислотным остатком ANP в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3. Кроме того, по меньшей мере 9 аминокислотных остатков присутствуют между последним аминокислотным остатком ANP и аминокислотным остатком HC res35a по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1; аминокислотным остатком HC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2; аминокислотным остатком HC res106 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3; аминокислотным остатком LC res 32 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1; аминокислотным остатком LC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или аминокислотным остатком LC res98 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3. Кроме того, настоящее изобретение относится к антителу или его фрагменту для применения в способе лечения, композиции, содержащей антитело или его фрагмент, нуклеиновой кислоте или смеси нуклеиновых кислот, кодирующей антитело или его фрагмент, клетке-хозяину, содержащей такую нуклеиновую кислоту или смесь нуклеиновых кислот, и к способу получения антитела или его фрагмента.
Предшествующий уровень техники настоящего изобретения
Натрийуретические пептиды представляют собой семейство трех структурно родственных пептидов с нейрогуморальным действием. Предсердный натрийуретический пептид (ANP) представляет собой пептид из 28 аминокислот, содержащий центральную кольцевую структуру, образованную дисульфидным мостиком между цистеиновыми остатками 7 и 23. Человеческий ANP экспрессируется в клетках миоцитов предсердий в виде пре-прогормона длиной 153 аминокислоты. Расщепление сигнального пептида дает форму прогормона, которая затем дополнительно расщепляется на зрелый ANP и N-концевой остаток, известный как NT-proANP. Подобно ANP, также мозговой натрийуретический пептид (BNP) и натрийуретический пептид C-типа (CNP) продуцируются из белков-предшественников и содержат центральную кольцевую структуру. BNP в основном продуцируется и высвобождается кардиомиоцитами левого и правого предсердий сердца, тогда как BNP в основном продуцируется кардиомиоцитами желудочков. CNP синтезируется эндотелиальными клетками кровеносных сосудов. Помимо этих мест, натрийуретические пептиды также продуцируются в меньших количествах в других частях тела, например, в мозге, почках и надпочечниках. Натрийуретический пептид кодируется тремя отдельными генами, NPPA, NPPB, и NPPC. Аминокислотные последовательности трех пептидов являются высоко консервативными у млекопитающих (Potter et al., Handb Exp Pharmacol. 2009; (191):341-66). Тем не менее, были описаны значительные модификации последовательности натрийуретических пептидов, такие как усечения, аминокислотные замены, а также химерные слияния (например, CD-NP (McKie et al., Curr Heart Fail Rep.2010 Sep; 7 (3): 93-9)), которые приводят к мощным натрийуретическим пептидам, которые активируют клеточные рецепторы или связываются с ними и могут вызывать соответствующие физиологические эффекты.
Натрийуретические пептиды связываются с тремя различными типами мембраносвязанных рецепторов - NPR-A, NPR-B и NPR-C, тем самым опосредуя их биологические эффекты. ANP и BNP с наибольшим сродством связываются с NPR-A; напротив, CNP имеет самое высокое сродство к рецептору NPR-B. NPR-A и NPR-B содержат (партикулярно) домен гуанилатциклазы (pGC), ферментативная активность которого вызывает повышение (внутриклеточного) циклического гуанозинмонофосфата (cGMP). В качестве вторичного посредника cGMP регулирует различные клеточные процессы. Рецептор NPR-C не проявляет активности в отношении гуанилатциклазы и также называется рецептором «клиренса», поскольку он может связывать натрийуретические пептиды, что приводит к их разрушению посредством эндоцитоза. Описана дополнительная сигнальная функция рецептора NPR-C посредством модуляции cAMP (Anand-Srivastava, Peptides. 2005 Jun; 26 (6): 1044-59).
Сердечные гормоны ANP и BNP выделяются при растяжении желудочков и предсердий, например. из-за чрезмерного объема плазмы. Они оказывают сосудорасширяющее действие за счет расслабления гладких мышц сосудов и приводят к снижению кровяного давления. В почках ANP вызывает среди прочего увеличение экскреции с мочой (диурез), а также повышение концентрации ионов натрия в моче (натрийурез). Полагают, что ANP представляет собой компенсаторный антагонист ренин-ангиотензин-альдостероновой системы (РААС), которая чрезмерно активируется при ряде сердечно-сосудистых заболеваний. Кроме того, ANP оказывает и другие нейрогуморальные эффекты, включая ингибирующее действие на симпатическую нервную систему, а также комплексное регулирующее действие на барорефлекс (Woods et al., Clin Exp Pharmacol Physiol. 2004 Nov; 31 (11): 791-4). Противовоспалительные, антигипертрофические и антифиброзные эффекты ANP, а также BNP и CNP были продемонстрированы на животных моделях для различных заболеваний (например, Knowles et al., 2001, J. Clin. Invest. 107: 975-984; Dahrouj et al., J Pharmacol Exp Ther. 2013 Jan; 344 (1): 96-102; Baliga et al., Br J Pharmacol. 2014 Jul; 171 (14): 3463-75; Mitaka et al. Intensive Care Med Exp.2014 Dec; 2 (1): 28; Werner et al., Basic Res Cardiol. 2016 Mar; 111 (2): 22; Kimura et al., Respir Res. 2016 Feb 19; 17: 19). Активация NPR-B посредством CNP играет существенную роль в росте костей (Yasoda et al., Clin. Calcium. 2009 Jul; 19 (7): 1003-8) и целостности эндотелия сосудов (Moyes et al., J Clin Invest. 2014 Sep; 124 (9): 4039-51).
Широкий спектр физиологических эффектов натрийуретических пептидов и их рецепторов делает их привлекательными целями при открытии новых лекарственных средств (Lumsden et al., Curr Pharm Des. 2010; 16 (37): 4080-8; Buglioni et al., Annu Rev Med. 2016; 67: 229-43). Например, натрийуретическая система cGMP может подавляться при различных патофизиологических состояниях, что может приводить к гипертонии, повышенной клеточной пролиферации, фиброзу, воспалению, эндотелиальной дисфункции, диабету, метаболическому синдрому, атеросклерозу, сердечной недостаточности, инфаркту миокарда, легочной гипертензии, глазным и почечным заболеваниям, костным заболеваниям, инсульту и/или сексуальная дисфункция.
Основным препятствием для терапевтического использования натрийуретических пептидов является их очень короткий период полужизни в плазме, составляющий всего несколько минут, в организме (Hunt et al., J Clin Endocrinol Metab. 1994 Jun; 78 (6): 1428-35; Kimura et al., Eur J Clin Pharmacol.2007 Jul; 63 (7): 699-702). Помимо эндоцитоза рецептором NPR-C, натрийуретические пептиды эффективно протеолитически расщепляются ферментами неприлизином (NEP) и разлагающим инсулин ферментом (IDE). Связанные с этим краткосрочные биологические эффекты вводимых натрийуретических пептидов ограничивают их терапевтическое использование в основном при до острых показаний. Например, инфузии рекомбинантного карперитида (ANP) и несиритида (BNP) одобрены для лечения острой декомпенсированной сердечной недостаточности в разных странах.
Лечению хронических заболеваний в значительной степени способствовало бы обеспечение агонистов NPR-A и NPR-B с увеличенным периодом полужизни в плазме, более высокой протеолитической стабильностью и увеличенной продолжительностью действия.
В последние годы были описаны несколько производных и вариантов натрийуретических пептидов, например, CD-NP (McKie et al., Curr Heart Fail Rep.2010 Sep; 7 (3): 93-9), ZD100 / MANP (McKie et al., Hypertension. 2010 Dec; 56 (6): 1152-9), PL-3994 (Edelson et al., Pulm Pharmacol Ther. 2013 Apr; 26 (2): 229-38), Ularitide (Anker et al., Eur Heart J. 2015 Mar 21; 36 (12): 715-2), ANX-042 (Pan et al., Proc Natl Acad Sci USA. 2009 Jul. 7; 106 (27): 11282-7) и BMN-111 (Wendt et al., J. Pharmacol Exp Ther. 2015 Apr; 353 (1): 132-49). Период полужизни CD-NP составляет около 18.5 мин (Lee et al., BMC Pharmacology 2007, 7 (Suppl I): P38). Другие производные ANP и CNP раскрыты в US 9,193,777 и EP 2 432 489 A, соответственно.
Кроме того, слияния натрийуретического пептида, включая слияния с Fc, слияние с альбумином и ПЭГилированные натрийуретические пептиды, были описаны. Слияния натрийуретический пептид-Fc, например, описаны в US 2010/0310561, WO 2008/154226, WO 2010/117760, WO 2006/107124, WO 2008/136611 и WO 2008/079995. Слияния натрийуретический пептид-альбумин описаны в US 7,521,424 и US 2014/0148390, и ПЭГилированные натрийуретические пептиды описаны в US 2014/0148390.
В WO 2005/060642 описано создание библиотек антител с привитыми пептидами ANP и BNP, полученных вставкой ANP или BNP с двумя рандомизированными фланкирующими аминокислотами на обоих концах в участок CDRH3 человеческого антитела, специфичного к столбнячному токсоиду. Аналогичным образом, в WO 2005/082004 раскрывается создание библиотеки антител с привитым миметиком ANP, полученной заменой всего исходного участка CDRH3 антитела 2G12 на пептид-миметик ANP, фланкированный двумя случайными аминокислотными остатками с каждой стороны. Ни одна из WO 2005/060642 и WO 2005/082004 не раскрывает какие-либо специфические антитела с привитым натрийуретическим пептидом, не говоря уже о функциональных характеристиках таких антител.
Задача настоящего изобретения
Исходя из предшествующего уровня техники задача настоящего изобретения состоит в обеспечении агонистов рецептора натрийуретического пептида с повышенной стабильностью в сыворотке по сравнению с натрийуретическими пептидами дикого типа природного происхождения.
Сущность изобретения
Вышеуказанная задача решается объектами изобретения, раскрытыми в независимых пунктах формулы изобретения. Авторами настоящего изобретения неожиданно было обнаружено, что биологически активные варианты натрийуретического пептида со значительно увеличенной стабильностью в сыворотке по сравнению с натрийуретическими пептидами дикого типа природного происхождения могут быть получены посредством включения аминокислотной последовательности натрийуретического пептида в один из CDR участков молекулы иммуноглобулина или ее фрагмента, несмотря на короткую длину и высокую консервативность последовательности участков CDR иммуноглобулина, что создает значительные конформационные ограничения для включения биологически активных пептидов. Однако активность натрийуретических пептидов, включенных в участок CDR иммуноглобулина, как было показано, значительно различается. Авторы настоящего изобретения обнаружили, что решающим фактором для успешного включения с получением биологически активного варианта натрийуретического пептида является число аминокислотных остатков между включенным натрийуретическим пептидом и ближайшими соседними соединениями CDR-каркаса, N-терминальными и C-терминальными от включенного натрийуретического пептида. Ниже определенного числа N-терминальных и C-терминальных фланкирующих аминокислотных остатков между натрийуретическим пептидом и соседними соединениями CDR-каркаса образуются только слитые конструкции натрийуретического пептида и иммуноглобулина без биологической активности или с резко пониженной биологической активностью. Было обнаружено, что специфические линкерные последовательности, фланкирующие включенный натрийуретический пептид, являются особенно предпочтительными для достижения высокой пептидной активности, хороших уровней экспрессии и/или низких уровней фрагментации белка.
Таким образом, первым объектом настоящего изобретения является антитело или его фрагмент, содержащее по меньшей мере одну гетерологичную аминокислотную, последовательность, включенную вовнутрь по меньшей мере одного CDR участка указанного антитела или его фрагмента, где указанная по меньшей мере одна гетерологичная аминокислотная последовательность содержит N-терминальную линкерную последовательность (Ntls), натрийуретический пептид и C-терминальную линкерную последовательность (Ctls), где необязательно по меньшей мере часть указанного по меньшей мере одного CDR участка замещена указанной по меньшей мере одной гетерологичной аминокислотной последовательностью, включенной в него, и где
a) по меньшей мере 12 аминокислотных остатков присутствуют между
i) аминокислотным остатком HC res25 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res S25) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res51 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res I51) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res92 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res C96) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res26 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res S25) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res49 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res Y51) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res88 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res C90) и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3; и где
b) по меньшей мере 9 аминокислотных остатков присутствуют между последним аминокислотным остатком натрийуретического пептида и
i) аминокислотным остатком HC res35a по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res M34) в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res57 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res T58) в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res106 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res G111) в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res 32 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res D34) в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res57 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res G59) в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res98 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res F102) в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3.
Другими объектами настоящего изобретения являются антитело или его фрагмент для применения в способе лечения, композиция, содержащая антитело или его фрагмент, нуклеиновая кислота или смесь нуклеиновых кислот, кодирующая антитело или его фрагмент клетка-хозяин, содержащая такую нуклеиновую кислоту или смесь нуклеиновых кислот, и способ получения антитела или его фрагмента.
Подробное описание настоящего изобретения
Настоящее изобретение может стать более понятным посредством последующего подробного описания настоящего изобретения и примеров, приведенных в настоящем документе.
Согласно первому аспекту настоящее изобретение относится к антителу или его фрагменту, содержащему по меньшей мере одну гетерологичную аминокислотную, последовательность, включенную вовнутрь по меньшей мере одного CDR участка указанного антитела или его фрагмента, где указанная по меньшей мере одна гетерологичная аминокислотная последовательность содержит N-терминальную линкерную последовательность (Ntls), натрийуретический пептид и C-терминальную линкерную последовательность (Ctls), где необязательно по меньшей мере часть указанного по меньшей мере одного CDR участка замещена указанной по меньшей мере одной гетерологичной аминокислотной последовательностью, включенной в него.
Авторы настоящего изобретения обнаружили, что биологически активные варианты натрийуретического пептида со значительно увеличенной стабильностью в сыворотке по сравнению с натрийуретическими пептидами дикого типа природного происхождения, могут быть получены посредством включения аминокислотной последовательности натрийуретического пептида в один из CDR участков молекулы иммуноглобулина или ее фрагмента. Это обнаружение было совершенно неожиданным. Как хорошо известно в данной области техники, короткая длина и высокая консервативность последовательности участков CDR иммуноглобулина, что особенно выражено в CDRL1, CDRL2, CDRL3, CDRH1 и CDRH2, создает значительные конформационные ограничения для включения биологически активных пептидов в окружающие иммуноглобулин последовательности могут отрицательно влиять на экспрессию, складывание и/или биологическую активность включенного пептида. Авторы настоящего изобретения неожиданно обнаружили, что активность натрийуретических пептидов, включенных в участок CDR иммуноглобулина, значительно меняется в зависимости от точного пути конструирования антитела с привитым натрийуретическим пептидом. Решающим фактором успешного включения с получением функционального, т.е. биологически активного варианта натрийуретического пептида, как показано, является число аминокислотных остатков между включенным натрийуретическим пептидом и ближайшими соседними соединениями CDR-каркаса, N-терминальными и C-терминальными от включенного натрийуретического пептида. Ниже определенного числа N-термнальных и C-терминальных фланкирующих аминокислотных остатков между натрийуретическим пептидом и соседними соединениями CDR-каркаса образуются только слитые конструкции натрийуретического пептида и иммуноглобулина без биологической активности.
Термины «включенный», «вставленный», «интегрированный», «привитый» и «внедренный», а также «включение», «вставка», «интеграция», «прививание» и «внедрение» используются в настоящем документе взаимозаменяемо. В контексте настоящего изобретения эти термины относятся к образованию гибридных полинуклеиновых кислот или гибридных полипептидов путем введения гетерологичной последовательности в исходную последовательность антитела или фрагмента антитела. Такое включение может быть осуществлено любыми способами. Обычно антитело или его фрагмент, содержащий натрийуретический пептид, фланкированный N-терминальной и C-терминальной линкерной последовательностью, получают с помощью методики и экспрессии рекомбинантной ДНК, как описано в данном документе.
Включение натрийуретического пептида, фланкированного N-терминальной и C-терминальной линкерной последовательностью, в CDR участок исходной последовательности антитела или его фрагмента, может привести к делеции по меньшей мере части указанного CDR участка. Например, клонирование последовательности нуклеиновой кислоты, кодирующей указанную гетерологичную аминокислотную последовательность, содержащую N-терминальную линкерную последовательность, натрийуретический пептид и C-терминальную линкерную последовательность, может быть осуществлено таким образом, что часть CDR-кодирующей последовательности замещается включенной гетерологичной последовательностью нуклеиновой кислоты. Согласно другим частным вариантам осуществления, включение гетерологичной аминокислотной последовательности, содержащей натрийуретический пептид, не приводит к делеции аминокислотных остатков CDR участка, в который гетерологичная аминокислотная последовательность вставлена.
В контексте настоящего изобретения термин «гетерологичная последовательность последовательностей» относится к аминокислотной последовательности, которая не происходит из исходного «пустого» антитела или его фрагмента, в который она включена. Внедрение гетерологической аминокислотной последовательности в антитело или его фрагмент, таким образом, дает сконструированную рекомбинантную молекулу антитела, состоящую из аминокислотных последовательностей различного происхождения.
Термин «натрийуретический пептид» относится к пептидам, которые могут вызывать натрийурез, выведение натрия почками. Натрийуретические пептиды включает включают атриальный натрийуретический пептид (ANP), мозговой натрийуретический пептид (BNP), натрийуретический пептид C-типа (CNP), натрийуретический пептид мамб (DNP) и Уродилатин. Натрийуретические пептиды в контексте настоящего изобретения могут быть любого происхождения. Натрийуретические пептиды включают натуральные натрийуретические пептиды, такие как натрийуретический пептид дикого типа и их мутантные варианты, а также гомолог гомологичные натрийуретические пептиды другого вида. Однако этот термин также включает искусственно созданные натрийуретические пептиды, такие как модифицированные химерные варианты отдельных натрийуретических пептидов. Известно, что использование кодонов у разных видов различно. Таким образом, при экспрессии гетерологичного белка в клетке-мишени может быть необходимо или, по меньшей мере, полезно адаптировать последовательность нуклеиновой кислоты к использованию кодона клеткой-мишенью. Способы разработки и конструирования производных данного белка хорошо известны любому специалисту в данной области техники.
Согласно частным вариантам осуществления натрийуретический пептид выбран из натрийуретического пептида дикого типа любого вида и функционального варианта любого такого натрийуретического пептида дикого типа. В контексте настоящего изобретения термин “функциональный вариант натрийуретического пептида” или “вариант функционального натрийуретического пептида” относится к натрийуретическому пептиду любого происхождения, включая природные и сконструированные пептиды, которые различны по аминокислотной последовательности и/или последовательности нуклеиновой кислоты, кодирующей аминокислотную последовательность данного натрийуретического пептида, как например натрийуретического пептида дикого типа данного вида, но все еще функционально активны. В контексте настоящего изобретения термин «функционально активный» относится к способности варианта натрийуретического пептида выполнять биологические функции природного натрийуретического пептида, в частности натрийуретического пептида дикого типа. В частности, «функционально активный» означает, что вариант натрийуретического пептида способен связываться со своим соответствующим рецептором. В случае лигандов NPR-A и NPR-B, «функционально активный», в частности, означает способность опосредовать увеличение (внутриклеточного) циклического гуанозинмонофосфата (cGMP) посредством связывания с одним или обоими этими рецепторами.
Согласно частным вариантам осуществления функциональные варианты натрийуретического пептида способны осуществлять одну или несколько биологических функций данного натрийуретического пептида, такого как натрийуретический пептид дикого типа данного вида на по меньшей мере около 50%, в частности по меньшей мере около 60%, по меньшей мере около 70%, по меньшей мере около 80% и самое большее, в частности, по меньшей мере около 90%, где одна или несколько биологических функций включают без ограничение, связывание натрийуретического пептида с его соответствующим рецептором и/или индукцию увеличения внутриклеточного cGMP.
Функциональная активность натрийуретических пептидов может быть измерена любыми методами, включая методы in vitro, которые позволяют либо измерить повышение (внутриклеточного) циклического гуанозинмонофосфата (cGMP), либо измерить изменения клеточных процессов, регулируемых cGMP, включая методы описанный в примерах 3 и 5. Согласно частным вариантам осуществления, вариант натрийуретического пептида (непривитый) считается функционально активным, если его значение EC50, определенное с помощью флуоресцентного анализа, описанного в примере 3, ниже 500 нМ, более конкретно ниже 250 нМ, более конкретно ниже 150 нМ, более конкретно ниже 100 нМ, более конкретно ниже 50 нМ, наиболее конкретно ниже 25 нМ.
Включение такого функционального варианта натрийуретического пептида в один из CDR участков молекулы иммуноглобулина или ее фрагмента, как описано в данном документе, дает иммуноглобулин, привитый натрийуретическим пептидом, с функциональной активностью натрийуретического пептида, и значительно повышенную стабильность в сыворотке по сравнению с непривитым функциональным вариантом натрийуретического пептида, как показано в примерах. Привитый натрийуретическим пептидом иммуноглобулин считается биологически активным (то есть функциональным), если он дает значительный положительный сигнал любым методом, который измеряет увеличение (внутриклеточного) циклического гуанозинмонофосфата (cGMP) прямо или косвенно путем оценки изменений в клеточных процессах, регулируемых cGMP. В частности, функциональную активность иммуноглобулина с привитым натрийуретическим пептидом можно оценить методами, описанными в примерах 3 и 5. В случае иммуноглобулинов, привитых натрийуретическим пептидом, значимость обычно оценивается на основании i) сравнения с отрицательным образцом, таким как пустой каркас иммуноглобулина, например, конструкция №209, антитело, содержащее SEQ ID NO 65 и SEQ ID NO 66, TPP-5657, ii) сравнение с положительным образцом, например, конструкция №117, антитело, содержащее SEQ ID NO 67 и SEQ ID NO 66, TPP-5661, и iii) дозозависимость.
Несмотря на то, что функциональный вариант натрийуретического пептида согласно настоящему изобретению может содержать любое количество мутаций, включающих добавления, делеции и/или замены одной или нескольких аминокислот по сравнению с эталонным натрийуретическим пептидом, функциональный вариант натрийуретического пептида обычно будет сохранять ключевые характеристики. соответствующего натрийуретического пептида, таких как ключевые остатки в центральном кольцевом домене. Консервативные остатки натрийуретических пептидов описаны, например, в Lincoln R. Potter et al. (Handb Exp Pharmacol. 2009; (191): 341-366). Таким образом, согласно частным вариантам осуществления, функциональный вариант натрийуретического пептида на по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичен последовательности согласно последовательности, показанной ниже:
X1CFGX2X3X4DRIX5X6X7SX8LGC
где X1 и X5 представляют собой G или S;
X3 представляет собой R или K;
X6 представляет собой A или S; и
X2, X4, X7 и X8 могут представлять собой любую аминокислоту.
На самом деле, натрийуретические пептиды любого типа могут быть включены в участок CDR иммуноглобулина или его фрагмента, как описано в настоящем документе. В частности, авторы настоящего изобретения обнаружили, что присутствие одного типа натрийуретического пептида достаточно для удовлетворения обоих минимальных требований достаточной биологической активности привитого натрийуретического пептида, и в частности подходящие N-концевые и C-концевые аминокислотные последовательности могут быть обеспечены другими типами натрийуретических пептидов. Не желая ограничиваться теорией, полагают, что эти схожие требования для успешного внедрения натрийуретического пептида в молекулу иммуноглобулина среди различных типов натрийуретического пептида могут быть обусловлены структурным сходством и/или механизмами действия в семействе натрийуретических пептидов.
Согласно частным вариантам осуществления натрийуретический пептид выбран из группы, состоящей из человеческого ANP, имеющего последовательность SEQ ID NO 23, человеческого BNP, имеющего последовательность согласно SEQ ID NO 24, человеческого CNP, имеющего последовательность согласно SEQ ID NO 25, и пептида, имеющего последовательность на по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или по меньшей мере 98% идентичную последовательности согласно любой из SEQ ID NO 23 - 25. Снова, натрийуретический пептид, имеющий последовательность, отличную от человеческих натрийуретических пептидов ANP, BNP и CNP дикого типа, может иметь любое естественное происхождение, например мутантная версия натрийуретического пептида человека дикого типа, или гомолог другого вида, или сконструированный натрийуретический пептид. Способы разработки и конструирования вариантов пептидов хорошо известны специалисту в данной области техники.
Согласно таким частным вариантам осуществления натрийуретический пептид, имеющий последовательность, на по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или по меньшей мере 98% идентичную последовательности согласно любой из SEQ ID NO 23 - 25, представляет собой функциональный вариант натрийуретического пептида.
«Процент (%) идентичности последовательности" относительно ссылочной полинуклеотидной или полипептидной последовательности, соответственно, определяли как процент остатков нуклеиновой кислоты или аминокислотных остатков, соответственно, в последовательности-кандидате, которые идентичны по остаткам нуклеиновой кислоты или аминокислотным остаткам, соответственно в ссылочной полинуклеотидной или полипептидной последовательности, соответственно, после выравнивания последовательностей и введение гэпов при необходимости, для достижения максимального процента идентичности последовательности. Консервативные замены не рассматриваются как часть идентичности последовательности. Согласно частным вариантам осуществления, любые гэпы, введенные в кандидатную последовательность и/или эталонную последовательность, не могут в общей сложности превышать более 50%, более 40%, более 30%, более 25%, более 20%, более 15% или более 10% от общего количества остатков эталонной последовательности. Согласно конкретному варианту осуществления идентичность последовательности в процентах определяется без введения каких-либо гэпов в кандидатную или эталонную последовательность (т.е. с использованием выравнивания без пробелов). Выравнивание с целью определения процента идентичности аминокислотной последовательности может быть достигнуто различными способами, которые находятся в пределах компетентности специалистов в данной области техники, например, с использованием общедоступного программного обеспечения, такое как BLAST, BLAST 2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить соответствующие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания сравниваемых полноразмерных последовательностей.
Натрийуретический пептид, который имеет определенный процент идентичности с последовательностью данного эталонного натрийуретического пептида, например, человеческий ANP, имеющий аминокислотную последовательность SEQ ID NO 23, может содержать одну или несколько мутаций, включающих добавление, делецию и/или замену одной или нескольких аминокислот по сравнению с эталонным натрийуретическим пептидом. Согласно настоящему изобретению указанные удаленные, добавленные и/или замещенные аминокислоты могут быть последовательными аминокислотами или могут быть разбросаны по длине аминокислотной последовательности натрийуретического пептида, которая имеет данный процент идентичности с последовательностью эталонного натрийуретического пептида, например, человеческий ANP, имеющий аминокислотную последовательность SEQ ID NO 23. На уровне ДНК, последовательность нуклеиновой кислоты, кодирующая натрийуретический пептид, которая имеет данный процент идентичности с последовательностью данного эталонного натрийуретического пептида может отличаться в большей степени из-за вырожденности генетического кода.
Согласно настоящему изобретению любое количество аминокислот может быть добавлено, удалено и/или заменено, до тех пор, пока сохраняется указанная идентичность с последовательностью эталонного натрийуретического пептида. Согласно частным вариантам осуществления предусмотренная идентичность аминокислотной последовательности соблюдается, и вариант натрийуретического пептида является биологически активным, т.е. является функциональным вариантом натрийуретического пептида. Предпочтительно, чтобы биологическая активность натрийуретического пептида, который имеет заданный процент идентичной последовательности с последовательностью данного эталонного натрийуретического пептида, например, человеческого ANP, имеющего аминокислотную последовательность SEQ ID NO 23, снижается менее чем на 90%, менее чем на 80%, менее чем на 70%, менее чем на 60%, менее чем на 50%, менее чем на 25% или менее чем на 10% по сравнению с указанным эталонным натрийуретическим пептидом, как измерено согласно описанному выше анализу.
Термин "антитело", как применяется в описании настоящего изобретения, описывает иммуноглобулиновые молекулы, предпочтительно состоящие из четырех полипептидных цепей, двух тяжелых (Н) цепей и двух легких (L) цепей, которые, как правило, связываются дисульфидными мостиками. Каждая тяжелая цепь содержит вариабельный домен тяжелой цепи (сокращаемые в настоящем изобретении как VH) и константный домен тяжелой цепи. Константный домен тяжелой цепи может содержать, например, три домена СН1, СН2 и СН3. Каждая легкая цепь содержит вариабельный домен легкой цепи (сокращаемый в настоящем изобретении как VL) и константный домен легкой цепи. Константный домен легкой цепи содержит один домен (CL). Домены VL и VH могут быть дополнительно подразделены на гипервариабельные участки, называемые участками, определяющими комплементарность (CDR), вкрапленные в области, которые являются более консервативными, называемые каркасными участками (FR). Каждый VH и VL, как правило, состоит из трех CDR и до четырех FR. расположенных от N-конца к С-концу, например, в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
Как применяется в описании настоящего изобретения, термин «участки, определяющие комплементарность» (CDR; например, CDR1, CDR2 и CDR3), относится к аминокислотным остаткам вариабельного домена антитела, присутствие которого необходимо для связывания антигена. Каждый вариабельный домен, как правило, имеет три участка CDR, идентифицируемые как CDR1, CDR2 и CDR3. Каждый участок, определяющий комплементарность, может содержать аминокислотные остатки из "участка, определяющего комплементарность", как определено по Кэботу (например, около остатков 24-34 (L1), 50-56 (L2) и 89-97 (L3) в вариабельной области легкой цепи и 31-35 (Н1), 50-65 (Н2) и 95-102 (Н3) в вариабельном домене тяжелой цепи; (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)) и/или остатки из "гипервариабельной петли" (например, около остатков 26-32 (L1), 50-52 (L2) и 91-96 (L3) в вариабельной области легкой цепи и 26-32 (Н1), 53-55 (Н2) и 96-101 (НЗ) в вариабельном домене тяжелой цепи (Chothia and Lesk; J Mol Biol 196:901-917 (1987)). В некоторых случаях участок, определяющий комплементарность, может включать аминокислоты как из участка CDR, определенного в соответствии с Кэботом, так и из гипервариабельной петли.
В зависимости от аминокислотной последовательности константного домена их тяжелых цепей интактные антитела могут быть отнесены к различным "классам". Существует пять главных классов интактных антител: IgA, IgD, IgE, IgG и IgM - и некоторые из них могут дополнительно разделяться на "подклассы" (изотипы), например, IgGI, IgG2, IgG3, IgG4, IgA и IgA2. В контексте настоящего изобретения термин “антитело” включает молекулы иммуноглобулина любого первичного класса - включая IgG, IgE, IgM, IgD, IgA и IgY - и любого подкласса - включая IgG1, lgG2, lgG3, lgG4, IgA1 и Ig A2 - природного происхождения или полученные рекомбинантными средствами и включает все в общем известные антитела. Предпочтительным классом иммуноглобулинов для применения согласно настоящему изобретению является IgG. Термин “антитело” также относится к другим белковым каркасам, которые способны ориентировать вставки CDR антител в ту же самую активную конформацию связывания, что и в природных антителах, так что связывание антигена-мишени, наблюдаемое с этими химерными белками, сохраняется относительно связывающей активности природного антитела, из которого были получены CDR.
В контексте настоящего изобретения термин «фрагмент» антитела/иммуноглобулина относится к любой части антитела /иммуноглобулина, которая содержит по меньшей мере один участок CDR. В частности, фрагмент антитела согласно настоящему изобретению сохраняет способность увеличивать время полужизни в сыворотке биологически активного пептида, предпочтительно натрийуретического пептида, включенного в него. Фрагменты антитела согласно настоящему изобретению включают фрагменты Fab, Fab', Fab'-SH, F(ab')2 и Fv; диатела; однодоменные антитела (Dabs); линейные антитела; одноцепочечные молекул антител (scFv) и дисульфид-стабилизированные фрагменты антитела Fv (dsFv); а также мультиспецифические фрагменты антитела и фрагменты, содержащие домен VL или VH, которые получают из интактных иммуноглобулинов или получают рекомбинантными средствами.
F(ab')2 или Fab могут быть разработаны для минимизации или полного удаления межмолекулярных дисульфидных взаимодействий, которые происходят между доменами CH1 и CL. Фрагменты антител в соответствии с настоящим изобретением могут включать вариабельный (вариабельные) участок (участки) отдельно или в комбинации со всеми или частично из следующего: шарнирная область, домены CH1, CH2, CH3 и CL. Также включены фрагменты антител, содержащие любую комбинацию вариабельного (вариабельных) участка (участков) с шарнирной областью, доменом CH1, CH2, CH3 и CL.
Антитело или его фрагмент составляет каркас, который придает стабильность включенному в него натрийуретическому пептиду. Например, время полужизни в сыворотке натрийуретического пептида, включенного в участок CDR антитела, как описано в настоящем документе, может быть увеличено по сравнению с временем полужизни в сыворотке натрийуретического пептида природного происхождения.
В принципе, гетерологичная аминокислотная последовательность, содержащая натрийуретический пептид, может быть включена в любую молекулу иммуноглобулина или ее фрагмент.В частности, иммуноглобулины любого вида (включая, но не ограничиваясь этим, человека, крупного рогатого скота, мыши, крысы, свиньи, собаки, акулы, ламы и верблюда) и любого первичного класса и подкласса могут использоваться в соответствии с настоящим изобретением. Однако для терапевтического использования может быть предпочтительным человеческое или гуманизированное антитело. В контексте настоящего изобретения термин «человеческое антитело» относится к антителам, имеющим аминокислотную последовательность человеческого иммуноглобулина, и включает антитела, выделенные из библиотек иммуноглобулинов человека, из В-клеток человека или от животных, трансгенных в отношении одного или нескольких иммуноглобулинов человека. а также синтетические человеческие антитела. Согласно частному варианту осуществления аминокислотные последовательности легкой цепи и тяжелой цепи вариабельного домена происходят из последовательностей человеческой зародышевой линии LV 1-40 и HV 3-23 соответственно (для получения дополнительной информации см. Пример 1).
В контексте настоящего изобретения термин «гуманизированное антитело» или «фрагмент гуманизированного антитела» относится к антителу или его фрагменту, которое (i) происходит из источника, отличного от человека (например, трансгенная мышь, несущая гетерологичную иммунную систему), антитело которой основано на последовательности зародышевой линии человека; или (ii) химерное, где вариабельный домен имеет нечеловеческое происхождение, а константный домен имеет человеческое происхождение, или (iii) с привитыми CDR, где CDR вариабельного домена имеют нечеловеческое происхождение, в то время как один или несколько каркасов вариабельного домена имеют человеческое происхождение, и константный домен (если таковой имеется) имеет человеческое происхождение.
Антитело или его фрагмент согласно настоящему изобретению может быть моноспецифическим, биспецифическим, триспецифическим или более мультиспецифическим.
В контексте настоящего изобретения термин «содержит» или «содержащий» означает «включая, но не ограничиваясь этим». Термин является открытым, означая наличие любых заявленных функций, элементов, целых чисел, стадий или компонентов, но не исключая наличие или добавление одной или нескольких других функций, элементов, целых чисел, стадий, компонентов или их группы. Термин «содержащий», таким образом, включает более ограничительные термины «состоящий из» и «по существу состоящий из». Согласно одному варианту осуществления термин «содержащий», используемый по всей заявке и, в частности, в формуле изобретения, может быть заменен термином «состоящий из».
В контексте настоящего изобретения термин “около” или “приблизительно” означает в пределах от 80% до 120%, альтернативно в пределах от 90% до 110%, включая в пределах от 95% до 105% от данного значения.
В антителе или его фрагменте согласно настоящему изобретению, a) по меньшей мере 12 аминокислотных остатков присутствуют между
i) аминокислотным остатком HC res25 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res S25) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res51 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res I51) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res92 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res C96) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res26 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res S25) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res49 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res Y51) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res88 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res C90) и первым аминокислотным остатком натрийуретического пептида в случае включения гетерологичной аминокислотной последовательности в CDRL3;
и b) по меньшей мере 9 аминокислотных остатков присутствуют между последним аминокислотным остатком натрийуретического пептида и
i) аминокислотным остатком HC res35a по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res M34) в случае включения гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res57 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res T58) в случае включения гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res106 по Кэботу (в тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO 65, это соответствует res G111) в случае включения гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res 32 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res D34) в случае включения гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res57 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res G59) в случае включения гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res98 по Кэботу (в легкой цепи, имеющей аминокислотную последовательность SEQ ID NO 66, это соответствует res F102) в случае включения гетерологичной аминокислотной последовательности в CDRL3.
Название перечисленных выше аминокислотных остатков относится к положению аминокислоты в исходной молекуле иммуноглобулина до включения гетерологичной аминокислотной последовательности. В контексте настоящего изобретения перечисленные выше аминокислотные остатки называются «эталонными аминокислотами» или «ссылочными аминокислотами». Эти эталонные аминокислотные остатки лежат на соединениях каркаса CDR или рядом с ними, но не обязательно соответствуют стандартным определениям границ CDR (стандартные определения границ CDR представляют собой аминокислотные остатки S25 и W36 для CDRH1; S49 и R67 для CDRH2; K98 и W108 для CDRH3; C22 и W37 для CDRL1; Y51 и G59 для CDRL2; C90 и F102 для CDRL3. Jarasch and Skerra, Proteins 2017 Jan; 85 (1): 65-71).
Ближайшая соседняя N-концевая эталонная аминокислота от вставленного натрийуретического пептида плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком, вставленного натрийуретического пептида, в настоящем документе обозначают как «N-концевой последовательностью». N-концевая последовательность содержит Ntls. Согласно частным вариантам осуществления N-концевая последовательность состоит из Ntls плюс соседней N-концевой эталонной аминокислоты.
Аминокислотное удлинение, присутствующее между аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней эталонной C-концевой аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота в настоящем документе обозначают как “C-концевая последовательность”. C-концевая последовательность содержит Ctls. Согласно частным вариантам осуществления C-концевая последовательность состоит из Ctls плюс соседней C- концевой эталонной аминокислоты.
Согласно частным вариантам осуществления, Ntls содержит GS линкерную последовательность; PN линкерную последовательность; аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно последовательность согласно любой из SEQ ID NO 1, 2 или 4, или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4; последовательность согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21; или последовательность, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21. Ntls также может содержать любую комбинацию перечисленных выше аминокислотных последовательностей.
Согласно таким частным вариантам осуществления, Ntls содержит GS линкерную последовательность; PN линкерную последовательность; аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно последовательность согласно любой из SEQ ID NO 1, 2 или 4, или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4; последовательность согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15 или 21; последовательность, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, или 21; или любую их комбинацию.
Согласно частным вариантам осуществления, Ctls содержит GS линкерную последовательность; PN линкерную последовательность; аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно последовательность согласно любой из SEQ ID NO 1, 3 или 5, или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 3 или 5; последовательность согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22; или последовательность, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22. Ctls также может содержать любую комбинацию перечисленных выше аминокислотных последовательностей.
Согласно частным вариантам осуществления, Ctls содержит GS линкерную последовательность; PN линкерную последовательность; аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно последовательность согласно любой из SEQ ID NO 1, 3 или 5, или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 3 или 5; последовательность согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 20 или 22; последовательность, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 20 или 22; или любую их комбинацию.
Согласно частным вариантам осуществления идентичность последовательности между последовательностью, содержащейся в Ntls и/или Ctls и любой из SEQ ID NO 1 - 22 составляет по меньшей мере 60%, в частности по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или 100%.
В контексте настоящего изобретения термин “GS линкерная последовательность” относится к пептидному линкеру, содержащему в основном глициновые и сериновые остатки. В частности, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или 100% аминокислотных остатков GS линкерной последовательности согласно настоящему изобретению выбраны из глициновых и сериновых остатков. GS линкерная последовательность согласно настоящему изобретению может, например, содержать от 1 до 30 аминокислотных остатков в общем. В частности, GS линкерная последовательность согласно настоящему изобретению не содержит более 3, 2 или 1 аминокислотных остатков, отличных от глицина или серина.
В контексте настоящего изобретения термин “PN линкерная последовательность” относится к пептидному линкеру, содержащему в основном пролиновый и аспарагиновый остатки. В частности, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или 100% аминокислотных остатков PN линкерной последовательности согласно настоящему изобретению выбраны из пролинового и аспарагинового остатка. PN линкерная последовательность согласно настоящему изобретению может, например, содержать от 1 до 30 аминокислотных остатков в общем. В частности, PN линкерная последовательность согласно настоящему не содержит более 3, 2 или 1 аминокислотных остатков, отличных от пролина или аспарагина. Другие аминокислотные остатки, которые могут присутствовать в PN линкерной последовательности согласно настоящему изобретению, представляют собой, например, остатки лизина или глутаминовой кислоты.
Согласно частным вариантам осуществления линкерная последовательность, содержащаяся в Ntls и/или Ctls и выбранная из GS линкерной последовательности; PN линкерной последовательности; линкерной последовательности каркаса антитела IgG человека; последовательности каркаса fab домена IgG человека; последовательности, которая по меньшей мере на 80% идентична последовательности линкерной последовательности, последовательности каркаса fab домена IgG человека или последовательности согласно любой из SEQ ID NO: 1-5; и последовательности, которая на по меньшей мере 60% идентична последовательности согласно любой из SEQ ID NO: 6 - 22, содержит по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных остатков. Линкерная последовательность, содержащаяся в Ntls и/или Ctls, может, например, содержать до 30, 28, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11 или 10 аминокислотных остатков.
В случае линкеров, содержащих последовательность каркаса антитела IgG человека или последовательность, которая на по меньшей мере 80% идентична ей, может быть особенно предпочтительно использована последовательность участка каркаса, которая примыкает к CDR, в которую включена гетерологичная аминокислотная последовательность. Например, Ntls и/или Ctls могут содержать линкер, содержащий аминокислотную последовательность, которая является частью каркасного участка FRH2 или FRH3 в случае, если гетерологическая аминокислотная последовательность включена в домен CDRH2. Подобным образом, Ntls и/или Ctls могут содержать линкер, содержащий аминокислотную последовательность, которая является частью каркасного участка FRL2 или FRL3 в случае, если гетерологическая аминокислотная последовательность включена в участок CDRL2.
Согласно частным вариантам осуществления, Ntls состоит из GS линкерной последовательности; PN линкерной последовательности; аминокислотной последовательности, которая является частью каркаса антитела IgG человека или последовательности, которая на по меньшей мере 80% идентична ей, в частности аминокислотной последовательности, которая является частью каркаса домена fab человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, более конкретно последовательности согласно любой из SEQ ID NO 1, 2 или 4 или последовательности, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4; последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21; последовательности, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21; или любой их комбинации.
Согласно частным вариантам осуществления Ctls состоит из GS линкерной последовательности; PN линкерной последовательности; аминокислотной последовательности, которая является частью каркаса человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, в частности аминокислотной последовательности, которая является частью каркаса домена fab человеческого антитела IgG или последовательности, которая на по меньшей мере 80% идентична ей, более конкретно последовательности согласно любой из SEQ ID NO 1, 3 или 5, последовательности, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 3 или 5; последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22; последовательности, которая на по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22; или любой их комбинации.
Согласно частным вариантам осуществления, как Ntls, так и Ctls содержат по меньшей мере одну из вышеперечисленных линкерных последовательностей или любую их комбинацию. На самом деле, любая из вышеперечисленных линкерных последовательностей Ntls может быть комбинирована с любой из вышеперечисленных линкерных последовательностей Ctls. На самом деле, любая линкерная последовательность может быть комбинирована с GS линкером. В качестве неограничивающего примера GS Ctls линкер может быть комбинирован с Ntls линкером, содержащим последовательность согласно любой из SEQ ID NO 6, 9 или 15 или последовательность, которая на по меньшей мере 60% идентична последовательности согласно любой из SEQ ID NO 6, 9 или 15Другим неограничивающим примером является GS Ntls линкер, комбинированный с Ctls линкером, содержащим последовательность согласно SEQ ID NO 15 или последовательность, которая на по меньшей мере 60% идентична ей.
Вышеуказанные линкерные последовательности оказались особенно полезными для достижения хороших активностей натрийуретических пептидов при достаточной общей длине N-концевой и C-концевой фланкирующих последовательностей. Не желая быть связанными теорией, полагают, что указанные выше линкерные пептидные удлинения приводят к конформации/складке, которая способствует благоприятному состоянию системы при представлении биологически активного натрийуретического пептида соответствующему рецептору с минимальными стерическими затруднениями.
Согласно частным вариантам осуществления i) Ntls содержит GS линкерную последовательность; PN линкерную последовательность; последовательность согласно SEQ ID NO 2, 4, 9, 11, 13 или 15; последовательность, которая на по меньшей мере 60% идентична последовательности согласно SEQ ID NO 2, 4, 9, 11, 13 или 15; или любую их комбинацию, и ii) Ctls содержит GS линкерную последовательность; PN линкерную последовательность; последовательность согласно SEQ ID NO 3, 5, 12, 14, 15 или 20; последовательность, которая на по меньшей мере 60% идентична последовательности согласно SEQ ID NO 3, 5, 12, 14, 15 или 20; или любую их комбинацию. Эти последовательности линкеров оказались особенно полезными, так как они не только для достижения высоких активностей натрийуретического пептида, хороших уровней экспрессии при рекомбинантной экспрессии и минимальной фрагментации белка или ее отсутствия, как показано в Таблице 9.
Эти линкерные последовательности оказались особенно полезными, поскольку они не только обеспечивают высокую активность натрийуретического пептида, но также обладают хорошими уровнями экспрессии при рекомбинантной экспрессии и не склонны к фрагментации белка при экспрессии (см. Таблицу 9).
Согласно частным вариантам осуществления, Ntls и Ctls каждая содержит GS линкерную последовательность; Ntls и Ctls каждая содержит PN линкерную последовательность; Ntls и Ctls каждая содержит аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно Ntls содержит последовательность согласно любой из SEQ ID NO 1, 2 или 4 или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4, и Ctls содержит последовательность согласно любой из SEQ ID NO 1, 3 или 5 или последовательность, которая на по меньшей мере 80% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 6 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 7 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 8 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 9 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 10 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 11 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 12 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 13 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 14 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 15 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 16 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 17 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 17 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 18 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 19 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 9 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 20 или последовательность, которая на по меньшей мере 60% идентична ей; или Ntls содержит последовательность согласно SEQ ID NO 21 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 22 или последовательность, которая на по меньшей мере 60% идентична ей.
Согласно таким частным вариантам осуществления, Ntls и Ctls каждая содержит GS линкерную последовательность; Ntls и Ctls каждая содержит PN линкерную последовательность; Ntls и Ctls каждая содержит аминокислотную последовательность, которая является частью каркаса человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, в частности аминокислотную последовательность, которая является частью каркаса домена fab человеческого антитела IgG или последовательность, которая на по меньшей мере 80% идентична ей, более конкретно Ntls содержит последовательность согласно любой из SEQ ID NO 1, 2 или 4 или последовательность, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4, и Ctls содержит последовательность согласно любой из SEQ ID NO 1, 3 или 5 или последовательность, которая на по меньшей мере 80% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 6 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 7 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 8 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 9 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 10 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 11 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 12 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 13 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 14 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 15 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 9 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 20 или последовательность, которая на по меньшей мере 60% идентична ей; или Ntls содержит последовательность согласно SEQ ID NO 21 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 22 или последовательность, которая на по меньшей мере 60% идентична ей.
Согласно таким частным вариантам осуществления, Ntls и Ctls каждая содержит GS линкерную последовательность; Ntls и Ctls каждая содержит PN линкерную последовательность; Ntls содержит последовательность согласно SEQ ID NO 2 или последовательность, которая на по меньшей мере 80% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 3 или последовательность, которая на по меньшей мере 80% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 4 или последовательность, которая на по меньшей мере 80% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 5 или последовательность, которая на по меньшей мере 80% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 11 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 12 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls содержит последовательность согласно SEQ ID NO 13 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 14 или последовательность, которая на по меньшей мере 60% идентична ей; Ntls и Ctls каждая содержит последовательность согласно SEQ ID NO 15 или последовательность, которая на по меньшей мере 60% идентична ей; или Ntls содержит последовательность согласно SEQ ID NO 9 или последовательность, которая на по меньшей мере 60% идентична ей, и Ctls содержит последовательность согласно SEQ ID NO 20 или последовательность, которая на по меньшей мере 60% идентична ей. Эти комбинации линкеров оказались особенно полезными для достижения высоких активностей натрийуретического пептида, хороших уровней экспрессии при рекомбинантной экспрессии и минимальной фрагментации белка или ее отсутствия, как показано в Таблице 9.
Согласно частным вариантам осуществления, Ntls дополнительно содержит якорный элемент A1 на ее С-терминальном конце, и/или Ctls дополнительно содержит якорный элемент A2 на ее N-терминальном конце, где A1 и A2 преимущественно содержат глициновый и сериновый остатки. Согласно частным вариантам осуществления, A1 и/или A2 содержат по меньшей мере 1, 2, 3, 4, или 5 аминокислотных остатков. A1 и/или A2 могут содержать до 10, 9, 8, 7, 6 или 5 аминокислотных остатков в общем. Согласно частным вариантам осуществления, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, или 100% аминокислотных остатков A1 и/или A2 выбраны из глициновых и сериновых остатков. В частности, A1 и/или A2 не содержит/содержат более 3, 2 или 1 аминокислотным остатков, отличных от глицина и серина
Согласно частным вариантам осуществления Ntls состоит из i) якорного элемента A1 на ее С-терминальном конце и ii) GS линкерной последовательности; PN линкерной последовательности; аминокислотной последовательности, которая является частью каркаса человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, в частности аминокислотной последовательности, которая является частью каркаса домена fab человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, более конкретно последовательности согласно любой из SEQ ID NO 1, 2 или 4, или последовательности, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 2 или 4; последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21; последовательности, которая на по меньшей мере 60% идентична последовательности согласно любой из SEQ ID NO 6, 7, 9, 11, 13, 15, 16, 17, 19 или 21; или любой их комбинацию.
Согласно частным вариантам осуществления, Ctls состоит из i) якорного элемента A2 на ее N-терминальном конце и ii) GS линкерной последовательности; PN линкерной последовательности; аминокислотной последовательности, которая является частью каркаса человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, в частности аминокислотной последовательности, которая является частью каркаса домена fab человеческого антитела IgG, или последовательности, которая на по меньшей мере 80% идентична ей, более конкретно последовательности согласно любой из SEQ ID NO 1, 3 или 5; последовательности, которая на по меньшей мере 80% идентична последовательности согласно любой из SEQ ID NO 1, 3 или 5; последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22; последовательности, которая на по меньшей мере 60% идентична последовательности согласно любой из SEQ ID NO 6, 8, 10, 12, 14, 15, 17, 18, 19, 20 или 22; или любой их комбинацию.
Согласно частным вариантам осуществления, Ntls и/или Ctls содержат (содержит) по меньшей мере 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных остатков в общем. Ntls и/или Ctls могут, например, содержать до 30, 28, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11 или 10 аминокислотных остатков в общем.
Согласно частным вариантам осуществления, аминокислотное удлинение, присутствующее между
i) аминокислотным остатком HC res25 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res51 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res92 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res26 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res49 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res88 по Кэботу и первым аминокислотным остатком натрийуретического пептида в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3
содержит последовательность согласно любой из SEQ ID NO 26 - 38 или последовательность, которая на по меньшей мере 80%, 85%, 90%, 95% или по меньшей мере 98% идентична последовательности согласно любой из SEQ ID NO 26 - 38.
Согласно частным вариантам осуществления, аминокислотное удлинение, присутствующее между последним аминокислотным остатком натрийуретического пептида и
i) аминокислотным остатком HC res35a по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res106 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res 32 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res98 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3
содержит последовательность согласно любой из SEQ ID NO 39 - 51 или последовательность, которая на по меньшей мере 80%, 85%, 90%, 95% или по меньшей мере 98% идентична последовательности согласно любой из SEQ ID NO 39 - 51.
Согласно частным вариантам осуществления, гетерологичная аминокислотная последовательность состоит из Ntls, натрийуретического пептида и Ctls.
Согласно частным вариантам осуществления, аминокислотное удлинение, присутствующее между
i) аминокислотным остатком HC res25 по Кэботу и аминокислотным остатком HC res35a по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH1;
ii) аминокислотным остатком HC res51 по Кэботу и аминокислотным остатком HC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH2;
iii) аминокислотным остатком HC res92 по Кэботу и аминокислотным остатком HC res106 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRH3;
iv) аминокислотным остатком LC res26 по Кэботу и аминокислотным остатком LC res 32 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL1;
v) аминокислотным остатком LC res49 по Кэботу и аминокислотным остатком LC res57 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL2; и/или
vi) аминокислотным остатком LC res88 по Кэботу and аминокислотным остатком LC res98 по Кэботу в случае включения указанной гетерологичной аминокислотной последовательности в CDRL3
содержит последовательность согласно любой из SEQ ID NO 52 - 64, или последовательность, которая на по меньшей мере 80%, 85%, 90%, 95% или по меньшей мере 98% идентична последовательности согласно любой из SEQ ID NO 52 - 64.
Согласно частным вариантам осуществления, антитело или его фрагмент содержит по меньшей мере два натрийуретических пептида. Согласно частным вариантам осуществления, оба натрийуретических пептида содержатся в гетерологичной аминокислотной последовательности, дополнительно содержащей Ntls и Ctls, и включены в CDR участок указанного антитела или его фрагмента, как описано в настоящем документе. По меньшей мере два натрийуретических пептида могут быть включены в два соответствующих участка CDR двух легких цепей или двух тяжелых цепей, или по меньшей мере два натрийуретических пептида могут быть включены в два отдельных участка CDR. По меньшей мере два натрийуретических пептида могут быть одинаковы или различными. Согласно таким частным вариантам осуществления, антитело или его фрагмент содержит по меньшей мере два различных натрийуретических пептида, которые включены в по меньшей мере два CDR участка.
Из-за димерной структуры молекул антител включение одной последовательности нуклеиновой кислоты, кодирующей гетерологичную аминокислотную последовательность (Ntls-натрийуретический пептид-Ctls), в нуклеиновую кислоту, кодирующую легкую или тяжелую цепь молекулы иммуноглобулина, как правило, дает белок антитела, несущий два натрийуретических пептида, расположенных в соответствующих участках CDR двух идентичных легких или двух идентичных тяжелых цепей. Однако также предусматривается вставка двух нуклеиновых кислот, кодирующих натрийуретический пептид, в два разных CDR кодирующих участка последовательности нуклеиновой кислоты, кодирующих легкую и/или тяжелую цепь, таким образом получая молекулу антитела с четырьмя натрийуретическими пептидами, расположенными в двух соответствующих парах CDR димерного антитела. Также охватываются димерные молекулы иммуноглобулинов, легкие цепи и/или тяжелые цепи которых не идентичны, например, включая димерные антитела, несущие один натрийуретический пептид, а также димерные антитела, несущие два разных натрийуретических пептида в двух соответствующих участках CDR двух легких или двух тяжелые цепей.
Согласно частным вариантам осуществления, натрийуретические пептиды вставлены в CDRH1 и CDRH2, CDRH1 и CDRH3, CDRH2 и CDRH3, CDRH1 и CDRL1, CDRH1 и CDRL2, CDRH1 и CDRL3, CDRH2 и CDRL1, или CDRH2 и CDRL2. Согласно частным вариантам осуществления, антитело или его фрагмент содержит одну ANP и одну BNP молекулу; одну ANP и одну CNP молекулу; или одну BNP и одну CNP молекулу.
Согласно частным вариантам осуществления, натрийуретический пептид, содержащийся в по меньшей мере одной гетерологичной аминокислотной последовательности, выключенной в по меньшей мере один участок CDR указанного антитела или его фрагмента, представляет собой ANP, и антитело или его фрагмент содержит по меньшей мере один дополнительный натрийуретический пептид. Согласно частным вариантам осуществления, по меньшей мере один дополнительный натрийуретический пептид также содержится в гетерологичной аминокислотной последовательности, дополнительно содержащей Ntls и Ctls и включенной в участок CDR указанного антитела или его фрагмента. Согласно частным вариантам осуществления, ANP и по меньшей мере один дополнительный натрийуретический пептид включены в два соответствующих участка CDR либо двух легких, либо двух тяжелых цепей антитела или его фрагмента. Согласно другим частным вариантам осуществления, ANP и по меньшей мере один дополнительный натрийуретический пептид включены в по меньшей два отдельных участка CDR. В частности, указанный по меньшей мере один дополнительный натрийуретический пептид выбран из ANP, BNP и CNP, более конкретно из BNP и CNP.
«Пустая» молекула антитела, не несущая гетерологичной аминокислотной последовательности, содержащей натрийуретический пептид, которая состоит из двух тяжелых цепей, имеющих последовательность согласно SEQ ID NO 65, и двух легких цепей, имеющих последовательность согласно SEQ ID NO 66, называется TPP-5657. Согласно частным вариантам осуществления молекула антитела, состоящая из двух тяжелых цепей, имеющих последовательность согласно SEQ ID NO 65, или последовательность, имеющую по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичность последовательности с ними. и две легкие цепи, имеющие последовательность согласно SEQ ID NO 66, или последовательность, имеющую по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичности последовательности с ними, служит в качестве исходного или родительского антитела, в которое включают гетерологичную аминокислотную последовательность, включающую натрийуретический пептид. Согласно таким частным вариантам осуществления гетерологичная аминокислотная последовательность, содержащая натрийуретический пептид включена в CDR участок одной или обеих тяжелых цепей такой молекулы антитела.
Согласно таким частным вариантам осуществления, тяжелая цепь (цепи), содержащая (содержащие) по меньшей мере одну гетерологичную аминокислотную последовательность, включенную в по меньшей мере один из ее CDR участков, имеет последовательность согласно любой из SEQ ID NO 67 - 79, или последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 67 - 79. Согласно частным вариантам осуществления, антитело согласно настоящему изобретению состоит из двух идентичных тяжелых цепей, имеющих последовательность согласно любой из SEQ ID NO 67 - 79, или последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 67 - 79, и две идентичные легкие цепи, имеющие последовательность согласно SEQ ID NO 66, или последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентична ей.
Согласно другим частным вариантам осуществления, гетерологичная аминокислотная последовательность, содержащая натрийуретический пептид, включена в CDR участок одной или обеих легких цепей такой молекулы антитела. Согласно таким частным вариантам осуществления, легкая цепь (цепи), содержащая (содержащие) по меньшей мере одну гетерологичную аминокислотную последовательность, включенную в по меньшей мере один из ее CDR участков, имеет (имеют) последовательность согласно любой из SEQ ID NO 80 или 81, последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 80 или 81. Согласно частным вариантам осуществления, антитело согласно настоящему изобретению состоит из двух идентичных легких цепей, имеющих последовательность согласно любой из SEQ ID NO 80 или 81, или последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентична последовательности согласно любой из SEQ ID NO 80 или 81, и две идентичные тяжелые цепи, имеющие последовательность согласно SEQ ID NO 65, или последовательность, которая на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичную им.
В таблице ниже показан состав тяжелой и легкой цепей примерных антител согласно настоящему изобретению.
Таблица 1: Примерные конструкции антитела с привитым натрийуретическим пептидом
Антитела согласно настоящему изобретению или их фрагменты включают природные очищенные продукты, продукты процедур химического синтеза и продукты, полученные с помощью рекомбинантных методов. В зависимости от происхождения антитело или его фрагмент согласно настоящему изобретению может быть гликозилированным или негликозилированным.
Например, стандартные методики рекомбинантной ДНК можно использовать для приготовления и/или получения нуклеиновых кислот, кодирующих тяжелую и легкую цепи, включения этих нуклеиновых кислот в экспрессионные векторы и введения векторов в клетки-хозяева для рекомбинантной экспрессии (см., например, Sambrook, Fritsch and Maniatis (eds.), Molecular Cloning; A Laboratory Manual, Second Edition, Cold Spring Harbor, N.Y., (1989); Ausubel, F. M. et al. (eds.) Current Protocols in Molecular Biology, Greene Publishing Associates, (1989); Goeddel, Gene Expression Technology, Methods in Enzymology 185, Academic Press, San Diego, Calif. (1990); and US 4,816,397 by Boss et al.).
Таким образом, согласно второму аспекту настоящее изобретение относится к нуклеиновой кислоте или смеси нуклеиновых кислот, кодирующей антитело или его фрагмент согласно настоящему изобретению. Эти последовательности нуклеиновых кислот могут быть оптимизированы в некоторых случаях для экспрессии в млекопитающих. Молекулы ДНК согласно настоящему изобретению не ограничиваются последовательностями, раскрытыми в данном документе, но также включают их варианты.
Настоящее изобретение дополнительно обеспечивает конструкции рекомбинантных нуклеиновых кислот, содержащие одну или несколько последовательность нуклеиновой кислоты согласно настоящему изобретению. Конструкция рекомбинантной нуклеиновой кислоты согласно настоящему изобретению может, например, содержать вектор нуклеиновой кислоты, такой как плазмида, в который была вставлена молекула нуклеиновой кислоты, кодирующая антитело или его фрагмент согласно настоящему изобретению. Понятно, что на дизайн вектора экспрессии, включая выбор регуляторных последовательностей, влияют такие факторы, как выбор клетки-хозяина, желаемый уровень экспрессии белка и то, желательна ли конститутивная или индуцибельная экспрессия.
Полезные экспрессионные векторы для использования в бактериях конструируются путем вставки одной или нескольких последовательностей нуклеиновой кислоты согласно настоящему изобретению вместе с подходящими сигналами инициирования трансляции и терминации в функционирующую рамку считывания с функциональным промотором. Бактериальные экспрессионные векторы, как правило, содержат один или несколько фенотипически селектируемых маркеров и сайт инициации репликации, чтобы гарантировать поддержания вектора и, если требуется, обеспечить амплификацию в бактериальном хозяине. Бактериальные экспрессионные векторы могут содержать элементы, полученные из коммерчески доступных плазмид, как например, хорошо известный клонирующий вектор pBR322 (ATCC 37017). Ряд бактериальных экспрессионных векторов может быть успешно выбран в зависимости от предполагаемого использования экспрессируемого антитела или его фрагмента. Например, если желательно большое количество такого антитела, могут быть желательны векторы, опосредующие высокий уровень экспрессии слитых белков антител, которые легко очищаются.
Конструкции рекомбинантных нуклеиновых кислот, предназначенные для экспрессии антител в эукариотической клетке-хозяине, могут содержать регуляторные последовательности, которые способны контролировать экспрессию открытой рамки считывания в эукариотической клетке, предпочтительно промотор и сигнал полиаденилирования. Промоторы и сигналы полиаденилирования предпочтительно выбираются так, чтобы они функционировали в пределах определенного типа клеток, предназначенных для экспрессии антител. Примеры подходящих промоторов включают, но не ограничиваются ими, промоторы цитомегаловируса (CMV), такие как сильный немедленно-ранний промотор CMV, вируса обезьян 40 (SV40), вируса опухоли молочной железы мыши (MMTV), вируса иммунодефицита человека (ВИЧ), как например промотор длинных концевых повторов ВИЧ (LTR), вируса Молони, вируса Эпштейна-Барра (EBV), аденовируса (например, главный поздний промотор аденовируса (AdMLP)), полиомы и вируса саркомы Рауса (RSV), синтетический промотор CAG состоящий из элемента раннего энхансера CMV, промотор, первый экзон и первый интрон гена бета-актина курицы и акцептор сплайсинга гена бета-глобина кролика, а также промоторы из генов млекопитающих, таких как актин, миозин, гемоглобин, мышечный креатин и металлотионеин. Согласно конкретному варианту осуществления кассета эукариотической экспрессии содержит промотор CMV. В контексте настоящего изобретения термин «промотор CMV» относится к сильному немедленно-раннему промотору цитомегаловируса.
Примеры подходящих сигналов полиаденилирования включают, но не ограничиваются ими, сайт полиаденилирования бычьего гормона роста (BGH), сигналы полиаденилирования SV40 и сигналы полиаденилирования LTR.
Кроме того, рекомбинантная последовательность нуклеиновой кислоты может содержать одну или несколько энхансерных последовательностей. Энхансер может быть, например, энхансером актина, миозина, гемоглобина, мышечного креатина или вирусным энхансером млекопитающих, например, энхансер из CMV, RSV, SV40 или EBV. Для дальнейшего описания вирусных регуляторных элементов и их последовательностей, см., например, US 5,168,062 от Stinski, US 4,510,245 от Bell et al. и US 4,968,615 от Schaffner et al.
Регуляторные последовательности и кодоны, как правило, зависят от вида, поэтому для максимального увеличения продукции белка регуляторные последовательности и кодоны предпочтительно выбирают так, чтобы они были эффективными для видов /типов клеток, предназначенных для экспрессии антител. Специалист в данной области техники может получить молекулы рекомбинантной ДНК, которые являются функциональными у данного вида субъектов.
Рекомбинантные экспрессионные векторы млекопитающих могут также включать точки начала репликации и селектируемые маркеры (см., например, US 4,399,216, US 4,634,665 и US 5,179,017). Подходящие селективные маркеры включают гены, которые придают устойчивость к лекарственным средствам, как например G418, пуромицин, гигромицин, бластицидин, цеоцин/блеомицин или метотрексат, или селективный маркер, которые используют ауксотрофии, как например глютаминсинтетаза, на клетке-хозяине, в которую был введен вектор. Например, ген дигидрофолатредуктазы (DHFR) придает устойчивость к метотрексату, ген neo обеспечивает устойчивость к G418, ген bsd из Aspergillus terreus придает устойчивость к бластидину, пуромицин-N-ацетилтрансферазу придает устойчивость к пуромицину, продукт гена Sh ble придает устойчивость к цеоцину, а устойчивость к гигромицину обеспечивается геном устойчивости к гигромицину E.coli (hyg или hph). Селектируемые маркеры, такие как DHFR или глютаминсинтетаза, также полезны для методов амплификации в сочетании с MTX и MSX.
Согласно некоторым вариантам осуществления последовательности нуклеиновой кислоты, кодирующие тяжелые и легкие цепи, вставлены в отдельные векторы. Согласно другим вариантам осуществления последовательности нуклеиновой кислоты, кодирующие тяжелые и легкие цепи, вставлены в один и тот же вектор. Кроме того, последовательности нуклеиновой кислоты, кодирующие вариабельные домены тяжелых и/или легких цепей, могут быть превращены, например, в полинуклеотидные последовательности, кодирующие полноразмерные цепи антитела, Fab фрагменты или scFv. Фрагмент ДНК, кодирующий VL- или VH может быть функционально связан, (таким образом, что аминокислотные последовательности, закодированные двумя фрагментами ДНК, оказались в одной рамке считывания) к другому фрагменту ДНК, кодирующему, например, константный домен антитела или гибкий линкер. В качестве примера, чтобы создать полинуклеотидную последовательность, которая кодирует scFv, нуклеиновые кислоты, кодирующие VH и VL, могут быть функционально связаны с другим фрагментом, кодирующим гибкий линкер, таким образом, чтобы последовательности VH и VL могли бы быть экспрессированы как белок с непрерывной единственной цепью с областями VL и VH, соединенными гибким линкером (см., например, Bird et al. (1988) Science 242:423-426; Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883; McCafferty et al, Nature (1990) 348:552-554). Последовательности человеческих константных доменов тяжелой цепи и легкой цепи известны специалистам в данной области техники (см., например, Kabat, E. A., el al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242) и фрагменты ДНК, охватывающие эти области, могут быть получены стандартной амплификацией с помощью ПЦР.
Согласно частным вариантам осуществления, последовательности нуклеиновой кислоты, кодирующие тяжелую цепь, в которую гетерологичная аминокислотная последовательность, содержащая натрийуретический пептид, включена содержат последовательность согласно любой из SEQ ID NO 82 или 83 или последовательность, на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичную последовательности согласно любой из SEQ ID NO 82 или 83. Согласно таким частным вариантам осуществления, последовательность нуклеиновой кислоты, кодирующая легкую цепь, содержит последовательность согласно SEQ ID NO 84 или последовательность на по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% идентичную ей.
Согласно третьему аспекту настоящее изобретение относится к клетке-хозяину, содержащей нуклеиновую кислоту или смесь нуклеиновых кислот согласно настоящему изобретению. В контексте настоящего изобретения термины «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» используются взаимозаменяемо и относятся к клеткам, в которые была введена экзогенная нуклеиновая кислота, включая потомство таких клеток. К клеткам-хозяевам относятся «трансформанты», «трансформированные клетки», «трансфектанты», «трансфицированные клетки» и «трансдуцированные клетки», которые включают первично трансформированную/трансфицированную/трансдуцированную клетку и потомство, полученное из нее, независимо от количества пассажей. Потомство не может быть полностью идентичным по содержанию нуклеиновой кислоты в родительской клетке, и содержащаяся экзогенная нуклеиновая кислота может содержать мутации. В настоящую заявку включено мутантное потомство, которое имеет ту же функцию или биологическую активность, что и скринированные или отобранные в первоначально трансформированной клетке.
Трансфекцию экспрессирующего вектора в клетку-хозяина можно проводить с использованием стандартных методов, таких как электропорация, нуклеофекция, кальций-фосфатная преципитация, липофекция, трансфекция на основе поликатиона, такая как трансфекция на основе поликатиона, такая как трансфекция на основе полиэтиленимина (PEI) и трансфекция DEAE-декстраном.
Подходящие клетки-хозяева включают прокариотические и эукариотические клетки. Примерами прокариотических клеток-хозяев являются бактерии и включают, без ограничения, Escherichia coli, Bacillus subtilis, Salmonella typhimurium и различные виды в пределах родов Pseudomonas, Streptomyces и Staphylococcus.
Неограничивающие примеры эукариотических клеток-хозяев включают дрожжи, насекомые и клетки насекомых, растения и растительные клетки, трансгенных животных и клетки млекопитающих. Подходящие клетки-хозяева млекопитающих для экспрессии антител включают яичник китайского хомячка (CHO клетки), такие как CHO-K1, CHO-S, CHO-K1SV [включая dhfr- CHO клетки, описанные в Urlaub and Chasin, (1980) Proc. Natl. Acad. Sci. USA 77:4216-4220 и Urlaub et al., Cell. 1983 Jun;33(2):405-12, с применением DHFR селектируемого маркера, например, как описано в R. J. Kaufman and P. A. Sharp (1982) Mol. Biol. 159:601-621; и другие нокаутные клетки, примеры которых приведены в Fan et al., Biotechnol Bioeng. 2012 Apr;109(4):1007-15], NS0 миеломные клетки, COS клетки, HEK293 клетки, HKB11 клетки, BHK21 клетки, CAP клетки, EB66 клетки, и SP2 клетки.
Экспрессия также может быть временной или полустабильной в экспрессионных системах экспрессии, таких как клетки HEK293, HEK293T, HEK293-EBNA, HEK293E, HEK293-6E, HEK293-Freestyle, HKB11, Expi293F, 293EBNALT75, CHO Freestyle, CHO-S, CHO-K1, CHO-K1SV, CHOEBNALT85, CHOS-XE, CHO-3E7 или CAP-T (например, Durocher et al., Nucleic Acids Res. 2002 Jan 15;30(2):E9).
Согласно четвертому аспекту настоящее изобретение относится к способу получения антитела или его фрагмента, включающему культивирование клетки-хозяина согласно настоящему изобретению. В частности, клетку-хозяин согласно настоящему изобретению культивируют в условиях, подходящих для экспрессии антитела или его фрагмента.
Экспрессия антител может быть конститутивной или регулируемой (например, индуцибельной). Для индуцибельной экспрессии антител клетку-хозяин согласно настоящему изобретению обычно выращивают до подходящей плотности клеток с последующей дерепрессией/индукцией выбранного промотора подходящими способами (например, температурным сдвигом или химической индукцией, такой как добавление или удаление низкомолекулярных индукторов, таких как тетрациклин в сочетании с системой Tet), и культивированием клетки-хозяина в течение дополнительного периода.
Согласно частным вариантам осуществления способ получения антитела или его фрагмента согласно настоящему изобретению дополнительно включает стадию выделения антитела или его фрагмента из культуры клеток-хозяев. Клетки можно, например, собирать центрифугированием, разрушать физическими или химическими средствами, а антитело или его фрагмент можно дополнительно очищать из полученного неочищенного экстракта. Согласно некоторым вариантам осуществления экспрессионный вектор сконструирован таким образом, что экспрессируемое антитело или его фрагмент секретируется в культуральную среду, в которой выращиваются клетки-хозяева. В этом случае антитело или его фрагмент можно непосредственно выделить из культуральной среды с использованием стандартных методов очистки белка.
Согласно частным вариантам осуществления способ согласно настоящему изобретению дополнительно включает стадию очистки выделенного антитела или его фрагмента. В частности, антитело очищают (1) до более чем 90%, как определено, например, с помощью аналитической хроматографии или SDS-капиллярного гель-электрофореза(например, на приборе Caliper LabChip GXII, GX 90 или Biorad Bioanalyzer) и, более конкретно, очистка дает гомогенность антител по меньшей мере около 92,5%, 95%, 98% или 99%; альтернативно, антитело очищают (2) до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности, или (3) до гомогенности с помощью SDS-PAGE в восстанавливающих или невосстанавливающих условиях с использованием кумасси синего или, желательно, серебряного красителя.
Антитела или их фрагменты согласно настоящему изобретению могут быть выделены и очищены из рекомбинантных клеточных культур известными методами включающими, но не ограниченные этим: осаждением сульфатом аммония или этанолом, экстракцией кислотой, хроматография с использованием белка А, хроматография с использованием белка G, эксклюзионная хроматография по размеру, анионная или катионная ионообменная хроматография, хроматография на фосфоцеллюлозе, гидрофобная хроматография, аффинная хроматография, хроматография на гидроксиапатите и хроматография с использованием белка лектина. Высокоэффективная жидкостная хроматография ("ВЭЖХ") может также использоваться для очистки (см., например, Colligan, Current Protocols in Immunology или Current Protocols in Protein Science, John Wiley & Sons, NY, N.Y., (1997-2001), например, Chapters 1, 4, 6, 8, 9, 10).
согласно пятому аспекту настоящее изобретение относится к композиции, содержащей антитело или его фрагмент согласно настоящему изобретению. В частности, композиция согласно настоящему изобретению представляет собой фармацевтическую композицию, подходящую для применения в способе лечения, где антитело или его фрагмент согласно настоящему изобретению содержится в количестве, эффективном для достижения намеченной цели, то есть предотвращения или лечения определенного болезненного состояния.
Композиция необязательно дополнительно содержит по меньшей мере один фармацевтически приемлемое вспомогательное вещество. В контексте настоящего изобретения термин «вспомогательное вещество» относится к природному или синтетическому веществу, составленному вместе с активным ингредиентом в лекарственное средство. Подходящие вспомогательные вещества включают антиадгезивные вещества, связующие, покрытия, дезинтегрирующие вещества, ароматизаторы, красители, смазывающие вещества, глиданты, сорбенты, консерванты и подсластители. Конкретные примеры фармацевтически приемлемых вспомогательных веществ включают, но не ограничиваются ими, физиологический раствор, забуференный физиологический раствор, декстрозу и воду. В контексте настоящего изобретения термин «фармацевтически приемлемый» относится к молекулярным компонентам и другим ингредиентам фармацевтических композиций, которые являются физиологически переносимыми и обычно не вызывают нежелательных реакций при введении млекопитающему (например, человеку). Термин «фармацевтически приемлемый» также может означать одобренный регулирующим органом федерального правительства или правительства штата или перечисленный в Фармакопее США или другой общепризнанной фармакопее для использования у млекопитающих и, более конкретно, у людей.
Композиция согласно настоящему изобретению может дополнительно содержать один или несколько дополнительных терапевтически активных агентов.
Фармацевтическая композиция может быть в форме раствора, суспензии, капсулы с энтеросолюбильным покрытием, лиофилизированного порошка или любой другой формы, подходящей для предполагаемого использования.
Фармацевтические композиции для перорального введения могут быть составлены с использованием фармацевтически приемлемых вспомогательных веществ, известных специалистам в данной области техники, в дозировках, подходящих для перорального введения. Такие вспомогательные вещества позволяют фармацевтическим композициям быть сформулированными в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, паст, суспензий и т.п., для проглатывания пациентом.
Фармацевтические препараты для перорального использования могут быть получены путем комбинирования активных соединений с твердым вспомогательным веществом, при необходимости размалывая (гранулируя) получающуюся смесь, и перерабатывая смесь гранул после добавления подходящих вспомогательных средств при необходимости, чтобы получить таблетки или ядро драже. Подходящими вспомогательными веществами являются углеводные или белковые наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; крахмал из кукурузы, пшеницы, риса, картофеля или других растений; целлюлозы, такие как метил целлюлоза, гидроксипропилметилцеллюлоза, или натрий карбоксиметилцеллюлоза; и камеди, включая гуммиарабик и трагакантовую камедь; и белки, такие как желатин и коллаген. При необходимости могут быть добавлены вещества для улучшения распадаемости таблеток или солюбилизирующие агенты, такие как поперечно сшитый поливинилпирролидон, агар, альгиновая кислота или ее соль, такая как альгинат натрия.
Ядра драже снабжаются подходящими покрытия, такими как концентрированные растворы сахаров, которые могут также содержать гуммиарабик, тальк, поливинилпирролидон, гель карбопола, полиэтиленгликоль и/или диоксид титана, глазировочные растворы, и подходящие органические растворители или смеси растворителей. Красители или пигменты могут быть добавлены к таблеткам или покрытиям драже для идентификации продукта или характеризации количества активного соединения, то есть дозировку.
Фармацевтические препараты, которые могут использоваться перорально, включают твердые капсулы, приготовленные из желатина, так же как мягкие, герметические капсулы, приготовленные из желатина и покрытия такого как глицерин или сорбит.Твердые капсулы могут содержать активные ингредиенты, смешанные с наполнителем или связующими веществами, такими как лактоза или крахмалы, лубрикантами, такими как тальк или стеарат магния, и при необходимости, стабилизаторами. В мягких капсулах активные соединения могут быть растворены или диспергированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкий полиэтиленгликоль с или без стабилизаторов.
Фармацевтические композиции для парентерального введения включают водные растворы терапевтически активных агентов. Для инъекции фармацевтические композиции в соответствии с настоящим изобретением могут быть составлены в водных растворах, предпочтительно в физиологически совместимых буферах, таких как раствор Хэнка, раствор Рингера или забуференный физиологический раствор. Водные инъекционные суспензии могут содержать вещества, которые увеличивают вязкость суспензий, такие как карбоксиметилцеллюлоза натрия, сорбит или декстран. Дополнительно, суспензии активного агента могут быть получены в виде соответствующих масляных инъекционных суспензий. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло или синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды или липосомы. При необходимости, суспензии могут также содержать подходящие стабилизирующие агенты или агенты, которые повышают растворимость терапевтически активного агента, что позволяет получить препарат высококонцентрированных растворов.
Для местного или назального введения используются в композиции пенетранты, соответствующие конкретному барьеру, через который должен быть пройден. Такие пенетранты известны специалистам в данной области техники.
Фармацевтические композиции в соответствии с настоящим изобретением могут производиться способом, который известен специалистам в данной области техники, например, посредством обычного смешивания, растворения, гранулирования, создания драже, отмачивания, эмульгирования, заключения в капсулу, включения или процессов лиофилизации.
Фармацевтическая композиция может обеспечиваться в виде соли и может быть сформирована с кислотами, включая, но не ограничиваясь этим: хлористоводородную, серную, уксусную, молочную, винную, яблочную, янтарную и т.д. Соли имеют тенденцию быть более растворимыми в водных или других протонных растворителях, которые являются соответствующими формами свободного основания. В других случаях предпочтительными препаратами могут быть лиофилизованные порошки в 1 мМ - 50 мМ гистидина, 0,1%-2% сахарозы, 2%-7% маннита в интервале рН от 4,5 до 7,5, которые объединяются с буфером пред использованием.
Дополнительные сведения о методах составления и введения можно найти в последнем выпуске Remington's Pharmaceutical Sciences (Ed. Maack Publishing Co, Easton, Pa.).
После приготовления фармацевтической композиции, содержащей антитело или его фрагмент согласно настоящему изобретению, она может быть помещена в соответствующий контейнер и помечена для лечения указанного состояния. Для введения антитела или его фрагмента согласно настоящему изобретению такая маркировка будет включать количество, частоту и способ введения.
Настоящее изобретение также относится к фармацевтическим упаковкам и наборам, содержащим один или несколько контейнеров, заполненных одним или несколькими ингредиентами вышеупомянутых композиций согласно настоящему изобретению. С таким контейнером (контейнерами) может быть связано уведомление в форме, предписанной государственным агентством, регулирующим производство, использование или продажу фармацевтических или биологических продуктов, отражающее одобрение агентством производства, использования или продажи продукта для введения человеку.
Согласно шестому аспекту настоящее изобретение относится к антителу или его фрагменту согласно настоящему изобретению или композиции согласно настоящему изобретению для применения в способе лечения.
В частности, такой способ лечения включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества антитела или его фрагмента согласно настоящему изобретению. Субъект может быть человеком или животным, не являющимся человеком (например, кроликом, крысой, мышью, собакой, обезьяной или другим приматом более низкого порядка).
В контексте настоящего изобретения термин «терапевтически эффективное количество» определяется как количество антитела или его фрагмента в соответствии с настоящим изобретением, которое достаточно для предотвращения или облегчения симптомов любого из расстройств и заболеваний, упомянутых в настоящем документе - либо в виде разовой дозы, либо в соответствии с режимом множественного приема, отдельно или в комбинации с другими агентами. Согласно частным вариантам осуществления, указанное «терапевтически эффективное количество» токсикологически переносимо. Определение эффективной дозы находится в пределах компетенции специалистов в данной области техники. Терапевтически эффективное количество терапевтического агента обычно в значительной степени зависит от конкретных характеристик пациента, таких как возраст, вес, пол и болезненное состояние, время, частота и способ введения, комбинация (комбинации) лекарственных средств и природа заболевания, которое лечат.Обычные дозировки антител варьируются от 0,1 до 100000 микрограммов, вплоть до общей дозы около 10 г, в зависимости от пути введения.
Общее руководство для его определения может быть найдено, например, в публикациях Международной конференции по вопросам гармонизации (International Conference on Harmonization) и в REMINGTON'S PHARMACEUTICAL SCIENCES, chapters 27 and 28, pp.484-528 (18th ed., Alfonso R. Gennaro, Ed., Easton, Pa.: Mack Pub. Co., 1990). Более тщательное определение терапевтически эффективного количества будет зависеть от таких факторов как токсичность и эффективность лекарства, которая может быть определена с использованием способов, известных специалистам в данной области техники и, которые можно найти в вышеупомянутых ссылках.
Вкратце, терапевтическая эффективность и токсичность терапевтических агентов могут быть определены в анализах клеточных культур или на животных моделях, например, как ED50 (доза, терапевтически эффективная для 50% населения) и LD50 (доза, летальная для 50% популяции), соответственно. Соотношение доз ED50 и LD50 является терапевтическим индексом.
Антитело или его фрагмент согласно настоящему изобретению подходит для лечения и/или профилактики сердечно-сосудистых, почечных, легочных, скелетных, глазных, тромбоэмболических и фиброзных заболеваний и нарушений, карликовости, ахондроплазии, а также других нарушений, связанных с cGMP и/или натрийуретическим пептидом. Таким образом, согласно частному варианту осуществления, антитело или его фрагмент предназначен для использования для лечения и/или профилактики любого из этих расстройств и заболеваний или любой их комбинации.
Антитело или его фрагмент согласно настоящему изобретению поэтому могут применяться в качестве лекарственных средств для лечения и/или профилактики сердечно-сосудистых заболеваний, например, артериальной и легочной гипертензии, резистентной и рефрактерной гипертензии, острой и хронической сердечной недостаточности, ишемической болезни сердца, синдрома облитерирующего бронхиолита (BOS), опухолевых и онкологических заболеваний, реакции трансплантат против хозяина, серповидно-клеточной анемии, стабильной и нестабильной стенокардии, периферических и сердечных сосудистых заболеваний, аритмии, нарушений ритма предсердий и желудочков, а также нарушений проводимости таких как, например, атриовентрикулярная блокада степени I-III (AB блок I-III), суправентрикулярной тахиаритмии, мерцательной аритмии, трепетания предсердий, фибрилляции желудочков, трепетания желудочков, вентрикулярной тахиаритмии, пируэтной тахикардии, экстрасистолы предсердий и желудочков, преждевременной деполяризации, исходящей из АВ соединения, синдрома слабости синусового узла, обморока, атриовентрикулярной узловой реципрокной тахикардии, синдрома Вольфа-Паркинсона-Уайта, острого коронарного синдрома (ACS), аутоиммунного заболевания сердца (перикардит, эндокардит, вальвулит, аортит, кардиомиопатии), шока, такого как шок кардиологического типа, септический шок и анафилактический шок, аневризмы, кардиомиопатии боксеров (преждевременное желудочковое сокращение (PVC)), кроме того, для лечения и/или профилактики тромбоэмболических заболеваний и ишемий, таких как миокардиальная ишемия, инфаркт миокарда, инсульт, гипертрофия сердца, транзисторные и ишемические атаки, преэклампсия, воспалительные сердечно-сосудистые заболевания, спазмы коронарных артерий и периферических артерий, образования отеков, таких как, например, отек легких, отек мозга, почечный отек или отек из-за сердечной недостаточности, нарушения периферического кровообращения, реперфузионные повреждения, артериальные и венозные тромбозы, микроальбуминурия, слабость сердечной мышцы, эндотелиальная дисфункция, микро- и макрососудистые повреждения (васкулит), а также для предотвращения рестенозов, например, после тромболитической терапии, чрескожно-транслюминальной ангиопластики (PTA), чрескожно-транслюминальной коронарной ангиопластики (PTCA), трансплантаций сердца и операций по шунтированию, а также микро- и макрососудистых повреждений (васкулит), повышенных уровней фибриногена и липопротеинов низкой плотности (LDL) и повышенных концентраций ингибитора активатора плазминогена 1 (PAI-1), а также для лечения и/или профилактики эректильной дисфункции и женской сексуальной дисфункции.
В контексте настоящего изобретения термин «сердечная недостаточность» включает в себя как острые, так и хронические формы проявления сердечной недостаточности, также как и специфические или родственные нозологические формы этого, такие как острая декомпенсированная сердечная недостаточность, недостаточность правых отделов сердца, недостаточность левых отделов сердца, глобальная сердечная недостаточность, ишемическая кардиомиопатия, дилатационная кардиомиопатия, гипертрофическая кардиомиопатия, идиопатическая кардиомиопатия, врожденный порок сердца, порок клапанов сердца, сердечная недостаточность при пороках клапанов сердца, стеноз митрального клапана, недостаточность митрального клапана, стеноз аортального клапана, недостаточность клапана аорты, трикуспидальный стеноз, недостаточность трехстворчатого клапана, стеноз клапана легочной артерии, недостаточность клапана легочной артерии, комбинированные пороки клапанов сердца, воспаление сердечной мышцы (миокардит), хронический миокардит, острый миокардит, вирусный миокардит, сердечная недостаточность, вызванная диабетом, токсическая алкогольная кардиомиопатия, кардиальные болезни накопления, а также диастолическая и систолическая сердечная недостаточность, сердечная недостаточность со сниженной фракцией выброса (HFrEF), сердечная недостаточность с сохраненной фракцией выброса (HFpEF) и острые фазы обострения существующей хронической сердечной недостаточности (обострение сердечной недостаточности).
Кроме того, антитело или его фрагмент согласно настоящему изобретению также можно использовать для лечения и/или профилактики артериосклероза, заболевания периферических артерий (PAD), нарушения липидного обмена, гиполипопротеинемии, дислипидемии, гипертриглицеридемии, гиперлипидемии, гиперхолестеринемии, абеталипопротеинемии, ситостеролемии, ксантоматоза, болезни Танжера, ожирения, тучности и комбинированной гиперлипидемии и метаболического синдрома.
Антитело или его фрагмент согласно настоящему изобретению дополнительно могут применяться для лечения и/или профилактики первичного и вторичного феномена Рейно, нарушений микроциркуляции, перемежающейся хромоты, периферических и автономных нейропатий, диабетических микроангиопатий, диабетической ретинопатии, диабетических язв на конечностях, гангрены, CREST-синдрома, эритематоза, оникомикоза, а также ревматических заболеваний, и для заживления ран.
Антитело или его фрагмент согласно настоящему изобретению также подходят для лечения и/или профилактики заболеваний мочеполовой системы, таких как, например, синдрома аденомы предстательной железы (BPS), гиперплазии предстательной железы (BPH), доброкачественной гиперплазии предстательной железы (BPE), нарушения опорожнения мочевого пузыря (BOO), симптомы со стороны нижних мочевыводящих путей (LUTS, включая кошачий урологический синдром (FUS)), нарушения мочеполовой системы, включая нейрогенный гиперактивный мочевой пузырь (OAB) и (IC), недержание мочи (UI), например, смешанное недержание мочи при напряжении, неотложное недержание мочи, стрессовое недержание мочи или недержание мочи от переполнения (MUI, UUI, SUI, OUI), боль в тазовой области, доброкачественные и злокачественные заболевания органов мужской и женской мочеполовой системы.
Антитело или его фрагмент согласно настоящему изобретению также подходит для лечения и/или профилактики заболеваний почек, в частности, острой и хронической почечной недостаточности, а также острого и хронического нарушения почек. В контексте настоящего изобретения термин «почечная недостаточность» охватывает как острые, так и хронические проявления почечной недостаточности, а также лежащие в основе или связанные с ними почечные нарушения, такие как почечная гипоперфузия, интрадиализная гипотензия, обструктивная уропатия, гломерулопатии, гломерулонефрит, острый гломерулонефрит, гломерулосклероз, тубулоинтерстициальные заболевания, нефропатические нарушения, такие как первичное и врожденное заболевание почек, нефрит, иммунологические заболевания почек, такие как отторжение трансплантата почки и иммунокомплексные заболевания почек, нефропатия, вызванная токсичными веществами, нефропатия, вызванная контрастными веществами, диабетическая и недиабетическая нефропатия, пиелонефрит, кисты почек, нефросклероз, гипертонический нефросклероз и нефротический синдром, которые можно охарактеризовать диагностически, например, аномально сниженным креатинином и/или экскрецией воды, аномально повышенными концентрациями в крови мочевины, азота, калия и/или креатинина, измененной активностью почечных ферментов, например глутамилсинтетазы, измененной осмолярностью или объемом мочи, повышенной микроальбуминурией, макроальбуминурией, поражением клубочков и артериол, расширением канальцев, гиперфосфатемией и/или необходимостью диализа. Настоящее изобретение также охватывает применение антитела или его фрагмента согласно настоящему изобретению для лечения и/или профилактики последствий почечной недостаточности, например, отека легких, сердечной недостаточности, уремии, анемии, электролитных нарушений (например, гиперкалиемии, гипонатриемии) и нарушений в костном и углеводном обмене.
Кроме того, антитело или его фрагмент согласно настоящему изобретению также подходят для лечения и/или профилактики астматических расстройств, легочной артериальной гипертензии (PAH) и других форм легочной гипертензии (PH), включая болезнь левых отделов сердца, ВИЧ, серповидно-клеточную анемию, тромбоэмболии (CTEPH), саркоидоз, COPD или легочную гипертензию, связанную с фиброзом легких, хроническую обструктивную болезнь легких (COPD), острый респираторный дистресс-синдром (ARDS), острое повреждение легких (ALI), дефицит альфа-1-антитрипсина (AATD), фиброз легких, эмфизему легких (например, эмфизема легких, вызванную сигаретным дымом). Синдром облитерирующего бронхиолита (BOS) и муковисцидоз (CF).
Антитело или его фрагмент согласно настоящему изобретению также подходит для борьбы с расстройствами центральной нервной системы, характеризующимися нарушениями системы NO/cGMP. Оно подходит, в частности, для улучшения восприятия, концентрации, обучения или памяти после когнитивных нарушений, подобных тем, которые возникают, в частности, в связи с ситуациями/заболеваниями/синдромами, такими как легкие когнитивные нарушения, возрастные нарушения обучения и памяти, связанные с возрастом потери памяти, сосудистая деменция, черепно-мозговая травма, инсульт, деменция, возникающая после инсульта (постинсультная деменция), посттравматическая черепно-мозговая травма, общие нарушения концентрации, нарушения концентрации внимания у детей с проблемами обучения и памяти, болезнь Альцгеймера, деменция с тельцами Леви, деменция с дегенерацией лобные доли, включая синдром Пика, болезнь Паркинсона, прогрессирующий надъядерный паралич, деменцию с кортикобазальной дегенерацией, амиолатеральный склероз (ALS), болезнь Хантингтона, демиелинизацию, рассеянный склероз, таламическую дегенерацию, деменцию Крейцфельда-Якоба, деменцию при ВИЧ, шизофрению с деменцией психоз или корсаковский синдром. Оно также подходит для лечения и/или профилактики заболеваний центральной нервной системы, таких как состояния тревоги, напряжения и депрессии, сексуальных дисфункций и нарушений сна, связанных с ЦНС, а также для контроля патологических нарушений приема пищи, стимуляторов и веществ, вызывающих привыкание.
Антитело или его фрагмент согласно настоящему изобретению, кроме того, также подходит для контроля церебрального кровотока и, таким образом, представляет собой эффективные агенты для контроля мигрени. Оно также подходит для профилактики и контроля последствий церебрального инфаркта (Apoplexia cerebri), таких как инсульт, церебральная ишемия и черепно-мозговая травма. Его также можно использовать для контроля состояния боли и тиннитуса.
Кроме того, антитело или его фрагмент согласно настоящему изобретению обладает противовоспалительным действием и, следовательно, может использоваться в качестве противовоспалительных средств для лечения и/или профилактики сепсиса (SIRS), полиорганной недостаточности (MODS, MOF), воспалительных заболеваний почек, хронические кишечные воспаления (IBD, болезнь Крона, UC), панкреатита, перитонита, ревматоидных заболеваний, воспалительных заболеваний кожи и воспалительных заболеваний глаз.
Кроме того, антитело или его фрагмент согласно настоящему изобретению может также применяться для лечения и/или профилактики аутоиммунных заболеваний.
Антитело или его фрагмент также подходит для лечения и/или профилактики фиброзных заболеваний внутренних органов, например, легких, сердца, почек, репродуктивной системы, костного мозга и, в частности, печени, а также дерматологических фиброзов и фиброзных поражений глаз. В контексте настоящего изобретения термин фиброзные заболевания включает, в частности, следующие термины: фиброз печени, цирроз печени, фиброз легких, эндомиокардиальный фиброз, нефропатия, гломерулонефрит, интерстициальный фиброз почек, фиброзное повреждение в результате диабета, миома матки, эндометриоз, фиброз костного мозга и подобные фиброзные расстройства, склеродермия, морфея, келоиды, гипертрофические рубцы (также после хирургических процедур), невусы, диабетическая ретинопатия, пролиферативная витроретинопатия и нарушения соединительной ткани (например, саркоидоз).
Антитело или его фрагмент согласно настоящему изобретению также подходит для борьбы с послеоперационными рубцами, например, в результате операций по поводу глаукомы.
Антитело или его фрагмент согласно настоящему изобретению можно также использовать в косметических целях для стареющей и ороговевшей кожи.
Более того, антитело или его фрагмент согласно настоящему изобретению подходит для лечения и/или профилактики гепатита, новообразований, остеопороза, глаукомы и гастропареза.
Антитело или его фрагмент согласно настоящему изобретению, кроме того, подходит для лечения и/или профилактики глазных заболеваний, таких как офтальмологические заболевания, реагирующие на натрийуретический пептид, заболевания сетчатки, глаукома, включая первичную открытоугольную глаукому (POAG), закрытоугольную глаукому и врожденную/развивающуюся глаукому, ретинопатии, травмы глаза, невропатии зрительного нерва, глазную гипертензию, повышенное внутриглазное давление, диабетическую ретинопатию, дегенерацию желтого пятна (AMD), возрастные заболевания глаз, отек желтого пятна, склерит, увеит, сухость глаз, ссадина эпителия роговицы, язва роговицы.
Более того, антитело или его фрагмент согласно настоящему изобретению подходит для лечения заболеваний костей и хрящей, таких как заболевания костей и хрящей, чувствительные к натрийуретическим пептидам, артрит, дегенеративные заболевания хрящевой ткани, остеоартрит, дегенерация хряща, переломы костей, дисплазия скелета, ахондроплазия, остеопороз, несовершенный остеогенез, костная болезнь Педжета (PDB), метаболическое заболевание костей, возрастные заболевания костей, остеомиелит, остеонекроз, рахит, остеомаляция, травмы и заболевания пластин роста, дефекты, связанные с заменой суставов и костей, синдром Марфана, спортивные травмы, мышечные дистрофии, мышечная дистрофия Дюшенна.
Таким образом, согласно другому аспекту настоящее изобретение относится к применению антитела или его фрагмент согласно настоящему изобретению для лечения и/или профилактики нарушений, в частности указанных выше нарушений.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению предназначено для применения в способе лечения и/или профилактики сердечной недостаточности, стенокардии, гипертонии, легочной гипертензии, ишемии, сосудистых заболеваний, почечной недостаточности, тромбоэмболических расстройств, фиброзных расстройств, заболеваний скелета и костей, глазных заболеваний и артериосклероза.
Согласно другому аспекту настоящее изобретение относится к применению антитела или его фрагмента согласно настоящему изобретению для получения лекарственного средства для лечения и/или профилактики нарушений, особенно вышеупомянутых нарушений.
Согласно частным вариантам осуществления настоящее изобретение относится к применению антитела или его фрагмента согласно настоящему изобретению для получения лекарственного средства для лечения и/или профилактики сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, ишемии, сосудистых расстройств, почечной недостаточности, тромбоэмболических расстройств, фиброзных нарушений, заболеваний с деменцией, артериосклероза, скелетных и костных заболеваний, глазных расстройств, карликовости, ахондроплазии и эректильной дисфункции.
Согласно другому аспекту настоящее изобретение относится к способу лечения и/или профилактики нарушений, в частности нарушений, упомянутых выше, с использованием эффективного количества по меньшей мере одного антитела или его фрагмента согласно настоящему изобретению.
Согласно частным вариантам осуществления настоящее изобретение относится к способу лечения и/или профилактики сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, ишемии, сосудистых нарушений, почечной недостаточности, тромбоэмболических нарушений, фиброзных нарушений, опухолевых и онкологических заболеваний, заболеваний скелета и костей, глазных нарушений, карликовости, ахондроплазии и артериосклероза с использованием эффективного количества по меньшей мере одного антитела или его фрагмента согласно настоящему изобретению.
Антитело согласно настоящему изобретению или его фрагмент согласно настоящему изобретению можно вводить как единственный фармацевтический агент или в комбинации с одним или несколькими дополнительными терапевтическими агентами, и в некоторых случаях само антитело может быть модифицировано. Например, антитело или его фрагмент могут быть конъюгированы с химическим соединением, например, для дальнейшего увеличения эффективности, стабильности и/или времени полужизни. В частности, антитело или его фрагмент согласно настоящему изобретению может быть ПЭГилирован и/или HESилирован.
Таким образом, согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению используют в комбинации с по меньшей мере одним дополнительным терапевтическим агентом в способе лечения, в частности для указанных выше целей.
Настоящее изобретение также обеспечивает фармацевтические комбинации, содержащие по меньшей мере одно антитело или его фрагмент согласно настоящему изобретению и по меньшей мере одно дополнительное терапевтическое средство.
В контексте настоящего изобретения термин «фармацевтическая комбинация» используется, как известно специалистам в данной области техники, причем такая комбинация может быть фиксированной комбинацией, нефиксированной комбинацией или набором частей.
В контексте настоящего изобретения термин «фиксированная комбинация» используется, как известно специалистам в данной области, и определяется как комбинация, в которой, например, первый активный ингредиент, такой как одно или несколько антител или их фрагментов в соответствии с настоящим изобретением, и дополнительный активный ингредиент присутствует вместе в одной стандартной дозе или в одном единственном объекте, например, в составе одной дозы. Одним из примеров «фиксированной комбинации» является фармацевтическая композиция, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют в смеси для одновременного введения, например, в составе. Другим примером «фиксированной комбинации» является фармацевтическая комбинация, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют в одной единице, но не в смеси. Таким образом, настоящее изобретение обеспечивает такие фармацевтические композиции, содержащие по меньшей мере одно антитело или его фрагмент и по меньшей мере одно дополнительное терапевтическое средство, в частности, для использования при лечении и/или профилактики вышеупомянутых нарушений.
В контексте настоящего изобретения термины «нефиксированная комбинация» и «набор частей» используются, как известно специалистам в данной области, и определяются как комбинация, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют в более чем одной единице, например, в отдельных лекарственных формах. Одним из примеров нефиксированной комбинации или набора частей является комбинация, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют отдельно.
Компоненты нефиксированной комбинации или набора частей можно вводить отдельно, последовательно, одновременно, в одно и то же время или в хронологическом порядке.
Антитело или его фрагмент согласно настоящему изобретению можно вводить одновременно с указанным дополнительным терапевтически активным агентом, до или после него. В контексте настоящего изобретения термин «одновременно с» означает введение антитела или его фрагмента согласно настоящему изобретению и, по меньшей мере, одного дополнительного терапевтически активного агента в тот же день, более конкретно в течение 12 часов, более конкретно в течение 2 часов.
Согласно частным вариантам осуществления введение антитела или его фрагмента согласно настоящему изобретению и одного другого терапевтически активного агента происходит в течение восьми недель подряд, более конкретно в течение от одной до шести недель подряд. Антитело или его фрагмент согласно настоящему изобретению и по меньшей мере один другой терапевтически активный агент может вводиться одним и тем же путем или разными путями.
Антитело или его фрагмент согласно настоящему изобретению можно, например, комбинировать с известными агентами той же группы лечения по показаниям, такими как агенты, используемые для лечения и/или профилактики заболеваний и/или состояний, связанных с гипертонией, сердечной недостаточностью, легочной гипертензией, COPD, астмой, муковисцидозом, ахондроплазией, гиперфосфатемией, хронической болезнью почек (CKD), кальцинозом мягких тканей, кальцинозом, связанным с хроническим заболеванием почек, кальцинозом, связанным с нехроническим заболеванием почек, медиальным кальцинозом, включая медиальный склероз Менкеберга, атеросклерозом, кальцинозом интимы, гипертрофией сердца, связанной с CKD, почечной дистрофией, связанной с CKD, остеопорозом, постменопаузальным остеопорозом, сахарным диабетом II, хроническим заболеванием почек, старением, гипофосфатурией, гиперпаратиреозом, нарушениями, связанными с витамином D, дефицитом витамина К, коагулянтами-антагонистами витамина К, болезнью Кавасаки, ACDC (артериальной кальцинозом в результате дефицита CD73), GACI (обобщенным артериальным кальцинозом младенцев), IBGC (идиопатическим кальцинозом подкорковых узлов), PXE (эластической псевдоксантомой), ревматоидным артритом, синдромом Синглтона-Мертена, P-талассемией, кальцификацией, гетеротрофной оссификацией, преждевременной кальцификацией плаценты, кальцинозом матки, фибромиомой матки с кальцинозом, болезнью Фара, микрокальцинатом и кальцинозом аортального клапана.
Предпочтительные примеры подходящих дополнительных терапевтических агентов для объединения с антителом или его фрагментом согласно настоящему изобретению:
 органические нитраты и NO-донаторы, как, например, нитропруссид натрия, нитроглицерин, изосорбид мононитрат, изосорбод динитрат, мол-сидомин или SIN-1, а также ингалятивный NO;
органические нитраты и NO-донаторы, как, например, нитропруссид натрия, нитроглицерин, изосорбид мононитрат, изосорбод динитрат, мол-сидомин или SIN-1, а также ингалятивный NO;
 соединения, которые ингибируют распад циклического гуанозинмонофос-фата (cGMP), например, ингибиторы фосфодиэстеразы (POE) 1, 2 и/или 5, в частности POE 5-ингибиторы, такие как силденафил, варденафил, тадала-фил, уденафил, дазантафил, аванафил, мироденафил, лоденафил или PF-00489791;
соединения, которые ингибируют распад циклического гуанозинмонофос-фата (cGMP), например, ингибиторы фосфодиэстеразы (POE) 1, 2 и/или 5, в частности POE 5-ингибиторы, такие как силденафил, варденафил, тадала-фил, уденафил, дазантафил, аванафил, мироденафил, лоденафил или PF-00489791;
 средства с антитромботическим действием, в качестве примера и предпочтительно, из группы ингибиторов агрегации тромбоцитов, антикоагулянтов или профибринолитических веществ;
средства с антитромботическим действием, в качестве примера и предпочтительно, из группы ингибиторов агрегации тромбоцитов, антикоагулянтов или профибринолитических веществ;
 активные вещества, снижающие кровяное давление, например, и предпочтительно, из группы антагонистов кальция, антагонистов ангиотензина AII, ингибиторов ACE, ингибиторов ACE, NEP-ингибиторов, ингибиторов вазопептидазы, антагонистов эндотелина, ингибиторов ренина, блокаторов альфа-рецепторов, блокаторов бета-рецепторов, антагонистов минералокортикоидных рецепторов, ингибиторов rho-киназы и диуретиков;
активные вещества, снижающие кровяное давление, например, и предпочтительно, из группы антагонистов кальция, антагонистов ангиотензина AII, ингибиторов ACE, ингибиторов ACE, NEP-ингибиторов, ингибиторов вазопептидазы, антагонистов эндотелина, ингибиторов ренина, блокаторов альфа-рецепторов, блокаторов бета-рецепторов, антагонистов минералокортикоидных рецепторов, ингибиторов rho-киназы и диуретиков;
 антиаритмические средства, в качестве примера и предпочтительно из группы блокаторов натриевых каналов, блокаторов бета-рецепторов, блокаторов калиевых каналов, антагонистов кальция, блокаторов If-каналов, дигиталиса, парасимпатолитиков (ваголитиков), симпатомиметиков и других антиаритмических средств, таких как аденозин, агонисты рецептора аденозина, а также вернакалант;
антиаритмические средства, в качестве примера и предпочтительно из группы блокаторов натриевых каналов, блокаторов бета-рецепторов, блокаторов калиевых каналов, антагонистов кальция, блокаторов If-каналов, дигиталиса, парасимпатолитиков (ваголитиков), симпатомиметиков и других антиаритмических средств, таких как аденозин, агонисты рецептора аденозина, а также вернакалант;
 положительные инотропные средства, например, сердечный гликозид (дигоксин), бета-адренергические и допаминргические агонисты, такие как изопреналин, адреналин, норадреналин, допамин или добутамин;
положительные инотропные средства, например, сердечный гликозид (дигоксин), бета-адренергические и допаминргические агонисты, такие как изопреналин, адреналин, норадреналин, допамин или добутамин;
 антагонисты рецепторы вазопрессина, в качестве примера и предпочтительно из группы кониваптана, толваптана, ликсиваптана, мозаваптана, сатаваптана, SR-121463, RWJ 676070 или BAY 86-8050, а также соединений, описанных в WO 2010/105770, WO2011/104322 и WO 2016/071212;
антагонисты рецепторы вазопрессина, в качестве примера и предпочтительно из группы кониваптана, толваптана, ликсиваптана, мозаваптана, сатаваптана, SR-121463, RWJ 676070 или BAY 86-8050, а также соединений, описанных в WO 2010/105770, WO2011/104322 и WO 2016/071212;
 активные вещества, изменяющие жировой обмен, в качестве примера и предпочтительно из группы агонистов тиреоидного рецептора, ингибиторов PCSK9, ингибиторов синтеза холестерина, таких как, например и предпочтительно, ингибиторы HMG-CoA-редуктазы или синтеза сквалена, ингибиторы ACAT, ингибиторы СЕТР, ингибиторы MTP, PPAR-альфа-, PPAR-гамма- и/или PPAR-дельта-агонисты, ингибиторы абсорбции холестерина, ингибиторы липазы, адсорберы полимерной желчной кислоты, ингибиторы реабсорбции желчных кислот и антагонисты липопротеина (а).
активные вещества, изменяющие жировой обмен, в качестве примера и предпочтительно из группы агонистов тиреоидного рецептора, ингибиторов PCSK9, ингибиторов синтеза холестерина, таких как, например и предпочтительно, ингибиторы HMG-CoA-редуктазы или синтеза сквалена, ингибиторы ACAT, ингибиторы СЕТР, ингибиторы MTP, PPAR-альфа-, PPAR-гамма- и/или PPAR-дельта-агонисты, ингибиторы абсорбции холестерина, ингибиторы липазы, адсорберы полимерной желчной кислоты, ингибиторы реабсорбции желчных кислот и антагонисты липопротеина (а).
 противовоспалительные средства, например и предпочтительно, из группы глюкокортикоидов, такие как, например и предпочтительно, преднизон, преднизолон, метилпреднизолон, триамцинолон, дексаметазон, бекломета-зон, бетаметазон, флунизолид, будесонид или флутиказон, а также нестеро-идные противовоспалительные агенты (NSAID), например и предпочтительно, ацетилсалициловая кислота (аспирин), ибупрофен и напроксен, производные 5-амино салициловой кислоты, антагонисты лейкотриена, ингибиторы TNF-альфа и антагонисты хемокинового рецептора, такие как ингибиторы CCR1, 2 и/или 5;
противовоспалительные средства, например и предпочтительно, из группы глюкокортикоидов, такие как, например и предпочтительно, преднизон, преднизолон, метилпреднизолон, триамцинолон, дексаметазон, бекломета-зон, бетаметазон, флунизолид, будесонид или флутиказон, а также нестеро-идные противовоспалительные агенты (NSAID), например и предпочтительно, ацетилсалициловая кислота (аспирин), ибупрофен и напроксен, производные 5-амино салициловой кислоты, антагонисты лейкотриена, ингибиторы TNF-альфа и антагонисты хемокинового рецептора, такие как ингибиторы CCR1, 2 и/или 5;
 агенты, которые ингибируют каскад сигнальных трансдукций, например, и предпочтительно, из группы ингибиторов киназы, например и предпочтительно, из группы ингибиторов тирозинкиназы и/или серин/треонинкиназы;
агенты, которые ингибируют каскад сигнальных трансдукций, например, и предпочтительно, из группы ингибиторов киназы, например и предпочтительно, из группы ингибиторов тирозинкиназы и/или серин/треонинкиназы;
 средства, которые ингибируют деградацию и модификацию внеклеточного матрикса, например и предпочтительно, из группы ингибиторов матриксных металлопротеаз (MMP), например и предпочтительно, ингибиторы химазы, стромелизина, коллагеназ, желатиназ и аггреканаз (предпочтительно из группы MMP-1, MMP-3, MMP-8, MMP-9, MMP-10, MMP-11 и с-13), а также металлоэластазы (MMP-12) и нейтрофилэластаза (HNE), например, сивелестат или DX-890;
средства, которые ингибируют деградацию и модификацию внеклеточного матрикса, например и предпочтительно, из группы ингибиторов матриксных металлопротеаз (MMP), например и предпочтительно, ингибиторы химазы, стромелизина, коллагеназ, желатиназ и аггреканаз (предпочтительно из группы MMP-1, MMP-3, MMP-8, MMP-9, MMP-10, MMP-11 и с-13), а также металлоэластазы (MMP-12) и нейтрофилэластаза (HNE), например, сивелестат или DX-890;
 агенты, которые блокируют связывание серотонина с его рецептором, например, и предпочтительно антагонисты 5-HT2b-рецептора;
агенты, которые блокируют связывание серотонина с его рецептором, например, и предпочтительно антагонисты 5-HT2b-рецептора;
 антифиброзные агенты, например и предпочтительно нинтеданиб, пирфенидон, антагонисты рецептора аденозина A2b, антагонисты сфингозин-1-фосфатного рецептора 3 (S1P3), ингибиторы аутотаксина, антагонисты рецептора 1 лизофосфатидной кислоты (LPA-1) и рецептора 2 лизофосфатидной кислоты (LPA-2), ингибиторы лизилоксидазы (LOX), ингибиторы лизилоксидаза подобного белка-2, ингибиторы CTGF, антагонисты IL-13, антагонисты интегрина, антагонисты TGF-бета, ингибиторы передачи сигналов wnt, антагонисты CCR2;
антифиброзные агенты, например и предпочтительно нинтеданиб, пирфенидон, антагонисты рецептора аденозина A2b, антагонисты сфингозин-1-фосфатного рецептора 3 (S1P3), ингибиторы аутотаксина, антагонисты рецептора 1 лизофосфатидной кислоты (LPA-1) и рецептора 2 лизофосфатидной кислоты (LPA-2), ингибиторы лизилоксидазы (LOX), ингибиторы лизилоксидаза подобного белка-2, ингибиторы CTGF, антагонисты IL-13, антагонисты интегрина, антагонисты TGF-бета, ингибиторы передачи сигналов wnt, антагонисты CCR2;
 агенты, которые действуют как бронходилататоры, например, предпочтительно антагонисты рецептора 5-HT2b; β2 («бета-два»)- адренергические агонисты (короткого и длительного действия), антихолинергические средства и теофиллин;
агенты, которые действуют как бронходилататоры, например, предпочтительно антагонисты рецептора 5-HT2b; β2 («бета-два»)- адренергические агонисты (короткого и длительного действия), антихолинергические средства и теофиллин;
 агенты, которые являются антагонистами цитокинов и хемокинов, например и предпочтительно антагонистами TGF-бета, CTGF, IL-1, IL-4, IL-5, IL-6, IL-8, IL-13, IL-25, IL-33, TSLP и интегрины;
агенты, которые являются антагонистами цитокинов и хемокинов, например и предпочтительно антагонистами TGF-бета, CTGF, IL-1, IL-4, IL-5, IL-6, IL-8, IL-13, IL-25, IL-33, TSLP и интегрины;
 органические нитраты и NO-донаторы, как, например, нитропруссид натрия, нитроглицерин, изосорбид мононитрат, изосорбод динитрат, мол-сидомин или SIN-1, а также ингаляционный NO;
органические нитраты и NO-донаторы, как, например, нитропруссид натрия, нитроглицерин, изосорбид мононитрат, изосорбод динитрат, мол-сидомин или SIN-1, а также ингаляционный NO;
 NO-независимые, однако гем-зависимые стимуляторы растворимой гуанилатциклазы, как например и предпочтительно соединения, раскрытые в WO 00/06568, WO 00/06569, WO 02/42301, WO 03/095451, WO 2011/147809, WO 2012/004258, WO 2012/028647 и WO 2012/059549;
NO-независимые, однако гем-зависимые стимуляторы растворимой гуанилатциклазы, как например и предпочтительно соединения, раскрытые в WO 00/06568, WO 00/06569, WO 02/42301, WO 03/095451, WO 2011/147809, WO 2012/004258, WO 2012/028647 и WO 2012/059549;
 NO-независимые, однако гем-зависимые активаторы растворимой гуанилатциклазы, как например и предпочтительно соединения, раскрытые в WO 01/19355, WO 01/19776, WO 01/19778, WO 01/19780, WO 02/070462 и WO 02/070510;
NO-независимые, однако гем-зависимые активаторы растворимой гуанилатциклазы, как например и предпочтительно соединения, раскрытые в WO 01/19355, WO 01/19776, WO 01/19778, WO 01/19780, WO 02/070462 и WO 02/070510;
 агенты, стимулирующие синтез cGMP, например, модуляторы sGC, например и предпочтительно, риоцигуат, цинацигуат, верицигуат;
агенты, стимулирующие синтез cGMP, например, модуляторы sGC, например и предпочтительно, риоцигуат, цинацигуат, верицигуат;
 аналоги простациклина или агонисты IP-рецепторов, например и предпочтительно илопрост, берапрост, трепростинил, эпопростенол или селексипаг;
аналоги простациклина или агонисты IP-рецепторов, например и предпочтительно илопрост, берапрост, трепростинил, эпопростенол или селексипаг;
 антагонисты рецепторов эндотелина, например и предпочтительно бозентан, дарузентан, амбрисентан или ситаксентан;
антагонисты рецепторов эндотелина, например и предпочтительно бозентан, дарузентан, амбрисентан или ситаксентан;
 средства, которые ингибируют растворимую эпоксидгидролазу (sEH), например и предпочтительно, N,N'-дициклогексилмочевина, 12-(3-адамантан-1-ил-уреидо)-додекановая кислота или 1-адамантан-1-ил-3-{5-[2-(2-этоксиэтокси)этокси]пентил}-мочевина;
средства, которые ингибируют растворимую эпоксидгидролазу (sEH), например и предпочтительно, N,N'-дициклогексилмочевина, 12-(3-адамантан-1-ил-уреидо)-додекановая кислота или 1-адамантан-1-ил-3-{5-[2-(2-этоксиэтокси)этокси]пентил}-мочевина;
 средства, которые влияют на метаболизмом глюкозы, например и предпочтительно, инсулин, бигуанид, тиазолидиндион, сульфонилмочевина, акарбоза, ингибиторы DPP4, аналоги GLP-1 или ингибиторы SGLT-1;
средства, которые влияют на метаболизмом глюкозы, например и предпочтительно, инсулин, бигуанид, тиазолидиндион, сульфонилмочевина, акарбоза, ингибиторы DPP4, аналоги GLP-1 или ингибиторы SGLT-1;
 натрийуретические пептиды, например и предпочтительно, предсердный натрийуретический пептид (ANP), натрийуретический пептид типа B (BNP, Несиритид), натрийуретический пептид типа C (CNP) или уродилатин;
натрийуретические пептиды, например и предпочтительно, предсердный натрийуретический пептид (ANP), натрийуретический пептид типа B (BNP, Несиритид), натрийуретический пептид типа C (CNP) или уродилатин;
 производные натрийуретических пептидов, например и предпочтительно, восоритид, цендеретид, PL 3994
производные натрийуретических пептидов, например и предпочтительно, восоритид, цендеретид, PL 3994
 активаторы сердечного миозина, например и предпочтительно, омекамтив мекарбил (CK-1827452);
активаторы сердечного миозина, например и предпочтительно, омекамтив мекарбил (CK-1827452);
 кальций-сенсибилизаторы, например и предпочтительно, левосимендан;
кальций-сенсибилизаторы, например и предпочтительно, левосимендан;
 средства, которые влияют на энергетический метаболизм сердца, например и предпочтительно, этомоксир, дихлорацетат, ранолазин или триметазидин, полные или частичные агонисты аденозиновых рецепторов A1, такие как GS-9667 (ранее известный как CVT-3619), кападенозон, неладенозон и не-ладенозон биаланат;
средства, которые влияют на энергетический метаболизм сердца, например и предпочтительно, этомоксир, дихлорацетат, ранолазин или триметазидин, полные или частичные агонисты аденозиновых рецепторов A1, такие как GS-9667 (ранее известный как CVT-3619), кападенозон, неладенозон и не-ладенозон биаланат;
 агенты, влияющие на частоту сердечных сокращений, например и предпочтительно, ивабрадин.
агенты, влияющие на частоту сердечных сокращений, например и предпочтительно, ивабрадин.
Под средствами с антитромботическим действием предпочтительно понимают соединения из группы ингибиторов агрегации тромбоцитов, антикоагулянтов или профибринолитических веществ.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором агрегации тромбоцитов, например и предпочтительно, аспирином, клопидогрелем, прасугрелем, тикагрелором, тиклопидином или дипиридамолом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором тромбина, таким как например и предпочтительно, ксимелагатран, дабигатран, мелагатран, бивалирудин или клексан.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с GPIIb/IIIa-антагонистами, такими как например и предпочтительно, тирофибан или абсиксимаб.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором фактора Ха, таким как например и предпочтительно, ривароксабан (BAY 59-7939), DU-176b, апиксабан, бетриксабан, отамиксабан, фидексабан, разаксабан, летаксабан, эрибаксабан, фондапаринукс, идапаринукс, PMD-3112, дарексабан (YM-150), KFA-1982, EMD-503982, MCM-17, MLN-1021, DX 9065a, DPC 906, JTV 803, SSR-126512 или SSR-128428.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с гепарином или производным гепарина с низкой молекулярной массой весом (LMW).
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом витамина К, таким как например и предпочтительно кумарин.
Под средствами, понижающими кровяное давление, предпочтительно понимают соединения из группы антагонистов кальция, антагонистов ангиотензина AII, ингибиторов фермента АСЕ, антагонистов эндотелина, ингибиторов ренина, блокаторов альфа-рецепторов, блокаторов бета-рецепторов, антагонистов мине-ралкортикоидных рецепторов, ингибиторов rho-киназы и диуретиков.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом кальция, таким как например и предпочтительно нифедипин, амлодипин, верапамил или дилтиазем.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с блокатором альфа-1-рецепторов, таким как например и предпочтительно празосин.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с блокатором бета-рецепторов, таким как например и предпочтительно пропранолол, атенолол, тимолол, пиндолол, альпренолол, окспренолол, пенбутолол, бупранолол, метипранолол, надолол, мепиндолол, каразалол, соталол, метопролол, бетаксолол, целипролол, бисопролол, картеолол, эсмолол, лабеталол, карведилол, адапролол, ландиолол, небиволол, эпанолол или бусиндолол.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом ангиотензина AII, таким как например и предпочтительно лосартан, кандесартан, валсартан, телмисартан или эмбусартан, или двойным антагонистом ангиотензина AII/ингибитором неприлизина, в качестве примера и предпочтительно с LCZ696 (валсартан/сакубитрил).
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором АСЕ, таким как например и предпочтительно эналаприл, каптоприл, лизиноприл, рамиприл, делаприл, фозиноприл, квиноприл, периндоприл или трандоприл.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом эндотелина, таким как например и предпочтительно бозентан, дарузентан, амбризентан или ситаксзентан.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором ренина, таким как например и предпочтительно алискирен, SPP-600 или SPP-800.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом минералкортикоидных рецепторов, таким как например и предпочтительно спиронолактон или эплеренон.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с петлевым диуретиком, например, фуросемидом, торасемидом, буметанидом и пиретанидом, с калийсберегающими диуретиками, например, амилоридом и триамтереном, с антагонистами альдостерона, например, спироно-лактоном, канреноатом калия и эплереноном, а также тиазидными диуретиками, например, гидрохлортиазидом, хлорталионом, ксипамидом и идапамидом.
Под средствами, изменяющими жировой обмен, понимают предпочтительно со-единения из группы ингибиторов СЕТР, агонистов тироидных рецепторов, ин-гибиторов синтеза холестерина, таких как ингибиторы HMG-CoA-редуктазы или синтеза сквалена, ингибиторов АСАТ, ингибиторов МТР, агонистов PPAR-альфа, PPAR-гамма и/или PPAR-дельта рецепторов, ингибиторов абсорбции хо-лестерина, полимерных адсорбентов желчной кислоты, ингибиторов реабсорбции желчной кислоты, ингибиторов липазы, а также антагонистов липопротеина (а).
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором СЕТР, таким как например и предпочтительно торсетрапиб (СР-529 414), JJT-705 или СЕТР-вакцина (Avant).
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с агонистом тироидных рецепторов, таким как например и предпочтительно D-тироксин, 3,5,3'-трийодотиронин (Т3), CGS 23425 или акситиром (CGS 26214).
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором HMG-CoA-редуктазы из класса статинов, таким как например и предпочтительно ловастатин, симвастатин, правастатин, флувастатин, аторвастатин, розувастатин или питавастатин.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором синтеза сквалена, таким как например и предпочтительно BMS-188494 или ТАК-475.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором АСАТ, таким как например и предпочтительно авазимиб, мелинамид, пактимиб, эфлусимиб или SMP-797.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором МТР, таким как например и предпочтительно имплитапид, BMS-201038, R-103757 или JTT-130.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с агонистом PPAR-гамма рецепторов, таким как например и предпочтительно пиоглитазон или росиглитазон.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с агонистом PPAR-дельта рецепторов, таким как например и предпочтительно GW-501516 или BAY 68-5042.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором абсорбции холестерина, таким как например и предпочтительно эзетимиб, тиквесид или памаквесид.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором липазы, таким как например и предпочтительно орлистат.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с полимерным адсорбентом желчной кислоты, в качестве примера и предпочтительно с холестирамином, колестиполом, колесолвамом, CholestaGel или колестимидом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором реабсорбции желчных кислот, в качестве примера и предпочтительно с ингибиторами ASBT (=IBAT), например, AZD-7806, S-8921, АК 105, BARI-1741, SC-435 или SC-635.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом липопротеина (а), в качестве примера и предпочтительно с гемкабеном кальцием (CI-1027) или никотиновой кислотой.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом липопротеина (а), в качестве примера и предпочтительно с гемкабеном кальцием (CI-1027) или никотиновой кислотой.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с модуляторами sGC, в качестве примера и предпочтительно с риоцигуатом, цинацигуатом или верицигуатом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации со средством, влияющим на метаболизм глюкозы, в качестве примера и предпочтительно с инсулином, сульфонилмочевиной, акарбозой, DPP4 ингибиторами, GLP-1 аналогами или SGLT-1 ингибиторами.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом TGFбета, в качестве примера и предпочтительно с пирфенидоном и фрезолимумабом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом CCR2, в качестве примера и предпочтительно с CCX-140.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистом TNFальфа, в качестве примера и предпочтительно с адалимумабом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором галектина-3, в качестве примера и предпочтительно с GCS-100.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором Nrf-2, в качестве примера и предпочтительно с бардоксолоном.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с агонистом BMP-7, в качестве примера и предпочтительно с THR-184.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором NOX1/4, в качестве примера и предпочтительно с GKT-137831.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с лекарственным средством, которое влияет на метаболизм витамина D, в качестве примера и предпочтительно с кальцитриолом, альфакальцидолом, доксеркальциферолом, максакальцитолом, парикальцитолом, холекальциферолом или паракальцитолом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с цитостатическим средством, в качестве примера и предпочтительно с циклофосфамидом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с иммуноподавляющим средством, в качестве примера и предпочтительно с циклоспорином.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с фосфатным связующим, в качестве примера и предпочтительно с колестиланом, севеламер гидрохлоридом и севеламер карбонатом, лантаном и карбонатом лантана.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с натрий-фосфатным со-транспортером почечного проксимального канальца, в качестве примера и предпочтительно с ниацином или никотинамидом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с кальцимиметиком для лечения гиперпаратиреоза.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации со средствами для лечения дефицита железа, в качестве примера и предпочтительно с продуктами железа.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации со средствами для лечения гиперурикемии, в качестве примера и предпочтительно с аллопуринолом или расбуриказом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с гликопротеиновым гормоном для лечения анемии, в качестве примера и предпочтительно с эритропоэтиом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с биологическими средствами для иммунной терапии, в качестве примера и предпочтительно с абатацептом, ритуксимабом, экулизумабом или белимумаом.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с антагонистами вазопрессина (группа ваптанов) для лечения сердечной недостаточности, в качестве примера и предпочтительно с толваптаном, кониваптаном, ликсиваптаном, мозаваптаном, сатаваптаном или релковаптаном.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибиторами Jak, в качестве примера и предпочтительно с рук-солитинибом, тофацитинибом, барицитинибом, CYT387, GSK2586184, лестаур-тинибом, пакритинибом (SB1518) или TG101348.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с аналогами простациклина для терапии микротромбов.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с щелочным лекарственным средством, в качестве примера и предпочтительно с бикарбонатом натрия.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором mTOR, в качестве примера и предпочтительно с эверолимусом или рапамицином.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором NHE3, в качестве примера и предпочтительно с AZD1722 или тенапанором.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с модулятором eNOS, в качестве примера и предпочтительно с сапроптерином.
Согласно частным вариантам осуществления, антитело или его фрагмент согласно настоящему изобретению вводят в комбинации с ингибитором CTGF, в качестве примера и предпочтительно с FG-3019.
Антитело или его фрагмент для применения в способе лечения согласно настоящему изобретению может быть составлен любым обычным способом с использованием одного или нескольких физиологически приемлемых носителей или вспомогательных веществ. Антитело или его фрагмент согласно настоящему изобретению можно вводить любыми подходящими средствами, которые могут варьироваться в зависимости от типа заболевания, подлежащего лечению. Возможные пути введения включают энтеральное (например, пероральное), парентеральное (например, внутривенное, внутриартериальное, внутрибрюшинное, внутримышечное, подкожное, внутрисердечное, внутрижелудочковое, интратекальное, интрамедуллярное, внутриочаговое), внутрилегочное и интраназальное введение. Кроме того, антитело или его фрагмент согласно настоящему изобретению можно вводить путем импульсной инфузии, например, с уменьшающимися дозами антитела или его фрагмента. Предпочтительно дозирование производят посредством инъекций, наиболее предпочтительно внутривенных или подкожных инъекций, частично в зависимости от того, является ли состояние острым или хроническим. Вводимое количество будет зависеть от множества факторов, таких как клинические симптомы, пол, возраст и/или вес индивидуума, вводятся ли другие лекарства и других. Квалифицированному специалисту понятно, что путь введения будет варьироваться в зависимости от заболевания или состояния, которое необходимо лечить.
Способы парентеральной доставки включают местное, внутриартериальное, внутриопухолевое, внутримышечное, подкожное, интрамедуллярное, интратекальное, внутрижелудочковое, внутривенное, внутрибрюшинное или интраназальное введение.
Согласно частным вариантам осуществления способ лечения включает однократное или многократное введение антитела или его фрагмента или фармацевтической композиции, содержащей его. Разовые дозы введений могут быть одинаковыми или разными. В частности, способ лечения включает 1, 2, 3, 4, 5 или 6 введений антитела или его фрагмента согласно настоящему изобретению, где предпочтительно множество введений происходит в течение от одного до шести последовательных месяцев. Антитело или его фрагмент согласно настоящему изобретению можно, например, вводить каждые 3-4 дня, каждую неделю, один раз каждые две недели или один раз каждые три недели, в зависимости от его времени полужизни и скорости выведения.
Краткое описание чертежей
Фиг. 1. Средние концентрации в плазме TPP-10992 и TPP-5661 после внутривенного введения 5 мг/кг крысе.
Фиг. 2. Средние концентрации в плазме TPP-12897 после внутрибрюшинного введения 5 мг/кг мышам.
Фиг. 3. Устойчивость ANP (A-C), TPP-10992 (D-F) и TPP-5661 (G-I) к протеолитическому расщеплению. Активность ANP, TPP-10992 и TPP-5661 тестировали на стабильной клеточной линии рецептора ANP крысы непосредственно (A, D, G) или после 4 ч инкубации при 37°C с 0,6 мкг/мл NEP (B, E, H) или 0,6 мкг/мл IDE (C, F, I).
Фиг. 4. Устойчивость BNP (A-C) и TPP-11155 (D-F) к протеолитическому расщеплению. Активность BNP и TPP-11155 тестировали на стабильной клеточной линии рецептора BNP крысы непосредственно (A, D), или после 4 ч инкубации при 37°C с 0,6 мкг/мл NEP (B, E) или 0.6 мкг/мл IDE (C, F).
Фиг. 5. Устойчивость CNP (A-C) и TPP-12897 (D-F) к протеолитическому расщеплению. Активность CNP и TPP-11155 тестировали на стабильной клеточной линии рецептора CNP крысы непосредственно (A, D), или после 4 ч инкубации при 37°C с 0,6 мкг/мл NEP (B, E) или 0.6 мкг/мл IDE (C, F).
Фиг. 6. Пептид ANP и TPP-10992 индуцировали кривые зависимости реакции вазодилатации от дозы в аортальных кольцах с PE-сокращением. Кривые "концентрация-ответ" (0,0001-10 мкМ; n=3 крысы) на пептид ANP (светлые кружки) и TPP-10992 (темные кружки) в аортальных кольцах эндотелий-интактных крыс, сокращенных фенилэфрином (1 мкМ). Экспериментальные значения были рассчитаны относительно максимальных изменений сокращения, производимого фенилэфрином в каждой ткани, которое было принято за 100%. Эффективность пептида ANP и TPP-10992 составляла -7,4 и -6,7, соответственно (значения logEC50). Данные представляют собой среднее значение±S.E.M. для 2 экспериментов.
Фиг. 7. Пептид ANP и TPP-5661 индуцировали кривые зависимости реакции вазодилатации от дозы в аортальных кольцах с PE-сокращением. Кривые "концентрация-ответ" (0,0001-10 мкМ; n=3 крысы) на пептид ANP (светлые кружки) и TPP-5661 (темные кружки) в аортальных кольцах эндотелий-интактных крыс, сокращенных фенилэфрином (1 мкМ). Экспериментальные значения были рассчитаны относительно максимальных изменений сокращения, производимого фенилэфрином в каждой ткани, которое было принято за 100%. Эффективность пептида ANP и TPP-5661 составляла -7,4 и -6,5, соответственно (значения logEC50). Данные представляют собой среднее значение±S.E.M. для 2 экспериментов.
Фиг. 8. Гемодинамический эффект ANP у крыс в сознании. Крысиный ANP вводили внутрибрюшинно в момент 0 часов. Доза 500 мкг ANP привела к снижению среднего артериального давления (MAP) примерно на 25% с продолжительностью эффекта около 6-8 часов.
Фиг. 9. Гемодинамический эффект TPP-5661 у крыс в сознании. TPP-5661 вводили внутрибрюшинно в момент 0 часов. Доза 15 мг/кг привела к снижению среднего артериального давления (MAP) примерно на 20% с продолжительностью эффекта более 6 дней.
Фиг. 10. Гемодинамический эффект PP-10992 у крыс в сознании. TPP-10992 вводили внутрибрюшинно в момент 0 часов. Доза 30 мг/кг привела к снижению среднего артериального давления (MAP) примерно на 20% с максимальным эффектом на момент времени 48 часов и продолжительностью эффекта более 6 дней
Фиг. 11. Активность конструкций антител с привитыми BNP на клетках hNPRA. Активность очищенных образцов соединений на стабильных клетках hNPRA-CHO k1 оценивали путем сравнения с эталонными образцами TPP-5661 и TPP-5657. Образцы тестировали в серии разведений в четыре раза.
Фиг. 12. Различные изотипы человеческого IgG обеспечивают одинаково подходящие каркасы антител. Примерное определение активности соединений 9, 33, 65, 91, 127 и 191 IgG1 (TPP-10294, TPP-10277, TPP-10279, TPP-10282, TPP-10269 и TPP-10355, соответственно), изотипов IgG2 и IgG4. Активность очищенных образцов соединения на стабильных клетках hNPRA-CHO k1 оценивали путем сравнения с контрольными образцами соединения 117 человеческого IgG1 TPP-5661 и соединения 209 человеческого IgG1 TPP-5657. Образцы тестировали в серии разведений в четыре раза
Фиг. 13. Одинаково подходящие каркасы антител IgG происходят из разных видов. Примерное определение активности соединения 117 человеческого IgG1 (TPP-5661) и соединения 9 человеческого IgG1 (TPP-10294) и их нечеловеческих аналогов IgG1. Активность очищенных образцов соединения на стабильных клетках hNPRA-CHO k1 оценивали путем сравнения с контрольным образцом соединения 209 человеческого IgG1 (TPP-5657). Образцы тестировали в серии разведений в четыре раза.
Фиг. 14. Одинаково подходящие каркасы антител человека IgG происходят из различных последовательностей зародышевой линии. Активность очищенных образцов соединения на стабильных клетках hNPRA-CHO k1 оценивали путем сравнения с эталонным образцом TPP-10992. Образцы тестировали в серии разведений в четыре раза.
Фиг. 15. Защитные эффекты TPP-12899 против LPS, IL-1β и проницаемости эндотелиального барьера, индуцированной тромбином, как оценено с помощью измерения импеданса в реальном времени.
Фиг. 16. Терапевтические эффекты TPP-13992 на выживаемость (A), прирост массы тела (B), соотношение белок/креатинин в моче (C) и массу левого предсердия (D); (n=8-12 (здоровый контроль, n=5), среднее±SEM, однофакторный дисперсионный анализ по сравнению с TPP-10155 (изотип-специфическое контрольное антитело).
Фиг. 17. Гемодинамическая оценка после введения плацебо, 0,1, 0,3 и 1,0 мг/кг TPP-10992. TPP-10992 показывает дозозависимое и длительное (>5 дней) снижение артериального давления. **p<0,01, ****p<0,0001 по сравнению с группой плацебо с использованием однофакторного теста ANOVA для повторных измерений с критерием множественного сравнения Тьюки.
Примеры
Пример 1. Конструкция кандидата TPP-5661
Кандидат TPP-5661 конструировали посредством слияния гетерологичной аминокислотной последовательности, содержащей Ntls, крысиный ANP дикого типа и Ctls, с C-концом HV 3-23 (SEQ ID NO 85) посредством замещения двух C-концевых остатков HV 3-23 на два N-концевых остатка гетерологичной аминокислотной последовательности, и с N-концом IGHJ1 (SEQ ID NO 86) посредством замещения девяти N-концевых остатков IGHJ1 на 9 C-концевых остатка гетерологичной аминокислотной последовательности. Соответствующая последовательность тяжелой цепи полной длины SEQ ID NO 67 дополнительно содержит аминокислотную последовательность Constant-H (SEQ ID NO 87).
Спаривание последовательности тяжелой цепи полной длины SEQ ID NO 67, несущей вставленный ANP крысы (rANP), с последовательностью легкой цепи полной длины SEQ ID NO 66, выполненное путем объединения последовательностей LV 1-40 (SEQ ID NO 88), IGLJ2 (SEQ ID NO 89) и Constant-L (SEQ ID NO 90) дает полный IgG кандидат TPP-5661 (см. Таблицу 1).
Ниже показана последовательность тяжелой цепи полной длины (SEQ ID NO 67); включенная гетерологичная аминокислотная последовательность (Ntls-rANP-Ctls) подчеркнута; последовательности, полученные из HV 3-23 и IGHJ1, выделены жирным шрифтом:
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSAISGSGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCTSVHQETKKYQSSPDGGSGGSLRRSSCFGGRIDRIGAQSGLGCNSFRYGSYSYTYNYEWHVDVWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
Сконструированная и синтезированная конструкция антитела была клонирована в соответствии с хорошо известными в данной области техники методами и подтверждена секвенированием ДНК с использованием плазмида-специфических олигонуклеотидов.
Пример 2. Вставка NP в участки CDR антитела приводит к увеличенному времени полужизни в сыворотке
Определение фармакокинетических параметров in vivo
Фармакокинетические параметры TPP-10992 (SEQ ID NO 76 и SEQ ID NO 66) и TPP-5661 (SEQ ID NO 67 и SEQ ID NO 66) определяли после внутривенного введения 5 мг/кг самцам крыс Wistar (n=3). TPP-10992 и TPP-5661 вводили в виде болюса через хвостовую вену. Образцы крови собирали из яремной вены через ранее имплантированные катетеры с временными интервалами до 14 дней (336 часов). Образованную EDTA-плазму хранили при -20°С до дальнейшего анализа
Количественное определение TPP-10992 и TPP-5661 в образцах плазмы проводили с использованием формата анти-IgG человека анализа ELISA(иммуноферментный анализ). Фармакокинетические параметры рассчитывали на основе временных профилей концентрации в плазме с использованием некомпартментного анализа данных.
Средние концентрации в плазме TPP-10992 и TPP-5661 после внутривенного введения с течением времени графически изображены на Фиг. 1.
Средний клиренс и время полужизни TPP-10992 и TPP-5661 приведены в Таблице 2 ниже.
Таблица 2. Средний клиренс (CL) и время полужизни (t1/2) для TPP-10992 и TPP-5661 после внутривенного введения 5 мг/кг крысе.
Определение фармакокинетических параметров in vivo
Фармакокинетические параметры TPP-12897 определяли после внутрибрюшинного введения самкам мышей Balb/c (n=3). Образцы крови собирали в период от 15 минут до 72 часов после применения. Образованную EDTA-плазму хранили при -20°С до дальнейшего анализа. Количественное определение TPP-12897 в образцах плазмы проводили с помощью анти-IgG человека формата анализа ELISA (иммуноглобулин G).
Фармакокинетические параметры рассчитывали из временных профилей концентрации в плазме с использованием некомпартментного анализа данных.
Средние концентрации TPP-12897 в плазме после внутрибрюшинного введения с течением времени графически изображены на Фиг. 2.
Средняя площадь под кривой (AUC) и время полужизни TPP-12897 приведены в Таблице 3 ниже.
Таблица 3. Средняя площадь под кривой (AUC) и время полужизни (t1/2) для TPP-12897 после внутрибрюшинного введения 5 мг/кг мышам.
Пример 3. In vitro, ex vivo и in vivo эффективность ANP-привитых антител
Данные по активности ANP-привитых антител на клеточной линии рецептора NPR-A
Клеточную линию крысиного рецептора ANP (NPR-A) на основе люминесценции получали, как описано ранее (Wunder et al. (2013), Eur J Pharmacol. 698: 131). Соответственно, линия клеток крысиного рецептора ANP (NPR-A) на основе флуоресценции была получена путем котрансфекции линии клеток CHO, стабильно экспрессирующих флуоресцентный кальций-сенсорный белок GCaMP6, плазмидными конструкциями, кодирующими CNGA2 (биосенсор cGMP) и крысиный NPR-A.
Клетки GCaMP6 рецептора ANP культивировали в течение одного дня на черных 384-луночных микротитровальных планшетах с прозрачным дном (2500 клеток/лунка). После удаления среды для культивирования клеток репортерные клетки загружали в течение 20 мин с Tyrode (130 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 20 мМ HEPES, 1 мМ MgCl2, 4,8 мМ NaHCO3 при pH 7,4), содержащим черный маскирующий краситель, при 37°C и 5% CO2. IBMX (0,2 мМ) использовали для предотвращения расщепления cGMP эндогенными фосфодиэстеразами.
Измерения флуоресценции (3 мин, кинетический режим) начинали сразу после добавления агониста. Рецепторные лиганды добавляли в Tyrode, содержащий черный маскирующий краситель и 0,1% BSA. Измерения проводили на FLIPR Tetra®.
ANP (Bachem, H-2100) стимулировал зависимые от концентрации сигналы флуоресценции на линии клеток NPR-A со значениями EC50 0,22 нМ. TPP-5661 и TPP-10992 стимулировали линию репортерных клеток рецептора ANP крысы со значениями EC50 17 нМ и 180 нМ, соответственно. Конструкция контрольного антитела TPP-5657 не стимулировала значимо клеточную линию NPR-A (тестировали до максимальной концентрации 460 нМ).
Чтобы определить чувствительность к протеолитической деградации, активность рецепторных лигандов также была охарактеризована после 4 часов инкубации с 0,6 мкг/мл нейтральной эндопептидазы (NEP, R&D Systems, 1182-ZNC) или 0,6 мкг/мл фермента, разрушающего инсулин (IDE, Merck, 407241-50UG) при 37°C.
На Фиг. 3 графически изображена стабильность ANP (A-C), TPP-10992 (D-F) и TPP-5661 (G-I) от протеолитического расщепления. Как показано на Фиг. 3, натрийуретический пептид ANP (Bachem, H-2100) показал высокую чувствительность к расщеплению NEP и IDE. Напротив, TPP-5661 и TPP-10992 показали высокую устойчивость к протеолитическому расщеплению NEP и IDE.
Данные по активности BNP-привитых антител на клеточной линии рецептора NPR-A
Клеточную линию крысиного рецептора BNP (NPR-A) на основе люминесценции получали, как описано ранее (Wunder et al. (2013), Eur J Pharmacol. 698: 131). Соответственно, линия клеток крысиного рецептора BNP (NPR-A) на основе флуоресценции была получена путем котрансфекции линии клеток CHO, стабильно экспрессирующих флуоресцентный кальций-сенсорный белок GCaMP6, плазмидными конструкциями, кодирующими CNGA2 (биосенсор cGMP) и крысиный NPR-A.
Клетки GCaMP6 рецептора BNP культивировали в течение одного дня на черных 384-луночных микротитровальных планшетах с прозрачным дном (2500 клеток/лунка). После удаления среды для культивирования клеток репортерные клетки загружали в течение 20 мин с Tyrode (130 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 20 мМ HEPES, 1 мМ MgCl2, 4,8 мМ NaHCO3 при pH 7,4), содержащим черный маскирующий краситель, при 37°C и 5% CO2. IBMX (0,2 мМ) использовали для предотвращения расщепления cGMP эндогенными фосфодиэстеразами.
Измерения флуоресценции (3 мин, кинетический режим) начинали сразу после добавления агониста. Рецепторные лиганды добавляли в Tyrode, содержащий черный маскирующий краситель и 0,1% BSA. Измерения проводили на FLIPR Tetra®.
BNP (Bachem, H-5968) стимулировал зависимые от концентрации сигналы флуоресценции на линии клеток NPR-A со значением EC50 2,9 нМ. TPP-9902, TPP-11153, TPP-1154, TPP-11155, TPP-11156 и TPP-11157 стимулировали репортерную клеточную линию рецептора BNP крысы со значениями EC50 2,3 мкМ,>1,9 мкМ, 7 нМ, 12 нМ, 1,2 мкМ и 11 нМ, соответственно. Конструкция контрольного антитела TPP-5657 не стимулировала значимо клеточную линию NPR-A (тестировали до максимальной концентрации 460 нМ).
Чтобы определить чувствительность к протеолитическому расщеплению, активность рецепторных лигандов также была охарактеризована после 4 часов инкубации с 0,6 мкг/мл нейтральной эндопептидазы (NEP, R&D Systems, 1182-ZNC) или 0,6 мкг/мл фермента, разрушающего инсулин (IDE, Merck, 407241-50UG) при 37°C. Натрийуретический пептид BNP (Bachem, H-5968) показал высокую чувствительность к расщеплению NEP и IDE. Напротив, TPP-11155 и TPP-11157 показали высокую устойчивость к протеолитическому расщеплению NEP и IDE.
На Фиг. 4 графически изображена устойчивость BNP (A-C) и TPP-11155 (D-F) к протеолитическому расщеплению.
Данные по активности CNP-привитых антител на клеточной линии рецептора NPR-B
Была создана линия репортерных клеток рецептора CNP крысы (NPR-B) на основе люминесценции, и измерения люминесценции были выполнены, как описано ранее (Wunder et al. (2013), Eur J Pharmacol. 698: 131).
Клетки рецептора CNP (2500 клеток/лунка) культивировали в течение 1 дня на непрозрачных 384-луночных микротитровальных планшетах. После удаления среды для культивирования клеток клетки нагружали в течение 3 ч 2,5 мкг/мл целентеразина в не содержащем Ca2+Tyrode (130 мМ NaCl, 5 мМ KCl, 20 мМ HEPES, 1 мМ MgCl2, 4,8 мМ NaHCO3 при pH 7,4) при 37°C и 5% CO2. Рецепторные лиганды добавляли в течение 10 мин в не содержащий Ca2+Tyrode, содержащий 0,1% BSA. IBMX (0,2 мМ) использовали для предотвращения расщепления cGMP эндогенными фосфодиэстеразами. Непосредственно перед добавлением ионов кальция (конечная концентрация 3 мМ) измерения люминесценции начинали с использованием камеры устройства с зарядовой связью (CCD) в светонепроницаемой коробке. Люминесценцию контролировали непрерывно в течение 50 с.
CNP (Bachem, H-1296) стимулировал зависимые от концентрации сигналы люминесценции на клеточной линии NPR-B крыс со значением EC50 0,024 нМ. TPP-9465, TPP-12377, TPP-12378, TPP-12897 и TPP-12899 стимулировали линию репортерных клеток рецептора CNP крысы со значениями EC50 5,2 нМ, 4,1 нМ, 25 нМ, 10 нМ и 3,2 нМ, соответственно. TPP-12374 стимулировал репортерную клеточную линию рецептора CNP крысы со значениями EC50 150 нМ, а TPP-12375, TPP-12376 показали лишь слабое указание активности.
Чтобы определить чувствительность к протеолитическому расщеплению, активность рецепторных лигандов также была охарактеризована после 4 часов инкубации с 0,6 мкг/мл нейтральной эндопептидазы (NEP, R&D Systems, 1182-ZNC) или 0,6 мкг/мл фермента, разрушающего инсулин (IDE, Merck, 407241-50UG) при 37°C
В отличие от натрийуретического пептида CNP (Bachem, H-1296), TPP-12377, TPP-12897 и TPP-12899 показали высокую устойчивость к протеолитическому расщеплению под действием NEP и IDE.
На Фиг. 5 графически изображена устойчивость CNP (A-C) и TPP-12897 (D-F) к протеолитическому расщеплению.
Данные по активности антител, привитых ANP, определяли с выделенными аортными кольцами крыс
Все эксперименты проводили в соответствии с установленными правилами и одобрены местным комитетом по экспериментам на животных. Самцов крыс Sprague-Dawley (весом 250-300 г) анестезировали пентобарбиталом натрия (40 мг/кг внутрибрюшинно), умерщвляли декапитацией и обескровливали. Грудную аорту вырезали и помещали в ледяной буфер Кребса следующего состава: 130 мМ NaCl, 14,9 мМ NaHCO3, 5,5 мМ декстрозы, 4,7 мМ KCl, 1,18 мМ KH2PO4, 1,17 мМ MgSO47H2O и 1,6 мМ CaCl22H2O. Сосуд вставляли в чашку Сильгарда Петри, наполненную охлажденным раствором Кребса, очищали от жира и соединительной ткани и разрезали на кольцевые сегменты длиной примерно 3-4 мм. аортные кольца устанавливали вертикально в камеры объемом 50 мл (ADIinstruments), содержащей раствор Кребса, при 37°C, непрерывно барботируемый смесью 95% O2 и 5% CO2. Изменения изометрической силы регистрировали с помощью системы сбора данных PowerLab (программное обеспечение Lab Chart 7.0)
После периода уравновешивания аортные кольца обрабатывали 80 мМ KCl для проверки жизнеспособности ткани. Затем определяли целостность эндотелия препаратов путем проверки чувствительности к ацетилхолину (ACh, 1 мкМ) в сосудах, предварительно сокращенных фенилэфрином (PE, 1 мкМ). После вымывания и периода уравновешивания использовали фенилэфрин (PE, 1 мкМ) для индукции сокращения, после чего натрийуретический пептид и IgG, привитые натрийуретическим пептидом, оценивали на вазорелаксацию. Пептид крысиного ANP (ADH-GM-10057T, Santai Labs) использовали в качестве эталона.
Как показано на Фиг. 6, как пептид ANP, так и TPP-10992 индуцировали дозозависимую вазодилатацию в PE-сокращенных аортных кольцах.
Как показано на Фиг. 7, как пептид ANP, так и TPP-5661 индуцировали дозозависимую вазодилатацию в PE-сокращенных аортных кольцах.
Данные по активности антител, привитых ANP, полученные на крысах в сознании
Артериальное давление и частоту сердечных сокращений контролировали у свободно движущихся находящихся в сознании животных с помощью радиотелеметрии (Data Sciences International). Для этих исследований использовали самок крыс со спонтанной гипертензией (SHR/N Crl BR, Charles River) с массой тела 210-300 г.Всех животных содержали в индивидуальных клетках при температуре окружающей среды 22-24°C и поддерживали 12-часовой цикл свет/темнота со свободным доступом к стандартному лабораторному корму для крыс и воде. Имплантацию телеметра (HD-10, DSI) проводили как минимум за 14 дней до того, как животных использовали для измерения артериального давления. Операция проводилась в асептических условиях. После бритья брюшной стенки был сделан разрез брюшной полости по средней линии, и сенсорный катетер, заполненный жидкостью, был вставлен выше по ходу потока в обнаженную нисходящую аорту между подвздошной бифуркацией и почечными артериями. Согласно рекомендациям DSI, кончик телеметрического катетера располагали каудально по отношению к почечным артериям и закрепляли тканевым клеем. Корпус передатчика прикрепляли к внутренней брюшной стенке перед закрытием брюшной полости. Для послеоперационной защиты от инфекций и против боли вводили разовую дозу антибиотика (Oxytetracyclin® 10%, 60 мг/кг подкожно, 0,06 мл/100 г массы тела, Beta-Pharma GmbH & Co, Германия) и анальгетика (Rimadyl®, 4 мг/кг подкожно, Pfizer, Германия). Сбор телеметрических данных выполнялся с помощью программного обеспечения DSI, которое было предопределено для выборки гемодинамических данных в течение 10 секунд, повторяемых каждые 5 минут.Сбор данных был начат менее чем за 2 часа до введения лекарственного средства и закончен после завершения циклов измерения. Данные выражены в% от базовых значений±SEM для по меньшей мере 4 животных на группу. Базальное значение для каждого животного рассчитывали как среднее значение, измеренное за два часа до применения вещества (7:00 - 9:00 утра). Затем данные выражали как среднее значение каждые полчаса, начиная с 15 минут после применения. Всем животным вводили однократное внутрибрюшинное (ip) введение тестируемых веществ, растворенных в фосфатно-солевом буфере (PBS). Введение лекарственного средства проводили в момент времени 9:00 утра (0 часов).
Гемодинамический эффект пептида ANP графически изображен на Фиг. 8. Гемодинамический эффект TPP-5661 графически изображен на Фиг. 9. Гемодинамический эффект TPP-10992 графически изображен на Фиг. 10
Пример 4. Получение различных конструкций антитела, привитого NP
Для конструкций с включением натрийуретического пептида в участок CDR, отличный от CDRH3, предположительно функционально нейтральный CDRH3 был сконструирован путем слияния удлинения из трех остатков Leu Thr Gly (IGHD7-27*01) с С-концом HV 3-23 и N-концом IGHJ1 (по сравнению с Примером 1). Соответствующая последовательность тяжелой цепи полной длины SEQ ID NO 65 дополнительно содержит аминокислотную последовательность Constant-H (SEQ ID NO 87).
Спаривание последовательности тяжелой цепи полной длины SEQ ID NO 65 без какой-либо вставки натрийуретического пептида с последовательностью легкой цепи полной длины SEQ ID NO 66, описанной в примере 1, дает синтетический и предположительно нейтральный IgG отрицательный контроль TPP-5657.
Сконструированная и синтезированная конструкция антитела была клонирована в соответствии с хорошо известными в данной области техники методами и подтверждена секвенированием ДНК с использованием плазмидоспецифичных олигонуклеотидов.
Исходя из этого каркаса антитела были созданы следующие конструкции антител с привитыми ANP.
Таблица 4. Конструирование конструкций антитела, привитого ANP
N-конце-вая1
C-конце-вая2
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком.
Таблица 4 (продолжение). Конструирование конструкций антитела с привитым ANP
3 N-концевая последовательность соответствует ближайшей соседней N-концевой аминокислоте от вставленного натрийуретического пептида, плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком вставленного натрийуретического пептида
4 C-концевая последовательность соответствует аминокислотному удлинению, присутствующему между последним аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней C-концевой эталонной аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота.
Кроме того, следующие конструкции человеческих антител IgG1 с привитыми BNP были получены на основе каркаса антител TPP-5657.
Таблица 5. Конструирование конструкций антитела, привитого BNP
N-концевая1
C-концевая2
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
3Соответствующее ANP соединение относится к конструкции антитела с привитым ANP с тем же локусом вставки и содержащей ту же N-концевую и C-концевую последовательность.
Таблица 5 (продолжение). Конструирование конструкций антитела, привитого BNP
3 N-концевая последовательность соответствует ближайшей соседней N-концевой аминокислоте от вставленного натрийуретического пептида, плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком вставленного натрийуретического пептида
4 C-концевая последовательность соответствует аминокислотному удлинению, присутствующему между последним аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней C-концевой эталонной аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота
Кроме того, были получены следующие конструкции IgG1 человека с привитым CNP.
Таблица 6. Конструирование конструкций антител, привитых CNP
N-кон-цевая1
C-кон-цевая2
pcs
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
3Соответствующее ANP соединение относится к конструкции антитела с привитым ANP с тем же локусом вставки и содержащей ту же N-концевую и C-концевую последовательность
Таблица 6 (продолжение). Конструирование конструкций антител, привитых CNP
3 N-концевая последовательность соответствует ближайшей соседней N-концевой аминокислоте от вставленного натрийуретического пептида, плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком вставленного натрийуретического пептида
4 C-концевая последовательность соответствует аминокислотному удлинению, присутствующему между последним аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней C-концевой эталонной аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота
Пример 5: In vitro активности полученных конструкций
Все конструкции были транзиентно экспрессированы в клетках HEK293 в соответствии с хорошо известными в данной области техники методами, с достижением плотности клеток около 2x10^6 клеток/мл, общей концентрации ДНК около 1 мкг/мл для двух плазмид, кодирующих легкую и тяжелую цепи, при 5-дневной инкубации для экспрессии.
Необработанные образцы (rcs) были экспрессированы в объеме культуры 0,4 мл, и супернатант, отделенный центрифугированием, был непосредственно использован для тестирования. Концентрацию соединения оценивали с помощью IgG-Fc количественного анализа ELISA в соответствии с хорошо известными в данной области техники способами. Вкратце, супернатант, разведенный 1: 1500, и серия 2-кратных разведений контрольной сыворотки человека (Bethyl, RS-110-4), начиная с 400 нг/мл, были иммобилизованы на черных микротитровальных планшетах Maxisorp 384 (MTP), покрытых анти-человеческим Fc. [Sigma I2136] при разведении 1: 440 в 1x покрывающем буфере (Candor, 121125) в течение 1 часа, 37°C. После блокирования с помощью 100%-ного блока SMART (Candor, 113125) применяли анти-человеческий Fc-HRP [Sigma, A0170] при разведении 1: 10000 для обнаружения антител в rcs и эталонных образцах. Кривые зависимости от дозы эталонного образца использовали для количественной оценки концентраций соединений, показанных в таблицах 7 и 8, столбец «мкг/мл rcs». Все образцы применяли четыре раза.
Выделенные образцы соединений (ics) были получены одностадийной очисткой через белок-A из 6 мл экспрессионной культуры и в соответствии с хорошо известными в данной области техники способами. Кислотные элюаты нейтрализовали добавлением 8% (об./об.) 1 М Трис/HCl с pH 9,0, определяли количественно по абсорбции при 280 нм и нормализовали до концентрации 125 нМ.
Образцы очищенных соединений (pcs) были получены путем двухэтапной очистки через белок-А и последующей SEC в буфере PBS из экспрессионной культуры объемом по меньшей мере 35 мл. Значения, приведенные в таблицах 7 и 8, столбец «мкг/мл pcs», относятся к концентрации соединения в супернатанте экспрессионной культуры, определенной аналитической хроматографией на белке А.
Все активности, показанные в таблицах 7 и 8, были измерены на клетках с гетерологичной сверхэкспрессией человеческого NPRA (hNPRA) с использованием количественного анализа cGMP, проводимого в соответствии с инструкциями производителя (cisbio; 62GM2PEH). Вкратце, анализ количественно определяет cGMP в буферном растворе или супернатантах клеточной культуры на основе конкуренции между cGMP, продуцируемым клеткой в результате стимуляции NPRA через образец (натрийуретический пептид), и cGMP, меченным d2, за связывание с антителом, меченным криптатом. Образец cGMP и меченный d2 cGMP конкурируют за связывание с ограниченным количеством сайтов на анти-cGMP антителах, меченных криптатом, и, следовательно, специфический флуоресцентный сигнал HTRF® (т.е. перенос энергии) обратно пропорционален концентрации cGMP в образце.
Данные кривой доза-ответ были проанализированы с помощью GraphPad Prism (версия 7.00 для Windows, GraphPad Software, La Jolla California USA) и EC50 были нанесены на график в соответствии с Y=дно+(вершина-дно)/(1+10^((LogEC50-X)*склон)) с применением ограничений для дна, вершины и склона (общее значение для всех наборов данных соответствующего эксперимента).
Активность необработанного образца соединения в отношении стабильных клеток hNPRA-CHO k1 сначала оценивали путем сравнения с отрицательным контролем TPP-5657 и с положительным образцом, в частности TPP-5661. Контроли и rcs тестировали с четырьмя повторениями в двух концентрациях с коэффициентом относительного разбавления 5, чтобы получить флуоресцентный сигнал (s) в динамическом диапазоне анализа. Окно анализа определялось как разница в сигнале неактивных (макс.сигнал, s_max) и высокоактивных образцов (мин. сигнал, s_min), и для обеих концентраций соединения активность в% была рассчитана как 100*(s_max - s) / (s_max - s_min). Значения, перечисленные в таблице 7, столбцы «активность rcs» и «stdev активность rcs», представляют собой среднее значение результатов для двух концентраций и соответствующее стандартное отклонение. Сигналы rcs, составляющие менее половины сигнала эталонного соединения TPP-5661 (36%), были оценены как неактивные (n.a.).
Активность нескольких необработанных образцов соединений на стабильных клетках hNPRA-CHO k1 повторно оценивали путем сравнения с эталонным образцом TPP-5661 в серии 2,5-кратных разведений (8 концентраций), начиная с 5-кратного разведения. Подходящее значение «logEC50» в качестве меры активности rcs было установлено по отношению к соответствующему значению эталонного rcs TPP-5661 путем вычисления дельты «logEC50» _соединение - «logEC50» _TPP-5661; итоговые значения приведены в таблице 7, столбец «относительная активность rcs». Примечательно, что концентрации соединения в rcs не учитывались, и, следовательно, на указанные значения в равной мере влияют активность соединения и концентрация. Все образцы применяли четыре раза.
Активность выделенных образцов соединений на стабильных клетках hNPRA-CHO k1 оценивали путем определения ЕС50 и сравнения с эталонным образцом TPP-5661. Образцы тестировали в серии 2,5-кратных разведений от 80 нМ до 0,13 нМ. Соответствующее значение logEC50 в качестве меры активности ics было установлено по отношению к соответствующему значению эталонного ics TPP-5661 (-8,8) путем вычисления дельты logEC50_compound - logEC50_TPP-5661; результирующие значения приведены в таблице 7, столбец «отн. logEC50 ics». Все образцы применяли четыре раза.
Активность очищенных образцов соединений на стабильных клетках hNPRA-CHO k1 оценивали в нескольких экспериментах путем определения ЕС50 и сравнения с эталонным образцом TPP-5661. Образцы испытывали в серии разведений по меньшей мере в четыре раза. Значения, указанные в таблице 7, столбцы «отн. logEC50 pcs 1, 3 и 4» являются результатом серии 5-кратных разведений (≥4 концентрации), начиная с 20 или 25 нМ. Значения приведены в таблице 7, столбец «отн. logEC50 pcs 2» являются результатом серии 10-кратных разведений (4 концентрации), начиная с 25 нМ. Значения, указанные в таблице 7, столбцы «отн. logEC50 pcs 5, 6, 7, 8 и 9» являются результатом серии 2,5-кратных разведений с 8 или 12 концентрациями, начиная с 40 до 200 нМ, соответственно. Соответствующее значение logEC50 в качестве меры активности pcs было установлено по отношению к соответствующему значению эталонного TPP-5661 в соответствующем эксперименте (в среднем -9,2, стандартное отклонение 0,5) путем вычисления дельты logEC50_compound - logEC50_TPP-5661.
Активность очищенных образцов соединения на транзиентных клетках hNPRA-HEK293 оценивали в трех экспериментах путем определения ЕС50 и сравнения с эталонным образцом TPP-5661. Образцы тестировали в серии 5-кратных разведений от 1000 нМ до 0,013 нМ. Подходящее значение logEC50 в качестве меры активности pcs устанавливали по отношению к соответствующему значению эталонного TPP-5661 в соответствующем эксперименте (среднее значение трех экспериментов -9,0, стандартное отклонение 0,4) путем вычисления дельты logEC50_compound - logEC50_TPP-5661; результирующие значения приведены в таблице 7, столбцы «отн. logEC50* pcs». Все образцы применяли дважды.
Обобщенная качественная оценка активности соединений приведена в графе «качественная активность», значения указаны в столбце «среднее отн. logEC50» рассчитывались как среднее данных относительных значений logEC50. Соединения, показывающие значения ЕС50>50 раз по сравнению с эталонным соединением TPP-5661, что означает среднее отн. logEC50>1,7, были качественно оценены как неактивные («-»), соединения, показывающие относительный logEC50 от 0,7 до 1,7, были оценены как активные («+»), соединения, показывающие относительное logEC50<0,7, были оценены как очень активные («++“); самые высокие активности наблюдались при относительном logEC50 ниже -0,7 («+++»). Соединения, показывающие активность в rcs без подтверждения, как ics или pcs, помечены единым «y», а соединения, оцененные как неактивные («na» в столбце «активность rcs»), вероятно, из-за их очень низкого уровня экспрессии (≤1 мкг / мл, «n.e.» в столбце «мкг/мл rcs»), отмечены соответствующим образом.
Таблица 7. Уровни экспрессии и активности конструкций антитела, привитого предсердным натрийуретическим пептидом
Не определено (n.d.), нет активности (n.a.), не экспрессируется (n.e.), не доступно (na)
logE
C50
ics
logE
C50
pcs 1
logE
C50
pcs 2
logE
C50
pcs 3
logE
C50
pcs 4
logE
C50
pcs 5
logE
C50
pcs 6
logE
C50
pcs 7
logE
C50
pcs 8
logE
C50
pcs 9
logE
C50
* pcs
logE
C50*
pcs
logEC
50*
pcs
50
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
Достоверные данные для соединений #104 и #135 не были получены. 12 соединений (#54, #61, #89, #139, #162, #168, #170, #171, #172, #173, #176, #196) показали очень низкие уровни экспрессии (≤ 1 мкг/мл в rcs) и соответственно отсутствие активности; активность соединения #61 была показана после обработки соединения (pcs). 7 соединений (#7, #24, #70, #83, #90, #154, #167) в большинстве случаев показали низкую активность как rcs, хотя их уровни экспрессии были очень низкими; активность соединений #24 и #90 были подтверждены при обработке соединения (pcs). Активность не наблюдалась для rcs соединений #18, #26, #29, #92, #96, #101, #104, #158, #164, #179; однако, активность соединений #18, #92, #158, #164 была показана при применении более высоких концентраций (относительная активность rcs); отсутствие активности соединения #26 было подтверждено таким образом.
Таблица 8. Уровни экспрессии и активности конструкций антитела, привитого мозговым натрийуретическим пептидом
не доступно (na)
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
3Соответствующее ANP соединение относится к конструкции ANP-привитого антитела в одними и теми же локусами вставки и содержащей ту же N-концевую и C-концевую последовательность
Очищенные образцы соединений тестировали, как описано в примере 3, в четырехкратных сериях разведений на стабильных клетках hNPRA-CHO k1. Активности конструкций BNP-привитых антител графически изображены на Фиг. 11.
TPP-11156, TPP-9902 и TPP-11153 показали значительную активность на клетках hNPRA по сравнению с TPP-1154, TPP-11155, и TPP-11157. Противоположные результаты наблюдались на rNPRA с EC50<20нМ для TPP-1154, TPP-11155, и TPP-11157, и EC50>1 мкМ для TPP-9902, TPP-11153, и TPP-11156 (см. Пример 3). Это можно объяснить присутствием последовательности BNP человека в TPP-11156, TPP-9902 и TPP-11153, тогда как TPP-1154, TPP-11155 и TPP-11157 содержат последовательность крысиного BNP (см. Таблицу 5). В отличие от всех других конструкций антитела, привитого BNP человека, TPP-18031 и TPP-18032 с низким числом добавленных N- и C-концевых аминокислот в BNP не показали активность на hNPRA.
Пример 6. Специфические линкерные последовательности являются особенно предпочтительными для достижения хорошей гомогенности и уровней экспрессии
Чистоту очищенных образцов соединения (пример 5, таблица 7, столбец «% чистоты pcs») определяли с помощью капиллярного гель-электрофореза в соответствии с инструкциями производителя (LabChip GX, Caliper Life Sciences) в восстанавливающих условиях. Чистоту в% рассчитывали как сумму площадей пиков, соответствующих интактной легкой и тяжелой цепи, относительно суммы всех наблюдаемых пиков.
Ntls последовательности, содержащие GS линкерную последовательность, PN линкерную последовательность или последовательность согласно SEQ ID NO 2, 4, 9, 11, 13 или 15, и Ctls последовательности, содержащие GS линкерную последовательность, PN линкерную последовательность или последовательность согласно SEQ ID NO 3, 5, 12, 14, 15 и 20, как было доказано, являются особенно полезными, так как они не только обеспечивают высокие активности натрийуретического пептида (при условии, что по меньшей мере 12 аминокислотных остатков присутствуют между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида), но также хорошие уровни экспрессии (в отличие, например, от последовательностей, используемых в соединениях #186, #195 и #202) и (в отличие, например, от последовательностей, используемых в соединениях 6 и 7) при низкой степени негомогенности (см. Таблицу 9). WB случае линкерных последовательностей, содержащих GS линкерную последовательность, а также линкерных последовательностей, содержащих PN линкерную последовательность, наблюдалась очень хорошая чистота, равная в среднем 98% Подобным образом, хорошие значения наблюдались для соединений с линкерами, содержащими последовательности SEQ ID NO 2, 3, 4, 5, 9, 11, 12, 13, 14, 15 и 20. А именно, Ntls, имеющая последовательность согласно SEQ ID NO 9, только в комбинации с Ctls, имеющим последовательность согласно SEQ ID NO 20, приводил к соединениям с очень хорошей чистотой; соединения с комбинацией Ntls, имеющего последовательность согласно SEQ ID NO 11, и Ctls, имеющая последовательность согласно SEQ ID NO 12, показали очень хорошую чистоту, только когда SEQ ID NO 11 была фланкирована с Asp (D) на N-концевом сайте, но не Thr (T) или Val (V), и когда SEQ ID NO 12 VNHLRSEKLT была фланкирована с Gly (G) на C-концевом сайте, но не Tyr (Y) или Phe (F), как в соединениях #126 и #135.
Таблица 9. Эффекты Ntls и Ctls на чистоту антитела (фрагмент Таблицы 7)
GSGSGS
GSGGSGG
SGSG
SGSGGGSGG
GSGM
GSGSGSGSP
DGGSGG
SGSGSGM
GSGSGSGS
PDGGSGG
GSGSGM
GSGG
GSGG
GQG
SGSGSPDG
GSGG
SGSGSGNR
PSG
SGSGSDG
GSGG
GSGSGF
GSGSGSPD
GGSGG
SGSGSGF
SGSGSGSP
DGGSGG
SGSGSGGF
NPNPGG
PNPGST
NPNPNPG
SGG
NPNPGST
NPNPNSPD
GGSGG
PNPNPGST
NPNPNSPD
GGSGG
PNPNPGST
NPNPNPD
GGSGG
NPHVDVW
GQG
NPNPNSPD
GGSGG
NPNPHVD
VWGQG
PNPNPNPN
GGSGG
NPNPNVF
VNHKPDG
GSGG
KKVEGST
NVNHKP
DGGSGG
KKVEGGST
SNVNHKP
DGGSGG
KKAEYFQ
HWGQG
LAITGPD
GGSGG
SKSGGST
LAITGPD
GGSGG
SKSGGGST
EKEKVST
AVGG
PKEKEK
EKVG
HQSPTPG
GSGG
KSLAST
HQAPGEG
GSGG
SLAST
HQAPGEG
GSGG
KSLAST
HPTPGEG
GSGG
KSLAST
HQSPTPG
GSGG
KSLAST
HQAPGSG
GSGG
KSLAST
HQAPSPG
STGG
KSLAST
HQAPTSG
GSGG
KSLAST
VKLELG
HRAPDG
GSGG
RSEKLT
GVVF
VKLELG
HRPDG
GSGG
KLTGVVF
LELGHRAP
DGGSGG
SEKGVVF
KLELGHR
PDGGSGG
EKLTYF
QHWGQG
VQVKLEL
GHRPDG
GSGG
EKLTFNY
FQHWGQG
NVRAPD
GGSGG
AIGGST
AVVNVR
APDGGS
GG
IAIWTT
GST
VNVRAD
GGSGG
AIGGST
IEILDRH
PDGGSGG
PISNGSG
FVVAM
IEILDRHP
DGGSGG
PISNGSG
FVVAM
FILPIEV
YGGSGG
DYDLFG
VVF
FILPIEVY
PDGGSGG
DYDLFG
VVF
FILPIEV
YFPDGG
SGG
RFDYDL
FGVVF
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
3 N-концевая последовательность соответствует ближайшей соседней N-концевой аминокислоте от вставленного натрийуретического пептида, плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком вставленного натрийуретического пептида
4 C-концевая последовательность соответствует аминокислотному удлинению, присутствующему между последним аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней C-концевой эталонной аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота
Пример 7. Изотипы IgG1, IgG2 и IgG4 обеспечивают в равной степени подходящие каркасы антител
Соединения 9, 33, 65, 91, 127 и 191 (человеческий IgG1 TPP-10294, TPP-10277, TPP-10279, TPP-10282, TPP-10269 и TPP-10355, соответственно) были созданы на основе различных изотипов IgG. Очищенные образцы соединений тестировали, как описано в примере 3, в четырехкратных сериях разведений на стабильных клетках hNPRA-CHO k1. Активности привитых ANP конструкций изотипов IgG2 и IgG4 человека (например, соединения 9 IgG4 TPP-10992) аналогичны их соответствующему изотипу IgG1, как графически изображено на Фиг. 12
Пример 8. Человеческие и нечеловеческие IgG обеспечивают в равной степени подходящие каркасы антител
Соединение 9 (человеческий IgG1 TPP-10294 и IgG4 TPP-10992) и соединение 117 (человеческий IgG1 TPP-5665) были получены на основе изотипов нечеловеческого IgG. Очищенные образцы соединений тестировали, как описано в примере 3, в четырехкратных сериях разведений на стабильных клетках hNPRA-CHO k1. Конструкции крысиного и мышиного изотипа с привитым ANP, например, соединение 9 крысиного IgG1 TPP-13992, показали активность, аналогичную их соответствующему изотипу человеческого IgG (Фиг. 13).
Пример 9. Человеческие IgG, содержащие различные последовательности зародышевой линии, обеспечивают одинаково подходящие каркасы антител
Были сконструированы 22 дополнительных антитела IgG4 с привитыми ANP (соединения A - S). В каждом случае ANP был включен в CDRH1. Тяжелые цепи этих конструкций содержат различные последовательности HV и CDRH3 и были спарены с различными легкими цепями лямбда или каппа. Структура соединений A - S представлена в таблицах 10 и 11.
Таблица 10. Конструирование ANP-привитых конструкций антител A - S
1 Число аминокислотных остатков, присутствующих между соответствующим N-концевым эталонным аминокислотным остатком и первой аминокислотой вставленного натрийуретического пептида;
2 Число аминокислотных остатков, присутствующих между последней аминокислотой вставленного натрийуретического пептида и соответствующим C-концевым эталонным аминокислотным остатком
3 N-концевая последовательность соответствует ближайшей соседней N-концевой аминокислоте от вставленного натрийуретического пептида, плюс аминокислотное удлинение, присутствующее между указанной эталонной аминокислотой и первым аминокислотным остатком вставленного натрийуретического пептида
4 C-концевая последовательность соответствует аминокислотному удлинению, присутствующему между последним аминокислотным остатком вставленного натрийуретического пептида и ближайшей соседней C-концевой эталонной аминокислотой от вставленного натрийуретического пептида, плюс указанная эталонная аминокислота
Таблица 11. Конструирование ANP-привитых конструкций антител A - S
Очищенные образцы соединений конструкций на основе IgG каркаса A - S, содержащие различные последовательности зародышевой линии, тестировали, как описано в Примере 3, в четырехкратных сериях разведений на стабильных клетках hNPRA-CHO k1. Примерные данные по активности графически изображены на Фиг. 14.
Пример 10. CNP-привитой IgG защищает от индуцированной проницаемости эндотелиального барьера
Проницаемость эндотелиального монослоя оценивали путем измерения импеданса в реальном времени с помощью системы xCELLigence RTCA с использованием микротитровальных луночных планшетов, покрытых микроэлектродами (E-планшеты). Изменения относительного импеданса выражали в виде значений безразмерного клеточного индекса (CI).
Первичные эндотелиальные клетки легочной артерии человека (HPAEC) высевали при низких пассированиях на Е-планшеты, предварительно покрытые коллагеном. После образования плотного монослоя и клеточного барьера с постоянными значениями CI, HPAEC предварительно обрабатывали указанными концентрациями соединения TPP-12899 или соответствующей конструкцией антитела отрицательного контроля TPP-5657, с последующим нарушением барьера EC разрушающими агонистами LPS (200 нг/мл), IL-1β (0,5 нг/мл) или тромбин (2 Ед/мл). CI регистрировали каждые 10 минут для отслеживания воздействия на рост клеток и проницаемость монослоя. Все индексы клеток были нормализованы в последней точке регистрации перед нанесением тестируемого вещества (=нормализованный CI).
Эксперименты проводили при n=4 с 3 техническими повторениями в каждом случае. Результаты выражали как среднее значение±SEM. Данные были статистически проанализированы с использованием однофакторного дисперсионного анализа с последующим многократным пост-тестом Сидака; Значения p<0,05 считались значимыми.
На Фиг. 15 графически изображено влияние на проницаемость эндотелиального монослоя, выраженное в виде значений индекса клеток. Как показано на Фиг. 15, предварительная обработка человеческих эндотелиальных монослойных культур ТРР-12899 защищала от индуцированной проницаемости эндотелиального барьера дозозависимым образом. Это не зависело от применяемого агента, разрушающего барьер; как при быстром и сильном действии тромбина, так и при длительных провоспалительных стимулах наблюдались значительные эффекты LPS и IL-1β. Соответствующий отрицательный контроль не показал эффекта.
Пример 11. Долгосрочные эффекты ANP -привитого IgG на крысиной модели хронической сердечной недостаточности (TGR(mRenR2)27
Крысиная модель TGR (mRenR2) 27 показывает гипертензию и эндотелиальную дисфункцию, а также повреждение органов-мишеней. Использовали самцов ренин-трансгенных крыс (Ganten D., Nature. 1990; 344 (6266): 541-4) в возрасте 8 недель. Неселективный ингибитор синтетаз оксида азота L-NAME (метиловый сложный эфир Nω-нитро-L-аргинина) хронически вводили с питьевой водой (20 мг/л) во всех исследуемых группах для индукции эндотелиальной дисфункции. TPP-13992, крысиный аналог IgG1 TPP-10294, использованный в примере 8, и TPP-10155, контрольное антитело изотипа IgG1 крысы, вводили один раз в неделю внутрибрюшинно. Оценивали массу тела и выживаемость. Группу плацебо обрабатывали носителем (PBS), а здоровую контрольную группу обрабатывали пищей с каптоприлом после отлучения от груди. Пищу и воду давали по желанию. Проводили ежедневное наблюдение за поведением и общим состоянием здоровья животных. По окончании эксперимента (14 неделя) крысам вводили анестезию. Затем крыс обескровливали и сердце извлекали из грудной полости для анализа. В конце исследования собирали мочу для определения различных параметров мочи, например, соотношение белок/креатинин в моче. Фиг. 16 графически изображает терапевтические эффекты TPP-13992 на выживаемость, увеличение массы тела, соотношение белок/креатинин в моче и массу левого предсердия.
Пример. 12. Гемодинамические эффекты ANP-привитого IgG у здоровых собак породы бигль
Влияния TPP-10992 на сердечно-сосудистые параметры и параметры ЭКГ после однократного подкожного введения оценивали в первичном фармакодинамическом исследовании на гончих собаках, находящихся в сознании, с телеметрическим оборудованием.
Телеметрические устройства (DSI™, США) были имплантированы хирургическим путем для измерения кровяного давления, а также частоты сердечных сокращений, после чего последовал период восстановления, позволяющий закрыть рану. В день исследования были активированы телеметрические датчики для непрерывных гемодинамических измерений. Передаваемые сигналы собирали приемниками телеметрии, расположенными в помещении для животных. Все собранные данные были обработаны программой сбора данных и усреднены за заранее определенный период в 12 часов. В качестве носителя для TPP-10992 использовали NaCl (0,9%), а дозы 0,1 мг/кг, 0,3 мг/кг и 1,0 мг/кг массы тела применяли посредством подкожной инъекции.
Результаты представлены графически на Фиг. 17. У здоровых собак TPP-10992 показал дозозависимое и продолжительное (>5 дней) снижение артериального давления, которое было значительным при дозе 1,0 мг/кг подкожно (по сравнению с плацебо). Никакого влияния на частоту сердечных сокращений не наблюдалось.
--->
Перечень последовательностей
<110> Bayer AG
<120> АНТИТЕЛА С ПРИВИТЫМ ПРЕДСЕРДНЫМ НАТРИЙУРЕТИЧЕСКИМ ПЕПТИДОМ
<130> BHC 18 1 016
<160> 447
<170> PatentIn version 3.5
<210> 1
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 1
Ser Tyr Ala Met Ser Trp Val Arg Gln Ala
1 5 10
<210> 2
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 2
Thr Tyr Ile Ser Asn Val Asn His Lys Pro
1 5 10
<210> 3
<211> 9
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 3
Ser Asn Thr Lys Val Asp Lys Lys Val
1 5
<210> 4
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 4
Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly
1 5 10
<210> 5
<211> 9
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 5
Asp Arg Phe Ser Gly Ser Lys Ser Gly
1 5
<210> 6
<211> 15
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 6
Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu Thr Ala Pro
1 5 10 15
<210> 7
<211> 14
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 7
Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
1 5 10
<210> 8
<211> 17
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 8
Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp Gly
1 5 10 15
Gln
<210> 9
<211> 12
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 9
Ser Val Val Val Thr Ser His Gln Ala Pro Gly Glu
1 5 10
<210> 10
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 10
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala
1 5 10
<210> 11
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 11
Gln Val Lys Leu Glu Leu Gly His Arg Ala
1 5 10
<210> 12
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 12
Val Asn His Leu Arg Ser Glu Lys Leu Thr
1 5 10
<210> 13
<211> 7
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 13
Ala Val Val Asn Val Arg Ala
1 5
<210> 14
<211> 7
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 14
Lys Gly Asp Lys Ile Ala Ile
1 5
<210> 15
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 15
Val Pro Lys Glu Lys Glu Lys Glu Lys Val
1 5 10
<210> 16
<211> 12
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 16
Ala Thr Lys Ala Val Ser Val Leu Lys Gly Asp Gly
1 5 10
<210> 17
<211> 9
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 17
Gln Gly Ile Ile Asn Phe Glu Gln Lys
1 5
<210> 18
<211> 11
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 18
Gly Pro Val Lys Val Trp Gly Ser Ile Lys Gly
1 5 10
<210> 19
<211> 7
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 19
Tyr Glu Lys Glu Lys Glu Lys
1 5
<210> 20
<211> 10
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 20
Gly Gly Ser Thr Pro Leu Lys Ser Leu Ala
1 5 10
<210> 21
<211> 14
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 21
Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
1 5 10
<210> 22
<211> 17
<212> PRT
<213> искусственная
<220>
<223> линкерная последовательность
<400> 22
Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp Gly
1 5 10 15
Gln
<210> 23
<211> 28
<212> PRT
<213> человека
<400> 23
Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile Gly
1 5 10 15
Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
20 25
<210> 24
<211> 28
<212> PRT
<213> человека
<400> 24
Met Val Gln Gly Ser Gly Cys Phe Gly Arg Lys Met Asp Arg Ile Ser
1 5 10 15
Ser Ser Ser Gly Leu Gly Cys Lys Val Leu Arg Arg
20 25
<210> 25
<211> 22
<212> PRT
<213> человека
<400> 25
Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu Asp Arg Ile Gly Ser
1 5 10 15
Met Ser Gly Leu Gly Cys
20
<210> 26
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 26
Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Gly
1 5 10 15
<210> 27
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 27
Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Pro Asp Gly Gly Ser Gly Gly
20
<210> 28
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 28
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 29
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 29
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 30
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 30
Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro Gly Ser Gly
1 5 10 15
Gly
<210> 31
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 31
Ser Gly Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 32
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 32
Ala Lys Val His Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 33
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 33
Ala Ala Trp Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Gly Gly
1 5 10 15
Ser Gly Gly
<210> 34
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 34
Ala Lys Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 35
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 35
Ser Gly Ser Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 36
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 36
Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 37
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 37
Gly Val Pro Lys Glu Lys Glu Lys Glu Lys Val Ser Thr Ala Val Gly
1 5 10 15
Gly
<210> 38
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (без эталонной aa)
<400> 38
Ser Val Val Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly Ser Gly
1 5 10 15
Gly
<210> 39
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 39
Gly Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly
1 5 10
<210> 40
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 40
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10
<210> 41
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 41
Gly Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro
1 5 10 15
Ser
<210> 42
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 42
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
<210> 43
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 43
Gly Ser Asn Pro Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser
1 5 10
<210> 44
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 44
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Gly Ser
1 5 10 15
<210> 45
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 45
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro His Val Asp Val Trp
1 5 10 15
Gly Gln
<210> 46
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 46
Gly Ser Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Val
1 5 10
<210> 47
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 47
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp
1 5 10 15
Gly Gln
<210> 48
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 48
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Gly Ser
1 5 10
<210> 49
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 49
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Ser
1 5 10
<210> 50
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 50
Gly Ser Ala Pro Leu Glu Val Pro Lys Glu Lys Glu Lys Glu Lys Val
1 5 10 15
<210> 51
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (без эталонной aa)
<400> 51
Gly Gly Ser Thr Pro Leu Lys Ser Leu Ala Ser
1 5 10
<210> 52
<211> 54
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 52
Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Gly Ser
1 5 10 15
Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile Gly Ala
20 25 30
Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Gly Ser Gly Gly
35 40 45
Ser Gly Ser Gly Ser Gly
50
<210> 53
<211> 65
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 53
Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Pro Asp Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly
20 25 30
Gly Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser
35 40 45
Phe Arg Tyr Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
50 55 60
Gly
65
<210> 54
<211> 64
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 54
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp
20 25 30
Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly
35 40 45
Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro Ser
50 55 60
<210> 55
<211> 63
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 55
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
20 25 30
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
35 40 45
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
50 55 60
<210> 56
<211> 59
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(wo ref
aas)
<400> 56
Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro Gly Ser Gly
1 5 10 15
Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile
20 25 30
Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser Asn
35 40 45
Pro Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser
50 55
<210> 57
<211> 63
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 57
Ser Gly Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
20 25 30
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
35 40 45
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Gly Ser
50 55 60
<210> 58
<211> 66
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 58
Ala Lys Val His Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
20 25 30
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
35 40 45
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro His Val Asp Val Trp
50 55 60
Gly Gln
65
<210> 59
<211> 61
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 59
Ala Ala Trp Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Gly Gly
1 5 10 15
Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp
20 25 30
Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly
35 40 45
Ser Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Val
50 55 60
<210> 60
<211> 66
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 60
Ala Lys Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
20 25 30
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
35 40 45
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp
50 55 60
Gly Gln
65
<210> 61
<211> 61
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 61
Ser Gly Ser Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp
20 25 30
Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly
35 40 45
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Gly Ser
50 55 60
<210> 62
<211> 59
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 62
Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg
20 25 30
Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser
35 40 45
Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Ser
50 55
<210> 63
<211> 61
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 63
Gly Val Pro Lys Glu Lys Glu Lys Glu Lys Val Ser Thr Ala Val Gly
1 5 10 15
Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile
20 25 30
Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser Ala
35 40 45
Pro Leu Glu Val Pro Lys Glu Lys Glu Lys Glu Lys Val
50 55 60
<210> 64
<211> 56
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность-NP-C-концевая последовательность
(без
эталонной aas)
<400> 64
Ser Val Val Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly Ser Gly
1 5 10 15
Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile
20 25 30
Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Gly Ser
35 40 45
Thr Pro Leu Lys Ser Leu Ala Ser
50 55
<210> 65
<211> 447
<212> PRT
<213> человека
<400> 65
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Leu Thr Gly Ala Glu Tyr Phe Gln His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 66
<211> 217
<212> PRT
<213> человека
<400> 66
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 67
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 67
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Ile
115 120 125
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 68
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 68
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
115 120 125
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 69
<211> 504
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 69
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
50 55 60
Pro Asp Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly
65 70 75 80
Gly Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser
85 90 95
Phe Arg Tyr Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
100 105 110
Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
115 120 125
Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
130 135 140
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu
145 150 155 160
Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
165 170 175
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
180 185 190
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
195 200 205
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
210 215 220
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
225 230 235 240
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
245 250 255
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
260 265 270
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
275 280 285
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
290 295 300
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
305 310 315 320
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
325 330 335
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
340 345 350
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
355 360 365
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
370 375 380
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
385 390 395 400
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
405 410 415
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
420 425 430
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
435 440 445
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
450 455 460
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
465 470 475 480
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
485 490 495
Lys Ser Leu Ser Leu Ser Pro Gly
500
<210> 70
<211> 504
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 70
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Ser
50 55 60
Pro Asp Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly
65 70 75 80
Gly Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser
85 90 95
Phe Arg Tyr Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro
100 105 110
Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
115 120 125
Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
130 135 140
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu
145 150 155 160
Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
165 170 175
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
180 185 190
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
195 200 205
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
210 215 220
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
225 230 235 240
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
245 250 255
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
260 265 270
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
275 280 285
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
290 295 300
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
305 310 315 320
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
325 330 335
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
340 345 350
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
355 360 365
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
370 375 380
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
385 390 395 400
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
405 410 415
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
420 425 430
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
435 440 445
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
450 455 460
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
465 470 475 480
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
485 490 495
Lys Ser Leu Ser Leu Ser Pro Gly
500
<210> 71
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 71
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val His Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
115 120 125
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
130 135 140
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 72
<211> 504
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 72
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Gly
20 25 30
Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly Ser Gly Gly
35 40 45
Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile Gly
50 55 60
Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser Tyr Gly
65 70 75 80
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Met Ser Trp Val Arg Gln
85 90 95
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly
100 105 110
Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
115 120 125
Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
130 135 140
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu
145 150 155 160
Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
165 170 175
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
180 185 190
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
195 200 205
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
210 215 220
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
225 230 235 240
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
245 250 255
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
260 265 270
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
275 280 285
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
290 295 300
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
305 310 315 320
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
325 330 335
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
340 345 350
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
355 360 365
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
370 375 380
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
385 390 395 400
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
405 410 415
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
420 425 430
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
435 440 445
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
450 455 460
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
465 470 475 480
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
485 490 495
Lys Ser Leu Ser Leu Ser Pro Gly
500
<210> 73
<211> 500
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 73
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro
50 55 60
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
65 70 75 80
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
85 90 95
Gly Ser Asn Pro Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser Thr Tyr
100 105 110
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
115 120 125
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu Tyr Phe Gln His
145 150 155 160
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
165 170 175
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
180 185 190
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
195 200 205
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
210 215 220
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
225 230 235 240
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
245 250 255
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
260 265 270
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
275 280 285
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
290 295 300
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
305 310 315 320
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
325 330 335
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
340 345 350
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
355 360 365
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
370 375 380
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
385 390 395 400
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
405 410 415
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
420 425 430
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
435 440 445
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
450 455 460
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
465 470 475 480
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
485 490 495
Leu Ser Pro Gly
500
<210> 74
<211> 502
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 74
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Thr Tyr Ile Ser Asn Val Asn His Lys Pro
50 55 60
Asp Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly
65 70 75 80
Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe
85 90 95
Arg Tyr Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Gly Ser
100 105 110
Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
115 120 125
Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
130 135 140
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu Tyr Phe
145 150 155 160
Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
165 170 175
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
180 185 190
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
195 200 205
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
210 215 220
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
225 230 235 240
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
245 250 255
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
260 265 270
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
275 280 285
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
290 295 300
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
305 310 315 320
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
325 330 335
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
340 345 350
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
355 360 365
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
370 375 380
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
385 390 395 400
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
405 410 415
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
420 425 430
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
435 440 445
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
450 455 460
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
465 470 475 480
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
485 490 495
Leu Ser Leu Ser Pro Gly
500
<210> 75
<211> 500
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 75
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp
50 55 60
Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg
65 70 75 80
Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg
85 90 95
Tyr Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Ser Thr Tyr
100 105 110
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
115 120 125
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu Tyr Phe Gln His
145 150 155 160
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
165 170 175
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
180 185 190
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
195 200 205
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
210 215 220
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
225 230 235 240
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
245 250 255
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
260 265 270
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
275 280 285
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
290 295 300
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
305 310 315 320
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
325 330 335
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
340 345 350
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
355 360 365
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
370 375 380
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
385 390 395 400
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
405 410 415
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
420 425 430
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
435 440 445
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
450 455 460
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
465 470 475 480
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
485 490 495
Leu Ser Pro Gly
500
<210> 76
<211> 501
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 76
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Gly
20 25 30
Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly Ser Gly Gly
35 40 45
Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile Gly
50 55 60
Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser Tyr Gly
65 70 75 80
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Met Ser Trp Val Arg Gln
85 90 95
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly
100 105 110
Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
115 120 125
Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
130 135 140
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu
145 150 155 160
Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
165 170 175
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
180 185 190
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
195 200 205
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
210 215 220
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
225 230 235 240
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
245 250 255
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
260 265 270
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
275 280 285
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
290 295 300
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
305 310 315 320
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
325 330 335
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
340 345 350
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
355 360 365
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
370 375 380
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
385 390 395 400
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
405 410 415
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
420 425 430
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
435 440 445
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
450 455 460
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
465 470 475 480
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
485 490 495
Ser Leu Ser Leu Gly
500
<210> 77
<211> 493
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 77
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Gly
20 25 30
Ser Gly Ser Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe
35 40 45
Gly Gly Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn
50 55 60
Ser Phe Arg Tyr Gly Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Met
65 70 75 80
Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ala
85 90 95
Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly
100 105 110
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
115 120 125
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys
130 135 140
Leu Thr Gly Ala Glu Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val
145 150 155 160
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
165 170 175
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
180 185 190
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
195 200 205
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
210 215 220
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
225 230 235 240
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
245 250 255
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
260 265 270
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
275 280 285
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
290 295 300
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
305 310 315 320
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
325 330 335
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
340 345 350
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
355 360 365
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
370 375 380
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
385 390 395 400
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
405 410 415
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
420 425 430
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
435 440 445
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
450 455 460
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
465 470 475 480
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
485 490
<210> 78
<211> 497
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 78
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Val Val Val Thr Ser His Gln Ala Pro Gly Glu Gly
50 55 60
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
65 70 75 80
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
85 90 95
Gly Gly Ser Thr Pro Leu Lys Ser Leu Ala Ser Thr Tyr Tyr Ala Asp
100 105 110
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr
115 120 125
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
130 135 140
Tyr Cys Ala Lys Leu Thr Gly Ala Glu Tyr Phe Gln His Trp Gly Gln
145 150 155 160
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
165 170 175
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
180 185 190
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
195 200 205
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
210 215 220
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
225 230 235 240
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
245 250 255
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
260 265 270
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
275 280 285
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
290 295 300
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
305 310 315 320
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
325 330 335
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
340 345 350
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
355 360 365
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
370 375 380
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
385 390 395 400
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
405 410 415
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
420 425 430
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
435 440 445
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
450 455 460
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
465 470 475 480
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
485 490 495
Gly
<210> 79
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 79
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly Arg Met
115 120 125
Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe Arg Tyr
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 80
<211> 267
<212> PRT
<213> искусственная
<220>
<223> NP привитая LC
<400> 80
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asn Pro Asn
85 90 95
Pro Asn Pro Asn Pro Asn Pro Asn Gly Gly Ser Gly Gly Ser Leu Arg
100 105 110
Arg Ser Ser Cys Phe Gly Gly Arg Met Asp Arg Ile Gly Ala Gln Ser
115 120 125
Gly Leu Gly Cys Asn Ser Phe Arg Tyr Gly Ser Asn Pro Asn Pro Asn
130 135 140
Pro Asn Pro Asn Pro Asn Val Phe Gly Ser Gly Thr Lys Val Thr Val
145 150 155 160
Leu Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser
165 170 175
Ser Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser
180 185 190
Asp Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser
195 200 205
Pro Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn
210 215 220
Asn Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp
225 230 235 240
Lys Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr
245 250 255
Val Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
260 265
<210> 81
<211> 274
<212> PRT
<213> искусственная
<220>
<223> NP привитая LC
<400> 81
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro
50 55 60
Asp Gly Gly Ser Gly Gly Ser Leu Arg Arg Ser Ser Cys Phe Gly Gly
65 70 75 80
Arg Met Asp Arg Ile Gly Ala Gln Ser Gly Leu Gly Cys Asn Ser Phe
85 90 95
Arg Tyr Gly Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn
100 105 110
Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr
115 120 125
Ser Ala Ser Leu Ala Ile Thr Gly Leu Gln Ala Glu Asp Glu Ala Asp
130 135 140
Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser Leu Ser Gly Val Val Phe Gly
145 150 155 160
Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Lys Ala Ala Pro Ser
165 170 175
Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln Ala Asn Lys Ala
180 185 190
Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly Ala Val Thr Val
195 200 205
Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly Val Glu Thr Thr
210 215 220
Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala Ser Ser Tyr Leu
225 230 235 240
Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser Tyr Ser Cys Gln
245 250 255
Val Thr His Glu Gly Ser Thr Val Glu Lys Thr Val Ala Pro Thr Glu
260 265 270
Cys Ser
<210> 82
<211> 366
<212> ДНК
<213> искусственная
<220>
<223> NP привитая HC кодирующая конструкция
<400> 82
gaagtgcagc tgctggaaag cggcggaggc ctggtgcagc ctggcggatc tctgagactg 60
agctgtgccg ccagcggctt caccttcagc agctacgcca tgagctgggt gcgccaggcc 120
cctggaaaag gcctggaatg ggtgtccgcc atctctggca gcggcggcag cacctactac 180
gccgattctg tgaagggccg gttcaccatc agccgggaca acagcaagaa caccctgtac 240
ctgcagatga acagcctgcg ggccgaggac accgccgtgt actactgtac aagcgtgcac 300
caggaaacaa agaagtacca gagcagcccc gacggcggca gtggcggaag tctgagaaga 360
agctcc 366
<210> 83
<211> 525
<212> ДНК
<213> искусственная
<220>
<223> NP привитая HC кодирующая конструкция
<400> 83
gaagttcagc tgctggaatc tggcggcgga ctggttcaac ctggcggatc tctgagactg 60
agctgtgccg ccagcggctt tacatttggc agcggctctg gatctggctc cggaagcgga 120
tctcctgatg gtggaagcgg aggcagcctg agaagaagca gctgtttcgg cggcagaatg 180
gacagaatcg gcgcccaatc tggcctgggc tgcaacagct ttagatacgg cagctacggc 240
tccggcagtg gttccggtag tggctctgga atgagctggg ttcgacaggc ccctggcaaa 300
ggccttgaat gggtgtccgc catttctggc agcggaggct ctacctacta cgccgatagc 360
gtgaagggca gattcaccat cagccgggac aacagcaaga acaccctgta cctgcagatg 420
aactccctga gagccgagga caccgccgtg tactattgcg ccaaactgac aggcgccgag 480
tacttccagc attggggaca gggaaccctg gtcacagtct cttca 525
<210> 84
<211> 333
<212> ДНК
<213> человека
<400> 84
cagtctgtgc tgacacagcc tcctagtgtg tctggcgccc ctggccagag agtgaccatc 60
agctgtaccg gcagcagctc caacatcgga gccggctatg acgtgcactg gtatcagcag 120
ctgcctggca ccgcccccaa actgctgatc tacggcaaca gcaaccggcc cagcggcgtg 180
cccgatagat tttccggcag caagagcggc accagcgcca gcctggctat tactggactg 240
caggccgagg acgaggccga ctactactgc cagagctacg acagcagcct gagcggcgtg 300
gtgtttggcg gcggaacaaa gctgaccgtg cta 333
<210> 85
<211> 98
<212> PRT
<213> человека
<400> 85
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys
<210> 86
<211> 17
<212> PRT
<213> человека
<400> 86
Ala Glu Tyr Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser
1 5 10 15
Ser
<210> 87
<211> 329
<212> PRT
<213> человека
<400> 87
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly
325
<210> 88
<211> 99
<212> PRT
<213> человека
<400> 88
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Gly
<210> 89
<211> 12
<212> PRT
<213> человека
<400> 89
Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
1 5 10
<210> 90
<211> 106
<212> PRT
<213> человека
<400> 90
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 91
<211> 18
<212> PRT
<213> искусственная
<220>
<223> NP вариант
<220>
<221> misc_признак
<222> (1)..(1)
<223> Xaa может быть любой природной аминокислотой
<220>
<221> misc_признак
<222> (5)..(7)
<223> Xaa может быть любой природной аминокислотой
<220>
<221> misc_признак
<222> (11)..(13)
<223> Xaa может быть любой природной аминокислотой
<220>
<221> misc_признак
<222> (15)..(15)
<223> Xaa может быть любой природной аминокислотой
<400> 91
Xaa Cys Phe Gly Xaa Xaa Xaa Asp Arg Ile Xaa Xaa Xaa Ser Xaa Leu
1 5 10 15
Gly Cys
<210> 92
<211> 7
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 92
Ser Gly Phe Thr Phe Ser Ser
1 5
<210> 93
<211> 10
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 93
Ser Gly Phe Thr Phe Gly Ser Gly Ser Gly
1 5 10
<210> 94
<211> 6
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 94
Gly Ser Gly Ser Gly Met
1 5
<210> 95
<211> 13
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 95
Ser Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10
<210> 96
<211> 9
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 96
Ser Gly Ser Gly Ser Gly Ser Gly Met
1 5
<210> 97
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 97
Ser Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Gly
1 5 10 15
<210> 98
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 98
Gly Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Met
1 5 10
<210> 99
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 99
Ser Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Gly
1 5 10 15
Ser Gly Gly
<210> 100
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 100
Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly Met
1 5 10
<210> 101
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 101
Ser Pro Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 102
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 102
Gly Ser Gly Arg Glu Val Pro Ile Ser Asn Gly Ser Gly Phe Val Val
1 5 10 15
Ala Met
<210> 103
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 103
Ser Gly Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 104
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 104
Ser Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu
1 5 10 15
Leu Thr Ala Pro Arg
20
<210> 105
<211> 24
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 105
Ser Gly Phe Thr Phe Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10 15
Ser Pro Asp Gly Gly Ser Gly Gly
20
<210> 106
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 106
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Met
1 5 10 15
<210> 107
<211> 25
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 107
Ser Gly Phe Thr Phe Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys
1 5 10 15
Leu Arg Ala Leu Leu Thr Ala Pro Arg
20 25
<210> 108
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 108
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Met
1 5 10
<210> 109
<211> 4
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 109
Ile Ser Gly Ser
1
<210> 110
<211> 4
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 110
Gly Gly Ser Thr
1
<210> 111
<211> 8
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 111
Ile Ser Gly Ser Gly Ser Gly Ser
1 5
<210> 112
<211> 8
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 112
Gly Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 113
<211> 9
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 113
Ile Ser Gly Ser Gly Ser Gly Ser Gly
1 5
<210> 114
<211> 10
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 114
Gly Ser Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 115
<211> 11
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 115
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10
<210> 116
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 116
Gly Ser Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 117
<211> 12
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 117
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly
1 5 10
<210> 118
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 118
Gly Glu Lys Glu Lys Glu Lys Val Ser Thr Ala Val Gly Ser Thr
1 5 10 15
<210> 119
<211> 13
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 119
Ile Ser Gly Ser Ala Val Val Asn Gly Gly Ser Gly Gly
1 5 10
<210> 120
<211> 9
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 120
Gly Lys Ile Ala Ile Gly Gly Ser Thr
1 5
<210> 121
<211> 14
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 121
Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Gly Gly
1 5 10
<210> 122
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 122
Gly Ser Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser Thr
1 5 10
<210> 123
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 123
Ile Ser Gly Ser Val Val Val Thr Ser His Gly Gly Ser Gly Gly
1 5 10 15
<210> 124
<211> 10
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 124
Gly Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 125
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 125
Ile Ser Gly Ser Ala Val Val Asn Val Arg Gly Gly Ser Gly Gly
1 5 10 15
<210> 126
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 126
Gly Gly Asp Lys Ile Ala Ile Gly Gly Ser Thr
1 5 10
<210> 127
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 127
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Ser Gly Gly
1 5 10 15
<210> 128
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 128
Ile Ser Gly Leu Ala Val Gln Ile Arg Arg Gly Gly Ser Gly Gly
1 5 10 15
<210> 129
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 129
Gly Gly Ser Gly Arg Glu Thr Leu Thr Leu Tyr Val Gly Ser Thr
1 5 10 15
<210> 130
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 130
Ile Ser Gly Ser Ala Val Val Asn Val Arg Ala Gly Gly Ser Gly Gly
1 5 10 15
<210> 131
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 131
Ile Ser Gly Ser Tyr Ala Met Ser Trp Val Arg Gly Gly Ser Gly Gly
1 5 10 15
<210> 132
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 132
Gly Ser Tyr Ala Met Ser Trp Val Arg Gln Gly Ser Thr
1 5 10
<210> 133
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 133
Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro Gly Gly
1 5 10 15
<210> 134
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 134
Gly Ser Asn Pro Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser Thr
1 5 10 15
<210> 135
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 135
Ile Ser Gly Ser Ala Val Val Asn Val Arg Ala Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 136
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 136
Gly Ser Gly Asp Lys Ile Ala Ile Gly Gly Ser Thr
1 5 10
<210> 137
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 137
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 138
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 138
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly
1 5 10 15
Gly
<210> 139
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 139
Ile Ser Gly Ser Val Val Val Thr Ser His Gln Ala Pro Gly Ser Gly
1 5 10 15
Gly
<210> 140
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 140
Gly Ser Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr Gly Ser Thr
1 5 10 15
<210> 141
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 141
Ile Ser Gly Arg Tyr Asn Ile Leu Lys Ile Gln Lys Val Gly Ser Gly
1 5 10 15
Gly
<210> 142
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 142
Gly Gly Ser Gly Glu Tyr Leu Ile Thr Tyr Gln Ile Met Gly Ser Thr
1 5 10 15
<210> 143
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 143
Ile Ser Gly Arg Gln Leu Leu Phe Cys Arg Val Thr Leu Gly Ser Gly
1 5 10 15
Gly
<210> 144
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 144
Gly Gly Ser Gly Glu Gln Ala Tyr Pro Glu Tyr Leu Ile Thr Tyr Gly
1 5 10 15
Ser Thr
<210> 145
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 145
Ile Ser Val Val Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly Ser
1 5 10 15
Gly Gly
<210> 146
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 146
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Ser Thr
1 5 10
<210> 147
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 147
Ile Ser Gly Val Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly Ser
1 5 10 15
Gly Gly
<210> 148
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 148
Gly Glu Lys Lys Lys Leu Lys Ser Leu Gly Ser Thr
1 5 10
<210> 149
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 149
Gly Glu Lys Lys Lys Leu Lys Ser Gly Gly Ser Thr
1 5 10
<210> 150
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 150
Ile Ser Gly Ser Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly Ser
1 5 10 15
Gly Gly
<210> 151
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 151
Gly Glu Lys Lys Lys Gly Lys Ser Gly Gly Ser Thr
1 5 10
<210> 152
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 152
Ile Ser Val Val Val Thr Ser His Gln Ala Pro Gly Ser Gly Gly Ser
1 5 10 15
Gly Gly
<210> 153
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 153
Ile Ser Val Val Val Thr Ser His Gln Ala Pro Thr Ser Gly Gly Ser
1 5 10 15
Gly Gly
<210> 154
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 154
Ile Ser Val Val Val Thr Ser His Gln Ser Pro Thr Pro Gly Gly Ser
1 5 10 15
Gly Gly
<210> 155
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 155
Gly Gly Ser Thr Pro Leu Lys Ser Leu Ala Ser Thr
1 5 10
<210> 156
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 156
Gly Ser Thr Pro Lys Leu Lys Ser Leu Ala Ser Thr
1 5 10
<210> 157
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 157
Ile Ser Val Val Val Thr Ser His Pro Thr Pro Gly Glu Gly Gly Ser
1 5 10 15
Gly Gly
<210> 158
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 158
Ile Ser Val Val Val Thr Ser His Gln Ala Pro Ser Pro Gly Ser Thr
1 5 10 15
Gly Gly
<210> 159
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 159
Ile Ser Val Val Val Thr Ser His Gln Ala Asn Gly Ser Gly Gly Ser
1 5 10 15
Gly Gly
<210> 160
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 160
Ile Ser Gly Ser Ala Val Val Asn Val Arg Ala Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 161
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 161
Gly Ser Lys Gly Asp Lys Ile Ala Ile Gly Gly Ser Thr
1 5 10
<210> 162
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 162
Ile Ser Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 163
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 163
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Ser Thr
1 5 10
<210> 164
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 164
Ile Ser Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 165
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 165
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Ser Thr
1 5 10
<210> 166
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 166
Ile Ser Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu Thr Ala
1 5 10 15
Pro Gly
<210> 167
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 167
Gly Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 168
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 168
Ile Ser Gly Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Gly Gly Ser
1 5 10 15
Gly Gly
<210> 169
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 169
Gly Ser Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Gly Ser Thr
1 5 10 15
<210> 170
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 170
Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro Gly Ser
1 5 10 15
Gly Gly
<210> 171
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 171
Ile His Pro Leu Gln Asn Arg Trp Ala Leu Trp Phe Phe Lys Gly Ser
1 5 10 15
Gly Gly
<210> 172
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 172
Gly Gly Ser Gly Asn Leu Arg Leu Ile Ser Lys Phe Asp Thr Val Thr
1 5 10 15
<210> 173
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 173
Ile Ser Gly Ser Val Thr Ile Phe Ser Leu Ala Thr Asn Glu Gly Ser
1 5 10 15
Gly Gly
<210> 174
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 174
Gly Gly Ser Gly Lys Thr Thr Trp His Arg Ile Ser Val Phe Gly Gly
1 5 10 15
Ser Thr
<210> 175
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 175
Ile Tyr Leu Glu Gly Lys Ile Asp Tyr Gly Glu Tyr Met Asp Gly Ser
1 5 10 15
Gly Gly
<210> 176
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 176
Gly Gly Ser Asn Val Arg Arg Gln Ala Thr Thr Ile Ile Ala Asp Asn
1 5 10 15
Ile Thr
<210> 177
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 177
Ile Ser Gly Ser Val Gln Gly Ile Ile Asn Phe Glu Gln Lys Gly Ser
1 5 10 15
Gly Gly
<210> 178
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 178
Gly Gly Ser Gly Pro Val Lys Val Trp Gly Ser Ile Lys Gly Gly Gly
1 5 10 15
Ser Thr
<210> 179
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 179
Ile Ser Gly Val Val Val Thr Ser His Gln Ala Pro Gly Glu Gly Gly
1 5 10 15
Ser Gly Gly
<210> 180
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 180
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Gly Ser Thr
1 5 10
<210> 181
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 181
Ile Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 182
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 182
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Ser Thr
1 5 10
<210> 183
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 183
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 184
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 184
Gly Ser Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 185
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 185
Ile Ser Gly Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 186
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 186
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Ser Thr
1 5 10
<210> 187
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 187
Ile Ser Gly Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 188
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 188
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Ser Thr
1 5 10
<210> 189
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 189
Ile Ser Gly Ser Val Val Val Thr Ser His Gln Ala Pro Gly Gly Gly
1 5 10 15
Ser Gly Gly
<210> 190
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 190
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr Gly Ser Thr
1 5 10
<210> 191
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 191
Gly Glu Lys Pro Lys Pro Lys Pro Leu Ala Tyr Gly Ser Thr
1 5 10
<210> 192
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 192
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Ser Thr
1 5 10
<210> 193
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 193
Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Pro Gly Gly
1 5 10 15
Ser Gly Gly
<210> 194
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 194
Ile Ser Gly Asp Ile Tyr Leu Ala Ile Asn Ile Thr Asn Gly Glu Gly
1 5 10 15
Ser Gly Gly
<210> 195
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 195
Gly Gly Ser Gly Asp Ile Tyr Leu Ala Ile Asn Ile Thr Asn Gly Glu
1 5 10 15
Ser Thr
<210> 196
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 196
Ile Ser Gly Ser Ala Thr Lys Ala Val Ser Val Leu Lys Gly Asp Gly
1 5 10 15
Ser Gly Gly
<210> 197
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 197
Gly Gly Ser Gly Val Gln Gly Ile Ile Asn Phe Glu Gln Lys Gly Gly
1 5 10 15
Ser Thr
<210> 198
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 198
Ile Ser Gly Ser Val Pro Lys Glu Lys Glu Lys Glu Lys Val Ser Thr
1 5 10 15
Ala Val Gly Gly
20
<210> 199
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 199
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10
<210> 200
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 200
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10 15
<210> 201
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 201
Ile Ser Gly Ser Ser Gly Ala Val Val Asn Val Arg Ala Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 202
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 202
Gly Ser Lys Gly Asp Lys Ile Ala Ile Trp Thr Thr Gly Ser Thr
1 5 10 15
<210> 203
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 203
Ile Ser Gly Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 204
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 204
Ile Ser Gly Ser Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 205
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 205
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Gly Ser Thr
1 5 10 15
<210> 206
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 206
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 207
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 207
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 208
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 208
Gly Ser Tyr Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10 15
<210> 209
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 209
Ile Ser Thr Gln Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 210
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 210
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Thr
1 5 10 15
<210> 211
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 211
Ile Ser Gly Ser Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 212
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 212
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Gly Ser Thr
1 5 10 15
<210> 213
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 213
Ile Ser Gly Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 214
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 214
Gly Ser Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Gly Ser Thr
1 5 10 15
<210> 215
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 215
Ile Ser Ala Val Gln Val Lys Leu Glu Leu Gly His Arg Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 216
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 216
Gly Ser Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Ser Thr
1 5 10 15
<210> 217
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 217
Ile Ser Gly Phe Ile Leu Pro Ile Glu Val Tyr Phe Lys Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 218
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 218
Gly Ser Pro Arg Lys Val Arg Phe Asp Tyr Asp Leu Phe Ser Thr
1 5 10 15
<210> 219
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 219
Ile Ser Gly Ser Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 220
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 220
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Gly Ser Thr
1 5 10 15
<210> 221
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 221
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10 15
<210> 222
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 222
Ile Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu
1 5 10 15
Thr Ala Pro Arg
20
<210> 223
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 223
Gly Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Ser Thr
1 5 10 15
<210> 224
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 224
Ile Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu
1 5 10 15
Thr Ala Pro Gly
20
<210> 225
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 225
Gly Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Thr
1 5 10 15
<210> 226
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 226
Ile Ser Gly Ser Ser Asp Lys Thr His Thr Ser Pro Pro Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 227
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 227
Gly Ser Lys Thr His Thr Ser Pro Pro Ser Pro Gly Gly Ser Thr
1 5 10 15
<210> 228
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 228
Ile Ser Gly Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 229
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 229
Gly Ser Tyr Ser Ser Tyr Ala Met Ser Trp Val Arg Gly Gly Ser Thr
1 5 10 15
<210> 230
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 230
Gly Ser Tyr Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Gly Ser Thr
1 5 10 15
<210> 231
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 231
Ile Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 232
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 232
Ile Ser Gly Ser Pro Asn Pro Asn Pro Asn Pro Asn Pro Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 233
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 233
Gly Ser Tyr Pro Asn Pro Asn Pro Asn Pro Asn Pro Ser Gly Ser Thr
1 5 10 15
<210> 234
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 234
Ile Ser Gly Pro Asn Pro Asn Lys Asn Pro Asn Pro Asn Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 235
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 235
Gly Ser Tyr Asn Pro Asn Glu Asn Pro Asn Pro Asn Pro Gly Ser Thr
1 5 10 15
<210> 236
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 236
Ile Ser Gly Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 237
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 237
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Gly Ser Thr
1 5 10 15
<210> 238
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 238
Ile Ser Gly Ser Val Val Val Thr Ser His Gln Ala Pro Gly Gly Ser
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 239
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 239
Ile Ser Gly Ser Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 240
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 240
Gly Ser Gly Arg Glu Val Pro Ile Ser Asn Gly Ser Gly Gly Ser Thr
1 5 10 15
<210> 241
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 241
Ile Ser Gly Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 242
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 242
Ile Ser Pro Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 243
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 243
Gly Ser Gly Arg Glu Val Pro Ile Ser Asn Gly Ser Gly Phe Ser Thr
1 5 10 15
<210> 244
<211> 11
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 244
Cys Ala Lys Ser Pro Asp Gly Gly Ser Gly Gly
1 5 10
<210> 245
<211> 4
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 245
Gly Ser Tyr Gly
1
<210> 246
<211> 9
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 246
Gly Ser Tyr Gln His Trp Gly Gln Gly
1 5
<210> 247
<211> 13
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 247
Cys Ala Lys Val His Gln Glu Thr Gly Gly Ser Gly Gly
1 5 10
<210> 248
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 248
Gly Ser Trp His Val Gln His Trp Gly Gln Gly
1 5 10
<210> 249
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 249
Cys Ala Lys Val His Gln Glu Thr Pro Asp Gly Gly Ser Gly Gly
1 5 10 15
<210> 250
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 250
Gly Ser Tyr Glu Trp His Val Gln His Trp Gly Gln Gly
1 5 10
<210> 251
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 251
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Gly Gly
1 5 10 15
<210> 252
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 252
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
1 5 10 15
Gly Gln Gly
<210> 253
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 253
Cys Thr Ser Val His Gln Glu Thr Ser Ser Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 254
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 254
Gly Ser Tyr Ser Tyr Glu Trp His Val Asp Val Trp Gly Gln Gly
1 5 10 15
<210> 255
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 255
Cys Ala Lys Thr His Thr Ser Pro Pro Ser Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 256
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 256
Gly Ser Ser Pro Pro Ser Pro Tyr Phe Gln His Trp Gly Gln Gly
1 5 10 15
<210> 257
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 257
Cys Thr Ser Val His Gln Glu Thr Lys Ser Ser Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 258
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 258
Gly Ser Tyr Ser Asn Tyr Glu Trp His Val Asp Val Trp Gly Gln Gly
1 5 10 15
<210> 259
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 259
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly
<210> 260
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 260
Cys Thr Ser Val His Gln Glu Thr Lys Lys Ser Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 261
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 261
Gly Ser Tyr Ser Tyr Asn Tyr Glu Trp His Val Asp Val Trp Gly Gln
1 5 10 15
Gly
<210> 262
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 262
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Gly Gly
1 5 10 15
Ser Gly Gly
<210> 263
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 263
Cys Thr Ser Val His Gln Glu Thr Lys Lys Gln Ser Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 264
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 264
Gly Ser Tyr Ser Tyr Tyr Asn Tyr Glu Trp His Val Asp Val Trp Gly
1 5 10 15
Gln Gly
<210> 265
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 265
Cys Ala Lys Val His Pro Asn Pro Asn Pro Asn Pro Asn Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 266
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 266
Gly Ser Asn Pro Asn Pro Asn Pro Asn Pro His Val Asp Val Trp Gly
1 5 10 15
Gln Gly
<210> 267
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 267
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly
20
<210> 268
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 268
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 269
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 269
Cys Ala Lys Leu Thr Val Val Val Thr Ser His Gln Ala Pro Gly Glu
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 270
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 270
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr Phe Gln His Trp Gly
1 5 10 15
Gln Gly
<210> 271
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 271
Cys Ala Lys Ser Ser Asp Lys Thr His Thr Ser Pro Pro Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 272
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 272
Gly Ser Lys Thr His Thr Ser Pro Pro Ser Pro Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 273
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 273
Cys Ala Lys Val Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 274
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 274
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Val Gln His Trp Gly Gln
1 5 10 15
Gly
<210> 275
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 275
Cys Ala Lys Val His Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 276
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 276
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr His Val Gln His Trp Gly Gln
1 5 10 15
Gly
<210> 277
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 277
Cys Ala Lys Leu Thr Val Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 278
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 278
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 279
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 279
Cys Ala Lys Leu Thr Ala Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 280
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 280
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Asn Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 281
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 281
Cys Ala Lys Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 282
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 282
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 283
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 283
Gly Ser Tyr Asp Tyr Val Trp Gly Ser Tyr Ala Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 284
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 284
Cys Ala Lys Leu Thr Ser Val Val Val Thr Ser His Gln Ala Pro Gly
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 285
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 285
Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 286
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 286
Cys Ala Lys Val His Pro Asn Pro Asn Pro Asn Pro Asn Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 287
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 287
Gly Ser Tyr Asn Pro Asn Pro Asn Pro Asn Pro His Val Asp Val Trp
1 5 10 15
Gly Gln Gly
<210> 288
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 288
Cys Ala Lys Leu Thr Gln Val Lys Leu Glu Leu Gly His Arg Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 289
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 289
Gly Ser Asn His Leu Arg Ser Glu Lys Leu Thr Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 290
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 290
Cys Ala Lys Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 291
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 291
Cys Ala Lys Thr Gln Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 292
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 292
Gly Ser Asn Thr Lys Val Asp Lys Lys Ala Glu Tyr Phe Gln His Trp
1 5 10 15
Gly Gln Gly
<210> 293
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 293
Gly Ser Tyr Ser Tyr Thr Thr Tyr Asn Tyr Glu Trp His Val Asp Val
1 5 10 15
Trp Gly Gln Gly
20
<210> 294
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 294
Cys Ala Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 295
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 295
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val His
1 5 10 15
Trp Gly Gln Gly
20
<210> 296
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 296
Cys Ala Lys Leu Thr Ala Glu Glu Trp Lys Lys Lys Tyr Glu Lys Glu
1 5 10 15
Lys Glu Lys Asn Lys Gly Ser
20
<210> 297
<211> 21
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 297
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ala Glu Tyr Phe Gln
1 5 10 15
His Trp Gly Gln Gly
20
<210> 298
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 298
Cys Ala Asp Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg
1 5 10 15
Ala Leu Leu Thr Ala Pro Arg
20
<210> 299
<211> 21
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 299
Gly Ser Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Tyr Phe Gln
1 5 10 15
His Trp Gly Gln Gly
20
<210> 300
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 300
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Tyr Gln Ser Ser
1 5 10 15
Pro Asp Gly Gly Ser Gly Gly
20
<210> 301
<211> 21
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 301
Gly Ser Tyr Ser Tyr Thr Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp
1 5 10 15
Val Trp Gly Gln Gly
20
<210> 302
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 302
Cys Ala Lys Leu Thr Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg
1 5 10 15
Ala Leu Leu Thr Ala Pro Arg
20
<210> 303
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 303
Cys Ala Lys Leu Thr Ala Val Gln Val Lys Leu Glu Leu Gly His Arg
1 5 10 15
Pro Asp Gly Gly Ser Gly Gly
20
<210> 304
<211> 25
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 304
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Tyr Gln
1 5 10 15
Ser Ser Pro Asp Gly Gly Ser Gly Gly
20 25
<210> 305
<211> 23
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 305
Gly Ser Tyr Ser Tyr Thr Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His
1 5 10 15
Val Asp Val Trp Gly Gln Gly
20
<210> 306
<211> 25
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 306
Cys Ala Lys Leu Thr Ala Val Gln Val Lys Leu Glu Leu Gly His Arg
1 5 10 15
Ala Gln Pro Asp Gly Gly Ser Gly Gly
20 25
<210> 307
<211> 23
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 307
Gly Ser Pro Val Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Tyr
1 5 10 15
Phe Gln His Trp Gly Gln Gly
20
<210> 308
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 308
Ser Ser Ser Asn Ile Gly Ser Lys Leu Arg Ala Leu Leu Thr Ala Pro
1 5 10 15
Arg
<210> 309
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 309
Gly Ser Gly Ser Gly Gly Ser Gly Gly Ser Gly Ser Gly Tyr Asp
1 5 10 15
<210> 310
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 310
Gly Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asp
1 5 10
<210> 311
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 311
Ser Ser Leu Gly Gln Ile Gln Leu Thr Ile Arg His Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 312
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 312
Gly Ser Asn Lys Leu Ile Val Val Val His Ala Ser Arg Asn Leu Ile
1 5 10 15
Gly Tyr Asp
<210> 313
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 313
Ser Pro Leu Gly Gln Ile Gln Leu Thr Ile Arg His Ser Ser Gln Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 314
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 314
Gly Ser Arg Asn Lys Leu Ile Val Val Val His Ala Ser Arg Asn Leu
1 5 10 15
Ile Ala Tyr Asp
20
<210> 315
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 315
Ser Ser Leu Gly Gln Ile Gln Leu Thr Ile Arg His Ser Ser Gln Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 316
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 316
Gly Ser Arg Asn Lys Leu Ile Val Val Val His Ala Ser Arg Asn Leu
1 5 10 15
Ile Gly Tyr Asp
20
<210> 317
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 317
Ser Ser Ser Asn Ile Gly Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala
1 5 10 15
Leu Leu Thr Ala Pro Arg
20
<210> 318
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 318
Gly Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu
1 5 10 15
Leu Thr Ala Asp
20
<210> 319
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 319
Gly Ser Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Ser Gly
1 5 10 15
Ser Gly Tyr Asp
20
<210> 320
<211> 24
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 320
Ser Ser Ser Asn Ile Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10 15
Ser Pro Asp Gly Gly Ser Gly Gly
20
<210> 321
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 321
Gly Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Tyr Asp
1 5 10 15
<210> 322
<211> 7
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 322
Asn Ser Asn Arg Pro Ser Gly
1 5
<210> 323
<211> 6
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 323
Tyr Gly Gly Ser Gly Ser
1 5
<210> 324
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 324
Gly Ser Gly Ser Asn Ser Asn Arg Pro Ser Gly
1 5 10
<210> 325
<211> 13
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 325
Tyr Gly Lys Thr His Thr Ser Pro Pro Ser Pro Gly Gly
1 5 10
<210> 326
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 326
Gly Gly Lys Thr His Thr Ser Pro Pro Ser Pro Gly Asn Arg Pro Ser
1 5 10 15
Gly
<210> 327
<211> 14
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 327
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Gly
1 5 10
<210> 328
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 328
Gly Gly Lys Thr His Thr Ser Pro Pro Ser Pro Ser Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 329
<211> 14
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 329
Tyr Gly Ser Lys Thr His Thr Ser Pro Pro Ser Pro Gly Gly
1 5 10
<210> 330
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 330
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Gly Ser Gly Gly
1 5 10 15
<210> 331
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 331
Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro Ser Gly
1 5 10 15
<210> 332
<211> 16
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 332
Tyr Gly Ser Ser Asp Lys Thr His Thr Ser Pro Pro Ser Pro Gly Gly
1 5 10 15
<210> 333
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 333
Gly Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn
1 5 10 15
Arg Pro Ser Gly
20
<210> 334
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 334
Tyr Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 335
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 335
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Asn Arg Pro Ser Gly
1 5 10 15
<210> 336
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 336
Tyr Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 337
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 337
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Asn Arg Pro Ser Gly
1 5 10 15
<210> 338
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 338
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Gly Ser Gly
1 5 10 15
Gly
<210> 339
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 339
Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro Ser
1 5 10 15
Gly
<210> 340
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 340
Tyr Gly Val Pro Lys Glu Lys Glu Lys Glu Lys Val Ser Thr Ala Val
1 5 10 15
Gly Gly
<210> 341
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 341
Gly Ser Ala Pro Leu Glu Val Pro Lys Glu Lys Glu Lys Glu Lys Val
1 5 10 15
Gly
<210> 342
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 342
Tyr Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 343
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 343
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Asn Arg Pro Ser
1 5 10 15
Gly
<210> 344
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 344
Tyr Gly Gly Ser Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 345
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 345
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10 15
Gly Gly
<210> 346
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 346
Gly Ser Tyr Glu Lys Glu Lys Glu Lys Asn Lys Thr Leu Lys Asn Val
1 5 10 15
Gly
<210> 347
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 347
Tyr Gly Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 348
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 348
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Asn Arg Pro Ser
1 5 10 15
Gly
<210> 349
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 349
Tyr Gly Ala Glu Glu Trp Lys Lys Lys Tyr Glu Lys Glu Lys Glu Lys
1 5 10 15
Gly Gly
<210> 350
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 350
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Gly
<210> 351
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 351
Tyr Gly Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 352
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 352
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Asn Arg Pro Ser
1 5 10 15
Gly
<210> 353
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 353
Tyr Gly Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu Thr Ala
1 5 10 15
Pro Gly
<210> 354
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 354
Gly Ser Asp Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 355
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 355
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 356
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 356
Tyr Gly Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 357
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 357
Gly Ser Asp Arg Phe Ser Gly Ser Lys Ser Gly Gly Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 358
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 358
Tyr Gly Gly Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 359
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 359
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Gly Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 360
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 360
Tyr Thr Gln Thr Tyr Ile Ser Asn Val Asn His Lys Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 361
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 361
Gly Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Asn Arg Pro
1 5 10 15
Ser Gly
<210> 362
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 362
Tyr Gly Gly Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 363
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 363
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 364
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 364
Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 365
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 365
Gly Ser Tyr Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn Arg Pro
1 5 10 15
Ser Gly
<210> 366
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 366
Tyr Gly Ser Gln Val Lys Leu Glu Leu Gly His Arg Ala Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 367
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 367
Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu Thr Ser Gly Asn Arg
1 5 10 15
Pro Ser Gly
<210> 368
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 368
Tyr Pro Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 369
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 369
Gly Ser Gly Arg Glu Val Pro Ile Ser Asn Gly Ser Gly Phe Asn Arg
1 5 10 15
Pro Ser Gly
<210> 370
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 370
Tyr Gly Gly Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 371
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 371
Gly Ser Gly Arg Glu Val Pro Ile Ser Asn Gly Ser Gly Gly Asn Arg
1 5 10 15
Pro Ser Gly
<210> 372
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 372
Tyr Gly Ala Val Val Tyr Ile Glu Ile Leu Asp Arg His Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 373
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 373
Tyr Gly Ser Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu
1 5 10 15
Thr Ala Pro Arg
20
<210> 374
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 374
Gly Ser Asp Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Asn
1 5 10 15
Arg Pro Ser Gly
20
<210> 375
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 375
Tyr Gly Ser Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu
1 5 10 15
Thr Ala Pro Gly
20
<210> 376
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 376
Tyr Gly Ser Ala Val Gln Val Lys Leu Glu Leu Gly His Arg Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 377
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 377
Gly Ser Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Ser Gly Asn
1 5 10 15
Arg Pro Ser Gly
20
<210> 378
<211> 15
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 378
Cys Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly Gly Ser Gly Gly
1 5 10 15
<210> 379
<211> 10
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 379
Gly Ser Gly Ser Gly Ser Gly Ser Gly Phe
1 5 10
<210> 380
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 380
Cys Gln Ser Tyr Asp Ile Leu Pro Ile Glu Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 381
<211> 11
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 381
Gly Ser Arg Phe Asp Tyr Asp Gly Val Val Phe
1 5 10
<210> 382
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 382
Cys Gly Ser Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly Gly Ser Gly
1 5 10 15
Gly
<210> 383
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 383
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Phe
1 5 10
<210> 384
<211> 17
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 384
Cys Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Gly Ser Gly
1 5 10 15
Gly
<210> 385
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 385
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Phe
1 5 10
<210> 386
<211> 18
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 386
Cys Gln Ser Tyr Asp Lys Leu Glu Leu Gly His Pro Asp Gly Gly Ser
1 5 10 15
Gly Gly
<210> 387
<211> 12
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 387
Gly Ser His Leu Arg Ser Glu Lys Gly Val Val Phe
1 5 10
<210> 388
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 388
Cys Gln Ser Tyr Asp Ile Leu Pro Ile Glu Val Tyr Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 389
<211> 13
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 389
Gly Ser Lys Val Arg Phe Asp Tyr Asp Gly Val Val Phe
1 5 10
<210> 390
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 390
Cys Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Pro Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 391
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 391
Cys Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Asp Gly Gly
1 5 10 15
Ser Gly Gly
<210> 392
<211> 19
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 392
Cys Gln Ser Tyr Asp Gly Phe Ile Leu Pro Ile Glu Val Tyr Gly Gly
1 5 10 15
Ser Gly Gly
<210> 393
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 393
Gly Ser Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Val Val Phe
1 5 10 15
<210> 394
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 394
Cys Gln Ser Tyr Asp Lys Leu Glu Leu Gly His Arg Ala Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 395
<211> 14
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 395
Gly Ser Val Asn His Leu Arg Ser Glu Lys Gly Val Val Phe
1 5 10
<210> 396
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 396
Cys Gln Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 397
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 397
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Val Phe
1 5 10 15
<210> 398
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 398
Cys Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 399
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 399
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Phe
1 5 10 15
<210> 400
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 400
Cys Gln Ser Tyr Asp Pro Asn Pro Asn Pro Asn Pro Asn Pro Asp Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 401
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 401
Gly Ser Asn Pro Asn Pro Asn Pro Asn Pro Ser Gly Val Val Phe
1 5 10 15
<210> 402
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 402
Cys Ala Ala Trp Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 403
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 403
Gly Ser Asn Pro Asn Pro Asn Pro Asn Pro Asn Pro Asn Val Phe
1 5 10 15
<210> 404
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 404
Cys Gln Ser Tyr Asp Gln Val Lys Leu Glu Leu Gly His Arg Ala Gly
1 5 10 15
Gly Ser Gly Gly
20
<210> 405
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 405
Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu Thr Gly Val Val Phe
1 5 10 15
<210> 406
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 406
Cys Gln Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 407
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 407
Cys Gln Ser Tyr Asp Gln Val Lys Leu Glu Leu Gly His Arg Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 408
<211> 15
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 408
Gly Ser Asn His Leu Arg Ser Glu Lys Leu Thr Gly Val Val Phe
1 5 10 15
<210> 409
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 409
Cys Gln Ser Tyr Asp Gly Phe Ile Leu Pro Ile Glu Val Tyr Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 410
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 410
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Phe
1 5 10 15
<210> 411
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 411
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Val Val Phe
1 5 10 15
<210> 412
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 412
Cys Gly Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly
20
<210> 413
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 413
Gly Ser Tyr Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Gly Phe
1 5 10 15
<210> 414
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 414
Cys Gln Ser Tyr Asp Ser Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala
1 5 10 15
Leu Leu Thr Ala Pro Arg
20
<210> 415
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 415
Cys Gln Ser Ala Val Gln Val Lys Leu Glu Leu Gly His Arg Ala Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 416
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 416
Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Val Phe
1 5 10 15
<210> 417
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 417
Cys Gln Ser Tyr Asp Gln Val Lys Leu Glu Leu Gly His Arg Ala Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 418
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 418
Cys Gln Ser Tyr Asp Gly Phe Ile Leu Pro Ile Glu Val Tyr Phe Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 419
<211> 16
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 419
Gly Ser Arg Lys Val Arg Phe Asp Tyr Asp Leu Phe Gly Val Val Phe
1 5 10 15
<210> 420
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 420
Cys Gln Ser Tyr Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro
1 5 10 15
Asp Gly Gly Ser Gly Gly
20
<210> 421
<211> 17
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 421
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Gly Val Val
1 5 10 15
Phe
<210> 422
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 422
Cys Gln Ser Tyr Asp Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser
1 5 10 15
Pro Asp Gly Gly Ser Gly Gly
20
<210> 423
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 423
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Ser Gly Val
1 5 10 15
Val Phe
<210> 424
<211> 24
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 424
Cys Gln Ser Tyr Asp Ala Val Gln Val Lys Leu Glu Leu Gly His Arg
1 5 10 15
Ala Pro Asp Gly Gly Ser Gly Gly
20
<210> 425
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 425
Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu Thr Phe Asn Gly Val
1 5 10 15
Val Phe
<210> 426
<211> 25
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 426
Cys Gln Ser Tyr Asp Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys
1 5 10 15
Leu Arg Ala Leu Leu Thr Ala Pro Arg
20 25
<210> 427
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 427
Gly Ser Gly Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu Thr Gly
1 5 10 15
Val Val Phe
<210> 428
<211> 21
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 428
Gly Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys Leu Arg Ala Leu Leu
1 5 10 15
Thr Ala Val Val Phe
20
<210> 429
<211> 25
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 429
Cys Gln Ser Tyr Asp Ser Ser Asp Arg Ser Ala Leu Leu Lys Ser Lys
1 5 10 15
Leu Arg Ala Leu Leu Thr Ala Pro Glu
20 25
<210> 430
<211> 23
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 430
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly Ser Gly
20
<210> 431
<211> 20
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 431
Gly Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val
1 5 10 15
Trp Gly Gln Gly
20
<210> 432
<211> 18
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 432
Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp Gly
1 5 10 15
Gln Gly
<210> 433
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 433
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp
1 5 10 15
Gly Gly Ser Gly Gly Ser
20
<210> 434
<211> 24
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 434
Gly Ser Gly Gly Tyr Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp
1 5 10 15
His Val Asp Val Trp Gly Gln Gly
20
<210> 435
<211> 21
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 435
Cys Gln Ser Tyr Asp Gln Val Lys Leu Glu Leu Gly His Arg Ala Gly
1 5 10 15
Gly Ser Gly Gly Ser
20
<210> 436
<211> 21
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 436
Gly Ser Gly Gly Ser Gly Ser Val Asn His Leu Arg Ser Glu Lys Leu
1 5 10 15
Thr Gly Val Val Phe
20
<210> 437
<211> 24
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 437
Gly Ser Gly Gly Ser Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp
1 5 10 15
His Val Asp Val Trp Gly Gln Gly
20
<210> 438
<211> 23
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 438
Gly Gly Gly Ser Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His
1 5 10 15
Val Asp Val Trp Gly Gln Gly
20
<210> 439
<211> 22
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 439
Cys Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Tyr
1 5 10 15
Lys Gly Ala Asn Lys Lys
20
<210> 440
<211> 20
<212> PRT
<213> искусственная
<220>
<223> N-концевая последовательность (с эталонной aa)
<400> 440
Ile Ser Gly Ser Val Val Val Thr Ser His Gln Ala Pro Gly Gly Gly
1 5 10 15
Ser Gly Gly Ser
20
<210> 441
<211> 19
<212> PRT
<213> искусственная
<220>
<223> C-концевая последовательность (с эталонной aa)
<400> 441
Gly Ser Gly Gly Ser Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr
1 5 10 15
Gly Ser Thr
<210> 442
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 442
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Met Val Gln Gly Ser Gly Cys Phe Gly Arg Lys Met
115 120 125
Asp Arg Ile Ser Ser Ser Ser Gly Leu Gly Cys Lys Val Leu Arg Arg
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 443
<211> 500
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 443
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Val Val Val Thr Ser His Gln Ala Pro Gly
50 55 60
Gly Gly Ser Gly Gly Met Val Gln Gly Ser Gly Cys Phe Gly Arg Lys
65 70 75 80
Met Asp Arg Ile Ser Ser Ser Ser Gly Leu Gly Cys Lys Val Leu Arg
85 90 95
Arg Gly Glu Lys Lys Lys Leu Lys Ser Leu Ala Tyr Gly Ser Thr Tyr
100 105 110
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
115 120 125
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Ala Lys Leu Thr Gly Ala Glu Tyr Phe Gln His
145 150 155 160
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
165 170 175
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
180 185 190
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
195 200 205
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
210 215 220
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
225 230 235 240
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
245 250 255
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
260 265 270
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
275 280 285
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
290 295 300
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
305 310 315 320
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
325 330 335
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
340 345 350
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
355 360 365
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
370 375 380
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
385 390 395 400
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
405 410 415
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
420 425 430
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
435 440 445
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
450 455 460
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
465 470 475 480
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
485 490 495
Leu Ser Pro Gly
500
<210> 444
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 444
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Ile Thr Gly Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Met Val Gln Gly Ser Gly Cys Phe Gly Arg Lys Met
115 120 125
Asp Arg Ile Ser Ser Ser Ser Gly Leu Gly Cys Lys Val Leu Arg Arg
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Ala Glu Tyr Phe Gln His Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 445
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 445
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Tyr Lys
100 105 110
Gly Ala Asn Lys Lys Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
115 120 125
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys Gly Ser Gly Gly Ser
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 446
<211> 499
<212> PRT
<213> искусственная
<220>
<223> NP привитая HC
<400> 446
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ser Val His Gln Glu Thr Lys Lys Tyr Gln Ser Ser Pro Asp Gly
100 105 110
Gly Ser Gly Gly Ser Gly Leu Ser Lys Gly Cys Phe Gly Leu Lys Leu
115 120 125
Asp Arg Ile Gly Ser Met Ser Gly Leu Gly Cys Gly Ser Gly Gly Tyr
130 135 140
Gly Ser Tyr Ser Tyr Thr Tyr Asn Tyr Glu Trp His Val Asp Val Trp
145 150 155 160
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
165 170 175
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
180 185 190
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
195 200 205
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
210 215 220
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
225 230 235 240
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
245 250 255
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly
<210> 447
<211> 217
<212> PRT
<213> человека
<400> 447
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Asp Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА С ПРИВИТЫМ МОЗГОВЫМ НАТРИЙУРЕТИЧЕСКИМ ПЕПТИДОМ | 2019 |
|
RU2839970C2 |
| АНТИТЕЛА С ПРИВИТЫМ НАТРИЙУРЕТИЧЕСКИМ ПЕПТИДОМ С-ТИПА | 2019 |
|
RU2828786C2 |
| АНТИ-СЕАСАМ6 АНТИТЕЛА И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2739163C2 |
| КОНЪЮГАТЫ СВЯЗУЮЩЕГО И АКТИВНОГО ВЕЩЕСТВА (ADC), ИМЕЮЩИЕ ФЕРМЕНТАТИВНО РАСЩЕПЛЯЕМЫЕ ГРУППЫ | 2017 |
|
RU2761390C2 |
| ТЕРАПЕВТИЧЕСКАЯ ПРОТИВОРАКОВАЯ НЕОЭПИТОПНАЯ ВАКЦИНА | 2017 |
|
RU2782422C2 |
| АФФИМЕРЫ, СВЯЗЫВАЮЩИЕСЯ С НЕОНАТАЛЬНЫМ FC РЕЦЕПТОРОМ | 2020 |
|
RU2817008C1 |
| МОЛЕКУЛЫ АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТ PD-L1 и CD137 | 2019 |
|
RU2826084C2 |
| МУЛЬТИВАЛЕНТНЫЕ И МУЛЬТИСПЕЦИФИЧЕСКИЕ 41BB-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2017 |
|
RU2789648C2 |
| АНТИТЕЛА К ТАУ И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2787779C2 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
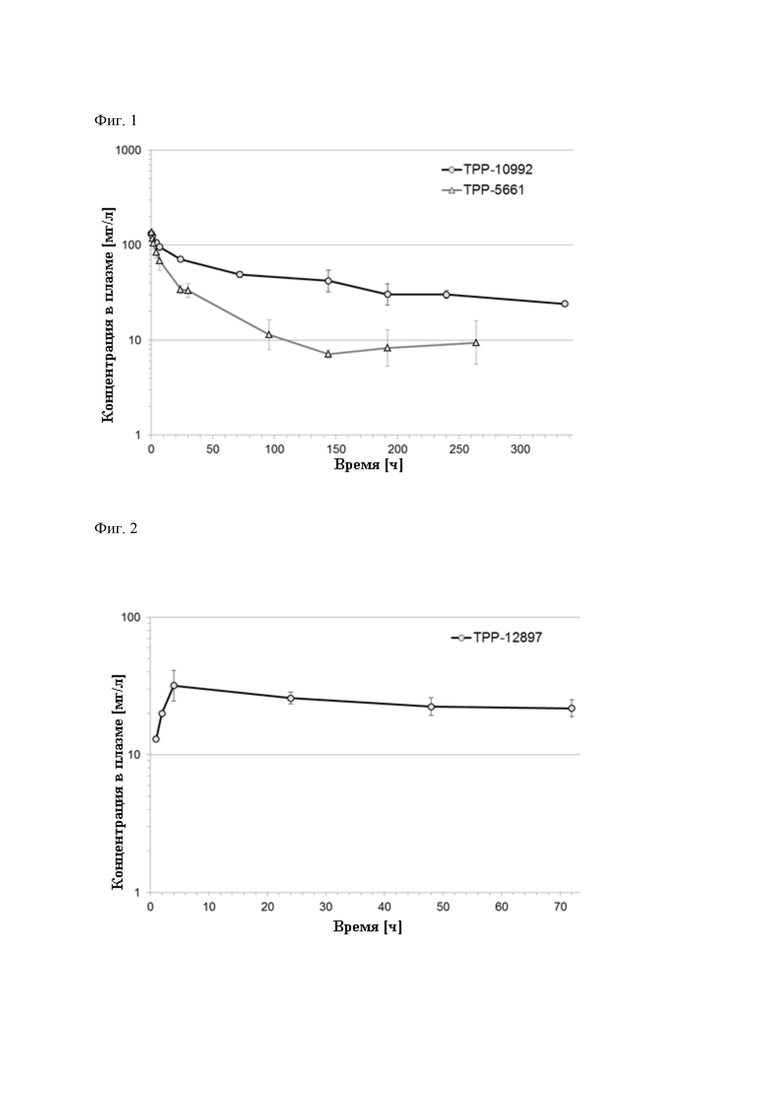
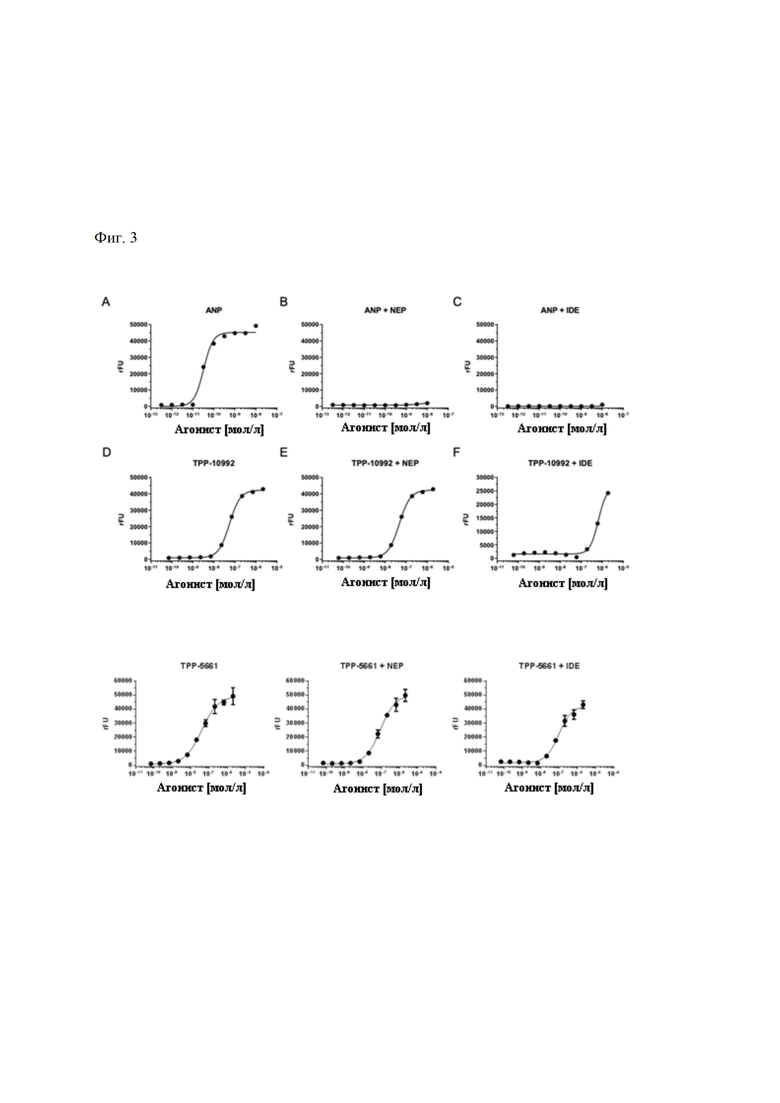


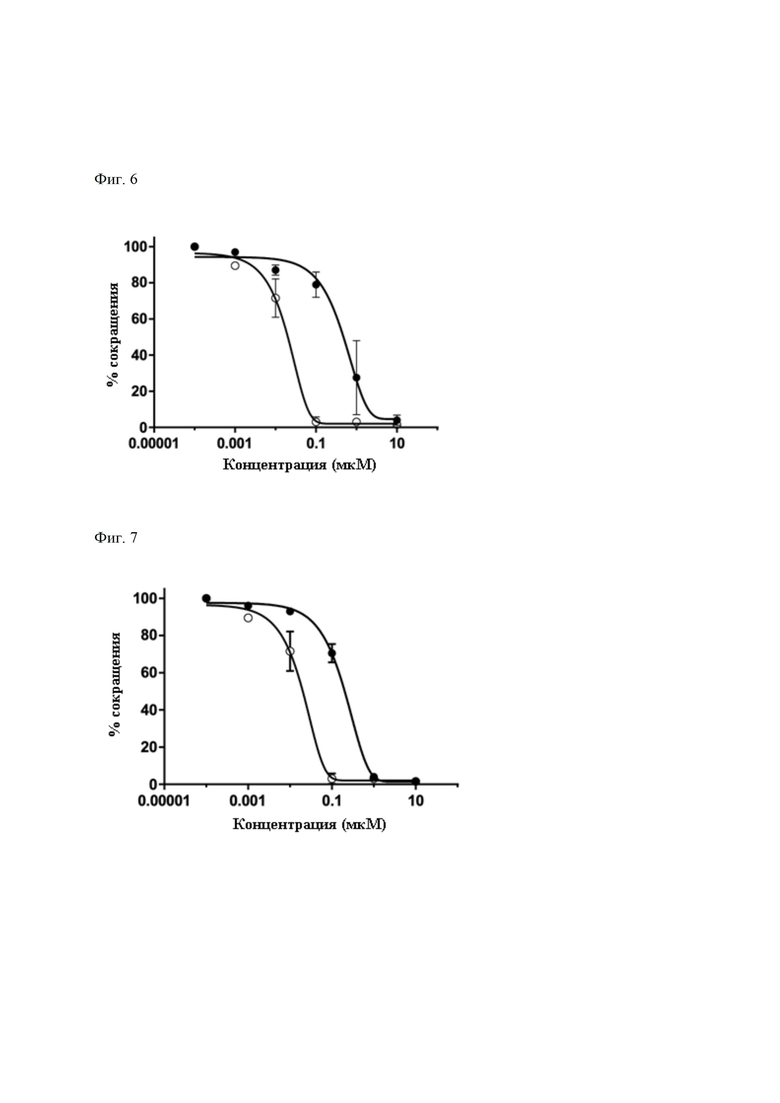
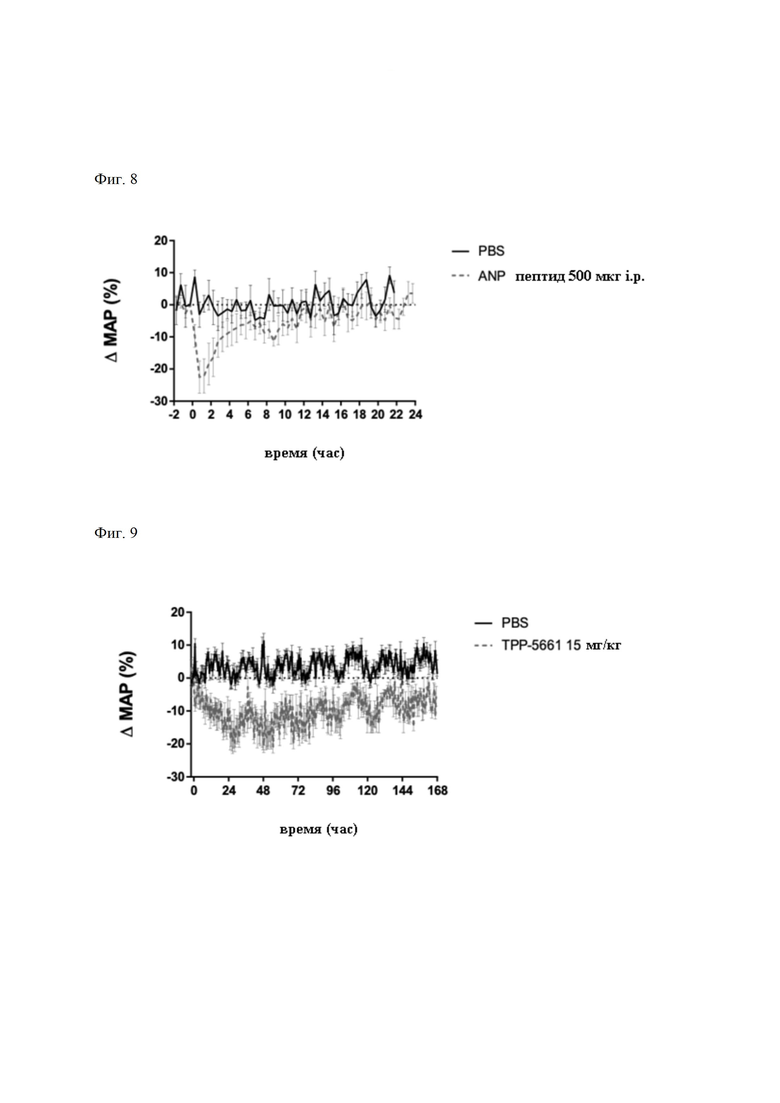
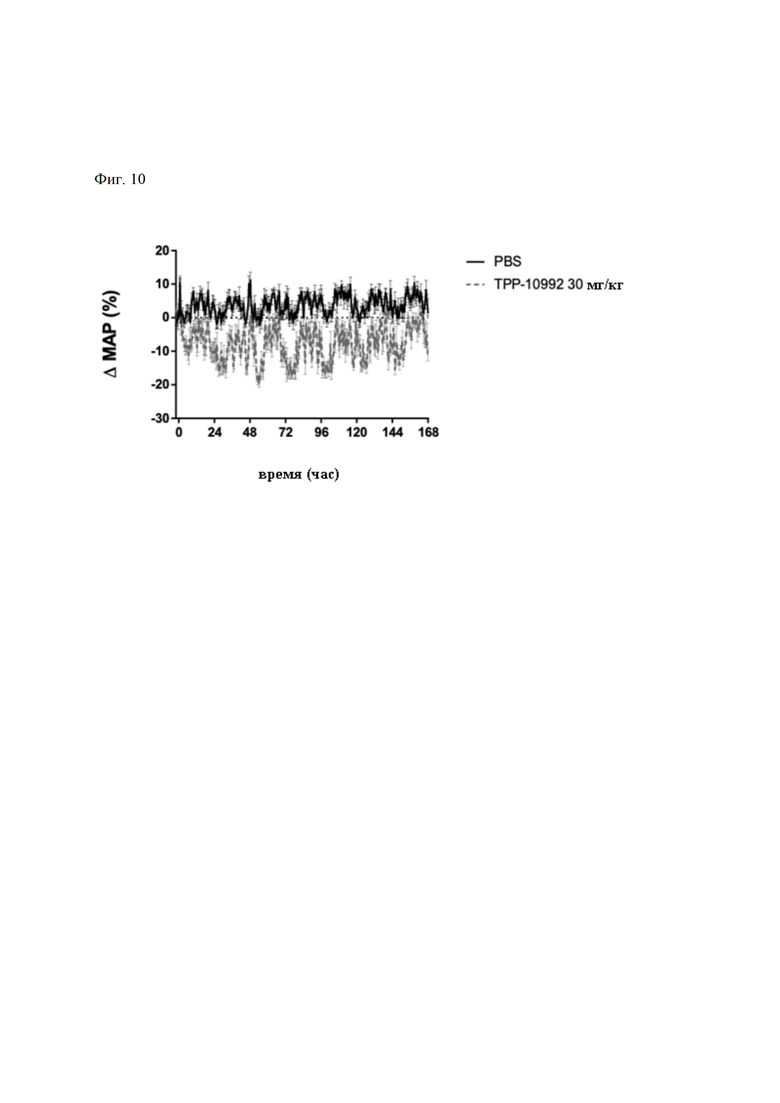
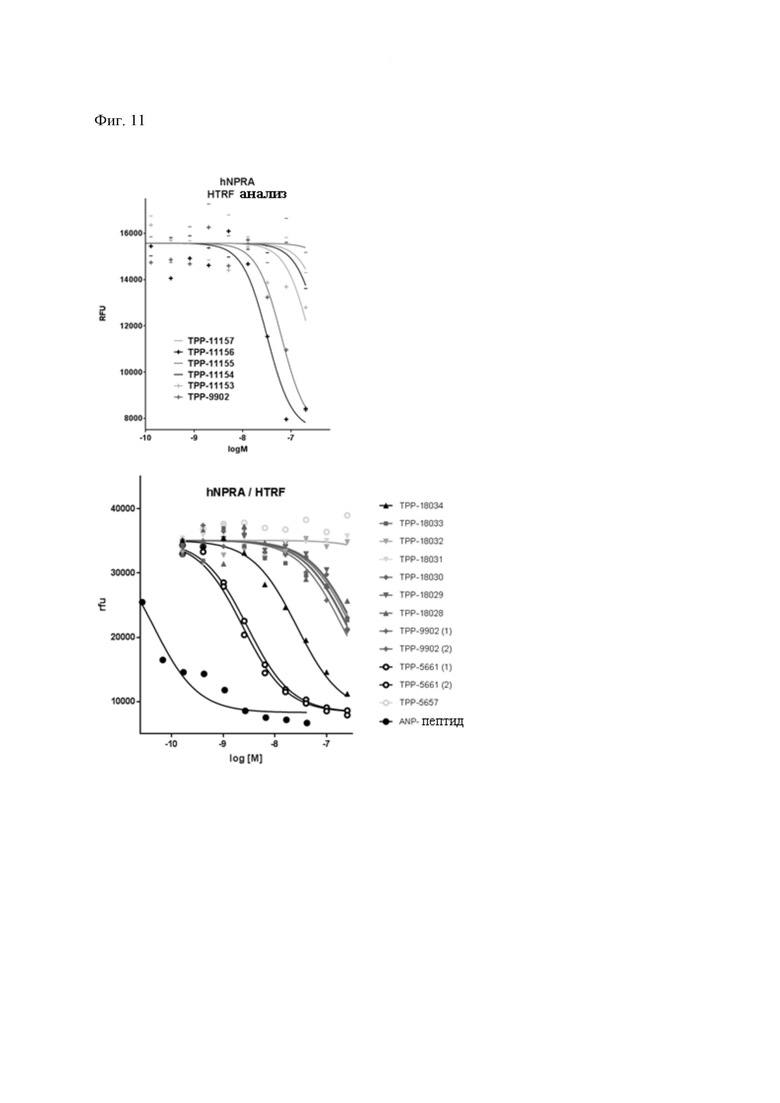
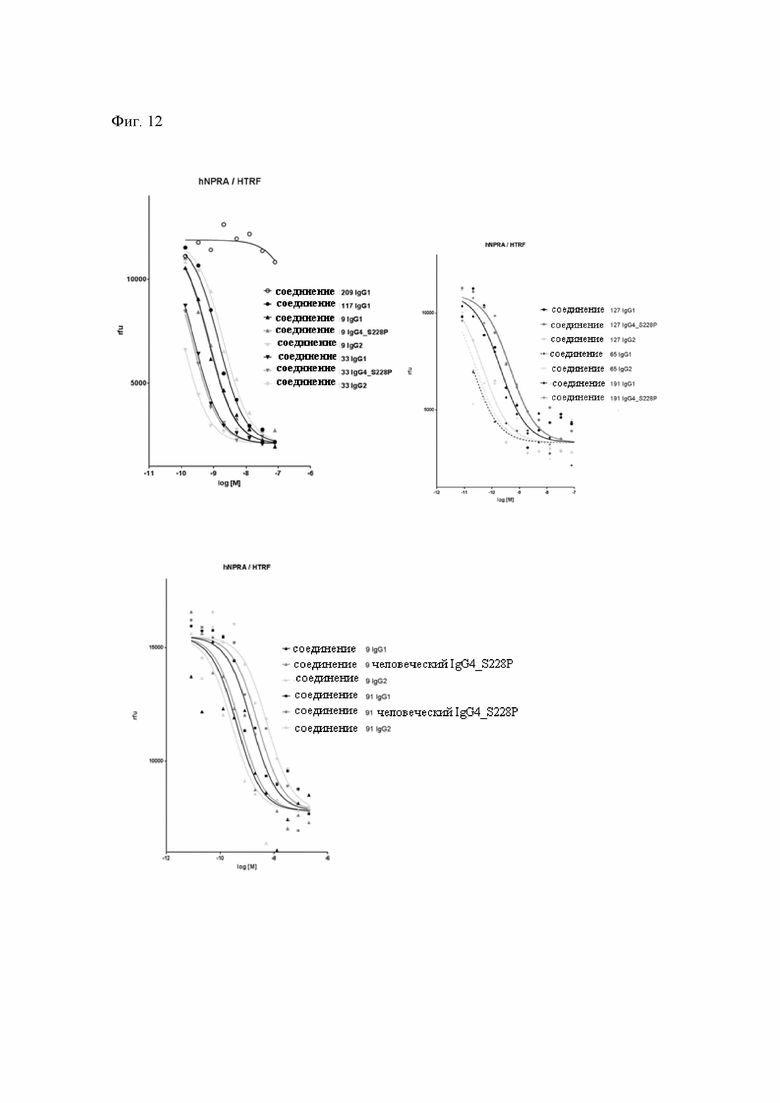
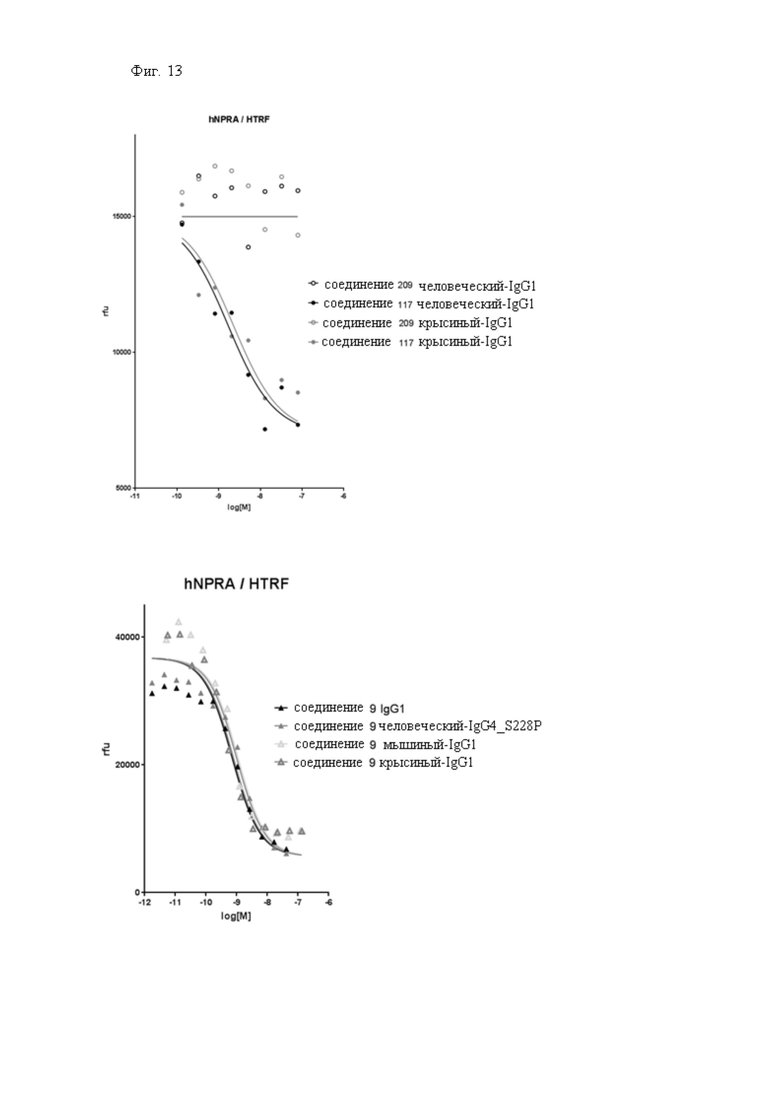
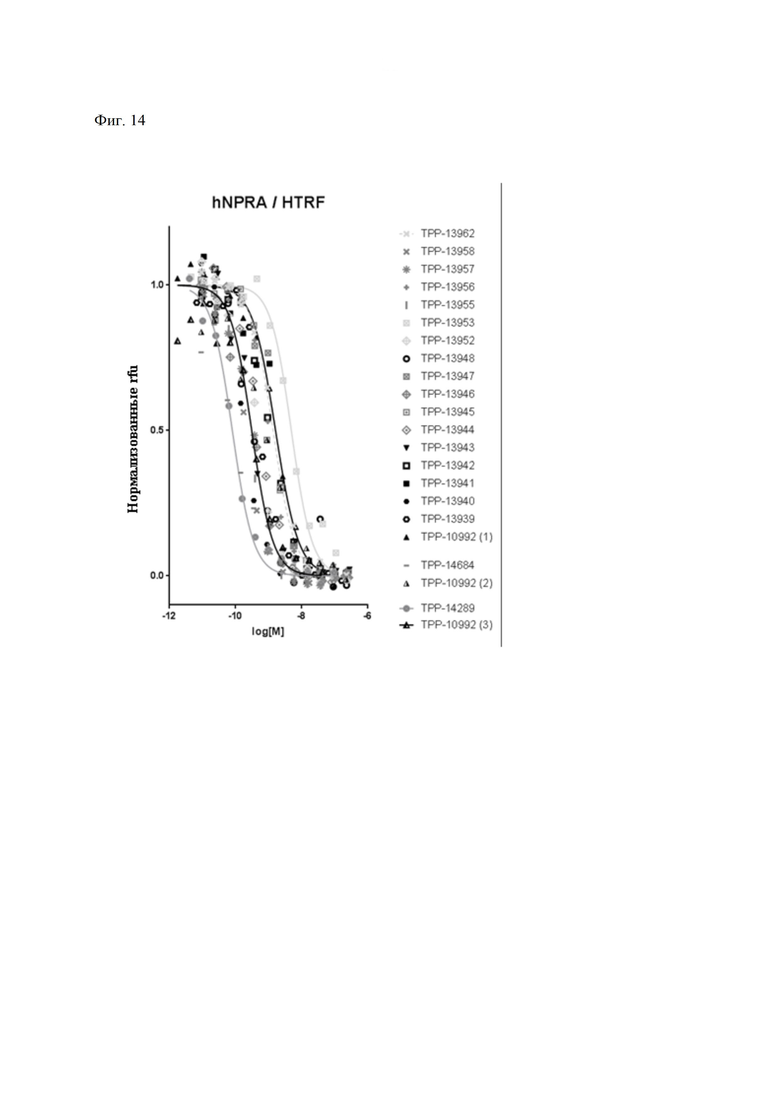
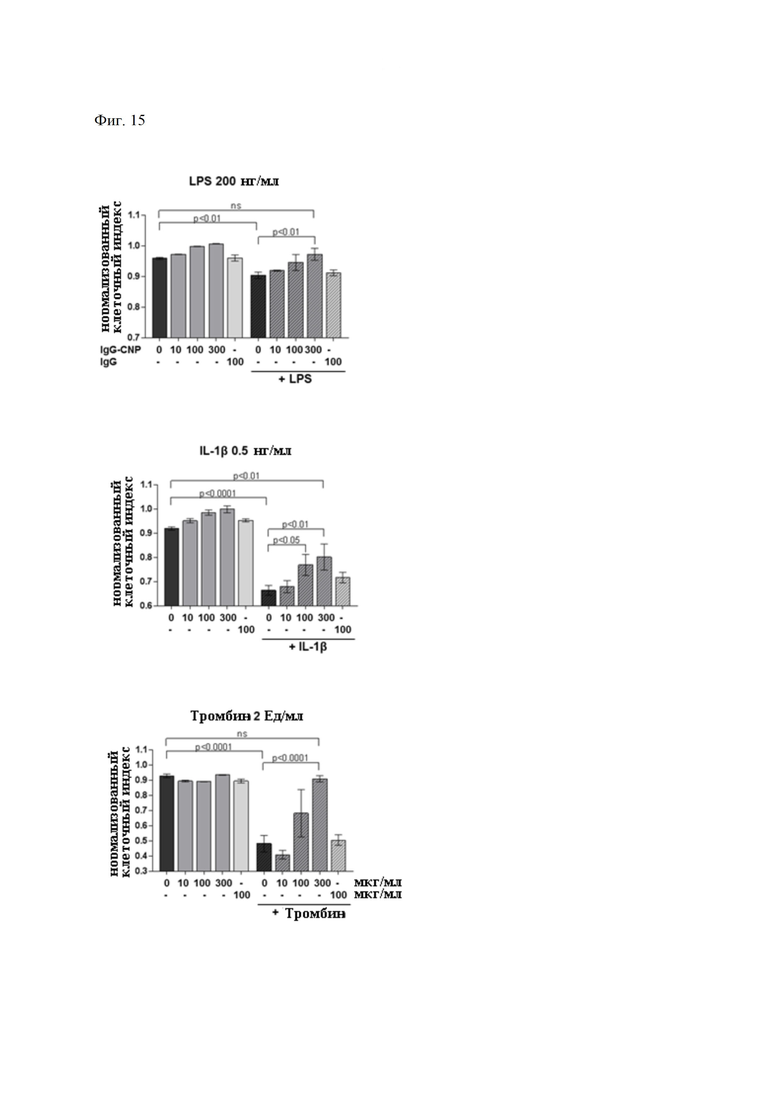
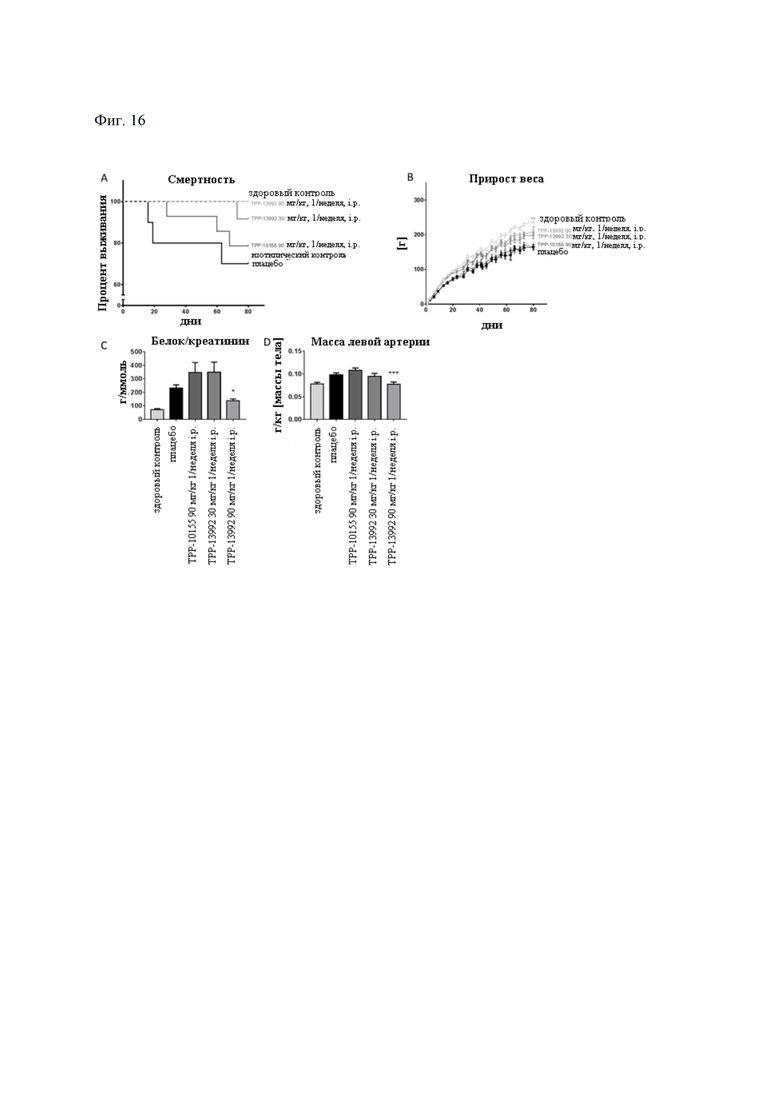
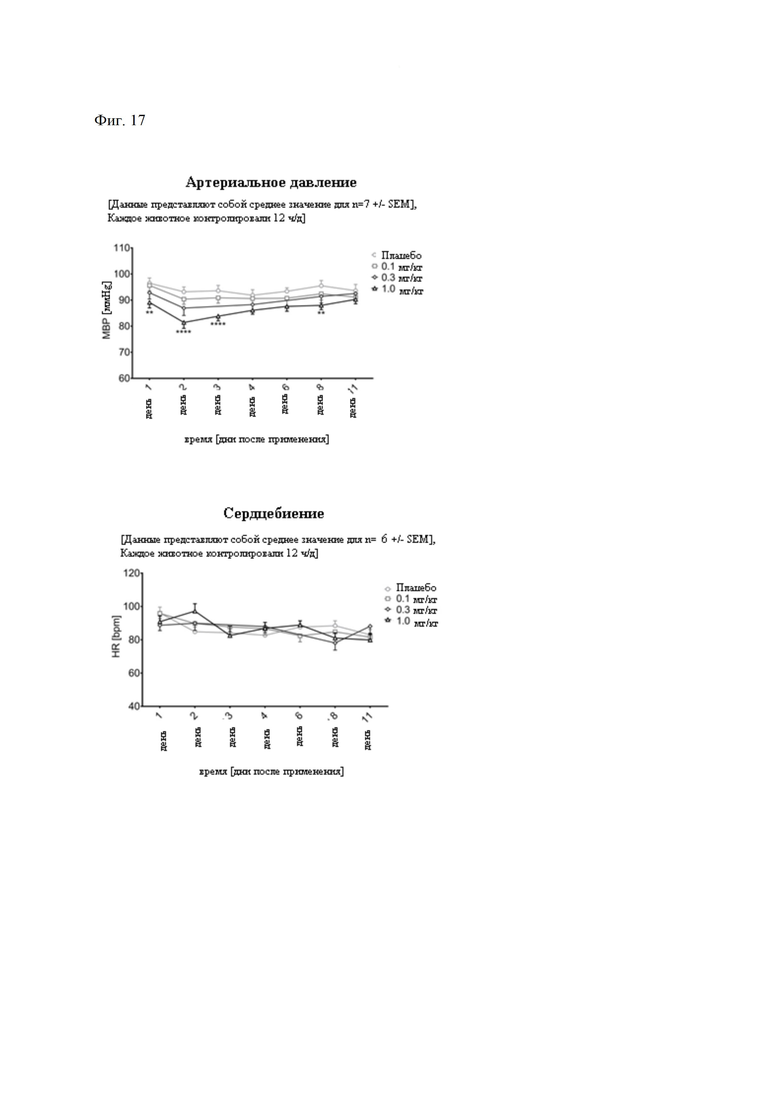
Изобретение относится к области биотехнологии. Предложены антитела или их фрагменты, пригодные в качестве агониста рецептора натрийуретического пептида. Антитела или их фрагменты содержат гетерологичную аминокислотную последовательность внутри CDR участка, где указанная гетерологичная аминокислотная последовательность содержит N-терминальную линкерную последовательность (Ntls), предсердный натрийуретический пептид (ANP) и C-терминальную линкерную последовательность (Ctls). Изобретение также относится к применению антитела или его фрагмента в способе лечения, композиции, содержащей антитело или его фрагмент, нуклеиновой кислоте или смеси нуклеиновых кислот, кодирующей антитело или его фрагмент, клетке-хозяину, содержащей такую нуклеиновую кислоту или такую смесь нуклеиновых кислот, а также к способу получения антитела или его фрагмента. Изобретение обеспечивает получение агонистов рецептора натрийуретического пептида с повышенной стабильностью в сыворотке по сравнению с натрийуретическими пептидами дикого типа природного происхождения. 11 н. и 1 з.п. ф-лы, 17 ил., 11 табл., 12 пр.
1. Антитело или его фрагмент, пригодные в качестве агониста рецептора натрийуретического пептида, где
(i) легкая цепь содержит или состоит из аминокислотной последовательности SEQ ID NO 66 или любой последовательности, имеющей по меньшей мере 95% идентичность с SEQ ID NO 66, и
(ii) тяжелая цепь содержит или состоит из аминокислотных последовательностей SEQ ID NOs 67 или 76; или любой последовательности, имеющей по меньшей мере 95% идентичность с SEQ ID NOs 67 или 76.
2. Антитело или его фрагмент, пригодные в качестве агониста рецептора натрийуретического пептида, где
(i) легкая цепь содержит или состоит из аминокислотной последовательности SEQ ID NO 66 и
(ii) тяжелая цепь содержит или состоит из аминокислотных последовательностей SEQ ID NOs 67 или 76.
3. Фрагмент антитела по п. 1 или 2, где указанный фрагмент антитела выбран из группы, состоящей из Fab, Fab’, Fab’-SH, F(ab’)2 и Fv фрагментов, диател, однодоменных антител (Dabs), линейных антител, одноцепочечных молекул антитела (scFv) и дисульфид-стабилизированных фрагментов антитела (dsFv).
4. Композиция, пригодная в качестве агониста рецептора натрийуретического пептида, содержащая антитело или его фрагмент по любому из пп. 1-3 и необязательно фармацевтически приемлемый носитель.
5. Нуклеиновая кислота, кодирующая антитело или его фрагмент по любому из пп. 1-3.
6. Смесь нуклеиновых кислот, кодирующих антитело или его фрагмент по любому из пп. 1-3.
7. Нуклеиновая кислота, кодирующая антитело или его фрагмент по любому из пп. 1-3, где
(i) тяжелая цепь кодируется последовательностью, включающей или состоящей из SEQ ID NOs 82 или 83, и
(ii) легкая цепь кодируется последовательностью, включающей или состоящей из SEQ ID NO 84.
8. Смесь нуклеиновых кислот, кодирующих антитело или его фрагмент по любому из пп. 1-3, где
(i) тяжелая цепь кодируется последовательностью, включающей или состоящей из SEQ ID NOs 82 или 83, и
(ii) легкая цепь кодируется последовательностью, включающей или состоящей из SEQ ID NO 84.
9. Клетка-хозяин для получения антитела или его фрагмента по любому из пп. 1-3, содержащая нуклеиновую кислоту по п. 5 или 7 или смесь нуклеиновых кислот по п. 6 или 8.
10. Способ получения антитела или его фрагмента по любому из пп. 1-3, включающий культивирование клетки-хозяина по п. 9 в условиях, подходящих для экспрессии антитела или его фрагмента, и извлечение антитела или его фрагмента.
11. Биологически активный агент, обладающий свойствами агониста рецептора натрийуретического пептида, представляющий собой антитело или его фрагмент по любому из пп. 1-3.
12. Применение антитела или его фрагмента по любому из пп. 1-3 для лечения сердечно-сосудистых, почечных, легочных, скелетных, глазных, тромбоэмболических или фиброзных заболеваний или нарушений, карликовости, ахондроплазии или других связанных с cGMP и/или натрийуретическим пептидом нарушений.
| WO 2005082004 A2, 09.09.2005 | |||
| US 2004253242 A1, 16.12.2004 | |||
| US 2010310561 A1, 09.12.2010 | |||
| ШАРОШИНА И.А | |||
| и др., Роль натрийуретических пептидов в диагностике сердечной недостаточности, РОССИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 2003, N 2(40), стр.81-86. |
Авторы
Даты
2024-07-05—Публикация
2019-04-10—Подача