РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка заявляет приоритет по предварительной заявке США №62/277028, поданной 11 января 2016 года, все содержание которой включено в данный документ посредством ссылки в полном объеме.
ОБЛАСТЬ ТЕХНИКИ
[0002] Данное изобретение относится в целом к молекулам, которые специфически взаимодействуют с 41BB, представителем суперсемейства рецепторов TNF (TNFRSF). Более конкретно, данное изобретение относится к мультивалентным и/или мультиспецифическим молекулам, которые связывают по меньшей мере 41BB.
УРОВЕНЬ ТЕХНИКИ
[0003] Суперсемейство рецепторов фактора некроза опухоли состоит из нескольких структурно родственных рецепторов клеточной поверхности. Активация мультимерными лигандами является общей особенностью многих из этих рецепторов. Многие представители TNFRSF характеризуются терапевтической эффективностью при многочисленных патологиях, если они активированы должным образом. Агонизм этого семейства рецепторов часто требует кластеризации более высокого порядка, а обычные двухвалентные антитела не идеальны для этой цели. Следовательно, существует терапевтическая потребность в более мощных агонистических молекулах TNFRSF.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0004] В данном изобретении предлагаются мультивалентные и мультиспецифические слитые полипептиды, связывающие рецепторы суперсемейства TNF (TNFRSF), которые связывают по меньшей мере 41BB (также известный как представитель 4 суперсемейства рецепторов фактора некроза опухоли (TNFRSF9) и/или CD137)). Применение термина "41BB" предназначено для охвата любого его варианта, например, в качестве неограничивающего примера, 41-BB и/или 4-1BB, при этом все варианты применяются в данном документе взаимозаменяемо. Эти молекулы, которые связывают по меньшей мере 41BB, упоминаются в данном документе как "41BB-нацеленные молекулы" или "41BB-нацеленные слияния" или "41BB-нацеленные белки" или "41BB-нацеленные слитые полипептиды" или "41BB-нацеленные слитые белки". В некоторых вариантах осуществления данного изобретения 41BB-нацеленная молекула представляет собой мультивалентную молекулу, например, мультивалентный 41BB-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения 41BB-нацеленная молекула представляет собой мультиспецифическую молекулу, например, мультиспецифический 41BB-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения 41BB-нацеленная молекула представляет собой мультивалентную и мультиспецифическую молекулу, например, мультивалентный и мультиспецифический 41BB-нацеленный слитый белок. В данном контексте термин "слитый белок" или "слитый полипептид" или "41BB-нацеленный слитый белок" или "41BB-нацеленный слитый полипептид", если не оговорено особо специально, относится к любому варианту осуществления слияния белка в данном изобретении, включая, но не ограничиваясь ими, мультивалентные слитые белки, мультиспецифические слитые белки или мультивалентные и мультиспецифические слитые белки.
[0005] В данном изобретении также предлагаются мультивалентные и мультиспецифические слитые полипептиды, которые связывают по меньшей мере лиганд программируемой смерти 1 (PDL1), также известный как PD-L1, CD274, B7-гомолог 1 и/или B7-H1. Применение термина "PDL1" предназначено для охвата любого его варианта, например, в качестве неограничивающего примера, PD-L1 и/или PDL-1, при этом все варианты применяются в данном документе взаимозаменяемо. Эти молекулы, которые связывают по меньшей мере PDL1, упоминаются в данном документе как "PDL1-нацеленные молекулы" или "PDL1-нацеленные слияния" или "PDL1-нацеленные белки" или "PDL1 -нацеленные слитые полипептиды" или "PDL1-нацеленные слитые белки". В некоторых вариантах осуществления данного изобретения PDL1-нацеленная молекула представляет собой мультивалентную молекулу, например, мультивалентный PDL1-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения PDL1-нацеленная молекула представляет собой мультиспецифическую молекулу, например, мультиспецифический PDL1-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения PDL1-нацеленная молекула представляет собой мультивалентную и мультиспецифическую молекулу, например, мультивалентный и мультиспецифический PDL1-нацеленный слитый белок. В данном контексте термин "слитый белок" или "слитый полипептид" или "PDL1-нацеленный слитый белок" или "PDL1-нацеленный слитый полипептид", если не оговорено особо специально, относится к любому варианту осуществления слияния белка в данном изобретении, включая, но не ограничиваясь ими, мультивалентные слитые белки, мультиспецифические слитые белки или мультивалентные и мультиспецифические слитые белки.
[0006] В данном изобретении также предлагаются мультивалентные и мультиспецифические слитые полипептиды, которые связывают по меньшей мере PDL1 и 41BB. Эти молекулы, которые связывают по меньшей мере PDL1, упоминаются в данном документе как "PDL1х41BB-нацеленные молекулы" или "PDL1х41BB-нацеленные слияния" или "PDL1х41BB-нацеленные белки" или "PDL1х41BB-нацеленные слитые полипептиды" или "PDL1х41BB-нацеленные слитые белки". В некоторых вариантах осуществления данного изобретения молекула, нацеленная на PDL1х41BB, представляет собой мультивалентную молекулу, например, мультивалентный PDL1х41BB-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения PDL1х41BB-нацеленная молекула представляет собой мультиспецифическую молекулу, например, мультиспецифический PDL1х41BB-нацеленный слитый белок. В некоторых вариантах осуществления данного изобретения PDL1х41BB-нацеленная молекула представляет собой мультивалентную и мультиспецифическую молекулу, например, мультивалентный и мультиспецифическый PDL1-нацеленный слитый белок. В данном контексте термин "слитый белок" или "слитый полипептид" или "PDL1х41BB-нацеленный слитый белок" или "PDL1х41BB-нацеленный слитый полипептид", если не оговорено особо специально, относится к любому варианту осуществления слияния белка в данном изобретении, включая, но не ограничиваясь ими, мультивалентные слитые белки, мультиспецифические слитые белки или мультивалентные и мультиспецифические слитые белки.
[0007] В некоторых вариантах осуществления данного изобретения мультивалентный и/или мультиспецифический слитый белок связывает по меньшей мере 41BB. Было продемонстрировано, что обычные антитела, нацеленные на представителей суперсемейства рецепторов TNF <g (TNFRSF), требуют экзогенного перекрестного сшивания для достижения достаточной агонистической активности, о чем свидетельствует необходимость наличия Fc-гамма-рецептора (FcγRs) для активности антител к DR4, DR5, GITR и OX40 (Ichikawa et al 2001 al Nat. Med. 7, 954-960, Li et al 2008 Drug Dev. Res. 69, 69-82; Pukac et al 2005 Br. J. Cancer 92, 1430-1441; Yanda et al 2008 Ann. Oncol. 19, 1060-1067; Yang et al 2007 Cancer Lett. 251: 146-157; Bulliard et al 2013 JEM 210(9): 1685; Bulliard et al 2014 Immunol and Cell Biol 92: 475-480). В дополнение к перекрестному сшиванию посредством FcγRs были продемонстрированы другие экзогенные агенты, включая добавление единиц олигомерных лигандов или связывающих антител (например, белка А и вторичных антител) для усиления кластеризации антител анти-TNFRSF и нисходящей передачи сигнала, например, добавление лиганда DR5 TRAIL усиливало способность антитела анти-DR5 индуцировать апоптоз (Graves et al 2014 Cancer Cell 26: 177-189). Эти данные свидетельствуют о необходимости кластеризации TNFRSF за пределами димера.
[0008] В данном изобретении предлагаются мультивалентные TNFRSF-связывающие слитые белки, которые содержат 2 или большее количество TNFRSF-связывающих доменов (TBD), при этом по меньшей мере один TBD связывает 41BB. В некоторых вариантах осуществления данного изобретения слитые белки по данному изобретению пригодны для применения в лечении новообразований.
[0009] В некоторых вариантах осуществления данного изобретения слитый белок содержит два или большее количество разных TBD, при этом каждый TBD связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит множество копий TBD, который связывает 41BB, например, в некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере две копии TBD, который связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере три копии TBD, который связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере четыре копии TBD, который связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере пять копий TBD, который связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере шесть копий TBD, который связывает 41BB. В некоторых вариантах осуществления данного изобретения слитый белок содержит шесть или большее количество копий TBD, который связывает 41BB.
[0010] В других вариантах осуществления данного изобретения слитые белки по данному изобретению связывают 41BB и второй представитель семейства TNFRSF, например GITR, OX40, CD27, TNFR2 и/или CD40. В этих вариантах осуществления данного изобретения слитые белки по данному изобретению модулируют иммунные клетки, что приводит к усилению разрушения опухоли. В других вариантах осуществления данного изобретения слитые белки по данному изобретению пригодны для применения в лечении воспалительных патологических состояний. В этих вариантах осуществления данного изобретения слитые белки по данному изобретению модулируют иммунные клетки, что приводит к затуханию воспалительного процесса, например, специфическое агонистическое воздействие на TNFR2 может усилить пролиферацию Treg, что приводит к иммунной супрессии.
[0011] Слитые белки по данному изобретению способны к усиленной кластеризации представителей семейства TNFRSF по сравнению с двухвалентными антителами, без сшивания. Усиленная кластеризация представителей семейства TNFRSF, опосредованная слитыми белками по данному изобретению, индуцирует усиленную TNFRSF-зависимую сигнализацию по сравнению с двухвалентными антителами, без сшивания. В большинстве вариантов осуществления данного изобретения слитый белок будет включать в себя более 2 TBD, например три, четыре, пять или шесть.
[0012] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими TBD и связывающий домен, направленный на второй антиген. В этих вариантах осуществления данного изобретения связывание со вторым антигеном способно обеспечить дополнительную функцию сшивания, а активацию TNFRSF можно получить только с помощью одного или двух TBD. В этих вариантах осуществления данного изобретения сигнализация TNFRSF усиливается и фокусируется наличием второго антигена. Эти мультиспецифические TBD, содержащие слитые белки, являются пригодным средством для достижения осуществляемой при определенных условиях сигнализации конкретного представителя семейства TNFRSF.
[0013] В этих вариантах осуществления данного изобретения связывание с представителем семейства TNFRSF посредством TBD вызывает минимальную сигнализацию, если второй антиген не является совместно вовлеченным в связывание, например, мультиспецифические слитые белки по данному изобретению способны связывать 41BB и PD-L1, при этом 41BB-зависимая сигнализация значительно усиливается, когда слитый белок связывается с клеткой, экспрессирующей PD-L1. В другом примере, мультиспецифические слитые белки по данному изобретению способны связывать 41BB и рецептор фолиевой кислоты альфа (FRα), при этом 41BB-зависимая сигнализация значительно усиливается, когда слитый белок связывается с клеткой, экспрессирующей FRα.
[0014] В данном изобретении предлагаются выделенные полипептиды, которые специфически связывают 41BB. В некоторых вариантах осуществления данного изобретения выделенный полипептид является производным от антител или фрагментов антител, включая scFv, Fabs, однодоменные антитела (sdAb), VNAR или VHH. В некоторых вариантах осуществления данного изобретения выделенный полипептид представляет собой человеческое или гуманизированное sdAb. Фрагменты sdAb могут быть производными от VHH, VNAR, сконструированных доменов VH или VK. VHH могут быть получены из верблюжьих антител только с тяжелой цепью. VNAR могут быть получены из антител хрящевых рыб только с тяжелой цепью. В практику воплощены различные способы получения мономерных sdAb из обычных гетеродимерных доменов VH и VK, включая конструирование взаимодействия и выбор семейств специфических зародышевых линий. В других вариантах осуществления данного изобретения выделенные полипептиды являются производными от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0015] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83. В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83.
[0016] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83. В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83.
[0017] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 17, 21, 26, 30, 50, 65 и 69; область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 27, 31, 42, 44, 48, 52, 61, 63, 71, 73, 75, 77 и 79; область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19, 22, 24, 28, 32, 55 и 57.
[0018] В данном изобретении предлагаются мультивалентные слитые белки, которые содержат 2 или большее количество связывающих доменов (BD), при этом по меньшей мере один BD связывает PDL1. В некоторых вариантах осуществления данного изобретения слитые белки по данному изобретению пригодны для применения в лечении новообразований.
[0019] В некоторых вариантах осуществления данного изобретения слитый белок содержит два или большее количество разных BD, при этом каждый BD связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит множество копий BD, который связывает PDL1, например, в некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере две копии BD, который связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере три копии BD, который связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере четыре копии BD, который связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере пять копий BD, который связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит по меньшей мере шесть копий BD, который связывает PDL1. В некоторых вариантах осуществления данного изобретения слитый белок содержит шесть или большее количество копий BD, который связывает PDL1.
[0020] В данном изобретении предлагаются выделенные полипептиды, которые специфически связывают 41BB. В некоторых вариантах осуществления данного изобретения выделенный полипептид является производным от антител или фрагментов антител, включая scFv, Fabs, однодоменные антитела (sdAb), VNAR или VHH. В некоторых вариантах осуществления данного изобретения выделенный полипептид представляет собой человеческое или гуманизированное sdAb. Фрагменты sdAb могут быть производными от VHH, VNAR, сконструированных доменов VH или VK. VHH могут быть получены из верблюжьих антител только с тяжелой цепью. VNAR могут быть получены из антител хрящевых рыб только с тяжелой цепью. В практику воплощены различные способы получения мономерных sdAb из обычных гетеродимерных доменов VH и VK, включая конструирование взаимодействия и выбор семейств специфических зародышевых линий. В других вариантах осуществления данного изобретения выделенные полипептиды являются производными от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0021] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124. В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 119-124.
[0022] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124. В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 119-124.
[0023] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 101, 105 и 109; область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 106, 110 и 117; область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 103, 107, 111, 113, 115 и 118.
[0024] В некоторых вариантах осуществления данного изобретения предлагаются выделенные полипептиды, которые специфически связывают по меньшей мере 41BB и PDL1. В некоторых вариантах осуществления данного изобретения каждый связывающий домен (BD) в выделенном полипептиде является производным от антител или фрагментов антител, включая scFv, Fabs, однодоменные антитела (sdAb), VNAR или VHH. В некоторых вариантах осуществления данного изобретения каждый BD представляет собой человеческое или гуманизированное sdAb. Фрагменты sdAb могут быть производными от VHH, VNAR, сконструированных доменов VH или VK. VHH могут быть получены из верблюжьих антител только с тяжелой цепью. VNAR могут быть получены из антител хрящевых рыб только с тяжелой цепью. В практику воплощены различные способы получения мономерных sdAb из обычных гетеродимерных доменов VH и VK, включая конструирование взаимодействия и выбор семейств специфических зародышевых линий. В других вариантах осуществления данного изобретения выделенные полипептиды являются производными от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0025] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает первую аминокислотную последовательность, которая связывает 4B11, выбранную из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, а также вторую аминокислотную последовательность, которая связывает PDL1, выбранную из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124.
[0026] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает первую аминокислотную последовательность, которая связывает 4B11, выбранную из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, а также вторую аминокислотную последовательность, которая связывает PDL1, выбранную из группы, состоящей из SEQ ID NO: 119-124.
[0027] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает первую аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, которая связывает 4B11, выбранной из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, а также вторую аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, которая связывает PDL1, выбранной из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124.
[0028] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает первую аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, которая связывает 4B11, выбранной из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, а также вторую аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, которая связывает PDL1, выбранной из группы, состоящей из SEQ ID NO: 119-124.
[0029] В некоторых вариантах осуществления настоящего изобретения выделенный полипептид включает (i) первую аминокислотную последовательность, которая связывает 4B11, и содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 17, 21, 26, 30, 50, 65 и 69; область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 27, 31, 42, 44, 48, 52, 61, 63, 71, 73, 75, 77 и 79; область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19, 22, 24, 28, 32, 55 и 57; и (ii) вторую аминокислотную последовательность, которая связывает PDL1, и содержит CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 101, 105 и 109; CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 106, 110 и 117; и CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 103, 107, 111, 113, 115 и 118.
[0030] В некоторых вариантах осуществления данного изобретения связывающие домены (BD) по данному изобретению, например, 41BB-связывающие домены и/или PDL1-связывающие домены, являются производным от антител или фрагментов антител, включая scFv, Fabs, однодоменные антитела (sdAb), VNAR или VHH. В некоторых вариантах осуществления данного изобретения BD представляют собой человеческое или гуманизированное sdAb. Фрагменты sdAb могут быть производными от VHH, VNAR, сконструированных доменов VH или VK. VHH могут быть получены из верблюжьих антител только с тяжелой цепью. VNAR могут быть получены из антител хрящевых рыб только с тяжелой цепью. В практику воплощены различные способы получения мономерных sdAb из обычных гетеродимерных доменов VH и VK, включая конструирование взаимодействия и выбор семейств специфических зародышевых линий. В других вариантах осуществления данного изобретения BD являются производными от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0031] Как правило, слитые белки по данному изобретению состоят из по меньшей мере двух или большего количества BD, функционально связанных посредством линкерного полипептида. Применение фрагментов sdAb в качестве специфического BD в слиянии по данному изобретению имеет преимущество в предотвращении проблемы неправильного спаривания "тяжелая цепь - легкая цепь", характерного для многих подходов с применением би/мультиспецифических антител. Кроме того, в слитых белках по данному изобретению уклоняются от применения длинных линкеров, требуемых многими биспецифическими антителами.
[0032] В некоторых вариантах осуществления данного изобретения все BD слитого белка представляют собой TBD, которые распознают один и тот же эпитоп у данного представителя семейства TNFRSF, например, слитые белки по данному изобретению могут включать в себя 2, 3, 4, 5 или 6 TBD с идентичной специфичностью к 41BB. В других вариантах осуществления данного изобретения слитый белок включает TBD, которые распознают отдельные эпитопы у данного представителя семейства TNFRSF, например, слитые белки по данному изобретению могут включать 2, 3, 4, 5 или 6 TBD с четко отличающейся специфичностью распознавания относительно различных эпитопов на 41BB. В этих вариантах осуществления данного изобретения слитые белки по данному изобретению содержат множество TBD, которые нацелены на отдельные области конкретного представителя семейства TNFRSF. В других вариантах осуществления данного изобретения TBD могут распознавать различные эпитопы у одного и того же представителя семейства TNFRSF или распознавать эпитопы на разных представителях семейства TNFRSF, например, в данном изобретении предлагается мультиспецифические слитые белки, включающие TBD, которые связывают GITR и 41BB или OX40 и 41BB, или CD27 и 41BB.
[0033] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1. В некоторых вариантах осуществления данного изобретения биспецифический слитый белок включает 41BB-нацеленный связывающий домен, выбранный из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, функционально связанный со вторым связывающим доменом (BD2), который связывает PDL1. В некоторых вариантах осуществления данного изобретения BD2 содержит аминокислотную последовательность, которая специфически связывает PDL1. В некоторых вариантах осуществления данного изобретения BD2 содержит PDL1-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124. В некоторых вариантах осуществления данного изобретения BD2 содержит PDL1-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 119-124. В некоторых вариантах осуществления данного изобретения BD2 содержит аминокислотную последовательность, которая специфически связывает PDL1 и выбрана из группы, состоящей из SEQ ID NO: 126-408.
[0034] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1. В некоторых вариантах осуществления данного изобретения биспецифический слитый белок включает 41BB-нацеленный связывающий домен, выбранный из группы, состоящей из SEQ ID NO: 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, функционально связанный со вторым связывающим доменом (BD2), который связывает PDL1. В некоторых вариантах осуществления данного изобретения BD2 содержит аминокислотную последовательность, которая специфически связывает PDL1. В некоторых вариантах осуществления данного изобретения BD2 содержит PDL1-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124. В некоторых вариантах осуществления данного изобретения BD2 содержит PDL1-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 119-124. В некоторых вариантах осуществления данного изобретения BD2 содержит аминокислотную последовательность, которая специфически связывает PDL1 и выбрана из группы, состоящей из SEQ ID NO: 126-408.
[0035] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1. В некоторых вариантах осуществления данного изобретения биспецифический слитый белок включает PDL1-нацеленный связывающий домен, выбранный из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124, функционально связанный со вторым TBD (TBD2), который связывает 41BB. В некоторых вариантах осуществления данного изобретения TBD2 содержит аминокислотную последовательность, которая специфически связывает 41BB. В некоторых вариантах осуществления данного изобретения TBD2 содержит 41BB-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83. В некоторых вариантах осуществления данного изобретения TBD2 содержит аминокислотную последовательность, которая специфически связывает 41BB и выбрана из группы, состоящей из SEQ ID NO: 84-99.
[0036] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1. В некоторых вариантах осуществления данного изобретения биспецифический слитый белок включает PDL1-нацеленный связывающий домен, выбранный из группы, состоящей из SEQ ID NO: 119-124, функционально связанный со вторым TBD (TBD2), который связывает 41BB. В некоторых вариантах осуществления данного изобретения TBD2 содержит аминокислотную последовательность, которая специфически связывает 41BB. В некоторых вариантах осуществления данного изобретения TBD2 содержит 41BB-нацеленный домен, выбранный из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83. В некоторых вариантах осуществления данного изобретения TBD2 содержит аминокислотную последовательность, которая специфически связывает 41BB и выбрана из группы, состоящей из SEQ ID NO: 84-99.
[0037] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1 и содержит аминокислотную последовательность, которая выбрана из группы, состоящей из SEQ ID NO: 448-456.
[0038] В некоторых вариантах осуществления данного изобретения мультиспецифический слитый белок представляет собой биспецифическую молекулу, которая нацелена на 41BB и PDL1 и содержит аминокислотную последовательность, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 448-456.
[0039] В некоторых вариантах осуществления данного изобретения все BD слитого белка распознают один и тот же эпитоп на PDL1, например, слитые белки по данному изобретению могут включать в себя 2, 3, 4, 5 или 6 BD с идентичной специфичностью к PDL1. В других вариантах осуществления данного изобретения слитый белок включает BD, которые распознают отдельные эпитопы на PDL1, например, слитые белки по данному изобретению могут включать 2, 3, 4, 5 или 6 BD с четко выраженной специфичностью распознавания относительно различных эпитопов на PDL1. В этих вариантах осуществления данного изобретения слитые белки по данному изобретению содержат множество BD, которые нацелены на отдельные области PDL1. В других вариантах осуществления данного изобретения BD могут распознавать различные эпитопы на PDL1.
[0040] В некоторых вариантах осуществления данного изобретения слитый белок по данному изобретению состоит из одного полипептида. В других вариантах осуществления данного изобретения слитый белок по данному изобретению состоит из более чем одного полипептида, например, при этом домен гетеродимеризации включен в слитый белок, в результате чего получают конструкцию асимметричного слитого белка, например, если область Fc иммуноглобулина включена в слитый белок, домен CH3 можно применять в качестве домена гомодимеризации, или область взаимодействия димера CH3 можно подвергать мутации с целью обеспечения гетеродимеризации.
[0041] В некоторых вариантах осуществления данного изобретения слитый белок содержит противоположные концы BD, например, BD расположены как на аминоконцевой (N-концевой) части слитого белка, так и на карбокси-концевой (С-концевой) части слитого белка. В некоторых вариантах осуществления данного изобретения все TBD находятся на одном и том же конце слитого белка, например, BD находятся либо на амино-, либо на карбокси-концевых частях слитого белка.
[0042] В некоторых вариантах осуществления данного изобретения линкерный полипептид содержит область Fc иммуноглобулина. В определенных вариантах осуществления данного изобретения область Fc иммуноглобулина представляет собой изотип IgG, выбранный из группы, состоящей из подкласса IgG1, подкласса IgG2, подкласса IgG3 и подкласса IgG4.
[0043] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или его иммунологически активный фрагмент представляет собой изотип IgG, например, область Fc иммуноглобулина слитого белка относится к подклассу IgG1 человека, имеющему аминокислотную последовательность:

[0044] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или его иммунологически активный фрагмент содержит полипептидную последовательность IgG1 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 1.
[0045] В некоторых вариантах осуществления данного изобретения область Fc IgG1 человека модифицирована в положении аминокислоты Asn297 (показана в рамке в SEQ ID NO: 1-4, нумерация по Кабату) с целью предотвращения гликозилирования слитого белка, например, Asn297Ala (N297A) или Asn297Asp (N297D). В некоторых вариантах осуществления данного изобретения область Fc слитого белка модифицирована в положении аминокислоты Leu235 (полужирный шрифт в SEQ ID NO: 1, нумерация по Кабату) с целью изменения взаимодействий рецептора Fc, например, Leu235Glu (L235E) или Leu235Ala (L235A). В некоторых вариантах осуществления данного изобретения область Fc слитого белка модифицирована в положении аминокислоты Leu234 (полужирный шрифт в SEQ ID NO: 1, нумерация по Кабату) с целью изменения взаимодействий рецептора Fc, например, Leu234Ala (L234A). В некоторых вариантах осуществления данного изобретения область Fc слитого белка модифицирована в положении аминокислоты Leu234 (в рамке, нумерация по Кабату), с целью изменения взаимодействий рецептора Fc, например, Leu235Glu (L235E). В некоторых вариантах осуществления данного изобретения область Fc слитого белка изменена как в положении аминокислоты 234, так и 235, например, Leu234Ala и Leu235Ala (L234A/L235A) или Leu234Val и Leu235Ala (L234V/L235A). В некоторых вариантах осуществления данного изобретения область Fc слитого белка не содержит аминокислоту в одном или большем количестве из следующих положений с целью уменьшения связывания рецептора Fc: Glu233 (E233, полужирный шрифт в SEQ ID NO: 1), Leu234 (L234), или Leu235 (L235). В некоторых вариантах осуществления данного изобретения область Fc слитого белка изменена в положении Gly235 с целью уменьшения связывания рецептора Fc, например, при этом Gly235 удалена из слитого белка. В некоторых вариантах осуществления данного изобретения область Fc IgG1 человека модифицирована в положении аминокислоты Gly236 (показана в рамке в SEQ ID NO: 1) с целью улучшения взаимодействия с CD32A, например, Gly236Ala (G236A). В некоторых вариантах осуществления данного изобретения в области Fc IgG1 человека отсутствует Lys447 (индекс ЕС по Kabat et al 1991 Sequences of Proteins of Immunological Interest).
[0046] В некоторых вариантах осуществления данного изобретения область Fc слитого белка изменена в одном или большем количестве из следующих положений с целью уменьшения связывания рецептора Fc: Leu 234 (L234), Leu235 (L235), Asp265 (D265), Asp270 (D270), Ser298 (S298), Asn297 (N297), Asn325 (N325) или Ala327 (A327), например, Leu 234Ala (L234A), Leu235Ala (L235A), Asp265Asn (D265N), Asp270Asn (D270N), Ser298Asn (S298N), Asn297Ala (N297A), Asn325Glu (N325E) или rAla327Ser (A327S). В предпочтительных вариантах осуществления данного изобретения модификации в пределах области Fc уменьшают связывание с рецепторами Fc-рецептор-гамма, при этом оказывая минимальное влияние на связывание с неонатальным рецептором Fc (FcRn).
[0047] В некоторых вариантах осуществления данного изобретения область Fc слитого белка не содержит аминокислоту в одном или большем количестве из следующих положений с целью уменьшения связывания рецептора Fc: Glu233 (E233), Leu234 (L234) или Leu235 (L235). В этих вариантах осуществления делеция Fc этих трех аминокислот уменьшает связывание комплемента белка C1q. Эти модифицированные полипептиды области Fc упоминаются в данном документе как полипептиды "делеции Fc".
PAPGGPSVFL FPPKPKDTLM ISRTPEVTCV VVDVSHEDPE VKFNWYVDGV EVHNAKTKPR EEQYNSTYRV VSVLTVLHQD WLNGKEYKCK VSNKALPAPI EKTISKAKGQ PREPQVYTLP PSRDELTKNQ VSLTCLVKGF YPSDIAVEWE SNGQPENNYK TTPPVLDSDG SFFLYSKLTV DKSRWQQGNV FSCSVMHEAL HNHYTQKSLS LSPGK (SEQ ID NO: 2)
[0048] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или его иммунологически активный фрагмент содержит полипептидную последовательность IgG1 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 2.
[0049] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или иммунологически активный фрагмент слитого белка относится к подклассу IgG2 человека, имеющему аминокислотную последовательность:

[0050] В некоторых вариантах осуществления данного изобретения слитый белок или его иммунологически активный фрагмент содержит полипептидную последовательность IgG2 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 3.
[0051] В некоторых вариантах осуществления данного изобретения область Fc IgG2 человека модифицирована в положении аминокислоты Asn297 (показана в рамке в SEQ ID NO: 1, 3, 4, и 5), с целью предотвращения гликозилирования антитела, например, Asn297Ala (N297A). В некоторых вариантах осуществления данного изобретения в области Fc IgG2 человека отсутствует Lys447, что соответствует остатку 217 из SEQ ID NO: 3 (индекс ЕС по Kabat et al 1991 Sequences of Proteins of Immunological Interest).
[0052] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или иммунологически активный фрагмент слитого белка относится к подклассу IgG3 человека, имеющему аминокислотную последовательность:

[0053] В некоторых вариантах осуществления данного изобретения антитело или его иммунологически активный фрагмент содержит полипептидную последовательность IgG3 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 4.
[0054] В некоторых вариантах осуществления данного изобретения область Fc IgG3 человека модифицирована в положении аминокислоты Asn297 (показана в рамке в SEQ ID NO: 1-4, нумерация по Кабату) с целью предотвращения гликозилирования антитела, например, Asn297Ala (N297A). В некоторых вариантах осуществления данного изобретения область Fc IgG3 человека модифицирована в положении аминокислоты 435, с целью продления периода полужизни, например, Arg435His (R435H, показана в рамке в SEQ ID NO: 3). В некоторых вариантах осуществления данного изобретения в области Fc IgG3 человека отсутствует Lys447, что соответствует остатку 218 из SEQ ID NO: 4 (индекс ЕС по Kabat et al 1991 Sequences of Proteins of Immunological Interest).
[0055] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или иммунологически активный фрагмент слитого белка относится к подклассу IgG4 человека, имеющему аминокислотную последовательность:

[0056] В некоторых вариантах осуществления данного изобретения антитело или его иммунологически активный фрагмент содержит полипептидную последовательность IgG4 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 5.
[0057] В других вариантах осуществления данного изобретения область Fc IgG4 человека модифицирована в положении аминокислоты 235 с целью изменения взаимодействий рецептора Fc, например, Leu235Glu (L235E). В некоторых вариантах осуществления данного изобретения область Fc IgG4 человека модифицирована в положении аминокислоты Asn297 (показана в рамке в SEQ ID NO: 1-4, нумерация по Кабату) с целью предотвращения гликозилирования антитела, например, Asn297Ala (N297A). В некоторых вариантах осуществления данного изобретения в области Fc IgG4 человека отсутствует Lys447, что соответствует остатку 218 из SEQ ID NO: 5 (индекс ЕС по Kabat et al 1991 Sequences of Proteins of Immunological Interest).
[0058] В некоторых вариантах осуществления данного изобретения область Fc иммуноглобулина или иммунологически активный фрагмент слитого белка относится к изотипу IgG4 человека, имеющему аминокислотную последовательность:

[0059] В некоторых вариантах осуществления данного изобретения антитело или его иммунологически активный фрагмент содержит полипептидную последовательность IgG4 человека, которая по меньшей мере на 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности SEQ ID NO: 6.
[0060] В некоторых вариантах осуществления данного изобретения область Fc IgG человека модифицирована с целью усиления связывания FcRn. Примерами мутаций Fc, которые усиливают связывание с FcRn, являются Met252Tyr, Ser254Thr, Thr256Glu (M252Y, S254T, T256E, соответственно) (нумерация по Кабату, Dall'Acqua et al 2006, J. Biol Chem Vol. 281(33) 23514-23524), Met428Leu и Asn434Ser (M428L, N434S) (Zalevsky et al 2010 Nature Biotech, Vol. 28(2) 157-159), или Met252Ile, Thr256Asp, Met428Leu (M252I, T256D, M428L, соответственно), (индекс ЕС по Kabat et al 1991 Sequences of Proteins of Immunological Interest). Met252 соответствует остатку 23 в SEQ ID NO: 1, 4 и 5, а также остатку 22 в SEQ ID NO: 3. Ser254 соответствует остатку 25 в SEQ ID NO: 1, 4 и 5, а также остатку 24 в SEQ ID NO: 3. Thr256 соответствует остатку 27 в SEQ ID NO: 1, 4 и 5, а также остатку 26 в SEQ ID NO: 3. Met428 соответствует остатку 199 в SEQ ID NO: 1, 4 и 5, а также остатку 198 в SEQ ID NO: 3. Asn434 соответствует остатку 205 в SEQ ID NO: 1, 4 и 5, а также остатку 204 в SEQ ID NO: 3. В некоторых вариантах осуществления данного изобретения, в которых слитый белок по данному изобретению включает полипептид Fc, полипептид Fc мутирован или модифицирован. В этих вариантах осуществления данного изобретения мутантный или модифицированный полипептид Fc включает следующие мутации: Met252Tyr и Met428Leu (M252Y, M428L) согласно системы нумерации Кабата.
[0061] В некоторых вариантах осуществления данного изобретения область Fc IgG человека модифицирована с целью изменения антителозависимой клеточной цитотоксичности (ADCC) и/или комплементзависимой цитотоксичности (CDC), например, модификации аминокислот, описанные в Natsume et al., 2008 Cancer Res, 68(10): 3863-72; Idusogie et al., 2001 J Immunol, 166(4): 2571-5; Moore et al.,2010 mAbs, 2(2): 181-189; Lazar et al., 2006 PNAS, 103(11): 4005-4010, Shields et al., 2001 JBC, 276(9): 6591-6604; Stavenhagen et al., 2007 Cancer Res, 67(18): 8882-8890; Stavenhagen et al., 2008 Advan. Enzyme Regul., 48: 152-164; Alegre et al, 1992 J Immunol, 148: 3461-3468; см. обзор в Kaneko and Niwa, 2011 Biodrugs, 25(1): 1-11. Примеры мутаций, которые усиливают ADCC, включают модификацию в положении Ser239 и Ile332, например, Ser239Asp и Ile332Glu (S239D, I332E). Примеры мутаций, которые усиливают CDC, включают модификации в положении Lys326, что соответствует остатку 97 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 96 последовательности SEQ ID NO: 2, и Glu333, что соответствует остатку 104 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 103 последовательности SEQ ID NO: 3. В некоторых вариантах осуществления данного изобретения область Fc модифицирована в одном или обоих этих положениях, например, Lys326Ala и/или Glu333Ala (K326A и E333A).
[0062] В некоторых вариантах осуществления данного изобретения область Fc IgG человека модифицирована с целью индуцирования гетеродимеризации, например, с модификацией аминокислоты в домене CH3 в положении Thr366, которое при замене на более объемную аминокислоту, например, Trp (T366W), есть возможность преимущественного спаривания со вторым доменом СН3, имеющим аминокислотные модификации до менее объемных аминокислот в положениях Thr366, что соответствует остатку 137 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 136 последовательности SEQ ID NO: 3, Leu368, что соответствует остатку 139 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 138 последовательности SEQ ID NO: 2, и Tyr407, что соответствует остатку 178 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 177 последовательности SEQ ID NO: 3, например, Ser, Ala и Val, соответственно (T366S/L368A/Y407V). Гетеродимеризацию посредством модификаций CH3 можно дополнительно стабилизировать путем введения дисульфидной связи, например, путем изменения Ser354, что соответствует остатку 125 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 124 последовательности SEQ ID NO: 3, до Cys (S354C) и Tyr349, что соответствует остатку 120 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 119 последовательности SEQ ID NO: 3, до Cys (Y349C) на противоположных доменах CH3 (см. обзор в Carter, 2001 Journal of Immunological Methods, 248: 7-15). В некоторых из этих вариантов осуществления данного изобретения область Fc может быть модифицирована на участке связывания белка-A на одном представителе гетеродимера, с целью предотвращения связывания белка-A и тем самым обеспечения более эффективной очистки гетеродимерного слитого белка. Типовой модификацией на этом участке связывания является Ile253, что соответствует остатку 24 последовательностей SEQ ID NO: 1, 4 и 5, а также остатку 23 последовательности SEQ ID NO: 3, например, Ile253Arg (I253R), например, модификация I253R может сочетаться с модификациями T366S/L368A/Y407V или с модификациями T366W. T366S/L368A/Y407V-модифицированный Fc способен формировать гомодимеры, поскольку нет стерической окклюзии взаимодействия димеризации, которая характерна в случае T336W-модифицированного Fc. Поэтому в некоторых вариантах осуществления данного изобретения модификацию I253R комбинируют с T366S/L368A/Y407V-модифицированным Fc, чтобы препятствовать очистке любого гомодимерного Fc, который может образоваться.
[0063] В некоторых вариантах осуществления данного изобретения область Fc IgG человека модифицирована с целью предотвращения димеризации. В этих вариантах осуществления данного изобретения слитые белки по данному изобретению являются мономерными, например, модификация в остатке Thr366 до заряженного остатка, например, Thr366Lys, Thr366Arg, Thr366Asp или Thr366Glu (T366K, T366R, T366D или T366E, соответственно), предотвращает димеризацию CH3-CH3.
[0064] В некоторых вариантах осуществления данного изобретения область Fc слитого белка изменена в одном или большем количестве из следующих положений с целью уменьшения связывания рецептора Fc: Leu 234 (L234), Leu235 (L235), Asp265 (D265), Asp270 (D270), Ser298 (S298), Asn297 (N297), Asn325 (N325) или Ala327 (A327), например, Leu 234Ala (L234A), Leu235Ala (L235A), Asp265Asn (D265N), Asp270Asn (D270N), Ser298Asn (S298N), Asn297Ala (N297A), Asn325Glu (N325E) или rAla327Ser (A327S). В предпочтительных вариантах осуществления данного изобретения модификации в пределах области Fc уменьшают связывание с рецепторами Fc-рецептор-гамма, при этом оказывая минимальное влияние на связывание с неонатальным рецептором Fc (FcRn).
[0065] В некоторых вариантах осуществления данного изобретения слитый белок содержит полипептид, производный от шарнирной области иммуноглобулина. Шарнирная область может быть выбрана из любого из подклассов IgG человека, например, слитый белок может содержать модифицированный шарнир IgG1, имеющий последовательность EPKSSDKTHTCPPC (SEQ ID NO: 7), при этом в Cys220, который образует дисульфид с С-концевым цистеином легкой цепи, мутирует до серина, например, Cys220Ser (C220S). В других вариантах осуществления данного изобретения слитый белок содержит усеченный шарнир, имеющий последовательность DKTHTCPPC (SEQ ID NO: 8).
[0066] В некоторых вариантах осуществления данного изобретения слитый белок имеет модифицированный шарнир из IgG4, который модифицирован для предотвращения или уменьшения обмена нитей, например, Ser228Pro (S228P), имеющий поседовательность ESKYGPPCPPC (SEQ ID NO: 9). В некоторых вариантах осуществления данного изобретения слитый белок содержит один или большее количество линкерных полипептидов. В других вариантах осуществления данного изобретения слитый белок содержит линкерные и шарнирные полипептиды.
[0067] В некоторых вариантах осуществления данного изобретения в слитых белках по данному отсутствует или содержится уменьшенное количество фукозы, присоединенной к N-связанной гликановой цепи в положении N297. Существует множество способов предотвращения фукозилирования, включая, но не ограничиваясь ими, продукцию в линии клеток с дефицитом FUT8; применение дополнительных ингибиторов присоединения к среде для культивирования клеток млекопитающих, например, кастаноспермина, 2-дезоксифукозы, 2-флурофукозы; применение продуцирующих линий клеток с естественно сниженной функцией путей фукозилирования, а также метаболического конструирования продуцирующей линии клеток.
[0068] В некоторых вариантах осуществления данного изобретения однодоменное антитело, VHH, или гуманизированное однодоменное антитело или однодоменное антитело человека сконструировано для устранения распознавания ранее существовавшими антителами, обнаруженными у людей. В некоторых вариантах осуществления данного изобретения однодоменные антитела по данному изобретению модифицированы посредством мутации положения Leu11, например, Leu11Glu (L11E) или Leu11Lys (L11K). В других вариантах осуществления данного изобретения однодоменные антитела по данному изобретению модифицированы посредством изменений в карбоксиконцевой области, например, терминальная последовательность состоит из GQGTLVTVKPGG (SEQ ID NO: 14) или GQGTLVTVEPGG (SEQ ID NO: 15) или их модификации. В некоторых вариантах осуществления данного изобретения однодоменные антитела по данному изобретению модифицированы посредством мутации положения 11 и посредством изменений в карбоксиконцевой области.
[0069] В некоторых вариантах осуществления данного изобретения BD слитых белков по данному изобретению являются функционально связанными посредством аминокислотных линкеров. В некоторых вариантах осуществления данного изобретения указанные линкеры состоят преимущественно из аминокислот глицин и серин, обозначенных в данном документе как GS-линкеры. GS-линкеры слитых белков по данному изобретению могут иметь разную длину, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 аминокислот в длину.
[0070] В некоторых вариантах осуществления настоящего изобретения GS-линкер содержит аминокислотную последовательность, выбранную из группы, состоящей из GGSGGS, то есть, (GGS)2 (SEQ ID NO: 10); GGSGGSGGS, т. e., (GGS)3 (SEQ ID NO: 11); GGSGGSGGSGGS, т. e., (GGS)4 (SEQ ID NO: 12); а также GGSGGSGGSGGSGGS, т. e., (GGS)5 (SEQ ID NO: 13).
[0071] В некоторых вариантах осуществления данного изобретения мультивалентный связывающий слитый белок является тетравалентным. В некоторых вариантах осуществления данного изобретения тетравалентный слитый белок имеет следующую структуру: BD-линкер-BD-линкер-шарнир-Fc. В некоторых вариантах осуществления данного изобретения тетравалентный слитый белок имеет следующую структуру: BD-линкер-шарнир-Fc-линкер-BD.
[0072] В некоторых вариантах осуществления данного изобретения BD тетравалентного слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения каждый BD тетравалентного слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения тетравалентный слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-шарнир-Fc, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH. В некоторых вариантах осуществления данного изобретения тетравалентный слитый белок имеет следующую структуру: VHH-линкер-шарнир-Fc-линкер-VHH, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0073] В некоторых вариантах осуществления данного изобретения мультивалентный TNFRSF-связывающий слитый белок является тетравалентным. В некоторых вариантах осуществления данного изобретения тетравалентный TNFRSF-связывающий слитый белок имеет следующую структуру: TBD-линкер-TBD-линкер-шарнир-Fc. В некоторых вариантах осуществления данного изобретения тетравалентный TNFRSF-связывающий слитый белок имеет следующую структуру: TBD-линкер-шарнир-Fc-линкер-TBD.
[0074] В некоторых вариантах осуществления данного изобретения TBD тетравалентного TNFRSF-связывающего слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения каждый TBD мультивалентного TNFRSF- связывающего слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения тетравалентный TNFRSF-связывающий слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-шарнир-Fc, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH. В некоторых вариантах осуществления данного изобретения тетравалентный TNFRSF-связывающий слитый белок имеет следующую структуру: VHH-линкер-шарнир-Fc-линкер-VHH, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0075] В некоторых вариантах осуществления настоящего изобретения GS-линкер содержит аминокислотную последовательность, выбранную из группы, состоящей из GGSGGS, то есть, (GGS)2 (SEQ ID NO: 10); GGSGGSGGS, т. e., (GGS)3 (SEQ ID NO: 11); GGSGGSGGSGGS, т. e., (GGS)4 (SEQ ID NO: 12); а также GGSGGSGGSGGSGGS, т. e., (GGS)5 (SEQ ID NO: 13).
[0076] В некоторых вариантах осуществления данного изобретения мультивалентный слитый белок является гексавалентным. В некоторых вариантах осуществления данного изобретения гексавалентный слитый белок имеет следующую структуру: BD-линкер-TBD-линкер-BD-линкер-шарнир-Fc. В некоторых вариантах осуществления данного изобретения гексавалентный слитый белок имеет следующую структуру: BD-линкер-BD-линкер-шарнир-Fc-линкер-BD, или BD-линкер-шарнир-Fc-линкер-BD-линкер-BD.
[0077] В некоторых вариантах осуществления данного изобретения BD гексавалентного слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения каждый BD гексавалентного слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения гексавалентный слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-шарнир-Fc, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH. В некоторых вариантах осуществления данного изобретения гексавалентный слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-шарнир-Fc-линкер-VHH, или VHH-линкер-шарнир-Fc-линкер-VHH-линкер-VHH, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0078] В некоторых вариантах осуществления данного изобретения мультивалентный TNFRSF-связывающий слитый белок является гексавалентным. В некоторых вариантах осуществления данного изобретения гексавалентный TNFRSF-связывающий слитый белок имеет следующую структуру: TBD-линкер-TBD-линкер-TBD-линкер-шарнир-Fc. В некоторых вариантах осуществления данного изобретения гексавалентный TNFRSF-связывающий слитый белок имеет следующую структуру: TBD-линкер-TBD-линкер-шарнир-Fc-линкер-TBD или TBD-линкер-шарнир-Fc-линкер-TBD-линкер-TBD.
[0079] В некоторых вариантах осуществления данного изобретения TBD гексавалентного TNFRSF-связывающего слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения каждый TBD гексавалентного TNFRSF- связывающего слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения гексавалентный TNFRSF-связывающий слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-шарнир-Fc, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH. В некоторых вариантах осуществления данного изобретения гексавалентный TNFRSF-связывающий слитый белок имеет следующую структуру: VHH-линкер-VHH-линкер-шарнир-Fc-линкер-VHH, или VHH-линкер-шарнир-Fc-линкер-VHH-линкер-VHH, при этом VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0080] В некоторых вариантах осуществления данного изобретения у мультивалентного слитого белка отсутствует область Fc. В некоторых из этих вариантов осуществления данного изобретения слитый белок является тетравалентным и имеет следующую структуру: BD-линкер-BD-линкер-BD-линкер-BD-линкер. В некоторых из этих вариантов осуществления данного изобретения слитый белок является пентавалентным и имеет следующую структуру: BD-линкер-BD-линкер-BD-линкер-BD-линкер-BD. В некоторых из этих вариантов осуществления данного изобретения слитый белок является гексавалентным и имеет следующую структуру: BD-линкер-BD-линкер-BD-линкер-BD-линкер-BD-линкер-BD.
[0081] В некоторых вариантах осуществления данного изобретения у мультивалентного TNFRSF-связывающего слитого белка отсутствует область Fc. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является тетравалентным и имеет следующую структуру: TBD-линкер-TBD-линкер-TBD-линкер-TBD-линкер. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является пентавалентным и имеет следующую структуру: TBD-линкер-TBD-линкер-TBD-линкер-TBD-линкер-TBD. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является гексавалентным и имеет следующую структуру: TBD-линкер-TBD-линкер-TBD-линкер-TBD-линкер-TBD-линкер-TBD.
[0082] В некоторых вариантах осуществления данного изобретения BD мультивалентного слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения у мультивалентного слитого белка отсутствует область Fc. В некоторых из этих вариантов осуществления данного изобретения слитый белок является тетравалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер. В некоторых из этих вариантов осуществления данного изобретения слитый белок является пентавалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH. В некоторых из этих вариантов осуществления данного изобретения слитый белок является гексавалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH. В любом из этих вариантов осуществления данного изобретения VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0083] В некоторых вариантах осуществления данного изобретения TBD мультивалентного TNFRSF-связывающего слитого белка представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения у мультивалентного TNFRSF-связывающего слитого белка отсутствует область Fc. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является тетравалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является пентавалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH. В некоторых из этих вариантов осуществления данного изобретения TNFRSF-связывающий слитый белок является гексавалентным и имеет следующую структуру: VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH-линкер-VHH. В любом из этих вариантов осуществления данного изобретения VHH представляет собой гуманизированную или полностью человеческую последовательность VHH.
[0084] В некоторых вариантах осуществления настоящего изобретения GS-линкер содержит аминокислотную последовательность, выбранную из группы, состоящей из GGSGGS, то есть,(GGS)2 (SEQ ID NO: 10); GGSGGSGGS, т. e., (GGS)3 (SEQ ID NO: 11); GGSGGSGGSGGS, т. e., (GGS)4 (SEQ ID NO: 12); а также GGSGGSGGSGGSGGS, т. e., (GGS)5 (SEQ ID NO: 13).
[0085] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими TBD и связывающий домен, направленный на второй антиген. В этих вариантах осуществления данного изобретения второй антигенсвязывающий домен может быть расположен во многих положениях внутри молекулы относительно TBD. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в N-концевом положении относительно TBD. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в С-концевом положении относительно TBD. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен на отдельном полипептиде, который связывается с первым полипептидом, содержащим TBD.
[0086] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими анти-41BB-связывающий домен и связывающий домен, направленный на второй антиген. В этих вариантах осуществления данного изобретения второй антигенсвязывающий домен может быть расположен во многих положениях внутри молекулы относительно анти-41BB-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в N-концевом положении относительно анти-41BB-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в С-концевом положении относительно анти-41BB-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен на отдельном полипептиде, который связывается с первым полипептидом, содержащим анти-41BB-связывающий домен.
[0087] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими анти-PDL1-связывающий домен и связывающий домен, направленный на второй антиген. В этих вариантах осуществления данного изобретения второй антигенсвязывающий домен может быть расположен во многих положениях внутри молекулы относительно анти-PDL1-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в N-концевом положении относительно анти-PDL1-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен в С-концевом положении относительно анти-PDL1-связывающего домена. В некоторых вариантах осуществления данного изобретения второй антигенсвязывающий домен расположен на отдельном полипептиде, который связывается с первым полипептидом, содержащим анти-PDL1-связывающий домен.
[0088] В некоторых вариантах осуществления данного изобретения TBD в мультиспецифическом TNFRSF-связывающем слитом белке представляет собой однодоменное антитело или VHH. В некоторых вариантах осуществления данного изобретения TBD в мультиспецифическом TNFRSF-связывающем слитом белке состоит из области вариабельной тяжелой цепи (VH) и вариабельной легкой цепи (VL) антитела. В некоторых вариантах осуществления данного изобретения VH и VL в TBD отформатированы в виде одноцепочечного вариабельного фрагмента (scFv), присоединенного посредством линкерной области. В некоторых вариантах осуществления данного изобретения VH и VL в TBD отформатированы в виде фрагмента FAB, который связывается посредством константного домена тяжелой цепи 1 (CH1) и константного домена легкой цепи (CL). В некоторых вариантах осуществления данного изобретения неантительные домены гетеродимеризации применяют для обеспечения надлежащей связи VH и VL в TBD. В некоторых вариантах осуществления данного изобретения TBD в мультиспецифическом TNFRSF-связывающем слитом белке является производным от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0089] В некоторых вариантах осуществления данного изобретения TBD в мультиспецифическом TNFRSF-связывающем слитом белке представляет собой однодоменное антитело или VHH, которое связывает 41BB. В некоторых вариантах осуществления данного изобретения анти-41BB-связывающий домен в мультиспецифическом TNFRSF-связывающем слитом белке состоит из области вариабельной тяжелой цепи (VH) и вариабельной легкой цепи (VL) антитела. В некоторых вариантах осуществления данного изобретения VH и VL в анти-41BB-связывающем домене отформатированы в виде одноцепочечного вариабельного фрагмента (scFv), присоединенного посредством линкерной области. В некоторых вариантах осуществления данного изобретения VH и VL в анти-41BB-связывающем домене отформатированы в виде фрагмента Fab, который связывается посредством константного домена тяжелой цепи 1 (CH1) и константного домена легкой цепи (CL). В некоторых вариантах осуществления данного изобретения неантительные домены гетеродимеризации применяют для обеспечения надлежащей связи VH и VL в анти-41BB-связывающем домене. В некоторых вариантах осуществления данного изобретения анти-41BB-связывающий домен в мультиспецифическом TNFRSF-связывающем слитом белке является производным от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0090] В некоторых вариантах осуществления данного изобретения связывающий домен в мультиспецифическом слитом белке представляет собой однодоменное антитело или VHH, которое связывает PDL1. В некоторых вариантах осуществления данного изобретения анти-PDL1-связывающий домен в мультиспецифическом TNFRSF-связывающем слитом белке состоит из области вариабельной тяжелой цепи (VH) и вариабельной легкой цепи (VL) антитела. В некоторых вариантах осуществления данного изобретения VH и VL в анти-PDL1-связывающем домене отформатированы в виде одноцепочечного вариабельного фрагмента (scFv), присоединенного посредством линкерной области. В некоторых вариантах осуществления данного изобретения VH и VL в анти-PDL1-связывающем домене отформатированы в виде фрагмента Fab, который связывается посредством константного домена тяжелой цепи 1 (CH1) и константного домена легкой цепи (CL). В некоторых вариантах осуществления данного изобретения неантительные домены гетеродимеризации применяют для обеспечения надлежащей связи VH и VL в анти-PDL1-связывающем домене. В некоторых вариантах осуществления данного изобретения анти-PDL1-связывающий домен в мультиспецифическом слитом белке является производным от неантительных каркасных белков, например, но не ограничиваясь ими, сконструированных белков с анкириновыми повторами (дарпины), авимеров, антикалин/липокалинов, центиринов и финомеров.
[0091] В некоторых вариантах осуществления данного изобретения анти-41BB-связывающий домен мультиспецифического TNFRSF-связывающего слитого белка представляет собой биспецифическое антитело или его антигенсвязывающий фрагмент.
[0092] В некоторых вариантах осуществления данного изобретения анти-PDL1-связывающий домен мультиспецифического слитого белка представляет собой биспецифическое антитело или его антигенсвязывающий фрагмент.
[0093] В любом из этих вариантов осуществления данного изобретения биспецифическое антитело или его антиген-фрагмент может быть в любом пригодном биспецифическом форматоме, известным в данной области техники, включая, в качестве неограничивающего примера, форматы на основе фрагментов антител, такие как, например, X-сшитые Fab, сшитые фрагменты Fab; tascFv/BiTE, тандем-scFv/привлекающий T-клетки биспецифический активатор; Db, диатело; taDb, тандемные диатела; форматы на основе Fc-слияний, такие как, например, Db-Fc, слияние "диатело-Fc"; taDb-Fc, тандемное слияние "диатело-Fc"; taDb-CH3, тандемное слияние "диатело-CH3"; (scFv) 4-Fc, тетра-слияние scFv-Fc; DVD-Ig, иммуноглобулин с двойным вариабельным доменом; форматы IgG, такие как, например, "выступ-во-впадину" и SEED, сконструированный домен с обменом цепей; CrossMab, "выступ-во-впадину" в комбинации с обменом тяжелой и легкой цепи домена; bsAb, биспецифическое антитело, производное от квадромы; sdAb, антитело на основе одного домена; и тела каппа-лямбда, такие как те, которые описаны в публикации PCT No. WO 2012/023053.
[0094] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83.
[0095] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83.
[0096] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 17, 21, 26, 30, 50, 65 и 69; область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 27, 31, 42, 44, 48, 52, 61, 63, 71, 73, 75, 77 и 79; область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19, 22, 24, 28, 32, 55 и 57.
[0097] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один BD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124.
[0098] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один BD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 119-124.
[0099] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один BD содержит CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 101, 105 и 109; CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 106, 110 и 117; и CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 103, 107, 111, 113, 115 и 118.
[00100] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 16, 20, 23, 25, 29, 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, и по меньшей мере один BD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 100, 104, 108, 112, 114, 116 и 119-124.
[00101] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 33, 39, 33-41, 43, 45-47, 49, 51, 53, 54, 56, 58-60, 62, 65, 66, 68, 70, 72, 74, 76, 78 и 80-83, и по меньшей мере один BD содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 119-124.
[00102] В любом из вышеприведенных вариантов осуществления данного изобретения по меньшей мере один TBD содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 17, 21, 26, 30, 50, 65 и 69; область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 27, 31, 42, 44, 48, 52, 61, 63, 71, 73, 75, 77 и 79; область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19, 22, 24, 28, 32, 55 и 57, и по меньшей мере один BD содержит CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 101, 105 и 109; CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 106, 110 и 117; и CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 103, 107, 111, 113, 115 и 118.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[00103] На Фигуре 1 приведена схема типовых мультивалентных и мультиспецифических слитых белков по данному изобретению.
[00104] На Фигурах 2A и 2B приведена пара графиков, демонстрирующих способность 41BB однодоменных антител (sdAb) связывать рекомбинантный 41BB человека (Фигура 2A) или 41BB яванского макака (Фигура 2B). Связывание оценивали с помощью ИФА, при этом рекомбинантный белок 41BB-mFc иммобилизовали на 96-луночном планшете Medisorp.
[00105] На Фигуре 3 приведен график, демонстрирующий способность 41BB однодоменных антител (sdAb) связывать 41BB на поверхности клетки. Связывание оценивали с помощью проточной цитометрии с применением клеток СНО, экспрессирующих 41BB, при этом данные представляли как медианную интенсивность флуоресценции.
[00106] На Фигуре 4 приведен график, демонстрирующий способность 41BB однодоменных антител, RH3 и 4H04, связывать 41BB яванского макака. Связывание оценивали с помощью ИФА, при этом рекомбинантный белок 41BB-mFc иммобилизовали на 96-луночном планшете Medisorp.
[00107] На Фигуре 5 приведен график, демонстрирующий способность 41BB однодоменных антител (VHH) блокировать взаимодействие между 41BB и 41BBL. Все анализируемые однодоменные антитела, за исключением RH3, блокируют взаимодействие между 41BB и 41BBL. Блокирование оценивали с помощью проточной цитометрии с применением рекомбинантного слитого белка 41BB и клеток СНО, экспрессирующих 41BB, при этом данные представляли как медианную интенсивность флуоресценции.
[00108] На Фигуре 6 приведен график, демонстрирующий неспособность обычного двухвалентного анти-41BB-антитела PF-05082566 индуцировать передачу сигналов 41BB, за исключением тех случаев, когда осуществляется дополнительная кластеризация с экзогенным сшивающим антителом против IgG человека. Передачу сигналов 41BB контролировали с применением NFkB репортерной клеточной линии 293, экспрессирующей 41BB.
[00109] На Фигурах 7A и 7B приведена пара графиков, демонстрирующих способность типового однодоменного антитела PDL1 (28A10) связывать PDL1 на поверхности клетки и блокировать взаимодействие с PD1. Связывание (Фигура 7А) оценивали с помощью проточной цитометрии на клетках СНО, экспрессирующих PDL1. Блокирование (Фигура 7B) оценивали с помощью проточной цитометрии с применением рекомбинантного слитого белка PD1 и клеток СНО, экспрессирующих PDL1, при этом данные представляли как медианную интенсивность флуоресценции.
[00110] Фигуры 8A, 8B и 8C представляют собой серию иллюстраций и график, изображающий PDL1-зависимый агонизм 41BB, опосредованный биспецифическими слитыми белками по данному изобретению, нацеленными на PDL1-41BB. На Фигурах 8А и 8В приведены концептуальные схемы, в которых биспецифические слитые белки имеют минимальные агонистические свойства 41BB (Фигура 8А), за исключением случаев, когда они связаны клеткой, экспрессирующей PD-L1 (Фигура 8В). На Фигуре 8С приведен график, демонстрирующий способность PDL1-позитивной клетки (в данном документе PDL1-трансфицированных клеток CHO) опосредовать передачу сигналов 41BB и неспособность PDL1-негативной клетки (в данном документе нетрансфицированных клеток CHO) опосредовать передачу сигналов 41BB. Передачу сигналов 41BB контролировали с применением NFkB репортерной клеточной линии 293, экспрессирующей 41BB.
[00111] На Фигурах 9A, 9B, 9C, 9D и 9E приведен ряд графиков, демонстрирующих связывание гуманизированных вариантов RH3 с 41BB человека (Фигура 9A и Фигура 9C) или яванского макака (Фигура 9B и Фигура 9D). Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB. На Фигуре 9Е приведен график, демонстрирующий, что гуманизированные варианты hzRH3v5-1 и hzRH3v9 не блокируют связывание 41BBL с 41BB на поверхности клетки. В этих исследованиях применяли рекомбинантный слитый белок 41BBL-mFc, содержащий область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00112] На Фигуре 10 приведен график, демонстрирующий специфическое связывание hzRH3v5-1 (40 нМ) с 41BB по сравнению с другими представителями семейства TNFRSF: OX40 и GITR. Связывание оценивали с помощью проточной цитометрии с применением клеток CHO, экспрессирующих данный представитель семейства TNFRSF.
[00113] На Фигурах 11A, 11B, 11C и 11D приведен ряд графиков, демонстрирующих связывание гуманизированных вариантов 4E01 с 41BB человека (Фигура 11A и Фигура 11C) или яванского макака (Фигура 11B). Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB. На Фигуре 11D приведен график, демонстрирующий, что гуманизированные варианты hz4E01v16, hz4E01v18, hz4E01v21, hz4E01v22 и hz4E01v23 блокируют связывание 41BBL с 41BB на поверхности клетки. В этих исследованиях применяли рекомбинантный слитый белок 41BBL-mFc, содержащий область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00114] На Фигуре 12 приведен график, демонстрирующий связывание гуманизированных однодоменных антител, нацеленных на PDL1. Связывание оценивали с помощью проточной цитометрии на клетках СНО, экспрессирующих PDL1.
[00115] На Фигуре 13 приведено схематическое изображение двух типовых форматов биспецифического PDL1х41BB, INBRX-105-1. INBRX-105-1-A (слева) имеет PDL1- и 41BB-связывающие домены, расположенные в противоположных конечных положениях от центральной области Fc, тогда как INBRX-105-1-B (справа) имеет PDL1- и 41BB-связывающие домены, расположенные в тандеме, на N-конце относительно области Fc.
[00116] На Фигурах 14A, 14B и 14C приведен ряд графиков, демонстрирующих эквивалентное связывание с 41BB человека (Фигура 14A) или яванского макака (Фигура 14B) посредством двух различных форматов биспецифического слитого белка, нацеленных на PDL1 и 41BB, и обозначенных в данном документе как INBRX-105-1-A и INBRX-105-1-B. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB. На Фигуре 14С приведен график, демонстрирующий, что биспецифический слитый белок, содержащий hzRh3v5-1, не блокирует связывание 41BBL с 41BB на поверхности клетки. В этих исследованиях применяли рекомбинантный слитый белок 41BBL и область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00117] На Фигурах 15A, 15B, 15C и 15D приведен ряд графиков, демонстрирующих эквивалентное связывание (Фигура 15А и Фигура 15С) и блокирование PD1 (Фигура 15B и Фигура 15D) посредством двух различных форматов биспецифического слитого белка, нацеленных на PDL1 и 41BB, и обозначенных в данном документе как INBRX-105-1-A и INBRX-105-1-B. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle человека (Фигура 15A) или яванского макака (Фигура 15С), экспрессирующих PDL1. Блокирование оценивали с помощью проточной цитометрии на клетках 293freestyle человека (Фигура 15В) или яванского макака (Фигура 15D), экспрессирующих PDL1, либо с рекомбинантным слитым белком PD1-mFc человека (Фигура 15B), либо яванского макака (Фигура 15D). Связывание PD1 обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00118] На Фигуре 16 приведен график, демонстрирующий способность гуманизированных версий биспецифического слитого белка PDL1х41BB (INBRX-105-1) индуцировать PDL1-зависимый агонизм 41BB. 41BB-экспрессирующую NFkB репортерную клеточную линию HEK293 применяли для оценки передачи сигналов 41BB, а в качестве источника PDL1 применяли PDL1-экспрессирующую линию клеток CHO.
[00119] На Фигурах 17A и 17B приведена пара графиков, демонстрирующих 41BB-специфическое связывание посредством 41BB-связывающей части биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB (Фигура 17A) или ближайший гомолог, TNFRSF21/DR6 (Фигура 17B). Антитело анти-DR6 (Invitrogen) применяли в качестве положительного контроля экспрессии DR6.
[00120] На Фигурах 18A, 18B и 18С приведен ряд графиков, демонстрирующих PDL1-специфическое связывание посредством PDL1-связывающей части биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих PDL1 (Фигура 18A) или его ближайший гомолог PDL2 (Фигура 18B) или VISTA/PDL3 (Фигура 18C)Антитела анти-PDL2 и анти-VISTA применяли в качестве положительных контролей экспрессии PDL2 и PDL3 соответственно.
[00121] На Фигурах 19A и 19B приведена пара графиков, демонстрирующих способность биспецифического слитого белка PDL1х41BB одновременно связывать PDL1 и 41BB. Связывание 41BB обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши. На Фигуре 19A приведен график, демонстрирующий связывание INBRX-105-1 с клетками K562, экспрессирующими PDL1. На Фигуре 19В приведен график, демонстрирующий связывание рекомбинантного 41BB с INBRX-105-1 на клетках, экспрессирующих PDL1.
[00122] На Фигуре 20 приведен график, демонстрирующий способность биспецифического слитого белка PDL1х41BB одновременно связывать рекомбинантный PDL1 и рекомбинантный 41BB в анализе ИФА. Связанный рекомбинантный 41BB обнаруживали с применением стрептавидина-HRP.
[00123] На Фигурах 21A, 21B и 21С приведен ряд графиков, демонстрирующих эффект биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению на активацию и пролиферацию Т-клеток. Продукцию INFγ в супернатанте клеток контролировали с помощью анализа ИФА и нормировали на стандартную кривую. Пролиферацию Т-клеток контролировали с помощью проточной цитометрии с применением CTV-мечения Т-клеток. Активацию Т-клеток оценивали по наличию активационного маркера CD25, контролируемого с помощью проточной цитометрии. Антитела применяли при концентрации 10 нМ.
[00124] На Фигурах 22A и 22B приведена пара графиков, демонстрирующих PDL1-зависимый агонизм 41BB, опосредованный биспецифическим слитым белком PDL1х41BB (INBRX-105-1) по данному изобретению. Пролиферацию CD8+ Т-клеток (Фигура 22A) контролировали с применением CTV-мечения, а продукцию INFγ (Фигура 22B) в супернатанте клеток контролировали с помощью анализа ИФА и нормировали на стандартную кривую.
[00125] На Фигуре 23 приведен график, демонстрирующий способность биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению усиливать фактор транскрипции, определяемый линией Th1, T-bet, экспрессирумый в популяциях Т-клеток. Экспрессию T-bet оценивали на популяции CD4+ и CD8+ T-клеток с помощью проточной цитометрии путем внутриклеточного окрашивания после фиксации и пермеабилизации.
[00126] На Фигурах 24A и 24B приведена пара графиков, сопоставляющих способность биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению и комбинации моноспецифических антител Атезолизумаб (анти-PDL1) и Утомилумаб (анти-41BB) индуцировать продукцию INFγ (Фигура 24A) или TNFα (Фигура 24B) из CD4+ или CD8+ T-клеток. Экспрессию цитокинов оценивали на популяции CD4+ и CD8+ T-клеток с помощью проточной цитометрии путем внутриклеточного окрашивания после фиксации и пермеабилизации.
[00127] На Фигурах 25A и 25B приведена пара графиков, демонстрирующих агонистическую способность тетравалентного 41BB-связывающего слитого белка и биспецифических слитых белков PDL1х41BB по данному изобретению в присутствии дополнительной PDL1-позитивной (Фигура 25A) или негативной (Фигура 25B) линии клеток. В этом исследовании применяли 41BB-экспрессирующую NFkB репортерную клетку HEK293 и совместно инкубировали либо с PDL1-негативной линией клеток K562 (Фигура 25B), либо со стабильно трансфицированной PDL1-экспрессирующей линией клеток K562 (Фигура 25A).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00128] Все патенты и публикации, упомянутые в этом описании, включены в настоящую заявку посредством ссылок в том же объеме, как если бы каждый независимый патент и публикация специально и отдельно были указаны как включенные в настоящую заявку посредством ссылки.
Определения
[00129] Если не указано иное, научные и технические термины, используемые в связи с данным изобретением, должны иметь значения, которые обычно понятны специалистам в данной области техники. Кроме того, если иное не требуется по контексту, термины в единственном числе включают формы в множественном числе, а термины в множественном числе включают формы в единственном числе. В общем случае, терминология, применяемая в связи со способами культивирования клеток и тканей, молекулярной биологией, иммунологией, химией белков и олиго- или полинуклеотидов, а также гибридизацией, описанными в настоящем документе, хорошо известна и широко применяется в данной области техники. Для получения рекомбинантной ДНК, синтеза олигонуклеотидов и культуры тканей, а также трансформации применяют стандартные методы (например, электропорацию, липофекцию). Ферментативные реакции и способы очистки проводят в соответствии со спецификацией производителя или так, как это обычно делают в данной области техники или как описано в данном документе. Приведенные далее процедуры и методики, как правило, осуществляют с применением общепринятых способов, хорошо известных в данной области техники и описанных в различных общих и более специализированных источниках, которые цитируются и обсуждаются в тексте данного описания. См., например, Sambrook et al. Molecular Cloning: A Laboratory Manual (2d ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y. (1989)). Терминология, применяемая в связи с лабораторными методиками и способами аналитической химии, синтетической органической химии, медицинской и фармацевтической химии, описанными в настоящем документе, хорошо известна и широко применяется в данной области техники. Стандартные методики применяются для химического синтеза, химического анализа, приготовления фармацевтического состава, составления и введения, и для лечения пациентов.
[00130] В соответствии с применением в данном описании, следующие термины, если не указано иное, следует понимать, как имеющие следующие значения:
[00131] В данном контексте термины "двухнацеленный слитый белок" и "антитело" могут быть синонимами. В данном контексте термин "антитело" относится к молекулам иммуноглобулина и иммунологически активным частям молекул иммуноглобулина (Ig), то есть, молекулам, которые содержат антигенсвязывающий участок, который специфически связывается (вступает в иммунную реакцию) с антигеном. Под терминами "специфически связывается" или "вступает в иммунную реакцию с" или "направленный против" подразумевается, что антитело вступает в реакцию с одним или большим количеством антигенных детерминант желаемого антигена и не вступает в реакцию с другими полипептидами или связывается с гораздо более низкой аффинностью (Kd > 10-6). Антитела включают, но не ограничиваются ими, поликлональное, моноклональное, химерное, dAb (доменное антитело), одноцепочечное, фрагменты Fab, Fab' и F(ab')2, Fv, scFvs, экспрессионную библиотеку Fab и фрагменты однодоменного антитела (sdAb), например, VHH, VNAR, сконструированные VH или VK.
[00132] Известно, что основная структурная единица антитела представляет собой тетрамер. Каждый тетрамер состоит из двух идентичных пар полипептидных цепей, каждая пара обладает одной "легкой" (около 25 кДа) и одной "тяжелой" цепью (около 50-70 кДа). Аминоконцевая часть каждой цепи содержит вариабельную область от около 100 до 110 или более аминокислот, главным образом ответственную за распознавание антигена. C-концевая часть каждой цепи определяет константную область, главным образом ответственную за эффекторную функцию. Как правило, молекулы антител, полученные от человека, относятся к любому из классов IgG, IgM, IgA, IgE и IgD, которые отличаются друг от друга по характеру тяжелой цепи, присутствующей в молекуле. Кроме того, некоторые классы имеют подклассы (также известные как изотипы), такие как IgG1, IgG2 и другие. Кроме того, у людей легкая цепь может быть каппа-цепью или лямбда-цепью.
[00133] В данном контексте термин "моноклональное антитело" (MAb) или "композиция моноклональных антител" относится к популяции молекул антител, которые содержат только один молекулярный вид молекулы антитела, состоящий из уникального генного продукта легкой цепи и уникального генного продукта тяжелой цепи. В частности, области, определяющие комплементарность (CDR) моноклонального антитела, являются идентичными во всех молекулах популяции. MAb содержат антигенсвязывающий участок, способный к иммунной реакции с определенным эпитопом антигена, характеризующимся уникальной аффинностью связывания с ним.
[00134] Термин "антигенсвязывающий участок" или "связывающая часть" относится к части молекулы иммуноглобулина, которая участвует в связывании антигена. Антигенсвязывающий участок образуется аминокислотными остатками N-концевых вариабельных ("V") областей тяжелой ("Н") и легкой ("L") цепей. Три сильно отклоняющихся участка в пределах V-областей тяжелой и легкой цепей, называемые "гипервариабельными областями", размещаются между более консервативными фланкирующими участками, известными как "каркасные области" или "FR". Таким образом, термин "FR" относится к аминокислотным последовательностям, которые в природных условиях обнаруживаются между гипервариабельными областями в иммуноглобулинах и соседствуют с ними. В молекуле антитела три гипервариабельные области легкой цепи и три гипервариабельные области тяжелой цепи расположены относительно друг друга в трехмерном пространстве, образуя антигенсвязывающую поверхность. Антигенсвязывающая поверхность дополняет трехмерную поверхность связанного антигена, а три гипервариабельные области каждой из тяжелой и легкой цепей называются "определяющими комплементарность областями" или "CDR". Назначение аминокислоты в каждом домене соответствуют определениям последовательностей Кабата из Proteins of Immunological Interest (National Institutes of Health, Bethesda, Md. (1987 and 1991)), или Chothia & Lesk J. Mol. Biol. 196: 901-917 (1987), Chothia et al. Nature 342: 878-883 (1989).
[00135] Части фрагментов однодоменного антитела (sdAb) слитых белков по данному изобретению упоминаются в данном документе взаимозаменяемо и обозначаются в данном документе термином "нацеленные полипептиды".
[00136] В данном контексте термин "эпитоп" включает любую детерминанту белка, способную специфически связываться с/с помощью иммуноглобулина или его фрагмента или рецептора Т-клеток. Термин "эпитоп" включает любую детерминанту белка, способную специфически связываться с/быть связанным иммуноглобулином или рецептором Т-клеток. Детерминанты эпитопов обычно состоят из химически активных поверхностных группировок молекул, таких как аминокислоты или боковые цепи сахара, и обычно имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Как утверждается, антитело специфически связывается с антигеном, когда константа диссоциации составляет ≤ 1 мМ, например, ≤ 1 мкМ; например, ≤ 100 нМ, например, ≤ 10 нМ и, например, ≤ 1 нМ.
[00137] В данном контексте термины "иммунологическое связывание" и "иммунологические связывающие свойства" относятся к нековалентным взаимодействиям определенного типа, который возникает между молекулой иммуноглобулина и антигеном, для которого иммуноглобулин является специфическим. Силу или аффинность иммунологических связывающих взаимодействий можно выразить в терминах константы диссоциации (Kd) взаимодействия, при этом меньшее значение Kd представляет более высокую аффинность. Иммунологические связывающие свойства выбранных полипептидов могут быть количественно определены с помощью способов, хорошо известных в данной области техники. Один из таких способов предполагает измерение скоростей образования комплекса "антигенсвязывающий участок/антиген" и диссоциации, причем эти скорости зависят от концентраций партнеров комплекса, аффинности взаимодействия и геометрических параметров, которые одинаково влияют на скорость в обоих направлениях. Таким образом, как "константу скорости ассоциации" (kon), так и "константу скорости диссоциации" (koff) можно определить путем расчета концентраций и фактических скоростей ассоциации и диссоциации. (См. Nature 361: 186-87 (1993)). Соотношение koff /kon позволяет исключить все параметры, не связанные с аффинностью, и является равным константе диссоциации Kd. (См., в общих чертах, Davies et al. (1990) Annual Rev Biochem 59: 439-473). Как утверждается, антитело по данному изобретению специфически связывается с антигеном, когда равновесная константа связывания (Kd) составляет от ≤1 μM, например, ≤100 нM, например, ≤10 нM, и, например, ≤100 пM до около 1 пМ, что измеряется с помощью анализов, таких как анализы связывания радиолиганда, поверхностный плазмонный резонанс (SPR), анализ связывания проточной цитометрии, или аналогичные анализы, известные специалистам в данной области техники.
[00138] В данном контексте термин "выделенный полинуклеотид" означает полинуклеотид геномного, кДНК или синтетического происхождения или их комбинацию, который в силу своей природы "выделенного полинуклеотида" (1) не связан с целым или частью полинуклеотида, в котором "выделенный полинуклеотид" встречается в природе, (2) функционально связан с полинуклеотидом, который не связан с полинуклеотидом, встречащимся в природе, или (3) не встречается в природе как часть большей последовательности.
[00139] Термин "выделенный белок", применяемый в данном описании, означает белок кДНК, рекомбинантную РНК или белок синтетического происхождения или некоторую их комбинацию, которые в силу своей природы или источника выведения являются "выделенным белком", который (1) не связан с белками, встречающимися в природе, (2) не содержит других белков из того же источника, например, не содержит морских белков, (3) экспрессируется клеткой из другого вида, или (4) не встречается в природе.
[00140] В данном контексте термин "полипептид" применяется как общий термин для обозначения нативного белка, фрагментов или аналогов полипептидной последовательности. Следовательно, фрагменты нативного белка и аналоги представляют собой виды полипептидного рода.
[00141] В данном контексте термин "встречающийся в природе", применяемый к объекту, относится к тому факту, что объект можно обнаружить в природе, например, полипептидная или полинуклеотидная последовательность, присутствующая в организме (включая вирусы), которую можно выделить из источника в природе и которая не была намеренно модифицирована человеком в лаборатории или иным образом, является "встречающейся в природе".
[00142] В данном контексте термин "функционально связанный" относится к положениям компонентов, определенных в такой взаимосвязи, что обеспечивает для них возможность функционировать по назначению. Регуляторная последовательность, являющаяся "функционально связанной" с кодирующей последовательностью, лигирована с ней таким образом, что экспрессия кодирующей последовательности достигается в условиях, совместимых с регуляторными последовательностями.
[00143] В данном контексте термин "регуляторная последовательность" относится к полинуклеотидным последовательностям, которые необходимы для осуществления экспрессии и процессинга кодирующих последовательностей, с которыми они лигированы. Природа таких регуляторных последовательностей отличается в зависимости от организма-хозяина в прокариот, такие контрольные последовательности, как правило, включают промотор, участок связывания рибосом и последовательность терминации транскрипции у эукариот, как правило, такие регуляторные последовательности включают промоторы и последовательность терминации транскрипции. Термин "регуляторные последовательности" предназначен для включения, как минимум, всех компонентов, присутствие которых является обязательным для экспрессии и процессинга, а также может включать дополнительные компоненты, присутствие которых является целесообразным, например, лидерные последовательности и последовательности партнеров слияния. В данном контексте термин "полинуклеотид" относится к полимерным нуклеотидам длиной не менее 10 оснований, либо рибонуклеотидам, либо дезоксинуклеотидам, либо модифицированной форме любого типа нуклеотида. Этот термин включает одно- и двухцепочечные формы ДНК.
[00144] В данном контексте термин "олигонуклеотид" включает встречающиеся в природе и модифицированные нуклеотиды, связанные вместе посредством встречающихся в природе и не встречающихся в природе олигонуклеотидных связей. Олигонуклеотиды представляют собой подмножество полинуклеотидов, как правило, содержащее в длину 200 оснований или меньше. В других вариантах осуществления данного изобретения длина олигонуклеотидов составляет от 10 до 60 оснований, например, 12, 13, 14, 15, 16, 17, 18, 19 или от 20 до 40 оснований в длину. Как правило, олигонуклеотиды являются одноцепочечными, например, для зондов, хотя олигонуклеотиды могут быть и двухцепочечными, например, для применения в конструкции мутанта гена. Олигонуклеотиды по данному изобретению могут быть либо смысловыми, либо антисмысловыми олигонуклеотидами.
[00145] В данном контексте термин "встречающиеся в природе нуклеотиды" включает в себя дезоксирибонуклеотиды и рибонуклеотиды. В данном контексте термин "модифицированные нуклеотиды" включает в себя нуклеотиды с модифицированными или замещенными группами сахаров и тому подобное. В данном контексте термин "олигонуклеотидные связи" включает в себя олигонуклеотидные связи, такие как фосфоротиоат, фосфородитиоат, фосфороселерлоат, фосфородиселеноат, фосфоранилотиоат, фосфораниладат, фосфоронмидат и тому подобное. См., например, LaPlanche et al. Nucl. Acids Res. 14: 9081 (1986); Stec et al. J. Am. Chem. Soc. 106: 6077 (1984), Stein et al. Nucl. Acids Res. 16: 3209 (1988), Zon et al. Anti Cancer Drug Design 6: 539 (1991); Zon et al. Oligonucleotides and Analogues: A Practical Approach, pp. 87-108 (F. Eckstein, Ed., Oxford University Press, Oxford England (1991)); Stec et al. в патенте США №5151510; Uhlmann and Peyman Chemical Reviews 90: 543 (1990). Олигонуклеотид может включать метку для обнаружения, если это является желательным.
[00146] В данном контексте термин "избирательно гибридизировать" означает обнаруживать и специфически связывать. Полинуклеотиды, олигонуклеотиды и их фрагменты в соответствии с данным изобретением избирательно гибридизуются с цепями нуклеиновых кислот в условиях гибридизации и промывания, что минимизирует заметные количества обнаруживаемого связывания с неспецифическими нуклеиновыми кислотами. Для достижения избирательных условий гибридизации, известных в данной области техники и обсуждаемых в данном документе, могут применяться условия высокой жесткости. Как правило, гомология последовательности нуклеиновой кислоты между полинуклеотидами, олигонуклеотидами и фрагментами по данному изобретению и представляющей интерес последовательности нуклеиновой кислоты будет составлять по меньшей мере 80% и более типично с увеличением гомологии по меньшей мере до 85%, 90%, 95% 99% и 100%. Две аминокислотные последовательности являются гомологичными, если отмечается частичная или полная идентичность между их последовательностями, например, 85%-ная гомология означает, что 85% аминокислот являются идентичными при выравнивании двух последовательностей для максимального соответствия. Предпочтительно, при определении максимальных значений длин совпадающих гэпов (в любой из двух соответствующих последовательностей), допускается 5 или менее, более предпочтительно - 2 или менее. В альтернативном варианте, две белковые последовательности (или полипептидные последовательности, полученные из них и состоящие по меньшей мере из 30 аминокислот в длину) являются гомологичными, как этот термин применяется в данном документе, если они имеют оценку выравнивания более чем 5 (в единицах стандартного отклонения), полученную с помощью программы ALIGN с матрицей данных мутаций и штрафом за гэпы 6 или выше. См. Dayhoff, M. O., в Atlas of Protein Sequence and Structure, стр. 101-110 (том 5, National Biomedical Research Foundation (1972)) и дополнение 2 к этому тому, стр. 1-10. Две последовательности или их части являются более предпочтительно гомологичными, если их аминокислоты являются на 50% или больше идентичными при оптимальном выравнивании с помощью программы ALIGN. Термин "соответствует" в данном документе применяется для обозначения того, что полинуклеотидная последовательность является гомологичной (то есть идентичной, а не строго эволюционно родственной) со всей или частью эталонной полинуклеотидной последовательности, или что полипептидная последовательность является идентичной эталонной полипептидной последовательности. В противоположном смысле термин "комплементарный" в данном документе применяется для обозначения того, что комплементарная последовательность является гомологичной всей или части эталонной полинуклеотидной последовательности. В целях иллюстрации, нуклеотидная последовательность "TATAC" соответствует эталонной последовательности "TATAC" и является комплементарной эталонной последовательности "GTATA".
[00147] Следующие термины применяются для описания отношений последовательностей между двумя или более полинуклеотидными или аминокислотными последовательностями: "эталонная последовательность", "окно сравнения", "идентичность последовательности", "процент идентичности последовательности" и "существенная идентичность". "Эталонная последовательность" представляет собой определенную последовательность, применяемую в качестве основы для сравнения последовательностей, эталонная последовательность может быть подмножеством большей последовательности, например, в виде сегмента полноразмерной кДНК или последовательности генов, приведенной в перечне последовательностей или может содержать полную последовательность кДНК или гена. Как правило, эталонная последовательность состоит по меньшей мере из 18 нуклеотидов или 6 аминокислот в длину, нередко - по меньшей мере из 24 нуклеотидов или 8 аминокислот в длину, и часто - по меньшей мере из 48 нуклеотидов или 16 аминокислот в длину. Поскольку две полинуклеотиды или аминокислотные последовательности могут каждая (1) содержать последовательность (то есть, часть полной полинуклеотидной или аминокислотной последовательности), которая является сходной между двумя молекулами, и (2) может дополнительно содержать последовательность, которая расходится между двумя полинуклеотидами или аминокислотными последовательностями, сравнение последовательностей между двумя (или большем количеством) молекулами обычно осуществляют путем сравнения последовательностей двух молекул в "окне сравнения" для идентификации и сравнения локальных области сходства последовательностей. В данном контексте термин "окно сравнения" относится к концептуальному сегменту по меньшей мере из 18 смежных положений нуклеотидов или 6 аминокислот, при этом полинуклеотидную последовательность или аминокислотную последовательность можно сравнивать с эталонной последовательностью по меньшей мере из 18 смежных нуклеотидов или последовательностями из 6 аминокислот и при этом часть полинуклеотидной последовательности в окне сравнения может содержать добавления, делеции, замены и т. п. (то есть, гэпы), составляющие 20 процентов или менее по сравнению с эталонной последовательностью (которая не содержит добавлений или делеций) для оптимального выравнивания двух последовательностей. Оптимальное выравнивание последовательностей для выравнивания окна сравнения можно выполнить с помощью алгоритма локальной гомологии согласно по Smith and Waterman Adv. Appl. Math. 2: 482 (1981), алгоритма выравнивания областей гомологии по Needleman and Wunsch J. Mol. Biol. 48: 443 (1970), с помощью способа поиска сходства по Pearson и Lipman, Proc. Natl. Acad. Sci. (U. S. A.) 85: 2444 (1988), компьютеризированных реализаций этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в пакете программного обеспечения Wisconsin Genetics Software Package Release 7. 0, (Genetics Computer Group, 575 Science Dr., Madison, Wis.), Geneworks или в пакетах программного обеспечения MacVector) или путем проверки, а также с помощью наилучшего выравнивания (то есть, приводящего к наибольшему проценту гомологии в окне сравнения), сгенерированного различными выбранными способами.
[00148] Термин "идентичность последовательности" означает, что две полинуклеотидные или аминокислотные последовательности являются идентичными (то есть, на основании принципа "нуклеотид-с-нуклеотидом" или "остаток-с-остатком") в окне сравнения. Термин "процент идентичности последовательности" вычисляют путем сравнения двух оптимально выровненных последовательностей в окне сравнения, определяя количество положений, в которых идентичное основание нуклеиновой кислоты (например, A, T, C, G, U или I) или аминокислотный остаток встречаются в составе обеих последовательностей, с получением количества совпадающих положений, после чего количество совпадающих положений делят на общее количество положений в окне сравнения (то есть, размер окна), и умножают результат на 100, таким образом получая процент идентичности последовательности. В данном контексте термины "существенная идентичность" означают характеристику полинуклеотидной или аминокислотной последовательности, при которой полинуклеотид или аминокислота содержит последовательность, которая имеет по меньшей мере 85 процентов идентичности последовательности, предпочтительно по меньшей мере от 90 до 95 процентов идентичности последовательностей, более предпочтительно по меньшей мере 99 процентов идентичности последовательности по сравнению с эталонной последовательностью в окне сравнения по меньшей мере с 18 нуклеотидными (6 аминокислотными) положениями, нередко - в окне сравнения по меньшей мере с 24-48 нуклеотидными (8-16 аминокислотными) положениями, при этом процент идентичности последовательности вычисляют путем сравнения эталонной последовательности с последовательностью, которая может включать в себя делеции или дополнения, составляющие 20 процентов или менее эталонной последовательности в окне сравнения. Эталонная последовательность может быть подмножеством большей последовательности.
[00149] В данном контексте, двадцать традиционных аминокислот и их аббревиатуры применяются традиционным образом. См. Immunology - A Synthesis (2nd Edition, E. S. Golub and D. R. Gren, Eds., Sinauer Associates, Sunderland7 Mass. (1991)). Стереоизомеры (например, D-аминокислоты) двадцати традиционных аминокислот, не встречающиеся в природе аминокислоты, такие как α- α-двузамещенные аминокислоты, N-алкил-аминокислоты, молочная кислота и другие нетрадиционные аминокислоты, также могут являться пригодными компонентами для полипептидов по данному изобретению. Примеры нетрадиционных аминокислот включают: 4-гидроксипролин, γ -карбоксиглутамат, ε-N, N, N-триметиллизин, ε-N-ацетиллизин, O-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метилгистидин, 5-гидроксилизин, σ-N-метиларгинин и другие аналогичные аминокислоты и иминокислоты (например, 4-гидроксипролин). В обозначении полипептида, применяемом в данном документе, левонаправленным является аминоконцевое направление, а правонаправленным является карбоксиконцевое направление, в соответствии со стандартом применения и конвенцией.
[00150] Аналогичным образом, если не указано иное левонаправленным концом одноцепочечной полинуклеотидной последовательности является 5' конец; при этом левое направление двухцепочечных полинуклеотидных последовательностей называется 5' направлением. Направление от 5' к 3', в котором происходит добавление растущих РНК-транскриптов, называется направлением транскрипции; области последовательности на цепи ДНК, имеющие такую же последовательность, что и РНК-транскрипт и которые расположены от 5' к 5' концу РНК-транскрипта, называются "последовательностями, расположенными против хода транскрипции"; области последовательности на цепи ДНК, имеющие такую же последовательность, что и РНК-транскрипт и которые расположены от 3' к 3' концу РНК-транскрипта, называются "последовательностями, расположенными за ходом транскрипции".
[00151] При применении к полипептидам термин "существенная идентичность" означает, что две последовательности пептидов при оптимальном выравнивании, например, с помощью программы GAP или BESTFIT с применением штрафа за делецию по умолчанию, имеют по меньшей мере 80% идентичности последовательности, например, по меньшей мере 90% идентичности последовательности, например, по меньшей мере 95% идентичности последовательности и, например, по меньшей мере 99% идентичности последовательности.
[00152] В некоторых вариантах осуществления данного изобретения положения неидентичных остатков отличаются консервативными аминокислотными заменами.
[00153] Консервативные аминокислотные замены относятся к взаимозаменяемости остатков, имеющих сходные боковые цепи, например, группа аминокислот, имеющих алифатические боковые цепи, представляет собой глицин, аланин, валин, лейцин и изолейцин; группа аминокислот, имеющих алифатически-гидроксильные боковые цепи, представляет собой серин и треонин; группа аминокислот, имеющих амидсодержащие боковые цепи, представляет собой аспарагин и глутамин; группа аминокислот, имеющих ароматические боковые цепи, представляет собой фенилаланин, тирозин и триптофан; группа аминокислот, имеющих основные боковые цепи, представляет собой лизин, аргинин и гистидин; и группа аминокислот, имеющих серосодержащие боковые цепи, представляет собой цистеин и метионин. Пригодными группами консервативных аминокислотных замен являются: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин.
[00154] Как обсуждалось в данном документе, незначительные изменения в аминокислотных последовательностях антител или молекул иммуноглобулина рассматриваются как охватываемые данным изобретением, при условии, что изменения в аминокислотной последовательности обеспечивают по меньшей мере 75%, например, по меньшей мере 80%, 90%, 95% и, например, 99%. В частности, предполагаются консервативные аминокислотные замены. Консервативные замены представляют собой те, которые происходят в семействе аминокислот, которые являются связанными в их боковых цепях. Генетически кодированные аминокислоты обычно делятся на семейства: (1) кислыми аминокислотами являются аспартат, глутамат; (2) основными аминокислотами являются лизин, аргинин, гистидин; (3) неполярными аминокислотами являются аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан и (4) незаряженными полярными аминокислотами являются глицин, аспарагин, глутамин, цистеин, серин, треонин, тирозин. Гидрофильные аминокислоты включают в себя аргинин, аспарагин, аспартат, глутамин, глутамат, гистидин, лизин, серин и треонин. Гидрофобные аминокислоты включают в себя аланин, цистеин, изолейцин, лейцин, метионин, фенилаланин, пролин, триптофан, тирозин и валин. Другие семейства аминокислот включают в себя (i) серин и треонин, которые являются алифатически-гидроксигруппой; (ii) аспарагин и глутамин, которые являются семейством, содержащим амид ; (iii) аланин, валин, лейцин и изолейцин, которые являются алифатическим семейством; и (iv) фенилаланин, триптофан и тирозин, которые являются ароматическим семейством, например, вполне можно ожидать, что изолированная замена лейцина на изолейцин или валин, замена аспартата на глутамат, замена треонина на серин или аналогичная замена аминокислоты на структурно родственную аминокислоту не будет характеризоваться существенным влиянием на связывание или свойства полученной молекулы, особенно если замена не включает аминокислоту в пределах каркасного участка. Приводит ли изменение аминокислоты к формированию функционального пептиду, можно легко определить, анализируя специфическую активность производного полипептида. Анализы подробно описаны в настоящем документе. Фрагменты или аналоги антител или молекул иммуноглобулина могут легко приготовить обычные специалисты в данной области техники. Пригодные амино- и карбокси-концевые фрагменты или аналоги встречаются вблизи границ функциональных доменов. Структурные и функциональные домены могут быть идентифицированы путем сравнения данных нуклеотидной и/или аминокислотной последовательности с общедоступными или защищенными правом собственности базами последовательностей. В некоторых вариантах осуществления данного изобретения компьютеризированные способы сравнения применяют для идентификации мотивов последовательности или доменов предполагаемой конформации белка, которые встречаются в других белках известной структуры и/или функции. Известны способы идентификации белковых последовательностей, которые складываются в известную трехмерную структуру. Bowie et al. Science 253: 164 (1991). Таким образом, приведенные выше примеры демонстрируют, что специалисты в данной области могут распознавать последовательности мотивов и структурные конформации, которые можно применять для определения структурных и функциональных доменов в соответствии с данным изобретением.
[00155] Пригодными аминокислотными заменами являются такие, которые: (1) снижают восприимчивость к протеолизу, (2) снижают восприимчивость к окислению, (3) изменяют аффинность связывания для образования белковых комплексов, (4) изменяют аффинности связывания и (4) придают или модифицируют другие физико-химические или функциональные свойства таких аналогов. Аналоги могут включать различные мутеины последовательности, не относящейся к числу встречающихся в природе пептидных последовательностей, например, одну или большее количество аминокислотных замен (например, консервативные аминокислотные замены) можно осуществить во встречающейся в природе последовательности (например, в части полипептида вне домена(ов), образующей межмолекулярные контакты. Консервативная аминокислотная замена не должна по существу изменять структурные характеристики родительской последовательности (например, замещающая аминокислота не должна стремиться разрушать спираль, которая определяется в родительской последовательности, или разрушать другие типы вторичной структуры, которые характеризуют родительскую последовательность). Примеры признанных в данной области техники полипептидных вторичных и третичных структур описаны в Proteins, Structures and Molecular Principles (Creighton, Ed., W. H. Freeman and Company, New York (1984)); Introduction to Protein Structure (C. Branden and J. Tooze, eds., Garland Publishing, New York, N. Y. (1991)); and Thornton et al. Nature 354: 105 (1991).
[00156] В данном контексте термин "полипептидный фрагмент" относится к полипептиду, который имеет аминоконцевую и/или карбокси-концевую делецию, но в котором оставшаяся аминокислотная последовательность является идентичной соответствующим положениям во встречающейся в природе последовательности, выведенной, например, из полноразмерной последовательности кДНК. Как правило, фрагменты имеют по меньшей мере 5, 6, 8 или 10 аминокислот в длину, например, по меньшей мере 14 аминокислот в длину, например, по меньшей мере 20 аминокислот в длину, обычно по меньшей мере 50 аминокислот в длину и, например, по меньшей мере 70 аминокислот в длину. В данном контексте термин "аналог" относится к полипептидам, которые состоят из сегмента по меньшей мере из 25 аминокислот, имеющего существенную идентичность с частью выведенной аминокислотной последовательности и характеризующегося специфическим связыванием с CD47 в подходящих условиях для связывания. Как правило, полипептидные аналоги включают консервативную аминокислотную замену (или добавление или делецию) по отношению к встречающейся в природе последовательности. Как правило, аналоги имеют по меньшей мере 20 аминокислот в длину, например, по меньшей мере 50 аминокислот в длину или больше, и часто могут достигать длины, характерной для встречающегося в природе полипептида.
[00157] Пептидные аналоги обычно применяются в фармацевтической промышленности в качестве непептидных лекарственных средств со свойствами, аналогичными свойствам матричного пептида. Эти типы непептидного соединения называются "пептидные миметики" или "пептидомиметики". Fauchere, J. Adv. Drug Res. 15: 29 (1986), Veber and Freidinger TINS p. 392 (1985); и Evans et al. J. Med. Chem. 30: 1229 (1987). Такие соединения часто разрабатываются с помощью компьютеризированного молекулярного моделирования. Пептидные миметики, которые структурно подобны пригодным для терапевтического применения пептидам, можно применять для получения эквивалентного терапевтического или профилактического эффекта. Как правило, пептидомиметики структурно сходны с эталонным полипептидом (то есть, полипептидом, который обладает биохимическим свойством или фармакологической активностью), таким как человеческое антитело, но имеют одну или большее количество пептидных связей, необязательно замененных на связь, выбранную из группы, состоящей из: -- CH2NH--, --CH2S-, --CH2-CH2--, --CH=CH--(цис и транс), --COCH2--, CH(OH)CH2--, и -CH2SO--, согласно способам, хорошо известным в данной области техники. Систематическую замену одной или большего количества аминокислот консенсусной последовательности на D-аминокислоту того же типа (например, D-лизин вместо L-лизина) можно применять для получения более стабильных пептидов. Кроме того, ограниченные пептиды, содержащие консенсусную последовательность или, по существу, вариацию идентичной консенсусной последовательности, могут быть получены с помощью способов, известных в данной области техники (Rizo and Gierasch Ann. Rev. Biochem. 61: 387 (1992)); например, путем добавления внутренних остатков цистеина, способных образовывать внутримолекулярные дисульфидные мостики, которые циклизируют пептид.
[00158] В данном контексте термин "агент" применяется для обозначения химического соединения, смеси химических соединений, биологической макромолекулы и/или экстракта, полученного из биологических материалов.
[00159] В данном контексте термин "метка" или "меченный" относится к включению детектируемого маркера, например, путем введения радиоактивно меченной аминокислоты или присоединения к полипептиду биотинильных фрагментов, которые могут быть обнаружены с помощью меченного авидина (например, стрептавидина, содержащего флуоресцентный маркер или ферментативную активность, который может быть обнаружен оптическими или калориметрическими методами). В определенных ситуациях метка или маркер также могут быть терапевтическими. В данной области техники известно множество способов мечения полипептидов и гликопротеинов, которые можно применять. Примеры меток для полипептидов включают, но не ограничиваются ими, следующие: радиоизотопы или радионуклиды (например, 3H, 14C, 15N, 35S, 90Y, 99Tc, 111In, 125I, 131I), флуоресцентные метки (например, FITC, родамин, люминофор на основе лантанида), ферментативные метки (например, пероксидаза хрена, β-галактозидаза, люцифераза, щелочная фосфатаза), хемилюминесцентные, биотинильные группы, предопределенные полипептидные эпитопы, распознаваемые вторичным репортером (например, парные последовательности лейциновых молний, участки связывания для вторичных антител, метал-связывающие домены, метки эпитопа). В некоторых вариантах осуществления данного изобретения метки прикрепляют с помощью спейсерных "ножек" различной длины для уменьшения потенциального пространственного затруднения. В данном контексте термин "фармацевтический агент или лекарственное средство" относится к химическому соединению или композиции, способным индуцировать желаемый терапевтический эффект при надлежащем введении пациенту.
[00160] В данном контексте термин "противоопухолевый агент" применяется для обозначения агентов, которые обладают функциональным свойством ингибировать развитие или прогрессирование новообразования у человека, особенно злокачественных (раковых) поражений, таких как карцинома, саркома, лимфома или лейкоз. Ингибирование метастазирования часто является одним из свойств противоопухолевых агентов.
[00161] В данном контексте термины "лечить", "лечащий" и "лечение" и тому подобное относятся к снижению тяжести и/или облегчению нарушения и/или симптомов, ассоциированных с ним. Под термином "облегчение" и/или "облегчать" подразумевается уменьшение, подавление, ослабление, затухание, ингибирование и/или стабилизация развития или прогрессирования заболевания, такого как, например, рак. Понятно, хотя не исключается, что лечение нарушения или патологического состояния, не требует, чтобы заболевание, патологическое состояние или симптомы, ассоциированные с ними, будут полностью устранены.
[00162] Другие химические термины применяются в данном документе в соответствии с обычным применением в данной области техники, как описано в The McGraw-Hill Dictionary of Chemical Terms (Parker, S., Ed., McGraw-Hill, San Francisco (1985)).
[00163] В данном контексте термин "по существу чистый" означает, что вид объекта является преобладающим из присутствующих видов (то есть, по молярной основе он более распространен, чем любые другие отдельные виды в композиции), и по существу очищенная фракция представляет собой композицию, в которой виды объекта содержат по меньшей мере около 50 процентов (по молярной основе) всех присутствующих макромолекулярных соединений.
[00164] Как правило, по существу чистая композиция будет содержать более 80% всех макромолекулярных компонентов, присутствующих в композиции, например, более 85%, 90%, 95% и 99%. В некоторых вариантах осуществления данного изобретения вид объекта очищают до необходимой гомогенности (виды загрязняющих веществ не могут быть обнаружены в композиции с помощью обычных способов обнаружения), при этом композиция состоит в основном из одного макромолекулярного вида.
[00165] В этом описании термины "содержит", "содержащий", "вмещающий", "имеющий" и тому подобное, могут иметь значения, обозначенное для них в Патентном законе США и могут означать "включает", "включая" и тому подобное; термины "состоящий в основном из" или "состоящий по существу из" также имеют значения, указанные в Патентном законе США и эти термины являются неограниченными, что позволяет охватывать больше, чем то, что изложено при том условии, что основные или новые характеристики того, что изложено, не изменяются присутствием большего, чем изложено, но исключают варианты осуществления предшествующего уровня техники.
[00166] Под "эффективным количеством" подразумевается количество, необходимое для улучшения симптомов заболевания по сравнению с необработанным пациентом. Эффективное количество активного соединения (соединений), применяемое для осуществления настоящего изобретения с целью терапевтического лечения заболевания, варьируется в зависимости от способа введения, возраста, массы тела и общего состояния здоровья субъекта. В конечном счете, лечащий врач или ветеринар определит надлежащее количество и схему введения. Такое количество упоминается в данном документе как "эффективное" количество.
[00167] Под термином "субъект" подразумевается млекопитающее, включая, но не ограничиваясь этим, человека или млекопитающего, не относящегося к человеку, такого как бык, лошадь, собака, грызун, овца, примат, верблюд или кошка.
[00168] В данном контексте термин "введение" относится к любому способу передачи, доставки, введения или транспортировки терапевтического агента субъекту, нуждающемуся в лечении таким агентом. Такие способы включают, но не ограничиваются ими, пероральное, местное, внутривенное, внутрибрюшинное, внутримышечное, внутрикожное, интраназальное и подкожное введение.
[00169] Под термином "фрагмент" подразумевается часть полипептида или молекулы нуклеиновой кислоты. Эта часть содержит, например, по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% всей длины эталонной молекулы нуклеиновой кислоты или полипептида. Фрагмент может содержать 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000 нуклеотидов или аминокислот.
[00170] Представленные в данном документе диапазоны следует понимать как подразумевающие все значений в пределах диапазона, например, следует понимать, что диапазон от 1 до 50 включает любое число, комбинацию чисел или субдиапазон из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50.
[00171] В настоящем описании термины в единственном числе включают соответствующие термины во множественном числе, если специально не указано или из контекста явно не следует иное. В настоящем описании термин "или" следует понимать как открытый, если специально не указано или из контекста явно не следует иное.
[00172] В настоящем описании термин "около" следует понимать как диапазон нормального предельно допустимого отклонения в данной области техники, например, в пределах 2 стандартных отклонений среднего значения, если специально не указано или из контекста явно не следует иное. "Около" можно понимать как значение в пределах 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1%, 0,05%, или 0,01% от установленного значения. Все числовые значения, представленные в данном документе, модифицируются термином "около", если из контекста явно не следует иное.
Нацеливание на 41BB (CD137, TNFRSF9)
[00173] 41BB является представителем суперсемейства рецепторов TNF, который преимущественно экспрессируется на активированных Т-клетках и NK-клетках и функционирует в качестве стимулирующей молекулы. агонистическое воздействие на 41BB усиливает пролиферацию и выживание Т-клеток, цитолитическую активность и секрецию цитокинов (например, IL-2, TNFα и INFγ). Показано, что у мышей задействование 41BB повышает противоопухолевый иммунитет. (Croft, 2009, Nat Rev Immunol 9: 271-285; Lynch, 2008, Immunol Rev. 22: 277-286). Важно отметить, что инфильтрирующие опухоль цитотоксические Т-клетки (CTL), как было показано, являются такими, что экспрессируют 41BB, и именно эти 41BB-позитивные CTL характеризуются самой высокой противоопухолевой цитотоксическойю активностью (Ye et al Clin Cancer Res; 20(1): 44-55). Лиганд для 41BB, 41BBL, по своей природе образует гомотример, что дает основания предположить, что сигнализация опосредуется кластеризацией 41BB более высокого порядка. Этот механизм активации разделяют многие представители TNFRSF. Интерес к применению сигнализации 41BB с целью противоопухолевой иммунотерапии обусловил разработку терапевтических антител 41BB. Однако способность двухвалентных антител 41BB к индуцированию сигнализации является слабой в отсутствие экзогенного фактора кластеризации. Это может быть достигнуто в некоторой степени благодаря взаимодействию с Fcγ-рецепторами (FcγRs), однако это также может привести к истощению 41BB-экспрессирующей клетки посредством эффекторных механизмов (например, ADCC и ADCP). Кроме того, конкуренция с высокой концентрацией IgG в сыворотке ослабляет эффективные взаимодействия FcγR. Следовательно, существующие двухвалентные антитела, нацеленные на 41BB, являются либо неэффективными агонистами, либо ответственны за истощение разных клеток, для которых требуется сигнализация 41BB. Ранее было показано, что терапевтическое антитело 41BB, PF-05082566, способно к опосредованной сигнализации 41BB только при сшивании с античеловеческим вторичным антителом (Fisher et al Cancer Immunol Immunother (2012) 61: 1721-1733). Следовательно, существует потребность в оптимизированном агонисте 41BB, способном опосредовать сигнализацию в отсутствие экзогенного сшивающего агента или взаимодействия Fcγ R. Слитые белки по данному изобретению способны опосредовать мощную сигнализацию 41BB 1) без каких-либо дополнительных взаимодействий при форматировании в виде многовалентного слитого белка или 2) при условии взаимодействия по меньшей мере со вторым антигеном при форматировании в виде мультиспецифического слитого белка. Слитые белки по данному изобретению способны к автономной (мультивалентные слитые белки) или осуществляемой при определенных условиях (мультиспецифические слитые белки) костимулирующей активности на Т-клетках и NK-клетках.
[00174] Примерные аминокислотные последовательности 41BB-связывающих однодоменных антител приведены ниже:











[00175] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, которая включает комбинацию последовательности вариабельной области тяжелой цепи (VH) и последовательности вариабельной области легкой цепи (VL), выбранной из группы, состоящей из:
последовательностей VH:
QVQLVQSGAEVKKPGSSVKVSCKASGGTFNSYAISWVRQAPGQGLEWMGGIIPGFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARKNEEDGGFDHWGQGTLVTVSS (SEQ ID NO: 84)
QVQLVESGGGLVQPGGSLRLSCAASGFTFSDYYMHWVRQAPGKGLEWVSVISGSGSNTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARLYAQFEGDFWGQGTLVTVSS (SEQ ID NO: 85)
QVQLVQSGAEVKKPGESLKISCKGSGYSFSTYWISWVRQMPGKGLEWMGKIYPGDSYTNYSPSFQGQVTISADKSISTAYLQWSSLKASDTAMYYCARGYGIFDYWGQGTLVTVSS (SEQ ID NO: 86)
EVQLVQSGAEVKKPGESLRISCKGSGYSFSTYWISWVRQMPGKGLEWMGKIYPGDSYTNYSPSFQGQVTISADKSISTAYLQWSSLKASDTAMYYCARGYGIFDYWGQGTLVTVSS (SEQ ID NO: 87)
последовательности VL:
DIELTQPPSVSVAPGQTARISCSGDNLGDYYASWYQQKPGQAPVLVIYDDSNRPSGIPERFSGSNSGNTATLTISGTQAEDEADYYCQTWDGTLHFVFGGGTKLTVL (SEQ ID NO: 88)
DIELTQPPSVSVAPGQTARISCSGDNIGSKYVSWYQQKPGQAPVLVIYSDSERPSGIPERFSGSNSGNTATLTISGTQAEDEADYYCQSWDGSISRVFGGGTKLTVL (SEQ ID NO: 89)
DIELTQPPSVSVAPGQTARISCSGDNIGDQYAHWYQQKPGQAPVVVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAEDEADYYCATYTGFGSLAVFGGGTKLTVL (SEQ ID NO: 90)
SYELTQPPSVSVSPGQTASITCSGDNIGDQYAHWYQQKPGQSPVLVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAMDEADYYCATYTGFGSLAVFGGGTKLTVL (SEQ ID NO: 91)
SYELTQPPSVSVSPGQTASITCSGDNIGDQYAHWYQQKPGQSPVVVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAMDEADYYCATYTGFGSLAVFGGGTKLTVL (SEQ ID NO: 92)
DIELTQPPSVSVAPGQTARISCSGDNIGDQYAHWYQQKPGQAPVVVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAEDEADYYCSTYTFVGFTTVFGGGTKLTVL (SEQ ID NO: 93)
SYELTQPPSVSVSPGQTASITCSGDNIGDQYAHWYQQKPGQSPVLVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAMDEADYYCSTYTFVGFTTVFGGGTKLTVL (SEQ ID NO: 94)
SYELTQPPSVSVSPGQTASITCSGDNIGDQYAHWYQQKPGQSPVVVIYQDKNRPSGIPERFSGSNSGNTATLTISGTQAMDEADYYCSTYTFVGFTTVFGGGTKLTVL (SEQ ID NO: 95)
[00176] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, которая включает комбинацию последовательности тяжелой цепи (HC) и последовательности легкой цепи (LC), выбранной из группы, состоящей из:
последовательностей HC:
QVQLQQWGAGLLKPSETLSLTCAVYGGSFSGYYWSWIRQSPEKGLEWIGEINHGGYVTYNPSLESRVTISVDTSKNQFSLKLSSVTAADTAVYYCARDYGPGNYDWYFDLWGRGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 96)
QVQLQQWGAGLLKPSETLSLTCAVYGGSFSGYYWSWIRQSPEKGLEWIGEINHGGYVTYNPSLESRVTISVDTSKNQFSLKLSSVTAADTAVYYCARDYGPGNYDWYFDLWGRGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 97)
последовательностей LC:
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPPALTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 98)
[00177] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в публикации заявки на патент США №20160244528, содержание которой включено в данный документ посредством ссылки в полном объеме.
[00178] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в патенте США №8337850, содержание которого включено в данный документ посредством ссылки в полном объеме.
[00179] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в публикации PCT №WO 2005/035584, содержание которой включено в данный документ посредством ссылки в полном объеме.
[00180] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в патенте EP №EP 1670828 B1, содержание которого включено в данный документ посредством ссылки в полном объеме.
[00181] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в публикации PCT №WO 2006/088447, содержание которой включено в данный документ посредством ссылки в полном объеме.
[00182] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, выбранной из последовательностей антител, описанных в публикации заявки на патент США №20080166336, содержание которой включено в данный документ посредством ссылки в полном объеме.
[00183] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности противоракового слитого белка или его антигенсвязывающего фрагмента, выбранной из последовательностей, описанных в публикации PCT №WO 2016/177802, содержание которой включено в данный документ посредством ссылки в полном объеме. В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от аминокислотной последовательности, содержащей:
QDSTSDLIPAPPLSKVPLQQNFQDNQFHGKWYVVGQAGNIRLREDKDPIKMMATIYELKEDKSYDVTMVKFDDKKCMYDIWTFVPGSQPGEFTLGKIKSFPGHTSSLVRVVSTNYNQHAMVFFKFVFQNREEFYITLYGRTKELTSELKENFIRFSKSLGLPENHIVFPVPIDQCIDG (SEQ ID NO: 99)
[00184] В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от последовательности полипептида, нацеленного на 41BB, или его антигенсвязывающего фрагмента, выбранной из последовательностей, описанных в публикации PCT №WO 2016/177762, содержание которой включено в данный документ посредством ссылки в полном объеме. В некоторых вариантах осуществления данного изобретения 41BB-связывающий домен содержит или является производным от аминокислотной последовательности, содержащей:
Нацеливание на PDL1-
[00185] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими по меньшей мере первый связывающий домен, например, TBD, и второй связывающий домен, направленный на лиганд программируемой смерти 1 (PD-L1). В этих вариантах осуществления данного изобретения связывание PD-L1 способно обеспечить дополнительную функцию сшивания, а активация TNFRSF достигается только с помощью одного или двух TBD. В этих вариантах осуществления данного изобретения сигнализация TNFRSF усиливается и фокусируется наличием PD-L1-экспрессирующей клетки.
[00186] PDL1 представляет собой трансмембранный белок типа 40 кДа типа I, который образует комплекс со своим белком 1 рецептора программированной смерти клетки (PD1), также известным как CD279. Взаимодействие PDL1 со своим рецептором PD1 на Т-клетках обеспечивает возникновение сигнала, который ингибирует TCR-опосредованную активацию продукции IL-2 и пролиферации Т-клеток. Аберрантная экспрессия и/или активность PDL1 и PDL1-родственная передача сигналов участвовали в патогенезе многих заболеваний и нарушений, такие как рак, воспаление и аутоиммунные состояния.
[00187] В некоторых вариантах осуществления данного изобретения PD-L1-связывающая часть представляет собой однодоменное антитело. В некоторых вариантах осуществления данного изобретения PDL1-связывающая часть слитого белка блокирует или ослабляет взаимодействие PDL1 и PD-1. Типовые PDL1-нацеленные однодоменные последовательности приведены ниже:




[00188] В других вариантах осуществления данного изобретения PD-L1-связывающая часть является производной от внеклеточного домена PD-1, содержащего по меньшей мере домен IgV, как показано ниже:
PTFSPALLVVTEGDNATFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQLPNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVT (SEQ ID NO: 125)
[00189] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от известной последовательности антитела анти-PDL1 или его антигенсвязывающего фрагмента. В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела, описанной в публикации PCT №WO 2016/149201, содержание которой включено в данный документ посредством ссылки в полном объеме.
[00190] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, которая включает комбинацию последовательности вариабельной области тяжелой цепи (VH) и последовательности вариабельной области легкой цепи (VL), выбранной из группы, состоящей из:
последовательностей VH:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYGFSWVRQAPGQGLEWMGWITAYNGNTNYAQKLQGRVTMTTDTSTSTVYMELRSLRSDDTAVYYCARDYFYGMDVWGQGTTVTVSS (SEQ ID NO: 126)
QVQLVQSGAEVKKPGSSVKVSCKTSGDTFSTYAISWVRQAPGQGLEWMGGIIPIFGKAHYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYFCARKFHFVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 127)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYDVHWVRQAPGQRLEWMGWLHADTGITKFSQKFQGRVTITRDTSASTAYMELSSLRSEDTAVYYCARERIQLWFDYWGQGT (SEQ ID NO: 128)
QVQLVQSGAEVKKPGSSVKVSCKVSGGIFSTYAINWVRQAPGQGLEWMGGIIPIFGTANHAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARDQGIAAALFDYWGQGTLVTVSS (SEQ ID NO: 129)
EVQLVESGGGLVQPGRSLRLSCAVSGFTFDDYVVHWVRQAPGKGLEWVSGNSGNIGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAVPFDYWGQGTLVTVSS (SEQ ID NO: 130)
QVQLVQSGAEVKKPGSSVKVSCKTSGDTFSSYAISWVRQAPGQGLEWMGGIIPIFGRAHYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYFCARKFHFVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 131)
QVQLVQSGAEVKKPGSSVKVSCKTSGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGKAHYAQKFQGRVTITADESTTTAYMELSSLRSEDTAVYYCARKYDYVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 132)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAINWVRQAPGQGLEWMGGIIPIFGSANYAQKFQDRVTITADESTSAAYMELSSLRSEDTAVYYCARDSSGWSRYYMDVWGQGTTVTVSS (SEQ ID NO: 133)
QVQLVQSGAEVKEPGSSVKVSCKASGGTFNSYAISWVRQAPGQGLEWMGGIIPLFGIAHYAQKFQGRVTITADESTNTAYMDLSSLRSEDTAVYYCARKYSYVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 134)
EVQLVESGGGLVQPGRSLRLSCAASGITFDDYGMHWVRQAPGKGLEWVSGISWNRGRIEYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAKGRFRYFDWFLDYWGQGTLVTVSS (SEQ ID NO: 135)
QMQLVQSGGGLVQPGGSLRLSCAASGFTFSSYWMSWVRQAPGKGLEWVANIKQDGSEKYYVDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCARDYFWSGFSAFDIWGKGTLVTVS (SEQ ID NO: 136)
последовательности VL:
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLVWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPRTFGQGTKVEIK (SEQ ID NO: 137)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPTFGQGTKVEIK (SEQ ID NO: 138)
DIQMTQSPSSLSASVGDRVTITCRASQGISSWLAWYQQKPEKAPKSLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYNSYPYTFGQGTKLEIK (SEQ ID NO: 139)
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSPWTFGQGTKVEIK (SEQ ID NO: 140)
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSPFGGGTKVEIK (SEQ ID NO: 141)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPTFGQGTRLEIK (SEQ ID NO: 142)
AIQLTQSPSSLSASVGDRVTITCRASQGISSALAWYQQKPGKAPKLLIYDASSLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQFNSYPFTFGPGTKVDIK (SEQ ID NO: 143)
DIVMTQSPSTLSASVGDRVTITCRASQGISSWLAWYQQKPGRAPKVLIYKASTLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPWTFGQGTKLEIK (SEQ ID NO: 144)
[00191] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательности VH:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSRYWMSWVRQAPGKGLEWVANIKQDGSEKYYVDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREGGWFGELAFDYWGQGTLVTVSS (SEQ ID NO: 145)
Последовательности VL:
EIVLTQSPGTLSLSPGERATLSCRASQRVSSSYLAWYQQKPGQAPRLLIYDASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSLPWTFGQGTKVEIK (SEQ ID NO: 146)
[00192] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSA (SEQ ID NO: 147)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSGSWIHWVRQAPGKGLEWVAWILPYGGSSYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSA (SEQ ID NO: 148)
последовательности VL:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKR (SEQ ID NO: 149).
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYNVPWTFGQGTKVEIKR (SEQ ID NO: 150).
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYAPPWTFGQGTKVEIKR (SEQ ID NO: 151)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYTVPWTFGQGTKVEIKR (SEQ ID NO: 152)
DIQMTQSPSSLSASVGDRVTITCRASQVINTFLAWYQQKPGKAPKLLIYSASTLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYTVPRTFGQGTKVEIKR (SEQ ID NO: 153).
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQGYGVPRTFGQGTKVEIKR (SEQ ID NO: 154)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLFTPPTFGQGTKVEIKR (SEQ ID NO: 155)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYFITPTTFGQGTKVEIKR (SEQ ID NO: 156)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYYTPPTFGQGTKVEIKR (SEQ ID NO: 157)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQFFYTPPTFGQGTKVEIKR (SEQ ID NO: 158)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSLFTPPTFGQGTKVEIKR (SEQ ID NO: 159)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSLYTPPTFGQGTKVEIKR (SEQ ID NO: 160)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSWYHPPTFGQGTKVEIKR (SEQ ID NO: 161)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYFYIPPTFGQGTKVEIKR (SEQ ID NO: 162)
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYWYTPTTFGQGTKVEIKR (SEQ ID NO: 163).
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYFIPPTFGQGTKVEIKR (SEQ ID NO: 164)
[00193] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
METGLRWLLLVAVLKGVQCLSVEESGGRLVTPGTPLTLTCTASGFTITNYHMFWVRQAPGKGLEWIGVITSSGIGSSSTTYYATWAKGRFTISKTSTTVNLRITSPTTEDTATYFCARDYFTNTYYALDIWGPGTLVTVSS (SEQ ID NO: 165)
QVQLVQSGAEVKKPGSSVKVSCKTSGDTFSTYAISWVRQAPGQGLEWMGGIIPIFGKAHYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYFCARKFHFVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 166)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYDVHWVRQAPGQRLEWMGWLHADTGITKFSQKFQGRVTITRDTSASTAYMELSSLRSEDTAVYYCARERIQLWFDYWGQGTLVTVSS (SEQ ID NO: 167)
QVQLVQSGAEVKKPGSSVKVSCKVSGGIFSTYAINWVRQAPGQGLEWMGGIIPIFGTANHAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARDQGIAAALFDYWGQGTLVTVSS (SEQ ID NO: 168)
EVQLVESGGGLVQPGRSLRLSCAVSGFTFDDYVVHWVRQAPGKGLEWVSGISGNSGNIGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAVPFDYWGQGTLVTVSS (SEQ ID NO: 169)
QVQLVQSGAEVKKPGSSVKVSCKTSGDTFSSYAISWVRQAPGQGLEWMGGIIPIFGRAHYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYFCARKFHFVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 170)
QVQLVQSGAEVKKPGSSVKVSCKTSGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGKAHYAQKFQGRVTITADESTTTAYMELSSLRSEDTAVYYCARKYDYVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 171)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAINWVRQAPGQGLEWMGGIIPIFGSANYAQKFQDRVTITADESTSAAYMELSSLRSEDTAVYYCARDSSGWSRYYMDVWGQGTTVTVSS (SEQ ID NO: 172)
QVQLVQSGAEVKEPGSSVKVSCKASGGTFNSYAISWVRQAPGQGLEWMGGIIPLFGIAHYAQKFQGRVTITADESTNTAYMDLSSLRSEDTAVYYCARKYSYVSGSPFGMDVWGQGTTVTVSS (SEQ ID NO: 173)
EVQLVESGGGLVQPGRSLRLSCAASGITFDDYGMHWVRQAPGKGLEWVSGISWNRGRIEYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAKGRFRYFDWFLDYWGQGTLVTVSS (SEQ ID NO: 174)
последовательности VL:
MDTRAPTQLLGLLLLWLPGARCALVMTQTPSSTSTAVGGTVTIKCQASQSISVYLAWYQQKPGQPPKLLIYSASTLASGVPSRFKGSRSGTEYTLTISGVQREDAATYYCLGSAGS (SEQ ID NO: 175)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLVWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPRTFGQGTKVEIK (SEQ ID NO: 176)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPTFGQGTKVEIK (SEQ ID NO: 177)
DIQMTQSPSSLSASVGDRVTITCRASQGISSWLAWYQQKPEKAPKSLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYNSYPYTFGQGTKLEIK (SEQ ID NO: 178)
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSPWTFGQGTKVEIK (SEQ ID NO: 179)
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSPFGGGTKVEIK (SEQ ID NO: 180)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPTFGQGTRLEIK (SEQ ID NO: 181)
AIQLTQSPSSLSASVGDRVTITCRASQGISSALAWYQQKPGKAPKLLIYDASSLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQFNSYPFTFGPGTKVDIK (SEQ ID NO: 182)
[00194] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYIMMWVRQAPGKGLEWVSSIYPSGGITFYADTVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARIKLGTVTTVDYWGQGTLVTVSS (SEQ ID NO: 183)
последовательности VL:
QSALTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTRVFGTGTKVTVL (SEQ ID NO: 184)
[00195] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVKLQESGPSLVKPSQTLSLTCSVTGYSITSDYWNWIRKFPGNKLEYVGYISYTGSTYYNPSLKSRISITRDTSKNQYYLQLNSVTSEDTATYYCARYGGWLSPFDYWGQGTTLTVSS (SEQ ID NO: 185)
EVQLQESGPGLVAPSQSLSITCTVSGFSLTTYSINWIRQPPGKGLEWLGVMWAGGGTNSNSVLKSRLIISKDNSKSQVFLKMNSLQTDDTARYYCARYYGNSPYYAIDYWGQGTSVTVSS (SEQ ID NO: 186)
EVKLQESGPSLVKPSQTLSLTCSVTGYSIISDYWNWIRKFPGNKLEYLGYISYTGSTYYNPSLKSRISITRDTSKNQYYLQLNSVTTEDTATYYCARRGGWLLPFDYWGQGTTLTVSS (SEQ ID NO: 187)
EVKLQESGPSLVKPGASVKLSCKASGYTFTSYDINWVKQRPGQGLEWIGWIFPRDNNTKYNENFKGKATLTVDTSSTTAYMELHSLTSEDSAVYFCTKENWVGDFDYWGQGTTLTLSS (SEQ ID NO: 188)
EVQLQQSGPDLVTPGASVRISCQASGYTFPDYYMNWVKQSHGKSLEWIGDIDPNYGGTTYNQKFKGKAILTVDRSSSTAYMELRSLTSEDSAVYYCARGALTDWGQGTSLTVSS (SEQ ID NO: 189)
EIVLTQSPATLSLSPGERATLSCRASSSVSYIYWFQQKPGQSPRPLIYAAFNRATGIPARFSGSGSGTDYTLTISSLEPEDFAVYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 190)
QVQLVQSGAEVKKPGASVKVSCKASGYTFPDYYMNWVRQAPGQGLEWMGDIDPNYGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGALTDWGQGTMVTVSS (SEQ ID NO: 191
QVQLVQSGAEVKKPGASVKVSCKASGYTFPDYYMNWVRQAPGQSLEWMGDIDPNYGGTNYNQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGALTDWGQGTMVTVSS (SEQ ID NO: 192)
EVQLVQSGAEVKKPGASVKVSCKASGYTFPDYYMNWVRQAPGQSLEWMGDIDPNYGGTNYNQKFQGRVTMTVDRSSSTAYMELSRLRSDDTAVYYCARGALTDWGQGTMVTVSS (SEQ ID NO: 193)
EVQLVESGGGLVQPGRSLRLSCTASGYTFPDYYMNWVRQAPGKGLEWVGDIDPNYGGTTYAASVKGRFTISVDRSKSIAYLQMSSLKTEDTAVYYCTRGALTDWGQGTMVTVSS (SEQ ID NO: 194)
EVQLVESGGGLVQPGRSLRLSCTASGYTFPDYYMNWVRQAPGKGLEWVGDIDPNYGGTTYNASVKGRFTISVDRSKSIAYLQMSSLKTEDTAVYYCARGALTDWGQGTMVTVSS (SEQ ID NO: 195)
последовательности VL:
DIVMTQSHKLMSTSVGDRVSITCKASQDVGTAVAWYQQKPGQSPKLLIYWASTRHTGVPDRFTGSGSGTDFTLTISNVQSEDLADYFCQQDSSYPLTFGAGTKVELK (SEQ ID NO: 196)
DIVTTQSHKLMSTSVGDRVSITCKASQDVGTAVAWYQQKPGQSPKLLIYWASTRHTGVPDRFTGSGSGTDFTLTISNVQSEDLADYFCQQDSSYPLTFGAGTKVELK (SEQ ID NO: 197)
DIVMTQSPSSLAVSVGEKVSMGCKSSQSLLYSSNQKNSLAWYQQKPGQSPKLLIDWASTRESGVPDRFTGSGSGTDFTLTISSVKAEDLAVYYCQQYYGYPLTFGAGTKLELK (SEQ ID NO: 198)
DIVMTQSPAIMSASPGEKVTMTCSASSSIRYMHWYQQKPGTSPKRWISDTSKLTSGVPARFSGSGSGTSYALTISSMEAEDAATYYCHQRSSYPWTFGGGTKLEIK (SEQ ID NO: 199)
QIVLSQSPAILSASPGEKVTMTCRASSSVSYIYWFQQKPGSSPKPWIYATFNLASGVPARFSGSGSGTSYSLTISRVETEDAATYYCQQWSNNPLTFGAGTKLELK (SEQ ID NO: 200)
EIVLTQSPATLSLSPGERATLSCRASSSVSYIYWFQQKPGQAPRLLIYAAFNRATGIPARFSGSGSGTDYTLTISSLEPEDFAVYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 201)
QIVLTQSPATLSLSPGERATLSCRASSSVSYIYWFQQKPGQSPRPLIYATFNLASGIPARFSGSGSGTSYTLTISRLEPEDFAVYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 202)
DIQLTQSPSSLSASVGDRVTITCRASSGVSYIYWFQQKPGKAPKLLIYAAFNLASGVPSRFSGSGSGTEYTLTISSLQPEDFATYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 203)
DIQLTQSPSSLSASVGDRVTITCRASSGVSYIYWFQQKPGKAPKPLIYAAFNLASGVPSRFSGSGSGTEYTLTISSLQPEDFATYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 204)
DIQLTQSPSILSASVGDRVTITCRASSSVSYIYWFQQKPGKAPKPLIYATFNLASGVPSRFSGSGSGTSYTLTISSLQPEDFATYYCQQWSNNPLTFGQGTKVEIK (SEQ ID NO: 205)
[00196] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYGISWVRQAPGQGLEWMGWISAYNGNTNYAQKLQGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARALPSGTILVGGWFDPWGQGTLVTVSS (SEQ ID NO: 206)
EVQLVQSGGGVVQPGRSLRLSCAASGFTFSSYALSWVRQAPGKGLEWVSAISGGGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDVFPETFSMNYGMDVWGQGTLVTVSS (SEQ ID NO: 207)
QVQLVQSGGGVVQPGGSLRLSCAASGFTFDDYAMHWVRQAPGKGLEWVSLISGDGGSTYYADSVKGRFTISRDNSKNSLYLQMNSLRTEDTALYYCAKVLLPCSSTSCYGSVGAFDIWGQGTTVTVSS (SEQ ID NO: 208)
QVQLVQSGGSVVRPGESLRLSCVASGFIFDNYDMSWVRQVPGKGLEWVSRVNWNGGSTTYADAVKGRFTISRDNTKNSLYLQMNNLRAEDTAVYYCVREFVGAYDLWGQGTTVTVSS (SEQ ID NO: 209)
QVQLVQSGAEVKKPGATVKVSCKVFGDTFRGLYIHWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITTDESTSTAYMELSSLRSEDTAVYYCASGLRWGIWGWFDPWGQGTLVTVSS (SEQ ID NO: 210)
EVQLVQSGAELKKPGSSVKVSCKAFGGTFSDNAISWVRQAPGQGPEWMGGIIPIFGKPNYAQKFQGRVTITADESTSTAYMVLSSLRSEDTAVYYCARTMVRGFLGVMDVWGQGTTVTVSS (SEQ ID NO: 211)
QVQLVQSGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSAISGSGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDQFVTIFGVPRYGMDVWGQGTTVTVSS (SEQ ID NO: 212)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADKSTSTAYMELSSLRSEDTAVYYCARGRQMFGAGIDFWGPGTLVTVSS (SEQ ID NO: 213)
EVQLVESGAEVKKPGSSVKVSCKVSGGTFGTYALNWVRQAPGQGLEWMGRIVPLIGLVNYAHNFEGRISITADKSTGTAYMELSNLRSDDTAVYYCAREVYGGNSDYWGQGTLVTVSS (SEQ ID NO: 214)
QVQLVQSGGEVKKPGASVKVSCKASGYTLSSHGITWVRQAPGQGLEWMGWISAHNGHASNAQKVEDRVTMTTDTSTNTAYMELRSLTADDTAVYYCARVHAALYYGMDVWGQGTLVTVSS (SEQ ID NO: 215)
QVQLQESGGGVVQPGRSLRLSCSASGFTFSRHGMHWVRQAPGKGLEWVAVISHDGSVKYYADSMKGRFSISRDNSNNTLYLQMDSLRADDTAVYYCARGLSYQVSGWFDPWGQGTLVTVSS (SEQ ID NO: 216)
NFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFSGSIDTSSNSASLTISGLKTKDEADYYCQSYDGITVIFGGGTKLTVL (SEQ ID NO: 217)
NFMLTQPHSVSGSPGKTVTLPCTRSSGSIASHYVQWYQQRPGSAPTTVIYEDNKRPSGVPDRFSGSIDSSSNSASLSISGLKTEDEADYYCQSYDSSNRWVFGGGTKLTVL (SEQ ID NO: 218)
LPVLTQPASLSASPGASASLTCTLRSGLNVGSYRIYWYQQKPGSRPQYLLNYKSDSNKQQASGVPSRFSGSKDASANAGILLISGLQSEDEADYYCMIWYSSAVVFGGGTKLTVL (SEQ ID NO: 219)
последовательности VL:
NFMLTQPHSVSESPGKTVTISCTRSSGNIASNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSYDSSNLWVFGGGTKLTVL (SEQ ID NO: 220)
SSELTQDPAVSVALGQTVRITCQGDSLRSYYASWYQQKPGQAPVLVIYGKNNRPSGIPDRFSGSSSGNTASLTITGAQAEDEADYYCNSRDSSGNHYVFGTGTKVTVL (SEQ ID NO: 221)
LPVLTQAPSVSVAPGKTARITCGGSDIGRKSVHWYQQKPGQAPALVIYSDRDRPSGISERFSGSNSGNTATLTISRVEAGDEADYYCQVWDNNSDHYVFGAGTELIVL (SEQ ID NO: 222)
QSALTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSTLPFGGGTKLTVL (SEQ ID NO: 223)
EIVLTQSPATLSLSPGERATLSCRASQSIGNSLAWYQQKPGQAPRLLMYGASSRATGIPDRFSGSGAGTDFTLTISSLEPEDFATYYCQQHTIPTFSFGPGTKVEVK (SEQ ID NO: 224)
DIVMTQTPSFLSASIGDRVTITCRASQGIGSYLAWYQQRPGEAPKLLIYAASTLQSGVPSRFSGSGSGTDFTLTISNLQPEDFATYYCQQLNNYPITFGQGTRLEIK (SEQ ID NO: 225)
QSALTQPPSVSVSPGQTANIPCSGDKLGNKYAYWYQQKPGQSPVLLIYQDIKRPSRIPERFSGSNSADTATLTISGTQAMDEADYYCQTWDNSVVFGGGTKLTVL (SEQ ID NO: 226)
NFMLTQPHSVSESPGKTVTISCTRSSGSIDSNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSYDSNNRHVIFGGGTKLTVL (SEQ ID NO: 227)
NFMLTQPHSVSESPGKTVTISCTRSSGNIGTNYVQWYQQRPGSAPVALIYEDYRRPSGVPDRFSGSIDSSSNSASLIISGLKPEDEADYYCQSYHSSGWEFGGGTKLTVL (SEQ ID NO: 228)
QSVLTQPPSVSVAPGQTARITCGGNNIGSKGVHWYQQKPGQAPVLVVYDDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHWVFGGGTKLTVL (SEQ ID NO: 229)
NFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSYDSTTPSVFGGGTKLTVL (SEQ ID NO: 230)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYGISWVRQAPGQGLEWMGWTSPHNGLTAFAQILEGRVTMTTDTSTNTAYMELRNLTFDDTAVYFCAKVHPVFSYALDVWGQGTLVTVSS (SEQ ID NO: 231)
EVQLVESGAEVMNPGSSVRVSCRGSGGDFSTYAFSWVRQAPGQGLEWMGRIIPILGIANYAQKFQGRVTITADKSTSTAYMELSSLRSDDTAVYYCARDGYGSDPVLWGQGTLVTVSS (SEQ ID NO: 232)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTNYGISWVRQAPGQGLEWMGWISAYNGNTNYAQKVQGRVTMTTDTSTSTGYMELRSLRSDDTAVYYCARGDFRKPFDYWGQGTLVTVSS (SEQ ID NO: 233)
[00197] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLVQSGPELKKPGASVKMSCKASGYTFTSYVMHWVKQAPGQRLEWIGYVNPFNDGTKYNEMFKGRATLTSDKSTSTAYMELSSLRSEDSAVYYCARQAWGYPWGQGTLVTVSS (SEQ ID NO: 234)
EVQLVQSGAEVKKPGASVKMSCKASGYTFTSYVMHWVKQAPGQRLEWIGYVNPFNDGTKYNEMFKGRATLTSDKSTSTAYMELSSLRSEDTAVYYCARQAWGYPWGQGTLVTVSS (SEQ ID NO: 235)
EVQLVQSGAEVKKPGASVKMSCKASGYTFTSYVMHWVRQAPGQRLEWIGYVNPFNDGTKYNEMFKGRATLTSDKSTSTAYMELSSLRSEDTAVYYCARQAWGYPWGQGTLVTVSS (SEQ ID NO: 236)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYVMHWVRQAPGQRLEWIGYVNPFNDGTKYNEMFKGRATLTSDKSTSTAYMELSSLRSEDTAVYYCARQAWGYPWGQGTLVTVSS (SEQ ID NO: 237)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYVMHWVRQAPGQRLEWIGYVNPFNDGTKYNEMFKGRATITSDKSTSTAYMELSSLRSEDTAVYYCARQAWGYPWGQGTLVTVSS (SEQ ID NO: 238)
последовательности VL:
DIVLTQSPASLALSPGERATLSCRATESVEYYGTSLVQWYQQKPGQPPKLLIYAASSVDSGVPSRFSGSGSGTDFTLTINSLEEEDAAMYFCQQSRRVPYTFGQGTKLEIK (SEQ ID NO: 239)
DIVLTQSPATLSLSPGERATLSCRATESVEYYGTSLVQWYQQKPGQPPKLLIYAASSVDSGVPSRFSGSGSGTDFTLTINSLEAEDAAMYFCQQSRRVPYTFGQGTKLEIK (SEQ ID NO: 240)
EIVLTQSPATLSLSPGERATLSCRATESVEYYGTSLVQWYQQKPGQPPKLLIYAASSVDSGVPSRFSGSGSGTDFTLTINSLEAEDAAMYFCQQSRRVPYTFGQGTKLEIK (SEQ ID NO: 241)
DIVLTQSPATLSLSPGERATLSCRATESVEYYGTSLVQWYQQKPGQPPKLLIYAASSVDSGVPSRFSGSGSGTDFTLTINSLEAEDAATYFCQQSRRVPYTFGQGTKLEIK (SEQ ID NO: 242)
[00198] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADKSTSTAYMELSSLRSEDTAVYYCAREGTIYDSSGYSFDYWGQGTLVTVSS (SEQ ID NO: 243)
EVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGIINPSGGSTSYAQKFQGRVSMTRDTSTSTVYMELSSLTSEDTAVYYCARDLFPHIYGNYYGMDIWGQGTTVTVSS (SEQ ID NO: 244)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADKSTSTAYMELSSLRSEDTAVYYCARLAVPGAFDIWGQGTMVTVSS (SEQ ID NO: 245)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARGQWLVTELDYWGQGTLVTVSS (SEQ ID NO: 246)
EVQLVESGSEVEKPGSSVKVSCKASGGTFSDSGISWVRQAPGQGLEWMGGIIPMFATPYYAQKFQDRVTITADESTSTVYMELSGLRSDDTAVFYCARDRGRGHLPWYFDLWGRGTLVTVSS (SEQ ID NO: 247)
EVQLVESGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARAPYYYYYMDVWGQGTTVTVSS (SEQ ID NO: 248)
EVQLLESGAEVKKPGSSVKVSCKASGGTLSRYALSWVRQAPGQGPEWVGAIIPIFGTPHYSKKFQDRVIITVDTSTNTAFMELSSLRFEDTALYFCARGHDEYDISGYHRLDYWGQGTLVTVSS (SEQ ID NO: 249)
QVQLVQSGSELKKPGSSVKVSCKASGYSFSGYYIHWVRQAPGQGLEWMGWIDPNSGVTNYVRRFQGRVTMTRDTSLSTAYMELSGLTADDTAVYYCARDENLWQFGYLDYWGQGTLVTVSS (SEQ ID NO: 250)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSRYGVHWVRQAPGQGLEWMGRLIPIVSMTNYAQKFQDRVSITTDKSTGTAYMELRSLTSEDTALYYCASVGQQLPWVFFAWGQGTLVTVSS (SEQ ID NO: 251)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 252)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 253)
EVQLVQSGGGLVQPGGSLRLSCAASGFTFSDYGMHWVRQPPGKGLEWLAVISYDGSYKIHADSVQGRFTISRDNAKNSVFLQMNSLKTEDTAVYYCTTDRKWLAWHGMDVWGQGTTVTVSS (SEQ ID NO: 254)
EVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARDGIVADFQHWGQGTLVTVSS (SEQ ID NO: 255)
EVQLVESGAEVKKPGASVKVSCKASGDTFSRYGITWVRQAPGRGLEWMGNIVPFFGATNYAQKFQGRLTITADKSSYTSYMDLSSLRSDDTAVYYCARDHFYGSGGYFDYWGQGTLVTVSS (SEQ ID NO: 256)
EVQLLESGAEVKKPGASVKVSCKASGYTFNSYDINWVRQAPGQGLEWMGGIIPVFGTANYAESFQGRVTMTADHSTSTAYMELNNLRSEDTAVYYCARDRWHYESRPMDVWGQGTTVTVSS (SEQ ID NO: 257)
EVQLVESGGGLVRPGGSLRLACAASGFSFSDYYMTWIRQAPGRGLEWIAYISDSGQTVHYADSVKGRFTISRDNTKNSLFLQVNTLRAEDTAVYYCAREDLLGYYLQSWGQGTLVTVSS (SEQ ID NO: 258)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNSAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAVSVKSRITINPDTSKNQFSLQLNSVTPEDTAVYYCARDEPRAVAGSQAYYYYGMDVWGQGTTVTVSS (SEQ ID NO: 259)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYYMHWVRQAPGQGLEWMGIINPSDGSTSYAQKFQGRVTMTRDTSTSTVHMELSSLRSEDTAVYYCARDLFPHIYGNYYGMDIWGQGTTVTVSS (SEQ ID NO: 260)
QMQLVQSGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 261)
QVQLVQSGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 262)
последовательности VL:
QSVLTQPPSVSAAPGQKVTISCSGNNSNIANNYVSWYQQLPGTAPKLLIYDNNYRPSGIPDRFSGSKSGTSATLDITGLQTGDEADYYCGVWDGSLTTGVFGGGTKLTVL (SEQ ID NO: 263)
AIQMTQSPSSLSASVGDRVTITCRASQGISNYLAWYQQKPGKVPKLLIYAASTLESGVPSRFSGSGSGTDFTLTISSLQPEDLATYYCQQLHTFPLTFGGGTKVEIK (SEQ ID NO: 264)
QPVLTQPPSASGSPGQSVTISCTGTSSDVGAYNFVSWYRQHPGKAPKLMIYEVNKRPSGVPDRFSGSKSGNTASLTVSGLQAEDEADYYCSSYAGTNSLGIFGTGTKLTVL (SEQ ID NO: 265)
QSVVTQPPSVSAAPGQKVTISCSGSSSDIGNHYVSWYQQLPGTAPKLLIYDNNQRPSGIPDRFSGSKSGTSATLAITGLQTGDEADYYCGTWDNSLSPHLLFGGGTKLTVL (SEQ ID NO: 266)
QSVLTQPPSVSAAPGQKVTISCSGSSSNMGNNYVSWYKQVPGTAPKLLIYENDKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDNSLSGFVFASGTKVTVL (SEQ ID NO: 267)
QSALTQPASVSGSLGQSVTISCTGSSSDVGSYNLVSWYQQHPGKAPNLMIYDVSKRSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTGISTVVFGGGTKLTVL (SEQ ID NO: 268)
QSVLTQPASVSGSPGQSITISCTGTSSDVGSYNLVSWYQQHPGKAPKLMIYEVSKRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYGGFNNLLFGGGTKLTVL (SEQ ID NO: 269)
DIVMTQSPSSLSASIGDRVTITCRASQRISAYVNWYQQKPGKAPKVLIYAASSLRSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQTYSSPWTFGQGTKVEIK (SEQ ID NO: 270)
QSVLTQPPSASGSPGQSVTISCTGTSSDIGGYDSVSWYQQHPGKAPKLMIYDVSKRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSIFFYVFGTGTKVTVL (SEQ ID NO: 271)
LPVLTQPASVSGSPGQSITISCTGTTSDIGGYDYVSWYQQHPGKAPKLMIYDVSKRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTHVFGTGTKLTVL (SEQ ID NO: 272)
QSALTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYRSSTLGPVFGGGTKLTVL (SEQ ID NO: 273)
QAGLTQPPSVSEAPRQRVTISCSGSSSNIGNNAVNWYQQLPGKAPKLLIYYDDLLPSGVSDRFSGSKSGTSASLAISGLQSEDEADYYCAAWDDSLNGYVFGTGTKLTVL (SEQ ID NO: 274)
QSALTQPRSVSGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSKRPSGVPDRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSTTHVFGTGTKVTVL (SEQ ID NO: 275)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSVWVFGGGTQLTVL (SEQ ID NO: 276)
QSVLTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGRAPRLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEGDYYCSSYTSGGTLGPVFGGGTKLTVL (SEQ ID NO: 277)
QAGLTQPPSASGTPGQRVTISCSGSSSNIGSNTVNWYQQLPGTAPKLLIYSNNQRPSGVPDRFSGSKSGTSASLAISGLQSEDEADYYCAAWDDSLNGWVFGGGTKLTVL (SEQ ID NO: 278)
AIRMTQSPSSLSASVGDRVTITCRASQSISNYLNWYQQRPGKAPNLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQTYSTPYTFGQGTKLEIK (SEQ ID NO: 279)
QSVLTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYRQHPGKAPKLMIYDVSYRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTDSSTRYVFGTGTKLTVL (SEQ ID NO: 280)
QPVLTQPPSASGTPGQRVAISCSGSRSNIEINSVNWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGSWDSSLSADVFGTGTKLTVL (SEQ ID NO: 281)
QSVLTQPPSVSAAPGKKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYRNNQRPSGVPDRFSGSKSGTSASLAISGLQSEDEADYYCATWDDSLNGWVFGGGTKLTVL (SEQ ID NO: 282)
QSVVTQPPSVSGAPGQRVTISCTGSSSNIGAGYDVHWYQQLPGTAPKLLIYGNNNRHSGVPDRFSGSKSGTSASLAITGLQAEDEAEFFCGTWDSRLTTYVFGSGTKLTVL (SEQ ID NO: 283)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSAVVFGGGTKLTVL (SEQ ID NO: 284)
VIWMTQSPSSLSASVGDRVTITCAASSLQSWYQQKPGKAPKLLIYEASTLESGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCQQSYSTPYTFGQGTKLEIK (SEQ ID NO: 285)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQVPGTAPKLLIYDNNKRPSGIPDRFSGSNSDTSATLGITGLQTGDEADYYCGTWDSSLSAWVFGGGTKLTVL (SEQ ID NO: 286)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSAGSVVFGGGTKLTVL (SEQ ID NO: 287)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCLVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 288)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 289)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 290)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 291)
[00199] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности тяжелой цепи (HC) и последовательности легкой цепи (LC), выбранной из группы, состоящей из:
последовательностей HC:
QVQLVQSGVEVKKPGASVKVSCKASGYTFTNYYMYWVRQAPGQGLEWMGGINPSNGGTNFNEKFKNRVTLTTDSSTTTAYMELKSLQFDDTAVYYCARRDYRFDMGFDYWGQGTTVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 292)
QVQLVESGGGVVQPGRSLRLDCKASGITFSNSGMHWVRQAPGKGLEWVAVIWYDGSKRYYADSVKGRFTISRDNSKNTLFLQMNSLRAEDTAVYYCATNDDYWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK (SEQ ID NO: 293)
последовательностей LC:
EIVLTQSPATLSLSPGERATLSCRASKGVSTSGYSYLHWYQQKPGQAPRLLIYLASYLESGVPARFSGSGSGTDFTLTISSLEPEDFAVYYCQHSRDLPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 294)
EIVLTQSPATLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSSNWPRTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 295)
[00200] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTK (SEQ ID NO: 296)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSS (SEQ ID NO: 297)
последовательностей HC:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG (SEQ ID NO: 298)
последовательности VL:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKR (SEQ ID NO: 299)
последовательностей LC:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 300)
[00201] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSRFWMSWVRQAPGKGLEWVANINQDGTEKYYVDSVKGRFTISRDNAKNSLYLQMNSLRAGDTAVYYCANTYYDFWSGHFDYWGQGTLVTVSS (SEQ ID NO: 301)
QEHLVESGGGVVQPGRSLRLSCEASGFTFSNFGMHWVRQAPGKGLEWVAALWSDGSNKYYADSVKGRVTISRDNSKNTLYLQMNSLRAEDTAVYYCARGRGAPGIPIFGYWGQGTLVTVSS (SEQ ID NO: 302)
EVQLVESGGGLVKPGGSLRLSCAASGFTFSNAWMSWVRQAPGKGLEWVGRIKRKTDGGTTDYAAPVKGRFTISRDDSKNTLHLQMNSLKTEDTAVYYCTTDDIVVVPAVMREYYFGMDVWGQGTTVTVSS (SEQ ID NO: 303)
QVQLVQSGAEVKKPGASVQVSCKASGYSFTGYYIHWVRQAPGQGLEWMGWINPNSGTKKYAHKFQGRVTMTRDTSIDTAYMILSSLISDDTAVYYCARDEDWNFGSWFDSWGQGTLVTVSS (SEQ ID NO: 304)
QVHLVQSGAEVKKPGASVKVSCKASGYTFTGYYIHWVRQAPGHGLEWMGWLNPNTGTTKYIQNFQGRVTMTRDTSSSTAYMELTRLRSDDTAVYYCARDEDWNYGSWFDTWGQGTLVTVSS (SEQ ID NO: 305)
EVQLVESGGGVVRPGGSLRLSCAASGFTFDDYGMTWVRQAPGRGLEWVSGIHWHGKRTGYADSVKGRFTISRDNAKKSLYLQMNSLKGEDTALYHCVRGGMSTGDWFDPWGQGTLVIVSS (SEQ ID NO: 306)
EVQLVESGGGVVRPGGSLRLSCAASGFTFDDYGMTWVRQVPGKGLEWVSGIHWSGRSTGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCARGGMSTGDWFDPWGQGTLVTVSS (SEQ ID NO: 307)
EVQLVESGGGLVQPGGSLRLSCAASGFTVGSNYMNWVRQAPGKGLEWVSVIYSGGSTYYADSVKGRFTISRLTSKNTLYLQMSSLRPEDTAVYYCARGIRGLDVWGQGTTVTVSS (SEQ ID NO: 308)
EERLVESGGDLVQPGGSLRLSCAASGITVGTNYMNWVRQAPGKGLEWVSVISSGGNTHYADSVKGRFIMSRQTSKNTLYLQMNSLETEDTAVYYCARGIRGLDVWGQGTMVTVSS (SEQ ID NO: 309)
QVQLVQSGAEVKMPGSSVRVSCKASGGIFSSSTISWVRQAPGQGLEWMGEIIPVFGTVNYAQKFQDRVIFTADESTTTAYMELSSLKSGDTAVYFCARNWGLGSFYIWGQGTMVTVSS (SEQ ID NO: 310)
EVQLVESGGDLVHPGRSLRLSCAASGFPFDEYAMHWVRQVPGKGLEWVSGISWSNNNIGYADSVKGRFTISRDNAKNSLYLQMNSLRPEDTAFYYCAKSGIFDSWGQGTLVTVSS (SEQ ID NO: 311)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVTLISYEGRNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDRTLYGMDVWGQGTTVTVSS (SEQ ID NO: 312)
QVTLRESGPALVKTTQTLTLTCTFSGFSLSTNRMCVTWIRQPPGKALEWLARIDWDGVKYYNTSLKTRLTISKDTSKNQVVLTMTNMDPVDTATFYCARSTSLTFYYFDYWGQGTLVTVSS (SEQ ID NO: 313)
EVQLVESGGGLVQPGGSLRLSCAASEFTVGTNHMNWVRQAPGKGLEWVSVIYSGGNTFYADSVKGRFTISRHTSKNTLYLQMNSLTAEDTAVYYCARGLGGMDVWGQGTTVTVSS (SEQ ID NO: 314)
EVQLVESGGGLVQRGESLRLYCAASGFTFSKYWMNWVRQAPGKGLEWVANIKGDGSEKYYVDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCARDYWGSGYYFDFWGQGTLVTVSS (SEQ ID NO: 315)
EVQLVESGGGLVQSGGSLRLSCAASGFTFSSYWMSWVRQAPGKGLEWVANIKQDGSEKYYVDSVKGRFTISRDNAKNSLYLQMNSLRADDTAVYYCARDDIVVVPAPMGYYYYYFGMDVWGQGTTVTVSS (SEQ ID NO: 316)
EVQLVESGGGLVQPGRSLRLSCAASGFTFDDFAMHWVRQAPGKGLEWVSGISWTGGNMDYANSVKGRFTISREDAKNSLYLQMNSLRAADTALYYCVKDIRGIVATGGAFDIWGRGTMVTVSS (SEQ ID NO: 317)
EVQLVESGGGLVQPGGSLRLSCAASGFTVGTNYMNWVRQAPGKGLEWISVIYSGGSTFYADSVKGRFTISRQTSQNTLYLQMNSLRPEDTAVYYCARGIRGFDIWGQGTMVTVSS (SEQ ID NO: 318)
EVQLVESGGGLVQPGGSLRLSCAASGFTISTNYMNWVRQAPGKGLEWVAVIYSSGSTYYIDSVKGRFTISRLTSKNTVYLQMSSLNSEDTAVYYCARGIRGFDIWGQGTMVTVSS (SEQ ID NO: 319)
EVQLVESGGGLVQPGRSLRLSCAASGFTIDDSAMHWVRQTPGKGLEWVSGISWKSGSIGYADSVRGRFTISRDNAKNSLYLQMNSLRVEDTALYYCVKDIRGNWNYGGNWFDPWGQGTLVTVSS (SEQ ID NO: 320)
EVQLVESGGGLVQPGGSLRLSCEASGFTVGVNHMNWVRQAPGKGLEWVSVIFSSGRTFYGDYVKGRLTIFRQTSQNTVYLQMNSLRSEDTAIYYCARGIGGLDIWGRGTMVTVSS (SEQ ID NO: 321)
EVQLVESGGGLVQPGRSLRLSCAASGFTFDDYALHWVRQAPGKGLEWVSGISWTGGTIDYADSVKGRFTISRDNAKNSLYLQMSSLRTEDTAIYYCTRDIRGNWKYGGWFDPWGQGTLVTVSS (SEQ ID NO: 322)
QVQLVQSGTEVKKPGASVKVSCKASGYTFTAYYMHWVRQAPGQGLDWMGWISPNSGFTNYAQKFQGRVTMTRDTSINTFYMELSGLRSDDTAVYYCAREGSTHHNSFDPWGQGTLVTVSS (SEQ ID NO: 323)
EVQLVESGGGLVQPGGSLRLSCAASGFTVGTNFMNWVRQAPGKGLEWVSAIYSGGTANYADSVKGRFTISRDTSRNTLYLQMNSLRTEDTAVYYCARGGGMDVWGQGTTVTVSS (SEQ ID NO: 324)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFNTYVLSWVRQAPGQGLEWMGEIIPILGAANYAQNFQGRVTFTTDESTNTAYMDLSSLRSEDTAVYYCARDRTSGGFDPWGQGTLVTVSS (SEQ ID NO: 325)
QVQLVQSGAEVEKPGASVKVSCKASGYIFTHYGISWVRQAPGQGLEWVGWISPYNGYTDYAQKLQGRVTLTTDTSTTTAYMELRNLRSDDTAMYYCSRGRGPYWSFDLWGRGTLVTVSS (SEQ ID NO: 326)
последовательности VL:
DIQMTQSPSTLSASVGDRVTITCRASQSISNWLAWYQQKPGKAPKLLIYKASSLESGVPSRFSGSGSGTEFTLTISSLQPDDFATYYCQQYHSYSYTFGQGTKEIK (SEQ ID NO: 327)
DIQMTQSPSSLSASVGDRVTITCRASQGIRNDLGWYQQKPGKAPKRLIYTASSLQSGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCLQHNSYPLTFGGGTKVAIK (SEQ ID NO: 328)
DIQMTQSPSSLSASVGDRVTITCRTSQGIRNDLGWYQQKPGKAPKRLIYAASSLQSGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCLQHNNYPYTFGQGTKLEIK (SEQ ID NO: 329)
DIVMTQTPLSSPVTLGQPASISCRSSQTLVHGDGNTYLSWIQQRPGQPPRLLIYKVSNQFSGVPDRFSGSGAGTDFTLKISRVEAEDVGLYFCMQATHFPITFGQGTRLEIK (SEQ ID NO: 330)
DIVMTQTPLSSPVTLGQPASISCRSSPSLVHSDGNTYLSWLQQRPGQPPRLLIYKISNRFSGVPDRFSGSGAGTDFTLKISRVEAEDVGVYYCMQATHFPITFGQGTRLEIR (SEQ ID NO: 331)
DIQMTQSPSSLSASLGDRVTITCRASQSINSYLNWYQQKPGKAPKLLIYVASSLQSGVPSRFSGSGSGTEFTLTISNLQPEDFATYYCQQSYSTPPITFGQGTRLEIK (SEQ ID NO: 332)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYVASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPPITFGQGTRLEIK (SEQ ID NO: 333)
DIQMTQSPSSLSASVGDRVTITCRASQTINIYLNWYQQKPGRAPRLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCHQSYSTPPITFGQGTRLEIK (SEQ ID NO: 334)
DIQMTQSPSSLSASVGDRVTITCRASQSMSSYLNWYQQKPGRAPKLLIFAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPPITFGQGTRLEIK (SEQ ID NO: 335)
EIVLTQSPGTLSLSPGERATLSCRASQSFNFNYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTINRLEPEDFGVFYCQQYESAPWTFGQGTKVEIK (SEQ ID NO: 336)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKLLIYAASSLQSGVPSRFSGGGSGTDFTLTISSLRPEDFATYYCQQSYCTPPITFGQGTRLEIK (SEQ ID NO: 337)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPPITFGQGTRLEIK (SEQ ID NO: 338)
DRVTITCRASQVISNYLAWYQQKPGKVPRLLIYAASTLQSGVPSRFSGSGSGTDFTLTISSLQPEDVATYYCQKYNSAPRTFGQGTKVEIK (SEQ ID NO: 339)
DIQMTQSPSSLSASVGDRVTITCRASQNINNYLNWYQQKPGKAPKLLIYAASSFQNAVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYNTPLTFGGGTKVEIK (SEQ ID NO: 340)
DIQMTQSPSSLSASVGDRVTITCRASQGIRNDLGWYQQKPGKAPKRLIYAASSLQSGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCLQHNSYPYTFGQGTKLEIK (SEQ ID NO: 341)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPPITFGQGTRLEIK (SEQ ID NO: 342)
[00202] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
QSLEESGGRLVKPDETLTITCTVSGIDLSSNGLTWVRQAPGEGLEWIGTINKDASAYYASWAKGRLTISKPSSTKVDLKITSPTTEDTATYFCGRIAFKTGTSIWGPGTLVTVSS (SEQ ID NO: 343)
последовательности VL:
AIVMTQTPSPVSAAVGGTVTINCQASESVYSNNYLSWFQQKPGQPPKLLIYLASTLASGVPSRFKGSGSGTQFTLTISGVQCDDAATYYCIGGKSSSTDGNAFGGGTEVVVR (SEQ ID NO: 344)
[00203] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
QMQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGNIVATITPLDYWGQGTLVTVSS (SEQ ID NO: 345)
QPVLTQPPSVSAAPGQKVTISCSGSSSNIANNYVSWYQQLPGTAPKLLIFANNKRPSGIPDRFSGSKSGTSAALDITGLQTGDEADYYCGTWDSDLRAGVFGGGTKLTVL (SEQ ID NO: 346)
EVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADKSTSTAYMELSSLRSEDTAVYYCAREGTIYDSSGYSFDYWGQGTLVTVSS (SEQ ID NO: 347)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 348)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 349)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 350)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 351)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 352)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 353)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSRYGVHWVRQAPGQGLEWMGRLIPIVSMTNYAQKFQDRVSITTDKSTGTAYMELRSLTSEDTALYYCASVGQQLPWVFFAWGQGTLVTVSS (SEQ ID NO: 354)
QMQLVQSGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 355)
QVQLVQSGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISFDGSNKYYADSVRGRFTISRDNSKNTLYLQMNSLRTEDTAVYYCARGWLDRDIDYWGQGTLVTVSS (SEQ ID NO: 356)
QMQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAYSWVRQAPGQGLEWMGGIIPSFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGPIVATITPLDYWGQGTLVTVSS (SEQ ID NO: 357)
QMQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAYSWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGPIVATITPLDYWGQGTLVTVSS (SEQ ID NO: 358)
QMQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAYSWVRQAPGQGLEWMGGIIPSFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGPIVATITPLDYWGQGTLVTVSS (SEQ ID NO: 359)
QMQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPAFGTANYAQKFQGRVTITADESTSTAYMELSSLRSEDTAVYYCARGPIVATITPLDYWGQGTLVTVSS (SEQ ID NO: 360)
последовательности VL:
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 361)
AIRMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYTTSSLKSGVPSRFSGSGSGTDFTLTISRLQPEDFATYYCQQSYSSTWTFGRGTKVEIK (SEQ ID NO: 362)
QSVLTQPPSVSAAPGQKVTISCSGNNSNIANNYVSWYQQLPGTAPKLLIYDNNYRPSGIPDRFSGSKSGTSATLDITGLQTGDEADYYCGVWDGSLTTGVFGGGTKLTVL (SEQ ID NO: 363)
LPVLTQPASVSGSPGQSITISCTGTTSDIGGYDYVSWYQQHPGKAPKLMIYDVSKRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTHVFGTGTKLTVL (SEQ ID NO: 364)
QSALTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYRSSTLGPVFGGGTKLTVL (SEQ ID NO: 365)
QAGLTQPPSVSEAPRQRVTISCSGSSSNIGNNAVNWYQQLPGKAPKLLIYYDDLLPSGVSDRFSGSKSGTSASLAISGLQSEDEADYYCAAWDDSLNGYVFGTGTKLTVL (SEQ ID NO: 366)
QSALTQPRSVSGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSKRPSGVPDRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSTTHVFGTGTKVTVL (SEQ ID NO: 367)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSVWVFGGGTQLTVL (SEQ ID NO: 368)
QSVLTQPASVSGSPGQSITISCTGTSSDVGGYNYVSWYQQHPGRAPRLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEGDYYCSSYTSGGTLGPVFGGGTKLTVL (SEQ ID NO: 369)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSAVVFGGGTKLTVL (SEQ ID NO: 370)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQVPGTAPKLLIYDNNKRPSGIPDRFSGSNSDTSATLGITGLQTGDEADYYCGTWDSSLSAWVFGGGTKLTVL (SEQ ID NO: 371)
QSVVTQPPSVSAAPGQKVTISCSGSSSNIGNNYVSWYQQLPGTAPKLLIYDNNKRPSGIPDRFSGSKSGTSATLGITGLQTGDEADYYCGTWDSSLSAGSVVFGGGTKLTVL (SEQ ID NO: 372)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCLVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 373)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 374)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 375)
SYELMQPPSVSVAPGKTATIACGGENIGRKTVHWYQQKPGQAPVLVIYYDSDRPSGIPERFSGSNSGNTATLTISRVEAGDEADYYCQVWDSSSDHRIFGGGTKLTVL (SEQ ID NO: 376)
[00204] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
QVQLVQSGSEVKKSGSSVKVSCKTSGGTFSITNYAINWVRQAPGQGLEWMGGILPIFGAAKYAQKFQDRVTITADESTNTAYLELSSLTSEDTAMYYCARGKRWLQSDLQYWGQGTLVTVSS (SEQ ID NO: 377)
последовательности VL:
QPVLTQPASVSGSPGQSITISCTGSSSDVGSYDLVSWYQQSPGKVPKLLIYEGVKRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYAGTRNFVFGGGTQLTVL (SEQ ID NO: 378)
[00205] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает комбинацию последовательности VH и последовательности VL, выбранной из группы, состоящей из:
последовательностей VH:
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGQSRPGFDYWGQGTLVTVSS (SEQ ID NO: 379)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGQSWPGFDYWGQGTLVTVSS (SEQ ID NO: 380)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGQSFPGFDYWGQGTLVTVSS (SEQ ID NO: 381)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSAAFDYWGQGTLVTVSS (SEQ ID NO: 382)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSAGYDYWGQGTLVTVSS (SEQ ID NO: 383)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSKGFDYWGQGTLVTVSS (SEQ ID NO: 384)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWKQGIVTVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTV (SEQ ID NO: 385)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRNGIVTVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 386)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSDIWKQGMVTVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 387)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRQGLATAYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 388)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSEIVATGILTSYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 389)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIGRQGLITVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 390)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWYQGLVTVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 391)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSDIWKQGFATADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 392)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWKQGIVTVYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 393)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRQGLATAYDSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSS (SEQ ID NO: 394)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRNGIVTVYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSAAFDYWGQGTLVTVSS (SEQ ID NO: 395)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRNGIVTVYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSAGYDYWGQGTLVTVSS (SEQ ID NO: 396)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWRNGIVTVYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSKGFDYWGQGTLVTVSS (SEQ ID NO: 397)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMetSWVRQAPGKGLEWVSSIWYQGLVTVYADSVKGRFTISRDNSKNTLYLQMetNSLRAEDTAVYYCAKWSAAFDYWGQGTLVTVSS (SEQ ID NO: 398)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWYQGLVTVYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSAGYDYWGQGTLVTVSS (SEQ ID NO: 399)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIWYQGLVTVYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKWSKGFDYWGQGTLVTVSS (SEQ ID NO: 400)
последовательности VL:
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYYASTLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNGYPSTFGQGTKVEIKR (SEQ ID NO: 401)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYYASTLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNGYPSTFGQGTKVEIKR (SEQ ID NO: 402)
DIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNGYPSTFGGGTKVEIKR (SEQ ID NO: 403)
[00206] В некоторых вариантах осуществления данного изобретения PDL1-связывающий домен содержит или является производным от последовательности антитела или его антигенсвязывающего фрагмента, который включает одноцепочечную последовательность Fv (scFv), выбранную из группы, состоящей из:
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSDITASGQRTTYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARSKIAFDYWGQGTLVTVSSGGGGSGGGGSGGGGSTDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYKASRLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQRALKPVTFGQGTKVEIKR (SEQ ID NO: 404)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSINKDGHYTSYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKNLDEFDYWGQGTLVTVSSGGGGSGGGGSGGGGSTDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPNTFGQGTKVEIKR (SEQ ID NO: 405)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIMATGAGTLYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDGAGFDYWGQGTLVTVSSGGGGSGGGGSGGGGSTDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYSASQLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQANSRPSTFGQGTKVEIKR (SEQ ID NO: 406)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLQWVSTITSSGAATYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKNYTGFDYWGQGTLVTVSSGGGGSGGGGSGGGGSTDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYNASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYTYGPGTFGQGTKVEIKR (SEQ ID NO: 407)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSSIYSTGGATAYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKSSAGFDYWGQGTLVTVSSGGGGSGGGGSGGGGSTDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYYASTLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNGYPSTFGQGTKVEIKR (SEQ ID NO: 408)
Двойное нацеливание на PDL1 и 41BB
[00207] В некоторых вариантах осуществления данного изобретения слитые белки являются биспецифическими молекулами, которые включают TBD, который связывает 41BB и связывающий домен, направленный на PDL1. В этих вариантах осуществления данного изобретения связывание PDL1 способно обеспечить дополнительную функцию сшивания, а активация TNFRSF может быть достигнута только с помощью одного или двух анти-41BB TBD. В этих вариантах осуществления данного изобретения сигнализация TNFRSF усиливается и фокусируется наличием PDL1-экспрессирующей клетки.
Тетравалентный агонист 41BB: hzRH3v5-1
EVQLLESGGGEVQPGGSLRLSCAASGFSFSINAMGWYRQAPGKRREFVAAIESGRNTVYAESVKGRFTISRDNAKNTVYLQMSSLRAEDTAVYYCGLLKGNRVVSPSVAYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGSGGGGSGGGGSEVQLLESGGGEVQPGGSLRLSCAASGFSFSINAMGWYRQAPGKRREFVAAIESGRNTVYAESVKGRFTISRDNAKNTVYLQMSSLRAEDTAVYYCGLLKGNRVVSPSVAYWGQGTLVTVKPGG (SEQ ID NO: 448)
Биспецифический PDL1 и 41BB: hz28A2v5 x hzRH3v5-1
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQPGGSLRLSCAASGFSFSINAMGWYRQAPGKRREFVAAIESGRNTVYAESVKGRFTISRDNAKNTVYLQMSSLRAEDTAVYYCGLLKGNRVVSPSVAYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 449)
Биспецифический PDL1 и 41BB: hz28A2v5 x hzRH3v5-2
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQPGGSLRLSCAASGFSFSINAMGWYRQAPGKRREFVAAIYSGRNTVYAESVKGRFTISRDNAKNTVYLQMSSLRAEDTAVYYCGLLKGNRVVSPSVAYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 450)
Биспецифический PDL1 и 41BB: hz28A2v5 x hzRH3v5-16
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQPGGSLRLSCAASGFSFSINAMGWYRQAPGKRREFVAAIYSGSSTVYAESVKGRFTISRDNAKNTVYLQMSSLRAEDTAVYYCGLLKGNRVVSPSVAYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 451)
Биспецифический PDL1 и 41BB: hz28A2v5 x hz4E01v16
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQLLESGGGEVQPGGSLRLSCAASGWAFGNYGMAWFRQAPGKEREFVSRLAWQGGSTDYVESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARQRSYSRYDIRTPQTYDYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 452)
Биспецифический PDL1 и 41BB: hz28A2v5 x hz4E01v18
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQLLESGGGEVQPGGSLRLSCAASGWAFGNYGMAWFRQAPGKEREFVSRLAWGGGSTDYVESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARQRSYSRYDIRTPQTYDYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 453)
Биспецифический PDL1 и 41BB: hz28A2v5 x hz4E01v21
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQLLESGGGEVQPGGSLRLSCAASGWAFSNYGMAWFRQAPGKEREFVSRLAWGGGSTDYVESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARQRSYSRYDIRTPQTYDYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 454)
Биспецифический PDL1 и 41BB: hz28A2v5 x hz4E01v22
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQLLESGGGEVQPGGSLRLSCAASGWAFGNYGMAWFRQAPGKEREFVSRLAWSGGSTDYVESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARQRSYSRYDIRTPQTYDYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 455)
Биспецифический PDL1 и 41BB: hz28A2v5 x hz4E01v23
EVQLLESGGGEVQPGGSLRLSCAASGGIFAIKPISWYRQAPGKQREWVSTTTSSGATNYAESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCNVFEYWGQGTLVTVKPGGSGGSEVQLLESGGGEVQLLESGGGEVQPGGSLRLSCAASGWAFSNYGMAWFRQAPGKEREFVSRLAWSGGSTDYVESVKGRFTISRDNAKNTLYLQMSSLRAEDTAVYYCARQRSYSRYDIRTPQTYDYWGQGTLVTVKPGGGGDKTHTCPPCPAPGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 456)
Нацеливание на рецептор фолиевой кислоты альфа (FRα)
[00208] В некоторых вариантах осуществления данного изобретения слитые белки являются мультиспецифическими, содержащими TBD и связывающий домен, направленный на рецептор фолиевой кислоты альфа (FRα). В этих вариантах осуществления данного изобретения связывание FRα способно обеспечить дополнительную функцию сшивания, а активация TNFRSF может быть достигнута только с помощью одного или двух TBD. В этих вариантах осуществления данного изобретения сигнализация TNFRSF усиливается и фокусируется наличием FRα-экспрессирующей клетки.
[00209] Типовые FRα -нацеленные однодоменные последовательности приведены ниже:



CDR1: GSIFSIDA (SEQ ID NO: 429)
CDR2: ITSSGST (SEQ ID NO: 430)
CDR3: NAITRMGGSTYDF (SEQ ID NO: 431)
[00210] Данное изобретение будет дополнительно описано в следующих примерах, которые не ограничивают объем изобретения, описанный в Формуле изобретения.
ПРИМЕРЫ
Пример 1. Связывание 41BB посредством 41BB-нацеленных однодоменных антител
[00211] Нацеленные на 41BB однодоменные антитела (sdAb), упоминаемые в данном документе как 1G3 (SEQ ID NO: 432), 1H4 (SEQ ID NO: 436), 1H1 (SEQ ID NO: 440), 4H4 (SEQ ID NO: 16), 1H8 (SEQ ID NO: 444), 4F5 (SEQ ID NO: 23) и 4E1 (SEQ ID NO: 20), связывают рекомбинантный 41BB человека (Фигура 2A) и 41BB яванского макака (Фигура 2B). Нацеленные на 41BB однодоменные антитела (sdAb), упоминаемые в данном документе как 4F5 (SEQ ID NO: 23), 4H04 (SEQ ID NO: 16), 4E01 (SEQ ID NO: 20), RH03 (SEQ ID NO: 25), и D1 (SEQ ID NO: 29), связывают 41BB человека, экспрессируемый на поверхности клеток СНО (Фигура 3). Нацеленные на 41BB антитела sdAb упоминаются в данном документе как 4H04, RH03 и связывают 41BB яванского макака. На Фигуре 2А, Фигуре 2В и Фигуре 4 проиллюстрированы результаты связывания, оцененного с помощью ИФА, при этом рекомбинантный слитый белок 41BB-mFc (слитый белок, содержащий 41BB, функционально связанный с областью Fc мыши) иммобилизовали на 96-луночном планшете Medisorp. На Фигуре 3 проиллюстрированы результаты связывания, оцененного с помощью проточной цитометрии с применением клеток СНО, экспрессирующих 41BB, при этом данные представляли как медианную интенсивность флуоресценции.
Пример 2. Блокирование 41BB посредством 41BB-нацеленных однодоменных антител
[00212] Нацеленные на 41BB однодоменные антитела (sdAb), упоминаемые в данном документе как 4F05 (SEQ ID NO: 23), 4H04 (SEQ ID NO: 16), 4E01 (SEQ ID NO: 20), RH03 (SEQ ID NO: 25), и D1 (SEQ ID NO: 29) блокировали взаимодействие между 41BB и его лигандом 41BBL. Все анализируемые однодоменные антитела, за исключением RH3, блокируют взаимодействие между 41BB и 41BBL. Блокирование оценивали с помощью проточной цитометрии с применением рекомбинантного слитого белка 41BB и клеток СНО, экспрессирующих 41BB, при этом данные представляли как медианную интенсивность флуоресценции.
[00213] В отличие от 41BB sdAb по данному изобретению, обычные двухвалентные антитела анти-41BB не индуцировали передачу сигналов 41BB, за исключением тех случаев, когда осуществляется дополнительная кластеризация с экзогенным сшивающим антителом против IgG человека. На Фигуре 6 продемонстрирована неспособность обычного двухвалентного анти-41BB-антитела PF-05082566, которое описано в патенте США №8337850, индуцировать передачу сигналов 41BB, за исключением тех случаев, когда осуществлялась дополнительная кластеризация с экзогенным сшивающим антителом против IgG человека. Передачу сигналов 41BB, изображенную на Фигуре 6 контролировали с применением NFkB репортерной клеточной линии 293, экспрессирующей 41BB.
Пример 3. Связывание PDL1 и блокирование взаимодействия между PLD1 и PD1 посредством PDL1-нацеленных однодоменных антител
[00214] В представленных в данном документе исследованиях применяют типовое однодоменное антитело PDL1 (sdAb), упоминаемое в данном документе как 28A10 (SEQ ID NO: 100), чтобы продемонстрировать, что PDL1-нацеленные sdAb по данному изобретению связывают PDL1 на поверхности клетки (Фигура 7A) и блокируют взаимодействие PDL1 с PD1 (Фигура 7B). Связывание оценивали с помощью проточной цитометрии на клетках СНО, экспрессирующих PDL1, а блокирование оценивали с помощью проточной цитометрии с применением рекомбинантного слитого белка PD1 и клеток СНО, экспрессирующих PDL1. Данные, приведенные на Фигурах 7А и 7В, представлены как медианная интенсивность флуоресценции.
Пример 4. Слитые белки, нацеленные на PDL1-41BB
[00215] В данном изобретении предлагаются слитые белки, которые нацелены по меньшей мере на PDL1 и 41BB. Эти биспецифические слитые белки, нацеленные на PDL1-41BB, являются агонистами PDL1-зависимой 41BB-опосредованной передачи сигналов. На Фигурах 8А и 8В приведены концептуальные схемы, в которых биспецифические слитые белки имеют минимальные агонистические свойства 41BB (Фигура 8А), за исключением случаев, когда они связаны клеткой, экспрессирующей PD-L1 (Фигура 8В). На Фигуре 8С продемонстрирована способность PDL1-позитивной клетки, в данном случае, популяции PDL1-трансфицированных клеток CHO, опосредовать передачу сигналов 41BB и неспособность PDL1-негативной клетки, в данном случае нетрансфицированных клеток CHO, опосредовать передачу сигналов 41BB. На этой фигуре проиллюстрированы два отдельных биспецифических слитых белка, каждый из которых содержит отдельную 41BB-связывающую VHH (например, 4E01 или RH3) и PD-L1-связывающую VHH, 28A10. Передачу сигналов 41BB контролировали с применением NFkB репортерной клеточной линии 293, экспрессирующей 41BB. Эта репортерная линия клеток задействует NF-kB-индуцируемую секретируемую щелочную фосфатазу, для мониторинга передачи сигналов NF-kB.
[00216] Слитые белки по данному изобретению, нацеленные на PDL1-41BB, включают гуманизированную анти-41BB последовательность. В исследованиях, представленных в данном документе, слитые белки по данному изобретению, нацеленные на PDL1-41BB, включают гуманизированную последовательность анти-41BB, такую как hzRH3v5-1 (SEQ ID NO: 30) и/или hzRH3v9 (SEQ ID NO: 82) и связывают 41BB как человека, так и яванского макака (Фигура 9A, 9B), включая 41BB человека и 41BB яванского макака, экспрессируемые на поверхности клеток CHO (Фигуры 9C, 9D). Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB.
[00217] Гуманизированные варианты hzRH3v5-1 и hzRH3v9 не блокируют связывание 41BBL с 41BB на поверхности клетки, как проиллюстрировано на Фигуре 9Е. В этих исследованиях применяли рекомбинантный слитый белок 41BBL-mFc, содержащий область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00218] Гуманизированный вариант hzRH3v5-1 специфически связывает 41BB по сравнению с другими представителями семейства TNFRSF: OX40 и GITR (Фигура 10). Связывание оценивали с помощью проточной цитометрии с применением клеток CHO, экспрессирующих данный представитель семейства TNFRSF.
[00219] Анализировали дополнительные гуманизированные варианты 41BB. На Фигурах 11A, 11B, 11C и 11D продемонстрировано связывание гуманизированных вариантов 4E01 с 41BB человека (Фигура 11A и Фигура 11C) или яванского макака (Фигура 11B). Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB. На Фигуре 11D продемонстрировано, что гуманизированные варианты hz4E01v16, hz4E01v18, hz4E01v21, hz4E01v22 и hz4E01v23 блокируют связывание 41BBL с 41BB на поверхности клетки. В этих исследованиях применяли рекомбинантный слитый белок 41BBL-mFc, содержащий область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00220] Слитые белки по данному изобретению, нацеленные на PDL1-41BB, также включают гуманизированную анти-PDL1 последовательность. В исследованиях, представленных в данном документе, слитые белки по данному изобретению, нацеленные на PDL1-41BB, включают гуманизированную последовательность анти-PDL1, такую как hz28A2v1 (SEQ ID NO: 120), hz28A2v2 (SEQ ID NO: 121), hz28A2v3 (SEQ ID NO: 122) и hz28A2v4-1 (SEQ ID NO: 123). На Фигуре 12 продемонстрировано связывание гуманизированных однодоменных антител, нацеленных на PDL1. Связывание оценивали с помощью проточной цитометрии на клетках СНО, экспрессирующих PDL1.
[00221] На Фигуре 13 приведено схематическое изображение двух типовых форматов биспецифического слитого белка PDL1х41BB по данному изобретению, упоминаемых в данном документе как INBRX-105-1. INBRX-105-1-A (слева) имеет PDL1- и 41BB-связывающие домены, расположенные в противоположных конечных положениях от центральной области Fc, тогда как INBRX-105-1-B (справа) имеет PDL1- и 41BB-связывающие домены, расположенные в тандеме, на N-конце относительно области Fc.
[00222] Эти два формата были дополнительно оценены на их способность связывать 41BB человека или яванского макака, блокировать взаимодействие между 41BB и 41BBL, связывать PDL1 и блокировать взаимодействие между PDL1 и PD1.
[00223] В частности, на Фигурах 14A, 14B и 14C продемонстрировано эквивалентное связывание с 41BB человека (Фигура 14A) или яванского макака (Фигура 14B) посредством двух различных форматов биспецифического слитого белка, нацеленных на PDL1 и 41BB, обозначенных в данном документе как INBRX-105-1-A и INBRX-105-1-B и проиллюстрированных на Фигуре 13. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB. В исследованиях, представленных в данном документе, hzRH3v5-1 (SEQ ID NO: 124) представляет собой 41BB-связывающий домен, применяемый в обоих форматах. Как проиллюстрировано на Фигуре 14С, биспецифический слитый белок, содержащий hzRh3v5-1, не блокирует связывание 41BBL с 41BB на поверхности клетки. В этих исследованиях применяли рекомбинантный слитый белок 41BBL и область Fc мыши, а связывание 41BBL обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши.
[00224] Более того, на Фигурах 15A, 15B, 15C и 15D продемонстрировано эквивалентное связывание (Фигура 15А и Фигура 15С) и блокирование PD1 (Фигура 15B и Фигура 15D) посредством двух различных форматов биспецифического слитого белка, нацеленных на PDL1 и 41BB, и обозначенных в данном документе как INBRX-105-1-A и INBRX-105-1-B. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle человека (Фигура 15A) или яванского макака (Фигура 15С), экспрессирующих PDL1. Блокирование оценивали с помощью проточной цитометрии на клетках 293freestyle человека (Фигура 15В) или яванского макака (Фигура 15D), экспрессирующих PDL1, либо с рекомбинантным слитым белком PD1-mFc человека (Фигура 15B), либо яванского макака (Фигура 15D). Связывание PD1 обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши. В исследованиях, представленных в данном документе, hz28A2v5 представляет собой PDL1-связывающий домен, применяемый в обоих форматах.
[00225] Биспецифические слитые белки PDL1х41BB были оценены на их способность индуцировать PDL1-зависимый агонизм 41BB. На Фигуре 16 продемонстрирована способность гуманизированных версий биспецифического слитого белка PDL1х41BB (INBRX-105-1) индуцировать PDL1-зависимый агонизм 41BB. В данном документе представлены два различных формата: INBRX-105-1-A и INBRX-105-1-B, имеющие PDL1- и 41BB-связывающие домены, расположенные на противоположных концах или в тандеме в слитом белке, соответственно. Примечательно, что INBRX-105-1-A по сравнению с INBRX-105-1-B демонстрирует эквивалентную PDL1-зависимую агонистическую активность. 41BB-экспрессирующую NFkB репортерную клеточную линию 293 применяли для оценки передачи сигналов 41BB, а в качестве источника PDL1 применяли PDL1-экспрессирующую линию клеток CHO. Эта репортерная линия клеток задействует NF-kB-индуцируемую секретируемую щелочную фосфатазу, для мониторинга передачи сигналов NF-kB.
[00226] Оценивали способность 41BB-специфического связывания и PDL1-специфического связывания посредством связывающих доменов в биспецифических слитых белках PDL1х41BB. На Фигурах 17A и 17B продемонстрировано 41BB-специфическое связывание посредством 41BB-связывающей части биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих 41BB (Фигура 17A) или ближайший гомолог, TNFRSF21/DR6 (Фигура 17B). Антитело анти-DR6 (Invitrogen) применяли в качестве положительного контроля экспрессии DR6. Кроме того, на Фигурах 18A, 18B и 18С продемонстрировано PDL1-специфическое связывание посредством PDL1-связывающей части биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению. Связывание оценивали с помощью проточной цитометрии на клетках 293freestyle, экспрессирующих PDL1 (Фигура 18A) или его ближайший гомолог PDL2 (Фигура 18B) или VISTA/PDL3 (Фигура 18C)Антитело анти-PDL2 и антитело анти-VISTA, известное как VSTB174, которое описано в публикации PCT №. WO 2015/097536, применяли в качестве положительных контролей экспрессии PDL2 и PDL3 соответственно.
[00227] Оценивали способность биспецифического слитого белка PDL1х41BB одновременно связывать PDL1 и 41BB. На Фигурах 19A и 19B продемонстрирована способность биспецифического слитого белка PDL1х41BB одновременно связывать PDL1 и 41BB. INBRX-105-1 титровали на клетках K562, экспрессирующих PDL1, и добавляли 25 нМ рекомбинантных белков 41BB-mFc. Связывание 41BB обнаруживали с применением специфического вторичного антитела против IgG-Fc мыши. На Фигуре 19A приведен график, демонстрирующий связывание INBRX-105-1 с клетками K562, экспрессирующими PDL1. На Фигуре 19В приведен график, демонстрирующий связывание рекомбинантного 41BB с INBRX-105-1 на клетках, экспрессирующих PDL1.
[00228] На Фигуре 20 продемонстрирована способность биспецифического слитого белка PDL1х41BB одновременно связывать рекомбинантный PDL1 и рекомбинантный 41BB в анализе ИФА. INBRX-105-1 титровали на иммобилизованный (планшет Medisorp) рекомбинантный PDL1, затем добавляли либо 2, либо 10μ г/мл биотинилированного рекомбинантного 41BB (His-меченого). Связанный рекомбинантный 41BB обнаруживали с применением стрептавидина-HRP.
[00229] Оценивали эффект биспецифических слитых белков PDL1х41BB на активацию и пролиферацию Т-клеток. На Фигурах 21A, 21B и 21С продемонстрирован эффект биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению на активацию и пролиферацию Т-клеток. В этом исследовании в течение 7 дней осуществляли аутологичное совместное культивирование in vitro с применением незрелого DC (iDC) и донорных соответствующих Т-клеток. PDL1+ iDC получали путем обогащения популяции моноцитов (Набор для обогащения моноцитов человека EasySep ™, STEMCELL Technologies Inc.) из человеческих донорских МКПК и их культивирования в 500 Ед/мл GM-CSF, и 250 Ед/мл IL-4, в течение 7 дней. Одновременно обогащали аутологичные Т-клетки (набор для обогащения Т-клеток человека EasySep™, STEMCELL Technologies Inc.) и криоконсервировали до завершения образования iDC. Обогащенные Т-клетки добавляли к iDC при приблизительном соотношении 20:1 (Т-клетка:iDC) и совместно культивировали в течение по меньшей мере 7 дней в присутствии IL-7. Биспецифический слитый белок PDL1х41BB, INBRX-105-1, превосходит моноспецифический слитый белок PDL1 sdAb-Fc (hz28A2v5-Fc), слитый белок sdAb-Fc 41BB (hzRH3v5-1-Fc), комбинацию hz28A2v5-Fc и hzRH3v5-1-Fc, антитело анти-PDL1 атезолизумаб, антитело анти-41BB, утомилумаб (PF-05082566, описанное в US8337850) или антитело анти-PD1 прембролизумаб и их комбинации при индуцировании INFγ (Фигура 21A) или опосредовании CD8+ пролиферации (Фигура 21В) и активации (Фигура 21С) Т-клеток. Продукцию INFγ в супернатанте клеток контролировали с помощью анализа ИФА и нормировали на стандартную кривую. Пролиферацию Т-клеток контролировали с помощью проточной цитометрии с применением CTV-мечения Т-клеток. Активацию Т-клеток оценивали по наличию активационного маркера CD25, контролируемого с помощью проточной цитометрии. Антитела применяли при концентрации 10 нМ. INBRX-105-1, по-видимому, повышает низкий уровень и/или активирует функцию активации/сигнализации Т-клеток, которая ослабляется при взаимодействии PDL1: PD1.
[00230] На Фигурах 22A и 22B продемонстрирован PDL1-зависимый агонизм 41BB, опосредованный биспецифическим слитым белком PDL1х41BB (INBRX-105-1) по данному изобретению. В этих исследованиях Т-клетки культивировали отдельно или с аутологичными незрелыми DC (iDC, PDL1-экспрессирующими), PDL1-экспрессирующей линией клеток K562 или родительской линией клеток K562 (PDL1-негативной) в присутствии или отсутствии 10 нМ INBRX-105-1 в течение 7 дней. Пролиферацию CD8+ Т-клеток (Фигура 22A) контролировали с применением CTV-мечения, а продукцию INFγ (Фигура 22B) в супернатанте клеток контролировали с помощью анализа ИФА и нормировали на стандартную кривую.
[00231] На Фигуре 23 продемонстрирована способность биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению усиливать фактор транскрипции, определяемый линией Th1, T-bet, экспрессируемый в популяциях Т-клеток. В этих исследованиях Т-клетки совместно культивировали с аутологичными незрелыми DC в присутствии или отсутствии INBRX-105-1 в течение 7 дней. Экспрессию T-bet оценивали на популяции CD4+ и CD8+ T-клеток с помощью проточной цитометрии путем внутриклеточного окрашивания после фиксации и пермеабилизации. INBRX-105-1 оказывал более сильный эффект на экспрессию T-bet в CD8+ T-клетках.
[00232] Биспецифические слитые белки PDL1х41BB по данному изобретению сравнивали с различными известными моноспецифическими антителами. На Фигурах 24A и 24B сопоставлена способность биспецифического слитого белка PDL1х41BB (INBRX-105-1) по данному изобретению и комбинации моноспецифических антител Атезолизумаб (анти-PDL1) и Утомилумаб (анти-41BB) индуцировать продукцию INFγ (Фигура 24A) или TNFα (Фигура 24B) из CD4+ или CD8+ T-клеток. В этих исследованиях Т-клетки совместно культивировали с аутологичными незрелыми DC в присутствии или отсутствии INBRX-105-1 в течение 7 дней, или комбинации моноспецифических антител. INBRX-105-1 характеризовался существенно большим эффектом при совместной стимуляции Т-клеток по сравнению с моноспецифическими антителами, нацеленными на одни и те же антигены. Экспрессию цитокинов оценивали на популяции CD4+ и CD8+ T-клеток с помощью проточной цитометрии путем внутриклеточного окрашивания после фиксации и пермеабилизации.
На Фигурах 25A и 25B продемонстрирована агонистическая способность тетравалентного 41BB-связывающего слитого белка и биспецифических слитых белков PDL1х41BB по данному изобретению в присутствии дополнительной PDL1-позитивной (Фигура 25A) или негативной (Фигура 25B) линии клеток. Примечательно, что только четырехвалентный 41BB- связывающий слитый белок был способен индуцировать передачу сигналов 41BB в отсутствие линии клеток, экспрессирующей PDL1. Биспецифические слитые белки PDL1х41BB (INBRX-105-1, INBRX-105-2 и INBRX-105-16) индуцировали передачу сигналов 41BB только при связывании с PDL1 на поверхности клетки, как проиллюстрировано на Фигуре 25A. Это демонстрирует, что двухвалентное взаимодействие 41BB, как и в случае с INBRX-105, является недостаточным для эффективной кластеризации и опосредования продуктивной передачи сигналов 41BB. Взаимодействие второго антигена поверхности клетки, PDL1, как в данном примере, обеспечивает дополнительную кластеризацию 41BB и продуктивную передачу сигналов. В этом исследовании применяли 41BB-экспрессирующую NFkB репортерную клетку HEK293 и совместно инкубировали либо с PDL1-негативной линией клеток K562 (Фигура 25B), либо со стабильно трансфицированной PDL1-экспрессирующей линией клеток K562 (Фигура 25A). INBRX-105-1 включает в себя 41BB-нацеленное sdAb: hzRH3v5-1, INBRX-105-2 включает в себя 41BB-нацеленное sdAb: hzRH3v5-2, а INBRX-105-16 включает в себя 41BB-нацеленное sdAb: hzRH3v5-16 и все включают в себя hz28A2v5 PDL1-нацеленное sdAb. Тетравалентный 41BB-нацеленный слитый белок, применяемый в данном изобретении, имеет следующий формат, содержащий hzRH3v5-1-Fc-hzRH3v5-1.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> INHIBRX LP
<120> МУЛЬТИВАЛЕНТНЫЕ И МУЛЬТИСПЕЦИФИЧЕСКИЕ 41BB-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ
<130> INHI-027001WO 322124-2114
<140> PCT/US2017/13040
<141> 2017-01-11
<150> US 62/277,028
<151> 2016-01-11
<160> 456
<170> PatentIn версия 3.5
<210> 1
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 1
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
35 40 45
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
50 55 60
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
65 70 75 80
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
85 90 95
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
100 105 110
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
115 120 125
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
130 135 140
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
145 150 155 160
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
165 170 175
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
180 185 190
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
195 200 205
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 2
<211> 215
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 2
Pro Ala Pro Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
1 5 10 15
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
20 25 30
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
35 40 45
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
50 55 60
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
65 70 75 80
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
85 90 95
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
100 105 110
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
115 120 125
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
130 135 140
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
145 150 155 160
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
165 170 175
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
180 185 190
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
195 200 205
Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 3
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 3
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
100 105 110
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
115 120 125
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
130 135 140
Ser Asp Ile Ser Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
145 150 155 160
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
165 170 175
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
180 185 190
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
195 200 205
Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 4
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 4
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp
35 40 45
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
50 55 60
Glu Gln Tyr Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu
65 70 75 80
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
85 90 95
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly
100 105 110
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
115 120 125
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
130 135 140
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu Asn
145 150 155 160
Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe
165 170 175
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
180 185 190
Ile Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr
195 200 205
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 5
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 5
Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
35 40 45
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
50 55 60
Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
65 70 75 80
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
85 90 95
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
100 105 110
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
115 120 125
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
130 135 140
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
145 150 155 160
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
165 170 175
Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
180 185 190
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
195 200 205
Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
210 215
<210> 6
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 6
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
35 40 45
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
50 55 60
Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
65 70 75 80
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
85 90 95
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
100 105 110
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
115 120 125
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
130 135 140
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
145 150 155 160
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
165 170 175
Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
180 185 190
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
195 200 205
Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
210 215
<210> 7
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 7
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys
1 5 10
<210> 8
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 8
Asp Lys Thr His Thr Cys Pro Pro Cys
1 5
<210> 9
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 9
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
1 5 10
<210> 10
<211> 6
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 10
Gly Gly Ser Gly Gly Ser
1 5
<210> 11
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 11
Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5
<210> 12
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 12
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5 10
<210> 13
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 13
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5 10 15
<210> 14
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 14
Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly
1 5 10
<210> 15
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 15
Gly Gln Gly Thr Leu Val Thr Val Glu Pro Gly Gly
1 5 10
<210> 16
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 16
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Asp
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Asp Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Gly Tyr Gly Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr
115 120
<210> 17
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 17
Gly Trp Ala Phe Asp Asn Tyr Gly
1 5
<210> 18
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 18
Leu Ala Trp Asn Gly Gly Ser Thr
1 5
<210> 19
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 19
Ala Arg Gln Arg Ser Tyr Ser Gly Tyr Gly Ile Arg Thr Pro Gln Thr
1 5 10 15
Tyr Asp Tyr
<210> 20
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 20
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Ala Gly Asp
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Arg Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Asn Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr
115 120
<210> 21
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 21
Gly Trp Ala Phe Gly Asn Tyr Gly
1 5
<210> 22
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 22
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
1 5 10 15
Tyr Asp Tyr
<210> 23
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 23
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Asp Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Gly Ile Arg Ala Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr
115 120
<210> 24
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 24
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Gly Ile Arg Ala Pro Gln Thr
1 5 10 15
Tyr Asp Tyr
<210> 25
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 25
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Leu
35 40 45
Ala Ala Ile Asp Ser Gly Arg Asn Thr Val Tyr Ala Val Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Gln Val Thr
115
<210> 26
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 26
Gly Phe Ser Phe Ser Ile Asn Ala
1 5
<210> 27
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 27
Ile Asp Ser Gly Arg Asn Thr
1 5
<210> 28
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 28
Gly Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr
1 5 10 15
<210> 29
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 29
Glu Val Gln Pro Val Gln Ser Gly Gly Gly Leu Val Gln Ala Gly Glu
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Ala Thr Ile Phe Ser Asn Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Thr Gly Gly Phe Thr Asn Tyr Arg Asp Ser Val Lys
50 55 60
Gly Arg Phe Asp Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Val Leu Arg Tyr Ser Arg Asp Tyr Ser Tyr Thr Thr Val Lys Glu
100 105 110
Tyr Trp Gly Gln Gly Thr Gln Val
115 120
<210> 30
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 30
Ala Thr Ile Phe Ser Asn Asn Ala
1 5
<210> 31
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 31
Ile Thr Thr Gly Gly Phe Thr
1 5
<210> 32
<211> 18
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 32
Asn Val Val Leu Arg Tyr Ser Arg Asp Tyr Ser Tyr Thr Thr Val Lys
1 5 10 15
Glu Tyr
<210> 33
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 33
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 34
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 34
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Gly Arg Glu Phe Val
35 40 45
Ala Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Ala Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 35
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 35
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Ala Glu Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu
65 70 75 80
Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln
100 105 110
Thr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys
115 120 125
<210> 36
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 36
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 37
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 37
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 38
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 38
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 39
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 39
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 40
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 40
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 41
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 41
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Gln Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 42
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 42
Leu Ala Trp Gln Gly Gly Ser Thr
1 5
<210> 43
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 43
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Ile
35 40 45
Gly Arg Leu Ala Trp Asn Ala Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Pro Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 44
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 44
Leu Ala Trp Asn Ala Gly Ser Thr
1 5
<210> 45
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 45
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gln Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 46
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 46
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Asn Ala Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 47
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 47
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 48
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 48
Leu Ala Trp Gly Gly Gly Ser Thr
1 5
<210> 49
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 49
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Ser Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 50
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 50
Gly Trp Ala Phe Ser Asn Tyr Gly
1 5
<210> 51
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 51
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Ser Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 52
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 52
Leu Ala Trp Ser Gly Gly Ser Thr
1 5
<210> 53
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 53
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Ser Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Ser Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 54
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 54
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Gly Tyr Asp Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 55
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 55
Ala Arg Gln Arg Ser Tyr Ser Gly Tyr Asp Ile Arg Thr Pro Gln Thr
1 5 10 15
Tyr Asp Tyr
<210> 56
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 56
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Gly Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 57
<211> 19
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 57
Ala Arg Gln Arg Ser Tyr Ser Arg Tyr Gly Ile Arg Thr Pro Gln Thr
1 5 10 15
Tyr Asp Tyr
<210> 58
<211> 126
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 58
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr
20 25 30
Gly Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ser Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Arg Ser Tyr Ser Gly Tyr Gly Ile Arg Thr Pro Gln Thr
100 105 110
Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
115 120 125
<210> 59
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 59
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Asp Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 60
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 60
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 61
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 61
Ile Glu Ser Gly Arg Asn Thr
1 5
<210> 62
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 62
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Tyr Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 63
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 63
Ile Tyr Ser Gly Arg Asn Thr
1 5
<210> 64
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 64
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 65
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 65
Gly Phe Thr Phe Ser Ile Asn Ala
1 5
<210> 66
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 66
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 67
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 67
Gly Phe Ser Phe Ser Ile Asn Ala
1 5
<210> 68
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 68
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 69
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 69
Gly Phe Thr Phe Ser Ser Asn Ala
1 5
<210> 70
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 70
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Ser Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 71
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 71
Ile Glu Ser Ser Arg Asn Thr
1 5
<210> 72
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 72
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Ser Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 73
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 73
Ile Glu Ser Gly Ser Asn Thr
1 5
<210> 74
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 74
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Ser Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 75
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 75
Ile Glu Ser Gly Arg Ser Thr
1 5
<210> 76
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 76
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Tyr Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 77
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 77
Ile Glu Ser Gly Arg Asn Thr
1 5
<210> 78
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 78
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Tyr Ser Gly Ser Ser Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 79
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 79
Ile Tyr Ser Gly Ser Ser Thr
1 5
<210> 80
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 80
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 81
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 81
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Val Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 82
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 82
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Gly Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 83
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 83
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Leu
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro
115 120
<210> 84
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 84
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asn Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Gly Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Asn Glu Glu Asp Gly Gly Phe Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 85
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 85
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Ser Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Tyr Ala Gln Phe Glu Gly Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 86
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 86
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Tyr
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Lys Ile Tyr Pro Gly Asp Ser Tyr Thr Asn Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Tyr Gly Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 87
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 87
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ser Thr Tyr
20 25 30
Trp Ile Ser Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Lys Ile Tyr Pro Gly Asp Ser Tyr Thr Asn Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Tyr Gly Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 88
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 88
Asp Ile Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Ser Cys Ser Gly Asp Asn Leu Gly Asp Tyr Tyr Ala
20 25 30
Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Asp Asp Ser Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Asp Gly Thr Leu His Phe
85 90 95
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 89
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 89
Asp Ile Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Ser Cys Ser Gly Asp Asn Ile Gly Ser Lys Tyr Val
20 25 30
Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Ser Asp Ser Glu Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Trp Asp Gly Ser Ile Ser Arg
85 90 95
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 90
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 90
Asp Ile Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Ser Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Val Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Tyr Thr Gly Phe Gly Ser Leu
85 90 95
Ala Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 91
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 91
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Tyr Thr Gly Phe Gly Ser Leu
85 90 95
Ala Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 92
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 92
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Val Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Tyr Thr Gly Phe Gly Ser Leu
85 90 95
Ala Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 93
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 93
Asp Ile Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Ser Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Val Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ser Thr Tyr Thr Phe Val Gly Phe Thr
85 90 95
Thr Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 94
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 94
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ser Thr Tyr Thr Phe Val Gly Phe Thr
85 90 95
Thr Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 95
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 95
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Ile Gly Asp Gln Tyr Ala
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Val Val Ile Tyr
35 40 45
Gln Asp Lys Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ser Thr Tyr Thr Phe Val Gly Phe Thr
85 90 95
Thr Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 96
<211> 448
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 96
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Glu Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Gly Gly Tyr Val Thr Tyr Asn Pro Ser Leu Glu
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Tyr Gly Pro Gly Asn Tyr Asp Trp Tyr Phe Asp Leu Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
210 215 220
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 97
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 97
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Glu Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Gly Gly Tyr Val Thr Tyr Asn Pro Ser Leu Glu
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Tyr Gly Pro Gly Asn Tyr Asp Trp Tyr Phe Asp Leu Trp Gly
100 105 110
Arg Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 98
<211> 216
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 98
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Ala Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys
115 120 125
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
130 135 140
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
145 150 155 160
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
165 170 175
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
180 185 190
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
195 200 205
Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 99
<211> 178
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 99
Gln Asp Ser Thr Ser Asp Leu Ile Pro Ala Pro Pro Leu Ser Lys Val
1 5 10 15
Pro Leu Gln Gln Asn Phe Gln Asp Asn Gln Phe His Gly Lys Trp Tyr
20 25 30
Val Val Gly Gln Ala Gly Asn Ile Arg Leu Arg Glu Asp Lys Asp Pro
35 40 45
Ile Lys Met Met Ala Thr Ile Tyr Glu Leu Lys Glu Asp Lys Ser Tyr
50 55 60
Asp Val Thr Met Val Lys Phe Asp Asp Lys Lys Cys Met Tyr Asp Ile
65 70 75 80
Trp Thr Phe Val Pro Gly Ser Gln Pro Gly Glu Phe Thr Leu Gly Lys
85 90 95
Ile Lys Ser Phe Pro Gly His Thr Ser Ser Leu Val Arg Val Val Ser
100 105 110
Thr Asn Tyr Asn Gln His Ala Met Val Phe Phe Lys Phe Val Phe Gln
115 120 125
Asn Arg Glu Glu Phe Tyr Ile Thr Leu Tyr Gly Arg Thr Lys Glu Leu
130 135 140
Thr Ser Glu Leu Lys Glu Asn Phe Ile Arg Phe Ser Lys Ser Leu Gly
145 150 155 160
Leu Pro Glu Asn His Ile Val Phe Pro Val Pro Ile Asp Gln Cys Ile
165 170 175
Asp Gly
<210> 100
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 100
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Thr Thr Ser Gly Gly Ile Phe Asn Ile Arg
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Met Gln Arg Glu Trp Val
35 40 45
Ala Thr Ile Ala Phe Gly Gly Ala Thr Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Ala Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Ala Phe Glu Ile Trp Gly Gln Gly Thr Gln Val Thr Val
100 105
<210> 101
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 101
Gly Gly Ile Phe Asn Ile Arg Pro
1 5
<210> 102
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 102
Ile Ala Phe Gly Gly Ala Thr
1 5
<210> 103
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 103
Asn Ala Phe Glu Ile
1 5
<210> 104
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 104
Gln Leu Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Arg Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Thr Thr Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Gln Glu Arg Glu Trp Val
35 40 45
Thr Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Val Ala Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asp Leu Lys Leu Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Gln Val Thr Val
100 105
<210> 105
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 105
Gly Gly Ile Phe Ala Ile Lys Pro
1 5
<210> 106
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 106
Thr Thr Ser Ser Gly Ala Thr
1 5
<210> 107
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 107
Asn Val Phe Glu Tyr
1 5
<210> 108
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 108
Gln Val Gln Leu Gln Glu Ser Gly Gly Asp Leu Val Gln Ala Gly Ser
1 5 10 15
Ser Leu Arg Leu Ala Cys Ala Thr Ser Gly Gly Val Phe Asn Ile Arg
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ala Thr Ile Ala Ser Gly Gly Ala Thr Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Ala Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Ala Phe Glu Val Trp Gly Gln Gly Thr Gln Val Thr Val
100 105
<210> 109
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 109
Gly Gly Val Phe Asn Ile Arg Pro
1 5
<210> 110
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 110
Ile Ala Ser Gly Gly Ala Thr
1 5
<210> 111
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 111
Asn Ala Phe Glu Val
1 5
<210> 112
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 112
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Thr Thr Ser Gly Gly Ile Phe Asn Ile Arg
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Met Gln Arg Glu Trp Val
35 40 45
Ala Thr Ile Ala Ser Gly Gly Ala Thr Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Ala Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Thr Leu Asn Phe Trp Gly Arg Gly Thr Gln Val Thr Val
100 105
<210> 113
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 113
Asn Thr Leu Asn Phe
1 5
<210> 114
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 114
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Thr Thr Ser Gly Gly Ile Phe Asn Ile Arg
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Met Gln Arg Glu Trp Val
35 40 45
Ala Thr Ile Ala Ser Gly Gly Ala Thr Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Ala Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Ile Trp Gly Gln Gly Thr Gln Val Thr Val
100 105
<210> 115
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 115
Asn Val Phe Glu Ile
1 5
<210> 116
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 116
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Ile Thr Ser Gly Gly Ile Phe Asn Ile Arg
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Pro Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ala Thr Ile Ala Ser Gly Gly Ala Ala Asn Tyr Ala Asn Ser Ile Lys
50 55 60
Gly Arg Phe Thr Ala Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Ala Phe Glu Asn Trp Gly Gln Gly Thr Gln Val Thr Val
100 105
<210> 117
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 117
Ile Ala Ser Gly Gly Ala Ala
1 5
<210> 118
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 118
Asn Ala Phe Glu Asn
1 5
<210> 119
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 119
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 120
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 120
Glu Val Gln Leu Gln Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 121
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 121
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 122
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 122
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 123
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 123
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Thr Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 124
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 124
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
100 105 110
<210> 125
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 125
Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala
1 5 10 15
Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn
20 25 30
Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe
35 40 45
Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr
50 55 60
Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg
65 70 75 80
Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro
85 90 95
Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr
100 105 110
<210> 126
<211> 117
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 126
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Thr Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Phe Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 127
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 127
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Asp Thr Phe Ser Thr Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Phe His Phe Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 128
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 128
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asp Val His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Leu His Ala Asp Thr Gly Ile Thr Lys Phe Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Ile Gln Leu Trp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
<210> 129
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 129
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Gly Ile Phe Ser Thr Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn His Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Gly Ile Ala Ala Ala Leu Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 130
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 130
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Val Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Asn Ser Gly Asn Ile Gly Tyr Ala Asp Ser Val Lys Gly Arg
50 55 60
Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met
65 70 75 80
Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys Ala Val Pro
85 90 95
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
100 105 110
<210> 131
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 131
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Asp Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Arg Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Phe His Phe Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 132
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 132
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Tyr Asp Tyr Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 133
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 133
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Ser Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Ala Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Ser Gly Trp Ser Arg Tyr Tyr Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 134
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 134
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Glu Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asn Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Leu Phe Gly Ile Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Tyr Ser Tyr Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 135
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 135
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Asp Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Arg Gly Arg Ile Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Gly Arg Phe Arg Tyr Phe Asp Trp Phe Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 136
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 136
Gln Met Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Phe Trp Ser Gly Phe Ser Ala Phe Asp Ile Trp Gly
100 105 110
Lys Gly Thr Leu Val Thr Val Ser
115 120
<210> 137
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 137
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Val Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 138
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 138
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 139
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 139
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 140
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 140
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 141
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 141
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 142
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 142
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Thr
85 90 95
Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 143
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 143
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Asn Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 144
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 144
Asp Ile Val Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 145
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 145
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly Trp Phe Gly Glu Leu Ala Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 146
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 146
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Leu Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 147
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 147
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 148
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 148
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Leu Pro Tyr Gly Gly Ser Ser Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 149
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 149
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 150
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 150
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Val Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 151
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 151
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ala Pro Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 152
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 152
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Val Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 153
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 153
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Val Ile Asn Thr Phe
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Val Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 154
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 154
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Gly Val Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 155
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 155
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Phe Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 156
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 156
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Phe Ile Thr Pro Thr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 157
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 157
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 158
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 158
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Phe Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 159
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 159
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Leu Phe Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 160
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Leu Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 161
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 161
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Trp Tyr His Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 162
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 162
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Phe Tyr Ile Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 163
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 163
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Tyr Thr Pro Thr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 164
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 164
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Phe Ile Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 165
<211> 141
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 165
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly
1 5 10 15
Val Gln Cys Leu Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro
20 25 30
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Thr Ile Thr
35 40 45
Asn Tyr His Met Phe Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
50 55 60
Trp Ile Gly Val Ile Thr Ser Ser Gly Ile Gly Ser Ser Ser Thr Thr
65 70 75 80
Tyr Tyr Ala Thr Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser
85 90 95
Thr Thr Val Asn Leu Arg Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala
100 105 110
Thr Tyr Phe Cys Ala Arg Asp Tyr Phe Thr Asn Thr Tyr Tyr Ala Leu
115 120 125
Asp Ile Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser
130 135 140
<210> 166
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 166
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Asp Thr Phe Ser Thr Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Phe His Phe Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 167
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 167
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asp Val His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Leu His Ala Asp Thr Gly Ile Thr Lys Phe Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Ile Gln Leu Trp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 168
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 168
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Gly Ile Phe Ser Thr Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn His Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Gly Ile Ala Ala Ala Leu Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 169
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 169
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Val Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Asn Ser Gly Asn Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Val Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser
<210> 170
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Asp Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Arg Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Phe His Phe Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 171
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 171
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Tyr Asp Tyr Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 172
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Ser Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Ala Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Ser Gly Trp Ser Arg Tyr Tyr Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 173
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 173
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Glu Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asn Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Leu Phe Gly Ile Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Tyr Ser Tyr Val Ser Gly Ser Pro Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 174
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 174
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Asp Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Arg Gly Arg Ile Glu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Gly Arg Phe Arg Tyr Phe Asp Trp Phe Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 175
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 175
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Pro Gly Ala Arg Cys Ala Leu Val Met Thr Gln Thr Pro Ser Ser
20 25 30
Thr Ser Thr Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser
35 40 45
Gln Ser Ile Ser Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
50 55 60
Pro Pro Lys Leu Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val
65 70 75 80
Pro Ser Arg Phe Lys Gly Ser Arg Ser Gly Thr Glu Tyr Thr Leu Thr
85 90 95
Ile Ser Gly Val Gln Arg Glu Asp Ala Ala Thr Tyr Tyr Cys Leu Gly
100 105 110
Ser Ala Gly Ser
115
<210> 176
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 176
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Val Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 177
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 177
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 178
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 178
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 179
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 179
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 180
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 180
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 181
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 181
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Thr
85 90 95
Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 182
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 182
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Asn Ser Tyr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 183
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 183
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ile Met Met Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Pro Ser Gly Gly Ile Thr Phe Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ile Lys Leu Gly Thr Val Thr Thr Val Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 184
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 184
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 185
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 185
Glu Val Lys Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Asp
20 25 30
Tyr Trp Asn Trp Ile Arg Lys Phe Pro Gly Asn Lys Leu Glu Tyr Val
35 40 45
Gly Tyr Ile Ser Tyr Thr Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Tyr Tyr Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Ser Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Tyr Gly Gly Trp Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 186
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 186
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Ser Ile Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Ala Gly Gly Gly Thr Asn Ser Asn Ser Val Leu Lys
50 55 60
Ser Arg Leu Ile Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Tyr Cys Ala
85 90 95
Arg Tyr Tyr Gly Asn Ser Pro Tyr Tyr Ala Ile Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 187
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 187
Glu Val Lys Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Ile Ser Asp
20 25 30
Tyr Trp Asn Trp Ile Arg Lys Phe Pro Gly Asn Lys Leu Glu Tyr Leu
35 40 45
Gly Tyr Ile Ser Tyr Thr Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Tyr Tyr Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Arg Gly Gly Trp Leu Leu Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 188
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 188
Glu Val Lys Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asp Ile Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Trp Ile Phe Pro Arg Asp Asn Asn Thr Lys Tyr Asn Glu Asn Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu His Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Thr Lys Glu Asn Trp Val Gly Asp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Leu Ser Ser
115
<210> 189
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 189
Glu Val Gln Leu Gln Gln Ser Gly Pro Asp Leu Val Thr Pro Gly Ala
1 5 10 15
Ser Val Arg Ile Ser Cys Gln Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Ile Leu Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Ser Leu Thr Val
100 105 110
Ser Ser
<210> 190
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 190
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Gln Ser Pro Arg Pro Leu Ile Tyr
35 40 45
Ala Ala Phe Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 191
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 191
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Met Val Thr Val
100 105 110
Ser Ser
<210> 192
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 192
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Ser Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Met Val Thr Val
100 105 110
Ser Ser
<210> 193
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 193
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Ser Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Val Asp Arg Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Met Val Thr Val
100 105 110
Ser Ser
<210> 194
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 194
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Thr Tyr Ala Ala Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Val Asp Arg Ser Lys Ser Ile Ala Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Met Val Thr Val
100 105 110
Ser Ser
<210> 195
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 195
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Tyr Thr Phe Pro Asp Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Asp Ile Asp Pro Asn Tyr Gly Gly Thr Thr Tyr Asn Ala Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Val Asp Arg Ser Lys Ser Ile Ala Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Leu Thr Asp Trp Gly Gln Gly Thr Met Val Thr Val
100 105 110
Ser Ser
<210> 196
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 196
Asp Ile Val Met Thr Gln Ser His Lys Leu Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Asp Tyr Phe Cys Gln Gln Asp Ser Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Val Glu Leu Lys
100 105
<210> 197
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 197
Asp Ile Val Thr Thr Gln Ser His Lys Leu Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg His Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Asp Tyr Phe Cys Gln Gln Asp Ser Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Val Glu Leu Lys
100 105
<210> 198
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 198
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Glu Lys Val Ser Met Gly Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Asp Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys
<210> 199
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 199
Asp Ile Val Met Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Ile Arg Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Thr Ser Pro Lys Arg Trp Ile Ser
35 40 45
Asp Thr Ser Lys Leu Thr Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ala Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys His Gln Arg Ser Ser Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 200
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 200
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Thr Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 201
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 201
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Ala Ala Phe Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 202
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 202
Gln Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Gln Ser Pro Arg Pro Leu Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 203
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 203
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Gly Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Ala Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 204
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 204
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Gly Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 205
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 205
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile
20 25 30
Tyr Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Asn Asn Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 206
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Leu Pro Ser Gly Thr Ile Leu Val Gly Gly Trp Phe Asp
100 105 110
Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 207
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 207
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Leu Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Gly Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Val Phe Pro Glu Thr Phe Ser Met Asn Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 208
<211> 128
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 208
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Asp Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Val Leu Leu Pro Cys Ser Ser Thr Ser Cys Tyr Gly Ser Val
100 105 110
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 209
<211> 117
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Gly Ser Val Val Arg Pro Gly Glu
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Ile Phe Asp Asn Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Val Asn Trp Asn Gly Gly Ser Thr Thr Tyr Ala Asp Ala Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Thr Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Asn Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Glu Phe Val Gly Ala Tyr Asp Leu Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 210
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 210
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Val Ser Cys Lys Val Phe Gly Asp Thr Phe Arg Gly Leu
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Thr Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Leu Arg Trp Gly Ile Trp Gly Trp Phe Asp Pro Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 211
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 211
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Leu Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Phe Gly Gly Thr Phe Ser Asp Asn
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Pro Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Lys Pro Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Val Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Met Val Arg Gly Phe Leu Gly Val Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 212
<211> 125
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 212
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gln Phe Val Thr Ile Phe Gly Val Pro Arg Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 213
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 213
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Arg Gln Met Phe Gly Ala Gly Ile Asp Phe Trp Gly Pro
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 214
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 214
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Gly Thr Phe Gly Thr Tyr
20 25 30
Ala Leu Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Val Pro Leu Ile Gly Leu Val Asn Tyr Ala His Asn Phe
50 55 60
Glu Gly Arg Ile Ser Ile Thr Ala Asp Lys Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Asn Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Val Tyr Gly Gly Asn Ser Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 215
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 215
Gln Val Gln Leu Val Gln Ser Gly Gly Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Leu Ser Ser His
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala His Asn Gly His Ala Ser Asn Ala Gln Lys Val
50 55 60
Glu Asp Arg Val Thr Met Thr Thr Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val His Ala Ala Leu Tyr Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 216
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 216
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Arg His
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser His Asp Gly Ser Val Lys Tyr Tyr Ala Asp Ser Met
50 55 60
Lys Gly Arg Phe Ser Ile Ser Arg Asp Asn Ser Asn Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Leu Ser Tyr Gln Val Ser Gly Trp Phe Asp Pro Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 217
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 217
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser Ile Ala Ser Asn
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ser Pro Thr Thr Val
35 40 45
Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Thr Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly
65 70 75 80
Leu Lys Thr Lys Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Gly
85 90 95
Ile Thr Val Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 218
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 218
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Gly Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Leu Pro Cys Thr Arg Ser Ser Gly Ser Ile Ala Ser His
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Thr Val
35 40 45
Ile Tyr Glu Asp Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Ser Ile Ser Gly
65 70 75 80
Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser
85 90 95
Ser Asn Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 219
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 219
Leu Pro Val Leu Thr Gln Pro Ala Ser Leu Ser Ala Ser Pro Gly Ala
1 5 10 15
Ser Ala Ser Leu Thr Cys Thr Leu Arg Ser Gly Leu Asn Val Gly Ser
20 25 30
Tyr Arg Ile Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Arg Pro Gln Tyr
35 40 45
Leu Leu Asn Tyr Lys Ser Asp Ser Asn Lys Gln Gln Ala Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Lys Asp Ala Ser Ala Asn Ala Gly Ile
65 70 75 80
Leu Leu Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys
85 90 95
Met Ile Trp Tyr Ser Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu
100 105 110
Thr Val Leu
115
<210> 220
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 220
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Asn Ile Ala Ser Asn
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Thr Val
35 40 45
Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly
65 70 75 80
Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser
85 90 95
Ser Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 221
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 221
Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala
20 25 30
Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Lys Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser
50 55 60
Ser Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly Asn His
85 90 95
Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105
<210> 222
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 222
Leu Pro Val Leu Thr Gln Ala Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Ser Asp Ile Gly Arg Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Ala Leu Val Ile Tyr
35 40 45
Ser Asp Arg Asp Arg Pro Ser Gly Ile Ser Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Asn Asn Ser Asp His
85 90 95
Tyr Val Phe Gly Ala Gly Thr Glu Leu Ile Val Leu
100 105
<210> 223
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 223
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Thr Leu Pro Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 224
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 224
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Gly Asn Ser
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Met
35 40 45
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ala Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Thr Ile Pro Thr Phe
85 90 95
Ser Phe Gly Pro Gly Thr Lys Val Glu Val Lys
100 105
<210> 225
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 225
Asp Ile Val Met Thr Gln Thr Pro Ser Phe Leu Ser Ala Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Gly Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Arg Pro Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn Asn Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 226
<211> 105
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 226
Gln Ser Ala Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Asn Ile Pro Cys Ser Gly Asp Lys Leu Gly Asn Lys Tyr Ala
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Leu Leu Ile Tyr
35 40 45
Gln Asp Ile Lys Arg Pro Ser Arg Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Ala Asp Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Asp Asn Ser Val Val Phe
85 90 95
Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 227
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 227
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser Ile Asp Ser Asn
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Thr Val
35 40 45
Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly
65 70 75 80
Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser
85 90 95
Asn Asn Arg His Val Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 228
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 228
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Asn Ile Gly Thr Asn
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Val Ala Leu
35 40 45
Ile Tyr Glu Asp Tyr Arg Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Ile Ile Ser Gly
65 70 75 80
Leu Lys Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr His Ser
85 90 95
Ser Gly Trp Glu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 229
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 229
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Gly Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Val Tyr
35 40 45
Asp Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 230
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 230
Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser Ile Ala Ser Asn
20 25 30
Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Thr Val
35 40 45
Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly
65 70 75 80
Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser
85 90 95
Thr Thr Pro Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 231
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 231
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Thr Ser Pro His Asn Gly Leu Thr Ala Phe Ala Gln Ile Leu
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Asn Leu Thr Phe Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Lys Val His Pro Val Phe Ser Tyr Ala Leu Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 232
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 232
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Met Asn Pro Gly Ser
1 5 10 15
Ser Val Arg Val Ser Cys Arg Gly Ser Gly Gly Asp Phe Ser Thr Tyr
20 25 30
Ala Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Tyr Gly Ser Asp Pro Val Leu Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 233
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 233
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Val
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Gly Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Phe Arg Lys Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 234
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 234
Glu Val Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Val Asn Pro Phe Asn Asp Gly Thr Lys Tyr Asn Glu Met Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ala Trp Gly Tyr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 235
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 235
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Val Asn Pro Phe Asn Asp Gly Thr Lys Tyr Asn Glu Met Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ala Trp Gly Tyr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 236
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 236
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Val Asn Pro Phe Asn Asp Gly Thr Lys Tyr Asn Glu Met Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ala Trp Gly Tyr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 237
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 237
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Val Asn Pro Phe Asn Asp Gly Thr Lys Tyr Asn Glu Met Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ala Trp Gly Tyr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 238
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 238
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Val Asn Pro Phe Asn Asp Gly Thr Lys Tyr Asn Glu Met Phe
50 55 60
Lys Gly Arg Ala Thr Ile Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ala Trp Gly Tyr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 239
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 239
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Val Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Val Asp Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Ser Leu Glu Glu Glu Asp Ala Ala Met Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Arg Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 240
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 240
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Val Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Val Asp Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Ser Leu Glu Ala Glu Asp Ala Ala Met Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Arg Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 241
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 241
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Val Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Val Asp Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Ser Leu Glu Ala Glu Asp Ala Ala Met Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Arg Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 242
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 242
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Glu Ser Val Glu Tyr Tyr
20 25 30
Gly Thr Ser Leu Val Gln Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Val Asp Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Ser Arg
85 90 95
Arg Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 243
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 243
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Thr Ile Tyr Asp Ser Ser Gly Tyr Ser Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 244
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 244
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Ser Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Phe Pro His Ile Tyr Gly Asn Tyr Tyr Gly Met Asp
100 105 110
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 245
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 245
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Ala Val Pro Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 246
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 246
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Ala Val Ile
35 40 45
Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly Arg
50 55 60
Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met
65 70 75 80
Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly
85 90 95
Gln Trp Leu Val Thr Glu Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 247
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 247
Glu Val Gln Leu Val Glu Ser Gly Ser Glu Val Glu Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Asp Ser
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Met Phe Ala Thr Pro Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Thr Ala Val Phe Tyr Cys
85 90 95
Ala Arg Asp Arg Gly Arg Gly His Leu Pro Trp Tyr Phe Asp Leu Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 248
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 248
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Pro Tyr Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 249
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 249
Glu Val Gln Leu Leu Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Leu Ser Arg Tyr
20 25 30
Ala Leu Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Pro Glu Trp Val
35 40 45
Gly Ala Ile Ile Pro Ile Phe Gly Thr Pro His Tyr Ser Lys Lys Phe
50 55 60
Gln Asp Arg Val Ile Ile Thr Val Asp Thr Ser Thr Asn Thr Ala Phe
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Phe Glu Asp Thr Ala Leu Tyr Phe Cys
85 90 95
Ala Arg Gly His Asp Glu Tyr Asp Ile Ser Gly Tyr His Arg Leu Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 250
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 250
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Ser Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Asn Ser Gly Val Thr Asn Tyr Val Arg Arg Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Leu Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Thr Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Asn Leu Trp Gln Phe Gly Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 251
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 251
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Leu Ile Pro Ile Val Ser Met Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Ser Ile Thr Thr Asp Lys Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Ser Val Gly Gln Gln Leu Pro Trp Val Phe Phe Ala Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 252
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 252
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 253
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 253
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 254
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 254
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Tyr Lys Ile His Ala Asp Ser Val
50 55 60
Gln Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Asp Arg Lys Trp Leu Ala Trp His Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 255
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 255
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ile Val Ala Asp Phe Gln His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 256
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 256
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Asp Thr Phe Ser Arg Tyr
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Val Pro Phe Phe Gly Ala Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Leu Thr Ile Thr Ala Asp Lys Ser Ser Tyr Thr Ser Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Phe Tyr Gly Ser Gly Gly Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 257
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 257
Glu Val Gln Leu Leu Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ser Tyr
20 25 30
Asp Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Phe Gly Thr Ala Asn Tyr Ala Glu Ser Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Ala Asp His Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Asn Asn Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Trp His Tyr Glu Ser Arg Pro Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 258
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 258
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ala Cys Ala Ala Ser Gly Phe Ser Phe Ser Asp Tyr
20 25 30
Tyr Met Thr Trp Ile Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Ser Asp Ser Gly Gln Thr Val His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Thr Lys Asn Ser Leu Phe
65 70 75 80
Leu Gln Val Asn Thr Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Asp Leu Leu Gly Tyr Tyr Leu Gln Ser Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 259
<211> 131
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 259
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Asp Glu Pro Arg Ala Val Ala Gly Ser Gln Ala
100 105 110
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
115 120 125
Val Ser Ser
130
<210> 260
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 260
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Asp Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val His
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Phe Pro His Ile Tyr Gly Asn Tyr Tyr Gly Met Asp
100 105 110
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 261
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 261
Gln Met Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 262
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 262
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 263
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 263
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Asn Asn Ser Asn Ile Ala Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Tyr Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Asp Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Val Trp Asp Gly Ser Leu
85 90 95
Thr Thr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 264
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 264
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Leu Ala Thr Tyr Tyr Cys Gln Gln Leu His Thr Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 265
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 265
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ala Tyr
20 25 30
Asn Phe Val Ser Trp Tyr Arg Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Val Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Ala Gly Thr
85 90 95
Asn Ser Leu Gly Ile Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 266
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 266
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asp Ile Gly Asn His
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Gln Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Ala Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Asn Ser Leu
85 90 95
Ser Pro His Leu Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 267
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 267
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Met Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Lys Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Glu Asn Asp Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Asn Ser Leu
85 90 95
Ser Gly Phe Val Phe Ala Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 268
<211> 109
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 268
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Leu Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Leu Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Asn Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Ser Gly Val Ser Asn Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu Gln
65 70 75 80
Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Gly Ile Ser
85 90 95
Thr Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 269
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 269
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Leu Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Gly Gly Phe
85 90 95
Asn Asn Leu Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 270
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 270
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Arg Ile Ser Ala Tyr
20 25 30
Val Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Arg Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Thr Tyr Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 271
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 271
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Ile Gly Gly Tyr
20 25 30
Asp Ser Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ile Phe Phe Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 272
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 272
Leu Pro Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Thr Ser Asp Ile Gly Gly Tyr
20 25 30
Asp Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr His Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 273
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 273
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Arg Ser Ser
85 90 95
Thr Leu Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 274
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 274
Gln Ala Gly Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Tyr Asp Asp Leu Leu Pro Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 275
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 275
Gln Ser Ala Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Thr Thr His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 276
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 276
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Val Trp Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 277
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 277
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Arg Ala Pro Arg Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Gly
85 90 95
Gly Thr Leu Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 278
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 278
Gln Ala Gly Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 279
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 279
Ala Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Arg Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Thr Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 280
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 280
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Arg Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Tyr Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Asp Ser
85 90 95
Ser Thr Arg Tyr Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 281
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 281
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Ala Ile Ser Cys Ser Gly Ser Arg Ser Asn Ile Glu Ile Asn
20 25 30
Ser Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Ser Trp Asp Ser Ser Leu
85 90 95
Ser Ala Asp Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 282
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 282
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Lys
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 283
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 283
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Asn Asn Arg His Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Glu Phe Phe Cys Gly Thr Trp Asp Ser Arg
85 90 95
Leu Thr Thr Tyr Val Phe Gly Ser Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 284
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 284
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 285
<211> 103
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 285
Val Ile Trp Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ala Ala Ser Ser Leu Gln Ser Trp Tyr
20 25 30
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Glu Ala Ser
35 40 45
Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
50 55 60
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
65 70 75 80
Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln
85 90 95
Gly Thr Lys Leu Glu Ile Lys
100
<210> 286
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 286
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Asn Ser Asp Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 287
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 287
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Gly Ser Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 288
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 288
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Leu Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 289
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 289
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 290
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 290
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 291
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 291
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 292
<211> 447
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 292
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 293
<211> 440
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 293
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
115 120 125
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
180 185 190
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
210 215 220
Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
225 230 235 240
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
245 250 255
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
260 265 270
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
275 280 285
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
290 295 300
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
305 310 315 320
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
325 330 335
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr
340 345 350
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
355 360 365
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
370 375 380
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
385 390 395 400
Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
405 410 415
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
420 425 430
Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 294
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 294
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 295
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 295
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 296
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 296
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120
<210> 297
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 297
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 298
<211> 447
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 298
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 299
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 299
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 300
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 300
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 301
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 301
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Asn Gln Asp Gly Thr Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Asn Thr Tyr Tyr Asp Phe Trp Ser Gly His Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 302
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 302
Gln Glu His Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Leu Trp Ser Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Val Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Arg Gly Ala Pro Gly Ile Pro Ile Phe Gly Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 303
<211> 130
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 303
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Arg Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu His Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Asp Asp Ile Val Val Val Pro Ala Val Met Arg Glu
100 105 110
Tyr Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
115 120 125
Ser Ser
130
<210> 304
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 304
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Gln Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Thr Lys Lys Tyr Ala His Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Asp Thr Ala Tyr
65 70 75 80
Met Ile Leu Ser Ser Leu Ile Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Asp Trp Asn Phe Gly Ser Trp Phe Asp Ser Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 305
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 305
Gln Val His Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly His Gly Leu Glu Trp Met
35 40 45
Gly Trp Leu Asn Pro Asn Thr Gly Thr Thr Lys Tyr Ile Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Thr Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Asp Trp Asn Tyr Gly Ser Trp Phe Asp Thr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 306
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 306
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Thr Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile His Trp His Gly Lys Arg Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Gly Glu Asp Thr Ala Leu Tyr His Cys
85 90 95
Val Arg Gly Gly Met Ser Thr Gly Asp Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Ile Val Ser Ser
115 120
<210> 307
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 307
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Gly Met Thr Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile His Trp Ser Gly Arg Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Met Ser Thr Gly Asp Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 308
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 308
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Ser Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Leu Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 309
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 309
Glu Glu Arg Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Val Gly Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Ser Gly Gly Asn Thr His Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Ile Met Ser Arg Gln Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Glu Thr Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Leu Asp Val Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 310
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 310
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Met Pro Gly Ser
1 5 10 15
Ser Val Arg Val Ser Cys Lys Ala Ser Gly Gly Ile Phe Ser Ser Ser
20 25 30
Thr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Ile Pro Val Phe Gly Thr Val Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Ile Phe Thr Ala Asp Glu Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Lys Ser Gly Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Asn Trp Gly Leu Gly Ser Phe Tyr Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 311
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 311
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val His Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Pro Phe Asp Glu Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ser Asn Asn Asn Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Phe Tyr Tyr Cys
85 90 95
Ala Lys Ser Gly Ile Phe Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 312
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 312
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Leu Ile Ser Tyr Glu Gly Arg Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Thr Leu Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 313
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 313
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Thr Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Asn
20 25 30
Arg Met Cys Val Thr Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Arg Ile Asp Trp Asp Gly Val Lys Tyr Tyr Asn Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Phe Tyr
85 90 95
Cys Ala Arg Ser Thr Ser Leu Thr Phe Tyr Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 314
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 314
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Glu Phe Thr Val Gly Thr Asn
20 25 30
His Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Thr Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Thr Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Leu Gly Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 315
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 315
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Arg Gly Glu
1 5 10 15
Ser Leu Arg Leu Tyr Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gly Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Trp Gly Ser Gly Tyr Tyr Phe Asp Phe Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 316
<211> 130
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 316
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Ile Val Val Val Pro Ala Pro Met Gly Tyr Tyr Tyr
100 105 110
Tyr Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
115 120 125
Ser Ser
130
<210> 317
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 317
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Phe
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Thr Gly Gly Asn Met Asp Tyr Ala Asn Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Glu Asp Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Ala Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Asp Ile Arg Gly Ile Val Ala Thr Gly Gly Ala Phe Asp Ile
100 105 110
Trp Gly Arg Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 318
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 318
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Val Ile Tyr Ser Gly Gly Ser Thr Phe Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Gln Thr Ser Gln Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 319
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 319
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Ile Ser Thr Asn
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Tyr Ser Ser Gly Ser Thr Tyr Tyr Ile Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Leu Thr Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Asn Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Arg Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 320
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 320
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Ile Asp Asp Ser
20 25 30
Ala Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Val Lys Asp Ile Arg Gly Asn Trp Asn Tyr Gly Gly Asn Trp Phe Asp
100 105 110
Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 321
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 321
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Thr Val Gly Val Asn
20 25 30
His Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Phe Ser Ser Gly Arg Thr Phe Tyr Gly Asp Tyr Val Lys
50 55 60
Gly Arg Leu Thr Ile Phe Arg Gln Thr Ser Gln Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Gly Gly Leu Asp Ile Trp Gly Arg Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 322
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 322
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Leu His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Thr Gly Gly Thr Ile Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Thr Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Thr Arg Asp Ile Arg Gly Asn Trp Lys Tyr Gly Gly Trp Phe Asp Pro
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 323
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 323
Gln Val Gln Leu Val Gln Ser Gly Thr Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Asp Trp Met
35 40 45
Gly Trp Ile Ser Pro Asn Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Asn Thr Phe Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Thr His His Asn Ser Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 324
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 324
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Gly Thr Asn
20 25 30
Phe Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Tyr Ser Gly Gly Thr Ala Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Thr Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser
<210> 325
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 325
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Asn Thr Tyr
20 25 30
Val Leu Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Ile Pro Ile Leu Gly Ala Ala Asn Tyr Ala Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Phe Thr Thr Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Thr Ser Gly Gly Phe Asp Pro Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 326
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 326
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr His Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Ser Pro Tyr Asn Gly Tyr Thr Asp Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Leu Thr Thr Asp Thr Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Asn Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ser Arg Gly Arg Gly Pro Tyr Trp Ser Phe Asp Leu Trp Gly Arg Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 327
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 327
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr His Ser Tyr Ser Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Glu Ile Lys
100 105
<210> 328
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 328
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Thr Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Ala Ile Lys
100 105
<210> 329
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 329
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Thr Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Asn Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 330
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 330
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Leu Val His Gly
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Ile Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Gln Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Phe Cys Met Gln Ala
85 90 95
Thr His Phe Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 331
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 331
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Pro Ser Leu Val His Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Thr His Phe Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Arg
100 105 110
<210> 332
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 332
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 333
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 333
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 334
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 334
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Thr Ile Asn Ile Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 335
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 335
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Met Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
Phe Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 336
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 336
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Phe Asn Phe Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Gly Val Phe Tyr Cys Gln Gln Tyr Glu Ser Ala Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 337
<211> 105
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 337
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Leu Leu Ile Tyr Ala Ala
35 40 45
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Gly Gly Ser
50 55 60
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Arg Pro Glu Asp Phe
65 70 75 80
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Cys Thr Pro Pro Ile Thr Phe
85 90 95
Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 338
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 338
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 339
<211> 91
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 339
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Val Ile Ser Asn Tyr
1 5 10 15
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Arg Leu Leu Ile
20 25 30
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
35 40 45
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
50 55 60
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg
65 70 75 80
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
85 90
<210> 340
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 340
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Phe Gln Asn Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 341
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 341
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 342
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 342
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 343
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 343
Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Lys Pro Asp Glu Thr
1 5 10 15
Leu Thr Ile Thr Cys Thr Val Ser Gly Ile Asp Leu Ser Ser Asn Gly
20 25 30
Leu Thr Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Ile Gly
35 40 45
Thr Ile Asn Lys Asp Ala Ser Ala Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Leu Thr Ile Ser Lys Pro Ser Ser Thr Lys Val Asp Leu Lys Ile
65 70 75 80
Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Gly Arg Ile
85 90 95
Ala Phe Lys Thr Gly Thr Ser Ile Trp Gly Pro Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 344
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 344
Ala Ile Val Met Thr Gln Thr Pro Ser Pro Val Ser Ala Ala Val Gly
1 5 10 15
Gly Thr Val Thr Ile Asn Cys Gln Ala Ser Glu Ser Val Tyr Ser Asn
20 25 30
Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
35 40 45
Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr Ile Ser Gly Val
65 70 75 80
Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Ile Gly Gly Lys Ser Ser
85 90 95
Ser Thr Asp Gly Asn Ala Phe Gly Gly Gly Thr Glu Val Val Val Arg
100 105 110
<210> 345
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 345
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Ile Val Ala Thr Ile Thr Pro Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 346
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 346
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Ala Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Phe Ala Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ala Leu Asp Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Asp Leu
85 90 95
Arg Ala Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 347
<211> 123
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 347
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Thr Ile Tyr Asp Ser Ser Gly Tyr Ser Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 348
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 348
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 349
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 349
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 350
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 350
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 351
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 351
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 352
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 352
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 353
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 353
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 354
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 354
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Leu Ile Pro Ile Val Ser Met Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Ser Ile Thr Thr Asp Lys Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Ser Val Gly Gln Gln Leu Pro Trp Val Phe Phe Ala Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 355
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 355
Gln Met Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 356
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 356
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Phe Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Leu Asp Arg Asp Ile Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 357
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 357
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Tyr Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ser Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Ile Val Ala Thr Ile Thr Pro Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 358
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 358
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Tyr Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Ile Val Ala Thr Ile Thr Pro Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 359
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 359
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Tyr Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ser Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Ile Val Ala Thr Ile Thr Pro Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 360
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 360
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ala Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Ile Val Ala Thr Ile Thr Pro Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 361
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 361
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 362
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 362
Ala Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Thr Thr Ser Ser Leu Lys Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ser Thr Trp
85 90 95
Thr Phe Gly Arg Gly Thr Lys Val Glu Ile Lys
100 105
<210> 363
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 363
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Asn Asn Ser Asn Ile Ala Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Tyr Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Asp Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Val Trp Asp Gly Ser Leu
85 90 95
Thr Thr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 364
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 364
Leu Pro Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Thr Ser Asp Ile Gly Gly Tyr
20 25 30
Asp Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr His Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 365
<211> 111
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 365
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Arg Ser Ser
85 90 95
Thr Leu Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 366
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 366
Gln Ala Gly Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Tyr Asp Asp Leu Leu Pro Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 367
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 367
Gln Ser Ala Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Thr Thr His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 368
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 368
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Val Trp Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 369
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 369
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Arg Ala Pro Arg Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Gly
85 90 95
Gly Thr Leu Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 370
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 370
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 371
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 371
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Asn Ser Asp Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 372
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 372
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Gly Ser Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 373
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 373
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Leu Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 374
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 374
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 375
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 375
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 376
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 376
Ser Tyr Glu Leu Met Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Thr Ile Ala Cys Gly Gly Glu Asn Ile Gly Arg Lys Thr Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Tyr Asp Ser Asp Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Asp Ser Ser Ser Asp His
85 90 95
Arg Ile Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 377
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 377
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Val Lys Lys Ser Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Gly Thr Phe Ser Ile Thr
20 25 30
Asn Tyr Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu
35 40 45
Trp Met Gly Gly Ile Leu Pro Ile Phe Gly Ala Ala Lys Tyr Ala Gln
50 55 60
Lys Phe Gln Asp Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr
65 70 75 80
Ala Tyr Leu Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Ala Arg Gly Lys Arg Trp Leu Gln Ser Asp Leu Gln Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 378
<211> 110
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 378
Gln Pro Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Ser Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asp Leu Val Ser Trp Tyr Gln Gln Ser Pro Gly Lys Val Pro Lys Leu
35 40 45
Leu Ile Tyr Glu Gly Val Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Ala Gly Thr
85 90 95
Arg Asn Phe Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 379
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 379
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ser Ser Ala Gly Gln Ser Arg Pro Gly Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 380
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 380
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ser Ser Ala Gly Gln Ser Trp Pro Gly Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 381
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 381
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ser Ser Ala Gly Gln Ser Phe Pro Gly Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 382
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 382
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Ala Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 383
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 383
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Ala Gly Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 384
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 384
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Lys Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 385
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 385
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Lys Gln Gly Ile Val Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val
<210> 386
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 386
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Asn Gly Ile Val Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 387
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 387
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asp Ile Trp Lys Gln Gly Met Val Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 388
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 388
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Gln Gly Leu Ala Thr Ala Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 389
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 389
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Glu Ile Val Ala Thr Gly Ile Leu Thr Ser Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 390
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 390
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Gly Arg Gln Gly Leu Ile Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 391
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 391
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Tyr Gln Gly Leu Val Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 392
<211> 114
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 392
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asp Ile Trp Lys Gln Gly Phe Ala Thr Ala Asp Ser Val Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
65 70 75 80
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Lys
85 90 95
Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
100 105 110
Ser Ser
<210> 393
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 393
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Lys Gln Gly Ile Val Thr Val Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 394
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 394
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Gln Gly Leu Ala Thr Ala Tyr Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 395
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 395
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Asn Gly Ile Val Thr Val Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Ala Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 396
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 396
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Asn Gly Ile Val Thr Val Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Ala Gly Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 397
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 397
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Arg Asn Gly Ile Val Thr Val Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Lys Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 398
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 398
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Glu Thr Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
35 40 45
Trp Val Ser Ser Ile Trp Tyr Gln Gly Leu Val Thr Val Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Glu Thr Asn Ser Leu Arg Ala Glu Asp Thr Ala
85 90 95
Val Tyr Tyr Cys Ala Lys Trp Ser Ala Ala Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 399
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 399
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Tyr Gln Gly Leu Val Thr Val Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Ala Gly Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 400
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 400
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Trp Tyr Gln Gly Leu Val Thr Val Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Trp Ser Lys Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 401
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 401
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Asp Asn Gly Tyr Pro Ser
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 402
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 402
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Asp Asn Gly Tyr Pro Ser
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 403
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 403
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Asp Asn Gly Tyr Pro Ser
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 404
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 404
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asp Ile Thr Ala Ser Gly Gln Arg Thr Thr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Lys Ile Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Lys Ala Ser Arg Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Ala
210 215 220
Leu Lys Pro Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
<210> 405
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 405
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Asn Lys Asp Gly His Tyr Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asn Leu Asp Glu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
210 215 220
Ser Thr Pro Asn Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
<210> 406
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 406
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Met Ala Thr Gly Ala Gly Thr Leu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gly Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ser Ala Ser Gln Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
210 215 220
Ser Arg Pro Ser Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
<210> 407
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 407
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Gln Trp Val
35 40 45
Ser Thr Ile Thr Ser Ser Gly Ala Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asn Tyr Thr Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Asn Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Thr
210 215 220
Tyr Gly Pro Gly Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
<210> 408
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 408
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Tyr Ser Thr Gly Gly Ala Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ser Ser Ala Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Asp Asn
210 215 220
Gly Tyr Pro Ser Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
<210> 409
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 409
Gln Leu Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Met Phe Tyr Ile Ser
20 25 30
Asp Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Phe Val
35 40 45
Ala Thr Ile Thr Ser Gly Gly Thr Thr Asn Tyr Ala Asp Ser Val Glu
50 55 60
Gly Arg Phe Ser Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Glu Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Ala His Gly Pro Thr Tyr Gly Ser Thr Trp Asp Asp Leu Trp Gly Gln
100 105 110
Gly Thr Gln Val Thr Val Lys Pro Gly Gly
115 120
<210> 410
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 410
Gly Ile Met Phe Tyr Ile Ser Asp
1 5
<210> 411
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 411
Thr Ile Thr Ser Gly Gly Thr Thr Asn Tyr
1 5 10
<210> 412
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 412
Thr Ala His Gly Pro Thr Tyr Gly Ser Thr Trp Asp Asp Leu
1 5 10
<210> 413
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 413
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Glu Thr Phe Gly Val Val Phe
20 25 30
Thr Leu Gly Trp Tyr Arg Gln Thr Pro Gly Lys Gln Arg Glu Phe Val
35 40 45
Ala Arg Val Thr Gly Thr Asp Thr Val Asp Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ser Asp Phe Ala Arg Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Thr Gly Ala Tyr Trp Gly Gln Gly Thr Gln Val Thr Val Lys Pro Gly
100 105 110
Gly
<210> 414
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 414
Thr Phe Gly Val Val Phe Thr
1 5
<210> 415
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 415
Val Thr Gly Thr Asp Thr Val
1 5
<210> 416
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 416
Asn Thr Gly Ala Tyr
1 5
<210> 417
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 417
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Thr Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Ala Ser Thr Tyr
20 25 30
Ser Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Gln Phe Val
35 40 45
Ala Arg Ile Ile Trp Ser Thr Gly Ser Thr Tyr Tyr Thr Asn Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Ile Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Glu Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ala Arg Glu Pro Thr Gly Tyr Asp Tyr Trp Gly Gln Gly Thr Gln
100 105 110
Val Thr Val Lys Pro Gly Gly
115
<210> 418
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 418
Gly Arg Thr Ala Ser Thr Tyr Ser
1 5
<210> 419
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 419
Ile Trp Ser Thr Gly Ser Thr
1 5
<210> 420
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 420
Thr Ala Arg Glu Pro Thr Gly Tyr Asp Tyr
1 5 10
<210> 421
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 421
Gln Leu Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Gly Leu Ser Cys Ala Ala Ser Gly Ser Ile Phe Arg Phe Gly
20 25 30
Ala Arg Gly Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Ile Ile Thr Ser Gly Gly Ser Thr Asn Tyr Ala Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Met Val Tyr Leu
65 70 75 80
Gln Met Asn Gly Leu Lys Ser Gly Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Ala Asp Arg Ser Asp Ala Val Gly Val Gly Trp Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Gln Val Thr Val Lys Pro Gly Gly
115 120
<210> 422
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 422
Gly Ser Ile Phe Arg Phe Gly Ala
1 5
<210> 423
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 423
Ile Thr Ser Gly Gly Ser Thr
1 5
<210> 424
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 424
Ala Ala Asp Arg Ser Asp Ala Val Gly Val Gly Trp Asp Tyr
1 5 10
<210> 425
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 425
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Thr Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Ala Ser Thr Tyr
20 25 30
Ser Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Gln Phe Val
35 40 45
Ala Arg Ile Ile Trp Ser Thr Gly Ser Thr Tyr Tyr Thr Asn Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Ile Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Glu Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ala Arg Asp Pro Thr Gly Tyr Asp Tyr Trp Gly Gln Gly Thr Gln
100 105 110
Val Thr Val Lys Pro Gly Gly
115
<210> 426
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 426
Ile Ile Trp Ser Thr Gly Ser Thr
1 5
<210> 427
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 427
Thr Ala Arg Asp Pro Thr Gly Tyr Asp Tyr
1 5 10
<210> 428
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 428
Gln Leu Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ser Ile Phe Ser Ile Asp
20 25 30
Ala Thr Ala Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Ile Ile Thr Ser Ser Gly Ser Thr Asn Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Asn Pro Glu Asp Thr Ala Leu Tyr Ser Cys Asn
85 90 95
Ala Ile Thr Arg Met Gly Gly Ser Thr Tyr Asp Phe Trp Gly Gln Gly
100 105 110
Thr Gln Val Thr Val Lys Pro Gly Gly
115 120
<210> 429
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 429
Gly Ser Ile Phe Ser Ile Asp Ala
1 5
<210> 430
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 430
Ile Thr Ser Ser Gly Ser Thr
1 5
<210> 431
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 431
Asn Ala Ile Thr Arg Met Gly Gly Ser Thr Tyr Asp Phe
1 5 10
<210> 432
<211> 117
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 432
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Pro Ala Gly Asp Gly Ser Thr Lys Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Lys Ser Arg Gly Trp Ser Thr Val Asp Asp Met Asp Tyr Trp Gly
100 105 110
Lys Gly Thr Gln Val
115
<210> 433
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 433
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 434
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 434
Ile Pro Ala Gly Asp Gly Ser Thr
1 5
<210> 435
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 435
Ala Lys Ser Arg Gly Trp Ser Thr Val Asp Asp Met Asp Tyr
1 5 10
<210> 436
<211> 117
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 436
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Val Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Asn Ser Gly Glu Ser Ser Thr Lys Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Asp Leu Lys Pro Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Lys His Arg Gly Trp Ser Thr Val Asp Asp Ile Asn Tyr Trp Gly
100 105 110
Lys Gly Thr Gln Val
115
<210> 437
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 437
Gly Phe Thr Phe Arg Ser Tyr Ala
1 5
<210> 438
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 438
Ile Asn Ser Gly Glu Ser Ser Thr
1 5
<210> 439
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 439
Ala Lys His Arg Gly Trp Ser Thr Val Asp Asp Ile Asn Tyr
1 5 10
<210> 440
<211> 119
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 440
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp His
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Trp Asn Gly His Tyr Thr Tyr Tyr Ala Glu Ser Met
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Lys Gly Trp Arg Gly Ser Tyr Thr Arg Asp Arg Pro Phe Ala Ser
100 105 110
Trp Gly Gln Gly Thr Gln Val
115
<210> 441
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 441
Gly Phe Thr Phe Asp Asp His Ala
1 5
<210> 442
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 442
Ile Ser Trp Asn Gly His Tyr Thr
1 5
<210> 443
<211> 16
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 443
Val Lys Gly Trp Arg Gly Ser Tyr Thr Arg Asp Arg Pro Phe Ala Ser
1 5 10 15
<210> 444
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 444
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Thr Asn Thr Gly Gly Gly Ser Thr Tyr Tyr Ala Tyr
50 55 60
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
65 70 75 80
Asn Thr Leu Tyr Leu Glu Met Asn Ser Leu Lys Pro Glu Asp Thr Ala
85 90 95
Gln Tyr Tyr Cys Val Arg Thr Arg Trp Glu Gly Val Tyr Asp Tyr Trp
100 105 110
Gly Leu Gly Thr Gln Val
115
<210> 445
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 445
Gly Phe Thr Phe Ser Ser Tyr Tyr
1 5
<210> 446
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 446
Ile Ser Thr Asn Thr Gly Gly Gly Ser Thr
1 5 10
<210> 447
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 447
Val Arg Thr Arg Trp Glu Gly Val Tyr Asp Tyr
1 5 10
<210> 448
<211> 482
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 448
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ile Asn
20 25 30
Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys Arg Arg Glu Phe Val
35 40 45
Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Gly
85 90 95
Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser Val Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly Gly Asp Lys Thr
115 120 125
His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro Ser Val Phe Leu
130 135 140
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
145 150 155 160
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
165 170 175
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
180 185 190
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
195 200 205
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
210 215 220
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
225 230 235 240
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
245 250 255
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
260 265 270
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
275 280 285
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
290 295 300
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
305 310 315 320
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
325 330 335
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Ser Gly Gly Gly
340 345 350
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly
355 360 365
Gly Glu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser
370 375 380
Gly Phe Ser Phe Ser Ile Asn Ala Met Gly Trp Tyr Arg Gln Ala Pro
385 390 395 400
Gly Lys Arg Arg Glu Phe Val Ala Ala Ile Glu Ser Gly Arg Asn Thr
405 410 415
Val Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
420 425 430
Ala Lys Asn Thr Val Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp
435 440 445
Thr Ala Val Tyr Tyr Cys Gly Leu Leu Lys Gly Asn Arg Val Val Ser
450 455 460
Pro Ser Val Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro
465 470 475 480
Gly Gly
<210> 449
<211> 466
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 449
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
130 135 140
Ser Phe Ser Ile Asn Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys
145 150 155 160
Arg Arg Glu Phe Val Ala Ala Ile Glu Ser Gly Arg Asn Thr Val Tyr
165 170 175
Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
180 185 190
Asn Thr Val Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Gly Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser
210 215 220
Val Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly
225 230 235 240
Gly Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly
245 250 255
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
260 265 270
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
275 280 285
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
290 295 300
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
305 310 315 320
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
325 330 335
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
340 345 350
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
355 360 365
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
370 375 380
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
385 390 395 400
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
405 410 415
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
420 425 430
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
435 440 445
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455 460
Gly Lys
465
<210> 450
<211> 466
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 450
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
130 135 140
Ser Phe Ser Ile Asn Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys
145 150 155 160
Arg Arg Glu Phe Val Ala Ala Ile Tyr Ser Gly Arg Asn Thr Val Tyr
165 170 175
Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
180 185 190
Asn Thr Val Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Gly Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser
210 215 220
Val Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly
225 230 235 240
Gly Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly
245 250 255
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
260 265 270
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
275 280 285
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
290 295 300
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
305 310 315 320
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
325 330 335
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
340 345 350
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
355 360 365
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
370 375 380
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
385 390 395 400
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
405 410 415
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
420 425 430
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
435 440 445
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455 460
Gly Lys
465
<210> 451
<211> 466
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 451
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
130 135 140
Ser Phe Ser Ile Asn Ala Met Gly Trp Tyr Arg Gln Ala Pro Gly Lys
145 150 155 160
Arg Arg Glu Phe Val Ala Ala Ile Tyr Ser Gly Ser Ser Thr Val Tyr
165 170 175
Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
180 185 190
Asn Thr Val Tyr Leu Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala
195 200 205
Val Tyr Tyr Cys Gly Leu Leu Lys Gly Asn Arg Val Val Ser Pro Ser
210 215 220
Val Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly
225 230 235 240
Gly Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly
245 250 255
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
260 265 270
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
275 280 285
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
290 295 300
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
305 310 315 320
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
325 330 335
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
340 345 350
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
355 360 365
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
370 375 380
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
385 390 395 400
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
405 410 415
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
420 425 430
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
435 440 445
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455 460
Gly Lys
465
<210> 452
<211> 481
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 452
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr Gly
145 150 155 160
Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val Ser
165 170 175
Arg Leu Ala Trp Gln Gly Gly Ser Thr Asp Tyr Val Glu Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr Tyr
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly
245 250 255
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro
260 265 270
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
275 280 285
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
290 295 300
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
305 310 315 320
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
325 330 335
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
340 345 350
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
355 360 365
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
370 375 380
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
385 390 395 400
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
405 410 415
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
420 425 430
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
435 440 445
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
450 455 460
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475 480
Lys
<210> 453
<211> 481
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 453
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr Gly
145 150 155 160
Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val Ser
165 170 175
Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr Tyr
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly
245 250 255
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro
260 265 270
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
275 280 285
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
290 295 300
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
305 310 315 320
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
325 330 335
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
340 345 350
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
355 360 365
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
370 375 380
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
385 390 395 400
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
405 410 415
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
420 425 430
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
435 440 445
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
450 455 460
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475 480
Lys
<210> 454
<211> 481
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 454
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Ser Asn Tyr Gly
145 150 155 160
Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val Ser
165 170 175
Arg Leu Ala Trp Gly Gly Gly Ser Thr Asp Tyr Val Glu Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr Tyr
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly
245 250 255
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro
260 265 270
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
275 280 285
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
290 295 300
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
305 310 315 320
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
325 330 335
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
340 345 350
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
355 360 365
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
370 375 380
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
385 390 395 400
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
405 410 415
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
420 425 430
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
435 440 445
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
450 455 460
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475 480
Lys
<210> 455
<211> 481
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 455
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Gly Asn Tyr Gly
145 150 155 160
Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val Ser
165 170 175
Arg Leu Ala Trp Ser Gly Gly Ser Thr Asp Tyr Val Glu Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr Tyr
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly
245 250 255
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro
260 265 270
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
275 280 285
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
290 295 300
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
305 310 315 320
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
325 330 335
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
340 345 350
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
355 360 365
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
370 375 380
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
385 390 395 400
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
405 410 415
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
420 425 430
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
435 440 445
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
450 455 460
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475 480
Lys
<210> 456
<211> 481
<212> PRT
<213> Искусственная последовательность
<220>
<223> химически синтезированная
<400> 456
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Gly Ile Phe Ala Ile Lys
20 25 30
Pro Ile Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Trp Val
35 40 45
Ser Thr Thr Thr Ser Ser Gly Ala Thr Asn Tyr Ala Glu Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Val Phe Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly
100 105 110
Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Glu
115 120 125
Val Gln Leu Leu Glu Ser Gly Gly Gly Glu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Trp Ala Phe Ser Asn Tyr Gly
145 150 155 160
Met Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val Ser
165 170 175
Arg Leu Ala Trp Ser Gly Gly Ser Thr Asp Tyr Val Glu Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gln Arg Ser Tyr Ser Arg Tyr Asp Ile Arg Thr Pro Gln Thr Tyr
225 230 235 240
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Lys Pro Gly Gly Gly
245 250 255
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Gly Gly Pro
260 265 270
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
275 280 285
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
290 295 300
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
305 310 315 320
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
325 330 335
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
340 345 350
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
355 360 365
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
370 375 380
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
385 390 395 400
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
405 410 415
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
420 425 430
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
435 440 445
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
450 455 460
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
465 470 475 480
Lys
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2020 |
|
RU2818588C2 |
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732042C2 |
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2827926C2 |
| НОВЫЕ ФЕРМЕНТЫ CRISPR И СИСТЕМЫ | 2016 |
|
RU2771826C2 |
| МУЛЬТИВАЛЕНТНЫЕ И МУЛЬТИСПЕЦИФИЧЕСКИЕ ГИБРИДНЫЕ БЕЛКИ, СВЯЗЫВАЮЩИЕСЯ С DR5 | 2016 |
|
RU2748620C2 |
| ЧАСТИЦЫ, КОНЪЮГИРОВАННЫЕ С ПЕПТИДОМ | 2014 |
|
RU2813163C2 |
| СВЯЗЫВАЮЩИЕСЯ С РЕЦЕПТОРАМИ АГОНИСТЫ TNF | 2016 |
|
RU2821343C2 |
| СЛИТЫЕ БЕЛКИ С АЛЬБУМИН-СВЯЗЫВАЮЩИМИ ДОМЕНАМИ | 2018 |
|
RU2786444C2 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
| АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА, СОДЕРЖАЩАЯ ДВА АНТИГЕНСВЯЗЫВАЮЩИХ ДОМЕНА, КОТОРЫЕ СВЯЗАНЫ ДРУГ С ДРУГОМ | 2019 |
|
RU2838581C2 |

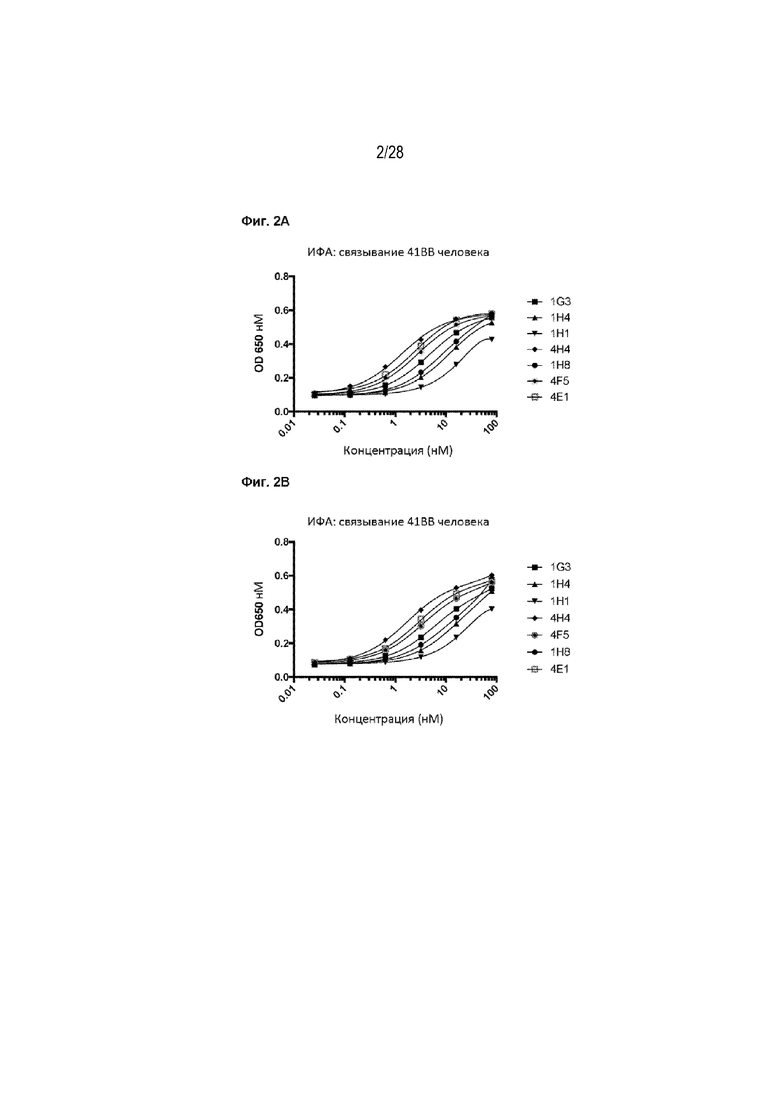


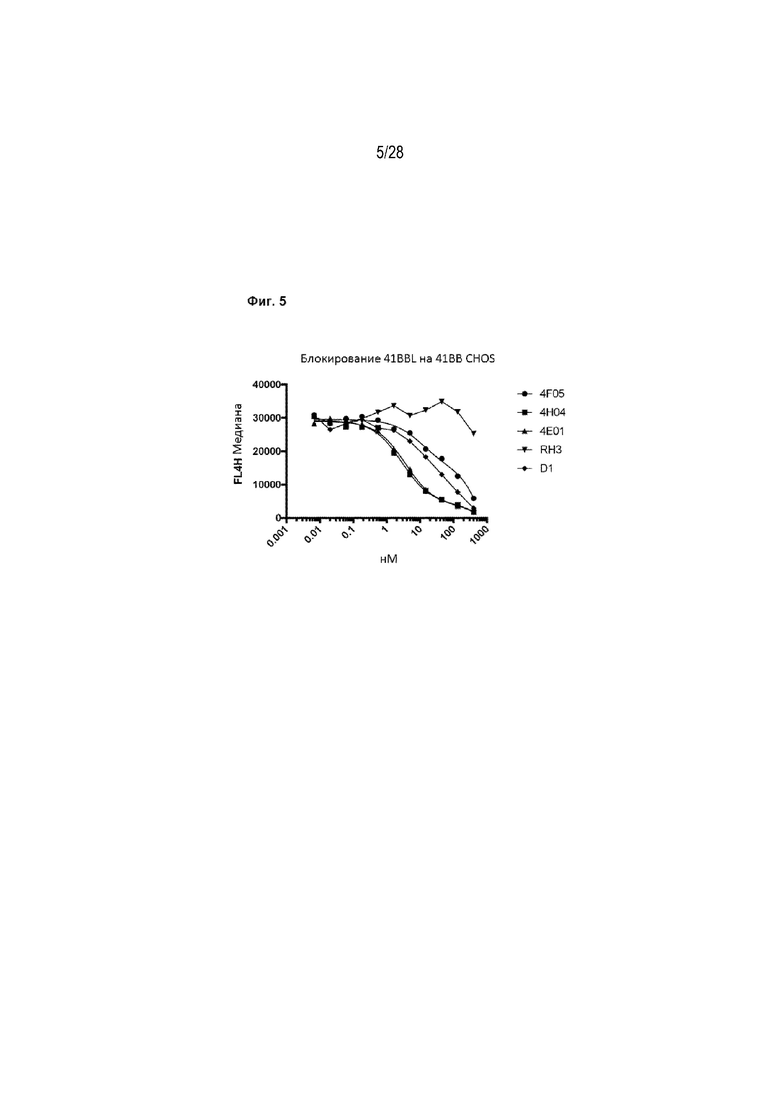


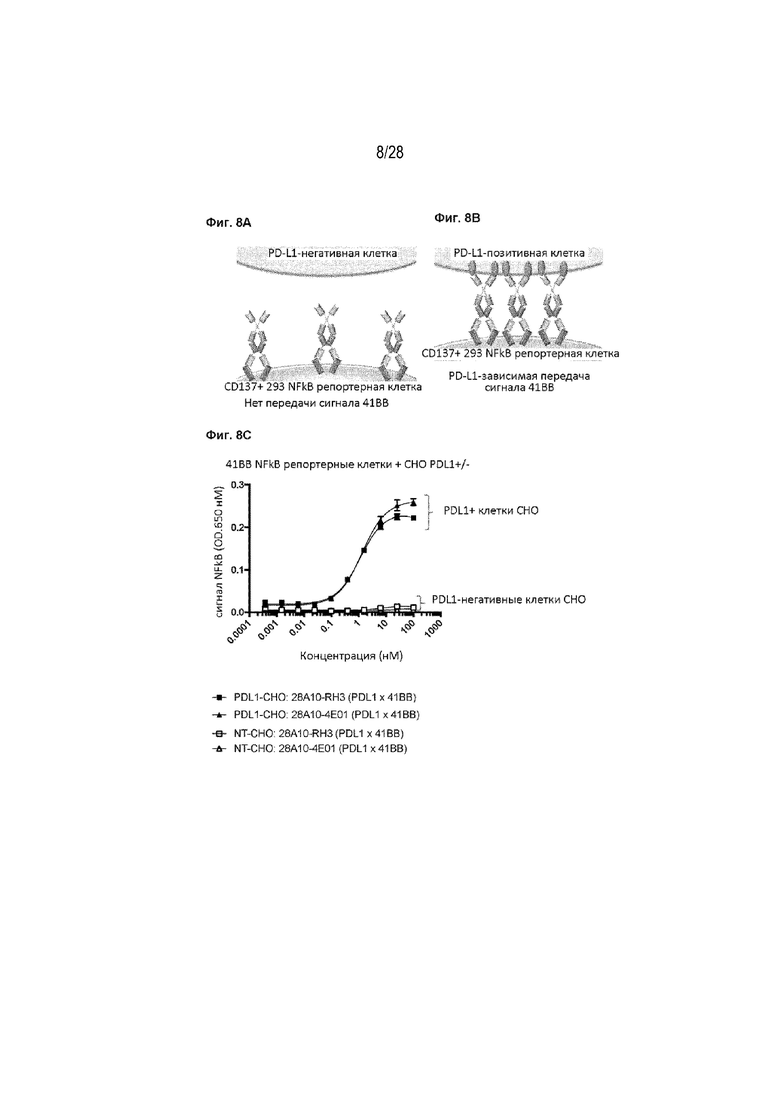
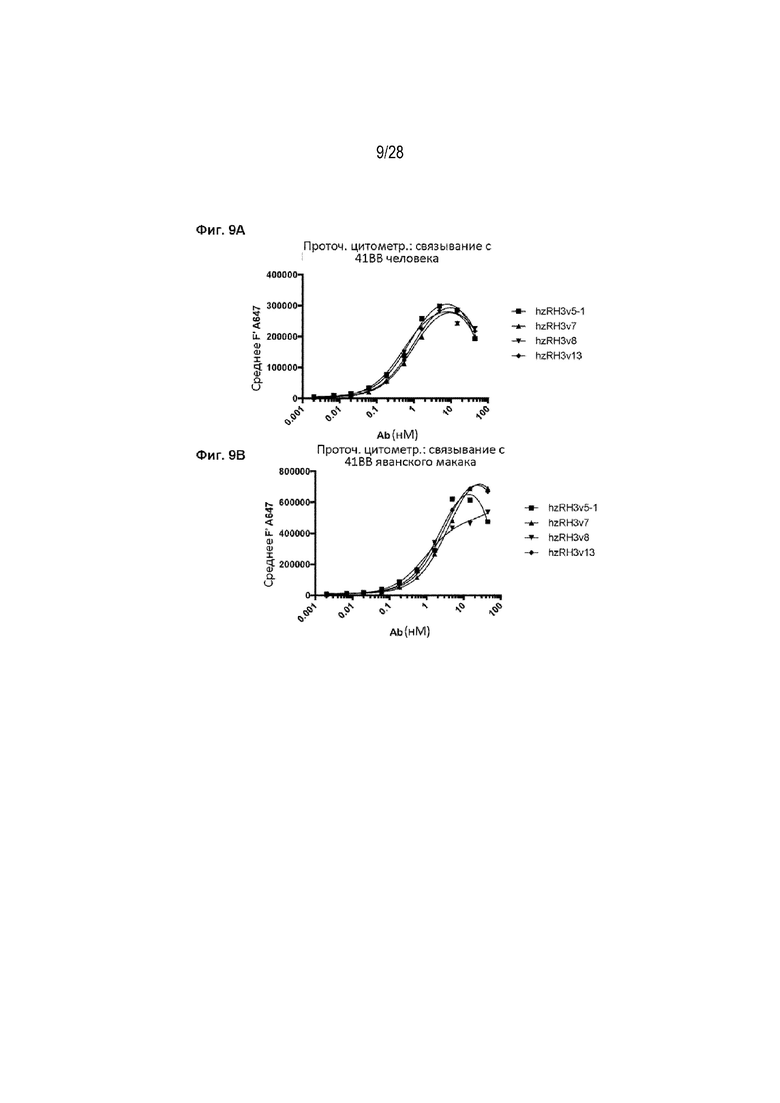
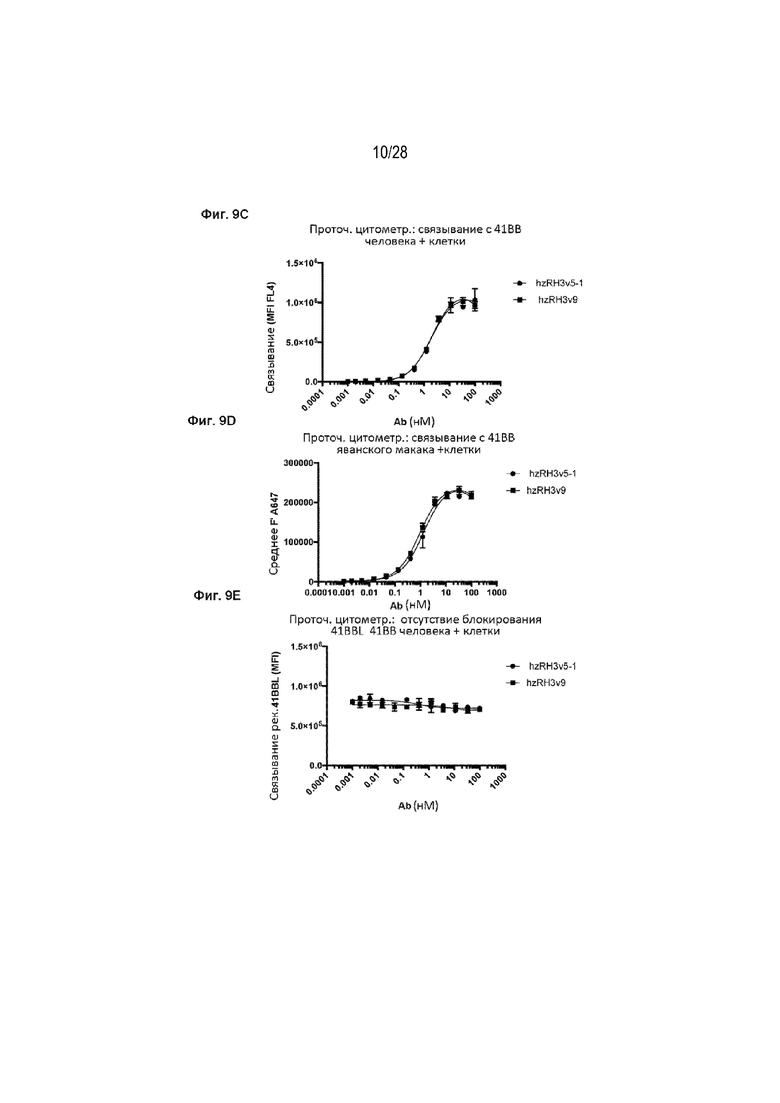


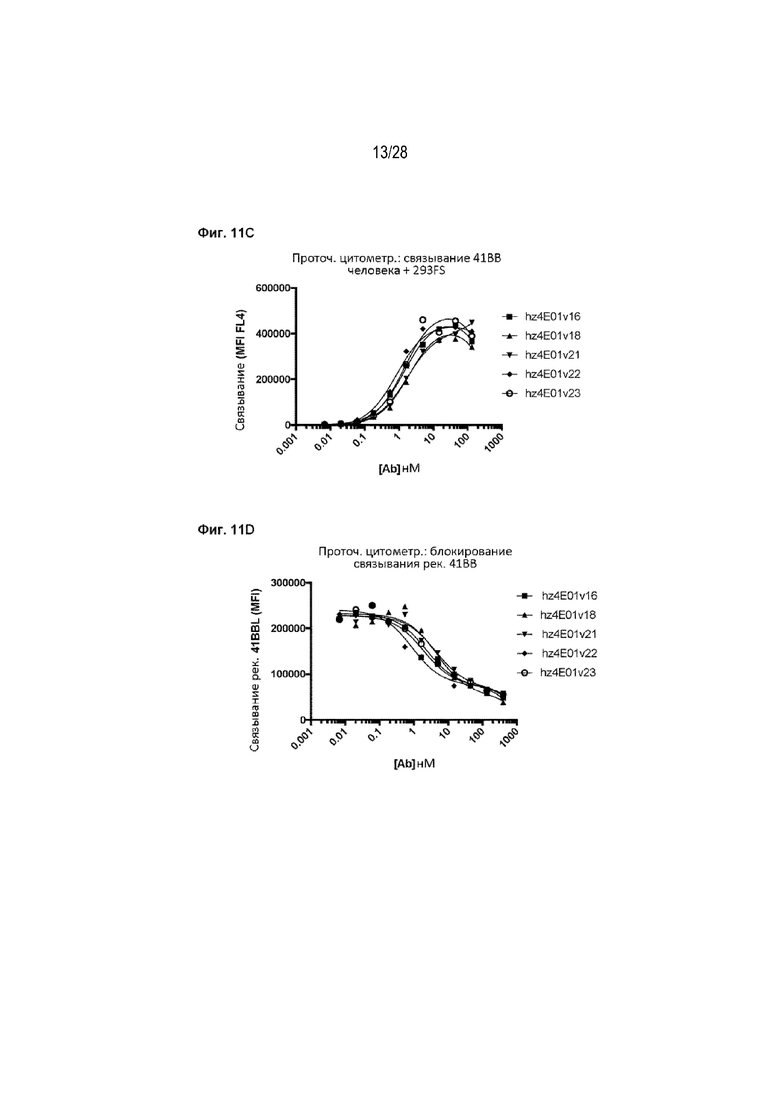


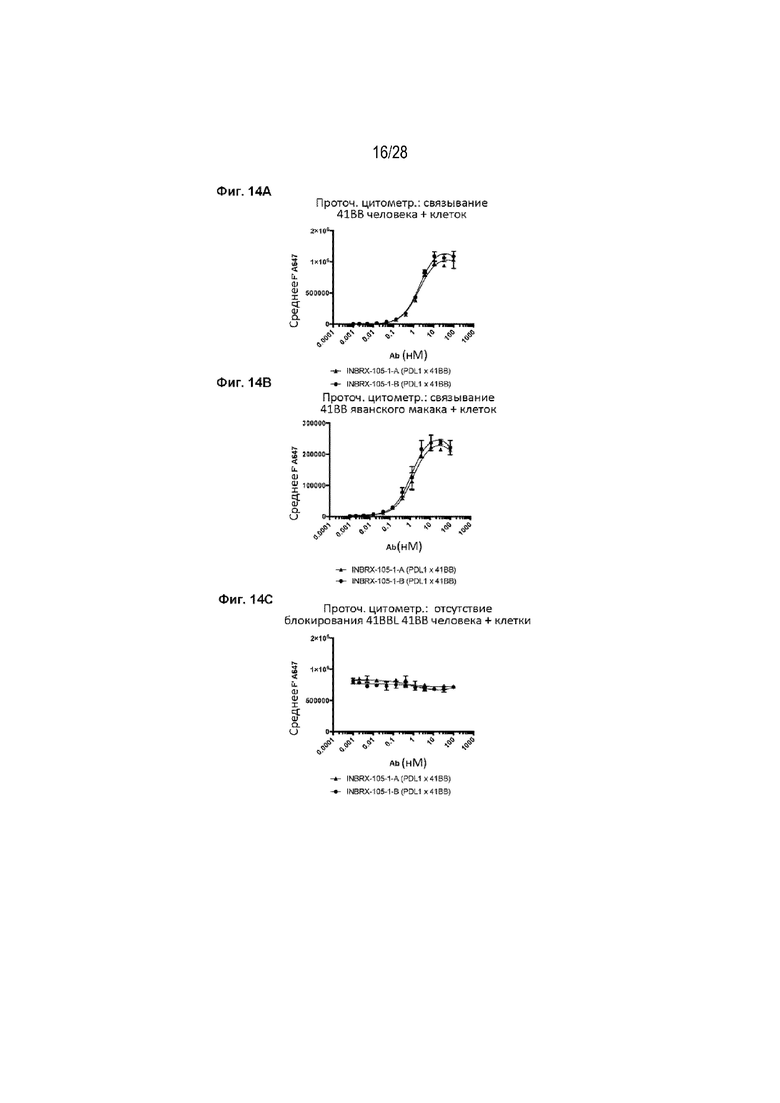
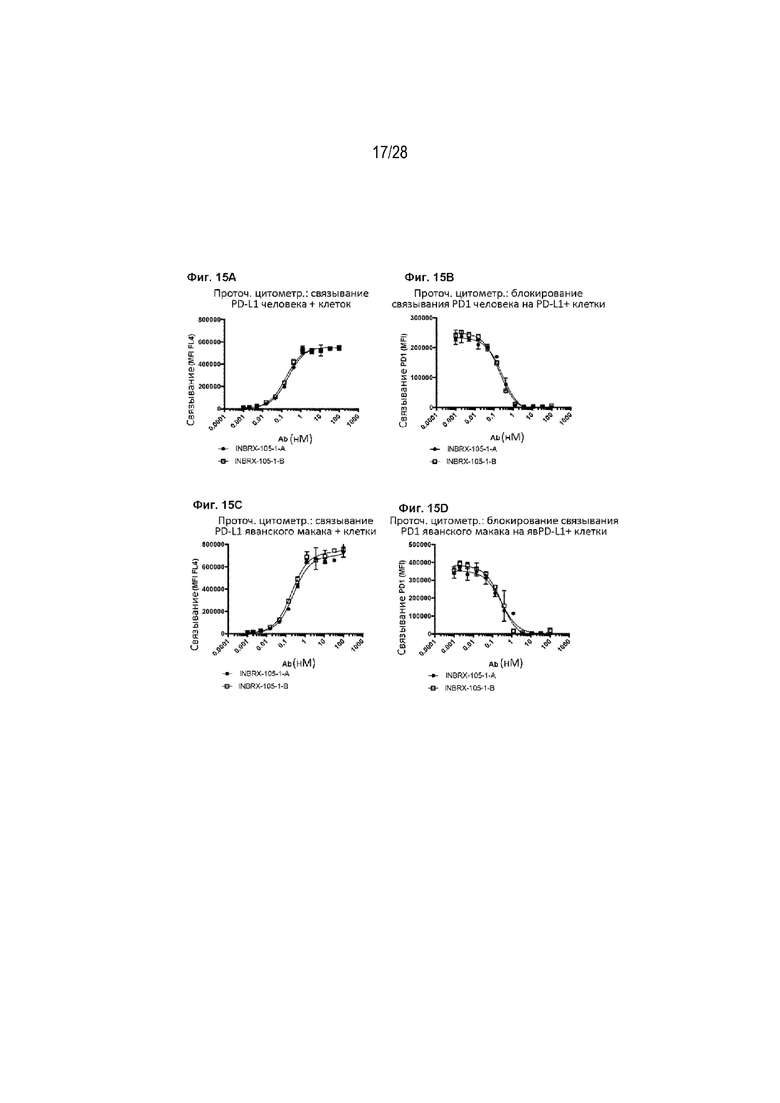
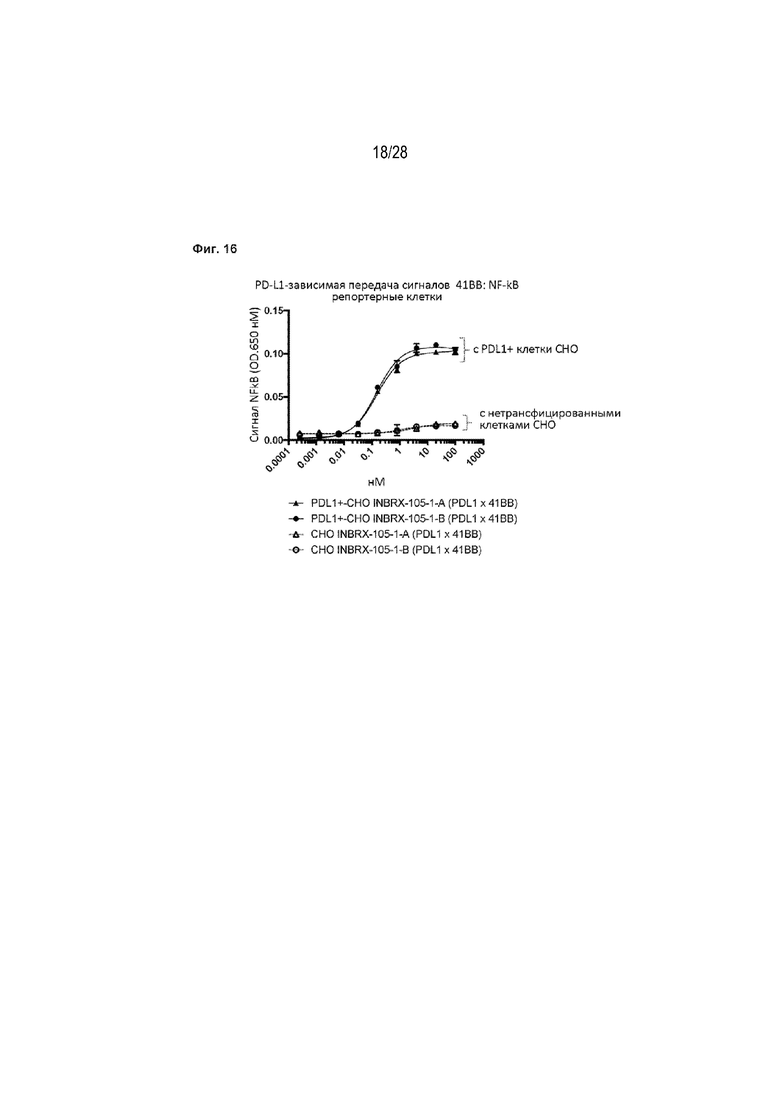
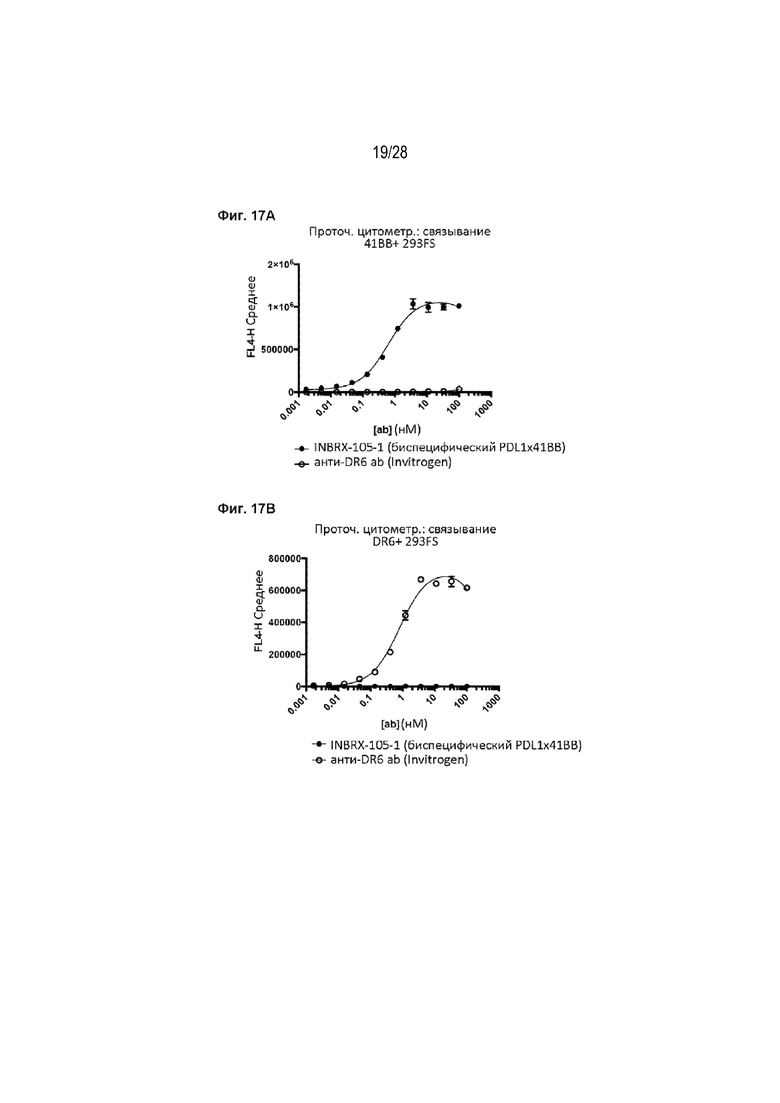



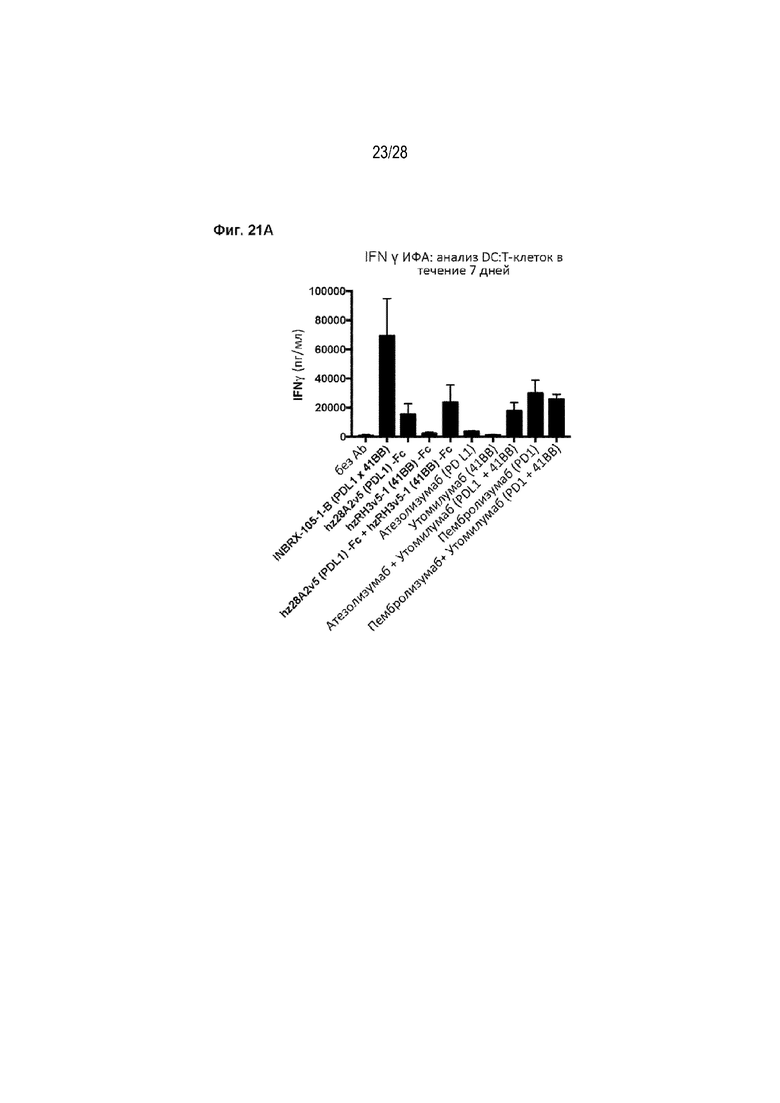


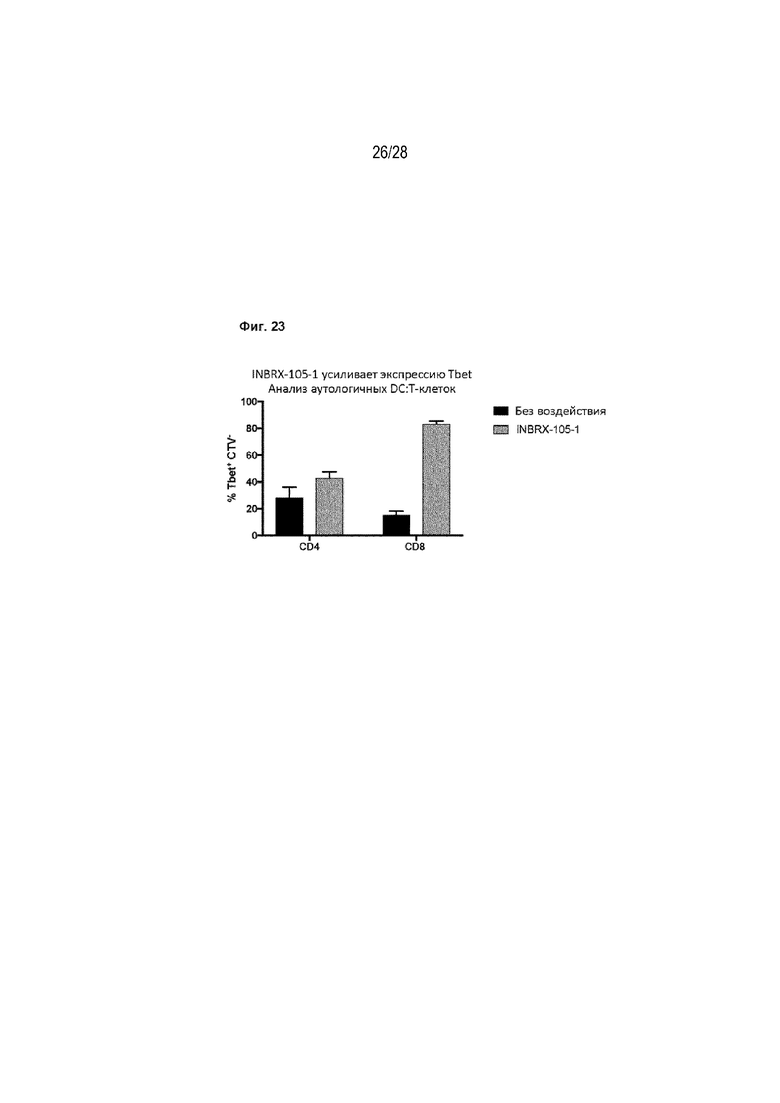

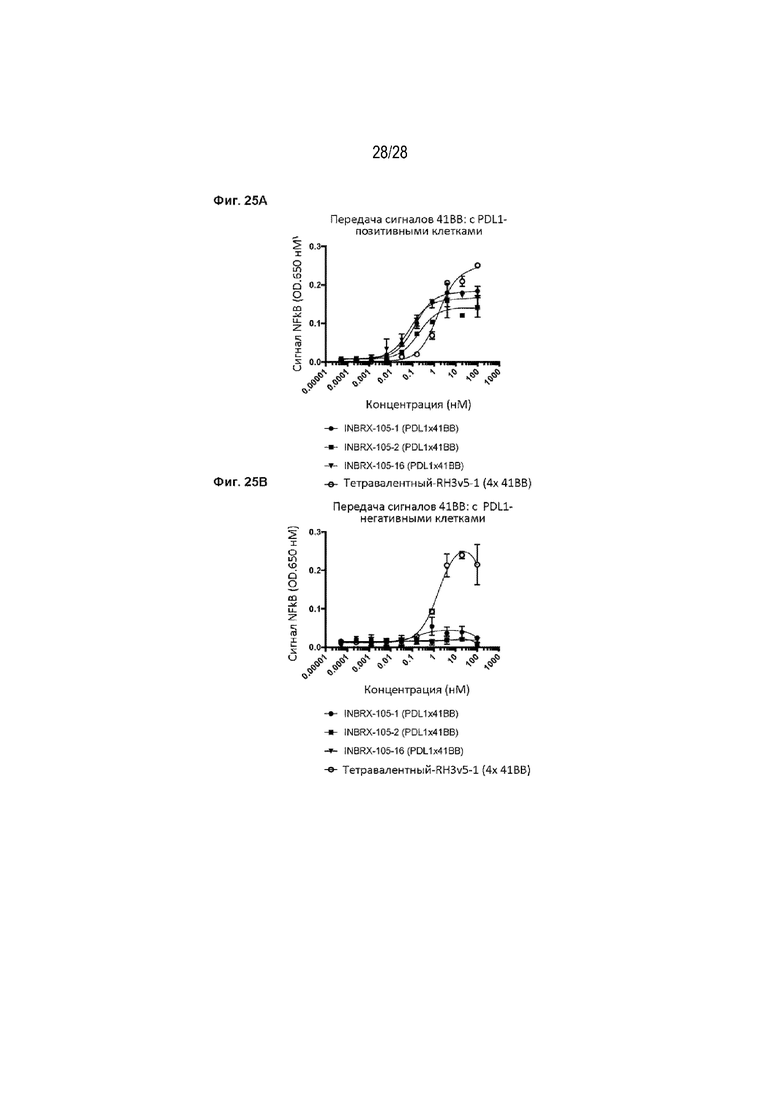
Изобретение относится к биохимии, в целом к молекулам, которые специфически взаимодействуют с 41BB - представителем суперсемейства рецепторов TNF (TNFRSF), в частности к мультивалентным и/или мультиспецифическим молекулам, которые связывают по меньшей мере 41BB. Слитые белки по изобретению способны к усиленной кластеризации представителей семейства TNFRSF по сравнению с двухвалентными антителами, без сшивания. Слитые белки по изобретению модулируют иммунные клетки, пригодны для применения в лечении новообразований, воспалительных патологических состояний. 7 н. и 9 з.п. ф-лы, 25 ил., 4 пр. 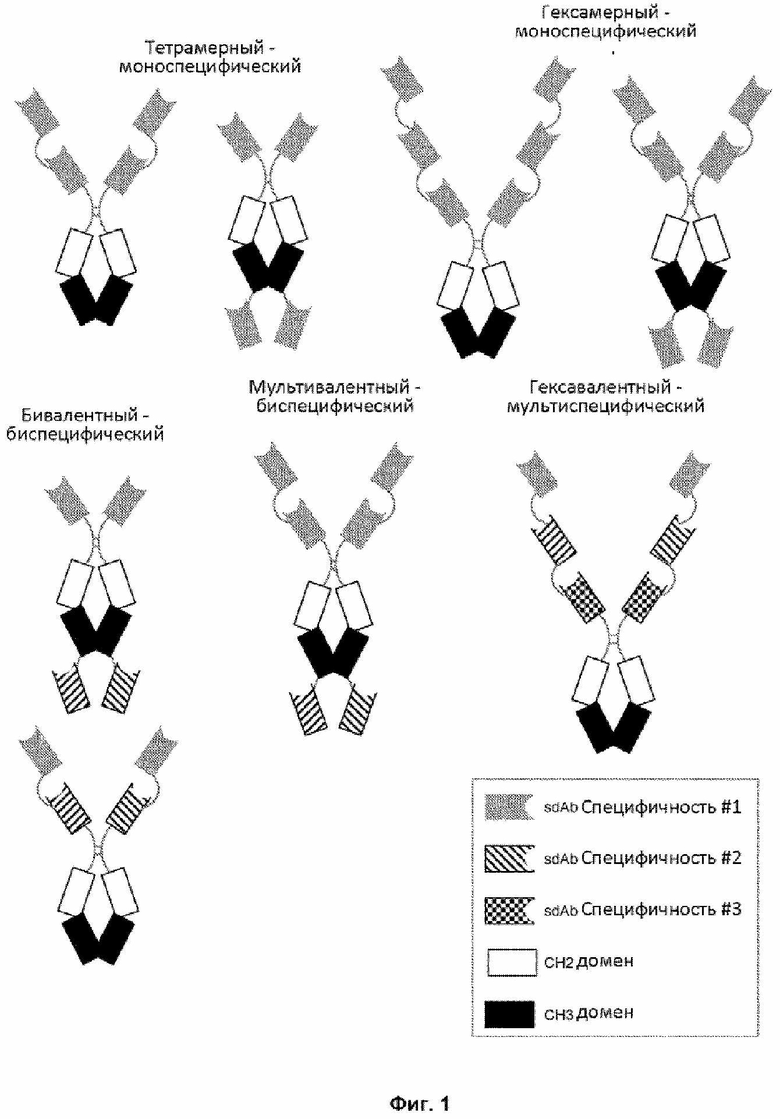
1. Выделенный полипептид, который связывает PDL1 и 41BB, где указанный полипептид содержит по меньшей мере один домен VHH, который связывает 41BB и содержит область 1, определяющую комплементарность (CDR1), содержащую аминокислотную последовательность SEQ ID NO: 26, область 2, определяющую комплементарность (CDR2), содержащую аминокислотную последовательность SEQ ID NO: 61, и область 3, определяющую комплементарность (CDR3), содержащую аминокислотную последовательность SEQ ID NO: 28; и по меньшей мере один домен VHH, который связывает PDL1 и содержит CDR1, содержащий аминокислотную последовательность SEQ ID NO: 105, CDR2, содержащий аминокислотную последовательность SEQ ID NO: 106, и CDR3, содержащий аминокислотную последовательность SEQ ID NO: 107.
2. Выделенный полипептид по п. 1, где по меньшей мере один домен VHH, связывающий 41BB, содержит аминокислотную последовательность, по меньшей мере на 95% идентичную SEQ ID NO: 60, и где по меньшей мере один домен VHH, связывающий PDL1, содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична SEQ ID NO: 124.
3. Выделенный полипептид по п. 1, где по меньшей мере один домен VHH, связывающий 41BB, содержит аминокислотную последовательность SEQ ID NO: 60, и где по меньшей мере один домен VHH, связывающий PDL1, содержит аминокислотную последовательность SEQ ID NO: 124.
4. Выделенный полипептид по любому из пп. 1-3, где по меньшей мере один домен VHH, который связывает 41BB, и по меньшей мере один домен VHH, который связывает PDL1, являются функционально связанными посредством линкерного полипептида.
5. Выделенный полипептид по любому из пп. 1-4, где каждый домен VHH представляет собой гуманизированный домен VHH.
6. Выделенный полипептид по любому из пп. 1-5, где указанный выделенный полипептид содержит полипептид области Fc иммуноглобулина.
7. Выделенный полипептид по п. 6, где указанный полипептид области Fc иммуноглобулина содержит аминокислотную последовательность, выбранную из SEQ ID NO: 1-6.
8. Выделенный полипептид по п. 7, где указанный полипептид области Fc иммуноглобулина содержит аминокислотную последовательность SEQ ID NO: 2.
9. Выделенный полипептид по любому из пп. 6-8, где указанный полипептид содержит структуру: VHH-линкер-VHH-линкер-шарнир-Fc, где каждый VHH представляет собой гуманизированную последовательность VHH.
10. Выделенный полипептид, который связывает PDL1 и 41BB, где указанный полипептид содержит аминокислотную последовательность SEQ ID NO: 449.
11. Выделенный полинуклеотид, который кодирует полипептид по любому из пп. 1-10.
12. Выделенная клетка, которая экспрессирует полипептид по любому из пп. 1-10, содержащая полинуклеотид по п. 11 и контрольную последовательность, содержащую по меньшей мере промотор и последовательность терминации транскрипции.
13. Способ получения полипептида по любому из пп. 1-10, включающий культивирование выделенной клетки по п. 12 в условиях, подходящих для экспрессирования указанного полипептида.
14. Применение полипептида по любому из пп. 1-10 для лечения новообразований.
15. Применение по п. 14, где указанное новообразование представляет собой рак.
16. Применение полипептида по любому из пп. 1-10 для модулирования иммунных клеток с целью усиления разрушения опухоли.
| WO 2014028776, 20.02.2014 | |||
| CHEN S | |||
| et al., Combination of 4-1BB agonist and PD-1 antagonist promotes antitumor effector/memory CD8 T cells in a poorly immunogenic tumor model, Cancer immunology research, 2015, vol | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Подъемник для выгрузки и нагрузки барж сплавными бревнами, дровами и т.п. | 1919 |
|
SU149A1 |
| KONTERMANN R | |||
| E | |||
| et al., Bispecific antibodies, Drug Discovery Today, 2015, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Углеподъемник для паровозов | 1924 |
|
SU838A1 |
Авторы
Даты
2023-02-07—Публикация
2017-01-11—Подача