Изобретение относится к медицине, а именно к челюстно-лицевой хирургии и офтальмологии, и предназначено для восстановления трофики (чувствительности) роговицы глаза.
В клинической практике повреждение лицевого нерва в ходе нейрохирургических операций нередко сочетается с повреждением тройничного нерва. Нарушение иннервации круговой мышцы глаза приводит к невозможности смыкания век, увеличению открытой глазной поверхности и нарушению прекорнеальной слезной пленки, адекватное восстановление которой невозможно из-за отсутствия полноценных мигательных движений [1, 2]. Поражение тройничного нерва проявляется снижением или отсутствием чувствительности в соответствующей части лица. Денервация роговицы сопровождается ее гипо- или анестезией, нейротрофическими расстройствами, что вызывает длительно текущий нейротрофический кератит рецидивирующего характера [3]. Существенное снижение регенераторных функций роговицы обусловлено отсутствием высвобождения нейропептидов из нервных окончаний, которые в норме способствуют пролиферации клеток эпителия, их дифференциации, миграции и адгезии [4-7].
С точки зрения лечения и прогноза нейротрофическая кератопатия (нейротрофический кератит) является одним из наиболее тяжелых заболеваний. Патологические изменения при нейротрофическом кератите могут существенно варьировать: от персистирующих эпителиальных дефектов до язв роговицы разной степени выраженности, плохо поддающихся лечению [4-7]. В результате даже при благоприятном исходе практически во всех случаях происходит формирование грубых помутнений, в том числе и в оптической области, с существенным снижением остроты зрения.
Таким образом, перечисленные факторы обусловливают необходимость этапного подхода к лечению этой категории пациентов, позволяющего воздействовать на те звенья патогенеза, которые приводят к развитию нейротрофического кератита.
Нейротрофический кератит (НТК) представляет собой дегенеративное заболевание роговицы, сопровождающееся нейрогенным воспалением. Оно обусловлено нарушением чувствительной иннервации тройничного нерва и характеризуется пониженной чувствительностью роговицы и нарушением процесса ее заживления. Вызывающие НТК повреждения тройничного нерва могут происходить на разных уровнях - от ядра до окончаний, расположенных в роговице, и быть обусловлены как глазными, так и системными заболеваниями. К наиболее распространенным причинам можно отнести герпетический кератит, диабет, химические ожоги, ятрогенные травмы при офтальмологических операциях, внутричерепные новообразования, нарушения мозгового кровообращения и нейрохирургические вмешательства. Изменения роговицы включают эпителиопатию (I степень), персистирующую эрозию (II степень), язву и ее осложнения (III степень). Определяющим диагностическим признаком НТК является снижение или потеря чувствительности роговицы. Морфологические характеристики нервов роговицы могут быть исследованы с помощью конфокальной микроскопии [8].
Классическое лечение нейротрофической кератопатии носит паллиативный характер и преимущественно направлено на защиту глазной поверхности. С этой целью используются различные консервативные методы лечения, включая медикаментозную терапию, аутосеротерапию, использование защитных контактных линз, хемоденервации леватора и др., а также хирургические методы (лечебная кератопластика, лечебные биологические покрытия, блефарорафия и др.) [9, 10].
Все вышеописанные методы лечения нейротрофических поражений роговицы носят паллиативный или вспомогательный характер и не позволяют радикально устранить симптомы нейротрофического поражения роговицы. Единственным патогенетически обоснованным способом, позволяющим купировать патологический процесс при нейротрофическом поражении, обеспечивающий структурный рост нерва, нервную трофику роговицы и восстановление ее чувствительности является невротизация роговицы.
Невротизация роговицы- это хирургическая операция, направленная на восстановление функции поврежденного нерва за счет подшивания к периферическому концу поврежденного нерва одного из неповрежденных соседних нервов [11] методом прямой невротизации, либо переноса здорового сегмента донорского нерва в ткань для восстановления моторной или сенсорной иннервации [12] методом непрямой невротизации.
Способ невротизации роговицы в качестве современного хирургического способа лечения нейротрофической кератопатии у пациентов с параличом мимической мускулатуры впервые раскрыт в [13]. В ходе шести операций проводили коронарный разрез, выделяли надглазничный и надблоковый нервы на контралатеральной стороне, далее проводили их к глазу на пораженной стороне и подшивали перилимбально. Полученные данные показали, что данный способ прямого переноса конечных ветвей n. ophthalmicus (n .supraorbitalis и n. supratrochlearis) улучшал чувствительность ранее анестезированных роговиц в кратчайшие сроки (а именно через 3-6 месяцев после операции) и создавал условия для улучшения состояния роговицы и восстановления зрительных функций.
Известен способ восстановления трофики роговицы глаза при нейротрофической кератопатии, вследствие частичного или полного повреждения тройничного нерва, заключающийся в следующем. Проводят коронарный разрез, рассекая кожу и подкожно-жировую клетчатку по намеченной линии в височно-теменных областях от одной до другой ушной раковины до надкостницы. Височно-теменной лоскут отделяют от надкостницы, доходя до поверхностных пластинок височных фасций и откидывают в лицевую сторону. Надкостницу рассекают, отступив от верхнеорбитальных краев на 8-11 см. Далее с двух сторон отслаивают надкостницу от лобной кости до верхнеорбитальных краев и костной пирамиды носа. На здоровой стороне высвобождают надглазничный и надблоковый нервы из мест выходов из глазницы. Из височно-теменного лоскута выделяют 4-8 ветвей надглазничного и/или надблокового нервов. В височно-теменном лоскуте формируют тоннель на пораженной стороне от надкостницы верхне-медиального края глазницы до верхне-конъюнктивального свода верхнего века, далее в местах разрезов конъюнктивы и теноновой капсулы вокруг лимба роговицы в склере формируют корнеосклеральные тоннели, проводя 3-5 перилимбальных разреза склеры шириной 2-4 мм на 1/2-1/3 ее толщины с последующим расслаиванием тканей склеры и роговицы по направлению от лимба к центру роговицы на 1-2 мм, и фиксацией фасцикул надглазничного и/или надблокового нервов в сформированных корнеосклеральных тоннелях. Далее височно-теменной лоскут укладывают на место [14].
Недостатком данного прямого способа невротизации роговицы является то, что зона восстановления чувствительной иннервации ограничивается роговицей глаза.
Наиболее ближайшим к заявляемому способу - прототипом, является способ восстановления трофики роговицы глаза при нейротрофической кератопатии, заключающийся в следующем. Проводят коронарный разрез, височно-теменной лоскут отделяют от надкостницы, доходя до поверхностных пластинок височных фасций и откидывают в лицевую сторону. Надкостницу рассекают, отступив от верхнеорбитальных краев на 8-11 см. Далее с двух сторон отслаивают надкостницу от лобной кости до верхнеорбитальных краев и костной пирамиды носа и откидывают вместе с височно-теменным лоскутом в лицевую сторону. На здоровой стороне визуализируют места выходов надглазничного и/или надблокового нервов из глазницы и их высвобождают. На здоровой стороне из височно-теменного лоскута выделяют 4-8 ветвей надглазничного и/или надблокового нервов. Далее дистальный конец одной из ветвей надглазничного или надблокового нервов со здоровой стороны сшивают с большей частью надглазничного нерва на пораженной стороне в месте его выхода из глазницы «конец-в-бок». Далее на пораженной стороне в откинутом височно-теменном лоскуте формируют тоннель от верхнего конъюнктивального свода верхнего века до надкостницы верхнемедиального края глазницы. Ветви надглазничного и/или надблокового нервов здоровой стороны проводят от надкостницы верхнемедиального края глазницы до верхнего конъюнктивального свода верхнего века пораженной стороны. Височно-теменной лоскут укладывают на место. На пораженной стороне вокруг лимба роговицы формируют тоннели для проведения ветвей надглазничного и/или надблокового нервов здоровой стороны. Выполняют 3-5 перилимбальных разрезов конъюнктивы и теноновой капсулы вокруг лимба роговицы, отступив от него 2-4 мм. Далее формируют тоннели в эписклеральном пространстве, соединяя разрезы между собой. Далее вокруг лимба роговицы в склере формируют корнеосклеральные тоннели в местах разрезов конъюнктивы и теноновой капсулы. Параллельно лимбу роговицы проводят 3-5 разрезов склеры шириной 2-4 мм в слое 1/3-1/2 ее толщины. Ткани склеры и роговицы расслаивают по направлению от лимба к центру роговицы на 1-2 мм. Далее от ранее сформированного тоннеля в височно-теменном лоскуте, заканчивающегося в верхнем конъюнктивальном своде верхнего века пораженной стороны, методом тупой и острой диссекции формируют тоннель под теноновой капсулой и конъюнктивой к ближайшему перилимбальному разрезу конъюнктивы. Ветви надглазничного и/или надблокового нервов проводят в сформированных тоннелях в височно-теменном лоскуте и в эписклеральном пространстве, разделяют на фасцикулы и фиксируют в сформированных корнеосклеральных тоннелях [15].
Недостатками известного способа являются травматичность доступа и диссекции. Относительным недостатком прямой невротизации роговицы является техническая сложность, связанная с обеспечением широкого доступа к донорским нервам, а также с прецизионным выделением их отдельных ветвей на значительном протяжении (от 8 до 10-12 см). Это требует дополнительного времени (от 3 до 4 ч), а также участия высококвалифицированной междисциплинарной хирургической бригады, включающей челюстно-лицевого хирурга, микрохирурга и офтальмохирурга.
Задачей изобретения является уменьшение травматичности способа, сокращение длительности операции и реабилитационного периода.
Технический результат: уменьшение травматичности операции, сокращение длительности операции и реабилитационного периода, ускорение заживление ран, более точное подведение нервных фасцикулов к роговице.
Предлагаемый способ заключается в следующем
Согласно предварительной разметке, через несколько разрезов на голени, выполняют забор аутонейротрансплантата сурального (икроножного) нерва длиной не более 30 см, раны на голени ушивают. Затем выполняют подбровный разрез на здоровой (непарализованной) стороне, выделяют надглазничный нерв, рассекают связку надглазничной вырезки для мобилизации нерва. На стороне повреждения выполняют аналогичный подбровный доступ и соединяют доступы, формируя подкожный тоннель. Трансплантат сурального нерва проводят в подкожном тоннеле. На здоровой стороне в условиях увеличения с помощью микроскопа, с использованием микрохирургических ножниц, выполняют эпиневральное окно в надглазничном нерве и производят эпиневральный шов сурального аутонейротрансплантата с надглазничным нервом по типу «конец-в-бок» узловыми швами нитью нейлон 9/0. Далее выполняют разрез в конъюнктивальном мешке и конец сурального аутонейротрансплантата проводят в конъюнктивальный мешок. Конъюнктиву и тенонову оболочку отсепаровывают вкруговую по лимбу. Конец сурального нерва заводят под конъюнктиву через разрез с латеральной стороны и разъединяют на 4 фасцикулы. Хирургическим расслаивателем формируют корнеосклеральные каналы в четырех секторах на 3, 6, 9, 12 часах. Фасцикулы погружают в каналы хирургическим шпателем, края корнеосклеральных каналов фиксируют нитью шелк 8/0. Конюънктиву ушивают поверх нерва отдельными узловыми швами нитью шелк 8/0. Субконъюнктивальное введение 4 мг дексаметазона. Блефарорафия нитью пролен 6/0. Накладывают асептическую повязку.
Определяющими отличиями предлагаемого способа от прототипа являются:
1). Невротизацию роговицы осуществляют через трансплантат сурального нерва, забор которого проводят через несколько разрезов на голени, а затем один конец подключают к нерву донору, а другой к роговице, что позволяет снизить травматичность способа (при прямой невротизации роговицы проводят коронарный разрез, височно-теменной лоскут отделяют от надкостницы, доходя до поверхностных пластинок височных фасций и откидывают в лицевую сторону).
2) Выполняют подбровный разрез на непарализованной стороне, выделяют надглазничный нерв, рассекают связку надглазничной вырезки для мобилизации нерва, на стороне повреждения выполняют аналогичный подбровный доступ и соединяют доступы, формируя подкожный тоннель, что позволяет уменьшить травматичность способа за счет менее травматичного доступа и ускорить заживление ран (при прямом методе невротизации роговицы проводят коронарный разрез).
3) Трансплантат сурального нерва проводят в подкожном тоннеле, затем на здоровой стороне выполняют эпиневральное окно в надглазничном нерве и производят эпиневральный шов сурального нерва с надглазничным нервом по типу конец-в-бок, что позволяет сократить длительность операции и реабилитационного периода.
4) Конец сурального нерва заводят под конъюнктиву через разрез с латеральной стороны, разъединяют на 4 фасцикулы, которые погружают и фиксируют к сформированным корнеосклеральным каналам на 3, 6, 9 и 12 часах, что обеспечивает более точное подведение нервных фасцикулов к роговице.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1.
Больной А., 39 лет обратился АНО «НИИ микрохирургии» с диагнозом: нейротрофический кератит. Из анамнеза известно, что в июне 2021 г - удаление опухоли мостомозжечкового угла с развитием моментального лицевого паралича и постепенным развитием нейротрофического кератита. Консервативное лечение кератита. Эпизоды тарзоррафии. Декабрь 2021 г - коррекция лагофтальма.
При осмотре максимально корригируемая острота зрения правого глаза составила Pr/certa, дефектов полей зрения при кинетической периметрии выявлено не было, прозопарез мягких тканей правой половины лица, ретракция верхнего и нижнего века, положительный симптом Белла, выраженная гиперемия конъюнктивы, незначительное количество слизистого отделяемого, отек эпителия роговицы и стромальное помутнение. По данным эстезиометрии правого глаза в пяти секторах чувствительность роговицы отсутствовала.
Пациенту проведена реиннервация роговицы заявляемым способом.
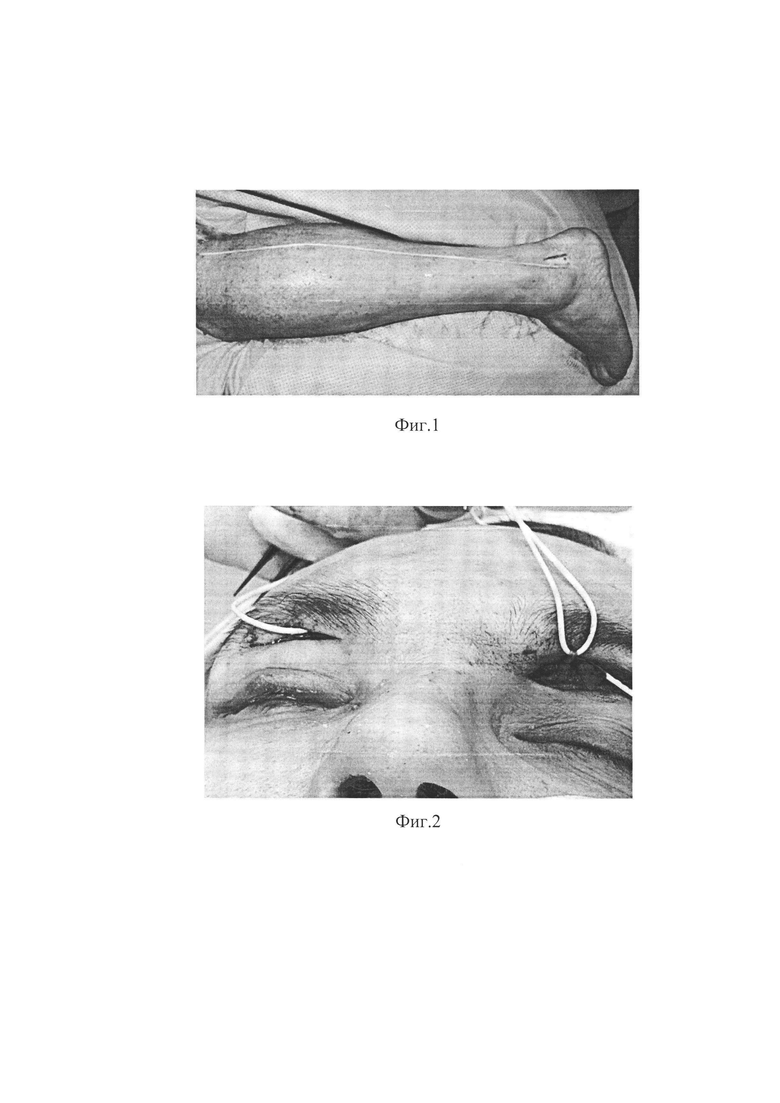
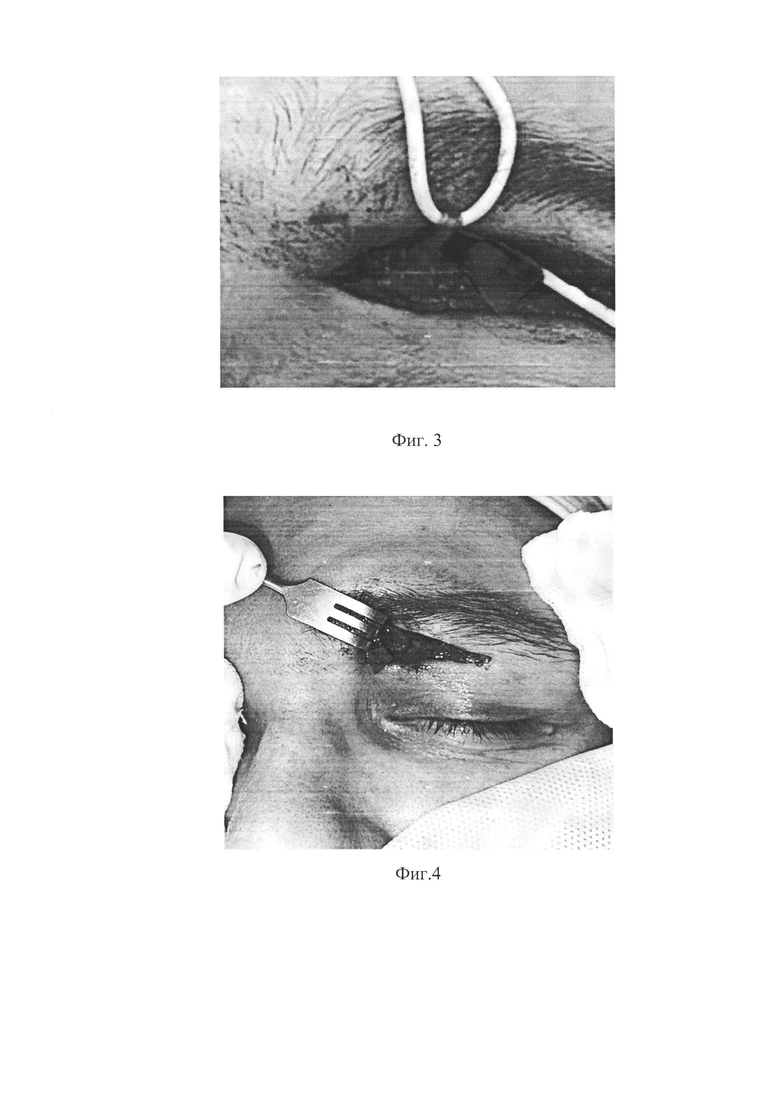
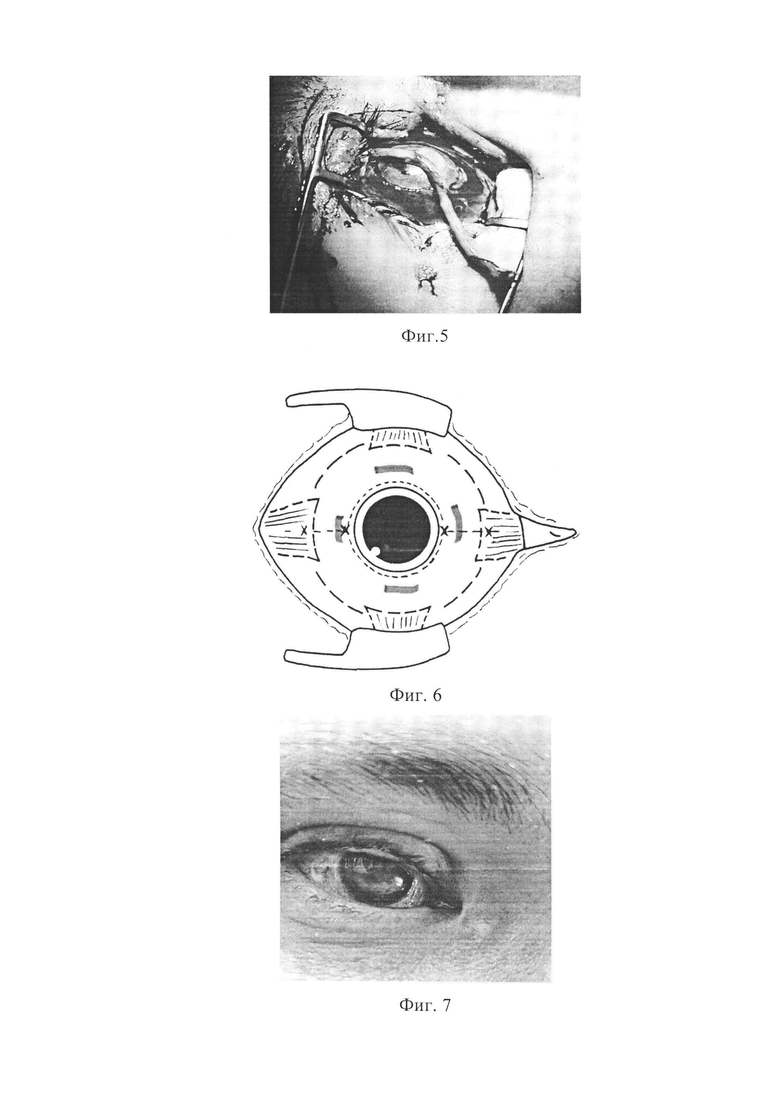
Согласно предварительной разметке через несколько разрезов на голени выполнен забор аутонейротрансплантата сурального нерва длиной 30 см, раны на голени ушиты (фиг. 1). Затем выполнен подбровный разрез на здоровой (непарализованной) стороне, выделен надглазничный нерв, рассечена связка надглазничной вырезки для мобилизации нерва (фиг. 2). На стороне повреждения выполнен аналогичный подбровный доступ и соеденены доступы, формируя подкожный тоннель. Трансплантат сурального нерва проведен в подкожном тоннеле (фиг. 3). На здоровой стороне в условиях увеличения с помощью микроскопа с использованием микрохирургических ножниц выполнено эпиневральное окно в надглазничном нерве и произведен эпиневральный шов сурального аутонейротрансплантата с надглазничным нервом по типу конец-в-бок узловыми швами нитью нейлон 9/0 (фиг. 4). Далее выполнен разрез в конъюнктивальном мешке и конец сурального аутонейротрансплантата проведен в конъюнктивальный мешок (фиг. 5). Конъюнктива и тенонова оболочка отсепарованы вкруговую по лимбу. Конец сурального нерва заведен под конъюнктиву через разрез с латеральной стороны и разъединен на 4 фасцикулы. Хирургическим расслаивателем сформированы корнеосклеральные каналы на 3, 6, 9, 12 часах (фиг. 6). Фасцикулы погружены в каналы хирургическим шпателем, края корнеосклеральных каналов фиксированы нитью шелк 8/0. Конъюнктива ушита поверх нерва отдельными узловыми швами нитью шелк 8/0. Субконъюнктивальное введение 4 мг дексаметазона. Блефарорафия нитью пролен 6/0. Наложена асептическая повязка.
Послеоперационные результаты операции через 6 месяцев (фиг. 7): Визометрия: 0.05 н.к. При биомикроскопии прослеживается ход нервных волокон в направлении лимба. Определение чувствительности роговицы в 5 секторах: в 3-х секторах результат положительный.
Через 2 месяца после операции у пациента отмечено восстановление чувствительности во всех пяти секторах роговицы (в верхненаружном и верхневнутреннем - 5, в нижненаружном, нижневнутреннем и центральном - 4 по шкале эстезиометра Cochet & Bonnet)
Пример 2.
Больная X., обратилась АНО «НИИ микрохирургии» с диагнозом: нейротрофический кератит. Госпитализирована с жалобами на сухость глаза, отсутствие чувствительности глазного яблока, нарушение зрения, помутнение роговицы. Симптомы появились внезапно после удаления опухоли мостомозжечкового угла в 2016 г. Неоднократно проходила курсы консервативного лечения у офтальмолога, эпизоды тарзоррафии, без эффекта. Локальный статус: Глаз спокоен. Умеренная перикорнеальная инъекция. Роговица: стромальное помутнение в центре с неоваскуляризацией. П/к нормальной глубины. Влага прозрачная. Зрачок круглый, реакция на свет живая. Остальные структуры глаза не визуализируются (под флером) из-за состояния роговицы.
По данным эстезиометрии правого глаза в пяти секторах чувствительность роговицы отсутствовала.
Больной проведена реиннервация роговицы заявляемым способом аналогично примеру 1, за исключением того, что выполнен забор аутонейротрансплантата сурального нерва длиной 27 см.
Послеоперационные результаты операции через 6 месяцев: При биомикроскопии прослеживается ход нервных волокон в направлении лимба. По данным эстезиометрии правого глаза в пяти секторах чувствительность роговицы восстановлена.
Предлагаемый способ позволяет уменьшить травматичность, сократить длительность операции и реабилитационного периода, а также восстанавливать чувствительность роговицы глаза у пациентов с нейротрофическим кератитом при повреждении тройничного нерва.
Источники информации
1. Allevi F, Fogagnolo P, Rossetti L, Biglioli F. Eyelid reanimation, neurotisation, and transplantation of the cornea in a patient with facial palsy. BMJ Case Rep.2014; 2014:1-3. https://doi.Org/10.1136/bcr-2014-205372
2. Груша Я.О., Федоров A.A., Фетцер Е.И. Паралитический лагофтальм. М.: ГЭОТАР-Медиа; 2019. Grusha YO, Fedorov АА, Fettser EI. Paraliticheskii lagoftal'm. Moscow: GEOTAR-Media; 2019. (In Russ.).
3. Bains RD, Elbaz U, Zuker RM. Corneal neurotization from the supratrochlear nerve with sural nerve grafts: a minimally invasive approach. Plast. Reconstr. Surg. 2015;135: 397e-400. https://doi.org/10.1097/PRS.0000000000000994
4. Lambiase A, Manni L, Bonini S, Rama P, Micera A, Aloe L. Nerve growth factor promotes corneal healing: structural, biochemical, and molecular analyses of rat and human corneas. Invest Ophthalmol. Vis Sci. 2000; 41:1063-1069.
5. Tan M, Bryars J, Moore J. Use of nerve growth factor to treat congenital neurotrophic corneal ulceration. Cornea. 2006; 25:352-355. https://doi.org/10.1097/01.ico.0000176609.42838.df
6. You L, Kruse FE, 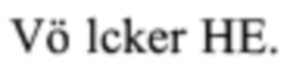 Neurotrophic factors in the human cornea. Invest Ophthalmol. Vis. Sci. 2000; 41:692-702.
Neurotrophic factors in the human cornea. Invest Ophthalmol. Vis. Sci. 2000; 41:692-702.
7. Каспарова E.A., Каспаров A.A., Собкова О.И., Каспарова Е.А., Розинова В.Н. Способ лечения гнойной язвы роговицы, развившейся на глазах с нейротрофическим кератитом и лагофтальмом. Вестник офтальмологии. 2019; 135(5 ч. 2):220-225. https://doi.org/10.17116/oftalma2019135052220
8. Каспарова Е.А., Марченко Н.Р. Нейротрофический кератит.Этиология, патогенез, клинические проявления. Обзор литературы. Часть 1. Офтальмология. 2022; 19(1):38-45. https://doi.org/10.18008/1816-5095-2022-1-38-45)
9. Комарова М.Г., Клюваева Т.Ю. Коррекция лагофтальма после эстетической блефаропластики мягкими контактными линзами. Вестник офтальмологии. 2006; 122(2):33-35.
10. Новиков С.А. Контактная линза как пролонгированная глазная лекарственная форма. Глаз. 2001; (4):6-18.
11. Большой медицинский энциклопедический словарь. Аветисов С.Э. и др. Под ред. Бородулина В.И. Изд. 4-е, испр. и доп. М.: РИПОЛ классик; 2007.
12. Malhotra R, Elalfy MS, Kannan R, Nduka C, Hamada S. Update on corneal neurotisation. Brit. J. Ophthalmol. 2018;103(l):26-35. https://doi.org/bjophthalmol-2018-312104
13. Terzis JK, Dryer MM, Bodner BI. Corneal neurotization: a novel solution to neurotrophic keratopathy. Plast. Reconstr. Surg. 2009; 123(1):112-120. https://doi.org/10.1097/PRS.0b01e3181904d3a
14. Патент RU 2722998 C1, опубл. 05.06.2020.
15. Патент RU 2803270 C1, опубл. 11.09.2023.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ восстановления трофики роговицы глаза при нейротрофической кератопатии | 2019 |
|
RU2722998C1 |
| Способ восстановления трофики роговицы глаза и чувствительности кожи в зоне иннервации первой ветви тройничного нерва при нейротрофической кератопатии | 2022 |
|
RU2803270C1 |
| СПОСОБ ПРОВЕДЕНИЯ МИКРОИНВАЗИВНОЙ НЕПРОНИКАЮЩЕЙ ГЛУБОКОЙ СКЛЕРЭКТОМИИ | 2013 |
|
RU2530760C1 |
| Способ поднадкостничной подтяжки лба через верхний блефаропластический доступ | 2024 |
|
RU2831640C1 |
| Способ фронто-темпорального лифтинга | 2023 |
|
RU2809695C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ | 1997 |
|
RU2143873C1 |
| СПОСОБ ФОРМИРОВАНИЯ ОПОРНО-ДВИГАТЕЛЬНОЙ КУЛЬТИ ПРИ ЭВИСЦЕРАЦИИ И ПРОТЕЗИРОВАНИЯ ГЛАЗА | 2003 |
|
RU2236205C1 |
| Способ микроинвазивной непроникающей глубокой склерэктомии при открытоугольной глаукоме | 2015 |
|
RU2613439C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФРАКТОРНОЙ ГЛАУКОМЫ | 2008 |
|
RU2385694C1 |
| СПОСОБ МИКРОИНВАЗИВНОЙ НЕПРОНИКАЮЩЕЙ ГЛУБОКОЙ СКЛЕРЭКТОМИИ ПРИ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЕ | 2014 |
|
RU2554231C1 |
Изобретение относится к медицине, а именно к челюстно-лицевой хирургии и офтальмологии. Выделяют надглазничный нерв, осуществляют подшивание к нему донорского нерва, проводят последний нерв к роговице на пораженной стороне и его подшивают. В качестве донорского нерва используют аутонейротрансплантат сурального нерва с длиной не более 30 см. Выполняют подбровные разрезы на здоровой и парализованной стороне лица, выделяют надглазничный нерв на здоровой стороне. Соединяют подбровные разрезы, формируя подкожный тоннель, суральный нерв проводят в подкожном тоннеле. Далее на здоровой стороне выполняют эпиневральное окно в надглазничном нерве и производят эпиневральный шов сурального нерва с надглазничным нервом по типу конец-в-бок. Затем конъюнктиву и тенонову оболочку отсепаровывают вкруговую по лимбу, конец сурального нерва заводят под конъюнктиву через разрез с латеральной стороны, разъединяют на 4 фасцикулы, которые погружают в сформированные корнеосклеральные каналы на 3, 6, 9 и 12 часах, а края корнеосклеральных каналов фиксируют узловыми швами. В частном случае суральный нерв сшивают с надглазничным нервом узловыми швами нитью нейлон 9/0. Края корнеосклеральных каналов фиксируют нитью шелк 8/0. Конъюнктиву ушивают поверх сурального нерва отдельными узловыми швами нитью шелк 8/0. Способ позволяет уменьшить травматичность операции, сократить длительность операции и реабилитационный период, ускорить заживление ран, осуществить более точное подведение нервных фасцикулов к роговице. 3 з.п. ф-лы, 2 пр., 7 ил.
1. Способ восстановления трофики роговицы глаза при нейротрофической кератопатии путем непрямой невротизации, включающий выделение надглазничного нерва, подшивание к нему донорского нерва, проведение последнего нерва к роговице на пораженной стороне и его подшивание, отличающийся тем, что в качестве донорского нерва используют аутонейротрансплантат сурального нерва с длиной не более 30 см, выполняют подбровные разрезы на здоровой и парализованной стороне лица, выделяют надглазничный нерв на здоровой стороне, соединяют подбровные разрезы, формируя подкожный тоннель, суральный нерв проводят в подкожном тоннеле, далее на здоровой стороне выполняют эпиневральное окно в надглазничном нерве и производят эпиневральный шов сурального нерва с надглазничным нервом по типу конец-в-бок, затем конъюнктиву и тенонову оболочку отсепаровывают вкруговую по лимбу, конец сурального нерва заводят под конъюнктиву через разрез с латеральной стороны, разъединяют на 4 фасцикулы, которые погружают в сформированные корнеосклеральные каналы на 3, 6, 9 и 12 часах, а края корнеосклеральных каналов фиксируют узловыми швами.
2. Способ по п. 1, отличающийся тем, что суральный нерв сшивают с надглазничным нервом узловыми швами нитью нейлон 9/0.
3. Способ по п. 1, отличающийся тем, что края корнеосклеральных каналов фиксируют нитью шелк 8/0.
4. Способ по п. 1, отличающийся тем, что конъюнктиву ушивают поверх сурального нерва отдельными узловыми швами нитью шелк 8/0.
| Способ восстановления трофики роговицы глаза и чувствительности кожи в зоне иннервации первой ветви тройничного нерва при нейротрофической кератопатии | 2022 |
|
RU2803270C1 |
| Способ восстановления трофики роговицы глаза при нейротрофической кератопатии | 2019 |
|
RU2722998C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТРОФИЧЕСКИХ ЯЗВ РОГОВИЦЫ И ПРОГРЕССИРУЮЩИХ КЕРАТИТОВ | 2012 |
|
RU2486879C1 |
| Байтингер В.Ф., Ежов А.А | |||
| Микрохирургия нейротрофических расстройств в мягких тканях таза и нижних конечностей | |||
| Вопросы реконструктивной и пластической хирургии | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Sarkar S., et al | |||
| Corneal Regeneration Using Gene Therapy Approaches | |||
| Cells | |||
Авторы
Даты
2024-07-29—Публикация
2024-02-19—Подача