Область техники настоящего изобретения
Различные варианты осуществления настоящего изобретения относятся к новому пептидному соединению или его фармацевтически приемлемой соли. В частности, различные варианты осуществления настоящего изобретения относятся к новому пептидному соединению или его фармацевтически приемлемой соли, имеющим противовоспалительную активность.
Уровень техники настоящего изобретения
В последнее время доля пожилых людей продолжает возрастать из-за развития медицинских технологий и увеличения продолжительности жизни в соответствии с экономическим развитием, а хронические воспалительные заболевания, такие как атопия и астма, увеличиваются, поскольку воспалительная реакция становится хронической из-за системной аномалии иммунной системы в связи с увеличением загрязнения окружающей среды и стресса.
В общем, воспалительная реакция представляет собой защитный механизм живой ткани от внешних раздражителей, таких как бактериальная инфекция, или внутренних раздражителей, таких как метаболиты in vivo, и возникает, когда продуцируются оксид азота (NO) и различные цитокины, такие как TNF-α, IL-1β и IL-6, которые являются различными регуляторами воспаления в клетках. Кроме того, липополисахарид (LPS), также известный как эндотоксин, присутствует в наружной клеточной мембране грамотрицательных бактерий и индуцирует активацию NF-κB (ядерный фактор-κB), внутриклеточного фактора транскрипции, в макрофагах или мононуклеарных клетках, тем самым индуцируя экспрессию генов воспалительных цитокинов, iNOS (индуцируемая синтаза оксида азота) и COX-2 (циклооксигеназа-2), и продуцируя медиаторы воспаления.
Следовательно, для регуляции воспалительной реакции ключевым фактором является регуляция экспрессии iNOS, COX-2 или NF-κB, а также секреция цитокинов и оксида азота, а вещества, регулирующие активность этих факторов, привлекают внимание как профилактические и лечебные средства при воспалительных заболеваниях.
Вещества, используемые в настоящее время для противовоспалительных целей, включают нестероиды, такие как флуфенамовая кислота, ибупрофен, бензидамин, индометацин и т.п.; и стероиды, такие как преднизолон, дексаметазон, гидрокортизон, бетаметазон и т.п. Однако эти вещества очень токсичны и вызывают несколько серьезных побочных эффектов, таких как повреждение печени, рак и инсульт, что ограничивает их использование. Кроме того, бывают случаи, когда возникает проблема индуцирования тяжелой иммуносупрессии, поскольку они не могут избирательно воздействовать на вещества, вызывающие воспаление. Соответственно, ведется разработка средства для лечения воспаления с использованием природного продукта, который безопасен для организма и имеет то преимущество, что его легко принимать в течение длительного периода времени по сравнению с обычными лекарственными средствами. Однако в случае противовоспалительного вещества, извлеченного из природного продукта, существуют проблемы, связанные со слабой эффективной концентрацией, при которой вещество проявляет эффективность, и требуются высокие производственные затраты, поскольку его необходимо выращивать на сельскохозяйственных угодьях и т. д.
Чтобы решить вышеуказанные проблемы, разрабатывается новая концепция противовоспалительного средства в качестве альтернативы существующему химическому средству для лечения воспаления или средству для лечения воспаления с использованием природного продукта, и, в частности, проводится много исследований по синтезу пептидов, обладающих противовоспалительной активностью.
Соответственно, авторы настоящего изобретения разработали пептид, который можно экономично производить в массовом масштабе, используя только 9 аминокислотных остатков, продолжая исследования веществ, проявляющих превосходную противовоспалительную активность, и обнаружили, что пептид не проявляет цитотоксичности и обладает превосходной противовоспалительной активностью. На основании вышеизложенного авторы настоящего изобретения завершили настоящее изобретение.
Подробное описание настоящего изобретения
Техническая задача
Различные варианты осуществления настоящего изобретения относятся к новому пептидному соединению или его фармацевтически приемлемой соли.
Решение задачи
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 1 ниже.
[Формула 1]
A1-A2-A3-A4-A5
в формуле 1, A1 - A5 связаны пептидной связью, представленной формулой 2 ниже,
A1 представляет собой замещенный или незамещенный пролин или глутамин,
A2 представляет собой замещенный или незамещенный глицин или аспарагиновую кислоту,
A3 представляет собой замещенный или незамещенный глутамин или глицин,
A4 представляет собой замещенную или незамещенную аспарагиновую кислоту или лейцин,
A5 представляет собой замещенный или незамещенный глицин или аланин, и
от нуля до двух из A1 - A5 могут быть независимо замещены одним заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина.
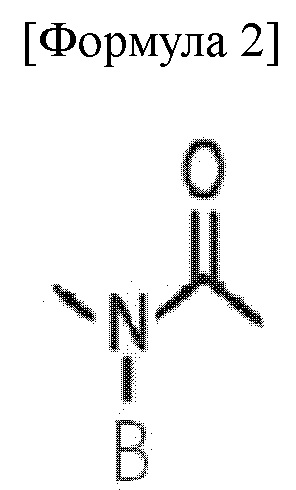
где B представляет собой водород или связан с по меньшей мере любым одним из A1 - A5, подлежащим циклизации.
Эффекты настоящего изобретения
Настоящее изобретение относится к новым пептидным соединениям, имеющим различные структуры, или их фармацевтически приемлемым солям, которые можно применять в различных областях.
Поскольку новое пептидное соединение или его фармацевтически приемлемая соль согласно настоящему изобретению имеет только от 5 до 8 аминокислотных остатков, возможно экономичное массовое производство. Кроме того, он не проявляет цитотоксичности, обладает отличной стабильностью и проявляет отличную противовоспалительную активность.
Краткое описание чертежей
Фиг. 1a, 1b и 1c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 10 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 2a, 2b и 2c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 32 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 3a, 3b и 3c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 41 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 4a, 4b и 4c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 55 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 5a, 5b и 5c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 59 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 6a, 6b и 6c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 91 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 7a, 7b и 7c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 30 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 8a, 8b и 8c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 11 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 9a, 9b и 9c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 86 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 10a, 10b и 10c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 103 в LPS-стимулирующих макрофагах, соответственно.
Фиг. 11a, 11b и 11c показывают результаты измерения уровней экспрессии IL-1β, IL-6 и TNFα в соответствии с лечением согласно Примеру 104 в LPS-стимулирующих макрофагах, соответственно.
Наилучший образ осуществления настоящего изобретения
Далее различные варианты осуществления настоящего изобретения описаны со ссылкой на прилагаемые чертежи. Варианты осуществления и термины, используемые в настоящем документе, не предназначены для ограничения технологии, описанной в настоящем документе, конкретными вариантами осуществления, и их следует понимать как включающие различные модификации, эквиваленты и/или замены вариантов осуществления.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 1 ниже.
[Формула 1]
A1-A2-A3-A4-A5
в формуле 1, A1 - A5 связаны пептидной связью, представленной формулой 2 ниже,
A1 представляет собой замещенный или незамещенный пролин или глутамин,
A2 представляет собой замещенный или незамещенный глицин или аспарагиновую кислоту,
A3 представляет собой замещенный или незамещенный глутамин или глицин,
A4 представляет собой замещенную или незамещенную аспарагиновую кислоту или лейцин,
A5 представляет собой замещенный или незамещенный глицин или аланин, и
от нуля до двух из A1 - A5 могут быть независимо замещены одним заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина.

где B представляет собой водород или связан с по меньшей мере любым одним из A1 - A5, подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 3 ниже.
[Формула 3]
A1-A2-A3-A4-A5-A6
в формуле 3, A1 - A6 связаны пептидной связью, представленной формулой 2 ниже,
A1 представляет собой замещенный или незамещенный пролин или глутамин,
A2 представляет собой замещенный или незамещенный глицин или аспарагиновую кислоту,
A3 представляет собой замещенный или незамещенный глутамин или глицин,
A4 представляет собой замещенную или незамещенную аспарагиновую кислоту или лейцин,
A5 представляет собой замещенный или незамещенный глицин или аланин,
A6 представляет собой замещенный или незамещенный лейцин или глицин, и
от нуля до двух из A1 - A6 могут быть независимо замещены одним заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина.

где B представляет собой водород или связан с по меньшей мере любым одним из A1 - A6, подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 4 ниже.
[Формула 4]
A1-A2-A3-A4-A5-A6-A7
в формуле 4, A1 - A7 связаны пептидной связью, представленной формулой 2 ниже,
A1 представляет собой замещенный или незамещенный пролин или глутамин,
A2 представляет собой замещенный или незамещенный глицин или аспарагиновую кислоту,
A3 представляет собой замещенный или незамещенный глутамин или глицин,
A4 представляет собой замещенную или незамещенную аспарагиновую кислоту или лейцин,
A5 представляет собой замещенный или незамещенный глицин или аланин,
A6 представляет собой замещенный или незамещенный лейцин или глицин,
A7 представляет собой замещенный или незамещенный аланин или пролин, и
от нуля до трех из A1 - A7 могут быть независимо замещены одним заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина.

где B представляет собой водород или связан с по меньшей мере любым одним из A1 - A7 подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 5 ниже.
[Формула 5]
A1-A2-A3-A4-A5-A6-A7-A8
в формуле 5, A1 - A8 связаны пептидной связью, представленной формулой 2 ниже,
A1 представляет собой замещенный или незамещенный пролин или глутамин,
A2 представляет собой замещенный или незамещенный глицин или аспарагиновую кислоту,
A3 представляет собой замещенный или незамещенный глутамин или глицин,
A4 представляет собой замещенную или незамещенную аспарагиновую кислоту или лейцин,
A5 представляет собой замещенный или незамещенный глицин или аланин,
A6 представляет собой замещенный или незамещенный лейцин или глицин,
A7 представляет собой замещенный или незамещенный аланин или пролин,
A8 представляет собой замещенный или незамещенный глицин или лизин, и
от нуля до трех из A1 - A8 могут быть независимо замещены одним заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина.

где B представляет собой водород или связан с по меньшей мере любым одним из A1 - A8 подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 6 ниже.
[Формула 6]

где R1 и R2 каждый независимо друг от друга представляет собой водород, замещенный или незамещенный C1-6алкил, -X2, -Rb, -O-, =O, -CH2Orb, или -ORb, где X2 представляет собой галоген, и Rb представляет собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, или замещенный или незамещенный гетероцикл,
R3 - R7 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S,
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл, и
B представляет собой водород или связан с по меньшей мере любым одним из R5 - R6 подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 7 ниже.
[Формула 7]
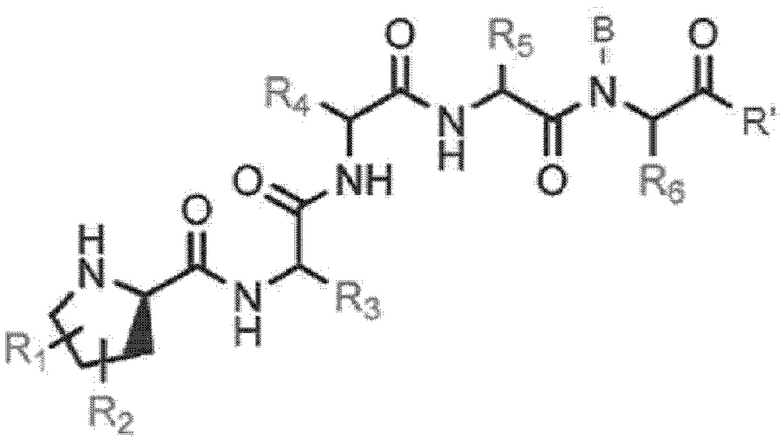
где R1 и R2 каждый независимо друг от друга представляет собой водород, замещенный или незамещенный C1-6алкил, -X2, -Rb, -O-, =O, -CH2Orb или -ORb, где X2 представляет собой галоген, и Rb представляет собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, или замещенный или незамещенный гетероцикл,
R3 - R6 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S,
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл,
B представляет собой водород или связан с по меньшей мере любым одним из R5 - R6 и R' подлежащим циклизации, и
R' представлен любой из формул 8 - 10 ниже.
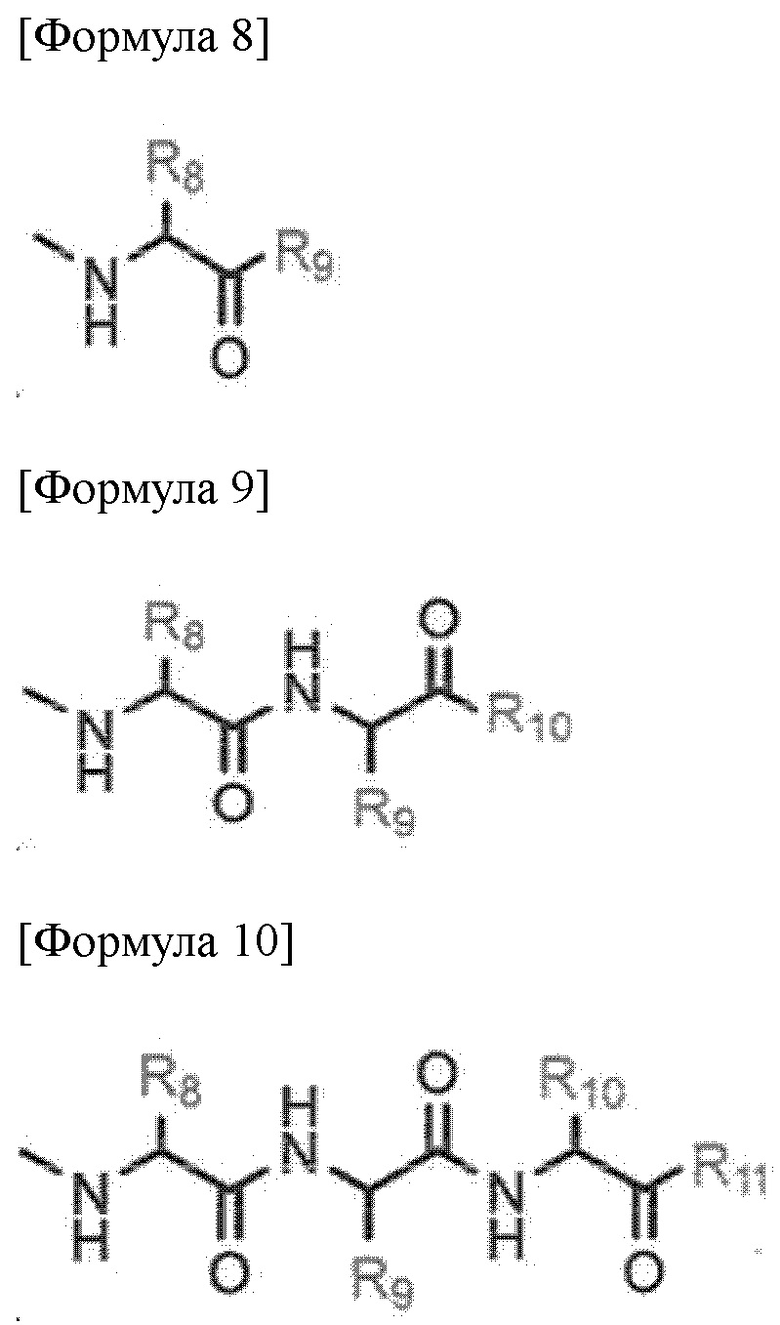
где R8 - R11 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S, и
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 11 ниже.
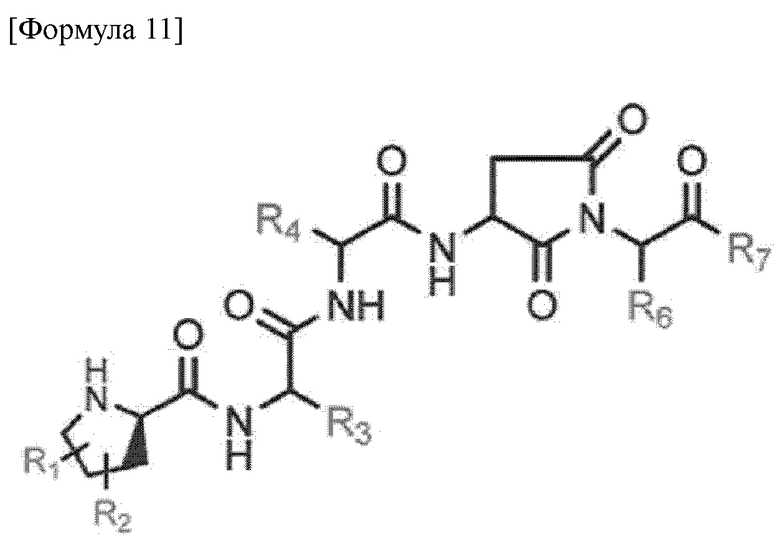
где R1 и R2 каждый независимо друг от друга представляет собой водород, замещенный или незамещенный C1-6алкил, -X2, -Rb, -O-, =O, -CH2Orb, или -ORb, где X2 представляет собой галоген, и Rb представляет собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, или замещенный или незамещенный гетероцикл,
R3 R4, R6 и R7 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S, и
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 12 ниже.
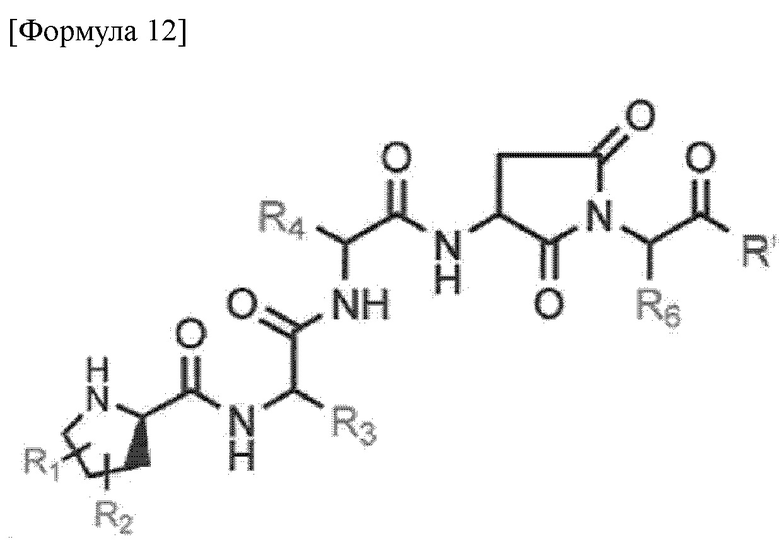
где R1 и R2 каждый независимо друг от друга представляет собой водород, замещенный или незамещенный C1-6алкил, -X2, -Rb, -O-, =O, -CH2Orb, или -ORb, где X2 представляет собой галоген, и Rb представляет собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, или замещенный или незамещенный гетероцикл,
R3, R4 и R6 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S,
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл, и
R' представлен любой из формул 13 - 15 ниже.

где R8 - R11 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S, и
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения имеет конфигурацию от 5-ти мерной до 8-ми мерной непрерывной или прерывающейся аминокислотной последовательности Hyp-Gly-Gln-Asp-Gly-Leu-Ala-Gly-Pro-Lys, где от 5-ти до 8-ми мерная последовательность является линейной, или по меньшей мере часть ее является циклизованной.
С другой стороны, пептид, по меньшей мере часть которого является циклизованной, может представлять собой пептид, содержащий Asu. В настоящем документе, Asu представляет собой апартимид или аминосукцинимид.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения имеет конфигурацию от 5-ти мерной до 8-ми мерной непрерывной или прерывающейся аминокислотной последовательности Hyp-Gly-Gln-Asp-Gly-Leu-Ala-Gly-Pro-Lys, где от 5-ти до 8-ми мерная последовательность является линейной, или по меньшей мере часть ее является циклизованной, и
имеет конфигурацию, в которой по меньшей мере любая одна из аминокислот замещена любым заместителем, выбранным из группы, состоящей из замещенного или незамещенного глицина, аланина, серина, треонина, цистеина, валина, лейцина, изолейцина, метионина, пролина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, аспарагина, глутамина, гистидина, лизина и аргинина, в конфигурации от 5-ти мера до 8-ми мера.
С другой стороны, пептид, по меньшей мере часть которого является циклизованной, может представлять собой пептид, содержащий Asu. В контексте настоящего изобретения Asu представляет собой апартимид или аминосукцинимид.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 16 ниже.
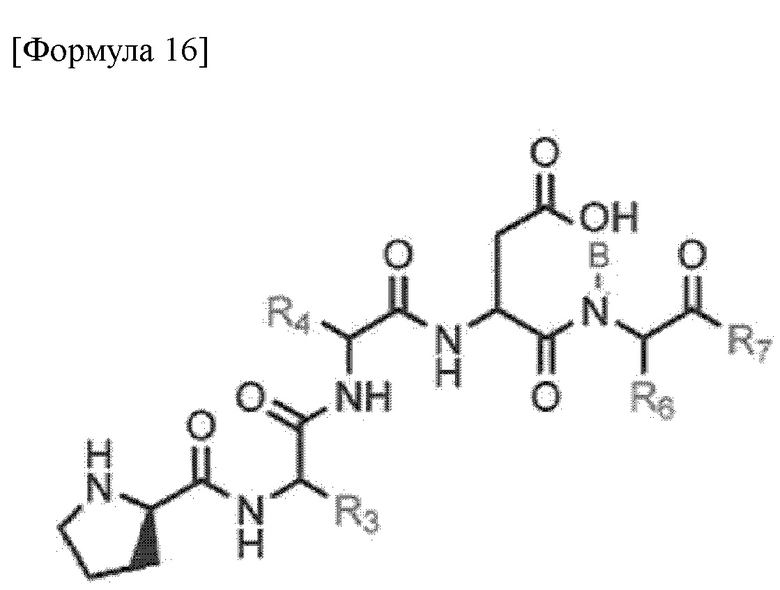
где R3, R4, R6 и R7 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S,
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл, и
B представляет собой водород или связан с по меньшей мере любым одним из аспарагиновая кислота и R6 подлежащим циклизации.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 17 ниже.
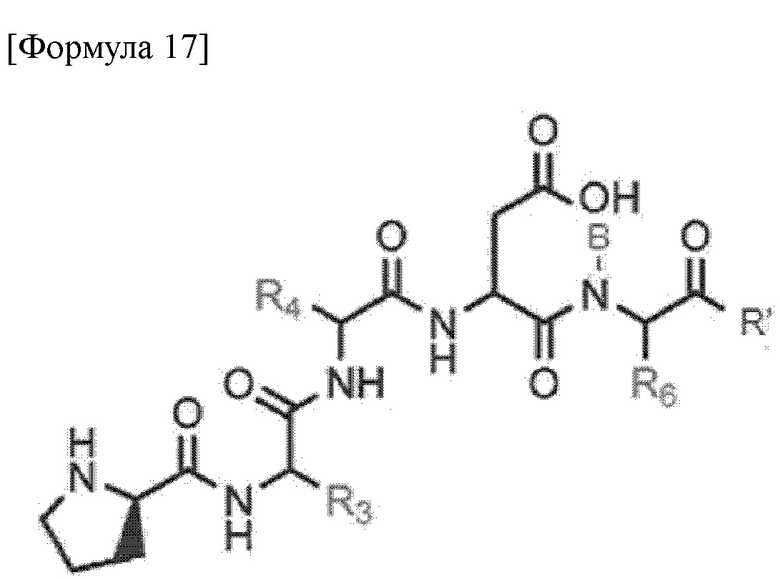
где R3, R4, и R6 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S,
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл,
B представляет собой водород или связан с по меньшей мере любым одним из аспарагиновая кислота и R6 подлежащим циклизации, и
R' представлен любой из формул 8 - 10 ниже.
[Формула 8]
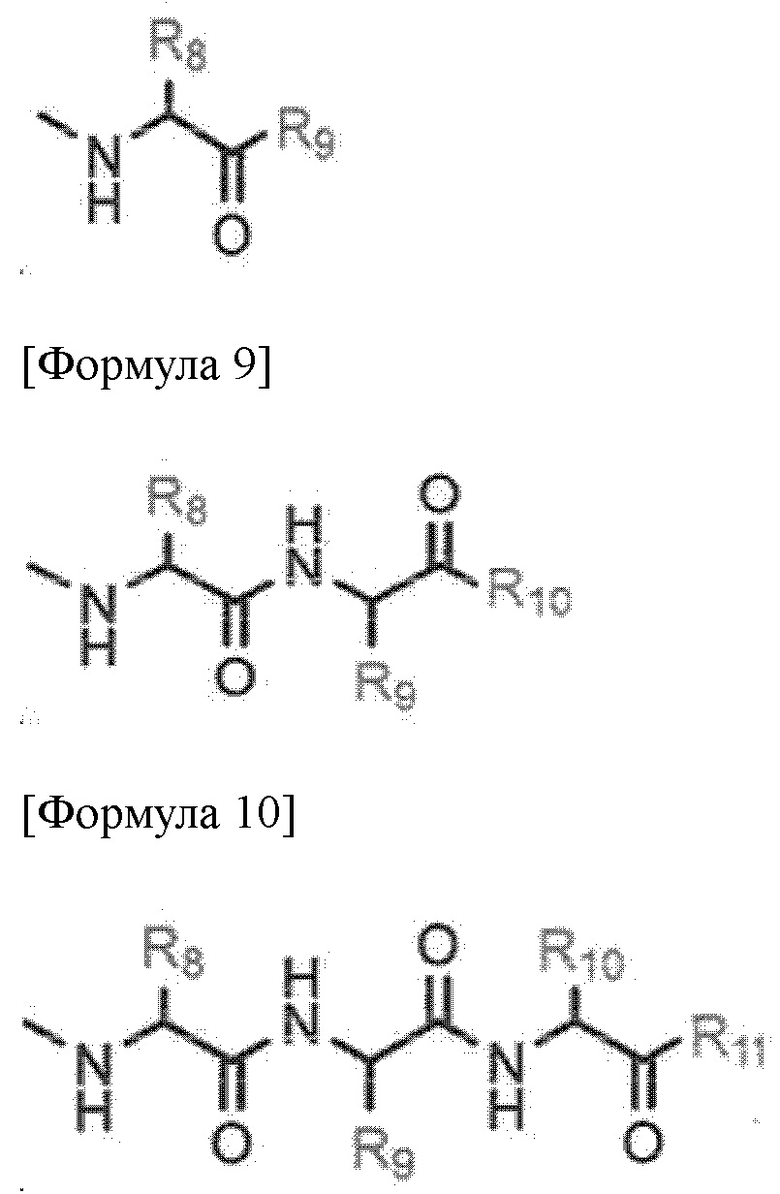
де R8 - R11 представляют собой водород, замещенный или незамещенный C1-6алкил, замещенный или незамещенный C1-10 алкокси, замещенный или незамещенный C1-10 галоалкил, замещенный или незамещенный C2-10 алкенил, замещенный или незамещенный C2-10 алкинил, замещенный или незамещенный C1-10 алкилен, замещенный или незамещенный C1-10 алкенилен, замещенный или незамещенный C1-10 алкинилен, замещенный или незамещенный C5-12 арил, замещенный или незамещенный C7-12 арилалкил, замещенный или незамещенный C5-14 арилалкинил, замещенный или незамещенный C8-16 арилалкенил, замещенный или незамещенный C3-10 гетероалкил, замещенный или незамещенный C3-10 циклоалкил, замещенный или незамещенный C3-10 гетероциклоалкил, или замещенный или незамещенный C5-12 гетероарил, где гетероалкил, гетероциклоалкил или гетероарил включает по меньшей мере один из N, O или S, и
замещение представляет собой замещение неводородным заместителем, где неводородным заместителем может быть один или несколько, выбранные из группы, состоящей из -RX, -Ra, -O-, =O, -ORa, -SRa, -S-, -N(Ra)2, -N+(Ra)3, =NRa, -C(RX)3, -CN, -OCN, -SCN, -N=C=O, -NSC, -NO, -NO2, =N-OH, =N2, -N3, -NHC(=O)Ra, -C(=O)Ra, -C(=O)NRaRa, -S(=O)2O-, -S(=O)2OH, -S(=O)2Ra, -OS(=O)2ORa, -S(=O)2NRa, -S(=O)Ra, -OP(=O)(ORa)2, -C(=O)Ra, алкилен-C(=O)Ra, -C(=S)Ra, -C(=O)ORa, алкилен-C(=O)ORa, -C(=O)O-, алкилен-C(=O)O-, -C(=S)ORa, -C(=O)SRa, -C(=S)SRa, -C(=O)NRaRa, алкилен-C(=O)NRaRa, -C(=S)NRaRa и -C(-NRa)NRaNRa, где RX представляет собой F, Cl, Br или I, и Ra представляет собой H, C1-6 алкил, C5-12 арил, C7-12 арилалкил или гетероцикл.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 17 ниже.
[Формула 17]
X1-X2-X3-X4-X5
в формуле 17,
X1 представляет собой любой, выбранный из группы, состоящей из Hyp, D Hyp, цис-4F-Pro, транс-4NH2-Pro, 4,4-дифтор-Pro, 4-метилен-Pro, 4,4-диметил Pro и Pro,
X2 представляет собой любой, выбранный из группы, состоящей из Gly, Ala, Val и Leu,
X3 представляет собой Gln или D Gln,
X4 представляет собой любой, выбранный из группы, состоящей из Asp, Ala, изопропиловый сложный эфир-замещенного Asp, D Asp, Glu, Leu и Asu, и
X5 представляет собой любой, выбранный из группы, состоящей из Val, Leu, Ala, Gly, Aib, и изопропиловый сложный эфир- замещенного Gly.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 18 ниже.
[Формула 18]
X1-X2-X3-X4-X5-X6
в формуле 18,
X1 представляет собой любой, выбранный из группы, состоящей из Hyp, D Hyp, цис-4F-Pro, транс-4NH2-Pro, 4,4-дифтор-Pro, 4-метилен-Pro, 4,4-диметил Pro и Pro,
X2 представляет собой любой, выбранный из группы, состоящей из Gly, Ala, Val и Leu,
X3 представляет собой Gln или D Gln,
X4 представляет собой любой, выбранный из группы, состоящей из Asp, Ala, изопропиловый сложный эфир-замещенного Asp, D Asp, Glu, Leu, Asu, Asn, His и Aib,
X5 представляет собой любой, выбранный из группы, состоящей из Val, Leu, Ala, Gly, Aib, и изопропиловый сложный эфир-замещенного Gly, и
X6 представляет собой любой, выбранный из группы, состоящей из Leu, D Leu, изопропиловый сложный эфир-замещенного Leu и Val.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 19 ниже.
[Формула 19]
X1-X2-X3-X4-X5-X6-X7
в формуле 19,
X1 представляет собой любой, выбранный из группы, состоящей из Hyp, D Hyp, цис-4F-Pro, транс-4NH2-Pro, 4,4-дифтор-Pro, 4-метилен-Pro, 4,4-диметил Pro и Pro,
X2 представляет собой любой, выбранный из группы, состоящей из Gly, Ala, Val и Leu,
X3 представляет собой Gln или D Gln,
X4 представляет собой любой, выбранный из группы, состоящей из Asp, Ala, изопропиловый сложный эфир-замещенного Asp, D Asp, Glu, Leu, Asu, Asn, His и Aib,
X5 представляет собой любой, выбранный из группы, состоящей из Val, Leu, Ala, Gly, Aib, изопропиловый сложный эфир-замещенного Gly, трет-Leu, фенил-Gly,
X6 представляет собой любой, выбранный из группы, состоящей из Leu, D Leu, изопропиловый сложный эфир-замещенного Leu и Val, и
X7 представляет собой любой, выбранный из группы, состоящей из Ala, D Ala и изопропиловый сложный эфир- замещенного Ala.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 20 ниже.
[Формула 20]
X1-X2-X3-X4-X5-X6-X7-X8
в формуле 20,
X1 представляет собой любой, выбранный из группы, состоящей из Hyp, D Hyp, цис-4F-Pro, транс-4NH2-Pro, 4,4-дифтор-Pro, 4-метилен-Pro, 4,4-диметил Pro и Pro,
X2 представляет собой любой, выбранный из группы, состоящей из Gly, Ala, Val и Leu,
X3 представляет собой Gln или D Gln,
X4 представляет собой любой, выбранный из группы, состоящей из Asp, Ala, изопропиловый сложный эфир-замещенного Asp, D Asp, Glu, Leu и Asu,
X5 представляет собой любой, выбранный из группы, состоящей из Val, Leu, Ala, Gly, Aib и изопропиловый сложный эфир-замещенного Gly,
X6 представляет собой любой, выбранный из группы, состоящей из Leu, D Leu, изопропиловый сложный эфир-замещенного Leu и Val,
X7 представляет собой любой, выбранный из группы, состоящей из Ala, D Ala, и изопропиловый сложный эфир-замещенного Ala, и
X8 представляет собой Gly.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 21 ниже.
[Формула 21]
X1-X2-X3-X4-X5-X6
в формуле 21,
X1 представляет собой Gln или Gly
X2 представляет собой любой, выбранный из группы, состоящей из Leu, Gln, Asp, Glu и Asu,
X3 представляет собой любой, выбранный из группы, состоящей из Gly, Asp и Ala,
X4 представляет собой Leu или Gly,
X5 представляет собой любой, выбранный из группы, состоящей из Ala, Leu и Pro, и
X6 представляет собой любой, выбранный из группы, состоящей из Gly, Ala и Lys.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 22 ниже.
[Формула 22]
X1- Gly-X3-X4- Gly-Pro-Lys
в формуле 22,
X1 представляет собой любой, выбранный из группы, состоящей из Asp, Leu, Hyp и Asu,
X3 представляет собой Leu или Gln, и
X4 представляет собой Ala или Asp.
Новое пептидное соединение или его фармацевтически приемлемая соль согласно одному варианту осуществления настоящего изобретения представлено формулой 23 ниже.
[Формула 23]
Gln-X2-Gly-Leu-Ala-Gly-Pro-Lys
в формуле 23,
X2 представляет собой по меньшей мере любой один из Asp, Leu и Asu.
В формулах 17 - 23 выше Hyp представляет собой (2S,4R) транс-4-гидрокси-L-пролин, Gly представляет собой глицин, Gln представляет собой глутамин, Asp представляет собой аспарагиновую кислоту, Leu представляет собой лейцин, Ala представляет собой аланин, Pro представляет собой пролин, Val представляет собой валин, трет-Leu представляет собой L-α-трет-бутилглицин, Asu представляет собой апартимид или аминосукцинимид, Lys представляет собой лизин, изопропиловый сложный эфир представляет собой производное, замещенное изопропиловым сложным эфиром при концевой аминокислотной группе, Aib представляет собой 2-аминоизомасляную кислоту, цис-4F-Pro представляет собой цис-4-фтор-L-пролин, транс-4NH2-Pro представляет собой транс-4-амино-L-пролин, 4,4-дифтор-Pro представляет собой 4-дифтор-L-пролин, 4-метилен-Pro представляет собой 4-метилен-L-пролин, 4,4-диметил Pro представляет собой 4,4-диметил-L-пролин, D Hyp представляет собой транс-4-гидрокси-D-пролин, D Gln представляет собой D-глутамин, D Asp представляет собой D-аспарагиновую кислоту, D Leu представляет собой D-лейцин, Asn представляет собой аспарагин, и His представляет собой гистидин.
Поскольку новое пептидное соединение или его фармацевтически приемлемая соль согласно настоящему изобретению имеет только от 5 до 8 аминокислотных остатков, возможно экономичное массовое производство.
Описанное выше новое пептидное соединение или его фармацевтически приемлемая соль не проявляют цитотоксичности, обладают превосходной стабильностью и обладают противовоспалительной активностью. Используемый в настоящем документе термин «противовоспалительный» означает предотвращение, лечение или ослабление воспаления. В настоящем документе под воспалением понимается заболевание, вызванное инфекцией из-за внешних инфекционных агентов (бактерий, грибков, вирусов, различных типов аллергенов и т.п.), ран, оперативных вмешательств, ожогов, обморожений, электростимуляции или химических веществ и т.д., и заболевание включает дерматит, воспалительное заболевание кишечника, язву желудка, колит, цистит, ринит, тонзиллит или астму и т.д., но конкретно не ограничивается этим.
Настоящее изобретение относится к фармацевтической композиции для профилактики или лечения воспаления, содержащей описанное выше новое пептидное соединение или его фармацевтически приемлемую соль в качестве активного ингредиента.
В фармацевтическую композицию для профилактики или лечения воспаления согласно настоящему изобретению может быть включено новое пептидное соединение или его фармацевтически приемлемая соль при концентрации от 0,001 до 10 мкМ. Композиция, содержащая противовоспалительный активный пептид при концентрации менее 0,001 мкМ, может оказывать слабое противовоспалительное действие, а если она имеет концентрацию более 10 мкМ, то усиление эффекта по мере увеличения концентрации является непропорциональным, поэтому может быть неэффективна, и есть проблема в том, что стабильность состава не обеспечена.
Фармацевтическая композиция для профилактики или лечения воспаления согласно настоящему изобретению может быть в виде нескольких лекарственных форм для перорального или парентерального введения. Когда она составлена, ее можно получить с использованием разбавителя или наполнителя, такого как наполнитель, объемообразующий агент, связующее, смачивающее вещество, разрыхлитель, поверхностно-активное вещество и т. д., которые обычно используются. Твердые препараты для перорального введения включают таблетки, пилюли, порошки, гранулы, капсулы и т.п., и такой твердый препарат можно приготовить путем смешивания одного или нескольких соединений по меньшей мере с одним вспомогательным веществом, например, крахмалом, карбонатом кальция, сахарозой или лактозой, желатином и т.п. В дополнение к вспомогательным веществам также могут быть использованы смазывающие вещества, такие как стеарат магния, тальк и т.п.
Жидкие препараты для перорального введения включают суспензии, растворы для внутреннего применения, эмульсии, сиропы и т.п. В дополнение к воде и жидкому парафину, которые обычно используются в качестве простых разбавителей, могут быть включены различные вспомогательные вещества, такие как смачивающий агент, подсластитель, отдушка, консервант и т.п.
Препараты для парентерального введения могут включать стерильные водные растворы, неводные растворители, суспензии, эмульсии, лиофилизированные препараты и суппозитории. В качестве неводного растворителя и суспендирующего растворителя можно использовать пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, сложные эфиры для инъекций, такие как этилолеат и т.п. В качестве основы суппозитория могут быть использованы витепсол, макрогол, твин 61, масло какао, лауриновое масло, глицерожелатин и т.п.
Лекарственная форма композиции согласно настоящему изобретению может быть использована в виде соли, а также может быть использована отдельно или в комбинации с другими активными соединениями, а также в соответствующей группе. В качестве соли, например, могут быть использованы соляная кислота, серная кислота, азотная кислота, фосфорная кислота, фтористоводородная кислота, бромистоводородная кислота, муравьиная кислота, уксусная кислота, винная кислота, молочная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, метансульфокислота, бензолсульфокислота, толуолсульфокислота, нафталинсульфокислота и т.п.
Композицию согласно настоящему изобретению можно вводить парентерально или перорально по желанию, и можно вводить от одного до нескольких раз в разделенных дозах в количестве от 0,1 до 500 мг, от 1 до 100 мг на 1 кг массы тела в день. Доза для конкретного пациента может варьироваться в зависимости от массы тела пациента, возраста, пола, состояния здоровья, диеты, времени введения, способа введения, скорости экскреции, тяжести заболевания и т.п.
Композиция согласно настоящему изобретению может быть получена и использована в любой форме, включая пероральные формы, такие как порошок, гранула, таблетка, капсула, суспензия, эмульсия, сироп и аэрозоль, препараты для наружного применения, такие как мазь. и крем, и суппозиторий, и стерильный раствор для инъекций, и т.п., соответственно, по общепринятым способам.
Композицию согласно настоящему изобретению можно вводить млекопитающим, таким как крысы, мыши, домашний скот и люди, различными путями, такими как парентеральное и пероральное введение, и можно ожидать всех способов введения, и ее можно вводить, например, путем пероральной, ректальной или внутривенной, внутримышечной, подкожной, внутриматочной, дуральной или интрацеребровентрикулярной инъекции.
С другой стороны, композиция согласно настоящему изобретению не обладает серьезной токсичностью и побочными эффектами, поэтому ее можно безопасно использовать даже при применении в течение длительного периода времени в профилактических целях.
Настоящее изобретение относится к пищевой композиции для профилактики или облегчения воспаления, содержащей описанное выше новое пептидное соединение или его фармацевтически приемлемую соль в качестве активного ингредиента.
В пищевую композицию для профилактики или облегчения воспаления согласно настоящему изобретению может быть включено новое пептидное соединение или его фармацевтически приемлемая соль при концентрации от 0,001 до 10 мкМ. Композиция, содержащая противовоспалительный активный пептид при концентрации менее 0,001 мкМ, может оказывать слабое противовоспалительное действие, а если она имеет концентрацию более 10 мкМ, то усиление эффекта по мере увеличения концентрации является непропорциональным, поэтому может быть неэффективна, и есть проблема в том, что стабильность состава не обеспечена.
Пищевая композиция для профилактики или облегчения воспаления предпочтительно представляет собой порошок, гранулу, таблетку, капсулу или напиток, но не ограничивается ими.
Пищевой продукт согласно настоящему изобретению может быть использован путем добавления нового пептидного соединения или его фармацевтически приемлемой соли согласно настоящему изобретению в чистом виде или в комбинации с другим пищевым продуктом или пищевыми ингредиентами, и может быть соответствующим образом использован в соответствии с обычным способом.
Тип пищевого продукта конкретным образом не ограничивается. Примеры пищевого продукта, к которому может быть добавлено новое пептидное соединение или его фармацевтически приемлемая соль согласно настоящему изобретению, включают мясо, колбасу, хлеб, шоколад, конфеты, закуски, кондитерские изделия, пиццу, рамен, другую лапшу, жевательную резинку, молочные продукты, включая мороженное, различные супы, напитки, чаи, питье, алкогольные напитки, витаминные комплексы и тому подобное, и включают в себя все продукты питания в обычном понимании.
Состав напитка согласно настоящему изобретению может содержать различные ароматизаторы, натуральные углеводы и т.п. в качестве дополнительных ингредиентов, как и обычные напитки. Вышеописанные природные углеводы представляют собой моносахариды, такие как глюкоза и фруктоза, дисахариды, такие как мальтоза и сахароза, и полисахариды, такие как декстрин и циклодекстрин, и сахарные спирты, такие как ксилит, сорбит и эритрит. В качестве подсластителя могут быть использованы натуральные подсластители, такие как тауматин и экстракт стевии, синтетические подсластители, такие как сахарин и аспартам, и т.п.
В дополнение к вышеперечисленному пищевой продукт согласно настоящему изобретению может содержать различные питательные вещества, витамины, электролиты, ароматизаторы, красители, пектиновую кислоту и ее соли, альгиновую кислоту и ее соли, органические кислоты, защитные коллоидные загустители, регуляторы рН, стабилизирующие вещества, консерванты, глицерин, спирт, газирующий агент, используемый в газированных напитках, и т.п. Кроме того, он может содержать мякоть для производства натурального фруктового сока, напитка из фруктового сока и напитка из овощей. Эти ингредиенты можно использовать независимо или в комбинации. Доля этих добавок не является критической, но обычно ее выбирают в диапазоне от 0,01 до 0,1 мас. частей на 100 мас. частей композиции согласно настоящему изобретению.
Пищевая композиция для профилактики или облегчения воспаления согласно настоящему изобретению может быть использована в качестве кормовой добавки или корма.
При использовании в качестве кормовой добавки композиция может представлять собой раствор с высокой концентрацией от 20 до 90% или может быть приготовлена в виде порошка или гранул. Кормовые добавки могут дополнительно включать любую из или одну или несколько органических кислот, таких как лимонная кислота, гуминовая кислота, адипиновая кислота, молочная кислота и яблочная кислота, фосфаты, такие как фосфат натрия, фосфат калия, кислый пирофосфат и полифосфат, природные антиоксиданты, такие как полифенол, катехин, альфа-токоферол, экстракт розмарина, витамин С, экстракт зеленого чая, экстракт солодки, хитозан, дубильная кислота и фитиновая кислота. При использовании в качестве корма композиция может быть составлена в форме обычного корма и может включать вместе традиционные ингредиенты корма.
Кормовые добавки и корма могут дополнительно включать зерна, такие как размолотая или дробленая пшеница, овес, ячмень, кукуруза и рис; растительно-белковые корма, такие как корма на основе рапса, сои и подсолнечника в качестве основного ингредиента; белковые корма животного происхождения, такие как кровяная мука, мясная мука, костная мука и рыбная мука; сухие ингредиенты, состоящие из сахара и молочных продуктов, например, различного сухого молока и сухой сыворотки и т.п., и могут дополнительно включать пищевые добавки, усилители пищеварения и всасывания, стимуляторы роста и т.п.
Кормовую добавку можно вводить животному отдельно или в комбинации с другими кормовыми добавками в съедобном носителе. Кроме того, кормовую добавку можно легко вводить животному в виде подкормки, непосредственно смешивая их с кормом для животных, или в пероральном составе отдельно от корма. Когда кормовую добавку вводят отдельно от корма для животных, ее можно комбинировать с фармацевтически приемлемым съедобным носителем, как хорошо известно в данной области техники, для получения лекарственной формы с немедленным высвобождением или замедленным высвобождением. Такие съедобные носители могут быть твердыми или жидкими, например, кукурузный крахмал, лактоза, сахароза, соевые хлопья, арахисовое масло, оливковое масло, кунжутное масло и пропиленгликоль. При использовании твердого носителя кормовая добавка может представлять собой таблетку, капсулу, порошок, пастилку или сахаросодержащую таблетку, подкормку в микродисперсном виде. При использовании жидкого носителя кормовая добавка может быть в виде мягкой желатиновой капсулы, либо сиропа, либо суспензии, эмульсии, либо раствора.
Кроме того, кормовая добавка и корм могут содержать вспомогательные вещества, например, консерванты, стабилизаторы, смачивающие или эмульгирующие вещества, усилители растворимости и т.п. Кормовую добавку можно использовать путем добавления в корм для животных путем погружения, распыления или смешивания.
Корм или кормовая добавка согласно настоящему изобретению могут применяться в рационе ряда животных, включая млекопитающих, домашнюю птицу и рыбу.
Их можно использовать для млекопитающих, включая свиней, крупный рогатый скот, овец, коз, лабораторных грызунов и лабораторных грызунов, а также домашних животных (например, собак, кошек) и т.п., можно использовать для домашней птицы, включая кур, индеек, уток, гусей, фазанов, перепелов и тому подобное, и можно использовать для рыбы, такой как форель, но без ограничения.
В одном варианте осуществления корм или кормовая добавка могут использоваться для профилактики или лечения воспаления у домашних животных. Домашние животные включают собак, кошек, мышей, кроликов и т.п., но без ограничения.
Настоящее изобретение относится к косметической композиции, обладающей противовоспалительным действием, содержащей описанное выше новое пептидное соединение или его фармацевтически приемлемую соль в качестве активного ингредиента.
В косметическую композицию согласно настоящему изобретению может быть включено новое пептидное соединение или его фармацевтически приемлемая соль при концентрации от 0,001 до 10 мкМ. Композиция, содержащая противовоспалительный активный пептид при концентрации менее 0,001 мкМ, может оказывать слабое противовоспалительное действие, а если она имеет концентрацию более 10 мкМ, то усиление эффекта по мере увеличения концентрации является непропорциональным, поэтому может быть неэффективна, и есть проблема в том, что стабильность состава не обеспечена.
Когда композицию согласно настоящему изобретению используют в качестве косметической композиции, в качестве активного ингредиента, помимо описанного выше нового пептидного соединения или его фармацевтически приемлемой соли, могут быть дополнительно включены компоненты, обычно используемые в косметической композиции. Например, она может включать обычные адъюванты, такие как антиоксиданты, стабилизаторы, солюбилизаторы, витамины, пигменты и отдушки и носители.
Косметическая композиция может быть также получены в любом составе, обычно получаемом в данной области техники, и может быть представлена в виде, например, раствора, суспензии, эмульсии, пасты, геля, крема, лосьона, порошка, мыла, очищающего масла, содержащего поверхностно-активные вещества, порошковой основы, эмульсионной основы, восковой основы и спрея и т.п., но без ограничения. Более конкретно, она может быть получена в виде питательного крема, вяжущего лосьона, смягчающего лосьона, лосьона, эссенции, питательного геля, массажного крема и т.п.
Когда состав косметической композиции представляет собой пасту, крем или гель, в качестве компонента-носителя могут быть использованы масло животного происхождения, растительное масло, воск, парафин, крахмал, трагакантовую камедь, производное целлюлозы, полиэтиленгликоль, силикон, бентонит, диоксид кремния, тальк или оксид цинка, или подобное.
Когда состав косметической композиции представляет собой порошок или спрей, в качестве компонента-носителя могут быть использованы лактоза, тальк, диоксид кремния, гидроксид алюминия, силикат кальция или порошок полиамида, и, в частности, в случае спрея, могут быть дополнительно включены пропелленты, такие как хлорфторуглеводород, пропан/бутан или диметиловый простой эфир.
Когда состав косметической композиции представляет собой раствор или эмульсию, в качестве компонента-носителя используется растворитель, солюбилизатор или эмульгатор, и он включает, например, воду, этанол, изопропанол, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, масло 1,3-бутилгликоля, алифатические сложные эфиры глицерина, сложные эфиры жирных кислот и полиэтиленгликоля или сорбитан.
Когда состав косметической композиции представляет собой суспензию, в качестве компонента-носителя используется жидкий разбавитель, такой как вода, этанол или пропиленгликоль, суспендирующий агент, такой как этоксилированный изостеариловый спирт, сложный эфир полиоксиэтиленсорбита и сложный эфир полиоксиэтиленсорбитана, микрокристаллическая целлюлоза, алюминий метагидроксид, бентонит, агар, трагакант и т.п.
При состав косметической композиции представляет собой очищающее средство, содержащее поверхностно-активное вещество, в качестве компонента-носителя используют сульфат алифатического спирта, сульфат эфира алифатического спирта, моноэфир сульфоянтарной кислоты, изетионат, производное имидазолиния, метилтаурат, саркозинат, сульфат эфира амида жирной кислоты, алкиламидобетаин, алифатический спирт, глицерид жирной кислоты, диэтаноламид жирной кислоты, растительное масло, производное ланолина, эфир этоксилированного глицерина и жирной кислоты и т.п.
Способ осуществления настоящего изобретения
Далее настоящее изобретение будет описано более подробно посредством примеров. Эти примеры предназначены для более подробной иллюстрации настоящего изобретения, и объем настоящего изобретения не ограничивается этими примерами.
Пример: Получение пептида
Получали пептиды согласно примерам 10 - 125, описанным в Таблице 1 ниже.
Таблица 1
(1) Пример 1 (стадия тритиловая смола - Lys (Boc))
2.2 л дихлорметана (далее MC) впрыскивали в 150 г 2-хлортритиловой смолы, перемешивали в течение 1 часа, а затем дегидратировали. 205.22 г Fmoc-Lys (Boc)-OH, 1.8 л MC и 153 мл N,N-диизопропилэтиламина (далее DIEA) впрыскивали в другую реакционную часть, и перемешивали в течение 10 минут до растворения, а затем впрыскивали в реакционную часть, содержащую смолу, и перемешивали при комнатной температуре в течение 4 часов. Перемешивали и затем дегидратировали. 1.8 л MC впрыскивали в дегидратированное твердое вещество и перемешивали в течение 10 минут, а затем дегидратировали, и этот процесс повторяли дважды. Растворенный раствор 1530 мл MC, 180 мл MeOH, 90 мл DIEA впрыскивали и перемешивали в течение 30 минут, а затем дегидратировали, и этот процесс повторяли дважды. После сушки азотом в течение 15 часов, высушенное твердое вещество сушили под вакуумом при 25°C в течение 15 часов с получением 267 г конечного твердого вещества. Обнаружили, что вычисленная скорость загрузки составляет 0.82 ммоль/г.
(2) Пример 2 (стадия тритиловая смола - Pro)
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.61 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Pro-OH.
(3)Пример 3 (стадия тритиловая смола - Gly)
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.96 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Gly-OH.
(4)Пример 4 (стадия тритиловая смола - Ala)
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.87 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Ala-OH.
(5) Пример 5 (стадия тритиловая смола - Leu)
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.97 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Leu-OH.
(6) Пример 6 (стадия тритиловая смола - Asp (OtBu))
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.94 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Asp (OtBu)-OH.
(7) Пример 7 (стадия тритиловая смола - Glu (OtBu))
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.62 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Glu (OtBu)-OH.
(8) Пример 8 (стадия тритиловая смола - Val)
Обнаружили, что вычисленная скорость загрузки составляет в общем 0.992 ммоль/г, тем же образом как в Примере 1 с применением Fmoc-Val-OH.
(9) Пример 9 (стадия расщепления)
99 мл 20% пиперидин/DMF (диметилформамид) впрыскивали в соединение, в котором желаемая аминокислотная последовательность связана с тритильная группа-индуцированной смолой, которое было синтезировано, и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 99 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 99 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. 30 мл MC, 70 мл TFA (трифторуксусная кислота), и 1 мл H2O впрыскивали в другую реакционную часть, и растворяли, а затем впрыскивали в реакционную часть. Перемешивали в течение 4 часов при комнатной температуре и фильтровали. Отфильтрованный раствор концентрировали до 1/2 при пониженном давлении на основе объема отфильтрованного раствора. Концентрированный раствор добавляли по каплям в реакционную часть, содержащую 300 мл IPE (изопропиловый простой эфир) и перемешивали в течение 30 минут. Неочищенное твердое вещество получали путем дегидратации осажденного твердого вещества.
(10) Пример 10
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.15 г Fmoc-Asp (OtBu)-OH, 13.52 г 1-гидрокси-1H-бензотриазола (далее HOBt), и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл диизопропилкарбодиимида (далее DIC) впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 16.7 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(11) Пример 11
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.7 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.1 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(12) Пример 12
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.3 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.4 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.0 г конечного твердого вещества.
(13) Пример 13
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.1 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.4 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(14) Пример 14
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.1 г Fmoc-Leu-OH, 13.52 г HOBt и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.2 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(15) Пример 15
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 27.5 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(16) Пример 16
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 28.3 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.2 г конечного твердого вещества.
(17) Пример 17
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.1 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.0 г конечного твердого вещества.
(18) Пример 18
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 26.4 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.9 г конечного твердого вещества.
(19) Пример 19
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.37 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.2 г конечного твердого вещества.
(20) Пример 20
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.25 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(21) Пример 21
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль валина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Val реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.25 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(22) Пример 22
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.76 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.4 г конечного твердого вещества.
(23) Пример 23
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.76 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(24) Пример 24
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 30.26 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(25) Пример 25
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 16.16 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.7 г конечного твердого вещества.
(26) Пример 26
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.63 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 3.0 г конечного твердого вещества.
(27) Пример 27
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.63 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 3.0 г конечного твердого вещества.
(28) Пример 28
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лизина, загруженного таким же образом, как в Примере 1 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.73 г Fmoc-Pro-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Lys реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.35 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.7 г конечного твердого вещества.
(29) Пример 29
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.80 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 3.3 г конечного твердого вещества.
(30) Пример 30
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.28 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(31) Пример 31
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль пролина, загруженного таким же образом, как в Примере 2 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Pro реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.87 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.4 г конечного твердого вещества.
(32) Пример 32
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.30 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.0 г конечного твердого вещества.
(33) Пример 33
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.10 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.5 г конечного твердого вещества.
(34) Пример 34
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.62 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(35) Пример 35
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.48 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.0 г конечного твердого вещества.
(36) Пример 36
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.12 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(37) Пример 37
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.32 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(38) Пример 38
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.80 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(39) Пример 39
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.50 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.7 г конечного твердого вещества.
(40) Пример 40
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.26 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.4 г конечного твердого вещества.
(41) Пример 41
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.91 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.5 г конечного твердого вещества.
(42) Пример 42
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.82 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(43) Пример 43
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.90 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.9 г конечного твердого вещества.
(44) Пример 44
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 14.32 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.7 г конечного твердого вещества.
(45) Пример 45
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.62 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.2 г конечного твердого вещества.
(46) Пример 46
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.00 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.5 г конечного твердого вещества.
(47) Пример 47
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.81 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.2 г конечного твердого вещества.
(48) Пример 48
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.81 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.2 г конечного твердого вещества.
(49) Пример 49
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.54 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.4 г конечного твердого вещества.
(50) Пример 50
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.23 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(51) Пример 51
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 9.14 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.5 г конечного твердого вещества.
(52) Пример 52
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.23 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.5 г конечного твердого вещества.
(53) Пример 53
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 10.56 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.9 г конечного твердого вещества.
(54) Пример 54
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 13.94 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.2 г конечного твердого вещества.
(55) Пример 55
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.15 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.29 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(56) Пример 56
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.69 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.1 г конечного твердого вещества.
(57) Пример 57
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.09 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(58) Пример 58
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.15 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.67 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.3 г конечного твердого вещества.
(59) Пример 59
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.15 г Fmoc-D Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.21 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.2 г конечного твердого вещества.
(60) Пример 60
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.48 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(61) Пример 61
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.32 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(62) Пример 62
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль D лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-D Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.76 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(63) Пример 63
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.68 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(64) Пример 64
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 24.15 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.7 г конечного твердого вещества.
(65) Пример 65
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-D Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 26.98 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.7 г конечного твердого вещества.
(66) Пример 66
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль D аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-D Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.78 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.9 г конечного твердого вещества.
(67) Пример 67
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 42.54 г Fmoc-Glu (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.18 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(68) Пример 68
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.11 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.8 г конечного твердого вещества.
(69) Пример 69
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.40 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.2 г конечного твердого вещества.
(70) Пример 70
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.78 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 3.1 г конечного твердого вещества.
(71) Пример 71
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль валина, загруженного таким же образом, как в Примере 8 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Val реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.24 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.1 г конечного твердого вещества.
(72) Пример 72
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.23 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.8 г конечного твердого вещества.
(73) Пример 73
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.04 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.6 г конечного твердого вещества.
(74) Пример 74
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.17 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(75) Пример 75
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 16.94 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(76) Пример 76
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль глицина, загруженного таким же образом, как в Примере 3 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Gly реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 16.87 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.1 г конечного твердого вещества.
(77) Пример 77
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.35 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(78) Пример 78
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.90 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.2 г конечного твердого вещества.
(79) Пример 79
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 14.37 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.8 г конечного твердого вещества.
(80) Пример 80
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 21.38 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.3 г конечного твердого вещества.
(81) Пример 81
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.27 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.7 г конечного твердого вещества.
(82) Пример 82
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.64 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.3 г конечного твердого вещества.
(83) Пример 83
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 450 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 14.68 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищеного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.5 г конечного твердого вещества.
(84) Пример 84
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль лейцина, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 29.73 г Fmoc-Gly-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 14.68 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.0 г конечного твердого вещества.
(85) Пример 85
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Aib (alpa-Me-Ala), загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.14 г Fmoc-Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Aib реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 8.96 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 1.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.3 г конечного твердого вещества.
(86) Пример 86
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.41 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.42 г конечного твердого вещества.
(87) Пример 87
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль аланина, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 17.53 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.53 г конечного твердого вещества.
(88) Пример 88
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.76 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.3 г конечного твердого вещества.
(89) Пример 89
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.81 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.6 г конечного твердого вещества.
(90) Пример 90
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 42.54 г Fmoc-Glu (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 18.66 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.6 г конечного твердого вещества.
(91) Пример 91
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Val, загруженного таким же образом, как в Примере 8 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 42.54 г Fmoc-Glu (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Val реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.74 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.4 г конечного твердого вещества.
(92) Пример 92
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Ala, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.48 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.11 г конечного твердого вещества.
(93) Пример 93
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Ala, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.35 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.65 г конечного твердого вещества.
(94) Пример 94
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Ala, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 23.91 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.67 г конечного твердого вещества.
(95) Пример 95
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Val, загруженного таким же образом, как в Примере 8 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Val реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 15.41 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.17 г конечного твердого вещества.
(96) Пример 96
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Ala, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 22.60 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.27 г конечного твердого вещества.
(97) Пример 97
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Ala, загруженного таким же образом, как в Примере 4 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 35.34 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Ala реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 19.39 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.08 г конечного твердого вещества.
(98) Пример 98
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, Fmoc-Leu-OH (35.34 g), 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.26 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.46 г конечного твердого вещества.
(99) Пример 99
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 20.76 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.13 г конечного твердого вещества.
(100) Пример 100
5 г неочищенного твердого вещества, полученного в Примере 10, впрыскивали, а затем 240 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 4.4 г могут быть получены. 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.15 г конечного твердого вещества.
(101) Пример 101
4 г неочищенного твердого вещества, полученного в Примере 11 впрыскивали, а затем 192 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 3.7 г могут быть получены. 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.86 г конечного твердого вещества.
(102) Пример 102
5 г неочищенного твердого вещества, полученного в Примере 12 впрыскивали, а затем 240 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 3.9 г могут быть получены. 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.15 г конечного твердого вещества.
(103) Пример 103
4 г неочищенного твердого вещества, полученного в Примере 15 впрыскивали, а затем 192 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 3.7 г могут быть получены. 3.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.41 г конечного твердого вещества.
(104) Пример 104
5 г неочищенного твердого вещества, полученного в Примере 16 впрыскивали, а затем 240 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 4.9 г могут быть получены. 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.14 г конечного твердого вещества.
(105) Пример 105
4 г неочищенного твердого вещества, полученного в Примере 19 впрыскивали, а затем 192 мл толуола впрыскивали. Реакционную часть нагревали до 110°C, и реакция протекала в течение 24 часов. После завершения реакции твердое вещество дегидратировали путем охлаждения - комнатная температура, и 3.7 г могут быть получены. 3.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.49 г конечного твердого вещества.
(106) Пример 106
1 г неочищенного твердого вещества, полученного в Примере 10 впрыскивали, а затем 4 мл IPA (изопропиловый спирт) впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.95 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.14 г конечного твердого вещества.
(107) Пример 107
3 г неочищенного твердого вещества, полученного в Примере 11 впрыскивали, а затем 12 мл IPA впрыскивали. 1.86 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 2.1 г неочищенного твердого вещества получали. 2 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.57 г конечного твердого вещества.
(108) Пример 108
4 г неочищенного твердого вещества, полученного в Примере 12 впрыскивали, а затем 16 мл IPA впрыскивали. 2.48 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 3.0 г неочищенного твердого вещества получали. 2 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.62 г конечного твердого вещества.
(109) Пример 109
1 г неочищенного твердого вещества, полученного в Примере 100 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.72 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.11 г конечного твердого вещества.
(110) Пример 110
1 г неочищенного твердого вещества, полученного в Примере 100 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.52 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.08 г конечного твердого вещества.
(111) Пример 111
1 г неочищенного твердого вещества, полученного в Примере 101 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.59 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.14 г конечного твердого вещества.
(112) Пример 112
1 г неочищенного твердого вещества, полученного в Примере 101 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.64 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.12 г конечного твердого вещества.
(113) Пример 113
1 г неочищенного твердого вещества, полученного в Примере 102 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.39 г неочищенного твердого вещества получали. 0.3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.07 г конечного твердого вещества.
(114) Пример 114
1 г неочищенного твердого вещества, полученного в Примере 102 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.79 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.20 г конечного твердого вещества.
(115) Пример 115
1 г неочищенного твердого вещества, полученного в Примере 10 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.48 г неочищенного твердого вещества получали. 0.3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.08 г конечного твердого вещества.
(116) Пример 116
1 г неочищенного твердого вещества, полученного в Примере 11 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.81 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.10 г конечного твердого вещества.
(117) Пример 117
1 г неочищенного твердого вещества, полученного в Примере 12 впрыскивали, а затем 4 мл IPA впрыскивали. 0.62 мл H2SO4 добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.69 г неочищенного твердого вещества получали. 0.5 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.11 г конечного твердого вещества.
(118) Пример 118
1 г неочищенного твердого вещества, полученного в Примере 30 впрыскивали, а затем 4 мл IPA впрыскивали. H2SO4 (0.62 мл) добавляли и перемешивали с возвратом флегмы с подтверждением завершения реакции посредством ВЭЖХ. Дегидратировали путем охлаждения - комнатная температура, и 0.48 г неочищенного твердого вещества получали. 0.4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.27 г конечного твердого вещества.
(119) Пример 119
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Val, загруженного таким же образом, как в Примере 8 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Val реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 11.94 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.07 г конечного твердого вещества.
(120) Пример 120
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Ala-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 13.57 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.44 г конечного твердого вещества.
(121) Пример 121
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 12.91 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 0.89 г конечного твердого вещества.
(122) Пример 122
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, Fmoc-Gly-OH (29.73 g), 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 11.82 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.26 г конечного твердого вещества.
(123) Пример 123
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 31.13 г Fmoc-Leu-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 12.44 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.08 г конечного твердого вещества.
(124) Пример 124
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 33.93 г Fmoc-Val-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 10.47 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 3 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 1.20 г конечного твердого вещества.
(125) Пример 125
400 мл 20% пиперидина/DMF впрыскивали в 50 ммоль Leu, загруженного таким же образом, как в Примере 5 и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл DMF впрыскивали и дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли дважды. 450 мл MC впрыскивали, а затем дегидартировали посредством перемешивания в течение 10 минут. Этот процесс повторяли три раза. В другой реакционной части, 41.15 г Fmoc-D Asp (OtBu)-OH, 13.52 г HOBt, и 900 мл DMF растворяли посредством перемешивания в течение 10 минут. Растворенный раствор впрыскивали в тритил-Leu реакционную часть, а затем 31.32 мл DIC впрыскивали и дегидартировали посредством перемешивания в течение 4 часов при комнатной температуре. 8.41 г неочищенного твердого вещества может быть получено посредством повторения ряда процессов согласно аминокислотной последовательности согласно Таблице 1 и проведения стадии расщепления (Пример 9). 4 г неочищенного твердого вещества очищали посредством Prep LC, а затем лиофилизировали с получением 2.06 г конечного твердого вещества.
Экспериментальный пример 1: Оценка стабильности при растворении
Для каждого из пептидов в приведенных выше примерах 10-125 изменение содержания было подтверждено при хранении в течение 7 дней при концентрации 1 мг/1 мл в растворенном состоянии при условиях хранения 40°C и относительной влажности 75%. Результаты показаны в Таблице 2 ниже.
Таблица 2
Ссылаясь на Таблицу 2 выше, можно увидеть, что в большинстве примеров содержание поддерживалось на уровне 50 % или более через 7 дней, и стабильность была очень хорошей.
Экспериментальный пример 2: in vitro оценка противовоспалительной эффективности с применением мышиного макрофага
Противовоспалительную эффективность оценивали для репрезентативных примеров вышеуказанных примеров. В частности, чтобы подтвердить, являются ли Примеры 10, 32, 41, 55, 59 и 91, которые являются репрезентативными примерами 5 аминокислотных остатков, Примеры 11 и 30, которые являются репрезентативными примерами 6 аминокислотных остатков, Пример 86, который является репрезентативным примером из 7 аминокислотных остатков, и Примеры 103 и 104, которые являются репрезентативными примерами из 8 аминокислотных остатков, обладают противовоспалительным действием, изменение количества секреции воспалительных цитокинов подтверждено иммуноферментным анализом (ELISA) с использованием клеток Raw 264.7, которые представляют собой клеточные линии макрофагов (моноцитов).
В частности, Примеры разводили в клетках Raw264.7 (Korean Cell Line Bank, 40071) при концентрации 10 нМ, 100 нМ, 1 мкМ и 10 мкМ, соответственно, и предварительно обрабатывали в течение 1 часа, а затем LPS (Sigma, L6529) при концентрации 1 мкг/мл добавляли для индукции воспалительной реакции. Через 24 часа после индукции супернатант клеточной культуры собирали и анализировали. Иммуноферментный анализ проводили с использованием набора Mouse IL-6 Quantikine ELISA (R&D systems, M6000B), набора TNF-alpha Quantikine ELISA (R&D systems, MTA00B), набора Mouse IL-1 beta/IL-1F2 Quantikine ELISA (R&D systems, MLB00C) в соответствии с руководством производителя.
В результате, ссылаясь на Фиг. 1а, Пример 10, который представляет собой 5-мер, значительно снизился уровень IL-1β, повышенный под действием LPS при концентрации 100 нМ и 1 мкМ, а ссылаясь на Фиг. 1с, значительно снизился уровень TNFα, повышенный под действием LPS при концентрации 10 нМ и 1 мкМ.
Ссылаясь на Фиг. 2а, пример 32, который представляет собой 5-мер, значительно снижал уровень IL-1β, повышенный под действием LPS при концентрации10 нМ, 100 нМ и 1 мкМ.
Ссылаясь на Фиг. 3а, пример 41, представляющий собой 5-мер, значительно снижал уровень IL-1β и уровень IL-6, повышенный под действием LPS при концентрации 100 нМ и 1 мкМ, соответственно.
Ссылаясь на Фиг. 4а и 5а, Примеры 55 и 59, которые являются 5-мерами, значительно снижали уровень IL-1β, повышенный под действием LPS при концентрации 100 нМ.
Ссылаясь на фиг. 6a и 6b, Пример 91, представляющий собой 5-мер, снижал уровень IL-1β, повышенный под действием LPS при всех концентрациях (10 нМ, 100 нМ, 1 мкМ и 10 мкМ), и значительно снижал только уровень IL-6, повышенный под действием LPS при концентрации 1 мкМ.
Ссылаясь на Фиг. 7b, Пример 30, который представляет собой 6-мер, значительно снижал уровень IL-6, повышенный под действием LPS при концентрации 10 нМ.
Ссылаясь на Фиг. 8c, пример 11, который представляет собой 6-мер, значительно снижает уровень TNFα, повышенный под действием LPS при концентрации 10 мкМ.
Ссылаясь на Фиг. 9а, Пример 86, который представляет собой 7-мер, значительно снижал уровень IL-1β, повышенный под действием LPS при концентрации 10 нМ, 1 мкМ и 10 мкМ.
Ссылаясь на Фиг. 10а, пример 103, который представляет собой 8-мер, значительно снижал уровень IL-1β, повышенный под действием LPS при концентрации 1 мкМ.
Ссылаясь на Фиг. 11c, Пример 104, который представляет собой 8-мер, значительно снижал уровень TNFα, повышенный под действием LPS при концентрации 10 нМ.
То есть Примеры 10, 32, 41, 55, 59, 86, 91 и 103, которые являются репрезентативными примерами настоящего изобретения, показали значительный противовоспалительный эффект за счет регуляции секреции IL-1β, секретируемого иммунными клетками, и Примеры 30, 32, 41, и 91 показали значительную противовоспалительную активность, регулируя секрецию IL-6, а Примеры 10, 11, 59, и 104 показали значительную противовоспалительную активность, регулируя секрецию TNFα, соответственно.
Признаки, структуры, эффекты и т.п., описанные в вышеописанных вариантах осуществления, включены по меньшей мере в один вариант осуществления настоящего изобретения и не обязательно ограничиваются только одним вариантом осуществления. Кроме того, признаки, структуры, эффекты и т.п., проиллюстрированные в каждом варианте осуществления, могут быть объединены или изменены для других вариантов осуществления специалистами в области техники, к которой относятся варианты осуществления. Следовательно, содержание, относящееся к таким комбинациям и модификациям, следует интерпретировать как входящее в объем настоящего изобретения.
Кроме того, хотя варианты осуществления были описаны выше, они являются всего лишь примерами и не ограничивают настоящее изобретение, и специалисты в данной области техники, к которым относится настоящее изобретение, поймут, что возможны различные модификации и применения, не приведенные в примерах выше, в диапазоне, который не выходит за рамки основных характеристик настоящего варианта осуществления. Например, каждый компонент, конкретно показанный в вариантах осуществления, может быть реализован путем модификации. Кроме того, различия, относящиеся к таким модификациям и применениям, следует рассматривать как входящие в объем настоящего изобретения, определенный в прилагаемой формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ ПЕПТИД И ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНОГО ЗАБОЛЕВАНИЯ, СОДЕРЖАЩИЙ ПЕПТИД В КАЧЕСТВЕ АКТИВНОГО ФАРМАЦЕВТИЧЕСКОГО ИНГРЕДИЕНТА | 2018 |
|
RU2766160C2 |
| ПЕПТИДЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2019 |
|
RU2819399C2 |
| ПРОИЗВОДНЫЕ МЕТАСТИНА И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2454425C2 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |
| СОЕДИНЕНИЯ, ИНГИБИРУЮЩИЕ MASP, И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2840441C2 |
| БЕЛКИ С ДВОЙНОЙ ФУНКЦИЕЙ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2741345C2 |
| ПРОЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ С ВЫСОКОЙ СТЕПЕНЬЮ ПРОНИКНОВЕНИЯ НА ОСНОВЕ ПЕПТИДОВ И РОДСТВЕННЫХ ПЕПТИДАМ СОЕДИНЕНИЙ | 2010 |
|
RU2627065C2 |
| ЦИКЛИЧЕСКИЕ ПЕПТИДЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2095368C1 |
| СИНТЕЗ ЛИКСИСЕНАТИДА С КЭППИРОВАНИЕМ | 2019 |
|
RU2782772C2 |
| АГОНИСТЫ ОКСИТОЦИНОВЫХ РЕЦЕПТОРОВ | 2010 |
|
RU2539692C2 |
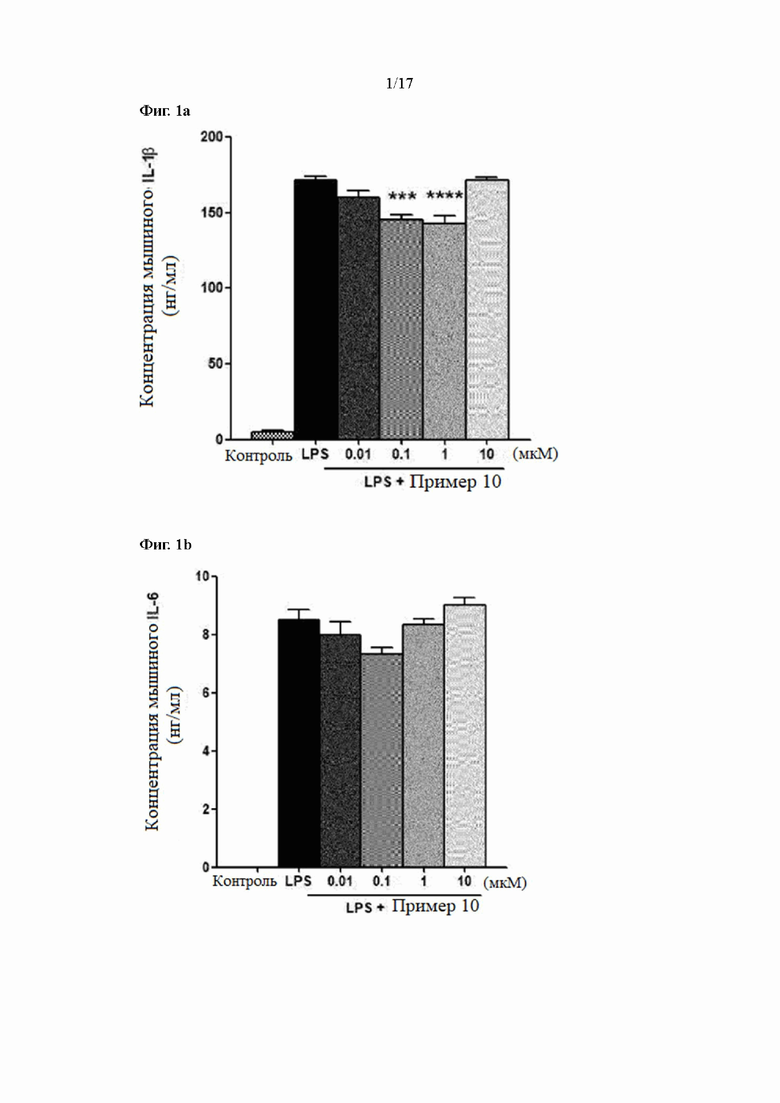

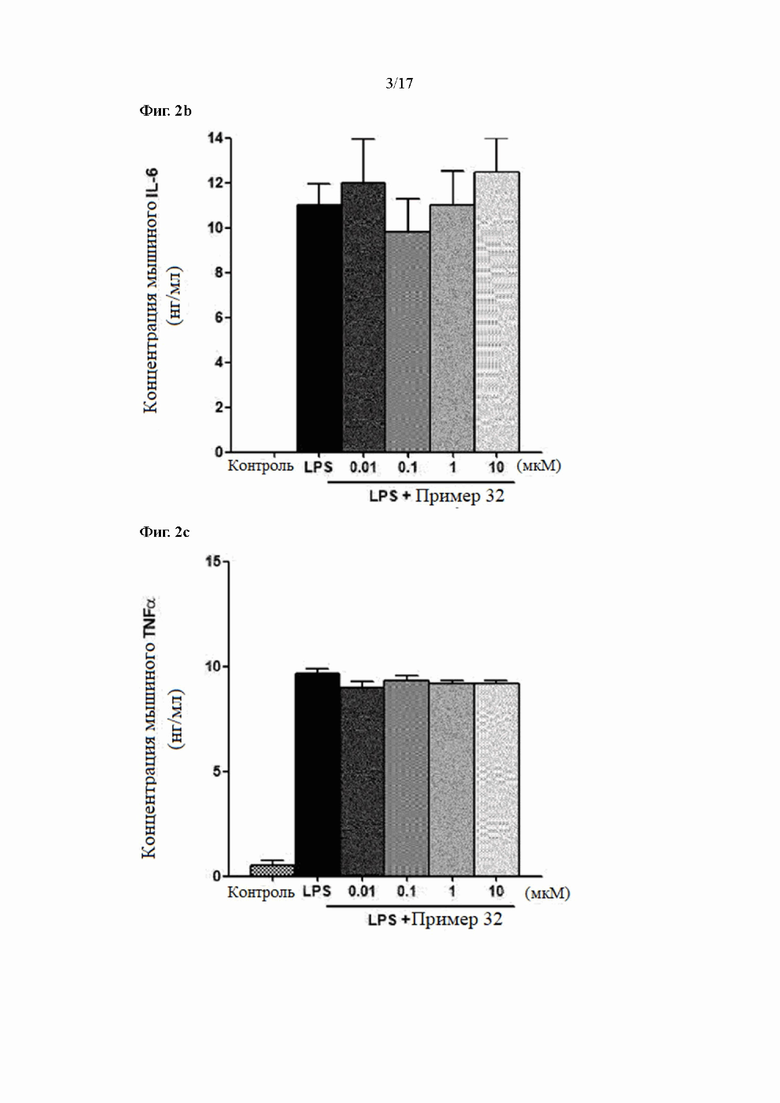
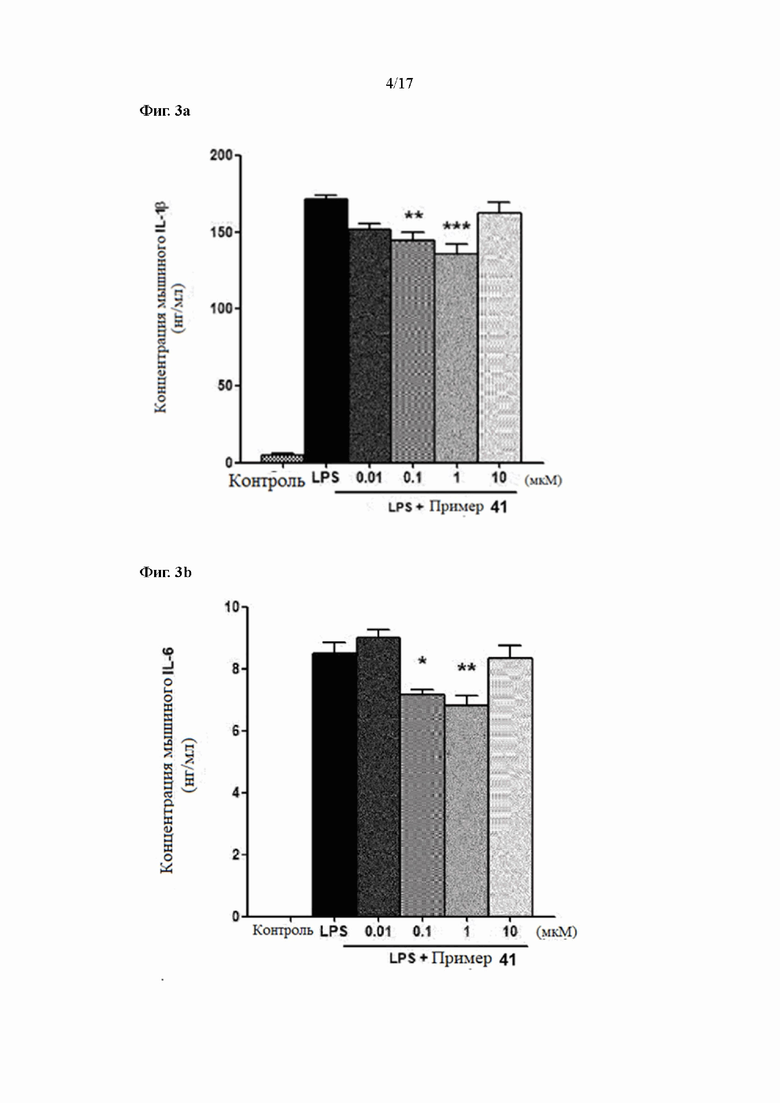
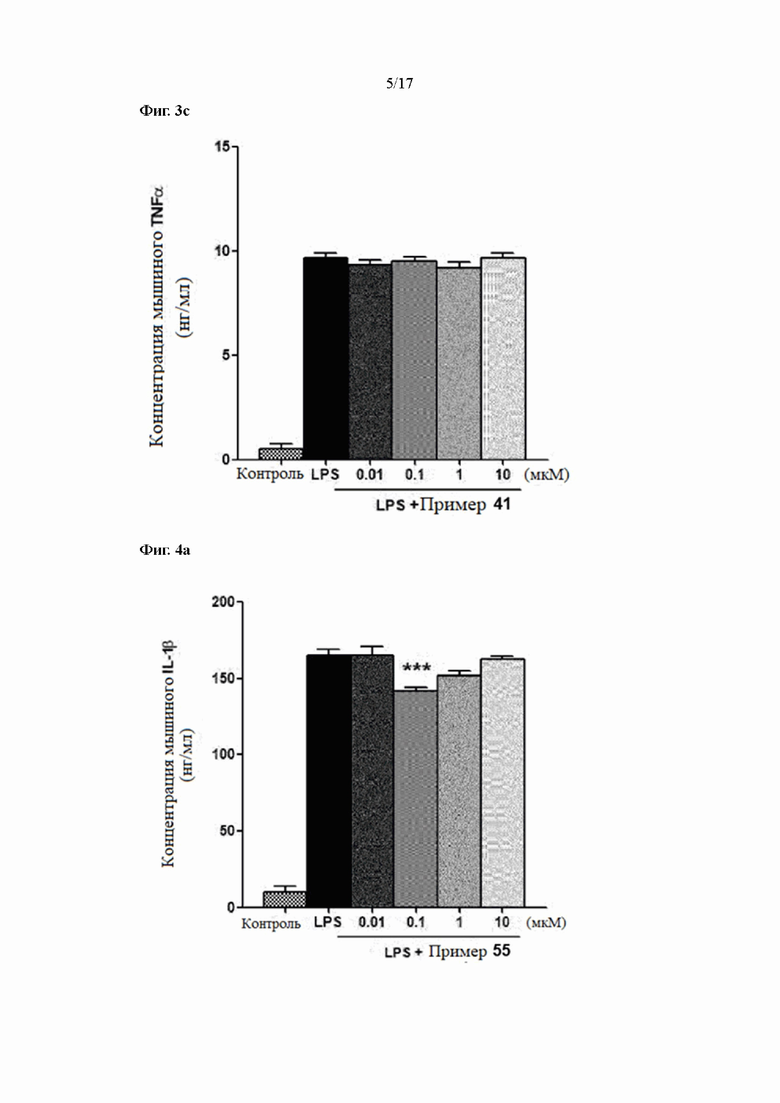
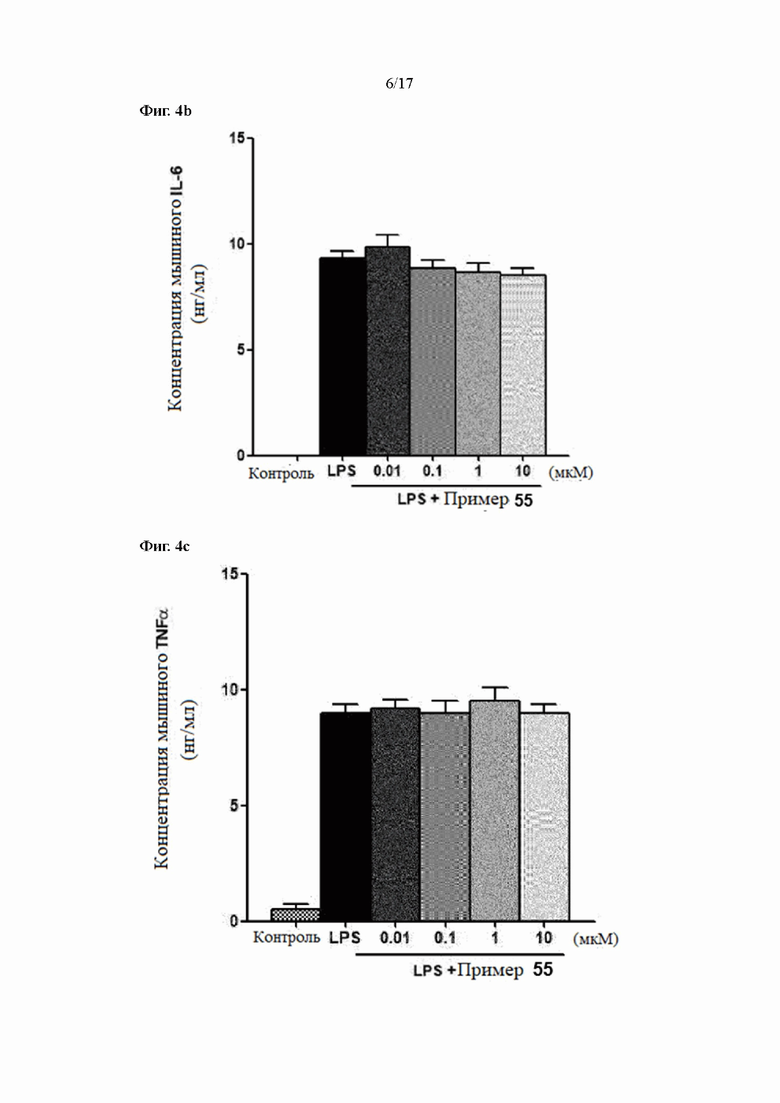
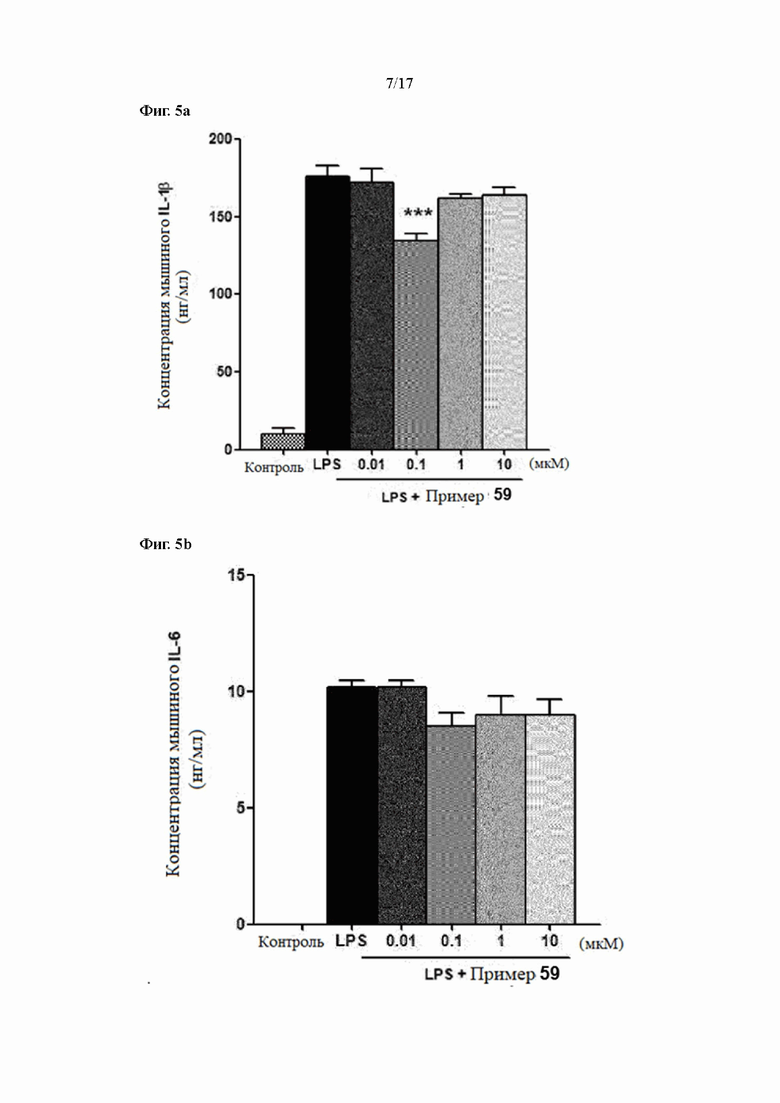
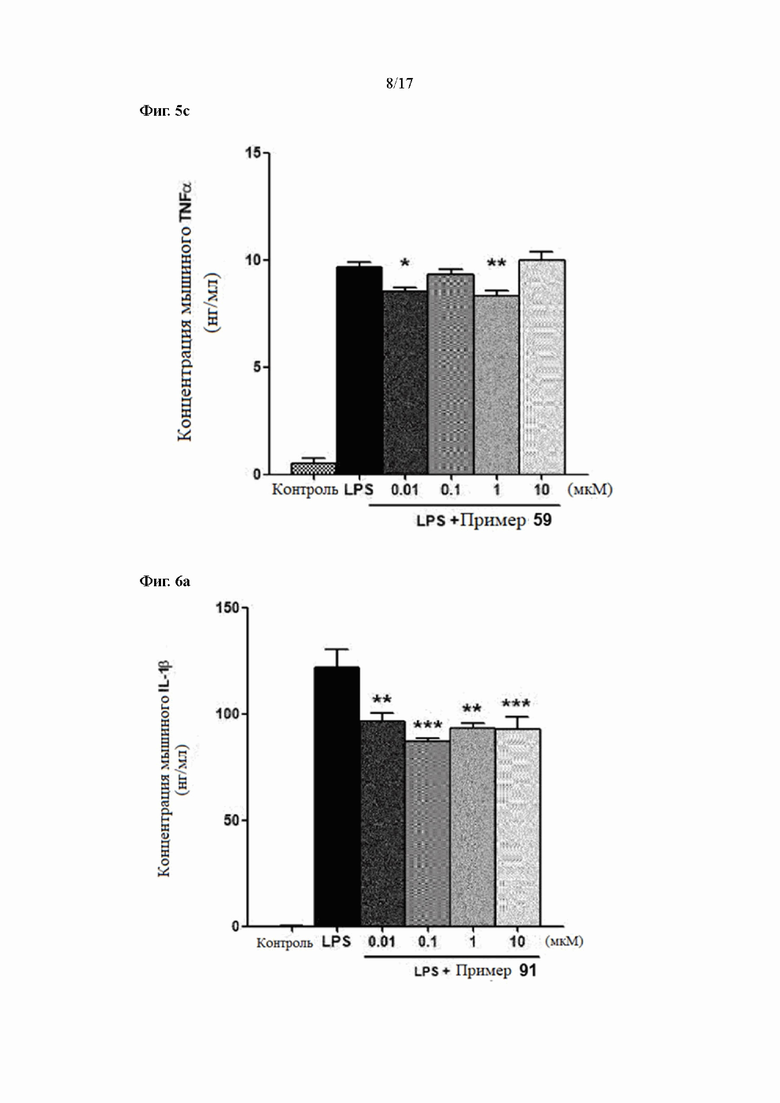
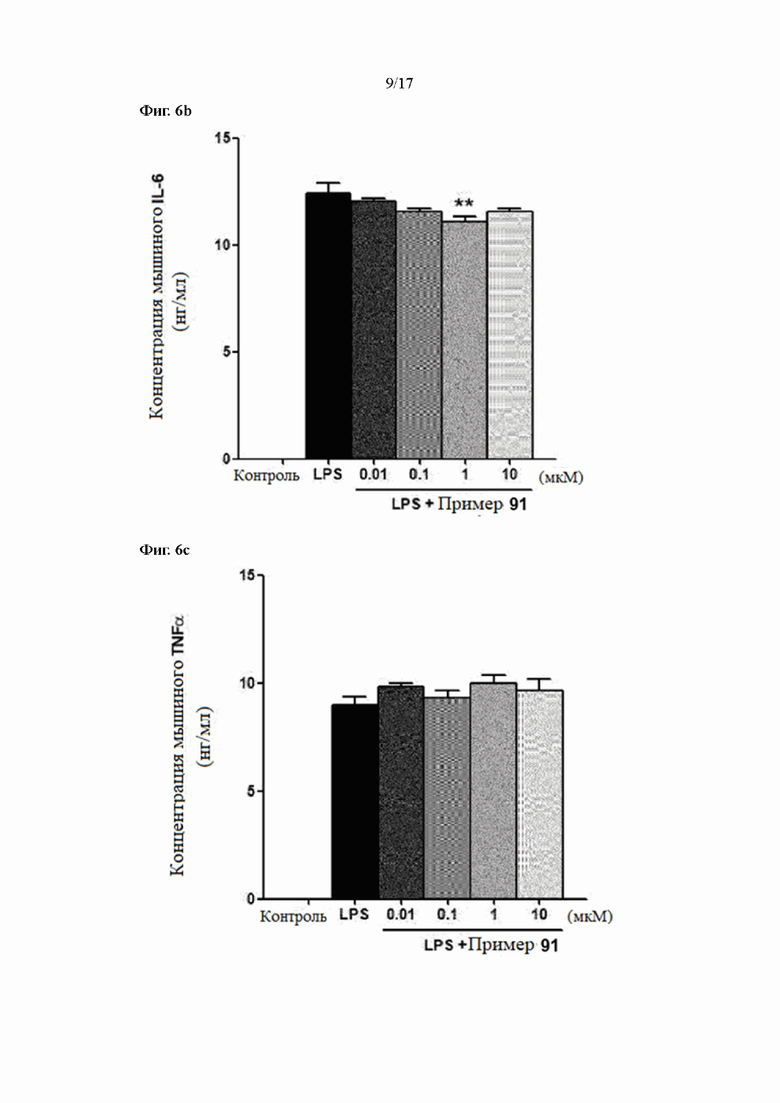
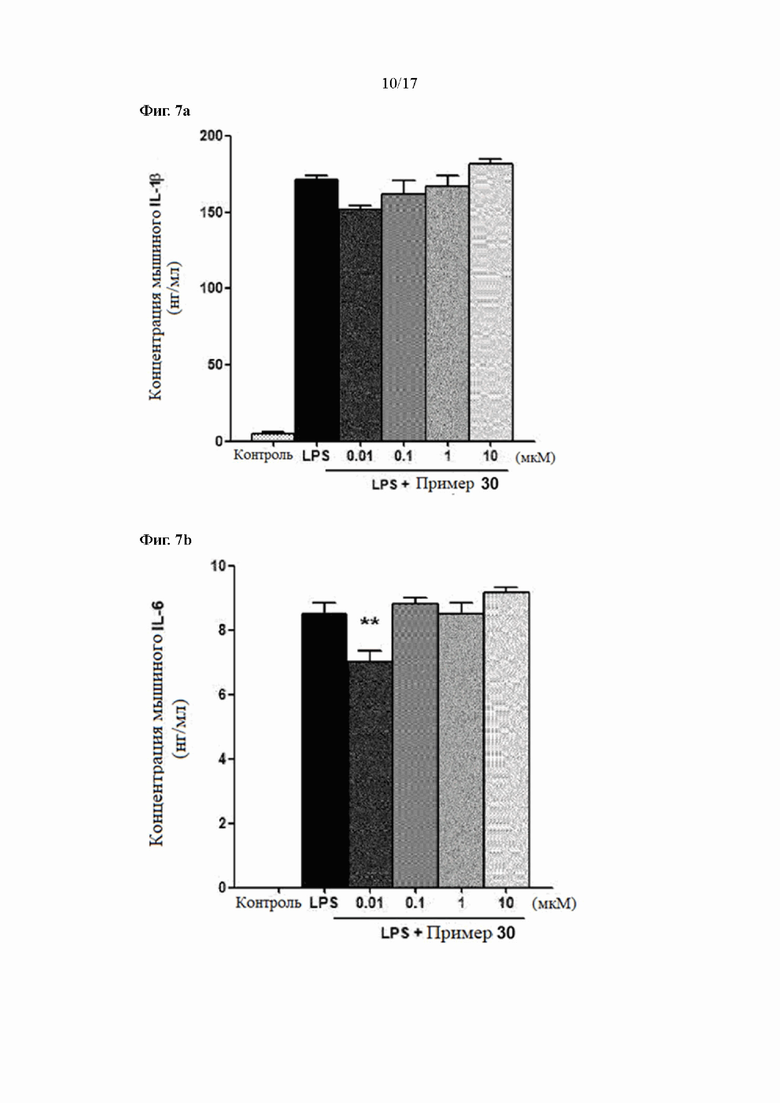
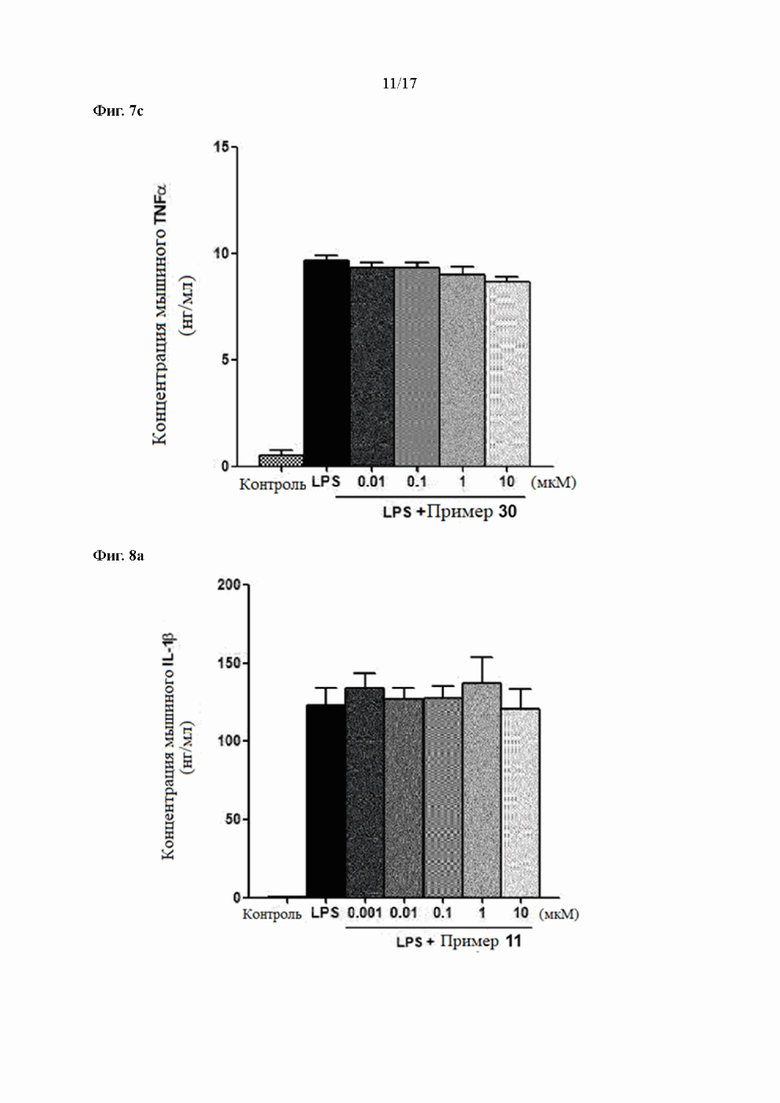
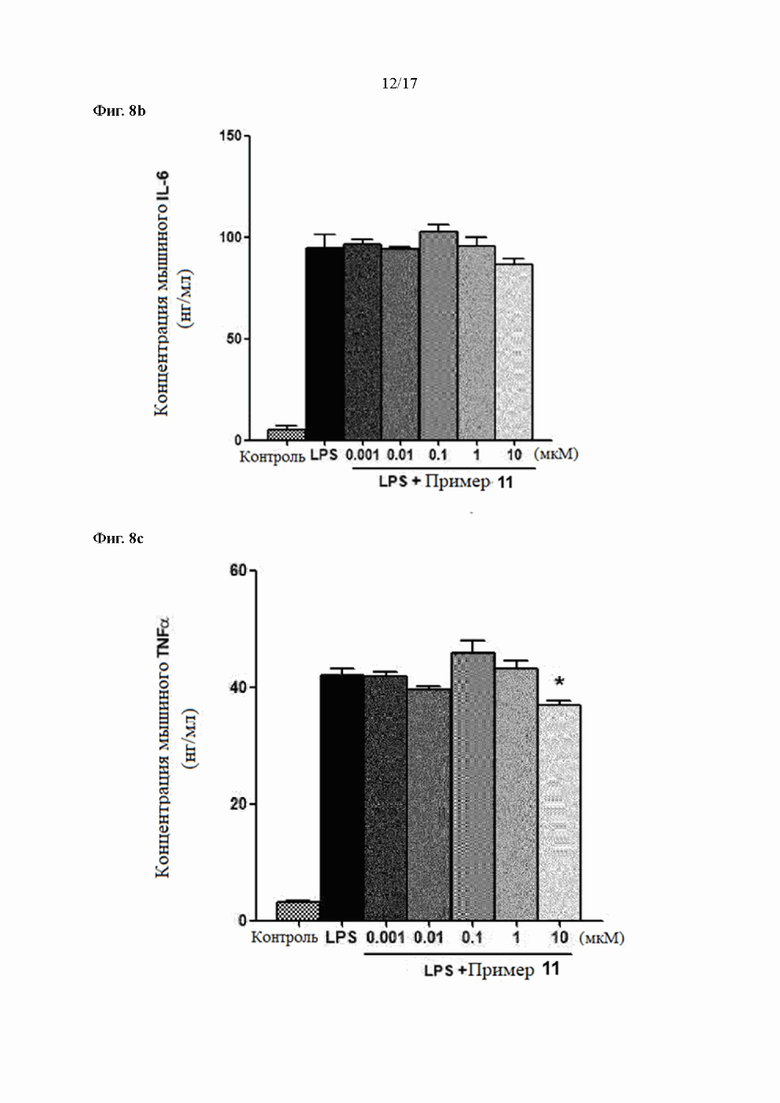
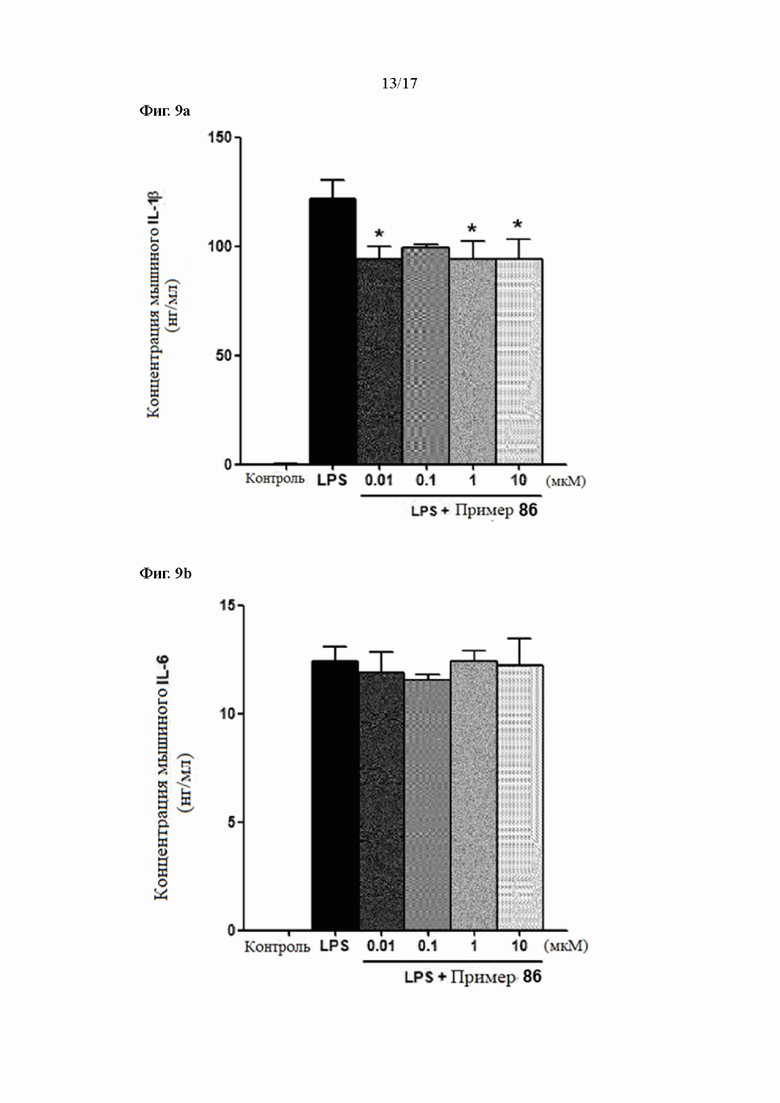
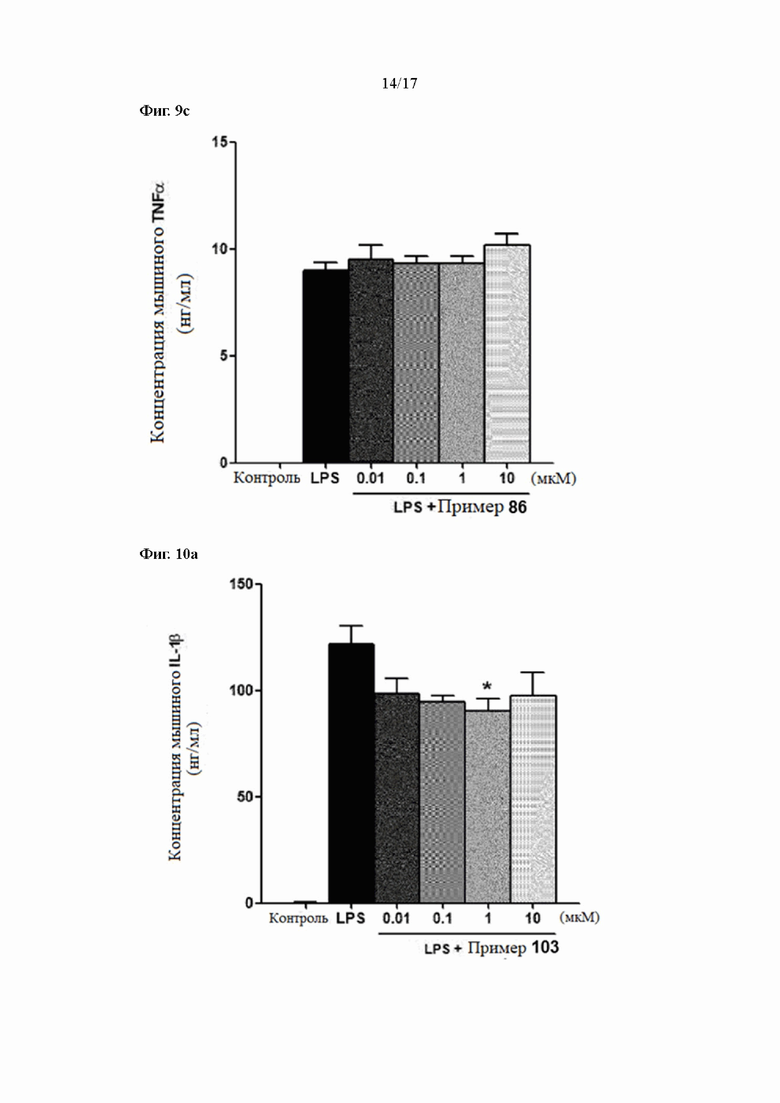


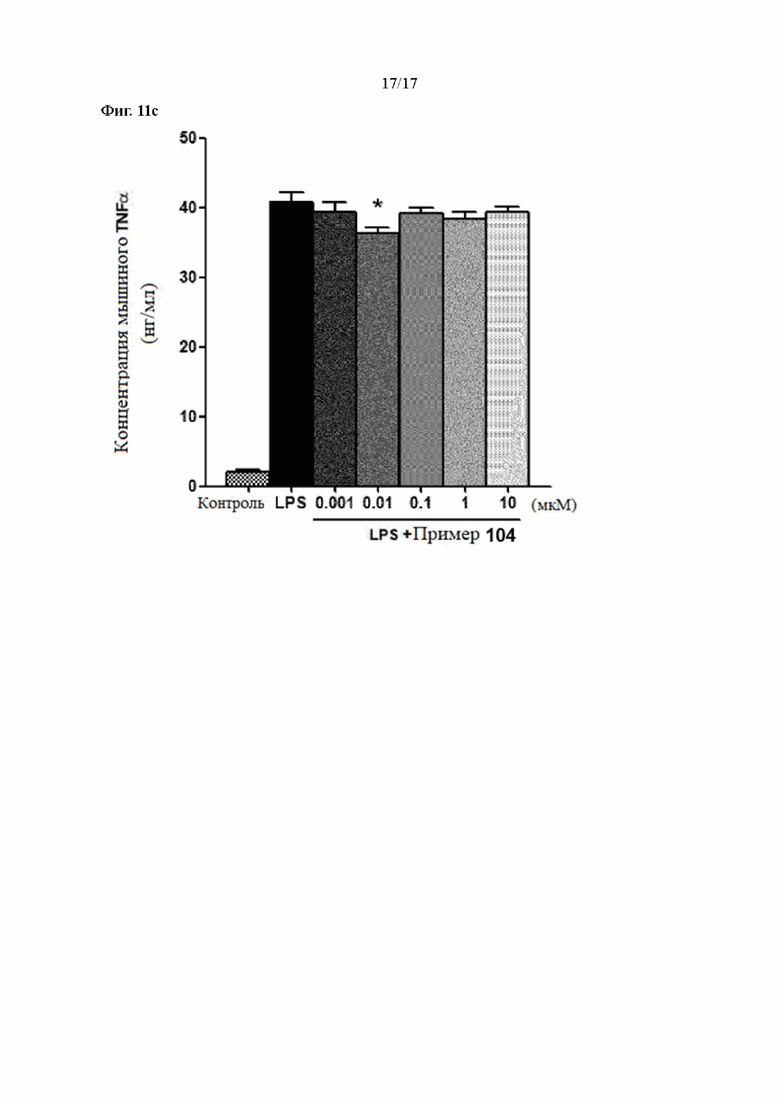
Настоящее изобретение относится к новому пептидному соединению, обладающему противовоспалительным эффектом, выбранному из Hyp-Gly-Gln-Glu-Leu-Leu-Ala, Hyp-Gly-Gln-Glu-Val-Leu-Ala и Hyp-Gly-Gln-Glu-Aib-Leu-Ala, или его фармацевтически приемлемой соли, а также к его фармацевтической, пищевой и косметической композиции. 5 н.п. ф-лы, 11 ил., 2 табл., 125 пр.
1. Новое пептидное соединение, выбранное из группы, состоящей из аминокислотной последовательности ниже, или его фармацевтически приемлемая соль:
Hyp-Gly-Gln-Glu-Leu-Leu-Ala,
Hyp-Gly-Gln-Glu-Val-Leu-Ala и
Hyp-Gly-Gln-Glu-Aib-Leu-Ala.
2. Новое пептидное соединение, имеющее аминокислотную последовательность Hyp-Gly-Gln-Glu-Aib-Leu-Ala, или его фармацевтически приемлемая соль.
3. Фармацевтическая композиция для профилактики или лечения воспаления, содержащая пептид по п. 1 или 2 в качестве активного ингредиента.
4. Пищевая композиция для профилактики или облегчения воспаления, содержащая пептид по п. 1 или 2 в качестве активного ингредиента.
5. Косметическая композиция, обладающая противовоспалительным эффектом, содержащая пептид по п. 1 или 2 в качестве активного ингредиента.
| WO 2018225961 A1,13.12.2018 | |||
| WO 2017175963 A1, 12.10.2017 | |||
| KR 101795653 B1, 09.11.2017 | |||
| US 2016215018 A1, 28.07.2016. |
Авторы
Даты
2024-08-12—Публикация
2020-05-20—Подача