Область техники
[0001] Настоящее изобретение относится к GD2-связывающей молекуле и тому подобное.
Уровень техники
[0002] Ганглиозиды представляют собой семейство гликолипидов и состоят из части сахарной цепи и липида (церамида: жирная кислота+длинноцепочечное основание). Ганглиозиды синтезируются серией ферментативных реакций и метаболизируются до конечных продуктов. GD2 синтезируется из GD3 с участием GM2/GD2 синтазы и далее синтезируется в GD1b с участием GM1/GD1b/GA1 синтазы.
[0003] В опухолевых клетках экспрессия GD2 синтазы является высокой, а экспрессия GD1b синтазы низкой, что приводит к высокой экспрессии GD2 на клеточной поверхности. Известно, что GD2, экспрессированный на клетках, участвует в клеточной адгезии и сигнальной трансдукции за счет сосуществования с молекулами адгезии, такими как интегрины, и участвует в росте и метастазировании рака.
[0004] Известно, что GD2 в высокой степени экспрессируется при меланоме, нейробластоме, глиобластоме, раке легкого, остеосаркоме и лейкозе. GD2 экспрессируется в нервных клетках и глиальных клетках в нормальных тканях, но его экспрессия в этих нормальных тканях низкая.
Список цитированных ссылок
Патентный документ
[0005] PTL 1: WO2012/033885
Сущность изобретения
Техническая задача
[0006] Поскольку GD2 считается хорошей молекулярной мишенью, то антитела, распознающие GD2, были выделены и использовались для лечения антителами или CAR терапии (PTL 1). Однако к настоящему времени указанные виды лечения имеют ограниченное применение, демонстрируя недостаточную терапевтическую эффективность. Например, как показано на фиг. 3 в PTL 1, цитотоксическое действие in vitro слабое, и обработка P1143 показывает примерно 20% лизис (отношение эффектора к мишени: 5:1), что было наиболее высоким эффектом, с наличием эффективности на уровне нескольких процентов для других. В PTL 1 также было показано, что клетки меланомы прививали внутривенно для воспроизведения рака легкого с последующей инфузией эффектора (1×107) (фиг. 6), и 20% мышей погибали на сутки 100, свидетельствуя о том, что в терапевтическом эксперименте не достигалось полного излечения.
[0007] Целью настоящего изобретения является разработка способа лечения или профилактики рака, который на молекулярном уровне нацелен на GD2.
Решение технической задачи
[0008] Авторы настоящего изобретения провели обширные исследования в связи вышеуказанной задачей и обнаружили, что эту задачу можно решить с использованием GD2-связывающей молекулы, которая включает вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1, CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3, и/или вариабельную область легкой цепи, содержащую CDR1 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9, CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11. Авторы изобретения провели дальнейшие исследования на основе этого открытия и завершили настоящее изобретение. В частности, настоящее изобретение включает следующий предмет изобретения.
[0009] Пункт 1. GD2-связывающая молекула, содержащая:
вариабельную область тяжелой цепи, содержащую:
CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1,
CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и
CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3, и/или
вариабельную область легкой цепи, содержащую:
CDR1 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9,
CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и
CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11.
[0010] Пункт 2. GD2-связывающая молекула по п.1, содержащая вариабельную область тяжелой цепи и вариабельную область легкой цепи.
[0011] Пункт 3. GD2-связывающая молекула по пп.1 или 2, где связывающая способность GD2-связывающей молекулы с ганглиозидом GD1a, ганглиозидом GD1b, ганглиозидом GD3, ганглиозидом GM1, ганглиозидом GM3, ганглиозидом GT1b или лактозилцерамидом равна или ниже 1/2 от связывающей способности GD2-связывающей молекулы с ганглиозидом GD2.
[0012] Пункт 4. GD2-связывающая молекула по любому из пп.1-3, которая представляет собой химерный антигенный рецептор.
[0013] Пункт 5. GD2-связывающая молекула по п.4, содержащая коровый домен, содержащий:
домен scFv, который содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи,
трансмембранный домен и
внутриклеточный домен TCR.
[0014] Пункт 6. GD2-связывающая молекула по п.5, где коровый домен дополнительно содержит внутриклеточный домен костимулятора.
[0015] Пункт 7. GD2-связывающая молекула по пп.5 или 6, содержащая домен GITRL через саморасщепляющийся пептидный домен в положении ближе к С-концу корового домена.
[0016] Пункт 8. GD2-связывающая молекула по любому из пп.1-3, которая представляет собой антитело.
[0017] Пункт 9. Полинуклеотид, кодирующий GD2-связывающую молекулу по любому из пп.1-8.
[0018] Пункт 10. Клетка, содержащая полинуклеотид по п.9.
[0019] Пункт 11. Т-клетка с химерным антигенным рецептором или NK-клетка с химерным антигенным рецептором, содержащая полинуклеотид, кодирующий GD2-связывающую молекулу по любому из пп.4-7.
[0020] Пункт 12. Фармацевтическая композиция, содержащая Т-клетку с химерным антигенным рецептором или NK-клетку с химерным антигенным рецептором по п.11, или GD2-связывающую молекулу, по п.8.
[0021] Пункт 13. Фармацевтическая композиция по п.12, кторая предназначена для применения в лечении или профилактике рака.
Преимущественные эффекты изобретения
[0022] Настоящее изобретение относится к способу лечения или профилактики рака, который на молекулярном уровне нацелен на GD2. В частности, с использованием настоящего изобретения можно лечить или профилактировать рак с использованием антитела, которое на молекулярном уровне нацелено на GD2, химерного антигенного рецептора, который на молекулярном уровне нацелен на GD2, и т. д.
Краткое описание фигур
[0023]
На фиг. 1 приведены результаты ELISA экспериментального примера 2. На вертикальной оси представлено поглощение, и на горизонтальной оси представлен коэффициент разбавления. В надписи к фигуре показаны иммобилизованные антигены.
На фиг. 2 приведены результаты тонкослойной хроматографии и иммуноокрашивания в экспериментальном примере 3. Дорожки 1, 2 и 3 на левой фотографии представляют собой дорожки с использованием 3 мкг, 2 мкг и 1 мкг смеси ганглиозидов головного мозга соответственно. Дорожки 1 и 2 на правой фотографии представляют собой дорожки с использованием 3 мкл и 1 мкл экстракта ганглиозидов из клеток SK-MEL-23 (Carney2) (гликолипид, экстрагированный из 10 г осадка после центрифугирования и растворенный в 2 мл C:M (1:1)). Дорожки 3 и 4 на правой фотографии представляют собой дорожки с использованием 1 мкл и 3 мкл экстракта клеток AS (гликолипид, экстрагированный из 1 г осадка после центрифугирования и растворенный в 0,5 мл C:M (1:1)).
На фиг.3 приведены результаты проточной цитометрии в экспериментальном примере 4. На вертикальной оси представлено количество клеток, и на горизонтальной оси представлена интенсивность флуоресценции. Черный пик указывает на образец, обработанный антителом 220-51, и серый (красный) пик указывает на образец, не обработанный антителом 220-51. Используемые клетки показаны над каждой гистограммой. AS, IMR32, Kohl-3 (SK-MEL-31) и YTN17 являются GD2-позитивными клетками, и CEM и MOLT4 являются GD2-негативными клетками.
На фиг.4 приведены результаты анализа RT-CES в экспериментальном примере 5. На вертикальной оси представлен клеточный индекс (рассчитанный по электрическому сопротивлению), и на горизонтальной оси представлено время, прошедшее с начала измерения клеточной адгезии.
На фиг. 5 схематично показаны структуры четырех CAR (28z CAR, zG CAR, 28z GITRL CAR и zG GITRL CAR).
На фиг. 6 приведены результаты экспериментального примера 8 (экспрессия в α/β-клетках при введении 28z CAR или 28z GITRL CAR экспрессионной плазмиды). Эффективность экспрессии анти-каппа CAR показана в процентах. Интенсивность экспрессии CAR-экспрессирующих клеточных фракций показана с использованием MFI.
На фиг.7 приведены результаты экспериментального примера 8 (экспрессия в альфа/бета-клетках при введении zG CAR или zG GITRL CAR экспрессионной плазмиды). Эффективность экспрессии анти-каппа CAR показана в процентах. Интенсивность экспрессии CAR-экспрессирующих клеточных фракций показана с использованием MFI.
На фиг.8 приведены результаты экспериментального примера 8 (экспрессия в альфа/бета-клетках без введения CAR экспрессионной плазмиды). Эффективность экспрессии анти-каппа CAR показана в процентах. Интенсивность экспрессии CAR-экспрессирующих клеточных фракций показана с использованием MFI.
На фиг.9 приведены результаты экспериментального примера 8 (экспрессия в альфа/бета-клетках при введении 28z GITRL CAR экспрессионной плазмиды). Относительное количество клеток, экспрессирующих GITRL, показано в процентах.
На фиг. 10 приведены результаты экспериментального примера 8 (экспрессия в альфа/бета-клетках при введении zG GITRL CAR экспрессионной плазмиды). Относительное количество клеток, экспрессирующих GITRL, показано в процентах.
На фиг. 11 приведены результаты экспериментального примера 8 (экспрессия в альфа/бета-клетках при введении CAR экспрессионной плазмиды). Относительное количество клеток, экспрессирующих GITRL, показано в процентах.
На фиг. 12 приведены результаты экспериментального примера 8 (экспрессия в гамма/дельта-клетках при введении 28z CAR или 28z GITRL CAR экспрессионной плазмиды и без введения CAR экспрессионной плазмиды). Относительное количество каппа-позитивных и Vd2-позитивных фракций показано в процентах.
На фиг. 13 приведены результаты экспериментального примера 8 (экспрессия в гамма/дельта клетках при введении 28z GITRL CAR экспрессионной плазмиды и без введения CAR экспрессионной плазмиды). Относительное количество клеток, экспрессирующих GITRL, показано в процентах.
На фиг. 14 показано распознавание клеток-мишеней гамма/дельта-клеток (результаты измерения внутриклеточной экспрессии IFNγ и CD107a с использованием проточного цитометра после сокультивирования клеток AS и CAR-T-клеток (в которые была введена 28z CAR экспрессионная плазмида) в течение 4 ч (экспериментальный пример 9)). Относительное количество IFNγ-экспрессирующих клеток и CD107a-экспрессирующих клеток представлено в процентах.
На фиг. 15 показано распознавание клеток-мишеней гамма/дельта-клеток (результаты измерения внутриклеточной экспрессии IFNγ и CD107a с использованием проточного цитометра после сокультивирования клеток AS и CAR-T-клеток (в которые была введена 28z GITRL CAR экспрессионная плазмида)) в течение 4 ч (экспериментальный пример 9)). Относительное количество IFNγ-экспрессирующих клеток и CD107a-экспрессирующих клеток представлено в процентах.
На фиг. 16 показано распознавание клеток-мишеней гамма/дельта-клеток (результаты измерения внутриклеточной экспрессии IFNγ и CD107a с использованием проточного цитометра после сокультивирования клеток AS и РВМС в течение 4 ч (экспериментальный пример 9)). Относительное количество IFNγ-экспрессирующих клеток и CD107a-экспрессирующих клеток представлено в процентах.
На фиг. 17 приведены результаты анализа xCELLigence в экспериментальном примере 10 (альфа/бета-клетки). На вертикальной оси представлена цитотоксическая активность (%), измеренная с помощью анализа xCELLigence, и на горизонтальной оси представлено время, прошедшее с момента добавления эффекторных клеток.
На фиг. 18 приведены результаты анализа xCELLigence в экспериментальном примере 10 (гамма/дельта-клетки). На вертикальной оси представлена цитотоксическая активность (%), измеренная с помощью анализа xCELLigence, и на горизонтальной оси представлено время, прошедшее с момента добавления эффекторных клеток.
На фиг. 19 приведены результаты нерадиоактивного анализа цитотоксичности в экспериментальном примере 10. На вертикальной оси представлено относительное количество цитотоксических клеток, рассчитанное на основе уровня люминесценции. Соотношение в надписи к фигуре указывает соотношение CAR-T-клеток и AS-клеток (количество CAR-T-клеток:количество AS-клеток).
На фиг. 20 приведены результаты экспериментального примера 11. На вертикальной оси представлен клеточный индекс, который отражает количество клеток Kelly на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 21 приведены результаты экспериментального примера 12. На вертикальной оси представлен клеточный индекс, который отражает количество клеток SK-N-SH на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 22 приведены результаты экспериментального примера 13. На вертикальной оси представлен клеточный индекс, который отражает количество клеток Hs578T-Luc на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 23 приведены результаты экспериментального примера 14. На вертикальной оси представлен клеточный индекс, который отражает количество клеток BT549-Luc на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 24 приведены результаты экспериментального примера 15. На вертикальной оси представлен клеточный индекс, который отражает количество клеток Kelly на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 25 приведены результаты экспериментального примера 16. На вертикальной оси представлен клеточный индекс, который отражает количество клеток D8 на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 26 приведены результаты экспериментального примера 17. На вертикальной оси представлен клеточный индекс, который отражает количество клеток C2 на Е-планшете. На горизонтальной оси представлено время, прошедшее с момента добавления клеток-мишеней.
На фиг. 27 приведены результаты экспериментального примера 18. На вертикальной оси представлен клеточный индекс, который отражает количество клеток NCI-N417 на Е-планшете. На горизонтальной оси представлено прошедшее время.
Подробное описание вариантов осуществления изобретения
[0024] 1. Определения
В рамках настоящего изобретения, термины «содержащий», «состоящий» и «включающий» включают понятия «содержащий», «состоящий», «состоящий по существу из» и «состоящий из».
[0025] В рамках настоящего изобретения, термин «идентичность» аминокислотных последовательностей относится к степени, в которой две или более разных аминокислотных последовательностей соответствуют друг другу. Таким образом, чем выше степень совпадения между двумя аминокислотными последовательностями, тем выше идентичность или сходство этих последовательностей. Уровень идентичности аминокислотной последовательности определяют, например, с использованием FASTA (инструмента для анализа последовательности) с параметрами по умолчанию. В качестве альтернативы уровень идентичности аминокислотной последовательности можно определить с использованием алгоритма BLAST, разработанного Karlin and Altschul (Karlin S., Altschul S.F. Methods for assessing the statistical significance of molecular sequence features by using general scorings schemes, Proc. Natl. Acad. Sci. USA, 87: 2264-2268(1990), Karlin S., Altschul S.F. Applications and statistics for multiple high-scoring segments in molecular sequences, Proc. Natl. Acad. Sci. USA, 90: 5873-7(1993)). На основе данного алгоритма BLAST была разработана программа под названием «BLASTX». Конкретные методы этих способов анализа известны, и их можно найти на веб-сайте Национального центра биотехнологической информации (NCBI) (http://www.ncbi.nlm.nih.gov/). «Идентичность» нуклеотидных последовательностей также определяется аналогично, как описано выше.
[0026] В рамках настоящего изобретения, термин «консервативная замена» означает замену аминокислотного остатка другим аминокислотным остатком, имеющим аналогичную боковую цепь. Например, замена между аминокислотными остатками, имеющими основную боковую цепь, такими как лизин, аргинин или гистидин, считается консервативной заменой. Следующие замены между другими аминокислотными остатками также считаются консервативными заменами: замена между аминокислотными остатками, имеющими кислую боковую цепь, такими как аспарагиновая кислота или глутаминовая кислота; замену между аминокислотными остатками, имеющими незаряженную полярную боковую цепь, такими как глицин, аспарагин, глутамин, серин, треонин, тирозин или цистеин; замену между аминокислотными остатками, имеющими неполярную боковую цепь, такими как аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин или триптофан; замену между аминокислотными остатками, имеющими бета-разветвленную боковую цепь, такими как треонин, валин или изолейцин; и замену между аминокислотными остатками, имеющими ароматическую боковую цепь, такими как тирозин, фенилаланин, триптофан или гистидин.
[0027] В рамках настоящего изобретения, термин «CDR» является аббревиатурой участка, определяющего комплементарность. CDR представляет собой участок в вариабельных областях иммуноглобулинов и активно участвующий в специфическом связывании антитела с его антигеном. Выражение «CDR легкой цепи» относится к CDR, присутствующему в вариабельных областях легкой цепи иммуноглобулинов, и выражение «CDR тяжелой цепи» относится к CDR, присутствующему в вариабельных областях тяжелой цепи иммуноглобулинов.
[0028] В рамках настоящего изобретения, выражение «вариабельная область» относится к области, содержащей CDR1-CDR3 (ниже просто «CDR 1-3»). Порядок, в котором расположены эти CDR 1-3, не ограничивается; однако вариабельная область предпочтительно относится к области, в которой CDR1, CDR2 и CDR3 расположены в указанном порядке в направлении от N-конца к С-концу или в обратном порядке либо последовательно, либо через другие указанные аминокислотные последовательности в качестве «каркасных областей» (FR), которые будут описаны ниже. Выражение «вариабельная область тяжелой цепи» относится к области, в которой находятся CDR 1-3 тяжелой цепи, и выражение «вариабельная область легкой цепи» относится к области, в которой находятся CDR 1-3 легкой цепи.
[0029] Области, отличные от CDR 1-3 в каждой вариабельной области, называются «каркасными областями» (FR), как указано выше. В частности, область между N-концом и CDR1 вариабельной области определяется как FR1, область между CDR1 и CDR2 - как FR2, область между CDR2 и CDR3 - как FR3, и область между CDR3 и C-концом вариабельной области определяется как FR2 - как FR4.
[0030] 2. GD2-связывающая молекула
В одном варианте осуществления настоящее изобретение относится к GD2-связывающей молекуле, содержащей вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1, CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3; и/или вариабельную область легкой цепи, содержащую CDR1 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9, CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11 (в настоящем описании «GD2-связывающая молекула по настоящему изобретению»). GD2-связывающая молекула по настоящему изобретению описана ниже.
[0031] GD2-связывающая молекула по настоящему изобретению может представлять собой любую GD2-связывающую молекулу при условии, что GD2-связывающая молекула содержит вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1, CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3, и/или вариабельную область легкой цепи, содержащую легкую CDR1 цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9, CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11, и при условии, что GD2-связывающая молекула, способна связываться с GD2.
[0032] GD2-связывающая молекула по настоящему изобретению может представлять собой молекулу, образованную одним типом полипептида, или молекулу, образованную комплексом двух или более типов полипептидов. GD2-связывающая молекула по настоящему изобретению может также представлять собой молекулу, образованную полипептидом или комплексом полипептидов, или молекулу, образованную полипептидом или комплексом полипептидов, к которой присоединено другое соединение (например, флуоресцентное соединение, радиоактивное соединение или неорганическая частица).
[0033] Способность к связыванию GD2 можно измерить в соответствии с известным методом, например, с использованием ELISA (в частности, например, с использованием метода, представленного в экспериментальном примере 2). Способность связывания GD2-связывающей молекулы по настоящему изобретению с GD2 составляет, например, по меньшей мере, 20%, по меньшей мере, 50%, по меньшей мере, 70%, по меньшей мере, 80%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 99% от связывающей способности антитела 220-51 к GD2 в примерах, описанных ниже, которая принимается за 100%.
[0034] GD2-связывающая молекула по настоящему изобретению предпочтительно содержит как вариабельную область тяжелой цепи, так и вариабельную область легкой цепи.
[0035] Вариабельная область тяжелой цепи предпочтительно представляет собой вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 4, или аминокислотную последовательность, имеющую, по меньшей мере, 90% (предпочтительно, по меньшей мере, 95%, предпочтительно, по меньшей мере, 98%, предпочтительно, по меньшей мере, 99%) идентичность с аминокислотной последовательностью, показанной в SEQ ID NO: 4. Вариабельная область легкой цепи предпочтительно представляет собой вариабельную область легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 12, или аминокислотную последовательность, имеющую, по меньшей мере, 90% (предпочтительно, по меньшей мере, 95%, предпочтительно, по меньшей мере, 98%, предпочтительно, по меньшей мере, 99%) идентичность с аминокислотной последовательностью, показанной в SEQ ID NO: 12. Если аминокислотная последовательность SEQ ID NO: 4 или 12 мутирована, то мутация предпочтительно представляет собой замену аминокислоты и более предпочтительно консервативную замену аминокислоты.
[0036] GD2-связывающая молекула по настоящему изобретению может специфически распознавать ганглиозид GD2. С этой точки зрения способность связывания GD2-связывающей молекулы по настоящему изобретению с другими антигенами, которые представляют собой, по меньшей мере, один член, выбранный из группы, состоящей из ганглиозида GD1a, ганглиозида GD1b, ганглиозида GD3, ганглиозида GM1, ганглиозида GM3, ганглиозида GT1b и лактозилцерамида (предпочтительно два члена или более, три члена или более, четыре члена или более, пять членов или более, шесть членов или более или семь членов (все)), предпочтительно составляет 1/2 или ниже (предпочтительно, 1/5 или ниже, 1/10 или ниже, 1/20 или ниже, 1/100 или ниже, 1/500 или ниже, 1/2000 или ниже или 1/10000 или ниже) от способности связываться GD2-связывающей молекулы по настоящему изобретению с ганглиозидом GD2.
[0037] GD2-связывающая молекула по настоящему изобретению может быть химически модифицирована. Полипептид, который составляет GD2-связывающую молекулу по настоящему изобретению, может иметь карбоксильную группу (-COOH), карбоксилатную группу (-COO-), амидную группу (-CONH2) или сложноэфирную группу (-COOR) на С-конце. «R» в сложном эфире представляет собой, например, C1-6 алкильную группу, такую как метил, этил, н-пропил, изопропил или н-бутил; C3-8 циклоалкильную группу, такую как циклопентил или циклогексил; C6-12 арильную группу, такую как фенил или α-нафтил; фенил-C1-2 алкильную группу, такую как бензил или фенэтил; C7-14 аралкильную группу, такую как α-нафтил-C1-2 алкильную группу, такую как α-нафтилметил; или пивалоилоксиметильную группу. Полипептид, который составляет GD2-связывающую молекулу по настоящему изобретению, может иметь амидированную или этерифицированную карбоксильную группу (или карбоксилат), которая не является карбоксильной группой на С-конце. Сложный эфир в данном случае может быть, например, сложным эфиром на С-конце, описанным выше. Полипептид, который составляет GD2-связывающую молекулу по настоящему изобретению, дополнительно включает полипептиды, имеющие аминогруппу N-концевого аминокислотного остатка, защищенную защитной группой (например, C1-6 ацильной группой, включая C1-6 алканоил, такую как формильная группа и ацетильная группа), полипептиды, имеющие пироглутаминированный N-концевой остаток глутамина, который может образоваться в результате расщепления in vivo; и полипептиды, имеющие заместитель (например, -ОН, -SH, аминогруппу, имидазольную группу, индольную группу и гуанидиногруппу) на стороне замены аминокислоты в молекуле, защищенной соответствующей защитной группой (например, C1-6 ацильная группа, включая C1-6 алканоильную группу, такую как формильная группа и ацетильная группа).
[0038] GD2-связывающая молекула по настоящему изобретению может иметь добавленный белок или пептид (например, известную белковую метку или сигнальную последовательность). Примеры белковых меток включают биотин, His-метку, FLAG-метку, Halo-метку, MBP-метку, HA-метку, Myc-метку, V5-метку, PA-метку и флуоресцентную белковую метку.
[0039] GD2-связывающая молекула по настоящему изобретению может представлять собой фармацевтически приемлемую соль, образованную кислотой или основанием. Соль может представлять собой любую фармацевтически приемлемую соль и может быть либо кислой, либо основной солью. Примеры кислых солей включают соли неорганических кислот, такие как гидрохлорид, гидробромид, сульфат, нитрат и фосфат; соли органических кислот, такие как ацетат, пропионат, тартарат, фумарат, малеат, малат, цитрат, метансульфонат и пара-толуолсульфонат; и соли аминокислот, такие как аспартат и глутамат. Примеры основных солей включают соли щелочных металлов, такие как соли натрия и соли калия; и соли щелочноземельных металлов, такие как соли кальция и соли магния.
[0040] GD2-связывающая молекула по настоящему изобретению может быть в форме сольвата. Растворителем может быть любой фармацевтически приемлемый растворитель, например вода, этанол, глицерин или уксусная кислота.
[0041] 2-1. Антитело
В предпочтительном варианте осуществления GD2-связывающая молекула по настоящему изобретению представляет собой антитело (в настоящем описании GD2-связывающая молекула по настоящему изобретению, представляющая собой антитело, может относиться к «антителу по настоящему изобретению»).
[0042] Антитело по настоящему изобретению представляет собой моноклональное антитело.
[0043] Антитело по настоящему изобретению может иметь любую молекулярную массу. Нижний предел составляет, например, 20000, предпочтительно 50000, предпочтительно 100000 и более предпочтительно 120000. Верхний предел составляет, например, 1000000, предпочтительно 500000 и более предпочтительно 200000.
[0044] Антитело по настоящему изобретению может иметь любую структуру. Антитело по настоящему изобретению может содержать константные области или не содержать константные области. Если антитело по настоящему изобретению содержит константные области, то антитело по настоящему изобретению может содержать все константные области тяжелой цепи (СН1, СН2 и СН3) и константные области легкой цепи (CL) или любую одну или комбинацию двух или более константных областей этих константных областей.
[0045] Конкретные примеры структуры антитела по настоящему изобретению включают иммуноглобулины, Fab, F(ab')2, миниантитело, scFv-Fc, Fv, scFv, диатело, триантитело и тетраантитело. Из них иммуноглобулин является предпочтительным с точки зрения эффекта по настоящему изобретению.
[0046] Иммуноглобулин имеет структуру, состоящую из комбинации двух структур, каждая из которых состоит из одной тяжелой цепи, содержащей вариабельную область тяжелой цепи и константную область тяжелой цепи, и одной легкой цепи, содержащей вариабельную область легкой цепи и константную область легкой цепи.
[0047] «Fab» содержит фрагмент тяжелой цепи, содержащий вариабельную область тяжелой цепи и СН1 в константной области тяжелой цепи, и легкую цепь, содержащую вариабельную область легкой цепи и константную область легкой цепи (CL), где вариабельная область тяжелой цепи и вариабельная область легкой цепи связаны нековалентным межмолекулярным взаимодействием, описанным выше, или связаны друг с другом посредством дисульфидной связи. В Fab CH1 и CL могут быть связаны дисульфидной связью между тиоловыми группами цистеиновых остатков, присутствующих в CH1 и CL.
[0048] «F(ab')2» содержит две пары Fab, где CH1 одного Fab связан с CH1 другого Fab посредством дисульфидной связи между тиоловыми группами их цистеиновых остатков.
[0049] «Мини-антитело» относится к структуре, в которой два фрагмента, каждый из которых содержит СН3, связанный с вариабельной областью тяжелой цепи, составляющей scFV, описанный ниже, связаны между СН3 и СН3 нековалентным межмолекулярным взаимодействием.
[0050] «scFv-Fc» относится к структуре, в которой два фрагмента антитела, каждый из которых содержит scFv, CH2 и CH3, связаны между CH3 и CH3 нековалентным межмолекулярным взаимодействием, как в случае с мини-антителом, и фрагменты связаны дисульфидной связью между тиоловыми группами цистеиновых остатков, находящихся в каждом СН3.
[0051] «Fv» считается наименьшей структурной единицей антитела с вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, связанными нековалентным межмолекулярным взаимодействием. В Fv тиоловая группа цистеинового остатка, присутствующего в вариабельной области тяжелой цепи, может быть связана с тиоловой группой цистеинового остатка, присутствующего в вариабельной области легкой цепи, посредством дисульфидной связи.
[0052] «scFv» имеет структуру, в которой С-конец вариабельной области тяжелой цепи и N-конец вариабельной области легкой цепи связаны через линкер, или N-конец вариабельной области тяжелой цепи и С-конец вариабельной области легкой цепи связаны через линкер, и это также относится к «одноцепочечному антителу».
[0053] В рамках настоящего изобретения, термины «диантитело», «триантитело» и «тетраантитело» соответственно относятся к димеру, тримеру и тетрамеру, образованному scFv, описанному выше, и каждое из них связано и структурно стабилизировано, например, нековалентным межмолекулярным взаимодействием вариабельных областей, как это имеет место в Fv.
[0054] Если антитело по настоящему изобретению представляет собой иммуноглобулин, то его класс особым образом не ограничивается. Классы включают, например, IgA, IgD, IgE, IgG и IgM, а также подклассы этих классов. Класс антител по настоящему изобретению представляет собой, например, IgG или IgM, предпочтительно IgG и более предпочтительно IgG1.
[0055] Источник антитела по настоящему изобретению особым образом не ограничивается. Антитело по настоящему изобретению может представлять собой, например, человеческое антитело, мышиное антитело, крысиное антитело, кроличье антитело, обезьянье антитело или антитело шимпанзе. Антитело по настоящему изобретению может быть химерным антителом (например, антителом, образованным заменой аминокислотной последовательности константной области антитела, полученного из организма, отличного от человека (например, мыши), на аминокислотную последовательность константной области человеческого антитела), гуманизированное антитело или полностью гуманизированное антитело.
[0056] Антитело по настоящему изобретению можно получить, например, способом, включающим культивирование хозяина, трансформированного полинуклеотидом, кодирующим антитело по настоящему изобретению, и сбор фракции, содержащей антитело по настоящему изобретению.
[0057] Полинуклеотид, кодирующий антитело по настоящему изобретению, может представлять собой любой полинуклеотид, точно содержащий последовательность антитела по настоящему изобретению, и может содержать другие последовательности в дополнение к кодирующей последовательности антитела по настоящему изобретению. Другие последовательности включают последовательность, кодирующую секреторный сигнальный пептид, последовательность промотора, последовательность энхансера, последовательность репрессора, последовательность инсулятора, ориджин репликации и последовательность, кодирующую ген лекарственной устойчивости, которые располагаются рядом с кодирующей последовательностью антитела по настоящему изобретению. Полинуклеотид, кодирующий антитело по настоящему изобретению, может также представлять собой линейный полинуклеотид или циклический полинуклеотид (например, вектор).
[0058] Конкретные примеры полинуклеотидов включают (I) полинуклеотиды, содержащие нуклеотидную последовательность, кодирующую, по меньшей мере, один член, выбранный из группы, состоящей из тяжелой цепи, вариабельной области тяжелой цепи, CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи антитела по настоящему изобретению, (II) полинуклеотиды, содержащие нуклеотидную последовательность, кодирующую, по меньшей мере, один член, выбранный из группы, состоящей из легкой цепи, вариабельной области легкой цепи, CDR1 легкой цепи, легкой CDR2 цепи и CDR3 легкой цепи антитела по настоящему изобретению, (III) полинуклеотиды, содержащие нуклеотидную последовательность, кодирующую, по меньшей мере, один член, выбранный из группы, состоящей из тяжелой цепи, вариабельной области тяжелой цепи, CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи антитела по настоящему изобретению, и полинуклеотиды, содержащие нуклеотидную последовательность, кодирующую, по меньшей мере, один член, выбранный из группы, состоящей из легкой цепи, вариабельной области легкой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи антитела по настоящему изобретению.
[0059] Хозяином может быть любой организм, например, клетки насекомых, эукариотические клетки или клетки млекопитающих. Из них клетки млекопитающих, такие как клетки HEK, клетки CHO, клетки NS0, клетки SP2/O или клетки P3U1, являются предпочтительными с точки зрения более эффективной экспрессии антитела. Способы трансформации, культивирования и сбора особым образом не ограничиваются, и можно использовать любой способ, известный в области получения антител. После сбора антитело по настоящему изобретению может быть необязательно очищено. Очистку можно проводить способом, известным в области получения антител, таким как хроматография или диализ.
[0060] 2-2. Химерный антигенный рецептор
В предпочтительном варианте осуществления GD2-связывающая молекула по настоящему изобретению представляет собой химерный антигенный рецептор. (В настоящем описании GD2-связывающая молекула по настоящему изобретению, представляющая собой химерный антигенный рецептор, может относиться к «химерному антигенному рецептору по настоящему изобретению».)
[0061] Химерный антигенный рецептор (CAR), как правило, представляет собой химерный белок, одноцепочечное антитело (scFv), которое состоит из легкой цепи (VL), связанной в тандеме с тяжелой цепью (VH) вариабельной области моноклонального антитела, расположенной ближе к N-концу в качестве домена, отвечающего за его способность связываться с антигеном, и его ξ-цепь Т-клеточного рецептора (TCR) находится ближе к C-концу. Т-клетки, экспрессирующие CAR, называются «CAR-T-клетками».
[0062] Домен, ответственный за способность связывания с антигеном (GD2) (GD2-связывающий домен) в химерном антигенном рецепторе по настоящему изобретению, особым образом не ограничивается, если данный домен содержит вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1, CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3, и/или вариабельную область легкой цепи, содержащую CDR1 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9, CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11.
[0063] GD2-связывающий домен предпочтительно имеет структуру scFv. Линкер, который связывает вариабельную область тяжелой цепи с вариабельной областью легкой цепи, может представлять собой любой линкер, который сохраняет функциональность химерного антигенного рецептора. Линкер предпочтительно представляет собой линкер GS (как правило, линкер, имеющий повторяющуюся последовательность, содержащую GGGGS (SEQ ID NO: 41) в качестве структурной единицы). Количество аминокислотных остатков линкера составляет, например, от 5 до 30, предпочтительно от 10 до 20 и более предпочтительно 15.
[0064] Химерный антигенный рецептор по настоящему изобретению обычно содержит коровый домен, содержащий домен scFv, имеющий вариабельную область тяжелой цепи и вариабельную область легкой цепи, трансмембранный домен и внутриклеточный домен TCR. В коровом домене домен scFv, трансмембранный домен и внутриклеточный домен TCR располагаются в указанном порядке от N-конца прямо или через другие домены.
[0065] Трансмембранный домен может быть любого типа, который не оказывает отрицательного влияния на функциональность химерного антигенного рецептора. Например, можно использовать CD28, CD3-дзета, CD4 или CD8-альфа, которые экспрессируются в клетках, таких как Т-клетки. Данные трансмембранные домены могут быть мутированы при условии, что при этом не нарушается функциональность химерного антигенного рецептора.
[0066] Внутриклеточный домен TCR может быть, например, внутриклеточным доменом, полученным из CD3, который также называется «ξ-цепью TCR». CD3 может быть мутирован при условии, что при этом не нарушается функциональность химерного антигенного рецептора. Мутация CD3 предпочтительно осуществляется таким образом, что CD3 содержит ITAM (мотив активации иммунорецепторов на основе тирозина).
[0067] Химерный антигенный рецептор по настоящему изобретению предпочтительно имеет спейсерную последовательность между доменом scFv и трансмембранным доменом. Спейсерная последовательность может быть любой длины и может быть образована из любых аминокислотных остатков при условии, что функциональность химерного антигенного рецептора не нарушается. Например, спейсерную последовательность можно сконструировать таким образом, чтобы она содержала примерно от 10 до 200 аминокислотных остатков. Используемая спейсерная последовательность предпочтительно представляет собой последовательность константной области легкой цепи.
[0068] Коровый домен в химерном антигенном рецепторе по настоящему изобретению предпочтительно дополнительно содержит внутриклеточный домен костимулятора. Внутриклеточный домен костимулятора может представлять собой любой внутриклеточный домен, полученный из костимулятора клеток, таких как Т-клетки. Например, можно подходящим образом выбрать и использовать, по меньшей мере, один член, выбранный из группы, состоящей из OX40, 4-1BB, GITR, CD27, CD278, CD28 и тому подобное. Внутриклеточный домен этих костимуляторов может быть мутирован при условии, что не нарушается функциональность химерного антигенного рецептора. Положение внутриклеточного домена костимулятора особым образом не ограничивается при условии, что внутриклеточный домен находится в положении ближе к С-концу трансмембранного домена; внутриклеточный домен может находиться ближе к N-концу или С-концу внутриклеточного домена TCR.
[0069] Химерный антигенный рецептор по настоящему изобретению предпочтительно содержит домен лиганда, такой как домен GITRL, домен 4-1BBL или домен ICOSL, в положении ближе к С-концу корового домена через саморасщепляющийся пептидный домен. Это может повысить эффективность экспрессии химерного антигенного рецептора или цитотоксическую активность CAR-T-клеток, содержащих химерный антигенный рецептор.
[0070] В рамках настоящего изобретения, выражение «саморасщепляющийся пептид» относится к пептидной последовательности с расщепляющейся активностью, находящейся между двумя аминокислотными остатками в пептидной последовательности. Примеры саморасщепляющихся пептидов включают 2А-пептиды и 2А-подобные пептиды. Например, в 2А-пептидах или 2А-подобных пептидах расщепление происходит между остатком глицина и остатком пролина этих пептидов. Это происходит за счет «механизма проскока рибосомы», при котором во время трансляции не образуется нормальная пептидная связь между остатком глицина и остатком пролина, и это не влияет на трансляцию ниже. Механизм проскока рибосомы известен в данной области и используется для экспрессии многочисленных белков, кодированных одной молекулярной информационной РНК (мРНК). Саморасщепляющийся пептид для применения в настоящем изобретении может быть получен из 2А-пептидов вирусов или 2А-подобных пептидов, обладающих эквивалентной функциональностью. Например, саморасщепляющийся пептид может быть выбран из группы, состоящей из 2А-пептидов, полученных из вируса ящура (FMDV) (F2A), 2А-пептидов, полученных из вируса ринита лошадей А (ERAV) (Е2А), пептидов, полученных из тешовируса свиней (PTV-1) (P2A), и 2A-пептидов, полученных из вируса Thosea asigna (TaV) (T2A). Домен саморасщепляющегося пептида может быть мутирован при условии, что активность саморасщепляющегося пептидного домена существенно не нарушается.
[0071] Домен GITRL особым образом не ограничивается. Домен GITRL представляет собой, например, предпочтительно домен, имеющий аминокислотную последовательность, показанную в SEQ ID NO: 40, или аминокислотную последовательность, имеющую, по меньшей мере, 90% идентичность (предпочтительно, по меньшей мере, 95%, предпочтительно, по меньшей мере, 98% и предпочтительно, по меньшей мере, 99%) с аминокислотной последовательностью, показанной в SEQ ID NO: 40. Если домен GITRL представляет собой аминокислотную последовательность, имеющую мутацию в аминокислотной последовательности, показанной в SEQ ID NO: 40, то мутация предпочтительно представляет собой замену аминокислоты и более предпочтительно консервативную замену аминокислоты.
[0072] Способы получения химерного антигенного рецептора и CAR-T-клетки, которая экспрессирует химерный антигенный рецептор, известны. Химерные антигенные рецепторы и CAR-T-клетки можно получить в соответствии с известным способом или аналогичным способом.
[0073] 3. Полинуклеотид
В одном варианте осуществления настоящее изобретение относится к полинуклеотиду, кодирующему GD2-связывающую молекулу по настоящему изобретению (который может относиться к «полинуклеотиду по настоящему изобретению» в настоящем описании). Полинуклеотид по настоящему изобретению описан ниже.
[0074] Полинуклеотид по настоящему изобретению может содержать другие последовательности в дополнение к последовательности, кодирующей GD2-связывающую молекулу по настоящему изобретению. Предпочтительно полинуклеотид по настоящему изобретению точно содержит последовательность GD2-связывающей молекулы по настоящему изобретению. Другие последовательности включают последовательности промотора, последовательности энхансера, последовательности репрессора, последовательности инсулятора, ориджин репликации, последовательности, кодирующие репортерный белок (например, флуоресцентные белки), и последовательности, кодирующие ген лекарственной устойчивости. Полинуклеотид по настоящему изобретению может быть линейным полинуклеотидом или циклическим полинуклеотидом (например, вектором). Вектор может представлять собой плазмидный вектор или вирусный вектор (например, аденовирусный или ретровирусный). Вектор также может быть, например, вектором для клонирования или для экспрессии. Вектор для экспрессии включает векторы для прокариотических клеток, таких как Escherichia coli или актиномицеты, и векторы для эукариотических клеток, таких как дрожжевые клетки, клетки насекомых или клетки млекопитающих.
[0075] Полинуклеотид по настоящему изобретению включает не только ДНК и РНК, но также известные химически модифицированные ДНК или РНК, описанные ниже. Для предупреждения деградации под действием гидролазах, таких как нуклеазы, фосфатный остаток (фосфат) каждого нуклеотида может быть заменен, например, химически модифицированным фосфатным остатком, таким как фосфоротиоат (PS), метилфосфонат или фосфородитионат. Гидроксильная группа в положении 2 рибозы каждого рибонуклеотида также может быть заменена на -OR (R представляет собой, например, CH3(2'-O-Me), CH2CH2OCH3(2'-O-MOE), CH2CH2NHC(NH)NH2, CH2CONHCH3 или CH2CH2CN). Кроме того, группа основания (пиримидинового, пуринового) может быть химически модифицирована, например, введением метильной группы или катионной функциональной группы в положение 5 пиримидинового основания или замещением карбонильной группы в положении 2 тиокарбонилом. Кроме того, полинуклеотиды по настоящему изобретению также включают, не ограничиваясь этим, полинуклеотиды, образованные модификацией фосфатной группы или гидроксильной группы, например, биотином, аминогруппой, низшей алкиламиногруппой или ацетильной группой. Термин «полинуклеотид» включает не только природные нуклеиновые кислоты, но также BNA (мостиковые нуклеиновые кислоты), LNA (замкнутые нуклеиновые кислоты) и PNA (пептидные нуклеиновые кислоты).
[0076] 4. Клетка
В одном варианте осуществления настоящее изобретение относится к клетке, содержащей полинуклеотид по настоящему изобретению (которая может относиться к «клетке по настоящему изобретению» в настоящем описании). Клетка по настоящему изобретению описана ниже.
[0077] Клетки, из которых происходят клетки по настоящему изобретению, особым образом не ограничиваются. С целью использования клетки по настоящему изобретению для получения GD2-связывающей молекулы по настоящему изобретению, то можно, например, использовать клетки, которые можно использовать для экспрессии белка (например, клетки насекомых, эукариотические клетки, клетки млекопитающих) используются в качестве исходных клеток.
[0078] Когда клетка по настоящему изобретению содержит полинуклеотид, кодирующий химерный антигенный рецептор по настоящему изобретению, то клетка предпочтительно представляет собой Т-клетку. Т-клетка предпочтительно представляет собой клетку, экспрессирующую химерный антигенный рецептор по настоящему изобретению. В более конкретном варианте осуществления Т-клетки по настоящему изобретению химерный антигенный рецептор по настоящему изобретению экспрессируется на клеточной мембране и предпочтительно экспрессируется в таком состоянии, что GD2-связывающий домен экспонируется снаружи клеточной мембраны.
[0079] Т-клетка или тому подобное, экспрессирующая химерный антигенный рецептор, распознает GD2 в GD2-связывающем домене, и затем внутриклеточно переносит сигнал распознавания для активации сигнала, индуцирующего цитотоксическую активность. В связи с этим клетка «атакует» другие клетки или ткани, экспрессирующие GD2, или проявляет цитотоксическую активность.
[0080] Когда клеткой, проявляющей такую функцию, является CTL, то такая клетка называется «Т-клеткой с химерным антигенным рецептором» («CAR-T-клетка»). Клетки, которые потенциально могут проявлять цитотоксическую активность, такие как NK-клетки, также могут проявлять цитотоксическую активность, когда GD2-связывающий домен связывается с GD2, как с Т-клеточным химерным антигенным рецептором. Таким образом, клетка-хозяин, содержащая полинуклеотид, кодирующий химерный антигенный рецептор (в частности, клетка-хозяин, обладающая цитотоксической активностью), является пригодной в качестве активного ингредиента фармацевтических композиций.
[0081] Такие CAR-T-клетки и т.п. применимы для лечения или профилактики рака и т.п., поскольку они специфически распознают раковую ткань (опухолевую ткань). Тип рака особым образом не ограничивается и включает солидную опухоль и рак крови. Примеры солидного рака включают рак легких, колоректальный рак, рак яичника, рак молочной железы, опухоль головного мозга, рак желудка, рак печени, рак языка, рак щитовидной железы, рак почки, рак предстательной железы, рак матки, остеосаркому, хондросаркому, рабдомиосаркому, меланому, нейробластому, рак мочевого пузыря и тому подобное.
[0082] Клетку по настоящему изобретению можно получить введением полинуклеотида по настоящему изобретению в клетки. При необходимости клетки, содержащие полинуклеотид по настоящему изобретению, можно сконцентрировать или можно сконцентрировать с использованием специфического маркера (антигена CD, такого как CD8) в качестве индикатора.
[0083] 5. Фармацевтическая композиция
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей Т-клетку с химерным антигенным рецептором или NK-клетку с химерным антигенным рецептором, содержащую полинуклеотид, кодирующий химерный антигенный рецептор по настоящему изобретению, или антитело по настоящему изобретению (которая может относиться к «фармацевтической композиции по настоящему изобретению» в настоящем описании). Фармацевтическая композиция по настоящему изобретению описана ниже.
[0084] Содержание клетки или антитела в фармацевтической композиции может быть соответствующим образом установлено с учетом типа целевого заболевания (например, солидного рака), желаемых терапевтических эффектов, способа введения, периода лечения, возраста пациента, массы тела пациента и т.д., например, содержание антитела в фармацевтической композиции может составлять примерно от 0,001 частей по массе до 10 частей по массе в расчете на 100 частей по массе всей фармацевтической композиции. Содержание клеток в фармацевтической композиции может составлять, например, примерно от 1 клетки/мл до 104 клеток/мл.
[0085] Форма введения фармацевтической композиции особым образом не ограничивается, при условии, что достигаются желаемые эффекты. Фармацевтическую композицию можно вводить млекопитающим, включая человека, любым из следующих способов введения: пероральное введение и парентеральное введение (например, внутривенная инъекция, внутримышечная инъекция, подкожное введение, ректальное введение, накожное введение и местное введение). Поскольку активным ингредиентом является клетка, то форма введения предпочтительно представляет собой парентеральное введение и более предпочтительно внутривенную инъекцию. Лекарственные формы для перорального введения и парентерального введения, а также способы их получения хорошо известны специалисту в данной области. Фармацевтическую композицию можно получить обычным способом, например, смешиванием антитела или клетки по настоящему изобретению с фармацевтически приемлемым носителем и т.д.
[0086] Примеры лекарственных форм для парентерального введения включают препараты для инъекций (например, внутривенные капельные вливания, внутривенные инъекции, внутримышечные инъекции, подкожные инъекции и эндодермальные инъекции), препараты для наружного применения (например, мази, катаплазмы и лосьоны), суппозитории, ингалянты, глазные капли, глазные мази, назальные капли, ушные капли, липосомальные агенты и т.п. Например, препарат для инъекций можно приготовить растворением или суспендированием антитела или клеток в дистиллированной воде для инъекций и необязательного добавлением солюбилизатора, буфера, регулятора pH, изотонического агента, успокаивающего агента, консерванта, стабилизатора, и т.д. Фармацевтическую композицию также можно использовать в виде лиофилизированного препарата, приготовленного перед применением.
[0087] Фармацевтическая композиция может дополнительно содержать другие лекарственные средства, эффективные для лечения или профилактики заболеваний. Фармацевтическая композиция может также содержать такие компоненты, как стерилизаторы, противовоспалительные средства, клеточные активаторы, витамины и аминокислоты, если это необходимо.
[0088] В качестве носителя, используемого для формуляции фармацевтической композиции, можно использовать эксципиенты, связующие вещества, дезинтеграторы, смазывающие вещества, красители и ароматизаторы, которые обычно используются в этой области техники; и также могут быть необязательно использованы стабилизаторы, эмульгаторы, усилители абсорбции, поверхностно-активные вещества, регуляторы pH, антисептики, антиоксиданты, наполнители, увлажнители, активаторы поверхности, диспергаторы, буферы, консерванты, солюбилизаторы, успокаивающие агенты и т.п.
[0089] Тип заболевания, которое лечится или профилактируется с использованием фармацевтической композиции особым образом не ограничивается, если лечение или профилактика могут быть достигнуты. Примеры конкретных целевых заболеваний включают опухоли. Предпочтительные примеры опухолей включают GD2-позитивные опухоли. Тип опухоли особым образом не ограничивается и включает солидную опухоль и рак крови. Примеры солидного рака включают рак легкого (в частности, мелкоклеточный рак легкого), колоректальный рак, рак яичника, рак молочной железы, опухоль головного мозга, рак желудка, рак печени, рак языка, рак щитовидной железы, рак почки, рак предстательной железы, рак матки, остеосаркому, хондросаркому, рабдомиосаркому, меланому, нейробластому, рак мочевого пузыря и т.п.
[0090] Целевым субъектом для введения (испытуемым субъектом) фармацевтической композиции является, например, животное, страдающее заболеванием, описанным выше, или животное с потенциальным риском развития такого заболевания. «Потенциальный риск развития такого заболевания» можно определить с использованием известного диагностического метода. Животное представляет собой, например, млекопитающее и предпочтительно человека.
[0091] Дозу фармацевтической композиции может определить лечащий врач с учетом различных факторов, таких как путь введения, тип заболевания, степень выраженности симптомов, возраст, пол и масса тела пациента, тяжесть заболевания, фармакологические данные, такие как фармакокинетика и токсикологические характеристики, использование или неиспользование системы доставки лекарственного средства и то, вводится ли композиция в виде части комбинированного лекарственного средства с другими лекарственными средствами. Например, когда активным ингредиентом является антитело, то доза фармацевтической композиции может составлять примерно от 1 мкг/кг (массы тела) до 10 г/кг (массы тела) в сутки. Когда активным ингредиентом является клетка, то доза может составлять примерно от 104 клеток/кг (массы тела) до 109 клеток/кг (массы тела). Схема введения фармацевтической композиции также может быть определена с учетом тех же факторов, что и при определении дозы. Например, композицию можно вводить от одного раза в сутки до одного раза в месяц в суточной дозе, приведенной выше.
Примеры
[0092] Настоящее изобретение подробно описано ниже со ссылкой на примеры. Однако настоящее изобретение не ограничивается приведенными примерами.
[0093] Материалы и экспериментальные методы
Если не указано иное, то в экспериментальных примерах использовали следующие материалы и методы.
[0094] (1) Клетка
Клетки Carney и AS были получены от доктора Old. IMR32, CEM, Kokl-3 и MOLT4 были получены от доктора Old/Ueda. YTN17 были получены от доктора Yodoi, и сублиния N1 клеток SK-MEL-28 была предоставлена доктором Lloyd. NCI-417, ACC-LC-171, ACC-LC-96 и ACC-LC-17 были предоставлены доктором Takashi Takahashi. Клетки C-2 D-18 получали введением GD3 синтазы в ACC-LC-17. GD2-экспрессирующие клетки S1 и S6 получали введением в сублинию N1 (GD3, не экспрессирующая GD3) клеток SK-MEL-28 pCDNA3.1neo, в который были включены кДНК GD3 синтазы и GM2/GD2 синтазы. Клетки V4 и V9 представляют собой клетки, в которые был введен пустой вектор pCDNA3.1neo.
[0095] (2) Антитело
Кроличье антитело против человеческой каппа-цепи (159) было получено от MBL. Alexa 488-меченное антикроличье IgG антитело (A11034) было получено от Invitrogen. PE-меченное антитело против GITRL (FAB6941P) было получено от BioLegend. PE-меченное антитело против человеческого 4-1BB (311504) было получено от BioLegend. PE-меченное антитело против ICOSL человека (309404) было получено от BioLegend. АРС-меченное антитело против человеческого CD4 (клон RPA-T4) было получено от Invitrogen. PE-меченное антитело против человеческого CD4 (555347) было получено от BD. APC/Cy7-меченное антитело против человеческого CD8 (клон HT8a) было получено от BioLegend. FITC-меченное антитело против человеческого Vd2 (клон B6, 331418) было получено от BioLegend. V450-меченное антитело против человеческого IFNγ (клон 45.83, 48-7319-42) было получено от BD Pharmingen. PE/Cy7-меченное антитело против человеческого TNFα (клон Mab11, 12-7349-82) было получено от eBioscience. АРС-меченное антитело против человеческого CD107a (560664) было получено от BD Pharmingen.
[0096] (3) Конструирование CAR экспрессионной плазмиды, получение ретровируса, карты и последовательности
CD1928 и CD1928z GITRL, приготовленные Eurofins, подвергали ферментативной обработке рестриктазами NotI и XhoI и рекомбинировали с pMS3 с получением плазмидных векторов. Экспрессионные векторы с люциферазой NGFR готовили обработкой этих указанных двух, полученных Eurofins обычным синтезом, с NotI и ClaI, и ClaI и XhoI соответственно, и их рекомбинацией в pMS3. Их вводили в Plat-A с использованием FuGENE с получением ретровирусов. Метод выполняли в соответствии с инструкциями производителя.
[0097] (4) Культивирование PBMC и перенос ретровирусного гена
После иммобилизации 2 мкг OKT3 и 10 мкг ретронектина в 12-луночном планшете мононуклеарные клетки периферической крови, доведенные Ficoll, культивировали в GT-T551 с добавлением 0,6% человеческой плазмы и IL-2 в конечной концентрации 600 Е/мл, собирали на сутки 4, инфицировали ретровирусами, иммобилизовали при 42°С в течение 2 ч при 2000×g, и культивировали.
Гамма/дельта-клетки готовили по методу Tanaka et al. Гамма/дельта-клетки (полученные культивированием мононуклеарных клеток периферической крови в среде YM-AB, содержащей новый препарат на основе бисфосфоната (PTA), с добавлением 25 нг/мл IL-7 и 25 нг/мл IL-15, и сбором их на сутки 4) инфицировали и культивировали в той же среде.
[0098] (5) Подтверждение экспрессии CAR и GITRL
Для оценки экспрессии CAR, анти-каппа-антитело подвергали реакции при 10 мкг/мл с последующим промыванием; Alexa 488-меченный антикроличий IgG (Invitrogen) реагировал при 5 мкг/мл с последующим промыванием; выполняли окрашивание APC/Cy7-меченным антителом против человеческого CD8 (BD) и APC-меченным антителом против человеческого CD4 (BioLegend); и измерение выполняли с использованием анализа FACSCanto. Для оценки экспрессии GITRL, PE-меченное антитело против человеческого GITRL (BioLegend) разбавляли в 100 раз и подвергали реакции, и измерение проводили с помощью анализа FACSCanto. Внутриклеточное окрашивание GITRL с использованием BD Cytofix/Cytoperm и BD Perm/Wash выполняли с использованием PE-меченного антитела против человеческого GITRL (BioLegend). Метод выполняли в соответствии с инструкциями производителя.
[0099] (6) Внутриклеточное окрашивание
После смешивания CAR-трансдуцированных PBMC и клеток-мишеней клетки подвергали взаимодействию с APC-меченным антителом против человеческого CD107a и культивировали в CO2-инкубаторе в течение 1 ч. После этого давали возможность действовать реагенту GolgiStop, и проводили культивирование в CO2-инкубаторе в течение 4 ч с последующим промыванием. Выполняли окрашивание антителом против человеческой каппа и Alexa 488-меченным антикроличьим IgG антителом и затем проводили окрашивание APC/Cy7-меченным антителом против человеческого CD8 и PE-меченным антителом против человеческого CD4. После обработки реагентами BD Cytofix/Cytoperm и BD Perm/Wash выполняли окрашивание V450-меченным антителом против человеческого IFNγ и PE/Cy7-меченным антителом против человеческого TNFα.
[0100] (7) Анализ xCELLigence
1,5×104 клеток-мишеней AS, суспендированных в 100 мкл среды RPMI 1640 с добавлением 10% FCS, помещали и выдерживали в СО2-инкубаторе на 24 ч. После этого помещали 1,5×104 эффекторных клеток, суспендированных в 100 мкл среды RPMI 1640 с добавлением 10% FCS, и регистрировали последующие изменения тока.
[0101] (8) Нерадиоактивный анализ цитотоксичности
Эксперимент проводили в соответствии с инструкциями производителя. В частности, сначала 4×105 клеток-мишеней AS суспендировали в 400 мкл 10% FCS/PRMI 1640 и добавляли к ним 1 мкл раствора BM-HT с последующим культивированием в CO2-инкубаторе в течение 15 мин. После промывания готовили 5×103 клеток и добавляли к ним 50×103, 15×103 и 5×103 CAR-T-клеток, клетки сокультивировали в течение 2 ч, и затем центрифугировали для сбора 25 мкл супернатанта. К этому добавляли 250 мкл раствора EU с последующим перемешиванием. После этого измеряли люминесценцию с помощью многофункционального ридера TriStar2 SLB942 (Berthold Technologies).
[0102] Экспериментальный пример 1: выделение моноклонального антитела
Мышей Balb/c x C57BL/6 F1 иммунизировали тремя подкожными инокуляциями клеток IMR32, и собранные клетки селезенки подвергали слиянию с клетками NS-1 с последующим культивированием в среде RPMI 1640, содержащей 10% FCS и HAT, с получением тем самым моноклональных антител. Полученные антитела подвергали скринингу с использованием проточной цитометрии для распознавания клеток IMR32. Далее получали субклоны полученного клона 220, и получали 220-51.
[0103] Экспериментальный пример 2: анализ антигенной специфичности 1
Антигенную специфичность антитела 220-51 анализировали с использованием ELISA. Ганглиозиды GD1a, GD1b, GD2, GD3, GM1, GM3, GT1b и лактозилцерамид (по 50 нг каждого) иммобилизовали метанолом. Каждое серийно разбавленное асцитное антитело подвергали реакции, и обеспечивали реагирование HRP-меченного антимышиного IgG антитела (Southern Biotech). Окрашивание развивали с помощью OPD и измеряли оптическую плотность.
[0104] На фиг. 1 приведены результаты. Антитело 220-51 распознавало только GD2 и не распознавало другие ганглиозиды.
[0105] Экспериментальный пример 3: анализ антигенной специфичности 2
Антигенную специфичность антитела 220-51 анализировали с использованием тонкослойной хроматографии. Смесь бычьих ганглиозида и GM3 и ганглиозидов, полученных из опухолевых клеток SK-MEL-23 (Carney2) и AS, анализировали тонкослойной хроматографией и переносили на мембрану PVDF с помощью промокательной термобумаги (ATTO TLC Thermal Blotter AC5970), Atto, Tokyo), и затем подвергали взаимодействию с антителом 220-51. После этого обеспечивали реакцию HRP-конъюгированного антимышиного IgG (цельный) (Cell Signaling), которые представляют собой HRP-меченные антимышиные вторичные антитела с последующей эмиссией света с использованием Western LightningTM Plus ECL (PerkinElmer Inc., Waltham, MA).
[0106] На фиг. 2 приведены результаты. Антитело 220-51 распознавало только GD2 и не распознавало другие ганглиозиды.
[0107] Экспериментальный пример 4: распознавание клеток, экспрессирующих GD2
1×105 клеток обрабатывали 100-кратно разведенным антителом в 0,5% BSA/PBS при комнатной температуре в течение 30 мин, промывали, обрабатывали FITC-меченым антимышиным IgG антителом (Cappel), промывали PBS и анализировали с использованием FACS Caliver или Accuri C6.
[0108] На фиг. 3 приведены результаты. Антитело 220-51 распознавало GD2+ AS, IMR32, Kohl-3 (SK-MEL-31) и YTN17, но не распознавало GD2- CEM или MOLT4.
[0109] Экспериментальный пример 5: ингибирование клеточной адгезии
Клетки GD2+ меланомы S1 и S6 и клетки GD2- V4 и V9 (количество клеток: 1×104) высевали на планшет, на котором был иммобилизован коллаген, и анализировали адгезию с использованием RT-CES, когда антитело 220-51 разводили в 50 раз и подвергали реакции, через 0,5 ч и 3 ч (S1-T: добавление антитела к S1).
[0110] На фиг. 4 приведены результаты. Антитело 220-51 ингибировало адгезию GD2+ клеток S1 и S6, но не ингибировало адгезию клеток GD2- V4 или V9.
[0111] Экспериментальный пример 6: анализ последовательности
Анализировали аминокислотную последовательность антитела 220-51 и нуклеотидную последовательность, кодирующую антитело. Результаты анализа представлены ниже. Последовательности CDR были выведены с использованием IMGIT.
[0112] Тяжелая цепь
Аминокислотная последовательность CDR1 тяжелой цепи: GFSLPSYG (SEQ ID NO: 1)
Аминокислотная последовательность CDR2 тяжелой цепи: IWAGGITN (SEQ ID NO: 2)
Аминокислотная последовательность CDR3 тяжелой цепи: ARGGSDYDGFAY (SEQ ID NO: 3)
Аминокислотная последовательность вариабельной области тяжелой цепи:
EVQLVESGPGLVAPSQSLSITCTVSGFSLPSYGVHWVRQPPGKGLEWLGVIWAGGITNYNSALMSRLTISKDNSKSQVFLKMNSLQTDDTAIYYCARGGSDYDGFAYWGQGTLVTVS (SEQ ID NO: 4)
Нуклеотидная последовательность CDR1 тяжелой цепи: GGG TTT TCA TTA CCC AGC TAT GGT (SEQ ID NO: 5)
Нуклеотидная последовательность CDR2 тяжелой цепи: ATC TGG GCT GGT GGA ATC ACA AAT (SEQ ID NO: 6)
Нуклеотидная последовательность CDR3 тяжелой цепи: GCC AGA GGC GGC TCT GAT TAC GAC GGC TTT GCT TAC (SEQ ID NO: 7)
Нуклеотидная последовательность вариабельной области тяжелой цепи:
GAGGTGCAGCTGGTGGAGTCTGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCATCACTTGCACTGTCTCTGGGTTTTCATTACCCAGCTATGGTGTTCACTGGGTTCGCCAGCCTCCAGGAAAGGGTCTGGAGTGGCTGGGAGTAATCTGGGCTGGTGGAATCACAAATTATAACTCGGCTCTCATGTCCAGACTGACCATCAGCAAAGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTTCAAACTGATGACACAGCCATATACTACTGTGCCAGAGGCGGCTCTGATTACGACGGCTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCATCA (SEQ ID NO: 8)
[0113] Легкая цепь
Аминокислотная последовательность CDR1 легкой цепи: QSLLSSRTRKNY (SEQ ID NO: 9)
Аминокислотная последовательность CDR2 легкой цепи: WAS (SEQ ID NO: 10)
Аминокислотная последовательность CDR3 легкой цепи: KQSYNLRT (SEQ ID NO: 11)
Аминокислотная последовательность вариабельной области легкой цепи:
DIVMTQSPSSLAVSAGEKVTMNCRSSQSLLSSRTRKNYLAWYQQKPGQSPKLLIYWASIRESGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCKQSYNLRTFGGGTKLEIK (SEQ ID NO: 12)
Нуклеотидная последовательность CDR1 легкой цепи: CAG AGT CTC CTC AGC AGT AGA ACC CGA AAG AAC TAC (SEQ ID NO: 13)
Нуклеотидная последовательность CDR2 легкой цепи: TGG GCA TCT (SEQ ID NO: 14)
Нуклеотидная последовательность CDR3 легкой цепи: AAG CAA TCT TAT AAT CTT CGG ACG (SEQ ID NO: 15)
Нуклеотидная последовательность вариабельной области легкой цепи:
GACATTGTGATGACACAGTCTCCATCCTCCCTGGCTGTGTCAGCAGGAGAGAAGGTCACTATGAACTGCAGATCCAGTCAGAGTCTCCTCAGCAGTAGAACCCGAAAGAACTACTTGGCTTGGTACCAGCAGAAACCAGGGCAGTCTCCTAAACTGCTGATCTACTGGGCATCTATTAGGGAATCTGGGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGGACAGATTTCACTCTCACCATCAGCAGTGTGCAGGCTGAAGACCTGGCAGTTTATTACTGCAAGCAATCTTATAATCTTCGGACGTTCGGTGGAGGCACCAAGCTGGAAATCAAA (SEQ ID NO: 16)
[0114] Экспериментальный пример 7: конструирование CAR экспрессионной плазмиды
Четыре CAR (28z CAR, zG CAR, 28z GITRL CAR и zG GITRL CAR) были сконструированы с использованием аминокислотной последовательности антитела 220-51 (на фиг. 5 схематично показаны структуры). Были приготовлены экспрессионные плазмиды для этих CAR. В частности, экспрессионные плазмиды готовили следующим образом.
[0115] Для 28z CAR и zG CAR с помощью Eurofins были созданы искусственные гены следующих двух последовательностей, вырезали NotI и XhoI и вставляли в pMS3 с получением экспрессионных плазмид.
[0116] Нуклеотидная последовательность искусственного гена для получения 28z CAR
Сайт NotI в последовательности Козака: GCGGCCGCCACC (SEQ ID NO: 17)-
лидерная последовательность mVH:
ATGAACTTTGGGCTCAGATTGATTTTCCTTGTCCTTACTTTAAAAGGTGTGAAGTGT (SEQ ID NO: 18)-
mVH: GAGGTGCAGCTGGTGGAGTCTGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCATCACTTGCACTGTCTCTGGGTTTTCATTACCCAGCTATGGTGTTCACTGGGTTCGCCAGCCTCCAGGAAAGGGTCTGGAGTGGCTGGGAGTAATCTGGGCTGGTGGAATCACAAATTATAACTCGGCTCTCATGTCCAGACTGACCATCAGCAAAGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTTCAAACTGATGACACAGCCATATACTACTGTGCCAGAGGCGGCTCTGATTACGACGGCTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCATCA (SEQ ID NO: 19)-
одинарная цепь:
GGAGGTGGAGGTTCTGGTGGAGGAGGTTCAGGTGGAGGTGGATCA(SEQ ID NO: 20)-
mVкаппа:
GACATTGTGATGACACAGTCTCCATCCTCCCTGGCTGTGTCAGCAGGAGAGAAGGTCACTATGAACTGCAGATCCAGTCAGAGTCTCCTCAGCAGTAGAACCCGAAAGAACTACTTGGCTTGGTACCAGCAGAAACCAGGGCAGTCTCCTAAACTGCTGATCTACTGGGCATCTATTAGGGAATCTGGGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGGACAGATTTCACTCTCACCATCAGCAGTGTGCAGGCTGAAGACCTGGCAGTTTATTACTGCAAGCAATCT TAT AAT CTT CGG ACG TTC GGT GGA GGC ACC AAG CTG GAA ATC AAA (SEQ ID NO: 21)-
hCкаппа: CGAACTGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCGGACTACGAGAAACACAAACTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGTGGCGCGCCA (SEQ ID NO: 22)-
трансмембранный домен hCD28:
ACTAGATTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTGAGG (SEQ ID NO: 23)-
Внутриклеточный домен hCD28:
AGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCC(SEQ ID NO: 24)-
hCD3 дзета:
CTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGCAGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC (SEQ ID NO: 25)TAA-
Сайт XhoI: TCGATTCTCGAG (SEQ ID NO: 26)
Аминокислотная последовательность 28z CAR
лидерная последовательность mVH: MNFGLRLIFLVLTLKGVKC (SEQ ID NO: 27)-
mVH:
EVQLVESGPGLVAPSQSLSITCTVSGFSLPSYGVHWVRQPPGKGLEWLGVIWAGGITNYNSALMSRLTISKDNSKSQVFLKMNSLQTDDTAIYYCARGGSDYDGFAYWGQGTLVTVS (SEQ ID NO: 28)-
одинарная цепь: GGGGSGGGGSGGGGS (SEQ ID NO: 29)-
mVкаппа:
DIVMTQSPSSLAVSAGEKVTMNCRSSQSLLSSRTRKNYLAWYQQKPGQSPKLLIYWASIRESGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCKQSYNLRTFGGGTKLEIK (SEQ ID NO: 30)-
hCкаппа:
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKLYACEVTHQGLSSPVTKSFNRGECGAP (SEQ ID NO: 31)-
трансмембанный домен hCD28:
TRFWVLVVVGGVLACYSLLVTVAFIIFWVR (SEQ ID NO: 32)-
внутриклеточный домен hCD28:
SKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRS (SEQ ID NO: 33)-
hCD3 дзета:
LRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPQRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR* (SEQ ID NO: 34)-
Нуклеотидная последовательность искусственного гена для получения zG CAR
Сайт NotI в последовательности Козака: GCGGCCGCCACC (SEQ ID NO: 17)-
лидерная последовательность mVH:
ATGAACTTTGGGCTCAGATTGATTTTCCTTGTCCTTACTTTAAAAGGTGTGAAGTGT (SEQ ID NO: 18)-
mVH:
GAGGTGCAGCTGGTGGAGTCTGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCATCACTTGCACTGTCTCTGGGTTTTCATTACCCAGCTATGGTGTTCACTGGGTTCGCCAGCCTCCAGGAAAGGGTCTGGAGTGGCTGGGAGTAATCTGGGCTGGTGGAATCACAAATTATAACTCGGCTCTCATGTCCAGACTGACCATCAGCAAAGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTTCAAACTGATGACACAGCCATATACTACTGTGCCAGAGGCGGCTCTGATTACGACGGCTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCATCA (SEQ ID NO: 19)-
одинарная цепь:
GGAGGTGGAGGTTCTGGTGGAGGAGGTTCAGGTGGAGGTGGATCA (SEQ ID NO: 20)-
mVкаппа:
GACATTGTGATGACACAGTCTCCATCCTCCCTGGCTGTGTCAGCAGGAGAGAAGGTCACTATGAACTGCAGATCCAGTCAGAGTCTCCTCAGCAGTAGAACCCGAAAGAACTACTTGGCTTGGTACCAGCAGAAACCAGGGCAGTCTCCTAAACTGCTGATCTACTGGGCATCTATTAGGGAATCTGGGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGGACAGATTTCACTCTCACCATCAGCAGTGTGCAGGCTGAAGACCTGGCAGTTTATTACTGCAAGCAATCT TAT AAT CTT CGG ACG TTC GGT GGA GGC ACC AAG CTG GAA ATC AAA (SEQ ID NO: 21)-
hCкаппа: CGAACTGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCGGACTACGAGAAACACAAACTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGTGGCGCGCCA (SEQ ID NO: 22)-
трансмембранный домен hCD28:
ACTAGATTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTGAGG (SEQ ID NO: 23)-
hCD3 дзета:
CTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGCAGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC (SEQ ID NO: 25)-
внутриклеточный домен hGITR:
AGGAGTCAGTGCATGTGGCCCCGAGAGACCCAGCTGCTGCTGGAGGTGCCGCCGTCGACCGAAGACGCCAGAAGCTGCCAGTTCCCCGAGGAAGAGCGGGGCGAGCGATCGGCAGAGGAGAAGGGGCGGCTGGGAGACCTGTGGGTG (SEQ ID NO: 35)TAA-
сайт XhoI: TCGATTCTCGAG (SEQ ID NO: 26)
Аминокислотная последовательность zG CAR
лидерная последовательность mVH: MNFGLRLIFLVLTLKGVKC (SEQ ID NO: 27)-
mVH:
EVQLVESGPGLVAPSQSLSITCTVSGFSLPSYGVHWVRQPPGKGLEWLGVIWAGGITNYNSALMSRLTISKDNSKSQVFLKMNSLQTDDTAIYYCARGGSDYDGFAYWGQGTLVTVS (SEQ ID NO: 28)-
одинарная цепь: GGGGSGGGGSGGGGS (SEQ ID NO: 29)-
mVкаппа:
DIVMTQSPSSLAVSAGEKVTMNCRSSQSLLSSRTRKNYLAWYQQKPGQSPKLLIYWASIRESGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCKQSYNLRTFGGGTKLEIK (SEQ ID NO: 30)-
hCкаппа:
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKLYACEVTHQGLSSPVTKSFNRGECGAP (SEQ ID NO: 31)-
трансмембранный домен hCD28: TRFWVLVVVGGVLACYSLLVTVAFIIFWVR (SEQ ID NO: 32)-
hCD3 дзета:
LRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPQRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR (SEQ ID NO: 34)-
внутриклеточный домен hGITR:
RSQCMWPRETQLLLEVPPSTEDARSCQFPEEERGERSAEEKGRLGDLWV* (SEQ ID NO: 36)
Для 28z GITRL CAR, экспрессионную плазмиду, в которую включали следующую нуклеотидную последовательность P2A-GITRL рядом с 3'-стороной нуклеотидной последовательности SEQ ID NO: 25, получали экспрессионную плазмиду 28z CAR, с использованием искусственного гена и ПЦР.
Нуклеотидная последовательность P2A-GITRL:
GGATCCGGCGCCACAAATTTTAGCCTCTTGAAGCAAGCCGGCGACGTGGAAGAGAATCCTGGGCCC (нуклеотидная последовательность P2A: SEQ ID NO: 37)-
ATGACCCTGCACCCCAGCCCCATCACCTGCGAGTTCCTGTTCAGCACCGCCCTGATCAGCCCCAAGATGTGCCTGAGCCACCTGGAGAACATGCCCCTGAGCCACAGCAGAACCCAGGGCGCCCAGAGAAGCAGCTGGAAGCTGTGGCTGTTCTGCAGCATCGTGATGCTGCTGTTCCTGTGCAGCTTCAGCTGGCTGATCTTCATCTTCCTGCAGCTGGAGACCGCCAAGGAGCCCTGCATGGCCAAGTTCGGCCCCCTGCCCAGCAAGTGGCAGATGGCCAGCAGCGAGCCCCCCTGCGTGAACAAGGTGAGCGACTGGAAGCTGGAGATCCTGCAGAACGGCCTGTACCTGATCTACGGCCAGGTGGCCCCCAACGCCAACTACAACGACGTGGCCCCCTTCGAGGTGAGACTGTACAAGAACAAGGACATGATCCAGACCCTGACCAACAAGAGCAAGATCCAGAACGTGGGCGGCACCTACGAGCTGCACGTGGGCGACACCATCGACCTGATCTTCAACAGCGAGCACCAGGTGCTGAAGAACAACACCTACTGGGGCATCATCCTGCTGGCCAACCCCCAGTTCATCAGC (нуклеотидная последовательность GITRL: SEQ ID NO: 38)
Аминокислотная последовательность P2A-GITRL является следующей: GSGATNFSLLKQAGDVEENPGP (аминокислотная последовательность P2A SEQ ID NO: 39)-
MTLHPSPITCEFLFSTALISPKMCLSHLENMPLSHSRTQGAQRSSWKLWLFCSIVMLLFLCSFSWLIFIFLQLETAKEPCMAKFGPLPSKWQMASSEPPCVNKVSDWKLEILQNGLYLIYGQVAPNANYNDVAPFEVRLYKNKDMIQTLTNKSKIQNVGGTYELHVGDTIDLIFNSEHQVLKNNTYWGIILLANPQFIS (аминокислотная последовательность GITRL: SEQ ID NO: 40).
[0117] Для zG GITRL CAR, получали экспрессионную плазмиду, в которую включали нуклеотидную последовательность P2A-GITRL рядом с 3'-стороной нуклеотидной последовательности SEQ ID NO: 35 экспрессионной плазмиды zG CAR, с использованием искусственного гена и ПЦР.
[0118] Экспериментальный пример 8: введение гена CAR в Т-клетку и подтверждение экспрессии
Каждую плазмидную ДНК, сконструированную, как описано выше, вводили в клетки Plat-A для получения ретровирусов. Культивированные РВМС человека инфицировали ретровирусами для получения Т-клеток, трансдуцированных CAR, и экспрессию CAR анализировали с использованием проточной цитометрии. Экспрессия CAR и лиганда была подтверждена в альфа/бета Т-клетках, как показано на фиг. 6-11, и в гамма/дельта Т-клетках, как показано на фиг. 12 и 13. Они являются эффекторными клетками. Было подтверждено, что эффективность экспрессии и интенсивность экспрессии (указанные по средней интенсивности флуоресценции; MFI) CAR повышались при коэкспрессии с GITRL (фиг. 6-8).
[0119] Экспериментальный пример 9: распознавание клетки-мишени эффекторной клеткой
CAR-T-клетки активируются и экспрессируют IFNγ и TNFα при сокультивировании с клетками-мишенями AS. Кроме того, CD107a транспортируется на поверхность клетки. Эти реакции указывают на то, что произошли многофункциональные реакции. Было подтверждено, что все виды CAR-T-клеток, полученных в данном эксперименте, активировались сокультивированием с клетками AS, и что происходили указанные ответные реакции (фиг. 14-16).
[0120] Экспериментальный пример 10: подтверждение цитотоксического действия эффекторной клетки
Цитотоксическое действие эффекторных клеток на клетки АС оценивали по изменениям во времени с помощью анализа xCELLigence. Результаты показали, что GD2 CAR обладал достаточной цитотоксической активностью в альфа/бета Т-клетках и гамма/дельта Т-клетках (фиг. 17 и 18). Это также наблюдали в нерадиоактивном анализе цитотоксичности (фиг. 19).
[0121] Экспериментальный пример 11: анализ 1 цитотоксического действия эффекторной клетки
После того, как GD2-позитивные клетки Kelly (20000 клеток) культивировали в Е-планшете в течение 20 ч, добавляли и культивировали каждый вид эффекторных клеток (альфа/бета) (40000 клеток), и определяли клеточный индекс во времени. Клеточный индекс отражает количество клеток Kelly на Е-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток Kelly непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Наблюдали эффективную цитотоксичность GD2 28z, GD2 zG и GITRL-коэкспрессирующих GD2 28z CAR-T-клеток, и не наблюдали цитотоксичности PBMC, в которые не вводили CAR (фиг. 20).
[0122] Экспериментальный пример 12: анализ 2 цитотоксического действия эффекторной клетки
После того, как GD2-негативные клетки SK-N-SH (20000 клеток) культивировали в E-планшете в течение 18 ч, каждому типу эффекторных клеток (альфа/бета) (40000 клеток) давали возможность воздействовали на них, и анализировали клеточный индекс во времени. Клеточный индекс отражает количество клеток SK-N-SH в Е-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток SK-N-SH непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Не наблюдали цитотоксичности для GD2 28z, GD2 zG или GITRL-коэкспрессирующих GD2 28z CAR-T-клеток (фиг. 21).
[0123] Экспериментальный пример 13: анализ 3 цитотоксического действия эффекторной клетки
После того, как GD2-позитивные клетки Hs578T-Luc (15000 клеток) культивировали в E-планшете в течение 20 ч, каждому виду эффекторных клеток (альфа/бета) (40000 клеток) давали возможность воздействовать на них, и анализировали клеточный индекс во времени. Клеточный индекс отражает количество клеток Hs578T-Luc в E-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток Hs578T-Luc непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Наблюдали эффективную цитотоксичность GD2 28z, GD2 zG и GITRL-коэкспрессирующих GD2 28z CAR-T-клеток, и не наблюдали цитотоксичности PBMC, в которые не вводили CAR (фиг. 22).
[0124] Экспериментальный пример 14: анализ 4 цитотоксического действия эффекторной клетки
После того, как GD2-негативные клетки BT549-Luc (20000 клеток) культивировали в E-планшете в течение 18 ч, каждому типу эффекторных клеток (альфа/бета) (40000 клеток) давали возможность воздействовать на них, и анализировали клеточный индекс во времени. Клеточный индекс клеток отражает количество клеток BT549-Luc в E-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток BT549-Luc непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Не наблюдали цитотоксичности для GD2 28z или GITRL-коэкспрессирующих GD2 28z CAR-T-клеток (фиг. 23).
[0125] Экспериментальный пример 15: анализ 5 цитотоксического действия эффекторной клетки
После того, как GD2-позитивные клетки Kelly (20000 клеток) культивировали в Е-планшете в течение 20 ч, каждому типу эффекторных клеток (альфа/бета) (30000 клеток) давали возможность воздействовать на них, и анализировали клеточный индекс во времени. Через сутки наблюдали эффективную цитотоксичность GD2 28z и GITRL-коэкспрессирующих GD2 28z CAR-T-клеток. Эффекторные клетки собирали и последовательно сокультивировали с клетками Kelly, культивируемыми на Е-планшете в течение 24 ч, и регистрировали изменения клеточного индекса во времени. Клеточный индекс отражает количество клеток Kelly в Е-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток Kelly непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Во втором последовательном тесте на цитотоксичность клетки 28z CAR-T, коэкспрессирующие GITRL, сохраняли более высокую цитотоксическую активность, чем 28z CAR (фиг. 24).
[0126] Экспериментальный пример 16: анализ 6 цитотоксического действия эффекторной клетки
Клетки D8 представляют собой GD2-позитивную клеточную линию, созданную введением генов GD3 синтазы и GD2 синтазы в GD2-негативные клетки мелкоклеточной карциномы легкого SK-LC-17 и селекцией G418. После того, как GD2-позитивные клетки D8 (10000 клеток) культивировали в E-планшете в течение 18 ч, каждому типу эффекторных клеток (альфа/бета) (30000 клеток) давали возможность воздействовать на них, и анализировали клеточный индекс во времени. Клеточный индекс отражает количество клеток D8 в Е-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток D8 непосредственно перед совместным культивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Наблюдали эффективную цитотоксичность GD2 28z, GD2 zG и GITRL-коэкспрессирующих GD2 28z CAR-T-клеток, и не наблюдали цитотоксичности PBMC, в которые не вводили CAR (фиг. 25).
[0127] Экспериментальный пример 17: анализ 6 цитотоксического действия эффекторной клетки
Клетки C2 представляют собой GD2-негативную клеточную линию, полученную введением плазмиды pCDNA3.1neo в GD2-негативные клетки мелкоклеточной карциномы легкого SK-LC-17 и селекцией G418. После того, как GD2-негативные клетки C2 (10000 клеток) культивировали в E-планшете в течение 18 ч, каждому типу эффекторных клеток (альфа/бета) (30000 клеток) давали возможность воздействовать на них, и клеточный индекс анализировали во времени. Клеточный индекс отражает количество клеток С2 в Е-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток С2 непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Не наблюдали цитотоксичности для GD2 28z, GD2 zG, GITRL-коэкспрессирующих GD2 28z CAR-T-клеток или РВМС, в которые не вводили CAR (фиг. 26).
[0128] Экспериментальный пример 18: анализ 7 цитотоксического действия эффекторной клетки
После того, как GD2-позитивные клетки NCI-N417 (20000 клеток) культивировали в E-планшете в течение 34 ч, каждому виду эффекторных клеток (альфа/бета) (60000 клеток) давали возможность воздействовать на них, и анализировали клеточный индекс во времени. Клеточный индекс отражает количество клеток NCI-N417 в E-планшете. Нормализованный клеточный индекс представляет собой клеточный индекс, нормализованный в предположении, что количество клеток NCI-N417 непосредственно перед сокультивированием с эффекторными клетками равно 1. На графике приведены средние значения (n=2). Наблюдали эффективную цитотоксичность GD2 28z, GD2 zG и GITRL-коэкспрессирующих GD2 28z CAR-T-клеток, и не наблюдали цитотоксичности PBMC, в которые не вводили CAR (фиг. 27).
--->
Список последовательностей
<110> MIE UNIVERSITY
CHUBU UNIVERSITY EDUCATIONAL FOUNDATION
<120> GD2-СВЯЗЫВАЮЩАЯ МОЛЕКУЛА
<130> P20-177WO
<150> JP 2019-142358
<151> 2019-08-01
<160> 41
<170> PatentIn version 3.5
<210> 1
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> H CDR1
<400> 1
Gly Phe Ser Leu Pro Ser Tyr Gly
1 5
<210> 2
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> H CDR2
<400> 2
Ile Trp Ala Gly Gly Ile Thr Asn
1 5
<210> 3
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> H CDR3
<400> 3
Ala Arg Gly Gly Ser Asp Tyr Asp Gly Phe Ala Tyr
1 5 10
<210> 4
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная область H
<400> 4
Glu Val Gln Leu Val Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Pro Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ala Gly Gly Ile Thr Asn Tyr Asn Ser Ala Leu Met
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Ser Asp Tyr Asp Gly Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser
115
<210> 5
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> H CDR1
<400> 5
gggttttcat tacccagcta tggt 24
<210> 6
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> H CDR2
<400> 6
atctgggctg gtggaatcac aaat 24
<210> 7
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> H CDR3
<400> 7
gccagaggcg gctctgatta cgacggcttt gcttac 36
<210> 8
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариабельная область H
<400> 8
gaggtgcagc tggtggagtc tggacctggc ctggtggcgc cctcacagag cctgtccatc 60
acttgcactg tctctgggtt ttcattaccc agctatggtg ttcactgggt tcgccagcct 120
ccaggaaagg gtctggagtg gctgggagta atctgggctg gtggaatcac aaattataac 180
tcggctctca tgtccagact gaccatcagc aaagacaact ccaagagcca agttttctta 240
aaaatgaaca gtcttcaaac tgatgacaca gccatatact actgtgccag aggcggctct 300
gattacgacg gctttgctta ctggggccaa gggactctgg tcactgtctc tgcatca 357
<210> 9
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> L CDR1
<400> 9
Gln Ser Leu Leu Ser Ser Arg Thr Arg Lys Asn Tyr
1 5 10
<210> 10
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> L CDR2
<400> 10
Trp Ala Ser
1
<210> 11
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> L CDR3
<400> 11
Lys Gln Ser Tyr Asn Leu Arg Thr
1 5
<210> 12
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная область L
<400> 12
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Asn Cys Arg Ser Ser Gln Ser Leu Leu Ser Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Ile Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 13
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> L CDR1
<400> 13
cagagtctcc tcagcagtag aacccgaaag aactac 36
<210> 14
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> L CDR2
<400> 14
tgggcatct 9
<210> 15
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> L CDR3
<400> 15
aagcaatctt ataatcttcg gacg 24
<210> 16
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариабельная область L
<400> 16
gacattgtga tgacacagtc tccatcctcc ctggctgtgt cagcaggaga gaaggtcact 60
atgaactgca gatccagtca gagtctcctc agcagtagaa cccgaaagaa ctacttggct 120
tggtaccagc agaaaccagg gcagtctcct aaactgctga tctactgggc atctattagg 180
gaatctgggg tccctgatcg cttcacaggc agtggatctg ggacagattt cactctcacc 240
atcagcagtg tgcaggctga agacctggca gtttattact gcaagcaatc ttataatctt 300
cggacgttcg gtggaggcac caagctggaa atcaaa 336
<210> 17
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Сайт NotI последовательности Козака
<400> 17
gcggccgcca cc 12
<210> 18
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Лидерная последовательность mVH
<400> 18
atgaactttg ggctcagatt gattttcctt gtccttactt taaaaggtgt gaagtgt 57
<210> 19
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mVH
<400> 19
gaggtgcagc tggtggagtc tggacctggc ctggtggcgc cctcacagag cctgtccatc 60
acttgcactg tctctgggtt ttcattaccc agctatggtg ttcactgggt tcgccagcct 120
ccaggaaagg gtctggagtg gctgggagta atctgggctg gtggaatcac aaattataac 180
tcggctctca tgtccagact gaccatcagc aaagacaact ccaagagcca agttttctta 240
aaaatgaaca gtcttcaaac tgatgacaca gccatatact actgtgccag aggcggctct 300
gattacgacg gctttgctta ctggggccaa gggactctgg tcactgtctc tgcatca 357
<210> 20
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Одинарная цепь
<400> 20
ggaggtggag gttctggtgg aggaggttca ggtggaggtg gatca 45
<210> 21
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mVkappa
<400> 21
gacattgtga tgacacagtc tccatcctcc ctggctgtgt cagcaggaga gaaggtcact 60
atgaactgca gatccagtca gagtctcctc agcagtagaa cccgaaagaa ctacttggct 120
tggtaccagc agaaaccagg gcagtctcct aaactgctga tctactgggc atctattagg 180
gaatctgggg tccctgatcg cttcacaggc agtggatctg ggacagattt cactctcacc 240
atcagcagtg tgcaggctga agacctggca gtttattact gcaagcaatc ttataatctt 300
cggacgttcg gtggaggcac caagctggaa atcaaa 336
<210> 22
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hCkappa
<400> 22
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc ggactacgag 240
aaacacaaac tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg tggcgcgcca 330
<210> 23
<211> 90
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Трансмембранный домен hCD28
<400> 23
actagatttt gggtgctggt ggtggttggt ggagtcctgg cttgctatag cttgctagta 60
acagtggcct ttattatttt ctgggtgagg 90
<210> 24
<211> 120
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Внутриклеточный домен hCD28
<400> 24
agtaagagga gcaggctcct gcacagtgac tacatgaaca tgactccccg ccgccccggg 60
cccacccgca agcattacca gccctatgcc ccaccacgcg acttcgcagc ctatcgctcc 120
<210> 25
<211> 342
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hCD3 zeta
<400> 25
ctgagagtga agttcagcag gagcgcagac gcccccgcgt accagcaggg ccagaaccag 60
ctctataacg agctcaatct aggacgaaga gaggagtacg atgttttgga caagagacgt 120
ggccgggacc ctgagatggg gggaaagccg cagagaagga agaaccctca ggaaggcctg 180
tacaatgaac tgcagaaaga taagatggcg gaggcctaca gtgagattgg gatgaaaggc 240
gagcgccgga ggggcaaggg gcacgatggc ctttaccagg gtctcagtac agccaccaag 300
gacacctacg acgcccttca catgcaggcc ctgccccctc gc 342
<210> 26
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Сайт XhoI
<400> 26
tcgattctcg ag 12
<210> 27
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Лидерная последовательность mVH
<400> 27
Met Asn Phe Gly Leu Arg Leu Ile Phe Leu Val Leu Thr Leu Lys Gly
1 5 10 15
Val Lys Cys
<210> 28
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> mVH
<400> 28
Glu Val Gln Leu Val Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Pro Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ala Gly Gly Ile Thr Asn Tyr Asn Ser Ala Leu Met
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Ser Asp Tyr Asp Gly Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser
115
<210> 29
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Одинарная цепь
<400> 29
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 30
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> mVkappa
<400> 30
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Asn Cys Arg Ser Ser Gln Ser Leu Leu Ser Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Ile Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 31
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> hCkappa
<400> 31
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Leu Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Ala Pro
100 105 110
<210> 32
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Трансмембранный домен hCD28
<400> 32
Thr Arg Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
1 5 10 15
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg
20 25 30
<210> 33
<211> 40
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Внутриклеточный домен hCD28
<400> 33
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
1 5 10 15
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
20 25 30
Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 34
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> hCD3 zeta
<400> 34
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
1 5 10 15
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
20 25 30
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
35 40 45
Lys Pro Gln Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
50 55 60
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
65 70 75 80
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
85 90 95
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
100 105 110
Pro Arg
<210> 35
<211> 147
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Внутриклеточный домен hGITR
<400> 35
aggagtcagt gcatgtggcc ccgagagacc cagctgctgc tggaggtgcc gccgtcgacc 60
gaagacgcca gaagctgcca gttccccgag gaagagcggg gcgagcgatc ggcagaggag 120
aaggggcggc tgggagacct gtgggtg 147
<210> 36
<211> 49
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Внутриклеточный домен hGITR
<400> 36
Arg Ser Gln Cys Met Trp Pro Arg Glu Thr Gln Leu Leu Leu Glu Val
1 5 10 15
Pro Pro Ser Thr Glu Asp Ala Arg Ser Cys Gln Phe Pro Glu Glu Glu
20 25 30
Arg Gly Glu Arg Ser Ala Glu Glu Lys Gly Arg Leu Gly Asp Leu Trp
35 40 45
Val
<210> 37
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> P2A
<400> 37
ggatccggcg ccacaaattt tagcctcttg aagcaagccg gcgacgtgga agagaatcct 60
gggccc 66
<210> 38
<211> 597
<212> ДНК
<213> Искусственная последовательность
<220>
<223> GITRL
<400> 38
atgaccctgc accccagccc catcacctgc gagttcctgt tcagcaccgc cctgatcagc 60
cccaagatgt gcctgagcca cctggagaac atgcccctga gccacagcag aacccagggc 120
gcccagagaa gcagctggaa gctgtggctg ttctgcagca tcgtgatgct gctgttcctg 180
tgcagcttca gctggctgat cttcatcttc ctgcagctgg agaccgccaa ggagccctgc 240
atggccaagt tcggccccct gcccagcaag tggcagatgg ccagcagcga gcccccctgc 300
gtgaacaagg tgagcgactg gaagctggag atcctgcaga acggcctgta cctgatctac 360
ggccaggtgg cccccaacgc caactacaac gacgtggccc ccttcgaggt gagactgtac 420
aagaacaagg acatgatcca gaccctgacc aacaagagca agatccagaa cgtgggcggc 480
acctacgagc tgcacgtggg cgacaccatc gacctgatct tcaacagcga gcaccaggtg 540
ctgaagaaca acacctactg gggcatcatc ctgctggcca acccccagtt catcagc 597
<210> 39
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> P2A
<400> 39
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 40
<211> 199
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> GITRL
<400> 40
Met Thr Leu His Pro Ser Pro Ile Thr Cys Glu Phe Leu Phe Ser Thr
1 5 10 15
Ala Leu Ile Ser Pro Lys Met Cys Leu Ser His Leu Glu Asn Met Pro
20 25 30
Leu Ser His Ser Arg Thr Gln Gly Ala Gln Arg Ser Ser Trp Lys Leu
35 40 45
Trp Leu Phe Cys Ser Ile Val Met Leu Leu Phe Leu Cys Ser Phe Ser
50 55 60
Trp Leu Ile Phe Ile Phe Leu Gln Leu Glu Thr Ala Lys Glu Pro Cys
65 70 75 80
Met Ala Lys Phe Gly Pro Leu Pro Ser Lys Trp Gln Met Ala Ser Ser
85 90 95
Glu Pro Pro Cys Val Asn Lys Val Ser Asp Trp Lys Leu Glu Ile Leu
100 105 110
Gln Asn Gly Leu Tyr Leu Ile Tyr Gly Gln Val Ala Pro Asn Ala Asn
115 120 125
Tyr Asn Asp Val Ala Pro Phe Glu Val Arg Leu Tyr Lys Asn Lys Asp
130 135 140
Met Ile Gln Thr Leu Thr Asn Lys Ser Lys Ile Gln Asn Val Gly Gly
145 150 155 160
Thr Tyr Glu Leu His Val Gly Asp Thr Ile Asp Leu Ile Phe Asn Ser
165 170 175
Glu His Gln Val Leu Lys Asn Asn Thr Tyr Trp Gly Ile Ile Leu Leu
180 185 190
Ala Asn Pro Gln Phe Ile Ser
195
<210> 41
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Линкер GS
<400> 41
Gly Gly Gly Gly Ser
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИГЕННЫЙ РЕЦЕПТОР | 2020 |
|
RU2832189C2 |
| ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К МЕЗОТЕЛИНУ И ИММУННЫЕ ЭФФЕКТОРНЫЕ КЛЕТКИ, НАЦЕЛЕННЫЕ НА МЕЗОТЕЛИН | 2016 |
|
RU2748281C2 |
| АНТИТЕЛО, НАЦЕЛЕННОЕ НА ВСМА, И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2799655C2 |
| АНТИТЕЛО К IL-13RA2 И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2756623C2 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА-3 И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2744245C2 |
| АНТИГЕН-СВЯЗЫВАЮЩИЙ БЕЛОК, РАСПОЗНАЮЩИЙ ПРОИСХОДЯЩИЙ ИЗ MAGE-A4 ПЕПТИД | 2018 |
|
RU2777074C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-T-КЛЕТКИ | 2020 |
|
RU2762942C1 |
| Терапевтические средства | 2016 |
|
RU2747733C1 |
| ПОЛИПЕПТИД, СПЕЦИФИЧНЫЙ К МУЦИНУ-1, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2805840C1 |
| АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2017 |
|
RU2773355C2 |






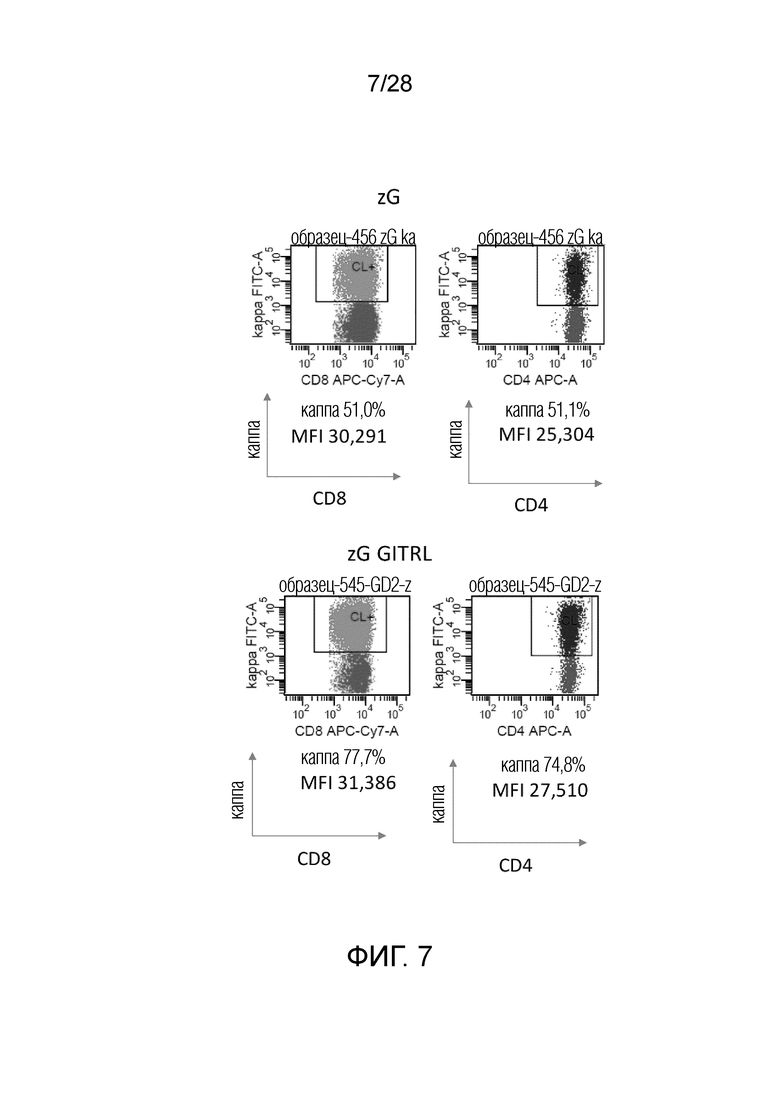

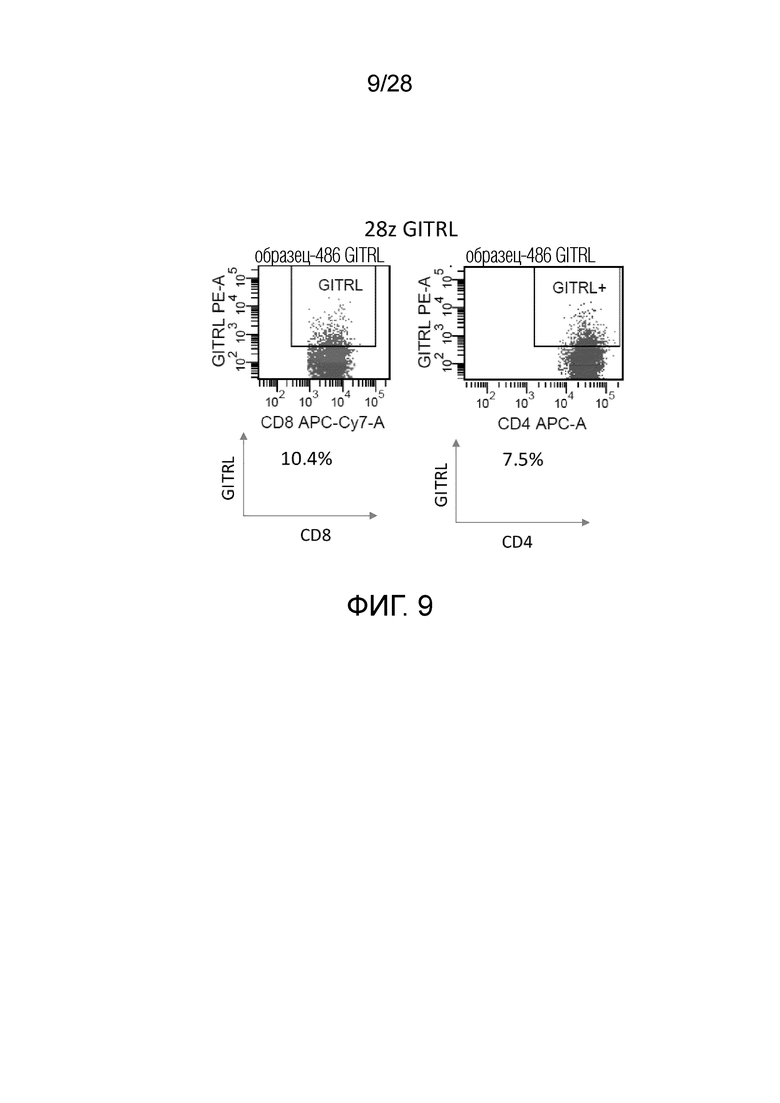
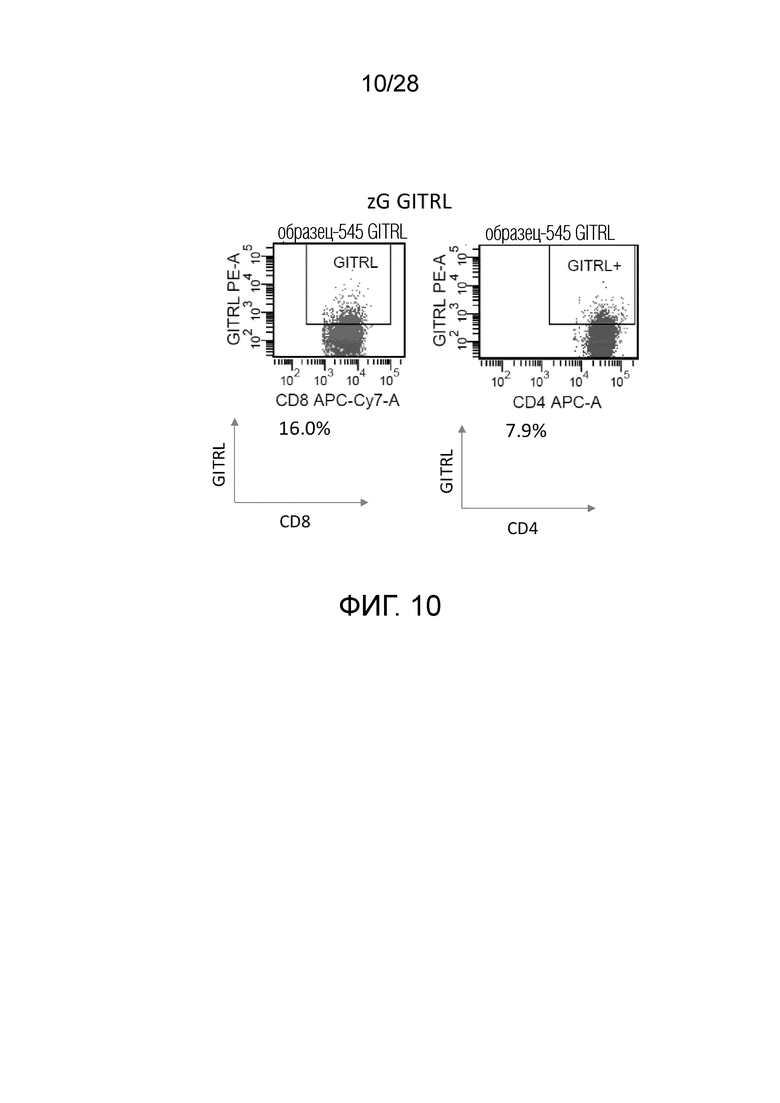




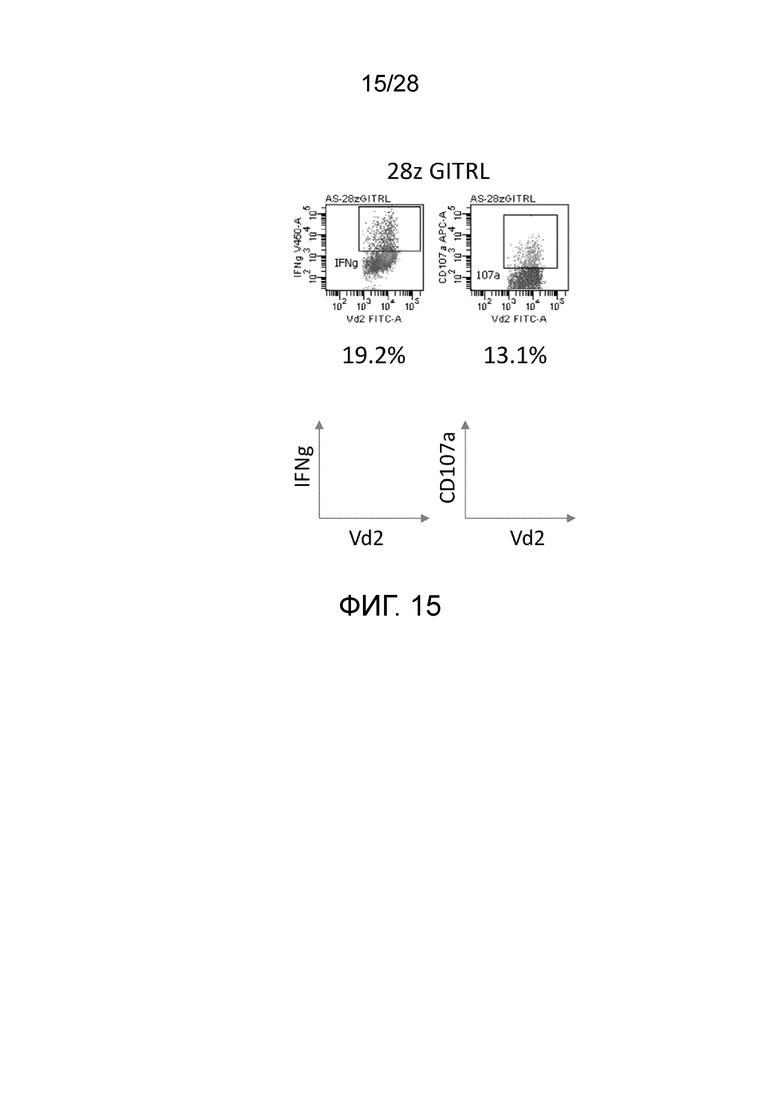


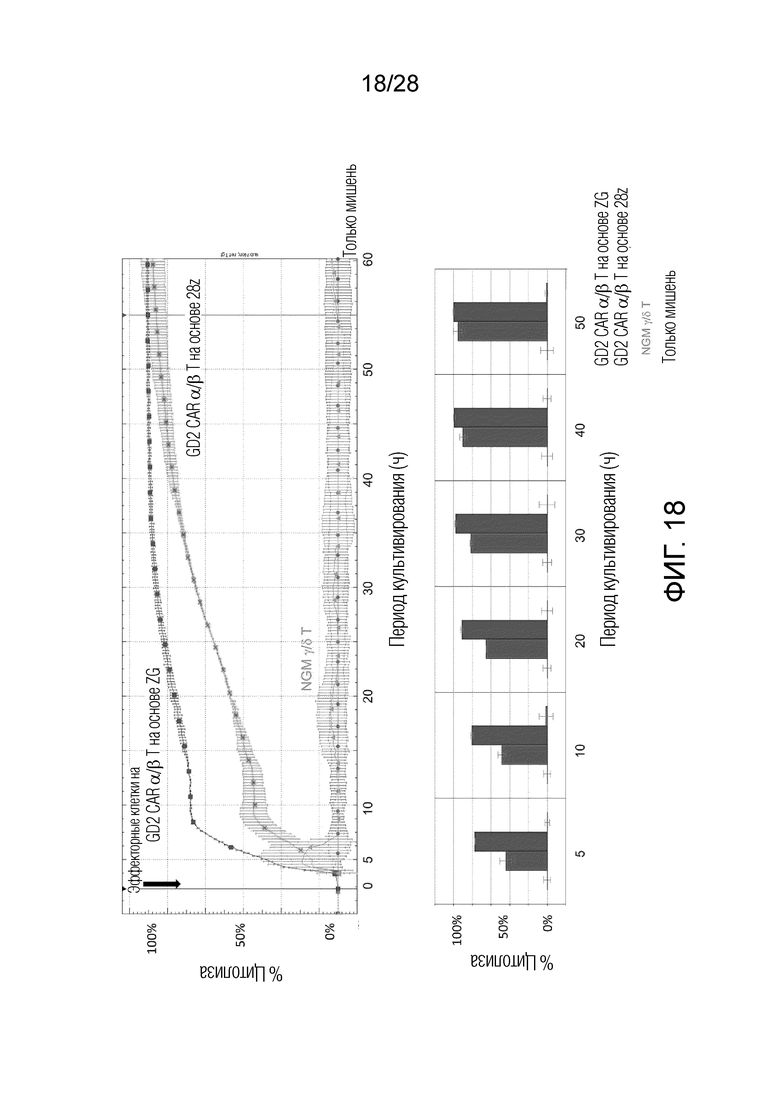
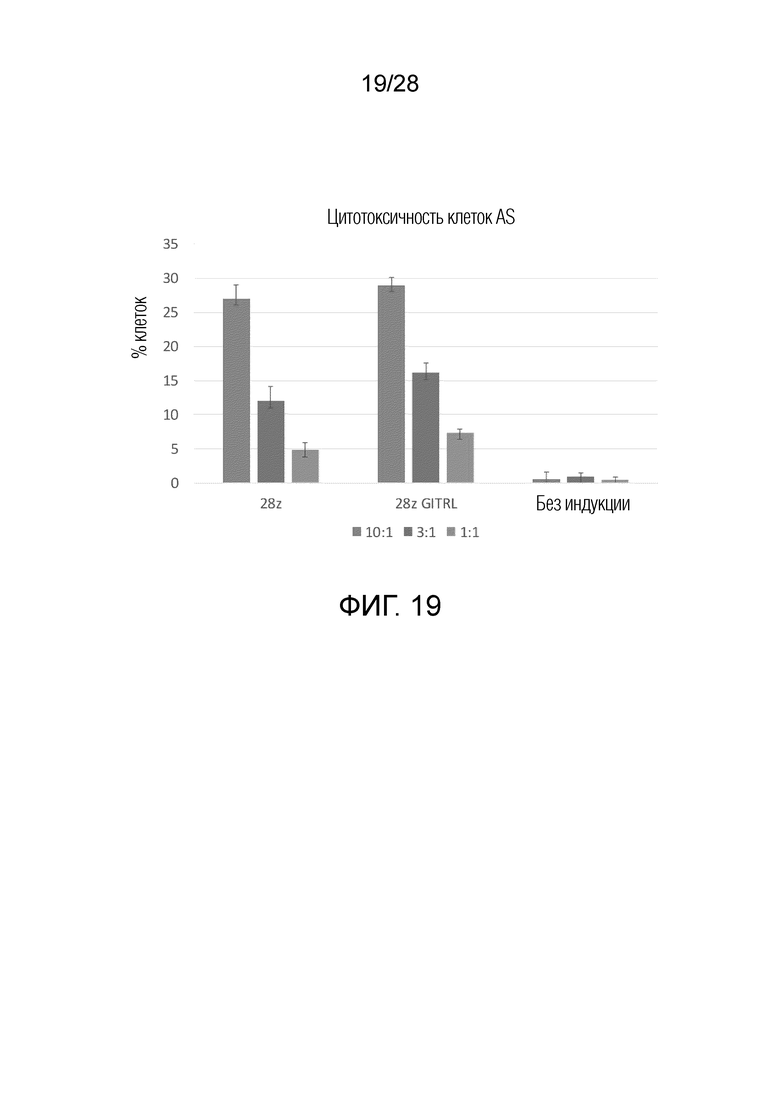

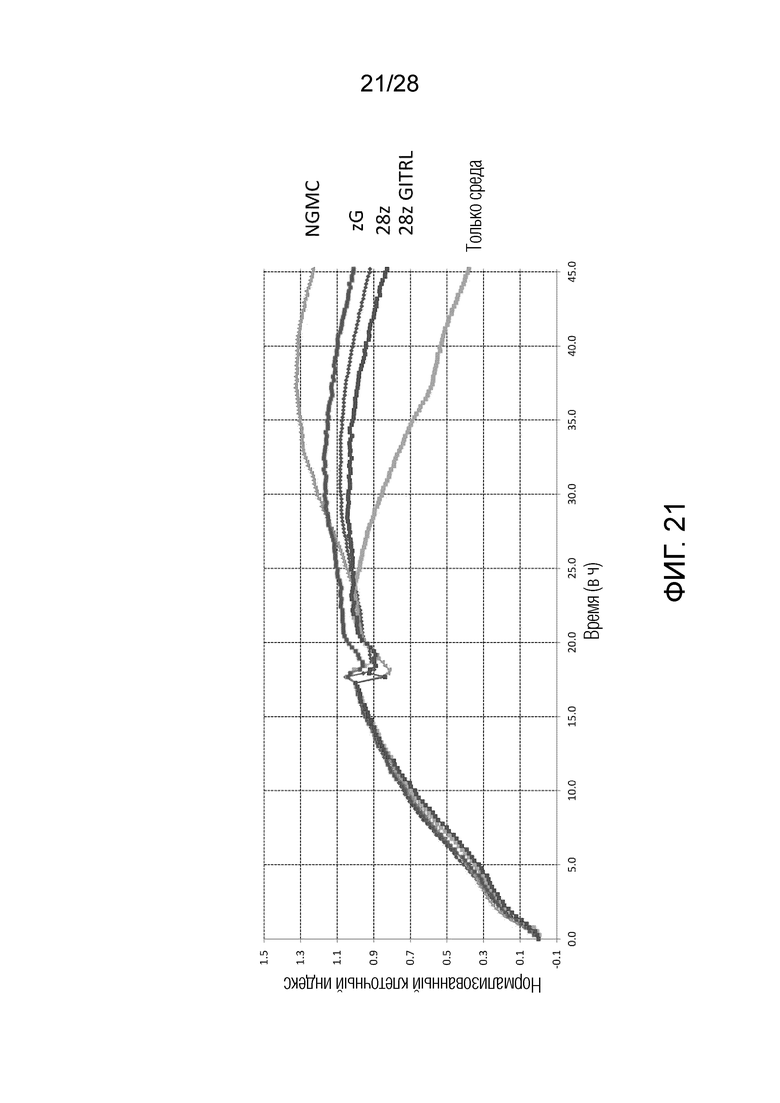

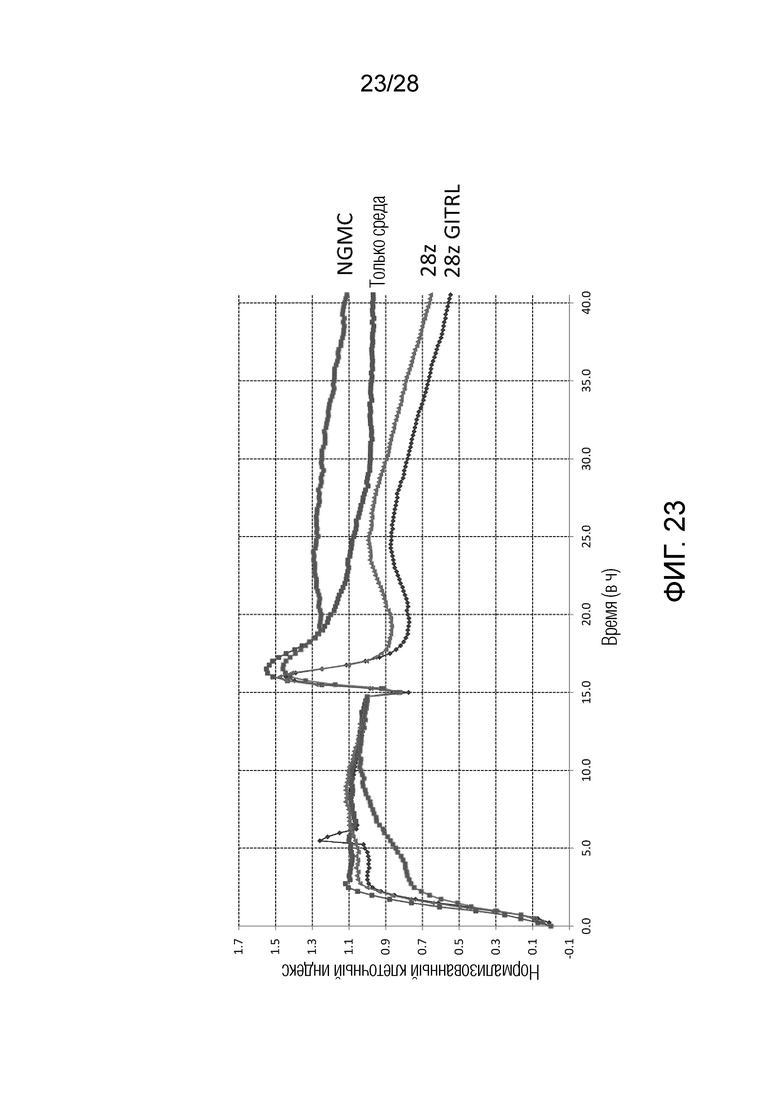
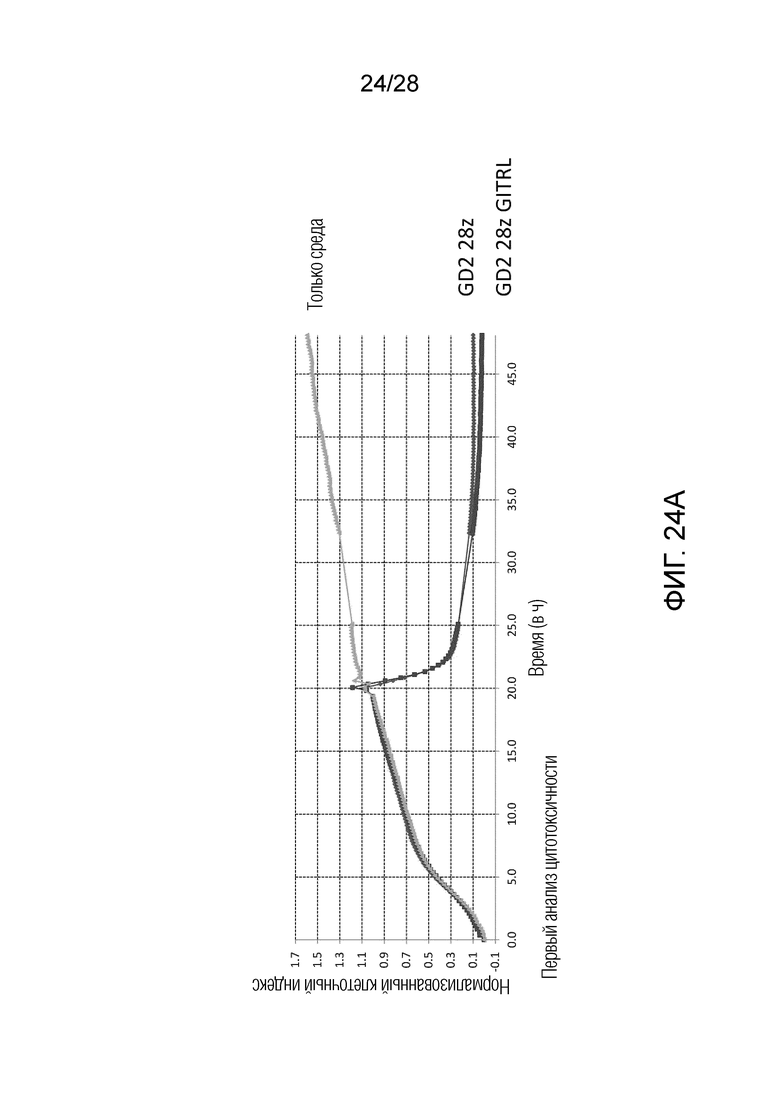



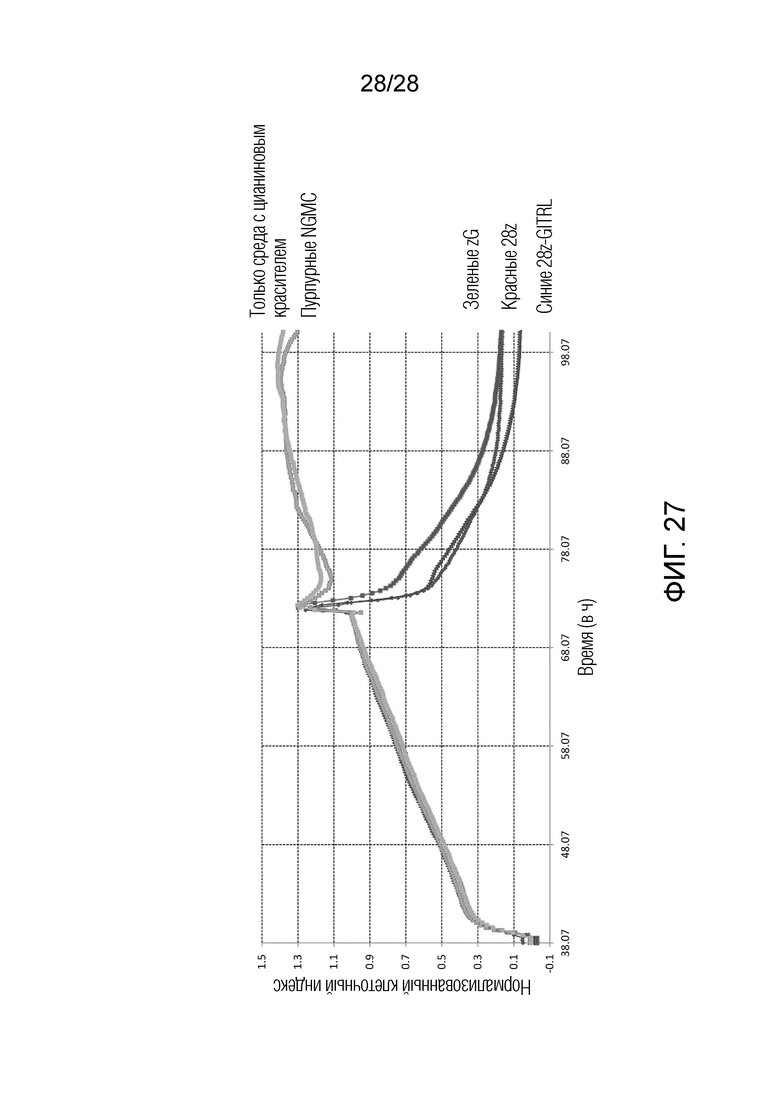
Изобретение относится к области биотехнологии, в частности к химерному антигенному рецептору. Указанный химерный антигенный рецептор специфически распознает ганглиозид GD2 и содержит GD2-связывающий домен, содержащий CDR1-CDR3 тяжелой цепи с последовательностями SEQ ID NO: 1-3, соответственно, а также CDR1-CDR3 легкой цепи с последовательностями SEQ ID NO: 9-11, соответственно. Настоящее изобретение также относится к полинуклеотиду, кодирующему указанный химерный антигенный рецептор, клетке, в том числе Т-клетке или NK-клетке, содержащей указанный полинуклеотид, а также фармацевтической композиции, содержащей эффективное количество Т-клеток или NK-клеток. Изобретение обеспечивает высокую цитотоксическую активность и терапевтическую эффективность при лечении рака, которое на молекулярном уровне нацелено на GD2. 5 н. и 4 з.п. ф-лы, 27 ил., 18 пр.
1. Химерный антигенный рецептор, содержащий
GD2-связывающий домен, содержащий
вариабельную область тяжелой цепи, содержащую
CDR1 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 1,
CDR2 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, и
CDR3 тяжелой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 3, и
вариабельную область легкой цепи, содержащую
CDR1 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 9,
CDR2 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 10, и
CDR3 легкой цепи, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 11,
где химерный антигенный рецептор специфически распознает ганглиозид GD2.
2. Химерный антигенный рецептор по п. 1, где связывающая способность химерного антигенного рецептора с ганглиозидом GD1a, ганглиозидом GD1b, ганглиозидом GD3, ганглиозидом GM1, ганглиозидом GM3, ганглиозидом GT1b или лактозилцерамидом равна или меньше 1/2 от связывающей способности химерного антигенного рецептора с ганглиозидом GD2.
3. Химерный антигенный рецептор по п. 1 или 2, содержащий коровый домен, содержащий:
домен scFv, который содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи,
трансмембранный домен и
внутриклеточный домен TCR.
4. Химерный антигенный рецептор по п. 3, где коровый домен содержит внутриклеточный домен костимулятора.
5. Химерный антигенный рецептор по п. 3 или 4, содержащий домен GITRL в положении ближе к С-концу корового домена через саморасщепляющийся пептидный домен.
6. Полинуклеотид, кодирующий химерный антигенный рецептор по любому из пп. 1-5.
7. Клетка, содержащая полинуклеотид по п. 6, где клетка экспрессирует химерный антигенный рецептор по любому из пп. 1-5.
8. Т-клетка с химерным антигенным рецептором или NK-клетка с химерным антигенным рецептором, содержащая полинуклеотид по п. 6, где клетка экспрессирует химерный антигенный рецептор по любому из пп. 1-5.
9. Фармацевтическая композиция, содержащая эффективное количество Т-клеток с химерным антигенным рецептором или NK-клеток с химерным антигенным рецептором по п. 8, которая предназначена для применения в лечении или профилактике рака, экспрессирующего GD2.
| ВЫСОКОАФФИННЫЕ АНТИТЕЛА К GD2 | 2014 |
|
RU2680267C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2015 |
|
RU2685479C2 |
| CN 108728460 A, 02.11.2018 | |||
| WO 2019059771 A2, 28.03.2019 | |||
| MARIUZZA R.A., The structural basis of antigen-antibody recognition, Ann | |||
| Rev | |||
| Biophys | |||
| Biophys | |||
| Chem., 1987, Vol | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| MULLER S | |||
| et al., Spliceosomal peptide P140 for immunotherapy of systemic lupus erythematosus: results of | |||
Авторы
Даты
2024-08-12—Публикация
2020-07-31—Подача