Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений - 3-ароил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[6]пирроло[1,2-d][1,4]тиазин-1,4(3aH)-дионов, которые могут участвовать в дальнейшем построении новых гетероциклических систем, а также использоваться в медицине, фармакологии, ветеринарии и сельском хозяйстве.
Структурными аналогами заявленных соединений являются 3-ароил-2-гидрокси- 3а-(2-оксоиндолин-3-ил)-5-фенилпирроло [1,2-a]хиноксалин-1,4(3aH,5H)-дионы, которые получают взаимодействием 3-ароил-5-фенилпирроло[1,2-a]хиноксалин-1,2,4(5H)-трионов с 2-оксиндолом в среде ацетонитрила при нагревании в течение 4 ч [Топанов П.А., Машевская И.В., Дмитриев М.В., Масливец А.Н. Журнал органической химии, 2020. Т. 56 (4). С.644-648. DOI 10.1134/S1070428020040247]. Синтез структурных аналогов осуществляется по следующей схеме:
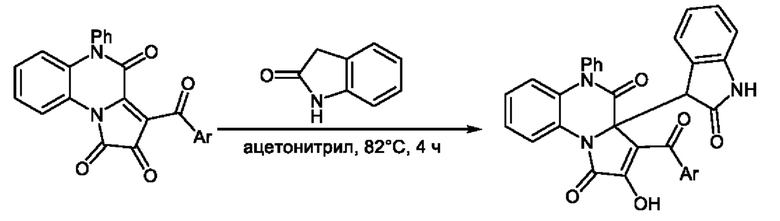
К недостаткам данного способа относится невозможность получения 3-ароил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[6]пирроло[1,2-d] [1,4]тиазин-1,4(3aH)-дионов.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 3-ароил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[6]пирроло[1,2-d] [1,4]тиазин-1,4(3aH)-дионов.
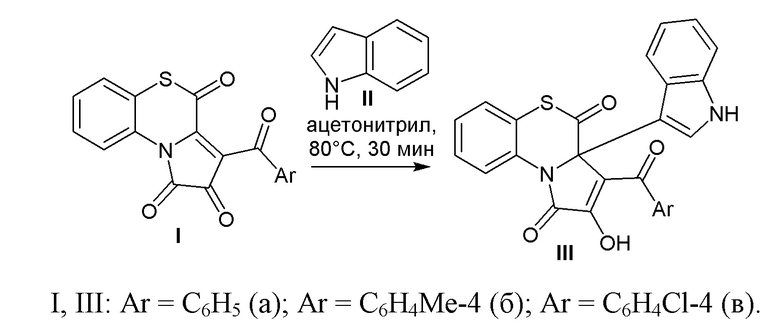
Поставленная задача осуществляется путем нагревания 3-ароилпирроло[2,1-с][1,4]бензотиазин-1,2,4-трионов (Ia-в) в присутствии индола (II) в безводном ацетонитриле при температуре 80°С в течение 30 мин по следующей схеме:
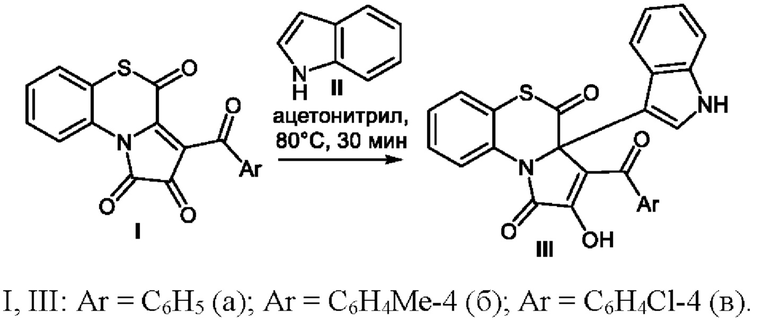
Выделение целевого продукта заключается в фильтровании порошкообразного осадка из реакционной массы.
Из патентной и технической литературы не были выявлены способы получения 3-ароил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[b]пирроло[1,2-d[1,4]тиазин-1,4(3aH)-дионов, имеющих сходные признаки с заявленным способом - не использовались исходные продукты, растворитель. На этом основании можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-Бензоил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[6]пирроло[1,2-d] [1,4]тиазин-1,4(3aH)-дион (IIIa).
Получение (IIIa): смесь, содержащую 0.05 г (0.149 ммоль) соединения (Ia) и 0.018 г (0.149 ммоль) индола (II), нагревают в безводном ацетонитриле в течение 30 мин при 80°С. Осадок фильтруют и промывают смесью толуол: хлороформ (1:1) при нагревании. Отфильтровывают, сушат при 145°С. Выход 0.050 г, (75%), т.ггл. 239-241°С.
Соединение (IIIa) - желтое порошкообразное вещество, легкорастворимое в ДМСО и ДМФА, ацетоне, труднорастворимое в ароматических углеводородах, хлороформе, нерастворимое в алканах. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIa) снят в виде пасты в вазелиновом масле: 3429, 3392, 1722, 1686, 1655 см-1.
Спектр ЯМР 1Н соединения (IIIa) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=11.88 (уш. с, 1H), 11.11 (м, 1H), 7.81 (м, 1H), 7.71 (м, 2Н), 7.58 (м, 1H), 7.46 (м, 2Н), 7.40 (м, 1H), 7.32 (м, 1H), 7.27 (м, 1H), 7.19 (м, 3Н), 7.08 -6.95 (м, 2Н) м. д.
Спектр ЯМР 13С соединения (IIIa) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=191.7, 189.3, 163.2, 149.0, 137.9, 136.5, 132.5, 129.7, 128.9 (2С), 128.1 (2С), 127.7, 126.5, 126.0, 125.8, 124.0, 123.6, 123.5, 121.4, 119.4, 117.6, 116.088, 112.1, 105.3,71.1 м. д.
Соединение C26H16N2O4S (IIIa). Вычислено, %: С, 69,02; Н, 3,56; N, 6,19. Найдено, %: С, 69,12; Н, 3,61; N, 6,25.
Пример 2. 2-Гидрокси-3а-(1H-индол-3-ил)-3-(4-метилбензоил)-1H-бензо[b]пирроло[1,2-d] [1,4]тиазин-1,4(3aH)-дион (IIIб).
Получение (IIIб): смесь, содержащую 0.05 г (0.143 ммоль) соединения (16) и 0.017 г (0.143 ммоль) индола (II), нагревают в безводном ацетонитриле в течение 30 мин при 80°С.Осадок фильтруют и промывают смесью толуол: хлороформ (1:1) при нагревании. Отфильтровывают, сушат при 145°С. Выход 0.049 г, (74%), т.пл. 244-246°С.
Соединение (IIIб) - желтое порошкообразное вещество, легкорастворимое в ДМСО и ДМФА, ацетоне, труднорастворимое в ароматических углеводородах, хлороформе, нерастворимое в алканах. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIб) снят в виде пасты в вазелиновом масле: 3322, 3193, 1699, 1666, 1645 см-1.
Спектр ЯМР 1Н соединения (IIIб) снят в растворе ДМСО-d6 при частоте400 МГц: δ=11.72 (уш. с, 1H), 11.09 (м, 1H), 7.80 (м, 1H), 7.61 (м, 2Н), 7.40 (м, 1H), 7.29 (м, 4Н), 7.19 (м, 3Н), 7.07-6.94 (м, 2Н), 2.37 (с, 3Н) м. д.
Спектр ЯМР 13С соединения (IIIб) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=191.9, 189.0, 163.4, 148.6, 143.0, 136.5, 135.4, 129.8, 129.3 (2С), 128.8 (2С), 127.8, 126.6, 126.2, 125.8, 124.1, 123.7, 123.5, 121.5, 119.5, 117.7, 116.3, 112.2, 105.4, 71.2,21.2 м. д.
Соединение C27H18N2O4S (IIIб). Вычислено, %: С, 69,52; Н, 3,89; N, 6,01. Найдено, %: С, 69,63; Н, 3,92; N, 6,12.
Пример 3. 2-Гидрокси-3а-(1H-индол-3-ил)-3-(4-хлорбензоил)-III-бензо[d]пирроло[1,2-d] [1,4]тиазин-1,4(3aH)-дион (IIIв).
Получение (IIIв): смесь, содержащую 0.05 г (0.135 ммоль) соединения (1в) и 0.016 г (0.135 ммоль) индола (II), нагревают в безводном ацетонитриле в течение 30 мин при 80°С. Осадок фильтруют и промывают смесью толуол: хлороформ (1:1) при нагревании. Отфильтровывают, сушат при 145°С. Выход 0.050 г, (76%), т.пл. 238-240°С.
Соединение (IIIв) - желтое порошкообразное вещество, легкорастворимое в ДМСО и ДМФА, ацетоне, труднорастворимое в ароматических углеводородах, хлороформе, нерастворимое в алканах. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIв) снят в виде пасты в вазелиновом масле: 3327, 3173, 1698, 1645, см-1.
Спектр ЯМР 1Н соединения (IIIв) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=12.00 (уш. с, 1H), 11.12 (м, 1H), 7.81 (м, 1H), 7.73 (м, 2Н), 7.53 (м, 2Н), 7.40 (м, 2Н), 7.29 (м, 1H), 7.27 (м, 1H), 7.21 (м,1H), 7.18 (м, 1Н), 7.07 -6.95 (м, 2Н) м. д.
Спектр ЯМР 13С соединения (IIIв) снят в растворе ДМСО-d6 при частоте 100 МГц: S=191.8, 188.2, 163.1,H 149.5, 137.4, 136.6, 136.5, 130.8 (2С), 129.7, 128.2 (2С), 127.7, 126.6, 126.1, 125.8, 124.0, 123.6, 123.5, 121.4, 119.4, 117.6, 115.6, 112.1, 105.2,71.0 м. д.
Соединение C26H15ClN2O4S (IIIв). Вычислено, %: С, 69,13; Н, 3,11; N, 5,75. Найдено, %: С, 69,22; Н, 3,15; N, 5,83.
Пример 4. Исследование 3-ароил-2-гидрокси-3а-(1H-индол-3-ил)-1H-бензо[b]пирроло[1,2-d][1,4]тиазин-1,4(3aH)-дионов (IIIa-в) на наличие росторегулирующей активности на культуре Chlorella vulgaris (штамм IMBR-19)
Для изучения росторегулирующей активности заявляемых соединений (IIIa-в) в отношении микроводорослей культуры Chlorella vulgaris (штамм IMBR-19, Институт морских биологических исследований имени А.О. Ковалевского Российской Академии Наук, г. Севастополь) выращивали стерильно на среде BG-11 [Гайсина Л.А., Фазлутдинова А.И., Кабиров P.P. Уфа: Изд-во БГПУ. 2008. 152 с]. Свежую (недельную) культуру засевали в заранее приготовленные колбы объемом 50 мл со средой (объем 30 мл) с добавлением соединений (IIIa-в) в концентрациях 1×10-4 М, 1×10-5 М, 1×10-6 М, 1×10-7 М в трехкратных повторностях. Стартовая концентрация клеток С.vulgaris составляла 1×10-7 клеток на колбу (контролировали подсчетом клеток в камере Горяева). Вещества (IIIa-в) растворяли в ДМСО. Дополнительно засевали культуры в контрольную среду, содержащую 1%-ый раствор ДМСО (повторность трехкратная).
Инкубация засеянных культур проходила в термостате при 28°С, интенсивность освещения 1000-1200 лк в режиме 12 ч света /12 ч темноты, при постоянном перемешивании 150 об/мин.
Через 5 дней инкубации вели подсчет общего числа клеток микроводорослей С.vulgaris в камере Горяева в 5 больших исчерченных квадратах (микроскоп Carl Zeiss, Axioastar Plus с окуляр-микрометром). Полученные данные обрабатывали с помощью дисперсионного анализа (ANOVA one-way) в программе Graph Pad Prism 8.
В 5-дневных культурах определяли содержание пигментов (хлорофилл а, b и каротиноиды) стандартным спектрофотометрическим методом в 95%-ом метано льном экстракте [Lichtenthaler Н. Chlorophylls and carotenoids: Pigments of photosynthetic biomembranes // Methods inEnzymolog. 1987. Vol. 148. P. 350-382. DOI: 10.1016/0076-6879(87)48036-1]. Анализ проводили в двухкратной повторности. Оптическую плотность экстрактов измеряли при длинах волн 750,470,652 и 665 нм. Концентрацию пигментов рассчитывали по уравнениям [Xiong J.Q., Kurade М.В., Abou-Shanab R.A.I, (et al.) Biodegradation of carbamazepine using freshwater microalgae Chlamydomonas mexicana and Scenedesmus obliquus and the determination of its metabolic fate // Bioresource Technology. 2016. Vol. 205. P. 183-190. DOI: 10.1016/j.biortech.2016.01.038]. Полученные данные обрабатывали с помощью гнездового анализа (Nested analysis) в программе Graph Pad Prism 8.
Полученные данные приведены в Таблице.
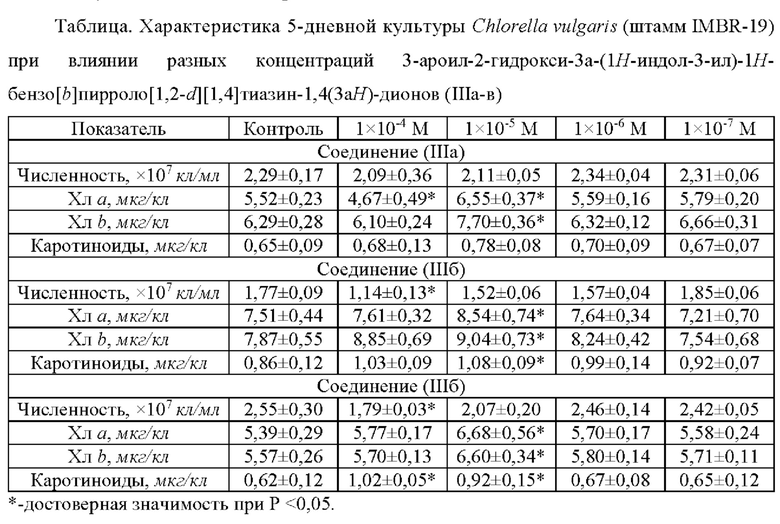
По результатам исследований установлено, что соединение (IIIa) проявляет ингибирующий эффект в отношении накопления хлорофилла а культурой Chlorella vulgaris (штамм IMBR-19) в концентрации 1×10-4 М. В концентрации 1×10-5 М наблюдается значительное накопление хлорофилла а и b.
Соединения (IIIб) и (IIIв) имеют ингибирующий эффект в отношении роста культуры Chlorella vulgaris (штамм IMBR-19) в концентрации 1×10-4 М, однако в данной концентрации соединение (IIIв) стимулирует накопление каротиноидов. Соединения (IIIб) и (IIIв) стимулируют накопление хлорофилла а и b и каротиноидов в концентрации 1×10-5 М.
Изобретение относится к области органической химии, а именно раскрывается способ получения 3-ароил-2-гидрокси-3a-(1H-индол-3-ил)-1H-бензо[b]пирроло[1,2-d][1,4]тиазин-1,4(3aH)-дионов (IIIа-в), при котором осуществляют взаимодействие 3-ароилпирроло[2,1-c][1,4]бензотиазин-1,2,4-трионов с эквивалентным количеством индола в апротонном растворителе ацетонитрил при нагревании при 80°С в течение 30 мин. Использование изобретения позволяет получить соединения формулы III с высоким выходом. 1 табл., 4 пр. 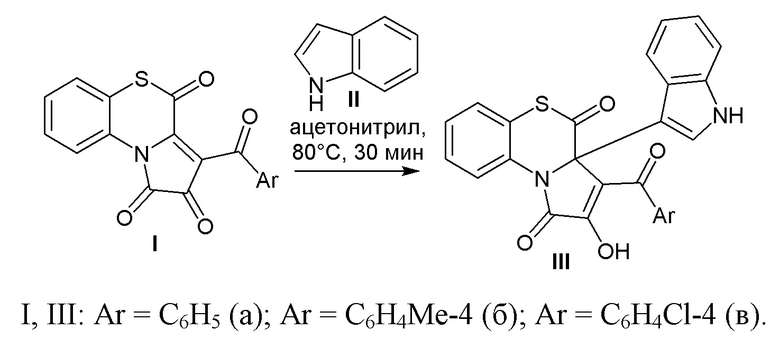
Способ получения 3-ароил-2-гидрокси-3a-(1H-индол-3-ил)-1H-бензо[b]пирроло[1,2-d][1,4]тиазин-1,4(3aH)-дионов (IIIа-в), при котором осуществляют взаимодействие 3-ароилпирроло[2,1-c][1,4]бензотиазин-1,2,4-трионов с эквивалентным количеством индола в апротонном растворителе ацетонитрил при нагревании при 80°С в течение 30 мин
| ТОПАНОВ П.А | |||
| и др | |||
| Нуклеофильное присоединение оксиндола к пирролохиноксалинтрионам | |||
| Журнал органической химии, 2020, т | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| ВОЗДУШНЫЙ МНОГОСТУПЕНЧАТЫЙ КОМПРЕССОР | 1923 |
|
SU644A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ получения 3-ароил-N-бензил-2-гидрокси-1-оксобензо[d]пирроло[2,1-b]тиазол-3а(1Н)-карбоксамидов | 2021 |
|
RU2764906C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АРОИЛ-3А-(3,4-ДИГИДРО-2Н-ПИРАН-5-ИЛ)-2-ГИДРОКСИПИРРОЛО[1,2-А]ХИНОКСАЛИН-1,4(3АН,5Н)-ДИОНОВ | 2015 |
|
RU2581268C1 |
Авторы
Даты
2024-08-21—Публикация
2023-12-03—Подача