Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса 2-гидрокси-2-2-оксоциклоалкил)пирроло[1,2-a]хиноксалина, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Известны структурные аналоги заявленных соединений - 3-ароил-2-гидрокси-2-(2-оксоциклоалкил)пирроло[2,1-с][1,4]бензоксазин-1,4(2H)-дионы, получаемые из 3-ароилпирроло[2,1-с][1,4]бензоксазин-1,2,4-трионов и циклоалканонов, путем выдерживания реагентов при температуре 110°С в течение 2-3 часов (Степанова Е.Е., Масливец А.Н., ЖОрХ, 2014, Т. 50, Вып. 9, с. 1394-1395). Синтез структурных аналогов осуществляется по следующей схеме:
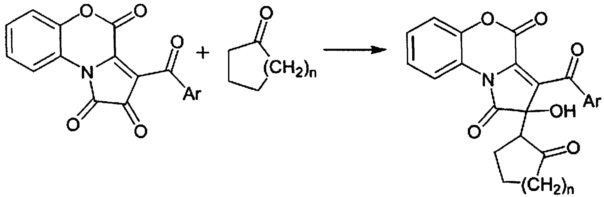
К недостаткам данного способа относится невозможность получения (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-а]хиноксалин-1,4(2H,5H)-дионов.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-a]хиноксалин-1,4(2H,5H)-дионов.
Поставленная задача осуществляется путем кипячения 3-ароилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионов с циклоалканонами в среде инертных апротонных растворителей по следующей схеме:
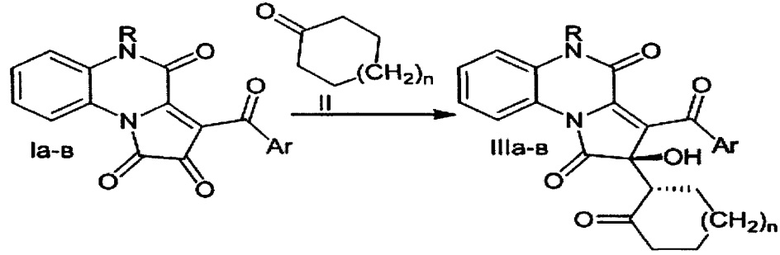 ,
,
где I, II и III: R=Ph, Ar=C6H4Cl-4, n=1 (a); R=H, Ar=C6H4Cl-4, n=1 (б); R=Ph, Ar=Ph, n=1 (в).
Процесс ведут при температуре 100°С, а в качестве растворителя используют безводный 1,4-диоксан.
Из патентной и технической литературы не были выявлены способы получения (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло [1,2-а]хиноксалин-1,4(2H,5H)-дионов, имеющие сходные признаки с заявленным способом, а именно, не использовались исходные продукты, растворитель, в котором проходит реакция, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. (R*)-2-Гидрокси-2-((S*)-2-оксоциклогексил)-5-фенил-3-(4-хлорбензоил)пирроло[1,2-а]хиноксалин-1,4(2H,5H)-дион (IIIa).
К суспензии 1.3 ммоль 5-фенил-3-(4-хлорбензоил)пирроло[1,2-a]хиноксалин-1,2,4(5H)-триона (Ia) в 10 мл безводного 1,4-диоксана добавляли 12.6 ммоль безводного циклогексанона (II), кипятили 3 ч (до исчезновения фиолетовой окраски), охлаждали, растворитель отгоняли под вакуумом, образовавшийся осадок перекристаллизовывали из тетрахлорметана, выпавший желтый осадок отфильтровали. Выход 76%, т. пл. 163-165°С (разл., тетрахлорметан). Соединение (IIIa) C30H23ClN2O5.
Найдено, %: С 68.46; Н 4.49; N 5.26.
Вычислено, %: С 68.38; Н 4.40; N 5.32.
Соединение (IIIa) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в ДМСО и ДМФА, растворимое в ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, этилацетате, ароматических углеводородах, труднорастворимое в тетрахлорметане, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIa), записанного в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы ОН (3458 см-1), лактамной карбонильной группы C4=O и кетонной карбонильной группы С2'=O (1743 см-1), лактамной карбонильной группы С1=O (1699 см-1), ароильной кетонной карбонильной группы С(Ar)=O (1638 см-1).
В спектре ЯМР 1Н соединения (IIIa), записанного в растворе в ДМСО-d6, кроме сигналов протонов метиленовых групп, ароматических колец и связанных с ними групп присутствуют дублет дублетов метинового протона С1'H при 3.38 м.д. (J1 13.8, J2 5.2 Гц) и синглет протона группы ОН при 6.40 м.д.
Пример 2. (R*)-2-Гидрокси-2-((S*)-2-оксоциклогексил)-3-(4-хлорбензоил)пирроло[1,2-а]хиноксалин-1,4(2H,5H)-дион (IIIб).
К суспензии 1.3 ммоль 3-(4-хлорбензоил)пирроло[1,2-a]хиноксалин-1,2,4(5H)-триона (Iб) в 10 мл безводного 1,4-диоксана добавляли 12.6 ммоль безводного циклогексанона (II), кипятили 3 ч (до исчезновения фиолетовой окраски), охлаждали, растворитель отгоняли под вакуумом, образовавшийся осадок перекристаллизовывали из бензола, выпавший желтый осадок отфильтровали. Выход 70%, т. пл. 219-220°С (разл., бензол). Соединение (IIIб) C24H19ClN2O5.
Найдено, %: С 63.82, Н 4.35, N 6.33.
Вычислено, %: С 63.93, Н 4.25, N 6.21.
Соединение (IIIб) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в ДМСО и ДМФА, растворимое в ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, этилацетате, труднорастворимое в ароматических углеводородах, тетрахлорметане, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIб), записанного в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний групп ОН и NH (3213 см-1), лактамной карбонильной группы С4=O и кетонной карбонильной группы С2'=O (1741 см-1), лактамной карбонильной группы С1=O (1710 см-1), ароильной кетонной карбонильной группы С(Ar)=O (1674 см-1).
В спектре ЯМР 1Н соединения (IIIб), записанного в растворе в ДМСО-d6, кроме сигналов протонов метиленовых групп, ароматических колец и связанных с ними групп присутствуют дублет дублетов метинового протона С1'Н при 3.16 м.д. (J1 13.0, J2 6.4 Гц), синглет протона группы ОН при 6.53 м.д., синглет протона группы NH при 11.21 м.д.
Пример 3. (R*)-3-Бензоил-2-гидрокси-2-((S*)-2-оксоциклогексил)-5-фенилпирроло[1,2-a]хиноксалин-1,4(2H,5H)-дион (IIIв).
К суспензии 1.3 ммоль 3-бензоил-5-фенилпирроло[1,2-a]хиноксалин-1,2,4(5H)-триона (Iв) в 10 мл безводного 1,4-диоксана добавляли 12.6 ммоль безводного циклогексанона (II), кипятили 10 ч (до исчезновения фиолетовой окраски), охлаждали, растворитель отгоняли под вакуумом, образовавшийся осадок перекристаллизовывали из бензола, выпавший желтый осадок отфильтровали. Выход 85%, т. пл. 160-162°С (разл., тетрахлорметан). Соединение (IIIв) C30H24N2O5.
Найдено, %: С 73.09; Н 4.95; N 5.72.
Вычислено, %: С 73.16; Н 4.91; N 5.69.
Соединение (IIIв) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в ДМСО и ДМФА, растворимое в ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, этилацетате, ароматических углеводородах, труднорастворимое в тетрахлорметане, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIв), записанного в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы ОН (3359 см-1), лактамной карбонильной группы С4=O и кетонной карбонильной группы С2'=O (1736 см-1), лактамной карбонильной группы С1=O (1707 см-1), ароильной кетонной карбонильной группы C(Ph)=O (1645 см-1).
В спектре ЯМР 1Н соединения (IIIв), записанного в растворе в ДМСО-d6, кроме сигналов протонов метиленовых групп, ароматических колец и связанных с ними групп присутствуют дублет дублетов метинового протона С1'Н при 3.38 м.д. (J1 13.4, J2 5.7 Гц), синглет протона группы ОН при 6.40 м.д.
Пример 4. Фармакологическое исследование (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-a]хиноксалин-1,4(2H,5H)-дионов (IIIб, в) на наличие противомикробной активности.
Для исследований использовали общепринятый метод двукратных серийных разведений [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ - М.: И-во Медицина, 2005]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME. После ряда разведений плотность суспензии в пробирке соответствовала 5,0×105 клеток/мл, конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
Противомикробные свойства химического вещества изучали на 2-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (штамм 906), Escherichia coli (штамм 1257), полученных в ФГБУ «Научный центр экспертизы средств медицинского применения» Минздравсоцразвития России.
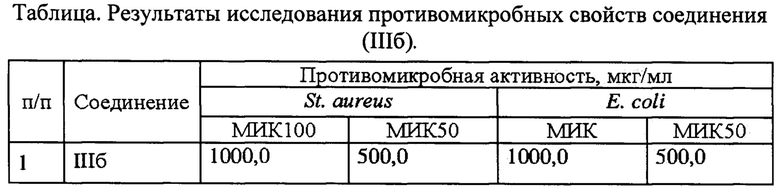
Примечание: Все препараты растворяли в диметилсульфоксиде;
В лунках стерильного 96 луночного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ для каждого вида тест-культур. В каждой лунке содержалось 100 мкл определенной концентрации испытуемого вещества и 100 мкл инокулята культуры. Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 0,5 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch с программным обеспечением Gen 5 и замеряли ОП при длине волны 540 нм. Через 24 часа вновь регистрировали ОП культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения.
МИК100 - концентрация субстанции в последней лунке, в которой отсутствует рост культуры, где ОП через 24 часа меньше первоначального измерения ОП.
МИК50 - концентрация субстанции, при которой рост культуры уменьшается на 50% от положительного контроля.
Проведенные исследования показали (табл.), что соединение (IIIб) обладает антимикробной активностью. Данные о фармакологической активности аналогов заявляемых соединений в доступной литературе отсутствуют.
Изобретение относится к области органической химии, а именно к способу получения соединений (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-a]хиноксалин-1,4(2H,5H)-дионов (IIIa-в), где R=Ph, Ar=C6H4Cl-4, n=1 (а); R=Н, Ar=C6H4Cl-4, n=1 (б); R=Ph, Ar=Ph, n=1 (в), путем взаимодействия 3-ароилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионов(Ia-в) и циклоалканов (II) при температуре кипения в течение 3–10 часов в среде инертных апротонных растворителей с последующим выделением целевых продуктов. Технический результат: разработан простой способ синтеза (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-a]хиноксалин-1,4(2H,5H)-дионов(IIIa-в), которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии. 1 табл., 3 пр.
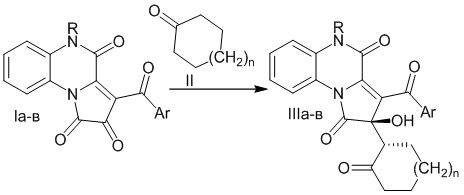
Способ получения (R*)-3-ароил-2-гидрокси-2-((S*)-2-оксоциклоалкил)пирроло[1,2-a]хиноксалин-1,4(2H,5H)-дионов, характеризующийся тем, что 3-ароилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионы подвергают взаимодействию с циклоалканонами при температуре кипения в течение 3–10 часов в среде инертных апротонных растворителей по следующей схеме:
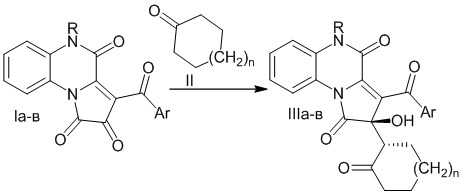 ,
,
где I, II и III: R=Ph, Ar=C6H4Cl-4, n=1 (а); R=Н, Ar=C6H4Cl-4, n=1 (б); R=Ph, Ar=Ph, n=1 (в);
с последующим выделением целевых продуктов.
| 3-АРОИЛ-2-(2-АРИЛГИДРАЗОНО)ПИРРОЛО[1,2-a]ХИНОКСАЛИН-1,4-(2H,5H)ДИОНЫ, ОБЛАДАЮЩИЕ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2471798C1 |
Авторы
Даты
2018-08-28—Публикация
2018-03-07—Подача