Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов, которые могут использоваться как исходные продукты для синтеза новых гетероциклических систем и лекарственных препаратов в фармакологии.
Известны структурные аналоги заявленных соединений, получаемые из 1,5-дигидро-2H-пиррол-2-онов [Армишева М.Н., Корниенко Н.А., Гейн В.Л., Вахрин М.И. Журнал общей химии. 2011. Т. 81. №9. С. 1556-1558. DOI: 10.1134/С107036321109026Х; Гейн В.Л., Гейн Л.Ф., Платонов В.С., Бобровская О.В. Журнал общей химии. 2014. Т. 84. №9. С. 1449-1453. DOI: 10.1134/С1070363214090072; Гейн В.Л., Булдакова Е.А., Дмитриев М.В., Мокрушин И.Г. Журнал общей химии. Т. 90. №1. С. 50-56. DOI: 10.1134/С1070363220010065; Abdul Rachid F.N.A., Mohammat М.F., Bouchamma F.Е., Сhааmeti Z., Hamzah A.C. Ruccian Journal of Organic Chemictry. 2020. Vol. 56. №6, pp. 1082-1088. DOI: 10.1134/С1070428020060184]. Синтез структурных аналогов осуществляется по следующей схеме с использованием полярных растворителей:
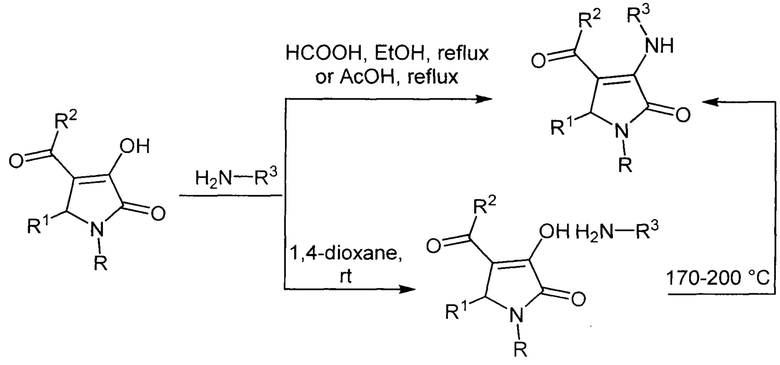
К недостаткам данных методов относится то, что 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионы невозможно получить с использованием свободного амина (например, циклогексиламина) (пример 6). Также для работы с диизопропиламином, который может быть выбран для получения класса 9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-8-(изопропиламино)-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов, требуется специальная защита кожи и глаз (согласно нормативу ГН 2.2.5.3532-18).
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов.
Поставленная задача осуществляется в несколько этапов по схеме ниже:
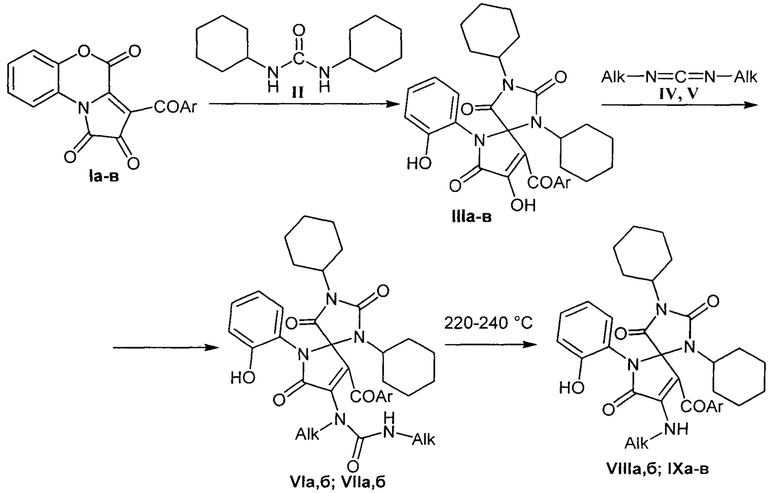
где: I, III: Ar=С6Н5 (а); Ar=C6H4Cl-4 (б); Ar=C6H4OMe-4 (в).
IV: Alk=(СН3)2СН; V: Alk=С6Н13.
VI, VIII: Ar=C6H4Cl-4, Alk=(СН3)2СН (а); Ar=C6H4OMe-4, Alk=(СН3)2СН (б).
VII, IX: Ar=С6Н5, Alk=С6Н13 (а); Ar=С6Н4С1-4, Alk=С6Н13 (б); Ar=C6H4OMe-4, Alk=С6Н13 (в).
1. кипячение 3-ароилпирроло[2,1-с][1,4]бензоксазин-1,2,4-трионов (Ia-в) с дициклогексилмочевиной (II) в среде инертного апротонного растворителя;
2. кипячение продукта (IIIa-в) с диалкилкарбодиимидом (IV) или (V) в среде инертного апротонного растворителя;
3. нагревание продуктов (VI), (VII) на металлической бане при 220-240°С до прекращения выделения газа.
Из патентной и технической литературы не были выявлены способы получения 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов, имеющие сходные признаки с заявленным способом - не использовались исходные продукты, растворитель, в котором проходит реакция. На основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 6-(2-Гидроксифенил)-8-изопропиламино-9-(4-хлорбензоил)-1,3-дицикло-гексил-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-трион (VIIIa).
Получение соединения (IIIб): К 0,5 г (1,4 ммоль) соединения (Ia) в 10 мл сухого толуола добавляют 0,066 г (1,4 ммоль) дициклогексилмочевины (II), кипятят в течение 30 минут (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывают. Выход 0,7 г (86%), т.пл. 155-157°С (разл.).
Получение соединения (VIa): К соединению (IIIб) 0,3 г (0,52 ммоль) добавляют 0,082 мл (0,52 ммоль) диизопропилкарбодиимида (IV), кипятят в течение 40 минут в 3 мл сухого толуола, выпавший осадок отфильтровывают. Выход (69%), т.пл. 155-157°С.
Получение соединения (VIIIa): 0,1 г (0,17 ммоль) соединения (VIa) нагревают на металлической бане при 220-240°С 7-10 минут (до прекращения выделения пузырьков газа). Охлаждают до комнатной температуры. Реакционную массу растирают в гексане, фильтруют, сушат. Выход 0,073 г (69%), т.пл. 151-153°С.
Соединение (IIIб) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIб) снят в виде пасты в вазелиновом масле: 3369, 3135, 1781, 1729, 1709, 1658 см-1.
Спектр ЯМР 1Н соединения (IIIб) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=9.89 (с, 1Н), 7.77 (м, 2Н), 7.58 (м, 2Н), 7.24 (м, 1Н), 6.99 (м, 1Н), 6.90 (м, 1Н), 6.81 (м, 1Н), 3.84 (м, 1Н), 3.08 (м, 1Н), 2.15-1.95 (м, 2Н), 1.87-1.58 (м, 8Н), 1.47 (м, 2Н), 1.35-1.05 (м, 7Н), 0.94 (м, 1Н) м.д.
Спектр ЯМР 13С соединения (IIIб) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=187.2, 169.2, 163.1, 156.3, 154.0, 153.8, 137.6, 136.1, 130.5 (2 С), 130.0, 128.4 (2 С), 126.7, 120.0, 118.9, 116.6, 112.6, 80.5, 52.0, 51.0, 30.0, 29.5, 28.7 (2 С), 25.7, 25.2, 25.2, 24.9, 24.8 (2 С) м. д.
Соединение (IIIб) C31H32ClN3O6. Найдено, %: С 64.52; Н 5.64; N 7.39. Вычислено, %: С 64.41; Н 5.58; N 7.27.
Соединение (VIa) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIa) снят в виде пасты в вазелиновом масле: 3173, 3083, 1702, 1681, 1666 см-1.
Спектр ЯМР 1H соединения (VIa) снят в растворе CDCl3 при частоте 400 МГц: δ=7.80 (м, 2Н), 7.46 (м, 2Н), 7.19 (м, 1Н), 6.99 (м, 2Н), 6.87 (м, 1Н), 4.87 (д, 1Н, J=4 Hz), 4.20 (м, 1Н), 4.02 (м, 1Н), 3.72 (м, 1Н), 2.96 (м, 1Н), 2.20 (м, 2Н), 2.00 (м, 1Н), 1.92-1.70 (м, 6Н), 1.63-1.62 (м, 1Н), 1.51-1.49 (м, 2Н), 1.44-1.23 (м, 6Н), 1.18-1.00 (м, 14Н) м. д.
Спектр ЯМР 13С соединения (VIa) снят в растворе CDCl3 при частоте 100 МГц: δ=188.1, 168.7, 165.4, 154.5, 154.3, 152.8, 142.7, 141.0, 134.0, 130.3 (2С), 129.2 (2С), 152.7, 121.3, 121.0, 119.0, 82.1, 54.6, 52.8, 51.3, 43.2, 30.4, 30.3, 29.1, 28.9, 26.1, 25.9, 25.8, 25.2, 25.0, 23.4, 23.0, 22.6, 21.9, 20.2 м.д.
Соединение (VIa) C38H46ClN5O6. Найдено, %: С 68.85; Н 6.63; N 9.89. Вычислено, %: С 68.81; Н 6.58; N 9.94.
Соединение (VIIIa) - белое высокоплавкое кристаллическое вещество, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIIIa) снят в виде пасты в вазелиновом масле: 3172, 1665 см-1.
Спектр ЯМР 1Н соединения (VIIIa) снят в растворе CDCl3 при частоте 400 МГц: δ=7.67 (м, 2Н), 7.47 (м, 2Н), 7.23 (м, 1Н), 7.06 (м, 1Н), 7.01 (м, 1Н), 6.90 (м, 1Н), 6.45 (уш. с, 1Н), 5.67 (д, 1Н, J=4 Hz), 3.96 (м, 1Н), 3.29 (м, 1Н), 2.80 (м, 1Н), 2.21-2.07 (м, 2Н), 1.95-1.66 (м, 7Н), 1.59-1.51 (м, 2Н), 1.39-0.85 (м, 15Н) м. д.
Спектр ЯМР 13С соединения (VIIIa) снят в растворе CDCl3 при частоте 100 МГц: δ=188.3, 170.0, 165.4, 154.5, 152.3, 139.3, 137.8, 130.5, 129.5 (2С), 129.3 (2С), 125.9, 122.0, 121.5, 119.9, 107.4, 83.0, 53.8, 52.3, 47.22, 30.5, 30.1, 29.0, 29.0, 26.4, 26.0, 25.9, 25.8, 25.2, 25.2, 22.7, 22.3 м. д.
Соединение (VIIIa) C34H39ClN4O5. Найдено, %: С 66.04; Н 6.30; N 9.11. Вычислено, %: С 65.96; Н 6.35; N 9.05.
Пример 2. 6-(2-Гидроксифенил)-8-изопропил-9-(4-метоксибензоил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-трион (VIIIб).
Получение соединения (IIIв): К 0,5 г (1.40 ммоль) соединения (Iв) в 10 мл сухого толуола добавляют 0,3 г (1.38 ммоль) дициклогексилмочевины (II), кипятят в течение 30 минут (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывают. Выход 0,73 г (90%), т.пл. 274-276°С.
Получение соединения (VIб): К соединению (IIIв) 0,3 г (0,5 ммоль) добавляют 0,164 мл (1.0 ммоль) диизопропилкарбодиимида (IV), кипятят в течение 40 минут, выпавший осадок отфильтровывают. Выход 0,22 г (31%), т.пл. 150-152°С.
Получение соединения (VIIIб): Соединение (VIб) 0,15 г (0,26 ммоль) нагревают на металлической бане при 220-240°С 7-10 минут (до прекращения выделения пузырьков газа). Охлаждают до комнатной температуры. Реакционную массу растирают в гексане, фильтруют, сушат. Выход 0,101 г (63%), т.пл. 148-150°С.
Соединение (IIIв) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIв) снят в виде пасты в вазелиновом масле: 3385, 3159, 1778,1727, 1716, 1683 см-1.
Спектр ЯМР 1Н соединения (IIIв) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=9.88 (с, 1Н), 7.77 (м, 2Н), 7.24 (м, 1Н), 7.05-6.98 (м, 3Н), 6.91 (м, 1Н), 6.81 (м, 1Н), 3.86-3.81 (м, 4Н), 3.06 (м, 1Н), 2.15-1.97 (м, 2Н), 1.83-1.70 (м, 5Н), 1.66-1.54 (м, 3Н), 1.49-1.41 (м, 2Н), 1.35-1.25 (м, 2Н), 1.21-1.08 (м, 5Н), 0.94 (м, 1Н) м. д.
Спектр ЯМР 13С соединения (IIIв) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=186.9, 169.2, 163.2, 154.1, 153.9, 131.1 (2С), 130.0, 129.8, 128.8, 128.1, 126.7, 120.1, 118.9, 116.6, 113.8, 113.5 (2С), 80.7, 55.4, 52.1, 51.0, 30.0, 29.5, 28.7 (2С), 28.6, 25.7, 25.2, 25.0, 24.8 (2С) м. д.
Соединение (IIIв) C32H33N3O7. Найдено, %: С 67.33; Н 6.19; N 7.42. Вычислено, %: С 67.00; Н 6.15; N 7.33.
Соединение (VIб) - белое высоко плавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIб) снят в виде пасты в вазелиновом масле: 3421, 3198, 1716, 1686, 1664, 1649 см-1.
Спектр ЯМР 1Н соединения (VIб) снят в растворе CDCl3 при частоте 400 МГц: δ=7.86 (м, 2Н), 7.18 (м, 1Н), 7.01 (м, 3Н), 6.94 (м, 2Н), 6.86 (м, 1Н), 4.88 (д, 1Н, J=8 Hz), 4.22 (м, 1Н), 4.02 (м, 1Н), 3.88 (с, 3Н), 3.76 (м, 1Н), 2.97 (м, 1Н), 2.27-2.14 (м, 2Н), 2.01 (м, 1Н), 1.92-1.69 (м, 6Н), 1.60 (м, 1Н), 1.51-1.47 (м, 2Н), 1.44-0.88 (м, 20Н) м. д.
Спектр ЯМР 13С соединения (VIб) снят в растворе CDCl3 при частоте 100 МГц: δ=187.5, 168.8, 165.8, 164.7, 154.5, 154.4, 152.8, 141.5, 131.6 (2С), 130.2, 128.5, 125.8, 121.6, 120.9, 119.1, 114.1 (2С), 82.3, 55.5, 54.6, 52.8, 51.2, 43.1, 30.4, 30.2, 29.2, 28.9, 26.1, 25.9, 25.9 (2С), 25.2, 25.0, 23.0, 22.6, 22.0, 20.2 м. д.
Соединение (VIб) C39H49N5O7. Найдено, %: С 67.02; Н 7.00; N 10.05. Вычислено, %: С 66.93; Н 7.06; N 10.01.
Соединение (VIIIб) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIIIб) снят в виде пасты в вазелиновом масле: 3121, 1700 см-1.
Спектр ЯМР 1Н соединения (VIIIб) снят в растворе CDCl3 при частоте 400 МГц: δ=7.74 (м, 2Н), 7.23 (м, 1Н), 7.09 (м, 2Н), 7.00 (м, 2Н), 6.90 (м, 1Н), 6.47 (уш. с, 1Н), 5.34 (д, 1Н, J=8 Hz), 3.99 (м, 1Н), 3.83 (с, 3Н), 3.27 (м, 1Н), 2.80 (м, 1Н), 2.22-2.12 (м, 2Н), 1.92-1.65 (м, 8Н), 1.54-1.49 (м, 2Н), 1.40-0.83 (м, 14Н) м. д.
Спектр ЯМР 13С соединения (VIIIб) снят в растворе CDCl3 при частоте 100 МГц: δ=188.4, 170.3, 166.0, 163.6, 154.7, 152.3, 142.0, 132.0, 130.6 (2С), 130.3, 125.9, 122.2, 121.5, 120.0, 114.2 (2С), 108.5, 83.2, 55.5, 53.8, 52.3, 47.0, 30.5, 30.0, 29.0 (2С), 26.4, 26.0, 25.9, 25.9, 25.2, 25.2, 22.8, 22.3 м. д.
Соединение (VIIIб) C35H42N4O6. Найдено, %: С 68.46; Н 6.92; N 9.08. Вычислено, %: С 68.38; Н 6.89; N 9.11.
Пример 3. 9-Бензоил-6-(2-гидроксифенил)-1,3-дициклогексил-8-циклогексиламино-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-трион (IXa).
Получение соединения (IIIa): К 0,5 г (1,49 ммоль) соединения (Ia) в 10 мл сухого толуола добавляют 0,33 г (1.47 ммоль) дициклогексилмочевины (II), кипятят в течение 30 минут (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывают. Выход 0,78 г (95%), т.пл. 287-289°С (разл.).
Получение соединения (VIIa): К соединению (IIIa) 0,3 г (0,55 ммоль) добавляли 1.0 ммоль дициклогексилкарбодиимида (V), кипятили в течение 40 минут, выпавший осадок отфильтровывали. Выход 0,33 г (80%), т.пл. 273-275°С.
Получение соединения (IXa): Соединение (VIIa) 0,1 г (1.0 ммоль) нагревают на металлической бане при 220-240°С 7-10 минут (до прекращения выделения пузырьков газа). Охлаждают до комнатной температуры. Реакционную массу растирают в гексане, фильтруют, сушат. Выход 0,08 г (96%), т.пл. 215-217°С.
Соединение (IIIa) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIIa) снят в виде пасты в вазелиновом масле: 3354, 3151, 1779, 1723, 1708, 1678 см-1.
Спектр ЯМР 1Н соединения (IIIa) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=9.90 (с, 1Н), 7.75 (м, 2Н), 7.62 (м, 1Н), 7.51 (м, 2Н), 7.24 (м, 1Н), 7.00 (м, 1Н), 6.91 (м, 1Н), 6.81 (м, 1Н), 3.84 (м, 1Н), 3.08 (м, 1Н), 2.16-1.96 (м, 2Н), 1.87-1.55 (м, 8Н), 1.46 (м, 2Н), 1.36-1.10 (м, 7Н), 0.95 (м, 1Н) м. д.
Спектр ЯМР 13С соединения (IIIa) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=188.5, 169.2, 163.1, 155.5, 154.0, 153.9, 137.3, 132.8, 130.0, 128.6 (2С), 128.2 (2С), 126.7, 120.0, 119.0, 116.7, 113.1, 80.6, 52.1, 51.0, 30.0, 29.5, 28.6 (2С), 25.7, 25.2, 25.2, 25.0, 24.8 (2С) м. д.
Соединение (IIIa) C31H33N3O6. Найдено, %: С 68.30; Н 6.07; N 7.93. Вычислено, %: С 68.49; Н 6.12; N 7.73.
Соединение (VIIa) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIIa) снят в виде пасты в вазелиновом масле: 3411, 3132, 1781, 1730, 1652 см-1.
Спектр ЯМР 1Н соединения (VIIa) снят в растворе CDCl3 при частоте 400 МГц: δ=7.85 (м, 2Н), 7.62 (м, 1Н), 7.47 (м, 2Н), 7.19 (м, 1Н), 7.01 (м, 2Н), 6.88 (м, 1Н), 6.73 (уш. с, 1Н), 4.85 (д, 1Н, J=4 Hz), 4.03 (м, 1Н), 3.74 (м, 1Н), 3.46 (м, 1Н), 2.99 (м, 1Н), 2.21 (м, 2Н), 2.00-1.50 (м, 22Н), 1.44-0.97 (м, 16Н) м. д.
Спектр ЯМР 13С соединения (VIIa) снят в растворе CDCl3 при частоте 100 МГц: δ=189.4, 168.7, 165.8, 154.5, 154.4, 152.7, 142.5, 135.8, 134.2, 130.2, 129.0 (2С), 128.7 (2С), 125.6, 121.7, 121.1, 119.4, 82.1, 59.7, 54.6, 52.8, 49.9, 33.3, 33.0, 31.9, 30.4, 30.4, 30.1, 29.1, 29.0, 26.3, 26.1. 26.1, 29.9, 25.8, 25.7, 25.6, 25.3, 25.2, 25.0, 24.9, 24.7 м. д.
Соединение (VIIa) C44H55N5O6. Найдено, %: С 70.38; Н 7.44; N 9.30. Вычислено, %: С 70.47; Н 7.39; N 9.34.
Соединение (IXa) - белое высокоплавкое кристаллическое вещество, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IXa) снят в виде пасты в вазелиновом масле: 3363, 3276, 1767, 1724, 1700, 1633 см-1.
Спектр ЯМР 1Н соединения (IXa) снят в растворе CDCl3 при частоте 400 МГц: δ=7.69 (м, 2Н), 7.59 (м, 1Н), 7.51 (м, 2Н), 7.24 (м, 1Н), 7.08 (м, 1Н), 7.03 (м, 1Н), 6.91 (м, 1Н), 6.45 (уш. с, 1Н), 5.60 (д, 1Н, J=8 Hz), 3.99 (м, 1Н), 2.84 (м, 1Н), 2.22-2.10 (м, 2Н), 1.97-1.82 (м, 6Н), 1.68-1.53 (м, 7Н), 1.45-0.75 (м, 16Н) м. д.
Спектр ЯМР 13С соединения (IXa) снят в растворе CDCl3 при частоте 100 МГц: δ=189.7, 170.3, 165.7, 154.7, 152.4, 139.9, 132.7, 130.4, 129.0 (2С), 128.1, 126.1, 122.1, 121.5 (2С), 120.0, 107.1, 83.1, 53.8, 52.3, 33.9, 32.9, 32.4, 30.5, 30.0, 29.1, 29.0, 26.4, 26.0, 25.9, 25.9, 25.2, 25.2, 25.1,24.5, 24.2 м. д.
Соединение (IXa) C37H44N4O5. Найдено, %: С 71.20; Н 7.17; N 8.93. Вычислено, %: С 71.13; Н 7.10; N 8.97.
Пример 4. 6-(2-Гидроксифенил)-1,3-дициклогексил-9-(4-хлорбензоил)-8-циклогексиламино-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-трион (IXб)
Получение соединения (VIIб): К соединению (IIIб) 0,3 г (0,5 ммоль) добавляли 0,10 г (0,5 ммоль) дициклогексилкарбодиимида (V), кипятили в течение 40 минут в 10 мл сухого толуола, выпавший осадок отфильтровывали. Выход 0,33 г (84%), т.пл. 203-204°С.
Получение соединения (IXб): Соединение (VIIб) 0,1 г (0,13 ммоль) нагревают на металлической бане при 220-240°С 7-10 минут (до прекращения выделения пузырьков газа). Расплав растирают в гексане, фильтруют, сушат. Выход 0,06 г (70%), т.пл. 174-175°С.
Соединение (VIIб) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIIб) снят в виде пасты в вазелиновом масле: 3345, 3181, 1780, 1731, 1718, 1655 см-1.
Спектр ЯМР 1Н соединения (VIIб) снят в растворе DMCO-d6 при частоте 400 МГц: δ=9.98 (с, 1Н), 7.86 (м, 2Н), 7.58 (м, 2Н), 7.23 (м, 1Н), 6.99 (м, 1Н), 6.90 (м, 1Н), 6.81 (м, 1Н), 5.94 (д, 1Н, J=4 Hz), 3.87 (м, 1Н), 3.73 (м, 1Н), 3.33 (м, 1Н), 3.03 (м, 1Н), 2.14-1.99 (м, 2Н), 1.82-1.40 (м, 20Н), 1.34-0.87 (м, 18Н) м. д.
Спектр ЯМР 13С соединения (VIIб) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=188.5, 168.3, 163.8, 154.2, 154.0, 153.5, 143.7, 139.0, 134.4, 130.4, 129.9, 128.8 (2С), 126.7, 120.5 (2С), 118.9, 116.6, 81.1, 57.4, 52.9, 51.4, 49.3, 32.5, 32.3 (2С), 31.2, 30.0, 29.8, 29.6, 28.6, 28.6 (2С), 25.6, 25.4, 25.2 (2С), 25.2, 25.1, 25.0, 24.8, 24.6 (2С), 24.6 м. д.
Соединение (VIIб) C44H54ClN5O6. Найдено, %: С 67.56; Н 6.99; N 8.96. Вычислено, %: С 67.37; Н 6.94; N 8.93.
Соединение (IXб) - белое высокоплавкое кристаллическое вещество, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IXб) снят в виде пасты в вазелиновом масле: 3379, 3278, 1767, 1724, 1701 см-1.
Спектр ЯМР 1Н соединения (IXб) снят в растворе CDCl3 при частоте 400 МГц: δ=7.65 (м, 2Н), 7.49 (м, 2Н), 7.24 (м, 1Н), 7.04 (м, 2Н), 6.92 (м, 1Н), 6.38 (с, 1Н), 5.77 (уш. с, 1Н), 3.97 (м, 1Н), 2.81 (м, 1Н), 2.21-2.09 (м, 2Н), 1.95-1.80 (м, 7Н), 1.68-1.46 (м, 9Н), 1.36-0.85 (м, 13Н) м. д.
Спектр ЯМР 13С соединения (IXб) снят в растворе CDCl3 при частоте 100 МГц: δ=188.4, 170.1, 165.5, 154.6, 152.3, 139.2, 138.1, 130.5, 129.5 (2 С), 129.3 (2 С), 126.0, 122.0, 121.6, 120.0, 106.8, 83.1, 53.8, 52.3, 32.9, 32.4, 32.4, 30.5, 30.1, 29.1, 29.0, 26.4, 26.0, 25.9, 25.9, 25.2, 25.2, 25.1, 24.5, 24.3 м. д.
Соединение (IXб) C37H43ClN4O5. Найдено, %: С 67.53; Н 6.61; N 8.47. Вычислено, %: С 67.41; Н 6.58; N 8.50.
Пример 5. 6-(2-Гидроксифенил)-9-(4-метоксибензоил)-1,3-дициклогексил-8-цикло-гексиламино-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-трион (IXв).
Получение соединения (VIIв): К соединению (IIIв) 0,3 г (0,52 ммоль) добавляют 0,11 г (0,52 ммоль) дициклогексилкарбодиимида (V), кипятят в течение 40 минут, выпавший осадок отфильтровывают. Выход 0,19 г (47%), т.пл. 274-276°С.
Получение соединения (IХв): Соединение (VIIв) 0,065 г (0,1 ммоль) нагревают на металлической бане при 220-240°С 7-10 минут (до прекращения выделения пузырьков газа). Охлаждают до комнатной температуры. Реакционную массу растирают в гексане, фильтруют, сушат. Выход 0,038 г (59%), т.пл. 275-277°С.
Соединение (VIIв) - белое высоко плавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (VIIв) снят в виде пасты в вазелиновом масле: 3341, 3176, 1779, 1732, 1716, 1645 см-1.
Спектр ЯМР 1Н соединения (VIIв) снят в растворе DMCO-d6 при частоте 400 МГц: δ=9.96 (с, 1Н), 7.88 (м, 2Н), 7.22 (м, 1Н), 6.98 (м, 3Н), 6.89 (м, 1Н), 6.81 (м, 1Н), 5.87 (д, 1Н, J=8 Hz), 3.91-3.84 (м, 4Н), 3.67 (м, 1Н), 3.43 (м, 1Н), 2.99 (м, 1Н), 2.11-2.01 (м, 2Н), 1.85-1.45 (м, 18Н), 1.39-0.86 (м, 20Н) м. д.
Спектр ЯМР 13С соединения (VIIв) снят в растворе ДМСО-d6 при частоте 100 МГц: δ=187.8, 168.2, 164.1, 164.0, 154.2, 153.6, 142.1, 131.4 (2С), 129.8, 128.6, 126.6, 120.7, 118.9, 116.5, 113.9 (2С), 81.36, 57.0, 55.6, 53.0, 51.4, 49.2, 32.5 (2С), 32.5, 31.2, 30.2, 29.8, 29.6, 28.7, 28.6, 25.6, 25.3, 25.2 (2С), 25.1, 24.8, 24.7, 24.7, 24.6 (2С), 24.5 м. д.
Соединение (VIIв) C45H57N5O7. Найдено, %: С 69.53; Н 7.45; N 8.89. Вычислено, %: С 69.30; Н 7.37; N 8.98.
Соединение (IХв) - белое высокоплавкое кристаллическое вещество, плавящееся с разложением, легкорастворимое в хлороформе, ДМСО и ДМФА, растворимое в ацетоне, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IХв) снят в виде пасты в вазелиновом масле: 3376, 3282, 1764, 1723, 1700 см-1.
Спектр ЯМР 1Н соединения (Хв) снят в растворе CDCl3 при частоте 400 МГц: δ=7.71 (м, 2Н), 7.23 (м, 1Н), 7.08-6.97 (м, 4Н), 6.90 (м, 1Н), 6.46 (уш. с, 1Н), 5.48 (д, 1Н, J=12 Hz), 4.00 (м, 1Н), 3.89 (с, 3Н), 2.81 (м, 1Н), 2.18 (м, 2Н), 1.91-1.82 (м, 7Н), 1.68-1.43 (м, 7Н), 1.37-0.75 (м, 15Н) м. д.
Спектр ЯМР 13С соединения (IХв) снят в растворе CDCl3 при частоте 100 МГц: δ=188.5, 170.4, 166.0, 163.6, 154.7, 152.3, 132.4, 130.5 (2С), 130.3, 125.9, 122.2, 121.5, 120.0, 114.2 (2С), 107.7, 83.0, 55.6, 53.8, 53.7, 52.3, 33.1, 32.4, 30.5, 30.0, 29.1, 29.0, 26.4, 26.0, 25.9, 25.9, 25.2, 25.2, 25.1, 24.6, 24.3 м. д.
Соединение (IХв) СН46N4О6. Найдено, %: С 69.79; Н 7.03; N 8.61. Вычислено, %: С 69.70; Н 7.08; N 8.56.
Пример 6. Взаимодействие 9-бензоил-8-гидрокси-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нон-8-ен-2,4,7-триона с циклогексиламином.
Взаимодействие соединения (IIIa) 0,01 г (0,018 ммоль) с циклогексиламином 0,002 мл (0,018 ммоль и более) в среде полярных (этанола, 1,4-диоксана, муравьиной кислоты) и неполярньгх (толуола) растворителей при нагревании или выдерживании при комнатной температуре в течение 1-24 ч не приводит к получению соединения (IXa) (по данным ультра-ВЭЖХ-УФ-МС).
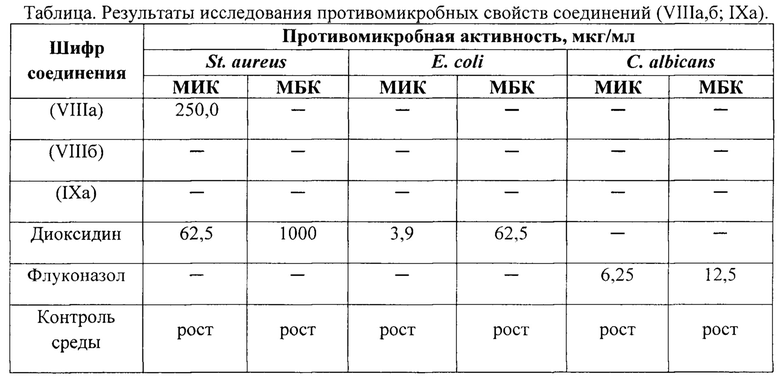
Пример 7. Фармакологическое исследование 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов (VIIIa,б; IXa) на наличие противомикробной активности.
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [А.Н. Миронов, Руководство по проведению доклинических исследований лекарственных средств / Часть первая. - М.: Гриф и К, 2012, с. 509].
В качестве тест-микроорганизмов использовали Staphylococcus aureus (штамм 906), Eccherichia coli (штамм 1257), полученных в Федеральном государственном бюджетном учреждении «Научный центр экспертизы средств медицинского применения» (ФГБУ «НЦЭСМП» Минздрава России, г. Москва); Candida albicans, РКПГУ 1353/1277, полученный в НИИ медицинской микологии им. П.Н. Кашкина ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России.
Культуры выращивали в пробирках на скошенной питательной среде (мясопептонный агар, Сабуро). Для приготовления рабочей взвеси микроорганизмов производили смыв выросшей культуры изотоническим раствором хлорида натрия и устанавливали плотность по стандарту McFarland 0,5 Ед с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
В качестве стандартной навески изучаемых соединений брали 20 мг. Растворяли в 1 мл ДМСО, а затем добавляли 9 мл дистиллированной воды, таким образом, получая концентрацию в 2000,0 мкг/мл испытуемого вещества. Далее в лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений соединений в бульоне МПБ, Сабуро. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культуры в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 0,5 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотность (ОП) при длине волны 540 нм. Через 24 часа и 7 суток вновь регистрировали ОП культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения
Анализ полученных данных показал: соединение (Villa) обладает ингибирующим действием в концентрации 250,0 мкг/мл соответственно в отношении штамма Staphylococcus aureus.
Изобретение относится к способу получения 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов, который заключается в том, что 3-ароилпирроло[2,1-с][1,4]бензоксазин-1,2,4-трионы подвергают последовательному взаимодействию с дициклогексилмочевиной, изопропилкарбодиимидом или дициклогексилкарбодиимидом в среде инертного апротонного растворителя, последующим термолизом полученных соединений с дальнейшим выделением целевых продуктов, по схеме
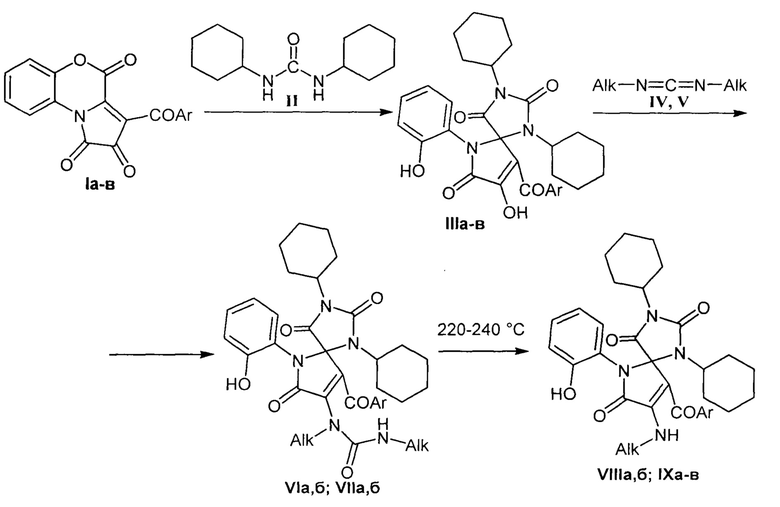
где I, III: Ar=C6H4Cl-4 (а); Ar=C6H4OMe-4 (б); IV: Alk=(СН3)2СН; V: Alk=С6Н13; VI, VIII: Ar=C6H4Cl-4, Alk=(СН3)2СН (а); Ar=C6H4OMe-4, Alk=(СН3)2СН (б); VII, IX: Ar=C6H4Cl-4, Alk=С6Н13 (а); Ar=C6H4OMe-4, Alk=С6Н13 (б). Технический результат – разработан способ получения новых соединений, которые могут использоваться как исходные продукты для синтеза новых гетероциклических систем и лекарственных препаратов в фармакологии. 1 табл., 7 пр.
Способ получения 8-(алкиламино)-9-ароил-6-(2-гидроксифенил)-1,3-дициклогексил-1,3,6-триазаспиро[4.4]нона-8-ен-2,4,7-трионов, отличающийся тем, что 3-ароилпирроло[2,1-с][1,4]бензоксазин-1,2,4-трионы подвергают последовательному взаимодействию с дициклогексилмочевиной, изопропилкарбодиимидом или дициклогексилкарбодиимидом в среде инертного апротонного растворителя, последующим термолизом полученных соединений с дальнейшим выделением целевых продуктов, по схеме
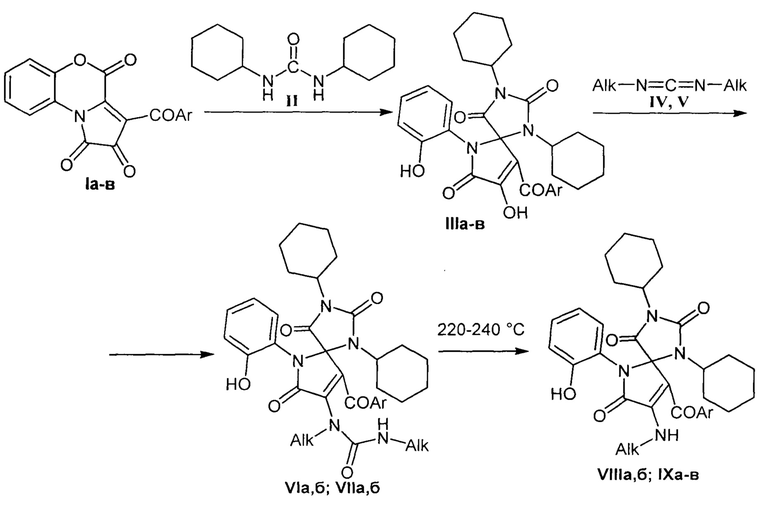
где I, III: Ar=C6H4Cl-4 (а); Ar=C6H4OMe-4 (б);
IV: Alk=(СН3)2СН; V: Alk=С6Н13;
VI, VIII: Ar=C6H4Cl-4, Alk=(СН3)2СН (а); Ar=C6H4OMe-4, Alk=(СН3)2СН (б);
VII, IX: Ar=C6H4Cl-4, Alk=С6Н13 (а); Ar=C6H4OMe-4, Alk=С6Н13 (б).
Авторы
Даты
2021-11-02—Публикация
2021-03-05—Подача