ОБЛАСТЬ ТЕХНИКИ
Настоящая заявка относится к области генной терапии и молекулярной биологии. Более конкретно, настоящее изобретение относится к выделенному модифицированному белку VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), который содержит одну или несколько аминокислотных замен по сравнению с белком VP1 капсида AAV9 дикого типа, которые повышают эффективность продукции (сборки) вектора на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), капсиду и вектору на основе вышеуказанного VP1, а также к их применению.
УРОВЕНЬ ИЗОБРЕТЕНИЯ
Аденоассоциированный вирус (AAV) представляет собой небольшой (25 нм), неспособный к самостоятельной репликации, безоболочечный вирус. У человека и приматов описано множество различных серотипов AAV. Геном аденоассоциированного вируса содержит (+ или -) одноцепочечную ДНК (ssDNA) длиной около 4,7 тысяч нуклеотидов. На концах молекулы геномной ДНК располагаются инвертированные концевые повторы (англ. inverted terminal repeats, ITRs). Геном содержит две открытые рамки считывания (англ. ORF): Rep и Сар, содержащие в себе несколько альтернативных рамок считывания, кодирующих различные белковые продукты. Продукты Rep имеют важное значение для репликации AAV, при этом ген Сар, помимо других альтернативных продуктов, кодирует 3 капсидных белка (VP1, VP2 и VP3). Белки VP1, VP2 и VP3 находятся в соотношении 1:1:10, образуя икосаэдрический капсид (Xie Q. et al. The atomic structure of adeno-associated virus (AAV-2), a vector for human gene therapy. Proc Natl Acad Sci USA, 2002; 99:10405-10410). При образовании рекомбинантного вектора AAV (rAAV) кассета экспрессии, фланкированная ITR, упаковывается в капсид AAV. Гены, необходимые для репликации AAV, не входят в кассету. Рекомбинантный AAV считается самым безопасным и одним из наиболее широко используемых вирусных векторов для переноса генов in vivo. Векторы могут инфицировать клетки множества типов тканей, обеспечивая эффективную и устойчивую экспрессию трансгена. Они также являются непатогенными и имеют низкий профиль иммуногенности (High КА et al., «rAAV human trial experience)) Methods Mol Biol. 2011; 807:429-57).
Одной из насущных целей исследований в области разработки эффективной генотерапии является оптимизация векторов для улучшения тех или иных свойств данных векторов.
Известно, что различные серотипы AAV характеризуются сродством к различным рецепторам на поверхности клеток-хозяев, к которым они обладают тропизмом. Так основным известным рецептором для AAV2 является гепарансульфат-протеогликан, корецепторами выступают интегриновый гетеродимер aVβ5, рецептор фактора роста фибробластов первого типа и рецептор фактора роста гепатоцитов, с-Met. AAV12 связывается с гепарансульфат-протеогликанами и сиаловой кислотой. AAV4 и AAV5 связываются с N- и О-связанными сиаловыми кислотами соответственно. AAV5 задействует рецептор фактора роста тромбоцитов. При этом установлена связь между аминокислотной последовательностью белков капсида AAV с процессом его сборки, инкапсидирования генома и сродством к различным типам рецепторов, репрезентированных на поверхности клеток-хозяев (Govindasamy L. et. al. Structural insights into adeno-associated virus serotype 5. J Virol. 2013 Oct; 87(20):11187-99).
В международной заявке WO 2012145601 описаны вирионы аденоассоциированного вируса (AAV) с вариантным капсидным белком, где вирионы AAV демонстрируют большую инфекционность ретинальных клеток, когда вводятся интравитреальной инъекцией, по сравнению с AAV дикого типа.
В международной заявке WO 2013158879 описан вектор на основе аденоассоциированного вируса (AAV) для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, содержащей капсидный белок VP1, который содержит одну или несколько замен лизина, где одна замена лизина представляет K137R, где упомянутая замена лизина является эффективной для ингибирования убиквитинилирования упомянутого капсидного белка, и тем самым увеличивается трансдукция упомянутого вектора AAV в клетке-мишени.
На данный момент существует потребность в высокоэффективной продукции (сборке) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), то есть в эффективном получении вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), которые содержат трансген (инкапсидированную гетерологичную нуклеиновую кислоту).
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторами изобретения было неожиданно установлено, что наличие одной или нескольких аминокислотных замен в белке VP1 капсида AAV9 дикого типа, которые выбраны из группы:
F422W,
F422W и Y446F,
I601M,
приводит к высокоэффективной продукции (сборке) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9) по сравнению со сборкой инкапсидированных вирусных векторов на основе rAAV9 дикого типа (без вышеуказанных мутаций), то есть при сборке инкапсидированных вирусных векторов на основе rAAV9, содержащих вышеуказанные модификации в капсиде AAV9, получают вирусные вектора на основе rAAV9, которые содержат трансген (инкапсидированную гетерологичную нуклеиновую кислоту), значительно чаще чем при сборке инкапсидированных вирусных векторов на основе rAAV9 дикого типа (без вышеуказанных мутаций).
Краткое описание изобретения
В одном из аспектов настоящее изобретение относится к выделенному модифицированному белку VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), который содержит аминокислотную последовательность белка VP1 капсида AAV9 дикого типа, кодируемую геном Сар, с одной или несколькими заменами, которые выбраны из группы:
F422W,
F422W и Y446F,
I601M,
где аминокислотная последовательность белка VP1 капсида AAV9 дикого типа имеет аминокислотную последовательность, представленную SEQ ID NO: 1.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замену в положении F422W.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность, представленную SEQ ID NO: 2.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замены F422W и Y446F.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность, представленную SEQ ID NO: 3.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замену I601М.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность, представленную SEQ ID NO: 4.
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, которая кодирует любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), использующихся для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9).
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F422W и представлена нуклеиновой последовательностью с SEQ ID NO: 6 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F422W и Y446F и представлена нуклеиновой последовательностью с SEQ ID NO: 7 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I601М и представлена нуклеиновой последовательностью с SEQ ID NO: 8 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
В одном из аспектов настоящее изобретение относится к выделенному капсиду для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), который включает любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), белок VP2 капсида AAV9 или его модифицированный вариант и белок VP3 капсида AAV9 или его модифицированный вариант.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP2 капсида AAV9 дикого типа.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP2 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 9.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 10.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 11.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 12.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP3 капсида AAV9 дикого типа.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP3 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 17.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 18.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 19.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 20.
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, которая кодирует любой из вышеуказанных капсидов, использующихся для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9).
В одном из аспектов настоящее изобретение относится к вектору на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9) для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, который включает:
1) любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) или любой из вышеуказанных капсидов, и
2) гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках.
В некоторых вариантах осуществления изобретения вектор на основе rAAV9 включает гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, где продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой терапевтический полипептид или репортерный полипептид.
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для доставки генного продукта нуждающемуся в этом субъекту, которая содержит:
a) любой из вышеуказанных векторов на основе rAAV9; и
b) фармацевтически приемлемый эксципиент.
В одном из аспектов настоящее изобретение относится к способу доставки генного продукта нуждающемуся в этом субъекту, который включает введение субъекту любого из вышеуказанных векторов на основе rAAV9 или вышеуказанной фармацевтической композиции.
В одном из аспектов настоящее изобретение относится к применению любого из вышеуказанных векторов на основе rAAV9 или вышеуказанной фармацевтической композиции для лечения заболевания у нуждающегося в этом субъекта.
В некоторых вариантах осуществления применения заболевание выбирают из группы: заболевания крови; заболевания центральной нервной системы; заболевания метаболизма; заболевания мышц; наследственные заболевания.
В одном из аспектов настоящее изобретение относится к способу получения любого из вышеуказанных векторов на основе rAAV9, который включает трансфекцию клеток-продуцентов, соответственно, любой из вышеуказанных нуклеиновых кислот, которые содержат последовательность, кодирующую модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), или вышеуказанной нуклеиновой кислотой, кодирующей капсид.
Краткое описание чертежей
Фигура 1 представляет собой кольцевую схему плазмиды pAAV-linker, предназначенной для клонирования библиотек случайных вариантов гена капсида AAV девятого серотипа.
GFP- последовательность, кодирующая зеленый флуоресцентный белок,
PolyA - сигнал полиаденилирования,
ITR - инвертированный концевой повтор аденоассоциированного вируса,
Т2А - последовательность, кодирующая 2А расщепляющийся пептид, который позволяет осуществлять коэкспрессию целевого и репортерного белков,
HBG intron - интрон бета-глобина человека,
CMVpromoter - промотор цитомегаловируса человека,
AmpR- последовательность гена бета-лактамазы, обеспечивающая устойчивость E.coli к ампициллину,
pUC origin - высококопийный ориджин репликации бактерий.
Фигура 2 представляет собой кольцевую схему плазмиды pAAV-GFP.
EGFP- последовательность, кодирующая модифицированный зеленый флуоресцентный белок,
PolyA - сигнал полиаденилирования,
ITR - инвертированный концевой повтор аденоассоциированного вируса,
HBG intron - интрон бета-глобина человека,
CMV promoter - промотор цитомегаловируса человека,
AmpR- последовательность гена бета-лактамазы, обеспечивающая устойчивость E.coli к ампициллину,
pUC origin - высококопийный ориджин репликации бактерий.
Фигура 3 представляет собой кольцевую схему плазмиды pAAV-Rep, предназначенной для наработки рекомбинантных вирусных препаратов дикого типа AAV девятого серотипа из библиотеки случайных вариантов.
AmpR- последовательность гена бета-лактамазы, обеспечивающая устойчивость E.coli к ампициллину,
pUC origin - высококопийный ориджин репликации бактерий,
AAV Rep genes - последовательность, кодирующая белки Rep, необходимые для жизненного цикла вируса.
Фигура 4 представляет собой кольцевую схему плазмиды pHelper, предназначенной для наработки рекомбинантных вирусных препаратов дикого типа AAV девятого серотипа из библиотеки случайных вариантов.
AmpR - ген бета-лактамазы, обеспечивающий устойчивость к ампициллину,
Ori- ориджин репликации в бактериях,
Adeno Е2А - последовательность гена хелперного аденовируса, участвующая в репликации вирусной ДНК,
Adeno Е4 - последовательность гена хелперного аденовируса, участвующая в репликации вирусной ДНК,
Adeno VARNA - последовательность гена хелперного аденовируса, отвечающая за стимуляцию трансляции как ранних, так и поздних вирусных генов.
Фигура 5 представляет собой график, который показывает эффективность наработки векторов на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9.
AAV9-01Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутацией F422W.
AAV9-02Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутацией I601M.
AAV9-03Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутациями Y446F и F422W.
AAV9-NullMut-GFP обозначает вектор на основе аденоассоциированного вируса 9 серотипа (rAAV9), включающий белок VP1 капсида AAV9 дикого типа.
Vg/ml кж обозначает количество вирусных геномов на миллилитр культуральной жидкости.
Фигура 6 представляет собой график, который показывает оценку эффективности трансдукции клеток препаратами на основе rAAV9, которые содержат одну или несколько точечных мутаций в белке VP1 капсида AAV9 дикого типа.
AAV9-01Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутацией F422W.
AAV9-02Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутацией I601M.
AAV9-03Mut-GFP обозначает вектор на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9), включающего модифицированный белок VP1 капсида AAV9 с мутациями Y446F и F422W.
AAV9-NullMut-GFP обозначает вектор на основе аденоассоциированного вируса 9 серотипа (rAAV9), включающий белок VP1 капсида AAV9 дикого типа.
Фигура 7 представляет собой схему положения структурных белков капсида AAV9 в последовательности кодирующей капсид AAV9.
1-737 ак-VPl,
138-737 ак-УР2,
203-737 ак-УРЗ.
Определения и общие методы
Если иное не определено в настоящем документе, научные и технические термины, используемые в связи с настоящим изобретением, будут иметь значения, которые обычно понятны специалистам в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
«Выделенный» означает измененный или удаленный из природного состояния. Например, нуклеиновая кислота или пептид, в природе присутствующие в живых организмах, не являются «выделенными», но те же нуклеиновая кислота или пептид, частично или полностью отделенные от материалов, сопутствующих им в их природном состоянии, являются «выделенными». Выделенная нуклеиновая кислота или белок могут существовать, по существу, в очищенной форме или могут существовать в неприродном окружении, таком как, например, генетически модифицированной клетке.
Определения «встречающийся в природе», «нативный» или «дикого типа» используют для описания объекта, который можно обнаружить в природе как отличающийся от получаемого искусственно. Например, белок или нуклеотидная последовательность, присутствующие в организме (включая вирус), которые можно изолировать из источника в природе, и которые не модифицированы умышленно специалистом в лаборатории, являются встречающимися в природе.
Термин «геном» относится к полному генетическому материалу организма.
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «включать» и «содержать» или их вариации, такие как «имеющий», «включает», «включающий», «содержит» или «содержащий», следует понимать как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых.
Белок (Пептид)
В настоящем описании термины «пептид», «полипептид» и «белок» используют взаимозаменяемо, и они относятся к соединению, состоящему из аминокислотных остатков, ковалентно связанных пептидными связями. Белок или пептид должен содержать по меньшей мере две аминокислоты, и не существует ограничений по максимальному количеству аминокислот, которые может содержать последовательность белка или пептида. Полипептиды включают любой пептид или белок, содержащий две или более аминокислот, соединенных друг с другом пептидными связями. Как применяют в настоящем описании, термин относится и к коротким цепям, также общепринято обозначаемым в этой области, например, как пептиды, олигопептиды и олигомеры, и к более длинным цепям, как правило, обозначаемым в этой области как белки, множество типов которых существует.«Полипептиды» включают, помимо прочего, например, биологически активные фрагменты, по существу, гомологичные полипептиды, олигопептиды, гомодимеры, гетеродимеры, варианты полипептидов, модифицированные полипептиды, производные, аналоги, слитные белки. Полипептиды включают природные пептиды, рекомбинантные пептиды, синтетические пептиды или их комбинацию. Молекулы нуклеиновых кислот
Термины «нуклеиновая кислота», «нуклеиновая последовательность» или «нуклеиновокислотная последовательность», «полинуклеотид», «олигонуклеотид», «полинуклеотидная последовательность» и «нуклеотидная последовательность», которые используются равнозначно в данном описании, обозначают четкую последовательность нуклеотидов, модифицированных или не модифицированных, определяющую фрагмент или участок нуклеиновой кислоты, содержащую или не содержащую неприродные нуклеотиды и являющуюся либо двухцепочечной ДНК или РНК, либо одноцепочечной ДНК или РНК, либо продуктами транскрипции указанных ДНК.
Как применяют в настоящем описании, полинуклеотиды включают, в качестве неограничивающих примеров, все последовательности нуклеиновой кислоты, получаемые любыми способами, доступными в этой области, включая, в качестве неограничивающих примеров, рекомбинантные способы, т.е. клонирование последовательностей нуклеиновой кислоты из рекомбинантной библиотеки или генома клетки, использование обычной технологии клонирования и ПЦР и т.п., и способами синтеза.
Здесь также следует упомянуть, что данное изобретение не относится к нуклеотидным последовательностям в их природной хромосомной среде, т.е. в природном состоянии. Последовательности данного изобретения были выделены и/или очищены, т.е. были взяты прямо или косвенно, например, путем копирования, при этом их среда была по меньшей мере частично модифицирована. Таким образом, также здесь следует подразумевать изолированные нуклеиновые кислоты, полученные путем генетической рекомбинации, например, с помощью принимающих клеток (клеток-хозяев), или полученные путем химического синтеза.
Термин нуклеотидная последовательность охватывает его комплемент, если не указано иное. Таким образом, нуклеиновую кислоту, имеющую определенную последовательность следует понимать как охватывающие ее комплементарную цепь с ее комплементарной последовательностью.
Аденоассоциированный вирус (AAV)
Вирусы семейства Parvoviridae представляют собой небольшие ДНК-содержащие вирусы животных. Семейство Parvoviridae может быть разделено на два подсемейства: Parvovirinae, представители которого инфицируют позвоночных животных, и Densovirinae, представители которого инфицируют насекомых. К 2006 году были описаны 11 серотипов аденоассоциированного вируса (Mori, S. ET AL., 2004, «Two novel adeno-associated viruses from cynomolgus monkey: pseudotyping characterization of capsid protein», Virology, T. 330 (2): 375-83). Все известные серотипы могут инфицировать клетки многих видов тканей. Тканевая специфичность определяется серотипом белков капсида, поэтому векторы на основе аденоассоциированого вируса конструируют, задавая необходимый серотип. Дополнительная информация по парвовирусам и другим представителям Parvoviridae описана в литературе (Kenneth I. Berns, «Parvoviridae: The Viruses and Their Replication», Chapter 69 in Fields Virology (3d Ed. 1996)).
Геномная организация всех известных серотипов AAV очень сходна. Геном AAV представляет собой линейную одноцепочечную молекулу ДНК, которая содержит менее чем примерно 5000 нуклеотидов (нт) в длину. Инвертированные концевые повторы (ITR) фланкируют уникальные кодирующие нуклеотидные последовательности белков (Rep), необходимых для обеспечения жизненного цикла вируса, а также последовательности перекрывающихся белков капсида (Сар). Ген Сар кодирует белки VP (VP1, VP2 и VP3), которые образуют капсид, а так же белки ААР (белок, активирующий сборку аденоассоциированного вируса (AAV) Sonntag F, Köther K, Schmidt K, et al. The assembly-activating protein promotes capsid assembly of different adeno-associated virus serotypes. J Virol. 2011;85(23):12686-12697. doi:10.1128/JVI.05359-11) и МААР (вспомогательный белок связывания с мембраной Ogden PJ, Kelsic ED, Sinai S, Church GM. Comprehensive AAV capsid fitness landscape reveals a viral gene and enables machine-guided design. Science. 2019;3 66(6469): 1139-1143. doi: 10.1126/science.aaw2900). Фланкирующие последовательности генома AAV длиной в 145 нуклеотидов являются самокомплементарными и организованы таким образом, что может быть сформирован энергетически стабильный внутримолекулярный дуплекс, образующий Т-образную шпилечную структуру. Такие шпилечные структуры функционируют как точки начала репликации ДНК вируса, являясь праймерами для клеточного ДНК-полимеразного комплекса. После инфекции клеток млекопитающих AAV дикого типа (wtAAV) гены Rep (например, Rep78 и Rep52) экспрессируются с помощью Р5 промотора и Р19 промотора, соответственно, и оба белка Rep выполняют определенную функцию в репликации генома вируса. Сплайсинг в открытой рамке считывания Rep (Rep ORF) приводит к экспрессии фактически четырех белков Rep (например, Rep78, Rep68, Rep52 и Rep40). Однако было показано, что несплайсированная мРНК, кодирующая белки Rep78 и Rep52, является достаточной для продукции вектора AAV в клетках млекопитающих.
Вектор на основе рекомбинантного аденоассоциированного вируса (rAAV)
Термин «вектор» при использовании в настоящем документе означает молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она соединена. Кроме того, термин «вектор» в данном настоящем документе означает вирусную частицу, способную транспортировать нуклеиновую кислоту.
Как применяют в настоящем описании, термин «экспрессия» определяют как транскрипцию и/или трансляцию конкретной нуклеотидной последовательности, запускаемую ее промотором.
Применение
«Генная терапия» представляет собой вставку генов в клетки и/или ткани субъекта для лечения заболевания, обычно, наследственных заболеваний, при этом дефектный мутантный аллель заменяется или дополняется функциональным аллелем.
«Лечить», «лечение» и «терапия» относятся к методу смягчения или устранения биологического расстройства и/или по меньшей мере одного из сопутствующих ему симптомов. Кроме того, содержащиеся в данном документе ссылки на «лечение» включает ссылки на лечебную, паллиативную и профилактическую терапию.
В одном аспекте субъект лечения или пациент является млекопитающим, предпочтительно человеческим субъектом. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Термин «нарушение» означает любое состояние, которое можно улучшить в результате лечения по настоящему изобретению.
«Заболевание» является состоянием здоровья субъекта, где субъект не может поддерживать гомеостаз, и где, если заболевание не облегчают, то здоровье субъекта продолжает ухудшаться.
Термин «субъект», «пациент», «индивидуум» и т.п. используют в настоящем описании взаимозаменяемо, и они относятся к любому животному, которое поддается воздействию способами, представленными в настоящем описании. В конкретных неограничивающих вариантах осуществления субъект, пациент или индивидуум является человеком. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Подробное описание изобретения
Выделенной модифицированной белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9)
В одном из аспектов настоящее изобретение относится к выделенному модифицированному белку VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), который содержит аминокислотную последовательность белка VP1 капсида AAV9 дикого типа, кодируемую геном Сар, с одной или несколькими заменами, которые выбраны из группы:
F422W,
F422W и Y446F,
I601M,
где аминокислотная последовательность белка VP1 капсида AAV9 дикого типа имеет аминокислотную последовательность 
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замену в положении F422W.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность 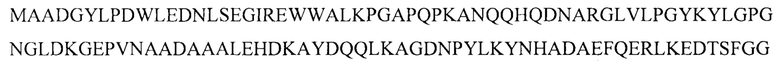

В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замены F422W и Y446F.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность 
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 включает замену I601М.
В некоторых вариантах осуществления изобретения выделенный модифицированный белок VP1 капсида AAV9 имеет аминокислотную последовательность 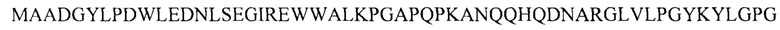

Выделенные модифицированные белки VP2 и VP3 капсида аденоассоциированного вируса 9 серотипа (ААV9)
«Правая часть» (+)-цепи геномной ДНК аденоассоциированного вируса содержит перекрывающиеся последовательности, кодирующие три белка капсида - VP1, VP2 и VP3. Транскрипция этих генов начинается с одного промотора, р40. Молекулярная масса соответствующих белков составляет 87, 72 и 62 кДа, соответственно. Все три белка транслируются с одной мРНК. После транскрипции пре-мРНК может подвергаться сплайсингу двумя разными способами, при этом вырезается более длинный или более короткий интрон и образуются мРНК длиной 2300 или 2600 нуклеотидов.
Таким образом, введение мутаций в ген Сар будет влиять не только на белок VP1 капсида AAV9, но и на VP2 и VP3 капсида AAV9.
На фигуре 7 приведено схематичное изображение положения структурных белков капсида AAV9 в последовательности гена Cap AAV:
1-737 ак-VP1,
138-737 ак-VP2,
203-737 ак-VP3.
С учетом перекрывающейся последовательности, кодирующей три белка капсида -VP1, VP2 и VP3, аминокислотная замена F422W в VP1 будет соответствовать:
аминокислотной замене в положении F285W в VP2;
аминокислотной замене в положении F220W в VP3.
С учетом перекрывающейся последовательности, кодирующей три белка капсида - VP1, VP2 и VP3, аминокислотная замена Y446F в VP1 будет соответствовать:
аминокислотной замене в положении Y309F в VP2;
аминокислотной замене в положении Y244F в VP3.
С учетом перекрывающейся последовательности, кодирующей три белка капсида -VP1, VP2 и VP3, аминокислотная замена I601М будет соответствовать:
аминокислотной замене в положении I464M в VP2;
аминокислотной замене в положении I399M в VP3.
Заявитель также считает целесообразным указать окружение найденных мутаций путем указания краткой аминокислотной последовательности, включающей данные мутации в VP 1/VP2/VP3:
Для F422W в VP 1 (F285W в VP2/ F220W в VP3) - NVPWHSS;
Для Y446F в VP1 (Y309F в VP2/ Y244F в VP3) - YLYFLSK;
Для I601M в VP1 (I464M в VP2/ I399M в VP3) - NQGMLPG.
В некоторых вариантах аминокислотная последовательность белка VP2 капсида AAV9 дикого типа имеет аминокислотную последовательность, представленную 
В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замену F285W.
В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замену F285W и имеет аминокислотную последовательность, представленную 

В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замены F285W и Y309F.
В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замены F285W и Y309F и имеет аминокислотную последовательность, представленную 
В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замену I464M.
В некоторых вариантах осуществления изобретения модифицированный белок VP2 капсида AAV9 содержит замену I464M и имеет аминокислотную последовательность, представленную 
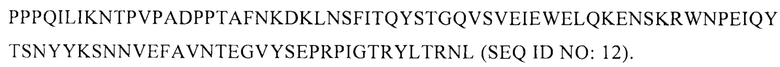
В некоторых вариантах осуществления изобретения белок VP3 капсида AAV9 дикого типа имеет аминокислотную последовательность, представленную 
В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замену F220W.
В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замену F220W и имеет аминокислотную последовательность, представленную 
В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замены F220W и Y244F.
В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замены F220W и Y244F и имеет аминокислотную последовательность, представленную 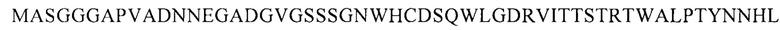

В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замену I399M.
В некоторых вариантах осуществления изобретения модифицированный белок VP3 капсида AAV9 содержит замену I399M и имеет аминокислотную последовательность, представленную 
Капсид
В одном из аспектов настоящее изобретение относится к выделенному капсиду для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), который включает любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), белок VP2 капсида AAV9 или его модифицированный вариант и белок VP3 капсида AAV9 или его модифицированный вариант.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP2 капсида AAV9 дикого типа.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP2 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 9.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 10.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 11.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 12.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP3 капсида AAV9 дикого типа.
В некоторых вариантах осуществления изобретения выделенный капсид включает белок VP3 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 17.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 18.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 19.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M.
В некоторых вариантах осуществления изобретения выделенный капсид включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 20.
Выделенная нуклеиновая кислота
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, которая кодирует любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), использующихся для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9).
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F422W и представлена нуклеиновой последовательностью с SEQ ID NO: 6 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F422W» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 6, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 2. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F422W и Y446F и представлена нуклеиновой последовательностью с SEQ ID NO: 7 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F422W и Y446F» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 7, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 3. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I601М и представлена нуклеиновой последовательностью с SEQ ID NO: 8 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I601М» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 8, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 4. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В одном из аспектов настоящее изобретение относится к выделенному капсиду для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), который включает любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, кодирующей вышеуказанный модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F285W и представлена нуклеиновой последовательностью с SEQ ID NO: 14 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F285W» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 14, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 10. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F285W и Y309F и представлена нуклеиновой последовательностью с SEQ ID NO: 15 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F285W и Y309F» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 15, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 11. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I464M и представлена нуклеиновой последовательностью с SEQ ID NO: 16 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP2 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I464М» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 16, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 12. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, кодирующей вышеуказанный модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9).
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F220W и представлена нуклеиновой последовательностью с SEQ ID NO: 22 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой F220W» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 22, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 18. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F220W и Y244F и представлена нуклеиновой последовательностью с SEQ ID NO: 23 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотными заменами F220W и Y244F» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 23, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 19. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В некоторых вариантах осуществления изобретения выделенная нуклеиновая кислота кодирует модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой I399M и представлена нуклеиновой последовательностью с SEQ ID NO: 24 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
Под «другой последовательностью, кодирующей соответствующую аминокислотную последовательность модифицированного белка VP3 капсида аденоассоциированного вируса 9 серотипа (AAV9) с аминокислотной заменой 1399М» подразумевается нуклеиновая последовательность, которая альтернативна нуклеиновой последовательности с SEQ ID NO: 24, так как с учетом вырожденности генетического кода широкий ряд различных ДНК-последовательностей может кодировать аминокислотную последовательность, раскрытую в данном документе как SEQ ID NO: 20. Специалистам в данной области хорошо известно получение таких альтернативных ДНК-последовательностей, кодирующих одни и те же аминокислотные последовательности. Такие вариантные ДНК-последовательности находятся в объеме настоящего изобретения.
В одном из аспектов настоящее изобретение относится к выделенной нуклеиновой кислоте, которая кодирует любой из вышеуказанных капсидов, использующихся для высокоэффективной продукции (сборки) инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9).
В некоторых вариантах выделенная нуклеиновая кислота, кодирующая вышеуказанный капсид, включает любую из вышеуказанных последовательностей нуклеиновых кислот.
Вектор на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9)
В одном из аспектов настоящее изобретение относится к вектору на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9) для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, который включает:
1) любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) или любой из вышеуказанных капсидов, и
2) гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках.
В одном из аспектов настоящее изобретение относится к вектору на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9) для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, который включает:
1) любой из вышеуказанных модифицированных белков VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), и
2) гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках.
В одном из аспектов настоящее изобретение относится к вектору на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9) для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, который включает:
1) любой из вышеуказанных капсидов, и
2) гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках.
Термины «вектор на основе рекомбинантного аденоассоциированного вируса 9 серотипа», «рекомбинантный вирус на основе AAV9», «вирусоподобная частица на основе AAV9», «рекомбинантный вирусный штамм AAV9», «рекомбинантный вектор AAV9» или «вектор на основе rAAV9» в контексте настоящего описания имеют одинаковое значение.
В некоторых вариантах осуществления изобретения rAAV9 включает гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, где продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой терапевтический полипептид или репортерный полипептид.
Вектор rAAV по изобретению не содержит нуклеотидные последовательности генов, кодирующих последовательности белков (Rep), необходимых для обеспечения жизненного цикла вируса, а также последовательности перекрывающихся белков капсида (Сар).
Характеристика капсида подробно описана в вышеуказанном разделе описания.
Под «регуляторными последовательностями, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках» подразумевается в рамках данного изобретения полинуклеотидные последовательности, которые необходимы для воздействия на экспрессию и процессинг кодирующих последовательностей, к которым они клонированы. Регулирующие экспрессию последовательности включают соответствующие последовательности инициации транскрипции, терминации, промотора и энхансера; эффективные сигналы процессинга РНК, такие как сплайсинг и сигналы полиаденилирования; последовательности, которые стабилизируют цитоплазматическую мРНК; последовательности, которые повышают эффективность трансляции (т.е. консенсусная последовательность Козака); последовательности, которые повышают стабильность белка; и, при желании, последовательности, которые усиливают секрецию белка. Характер таких регулирующих последовательностей различается в зависимости от организма-хозяина; в прокариотах такие контролирующие последовательности, как правило, включают промотор, сайт связывания рибосомы, а также последовательности терминации транскрипции; в эукариотах, как правило, такие контролирующие последовательности включают промоторы и последовательности терминации транскрипции. Термин «регуляторные последовательности» включает, как минимум, все компоненты, наличие которых имеет важное значение для экспрессии и процессинга, и может также включать дополнительные компоненты, чье присутствие является полезным, например, последовательности лидерных пептидов.
В контексте настоящего описания термин «промотор» относится к фрагменту нуклеиновой кислоты, который контролирует транскрипцию одной или нескольких кодирующих последовательностей, а также который структурно идентифицируется по наличию сайта связывания для ДНК-зависимой РНК-полимеразы, сайтов инициации транскрипции и других последовательностей ДНК, включающих, без ограничения, сайты связывания фактора транскрипции, сайты связывания репрессора и активатора белка, а также любые другие последовательности нуклеотидов, известные специалистам в данной области, которые непосредственно или опосредованно регулируют уровень транскрипции с данным промотором. «Конститутивный» промотор представляет собой такой промотор, который активен в большинстве тканей в обычных физиологических условиях и условиях развития. «Индуцибельный» промотор представляет собой промотор, который подвергается физиологической регуляции или регуляции в ходе развития, например, при воздействии химического индуктора. «Тканеспецифичный» промотор активен только в конкретных типах тканей или клеток.
Промоторы, которые используются для продукции высокого уровня полипептидов в эукариотических клетках и, в частности, в клетках млекопитающих, должны быть сильными и, предпочтительно, должны быть активными в широком диапазоне типов клеток. Сильные конститутивные промоторы, которые способны запускать экспрессию во многих типах клеток, хорошо известны в данной области и, поэтому, нет необходимости в их подробном описании в данном документе. В соответствии с идеей настоящего изобретения предпочтительно использовать промотор цитомегаловируса (CMV). Промотор или промотор/энхансер, полученные из немедленной ранней (IE) области цитомегаловируса (hCMV) человека, в особенности подходят в качестве промотора для вектора на основе rAAV9 по настоящему изобретению. Немедленная ранняя (IE) область цитомегаловируса (hCMV) человека и полученные из нее функциональные запускающие экспрессию фрагменты и/или функциональные усиливающие экспрессию фрагменты, например, описаны в ЕР0173177 и ЕР0323997, а также хорошо известны в данной области. Таким образом, несколько фрагментов немедленной ранней (IE) области hCMV могут использоваться в качестве промотора и/или промотора/энхансера.
Термины «энхансеры» или «энхансер», используемые в изобретении, могут относиться к последовательности ДНК, которая расположена как смежная с последовательностью ДНК, кодирующей рекомбинантный продукт. Энхансерные элементы обычно расположены в 5'-направлении от промоторного элемента или могут быть расположены ниже или в пределах кодирующей последовательности ДНК (например, последовательности ДНК, транскрибированной или транслированной в рекомбинантный продукт или продукты). Таким образом, энхансерный элемент может быть расположен на расстоянии 100 пар оснований, 200 пар оснований или 300 или больше пар оснований перед последовательностью ДНК, которая кодирует рекомбинантный продукт, или после этой последовательности. Энхансерные элементы могут увеличивать количество экспрессируемого рекомбинантного продукта от последовательности ДНК, превышая экспрессию, обусловленную одиночным промоторным элементом. Специалистам в данной области техники доступно множество энхансерных элементов.
В некоторых вариантах осуществления изобретения гетерологичная последовательность нуклеиновой кислоты, содержащая регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках может включать следующие элементы в направлении от 5'-конца к 3'-концу:
левый (первый) ITR (инвертированные концевые повторы);
CMV (цитомегаловирусный) энхансер;
CMV (цитомегаловирусный) промотер;
интрон гена hBG1 (ген субъединицы гемоглобина гамма-1);
нуклеиновая кислота, кодирующая продукт;
сигнал полиаденилирования hGH1 (сигнал полиаденилирования гена гормона роста человека);
правый (второй) ITR.
В некоторых вариантах реализации нуклеиновая кислота, кодирующая продукт (трансген) представляет собой по меньшей мере один ген, кодирующий белок. В некоторых вариантах реализации трансген кодирует по меньшей мере одну небольшую нуклеиновую кислоту-ингибитор. В некоторых вариантах реализации трансген кодирует по меньшей мере одну репортерную молекулу. В некоторых вариантах реализации малая ингибирующая нуклеиновая кислота представляет собой miRNA. В некоторых вариантах реализации малая ингибирующая нуклеиновая кислота представляет собой sponge miRNA или TuD-RNA, которая ингибирует активность по меньшей мере одной miRNA у животного. В некоторых вариантах реализации miRNA экспрессируется в клетке ткани-мишени. В некоторых вариантах реализации ткань-мишень представляет собой ткань печени, центральной нервной системы (ЦНС), глаз, желудочно-кишечного тракта, дыхательных путей, молочной железы, поджелудочной железы, мочевыводящих путей или ткани матки.
В некоторых вариантах вектор на основе rAAV9 имеет продукт экспрессии гетерологичной последовательности нуклеиновой кислоты, который представляет собой терапевтический полипептид или репортерный полипептид.
В некоторых вариантах вектор на основе rAAV9 содержит гетерологичную последовательность нуклеиновой кислоты, кодирующей продукт, который представляет собой терапевтический полипептид, где терапевтический полипептид представляет собой фактор свертывания крови, выбираемый из группы, состоящей из фактора VIII, фактора IX или их функционального варианта.
В некоторых вариантах вектор на основе rAAV9 содержит гетерологичную последовательность нуклеиновой кислоты, кодирующей продукт, который представляет собой фактор VIII или его функциональный вариант.
В некоторых вариантах вектор на основе rAAV9 содержит гетерологичную последовательность нуклеиновой кислоты, кодирующей продукт, который представляет собой фактор IX или его функциональный вариант.
В некоторых вариантах вектор на основе rAAV9 содержит гетерологичную последовательность нуклеиновой кислоты, кодирующей продукт, который представляет собой белок SMN1 (белок выживаемости моторных (двигательных) нейронов)
В некоторых вариантах вектор на основе rAAV9 содержит гетерологичную последовательность нуклеиновой кислоты, кодирующей продукт, который представляет собой полипептид RBD-S (рекомбинантный рецептор-связывающий домен гликопротеина S) вируса SARS-cov2 (коронавирус 2 типа, вызывающий тяжелый острый респираторный синдром).
Фармацевтическая композиция
В одном из аспектов настоящее изобретение относится к фармацевтической композиции для доставки генного продукта нуждающемуся в этом субъекту, которая содержит:
a) любой из вышеуказанных векторов на основе rAAV9; и
b) фармацевтически приемлемый эксципиент.
В некоторых вариантах фармацевтическая композиция используется для доставки генного продукта нуждающемуся в этом человеку.
В конкретных вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей вирусную частицу на основе rAAV9 по изобретению в фармацевтически приемлемом носителе или в других лекарственных соединениях, фармацевтические агенты, носители, адъюванты, разбавители и т.д. Носитель для инъекций обычно является жидким. Носитель для других способов введения может быть или твердым, или жидким, таким как стерильная апирогенная вода или стерильный апирогенный фосфатно-солевой буферный раствор. Для введения путем ингаляции носитель является вдыхаемым и предпочтительно находится в твердой или жидкой дисперсной форме. В качестве инъекционной среды предпочтительно использовать воду, содержащую добавки, общепринятые для инъекционных растворов, такие как стабилизирующие агенты, соли или солевые растворы и/или буферы.
В других вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей клетку, в которой вектор на основе rAAV9 интегрирован в геном, в фармацевтически приемлемом носителе или других лекарственных соединениях, фармацевтических агентах, носителях, адъювантах, разбавителях и т.д.
«Фармацевтическая композиция» обозначает композицию, включающую в себя вышеуказанный вектор на основе rAAV9, согласно изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых эксципиентов, таких как наполнители, растворители, разбавители, носители, вспомогательные, распределяющие, средства доставки, консерванты, стабилизаторы, эмульгаторы, суспендирующие агенты, загустители, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Фармацевтические композиции по настоящему изобретению и способы их изготовления будут бесспорно очевидными для специалистов в этой области. Производство фармацевтических композиций предпочтительно должно соответствовать требованиям GMP (надлежащей производственной практики). Композиция может включать буферную композицию, тонические агенты, стабилизаторы и солюбилизаторы.
«Фармацевтически приемлемым» считается материал, который не имеет биологических или других противопоказаний, например, материал можно вводить субъекту без каких-либо нежелательных биологических эффектов. Таким образом, такие фармацевтические композиции можно использовать, например, для трансфекции клетки ех vivo или для введения in vivo вирусной частицы или клетки непосредственно субъекту.
Термин «эксципиент» или «вспомогательное вещество» используется в данном документе для описания любого компонента, отличающегося от ранее описанных по данному изобретению. Это вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств.
Под «стабилизатором» понимается вспомогательное вещество или смесь двух и более вспомогательных веществ, которые обеспечивают физическую и/или химическую стабильность активного агента.
Под термином «буфер», «буферная композиция», «буферный агент» понимается раствор, способный сохранять значение рН, благодаря взаимодействию кислотных и щелочных компонентов, входящих в его состав, который дает возможность препарату вектора на основе rAAV9, проявлять устойчивость к изменениям рН. В общем случае, преимущественными являются значения рН фармацевтической композиции от 4,0 до 8,0. В качестве буферных агентов могут быть использованы, например, ацетатный, фосфатный, цитратный, гистидиновый, сукцинатный и т.п. буферные растворы, но, не ограничиваясь ими.
Фармацевтическая композиция является «стабильной», если активный агент сохраняет свою физическую стабильность и/или химическую стабильность и/или биологическую активность в течение заявленного срока годности при температуре хранения, например, при 2-8°С. Предпочтительно, чтобы активный агент сохранял и физическую, и химическую стабильность, а также биологическую активность. Период хранения выбирается на основании результатов исследования стабильности при ускоренном и естественном хранении.
Фармацевтическая композиция по данному изобретению может изготавливаться, упаковываться или широко продаваться в виде единичной стандартной дозы или множества единичных стандартных доз в виде готовой лекарственной формы. Используемый в данном документе термин «единичная стандартная доза» означает дискретное количество фармацевтической композиции, содержащей заранее определенное количество активного ингредиента. Количество активного ингредиента обычно равно дозировке активного ингредиента, который будет вводиться субъекту, или удобной части такой дозировки, например, половине или трети такой дозировки.
Способ доставки генного продукта
В одном из аспектов настоящее изобретение относится к способу доставки генного продукта нуждающемуся в этом субъекту, который включает введение субъекту любого из вышеуказанных векторов на основе rAAV9 или вышеуказанной фармацевтической композиции.
Под субъектом подразумевают любой живой организм, который поддается воздействию способами, представленными в настоящем описании. В конкретных неограничивающих вариантах осуществления субъект является человеком. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Любой способ введения вектора на основе rAAV9, принятый в данной области, может соответствующим образом использоваться для вышеуказанного вектора на основе rAAV9, по данному изобретению.
Примеры способов введения включают в себя местное применение, интраназальное, ингаляционное, чрезслизистое, трансдермальное, энтеральное (например, пероральное, ректальное), парентеральное (например, внутривенное, подкожное, внутрикожное, внутримышечное) введения, а также инъекции непосредственно в ткань или в орган.
Инъекционные препараты могут быть приготовлены в общепринятых лекарственных формах: в виде жидких растворов или суспензий, твердых форм, подходящих для приготовления растворов или суспензий в жидкости перед инъекцией, или в виде эмульсий. Альтернативно, можно вводить вышеуказанный рекомбинантный вирус на основе AAV9 по данному изобретению локально, а не системно, например, в виде депо или в композиции с замедленным высвобождением.
Рекомбинантный вирус на основе AAV9 вводят в организм в эффективном количестве. Рекомбинантный вирус на основе AAV9 предпочтительно вводят в организм в биологически эффективном количестве. «Биологически эффективное» количество рекомбинантного вируса представляет собой количество, которое достаточно, чтобы вызвать инфекцию (или трансдукцию) и экспрессию последовательности нуклеиновой кислоты в клетке. Если вирус вводят в клетку in vivo (например, вирус вводят субъекту, как описано ниже), «биологически эффективное» количество вирусного вектора представляет собой количество, которое достаточно, чтобы вызвать трансдукцию и экспрессию последовательности нуклеиновой кислоты в клетке-мишени.
Клетка для введения вышеуказанного рекомбинантного вируса на основе AAV9 по изобретению может быть клеткой любого типа, включая в себя без ограничения, моторные нейроны или прочие ткани нервной системы, эпителиальные клетки (например, эпителиальные клетки кожи, дыхательных путей и кишечника), печеночные клетки, мышечные клетки, клетки селезенки, фибробласты, эндотелиальные клетки и тому подобное.
Вышеуказанный рекомбинантный вирус на основе AAV9 по изобретению не используется для модификации генетической целостности клеток зародышевой линии человека.
Применение
В одном из аспектов настоящее изобретение относится к применению любого из вышеуказанных векторов на основе rAAV9 или вышеуказанной фармацевтической композиции для лечения заболевания у нуждающегося в этом субъекта.
В некоторых вариантах осуществления применения заболевание выбирают из группы: заболевания крови, заболевания центральной нервной системы, заболевания метаболизма, заболевания мышц, наследственные заболевания.
Под субъектом подразумевают любое животное, которое поддается воздействию способами, представленными в настоящем описании. В конкретных неограничивающих вариантах осуществления субъект является человеком. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Введение вектора на основе rAAV9 по настоящему изобретению субъекту-человеку или животному, нуждающемуся в этом, можно проводить любым известным в данной области способом для введения вирусных векторов.
Примеры способов введения включают в себя местное применение, интраназальное, ингаляционное, чрезслизистое, трансдермальное, энтеральное (например, пероральное, ректальное), парентеральное (например, внутривенное, подкожное, внутрикожное, внутримышечное) введения, а также инъекции непосредственно в ткань или в орган.
Инъекционные препараты могут быть приготовлены в общепринятых лекарственных формах: в виде жидких растворов или суспензий, твердых форм, подходящих для приготовления растворов или суспензий в жидкости перед инъекцией, или в виде эмульсий. Альтернативно, можно вводить вышеуказанный рекомбинантный вирус на основе AAV9 по данному изобретению локально, а не системно, например, в виде депо или в композиции с замедленным высвобождением.
В некоторых вариантах применения заболевание выбирают из группы: заболевания крови; заболевания центральной нервной системы; заболевания метаболизма; заболевания мышц; наследственные заболевания.
В некоторых вариантах применения заболевание представляет собой заболевание крови.
В некоторых вариантах применения заболевание представляет собой заболевание мышц.
В некоторых вариантах применения заболевание представляет собой наследственное заболевание.
В некоторых вариантах осуществления применения продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой фактор IX или его функциональный вариант.
В некоторых вариантах осуществления применения продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой фактор VIII или его функциональный вариант.
В некоторых вариантах осуществления применения продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой белок SMN1 (белок выживаемости моторных (двигательных) нейронов)
В некоторых вариантах осуществления применения продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой полипептид RBD-S (рекомбинантный рецептор-связывающий домен гликопротеина S) вируса SARS-cov2 (коронавирус 2 типа, вызывающий тяжелый острый респираторный синдром).
В некоторых вариантах осуществления применения любой из вышеуказанных векторов на основе rAAV9 или вышеуказанной фармацевтической композиции используются в терапевтически эффективном количестве.
Под «терапевтически эффективным количеством» подразумевается количество, которое достаточно для облегчения (например, для смягчения, уменьшения, снижения) по меньшей мере одного из симптомов, связанных с патологическим состоянием. Другими словами, «терапевтически эффективное» количество представляет собой количество, которое достаточно для обеспечения некоторого улучшения состояния субъекта.
Дозировки вышеуказанного рекомбинантного вируса на основе AAV9 по данному изобретению будут зависеть от способа введения, конкретного вирусного вектора и их можно определять рутинными способами. Примерными дозами для достижения терапевтического эффекта являются вирусные титры, составляющие по меньшей мере примерно 105, 106, 107, 108, 109, 1010, 10-11, 1012, 1013, 1014, 1015, 1016 трансдуцирующих единиц или больше, предпочтительно приблизительно от 109 до 1015 трансдуцирующих единиц, еще более предпочтительно 1014 трансдуцирующих единиц на килограмм.
Таким образом, рекомбинантный вирус на основе AAV9, реагенты и способы по настоящему изобретению можно использовать для направления нуклеиновой кислоты в делящиеся или неделящиеся клетки и для стабильной экспрессии в этих клетках гетерологичной нуклеиновой кислоты. С использованием этой векторной системы стало возможно вводить в клетки в условиях in vivo гены, которые кодируют белки, влияющие на физиологию клеток. Таким образом, векторы по настоящему изобретению могут быть полезными в генной терапии при патологических состояниях.
Настоящее изобретение можно использовать для доставки любой чужеродной нуклеиновой кислоты с биологическим эффектом для лечения или ослабления симптомов, связанных с каким-либо расстройством, обусловленным генной экспрессией. Примеры патологических состояний включают в себя без ограничения кистозный фиброз (и другие заболевания легких), гемофилию А, гемофилию В, талассемию, анемии и другие нарушения свертываемости крови, СПИД, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, боковой амиотрофический склероз, эпилепсию и другие неврологические расстройства, сахарный диабет, мышечные дистрофии (например, Дюшенна, Беккера, спинальная мышечная атрофия (SMA)), болезнь Гоше, болезнь Херлера, дефицит аденозиндеаминазы, болезни накопления гликогена и другие метаболические дефекты, заболевания солидных органов (например, мозга, печени, почек, сердца) и тому подобное.
Перенос генов обладает значительным потенциалом применения для понимания и создания способов лечения патологических состояний. Существует ряд наследственных заболеваний, для которых были изучены и клонированы дефектные гены. В некоторых случаях известна функция этих клонированных генов. В целом, упомянутые выше патологические состояния делятся на два класса: дефицитные состояния, как правило, дефицит ферментов, которые обычно наследуются рецессивным образом, и состояния нарушения баланса, иногда с вовлечением по меньшей мере регуляторных или структурных белков, которые наследуются доминантным образом. При дефицитных заболеваниях можно использовать перенос генов, чтобы внести нормальный ген в пораженные ткани для заместительной терапии. При патологических состояниях нарушения баланса перенос генов можно использовать для создания патологического состояния в смоделированной системе, которую затем можно использовать для разработки мер против этого патологического состояния. Таким образом, способы по настоящему изобретению позволяют лечить генетические заболевания. Согласно изобретению, патологическое состояние лечится путем частичного или полного устранения дефекта или дисбаланса, который вызывает заболевание или усугубляет степень его тяжести. Также возможно использование сайт-специфичной интеграции нуклеиновых последовательностей для запуска мутаций или исправления дефектов.
Способ получения вектора на основе rAAV9
В одном из аспектов настоящее изобретение относится к способу получения любого из вышеуказанных векторов на основе rAAV9, который включает трансфекцию клеток-продуцентов, соответственно, любой из вышеуказанных нуклеиновых кислот, которые содержат последовательность, кодирующую модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), или вышеуказанной нуклеиновой кислотой, кодирующей капсид.
Белки капсида могут быть экспрессированы из рекомбинантного вируса, вектора экспрессии или из линии клеток, в которую стабильно интегрированы гены описанных модифицированных капсидов AAV или кодирующие последовательности. Кроме того, изобретение обеспечивает получение капсидов AAV с описанными мутациями in vitro из белков капсидов AAV и конструирование упакованных капсидов in vitro. Изобретение также обеспечивает получение модифицированных капсидов AAV, которые были генетически сконструированы для экспрессии гетерологичных эпитопов клинически важных антигенов, чтобы вызвать иммунный ответ.
Способ получения вектора на основе rAAV9 подробно описан в примерах.
Трансгенное животное
Согласно некоторым аспектам раскрытия предоставляется способ создания модели соматических трансгенных животных. В некоторых вариантах реализации способ включает введение любого из вышеупомянутых rAAV не являющемуся человеком животному, где rAAV содержит по меньшей мере один трансген, и где rAAV инфицирует клетки ткани-мишени животного, не являющегося человеком.
В некоторых вариантах возможно использование описанных вариантов капсидов для создания модели соматических трансгенных животных, которые включают введение любого из вышеупомянутых rAAV не относящемуся к человеку животному, где rAAV содержит по меньшей мере один трансген. В некоторых вариантах реализации трансген представляет собой по меньшей мере один ген, кодирующий белок. В некоторых вариантах реализации трансген кодирует по меньшей мере одну небольшую нуклеиновую кислоту-ингибитор. В некоторых вариантах реализации трансген кодирует по меньшей мере одну репортерную молекулу.
Соматической трансгенной животной моделью может быть млекопитающее, такое как мышь, крыса, кролик, собака, кошка, овца, свинья, примат, не являющийся человеком.
В некоторых вариантах реализации предполагаемый терапевтический агент можно вводить модели соматического трансгенного животного для определения эффекта предполагаемого терапевтического агента на патологическое состояние животного.
Примеры
Для наилучшего понимания изобретения приводятся следующие примеры. Эти примеры приведены только в иллюстративных целях и не должны толковаться как ограничивающие сферу применения изобретения в любой форме.
Все публикации, патенты и патентные заявки, указанные в этой спецификации включены в данный документ путем отсылки. Хотя вышеупомянутое изобретение было довольно подробно описано путем иллюстрации и примера в целях исключения двусмысленного толкования, специалистам в данной области на основе идей, раскрытых в данном изобретении, будет вполне понятно, что могут быть внесены определенные изменения и модификации без отклонения от сущности и объема прилагаемых вариантов осуществления изобретения.
Материалы и общие методы
Методы рекомбинантной ДНК
Для манипуляций с ДНК использовали стандартные методы, описанные у Sambrook J. и др., Molecular cloning: A laboratory manual; Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 2012. Реагенты для молекулярной биологии использовали согласно инструкциям производителей.
Синтез генов
Требуемые сегменты генов получали из олигонуклеотидов, созданных путем химического синтеза. Генные сегменты длиной от 300 до 4000 п. н., которые фланкированы уникальными сайтами рестрикции, собирали путем отжига и лигирования олигонуклеотидов, включая ПЦР-амплификацию и последующее клонирование через указанные сайты рестрикции. Последовательности ДНК субклонированных генных фрагментов подтверждали путем секвенирования ДНК.
Определение последовательностей ДНК
Последовательности ДНК определяли путем секвенирования по Сенгеру.
Анализ последовательностей ДНК и белков и обработка данных о последовательностях
Применяли пакет программ SnapGene версии 5.1.4.1 для создания, картирования, анализа, аннотирования и иллюстрации последовательностей.
Статистический анализ данных
Результаты представлены в виде среднего значения±стандартное отклонение (SD), для сравнения результатов теста и контроля использовали дисперсионный анализ (ANOVA), и они были определены как статистически значимые.
Пример 1. Получение библиотек вариантов капсидов rAAV9
Получение библиотек вариантов капсидов rAAV9 производили методом случайного мутагенеза последовательности гена Cap (Davidsson М. et al., 2016). Вкратце, последовательность дикого типа гена Сар девятого серотипа (GenBank ID AY530579.1) была собрана de novo, после чего синтезированную нуклеотидную последовательность капсида AAV9 дикого типа фрагментировали с использованием урацил-ДНК-гликозилазы, полученные фрагменты собирали в полноразмерный ген Сар с помощью ДНК-полимеразы, не обладающей корректирующей активностью (в результате в последовательности возникали случайные мутации). Полноразмерные мутантные варианты клонировали в плазмиду-носитель pAAV-linker (Фиг. 1.) по сайтам рестрикции AscI/EcoRI в общую рамку считывания с зеленым флуоресцентным белком (GFP), продуцируя многообразную случайную библиотеку капсидов rAAV9, которую затем использовали для отбора вариантов капсидов с повышенной эффективностью сборки и/или трансдуцирующей активностью.
Положительный отбор вирусных частиц с повышенной эффективностью сборки проводили in vitro на клетках линии U-87 MG. При этом для трансдукции использовали частицы, очищенные с помощью УЦФ в градиенте йодиксанола. Спустя 48 часов клетки собирали и выделяли геномную ДНК для последующей амплификации последовательностей геномов вирусов, способных к эффективной трансдукции. Полученные последовательности затем переклонировали и повторно нарабатывали для последующих итераций отбора с целью обогащения библиотеки вариантами с наибольшей эффективностью сборки. После 5 раундов отбора гены капсидов 100 клонов просеквенировали для определения наиболее успешных мутаций и их сочетаний. По результатам секвенирования преобладающими сочетаниями мутаций оказались Y446F и F422W в VP1 AAV9- порядка 10% клонов, атак же клоны содержащие единичные мутации F422W или I601М в VP1 AAV9. Данные варианты капсидов клонировали в вектор для наработки вирусных частиц и в дальнейшем использовали для визуализации и сравнения профилей эффективности наработки rAAV частиц и трансдукции относительно AAV9 дикого типа.
Пример 2. Наработка и последующий отбор рекомбинантных вирусных частиц из полученной библиотеки последовательностей
Для наработки и последующего отбора рекомбинантных вирусных частиц из полученной библиотеки последовательностей была разработана серия плазмид: плазмида-носитель, плазмида, содержащая последовательность гена Rep, а также конструкция, содержащая аденовирусные гены, необходимые для репликации вирусных частиц.
Плазмида-носитель pAAV-linker (Фиг. 1), предназначенная для клонирования библиотек случайных вариантов гена капсида AAV девятого серотипа в одну рамку считывания с репортерным белком, была получена путем замены последовательности модифицированного зеленого флуоресцентного белка в исходной конструкции pAAV-GFP (Фиг. 2), с помощью рестриктазно-лигазного метода клонирования по сайтам HindIII/EcoRI, на последовательность T2A-GFP, синтезированную de novo с добавлением сайтов рестрикции EcoRI с 5'-конца и HindIII с 3'-конца.
Плазмида pAAV-Rep, содержащая последовательность гена Rep (Фиг. 3), полученную путем клонирования de novo синтезированной последовательности гена Rep AAV второго серотипа (GenBank ID AF043303.1) с добавлением сайта рестрикции Pcil на 5' конец и сайта рестикции Psil на 3' конце, в плазмиду pGem-T Easy так же обработанную рестриктазами PciI/PsiI.
В качестве источника аденовирусных генов для наработки рекомбинантных вирусных частиц была использована конструкция pHelper (Фиг. 4), содержащая AmpR - ген бета-лактамазы, обеспечивающий устойчивость к ампициллину, Ori- ориджин репликации в бактериях, Adeno Е2А - последовательность гена хелперного аденовируса, участвующая в репликации вирусной ДНК, Adeno Е4 - последовательность гена хелперного аденовируса, участвующая в репликации вирусной ДНК, Adeno VARNA - последовательность гена хелперного аденовируса отвечающая за стимуляцию трансляции как ранних, так и поздних вирусных генов.
Пример 3. Эффективность наработки векторов на основе модифицированного аденоассоциированного вируса 9 серотипа (rAAV9)
Для получения частиц rAAV с модифицированным капсидом 9 серотипа, клетки-продуценты НЕК293 трансфецировали с использованием полиэтиленимина одновременно 3 плазмидами:
1) Плазмидой, содержащей нуклеотидные последовательности аденовируса, кодирующие белки и РНК, необходимые для сборки частиц rAAV (хелперная плазмида);
2) Плазмидой, содержащей нуклеотидную природную последовательность гена Rep аденоассоциированного вируса, а также последовательность модифицированного гена Сар, которую выбирают из группы: нуклеотидная последовательность SEQ ID NO: 6, 7 или 8 или любая другая нуклеотидная последовательность, кодирующая белок VP1 с аминокислотными последовательностями SEQ ID No: 2, 3 или 4, и белки VP2 и VP3 с альтернативных рамок считывания используемой нуклеотидной последовательности, где
VP2 может иметь любую из аминокислотных последовательностей SEQ ID No: 9, 10, 11 или 12;
a VP3 может иметь любую из аминокислотных последовательностей SEQ ID No: 17, 18, 19 или 20;
3) Плазмидой, содержащей гетерологичный геном частицы rAAV, кодирующий целевой ген, предназначенный для доставки в клетки пациента.
Данный набор генов обеспечивает сборку вирусных частиц rAAV и инкапсидирование в них целевого генома в течение 72 часов. Через 72 часа после трансфекции клетки-продуценты подвергали лизису с высвобождением частиц rAAV, полученные вектора обрабатывали ДНКазой I в течение 2 часов при 37°С, затем еще 2 часа протеиназой К при 56°С. Титр полученных частиц rAAV определяли с помощью количественной ПЦР с использованием сета олигонуклеотидов состоящего из прямого праймера 5'- ACCACATGAAGCAGCACGAC -3', обратного праймера 5'-TCAGCTCGATGCGGTTCAC -3', и зонда 5'- HEX-CATGCCCGAAGGCTACGTCCAG-BHQ1 -3' специфичного к последовательности GFP.
Авторами изобретения было неожиданно установлено, что наличие единичной замены, выбранной из группы, включающей: F422W или I601М, или одновременное наличие мутаций Y446F и F422W в белке VP1 капсида AAV9 дикого типа, приводило к существенному увеличению выхода инкапсидированных вирусных частиц на основе rAAV9 с указанными выше мутациями. К примеру, при помощи метода количественной ПЦР удалось выявить изменение количества копий упакованного гетерологичного генома частицы rAAV, кодирующего целевой ген GFP (Фиг. 5).
При наличии мутации F422W (AAV9-01Mut-GFP) количество упакованных вирусных геномов, увеличивалось в 1,71 раза с 1,82Е+09 вг/мл до 3,12Е+09 вг/мл по сравнению с контрольным AAV9 с белком VP1 капсида дикого типа (AAV9-NullMut-GFP).
При наличии мутации I601М (AAV9-02Mut-GFP) количество упакованных вирусных геномов, увеличивалось в 2,1 раза с 1,82Е+09 вг/мл до 3,76Е+09 вг/мл по сравнению с контрольным AAV9 с белком VP1 капсида дикого типа (AAV9-NullMut-GFP).
При одновременном наличии мутаций Y446F и F422W (AAV9-03Mut-GFP) количество упакованных вирусных геномов, увеличивалось в 1,88 раза 1,82Е+09 вг/мл до 3,42Е+09 вг/мл по сравнению с контрольным AAV9 с белком VP 1 капсида дикого типа (AAV9-NullMut-GFP).
Пример 4. Оценка эффективности трансдукции клеток препаратами на основе rAAV9, которые содержат точечные мутации в белке VP1 капсида AAV9 дикого типа.
В лунки 24-луночных планшетов были посеяны клетки линии U-87 MG. Посев проводили в ростовую среду: ЕМЕМ с глутамином, 10% сыворотки крупного рогатого скота. Плотность посадки клеток составила 10 000 клеток/см2. При постановке трансдукции подготовленные заранее клетки были трансдуцированы при MOI 400000 вг/клетка. Все образцы были поставлены в трипликатах. Для негативного контроля были использованы интактные клетки.
Анализ эффективности трансдукции проводили по интенсивности сигнала репортерного белка GFP с помощью проточного цитометра Guava EasyCyte и программного обеспечения GuavaSoft.
Авторами изобретения было установлено, что наличие единичной мутации F422W или I601M, а также единовременное наличие мутаций Y446F и F422W, в белке VP1 капсида AAV9 дикого типа, не приводило к существенному снижению эффективности доставки трансгена векторами на основе rAAV с указанными выше мутациями. К примеру, при помощи метода проточной цитометрии удалось выявить изменение количества GFP позитивных клеток спустя 48 часов после трансдукции линии U-87 MG препаратами на основе rAAV с белком VP1 капсида AAV9 дикого типа или белком VP1 капсида AAV9 дикого типа, содержащим единичную мутацию F422W или I601М, а также варианты капсида одновременно содержащие мутации Y446F и F422W, в белке VP1 капсида AAV9 дикого типа (Фиг. 6).
При использовании контрольного препарата rAAV9 с белком VP1 капсида дикого типа (AAV9-NullMut-GFP) количество клеток, экспрессировавших GFP, составляло 95,58%.
При наличии мутации F422W (AAV9-01Mut-GFP) количество клеток, экспрессировавших GFP, составляло 96,15%.
При наличии мутации I601M (AAV9-02Mut-GFP) количество клеток, экспрессировавших GFP, составляло 93,75%.
При одновременном наличии мутации Y446F и F422W (AAV9-03Mut-GFP)
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ООО "АНАБИОН"
<120> Выделенный модифицированный белок VP1 капсида аденоассоциированного
вируса 9 серотипа (AAV9), капсид и вектор на его основе
<160> 24
<170> BiSSAP 1.3.6
<210> 1
<211> 736
<212> PRT
<213> Природная последовательность
<220>
<223> Природная последовательность белка VP1 капсида AAV9 дикого типа
(AAV9 CAP WT VP1)
<400> 1
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Gln Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Gln Ser Pro Gln Glu Pro Asp Ser Ser Ala Gly Ile Gly
145 150 155 160
Lys Ser Gly Ala Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Thr Glu Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Val Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Asp Asn Asn Gly Val Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Val Gln Val Phe Thr Asp Ser Asp Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Glu Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asp
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Glu
405 410 415
Phe Glu Asn Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser
435 440 445
Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln Gln Thr Leu Lys Phe Ser
450 455 460
Val Ala Gly Pro Ser Asn Met Ala Val Gln Gly Arg Asn Tyr Ile Pro
465 470 475 480
Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser Thr Thr Val Thr Gln Asn
485 490 495
Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala Ser Ser Trp Ala Leu Asn
500 505 510
Gly Arg Asn Ser Leu Met Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser Gly Ser Leu Ile Phe Gly
530 535 540
Lys Gln Gly Thr Gly Arg Asp Asn Val Asp Ala Asp Lys Val Met Ile
545 550 555 560
Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr Glu Ser
565 570 575
Tyr Gly Gln Val Ala Thr Asn His Gln Ser Ala Gln Ala Gln Ala Gln
580 585 590
Thr Gly Trp Val Gln Asn Gln Gly Ile Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Met
625 630 635 640
Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys Leu Asn Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala Val Asn Thr Glu Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 2
<211> 736
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP1 капсида AAV9, который
включает одну замену в положении F422W (AAV9 CAP F422W VP1)
<400> 2
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Gln Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Gln Ser Pro Gln Glu Pro Asp Ser Ser Ala Gly Ile Gly
145 150 155 160
Lys Ser Gly Ala Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Thr Glu Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Val Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Asp Asn Asn Gly Val Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Val Gln Val Phe Thr Asp Ser Asp Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Glu Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asp
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Glu
405 410 415
Phe Glu Asn Val Pro Trp His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser
435 440 445
Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln Gln Thr Leu Lys Phe Ser
450 455 460
Val Ala Gly Pro Ser Asn Met Ala Val Gln Gly Arg Asn Tyr Ile Pro
465 470 475 480
Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser Thr Thr Val Thr Gln Asn
485 490 495
Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala Ser Ser Trp Ala Leu Asn
500 505 510
Gly Arg Asn Ser Leu Met Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser Gly Ser Leu Ile Phe Gly
530 535 540
Lys Gln Gly Thr Gly Arg Asp Asn Val Asp Ala Asp Lys Val Met Ile
545 550 555 560
Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr Glu Ser
565 570 575
Tyr Gly Gln Val Ala Thr Asn His Gln Ser Ala Gln Ala Gln Ala Gln
580 585 590
Thr Gly Trp Val Gln Asn Gln Gly Ile Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Met
625 630 635 640
Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys Leu Asn Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala Val Asn Thr Glu Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 3
<211> 736
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP1 капсида AAV9, который
включает замены в положениях F422W и Y446F (AAV9 CAP F422W Y446F
VP1)
<400> 3
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Gln Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Gln Ser Pro Gln Glu Pro Asp Ser Ser Ala Gly Ile Gly
145 150 155 160
Lys Ser Gly Ala Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Thr Glu Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Val Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Asp Asn Asn Gly Val Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Val Gln Val Phe Thr Asp Ser Asp Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Glu Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asp
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Glu
405 410 415
Phe Glu Asn Val Pro Trp His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Phe Leu Ser
435 440 445
Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln Gln Thr Leu Lys Phe Ser
450 455 460
Val Ala Gly Pro Ser Asn Met Ala Val Gln Gly Arg Asn Tyr Ile Pro
465 470 475 480
Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser Thr Thr Val Thr Gln Asn
485 490 495
Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala Ser Ser Trp Ala Leu Asn
500 505 510
Gly Arg Asn Ser Leu Met Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser Gly Ser Leu Ile Phe Gly
530 535 540
Lys Gln Gly Thr Gly Arg Asp Asn Val Asp Ala Asp Lys Val Met Ile
545 550 555 560
Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr Glu Ser
565 570 575
Tyr Gly Gln Val Ala Thr Asn His Gln Ser Ala Gln Ala Gln Ala Gln
580 585 590
Thr Gly Trp Val Gln Asn Gln Gly Ile Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Met
625 630 635 640
Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys Leu Asn Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala Val Asn Thr Glu Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 4
<211> 736
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP1 капсида AAV9, который
включает одну замену в положении I601M (AAV9 CAP I601M VP1)
<400> 4
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Gln Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Gln Ser Pro Gln Glu Pro Asp Ser Ser Ala Gly Ile Gly
145 150 155 160
Lys Ser Gly Ala Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Thr Glu Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Val Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Asp Asn Asn Gly Val Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Val Gln Val Phe Thr Asp Ser Asp Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Glu Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asp
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Glu
405 410 415
Phe Glu Asn Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser
435 440 445
Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln Gln Thr Leu Lys Phe Ser
450 455 460
Val Ala Gly Pro Ser Asn Met Ala Val Gln Gly Arg Asn Tyr Ile Pro
465 470 475 480
Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser Thr Thr Val Thr Gln Asn
485 490 495
Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala Ser Ser Trp Ala Leu Asn
500 505 510
Gly Arg Asn Ser Leu Met Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser Gly Ser Leu Ile Phe Gly
530 535 540
Lys Gln Gly Thr Gly Arg Asp Asn Val Asp Ala Asp Lys Val Met Ile
545 550 555 560
Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr Glu Ser
565 570 575
Tyr Gly Gln Val Ala Thr Asn His Gln Ser Ala Gln Ala Gln Ala Gln
580 585 590
Thr Gly Trp Val Gln Asn Gln Gly Met Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Met
625 630 635 640
Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys Leu Asn Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala Val Asn Thr Glu Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 5
<211> 2211
<212> DNA
<213> Природная последовательность
<220>
<223> нуклеиновая кислота, кодирующая природную последовательность
белка VP1 капсида AAV9 дикого типа (AAV9 CAP WT VP1)
<400> 5
atggctgccg atggttatct tccagattgg ctcgaggaca accttagtga aggaattcgc 60
gagtggtggg ctttgaaacc tggagcccct caacccaagg caaatcaaca acatcaagac 120
aacgctcgag gtcttgtgct tccgggttac aaataccttg gacccggcaa cggactcgac 180
aagggggagc cggtcaacgc agcagacgcg gcggccctcg agcacgacaa ggcctacgac 240
cagcagctca aggccggaga caacccgtac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga gcagtctcct caggaaccgg actcctccgc gggtattggc 480
aaatcgggtg cacagcccgc taaaaagaga ctcaatttcg gtcagactgg cgacacagag 540
tcagtcccag accctcaacc aatcggagaa cctcccgcag ccccctcagg tgtgggatct 600
cttacaatgg cttcaggtgg tggcgcacca gtggcagaca ataacgaagg tgccgatgga 660
gtgggtagtt cctcgggaaa ttggcattgc gattcccaat ggctggggga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca atcacctcta caagcaaatc 780
tccaacagca catctggagg atcttcaaat gacaacgcct acttcggcta cagcaccccc 840
tgggggtatt ttgacttcaa cagattccac tgccacttct caccacgtga ctggcagcga 900
ctcatcaaca acaactgggg attccggcct aagcgactca acttcaagct cttcaacatt 960
caggtcaaag aggttacgga caacaatgga gtcaagacca tcgccaataa ccttaccagc 1020
acggtccagg tcttcacgga ctcagactat cagctcccgt acgtgctcgg gtcggctcac 1080
gagggctgcc tcccgccgtt cccagcggac gttttcatga ttcctcagta cgggtatctg 1140
acgcttaatg atggaagcca ggccgtgggt cgttcgtcct tttactgcct ggaatatttc 1200
ccgtcgcaaa tgctaagaac gggtaacaac ttccagttca gctacgagtt tgagaacgta 1260
cctttccata gcagctacgc tcacagccaa agcctggacc gactaatgaa tccactcatc 1320
gaccaatact tgtactatct ctcaaagact attaacggtt ctggacagaa tcaacaaacg 1380
ctaaaattca gtgtggccgg acccagcaac atggctgtcc agggaagaaa ctacatacct 1440
ggacccagct accgacaaca acgtgtctca accactgtga ctcaaaacaa caacagcgaa 1500
tttgcttggc ctggagcttc ttcttgggct ctcaatggac gtaatagctt gatgaatcct 1560
ggacctgcta tggccagcca caaagaagga gaggaccgtt tctttccttt gtctggatct 1620
ttaatttttg gcaaacaagg aactggaaga gacaacgtgg atgcggacaa agtcatgata 1680
accaacgaag aagaaattaa aactactaac ccggtagcaa cggagtccta tggacaagtg 1740
gccacaaacc accagagtgc ccaagcacag gcgcagaccg gctgggttca aaaccaagga 1800
atacttccgg gtatggtttg gcaggacaga gatgtgtacc tgcaaggacc catttgggcc 1860
aaaattcctc acacggacgg caactttcac ccttctccgc tgatgggagg gtttggaatg 1920
aagcacccgc ctcctcagat cctcatcaaa aacacacctg tacctgcgga tcctccaacg 1980
gccttcaaca aggacaagct gaactctttc atcacccagt attctactgg ccaagtcagc 2040
gtggagatcg agtgggagct gcagaaggaa aacagcaagc gctggaaccc ggagatccag 2100
tacacttcca actattacaa gtctaataat gttgaatttg ctgttaatac tgaaggtgta 2160
tatagtgaac cccgccccat tggcaccaga tacctgactc gtaatctgta a 2211
<210> 6
<211> 2211
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP1
капсида AAV9, который включает одну замену в положении F422W
(AAV9 CAP F422W VP1)
<400> 6
atggctgccg atggttatct tccagattgg ctcgaggaca accttagtga aggaattcgc 60
gagtggtggg ctttgaaacc tggagcccct caacccaagg caaatcaaca acatcaagac 120
aacgctcgag gtcttgtgct tccgggttac aaataccttg gacccggcaa cggactcgac 180
aagggggagc cggtcaacgc agcagacgcg gcggccctcg agcacgacaa ggcctacgac 240
cagcagctca aggccggaga caacccgtac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga gcagtctcct caggaaccgg actcctccgc gggtattggc 480
aaatcgggtg cacagcccgc taaaaagaga ctcaatttcg gtcagactgg cgacacagag 540
tcagtcccag accctcaacc aatcggagaa cctcccgcag ccccctcagg tgtgggatct 600
cttacaatgg cttcaggtgg tggcgcacca gtggcagaca ataacgaagg tgccgatgga 660
gtgggtagtt cctcgggaaa ttggcattgc gattcccaat ggctggggga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca atcacctcta caagcaaatc 780
tccaacagca catctggagg atcttcaaat gacaacgcct acttcggcta cagcaccccc 840
tgggggtatt ttgacttcaa cagattccac tgccacttct caccacgtga ctggcagcga 900
ctcatcaaca acaactgggg attccggcct aagcgactca acttcaagct cttcaacatt 960
caggtcaaag aggttacgga caacaatgga gtcaagacca tcgccaataa ccttaccagc 1020
acggtccagg tcttcacgga ctcagactat cagctcccgt acgtgctcgg gtcggctcac 1080
gagggctgcc tcccgccgtt cccagcggac gttttcatga ttcctcagta cgggtatctg 1140
acgcttaatg atggaagcca ggccgtgggt cgttcgtcct tttactgcct ggaatatttc 1200
ccgtcgcaaa tgctaagaac gggtaacaac ttccagttca gctacgagtt tgagaacgta 1260
ccttggcata gcagctacgc tcacagccaa agcctggacc gactaatgaa tccactcatc 1320
gaccaatact tgtactatct ctcaaagact attaacggtt ctggacagaa tcaacaaacg 1380
ctaaaattca gtgtggccgg acccagcaac atggctgtcc agggaagaaa ctacatacct 1440
ggacccagct accgacaaca acgtgtctca accactgtga ctcaaaacaa caacagcgaa 1500
tttgcttggc ctggagcttc ttcttgggct ctcaatggac gtaatagctt gatgaatcct 1560
ggacctgcta tggccagcca caaagaagga gaggaccgtt tctttccttt gtctggatct 1620
ttaatttttg gcaaacaagg aactggaaga gacaacgtgg atgcggacaa agtcatgata 1680
accaacgaag aagaaattaa aactactaac ccggtagcaa cggagtccta tggacaagtg 1740
gccacaaacc accagagtgc ccaagcacag gcgcagaccg gctgggttca aaaccaagga 1800
atacttccgg gtatggtttg gcaggacaga gatgtgtacc tgcaaggacc catttgggcc 1860
aaaattcctc acacggacgg caactttcac ccttctccgc tgatgggagg gtttggaatg 1920
aagcacccgc ctcctcagat cctcatcaaa aacacacctg tacctgcgga tcctccaacg 1980
gccttcaaca aggacaagct gaactctttc atcacccagt attctactgg ccaagtcagc 2040
gtggagatcg agtgggagct gcagaaggaa aacagcaagc gctggaaccc ggagatccag 2100
tacacttcca actattacaa gtctaataat gttgaatttg ctgttaatac tgaaggtgta 2160
tatagtgaac cccgccccat tggcaccaga tacctgactc gtaatctgta a 2211
<210> 7
<211> 2211
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP1
капсида AAV9, который включает замены в положениях F422W и Y446F
(AAV9 CAP F422W Y446F VP1)
<400> 7
atggctgccg atggttatct tccagattgg ctcgaggaca accttagtga aggaattcgc 60
gagtggtggg ctttgaaacc tggagcccct caacccaagg caaatcaaca acatcaagac 120
aacgctcgag gtcttgtgct tccgggttac aaataccttg gacccggcaa cggactcgac 180
aagggggagc cggtcaacgc agcagacgcg gcggccctcg agcacgacaa ggcctacgac 240
cagcagctca aggccggaga caacccgtac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga gcagtctcct caggaaccgg actcctccgc gggtattggc 480
aaatcgggtg cacagcccgc taaaaagaga ctcaatttcg gtcagactgg cgacacagag 540
tcagtcccag accctcaacc aatcggagaa cctcccgcag ccccctcagg tgtgggatct 600
cttacaatgg cttcaggtgg tggcgcacca gtggcagaca ataacgaagg tgccgatgga 660
gtgggtagtt cctcgggaaa ttggcattgc gattcccaat ggctggggga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca atcacctcta caagcaaatc 780
tccaacagca catctggagg atcttcaaat gacaacgcct acttcggcta cagcaccccc 840
tgggggtatt ttgacttcaa cagattccac tgccacttct caccacgtga ctggcagcga 900
ctcatcaaca acaactgggg attccggcct aagcgactca acttcaagct cttcaacatt 960
caggtcaaag aggttacgga caacaatgga gtcaagacca tcgccaataa ccttaccagc 1020
acggtccagg tcttcacgga ctcagactat cagctcccgt acgtgctcgg gtcggctcac 1080
gagggctgcc tcccgccgtt cccagcggac gttttcatga ttcctcagta cgggtatctg 1140
acgcttaatg atggaagcca ggccgtgggt cgttcgtcct tttactgcct ggaatatttc 1200
ccgtcgcaaa tgctaagaac gggtaacaac ttccagttca gctacgagtt tgagaacgta 1260
ccttggcata gcagctacgc tcacagccaa agcctggacc gactaatgaa tccactcatc 1320
gaccaatact tgtactttct ctcaaagact attaacggtt ctggacagaa tcaacaaacg 1380
ctaaaattca gtgtggccgg acccagcaac atggctgtcc agggaagaaa ctacatacct 1440
ggacccagct accgacaaca acgtgtctca accactgtga ctcaaaacaa caacagcgaa 1500
tttgcttggc ctggagcttc ttcttgggct ctcaatggac gtaatagctt gatgaatcct 1560
ggacctgcta tggccagcca caaagaagga gaggaccgtt tctttccttt gtctggatct 1620
ttaatttttg gcaaacaagg aactggaaga gacaacgtgg atgcggacaa agtcatgata 1680
accaacgaag aagaaattaa aactactaac ccggtagcaa cggagtccta tggacaagtg 1740
gccacaaacc accagagtgc ccaagcacag gcgcagaccg gctgggttca aaaccaagga 1800
atacttccgg gtatggtttg gcaggacaga gatgtgtacc tgcaaggacc catttgggcc 1860
aaaattcctc acacggacgg caactttcac ccttctccgc tgatgggagg gtttggaatg 1920
aagcacccgc ctcctcagat cctcatcaaa aacacacctg tacctgcgga tcctccaacg 1980
gccttcaaca aggacaagct gaactctttc atcacccagt attctactgg ccaagtcagc 2040
gtggagatcg agtgggagct gcagaaggaa aacagcaagc gctggaaccc ggagatccag 2100
tacacttcca actattacaa gtctaataat gttgaatttg ctgttaatac tgaaggtgta 2160
tatagtgaac cccgccccat tggcaccaga tacctgactc gtaatctgta a 2211
<210> 8
<211> 2211
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP1
капсида AAV9, который включает одну замену в положении I601M
(AAV9 CAP I601M VP1)
<400> 8
atggctgccg atggttatct tccagattgg ctcgaggaca accttagtga aggaattcgc 60
gagtggtggg ctttgaaacc tggagcccct caacccaagg caaatcaaca acatcaagac 120
aacgctcgag gtcttgtgct tccgggttac aaataccttg gacccggcaa cggactcgac 180
aagggggagc cggtcaacgc agcagacgcg gcggccctcg agcacgacaa ggcctacgac 240
cagcagctca aggccggaga caacccgtac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga gcagtctcct caggaaccgg actcctccgc gggtattggc 480
aaatcgggtg cacagcccgc taaaaagaga ctcaatttcg gtcagactgg cgacacagag 540
tcagtcccag accctcaacc aatcggagaa cctcccgcag ccccctcagg tgtgggatct 600
cttacaatgg cttcaggtgg tggcgcacca gtggcagaca ataacgaagg tgccgatgga 660
gtgggtagtt cctcgggaaa ttggcattgc gattcccaat ggctggggga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca atcacctcta caagcaaatc 780
tccaacagca catctggagg atcttcaaat gacaacgcct acttcggcta cagcaccccc 840
tgggggtatt ttgacttcaa cagattccac tgccacttct caccacgtga ctggcagcga 900
ctcatcaaca acaactgggg attccggcct aagcgactca acttcaagct cttcaacatt 960
caggtcaaag aggttacgga caacaatgga gtcaagacca tcgccaataa ccttaccagc 1020
acggtccagg tcttcacgga ctcagactat cagctcccgt acgtgctcgg gtcggctcac 1080
gagggctgcc tcccgccgtt cccagcggac gttttcatga ttcctcagta cgggtatctg 1140
acgcttaatg atggaagcca ggccgtgggt cgttcgtcct tttactgcct ggaatatttc 1200
ccgtcgcaaa tgctaagaac gggtaacaac ttccagttca gctacgagtt tgagaacgta 1260
cctttccata gcagctacgc tcacagccaa agcctggacc gactaatgaa tccactcatc 1320
gaccaatact tgtactatct ctcaaagact attaacggtt ctggacagaa tcaacaaacg 1380
ctaaaattca gtgtggccgg acccagcaac atggctgtcc agggaagaaa ctacatacct 1440
ggacccagct accgacaaca acgtgtctca accactgtga ctcaaaacaa caacagcgaa 1500
tttgcttggc ctggagcttc ttcttgggct ctcaatggac gtaatagctt gatgaatcct 1560
ggacctgcta tggccagcca caaagaagga gaggaccgtt tctttccttt gtctggatct 1620
ttaatttttg gcaaacaagg aactggaaga gacaacgtgg atgcggacaa agtcatgata 1680
accaacgaag aagaaattaa aactactaac ccggtagcaa cggagtccta tggacaagtg 1740
gccacaaacc accagagtgc ccaagcacag gcgcagaccg gctgggttca aaaccaagga 1800
atgcttccgg gtatggtttg gcaggacaga gatgtgtacc tgcaaggacc catttgggcc 1860
aaaattcctc acacggacgg caactttcac ccttctccgc tgatgggagg gtttggaatg 1920
aagcacccgc ctcctcagat cctcatcaaa aacacacctg tacctgcgga tcctccaacg 1980
gccttcaaca aggacaagct gaactctttc atcacccagt attctactgg ccaagtcagc 2040
gtggagatcg agtgggagct gcagaaggaa aacagcaagc gctggaaccc ggagatccag 2100
tacacttcca actattacaa gtctaataat gttgaatttg ctgttaatac tgaaggtgta 2160
tatagtgaac cccgccccat tggcaccaga tacctgactc gtaatctgta a 2211
<210> 9
<211> 599
<212> PRT
<213> Природная последовательность
<220>
<223> Природная последовательность белка VP2 капсида AAV9 дикого типа
(AAV9 CAP WT VP2)
<400> 9
Thr Ala Pro Gly Lys Lys Arg Pro Val Glu Gln Ser Pro Gln Glu Pro
1 5 10 15
Asp Ser Ser Ala Gly Ile Gly Lys Ser Gly Ala Gln Pro Ala Lys Lys
20 25 30
Arg Leu Asn Phe Gly Gln Thr Gly Asp Thr Glu Ser Val Pro Asp Pro
35 40 45
Gln Pro Ile Gly Glu Pro Pro Ala Ala Pro Ser Gly Val Gly Ser Leu
50 55 60
Thr Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly
65 70 75 80
Ala Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln
85 90 95
Trp Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu
100 105 110
Pro Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser
115 120 125
Gly Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp
130 135 140
Gly Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp
145 150 155 160
Trp Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu
165 170 175
Asn Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn
180 185 190
Gly Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe
195 200 205
Thr Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu
210 215 220
Gly Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr
225 230 235 240
Gly Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser
245 250 255
Phe Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn
260 265 270
Asn Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Phe His Ser Ser
275 280 285
Tyr Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp
290 295 300
Gln Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn
305 310 315 320
Gln Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val
325 330 335
Gln Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val
340 345 350
Ser Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly
355 360 365
Ala Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly
370 375 380
Pro Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu
385 390 395 400
Ser Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val
405 410 415
Asp Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr
420 425 430
Asn Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln
435 440 445
Ser Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile
450 455 460
Leu Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro
465 470 475 480
Ile Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro
485 490 495
Leu Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile
500 505 510
Lys Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp
515 520 525
Lys Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val
530 535 540
Glu Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro
545 550 555 560
Glu Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe
565 570 575
Ala Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr
580 585 590
Arg Tyr Leu Thr Arg Asn Leu
595
<210> 10
<211> 599
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP2 капсида AAV9, который
включает одну замену в положении F285W (AAV9 CAP F285W VP2)
<400> 10
Thr Ala Pro Gly Lys Lys Arg Pro Val Glu Gln Ser Pro Gln Glu Pro
1 5 10 15
Asp Ser Ser Ala Gly Ile Gly Lys Ser Gly Ala Gln Pro Ala Lys Lys
20 25 30
Arg Leu Asn Phe Gly Gln Thr Gly Asp Thr Glu Ser Val Pro Asp Pro
35 40 45
Gln Pro Ile Gly Glu Pro Pro Ala Ala Pro Ser Gly Val Gly Ser Leu
50 55 60
Thr Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly
65 70 75 80
Ala Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln
85 90 95
Trp Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu
100 105 110
Pro Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser
115 120 125
Gly Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp
130 135 140
Gly Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp
145 150 155 160
Trp Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu
165 170 175
Asn Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn
180 185 190
Gly Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe
195 200 205
Thr Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu
210 215 220
Gly Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr
225 230 235 240
Gly Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser
245 250 255
Phe Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn
260 265 270
Asn Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Trp His Ser Ser
275 280 285
Tyr Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp
290 295 300
Gln Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn
305 310 315 320
Gln Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val
325 330 335
Gln Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val
340 345 350
Ser Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly
355 360 365
Ala Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly
370 375 380
Pro Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu
385 390 395 400
Ser Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val
405 410 415
Asp Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr
420 425 430
Asn Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln
435 440 445
Ser Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile
450 455 460
Leu Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro
465 470 475 480
Ile Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro
485 490 495
Leu Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile
500 505 510
Lys Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp
515 520 525
Lys Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val
530 535 540
Glu Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro
545 550 555 560
Glu Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe
565 570 575
Ala Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr
580 585 590
Arg Tyr Leu Thr Arg Asn Leu
595
<210> 11
<211> 599
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP2 капсида AAV9, который
включает замены в положениях F285W и Y309F (AAV9 CAP F285W Y309F
VP2)
<400> 11
Thr Ala Pro Gly Lys Lys Arg Pro Val Glu Gln Ser Pro Gln Glu Pro
1 5 10 15
Asp Ser Ser Ala Gly Ile Gly Lys Ser Gly Ala Gln Pro Ala Lys Lys
20 25 30
Arg Leu Asn Phe Gly Gln Thr Gly Asp Thr Glu Ser Val Pro Asp Pro
35 40 45
Gln Pro Ile Gly Glu Pro Pro Ala Ala Pro Ser Gly Val Gly Ser Leu
50 55 60
Thr Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly
65 70 75 80
Ala Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln
85 90 95
Trp Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu
100 105 110
Pro Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser
115 120 125
Gly Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp
130 135 140
Gly Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp
145 150 155 160
Trp Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu
165 170 175
Asn Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn
180 185 190
Gly Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe
195 200 205
Thr Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu
210 215 220
Gly Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr
225 230 235 240
Gly Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser
245 250 255
Phe Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn
260 265 270
Asn Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Trp His Ser Ser
275 280 285
Tyr Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp
290 295 300
Gln Tyr Leu Tyr Phe Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn
305 310 315 320
Gln Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val
325 330 335
Gln Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val
340 345 350
Ser Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly
355 360 365
Ala Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly
370 375 380
Pro Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu
385 390 395 400
Ser Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val
405 410 415
Asp Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr
420 425 430
Asn Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln
435 440 445
Ser Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile
450 455 460
Leu Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro
465 470 475 480
Ile Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro
485 490 495
Leu Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile
500 505 510
Lys Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp
515 520 525
Lys Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val
530 535 540
Glu Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro
545 550 555 560
Glu Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe
565 570 575
Ala Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr
580 585 590
Arg Tyr Leu Thr Arg Asn Leu
595
<210> 12
<211> 599
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP2 капсида AAV9, который
включает одну замену в положении I464M (AAV9 CAP I464M VP2)
<400> 12
Thr Ala Pro Gly Lys Lys Arg Pro Val Glu Gln Ser Pro Gln Glu Pro
1 5 10 15
Asp Ser Ser Ala Gly Ile Gly Lys Ser Gly Ala Gln Pro Ala Lys Lys
20 25 30
Arg Leu Asn Phe Gly Gln Thr Gly Asp Thr Glu Ser Val Pro Asp Pro
35 40 45
Gln Pro Ile Gly Glu Pro Pro Ala Ala Pro Ser Gly Val Gly Ser Leu
50 55 60
Thr Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly
65 70 75 80
Ala Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln
85 90 95
Trp Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu
100 105 110
Pro Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser
115 120 125
Gly Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp
130 135 140
Gly Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp
145 150 155 160
Trp Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu
165 170 175
Asn Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn
180 185 190
Gly Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe
195 200 205
Thr Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu
210 215 220
Gly Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr
225 230 235 240
Gly Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser
245 250 255
Phe Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn
260 265 270
Asn Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Phe His Ser Ser
275 280 285
Tyr Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp
290 295 300
Gln Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn
305 310 315 320
Gln Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val
325 330 335
Gln Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val
340 345 350
Ser Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly
355 360 365
Ala Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly
370 375 380
Pro Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu
385 390 395 400
Ser Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val
405 410 415
Asp Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr
420 425 430
Asn Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln
435 440 445
Ser Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Met
450 455 460
Leu Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro
465 470 475 480
Ile Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro
485 490 495
Leu Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile
500 505 510
Lys Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp
515 520 525
Lys Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val
530 535 540
Glu Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro
545 550 555 560
Glu Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe
565 570 575
Ala Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr
580 585 590
Arg Tyr Leu Thr Arg Asn Leu
595
<210> 13
<211> 1800
<212> DNA
<213> Природная последовательность
<220>
<223> нуклеиновая кислота, кодирующая природную последовательность
белка VP2 капсида AAV9 дикого типа (AAV9 CAP WT VP2)
<400> 13
acggctcctg gaaagaagag gcctgtagag cagtctcctc aggaaccgga ctcctccgcg 60
ggtattggca aatcgggtgc acagcccgct aaaaagagac tcaatttcgg tcagactggc 120
gacacagagt cagtcccaga ccctcaacca atcggagaac ctcccgcagc cccctcaggt 180
gtgggatctc ttacaatggc ttcaggtggt ggcgcaccag tggcagacaa taacgaaggt 240
gccgatggag tgggtagttc ctcgggaaat tggcattgcg attcccaatg gctgggggac 300
agagtcatca ccaccagcac ccgaacctgg gccctgccca cctacaacaa tcacctctac 360
aagcaaatct ccaacagcac atctggagga tcttcaaatg acaacgccta cttcggctac 420
agcaccccct gggggtattt tgacttcaac agattccact gccacttctc accacgtgac 480
tggcagcgac tcatcaacaa caactgggga ttccggccta agcgactcaa cttcaagctc 540
ttcaacattc aggtcaaaga ggttacggac aacaatggag tcaagaccat cgccaataac 600
cttaccagca cggtccaggt cttcacggac tcagactatc agctcccgta cgtgctcggg 660
tcggctcacg agggctgcct cccgccgttc ccagcggacg ttttcatgat tcctcagtac 720
gggtatctga cgcttaatga tggaagccag gccgtgggtc gttcgtcctt ttactgcctg 780
gaatatttcc cgtcgcaaat gctaagaacg ggtaacaact tccagttcag ctacgagttt 840
gagaacgtac ctttccatag cagctacgct cacagccaaa gcctggaccg actaatgaat 900
ccactcatcg accaatactt gtactatctc tcaaagacta ttaacggttc tggacagaat 960
caacaaacgc taaaattcag tgtggccgga cccagcaaca tggctgtcca gggaagaaac 1020
tacatacctg gacccagcta ccgacaacaa cgtgtctcaa ccactgtgac tcaaaacaac 1080
aacagcgaat ttgcttggcc tggagcttct tcttgggctc tcaatggacg taatagcttg 1140
atgaatcctg gacctgctat ggccagccac aaagaaggag aggaccgttt ctttcctttg 1200
tctggatctt taatttttgg caaacaagga actggaagag acaacgtgga tgcggacaaa 1260
gtcatgataa ccaacgaaga agaaattaaa actactaacc cggtagcaac ggagtcctat 1320
ggacaagtgg ccacaaacca ccagagtgcc caagcacagg cgcagaccgg ctgggttcaa 1380
aaccaaggaa tacttccggg tatggtttgg caggacagag atgtgtacct gcaaggaccc 1440
atttgggcca aaattcctca cacggacggc aactttcacc cttctccgct gatgggaggg 1500
tttggaatga agcacccgcc tcctcagatc ctcatcaaaa acacacctgt acctgcggat 1560
cctccaacgg ccttcaacaa ggacaagctg aactctttca tcacccagta ttctactggc 1620
caagtcagcg tggagatcga gtgggagctg cagaaggaaa acagcaagcg ctggaacccg 1680
gagatccagt acacttccaa ctattacaag tctaataatg ttgaatttgc tgttaatact 1740
gaaggtgtat atagtgaacc ccgccccatt ggcaccagat acctgactcg taatctgtaa 1800
<210> 14
<211> 1800
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP2
капсида AAV9, который включает одну замену в положении F285W
(AAV9 CAP F285W VP2)
<400> 14
acggctcctg gaaagaagag gcctgtagag cagtctcctc aggaaccgga ctcctccgcg 60
ggtattggca aatcgggtgc acagcccgct aaaaagagac tcaatttcgg tcagactggc 120
gacacagagt cagtcccaga ccctcaacca atcggagaac ctcccgcagc cccctcaggt 180
gtgggatctc ttacaatggc ttcaggtggt ggcgcaccag tggcagacaa taacgaaggt 240
gccgatggag tgggtagttc ctcgggaaat tggcattgcg attcccaatg gctgggggac 300
agagtcatca ccaccagcac ccgaacctgg gccctgccca cctacaacaa tcacctctac 360
aagcaaatct ccaacagcac atctggagga tcttcaaatg acaacgccta cttcggctac 420
agcaccccct gggggtattt tgacttcaac agattccact gccacttctc accacgtgac 480
tggcagcgac tcatcaacaa caactgggga ttccggccta agcgactcaa cttcaagctc 540
ttcaacattc aggtcaaaga ggttacggac aacaatggag tcaagaccat cgccaataac 600
cttaccagca cggtccaggt cttcacggac tcagactatc agctcccgta cgtgctcggg 660
tcggctcacg agggctgcct cccgccgttc ccagcggacg ttttcatgat tcctcagtac 720
gggtatctga cgcttaatga tggaagccag gccgtgggtc gttcgtcctt ttactgcctg 780
gaatatttcc cgtcgcaaat gctaagaacg ggtaacaact tccagttcag ctacgagttt 840
gagaacgtac cttggcatag cagctacgct cacagccaaa gcctggaccg actaatgaat 900
ccactcatcg accaatactt gtactatctc tcaaagacta ttaacggttc tggacagaat 960
caacaaacgc taaaattcag tgtggccgga cccagcaaca tggctgtcca gggaagaaac 1020
tacatacctg gacccagcta ccgacaacaa cgtgtctcaa ccactgtgac tcaaaacaac 1080
aacagcgaat ttgcttggcc tggagcttct tcttgggctc tcaatggacg taatagcttg 1140
atgaatcctg gacctgctat ggccagccac aaagaaggag aggaccgttt ctttcctttg 1200
tctggatctt taatttttgg caaacaagga actggaagag acaacgtgga tgcggacaaa 1260
gtcatgataa ccaacgaaga agaaattaaa actactaacc cggtagcaac ggagtcctat 1320
ggacaagtgg ccacaaacca ccagagtgcc caagcacagg cgcagaccgg ctgggttcaa 1380
aaccaaggaa tacttccggg tatggtttgg caggacagag atgtgtacct gcaaggaccc 1440
atttgggcca aaattcctca cacggacggc aactttcacc cttctccgct gatgggaggg 1500
tttggaatga agcacccgcc tcctcagatc ctcatcaaaa acacacctgt acctgcggat 1560
cctccaacgg ccttcaacaa ggacaagctg aactctttca tcacccagta ttctactggc 1620
caagtcagcg tggagatcga gtgggagctg cagaaggaaa acagcaagcg ctggaacccg 1680
gagatccagt acacttccaa ctattacaag tctaataatg ttgaatttgc tgttaatact 1740
gaaggtgtat atagtgaacc ccgccccatt ggcaccagat acctgactcg taatctgtaa 1800
<210> 15
<211> 1800
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP2
капсида AAV9, который включает замены в положениях F285W и Y309F
(AAV9 CAP F285W Y309F VP2)
<400> 15
acggctcctg gaaagaagag gcctgtagag cagtctcctc aggaaccgga ctcctccgcg 60
ggtattggca aatcgggtgc acagcccgct aaaaagagac tcaatttcgg tcagactggc 120
gacacagagt cagtcccaga ccctcaacca atcggagaac ctcccgcagc cccctcaggt 180
gtgggatctc ttacaatggc ttcaggtggt ggcgcaccag tggcagacaa taacgaaggt 240
gccgatggag tgggtagttc ctcgggaaat tggcattgcg attcccaatg gctgggggac 300
agagtcatca ccaccagcac ccgaacctgg gccctgccca cctacaacaa tcacctctac 360
aagcaaatct ccaacagcac atctggagga tcttcaaatg acaacgccta cttcggctac 420
agcaccccct gggggtattt tgacttcaac agattccact gccacttctc accacgtgac 480
tggcagcgac tcatcaacaa caactgggga ttccggccta agcgactcaa cttcaagctc 540
ttcaacattc aggtcaaaga ggttacggac aacaatggag tcaagaccat cgccaataac 600
cttaccagca cggtccaggt cttcacggac tcagactatc agctcccgta cgtgctcggg 660
tcggctcacg agggctgcct cccgccgttc ccagcggacg ttttcatgat tcctcagtac 720
gggtatctga cgcttaatga tggaagccag gccgtgggtc gttcgtcctt ttactgcctg 780
gaatatttcc cgtcgcaaat gctaagaacg ggtaacaact tccagttcag ctacgagttt 840
gagaacgtac cttggcatag cagctacgct cacagccaaa gcctggaccg actaatgaat 900
ccactcatcg accaatactt gtactttctc tcaaagacta ttaacggttc tggacagaat 960
caacaaacgc taaaattcag tgtggccgga cccagcaaca tggctgtcca gggaagaaac 1020
tacatacctg gacccagcta ccgacaacaa cgtgtctcaa ccactgtgac tcaaaacaac 1080
aacagcgaat ttgcttggcc tggagcttct tcttgggctc tcaatggacg taatagcttg 1140
atgaatcctg gacctgctat ggccagccac aaagaaggag aggaccgttt ctttcctttg 1200
tctggatctt taatttttgg caaacaagga actggaagag acaacgtgga tgcggacaaa 1260
gtcatgataa ccaacgaaga agaaattaaa actactaacc cggtagcaac ggagtcctat 1320
ggacaagtgg ccacaaacca ccagagtgcc caagcacagg cgcagaccgg ctgggttcaa 1380
aaccaaggaa tacttccggg tatggtttgg caggacagag atgtgtacct gcaaggaccc 1440
atttgggcca aaattcctca cacggacggc aactttcacc cttctccgct gatgggaggg 1500
tttggaatga agcacccgcc tcctcagatc ctcatcaaaa acacacctgt acctgcggat 1560
cctccaacgg ccttcaacaa ggacaagctg aactctttca tcacccagta ttctactggc 1620
caagtcagcg tggagatcga gtgggagctg cagaaggaaa acagcaagcg ctggaacccg 1680
gagatccagt acacttccaa ctattacaag tctaataatg ttgaatttgc tgttaatact 1740
gaaggtgtat atagtgaacc ccgccccatt ggcaccagat acctgactcg taatctgtaa 1800
<210> 16
<211> 1800
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP2
капсида AAV9, который включает одну замену в положении I464M
(AAV9 CAP I464M VP2)
<400> 16
acggctcctg gaaagaagag gcctgtagag cagtctcctc aggaaccgga ctcctccgcg 60
ggtattggca aatcgggtgc acagcccgct aaaaagagac tcaatttcgg tcagactggc 120
gacacagagt cagtcccaga ccctcaacca atcggagaac ctcccgcagc cccctcaggt 180
gtgggatctc ttacaatggc ttcaggtggt ggcgcaccag tggcagacaa taacgaaggt 240
gccgatggag tgggtagttc ctcgggaaat tggcattgcg attcccaatg gctgggggac 300
agagtcatca ccaccagcac ccgaacctgg gccctgccca cctacaacaa tcacctctac 360
aagcaaatct ccaacagcac atctggagga tcttcaaatg acaacgccta cttcggctac 420
agcaccccct gggggtattt tgacttcaac agattccact gccacttctc accacgtgac 480
tggcagcgac tcatcaacaa caactgggga ttccggccta agcgactcaa cttcaagctc 540
ttcaacattc aggtcaaaga ggttacggac aacaatggag tcaagaccat cgccaataac 600
cttaccagca cggtccaggt cttcacggac tcagactatc agctcccgta cgtgctcggg 660
tcggctcacg agggctgcct cccgccgttc ccagcggacg ttttcatgat tcctcagtac 720
gggtatctga cgcttaatga tggaagccag gccgtgggtc gttcgtcctt ttactgcctg 780
gaatatttcc cgtcgcaaat gctaagaacg ggtaacaact tccagttcag ctacgagttt 840
gagaacgtac ctttccatag cagctacgct cacagccaaa gcctggaccg actaatgaat 900
ccactcatcg accaatactt gtactatctc tcaaagacta ttaacggttc tggacagaat 960
caacaaacgc taaaattcag tgtggccgga cccagcaaca tggctgtcca gggaagaaac 1020
tacatacctg gacccagcta ccgacaacaa cgtgtctcaa ccactgtgac tcaaaacaac 1080
aacagcgaat ttgcttggcc tggagcttct tcttgggctc tcaatggacg taatagcttg 1140
atgaatcctg gacctgctat ggccagccac aaagaaggag aggaccgttt ctttcctttg 1200
tctggatctt taatttttgg caaacaagga actggaagag acaacgtgga tgcggacaaa 1260
gtcatgataa ccaacgaaga agaaattaaa actactaacc cggtagcaac ggagtcctat 1320
ggacaagtgg ccacaaacca ccagagtgcc caagcacagg cgcagaccgg ctgggttcaa 1380
aaccaaggaa tgcttccggg tatggtttgg caggacagag atgtgtacct gcaaggaccc 1440
atttgggcca aaattcctca cacggacggc aactttcacc cttctccgct gatgggaggg 1500
tttggaatga agcacccgcc tcctcagatc ctcatcaaaa acacacctgt acctgcggat 1560
cctccaacgg ccttcaacaa ggacaagctg aactctttca tcacccagta ttctactggc 1620
caagtcagcg tggagatcga gtgggagctg cagaaggaaa acagcaagcg ctggaacccg 1680
gagatccagt acacttccaa ctattacaag tctaataatg ttgaatttgc tgttaatact 1740
gaaggtgtat atagtgaacc ccgccccatt ggcaccagat acctgactcg taatctgtaa 1800
<210> 17
<211> 534
<212> PRT
<213> Природная последовательность
<220>
<223> Природная последовательность белка VP3 капсида AAV9 дикого типа
(AAV9 CAP WT VP3)
<400> 17
Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly Ala
1 5 10 15
Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln Trp
20 25 30
Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro
35 40 45
Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly
50 55 60
Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly
65 70 75 80
Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp Trp
85 90 95
Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn
100 105 110
Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn Gly
115 120 125
Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe Thr
130 135 140
Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu Gly
145 150 155 160
Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr Gly
165 170 175
Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser Phe
180 185 190
Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn Asn
195 200 205
Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Phe His Ser Ser Tyr
210 215 220
Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp Gln
225 230 235 240
Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln
245 250 255
Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val Gln
260 265 270
Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser
275 280 285
Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala
290 295 300
Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly Pro
305 310 315 320
Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser
325 330 335
Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val Asp
340 345 350
Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn
355 360 365
Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln Ser
370 375 380
Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile Leu
385 390 395 400
Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile
405 410 415
Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro Leu
420 425 430
Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile Lys
435 440 445
Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys
450 455 460
Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu
465 470 475 480
Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu
485 490 495
Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala
500 505 510
Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg
515 520 525
Tyr Leu Thr Arg Asn Leu
530
<210> 18
<211> 534
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP3 капсида AAV9, который
включает одну замену в положении F220W (AAV9 CAP F220W VP3)
<400> 18
Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly Ala
1 5 10 15
Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln Trp
20 25 30
Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro
35 40 45
Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly
50 55 60
Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly
65 70 75 80
Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp Trp
85 90 95
Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn
100 105 110
Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn Gly
115 120 125
Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe Thr
130 135 140
Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu Gly
145 150 155 160
Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr Gly
165 170 175
Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser Phe
180 185 190
Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn Asn
195 200 205
Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Trp His Ser Ser Tyr
210 215 220
Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp Gln
225 230 235 240
Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln
245 250 255
Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val Gln
260 265 270
Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser
275 280 285
Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala
290 295 300
Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly Pro
305 310 315 320
Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser
325 330 335
Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val Asp
340 345 350
Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn
355 360 365
Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln Ser
370 375 380
Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile Leu
385 390 395 400
Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile
405 410 415
Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro Leu
420 425 430
Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile Lys
435 440 445
Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys
450 455 460
Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu
465 470 475 480
Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu
485 490 495
Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala
500 505 510
Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg
515 520 525
Tyr Leu Thr Arg Asn Leu
530
<210> 19
<211> 534
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP3 капсида AAV9, который
включает замены в положениях F220W и Y244F (AAV9 CAP F220W Y244F
VP3)
<400> 19
Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly Ala
1 5 10 15
Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln Trp
20 25 30
Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro
35 40 45
Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly
50 55 60
Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly
65 70 75 80
Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp Trp
85 90 95
Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn
100 105 110
Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn Gly
115 120 125
Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe Thr
130 135 140
Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu Gly
145 150 155 160
Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr Gly
165 170 175
Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser Phe
180 185 190
Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn Asn
195 200 205
Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Trp His Ser Ser Tyr
210 215 220
Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp Gln
225 230 235 240
Tyr Leu Tyr Phe Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln
245 250 255
Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val Gln
260 265 270
Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser
275 280 285
Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala
290 295 300
Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly Pro
305 310 315 320
Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser
325 330 335
Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val Asp
340 345 350
Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn
355 360 365
Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln Ser
370 375 380
Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Ile Leu
385 390 395 400
Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile
405 410 415
Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro Leu
420 425 430
Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile Lys
435 440 445
Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys
450 455 460
Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu
465 470 475 480
Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu
485 490 495
Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala
500 505 510
Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg
515 520 525
Tyr Leu Thr Arg Asn Leu
530
<210> 20
<211> 534
<212> PRT
<213> Искусственная последовательность
<220>
<223> выделенный модифицированный белок VP3 капсида AAV9, который
включает одну замену в положении I399M (AAV9 CAP I399M VP3)
<400> 20
Met Ala Ser Gly Gly Gly Ala Pro Val Ala Asp Asn Asn Glu Gly Ala
1 5 10 15
Asp Gly Val Gly Ser Ser Ser Gly Asn Trp His Cys Asp Ser Gln Trp
20 25 30
Leu Gly Asp Arg Val Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro
35 40 45
Thr Tyr Asn Asn His Leu Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly
50 55 60
Gly Ser Ser Asn Asp Asn Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly
65 70 75 80
Tyr Phe Asp Phe Asn Arg Phe His Cys His Phe Ser Pro Arg Asp Trp
85 90 95
Gln Arg Leu Ile Asn Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn
100 105 110
Phe Lys Leu Phe Asn Ile Gln Val Lys Glu Val Thr Asp Asn Asn Gly
115 120 125
Val Lys Thr Ile Ala Asn Asn Leu Thr Ser Thr Val Gln Val Phe Thr
130 135 140
Asp Ser Asp Tyr Gln Leu Pro Tyr Val Leu Gly Ser Ala His Glu Gly
145 150 155 160
Cys Leu Pro Pro Phe Pro Ala Asp Val Phe Met Ile Pro Gln Tyr Gly
165 170 175
Tyr Leu Thr Leu Asn Asp Gly Ser Gln Ala Val Gly Arg Ser Ser Phe
180 185 190
Tyr Cys Leu Glu Tyr Phe Pro Ser Gln Met Leu Arg Thr Gly Asn Asn
195 200 205
Phe Gln Phe Ser Tyr Glu Phe Glu Asn Val Pro Phe His Ser Ser Tyr
210 215 220
Ala His Ser Gln Ser Leu Asp Arg Leu Met Asn Pro Leu Ile Asp Gln
225 230 235 240
Tyr Leu Tyr Tyr Leu Ser Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln
245 250 255
Gln Thr Leu Lys Phe Ser Val Ala Gly Pro Ser Asn Met Ala Val Gln
260 265 270
Gly Arg Asn Tyr Ile Pro Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser
275 280 285
Thr Thr Val Thr Gln Asn Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala
290 295 300
Ser Ser Trp Ala Leu Asn Gly Arg Asn Ser Leu Met Asn Pro Gly Pro
305 310 315 320
Ala Met Ala Ser His Lys Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser
325 330 335
Gly Ser Leu Ile Phe Gly Lys Gln Gly Thr Gly Arg Asp Asn Val Asp
340 345 350
Ala Asp Lys Val Met Ile Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn
355 360 365
Pro Val Ala Thr Glu Ser Tyr Gly Gln Val Ala Thr Asn His Gln Ser
370 375 380
Ala Gln Ala Gln Ala Gln Thr Gly Trp Val Gln Asn Gln Gly Met Leu
385 390 395 400
Pro Gly Met Val Trp Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile
405 410 415
Trp Ala Lys Ile Pro His Thr Asp Gly Asn Phe His Pro Ser Pro Leu
420 425 430
Met Gly Gly Phe Gly Met Lys His Pro Pro Pro Gln Ile Leu Ile Lys
435 440 445
Asn Thr Pro Val Pro Ala Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys
450 455 460
Leu Asn Ser Phe Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu
465 470 475 480
Ile Glu Trp Glu Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu
485 490 495
Ile Gln Tyr Thr Ser Asn Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala
500 505 510
Val Asn Thr Glu Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg
515 520 525
Tyr Leu Thr Arg Asn Leu
530
<210> 21
<211> 1605
<212> DNA
<213> Природная последовательность
<220>
<223> нуклеиновая кислота, кодирующая природную последовательность
белка VP3 капсида AAV9 дикого типа (AAV9 CAP WT VP3)
<400> 21
atggcttcag gtggtggcgc accagtggca gacaataacg aaggtgccga tggagtgggt 60
agttcctcgg gaaattggca ttgcgattcc caatggctgg gggacagagt catcaccacc 120
agcacccgaa cctgggccct gcccacctac aacaatcacc tctacaagca aatctccaac 180
agcacatctg gaggatcttc aaatgacaac gcctacttcg gctacagcac cccctggggg 240
tattttgact tcaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatc 300
aacaacaact ggggattccg gcctaagcga ctcaacttca agctcttcaa cattcaggtc 360
aaagaggtta cggacaacaa tggagtcaag accatcgcca ataaccttac cagcacggtc 420
caggtcttca cggactcaga ctatcagctc ccgtacgtgc tcgggtcggc tcacgagggc 480
tgcctcccgc cgttcccagc ggacgttttc atgattcctc agtacgggta tctgacgctt 540
aatgatggaa gccaggccgt gggtcgttcg tccttttact gcctggaata tttcccgtcg 600
caaatgctaa gaacgggtaa caacttccag ttcagctacg agtttgagaa cgtacctttc 660
catagcagct acgctcacag ccaaagcctg gaccgactaa tgaatccact catcgaccaa 720
tacttgtact atctctcaaa gactattaac ggttctggac agaatcaaca aacgctaaaa 780
ttcagtgtgg ccggacccag caacatggct gtccagggaa gaaactacat acctggaccc 840
agctaccgac aacaacgtgt ctcaaccact gtgactcaaa acaacaacag cgaatttgct 900
tggcctggag cttcttcttg ggctctcaat ggacgtaata gcttgatgaa tcctggacct 960
gctatggcca gccacaaaga aggagaggac cgtttctttc ctttgtctgg atctttaatt 1020
tttggcaaac aaggaactgg aagagacaac gtggatgcgg acaaagtcat gataaccaac 1080
gaagaagaaa ttaaaactac taacccggta gcaacggagt cctatggaca agtggccaca 1140
aaccaccaga gtgcccaagc acaggcgcag accggctggg ttcaaaacca aggaatactt 1200
ccgggtatgg tttggcagga cagagatgtg tacctgcaag gacccatttg ggccaaaatt 1260
cctcacacgg acggcaactt tcacccttct ccgctgatgg gagggtttgg aatgaagcac 1320
ccgcctcctc agatcctcat caaaaacaca cctgtacctg cggatcctcc aacggccttc 1380
aacaaggaca agctgaactc tttcatcacc cagtattcta ctggccaagt cagcgtggag 1440
atcgagtggg agctgcagaa ggaaaacagc aagcgctgga acccggagat ccagtacact 1500
tccaactatt acaagtctaa taatgttgaa tttgctgtta atactgaagg tgtatatagt 1560
gaaccccgcc ccattggcac cagatacctg actcgtaatc tgtaa 1605
<210> 22
<211> 1605
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP3
капсида AAV9, который включает одну замену в положении F220W
(AAV9 CAP F220W VP3)
<400> 22
atggcttcag gtggtggcgc accagtggca gacaataacg aaggtgccga tggagtgggt 60
agttcctcgg gaaattggca ttgcgattcc caatggctgg gggacagagt catcaccacc 120
agcacccgaa cctgggccct gcccacctac aacaatcacc tctacaagca aatctccaac 180
agcacatctg gaggatcttc aaatgacaac gcctacttcg gctacagcac cccctggggg 240
tattttgact tcaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatc 300
aacaacaact ggggattccg gcctaagcga ctcaacttca agctcttcaa cattcaggtc 360
aaagaggtta cggacaacaa tggagtcaag accatcgcca ataaccttac cagcacggtc 420
caggtcttca cggactcaga ctatcagctc ccgtacgtgc tcgggtcggc tcacgagggc 480
tgcctcccgc cgttcccagc ggacgttttc atgattcctc agtacgggta tctgacgctt 540
aatgatggaa gccaggccgt gggtcgttcg tccttttact gcctggaata tttcccgtcg 600
caaatgctaa gaacgggtaa caacttccag ttcagctacg agtttgagaa cgtaccttgg 660
catagcagct acgctcacag ccaaagcctg gaccgactaa tgaatccact catcgaccaa 720
tacttgtact atctctcaaa gactattaac ggttctggac agaatcaaca aacgctaaaa 780
ttcagtgtgg ccggacccag caacatggct gtccagggaa gaaactacat acctggaccc 840
agctaccgac aacaacgtgt ctcaaccact gtgactcaaa acaacaacag cgaatttgct 900
tggcctggag cttcttcttg ggctctcaat ggacgtaata gcttgatgaa tcctggacct 960
gctatggcca gccacaaaga aggagaggac cgtttctttc ctttgtctgg atctttaatt 1020
tttggcaaac aaggaactgg aagagacaac gtggatgcgg acaaagtcat gataaccaac 1080
gaagaagaaa ttaaaactac taacccggta gcaacggagt cctatggaca agtggccaca 1140
aaccaccaga gtgcccaagc acaggcgcag accggctggg ttcaaaacca aggaatactt 1200
ccgggtatgg tttggcagga cagagatgtg tacctgcaag gacccatttg ggccaaaatt 1260
cctcacacgg acggcaactt tcacccttct ccgctgatgg gagggtttgg aatgaagcac 1320
ccgcctcctc agatcctcat caaaaacaca cctgtacctg cggatcctcc aacggccttc 1380
aacaaggaca agctgaactc tttcatcacc cagtattcta ctggccaagt cagcgtggag 1440
atcgagtggg agctgcagaa ggaaaacagc aagcgctgga acccggagat ccagtacact 1500
tccaactatt acaagtctaa taatgttgaa tttgctgtta atactgaagg tgtatatagt 1560
gaaccccgcc ccattggcac cagatacctg actcgtaatc tgtaa 1605
<210> 23
<211> 1605
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP3
капсида AAV9, который включает замены в положениях F220W и Y244F
(AAV9 CAP F220W Y244F VP3)
<400> 23
atggcttcag gtggtggcgc accagtggca gacaataacg aaggtgccga tggagtgggt 60
agttcctcgg gaaattggca ttgcgattcc caatggctgg gggacagagt catcaccacc 120
agcacccgaa cctgggccct gcccacctac aacaatcacc tctacaagca aatctccaac 180
agcacatctg gaggatcttc aaatgacaac gcctacttcg gctacagcac cccctggggg 240
tattttgact tcaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatc 300
aacaacaact ggggattccg gcctaagcga ctcaacttca agctcttcaa cattcaggtc 360
aaagaggtta cggacaacaa tggagtcaag accatcgcca ataaccttac cagcacggtc 420
caggtcttca cggactcaga ctatcagctc ccgtacgtgc tcgggtcggc tcacgagggc 480
tgcctcccgc cgttcccagc ggacgttttc atgattcctc agtacgggta tctgacgctt 540
aatgatggaa gccaggccgt gggtcgttcg tccttttact gcctggaata tttcccgtcg 600
caaatgctaa gaacgggtaa caacttccag ttcagctacg agtttgagaa cgtaccttgg 660
catagcagct acgctcacag ccaaagcctg gaccgactaa tgaatccact catcgaccaa 720
tacttgtact ttctctcaaa gactattaac ggttctggac agaatcaaca aacgctaaaa 780
ttcagtgtgg ccggacccag caacatggct gtccagggaa gaaactacat acctggaccc 840
agctaccgac aacaacgtgt ctcaaccact gtgactcaaa acaacaacag cgaatttgct 900
tggcctggag cttcttcttg ggctctcaat ggacgtaata gcttgatgaa tcctggacct 960
gctatggcca gccacaaaga aggagaggac cgtttctttc ctttgtctgg atctttaatt 1020
tttggcaaac aaggaactgg aagagacaac gtggatgcgg acaaagtcat gataaccaac 1080
gaagaagaaa ttaaaactac taacccggta gcaacggagt cctatggaca agtggccaca 1140
aaccaccaga gtgcccaagc acaggcgcag accggctggg ttcaaaacca aggaatactt 1200
ccgggtatgg tttggcagga cagagatgtg tacctgcaag gacccatttg ggccaaaatt 1260
cctcacacgg acggcaactt tcacccttct ccgctgatgg gagggtttgg aatgaagcac 1320
ccgcctcctc agatcctcat caaaaacaca cctgtacctg cggatcctcc aacggccttc 1380
aacaaggaca agctgaactc tttcatcacc cagtattcta ctggccaagt cagcgtggag 1440
atcgagtggg agctgcagaa ggaaaacagc aagcgctgga acccggagat ccagtacact 1500
tccaactatt acaagtctaa taatgttgaa tttgctgtta atactgaagg tgtatatagt 1560
gaaccccgcc ccattggcac cagatacctg actcgtaatc tgtaa 1605
<210> 24
<211> 1605
<212> DNA
<213> Искусственная последовательность
<220>
<223> нуклеиновая кислота, кодирующая модифицированный белок VP3
капсида AAV9, который включает одну замену в положении I399M
(AAV9 CAP I399M VP3)
<400> 24
atggcttcag gtggtggcgc accagtggca gacaataacg aaggtgccga tggagtgggt 60
agttcctcgg gaaattggca ttgcgattcc caatggctgg gggacagagt catcaccacc 120
agcacccgaa cctgggccct gcccacctac aacaatcacc tctacaagca aatctccaac 180
agcacatctg gaggatcttc aaatgacaac gcctacttcg gctacagcac cccctggggg 240
tattttgact tcaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatc 300
aacaacaact ggggattccg gcctaagcga ctcaacttca agctcttcaa cattcaggtc 360
aaagaggtta cggacaacaa tggagtcaag accatcgcca ataaccttac cagcacggtc 420
caggtcttca cggactcaga ctatcagctc ccgtacgtgc tcgggtcggc tcacgagggc 480
tgcctcccgc cgttcccagc ggacgttttc atgattcctc agtacgggta tctgacgctt 540
aatgatggaa gccaggccgt gggtcgttcg tccttttact gcctggaata tttcccgtcg 600
caaatgctaa gaacgggtaa caacttccag ttcagctacg agtttgagaa cgtacctttc 660
catagcagct acgctcacag ccaaagcctg gaccgactaa tgaatccact catcgaccaa 720
tacttgtact atctctcaaa gactattaac ggttctggac agaatcaaca aacgctaaaa 780
ttcagtgtgg ccggacccag caacatggct gtccagggaa gaaactacat acctggaccc 840
agctaccgac aacaacgtgt ctcaaccact gtgactcaaa acaacaacag cgaatttgct 900
tggcctggag cttcttcttg ggctctcaat ggacgtaata gcttgatgaa tcctggacct 960
gctatggcca gccacaaaga aggagaggac cgtttctttc ctttgtctgg atctttaatt 1020
tttggcaaac aaggaactgg aagagacaac gtggatgcgg acaaagtcat gataaccaac 1080
gaagaagaaa ttaaaactac taacccggta gcaacggagt cctatggaca agtggccaca 1140
aaccaccaga gtgcccaagc acaggcgcag accggctggg ttcaaaacca aggaatgctt 1200
ccgggtatgg tttggcagga cagagatgtg tacctgcaag gacccatttg ggccaaaatt 1260
cctcacacgg acggcaactt tcacccttct ccgctgatgg gagggtttgg aatgaagcac 1320
ccgcctcctc agatcctcat caaaaacaca cctgtacctg cggatcctcc aacggccttc 1380
aacaaggaca agctgaactc tttcatcacc cagtattcta ctggccaagt cagcgtggag 1440
atcgagtggg agctgcagaa ggaaaacagc aagcgctgga acccggagat ccagtacact 1500
tccaactatt acaagtctaa taatgttgaa tttgctgtta atactgaagg tgtatatagt 1560
gaaccccgcc ccattggcac cagatacctg actcgtaatc tgtaa 1605
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения модифицированного капсида аденоассоциированного вируса | 2021 |
|
RU2831732C1 |
| Выделенный модифицированный белок VP1 капсида аденоассоциированного вируса 5 серотипа (AAV5), капсид и вектор на его основе | 2019 |
|
RU2751592C2 |
| Синергетическое действие SMN1 и miR-23a при лечении спинальной мышечной атрофии | 2021 |
|
RU2839898C2 |
| Кодон-оптимизированная нуклеиновая кислота, которая кодирует белок SMN1, и ее применение | 2020 |
|
RU2742837C1 |
| РЕКОМБИНАНТНЫЕ ВИРУСНЫЕ ВЕКТОРЫ С МОДИФИЦИРОВАННЫМ ТРОПИЗМОМ И ПУТИ ИХ ПРИМЕНЕНИЯ ДЛЯ НАЦЕЛЕННОГО ВВЕДЕНИЯ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА В КЛЕТКИ ЧЕЛОВЕКА | 2018 |
|
RU2809246C2 |
| РЕКОМБИНАНТНЫЕ ВИРУСНЫЕ ЧАСТИЦЫ С МОДИФИЦИРОВАННЫМ ТРОПИЗМОМ И ПУТИ ИХ ПРИМЕНЕНИЯ ДЛЯ НАЦЕЛЕННОГО ВВЕДЕНИЯ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА В КЛЕТКИ ЧЕЛОВЕКА | 2018 |
|
RU2811426C2 |
| Вакцина на основе AAV5 для индукции специфического иммунитета к вирусу SARS-CoV-2 и/или профилактики коронавирусной инфекции, вызванной SARS-CoV-2 | 2020 |
|
RU2760301C1 |
| Вакцина на основе AAV5 для индукции специфического иммунитета к вирусу SARS-CoV-2 и/или профилактики коронавирусной инфекции, вызванной SARS-CoV-2 | 2021 |
|
RU2761879C1 |
| Вакцина на основе AAV5 для индукции специфического иммунитета к вирусу SARS-CoV-2 и/или профилактики коронавирусной инфекции, вызванной SARS-CoV-2 | 2020 |
|
RU2783313C1 |
| НОВЫЕ НАЦЕЛИВАЮЩИЕ НА ПЕЧЕНЬ АДЕНОАССОЦИИРОВАННЫЕ ВИРУСНЫЕ ВЕКТОРЫ | 2019 |
|
RU2793735C2 |

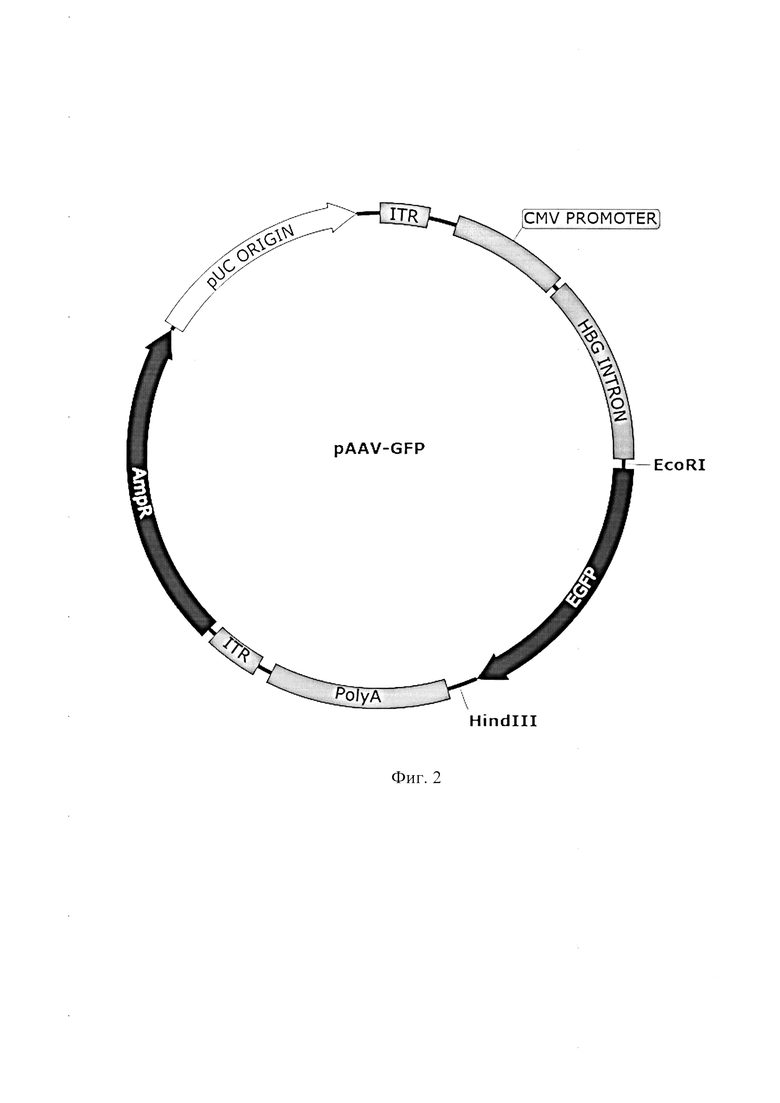
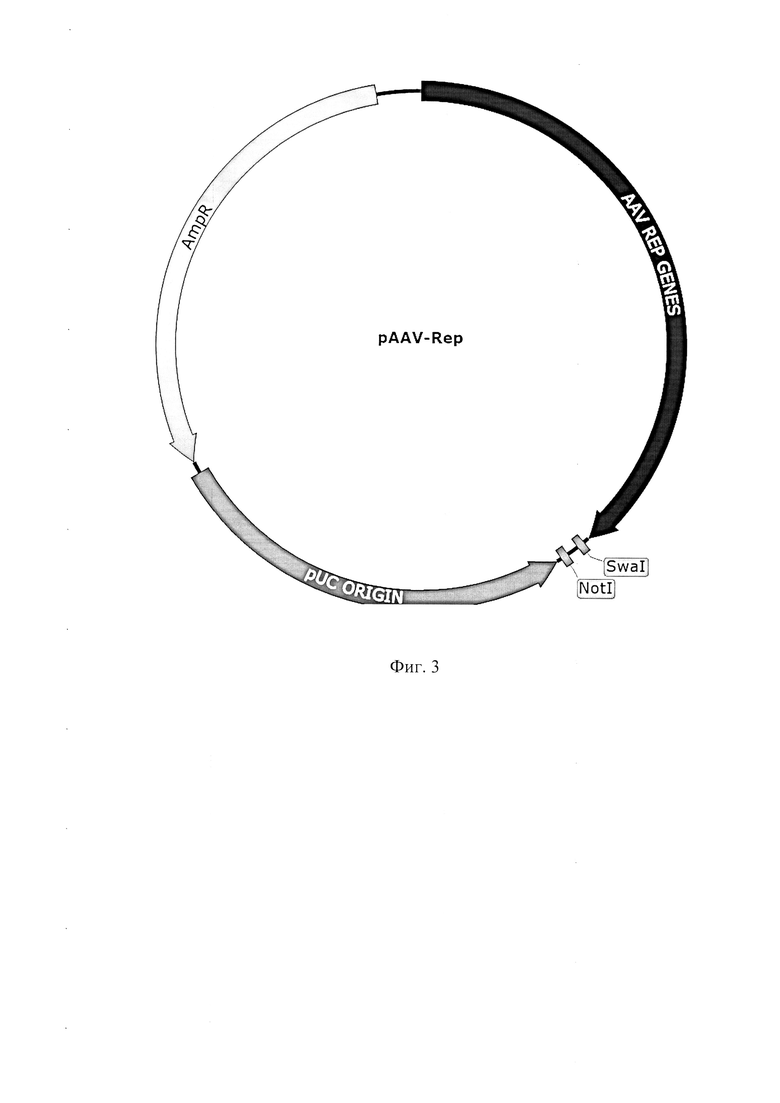
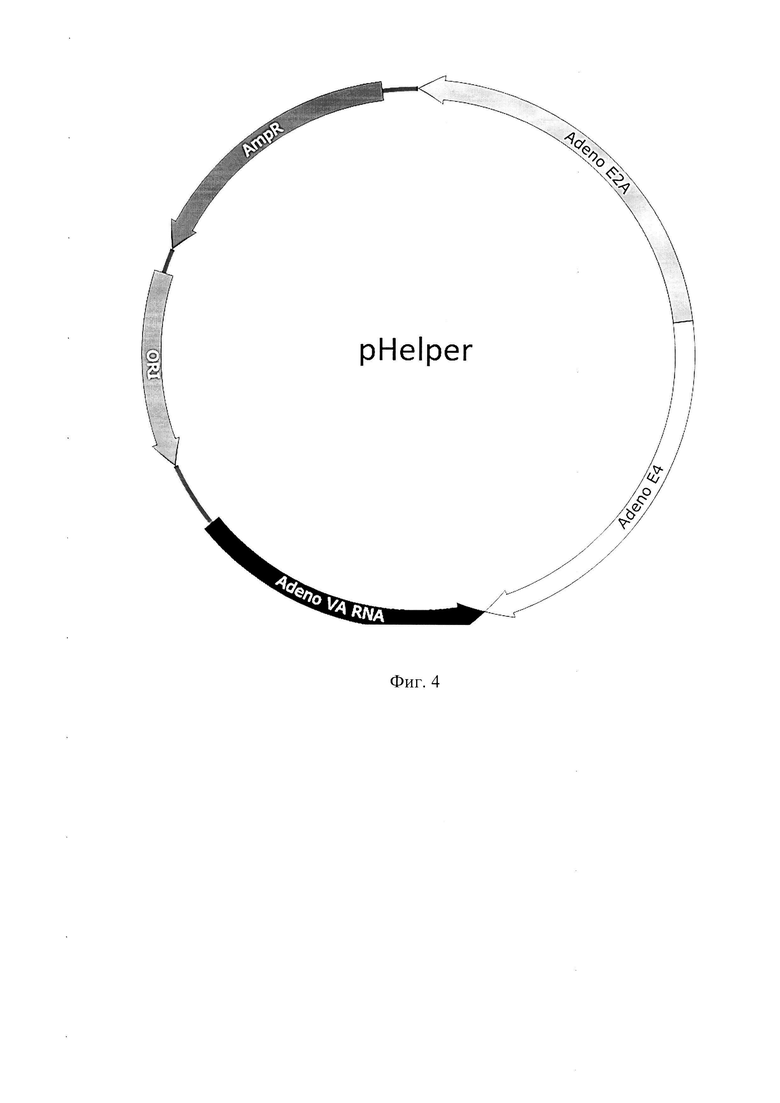
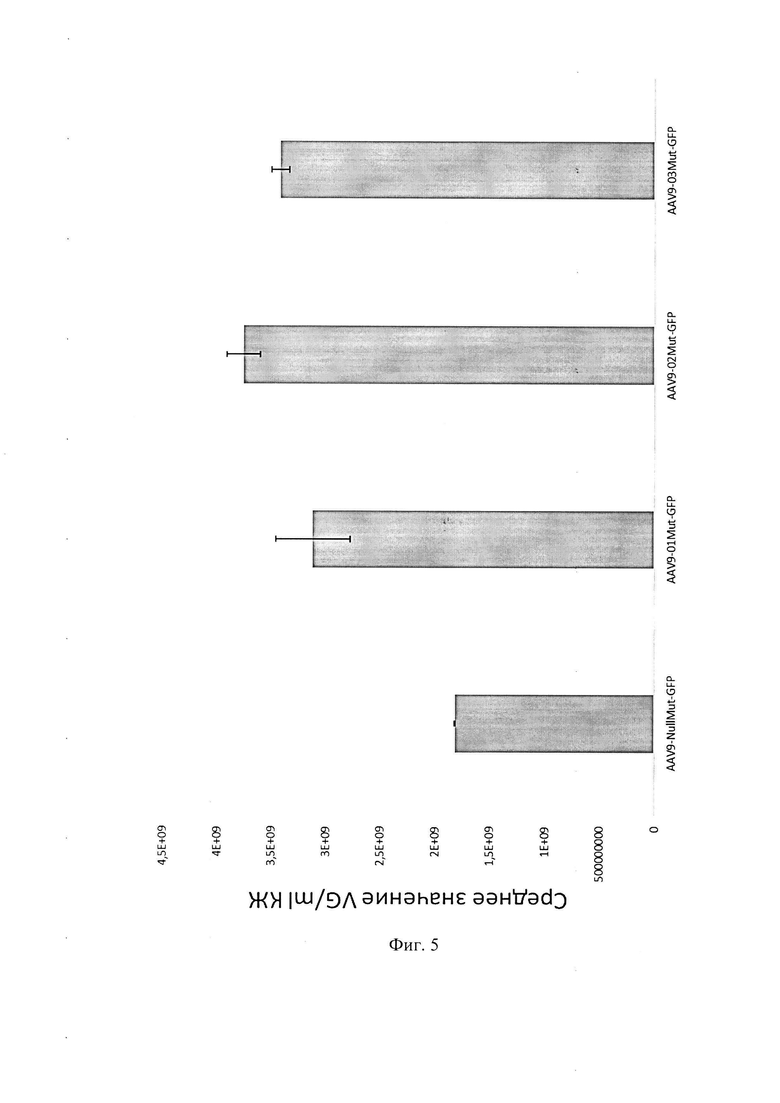
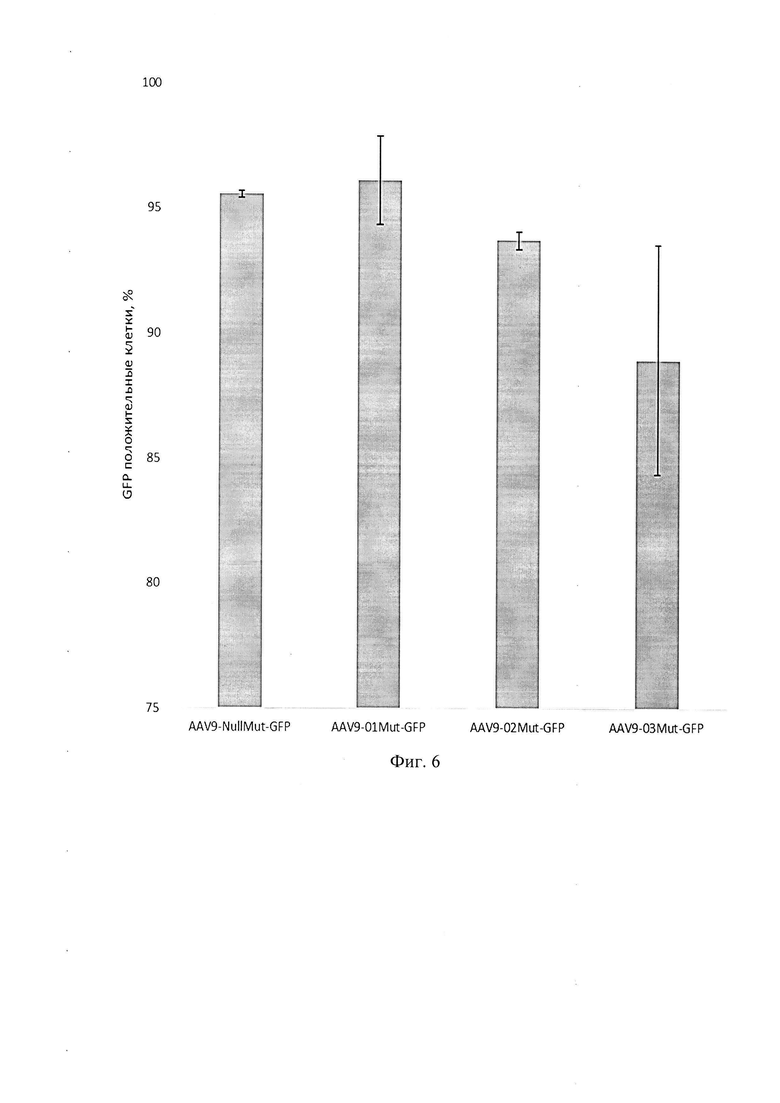
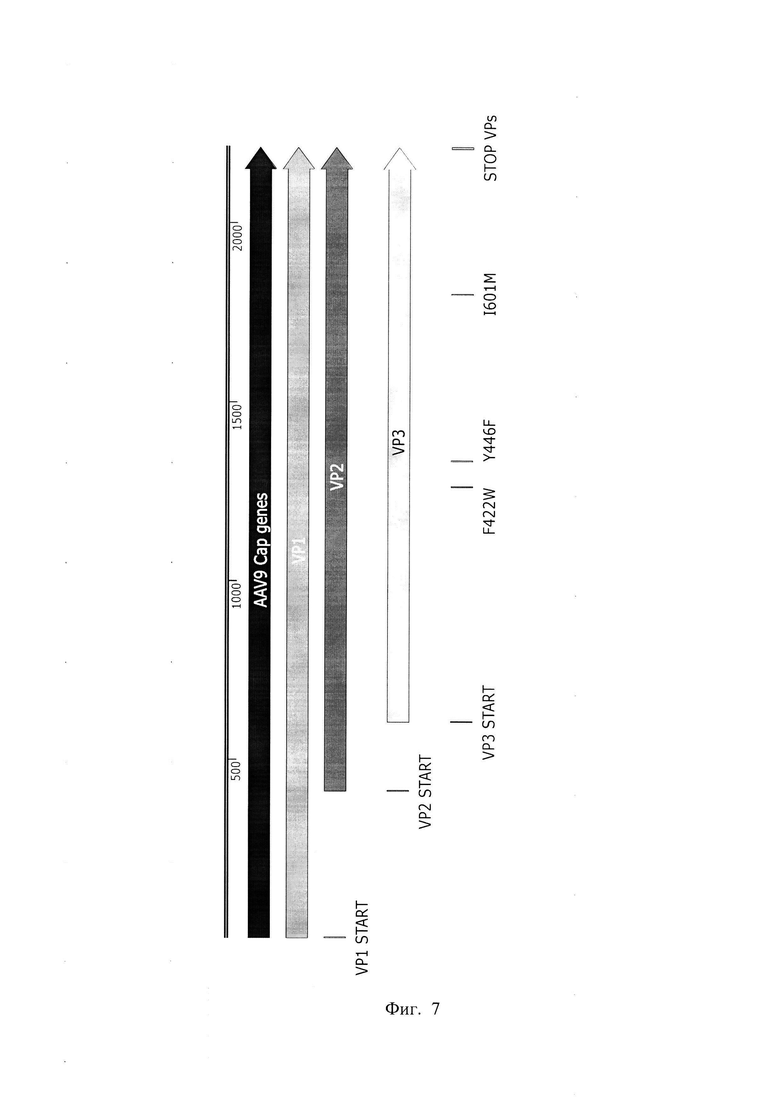
Настоящая заявка относится к области биотехнологии, в частности к области молекулярной биологии и генной инженерии. Изобретение раскрывает выделенный модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9), который содержит одну или несколько аминокислотных замен по сравнению с белком VP1 капсида AAV9 дикого типа, которые повышают эффективность продукции (сборки) вектора на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), капсид и вектор на основе вышеуказанного модифицированного VP1 AAV9, а также их применение для доставки генного продукта нуждающемуся в этом субъекту. 9 н. и 30 з.п. ф-лы, 4 пр., 7 ил.
1. Выделенный модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа (AAV9) для высокоэффективной продукции инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа (rAAV9), содержащий аминокислотную последовательность белка VP1 капсида AAV9 дикого типа, кодируемую геном Сар, с одной или несколькими заменами, которые выбраны из группы:
F422W,
F422W и Y446F,
I601M,
где аминокислотная последовательность белка VP1 капсида AAV9 дикого типа имеет аминокислотную последовательность, представленную SEQ ID NO: 1.
2. Выделенный модифицированный белок VP1 капсида AAV9 по п. 1, который включает замену в положении F422W.
3. Выделенный модифицированный белок VP1 капсида AAV9 по п. 2, который имеет аминокислотную последовательность, представленную SEQ ID NO: 2.
4. Выделенный модифицированный белок VP1 капсида AAV9 по п. 1, который включает замены F422W и Y446F.
5. Выделенный модифицированный белок VP1 капсида AAV9 по п. 4, который имеет аминокислотную последовательность, представленную SEQ ID NO: 3.
6. Выделенный модифицированный белок VP1 капсида AAV9 по п. 1, который включает замену I601M.
7. Выделенный модифицированный белок VP1 капсида AAV9 по п. 6, который имеет аминокислотную последовательность, представленную SEQ ID NO: 4.
8. Выделенная нуклеиновая кислота, кодирующая модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа по любому из пп. 1-7, который используется для высокоэффективной продукции инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа.
9. Выделенная нуклеиновая кислота по п. 8, кодирующая модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа с аминокислотной заменой F422W, которая представлена нуклеиновой последовательностью с SEQ ID NO: 6 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
10. Выделенная нуклеиновая кислота по п. 8, кодирующая модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа с аминокислотными заменами F422W и Y446F, которая представлена нуклеиновой последовательностью с SEQ ID NO: 7 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
11. Выделенная нуклеиновая кислота по п. 8, кодирующая модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа с аминокислотной заменой I601M, которая представлена нуклеиновой последовательностью с SEQ ID NO: 8 или любой другой последовательностью, кодирующей соответствующую аминокислотную последовательность.
12. Выделенный капсид для высокоэффективной продукции инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа, который включает модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа по любому из пп. 1-7.
13. Выделенный капсид по п. 12, который включает модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа по любому из пп. 1-7, белок VP2 капсида AAV9 или его модифицированный вариант и белок VP3 капсида AAV9 или его модифицированный вариант.
14. Выделенный капсид по п. 13, который включает белок VP2 капсида AAV9 дикого типа.
15. Выделенный капсид по п. 14, который включает белок VP2 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 9.
16. Выделенный капсид по п. 13, который включает модифицированный белок VP2 капсида аденоассоциированного вируса 9 серотипа.
17. Выделенный капсид по п. 16, который включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W.
18. Выделенный капсид по п. 17, который включает модифицированный белок VP2 капсида AAV9, который содержит замену F285W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 10.
19. Выделенный капсид по п. 16, который включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F.
20. Выделенный капсид по п. 19, который включает модифицированный белок VP2 капсида AAV9, который содержит замены F285W и Y309F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 11.
21. Выделенный капсид по п. 16, который включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M.
22. Выделенный капсид по п. 21, который включает модифицированный белок VP2 капсида AAV9, который содержит замену I464M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 12.
23. Выделенный капсид по п. 13, который включает белок VP3 капсида AAV9 дикого типа.
24. Выделенный капсид по п. 23, который включает белок VP3 капсида AAV9 дикого типа, который имеет аминокислотную последовательность, представленную SEQ ID NO: 17.
25. Выделенный капсид по п. 13, который включает модифицированный белок VP3 капсида аденоассоциированного вируса 9 серотипа.
26. Выделенный капсид по п. 25, который включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W.
27. Выделенный капсид по п. 26, который включает модифицированный белок VP3 капсида AAV9, который содержит замену F220W, и имеет аминокислотную последовательность, представленную SEQ ID NO: 18.
28. Выделенный капсид по п. 25, который включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F.
29. Выделенный капсид по п. 28, который включает модифицированный белок VP3 капсида AAV9, который содержит замены F220W и Y244F, и имеет аминокислотную последовательность, представленную SEQ ID NO: 19.
30. Выделенный капсид по п. 25, который включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M.
31. Выделенный капсид по п. 30, который включает модифицированный белок VP3 капсида AAV9, который содержит замену I399M, и имеет аминокислотную последовательность, представленную SEQ ID NO: 20.
32. Выделенная нуклеиновая кислота, кодирующая капсид по любому из пп. 12-31, который используется для высокоэффективной продукции инкапсидированных вирусных векторов на основе рекомбинантного аденоассоциированного вируса 9 серотипа.
33. Вектор на основе рекомбинантного аденоассоциированного вируса 9 серотипа для доставки субъекту гетерологичной последовательности нуклеиновой кислоты, который включает:
1) модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа по любому из пп. 1-7 или капсид по любому из пп. 12-31, и
2) гетерологичную последовательность нуклеиновой кислоты, содержащую регуляторные последовательности, которые обеспечивают экспрессию продукта, кодируемого гетерологичной последовательностью нуклеиновой кислоты, в целевых клетках.
34. Вектор на основе rAAV9 по п. 33, где продукт экспрессии гетерологичной последовательности нуклеиновой кислоты представляет собой терапевтический полипептид или репортерный полипептид.
35. Фармацевтическая композиция для доставки генного продукта нуждающемуся в этом субъекту, содержащая:
a) вектор на основе rAAV9 по любому из пп. 33, 34; и
b) фармацевтически приемлемый эксципиент.
36. Способ доставки генного продукта нуждающемуся в этом субъекту, который включает введение субъекту вектора на основе rAAV9 по любому из пп. 33, 34 или фармацевтической композиции по п. 35.
37. Применение вектора на основе rAAV9 по любому из пп. 33, 34 или фармацевтической композиции по п. 35 для лечения заболевания у нуждающегося в этом субъекта.
38. Применение по п. 37, где заболевание выбирают из группы: заболевания крови; заболевания центральной нервной системы; заболевания метаболизма; заболевания мышц; наследственные заболевания.
39. Способ получения вектора на основе rAAV9 по любому из пп. 33, 34, который включает трансфекцию клеток-продуцентов, соответственно, нуклеиновой кислотой, содержащей последовательность, кодирующую модифицированный белок VP1 капсида аденоассоциированного вируса 9 серотипа, по любому из пп. 8-11 или нуклеиновой кислотой, кодирующей капсид, по п. 32.
| RU 2019126509 A1, 04.06.2021 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| NASO M | |||
| et al | |||
| Adeno-Associated Virus (AAV) as a Vector for Gene Therapy, BioDrugs, 2017, v | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
Авторы
Даты
2024-08-28—Публикация
2021-08-20—Подача