ПЕРЕКРЕСТНАЯ ССЫЛКА
[0001] Настоящая заявка испрашивает приоритет предварительной заявки на патент США №62/836242, поданной 19 апреля 2019 года, содержание которой настоящим включено посредством ссылки во всей своей полноте.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка подается в электронном виде с помощью EFS-Web и включает перечень последовательностей, представленный в электронном виде в формате.txt. Файл с расширением.txt содержит перечень последовательностей под названием «AT-020_02WO_SL_ST25», созданный 16 апреля 2020 года и имеющий размер 40387 байт.Перечень последовательностей, содержащийся в данном файле с расширением.txt, является частью настоящего описания и включен в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ
[0003] Настоящее изобретение относится к антигенсвязывающим молекулам, таким как антитела, которые специфически связываются с scFv-частью химерных антигенных рецепторов (CAR), полученной из 4G7, которые связываются с CD19 человека, полинуклеотидам, кодирующим их, а также к способам их изготовления и лечения рака у пациента с их применением.
УРОВЕНЬ ТЕХНИКИ
[0004] Антиидиотипические антитела представляют собой подгруппу антител, вырабатываемых против иммунизирующих антител. Эти антиидиотипические антитела продемонстрировали специфическое связывание с идиотопами (уникальными антигенными детерминантами на поверхности антител) иммунизирующих антител. Антиидиотипические антитела, как правило, можно разделить на три отдельные группы: (1) антитела, которые распознают идиотопы, отличные от антигенсвязывающего сайта (ABS), на иммунизирующих антителах; (2) антитела, которые распознают эпитопы в пределах ABS и имитируют структуру номинального антигена; и (3) антитела, которые распознают эпитопы в пределах ABS без структурного сходства с номинальным антигеном (см., например, Pan et al., (1995) FASEB J 9: 43-49).
[0005] Известные способы выявления экспрессии CAR (например, антитело к мышиному Fab, растворимый человеческий слитый белок CD19-Fc) могут не обладать специфичностью, характеризоваться вариабельностью от партии к партии, генерировать сигналы низкой интенсивности в аналитических способах (например проточной цитометрии) или быть трудновоспроизводимыми в достаточных количествах, что может привести к недооценке истинного количества клеток, экспрессирующих CAR.
[0006] Таким образом, существует потребность в надежных реагентах для точного выявления экспрессии CAR на сконструированных Т-клетках или в анализах in vitro. В данном документе предусмотрены способы и композиции, удовлетворяющие эту и другие потребности.
КРАТКОЕ ОПИСАНИЕ
[0007] Настоящее изобретение предусматривает надежные реагенты со специфическим связыванием с высокой аффинностью для выявления CAR к CD19, содержащих scFv-часть, полученную из клона антитела 4G7 (например, UCART19, ALLO-501 и ALLO-501A). Описанные в данном документе антитела можно использовать в способе выявления экспрессии CAR к CD19 в контексте доклинических исследований, получения иммунных клеток, содержащих scFv, полученный из 4G7 (например, UCART19, ALLO-501 и ALLO-501A), в качестве фармакокинетического реагента на основании клинического потока и в клинических исследованиях иммуногенности.
[0008] В одном аспекте настоящее изобретение предусматривает выделенное антитело, которое специфически связывает молекулу, содержащую scFv к CD19, полученный из 4G7, и в одном варианте осуществления антитело является гуманизированным. В некоторых вариантах осуществления scFv к CD19, полученный из 4G7, содержит аминокислотную последовательность, которая характеризуется по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 99% или 100% идентичностью последовательности с аминокислотной последовательностью под SEQ ID NO: 36. В некоторых вариантах осуществления выделенное антитело не связывается с каркасной областью из 4G7. В некоторых вариантах осуществления выделенное антитело связывается с scFv к CD19, полученным из 4G7, с KD, составляющей не более чем 100 пМ, не более чем 90 пМ, не более чем 80 пМ, не более чем 70 пМ, не более чем 60 пМ, не более чем 50 пМ, не более чем 40 пМ, не более чем 30 пМ или не более чем 20 пМ, как определено посредством анализа Biacore при 25°С. В различных вариантах осуществления антиген связывающая молекула выбрана из группы, состоящей из антитела, scFv, Fab, Fab', Fv, F(ab')2, dAb, человеческого антитела, гуманизированного антитела, химерного антитела, моноклонального антитела, поликлонального антитела, рекомбинантного антитела, антитела IgE, антитела IgD, антитела IgM, антитела IgG1, антитела IgG1, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG2, антитела IgG2, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG3, антитела IgG3, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG4, антитела IgG4, содержащего по меньшей мере одну мутацию в шарнирной области, антитела, содержащего по меньшей мере одну не встречающуюся в природе аминокислоту, и любой их комбинации.
[0009] В дополнительных вариантах осуществления выделенное антитело содержит тяжелую цепь (НС), и в конкретных вариантах осуществления НС содержит последовательность вариабельной области тяжелой цепи (VH), выбранную из группы, состоящей из SEQ ID NO: 1-3. В дополнительных конкретных вариантах осуществления антитело, предусмотренное в данном документе, содержит CDR1 тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 15, 21, 24 и 29. В дополнительных конкретных вариантах осуществления антитело, предусмотренное в данном документе, содержит CDR2 тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 16, 22, 25, 30, 31 и 33. В еще одних вариантах осуществления антитело, предусмотренное в данном документе, содержит CDR3 тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 17, 23 и 26. В еще одних дополнительных вариантах осуществления тяжелая цепь антитела, предусмотренного в данном документе, содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи, при этом каждая CDR содержит аминокислотную последовательность, показанную в таблице 1с.
[0010] В некоторых вариантах осуществления антитело содержит аминокислотную последовательность VH, которая характеризуется по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100% идентичностью с VH антигенсвязывающей молекулы, предусмотренной в данном документе.
[0011] В некоторых вариантах осуществления выделенное антитело, предусмотренное в данном документе, содержит легкую цепь (LC), и в различных вариантах осуществления LC содержит последовательность вариабельной области легкой цепи (VL), выбранную из группы, состоящей из SEQ ID NO: 7-10. В некоторых вариантах осуществления вариабельная область легкой цепи (VL) антитела, предусмотренного в данном документе, содержит одну или более из (а) CDR1, (b) CDR2 и (с) CDR3. В дополнительных конкретных вариантах осуществления CDR1 легкой цепи антитела, предусмотренного в данном документе, может быть выбрана из группы, состоящей из SEQ ID NO: 18 и 27. В других вариантах осуществления CDR2 легкой цепи антитела, предусмотренного в данном документе, может содержать SEQ ID NO: 19. В еще одних дополнительных вариантах осуществления CDR3 легкой цепи антитела, предусмотренного в данном документе, может быть выбрана из группы, состоящей из SEQ ID NO: 20, 28 и 32. В еще одном дополнительном варианте осуществления легкая цепь антитела, предусмотренного в данном документе, содержит CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом каждая CDR содержит аминокислотную последовательность, представленную в таблице 1d.
[0012] В некоторых вариантах осуществления аминокислотная последовательность VL, которая характеризуется по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100% идентичностью с VL антигенсвязывающей молекулы, предусмотренной в данном документе.
[0013] В одном варианте осуществления антитело, предусмотренное в данном документе, содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 1, и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 7. В другом варианте осуществления антитело, предусмотренное в данном документе, содержит (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 18; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 19, и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 20. В дополнительном варианте осуществления антитело, предусмотренное в данном документе, содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 2, и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 8. В дополнительном варианте осуществления антитело, предусмотренное в данном документе, содержит (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 24; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 25; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 26; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27; (е) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 19, и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 28.
[0014] В одном варианте осуществления антитело, предусмотренное в данном документе, содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 3, и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 9. В конкретном варианте осуществления антитело, предусмотренное в данном документе, содержит (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 24; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 31; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 26; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27; (е) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 19, и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 32. В другом варианте осуществления антитело, предусмотренное в данном документе, содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 1, и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 10. В другом варианте осуществления антитело, предусмотренное в данном документе, содержит (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 18; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 19, и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 20.
[0015] В некоторых вариантах осуществления выделенное антитело содержит тяжелую цепь, кодируемую полинуклеотидом, содержащим нуклеиновую кислоту, характеризующуюся по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100% идентичностью с последовательностью нуклеиновой кислоты под SEQ ID NO: 37. В некоторых вариантах осуществления выделенное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 38 или 39. В некоторых вариантах осуществления выделенное антитело содержит легкую цепь, кодируемую полинуклеотидом, содержащим нуклеиновую кислоту, характеризующуюся по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100% идентичностью с последовательностью нуклеиновой кислоты под SEQ ID NO: 40. В некоторых вариантах осуществления выделенное антитело содержит легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 41 или 42.
[0016] В различных вариантах осуществления антитело, предусмотренное в данном документе, дополнительно содержит выявляемую метку, и выявляемая метка может быть выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена. Если требуется флуоресцентная метка, то флуоресцентная метка может быть выбрана из группы, состоящей из красителя Atto, красителя Alexafluor, квантовых точек, гидроксикумарина, аминокумарина, метоксикумарина, Cascade Blue, Pacific Blue, Pacific Orange, Lucifer Yellow, NBD, R-фикоэритрина (РЕ), конъюгатов PE-Cy5, конъюгатов РЕ-Су7, Red 613, PerCP, TruRed, FluorX, флуоресцеина, BODIPY-FL, Су2, Су3, Су3В, Су3.5, Су5, Су5.5, Су7, TRITC, Х-родамина, Lissamine Rhocamine В, Texas Red, аллофикоцианина (АРС), конъюгатов АРС-Су7, Indo-1, Fluo-3, Fluo-4, DCFH, DHR, SNARF, GFP (мутация Y66H), GFP (мутация Y66F), EBFP, EBFP2, азурита, GFPuv, T-Sapphire, Cerulean, mCFP, mTurquoise2, ECFP, CyPet, GFP (мутация Y66W), mKeima-Red, TagCFP, AmCyan1, mTFP1, GFP (мутация S65A), Midorishi Cyan, GFP дикого типа, GFP (мутация S65C), TurboGFP, TagGFP, GFP (мутация S65L), Emerald, GFP (мутация S65T), EGFP, Azami Green, ZsGreenl, TagYFP, EYFP, Topaz, Venus, mCitrine, YPet, TurboYFP, ZsYellow1, Kusabira Orange, mOrange, аллофикоцианина (АРС), mKO, TurboRFP, tdTomato, TagRFP, мономера DsRed, DsRed2 ("RFP"), mStrawberry, TurboFP602, AsRed2, mRFP1, J-Red, R-фикоэритрина (RPE), В-фикоэритрина (ВРЕ), mCherry, HcRed1, Katusha, Р3, перидинин-хлорофилла (PerCP), mKate (TagFP635), TurboFP635, mPlum и mRaspberry. В конкретных вариантах осуществления флуоресцентная метка может представлять собой R-фикоэритрин (РЕ) или аллофикоцианин (АРС).
[0017] В данном документе также предусмотрена композиция, содержащая антитело, предусмотренное в данном документе, и необязательно фармацевтически приемлемый носитель или среду-носитель.
[0018] В данном документе предусмотрены полинуклеотиды, кодирующие тяжелую цепь выделенного антитела из антитела, предусмотренного в данном документе. Кроме того, также предусмотрены полинуклеотиды, кодирующие легкую цепь выделенного антитела из антитела, предусмотренного в данном документе. Также предусмотрены векторы, содержащие полинуклеотид, кодирующий тяжелую цепь выделенного антитела из антитела, предусмотренного в данном документе, и кодирующий легкую цепь выделенного антитела из антитела, предусмотренного в данном документе. Также предусмотрены клетки, содержащие такие векторы, и в различных вариантах осуществления клетка предусматривает клетку, выбранную из группы, состоящей из клетки СНО, клетки Sp2/0, клетки кролика и клетки Е. coli.
[0019] В некоторых вариантах осуществления полинуклеотид содержит последовательность нуклеиновой кислоты под SEQ ID NO: 37 или 40. В некоторых вариантах осуществления полинуклеотид кодирует полипептид, содержащий аминокислотную последовательность под SEQ ID NO: 38, 39, 41 или 42.
[0020] Также предусмотрены способы получения выделенного антитела, предусмотренного в данном документе, и они могут включать инкубацию клетки, предусмотренной в данном документе, в подходящих условиях.
[0021] Предусмотрен способ определения количества клеток, экспрессирующих scFv, полученный из 4G7, и он может включать приведение образца в контакт с выделенным антителом, которое специфически связывает scFv, полученный из 4G7, конъюгированный с выявляемой меткой, и определение количества клеток, экспрессирующих scFv, полученный из 4G7, в образце. В вариантах осуществления выделенное антитело, которое специфически связывает scFv, полученный из 4G7, представляет собой антитело, предусмотренное в данном документе, или его гуманизированную форму.
[0022] Также предусмотрен способ определения количества клеток, представляющих полипептид, содержащий scFv к CD19, полученный из 4G7, где способ включает: (а) получение образца, содержащего клетки, которые, как известно или предполагается, представляют полипептид, содержащий scFv к CD19, полученный из 4G7; (b) приведение образца в контакт с выделенной антигенсвязывающей молекулой, предусмотренной в данном документе, или ее гуманизированной формой в условиях, которые обеспечивают связывание полипептида и антигенсвязывающей молекулы, и (с) определение количества клеток, представляющих полипептид, в образце.
[0023] В данном документе предусмотрен способ определения присутствия или отсутствия полипептида, содержащего scFv к CD19, полученный из 4G7, где способ включает: (а) получение образца, который, как известно или предполагается, содержит полипептид scFv к CD19, полученный из 4G7; (b) приведение образца в контакт с выделенной антигенсвязывающей молекулой, предусмотренной в данном документе, или ее гуманизированной формой в условиях, которые обеспечивают связывание полипептида и антигенсвязывающей молекулы, и (с) выявление присутствия или отсутствия комплекса полипептид:антигенсвязывающая молекула. В одном варианте осуществления способа образец представляет собой образец, фиксированный формалином. В другом варианте осуществления scFv, полученный из 4G7, представляет собой компонент химерного антигенного рецептора (CAR), и в дополнительных вариантах осуществления клетка, экспрессирующая CAR с scFv, полученным из 4G7, представляет собой иммунную клетку, выбранную из группы, состоящей из CD8+ Т-клеток, CD4+ Т-клеток, лимфоцитов, инфильтрирующих опухоль (TIL), NK-клеток, TCR-экспрессирующих клеток, дендритных клеток и NK-Т-клеток. В некоторых вариантах осуществления выделенная антигенсвязывающая молекула помечена выявляемой меткой, и выявляемая метка может быть выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена. Если выявляемая метка представляет собой флуоресцентную метку, то флуоресцентная метка может быть выбрана из группы, состоящей из красителя Atto, красителя Alexafluor, квантовых точек, гидроксикумарина, аминокумарина, метоксикумарина, Cascade Blue, Pacific Blue, Pacific Orange, Lucifer Yellow, NBD, R-фикоэритрина (PE), конъюгатов PE-Cy5, конъюгатов PE-Cy7, Red 613, PerCP, TruRed, FluorX, флуоресцеина, BODIPY-FL, Cy2, Су3, Су3В, Cy3.5, Cy5, Су5.5, Су7, TRITC, X-родамина, Lissamine Rhocamine В, Texas Red, аллофикоцианина (АРС), конъюгатов АРС-Су7, Indo-1, Fluo-3, Fluo-4, DCFH, DHR, SNARF, GFP (мутация Y66H), GFP (мутация Y66F), EBFP, EBFP2, азурита, GFPuv, T-Sapphire, Cerulean, mCFP, mTurquoise2, ECFP, CyPet, GFP (мутация Y66W), mKeima-Red, TagCFP, AmCyanl, mTFP1, GFP (мутация S65A), Midorishi Cyan, GFP дикого типа, GFP (мутация S65C), TurboGFP, TagGFP, GFP (мутация S65L), Emerald, GFP (мутация S65T), EGFP, Azami Green, ZsGreenl, TagYFP, EYFP, Topaz, Venus, mCitrine, YPet, TurboYFP, ZsYellow1, Kusabira Orange, mOrange, аллофикоцианина (АРС), mKO, TurboRFP, tdTomato, TagRFP, мономера DsRed, DsRed2 ("RFP"), mStrawberry, TurboFP602, AsRed2, mRFPl, J-Red, R-фикоэритрина (RPE), В-фикоэритрина (BPE), mCherry, HcRedl, Katusha, РЗ, перидинин-хлорофилла (PerCP), mKate (TagFP635), TurboFP635, mPlum и mRaspberry. В конкретном варианте осуществления флуоресцентная метка представляет собой R-фикоэритрин (РЕ) или аллофикоцианин (АРС). В некоторых вариантах осуществления клетка, экспрессирующая CAR с scFv, полученным из 4G7, представляет собой иммунную клетку, при этом иммунная клетка представляет собой Т-клетку, которая может находиться in vitro или in vivo. В вариантах осуществления Т-клетка находится в крови, выделенной ткани, ткани, выращенной ex vivo, или в среде для культивирования клеток. В одном варианте осуществления Т-клетка представляет собой аутологичную Т-клетку. В другом варианте осуществления Т-клетка представляет собой аллогенную Т-клетку.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0024] На ФИГ. 1 показан график, представляющий собой сенсограмму, демонстрирующую захват всех биотинилированных антиидиотипических субклонов («клон Е2» Е2153.1С4.Е2, «клон В4» E2153.1D9.B4, «клон Н5» E2153.1G5.H5, «клон А8» Е2153.2Н8 А8, «клон В7» Е2153.3 В11.В7, «клон Е11» E2153.4D7.E11) на поверхности чипа CAPture.
[0025] На ФИГ. 2А и 2В показаны графики кинетической подгонки для связывания m4G7-hFab с очищенными субклонами антиидиотипических антител, полученными из слитого белка 4G7 Е2153 (ФИГ. 2А), и связывания m4G7-hFab с отрицательным контролем (ФИГ. 2В) при 25°С.
[0026] На ФИГ. 3А и 3В показаны иллюстративные графики проточной цитометрии для сравнения коммерчески доступного антитела к мышиному F(ab')2 и клонов А8 и E11 антиидиотипических антител в отношении связывания с клетками UCART19. В пробирке А содержалась кровь здорового добровольца; пробирка В: кровь здорового добровольца + 100000 трансдуцированных клеток UCART19 на мл; пробирка С: кровь здорового добровольца+1 миллион трансдуцированных клеток UCART19 на мл, и пробирка D: 10 миллионов трансдуцированных клеток UCART19 на мл.
[0027] На ФИГ. 4А-4Е показаны иллюстративные результаты экспериментов по блокированию с применением антиидиотипического антитела А8, меченного против UCART19. На ФИГ. 4А показан линейный график % CAR+ клеток, выявляемых с помощью растворимого слитого белка CD19-Fc после предварительной обработки либо антиидиотипическим антителом, либо нерелевантным изотипическим контролем. На ФИГ. 4В и 4С показаны графики проточной цитометрии с ФИГ. 4А с повышающейся концентрацией Ab идиотипа А8 (Е2153.2Н8.А8) (ФИГ. 4В) и изотипический контроль, представляющий собой неконъюгированный мышиный IgG1 (ФИГ. 4С). На ФИГ. 4D и 4Е показана способность антиидиотипического m4G7 (А8) блокировать лизис опухолевых клеток при соотношениях Е:Т, составляющих 5:1 и 10:1 соответственно.
[0028] На ФИГ. 5А показаны иллюстративные графики проточной цитометрии из экспериментов с антиидиотипическими антителами для определения связывания с клетками Jurkat, экспрессирующими CAR, с scFv, полученным из мышиного 4G7 (m4G7), гуманизированного 4G7 (h4G7.7), мышиного scFv к CD19 FMC63 (не родственного 4G7) или ВС40, scFv человека к ВСМА. На ФИГ. 5В показаны графики проточной цитометрии положительного контроля с применением связывания sCD19-Fc со всеми CAR к CD19, экспрессируемыми на клетках Jurkat.
[0029] На ФИГ. 6А и ФИГ. 6 В показаны иллюстративные графики проточной цитометрии связывания антиидиотипических антител с h4G7.7 и UCART19, экспрессируемыми на первичных Т-клетках человека, но не связывающихся с CAR (CTL-019), полученным из FMC63 (ФИГ. 6А). sCD19-Fc использовали в качестве положительного контроля, демонстрирующего связывание со всеми CAR к CD19, экспрессируемыми на первичных Т-клетках человека (ФИГ. 6В).
[0030] На ФИГ. 7 показаны соотношения сигнал/шум антиидиотипических клонов El 1, Е2, А8 и В4 при повышающихся концентрациях.
[0031] На ФИГ. 8 показаны индекс окрашивания и графики проточной цитометрии антиидиотипического антитела А8, конъюгированного с флуоресцентными зондами на основе фикоэритрина (РЕ) или аллофикоцианина (АРС).
ПОДРОБНОЕ ОПИСАНИЕ
[0032] scFv-часть некоторых химерных антигенных рецепторов (CAR), например, по меньшей мере UCART19, ALLO-501 и ALLO-501А, получена из клона 4G7 мышиных антител к CD19 человека. Настоящее изобретение предусматривает реагенты для выявления CAR к CD19, содержащие scFv-часть, полученную из клона 4G7 антитела (например UCART19 и ALLO-501). В данном документе раскрыты антиидиотипические антитела (антиидиотипические), антитела, которые специфически связываются с клоном 4G7 к CD19 и молекулами к CD19, полученными из 4G7. Антиидиотипические антитела к молекулам, полученным из 4G7, раскрытые в данном документе, демонстрируют специфическое высокоаффинное связывание с химерными антигенными рецепторами (CAR), содержащими scFv, полученный из 4G7 (например, UCART19, ALLO-501 и ALLO-501А). Один неограничивающий пример scFv, полученного из 4G7, содержит аминокислотную последовательность под SEQ ID NO: 36.
[0033] При конъюгации с ярким флуорохромом антиидиотипические антитела, раскрытые в данном документе, окрашивают клетки, экспрессирующие химерные антигенные рецепторы (CAR), содержащие scFv, полученный из 4G7 (например, UCART19, ALLO-501 и ALLO-501A), с высоким MFI и низким фоном. Описанные в данном документе антитела можно использовать в способе выявления экспрессии CAR к CD19. Эти антитела можно использовать для идентификации, например, UCART19 и ALLO-501 как посредством проточной цитометрии, так и посредством иммуногистохимического анализа. Эти антитела также можно использовать в контексте доклинических исследований, получения иммунных клеток, содержащих scFv, полученный из 4G7 (например UCART19 и ALLO-501), в качестве фармакокинетического реагента на основании клинического потока и в клинических исследованиях иммуногенности.
[0034] 4G7 представляет собой моноклональное антитело к CD19, которое распознает CD19. Одноцепочечные вариабельные фрагменты (scFv), образованные из 4G7, содержат нацеливающий компонент некоторых химерных антигенных рецепторов (CAR) (см. WO2014184143A1, US 62/839455, поданную 26 апреля 2019 г., и US 63/005041, поданную 3 апреля 2020 г. ). В некоторых вариантах осуществления scFv, полученный из моноклонального антитела 4G7 к CD19, содержит часть тяжелой гамма-цепи 1 иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19 (GenBank: CAD88275.1; SEQ ID NO: 34), и часть легкой каппа-цепи иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19 (GenBank: CAD88204.1; SEQ ID NO: 35), связанные вместе посредством гибкого линкера. (Peipp М., D. Saul, et al., 2004. Efficient eukaryotic expression of fluorescent scFv fusion proteins directed against CD antigens for FACS applications. J. Immunol. Methods 285: 265-280). В некоторых вариантах осуществления scFv содержит вариабельные фрагменты тяжелой гамма-цепи 1 иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19, и вариабельные фрагменты легкой каппа-цепи иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19, связанные вместе посредством гибкого линкера.
[0035] Тяжелая гамма-цепь 1 иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19, содержит аминокислотную последовательность:
[0036]

(SEQ ID NO: 34, подчеркнута сигнальная последовательность, VH выделена жирным шрифтом и также показана под SEQ ID NO:)
[0037] Легкая каппа-цепь иммуноглобулина 4G7, представляющего собой моноклональное антитело к CD19, содержит аминокислотную последовательность:
[0038]

(SEQ ID NO: 35, подчеркнута сигнальная последовательность, VL выделена жирным шрифтом)
[0039] Иллюстративный scFv, полученный из 4G7, содержит аминокислотную последовательность:
[0040]

(SEQ ID NO: 36, каждая из CDR1, CDR2, CDR3 VH и CDR1, CDR2 и CDR3 VL подчеркнута)
[0041] В некоторых вариантах осуществления scFv содержит часть аминокислотных последовательностей под SEQ ID NO: 34 и/или SEQ ID NO: 35. В некоторых вариантах осуществления scFv содержит часть аминокислотных последовательностей под SEQ ID NO: 34 и/или SEQ ID NO: 35 с сигнальной последовательностью или без нее. В некоторых вариантах осуществления scFv характеризуется по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 97% или по меньшей мере 99% идентичностью последовательности с вариабельной областью из аминокислотной последовательности под SEQ ID NO: 34 и/или SEQ ID NO: 35. В некоторых вариантах осуществления scFv характеризуется по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 99% или 100% идентичностью последовательности с аминокислотной последовательностью под SEQ ID NO: 36. В данном документе раскрыты антигенсвязывающие молекулы, в том числе антитела, которые специфически связываются с scFv к CD19, полученным из 4G7, а также молекулы, содержащие данные последовательности, и клетки, представляющие такие молекулы. Гуманизированные формы антигенсвязывающих молекул также являются аспектом настоящего изобретения. Также раскрыты пути применения и использования данных антигенсвязывающих молекул.
I. Антигенсвязывающие молекулы и полинуклеотиды, кодирующие их
[0042] Используемый в данном документе термин «антигенсвязывающий домен» означает любой полипептид, который связывает конкретный целевой антиген, например, конкретный целевой антиген может представлять собой белок CD19 или его фрагмент (называемый в данном документе взаимозаменяемо как «антиген CD19», «целевой антиген CD19» или «целевой CD19»). В контексте антиидиотипического антитела по настоящему изобретению целевой антиген представляет собой антигенсвязывающую молекулу, которая специфически связывает CD19 (например клон 4G7 антитела и антигенсвязывающие молекулы, полученные из 4G7 или родственные ему, в том числе scFv).
[0043] В некоторых вариантах осуществления антигенсвязывающий домен связывается с антигеном CD19 на опухолевой клетке. В некоторых вариантах осуществления антигенсвязывающий домен связывается с антигеном CD19 на клетке, вовлеченной в гиперпролиферативное заболевание, или с вирусным или бактериальным антигеном.
[0044] Антигенсвязывающие домены включают без ограничения связывающие области антитела, которые являются иммунологически функциональными фрагментами. Термин «иммунологически функциональный фрагмент» (или «фрагмент») антигенсвязывающего домена представляет собой разновидность антигенсвязывающего домена, содержащую часть (независимо от того, как эта часть получена или синтезирована) антитела, в которой отсутствуют по меньшей мере некоторые аминокислоты, присутствующие в полноразмерной цепи, но которая все еще способна специфически связываться с целевым антигеном. Такие фрагменты являются биологически активными в том смысле, что они связываются с целевым антигеном и могут конкурировать с другими антигенсвязывающими доменами, включая интактные антитела, за связывание с данным эпитопом. В некоторых вариантах осуществления фрагменты представляют собой нейтрализующие фрагменты. В некоторых вариантах осуществления фрагменты могут блокировать или снижать активность CAR к CD19 (например, блокирующий эффект). В некоторых вариантах осуществления фрагменты могут противодействовать активности CAR к CD19.
[0045] В конкретных вариантах осуществления антиидиотипическое антитело по настоящему изобретению представляет собой антитело, идентифицированное в данном документе как клоны Е2, В4, А8, Е11, каждый из которых содержит аминокислотные последовательности тяжелой и легкой цепей, вариабельные последовательности, последовательности CDR и нуклеотидные последовательности, кодирующие такие последовательности, предусмотренные и обозначенные в данном документе.
[0046] Иммунологически функциональные фрагменты иммуноглобулина включают без ограничения scFv-фрагменты, Fab-фрагменты (Fab', F(ab')2 и т.п.), одну или более областей, определяющих комплементарность («CDR»), диатело (вариабельный домен тяжелой цепи на том же полипептиде, что и вариабельный домен легкой цепи, соединенные посредством короткого пептидного линкера, который является слишком коротким для обеспечения образования пары между двумя доменами в одной цепи), доменные антитела, бивалентные антигенсвязывающие домены (содержат два антигенсвязывающих сайта), полиспецифические антигенсвязывающие домены и одноцепочечные антитела. Данные фрагменты могут быть получены из любого источника, представляющего собой млекопитающее, в том числе без ограничения человека, мыши, крысы, верблюда или кролика. Специалисту в данной области техники будет понятно, что антигенсвязывающий домен может содержать небелковые компоненты.
[0047] Вариабельные области обычно демонстрируют одинаковую общую структуру относительно консервативных каркасных областей (FR), соединенных 3 гипервариабельными областями (CDR). CDR из двух цепей каждой пары обычно выравниваются по каркасным областям, что может обеспечить связывание со специфическим эпитопом. От N-конца к С-концу вариабельные области как легкой, так и тяжелой цепи обычно содержат домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Условно области CDR в тяжелой цепи обычно называются CDR1, CDR2 и CDR3 НС.Области CDR в легкой цепи как правило называются CDR1, CDR2 и CDR3 LC.
[0048] В некоторых вариантах осуществления антигенсвязывающие домены содержат одну или более областей, определяющих комплементарность (CDR), присутствующих в полноразмерной легкой или тяжелой цепи антитела, и в некоторых вариантах осуществления содержат одну тяжелую цепь и/или легкую цепь или ее часть. Эти фрагменты могут быть получены посредством методик рекомбинантной ДНК или могут быть получены посредством ферментативного или химического расщепления антигенсвязывающих доменов, в том числе интактных антител.
[0049] В некоторых вариантах осуществления антигенсвязывающий домен представляет собой антитело или его фрагмент, в том числе одну или более из его областей, определяющих комплементарность (CDR). В некоторых вариантах осуществления антигенсвязывающий домен представляет собой одноцепочечный вариабельный фрагмент (scFv), содержащий CDR легкой цепи CDR1, CDR2 и CDR3, а также CDR тяжелой цепи CDR1, CDR2 и CDR3.
[0050] Присвоение аминокислот каждому из каркасных областей, CDR и вариабельных доменов как правило осуществляется в соответствии со схемами нумерации по Kabat (см., например, Kabat et al. in Sequences of Proteins of Immunological Interest, 5th Ed., NIH Publication 91-3242, Bethesda Md. 1991), нумерации no Chothia (см., например, Chothia & Lesk, (1987), J Mol Biol 196: 901-917; Al-Lazikani et al., (1997) J Mol Biol 273: 927-948; Chothia et al., (1992) J Mol Biol 227: 799-817; Tramontano et al., (1990) J Mol Biol 215(1): 175-82; и патент США №7709226), нумерации «контакт» или схемой AbM (Antibody Modeling program, Oxford Molecular).
[0051] Соответственно, в некоторых вариантах осуществления CDR антиидиотипических антител, представленных в данном документе, пронумерованы в соответствии со схемой нумерации по Kabat. В других вариантах осуществления CDR антиидиотипических антител, представленных в данном документе, пронумерованы в соответствии со схемой нумерации по Chothia. В других вариантах осуществления CDR антиидиотипических антител, представленных в данном документе, пронумерованы в соответствии со схемой нумерации «контакт». В других вариантах осуществления CDR антиидиотипических антител, представленных в данном документе, пронумерованы в соответствии со схемой нумерации AbM.
[0052] В данном документе описаны гуманизированные антитела, которые можно получать посредством известных методик. В некоторых вариантах осуществления гуманизированное моноклональное антитело содержит вариабельный домен антиидиотипического антитела (или весь или часть его антигенсвязывающего сайта) и константный домен, полученный из человеческого антитела. В качестве альтернативы, фрагмент гуманизированного антитела может содержать антигенсвязывающий сайт моноклонального антитела мыши или кролика и фрагмент вариабельного домена (без антигенсвязывающего сайта), полученный из человеческого антитела. Процедуры получения сконструированных моноклональных антител включают процедуры, описанные, например, в Riechmann et al., (1988) Nature 332: 323, Liu et al., (1987) Proc. Nat. Acad. Sci. USA 84: 3439, Larrick et al., (1989) Bio/Technology 7: 934, и Winter et al., (1993) TIPS 14: 139. В некоторых вариантах осуществления химерное антитело представляет собой антитело с привитой CDR. Методики гуманизации антител обсуждаются, например, в патентах США №№5869619; 5225539; 5821337; 5859205; 6881557; Padlan et al., (1995) FASEB J. 9: 133-39; Tamura et al., (2000) J. Immunol. 164: 1432-41; Zhang et al., (2005) Mol. Immunol. 42(12): 1445-1451; Hwang et al, Methods. (2005) 36(1): 35-42; Dall'Acqua et al., (2005) Methods 36(1): 43-60, и Clark, (2000) Immunology Today 21(8): 397-402.
[0053] Варианты антиидиотипических антител также охватываются объемом настоящего изобретения, например вариабельные области легких и/или вариабельные области тяжелых цепей, каждая из которых характеризуется по меньшей мере 70-80%, 80-85%, 85-90%, 90-95% 95-97%, 97-99% или более 99%о идентичностью с аминокислотными последовательностями описанных в данном документе последовательностей антигенсвязывающего домена. В некоторых вариантах осуществления антиидиотипическое антитело характеризуется по меньшей мере приблизительно 75%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100%идентичностью с последовательностью вариабельной области тяжелой цепи, представленной в таблице 1а, и/или последовательностью вариабельной области легкой цепи, представленной в таблице 1b.
[0054] В некоторых случаях такие молекулы содержат по меньшей мере одну тяжелую цепь и одну легкую цепь, тогда как в других случаях вариантные формы содержат две вариабельные легкие цепи и две вариабельные тяжелые цепи (или их подчасти). Специалист в данной области техники сможет определить подходящие варианты антиидиотипических антител, представленных в данном документе, с применением хорошо известных методик. В определенных вариантах осуществления специалист в данной области техники может идентифицировать подходящие области молекулы, которые можно изменить без нарушения активности посредством нацеливания на области, которые, как считается, не являются важными для активности.
[0055] Антиидиотипическое антитело по настоящему изобретению также может представлять собой полностью человеческое моноклональное антитело. Полностью человеческие моноклональные антитела можно получать посредством любого количества методик, с которыми будут знакомы специалисты в данной области техники. Такие способы включают без ограничения трансформацию с помощью вируса Эпштейна-Барр (EBV) клеток периферической крови человека (например содержащих В-лимфоциты), иммунизацию В-клеток человека in vitro, слияние клеток селезенки от иммунизированных трансгенных мышей, несущих встроенные гены человеческих иммуноглобулинов, выделение из фаговых библиотек V-области человеческого иммуноглобулина или другие процедуры, известные из уровня техники и основанные на раскрытии в данном документе.
[0056] Антиидиотипическое антитело, которое специфически связывается с клоном 4G7 к CD19 и молекулами к CD19, полученными из 4G7, считается «селективным», если оно связывается с одной мишенью более прочно, чем со второй мишенью.
[0057] Считается, что антиидиотипическое антитело, которое специфически связывается с клоном 4G7 к CD19 и молекулами к CD19, полученными из 4G7, «специфически связывается» со своим целевым антигеном (например, 4G7 мыши и молекулами, полученными из 4G7), если константа диссоциации (Kd) составляет ~1 нМ. Антигенсвязывающий домен специфически связывает антиген с «высокой аффинностью», если Kd составляет 1-5 нМ, и с «очень высокой аффинностью», если Kd составляет 0,1-0,5 нМ. В одном варианте осуществления антигенсвязывающий домен характеризуется Kd, составляющей ~1 нМ. В одном варианте осуществления константа скорости диссоциации составляет <1×10-5. В других вариантах осуществления антигенсвязывающие домены будут связываться с 4G7 мыши и молекулами, полученными из 4G7, с Kd, составляющей от приблизительно 1×10-7 М до 1×10-12 М, и в еще одном варианте осуществления антигенсвязывающие домены будут связываться с Kd, составляющей от приблизительно 1×10-5 до 1×10-12.
[0058] Как предусмотрено в данном документе, антиидиотипические антитела по настоящему изобретению специфически связывают 4G7 мыши и молекулы, полученные из 4G7 (например, мышиный 4G7, гуманизированный 4G7, CAR, полученные из 4G7). В определенных вариантах осуществления антиидиотипические антитела по настоящему изобретению связывают мышиный 4G7 и молекулы, полученные из 4G7, с KD, составляющей менее чем 1×10-6 М, менее чем 1×10-7 М, менее чем 1×10-8 М или менее чем 1×10-9 М. В одном конкретном варианте осуществления антиидиотипические антитела связывают 4G7 мыши и молекулы, полученные из 4G7, с KD, составляющей менее чем 1×10-7 М. В другом варианте осуществления антиидиотипические антитела связывают 4G7 мыши и молекулы, полученные из 4G7, с KD, составляющей менее чем 1×10-8 М. В некоторых вариантах осуществления антиидиотипические антитела связывают 4G7 мыши и молекулы, полученные из 4G7, с Kd, составляющей приблизительно 1×10-7 М, приблизительно 2×10-7 М, приблизительно 3×10-7 М, приблизительно 4×10-7 М, приблизительно 5×10-7 М, приблизительно 6×10-7 М, приблизительно 7×10-7 М, приблизительно 8×10-7 М, приблизительно 9×10-7 М, приблизительно 1×10-8 М, приблизительно 2×10-8 М, приблизительно 3×10-8 М, приблизительно 4×10-8 М, приблизительно 5×10-8 М, приблизительно 6×10-8 М, приблизительно 7×10-8 М, приблизительно 8×10-8 М, приблизительно 9×10-8 М, приблизительно 1×10-9 М, приблизительно 2×10-9 М, приблизительно 3×10-9 М, приблизительно 4×10-9 М, приблизительно 5×10-9 М, приблизительно 6×10-9 М, приблизительно 7×10-9 М, приблизительно 8×10-9 М, приблизительно 9×10-9 М, приблизительно 1×10-10 М или приблизительно 5×10-10 М. В определенных вариантах осуществления Kd рассчитывается как соотношение Koff/Kon, а Kon и Koff определяются с применением моновалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления Kd рассчитывается как соотношение Koff/Kon, а Kon и Koff определяются с применением бивалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса BIAcore®.
[0059] В некоторых вариантах осуществления антиидиотипические антитела связывают мышиный 4G7 и молекулы, полученные из 4G7, со скоростью ассоциации (kon), составляющей менее чем 1×10-4 М-1 с-1, менее чем 2×10-4 М-1 с-1, менее чем 3×10-4 М-1 с-1, менее чем 4×10-4 М-1 с-1, менее чем 5×10-4 М-1 с-1, менее чем 7×10-4 М-1 с-1, менее чем 8×10-4 М-1 с-1, менее чем 9×10-4 М-1 с-1, менее чем 1×10-5 М-1 с-1, менее чем 2×10-5 М-1 с-1, менее чем 3×10-5 М-1 с-1, менее чем 4×10-5 М-1 с-1, менее чем 5×10-5 М" 1 с-1, менее чем 6×10-5 М-1 с-1, менее чем 7×10-5 М-1 с-1, менее чем 8×10-5 М-1 с-1, менее чем 9×10-5 М-1 с-1, менее чем 1×10-6 М-1 с-1, менее чем 2×10-6 М-1 с-1, менее чем 3×10-6 М-1 с-1, менее чем 4×10-6 М-1 с-1, менее чем 5×10-6 М-1 с-1, менее чем 6×10-6 М-1 с-1, менее чем 7×10-6 М-1 с-1, менее чем 8×10-6 М-1 с-1, менее чем 9×10-6 М-1 с-1 или менее чем 1×10-7 М-1 с-1. В определенных вариантах осуществления kon определяется с применением моновалентного антитела, такого как Fab-фрагмент, что измеряется, например, посредством технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления kon определяется с применением бивалентного антитела, что измеряется, например, посредством технологии поверхностного плазмонного резонанса BIAcore®.
[0060] В некоторых вариантах осуществления антиидиотипические антитела связывают мышиный 4G7 и молекулы, полученные из 4G7, со скоростью диссоциации (koff), составляющей менее чем 1×10-2 с-1, менее чем 2×10-2 с-1, менее чем 3×10-2 с-1, менее чем 4×10-2 с-1, менее чем 5×10-2 с-1, менее чем 6×10-2 с-1, менее чем 7×10-2 с-1, менее чем 8×10-2 с-1, менее чем 9×10-2 с-1, менее чем 1×10-3 с-1, менее чем 2×10-3 с-1, менее чем 3×10-3 с-1, менее чем 4×10-3 с-1, менее чем 5×10-3 с-1, менее чем 6×10-3 с-1, менее чем 7×10-3 с-1, менее чем 8×10-3 с-1, менее чем 9×10-3 с-1, менее чем 1×10-4 с-1, менее чем 2×10-4 с-1, менее чем 3×10-4 с-1, менее чем 4×10-4 с-1, менее чем 5×10-4 с-1, менее чем 6×10-4 с-1 менее чем 7×10-4 с-1, менее чем 8×10-4 с-1, менее чем 9×10-4 с-1, менее чем 1×10-5 с-1 или менее чем 5×10-4 с-1. В определенных вариантах осуществления koff определяется с применением моновалентного антитела, такого как Fab-фрагмент, что измеряется, например, посредством технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления koff определяется с применением бивалентного антитела, что измеряется, например, посредством технологии поверхностного плазмонного резонанса BIAcore®.
[0061] В данном документе предусмотрены антиидиотипические антитела (антиидиотипические), которые специфически связываются с клоном 4G7 к CD19 и антигенсвязывающими молекулами, полученными из 4G7, содержащими вариабельную тяжелую цепь (VH), где аминокислотная последовательность или полинуклеотидная последовательность VH выбрана из последовательностей VH, представленных в таблице 1а.


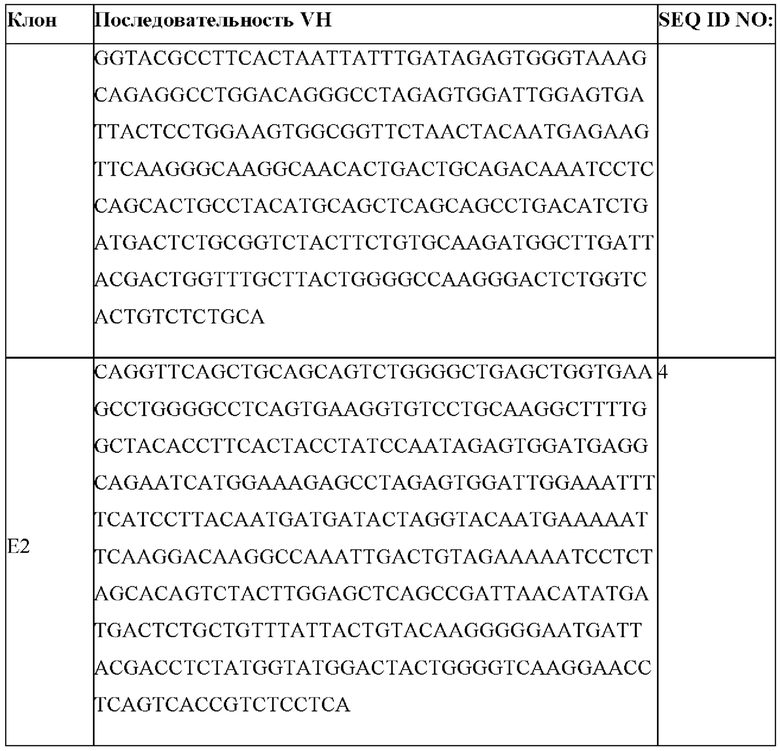
[0062] В данном документе предусмотрены антиидиотипические антитела (антиидиотипические), которые специфически связываются с клоном 4G7 к CD19, содержащие вариабельную легкую цепь (VL), где аминокислотная последовательность или полинуклеотидная последовательность VL выбрана из последовательностей VL, представленных в таблице 1b.



[0063] В данном документе предусмотрены антиидиотипические антитела (антиидиотипические) антитела, которые специфически связываются с клоном 4G7 к CD19 и антигенсвязывающими молекулами, полученными из 4G7, где антиидиотипические антитела содержат вариабельную тяжелую цепь (VH) и вариабельную легкую цепь (VL), где аминокислотная последовательность или полинуклеотидная последовательность VH выбрана из последовательностей VH, представленных в таблице 1а; и где аминокислотная последовательность или полинуклеотидная последовательность VL выбрана из последовательностей VL, представленных в таблице 1b.
[0064] В некоторых вариантах осуществления антиидиотипические антитела (антиидиотипические), которые специфически связываются с клоном 4G7 к CD19 и антигенсвязывающими молекулами, полученными из 4G7, содержат CDR1, CDR2 и CDR3 VH из последовательности VH, представленной в таблице 1а. В некоторых вариантах осуществления CDR1, CDR2 и CDR3 VH выбраны из последовательностей CDR, представленных таблице 1с.
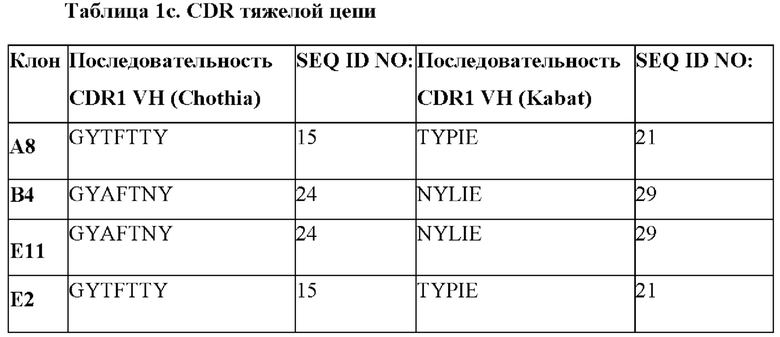
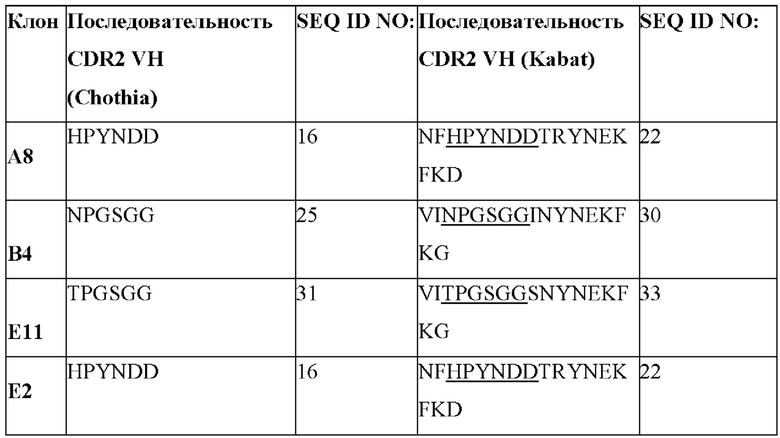
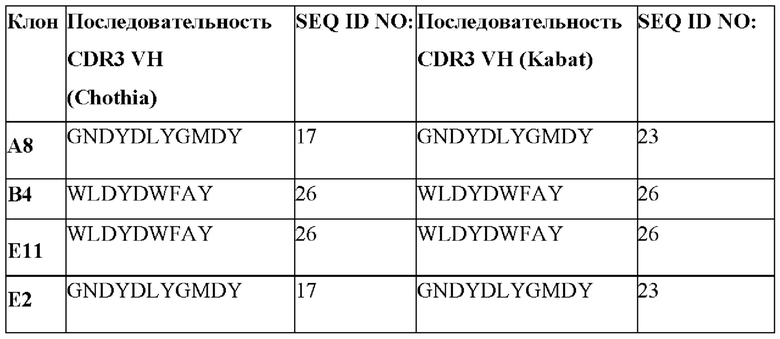
[0065] В некоторых вариантах осуществления антиидиотипические антитела (антиидиотипические), которые специфически связываются с клоном 4G7 к CD19 и антигенсвязывающими молекулами, полученными из 4G7, содержат CDR1, CDR2 и CDR3 VL из последовательности VL, представленной в таблице 1b. В некоторых вариантах осуществления CDR1, CDR2 и CDR3 VH выбраны из последовательностей CDR, представленных таблице 1d.
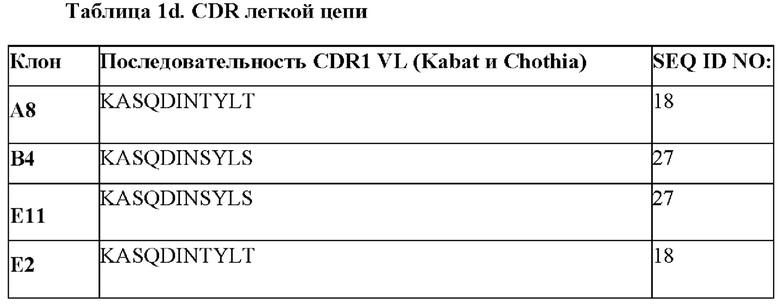
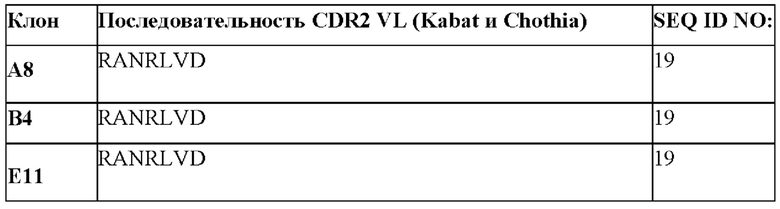


[0066] Последовательности ДНК и аминокислотные последовательности тяжелой цепи и легкой цепи клона А8 показаны ниже:
[0067] Последовательность ДНК тяжелой цепи мышиного IgG1 2153.2Н8А8


(SEQ ID NO: 37)
[0068] Аминокислотная последовательность тяжелой цепи мышиного IgG1 2153.2Н8А8
[0069]

(SEQ ID NO: 38, подчеркнута сигнальная последовательность)
[0070] Аминокислотная последовательность тяжелой цепи мышиного IgG1 2153.2Н8А8 без сигнальной последовательности
[0071]

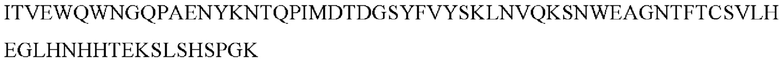
(SEQ ID NO: 39)
[0072] Последовательность ДНК мышиной легкой каппа-цепи 2153.2Н8.А8
[0073]

(SEQ ID NO: 40)
[0074] Аминокислотная последовательность мышиной легкой каппа-цепи 2153.2Н8А8
[0075]

(SEQ ID NO: 41, подчеркнута сигнальная последовательность)
[0076] Аминокислотная последовательность мышиной легкой каппа-цепи 2153.2Н8А8 без сигнальной последовательности
[0077]
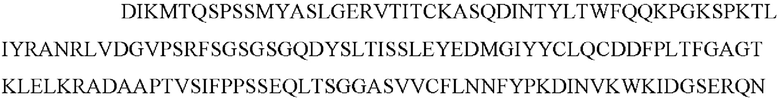
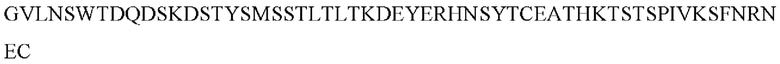
(SEQ ID NO: 42)
[0078] Настоящее изобретение охватывает модификации антиидиотипических антител, содержащие последовательности, показанные в таблицах 1a-1d, в том числе функционально эквивалентные антиидиотипические антитела, содержащие модификации, которые существенно не влияют на их свойства, и варианты, которые характеризуются повышенной или пониженной активностью и/или аффинностью. Например, аминокислотная последовательность может быть мутирована с получением антиидиотипического антитела с требуемой аффинностью связывания с клоном 4G7 к CD19 и антигенсвязывающими молекулами, полученными из 4G7. Модификация поли пептидов является рутинной практикой в данной области техники и поэтому не требует подробного описания в данном документе. Примеры модифицированных полипептидов включают полипептиды с консервативными заменами аминокислотных остатков, одной или более делециями или добавлениями аминокислот, которые существенно не изменяют функциональную активность или которые повышают (усиливают) аффинность полипептида к его лиганду, или применение химических аналогов.
[0079] Вставки аминокислотной последовательности включают амино- и/или карбоксиконцевые слияния длиной от одного остатка до полипептидов, содержащих сто или более остатков, а также вставки внутри последовательности одного или нескольких аминокислотных остатков. Примеры концевых вставок включают антитело с N-концевым метионильным остатком или антитело, слитое с эпитопной меткой. Другие варианты молекулы антитела со вставками включают слияние с N-или С-концом антитела, фермента или полипептида, что увеличивает период полужизни антитела в кровотоке.
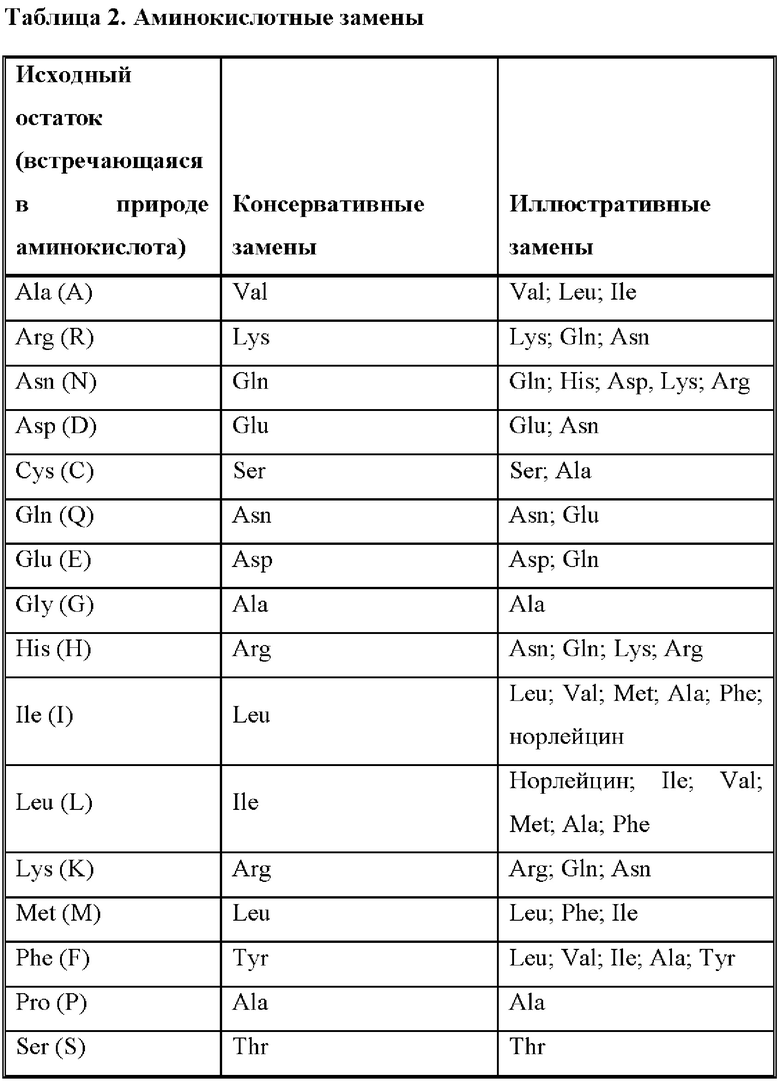
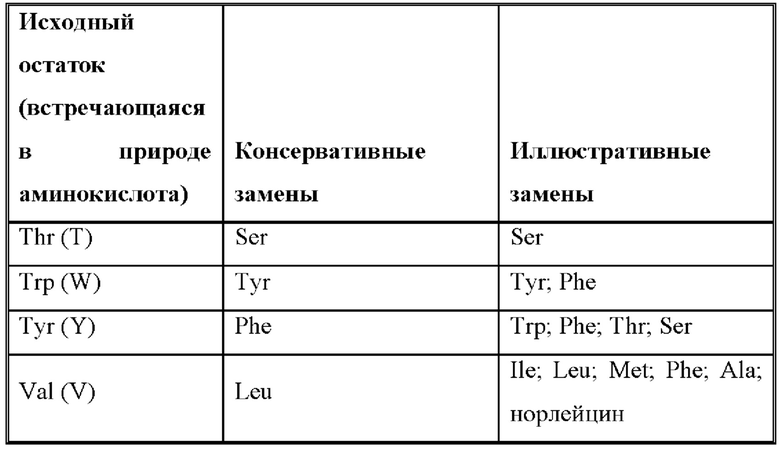
[0080] В вариантах с заменами удален по меньшей мере один аминокислотный остаток в антигенсвязывающем домене и на его место встроен другой остаток. В некоторых вариантах осуществления сайты, представляющие интерес для мутагенеза с заменами, включают гипервариабельные области/CDR, но также рассматриваются изменения FR. Консервативные замены показаны в таблице 2 под названием «консервативные замены». Если такие замены приводят к изменению биологической активности, то могут быть внесены более существенные изменения, обозначенные как «иллюстративные замены» в таблице 2 или как дополнительно описано ниже со ссылкой на классы аминокислот, и продукты подвергаются скринингу.
III. Способы получения антиидиотипических антител
[0081] Для клонирования полинуклеотидов вектор можно ввести в клетку-хозяина (выделенную клетку-хозяина), чтобы обеспечить репликацию самого вектора и таким образом амплифицировать копии содержащегося в нем полинуклеотида. Клонирующие векторы могут содержать компоненты последовательности, обычно включающие без ограничения точку начала репликации, промоторные последовательности, последовательности инициации транскрипции, энхансерные последовательности и селектируемые маркеры. Эти элементы могут быть выбраны соответствующим образом специалистом в данной области техники. Например, точка начала репликации может быть выбрана таким образом, чтобы способствовать автономной репликации вектора в клетке-хозяине.
[0082] В определенных вариантах осуществления настоящее изобретение предусматривает выделенные клетки-хозяева, содержащие вектор, предусмотренный в данном документе. Клетки-хозяева, содержащие вектор, можно использовать для экспрессии или клонирования полинуклеотида, содержащегося в векторе. Подходящие клетки-хозяева могут включать без ограничения прокариотические клетки, клетки грибов, дрожжевые клетки или клетки высших эукариот, такие как клетки млекопитающих. Подходящие прокариотические клетки для этой цели включают без ограничения эубактерии, такие как грамотрицательные или грамположительные организмы, например Enterobacteriaceae, такие как Escherichia, например, E. coli, Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella, например Salmonella typhimurium, Serratia, например Serratia marcescens, и Shigella, а также бациллы, такие как В. subtilis и В. licheniformis, Pseudomonas, например Р. aeruginosa, и Streptomyces.
[0083] Вектор может быть введен в клетку-хозяина с применением любых подходящих способов, известных из уровня техники, включая без ограничения доставку, опосредованную DEAE-декстраном, способ осаждения с фосфатом кальция, доставку, опосредованную катионными липидами, трансфекцию, опосредованную липосомами, электропорацию, бомбардировку микрочастицами, рецептор-опосредованную доставку генов, доставку, опосредованную полилизином, гистоном, хитозаном и пептидами. Стандартные способы трансфекции и трансформации клеток для экспрессии представляющего интерес вектора хорошо известны из уровня техники. В дополнительном варианте осуществления для генетической модификации донорной популяции иммунных эффекторных клеток, где каждый вектор кодирует отличающийся CAR, раскрытый в данном документе, может быть использована смесь различных векторов экспрессии. Полученные трансдуцированные иммунные эффекторные клетки образуют смешанную популяцию сконструированных клеток, при этом часть сконструированных клеток экспрессируют более чем один из различных CAR.
[0084] В одном варианте осуществления настоящее изобретение предусматривает способ оценки сконструированных посредством генной инженерии клеток, экспрессирующих CAR, который нацеливается на белок CD19. В некоторых вариантах осуществления сконструированные клетки оцениваются после размораживания криоконсервированных иммунных клеток.
[0085] В некоторых вариантах осуществления клетки составляются посредством их первоначального сбора из среды для культивирования, а затем промывания и концентрирования клеток в среде и системе контейнеров, подходящих для введения («фармацевтически приемлемый» носитель), в эффективном для лечения количестве. Подходящая инфузионная среда может представлять собой любой состав изотонической среды, стандартный нормальный солевой раствор, Normosol™ R (Abbott) или Plasma-Lyte™ A (Baxter), но также можно использовать 5% декстрозу в воде или лактат Рингера. Инфузионная среда может быть дополнена сывороточным альбумином человека.
[0086] В некоторых аспектах антиидиотипические антитела по настоящему изобретению используются для количественной оценки необходимых количеств клеток для лечения в композиции сконструированных Т-клеток, содержащих CAR, полученный из 4G7, например CAR к CD19 (такой как CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент.В некоторых вариантах осуществления требуемое количество для лечения, как правило, составляет по меньшей мере 2 типа клеток (например по меньшей мере 1 центральную CD8+ Т-клетку памяти и по меньшей мере 1 подгруппу CD4+ хелперных Т-клеток) или, более часто, более чем 102 клеток и до 106 клеток, до 108 или 109 клеток включительно и может составлять более чем 1010 клеток. Количество клеток будет зависеть от требуемого пути применения, для которого предназначена композиция, и типа клеток, содержащихся в ней. Плотность требуемых клеток как правило превышает 106 клеток/мл и как правило превышает 107 клеток/мл, как правило 108 клеток/мл или больше. Клинически значимое количество иммунных клеток может быть разделено на несколько инфузий, которое в совокупности равняется или превышает 105, 106, 107, 108, 109, 1010, 1011 или 1012 клеток. В некоторых аспектах настоящего изобретения, в частности, поскольку все клетки для инфузий будут перенаправлены на конкретный целевой антиген (CD19), можно вводить меньшие количества клеток в диапазоне 106/килограмм (106-1011 на пациента). Средства лечения на основе CAR можно вводить несколько раз в дозах, находящихся в пределах этих диапазонов. Клетки могут быть аутологичными, аллогенными или гетерологичными по отношению к пациенту, проходящему терапию.
[0087] Популяции клеток, экспрессирующие CAR по настоящему изобретению, можно вводить либо отдельно, либо в виде фармацевтической композиции в комбинации с разбавителями и/или с другими компонентами, такими как IL-2 или другие цитокины или популяции клеток. Фармацевтические композиции по настоящему изобретению могут содержать популяцию клеток, экспрессирующих CAR или TCR, такую как Т-клетки, описанные в данном документе, в комбинации с одним или более фармацевтически или физиологически приемлемыми носителями, разбавителями или вспомогательными веществами. Такие композиции могут содержать буферы, такие как нейтральный забуференный солевой раствор, забуференный фосфатом солевой раствор и т.п; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; анти оксид анты; хелатирующие средства, такие как ЭДТА или глутатион; адъюванты (например гидроксид алюминия) и консерванты. Композиции по настоящему изобретению могут быть составлены для внутривенного введения. Фармацевтические композиции (растворы, суспензии и т.п.) могут содержать одно или более из следующего: стерильные разбавители, такие как вода для инъекций, солевой раствор, такой как физиологический солевой раствор, раствор Рингера, изотонический хлорид натрия, нелетучие масла, такие как синтетические моно- или диглицериды, которые могут служить в качестве растворителя или суспендирующей среды, полиэтил енгликоли, глицерин, пропиленгликоль или другие растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабен; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатирующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и средства для регуляции тоничности, такие как хлорид натрия или декстроза. Препарат для парентерального введения может быть заключен в ампулы, одноразовые шприцы или флаконы с многократными дозами, сделанные из стекла или пластика. Фармацевтическая композиция для инъекций может быть стерильной.
IV. Способы определения количеств клеток, экспрессирующих CAR к CD19, полученный из 4G7
[0088] Настоящее изобретение предусматривает способ определения количества клеток, присутствующих в образце, которые экспрессируют CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19 или ALLO-501) или его фрагмент.Например, может быть необходимо определить количество иммунных клеток, присутствующих в образце, полученном от субъекта, которые экспрессируют CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, например, UCART19, или ALLO-501, или ALLO-501A) или его фрагмент.Или может быть необходимо определить количество трансфицированных клеток, экспрессирующих CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, например, UCART19, или ALLO-501, или ALLO-501A) или его фрагмент, что может быть использовано в качестве меры уровня эффективности трансфекции. Раскрытый способ может быть использован в этих и других путях применения, в которых необходимо определить количество клеток, присутствующих в образце, которые экспрессируют представляющую интерес молекулу, такую как CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A) или его фрагмент.
[0089] Таким образом, предусмотрен способ определения количества клеток, представляющих молекулу в образце, где молекула содержит полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент.
[0090] В некоторых вариантах осуществления предусмотрен образец, содержащий клетки, которые, как известно или предполагается, экспрессируют представляющую интерес молекулу, содержащую полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент.
[0091] Затем образец приводится в контакт с антигенсвязывающей молекулой, которая специфически связывает представляющую интерес молекулу, в условиях, которые обеспечивают образование связывающего комплекса, содержащего клетку, присутствующую в образце, и антигенсвязывающую молекулу. Антигенсвязывающая молекула может представлять собой антигенсвязывающую молекулу (или ее фрагмент), раскрытую в данном документе, например, на фигурах, в перечне последовательностей или в настоящем разделе настоящего раскрытия. Любая антигенсвязывающая молекула, которая специфически связывает полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A), или его фрагмент, может использоваться в раскрытом способе. В данном документе предусмотрены многочисленные примеры подходящих антигенсвязывающих молекул, например молекул, которые содержат одну или более CDR, показанных в таблицах 1с и 1d и описанных в данном документе.
[0092] Клетка может представлять собой клетку любого типа и может быть человеческой или отличной от человеческой (например, мыши, крысы, кролика, хомяка и т.д.). В некоторых вариантах осуществления клетка представляет собой иммунную клетку. Иммунная клетка по настоящему способу может представлять собой иммунную клетку любого типа (например, В-лимфоциты, моноциты, дендритные клетки, клетки Лангерганса, кератиноциты, эндотелиальные клетки, астроциты, фибробласты и олигодендроциты). В некоторых вариантах осуществления иммунные клетки представляют собой Т-клетки, в том числе Т-цитотоксические, Т-хелперные и Treg-клетки. В конкретных вариантах осуществления клетки представляют собой Т-клетки, которые можно получить, как описано в данном документе, посредством способов, известных из уровня техники. В этом варианте осуществления раскрытого способа можно использовать любой тип иммунной клетки, и клетка может быть человеческой клеткой или клеткой, отличной от человеческой (включая как прокариотические, так и эукариотические клетки). Иллюстративные клетки включают без ограничения иммунные клетки, такие как Т-клетки, лимфоциты, инфильтрирующие опухоль (TIL), NK-клетки, TCR-экспрессирующие клетки, дендритные клетки и NK-T-клетки. Т-клетки могут быть аутологичными, аллогенными или гетерологичными. В дополнительных вариантах осуществления клетки представляют собой Т-клетки, представляющие CAR. Т-клетки могут представлять собой CD4+ Т-клетки или CD8+ Т-клетки. При применении Т-клетки в раскрытых способах Т-клетка может представлять собой Т-клетку in vivo или Т-клетку in vitro. Более того, клетки могут находиться в любой среде или быть выделенными из любой среды, способной поддерживать клетки в жизнеспособной форме, такой как кровь, ткань или любой другой образец, полученный от субъекта, среды для культивирования клеток, ткани, выращенные ех vivo, подходящий буфер и т.п.
[0093] В некоторых вариантах осуществления образец, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, приводится в контакт с раскрытым в данном документе антиидиотипическим антителом, которое специфически связывает связывающую молекулу, полученную из 4G7. В некоторых вариантах осуществления антиидиотипическое антитело содержит выявляемую метку. В некоторых вариантах осуществления конъюгированное с выявляемой меткой антиидиотипическое антитело приводится в контакт с образцом, экспрессирующим CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A), в условиях, которые обеспечивают образование связывающего комплекса, содержащего клетку, присутствующую в образце, и антиидиотипическое антитело. В раскрытом способе можно использовать любое антиидиотипическое антитело, которое специфически связывает CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A). В данном документе предусмотрены многочисленные примеры подходящих антиидиотипических антител, например антител, которые содержат одну или более CDR, показанных в таблице 1с или 1d.
[0094] В способах, описанных в данном документе, можно использовать любую выявляемую метку, и подходящие метки могут быть выбраны с применением желаемого набора критериев. Примеры типов выявляемых меток включают флуоресцентные метки (например, флуоресцеин, родамин, тетраметилродамин, эозин, эритрозин, кумарин, метилкумарины, пирен, Malachite green, стильбен, Lucifer Yellow, Cascade Blue, Texas Red, IAEDANS, EDANS, BODIPY FL, LC Red 640, Cy 5, Cy 5.5, LC Red 705, Oregon green, красители Alexa-Fluor (Alexa Fluor 350, Alexa Fluor 430, Alexa Fluor 488, Alexa Fluor 546, Alexa Fluor 568, Alexa Fluor 594, Alexa Fluor 633, Alexa Fluor 647, Alexa Fluor 660, Alexa Fluor 680), Cascade Blue, Cascade Yellow и R-фикоэритрин (РЕ) (Molecular Probes), FITC, родамин и Texas Red (Pierce), Cy5, Cy5.5, Cy7 (Amersham Life Science) Подходящие оптические красители, в том числе флуорофоры, описаны в Johnson, Molecular Probes Handbook: A Guide to Fluorescent Probes and Labeling Techniques, 11th Edition, Life Technologies, (2010), настоящим явным образом включенном посредством ссылки, радиоактивные метки (например изотопные маркеры, такие как 3Н, 11С, 14С, 15N, 18F, 35S, 64CU, 90Y, 99Tc, 111In, 124I, 125I, 131I), фотохромные соединения, Halo-метка, красители Atto, красители Tracy, белковые флуоресцентные метки (например белковые флуоресцентные метки также включают без ограничения зеленый флуоресцентный белок, включая GFP из видов Renilla, Ptilosarcus или Aequorea (Chalfie et al., (1994) Science 263: 802-805), EGFP (Clontech Labs., Inc., номер доступа в Genbank U55762), синий флуоресцентный белок (BFP, Quantum Biotechnologies, Inc; Stauber, (1998) Biotechniques 24: 462-471; Heim et al., (1996) Curr. Biol 6: 178-182), усиленный желтый флуоресцентный белок (Clontech Labs., Inc.), люциферазу (Ichiki et al., (1993) J. Immunol 150: 5408-5417), магнитные метки (например DYNABEADS) и т.п. Стратегии мечения белков хорошо известны из уровня техники и могут быть использованы в раскрытом способе. См., например, Obermaier et al, (2015) Methods Mol Biol 1295: 153-65; Strack (2016) Nature Methods 13: 33; Site-Specific Protein Labeling: Methods and Protocols. (Gautier and Hinner, eds.) 2015, Springer. В некоторых вариантах осуществления выявляемая метка представляет собой флуоресцентный зонд на основе фикоэритрина (РЕ) или аллофикоцианина (АРС).
[0095] Метка может быть связана с антиидиотипическим антителом в любом положении в молекуле, хотя может потребоваться связать метку с антителом в положении (или положениях, если используется несколько меток) в такой точке, чтобы связывающие свойства молекулы не изменялись (если не требуется такая модифицированная связывающая активность). Может использоваться любая антигенсвязывающая молекула, которая специфически связывает связывающую молекулу, полученную из 4G7 (или ее фрагмент), такую как молекулы, описанные в данном документе, например молекулы, содержащие одну или более CDR, показанных в таблице 1с или 1d.
[0096] Антигенсвязывающая молекула может находиться на любой поверхности или может не находиться на поверхности. Например, антигенсвязывающая молекула может присутствовать в буфере, и система буфер-антигенсвязывающая молекула может быть приведена в контакт с образцом. В качестве альтернативы, антигенсвязывающая молекула может быть ассоциирована с поверхностью. Подходящие поверхности включают агарозные гранулы, магнитные гранулы, такие как DYNABEADS®, или пластиковый, стеклянный или керамический планшет, такой как планшет с лунками, пакет, например пакет для культивирования клеток, и т.п. Сама поверхность может быть расположена в другой структуре, такой как колонка.
[0097] Условия, которые обеспечивают образование связывающего комплекса, будут зависеть от множества факторов, однако как правило водные буферы при физиологических рН и ионной силе, такие как фосфатно-солевой буферный раствор (PBS), будут способствовать образованию связывающих комплексов и являются желательными в раскрытом способе.
[0098] Определяется количество клеток, присутствующих в связывающем комплексе в образце. Конкретный способ, используемый для определения количества клеток, присутствующих в связывающем комплексе, будет зависеть от природы выбранной метки. Например, при выборе флуоресцентной метки можно использовать FACS; при выборе изотопной метки можно использовать масс-спектрометрию, ЯМР или другую методику; при выборе магнитной метки можно использовать магнитную сортировку клеток; также можно использовать микроскопию. Данные, полученные посредством данных способов выявления, могут быть в виде количества клеток или данные могут быть в виде, который позволяет вычислить количество клеток на основании полученных данных.
V. Способы определения наличия или отсутствия CAR к CD19, полученного из 4G7
[0099] В некоторых вариантах осуществления достаточной информацией является информация о том, присутствует или отсутствует в образце молекула, содержащая CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19 или ALLO-501) или его фрагмент. Например, может быть полезно знать, что такая молекула экспрессируется, независимо от уровня экспрессии. В других случаях может потребоваться знать, были ли эффективными способ или стадия очистки, разработанные для удаления такой молекулы. Таким образом, качественное определение присутствия или отсутствия CAR к CD19 (например CAR, содержащего scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмента может быть полезным во многих путях применения.
[00100] В некоторых вариантах осуществления предусмотрен способ определения присутствия или отсутствия в образце полипептида, содержащего CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, в образце.
[00101] В некоторых вариантах осуществления способ включает получение образца, который, как известно или предполагается, содержит полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A), или его фрагмент.
[00102] Настоящее изобретение предусматривает антигенсвязывающую молекулу, которая специфически связывает полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, которые содержат выявляемую метку. Подходящие метки могут быть выбраны с применением желаемого набора критериев. Примеры типов выявляемых меток включают флуоресцентные метки (например, флуоресцеин, родамин, тетраметилродамин, эозин, эритрозин, кумарин, метилкумарины, пирен, Malachite green, стильбен, Lucifer Yellow, Cascade Blue, Texas Red, IAEDANS, EDANS, BODIPY FL, LC Red 640, Cy 5, Cy 5.5, LC Red 705, Oregon green, красители Alexa-Fluor (Alexa Fluor 350, Alexa Fluor 430, Alexa Fluor 488, Alexa Fluor 546, Alexa Fluor 568, Alexa Fluor 594, Alexa Fluor 633, Alexa Fluor 647, Alexa Fluor 660, Alexa Fluor 680), Cascade Blue, Cascade Yellow и R-фикоэритрин (РЕ) (Molecular Probes), FITC, родамин и Texas Red (Pierce), Cy5, Cy5.5, Cy7 (Amersham Life Science)). Подходящие оптические красители, в том числе флуорофоры, описаны в Johnson, Molecular Probes Handbook: A Guide to Fluorescent Probes and Labeling Techniques, 11th Edition, Life Technologies, (2010), настоящим явным образом включенным посредством ссылки, радиоактивные метки (например изотопные маркеры, такие как 3Н, 11С, 14С, 15N, 18F, 35S, 64CU, 90Y, 99Tc, 111In, 124I, 125I, 131I). Также могут быть использованы фотохромные соединения, Halo-метка, красители Atto, красители Tracy, белковые флуоресцентные метки (например белковые флуоресцентные метки также включают без ограничения зеленый флуоресцентный белок, в том числе GFP из видов Renilla, Ptilosarcus или Aequorea (Chalfie et al., (1994) Science 263: 802-805), EGFP (Clontech Labs, Inc., номер доступа в Genbank U55762), синий флуоресцентный белок (BFP, Quantum Biotechnologies, Inc.; Stauber, (1998) Biotechniques 24:462-471; Heim et al., (1996) Curr. Biol. 6: 178-182), усиленный желтый флуоресцентный белок (Clontech Labs, Inc.), люциферазу (Ichiki et al., (1993) J. Immunol. 150: 5408-5417), магнитные метки (например DYNABEADS®) и т.п. Стратегии мечения белков хорошо известны из уровня техники и могут быть использованы в раскрытых способах. Метка может быть связана с антигенсвязывающей молекулой в любом положении в молекуле, хотя может потребоваться связать метку с молекулой в положении (или положениях, если используется несколько меток) в такой точке, чтобы связывающие свойства молекулы не изменялись (если не требуется такая модифицированная связывающая активность). Можно использовать любую антигенсвязывающую молекулу, которая специфически связывает полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A) или его фрагмент, такую как молекулы, раскрытые в данном документе, например молекулы, содержащие одну или более CDR, описанных в таблицах 1 с и Id.
[00103] Затем образец приводится в контакт с антигенсвязывающей молекулой в условиях, которые обеспечивают образование связывающего комплекса, содержащего клетку, присутствующую в образце, и антигенсвязывающую молекулу.
[00104] Образец приводится в контакт с антигенсвязывающей молекулой в условиях, которые обеспечивают образование связывающего комплекса между полипептидом, содержащим CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, и антигенсвязывающей молекулой. Условия, которые обеспечивают образование связывающего комплекса, будут зависеть от множества факторов. Поскольку составные части связывающего комплекса могут находиться на поверхностях, как описано в данном документе, образованные связывающие комплексы также могут находиться на поверхностях.
[00105] На этой стадии может не образоваться связывающих комплексов или может образоваться множество связывающих комплексов, содержащих одну или более антигенсвязывающих молекул, связанных с полипептидом, содержащим CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A) или его фрагмент. Несвязанные молекулы, содержащие CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, и/или несвязанные антигенсвязывающие молекулы, также могут присутствовать в локальном окружении любых образованных связывающих комплексов.
[00106] Затем любые молекулы, не являющиеся частью связывающего комплекса, отделяются от любых образованных связывающих комплексов. Способ удаления будет зависеть от структуры и/или локального окружения связывающих комплексов. Например, если антигенсвязывающая молекула находится на грануле, в планшете или пакете, несвязанные компоненты реакционной смеси могут быть смыты с применением раствора, который оставляет образованные связывающие комплексы нетронутыми. В некоторых вариантах осуществления для выявления не требуется отделение связывающего комплекса.
[00107] Раствор, используемый для индукции образования связывающих комплексов, можно использовать, например, в качестве промывочного раствора для удаления несвязанных компонентов. Также можно использовать любой подходящий буфер или раствор, который не разрушает образованные связывающие комплексы. Как правило, при выполнении этой стадии способа следует избегать использования буферов с высокими концентрациями солей, нефизиологическим рН, содержащих хаотропы или денатурирующие вещества.
[00108] Может быть выявлено присутствие или отсутствие связывающего комплекса, который будет содержать полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, и антигенсвязывающую молекулу. Конкретный способ, используемый для выявления присутствия или отсутствия связывающего комплекса, как правило, будет зависеть от природы выбранной метки. В некоторых вариантах осуществления способ выявления представляет собой колориметрический анализ. Результатом способа является качественная оценка присутствия или отсутствия антигенсвязывающей молекулы, содержащей выявляемую метку, и, таким образом, присутствия или отсутствия ее партнера по связыванию, полипептида, содержащего CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501A) или его фрагмент.
[00109] Как и в случае с раскрытыми способами, полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, может находиться в любой среде. В некоторых вариантах осуществления полипептид, содержащий CAR к CD19 (например CAR, содержащий scFv, полученный из 4G7, такой как UCART19, или ALLO-501, или ALLO-501А) или его фрагмент, экспрессируется на поверхности клетки. В этом варианте осуществления клетка может представлять собой клетку любого типа и может быть человеческой или отличной от человеческой (например, мыши, крысы, кролика, хомяка и т.д.). В некоторых вариантах осуществления клетка представляет собой иммунную клетку. Иммунная клетка по настоящему способу может представлять собой иммунную клетку любого типа (например, В-лимфоциты, моноциты, дендритные клетки, клетки Лангерганса, кератиноциты, эндотелиальные клетки, астроциты, фибробласты и олигодендроциты). Особенно подходящими являются Т-клетки (в том числе Т-цитотоксические, Т-хелперные и Treg-клетки). В конкретных вариантах осуществления клетки представляют собой Т-клетки, которые можно получить, как описано в данном документе, посредством способов, известных из уровня техники. В этом варианте осуществления раскрытого способа можно использовать любой тип иммунной клетки, и клетка может быть человеческой клеткой или клеткой, отличной от человеческой. Иллюстративные клетки включают без ограничения иммунные клетки, такие как Т-клетки, лимфоциты, инфильтрирующие опухоль (TIL), NK-клетки, дендритные клетки и NK-T-клетки. Т-клетки могут быть аутологичными, аллогенными или гетерологичными. В дополнительных вариантах осуществления клетки представляют собой Т-клетки, представляющие TCR. Т-клетки могут представлять собой CD4+ Т-клетки или CD8+ Т-клетки. При применении Т-клетки в раскрытых способах Т-клетка может представлять собой Т-клетку in vivo или Т-клетку in vitro. Кроме того, клетки могут быть получены из стволовой клетки, такой как iPSC-клетка, клетка пуповинной крови или мезенхимальная стволовая клетка.
[00110] В некоторых вариантах осуществления клетка может находиться в любой среде или быть выделена из любой среды, способной поддерживать клетку в жизнеспособной форме, такой как кровь, ткань или любой другой образец, полученный от субъекта, среды для культивирования клеток, ткани, выращенные ех vivo, подходящий буфер и т.п. В некоторых вариантах осуществления клетка находится в образце, фиксированном формалином. В некоторых вариантах осуществления образец представляет собой фиксированную формалином ткань, заключенную в парафин (FFPE).
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[00111] Все публикации, патенты и заявки на патент, упомянутые в данном описании, включены в данный документ посредством ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент конкретно и отдельно была включена посредством ссылки. Однако цитирование ссылки в данном документе не должно толковаться как признание того, что такая ссылка является предшествующим уровнем техники для настоящего изобретения. В той степени, в которой любые определения или термины, приведенные в ссылках, включенных посредством ссылки, отличаются от терминов и обсуждения, приведенных в данном документе, настоящие термины и определения имеют преимущественную силу.
[00112] Вышеизложенное письменное описание считается достаточным, чтобы дать возможность специалисту в данной области техники осуществить настоящее изобретение на практике. Вышеприведенные описание и примеры, приведенные ниже, подробно описывают определенные варианты осуществления настоящего изобретения и описывают лучший способ, предлагаемый авторами настоящего изобретения. Однако будет понятно, что независимо от того, насколько подробно изложенное выше может быть представлено в тексте, настоящее изобретение может быть реализовано на практике посредством многих способов, и настоящее изобретение следует истолковывать в соответствии с прилагаемой формулой изобретения и любыми ее эквивалентами.
ПРИМЕРЫ
Пример 1. Получение антиидиотипических антител к клону 4G7 антитела к CD19 человека
[00113] Мышей Balb/c иммунизировали слитым белком 4G7-Fab человека-8xHis (E2153).("8xHis" раскрыт под SEQ ID NO: 45). Получали и клонировали гибридомы и секретируемые антитела подвергали скринингу в отношении специфичности связывания с 4G7. Шесть полученных субклонов Е2153 (Е2153.1С4.Е2, E2153.1D9.B4, E2153.1G5.H5, Е2153.2Н8.А8, Е2153.3 В11.В7, E2153.4D7.E11) очищали для дальнейшего анализа. Клоны антител идентифицировали и отбирали на основании их способности специфически связывать scFv, полученный из 4G7, в CAR UCART19 и ALLO-501.
Пример 2. Кинетический анализ антиидиотипических антител к клону 4G7 антитела к CD19 человека
[00114] Очищенные субклоны антител к m4G7 тестировали в отношении связывания с m4G7-hFab. Блокирующий эффект определяли с применением сэндвич-анализа и подтверждение связывания с m4G7-scFv-Fc определяли с применением анализа Biacore при 25°С. Пять очищенных антиидиотипических субклонов из слитого белка Е2153 демонстрируют связывание с m4G7-hFab. В качестве поверхности использовали сенсорный чип CAP (CAPture chip) №505. После регидратации сенсорного чипа САР водой при 42°С в течение 1 часа чип высушивали сжатым воздухом. Поверхность чипа кондиционировали с применением трех 1-минутных инъекций регенерирующего раствора со скоростью 10 мкл/мин. Раствор для регенерации содержал 3 части исходного раствора для регенерации 1 (8 М гуанидин-HCl) с 1 частью исходного раствора для регенерации 2 (1 М NaOH). За захватом реагента Biotin CAPture в течение 5 минут при 2 мкл/мин следовал захват биотинилированных очищенных субклонов антител Fusion Е2153 к m4G7 и контрольных антител при 10 мкг/мл в течение 1 мин при 10 мкл/мин. Как показано на ФИГ. 1, все биотинилированные антиидиотипические субклоны хорошо захватывались чипом CAPture.
[00115] Блокирование проводили с помощью 20 мкМ амин-РЕО-биотина в течение 1 мин при 10 мкл/мин. Поверхности регенерировали регенерирующим раствором (смесь из 3 частей регенерирующего исходного раствора 1 (8 М гуанидин-HCl) с 1 частью регенерирующего исходного раствора 2 (1 М NaOH)) в течение 2 минут при 10 мкл/мин. 6 очищенных антиидиотипических субклонов из слитого белка Е2153 от мышей Balb/c, иммунизированных с помощью m4G7-hFab, содержали Е2153.1С4.Е2 (0,51 мг/мл), E2153.1D9.B4 (0,41 мг/мл), E2153.1G5.H5 (0,37 мг/мл), Е2153.2Н8.А8 (0,45 мг/мл), Е2153.3 В11.В7 (0,49 мг/мл) и E2153.4D7.E11 (0,35 мг/мл).
[00116] Для кинетического анализа в указанных концентрациях также использовали следующие реагенты:
• m4G7-hFab: m4G7 hFab 8xHis, 0,92 мг/мл ("8xHis" раскрыт под SEQ ID NO: 45)
• m4G7-scFv-Fc: 0,8 мг/мл, предполагаемая молекулярная масса 52 кДа
• hCD19: hCD19-HIS-AVI, 33,386 кДа, предположительно активен на 18,4% по CFCA (активная концентрация 0,736 мкМ)
• каркасная область, контроль: контроль соответствия каркасной области для m4G7-Fab, 0,82 мг/мл
• a-hKappa: контроль: биотинилированный мышиный IgG1 к каппа-цепи человека - моноклональный, Southern Biotech, 0,5 мг/мл
• a-His: контроль: контрольное биотинилированное мышиное антитело к His. № по кат. R&D systems МАВ050В
[00117] Для анализа кинетики буфер и m4G7-hFab при 1 нМ, 10 нМ и 100 нМ вводили в течение 2 мин при 30 мкл/мин с последующей диссоциацией в течение 5 мин. Краткое описание кинетики связывания показано в таблице 3. Кинетические соответствия связывания m4G7-hFab с 6 очищенными антиидиотипическими субклонами из слитого белка Е2153 при 25°С показаны на ФИГ. 2А. Кинетические соответствия связывания m4G7-hFab с буфером в качестве отрицательного контроля при 25°С показаны на ФИГ. 2В.

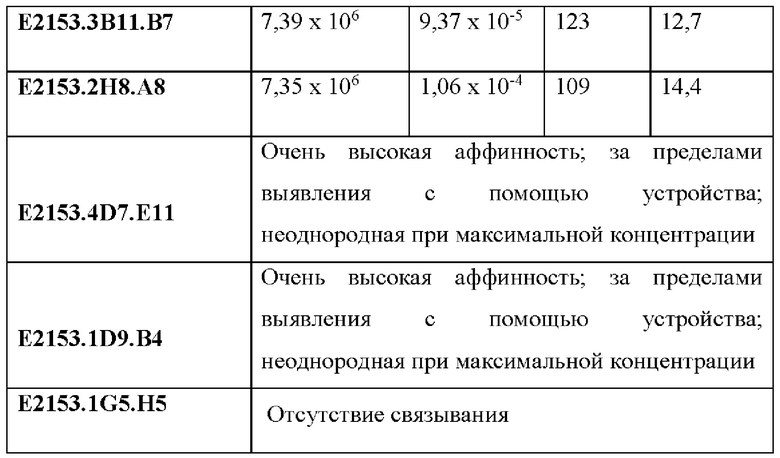
[00118] Для проверки связывания с контролем соответствия каркасной области для m4G7-hFab и m4G7-scFv-Fc вводили буфер, контроль соответствия каркасной области для m4G7-hFab при 100 нМ, m4G7-scFv-Fc при 100 нМ и m4G7-hFab при 100 нМ в течение 2 мин при 30 мкл/мин с последующей диссоциацией в течение 5 мин. Шесть очищенных антиидиотипических субклонов из слитого белка Е2153 не связывались с контролем соответствия каркасной области для m4G7-hFab. Кроме того, все антиидиотипические субклоны, за исключением Е2153.1G5.H5, связываются с m4G7-scFv-Fc. В таблице 4 обобщены определения связывания контроля соответствия каркасной области для m4G7-hFab и m4G7-scFv-Fc с очищенными антиидиотипическими субклонами из слитого белка Е2153 при 25°С.
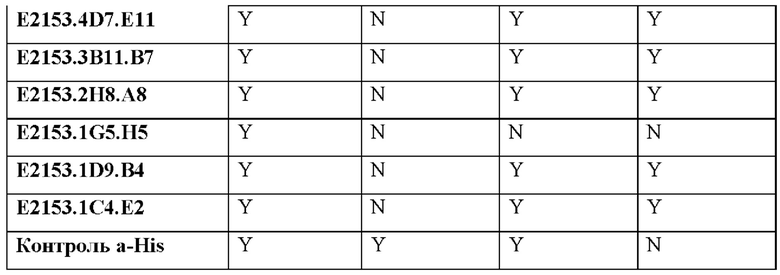
[00119] Блокирующий эффект связывания m4G7-hFab с hCD19 с помощью очищенных антиидиотипических субклонов из слитого белка Е2153 определяли посредством сэндвич-анализа при 25°С. Образец 1 вводили в течение 2 мин при 30 мкл/мин, затем в течение 10 сек в буфере, затем образец 2 вводили в течение 2 мин при 30 мкл/мин с последующей диссоциацией в течение 3 минут:
[00120]
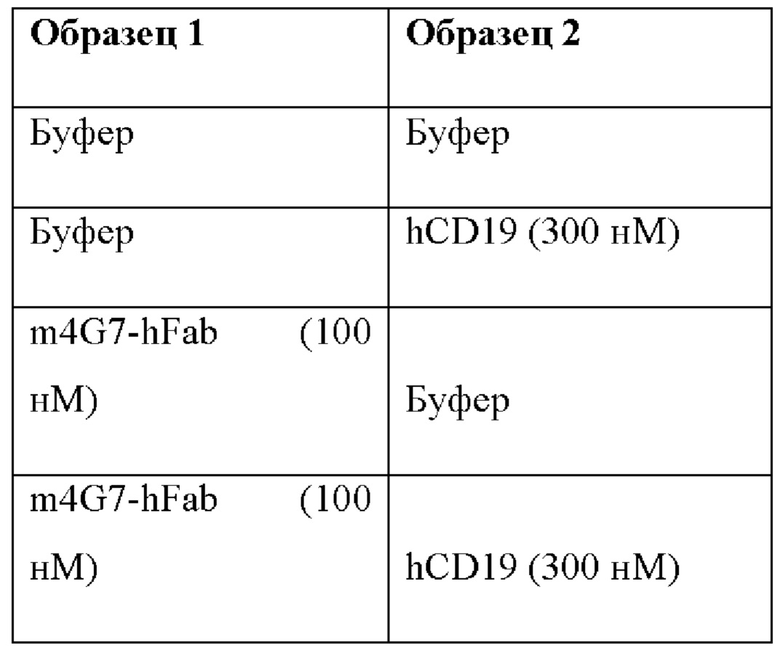
[00121] Как показано в таблице 5, сэндвичи с hCD19 не наблюдались ни с одним из антиидиотипических очищенных суб клонов m4G7. Эти данные свидетельствуют о том, что антиидиотипические субклоны не связываются с hCD19.
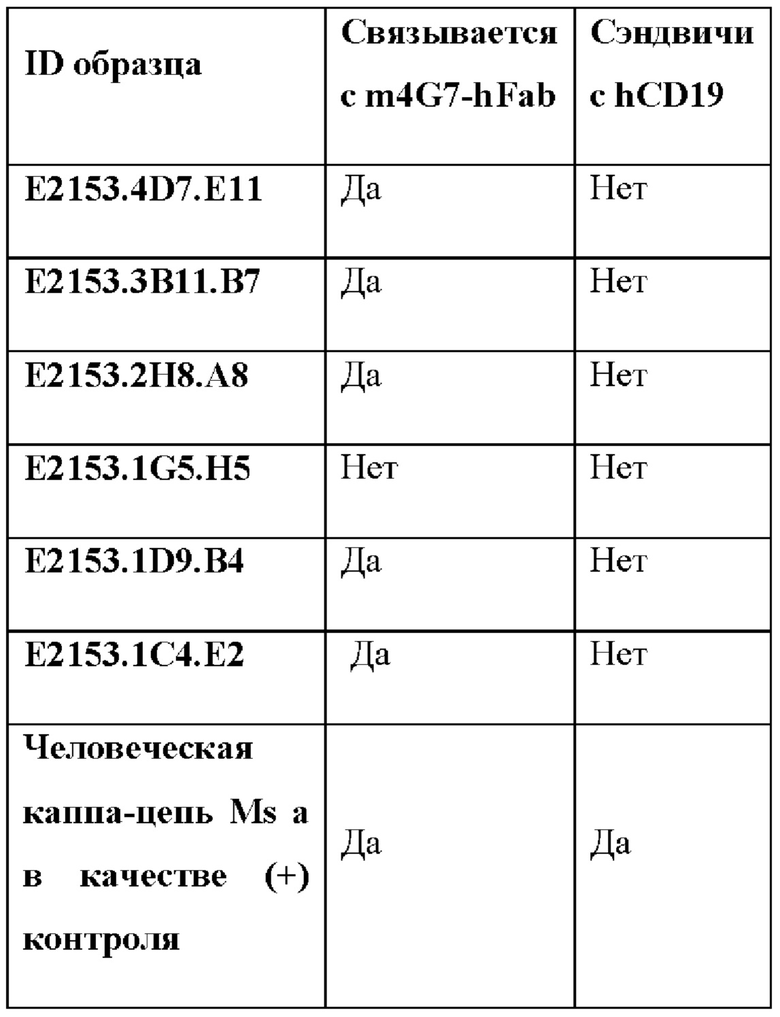
Пример 3. Сравнение антител к UCART19
[00122] Коммерчески доступное антитело к мышиному F(ab')2 от Jackson Immunoresearch и антитела А8 и Е11, описанные в примерах 1 и 2, тестировали при четырех концентрациях UCART19 (интактный контроль, 100000 клеток на мл в крови, 1 миллион клеток на мл в крови и 10 миллионов клеток на мл в PBS). Иллюстративные графики проточной цитометрии показаны на ФИГ. 3А и 3В. В пробирке А содержалась кровь здорового добровольца; пробирка В: кровь здорового добровольца + 100000 трансдуцированных клеток UCART19 на мл; пробирка С: кровь здорового добровольца + 1 миллион трансдуцированных клеток UCART19 на мл, и пробирка D: 10 миллионов трансдуцированных клеток UCART19 на мл.
[00123] Антитело А8 позволяет выявить клетки, положительные по UCART19, в отсутствие неспецифического связывания. Антитело Е11 демонстрирует слабое неспецифическое связывание. Антитела А8 и E11 генерируют сильный положительный сигнал РЕ, позволяющий четко различать клетки, положительные и отрицательные по UCART19. Десятикратное повышение % CAR+ клеток наблюдается между пробирками В и С для выявления с помощью антитела А8 и E11. Для пробирки D наблюдается 20-кратное повышение, а не ожидаемое 10-кратное повышение.
Пример 4. Блокирование UCART19
[00124] Свежие клетки UCART19 окрашивали посредством серийных разбавлений неконъюгированного идиотипического антитела А8 к UCART19 (Е2153.2Н8.А8) и неконъюгированного мышиного IgG1 в качестве изотипического контроля. Клетки инкубировали при 4°С в течение 20 мин с последующим промыванием буфером для окрашивания BD FACS. Вторичное окрашивание проводили с помощью растворимого CD19-hFc, конъюгированного с AF647, в течение 20 мин при 4°С. Клетки промывали буфером для окрашивания BD FACS с последующей проточной цитометрией. Как показано на ФИГ. 4А-4С, антитело к UCART19 блокирует связывание APC-sCD19. На ФИГ. 4В и 4С показаны графики проточной цитометрии с повышающейся концентрацией АЬ идиотипа А8 (Е2153.2Н8.А8) (ФИГ. 4В) и изотипический контроль, представляющий собой неконъюгированный мышиный IgG1 (ФИГ. 4С).
[00125] Блокирование клеток UCART19 антиидиотипическим антителом А8 также оценивали на размороженных клетках UCART19. Целевые клетки Raji-Luc-GFP высевали в количестве 5000 клеток/лунка в 50 мкл. Клетки UCART19 размораживали и оставляли для восстановления при 37°С в течение 1 часа. После восстановления концентрацию UCART19 регулировали до соотношений эффектор:мишень (Е:Т), составляющих 5:1 и 10:1, с применением данных по CAR % на день 13. Клетки UCART19 инкубировали при 37°С в течение 30 минут с применением различных концентраций антитела (антиидиотипическое антитело m4G7 и антитело изотипа IgG1). Каждое соотношение наносили в трех повторностях на Raji-Luc-GFP. Смесь клеток инкубировали при 37°С в течение приблизительно 24 часов. В каждую лунку добавляли 100 мкл реагента Promega Bright Glo, перемешивали, инкубировали при комнатной температуре в течение 3 минут и затем считывали на люминометре. Целевые клетки нормализовывали до 0% лизиса и % лизиса рассчитывали с применением только целевых клеток. На ФИГ. 4D и 4Е показана блокирующая способность антиидиотипического m4G7 (А8) при соотношениях Е:Т, составляющих 5:1 и 10:1 соответственно.
Пример 5. Связывание антиидиотипических антител с химерными антигенными рецепторами, полученными из 4G7
[00126] Этот пример демонстрирует специфическое связывание антиидиотипических антител как с CAR из человеческого h4G7.7, так и с CAR из мышиного m4G7. Как показано на ФИГ. 5А, антиидиотипические антитела, описанные в данном документе, связываются с клетками Jurkat, экспрессирующими CAR с scFv, полученным из мышиного 4G7 (m4G7) и гуманизированного 4G7 (h4G7.7). Антиидиотипические антитела по настоящему изобретению не связываются с CAR с мышиным scFv FMC63 к CD19 (не родственным 4G7) или ВС40, человеческим scFv к ВСМА. Связывание sCD19-Fc со всеми CAR к CD19, экспрессируемыми на клетках Jurkat, использовали в качестве положительного контроля (ФИГ. 5В).
[00127] Связывание антиидиотипических антител с CAR к CD19, экспрессируемыми на первичных Т-клетках человека. Антиидиотипические антитела демонстрируют специфическое связывание как с h4G7.7, так и с UCART19, экспрессируемыми на первичных Т-клетках человека, но не связываются с CAR (CTL-019), полученным из FMC63 (ФИГ. 6А). Связывание sCD19-Fc со всеми CAR к CD19, экспрессируемыми на первичных Т-клетках человека, использовали в качестве положительного контроля (ФИГ. 6В).
Пример 6. Конъюгация флуоресцентных зондов для FACS-анализа с антиидиотипическими антителами
[00128] Как показано на ФИГ. 7, клон А8 продемонстрировал лучшее соотношение сигнал/шум при меньшем тестируемом объеме, чем другие антиидиотипические антитела. Антиидиотипические антитела конъюгировали с флуоресцентными зондами на основе фикоэритрина (РЕ) или аллофикоцианина (АРС) для применения в качестве реагента для FACS-анализа. Как продукт конъюгации с АРС, так и конъюгированное с РЕ антитело А8 позволяли выявить UCART19, однако клон А8, конъюгированный с АРС, характеризовался индексом окрашивания, составляющим 102, а антитело А8, конъюгированное с РЕ, характеризовалось индексом окрашивания, составляющим 82 (фиг. 8). При конъюгации с ярким флуорохромом (например РЕ или АРС) А8 окрашивает клетки UCART19 или ALLO-501 с высоким MFI и низким фоном.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> АЛЛОДЖЕН ТЕРАПЬЮТИКС, ИНК.
<120> АНТИТЕЛА К ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРАМ, ПОЛУЧЕННЫМ ИЗ 4G7
<130> AT-020/02WO
<140>
<141>
<150> 62/836,242
<151> 2019-04-19
<160> 45
<170> Версия PatentIn 3.5
<210> 1
<211> 120
<212> БЕЛОК
<213> Mus musculus
<400> 1
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Phe Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Pro Ile Glu Trp Met Arg Gln Asn His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asn Phe His Pro Tyr Asn Asp Asp Thr Arg Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Ala Lys Leu Thr Val Glu Lys Ser Ser Ser Thr Val Tyr
65 70 75 80
Leu Glu Leu Ser Arg Leu Thr Tyr Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Gly Asn Asp Tyr Asp Leu Tyr Gly Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 2
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 2
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Thr
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr
20 25 30
Leu Ile Glu Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Asn Pro Gly Ser Gly Gly Ile Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Trp Leu Asp Tyr Asp Trp Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 3
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 3
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Thr
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr
20 25 30
Leu Ile Glu Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Thr Pro Gly Ser Gly Gly Ser Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Trp Leu Asp Tyr Asp Trp Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 4
<211> 360
<212> ДНК
<213> Mus musculus
<400> 4
caggttcagc tgcagcagtc tggggctgag ctggtgaagc ctggggcctc agtgaaggtg 60
tcctgcaagg cttttggcta caccttcact acctatccaa tagagtggat gaggcagaat 120
catggaaaga gcctagagtg gattggaaat tttcatcctt acaatgatga tactaggtac 180
aatgaaaaat tcaaggacaa ggccaaattg actgtagaaa aatcctctag cacagtctac 240
ttggagctca gccgattaac atatgatgac tctgctgttt attactgtac aagggggaat 300
gattacgacc tctatggtat ggactactgg ggtcaaggaa cctcagtcac cgtctcctca 360
<210> 5
<211> 354
<212> ДНК
<213> Mus musculus
<400> 5
caggtccagc tgcagcagtc tggagctgaa ctggtaaggc ctgggacttc agtgaaggtg 60
tcctgcaagg cttctggata cgccttcact aattatttga tagagtggat aaagcagagg 120
cctggacagg gccttgagtg gattggagtg attaatcctg gaagtggtgg tattaattat 180
aatgagaagt tcaagggcaa ggcaacactg acttcagaca aatcctccag cactgcctac 240
atgcagctca gcagcctgac atctgatgac tctgcggtct atttctgtgc aagatggctt 300
gattacgact ggtttgctta ctggggccaa gggactctgg tcactgtctc tgca 354
<210> 6
<211> 354
<212> ДНК
<213> Mus musculus
<400> 6
caggtccagc tgcagcagtc tggagctgag ctggtaaggc ctgggacttc agtgaaggtg 60
tcctgcaagg cctctgggta cgccttcact aattatttga tagagtgggt aaagcagagg 120
cctggacagg gcctagagtg gattggagtg attactcctg gaagtggcgg ttctaactac 180
aatgagaagt tcaagggcaa ggcaacactg actgcagaca aatcctccag cactgcctac 240
atgcagctca gcagcctgac atctgatgac tctgcggtct acttctgtgc aagatggctt 300
gattacgact ggtttgctta ctggggccaa gggactctgg tcactgtctc tgca 354
<210> 7
<211> 107
<212> БЕЛОК
<213> Mus musculus
<400> 7
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Thr Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Cys Asp Asp Phe Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 8
<211> 107
<212> БЕЛОК
<213> Mus musculus
<400> 8
Asp Ile Lys Met Thr Gln Phe Pro Ser Ser Met Tyr Ala Ser Val Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Cys Asp Glu Phe Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 9
<211> 107
<212> БЕЛОК
<213> Mus musculus
<400> 9
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Arg Gln Cys Asp Glu Phe Pro Ser
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 10
<211> 107
<212> БЕЛОК
<213> Mus musculus
<400> 10
Asp Ile Lys Met Thr Gln Phe Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Thr Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Cys Asp Asp Phe Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 11
<211> 321
<212> ДНК
<213> Mus musculus
<400> 11
gacatcaaga tgacccagtc tccatcttcc atgtatgcat ctctaggaga gagagtcact 60
atcacttgca aggcgagtca ggacattaat acctatttaa cctggttcca gcagaaacca 120
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 180
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 240
gaagatatgg gaatttatta ttgtctacag tgtgatgatt ttccgctcac gttcggtgct 300
gggaccaagc tggagctgaa a 321
<210> 12
<211> 321
<212> ДНК
<213> Mus musculus
<400> 12
gacatcaaga tgacccagtt tccatcttcc atgtatgcat ctgtaggaga gagagtcact 60
atcacttgca aggcgagtca ggacattaat agctatttaa gctggttcca gcagaaacca 120
gggaaatctc ctaagaccct gatttatcgt gcaaacagat tggtagatgg ggtcccatca 180
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 240
gaagatatgg gaatttatta ttgtctacag tgtgatgagt ttccgttcac gttcggaggg 300
gggaccaagc tggaaataaa a 321
<210> 13
<211> 321
<212> ДНК
<213> Mus musculus
<400> 13
gacatcaaga tgacccagtc tccatcttcc atgtatgcat ctctaggaga gagagtcact 60
atcacttgca aggcgagtca ggacattaat agctatttaa gctggttcca gcagaaacca 120
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 180
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 240
gaagatatgg gaatttatta ttgtcgacag tgtgatgagt ttccgtccac gttcggaggg 300
gggaccaagc tggaaataaa a 321
<210> 14
<211> 321
<212> ДНК
<213> Mus musculus
<400> 14
gacatcaaga tgacccagtt tccatcttcc atgtatgcat ctctaggaga gagagtcact 60
atcacttgca aggcgagtca ggacattaat acctatttaa cctggttcca gcagaaacca 120
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 180
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 240
gaagatatgg gaatttatta ttgtctacag tgtgatgatt ttccgctcac gttcggtgct 300
gggaccaagc tggagctgaa a 321
<210> 15
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 15
Gly Tyr Thr Phe Thr Thr Tyr
1 5
<210> 16
<211> 6
<212> БЕЛОК
<213> Mus musculus
<400> 16
His Pro Tyr Asn Asp Asp
1 5
<210> 17
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 17
Gly Asn Asp Tyr Asp Leu Tyr Gly Met Asp Tyr
1 5 10
<210> 18
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 18
Lys Ala Ser Gln Asp Ile Asn Thr Tyr Leu Thr
1 5 10
<210> 19
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 19
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 20
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 20
Leu Gln Cys Asp Asp Phe Pro Leu Thr
1 5
<210> 21
<211> 5
<212> БЕЛОК
<213> Mus musculus
<400> 21
Thr Tyr Pro Ile Glu
1 5
<210> 22
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 22
Asn Phe His Pro Tyr Asn Asp Asp Thr Arg Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asp
<210> 23
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 23
Gly Asn Asp Tyr Asp Leu Tyr Gly Met Asp Tyr
1 5 10
<210> 24
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 24
Gly Tyr Ala Phe Thr Asn Tyr
1 5
<210> 25
<211> 6
<212> БЕЛОК
<213> Mus musculus
<400> 25
Asn Pro Gly Ser Gly Gly
1 5
<210> 26
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 26
Trp Leu Asp Tyr Asp Trp Phe Ala Tyr
1 5
<210> 27
<211> 11
<212> БЕЛОК
<213> Mus musculus
<400> 27
Lys Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<210> 28
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 28
Leu Gln Cys Asp Glu Phe Pro Phe Thr
1 5
<210> 29
<211> 5
<212> БЕЛОК
<213> Mus musculus
<400> 29
Asn Tyr Leu Ile Glu
1 5
<210> 30
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 30
Val Ile Asn Pro Gly Ser Gly Gly Ile Asn Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 31
<211> 6
<212> БЕЛОК
<213> Mus musculus
<400> 31
Thr Pro Gly Ser Gly Gly
1 5
<210> 32
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 32
Arg Gln Cys Asp Glu Phe Pro Ser Thr
1 5
<210> 33
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 33
Val Ile Thr Pro Gly Ser Gly Gly Ser Asn Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 34
<211> 464
<212> БЕЛОК
<213> Mus musculus
<400> 34
Met Glu Trp Ser Trp Ile Phe Leu Phe Leu Leu Ser Gly Thr Ala Gly
1 5 10 15
Val His Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Ile Lys
20 25 30
Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Ser Tyr Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu
50 55 60
Glu Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn
65 70 75 80
Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Gly Thr Tyr Tyr Tyr Gly Ser Arg Val Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Lys Thr Thr
130 135 140
Pro Pro Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn
145 150 155 160
Ser Met Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro
165 170 175
Val Thr Val Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr
180 185 190
Phe Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val
195 200 205
Thr Val Pro Ser Ser Thr Trp Pro Ser Glu Thr Val Thr Cys Asn Val
210 215 220
Ala His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Val Pro Arg
225 230 235 240
Asp Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser
245 250 255
Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu Thr Ile Thr Leu
260 265 270
Thr Pro Lys Val Thr Cys Val Val Val Asp Ile Ser Lys Asp Asp Pro
275 280 285
Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu Val His Thr Ala
290 295 300
Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Ser Val
305 310 315 320
Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn Gly Lys Glu Phe
325 330 335
Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr
340 345 350
Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile
355 360 365
Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val Ser Leu Thr Cys
370 375 380
Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val Glu Trp Gln Trp
385 390 395 400
Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp
405 410 415
Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn Val Gln Lys Ser
420 425 430
Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val Leu His Glu Gly
435 440 445
Leu His Asn His His Thr Glu Lys Ser Leu Ser His Ser Pro Gly Lys
450 455 460
<210> 35
<211> 239
<212> БЕЛОК
<213> Mus musculus
<400> 35
Met Arg Cys Leu Ala Glu Phe Leu Gly Leu Leu Val Leu Trp Ile Pro
1 5 10 15
Gly Ala Ile Gly Asp Ile Val Met Thr Gln Ala Ala Pro Ser Ile Pro
20 25 30
Val Thr Pro Gly Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser
35 40 45
Leu Leu Asn Ser Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg
50 55 60
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala
65 70 75 80
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe
85 90 95
Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
100 105 110
Cys Met Gln His Leu Glu Tyr Pro Phe Thr Phe Gly Ala Gly Thr Lys
115 120 125
Leu Glu Leu Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro
130 135 140
Pro Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe
145 150 155 160
Leu Asn Asn Phe Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp
165 170 175
Gly Ser Glu Arg Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp
180 185 190
Ser Lys Asp Ser Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys
195 200 205
Asp Glu Tyr Glu Arg His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys
210 215 220
Thr Ser Thr Ser Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
225 230 235
<210> 36
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=Описание искусственной последовательности: синтетический
полипептид"
<400> 36
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Ile Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Tyr Tyr Gly Ser Arg Val Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ala Ala
130 135 140
Pro Ser Ile Pro Val Thr Pro Gly Glu Ser Val Ser Ile Ser Cys Arg
145 150 155 160
Ser Ser Lys Ser Leu Leu Asn Ser Asn Gly Asn Thr Tyr Leu Tyr Trp
165 170 175
Phe Leu Gln Arg Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Arg Met
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Ala Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val
210 215 220
Gly Val Tyr Tyr Cys Met Gln His Leu Glu Tyr Pro Phe Thr Phe Gly
225 230 235 240
Ala Gly Thr Lys Leu Glu Leu Lys
245
<210> 37
<211> 1392
<212> ДНК
<213> Mus musculus
<400> 37
atggcgtgga tctctatcat cctcttccta gtggcaacag ctataggtgt ccactcccag 60
gttcagctgc agcagtctgg ggctgagctg gtgaagcctg gggcctcagt gaaggtgtcc 120
tgcaaggctt ttggctacac cttcactacc tatccaatag agtggatgag gcagaatcat 180
ggaaagagcc tagagtggat tggaaatttt catccttaca atgatgatac taggtacaat 240
gaaaaattca aggacaaggc caaattgact gtagaaaaat cctctagcac agtctacttg 300
gagctcagcc gattaacata tgatgactct gctgtttatt actgtacaag ggggaatgat 360
tacgacctct atggtatgga ctactggggt caaggaacct cagtcaccgt ctcctcagcc 420
aaaacgacac ccccatctgt ctatccactg gcccctggat ctgctgccca aactaactcc 480
atggtgaccc tgggatgcct ggtcaagggc tatttccctg agccagtgac agtgacctgg 540
aactctggat ccctgtccag cggtgtgcac accttcccag ctgtcctgca gtctgacctc 600
tacactctga gcagctcagt gactgtcccc tccagcacct ggcccagcga gaccgtcacc 660
tgcaacgttg cccacccggc cagcagcacc aaggtggaca agaaaattgt gcccagggat 720
tgtggttgta agccttgcat atgtacagtc ccagaagtat catctgtctt catcttcccc 780
ccaaagccca aggatgtgct caccattact ctgactccta aggtcacgtg tgttgtggta 840
gacatcagca aggatgatcc cgaggtccag ttcagctggt ttgtagatga tgtggaggtg 900
cacacagctc agacgcaacc ccgggaggag cagttcaaca gcactttccg ctcagtcagt 960
gaacttccca tcatgcacca ggactggctc aatggcaagg agttcaaatg cagggtcaac 1020
agtgcagctt tccctgcccc catcgagaaa accatctcca aaaccaaagg cagaccgaag 1080
gctccacagg tgtacaccat tccacctccc aaggagcaga tggccaagga taaagtcagt 1140
ctgacctgca tgataacaga cttcttccct gaagacatta ctgtggagtg gcagtggaat 1200
gggcagccag cggagaacta caagaacact cagcccatca tggacacaga tggctcttac 1260
ttcgtctaca gcaagctcaa tgtgcagaag agcaactggg aggcaggaaa tactttcacc 1320
tgctctgtgt tacatgaggg cctgcacaac caccatactg agaagagcct ctcccactct 1380
cctggtaaat ga 1392
<210> 38
<211> 463
<212> БЕЛОК
<213> Mus musculus
<400> 38
Met Ala Trp Ile Ser Ile Ile Leu Phe Leu Val Ala Thr Ala Ile Gly
1 5 10 15
Val His Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Phe Gly Tyr Thr Phe
35 40 45
Thr Thr Tyr Pro Ile Glu Trp Met Arg Gln Asn His Gly Lys Ser Leu
50 55 60
Glu Trp Ile Gly Asn Phe His Pro Tyr Asn Asp Asp Thr Arg Tyr Asn
65 70 75 80
Glu Lys Phe Lys Asp Lys Ala Lys Leu Thr Val Glu Lys Ser Ser Ser
85 90 95
Thr Val Tyr Leu Glu Leu Ser Arg Leu Thr Tyr Asp Asp Ser Ala Val
100 105 110
Tyr Tyr Cys Thr Arg Gly Asn Asp Tyr Asp Leu Tyr Gly Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro
130 135 140
Pro Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser
145 150 155 160
Met Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val
165 170 175
Thr Val Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe
180 185 190
Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr
195 200 205
Val Pro Ser Ser Thr Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala
210 215 220
His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp
225 230 235 240
Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser Val
245 250 255
Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu Thr Ile Thr Leu Thr
260 265 270
Pro Lys Val Thr Cys Val Val Val Asp Ile Ser Lys Asp Asp Pro Glu
275 280 285
Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu Val His Thr Ala Gln
290 295 300
Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Ser Val Ser
305 310 315 320
Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys
325 330 335
Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile
340 345 350
Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro
355 360 365
Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val Ser Leu Thr Cys Met
370 375 380
Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val Glu Trp Gln Trp Asn
385 390 395 400
Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr
405 410 415
Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn
420 425 430
Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val Leu His Glu Gly Leu
435 440 445
His Asn His His Thr Glu Lys Ser Leu Ser His Ser Pro Gly Lys
450 455 460
<210> 39
<211> 444
<212> БЕЛОК
<213> Mus musculus
<400> 39
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Phe Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Pro Ile Glu Trp Met Arg Gln Asn His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asn Phe His Pro Tyr Asn Asp Asp Thr Arg Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Ala Lys Leu Thr Val Glu Lys Ser Ser Ser Thr Val Tyr
65 70 75 80
Leu Glu Leu Ser Arg Leu Thr Tyr Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Gly Asn Asp Tyr Asp Leu Tyr Gly Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro Pro Ser Val
115 120 125
Tyr Pro Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser Met Val Thr
130 135 140
Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr Val Thr
145 150 155 160
Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val Pro Ser
180 185 190
Ser Thr Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala His Pro Ala
195 200 205
Ser Ser Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp Cys Gly Cys
210 215 220
Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Val Leu Thr Ile Thr Leu Thr Pro Lys Val
245 250 255
Thr Cys Val Val Val Asp Ile Ser Lys Asp Asp Pro Glu Val Gln Phe
260 265 270
Ser Trp Phe Val Asp Asp Val Glu Val His Thr Ala Gln Thr Gln Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Ser Val Ser Glu Leu Pro
290 295 300
Ile Met His Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys Cys Arg Val
305 310 315 320
Asn Ser Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr
325 330 335
Lys Gly Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro Pro Pro Lys
340 345 350
Glu Gln Met Ala Lys Asp Lys Val Ser Leu Thr Cys Met Ile Thr Asp
355 360 365
Phe Phe Pro Glu Asp Ile Thr Val Glu Trp Gln Trp Asn Gly Gln Pro
370 375 380
Ala Glu Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr Asp Gly Ser
385 390 395 400
Tyr Phe Val Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn Trp Glu Ala
405 410 415
Gly Asn Thr Phe Thr Cys Ser Val Leu His Glu Gly Leu His Asn His
420 425 430
His Thr Glu Lys Ser Leu Ser His Ser Pro Gly Lys
435 440
<210> 40
<211> 705
<212> ДНК
<213> Mus musculus
<400> 40
atgaggaccc ctgctcagtt tcttggaatc ttgttgctct ggtttccagg tatcaaatgt 60
gacatcaaga tgacccagtc tccatcttcc atgtatgcat ctctaggaga gagagtcact 120
atcacttgca aggcgagtca ggacattaat acctatttaa cctggttcca gcagaaacca 180
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 240
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 300
gaagatatgg gaatttatta ttgtctacag tgtgatgatt ttccgctcac gttcggtgct 360
gggaccaagc tggagctgaa acgggctgat gctgcaccaa ctgtatccat cttcccacca 420
tccagtgagc agttaacatc tggaggtgcc tcagtcgtgt gcttcttgaa caacttctac 480
cccaaagaca tcaatgtcaa gtggaagatt gatggcagtg aacgacaaaa tggcgtcctg 540
aacagttgga ctgatcagga cagcaaagac agcacctaca gcatgagcag caccctcacg 600
ttgaccaagg acgagtatga acgacataac agctatacct gtgaggccac tcacaagaca 660
tcaacttcac ccattgtcaa gagcttcaac aggaatgagt gttag 705
<210> 41
<211> 234
<212> БЕЛОК
<213> Mus musculus
<400> 41
Met Arg Thr Pro Ala Gln Phe Leu Gly Ile Leu Leu Leu Trp Phe Pro
1 5 10 15
Gly Ile Lys Cys Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr
20 25 30
Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp
35 40 45
Ile Asn Thr Tyr Leu Thr Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro
50 55 60
Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser
85 90 95
Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Cys Asp
100 105 110
Asp Phe Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg
115 120 125
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln
130 135 140
Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr
145 150 155 160
Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln
165 170 175
Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg
195 200 205
His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro
210 215 220
Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
225 230
<210> 42
<211> 214
<212> БЕЛОК
<213> Mus musculus
<400> 42
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Thr Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Cys Asp Asp Phe Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Ala Asp Ala Ala
100 105 110
Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly
115 120 125
Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln Asn Gly Val Leu
145 150 155 160
Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr Tyr Ser Met Ser
165 170 175
Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg His Asn Ser Tyr
180 185 190
Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro Ile Val Lys Ser
195 200 205
Phe Asn Arg Asn Glu Cys
210
<210> 43
<211> 237
<212> БЕЛОК
<213> Mus musculus
<400> 43
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Ile Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Tyr Tyr Gly Ser Arg Val Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Lys Thr Thr Pro Pro Ser
115 120 125
Val Tyr Pro Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser Met Val
130 135 140
Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val Pro
180 185 190
Ser Ser Thr Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp Cys Gly
210 215 220
Cys Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser
225 230 235
<210> 44
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 44
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Ile Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu Asn Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Phe Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 45
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетическая
метка 8xHis"
<400> 45
His His His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| CD19-СПЕЦИФИЧЕСКИЙ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР И ЕГО ПРИМЕНЕНИЯ | 2014 |
|
RU2727447C2 |
| АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2017 |
|
RU2773355C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ВВЕДЕНИЯ ДОЗ АЛЛОГЕННЫХ T-КЛЕТОК С ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ | 2018 |
|
RU2776322C2 |
| УСТОЙЧИВЫЕ К РИТУКСИМАБУ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2816370C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) ПРОТИВ CD123 ДЛЯ ИСПОЛЬЗОВАНИЯ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2724999C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2017 |
|
RU2826270C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| НОВЫЕ КОНСТРУКЦИИ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА, СОДЕРЖАЩИЕ ДОМЕНЫ TNFR2 | 2019 |
|
RU2808254C2 |
| КЛЕТКА | 2015 |
|
RU2768019C2 |
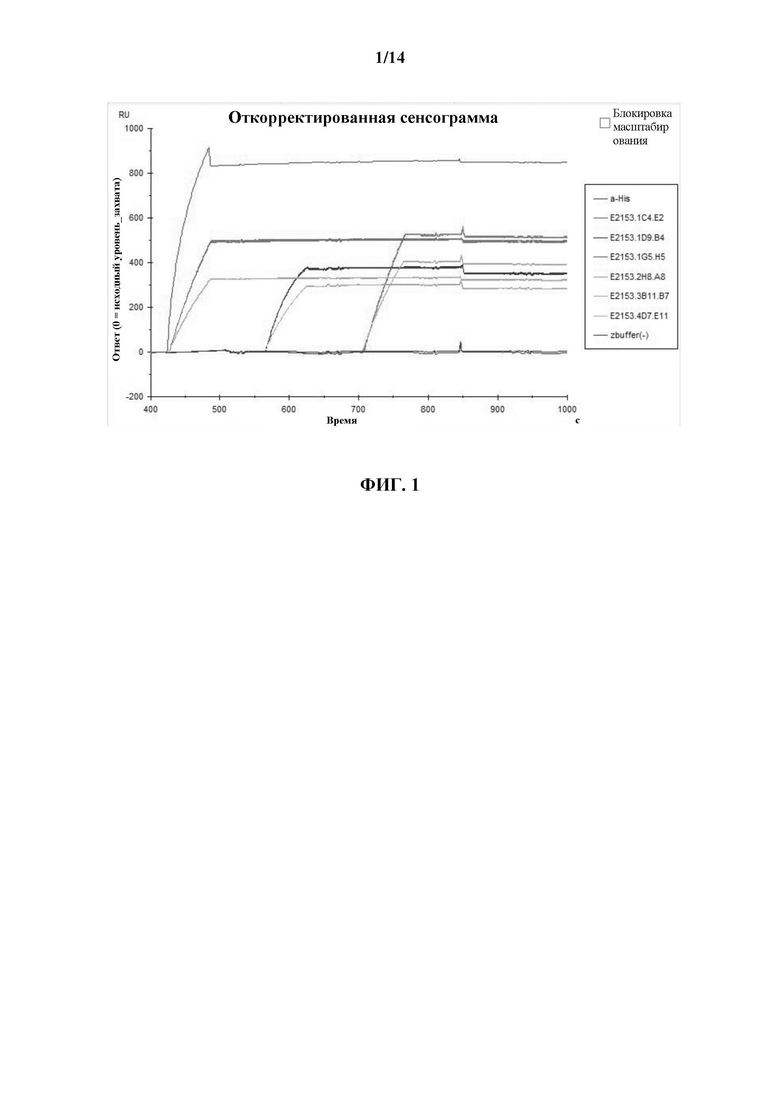
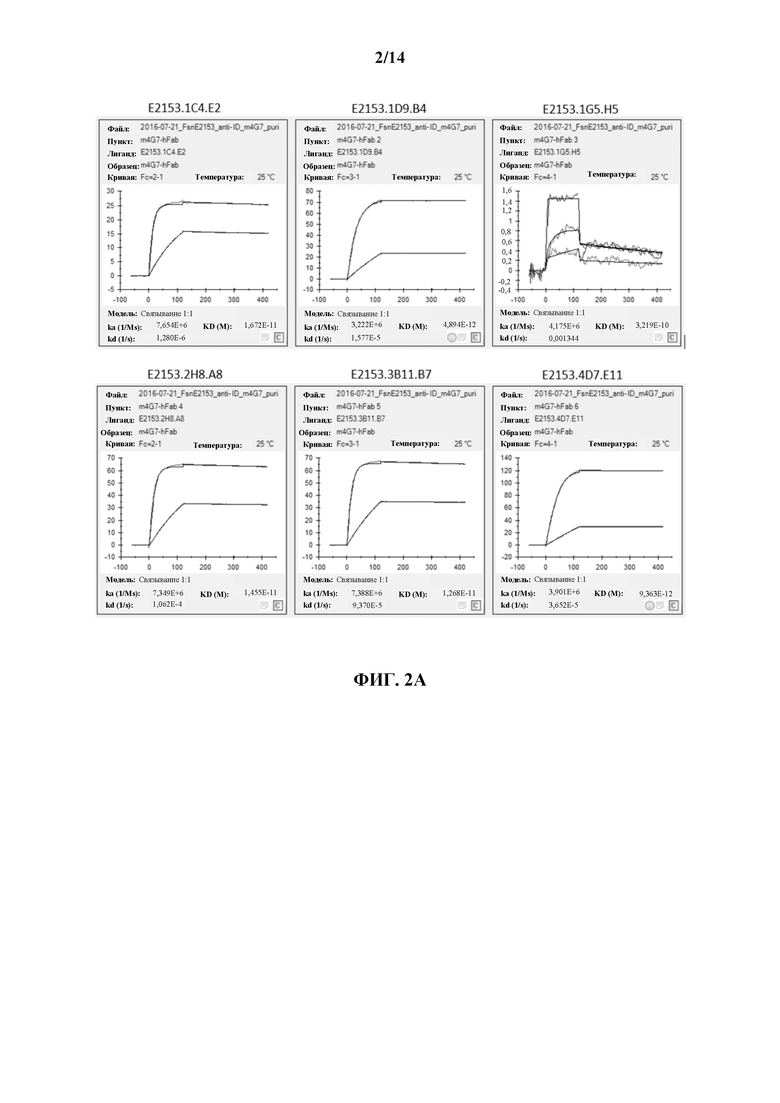
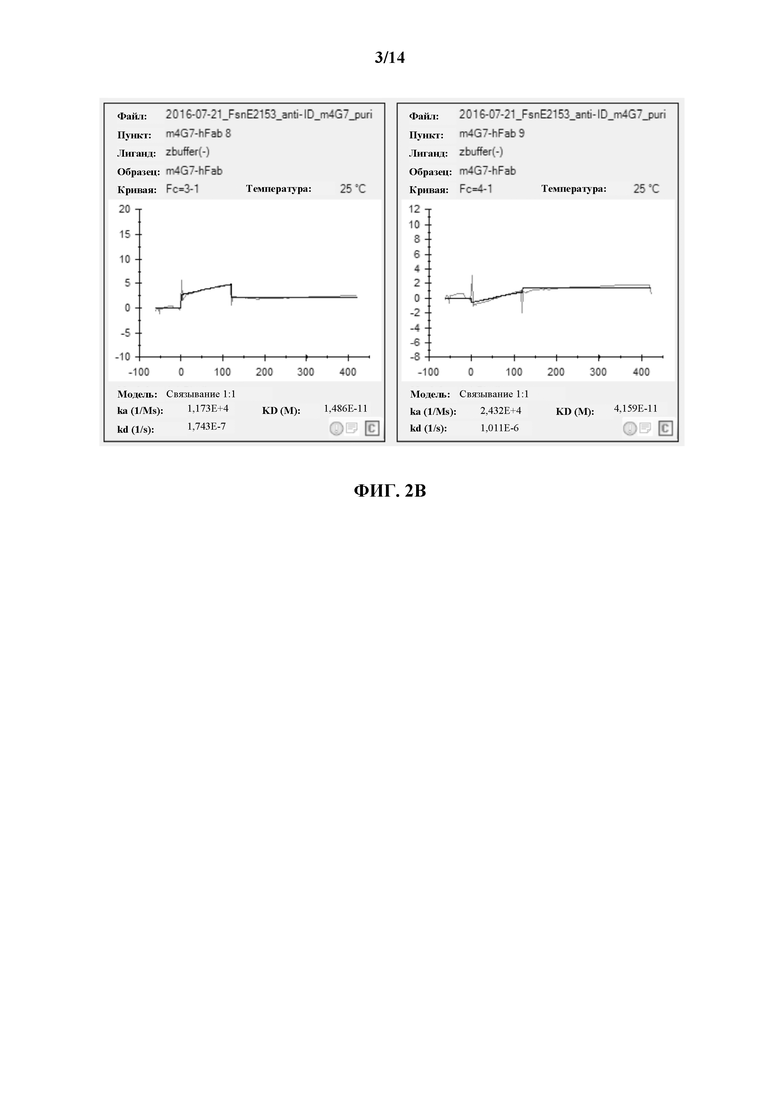
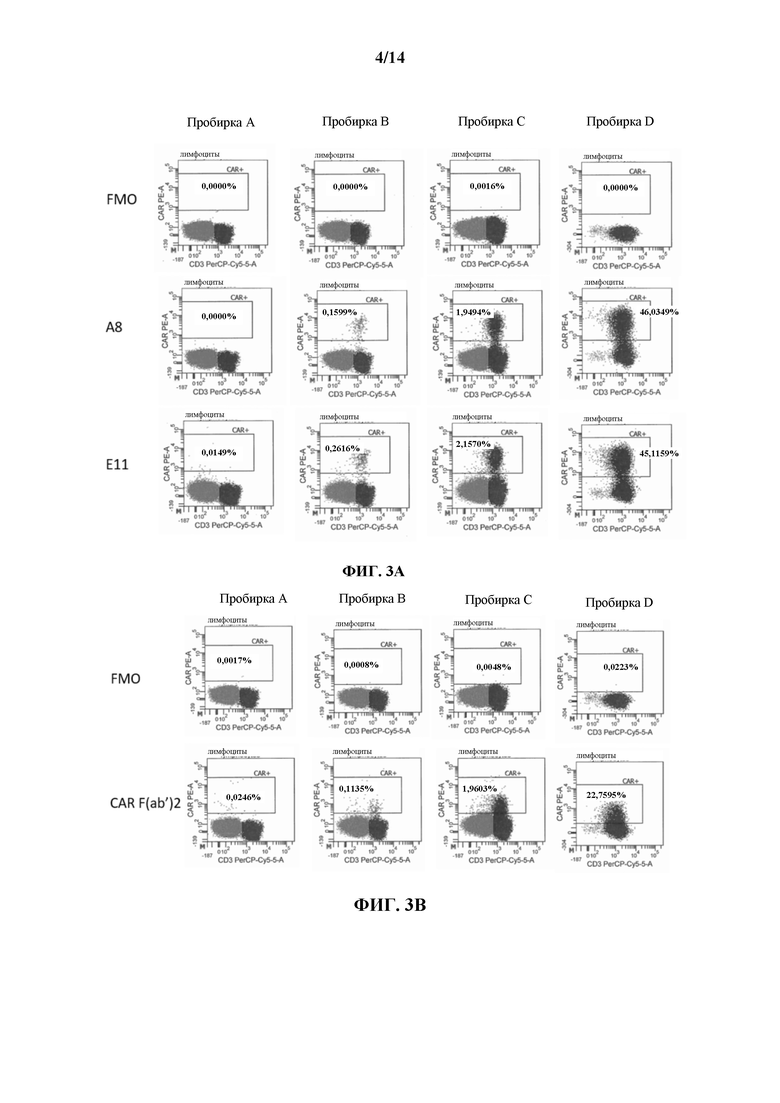
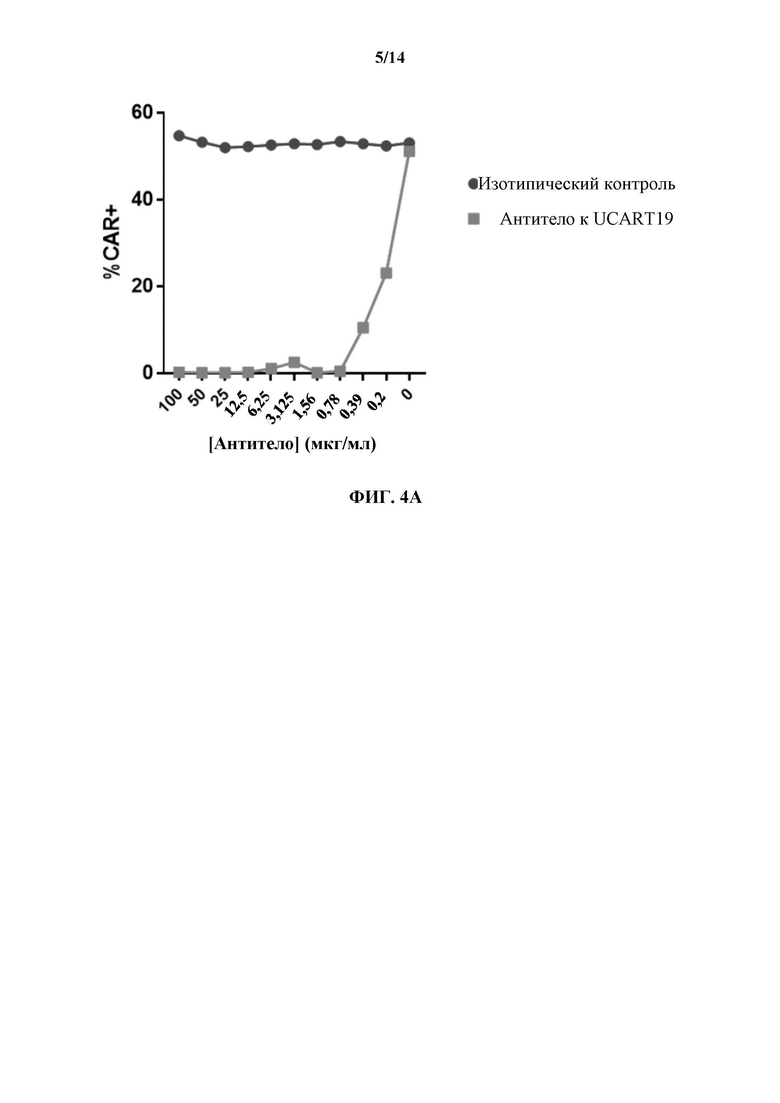


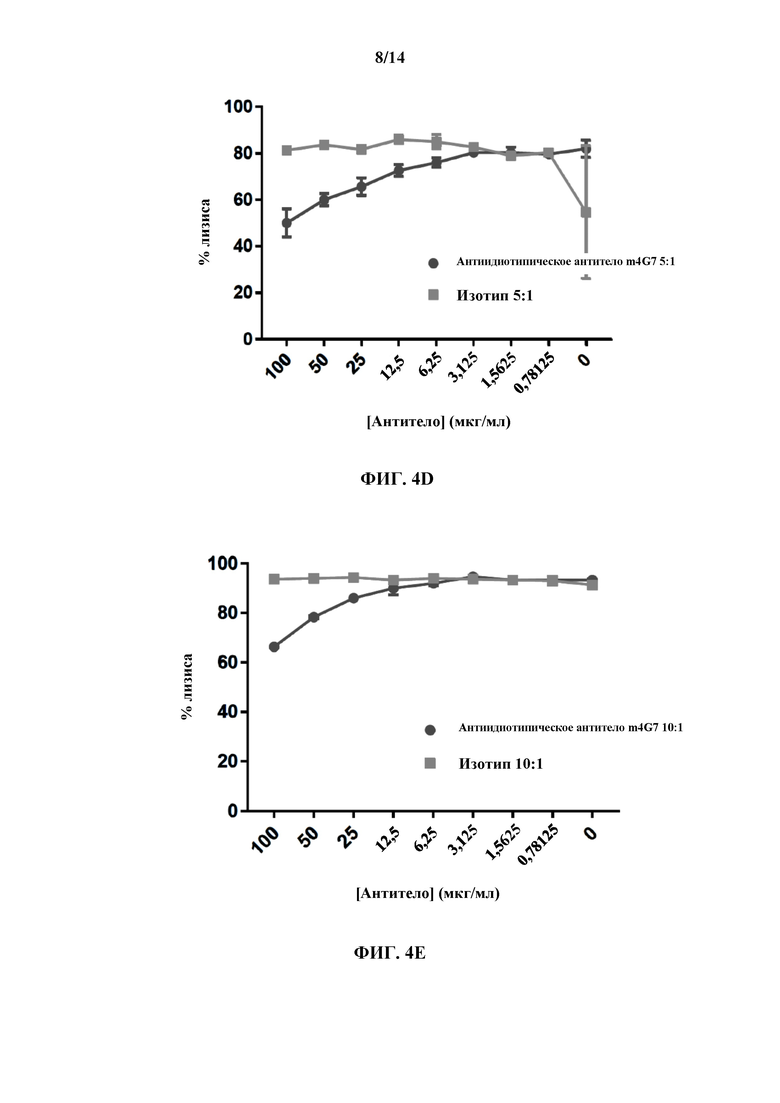

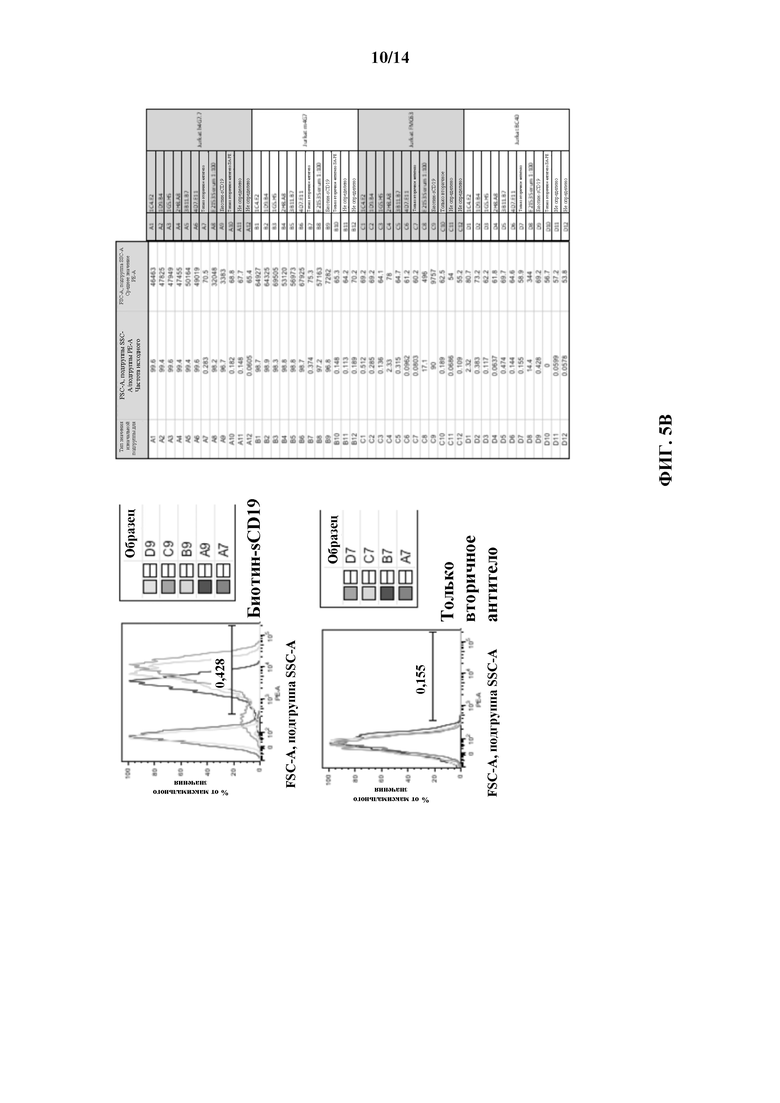
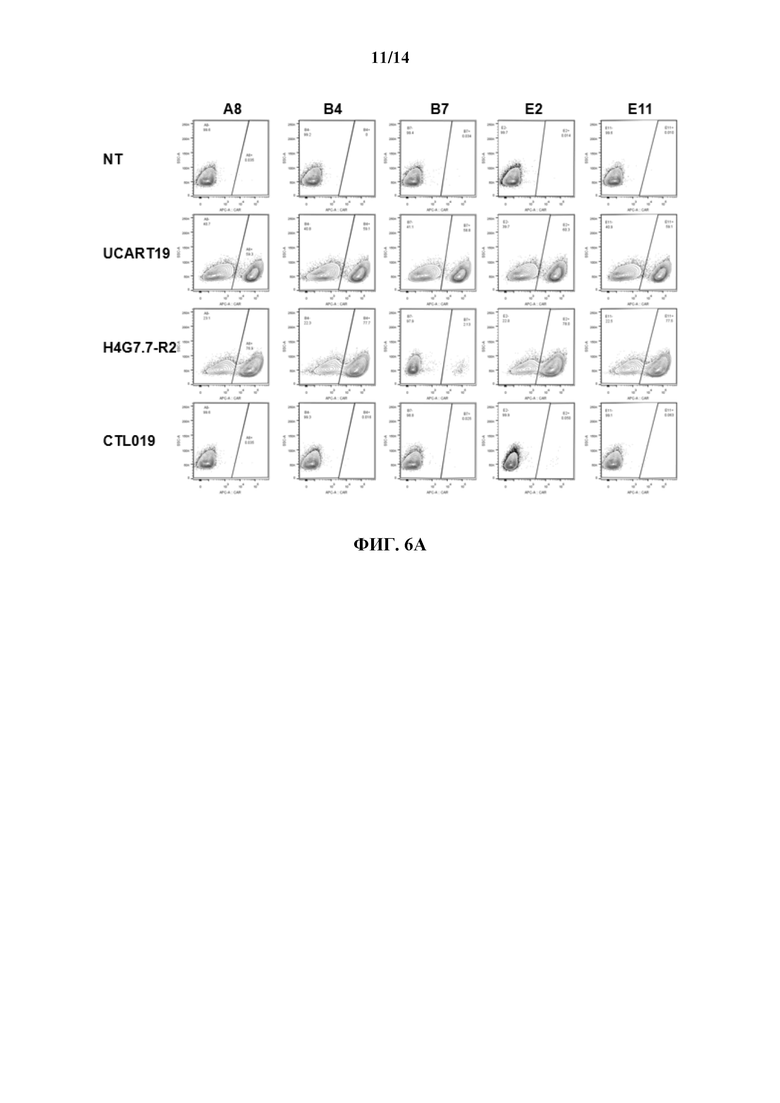
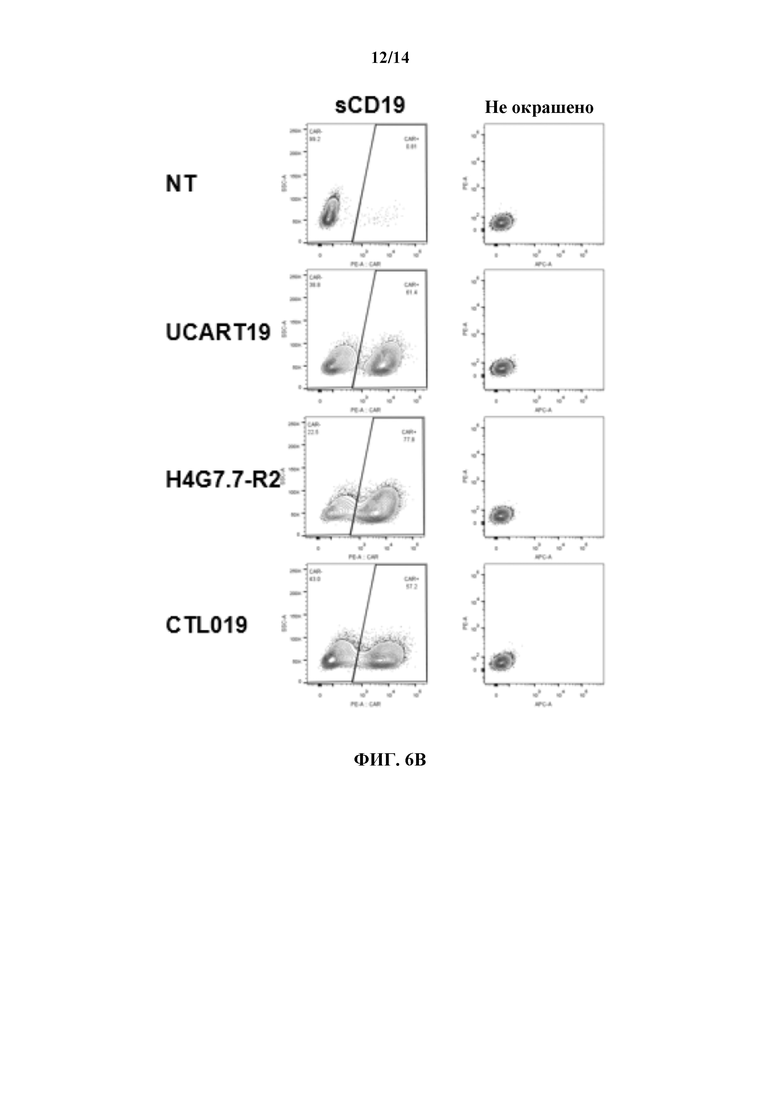
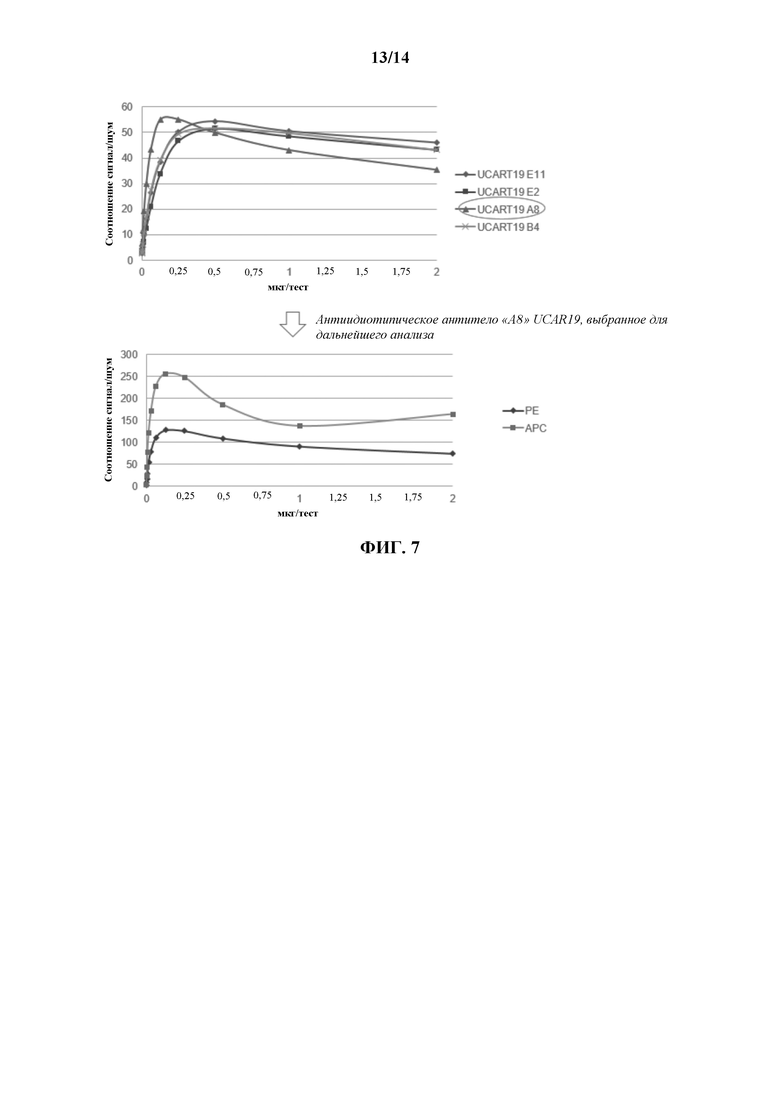
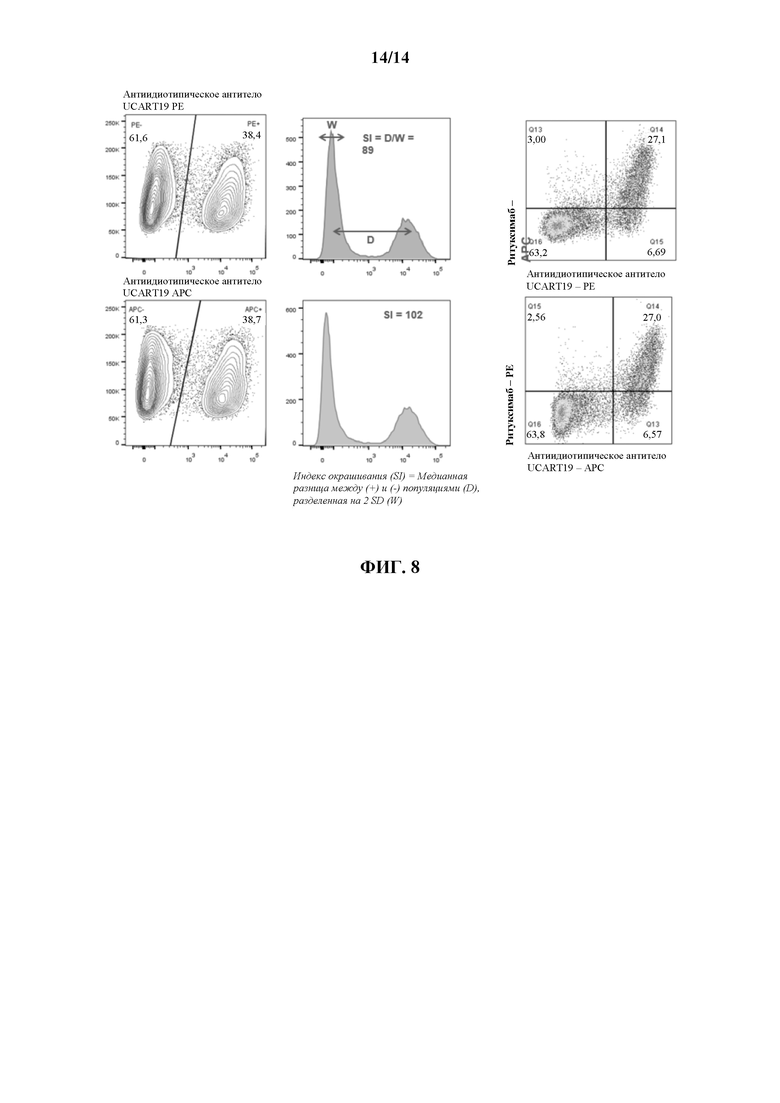
Изобретение относится к области биотехнологии. Предложены антитела, которые специфически связывают молекулу, содержащую scFv к CD19, и композиции, содержащие указанные антитела. Также предложены полинуклеотиды, кодирующие антитела, экспрессирующие векторы и клетки-хозяева, содержащие указанные полинуклеотиды, способ получения антител. Кроме того, изобретение относится к применению указанных антител для определения присутствия или отсутствия полипептида, содержащего scFv к CD19, или включающих его клеток. Изобретение может быть использовано для выявления экспрессии CAR к CD19, содержащих scFv из клона антитела 4G7, на сконструированных Т-клетках или в анализах in vitro. 9 н. и 18 з.п. ф-лы, 8 ил., 8 табл., 6 пр.
1. Выделенное антитело, которое специфически связывает молекулу, содержащую scFv к CD19, содержащий аминокислотную последовательность SEQ ID NO: 36, где выделенное антитело не связывается с каркасной областью; причем антитело содержит:
(a) CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 15; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 16; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 17; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 21; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 22; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 23; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 18; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19, и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 20; или
(b) CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 24; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 25; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 29; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 30; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 27; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19, и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 28; или
(с) CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 24; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 31; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 29; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 33; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 27; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19, и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 32.
2. Выделенное антитело по п. 1, где выделенное антитело связывается с scFv к CD19 с KD, составляющей не более чем 100 пМ, не более чем 80 пМ, не более чем 60 пМ или не более чем 50 пМ, как определено посредством анализа Biacore при 25°C.
3. Выделенное антитело по п. 1 или 2, содержащее:
(a) VH, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 1; и VL, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 7; или
(b) VH, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 2; и VL, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95% идентичностью с SEQ ID NO: 8; или
(c) VH, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 3; и VL, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 9; или
(d) VH, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 1; и VL, содержащую аминокислотную последовательность, которая характеризуется по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 10.
4. Выделенное антитело по любому из предыдущих пунктов, содержащее:
(a) VH, содержащую аминокислотную последовательность SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность SEQ ID NO: 7; или
(b) VH, содержащую аминокислотную последовательность SEQ ID NO: 2; и VL, содержащую аминокислотную последовательность SEQ ID NO: 8; или
(c) VH, содержащую аминокислотную последовательность SEQ ID NO: 3; и VL, содержащую аминокислотную последовательность SEQ ID NO: 9; или
(d) VH, содержащую аминокислотную последовательность SEQ ID NO: 1; и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
5. Выделенное антитело по п. 3 или 4, содержащее CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO:15; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 16; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 17; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 21; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 22; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 23; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 18; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19; и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 20.
6. Выделенное антитело по п. 3 или 4, содержащее CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 24; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 25; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 29; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 30; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 27; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19; и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 28.
7. Выделенное антитело по п. 3 или 4, содержащее CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 24; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 31; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; или CDR1 VH, содержащую аминокислотную последовательность SEQ ID NO: 29; CDR2 VH, содержащую аминокислотную последовательность SEQ ID NO: 33; CDR3 VH, содержащую аминокислотную последовательность SEQ ID NO: 26; и
CDR1 VL, содержащую аминокислотную последовательность SEQ ID NO: 27; CDR2 VL, содержащую аминокислотную последовательность SEQ ID NO: 19; и CDR3 VL, содержащую аминокислотную последовательность SEQ ID NO: 32.
8. Композиция для определения клеток, экспрессирующих scFv к CD19, содержащая выделенное антитело по любому из предыдущих пунктов и фармацевтически приемлемый носитель или среду-носитель.
9. Композиция по п. 8, в которой выделенное антитело конъюгировано с выявляемой меткой.
10. Полинуклеотид, кодирующий выделенное антитело по любому из пп. 1-7.
11. Экспрессирующий вектор, содержащий полинуклеотид по п. 10.
12. Клетка-хозяин для получения выделенного антитела по любому из пп. 1-7, причем клетка-хозяин содержит полинуклеотид по п. 10 или вектор по п. 11.
13. Клетка по п. 12, где клетка предусматривает клетку, выбранную из группы, состоящей из клетки CHO, клетки Sp2/0, клетки кролика и клетки E. coli.
14. Способ получения выделенного антитела, включающий инкубацию клетки по п. 12 или 13 в подходящих условиях.
15. Применение выделенного антитела по любому из пп. 1-7 для определения количества клеток, экспрессирующих scFv, который имеет по меньшей мере 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 36, в образце.
16. Применение по п. 15, где выделенное антитело конъюгировано с выявляемой меткой.
17. Применение выделенного антитела по любому из пп. 1-7 для определения количества клеток, представляющих полипептид, содержащий scFv к CD19, который имеет по меньшей мере 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 36, в образце, содержащем клетки, которые, как известно или предполагается, представляют полипептид, содержащий scFv к CD19.
18. Применение выделенного антитела по любому из пп. 1-7 для определения присутствия или отсутствия полипептида, содержащего scFv к CD19, который имеет по меньшей мере 90% идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 36, в образце, который, как известно или предполагается, содержит полипептид, содержащий scFv к CD19.
19. Применение по любому из пп. 15-18, где образец представляет собой образец, фиксированный формалином.
20. Применение по любому из пп. 15-19, где scFv представляет собой компонент химерного антигенного рецептора (CAR).
21. Применение по любому из пп. 15-20, где клетка представляет собой иммунную клетку.
22. Применение по п. 21, где иммунная клетка выбрана из группы, состоящей из CD8+ T-клеток, CD4+ T-клеток, лимфоцитов, инфильтрирующих опухоль (TIL), NK-клеток, TCR-экспрессирующих клеток, дендритных клеток, и NK-T-клеток.
23. Применение по п. 22, где Т-клетка находится in vitro.
24. Применение по п. 22 или 23, где Т-клетка находится в образце крови, образце выделенной ткани, ткани, выращенной ex vivo, или в среде для культивирования клеток.
25. Применение по любому из пп. 22-24, где Т-клетка представляет собой аутологичную Т-клетку, полученную от пациента.
26. Применение по любому из пп. 22-24, где Т-клетка представляет собой аллогенную Т-клетку, полученную от здорового добровольца.
27. Применение по любому из пп. 17-26, где выделенное антитело конъюгировано с выявляемой клеткой.
| WO 2018023100 A2, 01.02.2018 | |||
| US 2018044417 A1, 15.02.2018 | |||
| WO 2014190273 A1, 27.11.2014 | |||
| JENA B | |||
| et al | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| ПЕТУХОВ А.В | |||
| и др | |||
| Получение CAR T-лимфоцитов, специфичных к CD19, и оценка их функциональной | |||
Авторы
Даты
2024-09-03—Публикация
2020-04-17—Подача