Заявляемое изобретение относится к медицинской отрасли, а именно к фармацевтике, в том числе к фармацевтическим композициям на основе полициклических углеродных соединений. Заявляемое изобретение предназначается для лечения и профилактики заболеваний, связанных с паталогическими проявлениями иммунной системы. Фармацевтическая композиция является активной в отношении позвоночных млекопитающих, в том числе человека.
Из уровня техники известны производные пирролопиридина (WO 2004099205 - Azaindole compounds as kinase inhibitors, опубликовано 18.11.2004). Производные имидазопиридина (WO 2004099204 - Imidazo and thiazolopyridines as jak3 kinase inhibitors, опубликовано 18.11.2004). Производные пирролопиримидина (WO 1999065908 - PYRROLO[2,3-d]PYRIMIDINE COMPOUNDS, опубликовано 23.12.1999; WO 1999065909 - PYRROLO[2,3-d]PYRIMIDINE COMPOUNDS, опубликовано 23.12.1999; WO 2001042246 -PYRROLO[2,3-d]PYRIMIDINE COMPOUNDS, опубликовано 14.06.2001; WO 2002000661 PYRROLO[2,3-d]PYRIMIDINE COMPOUNDS AS IMMUNOSUPPRESSIVE AGENTS, опубликовано 03.01.2002). Известные соединения используют для подавления иммунных реакций, в том числе гиперпродукции цитокинов. Нарушения внутриклеточных сигнальных путей, в частности, осуществляемых через систему протеинкиназ (янус-киназы 1,2,3, тирозинкиназа 2), имеющих следствие дисбаланс продукции цитокинов, лежат в основе множества заболеваний и патологических состояний.
Так, например, одна из протеинкиназ, Янус-киназа 3 играет важную роль в передаче сигналов от интерлейкинов: IL-2, IL-4, IL-7, IL-9, IL-15 и 1L-21 (J.J. O'shea et al, Cell, Vol. 109 (suppl.), S121, 2002; K. Ozaki et al, Science, Vol. 298, p. 1630, 2002), что ведет к нарушению созревания Т- и В-клеток. Следовательно, заболевания, включающие пролиферативную аномалию Т-клеток, такую как отторжение трансплантата, и аутоиммунные заболевания, могут быть подвергнуты лечению путем контроля иммунного ответа через этот механизм.
Такой же принцип касается и других протеинкиназ (Янус-киназы 1, 2, тирозинкиназа 2).
Основное внимание современных исследователей в плане вышеуказанных патологических процессов, направлено на подавление функций данных киназ и, таким образом, получения искомого клинического эффекта.
Кроме того, с этой целью используются азаиндолы (RU 2403252 -АЗАИНДОЛЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK И ДРУГИХ ПРОТЕИНКИНАЗ, опубликовано 10.11.2010). Азаиндолы (пирролопиридины, диазаинданы) - ряд органических гетероциклических соединений с общей химической формулой C7H6N2. Различают 4-, 5-, 6-, 7-Азаиндолы.
Одним из наиболее близких источников к описываемой композиции, является RU 2472496 - ПРИМЕНЕНИЕ ФУЛЛЕРЕНОЛОВ С60(ОН)18-24 И С60(ОН)30-38 В КАЧЕСТВЕ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ (опубликовано 20.01.2013), в отношении вирусов гриппа, герпеса, аденовируса, РС-вируса.
Известные фармацевтические композиции в основном обладают низкой биодоступностью.
Целью заявляемого изобретения является достижение следующего технического результата: повышение биодоступности компонентов фармацевтической композиции в процессе регулировки иммунного ответа в живом организме.
Поставленная цель достигается следующим образом:
Фармацевтическая композиция, регулирующая иммунный ответ живого организма, представляющая собой смесь азотистых гетеро-циклических соединений - азаиндолов, включающих пирролидин и/или пирроло-пиримидины, и/или пирроло-пиридины, и/или их производные, характеризующаяся тем, что ее состав базируется на полициклическом органическом соединении на основе фуллеренола.
Фармацевтическая композиция, в которой, в частности, в качестве фуллеренола применен фуллеренол С60.
Фармацевтическая композиция, в которой, в частности, содержится 0,05-99,95 мас. % азаиндолов и фуллеренол - остальное.
Фармацевтическая композиция, в которой, в частности, содержится 0,05-99,95 мас. % фуллеренола и азаиндолы - остальное.
Фармацевтическая композиция, в которой, в частности, в качестве пирроло-пиримидинов применяют пирроло[2-b] пиримидиновые соединения.
Фармацевтическая композиция, в которой, в частности, в качестве пирроло-пиримидинов применяют пирроло[3-b] пиримидиновые соединения.
Фармацевтическая композиция, в которой, в частности, в качестве пирроло-пиримидинов применяют пирроло[2-d] пиримидиновые соединения.
Фармацевтическая композиция, в которой, в частности, в качестве пирроло-пиримидинов применяют пирроло[3-d] пиримидиновые соединения.
Фармацевтическая композиция, которая, в частности, дополнительно содержится в фармацевтическом растворителе.
Фармацевтическая композиция, которая, в частности, дополнительно содержит диазаинданы, и/или их производные.
Фармацевтическая композиция, которая, в частности, дополнительно содержит барицитиниб.
Фармацевтическая композиция, которая, в частности, дополнительно содержит руксолитиниб.
Фармацевтическая композиция, которая, в частности, дополнительно содержит природные антиоксиданты.
Фармацевтическая композиция, которая, в частности, дополнительно содержит витамин С и/или группы В.
На иллюстрирующем изображении представлено:
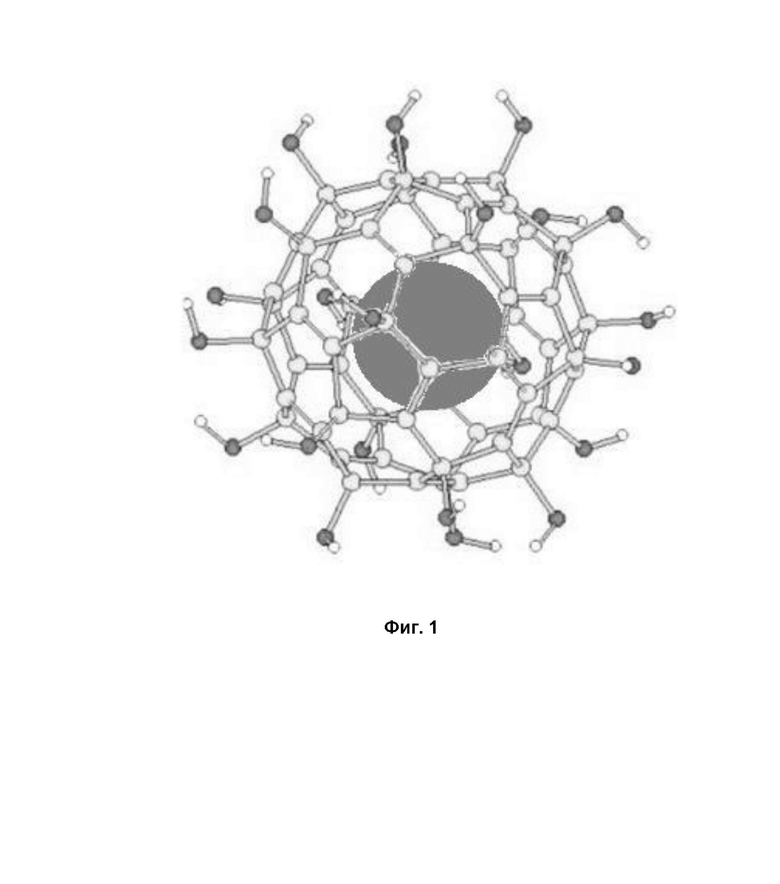
На Фиг. 1 схематично показано внедрение малой молекулы активного вещества внутрь полости молекулы фуллеренола.
Примеры осуществления заявляемой фармацевтической композиции и ее лечебное воздействие на живой организм.
Известно, что фуллеренол представляет собой молекулярное полигидроксилированное соединение, являющуюся комбинаций фуллерена с гидроксильными группами. В молекуле фуллерена атомы углерода соединяются между собой особым образом, образуя трехмерную «многоугольную» (в узлах находятся атомы углерода), в обобщенном приближении - сферическую фигуру (в частности, с шестьюдесятью атомами углерода - С60 в узлах). Фуллеренол на основе такого фуллерена в отдельных узлах этой фигуры содержит ряд функциональных групп ОН.
Известно также, что азаиндолы представляют собой органические гетероциклические соединения с общей химической формулой C7H6N2. Структурно представляются относительно плоскими 5-ти, 6-ти угольниками с функционально активными узлами NH. При использовании азаиндолов (пирроло-пиримидинов, в частности, барицитиниб, руксолитиниб и др.) происходит закономерное подавление синтеза провоспалительных цитокинов, в частности, интерлейкина 6. Указанные вещества, являющиеся ингибиторами JAKI-киназы, блокируют производство организмом цитокинов, снижая избыточный патогенный иммунный ответ, борясь при этом с аллергическими проявлениями (включая астматические), отторжениями органов при пересадке органов, аутоиммунными заболеваниями (красной волчанки, псориазов и др.), излишним опасным иммунным ответом («цитокиновым штормом»), в том числе, возникающим как следствие переносимых инфекций, в частности, коронавирусных, например COVID-19.
В заявляемой фармацевтической композиции фуллеренол играет роль вектора для адресной доставки препарата с различными видами азаиндолов, позволяющего транспортировать это лекарственное средство непосредственно в зону его максимального действия: в зараженные вирусом клетки, в лимфоузлы, ткани вблизи пересаженного органа и в другие места активного производства цитокинов. При этом фуллеренол захватывает с собой с помощью физико-химической связи, используя функциональные выступы гидроксильных групп, молекулы активных лекарственных препаратов (в частности, азаиндолов). Дополнительно таким же образом фуллеренолов могут быть захвачены молекулы природных антигистаминных средств, в качестве которых все чаще применяют натуральные антиоксиданты, например такие как бромелаин, кварцетин (в частности, применяемый в борьбе против астмы), снижающие выработку белка гистамина. Можно отметить, что и свободные от гидроксильных групп атомы углерода в узлах базового фуллерена в молекуле фуллеренола сами являются активными антиоксидантами.
Кроме того, полость углеродной сферы фуллерена, лежащая в основе соответствующего фуллеренола, оказывается достаточно вместительной, для проникновения внутрь ее атомов или молекул другого вещества, не превышающего диаметр этой внутренней полости. Такими могут быть, в частности, молекула аскорбиновой кислоты или витамины группы В (которые также являются достаточно сильными антиоксидантами). Захватывая внутрь себя частицы другого вещества, фуллеренол способен транспортировать их до необходимой конечной точки применения. Таким путем, в том числе, может быть осуществлен транзит необходимых соединений, минуя естественную защитную систему организма, в том числе: расщепляющие ферменты, макрофаги, лимфоциты и т.д. На Фиг. 1 схематично показано внедрение малой молекулы активного вещества внутрь полости молекулы фуллеренола.
Для большего лечебного воздействия заявляемой композиции, оба способа транспортировки (соединения с гидроксильными группами и внутри полости базового фуллерена) могут применяться комплексно.
Очевидно, что заявляемый фармацевтический комплекс на основе фуллеренола улучшает биодоступность активных лечебных препаратов, путем обеспечения их «адресной» доставки к органам и клеткам живого организма. Проникая таким образом в запланированную лечебную зону организма, заявляемая композиция учувствуют в требуемой регуляции иммунного ответа.
Одновременно, за счет повышения биодоступности составляющих заявляемой композиции веществ, для фармацевтического воздействия на организм требуются меньшие дозы веществ. Меньшие дозы веществ могут оказывать меньшие нежелательные влияния на организм (например, снижение побочных действий препарата), а также могут снижать нагрузку на живой организм, особенно в случаях и без того тяжелого состояния пациента вследствие, например, переносимого им «цитокинового шторма».
Примеры осуществления заявляемой фармацевтической композиции
Как известно, воспалительная реакция является неотьемлемой частью иммуногенеза. Избыточность или недостаточность воспаления играют значимую роль в патогенезе многих заболеваний, в том числе и тех, которые обусловлены вирусной инфекцией. ФНО-альфа и ИЛ-6 -цитокины, в значительной степени определяющие степень воспаления и основные маркеры «цитокинового шторма». Проведено исследование влияния на выработку этих цитокинов комплекса фуллеренол-ингибитор янус киназы.
Пример 1.
Исследование in vitro.
Исследование производили в культуре мононуклеарных клеток периферической крови (МНК) здоровых доноров. Фракция МНК получена путем выделения на градиенте плотности фиколла (Панэко, Россия) с р=1,077 по стандартной методике. После второй отмывки осадок клеток каждого донора был ресуспендирован в 1 мл среды RPMI-1640 (Панэко, Россия) с 10% эмбриональной бычьей сыворотки (Biosera, Франция) и антибиотиками - пенициллином 50 Ед и стрептомицином 50 мкг (далее - полная среда), производили подсчет количества и жизнеспособности клеток в камере Горяева, с окраской 1% трипановым синим. Выделенные клетки каждого донора развели полной средой до концентрации 2×106 в 1 мл и внесли по 200×105 в лунки A1:F6 96-луночного планшета (Nunc, Дания). В качестве индуктора экспрессии Янус киназ и продукции цитокинов использовали фитогемагглютинин (ФГА) в конечной концентрации 10 мкг/мл полной среды.
В эксперименте использовали Барицитиниб в концентрации 1 мкг/мл (контроль 2), смесь Барицитиниб-Фуллеренол (в соотношении 50/50%) в конечной концентрации 1 мкг/мл (опыт). В качестве контроля 1 использовали культуру клеток без добавления препаратов.
Препараты вносили в соответствующие лунки планшета по 10 мкл. Конечный объем среды во всех лунках - 250 мкл. Планшет помещали в условия влажной атмосферы с 5%CO2 при 37°С на 48 часов. После культивирования планшеты с клетками центрифугировали и в супернатанте определяли концентрацию фактора некроза опухолей альфа (TNFq) и интерлейкина 6 (IL-6). Анализ проведен методом цитометрических бус Bio-Plex ProTM Human Cytokine Grp I Panel 8-plex (Bio-RAD) по протоколу производителя. Результаты исследования представлены в таблицах 1 и 2.


Таким образом, добавление фуллеренола значительно усиливало эффект ингибитора янус киназ Барицитиниба в отношении выработки провоспалительных цитокинов.
Пример 2.
Исследование in vivo.
Как известно, клинические проявления пироплазмоза у собак во многом связаны с «цитокиновым штормом», когда высокий уровень провоспалительных цитокинов зачастую приводит к гибели животного.
Исследование проведено на 26 беспородных собаках, заболевших пироплазмозом в тяжелой форме. Всех животных разделили на 3 группы. Группа 1 (контроль 1, 6 собак) получали общепринятое при данной патологии лечение.
Группа 2 (контроль 2, 10 собак) получали дополнительно Барицитиниб из расчета 50 мкг/ кг веса.
Группа 3 (опыт, 10 собак) получали дополнительно смесь Барицитиниб - Фуллеренол (в соотношении 50/50%) из расчета 50 мкг/ кг веса.
При поступлении и через 3 дня после начала терапии у всех животных определяли уровень сывороточных ФНО альфа и Интерлейкина 6 (IL-6) с помощью иммуноферментных наборов MILLIPLEX MAP Canine Cytokine/Chemokine по регламенту производителя.
Результаты исследований представлены в таблицах 3 и 4.


Как видно из таблиц, использование препаратов - ингибиторов янус киназ при пироплазмозе у собак оказалось весьма эффективным, уровень провоспалительных цитокинов -ФНО альфа и IL-6 был достовернониже чем в контроле 1 и контроле 2. Это коррелировало с данными клинической картины. Животные быстрее поправлялись, начинали активнее двигаться, есть, нормализовалась температура.
В группе опыта (Барицитиниб+Фуллеренол) эти положительные изменения были особенно выражены, что подтверждается приведенными выше данными лабораторного анализа.
Из примеров видно, что использование в качестве основы лечебного процесса заявляемой фармацевтической композиции позволяет регулировать иммунный ответ организма путем ограничения его избыточного паталогического проявления.
Немаловажно и то, что применение заявляемой композиции в фармацевтической промышленности, может быть снижена нагрузка и на производственные мощности фармацевтических предприятий, в частности при массовом производстве сложных высокотехнологичных дорогостоящих лекарственных препаратов, например удовлетворяя повышенный спрос в вовремя эпидемий и пандемий.
Таким образом, заявляемая фармацевтическая композиция, регулирующая иммунный ответ живого организма, представляющая собой смесь азотистых гереро-циклических соединений - азаиндолов, на основе фуллеренола, обеспечивает повышение биодоступности активных компонентов в процессе регулировки иммунного ответа в живом организме.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармацевтическая композиция, стимулирующая иммунный ответ живого организма | 2021 |
|
RU2821633C1 |
| Способ получения фуллеренола | 2020 |
|
RU2750604C1 |
| КОМПОЗИЦИЯ ДЛЯ ТЕРАПИИ АТОПИЧЕСКОГО ДЕРМАТИТА НА ОСНОВЕ ФУЛЛЕРЕНА | 2016 |
|
RU2641041C1 |
| 2-(3-(4-(7H-пирроло[2,3-d]пиримидин-4-ил)-1H-пиразол-1-ил)-1-(этилсульфонил)азетидин-3-ил)ацетонитрила геминафтилдисульфонат в качестве ингибитора Янус киназ | 2016 |
|
RU2644155C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837215C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837316C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837533C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837548C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837216C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНОВ | 2024 |
|
RU2837221C1 |
Изобретение относится к области фармацевтики и медицины, а именно к фармацевтической композиции, регулирующей иммунный ответ живого организма, представляющей собой смесь азотистого гетероциклического соединения и фуллеренола, где в качестве азотистого гетероциклического соединения использован барицитиниб, а в качестве фуллеренола применен фуллеренол С60. Технический результат заключается в снижении уровня провоспалительных цитокинов в живом организме. 3 з.п. ф-лы, 1 ил., 4 табл., 2 пр.
1. Фармацевтическая композиция, регулирующая иммунный ответ живого организма, представляющая собой смесь азотистого гетероциклического соединения и фуллеренола, где в качестве азотистого гетероциклического соединения использован барицитиниб, а в качестве фуллеренола применен фуллеренол С60.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что дополнительно содержит природные антиоксиданты.
3. Фармацевтическая композиция по п. 1, отличающаяся тем, что дополнительно содержит витамин С и/или витамины группы В.
4. Фармацевтическая композиция по п. 1, отличающаяся тем, что содержится в фармацевтическом растворителе.
| CN 111514306 A, 11.08.2020 | |||
| MILES D | |||
| H | |||
| et al | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| - Vol | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| - No | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| - P | |||
| Кирпичный свод для кузнечных печей при паровых молотах | 1925 |
|
SU2244A1 |
| DJORDJEVIC A | |||
| et al | |||
| Review of synthesis and antioxidant potential of fullerenol nanoparticles // Journal of Nanomaterials | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| - | |||
Авторы
Даты
2024-09-03—Публикация
2021-10-29—Подача