Изобретение относится к пероральной тонкой пленке, способу ее получения, а также к применению такой пероральной тонкой пленки в качестве лекарственного средства.
Пероральные тонкие пленки представляют собой пленки, содержащие по меньшей мере одно фармацевтически активное вещество, которые помещают непосредственно в полость рта или наносят на слизистую оболочку полости рта и которые там растворяются или соответственно набухают и при этом высвобождают активное вещество. Речь при этом идет прежде всего об однослойных или многослойных содержащих действующее вещество тонких пленках на полимерной основе, которые после их укладывания на слизистую оболочку, в частности, на слизистую оболочку полости рта, могут выделять активное вещество непосредственно в полость рта. Очень хорошая циркуляция крови в слизистой оболочке полости рта обеспечивает быструю передачу активного вещества в кровоток. Преимущество данной системы введения состоит в том, что активное вещество в значительной степени всасывается через слизистую оболочку, и, таким образом исключается "метаболизм первого прохода", который происходит в случае обычной лекарственной формы активного вещества в виде таблеток. Активное вещество может быть растворено, эмульгировано или диспергировано в пленке.
Пероральные тонкие пленки в форме пены, в принципе, могут иметь высокую загрузку фармацевтически активного вещества. Данные пероральные тонкие пленки с высокой загрузкой в форме пены обычно демонстрируют очень быстрое время дезинтеграции, что выгодно для многих применений.
В других случаях, однако, может быть желательным, чтобы пероральные тонкие пленки с высокой загрузкой в форме пены дольше оставались в полости рта, чтобы, например, обеспечить более длительное трансмукозальное всасывание фармацевтически активного вещества.
Типичная проблема при производстве пероральных тонких пленок, которые медленно высвобождают фармацевтически активное вещество, заключается в том, что полимеры, обычно используемые для данной цели, образуют высоковязкие водные растворы и тем самым снижают содержание твердых веществ в растворе активного вещества, что помимо прочего значительно увеличивает время сушки.
Задача настоящего изобретения состояла в предоставлении пероральной тонкой пленки, включающей полимерную матрицу в форме отвержденной пены, имеющей полые пространства, скорость дезинтеграции которых можно регулировать в максимально широком диапазоне. Кроме того, пероральная тонкая пленка должна иметь возможность для как можно более простого и быстрого производства. В частности, следует избегать высоковязких растворов и длительного времени сушки.
Неожиданным образом данная задача была решена посредством пероральной тонкой пленки по п. 1. Такая пероральная тонкая пленка характеризуется тем, что имеет полимерную матрицу в форме отвержденной пены, имеющей полые пространства, причем полимерная матрица содержит по меньшей мере одно фармацевтически активное вещество, по меньшей мере один первый полимер, который включает водорастворимый полимер, и по меньшей мере один второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль.
Посредством добавления мукоадгезивного полимера со среднечисловой молекулярной массой, равной или больше 100000 г/моль, может быть предоставлена композиция пены, которая имеет более длительное время пребывания в ротовой полости. Кроме того посредством добавления мукоадгезивного полимера со среднечисловой молекулярной массой, равной или больше 100000 г/моль, достигается повышенная мукоадгезивность, так что пена лучше прилипает к слизистой оболочке и может удерживать активное вещество в месте абсорбции.
В принципе, пероральная тонкая пленка может быть получена так же, как и ранее известные пероральные тонкие пленки, поскольку добавленный мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, оказывает лишь незначительное влияние на физические характеристики во время суспензирования и сушки. Поскольку даже очень небольшое количество мукоадгезивного полимера со среднечисловой молекулярной массой, равной или больше 100000 г/моль, может вызвать замедленное по времени растворения, возможная загрузка активного вещества практически не изменяется.
В настоящем тексте термин «включающий» может также означать «состоящий из».
Водорастворимые полимеры включают химически самые различные природные или синтетические полимеры, общим признаком которых является их растворимость в воде или водной среде. Необходимым условием для этого является то, чтобы данные полимеры имели достаточное для растворимости в воде количество гидрофильных групп и не являлись сшитыми. Гидрофильные группы могут быть неионными, анионными, катионными и/или цвиттер-ионными группами.
Под «водорастворимым» предпочтительно понимают растворимость более 100 г/л в воде при 25°С.
На процесс мукоадгезии в основном влияют посредством свойств используемых полимеров, такие как степень сшивания, длина цепи и различные функциональные группы в структуре полимера. Мукоадгезивные системы используются во многих органеллах, покрытых слизистой оболочкой, для доставки активных веществ местного или системного действия.
Мукоадгезия может быть определена как явление молекулярных сил притяжения на границе раздела поверхностей слизистой оболочки, в данном случае слизистой оболочки полости рта, и мукоадгезивных полимеров, что позволяет полимерам держатся на слизистой оболочке в течение длительного периода времени.
Второй полимер, который включает по меньшей мере один мукоадгезивный полимер, имеет среднечисловую молекулярную массу равную или более 100000 г/моль, предпочтительно более 200000 г/моль, или более 300000 г/моль, или более 400000 г/моль или более 500000 г/моль, или более 600000 г/моль, или более 700000 г/моль, или более 800000 г/моль, или более 900000 г/моль.
Особенно предпочтительными также являются мукоадгезивные полимеры со среднечисловой молекулярной массой, равной или больше 1000000 г/моль, или 2000000 г/моль, или 3000000 г/моль, или 4000000 г/моль, или 5000000 г/моль, или 6000000 г/моль , или 7000000 г/моль.
Молекулярную массу определяют в соответствии со способами, известными специалисту в данной области, такими как, например, гель-проникающая хроматография.
Предпочтительно второй полимер, включающий по меньшей мере один мукоадгезивный полимер, имеющий среднечисловую молекулярную массу, равную или больше 100000 г/моль, представляет собой водорастворимый полимер, как определено выше.
Предпочтительно пероральная тонкая пленка согласно изобретению дополнительно характеризуется тем, что первый полимер включает полимер, имеющий среднечисловую молекулярную массу менее 100000 г/моль, предпочтительно менее 80000 или менее 60000.
Молекулярную массу определяют в соответствии со способами, известными специалисту в данной области, такими как, например, гель-проникающая хроматография.
Первый полимер, который включает водорастворимый полимер, предпочтительно выбран из группы, включающей крахмал и производные крахмала, декстраны, производные целлюлозы, такие как карбоксиметилцеллюлоза, гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилэтилцеллюлоза, натрийкарбоксиметилцеллюлоза, этил- или пропилцеллюлоза; полиакриловые кислоты, полиакрилаты, поливинилпирролидоны, сополимеры винилпирролидона и винилацетата, поливиниловые спирты, полиэтиленоксидные полимеры, полиакриламиды, полиэтиленгликоли, желатин, коллаген, альгинаты, пектин, пуллулан, трагакант, хитозан, альгиновую кислоту, арабиногалактан, галактоманнан, агар-агар, агарозу, карраген и природные каучуки, причем поливиниловые спирты являются особо предпочтительными.
Предпочтительно пероральная тонкая пленка согласно изобретению дополнительно характеризуется тем, что второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, выбран из группы, состоящей из поли(этилен)оксидных полимеров, производных крахмала, полиакриловых кислот, амилопектинов и/или поливиниловых спиртов, в частности смесей из полиакрилатов или соответственно полиакриловых кислот и амилопектинов.
Подходящими вторыми полимерами являются, например, поли(этилен)оксидные полимеры, такие как полиэтиленгликоли, со среднечисловой молекулярной массой примерно 1000000 г/моль или примерно 7000000 г/моль, которые доступны, например, под торговой маркой «Polyox WSR N12» или «Polyox WSR 303».
Другие подходящие вторые полимеры представляют собой смеси из полиакрилата или соответственно полиакриловой кислоты и амилопектина, которые доступны под торговым названием "Proloc 15".
Кроме того в качестве второго полимера подходящими являются длинноцепочечные поливиниловые спирты. Например, поливиниловый спирт со среднечисловой молекулярной массой около 200000 г/моль, который доступен, например, под торговым названием «PVA 40-88».
Пероральная тонкая пленка согласно изобретению предпочтительно отличается тем, что в пероральной тонкой пленке первый полимер содержится в количестве от 40 до 95 % масс., предпочтительно от 45 до 85 % масс. и особо особенно предпочтительно от 48 до 80 % масс., в пересчете на общую массу пероральной тонкой пленки.
Предпочтительно второй полимер присутствует в пероральной тонкой пленке в количестве от 0,1 до 20 % масс., предпочтительно от 2 до 18 % масс., особенно предпочтительно от 5 до 15 % масс., в пересчете на общую массу пероральной тонкой пленки.
По меньшей мере одно фармацевтически активное вещество в принципе не подлежит никаким ограничениям, но предпочтительно выбрано из всех фармацевтически активных веществ, подходящих для перорального и/или трансмукозального введения.
Предпочтительно активные вещества выбирают из группы, включающей классы активных веществ анальгетики, гормоны, снотворные, седативные средства, противоэпилептические средства, психотропные амины, психонейротропные средства, блокаторы нервно-мышечной системы, спазмолитики, антигистаминные средства, противоаллергические средства, кардиотоники, антиаритмические средства, диуретики, гипотензивные средства, вазопрессоры, антидепрессанты, противокашлевые средства, отхаркивающие средства, гормоны щитовидной железы, половые гормоны, противодиабетические средства, противоопухолевые средства, антибиотики, химиотерапевтические и наркотические средства, причем данная группа не является окончательной.
Особенно предпочтительно в случае по меньшей мере одного фармацевтически активного вещества речь идет о кетамине.
Под кетамином понимают (S)-(±)-2-(2-хлорфенил)-2-(метиламино)циклогексан-1-он, (R)-(±)-2-(2-хлорфенил)-2-(метиламино)циклогексан-1-он и рацемат (RS)-(±)-2-(2-хлорфенил)-2-(метиламино)циклогексан-1-он.
Особенно предпочтительно, чтобы (S)-кетамин был единственным стереоизомером кетамина, поскольку анальгетическая и анестезирующая активность (S)-кетамина примерно в три раза выше, чем у (R)-формы.
Содержание активного вещества в пероральной тонкой пленке может варьироваться в относительно широких пределах. В качестве пригодного можно привести диапазон от 10 до 60 % масс., в пересчете на общую массу (сухую общую массу) пероральной тонкой пленки. В одном варианте осуществления содержание активного вещества в пероральной тонкой пленке находится ближе к нижнему пределу диапазона, например, в случае, если активное вещество обладает чрезвычайно неприятным вкусом, для компенсации которого необходимо использовать большие количества маскирующих вкус средств. В данном случае в качестве подходящего содержания активного вещества можно привести диапазон от 10 до 40 % масс. В другом варианте осуществления содержание активного вещества в лекарственной форме согласно изобретению находится ближе к верхнему пределу диапазона, причем в качестве особенно предпочтительного может быть приведено содержание от 40 до 60 % масс., в частности содержание от 45 до 55 % масс.
Количество активного вещества в разовой дозе составляет до 100 мг, предпочтительно до 50 мг, особенно предпочтительно до 40 мг и наиболее предпочтительно до 35 мг. С другой стороны, минимальное количество активного вещества в разовой дозе предпочтительно должно составлять 5 мг, более предпочтительно 10 мг, наиболее предпочтительно 15 мг. В зависимости от конкретного применения содержание активного вещества может находиться в верхнем диапазоне указанных выше значений, например, в диапазоне от 50 до 100 мг. Также может быть приемлемым содержание действующего вещества от 30 до 50 мг.
Кроме того пероральная тонкая пленка согласно изобретению предпочтительно отличается тем, что пероральная тонкая пленка содержит по меньшей мере одно вспомогательное вещество, выбранное из группы, включающей красители, ароматизаторы, подсластители, пластификаторы, маскирующие вкус вещества, эмульгаторы, энхансеры, регуляторы рН, увлажнители, консерванты и/или антиоксиданты.
Каждое из данных вспомогательных веществ предпочтительно присутствует в количестве от 0,1 до 40 % масс., предпочтительно от 0,1 до 30 % масс., более предпочтительно от 0,1 до 15 % масс., наиболее предпочтительно от 0,1 до 10 % масс. или 0,1% до 5 % масс., в пересчете на общую массу пероральной тонкой пленки.
Многослойная пероральная тонкая пленка согласно изобретению в принципе не ограничена количеством содержащихся слоев.
Таким образом, возможны варианты осуществления, в которых пероральная тонкая пленка согласно изобретению имеет несколько содержащих активное вещество слоев.
Предпочтительно пероральная тонкая пленка согласно изобретению отличается тем, что она находится в форме отвержденной пены, имеющей полые пространства.
Преимущество данного варианта осуществления состоит в том, что, несмотря на сравнительно высокую массу единицы площади, ее получение в виде пены позволяет выполнять сушку быстрее по сравнению с сопоставимой не вспененной композицией.
Предпочтительно пероральная тонкая пленка согласно изобретению отличается тем, что полые пространства изолированы друг от друга и предпочтительно имеют форму пузырьков, причем полые пространства заполнены воздухом или газом, предпочтительно инертным газом, более предпочтительно азотом, углекислым газом, гелием или смесью по меньшей мере двух из данных газов.
Согласно другому варианту осуществления изобретения полые пространства соединены друг с другом и предпочтительно образуют сплошную канальную систему, пронизывающую полимерную матрицу.
Объемная доля указанных полых пространств в пересчете на общий объем матричного слоя предпочтительно составляет от 5 до 98 %, предпочтительно от 50 до 80 %. Таким образом благоприятно влияют на положительный эффект, заключающийся в укорененном растворении пероральной тонкой пленки.
Кроме того, для повышения стабильности пены перед или после сушки, к пероральной тонкой пленке используемой для образования пены, или к полученной пене перед или после сушки можно добавлять поверхностно-активные вещества, или соответственно тензиды.
Другим параметром, оказывающим влияние на свойства предлагаемой в изобретении пероральной тонкой пленки, является диаметр полых пространств или пузырьков. Пузырьки или полые пространства предпочтительно формируют с помощью взбивающего пену устройства, посредством которого диаметр пузырьков можно регулировать в широком, почти любом диапазоне. Так, например, диаметр пузырьков или полых пространств может находиться в диапазоне от 0,01 до 60 мкм. Диаметр пузырьков или полых пространств особенно предпочтительно составляет от 10 до 50 мкм.
Пероральная тонкая пленка согласно изобретению предпочтительно имеет площадь от 0,5 см2 до 10 см2, более предпочтительно от 2 см2 до 8 см2.
Масса единицы площади пероральной тонкой пленки согласно изобретению предпочтительно составляет по меньшей мере 10 г/м², более предпочтительно по меньшей мере 20 г/м² или по меньшей мере 30 г/м² или наиболее предпочтительно по меньшей мере 50 г/м² или менее или равно 400 г/м², более предпочтительно менее или равно 350 г/м², или менее или равно 300 г/м², или наиболее предпочтительно менее или равно 150 г/м². Предпочтительно масса единицы площади составляет от 10 до 400 г/м², более предпочтительно от 20 до 350 г/м² или от 30 до 300 г/м² и наиболее предпочтительно от 50 до 200 г/м².
Предпочтительно пероральная тонкая пленка согласно изобретению имеет толщину от примерно 10 мкм до примерно 1000 мкм, особенно предпочтительно от примерно 20 мкм до примерно 500 мкм.
Предпочтительно высвобожденное из пероральной тонкой пленки активное вещество либо всасывается в месте применения, например, через слизистую оболочку полости рта, либо транспортируется в другое место организма и всасывается в данном месте (например, в желудочно-кишечном тракте после проглатывания высвобожденного в ротовой полости активного вещества).
Время пребывания пероральной тонкой пленки согласно изобретению в месте ее применения (например, в ротовой полости), или соответственно время дезинтеграции предпочтительно находится в диапазоне от 10 секунд до 10 минут, более предпочтительно в диапазоне от 30 секунд до 8 минут, наиболее предпочтительно в диапазоне от 1 минуты до 5 минут.
Настоящее изобретение также относится к способу получения пероральной тонкой пленки, как описано выше, который включает следующие стадии:
a) получение раствора, дисперсии или расплава, который содержит по меньшей мере первый полимер, второй полимер и по меньшей мере одно фармацевтически активное вещество,
b) вспенивание раствора, дисперсии или расплава посредством введения газа или газовой смеси, в результате химического образования газа или в результате воздействия пониженного давления на растворенный газ, при необходимости реализуемое после предварительного добавления стабилизирующего пену средства,
с) распределение вспененного раствора, дисперсии или расплава на подложке для покрытия, и
d) отверждение распределенного раствора, дисперсии или расплава, посредством сушки и удаления растворителя или соответственно посредством охлаждения.
Под «сушкой» подразумевается удаление из пероральной тонкой пленки растворителя, в частности, воды. При этом не требуется удалять из пероральной тонкой пленки весь растворитель, в частности воду, а вполне достаточно удалить лишь основное количество растворителя из пероральной тонкой пленки, чтобы произошло отверждение пены. Таким образом, пероральная тонкая пленка после сушки может иметь остаточное содержание воды.
Вследствие удаления растворителя в процессе сушки пена отверждается, причем формируется долговременная структура образовавшихся полых пространств. Пероральные тонкие пленки с желаемыми размерами поверхности или геометрическими формами получают благодаря тому, что вспененную массу перед сушкой выливают в соответствующие формы или отдельные пероральные тонкие пленки выштамповывают из плоского куска большей площади.
На форму, количество и размер формируемых полых пространств можно оказывать воздействие посредством варьирования технологических параметров, например, типа и концентрации полимеров, вязкости полимерной композиции, а также благодаря регулированию процесса вспенивания, выбору стабилизирующего пену средства и так далее.
В качестве альтернативы описанному выше способу пероральную тонкую пленку согласно изобретению можно получать способом, в соответствии с которым формирование полых пространств внутри полимерной матрицы осуществляют посредством введения гидрофобного растворителя, который не смешивается с растворителем, используемым для получения указанного выше раствора или дисперсии.
При этом получают эмульсию, которая содержит гидрофобный растворитель в виде тонко распределенных капелек.
В результате удаления растворителя в процессе последующей сушки в полимерной матрице остаются каплеобразные или пузыреобразные полые пространства.
Кроме того, в варианте описанного выше способа полые пространства можно формировать посредством добавления к раствору или дисперсии, содержащему(-ей) полимер и активное вещество, вспомогательных веществ, которые образуют газ или газы, благодаря чему масса вспенивается. Подобное вспенивание посредством образования газа можно осуществлять во время получения полимерной массы или в процессе нанесения данной массы на подложку или только во время последующих процессов сушки. Пригодные для образования газа вещества или смеси веществ известны специалисту в данной области. Кроме того, вспенивание можно осуществлять также посредством воздействия пониженного давления на предварительно растворенный газ. В качестве газа, в частности, можно использовать инертный газ, например, азот, диоксид углерода или гелий, или смесь данных газов.
В качестве альтернативы при получении пероральной тонкой пленки согласно изобретению можно исходить также из расплава матричного полимера или соответственно смеси полимеров. Соответствующую переработку в принципе осуществляют подобно известному из уровня техники нанесению покрытий из масс горячего расплава ("hot melt").
При этом для вспенивания расплава в указанный полимерный расплав посредством одного из указанных выше методов вводят газ или газовую смесь. Затем полимерный расплав распределяют или экструдируют на пригодную подложку или выливают в форму и оставляют остывать или соответственно затвердевать. Технологию переработки из расплава нельзя использовать, если ответствующее активное вещество при температуре плавления полимерного расплава является нестабильным или летучим. В случае необходимости для снижения точки плавления к полимерному расплаву можно добавлять вспомогательные вещества.
Согласно другому варианту осуществления указанного выше способа получения сначала изготавливают полимерную матрицу в виде блока. Далее, т.е. после сушки или соответственно затвердевания, посредством разрезания от блока отделяют желаемую лекарственную форму.
Это означает, что в данном варианте осуществления описанные выше стадии c) и d), заменяют следующими стадиями c2) и d2):
с2) получение блока из раствора, дисперсии или расплава;
d2) разрезание затвердевшего блока для получения плоских форм.
Кроме того, настоящее изобретение относится к пероральной тонкой пленке получаемой описанным выше способом.
Кроме того, настоящее изобретение относится к пероральной тонкой пленке, как описано выше, или получаемой вышеописанным способом в качестве лекарственного средства.
Настоящее изобретение также относится к пероральной тонкой пленке, как описано выше, или получаемой способом, описанным выше, причем в качестве фармацевтически активного вещества присутствует кетамин, предпочтительно (S)-кетамин и/или его фармацевтически приемлемая соль, для применения при лечении болей и/или депрессий, в частности для снижения риска самоубийства и/или для применения в качестве общего анестетика, предпочтительно для инициирования или проведения общего наркоза или в качестве дополнения при местной анестезии и/или в качестве анальгетика.
Предпочтительные варианты осуществления, приведенные выше для многослойной тонкой пленки, также применимы к способу согласно изобретению, к полученной с помощью данного способа многослойной пероральной тонкой пленке, и ее применению в качестве лекарственного средства.
Настоящее изобретение далее более подробно разъясняется посредством неограничивающих притязания примеров.
Примеры
В далее следующих примерах используют следующие полимеры:
PVA 4-88: Поливиниловый спирт (MW < 100,000);
PVA 40-88: Поливиниловый спирт (MW > 100,000);
Polyox WSR N12: Поли(этилен)оксидный полимер (MW примерно 1000000);
Polyox WSR 303: Поли(этилен)оксидный полимер (MW примерно 7000000);
Proloc 15: Смесь из полиакрилата и амилопектина (MW > 100 000).
Пример 1
Вспененные пероральные тонкие пленки, имеющие составы в соответствии с таблицами 1-5, без фармацевтически активного вещества, были получены следующим образом.
Получение отдельных пероральных тонких пленок осуществляли посредством методов массового производства, известных специалисту в данной области, например, путем перемешивания/смешивания содержащихся компонентов с использованием перемешивающего двигателя и подходящих перемешивающих инструментов. В полученную таким образом массу вводят газ посредством перемешивания, например, с помощью машины для взбивания пены. Вспененную массу с помощью подходящего оборудования (роликовый аппликатор, ракель, короб для нанесения краски и т.д.) наносят с постоянной толщиной слоя на подложку для покрытия. В качестве подложки для покрытия могут служить все устойчивые к температуре лентообразные материалы, с которых можно повторно отделить сухую пленку. Это может быть обеспечено за счет выбора материала подложки для покрытия (различное поверхностное натяжение между пенообразной массой и подложкой) или посредством подходящих антиадгезионных покрытий подложки для покрытия, например, с помощью силиконов или фторполимеров. Содержащийся технологический растворитель (растворители), обычно вода или смеси из воды и органических, смешивающихся с водой растворителей, удаляют посредством сушки. Из полученного таким образом твердого вспененного слоя можно изготовить пероральные тонкие пленки соответствующего размера посредством разрезания или штамповки.
собой мукоадгезивный полимер
собой мукоадгезивный полимер
собой мукоадгезивный полимер
собой мукоадгезивный полимер
собой мукоадгезивный полимер
Пероральные тонкие пленки с составами в соответствии с таблицами 1-6 демонстрировали значительно более длительное время дезинтеграции, чем композиции, не содержащие полимера с молекулярной массой более 100000 г/моль.
Пример 2
Вспененные пероральные тонкие пленки, имеющие составы в соответствии с таблицами 6-7, с (S)-Кетамин ⋅ HCl в качестве активного вещества, были получены, как указано выше.
[мг/1,67 см3)
[% масс.]
собой мукоадгезивный полимер
[мг/1,67 см3)
[% масс.]
Пероральная тонкая пленка с составом в соответствии с таблицей 6 демонстрировала значительно более длительное время дезинтеграции, чем пероральная тонкая пленка с составом в соответствии с таблицей 7, которая не содержала полимера с молекулярной массой более 100000 г/моль.
Для вспененной пероральной тонкой пленки, имеющей состав в соответствии с таблицей 6, также определяли скорость высвобождения активного вещества.
Измерение высвобождения:
При in vitro высвобождении S-кетамин высвобождали из S-кетамин ⋅ HCl-содержащих пероральных тонких пленок (OTF) и определяли. Активное вещество высвобождали в фосфатном буфере с рН 6,8 USP и затем определяется методом градиентной ВЭЖХ с обращенной фазой. Количественное определение осуществляли по внешнему стандарту.
Растворение проводили с помощью устройства для растворения 2 - (лопасть над грузилом) в соответствии с USP <711>.
Средние скорости высвобождения представлены в таблице 9.
Высвобождение активного вещества из пероральной тонкой пленки в соответствии с таблицей 7 (англ. fast-release) сравнивали с высвобождением активного вещества из пероральной тонкой пленки, которая характеризуется намного более медленным высвобождением активного вещества (англ. slow-release).
Состав пероральной тонкой пленки с медленным высвобождением приведен в таблице 10.
[% масс.]
(замедляющий дезинтеграцию),
представляющий
собой мукоадгезивный полимер
Для вспененных пероральных тонких пленок, имеющих состав в соответствии с таблицей 7 и таблицей 10, также определяли скорость высвобождения активного вещества, как указано выше.
Средние скорости высвобождения представлены на фигуре 1.
Пример 3:
Вспененную пероральную тонкую пленку, имеющую состав в соответствии с таблицей 11 с (S)-кетамин ⋅ HCl в качестве активного вещества, получали, как указано выше.
[% масс.]
Для вспененной пероральной тонкой пленки, имеющей состав в соответствии с таблицей 11, также определяли скорость высвобождения активного вещества, как указано выше.
Средние скорости высвобождения представлены в таблице 12.
| название | год | авторы | номер документа |
|---|---|---|---|
| МНОГОСЛОЙНАЯ ПЕРОРАЛЬНАЯ ТОНКАЯ ПЛЕНКА | 2022 |
|
RU2832736C1 |
| ТОНКАЯ ПЛЕНКА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2021 |
|
RU2838392C1 |
| БЫСТРО РАСПАДАЮЩИЕСЯ ВСПЕНЕННЫЕ ПАСТИЛКИ С ВЫСОКОЙ МАССОЙ В ПЕРЕСЧЕТЕ НА ЕДИНИЦУ ПЛОЩАДИ | 2018 |
|
RU2826556C1 |
| КОНДИТЕРСКИЙ ПРОДУКТ | 2004 |
|
RU2347367C1 |
| ПЕРОРАЛЬНАЯ ТОНКАЯ ПЛЕНКА С ВЫСОКОЙ ЗАГРУЗКОЙ АКТИВНОГО ВЕЩЕСТВА | 2018 |
|
RU2754824C1 |
| РАСПАДАЮЩИЕСЯ ПЕРОРАЛЬНЫЕ ПЛЕНКИ | 2007 |
|
RU2436565C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОРАЛЬНОЙ ТОНКОЙ ПЛЕНКИ, СОДЕРЖАЩЕЙ МИКРОЧАСТИЦЫ | 2021 |
|
RU2811825C1 |
| ПРОДУКТЫ ПЕРОРАЛЬНОЙ ДОСТАВКИ, СОДЕРЖАЩИЕ ТРЕХМЕРНЫЕ ОБЪЕКТЫ | 2013 |
|
RU2598044C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ИЛИ НУТРИЦЕВТИЧЕСКИЙ СОСТАВ | 2010 |
|
RU2604861C2 |
| ТРАНСМУКОЗАЛЬНАЯ ТЕРАПЕВТИЧЕСКАЯ СИСТЕМА, СОДЕРЖАЩАЯ АГОМЕЛАТИН | 2020 |
|
RU2839934C1 |

Настоящее изобретение относится к пероральной тонкой пленке, включающей полимерную матрицу в форме отвержденной пены, имеющей полые пространства, причем полимерная матрица содержит по меньшей мере одно фармацевтически активное вещество, по меньшей мере один первый полимер, который включает водорастворимый полимер, и по меньшей мере один второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, к способу ее получения, а также к применению такой пероральной тонкой пленки в качестве лекарственного средства. 5 н. и 9 з.п. ф-лы, 1 ил., 12 табл., 3 пр.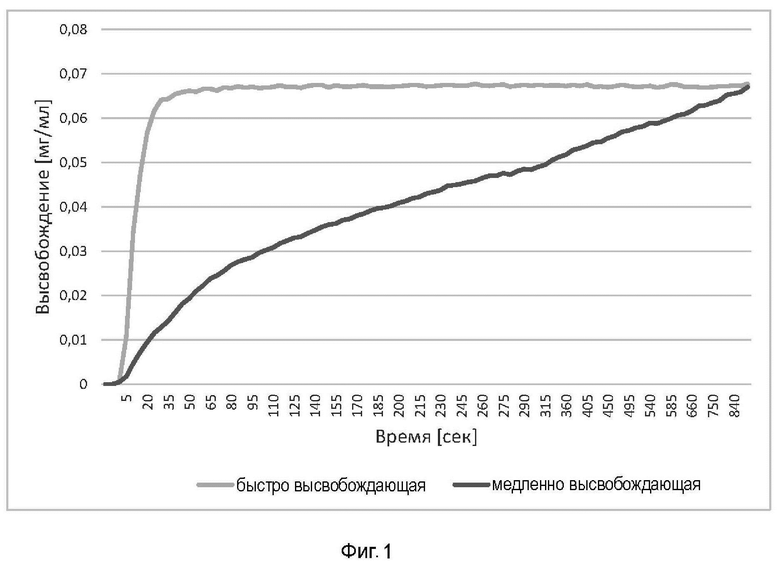
1. Пероральная тонкая пленка, включающая полимерную матрицу в форме отвержденной пены, имеющей полые пространства, причем полимерная матрица содержит по меньшей мере одно фармацевтически активное вещество, по меньшей мере один первый полимер, который включает водорастворимый полимер, и по меньшей мере один второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, причем по меньшей мере одно фармацевтически активное вещество содержится в пероральной тонкой пленке в количестве от 40 до 60% масс., в пересчете на общую массу пероральной тонкой пленки, причем первый полимер включает полимер, имеющий среднечисловую молекулярную массу менее 100000 г/моль.
2. Пероральная тонкая пленка по п. 1, отличающаяся тем, что по меньшей мере один мукоадгезивный полимер включает водорастворимый полимер.
3. Пероральная тонкая пленка по п. 1, отличающаяся тем, что первый полимер выбран из группы, включающей крахмал и производные крахмала, декстраны, производные целлюлозы, такие как карбоксиметилцеллюлоза, гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилэтилцеллюлоза, натрийкарбоксиметилцеллюлоза, этил- или пропилцеллюлоза; полиакриловую кислоту, полиакрилаты, поливинилпирролидоны, сополимеры винилпирролидона и винилацетата, поливиниловые спирты, поли(этилен)оксидные полимеры, полиакриламиды, полиэтиленгликоли, желатин, коллаген, альгинаты, пектин, пуллулан, трагакант, хитозан, альгиновую кислоту, арабиногалактан, галактоманнан, агар-агар, агарозу, карраген и/или природную камедь.
4. Пероральная тонкая пленка по п. 1, отличающаяся тем, что второй полимер выбран из группы, включающей поли(этилен)оксидные полимеры, производные крахмала, полиакриловые кислоты, амилопектины и/или поливиниловые спирты, в частности смеси из полиакрилатов или соответственно полиакриловых кислот и амилопектинов.
5. Пероральная тонкая пленка по п. 1, отличающаяся тем, что первый полимер содержится в пероральной тонкой пленке в количестве от 40 до 95% масс., в пересчете на общую массу пероральной тонкой пленки.
6. Пероральная тонкая пленка по п. 1, отличающаяся тем, что второй полимер содержится в пероральной тонкой пленке в количестве от 0,1 до 20% масс., в пересчете на общую массу пероральной тонкой пленки.
7. Пероральная тонкая пленка по п. 1, отличающаяся тем, что по меньшей мере одно фармацевтически активное вещество содержится в пероральной тонкой пленке в количестве от 45 до 55% масс., в пересчете на общую массу пероральной тонкой пленки.
8. Пероральная тонкая пленка по п. 1, отличающаяся тем, что полые пространства изолированы друг от друга и предпочтительно имеют форму пузырьков, причем полые пространства заполнены воздухом или газом, предпочтительно инертным газом, более предпочтительно азотом, углекислым газом, гелием или смесью по меньшей мере двух из данных газов.
9. Пероральная тонкая пленка по п. 1, отличающаяся тем, что полые пространства соединены друг с другом и предпочтительно образуют сплошную канальную систему, пронизывающую полимерную матрицу.
10. Пероральная тонкая пленка по одному из пп. 1-9, отличающаяся тем, что указанные полые пространства имеют объемную долю от 5 до 98%, предпочтительно от 50 до 80%, в пересчете на общий объем пероральной тонкой пленки.
11. Способ получения пероральной тонкой пленки по одному из пп. 1-10, отличающийся тем, что включает стадии:
a) получение раствора, дисперсии или расплава, который содержит по меньшей мере первый полимер, второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, и по меньшей мере одно фармацевтически активное вещество;
b) вспенивание раствора, дисперсии или расплава посредством введения газа или газовой смеси, в результате химического образования газа или в результате воздействия пониженного давления на растворенный газ, при необходимости после предварительного добавления стабилизирующего пену средства;
c) распределение вспененного раствора, дисперсии или расплава на подложке для покрытия; и
d) отверждение распределенного раствора, дисперсии или расплава посредством сушки и удаления растворителя или соответственно посредством охлаждения,
причем по меньшей мере одно фармацевтически активное вещество содержится в пероральной тонкой пленке в количестве от 40 до 60% масс., в пересчете на общую массу пероральной тонкой пленки,
причем первый полимер включает полимер, имеющий среднечисловую молекулярную массу менее 100000 г/моль.
12. Способ получения пероральной тонкой пленки по одному из пп. 1-10, отличающийся тем, что включает стадии:
a) получение раствора, дисперсии или расплава, который содержит по меньшей мере первый полимер, второй полимер, который включает мукоадгезивный полимер со среднечисловой молекулярной массой, равной или больше 100000 г/моль, и по меньшей мере одно фармацевтически активное вещество;
b) вспенивание раствора, дисперсии или расплава посредством введения газа или газовой смеси, в результате химического образования газа или в результате воздействия пониженного давления на растворенный газ, при необходимости после предварительного добавления стабилизирующего пену средства;
с2) получение блока из раствора, дисперсии или расплава;
d2) разрезание затвердевшего блока для получения плоских форм, причем по меньшей мере одно фармацевтически активное вещество содержится в пероральной тонкой пленке в количестве от 40 до 60% масс., в пересчете на общую массу пероральной тонкой пленки, причем первый полимер включает полимер, имеющий среднечисловую молекулярную массу менее 100000 г/моль.
13. Пероральная тонкая пленка, получаемая способом по одному из пп. 11 или 12.
14. Применение пероральной тонкой пленки по одному из пп. 1-10 или 13 в качестве лекарственного средства для перорального и/или трансмукозального введения.
| ПЛОСКИЙ ИЛИ ПЛАСТИНЧАТЫЙ ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ С ИСПРАВЛЕННЫМ ВКУСОМ | 2003 |
|
RU2316316C2 |
| БЫСТРО РАСПАДАЮЩАЯСЯ ФОРМА ДОЗИРОВКИ, ВЫСВОБОЖДАЮЩАЯ ДЕЙСТВУЮЩИЕ ИНГРЕДИЕНТЫ В РОТОВУЮ ПОЛОСТЬ ИЛИ ПОЛОСТИ ТЕЛА | 2005 |
|
RU2356533C2 |
| MASEK JOSEF et al | |||
| Multi-layered nanofibrous mucoadhesive films for buccal and sublingual administration of drug-delivery and vaccination nanoparticles - important step towards effective mucosal vaccines, JOURNAL OF CONTROLLED RELEASE, ELSEVIER, AMSTERDAM, NL, Band 249, 2016.07.25, Seite | |||
Авторы
Даты
2024-10-30—Публикация
2022-01-14—Подача