ПЕРЕКРЕСТНАЯ ССЫЛКА
[0001] Настоящая заявка испрашивает приоритет предварительной заявки на патент США №62/861214, поданной 13 июня 2019 года, содержание которой включено в данный документ посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит перечень последовательностей, который был представлен в электронном виде в формате ASCII и включен в данный документ посредством ссылки во всей своей полноте. Указанная копия ASCII, созданная 12 июня 2020 года, называется AT-021_02_SL_ST25.txt и имеет размер 26590 байт.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0003] Настоящее изобретение относится к антигенсвязывающим молекулам, в том числе без ограничения антителам, которые специфически связывают белки редактирования генов (например, белки TALEN, содержащие каталитический домен FokI, также упоминаемой как Fok-1 или Fok1), и кодирующим их полинуклеотидам, а также способам их применения.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0004] Инструменты редактирования генома, такие как эффекторные нуклеазы, подобные активатору транскрипции (TALEN®), нуклеазы типа «цинковый палец» (ZFN) и РНК-направляемые нуклеазы FokI (RFN), представляют собой мощные инструменты, позволяющие осуществлять точную проверку, вставку или делецию генов. TALEN, ZFN и RFN могут связываться с целевыми участками в геноме и осуществлять расщепление в них. Репарация полученной расщепленной ДНК осуществляется посредством эндогенного клеточного механизма репарации ДНК, представляющего собой негомологичное соединение концов (NHEJ), или посредством репарации, направляемой гомологией (HDR), при обеспечении матрицы репарации. В TALEN используется ДНК-связывающий домен эффектора TAL, слитый с ДНК-расщепляющим доменом (например, FokI). ZFN состоят из расщепляющего или каталитического домена рестрикционной эндонуклеазы, например, FokI, связанного со сконструированным «цинковым пальцем» Cys2His2, ДНК-связывающими полипептидами. RFN состоят из нуклеазы FokI, слитой с каталитически неактивной формой Cas9. Предполагается, что для эффективного редактирования генома у млекопитающих (например, людей, собак, крупного рогатого скота, приматов, отличных от человека, и т.д.) TALEN, ZFN и RFN будут экспрессироваться на высоком уровне. Из-за риска устойчивой нуклеазной активности и нецелевых эффектов, а также потенциальной иммуногенности в данной области существует потребность в антителах, которые распознают инструменты редактирования генома (например, антитела к TALEN и/или FokI), обладающих способностью связывать нуклеазные белки, с целью оценки безопасности и эффективности различных видов терапии, предусматривающих редактирование генов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0005] Настоящее изобретение предусматривает, среди прочего, антитела для выявления каталитических доменов FokI и полноразмерных белков TALEN в образце. Как описано в данном документе, в том числе в представленных ниже примерах, настоящее изобретение предусматривает антитела к TALEN, которые специфически связывают белки TALEN и FokI. В некоторых вариантах осуществления антитела к TALEN по настоящему изобретению могут применяться для оценки видов терапии и процессов, предусматривающих редактирование генов.
[0006] В одном аспекте настоящее изобретение предусматривает антитело к TALEN, содержащее аминокислотную последовательность вариабельной области тяжелой цепи, которая характеризуется по меньшей мере 85% идентичностью с SEQ ID NO: 3, и аминокислотную последовательность вариабельной области легкой цепи, которая характеризуется по меньшей мере 85% идентичностью с SEQ ID NO: 7. В одном варианте осуществления антитело к TALEN является гуманизированным. В различных вариантах осуществления антитело выбрано из группы, состоящей из антитела, scFv, Fab, Fab', Fv, F(ab')2, dAb, человеческого антитела, гуманизированного антитела, химерного антитела, моноклонального антитела, поликлонального антитела, рекомбинантного антитела, антитела IgE, антитела IgD, антитела IgM, антитела IgG1, антитела IgG1, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG2, антитела IgG2, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG3, антитела IgG3, содержащего по меньшей мере одну мутацию в шарнирной области, антитела IgG4, антитела IgG4, содержащего по меньшей мере одну мутацию в шарнирной области, антитела, содержащего по меньшей мере одну не встречающуюся в природе аминокислоту, и любой их комбинации.
[0007] В конкретных вариантах осуществления антитело содержит вариабельную область тяжелой цепи (НС), выбранную из группы, состоящей из SEQ ID NO: 3-6, и в дополнительных вариантах осуществления антитело к TALEN содержит CDR1 тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 12-14, и/или CDR2 тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 15-20, и/или CDR3 тяжелой цепи, содержащую SEQ ID NO: 21. В конкретных вариантах осуществления антитело к TALEN содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи, при этом каждая CDR содержит аминокислотную последовательность, показанную в табл. 1с. Также предусмотрено антитело к TALEN, содержащее аминокислотную последовательность VH, которая характеризуется по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100% идентичностью с VH антиген связывающей молекулы, предусмотренной в данном документе.
[0008] В других вариантах осуществления антитело к TALEN содержит последовательность вариабельной области легкой цепи (VL), выбранную из группы, состоящей из SEQ ID NO: 7-11. В конкретных вариантах осуществления антитело к TALEN содержит CDR1 легкой цепи, содержащую SEQ ID NO: 22, и/или CDR2 легкой цепи, выбранную из группы, состоящей из SEQ ID NO: 23-25, и/или CDR3 легкой цепи, выбранную из группы, состоящей из SEQ ID NO: 26-28. Дополнительно предусмотрено антитело к TALEN, где легкая цепь содержит CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом каждая CDR содержит аминокислотную последовательность, показанную в табл. 1d. Также предусмотрено антитело к TALEN, содержащее аминокислотную последовательность VL, которая характеризуется по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100% идентичностью с VL антиген связывающей молекулы, предусмотренной в данном документе.
[0009] В другом варианте осуществления в данном документе предусмотрено антитело к TALEN, содержащее (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 23; и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, и в дополнительном варианте осуществления антитело к TALEN содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 3; и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 7.
[0010] В другом варианте осуществления в данном документе предусмотрено антитело к TALEN, содержащее (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27, и в дополнительном варианте осуществления антитело к TALEN содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 3; и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 8.
[0011] В дополнительном варианте осуществления в данном документе предусмотрено антитело к TALEN, содержащее (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 13; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 25; и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, и в дополнительном варианте осуществления антитело к TALEN содержит (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 4; и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 9.
[0012] В еще одном дополнительном варианте осуществления в данном документе предусмотрено антитело к TALEN, содержащее (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15; (c)CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 28, и в дополнительном варианте осуществления антитело к TALEN содержит (а) VH, содержащую аминокислотную последовательность под SEQ ID NO: 5; и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 10.
[0013] Также предусмотрено антитело к TALEN, содержащее (a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12; (b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17; (с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; (d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; (e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; и (f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27, и в дополнительном варианте осуществления антитело к TALEN по п. Error! Reference source not found., содержащее (a) VH, содержащую аминокислотную последовательность под SEQ ID NO: 6; и (b) VL, содержащую аминокислотную последовательность под SEQ ID NO: 11.
[0014] В различных вариантах осуществления антитело к TALEN дополнительно содержит выявляемую метку, и в некоторых вариантах осуществления выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиометки и гаптена. Если выявляемая метка представляет собой флуоресцентную метку, то флуоресцентная метка может быть выбрана из группы, состоящей из красителя Atto, красителя Alexafluor, квантовых точек, гидроксикумарина, аминокумарина, метоксикумарина, Cascade Blue, Pacific Blue, Pacific Orange, Lucifer Yellow, NBD, R-фикоэритрина (PE), конъюгатов PE-Cy5, конъюгатов PE-Cy7, Red 613, PerCP, TruRed, FluorX, флуоресцеина, BODIPY-FL, Cy2, Су3, Су3В, Cy3.5, Cy5, Су5.5, Су7, TRITC, X-родамина, Lissamine Rhocamine В, Texas Red, аллофикоцианина (АРС), конъюгатов АРС-Су7, Indo-1, Fluo-3, Fluo-4, DCFH, DHR, SNARF, GFP (мутация Y66H), GFP (мутация Y66F), EBFP, EBFP2, азурита, GFPuv, T-Sapphire, Cerulean, mCFP, mTurquoise2, ECFP, CyPet, GFP (мутация Y66W), mKeima-Red, TagCFP, AmCyan1, mTFP1, GFP (мутация S65A), Midorishi Cyan, GFP дикого типа, GFP (мутация S65C), TurboGFP, TagGFP, GFP (мутация S65L), Emerald, GFP (мутация S65T), EGFP, Azami Green, ZsGreenl, TagYFP, EYFP, Topaz, Venus, mCitrine, YPet, TurboYFP, ZsYellow1, Kusabira Orange, mOrange, аллофикоцианина (АРС), mKO, TurboRFP, tdTomato, TagRFP, мономера DsRed, DsRed2 ("RFP"), mStrawberry, TurboFP602, AsRed2, mRFP1, J-Red, R-фикоэритрина (RPE), В-фикоэритрина (BPE), mCherry, HcRed1, Katusha, P3, перидинин-хлорофилла (PerCP), mKate (TagFP635), TurboFP635, mPlum и mRaspberry. В конкретных вариантах осуществления флуоресцентная метка представляет собой R-фикоэритрин (РЕ) или аллофикоцианин (АРС).
[0015] Также предусмотрена композиция, содержащая антитело к TALEN, предусмотренное в данном документе, и приемлемый носитель или среду-носитель, например, фармацевтически приемлемый носитель или среду-носитель.
[0016] Также предусмотрены полинуклеотиды, кодирующие тяжелую цепь антитела к TALEN, раскрытого в данном документе. Также предусмотрены полинуклеотиды, кодирующие легкую цепь антитела к TALEN, раскрытого в данном документе. Также предусмотрены векторы, содержащие один или оба из полинуклеотидов, кодирующих тяжелую и легкую цепь. Более того, предусмотрена клетка, содержащая один или оба из векторов, и клетка может предусматривать клетку, выбранную из группы, состоящей из клетки СНО, клетки Sp2/0, клетки кролика и клетки Е. coli. Предусмотрен способ получения антитела к TALEN, раскрытого в данном документе, и способ включает инкубирование клетки, содержащей один или оба из векторов, описанных выше, в подходящих условиях.
[0017] В еще одном дополнительном варианте осуществления предусмотрен способ определения наличия или отсутствия белка TALEN в образце, и в одном варианте осуществления способ включает приведение образца в контакт с антителом к TALEN, конъюгированным с выявляемой меткой, и определение наличия или отсутствия белка TALEN в образце; в некоторых вариантах осуществления антитело к TALEN предусматривает антитело, предусмотренное в данном документе, или его гуманизированную форму. Кроме того, образец может представлять собой образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ех vivo или в среде для культивирования клеток.
[0018] Различные аспекты настоящего изобретения подробно описаны в следующих разделах. Использование разделов не предназначено для ограничения настоящего изобретения. Каждый раздел может относиться к любому аспекту настоящего изобретения. В данной заявке использование «или» означает «и/или», если не указано иное. Все источники литературы, цитируемые в данном документе, включены посредством ссылки во всей своей полноте. Если не определено иное, то все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понятно специалисту в области, к которой принадлежит настоящее изобретение.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0019] Графические материалы, представленные в настоящем изобретении, предназначены только для иллюстрации, а не для ограничения.
[0020] На фиг. 1 показан результат анализа посредством вестерн-блоттинга супернатантов гибридомы из слияния №2299 (номера 13-16 отмечены на фиг.) и №2296 (номера 3, 6, 7, 8 и 11 отмечены на фиг.).
ОПРЕДЕЛЕНИЯ
[0021] Если не определено иное, то все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понятно специалисту в данной области (например, в области генной инженерии, культивирования клеток, молекулярной генетики, химии нуклеиновых кислот и биохимии).
[0022] Для лучшего понимания настоящего изобретения сначала ниже приводятся определения некоторых терминов. Дополнительные определения следующих терминов и других терминов изложены на протяжении настоящего изобретения.
[0023] Аффинность: Как известно из уровня техники, термин «аффинность» относится к мере прочности связывания конкретного лиганда с его партнером. Показатели аффинности могут быть измерены различными способами. В некоторых вариантах осуществления аффинность измеряют посредством количественного анализа. В некоторых вариантах осуществления концентрация партнера по связыванию и/или концентрация лиганда может варьировать. В некоторых таких вариантах осуществления аффинность можно сравнить с эталоном в сопоставимых условиях (например, концентрациях).
[0024] Аминокислота: в своем наиболее широком смысле термин относится к любому соединению и/или веществу, которое может быть включено в полипептидную цепь, например, посредством образования одной или более пептидных связей. В некоторых вариантах осуществления аминокислота имеет общую структуру H2N-C(H)(R)-СООН. В некоторых вариантах осуществления аминокислота представляет собой встречающуюся в природе аминокислоту. В некоторых вариантах осуществления аминокислота представляет собой синтетическую аминокислоту; в некоторых вариантах осуществления аминокислота представляет собой D-аминокислоту; в некоторых вариантах осуществления аминокислота представляет собой L-аминокислоту. Термин «стандартная аминокислота» относится к любой из двадцати стандартных L-аминокислот, обычно обнаруживаемых во встречающихся в природе пептидах. Термин «аминокислота, отличная от стандартной» относится к любой аминокислоте, за исключением стандартных аминокислот, независимо от того, получена она путем синтеза или из природного источника. В некоторых вариантах осуществления аминокислота, в том числе карбокси- и/или аминоконцевая аминокислота в полипептиде, может содержать структурную модификацию по сравнению с приведенной выше общей структурой. Например, в некоторых вариантах осуществления аминокислота может быть модифицирована путем метилирования, амидирования, ацетилирования и/или замещения по сравнению с общей структурой. Как будет ясно из контекста, в некоторых вариантах осуществления термин «аминокислота» используется для обозначения свободной аминокислоты; в некоторых вариантах осуществления он используется для обозначения аминокислотного остатка полипептида.
[0025] Антитело: Используемый в данном документе термин «антитело» относится к виду антигенсвязывающих белков, содержащих полипептид, который содержит элементы канонической последовательности иммуноглобулина, достаточные для обеспечения специфического связывания с конкретным целевым антигеном. Как известно из уровня техники, интактные антитела, продуцируемые в природе, представляют собой тетрамерные средства массой приблизительно 150 кДа, состоящие из двух идентичных полипептидов тяжелой цепи (приблизительно 50 кДа каждый) и двух идентичных полипептидов легкой цепи (приблизительно 25 кДа каждый), которые связываются друг с другом с получением того, что обычно называют «Y-образной» структурой. Каждая тяжелая цепь состоит по меньшей мере из четырех доменов (длина каждого составляет приблизительно ПО аминокислот), аминоконцевого вариабельного (VH) домена (расположенного на концах Y-образной структуры), за которым следуют три константных домена: CH1, СН2 и карбоксиконцевой СН3 (расположенный в основании «ствола» Y). Короткая область, обычно называемая «переключателем», соединяет вариабельную и константную области тяжелой цепи. «Шарнир» соединяет домены СН2 и СН3 с остальной частью антитела. Две дисульфидные связи в данной шарнирной области соединяют два полипептида тяжелой цепи друг с другом в интактном антителе. Каждая легкая цепь состоит из двух доменов: аминоконцевого вариабельного (VL) домена, за которым следует карбоксиконцевой константный (CL) домен, которые отделены друг от друга другим «переключателем». Тетрамеры интактных антител состоят из двух димеров: тяжелая цепь-легкая цепь, где тяжелая и легкая цепи связаны друг с другом одной дисульфидной связью; две другие дисульфидные связи соединяют шарнирные области тяжелой цепи друг с другом таким образом, что димеры соединяются друг с другом и образуется тетрамер. Антитела, продуцируемые естественным путем, также гликозилируются, как правило, по домену СН2. Каждый домен в природном антителе имеет структуру, характеризующуюся «иммуноглобулиновой складкой», образованной двумя бета-листами (например, 3-, 4- или 5-нитевыми листами), упакованными между собой в сжатый бета-цилиндр в антипараллельной ориентации. Каждый вариабельный домен содержит три гипервариабельные петли, известные как «области, определяющие комплементарность» (CDR1, CDR2 и CDR3), и четыре в некоторой степени инвариантные «каркасные» области (FR1, FR2, FR3 и FR4). При сворачивании природных антител FR-области образуют бета-листы, которые обеспечивают структурную основу для доменов, а области петель CDR как тяжелой, так и легкой цепей объединяются вместе в трехмерном пространстве таким образом, что они создают единый гипервариабельный антиген связывающий участок, расположенный на вершине Y-образной структуры. Fc-область встречающихся в природе антител связывается с элементами системы комплемента, а также с рецепторами на эффекторных клетках, в том числе, например, на эффекторных клетках, которые опосредуют цитотоксичность. В некоторых вариантах осуществления антитело является поликлональным; в некоторых вариантах осуществления антитело является моноклональным.
[0026] Связывание: Следует понимать, что используемый в данном документе термин «связывание», как правило, относится к нековалентной связи между или среди двух или более объектов. «Прямое» связывание предусматривает физический контакт между объектами или компонентами; «непрямое» связывание предусматривает физическое взаимодействие посредством физического контакта с одним или более промежуточными объектами.
[0027] Хромосома: Используемый в данном документе термин «хромосома» относится к линейной молекуле ДНК с ассоциированными белками в ядре эукариотических клеток, которая несет гены и участвует в передаче наследственной информации.
[0028] Соответствующий: как используется в данном документе, термин указывает на положение/обозначение аминокислотного остатка в полипептиде, представляющем интерес. Специалистам в данной области будет понятно, что для простоты остатки в полипептиде часто обозначаются с использованием канонической системы нумерации, основанной на эталонном родственном полипептиде, так что аминокислота, «соответствующая» остатку в положении 190, например, не обязательно должна являться 190-й аминокислотой в конкретной аминокислотной цепи, а скорее соответствует остатку, находящемуся в положении 190 в эталонном полипептиде; специалистам в данной области без труда будет понятно, как определить «соответствующие» аминокислоты.
[0029] Выявляемый компонент: Используемый в данном документе термин «выявляемый компонент» относится к любому элементу, молекуле, функциональной группе, соединению, фрагменту или компоненту, который является выявляемым. В некоторых вариантах осуществления выявляемый компонент обеспечивается или используется отдельно. В некоторых вариантах осуществления изобретения выявляемый компонент обеспечивается и/или используется совместно (например, соединен) с другим средством. Примеры выявляемых компонентов включают без ограничения различные лиганды, радионуклиды (например, 3Н, 14С, 18F, 19F, 32Р, 35S, 135I, 125I, 123I, 64Cu, 187Re, 111In, 90Y, 99mTc, 177Lu, 89Zr и т.д.), флуоресцентные красители (такие как, например, флуоресцеиновые красители, акридиновые красители, красители SYBR, родаминовые красители, оксазиновые красители и т.д.), хемилюминесцентные средства (такие как, например, сложные эфиры акридина, стабилизированные диоксетаны и т.п.), электрохемилюминесцентные средства (такие как, например, SULFO-TAG), биолюминесцентные средства (такие как, например, люциферин), спектрально различимые неорганические флуоресцентные полупроводниковые нанокристаллы (т.е. квантовые точки), наночастицы металлов (например, золото, серебро, медь, платина и т.д.), нанокластеры, парамагнитные ионы металлов, ферменты (такие как, например, пероксидаза хрена, щелочная фосфатаза и т.д.), колориметрические метки (такие как, например, красители, коллоидное золото и т.п.), биотин, дигоксигенин, гаптены, а также белки, для которых доступны антисыворотки или моноклональные антитела.
[0030] Сконструированный: В целом термин «сконструированный» относится к аспекту, подразумевающему манипуляцию со стороны человека в его отношении. Например, полинуклеотид считается «сконструированным», если две или более последовательностей, которые в природе не связаны друг с другом в данном порядке, подвергаются манипуляции со стороны человека так, чтобы они были непосредственно связаны друг с другом в сконструированном полинуклеотид е. Например, в некоторых вариантах осуществления настоящего изобретения сконструированный полинуклеотид может содержать регуляторную последовательность, которая встречается в природе в оперативной связи с первой кодирующей последовательностью, но не в оперативной связи со второй кодирующей последовательностью, соединенную человеком так, чтобы она была оперативно связана со второй кодирующей последовательностью. Аналогичным образом, клетка или организм считаются «сконструированными», если они подвергались манипуляции таким образом, чтобы их генетическая информация была изменена (например, новый генетический материал, ранее не присутствовавший, был введен, например, посредством трансформации, спаривания, соматической гибридизации, трансфекции, трансдукции или другого механизма, или ранее присутствовавший генетический материал изменяется или удаляется, например, посредством замены или делеционной мутации, или посредством протоколов спаривания). В соответствии с общепринятой практикой и как понятно специалистам в данной области, потомки сконструированного полинуклеотида или клетки, как правило, все еще называются «сконструированными», даже если фактические манипуляции осуществлялись в отношении предшествующего объекта.
[0031] Экспрессия: Используемый в данном документе термин «экспрессия» последовательности нуклеиновой кислоты относится к одному или более из следующих явлений: (1) получение матрицы РНК из последовательности ДНК (например, посредством транскрипции); (2) процессинг транскрипта РНК (например, посредством сплайсинга, редактирования, образования 5'-кэпа и/или образования 3'-конца); (3) трансляция РНК в полипептид или белок; и/или (4) посттрансляционная модификация полипептида или белка.
[0032] FokI: Используемый в данном документе термин «FokI» (в качестве альтернативы упоминаемый как Fok1 или Fok-1) относится к бактериальной рестрикционной эндонуклеазе IIS типа, которая встречается в природе в Flavobacterium okeanokoites. Природная FokI состоит из N-концевого ДНК-связывающего домена и неспецифического ДНК-расщепляющего домена на С-конце. ДНК-расщепляющий домен FokI может функционировать независимо от ДНК-связывающего домена. Как используется в данном документе, FokI относится к белку или нуклеиновой кислоте, кодирующей белок, которая содержит ДНК-расщепляющий домен (т.е. нуклеазный домен) FokI. FokI может относиться к целому белку FokI (SEQ ID NO: 2) или только к каталитическому нуклеазному домену (SEQ ID NO: 1). Термин «FokI» относится ко всем фрагментам и вариантам FokI, в том числе к мутантам, производным, аналогам, усеченным формам, слитым конструкциям и мультимерам FokI, включая димеры FokI. В некоторых вариантах осуществления FokI получают рекомбинантным способом. В некоторых вариантах осуществления полипептид FokI конъюгирован с дополнительным фрагментом или помечен с помощью дополнительного фрагмента, например, связывающего фрагмента и/или выявляемого фрагмента. Как будет ясно из контекста, в некоторых вариантах осуществления термин «FokI» используется для обозначения полипептида FokI или его фрагментов или вариантов; в некоторых вариантах осуществления термин «FokI» используется для обозначения нуклеиновых кислот, кодирующих полипептид FokI и его фрагменты и варианты.
[0033] Фрагмент: «Фрагмент» биологической молекулы, описанный в данном документе, имеет структуру, которая содержит дискретную часть целого, но не содержит один или более компонентов, присутствующих в целом (например, полипептид, в котором отсутствует одна или более аминокислот). В некоторых вариантах осуществления фрагмент состоит из такой дискретной части. В некоторых вариантах осуществления фрагмент состоит из характерного структурного элемента или компонента, присутствующего в целом (например, полипептидного домена), или содержит его. В некоторых вариантах осуществления биологическая молекула представляет собой полимер (например, полимер нуклеиновой кислоты или полипептид). В некоторых вариантах осуществления фрагмент полимера содержит или состоит из по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, ПО, 120, 130, 140, 150, 160, 170, 180, 190, 200,210, 220, 230, 240, 250,275, 300, 325, 350, 375, 400, 425, 450,475, 500 или более мономерных единиц (например, остатков), присутствующих в целом полимере. В некоторых вариантах осуществления фрагмент полимера содержит или состоит из по меньшей мере приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 25%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или более мономерных единиц (например, остатков), присутствующих в целом полимере. В некоторых вариантах осуществления целая биологическая молекула может быть названа «родительской» по отношению к целому.
[0034] Слитый: «Слитая молекула» представляет собой молекулу, где две или более субъединичные молекулы связаны, предпочтительно ковалентно. Субъединичные молекулы могут представлять собой молекулы одинакового химического типа или могут представлять собой молекулы различных химических типов. Примеры слияний молекул одинакового химического типа включают без ограничения слитые белки (например, слияние белка типа «цинковый палец» или ДНК связывающего домена TALEN с расщепляющим доменом FokI) и слитые нуклеиновые кислоты (например, нуклеиновую кислоту, кодирующую слитый белок, описанный выше). Примеры слияний молекул различных химических типов включают без ограничения слияния нуклеиновая кислота-полипептид (например, слияние молекулы РНК с расщепляющим доменом FokI).
[0035] Ген: Используемый в данном документе термин «ген» относится к последовательности ДНК, которая кодирует продукт (например, продукт, представляющий собой РНК, и/или полипептидный продукт). В некоторых вариантах осуществления ген содержит кодирующую последовательность (т.е. последовательность, которая кодирует конкретный продукт); в некоторых вариантах осуществления ген содержит некодирующую последовательность. В некоторых конкретных вариантах осуществления ген может содержать как кодирующую (например, экзонную), так и некодирующую (например, интронную) последовательность. В некоторых вариантах осуществления ген может содержать один или более регуляторных элементов, которые, например, могут регулировать или влиять на один или более аспектов экспрессии гена (например, клеточная типоспецифическая экспрессия, индуцируемая экспрессия и т.д.).
[0036] Генная или клеточная терапия: Используемый в данном документе термин «генная или клеточная терапия» относится к вставке или делеции конкретных последовательностей геномной ДНК для лечения или предупреждения нарушения или состояния, для которого требуется такая терапия. В некоторых вариантах осуществления вставка или делеция последовательностей геномной ДНК осуществляется в конкретных клетках (т.е. целевых клетках). Целевые клетки могут быть получены от млекопитающего и/или могут представлять собой клетки в организме субъекта-млекопитающего. Млекопитающие включают без ограничения людей, собак, кошек, коров, овец, свиней, лам, приматов, отличных от человека и т.д. В некоторых вариантах осуществления гетерологичную ДНК переносят в целевые клетки. Гетерологичная ДНК может вводиться в выбранные целевые клетки таким образом, что гетерологичная ДНК экспрессируется и производится кодируемый таким образом терапевтический продукт. Дополнительно или в качестве альтернативы гетерологичная ДНК может каким-либо образом опосредовать экспрессию ДНК, которая кодирует терапевтический продукт, или она может кодировать продукт, такой как пептид или РНК, который каким-либо образом опосредует, прямо или косвенно, экспрессию терапевтического продукта. Генная или клеточная терапия может также применяться для доставки нуклеиновой кислоты, кодирующей генный продукт, который замещает дефектный ген или дополняет генный продукт, производимый млекопитающим или клеткой, в которую он введен. Гетерологичная ДНК, кодирующая терапевтический продукт, может быть модифицирована перед введением в клетки пораженного субъекта с целью повышения или какого-либо иного изменения продукта или его экспрессии. Генная или клеточная терапия может также предусматривать доставку ингибитора, или репрессора, или другого модулятора экспрессии генов. Генная терапия может включать методики in vivo или ex vivo. В некоторых вариантах осуществления генная или клеточная терапия включает введение нуклеиновых кислот, кодирующих эффекторные нуклеазы, подобные активатору транскрипции (TALEN), нуклеазы типа «цинковый палец» (ZFN) или РНК-направляемые нуклеазы FokI (RFN). В некоторых вариантах осуществления вирусные и невирусные способы переноса генов могут применяться для введения нуклеиновых кислот, кодирующих TALEN, ZFN или RFN, в клетки млекопитающих или целевые ткани. Такие способы могут применяться для введения нуклеиновых кислот, кодирующих TALEN, ZFN или RFN, в клетки in vitro. Невирусные векторные системы доставки включают ДНК-плазмиды, чистую нуклеиновую кислоту и нуклеиновую кислоту в комплексе со средой-носителем для доставки, такой как полоксамеры или липосомы. Вирусные векторные системы доставки включают ДНК-содержащие и РНК-содержащие вирусы, которые имеют либо эписомальную, либо интегрированную форму генома после доставки в клетку. Обзор процедур генной терапии см., например, в Anderson, Science 256: 808-813 (1992); Miller, Nature 357: 455-460 (1992); Feuerbach et al. Kidney International 49:1791-1794 (1996); Urnov et al. Nature Reviews Genetics 11, 636 646 (2010); и Collins et al. Proceedings Biologicial Sciences / The Royal Society, 282(182l): pii 20143003 (2015).
[0037] Геном: Используемый в данном документе термин «геном» относится к совокупной генетической информации, которую несет отдельный организм или клетка, представленной в виде полных последовательностей ДНК их хромосом.
[0038] Высокоаффинное связывание: Используемый в данном документе термин «высокоаффинное связывание» относится к высокой степени прочности, с которой конкретный лиганд связывается со своим партнером. Аффинность может быть измерена любым доступным способом, в том числе способами, известными из уровня техники. В некоторых вариантах осуществления связывание считается высокоаффинным, если в анализах связывания Kd составляет приблизительно 500 пМ или менее (например, менее чем приблизительно 400 пМ, приблизительно 300 пМ, приблизительно 200 пМ, приблизительно 100 пМ, приблизительно 90 пМ, приблизительно 80 пМ, приблизительно 70 пМ, приблизительно 60 пМ, приблизительно 50 пМ, приблизительно 40 пМ, приблизительно 30 пМ, приблизительно 20 пМ, приблизительно 10 пМ, приблизительно 5 пМ, приблизительно 4 пМ, приблизительно 3 пМ, приблизительно 2 пМ и т.д.). В некоторых вариантах осуществления связывание считается высокоаффинным, если аффинность является более выраженной (например, Kd более низкая) в отношении представляющего интерес полипептида, чем в отношении выбранного эталонного полипептида. В некоторых вариантах осуществления связывание считается высокоаффинным, если соотношение Kd в отношении представляющего интерес полипептида и Kd в отношении выбранного эталонного полипептида составляет 1:1 или менее (например, 0,9:1, 0,8:1, 0,7:1, 0,6:1, 0,5:1. 0,4:1, 0,3:1, 0,2:1, 0,1:1, 0,05:1, 0,01:1 или менее). В некоторых вариантах осуществления связывание считается высокоаффинным, если Kd в отношении представляющего интерес полипептида составляет приблизительно 100% или менее (например, приблизительно 99%, приблизительно 98%), приблизительно 97%), приблизительно 96%, приблизительно 95%), приблизительно 90%, приблизительно 85%), приблизительно 80%), приблизительно 75%, приблизительно 70%), приблизительно 65%, приблизительно 60%, приблизительно 55%, приблизительно 50%), приблизительно 45%), приблизительно 40%), приблизительно 35%), приблизительно 30%, приблизительно 25%), приблизительно 20%, приблизительно 15%), приблизительно 10%, приблизительно 5%, приблизительно 4%, приблизительно 3%), приблизительно 2%, приблизительно 1% или менее) Kd в отношении выбранного эталонного полипептида.
[0039] Гомология: Используемый в данном документе термин «гомология» относится к общему родству между полимерными молекулами, например, между молекулами нуклеиновой кислоты (например, молекулами ДНК и/или РНК) и/или между полипептидными молекулами. В некоторых вариантах осуществления полимерные молекулы считаются «гомологичными» по отношению друг к другу, если их последовательности являются на по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичными. В некоторых вариантах осуществления полимерные молекулы считаются «гомологичными» по отношению друг к другу, если их последовательности являются на по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% схожими.
[0040] In vitro: Используемый в данном документе термин «in vitro» относится к явлениям, которые происходят скорее в искусственной среде, например, в пробирке или реакционном сосуде, в культуре клеток и т.д., чем в пределах многоклеточного организма.
[0041] In vivo: как используется в данном документе, термин относится к явлениям, которые происходят в пределах многоклеточного организма, такого как человек и животное, отличное от человека. В контексте систем на основе клеток термин может использоваться для обозначения явлений, которые происходят в пределах живой клетки (в отличие, например, от систем in vitro).
[0042] Выделенный: как используется в данном документе, термин относится к веществу и/или объекту, который (1) был отделен от по крайней мере некоторых компонентов, с которыми он был связан при первоначальном получении (будь то в природе и/или в экспериментальных условиях), и/или (2) был разработан, произведен, получен и/или изготовлен человеком. Выделенные вещества и/или объекты могут быть отделены от приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99% других компонентов, с которыми они были первоначально связаны. В некоторых вариантах осуществления выделенные средства характеризуются приблизительно 80%, приблизительно 85%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99% чистотой. Как используется в данном документе, вещество является «чистым», если оно по сути не содержит других компонентов. В некоторых вариантах осуществления, как будет понятно специалистам в данной области, вещество все еще может считаться «выделенным» или даже «чистым» после объединения с определенными другими компонентами, такими как, например, один или более носителей или вспомогательных веществ (например, буфер, растворитель, вода и т.д.); в таких вариантах осуществления процент выделения или чистоты вещества рассчитывают без включения таких носителей или вспомогательных веществ. В качестве лишь одного примера, в некоторых вариантах осуществления биологический полимер, такой как полипептид или полинуклеотид, который встречается в природе, считается «выделенным», если а) в соответствии со своим происхождением или источником происхождения он не связан с некоторыми или всеми из компонентов, которые сопутствуют ему в его естественном состоянии в природе; б) он по сути не содержит других полипептидов или нуклеиновых кислот той же разновидности от вида, который производит его в природе; с) он экспрессируется или каким-либо иным образом связан с компонентами из клетки или другой системы экспрессии, которая не относится к виду, который производит ее в природе. Таким образом, например, в некоторых вариантах осуществления полипептид, который получают посредством химического синтеза или который синтезируется в клеточной системе, отличной от той, которая производит его в природе, считается «выделенным» полипептидом. В качестве альтернативы или дополнительно в некоторых вариантах осуществления полипептид, который был подвергнут одной или более методикам очистки, может считаться «выделенным» полипептидом в том смысле, что он был отделен от других компонентов, а) с которыми он связан в природе; и/или b) с которыми он был связан при первоначальном получении.
[0043] Линкер: как используется в данном документе, термин используется для обозначения той части многоэлементного полипептида, которая соединяет различные элементы друг с другом. Например, специалистам в данной области понятно, что полипептид, структура которого содержит два или более функциональных или организационных доменов, часто содержит отрезок аминокислот между такими доменами, который связывает их друг с другом. В некоторых вариантах осуществления полипептид, содержащий линкерный элемент, имеет общую структуру общей формы S1-L-S2, где S1 и S2 могут являться одинаковыми или разными и представляют собой два домена, связанные друг с другом посредством линкера. В некоторых вариантах осуществления длина линкера составляет по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26,27,28, 29, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более аминокислот. В некоторых вариантах осуществления линкер характеризуется тем, что он, как правило, не принимает жесткую трехмерную структуру, а скорее обеспечивает гибкость полипептиду. Множество различных линкерных элементов, которые могут соответствующим образом применяться при конструировании полипептидов (например, слитых полипептидов), известны из уровня техники (см., например, Holliger, P., et al. (1993) Proc. Natl. Acad. Sci. USA 90: 6444-6448; Poljak, R.J., et al. (1994) Structure 2: 1121-1123).
[0044] Нуклеиновая кислота: как используется в данном документе, в своем наиболее широком смысле термин «нуклеиновая кислота» относится к любому соединению и/или веществу, которое включено или может быть включено в олигонуклеотидную цепь. В некоторых вариантах осуществления нуклеиновая кислота представляет собой соединение и/или вещество, которое включено или может быть включено в олигонуклеотидную цепь посредством фосфодиэфирной связи. Как будет ясно из контекста, в некоторых вариантах осуществления термин «нуклеиновая кислота» относится к отдельным остаткам нуклеиновой кислоты (например, нуклеотидам и/или нуклеозидам); в некоторых вариантах осуществления термин «нуклеиновая кислота» относится к олигонуклеотидной цепи, содержащей отдельные остатки нуклеиновой кислоты. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит РНК; в некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит ДНК. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, содержит или состоит из одного или более природных остатков нуклеиновых кислот. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, содержит или состоит из одного или более аналогов нуклеиновой кислоты. В некоторых вариантах осуществления нуклеиновая кислота имеет нуклеотидную последовательность, которая кодирует функциональный генный продукт, такой как РНК или белок. В некоторых вариантах осуществления нуклеиновая кислота содержит один или более интронов. В некоторых вариантах осуществления нуклеиновые кислоты получают посредством одного или более способов, представляющих собой выделение из природного источника, ферментативный синтез путем полимеризации на основе комплементарной матрицы (in vivo или in vitro), воспроизведение в рекомбинантной клетке или системе и химический синтез. В некоторых вариантах осуществления длина нуклеиновой кислоты составляет по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 600, 700, 800, 900, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000 или более остатков. В некоторых вариантах осуществления нуклеиновая кислота является однонитевой; в некоторых вариантах осуществления нуклеиновая кислота является двухнитевой. В некоторых вариантах осуществления нуклеиновая кислота имеет нуклеотидную последовательность, содержащую по меньшей мере один элемент, который кодирует или является комплементарным последовательности, которая кодирует полипептид. В некоторых вариантах осуществления нуклеиновая кислота обладает ферментативной активностью.
[0045] Физиологические условия: как используется в данном документе, термин имеет значение, понятное специалистам в данной области, относящееся к условиям, при которых клетки или организмы живут и/или размножаются. В некоторых вариантах осуществления термин относится к условиям внешней или внутренней среды, которые могут встречаться в природе с точки зрения организма или клеточной системы. В некоторых вариантах осуществления физиологические условия представляют собой те условия, которые присутствуют в пределах организма человека или животного, отличного от человека, в особенности те условия, которые присутствуют в области хирургического вмешательства и/или в ее пределах. Физиологические условия обычно включают, например, температуру в диапазоне от приблизительно 20°С до приблизительно 40°С, атмосферное давление, составляющее приблизительно 1, рН от приблизительно 6 до приблизительно 8, концентрацию глюкозы от приблизительно 1 мМ до приблизительно 20 мМ, концентрацию кислорода, соответствующую уровням в атмосфере, и силу притяжения, встречающуюся на земле. В некоторых вариантах осуществления условия в лаборатории регулируются и/или поддерживаются в соответствии с физиологическими условиями. В некоторых вариантах осуществления физиологические условия встречаются в организме.
[0046] Полипептид: используемый в данном документе термин «полипептид», как правило, имеет общепризнанное в данной области техники значение, представляющее собой полимер, состоящий по меньшей мере из трех аминокислот. Предполагается, что специалистам в данной области будет понятно, что термин «полипептид» является достаточно общим, чтобы охватывать не только полипептиды, содержащие полную последовательность, упоминаемую в данном документе, но также и полипептиды, которые представляют собой функциональные фрагменты (т.е. фрагменты, сохраняющие по меньшей мере один вид активности) таких полных полипептидов. Более того, специалистам в данной области понятно, что белковые последовательности, как правило, переносят некоторые замены без нарушения активности. Таким образом, любой полипептид, который сохраняет активность и характеризуется общей идентичностью последовательности, составляющей по меньшей мере приблизительно 30-40%, часто более чем приблизительно 50%, 60%, 70% или 80%, и дополнительно обычно содержит по меньшей мере одну область, характеризующуюся намного более высокой идентичностью, часто более чем 90% или даже 95%, 96%, 97%, 98% или 99% в одной или более высококонсервативных областях, обычно охватывающих по меньшей мере 3 4, а часто до 20 или более аминокислот, с другим полипептидом того же класса, охватывается соответствующим используемым в данном документе термином «полипептид». Полипептиды могут содержать L-аминокислоты, D-аминокислоты или и те, и другие, и могут содержать любую из разнообразных модификаций аминокислот или их аналогов, известных из уровня техники. Применимые модификации включают, например, терминальное ацетилирование, амидирование, метилирование и т.д. В некоторых вариантах осуществления белки могут содержать природные аминокислоты, неприродные аминокислоты, синтетические аминокислоты и их комбинации. Термин «пептид», как правило, используется для обозначения полипептида, длина которого составляет менее чем приблизительно 100 аминокислот, менее чем приблизительно 50 аминокислот, менее чем 20 аминокислот или менее чем 10 аминокислот. В некоторых вариантах осуществления белки представляют собой антитела, фрагменты антител, их биологически активные части и/или характерные для них части.
[0047] Белок: используемый в данном документе термин «белок» относится к одному или более полипептидам, которые функционируют как дискретная единица. Если отдельный полипептид представляет собой дискретную функциональную единицу и не требует постоянной или временной физической связи с другими полипептидами для образования дискретной функциональной единицы, термины «полипептид» и «белок» могут использоваться взаимозаменяемо. Если дискретная функциональная единица состоит из более чем одного полипептида, которые физически связаны друг с другом, термин «белок» может быть использован для обозначения множества полипептидов, которые физически связаны и функционируют вместе как дискретная единица. В некоторых вариантах осуществления белки могут содержать другие соединения, помимо аминокислот (например, гликопротеины, протеогликаны и т.д.), и/или могут быть обработаны или модифицированы каким-либо иным образом. Специалистам в данной области будет понятно, что в некоторых вариантах осуществления термин «белок» может относиться к полной полипептидной цепи, производимой клеткой (например, с сигнальной последовательностью или без нее), и/или к форме, которая является активной в пределах клетки (например, усеченной форме или форме в виде комплекса). В некоторых вариантах осуществления в случае, если белок состоит из нескольких полипептидных цепей, такие цепи могут быть ковалентно связаны друг с другом, например, посредством одной или более дисульфидных связей, или могут быть связаны другими способами.
[0048] Эталон: как используется в данном документе в научном контексте, термин описывает стандарт или контроль, относительно которого осуществляют сравнение. Например, в некоторых вариантах осуществления представляющее интерес средство, животное, индивидуум, популяция, образец, последовательность или значение сравнивают с эталонным или контрольным средством, животным, индивидуумом, популяцией, образцом, последовательностью или значением. В некоторых вариантах осуществления эталон или контроль тестируют и/или определяют по сути одновременно с тестированием или определением, представляющим интерес. В некоторых вариантах осуществления эталон или контроль представляет собой исторический эталон или контроль, необязательно воплощенный в материальном носителе. Как правило, как понятно специалистам в данной области, эталон или контроль определяется или характеризуется в условиях или обстоятельствах, сопоставимых с оцениваемыми. Специалистам в данной области будет понятно, если присутствует сходство, достаточное, чтобы оправдать использование и/или сравнение с конкретным возможным эталоном или контролем.
[0049] Образец: используемый в данном документе термин «образец», как правило, относится к биологическому образцу, полученному или происходящему из представляющего интерес источника, как описано в данном документе. В некоторых вариантах осуществления представляющий интерес источник предусматривает организм, такой как животное или человек. В некоторых вариантах осуществления биологический образец представляет собой или содержит биологическую ткань или жидкость. В некоторых вариантах осуществления биологический образец может представлять собой или содержать костный мозг; кровь; клетки крови любого типа (например, Т-клетки); асцитическую жидкость; образцы ткани или образцы, полученные посредством тонкоигольной биопсии; биологические жидкости, содержащие клетки; свободно плавающие нуклеиновые кислоты; мокроту; слюну; мочу; спинномозговую жидкость, перитонеальную жидкость; плевральную жидкость; фекалии; лимфу; жидкости, полученные из женских половых органов; мазки с кожи; мазки из влагалища; мазки из ротовой полости; мазки из носа; жидкости, полученные при промывании или лаваже, такие как жидкости, полученные при протоковом лаваже, или жидкости, полученные при бронхоальвеолярном лаваже; аспираты; материалы, полученные при соскобе; образцы костного мозга; образцы тканей, полученные при биопсии; образцы, полученные при хирургическом вмешательстве; фекалии, другие биологические жидкости, продукты секреции и/или выделения; и/или клетки, полученные из них, и т.д. В некоторых вариантах осуществления биологический образец представляет собой или содержит клетки, полученные от индивидуума. В некоторых вариантах осуществления полученные клетки представляют собой или включают клетки индивидуума, от которого получен образец. В некоторых вариантах осуществления образец представляет собой «первичный образец», полученный непосредственно из представляющего интерес источника любыми подходящими способами. Например, в некоторых вариантах осуществления первичный биологический образец получают способами, выбранными из группы, состоящей из биопсии (например, тонкоигольной аспирационной биопсии или биопсии ткани), хирургического вмешательства, сбора биологической жидкости (например, крови, лимфы, фекалий и т.д.) и т.д. В некоторых вариантах осуществления, как будет ясно из контекста, термин «образец» относится к препарату, который получают путем обработки (например, посредством удаления одного или более компонентов и/или добавления одного или более средств) первичного образца. Например, посредством фильтрации с использованием полупроницаемой мембраны. Такой «обработанный образец» может содержать, например, нуклеиновые кислоты или белки, выделенные из образца или полученные посредством применения в отношении первичного образца методик, таких как амплификация или обратная транскрипция мРНК, выделение и/или очистка от определенных компонентов и т.д.
[0050] Специфическое связывание: как используется в данном документе, термин относится к способности связывающего средства различать возможных партнеров в среде, в которой должно происходить связывание. Считается, что связывающее средство, которое взаимодействует с одной конкретной мишенью при наличии других потенциальных мишеней, «специфически связывается» с мишенью, с которой оно взаимодействует. В некоторых вариантах осуществления специфическое связывание оценивают посредством выявления или определения степени ассоциации между связывающим средством и его партнером; в некоторых вариантах осуществления специфическое связывание оценивают посредством выявления или определения степени диссоциации комплекса связывающее средство-партнер; в некоторых вариантах осуществления специфическое связывание оценивают посредством выявления или определения способности связывающего средства конкурировать с альтернативным взаимодействием между его партнером и другим объектом. В некоторых вариантах осуществления специфическое связывание оценивают посредством осуществления такого выявления или определения в пределах диапазона концентраций.
[0051] Субъект: под «субъектом» подразумевается млекопитающее (например, человек, в некоторых вариантах осуществления в том числе внутриутробные формы организма человека). В некоторых вариантах осуществления субъект страдает от соответствующего заболевания, нарушения или состояния. В некоторых вариантах осуществления субъект является восприимчивым к заболеванию, нарушению или состоянию. В некоторых вариантах осуществления субъект демонстрирует наличие одного или более симптомов или характеристик заболевания, нарушения или состояния. В некоторых вариантах осуществления субъект не демонстрирует наличие каких-либо симптомов или характеристик заболевания, нарушения или состояния. В некоторых вариантах осуществления субъект представляет собой кого-либо, имеющего один или более признаков, характеризующих восприимчивость к заболеванию, нарушению или состоянию или риск их возникновения. В некоторых вариантах осуществления субъект представляет собой пациента. В некоторых вариантах осуществления субъект представляет собой индивидуума, в отношении которого осуществляется, будет осуществляться и/или осуществлялась диагностика и/или терапия.
[0052] По сути: используемый в данном документе термин «по сути» относится к качественному состоянию, представляющему собой проявление полного или почти полного масштаба и степени характеристики или свойства, представляющего интерес. Специалисту в области биологии будет понятно, что биологические и химические явления крайне редко достигают завершения и/или протекают до конца, или достигают или избегают абсолютного результата. Термин «по сути», таким образом, используется в данном документе для отражения потенциального отсутствия завершенности, присущего многим биологическим и химическим явлениям.
[0053] Вариант: используемый в данном документе термин «вариант» относится к объекту, который демонстрирует значительную структурную идентичность по отношению к эталонному объекту, но структурно отличается от эталонного объекта по наличию или уровню одного или более химических компонентов по сравнению с эталонным объектом. Во многих вариантах осуществления вариант также функционально отличается от своего эталонного объекта. В целом то, рассматривают ли конкретный объект как «вариант» эталонного объекта, основано на степени его структурной идентичности по отношению к эталонному объекту. Как будет понятно специалистам в данной области, любой биологический или химический эталонный объект имеет определенные характерные структурные элементы. Вариант по определению представляет собой отдельный химический объект, который содержит общий один или более таких характерных структурных элементов. В качестве лишь нескольких примеров, малая молекула может содержать характерный ядерный структурный элемент (например, ядро макроцикла) и/или одно или более характерных подвешенных компонентов таким образом, что вариантом малой молекулы является вариант, который содержит общий ядерный структурный элемент и характерные подвешенные компоненты, но отличается по другим подвешенным компонентам и/или типам присутствующих связей (например, одиночные по сравнению с двойными, Е по сравнению с Z и т.д.) в пределах ядра, полипептид может содержать характерный элемент последовательности, состоящий из множества аминокислот, располагающихся в определенных положениях относительно друг друга в линейном или трехмерном пространстве и/или способствующих определенной биологической функции, нуклеиновая кислота может содержать характерный элемент последовательности, состоящий из множества нуклеотидных остатков, располагающихся в определенных положениях относительно друг друга в линейном или трехмерном пространстве. Например, вариантный полипептид может отличаться от эталонного полипептида как результат одного или более различий по аминокислотной последовательности и/или одного или более различий по химическим компонентам (например, углеводам, липидам и т.д.), ковалентно присоединенным к полипептидному каркасу. В некоторых вариантах осуществления вариантный полипептид демонстрирует общую идентичность последовательности по отношению к эталонному полипептиду, которая составляет по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%. В качестве альтернативы или дополнительно в некоторых вариантах осуществления вариантный полипептид не содержит общий с эталонным полипептидом по меньшей мере один характерный элемент последовательности. В некоторых вариантах осуществления эталонный полипептид обладает одним или более видами биологической активности. В некоторых вариантах осуществления вариантный полипептид обладает общим с эталонным полипептидом одним или более видами биологической активности. В некоторых вариантах осуществления вариантный полипептид не обладает одним или более видами биологической активности эталонного полипептида. В некоторых вариантах осуществления вариантный полипептид демонстрирует сниженный уровень одного или более видов биологической активности по сравнению с эталонным полипептидом. Во многих вариантах осуществления представляющий интерес полипептид считается «вариантом» родительского или эталонного полипептида, если представляющий интерес полипептид содержит аминокислотную последовательность, которая является идентичной родительской последовательности, за исключением небольшого числа изменений последовательности в определенных положениях. Как правило, менее чем 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% остатков в варианте являются замещенными по сравнению с родителем. В некоторых вариантах осуществления вариант содержит 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замещенный остаток по сравнению с родителем. Часто вариант содержит крайне небольшое число (например, менее чем 5, 4, 3, 2 или 1) замещенных функциональных остатков (т.е. остатков, которые участвуют в определенной биологической активности). Кроме того, вариант, как правило, содержит не более чем 5, 4, 3, 2 или 1 добавление или делецию и часто не содержит добавлений или делеций по сравнению с родителем. Более того, число любых добавлений или делеций обычно составляет менее чем приблизительно 25, приблизительно 20, приблизительно 19, приблизительно 18, приблизительно 17, приблизительно 16, приблизительно 15, приблизительно 14, приблизительно 13, приблизительно 10, приблизительно 9, приблизительно 8, приблизительно 7, приблизительно 6, и обычно составляет менее чем приблизительно 5, приблизительно 4, приблизительно 3 или приблизительно 2 остатка. В некоторых вариантах осуществления родительский или эталонный полипептид представляет собой полипептид, встречающийся в природе. В некоторых вариантах осуществления вариант является сконструированным. В некоторых вариантах осуществления вариант встречается в природе. Как будет понятно специалистам в данной области, в природе можно найти множество вариантов конкретного полипептида, представляющего интерес.
[0054] Вектор: как используется в данном документе, термин относится к молекуле нуклеиновой кислоты, способной переносить другую нуклеиновую кислоту, с которой она связана. Один тип вектора представляет собой «плазмиду», которая относится к кольцевой двухнитевой петле ДНК, в которую могут быть лигированы дополнительные сегменты ДНК. Другой тип вектора представляет собой вектор на основе вируса (например, лентивирусный вектор или гамма-ретровирусный вектор), где дополнительные сегменты ДНК могут быть лигированы в вирусный геном. Определенные векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальную природу репликации и эписомальные векторы млекопитающих). Другие векторы (например, векторы млекопитающих, отличные от эписомальных) могут быть интегрированы в геном клетки-хозяина при введении в клетку-хозяина, и, таким образом, реплицируются одновременно с геномом хозяина. Более того, определенные векторы способны направлять экспрессию генов, с которыми они оперативно связаны. Такие векторы в данном документе называются «векторами экспрессии».
[0055] Стандартные методики могут применяться для рекомбинантной ДНК, синтеза олигонуклеотидов, культивирования и трансформации ткани (например, электропорация, липофекция). Ферментативные реакции и методики очистки могут осуществляться в соответствии со спецификациями производителя, или как это обычно выполняется в данной области, или как описано в данном документе. Вышеописанные методики и процедуры могут, как правило, осуществляться в соответствии с традиционными способами, широко известными из уровня техники, и как это описано в различных общих и более конкретных источниках литературы, которые цитируются и обсуждаются в описании настоящего изобретения. См., например, Sambrook et al. Molecular Cloning: A Laboratory Manual (2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1989)), которая включена в данный документ посредством ссылки для любых целей.
[0056] Белок типа «цинковый палец»: используемый в данном документе термин «белок типа «цинковый палец» относится к полипептиду, который содержит «домен типа «цинковый палец», посредством которого он способен связываться с нуклеиновыми кислотами (например, с ДНК). Термин «домен типа «цинковый палец» относится к отдельному «пальцу», который содержит PfBa-складку, стабилизированную с помощью иона цинка. Каждый домен типа «цинковый палец» обычно содержит примерно 30 аминокислот. Домены типа «цинковый палец» являются в значительной степени структурно независимыми и могут сохранять свою структуру и функцию в различных видах окружающей среды.
[0057] Используемые в настоящей заявке термины «приблизительно» и «примерно» используются в качестве эквивалентов. Любые числовые значения, используемые в настоящей заявке с терминами «приблизительно»/«примерно» или без них, предназначены для охвата любых нормальных отклонений, понятных специалисту в данной области.
[0058] Другие признаки, объекты и преимущества настоящего изобретения очевидны из подробного описания, приведенного ниже. Однако следует понимать, что подробное описание, указывающее на варианты осуществления настоящего изобретения, приведено только в качестве иллюстрации, а не в качестве ограничения. Различные изменения и модификации в пределах объема настоящего изобретения будут очевидны для специалистов в данной области из подробного описания.
ПОДРОБНОЕ ОПИСАНИЕ ОПРЕДЕЛЕННЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0059] В настоящем изобретении предусмотрены антитела, которые связывают белки TALEN и/или каталитический ДНК-расщепляющий домен FokI, и пути их применения.
[0060] Как используется в данном документе, антитела включают без ограничения связывающие области антитела, которые представляют собой иммунологически функциональные фрагменты. Термин «иммунологически функциональный фрагмент» (или «фрагмент») антитела представляет собой разновидность антитела, содержащую часть (независимо от того, как эта часть получена или синтезирована) антитела, в которой отсутствуют по меньшей мере некоторые аминокислоты, присутствующие в полноразмерной цепи, но которая все еще способна специфически связываться с целевым антигеном (например, способна связываться с белками FokI и/или TALEN). Такие фрагменты являются биологически активными в том смысле, что они связываются с целевым антигеном и могут конкурировать с другими антигенсвязывающими молекулами, включая интактные антитела, за связывание с данным эпитопом. В некоторых вариантах осуществления фрагменты представляют собой нейтрализующие фрагменты. В некоторых вариантах осуществления фрагменты могут блокировать или снижать активность целевого антигена (например, блокирующий эффект). В некоторых вариантах осуществления фрагменты могут противодействовать активности целевого антигена.
[0061] В конкретных вариантах осуществления антитело к TALEN по настоящему изобретению представляет собой антитело, идентифицированное в данном документе как клоны 2299.2G3.C6, 2299.5D4.C8, 2299.6В3.В8.В6, 2299.6G5.C7 или 2299.7F11.В4, и каждый содержит аминокислотные, кодирующие, вариабельные последовательности и последовательности CDR тяжелой и легкой цепи, предусмотренные и обозначенные в данном документе. В некоторых вариантах осуществления клоны 2299.2G3.C6, 2299.5D4.C8, 2299.6В3.В8.В6, 2299.6G5.C7 или 2299.7F11.В4 специфически связывают молекулу, содержащую каталитический домен FokI.
[0062] Иммунологически функциональные фрагменты иммуноглобулина включают без ограничения scFv-фрагменты, Fab-фрагменты (Fab', F(ab')2 и т.п.), одну или более областей, определяющих комплементарность («CDR»), диатело (вариабельный домен тяжелой цепи на том же полипептиде, что и вариабельный домен легкой цепи, соединенные посредством короткого пептидного линкера, который является слишком коротким для обеспечения образования пары между двумя доменами в одной цепи), доменные антитела, бивалентные антигенсвязывающие домены (содержат два антигенсвязывающих участка), полиспецифические антигенсвязывающие домены и одноцепочечные антитела. Данные фрагменты могут быть получены из любого источника, представляющего собой млекопитающее, в том числе без ограничения человека, мыши, крысы, верблюда или кролика. Специалисту в данной области будет понятно, что антигенсвязывающая молекула может содержать небелковые компоненты.
[0063] Вариабельные области обычно демонстрируют одинаковую общую структуру относительно консервативных каркасных областей (FR), соединенных 3 гипервариабельными областями (CDR). CDR из двух цепей каждой пары обычно выравниваются по каркасным областям, что может обеспечить связывание со специфическим эпитопом. От N-конца к С-концу вариабельные области как легкой, так и тяжелой цепи обычно содержат домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Условно области CDR в тяжелой цепи обычно называются CDR1, CDR2 и CDR3 НС. Области CDR в легкой цепи, как правило, называются CDR1, CDR2 и CDR3 LC.
[0064] В некоторых вариантах осуществления антитела к TALEN содержат одну или более областей, определяющих комплементарность (CDR), присутствующих в полноразмерной легкой или тяжелой цепи антитела, и в некоторых вариантах осуществления содержат одну тяжелую цепь и/или легкую цепь или ее часть. Эти фрагменты могут быть получены посредством методик рекомбинантной ДНК или могут быть получены посредством ферментативного или химического расщепления антиген связывающих доменов, в том числе интактных антител.
[0065] В некоторых вариантах осуществления антигенсвязывающий домен представляет собой антитело или его фрагмент, в том числе одну или более из его областей, определяющих комплементарность (CDR). В некоторых вариантах осуществления антигенсвязывающий домен представляет собой одноцепочечный вариабельный фрагмент (scFv), содержащий CDR легкой цепи - CDR1, CDR2 и CDR3, а также CDR тяжелой цепи - CDR1, CDR2 и CDR3.
[0066] Причисление аминокислот к каждому из каркасных доменов, доменов CDR и вариабельных доменов, как правило, осуществляется в соответствии со схемами нумерации, представляющими собой схему нумерации по Kabat (см., например, Kabat et al. в Sequences of Proteins of Immunological Interest, 5th Ed., NIH Publication 91-3242, Bethesda Md. 1991), схему нумерации по Chothia (см., например, Chothia и Lesk, (1987), J Mol Biol 196: 901-917; Al-Lazikani et al. (1997) J Mol Biol 273: 927-948; Chothia et al. (1992) J Mol Biol 227: 799-817; Tramontano et al. (1990) J Mol Biol 215(1): 175-82; и патент США №7709226), контактную схему нумерации или схему AbM (программа Antibody Modeling, Oxford Molecular).
[0067] Соответственно, в некоторых вариантах осуществления CDR антител к TALEN, представленных в данном документе, пронумерованы в соответствии со схемой нумерации по Kabat. В других вариантах осуществления CDR антител к TALEN, представленных в данном документе, пронумерованы в соответствии со схемой нумерации по Chothia. В других вариантах осуществления CDR антител к TALEN, представленных в данном документе, пронумерованы в соответствии с контактной схемой нумерации. В других вариантах осуществления CDR антител к TALEN, представленных в данном документе, пронумерованы в соответствии со схемой нумерации AbM.
[0068] Гуманизированные антитела, представляющие собой антитела к TALEN, описанные в данном документе, могут быть получены посредством известных методик. В некоторых вариантах осуществления гуманизированное моноклональное антитело содержит вариабельный домен антитела к TALEN (или весь его антигенсвязывающий участок, или его часть) и константный домен, полученный из человеческого антитела. В качестве альтернативы фрагмент гуманизированного антитела может содержать антигенсвязывающий участок моноклонального антитела мыши или кролика и фрагмент вариабельного домена (без антигенсвязывающего участка), полученный из человеческого антитела. Процедуры получения сконструированных моноклональных антител включают процедуры, описанные, например, в Riechmann et al. (1988) Nature 332:323, Liu et al. (1987) Proc. Nat. Acad. Sci. USA 84:3439, Larrick et al. (1989) Bio/Technology 7:934, и Winter et al. (1993) TIPS 14:139. В некоторых вариантах осуществления химерное антитело представляет собой антитело с привитой CDR. Методики гуманизации антител обсуждаются, например, в патентах США №№5869619; 5225539; 5821337; 5859205; 6881557; Padlan et al. (1995) FASEB J. 9: 133-39; Tamura et al. (2000) J. Immunol. 164:1432-41; Zhang et al. (2005) Mol Immunol 42(12): 1445-1451; Hwang et al. Methods. (2005) 36(1): 35-42; Dall'Acqua et al. (2005) Methods 36(1): 43-60; и Clark, (2000) Immunology Today 21(8): 397-402.
[0069] Варианты антител к TALEN также охватываются объемом настоящего изобретения, например, вариабельные области легких цепей и/или вариабельные области тяжелых цепей, каждая из которых характеризуется по меньшей мере 70-80%, 80-85%, 85-90%, 90-95% 95-97%, 97-99% или более чем 99% идентичностью с аминокислотными последовательностями последовательностей антигенсвязывающего домена, описанных в данном документе. В некоторых вариантах осуществления антиидиотипическое антитело характеризуется по меньшей мере приблизительно 75%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 91%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100% идентичностью с последовательностью вариабельной области тяжелой цепи, представленной в табл. 1а, и/или последовательностью вариабельной области легкой цепи, представленной в табл. 1b.
[0070] В некоторых случаях такие молекулы содержат по меньшей мере одну тяжелую цепь и одну легкую цепь, тогда как в других случаях вариантные формы содержат две вариабельные области легкой цепи и две вариабельные области тяжелой цепи (или их подчасти). Специалист в данной области сможет определить подходящие варианты антител к TALEN, изложенных в данном документе, с применением хорошо известных методик. В определенных вариантах осуществления специалист в данной области может идентифицировать подходящие области молекулы, которые можно изменить без нарушения антигенсвязывающей активности посредством нацеливания на области, которые, как считается, не являются важными для активности.
[0071] Антитело к TALEN по настоящему изобретению также может представлять собой полностью человеческое моноклональное антитело. Полностью человеческие моноклональные антитела можно получать посредством любого количества методик, с которыми будут знакомы специалисты в данной области. Такие способы включают без ограничения трансформацию с помощью вируса Эпштейна-Барр (EBV) клеток периферической крови человека (например, содержащих В-лимфоциты), иммунизацию В-клеток человека in vitro, слияние клеток селезенки от иммунизированных трансгенных мышей, несущих встроенные гены человеческих иммуноглобулинов, выделение из фаговых библиотек V-области человеческого иммуноглобулина или другие процедуры, известные из уровня техники и основанные на раскрытии в данном документе.
[0072] Антитело к TALEN, которое специфически связывается с белком TALEN и/или каталитическим доменом FokI, считается «селективным», если оно связывается с одной мишенью более прочно, чем со второй мишенью. Считается, что антитело к TALEN, которое специфически связывается с белком TALEN и/или каталитическим доменом FokI, «специфически связывает» свой целевой антиген (например, белок TALEN и/или каталитический домен FokI), если константа диссоциации (Kd) находится в наномолярном диапазоне (например, ~1 нМ). Антигенсвязывающий домен специфически связывает антиген с «высокой аффинностью», если Kd составляет 1-5 нМ, и с «очень высокой аффинностью», если Kd составляет 0,1-0,5 нМ. В одном варианте осуществления антигенсвязывающий домен характеризуется Kd, составляющей ~ 1 нМ. В одном варианте осуществления константа скорости диссоциации составляет <1×10-5. В других вариантах осуществления антигенсвязывающие домены будут связываться с белками TALEN и молекулами, содержащими каталитический домен FokI, с Kd, составляющей от приблизительно 1×10-7 М до 1×10-12 М, и в еще одном варианте осуществления антигенсвязывающие домены будут связываться с Kd, составляющей от приблизительно 1×10-5 до 1×10-12.
[0073] Как предусмотрено в данном документе, антитела к TALEN по настоящему изобретению специфически связывают белки TALEN и/или нуклеазный домен FokI (например, SEQ ID NO: 1). В определенных вариантах осуществления антитела к TALEN по настоящему изобретению связывают белки TALEN и/или каталитический домен FokI с KD, составляющей менее 1×10-6 М, менее 1×10-7 М, менее 1×10-8 М или менее 1×10-9 М. В одном конкретном варианте осуществления антитела к TALEN связывают белки TALEN и/или каталитический домен FokI с KD, составляющей менее 1×10-7 М. В другом варианте осуществления антитела к TALEN связывают белки TALEN и/или каталитический домен FokI с KD, составляющей менее 1×10-8 М. В некоторых вариантах осуществления антитела к TALEN связывают белки TALEN и/или каталитический домен FokI с Kd, составляющей приблизительно 1×10-7 М, приблизительно 2×10-7 М, приблизительно 3×10-7 М, приблизительно 4×10-7 М, приблизительно 5×10-7 М, приблизительно 6×10-7 М, приблизительно 7×10-7 М, приблизительно 8×10-7 М, приблизительно 9×10-7 М, приблизительно 1×10-8 М, приблизительно 2×10-8 М, приблизительно 3×10-8 М, приблизительно 4×10-8 М, приблизительно 5×10-8 М, приблизительно 6×10-8 М, приблизительно 7×10-8 М, приблизительно 8×10-8 М, приблизительно 9×10-8 М, приблизительно 1×10-9 М, приблизительно 2×10-9 М, приблизительно 3×10-9 М, приблизительно 4×10-9 М, приблизительно 5×10-9 М, приблизительно 6×10-9 М, приблизительно 7×10-9 М, приблизительно 8×10-9 М, приблизительно 9×10-9 М, приблизительно 1×10-10 М или приблизительно 5×10-10 М. В определенных вариантах осуществления Kd рассчитывают как соотношение Koff/Kon, и Kon и Koff определяют с применением моновалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса Biacore®. В других вариантах осуществления Kd рассчитывают как соотношение Koff/Kon, и Kon и Koff определяют с применением бивалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса Biacore®.
[0074] В некоторых вариантах осуществления антитела к TALEN связывают белки TALEN и/или каталитический домен FokI со скоростью ассоциации (kon), составляющей менее чем 1×10-4 М-1 с-1, менее чем 2×10-4 М-1 с-1, менее чем 3×10-4 М-1 с-1, менее чем 4×10-4 М-1 с-1, менее чем 5×10-4 М-1 с-1, менее чем 7×10-4 М-1 с-1, менее чем 8×10-4 М-1 с-1, менее чем 9×10-4 М-1 с-1, менее чем 1×10-5 М-1 с-1, менее чем 2×10-5 М-1 с-1, менее чем 3×10-5 М-1 с-1, менее чем 4×10-5 М-1 с-1, менее чем 5×10-5 М-1 с-1, менее чем 6×10-5 М-1 с-1, менее чем 7×10-5 М-1 с-1, менее чем 8×10-5 М-1 с-1, менее чем 9×10-5 М-1 с-1, менее чем 1×10-6 М-1 с-1, менее чем 2×10-6 М-1 с-1, менее чем 3×10-6 М-1 с-1, менее чем 4×10-6 М-1 с-1, менее чем 5×10-6 М-1 с-1, менее чем 6×10-6 М-1 с-1, менее чем 7×10-6 М-1 с-1, менее чем 8×10-6 М-1 с-1, менее чем 9×10-6 М-1 с-1 или менее чем 1×10-7 М-1 с-1. В определенных вариантах осуществления коп может быть определена с применением моновалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления kon определяют с применением бивалентного антитела, как измерено, например, посредством технологии поверхностного плазмонного резонанса BIAcore®.
[0075] В некоторых вариантах осуществления антитела к TALEN связывают белки TALEN и/или каталитический домен FokI со скоростью диссоциации (koff), составляющей менее чем 1×10-2 с-1, менее чем 2×10-2 с-1, менее чем 3×10-2 с-1, менее чем 4×10-2 с-1, менее чем 5×10-2 с-1, менее чем 6×10-2 с-1, менее чем 7×10-2 с-1, менее чем 8×10-2 с-1, менее чем 9×10-2 с-1, менее чем 1×10-3 с-1, менее чем 2×10-3 с-1, менее чем 3×10-3 с-1, менее чем 4×10-3 с-1, менее чем 5×10-3 с-1, менее чем 6×10-3 с-1, менее чем 7×10-3 с-1, менее чем 8×10-3 с-1, менее чем 9×10-3 с-1, менее чем 1×10-4 с-1, менее чем 2×10-4 с-1, менее чем 3×10-4 с-1, менее чем 4×10-4 с-1, менее чем 5×10-4 с-1, менее чем 6×10-4 с-1 менее чем 7×10-4 с-1, менее чем 8×10-4 с-1, менее чем 9×10-4 с-1, менее чем 1×10-5 с-1 или менее чем 5×10-4 с-1. В определенных вариантах осуществления koff определяют с применением моновалентного антитела, такого как Fab-фрагмент, как измерено, например, посредством технологии поверхностного плазмонного резонанса BlAcore®. В других вариантах осуществления koff определяют с применением бивалентного антитела, как измерено, например, посредством технологии поверхностного плазмонного резонанса BlAcore®.
[0076] Предусмотренные антитела к TALEN связывают белки TALEN и/или каталитический домен FokI, при этом они содержат вариабельную область тяжелой цепи (VH), где аминокислотная последовательность или полинуклеотидная последовательность VH выбрана из последовательностей VH, представленных в табл. 1а. Антитела к TALEN, которые специфически связываются с каталитическим доменом FokI, содержат вариабельную область тяжелой цепи (VH), где аминокислотная последовательность или полинуклеотидная последовательность VH выбрана из последовательностей VH, представленных в табл. 1а. В некоторых вариантах осуществления аминокислотная последовательность VH характеризуется по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100% идентичностью с последовательностью VH, представленной в табл. 1а. Определения CDR по Kabat выделены жирным шрифтом, и определения CDR по Chothia подчеркнуты.
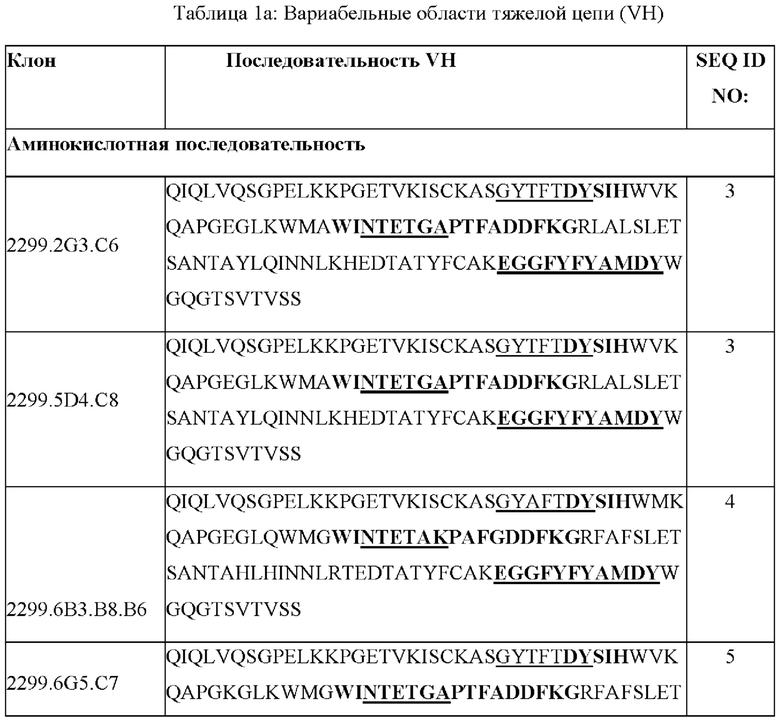



[0077] В данном документе предусмотрены антитела к TALEN, которые специфически связываются с каталитическим доменом FokI, содержащие вариабельную область легкой цепи (VL), где аминокислотная последовательность или полинуклеотидная последовательность VL выбрана из последовательностей VL, представленных в табл. 1b. В некоторых вариантах осуществления аминокислотная последовательность VL характеризуется по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или приблизительно 100%) идентичностью с последовательностью VL, представленной в табл. 1b. Определения CDR по Kabat выделены жирным шрифтом, и определения CDR по Chothia подчеркнуты.




[0078] В данном документе предусмотрены антитела к TALEN, которые специфически связываются с каталитическим доменом FokI, где антитела к TALEN содержат вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), где аминокислотная последовательность или полинуклеотидная последовательность VH выбрана из последовательностей VH, представленных в табл. 1а; и где аминокислотная последовательность или полинуклеотидная последовательность VL выбрана из последовательностей VL, представленных в табл. 1b.
[0079] В некоторых вариантах осуществления антитела к TALEN, которые специфически связываются с каталитическим доменом Fok1, содержат CDR1, CDR2 и CDR3 VH из последовательности VH, представленной в табл. 1а. В некоторых вариантах осуществления CDR1, CDR2 и CDR3 VH выбраны из последовательности CDR, представленной в табл. 1с.

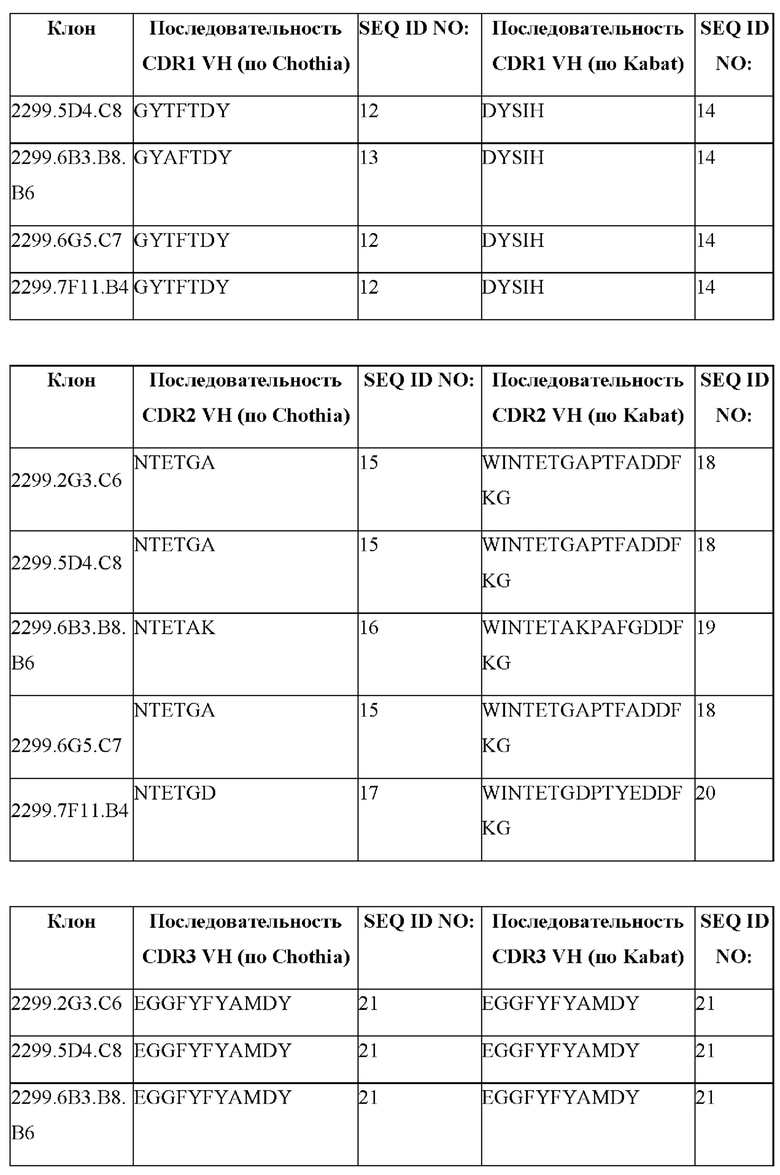
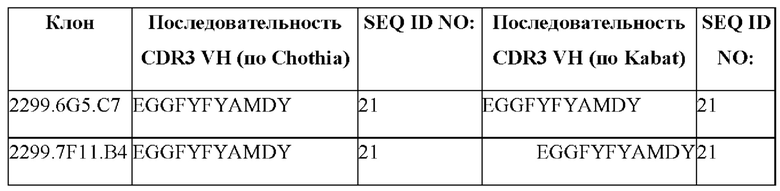
[0080] В некоторых вариантах осуществления антитела к TALEN, которые специфически связываются с каталитическим доменом Fok1, содержат CDR 1, CDR2 и CDR3 VL из последовательности VL, представленной в табл. 1b. В некоторых вариантах осуществления CDR 1, CDR2 и CDR3 VH выбраны из последовательности CDR, представленной в табл. 1d.
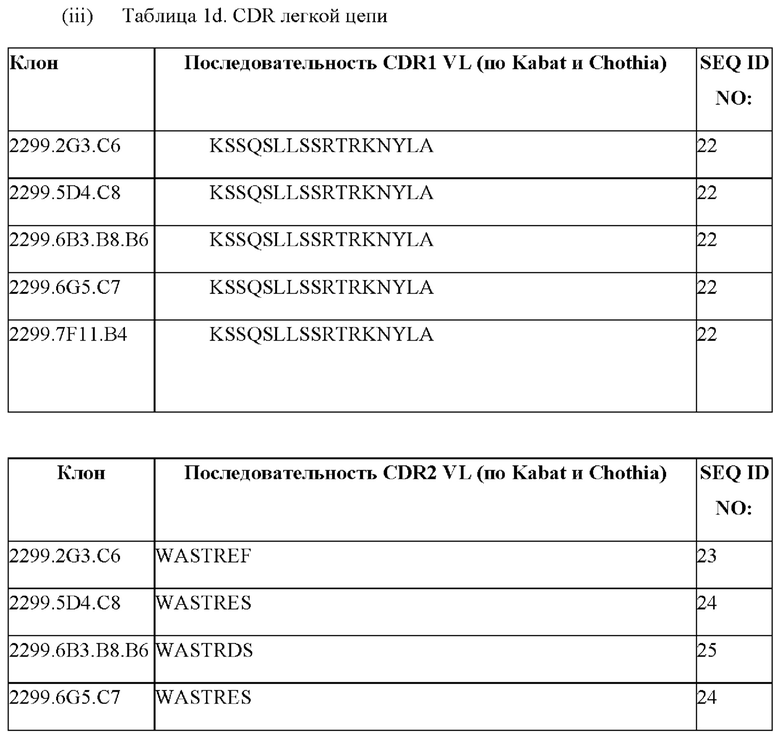
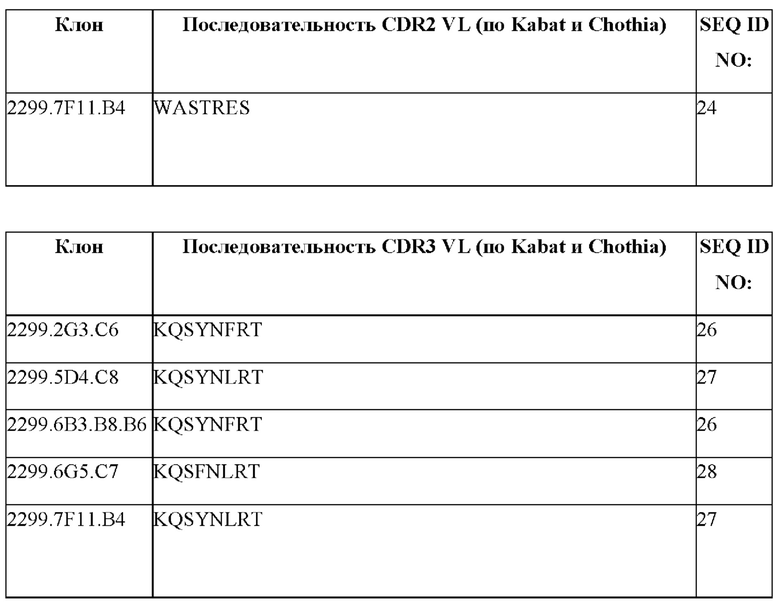
[0081] При практическом осуществлении способов, а также при получении и применении композиций, раскрытых в данном документе, используют, если не указано иное, традиционные методики молекулярной биологии, биохимии, вычислительной химии, белковой инженерии, структуры и функции антител, клеточной культуры, рекомбинантной ДНК и родственных областей, которые находятся в пределах компетенции специалиста в данной области. Данные методики полностью описаны в источниках литературы. См., например, Sambrook et al. MOLECULAR CLONING: A LABORATORY MANUAL, Second edition, Cold Spring Harbor Laboratory Press, 1989, и третье издание, 2001, и последующие издания; Ausubel et al. CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John Wiley & Sons, New York, 1987 и периодические изменения и дополнения; серию METHODS IN ENZYMOLOGY, Academic Press, San Diego; Wolffe, CHROMATIN STRUCTURE AND FUNCTION, Third edition, Academic Press, San Diego, 1998 и последующие издания.
Технологии редактирования генома
Эффекторные нуклеазы, подобные активатору транскрипции
[0082] Эффекторные нуклеазы, подобные активатору транскрипции (TALEN), обычно относятся к рестрикционным ферментам, которые могут быть сконструированы для разрезания конкретных последовательностей ДНК. Как правило, они содержат ДНК-связывающий домен эффектора TAL и ДНК-расщепляющий домен, т.е. нуклеазу, которая разрезает нити ДНК. Эффекторы, подобные активатору транскрипции (TALE), могут быть сконструированы для связывания практически любой требуемой последовательности ДНК. Таким образом, TALEN могут быть введены в клетки для применения в редактировании генов или для редактирования генома in situ.
[0083] Различные неспецифические ДНК-расщепляющие домены могут использоваться в конструкциях TALEN, в том числе без ограничения расщепляющий домен FokI дикого типа, части эндонуклеазы FokI, варианты расщепляющего домена FokI, как, например, те, которые содержат мутации, разработанные для повышения специфичности расщепления и активности расщепления. В некоторых вариантах осуществления домен FokI функционирует в качестве димера, при этом он содержит две конструкции, содержащие ДНК-связывающие домены для участков в целевом геноме, имеющие надлежащую ориентацию и расстояние между ними. В некоторых вариантах осуществления TALEN содержит расщепляющий домен эндонуклеазы (например, FokI) или расщепляющий полудомен. Раскрытые антитела могут применяться для любого TALEN-опосредованного редактирования генов, в том числе для целенаправленной интеграции; способы и композиции для опосредованной нуклеазой целенаправленной интеграции описаны в WO 2015127439 А1, которая включена в данный документ посредством ссылки во всей своей полноте.
Нуклеазы типа «цинковый палец»
[0084] Нуклеазы типа «цинковый палец» (ZFN) представляют собой белковые химеры, состоящие из ДНК-связывающего домена на основе «цинкового пальца» и ДНК-расщепляющего (т.е. нуклеазного) домена (например, FokI). ZFN способны вводить двухнитевые разрывы (DSB; разрывы в одинаковых или очень близких точках в обеих нитях двухнитевой молекулы ДНК) в конкретных положениях в пределах молекулы ДНК, которые затем могут быть использованы для блокирования, замены, вставки или редактирования целевой области генома.
[0085] «Цинковые пальцы» представляют собой одни из наиболее часто встречающихся ДНК-связывающих мотивов, обнаруженных у эукариот. Данные белки классифицируют в соответствии с числом и положением цистеиновых и гистидиновых остатков, доступных для координации цинка. «Цинковый палец» состоит из двух антипараллельных β-нитей и α-спирали. Ион цинка имеет ключевое значение для стабильности данного типа домена: при отсутствии иона металла домен разворачивается, так как он имеет слишком малый размер для того, чтобы содержать гидрофобное ядро. Одна очень хорошо изученная разновидность «цинковых пальцев» (класс С2Н2) содержит пару цистеиновых остатков в бета-нитях и два гистидиновых остатка в альфа-спирали, которые отвечают за связывание иона цинка. Два других класса белков типа «цинковый палец» представляют собой классы С4 и С6. «Цинковые пальцы» имеют важное значение в регуляции, поскольку при взаимодействии с ДНК и ионом цинка они обеспечивают получение уникального структурного мотива для ДНК-связывающих белков. Структура каждого отдельного «пальца» является высококонсервативной и состоит из приблизительно 30 аминокислотных остатков, сконструированных в виде ββα-складки и удерживаемых вместе посредством иона цинка. α-Спираль возникает в С-концевой части «пальца», в то время как β-лист возникает в N-концевой части.
[0086] ДНК-связывающий домен ZFN может состоять из от двух до восьми мотивов типа «цинковый палец», что обусловлено их предлагаемым модульным принципом конструкции. В некоторых вариантах осуществления ZFN содержит 2, 3, 4, 5, 6, 7 или 8 мотивов типа «цинковый палец». Как правило, считается, что каждый мотив типа «цинковый палец» распознает и связывается с последовательностью, состоящей из трех пар оснований, поэтому белок, содержащий большее число «цинковых пальцев», целенаправленно воздействует на более длинную последовательность и, следовательно, обладает большей специфичностью и аффинностью в отношении целевого участка. Способы конструирования связывающих доменов типа «цинковый палец» для связывания с выбранной последовательностью хорошо известны из уровня техники. См., например, Beerli et al. (2002) Nature Biotechnol. 20:135 141; Pabo et al. (2001) Ann. Rev. Biochem. 70:313 340; Isalan et al. (2001) Nature Biotechnol. 19:656-660; Segal et al. (2001) Curr. Opin. Biotechnol. 12:632-637; Choo et al. (2000) Curr. Opin. Struct. Biol. 10:411-416. Способы конструирования «цинковых пальцев», известные из уровня техники, включают без ограничения рациональное проектирование и различные типы отбора. Рациональное проектирование включает, например, использование баз данных, содержащих триплетные (или квадруплетные) нуклеотидные последовательности и отдельные аминокислотные последовательности «цинковых пальцев», при этом каждая триплетная или квадруплетная нуклеотидная последовательность связана с одной или более аминокислотными последовательностями «цинковых пальцев», которые связывают конкретную триплетную или квадруплетную последовательность. См., например, патенты США №6453242 и №6534261. В зависимости от требуемых характеристик конечного продукта, содержащиеся «цинковые пальцы» могут быть выбраны посредством параллельной, последовательной или двухсторонней методики или посредством методики на основе клеток in vitro. Иллюстративные способы отбора также известны из уровня техники, в том числе системы фагового дисплея и двойных гибридов, см. патенты США №№5789538; 5925523; 6007988; 6013453; 6410248; 6140466; 6200759 и 6242568; а также международные патентные публикации WO 98/37186; WO 98/53057; WO 00/27878; и WO 01/88197. Усиление специфичности связывания для связывающих доменов типа «цинковый палец» было описано ранее, например, в WO 02/077227.
[0087] Неспецифический нуклеазный домен FokI является функционально независимым от его природного ДНК-связывающего домена и, таким образом, может применяться в конструировании ZFN. Поскольку домен должен димеризоваться для осуществления двухнитевого разрыва, необходимо, чтобы нуклеаза также была связана с противоположной нитью посредством другой молекулы ZFN, связанной с ее целевой последовательностью, как показано на диаграмме. Два целевых участка не должны быть одинаковыми при условии, что присутствуют ZFN, нацеленные на оба сайта. С целью образования димера две молекулы ZFN должны встретиться со своими соответствующими участками распознавания на расстоянии не менее 4-6 пар оснований друг от друга, но и не настолько далеко друг от друга, чтобы они не могли димеризоваться. В то время как одна молекула ZFN связывает свою целевую последовательность на одной нити, другая молекула ZFN связывает свою целевую последовательность на противоположной нити, как показано на диаграмме. Нуклеазные домены димеризуются, и каждый из них расщепляет свою собственную нить, в результате чего получается DSB. FokI можно применять в виде гомо- или гетеродимера. В некоторых вариантах осуществления FokI представляет собой гомодимер. В некоторых вариантах осуществления FokI представляет собой гетеродимер.
РНК-направляемая нуклеаза FokI
[0088] РНК-направляемые нуклеазы FokI (RFN) представляют собой белковые химеры, состоящие из ДНК-связывающего домена нуклеазы Cas9 (Cas9) и ДНК-расщепляющего домена (например, расщепляющего домена FokI). RFN специфически нацеливаются на конкретные последовательности ДНК с помощью направляющей РНК (gRNA), несущей 17-20 нуклеотидов, комплементарных целевому участку, на 5'-конце. RFN требуют димеризации ДНК-расщепляющего домена FokI для введения двухнитевых разрывов (DSB; разрывов в одинаковых или очень близких точках в обеих нитях двухнитевой молекулы ДНК) в конкретных положениях в пределах молекулы ДНК, которые затем могут быть использованы для блокирования, замены, вставки или редактирования целевой области генома.
CRISPR
[0089] CRISPR-ассоциированные системы Cas в бактериях и археях развились таким образом, чтобы использовать короткие РНК для направления ДНК-расщепляющих комплексов к конкретным последовательностям нуклеотидов. Система CRISPR/Cas была адаптирована для редактирования генома в эукариотических клетках. Cas9 раскручивает ДНК и осуществляет проверку на наличие участка, комплементарного спейсерной области gRNA длиной 20 пар оснований, таким образом, специфически нацеливаясь на последовательности ДНК, предшествующие последовательностям мотивов, прилегающих к протоспейсеру (РАМ), в геномах клеток млекопитающих. Введение DSB обеспечивает возможность изменения целевой последовательности посредством одного из двух эндогенных механизмов репарации ДНК: либо посредством негомологичного соединения концов (NHEJ), либо посредством репарации, направляемой гомологией (HDR). Система CRISPR/Cas также применяется для регуляции генов, включая подавление и активацию транскрипции без изменения целевой последовательности. При целенаправленной регуляции генов, основанной на системе CRISPR/Cas, используется ферментативно неактивный Cas9 (dCas9). Дополнительные описания Cas9 и требования к gRNA для программируемого dCas9 включены без ограничения в патенты США №№14/536319, 14/320498 и 14/320467.
Системы редактирования генома
[0090] Вышеописанные TALEN, ZFN и RFN могут связываться и осуществлять расщепление в целевых участках в геноме, что позволяет осуществлять вставку или делецию конкретных последовательностей ДНК, особенно при обеспечении матрицы репарации. Селективное разрезание достигается посредством специфического по отношению к последовательности нацеливания посредством ДНК-связывающего домена (например, ДНК-связывающего домена эффектора TAL) и расщепления ДНК нуклеазами FokI. После того как конструкция на основе TALEN создает двухнитевой разрыв в целевом локусе, механизм гомологичной рекомбинации осуществляет проверку на наличие гомологии между поврежденной хромосомой и внехромосомным фрагментом и копирует последовательность фрагмента между двумя разорванными концами хромосомы, независимо от того, содержит ли фрагмент исходную последовательность, что приводит к вставке представляющего интерес гена в геном.
[0091] В дополнение к редактированию генов, опосредованному гомологией, подход TALEN также может применяться для редактирования генов (нокаутов и вставок), опосредованного негомологичным соединением концов.
[0092] В некоторых вариантах осуществления система редактирования генома содержит 1, 2, 3, 4, 5, 6, 7, 8 или более конструкций на основе нуклеиновых кислот, кодирующих «полуTALEN», которые подвергаются сборке с образованием полного TALEN, обладающего целенаправленной нуклеазной активностью, опосредованной FokI. В некоторых вариантах осуществления система редактирования генома включает две или четыре конструкции на основе нуклеиновых кислот, кодирующие «полуTALEN», обладающие целенаправленной нуклеазной активностью, опосредованной FokI. В некоторых вариантах осуществления нуклеиновые кислоты кодируют димерные TALEN или TALEN, содержащий два «полуTALEN».
[0093] В некоторых вариантах осуществления система редактирования генома включает полинуклеотидную конструкцию, несущую донорную последовательность, которая подвергается вставке в геном после расщепления с помощью нуклеазы. В некоторых вариантах осуществления донорная последовательность будет иметь одну или более гомологичных областей, характеризующихся общей идентичностью по отношению к геномной последовательности, с которой требуется рекомбинация. В некоторых вариантах осуществления донорная последовательность будет иметь одну или более гомологичных областей, которые характеризуются по меньшей мере 50% идентичностью последовательности с геномной последовательностью, с которой требуется рекомбинация. В некоторых вариантах осуществления отмечается 60%, 70%, 80%, 90%, 95%, 98%, 99% или 99,9% идентичность последовательности на протяжении гомологичной области. В зависимости от длины донорного полинуклеотида может отмечаться любое значение идентичности последовательности в диапазоне от 1% до 100%.
[0094] В некоторых вариантах осуществления в качестве части генной терапии введение ДНК в выбранные целевые клетки может осуществляться таким образом, что донорная ДНК экспрессируется и производится кодируемый таким образом терапевтический продукт. Дополнительно или в качестве альтернативы донорная ДНК может каким-либо образом опосредовать экспрессию ДНК, которая кодирует терапевтический продукт, или она может кодировать продукт, такой как пептид или РНК, который каким-либо образом опосредует, прямо или косвенно, экспрессию терапевтического продукта. В некоторых вариантах осуществления донорная ДНК кодирует терапевтический продукт для лечения или предупреждения заболевания или нарушения, развивающегося в результате генетического дефекта или недостаточности. В некоторых вариантах осуществления донорная ДНК кодирует терапевтический продукт для лечения или предупреждения рака или любого другого заболевания или нарушения, развивающегося в результате генетического дефекта или недостаточности. В некоторых вариантах осуществления донорная ДНК кодирует химерный антигенный рецептор (CAR).
[0095] Методики и протоколы для редактирования генома описаны в уровне техники. См., например, US 2005/0215502; US 2007/0134796; WO 2005/084190; WO 2014204578, Urnov et al. Nature Reviews Genetics 11, 636-646 (2010); Rahman et al. Human Gene Therapy 22(8): 925-933 (2011); Tsai et al. Nature Biotechnology (2014) 32: 569-576; и Collins et al. Proceedings Biological Sciences / The Royal Society, 282(1821):pii 20143003 (2015). Например, редактирование генома может осуществляться in vivo или ех vivo (например, in vitro). В некоторых вариантах осуществления вирусные и невирусные способы переноса генов могут применяться для введения нуклеиновых кислот, кодирующих TALEN, ZFN или RFN, в клетки млекопитающих или целевые ткани. Такие способы могут применяться для введения нуклеиновых кислот, кодирующих TALEN, ZFN или RFN, в клетки in vitro. В некоторых вариантах осуществления невирусные векторные системы доставки включают ДНК-плазмиды, чистую нуклеиновую кислоту и нуклеиновую кислоту в комплексе со средой-носителем для доставки, такой как полоксамеры или липосомы. В некоторых вариантах осуществления нуклеиновые кислоты, кодирующие TALEN, ZFN или RFN, трансфицируют с посредством электропорации. В некоторых вариантах осуществления невирусная система доставки включает прямой перенос мРНК, кодирующей TALEN, ZFN или RFN, например, посредством микроинъекции. Вирусные векторные системы доставки включают ДНК-содержащие и РНК-содержащие вирусы, которые имеют либо эписомальную, либо интегрированную форму генома после доставки в клетку. Примеры вирусных векторных систем доставки включают без ограничения дефектные по интегразе лентивирусные векторы, аденовирусные векторы и векторы на основе аденоассоциированного вируса. В некоторых вариантах осуществления компоненты системы редактирования генома смешиваются перед введением субъекту. В некоторых вариантах осуществления компоненты системы редактирования генома вводятся по отдельности. Отдельное введение компонентов системы редактирования генома может быть по сути одновременным, последовательным или разделенным определенным временным промежутком.
[0096] В данном документе описаны высокочувствительные и надежные способы выявления и/или измерения FokI в образце. Как показано в данном документе, данными способами можно выявлять FokI на физиологических уровнях.
Выявляемые компоненты
[0097] Используемые в данном документе выявляемые компоненты включают компоненты любой структуры, способные быть выявленными посредством любых способов, известных из уровня техники. Выявляемый компонент относится к любому элементу, молекуле, функциональной группе, соединению, фрагменту или компоненту, который является выявляемым. Выявляемые компоненты включают без ограничения радионуклиды (например, 3Н, 14С, 18F, 19F, 32Р, 35S, 135I, 125I, 123I, 64Cu, 187Re, 111In, 90Y, 99mTc, 177Lu, 89Zr и т.д.), флуоресцентные красители (такие как, например, флуоресцеиновые красители, акридиновые красители, красители SYBR, родаминовые красители, оксазиновые красители и т.д.), хемилюминесцентные средства (такие как, например, сложные эфиры акридина, стабилизированные диоксетаны и т.п.), электрохемилюминесцентные средства (такие как, например, SULFO-TAG), биолюминесцентные средства (такие как, например, люциферин), спектрально различимые неорганические флуоресцентные полупроводниковые нанокристаллы (т.е. квантовые точки), наночастицы металлов (например, золото, серебро, медь, платина и т.д.), нанокластеры, парамагнитные ионы металлов, ферменты (такие как, например, пероксидаза хрена, щелочная фосфатаза и т.д.), колориметрические метки (такие как, например, красители, коллоидное золото и т.п.), биотин, диоксигенин, гаптены, а также белки, для которых доступны антисыворотки или моноклональные антитела.
[0098] В некоторых вариантах осуществления антитело к FokI связано с выявляемым компонентом. Антитело к FokI может быть ковалентно или нековалентно связано с выявляемым компонентом. В некоторых вариантах осуществления выявляемый компонент выбран из Sulfo-Tag, пероксидазы хрена, щелочной фосфатазы, FITC, дигоксигенина, акридана, RPE, люциферина, флуорофоров, хромофоров, радиоизотопов или биотина.
[0099] В некоторых вариантах осуществления выявляемый компонент представляет собой электрохемилюминесцентную (ECL) метку. В целом анализы на основе ECL подразумевают использование электрохемилюминесцентных соединений в качестве меток (в данном документе упоминаемые как ECL-метки). Любые соединения, способные к электрохемилюминесценции, можно использовать в качестве ECL-меток. Примеры ECL-меток включают без ограничения металлоорганические соединения, такие как компонент на основе трис-бипиридил-рутения (RuBpy), где металл относится, например, к металлам из VII и VIII группы, в том числе Re, Ru, Ir и Os. В некоторых вариантах осуществления ECL-метка представляет собой метку Sulfo-Tag. Молекулы, которые вступают в реакцию с ECL-меткой в процессе ECL, в данном документе упоминаются как сореактанты ECL. Часто используемые сореактанты для ECL включают третичные амины (например, трипропиламин (ТРА)), оксалат и персульфат.
[0100] В некоторых вариантах осуществления антитело к TALEN связано с выявляемым компонентом. Выявляемый компонент может быть связан с антителом к TALEN посредством ковалентной конъюгации или посредством нековалентной связи. Ковалентная конъюгация выявляемого компонента с антителом к TALEN может быть прямой или может осуществляться посредством линкера. В некоторых вариантах осуществления выявляемый компонент выбран из ECL-метки (например, Sulfo-Tag), пероксидазы хрена, щелочной фосфатазы, FITC, дигоксигенина, акридана, RPE, люциферина, флуорофоров, хромофоров, радиоизотопов или биотина.
[0101] Антитела к TALEN, описанные в данном документе, могут применяться в любом анализе, известном из уровня техники, для измерения наличия или интенсивности выявляемого компонента в иммунологическом анализе. В некоторых вариантах осуществления выявление наличия или отсутствия молекулы, содержащей FokI (например, белка TALEN), включает измерение электрохемилюминесценции, люминесценции, флуоресценции или поглощения любыми способами, известными из уровня техники. Стадия выявления может включать количественное измерение, которое можно использовать для определения количества полипептида FokI в образце. Измерение (измерения) для определения наличия или интенсивности FokI может быть выполнено вручную или может быть выполнено с помощью аппарата, такого как анализатор. Например, в некоторых вариантах осуществления выявляемый компонент может производить цветовой результат. Способы могут включать визуальную оценку окрашенного продукта, и/или для выявления или количественного определения окрашенного продукта может быть использован прибор, такой как анализатор. В некоторых вариантах осуществления стадия выявления включает измерение электрохемилюминесценции, которое может осуществляться с помощью коммерчески доступного прибора.
[0102] В некоторых вариантах осуществления выявляемый компонент представляет собой флуоресцентную метку, фотохромное соединение, белковую флуоресцентную метку, магнитную метку, радиоактивную метку или гаптен. В некоторых вариантах осуществления выявляемая метка представляет собой флуоресцентную метку, выбранную из группы, состоящей из красителя Atto, красителя Alexa Fluor, квантовых точек, гидроксикумарина, аминокумарина, метоксикумарина, Cascade Blue, Pacific Blue, Pacific Orange, Lucifer Yellow, NBD, R-фикоэритрина (PE), конъюгатов PE-Cy5, конъюгатов PE-Cy7, Red 613, PerCP, TruRed, FluorX, флуоресцеина, BODIPY-FL, Cy2, Су3, Су3В, Cy3.5, Cy5, Су5.5, Су7, TRITC, X-родамина, Lissamine Rhocamine В, Texas Red, аллофикоцианина (АРС), конъюгатов АРС-Су7, Indo-1, Fluo-3, Fluo-4, DCFH, DHR, SNARF, GFP (мутация Y66H), GFP (мутация Y66F), EBFP, EBFP2, азурита, GFPuv, T-Sapphire, Cerulean, mCFP, mTurquoise2, ECFP, CyPet, GFP (мутация Y66W), mKeima-Red, TagCFP, AmCyan1, mTFP1, GFP (мутация S65A), Midorishi Cyan, GFP дикого типа, GFP (мутация S65C), TurboGFP, TagGFP, GFP (мутация S65L), Emerald, GFP (мутация S65T), EGFP, Azami Green, ZsGreenl, TagYFP, EYFP,Topaz, Venus, mCitrine, YPet, TurboYFP, ZsYellowl, Kusabira Orange, mOrange, аллофикоцианина (АРС), mKO, TurboRFP, tdTomato, TagRFP, мономера DsRed, DsRed2, mStrawberry, TurboFP602, AsRed2, mRFP1, J-Red, R-фикоэритрина (RPE), В-фикоэритрина (BPE), mCherry, HcRed1, Katusha, P3, перидинин-хлорофилла (PerCP), mKate (TagFP635), TurboFP635, mPlum и mRaspberry.
Рестрикционный фермент FokI 2 типа
[0103] FokI представляет собой бактериальную рестрикционную эндонуклеазу IIS типа, которая встречается в природе в Flavobacterium okeanokoites. Природная FokI состоит из N-концевого ДНК-связывающего домена и неспецифического ДНК-расщепляющего домена на С-конце (номер доступа в UniProt Р14870). Полноразмерная аминокислотная последовательность FokI дикого типа представляет собой 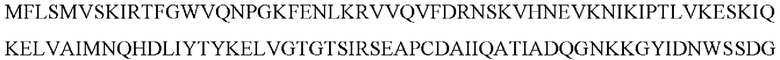

[0104] ДНК-расщепляющий домен FokI может функционировать независимо от ДНК-связывающего домена. В некоторых вариантах осуществления полипептид FokI состоит, по сути состоит или содержит нуклеазный домен FokI. В некоторых вариантах осуществления полипептид каталитического домена FokI представляет собой аминокислоты дикого типа 439-583 под SEQ ID NO: 2. В некоторых вариантах осуществления антитела к TALEN, описанные в данном документе, связываются с молекулой, содержащей SEQ ID NO: 1.

[0105] В некоторых вариантах осуществления белок FokI подвергается модификации. В некоторых вариантах осуществления модифицированный белок FokI содержит аминокислотную последовательность, характеризующуюся по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичностью по отношению к каталитическому домену FokI дикого типа (SEQ ID NO: 1). В некоторых вариантах осуществления белок FokI содержит биологически активные фрагменты FokI. В некоторых вариантах осуществления биологически активный фрагмент содержит каталитический домен FokI. В некоторых вариантах осуществления белок FokI содержит ДНК-расщепляющий домен FokI. В некоторых вариантах осуществления белок FokI содержит аминокислотную последовательность, которая отличается от SEQ ID NO: 1 на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 20 или более аминокислот.
Типы образцов
[0106] Типы образцов по настоящему изобретению включают любые материалы, которые содержат, предположительно содержат, вероятно содержат или для которых подтверждено содержание белков TALEN или молекул, содержащих каталитический домен FokI. В некоторых вариантах осуществления образец представляет собой образец in vitro. В некоторых вариантах осуществления образец представляет собой образец in vivo. В некоторых вариантах осуществления образец имеет биологическое происхождение (например, биологический образец). Биологические образцы включают все материалы, которые в какой-либо момент являлись частью живого организма. В некоторых вариантах осуществления биологический образец получен от млекопитающего. Млекопитающие включают без ограничения людей, собак, кошек, коров, свиней, овец, приматов, отличных от человека, и лам. Люди могут представлять собой людей любого возраста. Биологический образец может приобретать любую форму и может включать без ограничения клетки, ткань, цельную кровь, плазму крови, сыворотку крови, мочу, стул, слюну, пуповинную кровь, сперму, водянистую влагу или стекловидное тело, образец ворсин хориона и их комбинацию. В некоторых вариантах осуществления образец представляет собой образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ex vivo или в среде для культивирования клеток. В некоторых вариантах осуществления образец, например, образец сыворотки крови, подлежит анализу на наличие (или отсутствие) или уровень белка TALEN или FokI.
Наборы
[0107] Также в данном документе предусмотрены наборы для применения в выявлении и/или измерении FokI в образце (например, в биологическом образце), как описано в данном документе. Такие наборы, как правило, включают одно или более веществ, реагентов и/или материалов для применения в способах, предусмотренных в данном документе. Набор может содержать инструкции для осуществления таких способов. Наборы для выявления и/или измерения FokI могут содержать различные реагенты, необходимые для анализа 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 40, 50, 60, 70, 80, 90, 100, 150,200, 250, 300,400, 500, 600, 700, 800, 900, 1000 или более образцов. В некоторых вариантах осуществления набор может обеспечивать возможность для одновременного или почти одновременного анализа множества образцов, как, например, набор для анализа типа микропланшета. В некоторых вариантах осуществления набор может являться одноразовым, таким образом, реагенты и материалы предназначены для однократного применения и/или подлежат утилизации после осуществления анализа.
[0108] В некоторых вариантах осуществления набор для применения в выявлении и/или измерении FokI в образце содержит антитело к TALEN, описанное в данном документе и необязательно конъюгированное с выявляемым компонентом, или может содержать материалы, обеспечивающие лицу, применяющему набор, возможность для осуществления такой конъюгации. Субстраты для наборов для выявления FokI, описанных в данном документе, могут приобретать любую подходящую форму, которая обеспечивает связывание антител к FokI, описанных в данном документе, с комплексами, содержащими FokI. В некоторых вариантах осуществления субстрат содержится в микропланшете или является его частью. Можно применять любой подходящий выявляемый компонент, известный из уровня техники. Например, выявляемые компоненты включают без ограничения ECL-метку (например, Sulfo-Tag), пероксидазу хрена, щелочную фосфатазу, FITC, дигоксигенин, акридан, RPE, люциферин, флуорофоры, хромофоры, радиоизотопы или биотин. Кроме того, любые подходящие способы выявления могут применяться в сочетании с наборами для выявления FokI, описанными в данном документе. Набор может содержать или не содержать реагенты, материалы и/или инструменты для осуществления выявления или измерения сигнала. В некоторых вариантах осуществления применение набора может включать выявление сигнала, что предусматривает измерение электрохемилюминесценции, люминесценции, флуоресценции или поглощения. Выявление сигнала, связанного с анализом, представляющим собой выявление FokI с применением антител, может осуществляться любыми способами, известными из уровня техники. Соответствующие наборы могут содержать или не содержать инструкции для конкретного способа выявления. В некоторых вариантах осуществления набор может содержать направление пользователя к стандартным способам выявления. В некоторых вариантах осуществления набор может содержать направление пользователя к инструкциям, связанным с другими приборами для выявления.
Типичные пути применения
[0109] В некоторых вариантах осуществления способы и наборы по настоящему изобретению могут применяться для оценки и/или мониторинга клеточной или генной терапии, например, терапии CAR-T. В некоторых вариантах осуществления клеточная или генная терапия представляет собой генную терапию на основе ZFN. В некоторых вариантах осуществления клеточная или генная терапия представляет собой генную терапию на основе RFN. В некоторых вариантах осуществления клеточная терапия представляет собой генную терапию на основе TALEN. В некоторых вариантах осуществления клеточная или генная терапия предусматривает введение конструкции ДНК. В некоторых вариантах осуществления клеточная или генная терапия предусматривает заместительную терапию с применением мРНК. В некоторых вариантах осуществления клеточная или генная терапия предусматривает заместительную клеточную терапию, такую как терапия на основе химерных антигенных рецепторов (CAR), которая может предусматривать замещение с применением аллогенных или аутологичных клеток. Заместительная клеточная терапия может включать введение клеток, которые были трансдуцированы или трансфицированы с помощью конструкции на основе нуклеиновой кислоты, кодирующей белок FokI или его биологически активный фрагмент.
[0110] В некоторых вариантах осуществления образцы для оценки и/или мониторинга клеточной или генной терапии могут быть получены до начала терапии. В некоторых вариантах осуществления образцы получают после первого лечения или дозы клеточной или генной терапии. В некоторых вариантах осуществления образцы получают после завершения генной терапии. В некоторых вариантах осуществления образцы получают в конкретные моменты времени, через определенные интервалы или в какой-либо другой промежуток времени до, во время или после осуществления клеточной или генной терапии. В некоторых вариантах осуществления выявление FokI применяют для оценки потенциала клеточной или генной терапии.
Способы лечения
[0111] В некоторых вариантах осуществления антитела к TALEN по настоящему изобретению могут применяться для оценки и/или мониторинга генной терапии или клеточной заместительной терапии, такой как терапия CAR. В некоторых вариантах осуществления генная терапия включает введение пациенту популяции клеток, сконструированных с белком TALEN для экспрессии химерного антигенного рецептора (CAR). Содержащие CAR иммунные клетки могут быть использованы для лечения злокачественных новообразований, связанных с аберрантной экспрессией биомаркеров, в том числе рака. В некоторых вариантах осуществления содержащие CAR иммунные клетки по настоящему изобретению могут применяться для лечения неходжкинской лимфомы, например, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), лейкемии (например, CLL или ALL), множественной миеломы (ММ), мелкоклеточного рака легких, меланомы, глиом низкой степени злокачественности, глиобластомы, медуллярного рака щитовидной железы, карциноидных опухолей, рассеянных нейроэндокринных опухолей в поджелудочной железе, мочевом пузыре и предстательной железе, рака яичек и видов аденокарциномы легких с нейроэндокринными признаками.
[0112] Используемый в данном документе термин «рак» включает без ограничения солидные опухоли и опухоли, происходящие из системы крови. Термин «рак» относится к заболеванию тканей кожи, органов, крови и сосудов, включающему без ограничения виды рака мочевого пузыря, костей или крови, головного мозга, молочной железы, шейки матки, органов грудной клетки, толстой кишки, эндометрия, пищевода, глаза, головы, почки, печени, лимфатических узлов, легкого, ротовой полости, шеи, яичников, поджелудочной железы, предстательной железы, прямой кишки, желудка, яичка, гортани и матки. Конкретные виды рака включают без ограничения злокачественную опухоль на поздней стадии, амилоидоз, нейробластому, менингиому, гемангиоперицитому, множественные метастазы головного мозга, мультиформную глиобластому, глиобластому, глиому ствола головного мозга, злокачественную опухоль головного мозга с неблагоприятным прогнозом, злокачествленную глиому, рецидивирующую злокачествленную глиому, анапластическую астроцитому, анапластическую олигодендроглиому, нейроэндокринный рак, аденокарциному прямой кишки, колоректальный рак на стадиях С и D согласно системе стадирования по Дюку, неоперабельную колоректальную карциному, метастатическую гепатоклеточную карциному, саркому Капоши, острый миелобластный лейкоз с его кариотипом, лимфому Ходжкина, неходжкинскую лимфому (NHL), кожную Т-клеточную лимфому, кожную В-клеточную лимфому, диффузную крупноклеточную В-клеточную лимфому, низкодифференцированную фолликулярную лимфому, злокачественную меланому, злокачественную мезотелиому, синдром злокачественного плеврального выпота при мезотелиоме, перитонеальную карциному, папиллярную серозную карциному, саркому женских половых органов, саркому мягких тканей, склеродермию, кожный васкулит, гистиоцитоз из клеток Лангерганса, лейомиосаркому, оссифицирующую прогрессирующую фибродисплазию, гормонорезистентный рак предстательной железы, резецированную саркому мягких тканей с высоким риском, неоперабельную гепатоклеточную карциному, макроглобулинемию Вальденстрема, вялотекущую миелому, невыраженную миелому, рак фаллопиевой трубы, андрогеннезависимый рак предстательной железы, андрогензависимый неметастатический рак предстательной железы IV стадии, рак предстательной железы, нечувствительный к гормональной терапии, рак предстательной железы, нечувствительный к химиотерапии, папиллярную карциному щитовидной железы, фолликулярную карциному щитовидной железы, медуллярную карциному щитовидной железы и лейомиому. В конкретном варианте осуществления рак является метастатическим. В другом варианте осуществления рак является трудно поддающимся лечению или устойчивым к химиотерапии или лучевой терапии. В дополнительном варианте осуществления степень уменьшения рака была определена как меньшая, чем требовалось, и повторное лечение считалось подходящим.
ПРИМЕРЫ
Пример 1. Получение антител к TALEN
[0113] Для получения гибридомных клеток мышей Balb/c дикого типа иммунизировали белком, представляющим собой каталитический домен FokI, содержащим С-концевую метку 6xHis и линкер GSGS. При использовании повторных иммунизации в нескольких участках (RIMMS) клетки от мышей Balb/c в день 12 иммунизации подвергали слиянию с получением гибридомного слияния №2296. Полученные антитела подвергали скринингу по каталитическому домену FokI для получения положительных результатов ELISA и подвергали параллельному скринингу с применением антигена, представляющего собой гистидиновую метку. Образцы также были подвергали скринингу по полноразмерному белку TALEN, содержащему C-концевую метку 6xHis и линкер GSGS. Антитела анализировали посредством вестерн-блоттинга и оценивали с помощью Biacore® для подтверждения связывания и оценки кинетических свойств.
[0114] Для антител, полученных из слияния №2296, получали более 30 положительных результатов ELISA при скрининге по белку FokI и полноразмерному белку TALEN. Для данных антител были получены отрицательные результаты при скрининге по антигену, представляющему собой гистидиновую метку. При проведении анализа антител из слияния №2296 с помощью Biacore® получали значения kD в диапазоне от 5 нМ до 100 нМ. Результаты анализа кинетических свойств слияния №2296 дня 12 RIMMS с помощью Biacore® показаны в табл. 2 ниже.
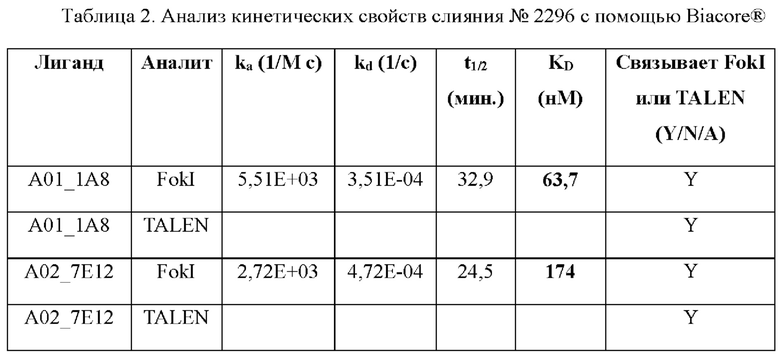
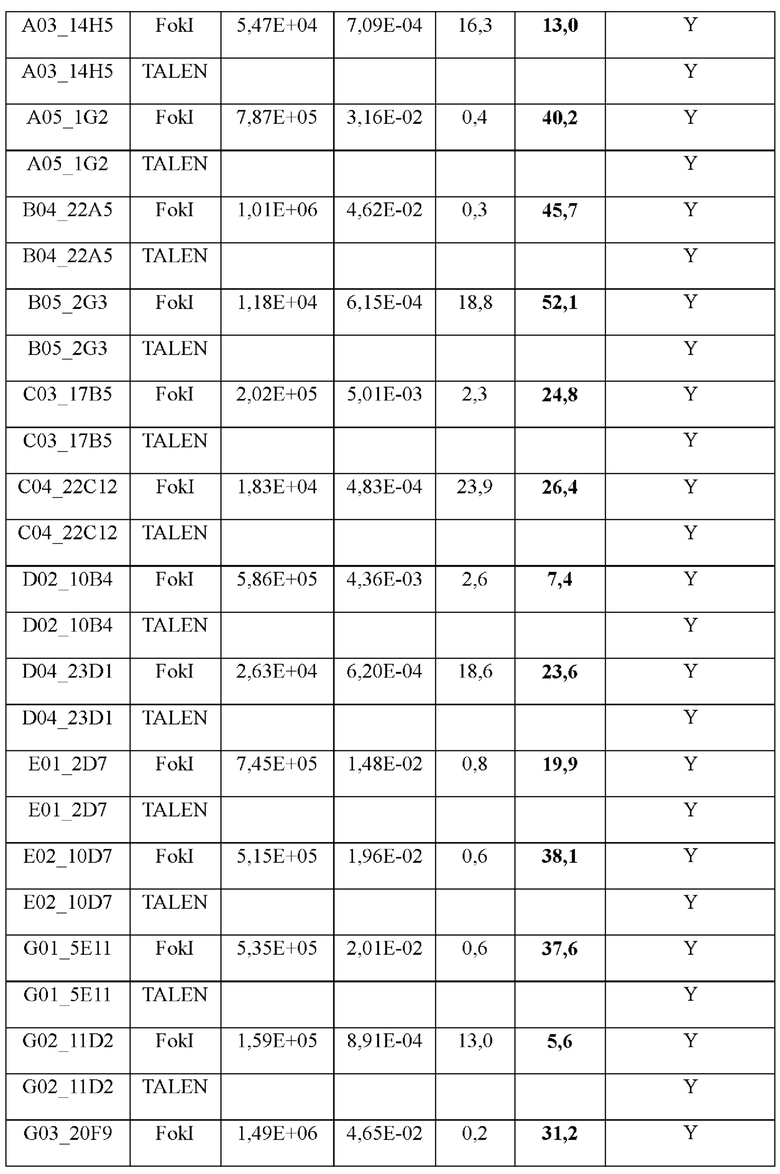
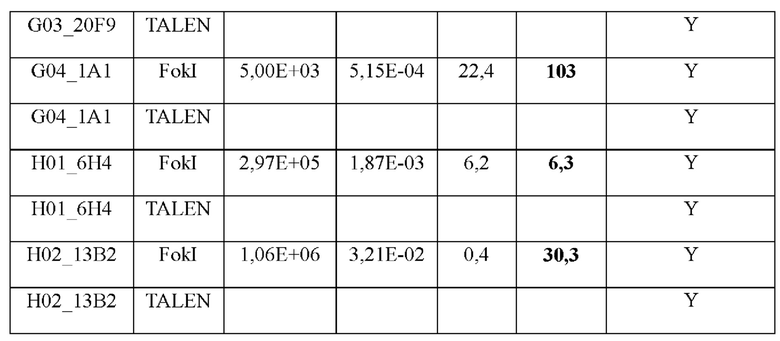
[0115] Клетки гибридомы из слияния №2299 получали в день 94 после длительной иммунизации. Для слияния выбирали мышь Balb/c №2299 с более высоким титром антител. Для антител, полученных из слияния №2299, получали более 68 положительных результатов ELISA при скрининге по белку FokI и полноразмерному белку TALEN. Для данных антител были получены отрицательные результаты при скрининге по антигену, представляющему собой гистидиновую метку. При проведении анализа антител из слияния №2299 с помощью Biacore® получали значения kD в диапазоне от суб нМ до 100 нМ. Для пяти из 12 образцов, демонстрирующих наилучшее связывание по результатам ELISA, получали положительные результаты при проведении анализа посредством вестерн-блоттинга с применением супернатанта (фиг. 1). Результаты анализа кинетических свойств иллюстративных антител из слияния №2299 с помощью Biacore® показаны в табл. 3 ниже.
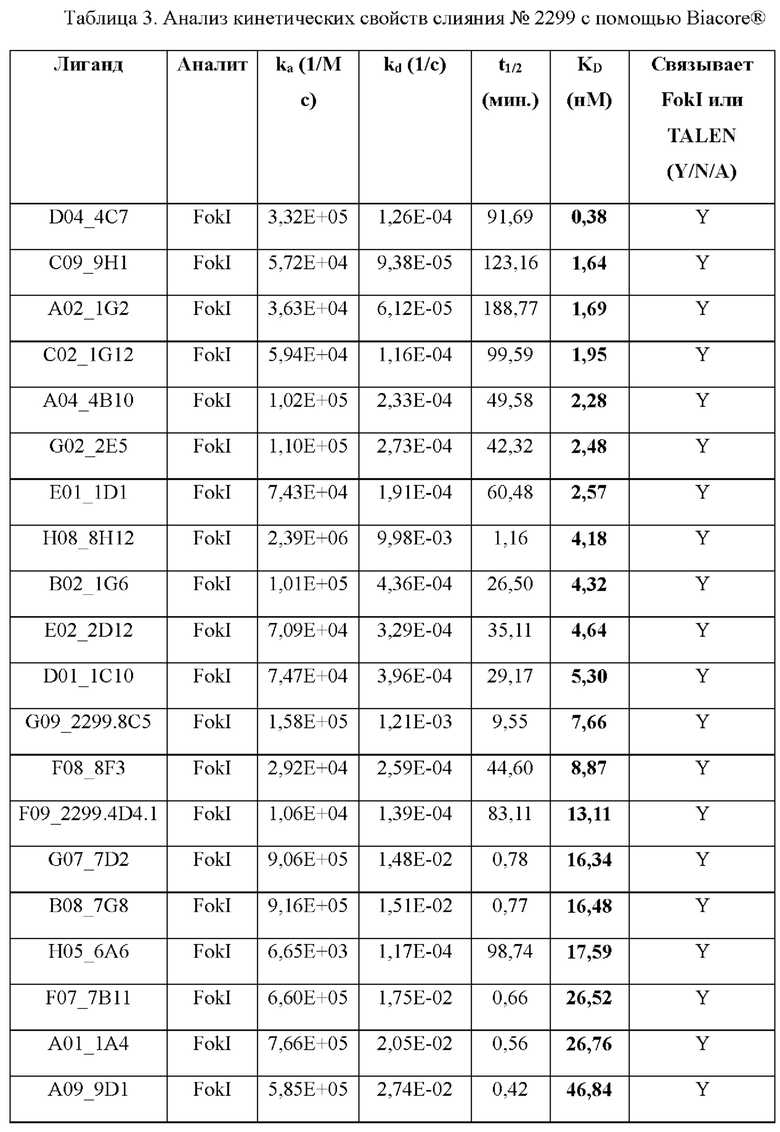
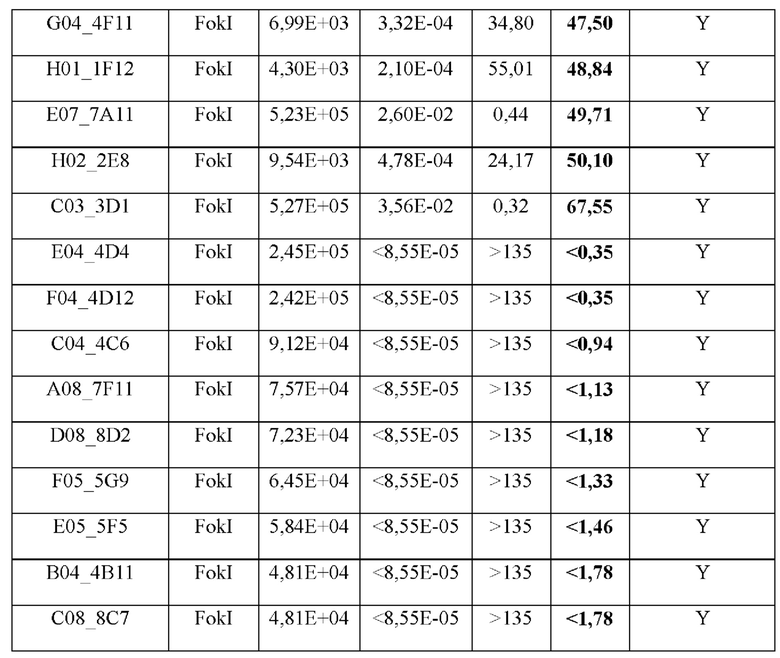
[0116] Очищенные антитела, показанные в табл. 4 ниже, выбирали для дальнейшего анализа и разработки способа анализа.
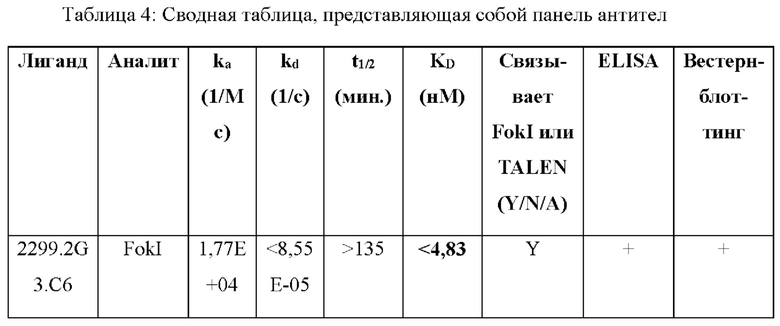
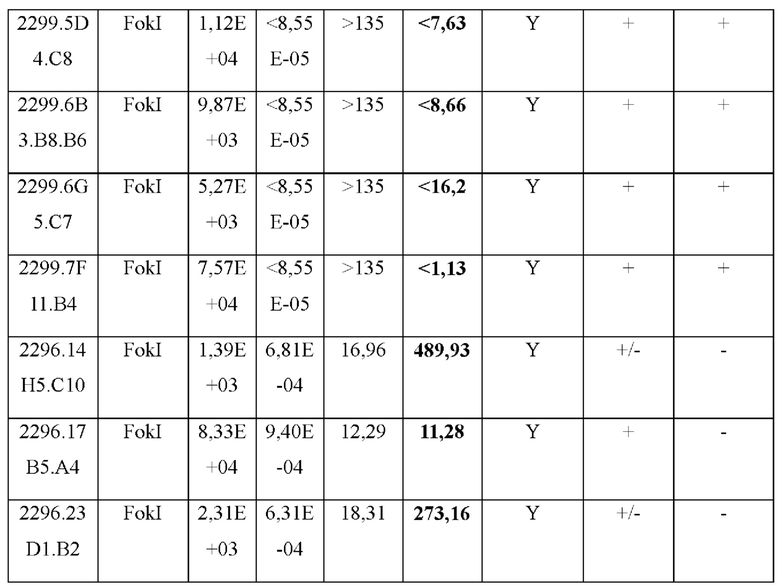
ЭКВИВАЛЕНТЫ И ОБЪЕМ ИЗОБРЕТЕНИЯ
[0117] Специалистам в данной области будет понятно, или они будут способны определить с помощью не более чем стандартных экспериментов, множество эквивалентов конкретных вариантов осуществления настоящего изобретения, описанных в данном документе. Предполагается, что объем настоящего изобретения не ограничивается приведенным выше описанием, а скорее соответствует изложенному в нижеследующей формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИБЛИОТЕКИ СИНТЕТИЧЕСКИХ ПОЛИПЕПТИДОВ И СПОСОБЫ ПОЛУЧЕНИЯ ВАРИАНТОВ ПОЛИПЕПТИДОВ С ЕСТЕСТВЕННЫМ РАЗНООБРАЗИЕМ | 2010 |
|
RU2562163C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ НЕКТИН-4, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2805252C2 |
| ANTI-CXCR4 АНТИТЕЛА И КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВО | 2014 |
|
RU2675516C2 |
| АНТИТЕЛА, КОТОРЫЕ СПЕЦИФИЧНО СВЯЗЫВАЮТ АЛЬФА-ТОКСИН STAPHYLOCOCCUS AUREUS, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2620065C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПОДАВЛЕНИЯ РАКОВЫХ СТВОЛОВЫХ КЛЕТОК | 2016 |
|
RU2752610C1 |
| АНТИ-C5 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2774716C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА К CD33 | 2015 |
|
RU2747384C2 |
| СВЯЗЫВАЮЩИЕ БЕЛКИ, СПЕЦИФИЧНЫЕ В ОТНОШЕНИИ LOX1, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2764993C2 |
| АНТИТЕЛА К ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРАМ, ПОЛУЧЕННЫМ ИЗ 4G7 | 2020 |
|
RU2826051C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ ИНТЕРЛЕЙКИНА-31 | 2012 |
|
RU2588462C2 |

Изобретение относится к области биотехнологии. Предложены антитела, специфичные к каталитическому домену FokI нуклеазы, и способы их получения. Также предложены конъюгаты указанных антител с выявляемой меткой. Также изобретение относится к применению антител и конъюгатов для определения наличия каталитического домена FokI нуклеазы в образце. Изобретение может применяться для оценки безопасности и эффективности различных видов терапии, предусматривающих редактирование генов. 10 н. и 18 з.п. ф-лы, 1 ил., 7 табл., 1 пр.
1. Антитело, специфичное к каталитическому домену FokI нуклеазы, содержащему аминокислотную последовательность SEQ ID NO: 1, причем антитело содержит аминокислотную последовательность вариабельной области тяжелой цепи (VH), которая характеризуется по меньшей мере 85% идентичностью с SEQ ID NO: 3, и аминокислотную последовательность вариабельной области легкой цепи (VL), которая характеризуется по меньшей мере 90% идентичностью с SEQ ID NO: 7, причем антитело содержит:
(a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14; CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 23; и CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, или содержит
(b) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 13 или 14; CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19; CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 25; и CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, или содержит
(c) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14; CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 28, или содержит
(d) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14; CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17 или 20; CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; и CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27, или содержит
(e) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14; CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18; CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21; CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22; CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24; и CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27.
2. Антитело по п. 1, содержащее аминокислотную последовательность VH, которая характеризуется по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 3, или аминокислотную последовательность VL, которая характеризуется по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью с SEQ ID NO: 7.
3. Антитело, специфичное к каталитическому домену FokI нуклеазы, содержащему аминокислотную последовательность SEQ ID NO:1, содержащее:
(a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 23, и
(f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26,
или содержащее
(g) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 13 или 14;
(h) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19;
(i) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(j) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(k) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 25, и
(l) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26,
или содержащее
(m) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(n) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(o) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(p) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(q) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(r) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 28,
или содержащее
(s) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(t) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17 или 20;
(u) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(v) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(w) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(x) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27,
или содержащее
(y) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(z) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(aa) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(bb) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(cc) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(dd) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27.
4. Конъюгат для определения наличия каталитического домена FokI нуклеазы, причем конъюгат содержит антитело по любому из пп. 1-3, конъюгированное с выявляемой меткой.
5. Конъюгат по п. 4, где выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена.
6. Конъюгат по п. 5, где флуоресцентная метка представляет собой R-фикоэритрин (PE) или аллофикоцианин (APC).
7. Композиция для определения наличия каталитического домена FokI нуклеазы, причем композиция содержит антитело по любому из пп. 1-3 и фармацевтически приемлемый носитель или среду-носитель.
8. Способ получения антитела по п. 1, включающий инкубирование клетки, содержащей один или более векторов, содержащих полинуклеотид, кодирующий тяжелую цепь антитела по п. 1, и полунуклеотид, кодирующий легкую цепь антитела по п. 1, в подходящих условиях.
9. Способ определения наличия каталитического домена FokI нуклеазы, содержащего аминокислотную последовательность SEQ ID NO:1, в образце, причем способ включает приведение образца в контакт с антителом по любому из пп. 1-3, конъюгированным с выявляемой меткой, и определение наличия указанного каталитического домена FokI нуклеазы в образце.
10. Способ по п. 9, причем выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена.
11. Способ по п. 9, где образец представляет собой образец иммунных клеток, образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ex vivo или в среде для культивирования клеток.
12. Способ по п. 10, где образец представляет собой образец иммунных клеток, образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ex vivo или в среде для культивирования клеток.
13. Антитело по п. 3, содержащее:
(a) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(b) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(с) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(d) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(e) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 23, и
(f) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, и VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 7.
14. Антитело по п. 3, содержащее:
(g) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 13 или 14;
(h) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 16 или 19;
(i) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(j) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(k) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 25, и
(l) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, и VH, содержащую аминокислотную последовательность SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность SEQ ID NO: 9.
15. Антитело по п. 3, содержащее:
(m) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(n) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(o) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(p) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(q) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(r) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 28, и VH, содержащую аминокислотную последовательность SEQ ID NO: 5, и VL, содержащую аминокислотную последовательность SEQ ID NO: 10.
16. Антитело по п. 3, содержащее:
(s) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(t) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 17 или 20;
(u) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(v) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(w) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(x) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27, и VH, содержащую аминокислотную последовательность SEQ ID NO: 6, и VL, содержащую аминокислотную последовательность SEQ ID NO: 11.
17. Антитело по п. 3, содержащее:
(y) CDR1 VH, содержащую аминокислотную последовательность под SEQ ID NO: 12 или 14;
(z) CDR2 VH, содержащую аминокислотную последовательность под SEQ ID NO: 15 или 18;
(aa) CDR3 VH, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(bb) CDR1 VL, содержащую аминокислотную последовательность под SEQ ID NO: 22;
(cc) CDR2 VL, содержащую аминокислотную последовательность под SEQ ID NO: 24, и
(dd) CDR3 VL, содержащую аминокислотную последовательность под SEQ ID NO: 27, и VH, содержащую аминокислотную последовательность SEQ ID NO: 3, и VL, содержащую аминокислотную последовательность SEQ ID NO: 8.
18. Способ определения наличия каталитического домена FokI нуклеазы, содержащего аминокислотную последовательность SEQ ID NO:1, в образце, причем способ включает приведение образца в контакт с антителом по любому из пп. 1-3 и 13-17, и определение наличия указанного каталитического домена FokI нуклеазы в образце.
19. Способ по п. 18, где антитело конъюгировано с выявляемой меткой.
20. Способ по п. 19, где выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена.
21. Способ по п. 18, где образец представляет собой образец иммунных клеток, образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ex vivo или в среде для культивирования клеток.
22. Способ по п. 19, где образец представляет собой образец иммунных клеток, образец ткани, образец крови, образец, фиксированный в формалине, ткань, выращенную ex vivo или в среде для культивирования клеток.
23. Способ получения антитела по п. 3, включающий инкубирование клетки, содержащей один или более векторов, содержащих полинуклеотид, кодирующий тяжелую цепь антитела по п. 3, и полунуклеотид, кодирующий легкую цепь антитела по п. 3, в подходящих условиях.
24. Применение антитела по любому из пп. 1-3, конъюгированного с выявляемой меткой, для определения наличия каталитического домена FokI нуклеазы, содержащего аминокислотную последовательность SEQ ID NO: 1.
25. Применение по п. 24, где выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена.
26. Применение антитела по любому из пп. 1-3 и 13-17 для определения наличия каталитического домена FokI нуклеазы, содержащего аминокислотную последовательность SEQ ID NO: 1.
27. Применение по п. 26, причем антитело конъюгировано с выявляемой меткой.
28. Применение по п. 27, где выявляемая метка выбрана из группы, состоящей из флуоресцентной метки, фотохромного соединения, белковой флуоресцентной метки, магнитной метки, радиоактивной метки и гаптена.
| RAMALINGAM S | |||
| et al | |||
| Creating Designed Zinc-Finger Nucleases with Minimal Cytotoxicity, Journal of Molecular Biology, 2011, Volume 405, Issue 3, pp | |||
| ПРОМЕЖУТОЧНАЯ ОПОРА ДЛЯ КАНАТНОГО ТРАНСПОРТЕРА | 1923 |
|
SU630A1 |
| MENGER L | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-11-13—Публикация
2020-06-12—Подача