Область техники
Настоящее изобретение относится к интравагинальным устройствам, содержащим прогестерон, способу изготовления таких устройств и применению указанных устройств.
УРОВЕНЬ ТЕХНИКИ
Прогестерон (прегн-4-ен-3,20-дион; C21H30O2) принадлежит к классу гормонов, называемых прогестогенами. Прогестерон представляет собой основной стероид природного происхождения, и он является предшественником в биосинтезе других стероидов, в частности глюкокортикоидов, андрогенов и эстрогенов.
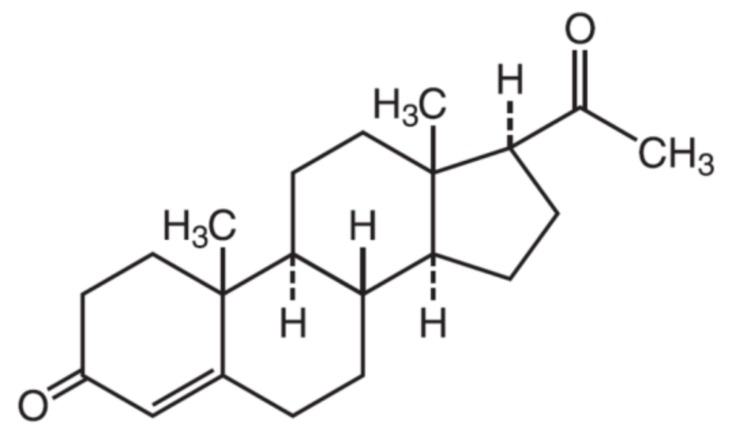
Прогестерон
Прогестерон в больших количествах вырабатывается в яичниках (желтым телом) от начала полового созревания до менопаузы, а также в меньших количествах вырабатывается надпочечниками после наступления преждевременной половой зрелости, вызванной гиперфункцией коры надпочечников (англ. adrenarche), как у мужчин, так и у женщин. В меньшей степени прогестерон вырабатывается в нервной ткани, в частности, в головном мозге, а также в жировой ткани. Во время беременности человека прогестерон во все более высоких количествах вырабатывается яичниками и плацентой. Сначала во время лютеиновой фазы или секреторной фазы менструального цикла и на ранних сроках беременности его источником является желтое тело, однако после 8-й недели беременности функция выработки прогестерона переходит к плаценте.
Прогестерон подготавливает матку к имплантации эмбриона, помогая эндометрию становиться толще и становиться более сосудистым, подготавливая его для размещения оплодотворенной яйцеклетки. Он также выполняет несколько функций во время беременности, включая увеличение молочных желез беременной женщины, подавление сократимости матки, иммунологическую защиту эмбриона и ингибирование синтеза простагландинов.
Прогестерон применяют при лечении ряда клинических расстройств, таких как дисфункциональное маточное кровотечение, эндометриоз, карцинома эндометрия, доброкачественное заболевание молочной железы, угроза выкидыша, преэклампсия, симптомы перименопаузы и недостаточность лютеиновой фазы.
Прогестерон также применяют для поддержания лютеиновой фазы при вспомогательных репродуктивных технологиях, также известных как искусственное оплодотворение. К сожалению, не все женщины репродуктивного возраста способны забеременеть естественным путем. Многие из указанных женщин обращаются к вспомогательным репродуктивным технологиям (ВРТ) для достижения беременности. Существуют по меньшей мере три основных типа ВРТ: экстракорпоральное оплодотворение (ЭКО), которое включает извлечение яйцеклеток, их оплодотворение в лабораторных условиях и перенос возникших эмбрионов в матку через шейку матки; перенос гаметы в маточную трубу (ГИФТ), при котором неоплодотворенные яйцеклетки и сперматозоиды помещаются в маточные трубы женщины с помощью лапароскопа через абдоминальный разрез; и перенос зиготы в маточную трубу (ЗИФТ), который включает извлечение яйцеклеток, их оплодотворение в лабораторных условиях и помещение оплодотворенной яйцеклетки (яйцеклеток) в маточные трубы женщины с помощью лапароскопа. Среди процедур ВРТ также рассматривают интрацитоплазматическую инъекцию сперматозоида (ИКСИ), метод ЭКО, при котором один сперматозоид вводится непосредственно в яйцеклетку; и пересаживание криоконсервированых эмбрионов (FET), при котором замороженный (криоконсервированный) эмбрион размораживают, а затем переносят в матку/маточную трубу женщины.
Для многих женщин в сочетании с ВРТ необходимо предпринять действия для подготовки матки к имплантации эмбриона. Разработано множество инструментов, способствующих данному процессу, среди которых выделяют введение экзогенного прогестерона.
Прогестерон часто вводят извне во время лютеиновой фазы, а иногда даже после лютеиновой фазы, хотя введение прогестерона, продолжающееся после надлежащей трансформации эндометрия в секреторную фазу, не является строго необходимым. Целью введения прогестерона в большинстве случаев является поддержание желтого тела, функция которого может быть нарушена при процедурах ВРТ и которое не способно обеспечить достаточное количество прогестерона для достижения трансформации эндометрия в секреторную фазу.
В данной области техники известны различные препараты прогестерона.
Прогестерон можно вводить перорально, однако из-за его быстрого выведения печенью (эффект первого прохождения через печень) его биодоступность в кровотоке, и в частности в матке, является невысокой, что приводит к значительной неэффективности пероральных составов прогестерона. Кроме того, для достижения уровней прогестерона внутри матки, достаточных для обеспечения пролиферации эндометрия, необходимо введение высоких доз прогестерона перорально, что неизбежно приводит к накоплению метаболитов прогестерона в крови, что, в свою очередь, может вызывать нежелательные побочные эффекты.
Широко используют внутримышечный (в/м) прогестерон, и, хотя с помощью внутримышечного введения могут быть достигнуты высокие уровни в сыворотке крови, прогестерон, доставленный таким образом, подвергается метаболизму в матке до того, как проявит свой терапевтический эффект (эффект первого прохождения через матку), и в результате значительно снижается его эффективность. Кроме того, внутримышечное введение требует ежедневных инъекций и является болезненным, некомфортным и причиняет пациентам неудобства.
Вагинальное введение прогестерона, как правило, приводит к более высоким уровням прогестерона в эндометрии по сравнению с указанными выше способами введения и к более низким уровням в сыворотке крови по сравнению с вводимым внутримышечно прогестероном, и, следовательно, может обеспечить более эффективное лечение с уменьшением системных побочных эффектов. Известны различные типы вагинального введения прогестерона.
Вагинальный гель, содержащий прогестерон, является менее болезненным и более простым в применении, чем внутримышечное введение прогестерона, но также требует ежедневного введения доз, может пачкать и из-за возможности вытекания может не обеспечивать дозу в полном объеме при каждом применении.
Также известно применение вагинальных вставок прогестерона для доставки в таблетках, но опять же требует введения высоких доз прогестерона по меньшей мере один раз в день. Также известны вагинальные капсулы, содержащие микронизированный прогестерон, но они требуют многократного ежедневного приема, что может быть обременительным для пациентов и может привести к прекращению лечения.
Другой известный тип вагинального препарата представляет собой интравагинальные кольца. Интравагинальные кольца предназначены для обеспечения непрерывного высвобождения прогестерона и, таким образом, как правило, не требуют ежедневного или даже частого применения препарата (то есть ежедневной или частой замены кольца), что обеспечивает повышенный комфорт для пациента.
В патенте США 5869081 раскрыто применение вагинальных колец, содержащих прогестерон, для подготовки эндометрия к имплантации эмбриона у ряда пациенток. Zegers-Hochschild et al. (Human Reproduction, 2000, 15 (10), 2093-2097) дополнительно сообщают о клиническом применении одного из таких вагинальных колец для успешного достижения беременности у ряда пациенток, у которых возник синдром преждевременного истощения яичников или отсутствие ответа на стимуляцию яичников.
Stadtmauer et al. (Fertility and Sterility, 2013, 99 (6), 1543-1549) аналогичным образом сообщают, что введение еженедельно вагинального кольца с прогестероном является эффективным для лютеиновой фазы и поддержания беременности в рамках лечения с помощью ВРТ для женщин с бесплодием.
В международной заявке на патент WO 2009/099586 также сообщают о применении вагинальных колец, содержащих прогестерон вместе с углеводородом или сложными эфирами глицерина и жирной кислоты, для лечения недостаточности лютеиновой фазы.
В клинических исследованиях, в которых используют содержащие прогестерон кольца для обеспечения достаточной пролиферации эндометрия, как правило в определенный момент на протяжении лечения, в частности в течение первых недель указанного лечения, у пациентов регистрируют вагинальное кровотечение. Так обстоит дело с упомянутыми выше вагинальными кольцами. Кровотечение, как правило, связано с низкими уровнями внутриматочного прогестерона и иногда устраняется во время лечения путем введения пациенту дополнительного прогестерона. Однако повышение уровней прогестерона не является особо желательным решением из-за возможных побочных эффектов, которые могут возникать в результате накопления прогестерона или его метаболитов. С другой стороны, следует учитывать, что кровотечение, даже если оно может не представлять собой признак осложнения беременности, всегда беспокоит пациентов и может привести к ненужной медицинской консультации. Таким образом, всегда желательно обеспечить лечение, при котором кровотечение на ранних сроках беременности исключается или сводится к минимуму.
Существует постоянная потребность в разработке новых альтернативных препаратов, которые устранят недостатки существующих лекарственных форм прогестерона. В частности, представляется весьма необходимым разработать препараты, обеспечивающие низкие уровни прогестерона в плазме крови при сохранении терапевтической эффективности, улучшении профиля безопасности/комфорта для пациентов и сведении к минимуму кровотечений на ранних сроках беременности.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения неожиданно обнаружили, что вагинальные устройства, содержащие прогестерон в виде полиморфной формы I или прогестерон, характеризующийся высоким процентным содержанием полиморфной формы I, являются эффективными при трансформации эндометрия в секреторную фазу, и при этом сводится к минимуму или не повышается риск вагинального кровотечения. Как следствие, прогестерон можно обеспечивать пациентам без необходимости замены устройства или добавления другого препарата прогестерона на протяжении лечения (по меньшей мере, до тех пор, пока не будет отмечена трансформации эндометрия в секреторную фазу). Предпочтительно вагинальные устройства по настоящему изобретению содержат прогестерон в малых количествах, обеспечивающих низкие уровни прогестерона в сыворотке крови.
Таким образом, настоящее изобретение относится к интравагинальному устройству, содержащему прогестерон, в котором по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I.
Другой аспект настоящего изобретения относится к способу изготовления вагинального устройства в соответствии с настоящим изобретением, включающему стадии:
а) Смешивания прогестерона, где по меньшей мере 75% прогестерона находится в виде полиморфной формы I, с фармацевтически приемлемой полимерной композицией.
б) Отверждения смеси, полученной на стадии а), при температуре 120°C или менее.
Авторы настоящего изобретения также обнаружили, что снижение количества прогестерона в устройствах по настоящему изобретению до уровней ниже, чем те, которые, как правило, используют в устройствах предшествующего уровня техники, приводит к появлению интравагинальных устройств, которые можно применять для успешной трансформации эндометрия в секреторную фазу и поддержания беременности, и при этом сводится к минимуму или даже предотвращается вагинальное кровотечение у беременных женщин.
Таким образом, в конкретном варианте реализации изобретения устройство по настоящему изобретению содержит от 17,4 мас.% до 2,9 мас.% прогестерона от общей массы устройства, более предпочтительно от 11,6 мас.% до 2,9 мас.% прогестерона, еще более предпочтительно от 8,7 мас.% до 2,9 мас.% прогестерона.
Авторы настоящего изобретения неожиданно обнаружили, что вагинальные устройства, изготовленные в соответствии со способом по настоящему изобретению, стабильны в течение по меньшей мере 3 лет при нормальных (комнатная температура) и ускоренных (до 30°C) условиях хранения, демонстрируют значительно меньшее «расплывание» (миграцию к поверхности кольца) прогестерона, способствуют меньшему «взрывному» эффекту (начальному чрезмерному высвобождению) прогестерона и показывают более медленное высвобождение прогестерона in vitro.
Другой аспект настоящего изобретения относится к применению интравагинального устройства по настоящему изобретению для лечения бесплодия у субъекта женского пола.
Еще один аспект настоящего изобретения относится к применению интравагинального устройства по настоящему изобретению для лечения симптомов перименопаузы.
В предпочтительном варианте реализации изобретения устройство представляет собой интравагинальное кольцо.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1. Рентгеновская дифрактограмма образца, полученного из интравагинального кольца в соответствии с настоящим изобретением.
Фиг. 2. Кривая дифференциальной сканирующей калориметрии для образца, полученного из интравагинального кольца в соответствии с настоящим изобретением.
Фиг. 3 и 4. Уровни в сыворотке плазмы крови после введения вагинальных колец по настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Хорошо известно, что органические соединения могут существовать в разных кристаллических формах, известных как полиморфы. Разные полиморфы или полиморфные соотношения определенного вещества могут обеспечивать заметно различающееся терапевтическое поведение.
Прогестерон является плохо растворимым в воде лекарственным средством, которое может представлять собой разные полиморфные формы, из которых наиболее изучены две: форма I (или альфа) и форма II (или бета) (Araya-Sibaja et al., Scanning, 2013, 35 (4), 213-221).
Прогестерон в чистой полиморфной форме I или в форме, обогащенной полиморфом I, может быть получен способами, известными в данной области техники (например, описанным в Barrio et al, Journal of Pharmaceutical Sciences, 2009, 98 (5), 1657-1670). Полиморфная форма I прогестерона образует характерные призматические кристаллы при кристаллизации из разбавленного спирта (O’Neil et al., The Merck Index, 13th Ed., 2001, 7866). Для обнаружения и/или количественного определения содержания полиморфной формы I прогестерона в данной области техники используют различные аналитические методы, а именно дифференциальную сканирующую калориметрию (ДСК), дифракцию рентгеновских лучей, инфракрасную спектроскопию или рамановскую спектроскопию (Wang et al., Organic Process Research & Development, 2000, 4, 391-395). Наиболее часто применяемым методом является дифференциальная сканирующая калориметрия, с помощью которой полиморфная форма I прогестерона демонстрирует характерную эндотерму примерно при 128-130°C, соответствующей ее температуре плавления.
В контексте настоящего изобретения прогестерон используют в его природной форме, то есть вырабатываемой яичниками. Тем не менее, в объем настоящего изобретения также входят фармацевтические соли или сольваты прогестерона. В частности, в объем настоящего изобретения входят фармацевтические соли или сольваты полиморфной формы I прогестерона.
В настоящем описании все выражения процентного количества, соотношений и т.п. даны «по весу», если не указано иное. В настоящем описании термин «по весу» тождественен термину «по массе» и указывает на то, что соотношение или процентное количество, представленные в данной заявке, определяется относительно массы, а не объема, толщины или какого-либо иного измеряемого параметра.
В настоящем описании термин «примерно» при использовании в сочетании с процентом или другой числовой величиной означает плюс или минус 1% от этого процента или другой числовой величины. Например, термин «примерно 80%» охватывает 80% плюс или минус 0,8%.
Предпочтительно интравагинальное кольцо по настоящему изобретению имеет кольцевую форму. В настоящем описании термин «кольцевой» обозначает форму кольца, относящийся кольцу или образующий кольцо. Кольцевые формы, пригодные для применения в настоящем изобретении, включают кольцо, овал, эллипс, тороид и т.п. Форма интравагинального кольца по настоящему изобретению может быть временно изменена или деформирована, то есть может временно принимать некольцевую форму, например, при введении во влагалище. Приведенные ниже значения диаметров колец характеризуют кольца по настоящему изобретению в недеформированном состоянии.
В варианте реализации настоящего изобретения по существу весь прогестерон в устройстве находится в виде полиморфной формы I. Используемый здесь термин «по существу» означает, что прогестерон, содержащийся в интравагинальном устройстве, содержит не более примерно 5%, предпочтительно примерно 2,5%, более предпочтительно примерно 1,5% или менее, предпочтительно примерно 0,5% или менее других полиморфных форм, в частности полиморфной формы II, или не содержит обнаруживаемых количеств других полиморфных форм, в частности полиморфной формы II.
По меньшей мере примерно 75% прогестерона, содержащегося в интравагинальном устройстве по настоящему изобретению, находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 80% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 85% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 90% прогестерона, содержащегося в интравагинальном кольце, находится в виде полиморфной формы I. В предпочтительном варианте реализации изобретения по меньшей мере примерно 95% прогестерона в интравагинальном устройстве, находится в виде полиморфной формы I.
В другом варианте реализации изобретения от примерно 75 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 80 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 85 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 90 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 95 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В предпочтительном варианте реализации изобретения примерно 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I.
Авторы настоящего изобретения неожиданно обнаружили, что интравагинальное устройство, содержащее прогестерон, в котором по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I, можно применять для успешного введения указанного гормона в схемах лечения бесплодия, в частности связанных с вспомогательными репродуктивными технологиями.
Авторы настоящего изобретения также неожиданно обнаружили, что снижение количества прогестерона в устройствах по настоящему изобретению до уровней ниже, чем те, которые, как правило, используют в устройствах известного уровня техники (при применении которых может наблюдаться вагинальное кровотечение во время периода введения прогестерона), все же приводит к появлению интравагинальных устройств, которые можно применять для успешной трансформации эндометрия в секреторную фазу и поддержания беременности, и при этом сводится к минимуму или даже предотвращается вагинальное кровотечение у беременных женщин.
В варианте реализации настоящего изобретения или в любом из вышеупомянутых вариантов реализации изобретения интравагинальное устройство содержит примерно 1,50 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,75 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,70 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,50 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,375 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,125 г прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 0,100 г прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 1,50 до примерно 0,100 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 1,50 до примерно 0,125 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 1,50 до примерно 0,25 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 1,50 до примерно 0,375 г прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 0,75 до примерно 0,100 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 0,75 до примерно 0,125 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 0,75 до примерно 0,25 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 0,75 до примерно 0,375 г прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 0,70 до примерно 0,100 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 0,70 до примерно 0,125 г прогестерона. В другом варианте реализации изобретения оно содержит от примерно 0,70 до примерно 0,25 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 0,70 до примерно 0,375 г прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 0,50 до примерно 0,100 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 0,50 до примерно 0,125 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 0,5 до примерно 0,25 г прогестерона. В более предпочтительном варианте реализации изобретения оно содержит от примерно 0,5 до примерно 0,375 г прогестерона.
В предпочтительном варианте реализации изобретения оно содержит от примерно 0,375 до примерно 0,100 г прогестерона. В более предпочтительном варианте реализации изобретения оно содержит от примерно 0,375 до примерно 0,125 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 0,375 до примерно 0,25 г прогестерона.
В конкретном варианте реализации изобретения оно содержит примерно 1,50 г прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 0,75 г прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 0,70 г прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 0,50 г прогестерона. В предпочтительном варианте реализации изобретения оно содержит примерно 0,375 г прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 0,25 г прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 0,125 г прогестерона.
В варианте реализации настоящего изобретения интравагинальное устройство содержит прогестерон в количестве примерно 34,8% или менее от общей массы кольца. В другом варианте реализации изобретения оно содержит примерно 17,4% прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 16,2% прогестерона или меньше. В предпочтительном варианте реализации изобретения оно содержит примерно 11,6% прогестерона или меньше. В более предпочтительном варианте реализации изобретения оно содержит примерно 8,7% прогестерона или меньше. В другом варианте реализации изобретения оно содержит примерно 2,9% прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 34,8% до примерно 2,9% прогестерона. В другом варианте реализации изобретения оно содержит от примерно 34,8% до примерно 5,8% прогестерона. В другом варианте реализации изобретения оно содержит от примерно 34,8% до примерно 8,7% прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 17,4% до примерно 2,9% прогестерона. В другом варианте реализации изобретения оно содержит от примерно 17,4% до примерно 5,8% прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 17,4% до примерно 8,7% прогестерона.
В другом варианте реализации изобретения оно содержит от примерно 16,2% до примерно 2,9% прогестерона. В другом варианте реализации изобретения оно содержит от примерно 16,2% до примерно 5,8% прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 16,2% до примерно 8,7% прогестерона.
В предпочтительном варианте реализации изобретения оно содержит от примерно 11,6% до примерно 2,9% прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 11,6% до примерно 5,8% прогестерона. В более предпочтительном варианте реализации изобретения оно содержит от примерно 11,6% до примерно 8,7% прогестерона.
В более предпочтительном варианте реализации изобретения оно содержит от примерно 8,7% до примерно 2,9% прогестерона. В предпочтительном варианте реализации изобретения оно содержит от примерно 8,7% до примерно 5,8% прогестерона.
В конкретном варианте реализации изобретения оно содержит примерно 34,8% прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 23,2% прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 17,4% прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 16,24% прогестерона. В предпочтительном варианте реализации изобретения оно содержит примерно 11,6% прогестерона. В более предпочтительном варианте реализации изобретения оно содержит примерно 8,7% прогестерона. В предпочтительном варианте реализации изобретения оно содержит примерно 5,8% прогестерона. В конкретном варианте реализации изобретения оно содержит примерно 2,9% прогестерона.
В конкретных вариантах реализации изобретения в любом и каждом из вышеупомянутых конкретных процентных диапазонов или процентов и/или конкретных диапазонов массы или масс по меньшей мере примерно 95% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I. В предпочтительном варианте реализации изобретения интравагинальное устройство содержит прогестерон в количестве от примерно 34% до примерно 3% от общей массы кольца и от примерно 90 до примерно 96, 97, 98, 99 или 100% прогестерона, содержащегося в интравагинальном кольце, находится в виде полиморфной формы I.
В другом предпочтительном варианте реализации изобретения интравагинальное устройство содержит прогестерон в количестве от примерно 17% до 6% от общей массы устройства, и по меньшей мере примерно 95% прогестерона в интравагинальном устройстве находится в виде полиморфной формы I.
В другом предпочтительном варианте реализации изобретения интравагинальное устройство содержит прогестерон в количестве от примерно 12% до 7% от общей массы устройства, и по меньшей мере примерно 99% прогестерона в интравагинальном устройстве находится в виде полиморфной формы I.
В другом предпочтительном варианте реализации изобретения интравагинальное устройство содержит прогестерон в количестве от примерно 9 до примерно 8% от общей массы устройства, и примерно 100% прогестерона, содержащегося в интравагинальном устройстве, находится в виде полиморфной формы I.
Авторы настоящего изобретения неожиданно обнаружили, что интравагинальное устройство по настоящему изобретению, предпочтительно в форме кольца, содержащее прогестерон в количествах менее 35 мас.%, при этом по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I, можно применять для успешного введения указанного гормона в схемах лечения бесплодия, в частности, связанных с вспомогательными репродуктивными технологиями, в течение по меньшей мере 14 дней без необходимости замены на другое устройство, содержащее прогестерон в более высоких количествах, и без необходимости введения другого препарата прогестерона.
В варианте реализации изобретения или в любом из вышеупомянутых вариантов реализации изобретения устройство дополнительно содержит фармацевтически приемлемую полимерную композицию в качестве фармацевтически приемлемого носителя. Фармацевтически приемлемый носитель, а также любой другой материал, используемый в интравагинальном устройстве по настоящему изобретению, подходит для введения в вагинальные пути субъекта и является нетоксичным для указанного субъекта. Указанные материалы также подходят для изготовления в виде интравагинального устройства определенной формы, предпочтительно кольца или аналогичных форм.
Фармацевтически приемлемые полимерные композиции, подходящие для применения в интравагинальных устройствах, описанных в данной заявке, включают, но не ограничены ими, полимеры олефинового и винилового типа, полимеры углеводного типа, полимеры конденсационного типа, полимеры каучукового типа и/или полисилоксаны. Другие примеры полимеров, которые могут быть использованы, включают полиэтиленвинилацетат, полиметилакрилат, полибутилметакрилат, пластифицированный поливинилхлорид, пластифицированный нейлон, пластифицированный полиэтилентерефталат, полиэтилен, полиакрилонитрил, политрифторхлорэтилен, поли(4,4'-изопропилендифениленкарбонат), сложные полиэтиленвиниловые эфиры, поливинилхлориддиэтилфумарат, сложные поли(эфиры акрилата и метакрилата), ацетат целлюлозы, ацилаты целлюлозы, частично гидролизованный поливинилацетат, поливинилбутираль, полиамиды, поливинилкарбонат, полиуретан, полиолефины, полистирол, поли(стирол-бутадиен) и их комбинации. Эти полимеры и их физические свойства, а также способы синтеза известны в данной области техники.
В конкретных вариантах реализации изобретения фармацевтически приемлемая полимерная композиция содержит по меньшей мере один эластомер.
Термин «эластомер» представляет собой термин, который понимается специалистом в данной области. В частности, эластомер относится к аморфной полимерной сетчатой структуре, образующейся при поперечном сшивании полимера или смеси полимеров. Каждый полимер состоит из мономерных звеньев, которые соединены друг с другом с формированием полимера. Мономерные звенья включают углерод, водород, кислород, кремний, галоген или их комбинацию. Эластомеры можно легко сгибать, растягивать, скручивать или деформировать, и после снятия напряжения они быстро возвращаются к своим приблизительным исходным размерам и форме. Эластомеры придают интравагинальным устройствам достаточную структурную целостность для обеспечения терапевтического применения и достаточную гибкость для адаптации к телу пациента и обеспечения максимального комфорта для пациента.
Предпочтительно фармацевтически приемлемая полимерная композиция содержит по меньшей мере один эластомер на основе силикона, например полисилоксан. В настоящем описании термин «полисилоксан» относится к любому из различных соединений, содержащих чередующиеся атомы кремния и кислорода, расположенные либо линейно, либо циклически. В конкретных вариантах реализации изобретения полисилоксан представляет собой диорганополисилоксан, такой как диарилполисилоксаны и диалкилполисилоксаны. В конкретном варианте реализации изобретения полисилоксан представляет собой полисилоксан с концевыми винилдиметильными группами. В более конкретном варианте реализации изобретения полисилоксан представляет собой диметилполисилоксан с концевыми винильными группами.
В других вариантах реализации изобретения фармацевтически приемлемый носитель содержит по меньшей мере один несиликоновый эластомер, например сополимер стирола, такой как поли(стирол-бутадиен).
В предпочтительном варианте реализации изобретения интравагинальное устройство по настоящему изобретению не содержит других материалов помимо прогестерона и фармацевтически приемлемой полимерной композиции. Однако в другом варианте реализации изобретения интравагинальное устройство по настоящему изобретению может содержать другие материалы в дополнение к прогестерону и фармацевтически приемлемой полимерной композиции.
В предпочтительном варианте реализации изобретения интравагинальное устройство по настоящему изобретению не содержит других материалов, помимо прогестерона, фармацевтически приемлемой полимерной композиции и любого вещества или вещества, производного от вещества или веществ, необходимых для изготовления устройства, а также составляющих часть устройства после его изготовления, например, любого, описанного в данной заявке, например, катализаторов сшивания или ингибиторов катализаторов.
В предпочтительном варианте реализации изобретения интравагинальное устройство по настоящему изобретению не содержит фармацевтически приемлемое вспомогательное вещество в дополнение к прогестерону и фармацевтически приемлемой полимерной композиции. Однако в другом варианте реализации изобретения интравагинальное устройство по настоящему изобретению может содержать фармацевтически приемлемое вспомогательное вещество в дополнение к прогестерону и фармацевтически приемлемой полимерной композиции. Неограничивающие примеры фармацевтически приемлемых вспомогательных веществ для вагинального применения включают смачивающие агенты, поверхностно-активные вещества, полоксамеры, карбополы, поливиниловый спирт, диоксид кремния, карбоксиметилцеллюлозу натрия, эмульгаторы, неионогенные поверхностно-активные вещества, твин, твин 80, полисорбат 80, альфа-липоевую кислоту, альфа-токоферол, аскорбилпальмитат, бензиловый спирт, биотин, бисульфиты, бор, бутилированный гидроксианизол, бутилированный гидрокситолуол, аскорбиновую кислоту, каротиноиды, цитрат кальция, ацетил-L-карнитин, хелатирующие агенты, хондроитин, хром, лимонную кислоту, кофермент Q-10, цистеин, гидрохлорид цистеина, 3-дегидрошикимовую кислоту, ЭДТА, сульфат железа (II), фолиевую кислоту, фумаровую кислоту, алкилгаллаты, чеснок, глюкозамин, экстракт виноградных косточек, гуггул, магний, яблочную кислоту, метабисульфит, N-ацетилцистеин, ниацин, никотинамид, корень крапивы, орнитин, пропилгаллат, пикногенол, со пальметто, селен, бисульфит натрия, метабисульфит натрия, сульфит натрия, сульфит калия, винную кислоту, тиосульфаты, тиоглицерин, тиосорбит, токоферол, токоферола ацетат, токоферола сукцинат, токотриенол, d-альфа-токоферола ацетат, витамин A, витамин B, витамин C, витамин D, витамин E, цинк, углеводы, углеводород или сложные эфиры глицерина и жирной кислоты или их комбинации.
В предпочтительном варианте реализации изобретения интравагинальное устройство по настоящему изобретению не содержит других активных фармацевтических ингредиентов помимо прогестерона. Однако в другом варианте реализации изобретения интравагинальное устройство по настоящему изобретению может содержать другие активные фармацевтические ингредиенты в дополнение к прогестерону. В конкретном варианте реализации изобретения другой активный фармацевтический ингредиент представляет собой вещество, подходящее для обеспечения овуляции, имплантации эмбриона и/или поддержания беременности на ранних сроках. В конкретном варианте реализации изобретения другим активным фармацевтическим ингредиентом является эстроген.
В другом предпочтительном варианте реализации изобретения интравагинальное устройство по настоящему изобретению не содержит фармацевтически приемлемого вспомогательного вещества или других активных фармацевтических ингредиентов в дополнение к прогестерону и фармацевтически приемлемой полимерной композиции, необязательного любого вещества или вещества, производного от веществ, необходимых для изготовления устройства, а также составляющих часть устройства после его изготовления.
В вариантах реализации изобретения, включающих фармацевтически приемлемый носитель, любые из указанных выше массовых процентов или процентных диапазонов прогестерона от массы устройства относится к массе прогестерона от общей массы прогестерона и фармацевтического носителя.
Любые из вышеупомянутых конкретных масс или диапазонов массы и массовых процентов или процентных диапазонов могут быть индивидуально объединены, чтобы обеспечить новые варианты реализации изобретения. В предпочтительном варианте реализации изобретения 0,375 г прогестерона соответствует примерно 8,7% прогестерона от общей массы кольца или от общей массы прогестерона и фармацевтического носителя, а другие конкретные массы, как описано выше, соответствуют массовому проценту на основе указанного соотношения.
В одном из вариантов реализации изобретения или в любом из вышеупомянутых вариантов реализации изобретения прогестерон по существу однородно распределены в интравагинальном устройстве.
В варианте реализации изобретения или в любом из вышеупомянутых вариантов реализации изобретения прогестерон может быть микронизированным. В настоящем описании термин «микронизированный» относится к частицам композиции, размеры которых были уменьшены до размера порядка микрон. В предпочтительном варианте реализации изобретения или в любом из вышеупомянутых предпочтительных вариантов реализации изобретения прогестерон является немикронизированным. Преимущественно, применение немикронизированного прогестерона может предотвращать «взрывной» эффект, при котором происходит начальное высвобождение из вагинального кольца прогестерона в большом количестве.
В варианте реализации изобретения или в любом из вышеупомянутых вариантов реализации изобретения интравагинальное устройство имеет форму кольца или форму, приблизительно аналогичную кольцу. Предпочтительно кольцо имеет внешний диаметр от примерно 40 до примерно 65 мм. В другом варианте реализации изобретения оно имеет внешний диаметр от примерно 50 до примерно 60 мм. В предпочтительном варианте реализации изобретения интравагинальное кольцо имеет внешний диаметр примерно 58 мм. В настоящем описании термин «внешний диаметр» относится к любому прямолинейному отрезку, который проходит через центр кольца, и конечные точки которого находятся на внешнем периметре кольца. Если внешний диаметр кольца является неодинаковымпо всему периметру, внешний диаметр относится к самому длинному прямолинейному отрезку, который проходит через центр кольца, и конечные точки которого находятся на внешнем периметре кольца.
В варианте реализации изобретения или в любом из вышеупомянутых вариантов реализации изобретения интравагинальное устройство, предпочтительно кольцо, имеет диаметр поперечного сечения от примерно 4 до примерно 10 мм. В другом варианте реализации изобретения оно имеет диаметр поперечного сечения от примерно 5 до примерно 8 мм. В предпочтительном варианте реализации изобретения интравагинальное кольцо имеет диаметр поперечного сечения примерно 5,5 мм. В настоящем описании термин «диаметр поперечного сечения» относится к любому прямолинейному отрезку, конечные точки которого находятся на внутреннем и внешнем периметре кольца.
В конкретном варианте реализации изобретения интравагинальное кольцо имеет внешний диаметр от примерно 50 до примерно 60 мм и диаметр поперечного сечения от примерно 5 до примерно 8 мм. В предпочтительном варианте реализации изобретения интравагинальное кольцо имеет внешний диаметр примерно 58 мм и диаметр поперечного сечения примерно 5,5 мм.
В варианте реализации изобретения интравагинальное устройство высвобождает (in vivo) не более или примерно 10 мг прогестерона в день в течение по меньшей мере 7 дней. В другом варианте реализации изобретения интравагинальное кольцо высвобождает (in vivo) не более или примерно 10 мг прогестерона в день в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. В одном из вариантов реализации изобретения интравагинальное устройство высвобождает (in vivo) от 4 до 8 мг прогестерона в день в течение по меньшей мере 7 дней. В предпочтительном варианте реализации изобретения интравагинальное устройство выделяет (in vivo) от 4 до 8 мг прогестерона в день в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. В более предпочтительном варианте реализации изобретения интравагинальное устройство высвобождает (in vivo) примерно 6 мг прогестерона в день в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. Скорость высвобождения измеряют путем вычитания оставшегося количества прогестерона в устройстве в конце лечения (например, 14 день) из количества прогестерона в устройстве в начале лечения (0 день) и деления результата на количество дней лечения (например, 14).
В варианте реализации изобретения интравагинальное устройство позволяет достичь среднего уровня прогестерона в сыворотке крови от 1 до 4 нг/мл в течение по меньшей мере 7 дней. В варианте реализации изобретения интравагинальное устройство позволяет достичь среднего уровня прогестерона в сыворотке крови от 1 до 4 нг/мл в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. В конкретном варианте реализации изобретения интравагинальное устройство позволяет достичь уровня прогестерона в сыворотке крови в диапазоне 1,5-3,5 нг/мл в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. В более конкретном варианте реализации изобретения интравагинальное устройство позволяет достичь уровня прогестерона в сыворотке крови примерно 2-3 нг/мл в течение по меньшей мере 14 дней, предпочтительно в течение периода времени от 14 до 18 дней, более предпочтительно в течение 14 дней. 2-3 нг/мл прогестерона соответствуют примерно 6,3-9,5 нмоль/мл прогестерона.
В варианте реализации изобретения уровни прогестерона в сыворотке крови, обеспечиваемые вагинальным устройством или кольцом по настоящему изобретению, приблизительно постоянны в течение периода применения указанного кольца, за исключением первых 24 часов применения, в течение которых уровни прогестерона в сыворотке крови возрастают. В конкретных вариантах реализации изобретения период применения составляет по меньшей мере 14 дней, предпочтительно от 14 до 18 дней, более предпочтительно 14 дней. «Постоянный» означает, что уровни прогестерона в сыворотке крови поддерживаются на уровне примерно от 3 до 14 нмоль/л, более конкретно от примерно 6 до примерно 14 нмоль/л, предпочтительно примерно от 6 до 12 нмоль/л.
В другом предпочтительном варианте реализации изобретения интравагинальное устройство или кольцо содержит от примерно 1,50 до примерно 0,125 г прогестерона, что соответствует от примерно 34,8% до примерно 2,9% прогестерона от общей массы устройства или от общей массы прогестерона и фармацевтического носителя, и обеспечивает постоянные уровни прогестерона в сыворотке крови от примерно 3 до 14 нмоль/л (за исключением первых 24 часов применения, в течение которых уровни прогестерона в сыворотке крови возрастают) в течение периода применения от 7 до 18 дней, предпочтительно примерно 14 дней, более предпочтительно 14 дней.
В особо предпочтительном варианте реализации изобретения интравагинальное устройство содержит от примерно 0,75 до 0,125 г прогестерона, что соответствует примерно от 17,4 до 2,9% прогестерона от общей массы устройства или от общей массы прогестерона и фармацевтического носителя, и обеспечивает постоянные уровни прогестерона в сыворотке крови от примерно 3 до 12 нмоль/л (за исключением первых 24 часов применения, в течение которых уровни прогестерона в сыворотке крови возрастают) в течение периода применения от 7 до 18 дней, предпочтительно примерно 14 дней, более предпочтительно 14 дней.
В особо предпочтительном варианте реализации изобретения интравагинальное устройство содержит примерно 0,375 г прогестерона, что соответствует примерно 8,7% прогестерона от общей массы устройства или от общей массы прогестерона и фармацевтического носителя, и обеспечивает постоянные уровни прогестерона в сыворотке крови примерно от 6 до 12 нмоль/л (за исключением первых 24 часов применения, в течение которых уровни прогестерона в сыворотке крови возрастают) в течение периода применения от 7 до 18 дней, предпочтительно примерно 14 дней, более предпочтительно 14 дней.
В другом конкретном варианте реализации изобретения интравагинальное устройство содержит от примерно 0,75 до примерно 0,25 г прогестерона, что соответствует от примерно 17,4% до примерно 5,8% прогестерона от общей массы прогестерона и фармацевтического носителя или от общей массы устройства, и обеспечивает постоянные уровни прогестерона в сыворотке крови от 1,5 до 3,5 нг/мл (за исключением первых 24 часов применения, в течение которых уровни прогестерона в сыворотке крови возрастают) в течение периода применения от 7 до 18 дней, предпочтительно примерно 14 дней, более предпочтительно 14 дней.
Таким образом, авторы настоящего изобретения неожиданно обнаружили, что интравагинальное устройство по настоящему изобретению, предпочтительно в форме кольца, содержащее прогестерон в количествах менее 35% по массе, где по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I, можно применять для успешного введения указанного гормона в схемах лечения бесплодия, в частности, связанных с вспомогательными репродуктивными технологиями, в течение по меньшей мере 14 дней без необходимости замены на другое устройство, содержащее прогестерон в более высоких количествах, и без необходимости добавления других препаратов прогестерона. Кроме того, авторы настоящего изобретения продемонстрировали, что применение такого интравагинального устройства, даже обеспечивающего уровни прогестерона в сыворотке крови менее или равные 10 мг/день, неожиданно предотвращает или сводит к минимуму вагинальное кровотечение во время периода введения прогестерона.
На Фиг. 3 и 4 показаны концентрации прогестерона в сыворотке крови, наблюдаемые для вагинальных колец в соответствии с настоящим изобретением, в частности интравагинальных колец, которые содержат от примерно 0,125 г прогестерона до примерно 1,50 г прогестерона.
Как упоминалось выше, настоящее изобретение также относится к способу изготовления вагинального устройства или кольца, как описано выше, причем способ включает стадии:
а) Смешивания прогестерона, где по меньшей мере 75% прогестерона находится в виде полиморфной формы I, с фармацевтически приемлемой полимер-образующей композицией; а затем
б) Отверждения смеси, полученной на стадии а), при температуре 120°C или менее.
Температура плавления полиморфной формы I прогестерона обычно указывается как 128-130°C. При воздействии температур, которые превышают его температуру плавления, прогестерон превращается в метастабильный расплав, и полиморфная форма исчезает (Barrio et al., Journal of Pharmaceutical Sciences, 2009, 98 (5), 1657-1670). Таким образом, при отверждении смеси, полученной на стадии а), при 120°C, в устройстве сохраняется процентное количество прогестерона в виде полиморфной формы I относительно количества исходного материала; то есть снижение количества полиморфной формы I сведено к минимуму.
Прогестерон, по меньшей мере 75% которого находится в виде полиморфной формы I, может быть получен способами, известными в данной области техники, например, описанными Barrio et al. Прогестерон в виде по существу чистой полиморфной формы I также коммерчески доступен.
В варианте реализации изобретения по существу весь прогестерон на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 75% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 80% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 85% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 90% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения по меньшей мере примерно 95% прогестерона на стадии а) находится в виде полиморфной формы I.
В другом варианте реализации изобретения от примерно 75 до примерно 100% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 80 до примерно 100% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 85 до примерно 100% прогестерона на стадии а) находится в виде полиморфной формы I. В другом варианте реализации изобретения от примерно 90 до примерно 100% прогестерона на стадии а) находится в виде полиморфной формы I.
В предпочтительном варианте реализации изобретения чистота полиморфной формы I на стадии а) соответствует чистоте полиморфной формы I в любом из описанных выше вариантов реализации интравагинального устройства и кольца. Как уже упоминалось, способ по настоящему изобретению предотвращает снижение полиморфной чистоты полиморфа I в вагинальном устройстве по отношению к содержащему прогестерон исходному материалу, используемому на стадии а).
Аналогично, масса используемого прогестерона или массовый процент используемого прогестерона могут быть любыми из тех, что описаны выше для вариантов реализации вагинального устройства.
Авторы настоящего изобретения обнаружили, что присутствие прогестерона в виде полиморфной формы I (в массовых процентах, описанных в приведенных выше вариантах реализации вагинального устройства) в смеси, полученной на стадии а), не ингибирует отверждение полимерной композиции на стадии б).
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа отверждение на стадии б) проводят в форме. В предпочтительном варианте реализации изобретения способ по настоящему изобретению включает литье смеси, полученной на стадии а), под давлением в форму на стадии б). В конкретном варианте реализации изобретения форма определяет полость, подходящую для изготовления интравагинальных колец с размерами, как описано выше.
Более того, авторы настоящего изобретения неожиданно обнаружили, что полученные в результате вагинальные устройства или кольца, содержащие по меньшей мере 75% прогестерона в виде полиморфной формы I, могут обладать следующими свойствами, представляющими собой преимущества по сравнению с устройствами или кольцами, содержащими меньшее количество прогестерона в виде полиморфной формы I:
- Значительно меньшее «расплывание» (миграцию к поверхности кольца) прогестерона;
- меньший «взрывной» эффект (начальное чрезмерное высвобождение) прогестерона;
- Более медленное высвобождение прогестерона.
В предпочтительном варианте реализации изобретения отверждение на стадии б) можно проводить за очень короткие периоды времени при использовании эластомер-образующей композиции, как описано ниже, в качестве фармацевтически приемлемой полимер-образующей композиции. Преимущественно, возможность выполнения стадии б) за такое короткое время обеспечивает способ изготовления содержащего прогестерон вагинального устройства по настоящему изобретению, которое, в частности, хорошо подходит для промышленного применения.
Таким образом, в конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа стадию б) осуществляют за время примерно 10 минут или менее, за время примерно 5 минут или менее, за время примерно 3 минуты или менее, за время примерно 45 секунд или менее, за время примерно 30 секунд или менее. В конкретном варианте реализации способа стадию б) осуществляют за время от примерно 10 минут до примерно 15 секунд, за время от примерно 5 минут до примерно 30 секунд, за примерно 3 минуты, за примерно 2 минуты, за примерно 90 секунд, за примерно 1 минуту, за примерно 45 секунд, за примерно 30 секунд. Предпочтительно стадию б) осуществляют за время от примерно 3 минут до примерно 45 секунд.
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа фармацевтически приемлемая полимер-образующая композиция представляет собой любой полимер-образующий материал, который сшивается при температуре менее или равной 120°C, предпочтительно за 10 минут или менее, с образованием фармацевтически приемлемой полимерной композиции, описанной в любом из вышеуказанных вариантов реализации изобретения.
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа фармацевтически приемлемая полимер-образующая композиция представляет собой эластомер-образующую композицию. В конкретном варианте реализации способа эластомер-образующая композиция содержит по меньшей мере один полисилоксан, предпочтительно по меньшей мере один диорганополисилоксан, предпочтительно диметилполисилоксан, любой из которых может быть сшит с эластомером. Предпочтительно полисилоксан содержит на молекулу по меньшей мере две силикон-связанные группы, имеющие алифатическую ненасыщенность, например полисилоксан с концевыми винильными группами. В предпочтительном варианте реализации способа полисилоксан содержит концевые винильные группы. Предпочтительно полисилоксан представляет собой полисилоксан с концевыми винилдиметильными группами. Предпочтительно полисилоксан представляет собой диметилполисилоксан с концевыми винильными группами. В других вариантах реализации способа эластомер-образующая композиция включает полимерный материал на несиликоновой основе, такой как поли(стирол-бутадиен).
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа, где это применимо, эластомер-образующая композиция содержит сшивающий агент, который может представлять собой, например, полисилоксан с концевыми H или OH группами, предпочтительно H группами, предпочтительно диорганополисилоксан с концевыми H или OH группами, предпочтительно H группами. В конкретном варианте реализации способа полисилоксан представляет собой полисилоксан с концевыми водородными и диметильными группами. В более конкретном варианте реализации способа сшивающий агент представляет собой диметилполисилоксан с концевыми H группами.
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа, где это применимо, эластомер-образующая композиция содержит катализатор сшивания, который может представлять собой металлорганическое соединение, например октоат олова (II), дилаурат дибутилолова, алкилтитанаты и хелаты титана, или комплекс платины. В предпочтительном варианте реализации способа катализатор сшивания представляет собой комплекс платины, в частности, который способствует реакции между ненасыщенными группами (например, вышеупомянутыми концевыми винильными группами) и силикон-связанными водородными группами (например, вышеупомянутыми концевыми H-группами), например, хлороплатиновая кислота, ацетилацетонат платины, комплекс галогенидов платины с ненасыщенными соединениями, такими как этилен, пропилен, органовинилсилоксаны и стирол, метилдиплатиновый (I) комплекс и Pt(CN)3. Предпочтительно комплекс платины представляет собой комплекс платины в винильном димере.
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа, где это применимо, эластомер-образующая композиция содержит ингибитор катализатора, например алкинильное соединение, такое как ацетилен-ненасыщенный вторичный или третичный спирт, например этинилциклогексанол. Алифатически-ненасыщенные группы представляют собой предпочтительно олефин-ненасыщенные группы.
В конкретном варианте реализации способа или в любом из вышеупомянутых вариантов реализации способа, где это применимо, эластомер-образующая композиция содержит кремнекислый наполнитель, такой как обработанный диоксид кремния.
Особо предпочтительными с промышленной точки зрения являются эластомер-образующие композиции, которые сшиваются при температуре 120°C или менее и за время примерно 10 минут или менее, такие как эластомер-образующие композиции, содержащие полисилоксан с концевыми винилдиметильными группами, полисилоксан с концевыми водородными и диметильными группами, катализатор на основе комплекса платины, который способствует гидросилилированию, и ингибитор катализатора. В конкретном варианте реализации способа эластомер-образующая композиция содержит полисилоксан с концевыми винилдиметильными группами, полисилоксан с концевыми водородными и диметильными группами, комплекс платины в винильном димере и этинилциклогексанол. В конкретном варианте реализации способа эластомер-образующая композиция представляет собой соединения DDR-4320 или DDU-4320 (коммерчески доступные от NuSil Technology LLC). В другом конкретном варианте реализации способа эластомер-образующая композиция представляет собой LSR92 или LSR86 (доступные от Bluestar/Elkem). В другом конкретном варианте реализации способа эластомер-образующая композиция представляет собой Silbione Biomaterial LSR D140 (доступный от Bluestar/Elkem).
Если устройство, предпочтительно кольцо, должно содержать один или более дополнительных фармацевтически приемлемых вспомогательных веществ, в зависимости от природы каждого фармацевтически приемлемого вспомогательного вещества, каждое фармацевтически приемлемое вспомогательное вещество будет добавлено либо на стадии а), либо на стадии б), либо после стадии б). Специалист в данной области техники понимает, когда и как можно добавлять вспомогательное вещество. В наиболее предпочтительном варианте реализации способа кольцо не содержит иного фармацевтически приемлемого вспомогательного вещества, кроме эластомера.
В предпочтительном варианте реализации способа по настоящему изобретению стадия а) включает:
а1) смешивание прогестерона с фармацевтически приемлемой полимер-образующей композицией и катализатором сшивания с образованием смеси А; и
а2) смешивание прогестерона с фармацевтически приемлемой полимер-образующей композицией и сшивающим агентом и ингибитором катализатора с образованием смеси B;
а3) смешивание смесей А и В,
где фармацевтически приемлемая полимер-образующая композиция, катализатор сшивания, сшивающий агент и ингибитор катализатора представляют собой такие, как описано в любом из вышеупомянутых вариантов реализации способа.
Концентрация прогестерона в смеси A может быть такой же, как и в смеси B, или может быть другой, при условии, что конечная концентрация соответствует описанной выше для любого из вышеупомянутых вариантов реализации вагинального устройства. В конкретном варианте реализации концентрация прогестерона в смеси A является такой же, как и в смеси B. Полиморфная чистота полиморфа I прогестерона в смеси A может быть такой же, как и в смеси B, или может быть другой, при условии, что конечная полиморфная чистота полиморфа I соответствует описанной выше для любого из вышеупомянутых вариантов реализации вагинального кольца. В конкретном варианте реализации способа полиморфная чистота полиморфа I прогестерона в смеси A такая же, как и в смеси B.
В варианте реализации способа, когда используют кремнекислый наполнитель из диоксида кремния, кремнекислый наполнитель составляет часть смеси А.
В конкретном варианте реализации изобретения смешивание на стадии а3) подразумевает добавление смеси А и смеси В в высокоскоростной смеситель и смешивание. В более конкретном варианте реализации смесь A и смесь B добавляют в высокоскоростной смеситель в соотношении приблизительно 1:1. В конкретном варианте реализации указанное добавление осуществляют путем перекачивания смесей в смеситель. В конкретном варианте реализации высокоскоростной смеситель представляет собой статический проточный смеситель. В конкретном варианте реализации смешение смесей A и B осуществляют за счет турбулентности.
В дополнительном аспекте настоящее изобретение относится к вагинальному устройству, предпочтительно кольцу, которое можно получить с помощью любого из вышеупомянутых вариантов реализации способа.
Настоящее изобретение дополнительно относится к интравагинальным устройствам, предпочтительно кольцам, как описано в любом из вышеупомянутых вариантов реализации изобретения, содержащим:
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель,
для применения в медицине.
Настоящее изобретение также относится к интравагинальным устройствам, предпочтительно кольцам, как описано в любом из вышеупомянутых вариантов реализации изобретения, содержащим
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель;
для применения для лечения бесплодия, в частности, во вспомогательных репродуктивных технологиях.
Настоящее изобретение также относится к интравагинальным устройствам, предпочтительно кольцам, как описано в любом из вышеупомянутых вариантов реализации изобретения, содержащим
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель;
для применения для лечения симптомов перименопаузы.
В контексте настоящего изобретения субъектом лечения является субъект женского пола. В конкретном варианте реализации изобретения субъект женского пола является субъектом женского пола, не являющимся человеком. В другом варианте реализации изобретения субъект женского пола является животным. В другом варианте реализации изобретения субъект женского пола является человеком.
Настоящее изобретение также относится к способу лечения бесплодия, в частности, вспомогательным репродуктивным технологиям, у нуждающегося в этом субъекта женского пола, при этом способ включает введение пациенту интравагинального устройства, предпочтительно кольца, как описано в любом из вышеупомянутых вариантов реализации изобретения, содержащим:
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель.
Настоящее изобретение также относится к способу лечения симптомов перименопаузы у нуждающегося в этом субъекта женского пола, при этом способ включает введение пациенту интравагинального устройства, предпочтительно кольца, как описано в любом из вышеупомянутых вариантов реализации изобретения, содержащим:
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель.
Настоящее изобретение также относится к способу изготовления интравагинального устройства, предпочтительно кольца, как описано в любом из вышеупомянутых вариантов реализации изобретения, для лечения бесплодия, в частности, с применением во вспомогательных репродуктивных технологиях, где интравагинальное устройство содержит:
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель.
Настоящее изобретение также относится к способу изготовления интравагинального устройства, предпочтительно кольца, как описано в любом из вышеупомянутых вариантов реализации изобретения, для лечения симптомов перименопаузы у субъекта женского пола, где интравагинальное устройство содержит:
- терапевтически эффективное количество прогестерона;
- фармацевтически приемлемый носитель.
В контексте настоящего изобретения термин «терапевтически эффективное количество» относится к количеству прогестерона в вагинальном устройстве, которое позволяет достичь внутриматочных уровней прогестерона, достаточных для оказания адекватного прогестагенного эффекта в эндометрии для обеспечения наступления и поддержания беременности на ранних сроках. Что касается лечения симптомов перименопаузы, термин «терапевтически эффективное количество» относится к количеству прогестерона в вагинальном устройстве, которое позволяет успешно лечить или облегчать симптом перименопаузы.
В настоящем описании, если не указано иное, выражения «лечение бесплодия», «лечение от бесплодия» и аналогичные означают купирование или предотвращение естественной или индуцированной неспособности субъекта женского пола к обеспечению имплантации эмбриона и поддержанию беременности на ранних сроках, в частности, относятся к поддержанию лютеиновой фазы во вспомогательных репродуктивных технологиях, также называемых искусственное оплодотворение. Эти термины также относят к облегчению, замедлению прогрессирования, купированию или предотвращению симптомов перименопаузы.
Поддержание лютеиновой фазы при лечении бесплодия
Лютеиновой фазой называют период от наступления овуляции до наступления беременности или возобновления менструации через 2 недели. В контексте вспомогательных репродуктивных технологий термин «поддержание лютеиновой фазы» (LPS) представляет собой термин, используемый для описания введения лекарственных средств с целью поддержания процесса имплантации.
Хорошо известно, что лютеиновая функция нарушается в циклах ЭКО. Причины нарушений лютеиновой фазы при ВРТ многочисленны. Было показано, что функция желтого тела нарушается процессом аспирации ооцитов из фолликула, поскольку гранулезные лютеиновые клетки механически разрушаются и аспирируются. Было доказано, что дефект лютеиновой фазы возникает при длительном протоколе приема агонистов гонадотропин-высвобождающего гормона и что в целом недостаточность желтого тела как следствие вспомогательных репродуктивных технологий частично вызвана процессом аспирации ооцитов из фолликула и применением лекарственных средств от бесплодия для стимуляции овуляции или стимуляции развития фолликулов, в частности, агонистов гонадотропин-высвобождающего гормона. В отсутствие поддержания лютеиновой фазы площадь под фармакокинетической кривой для прогестерона является субоптимальной, и это сопровождается преждевременным лютеолизом. В циклах без поддержания продолжительность лютеиновой фазы сокращалась, и происходило кровотечение на ранних сроках беременности. Многие метаанализы подтвердили, что поддержание лютеиновой фазы улучшает исход ЭКО. Поддержание лютеиновой фазы с помощью прогестерона, по сравнению с плацебо или отсутствием лечения в циклах приема агонистов гонадотропин-высвобождающего гормона и не агонистов гонадотропин-высвобождающего гормона, также привело к значительному увеличению количества клинических беременностей и живорождений.
Как следствие, поддержание лютеиновой фазы, в частности введением прогестерона, считают необходимым, а в некоторых случаях обязательным для противодействия любой лютеиновой недостаточности, которая может возникнуть во время лечения бесплодия. В частности, было доказано, что поддержание лютеиновой фазы с помощью прогестерона улучшает исходы беременности у ановуляторных пациентов, проходящих терапию стимуляции овуляции, и у овуляторных пациентов, проходящих стимуляцию развития множественных фолликулов перед ВРТ, например, ЭКО, или перед другими способами лечения бесплодия, такими как внутриматочная инсеминация (ВМИ).
Таким образом, в предпочтительном варианте реализации настоящего изобретения применение интравагинального устройства, предпочтительно кольца, как описано в любом из вышеупомянутых вариантов реализации изобретения, предназначено для поддержания лютеиновой фазы. В контексте настоящего изобретения поддержание лютеиновой фазы относится к введению или замене прогестерона у субъекта женского пола для содействия или улучшения имплантации эмбриона и поддержания беременности на ранних сроках.
В предпочтительном варианте реализации изобретения в любом из вышеупомянутых вариантов реализации изобретения интравагинальное устройство по настоящему изобретению применяют субъекты женского пола, проходящие протокол лечения бесплодия. В конкретном варианте реализации изобретения протокол лечения бесплодия включает введение лекарственного средства от бесплодия. В конкретном варианте реализации изобретения протокол лечения бесплодия включает стимуляцию овуляции или стимуляцию развития множественных фолликулов. В конкретном варианте реализации изобретения лекарственное средство от бесплодия применяют для стимуляции овуляции или стимуляции развития множественных фолликулов.
В конкретном варианте реализации изобретения протокол лечения бесплодия представляет собой протокол ВРТ. В еще более конкретном варианте реализации изобретения протокол ВРТ представляет собой ЭКО, ИКСИ, ГИФТ, ЗИФТ или пересаживание криоконсервированых эмбрионов. В предпочтительном варианте реализации изобретения протокол ВРТ представляет собой ЭКО или ИКСИ. В конкретном варианте реализации изобретения протокол ВРТ представляет собой ЭКО. В конкретном варианте реализации изобретения протокол ВРТ представляет собой ИКСИ.
В другом конкретном варианте реализации изобретения протокол лечения бесплодия представляет собой протокол искусственного оплодотворения. В еще более конкретном варианте реализации изобретения протокол искусственного оплодотворения представляет собой ВМИ. Следует отметить, что «протокол» используют в настоящем изобретении как синоним «цикла» или т.п.
В конкретном варианте реализации изобретения субъект женского пола является ановуляторным. В конкретном варианте реализации изобретения субъект женского пола является ановуляторным и проходит стимуляцию овуляции. В другом конкретном варианте реализации изобретения субъект женского пола является овуляторным. В другом конкретном варианте реализации изобретения субъект женского пола является овуляторным и проходит стимуляцию развития множественных фолликулов.
В другом варианте реализации изобретения, независимо от того, проходит или будет проходить субъект женского пола протокол лечения бесплодия, данный субъект женского пола испытывает дефект лютеиновой фазы (ДЛФ). Термин «дефект лютеиновой фазы» (ДЛФ) относится к нарушению нормального женского менструального цикла. ДЛФ также известен как недостаточность, несовершенство, дефект или дефицит лютеиновой фазы. Это может быть следствием нарушений на уровне гипоталамуса/гипофиза, яичников или эндометрия, в результате чего женский организм не вырабатывает достаточное количество гормона прогестерона или не в полной мере отвечает на природный уровень гормона. Это приводит к задержке развития слизистой оболочки матки (эндометрия) во время лютеиновой фазы. ДЛФ может привести к неспособности трансформировать эндометрий в секреторную фазу, в результате чего слизистая оболочка матки начинает разрушаться, вызывая менструальное кровотечение и вызывая выкидыш. В конкретном варианте реализации изобретения ДЛФ вызван ненормальным фолликулогенезом, недостаточным выбросом лютеинизирующего гормона, недостаточной секрецией прогестерона желтым телом, первичной недостаточностью яичников, отсутствием яичников, синдромом преждевременного истощения яичников, снижением овариального резерва, дисгенезией гонад, идиопатической недостаточностью яичников, дисфункцией гонад.
Как ясно из вышеупомянутого, вагинальное устройство по настоящему изобретению предусмотрено для применения у субъектов женского пола, у которых наблюдается природный дефицит прогестерона, но которые не проходят протокол лечения бесплодия, у субъектов женского пола, у которых не наблюдается природного дефицита прогестерона, но которые становятся или могут стать таковыми в результате протокола лечения бесплодия, или у субъектов женского пола с природным дефицитом прогестерона и которые проходят протокол лечения бесплодия.
В конкретном варианте реализации изобретения, в любом из вышеупомянутых вариантов реализации изобретения применение интравагинального устройства по настоящему изобретению снижает риск самопроизвольного аборта (выкидыша) в первом триместре беременности. В другом конкретном варианте реализации изобретения применение интравагинального устройства по настоящему изобретению снижает риск самопроизвольного аборта в первые два месяца беременности. В еще более конкретном варианте реализации изобретения снижает риск самопроизвольного аборта в первый месяц беременности.
В другом варианте реализации изобретения в любом из вышеупомянутых вариантов реализации изобретения лечение бесплодия включает введение по меньшей мере одного другого активного вещества, полезного для обеспечения овуляции, имплантации эмбриона и/или поддержания беременности на ранних сроках. В конкретном варианте реализации изобретения по меньшей мере одно другое активное вещество представляет собой эстроген, который может быть введен способами, известными в данной области техники. В конкретном варианте реализации изобретения по меньшей мере одно другое активное вещество и прогестерон содержатся в вагинальном устройстве по настоящему изобретению.
Вагинальные устройства в соответствии с настоящим изобретением эффективны в обеспечении поддержания лютеиновой фазы, в то же время характеризуются преимуществом, заключающимся в обеспечении предотвращения или снижения риска вагинального кровотечения. В настоящем описании термин «вагинальное кровотечение» или «кровотечение» относят к любому типу кровяных выделений из влагалища. Они могут варьироваться от кровянистых выделений (несколько капель крови) до кровотечения (более сильный поток крови). Предпочтительно данный термин относится к сильному кровотечению и кровоизлиянию.
Таким образом, в предпочтительном варианте реализации изобретения в любом из вышеупомянутых вариантов реализации изобретения вагинальные устройства по настоящему изобретению подходят для лечении бесплодия и одновременно для предотвращения или снижения риска вагинального кровотечения. В конкретном варианте реализации изобретения вагинальные устройства по настоящему изобретению применяют для замены лечения поддержанием лютеиновой фазы, которое привело к вагинальному кровотечению или чрезмерному вагинальному кровотечению.
В конкретном варианте реализации изобретения в любом из вышеупомянутых вариантов реализации изобретения интравагинальное устройство не заменяют в течение периода по меньшей мере 7 дней (считая с момента введения вагинального устройства). В предпочтительном варианте реализации изобретения интравагинальное устройство не заменяют в течение периода 14 дней. В конкретном варианте реализации изобретения интравагинальное устройство не заменяют в течение периода 15 дней, 16 дней, 17 дней или 18 дней.
Авторы настоящего изобретения обнаружили, что устройство, предпочтительно кольцо, в соответствии с настоящим изобретением можно применять без удаления или замены в течение данных периодов времени с обеспечением успешной трансформации эндометрия в секреторную фазу при отсутствии какого-либо наблюдаемого кровотечения у пациента. В конкретном варианте реализации изобретения интравагинальное устройство вводят за один-семь дней до переноса эмбриона, за два-шесть дней до переноса эмбриона, за три-пять дней до переноса эмбриона или за четыре дня до переноса эмбриона. В конкретном варианте реализации изобретения интравагинальное устройство вводят за день до переноса эмбриона.
Перименопауза
Как упоминалось выше, настоящее изобретение также подходит для лечения симптомов перименопаузы. В контексте настоящего изобретения дефицит прогестерона лежит в основе или способствует появлению симптомов перименопаузы.
Менопаузу определяют как отсутствие менструального цикла в течение 12 месяцев подряд у субъекта женского пола. Физические изменения у субъекта женского пола начинаются за несколько лет до последнего менструального цикла. Эта переходная фаза называется перименопаузой и может длиться от шести до десяти лет. Она начинается с изменения продолжительности периода времени между менструациями и заканчивается через двенадцать месяцев после последней менструации. Во время перименопаузального периода во время каждого менструального цикла набирается и стимулируется большее количество яйцеклеток, что приводит к более высоким, чем обычно, уровням эстрогена и более низким, чем обычно, уровням прогестерона.
Интравагинальные устройства по настоящему изобретению подходят для введения прогестерона в период перименопаузы. Дополнительно к применению устройства могут вводиться другие гормоны, либо прогестерон, либо другие гормоны, такие как эстрогены.
Примерами симптомов перименопаузы, которые можно лечить с помощью вагинальных устройств по настоящему изобретению, являются меноррагия, нерегулярные менструации, приливы, ночная потливость, недержание мочи, остеопороз, нарушение сна, перепады настроения, нервозность, беспокойство, учащенное сердцебиение, потеря памяти и/или концентрации, потеря либидо, усталость, урогенитальная атрофия, атрофия груди или сердечно-сосудистые заболевания. В предпочтительном варианте реализации изобретения симптомом перименопаузы является меноррагия, остеопороз, нарушение сна или сердечно-сосудистое заболевание.
Примеры
Приведенные ниже примеры являются исключительно иллюстративными и не ограничивают объем настоящего изобретения каким-либо образом. Таким образом, специалисту в данной области техники понятно, что в настоящее изобретение могут быть внесены различные изменения и модификации, не выходящие за пределы объема и сущности настоящего изобретения.
Пример 1: Способ изготовления и определения характеристик интравагинального кольца
DDR-4320 (коммерчески доступный от NuSil Technology LLC) используют при изготовлении вагинальных колец по настоящему изобретению. Состав DDR-4320 следующий:
Часть А представляет собой силиконовый полимер с концевыми винилдиметильными группами; комплекс платины в винильном димере.
Часть B представляет собой силиконовый полимер с концевыми винилдиметильными группами; силиконовый полимер с концевыми водородными и диметильными группами, этинилциклогексанол.
1,9675 г Части A смешивают с 0,1875 г прогестерона (при этом практически весь прогестерон в кольце находится в виде полиморфной формы I; коммерчески полученный). В отдельном сосуде 1,9675 г Части B смешивают с 0,1875 г прогестерона (тот же прогестерон, что используют для смешивания с Частью A).
Две смеси перекачивают в соотношении 1:1 в статический проточный смеситель, где их смешивают за счет турбулентности. Эту смесь вводят под давлением в форму, где кольца формируют путем отверждения при 120ºC в течение 45 секунд. Полученное таким образом интравагинальное кольцо весит 4,31 г и состоит из следующих компонентов:
Идентификация и количественное определение полиморфа I прогестерона в интравагинальном кольце с помощью дифракции рентгеновских лучей
Приборы и условия эксперимента
Полученное кольцо разрезали, чтобы получить образцы в форме диска толщиной около 1 миллиметра. Образцы в форме диска поместили между пленками из сложного полиэфира толщиной 3,6 мкм.
Образцы проанализировали с помощью порошкового дифрактометра PANalytical X’Pert PRO MPD θ/θ с радиусом 240 миллиметров в конфигурации сходящегося пучка с фокусирующим зеркалом и геометрии пропускания с плоскими образцами, помещенными между пленками с низким поглощением. Использовали следующие условия:
Излучение Cu Kα (= 1,5418 Å).
Рабочая мощность: 45 кВ - 40 мА.
Щели формирования падающего пучка, диафрагмирующие высоту пучка 0,4 миллиметра.
Щели Соллера 0,02 радиана регистрации падающего и дифрагированного пучка.
Детектор PIXcel: активная длина = 3,347 °.
2θ/θ сканы от 2 до 70 °2θ с размером шага 0,026 °2θ и временем измерения 600 секунд на шаг.
Полученные результаты
Наблюдаемые пики кристаллического образца указывают на присутствие кристаллической формы I (альфа-формы) прогестерона, а другие полиморфы, в частности, форма II, обнаружены не были. На Фиг. 1 представлена рентгеновская порошковая дифрактограмма образца с наложенными пиками, соответствующими эталонному образцу PDF#0-37-1690 формы I прогестерона (альфа-форма) (спектр эталонного образца изображен вертикальными линиями, спектр анализируемого образца изображен с помощью пиков). Для данной инструментальной техники и данного типа образца предел количественного определения составляет 1-5%. Следовательно, можно утверждать, что полиморфная чистота формы I составляет по меньшей мере 95%.
С помощью дифференциальной сканирующей калориметрии
Приборы и условия эксперимента
В контексте настоящего изобретения значения полиморфной чистоты рассчитывают на основе показаний энтальпии, полученных с помощью метода ДСК, описание которого представлено ниже.
Образцы приготовили в алюминиевом тигле емкостью 40 мкл. Образцы проанализировали с помощью Mettler Toledo DSC822e. Использовали следующие условия:
Газ: сухой азот 50 мл/мин.
Способ: Нагревание от 30°C до 200°C со скоростью 10°C/мин.
Полученные результаты
Полученная кривая указывает на присутствие кристаллической формы I (альфа-формы) прогестерона, а другие полиморфы, в частности, форма II, обнаружены не были. На Фиг. 2 представлена кривая ДСК, которая демонстрирует эндотермический эффект при температуре от 129°C с соответствующей теплотой 5,83 Дж/г. Эта эндотерма может быть связана с плавлением полиморфной формы I (альфа-формы) прогестерона. Другие характерные эндотермы не обнаружены.
Пример 2. Исследование фармакокинетики, фармакодинамики и переносимости у здоровых добровольцев женского пола в пременопаузе для оценки трех вагинальных колец, содержащих 0,375 г, 0,125 г и 0,040 г природного прогестерона
Данное исследование представляет собой одноцентровое, рандомизированное, контролируемое по активному препарату клиническое исследование фазы I-II типа доза-ответ в параллельных группах.
Цели:
1. Оценить фармакокинетический профиль трех вагинальных колец, содержащих 0,375 г, 0,125 г и 0,040 г прогестерона соответственно.
2. Оценить влияние трех вагинальных колец на обеспечение гестагенной трансформации эндометрия.
3. Оценить переносимость и приемлемость вагинальных колец, содержащих прогестерон.
Число субъектов исследования:
Всего 24 субъекта, по 8 в группе испытания
Исследуемое состояние здоровья или заболевание:
Испытуемая группа представляет собой здоровых добровольцев, хотя исследуемый препарат разработан для лечения дефицита лютеиновой фазы (ДЛФ) в контексте экстракорпорального оплодотворения (ЭКО)/вспомогательных репродуктивных технологий (ВРТ).
Критерии включения:
- Здоровая взрослая женщина детородного возраста (18-45 лет включительно).
- Предел диапазона индекса массы тела (ИМТ) 18-25 кг/м2 (оба значения включительно).
- Нормальное состояние влагалища.
- Нормальная цитология шейки матки.
- Серонегативная реакция в отношении поверхностного антигена гепатита B (HBsAg), антител к вирусу гепатита C (AbHCV), вирусу иммунодефицита человека (ВИЧ).
- Письменное информированное согласие, демонстрирующее осведомленность и готовность соблюдать процедуры протокола и оценки.
- Готовность отказаться от приема пероральных контрацептивов на период проведения исследования.
Критерии исключения:
- Соответствующая гинекологическая патология (эндометриоз, синдром поликистоза яичников (СПКЯ), аномалии матки, поражающие эндометриальную полость).
- Любая недавняя или сопутствующая патология, которая является противопоказанием к биопсии эндометрия или запрещает биопсию эндометрия.
- Соответствующий вульвовагинит (инфекционный или неинфекционный) в любое время за месяц до включения в исследование.
- Любые противопоказания к применению эстрогенов (новообразования и т.д.).
- Одновременное применение внутриматочной спирали (ВМС) и/или гормональных имплантатов.
- Активный курильщик (если старше 35 лет).
- Любое сопутствующее заболевание, которое, по мнению исследователя, может поставить под угрозу соблюдение требований исследования.
- Гиперчувствительность, аллергия или известная резистентность к активному ингредиенту или вспомогательным веществам лекарственных средств, используемых в данном исследовании (ацетату лейпрорелина, полугидрату эстрадиола, прогестерону).
- Беременность, намерение забеременеть или период лактации.
- Участие в другом клиническом испытании с участием нового химического соединения в течение 3 месяцев до включения в данное исследование. (При использовании дженериков в течение 4 недель до включения в это исследование).
- Нежелание или невозможность использования барьерных методов контрацепции.
- Неповрежденная девственная плева.
- Венозные тромбоэмболические заболевания (тромбоз глубоких вен, тромбоэмболия легочной артерии) или артериальные заболевания (стенокардия, инфаркт миокарда, инсульт).
- Коагулопатия или любое нарушение, которое может повлиять на состояние повышенной свертываемости крови субъекта.
Исследуемый вид лечения:
Исследуемый препарат и доза:
- T3: вагинальное кольцо с 0,375 г природного прогестерона.
- T4: вагинальное кольцо с 0,125 г природного прогестерона.
- T5: вагинальное кольцо с 0,040 г природного прогестерона.
Способ применения: однократное введение по одному кольцу каждому субъекту.
Помимо исследуемого вида лечения, каждый субъект получает следующие виды лечения:
- Инъекции агонистов гонадотропин-высвобождающего гормона для подавления выработки эндогенных гормонов.
- Пластыри с эстрогеном для стимуляции фазы пролиферации эндометрия.
- Необязательно субъект может получить один цикл пероральных контрацептивов в конце исследования.
Продолжительность лечения:
18±1 дней
Процедуры и оценки исследования:
Запланировали 20 визитов, включая скрининговые визиты, госпитализацию в клиническое отделение в первую фазу клинических испытаний на две ночи, контрольные визиты и заключительный контакт по телефону.
Участие каждого субъекта разделили на фазу скрининга/подготовки продолжительностью до 5 недель, период исследуемого вида лечения продолжительностью примерно 18 дней, период последующего наблюдения продолжительностью примерно 10 дней и период заключительного наблюдения продолжительностью 3 недели: в общей сложности 9 недель предусмотренных исследованием визитов и в общей сложности 12 недель участия в исследовании.
Отбор/скрининг:
Каждый субъект приходит в клиническое отделение (CU) для начального визита (визит 0), во время которого ему подробно объясняют исследование и запрашивают официальное согласие. Если есть согласие, субъект проходит общий медицинский осмотр, общее лабораторное исследование (клиническую биохимию, гематологию, серологию, анализ мочи) и цитологическое исследование.
Визит 1 включает гинекологическое обследование, тест на беременность, проверку соответствия критериям, влагалищную эхографию, взятие крови (для определения уровней гормонов) и внутримышечную инъекцию агонистов гонадотропин-высвобождающего гормона (Ginecrin Depot 3,75 мг).
Визит 2 должен быть проведен после окончания менструации у субъекта и включает гинекологическое обследование, подтверждение подавления гормона (путем влагалищной эхографии для подтверждения толщины эндометрия менее 7 мм и взятие крови для определения уровня 17-β-эстрадиола менее 60 пг/мл). Затем субъект начинает лечение эстрогеном (пластыри Estradot 75 мкг/сут).
Визит 3 включает вторую и заключительную внутримышечную инъекцию агонистов гонадотропин-высвобождающего гормона (Ginecrin Depot 3,75 мг).
Визит 4 включает гинекологическое обследование, влагалищную эхографию для подтверждения толщины эндометрия > 7 мм и взятие крови для определения уровня прогестерона, который должен быть менее 1 нг/мл.
Визит 5 представляет собой госпитализацию субъекта в клиническое отделение для рандомизации, лечение исследуемым препаратом и взятие крови для фармакокинетики. Визиты 6, 7 предполагают дальнейшее взятие образца для фармакокинетики.
Визит 8 включает гинекологическое обследование, влагалищную эхографию и взятие крови для определения уровня гормонов.
Визиты 9, 10 включают взятие крови для определения уровня гормонов.
Визит 11 включает гинекологическое обследование, влагалищную эхографию и взятие крови для определения уровня гормонов.
Визит 12 включает взятие крови для определения уровня гормонов.
Визит 13 включает гинекологическое обследование, влагалищную эхографию и взятие крови для определения уровня гормонов.
Визит 14 включает взятие крови для определения уровня гормонов.
Визит 15 включает гинекологическое обследование, влагалищную эхографию, взятие крови для определения уровня гормонов и биопсию эндометрия.
Визит 16 включает взятие крови для определения уровня гормонов.
Визит 17 включает гинекологическое обследование, влагалищную эхографию и взятие крови для определения уровня гормонов. На этом исследуемый вид лечения заканчивается удалением вагинального кольца и прекращением действия эстрогеновых пластырей.
Визит 18 (окончание исследования) включает общий медицинский осмотр, гинекологическое обследование, влагалищную эхографию, взятие крови для определения уровня гормонов, общее лабораторное исследование (клиническую биохимию, гематологию, анализ мочи, серологический тест на беременность). Субъекту будет предложен один курс пероральных контрацептивов (не обязательно).
Визит 19 (последующее наблюдение для оценки безопасности) проводят по телефону через 4 недели после окончания исследуемого вида лечения специально для оценки безопасности.
Критерии оценки:
1. Фармакокинетика:
Первичные параметры фармакокинетики
- Площадь под фармакокинетической кривой от введения до последней наблюдаемой концентрации прогестерона выше предела количественного определения (отличного от 0) в момент времени t: (AUC0-t).
- Площадь под фармакокинетической кривой от введения до последнего взятия крови через 408 часов (AUC0-408ч).
- Максимальная концентрация, полученная из концентраций прогестерона в сыворотке крови: (Cmax).
- Концентрация, полученная из концентраций прогестерона в сыворотке крови при последнем взятии крови через 408 часов (Cmin).
- Средняя концентрация, рассчитанная как значение AUC0-408ч/интервал введения (t). (Cav).
Вторичные параметры фармакокинетики
- Время достижения максимальной концентрации (Tmax).
- Площадь под фармакокинетической кривой, экстраполированная на бесконечное время: AUC0-∞.
- % флуктуации (Fl), рассчитанный как FI = ((Cmax-Cmin)/Cav) ×100).
2. Фармакодинамика:
- Гистологическая трансформация эндометрия через 14 дней лечения.
- Ультрасонографические особенности эндометрия в ответ на гормональное лечение.
3. Переносимость и безопасность:
- Оценка частоты, интенсивности, продолжительности и развития эпизодов кровотечения.
- Оценка переносимости вагинальных колец с оценкой местных симптомов и признаков.
- Оценка приемлемости вагинальных колец.
- Описание побочных эффектов.
Результаты и выводы
1. Результаты фармакокинетики
Концентрации прогестерона в сыворотке крови были представлены в виде таблицы для каждого лечения, как показано на Фиг. 4, и на основе концентраций получили или рассчитали фармакокинетические параметры.
Фармакокинетические параметры для каждого препарата перечислены в таблице ниже (среднее значение (стандартное отклонение (SD))).
N=8
N=8
N=8
2. Результаты фармакодинамики
Гистологическая трансформация эндометрия
Были отмечены различия между исследуемыми видами лечения. Существенную трансформацию эндометрия наблюдали в случае вагинальных колец Т3 и Т4, в то время как трансформация эндометрия в случае кольца Т5 с самой низкой дозой была слабой как по шкале трансформации эндометрия, так и по системе датирования Нойе. Т3 являлся единственным препаратом, который во всех случаях вызывал умеренную или выраженную трансформацию эндометрия.
Различия между T3 и T4 по сравнению с T5 являются статистически значимыми (p=0,004; p=0,011 соответственно), в то время как при сравнении T3 и T4 значимость не достигается.
Результаты по шкале трансформации эндометрия для каждого препарата приведены в таблице ниже:
Вагинальное кольцо с 0,375 г природного прогестерона
Вагинальное кольцо с 0,125 г природного прогестерона
Вагинальное кольцо с 0,040 г природного прогестерона
3. Результаты переносимости и безопасности
Вагинальное кровотечение
Наблюдали несколько эпизодов кровотечений у женщин, которым вводили вагинальные кольца в течение первых 14 дней лечения. Все случаи, наблюдаемые с T3, состояли из незначительных кровотечений (кровянистых выделений), в то время как все эпизоды тяжелых кровотечений в этот период наблюдали у женщин, получавших лечение посредством T4 и T5. У двух добровольцев, получавших лечение посредством Т4, и у 7 добровольцев, получавших лечение посредством Т5, вагинальные кольца были удалены преждевременно из-за сильного вагинального кровотечения. Эти пациенты преждевременно прекратили исследование, а биопсия для оценки трансформации эндометрия была выполнена за несколько дней до запланированного визита после 14 дней лечения. Из этих 9 пациентов только у одного из них, получавшего лечение посредством Т5, к моменту проведения биопсии был низкий уровень эстрадиола в сыворотке крови, в то время как у всех пациентов был низкий уровень прогестерона в сыворотке крови.
В заключительные дни исследования (визиты 17 и 18) наблюдали сильные кровотечения отмены во всех группах лечения.
Переносимость
Все женщины, которым вводили вагинальные кольца, во время всех визитов имели нормальное состояние влагалища. Ни у одной из них не было воспаления, эрозии слизистой оболочки влагалища, жжения, диспареунии или других местных признаков и симптомов. Только один доброволец, получавший лечение посредством Т3, почувствовал умеренную боль во время единственного визита. Ни одна из женщин, получавших лечение посредством Т4 и Т5, не отметила дискомфорт или зуд во время всех визитов. Некоторый дискомфорт наблюдали женщины, получавшие лечение посредством Т3 (две женщины испытывали легкий дискомфорт во время одного из визитов в рамках исследования, и одна женщина испытывала дискомфорт умеренной интенсивности во время 3 визитов в рамках исследования), а также некоторый зуд (умеренной интенсивности), но не имеющий ни клинической значимости, ни статистической значимости между курсами лечения. Участники исследования хорошо перенесли три вагинальных кольца.
Приемлемость
Три вагинальных кольца были приемлемы для участников исследования. Существенных различий между исследуемыми препаратами в отношении переносимости, гигиены и удобства не наблюдали.
Нежелательные явления
Во время исследования серьезных нежелательных явлений не зарегистрировали. Зарегистрировали тридцать три (33) легких и три (3) умеренных нежелательных явления при приеме Т3, из них двадцать восемь (28)
Выводы
Статистически значимые различия между препаратами Т3, Т4 и Т5 показаны в наиболее релевантных проанализированных фармакокинетических параметрах.
Линейный анализ показывает менее чем пропорциональное увеличение фармакокинетических параметров с увеличением дозы (от 0,040 до 0,375 г).
Все вагинальные кольца (0,375 г, 0,125 г и 0,04 г) вызывают гестагенную трансформацию эндометрия за счет действия прогестерона, высвобождаемого из колец.
При гистологическом анализе наблюдают эффект зависимости ответа от дозы в отношении гестагенной трансформации эндометрия. Из трех испытанных доз Т3 (0,375 г) вызвал самый высокий гестагенный эффект.
Системное воздействие прогестерона, продуцируемого дозой 0,375 г (T3), имеет такую же величину, что и наблюдаемое в предыдущем исследовании фармакокинетики и фармакодинамики. В этом исследовании также были проанализированы две более высокие дозы (1,5 г и 0,75 г), и не было показано различий в основных фармакокинетических параметрах между тремя дозами.
Принимая во внимание результаты обоих исследований, можно сделать вывод, что с фармакокинетической точки зрения доза 0,375 г представляет собой минимальную исследованную дозу, обеспечивающую максимальные системные уровни прогестерона. Кроме того, в этом исследовании фармакодинамический эффект дозы 0,375 г (Т3) имеет такую же величину, что и наблюдаемый в предыдущем исследовании, в котором не было показано различий между тремя испытанными дозами (1,5 г, 0,75 г и 0,375 г) в их способности вызывать гестагенную трансформацию эндометрия. Учитывая результаты обоих исследований, можно сделать вывод, что с точки зрения фармакодинамики доза 0,375 г (Т3) соответствует минимальной эффективной дозе.
Картина кровотечений различалась среди трех протестированных препаратов. Тяжелые вагинальные кровотечения произошли во время второй недели лечения посредством Т4 и Т5, тогда как для Т3 наблюдали лишь незначительные кровянистые выделения. Более ранние сильные кровотечения наблюдали у женщин, получавших Т5. Девять женщин (две получали Т4 и семь получали Т5) преждевременно прекратили участие в исследовании из-за сильного кровотечения.
Все виды лечения продемонстрировали хороший профиль переносимости/безопасности и не выявили каких-либо неожиданных нежелательных явлений. Большинство нежелательных явлений были умеренными, и различий между группами не выявлено.
Пример 3. Исследование фармакокинетики, фармакодинамики и переносимости у здоровых добровольцев женского пола в перименопаузе для оценки трех вагинальных колец, содержащих 1,5 г, 0,75 г и 0,375 г природного прогестерона
Клиническое испытание проводили по той же методике, что описана в Примере 2. Концентрации прогестерона в сыворотке крови в зависимости от времени показаны на Фиг. 3.
Пример 4: профили высвобождения прогестерона
Высвобождение прогестерона во времени для вагинального кольца согласно настоящему изобретению сравнивали с высвобождением прогестерона для вагинального кольца, содержащего другие полиморфные формы прогестерона.
Температура плавления полиморфа I (альфа) прогестерона составляет примерно 129°C. Когда прогестерон в виде полиморфной формы I используют для получения кольца по настоящему изобретению, и во время отверждения используют температуру выше температуры плавления прогестерона, подтверждено, что прогестерон плавится во время процесса полимеризации, и появляется полиморф II (бета) прогестерона.
Чтобы проверить, как появление полиморфа II может повлиять на конечный продукт, кольца с составом, описанным в Табл. I, изготовили при температурах ниже (120°C) и выше (150°C) температуры плавления прогестерона способом, описанным ниже. Затем определили характеристики колец и определили их профили высвобождения прогестерона in vitro.
Таблица I. Состав кольца
Для изготовления каждую из половин прогестерона смешивали с соответствующей частью соединения LSR, а затем оба компонента смешивали и заливали под давлением в форму, в которой проходил процесс отверждения с использованием различных температур для получения колец: первое кольцо подвергали отверждению при 120°C (настоящее изобретение), а другое кольцо подвергали отверждению при 150°C (сравнительное). Полученные кольца охарактеризовали с помощью сканирующей электронной микроскопии, рентгенодифракционного анализа и дифференциальной сканирующей калориметрии. Данные методы анализа подтвердили, что, если кольца изготавливают при температуре менее температуры плавления прогестерона, появляется только полиморф I, тогда как в противоположность этому при температуре выше температуры плавления появляются полиморф I, II и другие полиморфы.
Также проверили, что у колец, отвержденных при температурах ниже температуры плавления прогестерона, на поверхности наблюдаются лишь небольшое количество кристаллических частиц, в отличие от колец, изготовленных при температурах выше температуры плавления прогестерона, которые демонстрируют на поверхности резкое увеличение количества кристаллов прогестерона с другой морфологией и меньшим размером, чем исходный активный фармацевтический ингредиент.
Касательно профилей прогестерона in vitro, исследование проводили путем помещения колец в смесь изопропиловый спирт (ИПС)/вода (60/40) при 37°C в условиях предельного разбавления и при непрерывном перемешивании. Высвобождение исследовали в течение 11 дней. Прогестерон измеряли с помощью утвержденного метода ВЭЖХ. Было обнаружено, что кольца, отвержденные при 150°C, имели более сильный взрывной эффект и более высокую скорость высвобождения по сравнению с кольцами, отвержденными при 120°C (см. Табл. II).
Таблица II. Суммарное высвобождение прогестерона (мг) с течением времени
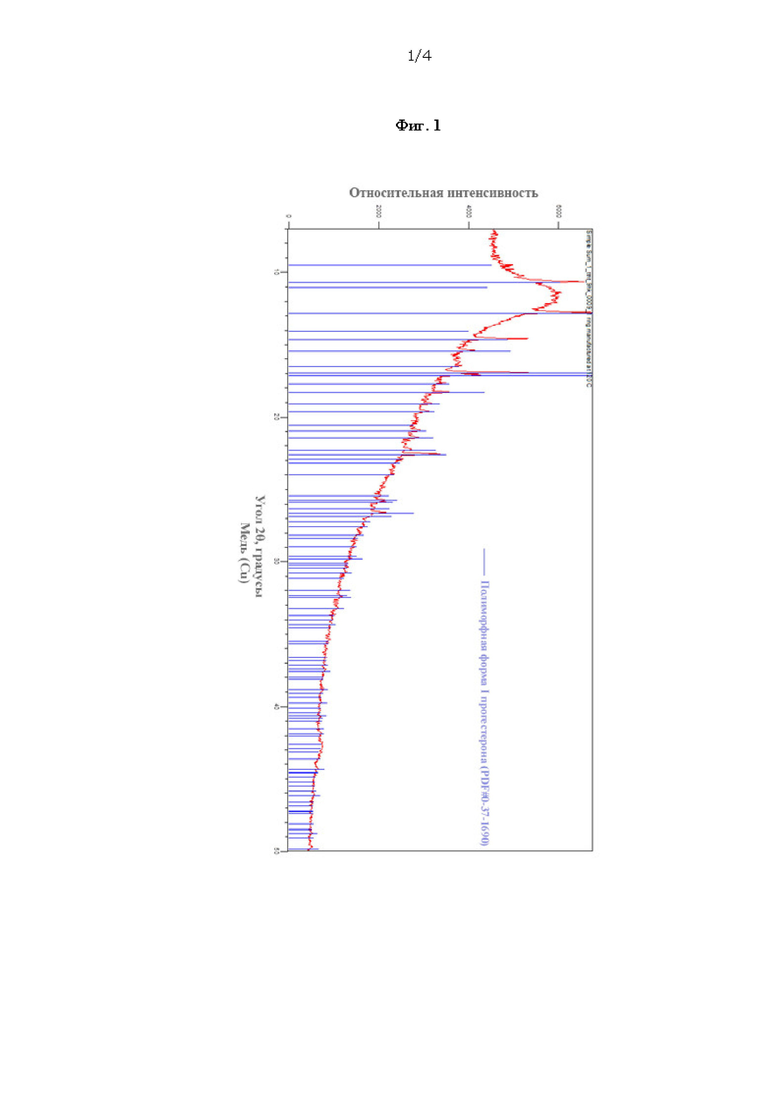
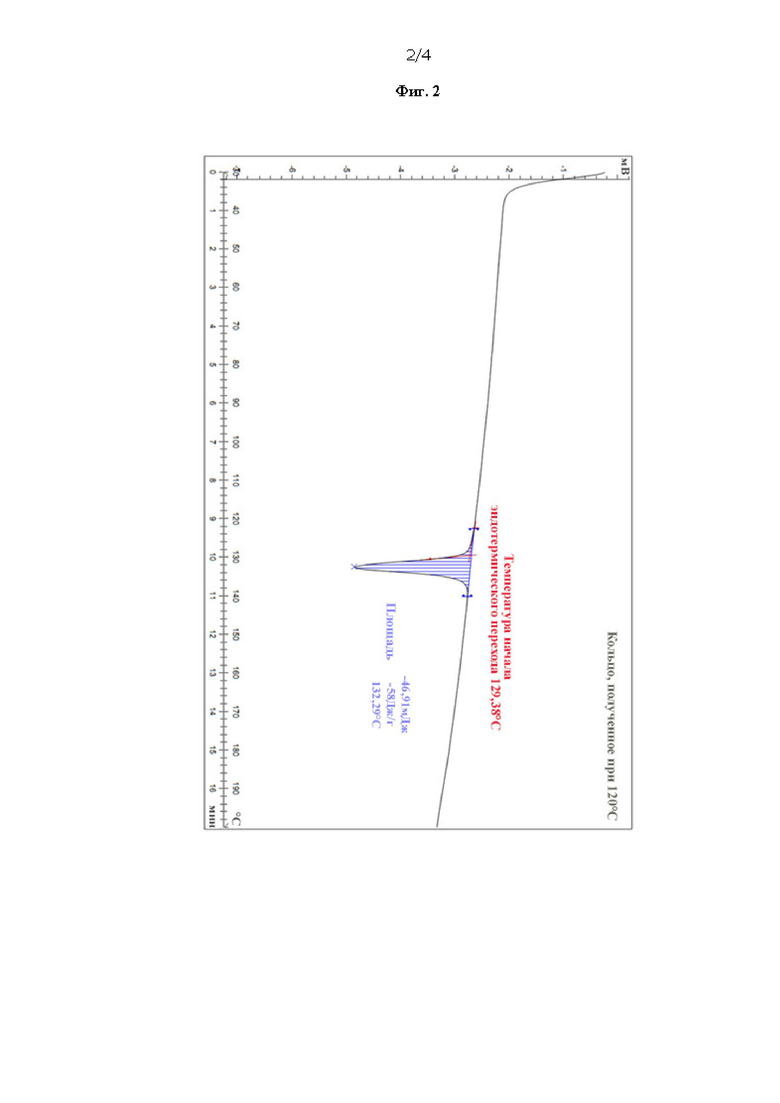
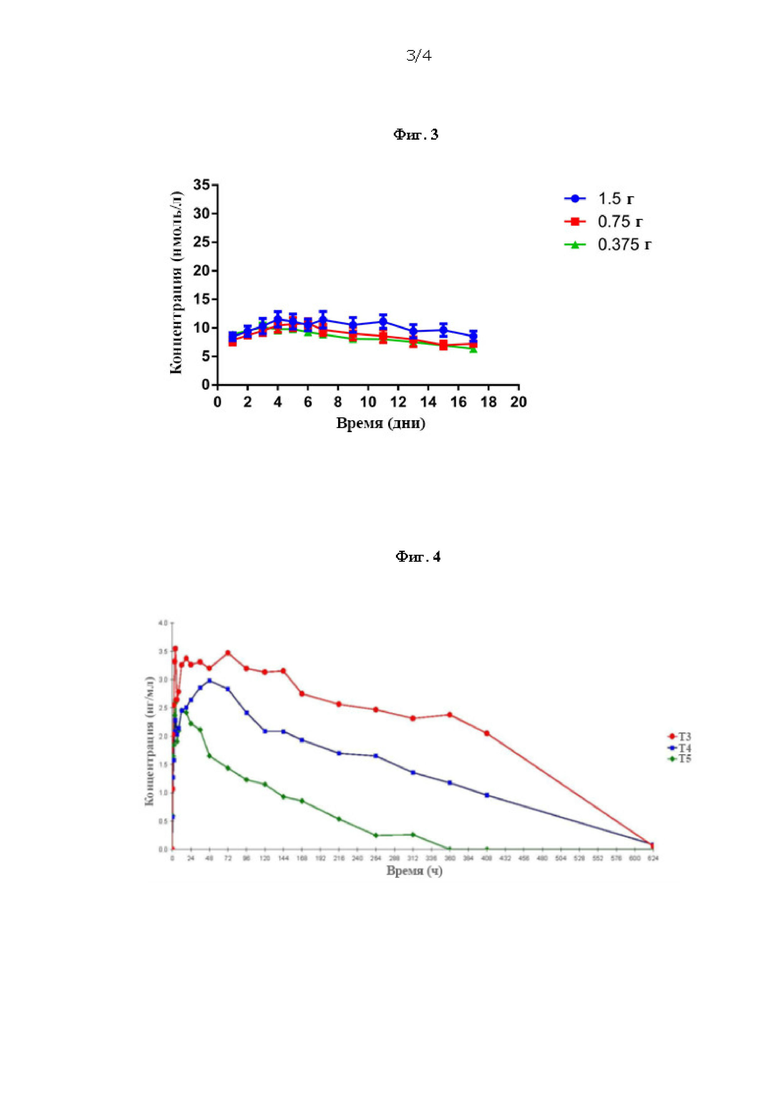
Изобретение относится к интравагинальным устройствам, в частности к кольцам, содержащим прогестерон определенной полиморфной чистоты, способам изготовления таких устройств и терапевтическим применениям указанных устройств. В частности, интравагинальные устройства содержат большое количество полиморфа I прогестерона и подходят для применения для лечения бесплодия у субъектов женского пола. 5 н. и 6 з.п. ф-лы, 4 ил., 2 табл., 4 пр.
1. Интравагинальное кольцо для лечения бесплодия, содержащее:
- от 0,10 до 0,75 г прогестерона, в котором по меньшей мере примерно 75% указанного прогестерона находится в виде полиморфной формы I; и
- по меньшей мере один эластомер на основе силикона в качестве фармацевтически приемлемого носителя.
2. Интравагинальное кольцо по п. 1, в котором по меньшей мере примерно 95% указанного прогестерона находится в виде полиморфной формы I.
3. Интравагинальное кольцо по п. 1, содержащее от 2,9 до 17,4 мас.% прогестерона относительно общей массы кольца.
4. Интравагинальное кольцо по п. 1, содержащее от 0,125 до 0,50 г прогестерона.
5. Способ изготовления вагинального кольца по любому из пп. 1-4, включающий стадии:
а) Смешивания от 0,10 до 0,75 г прогестерона, где по меньшей мере 75% прогестерона находится в виде полиморфной формы I, с фармацевтически приемлемой полимерной композицией, содержащей по меньшей мере один эластомер на основе силикона;
б) Отверждения смеси, полученной на стадии а), при температуре 120°C или менее.
6. Интравагинальное кольцо для лечения бесплодия, получаемое по способу по п. 5.
7. Применение интравагинального кольца, содержащего:
- от 0,10 до 0,75 г прогестерона, где по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I; и
- по меньшей мере один эластомер на основе силикона в качестве фармацевтически приемлемого носителя,
для лечения бесплодия.
8. Применение по п. 7, где лечение бесплодия представляет собой вспомогательную репродуктивную технологию.
9. Применение по п. 8, где лечение бесплодия включает поддержание лютеиновой фазы.
10. Применение по любому из пп. 7-9, где интравагинальное кольцо не заменяют в течение периода по меньшей мере 14 дней.
11. Применение интравагинального кольца, содержащего:
- от 0,10 до 0,75 г прогестерона, где по меньшей мере 75% указанного прогестерона находится в виде полиморфной формы I; и
- по меньшей мере один эластомер на основе силикона в качестве фармацевтически приемлемого носителя,
для лечения одного или более симптомов перименопаузы.
| HEREDIA V et al | |||
| "Polyisoprene matrix for progesterone release: In vitro and in vivo studies", 01 December 2009 (2009-12-01), Vol | |||
| Зеркальный стереовизир | 1922 |
|
SU382A1 |
| US 2009202612 A1, 2009.08.13 | |||
| Anindita Sarkar et al | |||
Авторы
Даты
2024-11-14—Публикация
2019-03-21—Подача