Предлагаемое изобретение относится к медицине, а именно к анестезиологии и реаниматологии и может быть использовано при оценке риска развития послеоперационной аритмии при операциях на органах брюшной полости.
Послеоперационная аритмия, входящая в состав больших сердечно-сосудистых осложнений (Sabate S., Mases Α., Guilera Ν., Canet J., et. al. Incidence and predictors of major perioperative adverse cardiac and cerebrovascular events in non-cardiac surgery. Br J Anaesth. 2011; 107(6):879-90.) и определяемая как электрокардиографические (ЭКГ) признаки трепетания предсердий (ТП), фибрилляции предсердий (ФП) или атриовентрикулярной блокады (AV-блокады) второй или третьей степени, регистрируемые в течение 30 дней после операции является серьезным опасным для жизни осложнением и тесно коррелирует с 30-дневной смертностью и долгосрочным исходом (Prasada S., Desai M.Y., Saad M., et al. Preoperative atrial fibrillation and cardiovascular outcomes after noncardiac surgery. J. Am. Coll. Cardiol. 2022; 79(25):2471-2485). У пациентов, у которых наблюдается послеоперационная аритмия, в два раза выше вероятность развития инсульта в течение одного года после операции. ФП является распространенной сердечной аритмией, связанной как с сердечнососудистой, так и с цереброваскулярной заболеваемостью и смертностью. Частота развития аритмий в послеоперационном периоде составляет от 3 до 10% (Danelich I.M., Lose J.M., Wright S.S., et al. Practical management of postoperative atrial fibrillation after noncardiac surgery. Journal of the American College of Surgeons 2014; 219: 831-41). Согласно прогнозам, распространенность ФП в ближайшие десятилетия увеличится из-за старения населения и более высокой распространенности факторов риска (Pistoia F., Sacco S., Tiseo С., et al. The epidemiology of atrial fibrillation and stroke. Cardiol Clin. 2016; 34:255-268). Периоперационные факторы, включающие гемодинамический стресс, травму тканей, боль, гиповолемию и электролитные нарушения усиливают симпатическую стимуляцию и адренергическую активность, что существенно повышает риск развития послеоперационной аритмии (Karamchandani K., Khanna А.K., Bose S., et al. Atrial fibrillation: current evidence and management strategies during the perioperative period. Anesth Analg. 2020; 130:2-13).
В связи с этим, выявление пациентов высокого риска позволяет целенаправленно применять способы профилактики послеоперационной аритмии и снижать риск ее развития.
Одним из аналогов является оценка исходного физического статуса по классификации Американского общества анестезиологов (ASA). Способ заключается в отнесении пациента к одному из классов (от одного до 6), в зависимости от тяжести сопутствующих заболеваний (Hurwitz ЕЕ, Simon M, Vinta SR.et al. Adding examples to the ASA-physical status classification improves correct assignment to patients. Anesthesiology. 2017; 126:(4):614-622 10.1097/ALN.0000000000001541).
Недостатки способа:
1. Субъективность.
2. Способ не учитывает влияния травматичности оперативного вмешательства.
3. Недостаточная точность прогнозирования.
4. Является приспособленным инструментом оценки риска развития послеоперационной аритмии.
Другим аналогом предлагаемого способа является пересмотренный индекс кардиального риска Т.Н. Lee (Lee Т.Н., Marcantonio E.R., Mangione С.М., et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery. Circulation. 1999; 100(10): 1043-1049). Способ заключается в том, что регистрируют имеющиеся у пациента предоперационные факторы: ишемическая болезнь сердца (ИБС), острое нарушение мозгового кровообращения (ОНМК), хроническая сердечная недостаточность (ХСН), сахарный диабет (СД) с инсулинотерапией, уровень креатинина сыворотки более 200 мкмоль/л и планируемое оперативное вмешательство высокого уровня риска. Каждому фактору присваивают 1 балл и при наличии суммы баллов не более 1 пациент относится к группе низкого кардиального риска, при наличии суммы баллов равной 2 - к группе промежуточного риска, 3 и более балов - к группе пациентов высокого риска.
Основными недостатками являются:
1. Способ не учитывает индивидуальных особенностей функционального состояния кардиореспираторной системы.
2. Имеет недостаточную точность прогнозирования для некардиальных операций.
3. В качестве послеоперационной аритмии рассматривает только фибрилляцию желудочков и полную AV-блокаду
Ближайшим аналогом способа является использование индекса кардиального риска L. Goldman, основанный на регистрации предоперационных факторов риска (Goldman L., Caldera D.L., Nussbaum S.R., et al. Multifactorial index of cardiac risk in noncardiac surgical procedures. N Engl J Med. 1977; 297(16): 845-850), включая возраст, инфаркт миокарда в течение последних 6 месяцев, набухание яремных вен или третий тон сердца при аускультации, ≥5 ЖЭ/мин, несинусовый ритм или преждевременные сокращения предсердий на предоперационной ЭКГ, аортальный стеноз, абдоминальная, торакальная или хирургия аорты, любая неотложная операция. Каждому фактору присваивают определенный балл и при наличии суммы баллов до 5, пациент относится к группе минимального кардиального риска, при наличии суммы баллов 26 и более - к группе пациентов наивысшего риска.
Недостатками способа являются:
1. В качестве послеоперационной аритмии оценивают только желудочковую тахикардию.
2. Недостаточная точность прогнозирования.
ЗАДАЧА: увеличение точности прогнозирования послеоперационной аритмии (трепетание и фибрилляция предсердий, атриовентрикулярная блокада второй или третьей степени) в плановой абдоминальной хирургии.
Технический результат - предлагаемый способ позволяет выявить пациентов с высоким риском развития послеоперационной аритмии после абдоминальных операций, путем определения предоперационных и послеоперационных факторов риска, достоверно влияющих на возникновение данных аритмий, что необходимо для оптимизации периоперационного периода у этих пациентов.
Сущностью предлагаемого способа является определение перед операцией длительности произвольного порогового апноэ в секундах посредством проведения пробы с задержкой дыхания на вдохе (F1), уровня гемоглобина в г/л (F2), возраста (F3), выявление наличия нарушения ритма сердца в анамнезе (F4), определение травматичности операции (F5), интраоперационное выявление потребности в вазопрессорах (F6) и затем определение риска развития послеоперационной аритмии по формуле: K=(-5,20563)+F1x(-0,039067)+F2x(-0,024462)+F3x0,058286+F4x2,14845+F5x0,74904+F6x1,35442, причем при наличии нарушения ритма сердца в анамнезе F4 принимают равной 1, при отсутствии - 0; F5 принимают за 1, если травматичность оперативного вмешательства высокая и за 0, если травматичность низкая и средняя; F6 принимают за 1, если интраоперационно применяют вазопрессоры и за 0, если вазопрессоры не применяют; и при значении К более -4,52, пациента относят к группе высокого риска развития послеоперационной аритмии, при значении К равном -4,52 и менее - к группе низкого риска.
Предлагаемый способ был обоснован следующим образом. Было произведено обследование 571 пациента, оперированных на органах брюшной полости с исходным физическим статусом 1-3 классов по классификации ASA. Регистрировали предоперационные и интраоперационные факторы, длительность произвольного порогового апноэ, предоперационный уровень гемоглобина, нарушение ритма сердца в анамнезе, определяли травматичность операции и потребность в вазопрессорах во время операции. В течение 30 дней после операции регистрировали наличие развития послеоперационной аритмии.
Травматичность хирургического вмешательства определяли по данным таблицы 1.

Длительность произвольного порогового апноэ определяли следующим образом. За день до операции, перед премедикацией, производили определение длительности произвольного порогового апноэ при проведении модифицированной пробы Штанге, для чего после максимального вдоха пациент производит задержку дыхания. Измеряли длительность произвольного порогового апноэ от начала пробы до появления рефлекторных сокращений диафрагмы, определяемых пальпаторно, для чего располагают ладонь над эпигастральной областью пациента. Пробу осуществляли три раза с интервалом в 10 минут, после чего вычисляли среднюю арифметическую длительность произвольного порогового апноэ.
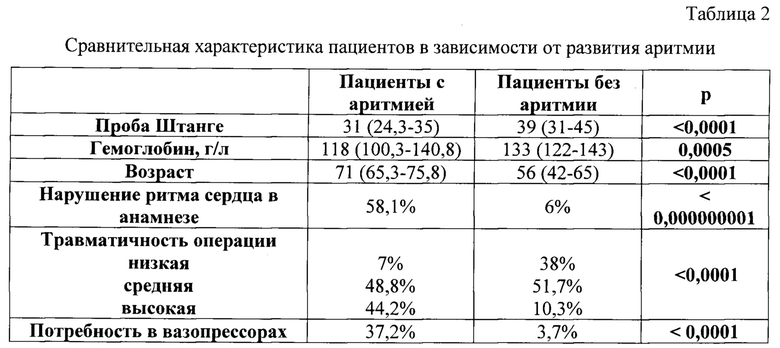
Сравнение предоперационных и послеоперационных факторов риска представлено в таблице 2. В данной таблице были определены и выделены значимые факторы риска развития послеоперационной аритмии.
Таблица 3
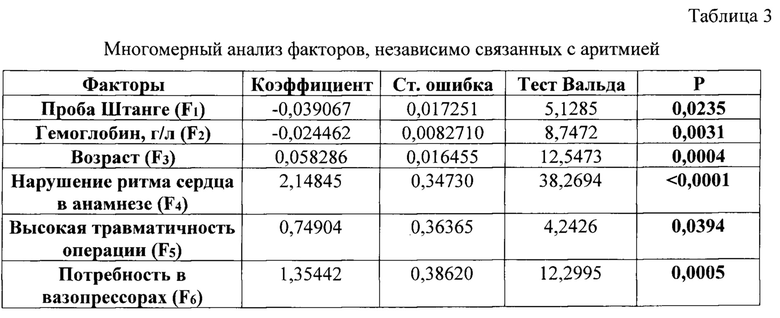
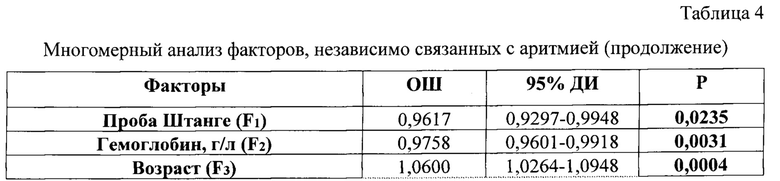
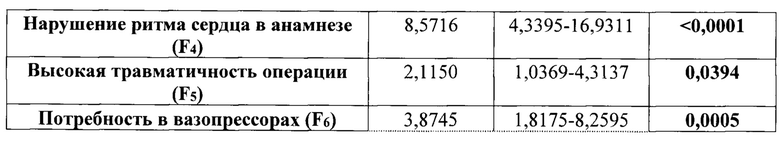
Проведенный логистический регрессионный анализ показал, что длительность произвольного порогового апноэ (проба Штанге), предоперационный уровень гемоглобина, возраст, нарушение ритма сердца в анамнезе, а также высокая травматичность операции и потребность в вазопрессорах во время анестезии достоверно влияют на риск развития аритмии (таблицы 3 и 4).
Прогнозирование послеоперационной аритмии определяют по формуле:
K=(-5,20563)+F1x(-0,039067)+F2x(-0,024462)+F3x0,058286+F4x2,14845+F5x0,74904+F6x1,35442
Цифровые коэффициенты выявлены и обоснованы путем проведения логистического регрессионного анализа и ROC-анализа. F1 - проба Штанге (длительность произвольного порогового апноэ в секундах), F2 - уровень гемоглобина в г/л, F3 - возраст, F4 - наличие нарушения ритма сердца в анамнезе (принимают за 1 при факте наличия и за 0 при отсутствии), F5 - травматичность операции (принимают за 1 при высокой травматичности операции и за 0 при низкой и средней травматичности), F6 - потребность в вазопрессорах (принимают за 1, если интраоперационно применяют вазопрессоры и за 0, если вазопрессоры не применяют).
При значении К более -4,52 пациента относят к группе высокого риска развития послеоперационной аритмии, при значении К равном -4,52 и менее - к группе низкого риска.
Проведенный ROC-анализ подтвердил отличную прогностическую ценность разработанного способа (площадь под ROC-кривой составила 0,931). Чувствительность и специфичность для полученной точки отсечения составили 81,4% и 88,2%, соответственно.
Предлагаемый способ может быть использован в практическом здравоохранении, не требует специальных условий для проведения, экономичен во времени, прост в эксплуатации.
1. Пациент К., 57 лет.
При обследовании в предоперационном периоде выявлена длительность произвольного порогового апноэ 37 секунд (F1), предоперационный уровень гемоглобина 137 г/л (F2), возраст 57 лет (F3), пароксизм фибрилляции предсердий в анамнезе (F4=1). Пациенту выполнена операция лапароскопическая герниопластика (F5=0). Потребности в вазопрессорах во время анестезии не было (F6=0).
Полученные величины подставлены в разработанное уравнение:
К=(-5,20563)+37х(-0,039067)+137х(-0,024462)+57х0,058286+1х2,14845+0x0,74904+0x1,35442=
=-4,53
Поскольку К=-4,53, пациент отнесен к группе низкого риска.
В послеоперационный период аритмии отсутствовали.
2. Пациентка Г., 74 года.
При обследовании в предоперационном периоде выявлена длительность произвольного порогового апноэ 22 секунды (F1), предоперационный уровень гемоглобина 113 г/л (F2), возраст 74 года (F3), нарушений ритма сердца в анамнезе не выявлено (F4=0). Пациентке выполнена операция лапароскопическая нефрэктомия (F5=0). Потребности в вазопрессорах во время анестезии не было (F6=0).
Полученные величины подставлены в разработанное уравнение:
К=(-5,20563)+22х(-0,039067)+113х(-0,024462)+74х0,058286+0х2,14845+0х0,74904+0х 1,3 5442=-4,51
Поскольку К=-4,51, пациентка отнесена к группе высокого риска.
В послеоперационный период на 3 сутки послеоперационного периода возник пароксизм ФП.
3. Пациент 3., 76 лет.
При обследовании в предоперационном периоде выявлена длительность произвольного порогового апноэ 32 секунды (F1), предоперационный уровень гемоглобина 102 г/л (F2), возраст 76 лет (F3), нарушений ритма сердца в анамнезе не выявлено (F4=0). Пациенту выполнена операция лапароскопическая холецистэктомия (F5=0). Потребности в вазопрессорах во время анестезии не было (F6=0).
Полученные величины подставлены в разработанное уравнение:
К=(-5,20563)+32х(-0,039067)+102х(-0,024462)+76х0,058286+0х2,14845+0х0,74904+0х 1,3 5442=-4,52
Поскольку К=-4,52, пациент отнесен к группе низкого риска.
В послеоперационный период аритмии отсутствовали.
Таким образом, применение предложенного способа позволяет достоверно прогнозировать развитие послеоперационной аритмии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ предоперационного прогнозирования послеоперационной фибрилляции предсердий в плановой абдоминальной хирургии | 2024 |
|
RU2841150C1 |
| Способ предоперационного прогнозирования больших кардиальных осложнений в плановой абдоминальной хирургии | 2024 |
|
RU2841151C1 |
| Способ прогнозирования риска 30-дневной летальности пациентов после плановых абдоминальных операций | 2024 |
|
RU2841147C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОЙ ДЫХАТЕЛЬНОЙ НЕДОСТАТОЧНОСТИ В ПЛАНОВОЙ АБДОМИНАЛЬНОЙ ХИРУРГИИ | 2023 |
|
RU2827125C1 |
| Способ предоперационного прогнозирования послеоперационной пневмонии в плановой абдоминальной хирургии | 2024 |
|
RU2841149C1 |
| СПОСОБ ПРЕДОПЕРАЦИОННОГО ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОГО ДЕЛИРИЯ В ПЛАНОВОЙ АБДОМИНАЛЬНОЙ ХИРУРГИИ | 2024 |
|
RU2840879C1 |
| Способ предоперационного прогнозирования послеоперационной дыхательной недостаточности в плановой абдоминальной хирургии | 2024 |
|
RU2841175C1 |
| Способ прогнозирования сердечно-сосудистых осложнений при проведении спинальной анестезии у гинекологических больных | 2015 |
|
RU2609061C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ ПЕРИОПЕРАЦИОННЫХ СЕРДЕЧНО-СОСУДИСТЫХ ОСЛОЖНЕНИЙ ПРИ ВНЕСЕРДЕЧНЫХ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ | 2009 |
|
RU2410017C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕАБИЛИТАЦИОННОГО ПОТЕНЦИАЛА У БОЛЬНЫХ ПОСЛЕ АОРТОКОРОНАРНОГО ШУНТИРОВАНИЯ | 2020 |
|
RU2746296C1 |
Изобретение относится к медицине, а именно к хирургии, анестезиологии и реаниматологии, и может быть использовано при оценке риска развития послеоперационной аритмии при операциях на органах брюшной полости. В предоперационном периоде определяют наличие нарушения ритма сердца в анамнезе, длительность произвольного порогового апноэ в секундах путем проведения пробы с задержкой дыхания на вдохе, уровень гемоглобина в г/л, возраст, травматичность операции, интраоперационно выявляют потребность в вазопрессорах. На основании полученных данных определяют риск развития послеоперационной аритмии (К) по заданной формуле, и при значении К более -4,52 пациента относят к группе высокого риска развития послеоперационной аритмии, при значении К равном -4,52 и менее - к группе низкого риска. Способ позволяет своевременно выявить пациентов с высоким риском развития послеоперационных аритмий после абдоминальных операций и осуществить оптимизацию периоперационного периода у данных пациентов за счет оценки совокупности наиболее значимых показателей. 4 табл., 3 пр.
Способ прогнозирования послеоперационной аритмии в плановой абдоминальной хирургии, включающий предоперационное выявление наличия нарушения ритма сердца в анамнезе (F4), отличающийся тем, что перед операцией дополнительно определяют длительность произвольного порогового апноэ в секундах путем проведения пробы с задержкой дыхания на вдохе (F1), уровень гемоглобина в г/л (F2), возраст (F3), травматичность операции (F5), интраоперационно выявляют потребность в вазопрессорах (F6) и затем определяют риск развития послеоперационной аритмии по формуле
К=(-5,20563) + F1 × (-0,039067) + F2 × (-0,024462) + F3 × 0,058286 + F4 × 2,14845 + F5 × 0,74904 + F6 × 1,35442,
причем при наличии нарушения ритма сердца в анамнезе F4 принимают равной 1, при отсутствии - 0;
F5 принимают за 1, если травматичность оперативного вмешательства высокая, и за 0, если травматичность низкая и средняя;
F6 принимают за 1, если интраоперационно применяют вазопрессоры, и за 0, если вазопрессоры не применяют;
и при значении К более -4,52 пациента относят к группе высокого риска развития послеоперационной аритмии, при значении К равном -4,52 и менее - к группе низкого риска.
Авторы
Даты
2024-11-18—Публикация
2023-12-18—Подача