Предполагаемое изобретение относится к медицине, а именно к анестезиологии и реаниматологии, и может быть использовано при оценке риска развития послеоперационной дыхательной недостаточности (ПДН) при операциях на органах брюшной полости.
ПДН, определяемая как потребность в искусственной вентиляции легких более 48 часов или незапланированная повторная интубация в течение 30 дней является серьезным опасным для жизни осложнением и тесно коррелирует с 30-дневной смертностью и долгосрочным исходом (Khuri SF, Henderson WG, DePalma RG, et al. Determinants of long-term survival after major surgery and the adverse effect of postoperative complications. Ann Surg. 2005; 242:323-326). Потребность в искусственной вентиляции легких может быть следствием невозможности отлучения от аппарата ИВЛ сразу после операции или может возникнуть после интубации трахеи в любое время в течение 30 дней после операции. Хотя частота развития ПДН относительно невысока (1-3%), она несет не только серьезные последствия для здоровья, но и значительно увеличивает финансовые затраты системы здравоохранения в целом (Carey K, Stefos Т, Shibei Z, et al. Excess costs attributable to postoperative complications. Med Care Res Rev. 2011; 68:490-503). ПДН тесно связана как с модифицируемыми, так и с немодифицируемыми факторами риска, в литературе встречается достаточно большое количество работ, посвященных выявлению предикторов ПДН (Johnson RG, Arozullah AM, Neumayer L, et al. Multivariable predictors of postoperative respiratory failure after general and vascular surgery: results from the patient safety in surgery study. J Am Coll Surg. 2007; 204:1188-1198; Gupta H, Gupta PK, Fang X, et al. Development and validation of a risk calculator predicting postoperative respiratory failure. Chest. 2011; 140:1207-1215; Milgrom DP, Njoku VC, Fecher AM, et al. Unplanned intubation: when and why does this deadly complication occur? Surgery. 2013; 154:376-383). Место хирургического вмешательства является одним из наиболее важных факторов риска, связанных с развитием послеоперационных респираторных осложнений (Smetana GW, Lawrence VA, Cornell JE. Preoperative pulmonary risk stratification for noncardiothoracic surgery: systematic review for the American College of Physicians. Ann Intern Med 2006; 144:581-95). Абдоминальные операции, особенно операции на брюшном отделе аорты, а также операции на верхних отделах брюшной полости, обладают самым высоким уровнем риска развития ПДН (Arozullah AM, Daley J, Henderson WM, Khuri SF for the National Veterans Administration Surgical Quality Improvement Program. Multifactorial risk index for predicting postoperative respiratory failure in men after major noncardiac surgery. Ann Surg 2000; 232:242-53; Johnson RG, Arozullah AM, Neumayer L, Henderson WG, Hosokawa P, Khuri SF. Multivariable predictors of postoperative respiratory failure after general and vascular surgery: results from the patient safety in surgery study. J Am Coll Surg 2007;204:1188-98). Близость кожного разреза к диафрагме, по-видимому, играет решающую роль в развитии ПДН (Ford GT, Rosenal TW, Clergue F, Whitelaw WA. Respiratory physiology in upper abdominal surgery. Clin Chest Med 1993;14:237-52; Dureuil B, Cantineau JP, Desmonts JM. Effects of upper or lower abdominal surgery on diaphragmatic function. Br J Anaesth 1987; 59:1230-5). Фактически, несколько исследований показали, что у пациентов, перенесших операции на верхнем этаже брюшной полости, снижение функции диафрагмы приводит к снижению вентиляции и расширению зависимых зон легких (Ford GT, Rosenal TW, Clergue F, Whitelaw WA. Respiratory physiology in upper abdominal surgery. Clin Chest Med 1993; 14:237-52; Dureuil B, Cantineau JP, Desmonts JM. Effects of upper or lower abdominal surgery on diaphragmatic function. Br J Anaesth 1987; 59:1230-5). Несколько недавних систематических обзоров и метаанализов доказали, что предоперационные физиотерапевтические маневры, тренировка инспираторных мышц и лечебная физкультура может помочь снизить частоту возникновения ПДН (Pouwels S, Willigendael ЕМ, van Sambeek MR, Nienhuijs SW, Cuypers PW, Teijink JA. Beneficial Effects of Pre-operative Exercise Therapy in Patients with an Abdominal Aortic Aneurysm: A Systematic Review. Eur J Vase Endovasc Surg 2015; 49:66-76., Katsura M, Kuriyama A, Takeshima T, Fukuhara S, Furukawa ТА. Preoperative inspiratory muscle training for postoperative pulmonary complications in adults undergoing cardiac and major abdominal surgery. Cochrane Database Syst Rev. 2015; 10:CD010356).
В связи с этим, выявление пациентов высокого риска позволяет целенаправленно применять способы профилактики ПДН и снижать риск ее развития.
Одним из аналогов способа является шкала оценки риска ПДН, разработанная экспертами Европейского общества анестезиологов (Canet J, Sabate S, Mazo V, et al. Development and validation of a score to predict postoperative respiratory failure in a multicentre European cohort: A prospective, observational study. Eur J Anaesthesiol. 2015; 32(7):458-470. doi:10.1097/EJA.0000000000000223). Способ заключается в том, что регистрируют предоперационную сатурацию по данным пульсоксиметрии, признаки респираторного заболевания, наличие и степень хронической сердечной недостаточности, возраст, длительность операции. Каждому фактору присваивают определенный балл и при наличии суммы баллов до 12 пациент относится к группе низкого риска ПДН, при наличии суммы баллов 12-22 - к группе среднего риска, более 22 - к группе пациентов высокого риска.
Основными недостатками являются
1. Способ не учитывает индивидуальных особенностей функционального состояния кардиореспираторной системы
2. Не учитывают важных факторов риска дыхательной недостаточности, связанных с оперативным вмешательством
Другим аналогом предлагаемого способа является способ, основанный на регистрации предоперационных факторов риска (Arozullah AM, Daley J, Henderson WG, Khuri SF. Multifactorial risk index for predicting postoperative respiratory failure in men after major noncardiac surgery. The National Veterans Administration Surgical Quality Improvement Program. Ann Surg 2000; 232(2):242-253), включая вид операции, возраст, уровень альбумина, уровень мочевины крови, наличия хронической обструктивной болезни легких (ХОБЛ).
Недостатками способа являются:
1. Отсутствие внешней валидации способа.
2. Необходимость выполнения сложных лабораторных исследований.
3. Недостаточная точность прогнозирования
Ближайшим аналогом является оценка исходного физического статуса по классификации Американского общества анестезиологов (ASA). Способ заключается в отнесении пациента к одному из классов (от одного до 6), в зависимости от тяжести сопутствующих заболеваний (Hurwitz ЕЕ, Simon М, Vinta SR.et al. Adding examples to the ASA-physical status classification improves correct assignment to patients. Anesthesiology. 2017; 126:(4):614-622 10.1097/ALN.0000000000001541).
Недостатки способа:
1. Субъективность
2. Способ не учитывает влияния травматичности оперативного вмешательства
3. Недостаточная точность прогнозирования
4. Является приспособленным инструментом оценки риска дыхательной недостаточности
ЗАДАЧА: увеличение точности прогнозирования послеоперационной дыхательной недостаточности в плановой абдоминальной хирургии.
Технический результат - предлагаемый способ позволяет достоверно выявить пациентов с высоким риском развития дыхательной недостаточности после абдоминальных операций.
Сущностью предлагаемого способа является определение перед операцией физического статуса по классификации ASA (F3), длительности произвольного порогового апноэ в секундах посредством проведения пробы с задержкой дыхания на вдохе (F1), выявление наличия полной функциональной зависимости (F2), наличия сопутствующей ХОБЛ (F6), интраоперационное определение длительности операции в минутах (F4), потребности в гемотрансфузии (F5) и затем определение риска развития послеоперационной дыхательной недостаточности по формуле: K=(-5,47106)+F1x(-0,031547)+F2x1,96548+F3x1,49812+F4x0,0067583+F5x1,69804+F6x11,77118, причем при наличии полной функциональной зависимости F2 принимают равной 1, при отсутствии - 0; F3 принимают за 1, если класс ASA более 2, и за 0, если класс ASA соответствует 1-2; F5 принимают за 1, если интраоперационно производят гемотрансфузию и за 0, если гемотрансфузии не было; F6 принимают за 1 при наличии ХОБЛ и за 0, если у пациента отсутствует ХОБЛ и при значении К более -4,3, пациента относят к группе высокого риска послеоперационной дыхательной недостаточности, при значении К равном -4,3 и менее - к группе низкого риска.
Предлагаемый способ был обоснован следующим образом. Было произведено обследование 1254 пациентов, оперированных на органах брюшной полости с исходным физическим статусом 1-4 классов по классификации ASA. Регистрировали предоперационные и интраоперационные факторы, длительность оперативного вмешательства, наличие полной функциональной зависимости, наличие сопутствующей ХОБЛ, длительность произвольного порогового апноэ, потребность в гемотрансфузии во время операции. В течение 30 дней после операции регистрировали наличие развития послеоперационной дыхательной недостаточности.
Физический статус оценивали по классификации Американского общества анестезиологов (таблица 1).

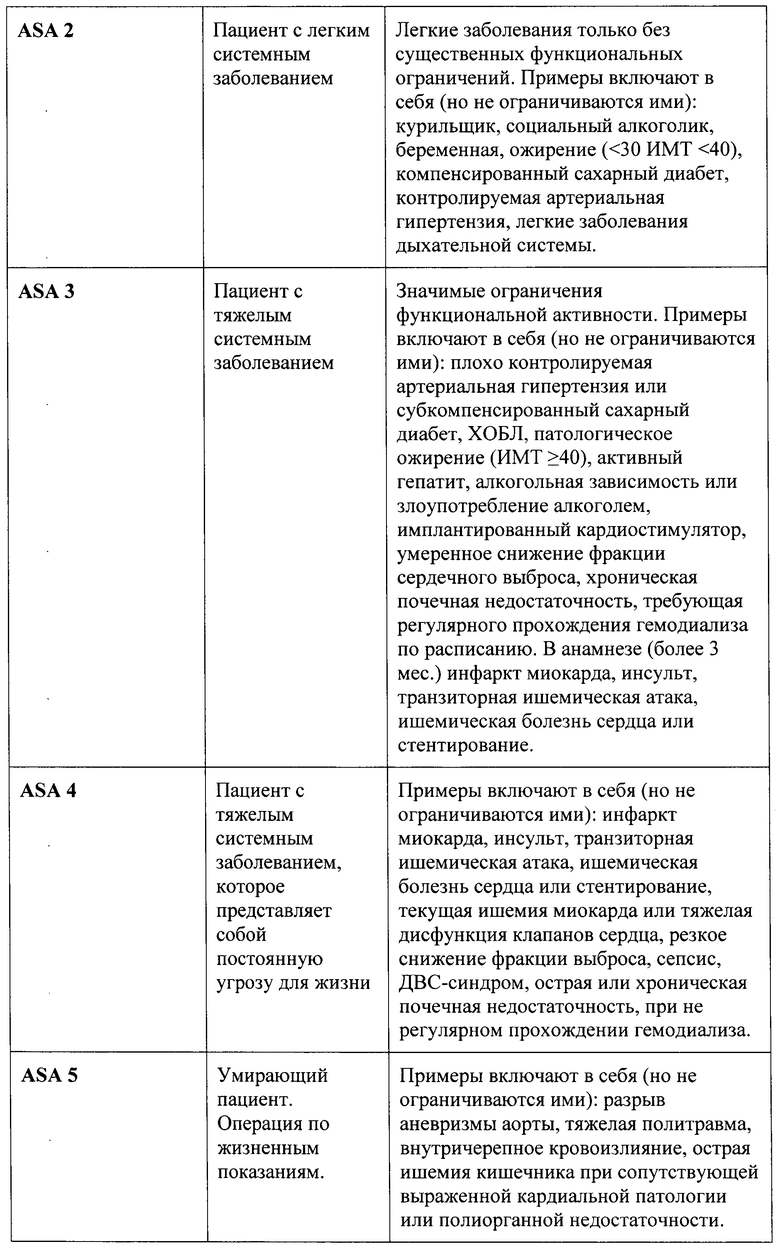

Функциональную зависимость пациента определяли как постоянную потребность в посторонней помощи в ежедневной активности по причине ухудшения их функционального статуса.
Длительность произвольного порогового апноэ определяли следующим образом. За день до операции, перед премедикацией, производили определение длительности произвольного порогового апноэ при проведении модифицированной пробы Штанге, для чего после максимального вдоха пациент производит задержку дыхания. Измеряли длительность произвольного порогового апноэ от начала пробы до появления рефлекторных сокращений диафрагмы, определяемых пальпаторно, для чего располагают ладонь над эпигастральной областью пациента. Пробу осуществляли три раза с интервалом в 10 минут, после чего вычисляли среднюю арифметическую длительность произвольного порогового апноэ.
Сравнение предоперационных и послеоперационных факторов риска представлено в таблице 2. В данной таблице были определены и выделены значимые факторы риска развития послеоперационной дыхательной недостаточности.
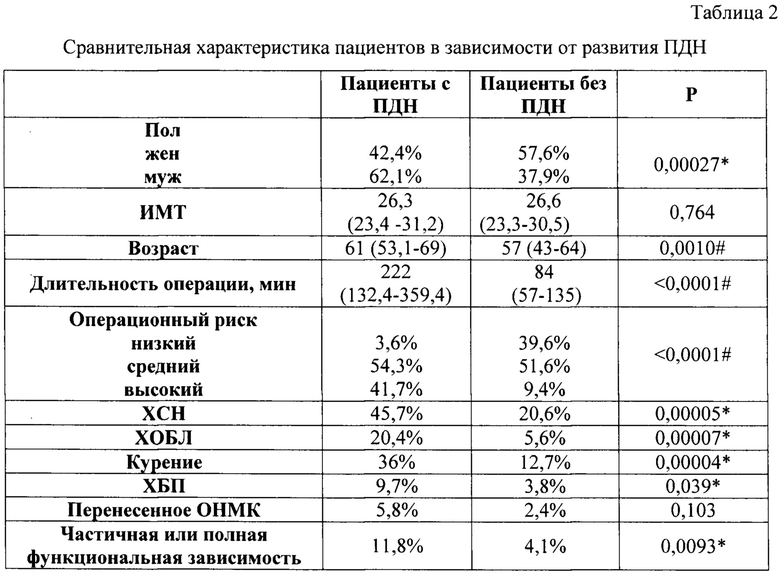
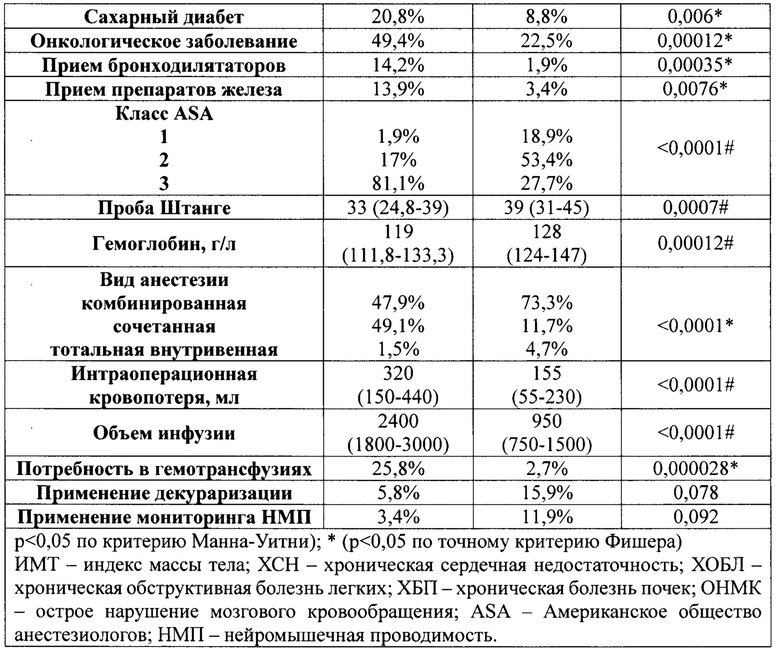
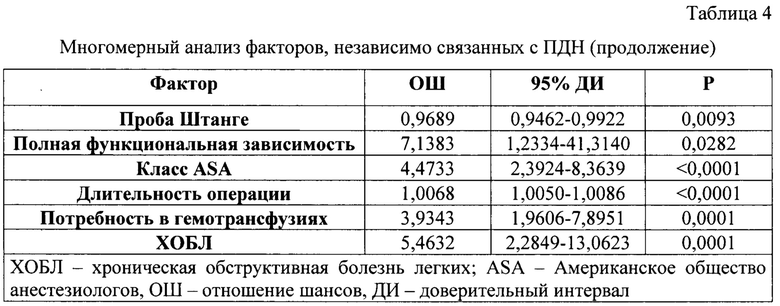
Проведенный логистический регрессионный анализ показал, что длительность произвольного порогового апноэ (проба Штанге), длительность операции, наличие полной функциональной зависимости, наличие сопутствующей ХОБЛ, физический класс по классификации ASA и потребность в гемотрансфузии достоверно влияют на риск развития дыхательной недостаточности (таблицы 3 и 4).
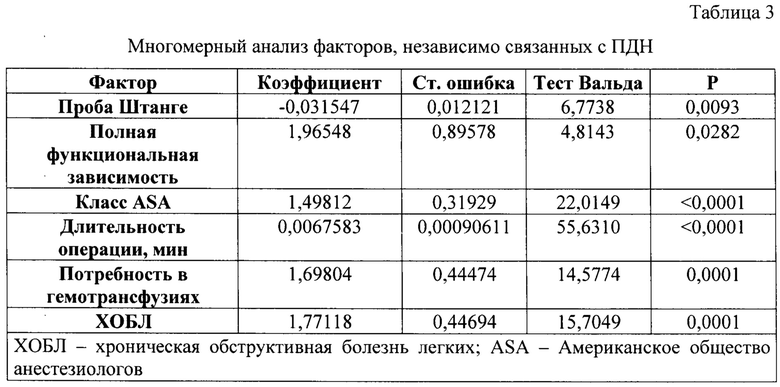
Прогнозирование послеоперационной дыхательной недостаточности определяют по формуле:
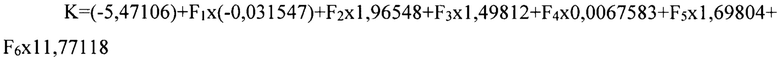
Цифровые коэффициенты выявлены и обоснованы путем проведения логистического регрессионного анализа и ROC-анализа. F1 - длительность произвольного порогового апноэ в секундах, F2 - полная функциональная зависимость (принимают за 1 при факте наличия и за 0 при отсутствии), F3 - физический класс по классификации ASA (принимают за 1, если класс более 2 и за 0, если класс ASA соответствует 1-2), F4 - длительность операции в минутах, F5 - потребность в гемотрансфузиях (принимают за 1, если интраоперационно производят гемотрансфузию и за 0, если гемотрансфузии не было), F6 - наличие ХОБЛ (принимают за 1 при факте наличия и за 0 при отсутствии).
При значении К более -4,3 пациента относят к группе высокого риска послеоперационной дыхательной недостаточности, при значении К равном -4,3 и менее - к группе низкого риска.
Проведенный ROC-анализ подтвердил высокую прогностическую ценность разработанного способа (площадь под ROC-кривой составила 0,880). Чувствительность и специфичность для полученной точки отсечения составили 80,6% и 82,4%, соответственно.
Предлагаемый способ может быть использован в практическом здравоохранении, не требует специальных условий для проведения, экономичен во времени, прост в эксплуатации.
1. Пациент М., 45 лет.
При обследовании в предоперационном периоде выявлена длительность произвольного порогового апноэ 50 секунд (F1), пациент без сопутствующей патологии, с учетом курения отнесен ко 2 классу по классификации физического статуса ASA (F3=0). Предоперационный уровень сатурации 100%, признаков ХОБЛ не выявлено (F6=0). Пациенту выполнена операция правосторонняя гемиколэктомия лапароскопическим доступом, длительность составила 406 минут (F4). Потребности в гемотрансфузии не было (F5=0).
Полученные величины подставлены в разработанное уравнение:

Поскольку K=-4,3, пациент отнесен к группе низкого риска. В послеоперационный период дыхательной недостаточности не было.
2. Пациент Т., 63 г.
При обследовании выявлена длительность произвольного порогового апноэ 23 секунды (F1), пациент перенес ОНМК 3 года назад, полностью функционально зависим (F2=1), отнесен к 3 классу по классификации физического статуса ASA (F3=1). Пациенту выполнена операция резекция желудка открытым доступом, длительность составила 180 минут (F4). Во время операции потребовалась трансфузия компонентов крови (F5=1). Предоперационный уровень сатурации 98%, признаков ХОБЛ не выявлено (F6=0).
Полученные величины подставлены в разработанное уравнение:
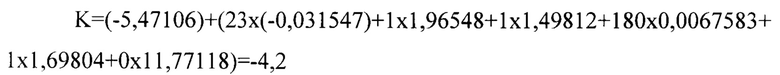
Поскольку K>-4,3, пациент отнесен к группе высокого риска.
В послеоперационный период на 5 сутки послеоперационного периода зафиксировано развитие дыхательной недостаточности.
3. Пациент Г., 25 лет.
При обследовании в предоперационном периоде выявлена длительность произвольного порогового апноэ 47 секунд (F1), пациент без сопутствующей патологии отнесен к 1 классу по классификации физического статуса ASA (F3=0). Предоперационный уровень сатурации 100%, признаков ХОБЛ не выявлено (F6=0). Пациенту выполнена операция спленэктомия лапароскопическим доступом, длительность составила 377 минут (F4). Потребности в гемотрансфузии не было (F5=0).
Полученные величины подставлены в разработанное уравнение:
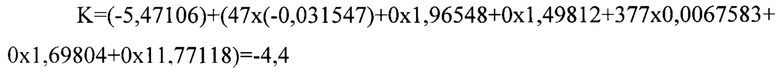
Поскольку K<-4,3, пациент отнесен к группе низкого риска.
В послеоперационный период дыхательной недостаточности не было.
Таким образом, применение предложенного способа позволяет достоверно прогнозировать развитие дыхательной недостаточности.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ предоперационного прогнозирования послеоперационной дыхательной недостаточности в плановой абдоминальной хирургии | 2024 |
|
RU2841175C1 |
| Способ предоперационного прогнозирования послеоперационной пневмонии в плановой абдоминальной хирургии | 2024 |
|
RU2841149C1 |
| Способ предоперационного прогнозирования больших кардиальных осложнений в плановой абдоминальной хирургии | 2024 |
|
RU2841151C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОЙ АРИТМИИ В ПЛАНОВОЙ АБДОМИНАЛЬНОЙ ХИРУРГИИ | 2023 |
|
RU2830282C1 |
| Способ прогнозирования риска 30-дневной летальности пациентов после плановых абдоминальных операций | 2024 |
|
RU2841147C1 |
| СПОСОБ ПРЕДОПЕРАЦИОННОГО ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОГО ДЕЛИРИЯ В ПЛАНОВОЙ АБДОМИНАЛЬНОЙ ХИРУРГИИ | 2024 |
|
RU2840879C1 |
| Способ предоперационного прогнозирования послеоперационной фибрилляции предсердий в плановой абдоминальной хирургии | 2024 |
|
RU2841150C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ИНФЕКЦИИ ОБЛАСТИ ХИРУРГИЧЕСКОГО ВМЕШАТЕЛЬСТВА ПРИ ОПЕРАЦИЯХ НА ПОЗВОНОЧНИКЕ | 2017 |
|
RU2674095C1 |
| Способ прогнозирования вероятности развития послеоперационных респираторных осложнений после лобэктомии | 2023 |
|
RU2825051C1 |
| Способ прогнозирования сердечно-сосудистых осложнений при проведении спинальной анестезии у гинекологических больных | 2015 |
|
RU2609061C1 |
Изобретение относится к медицине, а именно к анестезиологии и реаниматологии, и может быть использовано при оценке риска развития послеоперационной дыхательной недостаточности при операцих на органах брюшной полости. Перед операцией определяют длительность произвольного порогового апноэ в секундах путем проведения пробы с задержкой дыхания на вдохе, выявляют наличие полной функциональной зависимости, наличие сопутствующей хронической обструктивной болезни легких, интраоперационно определяют длительность операции в минутах, потребность в гемотрансфузии, учитывают физический статус по классификации ASA. С учетом полученных показателей определяют риск развития послеоперационной дыхательной недостаточности (К) по заданной формуле. И при значении К более -4,3, пациента относят к группе высокого риска послеоперационной дыхательной недостаточности, при значении K равном -4,3 и менее - к группе низкого риска. Способ позволяет повысить точность определения пациентов с высоким риском развития дыхательной недостаточности в послеоперационном периоде за счет оценки совокупности наиболее значимых показателей. 4 табл., 3 пр.
Способ прогнозирования послеоперационной дыхательной недостаточности в плановой абдоминальной хирургии, включающий предоперационное определение физического статуса по классификации ASA (F3), отличающийся тем, что перед операцией дополнительно определяют длительность произвольного порогового апноэ в секундах путем проведения пробы с задержкой дыхания на вдохе (F1), выявляют наличие полной функциональной зависимости (F2), наличие сопутствующей хронической обструктивной болезни легких (ХОБЛ, F6), интраоперационно определяют длительность операции в минутах (F4), потребность в гемотрансфузии (F5) и затем определяют риск развития послеоперационной дыхательной недостаточности по формуле:
K= (-5,47106) + F1 x (-0,031547) + F2 x 1,96548 + F3 x 1,49812 + F4 x 0,0067583 + F5 x 1,69804 + F6 x 11,77118,
причем при наличии полной функциональной зависимости F2 принимают равной 1, при отсутствии - 0;
F3 принимают за 1, если класс ASA более 2, и за 0, если класс ASA соответствует 1-2;
F5 принимают за 1, если интраоперационно производят гемотрансфузию и за 0, если гемотрансфузии не было;
F6 принимают за 1 при наличии ХОБЛ и за 0, если у пациента отсутствует ХОБЛ,
и при значении K более -4,3, пациента относят к группе высокого риска послеоперационной дыхательной недостаточности, при значении K равном -4,3 и менее - к группе низкого риска.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ПРИ ТОРАКАЛЬНЫХ ОПЕРАЦИЯХ | 2020 |
|
RU2745360C1 |
| КОТОВА Д,П | |||
| и др | |||
| Факторы риска респираторных осложнений у пациентов в периоперационном периоде | |||
| Клиницист | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| РОДИОНОВА Л.Н | |||
| и др | |||
| Прогностическое значение ультразвукового исследования легких и послеоперационная дыхательная недостаточность после обширных панкреатодуоденальных вмешательств | |||
Авторы
Даты
2024-09-23—Публикация
2023-11-24—Подача