Область техники, к которой относится изобретение
Настоящее изобретение относится в целом к новым активируемым протеазой антигенсвязывающим молекулам, которые содержат антиидиотипсвязывающий фрагмент, который обратимо маскирует связывание антигена молекулой. В частности, изобретение относится к связывающим Т-клетки молекулам, имеющим антиидиотипсвязывающий фрагмент, который маскирует CD3-связывающий фрагмент до расщепления протеазой. Это обеспечивает недоступность или «маскировку» CD3-связывающего фрагмента до его приближения к ткани-мишени, такой как опухоль, например, к инфильтрующим опухоль Т-клеткам. Кроме того, настоящее изобретение относится к полинуклеотидам, которые кодируют указанные актируемые протеазой связывающие Т-клетки молекулы и идиотипспецифические полипептиды, и к векторам и клеткам-хозяевам, которые содержат указанные полинуклеотиды. Изобретение относится также к способам получения активируемых протеазой связывающих Т-клетки молекул, предлагаемых в изобретении, и к способам их применения, например, для лечения заболевания.
Предпосылки создания изобретения
В различных клинических ситуациях часто требуется избирательная деструкция индивидуальной клетки-мишени или определенного типа клеток-мишеней. Например, основной задачей при терапии рака является разрушение именно опухолевых клеток с сохранением при этом в интактном и неповрежденном состоянии здоровых клеток и тканей.
Перспективным подходом для достижения этой цели является индукция иммунного ответа против опухоли, при котором иммунные эффекторные клетки, такие как естественные клетки-киллеры (NK) или цитотоксические Т-лимфоциты (CTL), атакуют и разрушают опухолевые клетки. В этом плане в последние годы возрос интерес к биспецифическим антителам, сконструированным таким образом, чтобы они связывались с помощью одного «плеча» с поверхностным антигеном на клетках-мишенях, а с помощью второго «плеча» с активирующим инвариантным компонентом комплекса Т-клеточного рецептора (TCR). Одновременное связывание такого антитела с обеими его мишенями должно усиливать временное взаимодействие между клеткой-мишенью и Т-клеткой, вызывая активацию любой цитотоксической Т-клетки и последующий лизис клетки-мишени. Таким образом, иммунный ответ переориентируется на клетки-мишени и не зависит от презентации пептидного антигена клеткой-мишенью или специфичности Т-клетки, что имеет место при нормальной ограниченной по ГКГС активации CTL. В этом контексте решающее значение имеет то, что CTL активируются только в условиях тесной близости к клетке-мишени, т.е. когда имеет место имитация иммунологического синапса. Наиболее предпочтительными являются активирующие Т-клетки биспецифические молекулы, для которых не требуется предварительное кондиционирование или костимуляция лимфоцитов для того, чтобы вызывать эффективный лизис клеток-мишеней. Разработано несколько форматов биспецифических антител и изучена их пригодность для опосредуемой Т-клетками иммунотерапии. Они включают молекулы BiTE (bispecific Т cell engager, биспецифический активатор (проводник) Т-клеток) (Nagorsen и Baeuerle Exp Cell Res 317, 2011, cc. 1255-1260), димерные антитела (диабоди) (Holliger и др., Prot Eng 9, 1996, cc. 299-305) и их производные, такие как тандемные диабоди (Kipriyanov и др., J Mol Biol 293, 1999, cc. 41-66), молекулы DART (dual affinity retargeting, переориентирующие молекулы с двойной аффинностью) (Moore и др., Blood 117, 2011, cc. 4542-51) и triomabs® (трифункциональные антитела) (Seimetz и др., Cancer Treat Rev 36, 2010, cc. 458-467).
Задача создания биспецифических молекул, пригодных для лечения, ставит несколькими технических проблем, связанных с требованиями к эффективности, токсичности, применимости и технологичности, которым они должны удовлетворять. В тех случаях, когда мишенью биспецифической молекулы является антиген на клетке-мишени, например, на раковой клетке, который экспрессируется также и в не являющейся мишенью ткани, может возникать токсичность. Таким образом, существует потребность в эффективных активирующих Т-клетки биспецифических молекулах, которые обеспечивают полную активацию Т-клеток в присутствии клеток-мишеней, но не в присутствии здоровых клеток или тканей.
Краткое изложение сущности изобретения
Изобретение относится в целом к активирующим Т-клетки биспецифическим молекулам, которые избирательно активируются в присутствии клетки-мишени.
Одним из объектов изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(а) первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3;
(б) второй антигенсвязывающий фрагмент, обладающий способностью специфически связываться с антигеном клетки-мишени; и
(в) маскирующий фрагмент, ковалентно присоединенный к биспецифической связывающей Т-клетки молекуле через расщепляемый протеазой линкер, где маскирующий фрагмент обладает способностью специфическим связываться с идиотипом первого или второго антигенсвязывающего фрагмента, тем самым обратимо скрывая («пряча») первый или второй антигенсвязывающий фрагмент.
В одном из вариантов осуществления изобретения маскирующий фрагмент активируемой протеазой активирующей Т-клетки биспецифической молекулы ковалентно присоединен к первому антигенсвязывающему фрагменту. В одном из вариантов осуществления изобретения маскирующий фрагмент ковалентно присоединен к вариабельной области тяжелой цепи первого антигенсвязывающего фрагмента. В одном из вариантов осуществления изобретения маскирующий фрагмент ковалентно присоединен к вариабельной области легкой цепи первого антигенсвязывающего фрагмента. В одном из вариантов осуществления изобретения маскирующий фрагмент представляет собой антиидиотипический scFv.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит второй маскирующий фрагмент, обратимо скрывающий второй антигенсвязывающий фрагмент.
В одном из вариантов осуществления изобретения протеаза, которая обладает способностью расщеплять расщепляемый протеазой линкер, экспрессируется клеткой-мишенью.
В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой обменены либо вариабельные, либо константные области легкой цепи Fab и тяжелой цепи Fab. В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой обменены константные области легкой цепи Fab и тяжелой цепи Fab. В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит не более одного антигенсвязывающего фрагмента, который обладает способностью специфически связываться с CD3. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит третий антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с антигеном клетки-мишени. В одном из конкретных вариантов осуществления изобретения третий антигенсвязывающий фрагмент идентичен второму антигенсвязывающему фрагменту. В одном из конкретных вариантов осуществления изобретения третий антигенсвязывающий фрагмент не идентичен второму антигенсвязывающему фрагменту. В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 или HER1. В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1, HER1 или мезотелином. В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1, HER1, HER2 или мезотелином.
В одном из вариантов осуществления изобретения первый и второй антигенсвязывающие фрагменты слиты друг с другом, необязательно через пептидный линкер. В одном из конкретных вариантов осуществления изобретения второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента. В одном из конкретных вариантов осуществления изобретения первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента. В одном из конкретных вариантов осуществления изобретения легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента слиты друг с другом, необязательно через пептидный линкер.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит дополнительно Fc-домен, состоящий из первой и второй субъединиц, обладающих способностью к стабильной ассоциации. В одном из вариантов осуществления изобретения Fc-домен представляет собой Fc-домен IgG, конкретно Fc-домен IgG1 или IgG4. В одном из вариантов осуществления изобретения Fc-домен представляет собой человеческий Fc-домен. В одном из вариантов осуществления изобретения Fc-домен характеризуется пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с нативным Fc-доменом IgG1. В одном из вариантов осуществления изобретения Fc-домен содержит одну или несколько аминокислотную(ых) замену(н), которая(ые) снижает(ют) связывание с Fc-рецептором и/или эффекторную функцию. В одном из конкретных вариантов осуществления изобретения одна или несколько аминокислотная(ых) замена(ы) находится(ятся) в одном или нескольких положениях, выбранных из следующей группы: L234, L235 и Р329 (нумерация по Кэботу). В одном из конкретных вариантов осуществления изобретения каждая субъединица Fc-домена содержит три аминокислотные замены, которые снижают связывание с активирующим Fc-рецептором и/или эффекторную функцию, где указанные аминокислотные замены представляют собой L234A, L235A и P329G. В одном из конкретных вариантов осуществления изобретения Fc-рецептор представляет собой Fcγ-рецептор. В одном из вариантов осуществления изобретения эффекторная функция представляет собой антитело-обусловленную клеточнозависимую цитотоксичность (ADCC). В одном из вариантов осуществления изобретения клетка-мишень представляет собой человеческую клетку.
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21); и
(в) аминокислотную последовательность CDR H3 PYDYDVLDY (SEQ ID NO: 22).
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(б) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(в) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21); и
(в) аминокислотную последовательность CDR H3 PYDYDVLDY (SEQ ID NO: 22);
и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27); и
(в) аминокислотную последовательность CDR H3 GITTVVDDYYAMDY (SEQ ID NO: 28).
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(б) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(в) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
В одном из вариантов осуществления изобретения маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27);
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28);
и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
В одном из вариантов осуществления изобретения расщепляемый протеазой линкер содержит по меньшей мере одну распознаваемую протеазой последовательность. В одном из вариантов осуществления изобретения расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность. В одном из вариантов осуществления изобретения распознаваемую протеазой последовательность выбирают из группы, состоящей из:
(а) RQARVVNG (SEQ ID NO: 36);
(б) VHMPLGFLGPGRSRGSFP (SEQ ID NO: 37);
(в) RQARVVNGXXXXXVPLSLYSG (SEQ ID NO: 38); и
(г) RQARVVNGVPLSLYSG (SEQ ID NO: 39),
(д) PLGLWSQ (SEQ ID NO: 40), где X обозначает любую аминокислоту.
В одном из вариантов осуществления изобретения расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность. В одном из вариантов осуществления изобретения распознаваемую протеазой последовательность выбирают из группы, состоящей из:
(а) RQARVVNG (SEQ ID NO: 36);
(б) VHMPLGFLGPGRSRGSFP (SEQ ID NO: 37);
(в) RQARVVNGXXXXXVPLSLYSG (SEQ ID NO: 38);
(г) RQARVVNGVPLSLYSG (SEQ ID NO: 39);
(д) PLGLWSQ (SEQ ID NO: 40);
(е) VHMPLGFLGPRQARVVNG (SEQ ID NO: 97);
(ж) FVGGTG (SEQ ID NO: 98);
(з) KKAAPVNG (SEQ ID NO: 99);
(и) PMAKKVNG (SEQ ID NO: 100);
(к) QARAKVNG (SEQ ID NO: 101);
(л) VHMPLGFLGP (SEQ ID NO: 102);
(м) QARAK (SEQ ID NO: 103);
(н) VHMPLGFLGPPMAKK (SEQ ID NO: 104);
(о) KKAAP (SEQ ID NO: 105); и
(п) PMAKK (SEQ ID NO: 106), где X обозначает любую аминокислоту.
В одном из вариантов осуществления изобретения протеазу, обладающую способностью расщеплять расщепляемый протеазой линкер, выбирают из группы, которая состоит из металлопротеиназы, например, матричной металлопротеиназы (ММР) 1-28 и «дезинтегрина и металлопротеиназы» (А Disintegrin And Metalloproteinase (ADAM)) 2, 7-12, 15, 17-23, 28-30 и 33, сериновой протеазы, например, активатора плазминогена урокиназного типа и матриптазы, цистеиновой протеазы, аспарагиновой протеазы и протеазы катепсина. В одном из конкретных вариантов осуществления изобретения протеаза представляет собой ММР9 или ММР2. В другом конкретном варианте осуществления изобретения протеаза представляет собой матриптазу. В одном из вариантов осуществления изобретения расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность RQARVVNG (SEQ ID NO: 36).
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, первый антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, который выбран из группы, состоящей из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, первый антигенсвязывающий фрагмент содержит гиперварибельные участки (CDR) тяжелой цепи, имеющие SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и CDR легкой цепи, имеющие SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 55.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 157, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 158.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 47, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 55.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 157, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 158.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 113, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 114.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи любого из антител, описанных в WO/2006/082515, которая полностью включена в настоящее описание в качестве ссылки.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, содержащий аминокислотную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 32, и вариабельную область легкой цепи, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 33.
В одном из вариантов осуществления изобретения в активируемой протеазой активирующей Т-клетки биспецифической молекуле, указанной в настоящем описании, второй антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 32, и легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 33.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, и второй и третий антигенсвязывающие фрагменты, которые обладают способностью специфически связываться с HER2, где второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 160, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161, где третий антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 159, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 2;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 1.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 4;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 1.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) по меньшей мере одну тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 32;
(б) по меньшей мере одну легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 34.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 72;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 1.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 85;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 1.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 73;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 3;
(в) первую легкую цепь, содержащую аминокислотную последовательность SEQ IDNO: 1; и
(г) вторую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 74.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 77;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 82;
(в) первую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 78; и
(г) вторую легкую цепь, содержащую аминокислотную последовательность SEQ IDNO: 81.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 76;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 77;
(в) первую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 78; и
(г) вторую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 79.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 132;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 136;
(в) первую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 81; и
(г) вторую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 133.
В одном из конкретных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, указанная в настоящем описании, содержит
(а) первую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 137;
(б) вторую тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 139;
(в) первую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 81; и
(г) вторую легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 138.
Одним из объектов изобретения является идиотипспецифический полипептид для обратимого сокрытия антигенсвязывающего сайта молекулы антитела к CD3. В одном из вариантов осуществления изобретения идиотипспецифический полипептид представляет собой антиидиотипический scFv. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через линкер. В одном из вариантов осуществления изобретения линкер представляет собой пептидный линкер. В одном из вариантов осуществления изобретения линкер представляет собой расщепляемый протеазой линкер. В одном из вариантов осуществления изобретения пептидный линкер содержит по меньшей мере один сайт, распознаваемый протеазой. В одном из вариантов осуществления изобретения протеазу выбирают из группы, которая состоит из металлопротеиназы, например, матричной металлопротеиназы (ММР) 1-28 и «дезинтегрина и металлопротеиназы» (ADAM) 2, 7-12, 15, 17-23, 28-30 и 33, сериновой протеазы, например, активатора плазминогена урокиназного типа и матриптазы, цистеиновой протеазы, аспарагиновой протеазы и протеазы катепсина.
В одном из конкретных вариантов осуществления изобретения протеаза представляет собой ММР9 или ММР2. В другом конкретном варианте осуществления изобретения протеаза представляет собой матриптазу. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через несколько линкеров. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через два линкера.
В одном из вариантов осуществления изобретения молекула, которая содержит антигенсвязывающий сайт антитела к CD3, представляет собой активирующую Т-клетки биспецифическую молекулу. В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21); и
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22).
В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(б) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(в) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21);
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22);
и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27); и
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28).
В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(б) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(в) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27);
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28);
и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
Другим объектом изобретения является выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или его фрагмент. Изобретение относится также к полипептидам, которые кодируются полинуклеотидами, предлагаемыми в изобретении. Изобретение относится также к экспрессионному вектору, который содержит выделенный полинуклеотид, предлагаемый в изобретении, и клетке-хозяину, которая содержит выделенный полинуклеотид или экспрессионный вектор, предлагаемый в изобретении. В некоторых вариантах осуществления изобретения клетка-хозяин представляет собой эукариотическую клетку, в частности, клетку млекопитающего.
Другим объектом изобретения является способ получения активируемой протеазой (активирующей) Т-клетки молекулы, предлагаемой в изобретении, который включает стадии а) культивирования клетки-хозяина, предлагаемой в изобретении, в условиях, пригодных для экспрессии активируемой протеазой (активирующей) Т-клетки молекулы, и (б) выделения активируемой протеазой (активирующей) Т-клетки молекулы. Изобретение относится также к активируемой протеазой (активирующей) Т-клетки молекуле, полученной способом, предлагаемым в изобретении.
Другим объектом изобретения является способ получения идиотипспецифического полипептида, предлагаемого в изобретении, который включает стадии а) культивирования клетки-хозяина, предлагаемой в изобретении, в условиях, пригодных для экспрессии активируемой протеазой (активирующей) Т-клетки молекулы, и (б) выделения идиотипспецифического полипептида. Изобретение относится также к полученному способом, предлагаемым в изобретении, идиотипспецифическому полипептиду.
Изобретение относится также к фармацевтической композиции, которая содержит активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, и фармацевтически приемлемый носитель.
Под объем изобретения подпадают также способы применения активируемой протеазой (активирующей) Т-клетки молекулы и фармацевтической композиции, предлагаемой в изобретении. Одним из объектов изобретения является активируемая протеазой (активирующая) Т-клетки молекула или фармацевтическая композиция, предлагаемая в изобретении, предназначенная для применения в качестве лекарственного средства. Одним из объектов изобретения является активируемая протеазой (активирующая) Т-клетки молекула или фармацевтическая композиция, предлагаемая в изобретении, предназначенная для применения для лечения заболевания у индивидуума, который нуждается в этом. В конкретном варианте осуществления изобретения заболевание представляет собой рак.
Предложено также применение активируемой протеазой (активирующей) Т-клетки молекулы, предлагаемой в изобретении, для приготовления лекарственного средства, предназначенного для лечения заболевания у индивидуума, который нуждается в этом; а также способ лечения заболевания у индивидуума, включающий введение указанному индивидууму в терапевтически эффективном количестве композиции, которая содержит активируемую протеазой (активирующую) Т-клетки молекулу, предлагаемую в изобретении, в фармацевтически приемлемой форме. В конкретном варианте осуществления изобретения заболевание представляет собой рак. В любом из указанных выше вариантов осуществления изобретения индивидуум предпочтительно представляет собой млекопитающее, прежде всего человека.
В изобретении предложен также способ индукции лизиса клетки-мишени, прежде всего опухолевой клетки, включающий приведение в контакт клетки-мишени с активируемой протеазой (активирующей) Т-клетки молекулой, предлагаемой в изобретении, в присутствии Т-клетки, прежде всего цитотоксической Т-клетки.
Другим объектом изобретения является также композиция, которая содержит активируемую протеазой активирующую Т-клетки биспецифическую молекулу, указанную в настоящем описании, и фармацевтически приемлемый носитель.
Другим объектом изобретения является также композиция, которая содержит идиотипспецифический полипептид, указанный в настоящем описании, и фармацевтически приемлемый носитель.
Другим объектом изобретения является также активируемая протеазой активирующая Т-клетки биспецифическая молекула или идиотипспецифический полипептид, указанные в настоящем описании, или композиция, указанная в настоящем описании, предназначенные для применения в качестве лекарственного средства. В одном из вариантов осуществления изобретения лекарственное средство предназначено для лечения или замедления развития рака, лечения или замедления развития связанного с иммунной системой заболевания и/или повышения или стимуляции иммунного ответа или функции у индивидуума.
Другим объектом изобретения является также активируемая протеазой активирующая Т-клетки биспецифическая молекула или идиотипспецифический полипептид, указанные в настоящем описании, предназначенные для лечения заболевания у индивидуума, который нуждается в этом. В одном из вариантов осуществления изобретения заболевание представляет собой пролиферативное нарушение, прежде всего рак.
Другим объектом изобретения является также способ лечения заболевания у индивидуума, включающий введение указанному индивидууму в терапевтически эффективном количестве композиции, которая содержит активируемую протеазой активирующую Т-клетки биспецифическую молекулу или композицию, указанную в настоящем описании.
Другим объектом изобретения является также способ индукции лизиса клетки-мишени, включающий приведение к контакт клетки-мишени с активируемой протеазой активирующей Т-клетки биспецифической молекулой или композицией, указанной в настоящем описании, в присутствии Т-клетки. В одном из вариантов осуществления изобретения способ индукции лизиса клетки-мишени представляет собой способ in vitro. В одном из вариантов осуществления изобретения клетка-мишень представляет собой раковую клетку. В одном из вариантов осуществления изобретения клетка-мишень экспрессирует протеазу, которая обладает способностью активировать активируемую протеазой активирующую Т-клетки биспецифическую молекулу.
Другим объектом изобретения является также антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент, специфические в отношении идиотипа анти-CD3 антигенсвязывающей молекулы, где антиидиотипическое антитело к CD3 или его фрагмент при связывании с анти-CD3 антигенсвязывающей молекулой специфически блокируют связывание анти-CD3 антигенсвязывающей молекулы с CD3.
В одном из вариантов осуществления изобретения антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент обратимо ассоциированы с анти-CD3 антигенсвязывающей молекулой через пептидный линкер, который содержит распознаваемый протеазой сайт. В одном из вариантов осуществления изобретения CD3 представляет собой мышиный, обезьяний или человеческий CD3.
Другим объектом изобретения является способ снижения токсичности in vivo активирующей Т-клетки биспецифической молекулы, который включает присоединение идиотипспецифического полипептида, указанного в настоящем описании, к активирующей Т-клетки биспецифической молекуле с помощью расщепляемого протеазой линкера с образованием активируемой протеазой активирующей Т-клетки биспецифической молекулы, где активируемая протеазой активирующая Т-клетки биспецифическая молекула имеет пониженную токсичность in vivo по сравнению с активирующей Т-клетки биспецифической молекулой.
Краткое описание чертежей
На чертежах показано:
на фиг. 1А-Д - схематическое изображение различных связывающих CD3 агентов с маскирующими фрагментами. На фиг. А1 - конструкция 7859: анти-ID (антиидиотипический) СН2527 scFv 4.15.64, сайт, распознаваемый матриптазой MK062, CD3 Fc. На фиг. 1Б - конструкция 7860: анти-ID СН2527 scFv 4.32.63, сайт, распознаваемый матриптазой MK062, CD3 Fc. На фиг. 1В - конструкция 7857: анти-ID СН2527 scFv 4.15.64, нерасщепляемый линкер, CD3 Fc. На фиг. 1Г - конструкция: ID (идентификационный номер) 7858 анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, CD3 Fc. На фиг. 1Д - конструкция 7861: одновалентное антитело к CD3, Fc;
на фиг. 2 - таблица, в которой обобщены данные об аффинностях антиидиотипических маскирующих фрагментов к связывающему CD3 агенту (СН2527);
на фиг. 3А-Г - результаты анализа методом капиллярного электрофореза в присутствии ДСН молекул, представленных на фиг. 1А и Б. На фиг. 3А-Б -результаты анализа методом капиллярного электрофореза в присутствии ДСН молекулы, представленной на фиг. 1А, в невосстанавливающих (фиг. 3А) и восстанавливающих (фиг. 3Б) условиях. Сравнение необработанной (I) и обработанной молекулы (III) продемонстрировало полное расщепление анти-ID scFv после обработки рекомбинантной (rh) матриптазой/ST14 в течение 48 ч при 37°С. Один образец (II) не обрабатывали, но инкубировали при 37°С в течение 48 ч. На фиг. 3В-Г - результаты анализа методом капиллярного электрофореза в присутствии ДСН молекулы, представленной на фиг. 1Б, в невосстанавливающих (фиг. 3В) и восстанавливающих (фиг. 3Г) условиях. Сравнение необработанной (I) и обработанной молекулы (III) продемонстрировало полное расщепление анти-ID scFv после обработки rh-матриптазой/ST14 в течение 48 ч при 37°С. Один образец (II) не обрабатывали, но инкубировали при 37°С в течение 48 ч;
на фиг. 4А-В - воздействие антиидиотипической маскировки на связывание CD3. На фиг. 4А и В - результаты репортерных анализов с использованием Jurkat NFAT, демонстрирующие маскирующий эффект антиидитипического специфического по отношению к CD3 scFv 4.15.64 (фиг. 4А) или антиидиотипического специфического по отношению к CD3 scFv 4.32.63 (фиг. 4Б). Одновалентные IgG к CD3 перекрестно сшивали через антитело к человеческому Fc-домену (нанесенному на планшет для анализа) перед добавление клеток Jurkat NFAT (репортерная клеточная линия острого лимфатического лейкоза с промотором NFAT, экспрессирующая человеческую CD3ε (ε-субъединицу человеческого CD3)). Репортерная клеточная линия Jurkat-NFAT (фирма Promega) представляет собой репортерную клеточную линию человеческого острого лимфатического лейкоза с промотором NFAT, которая экспрессирует человеческую CD3ε. Если CD3-связывающий агент связывается с CD3ε, то происходит экспрессия люциферазы и ее можно измерять по люминисценции после добавления субстрата One-Glo (фирма Promega). На фиг. 4В представлены результаты сравнения величин ЕС50, характеризующих связывание с CD3ε, для замаскированного  и незамаскированного CD3-связывающего агента;
и незамаскированного CD3-связывающего агента;
на фиг. 5А-З - схематическое изображение различных (активирующих) Т-клетки биспецифических молекул с маскирующими фрагментами. На фиг. 5А - конструкция 7344: анти-ID СН2527 scFv 4.15.64, сайт, распознаваемый матриптазой МК062, CD3 16D5 Fc. На фиг. 5Б - конструкция 7676: анти-ID СН2527 scFv 4.15.64, нерасщепляемый линкер, CD3 16D5 Fc. На фиг. 5В - конструкция 7496: анти-ID СН2527 scFv 4.32.63, сайт, распознаваемый матриптазой MK062, CD3 16D5 Fc. На фиг. 5Г - конструкция 7611: анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, CD3 16D5 Fc. На фиг. 5Д - конструкция 6298: GA916-D-16D5-02 sf W(1). FoIR1 16D5 классическая ТСВ (активирующая Т-клетки биспецифическая молекула) в формате 2+1 с общей легкой цепью. На фиг. 5Е - конструкция 6100: GA916-D-16D5 sf W(3a). FolR1 16D5 инвертированная ТСВ в формате 2+1 с общей легкой цепью. На фиг. 5Ж - конструкция ID 6182: DP47GS ТСВ sf СНО W(9a). DP47 инвертированная ТСВ в формате 2+1. На фиг. 5З - конструкция 7494: анти-ID СН2527 Fab 4.15.64, сайт, распознаваемый матриптазой MK062, CD3 16D5 Fc;
на фиг. 6 - результаты применения для трансфекции первого соотношения плазмид, полученные с помощью гель-фильтрации (1 («впадина»): 1 («выступ»): 3 (CLC) (общая легкая цепь);
на фиг. 7 - результаты применения для трансфекции второго соотношения плазмид, полученные с помощью гель-фильтрации (1 («впадина»): 2 («выступ»): 3 (CLC);
на фиг. 8 - результаты, полученные с помощью анализа методом капиллярного электрофореза в присутствии ДСН (КЭ-ДСН), ТСВ-молекулы, представленной на фиг. 5А (ID 7344) (полностью очищенный препарат): Полоса А = невосстанавливающие условия, полоса Б = восстанавливающие условия, полоса В = белковый стандарт;
на фиг. 9 - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ-молекулы, представленной на фиг. 5Б (ID 7676) (полностью очищенный препарат): Полоса А = невосстанавливающие условия, полоса Б = восстанавливающие условия, полоса В = белковый стандарт;
на фиг. 10 - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ-молекулы, представленной на фиг. 5В (ID 7496) (полностью очищенный препарат): Полоса А = невосстанавливающие условия, полоса Б = восстанавливающие условия, полоса В = белковый стандарт;
на фиг. 11 - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ-молекулы, представленной на фиг. 5Г (ID 7611) (полностью очищенный препарат): Полоса А = невосстанавливающие условия, полоса Б = восстанавливающие условия, полоса В = белковый стандарт;
на фиг. 12А-Г - результаты, полученные с помощью анализа методом капиллярного электрофореза в присутствии ДСН, молекул, представленных на фиг. 5А и В. На фиг. 12А и Б - результаты, полученные с помощью анализа методом капиллярного электрофореза, молекул, представленных на фиг. 5А (ID 7344) анти-ID СН2527 scFv 4.15.64, MK062, CD3 16D6 Fc, в невосстанавливающих (фиг. 12А) и восстанавливающих (фиг. 12Б) условиях. Сравнение необработанной (I) и обработанной (III) молекулы продемонстрировало полное расщепление анти-ID scFv после обработки rh-матриптазой/STH в течение 48 ч при 37°С. Один образец (II) не обрабатывали, но инкубировали при 37°С в течение 48 ч. Применяли предварительное окрашивание белковым маркером (IV) Mark 12 (фирма Invitrogen) для определения правильной молекулярной массы. На фиг. 12В и Г - результаты, полученные с помощью анализа методом капиллярного электрофореза, молекулы, представленной на фиг. 5В (ID 7496) анти-ID СН2527 scFv 4.32.63 MK062 CD3 16D6 Fc, в невосстанавливающих (фиг. 12В) и восстанавливающих (фиг. 12Г) условиях. Сравнение необработанной (I) и обработанной (III) молекулы продемонстрировало полное расщепление анти-ID scFv после обработки rh-матриптазой/БТИ в течение 48 ч при 37°С. Один образец (II) не обрабатывали, но инкубировали при 37°С в течение 48 ч. Применяли предварительное окрашивание белковым маркером (IV) Mark 12 (фирма Invitrogen) для определения правильной молекулярной массы;
на фиг. 13 - данные об уровне экспрессии FolR1, количественно установленные с помощью набора Qifikit (фирма Dako). Антитело к FolR1: № LS-C125620-100 (фирма LifeSpan Biosciences Inc); примененное в концентрации 20 мкг/мл; мышиный IgG1-изотип: №554121 (фирма BD);
на фиг. 14А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 14А - данные о цитолизе клеток Skov3, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 10 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 клонами, расщепляемым и нерасщепляемым линкером, предварительно обработанные очищенной rh-матриптазой/ST14) и человеческими РВМС после инкубации в течение 48 ч (Е:Т=7:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°C. На фиг. 14Б продемонстрирована активация Т-клеток из человеческих РВМС, индуцированная связыванием активируемой протеазой ТСВ в концентрации 10 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 фрагментами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) на клетках Skov3 после инкубации в течение 48 ч (Е:Т=7:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 15А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 15А - данные о цитолизе клеток Mkn-45, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 100 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 клонами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) и человеческими РВМС после инкубации в течение 48 ч (Е:Т=7:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. На фиг. 15Б продемонстрирована активация Т-клеток из человеческих РВМС, индуцированная связыванием активируемой протеазой ТСВ в концентрации 100 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 фрагментами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) на клетках Mkn-45 после инкубации в течение 48 ч (Е:Т=7:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 16 - данные о цитолизе клеток НТ29, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 10 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 клонами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) и человеческими РВМС после инкубации в течение 48 ч (Е:Т=7:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/БТИ (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. Столбиками слева направо обозначены следующие конструкции: 7344: анти-ID СН2527 scFv 4.15.64 MK062 CD3 16D6Fc; 7344: анти-ID СН2527 scFv 4.15.64 MK062 CD3 160Fc_обработанная; 7676: анти-ID СН2527 scFv 4.15.64 нерасщепляемый линкер CD3 16D6Fc; 7496: анти-ID СН2527 scFv 4.32.63 MK062 CD3 16D6 Fc; 7496: анти-ID CH2527 scFv 4.32.63 MK062 CD3 16D6 Fc_обработанная; 7611: анти-ID CH2527 scFv 4.32.63 нерасщепляемый линкер CD3 16D6 Fc; 6298: GA916-D-16D5-02 sf W(1); 6182: DP47GS TCB sf CHO W(9a);
на фиг. 17 - данные о цитолизе клеток Skov3, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 10 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 клонами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) и человеческими РВМС (РВМС из другого донора по сравнению с тем, клетки которого использовали при получении результатов, представленных на фиг. 14А) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли за 24 ч при 37°C. Столбиками слева направо обозначены следующие конструкции: 7344: анти-ID СН2527 scFv 4.15.64, МК062, CD3 16D6Fc; 7344: анти-ID СН2527 scFv 4.15.64, MK062, CD3 1606Fc_обработанная; 7676: анти-ID СН2527 scFv 4.15.64 нерасщепляемый линкер CD3 16D6Fc; 7496: анти-ID СН2527 scFv 4.32.63 MK062 CD3 16D6 Fc; 7496: анти-ID CH2527 scFv 4.32.63 MK062 CD3 16D6 Fc_обработанная; 7611: анти-ID CH2527 scFv 4.32.63 нерасщепляемый линкер CD3 16D6 Fc; 6298: GA916-D-16D5-02 sf W(1); 6182: DP47GS TCB sf CHO W(9a);
на фиг. 18A и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 18А - данные о цитолизе в зависимости от дозы клеток HeLa, индуцируемом активируемыми протеазой молекулами ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. На фиг. 18Б - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС, индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках HeLa после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 19А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 19А - данные о цитолизе в зависимости от дозы клеток HeLa, индуцируемом активируемыми протеазой молекулами ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым или нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. На фиг. 19Б - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС, индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках HeLa после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 20А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 20А - данные о цитолизе в зависимости от дозы клеток Skov3, индуцируемом активируемыми протеазой молекулами ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. На фиг. 20Б - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС, индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках Skov3 после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и С08+-Т-клеток;
на фиг. 21А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 21А - данные о цитолизе в зависимости от дозы клеток Skov3, индуцируемом активируемыми протеазой молекулами ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым или нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С. На фиг. 21Б - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС, индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках Skov3 после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 22А и Б - результаты оценки активации Т-клеток активируемыми протеазой ТСВ. На фиг. 22А - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС (из донора, отличного от донора, клетки которого использовали в описанных ранее экспериментах), индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках НТ29 после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток. На фиг. 22Б - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС (из другого донора по сравнению с тем, клетки которого использовали при получении результатов, представленных на фиг. 16), индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках НТ29 после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток.
на фиг. 23 - данные об активации в зависимости от дозы Т-клеток из человеческих РВМС (из донора, отличного от донора, клетки которого использовали в описанных ранее экспериментах), индуцированной связыванием активируемой протеазой ТСВ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым или нерасщепляемым линкером, обработанная молекула) на клетках HRCEpiC после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Маркеры Т-клеточной активации представляли собой CD25 (левые панели) и CD69 (правые панели). Представлены данные для CD4+- и CD8+-Т-клеток;
на фиг. 24 - данные о цитолизе клеток Ovcar3, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 50 нМ (ТСВ с различными маскирующими антиидиотипическими специфическими по отношению к CD3 клонами, расщепляемым и нерасщепляемым линкером, обработанные молекулы) и человеческими РВМС после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 10 мин при 37°C (неполное расщепление);
на фиг. 25 - данные о цитолизе клеток Skov3, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 10 нМ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.15.64, расщепляемым и нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС из трех других доноров). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч 37°С;
на фиг. 26 - данные о цитолизе клеток Skov3, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 10 нМ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым и нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС из трех других доноров). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С;
на фиг. 27 - данные о цитолизе клеток HeLa, индуцированном активируемыми протеазой молекулами ТСВ в концентрации 100 пМ (ТСВ с маскирующим антиидиотипическим специфическим по отношению к CD3 клоном 4.32.63, расщепляемым и нерасщепляемым линкером, обработанная молекула) и человеческими РВМС (выделенными из лейкоцитарной пленки) после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС из трех других доноров). Предварительную обработку rh-матриптазой/ST14 (фирма R&D Systems) осуществляли в течение 24 ч при 37°С;
на фиг. 28 - схематическое изображение конструкции анти-ID GA201 scFv, сайт, распознаваемый матричной металлопротеиназой, GA201 Fc (ОА201-анти-GA201-scFv);
на фиг. 29 - схематическое изображение антитела к HER1 GA201;
на фиг. 30А и Б - результаты, полученные с помощью анализа методом капиллярного электрофореза в присутствии ДСН, для молекулы, представленной на фиг. 28, в невосстанавливающих (фиг. 30А) и восстанавливающих условиях (фиг. 30Б). Молекулу, представленную на фиг. 28, очищали до гомогенного состояния на белке А и с помощью гель-фильтрации и подвергали анализом методом капиллярного электрофореза-ДСН;
на фиг. 31 - результаты FACS-анализа связывания GA201-анти-GA201-scFv и GA201 с HER1, который экспрессируется на клетках Н322М, для подтверждения маскирующего эффекта антиидиотипического GA201 scFv. GA201-aHTH-GA201-scFv инкубировали в течение ночи с матриксной металлопротеиназой ММР-2 и связывание с клетками Н322М сравнивали с нерасщепленной конструкцией GA201-анти-GA201-scFv, GA201 и антителом, применяемым в качестве контроля изотипа IgG1. Связывание с HER1 на клетках Н322М выявляли, используя в качестве вторичного антитела F(ab')2-фрагмент козьего античеловеческого IgG, Fc-специфического, конъюгированного с ФИТЦ, и анализировали с использованием FACS, применяя устройство BD FACS Canto II. Для анализа использовали медианную интенсивность флуоресценции (MFI);
на фиг. 32 - результаты, полученные методом поверхностного плазменного резонанса, анализа связывания HER1  с замаскированным и незамаскированным GA201 до и после расщепления с помощью ММР2;
с замаскированным и незамаскированным GA201 до и после расщепления с помощью ММР2;
на фиг. 33А-К - схематическое изображение различных (активирующих) Т-клетки биспецифических молекул с маскирующими фрагментами. На фиг. 33А - конструкция ID 8364: 16D5 ТСВ, классический формат, анти-ID СН2527 scFv 4.32.63 сайт ММР9-матриптазы MK062, слитый на N-конце с CD3. На фиг. 33Б - конструкция: ID 8363. 16D5 ТСВ, классический формат, анти-ID СН2527 scFv 4.32.63, сайт катепсина S/B, слитый на N-конце с CD3. На фиг. 33В - конструкция: ID 8365. 16D5 ТСВ, инвертированный формат, анти-ID СН2527 scFv 4.32.63, сайт матриптазы MK062, слитый на N-конце с общей легкой цепью. На фиг. 33Г - конструкция: ID 8366. 16D5 ТСВ, инвертированный формат, анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, слитый на N-конце с общей легкой цепью. На фиг. 33Д - конструкция: ID 8672. Антитело к мезотелину RG7787 с заряженными остатками ТСВ, классический формат, анти-ID СН2527 scFv 4.32.63 сайт ММР9-матриптазы МК062, слитый на N-конце с CD3 X Fab. На фиг. 33Е - конструкция ID 8673. Антитело с мезотелину RG7787 с ТСВ с заряженными остатками, классический формат, анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, слитый на N-конце с CD3 X Fab. На фиг. 33Ж - конструкция: ID 8674. Антитело к мезотелину RG7787 с ТСВ с заряженными остатками, инвертированный формат, анти-ID СН2527 scFv 4.32.63 сайт ММР9-матриптазы МК.062, слитый на N-конце с CD3 XFab. На фиг. 33З - конструкция: 8675. Антитело к мезотелину RG7787 с ТСВ с заряженными остатками, инвертированный формат, анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, слитый на N-конце с CD3 XFab. На фиг. 33И - конструкция: ID 8505. Антитело к мезотелину RG7787 с ТСВ с заряженными остатками CD3 XFab, инвертированный формат. На фиг. 33К - конструкция: ID 8676. CD3 XFab антитело к мезотелину RG7787 с ТСВ с заряженными остатками, классический формат;
на фиг. 34 - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ ID 8365 и ТСВ ID 8366 (полностью очищенный препарат): полоса А = белковый стандарт, полоса Б = белок, хранившийся при 4°C, полоса В = белок, предварительно обработанный rh-матриптазой/ST14 (фирма R&D Systems), полоса Г = белок, инкубированный в течение 72 ч при 37°С, и полоса Д = молекула 3;
на фиг. 35А и Б - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ, представленной на фиг. 33А (ID 8364) и ТСВ, представленной на фиг. 33Б (ID 8363). На фиг. 35А - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ 8364 (конечный очищенный препарат): полоса А = белковый стандарт, полоса Б = белок, хранившийся при 4°С, полоса В = белок, предварительно обработанный rh-матриптазой/ST14 (фирма R&D Systems), полоса Г = белок, инкубированный в течение 72 ч при 37°C, и полоса Д = конструкция с нерасщепляемым линкером. На фиг. 35Б - результаты, полученные с помощью анализа методом КЭ-ДСН, ТСВ 8363 (полностью очищенный препарат): полоса А = белковый стандарт, полоса Б = белок, хранившийся при 4°С, полоса В = белок, предварительно обработанный rh-матриптазой/ST14 (фирма R&D Systems), полоса Г = белок, инкубированный в течение 72 ч при 37°C, и полоса Д = конструкция с нерасщепляемым линкером;
на фиг. 36А и Б - полученный с использованием клеток Jurkat NFAT анализ активации, в котором в качестве клеток-мишеней применяли клетки HeLa и Skov-3. Каждая точка соответствует среднему значению, полученному по трем повторностям. Стандартное отклонение обозначено планками погрешностей. Репортерная клеточная линия Jurkat-NFAT (фирма Promega) представляет собой репортерную клеточную линию человеческого острого лимфатического лейкоза с промотором NFAT, которая экспрессирует человеческую CD3ε. Если CD3 связывающий агент ТСВ ТСВ связывается с опухолью-мишенью и CD3 (необходимо перекрестное сшивание) связывается с CD3ε, то экспрессию люциферазы можно измерять по люминисценции после добавления субстрата One-Glo (фирма Promega). Сравнивали FolR1-ТСВ (черные треугольники с направленной вниз вершиной) и предварительно обработанную протеазой активируемую ТСВ (8364, закрашенные серыми цветом квадраты), слитую на N-конце с анти-ID CD3 4.32.63 scFv и с сайтом ММР9-матриптазы MK062. Молекулу обрабатывали rh-матриптазой/ST14 (фирма R&D Systems) в течение примерно 20 ч при 37°C. Представлены также результаты, полученные для замаскированной ТСВ (содержащей нерасщепляемый линкер GS, серые треугольники с направленной вверх вершиной) и «ненацеленную» ТСВ, применяемую в качестве контроля (незакрашенный треугольник с направленной вниз вершиной). Пунктирной линией обозначена люминисценция клеток-мишеней и эффекторных клеток в отсутствии какой-либо ТСВ. На фиг. 36А - полученный с использованием клеток Jurkat NFAT анализ активации, в котором в качестве клеток-мишеней применяли клетки HeLa. На фиг. 36Б - полученный с использованием клеток Jurkat NFAT анализ активации, в котором в качестве клеток-мишеней применяли клетки Skov-3;
на фиг. 37А-Г - данные о цитотоксичности в отношении опухолевых клеток, обусловленной FolR1-TCB и человеческими РВМС (соотношение эффекторов : мишеней = 10: 1). Каждая точка соответствует среднему значению, полученному по трем повторностям. Стандартное отклонение обозначено планками погрешностей. На фиг. 37А - данные о цитотоксичности в отношении клеток-мишеней HeLa. Осуществляли сравнение двух различных форматов активируемых протеазой ТСВ, оба содержали антиидиотипический CD3 scFv, сцепленный с линкером с сайтом, распознаваемым матриптазой MK062. На фиг. 37Б - данные о цитотоксичности в отношении клеток-мишеней Skov-3. Осуществляли сравнение двух различных форматов активируемых протеазой ТСВ, оба содержали антиидиотипический CD3 scFv, сцепленный с линкером с сайтом, распознаваемым матриптазой MK062. На фиг. 37В - данные о цитотоксичности в отношении клеток-мишеней HeLa. Осуществляли сравнение классической активируемой протеазой ТСВ, содержащей антиидиотипический CD3 scFv и GS-линкеры с различными сайтами, распознаваемыми протеазой. Сравнивали активируемую протеазой ТСВ, содержащую линкер с сайтом ММР9-матриптазы MK062 (8364, серые квадраты), FolR1-TCB (светло-серые треугольники с направленной вниз вершиной), активируемую протеазой ТСВ, содержащую линкер только с сайтом матриптазы MK062 (светло-серый ромб)/сайтом катепсина (серые кружки) или нерасщепляемый линкер (черные треугольники с направленной вниз вершиной). На фиг. 37Г - данные о цитотоксичности в отношении клеток-мишеней Skov-3. Осуществляли сравнение классической активируемой протеазой ТСВ, содержащей антиидиотипический CD3 scFv и GS-линкеры с различными сайтами, распознаваемыми протеазой. Сравнивали активируемую протеазой ТСВ, содержащую линкер с сайтом ММР9-матриптазы MK062 (8364, серые квадраты), FolR1-TCB (светло-серые треугольники с направленной вниз вершиной), активируемую протеазой ТСВ, содержащую линкер только с сайтом матриптазы MK062 (светло-серый ромб)/сайтом катепсина (серые кружки) или нерасщепляемый линкер (черные треугольники с направленной вниз вершиной);
на фиг. 38А и Б - результаты количественной оценки позитивных по CD69 CD8-клеток после совместной инкубации первичных эпителиальных клеток коркового вещества почек человека (фиг. 38А) или бронхиальных эпителиальных клеток человека (фиг. 38Б) с различными ТСВ в концентрации 200 нМ и полученными из трех различных доноров человеческими РВМС. Т-клетки окрашивали после инкубации в течение 48 ч (Е:Т=10:1, эффекторные клетки представляли собой человеческие РВМС). Представлена медианная интенсивность флуоресценции маркера Т-клеточной активации CD69 в популяции CD8+-Т-клеток. Каждая точка соответствует среднему значению, полученному по трем повторностям для РВМС из трех различных доноров. Стандартное отклонение обозначено планками погрешностей. Для статистического анализа использовали непарный t-критерий;
на фиг. 39А и Б - данные о цитотоксичности в отношении опухолевых клеток, обусловленной MSLN-(мезотелин)-ТСВ и человеческими РВМС (соотношение эффекторов : мишеней = 10:1). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч перед определением ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ. Каждая точка соответствует среднему значению, полученному по трем повторностям. Стандартное отклонение обозначено планками погрешностей. На фиг. 39А - данные о цитотоксичности в отношении клеток-мишеней NCI Н596. Активируемая протеазой MSLN-TCB содержала антиидиотипический CD3 scFv, сцепленный с линкером с сайтом ММР9-матриптазы MK062. Сравнивали активируемую протеазой ТСВ (8672, светло-серые кружки), MSLN-TCB (темно-серые треугольники с направленной вниз вершиной) и актируемую протеазой ТСВ, содержащую нерасщепляемый линкер (8673, серые треугольники с направленной вверх вершиной). На фиг. 39Б - данные о цитотоксичности в отношении клеток-мишеней AsPC-1. Активируемая протеазой MSLN-TCB содержала антиидиотипический CD3 scFv, сцепленный с линкером с сайтом ММР9-матриптазы MK062. Сравнивали активируемую протеазой ТСВ (8672, светло-серые кружки), MSLN-TCB (темно-серые треугольники с направленной вниз вершиной) и актируемую протеазой ТСВ, содержащую нерасщепляемый линкер (8673, серые треугольники с направленной вверх вершиной);
на фиг. 40 - полученный с использованием клеток Jurkat NFAT анализ активации, в котором применяли образцы первичных опухолей и активируемые протеазой FolR1-TCB. Репортерные клетки Jurkat NFAT активировались после совместной инкубации с FolR1-TCB (6298) и активируемой протеазой FolR1-ТСВ, содержащей сайт расщепления ММР9-матриптазой (8364). Активируемые протеазой FolR1-TCB (8363, 8408) и контрольные ТСВ (8409, 7235) не индуцировали экспрессию люциферазы. Пунктирной линией обозначена базисная линия люминисценции для клеток Jurkat NFAT, которые совместно инкубировали с опухолью;
на фиг. 41А-В - полученные с помощью капиллярного электрофореза данные для активируемых протеазой ТСВ после инкубации в человеческой сыворотке. Молекулы инкубировали в течение 0 или 14 дней в истощенной по человеческому IgG сыворотке при 37°С во влажной камере (5% СО2). Все молекулы очищали с помощью аффинной хроматографии (белок А) и затем анализировали с помощью капиллярного электрофореза. На фиг. 41А - результаты КЭ-ДСН-анализа сыворотки для определения FolR1-TCB (6298) в сыворотке в день 0 и день 14. На фиг. 41Б - результаты КЭ-ДСН-анализа сыворотки для определения активируемой протеазой FolR1-TCB с линкером с сайтом ММР9-матриптазы (8364) в сыворотке в день 0 и день 14. На фиг. 41В - результаты КЭ-ДСН-анализа сыворотки для определения активируемой протеазой FolR1-TCB с линкером с сайтом матриптазы (8408) в сыворотке в день 0 и день 14 и предварительно расщепленной молекулы в сыворотке;
на фиг. 42А-Е - схематическое изображение различных (активирующих) Т-клетки биспецифических молекул с маскирующими фрагментами. На фиг. 42А -конструкция: ID 8955. Herceptarg-TCB, классический формат, анти-ID СН2527 scFv 4.32.63, линкер с MK062-ММР9, слитый на N-конце с VH. На фиг. 2Б - конструкция: ID 8957. Herceptarg-TCB, классический формат, анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, слитый на N-конце с VH. На фиг. 42В - конструкция: ID 8959. Herceptarg-TCB, классический формат. На фиг. 42Г - конструкция: ID 8997. FolR1 36F2-TCB, классический формат, анти-ID СН2527 scFv 4.32.63, линкер с МК062 ММР9, слитый на N-конце с VH. На фиг. 42Д - конструкция: ID 8998. FolR1 36F2-TCB, классический формат, анти-ID СН2527 scFv 4.32.63, нерасщепляемый линкер, слитый на N-конце с VH. На фиг. 42Е - конструкция: ID 8996. FolR1 36F2-TCB, классический формат;
на фиг. 43 - данные о токсичности в отношении бронхиальных эпителиальных клеток человека, опосредуемой человеческими РВМС и ТСВ в концентрации 100 или 10 нМ. Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч перед определением ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ. Каждая точка соответствует среднему значению, полученному по трем повторностям. Стандартное отклонение обозначено планками погрешностей;
на фиг. 44 - данные о цитотоксичности в отношении негативных по FolR1 клеток-мишеней (Mkn-45), опосредуемой FolR1-TCB в концентрации 100 нМ и человеческими РВМС. Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч перед определением ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ. Каждая точка соответствует среднему значению, полученному по трем повторностям. Стандартное отклонение обозначено планками погрешностей.
Подробное описание изобретения
Определения
Понятия, применяемые в настоящем описании, имеют значения, общепринятые в данной области, если специально не указано иное.
В контексте настоящего описания понятие «антигенсвязывающая молекула» в наиболее широком смысле относится к молекуле, которая специфически связывается с антигенной детерминантой. Примерами антигенсвязывающих молекул являются иммуноглобулины и их производные, например, их фрагменты.
Понятие «биспецифическая» означает, что антигенсвязывающая молекула обладает способностью специфически связываться по меньшей мере с двумя различными антигенными детерминантами. Как правило, биспецифическая антигенсвязывающая молекула содержит два антигенсвязывающих сайта, каждый из которых является специфическим в отношении различных антигенных детерминант. В некоторых вариантах осуществления изобретения биспецифическая антигенсвязывающая молекула обладает способностью одновременно связываться с двумя антигенными детерминантами, прежде всего с двумя антигенными детерминантами, эксирессируемыми на двух различных клетках.
В контексте настоящего описания понятие «валентность» означает наличие определенного количества антигенсвязывающих сайтов в антигенсвязывающей молекуле. Так, понятие «одновалентное связывание с антигеном» означает наличие одного (и не более одного) специфического в отношении антигена антигенсвязывающего сайта в антигенсвязывающей молекуле.
Понятие «антигенсвязывающий сайт» относится к сайту, т.е. одному или нескольким аминокислотным остаткам антигенсвязывающей молекулы, которые обеспечивают взаимодействие с антигеном. Например, антигенсвязывающий сайт антитела содержит аминокислотные остатки из гипервариабельных участков (определяющих комплементарность участков) (CDR). Нативная молекула иммуноглобулина имеет, как правило, два антигенсвязывающих сайта, молекула Fab, как правило, имеет один антигенсвязывающий сайт.
В контексте настоящего описания понятие «антигенсвязывающий фрагмент» относится к полипептидной молекуле, которая специфически связывается с антигенной детерминантой. В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент обладает способностью направлять субстанцию, к которой он присоединен (например, второй антигенсвязывающий фрагмент), к сайту-мишени, например, к специфическому типу опухолевой клетки или стромы опухоли, несущей антигенную детерминанту. В другом варианте осуществления изобретения антигенсвязывающий фрагмент обладает способностью активировать передачу сигналов через его антиген-мишень, например, антиген комплекса Т-клеточного рецептора. Антигенсвязывающие фрагменты включают антитела и их фрагменты, дополнительно описанные ниже. Конкретные антигенсвязывающие фрагменты включают антигенсвязывающий домен антитела, который содержит вариабельную область тяжелой цепи антитела и вариабельную область легкой цепи антитела. В некоторых вариантах осуществления изобретения антигенсвязывающие фрагменты могут включать константные области антитела, что дополнительно описано ниже и известно в данной области. Пригодные константные области тяжелых цепей включают любые из пяти изотипов: α, δ, ε, γ или μ. Пригодные константные области легких цепей включают любые из двух изотипов: κ и λ.
В контексте настоящего описания понятие «антигенная детерминанта» является синонимом понятий «антиген» и «эпитоп» и относится к сайту (например, участку, состоящему из смежных аминокислот, или конформационной конфигурации, состоящей из различных областей несмежных аминокислот) на полипептидной макромолекуле, с которой связывается антигенсвязывающий фрагмент с образованием комплекса антигенсвязывающий фрагмент-антиген. Пригодные антигенные детерминанты могут присутствовать, например, на поверхности опухолевых клеток, на поверхности инфицированных вирусом клеток, на поверхности других больных клеток, на поверхности иммунных клеток, клеток, находящихся в свободном состоянии в сыворотке крови и/или во внеклеточном матриксе (ЕСМ). В контексте настоящего описания белки, относящиеся к антигенам (например, FolR1, HER1, HER2, CD3, мезотелин), если не указано иное, могут представлять собой любые нативные формы белков из любого применяемого в качестве источника позвоночного животного, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы). В конкретном варианте осуществления изобретения антиген представляет собой человеческий белок. В контексте настоящего описания при ссылке на конкретный белок подразумевается «полноразмерный», непроцессированный белок, а также любая форма белка, полученная в результате процессинга в клетке. Под понятие подпадают также встречающиеся в естественных условиях варианты белка, например, сплайсинговые варианты или аллельные варианты. Примерами человеческих белков, пригодных в качестве антигенов, являются (но, не ограничиваясь только ими): FolR1, HER1 и CD3, прежде всего эпсилон-субъединица CD3 (см. UniProt № Р07766 (версия 130), NCBI RefSeq № NP_000724.1, SEQ ID NO: 54, человеческая последовательность; или UniProt № Q95LI5 (версия 49), NCBI GenBank, № BAB71849.1, последовательность обезьян циномолгус [Macaca fascicularis]). В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая антигенсвязывающая молекула, предлагаемая в изобретении, связывается с эпитопом CD3 или антигеном клетки-мишени, который является консервативным для CD3 или антигена-мишени из различных видов. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая антигенсвязывающая молекула, предлагаемая в изобретении, связывается с CD3 и FolR1, но не связывается с FolR2 или FolR3. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая антигенсвязывающая молекула, предлагаемая в изобретении, связывается с CD3 и HER1. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая антигенсвязывающая молекула, предлагаемая в изобретении, связывается с CD3 и мезотелином. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая антигенсвязывающая молекула, предлагаемая в изобретении, связывается с CD3 и HER2.
Понятие «специфически связывается» означает, что связывание является избирательным в отношении антигена и его можно отличать от нежелательных или неспецифических взаимодействий. Способность антигенсвязывающего фрагмента связываться со специфической антигенной детерминантой, можно определять с помощью твердофазного иммуноферментного анализа (ELISA) или других методик, известных специалисту в данной области, например, с помощью методики на основе поверхностного плазменного резонанса (осуществляя анализ с помощью устройства BIAcore) (Liljeblad и др., Glyco J 17, 2000, cc. 323-329), и традиционных анализов связывания (Heeley, Endocr Res 28, 2002, cc. 217-229). В одном из вариантов осуществления изобретения уровень связывания антигенсвязывающего фрагмента с неродственным белком составляет менее чем примерно 10% от уровня связывания антигенсвязывающего фрагмента с антигеном при измерении, например, с помощью SPR. В некоторых вариантах осуществления изобретения антигенсвязывающий фрагмент, который связывается с антигеном, или антигенсвязывающая молекула, содержащая антигенсвязывающий фрагмент, характеризуется величиной константы диссоциации (KD), составляющей ≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ, ≤0,1 нМ, ≤0,01 нМ или ≤0,001 нМ (например, 10-8 М или менее, например, от 10-8 М до 10-13 М, например, от 10-9 М до 10-13 М).
Понятие «аффинность» относится к суммарной силе всех нековалентных взаимодействий между индивидуальным сайтом связывания молекулы (например, рецептора) и ее партнера по связыванию (например, лиганда). Если не указано иное, то в контексте настоящего описания понятие «аффинность связывания» относится к присущей компонентам связывающейся пары (например, антигенсвязывающему фрагменту и антигену или рецептору и лиганду) аффинности связывания, отражающей взаимодействие по типу 1:1. Аффинность молекулы X к ее партнеру Y можно, как правило, характеризовать с помощью константы диссоциации (KD), которая представляет собой отношение констант скорости реакции диссоциации и ассоциации (koff и kon соответственно). Так, эквивалентные аффинности могут соответствовать различным константам скорости, если соотношение констант скорости остается таким же. Аффинность можно оценивать общепринятыми методами, известными в данной области, включая представленные в настоящем описании методы. Конкретным методом измерения аффинности является метод поверхностного плазмонного резонанса (SPR).
Понятие «пониженное связывание (пониженная способность к связыванию)», например, пониженная способность к связыванию с Fc-рецептором, относится к снижению аффинности касательно соответствующего взаимодействия, измеренной, например, с помощью SPR. Для ясности следует отметить, что понятие включает также снижение аффинности до нуля (или ниже предела обнаружения аналитического метода), т.е. полную элиминацию взаимодействия. И, наоборот, «повышенное связывание (повышенная способность к связыванию)» относится к повышению аффинности связывания касательно соответствующего взаимодействия.
Понятие «Т-клеточная активация (активация Т-клеток)» в контексте настоящего описания относится к одному или нескольким клеточным ответам Т-лимфоцита, в частности, цитотоксического Т-лимфоцита, выбранным из: пролиферации, дифференцировки, секреции цитокинов, высвобождения цитотоксических эффекторных молекул, цитотоксической активности и экспрессии маркеров активации. Активируемые протеазой активирующие Т-клетки биспецифические антигенсвязывающие молекулы, предлагаемые в изобретении, обладают способностью индуцировать Т-клеточную активацию. Приемлемые анализы оценки Т-клеточной активации, известные в данной области, представлены в настоящем описании.
Понятие «антиген клетки-мишени» в контексте настоящего описания относится к антигенной детерминанте, которая присутствует на поверхности клетки-мишени, например, клетки в опухоли, такой как раковая клетка или клетка стромы опухоли.
В контексте настоящего описания понятия «первый» и «второй» касательно антигенсвязывающих фрагментов и т.д. применяют с целью удобства различения, когда присутствует более одного типа каждого из фрагментов. Применение этих понятий не подразумевает их конкретный порядок или ориентацию в активируемой протеазой активирующей Т-клетки биспецифической антигенсвязывающей молекуле, если специально не указано иное.
Понятие «молекула Fab» относится к белку, состоящему из VH и СН1-домена тяжелой цепи («тяжелая цепь Fab») и VL и CL-домена легкой цепи («легкая цепь Fab») иммуноглобулина.
Под понятием «слитые» подразумевается, что компоненты (например, молекула Fab и субъединица Fc-домена) соединены пептидными связями, либо непосредственно, либо с помощью одного или нескольких пептидных линкеров.
В контексте настоящего описания понятие «одноцепочечная» относится к молекуле, содержащей аминокислотные мономеры, связанные линейно посредством пептидных связей. В некоторых вариантах осуществления изобретения один из антигенсвязывающих фрагментов представляет собой одноцепочечную молекулу Fab, т.е. молекулу Fab, в которой легкая цепь Fab и тяжелая цепь Fab соединены с помощью пептидного линкера с образованием одной пептидной цепи. В конкретном указанном варианте осуществления изобретения в одноцепочечной молекуле Fab С-конец легкой цепи Fab соединен с N-концом тяжелой цепи Fab.
Под кроссовер-молекулой Fab (которую обозначают также как «Crossfab») подразумевается молекула Fab, в которой либо вариабельные области, либо константные области тяжелой и легкой цепи Fab обменены друг на друга, т.е. кроссовер-молекула Fab содержит пептидную цепь, состоящую из вариабельной области легкой цепи и константной области тяжелой цепи, и пептидную цепь, состоящую из вариабельной области тяжелой цепи и константной области легкой цепи. Для простоты понимания, следует отметить, что в кроссовер-молекуле Fab, в которой обменены вариабельные области легкой цепи Fab и тяжелой цепи Fab, пептидную цепь, содержащую константную область тяжелой цепи, обозначают в контексте настоящего описания как «тяжелая цепь» кроссовер-молекулы Fab. И, наоборот, в кроссовер-молекуле Fab, в которой обменены константные области легкой цепи Fab и тяжелой цепи Fab, пептидную цепь, содержащую вариабельную область тяжелой цепи, обозначают в контексте настоящего описания как «тяжелая цепь» кроссовер-молекулы Fab.
В отличие от этого, понятие «каноническая» молекула Fab обозначает молекулу Fab в ее встречающемся в естественных условиях формате, т.е. содержащую тяжелую цепь, которая состоит из вариабельной и константной областей тяжелой цепи (VH-CH1), и легкую цепь, которая состоит из вариабельной и константной областей легкой цепи (VL-CL).
Понятие «молекула иммуноглобулина» относится к белку, имеющему структуру встречающегося в естественных условиях антитела. Например, иммуноглобулины класса IgG представляют собой гетеротетрамерные гликопротеины с молекулярной массой примерно 150000 Да, состоящие из двух легких цепей и двух тяжелых цепей, связанных дисульфидными мостиками. В направлении от N-конца к С-концу каждая тяжелая цепь содержит вариабельную область (VH), которую называют также вариабельным тяжелым доменом или вариабельным доменом тяжелой цепи, за которой расположены три константных домена (CH1, СН2 и CH3), которые называют также константной областью тяжелой цепи. Аналогично этому, в направлении от N- конца к С-концу каждая легкая цепь содержит вариабельную область (VL), которую называют также вариабельным легким доменом или вариабельным доменом легкой цепи, за которой расположен константный домен легкой цепи (CL), который называют также константной областью легкой цепи. Тяжелая цепь иммуноглобулина может относиться к одному из пяти типов, обозначенных как α (IgA), δ (IgD), ε (IgE), γ (IgG) или μ (IgM), некоторые из которых дополнительно подразделяют на подтипы, например, γ1 (IgG1), γ2 (IgG2), γ3 (IgG3), γ4 (IgG4), α1 (IgA1) и α2 (IgA2). Легкая цепь иммуноглобулина может относиться к одному из двух типов, обозначенных как каппа (κ) и лямбда (λ), на основе аминокислотной последовательности ее константного домена. Иммуноглобулин, как правило, состоит из двух молекул Fab и Fc-домена, которые соединены через шарнирную область иммуноглобулина.
В контексте настоящего описания понятие «антитело» используется в его наиболее широком смысле, и оно относится к различным структурам антител, включая (но, не ограничиваясь только ими) моноклональные антитела, поликлональные антитела и фрагменты антител, при условии, что они обладают требуемой антигенсвязывающей активностью.
Понятие «фрагмент антитела» относится к молекуле, отличной от интактного антитела, которая содержит часть интактного антитела, обладающую способностью связываться с антигеном, с которым связывается интактное антитело. Примерами фрагментов антител являются (но, не ограничиваясь только ими) Fv, Fab, Fab', Fab'-SH, F(ab')2, димерные антитела (диабоди), линейные антитела, одноцепочечные молекулы антител (например, scFv) и однодоменные антитела. Обзор некоторых фрагментов антител см., например, у Hudson и др., Nat Med 9, 2003, cc. 129-134. Обзор scFv-фрагментов см., например, у Plueckthun в: The Pharmacology of Monoclonal Antibodies, т.113, под ред. Rosenburg и Moore, изд-во Springer-Verlag, New York, 1994, cc. 269-315; см. также WO 93/16185; и US №№5571894 и 5587458. Обсуждение Fab- и F(ab')2-фрагментов, содержащих остатки эпитопа, связывающегося с рецептором спасения, и обладающих удлиненным временем полужизни in vivo, см. в US №5869046. Димерные антитела представляют собой фрагменты антител с двумя антигенсвязывающими сайтами, которые могут быть двухвалентными или биспецифическими (см., например, ЕР 404097; WO 1993/01161; Hudson и др., Nat Med 9, 2003, cc. 129-134; и Hollinger и др., Proc Natl Acad Sci USA 90, 1993, cc. 6444-6448. Тримерные (триабоди) и тетрамерные (тетрабоди) антитела описаны также у Hudson и др., Nat Med 9, 2003, cc. 129-134. Однодоменные антитела представляют собой фрагменты антител, содержащие весь вариабельный домен тяжелой цепи или его часть или весь вариабельный домен легкой цепи антитела или его часть. В некоторых вариантах осуществления изобретения однодоменное антитело представляет собой человеческое однодоменное антитело (фирма Domantis, Inc., Валтам, шт. Массачусетс; см., например, US №6248516 В1). Фрагменты антител можно создавать с помощью различных методик, включая (но, не ограничиваясь только ими) протеолитическое расщепление интактного антитела, а также получать с использованием рекомбинантных клеток-хозяев (например, Е. coli или фага), как указано в настоящем описании.
Понятие «антигенсвязывающий домен» относится к части антитела, которая содержит область, специфически связывающуюся и являющуюся комплементарной части антигена или полному антигену. Антигенсвязывающий домен может представлять собой, например, один или несколько вариабельных доменов антитела (которые называют также вариабельными областями антитела). Предпочтительно антигенсвязывающий домен содержит вариабельную область легкой цепи (VL) антитела и вариабельную область тяжелой цепи (VH) антитела.
Понятие «вариабельная область» или «вариабельный домен» относится к домену тяжелой или легкой цепи антитела, который участвует в связывании антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL соответственно) нативного антитела, как правило, имеют сходные структуры, при этом каждый домен содержит четыре консервативных каркасных участка (FR) и три гипервариабельных участка (HVR) (см., например, Kindt и др., Kuby Immunology, 6-е изд., изд-во W.H. Freeman and Co., 2007, с. 91). Одного VH- или VL-домена может быть достаточно для обеспечения специфичности связывания антигена.
Понятие «гипервариабельный участок» или «HVR» в контексте настоящего описания относится к каждому из участков вариабельного домена антитела, последовательности которых являются гипервариабельными, и/или которые образуют структуры в виде петель («гипервариабельные петли»). Как правило, нативные четырехцепочечные антитела содержат шесть HVR; три в VH (H1, Н2, Н3) и три в VL (L1, L2, L3). HVR, как правило, содержат аминокислотные остатки из гипервариабельных петель и/или из «определяющих комплементарность участков» (CDR), последние отличаются наиболее выраженной вариабельностью последовательности и/или участвуют в распознавании антигенов. За исключением CDR1 в VH, CDR, как правило, содержат аминокислотные остатки из гипервариабельных петель. Гипервариабельные участки (HVR) часто обозначают как «определяющие комплементарность участки» (CDR), и эти понятия в контексте настоящего описания используют взаимозаменяемо, и они относятся к участкам вариабельной области, которые образуют антигенсвязывающие области. Эта конкретная область описана у Kabat и др., U.S. Dept. of Health and Human Services, «Sequences of Proteins of Immunological Interest», 1983 и у Chothia и др., J. Mol. Biol. 196, 1987, cc. 901-917, причем эти определения относятся к перекрывающимся аминокислотным остаткам или поднаборам аминокислотных остатков при их сравнении друг с другом. Однако в контексте настоящего описания подразумевается возможность применения любого определения CDR антитела или его вариантов. Соответствующие аминокислотные остатки, из которых состоят CDR, как они определены в каждой из процитированных выше ссылок, представлены в сравнении ниже в таблице 1. Точные номера остатков, которые образуют конкретный CDR, должны варьироваться в зависимости от последовательности и размера CDR. Специалисты в данной области на основе данных об аминокислотной последовательности вариабельной области антитела легко могут определять, какие остатки входят в конкретный CDR.
1Нумерация всех входящих в CDR остатков в таблице 1 дана в соответствии с номенклатурой, предложенной Кэботом с соавторами (см. ниже).
2Обозначение «AbM» с прописной буквой «b», использованное в таблице 1, относится к CDR, как они определены программой для моделирования антител «AbM» компании Oxford Molecular Group.
Кэбот с соавторами предложили также систему нумерации (номенклатуру) последовательностей вариабельных областей, которую можно применять для любого антитела. Обычный специалист в данной области может однозначно применять эту систему «нумерации по Кэботу» к любой последовательности вариабельной области, не имея никаких экспериментальных данных, кроме сведений о самой последовательности. В контексте настоящего описания понятие «нумерация по Кэботу» относится к системе нумерации, описанной у Kabat и др., «Sequence of Proteins of Immunological Interest», изд-во U.S. Dept. of Health and Human Services, 1983. Если не указано иное, то ссылки на нумерацию положений конкретных аминокислотных остатков в вариабельной области антитела даны в соответствии с системой нумерации по Кэботу.
Нумерация полипептидных последовательностей в «Перечне последовательностей» не представляет собой нумерацию в соответствии с системой Кэбота. Однако в компетенции обычного специалиста в данной области является превращение нумерации последовательностей в «Перечне последовательностей» в нумерацию по Кэботу.
«Каркасные участки» или «FR»-участки представляют собой участки вариабельных доменов, отличные от остатков гипервариабельных участков (HVR). FR вариабельного домена, как правило, представлены четырьмя FR-доменами: FR1, FR2, FR3 и FR4. Таким образом, последовательности HVR и FR, как правило, расположены в VH (или VL) в следующем порядке: FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
Понятие «класс» антитела или иммуноглобулина относится к типу константного домена или константной области, входящего/входящей в тяжелую цепь. Существует пять основных классов антител: IgA, IgD, IgE, IgG и IgM, a некоторые из них можно дополнительно подразделять на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелых цепей, соответствующие различным классам иммуноглобулинов, обозначают как а, 8, 8, у и ц соответственно.
В контексте настоящего описания понятие «Fc-домен» или «Fc-область» относится к С-концевой области тяжелой цепи иммуноглобулина, которая содержит по меньшей мере часть константной области. Понятие относится к нативной последовательности Fc-областей и вариантам Fc-областей. Хотя пограничные последовательности Fc-области в тяжелой цепи IgG могут слегка варьироваться, как правило, Fc-область тяжелой цепи человеческого IgG простирается от Cys226 или от Pro230 до карбоксильного конца тяжелой цепи. Однако С-концевой лизин (Lys447) Fc-области может либо присутствовать, либо отсутствовать. Если специально не указано иное, то нумерация аминокислотных остатков в Fc-области или константном участке соответствует системе EU-нумерации, которую называют также EU-индексом, описанной у Kabat и др., Sequences of Proteins of Immunological Interest, 5-ое изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991. Понятие «субъединица» Fc-домена в контексте настоящего описания относится к одному из двух полипептидов, образующих димерный Fc-домен, т.е. к полипептиду, который содержит С-концевые константные области тяжелой цепи иммуноглобулина, обладающие способностью к стабильной самоассоциации. Например, субъединица Fc-домена IgG содержит константный домен СН2 IgG и СН3 IgG.
«Модификация, усиливающая ассоциацию первой и второй субъединиц Fc-домена» представляет собой манипуляцию с пептидным каркасом или посттрансляционные модификации субъединицы Fc-домена, которые уменьшают или препятствуют ассоциации полипептида, содержащего субъединицу Fc-домена, с идентичным полипептидом с образованием гомодимера. В контексте настоящего описания модификация, усиливающая ассоциацию, включает, прежде всего, различные модификации, осуществляемые с каждой из двух субъединиц Fc-домена, предназначенных для ассоциации (например, первой и второй субъединиц Fc-домена), при этом, модификации дополняют друг друга таким образом, чтобы усиливать ассоциацию двух субъединиц Fc-домена. Например, модификация, усиливающая ассоциацию, может изменять структуру или заряд одной или обеих субъединиц Fc-домена таким образом, чтобы улучшать их ассоциацию стерически или электростатически соответственно. Так, (гетеро)димеризация имеет место между полипептидом, который содержит первую субъединицу Fc-домена, и полипептидом, который содержит вторую субъединицу Fc-домена, которые могут быть неидентичными, поскольку дополнительные компоненты, слитые с каждой из субъединиц (например, антигенсвязывающие фрагменты), не являются одинаковыми. В некоторых вариантах осуществления изобретения модификация, усиливающая ассоциацию, представляет собой аминокислотную мутацию в Fc-домене, в частности, аминокислотную замену. В конкретном варианте осуществления изобретения модификация, усиливающая ассоциацию, представляет собой индивидуальную аминокислотную мутацию, в частности, аминокислотную замену, в каждой из двух субъединиц Fc-домена.
Понятие «эффекторные функции», используемое в настоящем описании, относится к видам биологической активности, присущим Fc-области антитела, которые варьируются в зависимости от изотипа антитела. Примерами эффекторных функций антитела являются: способность связываться с C1q и комплементзависимая цитотоксичность (CDC), способность связываться с Fc-рецептором, антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), антитело-обусловленный клеточнозависимый фагоцитоз (ADCP), секреция цитокинов, опосредованное иммунным комплексом поглощение антигена антигенпрезентирующими клетками, понижающая регуляция рецепторов клеточной поверхности (например, В-клеточного рецептора); и активация В-клеток.
В контексте настоящего описания подразумевается, что понятия «конструирование, сконструированный, инженерия» включают любую манипуляцию с пептидным каркасом или пост-трансляционные модификации встречающегося в естественных условиях или рекомбинантного полипептида или его фрагмента. Инженерия включает модификации аминокислотной последовательности, схемы гликозилирования или группы боковых цепей индивидуальных аминокислот, а также комбинации указанных подходов.
В контексте настоящего описания подразумевается, что понятие «аминокислотная мутация» относится к аминокислотным заменам, делециям, инсерциям и модификациям. Можно применять любую комбинацию замены, делеции, инсерции и модификации для создания конечной конструкции при условии, что конечная конструкция обладает требуемыми характеристиками, например, пониженной способностью связываться с Fc-рецептором или повышенной ассоциацией с другим пептидом. Аминокислотная последовательность с делециями и инсерциями включает амино- и/или карбоксиконцевые делеции и инсерции аминокислот. Конкретными аминокислотными мутациями являются аминокислотные замены. Для изменения, например, характеристик связывания Fc-области, наиболее предпочтительными являются неконсервативные аминокислотные замены, т.е. замена одной аминокислоты на другую аминокислоту, имеющую другие структурные и/или химические свойства. Аминокислотные замены включают замену на не встречающиеся в естественных условиях аминокислоты или на производные встречающихся в естественных условиях двадцати стандартных аминокислот (например, на 4-гидроксипролин, 3-метилгистидин, орнитин, гомосерин, 5-гидроксилизин). Аминокислотные мутации можно создавать с помощью генетических или химических методов, хорошо известных в данной области. Генетические методы могут включать сайтнаправленный мутагенез, ПЦР, синтез генов и т.п. Подразумевается, что можно применять также методы изменения боковой группы аминокислоты, отличные от методов генетической инженерии, такие как химическая модификация. Для обозначения одной и той же аминокислотной мутации можно использовать различные обозначения. Например, замену пролина в положении 329 Fc-домена на глицин можно обозначать как 329G, G329, G329, P329G или Pro329Gly.
В контексте настоящего описания понятие «полипептид» относится к молекуле, состоящей из мономеров (аминокислот), линейно связанных амидными связями (которые обозначают также как пептидные связи). Понятие «полипептид» относится к любой цепи, состоящей из двух или большего количества аминокислот, и не подразумевает, что продукт имеет конкретную длину. Так, пептиды, дипептиды, трипептиды, олигопептиды, «белок», «аминокислотная цепь» или любое иное принятое понятие, относящееся к цепи, состоящей из двух или большего количества аминокислот, все подпадают под определение «полипептид», и понятие «полипептид» можно применять вместо или взаимозаменяемо с любым из указанных понятий. Подразумевается также, что понятие «полипептид» относится в продуктам, которые несут пост-экспрессионные модификации полипептида, включая (но, не ограничиваясь только ими) гликозилирование, ацетилирование, фосфорилирование, амидирование, дериватизацию с использованием известных защитных/блокирующих групп, протеолитическое расщепление или модификацию с помощью не встречающихся в естественных условиях аминокислот. Полипептид можно получать из встречающегося в естественных условиях биологического источника или можно получать с помощью технологии рекомбинантной ДНК, и его не обязательно транслировать с созданной нуклеотидной последовательности. Его можно создавать любым путем, включая химический синтез. Полипептид, предлагаемый в изобретении, может состоять примерно из 3 или более, 5 или более, 10 или более, 20 или более, 25 или более, 50 или более, 75 или более, 100 или более, 200 или более, 500 или более, 1000 или более или 2000 или более аминокислот. Полипептиды могут иметь различную трехмерную структуру, хотя они необязательно должны иметь указанную структуру. Полипептиды с определенной трехмерной структурой обозначают как полипептиды, имеющие укладку, а полипептиды, которые не обладают определенной трехмерной структурой, но которые могут легче адаптироваться к большому количеству различных конформаций, обозначают как полипептиды, не имеющие укладку.
Под «выделенным» полипептидом или его вариантом, или производным подразумевают полипептид, который не находится в его естественном окружении. При этом не требуется наличия какого-либо конкретного уровня очистки. Например, выделенный полипептид можно удалять из его нативного или естественного окружения. Полученные путем рекомбинации полипептиды и белки, экспрессируемые в клетках-хозяевах, рассматриваются как выделенные для целей настоящего изобретения, если они представляют собой нативные или рекомбинантные полипептиды, которые отделены, фракционированы или частично или полностью очищены с помощью любого приемлемого метода.
«Процент (%) идентичности аминокислотной последовательности» относительно полипептидной референс-последовательности определяют как процент аминокислотных остатков в последовательности-кандидате, которые идентичны аминокислотным остаткам в полипептидной референс-последовательности, после выравнивания последовательностей и интродукции при необходимости брешей для достижения максимального процента идентичности последовательностей, и при этом какие-либо консервативные замены не учитываются при оценке идентичности последовательностей. Сравнительный анализ для определения процента идентичности аминокислотных последовательностей можно осуществлять различными путями, которые находятся в компетенции специалиста в данной области, например, с использованием публично доступных компьютерных программ, таких как программа BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области могут определять соответствующие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей. Однако для целей настоящего изобретения величину % идентичности аминокислотных последовательностей получают с использованием предназначенной для сравнения последовательностей компьютерной программы ALIGN-2. Предназначенная для сравнения последовательностей компьютерная программа ALIGN-2 разработана фирмой Genentech, Inc., и исходный код помещен на хранение вместе с документацией для пользователя в U.S. Copyright Office, Washington D.C., 20559, где он зарегистрирован под регистрационным номером U.S. Copyright Registration, № TXU510087. Программа ALIGN-2 представляет собой публично доступную программу фирмы Genentech, Inc., Южный Сан-Франциско, шт. Калифорния, или ее можно компилировать из исходного кода. Программу ALIGN-2 можно компилировать для применения в операционной системе UNIX, включая цифровую версию UNIX V4.0D. В программе ALIGN-2 все параметры для сравнения последовательностей являются заданными и не должны изменяться. В ситуациях, когда ALIGN-2 применяют для сравнения аминокислотных последовательностей, % идентичности аминокислотных последовательностей данной аминокислотной последовательности А относительно или по сравнению с данной аминокислотной последовательностью Б (которую другими словами можно обозначать как данная аминокислотная последовательность А, которая имеет или отличается определенным % идентичности аминокислотной последовательности относительно или по сравнению с данной аминокислотной последовательностью Б), рассчитывают следующим образом:
100 × частное X/Y,
где X обозначает количество аминокислотных остатков, оцененных программой сравнительного анализа последовательностей ALIGN-2 как идентичные совпадения при сравнительном анализе последовательностей А и Б с помощью указанной программы, и где Y обозначает общее количество аминокислотных остатков в Б. Должно быть очевидно, что, когда длина аминокислотной последовательности А не равна длине аминокислотной последовательности Б, то % идентичности аминокислотной последовательности А относительно аминокислотной последовательности Б не должен быть равен % идентичности аминокислотной последовательности Б относительно аминокислотной последовательности А. Если специально не указано иное, то в контексте настоящего описания все величины % идентичности аминокислотных последовательностей получают согласно процедуре, описанной в последнем из предшествующих параграфов, с помощью компьютерной программы ALIGN-2.
Понятие «полинуклеотид» относится к выделенной молекуле нуклеиновой кислоты или конструкции, например, матричной РНК (мРНК), РНК вирусного происхождения или плазмидной ДНК (пДНК). Полинуклеотид может содержать обычную фосфодиэфирную связь или нетрадиционную связь (например, амидную связь, такую, которая присутствует в пептидных нуклеиновых кислотах (ПНК)). Понятие «молекула нуклеиновой кислоты» относится к любому одному или нескольким сегментам нуклеиновой кислоты, например, фрагментам ДНК или РНК, присутствующим в полинуклеотиде.
Под «выделенной» молекулой нуклеиновой кислоты или полинуклеотидом подразумевается молекула нуклеиновой кислоты, т.е. ДНК или РНК, которая отделена от ее нативного окружения. Например, рекомбинантный полинуклеотид, кодирующий входящий в вектор полипептид, рассматривается как выделенный для целей настоящего изобретения. Другими примерами выделенного полинуклеотида являются рекомбинантные полинуклеотиды, присутствующие в гетерологичных клетках-хозяевах, или очищенные (частично или полностью) полинуклеотиды, находящиеся в растворе. Выделенный полинуклеотид включает молекулу полинуклеотида, входящую в клетки, которые в норме содержат молекулу полинуклеотида, но молекула полинуклеотида присутствует вне хромосомы или имеет локализацию в хромосоме, отличную от ее локализации в хромосоме в естественных условиях. Выделенные молекулы РНК включают полученные in vivo или in vitro РНК-транскрипты, предлагаемые в настоящем изобретении, а также формы с позитивной и негативной цепью и двухцепочечные формы. Выделенные полинуклеотиды или нуклеиновые кислоты, предлагаемые в настоящем изобретении, включают также указанные молекулы, полученные с помощью синтеза. Кроме того, полинуклеотид или нуклеиновая кислота может представлять собой или может включать регуляторный элемент, такой как промотор, сайт связывания рибосом или терминатор транскрипции.
Под нуклеиновой кислотой или полинуклеотидом, имеющей/имеющим нуклеотидную последовательность, которая, например, на 95% «идентична» нуклеотидной референс-последовательности, предлагаемой в настоящем изобретении, подразумевается, что нуклеотидная последовательность полинуклеотида идентична референс-последовательности за исключением того, что полинуклеотидная последовательность может включать вплоть до 5 точечные мутаций на каждые 100 нуклеотидов нуклеотидной референс-последовательности. Другими словами, для получения полинуклеотида, имеющего нуклеотидную последовательность, которая идентична по меньшей мере на 95% нуклеотидной референс-последовательности, вплоть до 5% нуклеотидов в референс-последовательности можно изымать путем делеции или заменять на другой нуклеотид, или вплоть до 5% нуклеотидов от общего количества нуклеотидов в референс-последовательности можно встраивать в референс-последовательность. Эти изменения референс-последовательности могут иметь место в положениях на 5'- или 3'-конце нуклеотидной референс- последовательности или в ином положении между этими концевыми положениями, и их встраивают либо индивидуально между остатками в референс-последовательности, либо их встраивают в референс-последовательность в виде одной или нескольких смежных групп. На практике решение вопроса о том, идентична ли конкретная полинуклеотидная последовательность по меньшей мере на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% нуклеотидной последовательности, предлагаемой в настоящем изобретении, можно решать, как правило, с использованием известных компьютерных программ, например, указанных выше для полипептидов (например, ALIGN-2).
Понятие «кассета экспрессии» относится к полинуклеотиду, полученному с помощью рекомбинации или синтеза, который содержит серии специфических нуклеотидных элементов, которые обеспечивают транскрипцию конкретной нуклеиновой кислоты в клетке-мишени. Рекомбинантную кассету экспрессии можно встраивать в плазмиду, хромосому, митохондриальную ДНК, пластидную ДНК, вирус или фрагмент нуклеиновой кислоты. Как правило, рекомбинантная кассета экспрессии, представляющая собой часть экспрессионного вектора, включает среди прочих последовательностей подлежащую транскрипции нуклеотидную последовательность и промотор. В некоторых вариантах осуществления изобретения кассета экспрессии, предлагаемая в изобретении, содержит полинуклеотидные последовательности, которые кодируют биспецифические антигенсвязывающие молекулы, предлагаемые в изобретении, или их фрагменты.
Понятие «вектор» или «экспрессионный вектор» является синонимом понятия «экспрессионная конструкция» и относится к молекуле ДНК, которую применяют для интродукции и обеспечения экспрессии конкретного гена, с которой он функционально связан в клетке-мишени. Понятие включает вектор, представляющий собой самореплицирующуюся структуру нуклеиновой кислоты, а также вектор, встроенный в геном клетки-хозяина, в которую он интродуцирован. Экспрессионный вектор, предлагаемый в настоящем изобретении, содержит кассету экспрессии. Экспрессионные векторы позволяют осуществлять транскрипцию стабильной мРНК в больших количествах. Когда экспрессионный вектор находится внутри клетки-мишени, то молекула рибонуклеиновой кислоты или белок, который кодируется геном, продуцируется в результате клеточного механизма транскрипции и/или трансляции. В одном из вариантов осуществления изобретения экспрессионный вектор, предлагаемый в изобретении, содержит кассету экспрессии, которая включает полинуклеотидные последовательности, которые кодируют биспецифические антигенсвязывающие молекулы, предлагаемые в изобретении, или их фрагменты.
В контексте настоящего описания понятия «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» используются взаимозаменяемо, и они относятся к клеткам, в которые интродуцирована экзогенная нуклеиновая кислота, включая потомство указанных клеток. К клеткам-хозяевам относятся «трансформанты» и «трансформированные клетки», которые включают первичные трансформированные клетки, а также потомство, выведенное из них, независимо от количества пересевов. Потомство может не быть строго идентичным родительской клетке по составу нуклеиновых кислот, а может нести мутации. Под данное понятие подпадает мутантное потомство, которое обладает такой же функцией или биологической активностью, что и отобранная путем скрининга или селекции исходная трансформированная клетка. Клетка-хозяин представляет собой любой тип клеточной системы, которую можно применять для создания биспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении. Клетки-хозяева включают культивируемые клетки, например, культивируемые клетки млекопитающих, такие как (но, не ограничиваясь только ими) СНО-клетки, BHK-клетки, NS0-клетки, 8Р2/0-клетки, клетки миеломы линии YO, клетки мышиной миеломы линии Р3Х63, PER-клетки, PER.С6-клетки или клетки гибридомы, клетки дрожжей, клетки насекомых и клетки растений, но также клетки, находящиеся в трансгенном животном, трансгенном растении или в культивируемой растительной или животной ткани.
«Активирующий Fc-рецептор» представляет собой Fc-рецептор, который после взаимодействия с Fc-доменом антитела осуществляет процесс передачи сигналов, которые стимулируют несущую рецептор клетку осуществлять эффекторные функции. Человеческие активирующие Fc-рецепторы включают FcγRIIIa (CD16a), FcγRI (CD64), FcγRIIa (CD32) и FcαRI (CD89).
Антитело-обусловленная клеточнозависимая цитотоксичность (ADCC) представляет собой иммунный механизм, приводящий к лизису сенсибилизированных антителом клеток-мишеней иммунными эффекторными клетками. Клетки-мишени представляют собой клетки, с которыми антитела или их производные, содержащие Fc-область, специфически связываются, как правило, через область белка, которая является N-концевой относительно Fc-области. В контексте настоящего описания понятие «пониженная ADCC» относится либо к снижению количества лизированных в данный момент времени клеток-мишеней при данной концентрации антитела в среде, окружающей клетки-мишени, путем указанного выше механизма ADCC, и/или к повышению концентрации антитела в среде, окружающей клетки-мишени, необходимой для достижения лизиса данного количества клеток-мишеней в данное время с помощью механизма ADCC. Понижение ADCC-активности определяют относительно ADCC, опосредуемой таким же антителом, которое получено с помощью такого же типа клеток-хозяев с использованием одинаковых стандартных методов получения, очистки, приготовления композиций и хранения (которые известны специалистам в данной области), но которое не подвергали инженерии. Например, понижение ADCC, опосредуемой антителом, которое содержит в его Fc-домене аминокислотную замену, которая снижает ADCC, определяют относительно ADCC, опосредуемой таким же антителом без указанной аминокислотной замены в Fc-домене. Приемлемые анализы оценки ADCC хорошо известны в данной области (см., например, публикацию РСТ WO 2006/082515 или публикацию РСТ WO 2012/130831).
Понятие «эффективное количество» агента относится к количеству, необходимому для обеспечения физиологического изменения в клетке или ткани, в которую его вводят.
Понятие «терапевтически эффективное количество» агента, например, фармацевтической композиции, относится к количеству, эффективному при применении в дозах и в течение периодов времени, необходимых для достижения требуемого терапевтического или профилактического результата. Терапевтически эффективное количество агента, например, элиминирует, снижает, замедляет, минимизирует или предупреждает нежелательные явления заболевания.
«Индивидуум» или «субъект» представляет собой млекопитающее. Млекопитающие представляют собой (но, не ограничиваясь только ими) одомашненных животных (например, коровы, овцы, кошки, собаки и лошади), приматов (например, люди и приматы кроме человека, такие как мартышки), кроликов и грызунов (например, мыши и крысы). Предпочтительно индивидуум или субъект представляет собой человека.
Понятие «фармацевтическая композиция» относится к препарату, который находится в такой форме, что он обеспечивает биологическую активность входящего в его состав действующего вещества, которое должно обладать эффективностью, и который не содержит дополнительных компонентов, которые обладают неприемлемой токсичностью для индивидуума, которому следует вводить композицию.
«Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтической композиции, отличному от действующего вещества, который является нетоксичным для индивидуума. Фармацевтически приемлемые носители включают (но, не ограничиваясь только ими) буфер, эксципиент, стабилизатор или консервант.
В контексте настоящего описания понятие «лечение» (и его грамматические вариации, такие как «лечить» или «процесс лечения») относится к клиническому вмешательству с целью изменения естественного течения болезни у индивидуума, подлежащего лечению, и его можно осуществлять либо для профилактики или в процессе развития клинической патологии. Требуемыми действиями лечения являются (но, не ограничиваясь только ими) предупреждение возникновения или рецидива болезни, облегчение симптомов, уменьшение любых прямых или косвенных патологических последствий болезни, предупреждение метастазов, снижение скорости развития болезни, облегчение или временное ослабление болезненного состояния и ремиссия или улучшение прогноза. В некоторых вариантах осуществления изобретения активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, применяют для задержки развития болезни или замедления прогрессирования болезни.
Понятие «листовка-вкладыш в упаковку» в контексте настоящего описания относится к инструкциям, которые обычно помещают в поступающие в продажу упаковки терапевтических продуктов, которые содержат информацию о показаниях, применении, дозе, пути введения, комбинированной терапии, противопоказаниях и/или мерах предосторожности при применении указанных терапевтических продуктов.
Понятие «идиотипспецифический полипептид» в контексте настоящего описания относится к полипептиду, который распознает идиотип антигенсвязывающего фрагмента, например, антигенсвязывающего фрагмента, специфического по отношению к CD3. Идиотипспецифический полипептид обладает способностью специфически связываться с вариабельной областью антигенсвязывающего фрагмента и тем самым снижает или предупреждает специфическое связывание антигенсвязывающего фрагмента с его когнатным антигеном. При ассоциации с молекулой, которая содержит антигенсвязывающий фрагмент, идиотипспецифический полипептид может функционировать в качестве маскирующего фрагмента молекулы. В настоящем описании представлены конкретно антиидиотипические антитела или фрагменты антиидиотипсвязывающего антитела, специфические по отношению к идиотину анти-CD3-связывающих молекул.
Понятие «протеаза» или «протеолитический фермент» в контексте настоящего описания относится к любому протеолитическому ферменту, который расщепляет линкер в сайте, распознаваемом ферментом, и который экспрессируется клеткой-мишенью. Указанные протеазы могут секретироваться клеткой-мишенью или оставаться ассоциированными с клеткой-мишенью, например, на поверхности клетки-мишени. Примеры протеаз включают (но, не ограничиваясь только ими) металлопротеиназы, например, матричную металлопротеиназу 1-28 и «дезинтегрин и металлопротеиназу» (ADAM) 2, 7-12, 15, 17-23, 28-30 и 33, сериновые протеазы, например, активатор плазминогена урокиназного типа и матриптазу, цистеиновые протеазы, аспарагиновые протеазы и представителей семейства катепсина.
В контексте настоящего описания понятие «активируемая протеазой» касательно активирующей Т-клетки биспецифической молекулы относится к активирующей Т-клетки биспецифической молекуле, которая обладает пониженной способностью или у которой аннулирована способность активировать Т-клетки благодаря маскирующему фрагменту, который снижает или аннулирует способность активирующей Т-клетки биспецифической молекулы связываться с CD3. После диссоциации маскирующего фрагмента путем протеолитического расщепления, например, протеолитического расщепления линкера, который соединяет маскирующий фрагмент с активирующей Т-клетки биспецифической молекулой, связывание с CD3 восстанавливается и тем самым активирующая Т-клетки биспецифическая молекула активируется.
Понятие «обратимое сокрытие» в контексте настоящего описания относится к такому связыванию маскирующего фрагмента или идиотипспецифического полипептида с антигенсвязывающим фрагментом или молекулой, которое мешает связыванию антигенсвязывающего фрагмента или молекулы с его/ее антигеном, например, CD3. Указанное сокрытие является обратимым в том смысле, что идиотипспецифический полипептид может высвобождаться из антигенсвязывающего фрагмента или молекулы, например, в результате расщепления протеазой, и тем самым освобождает антигенсвязывающий фрагмент или молекулу, давая им связываться с их антигеном.
Подробное описание вариантов осуществления изобретения Одним из объектов изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(а) первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3;
(б) второй антигенсвязывающий фрагмент, обладающий способностью специфически связываться с антигеном клетки-мишени; и
(в) маскирующий фрагмент, ковалентно присоединенный к связывающей Т-клетки биспецифической молекуле через расщепляемый протеазой линкер, где маскирующий фрагмент обладает способностью специфически связываться с идиотипом первого или второго антигенсвязывающего фрагмента, обеспечивая тем самым обратимое сокрытие первого или второго антигенсвязывающего фрагмента.
Первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3, содержит идиотип. В одном из вариантов осуществления изобретения маскирующий фрагмент активируемой протеазой активирующей Т-клетки биспецифической молекулы ковалентно присоединен к первому антигенсвязывающему фрагменту. В одном из вариантов осуществления изобретения маскирующий фрагмент ковалентно присоединен к вариабельной области тяжелой цепи первого антигенсвязывающего фрагмента. В одном из вариантов осуществления изобретения маскирующий фрагмент ковалентно присоединен к вариабельной области легкой цепи первого антигенсвязывающего фрагмента. Указанная ковалентная связь отличается от специфической связи маскирующего фрагмента с идиотипом первого антигенсвязывающего сайта, которая предпочтительно является нековалентной. Идиотип первого антигенсвязывающего фрагмента содержит его вариабельную область. В одном из вариантов осуществления изобретения маскирующий фрагмент связывается с аминокислотными остатками, которые обеспечивают контакт с CD3, когда первый антигенсвязывающий фрагмент связывается с CD3. В предпочтительном варианте осуществления изобретения маскирующий фрагмент не представляет собой когнатный антиген или его фрагменты первого антигенсвязывающего фрагмента, т.е. маскирующий фрагмент не представляет собой CD3 или его фрагменты. В одном из вариантов осуществления изобретения маскирующий фрагмент представляет собой антиидиотипическое антитело или его фрагмент. В одном из вариантов осуществления изобретения маскирующий фрагмент представляет собой антиидиотипический scFv. Приведенные в качестве примера варианты маскирующих фрагментов, которые представляют собой антиидиотипический scFv, и активируемых протеазой активирующих Т-клетки молекул, содержащих указанные маскирующие фрагменты, подробно описаны в примерах.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит второй маскирующий фрагмент, который обратимо скрывает второй антигенсвязывающий фрагмент.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, и который содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19;
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с антигеном клетки-мишени.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 55.
В конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolRl и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 157, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 158.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 32, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 33.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 115, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 116.
В конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В другом конкретном варианте осуществления изобретения второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19;
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55,
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19;
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55,
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 157, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 158.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19;
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с HER1, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55,
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с HER1, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 115, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 116.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области легкой цепи Fab и тяжелой цепи Fab обменены.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19;
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с мезотелином, содержащий по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
Одним из вариантов настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с CD3, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55,
(II) второй антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с мезотелином, содержащий вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
В одном из вариантов осуществления изобретения второй антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой константные области легкой цепи Fab и тяжелой цепи Fab обменены, а второй антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab. В другом конкретном варианте осуществления изобретения первый и второй антигенсвязывающие фрагменты слиты друг с другом, необязательно через пептидный линкер.
В конкретных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула дополнительно содержит Fc-домен, состоящий из первой и второй субъединиц, которые обладают способностью к стабильной ассоциации.
В другом конкретном варианте осуществления изобретения не более одного антигенсвязывающего фрагмента, обладающего способностью специфически связываться с CD3, присутствует в активируемой протеазой активирующей Т-клетки биспецифической молекуле (т.е. активируемая протеазой активирующая Т-клетки биспецифическая молекула характеризуется одновалентным связыванием с CD3).
Форматы активируемой протеазой активирующей Т-клетки биспецифической молекулы
Компоненты активируемой протеазой активирующей Т-клетки биспецифической молекулы можно сливать друг с другом в различных конфигурациях. Примеры конфигурацией представлены на фиг. 1А-Д и 5А-3. Дополнительные примеры конфигураций представлены на фиг. 33А-Л.
В конкретных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит Fc-домен, состоящий из первой и второй субъединиц, которые обладают способностью к стабильной ассоциации. В некоторых вариантах осуществления изобретения второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена.
В одном из указанных вариантов осуществления изобретения первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента. В конкретном указанном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула практически состоит из первого и второго антигенсвязывающих фрагментов, Fc-домена, состоящего и первой и второй субъединиц, и необязательно одного или нескольких пептидных линкеров, в которой первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента, а второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена. Необязательно легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента могут быть дополнительно слиты друг с другом.
В другом указанном варианте осуществления изобретения первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена. В конкретном указанном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула практически состоит из первого и второго антигенсвязывающих фрагментов, Fc-домена, состоящего и первой и второй субъединиц, и необязательно одного или нескольких пептидных линкеров, в которой первый и второй антигенсвязывающий фрагмент каждый слит на С-конце тяжелой цепи Fab с N-концом одной из субъединиц Fc-домена.
В других вариантах осуществления изобретения первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена.
В конкретном указанном варианте осуществления изобретения второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента. В конкретном указанном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула практически состоит из первого и второго антигенсвязывающих фрагментов, Fc-домена, состоящего и первой и второй субъединиц, и необязательно одного или нескольких пептидных линкеров, в которой второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента, а первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена. Необязательно легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента могут быть дополнительно слиты друг с другом.
Антигенсвязывающие фрагменты могут быть слиты с Fc-доменом или друг с другом непосредственно или через пептидный линкер, содержащий одну или несколько аминокислот, как правило, примерно 2-20 аминокислот. Пептидные линкеры известны в данной области, и они представлены в настоящем описании. Пригодные неиммуногенные пептидные линкеры включают, например, пептидные линкеры (G4S)n, (SG4)n, (G4S)n или G4(SG4)n. Как правило, «n» обозначает число от 1 до 10, как правило, от 2 до 4. Наиболее пригодным пептидным линкером для слияния друг с другом легких цепей Fab первого и второго антигенсвязывающих фрагментов является (G4S)2. Примером пептидного линкера, пригодного для соединения тяжелых цепей Fab первого и второго антигенсвязывающих фрагментов является EPKSC(D)-(G4S)2 (SEQ ID NO: 105 и 106). Линкеры могут дополнительно содержать шарнирную область иммуноглобулина (ее часть). В частности, когда антигенсвязывающий фрагмент слит с N-концом субъединицы Fc-домена, то он может быть слит посредством шарнирной области иммуноглобулина или ее части с использованием или без использования дополнительного пептидного линкера.
Ценной является активируемая протеазой активирующая Т-клетки биспецифическая молекула с одним антигенсвязывающим фрагментом, который обладает способностью специфически связываться с с антигеном клетки-мишени, прежде всего в случаях, когда ожидается интернализация антигена клетки-мишени после связывания с обладающим высокой аффинностью антигенсвязывающим фрагментом. В таких случаях присутствие нескольких антигенсвязывающих фрагментов, специфических в отношении антигена клетки-мишени, может повышать интернализацию антигена клетки-мишени, снижая тем самым его доступность.
Однако во многих других случаях целесообразно, чтобы активируемая протеазой активирующая Т-клетки биспецифическая молекула содержала два или большее количество антигенсвязывающих фрагментов, специфических в отношении антигена клетки-мишени (см. примеры, представленные на фиг. 5А-З), например, для оптимизации направленного переноса к сайту-мишени или для обеспечения перекрестного сшивания антигенов клетки-мишени.
Так, в некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, дополнительно содержит третий антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с антигеном клетки-мишени. В одном из вариантов осуществления изобретения третий антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab. В одном из вариантов осуществления изобретения третий антигенсвязывающий фрагмент обладает способностью специфически связываться с тем же самым антигеном клетки-мишени, что и второй антигенсвязывающий фрагмент. В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с антигеном клетки-мишени. В конкретном варианте осуществления изобретения второй и третий антигенсвязывающие фрагменты являются идентичными (т.е. они содержат одинаковые аминокислотные последовательности).
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с FolR1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с FolR1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с FolR1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с FolR1, при этом второй и третий антигенсвязывающие фрагменты содержат вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 115, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 116.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER2, при этом второй антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 142, SEQ ID NO: 143 и SEQ ID NO: 144, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150, а третий антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 145, SEQ ID NO: 146 и SEQ ID NO: 147, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER2, при этом второй антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 142, SEQ ID NO: 143 и SEQ ID NO: 144, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150, а третий антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 145, SEQ ID NO: 146 и SEQ ID NO: 147, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER2, при этом второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 160, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161, а третий антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 159, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с мезотелином, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с мезотелином, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с мезотелином, при этом второй и третий антигенсвязывающие фрагменты содержат вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
В одном из вариантов осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3, а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В конкретном варианте осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19; а второй и третий антигенсвязывающие фрагменты обладают способностью специфически связываться с HER1, при этом второй и третий антигенсвязывающие фрагменты содержат по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения третий антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой или второй субъединицы Fc-домена. В более конкретном варианте осуществления изобретения второй и третий антигенсвязывающий фрагмент каждый слит на С-конце тяжелой цепи Fab с N-концом одной из субъединиц Fc-домена, в первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента. Необязательно легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента могут быть дополнительно слиты друг с другом.
Второй и третий антигенсвязывающие фрагменты могут быть слиты с Fc-доменом непосредственно или через пептидный линкер. В конкретном варианте осуществления изобретения второй и третий антигенсвязывающий фрагмент каждый слит с Fc-доменом через шарнирную область иммуноглобулина. В конкретном варианте осуществления изобретения шарнирная область иммуноглобулина представляет собой шарнирную область человеческого IgG1. В одном из вариантов осуществления изобретения второй и третий антигенсвязывающие фрагменты и Fc-домен представляют собой часть молекулы иммуноглобулина. В конкретном варианте осуществления изобретения молекула иммуноглобулина представляет собой иммуноглобулин IgG-класса. В еще более конкретном варианте осуществления изобретения иммуноглобулин представляет собой иммуноглобулин IgG1-подкласса. В другом варианте осуществления изобретения иммуноглобулин представляет собой иммуноглобулин IgG4-подкласса. В другом варианте осуществления изобретения иммуноглобулин представляет собой человеческий иммуноглобулин. В других вариантах осуществления изобретения иммуноглобулин представляет собой химерный иммуноглобулин или гуманизированный иммуноглобулин. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула состоит в основном из молекулы иммуноглобулина, которая обладает способностью специфически связываться с антигеном клетки-мишени, и антигенсвязывающего фрагмента, который обладает способностью специфически связываться с CD3, в которой антигенсвязывающий фрагмент представляет собой молекулу Fab, прежде всего кроссовер-молекулу Fab, слитую с N-концом одной из тяжелых цепей иммуноглобулина, необязательно через пептидный линкер.
В конкретном варианте осуществления изобретения первый и третий антигенсвязывающий фрагмент каждый слит на С-конце тяжелой цепи Fab с N-концом одной из субъединиц Fc-домена, а второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента. В указанном конкретном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула практически состоит из первого, второго и третьего антигенсвязывающих фрагментов, Fc-домена, состоящего из первой и второй субъединиц, и необязательно одного или нескольких пептидных линкеров, в которой второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента, а первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой субъединицы Fc-домена, и в которой третий антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом второй субъединицы Fc-домена. Необязательно легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента могут быть дополнительно слиты друг с другом.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит гипервариабельный участок (CDR) 1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, CDR 2 легкой цепи, имеющий SEQ ID NO: 18, и CDR 3 легкой цепи, имеющий SEQ ID NO: 19, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, которая содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 14, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 15, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 16, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, легкой цепи, имеющий CDR 2 SEQ ID NO: 18, и CDR3 легкой цепи, имеющий SEQ ID NO: 19.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит гипервариабельный участок (CDR) 1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, CDR 2 легкой цепи, имеющий SEQ ID NO: 18, и CDR 3 легкой цепи, имеющий SEQ ID NO: 19, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, которая содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 151, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 152, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 153, CDR 1 легкой цепи, имеющий SEQ ID NO: 154, легкой цепи, имеющий CDR 2 SEQ ID NO: 155, и CDR 3 легкой цепи, имеющий SEQ ID NO: 156.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с FolR1, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 157, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 158.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит гипервариабельный участок (CDR) 1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, CDR 2 легкой цепи, имеющий SEQ ID NO: 18, и CDR 3 легкой цепи, имеющий SEQ ID NO: 19, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с HER1, которая содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 56, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 57, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 58, CDR 1 легкой цепи, имеющий SEQ ID NO: 59, легкой цепи, имеющий CDR 2 SEQ ID NO: 60, и CDR3 легкой цепи, имеющий SEQ ID NO: 61.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с HER1, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 115, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 116.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит гипервариабельный участок (CDR) 1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, CDR 2 легкой цепи, имеющий SEQ ID NO: 18, и CDR 3 легкой цепи, имеющий SEQ ID NO: 19, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с HER2, где второй антигенсвязывающий фрагмент содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 142, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 143, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 144, CDR 1 легкой цепи, имеющий SEQ ID NO: 148, легкой цепи, имеющий CDR 2 SEQ ID NO: 149, и CDR3 легкой цепи, имеющий SEQ ID NO: 150, и где третий антигенсвязывающий фрагмент содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 145, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 146, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 147, CDR 1 легкой цепи, имеющий SEQ ID NO: 148, легкой цепи, имеющий CDR 2 SEQ ID NO: 149, и CDR 3 легкой цепи, имеющий SEQ ID NO:150.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с HER2, где второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 160, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161, и где третий антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 159, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 161.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит гипервариабельный участок (CDR) 1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR 1 легкой цепи, имеющий SEQ ID NO: 17, CDR 2 легкой цепи, имеющий SEQ ID NO: 18, и CDR 3 легкой цепи, имеющий SEQ ID NO: 19, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с мезотелином, которая содержит CDR 1 тяжелой цепи, имеющий SEQ ID NO: 107, CDR 2 тяжелой цепи, имеющий SEQ ID NO: 108, CDR 3 тяжелой цепи, имеющий SEQ ID NO: 109, CDR 1 легкой цепи, имеющий SEQ ID NO: 110, легкой цепи, имеющий CDR 2 SEQ ID NO: 111, и CDR 3 легкой цепи, имеющий SEQ ID NO: 112.
Одним из вариантов осуществления настоящего изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(I) первый антигенсвязывающий фрагмент, представляющий собой молекулу Fab, обладающую способностью специфически связываться с CD3, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55, где первый антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области, прежде всего константные области, легкой цепи Fab и тяжелой цепи Fab обменены;
(II) второй и третий антигенсвязывающие фрагменты, каждый из которых представляет собой молекулу Fab, обладающую способностью специфически связываться с мезотелином, которая содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
Активируемая протеазой активирующая Т-клетки биспецифическая молекула по любому из десяти указанных выше вариантов осуществления изобретения может содержать также (III) Fc-домен, состоящий из первой и второй субъединиц, которые обладают способностью к стабильной ассоциации, в которой второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента, а первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом первой субъединицы Fc-домена и в которой третий антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом второй субъединицы Fc-домена.
В некоторых активируемых протеазой активирующих Т-клетки биспецифических молекулах, предлагаемых в изобретении, легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагмента слиты друг с другом, необязательно через линкерный пептид. В зависимости от конфигурации первого и второй антигенсвязывающих фрагментов легкая цепь Fab первого антигенсвязывающего фрагмента может быть слита на ее С-конце с N-концом легкой цепи Fab второго антигенсвязывающего фрагмента или легкая цепь Fab второго антигенсвязывающего фрагмента может быть слита на ее С-конце с N-концом легкой цепи Fab первого антигенсвязывающего фрагмента. Слияние легких цепей Fab первого и второго антигенсвязывающих фрагментов может дополнительно снижать ошибочное спаривание несоответствующих тяжелых и легких цепей Fab, а также уменьшать количество плазмид, необходимых для экспрессии некоторых активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором вариабельная область легкой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой вариабельная область тяжелой цепи заменена вариабельной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VL(1)-CH1(1)-CH2-CH3(-CH4)), и полипептид, в котором тяжелая цепь Fab второго антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(2)-CH1(2)-CH2-CH3(-CH4)). В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула дополнительно содержит полипептид, в котором вариабельная область тяжелой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента (VH(1)-CL(1)), и полипептид легкой цепи Fab второго антигенсвязывающего фрагмента (VL(2)-CL(2)). В некоторых вариантах осуществления изобретения полипептиды ковалентно связаны, например, дисульфидной связью.
В альтернативных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором вариабельная область тяжелой цепи Fab первого антигенсвязывающего объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой константная область тяжелой цепи заменена константной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(1)-CL(1)-СН2-СН3(-СН4)), и полипептид, в котором тяжелая цепь Fab второго антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(2)-CH1(2)-CH2-CH3(-CH4)). В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит дополнительно полипептид, в котором вариабельная область легкой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (VL(1)-CH1(1)), и полипептид легкой цепи Fab второго антигенсвязывающего фрагмента (VL(2)-CL(2)). В некоторых вариантах осуществления изобретения полипептиды ковалентно связаны, например, дисульфидной связью.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором вариабельная область легкой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой вариабельная область тяжелой цепи замена вариабельной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с тяжелой цепью Fab второго антигенсвязывающего фрагмента, который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VL(1)-CH1(1)-VH(2)-CH1(2)-CH2-CH3(-CH4)). В других вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором вариабельная область тяжелой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой константная область тяжелой цепи замена константной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с тяжелой цепью Fab второго антигенсвязывающего фрагмента, который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(1)-CL(1)-VH(2)-CH1(2)-CH2-CH3(-CH4)). В следующих вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором тяжелая цепь Fab второго антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с вариабельной областью легкой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой вариабельная область тяжелой цепи замена вариабельной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(2)-CH1(2)-VL(1)-CH1(1)-CH2-CH3(-CH4)). В других вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид, в котором тяжелая цепь Fab второго антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с вариабельной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с константно областью легкой цепи Fab первого антигенсвязывающего фрагмента (т.е. первый антигенсвязывающий фрагмент содержит тяжелую цепь кроссовер-молекулы Fab, в которой константная область тяжелой цепи замена константной областью легкой цепи), который в свою очередь объединен карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(2)-CH1(2)-VH(1)-CL(1)-CH2-CH3(-CH4)).
В некоторых из указанных вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептид содержит дополнительно полипептид легкой цепи кроссовер-молекулы Fab первого антигенсвязывающего фрагмента, в котором вариабельная область тяжелой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента (VH(1)-CL(1)), и полипептид легкой цепи Fab второго антигенсвязывающего фрагмента (VL(2)-CL(2)). В других указанных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит дополнительно полипептид легкой цепи кроссовер-молекулы Fab, в которой вариабельная область легкой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (VL(1)-CH1(1)), и полипептид легкой цепи Fab второго антигенсвязывающего фрагмента (VL(2)-CL(2)). В других указанных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит дополнительно полипептид вариабельной области легкой цепи Fab первого антигенсвязывающего фрагмента, которая объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с полипептидом легкой цепи Fab второго антигенсвязывающего фрагмента (VL(1)-CH1(1)-VL(2)-CL(2)), полипептид, в котором вариабельная область тяжелой цепи Fab первого антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с полипептидом легкой цепи Fab второго антигенсвязывающего фрагмента (VH(1)-CL(1)-VL(2)-CL(2)), полипептид, в котором полипептид легкой цепи Fab второго антигенсвязывающего фрагмента объединен карбоксиконцевой пептидной связью с вариабельной областью легкой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с константной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента (VL(2)-CL(2)-VL(1)-CH1(1)), или полипептид, в котором полипептид легкой цепи Fab второго антигенсвязывающего фрагмента объединен карбоксиконцевой пептидной связью с вариабельной областью тяжелой цепи Fab первого антигенсвязывающего фрагмента, которая в свою очередь объединена карбоксиконцевой пептидной связью с константной областью легкой цепи Fab первого антигенсвязывающего фрагмента (VL(2)-CL(2)-VH(1)-CL(1)).
Активируемая протеазой активирующая Т-клетки биспецифическая молекула согласно указанным вариантам осуществления изобретения может содержать дополнительно (I) полипептид субъединицы Fc-домена (СН2-СН3(-СН4)), или (II) полипептид, в котором тяжелая цепь Fab третьего антигенсвязывающего фрагмента объединена карбоксиконцевой пептидной связью с субъединицей Fc-домена (VH(3)-CH1(3)-CH2-CH3(-CH4)), и полипептид легкой цепи Fab третьего антигенсвязывающего фрагмента (VL(3)-CL(3)). В некоторых вариантах осуществления изобретения полипептиды ковалентно связаны, например, дисульфидной связью.
Согласно любому из указанных выше вариантов осуществления изобретения компоненты активируемой протеазой активирующей Т-клетки биспецифической молекулы (например, антигенсвязывающий фрагмент, Fc-домен) могут быть слиты непосредственно или через различные линкеры, прежде всего пептидные линкеры, содержащие одну или несколько аминокислот, как правило, примерно 2-20 аминокислот, которые указаны в настоящем описании и известны в данной области. Пригодные неиммуногенные пептидные линкеры включают, например, пептидные линкеры (G4S)n, (SG4)n, (G4S)n или G4(SG4)n, где, как правило, «n» обозначает число от 1 до 10, как правило, от 2 до 4.
Fc-домен
Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы состоит из пары полипептидных цепей, содержащих домены тяжелой цепи молекулы иммуноглобулина. Например, Fc-домен молекулы иммуноглобулина G (IgG) представляет собой димер, каждая субъединица которого содержит константные домены СН2 и СН3 тяжелой цепи IgG. Две субъединицы Fc-домена обладают способностью к стабильной ассоциации друг с другом. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, содержит не более одного Fc-домена.
В одном из вариантов осуществления изобретения Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы представляет собой Fc-домен IgG. В конкретном варианте осуществления изобретения Fc-домен представляет собой Fc-домен IgG1. В другом варианте осуществления изобретения Fc-домен представляет собой Fc-домен IgG4. В более конкретном варианте осуществления изобретения Fc-домен представляет собой Fc-домен IgG4, содержащий аминокислотную замену в положении S228 (нумерация по Кэботу), прежде всего аминокислотную замену S228P. Указанная аминокислотная замена снижает in vivo обмен в Fab-плече антител в виде IgG4 (см. Stubenrauch и др., Drug Metabolism and Disposition 38, 2010, cc. 84-91). В другом конкретном варианте осуществления изобретения Fc-домен является человеческим.
Модификации Fc-домена. способствующие гетеродимеризации
Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, содержат различные антигенсвязывающие фрагменты, слитые с одной или другой из двух субъединиц Fc-домена, при этом две субъединицы Fc-домена, как правило, содержатся в двух неидентичных полипептидных цепях. Рекомбинантная совместная экспрессия этих полипептидов и последующая димеризация приводит к нескольким возможным комбинациям двух полипептидов. Для повышения выхода и чистоты активируемых протеазой активирующих Т-клетки биспецифических молекул при их получении методами рекомбинации целесообразно интродуцировать в Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы модификацию, которая способствует ассоциации требуемых полипептидов.
Таким образом, в конкретных вариантах осуществления изобретения Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, содержит модификацию, которая способствует ассоциации первой и второй субъединиц Fc-домена. Сайт наиболее сильного белок-белкового взаимодействия двух субъединиц Fc-домена человеческого IgG находится в СН3-домене Fc-домена. Таким образом, в одном из вариантов осуществления изобретения указанная модификация находится в СН3-домене Fc-домена.
В конкретном варианте осуществления изобретения указанная модификация представляет собой так называемую модификацию типа «knob-in-hole» (типа «выступ-впадина»), которая включает модификацию, приводящую к образованию «выступа» на одной из двух субъединиц Fc-домена и модификацию, приводящую к образованию «впадины» в другой одной из двух субъединиц Fc-домена.
Технология «knob-into-hole» описана, например, в US №5731168; US №7695936; у Ridgway и др., Prot Eng 9, 1996, сс. 617-621 и Carter, J Immunol Meth 248, 2001, сс. 7-15. В целом, метод включает интродукцию выпуклости («выступ») на поверхности раздела первого полипептида и соответствующей полости («впадина») в поверхности раздела второго полипептида, в результате выпуклость может помещаться в полость, способствуя тем самым образованию гетеродимера и препятствуя образованию гомодимера. Выпуклости конструируют путем замены аминокислот с небольшими боковыми цепями на поверхности раздела первого полипептида на аминокислоты с более крупными боковыми цепями (например, на тирозин или триптофан). Компенсирующие полости идентичного или сходного с выпуклостями размера создают в поверхности раздела второго полипептида путем замены аминокислот с крупными боковыми цепями на аминокислоты с менее крупными боковыми цепями (например, аланин или треонин).
Таким образом, в конкретном варианте осуществления изобретения в СН3-домене первой субъединицы Fc-домена активируемой протеазой активирующей Т-клетки биспецифической молекулы аминокислотный остаток заменен аминокислотным остатком, который имеет больший объем боковой цепи, что приводит к образованию выпуклости на СН3-домене первой субъединицы, которая может помещаться в полость в СН3-домене второй субъединицы, и в СН3-домене второй субъединицы Fc-домена аминокислотный остаток заменен аминокислотным остатком, который имеет меньший объем боковой цепи, что приводит к образованию полости в СН3-домене второй субъединицы, в которую может помещаться выпуклость на СН3-домене первой субъединицы.
Выпуклость и полость можно создавать путем изменения нуклеиновых кислот, кодирующих полипептиды, например, с помощью сайтнаправленного мутагенеза или путем пептидного синтеза.
В конкретном варианте осуществления изобретения в СН3-домене первой субъединицы Fc-домена остаток треонина в положении 366 заменен остатком триптофана (T366W), а в СН3-домене второй субъединицы Fc-домена остаток тирозина в положении 407 заменен на остаток валина (Y407V). В одном из вариантов осуществления изобретения во второй субъединице Fc-домена дополнительно остаток треонина в положении 366 заменен на остаток серина (T366S) и остаток лейцина в положении 368 заменен на остаток аланина (L368A).
В следующем варианте осуществления изобретения в первой субъединице Fc-домена дополнительно остаток серина в положении 354 заменен на остаток цистеина (S354C), а во второй субъединице Fc-домена дополнительно остаток тирозина в положении 349 заменен на остаток цистеина (Y349C). Интродукция указанных двух остатков цистеина приводит к образованию дисульфидного мостика между двумя субъединицами Fc-домена, тем самым дополнительно стабилизируя димер (Carter, J Immunol Methods 248, 2001, cc. 7-15).
В конкретном варианте осуществления изобретения антигенсвязывающий фрагмент, обладающий способностью связываться с CD3, слит (необязательно через антигенсвязывающий фрагмент, обладающий способностью связываться с антигеном клетки-мишени) с первой субъединицей Fc-домена (которая содержит модификацию, приводящую к образованию «выступа»). Не вдаваясь в какую-либо теорию, слияние антигенсвязывающего фрагмента, обладающего способностью связываться с CD3, с содержащей «выступ» субъединицей Fc-домена должно (дополнительно) минимизировать образование антигенсвязывающих молекул, содержащих два антигенсвязывающих фрагмента, обладающих способностью связываться с CD3 (стерическое «столкновение» двух содержащих «выступ» полипептидов).
В альтернативном варианте осуществления изобретения модификация, способствующая ассоциации первой и второй субъединиц Fc-домена, представляет собой модификацию, опосредующую определяемые электростатическим действием воздействия, например, описанные в публикации РСТ WO 2009/089004. В целом, указанный метод включает замену одного или нескольких аминокислотных остатков на поверхности раздела двух субъединиц Fc-домена на заряженные аминокислотные остатки, в результате чего образование гомодимера становится электростатически невыгодным, а гетеродимеризация становится электростатически выгодной.
Модификации Fc-домена, приводящие к снижению связывания с Fc-рецептором и/или эффекторной функции
Fc-домен придает активируемой протеазой активирующей Т-клетки биспецифической антигенсвязывающей молекуле предпочтительные фармакокинетические свойства, включая продолжительное время полужизни в сыворотке, что обеспечивает хорошее накопление в ткани-мишени и предпочтительное соотношение распределения в ткани-крови. Однако в то же время он может приводить к нежелательной направленности активируемой протеазой активирующей Т-клетки биспецифической молекулы к клеткам, которые экспрессируют Fc-рецепторы, а не к предпочтительным несущим антиген клеткам. Кроме того, совместная активация путей передачи сигналов Fc-рецептора может приводить к высвобождению цитокинов, что в сочетании с обусловливающими активацию Т-клеток свойствами и продолжительным временем полужизни антигенсвязывающей молекулы приводит к избыточной активации цитокиновых рецепторов и серьезным побочным действиям при системном введении. Активация (несущих Fc-рецептор) иммунных клеток, отличных от Т-клеток, может даже снижать эффективность активируемой протеазой активирующей Т-клетки биспецифической молекулы из-за возможной деструкции Т-клеток, например, NK-клетками.
Таким образом, согласно конкретным вариантам осуществления изобретения Fc-домен активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, обладает пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с нативным Fc-доменом IgG1. В одном из указанных вариантов осуществления изобретения Fc-домен (или активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая указанный Fc-домен) характеризуется аффинностью связывания, составляющей менее чем 50%, предпочтительно менее чем 20%, более предпочтительно менее чем 10% и наиболее предпочтительно менее чем 5% от аффинности связывания с Fc-рецептором нативного Fc-домена IgG1 (или активируемой протеазой активирующей Т-клетку биспецифической молекулы, содержащей нативный Fc-домен IgG1), и/или эффекторной функцией, составляющей менее чем 50%, предпочтительно менее чем 20%, более предпочтительно менее чем 10% и наиболее предпочтительно менее чем 5% от эффекторной функции нативного Fc-домена IgG1 (или активируемой протеазой активирующей Т-клетки биспецифической молекулы, содержащей нативный Fc-домен IgG1). В одном из вариантов осуществления изобретения Fc-домен (или активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая указанный Fc-домен) практически не связывается с Fc-рецептором и/или не индуцирует эффекторную функцию. В конкретном варианте осуществления изобретения Fc-рецептор представляет собой Fcγ-рецептор. В одном из вариантов осуществления изобретения Fc-рецептор представляет собой человеческий Fc-рецептор. В одном из вариантов осуществления изобретения Fc-рецептор представляет собой активирующий Fc-рецептор. В конкретном варианте осуществления изобретения Fc-рецептор представляет собой активирующий человеческий Fcγ-рецептор, более конкретно человеческий FcγRIIIa, FcγRI или FcγRIIa, наиболее предпочтительно человеческий FcγRIIIa. В одном из вариантов осуществления изобретения эффекторная функция представляет собой одну или несколько функций, выбранных из группы, включающей CDC, ADCC, ADCP и секрецию цитокинов. В конкретном варианте осуществления изобретения эффекторная функция представляет собой ADCC. В одном из вариантов осуществления изобретения Fc-домен характеризуется практической такой же аффинностью связывания с неонатальным Fc-рецептором (FcRn), что и нативный Fc-домен IgG1. Практически такое же связывание с FcRn достигается, когда Fc-домен (или активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая указанный Fc-домен), характеризуется аффинностью связывания, составляющей более чем примерно 70%, предпочтительно более чем примерно 80%, более предпочтительно более чем примерно 90%, от аффинности связывания нативного Fc-домена IgG1 (или активируемой протеазой активирующей Т-клетки биспецифической молекулы, содержащий нативный Fc-домен IgG1) с FcRn.
Согласно некоторым вариантам осуществления изобретения Fc-домен конструируют так, чтобы он обладал пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с не подвергнутым инженерии Fc-доменом. В конкретных вариантах осуществления изобретения Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы содержит одну или несколько аминокислотных мутаций, которые снижают аффинность связывания Fc-домена с Fc-рецептором и/или эффекторную функцию. Как правило, в каждой из двух субъединиц Fc-домена присутствует(ют) одна или несколько одинаковых аминокислотных мутаций. В одном из вариантов осуществления изобретения аминокислотная мутация снижает аффинность связывания Fc-домена с Fc-рецептором. В одном из вариантов осуществления изобретения аминокислотная мутация снижает аффинность связывания Fc-домена с Fc-рецептором по меньшей мере в 2 раза, по меньшей мере в 5 раз или по меньшей мере в 10 раз. Согласно вариантам осуществления изобретения, в которых имеет место более одной аминокислотной мутации, которые снижают аффинность связывания Fc-домена с Fc-рецептором, комбинация указанных аминокислотных мутаций может снижать аффинность связывания Fc-домена с Fc-рецептором по меньшей мерс в 10 раз, по меньшей мере в 20 раз или даже по меньшей мере в 50 раз. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая сконструированный Fc-домен, характеризуется аффинностью связывания, составляющей менее чем 20%, в частности, менее чем 10%, более предпочтительно менее чем 5% от аффинности связывания с Fc-рецептором, характерной для активируемой протеазой активирующей Т-клетки биспецифической молекулы, содержащей не подвергнутый инженерии Fc-домен. В конкретном варианте осуществления изобретения Fc-рецептор представляет собой Fcγ-рецептор. В некоторых вариантах осуществления изобретения Fc-рецептор представляет собой человеческий Fc-рецептор. В некоторых вариантах осуществления изобретения Fc-рецептор представляет собой активирующий Fc-рецептор. В конкретном варианте осуществления изобретения Fc-рецептор представляет собой активирующий человеческий Fc-рецептор, более конкретно человеческий FcγRIIIa, FcγRI или FcγRIIa, наиболее предпочтительно человеческий FcγRIIIa. Предпочтительно уменьшается связывание с каждым из этих рецепторов. Согласно некоторым вариантам осуществления изобретения снижается также аффинность связывания с компонентом системы комплемента, в частности, аффинность связывания с C1q. Согласно одному из вариантов осуществления изобретения не снижается аффинность связывания с неонатальным Fc-рецептором (FcRn). Практически такое же связывание с FcRn, т.е. сохранение аффинности связывания Fc-домена с указанным рецептором, достигается, когда Fc-домен (или активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая указанный Fc-домен) характеризуется аффинностью связывания с FcRn, составляющей более чем примерно 70% от аффинности связывания с FcRn не подвергнутой инженерии формы Fc-домена (или активируемой протеазой активирующей Т-клетки биспецифической молекулы, содержащей указанную не подвергнутую инженерии форму Fc-домена). Fc-домен или активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, содержащие указанный Fc-домен, могут характеризоваться аффинностью, составляющей более чем примерно 80% и даже более чем примерно 90% от указанной выше аффинности. В некоторых вариантах осуществления изобретения Fc-домен активируемой протеазой активирующей Т-клетки биспецифической молекулы создают так, чтобы он обладал пониженной эффекторной функцией по сравнению с не подвергнутым инженерии Fc-доменом. Пониженная эффекторная функция может представлять собой (но, не ограничиваясь только ими) пониженную(ые) одну или несколько из следующих функций: пониженная комплементзависимая цитотоксичность (CDC), пониженная антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), пониженный антитело-обусловленный клеточнозависимый фагоцитоз (ADCP), пониженная секреция цитокинов, пониженное опосредованное иммунным комплексом поглощение антигена антигенпрезентирующими клетками, пониженное связывание с NK-клетками, пониженное связывание с макрофагами, пониженное связывание с моноцитами, пониженное связывание с полиморфоядерными клетками, пониженная непосредственная передача сигнала, индуцирующего апоптоз, пониженное перекрестное сшивание связанных с мишенью антител, пониженное созревание дендритных клеток или пониженное Т-клеточное примирование. В одном из вариантов осуществления изобретения пониженная эффекторная функция представляет собой одну или несколько функций, выбранных из группы, включающей пониженную CDC, пониженную ADCC, пониженный ADCP и пониженную секрецию цитокинов. В конкретном варианте осуществления изобретения пониженная эффекторная функция представляет собой пониженную ADCC. В одном из вариантов осуществления изобретения пониженная ADCC составляет меньше 20% от ADCC, индуцируемой не подвергнутым инженерии Fc-доменом (или активируемой протеазой активирующей Т-клетки биспецифической молекулой, содержащей не подвергнутый инженерии Fc-домен).
В одном из вариантов осуществления изобретения аминокислотная мутация, которая снижает аффинность связывания Fc-домена с Fc-рецептором и/или эффекторную функцию, представляет собой аминокислотную замену. В одном из вариантов осуществления изобретения Fc-домен содержит аминокислотную замену в положении, выбранном из Е233, L234, L235, N297, Р331 и Р329. В более конкретном варианте осуществления изобретения Fc-домен содержит аминокислотную замену в положении, выбранном из L234, L235 и Р329. В некоторых вариантах осуществления изобретения Fc-домен содержит аминокислотные замены L234A и L235A. В одном из указанных вариантов осуществления изобретения Fc-домен представляет собой Fc-домен IgG1, в частности, Fc-домен человеческого IgG1. В одном из вариантов осуществления изобретения Fc-домен содержит аминокислотную замену в положении Р329. В более конкретном варианте осуществления изобретения аминокислотная замена представляет собой Р329А или P329G, прежде всего P329G. В одном из вариантов осуществления изобретения Fc-домен содержит аминокислотную замену в положении Р329 и, кроме того, аминокислотную замену в положении, выбранном из Е233, L234, L235, N297 и Р331. В более конкретном варианте осуществления изобретения дополнительная аминокислотная замена представляет собой Е233Р, L234A, L235A, L235E, N297A, N297D или P331S. В конкретном варианте осуществления изобретения Fc-домен содержит аминокислотные замены в положениях Р329, L234 и L235. В более конкретном варианте осуществления изобретения Fc-домен содержит аминокислотные мутации L234A, L235A и P329G («P329G LALA»). В одном из указанных вариантов осуществления изобретения Fc-домен представляет собой Fc-домен IgG1, прежде всего Fc-домен человеческого IgG1. Комбинация аминокислотных замен «P329G LALA» практически полностью элиминирует связывание с Fcγ-рецептором Fc-домена человеческого IgG1 (а также с комплементом), что описано в публикации РСТ WO 2012/130831, которая полностью включена в настоящее описание в качестве ссылки. В WO 2012/130831 описаны также методы получения указанных мутантных Fc-доменов, методы изучения их свойств, таких как связывание с Fc-рецептором или эффекторные функции.
Антитела подкласса IgG4 обладают пониженной аффинностью к связыванию с Fc-рецепторами и пониженными эффекторными функциями по сравнению с антителами подкласса IgG1. Таким образом, в некоторых вариантах осуществления изобретения Fc-домен активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, представляет собой Fc-домен IgG4, в частности Fc-домен человеческого IgG4. В одном из вариантов осуществления изобретения Fc-домен IgG4 содержит аминокислотные замены в положении S228, конкретно аминокислотную замену S228P. Для дополнительного снижения аффинности связывания с Fc-рецептором и/или его эффекторной функции в одном из вариантов осуществления изобретения Fc-домен IgG4 содержит аминокислотную замену в положении L235, в частности, аминокислотную замену L235E. В другом варианте осуществления изобретения Fc-домен IgG4 содержит аминокислотную замену в положении Р329, в частности, аминокислотную замену P329G. В конкретном варианте осуществления изобретения Fc-домен IgG4 содержит аминокислотные замены в положениях S228, L235 и Р329, в частности, аминокислотные замены S228P, L235E и P329G. Указанные мутанты Fc-домена IgG4 и их особенности связывания с Fcγ-рецептором описаны в публикации РСТ WO 2012/130831, которая полностью включена в настоящее описание в качестве ссылки.
В конкретном варианте осуществления изобретения Fc-домен, характеризующийся пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с нативным Fc-доменом IgG1, представляет собой Fc-домен человеческого IgG1, содержащий аминокислотные замены L234A, L235A и необязательно P329G, или Fc-домен человеческого IgG4, содержащий аминокислотные замены S228P, L235E и необязательно P329G.
В некоторых вариантах осуществления изобретения элиминировали N-гликозилирование Fc-домена. В одном из указанных вариантов осуществления изобретения Fc-домен содержит аминокислотную мутацию в положении N297, в частности, аминокислотную замену аспарагина на аланин (N297A) или аспарагиновую кислоту (N297D).
Помимо Fc-доменов, описанных выше и в публикации РСТ WO 2012/130831, Fc-домены с пониженной способностью связываться с Fc-рецептором и/или эффекторной функцией включают также Fc-домены с заменой одного или нескольких остатков 238, 265, 269, 270, 297, 327 и 329 (US №6737056). К указанным мутантам Fc относятся мутанты Fc с заменами в двух или большем количестве из аминокислотных положений 265, 269, 270, 297 и 327, включая так называемый мутант Fc-домена «DANA» с заменой остатков 265 и 297 на аланин (US №7332581).
Мутантные Fc-домены можно получать путем аминокислотной делеции, замены, инсерции или модификации с использованием генетических или химических методов, хорошо известных в данной области. Генетические методы могут включать сайтнаправленный мутагенез кодирующей ДНК последовательности, ПЦР, синтез генов и т.п. Правильность нуклеотидных замен можно подтверждать, например, секвенированием.
Связывание с Fc-рецепторами можно легко определять, например, с помощью ELISA или поверхностного плазмонного резонанса (SPR) с использованием стандартного оборудования, такого как устройство BIAcore (фирма GE Healthcare), и с применением таких Fc-рецепторов, которые можно получать методом рекомбинантной экспрессии. Приемлемый указанный анализ связывания представлен в настоящем описании. Альтернативно этому, аффинность связывания Fc-доменов или активирующих клетки биспецифических антигенсвязывающих молекул, содержащих Fc-домен, с Fc-рецепторами можно оценивать с использованием клеточных линий, для которых известно, что они экспрессируют конкретные Fc-рецепторы, такие как человеческие NK-клетки, экспрессирующие FcγIIIa-рецептор.
Эффекторную функцию Fc-домена или активируемой протеазой активирующей Т-клетки биспецифической молекулы, содержащей Fc-домен, можно оценивать методами, известными в данной области. Приемлемый анализ для оценки ADCC представлен в настоящем описании. Другие примеры анализов in vitro, предназначенных для оценки ADCC-активности представляющей интерес молекулы, описаны в US №5500362; у Hellstrom и др., Proc Natl Acad Sci USA 83, 1986, сс. 7059-7063 и Hellstrom и др., Proc Natl Acad Sci USA 82, 1985, сс. 1499-1502; US №5821337; у Bruggemann и др., J Exp Med 166, 1987, сс. 1351-1361. Альтернативно этому, можно применять методы, основанные на нерадиоактивном анализе (см., например, ACTI™ - нерадиоактивный анализ цитотоксичности с помощью проточной цитометрии (фирма CellTechnology, Inc. Маунтин-Вью, шт. Калифорния); и CytoTox 96® - нерадиоактивный анализ цитотоксичности (фирма Promega, Мэдисон, шт. Висконсин)). Приемлемыми эффекторными клетками для таких анализов являются мононуклеарные клетки периферической крови (РВМС) и естественные клетки-киллеры (NK). В альтернативном или дополнительном варианте ADCC-активность представляющей интерес молекулы можно оценивать in vivo, например, с использованием созданных на животных моделей, описанных у Clynes и др., Proc Natl Acad Sci USA 95, 1998, сс. 652-656.
В некоторых вариантах осуществления изобретения снижают связывание Fc-домена с компонентом системы комплемента, в частности с C1q. Таким образом, в некоторых вариантах осуществления изобретения, в которых Fc-домен конструируют так, чтобы он обладал пониженной эффекторной функцией, указанная пониженная эффекторная функция включает пониженную CDC. Можно осуществлять анализы связывания C1q для решения вопроса о том, может ли активируемая протеазой активирующая Т-клетки биспецифическая молекула связываться с C1q и, как следствие, обладает ли она CDC-активностыо (см., например, анализы связывания с C1q и С3с, которые проводят с помощью ELISA, описанные в WO 2006/029879 и WO 2005/100402). Для оценки активации комплемента можно осуществлять анализ CDC (см., например, Gazzano-Santoro и др., J Immunol Methods 202, 1996, с. 163; Cragg и др., Blood 101, 2003, сс. 1045-1052 и Cragg и Glennie, Blood 103, 2004, сс. 2738-2743).
Антигенсвязывающие фрагменты
Антигенсвязывающая молекула, предлагаемая в изобретении, является биспецифической, т.е. она содержит по меньшей мере два антигенсвязывающих фрагмента, обладающих способностью специфически связываться с двумя различными антигенными детерминантами. Согласно изобретению антигенсвязывающие фрагменты представляют собой молекулы Fab (т.е. антигенсвязывающие домены, состоящие из тяжелой и легкой цепей, каждая из которых содержит вариабельную и константную области). В одном из вариантов осуществления изобретения указанные молекулы Fab являются человеческими. В другом варианте осуществления изобретения указанные молекулы Fab являются гуманизированными. Еще в одном варианте осуществления изобретения указанные молекулы Fab содержат человеческие константные области тяжелой и легкой цепей.
По меньшей мере один из антигенсвязывающих фрагментов представляет собой кроссовер-молекулу Fab. Указанная модификация препятствует ошибочному спариванию тяжелых и легких цепей из различных молекул Fab, повышая тем самым выход и чистоту активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, при производстве рекомбинантных молекул. В частности, в кроссовер-молекуле Fab, которую можно применять для создания активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, константные области легкой цепи Fab и тяжелой цепи Fab обменены. В другом варианте кроссовер-молекулы Fab, которую можно применять для создания активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, обменены вариабельные области легкой цепи Fab и тяжелой цепи Fab.
В конкретном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, обладает способностью одновременно связываться с антигеном клетки-мишени, в частности, антигеном опухолевой клетки, и CD3. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула обладает способностью перекрестно сшивать Т-клетку и клетку-мишень путем одновременного связывания с антигеном клетки-мишени и CD3. В еще более конкретном варианте осуществления изобретения указанное одновременное связывание приводит к лизису клетки-мишени, в частности, опухолевой клетки. В одном из вариантов осуществления изобретения указанное одновременное связывание приводит к активации Т-клетки. В других вариантах осуществления изобретения указанное одновременное связывание приводит к клеточному ответу Т-лимфоцита, в частности, цитотоксического Т-лимфоцита, выбранному из следующей группы: пролиферация, дифференцировка, секреция цитокинов, высвобождение эффекторной молекулы, цитотоксическая активность и экспрессия маркеров активации. В одном из вариантов осуществления изобретения связывание активируемой протеазой активирующей Т-клетки биспецифической молекулы с CD3 без одновременного связывания с антигеном клетки-мишени не приводит к Т-клеточной активации.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула обладает способностью перенаправлять цитотоксическую активность Т-клетки на клетку-мишень. В конкретном варианте осуществления изобретения указанная перенаправленность не зависит от опосредуемой ГКГС презентации пептидного антигена клеткой-мишенью и/или от специфичности Т-клетки.
В частности, согласно некоторым вариантам осуществления изобретения Т-клетка представляет собой цитотоксическую Т-клетку. В некоторых вариантах осуществления изобретения Т-клетка представляет собой CD4+ - или CD8+ -T-клетку, прежде всего CD8+ -Т-клетку.
CD3-связывающий фрагмент
Активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, содержит по меньшей мере один антигенсвязывающий фрагмент, обладающий способностью связываться с CD3 (в настоящее описании его обозначают также как «связывающий антиген CD3 фрагмент» или «первый антигенсвязывающий фрагмент»). В конкретном варианте осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит не более одного антигенсвязывающего фрагмента, обладающего способностью специфически связываться с CD3. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула характеризуется одновалентным связыванием с CD3. Связывающая антиген CD3 молекула представляет собой кроссовер-молекулу Fab, т.е. молекулу Fab, в которой либо вариабельные, либо константные области тяжелых и легких цепей Fab обменены. В вариантах осуществления изобретения, в которых не более одного антигенсвязывающего фрагмента, обладающего способностью специфически связываться с антигеном клетки-мишени, входит в активируемую протеазой активирующую Т-клетки биспецифическую молекулу, антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3, предпочтительно представляет собой кроссовер-молекулу Fab, а антигенсвязывающие фрагменты, обладающие способностью специфически связываться с антигеном клетки-мишени, представляют собой канонические молекулы Fab.
В конкретном варианте осуществления изобретения CD3 представляет собой CD3 человека или CD3 обезьян циномолгус, более конкретно, человеческий CD3. В конкретном варианте осуществления изобретения связывающий антиген CD3 фрагмент обладает перекрестной реактивностью с (т.е. специфически связывается с) CD3 человека и обезьян циномолгус. В некоторых вариантах осуществления изобретения первый антигенсвязывающий фрагмент обладает способностью специфически связываться с эпсилон-субъединицей CD3.
Связывающий антиген CD3 фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 11, SEQ ID NO: 12 и SEQ ID NO: 13, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19.
В одном из вариантов осуществления изобретения связывающий антиген CD3 фрагмент содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 11, CDR2 тяжелой цепи, имеющий SEQ ID NO: 12, CDR3 тяжелой цепи, имеющий SEQ ID NO: 13, CDR1 легкой цепи, имеющий SEQ ID NO: 17, CDR2 легкой цепи, имеющий SEQ ID NO: 18, и CDR3 легкой цепи, имеющий SEQ ID NO: 19.
В одном из вариантов осуществления изобретения связывающий антиген CD3 фрагмент содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 44, CDR2 тяжелой цепи, имеющий SEQ ID NO: 45, CDR3 тяжелой цепи, имеющий SEQ ID NO: 46, CDR1 легкой цепи, имеющий SEQ ID NO: 17, CDR2 легкой цепи, имеющий SEQ ID NO: 18, и CDR3 легкой цепи, имеющий SEQ ID NO: 19.
В одном из вариантов осуществления изобретения связывающий антиген CD3 фрагмент содержит последовательность вариабельной области тяжелой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и последовательность вариабельной области легкой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
В одном из вариантов осуществления изобретения связывающий антиген CD3 фрагмент содержит вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 55.
В одном из вариантов осуществления изобретения связывающий антиген CD3 фрагмент содержит последовательность вариабельной области тяжелой цепи SEQ ID NO: 43 и последовательность вариабельной области легкой цепи SEQ ID NO: 55.
Фрагмент, связывающий антиген клетки-мишени
Активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, содержит по меньшей мере один антигенсвязывающий фрагмент, обладающий способностью связываться с антигеном клетки-мишени (в настоящее описании его обозначают также как «связывающий антиген клетки-мишени фрагмент» или «второй» или «третий» антигенсвязывающий фрагмент»). В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит два антигенсвязывающих фрагмента, которые обладают способностью связываться с антигеном клетки-мишени. В конкретном указанном варианте осуществления изобретения каждый из указанных антигенсвязывающих фрагментов специфически связывается с одной и той же антигенной детерминантной. В еще более конкретном варианте осуществления изобретения все указанные антигенсвязывающие фрагменты являются идентичными. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит молекулу иммуноглобулина, которая обладает способностью специфически связываться с антигеном клетки-мишени. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит не более двух антигенсвязывающих фрагментов, которые обладают способностью связываться с антигеном клетки-мишени.
В предпочтительном варианте осуществления изобретения фрагмент, связывающий антиген клетки-мишени, представляет собой молекулу Fab, прежде всего каноническую молекулу Fab, которая связывается со специфической антигенной детерминантой и может направлять активируемую протеазой активирующую Т-клетки биспецифическую молекулу к сайту-мишени, например, специфическому типу опухолевой клетки, которая несет антигенную детерминанту.
В некоторых вариантах осуществления изобретения фрагмент, связывающий антиген клетки-мишени, специфически связывается с антигеном клеточной поверхности. В конкретном варианте осуществления изобретения фрагмент, связывающий антиген клетки-мишени, специфически связывается с фолатным рецептором 1 (FolR1) на поверхности клетки-мишени. В другом конкретном варианте осуществления изобретения фрагмент, связывающий антиген клетки-мишени, специфически связывается с рецептором эпидермального фактора роста (EGFR), в частности, с человеческим EGFR, например, HER1. В другом конкретном варианте осуществления изобретения фрагмент, связывающий антиген клетки-мишени, специфически связывается с HER2. В другом конкретном варианте осуществления изобретения фрагмент, связывающий антиген клетки-мишени, специфически связывается с мезотелином, в частности, с человеческим мезотелином.
В некоторых вариантах осуществления изобретения фрагмент, связывающий антиген клетки-мишени, направлен на антиген, ассоциированный с патологическим состоянием, таким как антиген, который презентируется на опухолевой клетке или инфицированной вирусом клетке. Приемлемыми антигенами являются антигены клеточной поверхности, например (но не ограничиваясь только ими) рецепторы клеточной поверхности. В конкретных вариантах осуществления изобретения антиген представляет собой человеческий антиген. В конкретном варианте осуществления изобретения антиген клетки-мишени выбирают из фолатного рецептора 1 (FolR1) и рецептора эпидермального фактора роста (EGFR), в частности, человеческого EGFR, например, HER1. В другом конкретном варианте осуществления изобретения антиген клетки-мишени представляет собой HER2. В другом конкретном варианте осуществления изобретения антиген клетки- мишени представляет собой мезотелин.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1. В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER1, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 56, SEQ ID NO: 57 и SEQ ID NO: 58, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 59, SEQ ID NO: 60 и SEQ ID NO: 61.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER1, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 56, CDR2 тяжелой цепи, имеющий SEQ ID NO: 57, CDR3 тяжелой цепи, имеющий SEQ ID NO: 58, CDR1 легкой цепи, имеющий SEQ ID NO: 59, CDR2 легкой цепи, имеющий SEQ ID NO: 60, и CDR3 легкой цепи, имеющий SEQ ID NO: 61.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER1, содержит последовательности CDR тяжелой и легкой цепей антитела к HER1, описанного в опубликованной заявке РСТ WO 2006/082515.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит по меньшей мере одну полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 32, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 33, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 34. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит по меньшей мере одну полипептидную последовательность SEQ ID NO: 32, полипептидную последовательность SEQ ID NO: 33 и полипептидную последовательность SEQ ID NO: 34.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно антиидиотипический по отношению к CD3 scFv (антиидиотипический CD3 scFv), который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR 3 легкой цепи, имеющий SEQ ID NO: 25. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно антиидиотипический CD3 scFv, содержащий полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 41 или 42. В одном из вариантов осуществления изобретения антиидиотипический CD3 scFv содержит полипептидную последовательность SEQ ID NO: 41 или 42.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно антиидиотипический HER1 scFv, который содержит по меньшей мере один CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно линкер, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 35.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно линкер, который имеет распознаваемый протеазой сайт, содержащий полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 97. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER1, содержит дополнительно линкер, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 86.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2. В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER2, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 142, SEQ ID NO: 143 и SEQ ID NO: 144, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150. В одном из дополнительных вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER2, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 145, SEQ ID NO: 146 и SEQ ID NO: 147, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 148, SEQ ID NO: 149 и SEQ ID NO: 150.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER2, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 142, CDR2 тяжелой цепи, имеющий SEQ ID NO: 143, CDR3 тяжелой цепи, имеющий SEQ ID NO: 144, CDR1 легкой цепи, имеющий SEQ ID NO: 148, CDR2 легкой цепи, имеющий SEQ ID NO: 149, и CDR3 легкой цепи, имеющий SEQ ID NO: 150. В одном из дополнительных вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении HER2, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 145, CDR2 тяжелой цепи, имеющий SEQ ID NO: 146, CDR3 тяжелой цепи, имеющий SEQ ID NO: 147, CDR1 легкой цепи, имеющий SEQ ID NO: 148, CDR2 легкой цепи, имеющий SEQ ID NO: 149, и CDR3 легкой цепи, имеющий SEQ ID NO: 150.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно антиидиотипический CD3 scFv, содержащий полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 41 или 42. В одном из вариантов осуществления изобретения антиидиотипический CD3 scFv содержит полипептидную последовательность SEQ ID NO: 41 или 42.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, содержащая по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно антиидиотипический HER2 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно линкер, содержащий полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 35.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно линкер, который имеет распознаваемый протеазой сайт, содержащий полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 97. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении HER2, содержит дополнительно линкер, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 86.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 132, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 136, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 81, и полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 133.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 132, полипептидную последовательность SEQ ID NO: 136, полипептидную последовательность SEQ ID NO: 81 и полипептидную последовательность SEQ ID NO: 133.
В конкретных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1. В одном из вариантов осуществления изобретения FolR1 представляет собой человеческий FolR1. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении человеческого FolR1, и не связывается с человеческим FolR2 или человеческим FolR3. В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 14, CDR2 тяжелой цепи, имеющий SEQ ID NO: 15, CDR3 тяжелой цепи, имеющий SEQ ID NO: 16, CDR1 легкой цепи, имеющий SEQ ID NO: 17, CDR2 легкой цепи, имеющий SEQ ID NO: 18, и CDR3 легкой цепи, имеющий SEQ ID NO: 19.
В другом варианте осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит последовательность вариабельной области тяжелой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 47, и последовательность вариабельной области легкой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 55, или их варианты, которые сохраняют функциональность.
В другом варианте осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит последовательность вариабельной области тяжелой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 47, и вариабельной области легкой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 55.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 151, CDR2 тяжелой цепи, имеющий SEQ ID NO: 152, CDR3 тяжелой цепи, имеющий SEQ ID NO: 153, CDR1 легкой цепи, имеющий SEQ ID NO: 154, CDR2 легкой цепи, имеющий SEQ ID NO: 155, и CDR3 легкой цепи, имеющий SEQ ID NO: 156.
В другом варианте осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит последовательность вариабельной области тяжелой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 157, и последовательность вариабельной области легкой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 158, или их варианты, которые сохраняют функциональность.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении FolR1, содержит последовательность вариабельной области тяжелой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 157, и вариабельной области легкой цепи, которая содержит аминокислотную последовательность SEQ ID NO: 158.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 2, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 1.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 2 и полипептидную последовательность SEQ ID NO: 1.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1, дополнительно содержит антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1, дополнительно содержит антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1, дополнительно содержит антиидиотипический CD3 scFv, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 41 или 42. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит полипептидную последовательность SEQ ID NO: 41 или 42.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1, дополнительно содержит линкер, имеющий распознаваемый протеазой сайт, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 97. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении FolR1, дополнительно содержит линкер, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 86.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 1, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 3, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 72.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 1, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 3, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 72.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 1, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 3, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 85.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 1, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 3, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 73 и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 74.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 1, полипептидную последовательность SEQ ID NO: 3 и полипептидную последовательность SEQ ID NO: 72.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 1, полипептидную последовательность SEQ ID NO: 3 и полипептидную последовательность SEQ ID NO: 85.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 1, полипептидную последовательность SEQ ID NO: 3, полипептидную последовательность SEQ ID NO: 73 и полипептидную последовательность SEQ ID NO: 74.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 137, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 139, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 81 и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 138.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 137, полипептидную последовательность SEQ ID NO: 139, полипептидную последовательность SEQ ID NO: 81 и полипептидную последовательность SEQ ID NO: 138.
В конкретных вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина. В одном из вариантов осуществления изобретения мезотелин представляет собой человеческий мезотелин. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении человеческого мезотелина. В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении мезотелина, содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении мезотелина, содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 107, CDR2 тяжелой цепи, имеющий SEQ ID NO: 108, CDR3 тяжелой цепи, имеющий SEQ ID NO: 109, CDR1 легкой цепи, имеющий SEQ ID NO: 110, CDR2 легкой цепи, имеющий SEQ ID NO: 111, и CDR3 легкой цепи, имеющий SEQ ID NO: 112.
В следующем варианте осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении мезотелина, содержит последовательность вариабельной области тяжелой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 113, и последовательность вариабельной области легкой цепи, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 114, или их варианты, которые сохраняют функциональность.
В одном из вариантов осуществления изобретения антигенсвязывающий фрагмент, специфический в отношении мезотелина, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 113, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 114.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина, дополнительно содержит антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина, дополнительно содержит антиидиотипический CD3 scFv, который содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина, дополнительно содержит антиидиотипический CD3 scFv, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 41 или 42. В одном из вариантов осуществления изобретения антиидиотипический scFv содержит полипептидную последовательность SEQ ID NO: 41 или 42.
В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина, дополнительно содержит линкер, имеющий распознаваемый протеазой сайт, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 97. В некоторых вариантах осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит по меньшей мере один антигенсвязывающий фрагмент, специфический в отношении мезотелина, дополнительно содержит линкер, который содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 86.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 77, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 78, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 81 и полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 82.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 76, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 77, полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 78, и полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 79.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 77, полипептидную последовательность SEQ ID NO: 78, полипептидную последовательность SEQ ID NO: 81 и полипептидную последовательность SEQ ID NO: 82.
В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 76, полипептидную последовательность SEQ ID NO: 77, полипептидную последовательность SEQ ID NO: 78 и полипептидную последовательность SEQ ID NO: 79.
Одним из вариантов осуществления изобретения является активирующая Т-клетки биспецифическая молекула, которая содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 76, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 77, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 78, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 81.
Одним из вариантов осуществления изобретения является активирующая Т-клетки биспецифическая молекула, которая содержит полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 77, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 78, полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 81, и полипептидную последовательность, идентичную по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 84.
В одном из вариантов осуществления изобретения активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 76, полипептидную последовательность SEQ ID NO: 77, полипептидную последовательность SEQ ID NO: 78 и полипептидную последовательность SEQ ID NO: 81.
В одном из вариантов осуществления изобретения активирующая Т-клетки биспецифическая молекула содержит полипептидную последовательность SEQ ID NO: 77, полипептидную последовательность SEQ ID NO: 78, полипептидную последовательность SEQ ID NO: 81 и полипептидную последовательность SEQ ID NO: 84.
Маскирующий фрагмент
Активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в изобретении, содержит по меньшей мере один маскирующий фрагмент. В других исследованиях предпринимались попытки маскировать связывание антитела путем кэппирования связывающего фрагмента фрагментом антигена, распознаваемым связывающим фрагментом (см., например, WO 2013/128194). Этот подход имеет несколько ограничений. Например, применение антигена уменьшает гибкость в отношении уменьшения аффинности связывающего фрагмента. Это обусловлено тем, что аффинность должна быть достаточно высокой для соответствующей маскировки маскирующим антигеном. Кроме того, после диссоциации антиген может потенциально связываться и взаимодействовать с его когнатным(ими) рецептором(ами) in vivo и вызывать нежелательные сигналы в клетках, экспрессирующих указанный рецептор. В противоположность этому, в подходе, представленном в настоящем описании, для маскировки применяют антиидиотипическое антитело или его фрагмент. Двумя альтернативными факторами, которые можно рассматривать для создания эффективного маскирующего фрагмента являются 1. эффективность маскировки и 2. обратимость маскировки. Если аффинность является слишком низкой, то маскировка может оказаться неэффективной. Однако, если аффинность является слишком высокой, то процесс маскировки может быть недостаточно обратимым. Нельзя предсказать, какой агент будет лучше «работать»: антиидиотипический маскирующий агент с высокой аффинностью или антиидиотипический маскирующий агент с низкой аффинностью. Как указано в настоящем описании, обладающие более высокой аффинностью маскирующие фрагменты в целом обеспечивали лучшую маскировку антигенсвязывающего сайта и одновременно могли эффективно быть удалены с целью активации молекулы. В одном из вариантов осуществления изобретения антиидиотипический маскирующий агент имеет KD 1-8нМ. В одном из вариантов осуществления изобретения антиидиотипический маскирующий агент имеет KD 2нМ при 37°С. В одном из конкретных вариантов осуществления изобретения антиидиотипический маскирующий фрагмент распознает идиотип первого антигенсвязывающего фрагмента, который обладает способностью специфически связываться с CD3, например, человеческим CD3. В одном из конкретных вариантов осуществления изобретения антиидиотипический маскирующий фрагмент распознает идиотип второго антигенсвязывающего фрагмента, который обладает способностью специфически связываться с антигеном клетки-мишени.
В одном из вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25. В одном из вариантов осуществления изобретения маскирующий фрагмент содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 20, CDR2 тяжелой цепи, имеющий SEQ ID NO: 21, CDR3 тяжелой цепи, имеющий SEQ ID NO: 22, CDR1 легкой цепи, имеющий SEQ ID NO: 23, CDR2 легкой цепи, имеющий SEQ ID NO: 24, и CDR3 легкой цепи, имеющий SEQ ID NO: 25.
В одном из вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 41. В одном из вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит полипептидную последовательность SEQ ID NO: 41.
В одном из предпочтительных вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31. В одном из вариантов осуществления изобретения маскирующий фрагмент содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 26, CDR2 тяжелой цепи, имеющий SEQ ID NO: 27, CDR3 тяжелой цепи, имеющий SEQ ID NO: 28, CDR1 легкой цепи, имеющий SEQ ID NO: 29, CDR2 легкой цепи, имеющий SEQ ID NO: 30, и CDR3 легкой цепи, имеющий SEQ ID NO: 31.
В одном из вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит полипептидную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% SEQ ID NO: 42. В одном из вариантов осуществления изобретения маскирующий фрагмент маскирует CD3-связывающий фрагмент и содержит полипептидную последовательность SEQ ID NO: 42.
В одном из предпочтительных вариантов осуществления изобретения маскирующий фрагмент маскирует HER1-связывающий фрагмент и содержит по меньшей мере один из CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53. В одном из вариантов осуществления изобретения анти-идиотипический scFv содержит CDR1 тяжелой цепи, имеющий SEQ ID NO: 48, CDR2 тяжелой цепи, имеющий SEQ ID NO: 49, CDR3 тяжелой цепи, имеющий SEQ ID NO: 50, CDR1 легкой цепи, имеющий SEQ ID NO: 51, CDR2 легкой цепи, имеющий SEQ ID NO: 52, и CDR3 легкой цепи, имеющий SEQ ID NO: 53.
Одним из объектов изобретения является идиотипспецифический полипептид, предназначенный для обратимого сокрытия сайта связывания антигена антигенсвязывающей молекулы. Одним из вариантов осуществления изобретения является идиотипспецифический полипептид, предназначенный для обратимого сокрытия анти-CD3 антигенсвязывающего сайта молекулы. Указанный идиотипспецифический полипептид, предназначенный для обратимого сокрытия анти-CD3 антигенсвязывающего сайта, должен обладать способностью специфически связываться с идиотипом анти-CD3 антигенсвязывающего сайта и тем самым снижать или аннулировать связывание анти-CD3 антигенсвязывающего сайта с CD3. Одним из вариантов осуществления изобретения является идиотипспецифический полипептид, предназначенный для обратимого сокрытия анти- HER1 антигенсвязывающего сайта молекулы. В одном из вариантов осуществления изобретения идиотипспецифический полипептид представляет собой антиидиотипический scFv. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через линкер. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через несколько линкеров. В одном из вариантов осуществления изобретения идиотипспецифический полипептид ковалентно присоединен к молекуле через два линкера. В одном из вариантов осуществления изобретения линкер представляет собой пептидный линкер. В одном из вариантов осуществления изобретения линкер представляет собой расщепляемый протеазой линкер. В одном из вариантов осуществления изобретения линкер содержит последовательность SEQ ID NO: 7, 8, 9 или 10. В одном из вариантов осуществления изобретения линкер содержит последовательность SEQ ID NO: 7, 8, 9, 10, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 или 96. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 7. В одном из вариантов осуществления изобретения линкер содержит полипептидную последовательность SEQ ID NO: 86. В одном из вариантов осуществления изобретения линкер содержит по меньшей мере один распознаваемый протеазой сайт. В одном из вариантов осуществления изобретения распознаваемый протеазой сайт содержит полипептидную последовательность SEQ ID NO: 36, 37, 38, 39, 40, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106. В одном из предпочтительных вариантов осуществления изобретения распознаваемый протеазой сайт содержит распознаваемую протеазой последовательность RQARVVNG (SEQ ID NO: 36). В другом варианте осуществления изобретения линкер содержит несколько распознаваемых протеазой сайтов. В одном из предпочтительных вариантов осуществления изобретения распознаваемый протеазой сайт содержит распознаваемую протеазой последовательность VHMPLGFLGPRQARVVNG (SEQ ID NO: 97). В одном из вариантов осуществления изобретения протеазу выбирают из группы, состоящей из металлопротеиназы, например, матричной металлопротеиназы 1-28 и «дезинтегрина и металлопротеиназы» (ADAM) 2, 7-12, 15, 17-23, 28-30 и 33, сериновой протеазы, например, активатора плазминогена урокиназного типа и матриптазы, цистеиновой протеазы, аспарагиновой протеазы и протеазы катепсина. В конкретных вариантах осуществления изобретения протеаза представляет собой ММР9 или ММР2. В другом конкретном варианте осуществления изобретения протеаза представляет собой матриптазу.
В одном из вариантов осуществления изобретения молекула, которая содержит анти-CD3 антигенсвязывающий сайт представляет собой активирующую Т-клетки биспецифическую молекулу. В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую по меньшей мере один из следующих участков: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность DYSIH (SEQ ID NO: 20); CDR Н2, имеющий аминокислотную последовательность WINTETGEPAYADDFKG (SEQ ID NO: 21); и CDR Н3, имеющий аминокислотную последовательность PYDYDVLDY (SEQ ID NO: 22). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область легкой цепи, содержащую по меньшей мере один из следующих участков: гипервариабельный участок легкой цепи (CDR L) 1, имеющий аминокислотную последовательность RASKSVSTSNYSYIH (SEQ ID NO: 23); CDR L2, имеющий аминокислотную последовательность YVSYLES (SEQ ID NO: 24); и CDR L3, имеющий аминокислотную последовательность QHSREFPWT (SEQ ID NO: 25). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность DYSIH (SEQ ID NO: 20); CDR Н2, имеющий аминокислотную последовательность WINTETGEPAYADDFKG (SEQ ID NO: 21); CDR Н3, имеющий аминокислотную последовательность PYDYDVLDY (SEQ ID NO: 22); и вариабельную область легкой цепи, содержащую: (CDR L) 1 легкой цепи, имеющий аминокислотную последовательность RASKSVSTSNYSYIH (SEQ ID NO: 23); CDR L2, имеющий аминокислотную последовательность YVSYLES (SEQ ID NO: 24); и CDR L3, имеющий аминокислотную последовательность QHSREFPWT (SEQ ID NO: 25). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую по меньшей мере один из следующих участков: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность SYGVS (SEQ ID NO: 26); CDR Н2, имеющий аминокислотную последовательность IIWGDGSTNYHSALIS (SEQ ID NO: 27); и CDR Н3, имеющий аминокислотную последовательность GITTVVDDYYAMDY (SEQ ID NO: 28). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область легкой цепи, содержащую по меньшей мере один из следующих участков: (CDR L) 1 легкой цепи, имеющий аминокислотную последовательность RASENIDSYLA (SEQ ID NO: 29); CDR L2, имеющий аминокислотную последовательность AATFLAD (SEQ ID NO: 30); и CDR L3, имеющий аминокислотную последовательность QHYYSTPYT (SEQ ID NO: 31). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность SYGVS (SEQ ID NO: 26); CDR Н2, имеющий аминокислотную последовательность IIWGDGSTNYHSALIS (SEQ ID NO: 27); CDR Н3, имеющий аминокислотную последовательность GITTVVDDYYAMDY (SEQ ID NO: 28); и вариабельную область легкой цепи, содержащую: (CDR L) 1 легкой цепи, имеющий аминокислотную последовательность RASENIDSYLA (SEQ ID NO: 29); CDR L2, имеющий аминокислотную последовательность AATFLAD (SEQ ID NO: 30); и CDR L3, имеющий аминокислотную последовательность QHYYSTPYT (SEQ ID NO: 31). В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую по меньшей мере один из следующих участков: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность SEQ ID NO: 48; CDR Н2 имеющий аминокислотную последовательность SEQ ID NO: 49; и CDR Н3 имеющий аминокислотную последовательность SEQ ID NO: 50. В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область легкой цепи, содержащую по меньшей мере один из следующих участков: гипервариабельный участок легкой цепи (CDR L) 1, имеющий аминокислотную последовательность SEQ ID NO: 51; CDR L2, имеющий аминокислотную последовательность SEQ ID NO: 52; и CDR L3, имеющий аминокислотную последовательность SEQ ID NO: 53. В одном из конкретных вариантов осуществления изобретения идиотипспецифический полипептид содержит вариабельную область тяжелой цепи, содержащую: гипервариабельный участок тяжелой цепи (CDR Н) 1, имеющий аминокислотную последовательность SEQ ID NO: 48; CDR Н2, имеющий аминокислотную последовательность SEQ ID NO: 49; и CDR Н3, имеющий аминокислотную последовательность SEQ ID NO: 50, и вариабельную область легкой цепи, содержащую: гипервариабельный участок легкой цепи (CDR L) 1, имеющий аминокислотную последовательность SEQ ID NO: 51; CDR L2, имеющий аминокислотную последовательность SEQ ID NO: 52; и CDR L3, имеющий аминокислотную последовательность SEQ ID NO: 53.
Полинуклеотиды
Изобретение относится также к выделенным полинуклеотидам, которые кодируют активируемую протеазой активирующую Т-клетки биспецифическую молекулу, представленную в настоящем описании, или ее фрагмент. В некоторых вариантах осуществления изобретения указанный фрагмент представляет собой антигенсвязывающий фрагмент.
Полинуклеотиды, предлагаемые в изобретении, включают полинуклеотиды, последовательности которых по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, или 100% идентичны последовательностям, представленным в SEQ ID NO: 62-71 или в SEQ ID NO:, включая их функциональные фрагменты или варианты. Полинуклеотиды, предлагаемые в изобретении, включают также полинуклеотиды, последовательности которых по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, или 100% идентичны последовательностям, представленным в SEQ ID NO: 117-131, включая их функциональные фрагменты или варианты. Полинуклеотиды, предлагаемые в изобретении, включают также полинуклеотиды, последовательности которых по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, или 100% идентичны последовательностям, представленным в SEQ ID NO: 162-170, включая их функциональные фрагменты или варианты.
Полинуклеотиды, кодирующие активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно экспрессировать в виде индивидуального полинуклеотида, который кодирует полную активируемую протеазой активирующую Т-клетки биспецифическую молекулу, или в виде нескольких (например, двух или большего количества) совместно экспрессируемых полинуклеотидов. Полипептиды, кодируемые совместно экспрессируемыми полинуклеотидами, можно соединять, например, через дисульфидные связи или другими путями с образованием функциональной активируемой протеазой активирующей Т-клетки биспецифической молекулы. Например, часть антигенсвязывающего фрагмента, представляющая собой легкую цепь, может кодироваться полинуклеотидом, отличным от полинуклеотида, кодирующего часть активируемой протеазой активирующей Т-клетки биспецифической молекулы, которая содержит часть антигенсвязывающего фрагмента, представляющую собой тяжелую цепь, субъединицу Fc-домена и необязательно (часть) другого антигенсвязывающего фрагмента. При совместной экспрессии полипептиды тяжелых цепей должны связываться с полипептидами легких цепей с образованием антигенсвязывающего фрагмента. В другом примере часть активируемой протеазой активирующей Т-клетки биспецифической молекулы, которая содержит одну из двух субъединиц Fc-домена и необязательно один или несколько (часть одного или нескольких) антигенсвязывающих фрагментов, может кодироваться полинуклеотидом, отличным от полинуклеотида, который кодирует часть активируемой протеазой активирующей Т-клетки биспецифической молекулы, которая содержит вторую из двух субъединиц Fc-домена и необязательно антигенсвязывающий фрагмент (его часть). При совместной экспрессии субъединицы Fc-домена должны связываться с образованием Fc-домена.
В некоторых вариантах осуществления изобретения выделенный полинуклеотид кодирует полную указанную в настоящем описании активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении. В других вариантах осуществления изобретения выделенный полинуклеотид кодирует полипептиды, входящие в указанную в настоящем описании активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении.
Другой вариант осуществления настоящего изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует последовательность вариабельной области. Другой вариант осуществления настоящего изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует полипептидную последовательность, представленную в SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 47 или 55. Другой вариант осуществления настоящего изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует полипептидную последовательность, представленную в SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 47, 55, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85. Другой вариант осуществления настоящего изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует полипептидную последовательность, представленную в SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 47, 55, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 132, 133, 134, 135, 136, 137, 138, 139, 140 или 141. Другим вариантом осуществления настоящего изобретения является также выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% нуклеотидной последовательности, представленной в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70 или 71. Другим вариантом осуществления настоящего изобретения является также выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% нуклеотидной последовательности, представленной в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130 или 131. Другим вариантом осуществления настоящего изобретения является также выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% нуклеотидной последовательности, представленной в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 162, 163, 164, 165, 166, 167, 168, 169 или 170. Другим вариантом осуществления изобретения является выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит нуклеотидную последовательность, представленную в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70 или 71. Другим вариантом осуществления изобретения является выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит нуклеотидную последовательность, представленную в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130 или 131. Другим вариантом осуществления изобретения является выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит нуклеотидную последовательность, представленную в SEQ ID NO: 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 162, 163, 164, 165, 166, 167, 168, 169 или 170. Другим вариантом осуществления изобретения является также выделенный полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, кодирующую последовательность вариабельной области, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% аминокислотной последовательности SEQ ID NO: 43, 47 или 55. Изобретение относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует последовательность вариабельной области SEQ ID NO: 43, 47 или 55 с консервативными аминокислотными заменами.
Другой вариант осуществления изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит последовательность, кодирующую последовательность вариабельной области, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% аминокислотной последовательности SEQ ID NO: 43, 47, 55, 113, 114, 115 или 116. Изобретение относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует последовательность вариабельной области SEQ ID NO: 43, 47, 55, 113, 114, 115 или 116 с консервативными аминокислотными заменами.
Другой вариант осуществления изобретения относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент, где полинуклеотид содержит последовательность, кодирующую последовательность вариабельной области, которая идентична по меньшей мере примерно на 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% аминокислотной последовательности SEQ ID NO: 43, 47, 55, 113, 114, 115, 116, 157, 158, 159, 160 или 161. Изобретение относится к выделенному полинуклеотиду, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу или ее фрагмент, где полинуклеотид содержит последовательность, которая кодирует последовательность вариабельной области SEQ ID NO: 43, 47, 55, 113, 114, 115, 116, 157, 158, 159, 160 или 161 с консервативными аминокислотными заменами.
В некоторых вариантах осуществления изобретения полинуклеотид или нуклеиновая кислота представляет собой ДНК. В других вариантах осуществления изобретения полинуклеотид, предлагаемый в настоящем изобретении, представляет собой РНК, например, в форме матричной РНК (мРНК). РНК, предлагаемая в настоящем изобретении, может быть одноцепочечной или двухцепочечной.
В изобретении предложены также выделенные полинуклеотиды, которые кодируют идиотипспецифический полипептид, указанный в настоящем описании, или его фрагмент. В некоторых вариантах осуществления изобретения указанный фрагмент представляет собой связывающий идиотип фрагмент, т.е. антиидиотипспецифическое антитело или его фрагмент. В одном из вариантов осуществления изобретения идиотипспецифический полипептид представляет собой антиидиотипический scFv.
Изобретение относится также к выделенному полинуклеотиду, который кодирует идиотиппецифический полипептид, предлагаемый в изобретении, или его фрагмент, где полинуклеотид содержит последовательность, которая кодирует одну или несколько из полипептидных последовательностей, представленных в SEQ ID NO: 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 48, 49, 50, 51, 52 и 53. Изобретение относится также к выделенному полинуклеотиду, который кодирует идиотиппецифический полипептид, предлагаемый в изобретении, или его фрагмент, где полинуклеотид содержит последовательность, которая кодирует одну или несколько из полипептидных последовательностей, представленных в SEQ ID NO: 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 48, 49, 50, 51, 52 и 53, с консервативными аминокислотными заменами.
Полинуклеотиды, кодирующие идиотипспецифические полипептиды, предлагаемые в изобретении, можно экспрессировать в виде индивидуального полинуклеотида, который кодирует полный идиотипспецифический полипептид, или в виде нескольких (например, двух или большего количества) совместно экспрессируемых полинуклеотидов. Полипептиды, кодируемые совместно экспрессируемыми полинуклеотидами, можно соединять, например, через дисульфидные связи или другими путями с образованием функционального идиотипспецифического полипептида, например, маскирующего фрагмента активируемой протеазой активирующей Т-клетки биспецифической молекулы. Например, в одном из вариантов осуществления изобретения идиотипспецифический полипептид представляет собой антиидиотипический scFv (одноцепочечный вариабельный фрагмент), в котором часть, представляющая собой легкую цепь антиидиотипического scFv, может кодироваться полинуклеотидом, отличным от полинуклеотида, кодирующего часть антиидиотипического scFv, представляющую собой вариабельную область тяжелой цепи антиидиотипического scFv. При совместной экспрессии полипептиды тяжелых цепей должны связываться с полипептидами легких цепей с образованием антиидиотипического scFv. В некоторых варрантах осуществления изобретения выделенный полинуклеотид кодирует указанный в настоящем описании идиотипспецифический полипептид, предлагаемый в изобретении.
В некоторых вариантах осуществления изобретения полинуклеотид или нуклеиновая кислота представляет собой ДНК. В других вариантах осуществления изобретения полинуклеотид, предлагаемый в настоящем изобретении, представляет собой РНК, например, в форме матричной РНК (мРНК). РНК, предлагаемая в настоящем изобретении, может быть одноцепочечной или двухцепочечной.
Методы рекомбинации
Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно получать, например, путем твердофазного пептидного синтеза (например, твердофазный синтез Меррифилда) или методом рекомбинации. Для рекомбинантного получения один или несколько полинуклеотидов, кодирующих активируемую протеазой активирующую Т-клетки биспецифическую молекулу (фрагмент), например, описанную выше, выделяют и встраивают в один или несколько векторов для дополнительного клонирования и/или экспрессии в клетке-хозяине. Указанный полинуклеотид можно легко выделять и секвенировать с помощью общепринятых процедур. Одним из вариантов осуществления изобретения является вектор, предпочтительно экспрессионный вектор, содержащий один или несколько полинуклеотидов, предлагаемых в изобретении. Методы, хорошо известные специалистам в данной области, можно применять для конструирования экспрессионных векторов, содержащих кодирующую последовательность активируемой протеазой активирующей Т-клетки биспецифической молекулы (фрагмента) наряду с приемлемыми контролирующими транскрипцию/трансляцию сигналами. Эти методы включают технологии рекомбинантной ДНК in vitro, методы синтеза и рекомбинации/генетической рекомбинации in vivo (см., например, методы, описанные у Maniatis и др., Maniatis и др., Molecular Cloning A Laboratory Manual, изд-во Cold Spring Harbor Laboratory, N.Y., 1989; и Ausubel и др., Current Protocols in Molecular Biology, изд-во Greene Publishing Associates and Wiley Interscience, N.Y., 1989). Экспрессионный вектор может представлять собой часть плазмиды, вируса или может представлять собой фрагмент нуклеиновой кислоты. Экспрессионный вектор включает кассету экспрессии, в которой полинуклеотид, кодирующий активируемую протеазой активирующую Т-клетки биспецифическую молекулу (фрагмент) (т.е. кодирующую область), клонируют с обеспечением функциональной связи с промотором и/или другими элементами, контролирующими транскрипцию или трансляцию. В контексте настоящего описания «кодирующая область» представляет собой часть нуклеиновой кислоты, которая состоит из кодонов, транслируемых в аминокислоты. Хотя «стоп-кодон» (TAG, TGA или ТАА) не транслируется в аминокислоту, он, в случае его присутствия, может рассматриваться как часть кодирующей области, однако любые фланкирующие последовательности, например, промоторы, сайты связывания рибосом, терминаторы транскрипции, интроны, 5'- и 3'-нетранслируемые области и т.п., не являются частью кодирующей области. Две или большее количество кодирующих областей может присутствовать в индивидуальной полинуклеотидной конструкции, например, индивидуальном векторе, или в отдельных полинуклеотидных конструкциях, например, отдельных (различных) векторах. Кроме того, любой вектор может содержать одну кодирующую область или может содержать две или большее количество кодирующих областей, например, вектор, предлагаемый в настоящем изобретении, может кодировать один или несколько полипептидов, которые пост- или котранляционно разделяются на конечные белки посредством протеолитического расщепления. Кроме того, вектор, полинуклеотид или нуклеиновая кислота, предлагаемый/предлагаемая в изобретении, может кодировать гетерологичные кодирующие области, либо слитые, либо не слитые с полинуклеотидом, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу (фрагмент), предлагаемую в изобретении, или ее вариант или производное. Гетерологичные кодирующие области включают (но, не ограничиваясь только ими) специализированные элементы или мотивы, такие как секреторный сигнальный пептид или гетерологичный функциональный домен. Функциональная связь имеет место, когда кодирующая область генного продукта, например, полипептида, ассоциирована с одной или несколькими регуляторными последовательностями таким образом, чтобы экспрессия генного продукта находилась под воздействием или контролем регуляторной(ых) последовательности(ей). Два ДНК-фрагмента (таких как кодирующая область полипептида и ассоциированный с ней промотор) являются «функционально связанными», если индукция промоторной функции приводит к транскрипции мРНК, кодирующей требуемый генный продукт, и если природа связи между двумя ДНК-фрагментами не оказывает воздействия на способность регулирующих экспрессию последовательностей направлять экспрессию генного продукта, или не оказывает воздействия на способность ДНК-матрицы к транскрипции. Таким образом, промоторная область должна быть функционально связана с нуклеиновой кислотой, кодирующей полипептид, если промотор обладает способностью осуществлять транскрипцию нуклеиновой кислоты. Промотор может представлять собой специфический для клетки промотор, который обеспечивает значительную транскрипцию ДНК только в предварительно отобранных клетках. Другие контролирующие транскрипцию элементы, помимо промотора, например, энхансеры, операторы, репрессоры и сигналы терминации транскрипции, можно функционально связывать с полинуклеотидом для обеспечения специфической для клетки транскрипции. Приемлемые промоторы и другие контролирующие транскрипцию области представлены в настоящем описании. Специалистам в данной области известно широкое разнообразие контролирующих транскрипцию областей. Они включают (но, не ограничиваясь только ими) контролирующие транскрипцию области, которые функционируют в клетках позвоночных животных, такие как (но, не ограничиваясь только ими) сегменты промоторов и энхансеров из цитомегаловирусов (например, немедленно-ранний промотор в сочетании с интроном-А), обезьяньего вируса 40 (например, ранний промотор) и ретровирусов (таких как вирус саркомы Рауса). Другие контролирующие транскрипцию области включают области, полученные из генов позвоночных животных, таких как ген актина, белка теплового шока, бычьего гормона роста и кроличьего α-глобина, а также другие последовательности, которые могут контролировать экспрессию генов в эукариотических клетках. Дополнительные приемлемые контролирующие транскрипцию области включают тканеспецифические промоторы и энхансеры, а также индуцибельные промоторы (например, промоторы, индуцируемые тетрациклинами). Аналогично этому, обычным специалистам в данной области известно широкое разнообразие контролирующих трансляцию элементов. Они включают (но, не ограничиваясь только ими) сайты связывания рибосом, кодоны инициации трансляции и терминирующие кодоны и элементы, полученные из вирусных систем (в частности внутренний сайт связывания (посадки) рибосом или IRES, который обозначают также как CITE-последовательность). Кассета экспрессии может включать также другие характерные структуры, такие как сайт инициации репликации и/или интегрированные в хромосому элементы, такие как длинные концевые повторы (LTR) ретровирусов, или инвертированные концевые повторы (ITR) аденоассоциированного вируса (AAV).
Кодирующие области полинуклеотида и нуклеиновой кислоты, предлагаемые в настоящем изобретении, могут быть ассоциированы с дополнительными кодирующими областями, кодирующими секреторные или сигнальные пептиды, которые направляют секрецию полипептида, кодируемого полинуклеотидом, предлагаемым в настоящем изобретении. Например, если требуется секреция активируемой протеазой активирующей Т-клетки биспецифической молекулы, то ДНК, кодирующую сигнальную последовательность, можно помещать против хода транскрипции относительно нуклеиновой кислоты, кодирующей активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, или ее фрагмент. Согласно гипотезе, касающейся сигналов, белки, секретируемые клетками млекопитающих, имеют сигнальный пептид или секреторную лидерную последовательность, который/которая отщепляется от зрелого белка после инициации экспорта растущей белковой цепи через шероховатый эндоплазматический ретикулум. Обычным специалистам в данной области должно быть очевидно, что полипептиды, секретируемые клетками позвоночных животных, как правило, имеют сигнальный пептид, слитый с N-концом полипептида, который отщепляется от транслируемого полипептида с образованием секретируемой или «зрелой» формы полипептида. В некоторых вариантах осуществления изобретения используют нативный сигнальный пептид, например, сигнальный пептид тяжелой цепи или легкой цепи иммуноглобулина или функциональное производное указанной последовательности, которое сохраняет способность обеспечивать секрецию полипептида, функционально связанного с ним. Альтернативно этому, можно применять гетерологичный сигнальный пептид млекопитающих или его функциональное производное. Например, лидерную последовательность дикого типа можно заменять на лидерную последовательность человеческого тканевого активатора плазминогена (TPA) или мышиной β-глюкуронидазы.
ДНК, кодирующую короткую белковую последовательность, которую можно применять для облегчения дальнейшей очистки (например, гистидиновую метку), или предназначенную для мечения активируемой протеазой активирующей Т-клетки биспецифической молекулы, можно включать внутрь или на концы полинуклеотида, кодирующего активируемую протеазой активирующую Т-клетки биспецифическую молекулу (фрагмент).
Дополнительным вариантом осуществления изобретения является клетка-хозяин, содержащая один или несколько полинуклеотидов, предлагаемых в изобретении. Некоторыми вариантами осуществления изобретения является клетка-хозяин, содержащая один или несколько векторов, предлагаемых в изобретении. Полинуклеотиды и векторы могут обладать любыми особенностями, индивидуально или в сочетании, указанными в настоящем описании касательно полинуклеотидов и векторов соответственно. В одном из таких вариантов осуществления изобретения клетка-хозяин содержит (например, трансформирована или трансфектирована) вектором, содержащим полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении (или ее часть). В контексте настоящего описания понятие «клетка-хозяин» относится к любому типу клеточной системы, которую можно конструировать для получения активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, или их фрагментов. Клетки-хозяева, пригодные для репликации и для поддержания экспрессии активируемых протеазой активирующих Т-клетки биспецифических молекул, хорошо известны в данной области. Такие клетки можно трансфектировать или трансдуцировать соответствующим образом конкретным экспрессионным вектором и можно выращивать в больших количествах содержащие вектор клетки с целью внесения их в ферментеры для крупномасштабных процессов получения активируемой протеазой активирующей Т-клетки биспецифической молекулы в достаточных для клинических применений количествах. Приемлемыми клетками-хозяевами являются прокариотические микроорганизмы, такие как Е. coli, или различные эукариотические клетки, такие как клетки яичника китайского хомячка (СНО), клетки насекомых или т.п. Например, полипептиды можно получать в бактериях, в частности, когда отсутствует потребность в гликозилировании. После экспрессии полипептид можно выделять из пасты бактериальных клеток в растворимую фракцию и можно дополнительно очищать. Помимо прокариот, в качестве хозяев для клонирования или экспрессии векторов, которые кодируют полипептид, можно использовать эукариотические микроорганизмы, такие как нитчатые грибы или дрожжи, включая штаммы грибов и дрожжей, пути гликозилирования которых были «гуманизированы», что позволяет получать полипептид с частично или полностью человеческой схемой гликозилирования (см. Gerngross, Nat. Biotech. 22, 2004, сс. 1409-1414 и Li и др., Nat. Biotech. 24, 2006, сс. 210-215). Клетки-хозяева, которые можно использовать для экспрессии (гликозилированных) полипептидов, получают также из многоклеточных организмов (беспозвоночных и позвоночных животных). Примерами клеток беспозвоночных являются клетки насекомых, а также можно применять клетки растений. Были выявлены многочисленные бакуловирусные штаммы и соответствующие пригодные для них в качестве хозяев клетки насекомых, прежде всего для трансфекции клеток Spodoptera frugiperda. В качестве хозяев можно применять также культуры растительных клеток (см., например, US №№5959177, 6040498, 6420548, 7125978 и 6417429 (описание технологии PLANTIBODIES™ для получения антител в трансгенных растениях). В качестве хозяев можно применять также клетки позвоночных животных. Например, можно использовать клеточные линии млекопитающих, которые адаптированы к росту в суспензии. Другими примерами приемлемых линий клеток-хозяев млекопитающих являются линия клеток почки обезьяны CV1, трансформированная с помощью SV40 (COS-7); линия клеток почки эмбриона человека (293 или клетки линии 293, субклонированные с целью выращивания в суспензионной культуре, Graham и др., J. Gen. Virol., 36, 1977, с. 59); клетки почки детеныша хомяка (ВНК); клетки Сертоли мыши (ТМ4-клетки, описанные, например, у Mather, Biol. Reprod., 23, 1980, сс. 243-251); клетки почки обезьяны (CV1); клетки почки африканской зеленой мартышки (VERO-76,); клетки карциномы шейки матки человека (HELA); клетки почки собаки (MDCK); клетки печени бычьей крысы (BRL 3А); клетки легкого человека (W138); клетки печени человека (Hep G2); клетки опухоли молочной железы мыши (ММТ 060562); клетки TRI, описанные, например, у Mather и др., Annals N.Y. Acad. Sci., 383, 1982, сс. 44-68); клетки MRC 5 и клетки FS4. Другими ценными линиями клеток-хозяев млекопитающих являются клетки яичника китайского хомячка (СНО), включая dhfr--CHO-клетки (Urlaub и др., Proc. Natl. Acad. Sci. USA, 77, 1980, с. 4216); и клеточные линии миеломы, такие как Y0, NS0 и Sp2/0. Обзор конкретных линий клеток-хозяев млекопитающих, которые можно применять для производства белка, см., например, у Yazaki и Wu, в: Methods in Molecular Biology под ред. В.K.С. Lo, изд-во Humana Press, Totowa, NJ, т. 248, 2003, cc. 255-268. Клетки-хозяева включают культивируемые клетки, например, культивируемые клетки млекопитающих, клетки дрожжей, клетки насекомых, клетки бактерий и клетки растений (но не ограничиваясь только ими), а также клетки, находящиеся в организме трансгенного животного, трансгенного растения или культивируемой растительной или животной ткани. В одном из вариантов осуществления изобретения клетка-хозяин представляет собой эукариотическую клетку, предпочтительно клетку млекопитающего, такую как клетка яичника китайского хомячка (СНО), клетка почки человеческого эмбриона (HEK) или лимфоидная клетка (например, клетка Y0, NS0, Sp20).
В данной области известны стандартные технологии для экспрессии чужеродных генов в этих системах. Клетки, экспрессирующие полипептид, содержащий либо тяжелую, либо легкую цепь антигенсвязывающего домена, такого как антитело, можно конструировать таким образом, чтобы в них происходила экспрессия других цепей антитела, например, таким образом, чтобы экспрессируемый продукт представлял собой антитело, которое имеет как тяжелую, так и легкую цепь.
Одним из вариантов осуществления изобретения является способ получения активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, заключающийся в том, что культивируют клетку-хозяина, содержащую полинуклеотид, который кодирует активируемую протеазой активирующую Т-клетки биспецифическую молекулу, представленную в настоящем описании, в условиях, пригодных для экспрессии активируемой протеазой активирующей Т-клетки биспецифической молекулы, и выделяют активируемую протеазой активирующую Т-клетки биспецифическую молекулу из клетки-хозяина (или культуральной среды клетки-хозяина).
Компоненты активируемой протеазой активирующей Т-клетки биспецифической молекулы генетически сливают друг с другом. Активируемую протеазой активирующую Т-клетки биспецифическую молекулу можно создавать так, чтобы ее компоненты сливать друг с другом непосредственно или косвенно через линкерную последовательность. Состав и длину линкера можно определять с помощью методов, хорошо известных в данной области, и можно оценивать эффективность. Примеры линкерных последовательностей, расположенных между различными компонентами активируемой протеазой активирующей Т-клетки биспецифической молекулы, представлены в приведенных в настоящем описании последовательностях. Можно включать также дополнительные последовательности для встраивания сайта расщепления, если требуется разделение индивидуальных компонентов слияния, например, последовательность, распознаваемую эндопептидазой.
В некоторых вариантах осуществления изобретения один или несколько антигенсвязывающих фрагментов активируемых протеазой активирующих Т-клетки биспецифических молекул содержит(ат) по меньшей мере вариабельную область антитела, обладающую способностью связываться с антигенной детерминантой. Вариабельные области могут образовывать часть встречающихся в естественных условиях или не встречающихся в естественных условиях антител или их фрагментов или могут быть получены из них. Методы получения поликлональных антител и моноклональных антител хорошо известны в данной области (см., например, Harlow и Lane, «Antibodies: а Laboratory Manual», изд-во Cold Spring Harbor Laboratory, 1988). He встречающиеся в естественных условиях антитела можно создавать с помощью твердофазного пептидного синтеза, можно получать с помощью методов рекомбинации (например, описанных в US №4186567) или можно получать, например, путем скрининга комбинаторных библиотек, содержащих вариабельные области тяжелых цепей и вариабельные области легких цепей (см., например, US №5969108 на имя McCafferty).
Антитела, фрагменты антител, антигенсвязывающие домены или вариабельные области из любых видов животных можно применять в активируемых протеазой активирующих Т-клетки биспецифических молекулах, предлагаемых в изобретении. Примерами антител, фрагментов антител, антигенсвязывающих доменов или вариабельных областей, которые можно применять согласно настоящему изобретению, являются (но, не ограничиваясь только ими) конструкции, полученные из организма мышей, приматов или человека. Если активируемая протеазой активирующая Т-клетки биспецифическая молекула предназначена для применения на человеке, то можно использовать химерную форму антитела, в которой константные области антитела получены из человеческого антитела. Гуманизированную или полностью человеческую форму антитела можно получать также с помощью методов, хорошо известных в данной области (см., например, US №5565332 на имя Winter). Для осуществления гуманизации можно применять различные методы, такие как (но, не ограничиваясь только ими) (а) трансплантация нечеловеческих (например, из антитела-донора) CDR в человеческий (например, антитело-реципиент) каркасный участок и константные области, сохраняющие или не сохраняющие имеющие решающее значение остатки каркасного участка (например, остатки, важные для сохранения хорошей антигенсвязывающей аффинности или функций антитела), (б) трансплантация только нечеловеческих определяющих специфичность участков (SDR или a-CDR; остатки имеют решающее значение для взаимодействия антитело-антиген) в человеческие каркасные и константные области, или (в) трансплантация полных нечеловеческих вариабельных доменов, но их «маскировка» напоминающим человеческий сегментом путем замены поверхностных остатков. Обзор гуманизированных антител и методов их получения см., например, у Almagro и Fransson, Front Biosci 13, 12008, сс. 1619-1633, и они описаны также, например, у Riechmann и др., Nature 332, 1988, сс. 323-329; Queen и др., Proc Natl Acad Sci USA 86, 1989, сс. 10029-10033; US, №№5821337, 7527791, 6982321 и 7087409; Jones и др., Nature 321, 1986, сс. 522-525; Morrison и др., Proc Natl Acad Sci 81, 1984, сс. 6851-6855; Morrison и Oi, Adv Immunol 44, 1988, cc. 65-92; Verhoeyen и др., Science 239, 1988, cc. 1534-1536; Padlan, Molec Immun 31(3), 1994, cc.169-217; Kashmiri и др., Methods 36, 2005, cc. 25-34) (описание трансплантации SDR (a-CDR)); Padlan, Mol Immunol 28, 1991, cc. 489-498 (описание метода изменения поверхности («повторное покрытие»)); Dall'Acqua и др., Methods 36, 2005, сс. 43-60 (описание «перестановки FR») и Osbourn и др., Methods 36, 2005, сс. 61-68, и Klimka и др., Br J Cancer 83, 2000, сс. 252-260 (описание подхода на основе «целенаправленной селекции» для перестановки FR). Человеческие антитела и человеческие вариабельные области можно получать с помощью различных методик, известных в данной области. Человеческие антитела описаны в целом, у van Dijk и van de Winkel, Curr Opin Pharmacol 5, 2001, cc. 368-374 и Lonberg, Curr Opin Immunol 20, 2008, cc. 450-459. Человеческие вариабельные области могут образовывать часть человеческих моноклональных антител или могут быть получены из них с помощью метода гибридом (см., например, Monoclonal Antibody Production Techniques and Applications, изд-во Marcel Dekker, Inc., New York, 1987, cc. 51-63). Человеческие антитела и человеческие вариабельные области можно получать также путем введения иммуногена трансгенному животному, которое модифицировано таким образом, что может продуцировать интактные человеческие антитела или интактные антитела с человеческими вариабельными областями в ответ на контрольное заражение антигеном (см., например, Lonberg, Nat Biotech 23, 2005, cc. 1117-1125). Человеческие антитела и человеческие вариабельные области можно создавать также путем выделения последовательностей вариабельных областей Fv-клона, отобранных из человеческих фаговых дисплейных библиотек (см., например, Hoogenboom и др. в: Methods in Molecular Biology, под ред. O'Brien и др., изд-во Human Press, Totowa, NJ, 178, 2001, cc. 1-37); и McCafferty и др., Nature 348, 552-554; Clackson и др., Nature 352, 1991, cc. 624-628). Фаг, как правило, экспонирует фрагменты антител либо в виде одноцепочечных Fv- (scFv)-фрагментов, либо в виде Fab-фрагментов.
В некоторых вариантах осуществления изобретения антигенсвязывающие фрагменты, пригодные для применения согласно настоящему изобретению, создают так, чтобы они обладали повышенной аффинностью связывания, например, с помощью методов, описанных в публикации заявки на патент США №2004/0132066, полное содержание которой включено в настоящее описание в качестве ссылки. Способность активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, связываться со специфической антигенной детерминантой, можно оценивать количественно либо с помощью твердофазного ферментного анализа (ELISA), либо другими методиками, известными специалисту в данной области, например, с помощью метода поверхностного плазмонного резонанса (осуществляя анализ с использованием системы BIACORE Т100) (Liljeblad и др., Glyco J 17, 2000, cc. 323-329), и традиционных анализов связывания (Heeley, Endocr Res 28, 2002, cc. 217-229). Анализы в условиях конкуренции можно применять для идентификации антитела, фрагмента антитела, антигенсвязывающего домена или вариабельного домена, конкурирующего с референс-антителом за связывание с конкретным антигеном, например, антитела, которое конкурирует с антителом V9 за связывание с CD3. В некоторых вариантах осуществления изобретения указанное конкурирующее антитело связывается с тем же эпитопом (например, линейным или конформационным эпитопом), с которым связывается референс-антитело. Подробные приведенные в качестве примеров методы картирования эпитопа, с которым связывается антитело, представлены у Morris, «Epitope Mapping Protocols)), в: Methods in Molecular Biology, изд-во Humana Press, Totowa, NJ, т. 66, 1996. При осуществлении приведенного в качестве примера анализа в условиях конкуренции иммобилизованный антиген (например, CD3) инкубируют в растворе, содержащем первое меченое антитело, которое связывается с антигеном (например, антитело V9, описанное в US 6054297), и второе немеченое антитело, которое подлежит тестированию в отношении его способности конкурировать с первым антителом за связывание с антигеном. Второе антитело может присутствовать в супернатанте гибридомы. В качестве контроля иммобилизованный антиген инкубируют в растворе, содержащем первое меченое антитело, но не содержащем второе немеченое антитело. После инкубации в условиях, обеспечивающих связывание первого антитела с антигеном, избыток несвязанного антитела удаляют и оценивают количество метки, ассоциированной с иммобилизованным антигеном. Если количество метки, ассоциированной с иммобилизованным антигеном, существенно снижено в тестируемом образце по сравнению с контрольным образцом, то это свидетельствует о том, что второе антитело конкурирует с первым антителом за связывание с антигеном (см. Harlow и Lane. Antibodies: A Laboratory Manual, изд-во Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, гл. 14, 1988).
Активируемые протеазой активирующие Т-клетки биспецифические молекулы, полученные с помощью представленных в настоящем описании методов, можно очищать с использованием известных в данной области методик, таких как жидкостная хроматография высокого разрешения, ионообменная хроматография, гель-электрофорез, аффинная хроматография, гель-фильтрация и т.п. Фактические условия, применяемые для очистки конкретного белка, зависят, в частности, от таких факторов, как чистый заряд, гидрофобность, гидрофильность и т.д., и они должны быть очевидны специалисту в данной области. Для очистки антитела с помощью аффинной хроматографии можно использовать лиганд, рецептор или антиген, с которым связывается активируемая протеазой активирующая Т-клетки биспецифическая молекула. Например, для очистки с помощью аффинной хроматографии активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, можно использовать матрикс с белком А или белком G. Например, последовательное применение аффинной хроматографии на белке А или G и гель-фильтрации можно применять для выделения активируемой протеазой активирующей Т-клетки биспецифической молекулы практически согласно методу, описанному в разделе «Примеры». Чистоту активируемой протеазой активирующей Т-клетки биспецифической молекулы можно определять с помощью любого из широкого разнообразия хорошо известных аналитических методов, включая гель-электрофорез, жидкостную хроматографию высокого давления и т.п. Например, установлено, что содержащие тяжелые цепи слитые белки, которые экспрессировали согласно описанным в разделе «Примеры» методам, являются интактными и правильно собранными, что продемонстрировано с помощью ДСН-ПААГ в восстанавливающих условиях (см., например, фиг. 8-12). Разделяли три полосы, соответствующие примерно Mr 25000, Mr 50000 и Mr 75000, которые соответствовали предсказанным молекулярным массам легкой цепи, тяжелой цепи и слитому белку тяжелая цепь/легкая цепь активируемой протеазой активирующей Т-клетки биспецифической антигенсвязывающей молекулы.
Анализы
Активируемые протеазой активирующие Т-клетки биспецифические молекулы, представленные в настоящем описании, можно идентифицировать, подвергать скринингу или характеризовать их физические/химические свойства и/или виды биологической активности с помощью различных анализов, известных в данной области.
Анализы аффинности
Аффинность активируемой протеазой активирующей Т-клетки биспецифической молекулы к Fc-рецептору или антигену-мишени можно определять с помощью методов, изложенных в разделе «Примеры», с помощью поверхностного плазмонного резонанса (SPR), используя стандартную инструментальную базу, например, устройство BIAcore (фирма GE Healthcare), и рецепторы или белки-мишени, которые можно получать с помощью рекомбинантной экспрессии. Альтернативно этому, связывание активируемых протеазой активирующих Т-клетки биспецифических молекул с различными рецепторами или антигенами-мишенями можно оценивать с использованием клеточных линий, экспрессирующих конкретный рецептор или антиген-мишень, например, с помощью проточной цитометрии (FACS). Конкретный иллюстративный и приведенный в качестве примера вариант измерения аффинности связывания описан ниже в разделе «Примеры».
Согласно одному из вариантов осуществления изобретения величину Ко измеряли методом поверхностного плазмонного резонанса с помощью устройства BIACORE® Т100 (фирма GE Healthcare) при 25°С.
Для анализа взаимодействия между Fc-областью и Fc-рецепторами меченный с помощью His рекомбинантный Fc-рецептор «захватывали» с помощью антитела к пента-His (фирма Qiagen), иммобилизованного на СМ5-чипах, и биспецифические конструкции применяли в качестве аналитов. В целом, метод состоял в следующем: биосенсорные чипы из карбоксиметилированного декстрана (СМ5, фирма GE Healthcare) активировали с помощью гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (EDC) и N-гидроксисукцинимида (NHS) согласно инструкциям поставщика. Антитело к пента-His разводили 10 мМ ацетатом натрия, рН 5,0 до концентрации 40 мкг/мл перед инъекцией со скоростью потока 5 мкл/мин для достижения уровня иммобилизации, соответствующего примерно 6500 единиц ответа (RU) связанного белка. После инъекции лиганда инъецировали 1М этаноламин для блокады непрореагировавших групп. Затем осуществляли «захват» Fc-рецептора в течение 60 с в концентрации 4 или 10 нМ. Для кинетических измерений инъецировали четырехкратные серийные разведения биспецифической конструкции (диапазон от 500 до 4000 нМ) в буфере HBS-EP+ (фирма GE Healthcare, 10 мМ HEPES, 150 мМ NaCl, 3 мМ ЭДТА, 0,05% сурфактанта Р20, рН 7,4) при 25°С со скоростью потока 30 мкл/мин в течение 120 с.
Для определения аффинности к антигену-мишени биспецифические конструкции «захватывали» с помощью специфического в отношении человеческого Fab антитела (фирма GE Healthcare), которое иммобилизовали на поверхности активированного сенсорного СМ5-чипа согласно методу, описанному для антитела к пента-His. Конечное количество сшитого белка соответствовало примерно 12000 RU. Осуществляли «захват» биспецифических конструкций в течение 90 с в концентрации 300 нМ. Антигены-мишени пропускали через проточные ячейки в течение 180 с в диапазоне концентраций от 250 до 1000 нМ со скоростью потока 30 мкл/мин. Мониторинг диссоциации осуществляли в течение 180 с.
Различия всех показателей преломления корректировали путем вычитания ответа, полученного в проточной референс-ячейке. Ответ на стационарной стадии использовали для определения константы диссоциации (KD) с помощью аппроксимации нелинейной кривой изотермы связывания Ленгмюра. Скорость реакции ассоциации (kon) и реакции диссоциации (koff) рассчитывали с использованием простой модели связывания Ленгмюра 1:1 (программа BIACORE ® Т100 Evaluation Software, версия 1.1.1) путем одновременной аппроксимации сенсограмм ассоциации и диссоциации. Константу равновесия реакции диссоциации (KD) рассчитывали как соотношение koff/kon (см., например, Chen и др., J Mol Biol 293, 1999, сс. 865-881).
Анализы активности
Биологическую активность активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, можно определять с помощью различных анализов, описанных в разделе «Примеры». Виды биологической активности могут включать, например, индукцию пролиферации Т-клеток, индукцию передачи сигнала в Т-клетках, индукцию экспрессии маркеров активации в Т-клетках, индукцию секреции цитокинов Т-клетками, индукцию лизиса клеток-мишеней, таких как опухолевые клетки, и индукцию регресса опухоли и/или повышение выживаемости.
Композиции, препаративные формы и пути введения
Следующим объектом изобретения являются фармацевтические композиции, содержащие любую из активируемых протеазой активирующих Т-клетки биспецифических молекул, представленных в настоящем описании, например, предназначенные для применения в любом из указанных ниже терапевтических способов. В одном из вариантов осуществления изобретения фармацевтическая композиция содержит любую из активируемых протеазой активирующих Т-клетки биспецифических молекул, представленных в настоящем описании, и фармацевтически приемлемый носитель. В другом варианте осуществления изобретения фармацевтическая композиция содержит любую из активируемых протеазой активирующих Т-клетки биспецифических молекул, представленных в настоящем описании, и по меньшей мере одно дополнительное терапевтическое средство, например, указанное ниже.
Кроме того, представлен способ получения активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, в форме, пригодной для введения in vivo, заключающийся в том, что (а) получают активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, и (б) объединяют в препаративной форме активируемую протеазой активирующую Т-клетки биспецифическую молекулу по меньшей мере с одним фармацевтически приемлемым носителем, где полученный препарат активируемой протеазой активирующей Т-клетки биспецифической молекулы пригоден для применения in vivo.
Фармацевтические композиции, предлагаемые в настоящем изобретении, содержат в терапевтически эффективном количестве одну или несколько активируемых протеазой активирующих Т-клетки биспецифических молекул, которая(ые) растворена(ы) или диспергирована(ы) в фармацевтически приемлемом носителе. Понятия «фармацевтически или фармакологически приемлемый» относится к молекулярным субстанциям и композициям, которые, в целом, нетоксичны для реципиентов в применяемых дозах и концентрациях, т.е. не вызывают вредные, аллергические или другие нежелательные реакции при введении при необходимости животному, такому, например, как человек. Приготовление фармацевтической композиции, которая содержит по меньшей мере одну активируемую протеазой активирующую Т-клетки биспецифическую молекулу и необязательно дополнительное действующее вещество, должно быть очевидно специалистам в данной области в свете настоящего описания, например, из справочника Remington's Pharmaceutical Sciences, 18-ое изд., изд-во Mack Printing Company, 1990, включенного в настоящее описание в качестве ссылки. Кроме того, очевидно, что препараты, предназначенные для введения животному (например, человеку), должны удовлетворять требованиям стандартов стерильности, пирогенности и общей безопасности и чистоты, разработанных отделением биологических стандартов FDA (Управление контроля пищевых продуктов и лекарственных средств) или соответствующим уполномоченным органом других стран. Предпочтительными композициями являются лиофилизированные препаративные формы или водные растворы. В контексте настоящего описания «фармацевтически приемлемый носитель» включает любые и все растворители, буферы, дисперсионные среды, покрытия, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактерильные агенты, противогрибные агенты), агенты для придания изотоничности, замедляющие абсорбцию агенты, соли, белки, лекарственные средства, стабилизаторы лекарственных средств, полимеры, гели, связующие вещества, эксципиенты, разрыхлители, замасливатели, подслащивающие вещества, корригенты, красители и подобные материалы и их комбинации, которые должны быть известны обычному специалисту в данной области (см., например, Remington's Pharmaceutical Sciences, 18-ое изд., изд-во Mack Printing Company, 1990, сс. 1289-1329, включенный в настоящее описание в качестве ссылки). В терапевтических или фармацевтических композициях можно применять любой общепринятый носитель, за исключением тех случаев, когда он несовместим с действующим веществом.
Композиция может содержать различные типы носителей в зависимости от того, вводят ли ее в твердой, жидкой или аэрозольной форме, и от того, должна ли она быть стерильной, как в случае использования таких путей введений, как инъекция. Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в настоящем изобретении (и любое дополнительное терапевтическое средство), можно вводить внутривенно, внутрикожно, внутриартериально, внутрибрюшинно, внутрь повреждения, внутрь черепа, внутрь сустава, внутрь предстательной железы, внутрь селезенки, внутриренально, внутриплеврально, внутритрахеально, внутриназально, внутрь стекловидного тела, внутривагинально, внутриректально, внутрь опухоли, внутримышечно, внутрибрюшинно, подкожно, подконъюнктивально, интравезикулярно, в слизистую оболочку, интраперикардиально, внутрь пуповины, интраокулярно, орально, топикально, место, путем ингаляции (например, аэрозольной ингаляции), инъекции, инфузии, непрерывной инфузии, локализованной перфузии, омывающей непосредственно клетки-мишени, через катетер, посредством лаважа, в виде кремов, в липидных композициях (например, липосомах), или с помощью любого другого метода или любой комбинации вышеуказанных путей, известных обычному специалисту в данной области (см., например, Remington's Pharmaceutical Sciences, 18-ое изд., изд-во Mack Printing Company, 1990, включенный в настоящее описание в качестве ссылки). Для введения молекул полипептидов, таких как активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, наиболее часто применяют парентеральное введение, в частности, внутривенную инъекцию.
Парентеральные композиции включают композиции, созданные для введения путем инъекции, например, подкожной, внутрикожной, внутрь повреждения, внутривенной, внутриартериальной, внутримышечной, подоболочечной или внутрибрюшинной инъекции. Для инъекции активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно включать в препаративные формы в виде водных растворов, предпочтительно в физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или физиологический соляной буфер. Раствор может содержать предназначенные для получения препаративной формы агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно этому, активируемые протеазой активирующие Т-клетки биспецифические молекулы могут находиться в порошкообразной форме, предназначенной для восстановления перед применением приемлемым наполнителем, например, стерильной не содержащей пирогенов водой. Стерильные инъецируемые растворы приготавливают путем включения активируемых протеазой активирующих Т-клетки биспецифических молекул, предлагаемых в изобретении, в требуемом количестве в соответствующий растворитель при необходимости в сочетании с различными другими ингредиентами, перечисленными ниже. Стерильность можно легко обеспечивать, например, путем фильтрации через стерильные фильтрующие мембраны. Как правило, дисперсии получают путем включения различных стерилизованных действующих веществ в стерильный наполнитель, который содержит основную дисперсионную среду и/или другие ингредиенты. В случае стерильных порошков для получения стерильных инъецируемых растворов, суспензий или эмульсий предпочтительными методами получения являются вакуумная сушка или сушка вымораживанием, которые позволяют получать порошок действующего вещества в сочетании с любым дополнительным требуемым ингредиентом из предварительно стерилизованной фильтрацией жидкой среды. При необходимости жидкая среда перед осуществлением инъекции может быть соответствующим образом забуферена и жидкому разбавителю сначала придана изотоничность с помощью достаточного количества соляного раствора или глюкозы. Композиция должны быть стабильной в условиях приготовления и хранения и защищена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Принято поддерживать загрязнение эндотоксинами на минимальном безопасном уровне, например, менее 0,5 нг/мг белка. Пригодные фармацевтически приемлемые носители включают (но, не ограничиваясь только ими): буферы, такие как фосфатный, цитратный и буферы на основе других органических кислот; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензиламмонийхлорид; гексаметонийхлорид; бензалконийхлорид; бензетонийхлорид; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол, резорцинол; циклогексанол; 3-пентанол и мета-крезол); низкомолекулярные (содержащие менее примерно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТК; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы с металлами (например, комплексы Zn-белок); и/или неионогенные поверхностно-активные вещества, такие как полиэтиленгликоль (ПЭГ). Водные суспензии для инъекций могут содержать соединения, которые повышают вязкость суспензии, такие как натриевая соль карбоксиметилцеллюлозы, сорбит, декстран или т.п. Необязательно суспензия может содержать также стабилизаторы или агенты, которые повышают растворимость соединений, что позволяет получать высококонцентрированные растворы. Кроме того, суспензии действующих веществ можно получать в виде соответствующих масляных предназначенных для инъекции суспензий. Приемлемые липофильные растворители или наполнители включают жирные нелетучие масла, такие как кунжутное масло, или синтетические эфиры жирных кислот, такие как этилолеаты или триглицериды, или липосомы.
Действующие вещества можно заключать в микрокапсулы, например, полученные с помощью методов коацервации или межфазной полимеризации, например в гидроксипропилметилцеллюлозные или желатиновые микрокапсулы и поли(метилметакрилатные) микрокапсулы соответственно, в коллоидные системы введения лекарственного средства (например, в липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие методы описаны в Remington's Pharmaceutical Sciences, под ред. A. Osol, 1980. Можно приготавливать препараты с замедленным высвобождением. Приемлемыми примерами препаратов с замедленным высвобождением являются полупроницаемые матрицы из твердых гидрофобных полимеров, включающие полипептид, такие матрицы представляют собой изделия определенной формы, например, пленки или микрокапсулы. В конкретном варианте осуществления изобретения для достижения пролонгированной абсорбции инъецируемой композиции можно применять в композиции агенты, замедляющие абсорбцию, такие, например, как моностеарат алюминия, желатин или их комбинации.
Помимо описанных выше композиций, активируемые протеазой активирующие Т-клетки биспецифические молекулы можно приготавливать также в виде препарата в форме депо. Указанные препаративные формы длительного действия можно применять путем имплантации (например, подкожной или внутримышечной) или внутримышечной инъекции. Так, например, активируемые протеазой активирующие Т-клетки биспецифические молекулы можно включать в препаративные формы в сочетании с приемлемыми полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами, или в виде умеренно растворимых производных, например, умеренно растворимой соли.
Фармацевтические композиции, содержащие активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно приготавливать с помощью общепринятых процессов смешения, растворения, эмульгирования, капсулирования, захвата или лиофилизации. Фармацевтические композиции можно включать в препаративные формы с помощью общепринятого метода с использованием одного или нескольких физиологически приемлемых носителей, разбавителей, эксципиентов или вспомогательных веществ, которые облегчают обработку белков, с получением препаратов, которые можно применять в фармацевтических целях. Соответствующая форма зависит от выбранного пути введения.
Активируемые протеазой активирующие Т-клетки биспецифические молекулы можно включать в композиции в виде свободной кислоты или свободного основания, в нейтральной форме или в форме соли. Фармацевтически приемлемые соли представляют собой соли, которые практически сохраняют биологическую активность свободной кислоты или свободного основания. Они включают кислотно-аддитивные соли, например, соли, образованные со свободными аминогруппами белковой композиции, или образованные с неорганическими кислотами, такими, например, как соляная или фосфорная кислота, или такими органическими кислотами, как уксусная, щавелевая, винная или миндальная кислота. Соли, образованные со свободной карбоксильной группой, можно получать также из неорганических оснований, таких, например, как гидроксиды натрия, калия, аммония, кальция или железа; или таких органических оснований как изопропиламин, триметиламин, гистидин или прокаин. Фармацевтические соли имеют тенденцию к более высокой растворимости в водных и других протонных растворителях по сравнению с соответствующими формами в виде свободных оснований.
Способы и композиции для терапевтического применения
Любую из активируемых протеазой активирующих Т-клетки биспецифических молекул, представленных в настоящем описании, можно применять в терапевтических способах. Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно использовать в качестве иммунотерапевтических агентов, например, при лечении различных видов рака.
Для применения в терапевтических способах активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно включать в состав препаративных форм, дозировать и вводить в соответствии с надлежащей клинической практикой. Рассматриваемые в этом контексте факторы включают конкретное нарушение, подлежащее лечению, конкретное млекопитающее, подлежащее лечению, клиническое состояние индивидуального пациента, причину заболевания, область введения агента, метод введения, схему введения и другие факторы, известные практикующим медикам.
Одним из объектов изобретения являются активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, предназначенные для применения в качестве лекарственного средства. Следующими объектами изобретения являются активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, предназначенные для применения при лечении заболевания. Некоторыми вариантами осуществления изобретения являются активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, предназначенные для применения в способе лечения. Одним из вариантов осуществления изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, представленная в настоящем описании, предназначенная для применения при лечении заболевания у индивидуума, который нуждается в этом. Некоторыми вариантами осуществления изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, предназначенная для применения в способе лечения индивидуума, который имеет заболевание, включающем введение индивидууму в терапевтически эффективном количестве активируемой протеазой активирующей Т-клетки биспецифической молекулы. В некоторых вариантах осуществления изобретения заболевание, подлежащее лечению, представляет собой пролиферативное нарушение. В конкретном варианте осуществления изобретения заболевание представляет собой рак. В некоторых вариантах осуществления изобретения способ включает также введение индивидууму в терапевтически эффективном количестве по меньшей мере одного дополнительного терапевтического средства, например, противоракового средства, если заболевание, подлежащее лечению, представляет собой рак. Дополнительными вариантами осуществления изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, представленная в настоящем описании, предназначенная для применения с целью индукции лизиса клетки-мишени, в частности опухолевой клетки. Некоторыми вариантами осуществления изобретения является активируемая протеазой активирующая Т-клетки биспецифическая молекула, предназначенная для применения в способе индукции лизиса клетки-мишени, в частности опухолевой клетки, у индивидуума, который включает введение индивидууму в эффективном количестве активируемой протеазой активирующей Т-клетки биспецифической молекулы для индукции лизиса клетки-мишени. «Индивидуум» в контексте любого из указанных выше вариантов осуществление изобретения представляет собой млекопитающее, предпочтительно человека.
Следующим объектом изобретения является применение активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, для производства или приготовления лекарственного средства. В одном из вариантов осуществления изобретения лекарственное средство предназначено для лечения заболевания у индивидуума, нуждающегося в этом. В одном из вариантов осуществления изобретения лекарственное средство предназначено для применения в способе лечения заболевания, включающем введение индивидууму, который имеет заболевание, в терапевтически эффективном количестве лекарственного средства. В некоторых вариантах осуществления изобретения заболевание, подлежащее лечению, представляет собой пролиферативное нарушение. В конкретном варианте осуществления изобретения заболевание представляет собой рак. В одном из вариантов осуществления изобретения способ включает также введение индивидууму в терапевтически эффективном количестве по меньшей мере одного дополнительного терапевтического средства, например, противоракового средства, если заболевание, подлежащее лечению, представляет собой рак. В другом варианте осуществления изобретения лекарственное средство предназначено для индукции лизиса клетки-мишени, в частности опухолевой клетки. В следующем варианте осуществления изобретения лекарственное средство предназначено для применения в способе индукции лизиса клетки-мишени, в частности опухолевой клетки, у индивидуума, включающему введение индивидууму в эффективном количестве лекарственного средства для индукции лизиса клетки-мишени. «Индивидуум» в контексте любого из указанных выше вариантов осуществления изобретения представляет собой млекопитающее, предпочтительно человека.
Следующим объектом изобретения является способ лечения заболевания. В одном из вариантов осуществления изобретения способ включает введение индивидууму, имеющему указанное заболевание, в терапевтически эффективном количестве активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении. В одном из вариантов осуществления изобретения указанному индивидууму вводят композицию, которая содержит активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, в фармацевтически приемлемой форме. В некоторых вариантах осуществления изобретения заболевание, подлежащее лечению, представляет собой пролиферативное нарушение. В конкретном варианте осуществления изобретения заболевание представляет собой рак. В некоторых вариантах осуществления изобретения способ включает также введение индивидууму в терапевтически эффективном количестве по меньшей мере одного дополнительного терапевтического средства, например, противоракового средства, если заболевание, подлежащее лечению, представляет собой рак. «Индивидуум» в контексте любого из указанных выше вариантов осуществления изобретения может представлять собой млекопитающее, предпочтительно человека.
Следующим объектом изобретения является способ индукции лизиса клетки-мишени, в частности, опухолевой клетки. В одном из вариантов осуществления изобретения способ включает приведение в контакт клетки-мишени с активируемой протеазой активирующей Т-клетки биспецифической молекулой, предлагаемой в изобретении, в присутствии Т-клетки, в частности, цитотоксической Т-клетки. Другим объектом изобретения является способ индукции лизиса клетки-мишени, в частности, опухолевой клетки. В одном из указанных вариантов осуществления изобретения способ включает введение индивидууму в эффективном количестве активируемой протеазой активирующей Т-клетки биспецифической молекулы для индукции лизиса клетки-мишени. В одном из вариантов осуществления изобретения «индивидуум» представляет собой человека.
В некоторых вариантах осуществления изобретения заболевание, подлежащее лечению, представляет собой пролиферативное нарушение, прежде всего рак. Примерами рака являются (но, не ограничиваясь только ими) рак мочевого пузыря, рак головного мозга, рак головы и шеи, рак поджелудочной железы, рак легкого, рак молочной железы, рак яичника, рак матки, рак шейки матки, рак эндометрия, рак пищевода, рак ободочной кишки, колоректальный рак, ректальный рак, рак желудка, рак предстательной железы, рак крови, рак кожи, плоскоклеточная карцинома, рак кости и рак почки. Другие нарушения клеточной пролиферации, которые можно лечить с использованием активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в настоящем изобретении, включают (но, не ограничиваясь только ими) неоплазмы, локализованные в: животе, кости, молочной железе, пищеварительной системе, печени, поджелудочной железе, брюшине, эндокринных железах (надпочечник, паращитовидная, гипофиз, яички, яичник, тимус, щитовидная железа), глазу, голове и шеи, нервной системе (центральной и периферической), лимфатической системе, тазовой области, коже, мягкой ткани, селезенке, грудном отделе и мочеполовой системе. Также под объем изобретения подпадают предраковые состояния или повреждения и метастазы рака. В некоторых вариантах осуществления изобретения рак выбирают из группы, включающей почечноклеточный рак, рак кожи, рак легкого, колоректальный рак, рак молочной железы, рак головного мозга, рак головы и шеи. Специалисту в данной области должно быть очевидно, что во многих случаях активируемая протеазой активирующая Т-клетки биспецифическая молекула не может обеспечивать исцеление, а может только оказывать частичное благоприятное воздействие. В некоторых вариантах осуществления изобретения физиологические изменения, характеризующиеся некоторым благоприятным действием, рассматриваются также как терапевтически ценные. Таким образом, в некоторых вариантах осуществления изобретения количество активируемой протеазой активирующей Т-клетки биспецифической молекулы, которое обеспечивает физиологическое изменение, рассматривается как «эффективное количество» или «терапевтически эффективное количество». Субъект, пациент или индивидуум, нуждающийся в лечении, представляет собой, как правило, млекопитающее, более конкретно человека.
В некоторых вариантах осуществления изобретения активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, вводят в эффективном количестве в клетку. В других вариантах осуществления изобретения активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, вводят в терапевтически эффективном количестве индивидууму для лечения болезни.
Для предупреждения или лечения заболевания соответствующая доза активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении (при ее применении индивидуально или в сочетании с одним или несколькими другими дополнительными терапевтическими средствами), должна зависеть от типа заболевания, подлежащего лечению, пути введения, веса тела пациента, типа активирующей Т-клетки биспецифической антигенсвязывающей молекулы, серьезности и течения заболевания, от того, вводят ли активирующую Т-клетки биспецифическую антигенсвязывающую молекулу в превентивных или терапевтических целях, предшествующих или осуществляемых одновременно терапевтических вмешательств, истории болезни пациента и ответа на активируемую протеазой активирующую Т-клетки биспецифическую молекулу и предписания лечащего врача. Практикующий специалист, ответственный за введение, в любом случае, должен определять концентрацию действующего(их) вещества(в) в композиции и соответствующую(ие) дозу(ы) для индивидуального пациента. Различные схемы введения доз включают (но, не ограничиваясь только ими) однократное введение или несколько введений в различные моменты времени, болюсное введение и пульсирующую инфузию.
Активируемую протеазой активирующую Т-клетки биспецифическую молекулу можно вводить пациенту в виде одной обработки или серий обработок. В зависимости от типа и серьезности заболевания возможная начальная доза активируемой протеазой активирующей Т-клетки биспецифической молекулы для введения пациенту, например, с использованием одного или нескольких индивидуальных введений или с помощью непрерывной инфузии, может составлять примерно от 1 мкг/кг до 15 мг/кг (например, 0,1-10 мг/кг). Типичная суточная доза может составлять от примерно 1 мкг/кг до 100 мг/кг или более в зависимости от отмеченных выше факторов. Для повторных введений в течение нескольких дней или более продолжительного периода в зависимости от состояния лечение, как правило, должно продолжаться до достижения требуемого подавления имеющихся симптомов заболевания. В качестве примера, доза активируемой протеазой активирующей Т-клетки биспецифической молекулы может составлять от примерно 0,005 до примерно 10 мг/кг. В другом примере (но, не ограничиваясь только указанным) доза на одно введение может составлять от примерно 1, примерно 5, примерно 10, примерно 50, примерно 100, примерно 200, примерно 350, примерно 500 мкг/кг веса тела, примерно 1, примерно 5, примерно 10, примерно 50, примерно 100, примерно 200, примерно 350, примерно 500 до примерно 1000 мг/кг веса тела или более, и находиться в любом указанном диапазоне. В качестве примеров (но, не ограничиваясь только ими) указанного диапазона значений, можно вводить от примерно 5 до примерно 100 мг/кг веса тела, от примерно 5 мкг/кг веса тела до примерно 500 мг/кг веса тела и т.д. с учетом указанных выше уровней доз. Так, пациенту можно вводить одну или несколько доз, составляющих примерно 0,5, 2,0, 5,0 или 10 мг/кг (или любую их комбинацию). Указанные дозы можно вводить прерывисто, например, каждую неделю или каждые три недели (например, таким образом, чтобы пациент получал от примерно двух до примерно двадцати или, например, примерно шесть доз активируемой протеазой активирующей Т-клетки биспецифической молекулы). Можно вводить начальную более высокую ударную дозу, после которой применять одну или несколько более низких доз. Однако можно использовать другие схемы введения доз. Успех такой терапии легко оценивать с помощью общепринятых методик и анализов.
Активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, как правило, следует применять в количестве, эффективном для достижения поставленной цели. При применении для лечения или предупреждения болезненного состояния активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, или их фармацевтические композиции, вводят или применяют в терапевтически эффективном количестве. Определение терапевтически эффективного количества находится в компетенции специалистов в данной области, прежде всего в свете представленного подробного описания изобретения.
Для системного введения терапевтически эффективную дозу можно сначала определять с помощью анализов in vitro, например, анализов с использованием клеточных культур. Затем дозу можно включать в форму для изучения на животных моделях для достижения концентрации в кровотоке, находящейся в диапазоне, включающем значение IC50, определенное на клеточной культуре. Указанную информацию можно использовать для более точного определения доз, которые можно применять на людях.
Начальные дозы можно оценивать также, исходя из данных, полученных in vivo, например, на животных моделях, используя методики, хорошо известные в данной области. Обычный специалист в данной области легко может оптимизировать применение на людях на основе данных, полученных на животных.
Уровень доз и интервал можно регулировать индивидуально для получения уровней в плазме активируемых протеазой активирующих Т-клетки биспецифических молекул, которые являются достаточными для поддержания терапевтического действия. Обычные дозы, предназначенные для введения пациенту путем инъекции, составляют от примерно 0,1 до 50 мг/кг/день, как правило, от примерно 0,5 до 1 мг/кг/день. Для достижения терапевтически эффективных уровней в плазме можно вводить несколько доз каждый день. Уровни в плазме можно оценивать, например, с помощью ЖХВР.
В случаях местного применения или избирательного поглощения эффективная местная концентрация активируемых протеазой активирующих Т-клетки биспецифических молекул может не соответствовать концентрации в плазме. Специалист в данной области может оптимизировать терапевтически эффективные местные дозы без чрезмерных экспериментов.
Применение в терапевтически эффективной дозе активируемых протеазой активирующих Т-клетки биспецифических молекул, представленных в настоящем описании, должно, как правило, обеспечивать терапевтическую пользу, не вызывая существенной токсичности. Токсичность и терапевтическую эффективность активируемой протеазой активирующей Т-клетки биспецифической молекулы можно определять с помощью стандартных фармацевтических процедур на культурах клеток или экспериментальных животных. Анализы на клеточных культурах или опыты на животных можно применять для определения значений LD50 (доза, смертельная для 50% популяции) и ED50 (доза, терапевтически эффективная для 50% популяции). Соотношение доз, характеризующих токсические и терапевтические действия, обозначают как терапевтический индекс, который можно выражать в виде соотношения LD50/ED50. Активируемые протеазой активирующие Т-клетки биспецифические молекулы, имеющие высокие терапевтические индексы, являются предпочтительными. В одном из вариантов осуществления изобретения активируемая протеазой активирующая Т-клетки биспецифическая молекула, предлагаемая в настоящем изобретении, характеризуется высоким терапевтическим индексом. Данные, полученные в анализах с использованием клеточных культур и в опытах на животных, можно применять для определения диапазона доз, которые можно применять на людях. Доза лежит предпочтительно в диапазоне концентраций в кровотоке, которые включают ED50, обладающих невысокой токсичностью или не обладающих токсичностью. Доза может варьироваться в зависимости от различных факторов, например, от применяемой лекарственной формы, применяемого пути введения, состояния индивидуума и т.п. Точную препаративную форму, путь введения и дозу может выбирать индивидуально врач в зависимости от состояния пациента (см., например, Fingl и др. в: The Pharmacological Basis of Therapeutics, гл. 1, 1975, с. 1, публикация полностью включена в настоящее описание в качестве ссылки).
Лечащему врачу пациентов, которым вводят активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, должно быть очевидно, как и когда заканчивать, прерывать или регулировать введение из-за токсичности, дисфункции органов и т.п. И, наоборот, лечащему врачу должно быть очевидно, как регулировать лечение в сторону применения более высоких доз, если клинический ответ является неадекватным (предотвращая при этом токсичность). Величина вводимой дозы при лечении представляющего интерес нарушения должна варьироваться в зависимости от серьезности состояния, подлежащего лечению, пути введения и т.п. Серьезность состояния можно, например, оценивать среди прочего с помощью стандартных прогностических методов оценки. Кроме того, доза и предполагаемая частота введения дозы должны также варьироваться в зависимости от возраста, веса тела и ответа индивидуального пациента.
Другие средства и варианты лечения
Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, при лечении можно вводить в сочетании с одним или несколькими другими средствами. Например, активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении, можно вводить совместно по меньшей мере с одним дополнительным терапевтическим средством. Понятие «терапевтическое средство» включает любое средство, которое вводят для лечения симптома или заболевания у индивидуума, который нуждается в таком лечении. Указанное дополнительное терапевтическое средство может представлять собой любое действующее вещество, которое можно применять при конкретном показании, подлежащем лечению, предпочтительно с дополнительными видами активности, которые не оказывают отрицательное действие друг на друга. В некоторых вариантах осуществления изобретения дополнительное терапевтическое средство представляет собой иммуномодулятор, цитостатическое средство, ингибитор клеточной адгезии, цитотоксическое средство, активатор клеточного апоптоза или средство, повышающее чувствительность клеток к индукторам апоптоза. В конкретном варианте осуществления изобретения дополнительное терапевтическое средство представляет собой противораковое средство, например, агент, разрушающий микротрубочки, антиметаболит, ингибитор топоизомеразы, интеркалятор ДНК, алкилирующий агент, средство гормональной терапии, ингибитор киназ, антагонист рецептора, активатор апоптоза опухолевых клеток или антиангиогенное средство.
Указанные другие средства могут присутствовать в комбинации в количествах, эффективных для указанных целей. Эффективное количество указанных других средств зависит от количества применяемой активируемой протеазой активирующей Т-клетки биспецифической молекулы, типа нарушения или лечения, и других указанных выше факторов. Активируемую протеазой активирующую Т-клетки биспецифическую молекулу, как правило, применяют в таких же дозах и с использованием указанных в настоящем описании путей введения, или в дозах, составляющих примерно от 1 до 99% от указанных в настоящем описании доз, или в любой дозе и с использованием любого пути введения, которые согласно эмпирическим/клиническим данным рассматриваются как приемлемые.
Отмеченные выше комбинированные терапии предусматривают совместное введение (когда два или большее количество терапевтических средств включают в одну и ту же или в отдельные композиции) и раздельное введение, в этом случае введение активируемой протеазой активирующей Т-клетки биспецифической молекулы, предлагаемой в изобретении, можно осуществлять до, одновременно и/или после введения дополнительного терапевтического средства и/или адъюванта. Активируемые протеазой активирующие Т-клетки биспецифические молекулы, предлагаемые в изобретении, можно применять также в сочетании с лучевой терапией.
Изделия
Другим объектом изобретения является изделие, которое содержит продукты, применяемые для лечения, предупреждения и/или диагностирования указанных выше нарушений. Изделие представляет собой контейнер и этикетку или листовку-вкладыш в упаковку, которая размещена на контейнере или прилагаются к нему. Приемлемыми контейнерами являются, например банки, пузырьки, шприцы, пакеты для внутривенного (IV) раствора и т.д. Контейнеры можно изготавливать из различных материалов, таких как стекло или пластмасса. Контейнер содержит композицию, которая сама по себе или в сочетании с другой композицией является эффективной для лечения, предупреждения и/или диагностирования состояния, и может иметь стерильный порт доступа (например, контейнер может представлять собой пакет для внутривенного раствора или пузырек, снабженный пробкой, которую можно прокалывать с помощью иглы для подкожных инъекций). По меньшей мере одно действующее вещество в композиции представляет собой активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении. На этикетке или листовке-вкладыше в упаковку указано, что композицию применяют для лечения выбранного состояния. Кроме того, изделие может включать (а) первый контейнер с находящейся в нем композицией, где композиция содержит активируемую протеазой активирующую Т-клетки биспецифическую молекулу, предлагаемую в изобретении; и (б) второй контейнер с находящейся в нем композицией, где композиция содержит дополнительное цитотоксическое или иное терапевтическое средство. Согласно этому варианту осуществления изобретения изделие может содержать листовку-вкладыш в упаковку, которая содержит информацию о том, что композиции можно использовать для лечения конкретного состояния. В альтернативном или дополнительном варианте изделие может дополнительно включать второй (или третий) контейнер с фармацевтически приемлемым буфером, таким как бактериостатическая вода для инъекций (БСВИ), забуференный фосфатом физиологический раствор, раствор Рингера и раствор декстрозы. Кроме того, оно может включать другие материалы, необходимые с коммерческой точки зрения и с точки зрения потребителя, в частности, другие буферы, разбавители, фильтры, иглы и шприцы.
Примеры вариантов осуществления изобретения
1. Активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(а) первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3;
(б) второй антигенсвязывающий фрагмент, обладающий способностью специфически связываться с антигеном клетки-мишени; и
(в) маскирующий фрагмент, ковалентно присоединенный к биспецифической связывающей Т-клетки молекуле через расщепляемый протеазой линкер, где маскирующий фрагмент обладает способностью специфическим связываться с идиотипом первого или второго антигенсвязывающего фрагмента, тем самым обратимо скрывая первый или второй антигенсвязывающий фрагмент.
2. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 1, в которой маскирующий фрагмент ковалентно присоединен к первому антигенсвязывающему фрагменту и обратимо скрывает первый антигенсвязывающий фрагмент.
3. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 1 или 2, в которой маскирующий фрагмент ковалентно присоединен к вариабельной области тяжелой цепи первого антигенсвязывающего фрагмента.
4. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 1 или 2, в которой маскирующий фрагмент ковалентно присоединен к вариабельной области легкой цепи первого антигенсвязывающего фрагмента.
5. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-4, в которой маскирующий фрагмент представляет собой антиидиотипический scFv.
6. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 2-5, где активируемая протеазой активирующая Т-клетки биспецифическая молекула содержит второй маскирующий фрагмент, который обратимо скрывает второй антигенсвязывающий фрагмент.
7. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-6, где протеаза экспрессируется клеткой-мишенью.
8. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-7, в которой второй антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области легкой цепи Fab и тяжелой цепи Fab обменены.
9. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-8, в которой второй антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой константные области легкой цепи Fab и тяжелой цепи Fab обменены.
10. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-9, в которой первый антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab.
11. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-10, содержащая не более одного антигенсвязывающего фрагмента, который обладает способностью специфически связываться с CD3.
12. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-11, содержащая третий антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с антигеном клетки-мишени.
13. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 12, в которой третий антигенсвязывающий фрагмент идентичен второму антигенсвязывающему фрагменту.
14. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-13, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 или HER1.
15. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-13, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с антигеном клетки-мишени, выбранным из группы, которая состоит из FolR1, HER1 и мезотелина.
16. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-13, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с антигеном клетки-мишени, выбранным из группы, которая состоит из FolR1, HER1, HER2 и мезотелина.
17. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-16, в которой первый и второй антигенсвязывающие фрагменты слиты друг с другом необязательно через пептидный линкер.
18. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-17, в которой второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента.
19. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-17, в которой первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента.
20. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-19, в которой легкая цепь Fab первого антигенсвязывающего фрагмента и легкая цепь Fab второго антигенсвязывающего фрагменты слиты друг с другом, необязательно через пептидный линкер.
21. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-20, дополнительно содержащая Fc-домен, который состоит из первой и второй субъединиц, обладающих способностью к стабильной ассоциации.
22. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 21, в которой Fc-домен представляет собой Fc-домен IgG, в частности, IgG1 или IgG4.
23. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 21 или 22, в которой Fc-домен представляет собой человеческий Fc-домен.
24. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 21-23, в которой Fc-домен характеризуется пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с нативным Fc-доменом IgG1.
25. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 24, в которой Fc-домен содержит одну или несколько аминокислотных замен, которые снижают связывание с Fc-рецептором и/или эффекторную функцию.
26. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 25, в которой указанная(ые) одна или несколько аминокислотная(ые) замена(ы) находится(ятся) в одном или нескольких положении(ях), выбранной(ых) из группы L234, L235 и Р329 (нумерация по Кэботу).
27. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 26, в которой каждая субъединица Fc-домена содержит три аминокислотные замены, которые снижают связывание с активирующим Fc-рецептором и/или эффекторную функцию, где указанные аминокислотные замены представляют собой L234A, L235A и P329G.
28. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 24-27, где Fc-рецептор представляет собой Fcγ-рецептор.
29. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 24-28, где эффекторная функция представляет собой антитело-обусловленную клеточнозависимую цитотоксичность (ADCC).
30. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-29, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21); и
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22).
31. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-30, в которой маскирующий фрагмент содержит вариабельную область легкой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
32. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-31, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21);
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22); и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
33. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-29, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27); и
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28).
34. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-29 и 33, в которой маскирующий фрагмент содержит вариабельную область легкой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
35. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-29 и 33-34, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27);
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28); и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
36. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-35, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYYIN (SEQ ID NO: 48);
(б) аминокислотную последовательность CDR Н2 VINPDSGGTDYNQNFKG (SEQ ID NO: 49); и
(в) аминокислотную последовательность CDR Н3 RDSYGFDY (SEQ ID NO: 50).
37. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-36, в которой маскирующий фрагмент содержит вариабельную область легкой цепи, содержащую по меньшей мере одну из следующих последовательностей:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 KASLSVTNDVA (SEQ ID NO: 51);
(д) аминокислотную последовательность CDR L2 YASNRNA (SEQ ID NO: 52); и
(е) аминокислотную последовательность CDR L3 QQDYTSPPT (SEQ ID NO: 53).
38. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-37, в которой маскирующий фрагмент содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYYIN (SEQ ID NO: 48);
(б) аминокислотную последовательность CDR Н2 VINPDSGGTDYNQNFKG (SEQ ID NO: 49);
(в) аминокислотную последовательность CDR Н3 RDSYGFDY (SEQ ID NO: 50); и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 KASLSVTNDVA (SEQ ID NO: 51);
(д) аминокислотную последовательность CDR L2 YASNRNA (SEQ ID NO: 52); и
(е) аминокислотную последовательность CDR L3 QQDYTSPPT (SEQ ID NO: 53).
39. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-38, в которой расщепляемый протеазой линкер содержит по меньшей мере одну распознаваемую протеазой последовательность.
40. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 39, в которой расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность.
41. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 40, в которой распознаваемая протеазой последовательность выбрана из группы, состоящей из:
(а) RQARVVNG (SEQ ID NO: 36);
(б) VHMPLGFLGPGRSRGSFP (SEQ ID NO: 37);
(в) RQARVVNGXXXXXVPLSLYSG (SEQ ID NO: 38); и
(г) RQARVVNGVPLSLYSG (SEQ ID NO: 39);
(д) PLGLWSQ (SEQ ID NO: 40), где X обозначает любую аминокислоту.
42. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 40, в которой распознаваемая протеазой последовательность выбрана из группы, состоящей из:
(а) RQARVVNG (SEQ ID NO: 36);
(б) VHMPLGFLGPGRSRGSFP (SEQ ID NO: 37);
(в) RQARVVNGXXXXXVPLSLYSG (SEQ ID NO: 38);
(г) RQARVVNGVPLSLYSG (SEQ ID NO: 39);
(д) PLGLWSQ (SEQ ID NO: 40);
(е) VHMPLGFLGPRQARVVNG (SEQ ID NO: 97);
(ж) FVGGTG (SEQ ID NO: 98);
(з) KKAAPVNG (SEQ ID NO: 99);
(и) PMAKKVNG (SEQ ID NO: 100);
(к) QARAKVNG (SEQ ID NO: 101);
(л) VHMPLGFLGP (SEQ ID NO: 102);
(м) QARAK (SEQ ID NO: 103);
(н) VHMPLGFLGPPMAKK (SEQ ID NO: 104);
(о) KKAAP (SEQ ID NO: 105); и
(п) PMAKK (SEQ ID NO: 106), где X обозначает любую аминокислоту.
43. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 39 или 40, в которой расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность RQARVVNG (SEQ ID NO: 36).
44. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 39 или 40, в которой расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность VHMPLGFLGPRQARVVNG (SEQ ID NO: 97).
45. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 39 или 40, в которой расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность RQARVVNG (SEQ ID NO: 36) или распознаваемую протеазой последовательность VHMPLGFLGPRQARVVNG (SEQ ID NO: 97).
46. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-45, где протеаза выбрана из группы, состоящей из металлопротеиназы, сериновой протеазы, цистеиновой протеазы, аспарагиновой протеазы и протеазы катепсина.
47. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 46, где металлопротеиназа представляет собой матричную металлопротеиназу (ММР), предпочтительно ММР9 или ММР2.
48. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по варианту осуществления изобретения 46, где сериновая протеаза представляет собой матриптазу.
49. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, в которой первый антигенсвязывающий фрагмент содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 44, SEQ ID NO: 45 и SEQ ID NO: 46, по меньшей мере один CDR легкой цепи, выбранный из группы, которая состоит из SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
50. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-49, в которой первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, содержащую:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 TYAMN (SEQ ID NO: 44);
(б) аминокислотную последовательность CDR Н2 RIRSKYNNYATYYADSVKG (SEQ ID NO: 45); и
(в) аминокислотную последовательность CDR Н3 HGNFGNSYVSWFAY (SEQ ID NO: 46); и вариабельную область легкой цепи, содержащую:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 GSSTGAVTTSNYAN (SEQ ID NO: 17);
(д) аминокислотную последовательность CDR L2 GTNKRAP (SEQ ID NO: 18); и
(е) аминокислотную последовательность CDR L3 ALWYSNLWV (SEQ ID NO: 19).
51. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-50, в которой первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
52. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-50, в которой первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 55.
53. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 14, SEQ ID NO: 15 и SEQ ID NO: 16, и по меньшей мере один CDR легкой цепи, выбранный из группы: SEQ ID NO: 17, SEQ ID NO: 18 и SEQ ID NO: 19.
54. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-53, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, содержащую:
а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 NAWMS (SEQ ID NO: 14);
б) аминокислотную последовательность CDR Н2 RIKSKTDGGTTDYAAPVKG (SEQ ID NO: 15); и
в) аминокислотную последовательность CDR Н3 PWEWSWYDY (SEQ ID NO: 16); и вариабельную область легкой цепи, содержащую:
г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 GSSTGAVTTSNYAN (SEQ ID NO: 17);
д) аминокислотную последовательность CDR L2 GTNKRAP (SEQ ID NO: 18); и
е) аминокислотную последовательность CDR L3 ALWYSNLWV (SEQ ID NO: 19).
55. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-54, в которой второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 47, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 55.
56. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-54, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 47, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 55.
57. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 151, SEQ ID NO: 152 и SEQ ID NO: 153, и по меньшей мере один CDR легкой цепи, выбранный из группы: SEQ ID NO: 154, SEQ ID NO: 155 и SEQ ID NO: 156.
58. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52 или 57, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, содержащую:
а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYYMH (SEQ ID NO: 151);
б) аминокислотную последовательность CDR Н2 IINPSGGSTSYAQKFQG (SEQ ID NO: 152); и
в) аминокислотную последовательность CDR Н3 SFFTGFHLDY (SEQ ID NO: 153); и вариабельную область легкой цепи, содержащую:
г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASQSVSSSYLA (SEQ ID NO: 154);
д) аминокислотную последовательность CDR L2 GASSRAT (SEQ ID NO: 155); и
е) аминокислотную последовательность CDR L3 QQYTNEHYYT (SEQ ID NO: 156).
59. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, 57 или 58, в которой второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 157, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 158.
60. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52 или 57, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с FolR1 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 157, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 158.
61. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит по меньшей мере один гипервариабельный участок (CDR) тяжелой цепи, выбранный из группы, которая состоит из SEQ ID NO: 107, SEQ ID NO: 108 и SEQ ID NO: 109, и по меньшей мере один CDR легкой цепи, выбранный из группы: SEQ ID NO: 110, SEQ ID NO: 111 и SEQ ID NO: 112.
62. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52 или 61, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит вариабельную область тяжелой цепи, содержащую:
а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 GYTMN (SEQ ID NO: 107);
б) аминокислотную последовательность CDR Н2 LITPYNGASSYNQKFRG (SEQ ID NO: 108); и
в) аминокислотную последовательность CDR Н3 GGYDGRGFDY (SEQ ID NO: 109); и вариабельную область легкой цепи, содержащую:
г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 SASSSVSYMH (SEQ ID NO: 110);
д) аминокислотную последовательность CDR L2 DTSKLAS (SEQ ID NO: 111); и
е) аминокислотную последовательность CDR L3 QQWSKHPLT (SEQ ID NO: 112).
63. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, 61 или 62, в которой второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 113, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 114.
64. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52 или 61-63, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с мезотелином и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 113, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 114.
65. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52, в которой второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 32, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая идентична по меньшей мере примерно на 95%, 96%, 97%, 98%, 99% или 100% аминокислотной последовательности SEQ ID NO: 33.
66. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-52 или 65, в которой второй антигенсвязывающий фрагмент обладает способностью специфически связываться с HER1 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 115, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 116.
67. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 2;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 1.
68. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 4;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 1.
69. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
а) по меньшей мере одну тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 32;
б) по меньшей мере одну легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 34.
70. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 72;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 1.
71. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 85;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 3; и
(в) легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 1.
72. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 73;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 3;
(в) первую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 1; и
(г) вторую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 74.
73. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 77;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 82;
(в) первую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 78; и
(г) вторую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 81.
74. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 76;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 77;
(в) первую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 78; и
(г) вторую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 79.
75. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 132;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 136;
(в) первую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 81; и
(г) вторую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 133.
76. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-48, содержащая
(а) первую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 137;
(б) вторую тяжелую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 139;
(в) первую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 81; и
(г) вторую легкую цепь, которая содержит аминокислотную последовательность SEQ ID NO: 138.
77. Идиотипспецифический полипептид, предназначенный для обратимого сокрытия анти-CD3 антигенсвязывающего сайта молекулы.
78. Идиотипспецифический полипептид по варианту осуществления изобретения 77, где идиотипспецифический полипептид представляет собой антиидиотипический scFv.
79. Идиотипспецифический полипептид по варианту осуществления изобретения 77 или 78, где идиотипспецифический полипептид ковалентно присоединен к молекуле через линкер.
80. Идиотипспецифический полипептид по варианту осуществления изобретения 79, где линкер представляет собой пептидный линкер.
81. Идиотипспецифический полипептид по варианту осуществления изобретения 79 или 80, где линкер представляет собой расщепляемый протеазой линкер.
82. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 79-81, где пептидный линкер содержит по меньшей мере один распознаваемый протеазой сайт.
83. Идиотипспецифический полипептид по варианту осуществления изобретения 82, где протеаза выбрана из группы, состоящей из металлопротеиназы, сериновой протеазы, цистеиновой протеазы, аспарагиновой протеазы и протеазы катепсина.
84. Идиотипспецифический полипептид по варианту осуществления изобретения 83, где металлопротеиназа представляет собой матричную металлопротеиназу (ММР), предпочтительно ММР9 или ММР2.
85. Идиотипспецифический полипептид по варианту осуществления изобретения 83, где сериновая протеаза представляет собой матриптазу.
86. Идиотипспецифический полипептид по варианту осуществления изобретения 82, где расщепляемый протеазой линкер содержит распознаваемую протеазой последовательность RQARVVNG (SEQ ID NO: 36) или распознаваемую протеазой последовательность VHMPLGFLGPRQARVVNG (SEQ ID NO: 97).
87. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-86, где молекула представляет собой активирующую Т-клетки биспецифическую молекулу.
88. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-87, содержащий вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21); и
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22).
89. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-88, содержащий вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
90. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-87, содержащий вариабельную область тяжелой цепи, которая содержит:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 DYSIH (SEQ ID NO: 20);
(б) аминокислотную последовательность CDR Н2 WINTETGEPAYADDFKG (SEQ ID NO: 21);
(в) аминокислотную последовательность CDR Н3 PYDYDVLDY (SEQ ID NO: 22); и вариабельную область легкой цепи, которая содержит:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASKSVSTSNYSYIH (SEQ ID NO: 23);
(д) аминокислотную последовательность CDR L2 YVSYLES (SEQ ID NO: 24); и
(е) аминокислотную последовательность CDR L3 QHSREFPWT (SEQ ID NO: 25).
91. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-87, содержащий вариабельную область тяжелой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27); и
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28).
92. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-87 и 91, содержащий вариабельную область легкой цепи, которая содержит по меньшей мере одну из следующих последовательностей:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
93. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-87, содержащий вариабельную область тяжелой цепи, которая содержит:
(а) аминокислотную последовательность гипервариабельного участка тяжелой цепи (CDR Н) 1 SYGVS (SEQ ID NO: 26);
(б) аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27);
(в) аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28); и вариабельную область легкой цепи, которая содержит:
(г) аминокислотную последовательность гипервариабельного участка легкой цепи (CDR L) 1 RASENIDSYLA (SEQ ID NO: 29);
(д) аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO: 30); и
(е) аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31).
94. Идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-93, в котором анти-CD3 антигенсвязывающий сайт содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 55.
95. Выделенный полинуклеотид, кодирующий активируемую протеазой активирующую Т-клетки биспецифическую антигенсвязывающую молекулу по одному из вариантов осуществления изобретения 1-76 или идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-94.
96. Полипептид, кодируемый полинуклеотидом по варианту осуществления изобретения 95.
97. Вектор, прежде всего экспрессионный вектор, содержащий полинуклеотид по варианту осуществления изобретения 95.
98. Клетка-хозяин, содержащая полинуклеотид по варианту осуществления изобретения 95 или вектор по варианту осуществления изобретения 97.
99. Способ получения активируемой протеазой активирующей Т-клетки биспецифической молекулы, включающий стадии, на которых а) культивируют клетку-хозяина по варианту осуществления изобретения 98 в условиях, пригодных для экспрессии активируемой протеазой активирующей Т-клетки биспецифической молекулы, и б) выделяют активируемую протеазой активирующую Т-клетки биспецифическую молекулу.
100. Активируемая протеазой активирующая Т-клетки биспецифическая молекула, полученная способом по варианту осуществления изобретения 99.
101. Способ получения идиотипспецифического полипептида, включающий стадии, на которых а) культивируют клетку-хозяина по варианту осуществления изобретения 98 в условиях, пригодных для экспрессии идиотипспецифического полипептида, и б) выделяют идиотипспецифический полипептид.
102. Идиотипспецифический полипептид, полученный способом по варианту осуществления изобретения 101.
103. Фармацевтическая композиция, содержащая активируемую протеазой активирующую Т-клетки биспецифическую молекулу по одному из вариантов осуществления изобретения 1-76 и фармацевтически приемлемый носитель.
104. Фармацевтическая композиция, содержащая идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-94 и фармацевтически приемлемый носитель.
105. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-76, идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-94 или композиция по варианту осуществления изобретения 103, предназначенные для применения в качестве лекарственного средства.
106. Активируемая протеазой активирующая Т-клетки биспецифическая молекула, предназначенная для применения по варианту осуществления изобретения 105, где лекарственное средство предназначено для лечения или замедления развития рака, лечения или замедления развития связанного с иммунной системой заболевания или повышения или стимуляции иммунного ответа или функции у индивидуума.
107. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из вариантов осуществления изобретения 1-76, идиотипспецифический полипептид по одному из вариантов осуществления изобретения 77-94 или композиция по варианту осуществления изобретения 103, предназначенные для применения для лечения заболевания у индивидуума, который нуждается в этом.
108. Активируемая протеазой активирующая Т-клетки биспецифическая молекула или идиотипспецифический полипептид, предназначенная/предназначенный для применения для лечения заболевания у индивидуума, который нуждается в этом, по варианту осуществления изобретения 107, где заболевание представляет собой рак.
109. Применение активируемой протеазой активирующей Т-клетки биспецифической молекулы по одному из вариантов осуществления изобретения 1-76 или идиотипспецифического полипептида по одному из вариантов осуществления изобретения 77-94 для приготовления лекарственного средства.
110. Применение по варианту осуществления изобретения 109, в котором заболевание представляет собой рак.
111. Способ лечения заболевания у индивидуума, включающий введение указанному индивидууму в терапевтически эффективном количестве композиции, содержащей активируемую протеазой активирующую Т-клетки биспецифическую молекулу по одному из вариантов осуществления изобретения 1-76, или композиции по варианту осуществления изобретения 103.
112. Способ индукции лизиса клетки-мишени, включающий приведение в контакт клетки-мишени с активируемой протеазой активирующей Т-клетки биспецифической молекулой по одному из вариантов осуществления изобретения 1-76 или композицией по варианту осуществления изобретения 103 в присутствии Т-клетки.
113. Способ по варианту осуществления изобретения 112, в котором клетка-мишень представляет собой раковую клетку.
114. Способ по варианту осуществления изобретения 112 или 113, в котором клетка-мишень экспрессирует протеазу, которая обладает способностью активировать активируемую протеазой активирующую Т-клетки биспецифическую молекулу.
115. Антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент, специфическое/специфически в отношении идиотипа анти-CD3 антигенсвязывающей молекулы, где антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент при связывании с анти-CD3 антигенсвязывающей молекулой специфически блокирует связывание анти-CD3 антигенсвязывающей молекулы с CD3.
116. Антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент по варианту осуществления изобретения 115, где антиидиотипическое антитело к CD3 или его фрагмент обратимо ассоциированы с анти-CD3 антигенсвязывающей молекулой через пептидный линкер, который содержит распознаваемый протеазой сайт.
117. Антиидиотипическое антитело к CD3 или его антигенсвязывающий фрагмент по варианту осуществления изобретения 115 или 116, где CD3 представляет собой мышиный, обезьяний или человеческий CD3.
118. Способ снижения токсичности in vivo активирующей Т-клетки биспецифической молекулы, включающий присоединение идиотипспецифического полипептида по одному из вариантов осуществления изобретения 77-94 к активирующей Т-клетки биспецифической молекуле с помощью расщепляемого протеазой линкера с получением активируемой протеазой активирующей Т-клетки биспецифической молекулы, при этом токсичность in vivo активируемой протеазой активирующей Т-клетки биспецифической молекулы снижается по сравнению с токсичностью активирующей Т-клетки биспецифической молекулы.
119. Изобретение как оно представлено выше в настоящем описании.
Примеры
Ниже представлены примеры способов и композиций, предлагаемых в изобретении. Как должно быть очевидно, можно воплощать на практике различные другие варианты осуществления изобретения в целом с учетом представленного выше описания изобретения.
Пример 1
Синтез одновалентных молекул анти-CD3 IgG с антиидиотипическим scFv
В настоящем описании представлены CD3-связывающие агенты, которые замаскированы с помощью связанного на N-конце антиидиотипического CD3 scFv. Эти конструкции включают распознаваемый протеазой сайт, который распознается специфической для опухоли протеазой. В присутствии экспрессирующих протеазу опухолевых клеток линкер, соединяющий маскирующий фрагмент, может расщепляться и в результате этого восстанавливается связывание CD3 CD3-связывающим агентом. Получали несколько одновалентных молекул анти-CD3 IgG с различными антиидиотипическими scFv, и они схематически представлены на фиг. 1А-Д под соответствующими им идентификационными (ID) номерами. Получали следующие молекулы:
Идентификационный №.7859: одновалентный CD3 IgG (антиидиотипический scFv 4.15.64 - сайт матриптазы MK062 - CD3 - слитый на N-конце с CD3 Fab - инертный Fc), слитый на N-конце с анти-CD3 scFv 4.15.64 и расщепляемым протеазой линкером.
Идентификационный №.7860: одновалентный CD3 IgG (антиидиотипический scFv 4.32.63 - сайт матриптазы MK062 - CD3 - слитый на N-конце с CD3 Fab - инертный Fc), слитый на N-конце с анти-CD3 scFv 4.32.63 и расщепляемым протеазой линкером.
Идентификационный №7857: одновалентный CD3 IgG (антиидиотипический scFv 4.15.64 - нерасщепляемый линкер - CD3 - слитый на N-конце с CD3 Fab - инертный Fc), слитый на N-конце с анти-CD3 scFv 4.15.64 и расщепляемым протеазой линкером.
Идентификационный №7858: одновалентный CD3 IgG (антиидиотипический scFv 4.32.63 - нерасщепляемый линкер - CD3 - слитый на N-конце с CD3 Fab - инертный Fc), слитый на N-конце с анти-CD3 scFv 4.32.63 и расщепляемым протеазой линкером.
Идентификационный №7861: одновалентный CD3 IgG (CD3 Fab - инертный Fc), слитый на N-конце с анти-CD3 scFv 4.15.64/4.32.63 и (расщепляемым) протеазой линкером.
Последовательности антиидиотипических (ID) связывающих агентов получали с помощью RACE-ПЦР (ПЦР с быстрой амплификацией концов кДНК) из РНК клеток гибридомы. Клетки гибридомы получали путем иммунизации мышей Fab-фрагментом СН2527 (VL_7-46(13)/VH_3-23(12)). Синтез последовательности одноцепочечного Fv (ScFv), включая необходимые для клонирования сайты рестрикции, заказывали на фирме Invitrogen. Сравнивали аффинность шести различных антиидиотипических СН2527-связывающих агентов (фиг. 2, результаты Biacore-анализа (фирма AG М. Schräml) при 25°С/37°С (аналит: MAK<CEA/CD3>rH)), и два из них клонировали в виде N-концевых слияний на тяжелой цепи CD3 Fab - Fc.
ДНК-последовательности анти-ID одноцепочечных Fv субклонировали в рамке считывания с CD3 VH-цепью, предварительно встроенной в соответствующий применяемый в качестве реципиента экспрессионный вектор для клеток млекопитающих. Экспрессия белка находилась под контролем MPSV-промотора, а на 3'-конце CDS присутствовала синтетическая сигнальная полиА-последовательность. Кроме того, каждый вектор содержал последовательность OriP EBV.
Молекулы получали путем совместной трансфекции растущих в суспензии клеток HEK293-EBNA экспрессионными векторами для клеток млекопитающих с использованием полиэтиленимина (ПЭИ). Клетки трансфектировали соответствующими экспрессионными векторами в соотношении 1:1: 2 («Fc «впадина» (СН2-СН3)»: «общая легкая цепь (CLC)» : «вектор тяжелой цепи с «выступом» (scFv-VH-CH1-CH2-CH3)»).
Для трансфекции клетки HEK293 EBNA культивировали в бессывороточной культуральной среде Excell, содержащей 6 мМ L-глутамин и 250 мг/л культуральной среды G418. Для производства высевали в центрифужные флаконы вместимостью 600 мл (максимальный рабочий объем 400 мл) 800 млн клеток HEK293 EBNA за 24 ч до трансфекции без G418. Для трансфекции 800 млн клеток центрифугировали в течение 5 мин при 210 × g, и супернатант заменяли 40 мл предварительно нагретой среды CD СНО, содержащей 6 мМ L-глутамин. Экспрессионные векторы смешивали в 40 мл среды CD СНО, содержащей 6 мМ L-глутамин, для получения конечного количества ДНК 400 мкг. После добавления 1080 мкл раствора ПЭИ (2,7 мкг/мл) смесь интенсивно перемешивали в течение 15 с и затем инкубировали в течение 10 мин при комнатной температуре. Затем клетки смешивали с раствором ДНК/ПЭИ, переносили в 600-миллилитровый центрифужный флакон и инкубировали в течение 3 ч при 37°С в инкубаторе в атмосфере, содержащей 5% СО2. После инкубации добавляли 360 мл среды Excell + 6 мМ L-глутамин + 5 г/л Pepsoy + 1,0 мМ VPA +3 г/л глюкозы, и клетки культивировали в течение 24 ч перед осуществлением подпитки 7% Feed 7. После культивирования в течение 6-7 дней супернатант собирали для очистки путем центрифугирования в течение 20-30 мин при 210 × g (центрифуга Sigma 8K). Раствор стерилизовали фильтрацией (фильтр с размером пор 0,22 мкм) и добавляли азид натрия в конечной концентрации 0,01% (мас./об.). Раствор хранили при 4°С до очистки. Секретированный белок очищали из супернатантов клеточных культур с помощью аффинной хроматографии, применяя аффинную хроматографию на белке А, с последующей(ими) одной или двумя стадией(ями) гель-фильтрации.
Для проведения аффинной хроматографии супернатант вносили на колонку HiTrap белок A FF (CV (объем колонки) = 5 мл, фирма GE Healthcare), уравновешенную 25 мл буфера, содержащего 20 мМ фосфат натрия, 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 7,5. Несвязанный белок удаляли промывкой, используя равный по меньшей мере 10 объемам колонки объем буфера, содержащего 20 мМ фосфат натрия, 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 7,5, требуемый белок элюировали, применяя равный 20 объемам колонки объем буфера (градиент от 0% до 100%), содержащего 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 2,5. Раствор белка нейтрализовали путем добавления 1/10 2М Трис, рН 10,5. Требуемый белок концентрировали с помощью ультра-концентратора Amicon®Ultra-15 Ultracel 30K (фирма Merck Millipore Ltd.) до объема, составляющего максимум 4 мл, перед загрузкой на колонку HiLoad Супердекс 200 (фирма GE Healthcare), уравновешенную буфером, содержащим 20 мМ гистидин, 140 мМ хлорид натрия, рН 6,0, 0,01% Твин-20.
При осуществлении анализа белка после гель-фильтрации чистоту и молекулярную массу молекул в виде единичных фракций определяли с помощью ДСН-ПААГ в отсутствии восстановителя и осуществляли окрашивание кумасси (InstantBlue™, фирма Expedeon). Применяли систему геля NuPAGE® Pre-Cast (4-12% Бис-Трис, фирма Invitrogen или 3-8% Трис-ацетата, фирма Invitrogen) согласно инструкции производителя.
Концентрацию белков в очищенных белковых образцах определяли, измеряя оптическую плотность (ОП) при 280 нм, осуществляя деление на коэффициент молярной экстинкции, рассчитанный на основе аминокислотной последовательности.
Чистоту и молекулярную массу молекул после конечной стадии очистки анализировали с помощью КЭ-ДСН в присутствии восстановителя и без него. Применяли систему Caliper LabChip GXII (фирма Caliper Lifescience) согласно инструкции производителя. Содержание агрегатов молекул определяли с использованием колонки для аналитической гель-фильтрации TSKgel G3000 SW XL (фирма Tosoh), применяя подвижный буфер, содержащий 25 мМ K2HPO4, 125 мМ NaCl, 200 мМ моногидрохлорид L-аргинина, 0,02% (мас./об.) NaN3, рН 6,7 при 25°С. Конечное качество всех молекул оказалось высоким с содержанием мономеров ≥92%.
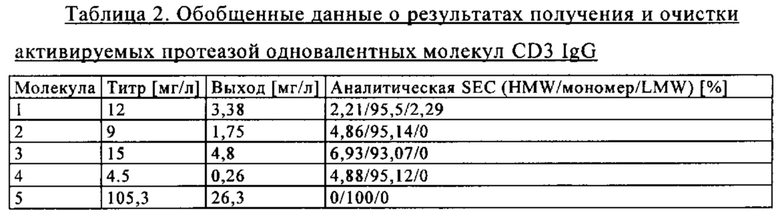
Пример 2
Расщепление и стабильность активируемых протеазой IgG
Активируемые протеазой молекулы IgG анализировали с помощью капиллярного электрофореза. Сравнение необработанного образца и обработанного образца продемонстрировало, что анти-ID scFv полностью отщеплялся после обработки rh-матриптазой/ST14 (фирма R&D Systems), о чем свидетельствовал сдвиг по размеру при анализе методом ДСН-ПААГ (фиг. 3). Анализ образцов, которые инкубировали в течение 48 ч при 37°С, подтвердил стабильность молекул в буфере для препаративной формы (фиг. 3А-Г).
Пример 3
Маскирующий эффект антиидиотипического scFv по отношению к CD3 IgG
Эффективность маскировки CD3-связывающего агента путем N-концевого слияния антиидиотипического CD3 scFv продемонстрирована с помощью репортерного анализа с использованием Jurkat-NFAT. Репортерные клетки Jurkat-NFAT (линия репортерных клеток острого человеческого лейкоза с регулируемой промотором NFAT экспрессией люциферазы, GloResponse Jurkat NFAT-RE-luc2P, фирма Promega, № CS176501) экспрессируют активную люциферазу светляка, если промотор NFAT активирован в результате связывания с CD3ε. Интенсивность сигнала люминесценции после добавления субстрата люциферазы пропорциональна интенсивности активации и передачи сигнала CD3. Полностью незамаскированные одновалентные молекулы CD3 служили в качестве положительного контроля. Обработку осуществляли с помощью rh-матриптазы/ST14 (фирма R&D Systems) в течение 48 ч при 37°С. В параллельном эксперименте для сенсибилизизации 96-луночного (плоского) планшета с белыми стенками и прозрачным дном (фирма Greiner Bio-One) использовали 8 мкг/мл антитела к человеческому Fc-домену (фирма BioLegends) из расчета 0,025 мкл/лунку в ЗФР в течение 48 ч при 4°С. ЗФР удаляли с помощью пипетки перед добавлением одновалентных IgG в указанном диапазоне концентраций 200 нМ - 2,56 пМ. Планшеты инкубировали в течение примерно 30 мин при 4°С. Затем репортерные клетки Jurkat-NFAT собирали и оценивали жизнеспособность с помощью устройства ViCell. Клетки ресуспендировали в среде Jurkat (RPMI1640, 2 г/л глюкозы, 2 г/л NaHCO3, 10% FCS, 25 мМ HEPES, 2 мМ L-глутамин, 1 × NEAA, 1 × пируват натрия) без гигромицина и добавляли 100 мкл на лунку (25000 клеток/лунку) к перекрестно сшитым одновалентным CD3 IgG. Клетки инкубировали в течение 3 ч при 37°С во влажной камере. Планшеты изымали из инкубатора примерно за 10 мин до считывания люминисценции для адаптации к комнатной температуре. Добавляли 100 мкл/лунку раствора ONE-Glo (1:1 об./об. ONE-Glo и среды для анализа на лунку) в лунки и инкубировали в течение 10 мин при комнатной температуре в темноте. Определение люминесценции осуществляли с помощью ридера WALLAC Victor3 ELISA (PerkinElmer2030), продолжительность детекции 1 лунки составляла 1 с. Для молекул 7857 (маскировка с помощью конструкции 4.15.64 с нерасщепляемым линкером) и 7859 (необработанная) обнаружено существенно сниженное связывание с CD3ε по сравнению с незамаскированной (7861) и предварительно обработанной молекулой (7859, обработанная) (фиг. 4А). Молекулу 7760 включали в качестве контроля для демонстрации того, что N-концевое связывание не блокировало связывание самого CD3. Для молекул 7858 (маскировка с помощью конструкции 4.32.63 с нерасщепляемым линкером) и 7860 (необработанная) обнаружено существенно сниженное связывание с CD3ε по сравнению с незамаскированной (7861) и предварительно обработанной молекулой (7860, обработанная) (фиг. 4Б). Согласно результатам оценки аффинности антиидиотипических CD3-связывающих агентов маскировка с помощью конструкции 4.32.63 являлась существенно более эффективной, чем с помощью 4.15.64. На основе величин ЕС50 (фиг. 4В) можно считать, что замаскированный 4.32.63 CD3-связывающий агент связывался в 54 слабее, чем незамаскированный CD3-связывающий агент 7861. Маскировка с помощью 4.15.64 снижала связывание лишь в 16 раз меньше по сравнению с 7861. В зависимости от опухоли-мишени и целевого связывающего агента можно определять наиболее эффективный маскирующий агент.
Пример 4
Получение анти-FolR1/анти-CD3 активирующих Т-клетки биспецифических (ТСВ) молекул с анти-CD3 scFv
Получали несколько активирующих Т-клетки биспецифических молекул (ТСВ) с различными антиидиотипическими scFv, и они схематично представлены на фиг. 5А-З под соответствующими ID-номерами. Получали следующие молекулы:
ID7344: FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.15.64 - сайт матриптазы MK062 - CD3 - слитый на N-конце с FolR1 VH - инертный Fc), со слитым на N-конце анти-CD3 scFv 4.15.64 и (расщепляемым) протеазой линкером (фиг. 5А, SEQ ID NO: 1, 2 и 3).
ID7496: FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.32.63 - сайт матриптазы MK062 - CD3 - слитый на N-конце с FolR1 VH - инертный Fc), со слитым на N-конце анти-CD3 scFv 4.32.63 и (расщепляемым) протеазой линкером (фиг. 5В, SEQ ID NO: 1, 3 и 4).
ID7676: FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.15.64 - сайт матриптазы MK062 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с FolR1 VH - инертный Fc), со слитым на N-конце анти-CD3 scFv 4.15.64 и (расщепляемым) протеазой линкером (фиг. 5Б, SEQ ID NO: 1, 3 и 6).
ID7611: FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.32.63 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с FolR1 VH - инертный Fc), со слитым на N-конце анти-CD3 scFv 4.32.63 и (расщепляемым) протеазой линкером (фиг. 5Г, SEQ ID NO: 1, 3 и 5).
Последовательности антиидиотипических (ID) связывающих агентов получали с помощью RACE-ПЦР (ПЦР с быстрой амплификацией концов кДНК) из РНК клеток гибридомы. Клетки гибридомы получали путем иммунизации мышей Fab-фрагментом СН2527 (VL_7-46(13)/VH_3-23(12)). Синтез последовательности одноцепочечного Fv (ScFv), включая необходимые для клонирования сайты рестрикции, заказывали на фирме Invitrogen. Сравнивали аффинности шести различных антиидиотипических СН2527-связывающих агентов (фиг. 2, результаты Biacore-анализа (фирма AG М. Schräml) при 25°С/37°С (аналит: MAK<CEA/CD3>rH)), и четыре из них клонировали в виде N-концевых слияний на НС CD3 - FolR1 16D5 ТСВ.
ДНК-последовательности анти-ID одноцепочечных Fv субклонировали в рамке считывания с CD3 VH-цепью, предварительно встроенной в соответствующий применяемый в качестве реципиента экспрессионный вектор для клеток млекопитающих. Экспрессия белка находилась под контролем MPSV - промотора, а на 3'-конце CDS присутствовала синтетическая сигнальная полиА-последовательность. Кроме того, каждый вектор содержал последовательность OriP EBV.
Молекулы получали путем совместной трансфекции растущих в суспензии клеток HEK293-EBNA экспрессионными векторами для клеток млекопитающих с использованием полиэтиленимина (ПЭИ). Клетки трансфектировали соответствующими экспрессионными векторами в соотношении 1:3:2 («вектор тяжелой цепи с «впадиной» (VH-CH1-CH2-CH3)»: «общая легкая цепь (CLC)»: «вектор тяжелой цепи с «выступом» (scFv-VH-CH1-VH-CH1-CH2-CH3)»).
Для трансфекции клетки HEK293 EBNA культивировали в бессывороточной культуральной среде Excell, содержащей 6 мМ L-глутамин и 250 мг/л культуральной среды G418. Для производства высевали в центрифужные флаконы вместимостью 600 мл (максимальный рабочий объем 400 мл) 800 млн клеток HEK293 EBNA за 24 ч до трансфекции без G418. Для трансфекции 800 млн клеток центрифугировали в течение 5 мин при 210 × g, и супернатант заменяли 40 мл предварительно нагретой среды CD СНО, содержащей 6 мМ L-глутамин. Экспрессионные векторы смешивали в 40 мл среды CD СНО, содержащей 6 мМ L-глутамин, для получения конечного количества ДНК 400 мкг. После добавления 1080 мкл раствора ПЭИ (2,7 мкг/мл) смесь интенсивно перемешивали в течение 15 с и затем инкубировали в течение 10 мин при комнатной температуре. Затем клетки смешивали с раствором ДНК/ПЭИ, переносили в 600-миллилитровый центрифужный флакон и инкубировали в течение 3 ч при 37°С в инкубаторе в атмосфере, содержащей 5% СО2. После инкубации добавляли 320 мл среды Excell + 6 мМ L-глутамин + 5 г/л Pepsoy + 1,0 мМ VPA +3 г/л глюкозы, и клетки культивировали в течение 24 ч перед осуществлением подпитки 7% Feed 7. После культивирования в течение 6-7 дней супернатант собирали для очистки путем центрифугирования в течение 20-30 мин при 210 × g (центрифуга Sigma 8K). Раствор стерилизовали фильтрацией (фильтр с размером пор 0,22 мкм) и добавляли азид натрия в конечной концентрации 0,01% (мас./об.). Раствор хранили при 4°С до очистки. Секретированный белок очищали из супернатантов клеточных культур с помощью аффинной хроматографии, применяя аффинную хроматографию на белке А, с последующей(ими) одной или двумя стадией(ями) гель-фильтрации.
Для проведения аффинной хроматографии супернатант вносили на колонку HiTrap белок A FF (CV = 5 мл, фирма GE Healthcare), уравновешенную 25 мл буфера, содержащего 20 мМ фосфат натрия, 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 7,5. Несвязанный белок удаляли промывкой, используя равный по меньшей мере 10 объемам колонки объем буфера, содержащего 20 мМ фосфат натрия, 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 7,5, требуемый белок элюировали, применяя равный 20 объемам колонки объем буфера (градиент от 0% до 100%), содержащего 20 мМ цитрат натрия, 0,5 М хлорид натрия, 0,01% Твин-20, рН 2,5. Раствор белка нейтрализовали путем добавления 1/10 2 М Трис, рН 10,5. Требуемый белок концентрировали с помощью ультра-концентратора Amicon®Ultra-15 Ultracel 30K (фирма Merck Millipore Ltd.) до объема, составляющего максимум 4 мл, перед загрузкой на колонку HiLoad Супердекс 200 (фирма GE Healthcare), уравновешенную буфером, содержащим 20 мМ гистидин, 140 мМ хлорид натрия, рН 6,0, 0,01% Твин-20.
При осуществлении анализа белка после гель-фильтрации определяли чистоту и молекулярную массу молекул в виде единичных фракций с помощью ДСН-ПААГ в отсутствии восстановителя и осуществляли окрашивание кумасси (InstantBlue™, фирма Expedeon). Применяли систему геля NuPAGE® Pre-Cast (4-12% Бис-Трис, фирма Invitrogen или 3-8% Трис-ацетата, фирма Invitrogen) согласно инструкции производителя.
Концентрацию белков в очищенных белковых образцах определяли, измеряя оптическую плотность (ОП) при 280 нм и осуществляя деление на коэффициент молярной экстинкции, рассчитанный на основе аминокислотной последовательности.
Чистоту и молекулярную массу молекул после конечной стадии очистки анализировали с помощью КЭ-ДСН в присутствии восстановителя и без него. Применяли систему Caliper LabChip GXII (фирма Caliper Lifescience) согласно инструкции производителя.
Содержание агрегатов молекул определяли с использованием колонки для аналитической гель-фильтрации TSKgel G3000 SW XL (фирма Tosoh), применяя подвижный буфер, содержащий 25 мМ K2HPO4, 125 мМ NaCl, 200 мМ моногидрохлорид L-аргинина, 0,02% (мас./об.) NaN3, рН 6,7 при 25°С. Конечное качество всех молекул оказалось высоким с содержанием мономеров ≥92%.
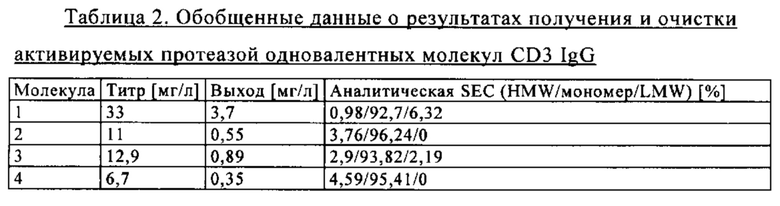
Пример 5
Кратковременная экспрессия активируемых протеазой ТСВ
Сравнивали методом гель-фильтрации различные соотношения плазмид, применяемых для трансфекции, поскольку ожидалась, что содержащая «выступ» цепь должна экспрессироваться с более низкими уровнями по сравнению с содержащей «впадину» цепью и легкой цепью. Как продемонстрировано на фиг. 6 и 7, применение плазмид в соотношении 1 («впадина») : 2 («выступ) : 3 (CLC) (фиг. 7) вместо 1 («впадина») : 1 («выступ») : 3 (CLC) (фиг. 6) повышало выход правильной молекулы (левый пик) и снижало количество гомодимеров типа «впадина»-«впадина» (правый пик).
Пример 6
Расщепление и стабильность активируемой протеазой ТСВ
Активируемые протеазой ТСВ анализировали с помощью капиллярного электрофореза. Сравнение необработанного образца и обработанного образца продемонстрировало, что анти-ID scFv полностью отщеплялся после обработки rh-матриптазой/ST14 (фирма R&D Systems). Анализ образцов, которые инкубировали в течение 48 ч при 37°С, подтвердил стабильность молекул в буфере для препаративной формы (фиг. 12А-Г).
Пример 7
Цитолиз клеток при использовании клеточных линий, которые экспрессируют различные уровни FolR1
Опосредуемый Т-клетками цитолиз клеток, индуцированный активируемыми протеазой ТСВ-молекулами, оценивали с использованием линий клеток-мишеней, экспрессирующих различные уровни FolR1 (фиг. 13). Человеческие РВМС применяли в качестве эффекторных клеток, и цитолиз клеток определяли после инкубации в течение 48 ч с активируемыми протеазой ТСВ-молекулами. Мононуклеарные клетки периферический крови (РВМС) человека выделяли из свежеполученных образцов крови или из лейкоцитарных пленок, которые получали из здоровых доноров. При использовании свежей крови, для получения применяли 50-миллилитровые пробирки Leucosep (фирма GreinerBioOne). При использовании обогащенных лимфоцитами препаратов (лейкоцитарные пленки) для получения применяли градиент плотности Histopaque-1077. Кровь/лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) плазму, находящуюся над содержащей РВМС интерфазой, отбрасывали и РВМС переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax, при 37°С, 5% CO2 в инкубаторе для клеток для последующего применения. В целом, метод состоял в следующем: прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали из расчета 0,4×106 клеток/мл в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в круглодонные 96-луночные планшеты. Для анализа цитолиза молекулы добавляли в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Цитолиз клеток-мишеней оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 1 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ.
Результаты (фиг. 14А, 15А, 16, 17, 18А, 19А и 20А) продемонстрировали, что активируемые протеазой ТСВ с антиидиотипическим CD3 scFv-фрагментом, связанным на N-конце с помощью нерасщепляемого линкера (№7676 и №7611, фиг. 5Б и Г соответственно), обладали способностью существенно снижать клеточный цитолиз клеток линий Skov3 и НТ29. Конструкция №7611 (фиг. 5Г) обеспечивала пониженный цитолиз клеток Hela, однако антиидиотипический CD3 scFv 4.15.64 в конструкции №7676 (фиг. 5Б) оказался менее эффективным в отношении снижения цитолиза клеток. Это согласуется с аффинностями антиидиотипического N-концевого фрагмента CD3 scFv. Обладающий более высокой аффинностью scFv-фрагмент обеспечивал более эффективную маскировку.
Сопоставимая эффективность обработанных и необработанных ТСВ позволяет предположить наличие экспрессии матриптазы на клетках Hela и Skov3. Вероятно, уровень экспрессии матриптазы ниже в клетках НТ29. Обработка Mkn-45, негативной по FolR1 клеточной линии, продемонстрировала, что при использовании всех применяемых в настоящем описании молекул цитолиз был очень слабым (фиг. 15А).
Пример 8
Т-клеточная активация после совместной инкубации линий опухолевых клеток с человеческими РВМС
Т-клеточную активацию, опосредуемую активируемыми протеазой ТСВ-молекулами, оценивали с использованием клеток Hela, Skov3 и НТ29. Человеческие РВМС применяли в качестве эффекторных клеток и активацию Т-клеток определяли после инкубации в течение 48 ч с клетками-мишенями и антителами. Клетки-мишени высевали с плотностью 20000 клеток/лунку в круглодонные 96-луночные планшеты. Молекулы добавляли в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Т-клеточную активацию оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного определения CD25 и CD69 на CD4-позитивных и CD8-позитивных Т-клетках. Результаты оценки Т-клеточной активации согласуются с результатами, полученными в предыдущем примере, в котором оценивали цитолиз клеток-мишеней (пример 7).
Пример 9
Т-клеточная активация, опосредуемая активируемыми протеазой ТСВ и линиями клеток-мишеней, которые экспрессируют низкие уровни антигена
Т-клеточную активацию, опосредуемую активируемыми протеазой ТСВ-молекулами, оценивали с использованием клеток НТ29, которые экспрессируют лишь низкие уровни FolR1 (фиг. 13). Человеческие РВМС, выделенные из лейкоцитарной пленки, применяли в качестве эффекторных клеток. При использовании обогащенных лимфоцитами препаратов (лейкоцитарные пленки) для получения применяли градиент плотности Histopaque-1077. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) плазму, находящуюся над содержащей РВМС интерфазой, отбрасывали и РВМС переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax, при 37°С, 5% CO2 в инкубаторе для клеток для последующего применения. В целом, метод состоял в следующем: прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали из расчета 0,4×106 клеток/мл в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в круглодонные 96-луночные планшеты. Молекулы добавляли в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Т-клеточную активацию оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного определения CD25 и CD69 на CD4-позитивных и CD8-позитивных Т-клетках. Эффективность обработанной активируемой протеазой ТСВ оказалась сопоставимой с эффективностью 16D5 ТСВ (6298). Эффективность 16D5 ТСВ (инвертированный формат)) оказалась более высокой по сравнению с классическим форматом. «Замаскированные» ТСВ с нерасщепляемым линкером или без предварительной обработки матриптазой не индуцировали Т-клеточную активацию при использовании указанной клеточной линии. Для клеточных линий с низким или умеренным уровнями экспрессии FolR1 оба антиидиотипических scFv обеспечивали достаточную маскировку CD3 Fab (фиг. 22А и Б).
Пример 10
Т-клеточная активация, опосредуемая активируемыми протеазой ТСВ, при использовании первичной клеточной линии HRCEpiC
Т-клеточную активацию, опосредуемую активируемыми протеазой ТСВ-молекулами, оценивали с использованием первичных эпителиальных клеток коркового вещества почек человека (фирма ScienceCell), которые экспрессируют лишь очень незначительные количества FolR1 (фиг. 13). Человеческие РВМС, выделенные из лейкоцитарной пленки, применяли в качестве эффекторных клеток. При использовании обогащенных лимфоцитами препаратов (лейкоцитарные пленки) для получения применяли градиент плотности Histopaque-1077. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) плазму, находящуюся над содержащей РВМС интерфазой, отбрасывали и РВМС переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2 -3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax, при 37°С, 5% CO2 в инкубаторе для клеток для последующего применения. В целом, метод состоял в следующем: прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали из расчета 0,4×106 клеток/мл в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в круглодонные 96-луночные планшеты. Молекулы добавляли в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Т-клеточную активацию оценивали после инкубации в течение 48 ч при 37°С, 5% CO2 путем количественного определения CD25 и CD69 на CD4-позитивных и CD8-позитивных Т-клетках. «Замаскированная» 16D5 ТСВ не индуцировала Т-клеточную активацию при инкубации с первичными эпителиальными клетками коркового вещества почек человека, несмотря на низкий уровень экспрессии FolR1, при наиболее высокой концентрации 10000 пМ ТСВ, что демонстрирует эффективность антиидиотипического маскирующего фрагмента. Небольшую активацию Т-клеток удалось обнаружить для 16D5 ТСВ (инвертированный и классический формат) (фиг. 23).
Пример 11
Анти-ID CD3 Fab, маскирующий CD3-связывающий агент молекулы 16D5 ТСВ. Цитолиз клеток Ovcar3
Опосредуемый Т-клетками цитолиз клеток-мишеней, вызываемый активируемыми протеазой ТСВ-молекулами, оценивали с использованием клеток OVCAR3 (фиг. 24). Человеческие РВМС применяли в качестве эффекторных клеток, и цитолиз клеток определяли после инкубации в течение 48 ч с молекулами. Мононуклеарные клетки периферический крови (РВМС) человека выделяли из свежеполученных образцов крови здорового донора. Для получения применяли 50-миллилитровые пробирки Leucosep (фирма GreinerBioOne). Кровь разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) плазму, находящуюся над содержащей РВМС интерфазой, отбрасывали и РВМС переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax, при 37°С, 5% СО2 в инкубаторе для клеток для последующего применения. В целом, метод состоял в следующем: прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали из расчета 0,4×106 клеток/мл в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в круглодонные 96-луночные планшеты. Для анализа цитолиза молекулы добавляли в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Цитолиз клеток-мишеней оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 1 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ. Результаты (фиг. 24) продемонстрировали, что в активируемой протеазой ТСВ с антиидиотипическим CD3 4.15.64, скрещенный Fab, связанный на N-конце с помощью нерасщепляемого линкера, не обеспечивается существенная маскировка CD3-связывающего агента. Кроме того, установлено, что клетки Ovcar3, вероятно, экспрессируют матриптазу, поскольку необработанная молекула также индуцировала цитолиз указанных клеток.
Пример 12
Цитолиз клеток Skov3 и HeLa с использованием человеческих РВМС из трех различных доноров
Цитолиз Т-клетками, опосредуемый активируемыми протеазой ТСВ-молекулами, оценивали с использованием двух различных клеточных линий, которые экспрессировали различные уровни FolR1 (фиг. 25-27). Человеческие РВМС применяли в качестве эффекторных клеток, и цитолиз клеток определяли после инкубации в течение 48 ч с молекулами. Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. При использовании обогащенных лимфоцитами препаратов (лейкоцитарные пленки) для получения применяли градиент плотности Histopaque-1077. Кровь/лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) плазму, находящуюся над содержащей РВМС интерфазой, отбрасывали и РВМС переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС замораживали в течение ночи при -80°С в камерах для охлаждения клеток (Cool Cell box) до их переноса в жидкий азот. За 24 ч до начала анализа РВМС подвергали оттаиванию и выдерживали в среде RPMI1640, содержащей 10% FCS и 1 × GlutaMax, при 37°С, 5% СО2 в инкубаторе для клеток. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали из расчета 0,4×106 клеток/мл в соответствующей среде. Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты. За 1 день до начала анализа подсчитывали количество РВМС и проверяли их жизнеспособность. РВМС центрифугировали при 350 × g в течение 5 мин и ресуспендировали в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Среду клеток-мишеней удаляли и добавляли РВМС к клеткам-мишеням перед добавлением разведенных антител в указанных концентрациях в трех повторностях. FolR1 16D5 ТСВ включали в качестве положительного контроля, а «ненацеленную» ТСВ-молекулу (которая связывается с CD3, но не с антигеном клетки-мишени) включали в качестве отрицательного контроля. РВМС добавляли к клеткам-мишеням в конечном соотношении Е:Т 10:1. Цитолиз клеток-мишеней оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 2 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ.
Результаты (фиг. 25-27) продемонстрировали, что FolR1 ТСВ с scFv 4.32.63, связанным на N-конце с помощью нерасщепляемого линкера (фиг. 5Г), индуцировала пониженный цитолиз клеток Hela в концентрации 100 пМ и клеток Skov3 в концентрации 10 нМ. FolR1 ТСВ с scFv 4.15.64, связанным на N-конце с помощью нерасщепляемого линкера (фиг. 5Б), была менее эффективной в отношении снижения цитолиза клеток Skov3 в концентрации 10 нМ. Установлено, что более сильная маскировка, обеспечиваемая антиидиотипическим scFv 4.32.63, обладающим более высокой аффинностью, является более эффективной в отношении CD3-связывающего агента, чем в случае более слабого антиидиотипический scFv 4.15.64. Сопоставимая эффективность обработанных и необработанных ТСВ позволяет предположить наличие экспрессии протеазы, например, матриптазы, на клетках Hela и Skov3.
Пример 13
Получение HER1-связывающего антитела GA201, замаскированного с помощью антиидиотипического GA201 scFv
В этом примере описано получение следующих молекул:
1: антитело GA201 IgG1-подкласса с N-концевым слиянием антиидиотипического GA201 scFv и сайтом матричной металлопротеиназы в глицин-сериновом линкере (SEQ ID NO: 32 и 34); и
2: HER1-связывающееся антитело IgG1-подкласса GA201 (SEQ ID NO: 32 и 33).
Их схематические изображения представлены на фиг. 28 и 29. Последовательность антиидиотипического (ID) связывающего GA201 агента получали с помощью ОТ-ПЦР (обратная транскрипция) из РНК клеток гибридомы, используя вырожденные праймеры, связывающиеся с концами вариабельных областей легкой и тяжелой цепи соответственно. Клетки гибридомы получали иммунизацией мышей. Синтез последовательности ДНК одноцепочечного Fv (ScFv) с фланкирующими уникальными сайтами рестриктаз заказывали на фирме Geneart и клонировали в виде N-концевого слияния на легкой цепи GA201.
Экспрессионный вектор фирмы Roche применяли для создания всех тяжелых и легких цепей слитого содержащего scFv слитого белка, который кодировался экспрессионными плазмидами. Вектор состоял из следующих элементов:
- ген, обусловливающий устойчивость к гигромицину в качестве маркера для селекции,
- сайт инициации репликации, oriP, из вируса Эпштейна-Барра (EBV),
- сайт инициации репликации из вектора pUC18, обеспечивающий репликацию этой плазмиды в Е. coli,
- ген бета-лактамазы, который придает устойчивость к ампициллину Е. coli,
- немедленно-ранний энхансер и промотор из цитомегаловируса человека (HCMV),
- сигнальная последовательность полиаденилирования («поли А») из человеческого иммуноглобулина 1 и
- уникальные сайты рестрикции BamHI и XbaI.
Молекулы получали путем совместной трансфекции клеток почки человеческого эмбриона 293-F, растущих в суспензии, экспрессионными векторами для клеток млекопитающих, используя систему для экспрессии FreeStyle™ 293 согласно инструкции производителя (фирма Invitrogen, США). В целом, метод состоял в следующем: суспензионные клетки FreeStyle™ 293-F культивировали в среде для экспрессии FreeStyle™ 293 при 37°С/8% CO2 и клетки высевали в свежую среду с плотностью 1-2 × 106 жизнеспособных клеток /мл в день трансфекции. Получали комплексы ДНК-293fectin™ в среде Opti-МЕМ I (фирма Invitrogen, США), используя 325 мкл 293fectin™ (фирма Invitrogen, Германия) и 250 мкг плазмидной ДНК тяжелой («GA201 тяжелая цепь») и легкой цепи («анти-GA201 VH-VL scFv расщепляемый ММР линкер G4S GA201 легкая цепь» или «GA201 легкая цепь») в молярном соотношении 1:1 в конечном объеме смеси для трансфекции 250 мл. Супернатанты клеточных культур, содержащих антитело, собирали через 7 дней после трансфекции путем центрифугирования при 14000 × g в течение 30 мин и фильтровали через стерильный фильтр (0,22 мкм). Супернатанты хранили при -20°С до очистки.
Секретированный белок очищали из супернатантов клеточных культур путем аффинной хроматографии, используя аффинную хроматографию на белка А, с последующей гель-фильтрацией. В целом, метод состоял в следующем: стерилизованные фильтрацией супернатанты клеточных культур вносили на колонку HiTrap белок A HP (5 мл), уравновешенную ЗФР-буфером (10 мМ Na2HPO4, 1 мМ KH2PO4, 137 мМ NaCl и 2,7 мМ KCl, рН 7,4). Несвязанные белки отмывали уравновешивающим буфером. Антитело и варианты антитела элюировали 0,1 М цитратным буфером, рН 2,8, и содержащие белок фракции нейтрализовали 0,1 мл 1М Трис, рН 8,5. Затем элюированные белковые фракции объединяли, концентрировали с помощью фильтрующей центрифуги Amicon Ultra (MWCO: 30 K, фирма Millipore) до объема 3 мл и вносили на колонку для гель-фильтрации Супердекс200 HiLoad 120 мл 16/60 (фирма GE Healthcare, Швеция), уравновешенную буфером, содержащим 20 мМ гистидин, 140 мМ NaCl, рН 6,0. Фракции, содержащие очищенный GA201-анти-GA201-scFv или GA201, с содержанием высокомолекулярных агрегатов менее 5%, объединяли и хранили в виде аликвот с концентрацией 1,0 мг/мл при -80°С.
При осуществлении анализа белка после гель-фильтрации чистоту и молекулярную массу молекул в виде единичных фракций определяли с помощью ДСН-ПААГ в отсутствии восстановителя и осуществляли окрашивание кумасси (InstantBlue™, фирма Expedeon). Применяли систему геля NuPAGE® Pre-Cast (4-12% Бис-Трис, фирма Invitrogen или 3-8% Трис-ацетата, фирма Invitrogen) согласно инструкции производителя.
Концентрацию белков в очищенных белковых образцах определяли, измеряя оптическую плотность (ОП) при 280 нм и осуществляя деление на коэффициент молярной экстинкции, рассчитанный на основе аминокислотной последовательности. Чистоту и молекулярную массу молекул после конечной стадии очистки анализировали с помощью КЭ-ДСН в присутствии восстановителя и без него. Применяли систему Caliper LabChip GXII (фирма Caliper Lifescience) согласно инструкции производителя.
Содержание агрегатов молекул определяли с помощью высокоэффективной SEC, используя колонку для аналитической гель-фильтрации Супердекс 200 (фирма GE Healthcare, Швеция) в подвижном буфере, содержащем 200 мМ KH2PO4, 250 мМ KCl, рН 7,0, при 25°С. 25 мкг белка инъецировали в колонку со скоростью потока 0,5 мл/мин и осуществляли изократическое элюирование в течение порядка 50 мин.
После конечной очистки во всех молекулах содержание мономера составляло ≥ 95% по данным высокоэффективной SEC. Молекулярная масса замаскированного антиидиотипическим scFv GA201, определенная с помощью КЭ-ДНС-анализа, составляла 216,3 кДа в невосстанавливающих условиях (фиг. 30А) и 58,3 кДа в восстанавливающих условиях касательно тяжелой цепи GA201 и 60,3 кДа касательно легкой цепи GA201, сцепленной с scFv (фиг. 30Б) соответственно. Молекулярная масса, рассчитанная на основе аминокислотной последовательности, составляла 49,2 кДа для тяжелой цепи и 51,9 кДа для легкой цепи GA201, сцепленной с scFv, что свидетельствует о гликозилировании обеих цепей в HEK293-клетках.

Пример 14
Маскирующий эффект антиидиотипического scFv в отношении GA201 IgG
Эффективность маскировки связывания HER1 GA201 посредством N-концевого слияния антиидиотипического GA201 scFv продемонстрирована с помощью FACS-анализа на экспрессирующих HER1 клетках Н322М и с помощью анализа методом поверхностного плазмонного резонанса (SPR) на сенсибилизированной HER1 поверхности чипа. Для протеолитического расщепления GA201-анти-GA201-scFv применяли рекомбинантную активную человеческую ММР2 (фирма Calbiochem). 1 мг антиидиотипического GA201 scFv, сшитого с GA201 с помощью глицин-серинового линкера, содержащего сайт расщепления ММР, инкубировали с 1,2 мкг ММР2 в течение ночи при 37°С в ЗФР.
Для FACS-анализа связывания HER1 расщепленной и нерасщепленной молекулой GA201-анти-GA201-scFv применяли линию клеток немелкоклеточного рака легкого Н322М. Плотность клеток доводили до 1×106/мл и вносили в 96-луночный круглодонный планшет. Добавляли молекулы и инкубировали на льду в течение 30 мин. Клетки промывали однократно FACS-буфером (ЗФР + 2% FCS + 0,1% азида натрия) и ресуспендировали с конъюгированным с ФИТЦ F(ab')2-фрагментом козьего античеловеческого IgG-Fc в качестве вторичного антитела (фирма ThermoFisher Scientific). После выдерживания еще в течение 20 мин на льду клетки провыли дважды и ресуспендировали в FACS-буфере и анализировали с помощью устройства BD FACS Canto II. Оценивали 10000 клеток и для анализа использовали медиану сигнала флуоресценции. До расщепления с помощью ММР-2 молекулы GA201-анти-GA201-scFv не обнаружено поддающегося измерению связывания с HER1 на Н322М-клетках, что свидетельствует о полной маскировке связывающих доменов GA201 антиидиотипическим scFv (фиг. 31). Связывание нерасщепленной молекулы GA201-анти-GA201-scFv оказалось сопоставимым со связыванием неспецифического применяемого в качестве контроля изотипа IgG антитела (фиг. 31). В противоположность этому, расщепление с помощью ММР антиидиотипического scFv приводило к активации GA201, и связывание с HER1 на Н322М-клетках восстанавливалось до уровней, сходных с уровнями незамаскированного родительского антитела GA201 (фиг. 31)
Для подтверждения полученных с помощью FACS результатов связывания замаскированного GA201 после расщепления с помощью ММР при создании изобретения осуществляли также эксперимент с применением SPR-анализа в качестве второго аналитического метода с использованием устройства Biacore Т100 (фирма GE Healthcare Biosciences АВ, Уппсала, Швеция). HER1 иммобилизовывали на поверхности биосенсорного чипа СМ5 с помощью стандартного метода аминного сочетания. Внеклеточный домен HER1 инъецировали в натрий-ацетатном буфере, рН 5,0 в концентрации 1 мкг/мл. Контрольные проточные референс-ячейки обрабатывали аналогичным образом, но используя только буфер в качестве носителя. Молекулы GA201-анти-GA201-scFv до и после расщепления в течение ночи с помощью ММР и GA201 разводили в 1×ЗФР, рН 7,4, 0,05% Твин20 (фирма Roche Diagnostics GmbH) и инъецировали в возрастающих концентрациях от 3,125 и до 50 нМ со скоростью потока 30 мкл/мин. Фаза ассоциации составляла 3 мин, а фаза диссоциации составляла 10 мин. Связывание HER1 восстанавливали путем инъекции 0,85% фосфорной кислоты в течение 30 с со скоростью потока 5 мкл/мин. Кинетические константы скорости и константы равновесия диссоциации рассчитывали, используя модель связывания 1:1 Лэнгмюра, с помощью программного обеспечения Biaevaluation. Величина KD, составляющая 1 нМ, характеризующая связывание HER1, установлена для родительского незамаскированного антитела GA201 (фиг. 32). После инкубации в течение ночи с ММР-2 для молекулы GA201-анти-GA201-scFv установлена величина KD 2 нМ со сходными с незамаскированным контрольным антителом константами скорости ассоциации и диссоциации (ka и kd), что свидетельствует о полном восстановлении способности связываться с HER1 в результате расщепления протеазой (фиг. 32). Для нерасщепленной молекулы GA201-анти-GA201-scFv не обнаружено никакое связывание с HER1 при использовании SPR-анализа (фиг. 32). В совокупности, при создании изобретения продемонстрирована полная утрата способности связываться с HER1 после слияния антиидиотипического scFv с N-концом антитела IgG 1-подкласса GA201 с использованием двух независимых аналитических методов. Кроме того, установлено, что связывание с HER1 полностью восстанавливалось после удаления scFv посредством расщепления протеазой в сайте расщепления ММР в глицин-сериновом линкере.
Пример 15
Получение анти-FolR1/анти-CD3 и анти-мезотелин/анти-CD3 связывающих Т-клетки биспецифических (ТСВ) молекул с анти-CD3 scFv
Получали несколько связывающих Т-клетки биспецифических (ТСВ) молекул с различными антиидиотипическими scFv, и они схематически изображены на фиг. 33А-К под соответствующим им IP-номером. Получали следующие молекулы:
IP 8364: «FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.32.63 - сайт ММР9 - матриптазы MK062 - CD3 - слитый на N-конце с FolR1 VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и линкером с сайтом протеазы ММР9 - MK062» (фиг. 33А, SEQ IP NO: 1, 3 и 72).
IP 8363: «FolR1 16D5 2+1 IgG, классический формат (антиидиотипический scFv 4.32.63 - сайт ММР9 - матриптазы MK062 - CD3 - слитый на N-конце с FolR1 VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и линкером с сайтом протеазы катепсина S/В» (фиг. 33Б, SEQ IP NO: 1, 3 и 85).
IP 8365: «FolR1 16D5 2+1 IgG, инвертированный формат (антиидиотипический scFv 4.32.63 - линкер с сайтом матриптазы MK062 - CD3 - слитый на N-конце с CD3 VL - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и линкером с сайтом матриптазы MK062» (фиг. 33В, SEQ IP NO: 1, 3, 73 и 74).
IP 8366: «FolR1 16D5 2+1 IgG, инвертированный формат (антиидиотипический scFv 4.32.63 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с CD3 VL - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и нерасщепляемым GS-линкером» (фиг. 33Г).
IP 8672: «Антитело к мезотелину (а-Мезотелин) 2+1 IgG, классический формат, MSLN-заряженные варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - сайт ММР9 - матриптазы MK062 - CD3 - слитый на N-конце с VH антитела к мезотелину - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и сайтом ММР9 - матриптазы MK062» (фиг. 33Д, SEQ ID NO: 77, 78, 81, 82).
ID 8673: «Антитело к мезотелину 2+1 IgG, классический формат, MSLN-заряженные варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с VH антитела к мезотелину - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63, нерасщепляемым GS-линкером» (фиг. 33Е).
ID 8674: «Антитело к мезотелину 2+1 IgG, инвертированный формат, MSLN-заряженные варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - сайт ММР9 - матриптазы MK062 - CD3 - слитый на N-конце с CD3 VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и сайтом ММР9 - матриптаза MK062» (фиг. 33Ж, SEQ ID NO: 76, 77, 78, 79).
ID 8675: «Антитело к мезотелину 2+1 IgG, инвертированный формат, MSLN-заряженные варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с CD3 VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и нерасщепляемым GS-линкером» (фиг. 33З).
ID 8505: «Антитело к мезотелину 2+1 IgG, инвертированный формат, MSLN-заряженные варианты, CD3 (НС антитела к мезотелину, слитая на N-конце с CD3 VL - инертный Fc)» (фиг. 33И).
ID 8676: «Антитело к мезотелину 2+1 IgG, классический формат, MSLN-заряженные варианты, скрещенный CD3 (антитело к мезотелину IgG-подкласса с CD3 - слитым на N-конце с VH антитела к мезотелину - инертный Fc)» (фиг. 33К)
Вариабельные домены субклонировали в рамке считывания с предварительно встроенными в соответствующий применяемый в качестве реципиента экспрессионный вектор для клеток млекопитающих доменами. Экспрессия белка находилась под контролем MPSV-промотора и на 3'-конце CDS присутствовала синтетическая сигнальная полиА-последовательность. Кроме того, каждый вектор содержал последовательность OriP EBV.
Молекулы (за исключением 8505, эту молекулу получали путем совместной трансфекции СНО-клеток, растущих в суспензии, с экспрессионными векторами для клеток млекопитающих. Кратковремннную трансфекцию осуществляли на фирме Evitria AG (Швейцария)) получали путем совместной трансфекции растущих в суспензии клеток HEK293-EBNA экспрессионными векторами для клеток млекопитающих с использованием полиэтиленимина (ПЭИ). Для трансфекции клетки HEK293 EBNA культивировали в бессывороточной культуральной среде Excell, содержащей 6 мМ L-глутамин и 250 мг/л культуральной среды G418. Для производства высевали в центрифужные флаконы вместимостью 600 мл (максимальный рабочий объем 400 мл) 800 млн клеток HEK293 EBNA за 24 ч до трансфекции без G418. Для трансфекции 800 млн клеток центрифугировали в течение 5 мин при 210 × g, и супернатант заменяли 40 мл предварительно нагретой среды CD СНО, содержащей 6 мМ L-глутамин. Экспрессионные векторы смешивали в 40 мл среды CD СНО, содержащей 6 мМ L-глутамин, для получения конечного количества ДНК 400 мкг. После добавления 1080 мкл раствора ПЭИ (2,7 мкг/мл) смесь интенсивно перемешивали в течение 15 с и затем инкубировали в течение 10 мин при комнатной температуре. Затем клетки смешивали с раствором ДНК/ПЭИ, переносили в 600-миллилитровый центрифужный флакон и инкубировали в течение 3 ч при 37°С в инкубаторе в атмосфере, содержащей 5% СО2. После инкубации добавляли 320 мл среды Excell + 6 мМ L-глутамин + 5 г/л Pepsoy + 1,0 мМ VPA +3 г/л глюкозы, и клетки культивировали в течение 24 ч перед осуществлением подпитки 7% Feed 7. После культивирования в течение 6-7 дней супернатант собирали для очистки путем центрифугирования в течение 20-30 мин при 210 × g (центрифуга Sigma 8K). Раствор стерилизовали фильтрацией (фильтр с размером пор 0,22 мкм) и добавляли азид натрия в конечной концентрации 0,01% (мас./об.). Раствор хранили при 4°С до очистки. Секретированный белок очищали из супернатантов клеточных культур с помощью аффинной хроматографии, применяя аффинную хроматографию на белке А, с последующей(ими) одной или двумя стадией(ями) гель-фильтрации.
Для проведения аффинной хроматографии супернатант вносили на колонку белок A MabSelectSure (CV = 5 мл, фирма GE Healthcare), уравновешенную буфером, содержим 20 мМ цитрат натрия, 20 мМ фосфат натрия, рН 7,5. Несвязанный белок удаляли промывкой, используя равный по меньшей мере 10 объемам колонки объем буфера, содержащего 20 мМ цитрат натрия, 20 мМ фосфат натрия, рН 7,5, а требуемый белок элюировали, применяя равный 20 объемам колонки объем буфера (градиент от 0% до 100%), содержащего 20 мМ цитрат натрия, 100 мМ хлорид натрия, 100 мМ глицин, рН 3,0. Раствор белка нейтрализовали, добавляя 1/10 0,5 М Na2HPO4, рН 8,0. Требуемый белок концентрировали с помощью ультра-концентратора Amicon®Ultra-15 Ultracel 30K (фирма Merck Millipore Ltd.) до объема, составляющего максимум 4 мл, перед загрузкой на колонку HiLoad Супердекс 200 (фирма GE Healthcare), уравновешенную буфером, содержащим 20 мМ гистидин, 140 мМ хлорид натрия, 0,01% Твин, рН 6,0.
Концентрацию белков в очищенных белковых образцах определяли, измеряя оптическую плотность (ОП) при 280 нм, осуществляя деление на коэффициент молярной экстинкции, рассчитанный на основе аминокислотной последовательности.
Чистоту и молекулярную массу молекул после конечной стадии очистки анализировали с помощью КЭ-ДСН-анализов в присутствии восстановителя или без него. Применяли систему Caliper LabChip GXII (фирма Caliper Lifescience) согласно инструкции производителя.
Содержание агрегатов молекул определяли с использованием колонки для аналитической гель-фильтрации TSKgel G3000 SW XL (фирма Tosoh), применяя подвижный буфер, содержащий 25 мМ K2HPO4, 125 мМ NaCl, 200 мМ моногидрохлорид L-аргинина, 0,02% (мас./об.) NaN3, рН 6,7 при 25°С.
Конечное качество всех молекул оказалось высоким с содержанием мономеров ≥95%.
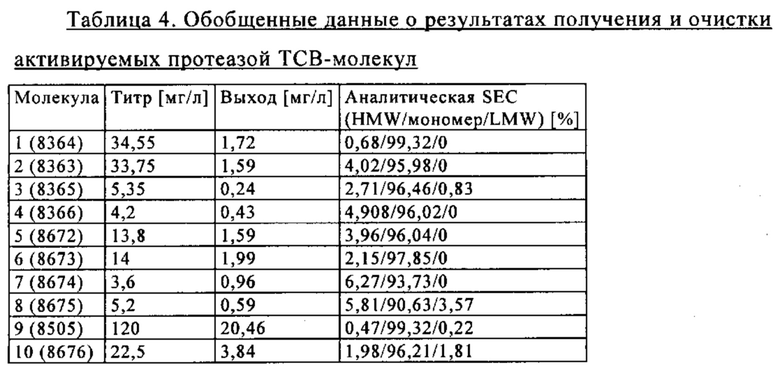
Пример 16
Контроль качества и стабильность - анализ методом капиллярного электрофореза в присутствии ДСН различных ТСВ-молекул
Чистоту и молекулярную массу молекул после конечной стадии очистки анализировали с помощью КЭ-ДСН-анализов в присутствии восстановителя или без него. Применяли систему Caliper LabChip GXII (фирма Caliper Lifescience) согласно инструкции производителя. Осуществляли сравнение необработанных молекул (которые хранили при 4°С), обработанных молекул (которые обрабатывали соответствующей рекомбинантной протеазой (фирма R&D Systems) в течение 24 ч при 37°С и молекулы, которую инкубировали в течение 72 ч при 37°С (фиг. 34, 35А и 35Б).
Сравнение необработанных и обработанных молекул продемонстрировало полное расщепление анти-ID scFv после обработки rh-матриптазой/ST14 в случае инвертированного формата, содержащего линкер с сайтом матриптазы MK062, но неполное расщепление в случае линкера с сайтом ММР9-матриптаза MK062. Обработка rh-катепсином В и rh-катепсином S также не обеспечивала полное расщепление. Условия для очищенных ферментов не были оптимальными.
Пробег молекул, инкубированных при 37°С в течение 72 ч, соответствовал такой же высоте, что и пробег чистых молекул, что позволяет предположить, что молекулы были стабильными при 37°С в течение времени, соответствующем продолжительности анализа in vitro. Предварительно окрашенный белковый маркер Mark 12 (фирма Invitrogen) применяли для определения правильной молекулярной массы.
Пример 17
Сравнение различных линкеров и форматов активируемых протеазой FolR1-ТСВ
Анализ активации Jurkat NFAT. Осуществляли анализ активации Jurkat NFAT для сравнения различных форматов и линкеров в активируемой протеазой ТСВ. Линия репортерных клеток Jurkat-NFAT (фирма Promega) представляет собой линию репортерных клеток острого человеческого лейкоза с промотором NFAT, экспрессирующую человеческую CD3ε. Если ТСВ связывается с опухолью-мишенью и CD3-связывающий агент связывается (перекрестное сшивание) с CD3ε, то экспрессию люциферазы можно измерять на основе люминисценции после добавления субстрата One-Glo (фирма Promega). 20000 клеток-мишеней высевали в 96-луночный планшет с белыми стенками и прозрачным дном (фирма Greiner Bio-One), используя 50 мкл /лунку среды Jurkat (RPMI1640, 2 г/л глюкозы, 2 г/л NaHCO3, 10% FCS, 25 мМ HEPES, 2 мМ L-глутамин, 1 × NEAA, 1 × пируват натрия) без гигромицина. Планшеты инкубировали в течение примерно 20 ч при 37°С. Репортерные клетки Jurkat-NFAT собирали и определяли жизнеспособность с помощью устройства ViCell. Клетки ресуспендировали в среде Jurkat без гигромицина и добавляли по 50 мкл на лунку (50000 клеток/лунку). Соотношение Е:Т составляло 2,5:1 (на основе количества высеянных клеток). Антитела разводили в среде Jurkat без гигромицина и добавляли из расчета 50 мкл/лунку. Клетки инкубировали при 37°С в течение 6 ч во влажной камере, после чего их изымали из камеры для адаптации к комнатной температуре примерно за 10 мин для оценки люминисценции. В лунки добавляли из расчета 50 мкл/лунку раствор ONE-Glo и инкубировали в течение 10 мин при комнатной температуре в темноте. Люминисценцию определяли с помощью ридера WALLAC Victor3 ELISA (PerkinElmer2030), продолжительность детекции составляла 1 с/лунку. Сравнение предварительно обработанной активируемой протеазой ТСВ (8364, закрашенные серым цветом квадраты) и FolR1-ТСВ (черные треугольники с направленной вниз вершиной) продемонстрировало, что эффективность после расщепления полностью восстанавливалась. Никакой люминисценции не удалось обнаружить в клетках, которые инкубировали с замаскированной ТСВ (содержащей нерасщепляемый GS-линкер, серые треугольники с направленной вверх вершиной) и контрольной «ненацеленной» ТСВ (незакрашенный треугольник с направленной вниз вершиной) для обеих линий клеток в указанном диапазоне концентраций. Штриховой линией обозначена люминисценция клеток-мишеней и эффекторных клеток без обработки какой-либо ТСВ (фиг. 36А и 36Б).
Пример 18
Цитотоксичность в отношении опухолевых клеток, обусловленная различными форматами активируемой протеазой ТСВ
Опосредуемый Т-клетками цитолиз опухолевых клеток, обусловленный активируемыми протеазой ТСВ-молекулами, оценивали на клеточных линиях, экспрессирующих различные уровни FolR1. Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) содержащую РВМС интерфазу переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС медленно замораживали в течение ночи при -80°С в контейнерах для замораживания клеток CoolCell® (фирма BioCision) и затем переносили в жидкий азот. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты и инкубировали в течение примерно 20 ч при 37°С во влажной камере. Примерно за 20 ч до начала анализа РВМС подвергали оттаиванию в среде RPMI1640 (10% FCS, 1 × GlutaMax). РВМС центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в свежей средой (RPMI1640, 2% FCS, 1 × GlutaMax) и инкубировали в течение максимум 24 ч при 37°С во влажной камере. За один день до начала анализа РВМС собирали и центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в среде для анализа и добавляли к клеткам-мишеням 0,2 млн РВМС из расчета 100 мкл/лунку (Е:Т 10:1, на основе количестве высеянных клеток-мишеней). Молекулы разводили средой для анализа (RPMI1640, 2% FCS, 1 × GlutaMax) и добавляли из расчета 50 мкл/лунку в указанных концентрациях в трех повторностях, после чего планшеты инкубировали в течение примерно 48 ч при 37°С во влажной камере. Цитолиз клеток-мишеней оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ.
Результаты (фиг. 37А и 37Б) представлены в виде сравнения двух различных форматов активируемых протеазой ТСВ, которые обе содержат антиидиотипический CD3 scFv 4.32.63, связанный с линкером с сайтом матриптазы MK062. Инвертированный формат активируемой протеазой ТСВ (8365, серые кружочки), вероятно, был более эффективным в отношении цитолиза (клетки-мишени HeLa и Skov-3), чем классический формат активируемой протеазой ТСВ (8408, темно-серые треугольники с направленной вверх вершиной). Однако инвертированная молекула, содержащая нерасщепляемый линкер (8366, светло-серые квадраты), оказалась менее эффективной с позиций маскировки, чем замаскированная классическая молекула (8409, темно-серые треугольники с направленной вниз вершиной).
На фиг. 37В представлены данные о цитотоксичности в отношении клеток-мишеней HeLa. Осуществляли сравнение классической активируемой протеазой ТСВ, содержащей антиидиотипический CD3 scFv 4.32.63 и GS-линкеры с различными сайтами, распознаваемыми протеазой. Активируемая протеазой ТСВ, содержащая линкер с сайтом ММР9-матриптазы MK062 (8364, серые квадраты) оказалась более эффективной, чем FolR1 ТСВ (светло-серые треугольники с направленной вниз вершиной), в то время как активируемая протеазой ТСВ, содержащая линкер только с сайтом матриптазы MK062 (светло-серый ромб), оказалась менее эффективной в отношении клеток HeLa. Эффективность молекул, содержащих сайт катепсина (серые кружки) или нерасщепляемый линкер (черные треугольники с направленной вниз вершиной), оказалась сопоставимой.
На фиг. 37Г представлены данные о цитотоксичности в отношении клеток-мишеней Skov-3. Осуществляли сравнение классической активируемой протеазой ТСВ, содержащей антиидиотипический CD3 scFv 4.43.63 и GS-линкеры с различными сайтами, распознаваемыми протеазой. Активируемая протеазой ТСВ, содержащая линкер с сайтом ММР9-матриптазы MK062 (8364, серые квадраты), практически имела такую же эффективность, что и FolR1-ТСВ (светло-серые треугольники с направленной вниз вершиной), в то время как активируемая протеазой ТСВ, содержащая линкер только с сайтом матриптазы MK062 (светло-серый ромб) оказалась менее эффективной в отношении цитолиза клеток Skov-3. Молекула, содержащая сайт катепсина (серые окружности) оказалась менее эффективной, чем молекула, содержащая только сайт матриптазы MK062, молекула, содержащая нерасщепляемый линкер (черные треугольники с направленной вниз вершиной), индуцировала в указанных концентрациях цитолиз лишь менее 10% клеток Skov-3.
Пример 19
Т-клеточная активация после совместной инкубации эпителиальных клеток коркового вещества почек человека или бронхиальных эпителиальных клеток человека с ТСВ и человеческими РВМС
Активацию Т-клеток, опосредуемую активируемыми протеазой ТСВ-молекулами, оценивали с использованием клеток HRCEpi (эпителиальные клетки коркового вещества почек человека) и HBEpiC (бронхиальные эпителиальные клетки человека), экспрессирующих лишь невысокие количества FolR1. Человеческие РВМС использовали в качестве эффекторных клеток и осуществляли окрашивание маркеров Т-клеточной активации после инкубации в течение 48 ч с молекулами и клетками. Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) содержащую РВМС интерфазу переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС медленно замораживали в течение ночи при -80°С в контейнерах для замораживания клеток CoolCell® (фирма BioCision) и затем переносили в жидкий азот. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты и инкубировали в течение примерно 20 ч при 37°С во влажной камере. Примерно за 20 ч до начала анализа РВМС подвергали оттаиванию в среде RPMI1640 (10% FCS, 1 × GlutaMax). РВМС центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в свежей среде (RPMI1640, 2% FCS, 1 × GlutaMax) и инкубировали в течение максимум 24 ч при 37°С во влажной камере. За один день до начала анализа РВМС собирали и центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в среде для анализа и добавляли к клеткам-мишеням 0,2 млн РВМС из расчета 100 мкл/лунку (Е:Т 10:1, соотношение определяли на основе количества высеянных клеток-мишеней). Молекулы разводили средой для анализа (RPMI1640, 2% FCS, 1 × GlutaMax) и добавляли в указанных концентрациях в трех повторностях, после чего планшеты инкубировали в течение примерно 48 ч при 37°С во влажной камере.
Т-клеточную активацию оценивали после инкубации в течение 48 ч при 37°С, 5% CO2 путем количественного определения CD25 и CD69 на CD4-позитивных и CD8-позитивных Т-клетках. FolR1 16D5 ТСВ (6298) и «ненацеленную» ТСВ (которая связывается с CD3, но не связывается с антигеном клетки-мишени, 7235) включали в качестве контролей. Каждая точка соответствует среднему значению, полученному по трем повторностям, для РВМС из трех различных доноров. Стандартное отклонение обозначено планками погрешностей. Для статистического анализа использовали непарный t-критерий. Результаты продемонстрировали повышение уровня CD69 в CD8-позитивных клетках при использовании FolR1-ТСВ, который существенно превышал медианную интенсивность флуоресценции, установленную для активируемых протеазой ТСВ (фиг. 38А и 38Б).
Пример 20
Цитотоксичность в отношении опухолевых клеток, опосредуемая различными форматами активируемой протеазой связывающейся с мезотелином (MSLN) ТСВ
Опосредуемый Т-клетками цитолиз опухолевых клеток, обусловленный активируемыми протеазой ТСВ-молекулами, оценивали на клеточных линиях, экспрессирующих различные уровни мезотелина (MSLN). Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, №Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) содержащую РВМС интерфазу переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл АСК-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС медленно замораживали в течение ночи при -80°С в контейнерах для замораживания клеток CoolCell® (фирма BioCision) и затем переносили в жидкий азот. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты и инкубировали в течение примерно 20 ч при 37°С во влажной камере. Примерно за 20 ч до начала анализа РВМС подвергали оттаиванию в среде RPMI1640 (10% FCS, 1 × GlutaMax). РВМС центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в свежей средой (RPMI1640, 2% FCS, 1 × GlutaMax) и инкубировали в течение максимум 24 ч при 37°С во влажной камере. За один день до начала анализа РВМС собирали и центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в среде для анализа и добавляли к клеткам-мишеням 0,2 млн РВМС из расчета 100 мкл/лунку (Е:Т 10:1, соотношение определяли на основе количества высеянных клеток-мишеней). Молекулы разводили средой для анализа (RPMI1640, 2% FCS, 1 × GlutaMax) и добавляли в указанных концентрациях в трех повторностях, после чего планшеты инкубировали в течение примерно 48 ч при 37°С во влажной камере. Цитолиз клеток-мишеней оценивали после инкубации в течение 48 ч при 37°С, 5% СО2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ.
Результаты (фиг. 39А и 39Б) позволили выявить цитолиз клеток-мишеней, опосредуемый активируемой протеазой MSLN ТСВ (8672) в отношении клеточных линий NCI Н596 и AsPC-1. Активируемые протеазой ТСВ практически соответствовали эффективности MSLN ТСВ (8676) в отношении клеток NCI Н596 и AsPC-1. Молекула, содержащая нерасщепляемый GS-линкер (8673), не индуцировала цитолиз обеих линий клеток в указанном диапазоне концентраций.
Пример 21
Репортерный анализ Jurkat-NFAT для мониторинга экспрессии мишени (FOLR1-TCB) и протеазной активности (активируемая протеазой FOLR1 ТСВ) в образцах первичных опухолей
Целью настоящего анализа было изучение экспрессии опухолевого антигена-мишени (FolR1) и активности опухольспецифических протеаз типа ММР9, матриптазы или катепсина, в образцах человеческих опухолей.
Линия репортерных клеток Jurkat-NFAT (фирма Promega) представляет собой линию репортерных клеток острого человеческого лейкоза с промотором NFAT, экспрессирующую человеческую CD3ε. Если активирующая Т-клетки биспецифическая молекула связывается с опухолью-мишенью и с CD3ε (перекрестное сшивание), то можно измерять экспрессию люциферазы. Люминисценцию измеряют после добавления субстрата One-Glo (фирма Promega).
Образцы первичных опухолей получали от фирмы Indivumed GmbH, Германия. Образцы доставляли в течение ночи в среде для транспортировки. Примерно через 24 ч после хирургической процедуры образец разрезали на небольшие кусочки. Подготавливали 96-луночный планшет с белыми стенками, плоским (прозрачным) дном путем добавления 18 мкл холодного матригеля (Matrigel (734-1101, фирма Corning/VWR). Планшет инкубировали в течение 2 мин при 37°С перед внесением кусочков опухоли (в трех повторностях). По 33 мкл холодного матригеля добавляли на лунку и планшет инкубировали вновь в течение 2 мин при 37°С. По 50 мкл разведения антитела (в среде Jurkat без гигромицина, но содержащей 2× пенициллин/стрептомицин) добавляли на лунку и планшет инкубировали в течение примерно 48 ч при 37°С, 5% CO2.
Репортерные клетки Jurkat-NFAT собирали и определяли жизнеспособность с помощью устройства ViCell. Клетки центрифугировали при 350 × g, 7 мин, после чего ресуспендировали в среде Jurkat без гигромицина и добавляли по 50 мкл на лунку (50000 клеток/лунку). Планшет инкубировали в течение 5 ч при 37°С во влажной камере, после чего изымали для определения люминисценции. По 80 мкл содержимого из каждой лунки переносили в 96-луночный планшет с белыми стенками. В каждую лунку добавляли 27 мкл/лунку раствора ONE-Glo и инкубировали в течение 10 мин при комнатной температуре в темноте. Люминисценцию определяли с помощью ридера WALLAC Victor3 ELISA (PerkinElmer2030), продолжительность детекции составляла 1 с/лунку.
Репортерные клетки Jurkat NFAT активировались после совместной инкубации с FolR1-TCB (6298) и активируемой протеазой FolR1-TCB, содержащей сайт расщепления ММР9-матриптазой (8364). Активируемые протеазой FolR1 ТСВ (8363, 8408) и контрольные ТСВ (8409, 7235) не индуцировали экспрессию люциферазы. Штриховой линией обозначена базисная линия люминисценции для клеток Jurkat NFAT, которые совместно инкубировали с опухолью (фиг. 40).
Пример 22
Стабильность в сыворотке активируемых протеазой ТСВ
Капиллярный электрофорез активируемых протеазой ТСВ после инкубации в человеческой сыворотке. Молекулы инкубировали в течение 0 или 14 дней в человеческой сыворотке с низким содержанием IgG при 37°С во влажной камере (5% CO2). Все молекулы очищали аффинной хроматографией (белок А) и затем анализировали с помощью капиллярного электрофореза.
100 мкг каждой молекулы добавляли либо в буфер (гистидиновый буфер (фирма Bichsel) с 0,01% Твин-20), либо в человеческую сыворотку (с низким содержанием IgG, SP1839, TL-15216, 16FSP63814). Концентрация молекул превышала 2 мг/мл и конечная концентрация составляла 0,5 мг/мл. Предварительную обработку одной молекулы (8408) осуществляли с помощью rh-матриптазы (фирма R&D Systems) в течение 24 ч при 37°С, 5% CO2 во влажной камере (в противном случае значение рН сыворотки могло изменяться). Образцы, соответствующие хранению в течение 0 дней, непосредственно замораживали в жидком азоте и хранили при - 80°С до анализа. Образцы, соответствующие хранению в течение 14 дней, инкубировали в течение 14 дней при 37°С, 5% CO2 во влажной камере, после чего их также быстро замораживали.
Перед анализом методом КЭ-ДСН все образцы очищали с помощью аффинной ЖХВР-хроматографии (устройство Agilent technologies 1200series, колонка: Upchurch-специфическая С-130В, материал для упаковки колонки: Applied Biosystems POROS 20А 60 мкл, буфер: 10 мМ Трис, 50 мМ глицин, 500 мМ NaCl, рН 8,0 и рН 2,0, инъецируемый объем: 100 мкл, скорость потока 1 мл/мин, сбор: на основе пика, нейтрализация: 0,5 М Na-фосфат рН 8,0, 10% объема). Активируемая протеазой ТСВ оказалась стабильной в человеческой сыворотке с низким содержанием IgG в течение минимум 14 дней (фиг. 41А-В).
Пример 23
Создание анти-Her2/анти-CD3 и анти-FolR1/анти-CD3 (активирующих) Т-клетки биспецифических (ТСВ) молекул с анти-CD3 scFv
Получали несколько (активирующих) Т-клетки биспецифических (ТСВ), и они схематически изображены на фиг. 42А-Е под соответствующим им ID-номером. Получали следующие молекулы:
ID 8955: «Herceptarg 2+1 IgG, классический формат, заряженные Herceptarg варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - ММР9 - матриптаза MK062 - CD3 - слитый на N-конце с Herceptarg VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и сайтом ММР9 - матриптазы MK062» (фиг. 42А, SEQ ID NO: 81, 132, 133 и 136).
ID 8957: «Herceptarg 2+1 IgG, классический формат, заряженные Herceptarg варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63-нерасщепляемый GS-линкер - CD3 - слитый на N-конце с Herceptarg VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и нерасщепляемым GS-линкером» (фиг. 42Б, SEQ ID NO: 81, 132, 133 и 135).
ID 8959: «Herceptarg 2+1 IgG, классический формат, заряженные Herceptarg варианты, скрещенный CD3 (Herceptarg IgG с CD3 - слитый на N-конце с Herceptarg VH - инертный Fc)» (фиг. 42В, SEQ ID NO: 81, 132, 133 и 134).
ID 8997: «FolR1 36F2 2+1 IgG, классический формат, заряженные FolR1 36F2 варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - ММР9 - матриптаза MK062 - CD3 - слитый на N-конце с FolR1 36F2 VH - инертный Fc) со слитым на N-конце анти-CD3 scFv 4.32.63 и сайтом ММР9 - матриптазы MK062» (фиг. 42Г, SEQ ID NO: 81, 137, 138 и 139).
ID 8998: «FolR1 36F2 2+1 IgG, классический формат, заряженные FolR1 36F2 варианты, скрещенный CD3 (антиидиотипический scFv 4.32.63 - нерасщепляемый GS-линкер - CD3 - слитый на N-конце с FolR1 36F2 VH - инертный Fc) с N-концевым слиянием анти-CD3 scFv 4.32.63 и нерасщепляемым GS-линкером» (фиг. 42Д, SEQ ID NO: 81, 137, 138 и 140).
ID 8996: «FolR1 36F2 2+1 IgG, классический формат, заряженные FolR1 36F2 варианты, скрещенный CD3 (FolR1 36F2 IgG с CD3 - слитый на N-конце с FolR1 36F2 VH - инертный Fc)» (фиг. 42Е, SEQ ID NO: 81, 137, 138 и 141).
Вариабельные домены субклонировали в рамке считывания с предварительно встроенными в соответствующий применяемый в качестве реципиента экспрессионный вектор для клеток млекопитающих доменами. Экспрессия белка находилась под контролем промотора MPSV или CMV (для Herceptarg), и синтетическая сигнальная полиА-последовательность присутствовала на 3'-конце CDS. Кроме того, каждый вектор содержал последовательность OriP EBV.
Пример 24
Цитотоксичность в отношении первичных клеток, опосредуемая активируемой протеазой FolR1 ТСВ
Опосредуемый Т-клетками цитолиз, обусловленный активируемой протеазой FolR1-TCB-молекулой, оценивали на первичных клеточных линиях, экспрессирующих низкие уровни FolR1 (фиг. 43). Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, № Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) содержащую РВМС интерфазу переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (400 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл ACK-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС медленно замораживали в течение ночи при -80°С в контейнерах для замораживания клеток CoolCell® (фирма BioCision) и затем переносили в жидкий азот. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали в среде для анализа (RPMI 1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты и инкубировали в течение примерно 20 ч при 37°С во влажной камере. Примерно за 20 ч до начала анализа РВМС подвергали оттаиванию в среде RPMI1640 (10% FCS, 1 × GlutaMax). РВМС центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в свежей средой (RPMI 1640, 2% FCS, 1 × GlutaMax) и инкубировали в течение максимум 24 ч при 37°С во влажной камере. За один день до начала анализа РВМС собирали и центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в среде для анализа и добавляли к клеткам-мишеням 0,2 млн РВМС из расчета 100 мкл/лунку (Е:Т 10:1, соотношение определяли на основе количестве высеянных клеток-мишеней). Молекулы разводили средой для анализа (RPMI1640, 2% FCS, 1 × GlutaMax) и добавляли в указанных концентрациях в трех повторностях, после чего планшеты инкубировали в течение примерно 48, 72 и 96 ч при 37°С во влажной камере. Цитолиз клеток-мишеней оценивали после инкубации в течение 48, 72 и 96 ч при 37°С, 5% CO2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ.
Токсичность в отношении бронхиальных эпителиальных клеток человека, опосредуемая человеческими РВМС и 100 нМ или 10 нм FolR1-TCB оказалась выше, чем при использовании активируемой протеазой ТСВ.
Пример 25
Цитотоксичность в отношении FolR1-негативных клеток, опосредуемая активируемой протеазой FolR1 ТСВ
Опосредуемый Т-клетками цитолиз, обусловленный активируемой протеазой FolR1-ТСВ-молекулой, оценивали на FolR1-негативной клеточной линии Mkn-45 (фиг. 44). Мононуклеарные клетки периферический крови (РВМС) человека выделяли из лейкоцитарных пленок, которые получали из здоровых доноров. Лейкоцитарную пленку разводили в соотношении 1:1 стерильным ЗФР и наслаивали на градиент Histopaque (фирма Sigma, № Н8889). После центрифугирования (450 × g, 30 мин, без перерыва, комнатная температура) содержащую РВМС интерфазу переносили в новую фальконовскую пробирку, которую затем заполняли 50 мл ЗФР. Смесь центрифугировали (40 × g, 10 мин, комнатная температура), супернатант отбрасывали и дебрис РВМС ресуспендировали в 2 мл ACK-буфера для лизиса эритроцитов. После инкубации при 37°С в течение примерно 2-3 мин пробирки заполняли стерильным ЗФР до 50 мл и центрифугировали при 350 × g в течение 10 мин. Указанную стадию промывки повторяли однократно перед ресуспендированием РВМС в среде RPMI1640, содержащей 2% FCS и 1 × GlutaMax и 10% ДМСО. РВМС медленно замораживали в течение ночи при -80°С в контейнерах для замораживания клеток CoolCell® (фирма BioCision) и затем переносили в жидкий азот. За 1 день до начала анализа прикрепленные клетки-мишени собирали с помощью трипсина/ЭДТА, подсчитывали, проверяли жизнеспособность и ресуспендировали в среде для анализа (RPMI1640, 2% FCS, 1 × GlutaMax). Клетки-мишени высевали с плотностью 20000 клеток/лунку в плоскодонные 96-луночные планшеты и инкубировали в течение примерно 20 ч при 37°С во влажной камере. Примерно за 20 ч до начала анализа РВМС подвергали оттаиванию в среде RPMI1640 (10% FCS, 1 × GlutaMax). РВМС центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в свежей средой (RPMI1640, 2% FCS, 1 × GlutaMax) и инкубировали в течение максимум 24 ч при 37°С во влажной камере. За один день до начала анализа РВМС собирали и центрифугировали при 350 × g в течение 7 мин. Дебрис ресуспендировали в среде для анализа и добавляли к клеткам-мишеням 0,2 млн РВМС из расчета 100 мкл/лунку (Е:Т 10:1, соотношение определяли на основе количестве высеянных клеток-мишеней). Молекулы разводили средой для анализа (RPMI1640, 2% FCS, 1 × GlutaMax) и добавляли в указанных концентрациях в трех повторностях, после чего планшеты инкубировали в течение примерно 48 и 72 ч при 37°С во влажной камере. Цитолиз клеток-мишеней оценивали после инкубации в течение 48, 72 и 96 ч при 37°С, 5% CO2 путем количественного анализа высвобождения ЛДГ в клеточные супернатанты апоптозными/некротическими клетками (набор для обнаружения ЛДГ, фирма Roche Applied Science, №11644793001). Максимальный лизис клеток-мишеней (=100%) достигался при инкубации клеток-мишеней в присутствии 1% Тритона Х-100 в течение 20 ч до определения ЛДГ. Минимальный лизис (=0%) соответствовал лизису при совместной инкубации клеток-мишеней с эффекторными клетками без какой-либо ТСВ. Активируемая протеазой ТСВ не индуцировала цитолиз клеток-мишеней при применении в концентрации 100 нМ.





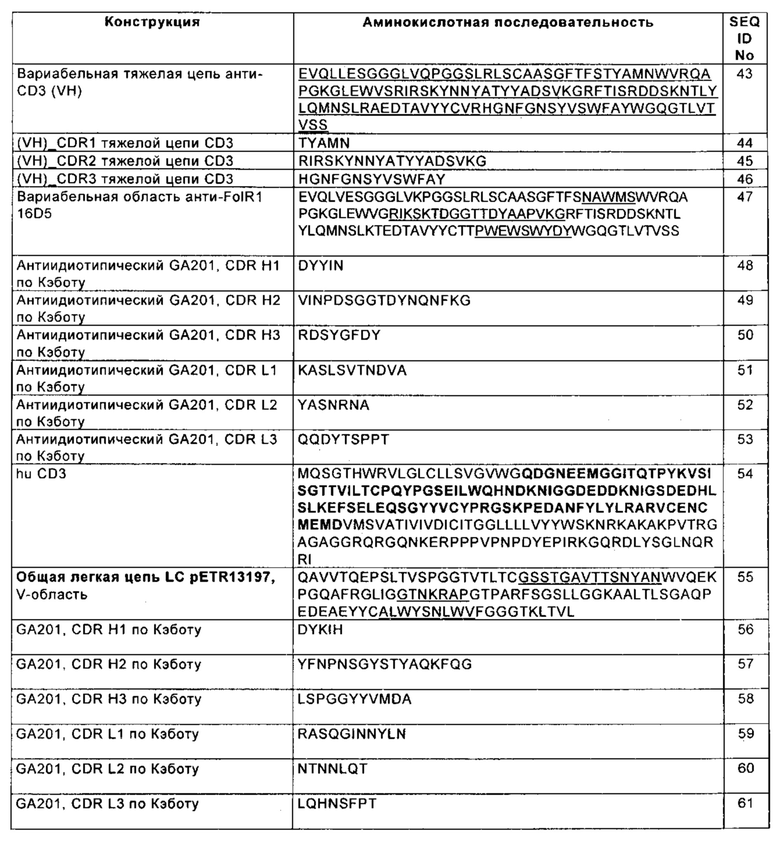












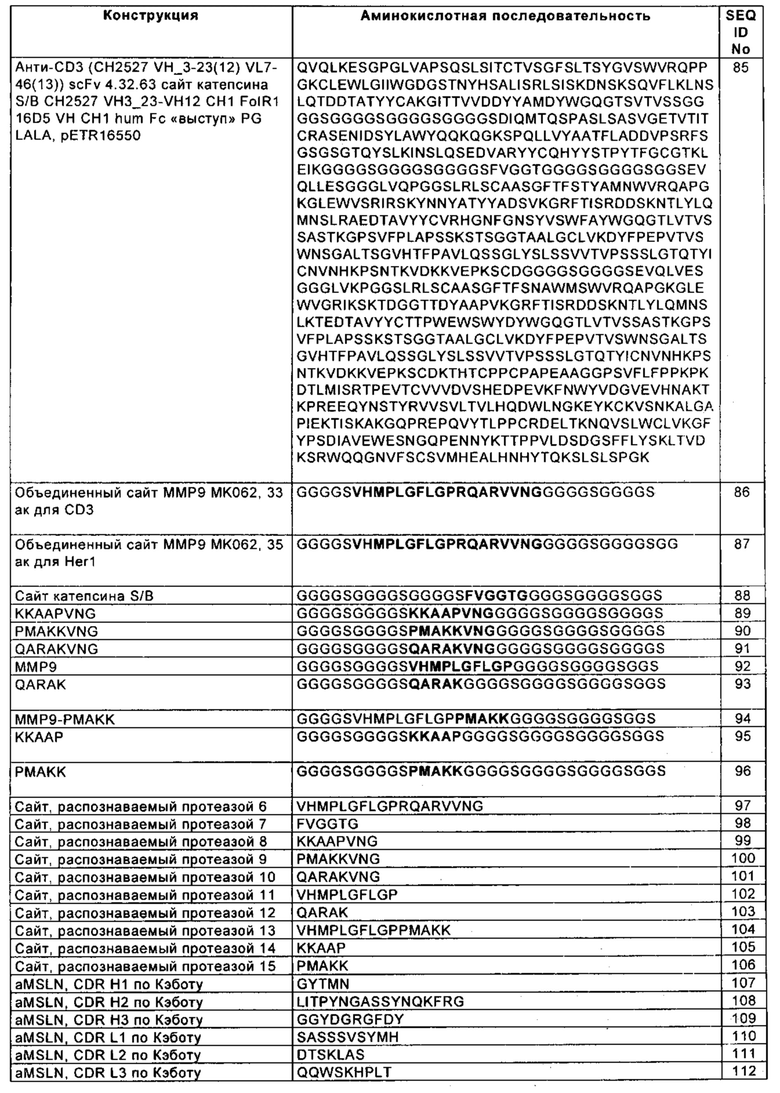

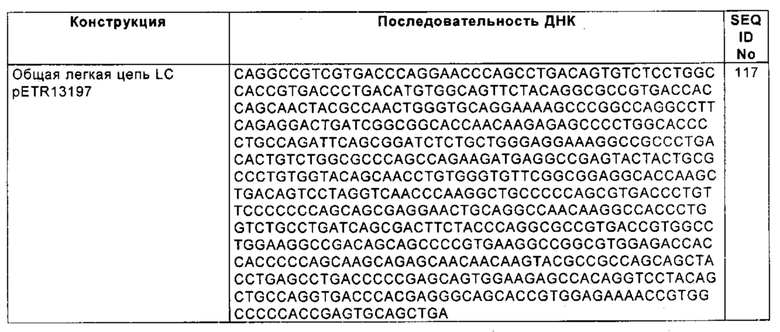












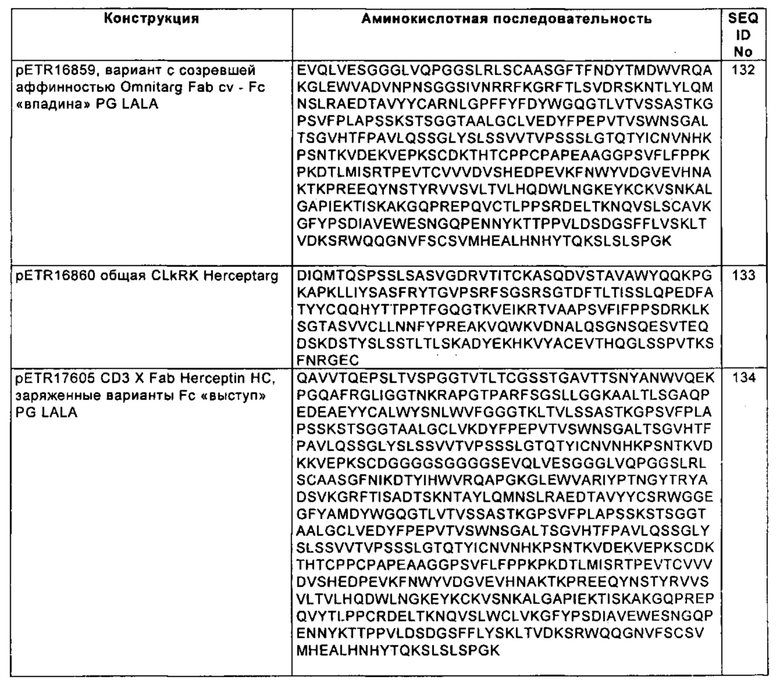


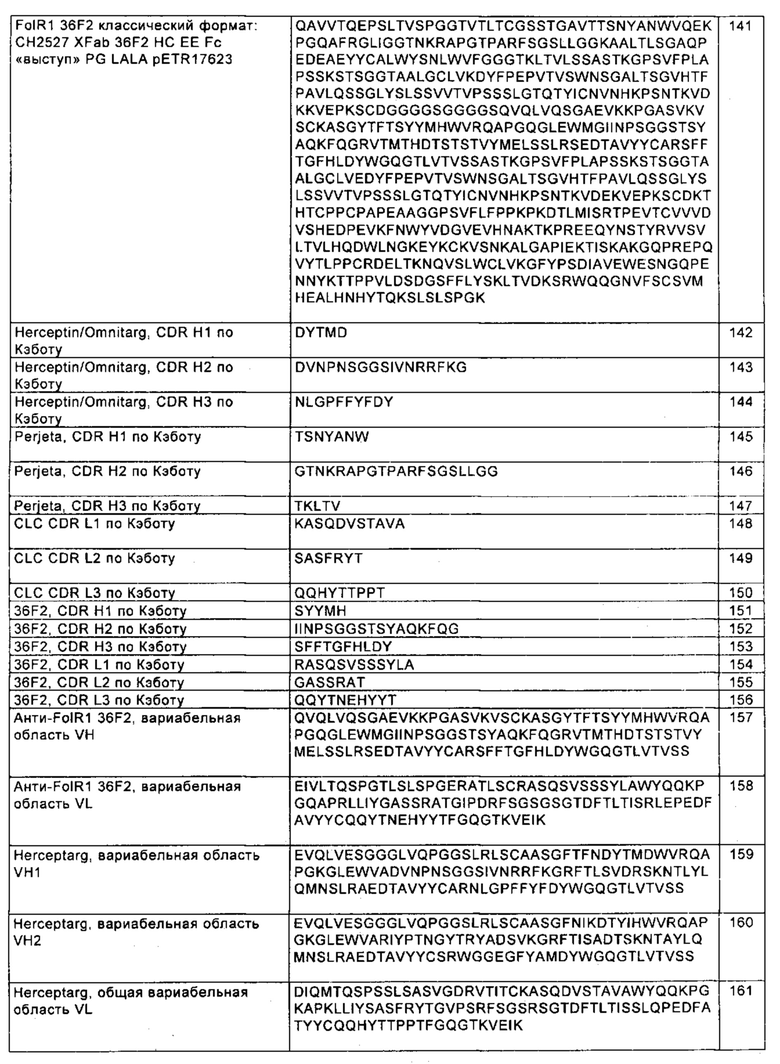







Хотя представленное выше изобретение подробно описано для целей лучшего понимания с помощью иллюстраций и примеров, описание и примеры ее следует рассматривать как ограничивающие объем изобретения. Содержание всех процитированных патентов и научной литературы полностью включены в настоящее описание в качестве ссылки.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Ф.Хоффманн-Ля Роше АГ
<120> Активируемые протеазой связывающие T-клетки биспецифические
молекулы
<130> P33331
<160> 170
<170> PatentIn version 3.5
<210> 1
<211> 215
<212> PRT
<213> Chimeric
<400> 1
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro
100 105 110
Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu
115 120 125
Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro
130 135 140
Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala
145 150 155 160
Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala
165 170 175
Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg
180 185 190
Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr
195 200 205
Val Ala Pro Thr Glu Cys Ser
210 215
<210> 2
<211> 971
<212> PRT
<213> Chimeric
<400> 2
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Arg Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile His Trp Val Lys Gln Ala Pro Gly Lys Cys Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Gly Glu Pro Ala Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ala His Pro Tyr Asp Tyr Asp Val Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Thr Val Leu Thr Gln
130 135 140
Ser Pro Ala Ser Leu Gly Val Ser Leu Gly Gln Arg Ala Thr Ile Ser
145 150 155 160
Cys Arg Ala Ser Lys Ser Val Ser Thr Ser Asn Tyr Ser Tyr Ile His
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Lys Tyr
180 185 190
Val Ser Tyr Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp
210 215 220
Ala Ala Thr Tyr Tyr Cys Gln His Ser Arg Glu Phe Pro Trp Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Arg Gln Ala Arg Val Val Asn Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 3
<211> 450
<212> PRT
<213> Chimeric
<400> 3
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Pro Trp Glu Trp Ser Trp Tyr Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 4
<211> 971
<212> PRT
<213> Chimeric
<400> 4
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Arg Gln Ala Arg Val Val Asn Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 5
<211> 971
<212> PRT
<213> Chimeric
<400> 5
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 6
<211> 971
<212> PRT
<213> Chimeric
<400> 6
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Arg Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile His Trp Val Lys Gln Ala Pro Gly Lys Cys Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Gly Glu Pro Ala Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ala His Pro Tyr Asp Tyr Asp Val Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Thr Val Leu Thr Gln
130 135 140
Ser Pro Ala Ser Leu Gly Val Ser Leu Gly Gln Arg Ala Thr Ile Ser
145 150 155 160
Cys Arg Ala Ser Lys Ser Val Ser Thr Ser Asn Tyr Ser Tyr Ile His
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Lys Tyr
180 185 190
Val Ser Tyr Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp
210 215 220
Ala Ala Thr Tyr Tyr Cys Gln His Ser Arg Glu Phe Pro Trp Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 7
<211> 33
<212> PRT
<213> Chimeric
<400> 7
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Gln Ala Arg Val Val
1 5 10 15
Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser
<210> 8
<211> 28
<212> PRT
<213> Chimeric
<400> 8
Gly Gly Gly Gly Ser Val His Met Pro Leu Gly Phe Leu Gly Pro Gly
1 5 10 15
Arg Ser Arg Gly Ser Phe Pro Gly Gly Gly Gly Ser
20 25
<210> 9
<211> 41
<212> PRT
<213> Chimeric
<400> 9
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Gln Ala Arg Val Val
1 5 10 15
Asn Gly Gly Gly Gly Gly Ser Val Pro Leu Ser Leu Tyr Ser Gly Gly
20 25 30
Gly Gly Gly Ser Gly Gly Gly Gly Ser
35 40
<210> 10
<211> 36
<212> PRT
<213> Chimeric
<400> 10
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Gln Ala Arg Val Val
1 5 10 15
Asn Gly Val Pro Leu Ser Leu Tyr Ser Gly Gly Gly Gly Gly Ser Gly
20 25 30
Gly Gly Gly Ser
35
<210> 11
<211> 5
<212> PRT
<213> Chimeric
<400> 11
Thr Tyr Ala Met Asn
1 5
<210> 12
<211> 19
<212> PRT
<213> Chimeric
<400> 12
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 13
<211> 14
<212> PRT
<213> Chimeric
<400> 13
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 14
<211> 5
<212> PRT
<213> Chimeric
<400> 14
Asn Ala Trp Met Ser
1 5
<210> 15
<211> 19
<212> PRT
<213> Chimeric
<400> 15
Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro
1 5 10 15
Val Lys Gly
<210> 16
<211> 9
<212> PRT
<213> Chimeric
<400> 16
Pro Trp Glu Trp Ser Trp Tyr Asp Tyr
1 5
<210> 17
<211> 14
<212> PRT
<213> Chimeric
<400> 17
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 18
<211> 7
<212> PRT
<213> Chimeric
<400> 18
Gly Thr Asn Lys Arg Ala Pro
1 5
<210> 19
<211> 9
<212> PRT
<213> Chimeric
<400> 19
Ala Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 20
<211> 5
<212> PRT
<213> Chimeric
<400> 20
Asp Tyr Ser Ile His
1 5
<210> 21
<211> 17
<212> PRT
<213> Chimeric
<400> 21
Trp Ile Asn Thr Glu Thr Gly Glu Pro Ala Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 22
<211> 9
<212> PRT
<213> Chimeric
<400> 22
Pro Tyr Asp Tyr Asp Val Leu Asp Tyr
1 5
<210> 23
<211> 15
<212> PRT
<213> Chimeric
<400> 23
Arg Ala Ser Lys Ser Val Ser Thr Ser Asn Tyr Ser Tyr Ile His
1 5 10 15
<210> 24
<211> 7
<212> PRT
<213> Chimeric
<400> 24
Tyr Val Ser Tyr Leu Glu Ser
1 5
<210> 25
<211> 9
<212> PRT
<213> Chimeric
<400> 25
Gln His Ser Arg Glu Phe Pro Trp Thr
1 5
<210> 26
<211> 5
<212> PRT
<213> Chimeric
<400> 26
Ser Tyr Gly Val Ser
1 5
<210> 27
<211> 16
<212> PRT
<213> Chimeric
<400> 27
Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile Ser
1 5 10 15
<210> 28
<211> 14
<212> PRT
<213> Chimeric
<400> 28
Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr
1 5 10
<210> 29
<211> 11
<212> PRT
<213> Chimeric
<400> 29
Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
1 5 10
<210> 30
<211> 7
<212> PRT
<213> Chimeric
<400> 30
Ala Ala Thr Phe Leu Ala Asp
1 5
<210> 31
<211> 9
<212> PRT
<213> Chimeric
<400> 31
Gln His Tyr Tyr Ser Thr Pro Tyr Thr
1 5
<210> 32
<211> 450
<212> PRT
<213> Chimeric
<400> 32
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Lys Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Tyr Phe Asn Pro Asn Ser Gly Tyr Ser Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Ser Pro Gly Gly Tyr Tyr Val Met Asp Ala Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 33
<211> 213
<212> PRT
<213> Chimeric
<400> 33
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Asn Thr Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Phe Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 34
<211> 492
<212> PRT
<213> Chimeric
<400> 34
Glu Val Gln Leu Glu Gln Ser Gly Pro Val Leu Val Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Ile Ile Gln Ser His Gly Lys Cys Leu Glu Trp Ile
35 40 45
Gly Val Ile Asn Pro Asp Ser Gly Gly Thr Asp Tyr Asn Gln Asn Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Thr Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Ser Tyr Gly Phe Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Thr
130 135 140
Pro Lys Phe Leu Leu Val Pro Ala Gly Asp Arg Ile Thr Met Thr Cys
145 150 155 160
Lys Ala Ser Leu Ser Val Thr Asn Asp Val Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ser Pro Lys Leu Leu Leu Tyr Tyr Ala Ser Asn Arg Asn
180 185 190
Ala Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe
195 200 205
Thr Phe Thr Ile Thr Thr Leu Gln Ala Glu Asp Leu Ala Val Tyr Phe
210 215 220
Cys Gln Gln Asp Tyr Thr Ser Pro Pro Thr Phe Gly Cys Gly Thr Lys
225 230 235 240
Leu Glu Ile Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Pro
245 250 255
Leu Gly Leu Trp Ser Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Asp Ile Gln Met Thr Gln Ser Pro Ser
275 280 285
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
290 295 300
Ser Gln Gly Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
305 310 315 320
Lys Ala Pro Lys Arg Leu Ile Tyr Asn Thr Asn Asn Leu Gln Thr Gly
325 330 335
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
340 345 350
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
355 360 365
Gln His Asn Ser Phe Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
370 375 380
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
385 390 395 400
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
405 410 415
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
420 425 430
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
435 440 445
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
450 455 460
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
465 470 475 480
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
485 490
<210> 35
<211> 35
<212> PRT
<213> Chimeric
<400> 35
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Pro Leu Gly Leu Trp
1 5 10 15
Ser Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser Gly Gly
35
<210> 36
<211> 8
<212> PRT
<213> Chimeric
<400> 36
Arg Gln Ala Arg Val Val Asn Gly
1 5
<210> 37
<211> 18
<212> PRT
<213> Chimeric
<400> 37
Val His Met Pro Leu Gly Phe Leu Gly Pro Gly Arg Ser Arg Gly Ser
1 5 10 15
Phe Pro
<210> 38
<211> 21
<212> PRT
<213> Chimeric
<220>
<221> X
<222> (9)..(13)
<223> X is an amino acid
<220>
<221> X
<222> (9)..(13)
<223> X or Xaa is an amino acid
<400> 38
Arg Gln Ala Arg Val Val Asn Gly Xaa Xaa Xaa Xaa Xaa Val Pro Leu
1 5 10 15
Ser Leu Tyr Ser Gly
20
<210> 39
<211> 16
<212> PRT
<213> Chimeric
<400> 39
Arg Gln Ala Arg Val Val Asn Gly Val Pro Leu Ser Leu Tyr Ser Gly
1 5 10 15
<210> 40
<211> 7
<212> PRT
<213> Chimeric
<400> 40
Pro Leu Gly Leu Trp Ser Gln
1 5
<210> 41
<211> 249
<212> PRT
<213> Chimeric
<400> 41
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Arg Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile His Trp Val Lys Gln Ala Pro Gly Lys Cys Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Gly Glu Pro Ala Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ala His Pro Tyr Asp Tyr Asp Val Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Thr Val Leu Thr Gln
130 135 140
Ser Pro Ala Ser Leu Gly Val Ser Leu Gly Gln Arg Ala Thr Ile Ser
145 150 155 160
Cys Arg Ala Ser Lys Ser Val Ser Thr Ser Asn Tyr Ser Tyr Ile His
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Lys Tyr
180 185 190
Val Ser Tyr Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp
210 215 220
Ala Ala Thr Tyr Tyr Cys Gln His Ser Arg Glu Phe Pro Trp Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys
245
<210> 42
<211> 249
<212> PRT
<213> Chimeric
<400> 42
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys
245
<210> 43
<211> 125
<212> PRT
<213> Chimeric
<400> 43
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 44
<211> 5
<212> PRT
<213> Chimeric
<400> 44
Thr Tyr Ala Met Asn
1 5
<210> 45
<211> 19
<212> PRT
<213> Chimeric
<400> 45
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 46
<211> 14
<212> PRT
<213> Chimeric
<400> 46
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 47
<211> 120
<212> PRT
<213> Chimeric
<400> 47
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Pro Trp Glu Trp Ser Trp Tyr Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 48
<211> 5
<212> PRT
<213> Chimeric
<400> 48
Asp Tyr Tyr Ile Asn
1 5
<210> 49
<211> 17
<212> PRT
<213> Chimeric
<400> 49
Val Ile Asn Pro Asp Ser Gly Gly Thr Asp Tyr Asn Gln Asn Phe Lys
1 5 10 15
Gly
<210> 50
<211> 8
<212> PRT
<213> Chimeric
<400> 50
Arg Asp Ser Tyr Gly Phe Asp Tyr
1 5
<210> 51
<211> 11
<212> PRT
<213> Chimeric
<400> 51
Lys Ala Ser Leu Ser Val Thr Asn Asp Val Ala
1 5 10
<210> 52
<211> 7
<212> PRT
<213> Chimeric
<400> 52
Tyr Ala Ser Asn Arg Asn Ala
1 5
<210> 53
<211> 9
<212> PRT
<213> Chimeric
<400> 53
Gln Gln Asp Tyr Thr Ser Pro Pro Thr
1 5
<210> 54
<211> 207
<212> PRT
<213> Homo sapiens
<400> 54
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr
20 25 30
Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr
35 40 45
Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys
50 55 60
Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp
65 70 75 80
His Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr
85 90 95
Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu
100 105 110
Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met
115 120 125
Ser Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu
130 135 140
Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys
145 150 155 160
Pro Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn
165 170 175
Lys Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg
180 185 190
Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile
195 200 205
<210> 55
<211> 109
<212> PRT
<213> Chimeric
<400> 55
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 56
<211> 5
<212> PRT
<213> Chimeric
<400> 56
Asp Tyr Lys Ile His
1 5
<210> 57
<211> 17
<212> PRT
<213> Chimeric
<400> 57
Tyr Phe Asn Pro Asn Ser Gly Tyr Ser Thr Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 58
<211> 11
<212> PRT
<213> Chimeric
<400> 58
Leu Ser Pro Gly Gly Tyr Tyr Val Met Asp Ala
1 5 10
<210> 59
<211> 11
<212> PRT
<213> Chimeric
<400> 59
Arg Ala Ser Gln Gly Ile Asn Asn Tyr Leu Asn
1 5 10
<210> 60
<211> 7
<212> PRT
<213> Chimeric
<400> 60
Asn Thr Asn Asn Leu Gln Thr
1 5
<210> 61
<211> 8
<212> PRT
<213> Chimeric
<400> 61
Leu Gln His Asn Ser Phe Pro Thr
1 5
<210> 62
<211> 648
<212> DNA
<213> Chimeric
<400> 62
caggccgtcg tgacccagga acccagcctg acagtgtctc ctggcggcac cgtgaccctg 60
acatgtggca gttctacagg cgccgtgacc accagcaact acgccaactg ggtgcaggaa 120
aagcccggcc aggccttcag aggactgatc ggcggcacca acaagagagc ccctggcacc 180
cctgccagat tcagcggatc tctgctggga ggaaaggccg ccctgacact gtctggcgcc 240
cagccagaag atgaggccga gtactactgc gccctgtggt acagcaacct gtgggtgttc 300
ggcggaggca ccaagctgac agtcctaggt caacccaagg ctgcccccag cgtgaccctg 360
ttccccccca gcagcgagga actgcaggcc aacaaggcca ccctggtctg cctgatcagc 420
gacttctacc caggcgccgt gaccgtggcc tggaaggccg acagcagccc cgtgaaggcc 480
ggcgtggaga ccaccacccc cagcaagcag agcaacaaca agtacgccgc cagcagctac 540
ctgagcctga cccccgagca gtggaagagc cacaggtcct acagctgcca ggtgacccac 600
gagggcagca ccgtggagaa aaccgtggcc cccaccgagt gcagctga 648
<210> 63
<211> 2916
<212> DNA
<213> Chimeric
<400> 63
cagatccagc tggtgcagag cggccctgag ctgaagaaac ccggcgagac agtgcggatc 60
agctgcaagg ccagcggcta caccttcacc gactacagca tccactgggt caagcaggcc 120
cctggcaagt gcctgaagtg gatgggctgg atcaacaccg agacaggcga gcccgcctac 180
gccgacgatt tcaagggcag attcgccttc agcctggaaa ccagcgccag caccgcctac 240
ctgcagatca acaacctgaa gaacgaggac accgccacct ttttctgcgc ccacccctac 300
gactacgacg tgctggatta ttggggccag ggcaccagcg tgaccgtgtc tagcggaggc 360
ggaggatctg gcggcggagg aagtggcgga gggggatctg ggggaggcgg atctgatacc 420
gtgctgacac agagccctgc cagcctggga gtgtccctgg gacagagagc caccatcagc 480
tgtcgggcca gcaagagcgt gtccaccagc aactacagct atatccactg gtatcagcag 540
aagcccggcc agccccccaa gctgctgatc aaatacgtgt cctacctgga aagcggcgtg 600
cccgccagat tttctggctc tggcagcggc accgacttca ccctgaacat ccaccccgtg 660
gaagaggaag atgccgccac ctactactgc cagcacagca gagagttccc ttggaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtaga 780
caggccagag tcgtgaacgg gggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg aggcggagga 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg attcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 64
<211> 1353
<212> DNA
<213> Chimeric
<400> 64
gaggtgcaat tggttgaatc tggtggtggt ctggtaaaac cgggcggttc cctgcgtctg 60
agctgcgcgg cttccggatt caccttctcc aacgcgtgga tgagctgggt tcgccaggcc 120
ccgggcaaag gcctcgagtg ggttggtcgt atcaagtcta aaactgacgg tggcaccacg 180
gattacgcgg ctccagttaa aggtcgtttt accatttccc gcgacgatag caaaaacact 240
ctgtatctgc agatgaactc tctgaaaact gaagacaccg cagtctacta ctgtactacc 300
ccgtgggaat ggtcttggta cgattattgg ggccagggca cgctggttac ggtgtcttcc 360
gctagcacca agggcccctc cgtgttcccc ctggccccca gcagcaagag caccagcggc 420
ggcacagccg ctctgggctg cctggtcaag gactacttcc ccgagcccgt gaccgtgtcc 480
tggaacagcg gagccctgac ctccggcgtg cacaccttcc ccgccgtgct gcagagttct 540
ggcctgtata gcctgagcag cgtggtcacc gtgccttcta gcagcctggg cacccagacc 600
tacatctgca acgtgaacca caagcccagc aacaccaagg tggacaagaa ggtggagccc 660
aagagctgcg acaaaactca cacatgccca ccgtgcccag cacctgaagc tgcaggggga 720
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 780
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 840
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 900
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 960
gagtacaagt gcaaggtctc caacaaagcc ctcggcgccc ccatcgagaa aaccatctcc 1020
aaagccaaag ggcagccccg agaaccacag gtgtgcaccc tgcccccatc ccgggatgag 1080
ctgaccaaga accaggtcag cctctcgtgc gcagtcaaag gcttctatcc cagcgacatc 1140
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 1200
ctggactccg acggctcctt cttcctcgtg agcaagctca ccgtggacaa gagcaggtgg 1260
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccgcttcacg 1320
cagaagagcc tctccctgtc tccgggtaaa tga 1353
<210> 65
<211> 2916
<212> DNA
<213> Chimeric
<400> 65
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtaga 780
caggccagag tcgtgaacgg gggagggggg ggaagtgggg gcggaggcag tgggggcgga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg gggcggagga 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg gttcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 66
<211> 2916
<212> DNA
<213> Chimeric
<400> 66
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg aggcggaggc 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg attcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 67
<211> 2916
<212> DNA
<213> Chimeric
<400> 67
cagatccagc tggtgcagag cggccctgag ctgaagaaac ccggcgagac agtgcggatc 60
agctgcaagg ccagcggcta caccttcacc gactacagca tccactgggt caagcaggcc 120
cctggcaagt gcctgaagtg gatgggctgg atcaacaccg agacaggcga gcccgcctac 180
gccgacgatt tcaagggcag attcgccttc agcctggaaa ccagcgccag caccgcctac 240
ctgcagatca acaacctgaa gaacgaggac accgccacct ttttctgcgc ccacccctac 300
gactacgacg tgctggatta ttggggccag ggcaccagcg tgaccgtgtc tagcggaggc 360
ggaggatctg gcggcggagg aagtggcgga gggggatctg ggggaggcgg atctgatacc 420
gtgctgacac agagccctgc cagcctggga gtgtccctgg gacagagagc caccatcagc 480
tgtcgggcca gcaagagcgt gtccaccagc aactacagct atatccactg gtatcagcag 540
aagcccggcc agccccccaa gctgctgatc aaatacgtgt cctacctgga aagcggcgtg 600
cccgccagat tttctggctc tggcagcggc accgacttca ccctgaacat ccaccccgtg 660
gaagaggaag atgccgccac ctactactgc cagcacagca gagagttccc ttggaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg aggcggaggc 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg attcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 68
<211> 99
<212> DNA
<213> Chimeric
<400> 68
ggcgggggag gctccggagg cggcggaagt agacaggcca gagtcgtgaa cgggggaggg 60
gggggaagtg ggggcggagg cagtgggggc ggaggatcc 99
<210> 69
<211> 1350
<212> DNA
<213> Chimeric
<400> 69
caggtgcagc tggtccagag cggcgccgag gtgaagaaac ccgggtcctc tgtcaaggtg 60
tcatgcaagg ctagcggatt cacctttaca gactacaaaa tccactgggt taggcaggca 120
cctggccaag gactcgaatg gatggggtat ttcaacccaa attccggcta ctctacctat 180
gcccagaagt ttcagggaag agtgactatt acagctgata agagtaccag cactgcatac 240
atggagctgt cctctcttcg ctcagaggac accgccgtct actattgtgc tcggctgagc 300
cccggtggct actatgtgat ggatgcatgg gggcagggaa caaccgtaac agtgtcctct 360
gcgtcgacta agggcccttc agtttttcca ctcgccccca gtagcaagtc cacatctggg 420
ggtaccgctg ccctgggctg ccttgtgaaa gactatttcc ctgaaccagt cactgtgtca 480
tggaatagcg gagccctgac ctccggtgta cacacattcc ccgctgtgtt gcagtctagt 540
ggcctgtaca gcctctcctc tgttgtgacc gtcccttcaa gctccctggg gacacagacc 600
tatatctgta acgtgaatca taagccatct aacactaaag tagataaaaa agtggagccc 660
aagagttgcg acaaaacaca cacctgtccc ccttgcccag cccccgagct tctgggaggc 720
cctagcgtct ttctcttccc acccaagcct aaggatactc tgatgatatc caggacccca 780
gaagttacat gcgtggtcgt ggacgtctca cacgaggacc ccgaagtgaa atttaactgg 840
tacgttgatg gtgtggaagt ccataatgcc aagaccaagc ctagagagga gcaatacaac 900
agtacatatc gcgtggtaag cgtgttgacc gttctccacc aggactggct caatgggaaa 960
gaatacaagt gtaaagtgtc caacaaagct ctgccagcac ccatcgagaa gactatttct 1020
aaggccaaag gccagccccg ggagcctcag gtctatacac ttccaccctc aagggatgaa 1080
ctgaccaaga accaagtgag cttgacttgc ctggtaaagg ggttctaccc ttccgacatc 1140
gctgtggagt gggagtctaa tggacaacca gaaaacaatt acaaaaccac accccctgtc 1200
ctcgacagtg atggcagctt tttcctgtat agcaaactta ccgttgacaa gtccagatgg 1260
cagcagggaa acgtgttctc atgtagcgtc atgcacgaag ctttgcataa ccactacaca 1320
cagaaaagcc tcagcctgag tccagggaag 1350
<210> 70
<211> 639
<212> DNA
<213> Chimeric
<400> 70
gacatccaaa tgacccagtc acctagtagc ctctccgcct ctgttggcga cagggtgaca 60
attacatgca gagcttcaca gggtatcaac aattacctga actggtatca gcagaaacca 120
gggaaggccc ccaagcgctt gatatataac accaataacc tgcaaactgg cgtccctagc 180
cggttctccg gatctggtag tggcaccgaa tttacactca ccatcagctc cctgcagcca 240
gaggatttcg ccacatacta ttgtcttcag cataattctt tccccacctt tgggcaagga 300
actaaactgg agattaagcg tactgtcgcc gctccctctg tgttcatttt tcctccaagt 360
gatgagcagc tcaaaagcgg taccgcatcc gttgtgtgcc tgcttaacaa cttctatccc 420
cgggaagcca aggtccaatg gaaggtggac aatgctctgc agtcaggaaa cagtcaggag 480
agcgtaaccg agcaggattc caaagactct acttactcat tgagctccac cctgacactc 540
tctaaggcag actatgaaaa gcataaagtg tacgcctgtg aggttaccca ccagggcctg 600
agtagccctg tgacaaagtc cttcaatagg ggagagtgc 639
<210> 71
<211> 1476
<212> DNA
<213> Chimeric
<400> 71
gaggttcagc tggagcagtc aggacctgtg ctggtgaagc ctgggacttc agtgaagatg 60
tcctgtaagg cttctggata cacattcact gactactata taaactggat aatacagagc 120
catggaaagt gtcttgagtg gattggagtt attaatcctg acagcggtgg tactgactac 180
aaccagaact tcaagggcaa ggccacattg actgttgaca agtcctccac cacagcctac 240
atggaactca ctagcctgac atctgaggac tctgcagtct attattgtgc aagaagggat 300
tcttacggct ttgactactg gggccaaggc accactctca cagtctcctc aggcggaggt 360
ggctcagggg gaggcggtag cggcggaggt ggctcagggg gaggcggtag cgacattgtg 420
ctgacccaga ctcccaaatt cctgcttgtg ccagcaggag acaggattac catgacctgc 480
aaggccagtc tgagtgtgac taatgatgta gcttggtatc aacagaaacc agggcagtct 540
cctaaactgc tgttatacta tgcatccaat cgcaacgctg gagtccctga tcgcttcact 600
ggcagtggat atgggacgga tttcactttc accatcacca ctttgcaggc tgaagacctg 660
gcagtttatt tctgtcagca ggattatacc tctcctccga cgttcggttg tggcaccaag 720
ctagaaatcc gtggtggcgg cggttctggc ggagggggtt ctggccccct ggggctatgg 780
agccagggtg gcggcggttc tggcggaggg ggttctggcg gtggtggctc tggcggtgac 840
atccaaatga cccagtcacc tagtagcctc tccgcctctg ttggcgacag ggtgacaatt 900
acatgcagag cttcacaggg tatcaacaat tacctgaact ggtatcagca gaaaccaggg 960
aaggccccca agcgcttgat atataacacc aataacctgc aaactggcgt ccctagccgg 1020
ttctccggat ctggtagtgg caccgaattt acactcacca tcagctccct gcagccagag 1080
gatttcgcca catactattg tcttcagcat aattctttcc ccacctttgg gcaaggaact 1140
aaactggaga ttaagcgtac tgtcgccgct ccctctgtgt tcatttttcc tccaagtgat 1200
gagcagctca aaagcggtac cgcatccgtt gtgtgcctgc ttaacaactt ctatccccgg 1260
gaagccaagg tccaatggaa ggtggacaat gctctgcagt caggaaacag tcaggagagc 1320
gtaaccgagc aggattccaa agactctact tactcattga gctccaccct gacactctct 1380
aaggcagact atgaaaagca taaagtgtac gcctgtgagg ttacccacca gggcctgagt 1440
agccctgtga caaagtcctt caatagggga gagtgc 1476
<210> 72
<211> 971
<212> PRT
<213> Chimeric
<400> 72
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Val His
245 250 255
Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val Asn Gly
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 73
<211> 689
<212> PRT
<213> Chimeric
<400> 73
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Pro Trp Glu Trp Ser Trp Tyr Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
225 230 235 240
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
245 250 255
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
260 265 270
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
275 280 285
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
290 295 300
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
305 310 315 320
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
325 330 335
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
340 345 350
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
355 360 365
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
370 375 380
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
385 390 395 400
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
405 410 415
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
420 425 430
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
435 440 445
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
450 455 460
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
465 470 475 480
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
485 490 495
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
500 505 510
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
515 520 525
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
530 535 540
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
545 550 555 560
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys
565 570 575
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
580 585 590
Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp
595 600 605
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
610 615 620
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
625 630 635 640
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
645 650 655
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
660 665 670
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
675 680 685
Lys
<210> 74
<211> 497
<212> PRT
<213> Chimeric
<400> 74
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Arg Gln Ala Arg Val Val Asn Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Lys Ala Ala Pro Ser Val
385 390 395 400
Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln Ala Asn Lys Ala Thr
405 410 415
Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly Ala Val Thr Val Ala
420 425 430
Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly Val Glu Thr Thr Thr
435 440 445
Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala Ser Ser Tyr Leu Ser
450 455 460
Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser Tyr Ser Cys Gln Val
465 470 475 480
Thr His Glu Gly Ser Thr Val Glu Lys Thr Val Ala Pro Thr Glu Cys
485 490 495
Ser
<210> 75
<211> 497
<212> PRT
<213> Chimeric
<400> 75
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Lys Ala Ala Pro Ser Val
385 390 395 400
Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln Ala Asn Lys Ala Thr
405 410 415
Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly Ala Val Thr Val Ala
420 425 430
Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly Val Glu Thr Thr Thr
435 440 445
Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala Ser Ser Tyr Leu Ser
450 455 460
Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser Tyr Ser Cys Gln Val
465 470 475 480
Thr His Glu Gly Ser Thr Val Glu Lys Thr Val Ala Pro Thr Glu Cys
485 490 495
Ser
<210> 76
<211> 674
<212> PRT
<213> Chimeric
<400> 76
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Gly
210 215 220
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln Glu
225 230 235 240
Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys Gly
245 250 255
Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val Gln
260 265 270
Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn Lys
275 280 285
Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly Gly
290 295 300
Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala Glu
305 310 315 320
Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly Gly
325 330 335
Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
340 345 350
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
355 360 365
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
370 375 380
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
385 390 395 400
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
405 410 415
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
420 425 430
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
435 440 445
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
450 455 460
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
465 470 475 480
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
485 490 495
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
500 505 510
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
515 520 525
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
530 535 540
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu
545 550 555 560
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
565 570 575
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
580 585 590
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
595 600 605
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
610 615 620
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
625 630 635 640
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
645 650 655
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
660 665 670
Gly Lys
<210> 77
<211> 449
<212> PRT
<213> Chimeric
<400> 77
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 78
<211> 213
<212> PRT
<213> Chimeric
<400> 78
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Lys His Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Arg Lys Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 79
<211> 514
<212> PRT
<213> Chimeric
<400> 79
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Val His
245 250 255
Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val Asn Gly
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Val Ala Ala Pro Ser Val Phe
405 410 415
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
420 425 430
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
435 440 445
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
450 455 460
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
465 470 475 480
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
485 490 495
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
500 505 510
Glu Cys
<210> 80
<211> 514
<212> PRT
<213> Chimeric
<400> 80
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Val Ala Ala Pro Ser Val Phe
405 410 415
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
420 425 430
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
435 440 445
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
450 455 460
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
465 470 475 480
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
485 490 495
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
500 505 510
Glu Cys
<210> 81
<211> 232
<212> PRT
<213> Chimeric
<400> 81
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Val
115 120 125
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys
130 135 140
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
145 150 155 160
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
165 170 175
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
180 185 190
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
195 200 205
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
210 215 220
Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 82
<211> 956
<212> PRT
<213> Chimeric
<400> 82
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Val His
245 250 255
Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val Asn Gly
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Val
500 505 510
Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser
515 520 525
Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
530 535 540
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Leu Ile Thr Pro
545 550 555 560
Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe Arg Gly Lys Ala Thr
565 570 575
Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser
580 585 590
Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Tyr
595 600 605
Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
610 615 620
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
625 630 635 640
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Glu
645 650 655
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
660 665 670
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
675 680 685
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
690 695 700
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
705 710 715 720
Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
725 730 735
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
740 745 750
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
755 760 765
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
770 775 780
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
785 790 795 800
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
805 810 815
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
820 825 830
Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
835 840 845
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
850 855 860
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
865 870 875 880
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
885 890 895
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
900 905 910
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
915 920 925
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
930 935 940
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 83
<211> 956
<212> PRT
<213> Chimeric
<400> 83
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Val
500 505 510
Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser
515 520 525
Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
530 535 540
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Leu Ile Thr Pro
545 550 555 560
Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe Arg Gly Lys Ala Thr
565 570 575
Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser
580 585 590
Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Tyr
595 600 605
Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
610 615 620
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
625 630 635 640
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Glu
645 650 655
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
660 665 670
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
675 680 685
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
690 695 700
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
705 710 715 720
Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
725 730 735
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
740 745 750
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
755 760 765
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
770 775 780
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
785 790 795 800
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
805 810 815
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
820 825 830
Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
835 840 845
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
850 855 860
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
865 870 875 880
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
885 890 895
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
900 905 910
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
915 920 925
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
930 935 940
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 84
<211> 674
<212> PRT
<213> Chimeric
<400> 84
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Ser Ser Ala
100 105 110
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
115 120 125
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
130 135 140
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
145 150 155 160
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
165 170 175
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
180 185 190
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
195 200 205
Val Glu Pro Lys Ser Cys Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly
210 215 220
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
225 230 235 240
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly
245 250 255
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
260 265 270
Met Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys
275 280 285
Phe Arg Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val
290 295 300
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
305 310 315 320
Cys Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln
325 330 335
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
340 345 350
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
355 360 365
Leu Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
370 375 380
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
385 390 395 400
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
405 410 415
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
420 425 430
Pro Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp
435 440 445
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
450 455 460
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
465 470 475 480
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
485 490 495
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
500 505 510
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
515 520 525
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
530 535 540
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu
545 550 555 560
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
565 570 575
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
580 585 590
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
595 600 605
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
610 615 620
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
625 630 635 640
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
645 650 655
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
660 665 670
Gly Lys
<210> 85
<211> 971
<212> PRT
<213> Chimeric
<400> 85
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Phe Val Gly Gly Thr Gly Gly Gly
260 265 270
Gly Ser Gly Gly Gly Gly Ser Gly Gly Ser Glu Val Gln Leu Leu Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Arg Ile Arg Ser Lys
325 330 335
Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
370 375 380
Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
385 390 395 400
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
405 410 415
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
420 425 430
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
435 440 445
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
450 455 460
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
465 470 475 480
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
485 490 495
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Gly
500 505 510
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
515 520 525
Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
530 535 540
Ala Ser Gly Phe Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln
545 550 555 560
Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr
565 570 575
Asp Gly Gly Thr Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr
580 585 590
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
595 600 605
Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Thr Pro Trp Glu
610 615 620
Trp Ser Trp Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
625 630 635 640
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
645 650 655
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
660 665 670
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
675 680 685
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
690 695 700
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
705 710 715 720
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
725 730 735
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
740 745 750
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
755 760 765
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
770 775 780
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
785 790 795 800
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
805 810 815
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
820 825 830
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
835 840 845
Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
850 855 860
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
865 870 875 880
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
885 890 895
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
900 905 910
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
915 920 925
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
930 935 940
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
945 950 955 960
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
965 970
<210> 86
<211> 33
<212> PRT
<213> Chimeric
<400> 86
Gly Gly Gly Gly Ser Val His Met Pro Leu Gly Phe Leu Gly Pro Arg
1 5 10 15
Gln Ala Arg Val Val Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser
<210> 87
<211> 35
<212> PRT
<213> Chimeric
<400> 87
Gly Gly Gly Gly Ser Val His Met Pro Leu Gly Phe Leu Gly Pro Arg
1 5 10 15
Gln Ala Arg Val Val Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser Gly Gly
35
<210> 88
<211> 33
<212> PRT
<213> Chimeric
<400> 88
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Phe
1 5 10 15
Val Gly Gly Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 89
<211> 33
<212> PRT
<213> Chimeric
<400> 89
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Lys Lys Ala Ala Pro Val
1 5 10 15
Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser
<210> 90
<211> 33
<212> PRT
<213> Chimeric
<400> 90
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Pro Met Ala Lys Lys Val
1 5 10 15
Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser
<210> 91
<211> 33
<212> PRT
<213> Chimeric
<400> 91
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Arg Ala Lys Val
1 5 10 15
Asn Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Ser
<210> 92
<211> 33
<212> PRT
<213> Chimeric
<400> 92
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Val His Met Pro Leu Gly
1 5 10 15
Phe Leu Gly Pro Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 93
<211> 33
<212> PRT
<213> Chimeric
<400> 93
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Arg Ala Lys Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 94
<211> 33
<212> PRT
<213> Chimeric
<400> 94
Gly Gly Gly Gly Ser Val His Met Pro Leu Gly Phe Leu Gly Pro Pro
1 5 10 15
Met Ala Lys Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 95
<211> 33
<212> PRT
<213> Chimeric
<400> 95
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Lys Lys Ala Ala Pro Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 96
<211> 33
<212> PRT
<213> Chimeric
<400> 96
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Pro Met Ala Lys Lys Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Ser
<210> 97
<211> 18
<212> PRT
<213> Chimeric
<400> 97
Val His Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val
1 5 10 15
Asn Gly
<210> 98
<211> 6
<212> PRT
<213> Chimeric
<400> 98
Phe Val Gly Gly Thr Gly
1 5
<210> 99
<211> 8
<212> PRT
<213> Chimeric
<400> 99
Lys Lys Ala Ala Pro Val Asn Gly
1 5
<210> 100
<211> 8
<212> PRT
<213> Chimeric
<400> 100
Pro Met Ala Lys Lys Val Asn Gly
1 5
<210> 101
<211> 8
<212> PRT
<213> Chimeric
<400> 101
Gln Ala Arg Ala Lys Val Asn Gly
1 5
<210> 102
<211> 10
<212> PRT
<213> Chimeric
<400> 102
Val His Met Pro Leu Gly Phe Leu Gly Pro
1 5 10
<210> 103
<211> 5
<212> PRT
<213> Chimeric
<400> 103
Gln Ala Arg Ala Lys
1 5
<210> 104
<211> 15
<212> PRT
<213> Chimeric
<400> 104
Val His Met Pro Leu Gly Phe Leu Gly Pro Pro Met Ala Lys Lys
1 5 10 15
<210> 105
<211> 5
<212> PRT
<213> Chimeric
<400> 105
Lys Lys Ala Ala Pro
1 5
<210> 106
<211> 5
<212> PRT
<213> Chimeric
<400> 106
Pro Met Ala Lys Lys
1 5
<210> 107
<211> 5
<212> PRT
<213> Chimeric
<400> 107
Gly Tyr Thr Met Asn
1 5
<210> 108
<211> 17
<212> PRT
<213> Chimeric
<400> 108
Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe Arg
1 5 10 15
Gly
<210> 109
<211> 10
<212> PRT
<213> Chimeric
<400> 109
Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr
1 5 10
<210> 110
<211> 10
<212> PRT
<213> Chimeric
<400> 110
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 111
<211> 7
<212> PRT
<213> Chimeric
<400> 111
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 112
<211> 9
<212> PRT
<213> Chimeric
<400> 112
Gln Gln Trp Ser Lys His Pro Leu Thr
1 5
<210> 113
<211> 119
<212> PRT
<213> Chimeric
<400> 113
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 114
<211> 106
<212> PRT
<213> Chimeric
<400> 114
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Lys His Pro Leu Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 115
<211> 120
<212> PRT
<213> Chimeric
<400> 115
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Thr Asp Tyr
20 25 30
Lys Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Tyr Phe Asn Pro Asn Ser Gly Tyr Ser Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Ser Pro Gly Gly Tyr Tyr Val Met Asp Ala Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 116
<211> 106
<212> PRT
<213> Chimeric
<400> 116
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Asn Thr Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Phe Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 117
<211> 648
<212> DNA
<213> Chimeric
<400> 117
caggccgtcg tgacccagga acccagcctg acagtgtctc ctggcggcac cgtgaccctg 60
acatgtggca gttctacagg cgccgtgacc accagcaact acgccaactg ggtgcaggaa 120
aagcccggcc aggccttcag aggactgatc ggcggcacca acaagagagc ccctggcacc 180
cctgccagat tcagcggatc tctgctggga ggaaaggccg ccctgacact gtctggcgcc 240
cagccagaag atgaggccga gtactactgc gccctgtggt acagcaacct gtgggtgttc 300
ggcggaggca ccaagctgac agtcctaggt caacccaagg ctgcccccag cgtgaccctg 360
ttccccccca gcagcgagga actgcaggcc aacaaggcca ccctggtctg cctgatcagc 420
gacttctacc caggcgccgt gaccgtggcc tggaaggccg acagcagccc cgtgaaggcc 480
ggcgtggaga ccaccacccc cagcaagcag agcaacaaca agtacgccgc cagcagctac 540
ctgagcctga cccccgagca gtggaagagc cacaggtcct acagctgcca ggtgacccac 600
gagggcagca ccgtggagaa aaccgtggcc cccaccgagt gcagctga 648
<210> 118
<211> 2916
<212> DNA
<213> Chimeric
<400> 118
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaagga ggcggcggaa gtgtgcacat gcccctgggc 780
ttcctgggcc ccagacaggc cagagtcgtg aacggggggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg gggcggagga 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg gttcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 119
<211> 2070
<212> DNA
<213> Chimeric
<400> 119
gaggtgcaat tggttgaatc tggtggtggt ctggtaaaac cgggcggttc cctgcgtctg 60
agctgcgcgg cttccggatt caccttctcc aacgcgtgga tgagctgggt tcgccaggcc 120
ccgggcaaag gcctcgagtg ggttggtcgt atcaagtcta aaactgacgg tggcaccacg 180
gattacgcgg ctccagttaa aggtcgtttt accatttccc gcgacgatag caaaaacact 240
ctgtatctgc agatgaactc tctgaaaact gaagacaccg cagtctacta ctgtactacc 300
ccgtgggaat ggtcttggta cgattattgg ggccagggca cgctggttac ggtgtcttcc 360
gctagcacaa agggccctag cgtgttccct ctggccccca gcagcaagag cacaagcggc 420
ggaacagccg ccctgggctg cctcgtgaag gactacttcc ccgagcccgt gacagtgtct 480
tggaacagcg gagccctgac aagcggcgtg cacactttcc ctgccgtgct gcagagcagc 540
ggcctgtact ccctgagcag cgtggtcacc gtgcctagca gcagcctggg cacccagacc 600
tacatctgca acgtgaacca caagcccagc aacaccaaag tggacaagaa ggtggagccc 660
aagagctgtg atggcggagg agggtccgga ggcggaggat ccgaggtgca gctgctggaa 720
tctggcggcg gactggtgca gcctggcgga tctctgagac tgagctgtgc cgccagcggc 780
ttcaccttca gcacctacgc catgaactgg gtgcgccagg cccctggcaa aggcctggaa 840
tgggtgtccc ggatcagaag caagtacaac aactacgcca cctactacgc cgacagcgtg 900
aagggccggt tcaccatcag ccgggacgac agcaagaaca ccctgtacct gcagatgaac 960
agcctgcggg ccgaggacac cgccgtgtac tattgtgtgc ggcacggcaa cttcggcaac 1020
agctatgtgt cttggtttgc ctactggggc cagggcaccc tcgtgaccgt gtcaagcgct 1080
agtaccaagg gccccagcgt gttccccctg gcacccagca gcaagagcac atctggcgga 1140
acagccgctc tgggctgtct ggtgaaagac tacttccccg agcccgtgac cgtgtcttgg 1200
aactctggcg ccctgaccag cggcgtgcac acctttccag ccgtgctgca gagcagcggc 1260
ctgtactccc tgtcctccgt ggtcaccgtg ccctctagct ccctgggaac acagacatat 1320
atctgtaatg tcaatcacaa gccttccaac accaaagtcg ataagaaagt cgagcccaag 1380
agctgcgaca aaactcacac atgcccaccg tgcccagcac ctgaagctgc agggggaccg 1440
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 1500
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 1560
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 1620
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 1680
tacaagtgca aggtctccaa caaagccctc ggcgccccca tcgagaaaac catctccaaa 1740
gccaaagggc agccccgaga accacaggtg tacaccctgc ccccatgccg ggatgagctg 1800
accaagaacc aggtcagcct gtggtgcctg gtcaaaggct tctatcccag cgacatcgcc 1860
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1920
gactccgacg gctccttctt cctctacagc aagctcaccg tggacaagag caggtggcag 1980
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 2040
aagagcctct ccctgtctcc gggtaaatga 2070
<210> 120
<211> 1494
<212> DNA
<213> Chimeric
<400> 120
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtaga 780
caggccagag tcgtgaacgg gggagggggg ggaagtgggg gcggaggcag tgggggcgga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtc ctaggtcaac ccaaggctgc ccccagcgtg 1200
accctgttcc cccccagcag cgaggaactg caggccaaca aggccaccct ggtctgcctg 1260
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 1320
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 1380
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 1440
acccacgagg gcagcaccgt ggagaaaacc gtggccccca ccgagtgcag ctga 1494
<210> 121
<211> 1494
<212> DNA
<213> Chimeric
<400> 121
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtc ctaggtcaac ccaaggctgc ccccagcgtg 1200
accctgttcc cccccagcag cgaggaactg caggccaaca aggccaccct ggtctgcctg 1260
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 1320
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 1380
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 1440
acccacgagg gcagcaccgt ggagaaaacc gtggccccca ccgagtgcag ctga 1494
<210> 122
<211> 2025
<212> DNA
<213> Chimeric
<400> 122
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac caggcgccag cgtgaaggtg 60
tcctgcaagg ccagcggcta cagcttcacc ggctacacca tgaactgggt gcgccaggct 120
cctggacagg gcctggaatg gatgggcctg atcaccccct acaacggcgc cagcagctac 180
aaccagaagt tccggggcaa ggccaccatg accgtggaca ccagcacctc caccgtgtat 240
atggaactga gcagcctgcg gagcgaggac accgccgtgt actattgtgc cagaggcggc 300
tacgacggca gaggcttcga ttattggggc cagggcaccc tcgtgaccgt gtcctctgct 360
agcaccaagg gcccctccgt gtttcctctg gccccttcca gcaagtccac ctctggcgga 420
actgccgctc tgggctgcct ggtggaagat tacttccccg agcccgtgac cgtgtcctgg 480
aattctggcg ctctgacctc cggcgtgcac acctttccag ctgtgctgca gtcctccggc 540
ctgtactccc tgtcctccgt cgtgacagtg ccctccagct ctctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gccctccaac accaaggtgg acgagaaggt ggaacccaag 660
tcctgcgacg gtggcggagg ttccggaggc ggaggatccc aggctgtcgt gacccaggaa 720
ccctccctga cagtgtctcc tggcggcacc gtgaccctga cctgtggatc ttctaccggc 780
gctgtgacca cctccaacta cgccaattgg gtgcaggaaa agcccggcca ggccttcaga 840
ggactgatcg gcggcaccaa caagagagcc cctggcaccc ctgccagatt ctccggttct 900
ctgctgggcg gcaaggctgc cctgactctg tctggtgctc agcctgagga cgaggccgag 960
tactactgcg ccctgtggta ctccaacctg tgggtgttcg gcggaggcac caagctgacc 1020
gtgctgtcca gcgcttccac caagggaccc agtgtgttcc ccctggcccc cagctccaag 1080
tctacatccg gtggcacagc tgccctggga tgtctcgtga aggactactt tcctgagcct 1140
gtgacagtgt cttggaacag cggagccctg accagcggag tgcacacatt ccctgcagtg 1200
ctgcagagca gcggcctgta tagcctgagc agcgtcgtga ccgtgccttc ctctagcctg 1260
ggaacacaga catatatctg taatgtgaat cataagccca gtaataccaa agtggataag 1320
aaagtggaac ctaagagctg cgataagacc cacacctgtc ccccctgccc tgctcctgaa 1380
gctgctggtg gccctagcgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 1440
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 1500
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 1560
gaacagtaca actccaccta ccgggtggtg tccgtgctga cagtgctgca ccaggactgg 1620
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgggcgc tcccatcgaa 1680
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac cctgccccca 1740
tgccgggatg agctgaccaa gaaccaggtc agcctgtggt gcctggtcaa aggcttctat 1800
cccagcgaca tcgccgtgga gtgggagagc aatgggcagc cggagaacaa ctacaagacc 1860
acgcctcccg tgctggactc cgacggctcc ttcttcctct acagcaagct caccgtggac 1920
aagagcaggt ggcagcaggg gaacgtcttc tcatgctccg tgatgcatga ggctctgcac 1980
aaccactaca cgcagaagag cctctccctg tctccgggta aatga 2025
<210> 123
<211> 1350
<212> DNA
<213> Chimeric
<400> 123
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac caggcgccag cgtgaaggtg 60
tcctgcaagg ccagcggcta cagcttcacc ggctacacca tgaactgggt gcgccaggct 120
cctggacagg gcctggaatg gatgggcctg atcaccccct acaacggcgc cagcagctac 180
aaccagaagt tccggggcaa ggccaccatg accgtggaca ccagcacctc caccgtgtat 240
atggaactga gcagcctgcg gagcgaggac accgccgtgt actattgtgc cagaggcggc 300
tacgacggca gaggcttcga ttattggggc cagggcaccc tcgtgaccgt gtcctctgct 360
agcaccaagg gcccctccgt gttccccctg gcccccagca gcaagagcac cagcggcggc 420
acagccgctc tgggctgcct ggtcgaggac tacttccccg agcccgtgac cgtgtcctgg 480
aacagcggag ccctgacctc cggcgtgcac accttccccg ccgtgctgca gagttctggc 540
ctgtatagcc tgagcagcgt ggtcaccgtg ccttctagca gcctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gcccagcaac accaaggtgg acgagaaggt ggagcccaag 660
agctgcgaca aaactcacac atgcccaccg tgcccagcac ctgaagctgc agggggaccg 720
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 780
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 840
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 900
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 960
tacaagtgca aggtctccaa caaagccctc ggcgccccca tcgagaaaac catctccaaa 1020
gccaaagggc agccccgaga accacaggtg tgcaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct ctcgtgcgca gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gctccttctt cctcgtgagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 1320
aagagcctct ccctgtctcc gggtaaatga 1350
<210> 124
<211> 642
<212> DNA
<213> Chimeric
<400> 124
gacatccaga tgacccagag ccccagcagc ctgtctgcca gcgtgggcga cagagtgacc 60
atcacctgta gcgccagcag cagcgtgtcc tacatgcact ggtatcagca gaagtccggc 120
aaggccccca agctgctgat ctacgacacc agcaagctgg cctccggcgt gcccagcaga 180
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct ccagcccgag 240
gacttcgcca cctactactg ccagcagtgg tccaagcacc ccctgacctt tggccagggc 300
accaagctgg aaatcaagcg tacggtggct gcaccatctg tcttcatctt cccgccatct 360
gatcggaagt tgaaatctgg aactgcctct gttgtgtgcc tgctgaataa cttctatccc 420
agagaggcca aagtacagtg gaaggtggat aacgccctcc aatcgggtaa ctcccaggag 480
agtgtcacag agcaggacag caaggacagc acctacagcc tcagcagcac cctgacgctg 540
agcaaagcag actacgagaa acacaaagtc tacgcctgcg aagtcaccca tcagggcctg 600
agctcgcccg tcacaaagag cttcaacagg ggagagtgtt ag 642
<210> 125
<211> 1545
<212> DNA
<213> Chimeric
<400> 125
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaagga ggcggcggaa gtgtgcacat gcccctgggc 780
ttcctgggcc ccagacaggc cagagtcgtg aacggggggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcgtg gccgctccct ccgtgttcat cttcccacct 1260
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 1320
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caacagccag 1380
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 1440
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 1500
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gctga 1545
<210> 126
<211> 1545
<212> DNA
<213> Chimeric
<400> 126
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcgtg gccgctccct ccgtgttcat cttcccacct 1260
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 1320
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caacagccag 1380
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 1440
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 1500
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gctga 1545
<210> 127
<211> 699
<212> DNA
<213> Chimeric
<400> 127
gaagtgcagc tgctggaatc cggcggagga ctggtgcagc ctggcggatc tctgagactg 60
tcttgtgccg cctccggctt caccttctcc acctacgcca tgaactgggt gcgacaggct 120
cctggcaagg gcctggaatg ggtgtcccgg atcagatcca agtacaacaa ctacgccacc 180
tactacgccg actccgtgaa gggccggttc accatctctc gggacgactc caagaacacc 240
ctgtacctgc agatgaactc cctgcgggcc gaggacaccg ccgtgtacta ttgtgtgcgg 300
cacggcaact tcggcaactc ctatgtgtct tggtttgcct actggggcca gggcaccctc 360
gtgaccgtgt catctgctag cgtggccgct ccctccgtgt tcatcttccc accttccgac 420
gagcagctga agtccggcac cgcttctgtc gtgtgcctgc tgaacaactt ctacccccgc 480
gaggccaagg tgcagtggaa ggtggacaac gccctgcagt ccggcaacag ccaggaatcc 540
gtgaccgagc aggactccaa ggacagcacc tactccctgt cctccaccct gaccctgtcc 600
aaggccgact acgagaagca caaggtgtac gcctgcgaag tgacccacca gggcctgtct 660
agccccgtga ccaagtcttt caaccggggc gagtgctga 699
<210> 128
<211> 2871
<212> DNA
<213> Chimeric
<400> 128
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaagga ggcggcggaa gtgtgcacat gcccctgggc 780
ttcctgggcc ccagacaggc cagagtcgtg aacggggggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtg ctgagcagcg cttccaccaa gggacccagt 1200
gtgttccccc tggcccccag ctccaagtct acatccggtg gcacagctgc cctgggatgt 1260
ctcgtgaagg actactttcc tgagcctgtg acagtgtctt ggaacagcgg agccctgacc 1320
agcggagtgc acacattccc tgcagtgctg cagagcagcg gcctgtatag cctgagcagc 1380
gtcgtgaccg tgccttcctc tagcctggga acacagacat atatctgtaa tgtgaatcat 1440
aagcccagta ataccaaagt ggataagaaa gtggaaccta agagctgcga tggcggagga 1500
gggtccggag gcggagggtc ccaggtgcag ctggtgcagt ctggcgccga agtgaagaaa 1560
ccaggcgcca gcgtgaaggt gtcctgcaag gccagcggct acagcttcac cggctacacc 1620
atgaactggg tgcgccaggc tcctggacag ggcctggaat ggatgggcct gatcaccccc 1680
tacaacggcg ccagcagcta caaccagaag ttccggggca aggccaccat gaccgtggac 1740
accagcacct ccaccgtgta tatggaactg agcagcctgc ggagcgagga caccgccgtg 1800
tactattgtg ccagaggcgg ctacgacggc agaggcttcg attattgggg ccagggcacc 1860
ctcgtgaccg tgtcctctgc tagcaccaag ggcccctccg tgttccccct ggcccccagc 1920
agcaagagca ccagcggcgg cacagccgct ctgggctgcc tggtcgagga ctacttcccc 1980
gagcccgtga ccgtgtcctg gaacagcgga gccctgacct ccggcgtgca caccttcccc 2040
gccgtgctgc agagttctgg cctgtatagc ctgagcagcg tggtcaccgt gccttctagc 2100
agcctgggca cccagaccta catctgcaac gtgaaccaca agcccagcaa caccaaggtg 2160
gacgagaagg tggagcccaa gagctgcgac aaaactcaca catgcccacc gtgcccagca 2220
cctgaagctg cagggggacc gtcagtcttc ctcttccccc caaaacccaa ggacaccctc 2280
atgatctccc ggacccctga ggtcacatgc gtggtggtgg acgtgagcca cgaagaccct 2340
gaggtcaagt tcaactggta cgtggacggc gtggaggtgc ataatgccaa gacaaagccg 2400
cgggaggagc agtacaacag cacgtaccgt gtggtcagcg tcctcaccgt cctgcaccag 2460
gactggctga atggcaagga gtacaagtgc aaggtctcca acaaagccct cggcgccccc 2520
atcgagaaaa ccatctccaa agccaaaggg cagccccgag aaccacaggt gtacaccctg 2580
cccccatgcc gggatgagct gaccaagaac caggtcagcc tgtggtgcct ggtcaaaggc 2640
ttctatccca gcgacatcgc cgtggagtgg gagagcaatg ggcagccgga gaacaactac 2700
aagaccacgc ctcccgtgct ggactccgac ggctccttct tcctctacag caagctcacc 2760
gtggacaaga gcaggtggca gcaggggaac gtcttctcat gctccgtgat gcatgaggct 2820
ctgcacaacc actacacgca gaagagcctc tccctgtctc cgggtaaatg a 2871
<210> 129
<211> 2871
<212> DNA
<213> Chimeric
<400> 129
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtg ctgagcagcg cttccaccaa gggacccagt 1200
gtgttccccc tggcccccag ctccaagtct acatccggtg gcacagctgc cctgggatgt 1260
ctcgtgaagg actactttcc tgagcctgtg acagtgtctt ggaacagcgg agccctgacc 1320
agcggagtgc acacattccc tgcagtgctg cagagcagcg gcctgtatag cctgagcagc 1380
gtcgtgaccg tgccttcctc tagcctggga acacagacat atatctgtaa tgtgaatcat 1440
aagcccagta ataccaaagt ggataagaaa gtggaaccta agagctgcga tggcggagga 1500
gggtccggag gcggagggtc ccaggtgcag ctggtgcagt ctggcgccga agtgaagaaa 1560
ccaggcgcca gcgtgaaggt gtcctgcaag gccagcggct acagcttcac cggctacacc 1620
atgaactggg tgcgccaggc tcctggacag ggcctggaat ggatgggcct gatcaccccc 1680
tacaacggcg ccagcagcta caaccagaag ttccggggca aggccaccat gaccgtggac 1740
accagcacct ccaccgtgta tatggaactg agcagcctgc ggagcgagga caccgccgtg 1800
tactattgtg ccagaggcgg ctacgacggc agaggcttcg attattgggg ccagggcacc 1860
ctcgtgaccg tgtcctctgc tagcaccaag ggcccctccg tgttccccct ggcccccagc 1920
agcaagagca ccagcggcgg cacagccgct ctgggctgcc tggtcgagga ctacttcccc 1980
gagcccgtga ccgtgtcctg gaacagcgga gccctgacct ccggcgtgca caccttcccc 2040
gccgtgctgc agagttctgg cctgtatagc ctgagcagcg tggtcaccgt gccttctagc 2100
agcctgggca cccagaccta catctgcaac gtgaaccaca agcccagcaa caccaaggtg 2160
gacgagaagg tggagcccaa gagctgcgac aaaactcaca catgcccacc gtgcccagca 2220
cctgaagctg cagggggacc gtcagtcttc ctcttccccc caaaacccaa ggacaccctc 2280
atgatctccc ggacccctga ggtcacatgc gtggtggtgg acgtgagcca cgaagaccct 2340
gaggtcaagt tcaactggta cgtggacggc gtggaggtgc ataatgccaa gacaaagccg 2400
cgggaggagc agtacaacag cacgtaccgt gtggtcagcg tcctcaccgt cctgcaccag 2460
gactggctga atggcaagga gtacaagtgc aaggtctcca acaaagccct cggcgccccc 2520
atcgagaaaa ccatctccaa agccaaaggg cagccccgag aaccacaggt gtacaccctg 2580
cccccatgcc gggatgagct gaccaagaac caggtcagcc tgtggtgcct ggtcaaaggc 2640
ttctatccca gcgacatcgc cgtggagtgg gagagcaatg ggcagccgga gaacaactac 2700
aagaccacgc ctcccgtgct ggactccgac ggctccttct tcctctacag caagctcacc 2760
gtggacaaga gcaggtggca gcaggggaac gtcttctcat gctccgtgat gcatgaggct 2820
ctgcacaacc actacacgca gaagagcctc tccctgtctc cgggtaaatg a 2871
<210> 130
<211> 2025
<212> DNA
<213> Chimeric
<400> 130
caggccgtcg tgacccagga acccagcctg acagtgtctc ctggcggcac cgtgaccctg 60
acatgtggca gttctacagg cgccgtgacc accagcaact acgccaactg ggtgcaggaa 120
aagcccggcc aggccttcag aggactgatc ggcggcacca acaagagagc ccctggcacc 180
cctgccagat tctccggttc tctgctgggc ggcaaggctg ccctgactct gtctggtgct 240
cagcctgagg acgaggccga gtactactgc gccctgtggt actccaacct gtgggtgttc 300
ggcggaggca ccaagctgac cgtgctgtcc agcgcttcca ccaagggacc cagtgtgttc 360
cccctggccc ccagctccaa gtctacatcc ggtggcacag ctgccctggg atgtctcgtg 420
aaggactact ttcctgagcc tgtgacagtg tcttggaaca gcggagccct gaccagcgga 480
gtgcacacat tccctgcagt gctgcagagc agcggcctgt atagcctgag cagcgtcgtg 540
accgtgcctt cctctagcct gggaacacag acatatatct gtaatgtgaa tcataagccc 600
agtaatacca aagtggataa gaaagtggaa cctaagagct gcgatggcgg aggagggtcc 660
ggaggcggag ggtcccaggt gcagctggtg cagtctggcg ccgaagtgaa gaaaccaggc 720
gccagcgtga aggtgtcctg caaggccagc ggctacagct tcaccggcta caccatgaac 780
tgggtgcgcc aggctcctgg acagggcctg gaatggatgg gcctgatcac cccctacaac 840
ggcgccagca gctacaacca gaagttccgg ggcaaggcca ccatgaccgt ggacaccagc 900
acctccaccg tgtatatgga actgagcagc ctgcggagcg aggacaccgc cgtgtactat 960
tgtgccagag gcggctacga cggcagaggc ttcgattatt ggggccaggg caccctcgtg 1020
accgtgtcct ctgctagcac caagggcccc tccgtgttcc ccctggcccc cagcagcaag 1080
agcaccagcg gcggcacagc cgctctgggc tgcctggtcg aggactactt ccccgagccc 1140
gtgaccgtgt cctggaacag cggagccctg acctccggcg tgcacacctt ccccgccgtg 1200
ctgcagagtt ctggcctgta tagcctgagc agcgtggtca ccgtgccttc tagcagcctg 1260
ggcacccaga cctacatctg caacgtgaac cacaagccca gcaacaccaa ggtggacgag 1320
aaggtggagc ccaagagctg cgacaaaact cacacatgcc caccgtgccc agcacctgaa 1380
gctgcagggg gaccgtcagt cttcctcttc cccccaaaac ccaaggacac cctcatgatc 1440
tcccggaccc ctgaggtcac atgcgtggtg gtggacgtga gccacgaaga ccctgaggtc 1500
aagttcaact ggtacgtgga cggcgtggag gtgcataatg ccaagacaaa gccgcgggag 1560
gagcagtaca acagcacgta ccgtgtggtc agcgtcctca ccgtcctgca ccaggactgg 1620
ctgaatggca aggagtacaa gtgcaaggtc tccaacaaag ccctcggcgc ccccatcgag 1680
aaaaccatct ccaaagccaa agggcagccc cgagaaccac aggtgtacac cctgccccca 1740
tgccgggatg agctgaccaa gaaccaggtc agcctgtggt gcctggtcaa aggcttctat 1800
cccagcgaca tcgccgtgga gtgggagagc aatgggcagc cggagaacaa ctacaagacc 1860
acgcctcccg tgctggactc cgacggctcc ttcttcctct acagcaagct caccgtggac 1920
aagagcaggt ggcagcaggg gaacgtcttc tcatgctccg tgatgcatga ggctctgcac 1980
aaccactaca cgcagaagag cctctccctg tctccgggta aatga 2025
<210> 131
<211> 2916
<212> DNA
<213> Chimeric
<400> 131
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtttcgtggg ggggaccggg ggcggaggca gtgggggggg aggatccggg 840
ggatccgagg tgcagctgct ggaatctggc ggcggactgg tgcagcctgg cggatctctg 900
agactgagct gtgccgccag cggcttcacc ttcagcacct acgccatgaa ctgggtgcgc 960
caggcccctg gcaaaggcct ggaatgggtg tcccggatca gaagcaagta caacaactac 1020
gccacctact acgccgacag cgtgaagggc cggttcacca tcagccggga cgacagcaag 1080
aacaccctgt acctgcagat gaacagcctg cgggccgagg acaccgccgt gtactattgt 1140
gtgcggcacg gcaacttcgg caacagctat gtgtcttggt ttgcctactg gggccagggc 1200
accctcgtga ccgtgtcaag cgctagcaca aagggcccta gcgtgttccc tctggccccc 1260
agcagcaaga gcacaagcgg cggaacagcc gccctgggct gcctcgtgaa ggactacttc 1320
cccgagcccg tgacagtgtc ttggaacagc ggagccctga caagcggcgt gcacaccttc 1380
cctgccgtgc tgcagagcag cggcctgtac tccctgagca gcgtggtcac cgtgcctagc 1440
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaaa 1500
gtggacaaga aggtggagcc caagagctgt gatggcggag gagggtccgg gggcggagga 1560
tccgaggtgc aattggttga atctggtggt ggtctggtaa aaccgggcgg ttccctgcgt 1620
ctgagctgcg cggcttccgg gttcaccttc tccaacgcgt ggatgagctg ggttcgccag 1680
gccccgggca aaggcctcga gtgggttggt cgtatcaagt ctaaaactga cggtggcacc 1740
acggattacg cggctccagt taaaggtcgt tttaccattt cccgcgacga tagcaaaaac 1800
actctgtatc tgcagatgaa ctctctgaaa actgaagaca ccgcagtcta ctactgtact 1860
accccgtggg aatggtcttg gtacgattat tggggccagg gcacgctggt tacggtgtct 1920
agcgctagta ccaagggccc cagcgtgttc cccctggcac ccagcagcaa gagcacatct 1980
ggcggaacag ccgctctggg ctgtctggtg aaagactact tccccgagcc cgtgaccgtg 2040
tcttggaact ctggcgccct gaccagcggc gtgcacacct ttccagccgt gctgcagagc 2100
agcggcctgt actccctgtc ctccgtggtc accgtgccct ctagctccct gggaacacag 2160
acatatatct gtaatgtcaa tcacaagcct tccaacacca aagtcgataa gaaagtcgag 2220
cccaagagct gcgacaaaac tcacacatgc ccaccgtgcc cagcacctga agctgcaggg 2280
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 2340
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 2400
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 2460
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 2520
aaggagtaca agtgcaaggt ctccaacaaa gccctcggcg cccccatcga gaaaaccatc 2580
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atgccgggat 2640
gagctgacca agaaccaggt cagcctgtgg tgcctggtca aaggcttcta tcccagcgac 2700
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 2760
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg 2820
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 2880
acgcagaaga gcctctccct gtctccgggt aaatga 2916
<210> 132
<211> 449
<212> PRT
<213> Chimeric
<400> 132
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Val Asn Arg Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Phe Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 133
<211> 214
<212> PRT
<213> Chimeric
<400> 133
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Arg Lys Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 134
<211> 675
<212> PRT
<213> Chimeric
<400> 134
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Ser Ser Ala
100 105 110
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
115 120 125
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
130 135 140
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
145 150 155 160
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
165 170 175
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
180 185 190
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
195 200 205
Val Glu Pro Lys Ser Cys Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly
210 215 220
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
225 230 235 240
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp
245 250 255
Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
260 265 270
Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser
275 280 285
Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala
290 295 300
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
305 310 315 320
Cys Ser Arg Trp Gly Gly Glu Gly Phe Tyr Ala Met Asp Tyr Trp Gly
325 330 335
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
340 345 350
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
355 360 365
Ala Leu Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val
370 375 380
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
385 390 395 400
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
405 410 415
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
420 425 430
Lys Pro Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys
435 440 445
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
450 455 460
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
465 470 475 480
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
485 490 495
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
500 505 510
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
515 520 525
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
530 535 540
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile
545 550 555 560
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
565 570 575
Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
580 585 590
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
595 600 605
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
610 615 620
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
625 630 635 640
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
645 650 655
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
660 665 670
Pro Gly Lys
675
<210> 135
<211> 957
<212> PRT
<213> Chimeric
<400> 135
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
500 505 510
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
515 520 525
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
530 535 540
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro
545 550 555 560
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
565 570 575
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
580 585 590
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
595 600 605
Glu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
610 615 620
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
625 630 635 640
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
645 650 655
Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
660 665 670
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
675 680 685
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
690 695 700
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
705 710 715 720
Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
725 730 735
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
740 745 750
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
755 760 765
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
770 775 780
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
785 790 795 800
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
805 810 815
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
820 825 830
Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys
835 840 845
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
850 855 860
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
865 870 875 880
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
885 890 895
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
900 905 910
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
915 920 925
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
930 935 940
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 136
<211> 957
<212> PRT
<213> Chimeric
<400> 136
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Val His
245 250 255
Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val Asn Gly
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
500 505 510
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
515 520 525
Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr Tyr Ile His Trp Val
530 535 540
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Tyr Pro
545 550 555 560
Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
565 570 575
Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
580 585 590
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Trp Gly Gly
595 600 605
Glu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
610 615 620
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
625 630 635 640
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
645 650 655
Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
660 665 670
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
675 680 685
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
690 695 700
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
705 710 715 720
Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
725 730 735
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
740 745 750
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
755 760 765
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
770 775 780
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
785 790 795 800
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
805 810 815
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
820 825 830
Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys
835 840 845
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
850 855 860
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
865 870 875 880
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
885 890 895
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
900 905 910
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
915 920 925
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
930 935 940
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 137
<211> 449
<212> PRT
<213> Chimeric
<400> 137
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr His Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Thr Gly Phe His Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 138
<211> 216
<212> PRT
<213> Chimeric
<400> 138
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Thr Asn Glu His
85 90 95
Tyr Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Arg Lys Leu Lys
115 120 125
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
130 135 140
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
145 150 155 160
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
165 170 175
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
180 185 190
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
195 200 205
Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 139
<211> 956
<212> PRT
<213> Chimeric
<400> 139
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Val His
245 250 255
Met Pro Leu Gly Phe Leu Gly Pro Arg Gln Ala Arg Val Val Asn Gly
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Val
500 505 510
Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser
515 520 525
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr Met His Trp Val
530 535 540
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Ile Ile Asn Pro
545 550 555 560
Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr
565 570 575
Met Thr His Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser
580 585 590
Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe
595 600 605
Thr Gly Phe His Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
610 615 620
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
625 630 635 640
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Glu
645 650 655
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
660 665 670
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
675 680 685
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
690 695 700
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
705 710 715 720
Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
725 730 735
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
740 745 750
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
755 760 765
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
770 775 780
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
785 790 795 800
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
805 810 815
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
820 825 830
Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
835 840 845
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
850 855 860
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
865 870 875 880
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
885 890 895
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
900 905 910
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
915 920 925
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
930 935 940
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 140
<211> 956
<212> PRT
<213> Chimeric
<400> 140
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Cys Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Asp Gly Ser Thr Asn Tyr His Ser Ala Leu Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Lys Gly Ile Thr Thr Val Val Asp Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Asp Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Ala
180 185 190
Ala Thr Phe Leu Ala Asp Asp Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Ser Glu Asp
210 215 220
Val Ala Arg Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Tyr Thr Phe
225 230 235 240
Gly Cys Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val Thr Gln
275 280 285
Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys
290 295 300
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp Val
305 310 315 320
Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly Leu Ile Gly Gly Thr Asn
325 330 335
Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly
340 345 350
Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp Glu Ala
355 360 365
Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe Gly Gly
370 375 380
Gly Thr Lys Leu Thr Val Leu Ser Ser Ala Ser Thr Lys Gly Pro Ser
385 390 395 400
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
405 410 415
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
420 425 430
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
435 440 445
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
450 455 460
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
465 470 475 480
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
485 490 495
Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Val
500 505 510
Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser
515 520 525
Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Tyr Met His Trp Val
530 535 540
Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Ile Ile Asn Pro
545 550 555 560
Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr
565 570 575
Met Thr His Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser Ser
580 585 590
Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe
595 600 605
Thr Gly Phe His Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
610 615 620
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
625 630 635 640
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Glu
645 650 655
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
660 665 670
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
675 680 685
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
690 695 700
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
705 710 715 720
Asp Glu Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
725 730 735
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
740 745 750
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
755 760 765
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
770 775 780
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
785 790 795 800
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
805 810 815
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
820 825 830
Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
835 840 845
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg
850 855 860
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
865 870 875 880
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
885 890 895
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
900 905 910
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
915 920 925
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
930 935 940
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
945 950 955
<210> 141
<211> 674
<212> PRT
<213> Chimeric
<400> 141
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Ser Ser Ala
100 105 110
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
115 120 125
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
130 135 140
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
145 150 155 160
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
165 170 175
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
180 185 190
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
195 200 205
Val Glu Pro Lys Ser Cys Asp Gly Gly Gly Gly Ser Gly Gly Gly Gly
210 215 220
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
225 230 235 240
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
245 250 255
Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
260 265 270
Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys
275 280 285
Phe Gln Gly Arg Val Thr Met Thr His Asp Thr Ser Thr Ser Thr Val
290 295 300
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
305 310 315 320
Cys Ala Arg Ser Phe Phe Thr Gly Phe His Leu Asp Tyr Trp Gly Gln
325 330 335
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
340 345 350
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
355 360 365
Leu Gly Cys Leu Val Glu Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
370 375 380
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
385 390 395 400
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
405 410 415
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
420 425 430
Pro Ser Asn Thr Lys Val Asp Glu Lys Val Glu Pro Lys Ser Cys Asp
435 440 445
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
450 455 460
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
465 470 475 480
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
485 490 495
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
500 505 510
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
515 520 525
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
530 535 540
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Gly Ala Pro Ile Glu
545 550 555 560
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
565 570 575
Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
580 585 590
Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
595 600 605
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
610 615 620
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
625 630 635 640
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
645 650 655
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
660 665 670
Gly Lys
<210> 142
<211> 5
<212> PRT
<213> Chimeric
<400> 142
Asp Tyr Thr Met Asp
1 5
<210> 143
<211> 17
<212> PRT
<213> Chimeric
<400> 143
Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Val Asn Arg Arg Phe Lys
1 5 10 15
Gly
<210> 144
<211> 10
<212> PRT
<213> Chimeric
<400> 144
Asn Leu Gly Pro Phe Phe Tyr Phe Asp Tyr
1 5 10
<210> 145
<211> 7
<212> PRT
<213> Chimeric
<400> 145
Thr Ser Asn Tyr Ala Asn Trp
1 5
<210> 146
<211> 20
<212> PRT
<213> Chimeric
<400> 146
Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser
1 5 10 15
Leu Leu Gly Gly
20
<210> 147
<211> 5
<212> PRT
<213> Chimeric
<400> 147
Thr Lys Leu Thr Val
1 5
<210> 148
<211> 11
<212> PRT
<213> Chimeric
<400> 148
Lys Ala Ser Gln Asp Val Ser Thr Ala Val Ala
1 5 10
<210> 149
<211> 7
<212> PRT
<213> Chimeric
<400> 149
Ser Ala Ser Phe Arg Tyr Thr
1 5
<210> 150
<211> 9
<212> PRT
<213> Chimeric
<400> 150
Gln Gln His Tyr Thr Thr Pro Pro Thr
1 5
<210> 151
<211> 5
<212> PRT
<213> Chimeric
<400> 151
Ser Tyr Tyr Met His
1 5
<210> 152
<211> 17
<212> PRT
<213> Chimeric
<400> 152
Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 153
<211> 10
<212> PRT
<213> Chimeric
<400> 153
Ser Phe Phe Thr Gly Phe His Leu Asp Tyr
1 5 10
<210> 154
<211> 12
<212> PRT
<213> Chimeric
<400> 154
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 155
<211> 7
<212> PRT
<213> Chimeric
<400> 155
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 156
<211> 10
<212> PRT
<213> Chimeric
<400> 156
Gln Gln Tyr Thr Asn Glu His Tyr Tyr Thr
1 5 10
<210> 157
<211> 119
<212> PRT
<213> Chimeric
<400> 157
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr His Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Thr Gly Phe His Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 158
<211> 109
<212> PRT
<213> Chimeric
<400> 158
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Thr Asn Glu His
85 90 95
Tyr Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 159
<211> 119
<212> PRT
<213> Chimeric
<400> 159
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asp Tyr
20 25 30
Thr Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asp Val Asn Pro Asn Ser Gly Gly Ser Ile Val Asn Arg Arg Phe
50 55 60
Lys Gly Arg Phe Thr Leu Ser Val Asp Arg Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Leu Gly Pro Phe Phe Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 160
<211> 120
<212> PRT
<213> Chimeric
<400> 160
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Glu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 161
<211> 107
<212> PRT
<213> Chimeric
<400> 161
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Arg Tyr Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 162
<211> 1350
<212> DNA
<213> Chimeric
<400> 162
gaagttcagc tggttgaaag cggtggtggt ctggttcagc ctggtggtag cctgcgtctg 60
agctgtgcag caagcggttt tacctttaac gattatacca tggattgggt tcgtcaggca 120
ccgggtaaag gtctggaatg ggttgcagat gttaatccga atagcggtgg tagcattgtt 180
aaccgtcgtt ttaaaggtcg ttttaccctg agcgttgatc gtagcaaaaa taccctgtat 240
ctgcaaatga atagtctgcg tgcagaggat accgcagtgt attattgtgc acgtaacctg 300
ggtccgttct tctactttga ttattggggt cagggcaccc tggttaccgt tagcagcgct 360
agcaccaagg gcccctccgt gttccccctg gcccccagca gcaagagcac cagcggcggc 420
acagccgctc tgggctgcct ggtcgaggac tacttccccg agcccgtgac cgtgtcctgg 480
aacagcggag ccctgacctc cggcgtgcac accttccccg ccgtgctgca gagttctggc 540
ctgtatagcc tgagcagcgt ggtcaccgtg ccttctagca gcctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gcccagcaac accaaggtgg acgagaaggt ggagcccaag 660
agctgcgaca aaactcacac atgcccaccg tgcccagcac ctgaagctgc agggggaccg 720
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 780
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 840
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 900
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 960
tacaagtgca aggtctccaa caaagccctc ggcgccccca tcgagaaaac catctccaaa 1020
gccaaagggc agccccgaga accacaggtg tgcaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct ctcgtgcgca gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gctccttctt cctcgtgagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 1320
aagagcctct ccctgtctcc gggtaaatga 1350
<210> 163
<211> 645
<212> DNA
<213> Chimeric
<400> 163
gacatccaga tgacccagag ccccagcagc ctgtctgcca gcgtgggcga cagagtgacc 60
atcacatgca aggccagcca ggacgtgtcc acagccgtgg cctggtatca gcagaagcct 120
ggcaaggccc ccaagctgct gatctacagc gccagcttcc ggtacaccgg cgtgcccagc 180
agattcagcg gcagcagatc cggcaccgac ttcaccctga ccatcagctc cctgcagccc 240
gaggacttcg ccacctacta ctgccagcag cactacacca ccccccccac atttggccag 300
ggcaccaagg tggaaatcaa gcgtacggtg gctgcaccat ctgtcttcat cttcccgcca 360
tctgatcgga agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat 420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag 480
gagagtgtca cagagcagga cagcaaggac agcacctaca gcctcagcag caccctgacg 540
ctgagcaaag cagactacga gaaacacaaa gtctacgcct gcgaagtcac ccatcagggc 600
ctgagctcgc ccgtcacaaa gagcttcaac aggggagagt gttag 645
<210> 164
<211> 2874
<212> DNA
<213> Chimeric
<400> 164
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaaggc gggggaggct ccggaggcgg cggaagtgga 780
ggcggcggaa gtggcggagg cggagggggg ggaagtgggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtg ctgagcagcg cttccaccaa gggacccagt 1200
gtgttccccc tggcccccag ctccaagtct acatccggtg gcacagctgc cctgggatgt 1260
ctcgtgaagg actactttcc tgagcctgtg acagtgtctt ggaacagcgg agccctgacc 1320
agcggagtgc acacattccc tgcagtgctg cagagcagcg gcctgtatag cctgagcagc 1380
gtcgtgaccg tgccttcctc tagcctggga acacagacat atatctgtaa tgtgaatcat 1440
aagcccagta ataccaaagt ggataagaaa gtggaaccta agagctgcga tggcggagga 1500
gggtccggag gcggagggtc cgaggtccag ctggtcgagt ctggaggagg actggtgcag 1560
ccaggcggat ctctgagact gagctgcgcc gccagcggat tcaacatcaa ggacacctac 1620
atccactggg tgaggcaggc ccctggaaag ggactggagt gggtggccag aatctacccc 1680
accaacggct acacaagata cgccgacagc gtgaagggca gattcaccat cagcgccgac 1740
accagcaaga acaccgccta cctgcagatg aacagcctga gagccgagga cacagccgtg 1800
tactactgct ctagatgggg aggcgagggc ttctacgcca tggactactg gggacagggc 1860
acactggtga ccgtgtccag cgctagcacc aagggcccct ccgtgttccc cctggccccc 1920
agcagcaaga gcaccagcgg cggcacagcc gctctgggct gcctggtcga ggactacttc 1980
cccgagcccg tgaccgtgtc ctggaacagc ggagccctga cctccggcgt gcacaccttc 2040
cccgccgtgc tgcagagttc tggcctgtat agcctgagca gcgtggtcac cgtgccttct 2100
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaag 2160
gtggacgaga aggtggagcc caagagctgc gacaaaactc acacatgccc accgtgccca 2220
gcacctgaag ctgcaggggg accgtcagtc ttcctcttcc ccccaaaacc caaggacacc 2280
ctcatgatct cccggacccc tgaggtcaca tgcgtggtgg tggacgtgag ccacgaagac 2340
cctgaggtca agttcaactg gtacgtggac ggcgtggagg tgcataatgc caagacaaag 2400
ccgcgggagg agcagtacaa cagcacgtac cgtgtggtca gcgtcctcac cgtcctgcac 2460
caggactggc tgaatggcaa ggagtacaag tgcaaggtct ccaacaaagc cctcggcgcc 2520
cccatcgaga aaaccatctc caaagccaaa gggcagcccc gagaaccaca ggtgtacacc 2580
ctgcccccat gccgggatga gctgaccaag aaccaggtca gcctgtggtg cctggtcaaa 2640
ggcttctatc ccagcgacat cgccgtggag tgggagagca atgggcagcc ggagaacaac 2700
tacaagacca cgcctcccgt gctggactcc gacggctcct tcttcctcta cagcaagctc 2760
accgtggaca agagcaggtg gcagcagggg aacgtcttct catgctccgt gatgcatgag 2820
gctctgcaca accactacac gcagaagagc ctctccctgt ctccgggtaa atga 2874
<210> 165
<211> 2874
<212> DNA
<213> Chimeric
<400> 165
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaagga ggcggcggaa gtgtgcacat gcccctgggc 780
ttcctgggcc ccagacaggc cagagtcgtg aacggggggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtg ctgagcagcg cttccaccaa gggacccagt 1200
gtgttccccc tggcccccag ctccaagtct acatccggtg gcacagctgc cctgggatgt 1260
ctcgtgaagg actactttcc tgagcctgtg acagtgtctt ggaacagcgg agccctgacc 1320
agcggagtgc acacattccc tgcagtgctg cagagcagcg gcctgtatag cctgagcagc 1380
gtcgtgaccg tgccttcctc tagcctggga acacagacat atatctgtaa tgtgaatcat 1440
aagcccagta ataccaaagt ggataagaaa gtggaaccta agagctgcga tggcggagga 1500
gggtccggag gcggagggtc cgaggtccag ctggtcgagt ctggaggagg actggtgcag 1560
ccaggcggat ctctgagact gagctgcgcc gccagcggat tcaacatcaa ggacacctac 1620
atccactggg tgaggcaggc ccctggaaag ggactggagt gggtggccag aatctacccc 1680
accaacggct acacaagata cgccgacagc gtgaagggca gattcaccat cagcgccgac 1740
accagcaaga acaccgccta cctgcagatg aacagcctga gagccgagga cacagccgtg 1800
tactactgct ctagatgggg aggcgagggc ttctacgcca tggactactg gggacagggc 1860
acactggtga ccgtgtccag cgctagcacc aagggcccct ccgtgttccc cctggccccc 1920
agcagcaaga gcaccagcgg cggcacagcc gctctgggct gcctggtcga ggactacttc 1980
cccgagcccg tgaccgtgtc ctggaacagc ggagccctga cctccggcgt gcacaccttc 2040
cccgccgtgc tgcagagttc tggcctgtat agcctgagca gcgtggtcac cgtgccttct 2100
agcagcctgg gcacccagac ctacatctgc aacgtgaacc acaagcccag caacaccaag 2160
gtggacgaga aggtggagcc caagagctgc gacaaaactc acacatgccc accgtgccca 2220
gcacctgaag ctgcaggggg accgtcagtc ttcctcttcc ccccaaaacc caaggacacc 2280
ctcatgatct cccggacccc tgaggtcaca tgcgtggtgg tggacgtgag ccacgaagac 2340
cctgaggtca agttcaactg gtacgtggac ggcgtggagg tgcataatgc caagacaaag 2400
ccgcgggagg agcagtacaa cagcacgtac cgtgtggtca gcgtcctcac cgtcctgcac 2460
caggactggc tgaatggcaa ggagtacaag tgcaaggtct ccaacaaagc cctcggcgcc 2520
cccatcgaga aaaccatctc caaagccaaa gggcagcccc gagaaccaca ggtgtacacc 2580
ctgcccccat gccgggatga gctgaccaag aaccaggtca gcctgtggtg cctggtcaaa 2640
ggcttctatc ccagcgacat cgccgtggag tgggagagca atgggcagcc ggagaacaac 2700
tacaagacca cgcctcccgt gctggactcc gacggctcct tcttcctcta cagcaagctc 2760
accgtggaca agagcaggtg gcagcagggg aacgtcttct catgctccgt gatgcatgag 2820
gctctgcaca accactacac gcagaagagc ctctccctgt ctccgggtaa atga 2874
<210> 166
<211> 1350
<212> DNA
<213> Chimeric
<400> 166
caggtgcaat tggttcaatc tggtgctgaa gtaaaaaaac cgggcgcttc cgttaaagtg 60
agctgcaaag catccggata caccttcact tcctattaca tgcactgggt tcgtcaagcc 120
ccgggccagg gtctggaatg gatgggcatc attaacccaa gcggtggctc tacctcctac 180
gcgcagaaat tccagggtcg cgtcacgatg acccatgaca ctagcacctc taccgtttat 240
atggagctgt ccagcctgcg ttctgaagat actgcagtgt actactgtgc acgctctttc 300
ttcactggtt tccatctgga ctattggggt caaggcaccc tcgtaacggt ttcttctgct 360
agcaccaagg gcccctccgt gttccccctg gcccccagca gcaagagcac cagcggcggc 420
acagccgctc tgggctgcct ggtcgaggac tacttccccg agcccgtgac cgtgtcctgg 480
aacagcggag ccctgacctc cggcgtgcac accttccccg ccgtgctgca gagttctggc 540
ctgtatagcc tgagcagcgt ggtcaccgtg ccttctagca gcctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gcccagcaac accaaggtgg acgagaaggt ggagcccaag 660
agctgcgaca aaactcacac atgcccaccg tgcccagcac ctgaagctgc agggggaccg 720
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 780
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 840
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 900
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 960
tacaagtgca aggtctccaa caaagccctc ggcgccccca tcgagaaaac catctccaaa 1020
gccaaagggc agccccgaga accacaggtg tgcaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct ctcgtgcgca gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gctccttctt cctcgtgagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 1320
aagagcctct ccctgtctcc gggtaaatga 1350
<210> 167
<211> 651
<212> DNA
<213> Chimeric
<400> 167
gaaatcgtgt taacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 60
ctctcttgca gggccagtca gagtgttagc agcagctact tagcctggta ccagcagaaa 120
cctggccagg ctcccaggct cctcatctat ggagcatcca gcagggccac tggcatccca 180
gacaggttca gtggcagtgg atccgggaca gacttcactc tcaccatcag cagactggag 240
cctgaagatt ttgcagtgta ttactgtcag cagtatacca acgaacatta ttatacgttc 300
ggccagggga ccaaagtgga aatcaaacgt acggtggctg caccatctgt cttcatcttc 360
ccgccatctg atcggaagtt gaaatctgga actgcctctg ttgtgtgcct gctgaataac 420
ttctatccca gagaggccaa agtacagtgg aaggtggata acgccctcca atcgggtaac 480
tcccaggaga gtgtcacaga gcaggacagc aaggacagca cctacagcct cagcagcacc 540
ctgacgctga gcaaagcaga ctacgagaaa cacaaagtct acgcctgcga agtcacccat 600
cagggcctga gctcgcccgt cacaaagagc ttcaacaggg gagagtgtta g 651
<210> 168
<211> 2871
<212> DNA
<213> Chimeric
<400> 168
caagtgcagc tgaaagagtc cggccctgga ctggtggccc ctagccagag cctgagcatc 60
acctgtaccg tgtccggctt cagcctgacc agctacggcg tgtcatgggt gcgccagcct 120
ccaggcaagt gtctggaatg gctgggcatc atctggggcg acggcagcac caattaccac 180
agcgccctga tcagcagact gagcatctcc aaggacaaca gcaagagcca ggtgttcctg 240
aagctgaaca gcctgcagac cgacgacacc gccacctact actgcgccaa gggcatcacc 300
accgtggtgg acgactacta cgctatggac tactggggcc agggcaccag cgtgacagtg 360
tctagcggag gcggaggatc tggcggcgga ggaagtggcg gagggggatc tgggggaggc 420
ggaagcgata tccagatgac ccagagccct gccagcctgt ctgcctctgt gggcgagaca 480
gtgaccatca catgccgggc cagcgagaac atcgacagct acctggcctg gtatcagcag 540
aagcagggca agagccccca gctgctggtg tacgccgcca cctttctggc cgacgatgtg 600
cccagcagat tcagcggcag cggaagcggc acacagtaca gcctgaagat caactccctg 660
cagagcgagg acgtggcccg gtactactgc cagcactact acagcacccc ctacaccttc 720
ggctgcggca ccaagctgga aatcaaagga ggcggcggaa gtgtgcacat gcccctgggc 780
ttcctgggcc ccagacaggc cagagtcgtg aacggggggg gcggaggcag tgggggggga 840
ggatcccagg ccgtcgtgac ccaggaaccc agcctgacag tgtctcctgg cggcaccgtg 900
accctgacat gtggcagttc tacaggcgcc gtgaccacca gcaactacgc caactgggtg 960
caggaaaagc ccggccaggc cttcagagga ctgatcggcg gcaccaacaa gagagcccct 1020
ggcacccctg ccagattcag cggatctctg ctgggaggaa aggccgccct gacactgtct 1080
ggcgcccagc cagaagatga ggccgagtac tactgcgccc tgtggtacag caacctgtgg 1140
gtgttcggcg gaggcaccaa gctgacagtg ctgagcagcg cttccaccaa gggacccagt 1200
gtgttccccc tggcccccag ctccaagtct acatccggtg gcacagctgc cctgggatgt 1260
ctcgtgaagg actactttcc tgagcctgtg acagtgtctt ggaacagcgg agccctgacc 1320
agcggagtgc acacattccc tgcagtgctg cagagcagcg gcctgtatag cctgagcagc 1380
gtcgtgaccg tgccttcctc tagcctggga acacagacat atatctgtaa tgtgaatcat 1440
aagcccagta ataccaaagt ggataagaaa gtggaaccta agagctgcga tggcggagga 1500
gggtccggag gcggagggtc ccaggtgcaa ttggttcaat ctggtgctga agtaaaaaaa 1560
ccgggcgctt ccgttaaagt gagctgcaaa gcatccggat acaccttcac ttcctattac 1620
atgcactggg ttcgtcaagc cccgggccag ggtctggaat ggatgggcat cattaaccca 1680
agcggtggct ctacctccta cgcgcagaaa ttccagggtc gcgtcacgat gacccatgac 1740
actagcacct ctaccgttta tatggagctg tccagcctgc gttctgaaga tactgcagtg 1800
tactactgtg cacgctcttt cttcactggt ttccatctgg actattgggg tcaaggcacc 1860
ctcgtaacgg tttcttctgc tagcaccaag ggcccctccg tgttccccct ggcccccagc 1920
agcaagagca ccagcggcgg cacagccgct ctgggctgcc tggtcgagga ctacttcccc 1980
gagcccgtga ccgtgtcctg gaacagcgga gccctgacct ccggcgtgca caccttcccc 2040
gccgtgctgc agagttctgg cctgtatagc ctgagcagcg tggtcaccgt gccttctagc 2100
agcctgggca cccagaccta catctgcaac gtgaaccaca agcccagcaa caccaaggtg 2160
gacgagaagg tggagcccaa gagctgcgac aaaactcaca catgcccacc gtgcccagca 2220
cctgaagctg cagggggacc gtcagtcttc ctcttccccc caaaacccaa ggacaccctc 2280
atgatctccc ggacccctga ggtcacatgc gtggtggtgg acgtgagcca cgaagaccct 2340
gaggtcaagt tcaactggta cgtggacggc gtggaggtgc ataatgccaa gacaaagccg 2400
cgggaggagc agtacaacag cacgtaccgt gtggtcagcg tcctcaccgt cctgcaccag 2460
gactggctga atggcaagga gtacaagtgc aaggtctcca acaaagccct cggcgccccc 2520
atcgagaaaa ccatctccaa agccaaaggg cagccccgag aaccacaggt gtacaccctg 2580
cccccatgcc gggatgagct gaccaagaac caggtcagcc tgtggtgcct ggtcaaaggc 2640
ttctatccca gcgacatcgc cgtggagtgg gagagcaatg ggcagccgga gaacaactac 2700
aagaccacgc ctcccgtgct ggactccgac ggctccttct tcctctacag caagctcacc 2760
gtggacaaga gcaggtggca gcaggggaac gtcttctcat gctccgtgat gcatgaggct 2820
ctgcacaacc actacacgca gaagagcctc tccctgtctc cgggtaaatg a 2871
<210> 169
<211> 2857
<212> DNA
<213> Chimeric
<400> 169
agagtccggc cctggactgg tggcccctag ccagagcctg agcatcacct gtaccgtgtc 60
cggcttcagc ctgaccagct acggcgtgtc atgggtgcgc cagcctccag gcaagtgtct 120
ggaatggctg ggcatcatct ggggcgacgg cagcaccaat taccacagcg ccctgatcag 180
cagactgagc atctccaagg acaacagcaa gagccaggtg ttcctgaagc tgaacagcct 240
gcagaccgac gacaccgcca cctactactg cgccaagggc atcaccaccg tggtggacga 300
ctactacgct atggactact ggggccaggg caccagcgtg acagtgtcta gcggaggcgg 360
aggatctggc ggcggaggaa gtggcggagg gggatctggg ggaggcggaa gcgatatcca 420
gatgacccag agccctgcca gcctgtctgc ctctgtgggc gagacagtga ccatcacatg 480
ccgggccagc gagaacatcg acagctacct ggcctggtat cagcagaagc agggcaagag 540
cccccagctg ctggtgtacg ccgccacctt tctggccgac gatgtgccca gcagattcag 600
cggcagcgga agcggcacac agtacagcct gaagatcaac tccctgcaga gcgaggacgt 660
ggcccggtac tactgccagc actactacag caccccctac accttcggct gcggcaccaa 720
gctggaaatc aaaggcgggg gaggctccgg aggcggcgga agtggaggcg gcggaagtgg 780
cggaggcgga ggggggggaa gtgggggcgg aggcagtggg gggggaggat cccaggccgt 840
cgtgacccag gaacccagcc tgacagtgtc tcctggcggc accgtgaccc tgacatgtgg 900
cagttctaca ggcgccgtga ccaccagcaa ctacgccaac tgggtgcagg aaaagcccgg 960
ccaggccttc agaggactga tcggcggcac caacaagaga gcccctggca cccctgccag 1020
attcagcgga tctctgctgg gaggaaaggc cgccctgaca ctgtctggcg cccagccaga 1080
agatgaggcc gagtactact gcgccctgtg gtacagcaac ctgtgggtgt tcggcggagg 1140
caccaagctg acagtgctga gcagcgcttc caccaaggga cccagtgtgt tccccctggc 1200
ccccagctcc aagtctacat ccggtggcac agctgccctg ggatgtctcg tgaaggacta 1260
ctttcctgag cctgtgacag tgtcttggaa cagcggagcc ctgaccagcg gagtgcacac 1320
attccctgca gtgctgcaga gcagcggcct gtatagcctg agcagcgtcg tgaccgtgcc 1380
ttcctctagc ctgggaacac agacatatat ctgtaatgtg aatcataagc ccagtaatac 1440
caaagtggat aagaaagtgg aacctaagag ctgcgatggc ggaggagggt ctggaggcgg 1500
agggtcccag gtgcaattgg ttcaatctgg tgctgaagta aaaaaaccgg gcgcttccgt 1560
taaagtgagc tgcaaagcat ccggatacac cttcacttcc tattacatgc actgggttcg 1620
tcaagccccg ggccagggtc tggaatggat gggcatcatt aacccaagcg gtggctctac 1680
ctcctacgcg cagaaattcc agggtcgcgt cacgatgacc catgacacta gcacctctac 1740
cgtttatatg gagctgtcca gcctgcgttc tgaagatact gcagtgtact actgtgcacg 1800
ctctttcttc actggtttcc atctggacta ttggggtcaa ggcaccctcg taacggtttc 1860
ttctgctagc accaagggcc cctccgtgtt ccccctggcc cccagcagca agagcaccag 1920
cggcggcaca gccgctctgg gctgcctggt cgaggactac ttccccgagc ccgtgaccgt 1980
gtcctggaac agcggagccc tgacctccgg cgtgcacacc ttccccgccg tgctgcagag 2040
ttctggcctg tatagcctga gcagcgtggt caccgtgcct tctagcagcc tgggcaccca 2100
gacctacatc tgcaacgtga accacaagcc cagcaacacc aaggtggacg agaaggtgga 2160
gcccaagagc tgcgacaaaa ctcacacatg cccaccgtgc ccagcacctg aagctgcagg 2220
gggaccgtca gtcttcctct tccccccaaa acccaaggac accctcatga tctcccggac 2280
ccctgaggtc acatgcgtgg tggtggacgt gagccacgaa gaccctgagg tcaagttcaa 2340
ctggtacgtg gacggcgtgg aggtgcataa tgccaagaca aagccgcggg aggagcagta 2400
caacagcacg taccgtgtgg tcagcgtcct caccgtcctg caccaggact ggctgaatgg 2460
caaggagtac aagtgcaagg tctccaacaa agccctcggc gcccccatcg agaaaaccat 2520
ctccaaagcc aaagggcagc cccgagaacc acaggtgtac accctgcccc catgccggga 2580
tgagctgacc aagaaccagg tcagcctgtg gtgcctggtc aaaggcttct atcccagcga 2640
catcgccgtg gagtgggaga gcaatgggca gccggagaac aactacaaga ccacgcctcc 2700
cgtgctggac tccgacggct ccttcttcct ctacagcaag ctcaccgtgg acaagagcag 2760
gtggcagcag gggaacgtct tctcatgctc cgtgatgcat gaggctctgc acaaccacta 2820
cacgcagaag agcctctccc tgtctccggg taaatga 2857
<210> 170
<211> 2025
<212> DNA
<213> Chimeric
<400> 170
caggccgtcg tgacccagga acccagcctg acagtgtctc ctggcggcac cgtgaccctg 60
acatgtggca gttctacagg cgccgtgacc accagcaact acgccaactg ggtgcaggaa 120
aagcccggcc aggccttcag aggactgatc ggcggcacca acaagagagc ccctggcacc 180
cctgccagat tcagcggatc tctgctggga ggaaaggccg ccctgacact gtctggcgcc 240
cagccagaag atgaggccga gtactactgc gccctgtggt acagcaacct gtgggtgttc 300
ggcggaggca ccaagctgac agtgctgagc agcgcttcca ccaagggacc cagtgtgttc 360
cccctggccc ccagctccaa gtctacatcc ggtggcacag ctgccctggg atgtctcgtg 420
aaggactact ttcctgagcc tgtgacagtg tcttggaaca gcggagccct gaccagcgga 480
gtgcacacat tccctgcagt gctgcagagc agcggcctgt atagcctgag cagcgtcgtg 540
accgtgcctt cctctagcct gggaacacag acatatatct gtaatgtgaa tcataagccc 600
agtaatacca aagtggataa gaaagtggaa cctaagagct gcgatggcgg aggagggtct 660
ggaggcggag ggtcccaggt gcaattggtt caatctggtg ctgaagtaaa aaaaccgggc 720
gcttccgtta aagtgagctg caaagcatcc ggatacacct tcacttccta ttacatgcac 780
tgggttcgtc aagccccggg ccagggtctg gaatggatgg gcatcattaa cccaagcggt 840
ggctctacct cctacgcgca gaaattccag ggtcgcgtca cgatgaccca tgacactagc 900
acctctaccg tttatatgga gctgtccagc ctgcgttctg aagatactgc agtgtactac 960
tgtgcacgct ctttcttcac tggtttccat ctggactatt ggggtcaagg caccctcgta 1020
acggtttctt ctgctagcac caagggcccc tccgtgttcc ccctggcccc cagcagcaag 1080
agcaccagcg gcggcacagc cgctctgggc tgcctggtcg aggactactt ccccgagccc 1140
gtgaccgtgt cctggaacag cggagccctg acctccggcg tgcacacctt ccccgccgtg 1200
ctgcagagtt ctggcctgta tagcctgagc agcgtggtca ccgtgccttc tagcagcctg 1260
ggcacccaga cctacatctg caacgtgaac cacaagccca gcaacaccaa ggtggacgag 1320
aaggtggagc ccaagagctg cgacaaaact cacacatgcc caccgtgccc agcacctgaa 1380
gctgcagggg gaccgtcagt cttcctcttc cccccaaaac ccaaggacac cctcatgatc 1440
tcccggaccc ctgaggtcac atgcgtggtg gtggacgtga gccacgaaga ccctgaggtc 1500
aagttcaact ggtacgtgga cggcgtggag gtgcataatg ccaagacaaa gccgcgggag 1560
gagcagtaca acagcacgta ccgtgtggtc agcgtcctca ccgtcctgca ccaggactgg 1620
ctgaatggca aggagtacaa gtgcaaggtc tccaacaaag ccctcggcgc ccccatcgag 1680
aaaaccatct ccaaagccaa agggcagccc cgagaaccac aggtgtacac cctgccccca 1740
tgccgggatg agctgaccaa gaaccaggtc agcctgtggt gcctggtcaa aggcttctat 1800
cccagcgaca tcgccgtgga gtgggagagc aatgggcagc cggagaacaa ctacaagacc 1860
acgcctcccg tgctggactc cgacggctcc ttcttcctct acagcaagct caccgtggac 1920
aagagcaggt ggcagcaggg gaacgtcttc tcatgctccg tgatgcatga ggctctgcac 1980
aaccactaca cgcagaagag cctctccctg tctccgggta aatga 2025
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МУЛЬТСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, МУЛЬТСПЕЦИФИЧЕСКИЕ АКТИВИРУЕМЫЕ АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2815683C2 |
| МУЛЬТСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, МУЛЬТСПЕЦИФИЧЕСКИЕ АКТИВИРУЕМЫЕ АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2727836C2 |
| ПОЛИПЕПТИД, СОДЕРЖАЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2017 |
|
RU2827545C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СОДЕРЖАЩИЕ АНТИ-FAP КЛОН 212 | 2019 |
|
RU2799429C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| АНТИ-ROR1/АНТИ-CD3 БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2831608C2 |
| Биспецифическое антитело анти-HER2/анти-4-1BB и его применение | 2020 |
|
RU2831838C2 |
| СУБСТРАТЫ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ И ДРУГИЕ РАСЩЕПЛЯЕМЫЕ ФРАГМЕНТЫ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2832636C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА К Vβ17/CD123 | 2020 |
|
RU2831786C2 |
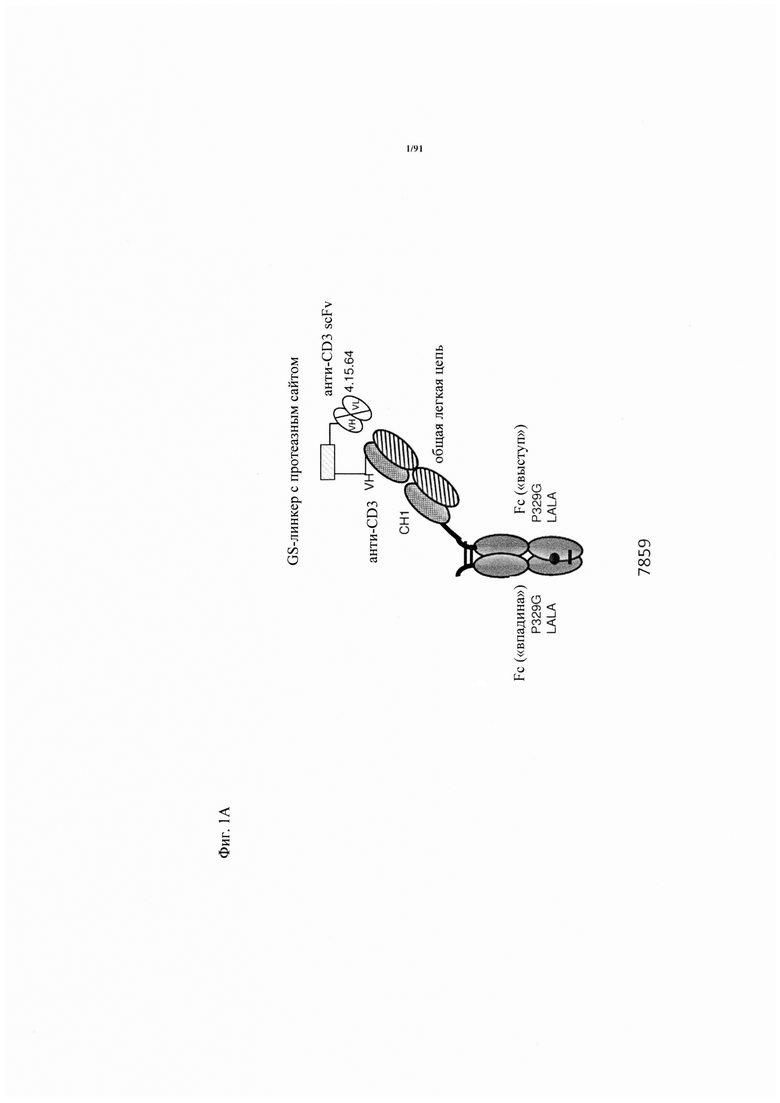
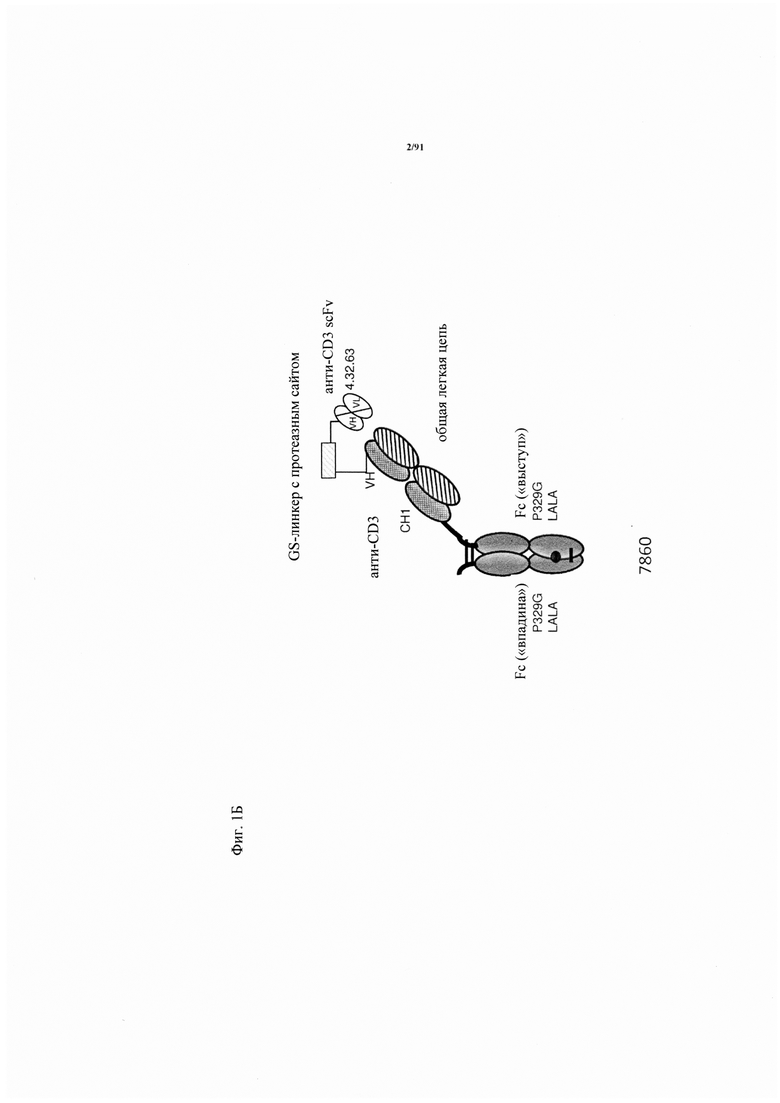
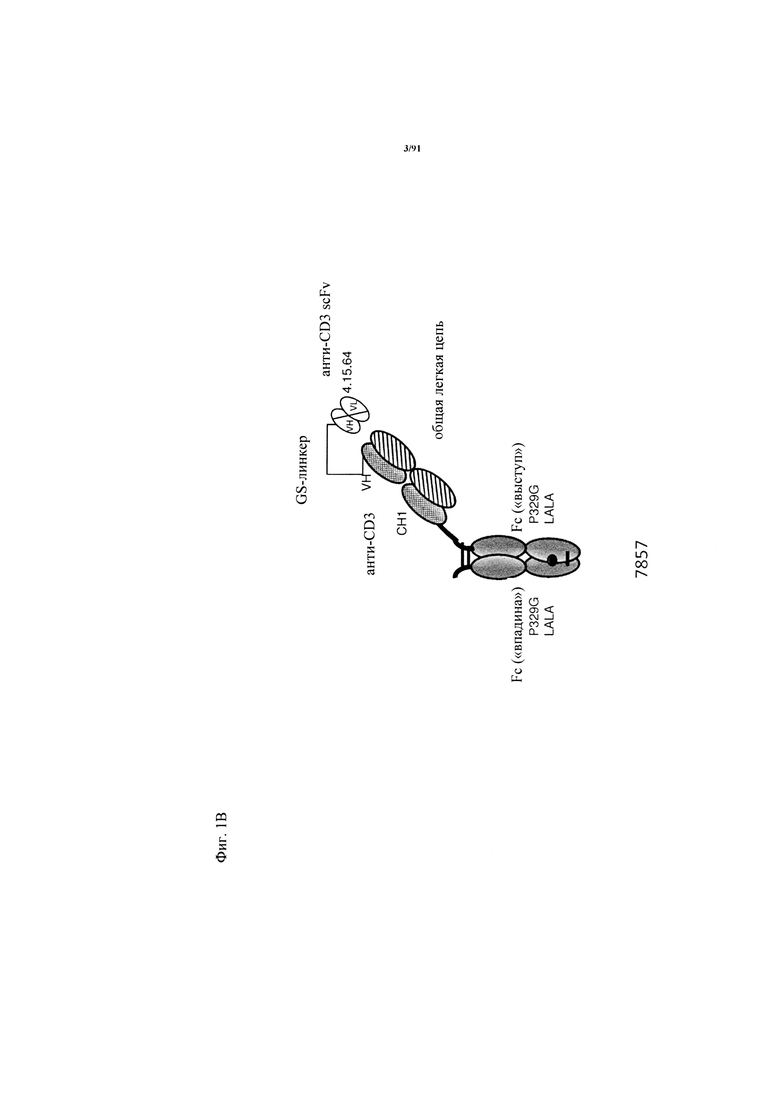
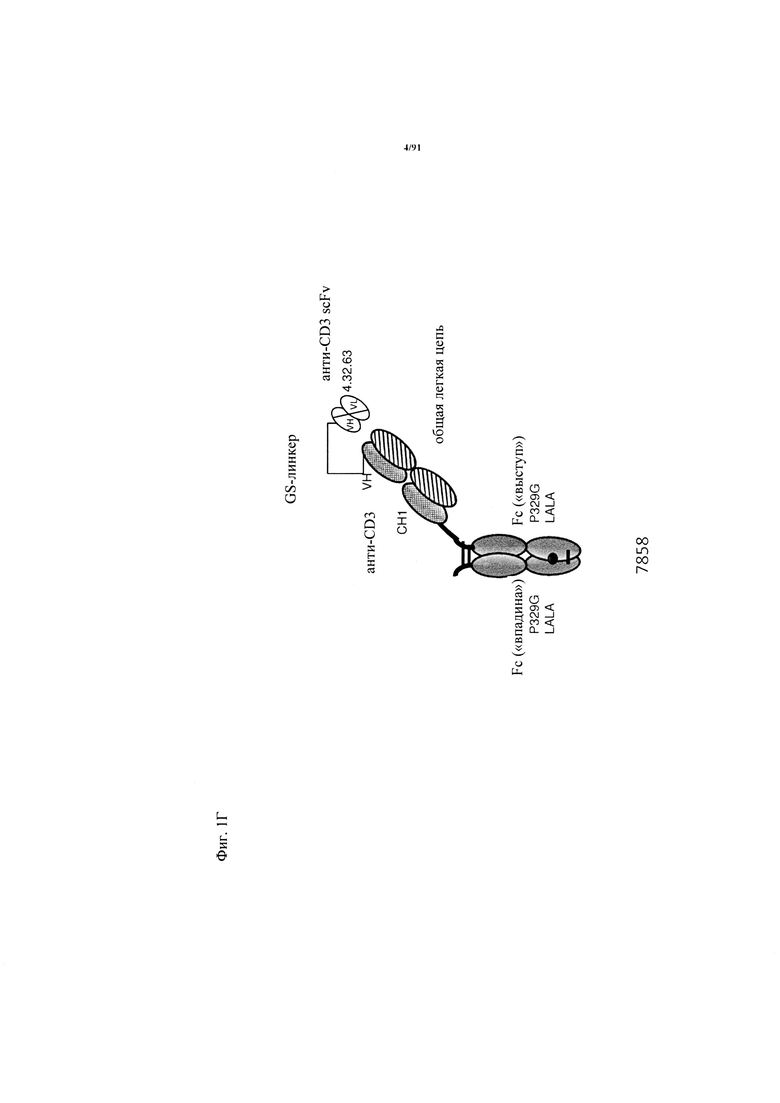




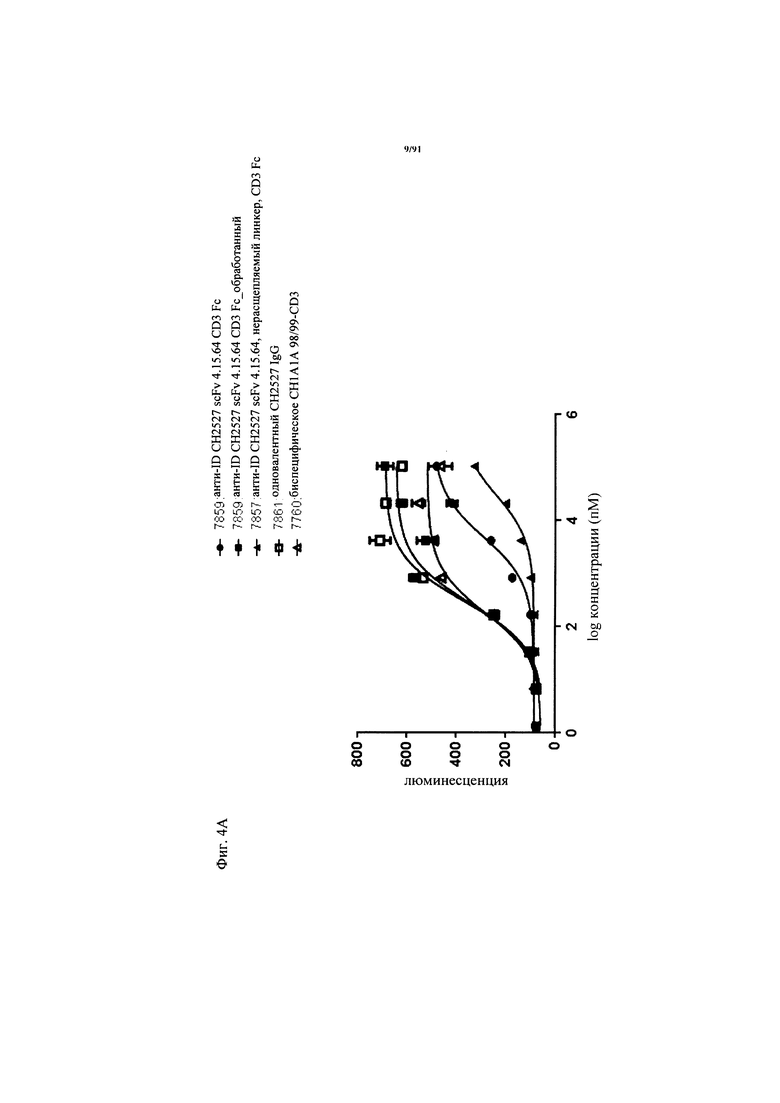
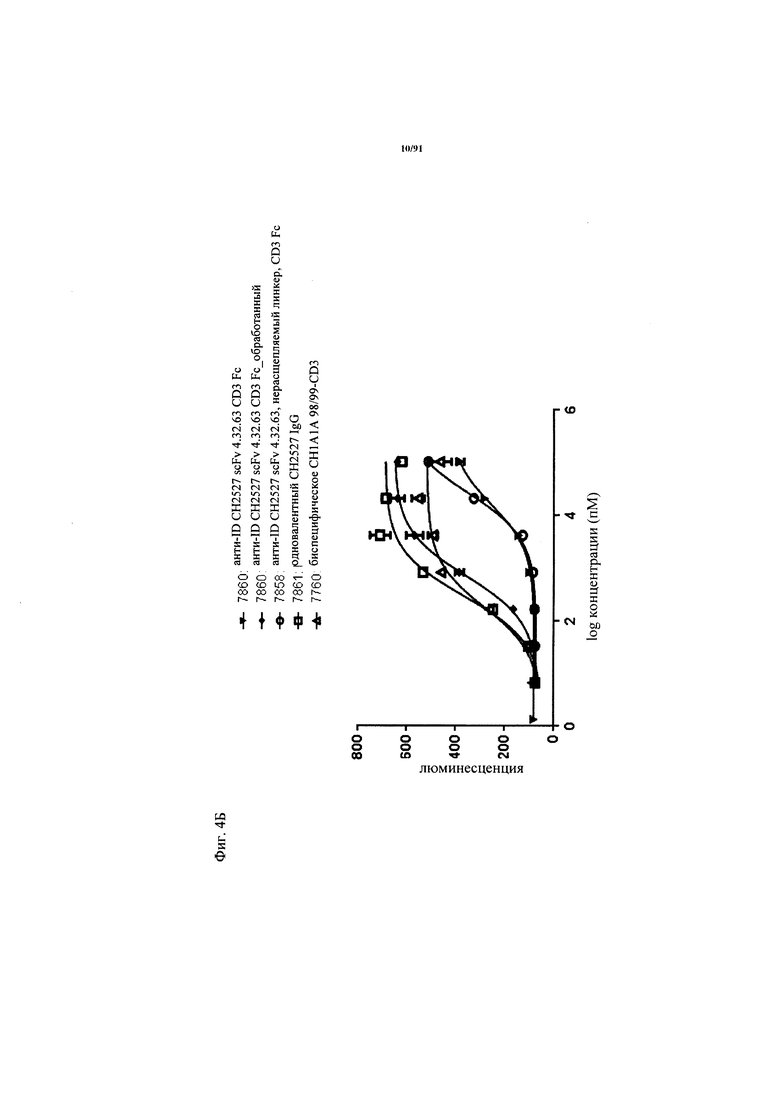

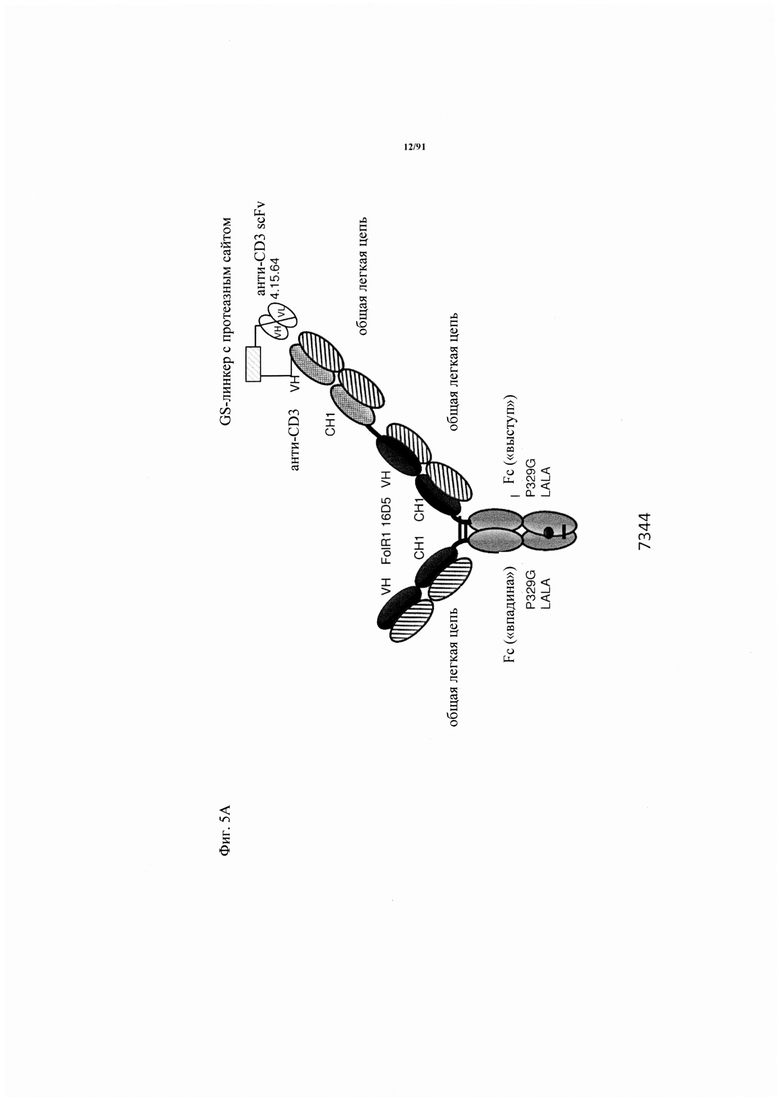
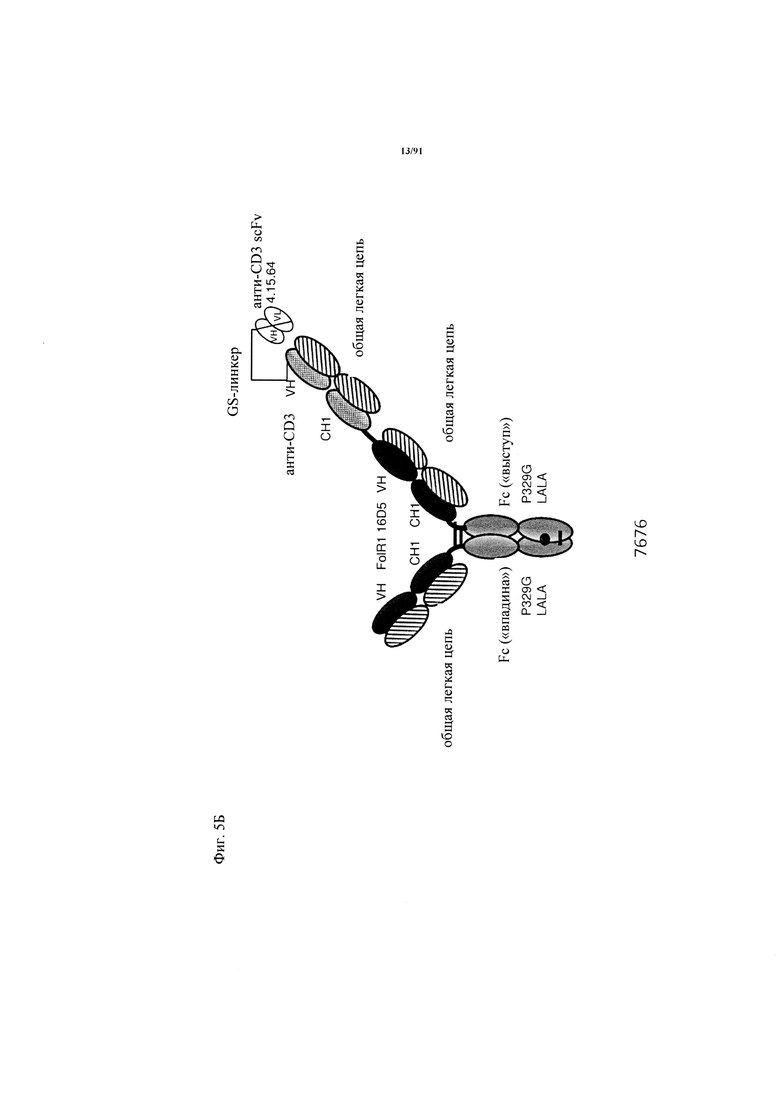
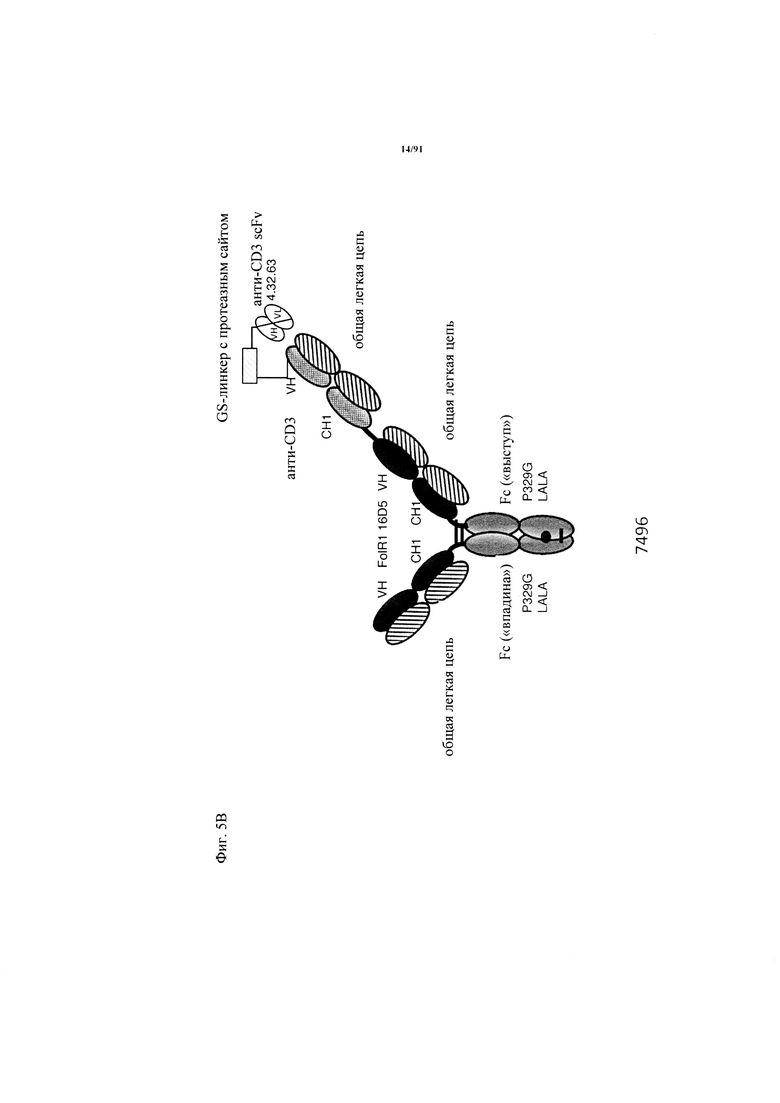
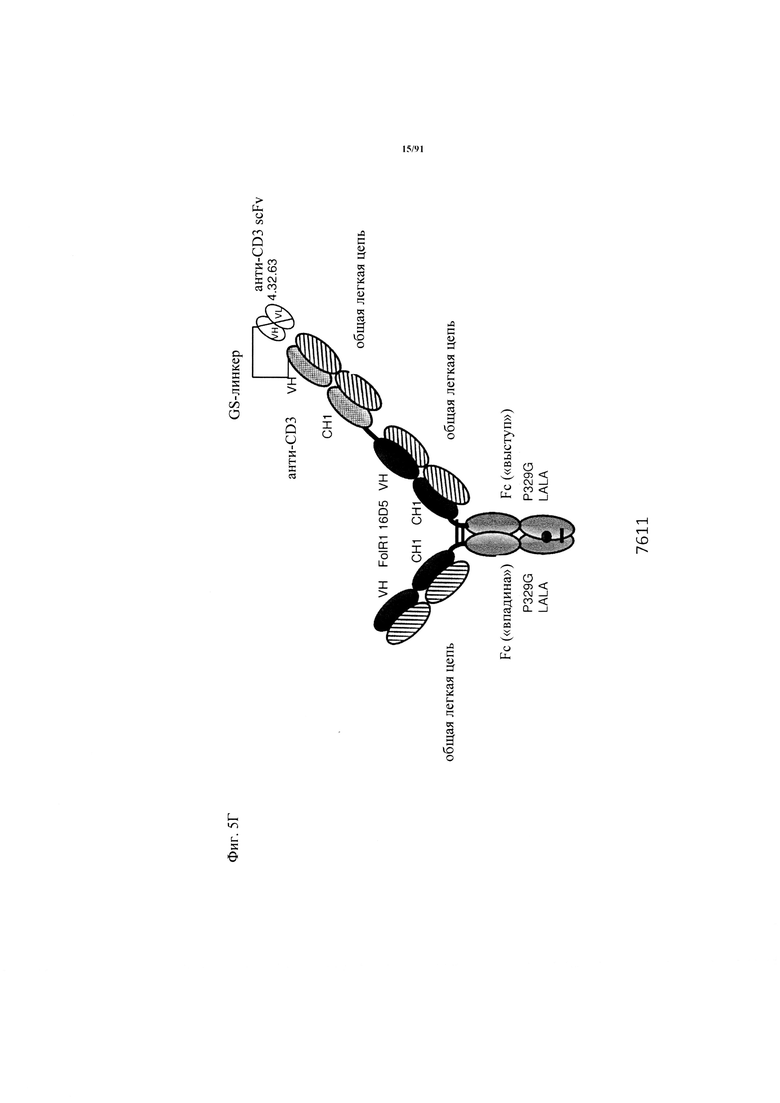
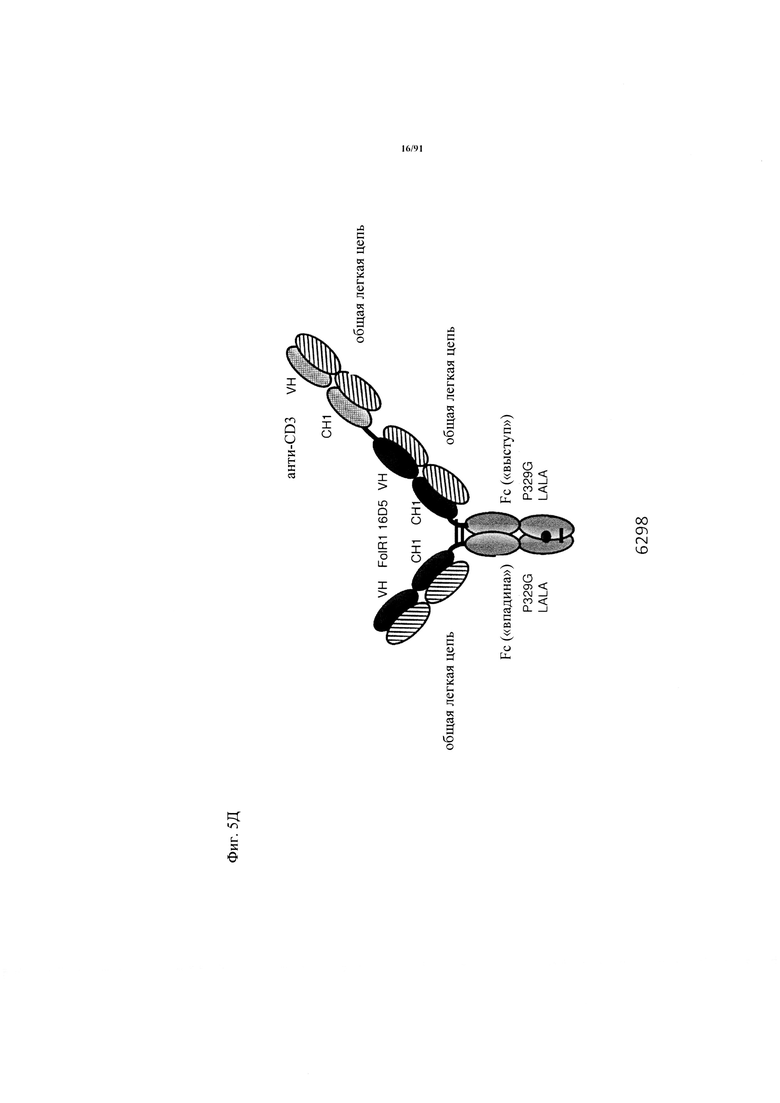
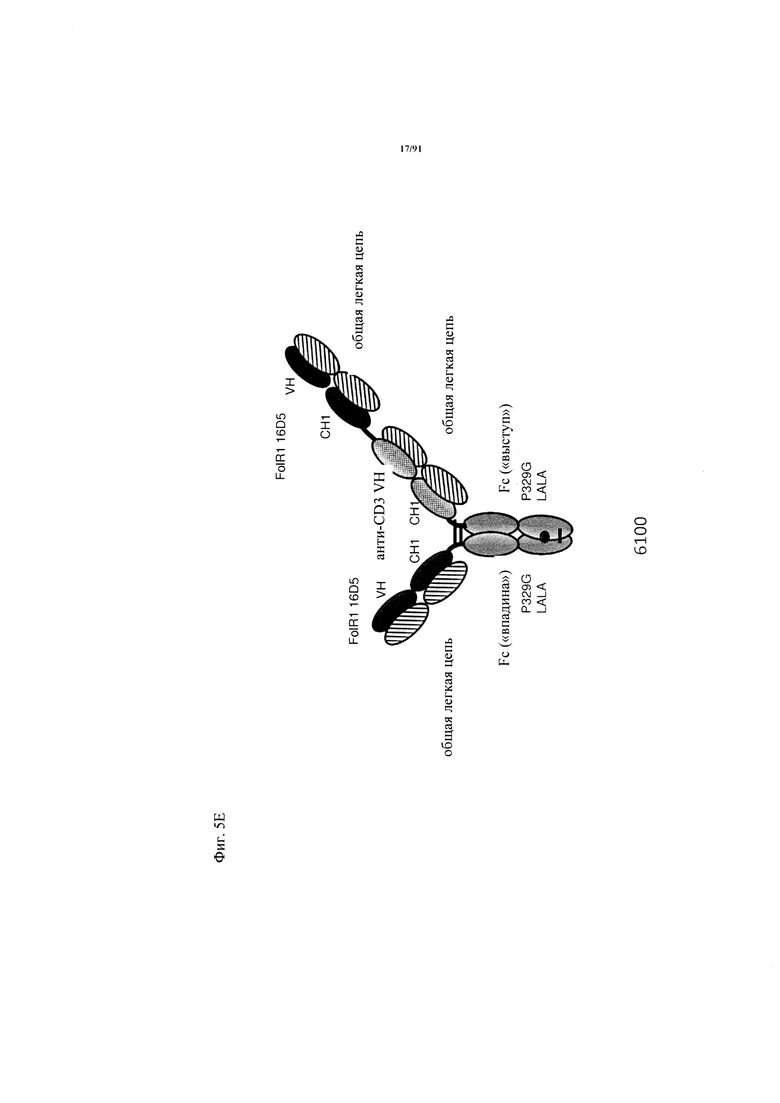

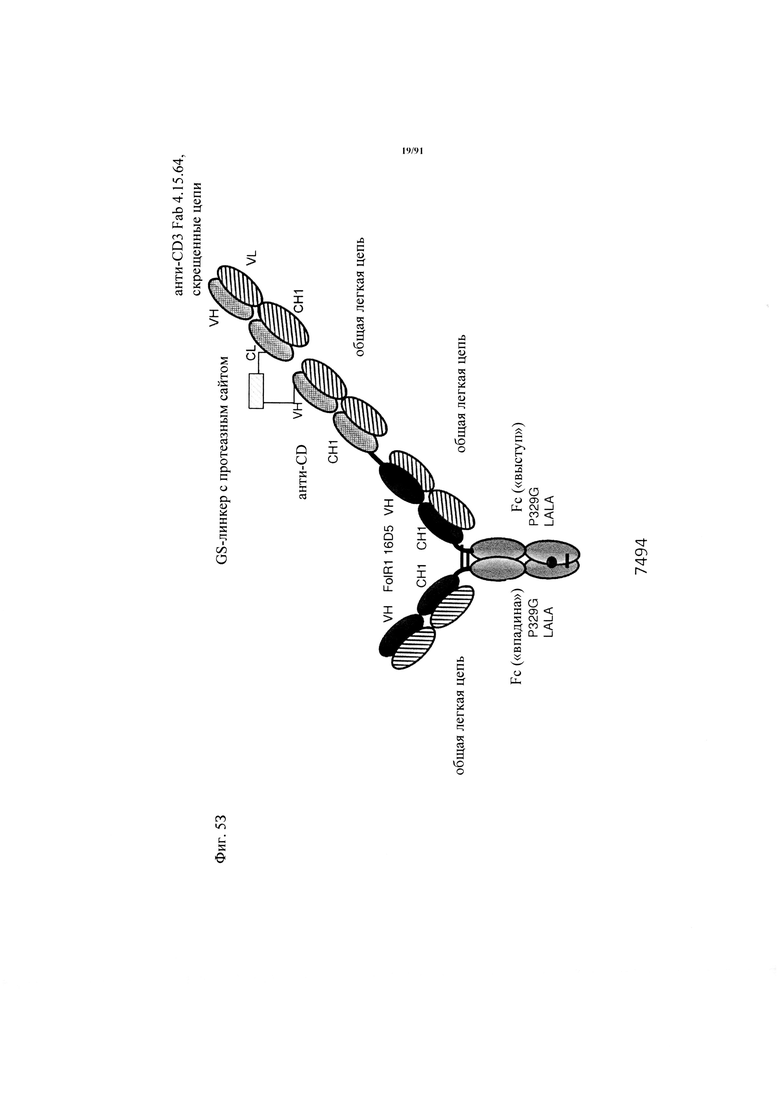
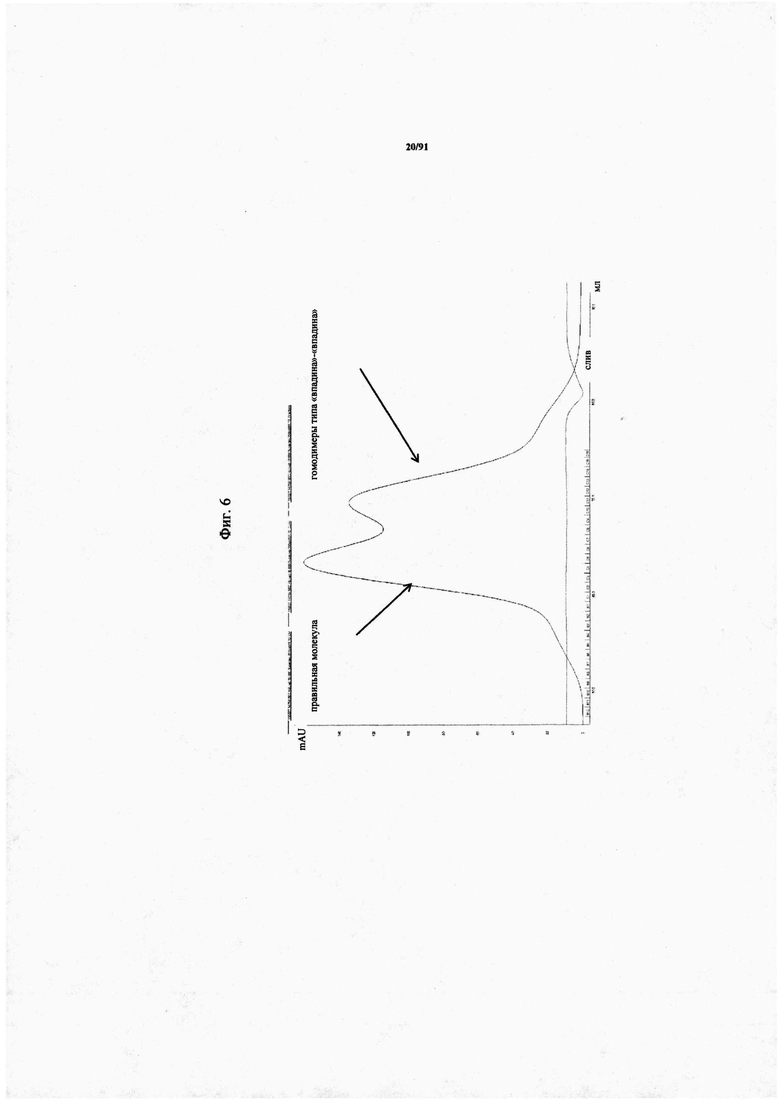
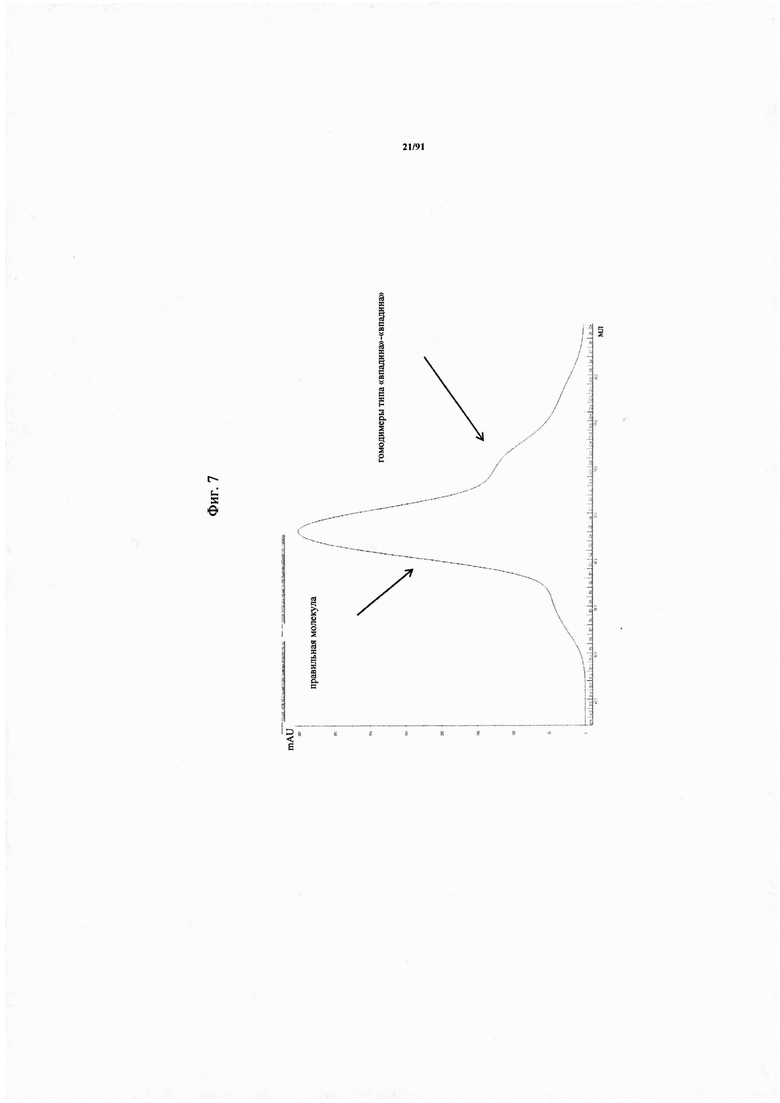







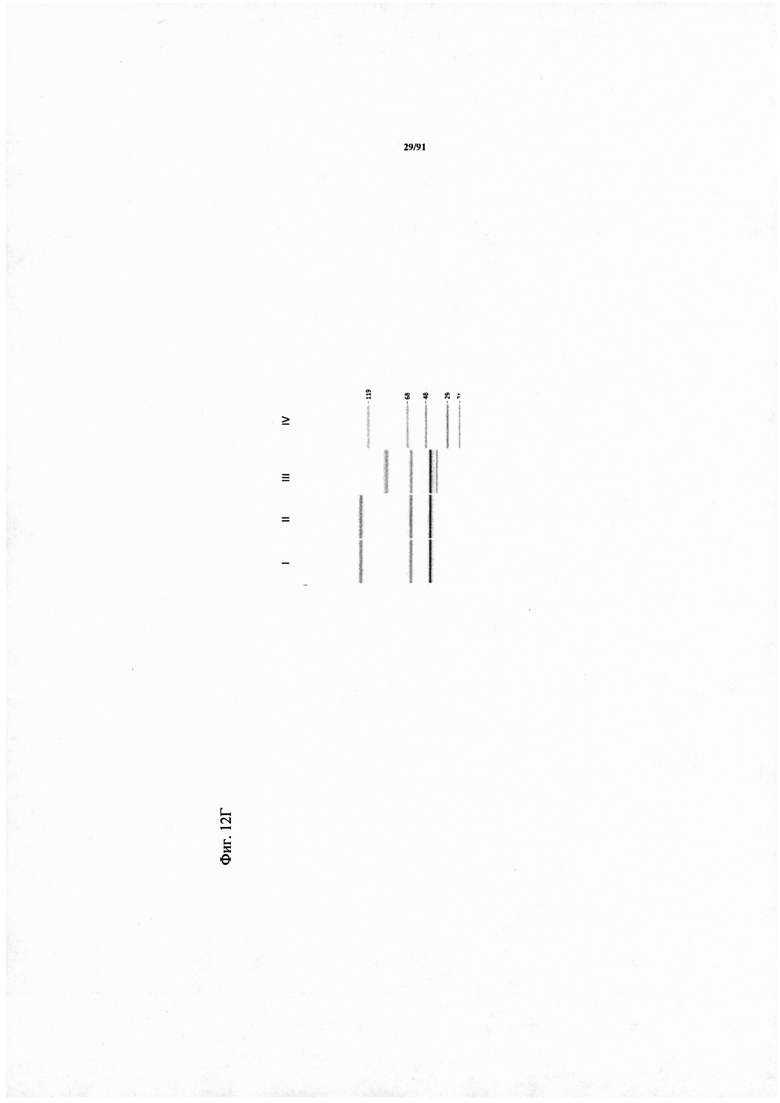


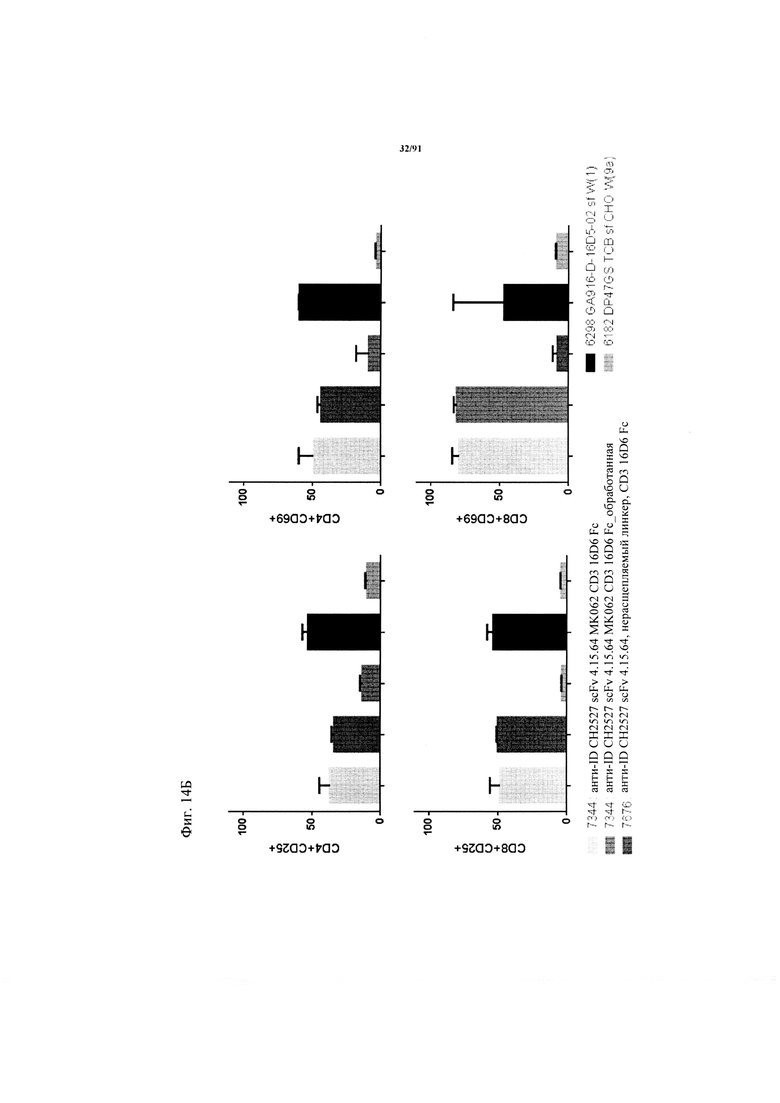

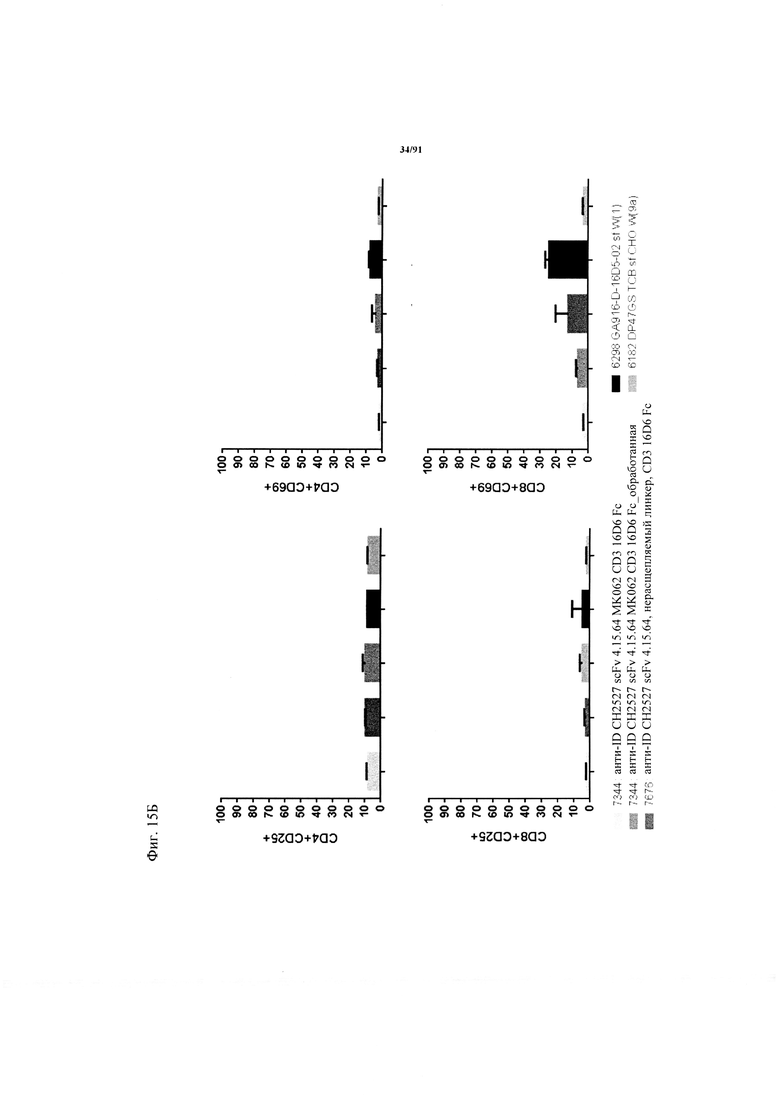


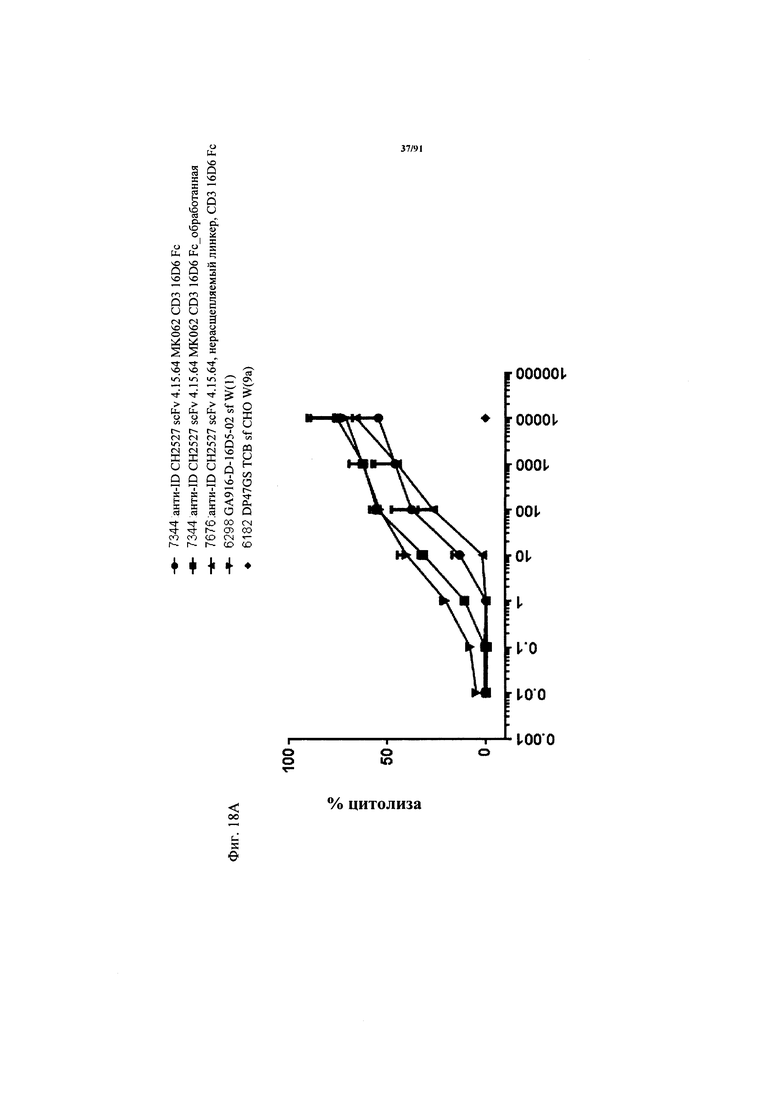
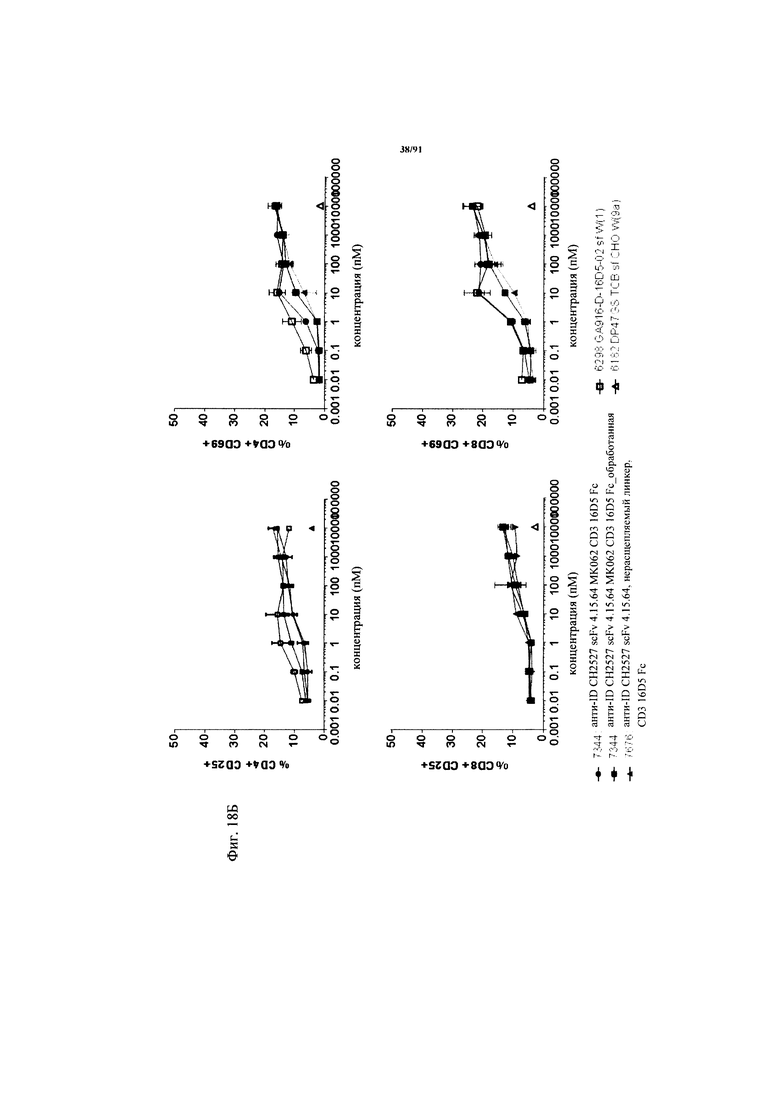
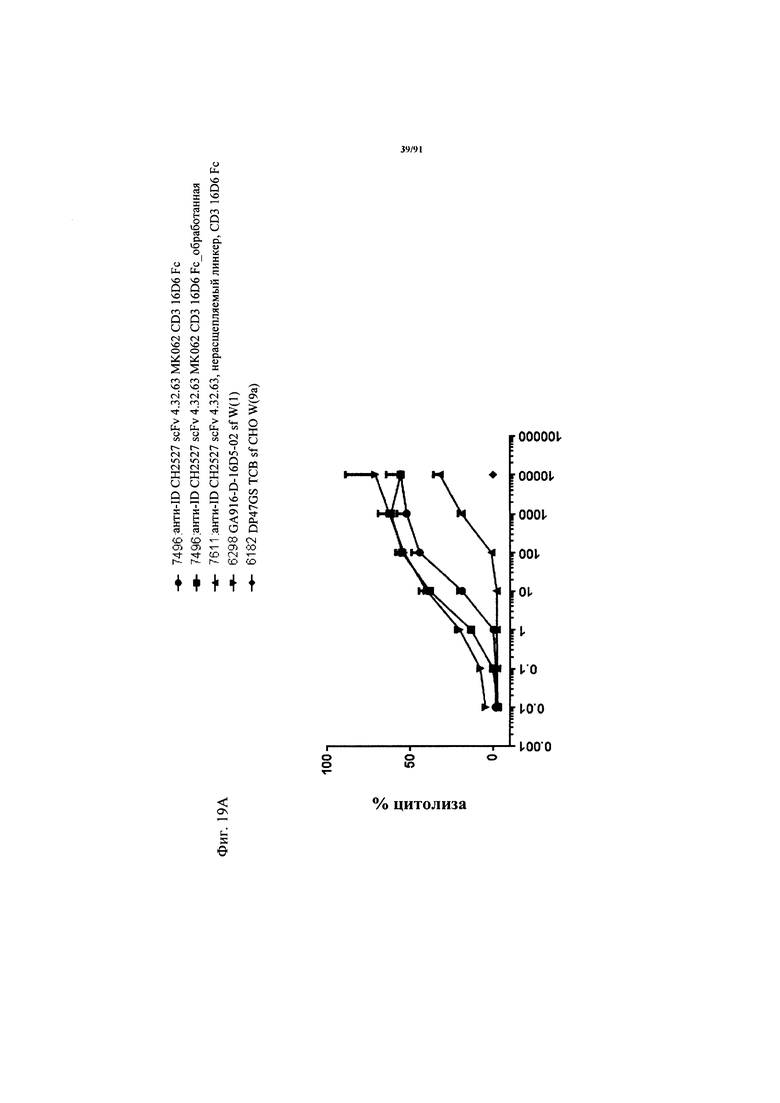
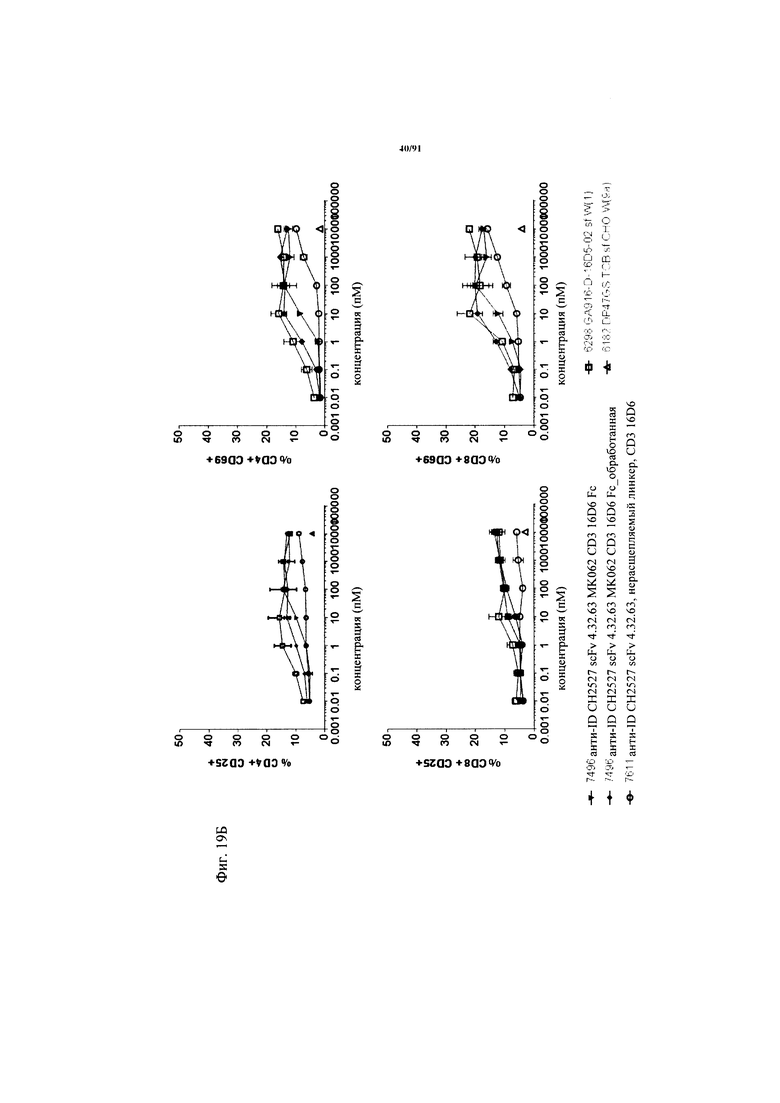
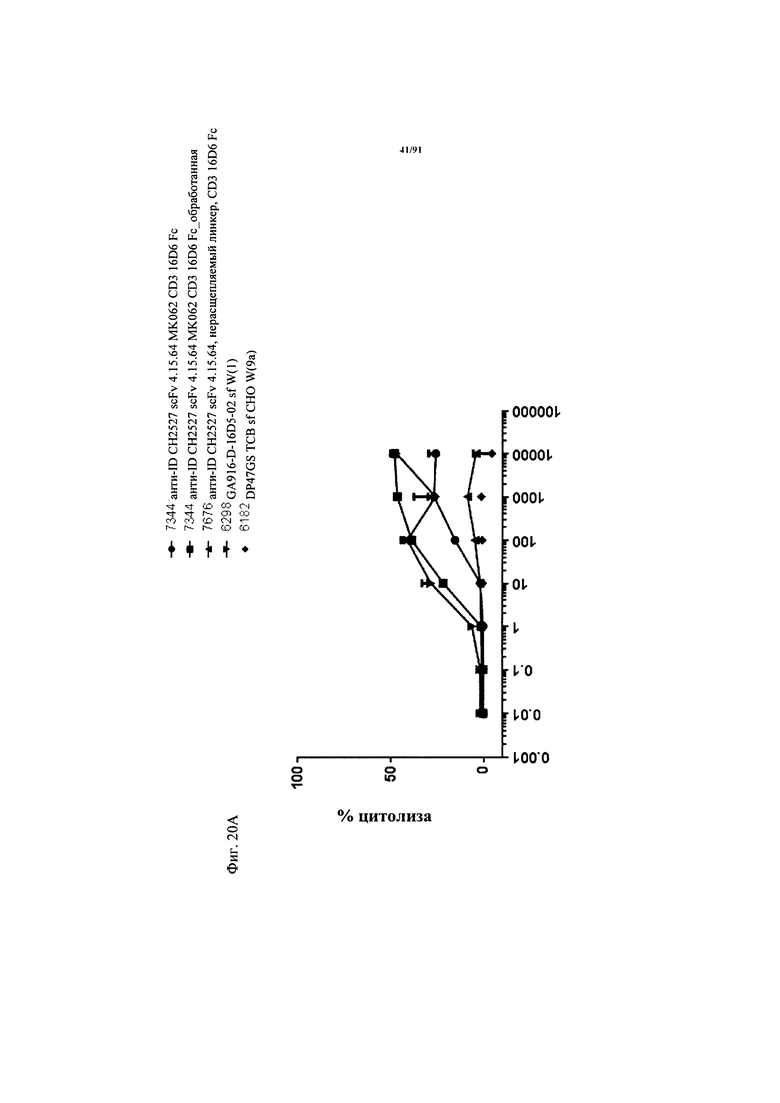
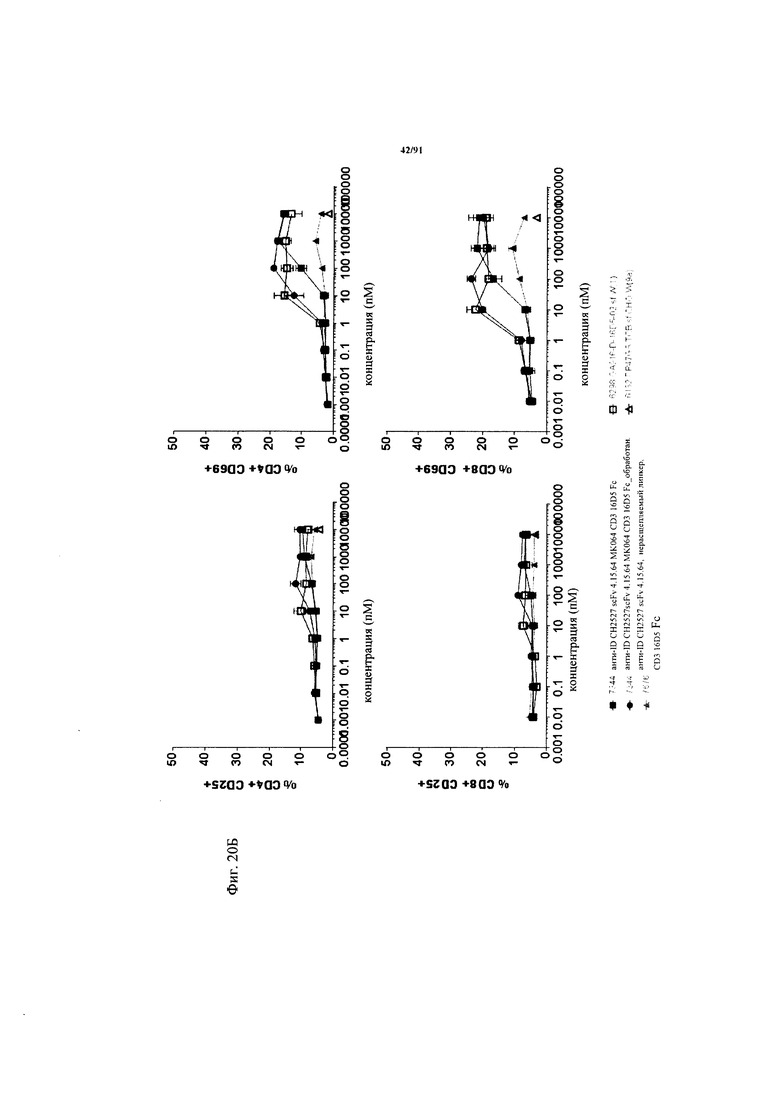
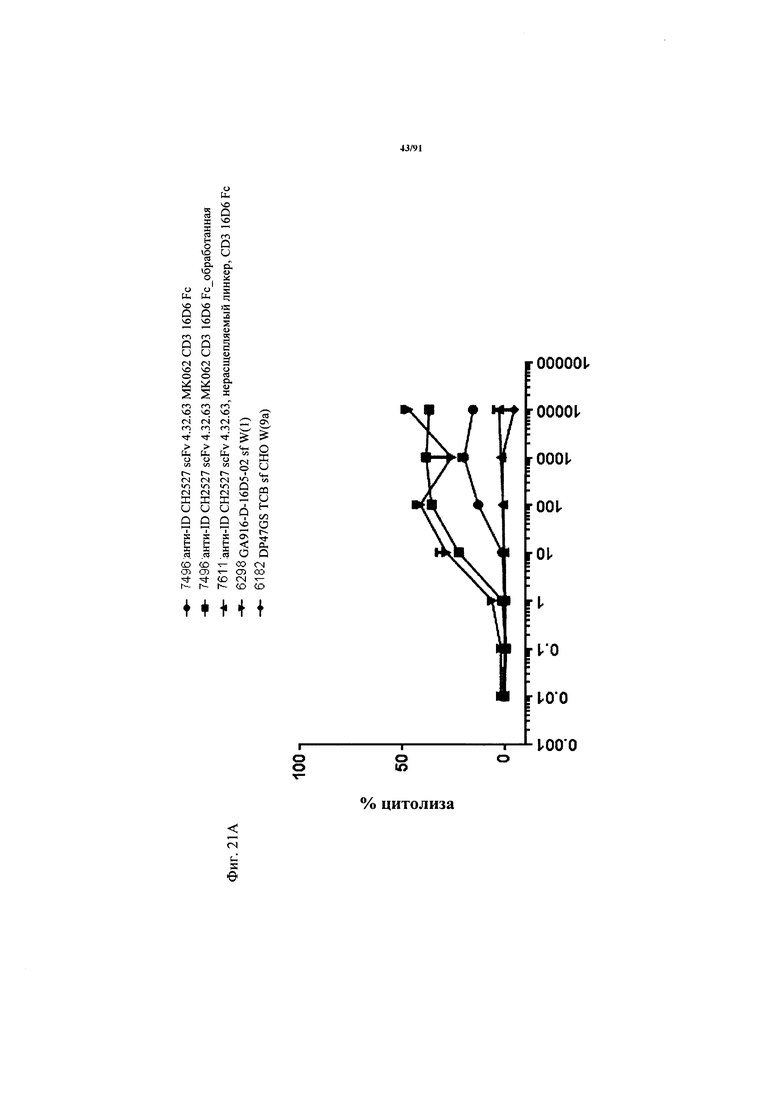
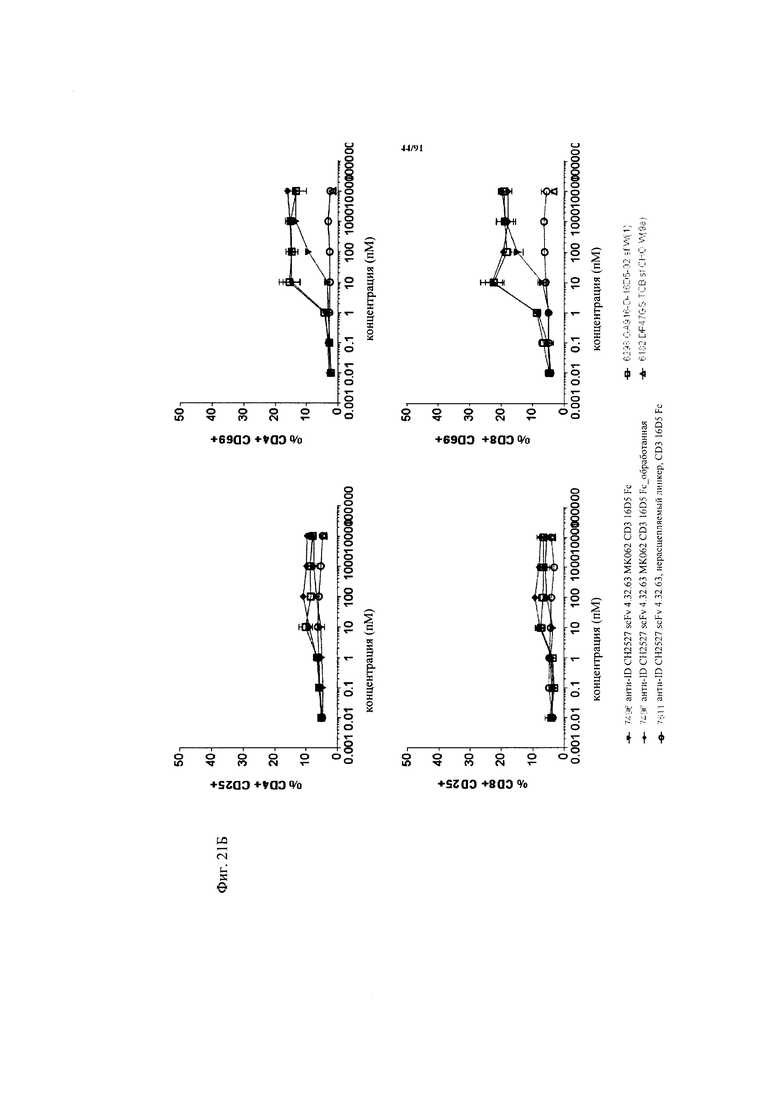
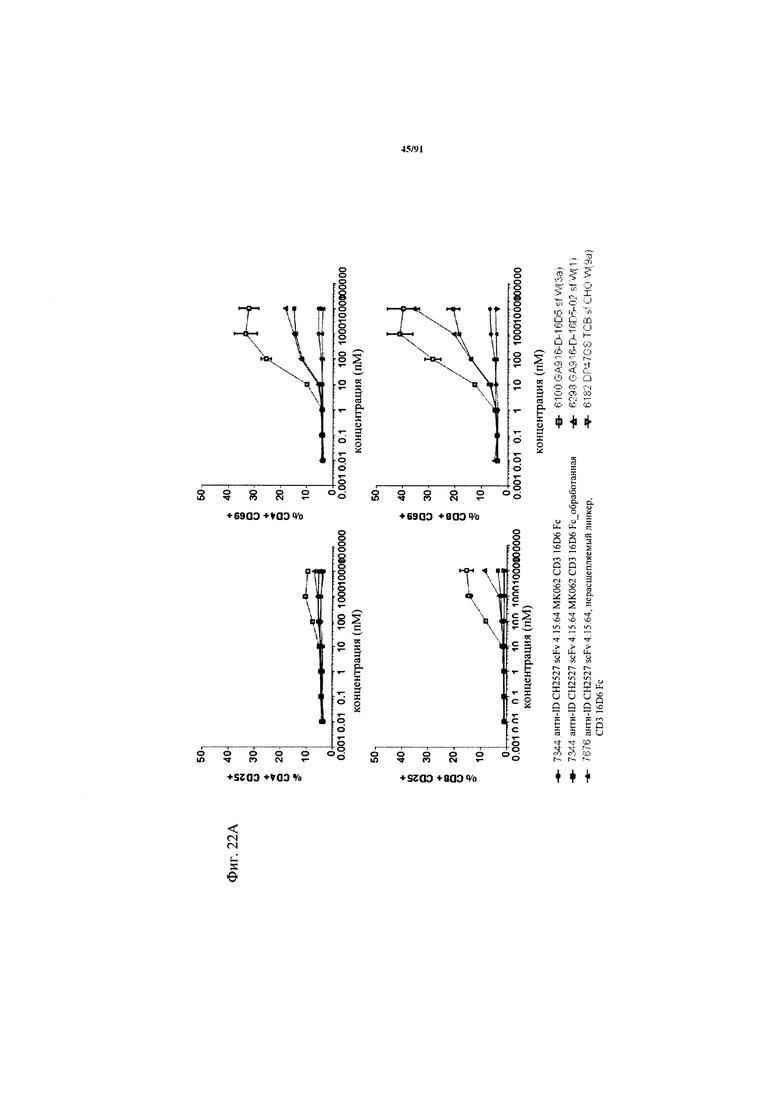
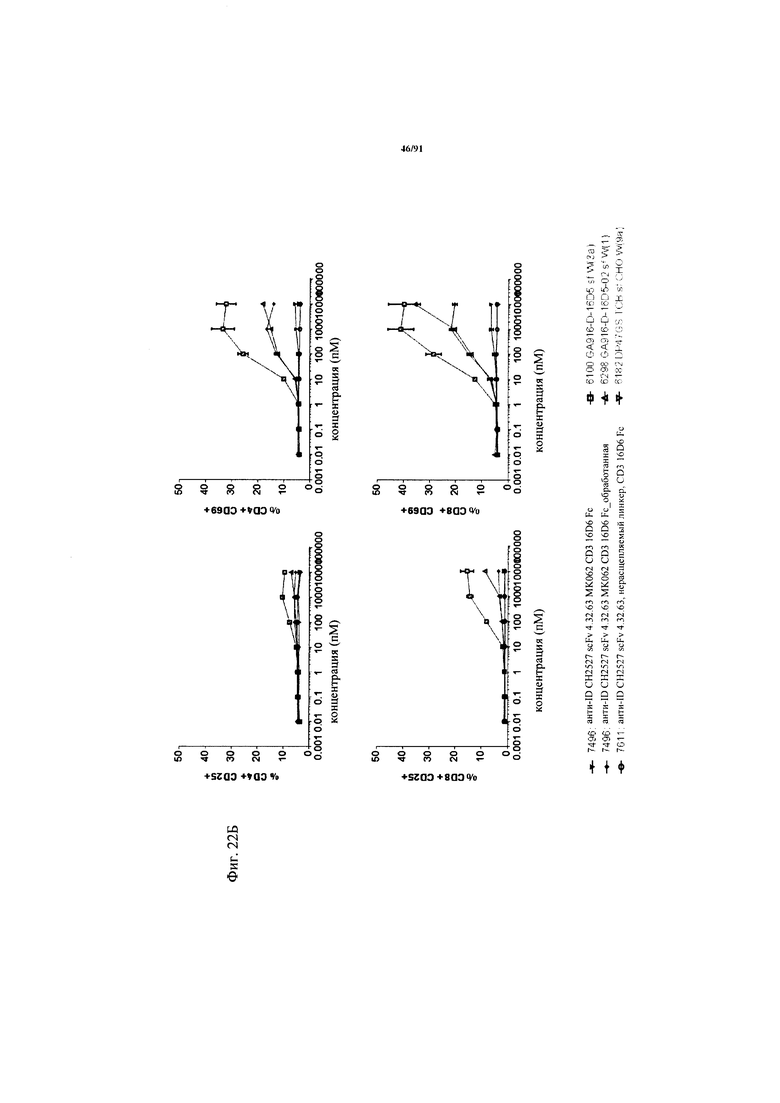
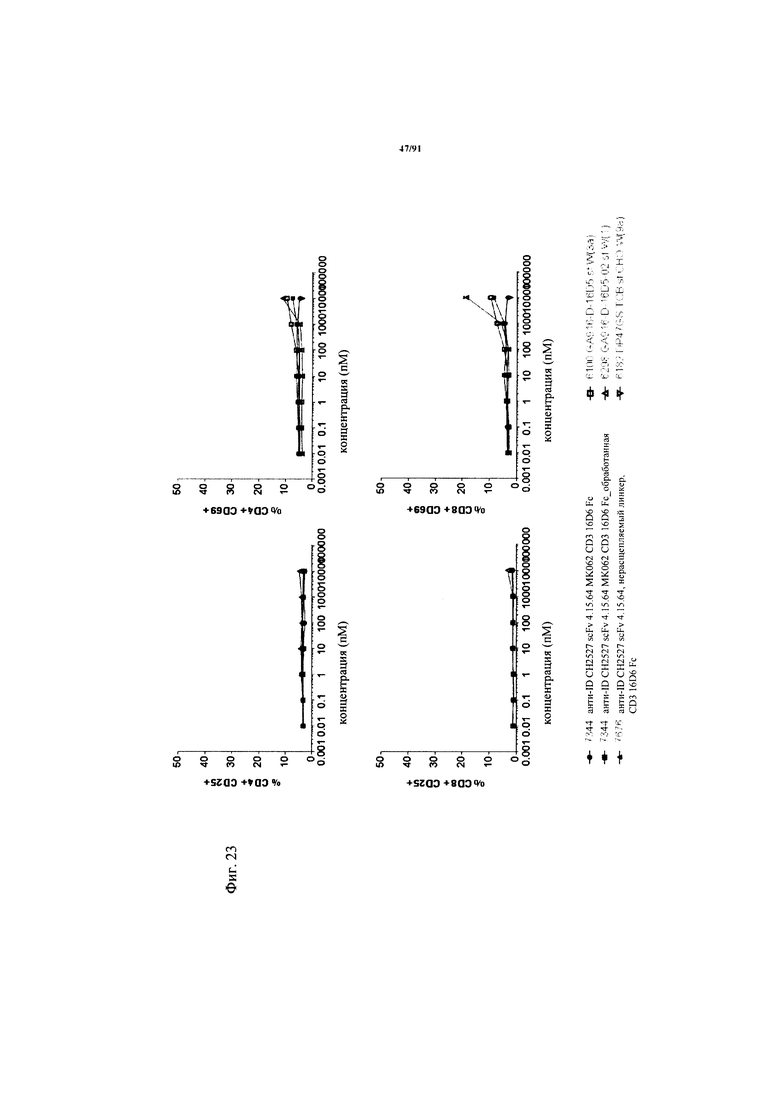
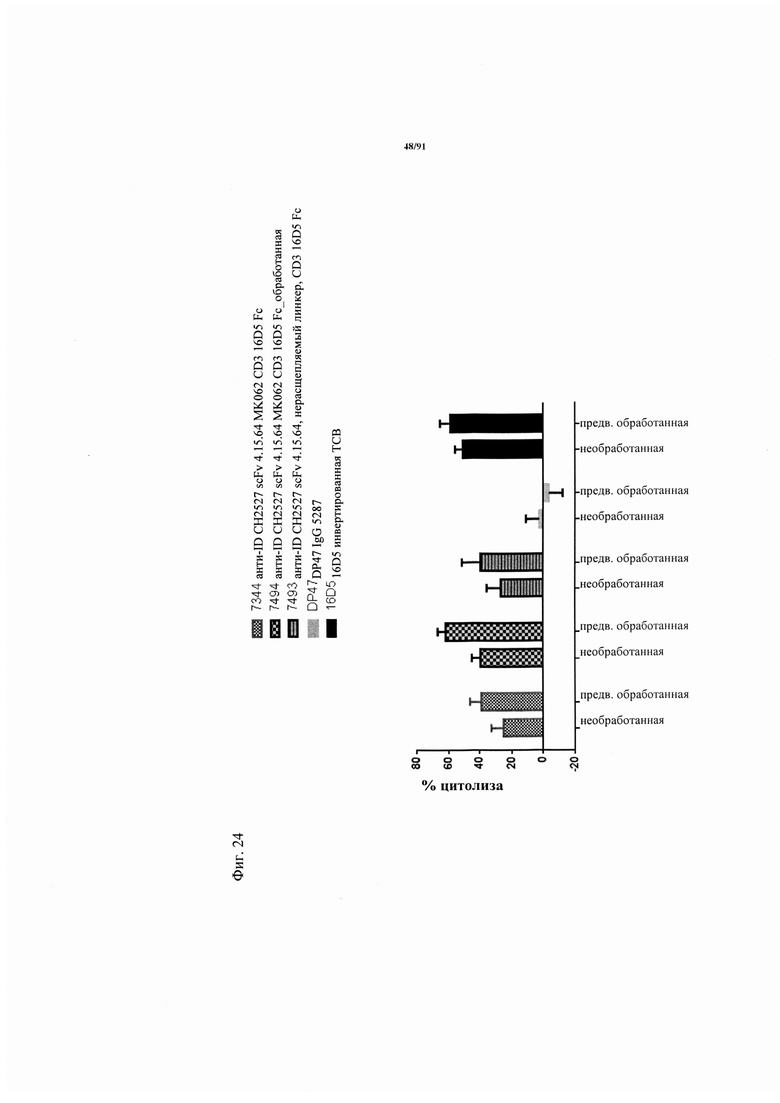
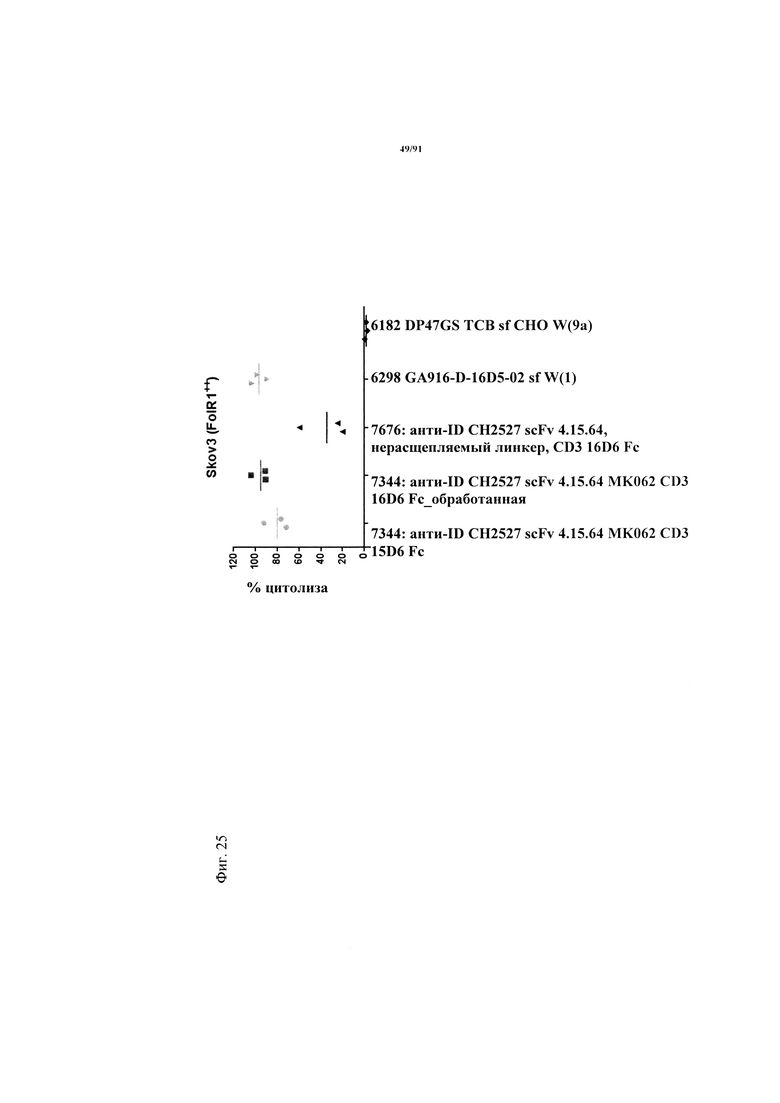

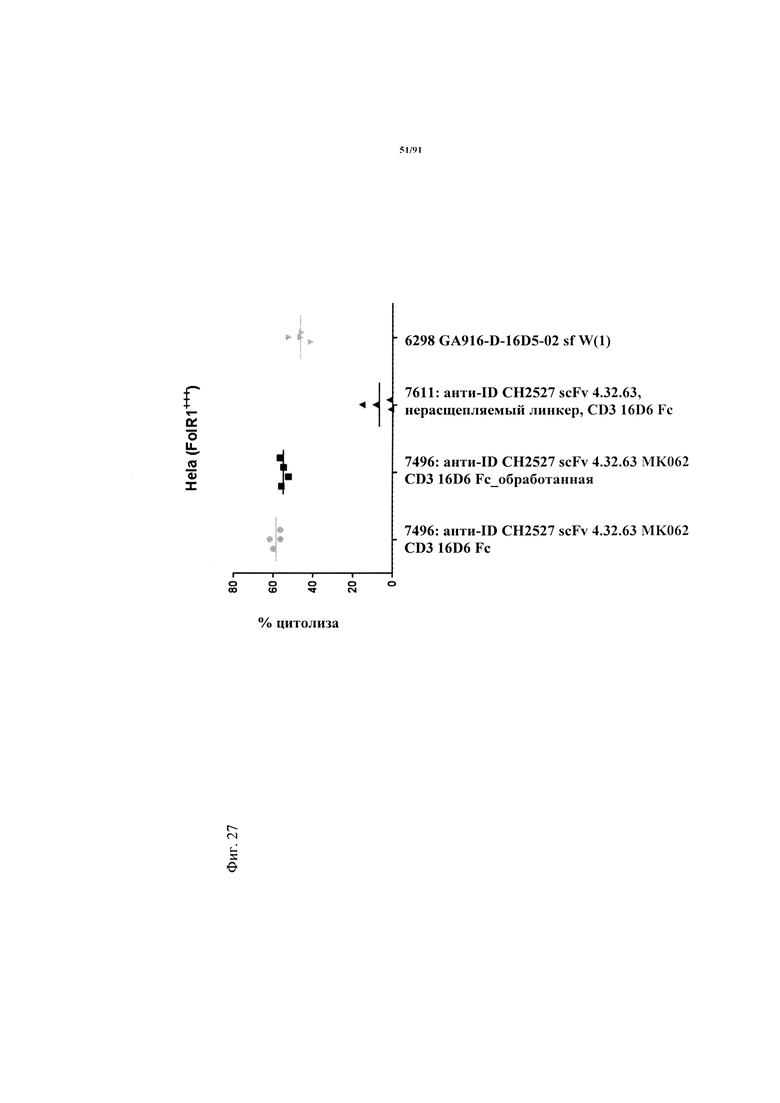
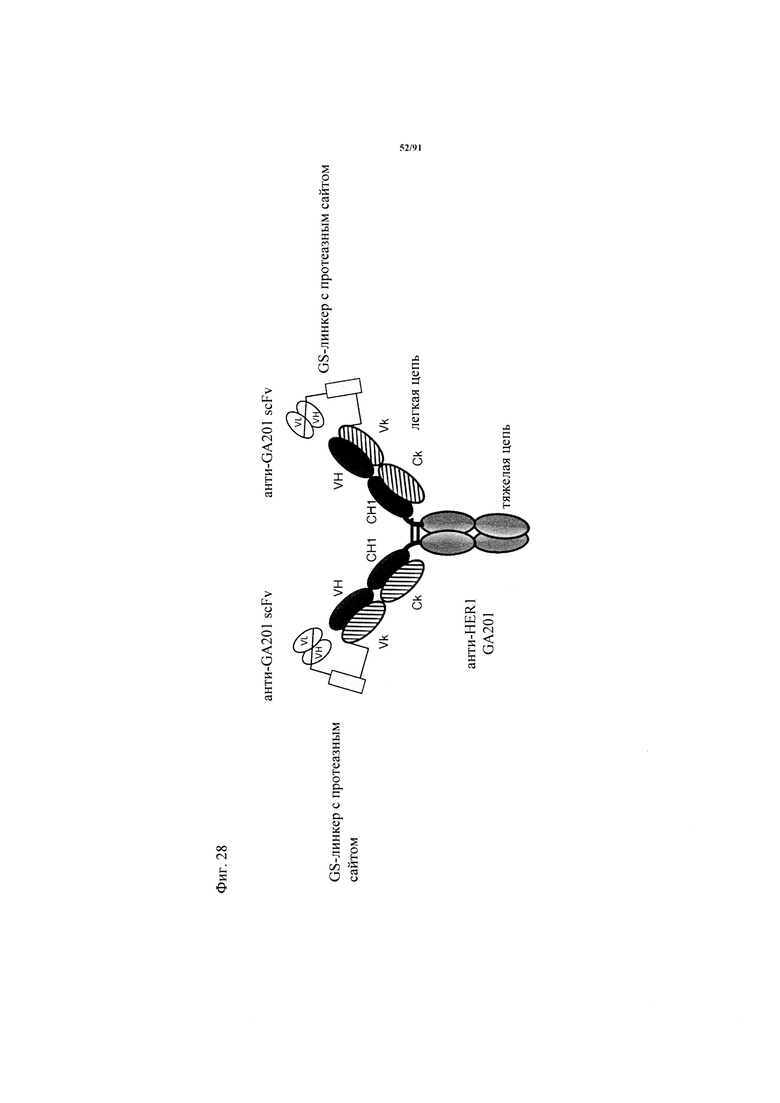


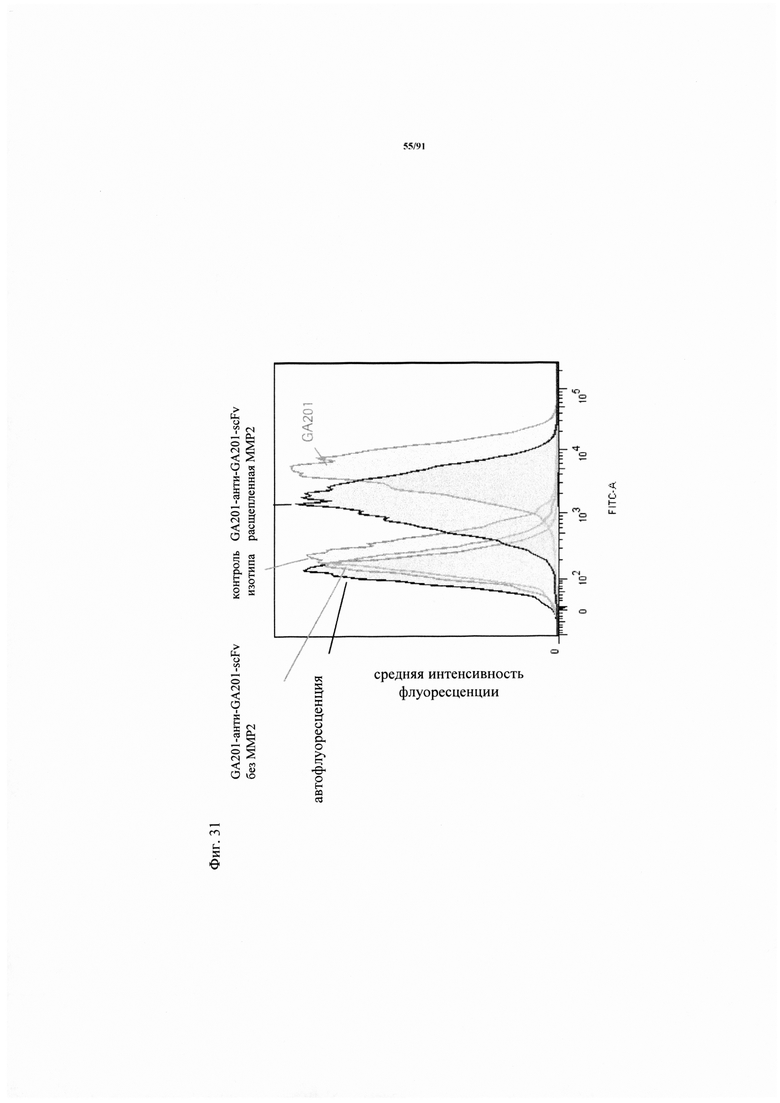

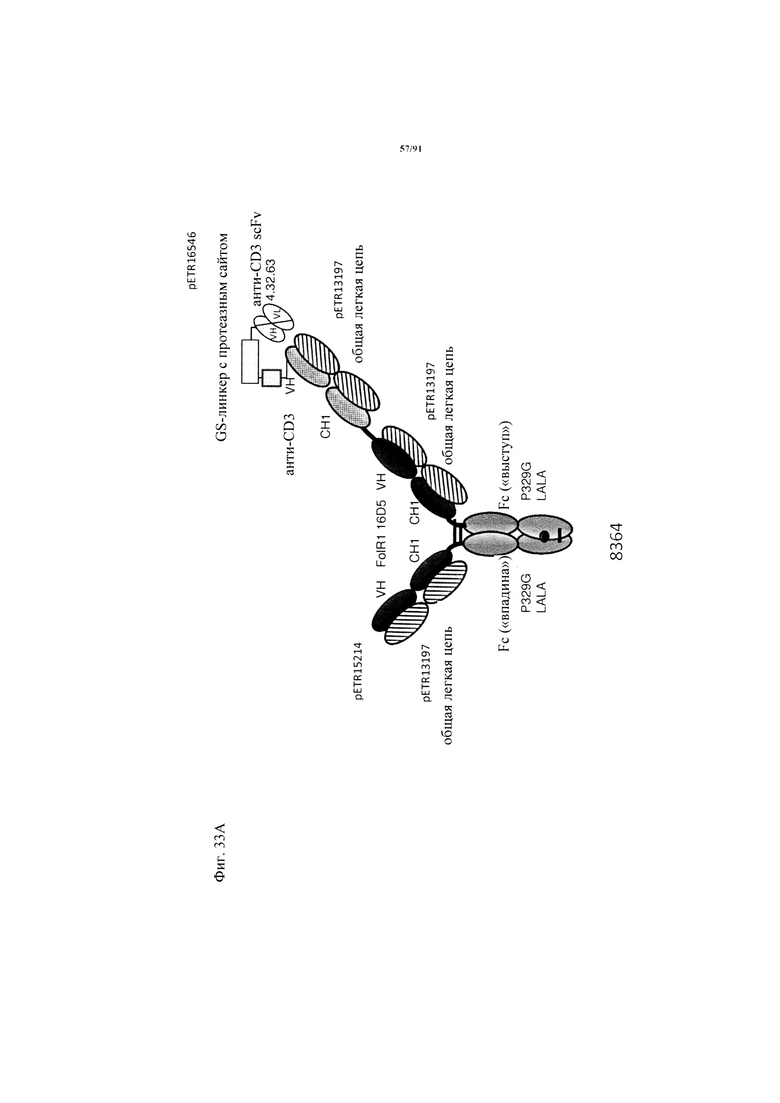
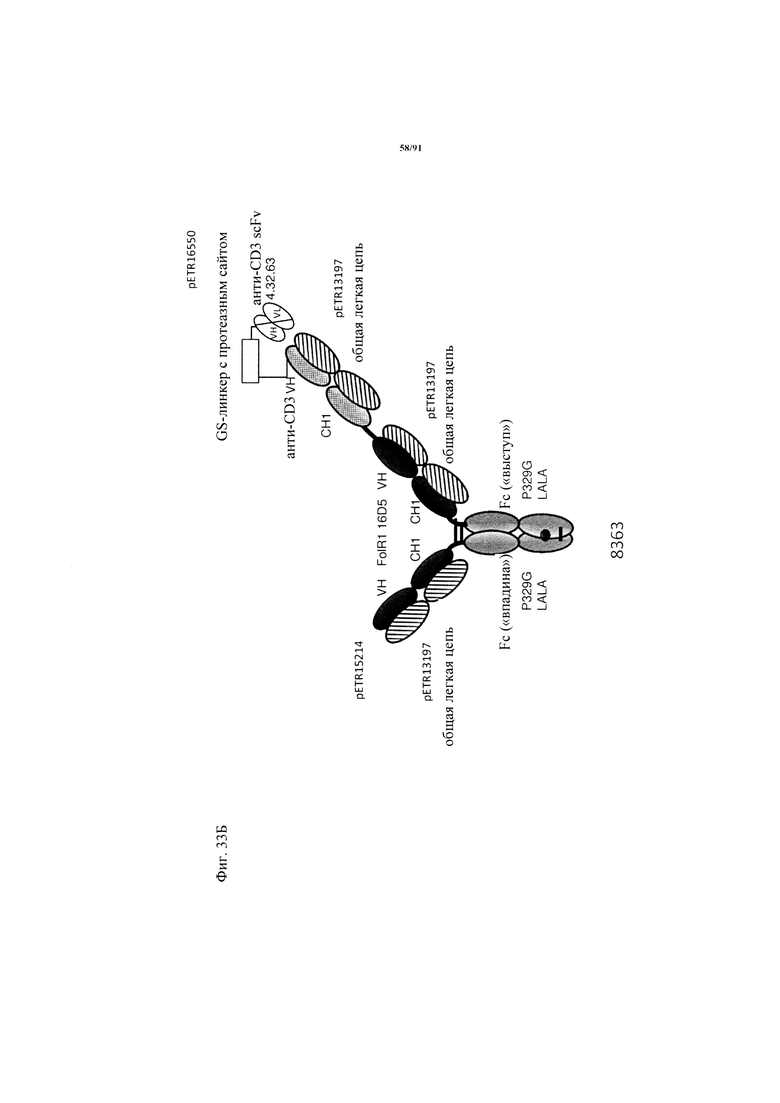
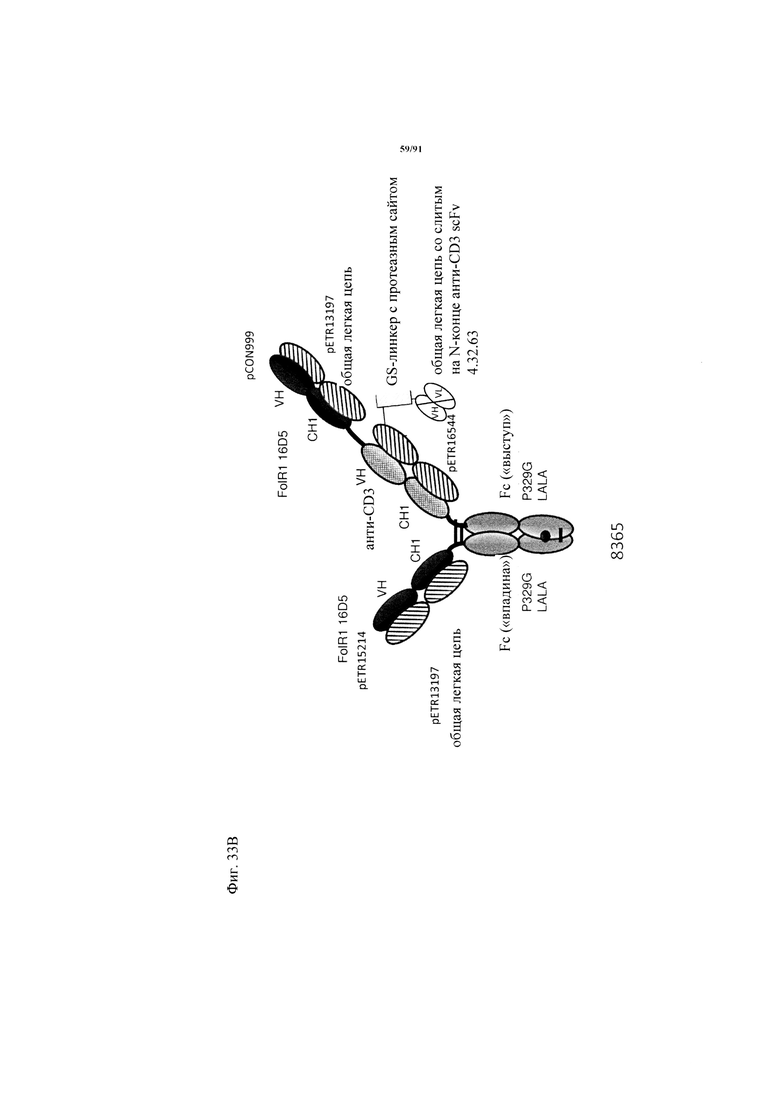
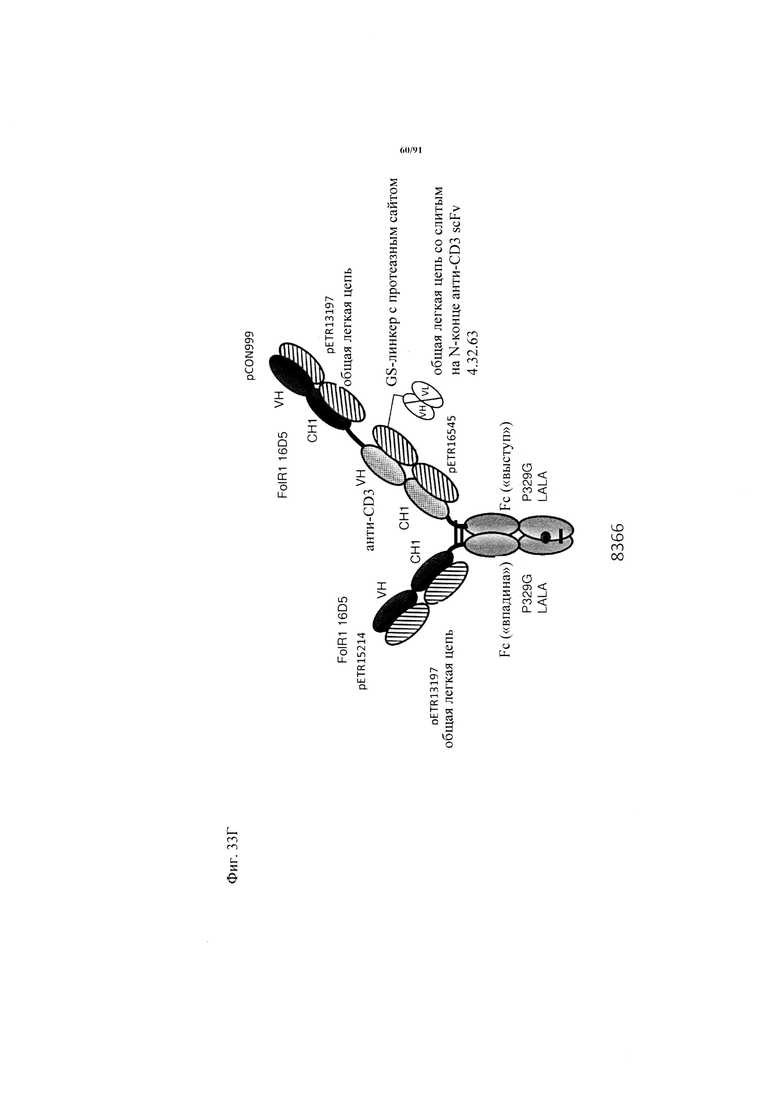
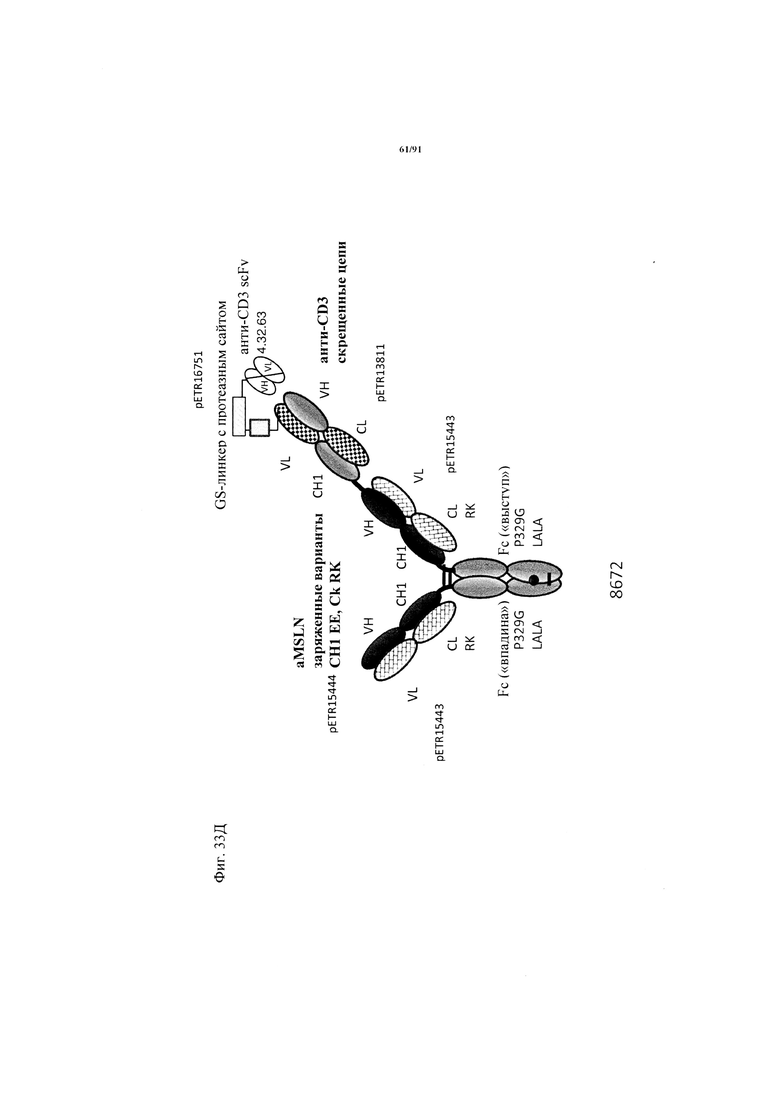
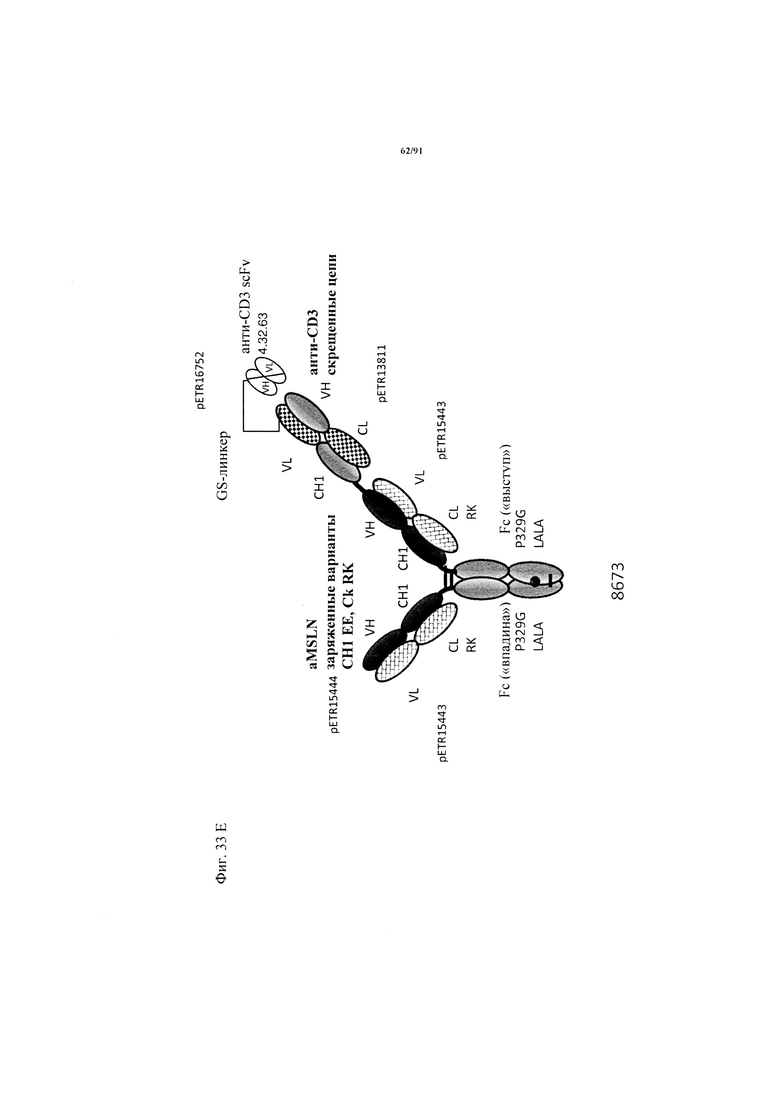
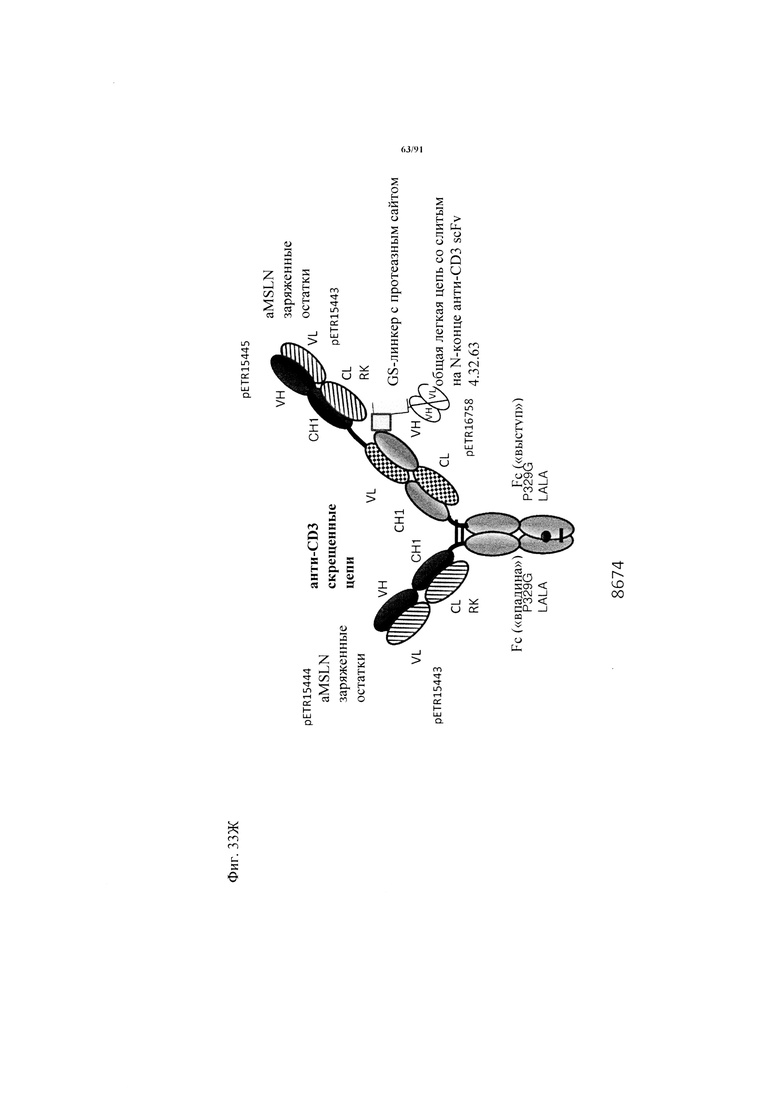
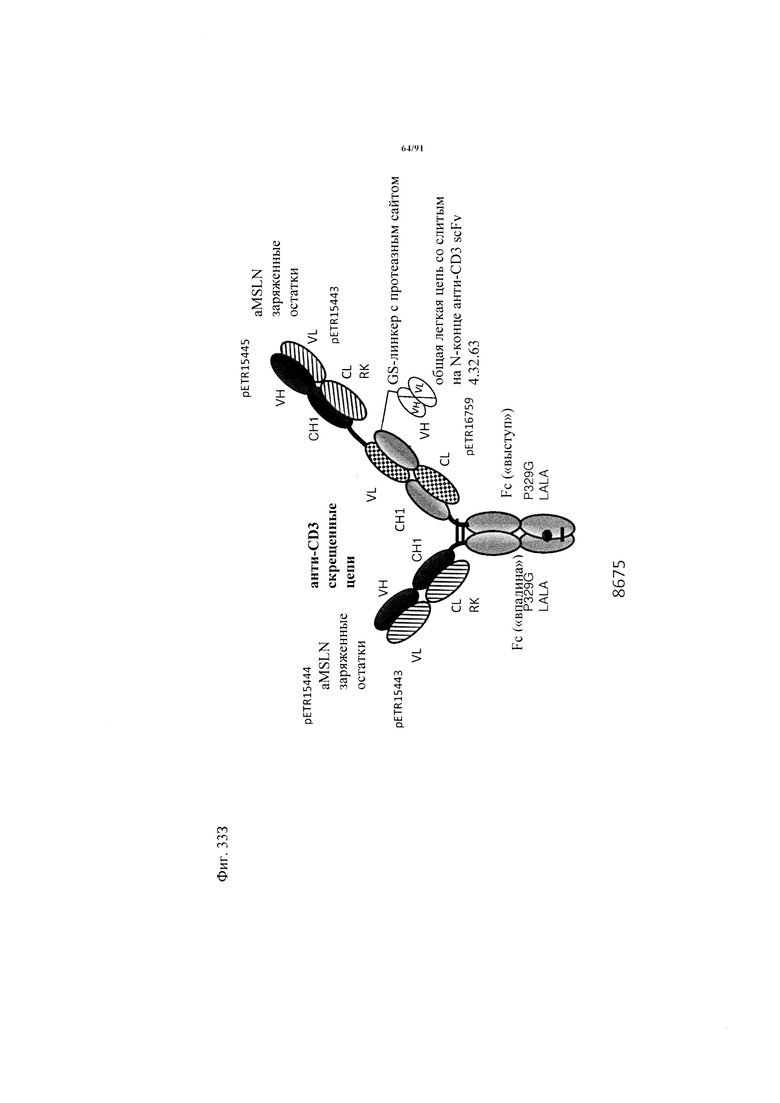
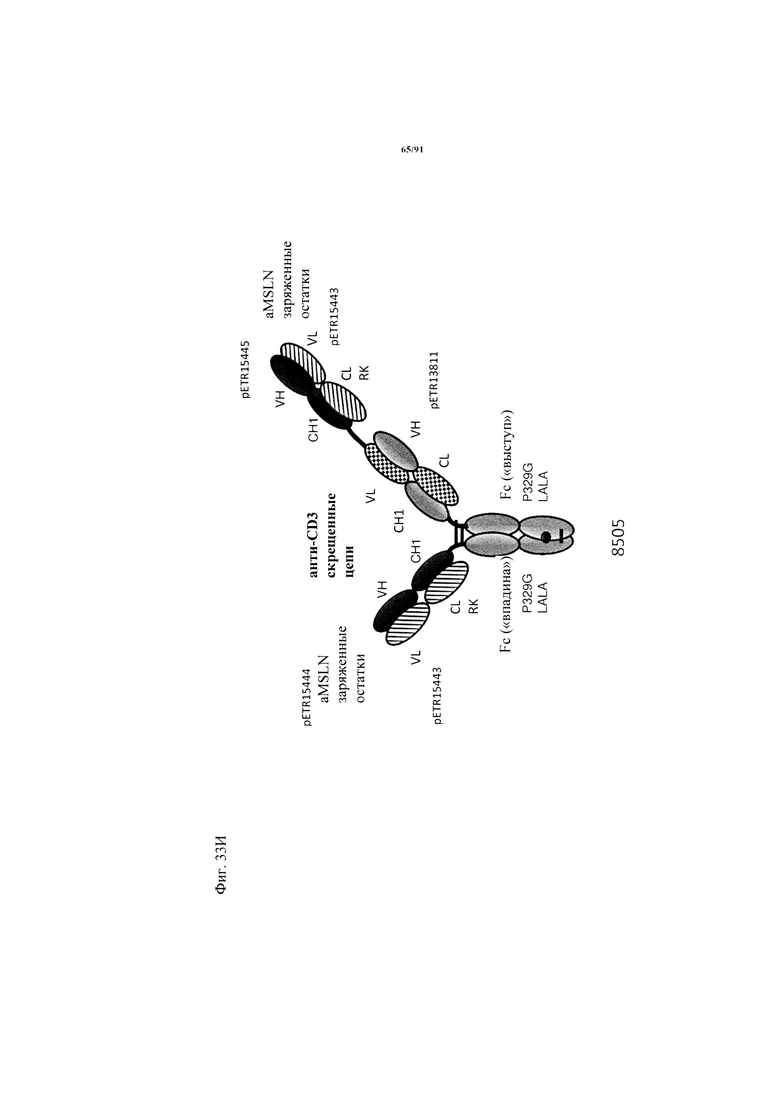
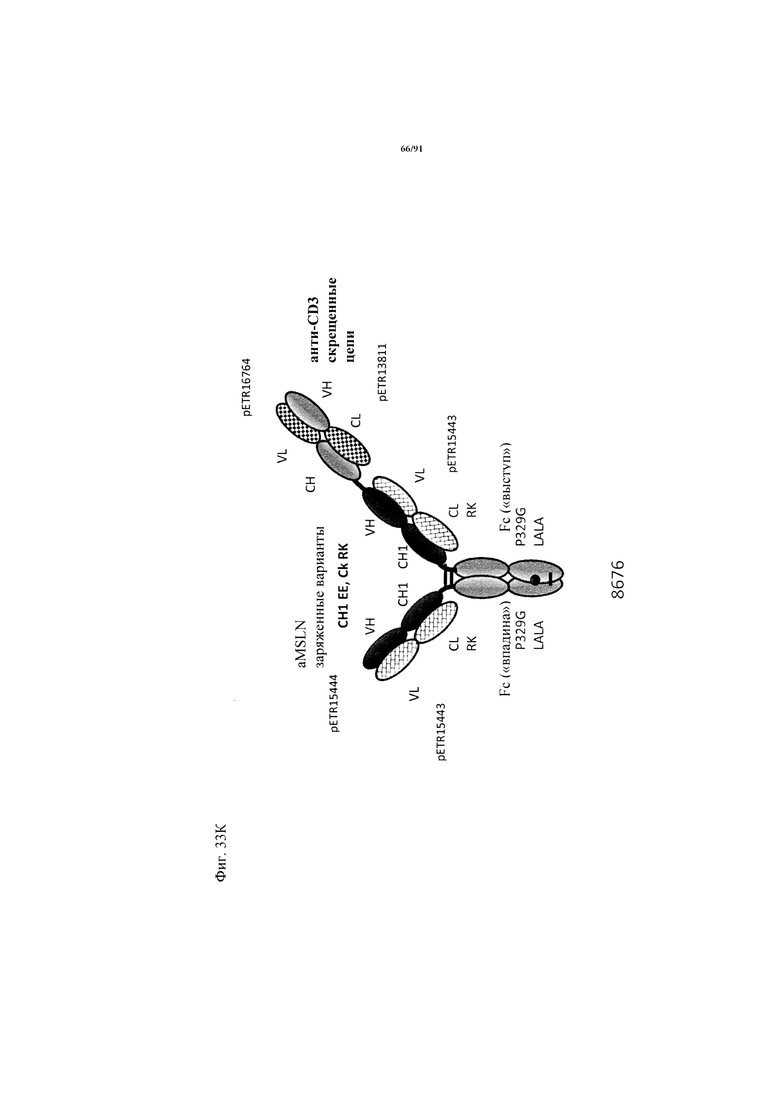



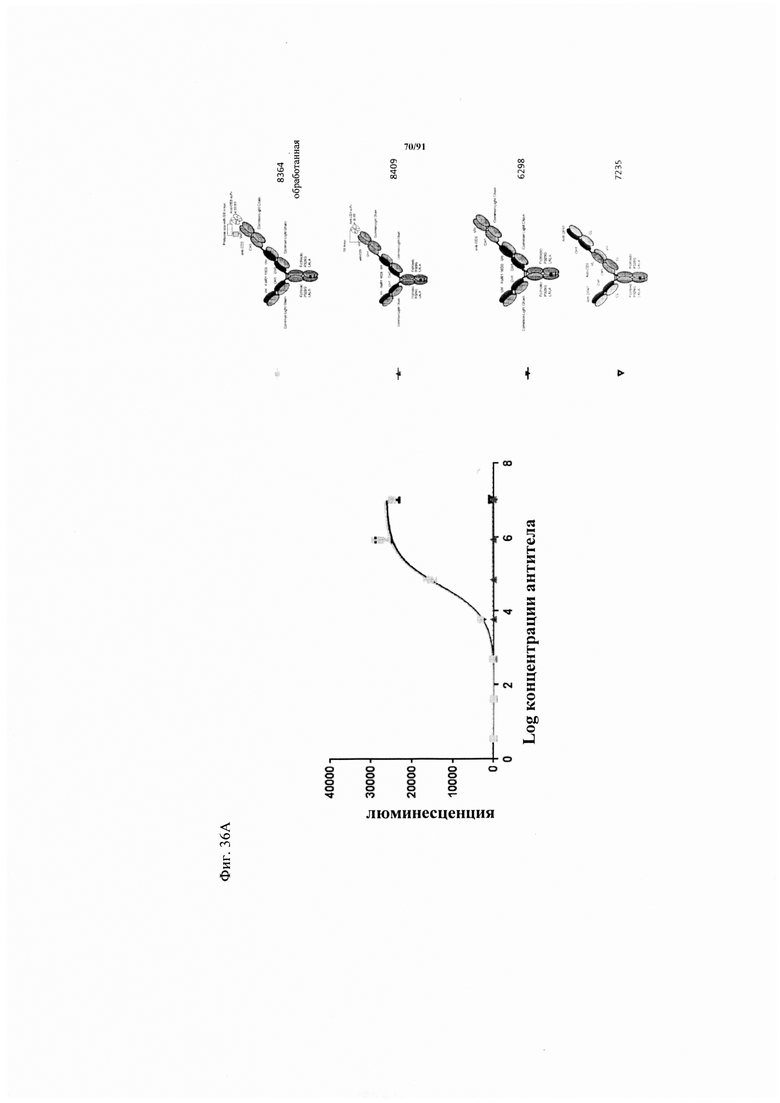
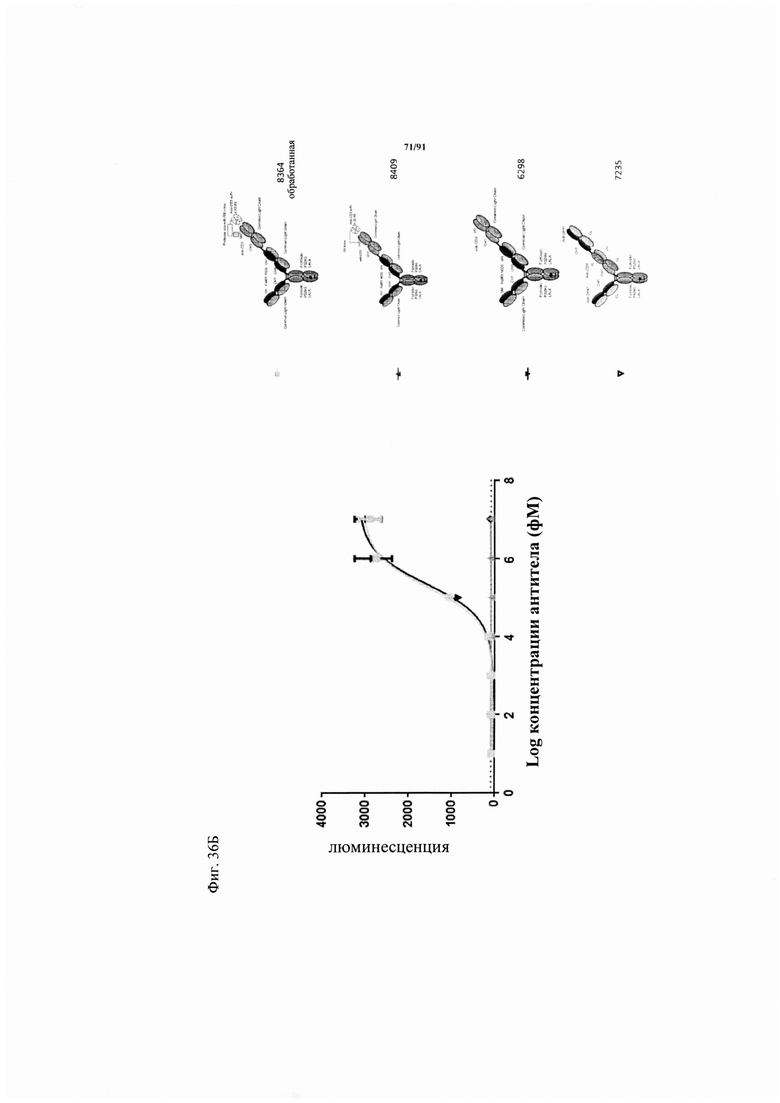
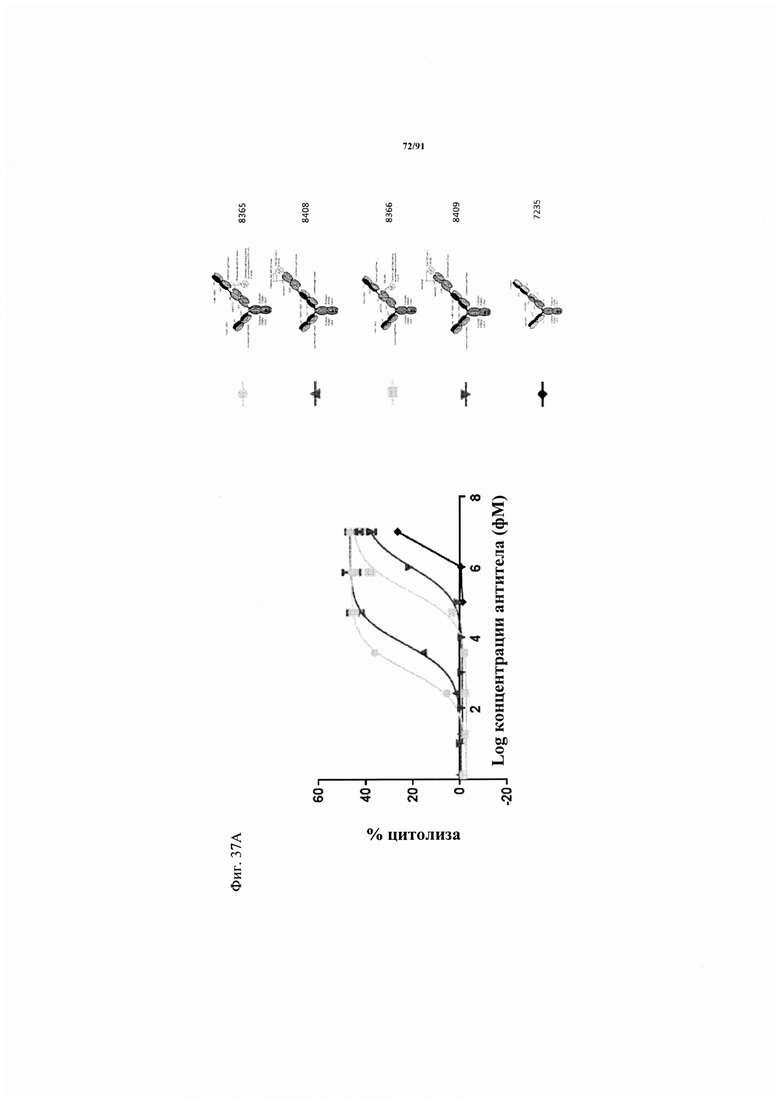
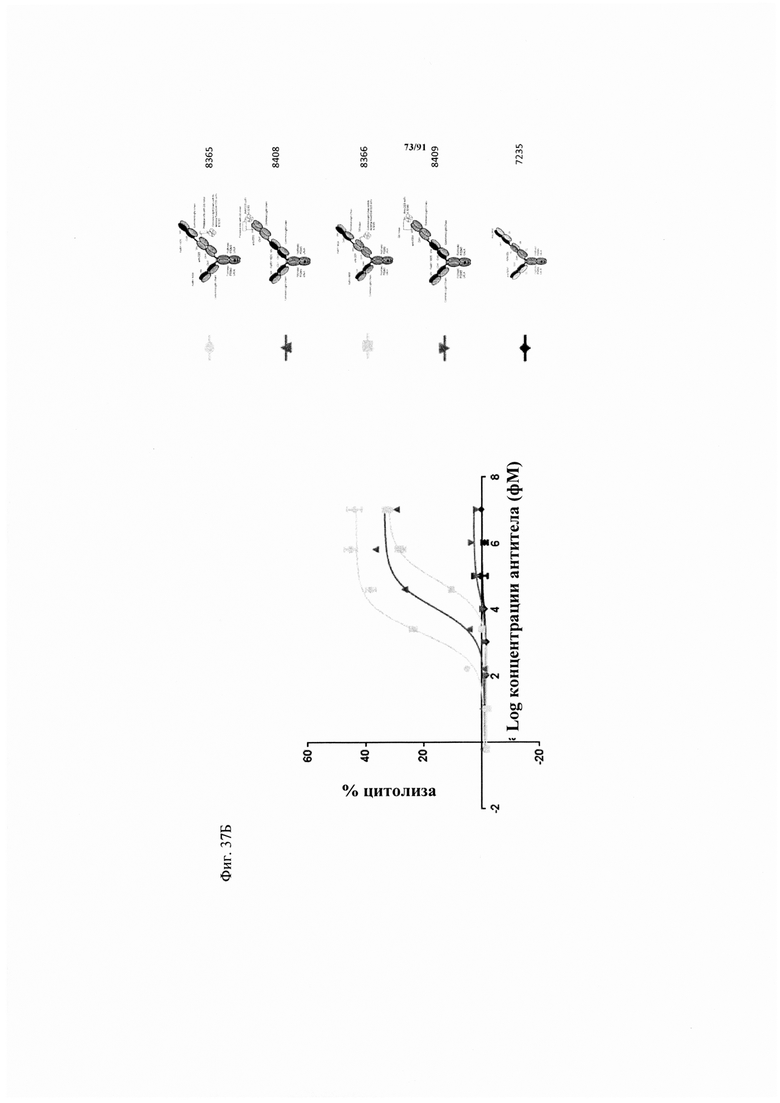
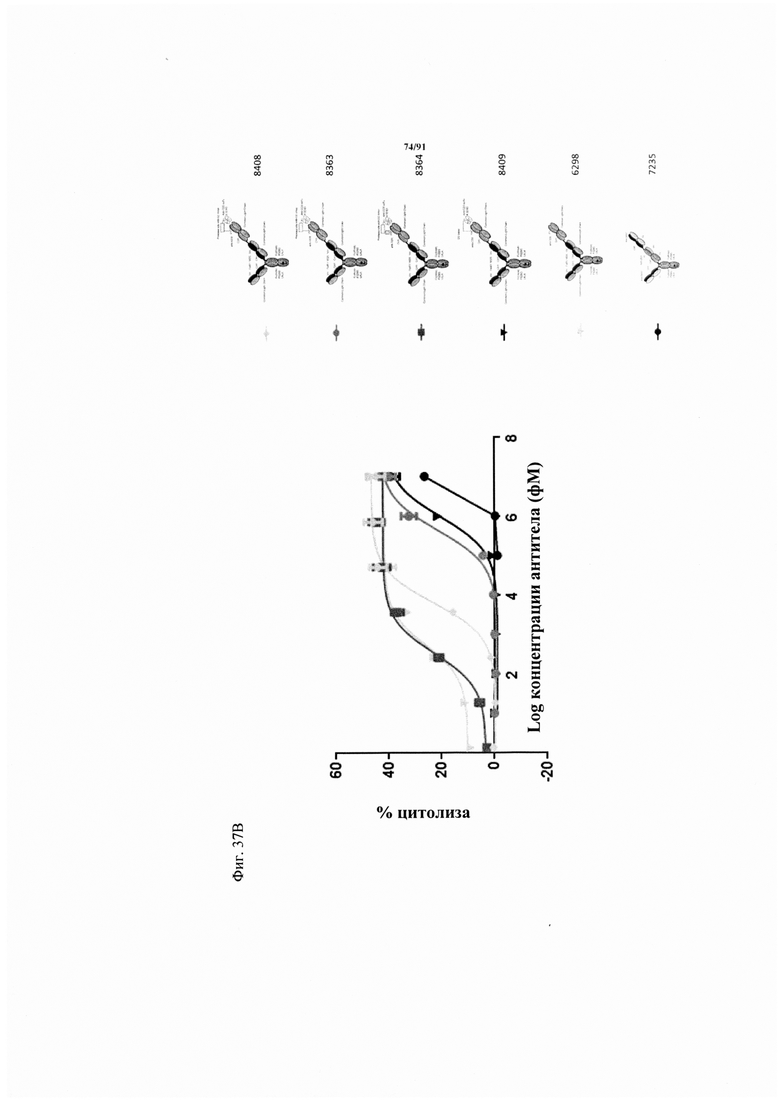
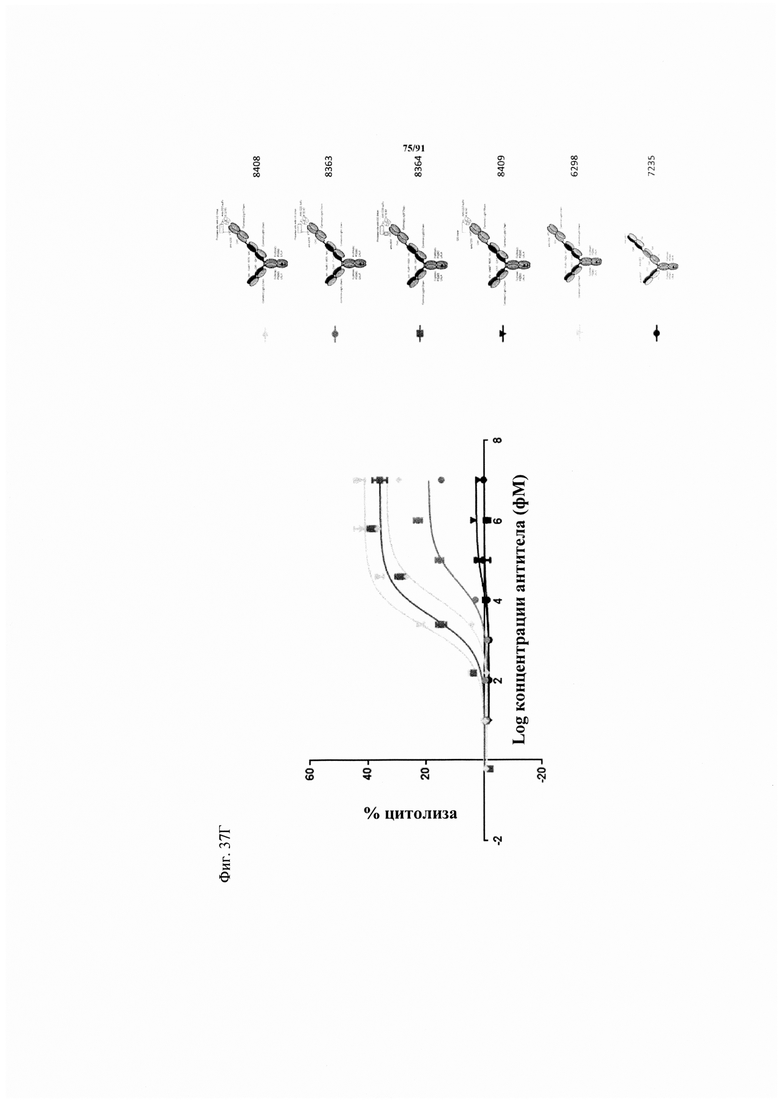
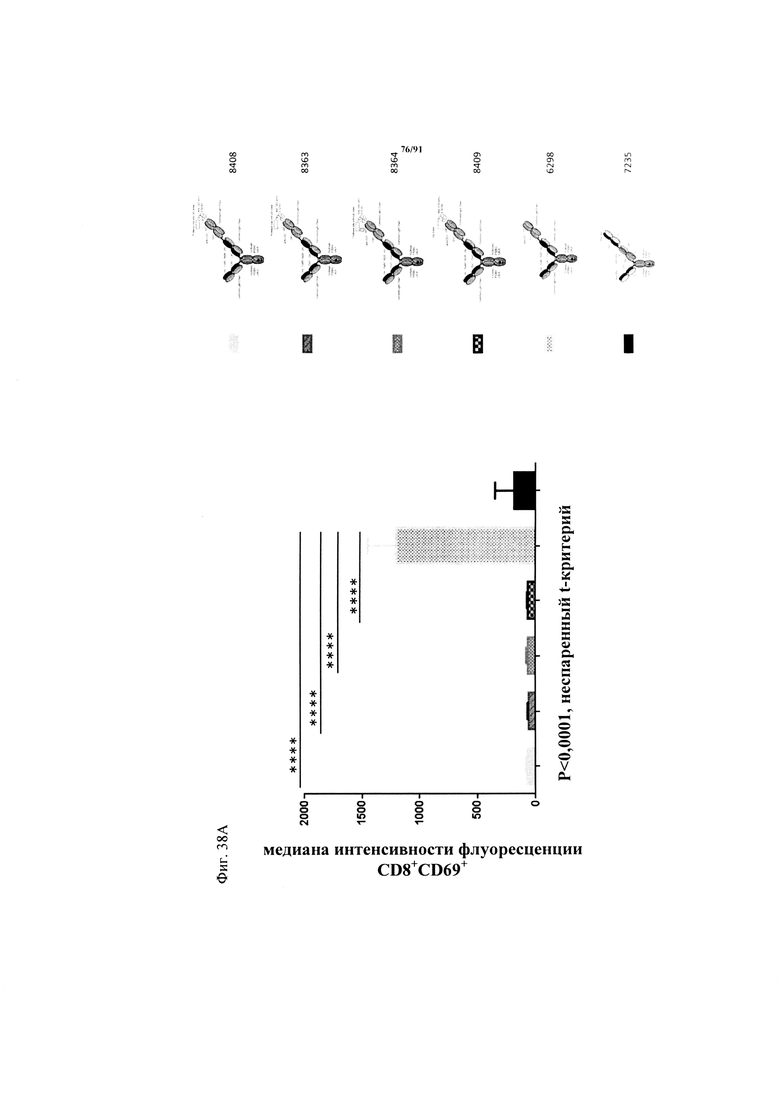
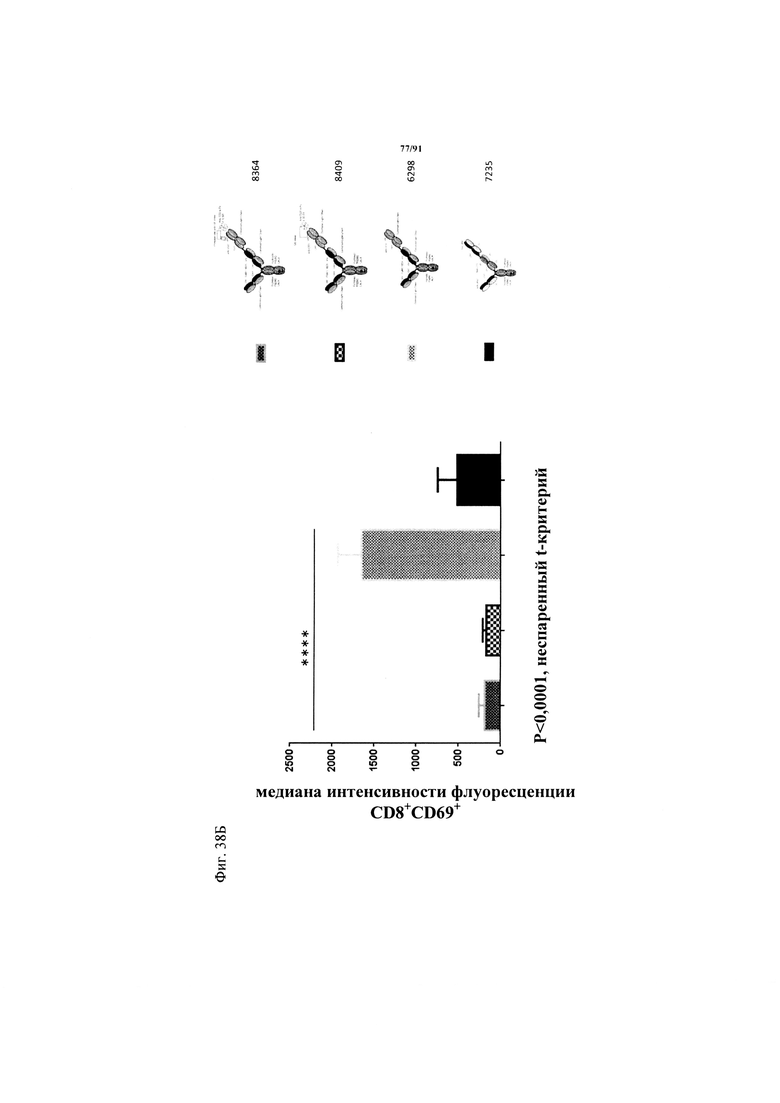
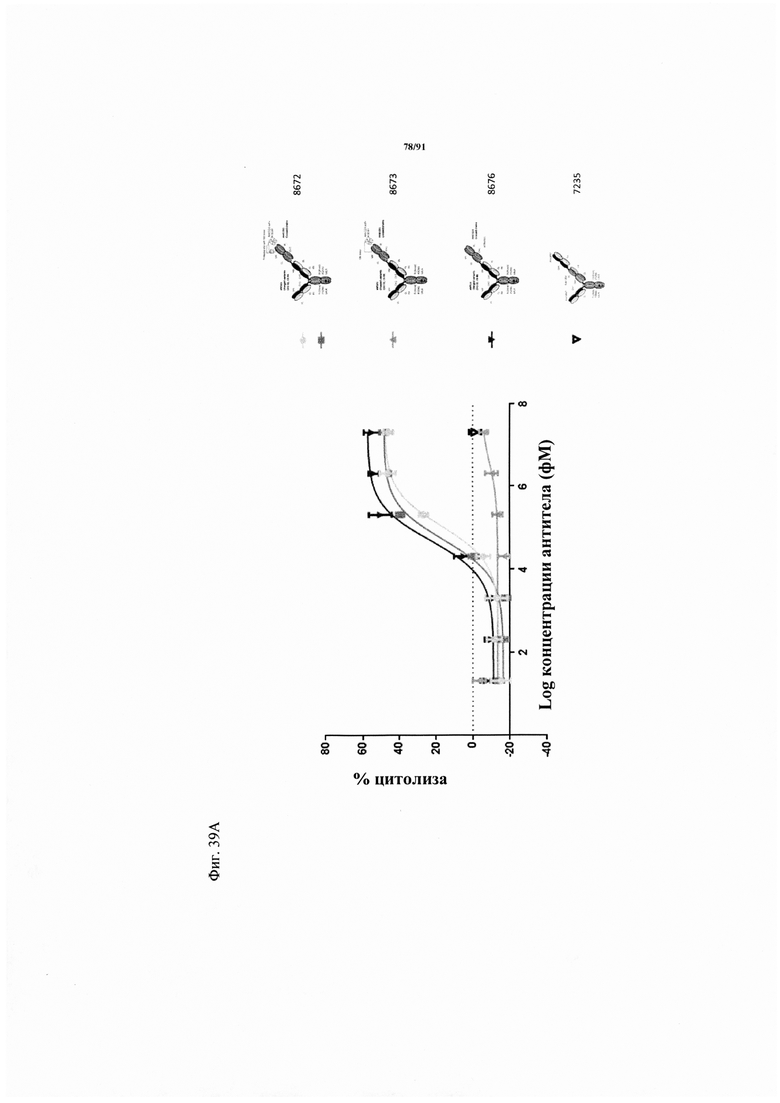
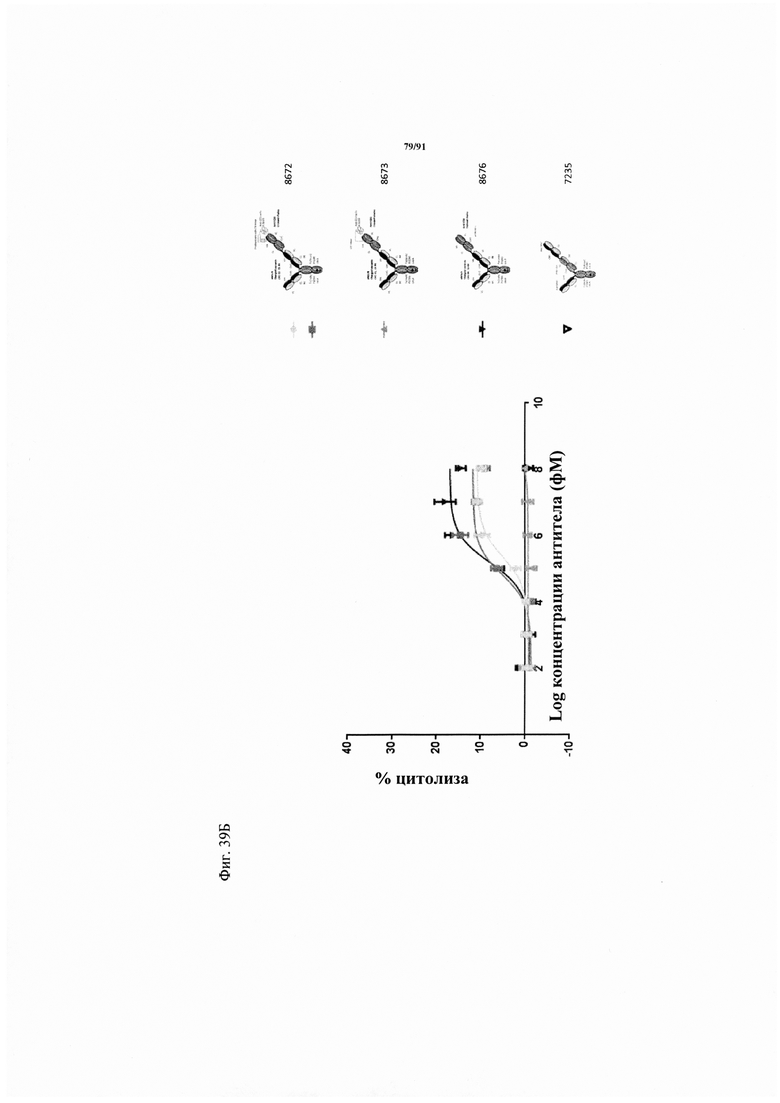

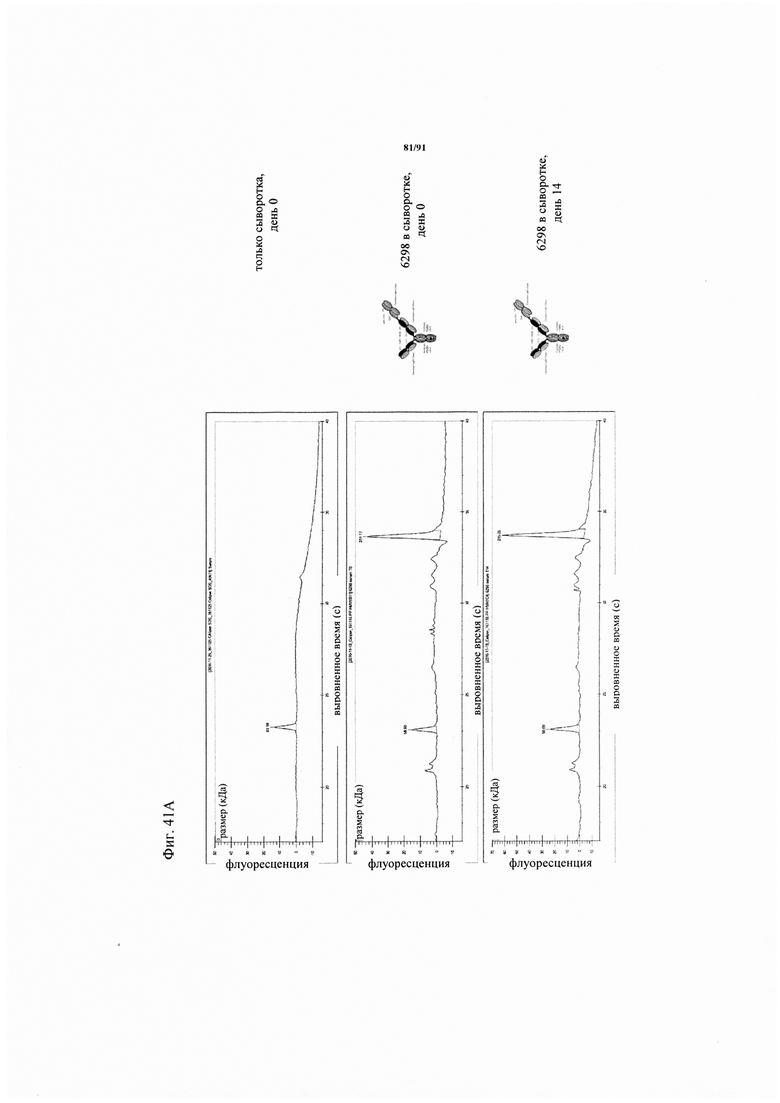
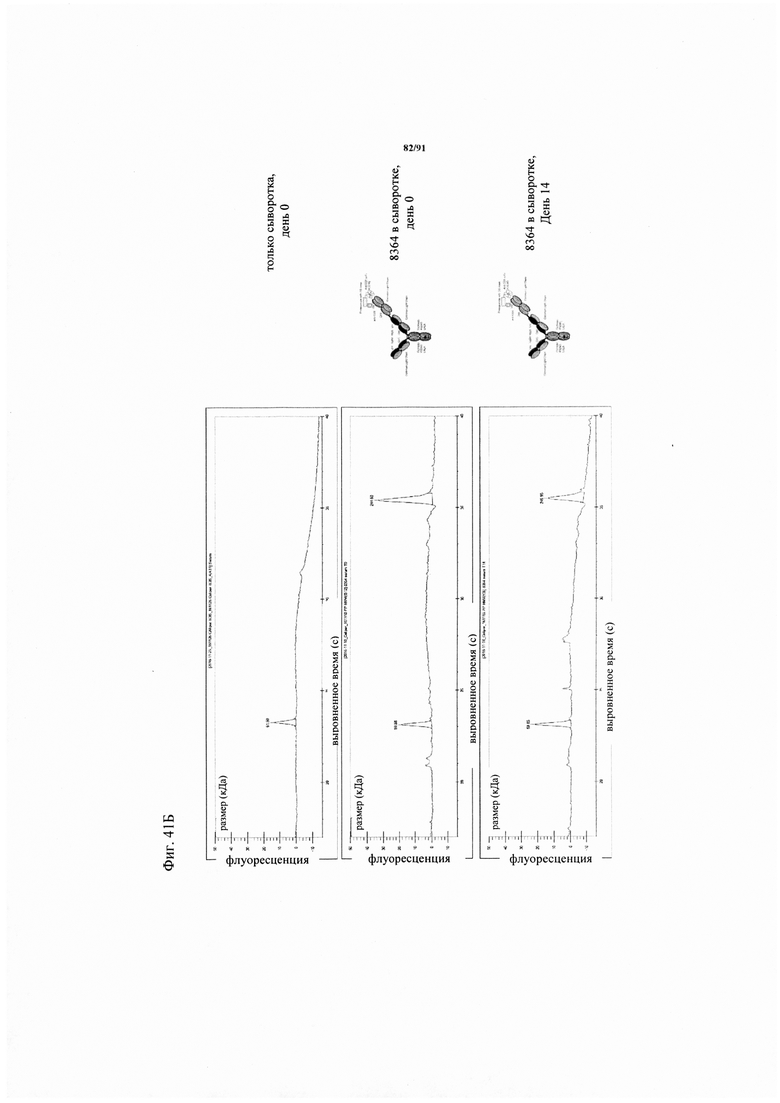
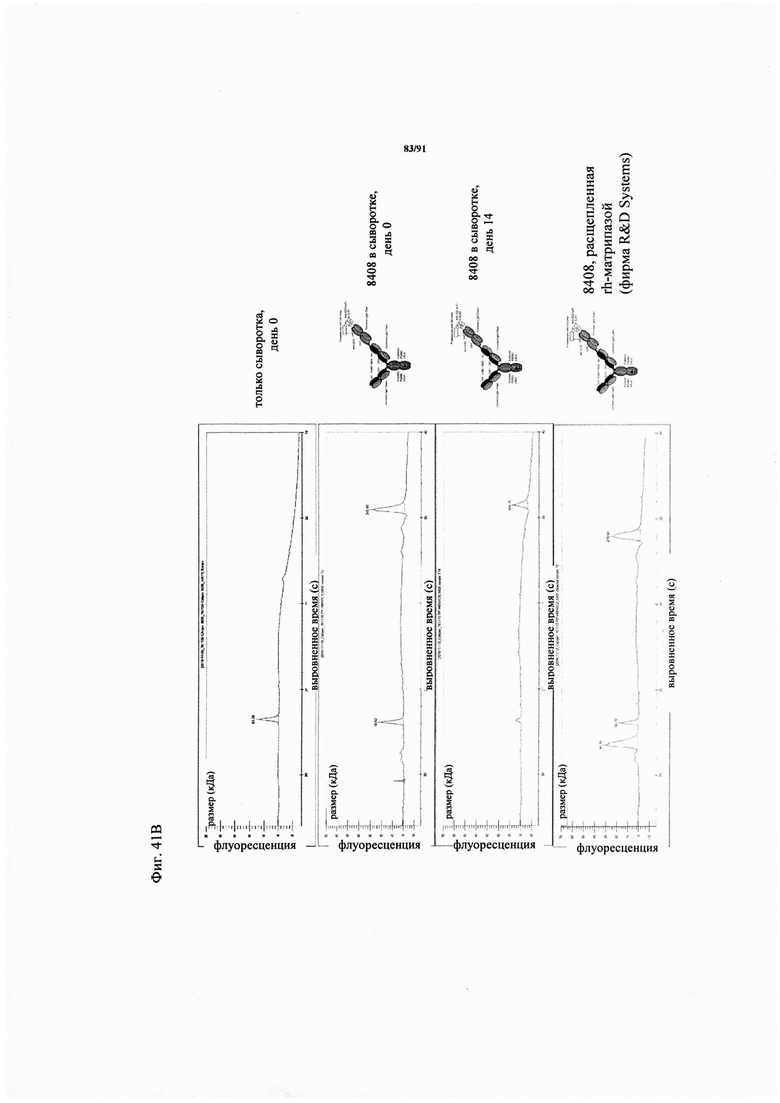
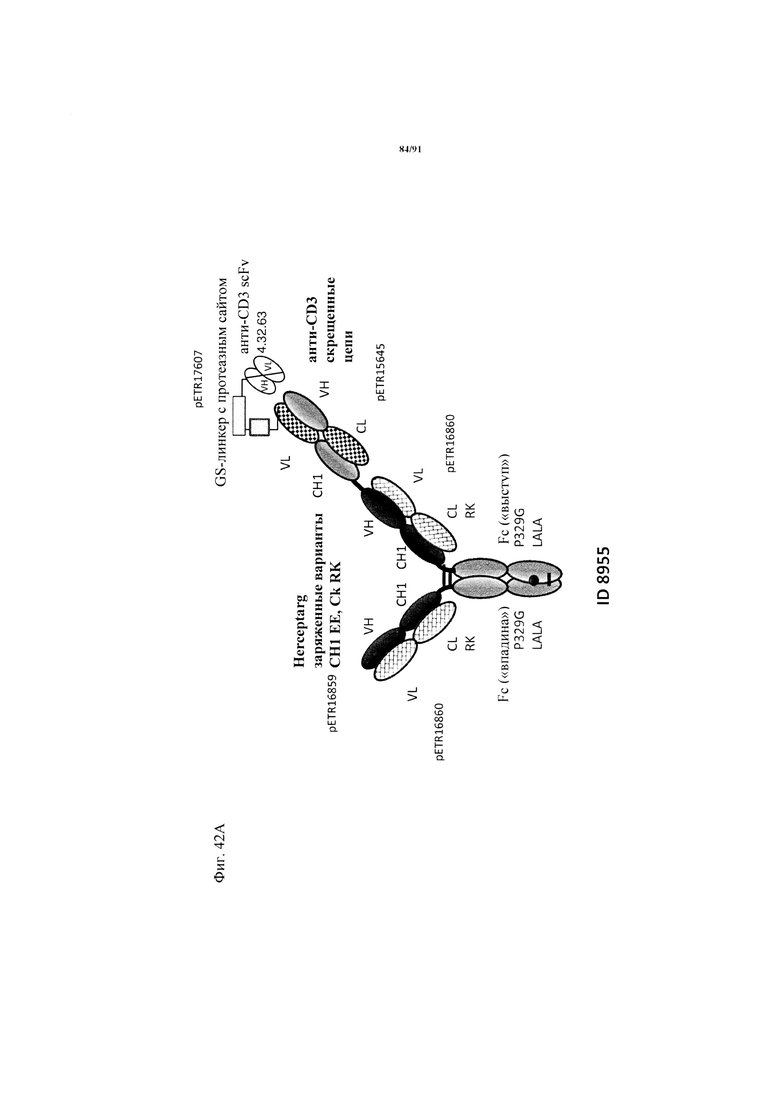
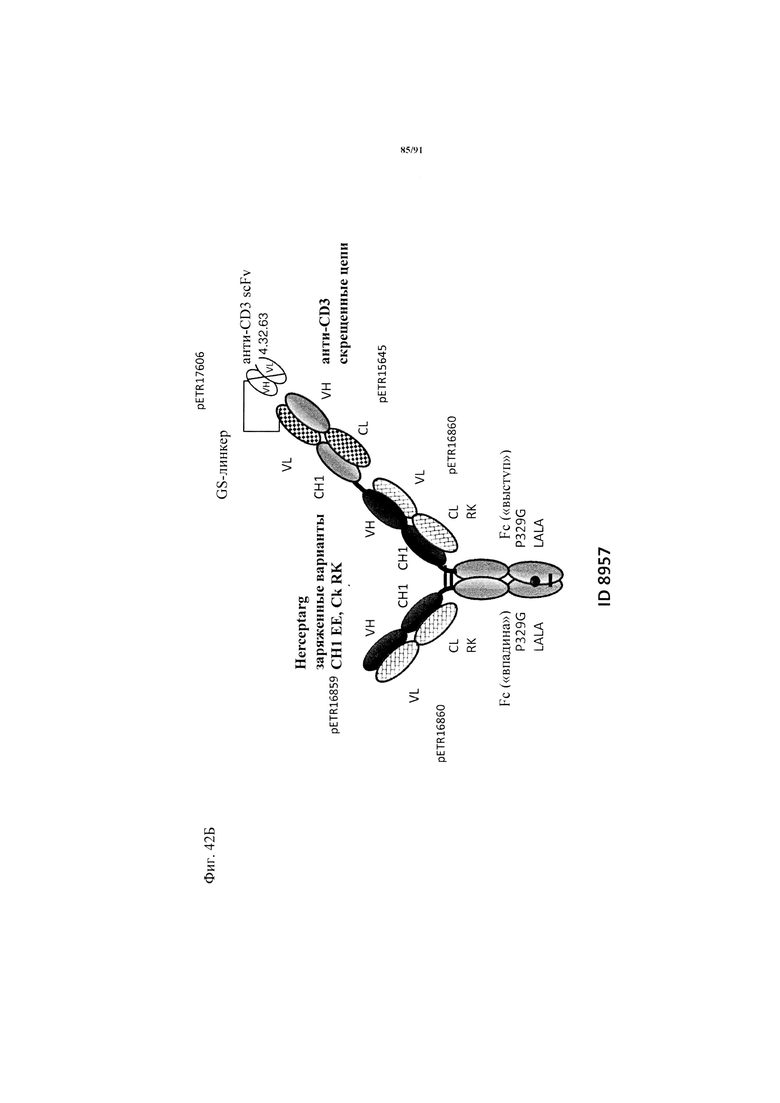
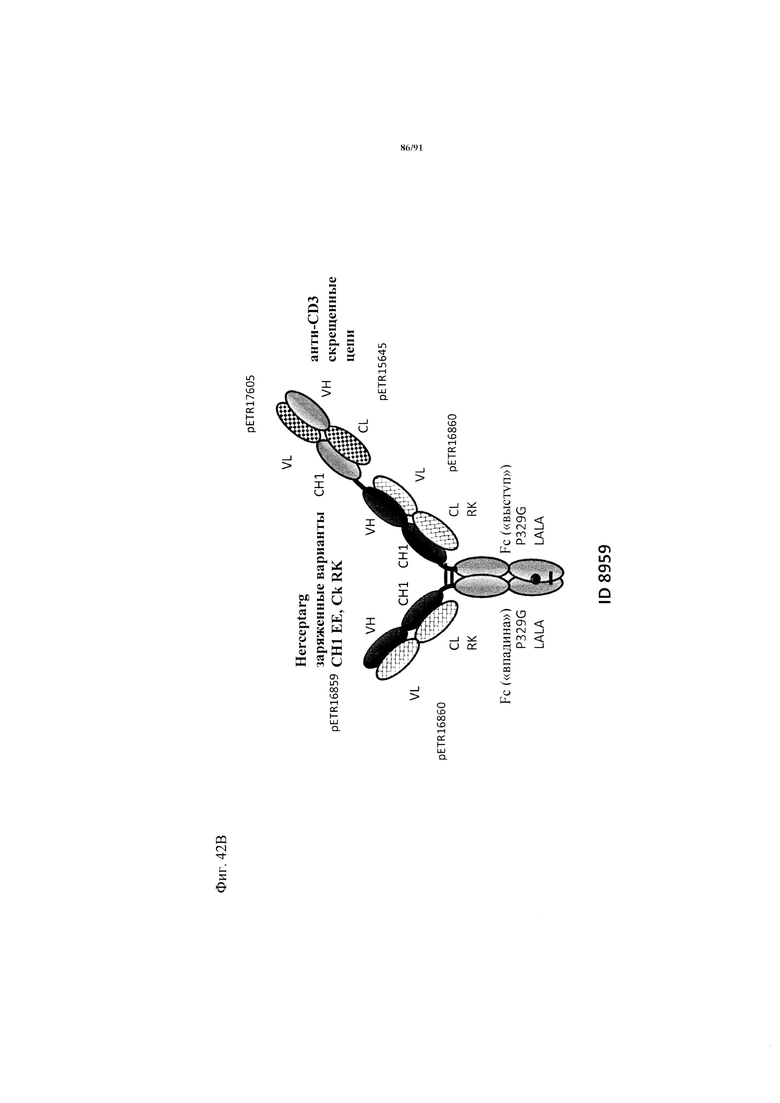
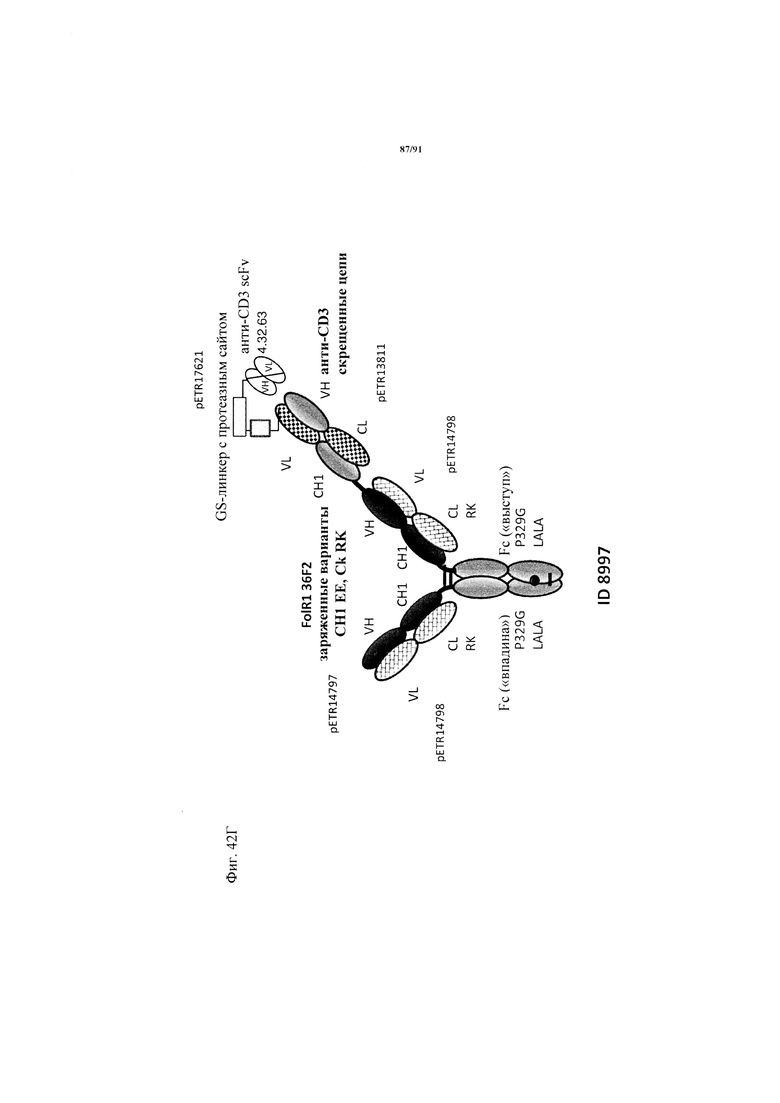
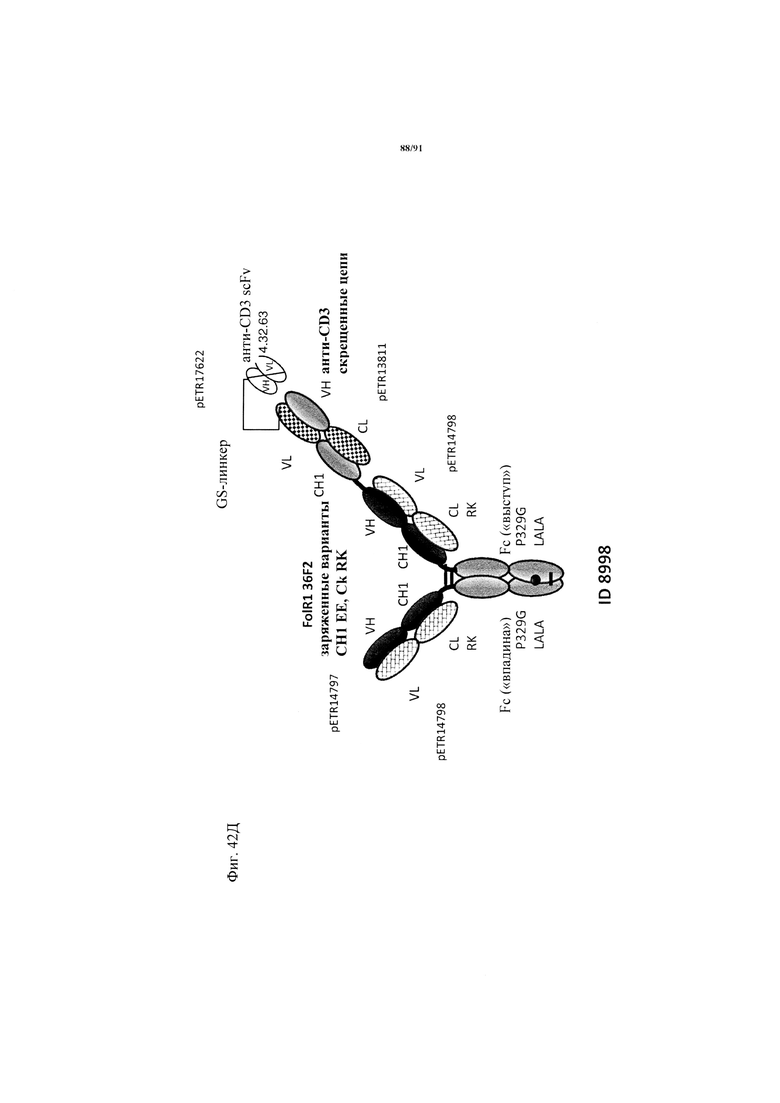
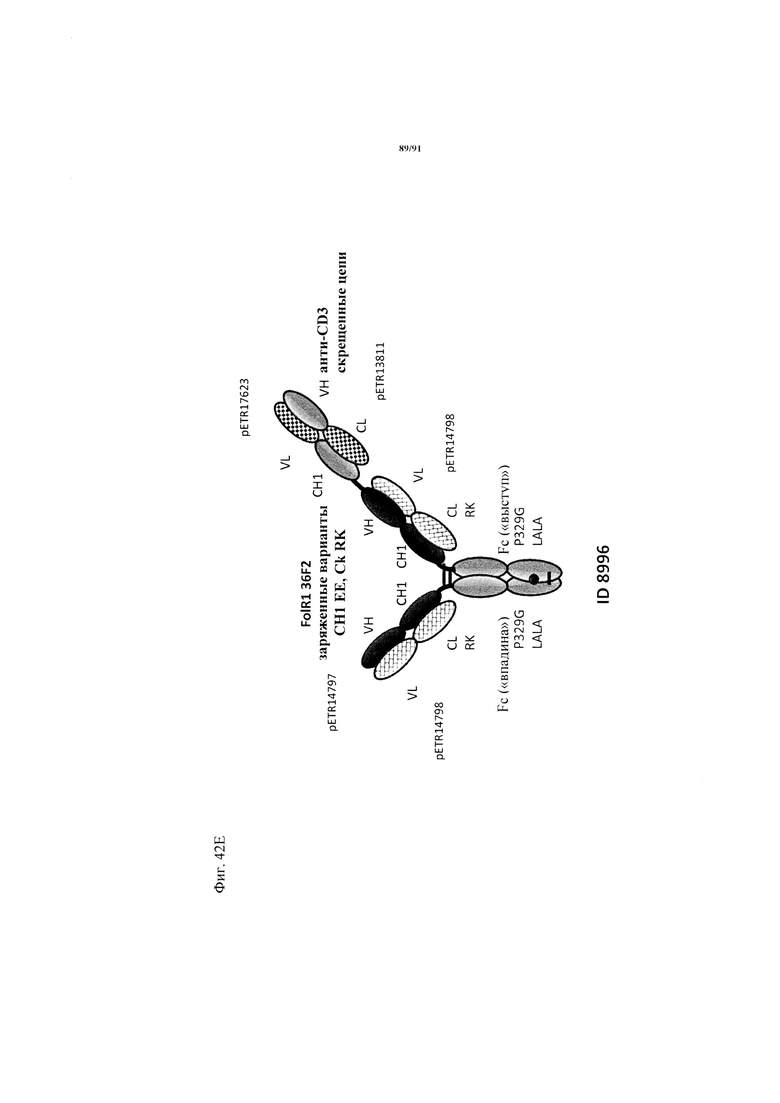
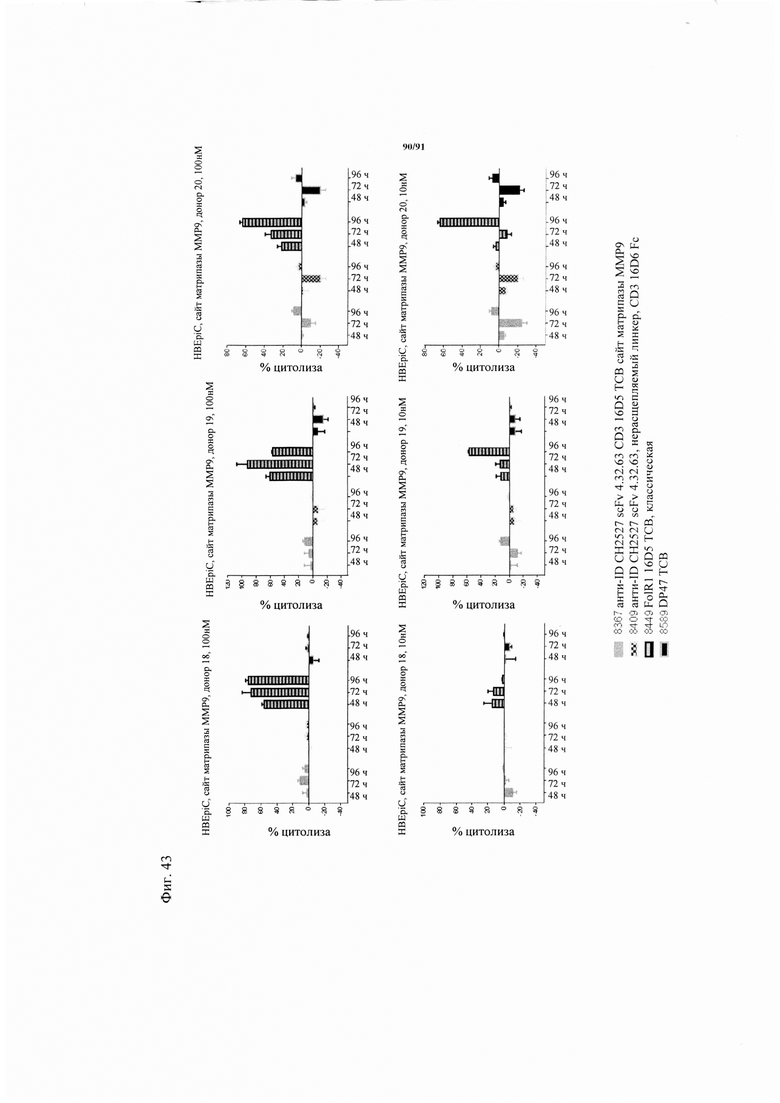

Изобретение относится к области биотехнологии, а именно к активируемой протеазой активирующей Т-клетки биспецифической молекуле, которая содержит первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3, и второй антигенсвязывающий фрагмент, обладающий способностью специфически связываться с FolRl, а также к фармацевтической композиции, ее содержащей. Изобретение эффективно для приготовления лекарственного средства для лечения или замедления прогрессирования рака. 3 н. и 17 з.п. ф-лы, 44 ил., 4 табл., 25 пр.
1. Активируемая протеазой активирующая Т-клетки биспецифическая молекула, которая содержит
(а) первый антигенсвязывающий фрагмент, обладающий способностью специфически связываться с CD3, причем первый антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность определяющей комплементарность области тяжелой цепи CDR H1 TYAMN (SEQ ID NO: 44), аминокислотную последовательность CDR Н2 RIRSKYNNYATYYADSVKG (SEQ ID NO: 45) и аминокислотную последовательность CDR Н3 HGNFGNSYVSWFAY (SEQ ID NO: 46) и вариабельную область легкой цепи, содержащую аминокислотную последовательность CDR L1 GSSTGAVTTSNYAN (SEQ ID NO: 17), аминокислотную последовательность CDR L2 GTNKRAP (SEQ ID NO: 18) и аминокислотную последовательность CDR L3 ALWYSNLWV (SEQ ID NO: 19);
(б) второй антигенсвязывающий фрагмент, обладающий способностью специфически связываться с FolRl, причем второй антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность гипервариабельного участка тяжелой цепи CDR H1 NAWMS (SEQ ID NO: 14), аминокислотную последовательность CDR Н2 RIKSKTDGGTTDYAAPVKG (SEQ ID NO: 15) и аминокислотную последовательность CDR Н3 PWEWSWYDY (SEQ ID NO: 16), и вариабельную область легкой цепи, содержащую аминокислотную последовательность гипервариабельного участка легкой цепи CDR L1 GSSTGAVTTSNYAN (SEQ ID NO: 17), аминокислотную последовательность CDR L2 GTNKRAP (SEQ ID NO: 18) и аминокислотную последовательность CDR L3 ALWYSNLWV (SEQ ID NO: 19);
(в) маскирующий фрагмент, который содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность гипервариабельного участка тяжелой цепи CDR H1 SYGVS (SEQ ID NO: 26), аминокислотную последовательность CDR Н2 IIWGDGSTNYHSALIS (SEQ ID NO: 27), аминокислотную последовательность CDR Н3 GITTVVDDYYAMDY (SEQ ID NO: 28) и вариабельную область легкой цепи, содержащую: аминокислотную последовательность гипервариабельного участка легкой цепи CDR L1 RASENIDSYLA (SEQ ID NO: 29), аминокислотную последовательность CDR L2 AATFLAD (SEQ ID NO:30) и аминокислотную последовательность CDR L3 QHYYSTPYT (SEQ ID NO: 31);
причем маскирующий фрагмент ковалентно присоединен к биспецифической связывающей Т-клетки молекуле через расщепляемый протеазой линкер, обладает способностью специфически связываться с идиотипом первого или второго антигенсвязывающего фрагмента, тем самым обратимо скрывая первый или второй антигенсвязывающий фрагмент, и представляет собой антиидиотипический scFv, а расщепляемый протеазой линкер содержит последовательность, распознаваемую протеазой, выбранную из группы, состоящей из:

где X представляет собой любую аминокислоту.
2. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по п. 1, в которой маскирующий фрагмент ковалентно присоединен к первому антигенсвязывающему фрагменту и обратимо скрывает первый антигенсвязывающий фрагмент.
3. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по п. 1 или 2, в которой маскирующий фрагмент ковалентно присоединен к вариабельной области тяжелой цепи первого антигенсвязывающего фрагмента.
4. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-3, в которой второй антигенсвязывающий фрагмент представляет собой кроссовер-молекулу Fab, в которой либо вариабельные, либо константные области легкой цепи Fab и тяжелой цепи Fab обменены.
5. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-4, в которой первый антигенсвязывающий фрагмент представляет собой каноническую молекулу Fab.
6. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-5, содержащая не более одного антигенсвязывающего фрагмента, который обладает способностью специфически связываться с CD3.
7. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-6, содержащая третий антигенсвязывающий фрагмент, который представляет собой молекулу Fab, обладающую способностью специфически связываться с антигеном клетки-мишени.
8. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по п. 7, в которой третий антигенсвязывающий фрагмент идентичен второму антигенсвязывающему фрагменту.
9. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-8, в которой первый и второй антигенсвязывающие фрагменты слиты друг с другом необязательно через пептидный линкер.
10. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-9, в которой второй антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab первого антигенсвязывающего фрагмента.
11. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-10, в которой первый антигенсвязывающий фрагмент слит на С-конце тяжелой цепи Fab с N-концом тяжелой цепи Fab второго антигенсвязывающего фрагмента.
12. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-11, содержащая Fc-домен, который состоит из первой и второй субъединиц, обладающих способностью к стабильной ассоциации.
13. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по п. 12, в которой Fc-домен представляет собой Fc-домен IgG, в частности, IgG1 или IgG4.
14. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по п. 12 или 13, в которой Fc-домен характеризуется пониженной аффинностью связывания с Fc-рецептором и/или пониженной эффекторной функцией по сравнению с нативным Fc-доменом IgGl.
15. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-14, в которой расщепляемый протеазой линкер содержит по меньшей мере одну распознаваемую протеазой последовательность.
16. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-15, в которой первый антигенсвязывающий фрагмент обладает способностью специфически связываться с CD3 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 43, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 55.
17. Активируемая протеазой активирующая Т-клетки биспецифическая молекула по одному из пп. 1-16, предназначенная для применения в качестве лекарственного средства для лечения или замедления прогрессирования рака.
18. Фармацевтическая композиция для лечения или замедления прогрессирования рака, содержащая активируемую протеазой активирующую Т-клетки биспецифическую молекулу по одному из пп. 1-16 и фармацевтически приемлемый носитель.
19. Фармацевтическая композиция по п. 18, предназначенная для применения в качестве лекарственного средства для лечения или замедления прогрессирования рака.
20. Применение активируемой протеазой активирующей Т-клетки биспецифической молекулы по одному из пп. 1-16 для приготовления лекарственного средства для лечения или замедления прогрессирования рака.
| WO 2016014974 A2, 28.01.2016 | |||
| WO 2015013671 A1, 29.01.2015 | |||
| CARRENO M | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| WO 2015001085 A1, 08.01.2015 | |||
| RU 2012143793 A, 10.05.2014. | |||
Авторы
Даты
2024-11-18—Публикация
2017-03-20—Подача