ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Данная заявка испрашивает приоритет в соответствии с предварительными заявками на патенты США с серийными номерами 62/607831, поданной 19 декабря 2017 года; 62/608569, поданной 20 декабря 2017 года; 62/625814, поданной 2 февраля 2018 года; и 62/760597, поданной 13 ноября 2018 года; полное содержание каждой из которых включено в данный документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[2] Заболевание, представляющее собой метахроматическую лейкодистрофию (MLD), представляет собой аутосомно-рецессивное расстройство, обусловленное дефицитом фермента арилсульфатазы A (ASA). ASA, кодируемая геном ARSA у людей, представляет собой фермент, разрушающий цереброзид-3-сульфат или сфинголипид-3-O-сульфогалактозилцерамид (сульфатид) до цереброзида и сульфата. При отсутствии фермента сульфатиды накапливаются в нервной системе (например, в миелиновых оболочках, нейронах и глиальных клетках) и в меньшей степени в висцеральных органах. Следствием этих молекулярных и клеточных событий является прогрессирующая демиелинизация и потеря аксонов в ЦНС и ПНС, что сопровождается клиническими проявлениями в виде тяжелой двигательной и когнитивной дисфункций.
[3] Определяющим клиническим признаком этого нарушения является дегенерация центральной нервной системы (ЦНС), которая приводит к нарушению когнитивных функций (например, среди прочего, к умственной отсталости, нервным расстройствам и слепоте).
[4] MLD может проявляться у маленьких детей (поздняя младенческая форма), при этом у пораженных детей, как правило, начинают проявляться симптомы вскоре по прошествии первого года жизни (например, в возрасте приблизительно 15-24 месяца), и дети обычно не живут дольше 5 лет. MLD может проявляться у детей (ювенильная форма), при этом у пораженных детей, как правило, проявляется нарушение когнитивных функций к возрасту приблизительно 3-10 лет, и продолжительность жизни может варьироваться (например, в диапазоне 10-15 лет после начала проявления симптомов). MLD может проявляться у взрослых (форма с возникновением в зрелом возрасте) и может появляться у индивидуумов в любом возрасте (например, как правило, в возрасте 16 лет и позднее) и прогрессирование заболевания может варьироваться в широких пределах.
[5] Заместительная ферментная терапия (ERT) является одобренной терапией для лечения MLD, которая предусматривает введение экзогенного заместительного фермента ASA, в частности рекомбинантной арилсульфатазы A (rhASA) (например, рекомбинантная человеческая арилсульфатаза A (rhASA)) пациентам с MLD.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[6] Настоящее изобретение предусматривает, помимо прочего, композиции, содержащие очищенный рекомбинантный белок ASA для заместительной ферментной терапии и способы его получения.
[7] Как описано в разделе «Примеры», иллюстративные рекомбинантные белки ASA, очищенные с применением определенных способов, описанных в данном документе, соответствуют требованиям чистоты для продажи в США и во многих других странах.
[8] Кроме того, рекомбинантный белок ASA, очищенный в соответствии с настоящим изобретением, обладает отличными характеристиками, такими как карта гликанов (например, пороговые количества манноза-6-фосфатированного рекомбинантного белка ASA (белок ASA с M6P)), которые могут способствовать биологической доступности, улучшенному целенаправленному воздействию и/или улучшенной эффективности рекомбинантного белка ASA.
[9] В одном аспекте настоящее изобретение предусматривает способ лечения метахроматической лейкодистрофии (MLD), при этом способ предусматривает введение интратекально субъекту, нуждающемуся в этом, терапевтически эффективной дозы состава, содержащего очищенный белок, представляющий собой рекомбинантную человеческую арилсульфатазу A (rhASA), где очищенный белок rhASA характеризуется картой протеогликанов, предусматривающей один или более пиков (т. е. видов), соответствующих нейтральному рекомбинантному белку ASA (нейтральному белку ASA), сиалированному рекомбинантному белку ASA (белку ASA с сиаловой кислотой), манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA с M6P), N-ацетил-глюкозамин-манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA, кэппированному M6P) и гибридному рекомбинантному белку ASA (гибридному белку ASA), и где введение состава приводит к стабилизации или уменьшению прогрессирования по меньшей мере одного симптома MLD.
[10] В одном варианте осуществления терапевтически эффективная доза очищенной rhASA составляет 100 мг.
[11] В одном варианте осуществления терапевтически эффективная доза очищенной rhASA составляет 150 мг.
[12] В одном варианте осуществления состав вводят один раз в неделю.
[13] В одном варианте осуществления у субъекта имеется поздняя младенческая форма MLD.
[14] В одном варианте осуществления стабилизацию или уменьшение прогрессирования MLD оценивают на основании изменения согласно системе классификации общей моторики (GMFC-MLD).
[15] В одном варианте осуществления введение состава приводит к изменению по уровню GMFC-MLD на ≤ 4, ≤ 3 или ≤ 2 уровням от исходного уровня через 2 года лечения у субъекта с поздней младенческой формой MLD.
[16] В одном варианте осуществления введение состава приводит к сохранению показателя GMFC-MLD через два года лечения.
[17] В одном варианте осуществления сохранение показателя GMFC-MLD представляет собой изменение согласно GMFC-MLD на не более чем 2 уровня от исходного уровня через два года лечения.
[18] В одном варианте осуществления исходный уровень представляет собой оценочный показатель согласно GMFC-MLD до первого введения состава.
[19] В одном варианте осуществления стабилизацию или уменьшение прогрессирования MLD оценивают на основании изменения по шкале оценки общей моторики (GMFM-MLD).
[20] В одном варианте осуществления введение состава приводит к сохранению показателя GMFM-MLD через два года лечения.
[21] В одном варианте осуществления показатель GMFM-MLD сохраняется на уровне > 40.
[22] В одном варианте осуществления стабилизацию или уменьшение прогрессирования MLD оценивают по уровням сульфатидов в спинномозговой жидкости.
[23] В одном варианте осуществления стабилизацию или уменьшение прогрессирования MLD оценивают по соотношению N-ацетиласпартата/креатина (NAA/cr) в головном мозге.
[24] В одном варианте осуществления стабилизацию или уменьшение прогрессирования MLD оценивают по уровням классификации функции экспрессивной речи при MLD (ELFC-MLD).
[25] В одном варианте осуществления субъект имеет исходный уровень GMFC-MLD 1-2.
[26] В одном варианте осуществления субъект имеет исходный уровень GMFC-MLD 3.
[27] В одном варианте осуществления субъект имеет исходный уровень GMFC-MLD 4.
[28] В одном варианте осуществления субъект находится на предсимптоматической стадии. В одном варианте осуществления возраст субъекта на предсимптоматической стадии менее 18 месяцев. В одном варианте осуществления субъекта на предсимптоматической стадии оценивают согласно Альбертской шкале двигательной функции у младенцев.
[29] В некоторых вариантах осуществления белок rhASA имеет аминокислотную последовательность, на по меньшей мере 70% идентичную SEQ ID NO:1.
[30] В одном аспекте настоящее изобретение предусматривает способ лечения поздней младенческой формы MLD, при этом способ предусматривает: введение субъекту состава, содержащего очищенный белок, представляющий собой рекомбинантную арилсульфатазу A (rhASA), с аминокислотной последовательностью, на по меньшей мере 70% идентичной SEQ ID NO:1, где очищенный белок rhASA характеризуется картой протеогликанов, предусматривающей один или более пиков (т. е. видов), соответствующих нейтральному рекомбинантному белку ASA (нейтральному белку ASA), сиалированному рекомбинантному белку ASA (белку ASA с сиаловой кислотой), манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA с M6P), N-ацетил-глюкозамин-манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA, кэппированному M6P) и гибридному рекомбинантному белку ASA (гибридному белку ASA), и состав вводят интратекально в дозе, составляющей 150 мг, с интервалом, предусматривающим введение один раз в неделю.
[31] В одном варианте осуществления состав содержит менее приблизительно 150 нг/мг белка клетки-хозяина (HCP).
[32] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA составляет по меньшей мере приблизительно 23% от общего очищенного рекомбинантного белка ASA, соответствующие манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA с M6P).
[33] В одном варианте осуществления карта протеогликанов очищенного рекомбинантного белка ASA предусматривает: от приблизительно 15% до приблизительно 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA), от приблизительно 35% до приблизительно 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой), от приблизительно 23% до приблизительно 33% манноза-6-фосфатированного рекомбинантного белка ASA (белок ASA с M6P), от приблизительно 1% до приблизительно 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и от приблизительно 5% до приблизительно 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
[34] В одном варианте осуществления карта протеогликанов очищенного рекомбинантного белка ASA предусматривает: от приблизительно 18% до приблизительно 22% нейтрального белка ASA, от приблизительно 37% до приблизительно 41% белка ASA с сиаловой кислотой, от приблизительно 26% до приблизительно 29% белка ASA с M6P, от приблизительно 4% до приблизительно 6% белка ASA, кэппированного M6P, и от приблизительно 7% до приблизительно 9% гибридного белка ASA.
[35] В одном варианте осуществления введение состава приводит к минимальным неблагоприятным эффектам (AE).
[36] В одном аспекте настоящее изобретение предусматривает новые способы очистки рекомбинантного белка ASA, которые могут предусматривать преимущества, такие как снижения финансовых затрат и затрат времени за счет улучшений эффективностей способа (например, снижение общего числа этапов для получения лекарственного вещества (DS) или лекарственного препарата (DP)) или за счет обеспечения возможности получения композиций с благоприятными характеристиками (например, композиция, содержащая очищенный рекомбинантный белок ASA с пороговым вмещением манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P), которая может обладать улучшенными биологической доступностью, целенаправленным воздействием или эффективностью) или композиций на основе DS, содержащих поверхностно-активное вещество (например, полисорбат-20 (P20)), которые могут обладать улучшенной стабильностью при хранении (например, холодильное хранение) или приводить к улучшенной эффективности способа в отношении получения DS или DP.
[37] В одном аспекте настоящее изобретение предусматривает композицию, содержащую очищенный белок, представляющий собой рекомбинантную арилсульфатазу A (rhASA), с аминокислотной последовательностью, на по меньшей мере 70% идентичной SEQ ID NO:1, где очищенный белок rhASA характеризуется одним или более видами протеогликанов, выбранными из нейтрального рекомбинантного белка ASA (нейтрального белка ASA), сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой), манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P), N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) или гибридного рекомбинантного белка ASA (гибридного белка ASA). В некоторых вариантах осуществления манноза-6-фосфатированный рекомбинантный белок ASA (белок ASA с M6P) присутствует в количестве, которое составляет по меньшей мере приблизительно 23% от содержания общего очищенного белка rhASA.
[38] В одном варианте осуществления настоящее изобретение предусматривает композицию, содержащую очищенный белок, представляющий собой рекомбинантную арилсульфатазу A (rhASA), с аминокислотной последовательностью, на по меньшей мере 70% идентичной SEQ ID NO:1, где очищенный белок rhASA присутствует в виде манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P) в количестве, которое составляет по меньшей мере приблизительно 23% от содержания общего очищенного белка rhASA; и очищенный рекомбинантный белок ASA содержит менее приблизительно 150 нг/мг белка клетки-хозяина (HCP).
[39] В одном аспекте настоящее изобретение предусматривает композицию, содержащую очищенный белок, представляющий собой рекомбинантную человеческую арилсульфатазу A (rhASA), с аминокислотной последовательностью, на по меньшей мере 70% идентичной SEQ ID NO:1, где по меньшей мере приблизительно 23% от общего очищенного рекомбинантного белка ASA соответствуют манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA с M6P), характеризующемуся картой протеогликанов; и композиция содержит менее приблизительно 150 нг/мг белка клетки-хозяина (HCP).
[40] В одном варианте осуществления белок ASA с M6P присутствует в композиции в количестве, которое составляет по меньшей мере приблизительно 26% от содержания общего очищенного белка rhASA. В одном варианте осуществления белок ASA с M6P присутствует в количестве, которое составляет по меньшей мере приблизительно 28% от содержания общего очищенного белка rhASA. В одном варианте осуществления белок ASA с M6P присутствует в композиции в количестве, которое составляет от приблизительно 20% до приблизительно 33% от содержания общего очищенного белка rhASA.
[41] В одном варианте осуществления общий очищенный белок rhASA предусматривает нейтральный рекомбинантный белок ASA (нейтральный белок ASA), сиалированный рекомбинантный белок ASA (белок ASA с сиаловой кислотой), N-ацетил-глюкозамин-манноза-6-фосфатированный рекомбинантный белок ASA (белок ASA, кэппированный M6P) или гибридный рекомбинантный белок ASA (гибридный белок ASA) или любую их комбинацию.
[42] В одном варианте осуществления общий очищенный белок rhASA предусматривает: от приблизительно 23% до приблизительно 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P), от приблизительно 15% до приблизительно 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA), от приблизительно 35% до приблизительно 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой), от приблизительно 1% до приблизительно 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и от приблизительно 5% до приблизительно 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
[43] В одном варианте осуществления нейтральный белок ASA присутствует в количестве, которое составляет от приблизительно 16% до приблизительно 22% от общего очищенного белка rhASA.
[44] В одном варианте осуществления нейтральный белок ASA присутствует в количестве, которое составляет от приблизительно 20% до приблизительно 25% от общего очищенного белка rhASA.
[45] В одном варианте осуществления белок ASA с сиаловой кислотой присутствует в количестве, которое составляет от приблизительно 35% до приблизительно 40% от общего очищенного белка rhASA.
[46] В одном варианте осуществления белок ASA с сиаловой кислотой присутствует в количестве, которое составляет от приблизительно 37% до приблизительно 42% от общего очищенного белка rhASA.
[47] В одном варианте осуществления белок ASA, кэппированный M6P, присутствует в количестве, которое составляет от приблизительно 3% до приблизительно 5% от общего очищенного белка rhASA.
[48] В одном варианте осуществления белок ASA, кэппированный M6P, присутствует в количестве, которое составляет от приблизительно 4% до приблизительно 6% от общего очищенного белка rhASA.
[49] В одном варианте осуществления белок ASA, кэппированный M6P, присутствует в количестве, которое составляет от приблизительно 4,5% до приблизительно 5,5% от общего очищенного белка rhASA.
[50] В одном варианте осуществления гибридный белок ASA присутствует в количестве, которое составляет от приблизительно 7% до приблизительно 10% от общего очищенного белка rhASA.
[51] В одном варианте осуществления гибридный белок ASA присутствует в количестве, которое составляет от приблизительно 7,5% до приблизительно 8,5% от общего очищенного белка rhASA.
[52] В одном варианте осуществления общий очищенный белок rhASA предусматривает: от приблизительно 16% до приблизительно 23% нейтрального белка ASA, от приблизительно 37% до приблизительно 42% белка ASA с сиаловой кислотой, от приблизительно 23% до приблизительно 27% белка ASA с M6P, от приблизительно 4% до приблизительно 8% белка ASA, кэппированного M6P, и от приблизительно 7% до приблизительно 10% гибридного белка ASA. В одном варианте осуществления общий очищенный белок rhASA предусматривает: от приблизительно 20% до приблизительно 23% нейтрального белка ASA, от приблизительно 35% до приблизительно 39% белка ASA с сиаловой кислотой, от приблизительно 26% до приблизительно 32% белка ASA с M6P, от приблизительно 3% до приблизительно 5% белка ASA, кэппированного M6P, и от приблизительно 7% до приблизительно 9% гибридного белка ASA.
[53] В одном варианте осуществления общий очищенный белок rhASA предусматривает: от приблизительно 18% до приблизительно 22% нейтрального белка ASA, от приблизительно 37% до приблизительно 41% белка ASA с сиаловой кислотой, от приблизительно 26% до приблизительно 29% белка ASA с M6P, от приблизительно 4% до приблизительно 6% белка ASA, кэппированного M6P, и от приблизительно 7% до приблизительно 9% гибридного белка ASA.
[54] В одном варианте осуществления общий очищенный белок rhASA присутствует в концентрации, составляющей от приблизительно 20 мг/мл до приблизительно 45 мг/мл. В одном варианте осуществления общий очищенный белок rhASA присутствует в концентрации, составляющей от приблизительно 25 мг/мл до приблизительно 34 мг/мл или от приблизительно 28 мг/мл до приблизительно 32 мг/мл. В одном варианте осуществления общий очищенный белок rhASA присутствует в концентрации, составляющей приблизительно 25 мг/мл, приблизительно 26 мг/мл, приблизительно 27 мг/мл, приблизительно 28 мг/мл, приблизительно 29 мг/мл, приблизительно 30 мг/мл, приблизительно 31 мг/мл, приблизительно 32 мг/мл, приблизительно 33 мг/мл или приблизительно 34 мг/мл.
[55] В одном варианте осуществления очищенный белок rhASA характеризуется специфической активностью, составляющей от приблизительно 50 до приблизительно 130 Ед./мл. В одном варианте осуществления очищенный белок rhASA характеризуется специфической активностью, составляющей от приблизительно 70 до приблизительно 100 Ед./мг. В одном варианте осуществления очищенный белок rhASA характеризуется специфической активностью, составляющей от приблизительно 80 до приблизительно 90 Ед./мг. В одном варианте осуществления очищенный белок rhASA характеризуется специфической активностью, составляющей от приблизительно 75 до приблизительно 95 Ед./мг.
[56] В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 140 нг/мг белка клетки-хозяина (HCP). В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 100 нг/мг HCP. В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 80 нг/мг HCP. В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 60 нг/мг HCP. В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 100 пг/мг ДНК клетки-хозяина (HCD). В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 50 пг/мг HCD. В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 10 пг/мг HCD. В одном варианте осуществления очищенный белок rhASA содержит менее приблизительно 5 пг/мг HCD, менее приблизительно 4 пг/мг HCD, менее приблизительно 3 пг/мг HCD, менее приблизительно 2 пг/мг HCD или менее приблизительно 1 пг/мг HCD.
[57] В одном варианте осуществления очищенный белок rhASA имеет аминокислотную последовательность, на по меньшей мере 80% идентичную SEQ ID NO:1. В одном варианте осуществления очищенный белок rhASA имеет аминокислотную последовательность, на по меньшей мере 90% идентичную SEQ ID NO:1. В одном варианте осуществления очищенный белок rhASA имеет аминокислотную последовательность, на по меньшей мере 95% идентичную SEQ ID NO:1.
[58] В одном варианте осуществления очищенный белок rhASA имеет аминокислотную последовательность, которая идентична SEQ ID NO:1.
[59] В одном варианте осуществления композиция содержит от приблизительно 0,001% до приблизительно 0,01% полисорбата-20 (P20). В одном аспекте настоящее изобретение предусматривает состав, содержащий композицию, которая подробно описана выше, и физиологически приемлемый носитель. В одном варианте осуществления состав подходит для внутривенного введения.
[60] В одном варианте осуществления состав подходит для интратекального введения. В одном варианте осуществления состав подходит для подкожного введения.
[61] В одном аспекте настоящее изобретение предусматривает способ очистки белка, представляющего собой рекомбинантную арилсульфатазу A (ASA), при этом способ предусматривает: очистку белка, представляющего собой рекомбинантную арилсульфатазу A (ASA), из неочищенного препарата путем проведения одного или более этапов хроматографии; объединения элюата из одного или более этапов хроматографии; необязательно регулирование pH объединенного элюата до pH, который составляет от приблизительно 6,0 до приблизительно 8,0; необязательно подвергание объединенного элюата или отрегулированного по pH элюата ультрафильтрации и/или диафильтрации; получение элюата, содержащего очищенный белок, представляющий собой рекомбинантную арилсульфатазу A (ASA); и добавление поверхностно-активного вещества к элюату, содержащему очищенный белок, представляющий собой рекомбинантную арилсульфатазу A (ASA).
[62] В одном варианте осуществления способ дополнительно предусматривает этап регулирования pH объединенного элюата до pH, который составляет от приблизительно 6,0 до приблизительно 8,0. В одном варианте осуществления имеет место этап подвергания отрегулированного по pH элюата ультрафильтрации и/или диафильтрации.
[63] В одном варианте осуществления указанное добавление поверхностно-активного вещества происходит до холодильного хранения элюата, содержащего очищенный рекомбинантный белок ASA.
[64] В одном варианте осуществления указанное поверхностно-активное вещество присутствует в концентрации, которая составляет от приблизительно 0,0001% (объем/объем) до приблизительно 0,01% (объем/объем). В одном варианте осуществления указанное поверхностно-активное вещество присутствует в концентрации, которая составляет от приблизительно 0,001% (объем/объем) до приблизительно 0,01% (объем/объем). В одном варианте осуществления указанное поверхностно-активное вещество представляет собой полисорбат-20 (P20).
[65] В одном варианте осуществления проведение одного или более этапов хроматографии предусматривает проведение анионообменной хроматографии, хроматографии в комбинированном режиме, хроматографии с гидрофобным взаимодействием, т. е. хроматографии с использованием фенильного сорбента, и катионообменной хроматографии, в указанном порядке. В некоторых вариантах осуществления при анионообменной хроматографии применяют колонку со смолой TMAE.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[66] Фигуры, описанные ниже, которые вместе составляют графические материалы, предназначены лишь для целей иллюстрации, а не ограничения.
[67] На фигурах 1A-1F показаны иллюстративные изображения иммуногистохимического окрашивания в отношении LAMP-1 у мышей с MLD, которых лечили с помощью rhASA, полученной по способу A или способу B, с соответствующим морфометрическим анализом в белом веществе (A) спинного мозга, (B) мозжечка, (C) бахромки гиппокампа, (D) ножки мозга, (E) коры больших полушарий и (F) полосатого тела иммуннотолерантных мышей с MLD, которых лечили с помощью rhASA в количестве 0,04 мг или 0,21 мг из способа A (iii, v) или способа B (iv, vi) или контроля (ii). Необработанные мыши C57/B16 служили контролями WT (i). LAMP-1, ассоциированный с лизосомой мембранный белок 1; MLD, метахроматическая лейкодистрофия; NS, незначимый; rhASA, рекомбинантная человеческая арилсульфатаза A; WT, дикий тип.
[68] На фигурах 2A и 2B показаны кривые зависимости концентрации от времени rhASA, полученной по способу A и способу B, в (фиг. 2A) сыворотке крови и (фиг. 2B) CSF после однократной интратекальной дозы, составляющей 6,0 мг, у яванских макаков подросткового возраста.
[69] На фигурах 3A и 3B показано биораспределение rhASA, полученной по способу A и способу B, у крыс. Из иллюстративных авторадиолюминограмм всего тела видно распределение в тканях радиоактивности через 4 часа после однократной интратекальной дозы, составляющей 0,62 мг [125I]-rhASA по (фиг. 3A) способу A и (фиг. 3B) способу B, у самцов крыс Sprague Dawley.
[70] На фигуре 4 показаны профили экскреции [125I]-rhASA по способу A и способу B в дозе 0,62 мг с мочой, фекалиями и в целом после однократной интратекальной дозы самцам крыс Sprague Dawley (n=2 и n=3, соответственно).
[71] На фигуре 5 показан план исследования с увеличением дозы и расширенного исследования для открытой оценки безопасности rhASA с увеличением дозы. CSF, спинномозговая жидкость; GMFM-88, шкала оценки общей моторики-88; IDDD, устройство для интратекальной доставки лекарственного средства; IT, интратекальный; MLD, метахроматическая лейкодистрофия; rhASA, рекомбинантная человеческая арилсульфатаза A.
[72] На фигуре 6 показаны клиническая PK/PD модель для концентраций rhASA в CSF, ЦНС и сыворотке крови и эффект в отношении концентраций сульфатидов в CSF. CL, клиренс лекарственного средства; CMT, компартмент; ЦНС, центральная нервная система; CSF, спинномозговая жидкость; kin, скорость образования сульфатидов; kout, константа скорости истощения сульфатидов; Ktrans, константа переходной скорости; PK/PD, фармакокинетические/фармакодинамические параметры; QCSF, межкомпартментный клиренс; rhASA, рекомбинантная человеческая арилсульфатаза A.
[73] На фигурах 7A, 7B и 7C показаны графики точности подбора предсказанных концентраций rhASA для популяции и индивидуума в CSF, концентрация сульфатидов в CSF и общие показатели GMFM-88 соответственно.
[74] На фигуре 8 показаны иллюстративные смоделированные остаточные концентрации rhASA в спинномозговой жидкости (CSF) (левая секция) и центральной нервной системе (ЦНС) (правая секция) по режиму дозирования и исходному возрасту. Сценарий 1: 100 мг раз в две недели; сценарий 2: 100 мг каждую неделю в течение 12 недель (первоначальное еженедельное введение дозы), затем 100 мг раз в две недели; сценарий 3: 150 мг каждую неделю в течение 12 недель (первоначальное еженедельное введение дозы), затем 150 мг раз в две недели; сценарий 4: стандартизированное по возрасту еженедельное введение дозы в течение 12 недель (первоначальное еженедельное введение дозы), затем раз в две недели (сценарий 4: 80 мг, < 8 месяцев; 120 мг, 8 - < 30 месяцев; 150 мг, ≥ 30 месяцев).
[75] На фигуре 9 показан смоделированный общий показатель GMFM-88, предсказанный для индивидуального уровня, согласно сценарию введения дозы. Четыре сценария введения дозы включали: сценарий 1, 100 мг раз в две недели (EOW); сценарий 2, 100 мг каждую неделю (EW) в течение 12 недель, затем 100 мг EOW; сценарий 3, 150 мг каждую неделю в течение 12 недель, затем 150 мг EOW; сценарий 4, стандартизированное по возрасту еженедельное введение дозы в течение 12 недель, затем EOW (80 мг, < 8 месяцев; 120 мг, 8 - < 30 месяцев; 150 мг, ≥ 30 месяцев).
[76] На фигуре 10 показан план исследования с увеличением дозы и расширенного исследования для открытой оценки безопасности rhASA с увеличением дозы. Решение к переходу на более высокую дозу основывалось на рассмотрении данных DSMB после того как пациенты в когорте получали по меньшей мере две дозы предшествующего уровня дозы. DSMB, независимый комитет по мониторингу данных; EOS, конец исследования; EOW, раз в две недели; GMFM-88, шкала оценки общей моторики-88; IDDD, устройство для интратекальной доставки лекарственного средства; MLD, метахроматическая лейкодистрофия; MRI, магниторезонансная визуализация; rhASA, рекомбинантная человеческая арилсульфатаза A.
[77] На фигуре 11 показан индивидуальный общий показатель GMFM-88 по возрасту пациента в течение периода исследования у пациентов, идентифицированных как отвечающие на лечение, и не отвечающих на лечение.
[78] На фигуре 12 показаны индивидуальные показатели тяжести MLD на исходном уровне и на неделе 40 для пациентов с доступными данными тех, кто ответил на лечение.
[79] На фигуре 13 показаны индивидуальные соотношения N-ацетиласпартат (NAA)/креатин в белом веществе передней теменной доли на исходном уровне и на неделе 40 для пациентов с доступными данными, тех кто ответил на лечение.
[80] На фигуре 14 показана средняя (± SD) концентрация rhASA в спинномозговой жидкости с течением времени.
[81] На фигуре 15 показаны наблюдаемые средние общие показатели GMFM-88 с течением времени для когорты 1 (способ A: 10 мг), когорты 2 (способ A: 30 мг), когорты 3 (способ A: 100 мг), когорты 4 (способ B: 100 мг). Планки погрешностей представляют собой стандартную ошибку среднего значения.
[82] На фигурах 16A и 16B показаны средние уровни сульфатидов в CSF и лизосульфатидов в CSF соответственно для когорты 1 (способ A: 10 мг), когорты 2 (способ A: 30 мг), когорты 3 (способ A: 100 мг), когорты 4 (способ B: 100 мг). Планки погрешностей представляют собой стандартную ошибку среднего значения. Верхний предел нормального значения для сульфатидов в CSF (0,113 мкг/мл) и для лизосульфатидов в CSF (0,0277 нг/мл) представляет собой наивысшую концентрацию, наблюдаемую в образцах CSF от 60 детей, у которых не было лейкодистрофии, но которые прошли спинномозговую пункцию (и, следовательно, могут иметь другие неврологические состояния). CSF, спинномозговая жидкость; LLOQ/2, нижний предел количественного определения.
[83] На фигурах 17A и 17B показано среднее изменение от исходного уровня с течением времени в (фигура 17A) соотношении NAA/креатин и (фигура 17B) соотношении холин/креатин в белом веществе правой передней доли. Исходные данные доступны для 16 пациентов и конечные данные исследования доступны для 12 пациенты. Планки погрешностей представляют собой стандартное отклонение от среднего значения.
[84] На фигурах 18A и 18B показано среднее изменение от исходного уровня с течением времени в (фигура 18A) соотношении NAA/креатин и (фигура 18B) соотношении холин/креатин в белом веществе правой передней теменной доли. Планки погрешностей представляют собой стандартное отклонение от среднего значения.
[85] На фигурах 19A и 19B показано среднее изменение от исходного уровня с течением времени в (фигура 19A) соотношении NAA/креатин и (фигура 19B) соотношении холин/креатин в белом веществе правой затылочно-теменной доли. Планки погрешностей представляют собой стандартное отклонение от среднего значения.
[86] На фигурах 20A и 20B показано среднее изменение от исходного уровня с течением времени в (фигура 20A) соотношении NAA/креатин и (фигура 20B) соотношении холин/креатин в сером веществе затылочной средней линии. Планки погрешностей представляют собой стандартное отклонение от среднего значения.
[87] На фигуре 21 показан средний общий показатель тяжести MLD с течением времени. Планки погрешностей представляют собой стандартную ошибку среднего значения.
[88] На фигуре 22 показан индивидуальный общий показатель GMFM-88 по возрасту в месяцах единокровных пар пациентов из клинического исследования rhASA.
ОПРЕДЕЛЕНИЯ
[89] В целях облегчения понимания настоящего изобретения ниже сперва определены некоторые термины. Дополнительные определения следующих терминов и других терминов изложены во всем настоящем описании.
[90] Примерно или приблизительно. Используемый в данном документе термин «примерно» или «приблизительно», применяемый в отношении одного или более значений, представляющих интерес, относится к значению, сходному с указанным эталонным значением. В определенных вариантах осуществления термин «примерно» или «приблизительно» относится к диапазону значений, находящихся в пределах 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или меньше в любую сторону (большую или меньшую) от указанного эталонного значения, если не указано иное или иное не очевидно из контекста (за исключением случаев, когда такое число будет превышать 100% от возможного значения).
[91] Биологически активный. Используемая в данном документе фраза «биологически активный» относится к характеристике какого-либо средства, обладающего активностью в биологической системе, и в частности в организме. Например, средство, которое при введении в организм оказывает биологический эффект на этот организм, считается биологически активным. В конкретных вариантах осуществления, в которых белок или полипептид является биологически активным, часть этого белка или полипептида, обладающая по меньшей мере одним видом биологической активности белка или полипептида, как правило, называется «биологически активной» частью.
[92] Катионнезависимый рецептор маннозо-6-фосфата (CI-MPR). Используемый в данном документе термин «катионнезависимый рецептор маннозо-6-фосфата (CI-MPR)» относится к клеточному рецептору, связывающему маннозо-6-фосфатные (M6P) метки на предшественниках кислой гидролазы в аппарате Гольджи, предназначенных для транспорта в лизосомы. В дополнение к маннозо-6-фосфатам, CI-MPR также связывает другие белки, в том числе IGF-II. CI-MPR также известен как «рецептор M6P/IGF-II», «рецептор CI-MPR/IGF-II», «рецептор IGF-II» или «рецептор IGF2». Эти термины и их сокращения используются в данном документе взаимозаменяемо.
[93] Хроматография. Используемый в данном документе термин «хроматография» относится к методике разделения смесей. Как правило, смесь растворена в текучей среде, называемой «подвижная фаза», которая переносит ее через структуру, содержащую другой материал, называемый «неподвижная фаза». Колоночная хроматография представляет собой методику разделения, в которой неподвижный слой находится внутри пробирки, т. е. колонки.
[94] Разбавитель. Используемый в данном документе термин «разбавитель» относится к фармацевтически приемлемому (например, безопасному и нетоксичному при введении человеку) разбавляющему веществу, применимому для получения разведенного состава. Приводимые в качестве примера разбавители включают в себя стерильную воду, бактериостатическую воду для инъекций (BWFI), pH-буферный раствор (например, физиологический раствор с фосфатным буфером), стерильный физиологический раствор, раствор Рингера или раствор декстрозы.
[95] Элюирование. Используемый в данном документе термин «элюирование» относится к способу извлечения одного материала из другого путем промывания растворителем. Например, в ионообменной хроматографии элюирование представляет собой способ промывки загруженных смол для удаления захваченных ионов.
[96] Элюат. Используемый в данном документе термин «элюат» относится к комбинации подвижной фазы «носителя» и анализируемого материала, который получают в результате хроматографии, как правило в результате элюирования.
[97] Заместительная ферментная терапия (ERT). Используемый в данном документе термин «заместительная ферментная терапия (ERT)» относится к любой терапевтической стратегии, с помощью которой корректируют дефицит фермента путем предоставления недостающего фермента. После введения фермент поглощается клетками и транспортируется в лизосомы, где фермент действует таким образом, чтобы устранить материал, накопившийся в лизосомах вследствие дефицита фермента. Как правило, для того, чтобы заместительная терапия лизосомными ферментами была эффективной, терапевтический фермент доставляется в лизосомы в соответствующие клетки в целевые ткани, где проявляется дефект накопления. Способы очистки, описанные в данном документе, можно применять для очистки и составления рекомбинантной арилсульфатазы A в качестве лекарственного вещества для ERT для MLD.
[98] Уравновешивание или установление равновесия. Используемые в данном документе термины «уравновешивать» или «установление равновесия» по отношению к хроматографии относятся к способу приведения первой жидкости (например, буфера) в равновесие с другой, в целом, для достижения стабильного и равномерного распределения компонентов жидкости (например, буфера). Например, в некоторых вариантах осуществления хроматографическая колонка может быть уравновешена путем пропускания одного или более объемов колонки необходимой жидкости (например, буфера) через колонку.
[99] Улучшать, увеличивать или снижать. Используемые в данном документе термины «улучшать», «увеличивать» или «снижать» или их грамматические эквиваленты указывают на значения по сравнению с измерением исходного уровня, таким как измерение у того же самого индивидуума до начала лечения, описанного в данном документе, или измерение у контрольного индивидуума (или нескольких контрольных индивидуумов) при отсутствии лечения, описанного в данном документе. «Контрольным индивидуумом» является индивидуум, пораженный той же формой лизосомной болезни накопления, что и индивидуум, подвергаемый лечению, который имеет приблизительно такой же возраст, как и индивидуум, подвергаемый лечению (для гарантирования того, что стадии заболевания у индивидуума, подвергаемого лечению, и контрольного(-ых) индивидуума(-ов) являются сопоставимыми).
[100] Примеси. Используемый в данном документе термин «примеси» относится к веществам внутри ограниченного количества жидкости, газа или твердого вещества, которые отличаются от химической композиции целевого материала или соединения. Примеси также называют загрязнителями.
[101] Загрузка. Используемый в данном документе термин «загрузка» относится, в хроматографии, к добавлению содержащих образец жидкости или твердого вещества в колонку. В некоторых вариантах осуществления конкретные компоненты образца, загруженные на колонку, затем захватываются по мере прохождения загруженного образца через колонку. В некоторых вариантах осуществления конкретные компоненты образца, загруженного на колонку, не захватываются, или «протекают сквозь», колонкой по мере прохождения загруженного образца через колонку.
[102] Полипептид. Используемый в данном документе «полипептид», говоря в целом, представляет собой нить по меньшей мере из двух аминокислот, соединенных друг с другом пептидной связью. В некоторых вариантах осуществления полипептид может содержать по меньшей мере 3-5 аминокислот, каждая из которых соединена с другими с помощью по меньшей мере одной пептидной связи. Средним специалистам в данной области будет понятно, что полипептиды необязательно иногда содержат «неприродные» аминокислоты или другие объекты, которые, тем не менее, способны встраиваться в полипептидную цепь.
[103] Объединенный материал. Используемый в данном документе термин «объединенный материал» по отношению к хроматографии относится к комбинированию одной или более фракций текучей среды, которые проходят через колонку вместе. Например, в некоторых вариантах осуществления одна или более фракций, которые содержат необходимый компонент образца, который был отделен с помощью хроматографии (например, «пиковые фракции»), могут быть «объединены» вместе с образованием одной «объединенной» фракции.
[104] Заместительный фермент. Используемый в данном документе термин «заместительный фермент» относится к любому ферменту, который может действовать таким образом, чтобы по меньшей мере частично замещать дефицитный или недостающий фермент при заболевании, подлежащем лечению. В некоторых вариантах осуществления термин «заместительный фермент» относится к любому ферменту, который может действовать таким образом, чтобы по меньшей мере частично замещать дефицитный или недостающий лизосомный фермент при лизосомной болезни накопления, подлежащей лечению. В некоторых вариантах осуществления заместительный фермент (например, rhASA) способен снижать количество накопившихся материалов в лизосомах млекопитающих или может обеспечивать избавление от одного или более симптомов лизосомной болезни накопления (например, MLD) или уменьшение их интенсивности. Заместительные ферменты, подходящие для настоящего изобретения, включают в себя как принадлежащие к дикому типу, так и модифицированные лизосомные ферменты и могут быть получены с помощью рекомбинантных и синтетических способов или очищены из природных источников. Заместительный фермент может представлять собой рекомбинантный, синтетический, ген-активированный или природный фермент.
[105] Растворимый. Используемый в данном документе термин «растворимый» относится к способности терапевтического средства образовывать гомогенный раствор. В некоторых вариантах осуществления растворимость терапевтического средства в растворе, в который его вводят и с помощью которого его переносят в целевое место действия, является достаточной для обеспечения доставки терапевтически эффективного количества терапевтического средства в целевое место действия. На растворимость терапевтических средств может влиять несколько факторов. Например, существенные факторы, которые могут влиять на растворимость белка, включают в себя ионную силу, аминокислотную последовательность и наличие других совместных солюбилизирующих средств или солей (например, солей кальция). В некоторых вариантах осуществления терапевтические средства в соответствии с настоящим изобретением являются растворимыми в их соответствующей фармацевтической композиции.
[106] Стабильность. Используемый в данном документе термин «стабильный» относится к способности терапевтического средства (например, рекомбинантного фермента) сохранять свою терапевтическую эффективность (например, свою предполагаемую биологическую активность и/или физико-химическую целостность полностью или по большей части) в течение продолжительных периодов времени. Стабильность терапевтического средства и способность фармацевтической композиции поддерживать стабильность такого терапевтического средства можно оценивать в течение продолжительных периодов времени (например, в течение по меньшей мере 1, 3, 6, 12, 18, 24, 30, 36 месяцев или дольше). Что касается состава, то стабильным составом является состав, в котором терапевтическое средство, содержащееся в нем, фактически сохраняет свою физическую и/или химическую целостность и биологическую активность при хранении и в ходе процессов (таких как замораживание/размораживание, механическое перемешивание и лиофилизация). Показателем стабильности белка может быть образование высокомолекулярных (HMW) агрегатов, потеря ферментативной активности, образование пептидных фрагментов и сдвиг профилей распределения зарядов.
[107] Обработка против вирусов. Используемый в данном документе термин «обработка против вирусов» относится к «удалению вирусов», при котором вирусы просто удаляют из образца (например, фильтрация для избавления от вирусов), или «инактивация вирусов», при которой вирусы остаются в образце, но в неактивной форме. В некоторых вариантах осуществления при удалении вирусов можно применять, среди прочего, нанофильтрацию и/или хроматографические методики. В некоторых вариантах осуществления при инактивации вирусов можно применять, среди прочего, инактивацию растворителем, инактивацию детергентом, пастеризацию, инактивацию кислым pH и/или инактивацию ультрафиолетом.
ПОДРОБНОЕ ОПИСАНИЕ
[108] Настоящее изобретение предусматривает, среди прочего, способы и композиции, предусматривающие очищенный рекомбинантный белок ASA (rhASA) для заместительной ферментной терапии. Настоящее изобретение по меньшей мере частично основано на обнаружении того, что rhASA является безопасной и хорошо переносимой младенцами и детьми; с возможностью сохранения увеличения дозы для более высокой терапевтической эффективности. Настоящее изобретение частично направлено на терапевтическую дозу улучшенной рекомбинантной rhASA и некоторый интервал между введениями для лечения MLD для улучшения двигательной функции, или по меньшей мере уменьшение или остановку прогрессирующего ухудшения двигательной функции у субъектов с дефицитом ASA.
[109] В одном аспекте настоящее изобретение относится к способу лечения MLD, включающему этапы введения терапевтически эффективной дозы rhASA с подходящим интервалом между дозами для уменьшения или остановки прогрессирования MLD.
[110] В некоторых вариантах осуществления терапевтически эффективная доза составляет 100 мг или больше. В некоторых вариантах осуществления подходящий интервал между дозами предусматривает введение один раз в две недели. В некоторых вариантах осуществления подходящий интервал между дозами предусматривает введение один раз в неделю. В некоторых вариантах осуществления способ включает введение состава, содержащего rhASA в дозе, составляющей 100 мг или больше, один раз в две недели (EOW). В некоторых вариантах осуществления состав, содержащий rhASA, вводят субъекту в дозе, составляющей 100 мг или больше, один раз в неделю (EW). В некоторых вариантах осуществления состав, содержащий rhASA, вводят субъекту в дозе, составляющей 150 мг, один EOW. В некоторых вариантах осуществления состав, содержащий rhASA, вводят субъекту в дозе, составляющей 150 мг, один EW.
[111] В некоторых вариантах осуществления субъект получает дозу, составляющую по меньшей мере 10 мг, в течение некоторого периода времени перед введением дозы, составляющей 100 мг. В некоторых вариантах осуществления субъект получает дозу, составляющую по меньшей мере 30 мг, в течение некоторого периода времени перед введением дозы, составляющей 100 мг. В некоторых вариантах осуществления субъект получает дозу, составляющую 100 мг, в течение некоторого периода времени и затем продолжает получать 100 мг rhASA. В некоторых вариантах осуществления некоторый период времени составляет 20 недель, 30 недель, 35 недель или 40 недель. В некоторых вариантах осуществления некоторый период времени составляет 40 недель.
[112] В некоторых вариантах осуществления субъекты, получающие дозу, составляющую по меньшей мере 100 мг, отвечали на предшествующее лечение с помощью 10 мг. В некоторых вариантах осуществления субъекты, получающие дозу, составляющую по меньшей мере 100 мг, отвечали на предшествующее лечение с помощью 30 мг. В некоторых вариантах осуществления субъекты, получающие дозу, составляющую по меньшей мере 100 мг, не отвечали на предшествующее лечение с помощью 10 мг. В некоторых вариантах осуществления субъекты, получающие дозу, составляющую по меньшей мере 100 мг, не отвечали на предшествующее лечение с помощью 30 мг. В некоторых вариантах осуществления у субъектов, получающих дозу, составляющую по меньшей мере 100 мг, не проявлялся какой-либо неблагоприятный эффект (AE) согласно предшествующему лечению с помощью 10 мг. В некоторых вариантах осуществления у субъектов, получающих дозу, составляющую по меньшей мере 100 мг, не проявлялся какой-либо AE согласно предшествующему лечению с помощью 30 мг. В некоторых вариантах осуществления у субъектов, получающих дозу, составляющую по меньшей мере 100 мг, не проявлялся какой-либо AE согласно предшествующему лечению с помощью 100 мг.
[113] В некоторых вариантах осуществления состав, содержащий rhASA, вводят в дозе, составляющей 100 мг или больше, один EW в течение 12 недель с последующим введение EOW. В некоторых вариантах осуществления состав, содержащий rhASA, вводят в дозе, составляющей 150 мг, один EW в течение 12 недель с последующим введение EOW. В некоторых вариантах осуществления у субъекта не проявляется неблагоприятный эффект при введении.
[114] Настоящее изобретение частично основано на обнаружении того, что терапевтическое применение rhASA является эффективным при лечении более широкого диапазона видов MLD, особенно поздней младенческой формы MLD. В одном аспекте настоящее изобретение предусматривает способ лечения поздней младенческой формы MLD. В некоторых вариантах осуществления способ включает введение состава, содержащего rhASA, субъекту, имеющему позднюю младенческую форму MLD. В некоторых вариантах осуществления способ включает введение эффективной терапевтической дозы состава, содержащего rhASA, с подходящим интервалом между дозами субъекту, имеющему позднюю младенческую форму MLD, для уменьшения или остановки прогрессирования поздней младенческой формы MLD. В некоторых вариантах осуществления способ включает интратекальное введение. В некоторых вариантах осуществления эффективная терапевтическая доза для лечения поздней младенческой формы MLD составляет 150 мг. В некоторых вариантах осуществления подходящий интервал между дозами для лечения поздней младенческой формы MLD предусматривает введение один раз в неделю.
[115] В некоторых вариантах осуществления субъект, имеющий позднюю младенческую форму MLD, имеет возраст 72 месяца или меньше. В некоторых вариантах осуществления субъект, имеющий позднюю младенческую форму MLD, имеет возраст 48 месяцев или меньше. В некоторых вариантах осуществления субъект, имеющий позднюю младенческую форму MLD, имеет возраст 24 месяца или меньше. В некоторых вариантах осуществления субъект, имеющий позднюю младенческую форму MLD, имеет возраст 18 месяцев или меньше. Субъектов выбирают и разделяют на категории на основании двигательной функции, которая определена по классификации общей моторики (GMFC).
[116] В некоторых вариантах осуществления способ включает введение состава, содержащего rhASA, интратекально субъекту, имеющему позднюю младенческую форму MLD, в дозе, составляющей 150 мг, один EW. В некоторых вариантах осуществления введение продолжали в течение по меньшей мере двух лет.
[117] Отбор субъектов для лечения поздней младенческой формы MLD с помощью состава, содержащего rhASA, предусматривает несколько факторов, основанных на возрасте, состоянии заболевания и определении характеристик двигательной функции. В некоторых вариантах осуществления лечение вводят субъекту с клиническими проявлениями на ранней стадии. В некоторых вариантах осуществления возраст субъекта с поздней младенческой формой MLD с клиническими проявлениями на ранней стадии составляет 18-48 месяцев. В некоторых вариантах осуществления субъект с поздней младенческой формой MLD с клиническими проявлениями на ранней стадии характеризуется уровнем 1-2 классификации общей моторики при MLD [GMFC-MLD].
[118] В некоторых вариантах осуществления лечение поздней младенческой формы MLD вводят субъекту с клиническими проявлениями на средней стадии. В некоторых вариантах осуществления возраст субъекта, представляющего собой субъекта с клиническими проявлениями на поздней стадии, составляет 18-72 месяца. В некоторых вариантах осуществления субъект, представляющий собой субъекта с клиническими проявлениями на поздней стадии, имеет уровень 4 GMFC MLD.
[119] В некоторых вариантах осуществления лечение поздней младенческой формы MLD вводят субъекту на предсимптоматической стадии или с клиническими проявлениями на минимальном уровне. В некоторых вариантах осуществления возраст субъекта на предсимптоматической стадии или с клиническими проявлениями на минимальном уровне составляет 18 месяцев или меньше, или единокровные родственники на предсимптоматической стадии из участников с одинаковым аллельным строением ASA. В одном варианте осуществления субъекта на предсимптоматической стадии оценивают с помощью Альбертской шкалы двигательной функции у младенцев (Piper M and Darrah J, “Motor Assessment of a Developing Infant,” Published February 9, 1994, страницы 222; ISBN: 9780721643076, Saunders).
[120] В некоторых вариантах осуществления настоящее изобретение предусматривает композицию на основе очищенной rhASA для введения субъекту с MLD.
Лечение заболевания, представляющего собой метахроматическую лейкодистрофию (MLD)
[121] Композиции и способы по настоящему изобретению можно применять для эффективного лечения индивидуумов, страдающих от MLD или подверженных ему, путем доставки в ЦНС. Определенные способы по настоящему изобретению для лечения MLD обычно включают этап интратекального введения субъекту, нуждающемуся в лечении, рекомбинантного фермента, представляющего собой арилсульфатазу A (ASA), в терапевтически эффективной дозе и с некоторым интервалом между введениями в течение периода лечения, достаточного для стабилизации или замедления прогрессирования двигательной дисфункции, которую оценивают по уровню GMFC-MLD (указывающему на ухудшение двигательной функции). В соответствии со многими способами, предусмотренными в настоящем изобретении, у субъекта не наблюдаются серьезные неблагоприятные эффекты, ассоциированные с введением рекомбинантной арилсульфатазы A.
Двигательные функции
[122] В некоторых вариантах осуществления неврологическое нарушение у пациента с MLD характеризуется ухудшением двигательной функции, например общей моторики. В некоторых вариантах осуществления эффективность лечения предусматривает шкалу оценки, которая связана с одной или более двигательными функциями.
[123] В некоторых вариантах осуществления предусмотрены способы лечения синдрома метахроматической лейкодистрофии (MLD), включающие этап интратекального введения субъекту, нуждающемуся в лечении, рекомбинантного фермента, представляющего собой арилсульфатазу A (ASA), в терапевтически эффективной дозе и с некоторым интервалом между введениями в течение периода лечения, достаточного для облегчения, стабилизации или снижения темпов ухудшения одной или более двигательных функций по сравнению с исходным уровнем. В некоторых вариантах осуществления введение рекомбинантного фермента ASA дополнительно приводит к облегчению, стабилизации или снижению темпов ухудшения одной или более когнитивных, адаптивных и/или исполнительных функций.
[124] Одна или более двигательных функций могут включать в себя, например, общую моторику. Будет понятно, что общую моторику можно оценивать с помощью любого соответствующего способа. Например, в некоторых вариантах осуществления общую моторику оценивают по изменению двигательной функции от исходного уровня с применением шкалы оценки общей моторики, такой как общий исходный показатель или доля в процентах шкалы оценки общей моторики-88 (GMFM-88) или классификация общей моторики (GMFC).
Шкала оценки общей моторики-88 (GMFM-88)
[125] В некоторых вариантах осуществления неврологическое нарушение у пациента с MLD характеризуется ухудшением общей моторики. Будет понятно, что общую моторику можно оценивать с помощью любого соответствующего способа. Например, в некоторых вариантах осуществления общую моторику оценивают по изменению двигательной функции от исходного уровня с применением общего исходного показателя шкалы оценки общей моторики-88 (GMFM-88). В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, превышающий 40%. В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, составляющий меньше 40%.
[126] В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к меньшему ухудшению двигательных функций, чем ухудшение, которое, как правило, будет наблюдаться без введения. Например, в некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами по настоящему изобретению приводит к уменьшению показателя GMFM-88 меньше чем на 10%, 20%, 30%, 40% или 50%.
[127] В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, составляющий 35. В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, составляющий больше 35. В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, составляющий 40. В некоторых вариантах осуществления субъект, подвергаемый лечению, имеет исходный показатель GMFM-88, составляющий больше 40. В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к сохранению двигательных функций относительно исходного уровня. В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к сохранению двигательных функций, оцененных с помощью показателя GMFM-88.
[128] В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к значительной стабилизации двигательной функции, например значительной стабилизации показателя, такого как показатель GMFM-88. Под «значительной стабилизацией» подразумевается, что ухудшение или усугубление отсутствует в течение некоторого периода времени, например в течение периода лечения и/или в течение периода, в ходе которого в обычных условиях будет ожидаться ухудшение или усугубление в отсутствие лечения.
[129] В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к улучшению двигательной функции, например улучшению показателя, такого как показатель GMFM-88.
[130] Также следует понимать, что для любого конкретного субъекта конкретные режимы дозирования необходимо корректировать с течением времени в соответствии с индивидуальной необходимостью и профессиональной оценкой специалиста, осуществляющего введение или контролирующего введение заместительной ферментной терапии, и что диапазоны доз, изложенные в данном документе, приводятся только в качестве примера и не предполагают ограничения объема или практической реализации заявляемого изобретения.
Классификация общей моторики (GMFC-MLD)
[131] Классификацию общей моторики (GMFC-MLD) можно применять в качестве инструмента для стандартизированной оценки общей моторики при MLD. GMFC-MLD состоит из семи уровней, представляющих все клинически связанные стадии от нормального (уровень 0) до потери всей общей моторики (уровень 6). В некоторых вариантах осуществления общую моторику оценивают с применением GMFC-MLD.
[132] В некоторых вариантах осуществления субъект, которого подвергают лечению, характеризуется исходным уровнем GMFC менее или равным 2 (способность стоять и ходить с помощью). В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к сохранению двигательных функций относительно исходного уровня, которое оценено по уровню GMFC. В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами, раскрытыми в данном документе, приводит к сохранению уровня GMFC, равным или менее 2.
[133] В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами по настоящему изобретению приводит к увеличению их уровня GMFC-MLD (указывающему на ухудшение двигательной функции) на не более чем 2 уровня от исходного уровня за 2 года. В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами по настоящему изобретению приводит к увеличению их уровня GMFC-MLD (указывающему на ухудшение двигательной функции) на не более чем 3 уровня от исходного уровня за 2 года. В некоторых вариантах осуществления введение рекомбинантного фермента ASA в соответствии со способами настоящего изобретения приводит к сохранению общей моторики, оцененной по изменению от исходного уровня на не более чем 2 уровня согласно GMFC-MLD.
Терапевтическое введение
[134] Очищенный рекомбинантный белок ASA можно вводить пациенту с MLD в соответствии с известными способами. Например, очищенный рекомбинантный белок ASA можно доставлять внутривенно, подкожно, внутримышечно, парентерально, трансдермально или через слизистую (например, перорально или назально).
[135] В некоторых вариантах осуществления рекомбинантную ASA или фармацевтическую композицию, содержащую ее, вводят субъекту с помощью внутривенного введения.
[136] В некоторых вариантах осуществления рекомбинантную ASA или фармацевтическую композицию, содержащую ее, вводят субъекту с помощью интратекального введения. Используемый в данном документе термин «интратекальное введение» или «интратекальная инъекция» относится к инъекции в позвоночный канал (интратекальное пространство, окружающее спинной мозг). Можно применять различные методики, включающие без ограничения интрацеребральную инъекцию в боковые желудочки головного мозга через трепанационное отверстие или с помощью цистернальной или люмбальной пункции или т. п. В некоторых вариантах осуществления «интратекальное введение» или «интратекальная доставка» в соответствии с настоящим изобретением относится к IT введению или доставке в поясничную зону или область, т. е. к люмбальным IT введению или доставке. Используемый в данном документе термин «поясничная область» или «поясничная зона» относится к зоне между третьим и четвертым поясничными позвонками (в нижнем отделе спины) и, более содержательно, к области L2-S1 позвоночника. В некоторых вариантах осуществления рекомбинантную ASA или фармацевтическую композицию, содержащую ее, вводят субъекту с помощью интратекального введения, как описано в международных публикациях согласно PCT WO2011/163648 и WO2011/163650, включенных в данном документе посредством ссылки в полном объеме.
[137] В некоторых вариантах осуществления рекомбинантную ASA или фармацевтическую композицию, содержащую ее, вводят субъекту с помощью подкожного (т. е. под кожу) введения. Для таких целей состав можно инъецировать с применением шприца. Однако, доступны и другие устройства для введения состава, такие как инъекционные устройства (например, устройства Inject-ease и Genject); шприц-ручки (такие как GenPen); безыгольные устройства (например, MediJector и BioJector) и пластырные системы подкожной доставки.
[138] В некоторых вариантах осуществления интратекальное введение можно применять в сочетании с другими путями введения (например, внутривенным, подкожным, внутримышечным, парентеральным, трансдермальным или через слизистую (например, пероральным или назальным)).
[139] Настоящее изобретение охватывает однократные, а также многократные введения терапевтически эффективного количества рекомбинантной ASA или фармацевтической композиции, содержащей ее, описанных в данном документе. Рекомбинантную ASA или фармацевтическую композицию, содержащую ее, можно вводить с равными интервалами в зависимости от природы, степени тяжести и степени выраженности состояния субъекта (например, лизосомной болезни накопления). В некоторых вариантах осуществления терапевтически эффективное количество рекомбинантной ASA или фармацевтической композиции, содержащей ее, можно вводить периодически с равными интервалами (например, один раз в год, один раз в шесть месяцев, один раз в пять месяцев, один раз в три месяца, каждые два месяца (один раз в два месяца), ежемесячно (один раз в месяц), каждые две недели (один раз в две недели), еженедельно, ежедневно или постоянно).
Доставка в ЦНС
[140] Считается, что различные стабильные составы, описанные в данном документе, в целом подходят для доставки терапевтических средств в ЦНС. Стабильные составы в соответствии с настоящим изобретением можно применять для доставки в ЦНС посредством различных методик и путей, в том числе без ограничения с помощью интрапаренхимального, интрацеребрального, интравентрикулярного интрацеребрального (ICV), интратекального (например, люмбального IT, IT в большую цистерну) введения и любых других методик и путей прямой или непрямой инъекции в ЦНС и/или CSF. Термин «большая цистерна» относится к пространству вокруг и ниже мозжечка в виде просвета между черепом и верхней частью позвоночника. Как правило, инъекция в большую цистерну также называется «доставкой в большую цистерну».
Интратекальная доставка
[141] В некоторых вариантах осуществления заместительный фермент доставляется в ЦНС в составе, описанном в данном документе. В некоторых вариантах осуществления заместительный фермент доставляется в ЦНС путем введения в спинномозговую жидкость (CSF) субъекта, нуждающегося в лечении. В некоторых вариантах осуществления для доставки необходимого заместительного фермента (например, белка ASA) в CSF применяют интратекальное введение. Как используется в данном документе, интратекальное введение (также называемое интратекальной инъекцией) относится к инъекции в позвоночный канал (интратекальное пространство, окружающее спинной мозг). Можно применять различные методики, включающие в себя без ограничения люмбальную пункцию. Приводимые в качестве примера способы описаны в Lazorthes et al. Advances in Drug Delivery Systems and Applications in Neurosurgery, 143-192, содержание которого включено в данный документ посредством ссылки.
[142] В соответствии с настоящим изобретением фермент можно инъецировать в любую область, окружающую позвоночный канал. В некоторых вариантах осуществления фермент инъецируют в поясничную зону. Используемый в данном документе термин «поясничная область» или «поясничная зона» относится к зоне между третьим и четвертым поясничными позвонками (в нижнем отделе спины) и, более содержательно, к области L2-S1 позвоночника. Как правило, интратекальная инъекция в поясничную область или поясничную зону также называется «люмбальной интратекальной доставкой» или «люмбальным интратекальным введением».
[143] В некоторых вариантах осуществления терапевтические белки, например рекомбинантную арилсульфатазу A, доставляют путем люмбального интратекального введения, например доставляют в область между третьим и четвертым поясничными позвонками (в нижнем отделе спины) и, более содержательно, в область L2-S1 позвоночника. Считается, что люмбальные интратекальные введение или доставка отличаются от доставки в большую цистерну тем, что люмбальные интратекальные введение или доставка в соответствии с настоящим изобретением обеспечивают лучшую и более эффективную доставку в дистальный отдел позвоночного канала, тогда как доставка в большую цистерну, помимо прочего, как правило, не обеспечивает хорошую доставку в дистальный отдел позвоночного канала.
Устройство для интратекальной доставки
[144] Для интратекальной доставки в соответствии с настоящим изобретением можно применять различные устройства. В некоторых вариантах осуществления устройство для интратекального введения содержит порт доступа жидкости (например, инъекционный порт); полый корпус (например, катетер), имеющий первую расходомерную диафрагму, находящуюся в гидравлическом сообщении с портом доступа жидкости, и вторую расходомерную диафрагму, выполненную с возможностью вставки в спинной мозг; и фиксирующий механизм для фиксации вставленного полого корпуса в спинном мозге. В качестве неограничивающего примера, подходящий фиксирующий механизм содержит один или более выступов, размещенных на поверхности полого корпуса, и шовное кольцо, устанавливаемое на один или более выступов, для предотвращения выскальзывания полого корпуса (например, катетера) из спинного мозга. В различных вариантах осуществления порт доступа жидкости включает в себя резервуар. В некоторых вариантах осуществления порт доступа жидкости включает в себя механический насос (например, инфузионный насос). В некоторых вариантах осуществления имплантированный катетер соединен с резервуаром (например, для болюсной доставки) или инфузионным насосом. Порт доступа жидкости может быть имплантированным или наружным.
[145] В некоторых вариантах осуществления интратекальное введение можно осуществлять с помощью люмбальной пункции (т. е. путем медленного болюсного введения) либо посредством системы доставки порт-катетер (т. е. путем инфузии или болюсного введения). В некоторых вариантах осуществления катетер вставляют между пластинками дуг поясничных позвонков, и наконечник осторожно продвигают в интратекальное пространство до необходимого уровня (обычно L3-L4).
[146] В некоторых вариантах осуществления интратекальное введение осуществляют посредством периодического или постоянного доступа к имплантированному устройству для интратекальной доставки лекарственных средств (IDDD).
[147] По сравнению с внутривенным введением объем однократной дозы, подходящий для интратекального введения, является, как правило, небольшим. Как правило, при интратекальной доставке в соответствии с настоящим изобретением поддерживается баланс состава CSF, а также внутричерепное давление субъекта. В некоторых вариантах осуществления интратекальную доставку осуществляют при отсутствии соответствующего удаления CSF из организма субъекта. В некоторых вариантах осуществления подходящий объем однократной дозы может составлять, например, меньше чем приблизительно 10 мл, 8 мл, 6 мл, 5 мл, 4 мл, 3 мл, 2 мл, 1,5 мл, 1 мл или 0,5 мл. В некоторых вариантах осуществления подходящий объем однократной дозы может составлять приблизительно 0,5-5 мл, 0,5-4 мл, 0,5-3 мл, 0,5-2 мл, 0,5-1 мл, 1-3 мл, 1-5 мл, 1,5-3 мл, 1-4 мл или 0,5-1,5 мл. В некоторых вариантах осуществления интратекальная доставка в соответствии с настоящим изобретением предусматривает этап первоначального удаления необходимого количества CSF. В некоторых вариантах осуществления перед интратекальным введением вначале удаляют меньше чем приблизительно 10 мл (например, меньше чем приблизительно 9 мл, 8 мл, 7 мл, 6 мл, 5 мл, 4 мл, 3 мл, 2 мл, 1 мл) CSF. В этих случаях подходящий объем однократной дозы может составлять, например, больше чем приблизительно 3 мл, 4 мл, 5 мл, 6 мл, 7 мл, 8 мл, 9 мл, 10 мл, 15 мл или 20 мл.
[148] Другие устройства для интратекального введения терапевтических композиций или составов индивидууму описаны в патенте США № 6217552, включенном в данный документ посредством ссылки. В качестве альтернативы, лекарственное средство можно давать интратекально, например, посредством однократной инъекции или непрерывной инфузии. Следует понимать, что лечение дозами может происходить в виде введения однократной дозы или многократных доз.
[149] Для инъекции составы по настоящему изобретению можно составлять в виде жидких растворов. В дополнение, фермент можно составлять в твердой форме и повторно растворять или суспендировать непосредственно перед применением. Также включены лиофилизированные формы. Инъекцию можно осуществлять, например, в виде болюсной инъекции или непрерывной инфузии фермента (например, с помощью инфузионных насосов).
Способы доставки, отличные от интратекальных
[150] Терапевтические ферменты, например рекомбинантную арилсульфатазу A, можно вводить с помощью способов, отличных от интратекальных, например путем интрацеребральной инъекции в боковые желудочки головного мозга субъекта. Инъекцию можно осуществлять, например, через трепанационное отверстие, проделанное в черепе субъекта. В другом варианте осуществления ферментный и/или другой фармацевтический состав вводят через вставленный хирургическим путем шунт в желудочек головного мозга субъекта. Например, инъекцию можно осуществлять в боковые желудочки, большие по размеру. В некоторых вариантах осуществления также можно осуществлять инъекцию в третий и четвертый желудочки, меньшие по размеру.
[151] В качестве альтернативы, фармацевтические композиции можно вводить посредством инъекции в большую цистерну или поясничную зону субъекта.
[152] Можно применять определенные устройства для выполнения введения терапевтической композиции. Например, составы, содержащие необходимые ферменты, можно предоставлять с помощью резервуара Оммайя, широко используемого для интратекального введения лекарственных средств при канцероматозе мозговых оболочек (Lancet 2: 983-84, 1963). Более конкретно, в этом способе вентрикулярную трубку вставляют через отверстие, образованное в переднем роге спинного мозга, и соединяют с резервуаром Оммайя, установленным под кожей волосистой части головы, и резервуар прокалывают под кожей для интратекальной доставки конкретного замещающего фермента, вводимого в резервуар.
Медленное высвобождение/стабильная доставка
[153] В другом варианте осуществления способа по настоящему изобретению фармацевтически приемлемый состав обеспечивает стабильную доставку, например «медленное высвобождение», ферментной или другой фармацевтической композиции, применяемой в настоящем изобретении, в организм субъекта в течение по меньшей мере одной, двух, трех, четырех недель или более длительных периодов времени после введения субъекту фармацевтически приемлемого состава.
[154] Используемый в данном документе термин «стабильная доставка» относится к непрерывной доставке фармацевтического состава по настоящему изобретению in vivo в течение некоторого периода времени после введения, предпочтительно по меньшей мере нескольких дней, недели или нескольких недель. Стабильная доставка композиции может быть продемонстрирована, например, по продолжительному терапевтическому эффекту фермента в течение некоторого времени (например, стабильная доставка фермента может быть продемонстрирована по продолжительному снижению количества накопительных гранул у субъекта). В качестве альтернативы, стабильная доставка фермента может быть продемонстрирована по выявлению наличия фермента in vivo в течение некоторого времени.
Доставка в целевые ткани
[155] Как обсуждается выше, одним из удивительных и важных признаков настоящего изобретения является то, что терапевтические средства, в частности, заместительные ферменты, вводимые с применением являющихся объектом настоящего изобретения способов и композиций по настоящему изобретению, способны к эффективной и обширной диффузии через поверхность головного мозга и к проникновению в различные слои или области головного мозга, в том числе в глубокие области головного мозга. В дополнение, являющиеся объектом настоящего изобретения способы и композиции по настоящему изобретению обеспечивают эффективную доставку терапевтических средств (например, фермента ASA) в различные ткани, нейроны или клетки спинного мозга, в том числе в поясничную область, нацеливание на которую с помощью существующих способов доставки в ЦНС, таких как ICV инъекция, является затруднительным. Кроме того, являющиеся объектом настоящего изобретения способы и композиции по настоящему изобретению обеспечивают доставку достаточного количества терапевтических средств (например, фермента ASA) в кровоток и различные периферические органы и ткани.
[156] Таким образом, в некоторых вариантах осуществления терапевтический белок (например, фермент ASA) доставляют в центральную нервную систему субъекта. В некоторых вариантах осуществления терапевтический белок (например, фермент ASA) доставляют в одну или более целевых тканей головного мозга, спинного мозга и/или периферических органов. Используемый в данном документе термин «целевые ткани» относится к любой ткани, пораженной лизосомной болезнью накопления, подлежащей лечению, или любой ткани, в которой в обычных условиях экспрессируется дефицитный лизосомный фермент. В некоторых вариантах осуществления целевые ткани включают в себя те ткани, в которых имеется выявляемое или аномально высокое количество субстрата фермента, например хранящегося в клеточных лизосомах ткани, у пациентов, страдающих от лизосомной болезни накопления или подверженных ей. В некоторых вариантах осуществления целевые ткани включают в себя те ткани, которые демонстрируют патологический процесс, симптом или признак, ассоциированный с заболеванием. В некоторых вариантах осуществления целевые ткани включают в себя те ткани, в которых дефицитный лизосомный фермент в обычных условиях экспрессируется на повышенном уровне. Как используется в данном документе, целевая ткань может представлять собой целевую ткань головного мозга, целевую ткань спинного мозга и/или периферическую целевую ткань. Приводимые в качестве примера целевые ткани подробно описаны ниже.
Целевые ткани головного мозга
[157] Как правило, головной мозг можно подразделить на различные области, слои и ткани. Например, менингеальная ткань представляет собой систему мембран, покрывающих центральную нервную систему, в том числе головной мозг. Мозговые оболочки содержат три слоя, включающие твердую мозговую оболочку, паутинную мозговую оболочку и мягкую мозговую оболочку. Как правило, основной функцией мозговых оболочек и спинномозговой жидкости является защита центральной нервной системы. В некоторых вариантах осуществления терапевтический белок в соответствии с настоящим изобретением доставляется в один или более слоев мозговых оболочек.
[158] Головной мозг имеет три основных подотдела, включающие большой мозг, мозжечок и ствол головного мозга. Полушария головного мозга расположены над большинством других структур головного мозга и покрыты кортикальным слоем. Под большим мозгом залегает ствол головного мозга, напоминающий стебель, к которому прикреплен большой мозг. В задней части головного мозга ниже большого мозга и сзади ствола головного мозга расположен мозжечок.
[159] Промежуточный мозг, расположенный возле средней линии головного мозга и над средним мозгом, содержит таламус, метаталамус, гипоталамус, эпиталамус, преталамус и претектальную область. Средний мозг, также называемый мезэнцефалоном, содержит крышу, покрышку, водопровод и ножки мозга, красное ядро и ядро III пары черепных нервов. Средний мозг связан со зрением, слухом, управлением движениями, циклом сон/бодрствование, концентрацией внимания и терморегуляцией.
[160] Области тканей центральной нервной системы, в том числе головного мозга, можно охарактеризовать по глубине залегания тканей. Например, ткани ЦНС (например, головного мозга) можно охарактеризовать как поверхностные или неглубокие ткани, ткани средней глубины залегания и/или глубокие ткани.
[161] В соответствии с настоящим изобретением терапевтический белок (например, заместительный фермент) можно доставлять в любую(-ые) соответствующую(-ие) целевую(-ые) ткань(-и) головного мозга, ассоциированную(-ые) с конкретным заболеванием, подлежащим лечению у субъекта. В некоторых вариантах осуществления терапевтический белок (например, заместительный фермент) в соответствии с настоящим изобретением доставляют в поверхностную или неглубокую целевую ткань головного мозга. В некоторых вариантах осуществления терапевтический белок в соответствии с настоящим изобретением доставляют в целевую ткань головного мозга средней глубины залегания. В некоторых вариантах осуществления терапевтический белок в соответствии с настоящим изобретением доставляют в глубокую целевую ткань головного мозга. В некоторых вариантах осуществления терапевтический белок в соответствии с настоящим изобретением доставляют в комбинацию поверхностной или неглубокой целевой ткани головного мозга, целевой ткани головного мозга средней глубины залегания и/или глубокой целевой ткани головного мозга. В некоторых вариантах осуществления терапевтический белок в соответствии с настоящим изобретением доставляется в глубокую ткань головного мозга, расположенную по меньшей мере на 4 мм, 5 мм, 6 мм, 7 мм, 8 мм, 9 мм, 10 мм или больше ниже наружной поверхности головного мозга (или по направлению внутрь от нее).
[162] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляются в одну или более поверхностных или неглубоких тканей большого мозга. В некоторых вариантах осуществления целевые поверхностные или неглубокие ткани большого мозга расположены в пределах 4 мм от поверхности большого мозга. В некоторых вариантах осуществления целевые поверхностные или неглубокие ткани большого мозга выбраны из тканей мягкой мозговой оболочки, тканей полосы коркового вещества головного мозга, гиппокампа, пространства Вирхова-Робена, кровеносных сосудов в пространстве VR, гиппокампа, частей гипоталамуса на нижней поверхности головного мозга, зрительных нервов и трактов, обонятельной луковицы и ее проекций и их комбинаций.
[163] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляются в одну или более глубоких тканей большого мозга. В некоторых вариантах осуществления целевые поверхностные или неглубокие ткани большого мозга расположены на 4 мм (например, 5 мм, 6 мм, 7 мм, 8 мм, 9 мм или 10 мм) ниже поверхности большого мозга (или по направлению внутрь от нее). В некоторых вариантах осуществления целевые глубокие ткани большого мозга включают в себя полосу коркового вещества головного мозга. В некоторых вариантах осуществления целевые глубокие ткани большого мозга включают в себя одно или более из промежуточного мозга (например, гипоталамуса, таламуса, преталамуса, субталамуса и т. д.), заднего мозга, чечевицеобразных ядер, базальных ганглиев, хвостатого ядра, скорлупы, миндалевидного тела, бледного шара и их комбинаций.
[164] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в одну или более тканей мозжечка. В определенных вариантах осуществления одна или более целевых тканей мозжечка выбраны из группы, состоящей из тканей молекулярного слоя, тканей слоя клеток Пуркинье, тканей зернистого слоя клеток, ножек мозжечка и их комбинации. В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в одну или более глубоких тканей мозжечка, в том числе без ограничения в ткани слоя клеток Пуркинье, ткани зернистого слоя клеток, глубокую ткань белого вещества мозжечка (например, глубокую по сравнению с зернистым слоем клеток) и глубокую ткань ядер мозжечка.
[165] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в одну или более тканей ствола головного мозга. В некоторых вариантах осуществления одна или более целевых тканей ствола головного мозга включают в себя ткань белого вещества ствола головного мозга и/или ткань ядер ствола головного мозга.
[166] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в различные ткани головного мозга, в том числе без ограничения в серое вещество, белое вещество, перивентрикулярные зоны, мягкую и паутинную мозговые оболочки, мозговые оболочки, новую кору, мозжечок, глубокие ткани в коре головного мозга, молекулярный слой, область хвостатого ядра/скорлупы, средний мозг, глубокие области варолиева моста или сердцевины и их комбинации.
[167] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в различные клетки в головном мозге, в том числе без ограничения в нейроны, глиальные клетки, периваскулярные клетки и/или менингеальные клетки. В некоторых вариантах осуществления терапевтический белок доставляют в олигодендроциты глубокого белого вещества.
Спинной мозг
[168] Как правило, области или ткани спинного мозга можно охарактеризовать по глубине залегания тканей. Например, ткани спинного мозга можно охарактеризовать как поверхностные или неглубокие ткани, ткани средней глубины залегания и/или глубокие ткани.
[169] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в одну или более поверхностных или неглубоких тканей спинного мозга. В некоторых вариантах осуществления целевая поверхностная или неглубокая ткань спинного мозга расположена в пределах 4 мм от поверхности спинного мозга. В некоторых вариантах осуществления целевая поверхностная или неглубокий ткань спинного мозга содержит мягкую мозговую оболочку и/или тракты белого вещества.
[170] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в одну или более глубоких тканей спинного мозга. В некоторых вариантах осуществления целевая глубокая ткань спинного мозга расположена в пределах 4 мм по направлению внутрь от поверхности спинного мозга. В некоторых вариантах осуществления целевая глубокая ткань спинного мозга предусматривает серое вещество и/или эпендимальные клетки спинного мозга.
[171] В некоторых вариантах осуществления терапевтические средства (например, ферменты) доставляют в нейроны спинного мозга.
Периферические целевые ткани
[172] Как используется в данном документе, периферические органы или ткани относятся к любым органам или тканям, не являющимся частью центральной нервной системы (ЦНС). Периферические целевые ткани могут включать в себя без ограничения систему крови, печень, почку, сердце, эндотелий, костный мозг и клетки, происходящие из костного мозга, селезенку, легкое, лимфатический узел, кость, хрящ, яичник и семенник. В некоторых вариантах осуществления терапевтический белок (например, заместительный фермент) в соответствии с настоящим изобретением доставляется в одну или несколько периферических целевых тканей.
Биораспределение и биодоступность
[173] В различных вариантах осуществления после доставки в целевую ткань терапевтическое средство (например, фермент ASA) локализуется внутриклеточно. Например, терапевтическое средство (например, фермент) может локализоваться в экзонах, аксонах, лизосомах, митохондриях или вакуолях целевых клеток (например, нейронов, таких как клетки Пуркинье). Например, в некоторых вариантах осуществления интратекально вводимые ферменты демонстрируют такую динамику транслокации, при которой фермент перемещается в периваскулярном пространстве (например, с помощью пульсационных конвективных механизмов). В дополнение, механизмы активного аксонального транспорта, связанные с ассоциацией вводимого белка или фермента с нейрофиламентами, также могут вносить вклад в распределение интратекально вводимых белков или ферментов в более глубоких тканях центральной нервной системы или иным образом способствовать ему.
[174] В некоторых вариантах осуществления терапевтическое средство (например, фермент ASA), доставляемое в соответствии с настоящим изобретением, может достигать терапевтически или клинически эффективных уровней или видов активности в различных целевых тканях, описанных в данном документе. Как используется в данном документе, терапевтически или клинически эффективными уровнем или активностью являются уровень или активность, достаточные для обеспечения терапевтического эффекта в целевой ткани. Терапевтический эффект может быть объективным (т. е. измеряемым с помощью определенного теста или маркера) или субъективным (т. е. субъект дает указание на эффект или ощущает его). Например, терапевтически или клинически эффективными уровнем или активностью могут являться уровень или активность фермента, достаточные для уменьшения интенсивности симптомов, ассоциированных с заболеванием, в целевой ткани (например, накопления GAG).
Терапевтически эффективная доза и интервал между введениями
[175] Терапевтически эффективное количество обычно вводят согласно режиму дозирования, который может предусматривать несколько разовых доз. Для любого конкретного терапевтического белка терапевтически эффективное количество (и/или соответствующая разовая доза в рамках эффективного режима дозирования) может варьироваться, например, в зависимости от пути введения, от комбинации с другими фармацевтическими средствами. Кроме того, конкретное терапевтически эффективное количество (и/или разовая доза) для любого конкретного пациента может зависеть от ряда факторов, включающих нарушение, подвергаемое лечению, и степень тяжести нарушения; активность конкретного используемого фармацевтического средства; конкретную используемую композицию; возраст, вес тела, общее состояние здоровья, пол и режим питания пациента; время введения, путь введения и/или скорость экскреции или метаболизма конкретного используемого слитого белка; продолжительность лечения и подобные факторы, хорошо известные в области медицины.
[176] В некоторых вариантах осуществления терапевтически эффективная доза составляет или превышает приблизительно 60 мг, 65 мг, 70 мг, 75 мг, 80 мг, 85 мг, 90 мг, 95 мг, 100 мг, 105 мг, 110 мг, 115 мг, 120 мг, 125 мг, 130 мг, 135 мг, 140 мг, 145 мг, 150 мг, 155 мг, 160 мг, 165 мг, 170 мг, 175 мг, 180 мг, 185 мг, 190 мг, 195 мг или приблизительно 200 мг. В конкретных вариантах осуществления терапевтически эффективная доза составляет или превышает приблизительно 150 мг. В некоторых вариантах осуществления терапевтически эффективная доза равняется или составляет меньше чем приблизительно 500 мг, 450 мг, 400 мг, 350 мг, 300 мг, 250 мг, 200 мг или 150 мг. В конкретных вариантах осуществления терапевтически эффективная доза составляет меньше чем приблизительно 200 мг. В некоторых вариантах осуществления терапевтически эффективная доза находиться в диапазоне приблизительно 10-200 мг, приблизительно 20-200 мг, приблизительно 30-200 мг, приблизительно 40-200 мг, приблизительно 50-200 мг, приблизительно 160-200 мг, приблизительно 70-200 мг, приблизительно 80-200 мг, приблизительно 90-200 мг, приблизительно 100-200 мг, приблизительно 125-200, приблизительно 150-200, приблизительно 50-300 мг, приблизительно 75-300 мг, приблизительно 100-300 мг, приблизительно 150-300 или приблизительно 10-50 мг. В некоторых вариантах осуществления терапевтически эффективная доза находится в диапазоне от приблизительно 100 мг до приблизительно 200 мг.
[177] В некоторых вариантах осуществления терапевтически эффективная доза находится в диапазоне от приблизительно 0,005 мг/кг веса головного мозга до 500 мг/кг веса головного мозга, например от приблизительно 0,005 мг/кг веса головного мозга до 400 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 300 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 200 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 100 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 90 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 80 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 70 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 60 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 50 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 40 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 30 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 25 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 20 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 15 мг/кг веса головного мозга, от приблизительно 0,005 мг/кг веса головного мозга до 10 мг/кг веса головного мозга.
[178] В некоторых вариантах осуществления терапевтически эффективная доза превышает приблизительно 0,1 мг/кг веса головного мозга, превышает приблизительно 0,5 мг/кг веса головного мозга, превышает приблизительно 1,0 мг/кг веса головного мозга, превышает приблизительно 3 мг/кг веса головного мозга, превышает приблизительно 5 мг/кг веса головного мозга, превышает приблизительно 10 мг/кг веса головного мозга, превышает приблизительно 15 мг/кг веса головного мозга, превышает приблизительно 20 мг/кг веса головного мозга, превышает приблизительно 30 мг/кг веса головного мозга, превышает приблизительно 40 мг/кг веса головного мозга, превышает приблизительно 50 мг/кг веса головного мозга, превышает приблизительно 60 мг/кг веса головного мозга, превышает приблизительно 70 мг/кг веса головного мозга, превышает приблизительно 80 мг/кг веса головного мозга, превышает приблизительно 90 мг/кг веса головного мозга, превышает приблизительно 100 мг/кг веса головного мозга, превышает приблизительно 150 мг/кг веса головного мозга, превышает приблизительно 200 мг/кг веса головного мозга, превышает приблизительно 250 мг/кг веса головного мозга, превышает приблизительно 300 мг/кг веса головного мозга, превышает приблизительно 350 мг/кг веса головного мозга, превышает приблизительно 400 мг/кг веса головного мозга, превышает приблизительно 450 мг/кг веса головного мозга, превышает приблизительно 500 мг/кг веса головного мозга.
[179] В некоторых вариантах осуществления терапевтически эффективная доза также может быть определена в мг/кг веса тела. Как будет понятно специалисту в данной области, значения веса головного мозга и значения веса тела могут коррелировать. Dekaban AS. “Changes in brain weights during the span of human life: relation of brain weights to body heights and body weights,” Ann Neurol 1978; 4:345-56. Таким образом, в некоторых вариантах осуществления дозы можно преобразовать, как показано в таблице 2.
[180] В некоторых вариантах осуществления терапевтически эффективная доза также может быть определена в мг/15 куб. см. CSF. Как будет понятно специалисту в данной области, терапевтически эффективные дозы в пересчете на значения веса головного мозга и значения веса тела можно преобразовать в мг/15 куб. см. CSF. Например, объем CSF у взрослых людей составляет примерно 150 мл (Johanson CE, et al. “Multiplicity of cerebrospinal fluid functions: New challenges in health and disease,” Cerebrospinal Fluid Res. 2008 May 14;5:10). Таким образом, инъекции взрослым однократной дозы от 0,1 мг до 50 мг белка будут составлять дозы примерно от 0,01 мг/15 куб. см. CSF (0,1 мг) до 5,0 мг/15 куб. см. CSF (50 мг) для взрослых.
[181] Также следует понимать, что для любого конкретного субъекта конкретные режимы дозирования необходимо корректировать с течением времени в соответствии с индивидуальной необходимостью и профессиональной оценкой специалиста, осуществляющего введение или контролирующего введение заместительной ферментной терапии, и что диапазоны доз, изложенные в данном документе, приводятся только в качестве примера и не предполагают ограничения объема или практической реализации заявляемого изобретения.
[182] В определенных вариантах осуществления рекомбинантный фермент арилсульфатазу A вводят с некоторым интервалом между введениями, например с равным интервалом. Например, интервал между введениями может составлять неделю, две недели или месяц.
[183] В определенных вариантах осуществления рекомбинантный фермент арилсульфатазу A вводят в течение периода лечения. Период лечения может быть предварительно определен, или он может быть скорректирован в зависимости от ответа пациента на лечение, в том числе без ограничения возможных нежелательных симптомов и/или свидетельств, указывающих на эффективность лечения, как обсуждается в данном документе. Например, период лечения может составлять по меньшей мере 6 месяцев, по меньшей мере 9 месяцев, по меньшей мере 12 месяцев, по меньшей мере 24 месяца или даже еще больше.
[184] Считается, что в некоторых вариантах осуществления лечение субъектов будет осуществляться в течение определенного периода лечения, при этом обеспечивается определенный период, в ходе которого они не получают лечение или получают альтернативное лечение, а затем снова обеспечивается другой период лечения.
[185] В некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может достигать уровня или активности фермента, составляющих по меньшей мере 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% от нормальных уровня или активности соответствующего лизосомного фермента в целевой ткани. В некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может достигать уровня или активности фермента, увеличенных по меньшей мере в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз или 10 раз по сравнению с контролем или с исходным уровнем (например, с эндогенными уровнями или видами активности при отсутствии лечения). В некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может достигать увеличенных уровня или активности фермента, составляющих по меньшей мере примерно 10 нмоль/ч./мг, 20 нмоль/ч./мг, 40 нмоль/ч./мг, 50 нмоль/ч./мг, 60 нмоль/ч./мг, 70 нмоль/ч./мг, 80 нмоль/ч./мг, 90 нмоль/ч./мг, 100 нмоль/ч./мг, 150 нмоль/ч./мг, 200 нмоль/ч./мг, 250 нмоль/ч./мг, 300 нмоль/ч./мг, 350 нмоль/ч./мг, 400 нмоль/ч./мг, 450 нмоль/ч./мг, 500 нмоль/ч./мг, 550 нмоль/ч./мг или 600 нмоль/ч./мг в целевой ткани.
[186] В некоторых вариантах осуществления являющиеся объектом настоящего изобретения способы в соответствии с настоящим изобретением являются особенно применимыми для нацеливания на поясничную область. В некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может достигать увеличенных уровня или активности фермента в поясничной области, составляющих по меньшей мере примерно 500 нмоль/ч./мг, 600 нмоль/ч./мг, 700 нмоль/ч./мг, 800 нмоль/ч./мг, 900 нмоль/ч./мг, 1000 нмоль/ч./мг, 1500 нмоль/ч./мг, 2000 нмоль/ч./мг, 3000 нмоль/ч./мг, 4000 нмоль/ч./мг, 5000 нмоль/ч./мг, 6000 нмоль/ч./мг, 7000 нмоль/ч./мг, 8000 нмоль/ч./мг, 9000 нмоль/ч./мг или 10000 нмоль/ч./мг.
[187] Как правило, терапевтические средства (например, заместительные ферменты), доставляемые в соответствии с настоящим изобретением, имеют достаточно длительный период полувыведения из CSF и целевых тканей головного мозга, спинного мозга и периферических органов. В некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может иметь период полувыведения, составляющий по меньшей мере примерно 30 минут, 45 минут, 60 минут, 90 минут, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 12 часов, 16 часов, 18 часов, 20 часов, 25 часов, 30 часов, 35 часов, 40 часов, до 3 дней, до 7 дней, до 14 дней, до 21 дня или до месяца. В некоторых вариантах осуществления, в некоторых вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, может сохранять выявляемые уровень или активность в CSF или кровотоке через 12 часов, 24 часа, 30 часов, 36 часов, 42 часа, 48 часов, 54 часа, 60 часов, 66 часов, 72 часа, 78 часов, 84 часа, 90 часов, 96 часов, 102 часа или неделю после введения. Выявляемые уровень или активность можно определить с помощью различных способов, известных из уровня техники.
[188] В определенных вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, достигает концентрации, составляющей по меньшей мере 30 мкг/мл, в тканях и клетках ЦНС субъекта после введения (например, через неделю, 3 дня, 48 часов, 36 часов, 24 часа, 18 часов, 12 часов, 8 часов, 6 часов, 4 часа, 3 часа, 2 часа, 1 час, 30 минут или меньше после интратекального введения фармацевтической композиции субъекту). В определенных вариантах осуществления терапевтическое средство (например, заместительный фермент), доставляемое в соответствии с настоящим изобретением, достигает концентрации, составляющей по меньшей мере 20 мкг/мл, по меньшей мере 15 мкг/мл, по меньшей мере 10 мкг/мл, по меньшей мере 7,5 мкг/мл, по меньшей мере 5 мкг/мл, по меньшей мере 2,5 мкг/мл, по меньшей мере 1,0 мкг/мл или по меньшей мере 0,5 мкг/мл, в целевых тканях или клетках субъекта (например, в тканях или нейронах головного мозга) после введения такому субъекту (например, через неделю, 3 дня, 48 часов, 36 часов, 24 часа, 18 часов, 12 часов, 8 часов, 6 часов, 4 часа, 3 часа, 2 часа, 1 час, 30 минут или меньше после интратекального введения таких фармацевтических композиций субъекту).
Терапевтические составы
[189] Рекомбинантную ASA или фармацевтическую композицию, содержащую ее, можно составлять с физиологически приемлемым носителем или вспомогательным веществом с получением фармацевтической композиции. Носитель и терапевтическое средство могут быть стерильными. Состав должен соответствовать способу введения.
[190] Подходящие фармацевтически приемлемые носители включают без ограничения воду, солевые растворы (например, NaCl), физиологический раствор, забуференный физиологический раствор, спирты, глицерин, этанол, аравийскую камедь, растительные масла, бензиловые спирты, полиэтиленгликоли, желатин, углеводы, такие как лактоза, амилоза или крахмал, сахара, такие как маннит, сахароза или другие, декстрозу, стеарат магния, тальк, кремниевую кислоту, вязкий парафин, парфюмерное масло, сложные эфиры жирных кислот, гидроксиметилцеллюлозу, поливинилпирролидон и т. д., а также их комбинации. Фармацевтические препараты можно, если требуется, смешивать со вспомогательными средствами (например, смазывающими веществами, консервантами, стабилизаторами, смачивающими средствами, эмульгаторами, солями для оказания влияния на осмотическое давление, буферами, красящими, вкусовыми и/или ароматными веществами и т. п.), которые не вступают во вредоносную реакцию с активными соединениями или не нарушают их активность. В некоторых вариантах осуществления применяют водорастворимый носитель, подходящий для внутривенного введения.
[191] Фармацевтическая композиция или лекарственный препарат, если это требуется, может также содержать незначительные количества смачивающих или эмульгирующих средств или буферных средств для установления рН. Композиция может представлять собой жидкий раствор, суспензию, эмульсию, таблетку, пилюлю, капсулу, состав с замедленным высвобождением или порошок. Композиция также может быть составлена в виде суппозитория с традиционными связывающими веществами и носителями, такими как триглицериды. Состав для перорального применения может содержать стандартные носители, такие как маннит, лактоза, крахмал, стеарат магния, поливинилпирролидон, сахаринат натрия, целлюлоза, карбонат магния и т. д. фармацевтической степени чистоты.
[192] Композиция или лекарственный препарат могут быть составлены в соответствии с обычными процедурами в виде фармацевтической композиции, приспособленной для введения людям. Например, в некоторых вариантах осуществления композиция для внутривенного введения обычно представляет собой раствор в стерильном изотоническом водном буфере. Если это необходимо, композиция также может содержать солюбилизирующее средство и анестезирующее средство местного действия для облегчения боли в месте инъекции. Обычно ингредиенты предоставляются либо по отдельности, либо смешанными друг с другом в единичной лекарственной форме, например в виде сухого лиофилизированного порошка или обезвоженного концентрата в герметично запечатанном контейнере, таком как ампула или саше, с указанием количества действующего средства. Если композиция предназначена для введения посредством инфузии, то она может быть распределена в инфузионную бутылку, содержащую стерильную воду, физиологический раствор или смесь декстроза/вода фармацевтической степени чистоты. Если композицию вводят посредством инъекции, то может быть предусмотрена ампула со стерильной водой для инъекций или физиологическим раствором, с тем чтобы ингредиенты можно было смешать перед введением.
[193] В некоторых вариантах осуществления арилсульфатаза A составлена в изотоническом растворе, таком как 154 мМ NaCl или 0,9% NaCl и 10-50 мМ фосфата натрия pH 6,5-8,0 или фосфата натрия, глицина, маннита или соответствующих солей калия. В вариантах осуществления осмоляльность состава составляет от приблизительно 250 до приблизительно 350 мосмоль/кг (например, от приблизительно 255 до приблизительно 320 мосмоль/кг, от приблизительно 260 до приблизительно 310 мосмоль/кг или от приблизительно 280 до приблизительно 300 мосмоль/кг).
[194] В другом варианте осуществления ASA составлен в физиологическом буфере, таком как:
a) буферный состав I, содержащий (в мМ): Na2HPO4 (3,50-3,90), NaH2PO4 (0-0,5), глицин (25-30), маннит (230-270) и воду для инъекций; или
b) буферный состав II, содержащий (в мМ): трис-HCl (10), глицин (25-30), маннит (230-270) и воду для инъекций.
[195] Арилсульфатазу A, очищенную согласно способу, описанному в данном документе, можно применять в качестве лекарственного препарата для снижения уровней сфинголипида 3-O-сульфогалактозилцерамида (галактозилсульфатида) в клетках в периферической нервной системе и/или в центральной нервной системе субъекта, страдающего от и/или у которого диагностировали метахроматическую лейкодистрофию. Введение ASA будет приводить к сниженному нарушению навыков двигательного научения и или к повышенной нервной двигательной скорости проведения и/или амплитуде нервной проводимости. Используемый в данном документе термин «терапевтически эффективное количество» в широком смысле определяется как общее количество терапевтического средства, содержащегося в фармацевтической композиции по настоящему изобретению. Обычно терапевтически эффективное количество является достаточным для достижения значимого благоприятного эффекта у субъекта (например, лечения, модулирования, излечения, предупреждения и/или уменьшения интенсивности первопричинного заболевания или состояния). Например, терапевтически эффективным количеством может являться количество, достаточное для достижения требуемого терапевтического и/или профилактического эффекта, такое как количество, достаточное для модулирования рецепторов лизосомных ферментов или их активности, с обеспечением, таким образом, лечения такой лизосомной болезни накопления или ее симптомов (например, снижения количества «полосатых телец» или устранения их присутствия или частоты их появления или клеточной вакуолизации после введения субъекту композиций по настоящему изобретению). Обычно количество терапевтического средства (например, рекомбинантного лизосомного фермента), вводимого субъекту, нуждающемуся в этом, будет зависеть от характеристик субъекта. Такие характеристики включают в себя состояние, степень тяжести заболевания, общее состояние здоровья, возраст, пол и вес тела субъекта. Средний специалист в данной области с легкостью сможет определить соответствующие дозы в зависимости от этих и других взаимосвязанных факторов. В дополнение, как объективные, так и субъективные анализы можно необязательно использовать для идентификации оптимальных диапазонов доз.
[196] В вариантах осуществления характерные особенности очищенного рекомбинантного белка ASA (например, характерная карта гликанов, как, например, очищенный рекомбинантный белок ASA с пороговым количеством манноза-6-фосфатированного рекомбинантного белка ASA), а также другие свойства, такие как характерный максимальный уровень белка клетки-хозяина (HCP), характерный максимальный уровень ДНК клетки-хозяина (HCD) и/или конкретная специфическая активность) могут приводить к необходимым свойствам композиций, содержащих очищенный рекомбинантный белок ASA (например, улучшенная стабильность при хранении, улучшенные терапевтические свойства и т. п.).
[197] В вариантах осуществления настоящее изобретение предусматривает способ очистки рекомбинантного белка ASA из неочищенного препарата (например, необработанных биологических материалов, таких как среда с содержащей ASA культурой клеток) с применением способа, предусматривающего только один этап ультрафильтрации/диафильтрации после хроматографической обработки. В вариантах осуществления данный одиночный этап способа UF/DF достигается путем объединения элюата из этапов хроматографии и регулирования pH объединенного элюата до приблизительно 6,0 или более. В некоторых вариантах осуществления данный упрощенный способ объединяют с этапами хроматографии с высокой загрузочной способностью для облегчения крупномасштабного получения рекомбинантного белка ASA.
[198] Различные аспекты настоящего изобретения подробно описаны в следующих подразделах. Использование подразделов не подразумевает ограничения настоящего изобретения. Каждый подраздел можно использовать в отношении любого аспекта настоящего изобретения. В настоящей заявке использование «или» означает «и/или», если не указано иное.
Арилсульфатаза A
[199] Арилсульфатаза A (ASA, ARSA или цереброзидсульфатаза) представляет собой фермент, который расщепляет цереброзид-3-сульфат (или сульфатид) до цереброзида и сульфата. В частности, галактозилсульфатид в обычных условиях метаболизируется путем гидролиза 3-O-сульфатной связи с образованием галактоцереброзида посредством объединенного действия лизосомального фермента арилсульфатазы A (EC 3.1.6.8) (Austin et al. Biochem J. 1964, 93, 15C-17C) и белка активатора сфинголипида под названием сапосин B. Дефицит арилсульфатазы A происходит во всех тканях пациентов с поздней младенческой, ювенильной и взрослой формами метахроматической лейкодистрофии (MLD). Как используется в данном документе белок, представляющий собой арилсульфатазу A, будут называть «ASA» или «ARSA» и сапосин B будут называть «Sap-B».
[200] Арилсульфатаза A представляет собой кислый гликопротеин с низкой изоэлектрической точкой. При значении pH выше 6,5 фермент существует в виде мономера с молекулярным весом, составляющим примерно 100 кДа. ASA существует в виде октамера весом 480 кДа в кислых условиях (pH ≤ приблизительно 5,0), но диссоциирует на димеры при уровнях нейтрального pH. В моче человека фермент состоит из двух неидентичных субъединиц весом 63 и 54 кДа (Laidler PM et al. Biochim Biophys Acta. 1985, 827, 73-83). Арилсульфатаза A, очищенная от печени, плаценты и фибробластов человека также состоит из двух субъединиц с немного отличающимся размером, варьирующим от 55 до 64 кДа (Draper RK et al. Arch Biochemica Biophys. 1976, 177, 525-538, Waheed A et al. Hoppe Seylers Z Physiol Chem. 1982, 363, 425-430, Fujii T et al. Biochim Biophys Acta. 1992, 15 1122, 93-98). Как и в случае с другими лизосомальными ферментами арилсульфатазу A синтезируют на мембраносвязанных рибосомах в виде гликозилированного предшественника. Затем она проходит через эндоплазматический ретикулум и аппарат Гольджи, где ее N-связанные олигосахариды процессируются с образованием фосфорилированного и сульфатированного олигосахарида комплексного типа (Waheed A et al. Biochim Biophys Acta. 1985, 847, 53-61, Braulke T et al. Biochem Biophys Res Commun. 1987, 143, 178-185). В нормальных культивируемых фибробластах образуется полипептид-предшественник весом 62 кДа, который транслоцируется посредством связывания рецептора манноза-6-фосфата (Braulke T et al. J Biol Chem. 1990, 265, 6650-6655) в кислую прелизосомальную эндосому (Kelly BM et al. Eur J Cell Biol. 1989, 48, 71-78).
[201] Способы, описанные в данном документе, можно применять для очистки арилсульфатазы A от любого источника, например от тканей или культивированных клеток (например, клеток человека (например, фибробластов), которые рекомбинантно продуцируют арилсульфатазу A). Арилсульфатазу A любого происхождения, в том числе без ограничения человека и других животных, таких как млекопитающие, можно получать способами, описанными в данном документе.
[202] Длина (18 аминокислот) сигнального пептида арилсульфатазы A человека основана на консенсусной последовательности и специфическом сайте обработки для сигнальной последовательности. Следовательно, из выведенной cDNA ASA человека (в EMBL, GenBank под номерами доступа J04593 и X521151) отщепление сигнального пептида происходит во всех клетках после остатка с номером 18 (Ala), что дает в результате зрелую форму арилсульфатазы A человека. Как используется в данном документе рекомбинантная арилсульфатаза A будет сокращена как «rASA». Зрелую форму арилсульфатазы A, в том числе зрелую форму арилсульфатазы A человека, будут называть «mASA» и зрелую рекомбинантную человеческую ASA будут называть «mrhASA».
[203] Показаны несколько форм арилсульфатазы A с помощью электрофореза и изоэлектрического фокусирования препаратов фермента из мочи (Luijten JAFM et al. J Mol Med. 1978, 3, 213), лейкоцитов (Dubois et al. Biomedicine. 1975, 23, 116-119, Manowitz P et al. Biochem Med Metab Biol. 1988, 39, 117-120), тромбоцитов (Poretz et al. Biochem J. 1992, 287, 979-983), культивированных фибробластов (Waheed A et al. Hoppe Seylers Z Physiol Chem. 1982, 363, 425-430, Stevens RL et al. Biochim Biophys Acta. 1976, 445, 661-671, Farrell DF et al. Neurology. 1979, 29, 16-20) и печени человека (Stevens RL et al. Biochim Biophys Acta. 1976, 445, 661-671, Farrell DF et al. Neurology. 1979, 29, 16-20, Sarafian TA et al. Biochem Med. 1985, 33, 372-380). Обработка эндоглюкозидазой H, сиалидазой и щелочной фосфатазой уменьшает молекулярный размер и сложность электрофоретического паттерна, что позволяет предположить, что большая часть гетерогенности заряда арилсульфатазы A обусловлена различиями в содержании углеводов фермента.
[204] Активный сайт арилсульфатазы A содержит остаток незаменимого гистидина (Lee GD and Van Etten RL, Arch Biochem Biophys. 1975, 171, 424-434) и два или более остатков аргинина (James GT, Arch Biochem Biophys. 1979, 97, 57-62). Многие анионы представляют собой ингибиторы фермента в концентрациях в миллимолярном диапазоне или ниже.
[205] Описана структура гена арилсульфатазы A человека. Как используется в данном документе данный ген будет называться «ARSA». Однако, в некоторых случаях «ARSA» также может относиться к белку, представляющему собой арилсульфатазу A. Ген ARSA расположен вблизи конца длинного плеча хромосомы 22 (22ql3.31-qter), он охватывает 3,2 т.н. (Kreysing et al. Eur J Biochem. 1990, 191, 627-631) и состоит из восьми экзонов, определяющих единицу фермента из 507 аминокислот (Stein et al. J Biol Chem. 1989, 264, 1252-1259). В клетках-фибробластах обнаружены матричные РНК длиной 2,1, 3,7 и 4,8 т.н., при этом матричная РНК длиной 2,1 т.н., по-видимому, ответственна за объем активной арилсульфатазы A, производимой клеткой (Kreysing et al. Eur J Biochem. 1990, 191, 627-631). Последовательность ARSA депонирована в EMBL, GenBank под номером доступа X521150. Отличия между опубликованной cDNA и кодирующей частью ARSA были описаны Kreysing et al. (Eur J Biochem. 1990, 191, 627-631). Последовательность cDNA, первоначально описанная Stein et al. (J Biol Chem. 1989, 264, 1252-1259), и последовательность cDNA, описанная Kreysing et al. (Eur J Biochem. 1990, 191, 627-631), депонированы в EMBL, GenBank под следующими номерами доступа J04593 и X521151 соответственно.
[206] В гене ARSA идентифицировано несколько полиморфизмов и более 40 связанных с заболеваниями мутаций (Gieselmann et al. Hum Mutat. 1994, 4, 233-242, Barth et al. Hum Mutat. 1995, 6, 170-176, Draghia et al. Hum Mutat. 1997, 9, 234-242). Связанные с заболеваниями мутации в гене ARSA можно разделить на две большие группы, которые довольно хорошо коррелируют с клиническим фенотипом MLD. Одна группа (I) не продуцирует активный фермент, не продуцирует иммунореактивный белок и не проявляет активность ASA при введении в культивируемые линии клеток животного. Другая группа (A) образует малые количества перекрестнореагирующего материала и низкие уровни функционального фермента в культивируемых клетках. У индивидуумов, гомозиготных по мутации в группе (I) или имеющих две отличные мутации из данной группы, проявляется поздняя младенческая форма MLD. У большинства индивидуумов с одной мутацией типа группы (I) и одной мутацией типа группы (A) развивается форма, возникающая в подростковый период, при этом у таковых с двумя мутациями типа группы (A), как правило, проявляется взрослая форма MLD. Некоторые мутации обнаруживаются относительно часто, тогда как другие обнаруживаются только в одиночных семьях. Можно отслеживать специфические мутации при участии представителей многих семей, однако общий скрининг в отношении носителей еще не является выполнимым.
[207] В дополнение к связанным с заболеваниями мутациям, описанным выше, в гене ARSA идентифицировали несколько полиморфизмов. Очень низкая активность ASA обнаружена у некоторых клинически здоровых родителей пациентов с MLD, а также в общей популяции. Данный так называемый псевдодефицит ASA ассоциирован с общим полиморфизмом гена ARSA (Gieselmann et al. Dev Neurosci. 1991, 13, 222-227).
Рекомбинантный белок ASA
[208] Используемый в данном документе термин «рекомбинантный белок ASA» относится к любой молекуле или части молекулы, которая может заменять по меньшей мере частично активность встречающегося в природе белка, представляющего собой арилсульфатазу A (ASA), или обеспечивать избавление от одного или более фенотипов или симптомов, ассоциированных с дефицитом ASA. Используемые в данном документе термины «рекомбинантный фермент ASA» и «рекомбинантный белок ASA» и грамматические эквиваленты используют взаимозаменяемо. В некоторых вариантах осуществления настоящее изобретение применяют для очистки рекомбинантного белка ASA, который представляет собой полипептид с аминокислотной последовательностью, в значительной степени подобной или идентичной зрелому белку ASA человека.
[209] Как правило, ASA человека вырабатывается в виде молекулы-предшественника, которая процессируется до зрелой формы. Этот процесс обычно происходит посредством удаления 18-аминокислотного сигнального пептида. Как правило, форма-предшественник также называется полноразмерным предшественником или полноразмерным белком ASA, который содержит 507 аминокислот. 18 N-концевых аминокислот отщепляются с получением в результате зрелой формы длиной 489 аминокислот. Таким образом, считается, что 18 N-концевых аминокислот обычно не требуются для активности белка ASA. Аминокислотные последовательности зрелой формы (SEQ ID NO: 1) и полноразмерного предшественника (SEQ ID NO: 2) типичного принадлежащего к дикому типу или встречающегося в природе белка ASA человека показаны в таблице 1.
ТАБЛИЦА 1. Арилсульфатаза A человека
[210] Таким образом, в некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, представляет собой зрелый человеческий белок ASA (SEQ ID NO:1). В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, может представлять собой гомолог или аналог зрелого белка ASA человека. Например, гомолог или аналог зрелого белка ASA человека может представлять собой модифицированный зрелый белок ASA человека, содержащий одну или более замен, делеций и/или вставок аминокислот по сравнению с принадлежащим к дикому типу или встречающимся в природе белком ASA (например, SEQ ID NO: 1) и сохраняющий при этом в значительной степени активность белка ASA. Таким образом, в некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, является в значительной степени гомологичным зрелому белку ASA человека (SEQ ID NO:1). В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, имеет аминокислотную последовательность, на по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более гомологичную SEQ ID NO:1. В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, является в значительной степени идентичным зрелому белку ASA человека (SEQ ID NO:1). В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, имеет аминокислотную последовательность, на по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичную SEQ ID NO:1. В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, содержит фрагмент или часть зрелого белка ASA человека.
[211] В качестве альтернативы рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, представляет собой полноразмерный белок ASA. В некоторых вариантах осуществления рекомбинантный белок ASA может быть гомологом или аналогом полноразмерного белка ASA человека. Например, гомолог или аналог полноразмерного белка ASA человека может представлять собой модифицированный полноразмерный белок ASA человека, содержащий одну или более замен, делеций и/или вставок аминокислот по сравнению с принадлежащим к дикому типу или встречающимся в природе полноразмерным белком ASA (например, SEQ ID NO: 2) и сохраняющий при этом в значительной степени активность белка ASA. Таким образом, в некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, является в значительной степени гомологичным полноразмерному белку ASA человека (SEQ ID NO:2). В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, имеет аминокислотную последовательность, на по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более гомологичную SEQ ID NO:2. В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, является в значительной степени идентичным SEQ ID NO:2. В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, имеет аминокислотную последовательность, на по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичную SEQ ID NO:2. В некоторых вариантах осуществления рекомбинантный белок ASA, очищенный согласно вариантам осуществления настоящего изобретения, содержит фрагмент или часть полноразмерного белка ASA человека. Как используется в данном документе, полноразмерный белок ASA, как правило, содержит последовательность сигнального пептида.
[212] Гомологи или аналоги белков ASA человека можно получать в соответствии со способами изменения полипептидной последовательности, известными обычному специалисту в данной области, такими как обнаруживаемые в источниках, в которых собраны такие способы. В некоторых вариантах осуществления консервативные замены аминокислот включают замены, выполненные среди аминокислот в следующих группах (a) M, I, L, V; (b) F, Y, W; (c) K, R, H; (d) A, G; (e) S, T; (f) Q, N и (g) E, D. В некоторых вариантах осуществления «консервативная аминокислотная замена» относится к аминокислотной замене, которая не изменяет такие характеристики, как относительный заряд или размер белка, в котором осуществляют аминокислотную замену.
[213] В некоторых вариантах осуществления рекомбинантные белки ASA могут содержать фрагмент, который связывается с рецептором на поверхности целевой клетки, для облегчения поглощения клетками и/или нацеливания на лизосомы. Например, такой рецептор может представлять собой катионнезависимый рецептор маннозо-6-фосфата (CI-MPR), связывающий остатки маннозо-6-фосфата (M6P). В дополнение, CI-MPR также связывает другие белки, в том числе IGF-II. В некоторых вариантах осуществления рекомбинантный белок ASA содержит остатки M6P на поверхности белка. В частности, рекомбинантный белок ASA может содержать бисфосфорилированные олигосахариды, обладающие более высокой аффинностью связывания с CI-MPR. В некоторых вариантах осуществления подходящий фермент содержит до приблизительно в среднем приблизительно по меньшей мере 20% бисфосфорилированных олигосахаридов на фермент. В других вариантах осуществления подходящий фермент может содержать приблизительно 10%, 15%, 18%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60% бисфосфорилированных олигосахаридов на фермент.
[214] В некоторых вариантах осуществления рекомбинантные ферменты ASA могут быть слиты с компонентом, нацеливающимся на лизосомы, который способен к связыванию с рецептором на поверхности целевых клеток. Подходящими компонентами, нацеливающимися на лизосомы, могут являться IGF-I, IGF-II, RAP, p97 и их варианты, гомологи или фрагменты (например, включающие в себя пептид, имеющий последовательность, на по меньшей мере 70%, 75%, 80%, 85%, 90% или 95% идентичную последовательности зрелого человеческого пептида IGF-I, IGF-II, RAP, p97 дикого типа). Компонент, нацеливающийся на лизосомы, может быть конъюгирован или слит с белком или ферментом ASA на N-конце, C-конце или внутри.
Очистка рекомбинантной арилсульфатазы A
[215] Варианты осуществления настоящего изобретения включают способы очистки для получения лекарственных веществ на основе арилсульфатазы A («ASA»), в частности рекомбинантного человеческого ASA («rhASA»).
[216] Разнообразие методик, в целом или частично, необязательно с модификациями, описанными в данном документе, можно применять для получения лекарственного вещества на основе очищенного ASA.
[217] Например, иллюстративный способ очистки включает один или более из приведенных этапов (например, 1, 2, 3, 4, 5, 6 или все 7 из данных этапов)
Оттаивание и объединение неочищенного массива rhASA (UPB).
Захват и фильтрация UPB посредством ультрафильтрации и диафильтрации («UFDF» или «захват UFDF»).
Далее фильтрация, захваченный материал можно подвергать инактивации вирусов перед хроматографической очисткой.
Способ, включающий последующее применение четырех хроматографических колонок: анионообменной колонки (например, колонки со смолой Fractogel TMAE HiCap), колонки с керамическим гидроксиапатитом типа I (HA), колонки для гидрофобного взаимодействия (HIC; например, колонки Phenyl Sepharose FF) и катионообменной (например, SP) колонки.
Объединение элюат из SP и регулирование pH объединенного элюат (например, регулирование до pH, составляющего от приблизительно 5,5 до приблизительно 6,5 (например, приблизительно 6,0)).
Полученный отрегулированный по pH катионообменный элюат затем фильтруют для избавления от вирусов с последующим этапом однократной концентрации и диафильтрации с достижением конечной целевой концентрации белка.
Добавление полисорбата 20 (P20) к элюату (например, до холодильного хранения).
[218] Используемый в данном документе «загрязнитель» представляет собой материал, который является отличным от необходимого полипептидного продукта, например арилсульфатазы A (ASA). Загрязнитель может быть вариантом необходимого полипептида (например, дезаминированным вариантом или амино-аспартатным вариантом необходимого полипептида) или другой молекулой, например полипептидом, нуклеиновой кислотой и эндотоксином.
[219] Используемое в данном документе «очистка» полипептида из композиции или образца, содержащих полипептид и один или более загрязнителей, подразумевает повышение степени чистоты полипептида в композиции или образце путем удаления (полностью или частично) по меньшей мере одного загрязнителя из композиции или образца.
[220] «Стадия очистки» может быть частью общего способа очистки, давая в результате композицию, содержащую по меньшей мере приблизительно 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 99,5%, 99,6%, 99,7%, 99,8% или 99,9% по весу представляющего интерес полипептида в пересчете на общий вес композиции.
[221] Степень чистоты арилсульфатазы A можно оценивать, например, с помощью одного или более из: вестерн-блоттинга белка клетки-хозяина (HCP), окрашивания кумасси при SDS-PAGE, окрашивания серебром при SDS-PAGE, обращенно-фазовой HPLC и эксклюзионной HPLC.
[222] Арилсульфатазу A, применяемую, например, в композициях и способах, описанных в данном документе, также можно описывать с помощью характерной карты гликанов (например, любой из иллюстративных карт гликанов, описанных в данном документе).
[223] В некоторых вариантах осуществления специфическая активность очищенной арилсульфатазы A составляет по меньшей мере приблизительно 50 ед./мг, 60 ед./мг, 70 ед./мг, 80 ед./мг, 90 ед./мг, 100 ед./мг, 110 ед./мг, 120 ед./мг, 130 ед./мг, 140 ед./мг, например, как определено с помощью способа, описанного в данном документе. В некоторых вариантах осуществления очищенный рекомбинантный ASA обладает специфической активностью, находящейся в диапазоне приблизительно 50-200 ед./мг (например, приблизительно 50-190 ед./мг, 50-180 ед./мг, 50-170 ед./мг, 50-160 ед./мг, 50-150 ед./мг, 50-140 ед./мг, 50-130 ед./мг, 50-120 ед./мг, 50-110 ед./мг, 50-100 ед./мг, 60-140 ед./мг, 60-130 ед./мг, 60-120 ед./мг, 60-110 ед./мг, 60-100 ед./мг, 70-140 ед./мг, 70-130 ед./мг, 70-120 ед./мг, 70-110 ед./мг, 70-100 ед./мг, 80-140 ед./мг, 80-130 ед./мг, 80-120 ед./мг, 80-110 ед./мг, 80-100 ед./мг, 90-140 ед./мг, 90-130 ед./мг, 90-120 ед./мг, 90-110 ед./мг, 90-100 ед./мг, 100-140 ед./мг, 100-130 ед./мг, 100-120 ед./мг, 100-110 ед./мг, 110-140 ед./мг, 110-130 ед./мг, 110-120 ед./мг, 120-140 ед./мг, 120-130 ед./мг или 130-140 ед./мг), например, как определено с помощью способа, описанного в данном документе.
[224] Исходным материалом для способа очистки является любой неочищенный препарат. Например, неочищенный препарат может быть необработанной средой с культурой клеток, содержащей рекомбинантный белок ASA, секретированный из клеток (например, клеток млекопитающих), продуцирующих белок ASA, или непереработанными клеточными лизатами, содержащими белок ASA. В некоторых вариантах осуществления неочищенный препарат может быть частично обработанными клеточной средой или лизатами клеток. Например, клеточная среда или лизаты клеток можно концентрировать, разбавлять, обрабатывать для инактивации вирусов, подвергать обработке от вирусов или удалять вирусы из них. В некоторых вариантах осуществления при удалении вирусов можно применять, среди прочего, нанофильтрацию и/или хроматографические методики. В некоторых вариантах осуществления при инактивации вирусов можно применять, среди прочего, инактивацию растворителем, инактивацию детергентом, пастеризацию, инактивацию кислым pH и/или инактивацию ультрафиолетом. Клеточная среда или лизаты клеток также можно обрабатывать протеазой, ДНКазой и/или РНКазой для снижения уровня белка и/или нуклеиновых кислот клетки-хозяина (например, ДНК или РНК). В некоторых вариантах осуществления необработанные или частично обработанные биологические материалы (например, клеточная среда или лизат клеток) можно замораживать и хранить при необходимой температуре (например, 2-8°C, -4°C, -25°C, -75°C) в течение периода времени и затем подвергать оттаиванию для очистки. Как используется в данном документе неочищенный препарат также называется исходным материалом или материалом для загрузки.
[225] Способы очистки, описанные в данном документе, могут включать без ограничения один или более из следующих этапов: глубинной фильтрации, инактивации вирусов, ионообменной хроматографии (например, анионообменной хроматографии и/или катионообменной хроматографии), хроматографии в комбинированном режиме, хроматографии с гидрофобным взаимодействием, ультрафильтрации/диафильтрации и фильтрации для избавления от вирусов. В некоторых вариантах осуществления способы очистки, описанные в данном документе, дополнительно включают аффинную хроматографию.
[226] На этапах хроматографии подходящий объем смолы, применяемой при упаковке в хроматографическую колонку, отражается размерами колонки, т. е. диаметром колонки и высотой смолы, и варьирует в зависимости, например, от количества белка в применяемом растворе и связывающей способности применяемой смолы. Однако, в пределах объема настоящего изобретения находится увеличение масштаба производственного процесса, а также способ очистки с целью получения производства и очистки ASA в промышленном масштабе. Соответственно параметры, такие как размер, диаметр колонки и скорость потока можно увеличивать, чтобы соответствовать скорости и эффективности такого крупномасштабного производства. В некоторых вариантах осуществления диаметр колонки находится в диапазоне приблизительно 50-100 мм, объем находится в диапазоне приблизительно 100-300 мл, и скорость потока составляет приблизительно 40-400 см/час (например, от приблизительно 100 см/час до 150 см/час) или приблизительно 5-100 мл.
Ультрафильтрация - захват
[227] В некоторых вариантах осуществления настоящего изобретения способы очистки, раскрытые в данном документе, включают один или более этапов восходящей ультрафильтрации с захватом ASA (например, человеческого рекомбинантного ASA), полученного из перфузионного биореактора. Ультрафильтрация, как используется в данном документе, относится к мембранной фильтрации с размером пор фильтра на уровне величины, составляющей от 0,001 до 0,1 мкм, которую можно применять для концентрирования и обессоливания растворенных молекул (белков, пептидов, нуклеиновых кислот, углеводов и других биологических молекул), замены буферов и грубого фракционирования. Способы ультрафильтрации для применения в вариантах осуществления настоящего изобретения предусматривают ультрафильтрацию с тангенциальным потоком или поперечноточную фильтрацию.
[228] Фильтрация и ультрафильтрация с тангенциальным потоком, как используется в данном документе, относятся к компоновкам, где сырьевой поток проходит параллельно лицевой стороне мембраны, по мере того как одна часть проходит через мембрану (пермиат), остальная часть (ретентат) рециркулирует обратно в подающий резервуар. В некоторых вариантах осуществления размер пор фильтров для ультрафильтрации с тангенциальным потоком выбирают так, чтобы обеспечить проникновение рекомбинантного ASA через фильтр. В других вариантах осуществления размер пор выбирают так, чтобы удерживать практически весь ASA в подаче, проходящей через фильтр. Как отмечалось в другом месте, ASA существует в виде октамера весом 480 кДа в кислых условиях (pH ≤ приблизительно 5,0), но диссоциирует на димеры при уровнях нейтрального pH. Таким образом, pH подачи можно регулировать совместно с выбором подходящего размера пор либо для удерживания ASA на мембране фильтра, либо для обеспечения прохождения через нее в качестве пермиата.
[229] Размер пор может быть выбран с отсечениями по молекулярному весу, составляющему по меньшей мере 10 кДа, по меньшей мере 20 кДа, по меньшей мере 30 кДа, по меньшей мере 40 кДа, по меньшей мере 50 кДа, по меньшей мере 60 кДа, по меньшей мере 70 кДа, по меньшей мере 80 кДа, по меньшей мере 90 кДа, по меньшей мере 100 кДа, по меньшей мере 300 кДа, по меньшей мере 400 кДа или по меньшей мере 500 кДа. Например, фильтр с размером пор, составляющим по меньшей мере 10 кДа, будет удерживать в подаче большую часть белков со значениями молекулярного веса, составляющими примерно 11 кДа или больше. В качестве другого примера, фильтр с размером пор, составляющим по меньшей мере 400 кДа, будет удерживать большую часть белков со значениями молекулярного веса больше 400 кДа. В некоторых вариантах осуществления процент удерживания подачи составляет по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или больше. Подобным образом, размер пор может быть выбран для выделения пермиатов с определенным размером. Например, фильтр с размером пор, составляющим по меньшей мере 500 кДа, будет обеспечивать проникание большей части белков со значениями молекулярного веса менее 500 кДа через него. В некоторых вариантах осуществления процент проникновения составляет по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или больше.
[230] Площадь фильтрации или фильтрующую способность также можно оптимизировать для применения в способах, раскрытых в данном документе. Соображения, влияющие на выбор площади фильтрации, предусматривают робастность, стоимость, скорость поступающего потока (т. е. скорость поперечного потока), трансмембранное давление, интенсивность потока пермиата, оборудование предприятия и производительность. В некоторых вариантах осуществления поток пермиата составляет приблизительно 50-100 литров на метр2 в час («LMH»). В некоторых вариантах осуществления поступающий поток составляет приблизительно 250-600 LMH, включительно. В некоторых вариантах осуществления поступающий поток составляет приблизительно 250-350 LMH, включительно. В некоторых вариантах осуществления поступающий поток составляет приблизительно 175-245 LMH, включительно. В некоторых вариантах осуществления поступающий поток составляет приблизительно 170-230 LMH, включительно. В некоторых вариантах осуществления поступающий поток составляет приблизительно 120-160 LMH, включительно. В некоторых вариантах осуществления поступающий поток составляет приблизительно 15-30 LMH, включительно. В некоторых вариантах осуществления взносовый поток составляет приблизительно 11-21 LMH, включительно. В некоторых вариантах осуществления площадь фильтрации составляет приблизительно 0,02 м2, приблизительно 0,14 м2, приблизительно 0,7 или приблизительно 3,5 м2. В конкретных вариантах осуществления трансмембранное давление составляет приблизительно 55-60 psi, включительно. В некоторых вариантах осуществления трансмембранное давление составляет приблизительно 15-25 psi, включительно. В некоторых вариантах осуществления трансмембранное давление составляет приблизительно 10-20 psi, включительно. В некоторых вариантах осуществления трансмембранное давление составляет приблизительно 5-15 psi.
[231] Ультрафильтрационные фильтры для применения в вариантах осуществления настоящего изобретения могут содержать мембранные материалы, известные специалистам в данной области, в том числе без ограничения полиэфирсульфон и стабилизированную целлюлозу.
[232] Одной иллюстративной фильтрующей кассетой для применения в вариантах осуществления настоящего изобретения является ECO® от Sartorius. Другой иллюстративной фильтрующей кассетой для применения в вариантах осуществления настоящего изобретения является стандартная мембрана с размером 30 кДа HYDROSART® от Sartorius. Еще одной иллюстративной фильтрующей кассетой для применения в вариантах осуществления настоящего изобретения является глубинный фильтр ZB от Cuno. В некоторых вариантах осуществления настоящего изобретения применяют глубинный фильтр Zeta Plus от Cuno.
Глубинная фильтрация
[233] Способы очистки, описанные в данном документе, могут включать один или более этапов глубинной фильтрации. Глубинные фильтры представляют собой разнообразие фильтров, в которых применяют пористую фильтрующую среду для удержания частиц по всей среде, а не только на поверхности среды. Они содержат фильтрующие среды с сортированной плотностью, что позволяет улавливать большие частицы ближе к поверхности фильтра, тогда как меньшие частицы проникают через большие открытые участки на поверхности фильтра, лишь для улавливания в меньших отверстиях ближе к центру фильтра. Хотя в некоторых вариантах осуществления применяют этапы глубинной фильтрации только во время восходящей фазы восстановления (т. е. перед последующими этапами хроматографической очистки), в других вариантах осуществления применяют глубинные фильтры во время одой или более дополнительных фаз очистки. В некоторых вариантах осуществления настоящего изобретения применяют глубинный фильтр Zeta Plus от Cuno.
[234] За глубинной фильтрацией необязательно может следовать фильтрация с отсечением по 0,45 микрона (± 2 мкм) для удаления частиц и снижения биологической нагрузки в препарате для последующей обработки.
Инактивация вирусов
[235] Способы очистки, описанные в данном документе, могут включать один или более этапов инактивации вирусов. В некоторых вариантах осуществления инактивация вирусов предусматривает растворитель и/или детергент. Растворитель или детергент могут предусматривать, например, полисорбат 20, полисорбат 80, три-н-бутил-фосфат (TnBP) или их комбинацию. Инактивация вирусов может длиться 3-24 часа инкубации в растворителе или детергенте. В другом варианте осуществления инактивация вирусов предусматривает фильтрацию для избавления от вирусов, например с помощью фильтра Planova™.
[236] Известно, что такие способы предназначены для обеспечения получения фермента, который по сути не содержит инфекционных вирусов и который может быть обозначен как «безопасный в отношении вирусов продукт». Кроме того, предполагается, что можно применять различные способы независимо или в комбинации.
[237] Инактивацию вирусов можно осуществлять путем добавления одного или более «инактивирующих вирусы средств» к раствору, содержащему фермент. В некоторых вариантах осуществления этап инактивации вирусов проводят перед этапом хроматографической очистки (т. е. перед загрузкой неочищенного препарата на первую хроматографическую колонку) с целью обеспечения того, что средство не присутствует в конечном продукте в любых количествах или концентрациях, которые будут нарушать безопасность продукта при применении в качестве фармацевтического вещества или в тех случаях, когда продукт применяют для получения фармацевтического вещества; в других вариантах осуществления применяют глубинные фильтры во время одной или более дополнительных фаз очистки. Например, в некоторых вариантах осуществления являющийся объектом настоящего изобретения способ в соответствии с настоящим изобретением дополнительно включает этап удаления вирусов после последней хроматографической колонки.
[238] Термин «инактивирующее вирус средство» предназначен для обозначения средства (например, детергента) или способа, которые можно применять с целью инактивации вирусов с липидной оболочкой, а также вирусов без липидной оболочки. Термин «инактивирующее вирус средство» следует понимать как охватывающий комбинацию таких средств и/или способов, когда это целесообразно, а также только один тип таких средства или способа.
[239] Типичные инактивирующие вирус средства представляют собой детергенты и/или растворители, более типично смесь детергента и растворителя. Следует понимать, что инактивирующее вирус средство представляет собой необязательно смесь одного или более детергентов с одним или более растворителями. Для инактивации вирусов можно использовать широкое разнообразие детергентов и растворителей. Детергент можно выбрать из группы, состоящей из неионогенных и ионогенных детергентов и выбрать так, чтобы оно по сути не приводило к денатурации. Как правило, применяют неионогенный детергент, поскольку он облегчает последующее устранение детергента из препарата на основе rASA при последующих этапах очистки. Подходящие детергенты описаны, например, в Shanbrom et al., в патенте США 4314997 и патенте США 4315919. Типичными детергентами являются такие, которые продаются под торговыми марками Triton X-100 и Tween 20 или Tween 80. Предпочтительными растворителями для применения в инактивирующих вирус средствах являются ди- или три-алкилфосфаты, которые описаны, например, в патенте США 4764369, под авторством Neurath и Horowitz. Типичный растворитель представляет собой три(н-бутил)фосфат (TnBP). Особенно предпочтительным инактивирующим вирус средством для практического осуществления настоящего изобретения является Tween 80, но, в качестве альтернативы, можно применять другие средства или комбинации средств. Типичное средство добавляют в таком объеме, что концентрация Tween-80 в содержащем ASA растворе находится в диапазоне приблизительно 0,5-4,0% по весу, предпочтительно при концентрации приблизительно 1% по весу. Затем можно добавлять TnBP до конечной концентрации, составляющей 0,3%, рассчитанной на основании нового объема образца, содержащего ASA.
[240] Этап инактивации вирусов выполняют в условиях, инактивирующих вирусы с оболочкой, что приводит к практически безопасному в отношении вирусов раствору, содержащему rhASA. В целом, такие условия предусматривают температуру, составляющую 4-37°C, такую как 19-28°C, 23-27°C, как правило приблизительно 25°C, и время инкубации, которое было определено как эффективное в ходе валидационных исследований. Как правило, время инкубации, составляющее 1-24 часа, является достаточным, предпочтительно 10-18 часов, как, например, приблизительно 14 часов, для обеспечения достаточной инактивации вирусов. Однако, подходящие условия (температура и значения времени инкубации) зависят от применяемого инактивирующего вирус средства, pH, и концентрации белка, и содержания липидов в растворе.
[241] Предполагается, что также можно применять другие способы удаления или инактивации вирусов с получением безопасного в отношении вирусов продукта, как, например, добавление метиленового синего с последующей инактивацией путем облучения ультрафиолетовым светом.
[242] Способы очистки, описанные в данном документе, могут включать один или более этапов фильтрации для удаления вирусов. Как правило, фильтрацию для избавления от вирусов проводят после очистки фермента с помощью одного или более этапов хроматографии. В некоторых вариантах осуществления этап фильтрации для избавления от вирусов проводят путем пропускания содержащего ASA раствора, который является результатом этапа очистки посредством стерильного фильтра, и затем пропускание стерильного профильтрованного раствора через нанофильтр. Под «стерильным фильтром» подразумевают фильтр, с помощью которого будут по сути удалять все микроорганизмы, способные к размножению и/или обуславливающие инфекцию. При этом обычным является то, что фильтр имеет размер пор, составляющий приблизительно 0,1 микрон, при этом размер пор может находиться в диапазоне от приблизительно 0,05 до 0,3 микрон. Может быть целесообразным заменять или объединять фильтрацию для избавления от вирусов образца, которую выполняли в способе очистки, с приведением образца в контакт с детергентом.
[243] Некоторые варианты осуществления настоящего изобретения включают по меньшей мере два этапа инактивации вирусов и/или фильтрации для избавления от вирусов. Например, инактивация вирусов перед колоночной хроматографией может быть объединена с удалением вирусов после завершения всех этапов хроматографии. Удаление вирусов после хроматографии может быть выполнено перед или после одного или более этапов ультрафильтрации/диафильтрации (UFDF) (например, ультрафильтрация с тангенциальным потоком). В конкретном примере элюат получают из конечного этапа хроматографической очистки (например, катионообменная (SP) хроматография) и pH объединенного материала, представляющего собой элюат, регулируют до приблизительно 5,5, приблизительно 6,0, приблизительно 6,5 или приблизительно 7,0 с последующим фильтрацией для избавления от вирусов. Таким образом, в некоторых вариантах осуществления однократному этапу UFDF предшествует фильтрация для избавления от вирусов (например, с применением фильтра Planova™). В других примерах элюат получают из конечной стадии хроматографической очистки (например, катионообменная (SP) хроматография), подвергают первому этапу UFDF без регулирования pH с последующей фильтрацией для избавления от вирусов и вторым этапом UFDF.
[244] В некоторых вариантах осуществления отрегулированный по pH объединенный материал, представляющий собой элюат, полученный в результате проведения катионообменной хроматографии, фильтруют для избавления от вирусов на фильтре Planova 20N. В некоторых вариантах осуществления выход относительно введения после фильтрации для избавления от вирусов отрегулированного по pH элюата, полученного в результате проведения катионообменной хроматографии, составляет приблизительно 90-100%; т. е. приблизительно 90%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более, как определено с помощью поглощения A280. Таким образом, в некоторых вариантах осуществления во время фильтрации для избавления от вирусов практически не теряется рекомбинантный ASA. Выход при фильтрации для избавления от вирусов является значительным, поскольку он подтверждает, что регулирование pH до приблизительно 6,0 позволяет октамерам ASA (которые составляют приблизительно 20 нм в диаметре) диссоциировать до димерной формы. Таким образом, размер пор фильтра для избавления от вирусов может быть выбран для обеспечения того, что только димерная форма отфильтруется (т. е. что октамерная форма может быть удержана фильтром или обуславливать закупоривание фильтра для избавления от вирусов). Для примеров, фильтр для избавления от вирусов с размером пор, составляющим 20 нм, будет удерживать октамерную форму ASA, но не димерную форму.
Аффинная хроматография
[245] Способы очистки, описанные в данном документе, могут включать один или более этапов аффинной хроматографии (например, иммуноаффинная хроматография, аффинная хроматография с иммобилизированным ионом металла и/или аффинная хроматография с иммобилизированным лигандом).
[246] Вкратце, аффинная хроматография представляет собой хроматографическую методику, которая основана на высокоспецифичном взаимодействии, таком как, например, между рецептором и лигандом, антигеном и антителом или ферментом и субстратом. Как будет известно специалисту в данной области, селективные молекулы, применяемые на этапе аффинной хроматографии в способах очистки, описанных в данном документе, могут основываться на различных свойствах (например, трехмерная структура, гликозилирование и т. д.) рекомбинантно полученного ASA, который может быть использован селективной молекулой. Иллюстративные селективные молекулы (или захватывающие реагенты), которые можно применять на этапе аффинной хроматографии включают в себя белок A, белок G, антитело, ион металла (например, никель), конкретный субстрат, лиганд или антиген. В некоторых вариантах осуществления в качестве подходящей селективной молекулы для этапа аффинной хроматографии по настоящему изобретению применяют антитело к арилсульфатазе A (например, антитело к арилсульфатазе A человека). Подходящие антитела к арилсульфатазе A можно получать коммерчески или посредством иммунизации отличных от человека животных (например, мышь, крыса, кролик, цыпленок, коза, овца, лошадь или другое подходящее животное для получения антител к белку человека).
[247] В целом, представляющую интерес молекулу (например, рекомбинантный ASA) улавливают на твердой или неподвижной фазе или среде посредством взаимодействия с селективной молекулой, тогда как другие, нежелательные молекулы, не улавливаются, поскольку они не связываются с селективной(-ыми) молекулой(-ами). Твердую среду затем можно удалять из смеси, необязательно промывать и представляющую интерес молекулу высвобождать из «ловушки» путем элюирования. В некоторых вариантах осуществления аффинные колонки можно элюировать путем изменения ионной силы посредством градиента. Например, значения концентрации солей, pH, pI и ионную силу можно применять для разделения или для получения градиента для разделения.
[248] В некоторых вариантах осуществления рекомбинантный белок ASA можно получать с меткой с целью облегчения очистки с помощью аффинной хроматографии. Как будет известно специалисту в данной области метки для белков могут включать, среди прочего, например, глутатион-S-трансферазу (GST), гексагистидин (His), связывающий мальтозу белок (MBP). В некоторых вариантах осуществления для разделения компонентов в образце при аффинной хроматографии применяют лектины. Например, некоторые лектины специфично связывают конкретную углеводную молекулу, и их можно применять для отделения гликопротеинов от негликозилированных белков или одной гликоформы от другой гликоформы.
Ионообменная хроматография
[249] Способы очистки, описанные в данном документе, могут включать один или более этапов ионообменной хроматографии (например, анионообменной хроматографии и/или катионообменной хроматографии).
[250] Как будет известно специалистам в данной области ионообменники (например, анионообменники и/или катионообменники) могут быть основаны на различных материалах по отношению к матрице, а также к присоединенным заряженным группам. Например, можно применять следующие матрицы, в которых упомянутые материалы могут быть в большей или меньшей степени сшиты: на основе агарозы (как, например, SEPHAROSE™ CL-6B, SEPHAROSE™ Fast Flow и SEPHAROSE™ High Performance), на основе целлюлозы (как, например, DEAE SEPHACEL®), на основе декстрана (как, например, SEPHADEX®), на основе диоксида кремния и на основе синтетических полимеров.
[251] Ионообменную смолу можно получать в соответствии с известными способами. Как правило, уравновешивающий буфер, с помощью которого обеспечивают возможность связывания смолы со своими противоионами, можно пропускать через ионообменную смолу до загрузки образца или композиции, содержащих полипептид и один или более загрязнителей, на смолу. В целях удобства, уравновешивающий буфер может быть таким же, как и загрузочный буфер, но это не является обязательным.
[252] В необязательном варианте осуществления настоящего изобретения ионообменную смолу можно восстанавливать с помощью восстанавливающего буфера после элюирования полипептида, так что колонку можно повторно применять. В целом, концентрация солей и/или pH восстанавливающего буфера могут быть такими, что практически все загрязнители и представляющий интерес полипептид элюируются из ионообменной смолы. Как правило, восстанавливающий буфер имеет очень высокую концентрацию солей для элюирования загрязнителей и полипептида из ионообменной смолы.
Анионообменная хроматография
[253] Варианты осуществления настоящего изобретения включают, например, предоставление образца арилсульфатазы A (например, рекомбинантная арилсульфатаза A) и подвергание образца анионообменной хроматографии, например анионообменной хроматографии, описанной в данном документе. Для анионоообменной смолы заряженные группы, которые ковалентно присоединены к матрице, могут представлять собой, например, диэтиламиноэтил (DEAE), четвертичный аминоэтил (QAE) и/или четвертичный аммоний (Q). В некоторых вариантах осуществления применяемая анионообменная смола представляет собой колонку Q Sepharose. Анионообменную хроматографию можно выполнять с применением, например, Q SEPHAROSE™ Fast Flow, Q SEPHAROSE™ High Performance, Q SEPHAROSE™ XL, CAPTO™ Q, DEAE, TOYOPEARL GIGACAP® Q, FRACTOGEL® TMAE (триметиламиноэтил, смола с четвертичным аммиаком), ESHMUNO™ Q, NUVIA™ Q или UNOSPHERE™ Q. В пределах объема настоящего изобретения можно применять другие анионообменники, включающий без ограничения, без ограничения, смолы с четвертичным амином или «Q-смолы» (например, CAPTOTM-Q, Q-SEPHAROSE®, QAE SEPHADEX®); смолы с диэтиламиноэтаном (DEAE) (например, DEAE-TRISACRYL®, DEAE SEPHAROSE®, бензоилированный нафтоилированный DEAE, диэтиламиноэтил SEPHACEL®); смолы AMBERJET®; смолы AMBERLYST®; смолы AMBERLITE® (например, AMBERLITE® IRA-67, сильноосновная AMBERLITE®, слабоосновная AMBERLITE®), смола с холестирамином, смолы ProPac® (например, PROPAC® SAX-10, PROPAC® WAX-10, PROPAC® WCX-10); смолы TSK-GEL® (например, TSKgel DEAE-NPR; TSKgel DEAE-5PW) и смолы ACCLAIM®.
[254] В вариантах осуществления анионообменную хроматографию проводят с применением FRACTOGEL® TMAE (триметиламиноэтил, смола с четвертичным аммиаком).
[255] В некоторых вариантах осуществления подвергание образца арилсульфатазы A анионообменной хроматографии проводят при температуре, составляющей приблизительно 23°C или меньше, приблизительно 18°C или меньше или приблизительно 16°C или меньше, например приблизительно 23°C, приблизительно 20°C, приблизительно 18°C или приблизительно 16°C.
[256] Типичные подвижные фазы для анионообменной хроматографии включают в себя относительно полярные растворы, такие как вода, ацетонитрил, органические спирты, такие как метанол, этанол и изопропанол, или растворы, содержащие 2-(N-морфолинo)-этансульфоновую кислоту (MES). Таким образом, в некоторых вариантах осуществления подвижная фаза включает приблизительно 0%, 1%, 2%, 4%, 6%, 8%, 10%, 12%, 14%, 16%, 18%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или приблизительно 100% полярного раствора. В некоторых вариантах осуществления подвижная фаза содержит от приблизительно 1% до приблизительно 100%, от приблизительно 5% до приблизительно 95%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 70% или от приблизительно 40% до приблизительно 60% полярного раствора в любое заданное время в ходе процесса разделения.
[257] В некоторых вариантах осуществления rhASA загружают при связывающей способности, составляющей приблизительно 23 произвольные ед./л смолы или меньше, например приблизительно 19 произвольных ед./л смолы или меньше, приблизительно 15 произвольных ед./л смолы или меньше или приблизительно 12 произвольных ед./л смолы или меньше, например от приблизительно 12 произвольных ед./л смолы до приблизительно 15 произвольных ед./л смолы или от приблизительно 15 произвольных ед./л смолы до приблизительно 19 произвольных ед./л смолы. В некоторых вариантах осуществления образец арилсульфатазы A загружают на колонку для анионообменной хроматографии при связывающей способности, составляющей по меньшей мере приблизительно 4,5 г/л смолы (например, по меньшей мере приблизительно 5 г/л смолы, 6 г/л смолы, 7 г/л смолы, 8 г/л смолы, 9 г/л смолы, 10 г/л смолы, 11 г/л смолы, 12 г/л смолы, 13 г/л смолы, 14 г/л смолы или 15 г/л смолы). В некоторых вариантах осуществления образец арилсульфатазы A загружают на колонку для анионообменной хроматографии при связывающей способности, находящейся в диапазоне приблизительно 4,5-20 г/л смолы (например, находящейся в диапазоне приблизительно 5-20 г/л смолы; 5-19 г/л смолы, 5-18 г/л смолы, 5-17 г/л смолы, 5-16 г/л смолы, 5-15 г/л смолы, 7,5-20 г/л смолы, 7,5-19 г/л смолы, 7,5-18 г/л смолы, 7,5-17 г/л смолы, 7,5-16 г/л смолы, 7,5-15 г/л смолы, 10-20 г/л смолы, 10-19 г/л смолы, 10-18 г/л смолы, 10-17 г/л смолы, 10-16 г/л смолы или 10-15 г/л смолы).
[258] Водный раствор, содержащий ASA и загрязнитель(-и) можно загружать на анионную смолу в качестве подвижной фазы с применением загрузочного буфера, который характеризуется концентрацией солей и/или pH такими, что полипептид и загрязнитель связываются с анионообменной смолой. Смолу затем можно промывать с помощью одного или более объемов колонки загрузочного буфера с последующими одним или более объемами колонки буфера для промывания, в котором концентрация солей увеличивается. Наконец, ASA можно элюировать с помощью элюирующего буфера с увеличивающейся концентрацией солей. Необязательно, элюирование фермента также можно опосредовать постепенным или поэтапным уменьшением pH. Фракции, предусматривающие активность ASA могут быть собраны и объединены для дополнительной очистки.
[259] В некоторых вариантах осуществления загрузка образца арилсульфатазы A на колонку для анионообменной хроматографии проводят с помощью загрузочного буфера. В одном варианте осуществления загрузочный буфер не содержит хлорид натрия. В другом варианте осуществления загрузочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия загрузочного буфера составляет от приблизительно 1 мМ до приблизительно 25 мМ, например от приблизительно 1 мМ до приблизительно 10 мМ, от приблизительно 1 мМ до приблизительно 5 мМ или от приблизительно 5 мМ до приблизительно 10 мМ. В некоторых вариантах осуществления концентрация солей в подвижной фазе представляет собой градиент (например, линейный или нелинейный градиент). В некоторых вариантах осуществления концентрация солей в подвижной фазе является постоянной. В некоторых вариантах осуществления концентрация солей в подвижной фазе может поэтапно увеличиваться или уменьшаться. В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для анионообменной хроматографии проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7.
[260] В некоторых вариантах осуществления промывание колонки для анионообменной хроматографии проводят с помощью одного или более промывочных буферов. Например, промывание анионообменной колонки может предусматривать два или более (например, первый и второй) этапов промывания, при этом при каждом применяют отличный промывочный буфер. В одном варианте осуществления промывочный буфер не содержит хлорид натрия. В другом варианте осуществления промывочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия промывочного буфера составляет от приблизительно 50 мМ до приблизительно 200 мМ, например от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 100 мМ до приблизительно 200 мМ или от приблизительно 100 мМ до приблизительно 150 мМ, например приблизительно 80 мМ, приблизительно 100 мМ, приблизительно 120 мМ или приблизительно 140 мМ. В некоторых вариантах осуществления промывание колонки для анионообменной хроматографии проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7.
[261] В одном варианте осуществления элюирующий буфер содержит фосфат натрия. Например, концентрация фосфата натрия элюирующего буфера составляет от приблизительно 20 мМ до приблизительно 50 мМ, например от приблизительно 25 мМ до приблизительно 45 мМ, например приблизительно 30 мМ, приблизительно 35 мМ или приблизительно 40 мМ. В другом варианте осуществления элюирующий буфер не содержит хлорид натрия. В еще одном варианте осуществления элюирующий буфер содержит хлорид натрия. Например, концентрация хлорида натрия элюирующего буфера составляет от приблизительно 200 мМ до приблизительно 300 мМ, например от приблизительно 240 мМ до приблизительно 280 мМ. В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для анионообменной хроматографии проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7.
[262] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для анионообменной хроматографии предусматривает один или более этапов сбора пиков элюирования. Например, сбор пиков элюирования начинается от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, например от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 200 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 200 мили-AU на убывающей стороне или от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, например, как определено с помощью спектрофотометрии, например при 280 нм.
[263] Для специалиста в данной области очевидно, что можно применять многочисленные разные буферы на этапах загрузки, промывания и элюирования. Как правило, однако, колонку можно уравновешивать с помощью 1-10 промываний колонки буфером, содержащим 0,05 М MES-трис, pH 7,0. Для удобства образец можно загружать в буфере из предыдущего этапа способа очистки или образец можно загружать с применением загрузочного буфера. Колонку можно промывать с помощью 1-10 объемов колонки буфера, применяемого для уравновешивания, после чего следует промывочный буфер, содержащий 0,02 MES-трис, 0,12 М NaCl, pH 7,0. В качестве альтернативы, колонку можно уравновешивать, загружать и промывать с помощью любого другого уравновешивающего, загрузочного и промывочного буферов, описанных в данном документе, для анионообменной хроматографии. Образец можно элюировать в буфере, содержащем 0,02 MES-трис, 0,26 М NaCl, pH 7,0. В качестве альтернативы, образец можно элюировать в любом другом элюирующем буфере, описанном в данном документе, для анионообменной хроматографии.
[264] Загрузочный буфер, промывочный буфер и элюирующий буфер, описанные в данном документе, могут включать одно или более буферных средств. Например, буферное средство может представлять собой трис, HEPES, MOPS, PIPES, SSC, MES, фосфат натрия, ацетат натрия или их комбинацию. Концентрация буферного средства составляет от приблизительно 1 мМ до приблизительно 500 мМ, например от приблизительно 10 мМ до приблизительно 250 мМ, от приблизительно 20 мМ до приблизительно 100 мМ, от приблизительно 1 мМ до 5 мМ, от приблизительно 5 мМ до 10 мМ, от приблизительно 10 мМ до 50 мМ или от приблизительно 50 мМ до приблизительно 100 мМ, например приблизительно 1 мМ, приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 20 мМ, приблизительно 30 мМ, приблизительно 40 мМ или приблизительно 50 мМ.
[265] Выход, активность и чистота после анионообменной хроматографии могут варьироваться. В некоторых вариантах осуществления выход, предусматривающий активность арилсульфатазы A, составляет по меньшей мере приблизительно 75%, например по меньшей мере приблизительно 85%, например от приблизительно 85% до приблизительно 99% или от приблизительно 90% до приблизительно 99%. В некоторых вариантах осуществления выход белка (AU или оптические единицы) составляет от приблизительно 10% до 50%, например от приблизительно 20% до приблизительно 35% или от приблизительно 25% до приблизительно 30%, например, как определено с помощью спектрофотометрии, например при 280 нм. В некоторых вариантах осуществления (например, таковые с применением колонки TMAE, которая описана ниже) выход, предусматривающий активность белка в объединенном материале при элюировании (AU или оптические единицы), составляет от приблизительно 70% до 400%, например от приблизительно 80% до приблизительно 390%, или от приблизительно 90% до приблизительно 350%, или от приблизительно 100% до 150%, более по меньшей мере 95%, например, как определено с помощью спектрофотометрии, например при 280 нм. В некоторых вариантах осуществления (например, таковые с применением колонки TMAE, которая описана ниже) значение логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) составляет от приблизительно 0,5 до приблизительно 1,1, например от приблизительно 0,6 до 0,9 или от приблизительно 0,7 до 0,8. В некоторых вариантах осуществления (например, таковые с применением колонки TMAE, которая описана ниже) чистота составляет по меньшей мере 75%, например по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или больше, как определено с помощью, например, капиллярного электрофореза-SDS PAGE. В предпочтительных вариантах осуществления выход, предусматривающий активность, LRV HCP и чистота (как определено с помощью капиллярного электрофореза-SDS PAGE) после анионообменной хроматографии составляет по меньшей мере приблизительно 90%, по меньшей мере приблизительно 0,6 и по меньшей мере приблизительно 80% соответственно.
[266] В предпочтительных вариантах осуществления настоящего изобретения применяют анионообменную колонку с высокой загрузочной способностью. В некоторых вариантах осуществления настоящего изобретения колонка характеризуется диапазоном нагрузки приблизительно 3-20 г/л (т. е. приблизительно 5-15 г/л, приблизительно 10-15 г/л, приблизительно 10-20 г/л). В некоторых вариантах осуществления загрузочная способность составляет значительно больше 4,3 г/л (например, составляет или превышает приблизительно 10 г/л, 12,5 г/л, 15 г/л, 17,5 г/л или 20 г/л). В некоторых вариантах осуществления связывающая способность смолы составляет приблизительно 75-100 произвольных ед./л (например, приблизительно 75 произвольных ед./л, приблизительно 80 произвольных ед./л, приблизительно 85 произвольных ед./л, приблизительно 90 произвольных ед./л, приблизительно 95 произвольных ед./л). В некоторых вариантах осуществления загрузочная способность составляет более приблизительно 80 произвольных ед./л. В некоторых вариантах осуществления колонка с высокой загрузочной способностью представляет собой колонку TMAE. В конкретных вариантах осуществления колонку выбирают из группы, состоящей из колонки Fractogel® TMAE, колонки Nuvia Q, колонки Q Sepharose Fast Flow, колонки Capto Q, колонки Q Sepharose XL, колонки Eshmuno Q, колонки UNOsphere Q или колонки GigaCap Q.
[267] В конкретных вариантах осуществления настоящего изобретения колонка TMAE предварительно уравновешена буфером, содержащим приблизительно 20 мМ MES-трис и 1000 мМ NaCl при pH, составляющем 7,0. В некоторых вариантах осуществления колонка уравновешена буфером, содержащим 50 мМ MES-трис при pH, составляющем 7,0. В некоторых вариантах осуществления скорость потока загрузки колонки TMAE составляет приблизительно 75-125 см/ч. (т. е. приблизительно 75-115 см/ч., приблизительно 75-110 см/ч., приблизительно 75-105 см/ч., приблизительно 75-100 см/ч., приблизительно 85-115 см/ч., приблизительно 85-110 см/ч., приблизительно 85-105 см/ч., приблизительно 85-100 см/ч., приблизительно 95-115 см/ч., приблизительно 95-110 см/ч., приблизительно 95-105 см/ч., приблизительно 95-100 см/ч., приблизительно 100-120 см/ч., приблизительно 100-115 см/ч., приблизительно 100-110 см/ч., приблизительно 100 см/ч.). Условия загрузки можно оптимизировать и оценивать по поглощению A280, как описано в данном документе.
[268] В конкретных вариантах осуществления при использовании колонки TMAE (например, колонка Fractogel TMAE) очень малое количество продукт теряется в потоке в течение загрузки, даже при значениях загрузочной способности более 15 г/л. Способность увеличивать загрузочную способность, в то же время минимизируя проточные потери, является значительным улучшением в методике очистки. В конкретных вариантах осуществления настоящего изобретения количество проточной потери продукта составляет менее 30% загрузки (например, менее приблизительно 25%, менее приблизительно 20%, менее приблизительно 15%, менее приблизительно 10% или менее приблизительно 5%).
[269] После загрузки в некоторых вариантах осуществления колонку TMAE промывают по меньшей мере единожды. В конкретных вариантах осуществления колонку промывают дважды. Первый или второй буфер для промывания может содержать оптимизированный уровень хлорида натрия. В некоторых вариантах осуществления количество хлорида натрия в первом или втором буфере для промывания составляет приблизительно 50-150 мМ (например, приблизительно 50-140 мМ, приблизительно 50-130 мМ, приблизительно 50-120 мМ, приблизительно 50-110 мМ, приблизительно 50-100 мМ, приблизительно 50-90 мМ, приблизительно 50-80 мМ, приблизительно 80-150 мМ, приблизительно 80-140 мМ, приблизительно 80-130 мМ, приблизительно 80-120 мМ, приблизительно 80-110 мМ, приблизительно 80-100 мМ, приблизительно 80-90 мМ, приблизительно 80 мМ или приблизительно 120 мМ). В некоторых вариантах осуществления первый буфер для промывания содержит 50 мМ MES-трис при pH 7,0. В некоторых вариантах осуществления второй буфер для промывания содержит 20 мМ MES-трис, 100 мМ NaCl при pH 7,0. Дополнительная оптимизация условий промывания, в частности условий второго промывания, охвачена вариантами осуществления настоящего изобретения. Например, увеличение концентрации солей при втором промывании может улучшить значения логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) и общую чистота, но снизить как активность, так и выход при A280. Как описано в данном документе, конкретные условия промывания должны быть сбалансированы с условиями элюирования, описанными ниже, с целью обеспечения оптимальной комбинации чистоты, активности и выхода.
[270] В вариантах осуществления настоящего изобретения, рекомбинантный ASA, связанный с колонкой TMAE, элюировали с помощью элюирующего буфера. В некотором варианте осуществления количество хлорида натрия в элюирующем буфере оптимизировано. В конкретных вариантах осуществления количество хлорида натрия в элюирующем буфере составляет приблизительно 150-300 мМ (например, приблизительно 150-290 мМ, приблизительно 150-280 мМ, приблизительно 150-270 мМ, приблизительно 150-260 мМ, приблизительно 150-250 мМ, приблизительно 150-240 мМ, приблизительно 150-230 мМ, приблизительно 150-220 мМ, приблизительно 150-210 мМ, приблизительно 170-290 мМ, приблизительно 170-280 мМ, приблизительно 170-270 мМ, приблизительно 170-260 мМ, приблизительно 170-250 мМ, приблизительно 170-240 мМ, приблизительно 170-230 мМ, приблизительно 170-220 мМ, приблизительно 170-210 мМ приблизительно 180-290 мМ, приблизительно 180-280 мМ, приблизительно 180-270 мМ, приблизительно 180-260 мМ, приблизительно 180-250 мМ, приблизительно 180-240 мМ, приблизительно 180-230 мМ, приблизительно 180-220 мМ, приблизительно 180-210 мМ, приблизительно 180, приблизительно 220 или приблизительно 260). В конкретном примере элюирующий буфер содержит 50 мМ MES-трис и 1 М NaCl при pH, составляющем 7,0. В некоторых вариантах осуществления выход при A280 после элюирования составляет более 60% загрузки (например, приблизительно 60%, приблизительно 70%, приблизительно 80% или больше). Дополнительная оптимизация условий элюирования охватывается вариантами осуществления настоящего изобретения. Например, увеличение концентрации солей при элюировании (т. е. проводимости) обеспечивает лучший выход, но приводит к худшим чистоте и удалению HCP. И как указано выше, конкретные условия промывания должны быть сбалансированы с условиями элюирования с целью обеспечения оптимальной комбинации чистоты, активности и выхода.
Катионообменная хроматография
[271] В некоторых вариантах осуществления способ дополнительно включает подвергание образца арилсульфатазы A катионообменной хроматографии, например катионообменной хроматографии с сульфопропилом (SP), например, которая описана в данном документе. В некоторых вариантах осуществления образец арилсульфатазы A подвергают анионообменной хроматографии перед катионообменной хроматографией. В типичном варианте осуществления катионообменная хроматография предусматривает катионообменную хроматографию с сульфопропилом (SP), но можно использовать другие катионные хроматографические мембраны или смолы, например мембрану MUSTANG™ S, смолу S-SEPHAROSE™ или смолу Blue SEPHAROSE™. В некоторых вариантах осуществления способ дополнительно включает концентрирование и/или фильтрование образца арилсульфатазы A, например с помощью ультрафильтрации и/или диафильтрации, например с помощью ультрафильтрации с тангенциальным потоком. Катионообменную хроматографию можно выполнять при оптимизированной температуре, например, которая описана в данном документе, для усиления связывания с мишенью и/или уменьшения степени связывания примесей. Например, катионообменную хроматографию можно выполнять при температуре, составляющей приблизительно 23°C, 18°C, 16°C или меньше.
[272] В одном варианте осуществления катионообменная хроматография предусматривает катионообменную хроматографию с сульфопропилом (SP). В другом варианте осуществления катионообменная хроматография представляет собой этап шлифования. Катионообменную хроматографию (например, катионообменная хроматографию с сульфопропилом (SP)) можно выполнять с применением, например, одного или более из: TOYOPEARL® SP-650, TOYOPEARL® SP-550, TSKGEL® SP-3PW, TSKGEL® SP-5PW, SP SEPHAROSE™ Fast Flow, SP SEPHAROSE™ High Performance, SP SEPHAROSE™ XL, мембраны SARTOBIND® S, POROS® HS50, UNOSPHERE™ S и MACROCAP™ S.
[273] Водный раствор, содержащий арилсульфатазу A и загрязнитель(-и) можно загружать на катионную смолу с применением загрузочного буфера, который характеризуется концентрацией солей и/или pH такими, что полипептид и загрязнитель связываются с катионообменной смолой. Смолу затем можно промывать с помощью одного или более объемов колонки уравновешивающего масла или загрузочного буфера и необязательно с последующими одним или более объемами колонки буфера для промывания, в котором концентрация солей увеличивается. Наконец, арилсульфатазу A можно элюировать в элюирующем буфере. Фракции, предусматривающие активность арилсульфатазы A, можно собирать и объединять для дополнительной очистки.
[274] В типичном варианте осуществления концентрацию NaCl и/или pH загрузочного буфера, промывочного буфера и/или элюирующего буфера, можно оптимизировать, например, как описано в данном документе, для усиления связывания с мишенью и/или уменьшения степени связывания примесей. В некоторых вариантах осуществления концентрация NaCl в загрузочном буфере составляет приблизительно 20 мМ, 15 мМ, 10 мМ или меньше. В некоторых вариантах осуществления загрузочный буфер характеризуется pH, составляющим приблизительно 4,5, 4,3, 4,0 или меньше. В некоторых вариантах осуществления концентрация NaCl в промывочном буфере составляет приблизительно 20 мМ, 15 мМ, 10 мМ или меньше. В некоторых вариантах осуществления концентрация NaCl в элюирующем буфере составляет приблизительно 55 мМ, 50 мМ, 45 мМ, 40 мМ или меньше.
[275] В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии предусматривает: загрузку образца арилсульфатазы A на колонку для катионной хроматографии (например, катионообменная колонка с сульфопропилом (SP)), промывание колонки для катионообменной хроматографии и элюирование арилсульфатазы A из колонки. В некоторых вариантах осуществления колонки можно уравновешивать с помощью более 3, например от 5 до 10, объемов колонки с 0,01 М NaAc, 0,01 М NaCl, 0,03 М уксусной кислоты, pH 4,2.
[276] В некоторых вариантах осуществления образец можно загружать в буфере из предыдущего этапа способа очистки или образец можно загружать с использованием загрузочного буфера. В одном варианте осуществления загрузочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия загрузочного буфера составляет от приблизительно 1 мМ до приблизительно 25 мМ, например от приблизительно 5 мМ до приблизительно 20 мМ, например приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 15 мМ или приблизительно 20 мМ. В другом варианте осуществления загрузочный буфер содержит ацетат натрия. Например, концентрация ацетата натрия загрузочного буфера составляет от приблизительно 10 мМ до приблизительно 100 мМ, например приблизительно 20 мМ, приблизительно 40 мМ или приблизительно 60 мМ. В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем от приблизительно 3,0 до приблизительно 6,0, например от приблизительно 4,0 до приблизительно 5,0, например приблизительно 4,0, приблизительно 4,3 или приблизительно 4,5. В некоторых вариантах осуществления образец арилсульфатазы A загружают на колонку для катионообменной хроматографии при связывающей способности, составляющей приблизительно 15 произвольных ед./л смолы или меньше, например приблизительно 14 произвольных ед./л смолы или меньше или приблизительно 12 произвольных ед./л смолы или меньше, например от приблизительно 10 произвольных ед./л смолы до приблизительно 14 произвольных ед./л смолы или от приблизительно 10 произвольных ед./л смолы до приблизительно 12 произвольных ед./л смолы.
[277] В некоторых вариантах осуществления промывание колонки для катионообменной хроматографии проводят с помощью одного или более промывочных буферов. Например, промывание катионообменной колонки может предусматривать два или более (например, первый и второй) этапов промывания, при этом при каждом применяют отличный промывочный буфер. Колонку можно промывать с помощью 1-10 объемов колонки буфера, применяемого для уравновешивания. В качестве альтернативы, колонку можно уравновешивать, загружать и промывать с помощью любого другого уравновешивающего, загрузочного и промывочного буферов, описанных в данном документе, для катионообменной хроматографии. В одном варианте осуществления промывочный буфер содержит хлорид натрия. Например концентрация хлорида натрия промывочного буфера составляет от приблизительно 1 мМ до приблизительно 25 мМ, например от приблизительно 5 мМ до приблизительно 20 мМ или от приблизительно 10 мМ до приблизительно 15 мМ, например приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 15 мМ или приблизительно 20 мМ. В другом варианте осуществления промывочный буфер содержит ацетат натрия. Например, концентрация ацетата натрия загрузочного буфера составляет от приблизительно 10 мМ до приблизительно 100 мМ, например приблизительно 20 мМ, приблизительно 40 мМ или приблизительно 60 мМ. В некоторых вариантах осуществления промывание колонки для катионообменной хроматографии проводят при pH, составляющем от приблизительно 3,0 до приблизительно 6,0, например от приблизительно 4,0 до приблизительно 5,0, например приблизительно 4,0, приблизительно 4,3 или приблизительно 4,5.
[278] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для катионообменной хроматографии проводят с помощью элюирующего буфера. В одном варианте осуществления элюирующий буфер содержит хлорид натрия. Например, концентрация хлорида натрия элюирующего буфера составляет от приблизительно 25 мМ до приблизительно 75 мМ, например от приблизительно 45 мМ до приблизительно 60 мМ, например приблизительно 45 мМ, приблизительно 50 мМ, приблизительно 55 мМ или приблизительно 55 мМ. В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для катионообменной хроматографии проводят при pH, составляющем от приблизительно 3,0 до приблизительно 6,0, например от приблизительно 4,0 до приблизительно 5,0, например приблизительно 4,0, приблизительно 4,3 или приблизительно 4,5. Таким образом, в качестве одного конкретного примера, образец можно элюировать в буфере, содержащем 0,02 М NaAc, 0,05 М NaCl, pH 4,5. В качестве альтернативы, образец можно элюировать в любом другом элюирующем буфере, описанном в данном документе, для катионообменной хроматографии.
[279] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для катионообменной хроматографии предусматривает один или более этапов сбора пиков элюирования. Например, сбор пиков элюирования начинается от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, например от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 200 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 200 мили-AU на убывающей стороне или от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, например, как определено с помощью спектрофотометрии, например при 280 нм. Собранные пики элюатов можно объединять.
[280] Загрузочный буфер, промывочный буфер и элюирующий буфер, описанные в данном документе, могут включать одно или более буферных средств. Например, буферное средство может представлять собой трис, HEPES, MOPS, PIPES, SSC, MES, фосфат натрия, ацетат натрия или их комбинацию. Концентрация буферного средства составляет от приблизительно 1 мМ до приблизительно 500 мМ, например от приблизительно 10 мМ до приблизительно 250 мМ, от приблизительно 20 мМ до приблизительно 100 мМ, от приблизительно 1 мМ до 5 мМ, от приблизительно 5 мМ до 10 мМ, от приблизительно 10 мМ до 50 мМ или от приблизительно 50 мМ до приблизительно 100 мМ, например приблизительно 1 мМ, приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 20 мМ, приблизительно 30 мМ, приблизительно 40 мМ или приблизительно 50 мМ.
[281] В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при температуре, составляющей приблизительно 23°C или меньше, приблизительно 18°C или меньше или приблизительно 16°C или меньше, например приблизительно 23°C, приблизительно 20°C, приблизительно 18°C или приблизительно 16°C. В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при от приблизительно 23°C до приблизительно 16°C, например при приблизительно 23°C, приблизительно 20°C, приблизительно 18°C или приблизительно 16°C, и загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем от приблизительно 4,5 до приблизительно 4,3, например при приблизительно 4,5, приблизительно 4,4 или приблизительно 4,3. В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при приблизительно 23°C и загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем приблизительно 4,5. В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при приблизительно 23°C и загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем приблизительно 4,3. В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при приблизительно 18°C и загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем приблизительно 4,5. В некоторых вариантах осуществления подвергание образца арилсульфатазы A катионообменной хроматографии проводят при приблизительно 18°C и загрузку образца арилсульфатазы A на колонку для катионообменной хроматографии проводят при pH, составляющем приблизительно 4,3.
[282] Выход после катионообменной хроматографии может варьироваться. В некоторых вариантах осуществления выход, предусматривающий активность арилсульфатазы A, составляет по меньшей мере приблизительно 75%, например по меньшей мере приблизительно 80%, например от приблизительно 80% до приблизительно 105%. В некоторых вариантах осуществления выход белка (AU или оптические единицы) составляет от приблизительно 65% до 100%, например от приблизительно 70% до приблизительно 95%, например, как определено с помощью спектрофотометрии, например при 280 нм.
[283] Степень чистоты и активность после катионообменной хроматографии значительно улучшаются. В некоторых вариантах осуществления значение логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) составляет от приблизительно 1,0 до приблизительно 2,5, например от приблизительно 1,5 до приблизительно 2,0 или от приблизительно 1,7 до приблизительно 1,9. Специфическая активность очищенной арилсульфатазы A может составлять по меньшей мере от приблизительно 50 ед./мг до приблизительно 140 ед./мг, например по меньшей мере приблизительно 70 ед./мг, по меньшей мере приблизительно 90 ед./мг, по меньшей мере приблизительно 100 ед./мг или по меньшей мере приблизительно 120 ед./мг, например, как определено согласно способу, описанному в данном документе. В некоторых вариантах осуществления арилсульфатазу A очищают до по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99%, по меньшей мере приблизительно 99,5%, по меньшей мере приблизительно 99,6%, по меньшей мере приблизительно 99,7%, по меньшей мере приблизительно 99,8% или по меньшей мере приблизительно 99,9%. Степень чистоты арилсульфатазы A можно оценивать, например, с помощью одного или более из: вестерн-блоттинга белка клетки-хозяина (HCP), окрашивания кумасси при SDS-PAGE, окрашивания серебром при SDS-PAGE, обращенно-фазовой HPLC и эксклюзионной HPLC. В некоторых вариантах осуществления уменьшение концентрации солей загрузочного буфера и снижение его pH усиливает связывание ASA с катионообменной колонкой, но не влияет на связывание примесей. Другими словами, оптимальный баланс концентрации солей и pH, которые изложены выше, могут увеличивать выход после катионообменной хроматографии без отрицательного воздействия на чистоту.
[284] В некоторых вариантах осуществления можно регулировать pH объединенного материала, представляющего собой элюат, полученный в результате проведения катионообменной хроматографии. В некоторых вариантах осуществления pH регулируют непосредственно перед фильтрацией для избавления от вирусов. Элюат, полученный в результате проведения катионообменной хроматографии (например, SP-элюат), можно регулировать по pH до приблизительно 5,5, приблизительно 6,0, приблизительно 6,5 или приблизительно 7,0 с применением буфера для регулирования pH, содержащего 0,25 M фосфата натрия, 1,33 M хлорида натрия, 0,34 M цитрата натрия, pH 7,0. В некоторых вариантах осуществления отрегулированный по pH объединенный материал, представляющий собой SP-элюат, фильтруют для избавления от вирусов на фильтре Planova 20N. В некоторых вариантах осуществления выход относительно введения после фильтрации для избавления от вирусов отрегулированного по pH элюата, полученного в результате проведения катионообменной хроматографии, составляет приблизительно 90-100%; т. е. приблизительно 90%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более, как определено с помощью поглощения A280. Выход при фильтрации для избавления от вирусов является значительным, поскольку он подтверждает, что регулирование pH до приблизительно 6,0 позволяет октамерам ASA (которые составляют приблизительно 20 нм в диаметре) диссоциировать до димерной формы. Таким образом, размер пор фильтра для избавления от вирусов может быть выбран для обеспечения того, что только димерная форма отфильтруется (т. е. что октамерная форма может быть удержана фильтром или обуславливать закупоривание фильтра для избавления от вирусов). Для примеров, фильтр для избавления от вирусов с размером пор, составляющим 20 нм, будет удерживать октамерную форму ASA, но не димерную форму.
Хроматография в комбинированном режиме
[285] Способы очистки, описанные в данном документе, могут включать один или более этапов хроматографии в комбинированном режиме. Хроматография в комбинированном режиме представляет собой тип хроматографии, при которой применяют несколько режимов разделения для разделения смеси разных молекул, как правило при жидкостной хроматографии. Например, разделение в комбинированном режиме может предусматривать комбинационные фазы с характеристиками ионообменной и обратной фазы в одно и то же время. Такие неподвижные фазы с более чем одним типом взаимодействия доступны от нескольких производителей колонок.
[286] В одном аспекте настоящее изобретение предусматривает способ очистки арилсульфатазы A из образца, где способ включает, например, обеспечение образца арилсульфатазы A (например, рекомбинантной арилсульфатазы A) и подвергание образца арилсульфатазы A хроматографии в комбинированном режиме, например хроматографии в комбинированном режиме, описанной в данном документе, как, например, способ, включающий хроматографию на колонке с керамическим гидроксиапатитом (HA), например хроматографию на колонке с гидроксиапатитом типа I или типа II. В некоторых вариантах осуществления хроматографию в комбинированном режиме проводят с применением одного или более из: среды с керамическим гидроксиапатитом типа I CHT™, среды с керамическим гидроксиапатитом типа II CHT™, гидроксиапатита BIO-GEL® HT и гидроксиапатита BIO-GEL® HTP.
[287] В некоторых вариантах осуществления подвергание образца арилсульфатазы A хроматографии в комбинированном режиме включает: загрузку образца арилсульфатазы A на колонку для хроматографии в комбинированном режиме (например, хроматография на колонке с HA), промывание колонки для хроматографии в комбинированном режиме и элюирование арилсульфатазы A из колонки. В некоторых вариантах осуществления подвергание образца арилсульфатазы A обменной хроматографии в комбинированном режиме проводят при температуре, составляющей приблизительно 23°C или меньше, приблизительно 18°C или меньше или приблизительно 16°C или меньше, например приблизительно 23°C, приблизительно 20°C, приблизительно 18°C или приблизительно 16°C.
[288] В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для хроматографии в комбинированном режиме проводят с помощью загрузочного буфера. В одном варианте осуществления загрузочный буфер содержит фосфат натрия. Например, концентрация фосфата натрия загрузочного буфера составляет от приблизительно 1 мМ до приблизительно 10 мМ, например от приблизительно 1 мМ до приблизительно 5 мМ, от приблизительно 5 мМ до приблизительно 10 мМ, например приблизительно 1 мМ, приблизительно 2 мМ или приблизительно 5 мМ. В другом варианте осуществления загрузочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия загрузочного буфера составляет от приблизительно 100 мМ до приблизительно 400 мМ, например от приблизительно 200 до приблизительно 300 мМ, например приблизительно 220 мМ, приблизительно 240 мМ, приблизительно 260 мМ или приблизительно 280 мМ.
[289] В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для хроматографии в комбинированном режиме проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7.
[290] В некоторых вариантах осуществления хроматография в комбинированном режиме предусматривает хроматографию на колонке с керамическим гидроксиапатитом (HA). Гидроксиапатит (HAP) обычно относится к кристаллической форме фосфата кальция. Механизм HAP предусматривает неспецифические взаимодействия между отрицательно заряженными карбоксильными группами белка и положительно заряженными ионами кальция на смоле и положительно заряженными амино-группами белка и отрицательно заряженными ионами фосфата на смоле. Основные или кислые белки можно адсорбировать селективным образом на колонке путем регулирования pH буфера; элюирования можно достигать путем изменения концентрации солей буфера. Как и ранее, очевидно, что можно применять множество буферных композиций, а также комбинации буферов. Однако, как правило, колонку можно уравновешивать с помощью 1-10 промываний колонки буфером, содержащим 0,001 М NaPO4, 0,02 М MES-трис, 0,26 М NaCl, pH 7,0. Для удобства образец можно загружать в буфере из предыдущего этапа способа очистки или образец можно загружать с применением загрузочного буфера. Колонку можно промывать с помощью 1-10 объемов колонки буфера, применяемого для уравновешивания, после чего следует промывочный буфер, содержащий 0,005 М NaPO4, 0,02 М MES-трис, 0,26 М NaCl, pH 7,0. В качестве альтернативы, колонку можно уравновешивать, загружать и промывать с помощью любого другого уравновешивающего, загрузочного и промывочного буферов, описанных в данном документе, для хроматографии в комбинированном режиме. Образец можно элюировать в буфере, содержащем 0,04 М NaPO4, pH 7,0. Необязательно, колонку можно зачищать путем промывания с помощью 1-10 объемов колонки с 0,4 М NaPO4, pH 12. В качестве альтернативы, образец можно элюировать в любом другом элюирующем буфере, описанном в данном документе, для хроматографии в комбинированном режиме.
[291] В некоторых вариантах осуществления промывание колонки для хроматографии в комбинированном режиме проводят с помощью одного или более промывочных буферов. Например, промывание колонки для хроматографии в комбинированном режиме может включать два или более (например, первый и второй) этапов промывания, при этом при каждом применяют отличный промывочный буфер.
[292] В одном варианте осуществления промывочный буфер содержит фосфат натрия. Например, концентрация фосфата натрия промывочного буфера составляет от приблизительно 1 мМ до приблизительно 10 мМ, например от приблизительно 1 мМ до приблизительно 5 мМ, от приблизительно 5 мМ до приблизительно 10 мМ, например приблизительно 1 мМ, приблизительно 5 мМ или приблизительно 10 мМ. В другом варианте осуществления промывочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия промывочного буфера составляет от приблизительно 50 мМ до приблизительно 600 мМ, например от приблизительно 100 мМ до приблизительно 500 мМ или от приблизительно 200 до приблизительно 400 мМ, например приблизительно 220 мМ, приблизительно 240 мМ, приблизительно 260 мМ или приблизительно 280 мМ.
[293] В некоторых вариантах осуществления промывание колонки для хроматографии в комбинированном режиме проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7.
[294] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для хроматографии в комбинированном режиме проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7. В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для хроматографии в комбинированном режиме предусматривает один или более этапов сбора пиков элюирования. Например, сбор пиков элюирования начинается от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, например от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 200 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 200 мили-AU на убывающей стороне или от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, например, как определено с помощью спектрофотометрии, например при 280 нм.
[295] Загрузочный буфер, промывочный буфер и элюирующий буфер, описанные в данном документе, могут включать одно или более буферных средств. Например, буферное средство может представлять собой трис, HEPES, MOPS, PIPES, SSC, MES, фосфат натрия, ацетат натрия или их комбинацию. Концентрация буферного средства составляет от приблизительно 1 мМ до приблизительно 500 мМ, например от приблизительно 10 мМ до приблизительно 250 мМ, от приблизительно 20 мМ до приблизительно 100 мМ, от приблизительно 1 мМ до 5 мМ, от приблизительно 5 мМ до 10 мМ, от приблизительно 10 мМ до 50 мМ или от приблизительно 50 мМ до приблизительно 100 мМ, например приблизительно 1 мМ, приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 20 мМ, приблизительно 30 мМ, приблизительно 40 мМ или приблизительно 50 мМ.
[296] В некоторых вариантах осуществления очистка ASA с помощью хроматографии в комбинированном режиме сменяет очистку с помощью ионообменной хроматографии (например, анионообменная хроматография). Однако, предполагается, что такие этапы можно проводить в обратном порядке.
[297] Выход после хроматографии в комбинированном режиме может варьироваться. В некоторых вариантах осуществления выход, предусматривающий активность арилсульфатазы A, составляет по меньшей мере приблизительно 80%, например по меньшей мере приблизительно 90%, например от приблизительно 80% до приблизительно 115%. В некоторых вариантах осуществления выход белка (AU или оптические единицы) составляет от приблизительно 30% до 80%, например от приблизительно 35% до приблизительно 75% или от приблизительно 50% до приблизительно 70%, например, как определено с помощью спектрофотометрии, например при 280 нм.
[298] Степень чистоты после хроматографии в комбинированном режиме значительно улучшается. В некоторых вариантах осуществления специфическая активность очищенной арилсульфатазы A составляет по меньшей мере от приблизительно 50 ед./мг до приблизительно 140 ед./мг, например по меньшей мере приблизительно 70 ед./мг, по меньшей мере приблизительно 90 ед./мг, по меньшей мере приблизительно 100 ед./мг или по меньшей мере приблизительно 120 ед./мг, например, как определено согласно способу, описанному в данном документе. В некотором варианте осуществления арилсульфатазу A очищают до по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99%, по меньшей мере приблизительно 99,5%, по меньшей мере приблизительно 99,6%, по меньшей мере приблизительно 99,7%, по меньшей мере приблизительно 99,8% или по меньшей мере приблизительно 99,9%. Степень чистоты арилсульфатазы A можно оценивать, например, с помощью одного или более из: вестерн-блоттинга белка клетки-хозяина (HCP), окрашивания кумасси при SDS-PAGE, окрашивания серебром при SDS-PAGE, обращенно-фазовой HPLC и эксклюзионной HPLC. В некоторых вариантах осуществления значение логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) составляет от приблизительно 0,3 до приблизительно 0,6, например от приблизительно 0,4 до 0, 5.
Хроматография с гидрофобным взаимодействием (HIC)
[299] Способы очистки, описанные в данном документе, могут включать подвергание образца арилсульфатазы A хроматографии с гидрофобным взаимодействием (HIC). В одном варианте осуществления хроматография с гидрофобным взаимодействием предусматривает хроматографию с использованием фенильного сорбента. В других вариантах осуществления хроматография с гидрофобным взаимодействием предусматривает хроматографию с использованием бутила или хроматографию с использованием октила. В некоторых вариантах осуществления подвергание образца арилсульфатазы A HIC проводят при температуре, составляющей приблизительно 23°C или меньше, приблизительно 18°C или меньше или приблизительно 16°C или меньше, например приблизительно 23°C, приблизительно 20°C, приблизительно 18°C или приблизительно 16°C. В некоторых вариантах осуществления образец арилсульфатазы A подвергают хроматографии в комбинированном режиме перед HIC.
[300] При хроматографии с гидрофобным взаимодействием используют притяжение данной молекулы в отношении полярного или неполярного окружения, и в отношении белка эта склонность обуславливается гидрофобностью или гидрофильностью остатков на подверженной воздействию наружной поверхности белка. Таким образом, белки фракционируют исходя из их различных степеней притяжения к гидрофобной матрице, как правило инертной подложке с алкильными линкерными плечами из 2-18 атомов углерода на длину цепи. Неподвижная фаза состоит из небольших неполярных групп (бутил, октил или фенил), присоединенных к главной цепи гидрофильного полимера (например, сшитой Sepharose™, декстрана или агарозы). Таким образом, колонка для HIC, как правило, представляет собой колонку Butyl SEPHAROSE™ или колонку Phenyl SEPHAROSE™, более типично колонку Phenyl SEPHAROSE™.
[301] В некоторых вариантах осуществления хроматография с гидрофобным взаимодействием предусматривает хроматографию с использованием фенильного сорбента с применением одного или более из Phenyl SEPHAROSE™ High Performance, Phenyl SEPHAROSE™ 6 Fast Flow (низкая плотность субстрата) или Phenyl SEPHAROSE™ 6 Fast Flow (высокая плотность субстрата).
[302] В некоторых вариантах осуществления подвергание образца арилсульфатазы A хроматографии с гидрофобным взаимодействием предусматривает: загрузку образца арилсульфатазы A на колонку для HIC, промывание колонки для HIC и элюирование арилсульфатазы A из колонки. Загрузка, промывание и элюирование при HIC в основном осуществляют согласно тому же принципу, как описано выше для ионообменной хроматографии, но часто применяют практически противоположные условия таковым, применяемым при ионообменной хроматографии. Таким образом, способ HIC предусматривает применение загрузочного буфера с высоким содержанием солей, который раскручивает белок для воздействия на гидрофобные сайты. Белок удерживается гидрофобными лигандами на колонке и подвергается воздействию градиента буферов, предусматривающих уменьшение значений концентрации солей. По мере уменьшения концентрации солей белок возвращается в свою нативную конформацию, и его впоследствии элюируют из колонки. В качестве альтернативы, белки можно элюировать с помощью PEG.
[303] В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для HIC проводят с помощью загрузочного буфера. В одном варианте осуществления загрузочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия загрузочного буфера составляет от приблизительно 0,5 М до приблизительно 2,5 М, например приблизительно 1 М или приблизительно 1,5 М. В другом варианте осуществления загрузочный буфер содержит фосфат натрия. Например, концентрация фосфата натрия загрузочного буфера составляет от приблизительно 10 мМ до приблизительно 100 мМ, например приблизительно 25 мМ, приблизительно 50 мМ или приблизительно 75 мМ. В некоторых вариантах осуществления загрузку образца арилсульфатазы A на колонку для HIC проводят при pH, составляющем от приблизительно 5 до приблизительно 7, например от приблизительно 5,5 до приблизительно 6,5, например приблизительно 5,5, приблизительно 6,0 или приблизительно 6,5. В некоторых вариантах осуществления образец арилсульфатазы A загружают на колонку для HIC при связывающей способности, составляющей приблизительно 12 произвольных ед./л смолы или меньше, например приблизительно 10 произвольных ед./л смолы или меньше, приблизительно 9 произвольных ед./л смолы или меньше, приблизительно 7 произвольных ед./л смолы или меньше или приблизительно 5 произвольных ед./л смолы или меньше, например от приблизительно 5 произвольных ед./л смолы до приблизительно 9 произвольных ед./л смолы или от приблизительно 5 произвольных ед./л смолы до приблизительно 7 произвольных ед./л смолы.
[304] Применение Phenyl SEPHAROSE™ в качестве твердой фазы при HIC типично в настоящем изобретении. Опять же, очевидно, что когда речь идет о точных условиях, а также буферах и комбинациях буферов, используемых для процессов загрузки, промывания и элюирования, существует большое количество различных возможностей. В типичном варианте осуществления колонку можно уравновешивать в буфере, который содержит 0,05 М NaPO4, 1 М NaCl, pH 5,5. Для удобства образец можно загружать в буфере из предыдущего этапа способа очистки или образец можно загружать с применением загрузочного буфера.
[305] В некоторых вариантах осуществления промывание колонки для HIC проводят с помощью одного или более промывочных буферов. Например, промывание колонки для HIC может предусматривать два или более (например, первый и второй) этапов промывания, при этом при каждом применяют отличный промывочный буфер. В некоторых вариантах осуществления промывочный буфер содержит хлорид натрия. Например, концентрация хлорида натрия промывочного буфера составляет от приблизительно 100 мМ до приблизительно 1,5 М, например от приблизительно 250 мМ до приблизительно 1 М, например приблизительно 250 мМ, приблизительно 500 мМ, приблизительно 750 мМ или приблизительно 1 М. В другом варианте осуществления промывочный буфер содержит фосфат натрия. Например, концентрация фосфата натрия загрузочного буфера составляет от приблизительно 10 мМ до приблизительно 100 мМ, например приблизительно 25 мМ, приблизительно 50 мМ или приблизительно 75 мМ. В некоторых вариантах осуществления промывание колонки для HIC проводят при pH, составляющем от приблизительно 5 до приблизительно 7, например от приблизительно 5,5 до приблизительно 6,5, например приблизительно 5,5, приблизительно 6,0 или приблизительно 6,5. Например, промывание можно осуществлять с применением 1-2 промываний колонки уравновешивающим буфером с последующими 1-5 объемами колонки с 0,02 М MES, 0,05 М NaPO4, 0,5 М NaCl, pH 5,5. В качестве альтернативы, колонку можно уравновешивать, загружать и промывать с помощью любого другого уравновешивающего, загрузочного и промывочного буферов, описанных в данном документе, для HIC.
[306] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для HIC проводят с помощью элюирующего буфера. В некоторых вариантах осуществления элюирующий буфер содержит хлорид натрия. Например, концентрация хлорида натрия элюирующего буфера составляет от приблизительно 30 мМ до приблизительно 100 мМ, например от приблизительно 45 мМ до приблизительно 85 мМ, например приблизительно 50 мМ, приблизительно 60 мМ, приблизительно 70 мМ или приблизительно 80 мМ. В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для HIC проводят при pH, составляющем от приблизительно 5 до приблизительно 9, например от приблизительно 6 до приблизительно 8, например приблизительно 7. Например, арилсульфатазу A можно элюировать с применением 0,02 М MES-трис, 0,06 М NaCl, pH 7,0. В качестве альтернативы образец можно элюировать в любом другом элюирующем буфере, описанном в данном документе, для HIC.
[307] В некоторых вариантах осуществления элюирование арилсульфатазы A из колонки для HIC предусматривает один или более этапов сбора пиков элюирования. Например, сбор пиков элюирования начинается от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, например от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 200 мили-AU на возрастающей стороне до приблизительно 50 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, от приблизительно 50 мили-AU на возрастающей стороне до приблизительно 200 мили-AU на убывающей стороне или от приблизительно 100 мили-AU на возрастающей стороне до приблизительно 100 мили-AU на убывающей стороне, например, как определено с помощью спектрофотометрии, например при 280 нм.
[308] В некоторых вариантах осуществления очистка арилсульфатазы A с помощью HIC сменяет очистку с помощью ионообменной хроматографии (например, анионообменная хроматография) и/или хроматографии в комбинированном режиме. Однако, предполагается, что такие этапы можно проводить в обратном порядке.
[309] Загрузочный буфер, промывочный буфер и элюирующий буфер, описанные в данном документе, могут включать одно или более буферных средств. Например, буферное средство может представлять собой трис, HEPES, MOPS, PIPES, SSC, MES, фосфат натрия, ацетат натрия или их комбинацию. Концентрация буферного средства составляет от приблизительно 1 мМ до приблизительно 500 мМ, например от приблизительно 10 мМ до приблизительно 250 мМ, от приблизительно 20 мМ до приблизительно 100 мМ, от приблизительно 1 мМ до 5 мМ, от приблизительно 5 мМ до 10 мМ, от приблизительно 10 мМ до 50 мМ или от приблизительно 50 мМ до приблизительно 100 мМ, например приблизительно 1 мМ, приблизительно 5 мМ, приблизительно 10 мМ, приблизительно 20 мМ, приблизительно 30 мМ, приблизительно 40 мМ или приблизительно 50 мМ.
[310] Выход после HIC может варьироваться. В некоторых вариантах осуществления выход, предусматривающий активность арилсульфатазы A, составляет по меньшей мере приблизительно 60%, например по меньшей мере приблизительно 70%, например от приблизительно 70% до приблизительно 100%. В некоторых вариантах осуществления выход белка (AU или оптические единицы) составляет от приблизительно 45% до 100%, например от приблизительно 50% до приблизительно 95% или от приблизительно 55% до приблизительно 90%, например, как определено с помощью спектрофотометрии, например при 280 нм.
[311] Степень чистоты после HIC значительно улучшается. В некоторых вариантах осуществления специфическая активность очищенной арилсульфатазы A составляет по меньшей мере от приблизительно 50 ед./мг до приблизительно 140 ед./мг, например по меньшей мере приблизительно 70 ед./мг, по меньшей мере приблизительно 90 ед./мг, по меньшей мере приблизительно 100 ед./мг или по меньшей мере приблизительно 120 ед./мг, например, как определено согласно способу, описанному в данном документе.
[312] В некоторых вариантах осуществления арилсульфатазу A очищают до по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99%, по меньшей мере приблизительно 99,5%, по меньшей мере приблизительно 99,6%, по меньшей мере приблизительно 99,7%, по меньшей мере приблизительно 99,8% или по меньшей мере приблизительно 99,9%. Степень чистоты арилсульфатазы A можно оценивать, например, с помощью одного или более из: вестерн-блоттинга белка клетки-хозяина (HCP), окрашивания кумасси при SDS-PAGE, окрашивания серебром при SDS-PAGE, обращенно-фазовой HPLC и эксклюзионной HPLC. В некоторых вариантах осуществления значение логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) составляет от приблизительно 0,6 до приблизительно 1,2, например от приблизительно 0,7 до 0,95,
Ультрафильтрация/диафильтрация
[313] Способы очистки, описанные в данном документе, могут включать один или более этапов нисходящей ультрафильтрации и/или диафильтрации. В некоторых вариантах осуществления способ дополнительно включает концентрирование и/или фильтрование образца арилсульфатазы A, например с помощью ультрафильтрации и/или диафильтрации, например с помощью ультрафильтрации с тангенциальным потоком.
[314] Ультрафильтрация относится к способу разделения с помощью мембраны, проводимому под давлением градиента, при котором с помощью мембраны разделяют на фракции компоненты жидкости в зависимости от их сольватированных размера и структуры. Диафильтрация представляет собой специализированный тип способа ультрафильтрации, при котором ретентат разбавляют водой и подвергают повторной ультрафильтрации для снижения концентрации растворимых компонентов пермиата и дополнительного увеличения концентрации удерживаемых компонентов. Ультрафильтрацию часто объединяют с диафильтрацией в этап очистки посредством ультрафильтрации/диафильтрации (UFDF).
[315] В вариантах осуществления настоящего изобретения используют по меньшей мере один, по меньшей мере два, по меньшей мере три или более этапов очистки посредством нисходящей UFDF. Одна или более стадий диафильтрации могут происходить на этапе UFDF (например, UFDFDF). В некоторых вариантах осуществления выход белка (AU или оптические единицы) после нисходящей UFDF, относительно количества из предыдущих этапов очистки, составляет от приблизительно 90% до 105%, например от приблизительно 95% до приблизительно 100%, например от приблизительно 97% до приблизительно 99%, как определено с помощью спектрофотометрии, например при 280 нм. В некоторых вариантах осуществления во время UFDF практически не наблюдаются потери белка.
[316] В некоторых вариантах осуществления настоящего изобретения нисходящая UFDF приводит к rASA, который является на по меньшей мере приблизительно 95%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или более чистым, как определено с помощью эксклюзионной хроматографии-высокоэффективной жидкостной хроматографии (SEC-HPLC) и/или обращенно-фазовой-высокоэффективной жидкостной хроматографии (RP-HPLC). В некотором варианте осуществления арилсульфатазу A очищают до по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99%, по меньшей мере приблизительно 99,5%, по меньшей мере приблизительно 99,6%, по меньшей мере приблизительно 99,7%, по меньшей мере приблизительно 99,8% или по меньшей мере приблизительно 99,9%. Степень чистоты арилсульфатазы A можно оценивать, например, с помощью одного или более из: вестерн-блоттинга белка клетки-хозяина (HCP), окрашивания кумасси при SDS-PAGE, окрашивания серебром при SDS-PAGE, обращенно-фазовой HPLC и эксклюзионной HPLC. Специфическая активность rASA составляет по меньшей мере от приблизительно 60 ед./мг до приблизительно 100 ед./мг, например по меньшей мере приблизительно 65 ед./мг, по меньшей мере приблизительно 90 ед./мг, по меньшей мере приблизительно 70 ед./мг или по меньшей мере приблизительно 90 ед./мг, например, как определено согласно анализу в отношении высвобождения сульфатазы, который описан ниже.
[317] В некоторых вариантах осуществления арилсульфатазу A очищают путем отделения от загрязнителей в соответствии с их размером в кислом окружении посредством фильтрации с тангенциальным потоком. Арилсульфатаза A образует октамер при низком значении pH с теоретическим молекулярным весом, составляющим 480 кДа, и, следовательно, будет удерживаться относительно открытой мембраной в то время как большинство загрязнителей пройдут через данную мембрану (Sommerlade et al., (1994) Biochem. J., 297; 123-130; Schmidt et al., (1995) Cell, 82 271-278; Lukatela et al., (1998) Biochemistry, 37, 3654-3664).
[318] В типичном варианте осуществления буфер для диафильтрации содержит 0,01 М фосфата-цитрата натрия, 0,137 М NaCl, pH 6,0.
[319] В некоторых вариантах осуществления, поскольку исходный материал для данного способа представляет собой суспензию арилсульфатазы A, которую элюируют из хроматографической колонки в предыдущей стадии способа, то pH в данной суспензии регулируют до 4-5 путем добавления 0,2-1 М ацетата Na, pH 4,5. Затем проводят диафильтрацию с помощью 1-10 объемов буфера с ацетатом Na, pH 4,0-5,5, способом, хорошо известным специалисту в данной области. Фильтрацию можно проводить с применением нескольких разных типов фильтра со значениями отсечения по номинальному весу, находящимися в диапазоне 20-450 кДа, однако обычно применяют фильтр со значением отсечения, находящимся в диапазоне 100-300 кДа. Для дальнейшей обработки содержащего арилсульфатазу A раствора регулируют pH до значения в диапазоне от 7 до 8 путем добавления трис-основания до конечной концентрации, составляющей примерно 20-50 мМ.
[320] В качестве альтернативы описанной выше фильтрации с кислым тангенциальным потоком отделение ASA от загрязнителей можно выполнять с помощью фильтрации через кислый гель с применением по сути тех же условий и композиций буферов. Фильтрацию проводят при низком значении pH через фильтрационную колонку с гелем, которую уравновешивали раствором при низком значении pH, например 0,2-0,9 М раствора ацетата Na при pH 4-5. В качестве варианта раствор арилсульфатазы A можно концентрировать с помощью фильтрации с тангенциальным потоком через фильтр с размером 20-50 кДа перед фильтрацией через гель. Степень концентрирования может значительно варьироваться, так что арилсульфатазу A можно концентрировать от приблизительно 0,1 мг/мл до приблизительно 50 мг/мл, предпочтительно до приблизительно 5 мг/мл.
[321] В некоторых вариантах осуществления объединенный материал образцов концентрируют за счет Biomax A-screen, 30 кДа. Диафильтрацию проводят путем 3-5 промываний колонки 20 мМ ацетата Na, pH 5,4-5,7.
[322] В вариантах осуществления поверхностно-активное вещество, такое как полисорбат-20 (P20), добавляют к композициям, содержащим очищенный белок ASA, перед холодильным хранением. В вариантах осуществления композиция содержит поверхностно-активное вещество, такое как P20, в концентрации, составляющей от приблизительно 0,0001% (объем/объем) до приблизительно 0,01% (объем/объем), от приблизительно 0,001% (объем/объем) до приблизительно 0,01% (объем/объем), приблизительно 0,001% (объем/объем), приблизительно 0,002% (объем/объем), приблизительно 0,003% (объем/объем), приблизительно 0,004% (объем/объем), приблизительно 0,005% (объем/объем), приблизительно 0,006% (объем/объем), приблизительно 0,007% (объем/объем), приблизительно 0,008% (объем/объем), приблизительно 0,009% (объем/объем) или приблизительно 0,01% (объем/объем).
Определение характеристик очищенных белков ASA
[323] Очищенный рекомбинантный белок ASA можно охарактеризовать с применением различных способов.
Чистота
[324] Степень чистоты очищенного рекомбинантного белка ASA, как правило, оценивают по уровню различных примесей (например, белка клетки-хозяина или ДНК клетки-хозяина), присутствующих в конечном продукте.
[325] Например, уровень белка клетки-хозяина (HCP) можно измерять с помощью ELISA или SDS-PAGE. В некоторых вариантах осуществления очищенный рекомбинантный белок ASA содержит менее 150 нг HCP/мг белка ASA (например, менее 140, 130, 120, 110, 100, 90, 80, 70, 60, 50, 40, 30, 30, 20, 10 нг HCP/мг белка ASA). В вариантах осуществления очищенный рекомбинантный белок ASA содержит менее приблизительно 100, приблизительно 80 или приблизительно 60 нг HCP/мг ASA.
[326] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA содержит менее приблизительно 150 пг/мг, 140 пг/мг, 130 пг/мг, 120 пг/мг, 110 пг/мг, 100 пг/мг, 90 пг/мг, 80 пг/мг, 70 пг/мг, 60 пг/мг, 50 пг/мг, 40 пг/мг, 30 пг/мг, 20 пг/мг или 10 пг/мг ДНК клетки-хозяина (HCD). В вариантах осуществления очищенный рекомбинантный белок ASA содержит менее приблизительно 50, приблизительно 10, приблизительно 9, приблизительно 8, приблизительно 7, приблизительно 6, приблизительно 5, приблизительно 4, приблизительно 3, приблизительно 2 или приблизительно 1 пг HCD/мг белка ASA.
[327] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA, при подвергании SDS-PAGE с окрашиванием кумасси бриллиантовым голубым, не характеризуется новыми полосами с интенсивностью, превышающей 0,05%, 0,01%, 0,15%, 0,2%, 0,25%, 0,3%, 0,35%, 0,4%, 0,45% или 0,5% аналитического контроля.
[328] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA, при подвергании SDS-PAGE с вестерн-блоттингом в отношении HCP, не характеризуется полосами с интенсивностью, превышающей аналитический контроль, представляющий собой полосу HCP размером 15 кДа, и новыми полосами с интенсивностью, превышающей 0,05%, 0,01%, 0,15%, 0,2%, 0,25%, 0,3%, 0,35%, 0,4%, 0,45%, 0,5% или 1,0% аналитического контроля. В вариантах осуществления выявляют не более трех полос HCP.
[329] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA, при подвергании SDS-PAGE с окрашиванием серебром, не характеризуется новыми полосами с интенсивностью, превышающей 0,05%, 0,01%, 0,15%, 0,2%, 0,25%, 0,3%, 0,35%, 0,4%, 0,45% или 0,5% аналитического контроля.
[330] В некоторых вариантах осуществления значение логарифмического уменьшения (LRV) белка клетки-хозяина (HCP) составляет от приблизительно 0,3 до приблизительно 0,6, например от приблизительно 0,4 до 0,5, Можно применять различные аналитические контроли, в частности таковые, приемлемые для контролирующих органов, таких как FDA.
[331] Степень чистоты очищенного рекомбинантного белка ASA также можно определять с помощью одной или более эксклюзионных хроматографий-высокоэффективных жидкостных хроматографий (SEC-HPLC), капиллярного электрофореза-SDS PAGE (CE-SDS PAGE) и/или обращенно-фазовой-высокоэффективной жидкостной хроматографии (RP-HPLC) (например, с применением колонок со связанным с октадецилом (C18) диоксидом кремния и проводят при кислом pH с TFA в качестве противоиона). В некоторых вариантах осуществления настоящего изобретения главный пик на хроматограмме представляет собой ASA. Параметры, которые можно изменять или оптимизировать для повышения степени разделения, включают в себя градиентные условия, органический модификатор, противоион, температуру, размер пор колонки и размер частиц, состав растворителей и скорость потока. Уровни чистоты можно различать по доле в процентах главного пика, как известно специалистам в данной области. Например, степень чистоты можно определять путем суммирования наблюдаемых главного и побочных пиков и расчета доли в процентах главного пика от общей площади.
[332] В некоторых вариантах осуществления настоящего изобретения степень чистоты ASA, очищенного согласно способам, раскрытым в данном документе, и которая определена по доли в процентах главного пика при SEC-HPLC, превышает или равняется 95% (например, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или больше). В некоторых вариантах осуществления настоящего изобретения степень чистоты ASA, очищенного согласно способам, раскрытым в данном документе, и которая определена по доли в процентах главного пика при SEC-HPLC, превышает или равняется 97% (например, приблизительно 97%, приблизительно 98%, приблизительно 99% или больше).
[333] В некоторых вариантах осуществления настоящего изобретения степень чистоты ASA, очищенного согласно способам, раскрытым в данном документе, и которая определена по доли в процентах главного пика при RP-HPLC, превышает или равняется 97% (т. е. приблизительно 97%, приблизительно 98%, приблизительно 99% или больше). В некоторых вариантах осуществления настоящего изобретения степень чистоты ASA, очищенного согласно способам, раскрытым в данном документе, и которая определена по доли в процентах главного пика при RP-HPLC, превышает или равняется 98% (т. е. приблизительно 98%, приблизительно 99% или больше).
Специфическая активность
[334] Очищенный рекомбинантный белок ASA также можно охарактеризовать с помощью оценки функциональной и/или биологической активности. Ферментативную активность композиции на основе рекомбинантного ASA можно определять с применением способов, известных в уровне техники. Как правило, способы предусматривают выявление удаления сульфата из синтетического субстрата, которое известно как анализ в отношении высвобождение сульфата. Один пример анализа в отношении ферментативной активности предусматривает применение ионной хроматографии. В данном способе количественно определяют количество ионов сульфата, которые ферментативно высвобождаются рекомбинантным ASA из субстрата. Субстрат может представлять собой природный субстрат или синтетический субстрат. В некоторых случаях субстрат представляет собой сульфат гепарина, дерматансульфат или их функциональные эквиваленты. Как правило, высвобожденный ион сульфата подвергают анализу с помощью ионной хроматографии с детектором по проводимости. В данном примере результаты можно выражать в виде ед./мг белка, где 1 единицу определяют как количество фермента, необходимого для высвобождения 1 мкмоля иона сульфата в час из субстрата. В некоторых вариантах осуществления очищенный рекомбинантный ASA характеризуется специфической активностью, составляющей по меньшей мере приблизительно 50 ед./мг, 60 ед./мг, 70 ед./мг, 80 ед./мг, 90 ед./мг, 100 ед./мг, 110 ед./мг, 120 ед./мг, 130 ед./мг, 140 ед./мг. В некоторых вариантах осуществления очищенный рекомбинантный ASA характеризуется специфической активностью, находящейся в диапазоне приблизительно 50-200 ед./мг (например, приблизительно 50-190 ед./мг, 50-180 ед./мг, 50-170 ед./мг, 50-160 ед./мг, 50-150 ед./мг, 50-140 ед./мг, 50-130 ед./мг, 50-120 ед./мг, 50-110 ед./мг, 50-100 ед./мг, 60-200 ед./мг, 60-190 ед./мг, 60-180 ед./мг, 60-170 ед./мг, 60-160 ед./мг, 60-150 ед./мг, 60-140 ед./мг, 60-130 ед./мг, 60-120 ед./мг, 60-110 ед./мг, 60-100 ед./мг, 70-200 ед./мг, 70-190 ед./мг, 70-180 ед./мг, 70-170 ед./мг, 70-160 ед./мг, 70-150 ед./мг, 70-140 ед./мг, 70-130 ед./мг, 70-120 ед./мг, 70-110 ед./мг, 70-100 ед./мг, 80-200 ед./мг, 80-190 ед./мг, 80-180 ед./мг, 80-170 ед./мг, 80-160 ед./мг, 80-150 ед./мг, 80-140 ед./мг, 80-130 ед./мг, 80-120 ед./мг, 80-110 ед./мг, 80-100 ед./мг, 90-200 ед./мг, 90-190 ед./мг, 90-180 ед./мг, 90-170 ед./мг, 90-160 ед./мг, 90-150 ед./мг, 90-140 ед./мг, 90-130 ед./мг, 90-120 ед./мг, 90-110 ед./мг, 90-100 ед./мг, 100-200 ед./мг, 100-190 ед./мг, 100-180 ед./мг, 100-170 ед./мг, 100-160 ед./мг, 100-150 ед./мг, 100-140 ед./мг, 100-130 ед./мг, 100-120 ед./мг, 100-110 ед./мг, 110-200 ед./мг, 110-190 ед./мг, 110-180 ед./мг, 110-170 ед./мг, 110-160 ед./мг, 110-150 ед./мг, 110-140 ед./мг, 110-130 ед./мг, 110-120 ед./мг, 120-200 ед./мг, 120-190 ед./мг, 120-180 ед./мг, 120-170 ед./мг, 120-160 ед./мг, 120-150 ед./мг, 120-140 ед./мг, 120-130 ед./мг, 130-200 ед./мг, 130-190 ед./мг, 130-180 ед./мг, 130-170 ед./мг, 130-160 ед./мг, 130-150 ед./мг или 130-140 ед./мг). В вариантах осуществления специфическая активность очищенного рекомбинантного ASA составляет от приблизительно 50 до приблизительно 130 ед./мг, от приблизительно 70 до приблизительно 100 ед./мг, от приблизительно 80 до приблизительно 90 ед./мг или от приблизительно 75 до приблизительно 95 ед./мг.
[335] В другом примере ферментативную активность композиции на основе рекомбинантного ASA можно определять путем измерения степени удаления сульфата из субстрата 4-метилумбеллиферил-сульфата (4-MUF-сульфата) с образованием флуоресцентного метилумбеллиферона. В данном примере флуоресцентный сигнал, образованный тестовым образцом, можно использовать для расчета ферментативной активности (в милиед./мл) с применением стандарта, представляющего собой 4-MUF. Одну милиединицу активности определяют как количество фермента, необходимое для превращения 1 наномоля 4-MUF-сульфата в 4-MUF за 1 минуту при 37°C. Специфическую активность затем можно рассчитывать путем деления ферментативной активности на концентрацию белка.
[336] В некоторых вариантах осуществления активность определяют по степени гидролиза синтетического хромогенного субстрата, сульфата пара-нитрокатехина (pNCS), который характеризуется конечным продуктом пара-нитрокатехином (pNC), который поглощает свет при 515 нм. Следующее уравнение можно применять для расчета ферментативной активности в мкмоль pNCS гидролизованный/мин. x мл (=единицы/мл):
Vоб. (мл) x ΔA=единицы/мл (1).
εM /1000 x Vобразец (мл) x время инкубации (мин.), где:
ΔA=поглощение образца - поглощение холостого раствора,
Vоб. (мл) = общий объем реакции в мл (в данном случае 0,15 мл),
Vобразец (мл) = добавленный объем образца в мл (в данном случае 0,05 мл),
εM=молярный коэффициент экстинкции для продукта pNC, который в данном случае составляет 12 400 М-1 см-1.
[337] Уравнение 1 может быть упрощено:
ΔA x (0,15 / (12 400/1000×0,05×30)) =X мкмоль / (минута x мл) (=единицы/мл) (1).
[338] Для расчета специфической активности в мкмоль pNC израсходованного/(минута x мг) (= единицы/мг), уравнение 1 делят на концентрацию белка образца:
Ур. 1/конц. белка (мг/мл) = Y мкмоль / (минута x мг) = единицы/мг (2).
[339] В любом примере концентрацию белка композиции на основе рекомбинантного ASA можно определять с помощью любого подходящего способа, известного в уровне техники для определения значений концентрации белка. В некоторых случаях концентрацию белка определяют с помощью анализа поглощения ультрафиолетового излучения. Такие анализы поглощения, как правило, проводят при длине волны, составляющей приблизительно 280 нм (A280).
[340] В некоторых вариантах осуществления очищенный рекомбинантный ASA характеризуется специфической активностью в отношении субстрата 4-метилумбеллиферона в диапазоне от приблизительно 1,0×103 милиед./мг до 100,0×103 милиед./мг, от приблизительно 1,0×103 милиед./мг до 50,0×103 милиед./мг, от приблизительно 1,0×103 милиед./мг до 40,0×103 милиед./мг, от приблизительно 1,0×103 милиед./мг до 30,0×103 милиед./мг, от приблизительно 1,0×103 милиед./мг до 20,0×103 милиед./мг, от приблизительно 1,0×103 милиед./мг до 10,0×103 милиед./мг, от приблизительно 4,0×103 милиед./мг до 8,0×103 милиед./мг, от приблизительно 4,0×103 милиед./мг до 10,0×103 милиед./мг, от приблизительно 4,5×103 милиед./мг до 10,0×103 милиед./мг, от приблизительно 5,0×103 милиед./мг до 10,0×103 милиед./мг, от приблизительно 5,5×103 милиед./мг до 15,0×103 милиед./мг или от приблизительно 4,0×103 милиед./мг до 20,0×103 милиед./мг. В некоторых вариантах осуществления очищенный рекомбинантный ASA характеризуется специфической активностью в отношении субстрата 4-метилумбеллиферона, составляющей приблизительно 1,0×103 милиед./мг, приблизительно 2,0×103 милиед./мг, приблизительно 3,0×103 милиед./мг, приблизительно 4,0×103 милиед./мг, приблизительно 5,0×103 милиед./мг, приблизительно 10,0×103 милиед./мг, приблизительно 15,0×103 милиед./мг, приблизительно 20,0×103 милиед./мг, приблизительно 25,0×103 милиед./мг, приблизительно 30,0×103 милиед./мг, приблизительно 35,0×103 милиед./мг, приблизительно 40,0×103 милиед./мг, приблизительно 45,0×103 милиед./мг, приблизительно 50,0×103 милиед./мг или более.
Профиль заряда
[341] Очищенный рекомбинантный ASA можно охарактеризовать по профилю заряда, ассоциированного с белком. Как правило, профиль заряда белка отражает паттерн зарядов остатков боковой цепи, как правило, присутствующих на поверхности белка. Профиль заряда можно определять путем проведения анализа с ионообменной (IEX) хроматографией (например, HPLC) в отношении белка. В некоторых вариантах осуществления «профиль заряда» относится к набору величин, представляющих количество белка, которое элюируется из ионообменной колонки в момент времени после добавления в колонку подвижной фазы, содержащей обменный ион.
[342] Как правило, подходящая ионообменная колонка представляет собой анионообменную колонку. Например, профиль заряда можно определять с помощью сильной анионообменной (SAX) хроматографии с применением системы высокоэффективной жидкостной хроматографии (HPLC). В целом, рекомбинантный ASA адсорбируется на фиксированном слое с положительным зарядом колонки для сильной анионообменной хроматографии, и градиент увеличивающейся ионной силы с помощью подвижной фазы при предварительно определенной скорости потока элюирует виды рекомбинантного ASA из колонки пропорционально силе их ионного взаимодействия с положительно заряженной колонкой. Более отрицательно заряженные (более кислые) виды ASA элюируются позднее, нежели менее отрицательно заряженные (менее кислые) виды ASA. Концентрацию белков в элюате выявляют по поглощению ультрафиолетового света (при 280 нм).
[343] В некоторых вариантах осуществления рекомбинантный ASA абсорбируется при приблизительно pH 8,0 в 20 мМ ТРИС-HCl на фиксированный слой с положительным зарядом колонки Mini Q PE, и градиент увеличивающейся ионной силы с применением подвижной фазы, состоящей из 20 мМ ТРИС-HCL, 1 М хлорида натрия, pH 8,0 при скорости потока, составляющей 0,8 мл/мин., элюирует виды рекомбинантного ASA из колонки пропорционально силе их ионного взаимодействия с положительно заряженной колонкой.
[344] В некоторых вариантах осуществления профиль заряда можно изображать с помощью хроматограммы в оптических единицах в зависимости от времени после элюирования из колонки для HPLC. Хроматограмма может содержать набор из одного или более пиков, при этом каждый пик в наборе идентифицирует субпопуляцию рекомбинантных ASA композиции, которые характеризуются подобными поверхностными зарядами.
Картирование гликанов
[345] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA можно охарактеризовать по его составу протеогликанов, как правило называемому картированием гликанов. Не желая ограничиваться какой-либо теорией, считают, что гликановые связи наряду с формой и сложностью разветвленной структуры, могут влиять на клиренс, нацеливание на лизосомы, биологическую доступность и/или эффективность in vivo.
[346] Как правило, карту гликанов можно определять с помощью ферментативного расщепления и последующего хроматографического анализа. Для ферментативного расщепления можно применять различные ферменты, в том числе без ограничения подходящие гликозилазы, пептидазы (например, эндопептидазы, экзопептидазы), протеазы и фосфатазы. В некоторых вариантах осуществления подходящий фермент представляет собой щелочную фосфатазу. В некоторых вариантах осуществления подходящий фермент представляет собой нейраминидазу. Гликаны (например, фосфогликаны) можно выявлять с помощью хроматографического анализа. Например, фосфогликаны можно выявлять с помощью высокоэффективной анионообменной хроматографии с импульсным амперометрическим детектированием (HPAE-PAD) или эксклюзионной высокоэффективной жидкостной хроматографии (HPLC). Количество гликана (например, фосфогликана), представленного каждым пиком на карте гликанов, можно рассчитывать с применением стандартной кривой гликана (например, фосфогликана) в соответствии со способами, известными в уровне техники и раскрытыми в данном документе.
[347] В вариантах осуществления очищенный рекомбинантный белок ASA присутствует в виде видов, предусматривающих: нейтральный рекомбинантный белок ASA (группа A), сиалированный рекомбинантный белок ASA (группа B), манноза-6-фосфатированный рекомбинантный белок ASA (группа C), N-ацетил-глюкозамин-манноза-6-фосфатированный рекомбинантный белок ASA (группа E) или гибридный рекомбинантный белок ASA (группа E) или любая их комбинация. В вариантах осуществления очищенный рекомбинантный белок ASA присутствует в виде нейтрального рекомбинантного белка ASA (группа A), сиалированного рекомбинантного белка ASA (группа B), манноза-6-фосфатированного рекомбинантного белка ASA (группа C), N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (группа E) и гибридного рекомбинантного белка ASA (группа E).
[348] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA в соответствии с настоящим изобретением характеризуется картой гликанов, содержащей по меньшей мере семь пиковых групп, указывающих на нейтральный (пиковая группа 1), моно-сиалированный (пиковая группа 2), кэпированный манноза-6-фосфатированный (пиковая группа 3), ди-сиалированный (пиковая группа 4), моно-манноза-6-фосфатированный (пиковая группа 5), гибридный (пиковая группа 6) и ди-манноза-6-фосфатированный (пиковая группа 7) белок ASA соответственно.
[349] Относительное количество гликана, соответствующее группе (например, любой из групп A-E или пиковых групп 1-7), можно определять на основе площади пиковой группы относительно площади соответствующей пиковой группы в предварительно определенном эталонном стандарте.
[350] В вариантах осуществления группа A (нейтральный рекомбинантный белок ASA) может характеризоваться площадью пиковой группы, которая находится в диапазоне от приблизительно 15 до приблизительно 25% (например, от приблизительно 16% до приблизительно 22% или от приблизительно 20% до приблизительно 25%) относительно площади соответствующей пиковой группы в эталонном стандарте. В вариантах осуществления площадь пиковой группы нейтрального рекомбинантного белка ASA находится в диапазоне, характерном для любого из иллюстративных составов в примере 3, с колебанием, составляющим от приблизительно 1% до приблизительно 10%, в любом из двух направлений для каждой конечной точки примерного диапазона (например, колебание, составляющее от приблизительно 1% до приблизительно 5%, для каждой конечной точки примерного диапазона).
[351] В вариантах осуществления группа B (сиалированный рекомбинантный белок ASA) может характеризоваться общей площадью пиковой группы видов сиалированного рекомбинантного белка ASA, которая находится в диапазоне от приблизительно 35% до приблизительно 45% (например, от приблизительно 35% до приблизительно 42% или от приблизительно 37% до приблизительно 42%) относительно любых площадей соответствующей пиковой группы в эталонном стандарте. В вариантах осуществления общая площадь пиковой группы сиалированного рекомбинантного белка ASA находится в диапазоне, характерном для любого из иллюстративных составов в примере 3, с колебанием, составляющим от приблизительно 1% до приблизительно 10%, в любом из двух направлений для каждой конечной точки примерного диапазона (например, колебание, составляющее от приблизительно 1% до приблизительно 5%, для каждой конечной точки примерного диапазона).
[352] В вариантах осуществления группа C (манноза-6-фосфатированный рекомбинантный белок ASA) может характеризоваться общей площадью пиковой группы видов манноза-6-фосфатированного рекомбинантного белка ASA, которая находится в диапазоне от приблизительно 20% до приблизительно 30% (например, от приблизительно 20% до приблизительно 26%, от приблизительно 25% до приблизительно 28% или от приблизительно 27% до приблизительно 32%) относительно любых площадей соответствующей пиковой группы в эталонном стандарте. В вариантах осуществления общая площадь пиковой группы манноза-6-фосфатированного рекомбинантного белка ASA находится в диапазоне, характерном для любого из иллюстративных составов в примере 3, с колебанием, составляющим от приблизительно 1% до приблизительно 10%, в любом из двух направлений для каждой конечной точки примерного диапазона (например, колебание, составляющее от приблизительно 1% до приблизительно 5%, для каждой конечной точки примерного диапазона).
[353] В вариантах осуществления группа D (N-ацетил-глюкозамин-манноза-6-фосфатированный рекомбинантный белок ASA) может характеризоваться общей площадью пиковой группы видов N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA, которая находится в диапазоне от приблизительно 1% до приблизительно 10% (например, от приблизительно 3% до приблизительно 5%, от приблизительно 4% до приблизительно 6% или от приблизительно 4,5% до приблизительно 5,5%) относительно любых площадей соответствующей пиковой группы в эталонном стандарте. В варианте осуществления общая площадь пиковой группы N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA находится в диапазоне, характерном для любого из иллюстративных составов в примере 3, с колебанием, составляющим от приблизительно 1% до приблизительно 10%, в любом из двух направлений для каждой конечной точки примерного диапазона (например, колебание, составляющее от приблизительно 1% до приблизительно 5%, для каждой конечной точки примерного диапазона).
[354] В вариантах осуществления группа E (гибридный рекомбинантный белок ASA) может характеризоваться площадью пиковой группы гибридного рекомбинантного белка ASA, которая находится в диапазоне от приблизительно 5% до приблизительно 15% (например, от приблизительно 7% до приблизительно 10%, от приблизительно 7% до приблизительно 9% или от приблизительно 7,5% до приблизительно 8,5%) относительно любых площадей соответствующей пиковой группы в эталонном стандарте. В вариантах осуществления общая площадь пиковой группы гибридного рекомбинантного белка ASA находится в диапазоне, характерном для любого из иллюстративных составов в примере 3, с колебанием, составляющим от приблизительно 1% до приблизительно 10%, в любом из двух направлений для каждой конечной точки примерного диапазона (например, колебание, составляющее от приблизительно 1% до приблизительно 5%, для каждой конечной точки примерного диапазона).
[355] Различные эталонные стандарты для картирования гликанов известны из уровня техники, и их можно применять для практической реализации настоящего изобретения.
[356] Предполагается, что паттерн гликозилирования очищенного рекомбинантного белка ASA (например, композиции, содержащей очищенный рекомбинантный белок ASA с пороговым вмещением манноза-6-фосфатированного рекомбинантного белка ASA (белок ASA с M6P)) может влиять на биологическую доступность, нацеливание или эффективность белка.
Картирование пептидов
[357] В некоторых вариантах осуществления можно применять картирование пептидов для определения композиции аминокислот, посттрансляционных модификаций и/или процессинга в клетке; как, например отщепление сигнального пептида и/или гликозилирование. Как правило, рекомбинантный белок можно разрушать на дискретные пептидные фрагменты либо с помощью контролируемого, либо случайного разрушения с получением паттерна или карты пептидов. В некоторых случаях очищенный белок ASA можно сначала подвергать ферментативному расщеплению перед аналитическим анализом. Расщепление можно проводить с применением пептидазы, гликозидгидролазы, фосфатазы, липазы или протеазы и/или их комбинаций перед аналитическим анализом. Структурную композицию пептидов можно определять с применением способов, широко известных в уровне техники. Иллюстративные способы включают без ограничения масс-спектрометрию, ядерный магнитный резонанс (NMR) или HPLC.
Анализ металлов
[358] В некоторых вариантах осуществления очищенный рекомбинантный белок ASA можно охарактеризовать с помощью анализа металлов. Различные способы анализа следов металлов в очищенных лекарственных веществах известны в уровне техники, и их можно применять при осуществлении на практике настоящего изобретения.
[359] В некоторых вариантах осуществления измеряют остаточный фосфор и сравнивают с эталонным образцом. Не желая ограничиваться какой-либо конкретной теорией, предполагают, что остаточный фосфор способствует сохранению pH лекарственного вещества. В некоторых вариантах осуществления настоящего изобретения остаточный фосфор составляет приблизительно 10-50 ppm (т. е. приблизительно 10-45 ppm, приблизительно 10-40 ppm, приблизительно 10-30 ppm, приблизительно 20-50 ppm приблизительно 20-45 ppm, приблизительно 20-40 ppm, приблизительно 20-30 ppm, приблизительно 30-50 ppm, приблизительно 30-40 ppm). В некоторых вариантах осуществления диапазон pH рекомбинантного ASA, очищенного в соответствии со способами, раскрытыми в данном документе, составляет приблизительно 5-7 (т. е. приблизительно 5,5-7,0, приблизительно 5,5-6,5, приблизительно 5,5-6,0, приблизительно 6,0-7,0, приблизительно 6,0-6,5, приблизительно 6,0-6,4, приблизительно 6,0-6,3, приблизительно 6,0-6,2, приблизительно 6,0-6,1, приблизительно 6,1-6,2).
[360] В некоторых вариантах осуществления рекомбинантный ASA, очищенный в соответствии со способами, раскрытыми в данном документе, содержит кальций. Не желая ограничиваться какой-либо конкретной теорией, предполагают, что ионы кальция, присутствующие в активном сайте ASA, могут быть необходимы для ферментативной активности. В некоторых вариантах осуществления настоящего изобретения кальций присутствует при уровнях, составляющих приблизительно 1-20 ppm (т. е. приблизительно 1-15 ppm, приблизительно 1-10 ppm, приблизительно 5-15 ppm, приблизительно 5-10 ppm, приблизительно 10-20 ppm, приблизительно 10-15 ppm, приблизительно 10-14 ppm, приблизительно 10-13 ppm, приблизительно 10-12 ppm).
ПРИМЕРЫ
Пример 1. Иллюстративный способ
[361] Очищенный рекомбинантный белок ASA получали в соответствии с иллюстративными способами, описанными в данном документе. В таблице 3 указаны определенные конкретные признаки иллюстративного способа получения очищенного рекомбинантного белка ASA. В вариантах осуществления способ очистки рекомбинантного белка ASA включает один или более из описанных в таблице 3 признаков.
Таблица 3
Скорость перфузии=1,40 VVD
Плотность целевых клеток=4,0E6 клеток/мл
Добавление полисорбата-20 при 0,005% (объем/объем) до конечного DS перед холодильным хранением
Пример 2. Иллюстративный состав
[362] Композиции, содержащие очищенный белок ASA, получали как описано в данном документе. В таблице 4 представлены характерные особенности композиции, содержащей очищенный белок ASA, при получении в соответствии с иллюстративным способом, описанным в данном документе. В вариантах осуществления композиция, содержащая очищенный рекомбинантный белок ASA, характеризуется одним или более из признаков, описанных в таблице 4. В вариантах осуществления, где представлены числовые диапазоны, каждая граница примерного диапазона может варьироваться на от приблизительно 1% до приблизительно 20% (например, от приблизительно 1% до приблизительно 15%, от приблизительно 1% до приблизительно 10%, от приблизительно 1% до приблизительно 7,5%, от приблизительно 1% до приблизительно 5% или от приблизительно 1% до приблизительно 2,5%).
Таблица 4. Иллюстративная композиция, содержащая лекарственное вещество (DS) на основе рекомбинантного ASA
Отсутствует более трех выявленных полос HCP
--
Пример 3. Исследования сравнимости
[363] Неклиническая программа сравнимости в качестве оценки активности, безопасности и фармакокинетики rhASA, полученного по способу B, по сравнению с rhASA, полученным по способу A, в неклинической программе сравнимости (таблица 5). Все дозы вводили интратекально. Фармакодинамическую сравнимость оценивали на иммуннотолерантных мышах с MLD с применением иммуногистохимического окрашивания ассоциированного с лизосомой мембранного белка 1 (LAMP-1). Фармакокинетическую сравнимость оценивали у яванских макаков подросткового возраста, которым однократно вводили 6,0 мг (эквивалент 100 мг/кг веса головного мозга) rhASA, полученного по способу A или способу B. Биораспределение сравнивали с помощью количественной авторадиографии всего тела у крыс. Потенциальную токсичность rhASA, полученного по способу B, оценивали путем повторного введения rhASA в дозах, составляющих 18,6 мг, яванским макакам подросткового возраста.
Таблица 5.
AUC, площадь под кривой зависимости концентрации от времени; CSF, спинномозговая жидкость; M6P, манноза-6-фосфат; MLD, метахроматическая лейкодистрофия; QWBA, количественная авторадиография всего тела; rhASA, рекомбинантная человеческая арилсульфатаза A.
Сравнимость по фармакодинамическим параметрам
[364] Иммуннотолерантные мыши с MLD, нокаутные по ASA (ASA-/-), которые имеют стабильно интегрированный трансген, кодирующий неактивный вариант ASA человека, что делает их иммунологически толерантными к инъецируемому rhASA. Животных распределяли в одну из шести групп: необработанные (n=6); со средой-носителем (154 мМ NaCl, 0,005% полисорбата 20, pH 6,0, n=4); rhASA, полученный по способу A, в дозе 0,04 мг (n=9) и 0,21 мг (n=10); rhASA, полученный по способу B, в дозе 0,04 мг (n=10) и 0,21 мг (n=10). Животным вводили дозы интратекально в 1, 8, 15 и 21 или 22 дни. Группа из семи необработанных мышей C57/B16 служила в качестве контролей дикого типа. Животных умерщвляли через 24 часа после их последней дозы rhASA.
[365] Гистологический анализ предусматривал иммуногистохимическое окрашивание ассоциированного с лизосомой мембранного белка 1 (LAMP-1), лизосомального белка-маркера, применяемого для обнаружения лизосомных болезней накопления и в качестве индикатора болезненного состояния. Иммуноокрашивание в отношении LAMP-1 головного мозга и спинного мозга мыши проводили в 5 мкм залитых парафином срезах с применением поликлонального антитела кролика к LAMP-1 (Abcam, номер по кат. ab24170, номер партии ER127402-2, 1:400, Cambridge, штат Массачусетс, США) и набора Bond™ Polymer Refine Detection Kit (Leica, номер по кат. DS9800, Buffalo Grove, штат Иллинойс, США). Сигнал от LAMP-1 получали посредством окрашивания 3,3-диаминобензидином и последующего контрокрашиванием гематоксилином. Первичное антитело заменяли антителом изотипа IgG для отрицательного контроля. Создавали и анализировали цифровые изображения окрашенных в отношении LAMP-1 срезов с применением сканера Aperio с программным обеспечением ImageScope (Leica Microsystems Inc., Buffalo Grove, штат Иллинойс, США). Относительную положительность окрашивания получали с применением следующего уравнения: положительность (%) = (количество положительных в отношении LAMP-1 пикселей/общее количество пикселей) × 100. Статистическое сравнение со средой-носителем и необработанных животных проводили для каждой ткани с применением критерия Манна-Уитни. На основе данной оценки (p > 0,01 между группами для всех тканей) данные объединяли в одну группу (далее в данном документе называемой контролем). Данные нормализовали в отношении контрольной группы и статистические сравнения проводили с применением однофакторного дисперсионного анализа с критерием множественного сравнения Тьюки. Результаты сравнения с p < 0,01 считали статистически значимыми.
[366] Значения специфической активности для rhASA, полученного по способу A и способу B, составляли 89 ед./мг и 106 ед./мг соответственно, оба из которых находились в целевом диапазоне для анализа. Сравнение двух материалов показало, что наибольшие изменения происходили в значениях содержания M6P и сиаловой кислоты, и значения специфической активности были схожими.
[367] Как показано на фигурах 1A-1F, окрашивание в отношении LAMP-1 у иммуннотолерантных мышей с MLD проводили у мышей для спинного мозга, белого вещества мозжечка и бахромки гиппокампа и для ножки мозга, коры больших полушарий и полосатого тела. Для оценки выбирали области, в которых показано влияние обработки материалом, полученным по способу A, из предыдущих исследований. Не наблюдали никаких статистически значимых отличий в окрашивании в отношении LAMP-1 для спинного мозга, белого вещества мозжечка и бахромки гиппокампа между животными, которым вводили дозы rhASA, полученного по способу A по сравнению со способом B. Подобным образом, никаких статистических отличий не наблюдали в окрашивании между rhASA, полученным по способу A и способу B, в ножке мозга, но отличия наблюдали в коре больших полушарий и полосатом теле. Эти отличия считали спорадическими и не имеющими биологической значимости, поскольку статистическая значимость была достигнута только для одной из двух тестируемых доз.
[368] По сравнению с контрольными животными наблюдали статистически значимые снижения в степени окрашивании в отношении LAMP-1 с rhASA, полученным как по способу A, так и по способу B, в спинном мозге (группы дозы 0,21 мг, p < 0,0001; фиг. 1A), в белом веществе мозжечка (группы доз 0,04 мг и 0,21 мг, p < 0,01; фиг. 1B), в ножке мозга (группы доз 0,04 мг и 0,21 мг; фиг. 1D) и в бахромке гиппокампа (группы дозы 0,04 мг, p < 0,01; фиг. 1C). Статистически значимые снижения в степени окрашивании в отношении LAMP-1 также происходили с rhASA, полученным по способу B, в коре больших полушарий (группы доз 0,04 мг и 0,21 мг, p ≤ 0,0001; фиг. 1E) и в полосатом теле (группа дозы 0,04 мг, p=0,0005; фиг. 1F).
Сравнимость по фармакокинетическим параметрам
[369] На 1 фазе животных рандомизировали на основании веса тела либо в группу rhASA, полученного по способу A, 6,0 мг (n=6 [3 самца, 3 самки]), либо в группу rhASA, полученного по способу B, 6,0 мг (n=6 [3 самца, 3 самки]). Интратекальный люмбальный катетер имплантировали хирургическим путем после предварительной обработки подкожно атропинсульфатом (0,01 мг/кг) с последующей анестезией внутримышечным кетамина гидрохлоридом (8 мг/кг), и примерно 1 л/мин. кислорода, и 2% изофлурана. Дозы rhASA вводили посредством имплантированного интратекального поясничного катетера в дозе объемом 1 мл. Доза, составляющая 6,0 мг, была эквивалентна 100 мг/кг веса головного мозга при нормировании к весу головного мозга, составляющему 60 г, у яванских макаков. Данная доза была основана на наивысшей дозе rhASA, которую вводили в фазе 1/2 клинического исследования детям с поздней младенческой формой MLD. В том клиническом исследовании наивысшая доза, которую вводили, составляла 100 мг эквивалентно 100 мг/кг веса головного мозга при нормировании к весу головного мозга, составляющему 1 кг (определено для возрастной группы участников исследования).
[370] На 2 фазе, которую начинали после периода отмывки, составляющего по меньшей мере 8 дней, животным вводили дозы rhASA, полученного по способу B, если им вводили дозы rhASA, полученного по способу A, на 1 фазе и, наоборот, животным вводили дозы rhASA, полученного по способу A, если им вводили дозы rhASA, полученного по способу B, на 1 фазе. Животных подвергали гуманной эвтаназии не более чем через 24 часа после последней дозы rhASA.
[371] Отслеживали значения веса тела, потребление корма и клинические параметры и образцы крови и CSF собирали до введения дозы и в предварительно указанные интервалы после введения дозы. Значения концентрации rhASA в сыворотке крови и CSF измеряли с применением твердофазного иммуноферментного анализа. Количественное определение уровней rhASA в сыворотке крови и CSF яванских макаков подросткового возраста выполняли с применением утвержденного GLP способа анализа ELISA. Микротитровальные планшеты покрывали поликлональным антителом кролика к rhASA (SH040). После инкубации с образцами и стандартами микротитровальные планшеты промывали и во все лунки добавляли конъюгированное с пероксидазой хрена моноклональное антитело мыши к ASA (клон 19-16-3). Нижний предел количественного определения для сыворотки крови обезьян составлял 39,1 нг/мл и для CSF обезьян составлял 19,5 нг/мл, и верхний предел количественного определения для каждого способа составлял 1250 нг/мл.
[372] Кривые зависимости концентрации от времени rhASA в сыворотке крови (фиг. 2A) и CSF (фиг. 2B) после однократной интратекальной дозы, составляющей 6,0 мг, яванским макакам подросткового возраста были схожи при использовании rhASA, полученного по способу A и способу B. rhASA, полученный по способу A и способу B, были схожи в отношении их фармакокинетических параметров, в том числе максимальной концентрации в плазме крови (Cmax), воздействия (площадь под кривой зависимости концентрации от момента времени 0 до последнего измерения [AUCпоследняя]) и клиренса (таблица 6).
Таблица 6. Средние фармакокинетические параметры в спинномозговой жидкости и сыворотке крови у яванских макаков подросткового возраста после интратекального поясничного введения 6,0 мг rhASA, изготовленного с применением способа A или способа B.
λz, t½, Vz, CL и MRTбеск. не могли быть определены в образцах сыворотки крови.
AUCбеск., площадь под кривой зависимости концентрации от времени с момента времени 0 до бесконечности; AUCпоследняя, площадь под кривой зависимости концентрации от времени от момента времени 0 до последнего измерения; CL, клиренс; Cmax, максимальная концентрация в плазме крови; λz, константа скорости переноса; ч., час; MRTбеск., от среднего времени удержания до бесконечности; n, количество; ND, не определено; t½, период полувыведения в конечной фазе; rhASA, рекомбинантная человеческая арилсульфатаза A; SD, стандартное отклонение; Tmax, время до максимальной концентрации в плазме крови; Vz, объем распределения.
Сравнимость биораспределения
[373] Исследование, в котором применяли количественную авторадиографию всего тела (QWBA) и гамма-радиометрию после однократной интратекальной дозы [125I]-rhASA. Для оценки распределения в тканях 28 крыс, которым имплантировали интратекальные порты, рандомизировали так, что каждая получала дозу [125I]-rhASA, составляющую 0,62 мг, изготовленного с применением либо способа A (14 животных), либо способа B (14 животных). Две крысы из каждой группы доз подвергали эвтаназии в каждый из семи моментов времени после введения дозы (примерно через 1, 4, 12, 24, 48, 96 и 168 часов после введения дозы) и обрабатывали для QWBA, при этом концентрацию радиоактивной метки определяли для выбранных тканей. Образцы крови собирали от анестезированных изофлураном животных с помощью кардиальной пункции перед эвтаназией. Для оценки фармакокинетических параметров аликвоты цельной крови, плазмы крови и ткани анализировали в отношении общей радиоактивности с применением гамма-радиометрии. Для оценки паттернов экскреции rhASA шесть самцов крыс Sprague Dawley распределяли в группы, получающие 0,62 мг [125I]-rhASA, изготовленного с применением либо способа A (3 животных), либо способа B (3 животных). Крыс помещали в отдельные камеры для исследования метаболизма для раздельного сбора моча и фекалий в течение 168 часов после введения [125I]-rhASA.
[374] Осаждение трихлоруксусной кислотой образцов плазмы крови показало, что примерно 33% 125I не связывалось с rhASA. Из иллюстративных авторадиолюминограмм всего тела видно распределение [125I]-rhASA, полученного по способу A (фиг. 3A) и способу B (фиг. 3B), у самцов крыс Sprague Dawley через 4 часа после введения однократной интратекальной дозы, составляющей 0,62 мг. Cmax и AUCпоследняя для rhASA, полученного по способу A и способу B, и соотношения rhASA, полученного по способу B, и rhASA, полученного по способу A, в разных тканях показаны в таблице 6. Наивысшую рассчитанную концентрацию (Cmax) [125I]-rhASA обнаруживали в щитовидной железе, вероятно, вследствие поглощения несвязанного йода. За ним следовали гипофиз, спинной мозг и печень, все из которых имели схожие уровни (таблица 7). Наименьшие концентрации [125I]-rhASA встречалась в жире, яичках, мышцах и глазах (таблица 7). При визуальном осмотре кажущаяся концентрация в спинном мозге была очень низкой относительно концентрации в прилегающих CSF и оболочках головного мозга, что позволяет предположить, что рассчитанные значения в спинном мозге могли быть завышены. Непосредственная близость к областям с высокой концентрацией 125I и небольшой количественный участок могли способствовать завышению значений в спинном мозге.
Таблица 7. Фармакокинетические параметры эквивалентов rhASA после однократной интратекальной дозы, составляющей 0,62 мг, [125I]-rhASA, полученного по способу A или способу B, у самцов крыс Sprague Dawley.
AUCпоследняя, площадь под кривой зависимости концентрации от времени от момента времени 0 до последнего измерения; Cmax, максимальная концентрация в плазме крови; rhASA, рекомбинантная человеческая арилсульфатаза A.
[375] Значения Cmax для rhASA, полученного по способу B, составляли примерно в 1,5 раза выше, чем таковые для [125I]-rhASA, полученного по способу A, для головного мозга, спинного мозга и легкого (наибольшие соотношения), и примерно в 0,2-0,6 раза ниже, чем таковые для [125I]-rhASA, полученного по способу A, для почки, надпочечной железы, желудка и поджелудочной железы (наименьшие соотношения; таблица 5). Отличия в уровнях воздействия (AUCпоследняя) для всех тканей были менее, чем в два раза, за исключением кожи и надпочечной железы, в которых соотношения составляли 2,27 и 2,19 соответственно для [125I]-rhASA, полученного по способу B и способу A (таблица 5). Период полувыведения в конечной фазе в плазме крови составлял 37,2 часа с [125I]-rhASA, полученным по способу A, и 42,5 часа с [125I]-rhASA, полученным по способу B.
[376] Профили экскреции в моче и фекалиях оценивали как показано на фигуре 4. Паттерны экскреции были схожи для [125I]-rhASA, полученного как по способу A, так и по способу B. Большая часть продукта, полученного по способу A и способу B, экскретировалась с мочой (76% и 71%, соответственно), что указывало на то, что rhASA системно выводится в основном за счет почечной элиминации, и приблизительно 6% экскретировалось с фекалиями в отношении обоих продуктов. Доля вводимой дозы, возвращенной в организм, составляла 6% для продукта, полученного по способу A, и 8% для продукта, полученного по способу B, при этом большая часть локализовалась в щитовидной железе, CSF и оболочках головного мозга. Общее извлечение (все выделения и возврат в организм объединены) составляло 90% и 83% для животных, которым вводили дозы [125I]-rhASA, полученного по способу A или способу B, соответственно.
Токсикология
[377] Интратекальный портальный катетер имплантировали хирургическим путем после предварительной обработки мелоксикамом (0,2 мг/кг) с последующими кетамина гидрохлоридом (5 мг/кг) и медетомидином (0,06 мг/кг). Дозы rhASA вводили с помощью болюсной доставки в медленном темпе с применением системы интратекального портального катетера. Животным вводили дозы каждые 2 недели в течение 11 недель (шесть доз в целом) либо rhASA, полученного по способу B, 18,6 мг (n=8 [4 самца, 4 самки]), либо контроль в виде среды-носителя (NaCl 154 мМ, 0,005% полисорбата 20, pH 6,0; n=8 [4 самца, 4 самки]) в дозе объемом 0,6 мл. Максимальную возможную дозу rhASA, составляющую 18,6 мг, применяли в данном исследовании, и она основывалась на наибольшем переносимом объеме у яванского макака подросткового возраста (0,6 мл) и на концентрации состава с rhASA, полученным по способу B (31,0 мг/мл).
[378] Оценки включали клинические исследования (оценки веса тела; потребления корма; физические, сердечно-сосудистые [электрокардиограмма и кровяное давление], неврологические и офтальмологические оценки) и функциональные исследования (биохимический анализ сыворотки крови; общий анализ крови; свертывание; анализ мочи; определение количества клеток CSF и биохимический анализ CSF). Антигенность rhASA, полученного по способу B, оценивали в сыворотке крови и CSF. Физические и неврологические исследования проводили на неседированных животных дважды во время фазы до введения дозы (перед хирургическим вмешательством и через ≥5 дней после хирургического вмешательства) и один раз в течение недель 1, 5 и 9 фазы введения доз (примерно через 24 часа после введения дозы), а также один раз перед аутопсией. Электрокардиографические исследования проводили на неанестезированных временно обездвиженных животных во время фазы до введения доз (после хирургического вмешательства) и на недели 11 фазы введения доз (сразу перед введением дозы и через 3 часа после введения дозы). Всех животных подвергали гуманной эвтаназии через 24 часа после конечной дозы. Собирали полные наборы тканей, но только целевые ткани, идентифицированные в первичном исследовании со способом A (т. е. спинной мозг и дорсальные корешковые ганглии), подвергали гистопатологической оценке.
[379] Интратекальное введение rhASA, полученного по способу B, хорошо переносилось яванскими макаками подросткового возраста, при этом не было никаких связанных с лекарственным средством эффектов в отношении результатов клинических, неврологических или функциональных исследований.
[380] Интратекальное введение rhASA, полученного по способу B, в дозе, составляющей 18,6 мг, каждые 2 недели в течение 11 недель яванским макакам подросткового возраста (шесть доз в целом) являлось уровнем, при котором отсутствовали наблюдаемые неблагоприятные эффекты. Введение rhASA, полученного по способу B, связывали с инфильтрацией эозинофилами в следующих областях: участки оболочек вокруг головного мозга и спинного мозга; околососудистые участки в головном мозге и спинном мозге; околоканальцевые (смежные с центральным каналом) участки в спинном мозге и участки пеневрия/эпиневрия вокруг корешков спинного мозга. Ни одно из таких изменений, связанных с rhASA, полученным по способу B, не характеризовалось тяжестью, которая, как разумно ожидали, могла бы изменить функцию нервной системы, и, на основании только строения, ни одно из таких изменений, связанных с rhASA, полученным по способу B, не рассматривалось как неблагоприятные эффекты. Наличие инфильтратов в спинном мозге согласовалось с тем, что было ожидаемо для животного с белком, введенным в интратекальное пространство.
[381] Средняя концентрация rhASA, полученного по способу B, составляла 544 нг/мл в сыворотке крови и 2185 нг/мл в CSF на 2 день; на 11 неделе она составляла 37 нг/мл в сыворотке крови и 171 нг/мл в CSF (фигура 2). У всех животных, которым вводили rhASA, вырабатывались антитела к лекарственному средству к 10 неделе с более высокими уровнями антител к лекарственному средству, наблюдаемыми в сыворотке крови, нежели в CSF (среднее значение: 391462 нг/мл по сравнению с 7383 нг/мл, соответственно); антитела к лекарственному средству не влияли на воздействие rhASA на целевые ткани, как подтверждено иммуногистохимическим исследованием и ELISA для тканей (данные не показаны).
Пример 4. Фармакокинетические/фармакодинамические профили рекомбинантной человеческой арилсульфатазы A у пациентов с MLD
[382] После интратекального введения пациентам с MLD изучали фармакокинетические/фармакодинамические (PK/PD) профили rhASA. Эффект rhASA в отношении уровней сульфатидов в спинномозговой жидкости (CSF) и изменения общего показателя шкалы оценки общей моторики-88 (GMFM-88) у пациентов с MLD, получающих rhASA, использовали для оценки его клинических эффектов и определения оптимального режима дозирования.
[383] Все пациенты получали rhASA раз в две недели в течение не более 338 недель через устройство для интратекальной доставки лекарственного средства (IDDD). Возраст пациентов в когортах 1, 2 и 3 составлял менее 12 лет на момент включения в первоначальное исследование с увеличением дозы, и они получали 10, 30 и 100 мг rhASA соответственно. Возраст пациентов в когорте 4 составлял менее 8 лет на момент включения, и они получали 100 мг rhASA, который изготавливали с применением проверенного способа. Все пациенты получали лекарственный препарат, составленный в виде 30 мг/мл rhASA в водном изотоническом растворе, содержащем 154 мМ хлорида натрия и 0,005% полисорбата 20, при pH 6,0, доставляемый с помощью IT введения через имеющееся на постоянной основе IDDD. Результаты нескольких оценок эффективности указывают на то, что rhASA может быть ассоциирован с замедлением прогрессирования заболевания.
[384] Пациенты, которые завершили исследование с увеличением дозы, могли продолжать получать rhASA раз в две недели через IDDD в течение расширенного исследования. Концентрацию rhASA в сыворотке крови оценивали после начальной дозы rhASA и на 38 неделе лечения. Пациенты в когорте 4 получали rhASA, который был изготовлен с применением проверенного способа. Образцы крови получали за ≤ 1 час до и через 0,5, 1, 2, 4, 8, 12, 24 и 48 часов после IT инъекции. Концентрацию rhASA в CSF оценивали каждые 2 или 4 недели во время исследования с увеличением дозы, и ежеквартально в недели 52-104, и два раза в год в недели 104-338 в расширенном исследовании. Наблюдения в отношении GMFM-88 оценивали на 0, 16, 24 и 40 неделях в исследовании с увеличением дозы, и ежеквартально в недели 52-104, и два раза в год в недели 104-338 в расширенном исследовании.
[385] Оценки включали возникшие во время лечения неблагоприятные явления (AE); биохимические анализы сыворотки; полученные данные электрокардиограммы (ECG) в 12 отведениях; основные показатели состояния организма; физические исследования; определения количества клеток, уровни глюкозы и белка в спинномозговой жидкости (CSF) и антитела к rhASA в CSF и сыворотке крови. AE определяли как все неблагоприятные явления, которые происходили в период времени от начальной дозы изучаемого продукта или хирургического вмешательства для внедрения устройства (в зависимости от того, что происходило раньше) и до последнего визита последующего наблюдения в исследовании. Последующую оценку выполняли через 4 недели после последней инъекции rhASA или через 2 недели после удаления последнего IDDD, в зависимости от того, что происходило позже, для пациентов, которых не включали в расширенное исследование. Для индивидуумов, которых включали в расширенное исследование последующую оценку выполняли при визите при окончании исследования (неделя 40).
[386] В отношении образцов сыворотки крови и CSF сперва проводили скрининг на антитела к лекарственному средству (ADA) с применением электрохемолюминесцентного мостикового иммуноферментного анализа (Meso Scale Diagnostics, LLC, Rockville, штат Мэриленд, США), в котором используют биотинилированный и меченный сульфогруппой rhASA для захвата и выявления соответственно. Положительные в отношении ADA образцы подтверждали с помощью конкурентного связывания лигандов с применением того же мостикового иммуноферментного анализа и впоследствии оценивали в отношении титра антител и нейтрализующей активности с применением анализа в отношении активности арилсульфатазы A с 4-нитрокатехинсульфатом в качестве субстрата.
[387] Оценивали фармакокинетические параметры rhASA в CSF и сыворотке крови после введения и изменения от исходного уровня в двигательной функции. Образцы сыворотки крови и CSF собирали от пациентов на неделе 0 (первая доза) и 38 (последняя доза). Концентрацию rhASA определяли с применением валидированных способов твердофазного иммуноферментного анализа. Изменение от исходного уровня в двигательной функции оценивали с применением общего показателя GMFM-88 (0-100%). Дополнительные конечные точки включали приведенные ниже. Уровни сульфатидов и лизосульфатидов в CSF, оцененные с помощью жидкостной хроматографии с тандемным масс-спектрометрическим обнаружением; уровни N-ацетиласпартата (NAA)/креатина и холина/креатина в глубоком белом и сером веществе головного мозга, оцененные с помощью спектроскопии протонного магнитного резонанса (MRS), изменение от исходного уровня в общем показателе тяжести MLD на основании магниторезонансной визуализации (MRI) головного мозга и функция переферических нервов, оцененная с помощью электронейрографии. Верхние пределы нормальных для CSF уровней сульфатидов и лизосульфатидов определяли как 0,113 мкг/мл и 0,0277 нг/мл соответственно на основании наивысшей концентрации, наблюдаемой в образцах от 60 детей, у которых не было лейкодистрофии, но которые прошли спинномозговую пункцию (и, следовательно, могут иметь другие неврологические состояния). Для каждого пациента проводили серийные измерения с помощью MRI головного мозга. На основании визуальной оценки способа MRI общий показатель тяжести MLD (диапазон: 0-34) рассчитывали для каждого индивидуума в каждый момент времени, где более высокие показатели указывали на более серьезное поражение головного мозга. Также проводили оценку функции периферических нервов с помощью электронейрографии. Измеряли скорость проводимости нерва, амплитуду, дистальную задержку и задержку F-зубца и трансформировали в z-показатели, если среднее значение и стандартное отклонение (SD) в популяции было доступно для подходящих возрастных диапазонов.
[388] Лечение с помощью rhASA хорошо переносилось, при этом никаких летальных исходов, никаких прерываний вследствие неблагоприятных явлений (AE) и никаких зарегистрированных опасных для жизни AE. IT rhASA, по-видимому, не обладает высоким иммуногенным потенциалом и, хотя у 10 пациентов вырабатывались индуцированные лечением антитела в сыворотке крови, не было корреляции между антителогенезом в сыворотке крови и AE.
[389] Концентрация rhASA медленно повышалась в сыворотке крови после IT введение (средний диапазон tmax 5,1-18,2 часа), при этом максимальная наблюдаемая концентрация в сыворотке крови (Cmax) и площадь под кривой зависимости концентрации в сыворотке крови от времени увеличивались относительно дозы. Концентрация rhASA, как правило, повышалась дозозависимым образом в CSF, при этом измеряемые концентрации, выявляемые при каждом визите перед введением дозы, позволяли предположить, что rhASA остается в CSF в течение 2 недель между дозами. Средние концентрации в CSF rhASA по когорте дозы и недели лечения представлены на фигуре 14. Фармакокинетические результаты были схожи у пациентов, которые получали 100 мг rhASA, изготовленного с применением либо способа A, либо способа B.
[390] Уменьшения среднего общего показателя GMFM-88 по сравнению с исходным уровнем наблюдали после лечения с помощью rhASA в каждой из четырех когорт (фигура 15). Среднее (SD) снижение на неделе 40 общего показателя GMFM-88 по сравнению с исходным уровнем в двух когортах со 100 мг (когорты 3 и 4) было схожим (-19,0 [16,12] по сравнению с -22,6 [25,48], соответственно). Однако, такие уменьшения были менее выраженными, чем таковые наблюдаемые в когортах с 10 мг и 30 мг (когорты 1 и 2; -29,2 [24,45] и -27,7 [17,76], соответственно). Изменение по сравнению с исходным уровнем общего показателя GMFM-88 с течением времени подытоживали в таблице 8. Снижения общей моторики, наблюдаемые у всех пациентов, показали тенденцию к меньшим ухудшениям по мере увеличения уровней доз rhASA. У пациентов, получающих 100 мг rhASA (когорта 3; способ A), показатель тяжести MLD оставался стабильным.
Таблица 8.

[391] Уровни сульфатидов в CSF оценивали в качестве индикатора активности лекарственного средства в ЦНС. Как показано на фигуре 16A, средние уровни сульфатидов в CSF упали ниже верхнего предела нормы к моменту окончания исследования в когортах 3 и 4 (0,07 [0,03] и 0,08 [0,03], соответственно). Уменьшения средних уровней лизосульфатидов в CSF также наблюдали во всех когортах с течением времени (фигура 16B). Средние уровни лизосульфатидов в CSF были стабильно ниже верхнего предела нормы с недели 2 в когорте 3, недели 4 в когорте 4 и недели 12 в когорте 2. Эти данные показывают, что rhASA является активным в ЦНС.
[392] Уровень NAA можно применять в качестве суррогатной оценки количества и/или плотности зрелых нейронов и аксонов, и при неврологических расстройствах сниженная концентрация NAA ассоциирована с повреждением и потерей нейронов и аксонов. Изменение соотношение NAA/креатина оценивали в качестве индикатора тяжести MLD у пациентов (фигура 17A). В белом веществе правой передней доли соотношение NAA/креатина, снижалось от исходного уровня до окончания исследования, хотя это было менее выражено для пациентов, которых лечили 30 мг или 100 мг rhASA (когорты 2-4) по сравнению с таковыми, которых лечили 10 мг (когорта 1) (фигура 17A). Подобные результаты были получены в белом веществе правой передней теменной доли и белом веществе правой затылочно-теменной доли (фигуры 18A и 19A). Соотношение NAA/креатина и доза rhASA в сером веществе показаны на фигуре 20A).
[393] Соотношение холина/креатина также оценивали во всех когортах. Было показано, что уровни холина у пациентов с MLD являются повышенными, и они могут возникать в результате повышения текучести мембраны, ассоциированного с деминерализацией. В белом веществе правой передней доли, белом веществе правой передней теменной доли и белом веществе правой затылочно-теменной доли соотношения холина/креатина стабильно повышались по сравнению с исходным уровнем у пациентов, которых лечили более низкими дозами (10 мг; когорта 1), но не было выраженной тенденции у тех, которых лечили 30 мг или 100 мг (когорты 2-4; фигура 17B, 18B и 19B). В сером веществе срединной затылочной доли соотношение холина/креатина было изменяющимся в когортах 1 и 2, но снижалось по сравнению с исходным уровнем в когорте 3 и оставалось стабильным в когорте 4 (фигура 20B).
[394] Средние общие показатели тяжести MLD повышались у пациентов, которых лечили 10 мг, 30 мг и 100 мг (B) rhASA с течением времени (когорты 1, 2 и 4), что указывало на прогрессирование заболевания (фигура 21). Наибольшее увеличение по сравнению с исходным уровнем было очевидным для пациентов, которые получали 10 мг rhASA (когорта 1; среднее изменение, 11,0). Напротив, средние общие показатели тяжести MLD оставались стабильными у пациентов, которых лечили 100 мг (A) rhASA (когорта 3), что может указывать на стабилизацию заболевания в ЦНС (фигура 21).
[395] Значительное ухудшение способности к нервной проводимости в медианном двигательном нерве возвышения большого пальца наблюдали на исходном уровне во всех когортах (таблица 9). Подобные результаты также обнаруживали в чувствительных нервах (данные не показаны). Функция нервов, по-видимому, не ухудшалась в четырех когортах в более поздние моменты времени.
Таблица 9. Z-показатели при визите для электронейрографии в медианном двигательном нерве возвышения большого пальца.
10 мг rhASA
EOW (n=6)
30 мг rhASA
EOW (n=6)
100 мг rhASA, EOW (n=6)
100 мг rhASA, EOW (n=6)
n
Среднее значение (SD)
Срединное значение
Диапазон
-7,9 (0,39)
-8,0
-8,4, -7,5
-6,9 (1,56)
-6,4
-9,4, -5,2
-5,6 (2,78)
-6,1
-8,3, -1,9
-6,7 (2,52)
-5,5
-10,5, -4,6
n
Среднее значение (SD)
Срединное значение
Диапазон
-8,3 (0,42)
-8,4
-8,7, -7,9
-7,3 (1,73)
-7,3
-9,4, -4,3
-5,0 (4,52)
-5,9
-10,5, 1,7
-7,7 (2,19)
-7,3
-10,5, -5,5
n
Среднее значение (SD)
Срединное значение
Диапазон
-8,3 (0,33)
-8,2
-8,6, -7,9
-6,3 (2,54)
-7,3
-8,5, -2,0
-6,4 (4,74)
-7,6
-10,5, 0,2
-6,6 (1,36)
-7,2
-7,7, -4,6
n
Среднее значение (SD)
Срединное значение
Диапазон
-8,2 (0,19)
-8,2
-8,4, -8,1
-7,1 (1,67)
-7,5
-8,5, -4,3
-5,5 (3,86)
-6,3
-10,2, -0,9
-6,9 (2,54)
-6,0
-10,5, -4,0
n
Среднее значение (SD)
Срединное значение
Диапазон
-1,6 (0,45)
-1,8
-2,0, -0,9
-1,3 (1,11)
-1,7
-2,6, 0,1
-1,3 (0,29)
-1,2
-1,6, -0,8
-0,9 (0,46)
-1,0
-1,5, -0,3
n
Среднее значение (SD)
Срединное значение
Диапазон
-1,6 (0,62)
-1,9
-2,1, -0,4
-1,5 (0,43)
-1,4
-2,2, -1,1
-1,1 (0,75)
-1,5
-1,6, 0,1
-1,3 (0,24)
-1,3
-1,4, -0,9
n
Среднее значение (SD)
Срединное значение
Диапазон
-1,5 (0,79)
-1,7
-2,0, -0,1
-1,4 (0,56)
-1,4
-2,2, -0,8
-1,5 (0,57)
-1,2
-2,3, -1,1
-0,7 (0,46)
-0,9
-1,1, 0,1
n
Среднее значение (SD)
Срединное значение
Диапазон
-1,5 (0,84)
-1,9
-2,2, -0,6
-1,3 (0,46)
-1,4
-1,6, -0,5
-1,1 (0,43)
-1,1
-1,6, -0,5
-1,0 (0,38)
-0,9
-1,4, -0,5
n
Среднее значение (SD)
Срединное значение
Диапазон
15,3 (5,35)
14,9
8,7, 23,8
8,2 (5,69)
5,9
3,3, 17,5
10,3 (9,76)
8,0
-0,8, 23,1
5,8 (3,49)
4,7
3,0, 11,9
n
Среднее значение (SD)
Срединное значение
Диапазон
12,9 (4,26)
12,4
7,2, 19,8
8,1 (4,82)
6,8
4,0, 17,0
8,1 (8,33)
6,1
-0,3, 19,3
8,8 (5,35)
7,7
4,0, 15,9
n
Среднее значение (SD)
Срединное значение
Диапазон
12,9 (4,63)
10,5
9,4, 20,5
7,9 (4,94)
6,7
4,2, 16,3
6,7 (6,54)
5,9
-0,1, 15,0
6,8 (4,68)
4,3
2,4, 13,1
n
Среднее значение (SD)
Срединное значение
Диапазон
13,8 (5,79)
11,0
10,0, 20,5
8,6 (5,66)
6,1
3,1, 14,9
7,4 (7,07)
7,0
-0,8, 17,5
7,1 (8,17)
3,8
2,4, 21,7
n
Среднее значение (SD)
Срединное значение
Диапазон
40,0 (25,02)
40,0
22,4, 57,7
19,4 (14,99)
27,8
2,1, 28,3
11,1 (17,54)
11,1
-1,3, 23,5
14,5 (18,54)
6,3
2,8, 47,1
n
Среднее значение (SD)
Срединное значение
Диапазон
48,0 (20,74)
59,5
24,1, 60,4
22,3 (16,67)
30,2
3,1, 33,5
4,6 (8,23)
4,6
-1,3, 10,4
26,2 (22,46)
17,3
9,6, 51,8
n
Среднее значение (SD)
Срединное значение
Диапазон
39,2 (21,07)
39,2
24,3, 54,1
22,6 (19,87)
23,4
2,5, 41,1
4,4 (8,53)
4,4
-1,6, 10,4
4,8 (2,12)
4,8
3,3, 6,3
n
Среднее значение (SD)
Срединное значение
Диапазон
52,3 (N/A)
52,3
52,3, 52,3
27,3 (23,40)
23,4
2,6, 60,4
4,6 (8,80)
4,6
-1,6, 10,8
6,3 (3,31)
6,3
3,0, 9,6
[396] В нескольких исследованиях также сообщалось об изменениях уровней метаболита в ЦНС у пациентов с неврологическими расстройствами, включая MLD. Например, снижения концентрации NAA ассоциированы с повреждением и потерей нейронов и аксонов, тогда как было показано, что уровни холина являются повышенными у пациентов с MLD. Как и ожидалось, авторы настоящего изобретения обнаружили, что соотношение NAA/креатина, как правило, снижается с течением времени в белом веществе головного мозга. Однако, это было менее выражено с дозами, составляющими 100 мг, нежели 10 мг или 30 мг, что потенциально указывает на меньшее повреждение нейронов при наивысшей дозе. Кроме того, соотношение холина/креатина в белом веществе головного мозга стабильно повышалось по сравнению с исходным уровнем у пациентов, которых лечили наименьшей дозой (10 мг; когорта 1), но результаты были более изменчивыми у пациентов, которых лечили наивысшими дозами. Авторы настоящего изобретения в своем исследовании не наблюдали никаких явных тенденций в отношении уровней других метаболитов, в том числе лактата, мио-инозитола и глутамина+глутамата. Для того, чтобы четко установить влияние лечения с помощью rhASA может потребоваться проведение анализов уровней метаболитов у большего количества пациентов и в разных участках головного мозга.
[397] В целом, эти обнаружения указывают на то, что IT лечение с помощью rhASA может быть ассоциировано со стабилизацией заболевания в ЦНС, в частности в дозе, составляющей 100 мг, EOW. Однако, малый размер выборки означает, что результаты, полученные авторами настоящего изобретения, должны интерпретироваться с осторожностью. В частности, количество пациентов с данными, доступными в каждый момент времени, варьирующихся для некоторых параметров и дополнительных исследований, потребуется в течение более длительного периода времени и большее количество пациентов для установления долговременной эффективности rhASA у пациентов с MLD. Кроме того, в возрасте включения между пациентами и когортами наблюдалась некоторая изменчивость, которая могла иметь последствия для сравнения ответов на лечение между различными группами доз. Подобным образом, данные об уровнях метаболитов, полученных с помощью MRS, не нормализовали с учетом возраста пациента.
[398] Несмотря на такие ограничения из обнаружений, полученных авторами настоящего изобретения, видно, что IT rhASA у детей с MLD в целом хорошо переносится. Хотя в целом наблюдалось ухудшение двигательной функции с течением времени, существовало доказательство сниженного прогрессирования заболевания у пациентов, которые получали rhASA, в частности при наивысшей дозе. Продолжали расширенное исследование для оценки долговременной безопасности, иммуногенности и клинических исходов, ассоциированных с лечением с помощью rhASA, и для дальнейшего исследования в клинической фазе rhASA при наивысших дозах начнут набирать пациентов в ближайшее время. Предполагают, что результаты таких исследований помогут определить дозирование и установить можно ли рассматривать rhASA в качестве потенциального лечения для пациентов с MLD в будущем.
Пример 5. Моделирование и имитация рекомбинантной человеческой арилсульфатазы A у пациентов с MLD
[399] Данные клинического исследования, описанного в примере 4, применяли для фармакокинетических (PD) и фармакодинамических (PD) моделирования и имитации рекомбинантной человеческой арилсульфатазы A у пациентов с MLD. Как описано на фигуре 5, для анализа в отношении PK-параметров все пациенты получали по меньшей мере одну дозу rhASA и имели по меньшей мере одно измерение концентрации rhASA в сыворотке крови или CSF. Для анализа в отношении PK/PD-параметров: все пациенты с оценкой PK-параметров, доступной из анализа в отношении PK-параметров и с по меньшей мере одним доступным измерением уровня сульфатидов в CSF или общего показателя GMFM-88. Популяционную модель PK-параметров на основе концентраций rhASA в сыворотке крови и CSF разрабатывали как показано на фигуре 6. Элиминацию rhASA представляли двумя моделями с компартментами в центральной нервной системе (ЦНС) с объемами распределения, VЦНС и VCSF, и межкомпартментным клиренсом, QCSF. Гипотетический переходный компартмент использовали для определения характеристик клиренса rhASA из CSF и его отсроченного появления в сыворотке крови.
[400] Были смоделированы взаимозависимости PK/PD, в том числе эффект rhASA на концентрацию сульфатидов, измеренный в CSF, и взаимосвязь воздействие-ответ (E-R) rhASA в отношении общего показателя GMFM-88. PK-промотор для взаимозависимости PK/PD представлял собой специфичные в отношении пациента непрерывные во времени PK-профили в CSF и ЦНС. PD эффекты моделировали последовательно и все связанные с PK-параметры фиксировали во время оценки PD параметров. Измерение уровня сульфатидов в CSF за период времени характеризовали с применением непрямой PK/PD модели ответа с rhASA, смоделированным в качестве увеличения элиминации сульфатида. Предсказанную согласно популяционной PK-модели концентрацию rhASA в компартменте ЦНС применяли в качестве ведущего элемента PD ответа. Взаимосвязь E-R воздействия rhASA согласно общему показателю GMFM-88 оценивали с применением модели бета-регрессии, ограниченной функцией логит-связи для ограничения предсказаний модели, лежащей в пределах диапазона 0-100%.
[401] Популяционные PK, PK/PD и E-R модели применяли для моделирования ожидаемых профилей rhASA зависимости концентрации от времени и общих показателей GMFM-88. Имитировали 750 профилей пациентов; произвольным образом равномерно отбирали 250 образцов для каждой возрастной группы. Все из массива данных, графиков и сводных таблиц получали с применением R (v3.3 или более поздняя; Lucent Technologies, Суиндон, Великобритания; http://www.rproject.org). Анализ популяционного PK, PK/PD и E-R моделирования и имитации проводили с применением программного обеспечения NONMEM (v7.3 или более поздняя; ICON Development Solutions, Ellicott City, штат Мэриленд, США).
[402] Как показано на фигуре 8, применяли четыре разных сценария введения доз. Сценарий 1 включал 100 мг раз в две недели, сценарий 2 включал 100 мг каждую неделю в течение 12 недель (первоначальное еженедельное введение дозы), затем 100 мг раз в две недели; сценарий 3 включал 150 мг каждую неделю в течение 12 недель (первоначальное еженедельное введение дозы), затем 150 мг раз в две недели, и сценарий 4: стандартизированное по возрасту еженедельное введение дозы в течение 12 недель (первоначальное еженедельное введение дозы), затем раз в две недели (сценарий 4: 80 мг, < 8 месяцев; 120 мг, 8 - < 30 месяцев; 150 мг, ≥ 30 месяцев). Все из массива данных, графиков и сводных таблиц получали с применением R (v3.3 или выше; Lucent Technologies, Суиндон, Великобритания; http://www.rproject.org). Имитировали 750 профилей пациентов; произвольным образом равномерно отбирали 250 образцов для каждой возрастной группы. Анализ популяционного PK, PK/PD и E-R моделирования и имитации проводили с применением программного обеспечения NONMEM (v7.3 или более поздняя; ICON Development Solutions, Ellicott City, штат Мэриленд, США).
[403] Пациентов (n=24) равномерно распределяли по четырем когортам. На исходном уровне средний возраст пациентов составлял 44,9 (стандартное отклонение [SD], 22,8; диапазон, 19,0-107,0) месяца, и средний вес составлял 15,4 (SD, 4,14; диапазон, 10,5-24,8) кг.
[404] Фиксированные эффекты оценивали с хорошей точностью, за исключением пропорциональных коэффициентов VCSF (76,1% RSE), VЦНС (121% RSE) и Ktrans (40,2% RSE). Точность оценочной межиндивидуальной вариабельности была низкой. Модель предполагала быстрое распределение rhASA в ткани головного мозга и системном кровотоке: медианный распределительный период полужизни rhASA в ЦНС составлял 1,02 (диапазон, 0,394-1,66) часа, и медианный период полужизни распределения из CSF в сыворотку крови составлял 1,19 (диапазон, 0,555-2,09) часа. Однако, медианный конечный период полужизни rhASA в ЦНС составлял примерно 20 дней (477 [диапазон, 256-1010] часов) (таблица 10). Медианная константа скорости перехода (выраженная как переходной период полужизни), составляющая 1,19 (диапазон, 0,555-2,09) часа, согласовалась с физиологической обработкой CSF (примерно 6 часов).
Таблица 10. Сводные статистические данные по оценкам отдельных PK-параметров
ЦНС, центральная нервная система; CSF, спинномозговая жидкость; PK, фармакокинетический; 0CSF; межкомпартментный клиренс в ЦНС; rhASA, рекомбинантная человеческая арилсульфатаза A; SD, стандартное отклонение
[405] Наблюдали зависимое от концентрации снижение уровней сульфатидов в CSF (установленная модель EC50: 184 нг/мл rhASA с крутым склоном, составляющим 3,59) и зависимое от концентрации подавление потери общей моторики (установленная модель IC50: 120 нг/мл rhASA, с пологим склоном, составляющим 0,554, в ткани головного мозга). Графики точности подбора предсказанных концентраций rhASA для популяции и индивидуума в CSF, концентрация сульфатидов в CSF и общие показатели GMFM-88 показаны на фигурах 7A, B и C соответственно. Все три модели показывают приемлемую характеристику наблюдаемых концентраций rhASA; точность моделей варьировала, что могло быть обусловлено небольшим количеством пациентов, включенных в исследование. Срединные имитационные остаточные концентрации rhASA перед введением дозы в CSF и ЦНС для четырех сымитированных сценариев введения доз показаны на фигуре 8.
[406] При 100 мг раз в две недели (сценарий 1) занимает примерно 16 недель для достижения сравнительно устойчивых PK-параметров, в соответствии со срединным элиминационными периодом полужизни rhASA, составляющим 477 часов. При 100 мг или 150 мг с введением раз в неделю в течение 12 недель с последующим введением доз раз в две недели (сценарии 2 и 3), достигали более высоких концентраций rhASA в CSF и ЦНС по сравнению со сценарием 1. Сценарий с введением доз в зависимости от возраста (сценарий 4) показал более стабильные сравнительно устойчивые остаточные концентрации rhASA с течением времени для всех трех возрастных групп. Однако, пациенты возрастом менее 8 месяцев не достигали таких же высоких остаточных концентраций rhASA во время фазы еженедельного введения как в сценариях 2 и 3.
[407] Имитации общего показателя GMFM-88 показали прогнозируемую стабилизацию с течением времени у некоторых пациентов (фигура 9), что согласуется с наблюдаемыми результатами клинического исследования. Сценарии 1-3 прогнозировали, что некоторые пациенты во всех группах продемонстрируют ранний ответ на лечение. Сценарий 3 прогнозирует наибольшее количество пациентов с общими показателями GMFM-88 выше 35 или 50 через 12 месяцев и 24 месяца соответственно. Введение дозы в зависимости от возраста (сценарий 4) прогнозировало, что меньшее количество пациентов в группах < 8 месяцев и 8 - < 30 месяцев будет отвечать на лечение, нежели в группе > 30 месяцев.
[408] Доставка rhASA с помощью IDDD может снижать уровни сульфатидов в CSF и замедлять скорость потери двигательной функции зависимым от дозы и воздействия образом у пациентов с MLD. Подходы с фармакокинетическим моделированием применяли для прогнозирования популяционных PK, PK/PD и E-R взаимозависимостей с общим показателем GMFM-88. Во всех случаях модели обеспечивали хорошее определение характеристик измерений, наблюдаемых у пациентов, получающих rhASA. С учетом небольшого количества пациентов изменчивость, наблюдаемая в отношении концентраций rhASA в CSF, и что концентрации в CSF наблюдали только в моменты времени до введения дозы, точность между различными моделями варьировалась. Однако, модель обеспечивала быстрое распределение rhASA в ткани головного мозга и системном кровотоке, но медленный конечный элиминационный период полужизни из ЦНС.
Пример 6. Анализ ответивших и неответивших пациентов на интратекальную доставку рекомбинантной человеческой арилсульфатазы A у детей с поздней младенческой формой метахроматической лейкодистрофии.
[409] Как показано на фигуре 10, пациенты получали rhASA с помощью устройства для интратекальной доставки лекарственного средства (IDDD) раз в две недели в течение недель 0-38. Когорта 1 (n=6) получала 10 мг rhASA, когорта 2 (n=6) получала 30 мг rhASA, когорта 3 (n=6) получала 100 мг rhASA, и когорта 4 (n=6) получала 100 мг rhASA, который получали с применением проверенного способа изготовления.
[410] Критерии отбора для когорт 1-4 включали в себя подтвержденный диагноз MLD (на основании дефицита ASA, оцениваемого с применением анализа в отношении лейкоцитов и повышенной концентрации сульфатидов в моче); первое проявление симптомов MLD в возрасте 30 месяцев или ранее; неврологический признаки MLD, присутствующие на момент скринингового обследования; ходячий (способный идти вперед на 10 шагов с одной удерживаемой рукой) на момент скрининга. Возраст пациентов, включенных в когорты 1-3, также составлял менее 12 лет на момент скрининга. Дополнительные критерии отбора для пациентов когорты 4 включали в себя общий показатель шкалы оценки общей моторики-88 (GMFM-88), составляющий по меньшей мере 40 на момент скрининга и по меньшей мере 35 при исходном уровне, и возраст менее 8 лет на момент скрининга.
[411] Каждому пациенту имплантировали хирургическим путем IDDD (PORT-A-CATH® II [Smiths Medical ASD, Inc., St Paul, штат Миннесота, США] или SOPH-A-PORT® Mini S [Sophysa, Орсе, Франция]) перед предоставлением им первой дозы rhASA. Местонахождение IDDD подтверждали после операции. Ответы на лечение оценивали post hoc у пациентов из когорт 3 и 4 с применением общего показателя GMFM-88 (0-100%), (Bjornson KF et al. Pediatr Phys Ther 1998;10:43-7), который предусматривал индикатор двигательной функции.
[412] Ответивших пациентов определяли как индивидуумов с исходным уровнем общего показателя GMFM-88, составляющим ≥ 35, и сохраняемым (снижение общего показателя GMFM-88 на ≤ 10) или увеличенным общим показателем GMFM-88 на момент окончания исследования относительно исходного уровня. Неответивших пациентов определяли как индивидуумов, которые не соответствуют данному критерию. Другие оцениваемые ключевые исходы включали в себя изменение концентрации сульфатидов в спинномозговой жидкости (CSF), изменение тяжести MLD, измеренное с помощью магниторезонансной визуализации (MRI) головного мозга с применением схожего способа оценки в баллах по Eichler et al. (Giugliani R et al. JIEMS 2017;5:314:A699) с получением показателя тяжести MLD-MRI, изменение уровней N-ацетиласпартата (NAA) в белом веществе головного мозга, оцененное с помощью магнитно-резонансной спектроскопии (MRS). На фигуре 22 показан индивидуальный общий показатель GMFM-88 по возрасту в месяцах единокровных пар пациентов из клинического исследования rhASA. По-видимому, биомаркеры и ответ двигательной функции совместно улучшаются. Дополнительно, по-видимому, уровни сульфатидов в CSF и NAA MRS совместно улучшаются. Ответ двигательной функции ассоциировался с зависимым от дозы снижением уровня накопленных сульфатидов в CSF.
[413] Из 12 пациентов, включенных в NCT01510028, которые получали 100 мг rhASA, четырех индивидуумов идентифицировали как ответивших пациентов: два из когорты 3 и два из когорты 4. Оставшихся восьми пациентов в когортах 3 и 4 идентифицировали как неответивших пациентов. На фигуре 11 показаны общие показатели GMFM-88 с течением времени для 12 пациентов. Демографические данные и исходные характеристики для четырех ответивших пациентов показаны в таблице 11.
Таблица 11. Демографические данные и исходные характеристики для индивидуумов, идентифицированных как ответившие пациенты
CSF, спинномозговая жидкость; GMFM-88, шкала оценки общей моторики-88; MLD, метахроматическая лейкодистрофия, MRS, магнитно-резонансная спектроскопия, NAA, N-ацетиласпартат.
[414] Ответившие пациенты 1, 2 и 3 имели концентрацию сульфатидов в CSF ниже верхнего предела нормы (0,113 мкг/мл) через 1 месяц; никакой информации последующего наблюдения в отношении концентрации сульфатидов в CSF не было доступно для ответившего пациента 4. На момент окончания исследования (неделя 40) сообщали, что концентрация сульфатидов в CSF составляла 0,0294 мкг/мл, 0,0489 мкг/мл и 0,0653 мкг/мл у ответивших пациентов 1, 2 и 3 соответственно.
[415] Один пациент из восьми неответивших пациентов имел концентрацию сульфатидов в CSF ниже верхнего предела нормы через 1 месяц. Значения концентраций сульфатидов в CSF падали ниже верхнего предела нормы через 8-36 недель у остальных пациентов. Один индивидуум из когорты 1 также соответствовал post hoc критериям ответившего пациента без уровней сульфатидов в CSF, нормализующихся к окончанию исследования.
[416] Показатель тяжести MLD-MRI от исходного уровня до недели 40 снижался у двух ответивших пациентов и повышался у одного из ответивших пациентов (фигура 12). Информация в отношении показателя тяжести MLD-MRI на момент окончания исследования не была доступна для ответившего пациента 4. Два из четырех ответивших пациентов имели соотношение NAA/креатина в белом веществе передней теменной доли, составляющее ≥ 1,0 на исходном уровне. Ни один из восьми неответивших пациентов, для которых были доступны исходные данные, не имел соотношение NAA/креатина на исходном уровне, составляющее ≥ 1,0.
[417] Соотношение NAA/креатина в белом веществе передней теменной доли повышалось на неделе 40 по сравнению с исходным уровнем у одного из ответивших пациентов и оставалось стабильным у двух других ответивших пациентов, для которых данные были доступны на исходном уровне и на неделе 40 (фигура 13).
[418] Четырех из двенадцати пациентов, которые получали 100 мг rhASA, идентифицировали как таких, которые ответили на лечение; возраст и исходные характеристики изменялись среди ответивших на лечение. Из этих обнаружений видна тенденция к стабилизации заболевания в подгруппе пациентов, которые получали наивысшую дозу и сохранению разработки интратекальной терапии с помощью rhASA для пациентов с LI-MLD. Факторы, которые влияют на ответ на лечение могут включать в себя концентрацию rhASA в CSF, исходное соотношение NAA/креатина, стабилизацию соотношения NAA/креатина, продолжительность заболевания, возраст и время, необходимое для уровней сульфатидов в CSF, чтобы прийти в норму.
Пример 7. Вводимая интратекально рекомбинантная человеческая арилсульфатаза A пациентам с поздней младенческой формой метахроматической лейкодистрофии
[419] Дефицит лизосомального фермента арилсульфатазы A при MLD приводит к накоплению сульфатированных гликосфинголипидов, в совокупности известных как сульфатиды. Они накапливаются в, и являются токсичными для, клетках, которые сохраняют миелиновую изолирующую оболочку аксонов как центральной, так и периферической нервных систем. IT введение рекомбинантной человеческой арилсульфатазы A может быть достаточным для гидролиза накопленных сульфатидов в клетках нервной системы и может замедлить или предотвратить дополнительное накопление, которое должно обуславливать благоприятное воздействие в отношении двигательной системы. Прямое введение в ЦНС посредством, например, IT доставки можно использовать для эффективного лечения пациентов с MLD. Данный пример иллюстрирует многоцентровое открытое клиническое исследование с сопоставимыми историческими контролями, разработанное для оценки эффективности введения интратекальной дозы, составляющей 150 мг rhASA, один раз в неделю пациентам с поздней младенческой формой MLD. В этом исследовании будет изучаться потенциал вводимых IT 150 мг rhASA для стабилизации или замедления прогрессирования двигательной дисфункции у субъектов детского возраста с поздней младенческой формой MLD.
[420] Примерно 35 пациентов будут включены для оценки безопасности и переносимости rhASA и его доставки с помощью устройства для интратекальной доставки лекарственного средства SOPH-A-PORT Mini S. Скорость и тяжесть прогрессирования заболевания точно задокументированы для поздней младенческой формы MLD. Отличительным признаком определения поздней младенческой формы MLD является ранний возраст возникновения симптомов заболевания, при этом у большей части пациентов с поздней младенческой формой MLD первые признаки двигательной дисфункции проявляются в возрасте до 18 месяцев. Четыре группы лечения будут включать на основании возраста и степени двигательной дисфункции на момент включения:
группа A - клинические проявления на ранней стадии (18-48 месяцев; классификация общей моторики согласно MLD [GMFC-MLD] уровень 1-2; n=16),
группа B - клинические проявления на средней стадии (18-72 месяца; уровень GMFC-MLD 3; n≤8),
группа C - клинические проявления на поздней стадии (18-72 месяца; уровень GMFC MLD 4; n≤8), и
группа D - на предсимптоматической стадии или с клиническими проявлениями на минимальном уровне (<18 месяцев; единокровные родственники на предсимптоматической стадии из участников, с одинаковым аллельным строением ASA; n=3).
[421] Возникновение симптомов должно быть до 30 месяцев в группах A-C. Все субъекты получали дозу IT rhASA, составляющую 150 мг, один раз в неделю в течение 105 недель. Исследование будет оценивать безопасность и эффективность схемы лечения в отношении общей моторики с применением GMFC-MLD и общего показателя GMFM-88 для измерения прогрессирования заболевания. Субъектов группы D будут оценивать с помощью Альбертской шкалы двигательной функции у младенцев (Piper and Darrah, 1994). Первичной конечной точкой будет доля детей в группе A с увеличением их уровня GMFC-MLD (указывающим на ухудшение двигательной функции) на не более чем 2 уровня от исходного уровня за 2 года. Вторичной конечной точкой будет доля детей в группе A с общим показателем шкалы оценки общей моторики-88, составляющим >40, через 2 года.
[422] Другие вторичные конечные точки будут включать оценивание эффектов IT введения rhASA в отношении периода времени до ухудшения общей моторики с применением GMFC-MLD; оценивание эффектов IT введения rhASA в отношении периода времени до ухудшения общей моторики с применением GMFM-88; оценивание эффектов IT введения rhASA в отношении экспрессивной речи с применением классификации функции экспрессивной речи (ELFC-MLD); оценивание эффектов IT введения rhASA в отношении биомаркеров в спинномозговой жидкости (CSF) (т. е. уровней сульфатидов) и оценивание эффектов IT введения rhASA в отношении спектроскопии протонного магнитного резонанса (MRS) головного мозга, в частности N-ацетиласпартата/креатина (NAA/Cr) в белом веществе. Исходы будут сравниваться с подобранными по показателю предрасположенности историческими контрольными данными у детей с MLD.
[423] Безопасность и переносимость IT rhASA будут основаны на частоте возникновения возникших во время лечения неблагоприятных явлений (TEAE), клинических лабораторных исследованиях (биохимический анализ сыворотки крови, общий анализ крови и анализ мочи) и основных показателях состояния организма, физическом исследовании, включающем задокументированные признаки и симптомы MLD, электрокардиограмму (ECG) с 12 отведениями, лабораторные параметры CSF (химические анализы и определения количества клеток), наличие и активность антител к rhASA в CSF и сыворотке крови и устройство SOPH-A-PORT® Mini S у субъектов с MLD.
[424] Дополнительные оценки эффектов введения IT rhASA могут основываться на биомаркерах в сыворотке крови и моче (т. е. уровнях сульфатидов), показателе тяжести, который измеряют по магниторезонансной визуализации (MRI) головного мозга, объемном анализе на основе MRI головного мозга, способности к глотанию, которую оценивают по эндоскопическому оцениванию глотания с помощью волокно-оптической системы (FEES), проводимости нервов по электронейрографии (ENG) и способности к коммуникации и распознаванию с применением реестра развития от Battelle (BDI-2NU). Нагрузка на опекуна и связанное с состоянием здоровья субъекта качество жизни, влияющие на ребенка с MLD, будут исследоваться путем оценки нагрузки на опекуна, которую проводят согласно опроснику влияния на опекуна (CIQ), и связанное с состоянием здоровья качество жизни (HRQOL), которое оценивают согласно пунктам Infant Toddler Quality of Life Questionnaire- 97 (ITQOL-97).
[425] Первичная конечная точка эффективности представляет собой ответ в группе A, определенный как сохранение общей моторики через 2 года (неделя 106), оцениваемое как изменение от исходного уровня на не более чем 2 уровня согласно GMFC-MLD. Ключевая вторичная конечная точка эффективности в группе A представляет собой сохранение общей моторики через 2 года (неделя 106), оцениваемое как общий показатель GMFM-88, составляющий >40. Эффективность rhASA будут оценивать путем сравнения включенных субъектов в группу A с субъектами сопоставимого исторического контроля. Данные от этих не подвергшихся лечению субъектов с MLD (т. е. субъектов, которые не получали исследовательских продукта или терапии) будут взяты из продолжающегося исследования естественного течения с помощью программы Global Leukodystrophy Initiative (GLIA-MLD). Также можно применять дополнительные сопоставимые исторические данные от субъектов с MLD, подвергшихся воздействию rhASA перед оценочным исследованием. Сопоставимые исторические контроли согласно GLIA-MLD и перед исследованиями Shire должны иметь данные для по меньшей мере исходного уровня и 1 оценки общей моторики после исходного уровня. Эти контроли будут иметь очень похожие критерии включения/исключения как включенные субъекты по настоящему исследованию и сравнимую оценку эффективности в подобные моменты времени.
[426] Несмотря на то, что несколько вариантов осуществления настоящего изобретения были описаны и проиллюстрированы в данном документе, специалистами в данной области будут легко предусмотрены различные другие средства и/или структуры для выполнения функции, и/или получение результатов и/или одно или более из преимуществ, описанных в данном документе, и каждое из таких изменений и/или модификаций рассматривается как находящиеся в пределах объема вариантов осуществления настоящего изобретения, описанных в данном документе. В более общем смысле, специалисты в данной области легко поймут, что все параметры, размеры, материалы и конфигурации, описанные в данном документе, предназначены для иллюстративного описания и что фактические параметры, размеры, материалы и/или конфигурации будут зависеть от конкретных применения или путей применения, для которого/которых идеи настоящего изобретения используются. Специалист в данной области поймет или сможет определить с применением лишь обычных экспериментов множество эквивалентов конкретных вариантов осуществления настоящего изобретения, описанных в данном документе. Таким образом, следует понимать, что вышеприведенные варианты осуществления представлены только в качестве примеров, и что в пределах объема прилагаемой формулы изобретения и ее эквивалентов, варианты осуществления настоящего изобретения могут быть реализованы на практике иным образом, как описано и заявлено. В соответствии с настоящим изобретением варианты осуществления настоящего описания направлены на каждое отдельное свойство, систему, изделие, материал, набор и/или способ, описанные в данном документе. Кроме того, любая комбинация двух или более таких свойств, систем, изделий, материалов, наборов и/или способов, если такие свойства, системы, изделия, материалы, наборы и/или способы не являются взаимоисключающими, включены в объем настоящего изобретения по настоящему изобретению.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SHIRE HUMAN GENETIC THERAPIES, INC.
<120> ОЧИЩЕННАЯ АРИЛСУЛЬФАТАЗА A И КОМПОЗИЦИИ НА ЕЕ ОСНОВЕ
<130> SHR-1320WO
<140> PCT/US2018/066583
<141> 2018-12-19
<150> 62/760,597
<151> 2018-11-13
<150> 62/625,814
<151> 2018-02-02
<150> 62/608,569
<151> 2017-12-20
<150> 62/607,831
<151> 2017-12-19
<160> 3
<170> PatentIn версия 3.5
<210> 1
<211> 489
<212> Белок
<213> Homo sapiens
<400> 1
Arg Pro Pro Asn Ile Val Leu Ile Phe Ala Asp Asp Leu Gly Tyr Gly
1 5 10 15
Asp Leu Gly Cys Tyr Gly His Pro Ser Ser Thr Thr Pro Asn Leu Asp
20 25 30
Gln Leu Ala Ala Gly Gly Leu Arg Phe Thr Asp Phe Tyr Val Pro Val
35 40 45
Ser Leu Cys Thr Pro Ser Arg Ala Ala Leu Leu Thr Gly Arg Leu Pro
50 55 60
Val Arg Met Gly Met Tyr Pro Gly Val Leu Val Pro Ser Ser Arg Gly
65 70 75 80
Gly Leu Pro Leu Glu Glu Val Thr Val Ala Glu Val Leu Ala Ala Arg
85 90 95
Gly Tyr Leu Thr Gly Met Ala Gly Lys Trp His Leu Gly Val Gly Pro
100 105 110
Glu Gly Ala Phe Leu Pro Pro His Gln Gly Phe His Arg Phe Leu Gly
115 120 125
Ile Pro Tyr Ser His Asp Gln Gly Pro Cys Gln Asn Leu Thr Cys Phe
130 135 140
Pro Pro Ala Thr Pro Cys Asp Gly Gly Cys Asp Gln Gly Leu Val Pro
145 150 155 160
Ile Pro Leu Leu Ala Asn Leu Ser Val Glu Ala Gln Pro Pro Trp Leu
165 170 175
Pro Gly Leu Glu Ala Arg Tyr Met Ala Phe Ala His Asp Leu Met Ala
180 185 190
Asp Ala Gln Arg Gln Asp Arg Pro Phe Phe Leu Tyr Tyr Ala Ser His
195 200 205
His Thr His Tyr Pro Gln Phe Ser Gly Gln Ser Phe Ala Glu Arg Ser
210 215 220
Gly Arg Gly Pro Phe Gly Asp Ser Leu Met Glu Leu Asp Ala Ala Val
225 230 235 240
Gly Thr Leu Met Thr Ala Ile Gly Asp Leu Gly Leu Leu Glu Glu Thr
245 250 255
Leu Val Ile Phe Thr Ala Asp Asn Gly Pro Glu Thr Met Arg Met Ser
260 265 270
Arg Gly Gly Cys Ser Gly Leu Leu Arg Cys Gly Lys Gly Thr Thr Tyr
275 280 285
Glu Gly Gly Val Arg Glu Pro Ala Leu Ala Phe Trp Pro Gly His Ile
290 295 300
Ala Pro Gly Val Thr His Glu Leu Ala Ser Ser Leu Asp Leu Leu Pro
305 310 315 320
Thr Leu Ala Ala Leu Ala Gly Ala Pro Leu Pro Asn Val Thr Leu Asp
325 330 335
Gly Phe Asp Leu Ser Pro Leu Leu Leu Gly Thr Gly Lys Ser Pro Arg
340 345 350
Gln Ser Leu Phe Phe Tyr Pro Ser Tyr Pro Asp Glu Val Arg Gly Val
355 360 365
Phe Ala Val Arg Thr Gly Lys Tyr Lys Ala His Phe Phe Thr Gln Gly
370 375 380
Ser Ala His Ser Asp Thr Thr Ala Asp Pro Ala Cys His Ala Ser Ser
385 390 395 400
Ser Leu Thr Ala His Glu Pro Pro Leu Leu Tyr Asp Leu Ser Lys Asp
405 410 415
Pro Gly Glu Asn Tyr Asn Leu Leu Gly Gly Val Ala Gly Ala Thr Pro
420 425 430
Glu Val Leu Gln Ala Leu Lys Gln Leu Gln Leu Leu Lys Ala Gln Leu
435 440 445
Asp Ala Ala Val Thr Phe Gly Pro Ser Gln Val Ala Arg Gly Glu Asp
450 455 460
Pro Ala Leu Gln Ile Cys Cys His Pro Gly Cys Thr Pro Arg Pro Ala
465 470 475 480
Cys Cys His Cys Pro Asp Pro His Ala
485
<210> 2
<211> 507
<212> Белок
<213> Homo sapiens
<400> 2
Met Gly Ala Pro Arg Ser Leu Leu Leu Ala Leu Ala Ala Gly Leu Ala
1 5 10 15
Val Ala Arg Pro Pro Asn Ile Val Leu Ile Phe Ala Asp Asp Leu Gly
20 25 30
Tyr Gly Asp Leu Gly Cys Tyr Gly His Pro Ser Ser Thr Thr Pro Asn
35 40 45
Leu Asp Gln Leu Ala Ala Gly Gly Leu Arg Phe Thr Asp Phe Tyr Val
50 55 60
Pro Val Ser Leu Cys Thr Pro Ser Arg Ala Ala Leu Leu Thr Gly Arg
65 70 75 80
Leu Pro Val Arg Met Gly Met Tyr Pro Gly Val Leu Val Pro Ser Ser
85 90 95
Arg Gly Gly Leu Pro Leu Glu Glu Val Thr Val Ala Glu Val Leu Ala
100 105 110
Ala Arg Gly Tyr Leu Thr Gly Met Ala Gly Lys Trp His Leu Gly Val
115 120 125
Gly Pro Glu Gly Ala Phe Leu Pro Pro His Gln Gly Phe His Arg Phe
130 135 140
Leu Gly Ile Pro Tyr Ser His Asp Gln Gly Pro Cys Gln Asn Leu Thr
145 150 155 160
Cys Phe Pro Pro Ala Thr Pro Cys Asp Gly Gly Cys Asp Gln Gly Leu
165 170 175
Val Pro Ile Pro Leu Leu Ala Asn Leu Ser Val Glu Ala Gln Pro Pro
180 185 190
Trp Leu Pro Gly Leu Glu Ala Arg Tyr Met Ala Phe Ala His Asp Leu
195 200 205
Met Ala Asp Ala Gln Arg Gln Asp Arg Pro Phe Phe Leu Tyr Tyr Ala
210 215 220
Ser His His Thr His Tyr Pro Gln Phe Ser Gly Gln Ser Phe Ala Glu
225 230 235 240
Arg Ser Gly Arg Gly Pro Phe Gly Asp Ser Leu Met Glu Leu Asp Ala
245 250 255
Ala Val Gly Thr Leu Met Thr Ala Ile Gly Asp Leu Gly Leu Leu Glu
260 265 270
Glu Thr Leu Val Ile Phe Thr Ala Asp Asn Gly Pro Glu Thr Met Arg
275 280 285
Met Ser Arg Gly Gly Cys Ser Gly Leu Leu Arg Cys Gly Lys Gly Thr
290 295 300
Thr Tyr Glu Gly Gly Val Arg Glu Pro Ala Leu Ala Phe Trp Pro Gly
305 310 315 320
His Ile Ala Pro Gly Val Thr His Glu Leu Ala Ser Ser Leu Asp Leu
325 330 335
Leu Pro Thr Leu Ala Ala Leu Ala Gly Ala Pro Leu Pro Asn Val Thr
340 345 350
Leu Asp Gly Phe Asp Leu Ser Pro Leu Leu Leu Gly Thr Gly Lys Ser
355 360 365
Pro Arg Gln Ser Leu Phe Phe Tyr Pro Ser Tyr Pro Asp Glu Val Arg
370 375 380
Gly Val Phe Ala Val Arg Thr Gly Lys Tyr Lys Ala His Phe Phe Thr
385 390 395 400
Gln Gly Ser Ala His Ser Asp Thr Thr Ala Asp Pro Ala Cys His Ala
405 410 415
Ser Ser Ser Leu Thr Ala His Glu Pro Pro Leu Leu Tyr Asp Leu Ser
420 425 430
Lys Asp Pro Gly Glu Asn Tyr Asn Leu Leu Gly Gly Val Ala Gly Ala
435 440 445
Thr Pro Glu Val Leu Gln Ala Leu Lys Gln Leu Gln Leu Leu Lys Ala
450 455 460
Gln Leu Asp Ala Ala Val Thr Phe Gly Pro Ser Gln Val Ala Arg Gly
465 470 475 480
Glu Asp Pro Ala Leu Gln Ile Cys Cys His Pro Gly Cys Thr Pro Arg
485 490 495
Pro Ala Cys Cys His Cys Pro Asp Pro His Ala
500 505
<210> 3
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетическая
метка 6xHis "
<400> 3
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКИЕ СЛИТЫЕ БЕЛКИ НАПРАВЛЕННОГО ДЕЙСТВИЯ НА ОСНОВЕ ЛИЗОСОМНЫХ ФЕРМЕНТОВ, СООТВЕТСТВУЮЩИЕ СОСТАВЫ И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2751235C2 |
| ИЗГОТОВЛЕНИЕ АКТИВНЫХ ВЫСОКОФОСФОРИЛИРОВАННЫХ ЛИЗОСОМАЛЬНЫХ ФЕРМЕНТОВ СУЛЬФАТАЗ ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2510820C2 |
| СПОСОБЫ И КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ОЧИЩЕННЫЕ РЕКОМБИНАНТНЫЕ ПОЛИПЕПТИДЫ | 2014 |
|
RU2793783C1 |
| НАПРАВЛЕННЫЕ ТЕРАПЕВТИЧЕСКИЕ ХИМЕРНЫЕ БЕЛКИ ЛИЗОСОМАЛЬНЫХ ФЕРМЕНТОВ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2680581C2 |
| РЕКОМБИНАНТНЫЕ БЕЛКИ ROBO2, КОМПОЗИЦИИ, СПОСОБЫ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2791486C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ДОСТАВКИ В ЦНС АРИЛСУЛЬФАТАЗЫ А | 2011 |
|
RU2671503C2 |
| ВАКЦИННЫЕ КОМПОЗИЦИИ, ХАРАКТЕРИЗУЮЩИЕСЯ УЛУЧШЕННОЙ СТАБИЛЬНОСТЬЮ И ИММУНОГЕННОСТЬЮ | 2016 |
|
RU2730625C2 |
| БЕЛКОВЫЕ КОМПОЗИЦИИ ПРОТИВ VEGF И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2020 |
|
RU2795973C1 |
| МОДИФИЦИРОВАННАЯ L-АСПАРАГИНАЗА | 2018 |
|
RU2775696C2 |
| КОМПОЗИЦИИ, СПОСОБЫ И ПРИМЕНЕНИЯ ПЕРЕНОСА ГЕНОВ ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2805606C2 |
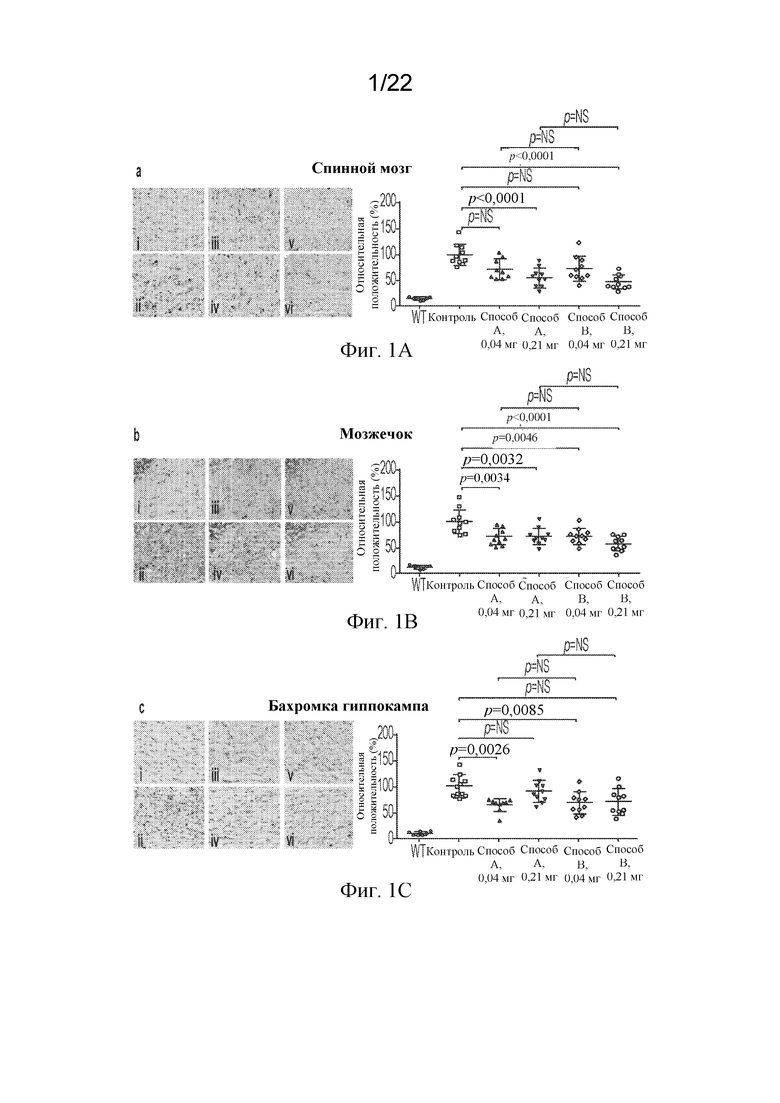
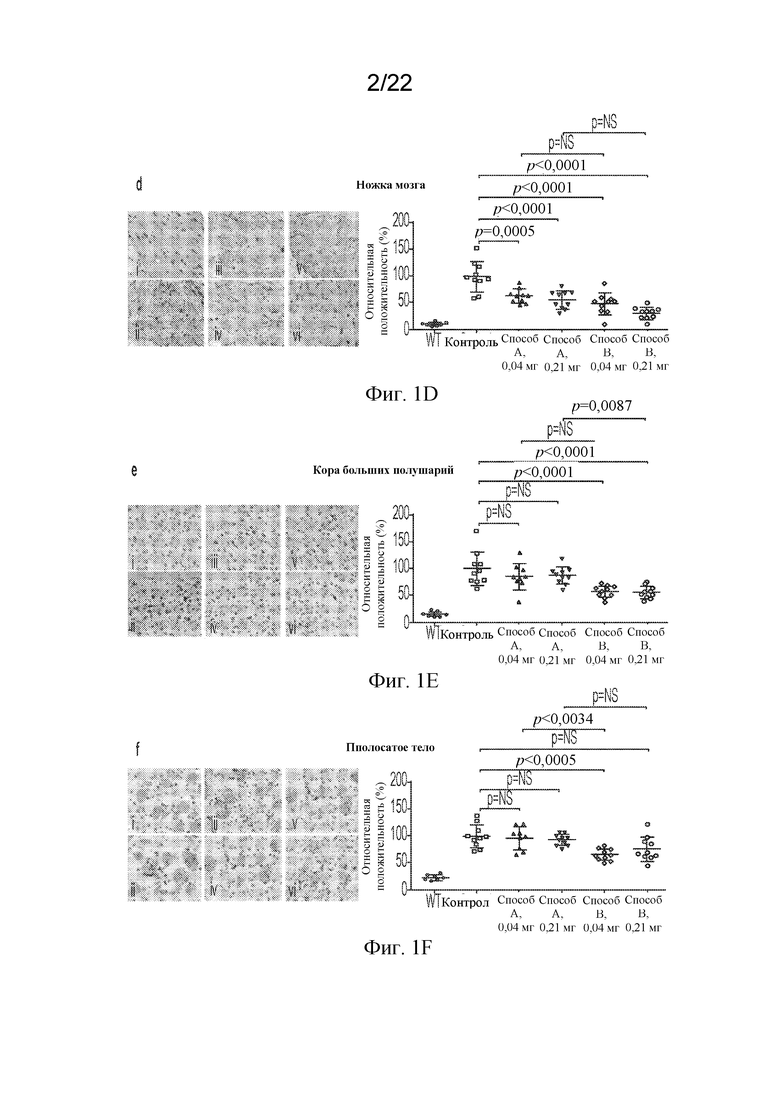
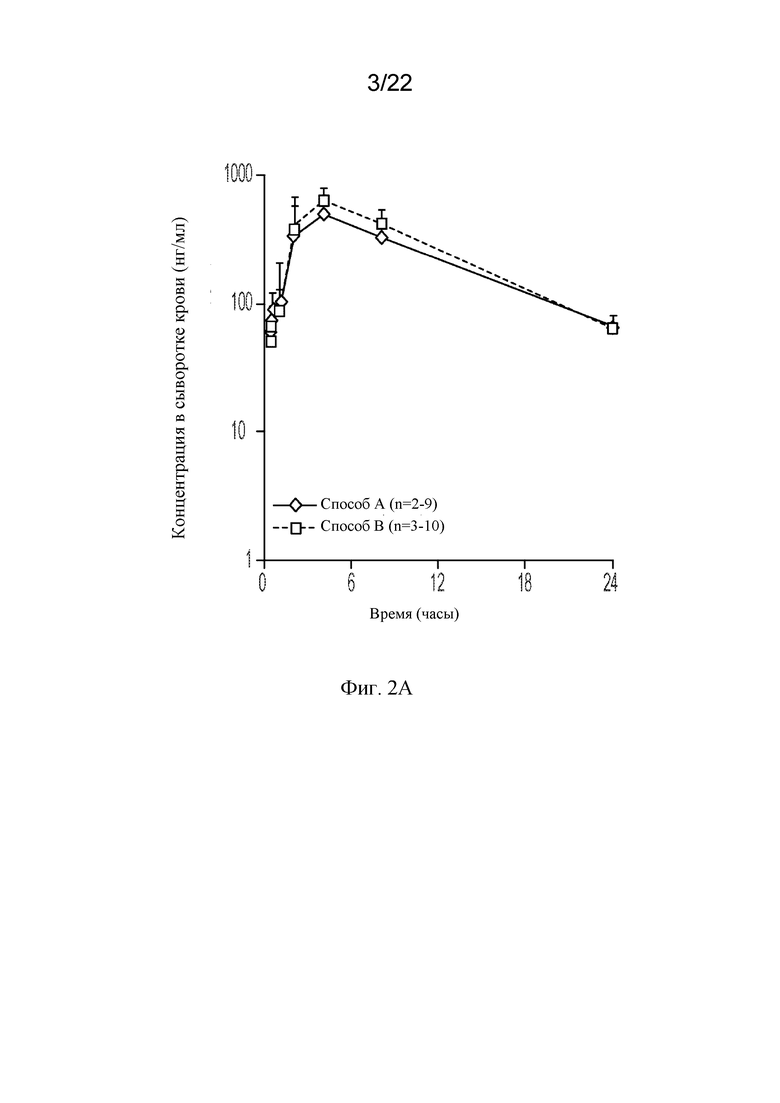
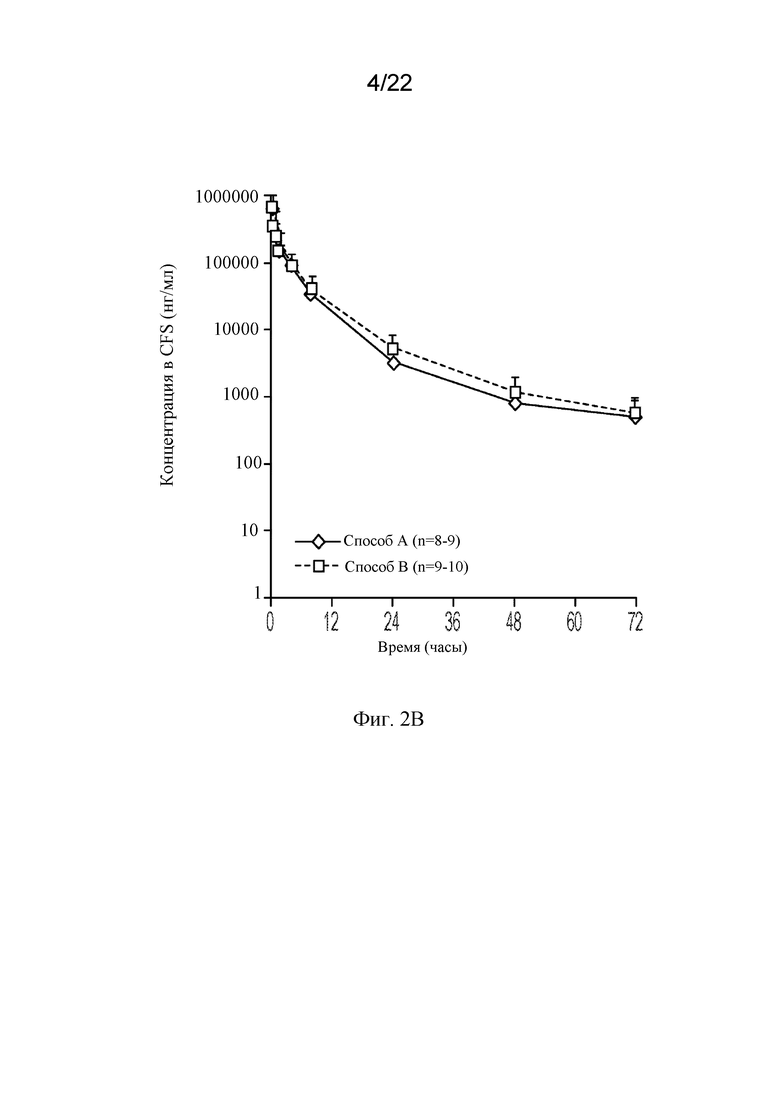
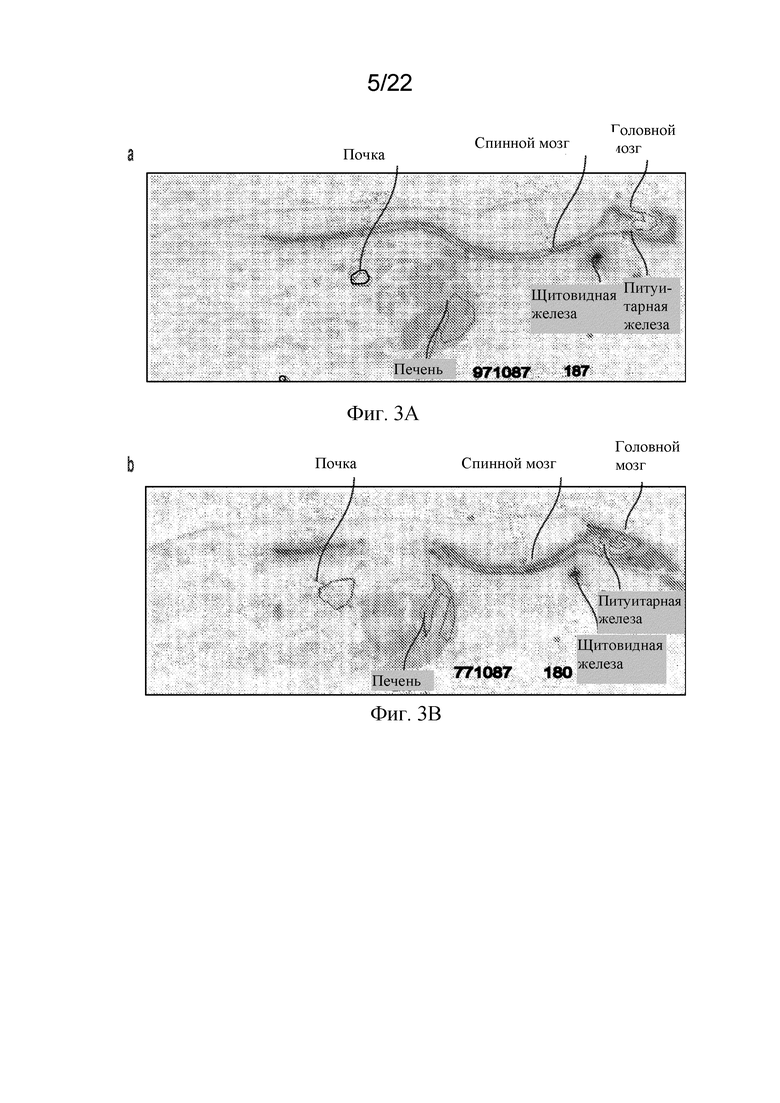
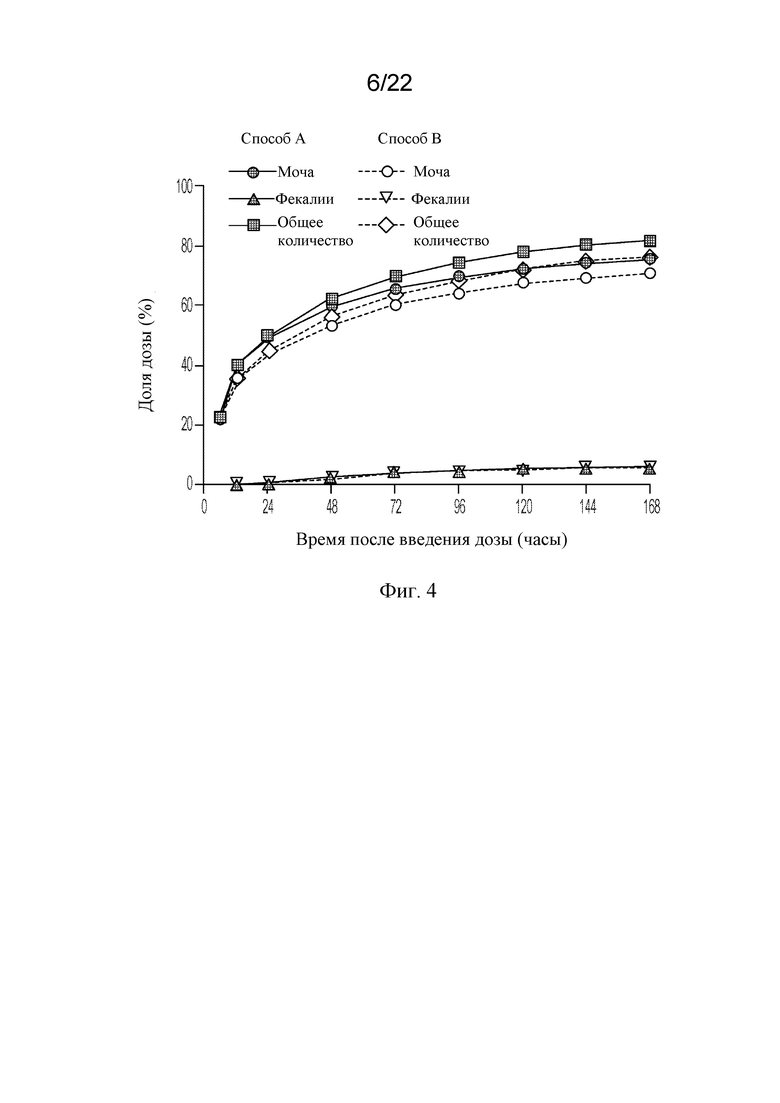
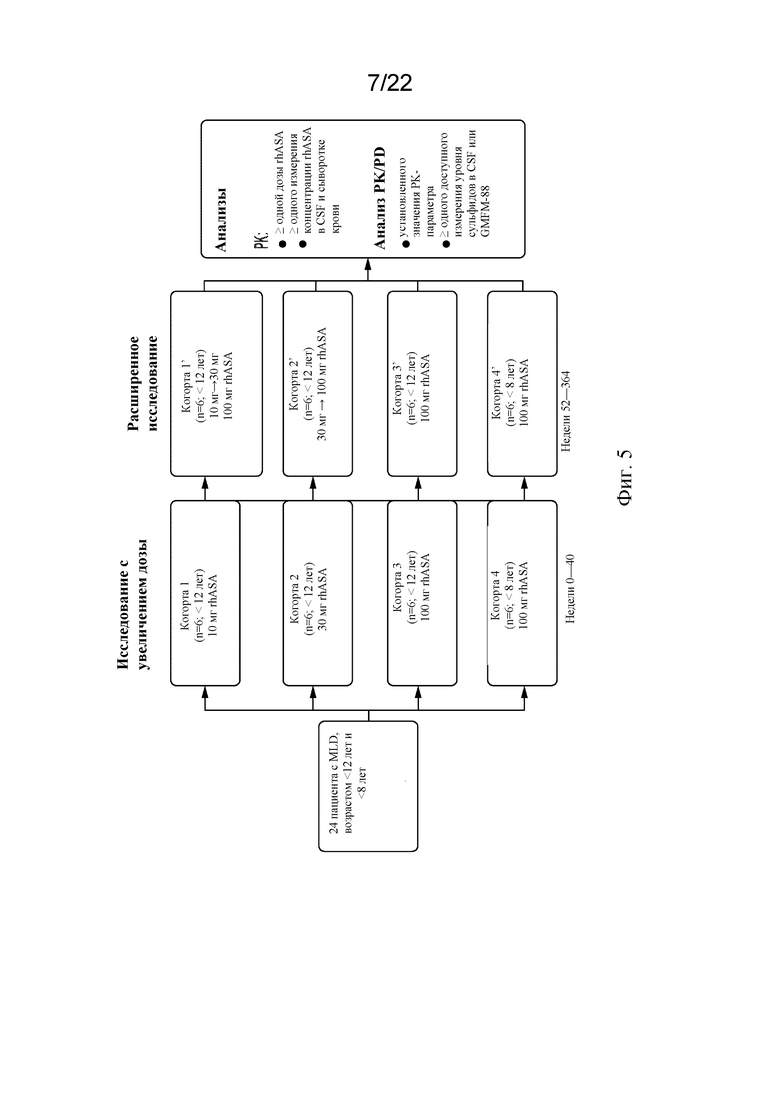
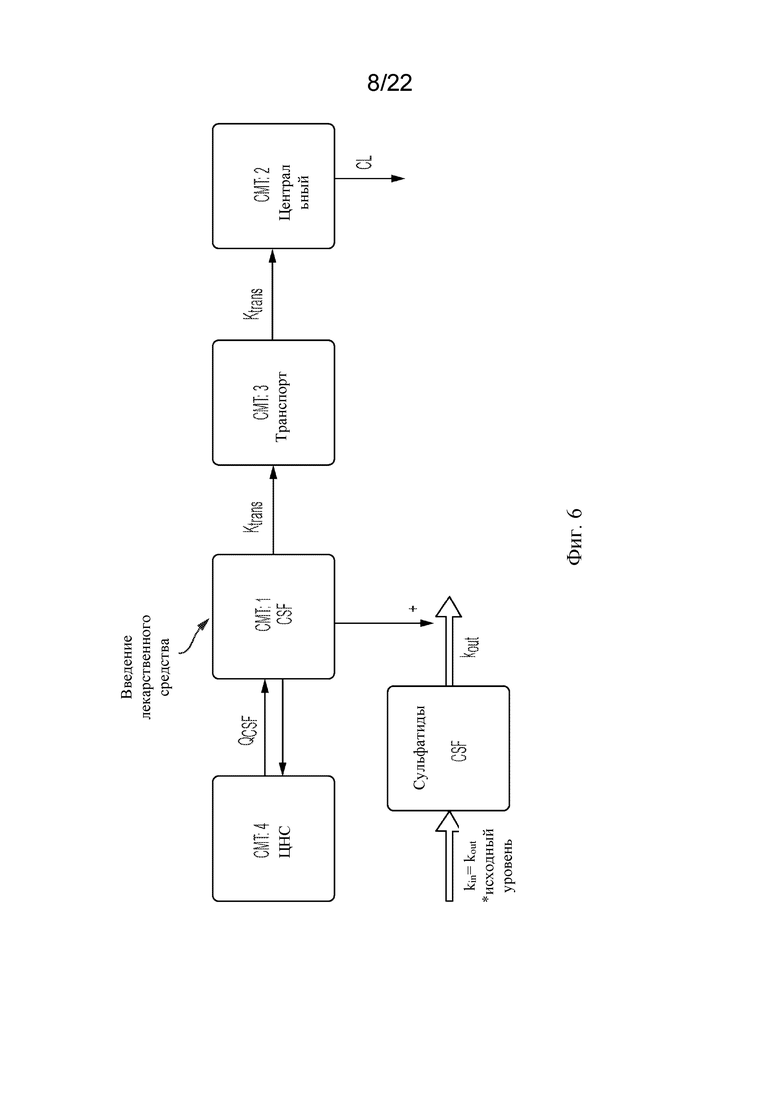
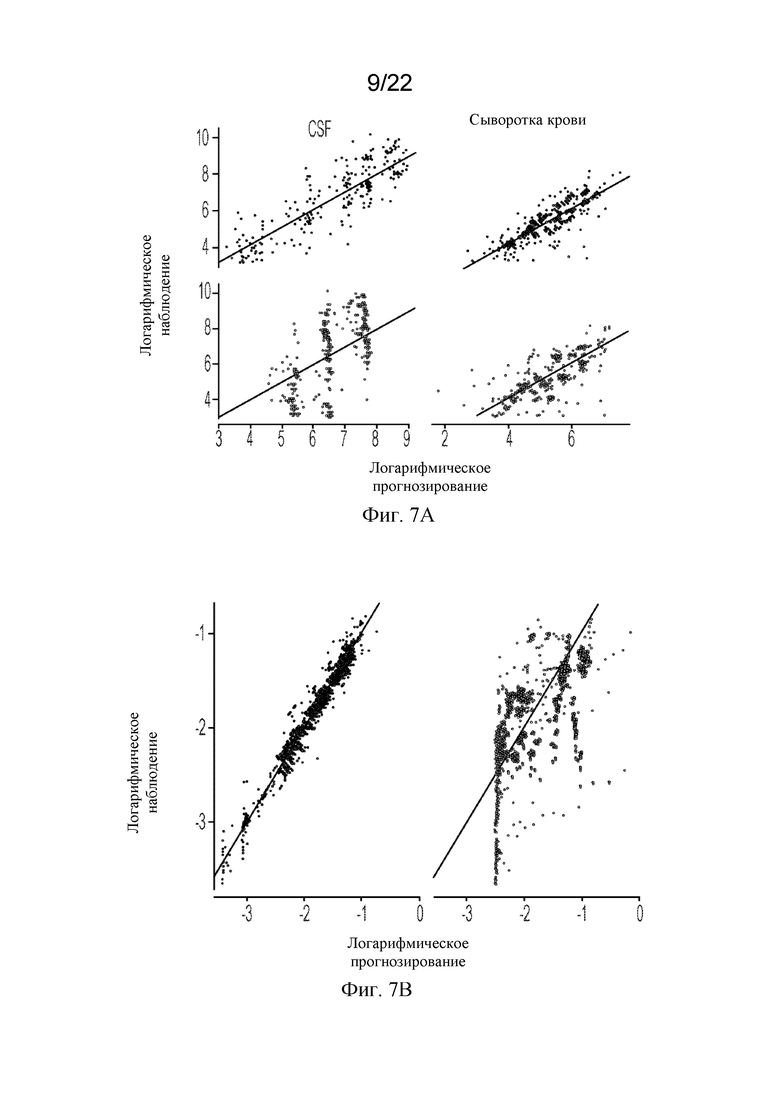
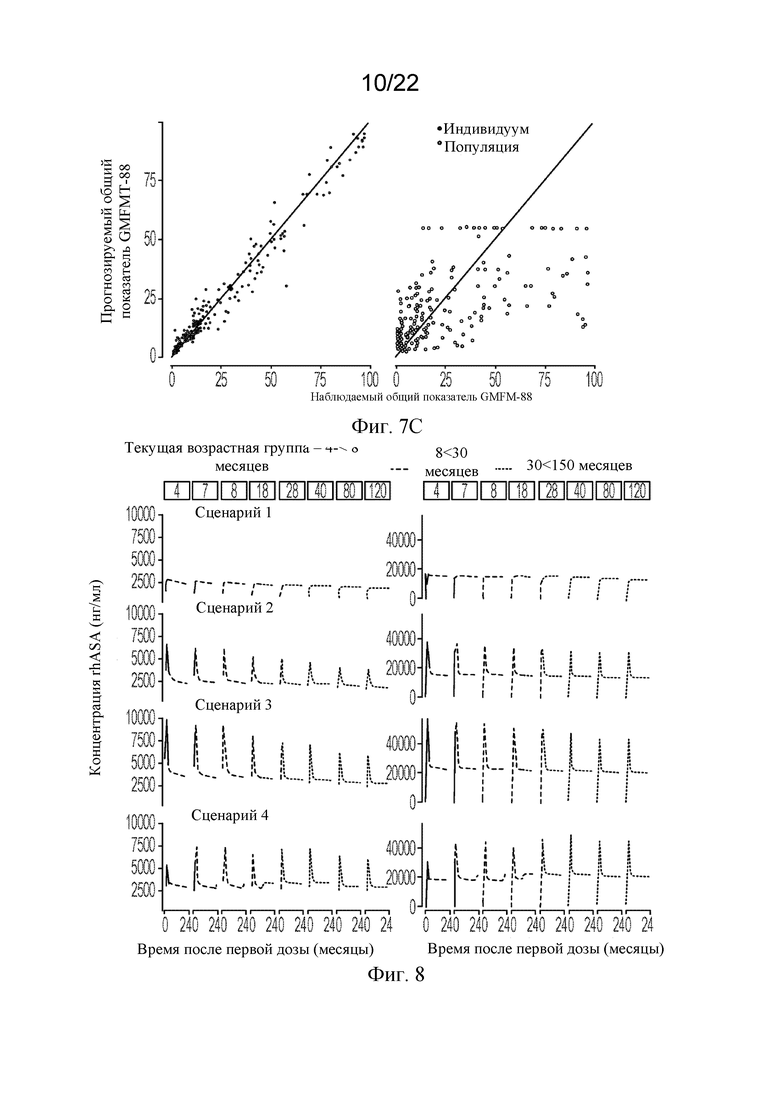
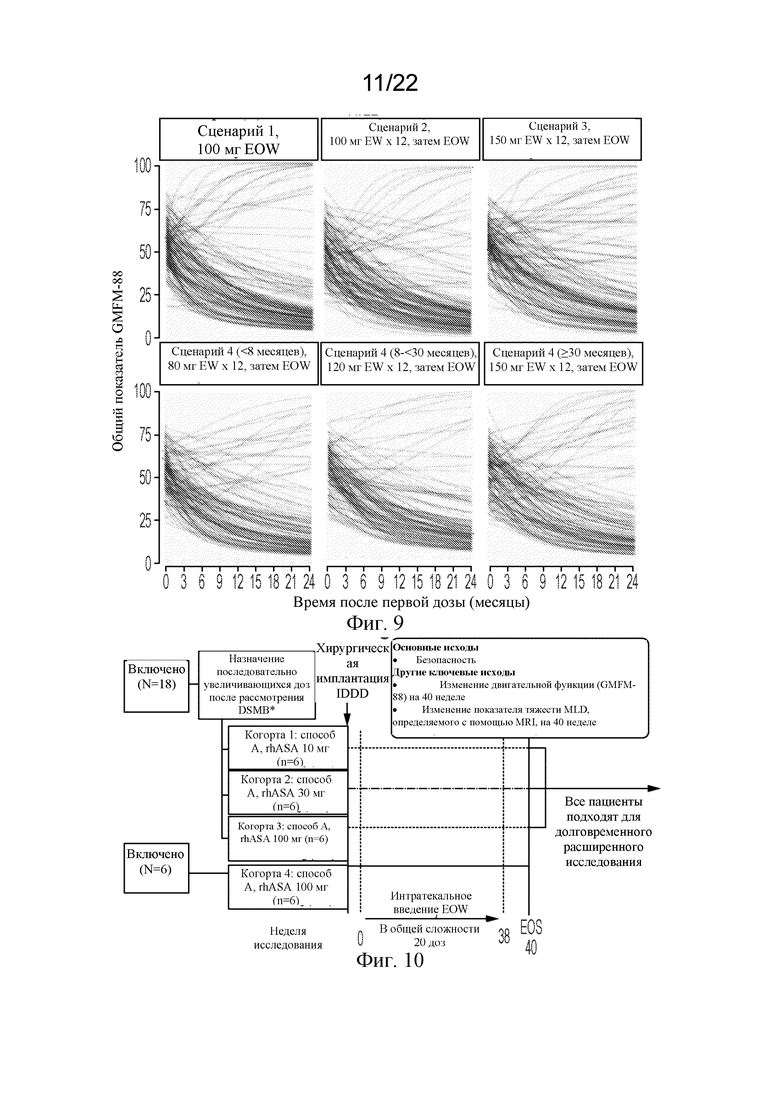

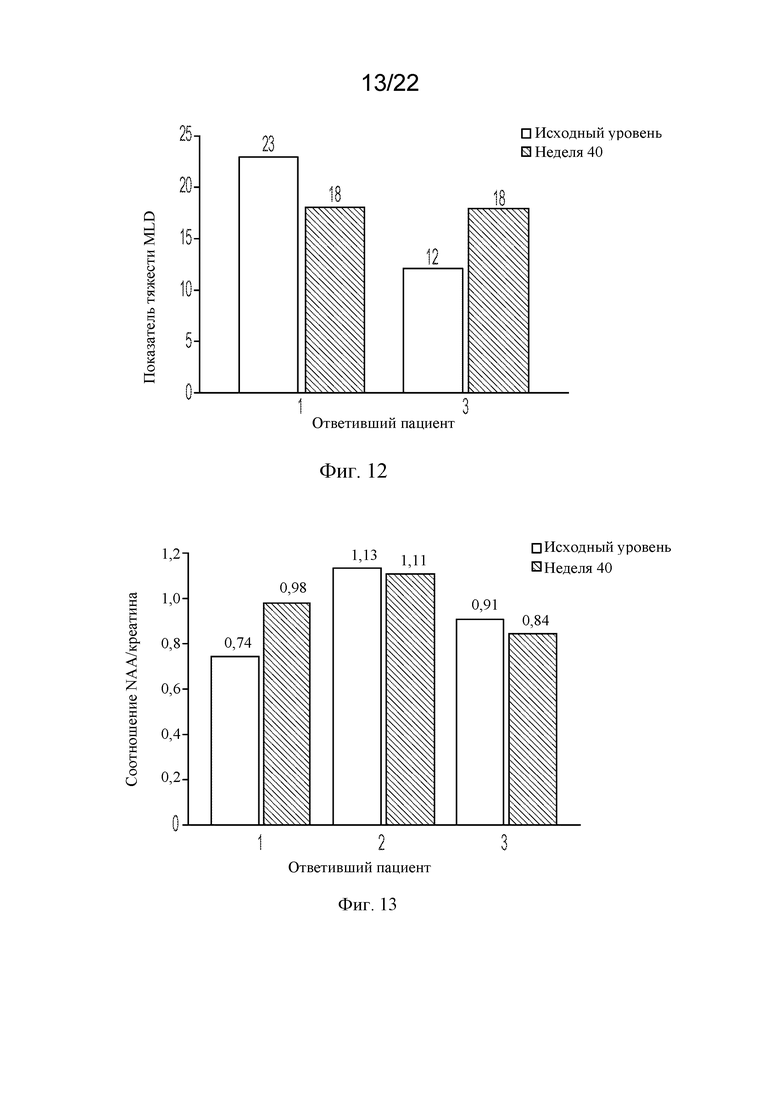


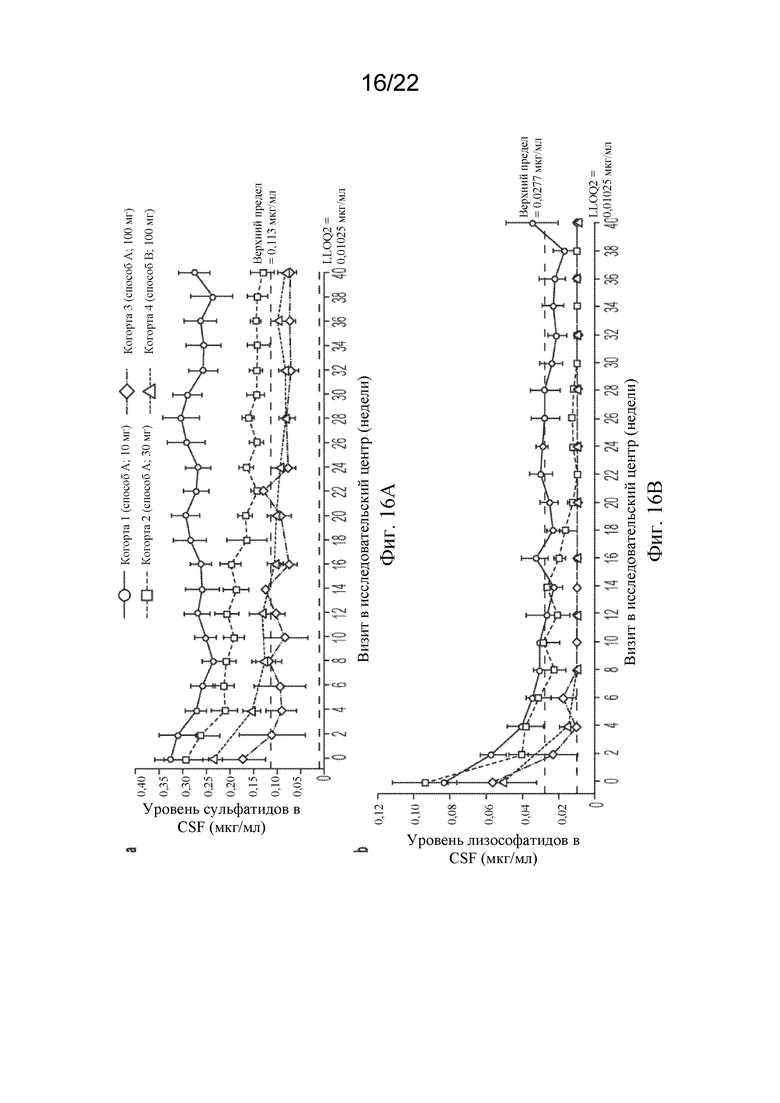
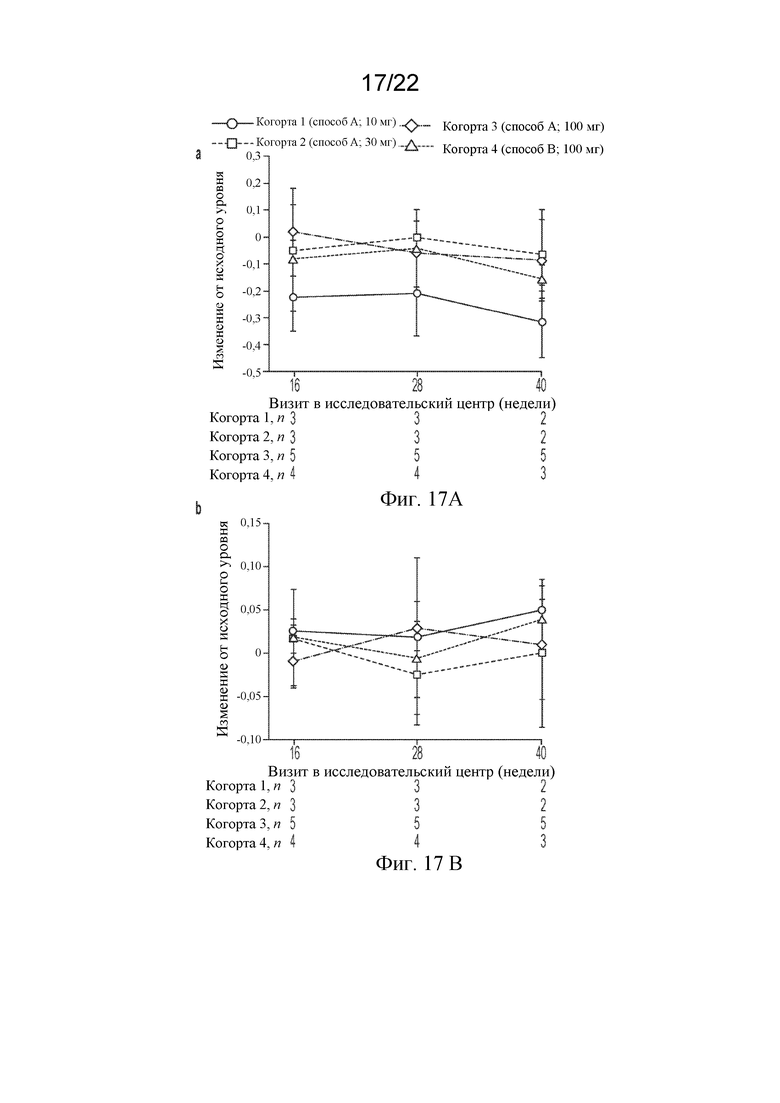

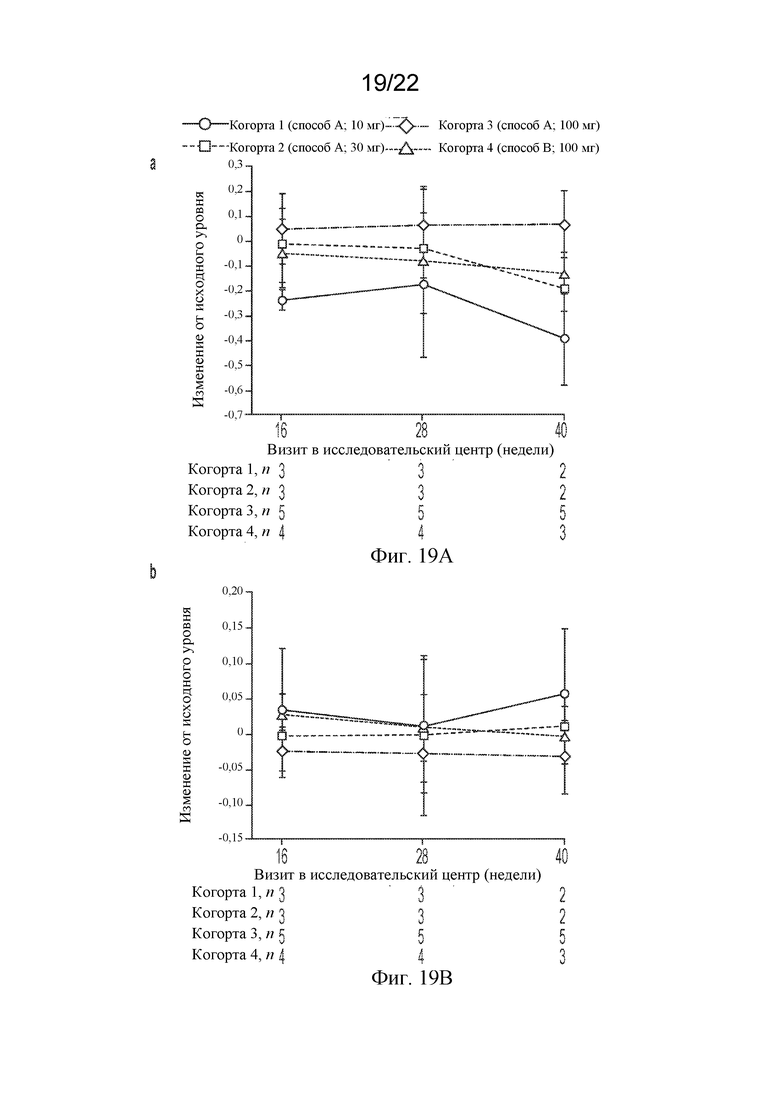
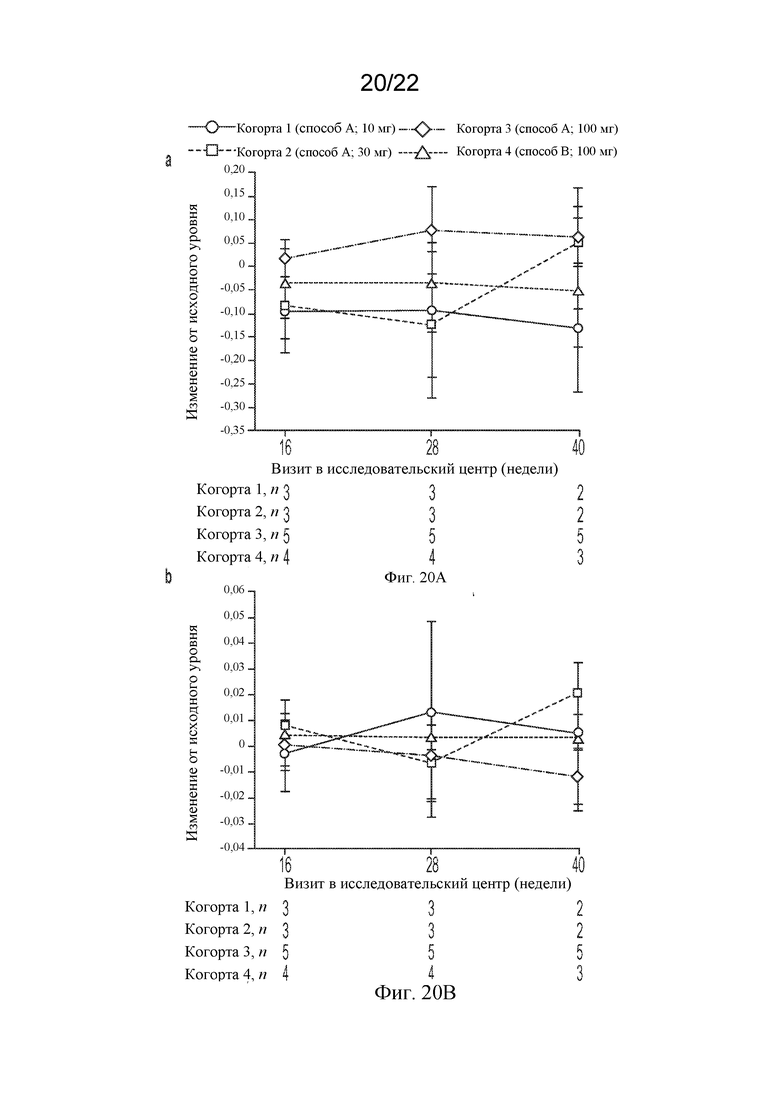
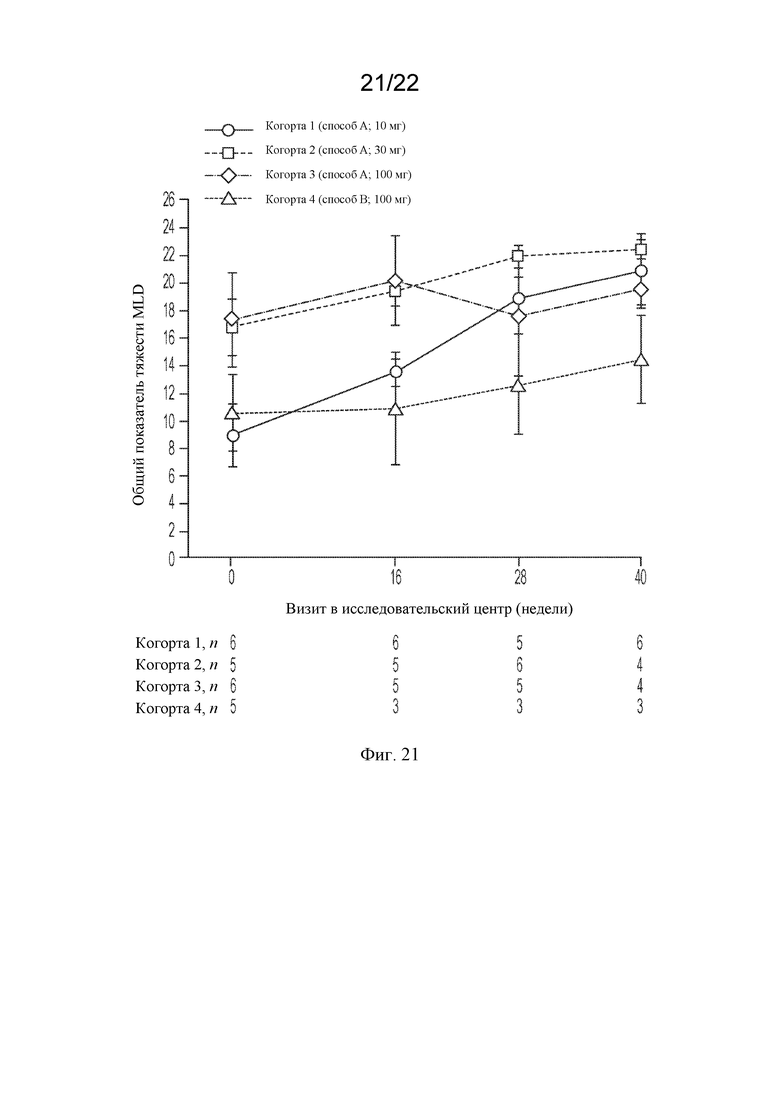
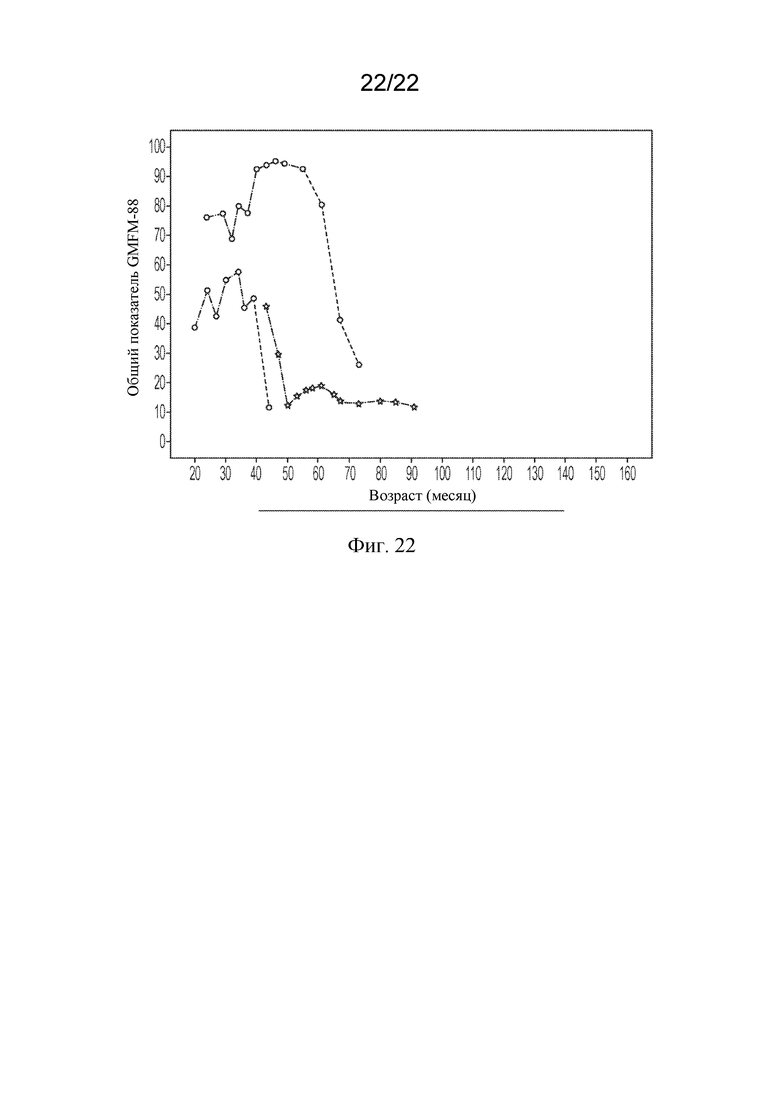
Изобретение относится к биотехнологии и представляет собой композицию для лечения метахроматической лейкодистрофии (MLD), содержащую очищенный белок, представляющий собой рекомбинантную человеческую арилсульфатазу A (rhASA), с аминокислотной последовательностью, по меньшей мере на 70% идентичной SEQ ID NO: 1, где очищенный белок rhASA характеризуется одним или более видами протеогликанов, выбранными из i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA), ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой), iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P), iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA). Изобретение позволяет повысить эффективность лечения метахроматической лейкодистрофии. 8 н. и 18 з.п. ф-лы, 22 ил., 11 табл., 7 пр.
1. Композиция для лечения метахроматической лейкодистрофии (MLD), содержащая очищенный белок, представляющий собой рекомбинантную человеческую арилсульфатазу A (rhASA), с аминокислотной последовательностью, по меньшей мере на 70% идентичной SEQ ID NO: 1, где очищенный белок rhASA характеризуется одним или более видами протеогликанов, выбранными из
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
2. Композиция по п. 1, где рекомбинантный ASA содержит менее приблизительно 150 нг/мг белка клетки-хозяина (HCP).
3. Композиция по п. 1, где по меньшей мере 23% от общего очищенного рекомбинантного белка ASA соответствует манноза-6-фосфатированному рекомбинантному белку ASA (белку ASA с M6P).
4. Композиция по п. 1, где общий очищенный белок rhASA присутствует в концентрации, составляющей от приблизительно 20 мг/мл до приблизительно 45 мг/мл.
5. Композиция по п. 1, где общий очищенный белок rhASA присутствует в концентрации, составляющей от приблизительно 25 мг/мл до приблизительно 34 мг/мл или от приблизительно 28 мг/мл до приблизительно 32 мг/мл.
6. Композиция по п. 1, где очищенный белок rhASA имеет специфическую активность, составляющую от приблизительно 50 до приблизительно 130 ед./мл.
7. Композиция по п. 6, где очищенный белок rhASA имеет специфическую активность, составляющую от приблизительно 70 до приблизительно 100 ед./мг.
8. Композиция по п. 1, где очищенный белок rhASA содержит менее приблизительно 140 нг/мг белка клетки-хозяина (HCP).
9. Композиция по п. 1, где очищенный белок rhASA содержит менее приблизительно 100 пг/мг ДНК клетки-хозяина (HCD).
10. Композиция по любому из пп. 1-9, содержащая от приблизительно 0,001% до приблизительно 0,01% полисорбата-20 (P20).
11. Состав для лечения метахроматической лейкодистрофии (MLD), содержащий композицию по любому из пп. 1-10 и физиологически приемлемый носитель.
12. Состав по п. 11, где состав является подходящим для внутривенного введения.
13. Состав по п. 11, где состав является подходящим для интратекального введения.
14. Состав по п. 11, где состав является подходящим для подкожного введения.
15. Способ лечения метахроматической лейкодистрофии (MLD), при этом способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективной дозы очищенного белка, представляющего собой рекомбинантную человеческую арилсульфатазу A (rhASA),
где очищенный белок rhASA характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
16. Способ лечения метахроматической лейкодистрофии (MLD), при этом способ включает введение фермента, представляющего собой рекомбинантную арилсульфатазу A (ASA), для применения в лечении метахроматической лейкодистрофии (MLD) у субъекта, имеющего исходный уровень менее уровня 4 согласно системе классификации общей моторики (GMFC), где фермент, представляющий собой рекомбинантную ASA, характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA),
при этом фермент, представляющий собой рекомбинантную ASA, предназначен для интратекального введения субъекту в терапевтически эффективной дозе.
17. Способ лечения метахроматической лейкодистрофии (MLD), при этом способ включает введение фермента, представляющего собой рекомбинантную арилсульфатазу A (ASA), для применения в лечении метахроматической лейкодистрофии (MLD) у субъекта, имеющего исходный уровень 1-4 согласно системе классификации общей моторики (GMFC), при этом фермент, представляющий собой рекомбинантную ASA, предназначен для интратекального введения субъекту в терапевтически эффективной дозе, и при этом фремент, представляющий собой рекомбинантную ASA, характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
18. Способ по любому из пп. 15-17, где очищенный белок rhASA характеризуется картой протеогликанов, содержащей:
i) от 18% до 22% нейтрального белка ASA,
ii) от 37% до 41% белка ASA с сиаловой кислотой,
iii) от 26% до 29% белка ASA с M6P,
iv) от 4% до 6% белка ASA, кэппированного M6P, и
v) от 7% до 9% гибридного белка ASA.
19. Способ по любому из пп. 15-17, где субъект имеет позднюю младенческую форму MLD.
20. Способ по любому из пп. 15-19, где субъект находится на предсимптоматической стадии.
21. Способ по п. 20, где возраст субъекта составляет менее 18 месяцев.
22. Способ по п. 21, где субъекта оценивают согласно Альбертской шкале двигательной функции у младенцев.
23. Способ по любому из пп. 15-22, где белок rhASA имеет аминокислотную последовательность, на по меньшей мере 70% идентичную SEQ ID NO: 1.
24. Применение очищенного белка, представляющего собой рекомбинантную человеческую арилсульфатазу A (rhASA), в производстве лекарственного средства для лечения метахроматической лейкодистрофии (MLD),
где очищенный белок rhASA характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
25. Применение фермента, представляющего собой рекомбинантную арилсульфатазу A (ASA), в производстве лекарственного средства для лечения метахроматической лейкодистрофии (MLD), где субъект характеризуется как имеющий исходный уровень менее уровня 4 согласно системе классификации общей моторики (GMFC),
где фермент, представляющий собой рекомбинантную ASA, характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA),
при этом фермент, представляющий собой рекомбинантную ASA, предназначен для интратекального введения субъекту в терапевтически эффективной дозе.
26. Применение фермента, представляющего собой рекомбинантную арилсульфатазу A (ASA), в производстве лекарственного средства для лечения метахроматической лейкодистрофии (MLD) у субъекта, который характеризуется как имеющий исходный уровень 1-4 согласно системе классификации общей моторики (GMFC), при этом фермент, представляющий собой рекомбинантную ASA, предназначен для интратекального введения субъекту в терапевтически эффективной дозе, и при этом фермент, представляющий собой рекомбинантную ASA, характеризуется картой протеогликанов, содержащей один или более видов протеогликанов, выбранных из:
i) от 15% до 25% нейтрального рекомбинантного белка ASA (нейтрального белка ASA),
ii) от 35% до 45% сиалированного рекомбинантного белка ASA (белка ASA с сиаловой кислотой),
iii) от 23% до 33% манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA с M6P),
iv) от 1% до 10% N-ацетил-глюкозамин-манноза-6-фосфатированного рекомбинантного белка ASA (белка ASA, кэппированного M6P) и
v) от 5% до 15% гибридного рекомбинантного белка ASA (гибридного белка ASA).
| WO 2014110246 A1, 17.07.2014 | |||
| WO 2017143233 A1, 24.08.2017 | |||
| US 9770410 B2, 26.09.2017 | |||
| CN 103282046 A, 04.09.2013 | |||
| ДОСТАВКА К ЦНС ЛЕЧЕБНЫХ АГЕНТОВ | 2011 |
|
RU2626514C2 |
Авторы
Даты
2024-11-18—Публикация
2018-12-19—Подача