ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к области биомедицины и, в частности, относится к комбинированной фармацевтической композиции для лечения рака почек.
УРОВЕНЬ ТЕХНИКИ
Почечно-клеточная карцинома (ПКК, RCC), также известная как рак почек, является наиболее распространенным злокачественным новообразованием мочеполовой системы. Последние статистические данные в Соединенных Штатах демонстрируют 65340 новых случаев онкологических заболеваний и 14970 смертей в Соединенных Штатах; онкологическое заболевание является ведущей причиной смертности. Годовой отчет Китайского онкологического регистра за 2018 год указывает, что заболеваемость раком почек в Китае достигла 40,2/100 тысяч, а смертность до 14,5/100 тысяч. 74,95% случаев представляли собой светлоклеточную почечно-клеточную карциному. Среди случаев остальных типов хромофобная почечно-клеточная карцинома, папиллярная почечно-клеточная карцинома, карцинома собирательных трубочек и другие виды рака составляют 3,21%, 2,75%, 0,56% и 18,54% случаев, соответственно.
Рак почек сам по себе не чувствителен к лучевой терапии и химиотерапии. Цитотерапия на основе интерлейкина-2 (IL-2) и интерферона-α (INF-α) начала широко применяться в клинической практике в качестве варианта первой линии адъювантной терапии с 1990 г. С 2000 года молекулярно-направленная терапия стала доминировать в клиническом лечении рака почек и оказалась очень эффективной в улучшении прогноза ПКК. В данное время низкомолекулярные препараты направленного действия, клинически одобренные FDA, в основном включают сунитиниб, сорафениб, пазопаниб, акситиниб, бевацизумаб, эверолимус и темсиролимус, а биологические препараты направленного действия в основном включают бевацизумаб, пембролизумаб, ипилимумаб, ниволумаб и авелумаб. Хотя в данное время достигнут большой прогресс в лечении рака почек, поиск других способов лечения по-прежнему имеет большое клиническое значение.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте в данной заявке предложена фармацевтическая комбинация или фармацевтическая композиция для применения при лечении рака почек, которые содержат: антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль.
В другом аспекте в данной заявке предложено применение фармацевтической комбинации или фармацевтической композиции антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли для приготовления лекарственного средства для лечения рака почек. В альтернативном варианте в данной заявке предложено применение фармацевтической комбинации или фармацевтической композиции, содержащих антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, для приготовления лекарственного средства для лечения рака почек.
В другом аспекте в данной заявке предложено применение фармацевтической комбинации или фармацевтической композиции антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли для лечения рака почек. В альтернативном варианте в данной заявке предложено применение фармацевтической комбинации или фармацевтической композиции, содержащих антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, для лечения рака почек.
В еще одном аспекте в данной заявке также предложен способ лечения рака почек, который включает введение нуждающемуся в этом пациенту эффективного количества фармацевтической комбинации или фармацевтической композиции антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли. В альтернативном варианте в данной заявке также предложен способ лечения рака почек, который включает введение нуждающемуся в этом пациенту эффективного количества фармацевтической комбинации или фармацевтической композиции, содержащих антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль.
В еще одном аспекте в данной заявке предложен набор для применения при лечении рака почек, содержащий: антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, при этом антитело против PD-L1 содержится в первом отделение, а анлотиниб или его фармацевтически приемлемая соль содержатся во втором отделении; их можно вводить одновременно, раздельно или последовательно нуждающемуся в этом пациенту. Набор дополнительно содержит инструкции по совместному применению антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли при лечении рака почек. В некоторых вариантах реализации данного изобретения набор содержит: фармацевтическую композицию антитела против PD-L1 и фармацевтическую композицию анлотиниба или его фармацевтически приемлемой соли.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: гуманизированное моноклональное антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: фармацевтическую композицию антитела против PD-L1 и фармацевтическую композицию анлотиниба или его фармацевтически приемлемой соли.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: фармацевтическую композицию, содержащую 600-2400 мг антитела против PD-L1, и фармацевтическую композицию, содержащую 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли в виде однократной дозе, при этом фармацевтическая композиция, содержащая антитело против PD-L1, находится в виде однократной дозы или в виде многократных доз; в некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция содержат: фармацевтическую композицию, содержащую 600-2400 мг антитела против PD-L1, представленную в виде многократной дозы, и фармацевтическую композицию, содержащую 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли в виде однократной дозы; в некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция представляют собой состав, подходящий для введения в рамках одного цикла лечения (например, 21-дневного цикла лечения), и содержат фармацевтическую композицию, содержащую 600-2400 мг антитела против PD-L1, и фармацевтическую композицию, содержащую 84-168 мг анлотиниба или его фармацевтически приемлемой соли.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль в массовом соотношении (0,35-29):1, предпочтительно (3,5-29):1, более предпочтительно (3,5-14,5):1, и наиболее предпочтительно (7-14,5):1. Антитело против PD-L1 и анлотиниб или его фармацевтически приемлемая соль могут быть упакованы отдельно или вместе. Анлотиниб может быть упакован в виде нескольких аликвот (например, 2 аликвоты, 7 аликвот, 14 аликвот, 28 аликвот или более); антитело против PD-L1 может быть упаковано в виде одной аликвоты или нескольких аликвот (например, 2 аликвоты, 4 аликвоты или более).
В некоторых вариантах реализации данного изобретения в данной заявке предложены фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, при этом антитело против PD-L1 и анлотиниб или его фармацевтически приемлемая соль находятся в форме фармацевтической композиции и могут быть введены одновременно, последовательно или через определенные промежутки времени. Кроме того, антитело против PD-L1 вводят один раз в неделю, каждые 2 недели, каждые 3 недели или каждые 4 недели; предпочтительно антитело против PD-L1 вводят в дозе 600-2400 мг при каждом введении. Кроме того, анлотиниб или его фармацевтически приемлемую соль вводят в дозе 6 мг, 8 мг, 10 мг или 12 мг один раз в день по схеме последовательного 2-недельного лечения с последующим 1-недельным перерывом.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат фармацевтическую композицию антитела против PD-L1 и фармацевтическую композицию анлотиниба, при этом антитело против PD-L1 получают в виде однократной дозы или в виде нескольких доз, подходящих для обеспечения пациента 600-2400 мг антитела против PD-L1 при первом введении, и анлотиниб или его фармацевтически приемлемую соль получают в виде однократных доз, подходящих для обеспечения пациента 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли ежедневно в течение 14 последовательных дней.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: фармацевтическую композицию антитела против PD-L1, в которой антитело против PD-L1 находится в концентрации 10-60 мг/мл, и фармацевтическую композицию, содержащую 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли, в виде однократной дозы.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: фармацевтическую композицию антитела против PD-L1, в которой антитело против PD-L1 находится в концентрации 10 мг/мл, и фармацевтическую композицию, содержащую 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли, в виде однократной дозы.
В некоторых вариантах реализации данного изобретения фармацевтическая комбинация или фармацевтическая композиция, содержащие антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль, описанные в данном документе, содержат: фармацевтическую композицию, содержащую 1200 мг антитела против PD-L1, представленную в виде многократной дозы, и фармацевтическую композицию, содержащую 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли, в виде однократной дозы.
В некоторых вариантах реализации данного изобретения набор подходит для введения в рамках одного цикла лечения (например, 21-дневного цикла лечения) и содержит фармацевтическую композицию, содержащую 600-2400 мг антитела против PD-L1, и фармацевтическую композицию, содержащую 84-168 мг анлотиниба или его фармацевтически приемлемой соли.
Анлотиниб или его фармацевтически приемлемая соль
Химическое название анлотиниба - 1-[[[4-(4-фтор-2-метил-1Н-индол-5-ил)окси-6-метоксихинолин-7-ил]окси]метил]циклопропиламин, который имеет следующую структурную формулу:
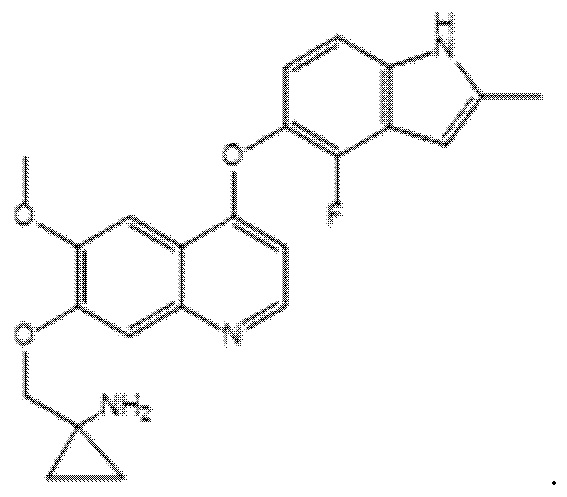
Фармацевтически приемлемые соли анлотиниба включают, но не ограничиваются ими, соли, образованные из анлотиниба и кислот, выбранных из группы, состоящей из следующих: соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, уксусная кислота, трифторуксусная кислота, пропионовая кислота, гексановая кислота, гептановая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфокислота, этансульфокислота, 1,2-этандисульфокислота, 2-гидроксиэтансульфокислота, бензолсульфокислота, p-хлорбензолсульфокислота, p-толуолсульфокислота, 3-фенилпропионовая кислота, триметилуксусная кислота, t-бутилуксусная кислота, додецилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота и стеариновая кислота; в некоторых вариантах реализации данного изобретения фармацевтически приемлемая соль представляет собой гидрохлорид или малеат; в некоторых вариантах реализации данного изобретения фармацевтически приемлемая соль представляет собой дигидрохлорид.
Доза анлотиниба или его фармацевтически приемлемой соли, указанная в данной заявке, основана на молекулярной массе свободного основания анлотиниба, если не указано иное.
Анлотиниб или его фармацевтически приемлемую соль можно вводить различными путями, включая, но не ограничиваясь ими, пероральное, парентеральное, внутрибрюшинное, внутривенное, внутриартериальное, трансдермальное, сублингвальное, внутримышечное, ректальное, трансбуккальное, интраназальное, ингаляционное, вагинальное, внутриглазное, местное, подкожное, внутрижировое, внутрисуставное и подоболочечное введение. В некоторых конкретных вариантах реализации данного изобретения лекарственный препарат вводят перорально. Вводимое количество анлотиниба или его фармацевтически приемлемой соли может быть определено в зависимости от тяжести заболевания, ответа заболевания, любой токсичности, связанной с лечением, а также возраста и состояния здоровья пациента. Например, суточная доза анлотиниба или его фармацевтически приемлемой соли может составлять от 2 мг до 20 мг. В некоторых вариантах реализации данного изобретения суточная доза анлотиниба или его фармацевтически приемлемой соли может составлять 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг и 16 мг. Анлотиниб или его фармацевтически приемлемую соль можно вводить один или несколько раз в день. В некоторых вариантах реализации данного изобретения анлотиниб или его фармацевтически приемлемую соль вводят один раз в сутки в виде твердого перорального состава.
Схема введения анлотиниба или его фармацевтически приемлемой соли может быть определена в зависимости от сочетания активности и токсичности лекарственного препарата, переносимости пациентом и т. д. Предпочтительно анлотиниб или его фармацевтически приемлемую соль вводят с интервалами. Интервальное введение включает период лечения и период перерыва. Анлотиниб или его фармацевтически приемлемую соль можно вводить один или несколько раз в день в период лечения. В некоторых вариантах реализации данного изобретения соотношение периода лечения к периоду перерыва в днях составляет 2:(0,5-5), предпочтительно 2:(0,5-3), более предпочтительно 2:(0,5-2), и даже более предпочтительно 2:(0,5-1). В некоторых вариантах реализации данного изобретения анлотиниб или его фармацевтически приемлемую соль вводят по схеме, состоящей из последовательного 2-недельного лечения с последующим 2-недельным перерывом. В некоторых вариантах реализации данного изобретения анлотиниб или его фармацевтически приемлемую соль вводят по схеме, состоящей из последовательного 2-недельного лечения с последующим 1-недельным перерывом. В некоторых вариантах реализации данного изобретения анлотиниб или его фармацевтически приемлемую соль вводят по схеме, состоящей из последовательного 5-дневного лечения с последующим 2-дневным перерывом. Например, анлотиниб или его фармацевтически приемлемую соль можно вводить перорально в дозе 6 мг, 8 мг, 10 мг или 12 мг один раз в день по схеме последовательного 2-недельного лечения с последующим 1-недельным перерывом.
Фармацевтическая композиция анлотиниба или его фармацевтически приемлемой соли
В некоторых вариантах реализации данного изобретения однократная доза фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли содержит 6 мг, 8 мг, 10 мг или 12 мг анлотиниба.
В некоторых вариантах реализации данного изобретения в соответствии с циклом лечения, состоящим из 2-недельного лечения с последующим 1-недельным перерывом, общая доза фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли, вводимой за цикл, составляет 84-168 мг. В некоторых вариантах реализации данного изобретения общая доза фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли включает количество, выбранное из группы, состоящей из 84 мг, 112 мг, 140 мг и 168 мг, или из диапазона, образованного любым из вышеупомянутых значений. В некоторых вариантах реализации данного изобретения общая доза фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли предпочтительно составляет 112-168 мг.
В некоторых вариантах реализации данного изобретения фармацевтическая композиция представляет собой состав для перорального применения; в некоторых вариантах реализации данного изобретения фармацевтическая композиция представляет собой твердый состав для перорального применения; в некоторых вариантах реализации данного изобретения фармацевтическая композиция включает, но не ограничивается ими, таблетку и капсулу.
Антитело против PD-L1
В некоторых вариантах реализации данного изобретения антитело против PD-L1 представляет собой антитело, раскрытое в WO2016022630 или CN107001463A.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: область CDR1 тяжелой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 1 или SEQ ID NO: 4; область CDR2 тяжелой цепи, имеющую, по меньшей мере 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 2 или SEQ ID NO: 5; область CDR3 тяжелой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 3 или SEQ ID NO: 6; область CDR1 легкой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 7 или SEQ ID NO: 10; область CDR2 легкой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 8 или SEQ ID NO: 11; и область CDR3 легкой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 9 или SEQ ID NO: 12.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: область CDR1 тяжелой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 1 и последовательности SEQ ID NO: 4; область CDR2 тяжелой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 2 и последовательности SEQ ID NO: 5; область CDR3 тяжелой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 3 и последовательности SEQ ID NO: 6; область CDR1 легкой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 7 и последовательности SEQ ID NO: 10; область CDR2 легкой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 8 и последовательности SEQ ID NO: 11; и область CDR3 легкой цепи, выбранную из группы, состоящей из последовательности SEQ ID NO: 9 и последовательности SEQ ID NO: 12.
В некоторых вариантах реализации данного изобретения выделенное антитело против PD-L1, описанное в данном документе, содержит: область CDR1 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 1; область CDR2 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 2; область CDR3 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 3; область CDR1 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 7; область CDR2 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 8; и область CDR3 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 9.
Каждая из областей CDR, описанных в данном документе, и их варианты, описанные выше, способны специфически распознавать и связываться с PD-L1, тем самым эффективно блокируя передачу сигналов между PD-L1 и PD-1.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 13 или SEQ ID NO: 14; и вариабельную область легкой цепи, имеющую, по меньшей мере, 80% (например, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%) гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 15 или SEQ ID NO: 16.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, представленную в SEQ ID NO: 13, и вариабельную область легкой цепи, представленную в SEQ ID NO: 15.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, представленную в SEQ ID NO: 14, и вариабельную область легкой цепи, представленную в SEQ ID NO: 16.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 17, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 18.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 19, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 20.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 21, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 18.
В одном конкретном варианте реализации данного изобретения гуманизированное мАт против PD-L1, описанное в данном документе, содержит один или более вариантов с консервативными заменами, выбранных из группы, состоящей из: SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20 и SEQ ID NO: 21. Гуманизированное мАт против PD-L1, содержащее варианты с консервативными заменами, сохраняет способность специфически распознавать и связываться с PD-L1.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 может представлять собой антитело IgG1 или IgG4.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 представляет собой антитело IgG1. В некоторых вариантах реализации данного изобретения антитело против PD-L1 представляет собой гликозилированное антитело IgG1.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит области, определяющие комплементарность (CDR), тяжелой цепи, выбранные из группы, состоящей из CDR тяжелой цепи, полученных из антител 13C5 и 5G11, и CDR легкой цепи, выбранных из группы, состоящей из CDR легкой цепи, полученных из антител 13C5 и 5G11. В одном варианте реализации данного изобретения антитело против PD-L1, описанное в данном документе, содержит: вариабельную область тяжелой цепи, выбранную из группы, состоящей из вариабельных областей тяжелой цепи химерных антител ch5G11-hIgG1, ch5G11-hIgG4, ch13C5-hIgG1 и ch13C5-hIgG4; и вариабельную область легкой цепи, выбранную из группы, состоящей из вариабельных областей легкой цепи химерных антител ch5G11-hIgG1, ch5G11-hIgG4, ch13C5-hIgG1 и ch13C5-hIgG4. В одном варианте реализации данного изобретения антитело против PD-L1, описанное в данном документе, содержит: вариабельную область тяжелой цепи, выбранную из группы, состоящей из вариабельных областей тяжелой цепи гуманизированных антител hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 и hu5G11-hIgG4; и вариабельную область легкой цепи, выбранную из группы, состоящей из вариабельных областей легкой цепи гуманизированных антител hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 и hu5G11-hIgG4. При этом можно сделать ссылку на описание патентов WO2016022630 или CN107001463A, в которых: 13C5, ch13C5-hIgG1, ch13C5-hIgG4, hu13C5-hIgG1 или hu13C5-hIgG4 содержат последовательность HCDR1 - SYGMS (SEQ ID NO: 4), последовательность HCDR2 - SISSGGSTYYPDSVKG (SEQ ID NO: 5), последовательность HCDR3 - GYDSGFAY(SEQ ID NO: 6), последовательность LCDR1 - ASQSVSTSSSSFMH (SEQ ID NO: 10), последовательность LCDR2 - YASNLES (SEQ ID NO: 11) и последовательность LCDR3 - QHSWEIPYT (SEQ ID NO: 12); 5G11, ch5G11-hIgG1, ch5G11-hIgG4, hu5G11-hIgG1 или hu5G11-hIgG4 содержат последовательность HCDR1 - TYGVH (SEQ ID NO: 1), последовательность HCDR2 - VIWRGVTTDYNAAFMS (SEQ ID NO: 2), последовательность HCDR3 - LGFYAMDY ( SEQ ID NO: 3), последовательность LCDR1 - KASQSVSNDVA (SEQ ID NO: 7), последовательность LCDR2 - YAANRYT (SEQ ID NO: 8) и последовательность LCDR3 QQDYTSPYT (SEQ ID NO: 9).
В некоторых вариантах реализации данного изобретения антитело против PD-L1 в фармацевтической комбинации может быть выбрано из одного или более антител. Используемый в контексте данного документа термин «более» относится к более чем одному, например, к двум, трем, четырем, пяти или более. Например, в некоторых вариантах реализации данного изобретения антитело против PD-L1 выбрано из группы, состоящей из антитела, содержащего вариабельную область тяжелой цепи, представленную в SEQ ID NO: 13, и вариабельную область легкой цепи, представленную в SEQ ID NO: 15, или выбрано из группы, состоящей из антитела, содержащего вариабельную область тяжелой цепи, представленную в SEQ ID NO: 14, и вариабельную область легкой цепи, представленную в SEQ ID NO: 16, или выбрано из группы, состоящей из их комбинации. В качестве другого примера, антитело против PD-L1 выбрано из группы, состоящей из антитела, содержащего аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 17, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 18, или выбрано из группы, состоящей из антитела, содержащего аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 19, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 20, или выбрано из группы, состоящей из антитела, содержащего аминокислотную последовательность тяжелой цепи, представленную в SEQ ID NO: 21, и аминокислотную последовательность легкой цепи, представленную в SEQ ID NO: 18, или выбранную из группы, состоящей из комбинаций любого из вышеперечисленных.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 содержит следующие аминокислотные последовательности: область CDR1 тяжелой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 1 или SEQ ID NO: 4; область CDR2 тяжелой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 2 или SEQ ID NO: 5; область CDR3 тяжелой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 3 или SEQ ID NO: 6; область CDR1 легкой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 7 или SEQ ID NO: 10; область CDR2 легкой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 8 или SEQ ID NO: 11; и область CDR3 легкой цепи, имеющую, по меньшей мере, 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 9 или SEQ ID NO: 12.
Фармацевтическая композиция антитела против PD-L1
В некоторых вариантах реализации данного изобретения однократная доза фармацевтической композиции антитела против PD-L1 содержит 300 мг или 600 мг антитела против PD-L1.
В некоторых вариантах реализации данного изобретения общая доза фармацевтической композиции антитела против PD-L1 составляет 600-2400 мг. В некоторых вариантах реализации данного изобретения общая доза фармацевтической композиции антитела против PD-L1 содержит количество, выбранное из группы, состоящей из 600 мг, 900 мг, 1200 мг, 1500 мг, 1800 мг, 2100 мг и 2400 мг, или из диапазона, образованного любым из вышеупомянутых значений. В некоторых вариантах реализации данного изобретения общая доза фармацевтической композиции антитела против PD-L1 предпочтительно составляет 600-2100 мг или 900-1500 мг.
В некоторых вариантах реализации данного изобретения фармацевтическая композиция антитела против PD-L1 представляет собой раствор для инъекций. В некоторых вариантах реализации данного изобретения фармацевтическая композиция антитела против PD-L1 содержит один или более буферов, модификатор изотоничности, стабилизатор и/или поверхностно-активное вещество. В частности, фармацевтическая композиция антитела против PD-L1 содержит 1-150 мг/мл антитела против PD-L1 (например, мАт), 3-50 мМ буфера, 2-150 мг/мл модификатора/стабилизатора изотоничности и 0,01-0,8 мг/мл поверхностно-активного вещества и имеет рН около 4,5-6,8.
В некоторых вариантах реализации данного изобретения в фармацевтической композиции антитела против PD-L1 мАТ против PD-L1 находится в концентрации около 5-150 мг/мл, предпочтительно около 10-60 мг/мл, и более предпочтительно около 10-30 мг/мл (масс./об.). В некоторых конкретных вариантах реализации данного изобретения мАт против PD-L1 находится в концентрации около 10 мг/мл, около 20 мг/мл, около 30 мг/мл, около 40 мг/мл, около 50 мг/мл, около 60 мг/мл, около 70 мг/мл, около 80 мг/мл, около 90 мг/мл, около 100 мг/мл, около 110 мг/мл или около 120 мг/мл; предпочтительно около 10 мг/мл, около 20 мг/мл, около 30 мг/мл, около 40 мг/мл, около 50 мг/мл или около 60 мг/мл; более предпочтительно около 10 мг/мл, около 20 мг/мл или около 30 мг/мл (масс./об.). В некоторых вариантах реализации данного изобретения концентрация мАт против PD-L1 составляет около 10 мг/мл (масс./об.). В других вариантах реализации данного изобретения концентрация мАт против PD-L1 составляет около 30 мг/мл (масс./об.). В других вариантах реализации данного изобретения концентрация мАт против PD-L1 составляет около 60 мг/мл (масс./об.).
В некоторых вариантах реализации данного изобретения буфер представляет собой гистидиновый солевой буфер. Гистидиновый солевой буфер имеет концентрацию около 5-30 мМ, предпочтительно около 10-25 мМ, более предпочтительно около 10-20 мМ и наиболее предпочтительно около 10-15 мМ. В некоторых конкретных вариантах реализации данного изобретения гистидиновый солевой буфер имеет концентрацию около 5 мМ, около 10 мМ, около 15 мМ, около 20 мМ, около 25 мМ или около 30 мМ. В некоторых вариантах реализации данного изобретения гистидиновый солевой буфер имеет концентрацию около 10 мМ. В других вариантах реализации данного изобретения гистидиновый солевой буфер имеет концентрацию около 15 мМ. В других вариантах реализации данного изобретения гистидиновый солевой буфер имеет концентрацию около 20 мМ. Гистидиновый солевой буфер содержит гистидин и соляную кислоту.
В некоторых вариантах реализации данного изобретения модификатор/стабилизатор изотоничности представляет собой сахарозу с концентрацией около 20-150 мг/мл, предпочтительно сахарозу с концентрацией около 40-100 мг/мл и более предпочтительно сахарозу с концентрацией около 60-80 мг/мл (масс./об.). В некоторых конкретных вариантах реализации данного изобретения концентрация сахарозы составляет около 40 мг/мл, 50 мг/мл, 60 мг/мл, 70 мг/мл, 80 мг/мл, 90 мг/мл или 100 мг/мл. В некоторых конкретных вариантах реализации данного изобретения концентрация сахарозы составляет около 60 мг/мл. В некоторых конкретных вариантах реализации данного изобретения концентрация сахарозы составляет около 70 мг/мл. В некоторых конкретных вариантах реализации данного изобретения концентрация сахарозы составляет около 80 мг/мл. В некоторых конкретных вариантах реализации данного изобретения концентрация сахарозы составляет около 90 мг/мл.
В некоторых вариантах реализации данного изобретения поверхностно-активное вещество выбрано из группы, состоящей из полисорбата 80, полисорбата 20 и полоксамера 188; предпочтительно полисорбата 80 и полисорбата 20; и более предпочтительно представляет собой полисорбат 80. В некоторых вариантах реализации данного изобретения концентрация поверхностно-активного вещества составляет около 0,05-0,6 мг/мл, предпочтительно около 0,1-0,4 мг/мл и более предпочтительно около 0,2-0,3 мг/мл (масс./об.).
В некоторых вариантах реализации данной заявки поверхностно-активное вещество представляет собой полисорбат 80 или полисорбат 20 в концентрации около 0,01-0,8 мг/мл (масс./об.). В некоторых конкретных вариантах реализации данного изобретения поверхностно-активное вещество представляет собой полисорбат 80 в концентрации около 0,05-0,6 мг/мл, предпочтительно полисорбат 80 в концентрации около 0,1-0,4 мг/мл, более предпочтительно полисорбат 80 в концентрации около 0,2-0,3 мг/мл и наиболее предпочтительно полисорбат 80 в концентрации около 0,2 мг/мл. В некоторых вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,1 мг/мл, 0,2 мг/мл, 0,3 мг/мл, 0,4 мг/мл, 0,5 мг/мл или 0,6 мг/мл; предпочтительно содержание полисорбата 80 в фармацевтической композиции составляет около 0,2 мг/мл, 0,3 мг/мл, 0,4 мг/мл или 0,5 мг/мл; более предпочтительно содержание полисорбата 80 в фармацевтической композиции составляет около 0,2 мг/мл, 0,3 мг/мл или 0,4 мг/мл; наиболее предпочтительно содержание полисорбата 80 в фармацевтической композиции составляет около 0,2 мг/мл. В некоторых вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,1 мг/мл. В других вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,2 мг/мл. В некоторых вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,3 мг/мл. В других вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,4 мг/мл. В некоторых вариантах реализации данного изобретения содержание полисорбата 80 в фармацевтической композиции составляет около 0,5 мг/мл.
В некоторых вариантах реализации данного изобретения водный раствор фармацевтической композиции имеет уровень pH, выбранный из диапазона 4,0-6,8, предпочтительно 4,5-6,5, более предпочтительно 5,5-6,0 и наиболее предпочтительно 5,5. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 4,5, около 4,8, около 5,0, около 5,2, около 5,4, около 5,5, около 5,6, около 5,8 или около 6,0, предпочтительно около 5,0, около 5,2, около 5,4, около 5,5 или около 5,6 и более предпочтительно около 5,5. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,0. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,2. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,4. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,5. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,6. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 5,8. В некоторых вариантах реализации данного изобретения рН водного раствора в фармацевтической композиции составляет около 6,0.
В некоторых конкретных вариантах реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 20 мг/мл (масс./об.), (b) сахарозу в концентрации около 70 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,1 мг/мл (масс./об.), (d) гистидин в концентрации около 20 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,0. В одном конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) мАт против PD-L1 в концентрации около 20 мг/мл (масс./об.), (b) сахарозу в концентрации около 70 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,1 мг/мл (масс./об.), (d) гистидин в концентрации около 20 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,0.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 10 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,2 мг/мл (масс./об.), (d) гистидин в концентрации около 10 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 50 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,3 мг/мл (масс./об.), (d) гистидин в концентрации около 10 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 100 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,5 мг/мл (масс./об.), (d) гистидин в концентрации около 10 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 30 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,2 мг/мл (масс./об.), (d) гистидин в концентрации около 10 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 60 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,2 мг/мл (масс./об.), (d) гистидин в концентрации около 10 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) антитело против PD-L1 в концентрации около 10 мг/мл (масс./об.), (b) сахарозу в концентрации около 70 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,4 мг/мл (масс./об.), (d) гистидин в концентрации около 20 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 6,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция содержит: (а) мАт против PD-L1 в концентрации около 10 мг/мл (масс./об.), (b) сахарозу в концентрации около 80 мг/мл (масс./об.), (c) полисорбат 80 в концентрации около 0,2 мг/мл (масс./об.), (d) гистидин в концентрации около 20 мМ и (e) необязательно подходящее количество соляной кислоты для доведения рН композиции до около 5,5.
В другом конкретном варианте реализации данного изобретения фармацевтическая композиция представляет собой водорастворимую инъекцию, включая, но не ограничиваясь этим, водорастворимый состав без лиофилизации или водорастворимый состав, восстановленный из лиофилизированного порошка. В некоторых вариантах реализации данного изобретения фармацевтическая композиция является лиофилизированной. Лиофилизированный состав относится к составу, полученному путем подвергания водного раствора процессу лиофилизации, при котором вещество сначала замораживают, а затем уменьшают количество растворителя путем сублимации (основного процесса сушки), а затем десорбции (дополнительного процесса сушки), до тех пор пока количество растворителя не уменьшится до значения, при котором больше не поддерживается биологическая активность или химическая реакция. Лиофилизированные составы по данной заявке также могут быть высушены другими способами, известными в данной области техники, такими как сушка распылением и барботажная сушка.
Рак почек
В данной заявке рак почек включает наследственный рак почек и спорадический рак почек.
В некоторых вариантах реализации данного изобретения рак почек включает светлоклеточную почечно-клеточную карциному и несветлоклеточную почечно-клеточную карциному.
В данной заявке рак почек включает, но не ограничивается ими, светлоклеточную почечно-клеточную карциному, мультилокулярную кистозную почечную опухоль низкой степени злокачественности, папиллярную почечно-клеточную карциному, наследственный лейомиоматоз и почечно-клеточную карциному, связанную с синдромом почечно-клеточной карциномы, хромофобную почечно-клеточную карциному, карциному собирательных трубочек, почечно-медуллярную карциному, почечно-клеточную карциному с транслокацией семейства MiT, почечно-клеточную карциному с дефицитом сукцинатдегидрогеназы, муцинозную, тубулярную и веретеноклеточную карциному, тубулокистозную почечно-клеточную карциному, приобретенную кистозную болезнь, связанную с почечно-клеточной карциномой, светлоклеточную папиллярную почечно-клеточную карциному, неклассифицированную почечно-клеточную карциному, папиллярную аденому и онкоцитому, на основании гистологического типирования.
В некоторых вариантах реализации данного изобретения рак почек выбран из светлоклеточной почечно-клеточной карциномы или из почечно-клеточной карциномы с преобладанием светлоклеточных компонентов.
В некоторых вариантах реализации данного изобретения пациент с раком почек представляет собой пациента с раком почек низкого риска, пациента с раком почек среднего риска или пациента с раком почек высокого риска. В некоторых вариантах реализации данного изобретения пациент с раком почки представляет собой пациента с почечно-клеточной карциномой низкого риска или пациента с почечно-клеточной карциномой среднего риска. В некоторых вариантах реализации данного изобретения пациент с раком почки представляет собой пациента с распространённой почечно-клеточной карциномой среднего риска.
В некоторых вариантах реализации данного изобретения рак почек включает, но не ограничивается ими, локализованный рак почек, местно-распространенный рак почек, синхронный метастатический рак почек и метахронный метастатический рак почек. В некоторых вариантах реализации данного изобретения рак почек представляет собой местно-распространенный рак почек. В других вариантах реализации данного изобретения рак почек представляет собой метастатический рак почек.
В некоторых вариантах реализации данного изобретения рак почек представляет собой почечно-клеточную карциному, ранее не подвергавшуюся лечению. В некоторых вариантах реализации данного изобретения рак почек представляет собой распространённую почечно-клеточную карциному, ранее не подвергавшуюся лечению. В некоторых вариантах реализации данного изобретения рак почек представляет собой распространённую светлоклеточную почечно-клеточную карциному, ранее не подвергавшуюся лечению, или распространённую несветлоклеточную почечно-клеточную карциному, ранее не подвергавшуюся лечению. В некоторых вариантах реализации данного изобретения рак почек представляет собой распространённую светлоклеточную почечно-клеточную карциному, ранее не подвергавшуюся лечению, или распространённую почечно-клеточную карциному с преобладанием светлоклеточных компонентов, ранее не подвергавшуюся лечению.
В некоторых вариантах реализации данного изобретения рак почек представляет собой рак, который ранее лечили с помощью одной или более схем лечения, которые закончились неудачей; в некоторых вариантах реализации данного изобретения рак почек представляет собой рак, который ранее лечили с помощью одной, двух, трех, четырех или пяти схем лечения, которые закончились неудачей.
В некоторых вариантах реализации данного изобретения рак почек выбран из рецидивирующего или рефрактерного рака почек; в некоторых вариантах реализации данного изобретения у пациента с раком почек возникает рецидив после лечения по предшествующей схеме лечения и достижения объективного ответа, или у пациента с раком почек не достигается объективный ответ на предшествующую схему лечения.
В некоторых вариантах реализации данного изобретения рак почек представляет собой рак, который ранее не подвергался системному лечению. В некоторых вариантах реализации данного изобретения рак почек представляет собой рак, который ранее лечился с использованием цитокиновой терапии, которая закончилась неудачей, и/или является резистентным к лекарству.
В данной заявке предшествующее лечение включает, но не ограничивается этим, хирургическое лечение, медикаментозное лечение, и/или интервенционное лечение.
В некоторых вариантах реализации данного изобретения предшествующее лечение включает, но не ограничивается этим, хирургическое лечение, лучевую терапию и/или медикаментозное лечение. Хирургическое лечение включает, но не ограничивается этим, нефронсберегающую операцию, радикальную нефрэктомию, диссекцию лимфатических узлов, операцию тромбоза опухоли нижней полой вены, опухоль-уменьшающую нефрэктомию, и резекцию олигометастаза. Лучевая терапия включает, но не ограничивается этим, лучевую терапию, уменьшающую симптомы, или радикальную лучевую терапию. Медикаментозное лечение включает, но не ограничивается этим, химиотерапию, цитокиновую терапию, и/или направленную медикаментозную терапию.
В некоторых вариантах реализации данного изобретения медикаментозное лечение включает, но не ограничивается этим, введение одного или более из следующего: циклофосфамида, ифосфамида, винкристина, преднизола, преднизолона, метилпреднизолона, фторурацилов (включая, но не ограничиваясь ими, 5-фторурацил, тегафур-гимерацил-отарацил калия, тегафур и капецитабин), бицинов (включая, но не ограничиваясь ими, адриамицин, пирарубицин, амрубицин, эпирубицин, акларубицин и идарубицин), антифолатов (включая, но не ограничиваясь им, метотрексат), цитарабина, азацитидина, флударабина, бендамустина, митоксантрона, этопозида, прокарбазина, гемцитабина, месна, дексаметазона, лейковорина, препараты платины (включая, но не ограничиваясь ими, оксалиплатин, цисплатин, карбоплатин, недаплатин, дициклоплатин и мириплатин), аналогов камптотецина (включая, но не ограничиваясь ими, камптотецин, гидроксикамптотецин, иринотекан и топотекан), таксанов (включая, но не ограничиваясь ими, паклитаксел, паклитаксел, связанный с альбумином, и доцетаксел), IL-2, INF-α, сунитиниба, сорафениба, пазопаниба, акситиниба, ленватиниба, кабозантиниба, эверолимуса, темсиролимуса, тивозаниба, бевацизумаба, пембролизумаба, ипилимумаба, ниволумаба и авелумаба.
В некоторых вариантах реализации данного изобретения медикаментозное лечение представляет собой комбинацию низкомолекулярного лекарственного препарата направленного действия, и биологического лекарственного препарата направленного действия, включая, но не ограничиваясь этим, комбинацию авелумаба и акситиниба, комбинацию ниволумаба и ипилимумаба, комбинацию пембролизумаба и акситинибаили комбинацию атезолизумаба и бевацизумаба.
В еще одном аспекте в настоящей заявке также предложено антитело против PD-L1 для применения при лечении рака почек. В данной заявке также предложен способ лечения рака почек, который включает введение нуждающемуся в этом пациенту эффективного количества антитела против PD-L1 по данной заявке. В данной заявке также предложено применение антитела против PD-L1 для лечения рака почек. В данной заявке также предложено применение антитела против PD-L1 для получения лекарственного средства для лечения рака почек.
Схема введения фармацевтической комбинации или фармацевтической композиции
В некоторых вариантах реализации данного изобретения при применении или способе лечения, описанном выше, антитело против PD-L1 и анлотиниб или его фармацевтически приемлемая соль находятся в форме фармацевтической композиции и могут вводиться одновременно, последовательно или через интервалы.
В некоторых вариантах реализации данного изобретения при применении или способе лечения, описанном выше, антитело против PD-L1 и анлотиниб вводят отдельно через определенные промежутки времени. В некоторых вариантах реализации данного изобретения антитело и анлотиниб вводят отдельно по одной и той же схеме или по разным схемам. В некоторых вариантах реализации данного изобретения эти два препарата вводят отдельно по разным схемам.
В некоторых вариантах реализации данного изобретения при применении или способе лечения, описанном выше, антитело против PD-L1 можно вводить один раз в неделю (q1w), один раз каждые 2 недели (q2w), один раз каждые 3 недели (q3w), или один раз каждые 4 недели (q4w). В одном конкретном варианте реализации данного изобретения антитело против PD-L1 вводят один раз каждые 3 недели. В некоторых вариантах реализации данного изобретения антитело против PD-L1 вводят в дозе 600-2400 мг при каждом введении.
Анлотиниб или его фармацевтически приемлемую соль можно вводить в дозе 6 мг, 8 мг, 10 мг или 12 мг один раз в день по схеме последовательного 2-недельного лечения с последующим 1-недельным перерывом.
В некоторых вариантах реализации данного изобретения антитело против PD-L1 и анлотиниб или его фармацевтически приемлемая соль применяют в одинаковых или разных циклах лечения. В некоторых конкретных вариантах реализации данного изобретения антитело против PD-L1 и анлотиниб применяют в одинаковых циклах лечения, например, в 1-недельных, 2-недельных, 3-недельных или 4-недельных циклах лечения.
В некоторых вариантах реализации данного изобретения при применении или способе лечения один цикл лечения составляет 21 день; антитело PD-L1 вводят в первый день каждого цикла лечения, а анлотиниб или его фармацевтически приемлемую соль вводят ежедневно в дни 1-14 каждого цикла. В некоторых вариантах реализации данного изобретения антитело против PD-L1 вводят один раз в первый день каждого цикла лечения, а анлотиниб или его фармацевтически приемлемую соль вводят один раз в день в дни 1-14 каждого цикла.
В некоторых вариантах реализации данного изобретения при применении или способе лечения антитело против PD-L1 можно вводить субъекту в дозе, выбранной из группы, состоящей из: от 0,01 до 40 мг/кг, от 0,1 до 30 мг/кг, от 0,1 до 20 мг/кг, от 0,1 до 15 мг/кг, от 0,1 до 10 мг/кг, от 1 до 15 мг/кг, от 1 до 20 мг/кг, от 1 до 3 мг/кг, от 3 до 10 мг/кг, от 3 до 15 мг/кг, от 3 до 20 мг/кг, от 3 до 30 мг/кг, от 10 до 20 мг/кг или от 15 до 20 мг/кг, или вводят субъекту в дозе от 60 мг до 2400 мг, от 90 мг до около 1800 мг, от 120 мг до 1500 мг, от 300 мг до 900 мг, от 600 мг до 900 мг, от 300 мг до 1200 мг, от 600 мг до 1200 мг или от 900 мг до 1200 мг.
В некоторых вариантах реализации данного изобретения при применении или способе лечения один цикл лечения составляет 21 день; 1200 мг антитела против PD-L1 вводят в первый день каждого цикла лечения и 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли вводят ежедневно в дни 1-14 каждого цикла лечения.
В некоторых вариантах реализации данного изобретения в 3-недельном цикле лечения субъекту вводят антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль в массовом соотношении (0,35-29):1, предпочтительно (3,5-29):1, более предпочтительно (3,5-14,5):1, и наиболее предпочтительно (7-14,5):1, при этом антитело против PD-L1 и анлотиниб или его фармацевтически приемлемую соль вводят в виде однократной дозы и многократных доз, соответственно.
Введение препарата
Приведенное ниже содержание не предназначено для ограничения введения фармацевтической комбинации, описанной в данном документе.
Компоненты фармацевтической комбинации или фармацевтической композиции по данной заявке можно вводить независимо, или некоторые или все компоненты вводят совместно различными подходящими путями, включая, но не ограничиваясь этим, пероральное введение или парентеральное введение (внутривенным, внутримышечным, местным или подкожным путем). В некоторых вариантах реализации данного изобретения компоненты фармацевтической комбинации, описанной в данном документе, можно вводить независимо, или некоторые или все компоненты вводят совместно посредством перорального введения или инъекции, например, внутривенной инъекции или внутрибрюшинной инъекции.
Компоненты в фармацевтической композиции, описанной в данном документе, могут быть приготовлены независимо в подходящих дозированных формах, или некоторые или все компоненты объединены в подходящие лекарственные формы, включая, но не ограничиваясь ими, таблетки, леденцы, пилюли, капсулы (например, твердая капсула, мягкая капсула, кишечнорастворимая капсула и микрокапсула), настойку, гранулу, сироп, инъекцию (внутримышечную, внутривенную и внутрибрюшинную), эмульсию, суспензию, раствор, диспергирующее вещество и лекарственные формы составов с замедленным высвобождением для перорального или неперорального введения.
Компоненты фармацевтической комбинации, описанной в данном документе, могут быть приготовлены независимо друг от друга, или некоторые или все компоненты могут быть приготовлены совместно с фармацевтически приемлемым носителем и/или эксципиентом.
Фармацевтическая комбинация, описанная в данном документе, может дополнительно содержать дополнительный терапевтический агент. В одном варианте реализации данного изобретения дополнительный терапевтический агент может представлять собой терапевтический агент для лечения рака почек, известный в данной области техники.
Фармацевтическая комбинация или фармацевтическая композиция по данной заявке, описанные выше, оказывают следующие полезные эффекты:
(1) лучшая эффективность в контроле роста опухоли или даже в устранении опухолей по сравнению с любым лекарственным средством из комбинации, вводимым отдельно;
(2) меньшие дозы по сравнению с любым лекарственным средством из комбинации, вводимым отдельно;
(3) хорошая переносимость пациентами и меньше побочных эффектов и/или осложнений по сравнению с любым лекарственным средством, вводимым отдельно;
(4) более высокий уровень контроля заболевания у пациентов, получавших лечение;
(5) большая выживаемость (например, медиана выживаемости, выживаемость без прогрессирования или общая выживаемость) у пациентов, получавших лечение;
(6) большая выживаемость (например, медиана выживаемости, выживаемость без прогрессирования или общая выживаемость) у пациентов, получавших лечение, по сравнению со стандартной химиотерапией;
(7) большая продолжительность ответа (DOR); и/или
(8) лучшая активность при лечении рака почек и лучший противоопухолевый синергетический эффект по сравнению с любым лекарственным средством из комбинации, вводимый отдельно.
Определения и описание
Если не указано иное, следующие термины, используемые в данном документе, имеют следующие значения. Отдельный термин, если не указано иное, не следует считать неопределенным или неясным, а следует толковать в соответствии с его общепринятым значением в данной области техники. Когда речь идет о торговом наименовании, подразумевается, что оно относится к соответствующему коммерческому продукту или его активному ингредиенту.
Если не указано иное, дозы и диапазоны, предложенные в данном документе для анлотиниба или его соли, основаны на молекулярной массе формы свободного основания анлотиниба.
Используемый в контексте данного документа термин «фармацевтическая комбинация» относится к комбинации двух или более активных ингредиентов (которые вводят в виде самих соответствующих активных ингредиентов или в виде их соответствующих производных, таких как фармацевтически приемлемые соли или сложные эфиры, пролекарства или композиции), которые вводят одновременно или последовательно. Активные вещества можно вводить субъекту одновременно или последовательно в любом порядке в виде одного состава.
Используемый в контексте данного документа термин «антитело» относится к связывающему белку, имеющего, по меньшей мере, один антигенсвязывающий домен. Антитело и его фрагмент по данной заявке могут представлять собой интактное антитело или любой его фрагмент. Таким образом, антитело и его фрагмент по данной заявке включают моноклональное антитело или его фрагмент и вариант антитела или его фрагмент, а также иммуноконъюгат. Примеры фрагмента антитела включают Fab-фрагмент, Fab'-фрагмент, F(ab')2 -фрагмент, Fv-фрагмент, выделенную область CDR, одноцепочечную молекулу Fv (scFv), Fd-фрагмент и другие известные в данной области техники фрагменты антител. Антитело и его фрагмент могут также включать рекомбинантный полипептид, слитый белок и биспецифическое антитело. Антитело против PD-L1 и его фрагмент, описанные в данном документе, могут относиться к изотипу IgG1, IgG2, IgG3 или IgG4. Термин «изотип» относится к классу антител, кодируемых геном константной области тяжелой цепи. В одном варианте реализации данного изобретения антитело против PD-L1 и его фрагмент, описанные в данном документе, могут относиться к изотипу IgG1 или IgG4. Антитело против PD-L1 и его фрагмент по данной заявке могут быть получены из любых видов, включая, но не ограничиваясь ими, мышь, крысу, кролика, примата, ламу и человека. Антитело против PD-L1 и его фрагмент могут представлять собой химерное антитело, гуманизированное антитело или интактное антитело человека. В одном варианте реализации данного изобретения антитело против PD-L1 представляет собой антитело, продуцируемое линией клеток гибридомы, полученной от мыши. Таким образом, в одном варианте реализации данного изобретения антитело против PD-L1 представляет собой мышиное антитело. В другом варианте реализации данного изобретения антитело против PD-L1 представляет собой химерное антитело. В другом варианте реализации данного изобретения химерное антитело представляет собой химерное антитело мыши-человека. В другом варианте реализации данного изобретения антитело представляет собой гуманизированное антитело. В другом варианте реализации данного изобретения антитело получено из мышиного антитела и является гуманизированным.
Термин «гуманизированное антитело» относится к антителу, содержащему области, определяющие комплементарность (CDR), полученные из нечеловеческого антитела, и каркасные и константные области, полученные из антитела человека. Например, антитело против PD-L1, описанное в данном документе, может содержать CDR, полученные из одного или более мышиных антител, а также каркасные и константные области антитела человека. Таким образом, в одном варианте реализации данного изобретения гуманизированное антитело, описанное в данном документе, связывается с тем же эпитопом на PD-L1, что и мышиное антитело, из которого получены CDR гуманизированного антитела. Иллюстративные гуманизированные антитела описаны в данном документе. Дополнительные антитела против PD-L1 или их варианты, содержащие CDR тяжелой и легкой цепей, описанные в данном документе, могут быть созданы с использованием любых каркасных последовательностей антитела человека, и они также включены в данную заявку. В одном варианте реализации данного изобретения каркасные последовательности, подходящие для использования по данной заявке, включают последовательности, сходные по структуре с каркасными последовательностями, описанными в данном документе. Дополнительные модификации могут быть сделаны в каркасных областях для улучшения свойств антител, описанных в данном документе. Такие дополнительные модификации каркасных областей могут включать: химические модификации, точечные мутации для снижения иммуногенности или удаления эпитопов Т-клеток, или модификации, возвращающие мутации к остаткам исходных последовательностей зародышевой линии. В некоторых вариантах реализации данного изобретения такие модификации включают модификации, соответствующие мутациям, приведенным в качестве примеров в данном документе, включая реверсии последовательностей зародышевой линии. Например, в одном варианте реализации данного изобретения одна или более аминокислот в каркасных областях VH и/или VL человека гуманизированных антител, описанных в данном документе, возвращаются к соответствующим аминокислотам в исходных мышиных антителах. Например, для VH и VL гуманизированных антител 5G11 и 13C5 несколько сайтов каркасных аминокислот матричных антител человека, описанных выше, возвращаются к соответствующим аминокислотным последовательностям мышиных антител 5G11 и 13C5. В одном варианте реализации данного изобретения аминокислоты в положении 53, 60 и/или 67 вариабельной области легкой цепи возвращаются к соответствующим аминокислотам, обнаруженных в положениях вариабельной области легкой цепи мышиных 5G11 или 13C5. В другом варианте реализации данного изобретения аминокислоты в положении 24, 28, 30, 49, 73, 83 и/или 94 вариабельной области тяжелой цепи возвращаются к соответствующим аминокислотам, обнаруженных в положениях вариабельной области тяжелой цепи мышиных 5G11 или 13C5. В одном варианте реализации данного изобретения гуманизированное антитело 5G11 содержит: вариабельную область легкой цепи, в которой аминокислота в положении 60 мутирована с Ser (S) на Asp (D), а аминокислота в положении 67 мутирована с Ser (S) на Tyr (Y); и вариабельную область тяжелой цепи, в которой аминокислота в положении 24 мутирована с Phe (F) на Val (V), аминокислота в положении 49 мутирована с Ala (A) на Gly (G), аминокислота в положении положение 73 мутирована с Thr (T) на Asn (N), и аминокислота в положении 83 мутирована с Thr (T) на Asn (N). В одном варианте реализации данного изобретения гуманизированное антитело 13C5 содержит: вариабельную область легкой цепи, в которой аминокислота в положении 53 мутирована с Tyr (Y) на Lys (K); и вариабельную область тяжелой цепи, в которой аминокислота в положении 28 мутирована с Thr (T) на Ile (I), аминокислота в положении 30 мутирована с Ser (S) на Arg (R), аминокислота в положении 49 мутирована с Ser (S) на Ala (A), и аминокислота в положении 94 мутирована с Tyr (Y) на Asp (D). Дополнительные или альтернативные реверсивные мутации могут быть сделаны в каркасных областях гуманизированных антител, описанных в данном документе, для улучшения свойств антител. Данная заявка также включает гуманизированные антитела, которые связываются с PD-L1 и содержат модификации каркаса, соответствующие иллюстративным модификациям, раскрытым в данном документе, относительно любой подходящей каркасной последовательности, а также другим модификациям каркаса, которые иным образом улучшают свойства антитела.
В данной заявке предложены выделенное антитело или его фрагмент, которые связываются с PD-L1, при этом антитело может быть получено с использованием гибридомы, выбранной из группы, состоящей из гибридом, обозначенных в данном документе как 13C5 и 5G11. Соответственно, данная заявка также включает гибридомы 13C5 и 5G11 и любые гибридомы, которые продуцируют описанные в данном документе антитела. В данной заявке также предложены выделенные полинуклеотиды, кодирующие антитела и их фрагменты, описанные в данном документе. Данная заявка также включает векторы экспрессии, содержащие выделенные полинуклеотиды, и клетки-хозяева, содержащие векторы экспрессии.
«Выделенное антитело» относится к антителу, которое, по существу, не содержит других антител, обладающих другой антигенной специфичностью (например, выделенное антитело, которое специфически связывается с PD-1, по существу, не содержит антител, которые специфически связываются с антигенами, отличными от PD-1). Однако выделенное антитело, которое специфически связывается с PD-1, может иметь перекрестную реактивность с другими антигенами (такими как молекулы PD-1 разных видов). Кроме того, выделенное антитело может, по существу, не содержать других клеточных материалов и/или химических веществ.
Термин «моноклональное антитело» («мАт») относится к не встречающемуся в природе составу молекул антител из отдельного компонента молекулы (т.е. молекул антител, последовательности оснований которых практически идентичны и которые проявляют одинаковую специфичность связывания и аффинность к конкретному эпитопу). мАт представляет собой пример выделенного антитела. мАт могут быть получены гибридомными способами, рекомбинантными способами, трансгенными способами или другими способами, известными специалистам в данной области техники.
Антитело или его антигенсвязывающий фрагмент, описанные в данном документе, специфичны в отношении PD-L1. В одном варианте реализации данного изобретения антитело или его фрагмент специфичны в отношении PD-L1. В одном варианте реализации данного изобретения антитело или его фрагмент, описанные в данном документе, связываются с PD-L1 человека или примата, но не связываются с PD-L1 любых других млекопитающих. В другом варианте реализации данного изобретения антитело или его фрагмент не связываются с PD-L1 мыши. Термины «PD-L1 человека», “hPD-L1” и “huPD-L1” и т.п. используются в данном документе взаимозаменяемо и относятся к PD-L1 человека и вариантам или изотипам PD-L1 человека. Термины «специфический», «специфичность» и «специфически» относятся к тому, что антитело или его фрагмент связываются с PD-L1 с большей аффинностью, чем с любыми другими мишенями.
Термины «лечить», «терапия» и «лечение» обычно относятся к получению необходимого фармакологического эффекта и/или физиологического эффекта. Что касается частичной или полной стабилизации или лечения заболевания и/или побочного эффекта заболевания, эффект может быть терапевтическим. Используемые в контексте данного документа термины «лечить», «терапия» и «лечение» охватывают любое лечение заболевания у пациента, включая (а) подавление симптома заболевания, т.е. блокирование прогрессирования заболевания; или (b) облегчение симптома заболевания, т.е. достижение ремиссии заболевания или симптома.
Термин «эффективное количество» относится к количеству соединения, описанного в данном документе, для (i) лечения конкретного заболевания, состояния или расстройства; (ii) облегчения, ослабления или устранения одного или более симптомов конкретного заболевания, состояния или расстройства, или (iii) предотвращения или задержки появления одного или более симптомов конкретного заболевания, состояния или расстройства, описанных в данном документе. Количество активного вещества (например, антитела или соединения, описанного в данном документе), составляющее «терапевтически эффективное количество», может варьироваться в зависимости от таких факторов, как состояние болезни, возраст, пол и масса тела индивидуума, а также от способности терапевтического средства или комбинации терапевтических средств вызывать желаемый ответ у индивидуума. Эффективное количество также может быть определено обычным образом специалистами в данной области техники в соответствии с их знаниями и данным изобретением.
Термины «вводить», «введение» и «применение» относятся к физическому введению композиции, содержащей терапевтическое средство, субъекту с использованием любого из множества способов и систем доставки, известных специалистам в данной области техники. Пути введения ингибиторов иммунных контрольных точек (например, антитела против PD-1 или антитела против PD-L1) включают внутривенный, внутримышечный, подкожный, внутрибрюшинный, спинальный или другие парентеральные пути введения, например, путем инъекции или инфузии. Используемая в контексте данного документа фраза «парентеральное введение» относится к способам введения помимо энтерального и местного введения, обычно путем инъекции, включая, но не ограничиваясь этим, внутривенную, внутримышечную, внутриартериальную подоболочечную, внутрилимфатическую, внутриочаговую, внутрикапсулярную, внутриглазничную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, подкапсулярную, субарахноидальную, интраспинальную, эпидуральную и интрастернальную инъекцию и инфузию и электропорацию in vivo. В некоторых вариантах реализации данного изобретения ингибитор контрольной точки иммунного ответа (например, антитело против PD-1 или антитело против PD-L1) вводят непарентеральным путем, а в некоторых вариантах реализации данного изобретения - путем перорального введения. Другие непарентеральные пути введения включают местный, эпидермальный или мукозальный пути, например, интраназальный, вагинальный, ректальный, сублингвальный или местный путь. Введение также может быть выполнено, например, один раз, несколько раз и/или в течение одного или более продолжительных периодов времени.
Термин «доза» относится к дозе, вводимой пациенту без учета массы тела или площади поверхности тела (ППТ) пациента. Например, человек с массой тела 60 кг и человек с массой тела 100 кг получат одинаковую дозу антитела (например, 240 мг антитела против PD-1).
Фраза «фармацевтически приемлемый» используется в данном описании для обозначения таких соединений, материалов, композиций и/или лекарственных форм, которые подходят для применения в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнения.
Термин «фармацевтически приемлемая соль» включает соли, образованные из свободного основания и кислоты, и соли, образованные из кислоты и свободного основания, например, гидрохлорид, гидробромид, нитрат, сульфат, фосфат, формиат, ацетат, трифторацетат, фумарат, оксалат, малеат, цитрат, сукцинат, мезилат, бензолсульфонат и p-метилбензолсульфонат, предпочтительно гидрохлорид, гидробромид, сульфат, формиат, ацетат, трифторацетат, фумарат, малеат, мезилат, p-метилбензолсульфонат, натриевая соль, калиевая соль, аммониевая соль и соль аминокислоты и так далее. В данной заявке при образовании фармацевтически приемлемой соли кислота и свободное основание находятся в молярном соотношении от около 1:0,2 до около 1:5, предпочтительно 1:0,5, 1:1, 1:2, 1:3, 1:4, 1:5, 1:6, 1:7 или же 1:8.
Используемые в контексте данного документа термины "субъект" и "пациент" используются взаимозаменяемо. В некоторых вариантах реализации данного документа термин «субъект» или «пациент» относится к млекопитающему. В некоторых вариантах реализации данного изобретения субъект или пациент представляет собой мышь. В некоторых вариантах реализации данного изобретения субъект или пациент представляет собой человека.
Под термином «около» следует понимать диапазон трех стандартных отклонений от среднего значения или стандартный диапазон допуска в конкретной области. В некоторых вариантах реализации данного документа термин «около» следует понимать как отклонение, не превышающее 0,5. Термин «около» изменяет все перечисленные после него значения. Например, «около 1, 2 и 3» означает «около 1», «около 2» и «около 3».
Термин «однократная доза» относится к наименьшей единице упаковки, содержащей определенное количество фармацевтического продукта; например, в коробке из семи капсул каждая капсула представляет собой однократную дозу; или флакон для инъекций представляет собой однократную дозу. Используемые в контексте данного документа термины «однократная доза» и «разовая доза» имеют одинаковое значение и используются взаимозаменяемо.
Термин «многократная доза» состоит из множества однократных доз.
Термин «фармацевтическая композиция» относится к смеси, состоящей из одного или более активных ингредиентов или их фармацевтических комбинаций по данной заявке и фармацевтически приемлемого эксципиента. Фармацевтическая композиция предназначена для облегчения введения субъекту соединения или его фармацевтической комбинации, описанных в данном документе.
Если в данном документе не указано иное, термины в единственном числе охватывают формы множественного числа, и наоборот.
Используемые в данном документе, если не указано иное, термины «содержать», «содержит» и «содержащий» или их эквиваленты являются открытыми утверждениями и означают, что элементы, компоненты и этапы, которые не указаны, могут быть включены в дополнение к перечисленным.
Пациенты с низким, средним и высоким риском стратифицированы в соответствии с критериями Международного консорциума по лечению метастатического рака почек (IMDC). В частности, критерии следующие:
Прогностическая стратификация риска
Примечание: а. формула расчета скорректированного кальция в сыворотке: скорректированный кальций в крови [Ca2+] (мг/л) = измеренный кальций [Ca2+] (мг/л) + 0,8 × (4 - значение альбумина)
Все патенты, патентные заявки и другие публикации прямо включены в данный документ в полном объеме посредством ссылки для целей описания и раскрытия данного изобретения. Данные публикации предоставлены исключительно потому, что они были раскрыты до даты подачи данной заявки. Все заявления относительно дат этих документов или описание содержания этих документов основаны на информации, доступной заявителю, и не являются признанием правильности дат или содержания этих документов. Кроме того, в любой стране или регионе любая ссылка на эти публикации в данном документе не должна рассматриваться как признание того, что публикации являются частью общепризнанных знаний в данной области техники.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Для ясности данная заявка дополнительно описана с помощью следующих примеров, которые, однако, не предназначены для ограничения объема данной заявки. Все реагенты, используемые в контексте данного документа, коммерчески доступны и могут использоваться без дополнительной очистки. В примерах антитело против PD-L1 получали, как описано в WO 2016022630, и после аффинной хроматографии элюат, содержащий антитело, получали обычными способами очистки антител.
Пример 1. Клиническое Исследование Рака Почек
Субъектам с раком почек, которые соответствовали критериям, вводили инъекции антитела против PD-L1 и давали капсулы анлотиниба гидрохлорида. Оценку ответа проводили каждые 6 недель (42 дня). Субъекты с контролем заболевания и переносимыми побочными эффектами могли непрерывно принимать лекарства до тех пор, пока клинические преимущества не были потеряны, пока токсичность не стала непереносимой, до тех пор, пока PD не было определено оценкой ответа, или пока исследователь не счел дальнейшее лечение нецелесообразным, в зависимости от того, что происходило раньше. Затем исследование заканчивалось.
1.1 Основные критерии включения:
1) гистопатологически подтвержденный светлоклеточный почечно-клеточный рак, включая распространенный почечно-клеточный рак с преобладанием светлоклеточных компонентов;
2) Не подвергались системному лечению местно-распространенных/метастатических заболеваний (были зарегистрированы те, у кого предыдущая цитокиновая терапия была неудачной/были резистентные к лекарственным препаратам);
3) Неоперабельные местно-распространенные/метастатические заболевания, имеющие, по меньшей мере, одно измеримое поражение в соответствии с Критериями оценки ответа солидных опухолей на лечение (RECIST 1.1); и
4) Возраст: 18-80 лет (рассчитывается на дату подписания формы согласия); мужчина или женщина; оценка по шкале ECOG: 0-1; ожидаемая выживаемость ≥ 3 месяцев.
1.2 Исследуемый лекарственный препарат
Инъекция антитела против PD-L1 - hu5G11-hIgG1: 1200 мг антитела против PD-L1 для инъекции разбавляли до 250 мл физиологическим раствором, а время инфузии составляло 60 ± 10 мин (от начала инфузии инъекции антитела против PD-L1 до окончания инфузии инъекции антитела против PD-L1 и завершения промывки трубки физиологическим раствором (рекомендуется 20 мл)). Инъекцию антитела против PD-L1 вводили в первый день и один раз в 21 день, то есть 21 день считали циклом лечения. (т.е. инъекция антитела против PD-L1: 1200 мг, d1/q3w) дозировка: 600 мг/20 мл.
Капсула анлотиниба гидрохлорида (действующее вещество - анлотиниб дигидрохлорид): один раз в сутки (перорально перед завтраком) по 1 капсуле (10 мг) каждый раз. Пероральное введение осуществляли в течение 2 недель подряд с перерывом на 1 неделю, то есть за цикл лечения засчитывали 21 день, и препарат вводили в дни 1-14 каждого цикла. За исключением особых обстоятельств, рекомендуется принимать его в определенное время каждый день. (например, капсула анлотиниба гидрохлорида: 10 мг/1 раз в день, 1-14 дней/q3w)
Исследователь может отрегулировать дозу капсул анлотиниба гидрохлорида, например, до 12 мг, 10 мг или 8 мг, в зависимости от состояния заболевания, безопасности и других аспектов.
1.3 Критерии оценки
Оценка безопасности: были приняты критерии NCI-CTCAE 5.0.
Оценка ответа: были приняты критерии RECIST 1.1 и критерии iRECIST.
1.4 Конечные точки
Основная конечная точка
Показатель эффективности: выживаемость без прогрессирования заболевания (PFS) согласно оценке Независимого наблюдательного комитета (IRC).
Дополнительные конечные точки
Показатели эффективности: выживаемость без прогрессирования (PFS), общая выживаемость (OS), частота объективных ответов (ORR = полный ответ (CR) + частичный ответ (PR)), скорость контроля заболевания (DCR = CR + PR + стабильное заболевание (SD)), продолжительность ответа (DOR), 12-месячная выживаемость без прогрессирования, 12-месячная и 24-месячная общая выживаемость и оценка качества жизни, данные по оценке исследователя; и показатели эффективности, связанные с иммунитетом (такие как iPFS).
Показатели безопасности: частота и тяжесть нежелательных явлений (НЯ), отклонение от нормы лабораторных показателей и серьезные нежелательные явления (СНЯ).
Биомаркер: корреляция экспрессии PD-L1 с ответом.
Иммуногенность инъекции антитела против PD-L1: положительная частота антител против лекарственного средства (ADA) и так далее.
1.5 Ответ
Предварительные исследования продемонстрировали, что субъекты могут получить пользу от лечения и добиться значимого ответа. На момент получения данных в этом исследовании применения гидрохлорида анлотиниба в сочетании с антителом против PD-L1 для лечения почечно-клеточной карциномы (капсулы анлотиниба гидрохлорида вводили субъектам в дозе 12 мг/qd, день1-14/q3w), 34 субъекта в исследуемой группе (группа анлотиниба гидрохлорида в сочетании с антителом против PD-L1) прошли не менее 2 циклов лечения, а некоторые из них завершили 10 циклов лечения; согласно статистике по наилучшему ответу, у 16 пациентов (16/34) достигнута стабилизация заболевания, а у 17 пациентов (17/34) достигнут частичный ответ, как указано в Таблице 1, в которой пациенты были классифицированы в соответствии с критериями IMDC на пациентов с низким риском, пациентов со средним риском и пациентов с высоким риском.
(0,00%)
(0,00%)
(0,00%)
(0,00%)
(58,33%)
(50,00%)
(33,33%)
(50,00%)
(41,67%)
(50,00%)
(50,00%)
(47,06%)
(0,00%)
(0,00%)
(16,67%)
(2,94%)
(58,33%)
(50,00%)
(33,33%)
(50,00%)
(100,00%)
(83,33%)
(97,06%)
Кроме того, результаты демонстрируют, что схема комбинированного лечения дает быстрый ответ при лечении рака почек; как представлено в Таблице 2, после 2 циклов лечения результаты оценки ответа продемонстрировали, что в основной группе у 25 пациентов (25/34) была стабилизация заболевание и у 8 пациентов (8/34) был частичный ответ: частота объективного ответа (ORR) составляла до 23,53%, а частота контроля заболевания (DCR) - до 97,06%.
(0,00%)
(0,00%)
(0,00%)
(0,00%)
(16,67%)
(37,50%)
(0,00%)
(23,53%)
(83,33%)
(62,50%)
(83,33%)
(73,53%)
(0,00%)
(0,00%)
(16,67%)
(2,94%)
(16,67%)
(37,50%)
(0,00%)
(23,53%)
(100,00%)
(83,33%)
(97,06%)
--->
Список Последовательностей
<110> CHIA TAI TIANQING PHARMACEUTICAL GROUP CO., LTD.
<120> КОМБИНИРОВАННЫЙ ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ РАКА ПОЧЕК
<130> 2020
<150> CN202010365735.X
<151> 2020-04-30
<160> 21
<170> SIPOSequenceListing 1.0
<210> 1
<211> 5
<212> БЕЛОК
<213> Mus sp.
<400> 1
Thr Tyr Gly Val His
1 5
<210> 2
<211> 16
<212> БЕЛОК
<213> Mus sp.
<400> 2
Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met Ser
1 5 10 15
<210> 3
<211> 8
<212> БЕЛОК
<213> Mus sp.
<400> 3
Leu Gly Phe Tyr Ala Met Asp Tyr
1 5
<210> 4
<211> 5
<212> БЕЛОК
<213> Mus sp.
<400> 4
Ser Tyr Gly Met Ser
1 5
<210> 5
<211> 16
<212> БЕЛОК
<213> Mus sp.
<400> 5
Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 6
<211> 8
<212> БЕЛОК
<213> Mus sp.
<400> 6
Gly Tyr Asp Ser Gly Phe Ala Tyr
1 5
<210> 7
<211> 11
<212> БЕЛОК
<213> Mus sp.
<400> 7
Lys Ala Ser Gln Ser Val Ser Asn Asp Val Ala
1 5 10
<210> 8
<211> 7
<212> БЕЛОК
<213> Mus sp.
<400> 8
Tyr Ala Ala Asn Arg Tyr Thr
1 5
<210> 9
<211> 9
<212> БЕЛОК
<213> Mus sp.
<400> 9
Gln Gln Asp Tyr Thr Ser Pro Tyr Thr
1 5
<210> 10
<211> 14
<212> БЕЛОК
<213> Mus sp.
<400> 10
Ala Ser Gln Ser Val Ser Thr Ser Ser Ser Ser Phe Met His
1 5 10
<210> 11
<211> 7
<212> БЕЛОК
<213> Mus sp.
<400> 11
Tyr Ala Ser Asn Leu Glu Ser
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Mus sp.
<400> 12
Gln His Ser Trp Glu Ile Pro Tyr Thr
1 5
<210> 13
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи hu5G11-hIgG1 и hu5G11-hIgG4
<400> 13
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 14
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи hu13C5-hIgG1 и hu13C5-hIgG4
<400> 14
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 15
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи hu5G11-hIgG1 и hu5G11-hIgG4
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 16
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи hu13C5-hIgG1 и hu13C5-hIgG4
<400> 16
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Gln Arg Ala Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Pro Val Glu Ala Asn Asp Thr Ala Asn Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 17
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> тяжелая цепь h5G11-hIgG1
<400> 17
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 18
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> легкая цепь h5G11-hIgG1 и h5G11-hIgG4
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 19
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> тяжелая цепь hu13C5-hIgG1
<400> 19
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 20
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> легкая цепь hu13C5-hIgG1 и hu13C5-hIgG4
<400> 20
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Gln Arg Ala Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Pro Val Glu Ala Asn Asp Thr Ala Asn Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 21
<211> 442
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> тяжелая цепь hu5G11-hIgG4
<400> 21
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОПУХОЛИ | 2020 |
|
RU2829637C2 |
| PD-L1 специфические антитела | 2017 |
|
RU2756236C2 |
| Анти-PD-L1 и IL-2 цитокины | 2017 |
|
RU2769282C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ PD-L1 и LAG-3 | 2017 |
|
RU2784388C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СЛИТОГО БЕЛКА РЕЦЕПТОРА ТРАНСФОРМИРУЮЩЕГО ФАКТОРА РОСТА БЕТА И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2791683C2 |
| НЕЙТРАЛИЗАЦИЯ ИНГИБИТОРНЫХ ПУТЕЙ В ЛИМФОЦИТАХ | 2015 |
|
RU2734771C2 |
| НОВАЯ КОМБИНАЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ | 2016 |
|
RU2742494C2 |
| АНТИТЕЛА ПРОТИВ PD-L1 И ИХ ВАРИАНТЫ | 2017 |
|
RU2770590C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ АНТИТЕЛА К PD-L1 И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2766590C2 |
| СПОСОБЫ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ, ВКЛЮЧАЮЩИЕ СРЕДСТВА, БЛОКИРУЮЩИЕ CTLA-4 И PD-1 | 2020 |
|
RU2833523C2 |
Группа изобретений относится к области биомедицины, в частности к лечению рака почек. Фармацевтическая комбинация для лечения рака почек содержит антитело против PD-L1, которое содержит область CDR1 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 1; область CDR2 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 2; область CDR3 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 3; область CDR1 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 7; область CDR2 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 8; и область CDR3 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 9, и анлотиниб или его фармацевтически приемлемую соль. Также раскрыты применение антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли для получения лекарственного средства для лечения рака почек и способ лечения рака почек. Группа изобретений обеспечивает быстрый ответ при лечении рака почек и стабилизацию заболевания. 3 н. и 23 з.п. ф-лы, 2 табл., 1 пр.
1. Фармацевтическая комбинация для лечения рака почек, содержащая:
антитело против PD-L1, которое содержит: область CDR1 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 1; область CDR2 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 2; область CDR3 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 3; область CDR1 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 7; область CDR2 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 8; и область CDR3 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 9, и
анлотиниб или его фармацевтически приемлемую соль.
2. Фармацевтическая комбинация по п. 1, отличающаяся тем, что фармацевтическая комбинация содержит: фармацевтическую композицию антитела против PD-L1 и фармацевтическую композицию анлотиниба или его фармацевтически приемлемой соли.
3. Фармацевтическая комбинация по любому из пп. 1, 2, отличающаяся тем, что антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 13; и вариабельную область легкой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 15.
4. Фармацевтическая комбинация по любому из пп. 1, 2, отличающаяся тем, что антитело против PD-L1 содержит: вариабельную область тяжелой цепи, выбранную из группы, состоящей из вариабельных областей тяжелой цепи гуманизированных антител hu5G11-hIgGl и hu5G11-hIgG4; и вариабельную область легкой цепи, выбранную из группы, состоящей из вариабельных областей легкой цепи гуманизированных антител hu5G11-hIgGl и hu5G11-hIgG4.
5. Фармацевтическая комбинация по любому из пп. 1, 2, отличающаяся тем, что антитело против PD-L1 содержит: тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 17; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18; или
тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 21; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18.
6. Применение антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли для получения лекарственного средства для лечения рака почек, при этом антитело против PD-L1 содержит: область CDR1 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 1; область CDR2 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 2; область CDR3 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 3; область CDR1 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 7; область CDR2 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 8; и область CDR3 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 9.
7. Применение по п. 6, отличающееся тем, что антитело против PD-L1 находится в форме фармацевтической композиции антитела против PD-L1 и анлотиниб или его фармацевтически приемлемая соль находится в форме фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли.
8. Применение по п. 7, отличающееся тем, что фармацевтическая композиция антитела против PD-L1 содержит 600-2400 мг антитела против PD-L1, предоставленного в форме многократной дозы или в форме однократной дозы.
9. Применение по п. 7 или 8, отличающееся тем, что фармацевтическая композиция анлотиниба или его фармацевтически приемлемой соли содержит 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли в виде однократной дозы.
10. Применение по любому из пп. 7-9, отличающееся тем, что фармацевтическая композиция антитела против PD-L1 представляет собой раствор для инъекций; фармацевтическая композиция анлотиниба или его фармацевтически приемлемой соли представляет собой твердый пероральный состав.
11. Применение по любому из пп. 6-10, отличающееся тем, что рак почек представляет собой распространенный рак почек;
рак почек представляет собой светлоклеточную почечно-клеточную карциному или не светлоклеточную почечно-клеточную карциному;
рак почек представляет собой светлоклеточную почечно-клеточную карциному или почечно-клеточную карциному с преобладанием светлоклеточных компонентов;
пациент с раком почек представляет собой пациента с раком почек низкого риска, или пациента с раком почек среднего риска, или пациента с раком почек высокого риска;
рак почек представляет собой почечно-клеточную карциному, ранее не подвергавшуюся лечению;
рак почек представляет собой распространенную почечно-клеточную карциному, ранее не подвергавшуюся лечению; или
рак почек представляет собой рак почек, который ранее не подвергался системному лечению.
12. Применение по любому из пп. 6-11, отличающееся тем, что антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 13; и вариабельную область легкой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 15.
13. Применение по любому из пп. 6-11, отличающееся тем, что антитело против PD-L1 содержит: вариабельную область тяжелой цепи, выбранную из группы, состоящей из вариабельных областей тяжелой цепи гуманизированных антител hu5G11-hIgG1 и hu5G11-hIgG4; и вариабельную область легкой цепи, выбранную из группы, состоящей из вариабельных областей легкой цепи гуманизированных антител hu5G11-hIgGl и hu5G11-hIgG4.
14. Применение по любому из пп. 6-11, отличающееся тем, что антитело против PD-L1 содержит: тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 17; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18; или
тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 21; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18.
15. Способ лечения рака почек, включающий раздельное введение нуждающемуся в этом пациенту эффективного количества антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли, при этом антитело против PD-L1 содержит: область CDR1 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 1; область CDR2 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 2; область CDR3 тяжелой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 3; область CDR1 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 7; область CDR2 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 8; и область CDR3 легкой цепи, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 9.
16. Способ по п. 15, отличающийся тем, что антитело против PD-L1 находится в форме фармацевтической композиции антитела против PD-L1 и анлотиниб или его фармацевтически приемлемая соль находится в форме фармацевтической композиции анлотиниба или его фармацевтически приемлемой соли.
17. Способ по п. 16, отличающийся тем, что указанная фармацевтическая композиция антитела против PD-L1 представляет собой состав, подходящий для введения в рамках одного цикла лечения, и содержит фармацевтическую композицию, содержащую 600-2400 мг антитела против PD-L1, представленную в форме многократной дозы или в форме однократной дозы.
18. Способ по п. 16 или 17, отличающийся тем, что указанная фармацевтическая композиция анлотиниба или его фармацевтически приемлемой соли представляет собой состав, подходящий для введения в рамках одного цикла лечения, и содержит фармацевтическую композицию, содержащую 84-168 мг анлотиниба; или
при этом указанная фармацевтическая композиция анлотиниба или его фармацевтически приемлемой соли содержит фармацевтическую композицию, содержащую 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли в виде однократной дозы.
19. Способ по любому из пп. 15-18, отличающийся тем, что антитело против PD-L1 вводят один раз в неделю, один раз каждые 2 недели, один раз каждые 3 недели или один раз каждые 4 недели.
20. Способ по любому из пп. 15-19, отличающийся тем, что один цикл лечения составляет 21 день; антитело против PD-L1 вводят в первый день каждого цикла лечения, а анлотиниб или его фармацевтически приемлемую соль вводят ежедневно в дни 1-14 каждого цикла.
21. Способ по п. 20, отличающийся тем, что 1200 мг антитела против PD-L1 вводят в первый день каждого цикла лечения и 6 мг, 8 мг, 10 мг и/или 12 мг анлотиниба или его фармацевтически приемлемой соли вводят ежедневно в дни 1-14 каждого цикла лечения.
22. Способ по любому из пп. 15-21, отличающийся тем, что каждый из антитела против PD-L1 и анлотиниба или его фармацевтически приемлемой соли представлен в форме фармацевтической композиции и вводят одновременно, последовательно или через определенные промежутки времени.
23. Способ по любому из пп. 15-22, отличающийся тем, что антитело против PD-L1 содержит следующие аминокислотные последовательности: вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 13; и вариабельную область легкой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, представленной в SEQ ID NO: 15.
24. Способ по любому из пп. 15-22, отличающийся тем, что антитело против PD-L1 содержит: вариабельную область тяжелой цепи, выбранную из группы, состоящей из вариабельных областей тяжелой цепи гуманизированных антител hu5G11-hIgG1 и hu5G11-hIgG4; и вариабельную область легкой цепи, выбранную из группы, состоящей из вариабельных областей легкой цепи гуманизированных антител hu5G11-hIgGl и hu5G11-hIgG4.
25. Способ по любому из пп. 15-22, отличающийся тем, что антитело против PD-L1 содержит: тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 17; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18; или
тяжелую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 21; и легкую цепь, имеющую аминокислотную последовательность, представленную в SEQ ID NO: 18.
26. Способ по любому из пп. 15-25, отличающийся тем, что рак почек представляет собой распространенный рак почек;
рак почек представляет собой светлоклеточную почечно-клеточную карциному или не светлоклеточную почечно-клеточную карциному;
рак почек представляет собой светлоклеточную почечно-клеточную карциному или почечно-клеточную карциному с преобладанием светлоклеточных компонентов;
пациент с раком почек представляет собой пациента с раком почек низкого риска, или пациента с раком почек среднего риска, или пациента с раком почек высокого риска;
рак почек представляет собой почечно-клеточную карциному, ранее не подвергавшуюся лечению;
рак почек представляет собой распространенную почечно-клеточную карциному, ранее не подвергавшуюся лечению; или
рак почек представляет собой рак почек, который ранее не подвергался системному лечению.
| CN 0111065411 А, 24.04.2020 | |||
| КОМБИНИРОВАННАЯ ТЕРАПИЯ НА ОСНОВЕ НАЦЕЛЕННЫХ НА ОПУХОЛЬ ИММУНОЦИТОКИНОВ, СОДЕРЖАЩИХ ВАРИАНТ IL-2, И АНТИТЕЛ К ЧЕЛОВЕЧЕСКОМУ PD-L1 | 2015 |
|
RU2710354C2 |
| SHEN G | |||
| Anlotinib: A novel multi-targeting tyrosine kinase inhibitor in clinical development // Journal of Hematology & Oncology, 19.09.2019, No.11(120), Электронный ресурс: URL: https://jhoonline.biomedcentral.com/articles/10.1186/s13045-018-0664-7 | |||
| Инструкция по медицинскому применению | |||
Авторы
Даты
2024-11-22—Публикация
2021-04-30—Подача