Область изобретения
Описаны антитела и способы использования антител. В частности, описаны антитела, которые специфически связывают антиген PD-L1 человека, и их использование при лечении различных заболеваний.
Вступление
Иммуноцитокины (гибридные белки антитело-цитокин) впервые были описаны в литературе в начале 1990-х годов и представляли собой продукты слияния цельных антител с цитокинами, такими как лимфотоксин (ФНО-α) или интерлейкин 2 (IL-2). Последующие исследования на моделях экспрессирующих GD2 опухолей у мышей показали, что антитело ch14.18 и иммуноцитокин ch14.18-IL2 оба обладают противоопухолевой активностью, но иммуноцитокин является гораздо более сильнодействующим, чем антитело, даже в сочетании со свободным IL-2 (см. Sabzevari Н et al., Proc. Natl. Acad. Sci. USA, 1994, 91:9626-30; Pancook JD, et al., Cancer Immunol. Immunother., 1996, 42:88-92; Becker JC, et al., Proc. Natl. Acad. Sci. USA, 1996, 93:2702-7). Кроме того, у иммунокомпетентных мышей, получавших иммуноцитокин, но не антитело плюс IL-2, вырабатывался адаптивный иммунный ответ, зависимый от CD8+ Т-клеток, который предотвращал последующую стимуляцию опухолью (Becker JC, et al., J. Exp. Med., 1996, 183:2361-6; Becker JC, et al., Proc. Natl. Acad. Sci. USA, 1996, 93:7826-31). Таким образом, нацеливание IL-2 на микроокружение опухоли индуцирует эффект противоопухолевой вакцины, что невозможно в случае антитела, будь то отдельно взятого либо вместе с свободным цитокином. Родственный гуманизированный иммуноцитокин, hu 14.18-IL2, обеспечил клиническое доказательство концепции при рецидивирующей нейробластоме без массивных поражений в качестве монотерапии, где он вызвал значительное количество полных ремиссий у пациентов без других вариантов лечения (см. Shusterman et al., Journal of Clinical Oncology, 2010, 28 (33), 4969-4975). В ряде публикаций описывается способность этой молекулы активировать несколько компонентов иммунной системы для уничтожения опухолевых клеток (в частности, NK-клеток и CD8+ Т-клеток), и создавать Т-клеточную память для противодействия последующей стимуляции опухолью (Yamane et и др. 2009; Expert Opi, Investig. Drugs, 18(7): 991-1000; Neal et al., 2004, Clin. Cancer Res., 1010, 4839-4847).
Поскольку иммуноцитокины на основе IL-2 могут иметь значительные побочные эффекты, в последнее время усилия были направлены на снижение токсичности при сохранении эффективности. Одним из примеров является селектикин (Selectikine, EMD 521873), имеющий замену аспарагиновой кислоты на треонин в положении 20 IL-2, являющимся ключевым остатком для связывания IL-2Rβ (Gillies et al., Clinical Cancer Research, 2011, 17 (11), 3673-3685). Было показано, что селектикин, который связывает некротическую ткань, обладает хорошей противоопухолевой активностью, несмотря на его селективность к высокоаффинному IL-2R по сравнению с промежуточным IL-2R, и хорошей переносимостью в исследованиях фазы I (Laurent et al., Journal of Translational Medicine, 2013, 11 (1), 5. http://doi.org/10.1186/1479-5876-11-5)
WO 02012/178137 (Gillies) и соответствующая журнальная статья (Gilles, Protein Engineering, Design and Selection, 2013, 26 (10), 561-569) описывают продукты слияния иммуноцитокинов легких цепей с нацеленными на опухоль антителами, и модуляцию активности IL-2 посредством укорачивания N-концевой части цитокина, что снижает передачу сигналов через IL-2R. Было показано, что гибридные белки IL-2, специфически нацеленные на IL-2R, обладают повышенной токсичностью по сравнению с диким типом (Vasquez-Lombardi et al. Nat Comm, 2017, DOI: 10.1038 / ncomms15373), что поддерживает точку зрения, в соответствии с которой уменьшение связывания IL-2R может быть полезным в отношении побочных эффектов.
Адаптивный иммунный ответ включает активацию, селекцию и клональную пролиферацию двух основных классов лимфоцитов, называемых Т-клетками и В-клетками. После встречи с антигеном Т-клетки пролиферируют и дифференцируются в антигенспецифические эффекторные клетки, тогда как В-клетки пролиферируют и дифференцируются в антителосекретирующие клетки. Активация Т-клеток представляет собой многоступенчатый процесс, требующий нескольких сигнальных явлений между Т-клеткой и антигенпредставляющей клеткой (АПК). Для активации Т-клеток в покоящуюся Т-клетку должны быть доставлены два типа сигналов. Первый тип опосредуется антигенспецифическим Т-клеточным рецептором (TcR) и придает специфичность иммунному ответу. Второй сигнал, являющийся сигналом костимуляторного типа, регулирует величину ответа и доставляется через вспомогательные рецепторы Т-клетки.
Первичный костимуляторный сигнал доставляется через активирующий рецептор CD28 после связывания с его лигандами В7-1 или В7-2. Напротив, связывание ингибирующего рецептора CTLA-4 с теми же лигандами В7-1 или В7-2 приводит к ослаблению ответа Т-клеток. Таким образом, сигналы CTLA-4 антагонизируют костимуляцию, опосредованную CD28. При высоких концентрациях антигена костимуляция CD28 перевешивает ингибирующий эффект CTLA-4. Временное регулирование экспрессии CD28 и CTLA-4 поддерживает баланс между активирующими и ингибирующими сигналами и обеспечивает развитие эффективного иммунного ответа, одновременно защищая от развития аутоиммунитета.
Рецептор программируемой смерти-1 (PD-1) представляет собой трансмембранный рецептор 50-55 кДа типа I, который является членом семейства CD28. PD-1 участвует в регуляции Т-клеточной активации и экспрессируется на Т-клетках, В-клетках и миелоидных клетках. Были идентифицированы два лиганда для PD-1 - лиганд 1 PD (PD-L1) и лиганд 2 (PD-L2), имеющие костимулирующие свойства.
Лиганд 1 рецептора программируемой клеточной смерти (PD-L1), также известный как кластер дифференцировки (CD274) или гомолог 1 В7 (В7-Н1), является членом семейства В7, который модулирует активацию или ингибирование рецептора PD-1. Открытая рамка считывания PD-L1 кодирует предполагаемый трансмембранный белок 1-го типа из 290 аминокислот, который включает два внеклеточных домена Ig (N-концевой V-подобный домен и С-подобный домен Ig), гидрофобный трансмембранный домен и цитоплазматический хвост из 30 аминокислот. Внутриклеточный (цитоплазматический) домен из 30 аминокислот не содержит явных сигнальных мотивов, но имеет потенциальный сайт фосфорилирования протеинкиназы С.
Полная аминокислотная последовательность для PD-L1 приведена в NCBI Reference Sequence: NP_054862.1 (SEQ ID NO: 1), которая ссылается на многие журнальные статьи, включая, например, Dong, Н., et al. (1999), "PD-L1, a third member of the B7 family, co-stimulates T-cell proliferation and interleukin-10 secretion," Nat. Med. 5 (12), 1365-1369. Ген PD-L1 сохраняется у шимпанзе, макаки-резус, собаки, коровы, мыши, крысы, курицы и полосатого данио. Мышиная форма PD-L1 имеет 69% аминокислотной идентичности с человеческой формой PD-L1, и также сохраняет консервативную структуру.
У людей PD-L1 экспрессируется на ряде типов иммунных клеток, включая активированные и анергические/истощенные Т-клетки, на наивных и активированных В-клетках, а также на миелоидных дендритных клетках (DC), моноцитах и тучных клетках. Он также экспрессируется на неиммунных клетках, включая островки поджелудочной железы, купферовые клетки печени, сосудистый эндотелий и выбранные эпителиальные ткани, например, эпителии дыхательных путей и эпителии почечных канальцов, где его экспрессия усиливается во время воспалительных эпизодов. Экспрессия PD-L1 также детектируется на повышенных уровнях на ряде опухолей, включая, без ограничений, рак молочной железы (включая, без ограничений, тройной отрицательный рак молочной железы и воспалительный рак молочной железы), яичников, шейки матки, толстой кишки, колоректальный, легкого, включая немелкоклеточный рак легкого, почек, в том числе карциному почек, желудка, пищевода, мочевого пузыря, гепатоцеллюлярный рак, плоскоклеточный рак головы и шеи (SCCHN) и рак поджелудочной железы, меланому и увеальную меланому.
Считается, что передача сигналов PD-1/PD-L1 служит критической нерезервированной функцией иммунной системы через отрицательную регуляцию ответов Т-клеток. Эта регуляция участвует в развитии Т-клеток в тимусе, в регуляции хронических воспалительных реакций и в обеспечении как периферической толерантности, так и иммунных привилегий. По-видимому, повышенная экспрессия PD-L1 может позволять раковым заболеваниям уклоняться от иммунной системы хозяина, и для многих раковых опухолей экспрессия PD-L1 ассоциирована с пониженной выживаемостью и неблагоприятным прогнозом. Терапевтические моноклональные антитела, способные блокировать путь PD-1/PD-L1, могут усилить противоопухолевые иммунные ответы у пациентов с раком. Опубликованные клинические данные позволяют предположить наличие корреляции между клиническими ответами и опухолевой мембранной экспрессией PD-L1 (Brahmer et al., Journal of Clinical Oncology, 2010, Topalian et al., NEJM, 2012) и более сильной корреляции между отсутствием клинических ответов и отсутствием белка PD-L1, локализованного на мембране (Brahmer et al., Journal of Clinical Oncology, 2010, Topalian et al., NEJM, 2012). Таким образом, экспрессия PD-L1 в опухолях или опухолепроникающих лейкоцитах (Herbst RS, et al., «Predictive correlates of response to the анти-PD-L1 antibody MPDL3280A in cancer patients», Nature, 2014, 27 Nov 515(7528)):563-7, doi: 10.1038/nature14011) является кандидатом молекулярного маркера для использования при отборе пациентов для иммунотерапии, например, иммунотерапии с использованием антител против PD-L1. Направленный отбор (enrichment) пациентов на основе поверхностной экспрессии PD-L1 может значительно улучшить клинический успех лечения препаратами, нацеленными на путь PD-1/PD-L1. Имеются также данные о сохраняющемся иммунном ответе, таком как опухолепроникающие CD8+ Т-клетки, или наличие характерных признаков активации цитокинов, таких как IFNγ ти
Дополнительные данные об экспрессии PD-L1 и корреляции с болезнью будут получены из многочисленных продолжающихся клинических испытаний. Атезолизумаб (Atezolizumab) является новейшим средством, и последние данные испытаний фазы II демонстрируют терапевтический эффект при метастатической уротелиальной карциноме и НМКРЛ, особенно у пациентов с PD-L1+ иммунными клетками в микроокружении опухоли (см. Fehrenbacher et al., 2016, The Lancet, http://doi.org/10.1016/S0140-6736 (16) 00587-0; Rosenberg et al., 2016, The Lancet, http://doi.org/10.1016/S0140-6736(16)00561-4). Недавние результаты исследования III фазы на 1225 пациентах с НМКРЛ показали улучшенную выживаемость пациентов, принимавших атезолизумаб, по сравнению с химиотерапией, независимо от экспрессии PD-L1 опухолью (Rittmeyer et al., 2017, The Lancet, 389 (10066), 255-265).
Краткое описание сущности изобретения
Антитела
В данном документе раскрыты антитела и их антигенсвязывающие фрагменты, которые специфически связываются с PD-L1. В одном варианте реализации, антитело или его антигенсвязывающий фрагмент специфически связывается с поверхностно экспрессированным PD-L1.
В первой конфигурации предусматривается антитело или его фрагмент, которые специфически связываются с hPD-L1, представлены SEQ ID NO:1, и конкурируют за связывание с указанным hPD-L1 с антителом 1D05, где антитело или фрагмент содержат домен VH, который включает CDRH3, содержащий мотив X1GSGX2YGX3X4FD, где X1, Х2 и Х3 независимо представляют собой любую аминокислоту, а Х4 присутствует или отсутствует, и в случае присутствия может означать любую аминокислоту.
Во второй конфигурации предусматривается антитело или его фрагмент, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 1D05, где антитело или фрагмент включают домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO:29 или 32, или последовательность CDRH3, представленную SEQ ID NO:29 или 32, содержащую 6 или меньше аминокислотных замещений.
В третьей конфигурации предусматривается антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 1D05.
В четвертой конфигурации предусматривается антитело или его фрагмент, который конкурирует за связывание с hPD-L1 с антителом 1D05.
В пятой конфигурации предусматривается биспецифическое антитело или гибридный белок, содержащие антитело или его фрагмент, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В шестой конфигурации предусматривается антитело или фрагмент, по результатам определения в любой другой конфигурации, варианте реализации или концепции, для использования при лечении или профилактике опосредованного hPD-L1 заболевания или состояния.
В седьмой конфигурации предусматривается использование антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции, при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики опосредованного hPD-L1 заболевания или состояния человека.
В восьмой конфигурации предусматривается способ лечения или профилактики опосредованного hPD-L1 заболевания или состояния у человека, включающий введение указанному человеку терапевтически эффективного количества антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции, в котором, тем самым, проводится лечение или профилактика опосредуемого hPD-L1 заболевания или состояния.
В девятой конфигурации предусматривается фармацевтическая композиция, содержащая антитело или фрагмент, определенные в любой другой конфигурации, варианте реализации или концепции, и фармацевтически приемлемом эксципиенте, разбавителе или носителе.
В десятой конфигурации предусматривается набор, включающий фармацевтическую композицию, содержащую антитело или фрагмент, определенные в любой другой конфигурации, варианте реализации или концепции, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
В одиннадцатой конфигурации предусматривается способ модуляции взаимодействия PD-1/PD-L1 у пациента, включающий введение эффективного количества антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции, указанному пациенту.
В двенадцатой конфигурации предусматривается способ ингибирования активности PD-L1 у пациента, включающий введение эффективного количества антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции, указанному пациенту.
В тринадцатой конфигурации предусматривается способ лечения пролиферативного заболевания у животного (например, человека), включающий введение эффективного количества антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции, указанному пациенту.
В четырнадцатой конфигурации предусматривается способ детектирования экспрессии PD-L1 в образце, включающий введение в контакт образца с антителом или фрагментом, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В пятнадцатой конфигурации предусматривается способ, включающий введение в контакт биологического образца с антителом или фрагментом, по результатам определения в любой другой конфигурации, варианте реализации или концепции, для образования комплекса с PD-L1, присутствующим в образце, и измерения присутствия, отсутствия или уровня комплекса в биологическом образце.
В шестнадцатой конфигурации предусматривается способ детектирования экспрессии PD-L1 в образце, включающий введение в контакт образца с антителом или фрагментом, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В семнадцатой конфигурации предусматривается способ, включающий введение в контакт биологического образца с антителом или фрагментом, по результатам определения в любой другой конфигурации, варианте реализации или концепции, для образования комплекса с PD-L1, присутствующим в образце, и измерения присутствия, отсутствия или уровня комплекса в биологическом образце.
В восемнадцатой конфигурации предусматривается способ идентификации партнеров по связыванию для PD-L1, который включает иммунопреципитацию интактного белкового комплекса, содержащего PD-L1, с использованием антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В девятнадцатой конфигурации предусматривается способ диагностики у человека заболевания, связанного с измененной экспрессией PD-L1, включающий стадии введения в контакт биологического образца человека с антителом, по результатам определения в другой конфигурации, варианте реализации или концепции, для образования комплекса между антителом и PD-L1, присутствующим в образце; и определения количества комплекса.
В двадцатой конфигурации предусматривается нуклеиновая кислота, кодирующая CDRH3 антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В двадцать первой конфигурации предусматривается нуклеиновая кислота, кодирующая домен VH и/или домен VL антитела или фрагмента, по результатам определения в любой другой конфигурации, варианте реализации или концепции.
В двадцать второй конфигурации предусматривается вектор, содержащий нуклеиновую кислоту в соответствии с любой другой конфигурацией, вариантом реализации или концепцией; где вектор, необязательно, представляет собой вектор СНО или HEK293.
В двадцать третьей конфигурации предусматривается хозяин, содержащий нуклеиновую кислоту в соответствии с любой другой конфигурацией, вариантом реализации или концепцией, или вектор в соответствии с любой другой конфигурацией, вариантом реализации или концепцией.
Иммуноцитокины
В первой конфигурации предусматривается иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, где тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1, представленным SEQ ID No: 1, и конкурирует за связывание с указанным hPD-L1 с антителом 1D05; и
иммуноцитокин содержит домен VH, который содержит CDRH3, содержащий мотив X1GSGX2YGX3X4FD, где X1, Х2 и Х3 независимо обозначают любую аминокислоту, и Х4 присутствует или отсутствует и, в случае его присутствия, может обозначать любую аминокислоту.
Во второй конфигурации предусматривается иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, где тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
где домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1 и конкурирует за связывание с указанным hPD-L1 с антителом 1D05, причем антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO:29 или 32, или последовательность CDRH3, представленную SEQ ID NO:29 или 32, содержащую 6 или меньше аминокислотных замещений.
В третьей конфигурации предусматривается иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, где тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1; и
причем домен VH содержит CDRH3, который состоит из 12-20 аминокислот и получен путем рекомбинации VH генного сегмента человека, D генного сегмента человека и JH генного сегмента человека, причем JH генный сегмент человека представляет собой IGHJ5 (например, IGHJ5*02).
В четвертой конфигурации предусматривается иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, где тяжелая цепь содержит, в направлении от N- к С-концу:
а) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 1D05.
В пятой конфигурации предусматривается иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, где тяжелая цепь содержит, в направлении от N- к С-концу:
а) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который конкурирует за связывание с hPD-L1 с антителом 1D05.
В шестой конфигурации предусматривается иммуноцитокин, по результатам определения в любой другой конфигурации, варианте реализации или аспекте, для использования при лечении или профилактике опосредованного hPD-L1 заболевания или состояния.
В седьмой конфигурации предусматривается использование иммуноцитокина, по результатам определения в любой другой конфигурации, варианте реализации или аспекте, при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики опосредованного hPD-L1 заболевания или состояния у человека.
В восьмой конфигурации предусматривается способ лечения или профилактики опосредованного hPD-L1 заболевания или состояния у человека, включающий введение указанному человеку терапевтически эффективного количества иммуноцитокина, по результатам определения в любой другой конфигурации, варианте реализации или аспекте, причем, тем самым, проводится лечение или профилактика опосредованного hPD-L1 заболевания или состояния.
В девятой конфигурации предусматривается фармацевтическая композиция, содержащая иммуноцитокин, по результатам определения в любой другой конфигурации, варианте реализации или аспекте, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
В десятой конфигурации предусматривается набор, включающий фармацевтическую композицию, содержащую иммуноцитокин, по результатам определения в любой другой конфигурации, варианте реализации или аспекте, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
В одиннадцатой конфигурации предусматривается нуклеиновая кислота, кодирующая тяжелую цепь и/или легкую цепь иммуноцитокина, по результатам определения в любой другой конфигурации, варианте реализации или аспекте.
В двенадцатой конфигурации предусматривается вектор, содержащий нуклеиновую кислоту, которая кодирует тяжелую цепь и/или легкую цепь иммуноцитокина, по результатам определения в любой другой конфигурации, варианте реализации или аспекте.
В тринадцатой конфигурации предусматривается хозяин, содержащий нуклеиновую кислоту в соответствии с любой другой конфигурацией, вариантом реализации или аспектом, или вектора, по результатам определения в любой другой конфигурации, варианте реализации или аспекте.
Биспецифические анти-ICOS антитела
В первой конфигурации предусматривается мультиспецифическое антитело (например, биспецифическое антитело или антитело с двойным связыванием), которое связывается с (и, необязательно, имеет специфичность к) ICOS (индуцируемый Т-клеточный ко-стимулятор) (например, человеческому ICOS) и другому целевому антигену.
Во второй конфигурации предусматривается композиция, содержащая мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием, как описано в данном документе, и фармацевтически приемлемый эксципиент, разбавитель или носитель.
В третьей конфигурации предусматривается мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием, как описано в данном документе, для использования при лечении или профилактике заболевания или состояния, выбранного из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей; таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно индуцируемые раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцируемые раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
В четвертой конфигурации предусматривается использование мультиспецифического, биспецифического антитела или антитела с двойным связыванием, как описано в данном документе, при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики заболевания или состояния у человека, выбранного из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно индуцируемые раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (таких как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
В пятой конфигурации предусматривается способ лечения или профилактики заболевания или состояния, выбранного из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и плоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома, или, например, вирусно индуцируемые раки (например, рак шейки матки и рак носоглотки) и саркомы мягких тканей) у человека, включающий введение указанному человеку терапевтически эффективного количества мультиспецифического, биспецифического антитела или антитела с двойным связыванием, как описано в данном документе, причем таким образом проводится лечение или профилактика заболевания или состояния.
В шестой конфигурации предусматривается нуклеиновая кислота, кодирующая тяжелую цепь и/или легкую цепь мультиспецифического антитела, как описано в данном документе.
В седьмой конфигурации предусматривается вектор, содержащий нуклеиновую кислоту, которая кодирует тяжелую цепь и/или легкую цепь мультиспецифического антитела, как описано в данном документе.
Описание Фигур
Фиг. 1: Анализ выбранных антител в реакции смешанной культуры лимфоцитов дендритных клеток-Т-клеток. Моноциты культивировали с GM-CSF (фактор, стимулирующий образование колоний гранулоцитов и макрофагов) и IL-4 в течение семи дней перед добавлением аллогенных очищенных CD3+ Т-клеток и титрованных антител. Супернатанты брали на 5-й день для анализа продуцирования IFNγ. Приведены данные для одного эксперимента. Следует отметить, что для 84G09 имеется по одной точке данных на концентрацию, поскольку одна репликация не удалась.
Фиг. 2: ИФА с прямой нейтрализацией PD-L1 с рецептором PD-1. Профили нейтрализации 1D05 и 84G09 по сравнению с калибровочным (benchmark) анти-PD-L1 антителом и изотипическим контролем. Данные представляют три независимых эксперимента.
Фиг. 3: Анализ методом FACS нейтрализации CHO-S с PD-L1 человека с помощью рецептора PD-1. Профили нейтрализации 1D05 и 84G09 по сравнению с калибровочным (benchmark) анти-PD-L1 антителом и изотипическим контролем. Данные представляют три независимых эксперимента.
Фиг. 4: Анализ методом FACS нейтрализации CHO-S с PD-L1 человека с помощью рецептора CD80. Профили нейтрализации 1D05 и 84G09 по сравнению с калибровочным анти-PD-L1 антителом и изотипическим контролем. Данные представляют три независимых эксперимента.
Фиг. 5: Связывание оптимизированных прототипов антитела (lead antibodies) с PD-L1, но не с PD-L2. Оптимизированные прототипы антител связываются с иммобилизованным на планшете PD-L1 (Фиг. 5а), но не с PD-L2 (Фиг. 5b). В качестве контроля использовали антитело против PD-L2. Данные выражены в единицах флуоресценции с временным разрешением при 615 нм. Данные представляют два независимых эксперимента.
Фиг. 6: Оптимизированные прототипы антител индуцируют продуцирование IFNγ в реакции смешанной культуры лимфоцитов дендритных клеток-Т-клеток. Незрелые дендритные клетки совместно культивировали с аллогенными CD4+ Т-клетками в присутствии антител в течение 5 дней. Измеряли IFNγ в супернатантах методом ИФА. Данные представляют три независимых экспериментов. В1 относится к калибровочным антителам.
Фиг. 7: Оптимизированные прототипы антител связываются с нативно экспрессируемым PD-L1 на дендритных клетках. Дендритные клетки были получены из моноцитарных предшественников с использованием GM-CSF и IL-4, и окрашивались оптимизированными прототипами антител (a) 1D05 и (b) 84G09 и изотипическим контролем, непосредственно помеченным AlexaFluor647. Приведены данные для одного донора крови, представляющего четырех доноров.
Фиг. 8а: Анализ методом ИФА прямой нейтрализации PD-L1 рецептором PD-1. Профили нейтрализации первично отобранных антител (hits) KM121, по сравнению с калибровочным анти-PD-L1-антителом и изотипическим контролем. Данные представляют три независимых эксперимента.
Фиг. 8b: Анализ методом ИФА прямой нейтрализации PD-L1 рецептором PD-1. Профили нейтрализации молекул-кандидатов оптимизированных прототипов антител KM122 по сравнению с калибровочным анти-PD-L1 антителом. Данные для одного эксперимента.
Фиг. 8с: ИФА с прямой нейтрализацией PD-L1 рецептором PD-1. Профиль нейтрализации молекулы-кандидата 416Е01 оптимизированного прототипа антитела KM122 по сравнению с калибровочным анти-PD-L1-антителом. Данные для одного эксперимента.
Фиг. 9а: Анализ методом ИФА прямой нейтрализации PD-L1 рецептором CD80. Профили нейтрализации первично отобранных антител (hits) КМ121, по сравнению с калибровочным анти-PD-L1-антителом и изотипическим контролем. Данные представляют три независимых эксперимента.
Фиг. 9b: Анализ методом ИФА прямой нейтрализации PD-L1 рецептором CD80. Профили нейтрализации молекул-кандидатов оптимизированных прототипов антител KM122 по сравнению с калибровочным анти-PD-L1 антителом. Данные для одного эксперимента.
Фиг. 9с: Анализ методом ИФА прямой нейтрализации PD-L1 рецептором CD80. Профили нейтрализации молекулы-кандидата 416Е01 оптимизированного прототипа антитела KM122 по сравнению с калибровочным анти-PD-L1 антителом. Данные для одного эксперимента.
Фиг. 10: Биспецифическое связывание, измеренное методом SPR, с PD-L1 в качестве первого антигена и TIGIT в качестве второго антигена. А) Биспецифическое 1, В) Биспецифическое 2, С) Биспецифическое 3, D) Биспецифическое 4. Подробная информация о получении каждого биспецифического конструкта приведена в Таблице 6.
Фиг. 11: Биспецифическое связывание, измеренное методом SPR, с TIGIT в качестве первого антигена и PD-L1 в качестве второго антигена. А) Биспецифическое 1, В) Биспецифическое 2, С) Биспецифическое 3, D) Биспецифическое 4. Подробная информация о получении каждого биспецифического конструкта приведена в Таблице 6.
Фиг. 12 (а): Способность конструктов иммуноцитокинов индуцировать пролиферацию в клетках TF-1, экспрессирующих IL-2Rαβγ, по сравнению с эквимолярными концентрациями свободного IL-2. Приведены данные для одного эксперимента, представляющего три эксперимента.
Фиг. 12 (b): Способность конструктов иммуноцитокинов индуцировать пролиферацию в клетках TF-1, экспрессирующих IL-2Rβγ, по сравнению с эквимолярными концентрациями свободного IL-2. Приведены данные для одного эксперимента, представляющего четыре эксперимента.
Фиг. 13 (а): Способность антитела 1D05 нейтрализовать взаимодействие между PD-1 и PD-L1 не зависит от слияния IL-2 с антителом, по результатам анализа нейтрализации методом ИФА. Приведены данные для одного эксперимента, представляющего три эксперимента.
Фиг. 13 (b): Способность антитела 1D05 нейтрализовать взаимодействие между CD80 и PD-L1 не зависит от слияния IL-2 с антителом, по результатам анализа нейтрализации методом ИФА. Приведены данные для одного эксперимента, представляющего три эксперимента.
Фиг. 14: Кривые роста NOD/SCID:ксенотрансплантат для in vivo исследований эффективности по группам в среднем и для индивидуальных животных.
Фиг. 14 (а): показывает среднюю для группы кривую роста опухоли (n=8/9), для этого графика, если животное исключалось из исследований из-за размера опухоли, последний результат измерений использовался для оставшейся части исследования. Заштрихованный участок показывает область, в которой использовался последний результат измерений.
На рисунках 14(b)-(е): показаны кривые роста опухолей индивидуальных животных для каждой группы, (б) только опухоли А375; (с) опухоли А375, введенные совместно с CD4+/8+ Т-клетками в соотношении 6:1. Для панелей (d) и (е) опухолевые клетки А375 вводили совместно с CD4+/8+ Т-клетками в соотношении 6:1; (d) изотипическое контрольное антитело в дозе 10 мг/кг и (е) анти-PD-L1-антитело 1D05 в дозе 10 мг/кг. Введение дозы проводилось через 1 час после имплантации опухоли/Т-клеток и в дни 3, 6, 8 и 10, как показано на графике пунктирными линиями.
Фиг. 15: График Каплана-Мейера для in vivo исследований эффективности NOD/SCID:ксенотрансплантат, показывающий количество животных, продолжающих участвовать в исследованиях. Этот график показывает небольшое увеличение времени участия в исследованиях при совместном введении CD4+/CD8+ Т-клеток с опухолевыми клетками (Т-клетки/А375) (n=9) по сравнению с одними лишь опухолевыми клетками А375 (n=9). Лечение с использованием изотипического контроля (Т-клетки/А375-изотип (n=8)) не влияло на выживаемость по сравнению с Т-клетками, вводимыми совместно с опухолевыми клетками без антитела. Лечение с использованием 10 мг/кг анти-PD-L1-антитела 1D05 (Т-клетки/А375-анти-PD-L1 (n=8)) значительно увеличивало время участия в исследованиях по сравнению с группой изотипического контроля. Введение дозы осуществляли через 1 час после инъекции Т-клеток/опухолевых клеток и в дни 3, 6, 8 и 10, как показано на графике пунктирными линиями.
Фиг. 16: Расширение лимфоцитов в ответ на дозирование иммуноцитокинов. Образцы крови натощак брали в предварительно обработанные ЭДТА пробирки перед введением исследуемых препаратов (0) и через 2, 5 и 7 дней после их введения. Количество клеток измеряли с помощью Bayer Advia 120. Результаты выражены в виде кратности изменения количества лимфоцитов.
Фиг. 17: Анализ стандартных гематологических параметров в ответ на дозирование иммуноцитокинов. Образцы крови натощак брали в предварительно обработанные ЭДТА пробирки перед введением исследуемых препаратов и через 7 дней после их введения. Анализ гемоглобина, гематокрита, количества эритроцитов и количества тромбоцитов проводили с использованием Bayer Advia 120. Результаты выражены как процент изменения параметра через 7 дней после введения дозы.
Фиг. 18: Уровни цитокинов в плазме яванских макак, получивших дозу молекул иммуноцитокина. Образцы плазмы получали до введения исследуемого препарата (РТ) и через 3 дня после введения дозы (D3) и анализировали методом MSD на уровни a) TNF-α; б) ИЛ-8; с) ИЛ-6; d) IFNγ; е) G-CSF и f) IL-2. Отсутствие столбиков показывает, что уровни цитокинов были ниже предела количественной оценки метода анализа. IL-4, ИЛ-5 и ИЛ-1β не были обнаружены ни в одном из образцов в любые моменты времени и потому не были включены в графики.
Фиг. 19: Уровни растворимого CD25 в плазме яванских макак, получивших дозу молекул иммуноцитокина. Образцы плазмы получали перед введением исследуемого препарата (РТ) и через 3 дня после введения дозы (D3) и анализировали с использованием коммерческого набора ИФА. * указывает, что значения уровней были выше верхнего предела количественной оценки (20 000 пг/мл).
Фиг. 20: Проточный цитометрический анализ субпопуляций МКПК (мононуклеарные периферические клетки крови). Цельную кровь окрашивали для маркеров а) Т-клеток и b) В-клеток, NK-клеток, нейтрофилов и моноцитов до лизиса и фиксации эритроцитов. Данные выражены как кратность изменения числа клеток через 5 дней после введения дозы. Данные для 1D05 LC D9-7 ICK отсутствуют из-за непригодности образца.
Фиг. 21: Фармакокинетический (ФК) анализ иммуноцитокинов. Сыворотку получали из образцов крови, взятых в различные моменты времени на протяжении 96 часов. На панелях а) и b) сыворотку инкубировали на планшетах, покрытых PD-L1, и иммуноцитокины детектировали с помощью детекторного биотинилированного анти-Fc человека антитела, и стрептавидина, меченого европием. На панелях с) и d) сыворотку инкубировали на планшетах, покрытых PD-L1, и иммуноцитокины детектировали с помощью биотинилированного анти-IL-2 человека антитела, и меченого европием стрептавидина. Результаты выражены в нг/мл.
Фиг. 22а: Индуцирование продуцирования IFNγ в анализе совместного культивирования моноцитов-Т-клеток анти-PD-L1 антителами в формате человеческого IgG1. Каждая точка данных представляет собой среднюю кратность индукции по результатам по меньшей мере из трех независимых экспериментов ± стандартная ошибка среднего.
Фиг. 22b: Индуцирование продуцирования IFNγ в анализе совместного культивирования моноцитов-Т-клеток анти-PD-L1-антителом в формате IgG4(PE) человека. Каждая точка данных представляет собой среднюю кратность индуцирования по результатам двух независимых экспериментов ± стандартное отклонение.
Фиг. 23 (а): Индукция IL-2 в анализе мышиной Т-клеточной гибридомы. Клетки LK35.2, трансфицированные человеческим PD-L1, нагружали пептидом овальбумина и совместно культивировали в течение ночи с клетками Т-клеточной гибридомы DO-11-10 в присутствии анти-PD-L1 антител или контролей, с последующим сбором супернатантов и анализом высвобождения IL-2. Каждая точка данных соответствует среднему значению высвобождения IL-2, скорректированному по фону, для трех независимых экспериментов ± стандартное отклонение.
Фиг. 23 (b): Индукция IL-2 в анализе мышиной Т-клеточной гибридомы. Клетки LK35.2, трансфицированные человеческим PD-L1, нагружали пептидом овальбумина и совместно культивировали в течение ночи с клетками Т-клеточной гибридомы DO-11-10 в присутствии биспецифических молекул ICOS/PD-L1 или отдельных антител, с последующим сбором супернатантов и анализом высвобождения IL-2. Каждая точка данных соответствует среднему значению высвобождения IL-2, скорректированному по фону, для трех независимых экспериментов ± стандартное отклонение.
Фиг. 24 (а): Индукция IFNγ в анализе DC-T-клеток методом MLR. Дендритные клетки, полученные из моноцитов (DC), активировали с помощью LPS Е. coli и совместно культивировали с аллогенными CD3+ Т-клетками в соотношении 1:1. IFNγ измеряли методом DELFIA после 5 дней совместного культивирования. Данные для одного эксперимента.
Фиг.24 (b): Индукция IL-2 в анализе DC-T-клеток методом MLR. Дендритные клетки, полученные из моноцитов (DC), активировали с помощью LPS Е. coli и совместно культивировали с аллогенными CD3+ Т-клетками в соотношении 1:1. IL-2 измеряли методом DELFIA после 3-х дней совместного культивирования. Данные для одного эксперимента.
Фиг. 25: Титрование молекул FIT-Ig, исходных моноспецифических антител и контрольных антител в анализе связывания PD-L1/TIGIT AlphaScreen® с использованием метода 1. Антитела инкубируют с белками PD-L1 и TIGIT в течение часа перед добавлением бусин с акцептором AlphaScreen® на один час с последующим добавлением бусин с донором AlphaScreen® еще на один час с последующим детектированием флуоресценции. А) титрование молекул FIT-Ig; В) Титрование моноспецифических антител. Представленные данные относятся к одному уникальному эксперименту.
Фиг. 26: титрование молекул FIT-Ig, исходных моноспецифических антител, а также контрольных антител в анализе связывания PD-L1/TIGIT AlphaScreen® с использованием метода 2. На бусины с донором и акцептором AlphaScreen® наносили в течение одного часа белки PD-L1 и TIGIT, соответственно, перед добавлением антител в течение одного часа с последующим детектированием флуоресценции. А) титрование молекул FIT-Ig; В) Титрование моноспецифических антител. Представленные данные относятся к одному уникальному эксперименту.
Фиг. 27: Титрование молекул FIT-Ig и контрольного антитела в анализе рекрутмента клеток с использованием PD-L1/TIGIT методом проточной цитометрии. СНО с PD-L1 человека и HEK с TIGIT человека окрашивали CellTrace™ Far Red и CellTrace™ Violet, соответственно, и совместно культивировали в присутствии антител в течение одного часа, после чего проводили детектирование флуоресценции и идентификацию дважды положительной популяции. Представленные данные относятся к одному уникальному эксперименту
Фиг. 28: Расширение лимфоцитов в ответ на введение дозы иммуноцитокинов. Образцы крови натощак брали в пробирки, предварительно обработанные ЭДТА, перед введением исследуемых препаратов (0) и через 2, 5 и 7, 10, 14 и 23 дня после их введения. Количество клеток измеряли с помощью Bayer Advia 120. Результаты выражены в виде кратности изменения количества лимфоцитов.
Фиг. 29: Уровни растворимого CD25 в плазме яванских макак, получивших дозу молекул иммуноцитокина. Образцы плазмы получали перед введением исследуемых препаратов (0) и через 3, 7 и 10 дней после введения дозы и анализировали с использованием коммерческого набора ИФА.
Фиг. 30: Анализ стандартных гематологических параметров в ответ на введение доз иммуноцитокинов. Образцы крови натощак брали в пробирки, предварительно обработанные ЭДТА, перед введением исследуемых препаратов (0) и через 2, 5, 7, 10, 14 и 23 дней после их введения. Анализ А) гемоглобина, В) гематокрита, С) количества эритроцитов и D) количества тромбоцитов проводили с использованием Bayer Advia 120. Результаты выражены как кратность изменения параметра в каждый момент времени.
Фиг. 31: Уровни цитокинов в плазме яванских макак, получивших дозу молекул иммуноцитокина. Образцы плазмы брали перед введением исследуемых препаратов (0) и через 1, 3, 7, 10, 14 и 23 дня после введения доз, и анализировали методом MSD для определения уровней a) TNF-α; б) IL-8; с) IL-6; d) IFNγ; е) G-CSF, f) IL-2, g) IL-4 и h) IL-5. Отсутствие столбиков показывает, что уровни цитокинов были ниже предела количественной оценки метода анализа. IL-1β не обнаруживался ни в каких образцах и потому не был включен в графики.
Фиг. 32: Фармакокинетический (ФК) анализ иммуноцитокинов. Сыворотку получали из образцов крови, взятых в различные моменты времени на протяжении 96 часов. Сыворотку инкубировали на планшетах, покрытых PD-L1, и иммуноцитокины детектировали с использованием биотинилированного детекторного антитела против Fc человека, и меченого европием стрептавидина. Результаты выражены в % от пиковой концентрации.
Фиг. 33: Расширение субпопуляций специфических Т-клеток молекулами ICK. Цельную кровь инкубировали с антителами для окрашивания перед лизисом эритроцитов, фиксацией и анализом методом проточной цитометрии. Результаты выражены в виде кратности изменения абсолютной численности (а) CD4+ Т-клеток и (b) CD8+ Т-клеток в каждый момент времени.
Фиг. 34: Эффекторная функция оптимизированных прототипов антител в анализе репортерных клеток. Клетки-мишени (ES2), экспрессирующие PD-L1, совместно культивировали в течение ночи с клетками Jurkat, генетически модифицированными для индуцированной NFAT экспрессии люциферазы, и FcγRIIIa, в присутствии PD-L1-антител. Каждая точка данных соответствует средней кратности индуцирования относительных световых единиц ± стандартное отклонение. Приведены данные для одного типичного эксперимента из трех независимых экспериментов
Фиг. 35: Связывание оптимизированных прототипов антитела с клеточно экспрессируемым PD-L1 яванского макака. Антитела титровали на клетках СНО, экспрессирующих PD-L1 яванского макака, и связанное антитело детектировали с помощью AlexaFluor 647 против IgG человека. Данные для одного эксперимента
Фиг. 36 (а): Анализ методом FACS нейтрализации CHO-S с PD-L1 человека рецептором PD-1. Профили нейтрализации оптимизированных прототипов антител по сравнению с калибровочным анти-PD-L1 антителом и изотипическим контролем. Данные представляют два независимых эксперимента
Фиг. 36 (b): Анализ нейтрализации методом FACS CHO-S с PD-L1 человека рецептором CD80. Профили нейтрализации оптимизированных прототипов антител по сравнению с калибровочным анти-PD-L1 антителом и изотипическим контролем. Данные представляют два независимых эксперимента
Фиг. 37: Индуцирование продуцирования IFNγ в анализе совместного культивирования моноцитов-Т-клеток анти-PD-L1 антителами в формате человеческого IgG1. Каждая точка данных представляет собой среднюю кратность индуцирования IFNγ по результатам по меньшей мере трех независимых экспериментов, ± стандартная ошибка среднего
Детальное описание
1. Определения
Если иное не определено в данном документе, научные и технические термины должны иметь значения, являющиеся общепринятыми для рядовых специалистов в данной области техники. Кроме того, если иное не требуется по контексту, термины в единственном числе должны включать множественное число, а термины во множественном числе должны включать единственное число.
Термины в единственном числе (в английском тексте - с артиклями «a», «an» и «the») включают обозначаемые объекты во множественном числе, если контекст явно не указывает иное. Аналогично, слово «или» должно включать «и», если контекст явно не указывает иное. Хотя способы и материалы, аналогичные или эквивалентные описанным в данном документе, могут быть использованы в практике или при тестировании данного изобретения, пригодные способы и материалы описаны ниже. Аббревиатура "e.g." происходит от латинского выражения «exempli gratia» и используется в данном документе для обозначения неограничивающего примера. Таким образом, аббревиатура "e.g." является синонимом термина «например».
В описании и формуле изобретения термин «приблизительно» используется для модификации, например, количества ингредиента в композиции, концентрации, объема, температуры процесса, времени процесса, выхода, расхода, давления и подобных значений, и их диапазонов, используемых при описании вариантов реализации изобретения. Термин «приблизительно» относится к изменению численной величины, которое может иметь место, например, при типичных процедурах измерения и обработки, используемых для получения соединений, композиций, концентратов или применения композиций; вследствие непреднамеренной ошибки в этих процедурах; вследствие различий в производстве, источниках или в чистоте исходных материалов или ингредиентов, используемых для осуществления этих методов, и из-за подобных соображений. Термин «приблизительно» также охватывает количества, которые отличаются из-за старения композиции с определенной начальной концентрацией или смесью, и количества, которые отличаются из-за смешивания или обработки композиции с определенной начальной концентрацией или смесью. В случае изменения с помощью термина «приблизительно», связанные с ним притязания включают эквиваленты этих величин.
В используемом в данном документе значении, термин «вводить» или «введение» относится к акту инъекции или физической доставки иным образом вещества, существующего вне организма (например, антитела против hPD-L1, предложенного в данном документе), пациенту, например, через слизистую оболочку, путем внутрикожной, внутривенной, внутримышечной доставки и/или любы другим способом физической доставки, описанным в данном документе или известным в данной области. При лечении заболевания или его симптома, введение вещества обычно происходит после начала проявления заболевания или его симптомов. При профилактике болезни или ее симптомов, введение вещества обычно происходит до начала проявления заболевания или его симптомов.
Термины «антитело», «иммуноглобулин» или «Ig» могут использоваться в данном документе взаимозаменяемо и означают молекулу иммуноглобулина, которая распознает и специфически связывается с мишенью, такой как белок, полипептид, пептид, углевод, полинуклеотид, липид или комбинации вышеуказанных, посредством по меньшей мере одного сайта распознавания антигена в вариабельной области молекулы иммуноглобулина. В используемом в данном документе значении, термин «антитело» включает интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител (такие как фрагменты Fab, Fab', F(ab')2 и Fv), одноцепочечные мутанты Fv (scFv), мультиспецифические антитела такие как биспецифические антитела (включая антитела с двойным связыванием), химерные антитела, гуманизированные антитела, человеческие антитела, гибридные белки, содержащие антигенопределяющую область антитела, и любую другую модифицированную молекулу иммуноглобулина, содержащую антигенраспознающий сайт, при условии, что антитела проявляют желательную биологическую активность. Термин «антитело» также может относиться к Y-образному гликопротеину с молекулярным весом приблизительно 150 кДа, состоящему из четырех полипептидных цепей: двух легких (L) цепей и двух тяжелых (Н) цепей. Существует пять типов изотипов тяжелой цепи Ig млекопитающих, обозначаемых греческими буквами альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ). Тип тяжелой цепи определяет класс антитела, т.е. IgA, IgD, IgE, IgG и IgM, соответственно. Классы γ и α дополнительно делятся на подклассы на основе различий в последовательности и функции константной области, например, IgG1, hIgG2, mIgG2A, mIgG2B, IgG3, IgG4, IgA1 и IgA2. У млекопитающих существуют два типа легких цепей иммуноглобулина, λ и κ. «Вариабельная область» или «вариабельный домен» антитела относится к аминоконцевым доменам тяжелой или легкой цепи антитела. Вариабельные домены тяжелой цепи и легкой цепи могут обозначаться «VH» и «VL», соответственно. Эти домены обычно являются наиболее вариабельными частями антитела (по сравнению с другими антителами того же класса) и содержат антигенсвязывающие сайты.
Антитела, раскрытые в данном документе, могут быть олигоклональными, поликлональными, моноклональными (включая полноразмерные моноклональные антитела), камелизированными, химерными, CDR-привитыми, мультиспецифическими, биспецифическими (включая антитела с двойным связыванием), каталитическими, химерными, гуманизированными, полностью человеческими, антиидиотипическими, включая антитела, которые могут быть мечеными в растворимой или связанной форме, а также их фрагментами, вариантами или производными, взятыми либо отдельно, либо в сочетании с другими аминокислотными последовательностями, обеспечиваемыми известными способами. Антитело может принадлежать любому виду. Антитела, раскрытые в данном документе, могут быть голыми или конъюгированными с другими молекулами, такими как токсины, радиоизотопы и т.д.
Термин «антигенсвязывающий домен», «антигенсвязывающая область», «антигенсвязывающий фрагмент» и подобные термины относятся к той части антитела, которая содержит аминокислотные остатки, взаимодействующие с антигеном, и придающие связывающему агенту его специфичность и аффинность к антигену (например, гипервариабельные участки (CDR)). Антигенсвязывающая область может быть получена от любых видов животных, таких как грызуны (например, кролик, крыса или хомяк) и люди. Предпочтительно, антигенсвязывающая область, будет иметь человеческое происхождение.
Описанные в данном документе антигенсвязывающие фрагменты могут включать одноцепочечные Fv (scFv), одноцепочечные антитела, однодоменные антитела, доменные антитела, фрагменты Fv, фрагменты Fab, фрагменты F(ab'), фрагменты F(ab')2, фрагменты антител, проявляющие желательную биологическую активность, стабилизированную дисульфидными связями вариабельную область (dsFv), димерную вариабельную область (диатело), антиидиотипические (анти-Id) антитела (включая, например, антитела против Id к антителам), внутриклеточные антитела, линейные антитела, одноцепочечные молекулы антител и мультиспецифические антитела, образованные из фрагментов антител и эпитопсвязывающих фрагментов любого из вышеуказанного. В частности, антитела и фрагменты антител, раскрытые в данном документе, могут включать молекулы иммуноглобулина и иммунологически активные фрагменты молекул иммуноглобулина, т.е. молекулы, содержащие антигенсвязывающий сайт. Гидролиз антител с ферментом папаином дает два идентичных антигенсвязывающих фрагмента, известных также как фрагменты «Fab», и фрагмент «Fc», не обладающий антигенсвязывающей активностью, но способный кристаллизоваться. «Fab» при использовании в данном документе относится к фрагменту антитела, который включает один константный и один вариабельный домен каждой из тяжелой и легкой цепей. Термин «область Fc» используется в данном документе для определения С-концевого участка тяжелой цепи иммуноглобулина, включая Fc-области с нативной последовательностью и варианты Fc-областей. «Fc-фрагмент» относится к карбоксиконцевым частям обеих Н-цепей, удерживаемых вместе дисульфидными связями. Эффекторные функции антител определяются последовательностями в области Fc - области, которая также распознается Fc-рецепторами (FcR), присутствующими на определенных типах клеток. Гидролиз антител с ферментом пепсином дает фрагмент F(ab')2, в котором два плеча молекулы антитела остаются связанными и содержат два антигенсвязывающих сайта. Фрагмент F(ab')2 обладает способностью сшивать антиген.
«Fv» при использовании в данном документе относится к минимальному фрагменту антитела, которое сохраняет как антигенраспознающие, так и антигенсвязывающие сайты. Эта область состоит из димера вариабельного домена одной тяжелой и одной легкой цепи с сильной нековалентной или ковалентной связью. В такой конфигурации три CDR каждого вариабельного домена взаимодействуют, образуя антигенсвязывающий сайт на поверхности димера VH-VL. В совокупности, шесть CDR обеспечивают антигенсвязывающую специфичность антитела. Однако, даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфичных по отношению к антигену) обладает способностью распознавать и связывать антиген, хотя и с более низким сродством, чем цельный сайт связывания.
В используемом в данном документе значении, термин «моноклональное антитело» относится к антителу, полученному из популяции по существу гомогенных антител, то есть индивидуальные антитела, составляющие популяцию, являются идентичными, за исключением возможных естественных мутаций и/или посттрансляционных модификаций (например, изомеризации, амидирования) которые могут присутствовать в незначительных количествах. Моноклональные антитела являются высокоспецифичными и направлены против одной антигенной детерминанты или эпитопа. В отличие от них, препараты поликлональных антител обычно включают различные антитела, направленные против различных антигенных детерминант (или эпитопов). В используемом в данном документе значении, термин «моноклональное антитело» охватывает как интактные, так и полноразмерные моноклональные антитела, а также фрагменты антител (такие как Fab, Fab', F(ab')2, Fv), одноцепочечные (scFv) мутанты, гибридные белки, содержащие часть антитела и любую другую модифицированную молекулу иммуноглобулина, содержащую антигенараспознающий сайт. Кроме того, «моноклональное антитело» относится к таким антителам, полученным любым количеством способов, включая, без ограничений, гибридому, фаговую селекцию, рекомбинантную экспрессию и трансгенных животных.
Моноклональные антитела в данном документе могут включать «химерные» антитела (иммуноглобулины), в которых часть тяжелой и/или легкой цепи является идентичной или гомологичной соответствующим последовательностям в антителах, полученных от определенного вида или принадлежащих к определенному классу или подклассу антител, в то время как остальная часть цепи (цепей) является идентичной или гомологичной соответствующим последовательностям в антителах, полученных от другого вида или принадлежащих к другому классу или подклассу антитела, а также к фрагментам таких антител, проявляющим желательную биологическую активность.
Термин «гуманизированное антитело» относится к субпопуляции химерных антител, в которых «гипервариабельная область» из нечеловеческого иммуноглобулина (донорное антитело) заменяет остатки из гипервариабельной области в иммуноглобулине человека (антитело-реципиент). В общем, гуманизированное антитело будет включать по существу все из по меньшей мере одного, и типично двух вариабельных доменов, в которых все или по существу все гипервариабельные петли соответствуют последовательности нечеловеческого иммуноглобулина, и все или по существу все каркасные области представляют собой последовательность человеческого иммуноглобулина, хотя каркасные области могут включать одно или несколько замещений, которые улучшают характеристики антител, такие как аффинность связывания, изомеризация, иммуногенность и т.д.
Термин «биспецифическое антитело» означает антитело, которое содержит специфичность к двум молекулам-мишеням и включает, без ограничений, такие форматы, как DVD-Ig (см. DiGiammarino et al., "Design and generation of DVD-Ig™ molecules for dual-specific targeting", Meth. Mol. Biol., 2012, 889, 145-156), mAb2 (см. WO 2008/003103, описание формата mAb2 включено в данный документ посредством ссылки), FIT-Ig (см. WO 2015/103072, описание каркаса FIT-Ig включено в данный документ посредством ссылки), mAb-dAb, dock and lock, обмен Fab-плечо, SEEDbody, Triomab, LUZ-Y, Fcab, κλ-body (антитело к каппа-лямбда легким цепям иммуноглобулинов), ортогональный Fab, scDiabody-Fc (одноцепочечное диатело-Fc), диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело, BiTE, диатело, DART, TandAb, scDiabody (одноцепочечное диатело), scDiabody-СН3 (одноцепочечное диатело-СН3), Diabody-СН3 (диатело-СН3), Triple body (тройное антитело), миниантитело, минитело, минитело TriBi, scFv-СН3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, тетравалентный HCab, ImmTAC, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами (charge pairs), заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig и zybody. Обзор биспецифических форматов приведен в Spiess, С, et al., Mol. Immunol. (2015). В другом варианте реализации, биспецифическая молекула содержит антитело, слитое с другим не-Ig-форматом, например, связывающий домен Т-клеточного рецептора; домен суперсемейства иммуноглобулина; вариабельный лимфоцитарный рецептор бесчелюстных; домен фибронектина (например, аднектин (Adnectin™)); константный домен антитела (например, домен СН3, например, СН2 и/или СН3, принадлежащий Fcab™), где константный домен не является функциональным доменом CH1; scFv; (scFv)2; одноцепочечное диатело (sc-diabody); scFab; центирин и эпитопсвязывающий домен, полученный из каркаса, выбранного из CTLA-4 (Evibody™); липокалиновый домен; белок А, такой как Z-домен белка А (например, Affibody™ или SpA); А-домен (например, Avimer™ или Maxibody™); белок теплового шока (такой как эпитопсвязывающий домен, полученный из GroEI и GroES); трансферриновый домен (например, trans-body); белок с анкириновым повтором (например, DARPin™); пептидный аптамер; лектиновый домен С-типа (например, тетранектин (Tetranectin™)); человеческий γ-кристаллин или убиквитин человека (аффилин); домен PDZ; токсин скорпиона; и домен Кунитц-типа ингибитора протеазы человека.
В одном варианте реализации, биспецифическое антитело представляет собой mAb2. MAb2 содержит домен VH и VL интактного антитела, слитый с модифицированной константной областью, которая была генетически модифицирована для образования антигенсвязывающего сайта, известного как «Fcab». Технология, лежащая в основе формата Fcab/mAb2, более подробно описана в WO 2008/003103, и описание формата mAb2 включено в данный документ посредством ссылки.
В одном варианте реализации, «биспецифическое антитело» не включает формат FIT-Ig. В одном варианте реализации, «биспецифическое антитело» не включает формат mAb2. В одном варианте реализации, «биспецифическое антитело» не включает ни формат FIT-Ig, ни формат mAb2.
В другом варианте реализации, биспецифическое антитело представляет собой «антитело с двойным связыванием». В используемом в данном документе значении, термин «антитело с двойным связыванием» представляет собой биспецифическое антитело, в котором оба антигенсвязывающих домена образованы парой VH/VL и включают FIT-Ig (см. WO 2015/103072, включенную в данный документ посредством ссылки), mAb-dAb, dock and lock, обмен Fab-плечо, SEEDbody, Triomab, LUZ-Y, Fcab, κλ-body, ортогональный Fab, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab- scFv, внутриклеточное антитело, BiTE, диатело, DART, TandAb, scDiabody, scDiabody-CH3, Diabody-СН3, Triple body, миниантитело, минитело, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, тетравалентный HCab, ImmTAC, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv и scFv4-Ig.
Термины «гипервариабельная область», «область CDR» или «CDR» относятся к областям вариабельного домена антитела, являющимся гипервариабельными в последовательности и/или образующим структурно определенные петли. Как правило, сайты связывания антигена антитела включают шесть гипервариабельных областей: три в VH (CDRH1, CDRH2, CDRH3) и три в VL (CDRL1, CDRL2, CDRL3). Эти области тяжелой и легкой цепей антитела обеспечивают антигенсвязывающую специфичность антитела. CDR (гипервариабельные участки) могут быть определены в соответствии с системой Кабата (см. Kabat, Е.А. et al., 1991, "Sequences of Proteins of Immunological Interest", 5th edit., NIH Publication no. 91-3242, U.S. Department of Health and Human Services). Для определения CDR могут использоваться другие системы, такие как (which as) система, разработанная Chothia et al. (см. Chothia, С. & Lesk, A.M., 1987, "Canonical structures for the hypervariable regions of immunoglobulins", J. Mol. Biol., 196, 901-917) и система IMGT (см. Lefranc, M.P., 1997, "Unique database numbering system for immunogenetic analysis", Immunol. Today, 18, 50). Антитело обычно содержит 3 CDR тяжелой цепи и 3 CDR легкой цепи. Термин CDR или CDRs используется в данном документе для обозначения одной или нескольких из этих областей. Специалист в данной области способен легко сравнить различные системы номенклатуры и определить, может ли конкретная последовательность быть определена как CDR.
«Человеческое антитело» представляет собой антитело, которое обладает аминокислотной последовательностью, соответствующей последовательности антитела, продуцируемого человеком, и/или было получено с использованием любого из способов получения человеческих антител и определенно исключает гуманизированное антитело, содержащее нечеловеческие антигенсвязывающие остатки. Термин «специфически связывается» относится к измеримым и воспроизводимым взаимодействиям, таким как связывание между мишенью и антителом, которое позволяет определить присутствие мишени в присутствии гетерогенной популяции молекул, включая биологические молекулы. Например, антитело, специфически связывающееся с мишенью (которая может быть эпитопом), представляет собой антитело, которое связывает эту мишень с большей аффинностью, авидностью, более легко и/или с большей продолжительностью, чем оно связывается с другими мишенями. В одном варианте реализации, степень связывания антитела с несвязанной мишенью составляет менее примерно 10% от связывания антитела с мишенью, при измерении, например, методом радиоиммуноанализа (RIA).
Антитело или его фрагмент, которые специфически связываются с антигеном hPD-L1, могут быть перекрестно-реактивными с родственными антигенами. Предпочтительно, антитело или его фрагмент, которые специфически связываются с антигеном hPD-L1, не реагируют перекрестно с другими антигенами (но могут, необязательно, перекрестно реагировать с PD-L1 другого вида, например, макака-резуса или мыши). Антитело или его фрагмент, которые специфически связываются с антигеном hPD-L1, можно идентифицировать, например, с помощью иммуноанализов, BIAcore™ или других методов, известных специалистам в данной области. Антитело или его фрагмент специфически связываются с антигеном PD-L1, если они связываются с антигеном hPD-L1 с более высокой аффинностью, чем с любым перекрестно-реактивным антигеном, при определении с использованием экспериментальных методов, таких как радиоиммуноанализы (RIA) и твердофазовые иммуноферментные анализы (ИФА). Как правило, специфическая или селективная реакция будет по меньшей мере вдвое превышать фоновый сигнал или шум, и наиболее характерно, будет превышать фон более чем в 10 раз (например, более чем в 15 раз, более чем в 20 раз, более чем в 50 раз или более чем в 100 раз). См., например, Paul, ed., 1989, Fundamental Immunology Second Edition, Raven Press, New York, где на стр. 332-336 приведено обсуждение специфичности антител.
Термин «алифатическая аминокислота» означает, что группы R аминокислот являются неполярными и гидрофобными. Гидрофобность возрастает с увеличением числа атомов С в углеводородной цепи. Алифатическими аминокислотами являются глицин, аланин, валин, лейцин и изолейцин.
Термин «ароматическая аминокислота» означает, что группы R аминокислот содержат ароматическую кольцевую систему. Ароматическими аминокислотами являются фенилаланин, тирозин и триптофан.
Термин «гидроксилсодержащая аминокислота» означает, что группы R аминокислот содержат гидроксильную группу и являются гидрофильными. Гидроксилсодержащими аминокислотами являются серии, цистеин, треонин и метионин.
Термин «основная аминокислота» означает, что группы R аминокислот содержат азот и являются основными при нейтральном рН. Основными аминокислотами являются гистидин, лизин и аргинин.
Термин «циклическая аминокислота» означает, что группы R аминокислот имеют алифатическую циклическую структуру. Единственной циклической алифатической аминокислотой является пролин.
Термин «кислотная аминокислота» означает, что группы R аминокислот являются полярными и отрицательно заряжены при физиологическом рН. Кислотными аминокислотами являются аспартат и глутамат.
Термин «амидная аминокислота» означает, что группы R аминокислот содержат амидную группу. Амидными аминокислотами являются аспарагин и глутамин.
В используемом в данном документе значении, термин «номер авторизации» или «номер разрешения на продажу» относится к номеру, присвоенному регулирующим органом после того, как данный орган определит, что конкретный медицинский продукт и/или композиция могут быть выпущены на рынок и/или в продажу на территории, находящейся под юрисдикцией органа. В используемом в данном документе значении, термин «регулирующий орган» относится к одному из агентств, ответственных за оценку, например, безопасности и эффективности медицинского продукта и/или композиции, а также за контроль продаж/сбыта таких продуктов и/или композиций на данной территории. Управление по контролю за пищевыми продуктами и лекарствами (FDA) в США и Европейское агентство по лекарственным средствам (ЕРА) в Европе являются всего лишь двумя примерами таких регулирующих органов. Другие неограничивающие примеры могут включать SDA, МРА, MHPRA, IMA, ANMAT, отдел лекарственных средств Департамента здравоохранения Гонконга, CDSCO, Medsafe и KFDA.
В используемом в данном документе значении, термин «биомаркер» относится к гену, который дифференциально экспрессируется у особ, имеющих представляющее интерес заболевание, например, ген, дифференциально экспрессирующийся у особ с раком. В одном варианте реализации, PD-L1 представляет собой биомаркер, экспрессия которого в опухолях может указывать, будет ли пациент реагировать на конкретный тип лечения, в частности, будет ли пациент отвечать на лечение, нацеленное на PD-L1, например, иммунотерапию с использованием антител против PD-L1. В одном варианте реализации, PD-L1 представляет собой биомаркер, экспрессия которого в опухолях может указывать на то, будет ли пациент реагировать на конкретный вид лечения, в частности, будет ли пациент отвечать на лечение, нацеленное на PD-1, например, иммунотерапию с использованием антител против PD-1. В другом варианте реализации, PD-L1 может быть свободным или мембранно-связанным. В другом варианте реализации, PD-L1 может быть зафиксированным или нефиксированным.
В используемом в данном документе значении, термин «буфер» относится к химическому агенту, который способен поглощать определенное количество кислоты или основания без значительного изменения рН.
В используемом в данном документе значении, термин «носитель» относится к разбавителю, адъюванту (например, адъюванту Фрейнда (полному и неполному)), эксципиенту или носителю, с которым вводится терапевтическое средство. Такие фармацевтические носители могут быть стерильными жидкостями, такие как вода и масла, в том числе минерального, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Вода является предпочтительным носителем, когда фармацевтическая композиция вводится внутривенно. Солевые растворы и водные растворы декстрозы и глицерина также могут быть использованы в качестве жидких носителей, особенно для инъекционных растворов.
Термин «химиотерапевтическое средство» или «химиотерапия» относится к терапевтическому агенту, основной целью которого является уничтожение раковых клеток, как правило, путем нарушения способности опухолевых клеток к росту или размножению. Существует много разных типов химиотерапевтических средств, причем доступными являются более 50 одобренных препаратов для химиотерапии. Химиотерапевтические препараты можно классифицировать в зависимости от способа их действия. Алкилирующие препараты убивают раковые клетки, непосредственно атакуя ДНК, являющуюся генетическим материалом генов. Циклофосфамид представляет собой алкилирующий препарат. Антиметаболиты препятствуют продуцированию ДНК и препятствуют росту и размножению клеток. Примером антиметаболита является 5-фторурацил (5-FU). Противоопухолевые антибиотики производят из природных веществ, таких как почвенные грибки. Они нарушают важным функциям клетки, включая продуцирование ДНК и клеточных белков. К этой группе химиотерапевтических препаратов относятся доксорубицин и блеомицин. Алкалоиды растений препятствуют нормальному делению клеток. Винбластин и винкристин являются растительными алкалоидами, полученными из растения барвинка. Стероидные гормоны замедляют рост некоторых видов рака, зависящих от гормонов. Например, тамоксифен используется для лечения рака молочной железы, рост которого зависит от гормона эстрогена. Ингибиторы ответа на повреждения ДНК (DDR), такие как ингибиторы PARP, блокируют механизмы репарации ДНК после одно- или двухцепочечных разрывов.
Примеры химиотерапевтических средств включают адриамицин, доксорубицин, 5-фторурацил, цитозин-арабинозид (Ara-С), циклофосфамид, тиотепа, таксотер (доцетаксел), бусульфан, цитоксин, таксол, метотрексат, цисплатин, мелфалан, винбластин, блеомицин, этопозид, ифосфамид, митомицин С, митоксантрон, винкристин (Vincreistine), винорелбин, карбоплатин, тенипозид, дауномицин, карминомицин, аминоптерин, дактиномицин, митомицины, эсперамицины (см. патент США №4675187), мелфалан и другие родственные производные азотных ипритов. Пригодные токсины и химиотерапевтические средства описаны в Remington's Pharmaceutical Sciences, 19 Ed. (Mack Publishing Co. 1995), а также в Goodman and Gilman's The Pharmacological Basis of Therapeutics, 7th Ed. (MacMillan Publishing Co. 1985). Другим примером химиотерапевтических средств является класс антитело-конъюгированных токсинов, включая, без ограничений, пирролобензодиазепины (pyrrolobenzodiazepiness), майтансаноиды, калихеамицин и т.д. Другие пригодные токсины и/или химиотерапевтические средства известны специалистам в данной области.
В используемом в данном документе значении, термин «композиция» должен охватывать продукт, содержащий указанные ингредиенты (например, антитело по изобретению), необязательно, в указанных количествах, а также любой продукт, который прямо или косвенно образуется при сочетании указанных ингредиентов, необязательно, в указанных количествах.
В используемом в данном документе значении, термин «содержащий» или «содержит» используется по отношению к антителам, фрагментам, применениям, композициям, способам и их соответствующему компоненту (компонентам), являющимся существенными для способа или композиции, но допускает возможность включения неуточненных элементов, независимо от того, являются они существенными или нет.
Термин «состоящий из» относится к антителам, фрагментам, применениям, композициям, методам и их соответствующим компонентам, как описано в данном документе, которые не содержат какого-либо элемента, не указанного в данном описании варианта реализации.
В используемом в данном документе значении, термин «состоящий по существу из» относится к элементам, необходимым для данного варианта реализации. Этот термин предусматривает возможность присутствия элементов, не оказывающих существенного влияния на основную и новую или функциональную характеристику (характеристики) этого варианта реализации.
В контексте полипептида, используемый в данном документе термин «производное» относится к полипептиду, который содержит аминокислотную последовательность полипептида hPD-L1, фрагмента полипептида hPD-L1 или антитела, специфически связывающегося с hPD-L1, которая была изменена путем введения замещений, делеций или аддиций аминокислот. В используемом в данном документе значении, термин «производное» также относится к полипептиду hPD-L1, фрагменту полипептида hPD-L1 или антителу, которое специфически связывается с полипептидом hPD-L1, которые были химически модифицированы, например, путем ковалентного присоединения к полипептиду молекулы любого типа. Например, но не в качестве ограничения, полипептид hPD-L1, фрагмент полипептида hPD-L1 или антитело hPD-L1 могут быть химически модифицированы, например, путем гликозилирования, ацетилирования, пегилирования, фосфорилирования, амидирования, дериватизации известными защитными/блокирующими группами, протеолитического расщепление, связывания с клеточным лигандом или другим белком и т.д. Производные модифицируют таким образом, чтобы они отличались от встречающегося в природе или исходного пептида или полипептидов по типу или месту присоединения молекул. Производные дополнительно включают делецию одной или нескольких химических групп, которые естественно присутствуют на пептиде или полипептиде. Производное полипептида hPD-L1, фрагмент полипептида hPD-L1 или антитело hPD-L1 могут быть химически модифицированы путем проведения химических модификаций с использованием методов, известных специалистам в данной области, включая, без ограничений, специфическое химическое расщепление, ацетилирование, формилирование (formulation), метаболический синтез туникамицина и т.д. Кроме того, производное полипептида hPD-L1, фрагмент полипептида hPD-L1 или антитело hPD-L1 могут содержать одну или несколько неклассических аминокислот. Полипептидное производное обладает функцией, аналогичной или идентичной полипептиду hPD-L1, фрагменту полипептида hPD-L1 или антителу hPD-L1, описанным в данном документе.
В используемом в данном документе значении, термин «эффекторная функция» относится к чему-то одному или нескольким из опосредованной антителами клеточной цитотоксичности (ADCC), ответов, опосредованных комплементзависимой цитотоксичностью (CDC), опосредованного Fc фагоцитоза, или антителозависимого клеточного фагоцитоза (ADCP) и рециркуляции антител через рецептор FcRn.
«Эффективное количество» относится к количеству, эффективному при дозировках и в течение периодов времени, необходимых для достижения желательного эффекта, включая терапевтический или профилактический результат. «Терапевтически эффективное количество» относится к минимальной концентрации, необходимой для достижения измеримого улучшения или профилактики конкретного расстройства. Терапевтически эффективное количество здесь может меняться в зависимости от таких факторов, как состояние болезни, возраст, пол и вес пациента, а также способность антитела вызывать желательный ответ у индивидуума. Терапевтически эффективное количество также является таким, при котором токсические или вредные эффекты антитела перевешиваются терапевтически благоприятными эффектами. «Профилактически эффективное количество» относится к количеству, эффективному при дозировках и в течение периодов времени, необходимых для достижения желательного профилактического результата. В некоторых вариантах реализации, эффективное количество антитела по изобретению составляет от примерно 0,1 мг/кг (мг антитела на кг веса пациента) до примерно 100 мг/кг. В некоторых вариантах реализации, эффективное количество предусматриваемого в них антитела составляет около 0,1 мг/кг, около 0,5 мг/кг, около 1 мг/кг, 3 мг/кг, 5 мг/кг, около 10 мг/кг, около 15 мг/кг, около 20 мг/кг, около 25 мг/кг, около 30 мг/кг, около 35 мг/кг, около 40 мг/кг, около 45 мг/кг, около 50 мг/кг, около 60 мг/кг, около 70 мг/кг, около 80 мг/кг около 90 мг/кг или около 100 мг/кг (или представляет собой диапазон в указанных пределах). В некоторых вариантах реализации, «эффективное количество», в используемом в данном документе значении, также относится к количеству антитела по изобретению, (необходимому) для достижения определенного результата (например, ингибирования связанной с hPD-L1 биологической активности клетки).
В используемом в данном документе значении, термин «эпитоп» относится к локализованной области на поверхности антигена, такого как полипептид hPD-L1 или фрагмент полипептида hPD-L1, способного связываться с одной или несколькими антигенсвязывающими областями антитела, и обладающего антигенной или иммуногенной активностью у животного, предпочтительно, млекопитающего, и наиболее предпочтительно, у человека, которая способна вызывать иммунный ответ. Эпитоп, обладающий иммуногенной активностью, представляет собой часть полипептида, которая вызывает гуморальный иммунный ответ у животного. Эпитоп, обладающий антигенной активностью, представляет собой часть полипептида, с которым специфически связывается антитело, по результатам определения любым способом, хорошо известным в данной области, например, с помощью описанных в данном документе иммуноанализов. Антигенные эпитопы необязательно, должны быть иммуногенными. Эпитопы обычно состоят из химически активных поверхностных группировок молекул, таких как аминокислоты или боковые цепи сахаров, и имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Область полипептида, участвующая в образовании эпитопа, может состоять из последовательно расположенных аминокислот полипептида, или эпитоп может быть образована двумя или более несмежными областями полипептида. Эпитоп может быть или не быть трехмерным поверхностным образованием антигена. В некоторых вариантах реализации, эпитоп hPD-L1 представляет собой трехмерное поверхностное образование полипептида hPD-L1 (например, в тримерной форме полипептида hPD-L1). В других вариантах реализации, эпитоп hPD-L1 является линейной структурой полипептида hPD-L1 (например, в тримерной форме или мономерной форме полипептида hPD-L1). Антитела, представленные в данном документе, могут специфически связываться с эпитопом мономерной (денатурированной) формы hPD-L1, эпитопом тримерной (нативной) формы hPD-L1, или как с мономерной (денатурированной) формой, так и с тримерной (нативной) формой hPD-L1. В конкретных вариантах реализации, антитела, представленные в данном документе, специфически связываются с эпитопом тримерной формы hPD-L1, но не связываются специфически с мономерной формой hPD-L1.
В используемом в данном документе значении, термин «эксципиенты» относится к инертным веществам, которые обычно используются в качестве разбавителя, носителя, консервантов, связующих веществ или стабилизирующего агента для лекарственных средств и включают, без ограничений, белки (например, сывороточный альбумин и т.д.), аминокислоты (например, аспарагиновая кислота, глутаминовая кислота, лизин, аргинин, глицин, гистидин и т.д.), жирные кислоты и фосфолипиды (например, алкилсульфонаты, каприлат и т.д.), поверхностно-активные вещества (например, ДСН, полисорбат, неионное поверхностно-активное вещество и т.д.), сахариды (например, сахароза, мальтоза, трегалоза и т.д.) и полиолы (например, маннит, сорбит и т.д.). См. также Remington's Pharmaceutical Sciences (1990) Mack Publishing Co., Easton, Pa., которая включена в настоящее описание посредством ссылки в полном объеме.
В используемом в данном документе значении, термин «фиксированный» или «фиксация» относится к химическому процессу, посредством которого биологические ткани сохраняются от разложения, для предотвращения аутолиза или гниения. В общем, фиксация включает воздействие на ткань химическими соединениями, такими как спирты или альдегиды, такие как формальдегид, для остановки протекающих биохимических реакций. В некоторых случаях фиксация может также увеличивать механическую прочность или стабильность обработанных тканей. Термин «нефиксированный» относится к ткани, которая не подвергалась химической обработке для предотвращения разложения ткани. В используемом в данном документе значении, термин «поверхностно экспрессируемый» означает, что белок внедрен в клеточную мембрану или проходит через нее, или связан с белком, который внедрен в или проходит через клеточную мембрану (т.е. мембранно-связанный белок). В одном варианте реализации, поверхностно экспрессируемый белок включает один или несколько трансмембранных доменов. В другом варианте реализации, белок связан с наружной или внутренней поверхностью клеточной мембраны опосредованно посредством ассоциации с другим белком, «прошивающим» мембрану (т.е. сам поверхностно экспрессируемый белок не проходит через клеточную мембрану). В общем, поверхностно экспрессируемые белки, которые интегрированы в клеточную мембрану или экспрессируются эндогенно внутри клетки, имеют большую склонность складываться в правильной конформации, чем рекомбинантно полученные свободные формы этого же белка.
В контексте пептида или полипептида термин «фрагмент», в используемом в данном документе значении, относится к пептиду или полипептиду, содержащему менее чем полноразмерную аминокислотную последовательность. Такой фрагмент может образовываться, например, в результате усечения на аминоконце, усечения на карбоксильном конце и/или внутренней делеции остатка (остатков) из аминокислотной последовательности. Фрагменты могут, например, образовываться в результате альтернативного сплайсинга РНК или активности протеазы in vivo. В некоторых вариантах реализации, фрагменты PD-L1 включают полипептиды, содержащие аминокислотную последовательность из по меньшей мере 5 смежных аминокислотных остатков, по меньшей мере 10 смежных аминокислотных остатков, по меньшей мере 15 смежных аминокислотных остатков, по меньшей мере 20 смежных аминокислотных остатков, по меньшей мере 25 смежных аминокислотных остатков, по меньшей мере 40 смежных аминокислотных остатков, по меньшей мере 50 смежных аминокислотных остатков, по меньшей мере 60 смежных аминокислотных остатков, по меньшей мере 70 смежных аминокислотных остатков, по меньшей мере 80 смежных аминокислотных остатков, по меньшей мере 90 смежных аминокислотных остатков, по меньшей мере 100 смежных аминокислотных остатков, по меньшей мере 125 смежных аминокислотных остатков, по меньшей мере 150 смежных аминокислотных остатков, по меньшей мере 175 смежных аминокислотных остатков, по меньшей мере 200 смежных аминокислотных остатков или по меньшей мере 250 смежных аминокислотных остатков аминокислотной последовательности полипептида hPD-L1 или антитела, специфически связывающегося с полипептидом hPD-L1. В конкретном варианте реализации, фрагмент полипептида hPD-L1 или антитело, которое специфически связывается с антигеном hPD-L1, сохраняет по меньшей мере 1, по меньшей мере 2 или по меньшей мере 3 функции полипептида или антитела.
Термин «свободный» относится к полипептиду, например, PD-L1 или его фрагментам и его вариантам, которые объединены с буфером, причем полипептид не связан с клеточной поверхностью или клеточной мембраной. По существу, термин «свободный» может относиться к полипептиду, который способен к поверхностной экспрессии (т.е. включает один или несколько трансмембранных доменов или ассоциациированных с мембраной доменов), но, в его текущем состоянии, не экспрессируется на поверхности клетки или не связан с белком, экспрессирующимся на поверхности клетки. Свободный полипептид может также относиться к свободному рекомбинантному или нативному или несвязанному полипептиду. В контексте фагового дисплея, выбор свободного антигена может проводиться в растворе (называется в данном документе «выбором в растворе») или в адсорбированном на поверхности состоянии, например, адсорбированным на поверхности 96-луночного планшета (называется в данном документе «выбор методом биопэннинга»).
В используемом в данном документе значении, термин «гибридный белок» относится к полипептиду, который содержит аминокислотную последовательность антитела и аминокислотную последовательность гетерологичного полипептида или белка (т.е. полипептида или белка, обычно не являющегося частью антитела (например, антитела, не направленного против hPD-L1-антигена)). Термин «слияние» при использовании по отношению к hPD-L1 или к антителу против hPD-L1 относится к соединению пептида или полипептида, или его фрагмента, варианта и/или производного, с гетерологичным пептидом или полипептидом. Предпочтительно, гибридный белок сохраняет биологическую активность hPD-L1 или анти-hPD-LI антитела. В некоторых вариантах реализации, гибридный белок содержит домен VH, домен VL.CDR VH (один, два или три CDR VR) и/или CDR VL (один, два или три CDR VL) антитела hPD-L1, где гибридный белок специфически связывается с эпитопом hPD-L1.
Термин «тяжелая цепь» при использовании по отношению к антителу касается пяти различных типов, называемых альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ), на основе аминокислотной последовательность константного домена тяжелой цепи. Эти различные типы тяжелых цепей хорошо известны и обусловливают существование пяти классов антител, IgA, IgD, IgE, IgG и IgM, соответственно, включая четыре подкласса IgG, а именно IgG1, IgG2, IgG3 и IgG4. Предпочтительно, тяжелая цепь представляет собой тяжелую цепь человека. В человеческой популяции существуют множественные аллели константной области тяжелой цепи каждого иммуноглобулина или подкласса иммуноглобулина. Нуклеотидные и аминокислотные последовательности этих аллельных вариантов представлены в общедоступных базах данных, таких как IMGT, ENSEMBL Swiss-Prot и Uniprot. Аллельные варианты также могут быть идентифицированы в различных проектах секвенирования генома. В одном варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат тяжелую цепь, кодируемую аллелем константной области IgG1, который включает, без ограничений, человеческие IGHG1*01 (SEQ ID NOs:340, 341 и 537), IGHG1*02 (SEQ ID NOs:340, 341 и 537), IGHG1*03 (SEQ ID NOs:523 и 524), IGHG1*04 (SEQ ID NOs:525 и 526) и IGHG1*05 (SEQ ID NOs:340, 341 и 537). В одном варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG2, который включает, без ограничений, человеческие IGHG2*01 (SEQ ID NOs:527 и 528), IGHG2*02 (SEQ ID NOs:529 и 530), IGHG2*03 (SEQ ID NOs:527 и 528), IGHG2*04 (SEQ ID NOs:531 и 532), IGHG2*05 (SEQ ID NOs:527 и 528) и IGHG2*06 (SEQ ID NOs:533 и 534). В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG3, который включает, без ограничений, человеческие IGHG3*01, IGHG3*02, IGHG3*03, IGHG3*04, IGHG3*05, IGHG3*06, IGHG3*07, IGHG3*08, IGHG3*09, IGHG3*10, IGHG3*11, IGHG3*12, IGHG3*13, IGHG3*14, IGHG3*15, IGHG3*16, IGHG3*17, IGHG3*18 и IGHG3*19. В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области IgG4, который включает, без ограничений, IGHG4*01 (SEQ ID NOs:192 и 193), IGHG4*02 (SEQ ID NOs:194 и 195), IGHG4*03 (SEQ ID NOs:196 & 197) и IGHG4*04 (SEQ ID NOs:192 и 193) человека. В другом примере, тяжелая цепь представляет собой инактивированный изотип IgG, например, инактивированный IgG4. В некоторых вариантах реализации, антитела по изобретению содержат константную область гамма-4 человека. В другом варианте реализации, константная область тяжелой цепи не связывает Fc-γ-рецепторы и, например, включает мутацию Leu235Glu. В другом варианте реализации, константная область тяжелой цепи содержит мутацию Ser228Pro для повышения стабильности. В другом варианте реализации, константная область тяжелой цепи представляет собой IgG4-PE (SEQ ID NO: 199). В другом варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи, кодируемую аллелем константной области мышиного IgG1, который включает, без ограничений, IGHG1*01 или IGHG1*02 мыши. В одном варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи, кодируемую аллелем константной области мышиной IgG2, который включает, без ограничений, мышиные IGHG2A*01, IGHG2A*02, IGHG2B*01, IGHG2B*02, IGHG2C*01, IGHG2C*02 или IGHG2C*03. В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем константной области мышиного IgG3, который включает, без ограничений, IGHG3*01 мыши.
В используемом в данном документе значении, термин «хозяин» относится к животному, предпочтительно, млекопитающему и наиболее предпочтительно, человеку.
В используемом в данном документе значении, термин «клетка-хозяин» относится к конкретной клетке субъекта, трансфицированной молекулой нуклеиновой кислоты, и потомству или потенциальному потомству такой клетки. Потомство такой клетки не может быть идентично родительской клетке, трансфицированной молекулой нуклеиновой кислоты, из-за мутаций или воздействий окружающей среды, которые могут возникать в последующих поколениях, или интеграции молекулы нуклеиновой кислоты в геном клетки-хозяина.
В используемом в данном документе значении, термин «цитокин IL-2» относится к цитокиноподобной молекуле, имеющей активность, схожую с IL-2 дикого типа. Он может проявлять активность по высокоаффинному (αβγ) рецептору IL-2 и/или по рецептору IL-2 промежуточной аффинности (αβ). Цитокин может быть вариантом цитокина IL-2, имеющим одну или несколько делеций, замещений или вставок аминокислот. Варианты цитокинов описаны более подробно ниже.
Используемый в данном документе термин «иммуномодулирующее средство» и его варианты, включая, без ограничений, иммуномодулирующие средства, относится к агенту, который модулирует иммунную систему хозяина. В некоторых вариантах реализации, иммуномодулирующим агентом является иммунодепрессант. В некоторых других вариантах реализации, иммуномодулирующим агентом является иммуностимулирующий агент. В соответствии с изобретением, иммуномодулирующий агент, используемый в комбинированных терапиях по изобретению, не включает антитело против hPD-L1 или антигенсвязывающий фрагмент. Иммуномодулирующие агенты включают, без ограничений, малые молекулы, пептиды, полипептиды, белки, гибридные белки, антитела, неорганические молекулы, миметики и органические молекулы.
Термин «в комбинации» в контексте проведения других методов лечения относится к использованию более чем одной терапии. Использование термина «в комбинации» не ограничивает порядок проведения терапий для субъекта с заболеванием. Первую терапию можно вводить до (например, за 1 минуту, 45 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель), одновременно или после (например, через 1 минуту, 45 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель) введения второй терапии субъекту, имевшему, имеющему или являющемуся восприимчивым к опосредованному hPD-L1 заболеванию. Любая дополнительная терапия может проводиться в любом порядке с другими дополнительными терапиями. В некоторых вариантах реализации, антитела по изобретению можно вводить в комбинации с одной или несколькими терапиями (например, терапиями, которые не являются антителами по изобретению, применяемыми в настоящее время для профилактики, лечения, ведения и/или облегчения hPD-L1-опосредованного заболевания. Неограничивающие примеры методов лечения, которые можно проводить в комбинации с антителом по изобретению, включают анальгетики, анестетики, антибиотики или иммуномодулирующие средства или любое другое средство, указанное в Фармакопее США и/или в справочнике врача (Physician's Desk Reference).
В используемом в данном документе значении, термин «иммуноцитокин» относится к формату антител, слитых с молекулой цитокина. Формат антител может быть любым из описанных в данном документе, и цитокин может быть присоединен непосредственно или с помощью линкера или химической связи к N-либо к С-концу тяжелой или легкой цепи формата антитела.
В используемом в данном документе значении, термин «инъекционное устройство» относится к устройству, предназначенному для выполнения инъекций, где инъекция включает стадии установления временного канала прохождения жидкости между инъекционным устройством и тканью особы, обычно, подкожной тканью. Инъекция дополнительно включает введение некоторого количества жидкого лекарственного средства в ткань и отсоединение или удаление инъекционного устройства из ткани. В некоторых вариантах реализации, инъекционное устройство может быть внутривенным устройством или схеме для внутривенного введения (IV), которое является типом инъекционного устройства, используемым, когда целевой тканью является кровь в системе кровообращения, например, кровь в вене. Обычным, но не ограничивающим примером инъекционного устройства являются игла и шприц.
В используемом в данном документе значении, термин «инструкции» относится к отображению письменного, печатного или графического материала на первичном контейнере изделия, например, к письменному материалу, отображаемому на флаконе, содержащем фармацевтически активный агент, или к подробной информации о составе и использовании представляющего интерес продукта, включенного в набор, содержащий представляющую интерес композицию. В инструкциях излагается способ лечения, который предполагается провести или выполнить.
«Выделенным» или «очищенным» антителом или белком являются материалы, которые были идентифицированы, выделены и/или извлечены из компонента его производственной среды (например, природного или рекомбинантного). Например, антитело или белок по существу не содержат клеточного материала или других загрязняющих белков из источника клеток или ткани, из которого было получено антитело, или по существу не содержит химических прекурсоров или других химических веществ при использовании химического синтеза. Фраза «по существу не содержащий клеточного материала» включает препараты антитела, в которых антитело отделено от клеточных компонентов клеток, из которых оно было выделено или получено рекомбинантными способами. Таким образом, антитело, по существу не содержащее клеточного материала, включает препараты антитела, имеющие менее 30%, 20%, 10% или 5% (по сухой массе) гетерологичного белка (также называемого в данном документе «загрязняющий белок»)). Когда антитело получают рекомбинантными методами, оно также, предпочтительно, по существу не содержит культуральной среды, то есть культуральная среда составляет менее примерно 20%, 10% или 5% от объема белкового препарата. Когда антитело получают методом химического синтеза, оно, предпочтительно, по существу не содержит химических прекурсоров или других химических веществ, то есть оно отделено от химических прекурсоров или других химических веществ, принимающих участие в синтезе белка. Соответственно, такие препараты антитела содержат менее примерно 30%, 20%, 10%, 5% (по сухой массе) химических прекурсоров или соединений, отличных от представляющего интерес антитела. В предпочтительном варианте реализации, антитела по изобретению являются выделенными или очищеными.
Термины «нумерация по Кабату» и подобные термины являются общеизвестными в данной области техники и относятся к системе нумерации аминокислотных остатков, являющихся более вариабельными (т.е. гипервариабельными), чем другие аминокислотные остатки в вариабельных областях тяжелой цепи антитела, или его антигенсвязывающей части (Kabat et al., (1971) Ann. NY Acad. Sci., 190: 382-391 и, Kabat et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242). Для вариабельной области тяжелой цепи, гипервариабельная область обычно находится в диапазонах положений аминокислот 31-35 для CDR1, положений аминокислот 50-65 для CDR2 и положений аминокислот 95-102 для CDR3.
«Метка» или «меченый», в используемом в данном документе значении, относится к добавлению к полипептиду детектируемого фрагмента, например, радиоактивной метки, флуоресцентной метки, ферментативной метки, хемилюминесцентной метки или биотинильной группы или золота. Радиоизотопы или радионуклиды могут включать 3Н, 14С, 15N, 35S, 90Y, 99Тс, 115In, 125I, 131I, флуоресцентные метки могут включать родамин, лантаноидные люминофоры или FITC, и ферментативные метки могут включать пероксидазу хрена, β-галактозидазу, люциферазу, щелочную фосфатазу. Дополнительные метки включают, в качестве иллюстрации и без ограничений: ферменты, такие как глюкозо-6-фосфатдегидрогеназа («G6PDH»), альфа-D-галактозидаза, глюкозооксидаза, глюкоамилаза, карбоангидраза, ацетилхолинэстераза, лизоцим, малатдегидрогеназа и пероксидаза; красители (например, цианиновые красители, например, Cy5™, Cy5.5™ или Cy7™); дополнительные флуоресцентные метки или флуоресцирующие агенты включают флуоресцеин и его производные, флуорохром, GFP (GFP означает «зеленый флуоресцентный белок»), другие флуоресцентные белки (например, mCherry, mTomato), дансил, умбеллиферон, фикоэритрин, фикоцианин, аллофикоцианин, о-фтальдегид, и флуорескамин; флуорофоры, такие как криптаты лантанидов и хелаты, например, европия и т.д. (Perkin Elmer и Cisbio Assays); хемилюминесцентные метки или хемилюминесцентные агенты, такие как изолюминол, люминол и диоксетаны; сенсибилизаторы; коферменты; ферментные субстраты; частицы, такие как латексные или углеродные частицы; металлический золь; кристаллиты; липосомы; клетки и т.д., которые могут быть дополнительно мечены красителем, катализатором или другой детектируемой группой; такие молекулы, как биотин, дигоксигенин или 5-бромдезоксиуридин; фрагменты токсинов, такие как, например, фрагмент токсина, выбранный из группы экзотоксина Pseudomonas (РЕ или его цитотоксический фрагмент или мутант), дифтерийный токсин или его цитотоксический фрагмент или мутант, ботулинический токсин А, В, С, D, Е или F, рицин или его цитотоксический фрагмент, например, рицин А, абрин или его цитотоксический фрагмент, сапорин или его цитотоксический фрагмент, противовирусный токсин фитолакки или его цитотоксический фрагмент и бриодин 1 или его цитотоксический фрагмент.
Термин «легкая цепь» при использовании по отношению к антителу относится к легким цепям иммуноглобулина, два типа которых встречаются у млекопитающих - лямбда (λ) и каппа (κ). Предпочтительно, легкая цепь представляет собой легкую цепь человека. Предпочтительно, константная область легкой цепи является константной областью человека. В человеческой популяции существуют множественные аллели константной области легкой цепи. Нуклеотидные и аминокислотные последовательности этих аллельных вариантов представлены в общедоступных базах данных, таких как IMGT, ENSEMBL, Swiss-Prot и Uniprot. В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем к константной области человека, который включает, без ограничений, IGKC*01 (SEQ ID NOs:206 и 207), IGKC*02 (SEQ ID NOs:208 и 209), IGKC*03 (SEQ ID NOs:210 и 211), IGKC*04 (SEQ ID NOs:212 и 213) и IGKC*05 (SEQ ID NOs:214 и 215). В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат белок, кодируемый аллелем А константной области человека, который включает, без ограничений, IGLC1*01 (SEQ ID NOs:216 и 217), IGLC1*02 (SEQ ID NOs:218, 219 и 220), IGLC2*01 (SEQ ID NOs:221, 222 и 538), IGLC2*02 (SEQ ID NOs:224 и 225), IGLC2*03 (SEQ ID NOs:224 и 225), IGLC3*01 (SEQ ID NOs:226 и 227), IGLC3*02 (SEQ ID NOs:228 и 229), IGLC3*03 (SEQ ID NOs:230 и 231), IGLC3*04 (SEQ ID NOs:232 и 233), IGLC6*01 (SEQ ID NOs:234 и 235), IGLC7*01 (SEQ ID NOs:236 и 237), IGLC7*02 (SEQ ID NOs:236 и 237), IGLC7*03 (SEQ ID NOs:535 и 536). В другом варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат константную область легкой цепи, кодируемую аллелем константной области к мыши, который включает, без ограничений, IGKC*01, IGKC*03 или IGKC*03. В другом варианте реализации, антитела и фрагменты антител, раскрытые в данном документе, содержат константную область легкой цепи, кодируемую аллелем константной области λ мыши, который включает, без ограничений, IGLC1*01, IGLC2*01 или IGLC3*01.
«Процент (%) идентичности аминокислотной последовательности» и «гомология», по отношению к последовательности пептида, полипептида или антитела, определяются как процент аминокислотных остатков в последовательности-кандидате, которые идентичны аминокислотным остаткам в конкретной пептидной или полипептидной последовательности после выравнивания последовательностей и введения разрывов, при необходимости, для достижения максимальной процентной идентичности последовательностей и без учета каких-либо консервативных замещений как части идентичности последовательностей. Выравнивание с целью определения процента идентичности аминокислотной последовательности может быть осуществлено различными способами, доступными специалистам в данной области, например, с использованием общедоступного компьютерного программного обеспечения, такого как прикладные программы BLAST, BLAST-2, ALIGN или MEG ALIGN™ (DNASTAR), В одном варианте реализации, % гомологии составляет примерно 70%. В одном варианте реализации, % гомологии составляет примерно 75%. В одном варианте реализации, % гомологии составляет примерно 80%. В одном варианте реализации, % гомологии составляет примерно 85%. В одном варианте реализации, % гомологии составляет примерно 90%. В одном варианте реализации, % гомологии составляет примерно 92%. В одном варианте реализации, % гомологии составляет примерно 95%. В одном варианте реализации, % гомологии составляет примерно 97%. В одном варианте реализации, % гомологии составляет примерно 98%. В одном варианте реализации, % гомологии составляет примерно 99%. В одном варианте реализации, % гомологии составляет 100%.
Термин «природный» или «нативный» при использовании в связи с биологическими материалами, такими как молекулы нуклеиновых кислот, полипептиды, клетки-хозяева и т.п., относится к материалам, существующим в природе и не подвергнутым манипуляциям со стороны человека.
В используемом в данном документе значении, термин «упаковка» относится к тому, каким образом компоненты организованы и/или удерживаются в единице, пригодной для распространения и/или использования. Упаковка может включать, например, коробки, мешки, шприцы, ампулы, флаконы, пробирки, двустворчатые упаковки типа раковины-складня, изолирующие слои (barriers) и/или контейнеры для поддержания стерильности, маркировки и т.д.
В используемом в данном документе значении, термин «фармацевтически приемлемый» означает получивший одобрение регулирующего органа федерального правительства или правительства штата или включенный в Фармакопею США, Европейскую фармакопею или другую общепризнанную фармакопею для использования у животных и, более конкретно, у людей.
В используемом в данном документе значении, термины «полинуклеотид», «нуклеотид», «нуклеиновая кислота» «молекула нуклеиновой кислоты» и другие подобные термины используются взаимозаменяемо и включают ДНК, РНК, мРНК и т.п.
Используемые здесь термины «предотвращать», «профилактический» и «профилактика» относятся к полному или частичному ингибированию развития, рецидива, начала или распространения опосредованного hPD-L1 заболевания и/или связанного с ним симптома, в результате проведения терапии или комбинации предлагаемых в данном документе терапий (например, комбинации профилактических или терапевтических средств, таких как антитело по изобретению).
Термин «растворимый» относится к полипептиду, такому как PD-L1, и его вариантам или фрагментам, не содержащим одного или нескольких трансмембранных или цитоплазматических доменов, присутствующих в нативной или мембранно-связанной форме. В одном варианте реализации, «растворимая» форма PD-L1 не содержит ни трансмембранного домена, ни цитоплазматического домена.
Термин «субъект» или «пациент» относится к любому животному, включая, без ограничений, млекопитающих. В используемом в данном документе значении, термин «млекопитающее» относится к любому позвоночному животному, которое вскармливает своих детенышей и либо рождает живых детенышей (плацентарные (eutharian or placental) млекопитающие), либо является яйцекладущим (сумчатые (metatharian) или неплацентарные млекопитающие). Примеры видов млекопитающих включают, без ограничений, людей и других приматов, включая не являющихся человеком приматов, таких как шимпанзе и другие виды человекообразных обезьян и не-человекообразных обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, овец, свиней, коз и лошадей; домашних млекопитающих животных, такие как собаки и кошки; лабораторных животных, включая грызунов, таких как мыши, крысы (включая хлопковых хомяков) и морских свинок; птиц, включая домашних, диких и охотничьих птиц, таких как куры, индейки и другие куриноподобные птицы, утки, гуси и т.п.
В используемом в данном документе значении, термин «по существу все» означает по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере, примерно 75%, по меньшей мере примерно 80%, по меньшей мере примерно 85%, по меньшей мере примерно 90%, по меньшей мере примерно 95%, по меньшей мере примерно 98%, по меньшей мере примерно 99% или примерно 100%.
В используемом в данном документе значении, термин «по существу не содержащий поверхностно-активного вещества» относится к композиции антитела, которое специфически связывается с антигеном hPD-L1, причем указанная композиция содержит менее 0,0005%, менее 0,0003% или меньше 0,0001% поверхностно-активных веществ и/или меньше 0,0005%, менее 0,0003% или меньше 0,0001% поверхностно-активных веществ.
В используемом в данном документе значении, термин «по существу не содержащий соли» относится к композиции антитела, которое специфически связывается с антигеном hPD-L1, причем указанная композиция содержит менее 0,0005%, менее 0,0003% или меньше 0,0001% неорганических солей.
В используемом в данном документе значении, термин «поверхностно-активное вещество» относится к органическим веществам, имеющим амфипатическое строение; а именно, они состоят из групп с противоположными тенденциями растворимости, как правило, маслорастворимой углеводородной цепи и водорастворимой ионной группы. Поверхностно-активные вещества можно классифицировать в зависимости от заряда поверхностно-активного фрагмента на анионные, катионные и неионные поверхностно-активные вещества. Поверхностно-активные вещества часто используются в качестве смачивающих, эмульгирующих, солюбилизирующих и диспергирующих агентов для различных фармацевтических композиций и препаратов биологических материалов.
В используемом в данном документе значении, термин «метка» относится к любому типу фрагмента, который присоединен к, например, полипептиду и/или полинуклеотиду, кодирующему hPD-L1 или антитело hPD-L1 или его антигенсвязывающий фрагмент. Например, полинуклеотид, кодирующий hPD-L1, антитело hPD-L1 или его антигенсвязывающий фрагмент, может содержать одну или несколько дополнительных кодирующих метку нуклеотидных последовательностей, которые кодируют, например, детектируемый фрагмент или фрагмент, способствующий аффинной очистке. При трансляции, метка и антитело могут представлять собой гибридный белок. Термин «детектируемый» или «детектирование» по отношению к метке относится к любой метке, которая может быть визуализирована, или к случаям, когда присутствие метки может быть определено и/или измерено иными способами (например, путем количественной оценки). Неограничивающим примером детектируемой метки является флуоресцентная метка.
В используемом в данном документе значении, термин «терапевтическое средство» относится к любому агенту, который может быть использован для лечения, ведения или улучшения опосредованного hPD-L1 заболевания и/или связанного с ним симптома. В некоторых вариантах реализации, термин «терапевтическое средство» относится к антителу по изобретению. В некоторых других вариантах реализации, термин «терапевтическое средство» относится к агенту, отличному от антитела по изобретению. Предпочтительно, терапевтическое средство является агентом, который, как известно, является полезным, или использовался, или в настоящее время используется для лечения, ведения или улучшения опосредованного hPD-L1 заболевания или одного или нескольких связанных с ним симптомов. В конкретных вариантах реализации, терапевтическое средство представляет собой полностью человеческое антитело против hPD-L1, такое как полностью человеческое анти-hPD-L1 моноклональное антитело.
В используемом в данном документе значении, термин «терапия» относится к любому протоколу, способу и/или агенту, которые могут использоваться для профилактики, ведения, лечения и/или улучшения опосредованного hPD-L1 заболевания (например, рака). В некоторых вариантах реализации, термины «терапии» и «терапия» относятся к биологической терапии, поддерживающей терапии и/или другим методам лечения, полезным для профилактики, ведения, лечения и/или улучшения опосредованного hPD-L1 заболевания, известным квалифицированным специалистам в данной области, таким как медицинский персонал.
Термины «лечить», «лечение» и «проведение лечения» относятся к ослаблению или улучшению прогрессирования, тяжести и/или продолжительности опосредованного hPD-L1 заболевания (например, рака), возникающим в результате проведения одной или нескольких терапий (включая, без ограничений, введение одного или нескольких профилактических или терапевтических средств, таких как антитело по изобретению). В конкретных вариантах реализации, такие термины относятся к снижению или ингибированию связывания hPD-L1 с PD-1, снижению или ингибированию связывания hPD-L1-CD80 и/или ингибированию или снижению одного или нескольких симптомов, связанных с опосредованным hPD-L1 заболеванием, таким как рак. В конкретных вариантах реализации, такие термины относятся к снижению или ингибированию связывания hPD-L1 с PD-1 и/или CD80, и/или ингибированию или ослаблению одного или нескольких симптомов, связанных с опосредованным hPD-L1 заболеванием, таких как рак. В примере, клетка представляет собой человеческую клетку. В конкретных вариантах реализации, профилактический агент представляет собой полностью человеческое антитело против hPD-L1, такое как полностью человеческое анти-hPD-L1 моноклональное антитело.
Термин «вариабельная область» или «вариабельный домен» относится к части легкой и тяжелой цепей, обычно к примерно 120-130 аминоконцевым аминокислотам тяжелой цепи и примерно от 100 до 110 аминокислотам легкой цепи, последовательности которых сильно различаются в разных антителах, и которые участвуют (are used) в связывании и специфичности каждого конкретного антитела с его конкретным антигеном. Изменчивость последовательностей сосредоточена в областях, которые называются гипервариабельными участками (участками, определяющими комплементарность (CDR)), в то время как более высококонсервативные области вариабельного домена называются каркасными областями (FR). CDR PD-L1 и тяжелые цепи несут основную ответственность за взаимодействие антитела с антигеном. Нумерация положений аминокислот, используемая в данном документе, соответствует индексу EU, как описано у Kabat et al. (1991) Sequences of proteins of immunological interest. (U.S. Department of Health and Human Services, Washington, D.C.) 5th ed. ("Kabat et al."). В предпочтительных вариантах реализации, вариабельная область представляет собой вариабельную область человека.
Определения общих терминов клеточной биологии и молекулярной биологии можно найти в "The Merck Manual of Diagnosis and Therapy", 19th Edition, опубликовано Merck Research Laboratories, 2006 (ISBN 0-911910-19-0); Robert S. Porter et al. (eds.), The Encyclopedia of Molecular Biology, опубликовано Blackwell Science Ltd., 1994 (ISBN 0-632-02182-9); Benjamin Lewin, Genes X, опубликовано Jones & Bartlett Publishing, 2009 (ISBN-10: 0763766321); Kendrew et al. (Eds.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, опубликовано VCH Publishers, Inc., 1995 (ISBN 1-56081-569-8) и Current Protocols in Protein Sciences 2009, Wiley Intersciences, Coligan et al., eds.
Если не указано иное, настоящее изобретение было выполнено с использованием стандартных процедур, как описано, например, в Sambrook et al., Molecular Cloning: A Laboratory Manual (4 ed.), Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., USA (2012); Davis et al., Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (1995); или Methods in Enzymology: Guide to Molecular Cloning Techniques Vol. 152, S.L. Berger and A.P. Kimmel Eds., Academic Press Inc., San Diego, USA (1987); Current Protocols in Protein Science (CPPS) (John E. Coligan, et al., ed., John Wiley and Sons, Inc.), Current Protocols in Cell Biology (CPCB) (Juan S. Bonifacino et al. ed., John Wiley and Sons, Inc.), и Culture of Animal Cells: A Manual of Basic Technique by R. Ian Freshney, Publisher: Wiley-Liss; 5th edition (2005), Animal Cell Culture Methods (Methods in Cell Biology, Vol. 57, Jennie P. Mather and David Barnes editors, Academic Press, 1st edition, 1998), которые все включены в данный документ посредством ссылок в полном объеме.
Определения других терминов приведены в данном документе в описании различных аспектов изобретения.
2. Антитела PD-L1
Многие опухолевые клетки экспрессируют поверхностные молекулы, являющиеся специфическими для рака, которые могут служить диагностическими и/или терапевтическими мишенями для антител. Примеры белков клеточной поверхности, экспрессируемых опухолями, представляющих собой молекулы, которые могут быть полезны в качестве биомаркеров, включают, например, члены семейства В7 белков, молекулы главного комплекса гистосовместимости (МНС), рецепторы цитокинов и факторов роста, такие как рецептор эпидермального фактора роста (EGFR). Семейство В7 представляет собой группу белков, являющихся членами иммуноглобулинового суперсемейства (Ig) белков клеточной поверхности, которые связываются с рецепторами на лимфоцитах для регулирования иммунных реакций. Это семейство включает трансмембранные или гликозилфосфатидилинозит(GPI)-связанные белки, характеризующиеся внеклеточными Ig-подобными доменами (IgV и IgC-домены, родственные с вариабельными и константными доменами иммуноглобулинов). Все члены имеют короткие цитоплазматические домены. Существует семь известных членов семейства В7: В7-1, В7-2, PD-L1 (В7-Н1), PD-L2, В7-Н2, В7-Н3 и В7-Н4.
Полная аминокислотная последовательность PD-L1 представлена NCBI Reference Sequence: NP_054862.1 (SEQ ID NO: 1), которая имеет ссылки (refers to) на многие журнальные статьи, включая, например, Dong, Н., et al. (1999), "PD-L1, а third member of the B7 family, co-stimulates T-cell proliferation and interleukin-10 secretion," Nat. Med. 5 (12), 1365-1369, описание которой включено в данный документ посредством ссылки в полном объеме. Аминокислотная последовательность PD-L1 включает цитоплазматический домен длиной 30 аминокислот, являющийся уникальным для PD-L1, который демонстрирует незначительную гомологию с другими молекулами, включая другие члены семейства В7.
В одном варианте реализации, антитело представляет собой поликлональное антитело. Способы получения поликлональных антител известны и включают, например, инокуляцию пригодного млекопитающего антигеном для индуцирования иммунной системы животного с целью получения иммуноглобулинов (IgG), специфически связывающих введенный антиген. Примеры пригодных млекопитающих включают, например, мышь, морскую свинку, хомяка, крысу, кролика, овцу или козу. Поликлональный IgG затем обычно очищают от сыворотки млекопитающего. В одном варианте реализации, антитело представляет собой поликлональное антитело, которое связывается с поверхностно экспрессированным белком. В другом варианте реализации, антитело представляет собой поликлональное антитело, которое специфически связывается с членом семейства В7 белков. В более конкретном варианте реализации, антитело представляет собой поликлональное антитело, которое специфически связывает PD-L1. В другом варианте реализации, антитело представляет собой поликлональное антитело, которое специфически связывает поверхностно экспрессированный PD-L1. В более конкретном варианте реализации, поликлональное антитело или его антигенсвязывающий фрагмент специфически связывают PD-L1 человека. В другом варианте реализации, антитело представляет собой поликлональное антитело, которое специфически связывает растворимый PD-L1. Термин «растворимый» также относится к белку, такому как PD-L1, не имеющему одного или нескольких из трансмембранного домена или цитоплазматических доменов. В одном варианте реализации, «растворимая» форма PD-L1 не содержит ни трансмембранного домена, ни цитоплазматического домена. В одном варианте реализации, антитело представляет собой поликлональное антитело, которое связывает «свободный» PD-L1 (т.е. PD-L1, не связанный с клеточной мембраной или поверхностью, прямо или косвенно).
В другом варианте реализации, антитело может быть моноклональным антителом. Способы получения моноклональных антител известны и включают, например, слияние клеток миеломы с клетками животного, которое было иммунизировано желательным антигеном. В других вариантах реализации, моноклональные антитела могут быть получены с использованием технологии рекомбинантной ДНК. В одном варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывает поверхностно экспрессируемый белок. В одном варианте реализации, антитело является полностью человеческим моноклональным антителом. В другом варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывается с членом семейства В7 белков. В более конкретном варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывает PD-L1. В другом варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывается с поверхностно экспрессированным PD-L1. В более конкретном варианте реализации, моноклональное антитело или его антигенсвязывающий фрагмент специфически связывают PD-L1 человека. В другом варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывает растворимый PD-L1. В одном варианте реализации, антитело представляет собой моноклональное антитело, специфически связывающее растворимый PD-L1, в котором отсутствует один или несколько из трансмембранного домена или цитоплазматических доменов. В одном варианте реализации, антитело представляет собой моноклональное антитело, которое специфически связывает растворимый PD-L1, не имеющий ни трансмембранного домена, ни цитоплазматического домена. В одном варианте реализации, антитело представляет собой моноклональное антитело, связывающее «свободный» PD-L1 (т.е. PD-L1, который не связан с клеточной мембраной или поверхностью, прямо или косвенно).
В примере, сайт (сайты) связывания антитела или фрагмента выбирают из множества (например, библиотеки) сайтов связывания. Например, множество сайтов связывания содержит или состоит из множества 4-цепочечных антител или их фрагментов, например, dAb, Fab или scFv. Пригодные способы получения множеств сайтов связывания для скрининга включают фаговый дисплей (получение библиотеки фагового дисплея сайтов связывания антител), рибосомный дисплей (создание библиотеки рибосомного дисплея сайтов связывания антител), дрожжевой дисплей (создание библиотеки дрожжевого дисплея сайтов связывания антител), или иммунизацию неявляющегося человеком позвоночного животного (например, грызуна, например, мыши или крысы, например, Velocimouse™, Kymouse™, Xenomouse™, Aliva Mouse™, HuMAb Mouse™, Omnimouse™, Omnirat™ или Memo Mouse™) hPD-L1 или эпитопом hPD-L1 и выделение репертуара антителопродуцирующих клеток (например, репертуара В-клеток, плазматических клеток или плазмобластов) и/или репертуара выделенных антител, фрагментов или сайтов связывания.
Связывающая способность, специфичность и аффинность PD-L1 (Kd, Koff и/или Kon) могут быть определены любым обычным способом в данной области техники, например, методом поверхностного плазмонного резонанса (SPR). В используемом в данном документе значении, термин «Kd» или «KD» предназначен для обозначения равновесной константы диссоциации конкретного взаимодействия антитело-антиген. Такие измерения связывания могут быть проведены с использованием различных анализов связывания, известных в данной области, например, с использованием метода поверхностного плазмонного резонанса (SPR), такого как Biacore™, или с использованием ProteOn XPR36™ (Bio-Rad®), с использованием KinExA® (Sapidyne Instruments, Inc), или с использованием ForteBio Octet (Pall ForteBio Corp.).
В одном варианте реализации, поверхностный плазмонный резонанс (SPR) проводят при 25°С. В другом варианте реализации, SPR проводят при 37°С.
В одном варианте реализации, SPR проводят при физиологическом pH, таком как pH 7 или pH 7,6 (например, с использованием забуференного Hepes физиологического раствора при pH 7,6 (также называемого HBS-EP)).
В одном варианте реализации, SPR проводят при физиологическом уровне содержания соли, например 150 мМ NaCl.
В одном варианте реализации, SPR проводят при уровне содержания детергента не более 0,05% об., например, в присутствии Р20 (полисорбат 20, например, Tween 20™), в количестве 0,05%, и 3 мМ ЭДТА.
В одном примере, SPR проводят при 25°С или 37°С в буфере при pH 7,6, 150 мМ NaCl, 0,05% детергента (например, Р20) и 3 мМ ЭДТА. Буфер может содержать 10 мМ Hepes. В одном примере, SPR проводят при 25°С или 37°С в HBS-EP. HBS-EP поставляется фирмой Teknova Inc. (California, номер по каталогу Н8022).
В примере, аффинность антитела или фрагмента определяют методом SPR путем:
1. Связывания анти-мышиного (или другого соответствующего человеческого, крысиного или принадлежащего не являющемуся человеком позвоночному животному, подобранного с учетом видового соответствия константной области антитела) IgG (например, Biacore™ BR-1008-38) с биосенсорным чипом (например, чипом GLM), например, с помощью первичной аминной связи;
2. Воздействия на анти-мышиный IgG (или другое антитело, подобранное с учетом видового соответствия) тестируемым IgG-антителом для связывания тестируемого антитела на чипе;
3. Пропускания тест-антигена по поверхности связывания чипа при концентрации 1024 нМ, 256 нМ, 64 нМ, 16 нМ, 4 нМ и 0 нМ (т.е. только буфер); и
4. И определения аффинности связывания тестируемого антитела с тест-антигеном с использованием метода поверхностного плазмонного резонанса, например, в условиях SPR, описанных выше (например, при 25°С в физиологическом буфере). SPR может выполняться с использованием любого стандартного аппарата SPR, такого как Biacore™, или с использованием ProteOn XPR36™ (Bio-Rad®).
Регенерацию поверхности связывания можно проводить с помощью 10 мМ глицина при pH 1,7. Такая обработка удаляет связанное антитело и позволяет использовать поверхность для другого взаимодействия. Данные связывания могут быть аппроксимированы моделью 1:1, обычно используемой в стандартных методах, например, путем использования модели, заложенной в прикладной программе анализа ProteOn XPR36™.
Авторы настоящего изобретения идентифицировали ряд антител, обладающих специфичностью по отношению к hPD-L1, которые обладают рядом потенциальных возможностей и преимуществ по сравнению с существующими антителами. Например, раскрытые в данном документе антитела могут обладать одним или несколькими из следующих свойств:
a. Специфичность к блокированию только одним из лигандов PD-L1 (например, блокирует взаимодействие CD80/PD-L1, но не взаимодействие PD-1/PD-L1)
b. Иммуногенность/отсутствие побочных эффектов
c. Растворимость
d. Стабильность
e. Простота составления композиции
f. Частота дозирования и/или путь введения, например, из-за улучшенного периода полувыведения по сравнению с существующими антителами против PDL1
g. Технологичность (например, экспрессия, простота очистки, изоформы)
1D05 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 33, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 34. 1D05 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 43, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 35 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 36). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
84G09 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 13, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 7 (IMGT) или SEQ ID NO: 10 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 8 (IMGT) или SEQ ID NO: 11 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 9 (IMGT) или SEQ ID NO: 12 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 14. 84G09 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 23, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 17 (IMGT) или SEQ ID NO: 20 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 18 (IMGT) или SEQ ID NO: 21 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 19 (IMGT) или SEQ ID NO: 22 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 24. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 15 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 16). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 25 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 26).
Мутант 1 1D05 НС имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 47, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Мутант 1 1D05 НС имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 43, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
Мутант 2 1D05 НС имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 48, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Мутант 2 1D05 НС имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 43, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
Мутант 3 1D05 НС имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 49, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Мутант 3 1D05 НС имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 43, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
Мутант 4 1D05 НС имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 342, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Мутант 4 1D05 НС имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 43, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
Мутант 1 1D05 LC имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 33, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 34. Мутант 1 1D05 LC имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 50, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность CDRL2 мутанта 1 1D05 LC определяется по системам Кабата или IMGT по последовательности VL, представленной SEQ ID NO: 50. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 35 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 36).
Мутант 2 1D05 LC имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 33, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 34. Мутант 2 1D05 LC имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 51, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 38 (IMGT) или SEQ ID NO: 41 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 35 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 36).
Мутант 3 1D05 LC имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 33, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 27 (IMGT) или SEQ ID NO: 30 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 28 (IMGT) или SEQ ID NO: 31 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 29 (IMGT) или SEQ ID NO: 32 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 34. Мутант 3 1D05 LC имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 298, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 37 (IMGT) или SEQ ID NO: 40 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 39 (IMGT) или SEQ ID NO: 42 (Кабат). Последовательность CDRL2 мутанта 3 1D05 LC определяется по системам Кабата или IMGT по последовательности VL, представленной SEQ ID NO: 298. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 44. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 35 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 36). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 45 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 46).
411В08 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 58, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 52 (IMGT) или SEQ ID NO: 55 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 53 (IMGT) или SEQ ID NO: 56 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 54 (IMGT) или SEQ ID NO: 57 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 59. 411В08 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 68, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 62 (IMGT) или SEQ ID NO: 65 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 63 (IMGT) или SEQ ID NO: 66 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 64 (IMGT) или SEQ ID NO: 67 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 69. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 60 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 61). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 70 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 71).
411С04 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 78, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 72 (IMGT) или SEQ ID NO: 75 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 73 (IMGT) или SEQ ID NO: 76 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 74 (IMGT) или SEQ ID NO: 77 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 79. 411С04 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 88, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 82 (IMGT) или SEQ ID NO: 85 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 83 (IMGT) или SEQ ID NO: 86 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 84 (IMGT) или SEQ ID NO: 87 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 89. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 80 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 81). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 90 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 91).
411D07 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 98, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 92 (IMGT) или SEQ ID NO: 95 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 93 (IMGT) или SEQ ID NO: 96 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 94 (IMGT) или SEQ ID NO: 97 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 99. 411D07 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 108, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 102 (IMGT) или SEQ ID NO: 105 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 103 (IMGT) или SEQ ID NO: 106 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 104 (IMGT) или SEQ ID NO: 107 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 109. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 100 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 101). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 110 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 111).
385F01 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 118, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 112 (IMGT) или SEQ ID NO: 115 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 113 (IMGT) или SEQ ID NO: 116 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 114 (IMGT) или SEQ ID NO: 117 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 119. 385F01 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 128, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 122 (IMGT) или SEQ ID NO: 125 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 123 (IMGT) или SEQ ID NO: 126 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 124 (IMGT) или SEQ ID NO: 127 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 129. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 120 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 121). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 130 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 131).
386Н03 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 158, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 152 (IMGT) или SEQ ID NO: 155 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 153 (IMGT) или SEQ ID NO: 156 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 154 (IMGT) или SEQ ID NO: 157 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 159. 386Н03 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 168, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 162 (IMGT) или SEQ ID NO: 165 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 163 (IMGT) или SEQ ID NO: 166 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 164 (IMGT) или SEQ ID NO: 167 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 169. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 160 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 161). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 170 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 171).
389А03 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 178, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 172 (IMGT) или SEQ ID NO: 175 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 173 (IMGT) или SEQ ID NO: 176 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 174 (IMGT) или SEQ ID NO: 177 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 179. 389А03 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 188, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 182 (IMGT) или SEQ ID NO: 185 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 183 (IMGT) или SEQ ID NO: 186 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 184 (IMGT) или SEQ ID NO: 187 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 189. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 180 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 181). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 190 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 191).
413D08 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 138, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 132 (IMGT) или SEQ ID NO: 135 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 133 (IMGT) или SEQ ID NO: 136 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 134 (IMGT) или SEQ ID NO: 137 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 139. 413D08 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 148, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 142 (IMGT) или SEQ ID NO: 145 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 143 (IMGT) или SEQ ID NO: 146 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 144 (IMGT) или SEQ ID NO: 147 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 149. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 140 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 141). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 150 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 151).
413G05 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 244, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 238 (IMGT) или SEQ ID NO: 241 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 239 (IMGT) или SEQ ID NO: 242 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 240 (IMGT) или SEQ ID NO: 243 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 245. 413G05 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 254, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 248 (IMGT) или SEQ ID NO: 251 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 249 (IMGT) или SEQ ID NO: 252 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 250 (IMGT) или SEQ ID NO: 253 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 255. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 246 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 247). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 256 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 257).
413F09 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 264, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 258 (IMGT) или SEQ ID NO: 261 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 259 (IMGT) или SEQ ID NO: 262 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 260 (IMGT) или SEQ ID NO: 263 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 265. 413F09 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 274, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 268 (IMGT) или SEQ ID NO: 271 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 269 (IMGT) или SEQ ID NO: 272 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 270 (IMGT) или SEQ ID NO: 273 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 275. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 266 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 267). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 276 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 277).
414В06 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 284, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 278 (IMGT) или SEQ ID NO: 281 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 279 (IMGT) или SEQ ID NO: 282 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 280 (IMGT) или SEQ ID NO: 283 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 285. 414В06 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 294, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 288 (IMGT) или SEQ ID NO: 291 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 289 (IMGT) или SEQ ID NO: 292 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 290 (IMGT) или SEQ ID NO: 293 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 295. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 286 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 287). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 296 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 297).
416Е01 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 349, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 343 (IMGT) или SEQ ID NO: 346 (Кабат), аминокислотную последовательность CDRH2, представленную SEQ ID NO: 344 (IMGT) или SEQ ID NO: 347 (Кабат), и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 345 (IMGT) или SEQ ID NO: 348 (Кабат). Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 350. 416Е01 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 359, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 353 (IMGT) или SEQ ID NO: 356 (Кабат), аминокислотную последовательность CDRL2, представленную SEQ ID NO: 354 (IMGT) или SEQ ID NO: 357 (Кабат), и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 355 (IMGT) или SEQ ID NO: 358 (Кабат). Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 360. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 351 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 352). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 361 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 362).
Антитела по изобретению описаны в отношении следующих концепций, аспектов, предложений, компоновок и вариантов реализации. Если не указано иное, все понятия, варианты реализации, предложения, аранжировки и аспекты должны рассматриваться как способные сочетаться с любыми другими концепциями, аспектами, предложениями, компоновками или вариантами реализации, за исключением случаев, когда такая комбинация не будет иметь технического смысла, или когда явным образом будет указано иное.
Концепция 1. Антитело или его фрагмент, которые специфически связываются с hPD-L1, представленным SEQ ID NO: 1, и конкурируют за связывание с указанным hPD-L1 с антителом 1D05, причем антитело или фрагмент содержат домен VH, который содержит CDRH3, содержащий мотив X1GSGX2YGX3X4FD, где X1, Х2 и Х3 независимо обозначают любую аминокислоту, а Х4 присутствует или отсутствует, и, в случае его присутствия, может обозначать любую аминокислоту.
В этих концепциях антитела или фрагменты могут включать или не включать биспецифические антитела. В одном варианте реализации, в этих концепциях, антитела или фрагменты включают биспецифические антитела. В одном варианте реализации, биспецифическое антитело не включает формат FIT-Ig. В одном варианте реализации, биспецифическое антитело не включает формат mAb2. В одном варианте реализации, биспецифическое антитело не включает ни формат FIT-Ig, ни формат mAb2. В одном варианте реализации, антитело или фрагмент, в этих концепциях, включают биспецифическое антитело, но не включают биспецифическое антитело, имеющее формат FIT-Ig. В одном варианте реализации, антитело или фрагмент, в этих концепциях, включают биспецифическое антитело, но не включают биспецифическое антитело, имеющее формат mAb2. В одном варианте реализации, антитело или фрагмент, в этих концепциях, включают биспецифическое антитело, но не включают биспецифическое антитело, имеющее формат FIT-Ig или формат mAb2. В другом варианте реализации, в этих концепциях, антитела или фрагменты включают антитела с двойным связыванием.
Предпочтительно, антитело или его фрагмент, которые специфически связываются с антигеном hPD-L1, не реагируют перекрестно с другими антигенами (но могут, необязательно, перекрестно реагировать с PD-L1 другого вида, например, макака-резуса, яванского макака или мыши). Антитело или его фрагмент, которые специфически связываются с антигеном hPD-L1, можно идентифицировать, например, с помощью иммуноанализов, BIAcore™ или других методов, известных специалистам в данной области. Антитело или его фрагмент специфически связываются с антигеном hPD-L1, когда они связываются с антигеном hPD-L1 с более высокой аффинностью, чем с любым перекрестно-реактивным антигеном, при определении с использованием экспериментальных методов, таких как радиоиммуноанализ (RIA) и твердофазные иммуноферментные анализы (ИФА). Как правило, специфическая или селективная реакция будет по меньшей мере вдвое превышать фоновый сигнал или шум, и наиболее характерно, более чем в 10 раз превышать фон. См., например, Paul, ed., 1989, Fundamental Immunology Second Edition, Raven Press, New York, где на стр. 332-336 приведено обсуждение специфичности антител.
В одном варианте реализации, антитело или фрагмент представляют собой человеческое антитело. В одном варианте реализации, антитело или фрагмент представляют собой человеческое антитело или фрагмент. В одном варианте реализации, антитело или фрагмент представляют собой полностью человеческое антитело или фрагмент. В одном варианте реализации, антитело или фрагмент представляют собой полностью человеческое моноклональное антитело или фрагмент.
Также предлагается концепция 1а: антитело или его фрагмент, которые специфически связываются с hPD-L1, представленным SEQ ID NO: 1, и конкурируют за связывание с указанным hPD-L1 с антителом 411В08, где антитело или фрагмент содержат домен VH, который содержит CDRH3, содержащий мотив ARX1RX2X3SDX4X5D, где Х1, Х2, Х3, Х4 и Х5 независимо обозначают любую аминокислоту.
Также предлагается концепция 1b: антитело или его фрагмент, которые специфически связываются с hPD-L1, представленным SEQ ID NO: 1, и конкурируют за связывание с указанным hPD-L1 с антителом 411В08, где антитело или фрагмент содержат домен VH, который содержит CDRH3, содержащий мотив X1RDGSGSY, где X1 обозначает любую аминокислоту.
Как предусмотрено в концепциях или аспектах настоящего изобретения, анти-PD-L1 антитело или иммуноцитокин могут связываться с PD-L1, например, PD-L1 человека, со значением KD менее 50 нМ, менее 40 нМ, менее 30 нМ, по результатам определения методом поверхностного плазмонного резонанса. В другом варианте реализации, анти-PD-L1 антитело или иммуноцитокин могут связываться с PD-L1, например, PD-L1 человека, с KD менее 20 нМ, менее 15 нМ, менее 10 нМ, по результатам определения методом поверхностного плазмонного резонанса. Анти-PD-L1 антитело или иммуноцитокин могут связываться с PD-L1, например, PD-L1 человека, с KD менее 8 нМ, менее 5 нМ, менее 4 нМ, менее 3 нМ, менее 2 нМ или меньше 1 нМ, по результатам определения методом поверхностного плазмонного резонанса. KD может иметь значение 0,9 нМ или меньше, 0,8 нМ или меньше, 0,7 нМ или меньше, 0,6 нМ или меньше, 0,5 нМ или меньше, 0,4 нМ или меньше, 0,3 нМ или меньше, 0,2 нМ или меньше, или 0,1 нМ или меньше.
В другом варианте реализации, KD находится в диапазоне от 0,01 до 1 нМ, или от 0,05 до 2 нМ, или от 0,05 до 1 нМ. KD может определяться для hPD-L1, cynoPD-L1 (PD-L1 яванского макака) и/или мышиного PD-L1.
В другом варианте реализации, антитела против PD-L1, раскрытые в данном документе, имеют константу скорости ассоциации KON (например, по результатам измерений методом SPR, например, при 25°С или при 37°С) приблизительно от 0,5 до 10 мкМ, например, приблизительно от 1 до 8 мкМ или приблизительно от 1 до 7 мкМ. В другом варианте реализации, константа скорости ассоциации KON составляет приблизительно от 1 до 5 мкМ, например, приблизительно 1 мкМ, приблизительно 1,5 мкМ, приблизительно 2 мкМ, приблизительно 2,5 мкМ или приблизительно 3 мкМ. В другом варианте реализации, скорость KON составляет приблизительно 3,5 мкМ, приблизительно 4 мкМ, приблизительно 4,5 мкМ, приблизительно 5 мкМ или приблизительно 5,5 мкМ.
В другом варианте реализации, антитела против PD-L1, раскрытые в данном документе, имеют константу скорости диссоциации KOFF (например, по результатам измерений методом SPR, например, при 25°С или при 37°С), приблизительно от 0,01 до 100 мМ, например, приблизительно от 0,1 до 50 мМ, или приблизительно от 0,5 до 50 мМ. В другом варианте константа скорости диссоциации KOFF составляет приблизительно от 0,5 до 10 мМ, или приблизительно от 0,5 до 10 мМ, например, приблизительно 1 мМ, приблизительно 2 мМ, приблизительно 3 мМ, приблизительно 4 мМ или приблизительно 5 мМ. В другом варианте константа скорости диссоциации KOFF составляет приблизительно 0,6 мМ, приблизительно 0,7 мМ, приблизительно 0,8 мМ или приблизительно 0,9 мМ.
В другом варианте реализации, антитела против PD-L1 (и иммуноцитокины), описанные в концепциях и аспектах настоящего изобретения, обеспечивают улучшенные уровни транзиентной экспрессии по сравнению с другими анти-PD-L1-антителами и иммуноцитокинами. Таким образом, в одном варианте реализации, анти-PD-L1 антитело (или иммуноцитокин) экспрессируется в клетке HEK293, например, клетке HEK293T, с уровнем экспрессии приблизительно 100 мкг/мл или в диапазоне приблизительно от 100 до 350 мкг/мл. В другом варианте реализации, уровень экспрессии имеет значение выше приблизительно 350 мкг/мл.
В другом варианте реализации, анти-PD-L1 антитело (или иммуноцитокин) экспрессируется в клетке СНО, например, клетке Expi-CHO, с уровнем экспрессии приблизительно 100 мкг/мл, или в диапазоне значений приблизительно от 100 до 350 мкг/мл. В другом варианте реализации, уровень экспрессии имеет значение выше приблизительно 350 мкг/мл.
В другом варианте реализации, анти-PD-L1 антитело (или иммуноцитокин) экспрессируется в клетке СНО, например, клетке Expi-CHO или клетке СНО-Е7 EBNA, с уровнем экспрессии приблизительно 100 мкг/мл или в диапазоне значений приблизительно от 100 до 350 мкг/мл. В другом варианте реализации, уровень экспрессии имеет значение выше приблизительно 350 мкг/мл. Антитело, описанное в данном документе как 1D05, в формате человеческого IgG1 (SEQ ID NO: 340, в объеме 2 л, в клетках СНО-Е7 EBNA, имеет уровень экспрессии приблизительно 115 мкг/мл. Антитело, описанное в данном документе как 416Е01, в формате человеческого IgG1 (SEQ ID NO: 340), в объеме 2 л, в клетках СНО-Е7 EBNA, имеет уровень экспрессии приблизительно 160 мкг/мл. Антитело, описанное в данном документе как 1414В06, в формате человеческого IgG1 (SEQ ID NO: 340), в объеме 2 л, в клетках СНО-Е7 EBNA, имеет уровень экспрессии приблизительно 783 мкг/мл. Антитело, описанное в данном документе как 413G05, в формате человеческого IgG1 (SEQ ID NO: 340), в объеме 2 л, в клетках СНО-Е7 EBNA, имеет уровень экспрессии приблизительно 383 мкг/мл.
В любой из этих систем экспрессии, экспрессия проводится в масштабе от приблизительно 0,5 мл до 3 мл, например, приблизительно от 0,5 мл до 2 мл. В любой из этих систем экспрессии, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться из вектора рТТ5. В любой из этих систем экспрессии, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться в сочетании с липидным трансфекционным реагентом и может, необязательно, экспрессироваться в клетке СНО, например, в клетке Expi-CHO. В любой из этих систем экспрессии, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться в сочетании с полиэтилениминовым (PEI) трансфекционным реагентом и может, необязательно, экспрессироваться в клетке СНО, например, клетке СНО-Е7 EBNA. В любой из этих систем экспрессии, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться в сочетании с хелперной плазмидой (например, AKT-хелперной плазмидой) и может, необязательно, экспрессироваться в клетке СНО, например, в клетке СНО-Е7 EBNA.
В любой из этих систем экспрессии, уровень экспрессии составляет от приблизительно от 100 мкг/мл до приблизительно 1500 мкг/мл, например, от приблизительно 100 мкг/мл до приблизительно 1000 мкг/мл, или от приблизительно 200 мкг/мл до приблизительно 1000 мкг/мл, или от приблизительно 350 мкг/мл до приблизительно 1000 мкг/мл. В любой из этих систем экспрессии, нижний предел экспрессии может составлять приблизительно 100 мкг/мл, приблизительно 200 мкг/мл, приблизительно 300 мкг/мл, или приблизительно 400 мкг/мл. В другом варианте реализации, нижний предел экспрессии может составлять приблизительно 500 мкг/мл, приблизительно 600 мкг/мл, приблизительно 700 мкг/мл, или приблизительно 800 мкг/мл. В любой из этих систем экспрессии, верхний предел экспрессии может составлять приблизительно 2000 мкг/мл, приблизительно 1800 мкг/мл, приблизительно 1600 мкг/мл, или приблизительно 1500 мкг/мл. В другом варианте реализации, верхний предел экспрессии может составлять приблизительно 1250 мкг/мл, приблизительно 1000 мкг/мл, приблизительно 900 мкг/мл, или приблизительно 800 мкг/мл.
В другом варианте реализации, система экспрессии представляет собой систему экспрессии Lonza, например, систему Lonza X-Ceed®. В системе экспрессии Lonza, экспрессию можно проводить в масштабе от примерно 30 мл до 2 л, например, от 50 мл до 1 л, или от 1 л до (tp) 2 л. В системе экспрессии Lonza, анти-PD-L1 антитело (или иммуноцитокин) может быть выражено в сочетании с электропорацией и, необязательно, без каких-либо вспомогательных плазмид. В системе экспрессии Lonza, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться на уровне приблизительно 1 г/л или приблизительно 900 мг/л или приблизительно 800 мг/л или приблизительно 700 мг/л, В другом варианте реализации, в системе экспрессии Lonza, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться на уровне приблизительно 600 мг/л или приблизительно 500 мг/л или приблизительно 400 мг/л. В системе экспрессии Lonza, анти-PD-L1 антитело (или иммуноцитокин) может экспрессироваться на уровне от приблизительно 400 мг/л до приблизительно 2 г/л, например, от приблизительно 500 мг/л до приблизительно 1,5 г/л, или от приблизительно 500 мг/л до приблизительно 1 г/л. В другом варианте реализации, уровень экспрессии превышает 1 г/л. В другом варианте реализации, антитела против PD-L1, описанные в концепциях, обеспечивают улучшенный период полувыведения по сравнению с другими анти-PD-L1 антителами, как описано далее в Аспекте 1 ниже.
Концепция 2. Антитело или фрагмент согласно концепции 1, где X1 представляет собой гидроксилсодержащую аминокислоту, необязательно, Т.
В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или цистеин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин или треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин или метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой треонин или метионин.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из серина, цистеина, треонина и метионина.
Концепция 2а. Антитело или фрагмент согласно концепции 1а, где X1 представляет собой алифатическую аминокислоту или амидную аминокислоту.
В одном варианте реализации, X1 выбирают из аспарагина (N) и валина (V). В одном варианте реализации, X1 представляет собой валин. В одном варианте реализации, X1 представляет собой аспарагин.
Концепция 2b. Антитело или фрагмент согласно концепции 1b, где X1 представляет собой алифатическую аминокислоту.
В одном варианте реализации, X1 выбирают из аланина (А) или валина (V). В одном варианте реализации, X1 представляет собой валин. В одном варианте реализации, X1 представляет собой аланин.
Концепция 3. Антитело или фрагмент согласно концепции 1 или концепции 2, где Х2 представляет собой основную аминокислоту, необязательно, K.
В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой гистидин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой лизин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой аргинин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой гистидин или лизин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой гистидин или аргинин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой лизин или аргинин.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из гистидина, лизина и аргинина.
Концепция 3а. Антитело или фрагмент согласно концепции 1а или концепции 2а, где Х2 представляет собой алифатическую аминокислоту или амидную аминокислоту.
В одном варианте реализации, Х2 выбирают из лейцина (L), изолейцина (I), валина (V), аспарагина (N) и глутамина (Q). В одном варианте реализации, Х2 выбирают из лейцина (L), изолейцина (I) и валина (V). В одном варианте реализации, Х2 выбирают из аспарагина (N) и глутамина (Q). В одном варианте реализации, Х2 выбирают из лейцина (L) и глутамина (Q). В одном варианте реализации, Х2 представляет собой лейцин (L). В одном варианте реализации, Х2 представляет собой глутамин (Q).
Концепция 4. Антитело или фрагмент согласно любой из концепций 1-3, где Х2 представляет собой гидроксилсодержащую аминокислоту, необязательно, S или Т.
В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или цистеин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой серии или метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин или треонин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой цистеин или метионин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой треонин или метионин.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из серина, цистеина, треонина и метионина.
Концепция 4а. Антитело или фрагмент согласно любой из концепций 1а, 2а или 3а, где Х3 представляет собой ароматическую аминокислоту.
В одном варианте реализации, Х3 выбирают из фенилаланина (F), тирозина (Y) и триптофана (W). В одном варианте реализации, Х3 выбирают из тирозина (Y) и триптофана (W). В одном варианте реализации, Х3 представляет собой тирозин (Y). В одном варианте реализации, Х3 представляет собой триптофан (W).
Концепция 5. Антитело или фрагмент согласно любой из концепций 1-4, где Х3 представляет собой ароматическую аминокислоту, необязательно, W.
В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой фенилаланин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой тирозин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой триптофан. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой фенилаланин или тирозин. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой фенилаланин или триптофан. В одном варианте реализации, гидроксилсодержащая аминокислота представляет собой тирозин или триптофан.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из фенилаланина, тирозина и триптофана.
Концепция 5а. Антитело или фрагмент согласно любой из концепций 1а, 2а, 3а или 4а, где X4 представляет собой ароматическую аминокислоту.
В одном варианте реализации, Х4 выбирают из фенилаланина (F), тирозина (Y) и триптофана (W). В одном варианте реализации, Х4 выбирают из тирозина (Y) и фенилаланина (F). В одном варианте реализации, Х4 представляет собой тирозин (Y). В одном варианте реализации, Х4 представляет собой фенилаланин (F).
Концепция 6. Антитело или фрагмент согласно любой из концепций 1-5, где Х4 отсутствует.
Концепция 6а. Антитело или фрагмент согласно любой из концепций 1а, 2а, 3а, 4а или 5а, где Х5 представляет собой алифатическую аминокислоту или гидроксилсодержащую аминокислоту.
В одном варианте реализации, X5 выбран из лейцина (L), изолейцина (I), валина (V), серина (S), цистеина (С) и треонина (Т). В одном варианте реализации, Х5 выбран из лейцина (L), изолейцина (I) и валина (V). В одном варианте реализации, Х5 выбирают из серина (S), цистеина (С) и треонина (Т). В одном варианте реализации, Х5 выбран из лейцина (L) и серина (S). В одном варианте реализации, Х5 представляет собой серии (S). В одном варианте реализации, Х5 представляет собой лейцин (L).
Концепция 7. Антитело или фрагмент согласно любой из концепций 1-5, где Х4 присутствует.
Концепция 8. Антитело или фрагмент согласно концепции 7, где Х4 представляет собой алифатическую аминокислоту, необязательно, G.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из глицина, аланина, валина, лейцина и изолейцина.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из глицина и аланина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из глицина и валина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из глицина и лейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из глицина и изолейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из аланина и валина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из аланина и лейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из аланина и изолейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из валина и лейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из валина и изолейцина. В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из лейцина и изолейцина.
В одном варианте реализации, гидроксилсодержащая аминокислота выбрана из трех из всех из (selected from three of each of) глицина, аланина, валина, лейцина и изолейцина. В одном варианте реализации, гидроксилсодержащая аминокислота, выбранная из четырех из каждого из глицина, аланина, валина, лейцина и изолейцина.
Концепция 9. Антитело или его фрагмент, необязательно, согласно любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 1D05, где антитело или фрагмент содержат домен VH, содержащий последовательность CDRH3, представленную SEQ ID NO: 29 или 32, или последовательность CDRH3, представленную SEQ ID NO: 29 или 32, содержащую 6 или меньше аминокислотных замещений.
Концепция 9а: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 84G09, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 9 или 12, или последовательность CDRH3, представленную SEQ ID NO: 9 или 12, содержащую 6 или меньше аминокислотных замещений.
Концепция 9b: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 411В08, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 54 или 57, или последовательность CDRH3, представленную Seq ID NO: 54 или 57, содержащую 6 или меньше аминокислотных замещений.
Концепция 9с: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 411С04, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 74 или 77, или последовательность CDRH3, представленную SEQ ID NO: 74 или 77, содержащую 6 или меньше аминокислотных замещений.
Концепция 9d: антитело или его фрагмент, необязательно, согласно любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 411D07, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 94 или 97, или последовательность CDRH3, представленную SEQ ID NO: 94 или 97, содержащую 3 или меньше аминокислотных замещений.
Концепция 9е: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 385F01, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 114 или 117, или последовательность CDRH3, представленную Seq ID NO: 114 или 117, содержащую 6 или меньше аминокислотных замещений.
Понятие 9f: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 386Н03, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 144 или 147, или последовательность CDRH3, представленную Seq ID NO: 144 или 147, содержащую 3 или меньше аминокислотных замещений.
Концепция 9g: антитело или его фрагмент, необязательно, согласно любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 389А03, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 174 или 177, или последовательность CDRH3, представленную SEQ ID NO: 174 или 177, содержащую 6 или меньше аминокислотных замещений.
Концепция 9h: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 413D08, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 134 или 137, или последовательность CDRH3, представленную SEQ ID NO: 134 или 137, содержащую 5 или меньше аминокислотных замещений.
Концепция 9i: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 413G05, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 240 или 243, или последовательность CDRH3, представленную SEQ ID NO: 240 или 243, содержащую 6 или меньше аминокислотных замещений.
Концепция 9j: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 413F09, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 260 или 263, или последовательность CDRH3, представленную Seq ID NO: 260 или 263, содержащую 6 или меньше аминокислотных замещений.
Концепция 9k: антитело или его фрагмент, необязательно, по любой из концепций 1-8, которые специфически связываются с hPD-L1 и конкурируют за связывание с указанным hPD-L1 с антителом 414В06, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 280 или 283, или последовательность CDRH3, представленную Seq ID NO: 280 или 283, содержащую 6 или меньше аминокислотных замещений.
Понятие 9l: антитело или его фрагмент, необязательно, по любой из концепций 1-8, который специфически связывается с hPD-L1 и конкурирует за связывание с указанным hPD-L1 с антителом 416Е01, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 345 или 348 или последовательность CDRH3, представленную SEQ ID NO: 345 или 348, содержащую 6 или меньше аминокислотных замещений.
Во всех концепциях 9, 9а-l, 17, 17а-l, 18, 18а-l, 19, 19а-l, 22, 22a-l, 23, 23a-l, 24 и 24a-l, в одном варианте реализации, CDR содержит одно аминокислотное замещение, которое может быть консервативным аминокислотным замещением. Во всех концепциях 9, 9a-l, 17, 17а-l, 18, 18а-l, 19, 19а-l, 22, 22a-l, 23, 23а, 24 и 24а-l, в одном варианте реализации, CDR содержит два аминокислотных замещения, которые могут быть консервативными аминокислотными замещениями. Во всех концепциях 9, 9a-l, 17, 17а-l, 18, 18а-l, 19, 19а-l, 22, 22а, 22b, 22d, 22f, 22g, 24 и 24a-l, в одном варианте реализации, CDR включает три аминокислотных замещения, которые могут быть консервативными аминокислотными замещениями. Во всех концепциях 9, 9а-с, 9е, 9g-1, 17, 17а-с, 17е, 17g-l, 19, 19а, 22, 22d, 22f, 22g, 24 и 24a-l, в одном варианте реализации, CDR содержит четыре аминокислотных замещения, которые могут быть консервативными аминокислотными замещениями. Во всех концепциях 9, 9а-с, 9е, 9g-l, 17, 17а-с, 17е, 17g-l, 22d, 22f и 22g в одном варианте реализации, CDR содержит пять аминокислотных замещений, которые могут быть консервативными аминокислотными замещениями. Во всех концепциях 9, 9а-с, 9е, 9g, 9i-l, 17, 17а-с, 17е, 17g и 17i-l, в одном варианте реализации, CDR включает шесть аминокислотных замещений, которые могут быть консервативными аминокислотными замещениями.
Аминокислотные замещения включают изменения, при которых аминокислоту заменяют на другой природный аминокислотный остаток. Такие замещения могут быть классифицированы как «консервативные», и в этом случае аминокислотный остаток, содержащийся в полипептиде, заменяется другой природной аминокислотой аналогичного характера либо по показателю полярности, функциональности или размеру боковой цепи. Такие консервативные замещения хорошо известны в данной области. Замещения, охватываемые настоящим изобретением, также могут быть «неконсервативными», в которых аминокислотный остаток, присутствующий в пептиде, замещен аминокислотой, имеющей отличные свойства, например, природной аминокислотой из другой группы (например, замещение заряженной или гидрофобной аминокислотой (amino; acid) аланином) или, альтернативно, в которых природная аминокислота замещена нетрадиционной аминокислотой.
В одном варианте реализации, консервативные аминокислотные замещения являются такими, как описано в данном документе. Например, замещением может быть замена Y на F, Т на S или K, Р на А, Е на D или Q, N на D или G, R на K, G на N или А, Т на S или K, D на N или Е, I на L или V, F на Y, S на Т или A, R на K, G на N или А, K на R, А на S, K или Р. В другом варианте реализации, консервативные аминокислотные замещения могут быть случаями замещения Y на F, Т А или S, I на L или V, W на Y, М на L, N на D, G на А, Т на А или S, D на N, I на L или V, F на Y или L, S на А или Т, и А на S, G, Т или V.
Концепция 10. Антитело или фрагмент, которые специфически связываются с HPD-L1 и содержит домен VH, содержащий CDRH3 размером от 12 до 20 аминокислот, и которые получены в результате рекомбинации VH генного сегмента человека, D генного сегмента человека и JH генного сегмента человека, где JH генным сегментом человека является IGHJ5 (например, IGHJ5*02).
В одном варианте реализации, CDRH3 составляет от 14 до 17 аминокислот, a JH генный сегмент человека представляет собой IGHJ5 (например, IGHJ5*02).
В качестве концепции 10а предлагается также антитело или фрагмент, которые специфически связываются с hPD-L1 и содержат домен VH, содержащий CDRH3 размером от 8 до 16 аминокислот, и которые получены путем рекомбинации VH генного сегмента человека, D генного сегмента человека и JH генного сегмента человека, где JH генный сегмент человека выбран из IGHJ4 (например, IGHJ4*02), IGHJ5 (например, IGHJ5*02) и IGHJ6 (например, IGHJ6*02).
В другом варианте реализации, JH генный сегмент человека представляет собой IGHJ6 (например, IGHJ6*02). В другом варианте реализации, CDRH3 содержит от 10 до 17 аминокислот, a JH сегмент человека представляет собой IGHJ6 (например, IGHJ6*02).
В другом варианте реализации, JH генный сегмент человека представляет собой IGHJ4 (например, IGHJ4*02). В другом варианте реализации, CDRH3 содержит от 7 до 17 аминокислот, a JH генный сегмент человека представляет собой IGHJ4 (например, IGHJ4*02).
Необязательно, антитело по концепции 10 или 10а имеет любые признаки концепций 1-9, включая аффинность связывания, константы скоростей ассоциации (Kon) и диссоциации (Koff), уровни экспрессии, период полувыведения и т.д.
Концепция 11. Антитело или фрагмент согласно концепции 10 или 10а, где VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-9, такой как IGHV3-9*01).
В качестве концепции 11а предусматриваются также антитело или фрагмент согласно концепции 10 или 10а, где VH генный сегмент человека выбран из IGHV3 (например, IGHV3-9, такой как IGHV3-9*01 или, например, IGHV3-7, такой как IGHV3-7*01 или, например, IGHV3-33, такой как IGHV3-33*01 или, например, IGHV3-11, такой как IGHV3-11*01 или, например, IGHV3-23, такой как IGHV3-23*04) или IGHV4 (например, IGHV4-4, такой как IGHV4-4*02 или, например, IGHV4-39, такой как IGHV4-39*01).
В одном варианте реализации, VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-7, такой как IGHV3-7*01). В одном варианте реализации, VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-33, такой как IGHV3-33*01). В одном варианте реализации, VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-11, такой как IGHV3-11*01). В одном варианте реализации, VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-23, такой как IGHV3-23*04).
В одном варианте реализации, VH генный сегмент человека представляет собой IGHV4 (например, IGHV4-4, такой как IGHV4-4*02). В одном варианте реализации, VH генный сегмент человека представляет собой IGHV4 (например, IGHV4-39, такой как IGHV4-39*01).
В качестве концепции 11b предусматриваются также антитело или фрагмент согласно концепциям 10, 10а, 11 или 11а, где D генный сегмент человека выбран из IGHD1 (например, IGHD1-20, такой как IGHD1-20*01), IGHD3 (например, IGHD3-10, такой как IGHD3-10*01), IGHD4 (например, IGHD4-11, такой как IGHD4-11*01), IGHD5 (например, IGHD5-7, такой как IGHD5-18*01) и IGHD6 (например, IGHD6-13, такой как IGHD6-13*01).
В одном варианте реализации, D генный сегмент человека представляет собой IGHD1 (например, IGHD1-20, такой как IGHD1-20*01). В одном варианте реализации, D генный сегмент человека представляет собой IGHD3 (например, IGHD3-10, такой как IGHD3-10*01). В одном варианте реализации, D генный сегмент человека представляет собой IGHD4 (например, IGHD4-11, такой как IGHD4-11*01). В одном варианте реализации, D генный сегмент человека представляет собой IGHD5 (например, IGHD5-18, такой как IGHD5-19*01). В одном варианте реализации, D генный сегмент человека представляет собой IGHD6 (например, IGHD6-13, такой как IGHD6-13*01).
В любой из концепций 10, 11 и 11а VH, DH и JH генные сегменты являются такими, как описано в комбинациях антител в таблице 5 ниже. В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-7, такой как IGHV3-7*01), IGHD4 (например, IGHD4-11, такой как IGHD4-11*01) и IGHJ4 (например, IGHJ4*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV4 (например, IGHV4-4, такой как IGHV4-4*02), IGHD3 (например, IGHD3-10, такой как IGHD3-10*01) и IGHJ4 (например, IGHJ4*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV4 (например, IGHV4-39, такой как IGHV4-39*01), IGHD6 (например, IGHD6-13, такой как IGHD6-13*01) и IGHJ1 (например, IGHJ1*01). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-33, такой как IGHV3-33*01), IGHD5 (например, IGHD5-18, такой как IGHD5-18*01) и IGHJ6 (например, IGHJ6*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-11, такой как IGHV3-11*01), IGHD1 (например, IGHD1-20, такой как IGHD1-20*01) и IGHJ6 (например, IGHJ6*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-23, такой как IGHV3-23*04), IGHD5 (например, IGHD5-18, такой как IGHD5-18*01) и IGHJ4 (например, IGHJ4*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-7, такой как IGHV3-7*01), IGHD5 (например, IGHD5-24, такой как IGHD5-24*01) и IGHJ4 (например, IGHJ4*02). В одном варианте реализации, тяжелая цепь антитела получена из комбинации IGHV3 (например, IGHV3-23, такой как IGHV3-23*04), IGHD6 (например, IGHD6-13, такой как IGHD6-13*01) и IGHJ4 (например, IGHJ4*02).
Концепция 12. Антитело или фрагмент согласно концепциям 10, 10а, 11, 11а или 11b, где антитело или фрагмент содержат домен VL, который получен путем рекомбинации Vκ генный сегмент человека и Jκ генный сегмент человека, где Vκ генный сегмент человека представляет собой IGκV1D (например, IGκV1D-39, такой как IGκV1D-39*01).
В качестве концепции 12а предусматриваются также антитело или фрагмент согласно любой из концепций 10, 10а, 11, 11а или 11b, где Vκ генный сегмент человека выбран из IGκV1 (например, IGκV1-17, такой как IGκV1-17*01 или например, IGKV1-9, такой как IGκV1-9*d01 или, например, IGκV1D-12, такой как IGκV1D-12*02 или, например, IGκV1D-39, такой как IGκV1D-39*01) и IGκV4 (например, IGκV4-1, такой как IGκV4-1*01).
В одном варианте реализации, Vκ генный сегмент человека представляет собой IGκV1 (например, IGκV1-17, такой как IGκV1-17*01). В одном варианте реализации, Vκ генный сегмент человека представляет собой IGκV1 (например, IGκV1-9, такой как IGκV1-9*d01). В одном варианте реализации, Vκ генный сегмент человека представляет собой IGκV1 (например, IGκV1D-12, такой как IGκV1D-12*02). В одном варианте реализации, Vκ генный сегмент человека представляет собой IGκV1 (например, IGκV1D-39, такой как IGκV1D-39*01).
В одном варианте реализации, Vκ генный сегмент человека представляет собой IGκV1 IGκV4 (например, IGκV4-1, такой как IGκV4-1*01)
В качестве концепции 12b предусматриваются также антитело или фрагмент согласно концепции 10, 10а, 11 или 11а, где Jκ генный сегмент человека выбран из IGκJ1 (например, IGκJ1*01), IGκJ2 (например, IGκJ2*04), IGκJ3 (например, IGκJ3*01), IGκJ4 (например, IGκJ4*01) или IGκJ5 (например, IGκJ5*01).
В одном варианте реализации, Jκ генный сегмент человека представляет собой IGκJ1 (например, IGκJ1*01). В одном варианте реализации, Jκ генный сегмент человека представляет собой IGκJ2 (например, IGκJ2*04). В одном варианте реализации, Jκ генный сегмент человека представляет собой IGκJ3 (например, IGκJ3*01). В одном варианте реализации, Jκ генный сегмент человека представляет собой IGκJ4 (например, IGκJ4*01). В одном варианте реализации, Jκ генный сегмент человека представляет собой IGκJ5 (например, IGκJ5*01).
В любой из концепций 12 и 12а Vκ и Jκ генные сегменты являются такими, как описано в комбинациях антител в таблице 5 ниже. В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV1D (например, IGKV1D-12, такой как IGKV1D-12*02) и IGKJ3 (например, IGKJ3*01). В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV4 (например, IGKV4-1, такой как IGKV14-1*01) и IGKJ2 (например, IGKJ2*04). В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV1 (например, IGKV1-17, такой как IGKV1-17*01) и IGKJ1 (например, IGKJ1*01). В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV1D (например, IGKV1D-12, такой как IGKV1D-12*02) и IGKJ4 (например, IGKJ4*01). В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV1 (например, IGKV1-9, такой как IGKV1-9*d01) и IGKJ5 (например, IGKJ5*01). В одном варианте реализации, легкая цепь антитела получена из комбинации IGKV1D (например, IGKV1D-12, такой как IGKV1D-12*02) и IGKJ5 (например, IGKJ5*01).
Концепция 13. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 1D05.
Концепция 13а. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 84G09.
Концепция 13b. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 411В08.
Концепция 13с. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 411С04.
Концепция 13d. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 411D07.
Концепция 13е. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 385F01.
Концепция 13f. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 386Н03.
Концепция 13g. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 389А03.
Концепция 13h. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 413D08.
Концепция 13i. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 413G05.
Концепция 13j. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 413F09.
Концепт 13k. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 414В06.
Концепт 13l. Антитело или его фрагмент, которые специфически связываются с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 416Е01.
Антитела, описанные в этих концепциях, имеют последовательности, описанные выше.
В одном варианте реализации, предлагается антитело, специфически связывающееся с эпитопом, который по существу подобен эпитопу, с которым связывается любое из антител в концепции 13, 13а-13l.
Контактные аминокислотные остатки, участвующие во взаимодействии антитела и антигена, могут быть определены различными способами, известными специалистам в данной области.
В одном варианте реализации, последовательная замена аминокислот антигенной последовательности (с использованием стандартных методов молекулярной биологии для мутации ДНК кодирующей последовательности антигена), в этом случае hPD-L1 с аланином (аланиновое сканирование) или другой неродственной аминокислотой, может содержать остатки, мутация которых будет уменьшать или устранять способность антитела распознавать рассматриваемый антиген. Связывание может быть оценено с использованием стандартных методов, таких как, без ограничений, SPR, HTRF, ИФА (которые описаны в другой части данного документа). Могут быть сделаны другие замены для усиления нарушения связывания, такого как изменение заряда боковой цепи аминокислот антигенной последовательности (например, замена лизина на глутаминовую кислоту), взаимные замены полярных и неполярных остатков (например, замена серина на лейцин). Аланиновое сканирование или другой способ замещения аминокислот могут быть проведены либо с рекомбинантным растворимым антигеном, либо в том случае, когда мишень является мишенью клеточной мембраны, непосредственно на клетках с использованием транзиентной или стабильной экспрессии мутированных версий.
В одном варианте реализации, кристаллография белка может использоваться для определения контактных остатков между антителом и антигеном (т.е. для определения эпитопа, с которым связывается антитело), кристаллография позволяет непосредственно визуализировать контактные остатки, участвующие в взаимодействии антитело-антиген. Как и стандартная рентгеновская кристаллография, криоэлектронная микроскопия использовалась для определения контактных остатков антител и белка капсида ВИЧ (см. Lee, Jeong Hyun, et al. "Antibodies to a conformational epitope on gp41 neutralize HIV-1 by destabilizing the Env spike", Nature communications, 6, (2015)).
В одном варианте реализации, если антитело распознает линейный эпитоп, могут быть получены короткие пептиды на основе последовательности антигена, и связывание антитела с этими пептидами можно проанализировать с использованием стандартных методов, таких как, без ограничений, SPR, HTRF, ИФА (которые описаны в другой части данного документа). Дальнейшее исследование эпитопа может быть обеспечено путем проведения аланинового сканирования на любых пептидах, которые демонстрируют связывание. Альтернативу линейным пептидам, конформационное сканирование может быть выполнено с использованием технологии Pepscan (http://www.pepscan.com/) с использованием их химического связывания пептидов со скаффолдом, которая была использована для определения прерывистых эпитопов на антителах, нацеленных на CD20 (Niederfellner, Gerhard, et al. "Epitope characterization and crystal structure of GA101 provide insights into the molecular basis for type I/II distinction of CD20 antibodies.", Blood, 118.2, (2011), 358-367.).
В одном варианте реализации, для идентификации связывающих эпитопов могут быть использованы ограниченное протеолитическое расщепление и масс-спектрофотометрия. Комплекс антитело-антиген гидролизуется протеазой, такой как, без ограничений, трипсин. Гидролизованные комплексные пептиды сравнивают с результатами масс-спектрофотометрии отдельно взятых продуктов гидролиза антитела и антигена, чтобы определить, защищен ли конкретный эпитоп комплексообразованием. Дальнейшую работу по замещению аминокислот, конкурентному связыванию, можно затем использовать для выделения отдельных аминокислотных остатков, участвующих в взаимодействии (см., например, Suckau, Detlev, et al. "Molecular epitope identification by limited proteolysis of an immobilized antigen-antibody complex and mass spectrometric peptide mapping.", Proceedings of the National Academy of Sciences, 87.24, (1990), 9848-9852).
Таким образом, в одном варианте реализации, контактные остатки эпитопа идентифицируют путем сканирования неродственной аминокислотой (например, сканирования аланином). В другом варианте реализации, сканирование неродственной аминокислотой (например, сканирование аланином) проводят с использованием технологии, выбранной из SPR, HTRF, ИФА, рентгеновской кристаллографии, криоэлектронной микроскопии и комбинации ограниченного протеолитического расщепления и масс-спектрометрии. В одном варианте реализации, сканирование неродственной аминокислотой (например, сканирование аланином) проводят с использованием HTRF. В одном варианте реализации, сканирование неродственной аминокислотой (например, сканирование аланином) проводят с использованием ИФА.
Когда сканирование аланином проводят методом ИФА или HTRF, аминокислотный остаток идентифицируют как участвующий в образовании эпитопа, если снижение сигнала составляет по меньшей мере 25%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 30%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 35%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 40%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 45%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 50%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 55%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 60%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 70%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 75%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 80%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 85%. В одном варианте реализации, уменьшение сигнала составляет по меньшей мере 90%.
Когда сканирование аланином проводят методом SPR, аминокислотный остаток идентифицируют как участвующий в образовании эпитопа, если наблюдается по меньшей мере 10-кратное уменьшение аффинности. В одном варианте реализации, уменьшение аффинности является по меньшей мере 15-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 20-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере в 30-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 40-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 50-кратным. В одном варианте реализации, уменьшение аффинности составляет, по меньшей мере, 100-кратным.
В одном варианте реализации, контактные остатки эпитопа идентифицируют методом рентгеновской кристаллографии. В одном варианте реализации, контактные остатки эпитопа идентифицируют методом криоэлектронной микроскопии. В одном варианте реализации, контактные остатки эпитопа идентифицируют комбинацией ограниченного протеолитического расщепления и масс-спектрометрии.
Концепция 14. Антитело или фрагмент согласно концепции 13, где эпитоп идентифицируют сканированием неродственной аминокислотой или рентгеновской кристаллографией.
Концепция 15. Антитело или фрагмент согласно концепции 14, где контактные остатки эпитопа определяют по снижению аффинности по меньшей мере в 10 раз при сканировании неродственной аминокислотой, например, сканировании аланином, по результатам определения методом SPR.
В одном варианте реализации, уменьшение аффинности является по меньшей мере 15-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 20-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере в 30-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 40-кратным. В одном варианте реализации, уменьшение аффинности является по меньшей мере 50-кратным. В одном варианте реализации, уменьшение аффинности составляет, по меньшей мере, 100-кратным.
SPR может проводиться, как описано выше.
Концепция 16. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 1D05.
Конкуренция может определяться методом поверхностного плазмонного резонанса (SPR), причем такие методики легко доступны квалифицированному специалисту. SPR может проводиться с использованием Biacore™, Proteon™ или другого стандартного метода SPR. Такая конкуренция может быть вызвана, например, связыванием антител или фрагментов с идентичными или перекрывающимися эпитопами hPD-L1. В одном варианте реализации, конкуренцию определяют методом ИФА, причем такие методы легко доступны квалифицированному специалисту. В одном варианте реализации, конкуренцию определяют методом гомогенной флуоресценции с временным разрешением (HTRF), причем такие методы легко доступны квалифицированному специалисту. В одном варианте реализации, конкуренцию определяют с помощью сортировки клеток с активированной флуоресценцией (FACS), причем такие методы легко доступны квалифицированному специалисту. В одном варианте реализации, конкуренцию определяют методом интерферометрии биослоя (BLI) ForteBio Octet®, причем такие методы легко доступны квалифицированному специалисту.
В одном варианте реализации, антитело или фрагмент конкурируют (например, зависимым от дозы образом) с hPD-1 (или его гибридным белком) для связывания с экспрессируемым на поверхности hPD-L1. В одном варианте реализации, антитело или фрагмент конкурируют (например, зависимым от дозы образом) с hPD-1 (или его гибридным белком) за связывание с растворимым hPDL-1.
В одном варианте реализации, антитело или фрагмент частично или полностью ингибируют связывание PD-1 и/или CD80 с экспрессируемым на клеточной поверхности PD-L1, таким как hPD-L1. В другом варианте реализации, антитело или фрагмент частично или полностью ингибируют связывание hPD-1 и/или CD80 с растворимым hPD-L1. В некоторых вариантах реализации, антитело или фрагмент частично или полностью увеличивают секрецию IFNγ, CD25 и IL-2 из клетки с поверхностно-экспрессируемым PD-1. В одном варианте реализации, антитело или фрагмент частично или полностью ингибируют связывание CD80 с растворимым hPD-L1, но не обнаруживают какого-либо детектируемого ингибирования связывания PD-1 с экспрессируемым на поверхности клетки PD-L1. В одном варианте реализации, антитело или фрагмент частично или полностью ингибируют связывание CD80 с растворимым hPD-L1, но не обнаруживают какого-либо детектируемого ингибирования связывания PD-1 с растворимым PD-L1.
В используемом в данном документе значении, термин «ингибирует», «ингибирование», «ингибирующий» и т.п., в используемом в данном документе значении, относится к способности антагониста (например, антитела или его фрагмента) связываться с эпитопом, который либо частично, либо полностью предотвращает связывание рецептора (например, CD80 или PD-1) с лигандом (например, PD-L1). Если эпитоп, с которым связывается антагонист, полностью блокирует сайт связывания лиганда, то связывание лиганда полностью предотвращается (что может быть физической блокировкой - в случае перекрывающихся эпитопов, или стерической блокировкой - когда антагонист является настолько большим, что он препятствует связыванию лиганда с его особым эпитопом), и лиганд не удаляется из кровообращения. Таким образом, концентрация циркулирующего лиганда может быть увеличена. Если эпитоп, с которым связывается антагонист, частично блокирует сайт связывания лиганда, лиганд может быть способен связываться, но только слабо (в случае частичного ингибирования) или в ориентации, отличной от естественного взаимодействия связывания. В этом случае, некоторая часть лиганда может быть удалена из кровообращения, но не в таком количестве, как при полностью свободном и доступном для связывания сайте связывания лиганда. Таким образом, ингибирование относится к физическому взаимодействию лиганда и рецептора. Ингибирование можно измерить с помощью HTRF, который более подробно описан в другой части данного документа и у Mathis (1995) Clinical Chemistry 41 (9), 1391-1397. Ингибирование также может быть измерено методом проточной цитометрии, где рецептор экспрессируется на клетках, или методом ИФА, где рецептор адсорбируется на планшетах.
Концепция 16а. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 84G09.
Концепция 16b. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 411В08.
Концепция 16с. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 411С04.
Концепция 16d. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 411D07.
Концепция 16е. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 385F01.
Концепция 16f. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 386Н03.
Концепция 16g. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 389А03.
Концепция 16h. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 413D08.
Концепция 16i. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 413G05.
Концепция 16j. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 413F09.
Концепция 16k. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 414В06.
Концепция 16l. Антитело или его фрагмент, которые конкурируют за связывание с hPD-L1 с антителом 416Е01.
Антитела имеют последовательности, описанные выше.
Концепция 17. Антитело или фрагмент согласно любой из концепций 10-16, где домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 29 или 32, или последовательность CDRH3, представленную SEQ ID NO: 29 или 32, содержащую 6 или меньше аминокислотных замещений.
Концепция 17а: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, и в случае зависимости от концепции 16 оно зависит от концепции 16а), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 9 или 12, или последовательность CDRH3, представленную SEQ ID NO: 9 или 12, содержащую 6 или меньше аминокислотных замещений.
Концепция 17b: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16b), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 54 или 57, или последовательность CDRH3, представленную SEQ ID NO: 54 или 57, содержащую 6 или меньше аминокислотных замещений.
Концепция 17с: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16с), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 74 или 77, или последовательность CDRH3, представленную SEQ ID NO: 74 или 77, содержащую 6 или меньше аминокислотных замещений.
Концепция 17d: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16d), в которой V н содержит последовательность CDRH3, представленную SEQ ID NO: 94 или 97, или последовательность CDRH3, представленную SEQ ID NO: 94 или 97, содержащую 3 или меньше аминокислотных замещений.
Концепция 17е: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16е), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 114 или 117, или последовательность CDRH3, представленную SEQ ID NO: 114 или 117, содержащую 6 или меньше аминокислотных замещений.
Концепция 17f: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16f), в которой домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 144 или 147, или последовательность CDRH3, представленную SEQ ID NO: 144 или 147, содержащую 3 или меньше аминокислотных замещений.
Концепция 17g: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16g), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 174 или 177, или последовательность CDRH3, представленную SEQ ID NO: 174 или 177, содержащую 6 или меньше аминокислотных замещений.
Концепция 17h: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16h), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 134 или 137, или последовательность CDRH3, представленную SEQ ID NO: 134 или 137, содержащую 5 или меньше аминокислотных замещений.
Концепция 17i: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16i), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 240 или 243, или последовательность CDRH3, представленную SEQ ID NO: 240 или 243, содержащую 6 или меньше аминокислотных замещений.
Концепция 17j: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16j), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 260 или 263, или последовательность CDRH3, представленную SEQ ID NO: 260 или 263, содержащую 6 или меньше аминокислотных замещений.
Концепция 17k: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16k), при этом VH содержит последовательность CDRH3, представленную SEQ ID NO: 280 или 283 или последовательность CDRH3, представленную SEQ ID NO: 280 или 283, содержащую 6 или меньше аминокислотных замещений.
Концепция 17l: Антитело или его фрагмент согласно любой из концепций 10-16 (но в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, и в случае зависимости от концепции 16, они являются зависимыми от концепции 16l), при этом домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 345 или 348, или последовательность CDRH3, представленную SEQ ID NO: 345 или 348, содержащую 6 или меньше аминокислотных замещений.
Концепция 18. Антитело или фрагмент согласно любой из предшествующих концепций, в которых домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 27 или 30, или последовательность CDRH1, представленную SEQ ID NO: 27 или 30, содержащую 3, 2 или 1 аминокислотных замещения.
Концепция 18а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17а), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 7 или 10, или последовательность CDRH1, представленную SEQ ID NO: 7 или 10 содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17b), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 52 или 55, или последовательность CDRH1, представленную SEQ ID NO: 52 или 55, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17с), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 72 или 75, или последовательность CDRH1, представленную SEQ ID NO: 72 или 75, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17d), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 92 или 95, или последовательность CDRH1, представленную SEQ ID NO: 92 или 95, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17е), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 112 или 115, или последовательность CDRH1, представленную SEQ ID NO: 112 или 115, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17f), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 142 или 145, или последовательность CDRH1, представленную SEQ ID NO: 142 или 145, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17g), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 172 или 175, или последовательность CDRH1, представленную SEQ ID NO: 172 или 175, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17h), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 132 или 135, или последовательность CDRH1, представленную SEQ ID NO: 132 или 135, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17i), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 238 или 241, или последовательность CDRH1, представленную SEQ ID NO: 238 или 241, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17j), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 258 или 261, или последовательность CDRH1, представленную SEQ ID NO: 258 или 261, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17k), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 278 или 281, или последовательность CDRH1, представленную SEQ ID NO: 278 или 281, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 18l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, и в случае зависимости от концепции 17, они являются зависимыми от концепции 17l), где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 343 или 346, или последовательность CDRH1, представленную SEQ ID NO: 343 или 346, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19. Антитело или фрагмент согласно любой из предшествующих концепций, в которых домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 28 или 31, или последовательность CDRH2, представленную SEQ ID NO: 28 или 31, содержащую 4 или меньше аминокислотных замещений.
Концепция 19а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18а), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 8 или 11, или последовательность CDRH2, представленную SEQ ID NO: 8 или 11, содержащую 4 или меньше аминокислотных замещений.
Концепция 19b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18b), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 53 или 56, или последовательность CDRH2, представленную SEQ ID NO: 53 или 56, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18с), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 73 или 76, или последовательность CDRH2, представленную SEQ ID NO: 73 или 76, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18d), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 93 или 96, или последовательность CDRH2, представленную SEQ ID NO: 93 или 96, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18е), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 113 или 116, или последовательность CDRH2, представленную SEQ ID NO: 113 или 116, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18f), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 143 или 146, или последовательность CDRH2, представленную SEQ ID NO: 143 или 146, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18g), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 173 или 176, или последовательность CDRH2, представленную SEQ ID NO: 173 или 176, содержащую 3, 2 или 1 аминокислотную замену (и).
Концепция 19h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18h), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 133 или 136, или последовательность CDRH2, представленную SEQ ID NO: 133 или 136, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18i), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 239 или 242, или последовательность CDRH2, представленную SEQ ID NO: 239 или 242, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18j), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 259 или 262, или последовательность CDRH2, представленную SEQ ID NO: 259 или 262, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18k), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 279 или 282, или последовательность CDRH2, представленную SEQ ID NO: 279 или 282, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 19l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, и в случае зависимости от концепции 18, они являются зависимыми от концепции 18l), где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 344 или 347, или последовательность CDRH2, представленную SEQ ID NO: 344 или 347, содержащую 3, 2 или 1 аминокислотных замещений.
Концепция 20. Антитело или фрагмент согласно любой из предшествующих концепций, где домен VH содержит аминокислотную последовательность SEQ ID NO: 33 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 33.
Концепция 20а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, в случае зависимости от концепции 18, они являются зависимыми от концепции 18а, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19а), где домен VH содержит аминокислотную последовательность SEQ ID NO: 13 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 13.
Концепция 20b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, в случае зависимости от концепции 18, они являются зависимыми от концепции 18b, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19b), где домен VH содержит аминокислотную последовательность SEQ ID NO: 58 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 58.
Концепция 20с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, в случае зависимости от концепции 18, они являются зависимыми от концепции 18с, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19с), где домен VH содержит аминокислотную последовательность SEQ ID NO: 78 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 78.
Концепция 20d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, в случае зависимости от концепции 18, они являются зависимыми от концепции 18d, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19d), где домен VH содержит аминокислотную последовательность SEQ ID NO: 98 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 98.
Концепция 20е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, в случае зависимости от концепции 18, они являются зависимыми от концепции 18е, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19е), где домен VH содержит аминокислотную последовательность SEQ ID NO: 118 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 118.
Концепция 20f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, в случае зависимости от концепции 18, они являются зависимыми от концепции 18f, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19f), где домен VH содержит аминокислотную последовательность SEQ ID NO: 158 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 158.
Концепция 20g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, в случае зависимости от концепции 18, они являются зависимыми от концепции 18g, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19g), где домен VH содержит аминокислотную последовательность SEQ ID NO: 178 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 178.
Концепция 20h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, в случае зависимости от концепции 18, они являются зависимыми от концепции 18h, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19h), где домен VH содержит аминокислотную последовательность SEQ ID NO: 138 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 138.
Концепция 20i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, в случае зависимости от концепции 18, они являются зависимыми от концепции 18i, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19i), где домен VH содержит аминокислотную последовательность SEQ ID NO: 244 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 244.
Концепция 20j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, в случае зависимости от концепции 18, они являются зависимыми от концепции 18j, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19j), где домен VH содержит аминокислотную последовательность SEQ ID NO: 264 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 264.
Концепция 20k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, в случае зависимости от концепции 18, они являются зависимыми от концепции 18k, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19k), где домен VH содержит аминокислотную последовательность SEQ ID NO: 284 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 284.
Понятие 20l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, в случае зависимости от концепции 18, они являются зависимыми от концепции 18l, и в случае зависимости от концепции 19, они являются зависимыми от концепции 19l), где домен VH содержит аминокислотную последовательность SEQ ID NO: 349 или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 349.
В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Концепция 21. Антитело или фрагмент согласно любой из предшествующих концепций, включающие первую и вторую копии указанного домена VH.
Концепция 22. Антитело или фрагмент согласно любой из предшествующих концепций, содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 37 или 40, или последовательность CDRL1, представленную SEQ ID NO: 37 или 40, содержащую 3 или меньше аминокислотных замещений.
Концепция 22а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, в случае зависимости от концепции 18, они являются зависимыми от концепции 18а, в случае зависимости от концепции 19, они являются зависимыми от концепции 19а, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20а), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 17 или 20 или последовательность CDRL1, представленную SEQ ID NO: 17 или 20, содержащую 3 или меньше аминокислотных замещений.
Концепция 22b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, в случае зависимости от концепции 18, они являются зависимыми от концепции 18b, в случае зависимости от концепции 19, они являются зависимыми от концепции 19b, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20b), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 62 или 65, или последовательность CDRL1, представленную SEQ ID NO: 62 или 65, содержащую 3 или меньше аминокислотных замещений.
Концепция 22с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, в случае зависимости от концепции 18, они являются зависимыми от концепции 18с, в случае зависимости от концепции 19, они являются зависимыми от концепции 19с, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20с), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 82 или 85, или последовательность CDRL1, представленную SEQ ID NO: 82 или 85, содержащую 2 или 1 аминокислотных замещений,
Концепция 22d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, в случае зависимости от концепции 18, они являются зависимыми от концепции 18d, в случае зависимости от концепции 19, они являются зависимыми от концепции 19d, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20d), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 102 или 105, или последовательность CDRL1, представленную SEQ ID NO: 102 или 105, содержащую 5 или меньше аминокислотных замещений.
Концепция 22е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, в случае зависимости от концепции 18, они являются зависимыми от концепции 18е, в случае зависимости от концепции 19, они являются зависимыми от концепции 19е, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20е), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 122 или 125 или последовательность CDRL1, представленную SEQ ID NO: 122 или 125, содержащую 2 или 1 аминокислотных замещений.
Концепция 22f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, в случае зависимости от концепции 18, они являются зависимыми от концепции 18f, в случае зависимости от концепции 19, они являются зависимыми от концепции 19f, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20f), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 162 или 165, или последовательность CDRL1, представленную SEQ ID NO: 162 или 165, содержащую 5 или меньше аминокислотных замещений.
Концепция 22g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, в случае зависимости от концепции 18, они являются зависимыми от концепции 18g, в случае зависимости от концепции 19, они являются зависимыми от концепции 19g, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20g), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 182 или 185 или последовательность CDRL1, представленную SEQ ID NO: 182 или 185, содержащую 5 или меньше аминокислотных замещений.
Концепция 22h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, в случае зависимости от концепции 18, они являются зависимыми от концепции 18h, в случае зависимости от концепции 19, они являются зависимыми от концепции 19h, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20h), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 142 или 145, или последовательность CDRL1, представленную SEQ ID NO: 142 или 145, содержащую 2 или 1 аминокислотных замещений.
Концепция 22i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, в случае зависимости от концепции 18, они являются зависимыми от концепции 18i, в случае зависимости от концепции 19, они являются зависимыми от концепции 19i, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20i), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 248 или 251 или последовательность CDRL1, представленную SEQ ID NO: 248 или 251, содержащую 2 или 1 аминокислотных замещений.
Концепция 22j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, в случае зависимости от концепции 18, они являются зависимыми от концепции 18j, в случае зависимости от концепции 19, они являются зависимыми от концепции 19j, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20j), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 268 или 271, или последовательность CDRL1, представленную SEQ ID NO: 268 или 271, содержащую 2 или 1 аминокислотных замещений.
Концепция 22k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, в случае зависимости от концепции 18, они являются зависимыми от концепции 18k, в случае зависимости от концепции 19, они являются зависимыми от концепции 19k, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20k), содержащие домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 288 или 291, или последовательность CDRL1, представленную SEQ ID NO: 288 или 291, содержащую 2 или 1 аминокислотных замещений.
Концепция 22l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, в случае зависимости от концепции 18, они являются зависимыми от концепции 18l, в случае зависимости от концепции 19, они являются зависимыми от концепции 19l, и в случае зависимости от концепции 20, они являются зависимыми от концепции 20l), содержащие домен VL который содержит последовательность CDRL1, представленную SEQ ID NO: 353 или 356, или последовательность CDRL1, представленную SEQ ID NO: 353 или 356, содержащую 2 или 1 аминокислотных замещений,
Концепция 23. Антитело или фрагмент согласно любой из предшествующих концепций, содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 38 или 41, или последовательность CDRL2, представленную SEQ ID NO: 38 или 41, содержащую 2 или 1 аминокислотных замещений, например, последовательность CDRL2, представленную SEQ ID NO: 50.
Концепция 23а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, в случае зависимости от концепции 18, они являются зависимыми от концепции 18а, в случае зависимости от концепции 19, они являются зависимыми от концепции 19а, в случае зависимости от концепции 20, они являются зависимыми от концепции 20а, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22а), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 18 или 21, или последовательность CDRL2, представленную SEQ ID NO: 18 или 21, содержащую 2 или 1 аминокислотных замещений.
Концепция 23b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, в случае зависимости от концепции 18, они являются зависимыми от концепции 18b, в случае зависимости от концепции 19, они являются зависимыми от концепции 19b, в случае зависимости от концепции 20, они являются зависимыми от концепции 20b, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22b), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 63 или 66, или последовательность CDRL2, представленную SEQ ID NO: 63 или 66, содержащую одно аминокислотное замещение.
Концепция 23с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, в случае зависимости от концепции 18, они являются зависимыми от концепции 18с, в случае зависимости от концепции 19, они являются зависимыми от концепции 19с, в случае зависимости от концепции 20, они являются зависимыми от концепции 20с, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22с), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 83 или 86, или последовательность CDRL2, представленную SEQ ID NO: 83 или 86, содержащую одно аминокислотное замещение.
Концепция 23d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, в случае зависимости от концепции 18, они являются зависимыми от концепции 18d, в случае зависимости от концепции 19, они являются зависимыми от концепции 19d, в случае зависимости от концепции 20, они являются зависимыми от концепции 20d, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22d), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 103 или 106, или последовательность CDRL2, представленную SEQ ID NO: 103 или 106, содержащую одну аминокислотную замену.
Концепция 23е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, в случае зависимости от концепции 18, они являются зависимыми от концепции 18е, в случае зависимости от концепции 19, они являются зависимыми от концепции 19е, в случае зависимости от концепции 20, они являются зависимыми от концепции 20е, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22е), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 123 или 126, или последовательность CDRL2, представленную SEQ ID NO: 123 или 126, содержащую одну аминокислотную замену.
Концепция 23f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, в случае зависимости от концепции 18, они являются зависимыми от концепции 18f, в случае зависимости от концепции 19, они являются зависимыми от концепции 19f, в случае зависимости от концепции 20, они являются зависимыми от концепции 20f, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22f), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 153 или 156 или последовательность CDRL2, представленную SEQ ID NO: 153 или 156, содержащую одно аминокислотное замещение.
Концепция 23g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, в случае зависимости от концепции 18, они являются зависимыми от концепции 18g, в случае зависимости от концепции 19, они являются зависимыми от концепции 19g, в случае зависимости от концепции 20, они являются зависимыми от концепции 20g, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22g), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 183 или 186, или последовательность CDRL2, представленную SEQ ID NO: 183 или 186, содержащую одно аминокислотное замещение.
Концепция 23h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, в случае зависимости от концепции 18, они являются зависимыми от концепции 18h, в случае зависимости от концепции 19, они являются зависимыми от концепции 19h, в случае зависимости от концепции 20, они являются зависимыми от концепции 20h, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22h), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 143 или 146, или последовательность CDRL2, представленную SEQ ID NO: 143 или 146, содержащую одно аминокислотное замещение.
Концепция 23i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, в случае зависимости от концепции 18, они являются зависимыми от концепции 18i, в случае зависимости от концепции 19, они являются зависимыми от концепции 19i, в случае зависимости от концепции 20, они являются зависимыми от концепции 20i, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22i), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 249 или 252, или последовательность CDRL2, представленную SEQ ID NO: 249 или 252, содержащую одно аминокислотное замещение.
Концепция 23j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, в случае зависимости от концепции 18, они являются зависимыми от концепции 18j, в случае зависимости от концепции 19, они являются зависимыми от концепции 19j, в случае зависимости от концепции 20, они являются зависимыми от концепции 20j, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22j), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 269 или 272, или последовательность CDRL2, представленную SEQ ID NO: 269 или 272, содержащую одно аминокислотное замещение.
Концепция 23k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, в случае зависимости от концепции 18, они являются зависимыми от концепции 18k, в случае зависимости от концепции 19, они являются зависимыми от концепции 19k, в случае зависимости от концепции 20, они являются зависимыми от концепции 20k, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22k), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную SEQ ID NO: 289 или 292, или последовательность CDRL2, представленную SEQ ID NO: 289 или 292, содержащую одну аминокислотную замену.
Концепция 23l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, в случае зависимости от концепции 18, они являются зависимыми от концепции 18l, в случае зависимости от концепции 19, они являются зависимыми от концепции 19l, в случае зависимости от концепции 20, они являются зависимыми от концепции 20l, и в случае зависимости от концепции 22, они являются зависимыми от концепции 22l), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2 из SEQ ID NO: 354, или 357, или последовательность CDRL2, представленную SEQ ID NO: 354 или 357, содержащую одно аминокислотное замещение.
Концепция 24. Антитело или фрагмент согласно любой из предшествующих концепций, содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 39 или 42, или последовательность CDRL3, представленную SEQ ID NO: 39 или 42, содержащую 4 или меньше аминокислотных замещений.
Концепция 24а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, в случае зависимости от концепции 18, они являются зависимыми от концепции 18а, в случае зависимости от концепции 19, они являются зависимыми от концепции 19а, в случае зависимости от концепции 20, они являются зависимыми от концепции 20а, в случае зависимости от концепции 22, они являются зависимыми от концепции 22а, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23а), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 19 или 22, или последовательность CDRL3, представленную SEQ ID NO: 19 или 22, содержащую 4 или меньше аминокислотных замещений.
Концепция 24b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, в случае зависимости от концепции 18, они являются зависимыми от концепции 18b, в случае зависимости от концепции 19, они являются зависимыми от концепции 19b, в случае зависимости от концепции 20, они являются зависимыми от концепции 20b, в случае зависимости от концепции 22, они являются зависимыми от концепции 22b, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23b), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 64 или 67, или последовательность CDRL3, представленную SEQ ID NO: 64 или 67, содержащую 4 или меньше аминокислотных замещений.
Концепция 24с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, в случае зависимости от концепции 18, они являются зависимыми от концепции 18с, в случае зависимости от концепции 19, они являются зависимыми от концепции 19с, в случае зависимости от концепции 20, они являются зависимыми от концепции 20с, в случае зависимости от концепции 22, они являются зависимыми от концепции 22с, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23с), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 84 или 87, или последовательность CDRL3, представленную SEQ ID NO: 84 или 87, содержащую 4 или меньше аминокислотных замещений.
Концепция 24d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, в случае зависимости от концепции 18, они являются зависимыми от концепции 18d, в случае зависимости от концепции 19, они являются зависимыми от концепции 19d, в случае зависимости от концепции 20, они являются зависимыми от концепции 20d, в случае зависимости от концепции 22, они являются зависимыми от концепции 22d, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23d), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 104 или 107, или последовательность CDRL3, представленную SEQ ID NO: 104 или 107, содержащую 4 или меньше аминокислотных замещений.
Концепция 24е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, в случае зависимости от концепции 18, они являются зависимыми от концепции 18е, в случае зависимости от концепции 19, они являются зависимыми от концепции 19е, в случае зависимости от концепции 20, они являются зависимыми от концепции 20е, в случае зависимости от концепции 22, они являются зависимыми от концепции 22е, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23е), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 124 или 127, или последовательность CDRL3, представленную SEQ ID NO: 124 или 127, содержащую 4 или меньше аминокислотных замещений.
Концепция 24f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, в случае зависимости от концепции 18, они являются зависимыми от концепции 18f, в случае зависимости от концепции 19, они являются зависимыми от концепции 19f, в случае зависимости от концепции 20, они являются зависимыми от концепции 20f, в случае зависимости от концепции 22, они являются зависимыми от концепции 22f, и в случае зависимости от концепции 23, они являются зависимыми концепции 23f), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 164 или 167, или последовательность CDRL3, представленную SEQ ID NO: 164 или 167, содержащую 4 или меньше аминокислотных замещений.
Концепция 24g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, в случае зависимости от концепции 18, они являются зависимыми от концепции 18g, в случае зависимости от концепции 19, они являются зависимыми от концепции 19g, в случае зависимости от концепции 20, они являются зависимыми от концепции 20g, в случае зависимости от концепции 22, они являются зависимыми от концепции 22g, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23g), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 184 или 187, или последовательность CDRL3, представленную SEQ ID NO: 184 или 187, содержащую 4 или меньше аминокислотных замещений.
Концепция 24h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, в случае зависимости от концепции 18, они являются зависимыми от концепции 18h, в случае зависимости от концепции 19, они являются зависимыми от концепции 19h, в случае зависимости от концепции 20, они являются зависимыми от концепции 20h, в случае зависимости от концепции 22, они являются зависимыми от концепции 22h, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23h), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 144 или 147, или последовательность CDRL3, представленную SEQ ID NO: 144 или 147, содержащую 4 или меньше аминокислотных замещений.
Концепция 24i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, в случае зависимости от концепции 18, они являются зависимыми от концепции 18i, в случае зависимости от концепции 19, они являются зависимыми от концепции 19i, в случае зависимости от концепции 20, они являются зависимыми от концепции 20i, в случае зависимости от концепции 22, они являются зависимыми от концепции 22i, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23i), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 250 или 253, или последовательность CDRL3, представленную SEQ ID NO: 250 или 253, содержащую 4 или меньше аминокислотных замещений.
Концепция 24j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, в случае зависимости от концепции 18, они являются зависимыми от концепции 18j, в случае зависимости от концепции 19, они являются зависимыми от концепции 19j, в случае зависимости от концепции 20, они являются зависимыми от концепции 20j, в случае зависимости от концепции 22, они являются зависимыми от концепции 22j, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23j), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 270 или 273, или последовательность CDRL3, представленную SEQ ID NO: 270 или 273, содержащую 4 или меньше аминокислотных замещений.
Концепция 24k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, в случае зависимости от концепции 18, они являются зависимыми от концепции 18k, в случае зависимости от концепции 19, они являются зависимыми от концепции 19k, в случае зависимости от концепции 20, они являются зависимыми от концепции 20k, в случае зависимости от концепции 22, они являются зависимыми от концепции 22k, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23k), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 290 или 293, или последовательность CDRL3, представленную SEQ ID NO: 290 или 293, содержащую 4 или меньше аминокислотных замещений.
Концепция 24l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, в случае зависимости от концепции 18, они являются зависимыми от концепции 18l, в случае зависимости от концепции 19, они являются зависимыми от концепции 19l, в случае зависимости от концепции 20, они являются зависимыми от концепции 20l, в случае зависимости от концепции 22, они являются зависимыми от концепции 22l, и в случае зависимости от концепции 23, они являются зависимыми от концепции 23l), содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную SEQ ID NO: 355 или 358, или последовательность CDRL3, представленную SEQ ID NO: 355 или 358, содержащую 4 или меньше аминокислотных замещений.
Концепция 25. Антитело или фрагмент согласно любой из предшествующих концепций, содержащие (а) или указанный домен VL, где домен VL содержит аминокислотную последовательность SEQ ID NO: 43 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85% или по меньшей мере на 90%), идентичную SEQ ID NO: 43 (например, последовательность домена VL в последовательности легкой цепи, представленной SEQ ID NO: 50, 51 или 298).
Концепция 25а: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9а, в случае зависимости от концепции 13, они являются зависимыми от концепции 13а, в случае зависимости от концепции 16, они являются зависимыми от концепции 16а, в случае зависимости от концепции 17, они являются зависимыми от концепции 17а, в случае зависимости от концепции 18, они являются зависимыми от концепции 18а, в случае зависимости от концепции 19, они являются зависимыми от концепции 19а, в случае зависимости от концепции 20, они являются зависимыми от концепции 20а, в случае зависимости от концепции 22, они являются зависимыми от концепции 22а, в случае зависимости от концепции 23, они являются зависимыми от концепции 23а, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24а), где домен VL содержит аминокислотную последовательность SEQ ID NO: 23 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 23.
Концепция 25b: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9b, в случае зависимости от концепции 13, они являются зависимыми от концепции 13b, в случае зависимости от концепции 16, они являются зависимыми от концепции 16b, в случае зависимости от концепции 17, они являются зависимыми от концепции 17b, в случае зависимости от концепции 18, они являются зависимыми от концепции 18b, в случае зависимости от концепции 19, они являются зависимыми от концепции 19b, в случае зависимости от концепции 20, они являются зависимыми от концепции 20b, в случае зависимости от концепции 22, они являются зависимыми от концепции 22а, в случае зависимости от концепции 23, они являются зависимыми от концепции 23b, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24b), где домен VL содержит аминокислотную последовательность SEQ ID NO: 68 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 68.
Концепция 25с: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9с, в случае зависимости от концепции 13, они являются зависимыми от концепции 13с, в случае зависимости от концепции 16, они являются зависимыми от концепции 16с, в случае зависимости от концепции 17, они являются зависимыми от концепции 17с, в случае зависимости от концепции 18, они являются зависимыми от концепции 18с, в случае зависимости от концепции 19, они являются зависимыми от концепции 19с, в случае зависимости от концепции 20, они являются зависимыми от концепции 20с, в случае зависимости от концепции 22, они являются зависимыми от концепции 22с, в случае зависимости от концепции 23, они являются зависимыми от концепции 23с, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24с), где домен VL содержит аминокислотную последовательность SEQ ID NO: 88 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 88.
Концепция 25d: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9d, в случае зависимости от концепции 13, они являются зависимыми от концепции 13d, в случае зависимости от концепции 16, они являются зависимыми от концепции 16d, в случае зависимости от концепции 17, они являются зависимыми от концепции 17d, в случае зависимости от концепции 18, они являются зависимыми от концепции 18d, в случае зависимости от концепции 19, они являются зависимыми от концепции 19d, в случае зависимости от концепции 20, они являются зависимыми от концепции 20d, в случае зависимости от концепции 22, они являются зависимыми от концепции 22d, в случае зависимости от концепции 23, они являются зависимыми от концепции 23d, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24d), где домен VL содержит аминокислотную последовательность SEQ ID NO: 108 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 108.
Концепция 25е: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9е, в случае зависимости от концепции 13, они являются зависимыми от концепции 13е, в случае зависимости от концепции 16, они являются зависимыми от концепции 16е, в случае зависимости от концепции 17, они являются зависимыми от концепции 17е, в случае зависимости от концепции 18, они являются зависимыми от концепции 18е, в случае зависимости от концепции 19, они являются зависимыми от концепции 19е, в случае зависимости от концепции 20, они являются зависимыми от концепции 20е, в случае зависимости от концепции 22, они являются зависимыми от концепции 22е, в случае зависимости от концепции 23, они являются зависимыми от концепции 23е, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24е), где домен VL содержит аминокислотную последовательность SEQ ID NO: 128 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 128.
Концепция 25f: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9f, в случае зависимости от концепции 13, они являются зависимыми от концепции 13f, в случае зависимости от концепции 16, они являются зависимыми от концепции 16f, в случае зависимости от концепции 17, они являются зависимыми от концепции 17f, в случае зависимости от концепции 18, они являются зависимыми от концепции 18f, в случае зависимости от концепции 19, они являются зависимыми от концепции 19f, в случае зависимости от концепции 20, они являются зависимыми от концепции 20f, в случае зависимости от концепции 22, они являются зависимыми от концепции 22f, в случае зависимости от концепции 23, они являются зависимыми от концепции 23f, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24f), где домен VL содержит аминокислотную последовательность SEQ ID NO: 168 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 168.
Концепция 25g: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9g, в случае зависимости от концепции 13, они являются зависимыми от концепции 13g, в случае зависимости от концепции 16, они являются зависимыми от концепции 16g, в случае зависимости от концепции 17, они являются зависимыми от концепции 17g, в случае зависимости от концепции 18, они являются зависимыми от концепции 18g, в случае зависимости от концепции 19, они являются зависимыми от концепции 19g, в случае зависимости от концепции 20, они являются зависимыми от концепции 20g, в случае зависимости от концепции 22, они являются зависимыми от концепции 22g, в случае зависимости от концепции 23, они являются зависимыми от концепции 23g, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24g), где домен VL содержит аминокислотную последовательность SEQ ID NO: 188 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 188.
Концепция 25h: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9h, в случае зависимости от концепции 13, они являются зависимыми от концепции 13h, в случае зависимости от концепции 16, они являются зависимыми от концепции 16h, в случае зависимости от концепции 17, они являются зависимыми от концепции 17h, в случае зависимости от концепции 18, они являются зависимыми от концепции 18h, в случае зависимости от концепции 19, они являются зависимыми от концепции 19h, в случае зависимости от концепции 20, они являются зависимыми от концепции 20h, в случае зависимости от концепции 22, они являются зависимыми от концепции 22h, в случае зависимости от концепции 23, они являются зависимыми от концепции 23h, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24h), где домен VL содержит аминокислотную последовательность SEQ ID NO: 148 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 148.
Концепция 25i: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9i, в случае зависимости от концепции 13, они являются зависимыми от концепции 13i, в случае зависимости от концепции 16, они являются зависимыми от концепции 16i, в случае зависимости от концепции 17, они являются зависимыми от концепции 17i, в случае зависимости от концепции 18, они являются зависимыми от концепции 18i, в случае зависимости от концепции 19, они являются зависимыми от концепции 19i, в случае зависимости от концепции 20, они являются зависимыми от концепции 20i, в случае зависимости от концепции 22, они являются зависимыми от концепции 22i, в случае зависимости от концепции 23, они являются зависимыми от концепции 23i, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24i), где домен VL содержит аминокислотную последовательность SEQ ID NO: 254 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 254.
Концепция 25j: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9j, в случае зависимости от концепции 13, они являются зависимыми от концепции 13j, в случае зависимости от концепции 16, они являются зависимыми от концепции 16j, в случае зависимости от концепции 17, они являются зависимыми от концепции 17j, в случае зависимости от концепции 18, они являются зависимыми от концепции 18j, в случае зависимости от концепции 19, они являются зависимыми от концепции 19j, в случае зависимости от концепции 20, они являются зависимыми от концепции 20j, в случае зависимости от концепции 22, они являются зависимыми от концепции 22j, в случае зависимости от концепции 23, они являются зависимыми от концепции 23j, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24j), где домен VL содержит аминокислотную последовательность SEQ ID NO: 274 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 274.
Концепция 25k: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9k, в случае зависимости от концепции 13, они являются зависимыми от концепции 13k, в случае зависимости от концепции 16, они являются зависимыми от концепции 16k, в случае зависимости от концепции 17, они являются зависимыми от концепции 17k, в случае зависимости от концепции 18, они являются зависимыми от концепции 18k, в случае зависимости от концепции 19, они являются зависимыми от концепции 19k, в случае зависимости от концепции 20, они являются зависимыми от концепции 20k, в случае зависимости от концепции 22, они являются зависимыми от концепции 22k, в случае зависимости от концепции 23, они являются зависимыми от концепции 23k, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24k), где домен VL содержит аминокислотную последовательность SEQ ID NO: 294 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 294.
Концепция 25l: Антитело или его фрагмент согласно любой предшествующей концепции (но в случае зависимости от концепции 9, они являются зависимыми от концепции 9l, в случае зависимости от концепции 13, они являются зависимыми от концепции 13l, в случае зависимости от концепции 16, они являются зависимыми от концепции 16l, в случае зависимости от концепции 17, они являются зависимыми от концепции 17l, в случае зависимости от концепции 18, они являются зависимыми от концепции 18l, в случае зависимости от концепции 19, они являются зависимыми от концепции 19l, в случае зависимости от концепции 20, они являются зависимыми от концепции 20l, в случае зависимости от концепции 22, они являются зависимыми от концепции 22l, в случае зависимости от концепции 23, они являются зависимыми от концепции 23l, и в случае зависимости от концепции 24, они являются зависимыми от концепции 24l), где домен VL содержит аминокислотную последовательность SEQ ID NO: 359 или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 80% (например, по меньшей мере на 85%, или по меньшей мере на 90%) идентичную SEQ ID NO: 359.
В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Концепция 26. Антитело или фрагмент согласно любой из концепций 12-21, включающие первую и вторую копии (а) или указанного домена VL.
Концепция 27. Антитело или фрагмент согласно любой из предшествующих концепций, которые специфически связываются с PD-L1 яванского макака, представленным SEQ ID NO: 2.
В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью менее 1 нМ (например, от 1 нМ до 0,01 пМ или от 1 нМ до 0,1 пМ или от 1 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью менее 10 нМ (например, от 10 нМ до 0,01 пМ или от 10 нМ до 0,1 пМ или от 10 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью менее 0,1 нМ (например, от 0,1 нМ до 0,01 пМ или от 0,1 нМ до 0,1 пМ или от 0,1 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью менее 0,01 нМ (например, от 0,011 нМ до 0,01 пМ или от 0,01 нМ до 0,1 пМ).
В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 2-кратную аффинность к hPD-L1. В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 4-кратную аффинность к hPD-L1. В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 5-кратную аффинность к hPD-L1. В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 6-кратную аффинность к hPD-L1. В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 8-кратную аффинность к hPD-L1. В одном варианте реализации, антитело или фрагмент связываются с PD-L1 яванского макака с аффинностью, не превышающей 10-кратную аффинность к hPD-L1.
В одном варианте реализации, антитело или фрагмент не связываются детектируемо с PD-L1 яванского макака. В одном варианте реализации, антитело или фрагмент не связываются детектируемо с мышиным PD-L1.
В одном варианте реализации, антитело или фрагмент связываются с мышиным PD-L1 с аффинностью менее 1 нМ (например, от 1 нМ до 0,01 пМ или от 1 нМ до 0,1 пМ или от 1 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с мышиным PD-L1 с аффинностью менее 10 нМ (например, от 10 нМ до 0,01 пМ или от 10 нМ до 0,1 пМ или от 10 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с мышиным PD-L1 с аффинностью менее 0,1 нМ (например, от 0,1 нМ до 0,01 пМ или от 0,1 нМ до 0,1 пМ или от 0,1 нМ до 1 пМ). В одном варианте реализации, антитело или фрагмент связываются с мышиным PD-L1 с аффинностью менее 0,01 нМ (например, от 0,011 нМ до 0,01 пМ или от 0,01 нМ до 0,1 пМ).
Концепция 28. Антитело или фрагмент согласно любой из предшествующих концепций, где антитело или фрагмент содержат легкую цепь каппа.
Аминокислотные и нуклеотидные последовательности константной области легкой цепи каппа представлены в SEQ ID NOs: 206-215.
В одном варианте реализации, легкая цепь может быть легкой цепью лямбда. Аминокислотные и нуклеотидные последовательности константного участка легкой цепи лямбда представлены в SEQ ID NOs: 216-237 и SEQ ID NO: 535, SEQ ID NO: 536 и SEQ ID NO: 538.
Концепция 29. Антитело или фрагмент согласно любой из концепций 9-28, где аминокислотные замещения представляют собой консервативные аминокислотные замещения, где, необязательно, консервативные заместители относятся к одной из шести групп (каждая группа, включает аминокислоты, являющиеся консервативными замещениями друг для друга), выбранных из:
1) аланин (А), серин (S), треонин (Т);
2) аспарагиновая кислота (D), глутаминовая кислота (Е);
3) аспарагин (N), глутамин (Q);
4) аргинин (R), лизин (K);
5) изолейцин (I), лейцин (L), метионин (М), валин (V); и
6) фенилаланин (F), тирозин (Y), триптофан (W).
Консервативные замены могут быть такими, как описано выше в концепции 9.
Концепция 30. Антитело или фрагмент согласно любой из предшествующих концепций, в которых антитело или фрагмент содержат константную область, такую как константная область человека, например, нуль-эффекторная (effector-null) константная область человека, например, константная область IgG4 или константная область IgG1, где, необязательно, константная область представляет собой IgG4-PE (SEQ ID NO: 199) или инактивированный IgG1, представленный SEQ ID NO: 205.
В других вариантах реализации, антитело или фрагмент представляют собой любые из изотипов или константных областей, как было определено выше. В одном варианте реализации, константная область представляет собой IgG1 человека дикого типа (SEQ ID NO: 340). Например, константная область представляет собой константную область IgG1 с активированным эффектором, необязательно, обладающую ADCC (опосредованная антителами клеточная цитотоксичность) и/или CDC (комплементзависимая цитотоксичность) активностью. В одном варианте реализации, константная область сконструирована для улучшения ADCC и/или CDC и/или ADCP (антителозависимый клеточно-опосредованный фагоцитоз). В другом варианте реализации, константная область модифицирована для улучшения эффекторной функции.
Константная область IgG4 может быть любой из аминокислотных последовательностей константной области IgG4, или может кодироваться любой из последовательностей нуклеиновой кислоты SEQ ID NOs: 192-203. Константной областью тяжелой цепи может быть IgG4, содержащий как мутацию Leu235Glu, так и мутацию Ser228Pro. Такая константная область тяжелой цепи IgG4-PE (SEQ ID NOs: 198, кодируемая SEQ ID NOs: 199, 200 и 201) является нуль-эффекторной.
Альтернативной нуль-эффекторной константной областью человека является инактивированный IgG1, представляющий собой аллель IgG1*01, содержащий мутации L235A и/или G237A (например, LAGA, SEQ ID NO: 204, кодируемый SEQ ID NO: 205). В одном варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, содержат константную область тяжелой цепи IgG1, где последовательность содержит аланин в положении 235 и/или 237 (нумерация по индексу EU).
Механизм антителозависимого клеточно-опосредованного фагоцитоза (ADCP) описан в  et al., "Antibody-Dependent Phagocytosis of Tumor Cells by Macrophages: A Potent Effector Mechanism of Monoclonal Antibody Therapy of Cancer", Cancer Res., 75(23), December 1, 2015.
et al., "Antibody-Dependent Phagocytosis of Tumor Cells by Macrophages: A Potent Effector Mechanism of Monoclonal Antibody Therapy of Cancer", Cancer Res., 75(23), December 1, 2015.
Действенность Fc-опосредованных эффектов может быть усилена путем модификации домена Fc различными установленными методами. Такие методы повышают аффинность к определенным Fc-рецепторам, тем самым создавая потенциальные разнообразные профили усиления активации. Такой результат может быть достигнут путем модификации одного или нескольких аминокислотных остатков (например, как описано в Lazar et al., 2006, Proc. Natl. Acad. Sci. U.S.A., Mar 14; 103(11):4005-10; раскрытые в этом документе модификации включены в данный документ посредством ссылок). Было показано, что константные области IgG1 человека, содержащие определенные мутации или имеющие измененное гликозилирование на остатке Asn297 (например, N297Q, нумерация по индексу EU), улучшают связывание с Fc-рецепторами. В одном варианте реализации, такие мутации касаются одного или нескольких остатков, выбранных из 239, 332 и 330, для константных областей IgG1 человека (или эквивалентных положений в других изотипах IgG). В одном варианте реализации, антитело или фрагмент содержат константную область IgG1 человека, имеющую одну или несколько мутаций, независимо выбранных из N297Q, S239D, I332E и A330L (нумерация по индексу EU).
В другом варианте реализации, увеличение аффинности к Fc-рецепторам достигается в результате изменения естественного профиля гликозилирования Fc-домена путем, например, генерации вариантов с пониженной степенью фукозилирования (under fucosylated) или дефукозилированных вариантов (как описано в Natsume et al., 2009, Drug Des Devel. Ther., 3:7-16, или Zhou Q., Biotechnol. Bioeng., 2008, Feb 15, 99 (3): 652-65, раскрытые в этих документах модификации включены в данный документ посредством ссылок). Нефукозилированные антитела содержат триманнозильную коровую структуру N-гликанов комплексного типа Fc без остатка фукозы. Эти антитела с модифицированной схемой гликозилирования, не содержащие корового остатка фукозы из N-гликанов Fc, могут проявлять более сильный ADCC, чем фукозилированные эквиваленты, из-за усиления связывающей способности FcγRIIIa. Например, для увеличения ADCC, остатки в области шарнира могут быть изменены для увеличения связывания с Fc-γRIII (см., например, Shields et al., 2001, J. Biol. Chem., Mar 2; 276(9):6591-604; раскрытые в этом документе модификации включены в данный документ посредством ссылок). Таким образом, в одном варианте реализации, антитело или фрагмент содержат константную область тяжелой цепи человеческого IgG, которая представляет собой вариант константной области тяжелой цепи человеческого IgG дикого типа, причем вариант константной области тяжелой цепи человеческого IgG связывается с человеческими рецепторами Fcγ, выбранными из группы, состоящей из FcγRIIB и FcγRIIA, с более высокой аффинностью, чем при связывании константной области тяжелой цепи человеческого IgG дикого типа с человеческими рецепторами Fcγ. В одном варианте реализации, антитело или фрагмент содержат константную область тяжелой цепи человеческого IgG, которая представляет собой вариант константной области тяжелой цепи человеческого IgG дикого типа, причем вариант константной области человеческого IgG человека связывается с FcγRIIB человека с большей аффинностью, чем при связывании константной области тяжелой цепи человеческого IgG дикого типа с человеческим FcγRIIB. В одном варианте реализации, вариант константной области тяжелой цепи IgG человека представляет собой вариант IgG1 человека, вариант IgG2 человека или вариант константной области тяжелой цепи человеческого IgG4. В одном варианте реализации, вариант константной области тяжелой цепи IgG человека содержит одну или несколько аминокислотных мутаций, выбранных из G236D, P238D, S239D, S267E, L328F и L328E (система нумерации по индексу EU). В другом варианте реализации, вариант константной области тяжелой цепи человеческого IgG содержит набор аминокислотных мутаций, выбранных из группы, состоящей из: S267E и L328F; P238D и L328E; P238D и одно или несколько замещений, выбранных из группы, состоящей из E233D, G237D, H268D, P271G и A330R; P238D, E233D, G237D, H268D, P271G и A330R; G236D и S267E; S239D и S267E; V262E, S267E и L328F; и V264E, S267E и L328F (система нумерации по индексу EU). В другом варианте реализации, вариант константной области тяжелой цепи человеческого IgG дополнительно содержит одну или несколько мутаций аминокислот, которые уменьшают аффинность IgG к FcγRIIIA человека, FcγRIIA человека или FcγRI человека. В одном варианте реализации, FcγRIIB экспрессируется на клетке, выбранной из группы, состоящей из макрофагов, моноцитов, В-клеток, дендритных клеток, эндотелиальных клеток и активированных Т-клеток. В одном варианте реализации, вариант константной области тяжелой цепи человеческого IgG содержит одну или несколько следующих аминокислотных мутаций G236A, S239D, F243L, Т256А, K290A, R292P, S298A, Y300L, V305I, A330L, I332E, Е333А, K334A, А339Т и P396L (система нумерации по индексу EU). В одном варианте реализации, вариант константной области тяжелой цепи человеческого IgG содержит набор аминокислотных мутаций, выбранных из группы, состоящей из: S239D; Т256А; K290A; S298A; I332E; Е333А; K334A; А339Т; S239D и I332E; S239D, A330L и I332E; S298A, Е333А и K334A; G236A, S239D и I332E; и F243L, R292P, Y300L, V305I и P396L (система нумерации по индексу EU). В одном варианте реализации, вариант константной области тяжелой цепи человеческого IgG содержит аминокислотные мутации S239D, A330L или I332E (система нумерации по индексу EU). В одном варианте реализации, вариант константной области тяжелой цепи человеческого IgG содержит аминокислотные мутации S239D и I332E (система нумерации по индексу EU). В одном варианте реализации, вариант константной области тяжелой цепи человеческого IgG представляет собой вариант константной области тяжелой цепи человека IgG1, содержащий аминокислотные мутации S239D и I332E (система нумерации по индексу EU). В одном варианте реализации, антитело или фрагмент содержат афукозилированную область Fc. В другом варианте реализации, антитело или его фрагмент являются дефукозилированными. В другом варианте реализации, антитело или фрагмент имеют пониженную степень фукозилирования.
В другом варианте реализации, раскрытые в данном документе антитела и фрагменты могут содержать тройную мутацию (M252Y/S254T/T256E), которая усиливает связывание с FcRn. См. Dall et al., Immunol 2002; 169: 5171-5180, обсуждение влияния мутаций со связыванием FcRn приведено в таблице 2, описанные в этом документе мутации включены в данный документ посредством ссылок.
В равной степени, усиление CDC может быть достигнуто за счет аминокислотных замен, которые увеличивают аффинность к C1q, первому компоненту классического каскада активации комплемента (см. Idusogie et al., J. Immunol., 2001, 166: 2571-2575; описанные модификации включены в данный документ посредством ссылок). Другой подход заключается в создании химерного домена Fc, созданного из сегментов человеческого IgG1 и человеческого IgG3, которые используют более высокую аффинность IgG3 к C1q (Natsume et al., 2008, Cancer Res., 68: 3863-3872; модификации включены в данный документ посредством ссылок). В другом варианте реализации, раскрытые в данном документе антитела или фрагменты антител могут содержать мутированные аминокислоты в остатках 329, 331 и/или 322 для изменения связывания C1q и/или снижения или уничтожения активности CDC. В другом варианте реализации, антитела или фрагменты антител, раскрытые в данном документе, могут содержать Fc-области с модификациями в остатках 231 и 239, в результате чего аминокислоты заменяют с целью изменения способности антитела фиксировать комплемент. В одном варианте реализации, антитело или фрагмент имеет константную область, содержащую одну или несколько мутаций, выбранных из E345K, E430G, R344D и D356R, в частности, двойную мутацию, содержащую R344D и D356R (система нумерации по индексу EU).
Антитело может иметь константную область тяжелой цепи, которая связывает один или несколько типов Fc-рецептора, но не индуцирует клеточные эффекторные функции, то есть, которая не опосредует активность ADCC, CDC или ADCP. Такая константная область может быть неспособна связывать специфический Fc-рецептор (рецепторы), ответственный за запуск активности ADCC, CDC или ADCP. Антитело может иметь константную область тяжелой цепи, которая не связывает рецепторы Fcγ. Таким образом, в одном варианте реализации, константная область может содержать мутацию Leu235Glu (система нумерации по индексу EU).
В другом варианте реализации, антитела и фрагменты, раскрытые в данном документе, модифицированы для увеличения или уменьшения периода полувыведения из сыворотки. В одном варианте реализации, вводят одну или несколько из следующих мутаций: T252L, T254S или T256F, для увеличения биологического периода полувыведения антитела. Биологический период полувыведения также может быть увеличен путем изменения домена CH1 константной области тяжелой цепи или области CL с целью введения эпитопа связывания рецептора реутилизации, взятого из двух петель домена СН2 Fc-области IgG, как описано в патентах США №№5869046 и 6121022, причем раскрытые в этом документе модификации включены в данный документ посредством ссылок. В другом варианте реализации, шарнирную область Fc антитела или антигенсвязывающего фрагмента по изобретению мутируют для уменьшения биологического периода полувыведения антитела или фрагмента. Одну или несколько аминокислотных мутаций вводят в область интерфейса домена СН2-СН3 фрагмента Fc-шарнира, так чтобы антитело или фрагмент имели нарушенное связывание со стафилококковым (Staphylococcyl) белком A (SpA) по сравнению со связыванием нативного SpA с шарнирным доменом Fc. Специалистам в данной области известны другие способы увеличения периода полувыведения из сыворотки. Так, в одном варианте реализации, антитело или фрагмент пегилируют. В другом варианте реализации, антитело или фрагмент сливают с альбуминсвязывающим (albumin-binding) доменом, например, альбуминсвязывающим однодоменным антителом (dAb). В другом варианте реализации, антитело или фрагмент ПАСилируют (PASylated) (т.е. проводят сплайсинг (genetic fusion) полипептидных последовательностей, состоящих из PAS (XL-Protein GmbH), которые образует незаряженные структуры неупорядоченных клубков с большим гидродинамическим объемом). В другом варианте реализации, антитело или фрагмент представляют собой XTENylated®/rPEGylated продукты (т.е. проводят сплайсинг пептидной последовательности с неточными повторами (Amunix, Versartis) с терапевтическим пептидом). В другом варианте реализации, антитело или фрагмент представляют собой ELPylated продукты (т.е. проводят сплайсинг с последовательностью с ELP (эластин-подобный полипептид)-повторами (PhaseBio)). Различные такие гибридные продукты, позволяющие увеличить периоды полувыведения, описаны более подробно в Strohl, BioDrugs (2015) 29: 215-239, и эти гибридные продукты, например, приведенные в таблицах 2 и 6, включены в данный документ посредством ссылок.
Антитело может иметь модифицированную константную область, которая повышает стабильность. Так, в одном варианте реализации, константная область тяжелой цепи содержит мутацию Ser228Pro. В другом варианте реализации, раскрытые в данном документе антитела и фрагменты содержат шарнирную область тяжелой цепи, модифицированную с целью изменения числа цистеиновых остатков. Эта модификация может быть использована для облегчения сборки легкой и тяжелой цепей или для повышения или снижения стабильности антитела.
Концепция 31. Антитело или фрагмент согласно концепции 30, где константная область представляет собой константную область мыши.
В других вариантах реализации, константная область может быть получена от любого млекопитающего, не являющегося человеком, например, крысы, мыши, хомяка, морской свинки, собаки, кошки, лошади, курицы, ламы, дромадера и т.д. В одном варианте реализации, константная область представляет собой константную область крысы. В другом варианте реализации, константная область является константной областью ламы. Константная область мыши может быть любым из изотипов или аллелей, описанных выше.
Концепция 32. Антитело или фрагмент согласно концепции 30 или концепции 31, где константная область обладает активностью CDC и/или ADCC.
Концепция 33. Антитело согласно любой из предшествующих концепций, в котором:
a) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
b) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 43;
c) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
d) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
e) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
f) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
g) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
h) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
i) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
j) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
k) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
l) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
m) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
n) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
о) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
p) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
q) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
r) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
s) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
t) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
u) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
v) домен VH содержит аминокислотную последовательность SEQ ID NO: 58, а домен VL содержит аминокислотную последовательность SEQ ID NO: 68;
w) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 58, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 68;
х) домен VH содержит аминокислотную последовательность SEQ ID NO: 78, а домен VL содержит аминокислотную последовательность SEQ ID NO: 88;
у) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 78, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 88;
z) домен VH содержит аминокислотную последовательность SEQ ID NO: 98, а домен VL содержит аминокислотную последовательность SEQ ID NO: 108;
аа) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 98, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 108;
bb) домен VH содержит аминокислотную последовательность SEQ ID NO: 118, а домен VL содержит аминокислотную последовательность SEQ ID NO: 128;
сс) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 118, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 128;
dd) домен VH содержит аминокислотную последовательность SEQ ID NO: 158, а домен VL содержит аминокислотную последовательность SEQ ID NO: 168;
ее) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 158, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 168;
ff) домен VH содержит аминокислотную последовательность SEQ ID NO: 178, а домен VL содержит аминокислотную последовательность SEQ ID NO: 188;
gg) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 178, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 188;
hh) домен VH содержит аминокислотную последовательность SEQ ID NO: 138, а домен VL содержит аминокислотную последовательность SEQ ID NO: 148;
ii) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 138, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 148;
jj) домен VH содержит аминокислотную последовательность SEQ ID NO: 244, а домен VL содержит аминокислотную последовательность SEQ ID NO: 254;
kk) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 244, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 254;
ll) домен VH содержит аминокислотную последовательность SEQ ID NO: 264, а домен VL содержит аминокислотную последовательность SEQ ID NO: 274;
mm) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 264, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 274;
nn) домен VH содержит аминокислотную последовательность SEQ ID NO: 284, а домен VL содержит аминокислотную последовательность SEQ ID NO: 294; и
оо) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 284, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 294;
pp) домен VH содержит аминокислотную последовательность SEQ ID NO: 349, а домен VL содержит аминокислотную последовательность SEQ ID NO: 359; и
qq) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 349, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 359. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Концепция 34. Антитело согласно любой из предшествующих концепций, где антитело содержит тяжелую цепь и легкую цепь, и
a) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
b) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 35, и аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 45;
c) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 47, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
d) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 48, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
e) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 49, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
f) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 342, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 45;
g) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
h) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 47, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
i) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 48, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
j) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 49, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
k) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 342, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
l) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
m) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 47, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
n) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 48, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
о) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 49, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
p) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 342, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 51;
q) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 35, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 298;
r) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 47, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 298;
s) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 48, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 298;
t) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 49, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 298;
u) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 342, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 298;
v) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 60, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 70;
w) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 60, и аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 70;
x) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 80, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 90;
у) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 80, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 90;
z) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 100, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 110;
aa) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 100, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 110;
bb) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 120, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 130;
cc) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 120, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 130;
dd) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 160, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 170;
ее) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 160, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 170;
ff) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 180, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 190;
gg) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 180, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 190
hh) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 140, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 150;
ii) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 140, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 150;
jj) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 246, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 256;
kk) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 246, и аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 256;
ll) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 266, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 276;
mm) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 266, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 276;
nn) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 286, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 296; и
oo) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 286, и аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 296;
pp) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 351, а аминокислотная последовательность легкой цепи содержит аминокислотную последовательность SEQ ID NO: 361; и
gg) аминокислотная последовательность тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 351, и аминокислотная последовательность легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 361, В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Концепция 35. Антитело или фрагмент согласно любой из предшествующих концепций, которые конкурируют за связывание с hPD-L1 с антителом 1D05, причем, необязательно, конкуренцию за связывание с hPD-L1 проводят с использованием метода SPR.
SPR может проводиться, как описано выше, или как описано в концепции 16.
Концепция 36. Антитело или фрагмент согласно любой из предшествующих концепций, в которых антитело или фрагмент способны ингибировать супрессию Т-клеток, опосредованное PD-L1, где, необязательно, супрессию Т-клеток измеряют по увеличению одного или нескольких показателей из IFNγ, IL-2, CD25 или пролиферации Т-клеток в анализе, обеспечивающем костимуляцию посредством прямой стимуляции CD3/CD28, стимуляции суперантигеном, или обеспечивающем костимуляцию путем совместной инкубации с клетками, способными индуцировать Т-клеточный ответ.
Измерения могут проводиться с использованием любой пригодной методики. Например, измерения могут проводиться с использованием ИФА, HTRF, включения BRDU (пролиферация), электрохемилюминесценции (ECL) или проточной цитометрии (например, FACS). Эти способы хорошо известны специалистам в данной области и описаны в других разделах данного документа. В одном варианте реализации, анализ представляет собой проточную цитометрию. В одном варианте реализации, анализ представляет собой ИФА. В одном варианте реализации, анализ представляет собой HTRF.
В одном варианте реализации, супрессию Т-клеток измеряется по увеличению IFNγ. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению IL-2. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению CD25. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению IFNγ и IL-2. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению IFNγ и CD25. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению CD25 и IL-2. В одном варианте реализации, супрессию Т-клеток измеряется по увеличению IFNγ, IL-2 и CD25.
В одном варианте реализации, костимуляция обеспечивается прямой стимуляцией CD3/CD28.
В одном варианте реализации, костимуляция обеспечивается суперантигеном, таким как стафилококковый энтеротоксин В (SEB).
В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с клетками, способными индуцировать Т-клеточный ответ. Такие клетки могут представлять собой антигенпредставляющие клетки (АПК), например, моноциты, В-клетки или дендритные клетки. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с АПК. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с моноцитами. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с В-клетками. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с дендритными клетками.
Концепция 37. Биспецифическое антитело или гибридный белок, содержащие антитело или его фрагмент, как определено в любой предшествующей концепции.
Концепция 37а. Антитело с двойным связыванием или гибридный белок, содержащий антитело или его фрагмент, как определено в любой предшествующей концепции.
Антитело с двойным связыванием имеет значение, указанное выше.
Концепция 38. Биспецифическое антитело согласно концепции 37, где биспецифический формат выбран из DVD-Ig, mAb2, FIT-Ig, mAb-dAb, dock and lock, SEEDbody, scDiabody (одноцепочечное диатело)-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело (intrabody), BiTE, диатело, DART, TandAb, scDiabody, scDiabody-СН3, Diabody-CH3, минитело, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, в частности, mAb2, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами и FIT-Ig, например, mAb2 и FIT-Ig.
В одном варианте реализации, биспецифический формат выбирают из DVD-Ig, mAb2, FIT-Ig, mAb-dAb, dock and lock, обмена Fab-плечо, SEEDbody, Triomab, LUZ-Y, Fcab, κλ-body, ортогонального Fab, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело, BiTE, диатело, DART, TandAb, scDiabody, scDiabody-CH3, Diabody-CH3, тройное антитело (Triple body), миниантитело, минитело, минитело TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2- scFv, scFv-KIH, Fab-scFv-Fc, тетравалентный HCab, ImmTAC, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H) IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig и zybody.
В одном варианте реализации, биспецифический формат выбирают из DVD-Ig, FIT-Ig, mAb-dAb, dock and lock, обмена Fab-плечо, SEEDbody, Triomab, LUZ-Y, Fcab, κλ-body, ортогонального Fab, scDiabody-Fc, диатело-Fc, тандема scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточного антитела, BiTE, диатела, DART, TandAb, scDiabody, scDiabody-CH3) диатело-СН3, тройного антитела, миниантитела, минитела, TriBi, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2-scFv, scFv-KIH, Fab-scFv-Fc, тетравалентного HCab, ImmTAC, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig и zybody, например, DVD-Ig, FIT-Ig, mAb-dAb, dock and lock, SEEDbody, scDiabody-Fc, диатела-Fc, тандема scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточного антитела, BiTE, диатела, DART, TandAb, scDiabody, scDiabody-CH3, Diabody-CH3, минитела, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженных пар, заряженных пар с общей легкой цепью, в частности, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с обычными цепями легкой цепи и зарядов и FIT-Ig, например, FIT-Ig.
В одном варианте реализации, биспецифический формат выбирают из DVD-Ig, mAb2, mAb-dAb, dock and lock, обмена Fab-плечо, тела SEED, Triomab, LUZ-Y, Fcab, κλ-body, ортогонального Fab, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутрибрюшинье, BiTE, диатела, DART, TandAb, scDiabody, scDiabody-CH3, Diabody-CH3, Тройной организм, миниантитело, минитело, TriBi минитело, scFv-CH3 KIH, scFv-CH-CL-scFv, F(ab')2- scFv, scFv-KIH, Fab-scFv-Fc, тетравалентный HCab, ImmTAC, knobs-in-holes, дырки с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig и zybody, например, DVD-Ig, mAb2, mAb-dAb, dock and lock, SEEDbody, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело, BiTE, диатело, DART, TandAb, scDiabody, scDi abody-CH3, Diabody-CH3, микроволны, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, в частности, mAb2, knobs-in-holes, knobs-in-holes с общей легкой цепью и заряженными парами, и knobs-in-holes с общей легкой цепью, например, mAb2.
В одном варианте реализации, биспецифический формат выбирают из DVD-Ig, mAb-dAb, dock and lock, обмена Fab-плечо, тела SEED, Triomab, LUZ-Y, Fcab, κλ-body, ортогонального Fab, scDiabody-Fc, diabody- Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутрибрюшинье, BiTE, диатело, DART, TandAb, scDiabody, scDiabody-CH3, Diabody-CH3, Тройной организм, миниантитело, минитело, TriBi минитело, scFv-СН3 KIH, scFv-CH-CL-scFv, F(ab')2- scFv, scFv-KIH, Fab-scFv-Fc, тетравалентный HCab, ImmTAC, knobs-in-holes, knobs-in-holes с общими легкая цепь, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, DT-IgG, DutaMab, IgG(H)-scFv, scFv-(H)IgG, IgG(L) (L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig и zybody, например, DVD-Ig, mAb-dAb, dock and lock, SEEDbody, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело, BiTE, диатело, DART, TandAb, scDiabody, scDiabody-CH3, Dia корпус-СН3, мини-отсек, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, в частности, knobs-in-holes, knobs-in-holes с общей легкой цепью и заряженными парами и knobs-in-holes с общей легкой цепью.
Концепция 39. Биспецифическое антитело согласно концепции 37 или концепции 38, где биспецифическое антитело специфически связывается с hPD-L1 и другим антигеном-мишенью, выбранным из ингибиторов иммунной контрольной точки (таких как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммуномодуляторов (таких как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CXCL11 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R), иммунных активаторов (таких как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические антитела против CXCR3), CD27, CD3, ICOS (например, агонистические антитела против ICOS), например, ICOS, CD137, GITR и ОХ40).
Концепция 39а. Биспецифическое антитело, связывающееся с hPD-L1, в котором VH, VL, или спаренные VH и VL содержат один или несколько CDR (например, CDRH3 и CDRL3) или последовательности вариабельной области любого из антител, описанных в Аспекте 1а ниже, и другим антигеном-мишенью, выбранным из ингибиторов иммунной контрольной точки (таких как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммуномодуляторов (таких как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CXCL11 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R), иммунных активаторов (таких как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические антитела против CXCR3), CD27, CD3, ICOS (например, агонистические антитела против ICOS). ICOS, CD137, GITR и ОХ40).
Концепция 39b. Биспецифическое антитело согласно концепции 37 или концепции 38, где биспецифическое антитело специфически связывается с hPD-L1 и другим антигеном-мишенью, выбранным из ингибиторов иммунной контрольной точки (таких как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммуномодуляторов (таких как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R), иммунных активаторов (таких как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические антитела против CXCR3), CD3, ICOS (например, агонистические анти-ICOS антитела), например, ICOS, CD137, GITR и ОХ40).
В одном варианте реализации, другим антигеном-мишенью является ингибитор иммунной контрольной точки, такой как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, CTLA-4, TIM-3 и LAG-3. В одном варианте реализации, другим антигеном-мишенью является иммунный модулятор, такой как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CXCL11 и CD155, или такой как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R. В одном варианте реализации, другим антигеном-мишенью является иммунный активатор, такой как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические анти-CXCR3 антитела), CD27, CD3 и ICOS (например, агонистические анти-ICOS антитела), или CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические анти-CXCR3 антитела), CD3 и ICOS (например, агонистические анти-ICOS антитела), например, ICOS, CD137, GITR и ОХ40). В одном варианте реализации, другим антигеном-мишенью является CTLA-4. В одном варианте реализации, другим антигеном-мишенью является TIGIT. В одном варианте реализации, другим антигеном-мишенью является TIM-3. В одном варианте реализации, другим антигеном-мишенью является LAG-3. В одном варианте реализации, другим антигеном-мишенью является GITR. В одном варианте реализации, другим антигеном-мишенью является VISTA. В одном варианте реализации, другим антигеном-мишенью является CD137. В одном варианте реализации, другим антигеном-мишенью является SIRPα. В одном варианте реализации, другим антигеном-мишенью является CXCL10. В одном варианте реализации, другим антигеном-мишенью является CD155. В одном варианте реализации, другим антигеном-мишенью является CD40.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой PD-1, и связывание с PD-1 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CTLA4, и связывание с CTLA4 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой TIGIT, и связывание с TIGIT обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой TIM-3, и связывание с TIM-3 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой LAG3, и связывание с LAG3 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой VISTA, и связывание с VISTA обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой BTLA, и связывание с BTLA обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой hHVEM, и связывание с hHVEM обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CSF1R, и связывание с CSF1R обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CCR4, и связывание с CCR4 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD39, и связывание с CD39 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD40, и связывание с CD40 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD73, и связывание с CD73 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD96, и связывание с CD96 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CXCR2, и связывание с CXCR2 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CXCR4, и связывание с CXCR4 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD200, и связывание с CD200 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой GARP, и связывание с GARP обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой SIRPα, и связывание с SIRPα обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CXCL9, и связывание с CXCL9 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CXCL10, и связывание с CXCL10 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD155, и связывание с CD155 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD137, и связывание с CD137 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой GITR, и связывание с GITR обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой ОХ40, и связывание с ОХ40 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD40, и связывание с CD40 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CXCR3, и связывание с CXCR3 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD27, и связывание с CD27 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой CD3, и связывание с CD3 обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в Аспекте 1А ниже.
В другом варианте реализации, биспецифическое антитело связывает другой антиген-мишень, представляющий собой ICOS, и связывание с ICOS обеспечивается антигенсвязывающим доменом (например, VH, VL или спаренными VH и VL), имеющим любую из последовательностей, включая последовательности CDR (например, CDRH3 и/или CDRL3) или последовательности вариабельных областей, как описано в схеме (arrangement) 5 и схеме 5а ниже, и любое из антител против ICOS, описанных в предложениях (sentences) 1-102, и предложениях 1а-21а.
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает GITR (необязательно, GITR Fab имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, СН1, СН2 и СН3), которое связывает GITR (необязательно, антитело к GITR имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключается эффектором (например, представляет собой формат IgG4, или как описано в любой из концепций 30-31).
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, СН1, СН2 и СН3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает ICOS (например, связывается с агонистической активностью и, необязательно, ICOS Fab имеет последовательность, включающую CDR и вариабельные области, как определено в схеме 5 или в схеме 5а, или в предложениях 1-102 или в предложениях 1а-21а ниже). В одном варианте реализации, ICOS Fab имеет последовательность любого из антител ICOS, описанных в данном документе в предложениях 1-102 или в предложениях 1а-21а). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который включает полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывает ICOS (например, связывается с агонистической активностью или необязательно, антитело ICOS имеет последовательность, включающую CDR и вариабельные области, как определено в схеме 5 или в схеме 5а, или в предложениях 1-102 или в предложениях 1а-21а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1А ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, СН1, СН2 и СН3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает TIM-3 (необязательно, TIM-3 Fab имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, СН1, СН2 и СН3), которое связывает TIM-3 (необязательно, антитело TIM-3 имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает CD137 (необязательно, CD137 Fab имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывается с CD137 (необязательно, антитело CD137 имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3) который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает CD3 (необязательно, CD3 Fab имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3) который связывает CD3 (необязательно, антитело CD3 имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
Любая из перечисленных выше мишеней (и Fab и/или полных антител, описанных более подробно в Аспекте 1А) может быть применена к структуре FIT-Ig.
Концепция 40. Биспецифическое антитело согласно концепции 39, где другим антигеном-мишенью является TIGIT или LAG3.
В любой из концепций 37-40, если антитело или его фрагмент имеют последовательности вариабельных областей тяжелой и легкой областей 84G09, то биспецифическое антитело должно рассматриваться как не включающее формат mAb2, где Fcab имеет аффинность связывания с LAG3.
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, CH2 и CH3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает TIGIT (необязательно, Fab TIGIT имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывается с TIGIT (необязательно, антитело TIGIT имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, CH2 и CH3), которое связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает LAG3 (необязательно, Fab LAG3 имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, биспецифическое антитело имеет формат FIT-Ig, который содержит полное антитело (например, антитело, содержащее легкую цепь, содержащую VL и CL, и тяжелую цепь, содержащую VH, CH1, СН2 и СН3), которое связывает LAG3 (необязательно, антитело LAG3 имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже), и Fab, который связывает hPD-L1 (необязательно, антитело имеет структуру, как определено в любой из концепций 1-40, или антитело имеет последовательность, включающую CDR и вариабельные области, как определено в Аспекте 1а ниже). В одном варианте реализации, FIT-Ig активируется эффектором (например, как описано в любой из концепций 30-32). В другом варианте реализации, FIT-Ig отключен эффектором (например, представляет собой формат IgG4, или является таким, как описано в любой из концепций 30 или 31).
Концепция 41. Антитело или фрагмент, как определено в любой предшествующей концепции для использования в лечении или профилактике опосредованного hPD-L1 заболевания или состояния, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные новообразования, таких как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома) (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Концепция 42. Использование антитела или фрагмента, как определено в любой из концепций 1-40, при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики опосредованного hPD-L1 заболевания или состояния у человека, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные виды рака (например, рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Концепция 43. Способ лечения или профилактики опосредованного hPD-L1 заболевания или состояния, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (таких как рак шейки матки и рак носоглотки) и саркомы мягких тканей), у человека, включающий введение указанному человеку терапевтически эффективного количества антитела или фрагмента, как определено в любой из концепций 1-40, в результате чего проводится лечение или профилактика опосредованного hPD-L1 заболевания или состояния.
В любой из концепций 41-43, опосредованное hPD-L1 заболевание может быть любым из описанных в данном документе. В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание является вирусно-индуцированным раковым заболеванием, таким как рак шейки матки и рак носоглотки, например, рак шейки матки, вызванный инфекцией ВПЧ (вирус папилломы человека). В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание представляет собой хроническую вирусную инфекцию. В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание является неопластическим заболеванием. В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание является не связанным с новообразованиями заболеванием. В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание является злокачественной опухолью. В одном из вариантов реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание представляет собой рак, который, как известно, реагирует на терапию PD-L1, такой как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома. В одном варианте реализации, в любой из концепций 41-43 опосредованное hPD-L1 заболевание представляет собой рак, который является саркомой мягких тканей.
Концепция 44. Антитело или фрагмент согласно концепции 41, использование согласно концепции 42, или способ согласно концепции 43, где заболевание или состояние, опосредованное hPD-L1, является раком.
Концепция 44а. Антитело или фрагмент согласно концепции 41, использование согласно концепции 42, или способ согласно концепции 43, где заболевание или состояние, опосредованное hPD-L1, является нейродегенеративным заболеванием, расстройством или состоянием, где, необязательно, нейродегенеративное заболевание, расстройство или состояние выбрано из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона, болезни Хантингтона, первичного прогрессирующего рассеянного склероза, вторичного прогрессирующего рассеянного склероза, кортикобазальной дегенерации, синдрома Ретта, расстройства дегенерации сетчатки, выбранного из возрастной макулярной дегенерации и пигментного ретинита; передней ишемической оптической нейропатии, глаукомы, увеита, депрессии, связанного с травмой стресса или посттравматического стрессового расстройства, лобно-височной деменции, деменций тела Леви, легких когнитивных нарушений, атрофии задней коры головного мозга, первичной прогрессирующей афазии и прогрессирующего супрануклеарного паралича или связанной с возрастом деменции, в частности, болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона и болезни Хантингтона и, например, болезни Альцгеймера.
В концепции 44а, терапевтически эффективное количество антитела или фрагмента может содержать антигенсвязывающий сайт, который специфически связывает PD-L1, например, hPD-L1.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает PD-L1, например, hPD-L1. В одном варианте реализации, антигенсвязывающий сайт PD-L1 содержит области CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или VH и VL, любого из антител против PD-L1, выбранных из атезолизумаба (Roche), авелумаба (Merck), BMS-936559/MDX-1105 (BMS), дурвалумаба/Medi4736 (Medimmune), KN-035, СА-170, FAZ-053 М7824, ABBV-368, LY-3300054, GNS-1480, YW243.55.S70, REGN3504 и любого из антител PD-L1, раскрытых в WO 2017/034916, WO 2017/020291, WO 2017/020858, WO 2017/020801, WO 2016/111645, WO 2016/197367, WO 2016/141101, WO 2016/000619, WO 2016/160792, WO 2016/022630, WO 2015/007235, WO 2015/179654, WO 2015/173267, WO 2000/181342, WO 2015/109124, WO 2015/112805, WO 2015/061668, WO 2014/159562, WO 2014/165082, WO 2014/100079, WO 2014/055897, WO 2013/181634, WO 2013/173223, WO 2013/079174, WO 2012/145493, WO 2011/066389, WO 2010/077634, WO 2010/036959, WO 2010/089411 или WO 2007/005874, причем указанные антитела и последовательности включены в данный документ посредством ссылок.
В другом варианте реализации концепции 44а, антигенсвязывающий сайт PD-L1 содержит область CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или VH и VL, любого из антител против PD-L1, выбранных из антитела против PD-L1, раскрытого в данном документе, в частности, клоны антител против PD-L1, раскрытых в концепциях 16а-161 и, более конкретно, клон 84G09 антитела против PD-L1.
В другом варианте реализации концепции 44а, антигенсвязывающий сайт PD-L1 содержит область CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или VH и VL, клона 84G09 анти-PD-L1 антитела, и опосредованное hPD-L1 заболевание или состояние представляет собой болезнь Альцгеймера.
Концепция 45. Антитело или фрагмент, применение или способ согласно концепции 44, где рак выбирают из меланомы, карциномы клеток Меркеля, немелкоклеточного рака легкого (плоскоклеточного и некемного), рака почки, рака мочевого пузыря, головы и карциномы шейки матки и мезотелиомы, или выбирают из вирусно-индуцированного рака (например, рака шейки матки и рака носоглотки) и саркомы мягких тканей.
Концепция 46. Антитело или фрагмент, использование или способ согласно любой из концепций 41-45, дополнительно включающие проведение для человека дополнительной терапии, например, введение дополнительного терапевтического агента, причем, необязательно, дополнительный терапевтическое средство независимо выбирают из группы, состоящей из:
a. других ингибиторов иммунных контрольных точек (таких как антитела против TIM-3, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
b. иммунных стимуляторов (таких как антитела против ОХ40, антитела против GITR, антитела против CD137, антитела против ICOS и антитела против CD40);
c. антагонистов хемокиновых рецепторов (таких как CXCR4, CCR4 и CXCR2);
d. таргетных ингибиторов киназ (таких как ингибиторы CSF-1R или VEGFR);
e. ингибиторов ангиогенеза (таких как анти-VEGF-A или дельта-подобный лиганд-4);
f. иммуностимулирующих пептидов или хемокинов (таких как CXCL9 или CXCL10);
g. цитокинов (таких как IL-15 и IL-21);
h. биспецифических антагонистов Т-клеток (BiTE), имеющих по меньшей мере одну специфичность против CD3 (например, CD3/CD19 BiTE);
i. других биспецифических молекул (например, IL-15-содержащих молекул, нацеленных на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (NY-ESO-1), GD2, EpCAM или ассоциированный с меланомой антиген-3 (MAGE-А3));
j. онколитических вирусов (таких как вирус HSV (вирус герпеса человека) (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины); к. вакцинации опухоль-ассоциированными антигенами (такими как рака пищевода New York Esophageal Cancer-1 [NY-ESO-1], ассоциированный с меланомой антиген-3 [MAGE-3]);
l. клеточных терапий (таких как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или антимезотелин);
m. биспецифические активаторы (engagers) NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a; и
n. адоптивного переноса опухолеспецифических Т-клеток или клеток LAK, или, необязательно, дополнительная терапия представляет собой химиотерапию, лучевую терапию и хирургическое удаление опухолей.
Лучевая терапия может проводиться с однократной дозой или дробными дозами, с облучением непосредственно пострадавших тканей либо всего организма.
Химиотерапевтические средства могут быть такими, как описано выше, в частности, агентами, индуцирующими иммуногенную гибель клеток, например, платиновыми терапиями, такими как оксалиплатин. В одном варианте реализации, химиотерапия является стандартом цитотоксической химиотерапии для лечения рака.
В этом аспекте, биспецифические молекулы включают «биспецифические антитела» и гибридные белки антител, включая форматы и молекулы, описанные в концепциях 37-40.
Антитела могут представлять собой любую из последовательностей или антител, описанных в схеме 5, 5а, или подробно описанных в Аспекте 1а.
Дополнительные терапевтические средства в этой концепции могут быть доставлены любым их способов, хорошо известных специалистам в данной области. Например, дополнительные терапевтические средства могут быть доставлены перорально, системно или местно (в среду опухоли). В одном варианте реализации, дополнительный терапевтическое средство доставляется перорально. В одном варианте реализации, дополнительный терапевтическое средство поставляется системно (например, внутривенно). В одном варианте реализации, дополнительный терапевтическое средство доставляется местно в среду опухоли.
Композиции и пути введения описаны более подробно ниже.
Концепция 47. Антитело или фрагмент, использование или способ согласно концепции 46, где дополнительный терапевтическое средство вводят последовательно или одновременно с анти-hPD-L1 антителом или фрагментом.
Концепция 48. Фармацевтическая композиция, содержащая антитело или фрагмент, как определено в любой из концепций 1-40, и фармацевтически приемлемый эксципиент, разбавитель или носитель и, необязательно, дополнительно содержащая дополнительный терапевтическое средство, независимо выбранный из группы, состоящей из:
a) других ингибиторов иммунных контрольных точек (таких как антитела против TIM-3, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
b) иммунных стимуляторов (таких как антитела против ОХ40, антитела против GITR, анти-С0137-антитела, анти-ICOS антитела и антитела против CD40);
c) антагонистов хемокиновых рецепторов (такие как CXCR4, CCR4 и CXCR2);
d) нацеленные ингибиторы киназы (такие как ингибиторы CSF-1R или VEGFR);
e) ингибиторы ангиогенеза (например, анти-VEGF-A или дельта-подобный лиганд-4);
f) иммуностимулирующие пептиды или хемокины (такие как CXCL9 или CXCL10);
g) цитокины (такие как IL-15 и IL-21);
h) биспецифические активаторы Т-клеток (BiTE), имеющие по меньшей мере одну специфичность против CD3 (например, BiTE CD3/CD19);
i) другие биспецифические молекулы (например, IL-15-содержащие молекулы, нацеленные на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (плоскоклеточная карцинома пищевода, Нью-Йорк-1) (NY-ESO-1), GD2, ЕрСАМ или ассоциированный с меланомой антиген-3 (MAGE-A3));
j) онколитические вирусы (такие как вирус HSV (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины);
k) вакцинация ассоциированными с опухолью антигенами (такими как плоскоклеточной карциномы пищевода, Нью-Йорк-1 [NY-ESO-1], связанный с меланомой антиген-3 [MAGE-3]);
l) клеточные методы лечения (такие как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или анти-мезотелиновые антитела);
m) биспецифические активаторы NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a; и
n) адоптивный перенос опухолеспецифических Т-клеток или клеток LAK. Фармацевтические композиции хорошо известны специалистам в данной области. В одном варианте реализации, антитело или фрагмент вводят внутривенно. В одном варианте реализации, антитело или фрагмент вводят подкожно.
В одном примере, антитело или фрагмент, раскрытые в данном документе, содержатся в медицинском контейнере, например, флаконе, шприце, контейнере для внутривенного введения (IV) или инъекционном устройстве (таком как интраокулярное или интравитреальное инъекционное устройство). В примере, антитело или фрагмент находятся in vitro, например, в стерильном контейнере.
В одном варианте реализации, композиция составлена в соответствии с обычными процедурами в виде фармацевтической композиции, адаптированной для внутривенного введения людям. Как правило, композиции для внутривенного введения представляют собой растворы в стерильном изотоническом водном буфере. При необходимости, композиция может также включать солюбилизирующий агент и местный анестетик, такой как лигнокаин (lignocamne), для облегчения боли в месте инъекции. Однако, такие композиции можно вводить путем, отличным от внутривенного.
Как правило, ингредиенты композиций либо поставляются отдельно, либо смешиваются вместе в стандартной дозированной форме, например, в виде сухого лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, таком как ампула или саше, с указанием количества активного агента. В тех случаях, когда композиция должна вводиться путем инфузии, она может дозироваться из инфузионной бутылки, содержащей стерильную воду или физиологический раствор для фармацевтического применения. Когда композицию вводят путем инъекции, может быть предусмотрена ампула стерильной воды для инъекций или физиологического раствора, так чтобы ингредиенты могли быть смешаны перед введением.
В этом аспекте, биспецифические молекулы включают «биспецифические антитела» и гибридные белки антител, включая форматы и молекулы, описанные в концепциях 37-40.
Дополнительные терапевтические средства в этой концепции могут быть доставлены любым их способов, хорошо известных специалистам в данной области. Например, дополнительные терапевтические средства могут быть доставлены перорально, системно или местно (в среду опухоли). В одном варианте реализации, дополнительный терапевтическое средство доставляется перорально. В одном варианте реализации, дополнительный терапевтическое средство поставляется системно (например, внутривенно). В одном варианте реализации, дополнительный терапевтическое средство доставляется местно в среду опухоли.
Антитела могут иметь любую из последовательностей, или могут быть любыми из антител, описанных в схеме 5, 5а, или подробно описанных в Аспекте 1а.
Концепция 49. Фармацевтическая композиция согласно концепции 48 или набор, включающий фармацевтическую композицию, как определено в концепции 48, где композиция предназначена для лечения и/или профилактики опосредованного hPD-L1 состояния или заболевания, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (например, рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная В-клеточная лимфома.
Концепция 50. Фармацевтическая композиция согласно концепции 48 или концепции 49 в комбинации с, или набор согласно концепции 49, содержащие этикетку или инструкции по использованию для лечения и/или профилактики указанного заболевания или состояния у человека; где, необязательно, этикетка или инструкции содержат номер регистрационного удостоверения лекарственного средства (например, регистрационный номер FDA или ЕМА); где, необязательно, набор включает устройство для внутривенного введения (IV) или инъекционное устройство, содержащее антитело или фрагмент.
Концепция 51. Способ модуляции взаимодействия PD-1/PD-L1 у пациента, включающий введение эффективного количества антитела или фрагмента, как определено в любой из концепций 1-40, указанному пациенту.
В другом варианте реализации, предлагается способ модуляции взаимодействия CD80/PD-L1 у пациента, включающий введение эффективного количества антитела или фрагмента, как определено в любой из концепций 1-40, указанному пациенту. В другом варианте реализации, антитело или фрагмент модулируют взаимодействие CD80/PD-L1, но не модулируют взаимодействие PD-1/PD-L1. В другом варианте реализации, антитело или фрагмент блокируют взаимодействие CD80/PD-L1, но не блокируют взаимодействие PD-1/PD-L1. В другом варианте реализации, антитело или фрагмент ингибируют взаимодействие CD80/PD-L1, но не ингибируют взаимодействие PD-1/PD-L1.
Концепция 52. Способ ингибирования активности PD-L1 у пациента, включающий введение эффективного количества антитела или фрагмента, как определено в любой из концепций 1-40, указанному пациенту.
В одном варианте реализации, антитело или фрагмент блокируют или ингибируют связывание PD-1 с PD-L1. В одном варианте реализации, антитело или фрагмент блокируют или ингибируют связывание CD80 с PD-L1.
Концепция 53. Способ лечения пролиферативного заболевания у животного (например, человека), включающий введение эффективного количества антитела или фрагмента, как определено в любой из концепций 1-40, указанному пациенту.
Пролиферативные заболевания могут быть любыми из описанных в других разделах данного документа.
Концепция 54. Способ детектирования экспрессии PD-L1 в образце, включающий введение в контакт образца с антителом или фрагментом, как определено в любой из концепций 1-40.
Концепция 55. Способ, включающий введение в контакт биологического образца с антителом или фрагментом, как определено в любой из концепций 1-40, с образованием комплекса с PD-L1, присутствующим в образце, и измерение присутствия, отсутствия или уровня содержания комплекса в биологическом образце.
Концепция 56. Способ согласно концепции 55, в котором присутствие, отсутствие и/или уровень экспрессии PD-L1 детектируется до начала лечения, а высокий уровень экспрессируемого на поверхности PD-L1 свидетельствует об успешном лечении.
Концепция 57. Способ согласно концепции 55, где присутствие, отсутствие и/или уровень экспрессии PD-L1 детектируют во время лечения в качестве биомаркера раннего ответа.
Концепция 58. Способ согласно концепции 55 или концепции 57, в котором присутствие, отсутствие и/или уровень экспрессии PD-L1 детектируют во время или после лечения, чтобы помочь определить один или несколько показателей из следующих: было ли лечение успешным, следует ли продолжать лечение, и/или следует ли модифицировать лечение.
Концепция 59. Способ по любой из концепций 55-58, где терапия включает проведение лечения анти-PD-LI антителом, необязательно, как определено в любой из концепций 1-40.
Концепция 60. Способ контроля эффективности терапии, включающий детектирование экспрессии поверхностно экспрессируемого PD-L1 у пациента до терапии и во время или после терапии, в котором антитело или фрагмент, как определено в любой из концепций 1-40, используют для детектирования экспрессии поверхностно экспрессируемого PD-L1.
Концепция 61. Способ согласно концепции 60, в котором поверхностно экспрессируемый PD-L1 детектируется in vivo.
Концепция 62. Способ согласно концепции 60, в котором поверхностно экспрессируемый PD-L1 детектируется в образце ткани in vitro.
Концепция 63. Способ идентификации связывающих партнеров для PD-L1, включающий иммунопреципитацию интактного белкового комплекса, содержащего PD-L1, с использованием антитела или фрагмента, как определено в любой из концепций 1-40.
Концепция 64. Способ диагностики у человека заболевания, связанного с измененной экспрессией PD-L1, включающий стадии введения в контакт биологического образца человека с антителом, как определено в концепциях 1-40, с образованием комплекса между антителом и PD-L1, присутствующим в образце; и детектирование количества комплекса.
Концепция 65. Нуклеиновая кислота, кодирующая CDRH3 антитела или фрагмента, как определено в любой из концепций 1-40.
Концепция 65а. Также предусматривается нуклеиновая кислота, кодирующая CDRH2 антитела или фрагмента, как определено в любой из концепций 1-40. Концепция 65b. Также предусматривается нуклеиновая кислота, кодирующая CDRH1 антитела или фрагмента, как определено в любой из концепций 1-40. Концепция 65 с. Также предусматривается нуклеиновая кислота, кодирующая CDRL1 антитела или фрагмента, как определено в любой из концепций 1-40.
Концепция 65d. Также предусматривается нуклеиновая кислота, кодирующая CDRL2 антитела или фрагмента, как определено в любой из концепций 1-40. Концепция 65е. Также предусматривается нуклеиновая кислота, кодирующая CDRL3 антитела или фрагмента, как определено в любой из концепций 1-40.
В одном варианте реализации, нуклеиновая кислота представляет собой выделенную и очищенную нуклеиновую кислоту.
Концепция 66. Нуклеиновая кислота, кодирующая домен VH и/или домен VL антитела или фрагмента, как определено в любой из концепций 1-40.
Последовательности нуклеиновых кислот доменов VH и VL по изобретению приведены в перечне последовательностей. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 70% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 75% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 95% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты, по меньшей мере, на 96% идентична указанному ID-идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 97% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 98% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 99% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 99,5%, идентична указанному идентификатору SEQ ID No.
Концепция 67. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 36 и/или SEQ ID NO: 46.
Концепция 67а. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 16 и/или SEQ ID NO: 26.
Концепция 67b. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 61 и/или SEQ ID NO: 71.
Концепция 67с. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 81 и/или SEQ ID NO: 91.
Концепция 67d. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 101 и/или SEQ ID NO: 111.
Концепция 67е. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 121 и/или SEQ ID NO: 131.
Концепция 67f. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 161 и/или SEQ ID NO: 171.
Концепция 67g. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 181 и/или SEQ ID NO: 191.
Концепция 67h. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 141 и/или SEQ ID NO: 151.
Концепция 67i. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 247 и/или SEQ ID NO: 257.
Концепция 67j. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 267 и/или SEQ ID NO: 277.
Концепция 67k. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 287 и/или SEQ ID NO: 297.
Концепция 67l. Нуклеиновая кислота согласно концепции 66, содержащая нуклеотидную последовательность, которая по меньшей мере на 80% идентична последовательности SEQ ID NO: 352 и/или SEQ ID NO: 362.
В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 70% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 75% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 95% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты, по меньшей мере, на 96% идентична указанному ID-идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 97% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 98% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 99% идентична указанному идентификатору SEQ ID No. В одном варианте реализации, последовательность нуклеиновой кислоты по меньшей мере на 99,5%, идентична указанному идентификатору SEQ ID No.
Концепция 68. Нуклеиновая кислота, кодирующая тяжелую цепь или легкую цепь антитела, как определено в любой из концепций 1-40.
Концепция 69. Вектор, содержащий нуклеиновую кислоту согласно любой из концепций 65-68; где вектор, необязательно, представляет собой вектор СНО или HEK293.
Концепция 70. Хозяин, содержащий нуклеиновую кислоту согласно любой из концепций 65-68 или вектор согласно концепции 69.
3. Иммуноцитокины
Изобретатели описали иммуноцитокины, которые содержат антитело, связывающееся с ингибитором иммунной контрольной точки, таким как PD-L1, слитый с N-концом или С-концом тяжелой цепи или легкой цепи (например, С-концом тяжелой или легкой цепь, и в частности, легкой цепи). Иммуноцитокины содержат молекулу цитокина, которая может быть IL-2 или его вариантом (включая вариант, имеющий делецию от 1 до 10 аминокислот на N-конце). Описанные выше антитела могут быть использованы в любом иммуноцитокине, описанном в данном документе.
Без ограничения теорией, иммуноцитокины по изобретению могут обеспечивать одно или несколько из следующих преимуществ:
• синергетическая активность (в силу терапевтической активности фрагмента Fab антитела в комбинации с цитокином)
• улучшенное нацеливание на опухоль
• способность сохранять эффекторные функции, такие как CDC, ADCC и/или ADCP
• уменьшенное воздействие за пределами мишени
• пониженная токсичность (например, по сравнению с свободным цитокином или цитокином, слитым с тяжелой цепью иммуноцитокина)
• пониженная иммуногенность
• более низкая доза/частота дозирования, в частности, из-за улучшенного периода полувыведения продуктов слияния цитокинов с легкой цепью по сравнению с эквивалентными продуктами слияния с тяжелыми цепями
• Специфичность к блокированию только одним из лигандов PD-L1 (например, блокирует взаимодействие CD80/PD-L1, но не взаимодействие PD-1/PD-L1)
• Растворимость
• Стабильность
• Простота составления композиции
• Частота дозирования и/или пути введения
• Технологичность (например, экспрессия, простота очистки, изоформы)
1D05 ICK содержит аминокислотную последовательность тяжелой цепи SEQ ID NO: 299 и аминокислотную последовательность легкой цепи SEQ ID NO: 300. Легкая цепь содержит домен VL, содержащий CDR, и последовательность VL антитела 1D05, как описано выше, слитую в тяжелой цепи с полноразмерным человеческим цитокином IL-2 дикого типа. Он не содержит линкерного пептида. Тяжелая цепь содержит домен VH, содержащий CDR, и последовательность VH антитела 1D05, как описанно выше, слитую с инактивированной константной областью IgG (SEQ ID NO: 205).
1D05 D5-9 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D5-9 IL-2 (SEQ ID NO: 303), которая непосредственно слита с аминокислотами 21-133 hlL-2 (SEQ ID NO:324).
1D05 D1-9 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-9 IL-2 (SEQ ID NO: 304), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D5-7 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID N0:33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D5-7 IL-2 (SEQ ID NO: 305), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1 IL-2 (SEQ ID NO: 306), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-2 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-2 IL-2 (SEQ ID NO: 307), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-3 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-3 IL-2 (SEQ ID NO: 308), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-4 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-4 IL-2 (SEQ ID NO: 309), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-5 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-5 IL-2 (SEQ ID NO: 310), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-6 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-6 IL-2 (SEQ ID NO: 311), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-7 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-7 IL-2 (SEQ ID NO: 312), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D1-8 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-8 IL-2 (SEQ ID NO: 313), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9 IL-2 (SEQ ID NO: 314), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-8 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-8 IL-2 (SEQ ID NO: 315), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-7 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-7 IL-2 (SEQ ID NO: 316), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-6 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-6 IL-2 (SEQ ID NO: 317), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-4 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-4 IL-2 (SEQ ID NO: 318), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-3 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-3 IL-2 (SEQ ID NO: 319), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D9-2 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-2 IL-2 (SEQ ID NO: 320), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D2-6 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D2-6 IL-2 (SEQ ID NO: 321), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D3-7 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D3-7 IL-2 (SEQ ID NO: 322), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
1D05 D4-8 ICK содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 33 (содержащую CDR 1D05, как описано выше), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D4-8 IL-2 (SEQ ID NO: 323), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
В любом из конструктов ICK, описанных выше, связывающий участок IL-2 может быть вариантом IL-2, в частности, IL-2, имеющим мутацию R38A (как описано в аминокислотах 21-133 варианта IL-2, описанного как SEQ ID NO: 517) или мутацию R38Q (как описано в аминокислотах 21-133 варианта IL-2, описанного как SEQ ID NO: 518).
В любом из вышеописанных конструктов ICK область VH антитела 1D05 может быть заменена на область VH мутированного 1D05 - мутант тяжелой цепи 1 (SEQ ID NO: 47), мутированного 1D05 - мутант тяжелой цепи 2 (SEQ ID NO: 48), мутированного 1D05 - мутант тяжелой цепи 3 (SEQ ID NO: 49) или мутированного 1D05 - мутант тяжелой цепи 4 (SEQ ID NO: 342). Предпочтительной мутированной областью VH тяжелой цепи 1D05 является мутированный 1D05 - мутант тяжелой цепи 4 (SEQ ID NO: 342).
Таким образом, некоторые конструкты ICK включают:
Мутированный 1D05 - мутант тяжелой цепи 4 D5-9 ICK, который содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 342 (содержащую CDR мутированного 1D05 - мутанта тяжелой цепи 4, как описано в данном документе), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D5-9 IL-2 (SEQ ID NO: 303), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
Мутированный 1D05 - мутант тяжелой цепи 4 D1-9 ICK, который содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 342 (содержащую CDR мутированного 1D05 - мутанта тяжелой цепи 4, как описано в данном документе), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-9 IL-2 (SEQ ID NO: 304), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
Мутированный 1D05 - мутант тяжелой цепи 4 D1-8 ICK, который содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 342 (содержащую CDR мутированного 1D05 - мутанта тяжелой цепи 4, как описано в данном документе), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D1-8 IL-2 (SEQ ID NO: 313), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
Мутированный 1D05 - мутант тяжелой цепи 4 D9-7 ICK, который содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 342 (содержащую CDR мутантного мутанта 4D55 с тяжелой цепью, как описано в данном документе), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-7 IL-2 (SEQ ID NO: 316), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
Мутированный 1D05 - мутант тяжелой цепи 4 D9-2 ICK, который содержит тяжелую цепь, содержащую аминокислотную последовательность области VH SEQ ID NO: 342 (содержащую CDR мутированного 1D05 - мутанта тяжелой цепи 4, как описано в данном документе), слитую с инактивированной константной областью IgG1 с аминокислотной последовательностью SEQ ID NO: 205. Легкая цепь содержит аминокислотную последовательность VL SEQ ID NO: 43 (содержащую CDR 1D05, как описано выше), непосредственно слитую на С-конце с D9-2 IL-2 (SEQ ID NO: 320), которая непосредственно слита с аминокислотами 21-133 hIL-2 (SEQ ID NO: 324).
В любом из вышеописанных конструктов ICK, область VL антитела 1D05 может быть заменена на область VL мутированного 1D05 - мутанта легкой цепи 1 (SEQ ID NO: 50), мутированного 1D05 - мутанта легкой цепи 2 (SEQ ID NO: 51) или мутированного 1D05 - мутанта легкой цепи 3 (SEQ ID NO: 298).
В любом из конструктов ICK, описанных выше, обе области VH и VL антитела 1D05 могут быть заменены на две области VH и VL любого из других антител, описанных в данном документе, т.е. 84G09, 411В08, 411С04, 411D07, 385F01, 413D08, 386Н03, 389А03, 413G05, 413F09 и 414В06.
В любом из конструктов ICK, описанных выше, константная область тяжелой цепи SEQ ID NO: 205 может быть заменена на любую из константных областей тяжелой цепи SEQ ID NOs: 193, 195, 197, 199, 203, 205, 340, 524, 526, 528, 530, 532 или 534.
Иммуноцитокины могут быть описаны в приведенных ниже предложениях или аспектах. Если не оговорено иное, признаки любой из концепций, описанных выше, являются применимыми mutatis mutandis к любому из приведенных ниже аспектов.
Аспект 1. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1, представленным SEQ ID No: 1, и конкурирует за связывание с указанным hPD-L1 с антителом 1D05; и
иммуноцитокин содержит домен VH, который содержит CDRH3, содержащий мотив X1GSGX2YGX3X4FD, где Х1, Х2 и Х3 независимо обозначают любую аминокислоту, и Х4 присутствует или отсутствует и, в случае его присутствия, может обозначать любую аминокислоту.
В описанных в данном документе аспектах, последовательности CDR могут быть определены в соответствии с любым способом, известным специалистам в данной области, таким как использование системы Кабата (Кабат), метода IMGT или метода Чотиа (Chothia), каждый из которых описан более подробно в данном документе. В одном варианте реализации, области CDR представляют собой области CDR человека.
В дополнение к областям CDR, домены VH и/или VL могут дополнительно содержать каркасные области, такие как FW1, FW2 и FW3. Домены VH и/или VL могут иметь любое происхождение, описанное в данном документе, и могут быть, например, полностью человеческими, гуманизированными, мышиными или верблюжьими. В одном варианте реализации, домены VH и/или VL являются доменами VH и/или VL человека. CDR могут иметь нечеловеческое происхождение (например, мышиное происхождение) и быть пересажены в каркасные области человека. В другом варианте реализации, CDR являются синтетическими.
В другом варианте реализации, области VH могут быть выбраны из группы, состоящей из вариабельного домена антитела (например, VL или VH, вариабельного домена антитела (antibody single variable domain) (доменного антитела или dAb), вариабельного домена Vhh верблюжьего антитела, вариабельного домена акульего иммуноглобулина (NARV), нанотела (Nanobody™) или вариабельного домена камелизированного VH); связывающего домена рецептора Т-клеток; домена суперсемейства иммуноглобулина; вариабельного лимфоцитарного рецептора бесчелюстных (agnathan); домена фибронектина (например, аднектин (Adnectin™)); константного домена антитела (например, домена СН3, например, СН2 и/или СН3 Fcab™), где константный домен не является функциональным доменом СН1; scFv; (scFv)2; одноцепочечного диатела (sc-diabody); scFab; центирина и эпитопсвязывающего домена, полученных из каркаса, выбранного из CTLA-4 (Evibody™); липокалинового домена; белка А, такого как Z-домен белка А (например, Affibody™ или SpA); А-домена (например, Avimer™ или Maxibody™); белка теплового шока (такого как эпитопсвязывающий домен, полученный из GroEI и GroES); трансферринового домена (например, trans-body); белка с анкириновым повтором (например, DARPin™); пептидного аптамера; лектинового домена С-типа (например, тетранектина (Tetranectin™)); человеческого γ-кристаллина или убиквитина человека (аффилина); домена PDZ; токсина скорпиона; и домена Кунитц-типа ингибитора протеазы человека.
Константная область содержит по меньшей мере два домена константной области тяжелой цепи, выбранных из CH1, СН2, СН3 и СН4. В одном варианте реализации, константная область содержит (или состоит из) домена CH1 и домена СН2. В одном варианте реализации, константная область содержит (или состоит из) домена CH1, шарнирной области и домена СН2. В одном варианте реализации, константная область содержит (или состоит из) домена CH1 и домена СН3 и, необязательно, шарнирной области. В одном варианте реализации, константная область содержит (или состоит из) домена CH1 и домена СН4 и, необязательно, шарнирной области. В одном варианте реализации, константная область содержит (или состоит из) домена CH1, домена СН2 и домена СН3 и, необязательно, шарнирной области. В одном варианте реализации, константная область содержит (или состоит из) домена CH1, домена СН2 и домена СН4 и, необязательно, шарнирной области. В одном варианте реализации, константная область содержит (или состоит из) домена CH1, домена СН3 и домена СН4 и, необязательно, шарнирной области. В одном варианте реализации, константная область содержит (или состоит из) полной константной области.
Константная область может принадлежать к любому изотипу, описанному в данном документе, например, IgA, IgD, IgE, IgG и IgM. В одном варианте реализации, константная область имеет любое происхождение, описанное в данном документе, и может быть, например, человеческой, мышиной или верблюжьей. В одном варианте реализации, константная область является (полной) константной областью человека. В одном варианте реализации, константная область представляет собой константную область IgG человека. В одном варианте реализации, константная область является (полной) константной областью IgG1 человека. В одном варианте реализации, константная область представляет собой нуль-эффекторную (полную) константную область IgG1 человека. В одном варианте реализации, константная область имеет активность CDC и/или ADCC и/или ADCP. В одном варианте реализации, константная область генетически модифицирована для усиления активности CDC и/или ADCC и/или ADCP. Константная область может быть любой из константных областей, описанных в концепциях 30-32 выше.
Константная область легкой цепи может быть константной областью каппа- или лямбда-легкой цепи. Константная область легкой цепи может быть такой, как описано в концепции 28 выше.
Цитокин IL-2 представляет собой молекулу цитокина, которая придает активность IL-2 одному или обоим из рецептора IL-2 с промежуточной ааффинностью (αβ) и высокоаффинного рецептора IL-2 (αβγ). Цитокин IL-2 включает варианты цитокинов IL-2. Цитокин IL-2 может иметь человеческое или нечеловеческое происхождение, например, принадлежать млекопитающему, не являющемуся человеком, включая, без ограничений, приматов (например, обезьян, таких как макак-резус или яванский макак), грызунов (таких как мыши, крысы и морские свинки) сельскохозяйственных животных (таких как крупный рогатый скот, овцы, свиньи, козы, лошади, куры, индюки, утки и гуси) и домашних млекопитающих (таких как собаки и кошки). В одном варианте реализации, цитокин IL-2 представляет собой человеческий цитокин IL-2.
В используемом в данном документе значении, термин «вариант IL-2 цитокин» обозначает цитокин, имеющий делецию до 10 аминокислот из N-концевой последовательности, в сочетании с замещениями до 5 аминокислот, делециями или вставками в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 5 (например, 1, 2, 3, 4 или 5) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 15 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 5 (например, 1, 2, 3, 4 или 5) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 5 (например, 1, 2, 3, 4 или 5) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с 1 аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 9 (например, 1, 2, 3, 4, 5, 6, 7, 8 или 9) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 9 (например, 1, 2, 3, 4, 5, 6, 7, 8 или 9) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 9 (например, 1, 2, 3, 4, 5, 6, 7, 8 или 9) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 9 (например, 1, 2, 3, 4, 5, 6, 7, 8 или 9) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 8 (например, 1, 2, 3, 4, 5, 6, 7 или 8) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 8 (например, 1, 2, 3, 4, 5, 6, 7 или 8) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 8 (например, 1, 2, 3, 4, 5, 6, 7 или 8) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 8 (например, 1, 2, 3, 4, 5, 6, 7 или 8) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 7 (например, 1, 2, 3, 4, 5, 6 или 7) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 7 (например, 1, 2, 3, 4, 5, 6 или 7) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 7 (например, 1, 2, 3, 4, 5, 6 или 7) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 7 (например, 1, 2, 3, 4, 5, 6 или 7) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 6 (например, 1, 2, 3, 4, 5 или 6) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 6 (например, 1, 2, 3, 4, 5 или 6) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 6 (например, 1, 2, 3, 4, 5 или 6) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 5 (например, 1, 2, 3, 4 или 5) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 5 (например, 1, 2, 3, 4 или 5) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 5 (например, 1, 2, 3, 4 или 5) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 6 (например, 1, 2, 3, 4, 5 или 6) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 4 (например, 1, 2, 3 или 4) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 4 (например, 1, 2, 3 или 4) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 4 (например, 1, 2, 3 или 4) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 4 (например, 1, 2, 3 или 4) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 3 (например, 1, 2 или 3) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в комбинации с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 3 (например, 1, 2 или 3) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в комбинации с до 3 (например 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 3 (например, 1, 2 или 3) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в комбинации с до 2 (например 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) до 3 (например, 1, 2 или 3) делеций аминокислот в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) 1 или 2 аминокислотных делеций в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 4 (например, 1, 2, 3 или 4) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) 1 или 2 аминокислотных делеций в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 3 (например, 1, 2 или 3) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) 1 или 2 аминокислотных делеций в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа) в сочетании с до 2 (например, 1 или 2) аминокислотных замещений в других местах цитокина IL-2. В одном варианте реализации, вариант цитокина IL-2 содержит (или состоит из) 1 или 2 аминокислотных делеций в N-концевой последовательности (например, в пределах первых 20, или первых 15, или первых 10 аминокислот рассматриваемой последовательности IL-2 дикого типа), в сочетании с одним аминокислотным замещением в другом месте цитокина IL-2.
Замещения в других местах цитокина IL-2 дополнительно определены в аспекте 44 ниже.
Конкретные цитокины IL-2 и варианты цитокинов IL-2 дополнительно определены в аспектах 40-45 ниже.
Аминокислотная последовательность α-цепи IL-2 человека представлена в SEQ ID NO: 327. Аминокислотная последовательность β-цепи IL-2 человека представлена в SEQ ID NO: 328. Аминокислотная последовательность γ-цепи IL-2 человека представлена в SEQ ID NO: 239.
В любых аспектах или концепциях данного документа, иммуноцитокин или анти-PDL1 антитело или фрагмент могут иметь период полувыведения, составляющий по меньшей мере 4 часа, 5 часов, 6 часов, 7 часов или 8 часов. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 9 часов, или по меньшей мере 10 часов, или по меньшей мере 11 часов, или по меньшей мере 12 часов. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 13 часов, или по меньшей мере 14 часов, или по меньшей мере 15 часов, или по меньшей мере 16 часов. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 17 часов, или по меньшей мере 18 часов, или по меньшей мере 19 часов, или по меньшей мере 20 часов. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 21 час или, по меньшей мере, 22 часа или по меньшей мере 23 часа или по меньшей мере 24 часа. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 25 часов, или по меньшей мере 26 часов, или по меньшей мере 27 часов, или по меньшей мере 30 часов. В другом варианте реализации, период полувыведения любого из иммуноцитокинов или анти-PD-L1 антител или фрагментов, предусматриваемых в данном документе, составляет по меньшей мере 32 часа, или по меньшей мере 34 часа, или по меньшей мере 36 часов, или по меньшей мере 40 часов. В одном варианте реализации, период полувыведения определяют в мышиной модели (например, нокин (knock-in)-мыши с PD-L1 человека, например, как описано в Примере 22 ниже, или у иммунокомпрометированной мыши с ксенотрансплантатом человеческих Т-клеток). В другом варианте реализации, период полувыведения определяют в исследовании с введением однократной дозы яванским макакам (например, как описано в Примере 18 или Примере 23 ниже). В другом варианте реализации, период полувыведения определяют в искусственно размноженных исследованиях с однократной дозой у яванских макак (например, как описано в Примере 19 или Примере 26 ниже).
Аспект 1а. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константная область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константная область легкой цепи, (CL);
e) необязательно, линкер, (L); и
f) цитокин IL-2;
где домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с антигеном, выбранным из: ингибитора иммунной контрольной точки (такого как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммунного модулятора (такого как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CXCL11 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R) и иммунного активатора (такого как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистическая активность против CXCR3), CD27, CD3 и ICOS (например, агонистическая активность против ICOS), например, ICOS, CD137, GITR и ОХ40).
В другом варианте реализации, антигенсвязывающий сайт специфически связывается с антигеном, выбранным из: ингибитора иммунной контрольной точки (такого как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммунного модулятора (такого как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R) и иммунного активатора (такого как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистическая активность против CXCR3), CD3 и ICOS (например, агонистическая активность против ICOS), например, ICOS, CD137, GITR и ОХ40).
Любой из вариантов реализации аспекта 1 являются применимыми mutatis mutandis (с необходимыми изменениями) к аспекту 1а. Любые из признаков или вариантов реализации аспектов 2-54 являются применимыми mutatis mutandis к аспекту 1а. Любые из признаков антител или других вариантов реализации или признаков концепций 1-70 являются применимыми mutatis mutandis к аспекту 1а.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает PD-L1, например, hPD-L1. В одном варианте реализации, антигенсвязывающий сайт PD-L1 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL любого анти-PD-L1 антитела, выбранного из атезолизумаба/MPDL3280A (Roche), авелумаба/MSB0010718C (Merck), BMS-936559/MDX-1105 (BMS), дурвалумаба/Medi4736 (Medimmune), KN-035, СА-170, FAZ-053 М7824, ABBV-368, LY-3300054, GNS-1480, YW243.55.S70, REGN3504 и любых из PD-L1-антител, раскрытых в WO 2017/034916, WO 2017/020291, WO 2017/020858, WO 2017/020801, WO 2016/111645, WO 2016/00735, WO 2016/176654, WO 2016/197367, WO 2016/061142, WO 2016/149201, WO 2016/00619, WO 2016/022630, WO 2016/007235, WO 2015/173267, WO 2015/181342, WO 2015/109124, WO 2015/195163, WO 2015/112805, WO 2015/061668, WO 2014/159562, WO 2014/165082, WO 2014/100079, WO 2014/055897, WO 2013/181634, WO 2013/173223, WO 2013/079174, WO 2012/145493, WO 2011/066389, WO 2010/077634, WO 2010/036959, WO 2010/089411 или WO 2007/005874, причем указанные антитела и последовательности включены в настоящее описание посредством ссылки.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает ICOS, например, hICOS. В одном варианте реализации, антигенсвязывающий сайт специфически связывает ICOS, например, hICOS, и является агонистом ICOS, например, hICOS. В одном варианте реализации, антигенсвязывающий сайт специфически связывает ICOS, например, hICOS, и является антагонистом ICOS, например, hICOS. В одном варианте реализации, антигенсвязывающий сайт ICOS содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL любого из антител против ICOS, описанных в схеме 5 и схеме 5а ниже, и любых антител против ICOS, описанных в предложениях 1-102, и предложениях 1а-21а.
В любом из следующих вариантов реализации, конкретный антигенсвязывающий сайт специфически связывается с человеческой мишенью. В одном варианте реализации, антигенсвязывающий сайт специфически связывает ингибитор иммунной контрольной точки. В одном варианте реализации, антигенсвязывающий сайт специфически связывает ингибитор иммунной контрольной точки, выбранный из PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA. В одном варианте реализации, антигенсвязывающий сайт специфически связывает ингибитор иммунной контрольной точки, выбранный из TIGIT, CTLA-4, TIM-3 и LAG-3.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает PD-1, например, PD-1 человека. В одном варианте реализации, антигенсвязывающий сайт PD-1 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из пембролизумаба (Keytruda®/MK-3475), ниволумаб (Opdivo®/BMS-936558/MDX-1106), MEDI-0680/АМР514, PDR001, ламбролизумаба, BMS-936558, REGN2810, BGB-A317, BGB-108, PDR-001, SHR-1210, JS-001, JNJ-63723283, AGEN-2034, PF-06801591, генолимзумаба, MGA-012, IBI-308, BCD-100, TSR-042 ANA011, AUNP-12, KD033, MCLA-134, mDX400, muDX400, STI-A1110, АВ011, 244С8, 388D4, ХСЕ853 или пидилизумаба/СТ-011, или из любого из антител против PD-1, описанных в WO 2015/112800 и US 2015/0203579 (включая антитела в таблицах 1-3) US 9394865 и US 4888802, WO 2017/087599 (включая антитело SSI-361 и SHB-617), WO 2017/079112, WO 2017/071625 (включая депозит С2015132, гибридому LT004 и антитела 6F5/6F5 (Re), 6F5H1 L1 и 6F5 H2L2), WO 2017/058859 (включая PD1AB-1 до PD1AB-6), WO 2017/058115 (включая 67D9, C67D9, и hu67D9), WO 2017/555547 (включая 12819.15384, 12748.15381, 12748.16124, 12865.15377, 12892.15378, 12796.15376, 12777.15382, 12760.15375 и 13112.15380), WO 2017/040790 (включая AGEN2033w, AGEN2034w, AGEN2046w, AGEN2047w, AGEN2001w и AGEN2002w), WO 2017/025051 и WO 2017/024515 (включая 1.7.3 hAb, 1.49.9 hAb, 1.103.11 hAb, 1.103.11-v2 hAb, 1.139.15 hAb и 1.153.7 hAb), WO 2017/025016 и WO 2017/024465 (включая антитела А-I), WO 2017/020858 и WO 2017/020291 (включая 1.4.1, 1.14.4, 1.20.15 и 1.46.11), WO 2017/019896 и WO 2015/112900 и US 2015/0210769 (включая BAP049-hum01 - BAP049-hum16 и BAP049-Clone-A - BAP049-Clone-E), WO 2017/019846 (включая mAb 1 PD-1 - mAb 15 PD-1), WO 2017/016497 (включая МНС723, МНС724, МНС725, МНС728, МНС729, m136-M13, m136-М19, m245-M3, m245-M5 и m136-M14), WO 2016/201051 (включая антитело ЕН12.2Н7, антитело hPD-1 mAb2, антитело hPD-1 mAb7, антитело hPD-1 mAb9, антитело hPD-1 mAb15 или антитело против PD-1, выбранное из Таблицы 1), WO 2016/197497 (включая DFPD1-1 - DFPD1-13), WO-2016/197367 (включая 2.74.15 и 2.74.15Ab4 - 2.74.15Ab8), WO 2016/196173 (включая антитела в Таблице 5 и Фигуры 1-5), WO 2016/127179 (включая R3A1, R3A2, R4B3 и R3D6), WO 2016/077397 (включая антитела, описанные в Таблице 1 Примера 9), WO 2016/106159 (включая мышиные антитела в Таблице 3 Примера 2 и гуманизированные антитела в Таблицах 7, 8 и 9 Примера 3), WO 2016/092419 (включая С1, С2, С3, ЕН12.1, mAb7-G4, mAb15-G4, mAb-AAA, mAb15-AAA), WO 2016/068801 (включая клон A3 и его варианты и другие антитела, описанные на Фиг. 1-4), WO 026/014688 (включая 10D1, 4С10, 7D3, 13F1, 15Н5, 14А6, 22А5, 6Е1, 5А8, 7А4 и 7A4D и гуманизированные антитела из Примеров 9/10), WO 2016/015685 (включая 10F8, ВА08-1, ВА-08-2 и 15Н6), WO 2015/091911 и WO 2015/091910 (включая антисобачьи антитела PD-1 в Примерах 2, 3 и 4), WO 2015/091914 (включая антисобачьи антитела PD-1 в Таблице 3), WO 2015/085847 (включая mAb005, Н005-1 - Н005-4), WO 2015/058573 (включая сАВ7), WO 2015/036394 (включая LOPD180), WO 2015/035606 (включая антитела в Таблице 1 Примера 2, в Таблицах 14, 15 и 16 Примера 7 и в Таблицах 20, 21 и 22 Примера 11) WO 2014/194302 (включая GA2, RG1B3, RG1H10, RG2A7, RG2H10, SH-A4, RG4A6, GA1, GB1, GB6, GH1, А2, С7, Н7, SH-A4, SH-A9, RG1H11 и RG6B), WO 2014/179664 (включая 9А2, 10В11, 6Е9, АРЕ1922, АРЕ1923, АРЕ1924, АРЕ1950, АРЕ1963 и АРЕ2058), WO 2014/206107 (включая клоны 1, 10, 11, 55, 64, 38, 39, 41 и 48), WO 2012/135408 (включая h409A11, h409A16 и h409A17), WO 2012/145493 (включая антитела 1Е3, 1Е8, 1Н3 и h1H3 Var 1 - h1H3 Var 14), WO 2011/110621 (включая антитело 949 и модифицированные варианты, раскрытые на Фиг. 1-11), WO 2011/110604 (включая антитело 948 и модифицированные варианты, раскрытые на Фиг. 3-11), WO 2010/089411 (включая депозиты в CNCM №№1-4122, 1-4080 или 1-4081), WO 2010/036959 (включая антитела в Таблице 1 Примера 1), WO 2010/029435 и WO 2010/029434 (включая клоны 2, 10 и 19), WO 2008/156712 (включая hPD-1.08A, hPD-1.09A, h409A11, h409A16 и h409A17, и антитела, описанные в Примере 2, Таблица Н, Примере 4 и Таблице IV), WO 2006/121168 (включая клоны 17D8, 4Н1, 5С4, 4А11, 7D3, 5F4 и 2D3), WO 2004/004771 или WO 2004/056875 (включая PD1-17, PD1-28, PD1-33, PD1-35, PD1-F2 и Abs, описанные в Таблице 1); последовательности и признаки антител против PD-1 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CTLA-4, например, hCTLA-4. В одном варианте реализации, антигенсвязывающий сайт CTLA-4 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из ипилимумаба (MDX-010, CAS No. 477202-00-9), тремелимумаб (тицилимумаб/СР-675, 206), клона 2F1 антитела, клона 1F4 (Abnova Corporation), клона 9Н10 (EMD Millipore), клона BNU3 (GeneTex), клона 1 Е2, клона AS32 (Biosciences) клона А3.4Н2.Н12 (Acris Antibodies), клона 060 (Sino Biological), клона BU5G3 (Creative Diagnostics), клона MIH8 (MBL International), клона A3.6B10.G1 или клона L3D10 (BioLegend) или из любого из антител против CTLA-4, описанных в WO 2017/087588 (ISV, раскрытые на Фигуре 2), WO 2017/084078 (клоны С2, С4, С10, С11, С12 и С13 и Фигуры 4-7), WO 2016/196237 (включая AGEN1884w, AGEN2041w, последовательности на Фиг. 19А, 19В и Таблицы 1-6), WO 2016/130986 и WO 2016/130898 (включая Е8, F7 и антитела (Abs), описанные в Таблице 4), WO 2016/015675 (включая гибридому LT001 и антитела 8D2, 8D2H1L1, 8D2H2L2, 8D2H3L3, 8D2H2L15 и 8D2H2L17), WO 2012/120125 (включая 3В10, 8Н5 и антитела (Abs), идентифицированные в Примерах 1, 2, 3 и 5), WO 2010/097597 (включая JMW-3B3 и раскрытые варианты и фрагменты), WO 2009/100140 (включая 10D1, 1Н5, 3А4, 6С10 и антитела, описанные на Фиг. 1-6), WO 2007/008463 и WO 2006/101692 и WO 2006/101691 и WO 2006/048749 и WO 2005/09238 (включая 4.1.1, 4.8.1, 4.10.2, 4.13.1, 4.14.3, 6.1.1, 11.2.1, 11.6.1, 11.7.1, 12.3.1.1, 12.9.1.1 и 10D1), WO 2006/096491 (включая депозит АТСС №11.2.1 11.2.1.4 РТА-5169 и 4.1.1 4.1.1.1 РТА-5166), WO 2006/066568 (включая TGN2122.C, TGN2422.C, 4.8Н10Н5 и 4.3F6B5 и антитела, описанные в Таблицах 3-14), WO 2006/029219 (включая L3D10, L1B11, K4G4, KM10 и YL2), WO 2004/029069 (включая депозит АТСС №РТА-4537), WO 01/54732 (включая антитела 25, 26, 27, 29, 33, 34, 35, 36 и 38), WO 01/14424 (включая 3А4, 9А5, 2Е2, 2Е7, 4В6, 4Е10, 5С4, 5G1, 11Е8 и 11G1 и антитела, идентифицированные в Примерах 3 и 4 и Таблице 3) и WO 00/37504 (включая 3.1.1, 4.1.1, 4.8.1, 4.10.2, 4.13.1, 4.14.3, 6.1.1, 11.2.1, 11.6.1, 11.7.1, 12.3.1.1 и 12.9.1.1); последовательности и признаки антител против CTLA-4 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает TIGIT, например, человеческий TIGIT. В одном варианте реализации, антигенсвязывающий сайт TIGIT содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из RG-6058 (MTIG-7192A) или из любого из антител против TIGIT, описанных в WO 2017/053748 (включая 1А4, 1D3, 4А3, 10А7, 4.1D3.Q1E, h10A7.K4G3, 4.1D3 и другие антитела, описанные в Примерах 1 и 2), WO 2017/037707 (включая VSIG9#1 и 258-csl#4), WO 2017/030823 (включая 14D7, 26В10 и гуманизированные варианты в Примере 3), WO 2016/191643 (включая 313R11, 313R12, 313R14, 313R19, 313R20, АТСС РТА-122180 и АТСС РТА-122181), WO 2016/106302 (включая 14В2, 13Е6, 6F9, 11G11, 10С9, 16F6, 11С9, 27А9, 10D7, 20G6, 24Е8, 24G1, 27F1, 15А6, 4Е4, 13D1, 9В11, 10В8, 22G2, 19Н2, 8С8, 17G4, 25Е7, 26D8 и 16А8), WO 2016/028656 (включая 14А6, 28Н5 или 31С6 и гуманизированные варианты из Примера 6) и WO 2009/126688 (US 2013/0251720, включая 10А7 и 1F4); последовательности и признаки антител против TIGIT включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает TIM-3, например, человеческий TIM-3. В одном варианте реализации, антигенсвязывающий сайт TIM-3 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL- из F38-2E2 (BioLegend), клона 2Е2 (Merck Millipore), клона 6В6Е2, клона 024 (Sino Biological) клона 344801 (R&D Systems), клона Е-18, клона Н-191 (Santa Cruz Biotechnology) или клона 13А224 (United States Biological), TSR-022 (Tesaro) или из любого из антител против TIM-3, описанных в WO 2017/079115 (включая антитела против TIM3, перечисленные в таблицах 30-38), WO 2017/055404 (включая PD1TIM3-0389, PD1TIM3-0168, PD1TIM3-0166, TIM3-0038, TIM3-0018, TIM3-0028, TIM3-0438 - Таблица С), WO 2017/031242 (таблица 10), WO 2016/179194 (включая антитела на Фигуре 1b, включая mAb F38-2E2 и 2Е2), WO 2016/171722 (включая 344823 и антитела из гибридом 7D11, 10G12, 11G8, 8В.2С12 и 25F.1D6), WO 2016/161270 (включая АРЕ5137 и АРЕ5121), WO 2016/111947 (включая mAb5, mAb13, mAb15, mAb17, mAb21, mAb22, mAb26, mAb27, mAb48, mAb58 и mAb91), WO 2016/071448 (включая TIM3-0016, TIM3-0018, TIM3-0021, TIM3-0022, TIM3-0026, TIM3-0028, TIM3-0030, TIM3-0033, TIM3-0038, TIM3-0433, TIM3-0434, TIM3-0438 и TIM3-0443), WO 2016/068802 (включая 1В9, 1Н9, 1Н10, 2С7, 2F4, 2G6, 1D9, 1F4 и 2С8 - Фигуры 1, 2 и 3), WO 2016/068803 (включая A3, В10, G6, G7, G9, А11 и A11_gl - Фигуры 1, 2 и 3), WO 2015/117002 (включая ABTIM3, ABTIM3-hum02, ABTIM3-hum05, ABTIM3-hum06, ABTIM3-hum09, ABTIM3-hum10, ABTIM3-hum12, ABTIM-hum01, ABTIM-hum04, ABTIM3-hum07, ABTIM3-hum08, ABTIM3-hum04, ABTIM3-hum21, ABTIM3-hum03, ABTIM3-hum11 и антитела, перечисленные в таблице 9), WO 2015/048312 (включая 5D12) WO 2014/022332 (включая 2С12), WO 2013/006490 (включая антитела в таблице 1), WO 2011/155607 (включая 512, 644, 4545, 4177, 8213, 344823 и 34823), WO 2003/063792 (включая антитела 8В.2С12 и 25F.1D6), WO 2017/019897 (включая молекулы антител, раскрытые в Таблицах 1-4, включая ABTIM3, ABTIM3-hum20, ABTIM3-hum22 и ABTIM3-hum23), WO 2016/079050 и WO 2016/079050 (включая Tim3_0022, Tim3_0016, Tim3_0018, Tim3_00122, Tim3_0022, Tim3_0021, Tim3_0028, Tim3_0026, Tim3_0033, Tim3_0038, Tim3_0030, 1.7.Е10, F38-2EL и 27-12E12); последовательности и признаки антител против TIM-3 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает LAG-3, например, LAG-3 человека. В одном варианте реализации, антигенсвязывающий сайт LAG-3 включает CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из клона антитела 17В4 (Enzo Life Sciences) или клона 333210 (R&D Systems), или клона 14L676 (United States Biological), или C9B7W (PharMingen), или 11Е, или IMO321, или mAb C9B7W (BioXcell), или из любого из антител против LAG-3, описанных в WO 95/30750, WO 2004/788928, WO 2008/132601 (включая IMP731 Lag-3 Ab, IMP321, А9Н12 Lag-3 mAb и 31G11), WO 2010/019570 (включая 25F7, 26Н10, 25Е3, 8В7, 11F2 и 17Е5), WO 2014/140180 (включая H5L7, H5L7BW, IMP731 и антитела в Таблицах 3 и Таблице 7), WO 2014/179664 (включая АРЕ03109), WO 2014/008218 (включая Lag3.1, Lag3.5, Lag3.6, Lag3.7 и Lag3.8), WO 2015/042246, WO 2015/116539 (включая BMS-986016), WO 2015/138920 (включая BAP050-hum01 - BAP050-hum20, huBAP050(Ser), BAP050-hum01-Ser - BAP050-hum20-Ser, BAP050-Clone-F, BAP050-Clone-G, BAP050-Clone-H, BAP050-Clone-I, BAP050-Clone-J, BAP050 и BAP050-chi), WO 2015/198312, WO 2016/028672 (включая Ab1, Ab2, Ab3, Ab4, Ab5, Ab6, Ab7, Ab8 и Ab9), WO 2016/126858, WO 2016/200782 (включая LAG-3 mAb1 - LAG-3 mAb6), WO 2017/015560 (включая L32D10, L3E3, L3C5, L35D4, L35G6, L33H11, L32A9, L32A4, L3A1 и антитела, перечисленные в Таблице 3), WO 2017/062888 (включая mAb1, Н4Н15477Р, Н4Н15483Р, Н4Н15484Р, Н4Н15491, Н4Н17823Р, Н4Н17826Р2, Н4Н17828Р2, H4sH15460P, H4sH15462P, H4sH15463P, H4sH15464P, H4sH15466P, H4sH15467P, H4sH15470P, H4sH15475P, H4sH15479P, H4sH15480P, H4sH15482P, H4sH15488P, H4sH15496P2, H4sH15498P2, H4sH15505P2, H4sH15518P2, H4sH15523P2, H4sH15530P2, H4sH15555P2, H4SH15558P2, H4sH15567P2 и H4H17819P), WO 2017/019894, WO 2017/037203 (включая 8E2, 13E2, 34F4, 17B4 и IMP761), WO 2017/087589 (включая 11В09) или WO 2017/087901; последовательности и признаки антител против LAG-3 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает VISTA, например, человеческий VISTA. В одном варианте реализации, антигенсвязывающий сайт VISTA содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из любого из антител против VISTA, описанных в WO 2016/207717 и WO 2015/097536 (включая VSTB50, VSTB53, VSTB60, VSTB95, VSTB112, VSTB116, VSTB174, VSTB175, VSTB149, VSTB140 и антитела в Таблице 1А и Примерах 7 и 8) и WO 2014/190356 (включая клоны 2D3 и 18С3); последовательности и признаки анти-VISTA-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный модулятор. В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный модулятор, выбранный из BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CXCL11 и CD155, или из BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155. В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный модулятор, выбранный из GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает GARP, например, GARP человека. В одном варианте реализации, антигенсвязывающий сайт GARP содержит CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из G14D9, Plato-1, 272, G6, 50 G10 или 7В11, или из любого из антител против GARP, описанных в WO 2007/113301 и WO 2015/015003 (включая MHGARP8, LHG-10, LHG-10-D, LHG-10.3-D, LHG-10.4-D, LHG-10.5-D, LHG-10.6-D, LHG-10.3, LHG-10.4, LHG-10.5, LHG-10.6, 27Е10, MHGARP1, MHGARP2, MHGARP3, MHGARP4, MHGARP5, MHGARP6, MHGARP7 и MHGARP9), WO 2017/051888 (включая 110F, 105F, c151D, c198D, h198D, h151D, h151D-H1L1 и h198D-H3L4); последовательности и признаки анти-GARP-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает SIRPα, например, SIRPαчеловека. В одном варианте реализации, антигенсвязывающий сайт SIRPα содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из ED9 (ThermoFisher) или 602411 (Novus Biologicals), или из любого из антител против SIRPα, описанных в WO 97/48723, WO 00/24869 (включая 10С4), WO 00/66159 (включая ED9 и ED17), WO 01/40307, WO 02/092784 (включая SE5A5, SE7C2 и SE12C3), WO 2004/108923 (включая SE12C3 и 2F34), WO 2009/046541 (включая Р84), WO 2011/076781, WO 2012/172521, WO 2012/040207 (включая SE5A5 и мышиный Р84), WO 2013/056352 (включая 29-АМ4-5, Ab АМ4-5, АМ5-1, АМ5-3, АМ5-5, АМ5-6, SIRPalpha-AM3-35, АМ4-1, SIRP29-AM3-35, SIRP29-AM4-5, SIRP29-AM4-1, 29-АМ2-2, 29-АМ4-4, 29-АМ4-1, 29-АМ4-5, 29-АМ3-35 и SIRP29-AM3-63), WO 2016/063233, WO 2016/205042 (включая Р362) или WO 2015/138600 (включая KWAR23); последовательности и признаки анти-SIRPα антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CXCR4, например, CXCR4 человека. В одном варианте реализации, антигенсвязывающий сайт CXCR4 включает CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL улокуплумаба/BMS-936564, клона 44717.111 или PF-06747143, или из любого из антител против CXCR4, описанных в WO 97/49424 (включая MAB12G5), WO 99/50461, WO 01/42308, WO 03/06830 и WO 2003/066830 (включая Ab124 и Ab125), WO 2004/059285 (включая ALX40-4C), WO 2006/089141 (включая mAb 2N, 6R, 18, 19, 20, 33 и 48), WO 2007/005605, WO 2008/142303 (включая МАВ170, МАВ171, МАВ173 и МАВ172), WO 2008/060367 и WO 2013/071068 и WO 2015/015401 (включая BMS-936564/MDX-1338), WO 2009/140124 (включая антитела I, II, III, IV и V), WO 2009/117706 (включая 701, 708, 716, 717, 718 и 4G10), WO 2011/161266 (включая 4CXCR100, 4CXCR103, 4CXCR104, 4CXCR101, 4CXCR238D2 и 4CXCR238D4), WO 2011/098762 (включая С-9Р21 (Таблица 1), В-1М22 (Таблица 2), С1124 (Таблица 3), D-1K21 (Таблица 4) и 9N10 (Таблица 5)), WO 2012/175576, WO 2013/013025 (включая 2А4, 6С7, 4С1, 7С8, 5С9 и 5Е1), WO 2013/017566 (включая Mab 427аВ1 и 515Н7), WO 2013/017562 (включая 1-3859 Mab и 515Н7), WO 2015/069874 (включая антитела, соответствующие SEQ ID Nos 25 и 29), WO 2015/015401 (включая 12А11, 6В6, 3G10, m3G10.hlgG1, m3G10.hlgG4, h3G10.A57.hlgG1, h3G10.A57.A58A.hlgG1, h3G10.1.91.A58A.hlgG1, h3G10.1.91.A58B.hlgG1 и h3G10.2.37.2.72.hlgG1), WO 2016/156570 (включая 281F12, 281A6 и 281D4), WO 2016/109872 (включая антитела, перечисленные в Таблицах 1, 2, 9 и 12, М3-114-6Н, АМ4-272-6Н, АМ3-523-6Н, АМ4-272, АМ3-114, АМ3-523, АМ4-746 и АМ4-1121), WO 2017/071625, WO 2012/175576, WO 2010/125162 и WO 2012/055980 и WO 2011/121040 и WO 2010/037831 (включая с414Н5 (414Н5), с515Н7 (515Н7) и 301аЕ5), WO 2009/138519 (включая ALX40-4C, 238D2, 238D4, 237В5, антитела и последовательности перечисленные в Таблице 1, Таблице 1.1, Таблице А-I, Таблице В-1.1 и В-5), WO 2011/042398 (включая 238D2 и 238D4), WO 2011/083140 (включая раскрытые в Таблицах С-2, С-3, С-4 и С-5, на Фигуре 2, и ALX-0651, 15Н3, 10Е12, 10G10, 238В6, 10Е9, 281Е10, 10А10, 14А2 и 15А1) или WO 2011/083141; последовательности и признаки анти-CXCR4-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает BTLA, например, hBTLA. В одном варианте реализации, антигенсвязывающий сайт BTLA включает CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из клона антитела 1В7, клона 2G8, клона 4С5 (Abnova Corporation), клона 4В8 (antibodies-online), клона MIH26 (Thermo Scientific Pierce Antibodies), клона UMAB61 (OriGene Technologies), клона 330104 (R&D Systems), клона 1B4 (Lifespan Biosciences), клона 440205, клона 5E7 (Creative Diagnostics) или из любого из антител против BTLA, описанных в WO 2016/176583 (включая клон 6F4), WO 2011/014438 (включая 8D5, 8А3, 20Н4, 21Н6, 15С5, 19А7 и 4С7), WO 2010/106051 (включая депозит CNCM №1-4123) и WO 2008/076560 (включая 1В4, Е4Н9, 3С2, 3С2а, 6А5, 11Е2, E8D9, 10Н6 и 4С9, как описано в Примере 2); последовательности и признаки анти-BTLA-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает hVEM, например, hVEM человека. В одном варианте реализации, антигенсвязывающий сайт HVEM содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL- из любого из антител против HVEM, описанных в WO 2008/083169 (включая LBH1); последовательности и признаки анти-BTLA-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CSF1R. В одном варианте реализации, антигенсвязывающий сайт CSF1R содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL- из любого из антител против CSF1R, описанных в WO 2009/026303 (включая 1.2, 1.109, 2.360 и 1.2.SM и антитела на Фиг. 1 и 2), WO 2009/112245 (включая CXIIG6), WO 2011/070024 (включая Mab 2F11, 2Е10, 2Н7 и 1G10, и их производные), WO 2011/107553 (включая 7H5.2G10/DSM АСС2922), WO 2011/123381 (включая антитело 1 и антитело 2), WO 2011/131407 (включая 7G5.3B6/DSM АСС2921), WO 2011/140249 (включая 0301, 0302, и 0311, их производные, и антитела в Таблицах 2, 3 и 5), WO 2013/169264 и WO 2014/036357 и WO 2016/106180 и WO 2016/168149 (включая huAb1 - huAb16), WO 2012/110360 и WO 2013/057281 (включая CXIIG6, H19K12, H27K5 и H27K15 и гуманизированные антитела в Таблицах 1 и 2), WO 201/087699 (включая 9D11.2E8 и 10H2.2F12), WO 2014/072441 (включая H27K15), WO 201/173814 и WO 2013/1320 44 (включая Mab 2F11, Mab 2Е10, Mab 2Н7, Mab 1G10 и sc2-4A5, и антитела в Таблицах 3 и 3b), WO 2015/028455 и WO 2015/028454 (включая Ab535, Ab969 и производные, например, Ab969.g2), WO 2015/036511 и WO 2016/207312 (включая 2F11, 2Е10 и производные, описанные в варианте реализации 33) и WO 2017/049038 (включая ALM-423 и антитела, перечисленные в Таблице 2); последовательности и признаки анти-CSF1R-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD39, например, человеческий CD39. В одном варианте реализации, антигенсвязывающий сайт CD39 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из BY40, BY12, BA54g (Biolegend), BU61 (Santa Cruz Biotech), A1 (Ebiosciences), AC2 (Immunotech), 22A9 (Abcam), 24DMS1 или любое из анти-CD39-антител, описанных в WO 96/32471, WO 00/04041, WO 01/10205 (включая CD39L4), WO 2009/09547 (включая CNCM-I-3889/BY40), WO 2014/169255, WO 2012/085132 (включая антитела VY12, BY40 и BA54g), WO 2016/073845 (включая R29-5-13A, R29-5-71A, R29-5-165C и R29-9-8B), WO 2017/089334 (включая 1-391, 1-392 и антитела, полученные из гибридом I-3889 и CNCM I-41171) и WO 2009/095478; последовательности и признаки анти-CD39-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD40, например, человеческий CD40. В одном варианте реализации, антигенсвязывающий сайт CD40 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из BMS3h-56-269, СР-870893, дацетузумаба, SEA-CD40, ADC-1013, RO7009789 и Chi Lob 7/4, или из любого из анти-CD40-антител, описанных в WO 2017/059243, WO 2017/059196, WO 2017/040932, WO 2017/040566, WO 2017/004016, WO 2017/004006, WO 2016/196314, WO 2016/028810, WO 2016/023875, WO 2015/134988, WO 2015/091853, WO 2014/070934, WO 2014/065403, WO 2014/065402, WO 2014/04298, WO 2013/164789, WO 2012/149354, WO 2012/149356, WO 2012/125569, WO 2012/111762, WO 2012/075111, WO 2012/065950, WO 2012/041635, WO 2011/123489, WO 2010/123012, WO 2010/104761, WO 2010/121231, WO 2009/062125, WO 2010/104747, WO 2010/104748, WO 2010/104749, WO 2010/024676, WO 2009/094391, WO 2009/062054, WO 2008/091954, WO 2007/129895, WO 2007/124299, WO 2007/053767, WO 2007/053661, WO 2006/128103, WO 2006/073443, WO 2005/063981, WO 2005/063289 (US 2012/0263732), WO 2005/044855, WO 2005/044306, WO 2005/044304, WO 2005/044304, WO 2005/044854, WO 2005/044305, WO 03/40170 (US 5763442 В, US 6718633 В, US 3338660 В, US 7288251 В, US 7626012 B, US 8388971 B, US 2013/0024956), WO 03/029296, WO 02/088186, WO 01/83755, WO 02/28905, WO 02/28480, WO 02/28481, WO 02/28904, WO 01/37870, WO 01/16180, WO 00/75348, WO 99/61057, WO 99/47575, WO 97/31025, WO 95/17202 и WO 95/96653; последовательности и признаки анти-CD40-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD73, например, человеческий CD73. В одном варианте реализации, антигенсвязывающий сайт CD73 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из 1Е9 (Santa Cruz Biotechnology), AD2, 7G2, 4G4, или из любого из анти-CD73-антител, описанных в WO 2017/064043 (включая 7Н10, 12F9, 15D7, 4В11, 11D9 и 9D2), WO 2016/081748 (включая 4С3, 7А11, 6Е11, 5F8, 4С3, 11F11, 11А6, CD73.4-1, CD73.4-2, CD73.3, 11F11-1, 11F11-2, 11F11, 4С3-1, 4С3-2, 4С3-3, 4D4, 10D2-1, 10D2-2, 11А6, 24Н2, 5F8-1, 5F8-2 и 5F8-3), WO 2016/131950 (включая 11Е1, 8С7, 3С12 и 6Е1), WO 2016/075176 (включая MEDI9447, клон 10.3 и клон 2С5) и WO 2016/075099 (включая CD730004, CD730008, CD7300011, CD730021, CD730042, CD730046, CD730047, CD730068 и CD730069), WO 2016/055609 (включая 11Е1, 6Е1, 3С12 и 8С7); последовательности и признаки анти-CD73-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD96, например, человеческий CD96. В одном варианте реализации, антигенсвязывающий сайт CD96 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL 6А6 или NK92.39 (Е bioscience), 1С8, 3Н8, МАА6359, или из любого из антител против CD96, описанных в WO 2008/073316, WO 2009/007124, WO 2013/184912, WO 2014/089169, WO 2014/149310 (включая антитело 3.3), WO 2015/024060 или WO 2015/024042, WO 2015/024060 (включая mAb 3.3); последовательности и признаки анти-CD96-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CXCR2, например, CXCR2 человека. В одном варианте реализации, антигенсвязывающий сайт CXCR2 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL- из любого из антител против CXCR2, описанных в WO 2015/169811 (включая HY29 и HY29GL), WO 201/170317 (включая СХ2-Mab, №№1-19), WO 2012/062713, WO 2013/168108 (включая 163D2-127D1, 163E3-127D1, 163Е3-54В12, 163D2-54B12, 2В2-163Е3, 2B2-163D2, 97А9-2В2, 97А9-54В12, 127D1-163D2, 127D1-163E3, 2В2-97А9, 54B12-163D2, 54В12-163Е3, 163D2-2B2, 163Е3-2В2, 127D1-97A9, 54В12-97А9, 97A9-127D1 и их производные), WO 2009/117706 (включая 48311.211, 5Е8 / CXCR2, клон 19 и их производные), WO 2009/120186 (включая RII115, 48311 и их производные) и WO 2002/26249; последовательности и признаки анти-CXCR2-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD200, например, CD200 человека. В одном варианте реализации, антигенсвязывающий сайт CD200 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из DX-109, самализумаба/ALXN-6000, TTI-200.7, или любого из антител против CD200, описанных в WO 99/256565 (включая М3В5 и антитела в Примерах 4 и 5), WO 02/11762 (включая 3В6 и антитела в примерах), WO 2004/060295 (US 2004/0213783), WO 2004/078938 (включая scFv-9), WO 2006/020266 (US 8840885 В2, включая CG1R3A10, cG2aR3A10, cG2aR3B7, dGIR3A5, dGIR3B5 и dGIR3B10 и антитела, описанные на Фиг. 9А-9С, Фиг. 21А и 21В), WO 2007/084321 (US 8709415 В2, включая ALXN5200, hB7VH3VL2, C2aB7G1, C2aB7G2/G4, V3V2-G1 и V3V2-G2/G4), WO 2009/014745 (включая OX90mG2a (Фиг. 10), OX90NE и OX90NE-AG) и WO 2011/100538 и US 2013/0189258 (включая антитело 1 и антитело 2); последовательности и признаки анти-CD200-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывается с CCR4, например, CCR4 человека. В одном варианте реализации, антигенсвязывающий сайт CCR4 включает CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из могамулизумаб, KM3060 (см. Niwa et al., 2004, Cancer Research 64, 2127-2133) и KW-0761 (см. Ishida et al., Annals of Oncology 2008, vol. 19, supplement 4, 513) или из любого из антител против CCR4, описанных в WO 2016/178779 и WO 2016/057488 (включая mAb2-3, 1-44, 1-49, 2-1 и 2-2), WO 2015/179236 (включая KW-0761), WO 201/166500 (включая mAb1567, с1567, h1567, mAb1-4 и 2-3 и антитела в Примерах 6 и 13), WO 2012/076883 (включая антитела 208, 306, 308, 406, 501, 503, 601, 603 и 803 - Таблицы 1-9), WO 2010/142952 (включая 17G, 9Е, 11F, 9Е10, 9E10J и 9E1D - см. Таблицы 1-16), WO 2009/086514 (включая mAb1567 и гуманизированные mAb в Примере 14), WO 2005/035582 (включая антитело DG44/CCR4 и антитело Ms705/CCR4 (FERM ВР-8467)), WO 2005/053741 и WO 01/64754 (US 6989145 В, US 7666418 В, US 8197814 В, US 8632996 В, включая KM2160 (FERM ВР-10090), KM2760 (депозит FERM ВР-7054)), WO 2003/018635 (включая KM2160, KM8759 (FERM ВР-8129) и KM8760 (FERM ВР-8130), WO 00/47474 (US 6488930 В, US 7138117 В, включая 2В10, 10Е4, 1G1 и антитела, депонированные с номерами доступа АТСС НВ-12624 и НВ-12625) и WO 00/41724 (US 6881406 В, US 6245332 В, включая 1G1 и антитело, депонированное с номером доступа АТСС НВ-12624); последовательности и признаки анти-CCR4-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CXCL9, например, человеческий CXCL9. В одном варианте реализации, антигенсвязывающий сайт CXCL9 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из mAb 392-100 или AF392 (R&D Systems).
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CXCL10, например, человеческий CXCL10. В одном варианте реализации, антигенсвязывающий сайт CXCL10 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL mAb266 (R&D Systems) или из любого из антител против CXCL10, описанных в WO 017/8708 (включая CR.G (IP-10) (IgG1) (PharMingen) и IP-10 (IgG) (A. Luster), WO 02/15932, WO 03/006045, WO 2004/082714, WO 2004/045525, WO 2004/045526, WO 2004/101511 (включая антитела в Таблице 1 и AIP12, HuAIP12, MuAIP12, AIP13, HuAIP13, MuAIP13, AIP6, AIP8, AIP14, AIP18, AIP21, AIP22, AIP5 и AIP17), WO 2005/060457 (включая AIP5, AIP6, AIP8, AIP10, AIP12, AIP13, AIP14, AIP17, AIP18, AIP21, AIP22, AIP32 и AIP36), WO 2005/011605, WO 2005/023201, WO 2005/058815 (включая 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 10A12S13C4), WO 2005/084708, WO 2006/039819, WO 2006/118085, WO 2008/047486, WO 2008/044824 (включая антитела №124, №31, №28, №43 и №137), WO 2008/106200, WO 2009/023566, WO 2012/149320 (включая MSX-1100 и 6А5), WO 2014/003742 (включая антитело Примера 14), WO 201/170735, WO 2014/189306, WO 2015/063187; последовательности и признаки антител против CXCL10 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD155, например, человеческий CD155. В одном варианте реализации, антигенсвязывающий сайт CD155 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из клона SKII.4 (BioLegend).
В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный активатор. В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный активатор, выбранный из CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистическая активность против CXCR3), CD3 и ICOS (например, агонистическая активность против ICOS). В одном варианте реализации, антигенсвязывающий сайт специфически связывает иммунный активатор, выбранный из ICOS, CD137, GITR и ОХ40.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD137, например, hCD137. В одном варианте реализации, антигенсвязывающий сайт CD137 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из урелумаба, BMS-663513, PF-05082566 (Pfizer), 1D8 и 3Е1, 4В4 (BioLegend 309809), Н4-1ВВ-М127 (BD Pharmingen 552532), BBK.2 (Thermo Fisher M S621PABX), 145501 (Leinco Technologies B591), антитело, продуцируемое клеточной линией, депонированной как АТСС № НВ-11248 (патент США 6974863) или XmAb-5592, или из любого из анти-CD137-антител, описанных в WO 2017/04945, WO 2016/134358, WO 2015/179236, WO 2012/177788, WO 2012/145183, WO 2012/032433, WO 2009/135019, WO 2005/035584, патенте США 6974863, WO 2004/055513 и WO 2004/010947; последовательности и признаки анти-CD137-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает GITR, например, hGITR. В одном варианте реализации, антигенсвязывающий сайт GITR содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из MK4166, TRX518, TRX385, МАВ689 (R&D Systems), YGITR765 (Novus Biologicals) или 1D8 (Novus Biologicals), или из любого из антител против GITR, описанных в WO 025/187835 (включая 28F3, 3С3-1, 3С3-2, 2G6, 8А6, 9G7-1, 9G7-2, 14Е3, 19Н8-1, 19Н8-2, 19D3, 18Е10 и 6G10), WO 2015/184099 (включая 1042-7, 32-15, 1039-45, 1333-21, 231-1039-45, 231-32-15, Hum231#1, Hum231#2, m6C8, pab1964, pab1973, pab1975 - pab1977, pab1979 - pab1981, pab1983, pab2159, pab2160, pab2161 и антитела в Таблицах 1 и 2), WO 2015/031667 (включая антитела Ab1 - Ab59 в Таблице 1), WO 2015/026684 (включая антитело с CDR-последовательностями SEQ ID 1-66), WO 2013/039954 (включая 2155, 1718, 1649, 1362, 954, 827, 698, 706 и антитела, перечисленные в Таблицах 1 и 3), WO 2011/051726 (включая антитела, содержащие CDR а-f, перечисленные на странице 17), WO 2011/028683 (включая антитела 36Е5, 61F6, 61G6, 3D6, 6Н6, 1D8, 17F10, 35D8, 49А1, 9Е5, 31Н6 и антитела из гибридом РТА-9889, РТА-9890, РТА-9891, РТА-9892, РТА-9893, РТА-10286, РТА-10287, РТА-10288, РТА-10289, РТА-10290 и РТА-10291), WO 2009/009116 (включая антитело 2F8), WO 2007/133822 (включая антитела, перечисленные в Таблице 1), WO 2006/105021 (включая 6С8, 2F8, HuN6C8-Agly, HuQ6C8-Gly и HuQ6C8-Agly), WO 2006/050172 и WO 2004/084942 (включая DTA-1), WO 03/006058 (включая anti-GITR/TNFRSF18# AF524), WO 2016/054638 (включая mAb №1-81, №3-167, №5-139, №7-192, №10-116, №11-126, №12-46, №13-169, №14-182, №15-68 и №17-60), WO 2016/196792 (включая 6G10, 28F3, 19D3, 18Е10, 3С3, 2G6, 8А6, 9G7, 14Е3 и 19Н8), WO 201/87678 (включая 28F3, 19D3, 18Е10, 3С3-1, 3С3-2, 2G6, 8А6, 9G7-1, 9G7-2, 14Е3, 19Н8-1, 19Н8-2 и 6G10); последовательности и признаки анти-GITR-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает ОХ40, например, hOX40. В одном варианте реализации, антигенсвязывающий сайт ОХ40 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из GSK3174998, L106 BD (Pharmingen, продукт №340420), АСТ35 (Santa Cruz Biotechnology, № по каталогу 20073), MOXR0916, MEDI-6469, MEDI-0562, 9B12 (Weinberg, AD, et al., J Immunother 29, 575-585 (2006)), гуманизированное анти-ОХ40 Ab, описанное в Morris et al., Mol Immunol. May 2007; 44(12):3112-3121, или из любого из антител против ОХ40, описанных в WO 2000/077085 (включая SAP9, SAP28.2, SAP15.3, SAP 29-50, SAP 25-29 и SAP 29-23 и гуманизированные варианты, описанные в Примерах 4 и 5), WO 2017/063162 (включая О3, 019, 021 и вариант со зрелой аффинностью в Примере 5 - Таблица 2, включая 21#Н28Н33, 21#Н65, 21#Н96, 21#VHnew-L80, 21#H96-L80), WO 2017/050729 (включая SP197), WO 2017/021912 и WO 2017/021910 (включая ANTIBODY 106-222, OX86 и антитела, описанные на Фиг. 6 и 7), WO 2016/200836 и WO 2016/200835 (включая MOXR0916/1A7.gr1 IgG1), WO 2016/196228 (включая 3F4, 14В6-1, 14В6-2, 23Н3, 18Е9, 8В11, 20В3, 20С1, 6Е1-1, 6Е1-2, 14А2, 14А2-1, 14А2-2, L106, ОХ40.1, ОХ40.5, ОХ40.8, ОХ40.6 и ОХ40.16 и ОХ40.21 - Фигуры 1-10), WO 2016/179517 (включая 11D4, pab1949, pab1949-1, pab2044, pab2193-1, Таблицы 1-4), WO 2016/057667 (включая 9В12 и OX40mAb24), WO 2015/153513 (включая 3С8, 1D2, 1А7 и их варианты, описанные в перечне последовательностей, включая A1A7.gr1 и 3C8.gr.5, антитела, описанные на Фигуре 1), WO 2014/148895 (включая АСТ35, 12Н3, 12Н3 (Фиг. 25) - и гуманизированные версии VL1H1, VL1VH2, VL1VH3, VL2H1, VL2VH2 и VL2VH3 (Фиг. 43 и 44) и 20Е5 (Фиг. 24)), WO 2013/068563 (включая А26 [Фиг. 2]), WO 2013/038191 (включая АСТ35, 12Н3 и 12Н3), WO 2013/028231 (включая 119-122, 119-43-1, 106-222 и антитела в Таблице 1), WO 2013/008171 (включая 2F8, 1D4 и их производные, включая VH6/VL9, и антитела на Фиг. 4 и 5, и Таблицы 6 и 7), WO 2012/027328 (включая 119-122, 119-43-1, Hu106 и Hu106-222), WO 2010/096418 (включая А26), WO 2008/106116 (включая антитела в Таблицах 1 и 2 и А10 (включая A10A-F), В66 - Fig14 - В2, В24, В36, В37 и В39) и WO 2007/062245 (включая 112V8 (АТСС № РТА-7219), 112Y55 (АТСС № РТА-7220), 112Y131 (АТСС № РТА-7218), 112F32 (АТСС № РТА-7217) и 112Z5 (АТСС №РТА-7216); последовательности и признаки антител против ОХ40 включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CXCR3, например, CXCR3. В одном варианте реализации, антигенсвязывающий сайт CXCR3 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из GSK3174998 или из любого из анти-CXCR3 антител, описанных в WO 2016/200836, WO 2016/200835, WO 2016/196228, WO 2016/179517, WO 2016/057667, WO 2015/153513, WO 2014/148895, WO 2013/068563, WO 2013/038191, WO 2013/028231, WO 2013/008171, WO 2012/027328, WO 2010/096418, WO 2011/073180, WO 2008/106116 и WO 2007/062245; последовательности и признаки анти-CXCR3-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD27, например, hCD27. В одном варианте реализации, антигенсвязывающий сайт CD27 содержит CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL- из любого из антител против CD27, описанных в WO 2016/145085 (в том числе 1F5), WO 2015/016718 (включая hCD27.15 и 1F5), WO 2014/140374 (включая 2F2, 5F24, 5F32, 10F13, 10F31, 11F26, 1052-015, F2A4B2 и их производные, включая hz5F24VH+V5Q, hz5F24VL+K45Q), WO 2013/138586 (включая С2177, С2186, С2191 и С2192 и производные в Примерах 8-12 и Таблицах 7-42), WO 2012/004367 (включая hCD27.15/ATCC № РТА-11008), WO 2011/130434 (включая 1G5, 1Н8, 3Н12, 3Н8, 2G9, 1F5, 3А10, 2С2, ms 1А4, ms 9F4 и ms М-Т271), WO 2011/081164 и WO 2010/001908 (включая KM4027, KM4028, KM4026, KM4030, KM4032 и их производные), WO 2008/051424 (включая LG3A10 и АТ124-1); последовательности и признаки анти-CD27-антител включены в данный документ посредством ссылок.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает CD3, например, hCD3. В одном варианте реализации, антигенсвязывающий сайт CD3 включает CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL из антитела OKT3, отеликсизумаба, теплизумаба или висилизумаба, или из любого из анти-CD3-антител, описанных в WO 2017/010874, WO 2017/009442, WO 2016/204966, WO 2016/180721, WO 2016/179003, WO 2016/116626, WO 2016/014974, WO 2015/104346, WO 2015/095392, WO 2015/001085, WO 2014/047231, WO 2013/188693, WO 2013/186613, WO 2013/158856, WO 2012/173819, WO 2012/162067, WO 2005/118635, WO 2004/108158, WO 2004/052397, WO 2004/024771, WO 01/51644, WO 00/05268, WO 97/44362, WO 93/19196, WO 92/06193 и WO 91/09968; последовательности и признаки анти-CD3-антител включены в данный документ посредством ссылок.
Аспект 1b. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
а) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
б) константная область тяжелой цепи;
c) необязательно, линкер, (L); и
d) цитокин IL-2;
и легкая цепь содержит, в направлении от N- к С-концу:
e) домен VL, содержащий CDRL1, CDRL2 и CDRL3; и
f) константную область легкой цепи (CL);
где домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с антигеном, выбранным из: ингибитора иммунной контрольной точки (такого как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммунного модулятора (такого как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R) и иммунного активатора (такого как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические антитела против CXCR3), CD27, CD3 и ICOS (например, агонистические анти-ICOS антитела), например, ICOS, CD137, GITR и ОХ40).
В другом варианте реализации, антигенсвязывающий сайт, который специфически связывается с антигеном, выбран из: ингибитора иммунной контрольной точки (такого как PD-1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, TIGIT, TIM-3 и LAG-3), иммунного модулятора (такого как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R) и иммунного активатора (такого как CD137, GITR, ОХ40, CD40, CXCR3 (например, агонистические антитела против CXCR3), CD3 и ICOS (например, агонистические анти-ICOS антитела), например, ICOS, CD137, GITR и ОХ40).
Любой из вариантов реализации аспекта 1 и/или аспекта 1а является применимым mutatis mutandis (с необходимыми изменениями) к аспекту 1b. Любые из признаков или вариантов реализации аспектов 2-54 являются применимыми mutatis mutandis к аспекту 1b. Любой из признаков антител или других вариантов реализации или признаков концепций 1-70 является применимым mutatis mutandis к аспекту 1b.
В одном варианте реализации, антигенсвязывающий сайт специфически связывает любой из антигенов, как указано в Аспекте 1а.
В одном варианте реализации, антигенсвязывающий сайт специфически связывается с hPD-L1, представленным SEQ ID NO: 1, и конкурирует за связывание с указанным hPD-L1 с антителом 1D05; причем иммуноцитокин содержит домен VH, который содержит CDRH3, содержащий мотив X1GSGX2YGX3X4FD, где X1, Х2 и Х3 независимо представляют собой любую аминокислоту, а Х4 либо присутствует, либо отсутствует, и, в случае его присутствия, может быть любой аминокислотой.
В любом из аспектов 1 или 1а, формулировка части f) может быть изменена следующим образом: «f) цитокин, например, выбранный из IL-7, IL-15, IL-21, IL-12, GM-CSF, TNFα, TGFβ, CXCL9, CXCL10 и интерферона-α". В 1b формулировка части d) может быть заменена на «d) цитокин, например, выбранный из IL-7, IL-15, IL-21, IL-12, GM-CSF, TNFα, TGFβ, CXCL9, CXCL10 и интерферона-α". Таким образом, раскрытые в данном документе иммуноцитокины могут содержать цитокины, отличные от цитокина, обладающего активностью цитокина IL-2. В одном варианте реализации, цитокин представляет собой IL-7 (SEQ ID NO: 330). В одном варианте реализации, цитокин представляет собой IL-15 (SEQ ID NO: 331). В одном варианте реализации, цитокин представляет собой IL-21 (SEQ ID NO: 332). В одном варианте реализации, цитокин представляет собой IL-12, содержащий a-цепь (SEQ ID NO: 336) и В-цепь (SEQ ID NO: 337). В одном варианте реализации, цитокин представляет собой GM-CSF (SEQ ID NO: 333). В одном варианте реализации, цитокин представляет собой TNFα (SEQ ID NO: 335). В одном варианте реализации, цитокин представляет собой TGFβ. В одном варианте реализации, цитокин представляет собой CXCL9 (SEQ ID NO: 338). В одном варианте реализации, цитокин представляет собой CXCL10 (SEQ ID NO: 339). В одном варианте реализации, цитокин представляет собой интерферон-α (SEQ ID NO: 334).
В другом варианте реализации, цитокин является иммуностимулирующим цитокином. В другом варианте реализации, цитокин является стимулирующим Т-клеточным цитокином.
Аспект 2. Иммуноцитокин согласно аспекту 1, где X1 представляет собой гидроксилсодержащую аминокислоту, необязательно, Т.
Аспект 3. Иммуноцитокин согласно аспекту 1 или аспекту 2, где Х2 представляет собой основную аминокислоту, необязательно, K.
Аспект 4. Иммуноцитокин согласно любому из аспектов 1-3, где Х2 представляет собой гидроксилсодержащую аминокислоту, необязательно, S или Т.
Аспект 5. Иммуноцитокин по любому из пп. 1-4, отличающийся тем, что Х3 представляет собой ароматическую аминокислоту, необязательно, W.
Аспект 6. Иммуноцитокин согласно любому из аспектов 1-5, где Х4 отсутствует.
Аспект 7. Иммуноцитокин согласно любому из аспектов 1-5, где Х4 присутствует.
Аспект 8. Иммуноцитокин согласно аспекту 7, где Х4 представляет собой алифатическую аминокислоту, необязательно, G.
Признаки аспектов 2-7 могут быть такими, как определено в любой из концепций 2-7 выше.
Аспект 9. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
где домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1 и конкурирует за связывание с указанным hPD-L1 с антителом 1D05, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 29 или 32, или последовательность CDRH3, представленную SEQ ID NO: 29 или 32, содержащую 6 или меньше аминокислотных замещений, где, необязательно, иммуноцитокин соответствует любому из аспектов 2-8.
В этом аспекте, любые признаки CDRH3, описанные в концепциях 9 и 9a-l, и любые варианты реализации концепции 9, являются применимыми mutatis mutandis.
Аспект 10. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1; и
причем домен VH содержит CDRH3, который состоит из 12-20 аминокислот и получен путем рекомбинации VH генного сегмента человека, D генного сегмента человека и JH генного сегмента человека, причем JH генный сегмент человека представляет собой IGHJ5 (например, IGHJ5*02).
В этом аспекте, любые признаки CDRH3, описанные в концепциях 10 и 10а, являются применимыми mutatis mutandis.
Аспект 11. Иммуноцитокин согласно аспекту 10, где VH генный сегмент человека представляет собой IGHV3 (например, IGHV3-9, такой как IGHV3-9*01).
В этом аспекте, любые признаки генных сегментов, описанные в концепциях 11, 11а или 11b, являются применимыми mutatis mutandis.
Аспект 12. Иммуноцитокин согласно аспекту 10 или аспекту 11, где антитело или фрагмент содержат домен VL, который получен путем рекомбинации Vκ генный сегмент человека и Jκ генный сегмент человека, где VL генный сегмент человека представляет собой IGκVID (например, IGKV1D-39, такой как IGκV1D-39*01).
В этом аспекте, любые признаки генных сегментов, описанные в концепциях 12, 12а или 12b, являются применимыми mutatis mutandis.
Аспект 13. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
а) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с эпитопом, идентичным эпитопу, с которым специфически связывается антитело 1D05.
В этом аспекте, любые признаки эпитопов, анализов и других вариантов реализации, описанные в любой из концепций 13 и 13а-13l, являются применимыми mutatis mutandis.
Аспект 14. Иммуноцитокин согласно аспекту 13, где эпитоп идентифицируют сканированием неродственной аминокислотой или рентгеновской кристаллографией.
Аспект 15. Иммуноцитокин согласно аспекту 14, где контактные остатки эпитопа определяют по снижению аффинности, по меньшей мере, в 10 раз при сканировании неродственной аминокислотой, например, сканировании аланином, по результатам определения методом SPR.
В этом аспекте, любые признаки концепции 15 являются применимыми mutatis mutandis.
Аспект 16. Иммуноцитокин, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1, CDRH2 и CDRH3; и
b) константную область тяжелой цепи;
и легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1, CDRL2 и CDRL3;
d) константную область легкой цепи (CL);
e) необязательно, линкер (L); и
f) цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который конкурирует за связывание с hPD-L1 с антителом 1D05.
В этом аспекте, любые признаки антител концепций 16а-16l или любого из конкурентных анализов и других вариантов реализации, описанных в концепции 16, или признаки концепции 35 являются применимыми mutatis mutandis.
Аспект 17. Иммуноцитокин согласно любому из аспектов 10-16, где домен VH содержит последовательность CDRH3, представленную SEQ ID NO: 29 или 32, или последовательность CDRH3, представленную SEQ ID NO: 29 или 32, содержащую 6 или меньше аминокислотных замещений.
В этом аспекте, любые признаки антител концепций 17а-17l являются применимыми mutatis mutandis.
Аспект 18. Иммуноцитокин согласно любому из предшествующих аспектов, где домен VH содержит последовательность CDRH1, представленную SEQ ID NO: 27 или 30, или последовательность CDRH1, представленную SEQ ID NO: 27 или 30, содержащую 3, 2 или 1 аминокислотных замещений.
В этом аспекте, любые признаки антител концепций 18а-18l являются применимыми mutatis mutandis.
Аспект 19. Иммуноцитокин согласно любому из предшествующих аспектов, где домен VH содержит последовательность CDRH2, представленную SEQ ID NO: 28 или 31, или последовательность CDRH2, представленную SEQ ID NO: 28 или 31, содержащую 4 или меньше аминокислотных замещений.
В этом аспекте, любые признаки антител концепций 19а-19l являются применимыми mutatis mutandis.
Аспект 20. Иммуноцитокин согласно любому из предшествующих аспектов, где домен VH содержит аминокислотную последовательность SEQ ID NO: 33 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 80% (например, по меньшей мере 85%, или по меньшей мере 90%), идентична SEQ ID NO: 33 (например, последовательности домена VH в любой из последовательностей тяжелой цепи, представленных SEQ ID Nos: 47-49).
В этом аспекте, любые признаки антител концепций 20a-20l или любого из вариантов реализации концепции 20 являются применимыми mutatis mutandis.
Аспект 21. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий первую и вторую копии указанной тяжелой цепи.
Аспект 22. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий домен VL, который содержит последовательность CDRL1, представленную SEQ ID NO: 37 или 40, или последовательность CDRL1, представленную SEQ ID NO: 37 или 40, содержащую 3 или меньше аминокислотных замещений.
В этом аспекте, любые признаки антител концепций 22a-22l являются применимыми mutatis mutandis.
Аспект 23. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий домен VL, который содержит последовательность CDRL2, представленную SEQ ID NO: 38 или 41, или последовательность CDRL2, представленную SEQ ID NO: 38 или 41, содержащую 2 или 1 аминокислотных замещений, например, последовательность CDRL2, представленную SEQ ID NO: 50.
В этом аспекте, любые признаки антител концепций 23a-23l являются применимыми mutatis mutandis.
Аспект 24. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий домен VL, который содержит последовательность CDRL3, представленную SEQ ID NO: 39 или 42, или последовательность CDRL3, представленную SEQ ID NO: 39 или 42, содержащую 4 или меньше аминокислотных замещений.
В этом аспекте, любые признаки антител концепций 24a-24l являются применимыми mutatis mutandis.
Аспект 25. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий домен VL, который содержит аминокислотную последовательность SEQ ID NO: 43 или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 80% (например, по меньшей мере 85%, или по меньшей мере 90%), идентична SEQ ID NO: 43 (например, последовательности домена VL в последовательности легкой цепи, представленной SEQ ID NO: 50 или 51).
В этом аспекте, любые признаки антител концепций 25a-25l или любого из вариантов реализации концепции 25 являются применимыми mutatis mutandis.
Аспект 26. Иммуноцитокин согласно любому из предшествующих аспектов, содержащий первую и вторую копии указанной легкой цепи.
Аспект 27. Иммуноцитокин согласно любому из предшествующих аспектов, который специфически связывается с PD-L1 яванского макака, представленным SEQ ID NO: 2.
В этом аспекте, любые варианты реализации концепции 27 являются применимыми mutatis mutandis.
Аспект 28. Иммуноцитокин согласно любому из предшествующих аспектов, где антитело или фрагмент содержат легкую цепь каппа.
В этом аспекте, любые варианты реализации концепции 28 являются применимыми mutatis mutandis.
Аспект 29. Иммуноцитокин по любому из аспектов 9-28, где аминокислотные замещения представляют собой консервативные аминокислотные замещения, где, необязательно, консервативные замещения относятся к одной из шести групп (каждая группа содержит аминокислоты, являющиеся консервативными замещениями друг для друга), выбранных из:
1) аланин (А), серии (S), треонин (Т);
2) аспарагиновая кислота (D), глутаминовая кислота (Е);
3) аспарагин (N), глутамин (Q);
4) аргинин (R), лизин (K);
5) изолейцин (I), лейцин (L), метионин (М), валин (V); и
6) фенилаланин (F), тирозин (Y), триптофан (W).
В этом аспекте, любые варианты реализации концепции 9 являются применимыми mutatis mutandis.
Аспект 30. Иммуноцитокин согласно любому из предшествующих аспектов, где антитело или фрагмент содержат константную область, например, константную область IgG1, где, необязательно, константная область представляет собой инактивированный (disabled) IgG1, представленный SEQ ID NO: 205.
В этом аспекте, любые признаки или варианты реализации концепций 30, 31 или 32 являются применимыми mutatis mutandis.
Аспект 31. Иммуноцитокин согласно любому из предшествующих аспектов, где:
A) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
B) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 43;
C) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
D) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
E) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
F) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
G) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
H) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
I) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 50;
J) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
K) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
L) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
М) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
N) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
О) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
Р) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
Q) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 298;
R) домен VH содержит аминокислотную последовательность SEQ ID NO: 58, а домен VL содержит аминокислотную последовательность SEQ ID NO: 68;
S) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 58, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 68;
Т) домен VH содержит аминокислотную последовательность SEQ ID NO: 78, а домен VL содержит аминокислотную последовательность SEQ ID NO: 88;
U) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 78, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 88;
V) домен VH содержит аминокислотную последовательность SEQ ID NO: 98, а домен VL содержит аминокислотную последовательность SEQ ID NO: 108;
W) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 98, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 108;
X) домен VH содержит аминокислотную последовательность SEQ ID NO: 118, а домен VL содержит аминокислотную последовательность SEQ ID NO: 128;
Y) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 118, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 128;
Z) домен VH содержит аминокислотную последовательность SEQ ID NO: 158, а домен VL содержит аминокислотную последовательность SEQ ID NO: 168;
АА) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 158, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 168;
ВВ) домен VH содержит аминокислотную последовательность SEQ ID NO: 178, а домен VL содержит аминокислотную последовательность SEQ ID NO: 188;
СС) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 178, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 188;
DD) домен VH содержит аминокислотную последовательность SEQ ID NO: 138, а домен VL содержит аминокислотную последовательность SEQ ID NO: 148;
ЕЕ) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 13, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 148;
FF) домен VH содержит аминокислотную последовательность SEQ ID NO: 244, а домен VL содержит аминокислотную последовательность SEQ ID NO: 254;
GG) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 244, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 254;
НН) домен VH содержит аминокислотную последовательность SEQ ID NO: 264, а домен VL содержит аминокислотную последовательность SEQ ID NO: 274;
II) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 264, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 274;
JJ) домен VH содержит аминокислотную последовательность SEQ ID NO: 284, а домен VL содержит аминокислотную последовательность SEQ ID NO: 294;
KK) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 284, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 294;
LL) домен VH содержит аминокислотную последовательность SEQ ID NO: 13, а домен VL содержит аминокислотную последовательность SEQ ID NO: 23; и
ММ) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 13, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 23;
NN) домен VH содержит аминокислотную последовательность SEQ ID NO: 349, а домен VL содержит аминокислотную последовательность SEQ ID NO: 359; и
OO) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 349, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 359.
В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Аспект 32. Иммуноцитокин согласно любому из предшествующих аспектов, где:
A) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 299, и VL и CL содержат аминокислотную последовательность SEQ ID NO: 45;
B) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 299, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 45;
C) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 47, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 45;
D) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 48, a VL и CL, содержат аминокислотную последовательность SEQ ID NO: 45;
E) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 49, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 45;
F) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 342, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 45;
G) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 238, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 50;
H) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 47, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 50;
I) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 48, a VL и CL, содержат аминокислотную последовательность SEQ ID NO: 50;
J) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 49, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 50;
K) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 342, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 50;
L) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 299, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 51;
М) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 47, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 51;
N) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 48, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 51;
О) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 49, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 51;
Р) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 342, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 51;
Q) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 299, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 298;
R) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 47, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 298;
S) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 48, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 298;
Т) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 49, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 298;
U) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 342, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 298;
V) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 60, и VL и CL содержат аминокислотную последовательность SEQ ID NO: 70;
W) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 60, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 70;
X) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 80, и VL и CL содержат аминокислотную последовательность SEQ ID NO: 90;
Y) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 80, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 90;
Z) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 100, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 110;
АА) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 100, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 110;
ВВ) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 120, и VL и CL содержат аминокислотную последовательность SEQ ID NO: 130;
СС) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 120, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 130;
DD) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 160, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 170;
ЕЕ) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 160, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 170;
FF) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 180, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 190;
GG) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 180, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 190;
НН) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 140, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 150;
II) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 140, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 150;
JJ) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 246, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 256;
KK) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 246, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 256;
LL) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 266, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 276;
MM) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 266, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 276;
NN) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 286, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 296; и
OO) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 286, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 296;
РР) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 15, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 25; и
QQ) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 15, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 25;
RR) VH и константная область содержат аминокислотную последовательность SEQ ID NO: 351, a VL и CL содержат аминокислотную последовательность SEQ ID NO: 361; и
SS) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 351, a VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 85% идентична SEQ ID NO: 361.
В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 70% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 75% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 95% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 96% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 97% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 98% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99% идентична последовательности с указанным идентификатором SEQ ID. В одном варианте реализации, аминокислотная последовательность, по меньшей мере на 99,5% идентична последовательности с указанным идентификатором SEQ ID.
Аспект 33. Иммуноцитокин согласно любому из предшествующих аспектов, где антигенсвязывающий сайт специфически связывает PD-L1, тогда как цитокин IL-2 связывает высокоаффинный (αβγ) рецептор IL-2 (IL-2R).
В одном варианте реализации, антигенсвязывающий сайт связывает PD-L1 одновременно со связыванием цитокином IL-2 αβγ IL-2R. В одном варианте реализации, антигенсвязывающий сайт связывает PD-L1 последовательно со связыванием цитокином IL-2 αβγ IL-2R. В одном варианте реализации, цитокин IL-2 дополнительно связывает промежуточный (βγ) IL-2R.
Аспект 34. Иммуноцитокин согласно любому из предшествующих аспектов, где иммуноцитокин способен ингибировать супрессию Т-клеток, опосредованную PD-L1.
В одном варианте реализации, иммуноцитокин ингибирует PD-L1-опосредованную супрессию Т-клеток. В одном варианте реализации, иммуноцитокин ингибирует PD-L1-опосредованную супрессию Т-клеток в анализе in vitro. В другом варианте реализации, антигенсвязывающий сайт имеет любые из признаков или вариантов реализации концепций 51 или 52.
В другом варианте реализации, антигенсвязывающий сайт блокирует или ингибирует связывание PD-1 с PD-L1. В одном варианте реализации, антигенсвязывающий сайт блокирует или ингибирует связывание CD80 с PD-L1.
Аспект 35. Иммуноцитокин согласно любому из предшествующих аспектов, где иммуноцитокин способен усиливать опосредованную IL-2R активацию Т-клеток.
В одном варианте реализации, иммуноцитокин усиливает активацию Т-клеток, опосредованную IL-2R. В одном варианте реализации, иммуноцитокин усиливает опосредованную IL-2R активацию Т-клеток в анализе in vitro.
Аспект 36. Иммуноцитокин согласно аспекту 34 или аспекту 35, где супрессию Т-клеток или усиление опосредованной IL-2R активации Т-клеток измеряют по увеличению одного или нескольких показателей из IFNγ, IL-2, CD25 или пролиферации Т-клеток в анализе, обеспечивающем костимуляцию посредством прямой стимуляции CD3/CD28, стимуляции суперантигеном, или обеспечивающем костимуляцию путем совместной инкубации с клетками, способными индуцировать Т-клеточный ответ.
Измерения могут проводиться с использованием любой пригодной методики. Например, измерения могут проводиться с использованием ИФА, HTRF, включения BRDU (пролиферация), электрохемилюминесценции (ECL) или проточной цитометрии (например, FACS). Эти способы хорошо известны специалистам в данной области и описаны в других разделах данного документа. В одном варианте реализации, анализ представляет собой проточную цитометрию. В одном варианте реализации, анализ представляет собой ИФА. В одном варианте реализации, анализ представляет собой HTRF.
В этом аспекте, когда аспект 36 является зависимым от аспекта 34, любые признаки или варианты реализации концепции 36 являются применимыми mutatis mutandis.
Когда Аспект 36 является зависимым от Аспекта 35, в одном варианте реализации, усиление опосредованной IL-2R активации Т-клеток измеряют по увеличению одного или обоих показателей из IFNγ и CD25.
Когда Аспект 36 является зависимым от Аспекта 35, в одном варианте реализации, костимуляция обеспечивается прямой стимуляцией CD3/CD28.
Когда Аспект 36 является зависимым от Аспекта 35, в одном варианте реализации, костимуляция обеспечивается суперантигеном, таким как стафилококковый энтеротоксин В (SEB).
Когда Аспект 36 является зависимым от Аспекта 35, в одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с клетками, способными индуцировать Т-клеточный ответ. Такие клетки могут представлять собой антигенпредставляющие клетки (АПК), например, моноциты, В-клетки или дендритные клетки. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с АПК. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с моноцитами. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с В-клетками. В одном варианте реализации, анализ обеспечивает костимуляцию путем совместной инкубации с дендритными клетками.
Аспект 37. Иммуноцитокин согласно любому из предшествующих аспектов, который не содержит линкер (L), или иммуноцитокин согласно любому из предыдущих пунктов, где CL в соответствии с d) непосредственно сливается с цитокином в соответствии с f).
В одном варианте реализации, CL легкой цепи или тяжелой цепи непосредственно сливают с цитокином.
В одном варианте реализации аспекта 1b CL в соовтетствии с b) непосредственно сливают с цитокином в соответствии с d).
Аспект 38. Иммуноцитокин согласно любому из аспектов 1-37, где линкер представляет собой пептидный линкер длиной от 1 до 20 аминокислот.
В одном варианте реализации, линкер представляет собой пептидный линкер длиной от 1 до 15 аминокислот. В одном варианте реализации, линкер представляет собой пептидный линкер длиной от 1 до 10 аминокислот. В одном варианте реализации, линкер представляет собой пептидный линкер длиной от 1 до 5 аминокислот.
В одном варианте реализации, линкер может быть химическим линкером. В случае рекомбинантных гибридных белков линкеры кодируются последовательностями нуклеиновых кислот, расположенными в рамке, между кодирующими областями различных участков иммуноцитокина. В случае синтетических белков, линкерные пептиды вводят во время синтеза.
Линкеры хорошо известны квалифицированным специалистам в данной области. Например, см. описание в Denardo et al., 1998, Clin. Cancer Res., 4(10):2483-90; Peterson et al., 1999, Bioconjug. Chem. 10(4):553-7; и Zimmerman et al., 1999, Nucl. Med. Biol., 26(8):943-50, раскрытые в этих документах модификации включены в данный документ посредством ссылок.
Аспект 39. Иммуноцитокин согласно аспекту 38, где линкерный пептид выбран из поли-G или (G4S)X, где X равно 1, 2, 3 или 4.
В других вариантах реализации, линкер может быть выбран из STG, GSTG, RS, TVAAPS, GGGGS, GSTVAAPS, TVAAPSGS или GSTVAAPSGS. В другом варианте реализации, линкер представляет собой Gln-Arg-Val-Asp (получен из N-конца константной области каппа собаки). В другом варианте реализации, линкером представляет собой GGNGT или YGNGT.
Аспект 40. Иммуноцитокин согласно любому из предшествующих аспектов, где цитокин IL-2 представляет собой человеческий IL-2 (hIL-2) или его вариант.
Варианты IL-2 описаны в аспекте 1.
Также предлагается вариант цитокина, который может быть любым из не относящихся к IL-2 цитокинов, описанных в данном документе (включая не относящиеся к IL-2 цитокины, описанные в Аспекте 1, например, выбранные из IL-7, IL-15, IL-21, IL-12, GM-CSF, TNFα, αCXCL9, αCXCL10 и интерферон-α). Определение варианта IL-2 цитокина является применимым mutatis mutandis к другим цитокинам (включая иммуностимулирующие цитокины и цитокины, стимулирующие Т-клетки), раскрытым в данном документе, например, включающим любую из N-концевых делеций, описанных для IL-2 в аспекте 1.
Аспект 41. Иммуноцитокин согласно аспекту 40, где hIL-2 содержит или состоит из аминокислотной последовательности SEQ ID NO: 301.
Аспект 42. Иммуноцитокин согласно аспекту 40, где hIL-2 содержит вариант IL-2, который содержит модификацию на N-конце, необязательно, делецию от 1 до 10 аминокислот.
В используемом в этом аспекте значении, модификация на N-конце любого из описанных в данном документе цитокинов (включая не относящиеся к IL-2 цитокины, описанные в Аспекте 1, например, выбранные из IL-7, IL-15, IL-21, IL-12, GM-CSF, TNFα, αCXCL9, αCXCL10 и интерферон-α) относится к одному или нескольким (например, от 1 до 10, например, 1-5) аминокислотным замещениям, делециям или вставкам.
В одном варианте реализации, модификация представляет собой одно или несколько (например, от 1 до 10, например, 1-5) аминокислотных замещений на N-конце цитокина. Замещения могут быть консервативными замещениями, например, как определено в концепции 9, концепции 29 или аспекте 29. В одном варианте реализации, модификация является делецией. В другом варианте реализации, модификация представляет собой N-терминальную делецию, например, любую из делеций, описанных в концепции 9 и аспекте 1. В одном варианте реализации, модификация (такая как делеция от 1 до 10 аминокислот) находится в пределах конечных 50 аминокислот на N-конце цитокина, например, цитокина IL-2. В одном варианте реализации, модификация (например, делеция от 1 до 10 аминокислот) находится в пределах конечных 30 аминокислот N-конца цитокина, например, цитокина IL-2. В одном варианте реализации, модификация (такая как делеция от 1 до 10 аминокислот) находится в пределах конечных 25 аминокислот N-конца цитокина, например, цитокина IL-2. В одном варианте реализации, модификация (например, делеция от 1 до 10 аминокислот) находится в пределах конечных 20 аминокислот N-конца цитокина, например, цитокина IL-2. В одном варианте реализации, модификация (например, делеция от 1 до 10 аминокислот) находится в пределах конечных 15 аминокислот N-конца цитокина, например, цитокина IL-2. В одном варианте реализации, модификация (такая как делеция от 1 до 10 аминокислот) находится в пределах конечных 10 аминокислот N-конца цитокина, например, цитокина IL-2.
В одном варианте реализации, модификация представляет собой делецию от 1 до 9 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-9 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 8 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-8 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 7 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-7 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 6 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-6 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 5 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-5 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 4 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-4 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию от 1 до 3 аминокислот из конечных 10 аминокислот N-конца цитокина, такую как делеция конечных 1-3 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию 1 или 2 аминокислот из конечных 10 аминокислот N-конца цитокина, таких как делеция конечных 1 или 2 аминокислот N-конца цитокина. В одном варианте реализации, модификация представляет собой делецию 1 аминокислоты из конечных 10 аминокислот N-конца цитокина, такую как делеция конечной аминокислоты N-конца цитокина. В конкретном варианте реализации, цитокин представляет собой цитокин IL-2, такой как цитокин IL-2 человека.
В одном варианте реализации, делеции подвергается 9-я аминокислота с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, делеции подвергаются 8-я и 9-я аминокислоты с N-конца цитокина, например, цитокина IL-2, например, к цитокину IL-2 человека. В одном варианте реализации, делеции подвергаются 7-я, 8-я и 9-я аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, делеции подвергаются от 6-й до 9-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, делеции подвергаются от 4-й до 9-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, изобретения, делеции подвергаются от 3-й до 9-й аминокислоты с N-конца цитокина, например, IL-2 цитокина, например, человеческого цитокина IL-2. В одном варианте реализации, делеции подвергаются от 2-й до 9-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, делеции подвергаются от 2-й до 6-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, делеции подвергаются от 3-й до 7-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. В одном варианте реализации, изобретения, делеции подвергаются от 4-й до 8-й аминокислоты с N-конца цитокина, например, цитокина IL-2, например, цитокина IL-2 человека. Любая из делеции, описанных в Аспекте 1 выше, может быть применена mutatis mutandis к не относящимся к IL-2 цитокинам в соответствии сданным аспектом.
Аспект 42а. Вариант hIL-2, содержащий N-концевую модификацию по любому из аспектов или признаков аспекта 42. В одном варианте реализации аспекта 42а вариант hIL-2 представляет собой очищенный вариант hIL-2. В другом варианте реализации аспекта 42а вариант hIL-2 представляет собой выделенный и очищенный вариант hIL-2.
Аспект 42b. Вариант цитокина, выбранный из IL-7, IL-15, IL-21, IL-12, GM-CSF, TNF, CXCL9, CXCL10 и интерферона-α, содержащий N-концевую модификацию по любому из аспектов или признаков аспекта 42. В одном варианте реализации аспекта 42а вариант цитокина представляет собой очищенный вариант цитокина. В другом варианте реализации аспекта 42а вариант цитокина представляет собой выделенный и очищенный вариант цитокина.
Аспект 43. Иммуноцитокин согласно аспекту 40 или аспекту 42, где hIL-2 содержит вариант IL-2, содержащий N-концевую последовательность, выбранную из SEQ ID NO: 303-323.
Аспект 43а. Вариант hIL-2, содержащий N-концевую последовательность, выбранную из SEQ ID NO: 303-323.
В одном варианте реализации аспекта 43а вариант hIL-2 представляет собой очищенный вариант hIL-2. В другом варианте реализации аспекта 43а вариант hIL-2 представляет собой выделенный и очищенный вариант hIL-2. В одном варианте реализации, вариант hIL-2 содержит (или состоит из) N-концевой последовательности, выбранной из SEQ ID NO: 303-323, непосредственно слитой с последовательностью IL-2, выбранной из SEQ ID NO: 324, 517 и 518.
Аспект 44. Иммуноцитокин согласно любому из аспектов 40, 42 или 43, где вариант hIL-2 содержит одну или несколько (например, от 1 до 5, например, одну или две) мутаций, независимо выбранных из следующих:
1) D20 (например, D20T);
2) R38 (например, R38W, R38A или R38Q);
3) F42 (например, F42A или F42K);
4) Y45 (например, Y45A);
5) Е62 (например, Е62А);
6) N88 (например, N88R);
7) С125 (например, C125S);
8) Q126 (например, Q126W); или
9) R38 и F42 (такие как R38W и F42K, или R38A и F42A);
причем нумерация остатка определена по отношению к последовательности IL-2 дикого типа человека, SEQ ID NO: 301.
Аспект 44а. Вариант hIL-2 по любому из аспектов 42а или 43а, где вариант hIL-2 содержит одну или несколько (например, от 1 до 5, например, одну или две) мутаций, независимо выбранных из следующих:
1) D20 (например, D20T);
2) R38 (например, R38W, R38A или R38Q);
3) F42 (например, F42A или F42K);
4) Y45 (например, Y45A);
5) Е62 (например, Е62А);
6) N88 (например, N88R);
7) С125 (например, C125S);
8) Q126 (например, Q126W); или
9) R38 и F42 (такие как R38W и F42K, или R38A и F42A);
причем нумерация остатка определена по отношению к последовательности IL-2 дикого типа человека, SEQ ID NO: 301.
В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации F42 (такой как F42A или F42K, например, F42A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации Y45 (например, Y45A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации Е62 (такой как Е62А).
В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A) и мутации F42 (такой как F42A или F42K, например, F42A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A) и мутации Y45 (такой как Y45A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A) и Е62 (такой как Е62А). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации Y45 (такой как Y45A) и Е62 (такой как Е62А). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации F42 (такой как F42A или F42K, например, F42A) и мутации Е62 (такой как Е62А). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации F42 (такой как F42A или F42K, например, F42A) и мутации Y45 (например, Y45A).
В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A), мутации F42 (такой как F42A или F42K, например, F42A) и мутации Y45 (такой как Y45A). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A), мутации F42 (такой как F42A или F42K, например, F42A) и мутации Е62 (такой как Е62А). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A), мутации Y45 (такой как Y45A) и мутации Е62 (такой как Е62А).
В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38 (такой как R38W, R38A или R38Q, например, R38A), мутации F42 (такой как F42A или F42K, например, F42A), мутации Y45 (такой как Y45A) и мутацию Е62 (такой как Е62А). В одном варианте реализации, вариант hIL-2 содержит (или состоит из) мутации R38A, F42A, Y45A и Е62А.
Другие мутации hIL-2 известны специалистам в данной области техники. В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2012/062228 (см. Пункты 2-7 формулы изобретения, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 1999/60128 (см. пункты формулы изобретения 6, 7, 8, 10, 11 и 12, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 1993/20849 (см. пункты формулы изобретения 4 и 5, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2003/015697 (см. пункты формулы изобретения 7 и 10, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2005/007121 (см. пункты формулы изобретения 9-14, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2005/086798 (см. пункты формулы изобретения 5-10, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2005/086751 (см. пункты формулы изобретения 5-9, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2009/061853 (см. пункт 5 формулы изобретения, включенную в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2012/088446 (см. пункты формулы изобретения 3-8 и 11-13, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2012/107417 (см. пункты формулы изобретения 2, 4, 6 и 9, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2012/119093 (см. пункты формулы изобретения 1-7 формулы изобретения, включенные в данный документ посредством ссылки). В одном варианте реализации, мутации hIL-2 представляют собой мутации, описанные в WO 2015/164815 (см. пункты формулы изобретения 3-19, включенные в данный документ посредством ссылки).
В этих аспектах, где нумерация остатков определяется со ссылкой на последовательность IL-2 человека дикого типа, если, например, присутствует одна делеция аминокислоты на N-конце цитокина, а в заявке описывается аминокислотная мутация N88, то для варианта IL-2, имеющего одну делецию аминокислоты, N фактически будет находиться в положении 87. Если цитокин имеет 3 делеции аминокислот на N-конце, а мутация представляет собой мутацию F42A, то фактическим положением мутации в варианте последовательности будет F39.
Аспект 45. Иммуноцитокин согласно аспекту 40, где hIL-2 содержит вариант IL-2, состоящий из N-концевой последовательности, выбранной из SEQ ID NO: 242-262, слитой с аминокислотной последовательностью SEQ ID NO: 324.
В одном варианте реализации, вариант hIL-2 содержит (или состоит из) N-концевой последовательности, выбранной из SEQ ID NO: 303-323, слитой с аминокислотной последовательностью, выбранной из SEQ ID NO: 324, 517 и 518.
В одном варианте реализации, иммуноцитокин представляет собой 1D05 D1-9 ICK. В одном варианте реализации, иммуноцитокин представляет собой 1D05 D1-9. В одном варианте реализации, иммуноцитокин представляет собой 1D05 D9-2 ICK. В одном варианте реализации, иммуноцитокин представляет собой 1D05 D9-7 ICK.
Аспект 45а. Вариант hIL-2, содержащий N-концевую последовательность, выбранную из SEQ ID NO: 303-323, слитую с аминокислотной последовательностью SEQ ID NO: 324.
В одном варианте реализации аспекта 45а, вариант hIL-2 представляет собой очищенный вариант hIL-2. В другом варианте реализации аспекта 44а, вариант hIL-2 представляет собой выделенный и очищенный вариант hIL-2.
Аспект 46. Иммуноцитокин согласно любому из предшествующих аспектов, где цитокин IL-2 связывается с высокоаффинным (αβγ) рецептором IL-2 с меньшей эффективностью, чем свободный IL-2, например, с ЕС50 больше 20 пМ, больше 50 пМ, или больше 100 пМ, например, при измерении путем клеточного пролиферативного анализа.
Свободный IL-2 имеет эффективность приблизительно 10 пМ по отношению к αβγ рецептору (высокоаффинному) в клеточном пролиферативном анализе. В используемом в данном документе значении, ЕС50 относится к эффективной концентрации, обеспечитвающей 50% от максимальной активации IL2R. Чем выше ЕС50, тем менее сильнодействующим является вещество, поэтому вещество, имеющее ЕС50, равную 1 пМ, является более сильным, чем вещество с ЕС50, равным 1 нМ. Последовательности α-цепи, β-цепи и γ-цепи представлены в SEQ ID NOs: 327, 328 и 329 соответственно.
В одном варианте реализации, цитокин IL-2 имеет значение ЕС50 в диапазоне от 5 до 20 пМ. В одном варианте реализации, ЕС50 находится в диапазоне от 5 пМ до 1 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 5 до 750 пМ, от 5 до 500 пМ, от 5 до 250 пМ или от 5 до 100 пМ, например, от 5 до 50 пМ.
В одном варианте реализации, ЕС50 находится в диапазоне от 10 пМ до 1 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 10 до 750 пМ, от 10 до 500 пМ, от 10 до 250 пМ, или от 10 до 100 пМ, например, от 10 до 50 пМ, или от 10 до 30 пМ.
В одном варианте реализации, ЕС50 находится в диапазоне от 20 пМ до 1 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 20 до 750 пМ, от 20 до 500 пМ, от 20 до 250 пМ, или от 20 до 100 пМ, например, от 20 до 50 пМ.
В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 50 пМ до 1 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 50 до 750 пМ, от 50 до 500 пМ, от 50 до 250 пМ или от 50 до 100 пМ, например, от 50 до 75 пМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 100 пМ до 1 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 100 до 800 пМ, от 100 до 700 пМ, от 100 до 600 пМ или от 100 до 500 пМ, например, от 100 до 400 пМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 100 до 300 пМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 100 до 200 пМ.
В другом варианте реализации, ЕС50 имеет значение больше 5 пМ. В другом варианте реализации, ЕС50 имеет значение больше 10 пМ. В другом варианте реализации, ЕС50 имеет значение больше 20 пМ. В другом варианте реализации, ЕС50 имеет значение более 30 пМ, более 40 пМ, более 50 пМ, более 60 пМ или более 70 пМ. В другом варианте реализации, ЕС50 имеет значение более 100 пМ, более 125 пМ, более 150 пМ, более 175 пМ или более 200 пМ. В другом варианте реализации, ЕС50 имеет значение более 250 пМ, более 300 пМ, более 350 пМ, более 400 пМ. В другом варианте реализации, ЕС50 имеет значение более 500 пМ, более 600 пМ, более 700 пМ или более 800 пМ.
В одном варианте реализации, ЕС50 имеет значение менее 5 нМ. В одном варианте реализации, ЕС50 имеет значение менее 1 нМ. В одном варианте реализации, ЕС50 имеет значение менее 800 пМ. В одном варианте реализации, ЕС50 имеет значение менее 700 пМ. В одном варианте реализации, ЕС50 имеет значение менее 600 пМ. В одном варианте реализации, ЕС50 имеет значение менее 500 пМ. В одном варианте реализации, ЕС50 имеет значение менее 400 пМ. В одном варианте реализации, ЕС50 имеет значение менее 300 пМ. В одном варианте реализации, ЕС50 имеет значение менее 200 пМ. В одном варианте реализации, ЕС50 имеет значение менее 100 пМ. В одном варианте реализации, ЕС50 имеет значение менее 50 пМ.
αЭффективность иммуноцитокина против αβγ IL-2R может быть измерена путем клеточного пролиферативного анализа, который хорошо известен специалистам в данной области и подробно описан в Примерах ниже (см. Пример 13 и Фигуру 12),
Аспект 47. Иммуноцитокин согласно любому из предшествующих аспектов, где IL-2 связывается с рецептором IL-2 промежуточной аффинности (βγ) с эффективностью меньшей, чем у свободного IL-2, например, с ЕС50 более 1 нМ, более 5 нМ или более 10 нМ, например, при измерении в клеточном пролиферативном анализе.
Свободный IL-2 имеет активность приблизительно 100 пМ по отношению к рецептору βγ (промежуточной аффинности) в клеточном пролиферативном анализе. В используемом в данном документе значении, ЕС50 относится к эффективной концентрации, обеспечивающей 50% от максимальной активации IL-2R. Чем выше EC50, тем менее сильнодействующим является вещество, поэтому вещество, имеющее ЕС50, равную 1 пМ, является более сильным, чем вещество с ЕС50, равным 1 нМ. Последовательности α-цепи, β-цепи и γ-цепи представлены в SEQ ID NOs: 327, 328 и 329 соответственно.
В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 100 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 10 до 100 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 20 до 100 нМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 30 до 100 нМ, от 40 до 100 нМ, от 50 до 100 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 50 до 100 нМ, от 60 до 100 нМ, от 70 до 100 нМ.
В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 50 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 10 до 50 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 20 нМ до 50 нМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 30 до 50 нМ, или от 40 до 50 нМ.
В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 10 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 20 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 30 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 9 нМ. В одном варианте реализации, ЕС50 находится в диапазоне от 1 до 8 нМ. В другом варианте реализации, цитокин IL-2 имеет ЕС50 в диапазоне от 1 до 7 нМ, от 1 до 6 нМ, или от 1 до 5 нМ.
В другом варианте реализации, ЕС50 имеет значение более 0,5 нМ, более 0,6 нМ, более 0,7 нМ, более 0,8 нМ или более 0,9 нМ. В другом варианте реализации, ЕС50 имеет значение более 1 нМ, более 1,25 нМ, более 1,5 нМ, более 1,75 нМ, или более 2 нМ. В другом варианте реализации, ЕС50 имеет значение более 2,5 нМ, более 3 нМ, более 3,5 нМ, более 4 нМ. В другом варианте реализации, ЕС50 имеет значение более 5 нМ, более 6 нМ, более 7 нМ или более 8 нМ. В конкретном варианте реализации, ЕС50 имеет значение более 1 нМ.
В одном варианте реализации, ЕС50 имеет значение менее 10 нМ. В одном варианте реализации, ЕС50 имеет значение менее 20 нМ. В одном варианте реализации, ЕС50 имеет значение менее 30 нМ. В одном варианте реализации, ЕС50 имеет значение менее 40 нМ. В одном варианте реализации, ЕС50 имеет значение менее 50 нМ.
В одном варианте реализации, ЕС50 имеет значение менее 100 нМ. В одном варианте реализации, ЕС50 имеет значение менее 200 нМ. В одном варианте реализации, ЕС50 имеет значение менее 300 нМ.
В другом варианте реализации, ЕС50 имеет значение менее 75 нМ или менее 50 нМ.
В одном варианте реализации, IL-2 не демонстрирует детектируемой активности против βγ IL-2R в клеточном пролиферативном анализе.
Эффективность иммуноцитокина против βγ IL-2R может быть измерена в клеточном пролиферативном анализе, который хорошо известен специалистам в данной области и подробно описан в Примерах ниже (см. Пример 13 и Фигуру 12).
Аспект 48. Иммуноцитокин согласно любому из предшествующих аспектов, где IL-2 предпочтительно связывается с высокоаффинным (αβγ) рецептором IL-2 по сравнению с рецептором IL-2 промежуточной аффинности (βγ).
Аспект 49. Иммуноцитокин согласно аспекту 48, где отношение активности по отношению к IL-2 высокоаффинного (αβγ) рецептора IL-2 и рецептора IL-2 промежуточной аффинности (βγ) составляет по меньшей мере 2:1.
В одном варианте реализации, соотношение составляет по меньшей мере 3:1. В одном варианте реализации, соотношение составляет по меньшей мере 4:1. В одном варианте реализации, соотношение составляет по меньшей мере 5:1. В одном варианте реализации, соотношение составляет по меньшей мере 7,5:1. В одном варианте реализации, соотношение составляет по меньшей мере 10:1. В одном варианте реализации, соотношение составляет по меньшей мере 12,5:1. В одном варианте реализации, соотношение составляет по меньшей мере 15:1. В одном варианте реализации, соотношение составляет по меньшей мере 17,5:1. В одном варианте реализации, соотношение составляет по меньшей мере 20:1.
В другом варианте реализации, соотношение составляет по меньшей мере 50:1. В другом варианте реализации, соотношение составляет по меньшей мере 75:1. В другом варианте реализации, соотношение составляет по меньшей мере 100:1. В другом варианте реализации, соотношение составляет по меньшей мере 250:1. В другом варианте реализации, соотношение составляет по меньшей мере 500:1. В другом варианте реализации, соотношение составляет по меньшей мере 750:1. В другом варианте реализации, соотношение составляет по меньшей мере 1000:1.
В другом варианте реализации, соотношение составляет по меньшей мере 1250:1. В другом варианте реализации, соотношение составляет по меньшей мере 1500:1. В другом варианте реализации, соотношение составляет по меньшей мере 1750:1. В другом варианте реализации, соотношение составляет по меньшей мере 2000:1.
Аспект 50. Иммуноцитокин согласно любому из предшествующих аспектов, где антигенсвязывающий сайт связывается с hPD-L1 с аффинностью менее 500 пМ (например, менее 300 пМ, или меньше 200 пМ), где, необязательно, иммуноцитокин обеспечивает соотношение активности IL-2 против высокоаффинного (αβγ) рецептора IL-2 к аффинности антигенсвязывающего сайта анти-PD-L1 против hPD-L1, равное по меньшей мере 2:1.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью менее 200 пМ. В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью менее 100 пМ или меньше 50 пМ.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 50 до 500 пМ или от 75 до 500 пМ или от 100 до 500 пМ или от 200 пМ до 500 пМ.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 50 до 400 пМ или от 50 до 300 пМ или от 50 до 200 пМ или от 50 до 100 пМ.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 100 до 500 пМ или от 100 до 400 пМ или от 100 до 300 пМ.
В одном варианте реализации, соотношение активности цитокина IL-2 против высокоаффинного (αβγ) рецептора к аффинности антигенсвязывающего сайта против PD-L1 к hPD-L1 составляет по меньшей мере 3:1. В одном варианте реализации, соотношение активности цитокина IL-2 против высокоаффинного (αβγ) рецептора к аффинности антигенсвязывающего сайта против PD-L1 к hPD-L1 составляет по меньшей мере 4:1. В одном варианте реализации, соотношение активности цитокина IL-2 против высокоаффинного (αβγ) рецептора к аффинности антигенсвязывающего сайта против PD-L1 к hPD-L1 составляет по меньшей мере 5:1. В одном варианте реализации, соотношение активности цитокина IL-2 против высокоаффинного (αβγ) рецептора к аффинности антигенсвязывающего сайта против PD-L1 к hPD-L1 составляет по меньшей мере 7:1. В одном варианте реализации, соотношение активности цитокина IL-2 против высокоаффинного (αβγ) рецептора к аффинности антигенсвязывающего сайта анти-PD-L1 против hPD-L1 составляет по меньшей мере 10:1.
Любые из показателей периода полувыведения, константы скорости ассоциации (KON), константы скорости диссоциации (KOFF) или характеристик связывания анти-PD-L1 антител в концепциях 1-40 являются применимыми, с соответствующими изменениями (mutatis mutandis) к иммуноцитокинам, раскрытым в данном документе.
Аспект 50а. Иммуноцитокин согласно любому из предшествующих аспектов, где антигенсвязывающий сайт связывается с mPD-L1 (SEQ ID NO: 325) с аффинностью менее 500 нМ (например, менее 100 нМ, менее 10 нМ или меньше 1 нМ).
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 1 до 500 нМ, или от 1 до 250 нМ, или от 1 до 100 нМ, или от 1 до 50 нМ.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 10 до 500 нМ, или от 10 до 250 нМ, или от 10 до 100 нМ, или от 1 до 50 нМ, в частности, от 10 до 100 нМ.
В одном варианте реализации, антигенсвязывающий сайт связывается с hPD-L1 с аффинностью от 100 до 500 нМ, или от 100 до 400 нМ, или от 100 до 300 нМ, или от 100 до 200 нМ.
Аффинность антигенсвязывающего сайта с hPD-L1 или mPD-L1 может быть измерена любым способом, хорошо известным специалистам в данной области. В одном варианте реализации, аффинность измеряют методом SPR, который детально описан выше.
Аспект 51. Иммуноцитокин, как определено в любом предшествующем аспекте, для использования при лечении или профилактике опосредованного hPD-L1 заболевания или состояния, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (таких как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная B-клеточная лимфома (например, меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого рак (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи и мезотелиома, или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Аспект 52. Использование иммуноцитокина, как определено в любом из аспектов 1-50, при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики опосредованного hPD-L1 заболевания или состояния у человека, например, где опосредованное hPD-L1 заболевание или состояние выбрано из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная B-клеточная лимфома (например, меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Аспект 53. Способ лечения или профилактики опосредованного hPD-L1 заболевания или состояния, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная B-клеточная лимфома (например, меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей) у человека, включающий введение указанному человеку терапевтически эффективного количества иммуноцитокина, как определено в любом из аспектов 1-50, посредством чего осуществляется лечение или профилактика опосредуемого hPD-L1 заболевания или состояния.
В любом из аспектов 51-53, опосредованное hPD-L1 заболевание может быть любым из описанных в данном документе. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание представляет собой вирусно-индуцированное раковое заболевание, такое как рак шейки матки и рак носоглотки, например, рак шейки матки, вызванный инфекцией ВПЧ. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание представляет собой хроническую вирусную инфекцию. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание является неопластическим заболеванием. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание является не связанным с новообразованиями заболеванием. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание является злокачественной опухолью. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание представляет собой рак, который, как известно, реагирует на терапию PD-L1, такой как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание представляет собой рак, являющийся саркомой мягких тканей. В одном варианте реализации, в любом из аспектов 51-53, опосредованное hPD-L1 заболевание представляет собой нейродегенеративное заболевание, расстройство или состояние где нейродегенеративное заболевание, расстройство или состояние, необязательно, выбраны из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона, болезни Хантингтона, первичного прогрессирующего рассеянного склероза, вторичного прогрессирующего рассеянного склероза, кортикобазальной дегенерации, синдрома Ретта, дегенеративного расстройства сетчатки, выбранного из возрастной дегенерации желтого пятна и пигментного ретинита; передней ишемической оптической нейропатии, глаукомы, увеита, депрессии, связанного с травмой стресса или посттравматического стрессового расстройства, лобно-височной деменции, деменций тела Леви, легких когнитивных нарушений, атрофии задней коры головного мозга, первичной прогрессирующей афазии и прогрессирующего супрануклеарного паралича или связанной с возрастом деменции, в частности, болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона и болезни Хантингтона и, например, болезни Альцгеймера.
Аспект 54. Иммуноцитокин согласно аспекту 51, применение согласно аспекту 52 или способ согласно аспекту 53, где опосредованное hPD-L1 заболевание или состояние является раком.
Аспект 55. Иммуноцитокин, использование или способ согласно аспекту 54, где рак выбран из меланомы, рака клеток Меркеля, немелкоклеточного рака легкого, рака мочевого пузыря, неходжкинских лимфом, колоректального рака с микросателлитной нестабильностью (MSI) или рака, выбранного из рака молочной железы, рака яичников, колоректального рака (без MSI или микросателлитной нестабильности), в частности, меланомы и почечно-клеточного рака.
В одном варианте реализации, рак представляет собой рак, который, как известно, реагирует как на терапию IL-2, так и на терапию PD-L1, такой как меланома и почечно-клеточный рак.
В одном варианте реализации, рак представляет собой колоректальный рак с микросателлитной нестабильностью (MSI). В одном варианте реализации, рак представляет собой рак молочной железы. В одном варианте реализации, рак представляет собой рак яичников.
Аспект 56. Иммуноцитокин, использование или способ по любому из аспектов 51-55, дополнительно включающий введение человеку дополнительной терапии, например, дополнительного терапевтического агента, где, необязательно, дополнительный терапевтическое средство независимо выбирают из группы, состоящей из:
A) других ингибиторов иммунных контрольных точек (таких как антитела против TIM-3, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
B) иммунных стимуляторов (таких как антитела против ОХ40, антитела против GITR, антитела против CD137, антитела против ICOS и антитела против CD40);
C) антагонистов хемокиновых рецепторов (таких как CXCR4, CCR4 и CXCR2);
D) таргетных ингибиторов киназ (таких как ингибиторы CSF-1R или VEGFR);
E) ингибиторов ангиогенеза (таких как анти-VEGF-A или дельта-подобный лиганд-4);
F) иммуностимулирующих пептидов или хемокинов (таких как CXCL9 или CXCL10);
G) цитокинов (таких как IL-15 и IL-21);
H) биспецифических антагонистов Т-клеток (BiTE), имеющих по меньшей мере одну специфичность против CD3 (например, CD3/CD19 BiTE);
I) других биспецифических молекул (например, IL-15-содержащих молекул, нацеленных на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (NY-ESO-1), GD2, EpCAM или ассоциированный с меланомой антиген-3 (MAGE-А3));
J) онколитических вирусов (таких как вирус HSV (вирус герпеса человека) (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины);
K) вакцинации опухоль-ассоциированными антигенами (такими как рака пищевода New York Esophageal Cancer-1 [NY-ESO-1], ассоциированный с меланомой антиген-3 [MAGE-3]);
L) клеточных терапий (таких как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или антимезотелин);
М) биспецифические активаторы (engagers) NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a; и
N) адоптивного переноса опухолеспецифических Т-клеток или клеток LAK,
или, необязательно, дополнительная терапия представляет собой химиотерапию, лучевую терапию и хирургическое удаление опухолей.
Лучевая терапия может проводиться с однократной дозой или дробными дозами, с облучением непосредственно пострадавших тканей либо всего организма.
В этом аспекте, любые признаки и варианты реализации концепции 46 являются применимыми mutatis mutandis.
В этом аспекте, биспецифические молекулы включают «биспецифические антитела» и гибридные белки антител, включая форматы и молекулы, описанные в концепциях 37-40.
Антитела могут представлять собой любую из последовательностей или антител, описанных в схеме 5, 5а, или подробно описанных в Аспекте 1а.
Аспект 57. Фармацевтическая композиция, содержащая иммуноцитокин, как определено в любом из аспектов 1-50, и фармацевтически приемлемый эксципиент, разбавитель или носитель и, необязательно, дополнительно содержащая дополнительный терапевтическое средство, независимо выбранный из группы, состоящей из:
A) других ингибиторов иммунных контрольных точек (таких как антитела против TIM-3, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
B) иммунных стимуляторов (таких как антитела против ОХ40, антитела против GITR, антитела против CD137, антитела против ICOS и антитела против CD40);
C) антагонистов хемокиновых рецепторов (таких как CXCR4, CCR4 и CXCR2);
D) таргетных ингибиторов киназ (таких как ингибиторы CSF-1R или VEGFR);
E) ингибиторов ангиогенеза (таких как анти-VEGF-A или дельта-подобный лиганд-4);
F) иммуностимулирующих пептидов или хемокинов (таких как CXCL9 или CXCL10);
G) цитокинов (таких как IL-15 и IL-21);
H) биспецифических антагонистов Т-клеток (BiTE), имеющих по меньшей мере одну специфичность против CD3 (например, CD3/CD19 BiTE);
I) других биспецифических молекул (например, IL-15-содержащих молекул, нацеленных на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (NY-ESO-1), GD2, EpCAM или ассоциированный с меланомой антиген-3 (MAGE-А3));
J) онколитических вирусов (таких как вирус HSV (вирус герпеса человека) (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины);
K) вакцинации опухоль-ассоциированными антигенами (такими как рака пищевода New York Esophageal Cancer-1 [NY-ESO-1], ассоциированный с меланомой антиген-3 [MAGE-3]);
L) клеточных терапий (таких как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или антимезотелин);
М) биспецифические активаторы (engagers) NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a; и
N) адоптивного переноса опухолеспецифических Т-клеток или клеток LAK.
В одном варианте реализации, дополнительный терапевтическое средство вводят последовательно или одновременно с иммуноцитокином.
В этом аспекте, любые признаки и варианты реализации концепции 48 являются применимыми mutatis mutandis (с учетом соответствующих различий).
В этом аспекте, биспецифические молекулы включают «биспецифические антитела» и гибридные белки антител, включая форматы и молекулы, описанные в концепциях 37-40.
Антитела могут представлять собой любую из последовательностей или антител, описанных в схеме 5, 5а, или подробно описанных в Аспекте 1а.
Аспект 58. Фармацевтическая композиция согласно аспекту 57 или набор, включающий фармацевтическую композицию, как определено в аспекте 57, где композиция предназначена для лечения и/или профилактики опосредованного hPD-L1 заболевания или состояния, например, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (например, рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная B-клеточная лимфома (например, меланома, рак молочной железы, рак яичников, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, колоректальный рак (без MSI или микросателлитной нестабильности), плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Аспект 59. Фармацевтическая композиция согласно аспекту 57 или аспекту 58 в комбинации с, или набор согласно аспекту 58, содержащий этикетку или инструкции по применению для лечения и/или профилактики указанного заболевания или состояния у человека; где, необязательно, этикетка или инструкции содержат номер регистрационного удостоверения лекарственного средства (например, номер разрешения FDA или ЕМА); где, необязательно, набор включает устройство для внутривенного введения (IV) или инъекционное устройство, содержащее иммуноцитокин.
Аспект 60. Способ лечения пролиферативного заболевания у животного (например, человека), включающий введение эффективного количества иммуноцитокина, как определено в любом из аспектов 1-50, указанному пациенту.
Пролиферативные заболевания могут быть любыми из описанных в других разделах данного документа.
Аспект 61. Нуклеиновая кислота, кодирующая тяжелую цепь и/или легкую цепь иммуноцитокина, как определено в любом из аспектов 1-50.
В одном варианте реализации, нуклеиновая кислота кодирует легкую цепь иммуноцитокина, как определено в любом из аспектов 1-50.
Аспект 62. Вектор, содержащий нуклеиновую кислоту, как определено в аспекте 61; где вектор, необязательно, представляет собой вектор СНО или HEK293.
Аспект 63. Хозяин, содержащий нуклеиновую кислоту, как определено в аспекте 61, или вектор, как определено в аспекте 62.
4. ICOS-антитела
В данном документе предусматриваются ICOS-антитела. Антитела ICOS могут быть любыми из описанных в патентной заявке GB 1620414.1 (поданной 1 декабря 2016 г.), раскрытые в ней последовательности анти-ICOS антител включены в данный документ посредством ссылок.
STIM001 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 366, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 363, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 364, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 365. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 367. STIM001 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 373, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 370, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 371, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 372. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 374. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 368 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 369). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 375 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 376).
STIM002 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 380, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 377, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 378, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 379. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 381. STIM002 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 387, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 384, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 385, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 386. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 388 или SEQ ID NO: 519. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 382 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 383). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 389 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 390 или SEQ ID NO: 520).
STIM002-B имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 394, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 391, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 392, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 393. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 395. STIM002-B имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 401, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 398, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 399, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 400. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 402. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 396 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 397). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 403 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 404).
STIM003 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 408, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 405, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 406, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 407. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 409 или SEQ ID NO: 521. STIM003 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 415, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 412, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 413, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 414. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 4416. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 410 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 411 или SEQ ID NO: 522). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 417 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 418).
STIM004 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 422, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 419, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 420, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 421. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 423. STIM004 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 429, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 426, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 427, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 428. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 430 или SEQ ID NO: 431. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 424 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 425). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 432 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 433 или SEQ ID NO: 434).
STIM005 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 438, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 435, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 436, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 437. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 439. STIM005 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 445, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 442, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 443, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 444. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 446. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 440 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 441). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 447 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 448).
STIM006 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 452, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 449, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 450, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 451. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 453. STIM006 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 459, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 456, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 457, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 458. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 460. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 454 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 455). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 461 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 462).
STIM007 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 466, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 463, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 464, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 465. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 467. STIM007 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 473, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 470, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 471, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 472. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 474. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 468 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 469). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 475 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 476).
STIM008 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 480, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 477, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 478, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 479. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 481. STIM008 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 487, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 484, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 485, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 486. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 488. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 482 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 483). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 489 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 490).
STIM009 имеет аминокислотную последовательность вариабельной области тяжелой цепи (VH), представленную SEQ ID NO: 494, содержащую аминокислотную последовательность CDRH1, представленную SEQ ID NO: 491, аминокислотную последовательность CDRH2, представленную SEQ ID NO: 492, и аминокислотную последовательность CDRH3, представленную SEQ ID NO: 493. Последовательность нуклеиновой кислоты тяжелой цепи домена VH представлена SEQ ID NO: 495. STIM009 имеет аминокислотную последовательность вариабельной области легкой цепи (VL), представленную SEQ ID NO: 501, содержащую аминокислотную последовательность CDRL1, представленную SEQ ID NO: 498, аминокислотную последовательность CDRL2, представленную SEQ ID NO: 499, и аминокислотную последовательность CDRL3, представленную SEQ ID NO: 500. Последовательность нуклеиновой кислоты легкой цепи домена VL представлена SEQ ID NO: 502. Домен VH может быть объединена с любой из последовательностей константной области тяжелой цепи, описанной в данном документе, например, SEQ ID NO: 193, SEQ ID NO: 195, SEQ ID NO: 197, SEQ ID NO: 199, SEQ ID NO: 201, SEQ ID NO: 203, Seq ID Nos: 205, Seq ID Nos: 340, Seq ID Nos: 524, Seq ID Nos: 526, Seq ID Nos: 528, Seq ID Nos: 530, SEQ ID NO: 532 или SEQ ID NO: 534. Область VL может быть объединена с любой из последовательностей константной области легкой цепи, описанной в данном документе, например, SEQ ID NOs: 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 536 и 538. Полноразмерная аминокислотная последовательность тяжелой цепи представлена SEQ ID NO: 496 (последовательность нуклеиновой кислоты тяжелой цепи - SEQ ID NO: 497). Полноразмерная аминокислотная последовательность легкой цепи представлена SEQ ID NO: 503 (последовательность нуклеиновой кислоты легкой цепи - SEQ ID NO: 504).
Антитела STIM001-009 описаны более подробно в патентной заявке GB 1620414.1 (поданной 1 декабря 2016 г.), содержание которой включено в данный документ посредством ссылки. Антитела ICOS также могут быть описаны, как указано в пронумерованных предложениях ниже:
Предложение 1. Выделенное антитело, которое связывает внеклеточный домен ICOS человека и/или мыши, содержащее:
домен VH антитела, содержащий гипервариабельные участки (CDR) HCDR1, HCDR2 и HCDR3, и
домен VL антитела, содержащий гипервариабельные участки LCDR1, LCDR2 и LCDR3, где
HCDR1 представляет собой HCDR1 STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой HCDR1 с 1, 2, 3, 4 или 5 аминокислотными изменениями,
HCDR2 представляет собой HCDR2 STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой HCDR2 с 1, 2, 3, 4 или 5 аминокислотными изменениями и/или
HCDR3 представляет собой HCDR3 STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой HCDR3 с 1, 2, 3, 4 или 5 аминокислотными изменениями.
Предложение 2. Антитело согласно предложению 1, где CDR тяжелой цепи антитела являются CDR STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержат CDR тяжелой цепи STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009 с 1, 2, 3, 4 или 5 аминокислотными изменениями.
Предложение 3. Антитело согласно предложению 2, где домен VH антитела имеет CDR тяжелой цепи STIM003.
Предложение 4. Выделенное антитело, которое связывает внеклеточный домен ICOS человека и/или мыши, содержащее:
домен VH антитела, содержащий гипервариабельные участки HCDR1, HCDR2 и HCDR3, и
домен VL антитела, содержащий гипервариабельные участки LCDR1, LCDR2 и LCDR3,
где LCDR1 представляет собой LCDR1 STIM001, STIM002, STIM002-B, STIM003, STIM004 STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой LCDR1 с 1, 2, 3, 4 или 5 аминокислотными изменениями,
LCDR2 представляет собой LCDR2 STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой LCDR2 с 1, 2, 3, 4 или 5 аминокислотными изменениями и/или
LCDR3 представляет собой LCDR3 STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержит такой LCDR3 с 1, 2, 3, 4 или 5 аминокислотными изменениями.
Предложение 5. Антитело согласно любому из предшествующих предложений, в котором CDR легкой цепи антитела являются CDR STIM001, STIM002, STIM002-В, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или содержат CDR легкой цепи STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009 с 1, 2, 3, 4 или 5 аминокислотными изменениями.
Предложение 6. Антитело согласно предложению 5, где домен VL антитела имеет CDR легкой цепи STIM003.
Предложение 7. Антитело согласно любому из предшествующих предложений, содержащее каркасные области доменов VH и/или VL последовательностей генных сегментов зародышевой линии человека.
Предложение 8. Антитело согласно любому из предшествующих предложений, содержащее домен VH, который
(i) получают в результате рекомбинации V генного сегмента тяжелой цепи человека, D генного сегмента тяжелой цепи человека и J генного сегмента тяжелой цепи человека, где
V сегмент представляет собой IGHV1-18 (например, V1-18*01), IGVH3-20 (например, V3-20*d01), IGVH3-11 (например, V3-11*01) или IGVH2-5 (например, V2-5*10);
D генный сегмент представляет собой IGHD6-19 (например, IGHD6-19*01), IGHD3-10 (например, IGHD3-10*01) или IGHD3-9 (например, IGHD3-9*01); и/или
J генный сегмент представляет собой IGHJ6 (например, IGHJ6*02), IGHJ4 (например, IGHJ4*02) или IGHJ3 (например, IGHJ3*02), или
(ii) содержит каркасные области FR1, FR2, FR3 и FR4, где
FR1 выравнивается с V генным сегментом зародышевой линии человека IGHV1-18 (например, V1-18*01), IGVH3-20 (например, V3-20*d01), IGVH3-11 (например, V3-11*01) или IGVH2-5 (например, V2-5*10), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями,
FR2 выравнивается с V генным сегментом зародышевой линии человека IGHV1-18 (например, V1-18*01), IGVH3-20 (например, V3-20*d01), IGVH3-11 (например, V3-11*01) или IGVH2-5 (например, V2-5*10), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями,
FR3 выравнивается с V генным сегментом зародышевой линии человека IGHV1-18 (например, V1-18*01), IGVH3-20 (например, V3-20*d01), IGVH3-11 (например, V3-11*01) или IGVH2-5 (например, V2-5*10), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями и/или
FR4 выравнивается с J генным сегментом зародышевой линии IGJH6 (например, JH6*02), IGJH4 (например, JH4*02) или IGJH3 (например, JH3*02), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями,
Предложение 9. Антитело согласно любому из предшествующих предложений, содержащее домен VL антитела, который
(i) получают в результате рекомбинации V генного сегмента легкой цепи человека и J генного сегмента легкой цепи человека, где
V сегмент представляет собой IGKV2-28 (например, IGKV2-28*01), IGKV3-20 (например, IGKV3-20*01), IGKV1D-39 (например, IGKV1D-39*01), или IGKV3-11 (например, IGKV3-11*01), и/или
J генный сегмент представляет собой IGKJ4 (например, IGKJ4*01), IGKJ2 (например, IGKJ2*04), IGLJ3 (например, IGKJ3*01) или IGKJ1 (например, IGKJ1 *01); или
(ii) содержит каркасные области FR1, FR2, FR3 и FR4, где
FR1 выравнивается с V генным сегментом зародышевой линии человека IGKV2-28 (например, IGKV2-28*01), IGKV3-20 (например, IGKV3-20*01), IGKV1D-39 (например, IGKV1D-39*01) или IGKV3-11 (например, IGKV3-11*01), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями,
FR2 выравнивается с V генным сегментом зародышевой линии человека IGKV2-28 (например, IGKV2-28*01), IGKV3-20 (например, IGKV3-20*01), IGKV1D-39 (например, IGKV1D-39*01) или IGKV3-11 (например, IGKV3-11*01), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями,
FR3 выравнивается с V генным сегментом зародышевой линии человека IGKV2-28 (например, IGKV2-28*01), IGKV3-20 (например, IGKV3-20*01), IGKV1D-39 (например, IGKV1D-39*01) или IGKV3-11 (например, IGKV3-11*01), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями и/или
FR4 выравнивается с J генным сегментом зародышевой линии человека IGKJ4 (например, IGKJ4*01), IGKJ2 (например, IGKJ2*04), IGKJ3 (например, IGKJ3*01) или IGKJ1 (например, IGKJ1*01), необязательно, с 1, 2, 3, 4 или 5 аминокислотными изменениями.
Предложение 10. Антитело согласно любому из предшествующих предложений, включающее домен VH антитела, который является доменом VH STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или который имеет аминокислотную последовательность, по меньшей мере на 90% идентичную последовательности домена VH антитела STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009.
Предложение 11. Антитело согласно любому из предшествующих предложений, содержащее домен VL антитела, который является доменом VL STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или который имеет аминокислотную последовательность, по меньшей мере на 90% идентичную последовательности домена VL антитела STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009.
Предложение 12. Антитело согласно предложению 11, содержащее
домен антитела VH, который выбирают из домена VH STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, или который имеет аминокислотную последовательность, по меньшей мере на 90% идентичную последовательности домена VH антитела STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009, и
домен VL антитела, который является доменом VL указанного выбранного антитела, или который имеет аминокислотную последовательность, по меньшей мере на 90% идентичную последовательности домена VL указанного выбранного антитела.
Предложение 13. Антитело согласно предложению 12, содержащее домен VH STIM003 и домен VL STIM003.
Предложение 14. Антитело согласно любому из предшествующих предложений, содержащее константную область антитела.
Предложение 15. Антитело согласно предложению 14, в котором константная область содержит константную область тяжелой и/или легкой цепи человека.
Предложение 16. Антитело согласно предложению 14 или предложению 15, где константная область является положительной к Fc-эффектору.
Предложение 17. Антитело согласно предложению 16, содержащее Fc-область, которая имеет улучшенную функцию ADCC, ADCP и/или CDC по сравнению с нативной Fc-областью человека.
Предложение 18. Антитело согласно любому из предложений 14-17, где антитело представляет собой IgG1.
Предложение 19. Антитело согласно предложению 17 или предложению 18, в котором антитело является афукозилированным.
Предложение 20. Антитело согласно любому из предшествующих предложений, конъюгированное с цитотоксическим лекарственным средством или пролекарством.
Предложение 21. Антитело согласно любому из предшествующих предложений, которое является мультиспецифическим антителом.
Предложение 22. Выделенное антитело, которое конкурирует за связывание с человеческим ICOS с антителом IgG1 человека, содержащим гипервариабельные участки тяжелой и легкой цепей STIM001, STIM002, STIM002-B, STIM003, STIM004, STIM005, STIM006, STIM007, STIM008 или STIM009,
Предложение 23. Выделенное антитело, которое связывает внеклеточный домен ICOS человека и мыши с аффинностью (KD) менее 50 нМ, по результатам определения методом поверхностного плазмонного резонанса.
Предложение 24. Антитело согласно предложению 23, где антитело связывает внеклеточный домен ICOS человека и мыши с аффинностью (KD) менее 5 нМ, по результатам определения методом поверхностного плазмонного резонанса.
Предложение 25. Антитело согласно предложению 23 или предложению 24, где KD связывания внеклеточного домена ICOS человека находится в пределах 10-кратного по сравнению с KD связывания внеклеточного домена ICOS мыши.
Предложение 26. Композиция, содержащая выделенное антитело согласно любому из предшествующих предложений и фармацевтически приемлемый эксципиент.
Предложение 27. Композиция, содержащая выделенную нуклеиновую кислоту, кодирующую антитело согласно любому из предложений 1-25 и фармацевтически приемлемый эксципиент.
Предложение 28. Способ истощения регуляторных Т-клеток и/или усиления эффекторного ответа Т-клеток у пациента, включающий введение пациенту композиции согласно предложению 26.
Предложение 29. Способ лечения заболевания или состояния, восприимчивых к терапии путем истощения регуляторных Т-клеток и/или усиление эффекторного ответа Т-клеток у пациента, включающий введение пациенту композиции согласно предложению 26.
Предложение 30. Композиция согласно предложению 26 для использования в методе лечения человеческого организма путем терапии.
Предложение 31. Композиция для использования согласно предложению 30, предназначенная для использования при истощении регуляторных Т-клеток и/или усилении эффекторного ответа Т-клеток у пациента.
Предложение 32. Композиция для применения согласно предложению 30, предназначенная для использования при лечении заболевания или состояния, восприимчивого к лечению путем истощения регуляторных Т-клеток и/или усиления эффекторного ответа Т-клеток у пациента.
Предложение 33. Способ согласно предложению 29 или композиция для использования согласно предложению 32, где заболевание представляет собой рак или солидную опухоль.
Предложение 34. Способ или композиция для использования согласно любому из предложений 29-33, где способ включает введение пациенту антитела и другого терапевтического агента.
Предложение 35. Способ или композиция для использования согласно предложению 34, где терапевтическое средство представляет собой антитело против PDL1.
Предложение 36. Способ или композиция для использования согласно предложению 35, в котором антитело против ICOS и антитело против PDL1 могут каждое медиировать ADCC, ADCP и/или CDC.
Предложение 37. Способ или композиция для использования согласно предложению 35, где антитело против ICOS представляет собой антитело IgG1 человека, и антитело против PDL1 представляет собой антитело IgG1 человека.
Предложение 38. Способ или композиция для использования согласно предложению 34, где другим терапевтическим агентом является IL-2.
Предложение 39. Способ или композиция для использования согласно любому из предложений 34-38, где способ включает введение анти-ICOS антитела после введения другого терапевтического агента.
Предложение 40. Способ или композиция для использования согласно любому из предложений 28-39, где
антитело против ICOS конъюгировано с пролекарством, и где
способ или применение включают
введение пациенту анти-ICOS антитела и
селективную активацию пролекарства в области ткани-мишени.
Предложение 41. Способ или композиция для использования согласно предложению 40, в которых у пациента имеется солидная опухоль, и способ включает селективную активацию пролекарства в опухоли.
Предложение 42. Способ или композиция для использования согласно приговору 40 или предложению 41, включающие селективную активацию пролекарства посредством фотоактивации.
Предложение 43. Комбинация антитела IgG1 против ICOS человека и антитела IgG1 против PDL1 человека для использования в способе лечения рака.
Предложение 44. Комбинация согласно предложению 43, где антитело против ICOS и антитело против PDL1 предусматриваются в отдельных композициях для введения.
Предложение 45. Способ или композиция для использования согласно предложению 37 или комбинация согласно предложению 43 или предложению 44, в которых константная область IgG1 человека имеет аминокислотную последовательность дикого типа, представленную в приложенном перечне последовательностей.
Предложение 46. Анти-ICOS антитело для использования в способе уменьшения или реверсирования скачка ICOS-положительных регуляторных Т-клеток у пациента, при этом скачок возникает в результате лечения пациента другим терапевтическим агентом.
Предложение 47. Способ лечения пациента, включающий уменьшение или реверсирование скачка ICOS-положительных регуляторных Т-клеток у пациента, при этом скачок возникает в результате лечения пациента другим терапевтическим агентом.
Предложение 48. Анти-ICOS антитело для использования в способе лечения пациента, включающем введение анти-ICOS антитела пациенту с повышенным уровнем ICOS-положительных регуляторных Т-клеток после лечения другим терапевтическим агентом.
Предложение 49. Способ лечения пациента, включающий введение анти-ICOS антитела пациенту с повышенным уровнем ICOS-положительных регуляторных Т-клеток после лечения другим терапевтическим агентом.
Предложение 50. Анти-ICOS антитело для использования согласно предложению 46 или предложению 48, или способ согласно предложению 47 или предложению 49, где способ включает введение терапевтического агента пациенту, определение того, что пациент имеет повышенный уровень ICOS-положительных регуляторных Т-клеток после лечения указанным агентом, и введение пациенту анти-ICOS антитела для снижения уровня регуляторных Т-клеток.
Предложение 51. Антитело против ICOS для использования или способ согласно любому из предложений 46-50, где терапевтическим агентом является IL-2 или иммуномодулирующее антитело (например, анти-PDL-1, анти-PD-1 или анти-CTLA-4).
Предложение 52. Антитело против ICOS для использования или способ согласно любому из предложений 46-51, где способ включает лечение опухоли, например, меланомы, такой как метастазирующая меланома.
Предложение 53. Анти-ICOS антитело для использования в способе лечения рака у пациента путем вакцинации пациента in vivo против его раковых клеток, причем способ включает
лечение пациента терапией, которая вызывает иммунологическую гибель раковых клеток, что приводит к презентации антигена антигенспецифическим эффекторным Т-клеткам, и
введение пациенту анти-ICOS антитела, причем анти-ICOS антитело усиливает антигенспецифический эффекторный T-клеточный ответ.
Предложение 54. Способ лечения рака у пациента путем in vivo вакцинации пациента против его раковых клеток, включающий
лечение пациента терапией, которая вызывает иммунологическую гибель раковых клеток, что приводит к презентации антигена антигенспецифическим эффекторным Т-клеткам, и
введение пациенту анти-ICOS антитела, причем анти-ICOS антитело усиливает антигенспецифический эффекторный T-клеточный ответ.
Предложение 55. Способ лечения рака у пациента путем in vivo вакцинации пациента против его раковых клеток, причем способ включает введение пациенту анти-ICOS антитела, где
пациентом является тот, кто ранее лечился терапией, вызывающей иммунологическую гибель раковых клеток, что приводит к презентации антигена антигенспецифическим эффекторным Т-клеткам, и где
анти-ICOS антитело усиливает антигенспецифический эффекторный T-клеточный ответ.
Предложение 56. Анти-ICOS антитело для использования или способ согласно любому из предложений 53-55, где терапия, которая вызывает иммунологическую гибель клеток, представляет собой облучение раковых клеток, введение химиотерапевтического агента и/или введение антитела, нацеленного на опухоль-ассоциированный антиген.
Предложение 57. Анти-ICOS антитело для использования или способ согласно предложению 56, где химиотерапевтическим агентом является оксалиплатин.
Предложение 58. Анти-ICOS антитело для использования или способ согласно предложению 56, где опухоль-ассоциированный антиген представляет собой HER2 или CD20.
Предложение 59. Анти-ICOS антитело для использования в способе вакцинации пациента, где способ включает введение пациенту антитела и композиции вакцины.
Предложение 60. Способ вакцинации пациента, включающий введение пациенту анти-ICOS антитела и композиции вакцины.
Предложение 61. Анти-ICOS антитело для использования согласно предложению 59 или способ согласно предложению 60, в котором композиция вакцины представляет собой вакцину против гепатита В, малярии или ВИЧ.
Предложение 62. Анти-ICOS антитело для использования в способе лечения рака у пациента, где рак является или был охарактеризован как положительный по экспрессии лиганда ICOS и/или FOXP3.
Предложение 63. Способ лечения рака у пациента, у которого рак является или был охарактеризован как положительный по экспрессии лиганда ICOS и/или FOXP3, причем способ включает введение пациенту антитела против ICOS.
Предложение 64. Анти-ICOS антитело для использования согласно предложению 62 или способ согласно предложению 63, в котором способ включает:
тестирование образца от пациента для определения того, экспрессирует ли рак лиганд ICOS и/или FOXP3;
выбор пациента для лечения антителом против ICOS; и
введение пациенту анти-ICOS антитела.
Предложение 65. Анти-ICOS антитело для использования согласно предложению 62 или способ согласно предложению 63, где способ включает введение анти-ICOS антитела пациенту, для которого тестируемый образец показал, что рак является положительным по экспрессии лиганда ICOS и/или FOXP3.
Предложение 66. Анти-ICOS антитело для использования или способ согласно предложению 64 или предложению 65, где образец представляет собой биопсийный образец солидной опухоли.
Предложение 67. Анти-ICOS антитело для использования в способе лечения рака у пациента, где рак является или был охарактеризован как невосприимчивый к лечению иммуноонкологическим препаратом, например, антителом против CTLA-4, антителом против PD1, антителом против PD-L1, антителом против CD137 или антителом против GITR.
Предложение 68. Способ лечения рака у пациента, у которого рак является или был охарактеризован как невосприимчивый к лечению иммуноонкологическим лекарственным средством, например, антителом против CTLA-4, антителом против PD1, анти-PD-L1 антителом, анти-CD137-антитело или антитело против GITR, причем способ включает введение пациенту анти-ICOS антитела.
Предложение 69. Анти-ICOS антитело для использования согласно предложению 67 или способ согласно предложению 68, где способ включает:
лечение пациента иммуноонкологическим препаратом;
определение того, что рак не реагирует на препарат;
выбор пациента для лечения антителом против ICOS; и
введение пациенту анти-ICOS антитела.
Предложение 70. Анти-ICOS антитело для использования согласно предложению 67 или способ согласно предложению 68, в котором способ включает введение анти-ICOS антитела пациенту, у которого рак не реагирует на предыдущее лечение иммуноонкологическим препаратом.
Предложение 71. Анти-ICOS антитело для использования или способ согласно любому из предложений 62-70, где рак представляет собой опухоль, образовавшуюся из клеток, которые приобрели способность экспрессировать лиганд ICOS.
Предложение 72. Анти-ICOS антитело для использования или способ согласно предложению 71, где рак является меланомой.
Предложение 73. Анти-ICOS антитело для использования или способ согласно любому из предложений 62-70, где рак происходит от антигенпрезентирующей клетки, такой как В-лимфоцит (например, B-клеточная лимфома, такая как диффузная крупноклеточная B-клеточная лимфома) или Т-лимфоцит.
Предложение 74. Анти-ICOS антитело для использования или способ согласно любому из предложений 62-70, где рак является невосприимчивым к лечению анти-CD20 антителом.
Предложение 75. Анти-ICOS антитело для использования или способ согласно предложению 74, где рак является B-клеточной лимфомой.
Предложение 76. Анти-ICOS антитело для использования или способ согласно предложению 75, где анти-CD20 антитело представляет собой ритуксимаб.
Предложение 77. Анти-ICOS антитело для использования или способ согласно любому из предложений 74-76, где способ включает лечение пациента анти-CD20 антителом;
определение того, что рак не реагирует на анти-CD20 антитело;
тестирование образца пациента для определения того, экспрессирует ли рак лиганд ICOS;
выбор пациента для лечения антителом против ICOS; и
введение пациенту анти-ICOS антитела.
Предложение 78. Анти-ICOS антитело для использования или способ согласно любому из предложений 74-76, где способ включает введение анти-ICOS антитела пациенту, у которого рак не реагирует на предшествующее лечение анти-CD20 антителом.
Предложение 79. Анти-ICOS антитело для использования или способ согласно любому из предложений 52-78, где рак представляет собой солидную опухоль.
Предложение 80. Анти-ICOS антитело для использования или способ согласно любому из предложений 52-78, где рак представляет собой гематологическую жидкую опухоль.
Предложение 81. Анти-ICOS антитело для использования или способ согласно предложению 79 или 80, где опухоль имеет высокое содержание регуляторных Т-клеток.
Предложение 82. Анти-ICOS антитело для использования или способ согласно любому из предложений 43-81, где антитело против ICOS является таким, как определено в любом из предложений 1-25, или предусматривается в композиции согласно предложению 26.
Предложение 83. Трансгенное млекопитающее, не являющееся человеком, имеющее геном, содержащий человеческий или гуманизированный локус иммуноглобулина, кодирующий генные сегменты вариабельной области человека, где млекопитающее не экспрессирует ICOS.
Предложение 84. Способ получения антитела, которое связывает внеклеточный домен человеческого или нечеловеческого ICOS, включающий
(a) иммунизацию млекопитающего согласно предложению 83 антигеном ICOS человека;
(b) выделение антител, продуцируемых млекопитающим;
(c) тестирование антител на способность связывать человеческий и нечеловеческий ICOS; и
(d) выбор одного или нескольких антител, которые связывают как человеческий, так и нечеловеческий ICOS.
Предложение 85. Способ согласно предложению 84, включающий иммунизацию млекопитающего клетками, экспрессирующими ICOS человека.
Предложение 86. Способ согласно предложению 84 или предложению 85, включающий
(c) тестирование антител на способность связывать человеческие ICOS и нечеловеческие ICOS с использованием метода поверхностного плазмонного резонанса и определения аффинностей связывания; и
(d) выбор одного или нескольких антител, для которых KD связывания с ICOS человека составляет менее 50 нМ, a KD связывания с нечеловеческим ICOS составляет менее 500 нМ.
Предложение 87. Способ согласно предложению 86, включающий
(d) выбор одного или нескольких антител, для которых KD связывания с ICOS человека составляет менее 10 нМ, a KD связывания с нечеловеческим ICOS составляет менее 100 нМ.
Предложение 88. Способ согласно любому из предложений 84-87, включающий
(c) тестирование антител на способность связывать человеческие ICOS и нечеловеческие ICOS с использованием метода поверхностного плазмонного резонанса и определения аффинностей связывания; и
(d) выбор одного или нескольких антител, для которых KD связывания с ICOS человека находится в пределах 10-кратного значения KD связывания с нечеловеческим ICOS.
Предложение 89. Способ согласно предложению 88, включающий
(d) выбор одного или нескольких антител, для которых KD связывания с ICOS человека находится в пределах 5-кратного значения KD связывания с нечеловеческим ICOS.
Предложение 90. Способ согласно любому из предложений 84-89, включающий тестирование антител на способность связывать нечеловеческие ICOS от того же вида, к которому относится млекопитающее.
Предложение 91. Способ согласно любому из предложений 84-90, включающий тестирование антител на способность связывать нечеловеческие ICOS от вида, отличного от того, к которому относится млекопитающее.
Предложение 92. Способ согласно любому из предложений 84-91, в котором млекопитающее представляет собой мышь или крысу.
Предложение 93. Способ согласно любому из предложений 84-92, где нечеловеческий ICOS представляет собой ICOS мыши или ICOS крысы.
Предложение 94. Способ согласно любому из предложений 84-93, где человеческий или гуманизированный локус иммуноглобулина включает генные сегменты вариабельной области человека, расположенные слева от (upstream) эндогенной константной области.
Предложение 95. Способ согласно предложению 94, включающий
(a) иммунизацию млекопитающего согласно предложению 83 антигеном человеческого ICOS, где млекопитающее представляет собой мышь;
(b) выделение антител, продуцируемых мышью;
(c) тестирование антител на способность связывать ICOS человека и ICOS мыши; и
(d) выбор одного или нескольких антител, которые связывают ICOS как человека, так и мыши.
Предложение 96. Способ согласно любому из предложений 84-95, включающий выделение нуклеиновой кислоты, кодирующей вариабельный домен тяжелой цепи антитела и/или вариабельный домен легкой цепи антитела.
Предложение 97. Способ согласно любому из предложений 84-96, в котором млекопитающее генерирует антитела посредством рекомбинации генных сегментов вариабельной области человека и эндогенной константной области.
Предложение 98. Способ согласно предложению 96 или предложение 97, включающий конъюгирование нуклеиновой кислоты, кодирующей вариабельный домен тяжелой и/или легкой цепи, с нуклеотидной последовательностью, кодирующей константную область тяжелой цепи человека и/или константную область легкой цепи человека, соответственно.
Предложение 99. Способ согласно любому из предложений 96-98, включающий введение нуклеиновой кислоты в клетку-хозяина.
Предложение 100. Способ согласно предложению 99, включающий культивирование клетки-хозяина в условиях экспрессии антитела или вариабельного домена тяжелой и/или легкой цепи антитела.
Предложение 101. Антитело или вариабельный домен тяжелой и/или легкой цепи антитела, продуцируемый способом согласно любому из предложений 84-100.
Sentence 102. Способ выбора антитела, которое связывает ICOS, необязательно, для выбора агонистического антитела ICOS, в котором анализ включает:
обеспечение матрицы антител, иммобилизованных (присоединенных или прикрепленных) к субстрату в тестовой лунке;
добавление экспрессирующих ICOS клеток (например, активированных первичных Т-клеток или клеток MJ) в тестовую лунку;
наблюдение морфологии клеток;
детектирование изменения формы в лунках от округлой до сплюснутой к подложке внутри лунки; где изменение формы указывает, что антитело представляет собой антитело, которое связывает ICOS, необязательно, антитело к агонисту ICOS;
выбор антитела из тестовой лунки;
экспрессию нуклеиновой кислоты, кодирующей CDR выбранного антитела; и
составление композиции антитела, содержащей один или несколько дополнительных компонентов.
Альтернативные предложения, описывающие анти-ICOS антитела, описаны ниже:
Предложение 1а. Антитело или его фрагмент, которые специфически связываются с ICOS человека (hICOS) (SEQ ID NO: 508, 507 и/или 506) и:
a) конкурируют за связывание с указанным hICOS с антителом STIM001, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 365, или последовательность CDRH3, представленную Seq ID NO: 365, содержащую 3, 2 или 1 аминокислотных замещений;
b) конкурируют за связывание с указанным hICOS с антителом STIM002, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 379, или последовательность CDRH3, представленную Seq ID NO: 379, содержащую 3, 2 или 1 аминокислотных замещений;
c) конкурируют за связывание с указанным hICOS с антителом STIM002-B, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 393, или последовательность CDRH3, представленную SEQ ID NO: 393, содержащую 3, 2 или 1 аминокислотных замещений;
d) конкурируют за связывание с указанным hICOS с антителом STIM003, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 407, или последовательность CDRH3, представленную SEQ ID NO: 407, содержащую 3, 2 или 1 аминокислотных замещений;
e) конкурируют за связывание с указанным hICOS с антителом STIM004, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 421, или последовательность CDRH3, представленную Seq ID NO: 421, содержащую 3, 2 или 1 аминокислотных замещений;
f) конкурируют за связывание с указанным hICOS с антителом STIM005, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 437, или последовательность CDRH3, представленную SEQ ID NO: 437, содержащую 3, 2 или 1 аминокислотных замещений;
д) конкурируют за связывание с указанным hICOS с антителом STIM006, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 451, или последовательность CDRH3, представленную SEQ ID NO: 451, содержащую 3, 2 или 1 аминокислотных замещений;
h) конкурируют за связывание с указанным hICOS с антителом STIM007, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 465, или последовательность CDRH3, представленную Seq ID NO: 465, содержащую 3, 2 или 1 аминокислотных замещений;
i) конкурируют за связывание с указанным hICOS с антителом STIM008, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 479 или последовательность CDRH3, представленную Seq ID NO: 479, содержащую 3, 2 или 1 аминокислотных замещений; или
j) конкурирует за связывание с указанным hICOS с антителом STIM009, где антитело или фрагмент содержат домен VH, который содержит последовательность CDRH3, представленную SEQ ID NO: 493, или последовательность CDRH3, представленную Seq ID NO: 493, содержащую 3, 2 или 1 аминокислотных замещений.
Предложение 2а. Антитело или его фрагмент согласно предложению 1а, где домен VH содержит последовательность CDRH1, представленную:
a) SEQ ID NO: 363, или последовательность CDRH1, представленную SEQ ID NO: 363, содержащую 1 аминокислотное замещение;
b) SEQ ID NO: 377, или последовательность CDRH1, представленную SEQ ID NO: 377, содержащую 1 аминокислотное замещение;
c) SEQ ID NO: 391, или последовательность CDRH1, представленную SEQ ID NO: 391, содержащую 1 аминокислотное замещение;
d) SEQ ID NO: 405, или последовательность CDRH1, представленную SEQ ID NO: 405, содержащую 1 аминокислотное замещение;
e) SEQ ID NO: 419, или последовательность CDRH1, представленную SEQ ID NO: 419, содержащую 1 аминокислотное замещение;
f) SEQ ID NO: 435, или последовательность CDRH1, представленную SEQ ID NO: 435, содержащую 1 аминокислотное замещение;
g) SEQ ID NO: 449, или последовательность CDRH1, представленную SEQ ID NO: 449, содержащую 1 аминокислотное замещение;
h) SEQ ID NO: 463, или последовательность CDRH1, представленную SEQ ID NO: 463, содержащую 1 аминокислотное замещение; или
i) SEQ ID NO: 477, или последовательность CDRH1, представленную SEQ ID NO: 477, содержащую 1 аминокислотное замещение;
j) SEQ ID NO: 491, или последовательность CDRH1, представленную SEQ ID NO: 491, содержащую 1 аминокислотное замещение.
Предложение 3а. Антитело или его фрагмент согласно предложению 1а или предложению 2а, где домен VH содержит последовательность CDRH2, представленную:
a) SEQ ID NO: 364, или последовательность CDRH2, представленную SEQ ID NO: 364, содержащую 2 или 1 аминокислотных замещений;
b) SEQ ID NO: 378, или последовательность CDRH2, представленную SEQ ID NO: 378, содержащую 2 или 1 аминокислотных замещений;
c) SEQ ID NO: 392, или последовательность CDRH2, представленную SEQ ID NO: 392, содержащую 2 или 1 аминокислотных замещений;
d) SEQ ID NO: 406, или последовательность CDRH2, представленную SEQ ID NO: 406, содержащую 2 или 1 аминокислотных замещений;
e) SEQ ID NO: 420, или последовательность CDRH2, представленную SEQ ID NO: 420, содержащую 2 или 1 аминокислотных замещений;
f) SEQ ID NO: 436, или последовательность CDRH2, представленную SEQ ID NO: 436, содержащую 2 или 1 аминокислотных замещений;
g) SEQ ID NO: 450, или CDRH2 последовательность SEQ ID NO: 450, содержащая 2 или 1 аминокислотных замещений;
h) SEQ ID NO: 464, или последовательность CDRH2, представленную SEQ ID NO: 464, содержащую 2 или 1 аминокислотных замещений;
i) SEQ ID NO: 478, или последовательность CDRH2, представленную SEQ ID NO: 478, содержащую 2 или 1 аминокислотных замещений; или
j) SEQ ID NO: 492, или последовательность CDRH2, представленную SEQ ID NO: 492, содержащую 2 или 1 аминокислотных замещений.
Предложение 4а. Антитело или его фрагмент согласно любому из предшествующих предложений, в которых домен VH содержит:
a) аминокислотную последовательность SEQ ID NO: 366 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 366;
b) аминокислотную последовательность SEQ ID NO: 380 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 380;
c) аминокислотную последовательность SEQ ID NO: 394 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 394;
d) аминокислотную последовательность SEQ ID NO: 408 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 408;
e) аминокислотную последовательность SEQ ID NO: 422 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 422;
f) аминокислотную последовательность SEQ ID NO: 438 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 438;
g) аминокислотную последовательность SEQ ID NO: 452 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 452;
h) аминокислотную последовательность SEQ ID NO: 466 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 466;
i) аминокислотную последовательность SEQ ID NO: 480 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 480; или
j) аминокислотную последовательность SEQ ID NO: 494 или аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 494.
Предложение 5а. Антитело или фрагмент согласно любому из предшествующих предложений, содержащие первую и вторую копии указанного домена VH.
Предложение 6а. Антитело или его фрагмент согласно любому из предшествующих предложений, содержащие домен VL, которая содержит последовательность CDRL1, представленную:
a) SEQ ID NO: 370, или последовательность CDRL1, представленную SEQ ID NO: 370, содержащую одно аминокислотное замещение;
b) SEQ ID NO: 384, или последовательность CDRL1, представленную SEQ ID NO: 384, содержащую одно аминокислотное замещение;
c) SEQ ID NO: 398, или последовательность CDRL1, представленную SEQ ID NO: 398, содержащую одно замещение аминокислоты;
d) SEQ ID NO: 412, или последовательность CDRL1, представленную SEQ ID NO: 412, содержащую одно аминокислотное замещение;
e) SEQ ID NO: 426, или последовательность CDRL1, представленную SEQ ID NO: 426, содержащую одно аминокислотное замещение;
f) SEQ ID NO: 442, или последовательность CDRL1, представленную SEQ ID NO: 442, содержащую одно аминокислотное замещение;
g) SEQ ID NO: 456, или последовательность CDRL1, представленную SEQ ID NO: 456, содержащую одно аминокислотное замещение;
h) SEQ ID NO: 470, или последовательность CDRL1, представленную SEQ ID NO: 470, содержащую одну аминокислотную замену; или
i) SEQ ID NO: 484, или последовательность CDRL1, представленную SEQ ID NO: 484, содержащую одно аминокислотное замещение.
j) SEQ ID NO: 498, или последовательность CDRL1, представленную SEQ ID NO: 498, содержащую одно аминокислотное замещение.
Предложение 7а. Антитело или его фрагмент согласно любому из предшествующих предложений, содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL2, представленную:
a) SEQ ID NO: 371, или последовательность CDRL2, представленную SEQ ID NO: 371, содержащую 1 аминокислотное замещение;
b) SEQ ID NO: 385, или последовательность CDRL2, представленную SEQ ID NO: 385, содержащую 1 аминокислотное замещение;
c) SEQ ID NO: 399, или последовательность CDRL2, представленную SEQ ID NO: 399, содержащую 1 аминокислотное замещение;
d) SEQ ID NO: 413, или последовательность CDRL2, представленную SEQ ID NO: 413, содержащую 1 аминокислотное замещение;
e) SEQ ID NO: 427, или последовательность CDRL2, представленную SEQ ID NO: 427, содержащая 1 аминокислотную замену;
f) SEQ ID NO: 443, или последовательность CDRL2, представленную SEQ ID NO: 443, содержащая 1 аминокислотную замену;
g) SEQ ID NO: 457, или последовательность CDRL2, представленную SEQ ID NO: 457, содержащую 1 аминокислотное замещение;
h) SEQ ID NO: 471, или последовательность CDRL2, представленную SEQ ID NO: 471, содержащая 1 аминокислотную замену;
i) SEQ ID NO: 485, или последовательность CDRL2, представленную SEQ ID NO: 485, содержащую 1 аминокислотное замещение; или
j) SEQ ID NO: 499, или последовательность CDRL2, представленную SEQ ID NO: 499, содержащую 1 аминокислотное замещение.
Предложение 8а. Антитело или его фрагмент согласно любому из предшествующих предложений, содержащие (а) или указанный домен VL, где домен VL содержит последовательность CDRL3, представленную:
a) SEQ ID NO: 372, или последовательность CDRL3, представленную SEQ ID NO: 372, содержащую 2 или 1 аминокислотных замещений;
b) SEQ ID NO: 386, или последовательность CDRL3, представленную SEQ ID NO: 386, содержащую 2 или 1 аминокислотных замещений;
c) SEQ ID NO: 400, или последовательность CDRL3, представленную SEQ ID NO: 400, содержащую 2 или 1 аминокислотных замещений;
d) SEQ ID NO: 414, или последовательность CDRL3, представленную SEQ ID NO: 414, содержащую 2 или 1 аминокислотных замещений;
e) SEQ ID NO: 428, или последовательность CDRL3, представленную SEQ ID NO: 428, содержащую 2 или 1 аминокислотных замещений;
f) SEQ ID NO: 444, или последовательность CDRL3, представленную SEQ ID NO: 444, содержащую 2 или 1 аминокислотных замещений;
g) SEQ ID NO: 458, или последовательность CDRL3, представленную SEQ ID NO: 458, содержащую 2 или 1 аминокислотных замещений;
h) SEQ ID NO: 472, или последовательность CDRL3, представленную SEQ ID NO: 472, содержащую 2 или 1 аминокислотных замещений;
i) SEQ ID NO: 486, или последовательность CDRL3, представленную SEQ ID NO: 486, содержащую 2 или 1 аминокислотных замещений; или
j) SEQ ID NO: 500, или последовательность CDRL3, представленную SEQ ID NO: 500, содержащую 2 или 1 аминокислотных замещений.
Предложение 9а. Антитело или его фрагмент согласно любому из предшествующих предложений, содержащие (а) или указанный домен BL, где домен VL содержит аминокислотную последовательность, представленную:
a) SEQ ID NO: 373, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 373;
b) SEQ ID NO: 387, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 387;
c) SEQ ID NO: 401, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 401;
d) SEQ ID NO: 415, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 415;
e) SEQ ID NO: 429, или аминокислотной последовательности вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 429;
f) SEQ ID NO: 445, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 445;
g) SEQ ID NO: 459, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 459;
h) SEQ ID NO: 473, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 473;
i) SEQ ID NO: 487, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 487; или
j) SEQ ID NO: 501, или аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 98% идентична SEQ ID NO: 501.
Предложение 10а. Антитело или фрагмент согласно любому из предложений 6а-9а, содержащие первую и вторую копии (а) или указанного домена VL.
Предложение 11. Антитело или фрагмент согласно любому из предшествующих предложений, в которых аминокислотные замещения представляют собой консервативные аминокислотные замещения, где, необязательно, консервативные заместители относятся к одной из шести групп (каждая группа содержит аминокислоты, которые являются консервативными заменами друг для друга), выбранных из:
1) аланин (А), серин (S), треонин (Т);
2) аспарагиновая кислота (D), глутаминовая кислота (Е);
3) аспарагин (N), глутамин (Q);
4) аргинин (R), лизин (K);
5) изолейцин (I), лейцин (L), метионин (М), валин (V); и
6) фенилаланин (F), тирозин (Y), триптофан (W).
Предложение 12а. Антитело или его фрагмент, которые специфически связываются с эпитопом, который является:
a) Идентичным эпитопу, с которым специфически связывается антитело STIM001;
b) Идентичным эпитопу, с которым специфически связывается антитело STIM002;
c) Идентичным эпитопу, с которым специфически связывается антитело STIM002-B;
d) Идентичным эпитопу, с которым специфически связывается антитело STIM003;
e) Идентичным эпитопу, с которым специфически связывается антитело STIM004;
f) Идентичным эпитопу, с которым специфически связывается антитело STIM005;
g) Идентичным эпитопу, с которым специфически связывается антитело STIM006;
h) Идентичным эпитопу, с которым специфически связывается антитело STIM007;
i) Идентичным эпитопу, с которым специфически связывается антитело STIM008; или
j) Идентичным эпитопу, с которым специфически связывается антитело STIM009.
Предложение 13а. Антитело или фрагмент согласно предложению 12а, где эпитоп идентифицируют путем сканирования неродственной аминокислотой или рентгеновской кристаллографией.
Предложение 14а. Антитело или фрагмент согласно предложению 13а, где контактные остатки эпитопа определяют по снижению аффинности, по меньшей мере, в 10 раз при сканировании неродственной аминокислотой, например, сканировании аланином, по результатам определения методом SPR.
Предложение 15а. Антитело или его фрагмент, которые:
a) Конкурируют за связывание с hICOS с антителом STIM001;
b) Конкурируют за связывание с hICOS с антителом STIM002;
c) Конкурируют за связывание с hICOS с антителом STIM002-B;
d) Конкурируют за связывание с hICOS с антителом STIM003;
e) Конкурируют за связывание с hICOS с антителом STIM004;
f) Конкурируют за связывание с hICOS с антителом STIM005;
g) Конкурируют за связывание с hICOS с антителом STIM006;
h) Конкурируют за связывание с hICOS с антителом STIM007;
i) Конкурируют за связывание с hICOS с антителом STIM008; или
j) Конкуренты за связывание с hICOS с антителом STIM009.
Предложение 16а. Антитело или фрагмент согласно любому из предшествующих предложений, которые специфически связываются с ICOS яванского макака (SEQ ID NO: 513, SEQ ID NO: 513 или SEQ ID NO: 514) и/или ICOS мыши (SEQ ID NO: 510, SEQ ID NO: 511 или SEQ ID NO: 512).
Предложение 17а. Антитело или фрагмент согласно любому из предшествующих предложений, которые специфически связываются с изоформой hICOS или природным вариантом, изоформой ICOS мыши или природным вариантом и/или изоформой ICOS яванского макака или природным вариантом.
Предложение 18а. Антитело или фрагмент согласно предложению 17а, где изоформа hICOS содержит аминокислотную последовательность SEQ ID NO: 509.
Предложение 19а. Антитело или фрагмент согласно любому из предшествующих предложений, в которых антитело или фрагмент содержат константную область, такую как константная область человека, например, константная область эффекторно-нулевого человека, например, константная область IgG4 или константная область IgG1, где, необязательно, константная область представляет собой IgG4-PE (SEQ ID NO: 199) или инактивированный IgG1 (SEQ ID NO: 205).
Предложение 20а. Антитело или фрагмент согласно предложению 19а, где константная область представляет собой константную область мыши.
Предложение 21а. Антитело или фрагмент согласно предложению 19а или предложение 20а, где константная область имеет активность CDC и/или ADCC.
5. Биспецифические анти-ICOS антитела
Как описано выше, антитела PD-L1, предусматриваемые в данном документе, могут иметь формат мультиспецифического (например, биспецифического) антитела, как описано выше в концепциях 37-40. В одном варианте реализации, раскрытом там, антитела PD-L1, раскрытые в данном документе, могут иметь формат биспецифического антитела, которое имеет специфичность как к PD-L1 (например, PD-L1 человека), так и к ICOS (например, агонист ICOS, такого как ICOS человека).
Таким образом, предусматривается мультиспецифическое (например, биспецифическое антитело или антитело с двойным связыванием), которое имеет специфичность к PD-L1 (например, PD-L1 человека) и ICOS (например, ICOS человека). В одном варианте реализации, мультиспецифическое (например, биспецифическое или с двойным связыванием) антитело обладает агонистической активностью против ICOS (например, ICOS человека).
Различные ICOS-содержащие мультиспецифические антитела описаны в приведенных ниже схемах:
Схема 1. Мультиспецифическое антитело (например, биспецифическое антитело или антитело с двойным связыванием), которое связывает (и, необязательно, имеет специфичность к) ICOS (например, ICOS человека) и другому целевому антигену.
В одном варианте реализации, предусматривается биспецифическое антитело или антитело с двойным связыванием, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень. В одном варианте реализации, предусматривается биспецифическое антитело или антитело с двойным связыванием, которое имеет специфичность к ICOS (например, ICOS человека) и другому целевому антигену. В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, причем биспецифическое антитело имеет формат mAb2. В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, причем биспецифическое антитело имеет формат mAb2, а связывание с другим антигеном-мишенью обеспечивается модифицированной константной областью (т.е. Fcab). В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, который представляет собой PD-L1 (например, PD-L1 человека), и где биспецифическое антитело имеет формат mAb2, а связывание с ICOS обеспечивается модифицированной константной областью (т.е. Fcab). В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, который представляет собой PD-L1 (например, PD-L1 человека), причем биспецифическое антитело имеет формат mAb2, и связывание с ICOS обеспечивается модифицированной константной областью (т.е. Fcab), а связывание с PD-L1 обеспечивается любым из антител, описанных в концепциях 1-70, или любым из антител PD-L1, описанных в схеме 5 или 5а ниже. В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, который представляет собой PD-L1 (например, PD-L1 человека), причем биспецифическое антитело имеет формат mAb2, а связывание с PD-L1 обеспечивается модифицированной константной областью (т.е. Fcab). В одном варианте реализации, предусматривается биспецифическое антитело, которое связывает ICOS (например, ICOS человека) и другой антиген-мишень, который представляет собой PD-L1 (например, PD-L1 человека), причем биспецифическое антитело имеет формат mAb2, и связывание с PD-L1 обеспечивается модифицированной константной областью (т.е. Fcab), а связывание с ICOS обеспечивается любым из антител, описанных в предложениях 1-102 или предложениях 1а-21а.
В одном варианте реализации, мультиспецифическое (например, биспецифическое или с двойным связыванием) антитело обладает агонистической активностью против ICOS (например, ICOS человека). Другим антигеном-мишенью может быть любой из антигенов-мишеней, указанных в концепции 39. В одном варианте реализации, другой антиген-мишень представляет собой ингибитор иммунной контрольной точки, такой как PD-1, PD-L1, CTLA-4, TIGIT, TIM-3, LAG-3 и VISTA, например, PD-L1, TIGIT, CTLA-4, TIM-3 и LAG-3. В одном варианте реализации, другим антигеном-мишенью является иммунный модулятор, такой как BTLA, hHVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10 и CD155, например, GARP, SIRPα, CXCR4, BTLA, hVEM и CSF1R. В одном варианте реализации, другим антигеном-мишенью является иммунный активатор, такой как CD137, GITR, OX40, CD40, CXCR3 (например, агонистические анти-CXCR3 антитела), CD27 и CD3, или CD137, GITR, OX40, CD40, CXCR3 (например, агонистические анти-CXCR3 антитела) и CD3, например, CD137, GITR и OX40). В одном варианте реализации, другим антигеном-мишенью является PD-L1. В одном варианте реализации, другим антигеном-мишенью является CTLA-4. В одном варианте реализации, другим антигеном-мишенью является TIGIT. В одном варианте реализации, другим антигеном-мишенью является TIM-3. В одном варианте реализации, другим антигеном-мишенью является LAG-3. В одном варианте реализации, другим антигеном-мишенью является GITR. В одном варианте реализации, другим антигеном-мишенью является VISTA. В одном варианте реализации, другим антигеном-мишенью является CD137. В одном варианте реализации, другим антигеном-мишенью является SIRPα. В одном варианте реализации, другим антигеном-мишенью является CXCL10. В одном варианте реализации, другим антигеном-мишенью является CD155. В одном варианте реализации, другим антигеном-мишенью является CD40. Антителами против таких других антигенов-мишеней могут быть любые из описанных в Аспекте 1а выше.
Формат мультиспецифических, биспецифических антител или антител с двойным связыванием может быть любым из форматов, раскрытых в данном документе, например, как описано в концепциях 37-40. В частности, связывание и/или специфичность к ICOS могут быть обеспечены не-иммуноглобулиновым форматом, например, связывающим доменом рецептора Т-клеток; доменом суперсемейства иммуноглобулина; вариабельным лимфоцитарным рецептором бесчелюстных; фибронектиновым доменом (например, Adnectin™); константным доменом антитела (например, доменом СН3, например, СН2 и/или СН3 Fcab™), где константный домен не является функциональным доменом СН1; scFv; (scFv)2; одноцепочечным диателом (sc-diabody); scFab; центрином и эпитопсвязывающим доменом, полученным из каркаса, выбранного из CTLA-4 (Evibody™); липокалиновым доменом; белком А, таким как Z-домен белка А (например, Affibody™ или SpA); А-доменом (например, Avimer™ или Maxibody™); белком теплового шока (таким как эпитопсвязывающий домен, полученный из GroEI и GroES); трансферриновым доменом (например, транс-тело); белком с анкириновым повтором (например, DARPin™); пептидным аптамером; лектиновым доменом С-типа (например, Tetranectin™); человеческим γ-кристаллином или убиквитином (аффилином) человека; доменом PDZ; токсином скорпиона; и доменом Кунитц-типа ингибитора протеазы человека. Связывание м и/или специфичность к другому антигену-мишени могут быть обеспечены с помощью антигенсвязывающего белка, производного от иммуноглобулина.
«Специфически связывает» имеет значение, указанное выше. Константы связывания, например, KD, могут быть определены, как описано в другой части данного документа, и конкретные KD, представляющие интерес, описаны в схеме 2 ниже и в концепции 1 выше (хотя значения KD описаны для связывания PD-L1, они в равной степени могут применяться к связыванию ICOS).
Схема 2. Мультиспецифическое антитело согласно схеме 1, где ICOS представляет собой ICOS человека.
Последовательности ICOS человека представлены в SEQ ID NOs: 506, 507 и 508. В одном варианте реализации, мультиспецифическое антитело является специфичным к ICOS человека дикого типа. В другом варианте реализации, мультиспецифическое антитело является перекрестно-реактивным к изоформе или природному варианту hICOS, например, изоформе SEQ ID NO: 509. Другие изоформы и природные варианты хорошо известны специалистам в данной области техники. В другом варианте реализации, Мультиспецифическое антитело является специфичным к изоформе или природному варианту (например, изоформе ICOS, имеющей аминокислотную последовательность SEQ ID NO: 509) по сравнению с hICOS дикого типа.
Один из способов количественной оценки степени видовой перекрестно-реактивности антитела, например, мультиспецифического, биспецифического антитела или антитела с двойным связыванием, заключается в определении кратности разницы в его аффинности к антигену по сравнению с другим антигеном (например, кратности разницы в аффинности к человеческому ICOS по сравнению с мышиным ICOS, или кратности разницы в аффинности к hICOS дикого типа по сравнению с изоформой hICOS). Аффинность может быть количественно определена как KD, представляющий собой равновесную константу диссоциации реакции антитело-антиген, по результатам определения методом SPR (необязательно, с антителом в формате Fab, как описано в другой части данного документа). Перекрестно-реактивное антитело против ICOS для вида или изоформы может иметь разницу в аффинности связывания ICOS человека и мыши, составляющую 30-кратную или меньше, 25-кратную или меньше, 20-кратную или меньше, 15-кратную или меньше, 10-крвтную или меньше, или 5-кратную или меньше. Иными словами, KD связывания внеклеточного домена hICOS может иметь значение в пределах 30-кратного, 25-кратного, 20-кратного, 15-кратного, 10-кратного или 5-кратного от KD связывания с внеклеточным домена ICOS мыши. Антитела также могут считаться перекрестно-реактивными, если KD связывания антигена для обоих видов соответствуют пороговому значению, например, если KD связывания hICOS и KD связывания ICOS мыши составляют 10 мМ или меньше, предпочтительно, 5 мМ или меньше, более предпочтительно, 1 мМ или меньше. Величина KD может составлять 10 нМ или меньше, 5 нМ или меньше, 2 нМ или меньше, или 1 нМ или меньше. Величина KD может составлять 0,9 нМ или меньше, 0,8 нМ или меньше, 0,7 нМ или меньше, 0,6 нМ или меньше, 0,5 нМ или меньше, 0,4 нМ или меньше, 0,3 нМ или меньше, 0,2 нМ или меньше, или 0,1 нМ или меньше.
Альтернативной мерой перекрестно-реактивности для связывания hICOS и ICOS мыши, или hICOS дикого типа (WT) и изоформы hICOS, является способность антитела нейтрализовать связывание лиганда ICOS с рецептором ICOS, например, в анализе HTRF (как описано в другой части данного документа). Примеры видовых перекрестно-реактивных антител представлены в данном документе, включая STIM001, STIM002, STIM002-B, STIM003, STIM005 и STIM006, для каждого из которых были подтверждены как нейтрализация связывания человеческого В7-Н2 (лиганд ICOS) с hICOS, так и нейтрализация связывания мыши В7-Н2 с мышиным ICOS в анализе HTRF. Любое из этих антител или их вариантов может быть выбрано, когда требуется антитело, перекрестно-реактивное к ICOS человека и мыши. Видовое перекрестно-реактивное антитело против ICOS может иметь IC50 ингибирования связывания hICOS с рецептором ICOS человека, находящуюся в пределах 25-кратного, 20-кратного, 15-кратного, 10-кратного или 5-кратного значения IC50 для ингибирования связывания ICOS мыши с мышиным рецептором ICOS, по результатам определения в анализе HTRF. Антитела также могут считаться перекрестно-реактивными, если IC50 для ингибирования связывания hICOS с рецептором ICOS человека и IC50 для ингибирования связывания ICOS мыши с рецептором ICOS мыши оба имеют значения 1 мМ или меньше, предпочтительно, 0,5 мМ или меньше, например, 30 нМ или меньше, 20 нМ или меньше, 10 нМ или меньше. Значения IC50 могут составлять 5 нМ или меньше, 4 нМ или меньше, 3 нМ или меньше или 2 нМ или меньше. В некоторых случаях, IC50 будут составлять по меньшей мере 0,1 нМ, по меньшей мере 0,5 нМ или по меньшей мере 1 нМ.
Аффинности также могут быть такими, как раскрыто в концепции 27 выше.
Схема 3. Мультиспецифическое антитело согласно схеме 2, которое содержит домен VH, содержащий CDRH1, CDRH2 и CDRH3, причем домен VH связывается с (и, необязательно, имеет специфичность к) hICOS.
В одном варианте реализации, мультиспецифическое антитело содержит по меньшей мере один домен VH, который связывается с hICOS. Например, мультиспецифическое антитело может содержать одноцепочечный Fv (scFv), одноцепочечное антитело, однодоменное антитело или доменное антитело, которое содержит только домен VH, связывающийся с (и, необязательно, имеющий специфичность к) hICOS.
Схема 4. Мультиспецифическое антитело согласно схеме 2 или схеме 3, которое содержит домен VL, содержащий CDRL1, CDRL2 и CDRL3, причем домен VL связывается с (и, необязательно, имеет специфичность к) hICOS.
В одном варианте реализации, мультиспецифическое антитело содержит по меньшей мере один домен VL, который связывается с hICOS. Например, мультиспецифическое антитело может содержать одноцепочечный Fv (scFv), одноцепочечное антитело, однодоменное антитело или доменное антитело, содержащее только домен VL, который связывается с (и, необязательно, имеет специфичность к) hICOS.
В другом варианте реализации, мультиспецифическое антитело содержит спаренный домен VH и VL, включая, без ограничений, интактное или полноразмерное антитело, фрагмент Fab, фрагмент Fab', фрагмент F(ab')2 или фрагмент Fv.
Схема 5. Мультиспецифическое антитело согласно схеме 3 или 4, где домен VH и/или VL представляет собой любой из доменов VH и/или VL:
а. антител 7F12, 37А10, 35А9, 36Е10, 16G10, 37A10S713, 37A10S714, 37A10S715, 37A10S716, 37A10S717, 37A10S718, 16G10S71, 16G10S72, 16G10S73, 16G10S83, 35A9S79, 35A9S710, 35A9S89 или любого другого антитела, описанного в WO 2016/154177 и US 2016/0304610;
b. антител 422.2, H2L5 или любого другого антитела, описанного в WO 2016/120789 и US 2016/0215059;
с. антитела 314-8, антитела, продуцируемого гибридомой CNCM I-4180, или любого другого антитела, описанного в WO 2014/033327 и US 2015/0239978;
d. антитела Icos145-1, антитела, продуцируемого гибридомой CNCM I-4179, или любого другого антитела, описанного в WO 2012/131004, US 9376493 и US 2016/0264666;
е. антител JMAb 136, "136" или любого другого антитела, описанного в WO 2010/056804;
f. антител MIC-944, 9F3 или любого другого антитела, описанного в WO 99/15553, US 7259247, US 7132099, US 7125551, US 7306800, US 7722872, WO 05/103086, US 8318905 и US 8916155;
g. любого JMAb-антитела, например, любого из JMAb-124, JMAb-126, JMAb-127, JMAb-128, JMAb-135, JMAb-136, JMAb-137, JMAb-138, JMAb-139, JMAb-140, JMAb -141, например, JMAb136, или любого другого антитела, описанного в WO 98/3821, US 7932358 B2, US 2002/156242, US 7030225, US 7045615, US 7279560, US 7226909, US 7196175, US 7932358, US 8389690, WO 02/070010, US 7438905, US 7438905, WO 01/87981, US 6803039, US 7166283, US 7988965, WO 01/15732, US 7465445 и US 7998478;
h. антитела 17G9 или любого другого антитела, описанного в WO 2014/08911;
i. любого антитела, описанного в WO 2012/174338;
j. любого антитела, описанного в US 2016/0145344;
k. любого антитела, описанного в WO 2011/020024, US 2016/002336, US 2016/024211 и US 8840889;
l. любого антитела, описанного в US 8497244;
m. антитела, известного как GSK 3359609;
n. антитела, известного как JTX-2011; или
о. клона антитела ISA-3 (eBioscience), клона SP98 (Novus Biologicals), клона 1 G1, клона 3G4 (Abnova Corporation), клона 669222 (R&D Systems), клона TQ09 (Creative Diagnostics) или клона С398.4А (BioLegend),
Схема 5а. Мультиспецифическое антитело согласно любой из предшествующих схем, которое содержит CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или VH, или VL, или область VH и VL:
а. антител 7F12, 37А10, 35А9, 36Е10, 16G10, 37A10S713, 37A10S714, 37A10S715, 37A10S716, 37A10S717, 37A10S718, 16G10S71, 16G10S72, 16G10S73, 16G10S83, 35A9S79, 35A9S710, 35A9S89 или любого другого антитела, описанного в WO 2016/154177 и US 2016/0304610;
b. антител 422.2, H2L5 или любого другого антитела, описанного в WO 2016/120789 и US 2016/0215059;
с. антитела 314-8, антитела, продуцируемого гибридомой CNCM I-4180, или любого другого антитела, описанного в WO 2014/033327 и US 2015/0239978;
d. антитела Icos145-1, антитела, продуцируемого гибридомой CNCM I-4179, или любого другого антитела, описанного в WO 2012/131004, US 9376493 и US 2016/0264666;
е. антител JMAb 136, "136" или любого другого антитела, описанного в WO 2010/056804;
f. антител MIC-944, 9F3 или любого другого антитела, описанного в WO 99/15553, US 7259247, US 7132099, US 7125551, US 7306800, US 7722872, WO 05/103086, US 8318905 и US 8916155;
g. любого JMAb-антитела, например, любого из JMAb-124, JMAb-126, JMAb-127, JMAb-128, JMAb-135, JMAb-136, JMAb-137, JMAb-138, JMAb-139, JMAb-140, JMAb -141, например, JMAb136 или любого другого антитела, описанного в WO 98/3821, US 7932358 B2, US 2002/156242, US 7030225, US 7045615, US 7279560, US 7226909, US 7196175, US 7932358, US 8389690, WO 02/070010, US 7438905, US 7438905, WO 01/87981, US 6803039, US 7166283, US 7988965, WO 01/15732, US 7465445 и US 7998478;
h. антитела 17G9 или любого другого антитела, описанного в WO 2014/0889;
i. любого антитела, описанного в WO 2012/174338;
j. любого антитела, описанного в US 2016/0145344;
k. любого антитела, описанного в WO 2011/020024, US 2016/002336, US 2016/024211 и US 8840889;
l. любого антитела, описанного в US 8497244;
m. антитела, известного как GSK 3359609;
n. антитела, известного как JTX-2011; или
о. клона антитела ISA-3 (eBioscience), клона SP98 (Novus Biologicals), клона 1 G1, клона 3G4 (Abnova Corporation), клона 669222 (R&D Systems), клона TQ09 (Creative Diagnostics) или клона С398.4А (BioLegend),
Схема 6. Мультиспецифическое антитело согласно схеме 3 или 4, где домен VH и/или VL представляет собой любой из доменов VH и/или VL, определенных в предложениях 1-102 или предложениях 1а-21а.
В одном варианте реализации, VH и/или VL анти-ICOS являются такими, как описано в патентной заявке GB 1620414.1 (поданной 1 декабря 2016 г.), содержание которой включено в данный документ посредством ссылки.
Схема 7. Мультиспецифическое антитело согласно любой из предшествующих схем, обладающее агонистической активностью против ICOS.
Наличие сродства к рецептору можно тестировать с помощью in vitro анализов активации Т-клеток, используя антитело в растворимой форме (например, в формате иммуноглобулина или в другом формате антител, включающем два пространственно разделенных антигенсвязывающих сайта, например, две пары VH-VL), либо со сшивающим агентом или без него, или используя антитело (например, Мультиспецифическое антитело), связанное с твердой поверхностью, для создания матрицы связанных антигенсвязывающих сайтов. В анализах на наличие сродства к рецептору может использоваться hICOS-положительная клеточная линия Т-лимфоцитов, такая как MJ-клетки (АТСС CRL-8294) в качестве Т-клетки-мишени для активации в таких анализах. Один или несколько показателей активации Т-клеток могут быть определены для тестируемого антитела и сравнены с эталонной молекулой или отрицательным контролем для определения того, имеется ли статистически значимая (р<0,05) разница в активации Т-клеток, вызываемая тестовым антителом (например, мультиспецифическим антителом) по сравнению с эталонной молекулой или контролем. Одним из пригодных показателей активации Т-клеток является продуцирование цитокинов, например, IFNγ, TNFα или IL-2. Квалифицированный специалист будет включать пригодные контроли, по мере необходимости, стандартизируя условия анализа для тестируемого антитела и контроля. Пригодным отрицательным контролем является антитело в том же формате (например, изотипический контроль), которое не связывает ICOS, например, антитело (например, мультиспецифическое антитело), специфичное к антигену, не присутствующему в аналитической системе. Существенное различие, наблюдаемое для тестового антитела по сравнению с родственным изотипическим контролем в динамическом диапазоне анализа, указывает на то, что антитело действует как агонист рецептора ICOS в этом анализе.
Агонистическое антитело может быть определено как такое, которое при тестировании в анализе активации Т-клеток:
имеет значительно более низкую EC50 для индукции продуцирования IFNγ по сравнению с контрольным антителом;
индуцирует значительно более высокое максимальное продуцирование IFNγ по сравнению с контрольным антителом;
имеет значительно более низкую EC50 для индукции продуцирования IFNγ по сравнению с ICOSL-Fc;
индуцирует значительно более высокое максимальное продуцирование IFNγ по сравнению с ICOSL-Fc;
имеет значительно более низкую EC50 для индукции продуцирования IFNγ по сравнению с контрольным антителом С398.4А; и/или
индуцирует значительно более высокое максимальное продуцирование IFNγ по сравнению с контрольным антителом С398.4А.
Значительно более низкое или значительно более высокое значение может иметь, например, разность до 0,5-кратной, до 0,75-кратной, до 2-кратной, до 3-кратной, до 4-кратной или до 5-кратной по сравнению с эталонным или контрольным значением.
Таким образом, в одном примере антитело (например, мультиспецифическое антитело), представленное в данном документе, имеет значительно более низкое, например, по меньшей мере, в 2 раза более низкое значение EC50 для индукции IFNγ в анализе активации клеток MJ с использованием антитела в формате, иммобилизованном на бусинах, по сравнению с контролем.
Анализы с иммобилизацией на бусинах используют антитело (например, мультиспецифическое антитело) (и, для экспериментов с эталоном или контролем, контрольное антитело, эталонное антитело или ICOSL-Fc), связанное с поверхностью бусин. Могут использоваться магнитные бусины, различные виды которых являются коммерчески доступными, например, тозил-активированные DYNABEADS M-450 (DYNAL Inc, 5 Delaware Drive, Lake Success, NY 11042 Prod No. 140,03, 140,04). На бусины может быть нанесено покрытие (способы нанесения покрытий хорошо известны специалистам), обычно, путем растворения материала покрытия в карбонатном буфере (рН 9,6, 0,2 М), или другим способом, известным специалистам. Использование бусинок удобно позволяет определять количество белка, связанного с поверхностью бусин, с хорошей степенью точности. Стандартные методы количественного определения Fc-белка могут быть использованы для количественной оценки белка, связанного на бусинах. Может быть использован любой пригодный метод, со ссылкой на соответствующий стандарт в динамическом диапазоне анализа. Могут быть использованы DELFIA, ИФА или другие методы.
Агонистическая активность антитела также может быть измерена ex vivo у первичных Т-лимфоцитов человека. Способность антитела (например, мультиспецифического антитела) индуцировать экспрессию IFNγ в таких Т-клетках указывает на агонизм ICOS. Предпочтительно, антитело будет демонстрировать значительную (р<0,05) индукцию IFNγ при 5 мкг/мл по сравнению с контрольным антителом в анализе активации Т-клеток. Антитело против ICOS может стимулировать активацию Т-клеток в большей степени, чем ICOS-L или С398.4 в таком анализе. Таким образом, антитело может демонстрировать значительно большую (р<0,05) индукцию IFNγ при 5 мкг/мл по сравнению с контрольным или эталонным антителом в анализе активации Т-клеток. В качестве альтернативного результата анализа может быть измерена индукция TNFα или IL-2.
Агонизм анти-ICOS антитела может увеличивать его способность изменять баланс между популяциями регуляторных (TReg) и эффекторных (TEff) Т-клеток in vivo, например, на участке патологии, таком как микроокружение опухоли, в пользу TEff-клеток. Способность антитела усиливать уничтожение опухолевых клеток активированными ICOS-положительными эффекторными Т-клетками может быть определена, как описано в другом месте.
Схема 8. Мультиспецифическое антитело согласно любой из предшествующих схем, которое связывается с (и, необязательно, имеет специфичность к) мышиному ICOS и/или ICOS яванского макака.
Мультиспецифические антитела, описанные в данном документе, могут быть перекрестно-реактивными и могут, например, связывать внеклеточный домен ICOS мыши, а также ICOS человека. Мультиспецифические антитела могут связывать другие нечеловеческие ICOS, включая ICOS приматов, таких как яванский макак. Мультиспецифическое антитело против ICOS, предназначенное для терапевтического использования у людей, должно связывать ICOS человека, в то время как связывание с ICOS других видов не будет иметь прямой терапевтической значимости в клиническом контексте человека. Однако, независимо от основополагающей теории, перекрестно-реактивные антитела имеют высокую ценность и являются превосходными кандидатами в терапевтические молекулы для доклинических и клинических исследований. Перекрестная реактивность может быть определена, как описано для схемы 2 выше.
Схема 9. Мультиспецифическое антитело согласно любой из предшествующих схем, которое является биспецифическим антителом.
Биспецифическое антитело имеет любое из значений, указанных выше.
Схема 10. Биспецифическое антитело согласно схеме 9, где формат биспецифического антитела выбирают из DVD-Ig, mAb2, FIT-Ig, mAb-dAb, dock and lock, SEEDbody, scDiabody-Fc, диатело-Fc, тандем scFv-Fc, Fab-scFv-Fc, Fab-scFv, внутриклеточное антитело, BITE, диатело, DART, TandAb, одноцепочечное диатело (scDiabody), scDiabody-СН3, диатело-СН3, мини-антитело (minibody), knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами, заряженные пары, заряженные пары с общей легкой цепью, в частности, mAb2, knobs-in-holes, knobs-in-holes с общей легкой цепью, knobs-in-holes с общей легкой цепью и заряженными парами и FIT-Ig, например, mAb2 и FIT-Ig.
В одном варианте реализации, формат биспецифического антитела является таким, как описано в любой из концепций 37-40 выше, или как описано в разделе определений. В одном варианте реализации, биспецифическое антитело имеет формат mAb2, где связывание ICOS обеспечивается участком Fcab биспецифического антитела. В другом варианте реализации, биспецифическое антитело имеет формат mAb2, где связывание ICOS обеспечивается участком Fab биспецифического антитела.
В другом варианте реализации, биспецифическое антитело не является биспецифическим антителом mAb2.
Схема 11. Мультиспецифическое антитело в соответствии с любой из схем 1-8, которое является антителом с двойным связыванием.
Антитело с двойным связыванием имеет любое из значений, указанных выше.
Схема 12. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно любой из схем 1-11, где другой антиген-мишень выбран из ингибиторов иммунных контрольных точек, иммуномодуляторов и иммунных активаторов.
Схема 13. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 12, где другой антиген-мишень выбран из PD-1, PD-L1, CTLA-4, TIGIT, TIM-3, LAG-3, VISTA, BTLA, HVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CD155, CD137, GITR, OX40, CXCR3, CD27 и CD3.
Схема 13а. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 12, где другой антиген-мишень выбран из PD-1, PD-L1, CTLA-4, TIGIT, TIM-3, LAG-3, VISTA, BTLA, HVEM, CSF1R, CCR4, CD39, CD40, CD73, CD96, CXCR2, CXCR4, CD200, GARP, SIRPα, CXCL9, CXCL10, CD155, CD137, GITR, OX40, CXCR3 и CD3.
В одном варианте реализации, антигенсвязывающий сайт, который связывает другой антиген-мишень, обеспечивается любым из CDRH1, CDRH2, CDR3, CDRL1, CDRL2 и CDRL3, или областями VH или VL, или VH и VL, любого из антител против мишеней, перечисленных в Схеме 13, которые более подробно описаны в Аспекте 1а выше.
Схема 14. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 13, где другой антиген-мишень выбран из PD-L1, TIGIT, TIM-3, LAG-3, GARP, SIRPα, CXCR4, BTLA, HVEM, CSF1R, агонистических анти-CXCR3 антител), CD137, GITR и OX40.
Схема 15. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 14, где другим антигеном-мишенью является PD-L1 (например, PD-L1 человека).
Схема 16. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 15, где связывание с (и, необязательно, специфичность к) PD-L1 обеспечивается любым из антител или фрагментов, как определено в концепциях 1-70.
Схема 17. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 15 или схеме 16, которое содержит домен VH, содержащий CDRH1, CDRH2 и CDRH3, который домен VH обладает специфичностью для PD-L1 человека.
Схема 18. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно любой из схем 15-17, которое содержит домен VL, содержащий CDRL1, CDRL2 и CDRL3, причем домен VL является специфичным к PD-L1 человека.
Схема 19. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 17 или схеме 18, где домен VH и/или VL представляет собой любой из доменов VH и/или VL атезолизумаба (Roche), авелумаба (Merck), BMS-936559 (BMS), дурвалумаба (Medimmune) или любого из антител PD-L1, описанных в WO 2016/061142, WO 2016/022630, WO 2015/173267, WO 2015/181342, WO 2015/109124, WO 2015/112805, WO 2015/061668, WO 2014/159562, WO 2014/165082, WO 2014/100079, WO 2014/055897, WO 2013/181634, WO 2013/173223, WO 2013/079174, WO 2012/145493, WO 2011/066389, WO 2010/077634, WO 2010/036959 или WO 2007/005874.
Схема 20. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 17 или схеме 18, где домен VH и/или VL представляет собой любой из доменов VH и/или VL, описанных в концепциях 1-70.
Схема 21. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно любой из схем 15-20, которое связывает (и, необязательно, имеет специфичность к) PD-L1 мыши и/или PD-L1 яванского макака.
Перекрестная реактивность может быть такой, как описано выше для схемы 2 или концепции 27.
Схема 22. Композиция, содержащая мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием, как определено в любой из предшествующих схем, и фармацевтически приемлемый эксципиент, разбавитель или носитель и, необязательно, дополнительно содержащая дополнительный терапевтическое средство, независимо выбранный из группы, состоящей из:
a) других ингибиторов иммунной контрольной точки (таких как антитела против TIM-3, антитела против PD-1, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
b) иммунных стимуляторов (таких как антитела против OX40, антитела против GITR, анти-CD137-антитела, анти-ICOS антитела и антитела против CD40);
c) антагонистов хемокиновых рецепторов (такие как CXCR4, CCR4 и CXCR2);
d) нацеленные ингибиторы киназы (такие как ингибиторы CSF-1R или VEGFR);
e) ингибиторы ангиогенеза (например, анти-VEGF-A или дельта-подобный лиганд-4);
f) иммуностимулирующие пептиды или хемокины (такие как CXCL9 или CXCL10);
g) цитокины (такие как IL-15 и IL-21);
h) биспецифические активаторы Т-клеток (BiTE), имеющие по меньшей мере одну специфичность против CD3 (например, BiTE CD3/CD19);
i) другие биспецифические молекулы (например, IL-15-содержащие молекулы, нацеленные на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (плоскоклеточная карцинома пищевода, Нью-Йорк-1) (NY-ESO-1), GD2, ЕрСАМ или ассоциированный с меланомой антиген-3 (MAGE-A3));
j) онколитические вирусы (такие как вирус HSV (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины);
k) вакцинация ассоциированными с опухолью антигенами (такими как плоскоклеточной карциномы пищевода, Нью-Йорк-1 [NY-ESO-1], связанный с меланомой антиген-3 [MAGE-3]);
l) клеточные методы лечения (такие как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или анти-мезотелиновые антитела);
m) биспецифические активаторы NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a;и
n) адоптивный перенос опухолеспецифических Т-клеток или клеток LAK.
Антитела могут представлять собой любую из последовательностей или антител, описанных в схеме 5 или подробно описанных в Аспекте 1а. Другие признаки этой схемы могут быть такими, как описано в концепции 49.
Схема 22а. Фармацевтическая композиция согласно схеме 22 или набор, включающий фармацевтическую композицию, как определено в схеме 22, где композиция предназначена для лечения и/или профилактики состояния или заболевания, выбранного из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома, диффузная крупноклеточная В-клеточная лимфома.
Схема 22b. Фармацевтическая композиция согласно схеме 22 или схеме 22а, в сочетании с, или набор согласно схеме 22а, содержащие этикетку или инструкции по применению для лечения и/или профилактики указанного заболевания или состояния у человека; где, необязательно, этикетка или инструкции содержат номер регистрационного удостоверения лекарственного средства (например, номер разрешения FDA или ЕМА); где, необязательно, набор включает устройство для внутривенного введения (IV) или инъекционное устройство, которое содержит мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием.
Схема 23. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием, как определено в любой из схем 1-21, для использования при лечении или профилактике заболевания или состояния, выбранных из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей; таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Схема 24. Использование мультиспецифического, биспецифического антитела или антитела с двойным связыванием, как определено в любой из схем 1-21 при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики заболевания или состояния человека, выбранного из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки) и саркомы мягких тканей).
Схема 25. Способ лечения или профилактики у человека заболевания или состояния, выбранного из неврологического заболевания, неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, таких как меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоскоклеточный рак головы и шеи, мезотелиома, вирусно-индуцированные раковые заболевания (такие как рак шейки матки и рак носоглотки), саркомы мягких тканей, гематологические злокачественные опухоли, такие как болезнь Ходжкина и неходжкинская лимфома и диффузная крупноклеточная В-клеточная лимфома (например, меланома, карцинома клеток Меркеля, немелкоклеточный рак легкого (плоскоклеточный и неплоскоклеточный), почечно-клеточный рак, рак мочевого пузыря, плоско клеточный рак головы и шеи и мезотелиома или, например, вирусно-индуцированные раковые заболевания (например, рак шейки матки и рак носоглотки) и саркомы мягких тканей), включающий введение указанному человеку терапевтически эффективного количества мультиспецифического, биспецифического антитела или антитела с двойным связыванием, как определено в любой из схем 1-21, причем тем самым проводится лечение или профилактика заболевания или состояния.
Заболевания и состояния, лечение или профилактика которых могут проводиться с помощью мультиспецифических, биспецифических антител или антител с двойным связыванием, предусмотренных в этих схемах, могут быть любыми заболеваниями, предусмотренными, например, с концепциях 41-45, аспектах 51-55 или в любом из предложений, описанных в данном документе.
Схема 26. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 23, использование согласно схеме 24 или способ согласно схеме 25, где неврологическое заболевание является нейродегенеративным заболеванием, расстройством или состоянием, где, необязательно, нейродегенеративное заболевание, расстройство или состояние выбирают из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона, болезни Хантингтона, первичного прогрессирующего рассеянного склероза, вторичного прогрессирующего рассеянного склероза, кортикобазальной дегенерации, синдрома Ретта, расстройства дегенерации сетчатки, выбранного из возрастной макулярной дегенерации и пигментного ретинита; передней ишемической оптической нейропатии, глаукомы, увеита, депрессии, связанного с травмой стресса или посттравматического стрессового расстройства, лобно-височной деменции, деменций тела Леви, легких когнитивных нарушений, атрофии задней коры головного мозга, первичной прогрессирующей афазии и прогрессирующего супрануклеарного паралича или связанной с возрастом деменции, в частности, болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона и болезни Хантингтона и, например, болезни Альцгеймера.
Схема 27. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием согласно схеме 23, использование согласно схеме 24 или способ согласно схеме 25, где рак выбран из меланомы, карциномы клеток Меркеля, немелкоклеточного рака легкого (плоскоклеточного и неплоскоклеточного), почечно-клеточного рака, рака мочевого пузыря, плоскоклеточного рака головы и шеи и мезотелиомы, или выбран из вирусно-индуцированных раковых заболеваний (например, рака шейки матки и рака носоглотки) и саркомы мягких тканей.
Схема 28. Мультиспецифическое, биспецифическое антитело или антитело с двойным связыванием, использование или способ согласно любой из схем 23-27, дополнительно включающие введение человеку дополнительной терапии, например, дополнительного терапевтического агента, где, необязательно, дополнительный терапевтическое средство независимо выбран из группы, состоящей из:
а. других ингибиторов иммунной контрольной точки (таких как антитела против TIM-3, антитела против PD-1, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3);
b. иммунных стимуляторов (таких как анти-ОХ40 антитела, анти-GITR антитела, анти-CD137-антитела и анти-CD40-антитела);
с. антагонистов хемокиновых рецепторов (таких как CXCR4, CCR4 и CXCR2);
d. таргетных ингибиторов киназ (таких как ингибиторы CSF-1R или VEGFR);
е. ингибиторов ангиогенеза (таких как анти-VEGF-A или дельта-подобный лиганд-4);
f. иммуностимулирующих пептидов или хемокинов (таких как CXCL9 или CXCL10);
g. цитокинов (таких как IL-15 и IL-21);
h. биспецифических антагонистов Т-клеток (BiTE), имеющих по меньшей мере одну специфичность против CD3 (например, CD3/CD19 BiTE);
i. других биспецифических молекул (например, IL-15-содержащих молекул, нацеленных на ассоциированные с опухолью антигены, например, рецепторы эпидермального фактора роста, такие как EGFR, Her-2, New York Esophageal Cancer-1 (NY-ESO-1), GD2, EpCAM или ассоциированный с меланомой антиген-3 (MAGE-A3));
j. онколитических вирусов (таких как вирус HSV (вирус герпеса человека) (который, необязательно, секретирует GMCSF), вирус болезни Ньюкасла и вирус осповакцины);
k. вакцинации опухоль-ассоциированными антигенами (такими как рака пищевода New York Esophageal Cancer-1 [NY-ESO-1], ассоциированный с меланомой антиген-3 [MAGE-3]);
l. клеточных терапий (таких как Т-клетки с химерными антигенными рецепторами (CAR-T), например, экспрессирующие анти-CD19, анти-EpCam или антимезотелин);
m. биспецифические активаторы (engagers) NK-клеток, обладающие специфичностью против активирующего рецептора MK, такого как NKG2D или CD16a; и
n. адоптивного переноса опухолеспецифических Т-клеток или клеток LAK,
или, необязательно, дополнительная терапия представляет собой химиотерапию, лучевую терапию и хирургическое удаление опухолей.
Лучевая терапия может проводиться с однократной дозой или дробными дозами, с облучением непосредственно пострадавших тканей либо всего организма.
В этой схеме любые признаки и варианты реализации концепции 46 являются применимыми mutatis mutandis.
В этом аспекте, биспецифические молекулы включают «биспецифические антитела» и гибридные белки антител, включая форматы и молекулы, описанные в концепциях 37-40.
Схема 29. Нуклеиновая кислота, кодирующая тяжелую цепь и/или легкую цепь мультиспецифического, биспецифического антитела или антитела с двойным связыванием, как определено в любой из схем 1-21.
Схема 30. Вектор, содержащий нуклеиновую кислоту, как определено в схеме 29; где вектор, необязательно, представляет собой вектор СНО или HEK293.
Схема 31. Хозяин, содержащий нуклеиновую кислоту, как определено в схеме 29, или вектор, как определено в схеме 30.
6. Применение антител и иммуноцитокинов
Если иное не очевидно из контекста, использование антител или фрагментов является применимым mutatis mutandis к иммуноцитокинам и мультиспецифическим (например, биспецифическим антителам или антителам с двойным связыванием) по изобретению.
Терапевтическое
В одном варианте реализации, раскрытые в данном документе специфические к PD-L1 антитела и их антигенсвязывающие фрагменты могут быть использованы для терапевтической модуляции пути PD-1/PD-L1. В одном варианте реализации, специфическое к PD-L1 антитело или его фрагмент являются такими, как описано в любой концепции, аспекте или варианте реализации настоящего изобретения.
В одном варианте реализации, антитело или связывающий фрагмент антитела специфически связываются с PD-L1 и тем самым ингибируют активность PD-L1. В другом варианте реализации, антитело или связывающий фрагмент антитела специфически связываются с PD-L1 и тем самым ингибируют связывание PD-L1 с PD-1. В другом варианте реализации, антитело или связывающий фрагмент антитела специфически связываются с PD-L1 и тем самым ингибируют связывание PD-L1 с В7-1. В еще одном варианте реализации, антитело или его антигенсвязывающий фрагмент блокируют индуцированную PD-L1 супрессию Т-клеток и тем самым усиливают противоопухолевый иммунитет.
В еще одном варианте реализации, антитело или его антигенсвязывающий фрагмент способны стимулировать один или несколько из следующих видов активности: пролиферацию Т-клеток, секрецию IFN-γ, CD25 и/или IL-2 в реакциях смешанных культур лимфоцитов.
В одном варианте реализации, антитело или его антигенсвязывающий фрагмент специфически связывают PD-L1 и ингибируют индуцируемую PD-L1 пролиферацию клеток, например, пролиферацию опухолевых клеток и/или ингибируют выживаемость опухолевых клеток. В другом варианте реализации, антитело или его связывающий антиген фрагмент специфически связывают PD-L1 и тем самым ингибируют опосредованную PD-L1 супрессию Т-клеток, включая, без ограничений, реакционноспособные к опухоли Т-клетки, тем самым усиливая противоопухолевую цитолитическую Т-клеточную активность. В других вариантах реализации, антитела или их связывающие фрагменты, как описано в данном документе, ингибируют адгезию опухолевых клеток, подвижность, инвазию и метастаз клеток и уменьшают рост опухоли. В других вариантах реализации, антитела или их связывающие фрагменты могут связываться с клетками, экспрессирующими PD-L1, включая опухолевые и неопухолевые клетки, и рекрутировать, посредством взаимодействия с фрагментом Fc антитела, клеточные эффекторные функции против клеток-мишеней по механизмам, включающим, без ограничений, антителозависимую клеточную цитотоксичность (ADCC) и антителозависимый клеточный фагоцитоз (ADCP).
Другие варианты реализации включают способы лечения пролиферативного или инвазионного заболевания у млекопитающего путем введения животному терапевтически эффективной дозы антитела или его антигенсвязывающего фрагмента. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы в способе лечения млекопитающего, страдающего заболеванием, выбранным из: неопластического или не связанного с новообразованиями заболевания, хронической вирусной инфекции и злокачественной опухоли, причем способ включает введение млекопитающему терапевтически эффективной дозы антитела или его антигенсвязывающего фрагмента.
Другие варианты реализации включают способы лечения заболевания иммунологической дисфункции у млекопитающего путем введения животному терапевтически эффективной дозы антитела или его антигенсвязывающего фрагмента, как описано в данном документе. Примеры иммунологической дисфункции у людей включает заболевания неврологического дефицита, такие как болезнь Альцгеймера.
Кроме того, было выдвинуто предположение, что иммунный ответ, особенно IFNv-зависимый системный иммунный ответ, может быть полезным при лечении болезни Альцгеймера и других патологий ЦНС, имеющих в качестве общего признака нейровоспалительный компонент. WO 2015/136541 (включенный в данный документ посредством ссылки) предлагает лечение болезни Альцгеймера с использованием антитела против PD-1 (см. также Baruch K. et al., PD-1 immune checkpoint blockade reduces pathology and improves memory in mouse models of Alzheimer's disease, Nature Medicine, 2016, 22(2): 137-137).
Таким образом, в одном варианте реализации, антитело или его антигенсвязывающий фрагмент специфически связывают PD-L1 и снижают уровень системной иммуносупрессии у индивидуума путем снятия ограничения, налагаемого на иммунную систему путем иммунной контрольной точки PD-1/PD-L1. В одном аспекте, ингибирующая блокада пути иммунной контрольной точки PD-1/PD-L1 приводит к преходящему облегчению системной адаптивной иммунной активности от супрессии, что приводит к транзиентно усиленному иммунному ответу на периферии, проявляющемуся главным образом в повышении секреции IFN-γ посредством IFN-γ-продуцирующими клетками. Повышенная активность IFN-γ может позволить хориоидному сплетению головного мозга обеспечить возможность селективного графика лейкоцитов и инфильтрации Т-клеток и моноцитов в поврежденную ЦНС, самонаведение этих иммунных клеток в места нейродегенеративной патологии и нейровоспаления, и может модулировать среду, чтобы она стала менее токсичной и более пермиссивной для клиренса токсичных веществ, спасения нейронов, регенерации и ремонта.
Таким образом, опосредованное PD-L1 заболевание или состояние представляет собой нейродегенеративное заболевание, расстройство или состояние. В одном варианте реализации, нейродегенеративным заболеванием, расстройством или состоянием является болезнь Альцгеймера. В другом варианте реализации, нейродегенеративное заболевание, расстройство или состояние выбирают из амиотрофического бокового склероза, болезни Паркинсона, болезни Хантингтона, первичного прогрессирующего рассеянного склероза, вторичного прогрессирующего рассеянного склероза, кортикобазальной дегенерации, синдрома Ретта, расстройства дегенерации сетчатки, выбранного из возрастной макулярной дегенерации и пигментного ретинита; передней ишемической оптической нейропатии, глаукомы, увеита, депрессии, связанного с травмой стресса или посттравматического стрессового расстройства, лобно-височной деменции, деменций телец Леви, легких когнитивных нарушений, атрофии задней коры, первичной прогрессирующей афазии и прогрессирующего супрануклеарного паралича или возрастной деменции. В другом варианте реализации, нейродегенеративное заболевание, расстройство или состояние выбирают из болезни Альцгеймера, бокового амиотрофического склероза, болезни Паркинсона и болезни Хантингтона.
Анти-PD-L1 антитела, как описано в данном документе, могут быть использованы для лечения болезни Альцгеймера или других нейродегенеративных заболеваний, необязательно, в сочетании с одним или несколькими другими ингибиторами иммунной контрольной точки (такими как антитела против TIM-3, антитела против CTLA-4, антитела против TIGIT и антитела против LAG-3), или одним или несколькими другими иммунными стимуляторами (такими как антитела против OX40, антитела против GITR, антитела против CD137, антитела против ICOS и антитела против CD40, включая конкретно описанные в Аспекте 1а данного документа). Другие партнеры для комбинаций включают любой из активных агентов, перечисленных в п. 10 формулы WO 2015/136541, который включен в данный документ посредством ссылки.
Любое из описанных в данном документе антител PD-L1 (включая, по меньшей мере, антитела, описанные в любой из концепций 1-40, и антитела PD-L1, описанные в Аспекте 1а), можно использовать для лечения нейродегенеративных заболеваний, расстройств или состояний, описанных выше.
Типичные примеры рака у людей включают карциному клеток Меркеля, рак молочной железы, рак предстательной железы, базальноклеточный рак, рак желчных путей, рак мочевого пузыря, рак кости, рак головного мозга и ЦНС (например, глиобластома), рак шейки матки, хориокарциному, рак ободочной и прямой кишки, рак соединительной ткани, рак пищеварительной системы; рак эндометрия, рак пищевода; рак глаз; рак головы и шеи; рак носоглотки; рак желудка; внутриэпителиальное новообразование; рак почки; рак гортани; лейкоз; рак печени; рак легких (например, мелкоклеточный и немелкоклеточный); лимфому, включая болезнь Ходжкина и неходжкинскую лимфому, включая, без ограничений, диффузную крупноклеточную В-клеточную лимфому (DLBCL); хронический лимфоцитарный лейкоз, меланому; увеальную меланому, миелому, нейробластому, рак полости рта (например, губы, языка, рта и глотки); рак яичников; рак поджелудочной железы, ретинобластому; рабдомиосаркому; рак прямой кишки, почечно-клеточный рак (карцинома почек (RCC)), рак дыхательной системы; саркому, рак кожи; рак желудка, рак яичек, рак щитовидной железы; рак матки, рак мочевой системы, а также другие карциномы и саркомы. Другие примеры вирусно-индуцированных раков включают: назофарингеальную карциному, некоторые виды неходжкинской лимфомы (НХЛ) (например, без ограничений, EBV+ (положительные по вирусу Эпштейна-Барр) лимфомы ЦНС, диффузная крупноклеточная В-клеточная лимфома (DLBCL) и лимфома Беркитта (BL), лимфомы Ходжкина (предположительно, инициируемые EBV), связанные с вирусом папилломы человека (HPV) плоскоклеточные карциномы шейки матки и головы и шеи); связанная с вирусом гепатита В (HBV) гепатоцеллюлярная карцинома.
Примерами хронических инфекций у людей являются ВИЧ, вирус гепатита В (HBV) и вирус гепатита С (HCV).
Пролиферативные или инвазионные заболевания, которые можно лечить антителами или антигенсвязывающими фрагментами, описанными в данном документе, включают неопластические заболевания и метастазы, связанные с таким неопластическим заболеванием, таким как меланома, увеальная меланома, рак кожи, мелкоклеточный рак легкого, немелкоклеточный рак легкого, рак слюнной железы, глиома, гепатоцеллюлярная (печеночная) карцинома, рак желчного пузыря, опухоль щитовидной железы, рак кости, рак желудка, рак предстательной железы, рак молочной железы (включая трижды негативный рак молочной железы), рак яичников, рак шейки матки, рак матки, рак вульвы, рак эндометрия, рак яичек, рак мочевого пузыря, рак легкого, глиобластома, рак щитовидной железы, рак эндометрия, рак почки, рак толстой кишки, колоректальный рак, рак поджелудочной железы, рак пищевода, рак мозга/ЦНС, раки нейронов, раки головы и шеи (включая, без ограничений, плоскоклеточный рак головы и шеи (SCCHN)), мезотелиома, саркомы, рак желчных протоков (холангиокарцинома), аденокарцинома тонкой кишки, педиатрические злокачественные опухоли, эпидермоидная карцинома, саркомы, рак плевральных/перитонеальных мембран и лейкоз, включая острый миелоидный лейкоз, острый лимфобластный лейкоз и множественную миелому. Поддающиеся лечению хронические вирусные инфекции включают ВИЧ, вирус гепатита В (HBV) и вирус гепатита С (HCV) у людей, вирус иммунодефицита обезьян (SIV) у обезьян и вирус лимфоцитарного хориоменингита (LCMV) у мышей.
Антитело или его антигенсвязывающий фрагмент можно вводить отдельно или в комбинации с другими антителами или химиотерапевтическими лекарственными средствами, лучевой терапией или терапевтическими вакцинами. В одном варианте реализации, антитело или его антигенсвязывающий фрагмент вводят в виде конъюгата антитело-лекарственное средство, в котором антитело или его антигенсвязывающий фрагмент связаны с фрагментом лекарственного средства, таким как цитотоксический или цитостатический агент. Использование конъюгатов антитело-лекарственное средство для местной доставки цитотоксических или цитостатических агентов при лечении рака позволяет осуществлять целенаправленную доставку фрагмента лекарственного средства к опухолям и внутриклеточное накопление в них, когда системное введение неконъюгированного лекарственного средства может привести к неприемлемым уровням токсичности. Лекарственные средства в конъюгатах лекарственное средство-антитело могут включать, без ограничений, дауномицин, доксорубицин, метотрексат и виндезин. Токсины также могут быть использованы в конъюгатах антитело-токсин, включая, например, бактериальные токсины, такие как дифтерийный токсин, растительные токсины, такие как рицин, токсины на основе малых молекул, такие как гелданамицин. Токсины могут проявлять свои цитотоксические и цитостатические эффекты по механизмам, включающим связывание тубулина, связывание ДНК или топоизомеразу.
Детектирование
В другом варианте реализации, антитела или антигенсвязывающие фрагменты могут быть использованы для детектирования присутствия, отсутствия и/или уровня поверхностной экспрессии экспрессируемого PD-L1 в образце. Поверхностная экспрессия PD-L1 может быть обнаружена in vivo и/или in vitro и полезна для диагностики заболеваний или состояний, связанных с экспрессией и/или сверхэкспрессией PD-L1.
In vitro диагностика
В другом варианте реализации, специфичные к PD-L1 антитела или их антигенсвязывающие фрагменты могут быть использованы для оценки экспрессии и локализации PD-L1 в биологическом образце от пациента. В одном варианте реализации, биологический образец представляет собой образец ткани и экспрессию PD-L1 детектируют с использованием известных методов, таких как проточная цитометрия, иммуногистохимия (IHC) свежей ткани, IHC ткани FFPE (фиксированной формалином и залитой парафином) и/или IHC замороженной ткани. В других вариантах реализации, биологическим образцом является кровь, плазма или сыворотка.
В одном варианте реализации, описанный в данном документе фрагмент антитела или антитела помечен детектируемым фрагментом, например, радиоактивной меткой, флуоресцентной меткой, ферментативной меткой хемилюминесцентной меткой или биотинильной группой. Радиоизотопы или радионуклиды могут включать 3H, 14C, 15N, 35S, 90Y, 99Tc, 115In, 125I, 131I, флуоресцентные метки могут включать родамин, лантаноидные люминофоры или FITC, и ферментативные метки могут включать пероксидазу хрена, β-галактозидазу, люциферазу, щелочную фосфатазу. Дополнительные метки включают, в качестве иллюстрации, без ограничений: ферменты, такие как глюкозо-6-фосфатдегидрогеназа («G6PDH»), альфа-D-галактозидаза, глюкозооксидаза, глюкоамилаза, карбоангидраза, ацетилхолинэстераза, лизоцим, малатдегидрогеназа и пероксидаза; красители; дополнительные флуоресцентные метки или люминофоры включают такие, как флуоресцеин и его производные, флуорохром, GFP (GFP обозначает «зеленый флуоресцентный белок»), дансил, умбеллиферон, фикоэритрин, фикоцианин, аллофикоцианин, о-фталевый альдегид и флуорескамин; флуорофоры, такие как криптаты и хелаты лантанидов, например, европия и т.д. (Perkin Elmer и Cisbio Assays); хемилюминесцентные метки или хемилюминесцентные вещества, такие как изолюминол, люминол и диоксетаны; сенсибилизаторы; коферменты; ферментные субстраты; частицы, такие как латексные или углеродные частицы; металлический золь; кристаллиты; липосомы; клетки и т.д., которые могут быть дополнительно мечены красителем, катализатором или другой детектируемой группой; молекулы, такие как биотин, дигоксигенин или 5-бромдезоксиуридин; фрагменты токсинов, такие как, например, фрагмент токсина, выбранного из группы экзотоксина Pseudomonas (РЕ или его цитотоксический фрагмент или мутант), дифтерийный токсин или его цитотоксический фрагмент или мутант, ботулинический токсин А, В, С, D, Е или F, рицин или его цитотоксический фрагмент, например, рицин А, абрин или его цитотоксический фрагмент, сапорин или его цитотоксический фрагмент, противовирусный токсин фитолакки (pokeweed) или его цитотоксический фрагмент и бриодин 1 или его цитотоксический фрагмент.
In vivo диагностика
В одном варианте реализации, антитело или его антигенсвязывающий фрагмент могут быть введены пациенту, где антитело или антигенсвязывающий фрагмент конъюгированы с меткой. Наличие метки у пациента можно измерить или наблюдать, при этом относительно высокое количество метки может указывать на высокий риск заболевания, и относительно низкое количество метки может указывать на относительно низкий риск заболевания. В одном варианте реализации, метка представляет собой контрастный агент, изотопную метку или флуоресцентный маркер, такой как зеленый флуоресцентный белок.
В одном варианте реализации, антитело или антигенсвязывающий фрагмент используют для контроля терапии, включающей использование других терапевтических средств, включая, например, химиотерапевтические средства или другие антитела, которые специфически связывают PD-L1. В одном варианте реализации, антитело не конкурирует с терапевтическими антителами PD-L1.
Руководство по выбору пациента
В одном варианте реализации, детектирование экспрессии PD-L1 может использоваться для управления выбором пациентов. В одном варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для оказания помощи в выборе пациента для терапевтического лечения антителами с использованием анти-PD-L1 антитела, включая, без ограничений, анти-PD-L1 антитела, раскрытые в WO 2011/066389, озаглавленной «Targeted Binding Agents Against B7-H1», причем указанные антитела и последовательности включены в данный документ посредством ссылок. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для оказания помощи в выборе пациента для лечения иммунотерапиями, такими как анти-PD-L1, анти-CTLA4, анти-ОХ40, анти-PD-l, вакцинами и т.д. В некоторых случаи, более высокие уровни PD-L1 могут указывать на успешную терапию, тогда как более низкие уровни могут указывать на пониженную вероятность успеха. Предпочтительная экспрессия сплайс-вариантов и/или процессинг белка могут давать уникальные профили белковой смеси, которые могут влиять на реакцию пациента на лечение или могут изменяться после лечения. Эти профили могут помочь идентифицировать пациентов и определить подгруппы пациентов, которые должны получать лечение, продолжать получать лечение, или получать альтернативное лечение. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для детектирования изоформ PD-L1. Образцы пациентов могут включать, например, кровь, плазму, сыворотку, мокроту, слюну, мочу, цереброспинальную жидкость (CSF), слезы, выдыхаемые образцы экзогенных частиц, клеточный супернатант, клеточный или тканевый лизат, или образцы тканей.
В одном варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для идентификации присутствия, отсутствия и/или уровня экспрессии PD-L1 в начальный момент времени, т.е. до лечения.
В другом варианте реализации, специфичные к PD-L1 антитела или их антигенсвязывающие фрагменты могут использоваться в качестве маркера исключения, чтобы предлагать лечение с помощью методов, не нацеленных на PD-L1. В другом варианте реализации, специфичные к PD-L1 антитела или их антигенсвязывающие фрагменты могут быть использованы в качестве прогностического маркера ожидаемой продолжительности жизни. В частности, экспрессия PD-L1 на опухолях связана с плохим прогнозом, а ожидаемая продолжительность жизни может быть оценена на основе исторических данных по типам опухолей.
Способы детектирования белков известны и включают, например, иммуногистохимию (IHC), проточную цитометрию, вестерн-блоттинг и масс-спектроскопию, иммунопреципитацию, аптамеры, иммуно-ПЦР и белковые матрицы.
Корректирование терапии
Антитела могут использоваться для регулирования терапии. Например, антитела или их антигенсвязывающие фрагменты могут быть использованы для идентификации присутствия, отсутствия и/или уровня экспрессии PD-L1 во время или после лечения. В одном варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы в качестве биомаркеров раннего ответа для помощи в ведении пациентов, одобрении лекарств и возмещении расходов. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для идентификации присутствия, отсутствия и/или уровня экспрессии PD-L1, чтобы помочь регулировать терапию. Например, экспрессия PD-L1 может помочь определить, было ли лечение эффективно и, следовательно, следует ли продолжать лечение или откорректировать дозу (увеличить или уменьшить), и следует ли изменить схему комбинированного лечения. Например, в одном варианте реализации, специфичные к PD-L1 антитела или их антигенсвязывающие фрагменты могут быть использованы для определения степени заполнения рецепторов PD-L1 на клетках пациента, получающего анти-PD-L1-терапию, для установления дозы (PK/PD). В частности, степень заполнения рецепторов может использоваться в качестве меры охвата мишени или покрытия мишени. Оценки количества или продолжительности покрытия мишени, необходимого для проявления биологического или клинического ответа, могут быть использованы для определения того, получил ли пациент достаточную дозу или нет. В частности, антитела могут использоваться для оценки соотношения между дозой, экспозицией, заполнением рецепторов, фармакодинамическим ответом и клинической пользой.
Мониторинг эффективности терапии
В другом варианте реализации, специфичные к PD-L1 антитела или их антигенсвязывающие фрагменты могут использоваться для мониторинга пациентов, чтобы помочь оценить, эффективен ли курс лечения и следует ли продолжать лечение. Например, в одном варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы для определения экспрессии до получения пациентом терапевтического лечения, нацеленного на PD-L1. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут использоваться для определения экспрессии во время терапии или после получения пациентом терапевтического лечения против PD-L1. В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы в качестве маркера раннего ответа, чтобы помочь в определении того, эффективен ли курс терапии и должен ли он быть продолжен или прекращен. В одном варианте реализации, экспрессия PD-L1 детектируется после вымывания, где термин «вымывание» относится к периоду времени, после которого вводимый препарат удаляется из организма. В частности, экспрессия PD-L1 может детектироваться после вымывания, если пациент получает анти-PD-L1 терапию, которая конкурирует с детектируемым антителом. Однако, если пациента лечат антителом, которое не конкурирует с анти-PD-L1 антителом, таким как анти-CTLA-4 или анти-PD-l, детектирование может быть проведено без ожидания вымывания. В другом варианте реализации, детектируемое антитело может связываться с PD-L1, но не конкурировать с терапевтическим антителом, которое связывается с PD-L1. В этой ситуации вымывание может не понадобиться. Период вымывания может меняться в зависимости от многих факторов, но обычно представляет собой период продолжительностью, по меньшей мере, примерно 1, 2, 3, 4, 5 или 6 недель и до 1, 2, 3, 4, 5 или 6 месяцев после лечения новейшими методами химиотерапии или иммунотерапии. Антитела или их антигенсвязывающие фрагменты могут быть использованы для определения экспрессии PD-L1 на образцах биопсии или на циркулирующих опухолевых клетках (СТС).
В одном варианте реализации, меченые антитела или их антигенсвязывающие фрагменты могут быть использованы для определения корреляционных зависимостей с периферическими участками для обеспечения неинвазивной оценки состояния опухоли до, во время и после лечения.
Способы детектирования белков являются известными и включают, например, иммуногистохимию (IHC), проточную цитометрию, вестерн-блоттинг и масс-спектроскопию, иммунопреципитацию, аптамеры, иммуно-ПЦР и белковые матрицы.
Определение партнеров по связыванию белка для PD-L1
В другом варианте реализации, антитела или их антигенсвязывающие фрагменты могут быть использованы в качестве реагента захвата или детектирующего реагента для исследования партнеров белков PD-L1 по связыванию белка в контексте «осаждения» (pull-down) белков. «Осаждение» (pull down) белка относится к иммунопреципитации комплексов интактного белка, такого как антиген, наряду с любыми связанными с ним белками или лигандами, и также известно как совместная иммунопреципитация (Co-IP). Co-IP работает путем выбора антитела, нацеленного на известный белок, который, как полагают, является членом более крупного комплекса белков. Нацеливание антитела на известный член может позволить извлечь из раствора весь белковый комплекс и тем самым идентифицировать неизвестные члены комплекса. В настоящее время отсутствует полное понимание регуляции иммунного распознавания посредством и отличия оси PD-1 от CTLA-4 и т.д. Таким образом, антитела и антигенсвязывающие фрагменты могут улучшить понимание взаимодействий между вспомогательными белками и факторами, которые могут определять склонность пациента реагировать на конкретные методы лечения или иммунотерапию в целом.
7. Фармацевтические композиции
Если иное не очевидно из контекста, композиции антител или фрагментов являются применимыми mutatis mutandis к иммуноцитокинам и мультиспецифическим (например, биспецифическим антителам или антителам с двойным связыванием) по изобретению.
В одном варианте реализации, предложена фармацевтическая композиция, содержащая эффективное количество антитела или антигенсвязывающего фрагмента и фармацевтически приемлемый носитель. Эффективное количество антитела для терапевтического использования, будет зависеть, например, от терапевтических целей, пути введения и состояния пациента. В одном варианте реализации, композиция включает другие эксципиенты или стабилизаторы.
Фармацевтически приемлемые носители известны и включают носители, эксципиенты или стабилизаторы, которые являются нетоксичными для клеток или млекопитающих, подвергающихся воздействию, при используемых дозировках и концентрациях. Часто физиологически приемлемый носитель представляет собой водный раствор с забуференным рН. Примеры физиологически приемлемых носителей включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту; низкомолекулярный полипептид (менее примерно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как этилендиаминтетрауксусная кислота (ЭДТА); сахароспирты, такие как маннит или сорбит; солеобразующие противоионы, такие как натрий; и/или неионные поверхностно-активные вещества, такие как TWEEN™, полиэтиленгликоль (ПЭГ) и PLURONICS™.
Антитела или антигенсвязывающие фрагменты можно вводить внутривенно или через нос, легкие, например, в виде жидкого или порошкообразного аэрозоля (лиофилизированного). Композицию можно также вводить парентерально или подкожно. При системном введении композиция должна быть стерильной, апирогенной и в физиологически приемлемом растворе с учетом рН, изотоничности и стабильности. Эти условия известны специалистам в данной области техники.
Способы введения профилактического или терапевтического агента (например, антитела, как раскрыто в данном документе) или фармацевтическая композиция включают, без ограничений, парентеральное введение (например, внутрикожное, внутримышечное, внутрибрюшинное, внутривенное и подкожное), эпидуральное и мукозальное (например, интраназальный и пероральный пути). В конкретном варианте реализации, профилактический или терапевтическое средство (например, антитело, как раскрыто в данном документе), или фармацевтическую композицию вводят интраназально, внутримышечно, внутривенно или подкожно. Профилактические или терапевтические средства или композиции могут быть введены любым удобным путем, например, путем инфузиг или болюсной инъекции, путем абсорбции через эпителиальные или слизистые оболочки (например, слизистую оболочку полости рта, слизистую оболочку полости носа, слизистую оболочку прямой кишки и кишечника и т.д.) и могут быть введены вместе с другими биологически активными агентами. Введение может быть системным или местным. Каждая доза может быть введена одним и тем же путем введения или разными. В одном варианте реализации, анти-PD-L1 антитело или фрагмент, как раскрыто в данном документе, могут быть введены несколькими путями введения одновременно или последовательно с другими дозами того же самого или другого анти-PD-L1 антитела или фрагмента, как раскрыто в данном документе.
Различные системы доставки известны и могут быть использованы для введения профилактического или терапевтического агента (например, антитела или фрагмента, как раскрыто в данном документе), включая, без ограничений; инкапсулирование в липосомах, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать антитело, рецептор-опосредованный эндоцитоз (см., например, Wu and Wu, J. Biol. Chem. 262: 4429-4432 (1987)); конструирование нуклеиновой кислоты как части ретровирусного или другого вектора и т.д. Кроме того, также может быть использовано легочное введение, например, с использованием ингалятора или распылителя и композиции препарата с аэрозольным агентом. См., например, патенты США №№6019968, 5985320, 5985309, 5934272, 5874064, 5855913, 5290540 и 4880078; и в публикациях РСТ WO 92/19244, WO 97/32572, WO 97/44013, WO 98/31346 и WO 99/66903, каждый из которых включен в данный документ посредством ссылки в полном объеме.
В конкретном варианте реализации, может быть желательным местное введение профилактического или терапевтического агента или фармацевтической композиции, как описано в данном документе, в область, нуждающуюся в лечении. Это может быть достигнуто, например, путем локальной инфузии, путем местного введения (например, в виде интраназального спрея), путем инъекции или с помощью имплантата, причем указанный имплантат представляет собой пористый, непористый или желатинообразный материал, включая мембраны, таких как силастиковые (sialastic) мембраны, или волокна. При введении анти-PD-L1 антитела или фрагмента следует следить за тем, чтобы использовались материалы, которые не абсорбируют антитело.
8. Наборы и готовые изделия
Если из контекста не следует иное, наборы и готовые изделия для антител или фрагментов являются применимыми mutatis mutandis к иммуноцитокинам и мультиспецифическим (например, биспецифическим антителам или антителам с двойным связыванием) по изобретению.
В одном варианте реализации, изобретение предусматривает набор для детектирования PD-L1 в биологическом образце. Набор может использоваться для скрининга заболеваний, связанных с PD-L1. В одном варианте реализации, набор включает антитело или антигенсвязывающий фрагмент и средство для определения того, связано ли антитело или антигенсвязывающий фрагмент с PD-L1 в образце. В одном варианте реализации, антитело или антигенсвязывающий фрагмент являются мечеными. В другом варианте реализации, антитело или антигенсвязывающий фрагмент представляют собой немеченое первичное антитело, и набор включает средство для детектирования первичного антитела. В одном варианте реализации, средство для детектирования включает меченое вторичное антитело, которое является антииммуноглобулиновым антителом. Антитело может быть помечено любым пригодным маркером, включая, например, флуорохром, фермент, радионуклид и рентгеноконтрастный материал. Пригодные антитела и антигенсвязывающие фрагменты подробно описаны выше.
В одном варианте реализации, предлагается набор для детектирования PD-L1, где набор включает антитело или антигенсвязывающий фрагмент, описанные в данном документе. В одном варианте реализации, набор может также включать инструкции и один или несколько реагентов для детектирования PD-L1. В одном варианте реализации, набор включает антиген или антигенсвязывающий фрагмент, описанные в данном документе, вместе с инструкциями по приготовлению фиксированного формалином залитого парафином (FFPE) образца ткани для иммуногистохимии (IHC) и/или одного или нескольких реагентов для IHC. В одном варианте реализации, набор включает антиген или антигенсвязывающий фрагмент, описанные в данном документе, в качестве первичного антитела, и вторичное антитело, которое специфически связывается с ними. В одном варианте реализации, набор включает меченый антиген или антигенсвязывающий фрагмент, описанные в данном документе, где метка включает флуоресцентную метку, такую как флуоросцеин или родамин, или ферментативный репортер, такой как пероксидаза хрена (HRP) или щелочная фосфатаза (АР). В одном варианте реализации, набор включает блокирующий реагент, который содержит по меньшей мере примерно 1% и до примерно 5%, или от примерно 2% до 3%, или примерно 2% белка желатина шкур холодноводных (CWF) рыб в буфере, таких как забуференный фосфатом физиологический раствор (PBS). В одном варианте реализации, набор включает буфер для извлечения антигена, такой как цитратный буфер, например, цитрат натрия, в концентрации по меньшей мере примерно 1, 2, 5 или 10 мМ, и до примерно 10, 15 или 20 мМ, и при рН от примерно 5,5 до 9 или рН около 6.
В другом варианте реализации, предусматривается набор для лечения заболеваний, связанных с экспрессией PD-L1, где набор включает антитело или антигенсвязывающий фрагмент, описанные в данном документе, и инструкции по введению антитела или антигенсвязывающего фрагмента субъекту, нуждающемуся в лечении. Также предлагается фармацевтический или диагностический пакет или набор, содержащий один или несколько контейнеров, заполненных одним или несколькими ингредиентами фармацевтических композиций, раскрытых в данном документе, такими как одно или несколько антител против PD-L1 или фрагментов, представленных в данном документе. Такой контейнер (контейнеры) могут быть необязательно связаны с уведомлением в форме, предписанной правительственным агентством, регулирующим производство, использование или продажу фармацевтических препаратов или биологических продуктов, в котором указывается на разрешение со стороны агентства на производство, использование или продажу для введения людям, например, регистрационный номер.
В другом варианте реализации, предусматриваются промышленное изделие, которое включает контейнер, содержащий композицию, содержащую антитело или антигенсвязывающий фрагмент, раскрытые в данном документе, и вкладыш или этикетка, указывающие, что композиция может использоваться для лечения заболеваний, характеризующихся экспрессией или сверхэкспрессией PD-L1. В одном варианте реализации, предусматривается набор для лечения и/или профилактики состояния или заболевания, опосредованного PD-L1, причем набор содержит антитело или фрагмент, как раскрыто в данном документе в любом варианте реализации или комбинации вариантов реализации (и, необязательно, дополнительный терапевтическое средство, как раскрыто в другой части данного документа), необязательно, в комбинации с этикеткой или инструкциями по использованию для лечения и/или профилактики указанного заболевания или состояния у человека; где, необязательно, этикетка или инструкция содержат номер регистрационного удостоверения лекарственного средства (например, регистрационный номер FDA или ЕМА); где, необязательно, набор включает устройство для внутривенного введения (IV) или инъекционное устройство, содержащее антитело или фрагмент. В другом варианте реализации, набор содержит антитело или его антигенсвязывающий фрагмент, содержащиеся в контейнере или в пакете для внутривенного (IV) введения. В другом варианте реализации, контейнер или пакет для внутривенного (IV) введения представляет собой стерильный контейнер или стерильный для внутривенного введения. В другом варианте реализации, таким образом, составлена фармацевтическая композиция антитела или антигенсвязывающего фрагмента, содержащаяся в (стерильном) контейнере или содержащаяся внутри (стерильного) пакета для внутривенного (IV) введения. В дополнительном варианте реализации, комплект дополнительно содержит инструкции по использованию.
9. Примеры
Пример 1 - Получение антигена, процедуры иммунизации и получение гибридомы
В следующем примере представлено подробное описание получения и идентификации панели моноклональных антител против PD-L1 человека с использованием системы KyMouse™ (см., например, WO 2011/004192, WO 2011/158009 и WO 2013/061098). С этой целью, генетически модифицированных мышей, содержащих большое количество генов человеческого иммуноглобулина, иммунизируют растворимым рекомбинантным PD-L1 человека или поверхностно экспрессированным PD-L1 человека, презентированным (displayed) на клетках эмбриональных фибробластов мыши (MEF). Были разработаны различные схемы иммунизации, включая обычные внутрибрюшинные инъекции, а также режим быстрой иммунизации на нескольких участках (RIMMS), которые обеспечивали бустер-иммунизацию животных в течение нескольких недель (см. подробное описание методов ниже). В конце каждой схемы удаляли вторичную лимфоидную ткань, такую как селезенка, а в некоторых случаях и лимфатические узлы. Из тканей готовили суспензию отдельных клеток и сливали с клетками SP2/0 для создания стабильной гибридомной клеточной линии.
Материалы и методы
a) Получение стабильно трансфицированных клеток MEF и CHO-S. экспрессирующих PD-L1 человека:
Полноразмерная последовательность PD-L1 человека (SEQ ID NO: 1, также известная как В7-Н1) была подвергнута оптимизации кодонов для экспрессии у млекопитающих и клонирована в экспрессионный вектор под управлением промотором CMV, фланкированным специфическими 3'- и 5'-терминальными повторными последовательностями piggyBac, облегчающими стабильную интеграцию в клеточный геном (см. "A hyperactive piggyBac транспозаза for mammalian applications"; Yusa K., et al., Proc. Natl. Acad. Sci. USA., 108(4): 1531-6, 2011 Jan 25). Кроме того, экспрессионный вектор содержал кассету для селекции пуромицином для облегчения получения стабильной клеточной линии. Проводили трансфекцию плазмиды, экспрессирующей PD-L1 человека, совместно с плазмидой, кодирующей транспозазу piggyBac, в самостоятельно полученную клеточную линию мышиных эмбриональных фибробластов мыши (MEF) (эмбрионы, используемые для генерации этой линии, были получены от 129S5, скрещенного с самкой мыши C57/BL6) и CHO-S с использованием реагента трансфекции FreeStyle Max (Invitrogen) в соответствии с инструкциями производителя. Через 24 часа после трансфекции среду дополняли пуромицином и выращивали в течение по меньшей мере двух недель, чтобы выбрать стабильную клеточную линию, с полной заменой среды каждые 3-4 дня. Экспрессию DPD-L1 оценивали методом проточной цитометрии с использованием конъюгированного антитела против человеческого PD-L1-РЕ (eBioscience). Полные среды MEF состояли из модифицированной по Дульбекко среды Игла (Gibco), дополненной 10% об./об. фетальной бычьей сыворотки (Gibco). Полные среды CHO-S состояли из сред CD-CHO (Gibco), дополненных 8 мМ Glutamax (Gibco). Трансфицированные клетки СНО использовали для скрининга (см. Пример 2).
b) Получение клеток MEF для иммунизации мыши:
Среду клеточной культуры удаляли и клетки промывали один раз 1× PBS. Клетки обрабатывали в течение 5 минут трипсином для отделения клеток от поверхности тканевой культуры. Клетки собирали и трипсин нейтрализовали добавлением полных сред MEF. Клетки затем центрифугировали при 300×g в течение 10 минут и промывали 25 мл 1× PBS. Клетки подсчитывали и ресуспендировали в соответствующей концентрации в 1× PBS.
c) Иммунизация с помощью PD-L1
Генетически модифицированный штамм Kymouse™ HK, содержащий гены человеческого иммуноглобулина, продуцирующие человеческие антитела легкой цепи каппа (HK) (Lee et al, Nature Biotechnology, 32, 6-363, 2014), был иммунизирован по различным схемам иммунизации для получения антител анти-PD-L1 человека.
Мышей иммунизировали либо с помощью растворимых рекомбинантных hPD-L1 (R&D Systems, 156-B7, Fc-химера) с использованием модифицированной процедуры подкожной иммунизации (RIMMS, модифицированной по Kilpatrick et al., "Rapid development of affinity matured monoclonal antibodies using RIMMS"; Hybridoma. 1997 Aug, 16 (4): 381-9, далее КМ031), или с использованием растворимого рекомбинантного hPD-L1 по схеме первичной иммунизации-отдыха-вторичной иммунизации (prime-rest-boost) путем подкожного введения (далее КМ032), или комбинацией растворимого рекомбинантного hPD-L1 и стабильно трансфицированных MEF-клеток, экспрессирующих hPD-L1, вводимых внутрибрюшинно (далее КМ033). Система Sigma Adjuvant использовалась для всех иммунизации, а интервалы отдыха обычно составляли от 2 до 3 недель. При использовании в качестве иммуногена белка, также вводили CpG (Hokkaido System Science). Сыворотку из серийных или терминальных образцов крови анализировали на присутствие специфических антител методами ИФА и проточной цитометрии, и данные о титрах использовались (когда это было возможно) для отбора мышей, которые будут использоваться для гибридомных слияний. Была также проведена еще одна схема иммунизации КМ042, с использованием только клеток MEF-PD-L1, или только один белок по схеме первичная иммунизация-отдых-вторичная иммунизация, но среди шести антител с подтвержденным связыванием с hPD-L1 не было идентифицировано нейтрализующих антител.
d) Клонирование и экспрессия рекомбинантных белков
Последовательности ДНК, кодирующие PD-L1, были приобретены в виде синтетических цепочек ДНК и клонированы в соответствующие векторы экспрессии млекопитающих для транзиентной экспрессии в клетках Expi293 и СНО. В перечне последовательностей приведены последовательности антигенов, когда они были доступны, и аффинные метки для очистки/мечения (выделены жирным шрифтом и подчеркиванием), см. SEQ ID NOs: 3-6.
е) Определение титра сыворотки по обратному протоколу ИФА PD-L1
Титры в образцах мышиной сыворотки определяли с использованием протокола обратного ИФА PD-L1. Анти-мышиное антитело для захвата IgG (Southern Biotech) (4 мкг/мл, разведенное в PBS, 50 мкл/лунку) адсорбировалось на 96-луночных планшетах с низкой автофлуоресценцией и высоким связыванием белка (Costar) в течение ночи при 4°С. Избыток IgG удаляли промыванием три раза PBS-Tween (0,1% об./об.) и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего пластины трижды промывали PBS-Tween (0,1% об./об.). Готовили серийные десятикратные разведения мышиной сыворотки, разбавляя образцы разбавителем для реагентов (0,1% мас./об. BSA/PBS). Затем на ИФА-планшеты добавляли 50 мкл/лунку продукта этого титрования. Для определения изменения уровня активности в результате иммунизации сыворотку от каждого животного до иммунизации разбавляли до 1/100 разбавителем для реагентов и добавляли на ИФА-планшеты по 50 мкл/лунку. После инкубации планшеты промывали, как прежде, для удаления несвязанных белков. Затем добавляли в планшеты биотинилированный hPD-L1-his (белок собственного приготовления, SEQ ID NO: 3, помеченный на месте с использованием Sulfo-NHS-LC-Biotin (Thermo)), используемый в концентрации 100 нг/мл в разбавителе для реагентов; 50 мкл/лунку), и инкубировали при комнатной температуре в течение 1 часа. Несвязанный биотинилированный hPD-L1 удаляли промыванием PBS-Tween (0,1% об./об.), а оставшийся биотинилированный hPD-L1 детектировали путем добавления стрептавидина-HRP (Sigma), разбавленного 1/10000 разбавителем для реагентов. После инкубации в течение 1 часа при комнатной температуре планшеты промывали, как описано выше, и в планшет прибавляли 50 мкл тетраметилбензидина (ТМВ) (Sigma). Реакцию останавливали добавлением 50 мкл 1М серной кислоты (Fluka Analytical). Оптическую плотность (OD) при 450 нм измеряли планшет-ридером Envision (PerkinElmer). Титры не проводились для KM032, поскольку была иммунизирована только одна мышь. Для KM031 титры выполнялись только для терминальных образцов крови.
f) Определение титров сыворотки проточной цитометрией с использованием hPD-L1, эспрессируемого CHO-S
Клетки CHO-S, экспрессирующие hPD-L1, суспендированные в буфере FACS (PBS + 1% мас./об. BSA + 0,1% мас./об. азида натрия), распределяли на 96-луночном планшете с V-образными лунками (Greiner) с плотностью 105 клеток на лунку. Титрование сыворотки мыши готовили, разбавляя образцы буфером FACS. Затем к ячейке прибавляли 25 мкл/лунку продукта этого титрования. Чтобы определить изменение уровня активности в результате иммунизации, сыворотку от каждого животного до иммунизации разбавляли до 1/100 в буфере FACS и добавляли к клеткам по 25 мкл/лунку. Клетки инкубировали при 4°С в течение 1 часа. Клетки дважды промывали 150 мкл PBS, центрифугировали после каждой стадии промывки и аспирации супернатанта (центрифугирование при 300×g в течение 3 минут). Для детектирования связывания антител, конъюгат фикоэритрина (РЕ) с козьим антимышиным IgG (Jackson ImmunoResearch) разбавляли 1/500 в буфере FACS и добавляли к клеткам по 50 мкл. Клетки инкубировали 1 час при 4°С в темноте, затем дважды промывали 150 мкл PBS, как описано выше. Для фиксации клеток добавляли 100 мкл 2% об./об. параформальдегида и клетки инкубировали в течение 30 минут при 4°С. Затем клетки осаждали центрифугированием при 300×g и планшеты ресуспендировали в 100 мкл буфера FACS. Интенсивность сигнала фикоэритрина (РЕ) (среднее геометрическое) измеряли методом проточной цитометрии с использованием инструмента BD FACS Array. Определение титров этим методом проводили только для KM033.
g) Выделение и подготовка мышиных тканей
После окончательной иммунизации мышей умерщвляли (culled) и селезенку вырезали у иммунизированных мышей, промывали в 1× PBS и хранили на льду до последующей обработки. Ткани готовили в буфере, содержащем 1× PBS (Invitrogen) и 3% инактивированной нагреванием FBS (Invitrogen). Спленоциты диспергировали путем протирания ткани через сито с размером отверстий 45 мкм (BD Falcon) и промывали 30 мл 3% буфера FBS/PBS перед центрифугированием при 700 g в течение 10 минут при 4°С. Для удаления эритроцитов, гранулированные спленоциты ресуспендировали в 4 мл буфера для лизиса эритроцитов (Sigma). После 4 минут инкубации реакцию лизиса останавливали добавлением буфера 3% FBS/1× PBS. Агрегаты клеток отфильтровывали с помощью сита 45 мкм. Оставшиеся спленоциты осаждали центрифугированием для дальнейших процедур. Для KM031 и KM032 также извлекали подмышечные, паховые и брыжеечные лимфатические узлы и помещали в стерильный 1× PBS на льду до последующей обработки. Лимфатические узлы обрабатывались отдельно от спленоцитов. Клетки лимфатических узлов готовили, как указано выше, но без проведения лизиса эритроцитов. Оставшиеся клетки лимфатических узлов осаждали центрифугированием для дальнейших процедур.
h) Слияние гибридом
Объединяли клетки селезенки и лимфатических узлов для KM031, а также KM032, и подвергали негативному отбору с использованием системы MACS® Separation. Вкратце, в случае использования лимфатических узлов, эти клетки объединяли со спленоцитами от соответствующих мышей после лизиса эритроцитов и определяли общее количество клеток. Клетки ресуспендировали в 100 мкл 3%-ного буфера FBS/PBS на 107 клеток, перед добавлением 10 мкл коктейля Pan В Cell Biotin-Antibody (№ кат. 130-095-813) на 107 клеток и 10 мкл антитела анти-IgD-биотин (№ кат. 130-096-979) и инкубировали в течение 10 минут при 4°С. Добавляли 2 мл буфера FBS/PBS и клетки центрифугировали при 700 g в течение 10 минут. Супернатант полностью удаляли аспирацией и добавляли 100 мкл свежего буфера, затем добавляли 30 мкл Anti-Biotin MicroBeads (№кат.130-047-302) на 107 клеток вместе с 7 мкл Anti-Mouse IgM MicroBeads (Miltenyi Biotec). Клетки инкубировали в холодильнике в течение 15 минут. Затем смесь клеток/микросфер наносили на предварительно смоченную колонку LD (Miltenyi Biotec), помещенную в магнитный сепаратор MACS, и промывали 3% буфером FBS/PBS. Немеченые клетки, которые проходили через колонку, собирали в 3%-ном буфере FBS/PBS.
Клетки KM033 подвергали положительному отбору с использованием системы MACS® Separation. После лизиса эритроцитов спленоциты ресуспендировали в 80 мкл 3% буфера FBS/PBS на 107 клеток перед добавлением антимышиного IgG1 (№ кат. 130-047-101) плюс микросферы с антимышиным IgG2a+b (№ кат. 130 -047-201) и инкубировали в течение 15 минут при 4°С. Смесь клеток/микросфер наносят затем на предварительно смоченную колонку LS (Miltenyi Biotec), помещенную в магнитный сепаратор MACS, и промывают 3% FBS/PBS-буфером. IgG-положительные клетки собирают в меченной фракции, связанной на колонке, в 3%-ном буфере FBS/PBS.
Обогащенные В-клетки обрабатывали CpG (Hokkaido System Science) в течение ночи (конечная концентрация 25 мкМ) и на следующий день промывали один раз буфером для слияния BSA (0,3 М D-сорбит, 0,11 мМ гидрат ацетата кальция, 0,5 мМ тетрагидрат ацетата магния и 0,1% BSA (об./об.), доведенный до рН 7,2). Промытые клетки ресуспендировали в 200 мкл буфера для слияния BSA и определяли количество клеток. Клетки SP2/0 обрабатывали таким же образом, но промывали буфером слияния BSA дважды, а не один раз. В-клетки, слитые в соотношении 3:1 с клетками миеломы SP2/0, путем электрослияния с использованием манипулятора ВТХ ЕСМ 2001 Electro Cell Manipulator (Harvard Apparatus). Каждый продукт слияния оставляли на ночь в среде для восстановления (модифицированная по Дульбекко среда Игла (высокое содержание глюкозы, без фенолового красного), с добавкой OPI (оксалоацетат, пируват, инсулин) (Sigma), 1× L-глутамакса (Gibco), 20% FBS (Gibco, с испытаниями каждой партии для использования с гибридомами) и 0,05 мМ 2-меркаптоэтанола), затем ресуспендировали в 1 части среды для восстановления и 9 частях полутвердой среды (ClonaCell-HY Hybridoma Selection Medium D, Stemcell Technologies) и высеивали на 10 см чашки Петри. Видимые колонии выбирали через 12 дней в 96-луночные планшеты и культивировали в течение еще 2-3 дней перед скринингом.
Пример 2 - Скрининг супернатантов гибридомы
После получения гибридомных клонов супернатант гибридомы оценивали последовательно первичным и вторичным скринингом, и соответствующие гибридомные клоны выбирали на основе критериев связывания антитела с PD-L1 человека и активности нейтрализации рецептора. В описанных каскадах скрининга было проведено тестирование 9317 гибридомных клонов, и 120 были идентифицированы как первично отобранные. После этого, свойства 36 гибридомных клонов были подтверждены с использованием критериев вторичного скрининга (см. подробнее в разделе Материалы и методы и в Таблице 1). Из клонов, идентифицированных вторичным скринингом, авторы изобретения выбрали четыре клона для включения в список предварительно отобранных антител, в соответствии с желательными критериями отбора (см. подробнее в Примере 3).
Материалы и методы
а) Первичный скрининг - Связывание с экспрессируемым клетками PD-L1 человека
Супернатанты, собранные с клеток гибридомы, подвергали скринингу на способность секретируемых антител связываться с hPD-L1, экспрессируемым на поверхности клеток CHO-S. Для определения связывания CHO-S клетки hPD-L1 высеивали в 384-луночные обработанные планшеты для тканевых культур с черными стенками и прозрачным дном (Costar) в количестве 1×104/лунку в 80 мкл среды F12 (Gibco) с добавкой 10% FBS (Gibco) и культивировали в течение ночи при 37°С, 5% CO2. Культуральную среду удаляли из 384-луночных планшетов для анализа. Добавляли в каждую лунку не менее 5 мкл супернатанта гибридомы, или 5 мкл MIH1 с концентрацией 2 мкг/мл в гибридомной поддерживающей среде (НММ), или контрольное антитело изотипа IgG1 (называемое в некоторых случаях Cm7, Sigma M9269, в конечной концентрации 1 мкг/мл), разбавленное в НММ. НММ состояла из среды Advanced DMEM (Gibco), дополненной 1× Glutamax (Gibco), 20% об./об. FBS (Gibco), 0,05 мМ β-меркаптоэтанола, 1× НТ-добавки (Gibco) и 1× пенициллин/стрептомицин (Gibco). В каждую лунку добавляли 45 мкл буфера FACS, содержащего 500 нг/мл антимышиного антитела IRDye 800CW anti-Mouse Ab (LICOR) и 0,2 мкМ DRAQ5 (Biostatus). DRAQ5 не добавляли в фоновые лунки. Планшеты инкубировали в течение 1 часа при 4°С. Супернатант удаляли аспирацией и добавляли 25 мкл 4% об./об. параформальдегида и планшеты инкубировали в течение 15 минут при комнатной температуре. Планшеты дважды промывали 100 мкл PBS и затем промывочный буфер полностью удаляли. Интенсивность флуоресценции считывали путем сканирования планшетов с использованием инфракрасной системы визуализации Odyssey Infrared Imaging System (LI-COR ®). Связывание с антимышиным антителом (канал 800 нм) нормировали по числу клеток (канал 700 нм) в соответствии с алгоритмом, рекомендованным LI-COR®. Процент эффекта рассчитывали, как описано ниже (Уравнение 1). Полное связывание определяли с использованием эталонного антитела при конечной концентрации анализа 0,2 мкг/мл. Неспецифическое связывание определяли с использованием изотипического контроля мышиного IgG1 (Sigma) при конечной концентрации анализа 0,2 мкг/мл. Критерии первичного отбора антител были основаны на анализируемом сигнале и визуальном осмотре отсканированных планшетов.
Уравнение 1: Расчет процента эффекта по результатам первичного скрининга (LI-COR) и HTRF
Использование значений 800% отклика (LI-COR) или отношения 665/620 нм (см. Уравнение 2) (HTRF)
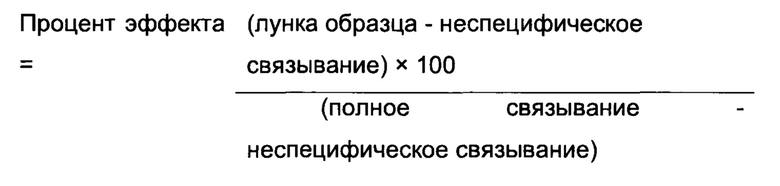
Неспецифическое связывание = значения для лунок, содержащих изотипический контроль мышиного IgG1
Полное связывание = значения для лунок, содержащих эталонное антитело
б) Первичный скрининг: связывание с рекомбинантным человеческим PD-L1
Параллельно со скринингом связывания с PD-L1, экспрессируемым CHO-S, супернатанты, собранные из лунок гибридомы, подвергали скринингу на способность секретируемых антител связываться с hPD-L1, экспрессируемым в виде рекомбинантного белка (собственного приготовления). Связывание секретируемых антител с рекомбинантным PD-L1 идентифицировали методом HTRF® (гомогенная флуоресценция с временным разрешением, Cisbio) в формате анализа с использованием биотинилированного hPD-L1. 10 мкл супернатанта гибридомы переносили в белый 384-луночный полистирольный планшет малого объема с несвязывающей поверхностью (Greiner). 5 мкл 230 нМ биотинилированного hPD-L1 his, разбавленного в буфере для анализа методом HTRF (PBS (Sigma) + 0,53 М KF (Sigma) + 0,1% мас./об. BSA (Sigma)), предварительно инкубировали с 10 мкл супернатанта гибридомы или 10 мкл эталонного антитела, разведенного до рабочей концентрации 3,3 нМ, в течение 1 часа при комнатной температуре. В лунки отрицательного контроля добавляли 10 мкл НММ. Стрептавидин D2 (Cisbio) и козьи антитела против мышиного IgG (Southern Biotech), меченые криптатом европия (Cisbio), были разбавлены 1/100 в буфере для анализа HTRF и 5 мкл этой смеси добавляли во все лунки. Планшет оставляли для инкубации в темноте в течение 2 часов до момента считывания флуоресценции с временным разрешением при длинах волн излучения 620 нм и 665 нм с помощью планшет-ридера EnVision (Perkin Elmer). Более подробную информацию о технологии HTRF® можно найти в работе Mathis (1995) Clinical Chemistry 41 (9), 1391-1397.
Данные анализировали путем вычисления отношения 665/620 и процента эффекта для каждого образца согласно уравнению 2 и уравнению 1, соответственно.
Уравнение 2: Расчет отношения 665/620
отношение 665/620 = (значение для образца 665/620 нм) × 10000
В общем, критерии выбора первично отобранных антител основывались на величине эффекта, большей или равной 10%. В некоторых случаях выбор первично отобранных антител основывался на величине эффекта, большей или равной 20%.
Переход ко вторичному скринингу основывался на комбинации данных для антител, первично отобранных по связыванию рекомбинантного PD-L1 и по связыванию с PD-L1 человека, экспрессируемым на клетках СНО.
c) Вторичный скрининг: Связывание с клеточно экспрессируемым рекомбинантным человеческим PD-L1 или нативно экспрессируемым hPD-L1 и аффинность связывания
Для определения того, имели ли лунки, выбранные с использованием критериев выбора первичного скрининга, требуемые характеристики, установленные авторами изобретения, был проведен ряд анализов. Клоны гибридомы, отобранные при первичном скрининге, культивировали в течение 3 дней, и супернатанты, собранные с клеток гибридомы, испытывали для оценки того, связываются ли секретируемые антитела, в некоторых случаях, с экспрессируемым CHO-S hPD-L1 или, в некоторых случаях, с клетками ES2. Кроме того, была также оценена способность нейтрализовать рекомбинантный hpD-1 Fc, связывание с hPD-L1 CHO-S или клетками ES2. Также тестировали связывание антител с PD-L1 человека методом SPR.
d) Связывание с клеточно экспрессируемым hPD-L1 и нейтрализация, и связывание hPD-L1 с PD-1
Было проведено тестирование связывания супернатантов гибридомы на способность связываться с клетками CHO-S, экспрессирующими hPD-L1, или с клетками ES2. Клетки CHO-S, экспрессирующие hPD-L1 (собственного приготовления) или клетки ES2 (АТСС CRL-1978), нативно экспрессирующие hPD-L1, разводили в буфере FACS и распределяли на 96-луночном планшете с V-образными лунками (Greiner) при плотности от 0,5 до 1×105 клеток на лунку. Клетки промывали 150 мкл PBS и центрифугировали при 300 g в течение 3 минут. Супернатант удаляли аспирацией и добавляли 150 мкл PBS. Эта стадия промывки повторялась.
К промытым клеткам добавляли 50 мкл супернатанта гибридомы или очищенного гибридомного материала, к которому добавляли 500 нг/мл Fc человеческого PD-1 (собственного приготовления, SEQ ID NO: 6). Эталонное антитело добавляли в среду в количестве 2 мкг/мл. При использовании очищенного материала, титрования готовили из максимальной концентрации 600 нМ перед добавлением к клеткам. При использовании супернатантов, к клеткам добавляли неразбавленный супернатант и три последовательных двукратных разведения. Клетки инкубировали при 4°С в течение 30 минут. Клетки дважды промывали 150 мкл буфера FACS, центрифугировали при 300 g в течение 3 минут после каждой стадии промывки и удаляли супернатант аспирацией.
Для детектирования связывания антител и рецепторов, к клеткам добавляли 50 мкл козьего анти-человеческого IgG-PE (Jackson ImmunoResearch) и АРС анти-мышиного IgG (Jackson ImmunoResearch), разбавленных 1/500 в буфере FACS. Клетки инкубировали в течение 30 минут при 4°С в темноте. Клетки промывали дважды, как описано выше, и ресуспендировали в буфере FACS для анализа. Интенсивность сигнала РЕ и АРС (среднее геометрическое) измеряли методом проточной цитометрии с использованием инструмента BD FACS Array. Графики данных построены как средние геометрические значения без дополнительных вычислений.
е) Определение аффинности методом поверхностного плазмонного резонанса
Анализ методом поверхностного плазмонного резонанса (SPR) без использования меток проводили на приборе SPR с матрицей ProteOn XPR36 (BioRad). Поверхность захвата антимышиного IgG была создана на чипе биосенсора GLC с использованием реакции аминного сочетания антимышиного IgG фирмы GE Healthcare. Тестируемые антитела захватывали на этой поверхности и человеческий PD-L1 (собственного приготовления) использовали в качестве аналита в концентрациях 256 нМ, 64 нМ, 16 нМ, 4 нМ и 1 нМ. Анализ проводили при 25°С с использованием HBS-EP (Teknova Н8022). В качестве эталона для сенсограмм связывания использовался один лишь буфер. Данные были проанализированы с использованием модели 1:1, встроенной в программу анализа данных ProteOn XPR36. В некоторых случаях в качестве источника антитела использовали супернатанты гибридомы; в других случаях антитело выделяли из супернатанта гибридомы до проведения анализа (см. ниже). В некоторых случаях использовали поверхность захвата белка A/G. Она была создана на чипе биосенсора GLM с использованием реакции аминного сочетания белка A/G фирмы Biorbyt.
f) Очистка антител от супернатантов гибридомы
Смолу с белком G в колонке с гравитационным потоком сначала промывали водой, затем 50 мМ гидроксидом натрия или IgG Elute (Pierce) и затем уравновешивали PBS для тканевых культур. Осветленный супернатант гибридомы, содержащий 10% об./об. 10× PBS для тканевых культур, несколько раз наносили на уравновешенную колонку с белком G. Смолу промывали PBS для тканевых культур, чтобы удалить несвязанный материал. Затем антитело элюировали IgG Elute (Pierce) и элюированную фракцию затем нейтрализовали TRIS с конечной концентрацией 100 мМ при рН 8,0. Элюированную фракцию затем концентрировали до объема менее 1,5 мл центрифугированием в центрифужном фильтрующем элементе с порогом отсечения 10 кДа. Затем добавляли PBS для тканевых культур и образец снова концентрировали до объема менее 1,5 мл. Концентрацию белка определяли количественно при OD280 с использованием молярного коэффициента экстинкции, заложенного в Nanodrop для IgG. Наконец, образец анализировали методом ДСН-ПААГ для оценки чистоты.
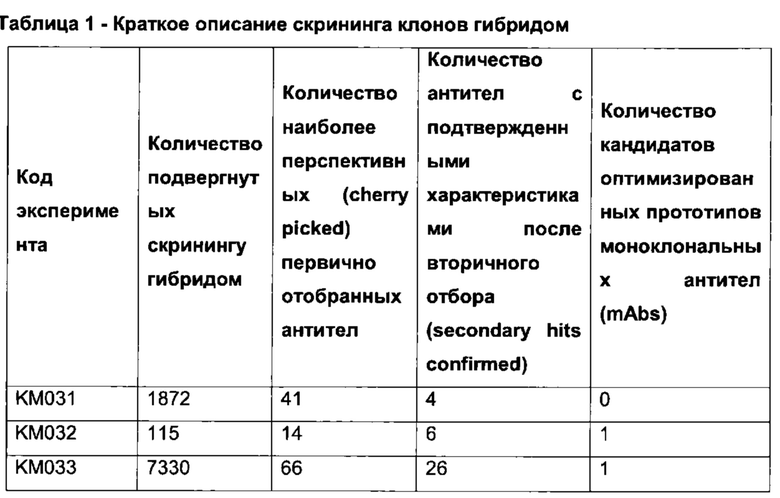
Пример 3 - Критерии включения в список предварительно отобранных антител
Связывание с hPD-L1, нативно экспрессируемым на клетках ES2, и нейтрализация связывания рекомбинантного PD-1 человека с клетками ES2 использовались в качестве критериев отбора при вторичном скрининге. Антитела, отбираемые для дальнейшей очистки и дополнительных анализов, определяли по сочетанию высокой аффинности к PD-L1 человека и нейтрализующей способности.
После отбора и определения характеристик выбранных антител их полностью человеческие вариабельные домены были выделены методом ОТ-ПЦР (RT-PCR) с использованием смеси прямого и обратного праймеров. Антитела переформатировали в остов IgG1 человека и экспрессировали с использованием системы транзиентной экспрессии в клетках CHO-S.
Материалы и методы
а) Выделение РНК из клеток гибридомы
Общую РНК экстрагировали из клеток гибридомы с использованием реагента TRIzol™ (Invitrogen). Количество и качество выделенной РНК анализировали спектрофотометрически.
b) Выделение вариабельного домена антитела методом ОТ-ПЦР
Выбранные клоны использовали для получения полной РНК, которую использовали в реакции ОТ-ПЦР для выделения V-областей тяжелой и легкой цепей. Для тяжелых цепей использовали мышиные IgG-специфические обратные праймеры и наборы специфических к лидерной последовательности человеческого Ig прямых праймеров. Для легких цепей каппа использовались обратные праймеры, специфические к мышиной константой области каппа и наборы прямых праймеров, специфических к лидерной последовательности человеческой каппа. Продукты ОТ-ПЦР разделяли электрофорезом на агарозном геле, причем ДНК предсказанного размера очищали на геле и секвенировали в прямом и обратном направлениях. Альтернативно, продукты ОТ-ПЦР субклонировали в клонирующий вектор и ДНК отдельных колоний, представленных для секвенирования.
Пример 4 - Выбор окончательной панели оптимизированных прототипов антител (final lead panel)
Рекомбинантно экспрессируемые антитела анализировали методом SPR для подтверждения связывания с PD-L1 яванского макака, а также с PD-L1 человека. Антитела также тестировали в реакции смешанной культуры лимфоцитов (MLR) дендритных клеток-Т-клеток на способность повышать продуцирование IFNγ (Фиг. 1). Антитела со стабильным иммуномодулирующим эффектом в MLR и со связыванием с PD-L1 человека и яванского макака были выбраны в качестве окончательной панели - они были обозначены как клон 84G09 и клон 1D05. Данные на Фигуре 1 относятся к одному эксперименту. Было проведено еще пять экспериментов, которые показали сходные результаты (84G09 продемонстрировал активность в 3 из 5 экспериментов, 1D05 продемонстрировал активность в 3 из 4 экспериментов, 1А01 продемонстрировал активность в 1 из 3 экспериментов, и 8В09 продемонстрировал активность в 0 из 3 экспериментов). Один из дополнительных экспериментов был неудачным (включая положительный контроль).
Материалы и методы
а) Использование поверхностного плазмонного резонанса для анализа антител с константной областью человека
Анализ методом поверхностного плазмонного резонанса (SPR) без использования меток проводили на приборе SPR с матрицей ProteOn XPR36 (BioRad). Поверхность захвата антитела против человеческого IgG была создана на чипе биосенсора GLC с использованием комбинации антител против Fc человека (Jackson Labs 09-005-008,109-006-008 и 309-006-008) путем реакции аминного сочетания. Тестируемые антитела захватывали на этой поверхности, и человеческий PD-L1-his и PD-L1-FLAG яванского макака (собственного приготовления, SEQ ID NO: 5) использовали в качестве аналита в концентрациях 128 нМ, 32 нМ, 8 нМ, 2 нМ, 0,5 нМ и 0 нМ. Данные были проанализированы с использованием модели 1:1, встроенной в программу анализа данных ProteOn XPR36.
b) Реакция смешанной культуры лимфоцитов (MLR) дендритных клеток - Т-клеток
Дендритные клетки были получены из моноцитарных предшественников. Моноцитарные предшественники были выделены из мононуклеарных клеток периферической крови (РВМС), выделенных с использованием центрифугирования в градиенте плотности Ficoll-Paque plus (GE Healthcare) из камер системы лейкофильтрации (лейкоредукция) (NHSBT). Моноциты были выделены из РВМС с использованием магнитных разделительных микросфер для отрицательной селекции (Miltenyi Biotec). Моноциты высеивали в 96-луночные плоскодонные планшеты для тканевых культур (ТС) в количестве 5×104/лунку и 1×104/лунку и культивировали с цитокинами GM-CSF и IL-4 (оба Peprotech) в концентрации 100 нг/мл в течение 7 дней в культуральных средах (Advanced RPMI (Gibco), дополненная 10% об./об. FBS и 2 нМ глутамином (культуральная среда).
Через 7 дней Т-клетки очищали от аллогенных РВМС с использованием магнитных разделительных микросфер для отрицательной селекции (Miltenyi). После очистки, буфер для выделения удаляли центрифугированием и аспирацией. Клетки ресуспендировали в количестве 1×106 клеток/мл в культуральной среде и 100 мкл Т-клеток добавляли во все лунки, за исключением лунок для одних дендритных клеток (DC). Еще 100 мкл культуральной среды добавляли в лунки для одних лишь дендритных клеток (DC) и одних лишь Т-клеток. Были приготовлены последовательные трехкратные разведения антител в культуральной среде (конечная верхняя концентрация 60 нМ). К клеткам добавляли по 10 мкл каждого разведения.
Клетки инкубировали в течение пяти дней при 37°С. После этого периода измеряли IFN-γ с помощью Duoset ELISA (R&D Systems) в соответствии с инструкциями производителя.
Пример 5 - Углубленная характеристика оптимизированных прототипов антитела
Оптимизированные прототипы антител 84G09 и 1D05 были подвергнуты углубленному анализу, включая SPR при 37°С, полные титрования антител в анализах нейтрализации и подтверждение связывания с PD-L1, но не с PD-L2. Антитела также экспрессировали с константной областью IgG4(PE) человека (SEQ ID NO: 199) для анализа реакцией смешанной культуры лимфоцитов. Оптимизированные прототипы антител сохраняют субнаномолярную аффинность при 37°С и демонстрируют сильную нейтрализацию связывания PD-L1 как с PD-1, так и с CD80. Антитела не реагируют перекрестно с PD-L2, связывают нативно экспрессируемые PD-L1 на дендритных клетках и являются мощными стимуляторами продуцирования IFNγ в MLR.
а) Анализ нейтрализации PD-L1/PD-1 человека (ИФА)
Fc PD-1 (собственного приготовления, SEQ ID NO: 6), разбавленный до 1 мкг/мл, адсорбировали на 96-луночных планшетах с низкой автофлуоресценцией и высоким связыванием белка (Costar) в течение ночи при 4°С. Избыточный белок удаляли промыванием PBS-Tween (0,1% об./об.), и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего планшеты промывали, как описано выше. Добавляли в 96-луночный несвязывающий планшет 30 мкл титрования (разведение 1/3) антитела, разведенного в буфере для анализа ИФА (PBS + 0,1% BSA). Добавляли в планшет 30 мкл биотинилированного PD-L1 his (собственного приготовления, SEQ ID NO: 3) при рабочей концентрации 50 нМ (конечная концентрация анализа [FAC] 25 нМ), за исключением контрольных лунок, куда добавляли 30 мкл буфера для анализа ИФА. Планшет инкубировали в течение 30 минут перед переносом 50 мкл на планшеты с нанесеным покрытием, планшеты с покрытием инкубировали в течение 1 часа при комнатной температуре. Избыток белка удаляли промыванием PBS-Tween (0,1% об./об.). Связывание PD-L1 детектировали с использованием меченого стрептавидином европия (streptavidin labelled Europium) (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный Tris физиологический раствор)-Tween (0,1% об./об.) и 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Процент специфического связывания рассчитывали с использованием Уравнения 3. Значения IC50 определяли с использованием прикладной программы GraphPad Prism путем аппроксимации кривой с использованием четырехпараметрического логистического уравнения (уравнение 4). Результаты приведены на Фигуре 2 и приведены в Таблице 2.
Уравнение 3: Процент связывания рецептора (ИФА)
На основе данных флуоресценции при 615 нм
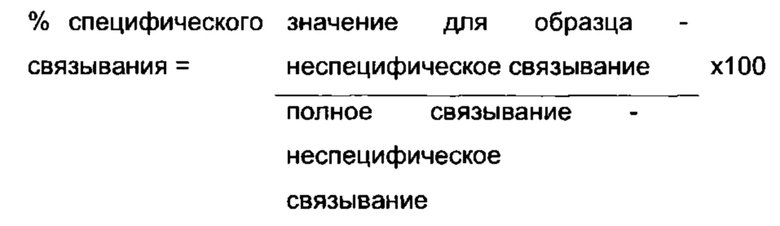
Полное связывание = биотинилированный PD-L1 (без антител)
Неспецифическое связывание = без биотинилированного PD-L1
Уравнение 4: Четырехпараметрический логистический расчет

X = логарифм концентрации.
Y = специфическое связывание (Уравнение 3)
Верхнее и нижнее значения = Значения на участках плато, выраженные в тех же единицах, что и Y (специфическое связывание)
Log IC50 выражено в тех же единицах, что и X. Y начинается с нижнего значения и возрастает до верхнего значения по кривой сигмоидной формы. Специфическое связывание уменьшается по мере увеличения X.
с) Анализ нейтрализации СНО человеческого PD-L1/PD-1 или CD80 (проточная цитометрия)
Клетки CHO-S, нетрансфицированные (обозначаемые как дикий тип (WT)) или трансфицированные hPD-L1, разводили буфером FACS и распределяли на 96-луночный планшет с V-образными лунками (Greiner) с плотностью 1×105 клеток на лунку в 50 мкл. Биотинилированный PD-1-Fc человека (экспрессированный, собственного приготовления, SEQ ID NO: 6) или CD80-Fc (R&D Systems) готовили путем титрования из конечной концентрации для анализа (FAC) 1 мкМ, серийными разбавлениями 1/2 в буфере FACS. Титры антител готовили из рабочей концентрации 300 нМ, FAC 150 нМ, в виде серии разбавлений 1/3 в буфере FACS. Биотинилированный PD-1 или CD80 разбавляли в буфере FACS до рабочей концентрации 60 нМ, FAC 30 нМ. Планшеты центрифугировали при 300×g в течение 3 минут до аспирации супернатанта. Прибавляли к клеткам 25 мкл лиганда и 25 мкл раствора антитела (или 50 мкл титра лиганда) и инкубировали при 4°С в течение 1 часа. Клетки промывали 150 мкл PBS и центрифугировали при 300 g в течение 3 минут. Супернатант удаляли аспирацией и добавляли 150 мкл PBS. Эта стадия промывки повторялась. Присутствие связанного CD80 или PD-1 детектировали добавлением 50 мкл комплекса стрептавидин-AlexaFluor 647 (Jackson ImmunoResearch), разбавленного 1/500 в буфере FACS. Клетки инкубировали 30 минут при 4°С в темноте. Клетки промывали, как описано выше. Для фиксации клеток добавляли 100 мкл 2% об./об. параформальдегида и клетки инкубировали в течение 30 минут при 4°С, осадок клеток собирали центрифугированием при 300×g и планшеты ресуспендировали в 100 мкл буфера FACS. Уровень сигнала AlexaFluor 647 (среднее геометрическое) измеряли методом проточной цитометрии с использованием прибора BD FACS Array. Результаты показаны на Фиг. 3 и 4 и приведены в Таблице 2.
Уравнение 5: Процент связывания рецептора (проточная цитометрия)
На основе геометрического среднего флуоресценции
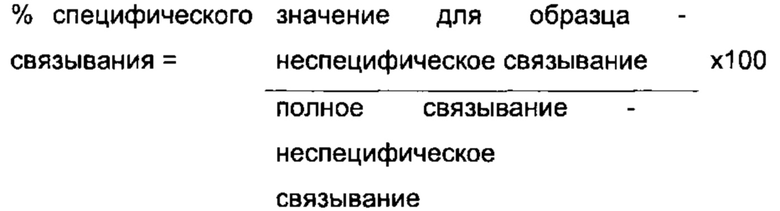
Полное связывание = только биотинилированный PD-1 или CD80 (без антител)
Неспецифическое связывание = только стрептавидин AlexaFluor 647, без лиганда
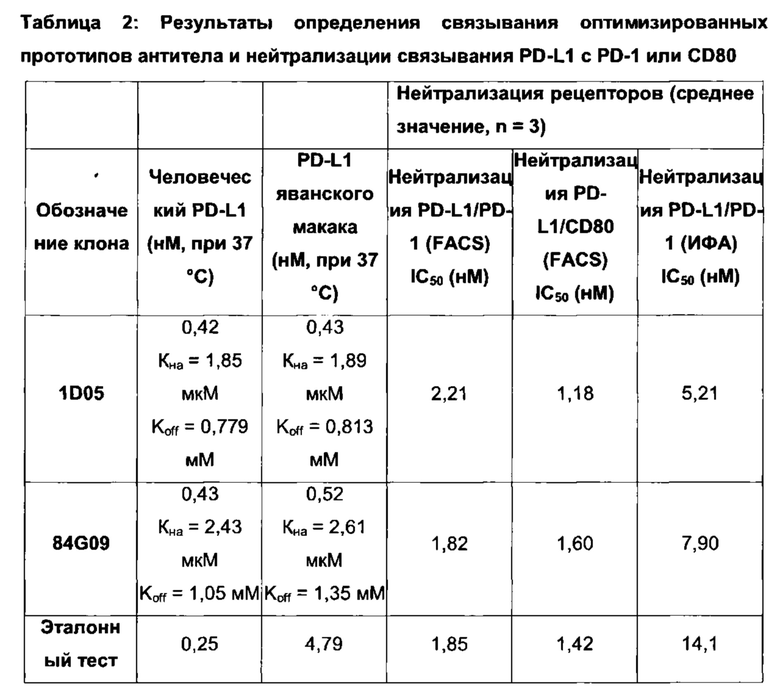
d) Связывание PD-L1/PD-L2
PD-L1-Fc (R&D Systems) и PD-L2-Fc (R&D Systems) разбавляли до 2 мкг/мл и отдельно адсорбировали на 96-луночных планшетах с высоким связыванием белка (Greiner) в течение ночи при 4°С, 50 мкл/лунку. Избыток белка удаляли промыванием PBS-Tween (0,1% об./об.), и лунки блокировали 250 мл/лунку буфера Pierce Protein Free Blocking Buffer (Thermo, 37572) в течение 1 часа, после чего планшеты промывали, как описано выше. Биотинилированные антитела против PD-L1 (собственного приготовления) или контрольные анти-PD-L2 антитела (R&D Systems) разбавляли в блокирующем буфере, проводя серийное трехкратное разведение, начиная с 10 мкг/мл. 100 мкл каждого разведения антител добавляли на планшеты в двух параллельных экспериментах и инкубировали в течение 1 часа при комнатной температуре перед промыванием, как указано выше. Связывание антител детектировали с использованием стрептавидина, меченого европием (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный Tris физиологический раствор)-Tween (0,1% об./об.) и 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Результаты представлены на Фигуре 5.
е) Анализ SPR
Анализ методом поверхностного плазмонного резонанса (SPR) без использования метки проводили, как описано в Примере 4, за исключением того, что анализ проводили при 37°С. Кроме того, из-за артефактов, возникающих при проведении анализа при 37°С, было установлено, что наилучшие условия сравнения сенсограмм связывания обеспечиваются при использовании сенсограмм антитела отрицательного контроля с использованием тех же концентраций человеческого PD-L1. Результаты приведены в Таблице 2.
f) Реакция смешанных лимфоцитов
Искусственно размноженные CD4+ Т-клетки оттаивали и переводили в состояние покоя в среде AIM V© (Gibco) при 37°С, 5% CO2, в течение ночи перед днем анализа. Серийные разведения античеловеческих mAb PD-L1 были приготовлены в среде AIM с конечной концентрацией 4×. 50 мкл разбавленных mAb добавляли в 96-луночные планшеты с U-образным дном. 1×104 незрелых дендритных клеток (iDC) в 50 мкл среды AIM и 1×105 искусственно размноженных CD4+ Т-клеток (искусственно размноженных с использованием активатора Dynabeads Human T-Activator CD3/CD28 фирмы Life Technologies (Invitrogen/Applied Biosystems; № кат. 11131D) в соответствии с инструкциями производителя) в 100 мкл среды AIM добавляли к разведениям антител в каждой лунке. Контрольные лунки включали: только CD4+ Т-клетки, только iDC, CD4+ Т-клетки и iDC с IgG-изотиповыми контрольными антителами или без них в 200 мкл среды AIM. Реакционные планшеты инкубировали в течение 5 дней в увлажненном инкубаторе (37°С в 5% СО2). В конце анализа планшет центрифугировали (528×g в течение 3 минут) и 100 мкл супернатанта собирали из лунок путем осторожного пипетирования. Супернатанты анализировали с использованием набора для ИФА человеческого IFNγ Quantikine ELISA (R&D Systems) в соответствии с инструкциями производителя. Результаты приведены на Фигуре 6.
g) Секвенирование и характеристика использования генных сегментов 1D05 и 84G09
Секвенирование антител проводилось фирмой Source Bioscience, гены V сопоставлялись с последовательностями зародышевой линии.
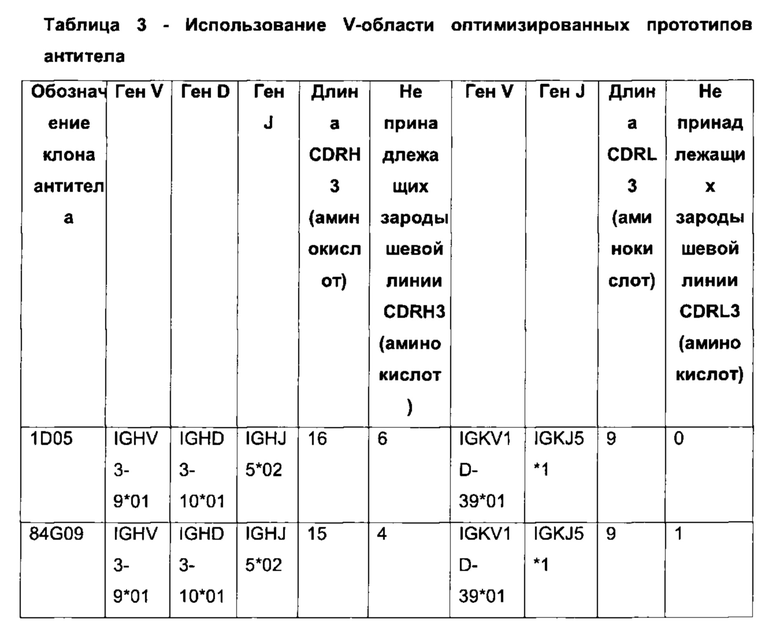
h) Связывание оптимизированных прототипов антитела с нативно экспрессируемым PD-L1
84G09 и 1D05 были помечены AlexaFluor647 и использованы для окрашивания дендритных клеток, полученных из моноцитарных предшественников. Это показывает, что оптимизированные прототипы антител связывают PD-L1, который нативно экспрессируется на человеческих дендритных клетках. Данные показаны на Фигуре 7.
Материалы и методы
МКПК суспендировали в среде RPMI 1640 без добавок и оставляли для прилипания к колбе для тканевых культур в течение двух часов при 37°С. Неадгезивные клетки удаляли и колбу промывали три раза PBS. PBS удаляли и заменяли на RPMI 10% hiFBS (Gibco), содержащим 100 нг/мл GM-CSF и IL-4 (оба Peprotech). Клетки культивировали при 37°С в течение 7 дней, а затем удаляли из колбы с использованием скребка для клеток.
Клетки ресуспендировали в буфере FACS (PBS, 1% мас./об. BSA, 0,1% мас./об. азида натрия) и высевали при 105 клеток/лунку и инкубировали с Trustain FcX (Biolegend) в течение 10 мин для предотвращения связывания антитела с FcγR. Добавляли меченые AlexaFluor647 антитела при конечной концентрации 5 мкг/мл и инкубировали при 4°С в течение 1 часа. Клетки затем промывали три раза в буфере FACS и фиксировали в течение 20 минут в 4% параформальдегиде (Affymetrix). После фиксации клетки промывали три раза, как указано выше, и ресуспендировали в буфере FACS для анализа методом проточной цитометрии. Данные получали с использованием проточного цитометра MACSQuant (Miltenyi Biotec) и проанализированы в FlowJo v10.
Пример 6 - Получение антигена, процедуры иммунизации и сортировка антигенспецифических В-клеток и выделение V-области
Дополнительные моноклональные антитела против PD-L1 человека были получены с использованием ранее описанной системы KyMouse™. Генетически модифицированных мышей HK иммунизировали растворимым рекомбинантным PD-L1 человека и мыши или поверхностно экспрессируемым PD-L1 человека и мыши, представляемым на клетках эмбриональных фибробластов мыши (MEF). Титры сыворотки определяли методом обратного ИФА, и для проведения анализов были выбраны мыши с самыми высокими титрами. В конце каждого эксперимента извлекали селезенку и лимфатические узлы. Из тканей готовили суспензию отдельных клеток и окрашивали для сортировки антигенспецифических В-клеток методом FACS.
Материалы и методы
а) Иммунизация мышей
Мышей иммунизировали растворимым рекомбинантным человеческим PD-L1 или комбинацией человеческого и мышиного белков PD-L1 (собственного приготовления) в соответствии со схемой, описанной в Примере 1 для KM032 (далее KM121). Мышей также иммунизировали человеческим PD-L1-белком и клетками MEF, экспрессирующими PD-L1 человека или мыши, согласно схеме, описанной в Примере 1 для KM033 (далее KM122). MEF-клетки, экспрессирующие PD-L1 мыши, были получены в соответствии с Примером 1, но с заменой мышиных последовательностей PD-L1 на человеческие последовательности PD-L1 и с заменой анти-мышиного детектирующего антитела PD-L1 (eBioscience) на анти-человеческое детектирующее антитело PD-L1.
b) Определение титра сыворотки по протоколу обратного ИФА PD-L1
Титры в образцах сыворотки мыши определяли с использованием
протокола обратного ИФА PD-L1 в соответствии с Примером 1 со следующими изменениями. hPD-L1 собственного приготовления самостоятельно метили с использованием набора Lightning Link (Innova Biosciences), и использовали в концентрации 1 мкг/мл в разбавителе для реагентов; 50 мкл/лунку). Связанный hPD-L1 детектировали путем добавления комплекса стрептавидин-европий (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). После инкубации в течение 1 часа при комнатной температуре в темноте планшеты промывали с использованием TBS (забуференный трис солевой раствор)-Tween (0,1% об./об.) и 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Графики данных флуоресценции строили по подсчитанным импульсам европия.
c) Сортировка антигенспецифических В-клеток и выделение областей V
Используемые методы были по существу такими же, как описано в Примере 1 заявки РСТ WO 2015/040401, которая включена в данный документ посредством ссылки. Вкратце, спленоциты и клетки лимфатических узлов, выделенные в экспериментах по иммунизации KM121 и KM122, окрашивали коктейлем антител, содержащим маркеры для селекции представляющих интерес клеток (CD19), в то время как нежелательные клетки были исключены из конечной отсортированной популяции (IgM, IgD, 7AAD). CD19+ В-клетки дополнительно метили человеческим PD-L1 (SEQ ID NO: 1) и мышиным PD-L1 (SEQ ID NO: 325, самостоятельно меченые AlexaFluor647 и AlexaFluor488, соответственно, с использованием наборов Lightning Link) для детектирования В-клеток, продуцирующих специфические антитела - клеток, связывающих PD-L1 человека или PD-L1 как человека, так и мыши. Эти клетки сортировали по одной методом FACS в буфере для лизиса. Последовательности V-области были выделены с использованием ОТ-ПЦР и двух дополнительных циклов ПЦР, затем были присоединены мостиковыми связями к константной области IgG1 мыши и экспрессированы в клетках HEK293. Супернатанты клеток HEK293 подвергали скринингу на присутствие PD-L1-связывающих антител. Этот метод далее упоминается как ВСТ.
Пример 7. Скрининг супернатанта
Супернатанты ВСТ подвергали скринингу методом HTRF, и первично отобранные антитела подвергали дополнительному скринингу на связывание с клеточно экспрессируемым рекомбинантным hPD-L1 и нейтрализацию связывания PD-1, и на аффинность связывания с рекомбинантным белком PD-L1 человека, яванского макака и мыши методом SPR, как описано в этом Примере. Антитела KM121 с аффинностью 1 нМ или выше к PD-L1 человека, а в некоторых случаях -также яванского макака, были отобраны для дополнительного анализа. Для KM122 были отобраны антитела, обладающие способностью нейтрализовать связывание PD-1 с экспрессируемым клеткой PD-L1, вместе с высокой аффинностью связывания (<1 нМ) к PD-L1 человека и яванского макака. Антитела не связывались с мышиным PD-L1.
а) Первичный скрининг. Связывание с рекомбинантным человеческим PD-L1 (супернатанты ВСТ)
Супернатанты, собранные в экспериментах с экспрессией ВСТ, подвергали скринингу на способность секретируемых антител связываться с hPD-L1, экспрессируемыми в виде рекомбинантного белка (собственного приготовления). Связывание секретируемых антител с рекомбинантным PD-L1 человека и мыши идентифицировали методом HTRF® (гомогенная флуоресценция с временным разрешением, Cisbio) с использованием PD-L1, меченых FluoProbes® 647Н (Innova Biosciences) (обозначаемых в данном документе как 647 hPD-L1 или 647 mPD-L1 для меченых FluoProbes® 647Н человеческого PD-L1 и мышиного PD-L1, соответственно). 5 мкл супернатанта ВСТ переносили на белый 384-луночный полистирольный планшет с лунками малого объема и несвязывающей поверхностью (Greiner). Во все лунки добавляли 5 мкл 25 нМ 647 hPD-L1 или 647 mPD-L1, разбавленных в буфере для анализа HTRF. Эталонное антитело разбавляли в среде ВСТ (Gibco #А14351-01) до 40 нМ и добавляли по 5 мкл на планшет. Для лунок отрицательного контроля добавляли 5 мкл мышиного IgG1 (Sigma М9269, в некоторых случаях называемого СМ7), разбавленного до 40 нМ в среде ВСТ. Связывание секретируемых антител к PD-L1 детектировали добавлением 10 мкл козьего антимышиного IgG (Southern Biotech), непосредственно меченого криптатом европия (Cisbio), разбавленным 1/2000 в буфере для анализа HTRF. Планшет оставляли для инкубации в темноте в течение 2 часов до момента считывания флуоресценции с временным разрешением при длинах волн излучения 620 нм и 665 нм с помощью планшет-ридера EnVision (Perkin Elmer).
Данные анализировали путем вычисления отношения 665/620 и процента эффекта для каждого образца согласно уравнению 2 и уравнению 1, соответственно.
Для KM121 первично отобранные антитела выбирали на основе эффекта, равного или превышающего 30 процентов, тогда как для KM122 первично отобранные антитела выбирали на основе эффекта, равного или превышающего 40 процентов.
Переход ко вторичному скринингу была основан на данных связывания рекомбинантного PD-L1.
b) Вторичный скрининг - связывание с экспрессируемым клеткой hPD-L1 и нейтрализация связывания hPD-L1 с PD-1 (супернатанты ВСТ)
Связывание супернатантов ВСТ определяли путем тестирования на способность связываться с клетками CHO-S, экспрессирующими hPD-L1. Клетки CHO-S, экспрессирующие hPD-L1 (собственного приготовления), разводили в буфере FACS (PBS, 1% BSA, 0,1% азида натрия) и распределяли на 96-луночном планшете с V-образными лунками (Greiner) с плотностью 0,5-1×105 клеток на лунку. Клетки промывали 150 мкл PBS и центрифугировали при 300 g в течение 3 минут. Супернатант удаляли аспирацией и добавляли 150 мкл PBS. Эта стадия промывки повторялась.
К промытым клеткам добавляли 25 мкл неразведенного супернатанта ВСТ, эталонного антитела или контрольного антитела, разбавленного до 300 нМ в среде ВСТ. Добавляли 25 мкл 30 нМ биотинилированного PD-1 человека (собственного приготовления) и клетки инкубировали при 4°С в течение 60 минут. Добавляли 150 мкл буфера FACS и клетки промывали, как описано выше. Для детектирования связывания биотинилированных PD-1 и антител против PD-L1, стрептавидин-647 (стрептавидин-647, Jackson ImmunoResearch) и анти-мышиный РЕ (Jackson ImmunoResearch) разводили все 1/500 в буфере FACS и добавляли к клеткам 50 мкл этой смеси. Клетки инкубировали 4°С в течение 60 минут. Клетки дважды промывали 150 мкл буфера FACS, центрифугировали при 300 g в течение 3 минут после каждой стадии промывки и удаляли супернатант аспирацией. Клетки фиксировали добавлением 50 мкл 4% параформальдегида в течение ночи. Клетки промывали один раз, как описано выше, и ресуспендировали в буфере FACS для анализа. Интенсивность сигналов РЕ и АРС (среднее геометрическое) измеряли методом проточной цитометрии с использованием прибора BD FACS Array. Графики данных построены как средние геометрические значения без дополнительных вычислений.
Для KM121 антитела вторичного отбора выбирали на основе связывания с высокой аффинностью (<1 нМ) с человеческим PD-L1. Для KM122 антитела вторичного отбора выбирали на основе сопоставимой высокой аффинности связывания (<1 нМ) с PD-L1 человека и яванского макака и способности нейтрализовать связывание PD-1 с экспрессируемым клетками PD-L1. Результаты приведены в Таблице 4.
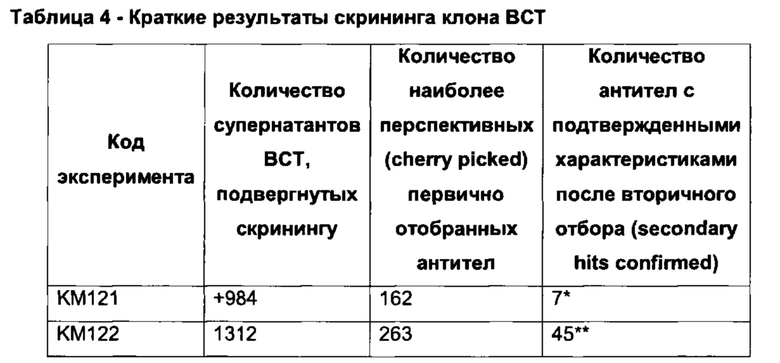
* три из этих антител вторичного отбора не проходили первичный скрининг и были подвергнуты скринингу только методами SPR и нейтрализации
** одно из первично отобранных антител было идентифицировано с помощью первичного скрининга, но количество материала было недостаточным для вторичного скрининга. Было показано, что после повторной экспрессии клон связывает PD-L1 человека и яванского макака с аффинностью <1 нМ, и его исследования были продолжены.
с) Анализ связывания методом поверхностного плазмонного резонанса
Анализ SPR проводили с помощью системы ProteOn XPR36 Array. Антимышиный IgG (GE Healthcare BR-1008-38) иммобилизовали на чипе GLM путем сочетания с первичным амином. Антитела захватывали непосредственно из супернатантов ВСТ. PD-L1 человека, мыши и яванского макака использовали в качестве аналитов и пропускали над захваченными антителами в одной концентрации. Устанавливают нулевое значение сенсограмм связывания по двум холостым образцам с 0 нМ (т.е. только буфер), и данные анализируют с использованием модели 1:1, встроенной в программы для анализа ProteOn. Анализ проводят при 25°С и используют HBS-EP в качестве подвижного буфера.
Пример 8 - Характеристика выбранных антител
Первично отобранные антитела повторно экспрессировали с константной областью IgG1 человека и отправляли для секвенирования в Source Bioscience. Использование V-области приведено в таблице 5. Попадания затем анализировали методом ИФА для определения их способности нейтрализовать взаимодействия PD-L1/PD-1 и взаимодействия PD-L1/CD80. Все семь первично отобранных антител KM121 нейтрализовали взаимодействия PD-L1/CD80; однако, четыре антитела не нейтрализовали PD-L1/PD-1. Четыре из пяти первично отобранных антител KM122 нейтрализуют как PD-L1/PD-1, так и PD-L1/CD80. Результаты показаны на Фиг. 8 и 9. Антитела, продемонстрировавшие нейтрализацию взаимодействий как PD-1, так и CD80 с PD-L1, дополнительно подвергали скринингу на их способность повышать ИФНγ в аутологичном анализе совместного культивирования с использованием моноцитов и Т-клеток.
Материалы и методы
а) ИФА нейтрализации PD-L1/PD-1 и PD-L1/CD80
CD80 (R&D Systems) или PD-1 (собственного приготовления), разбавленный до 2,5 мкг/мл, адсорбировали на 96-луночных планшетах с низкой аутофлуоресценцией и высоким связыванием белка (Costar) в течение ночи при 4°С. Избыточный белок удаляли промыванием PBS-Tween (0,1% об./об.), и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего планшеты промывали PBS-Tween, как описано выше. К 96-луночному планшету без связывания добавляли 60 мкл титрованного (трехкратное серийное разведение) антитела, растворенного в буфере для анализа ИФА (PBS + 0,1% BSA). К планшету добавляли 60 мкл меченного биотином PD-L1 с рабочей концентрацией 16 нМ (8 нМ FAC), за исключением контрольных лунок, в которые добавляли 60 мкл аналитического буфера для ИФА. Планшет инкубировали в течение 30 минут перед переносом 50 мкл на планшеты с нанесенным покрытием, планшеты с покрытием инкубировали в течение 1 часа при комнатной температуре. Избыток белка удаляли промыванием PBS-Tween (0,1% об./об.). Связывание PD-L1 детектировали с использованием меченого стрептавидином европия (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный трисом физиологический раствор)-Твин (0,1% об./об.) и добавляли к планшету 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Процент специфического связывания рассчитывали по Уравнению 3. Значения IC50 определяли с использованием прикладной программы GraphPad Prism путем аппроксимации кривой с использованием четырехпараметрического логистического уравнения (уравнение 4). Результаты приведены в Таблице 4а ниже. Значения для антител KM121 являются средним для трех независимых экспериментов. Значения для KM122 получены из одного эксперимента. Н.д. (ND) указывает, что значение IC50 не было определено, так как полная кривая не может быть сгенерирована.
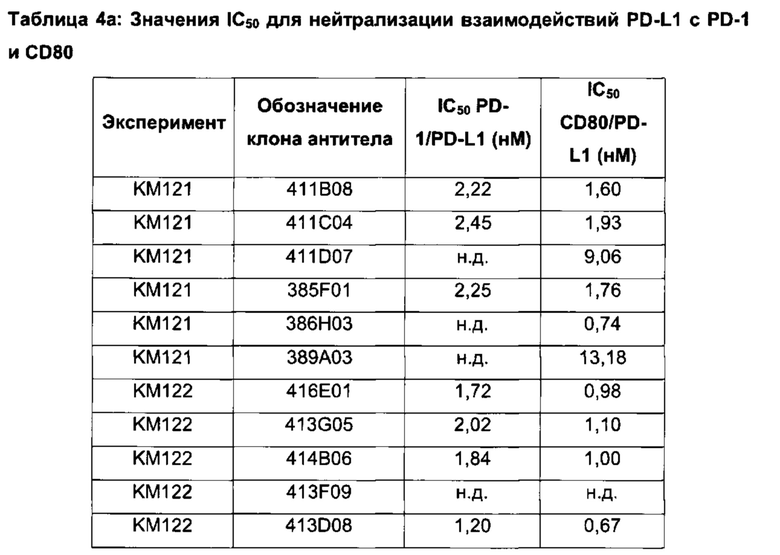
Выбранные оптимизированные прототипы антител, активные в анализе совместного культивирования моноцитов и Т-клеток (см. Пример 9), анализировали методом SPR при 25 и 37°С. Оптимизированные прототипы антител сохраняли субнаномолярную аффинность связывания с PD-L1 даже при 37°С. Антитела не связывали мышиный PD-L1. Результаты приведены в Таблице 4b.
Материалы и методы
Анализ SPR проводили согласно примеру 4 со следующими поправками: анализ проводили при 37°С, а также при 25°С для повышения жесткости анализа. PD-L1 человека, яванского макака и мыши (с his-меткой) были приготовлены самостоятельно (SEQ ID Nos 3, 5 и 326, соответственно).
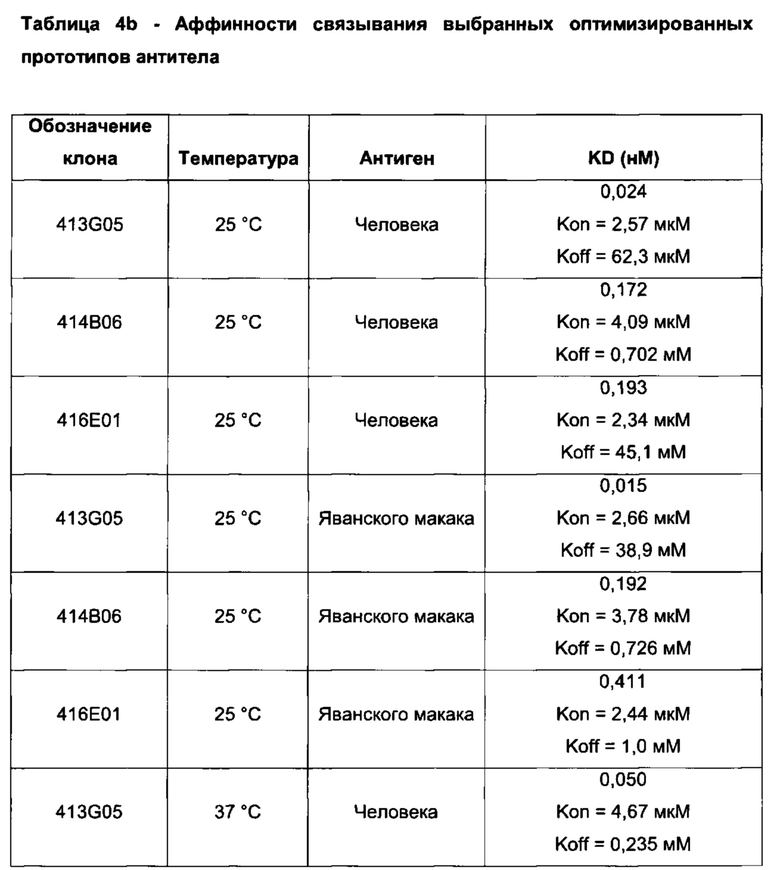

Пример 9 - Тестирование анти-PD-L1 оптимизированных прототипов антитела в аутологичном анализе совместной культуры
Эффекты анти-PD-L1 антител на продуцирование ИФНγ анализировали в совместной культуре очищенных моноцитов периферической крови и CD45RO+ Т-клеток памяти того же донора. Вкратце, моноциты выделяли путем отрицательного отбора с использованием бусин для магнитной сепарации (Miltenyi Biotec). CD45RO+ Т-клетки выделяют посредством первого раунда отрицательной селекции CD3+ Т-клеток и одного раунда положительной селекции CD45RO+ клеток (Miltenyi Biotec). Подмножества клеток совместно культивируют в соотношении 1:1 в RPMI 10% hiFBS в присутствии анти-CD3 (UCHT1, eBioscience), используемого для обеспечения стимуляции TCR, и исследуемых антител. Супернатанты отбирают через 4 дня для анализа IFNγ с помощью MSD (Meso Scale Discovery).
Эксперименты проводили, как описано, за исключением того, что продуцирование IFNγ, измеряли с помощью ИФА Human IFNγ Duoset® (R&D Systems™), при использовании для детектирования Eu-N1 стрептавидин (Delfia®).
Строили график зависимости отклика для стандарта IFNγ (пг/мл) от относительной флуоресценции при 615 нм. Концентрацию IFNγ определяли интерполяцией по калибровочной кривой в пг/мл с использованием 4-параметрической логистической аппроксимации, согласно Уравнению 4. Антитело-индуцированный IFNγ представлен в виде кратности индуцирования по сравнению с сигналом анализа лунок, показывающим уровни фонового уровня ответа, согласно Уравнению 6. Каждый график представляет собой зависимость средней кратности индуцирования для отдельных доноров, с представленными как минимум двумя различными донорами, от концентрации антител Log (М). Результаты показаны на Фиг. 22 и 37.
Уравнение 6
Кратность индукцирования = результат определения отклика при анализе (пг/мл) / фоновый отклик (пг/мл)
Фоновый отклик IFNγ = концентрация IFNγ (пг/мл) из лунок, содержащих совместную культуру моноциты-Т-клетки с анти-CD3-стимуляцией, без антитела.
Все пять антител в формате человеческого IgG1 индуцировали специфическое дозозависимое увеличение продуцирования IFNγ Т-клетками после 4-х дней совместного культивирования с аутологичными моноцитами и анти-CD3 (см. Фигуры 22а и 22b). Два антитела, которые индуцировали наибольшее увеличение продуцирования цитокинов, 413G05 и 414В06, были выбраны для повторного анализа методом SPR (см. Пример 8). Антитело 416Е01 в формате человеческого IgG4(PE) (SEQ ID NO: 199) также индуцировало специфическое дозозависимое увеличение продуцирования IFNγ в анализе совместной культуры. Это антитело также было отобрано для повторного анализа методом SPR.
Три отобранных антитела также анализировали вместе с двумя оптимизированными прототипами антител, отобранными в Примере 4 (1D05 и 84G09), и коммерческим активируемым эффектором антителом сравнения. Антитела имели формат человеческого IgG1. Все антитела индуцировали дозозависимое продуцирование IFNγ в этом анализе (Фиг. 37 и Таблица 22).
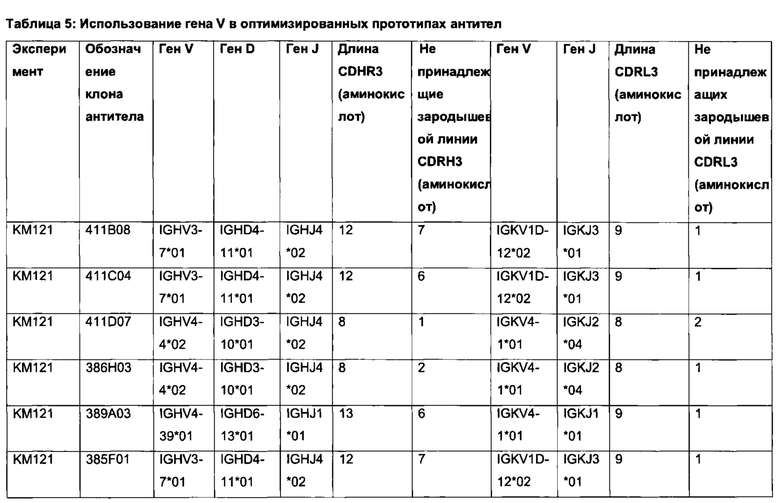
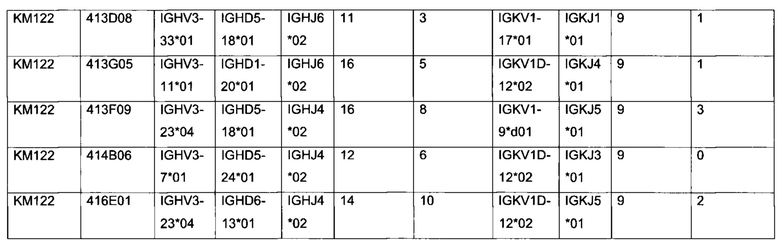
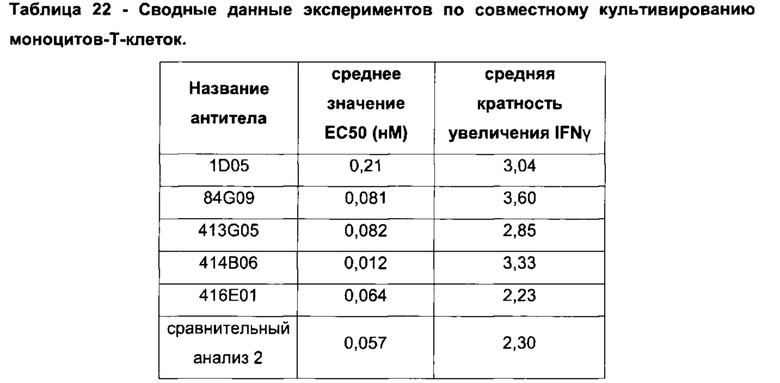
Пример 10 - Биспецифические молекулы FIT-Ig, нацеленные на PD-L1 и TIGIT
Биспецифические конструкты FIT-Ig были сконструированы по существу как описано в Примере 1 международной заявки WO 2015/103072 (на имя EpiMab Biotherapeutics, включена в данный документ посредством ссылки).
Биспецифические конструкты, имеющие структуру FIT-Ig, как представлено на Фиг. 1 WO 2015/103072, экспрессировали в клетках СНО при соотношении векторов: ДНК конструкта 1: 50%, ДНК конструкта 2: 25%, ДНК конструкта 3 25% от общей ДНК при транзиентной трансфекции. Биспецифические молекулы очищали стандартными методами хроматографии с белком А и эксклюзионной хроматографии. В этом отношении Конструкт 1 представляет собой полипептидную цепь, состоящую из VLA-CL-VHB-CH1-CH2-CH3, на Фигуре 1 WO 2015/103072. Конструкт 2 представляет собой полипептидную цепь, состоящую из VHA-CH1, на Фигуре 1 WO 2015/103072, и Конструкт 3 представляет собой полипептидную цепь, состоящую из VLB-CL, на Фигуре 1 WO 2015/103072.
Анализ методом SPR использовали для определения аффинности различных плеч биспецифического антитела, а исходные моноспецифические антитела использовались для определения того, происходило ли изменение аффинности в биспецифической молекуле. Последовательное связывание антигенов использовалось для проверки того, способны ли биспецифические конструкты связываться на обоих плечах биспецифического антитела.

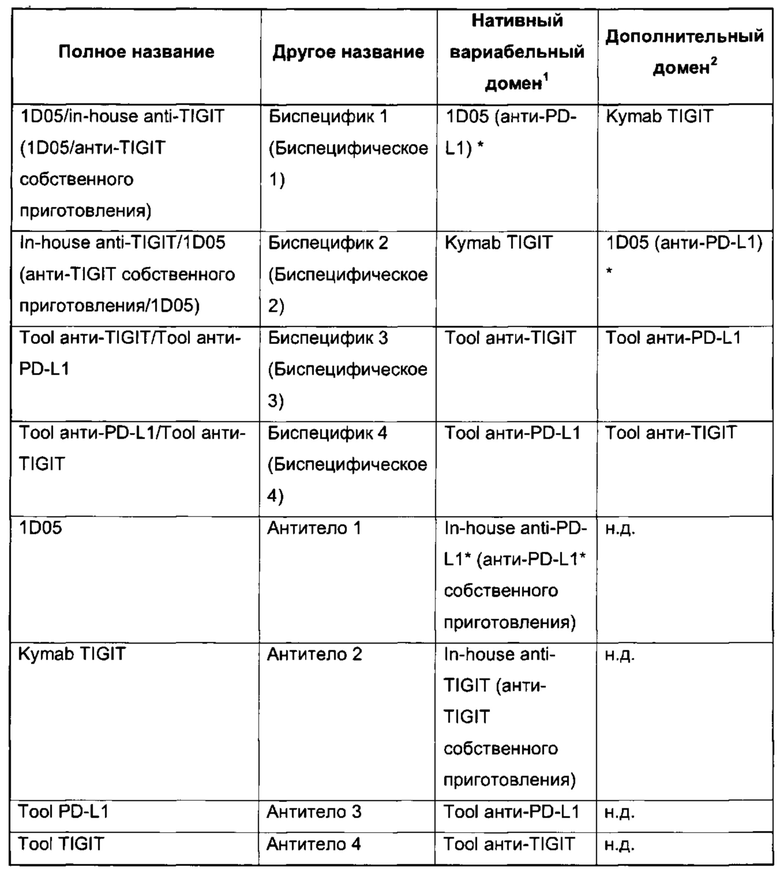
* 1D05 имеет последовательность VH SEQ ID NO: 33 и последовательность VL SEQ ID NO: 43 и константную область тяжелой цепи SEQ ID NO: 205
1 «Нативный вариабельный домен» соответствует сайту связывания антигена, образованному VHB и VLB на Фигуре 1 WO 2015/103072
2 «Дополнительный домен» соответствует сайту связывания антигена, образованному VHA и VLA на Фигуре 1 WO 2015/103072
а) Кинетический анализ
Поверхность захвата антитела против IgG человека была создана с использованием смеси 3 антител против человеческого Fc (Jackson Labs 109-005-008, 109-006-008 и 309-006-008), иммобилизованных на чипе GLC с использованием реакции сочетания с первичным амином. Контрольные моноспецифические антитела или конструкты биспецифических антител захватывали на этой поверхности, а человеческий PD-L1 или TIGIT использовали в качестве аналита в концентрациях 512 нМ, 128 нМ, 32 нМ, 8 нМ и 2 нМ, причем 0 нМ (т.е. только буфер) использовали в качестве двойного эталона на сенсограммах связывания. Анализ проводили при 25°С, используя HBS-EP в качестве подвижного буфера. Сенсограммы аппроксимировали моделью 1:1, включенной в программу анализа данных ProteOn.
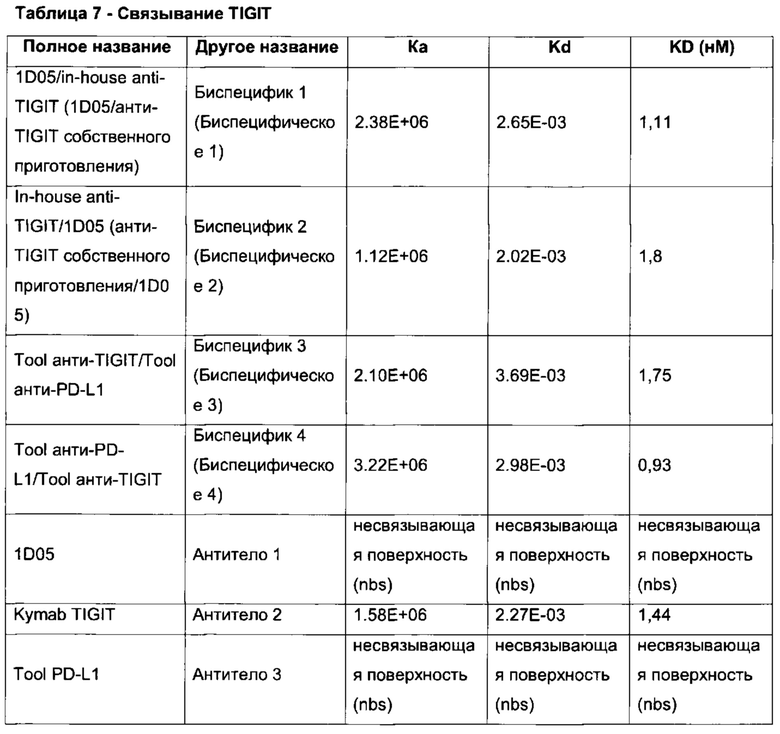
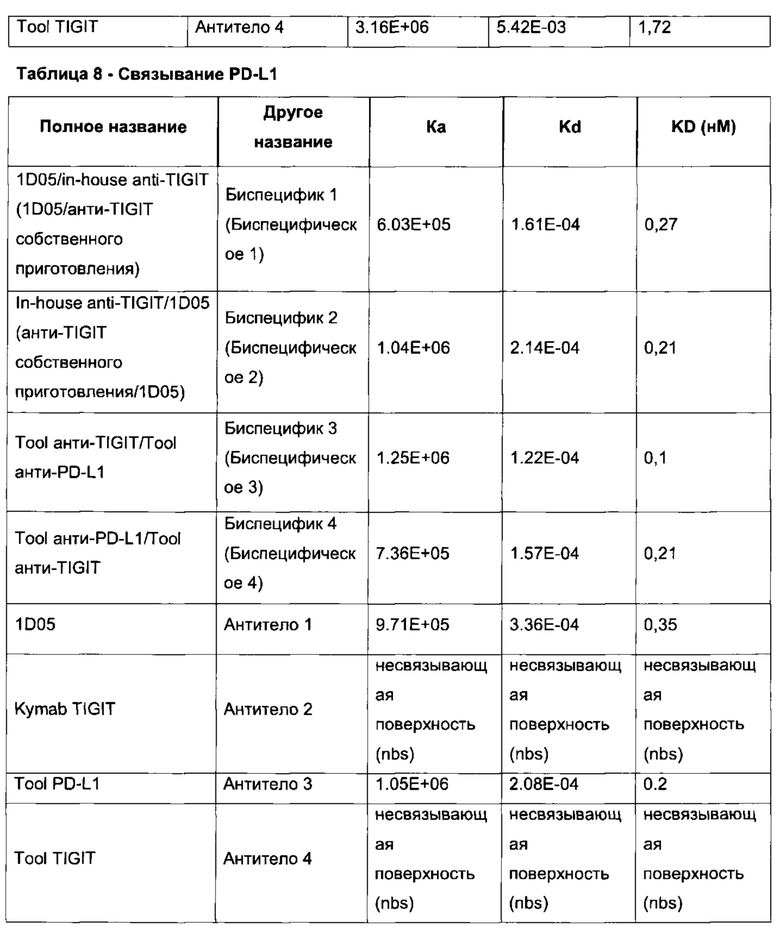
b) Биспецифическое связывание
Используя эту же поверхность захвата против IgG человека, созданную для кинетического анализа, захватывали на этой поверхности конструкты биспецифических антител, а рекомбинантный PD-L1 или TIGIT использовали в качестве аналита в концентрациях 512 нМ, 128 нМ, 32 нМ, 8 нМ и 2 нМ, причем 0 нМ (т.е. только буфер) использовали как двойной эталон на сенсограммах связывания. Анализ проводили путем впрыскивания PD-L1, а затем TIGIT, без регенерации между впрыскиваниями аналита, а также TIGIT, а затем PD-L1. Сенсограммы для 512 нМ, определенные по двум образцам (double referenced), показаны на Фиг. 10 и 11.
c) Характеристика молекул биспецифических FIT-Iq, связывающихся с PD-L1 и TIGIT, с помощью AlphaScreen®
Анализ связывания AlphaScreen® был разработан для оценки биспецифического связывания молекул FIT-Ig PD-L1/TIGIT. Анализ проводили с использованием биотинилированного His-PD-L1 (SEQ ID NO: 3) и His-FLAG-TIGIT (SEQ ID NO: 539), детектируемых, соответственно, с помощью донорных шариков со стрептавидином и анти-FLAG-акцепторных шариков (оба Perkin Elmer, 6760613). Человеческий IgG1 (Sigma 15154) и исходные моноспецифические антитела отдельно или в комбинации использовали в качестве отрицательных контролей, а анти-His антитело (Qiagen 34660) использовали в качестве положительного контроля.
Было разработано два протокола для исследования способности молекул FIT-Ig усиливать сближение с покрытыми TIGIT и PD-L1 шариками с четко выраженной жесткостью. Антитела либо инкубировали с белками PD-L1 и TIGIT перед добавлением детектирующих шариков AlphaScreen® (Метод 1), либо инкубировали с детектирующими шариками, предварительно покрытыми соответствующими белками TIGIT и PD-L1 (Метод 2). Второй способ был разработан для имитации рекрутмента клеток биспецифическими антителами.
i) Метод 1
Биспецифические антитела, исходные моноспецифические антитела и контрольные антитела были приготовлены в буфере (PBS рН 7,4 (Gibco) и 0,1% мас./об. BSA (Sigma)) в концентрации 150 нМ и серийно разбавлялись в соотношении 1:3, 8 значений концентрации. 5 мкл каждого серийного разведения антитела смешивали в 384-луночном аналитическом планшете AlphaLISA® (Perkin Elmer 6005350) с 5 мкл биотинилированного His-PD-L1 и 5 мкл His-FLAG-TIGIT, с концентрацией 50 нМ в буфере. Исходные моноспецифические антитела также готовили, как описано выше, начиная с 300 нМ, для тестирования в комбинациях. Добавляли 2,5 мкл первого антитела к такому же объему второго антитела, затем 5 мкл каждой комбинации исходных моноспецифических антител смешивали в аналитических планшетах с 5 мкл биотинилированного His-PD-L1 и 5 мкл His-FLAG-TIGIT, с концентрацией 50 нМ в буфере. Аналитические планшеты инкубировали в течение 1 часа при комнатной температуре перед добавлением 5 мкл анти-FLAG акцепторных шариков в количестве 0,1 г/л еще на час при комнатной температуре в темноте. Наконец, добавляли 5 мкл донорных шариков со стрептавидином в количестве 0,1 г/л в аналитические планшеты на 2 часа 30 минут. Аналитические планшеты считывали с использованием планшет-ридера EnVision (Perkin Elmer) с длинами волн возбуждения/излучения 680/615 нм. Строили графики измеренных отсчетов флуоресценции (альфа-сигнал) при титровании антител в программе Prism. Результаты приведены на Фигуре 25. Связывание молекул FIT-Ig с PD-L1 и TIGIT увеличивается с концентрацией антитела до 10 нМ. Не наблюдается связывания моноспецифических исходных антител и изотипического контроля.
ii) Метод 2
Донорные шарики со стрептавидином, приготовленные в количестве 0,05 г/л в буфере (PBS, рН 7,4 (Gibco 14190169) и 0,1% мас./об. BSA (Sigma)), покрывали биотинилированным His-PD-L1 (SEQ ID NO: 3) с концентрацией 25 нМ, в то время как His-FLAG-TIGIT (SEQ ID NO: 539) с концентрацией 25 нМ использовали для мечения анти-FLAG акцепторных шариков в количестве 0,05 г/л в буфере. Как акцепторные, так и донорные шарики инкубировали в течение 1 часа при комнатной температуре в темноте.
Биспецифические антитела, исходные моноспецифические антитела, отдельно взятые и в комбинациях, и контрольные антитела готовили в буфере с концентрацией 300 нМ и серийно разбавляли в соотношении 1:3, 8 значений концентрации. 5 мкл каждого серийного разведения антитела смешивали в 384-луночном аналитическом планшете AlphaLISA® (Perkin Elmer 6005350) с 10 мкл предварительно покрытых донорных шариков и 10 мкл предварительно покрытых акцепторных шариков. Аналитические планшеты инкубировали при комнатной температуре в течение 4 часов в темноте и затем считывали, как описано для способа 1. Строили графики измеренных отсчетов флуоресценции (альфа-сигнал) при титровании антител в программе Prism. Результаты приведены на Фигуре 26. Связывание молекул FIT-Ig с PD-L1 и TIGIT увеличивается с концентрацией антитела до 20 нМ. Не наблюдается связывания моноспецифических исходных антител и изотипического контроля.
d) Характеристика биспецифических молекул FIT-Ig, связывающихся с PD-L1 и TIGIT, методом проточной цитометрии
Протокол проточной цитометрии был разработан для оценки способности молекул FIT-Ig способствовать рекрутменту клеток, экспрессирующих TIGIT и PD-L1. С этой целью, клетки СНО, трансфицированные человеческим PD-L1, окрашивали CellTrace™ Far Red (Invitrogen С34572), имеющим максимум излучения при 661 нм, а клетки HEK, трансфицированные человеческим TIGIT, окрашивали CellTrace™ Violet (Invitrogen С34571), имеющим максимум излучения при 450 нм.
Клетки СНО с PD-L1 человека и HEK с TIGIT человека собирали, подсчитывали, промывали и повторно суспендировали в PBS (Gibco 14190169) в количестве 1 миллион клеток на миллилитр. Красители CellTrace™ Far Red и CellTrace™ Violet разводили 1:2000 и инкубировали с клетками в течение 20 мин при 37°С в темноте, согласно рекомендациям производителя. Затем добавляли избыток буфера (PBS (Gibco 14190169), 1% BSA (Sigma), 0,1% азида натрия (Severn Biotech 40-2010-01)) для дополнительной 5-минутной стадии инкубации. Клетки осаждали центрифугированием, повторно суспендировали в буфере в количестве 0,5 миллиона клеток на миллилитр и инкубировали по меньшей мере 10 минут при 37°С, прежде чем приступить к протоколу связывания. Неокрашенные ячейки сохраняли и использовали для создания стратегии гейтирования.
Биспецифические антитела и человеческий IgG1 были приготовлены в буфере с концентрацией 150 нМ и серийно разбавлены в соотношении 1:3, 8 значений концентрации. 50 мкл каждого серийного разведения антитела, 50 мкл клеток СНО с PD-L1 человека, меченых CellTrace™ Far Red, и 50 мкл HEK с TIGIT человека, меченых CellTrace™ Violet, добавляли в 96-луночный полистирольный (PS) планшет с V-образным дном (Greiner 651901). Аналитические планшеты инкубировали при комнатной температуре в течение 1 часа при осторожном перемешивании (450 об/мин) перед считыванием с использованием проточного цитометра Attune N×T (Thermo Fisher). CellTrace™ Violet возбуждали с использованием фиолетового лазера и детектировали в канале VL1 с полосовым фильтром 440/50. CellTrace™ Far Red возбуждали с использованием красного лазера и детектировали в канале RL1 с полосовым фильтром 670/14. Сбор проб проводили без интенсивного перемешивания образцов. Данные проточной цитометрии (FCS files) анализировали с помощью программного обеспечения FlowJo®. Одиночные клетки и дуплеты гейтировали на основе точечной диаграммы прямого и бокового рассеяния.
Анализ данных позволил идентифицировать четыре разных гейта: дважды отрицательный квадрант, соответствующий неокрашенным СНО с человеческим PD-L1 и неокрашенным HEK с человеческим TIGIT; два квадранта, положительных по одиночному окрашиванию (в канале VL1 или RL1); и квадрант, положительный по двойному окрашиванию (в обоих каналах VL1 и RL1), состоящий из окрашенных СНО с PD-L1 человека и окрашенных HEK с TIGIT человека, рекрутированных молекулами FIT-Ig. Графики процентного содержания дважды положительных клеток при титровании антител строили в программе Prism. Результаты приведены на Фигуре 27. Процент дважды положительных клеток увеличивается с концентрацией молекул FIT-Ig до 1 нМ.
Моноспецифическое связывание тестируемых молекул с мишенью было подтверждено на окрашенных клетках с использованием моноспецифических антител, меченых R-фикоэритрином (РЕ), имеющим максимум излучения при 590 нм. Меченые фикоэритрином антитело 1, антитело 2 и человеческий IgG1 разводили в буфере с концентрацией 150 нМ. 50 мкл каждого антитела смешивали с 50 мкл окрашенных СНО с PD-L1 человека и 50 мкл окрашенных HEK с TIGIT человека в 96-луночном полистирольном (PS) планшете с V-образным дном (Greiner 651901). После 1 часа инкубации при комнатной температуре, клетки промывали 3 раза 200 мкл/лунку PBS и повторно суспендировали в 150 мкл/лунку буфера. Аналитические пластины считывали с использованием проточного цитометра Attune N×T (Thermo Fisher) для регистрации флуоресценции. Как указано выше, были обнаружены Cell Trace™ Violet и Far Red. Фитоэритрин (РЕ) возбуждали с использованием желтого лазера и детектировали в канале YL1 с полосовым фильтром 585/16. Геометрические средние (GeoMean) значения в канале YL1 использовали для определения моноспецифического связывания с окрашенными СНО с человеческим PD-L1 или окрашенными HEK с человеческим TIGIT.
Пример 11. Создание и экспрессия конструктов анти-PD-L1-IL-2 иммуноцитокинов
Иммуноцитокины были получены путем слияния IL-2 дикого типа (SEQ ID NO: 301) или IL-2, содержащего делеции в первых девяти аминокислотах (см. SEQ ID NO: 303-323, слитые с SEQ ID NO: 324), с легкой цепью анти-PD-L1-антитела 1D05 (см. SEQ ID NO: 45). Они были сопряжены с вариантом тяжелой цепи 1D05 IgG1 с инактивированным эффектором (SEQ ID NO: 205). IL-2 дикого типа, слитый с тяжелой цепью 1D05, был приготовлен для использования в качестве контроля (SEQ ID NO: 302) и соединен с немодифицированной легкой цепью 1D05 (SEQ ID NO: 45). Двадцать два иммуноцитокина были успешно экспрессированы и в дальнейшем охарактеризованы. Один конструкт легкой цепи, 1D05 D1, не экспрессировался успешно.
Материалы и методы
Последовательности ДНК, кодирующие анти-PD-L1 иммуноцитокин (антитело 1D05) (С-терминальное слияние IL-2 с легкой цепью), были приобретены в виде синтетических цепочек ДНК и клонированы в экспрессионный вектор рТТ5 с использованием стратегии клонирования Golden Gate. Последовательность тяжелой цепи 1D05 включает константную область, которая является инактивированным вариантом IgG1, содержащим изменения по сравнению с диким типом, выделенные жирным шрифтом (SEQ ID NO: 299). Легкая цепь антитела 1D05 имеет полноразмерную последовательность IL-2 дикого типа (выделена подчеркиванием), слитую с С-концом константной области каппа (SEQ ID NO: 300). ПЦР по методу перекрывающегося сплайсинг-расширения с использованием соответствующих олигонуклеотидных праймеров использовалась для генерации вариантов N-конца IL-2 (см. SEQ ID NO: 300, где последовательность IL-2 выделена подчеркиванием, а область, подлежащая изменению, выделена жирным шрифтом). Варианты последовательностей клонировали в экспрессионный вектор рТТ5 с использованием метода Golden Gate. Последовательности дикого типа и конструкты вариантов были трансфицированы в клетки Expi293™ для экспрессии.
Пример 12 - Получение клеток, трансфицированных IL-2R, для скрининга
Чтобы дифференцировать активность иммуноцитокинов по отношению к рецепторам IL-2, имеющим высокую аффинность (αβγ) и промежуточную аффинность (βγ), были получены трансфектанты IL-2R. Клетки TF-1, экспрессирующие эндогенную общую цепь γ, трансфицировали рецепторными субъединицами β или α и β для придания реактивности к IL-2. Затем анализировали пролиферативный ответ на иммуноцитокины с использованием этих клеток (см. Пример 13).
Материалы и методы
Были созданы две рекомбинантные клеточные линии для определения различий между сигнализациями через IL-2R высокой аффинности (αβγ) и промежуточной аффинности (βγ). Клеточная линия эритролейкемии TF-1 (Европейская коллекция аутентифицированных клеточных культур) продемонстрировала полную зависимость роста от гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) или интерлейкина-3 (IL-3). Первую сгенерированную клеточную линию трансфицировали только полноразмерным человеческим IL-2Rβ (CD122). Вторая клеточная линия была получена путем трансфекции полноразмерного IL-2Rα (CD25) человека в первую клеточную линию.
Трансфецированные последовательности были оптимизированы по использованию кодонов для экспрессии у млекопитающих и клонировались в экспрессионный вектор под управлением промотора CMV, фланкированного последовательностями специфических 3'-и 5'-терминальных повторов piggyBac, улучшающими стабильную интеграцию в клеточный геном (см. "A hyperactive piggyBac транспозаза for mammalian applications"; Yusa K., et al., Proc. Natl. Acad. Sci. USA., 108(4): 1531-6, 2011 Jan 25). Кроме того, экспрессионный вектор для каждой субъединицы содержал отличную от других селекционную кассету для облегчения получения стабильной клеточной линии. Селекцию субъединицы β проводили с использованием пуромицина (Sigma), а субъединицы α - с использованием генетицина (Gibco). Субъединицу α трансфицировали в клетки, уже экспрессирующие субъединицу β.
Экспрессионные плазмиды трансфицировали совместно с плазмидой, кодирующей транспозазу piggyBac, в клеточную линию TF1 путем электропорации с использованием системы набора Lonza 4-D nucleofector transfection X в соответствии с инструкциями производителя. Через 24 часа после трансфекции полную среду дополняли для соответствующей селекции и клетки выращивали в течение по меньшей мере 3 недель для селекции стабильной линии, при этом среду заменяли каждые 3-4 дня. Экспрессию рекомбинантных человеческих субъединиц оценивали методом проточной цитометрии с использованием АРС-конъюгированного антитела против CD122 человека (IL-2Rβ) (eBioscience) и РЕ-конъюгированного антитела против CD25 человека (IL-2Rα) (eBioscience), Экспрессия эндогенной общей γ-цепи была подтверждена с помощью РЕ-конъюгированного антитела против CD132 человека (общая γ-цепь) (eBioscience). Поскольку экспрессия была низкой, клетки CD122+ сортировали по методу использования флуоресценции клеток (FACS) и затем культивировали при селекции. После трансфекции наблюдалась однородная экспрессия цепи α, и поэтому эти клетки не сортировали.
Полная среда TF1 состояла из среды RPMI 1640 (Gibco) плюс GM-CSF (2 нг/мл) и была дополнена 10% об./об. термоинактивированной фетальной бычьей сывороткой (hiFBS, Gibco). После подтверждения реакции на IL-2, трансфицированные клеточные линии поддерживали в RPMI 1640, 10% hiFBS и 5 нг/мл рекомбинантного IL-2 человека с генетицином (αβ) или без него (β).
Пример 13 - Оценка способности иммуноцитокиновых конструктов к сигнализации посредством IL-2R
Иммуноцитокины оценивали по их способности индуцировать пролиферацию клеточных линий TF1, трансфицированных субъединицей β либо субъединицами α и β IL-2R. Клетки истощали по цитокинам в течение ночи, затем стимулировали титрованием каждого иммуноцитокина. Использовали CellTiter-Glo® для определения количества жизнеспособных клеток в культуре через 3 дня на основе количественного определения присутствующего АТФ. Наблюдался широкий спектр влияния иммуноцитокинов на IL-2Rβγ, причем наибольшие делециия IL-2 давали наибольшее снижение пролиферации по сравнению с эквимолярными количествами свободного IL-2. Эффект на активность αβγ выражен слабее, но наибольшее снижение пролиферации также наблюдается при наибольших делециях IL-2. Делеции в первых нескольких N-концевых аминокислотах IL-2 позволяют осуществлять точную настройку активности цитокинов. Репрезентативный эксперимент показан на Фиг. 12(a) и (б).
Материалы и методы
Трансфицированные IL-2R клетки TF1 культивировали в обычном порядке в RPMI + 10% фетальной бычьей сыворотке (культуральная среда) с добавкой IL-2 (Peprotech) в количестве 5 нг/мл для β-трансфицированной клеточной линии и IL-2 в количестве 5 нг/мл и генетицина (Gibco) в количестве 350 мкг/мл для αβ-трансфицированной клеточной линии. Перед тестированием конструктов иммуноцитокинов клетки собирали центрифугированием и удаляли супернатант аспирацией. Клетки промывали в PBS для удаления цитокинов и антибиотиков. Клетки ресуспендировали в свежей культуральной среде при 105 клеток/мл, без добавок, и снова помещали в инкубатор на ночь.
Клетки собирали центрифугированием и удаляли супернатант аспирацией. Клетки ресуспендировали в полной среде и добавляли в лунки планшета 30 мкл клеточного раствора (384-луночный планшет с белыми стенками, обработанный для тканевых культур), для получения начальной концентрации клеток 1250 клеток/лунку.
Лиганд IL-2 готовили в виде серийных четырехкратных разведений из конечной аналитической концентрации (FAC) 300 нг/мл (рабочая - 600 нг/мл) в культуральной среде. Конструкты иммуноцитокинов титровали от 0,1 мкг/мл (трехкратные разведения) для тестирования клеточной линии αβγ и 10 мкг/мл (трехкратные разведения) для клеточной линии βγ. Добавляли 30 мкл титрования в планшет с клетками. В контрольные лунки добавляли 30 мкл культуральной среды без IL-2. Для уменьшения эффекта испарения, крайние ряды/колонки планшета заполняли 80 мкл культуральной среды. Планшеты затем инкубировали в течение 3 дней при 37°С, 5% CO2. После периода культивации пролиферацию клеток TF-1 оценивали добавлением 30 мкл Cell Titre Glo (Promega) во все лунки. Планшет инкубировали при комнатной температуре в течение 10 минут, затем считывали с использованием ультрачувствительного люминесцентного фильтра.
Уравнение 7: Расчет кратности по отношению к фону в анализе пролиферации TF-1
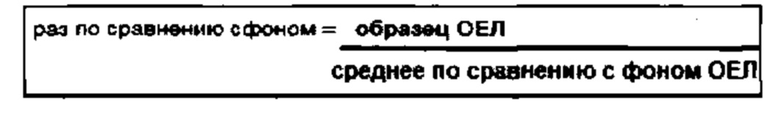
ОЕЛ = относительные единицы люминесценции
Данные выражены в виде кратности по отношению к фону. Фон определяли по лункам, содержащим клетки без цитокина
Пример 14 - Связывание иммуноцитокинов с PD-L1
Поверхностный плазмонный резонанс использовали для подтверждения способности конструктов иммуноцитокинов связывать PD-L1. Присутствие IL-2 в легкой цепи не оказывает отрицательного влияния на связывание (Таблица 9). Четыре конструкта с диапазоном активностей IL-2 были отобраны для проведения дополнительных анализов -это были 1D05 D1-9 ICK, 1D05 D1-8 ICK, 1D05 D9-2 ICK и 1D05 D9-7 ICK.
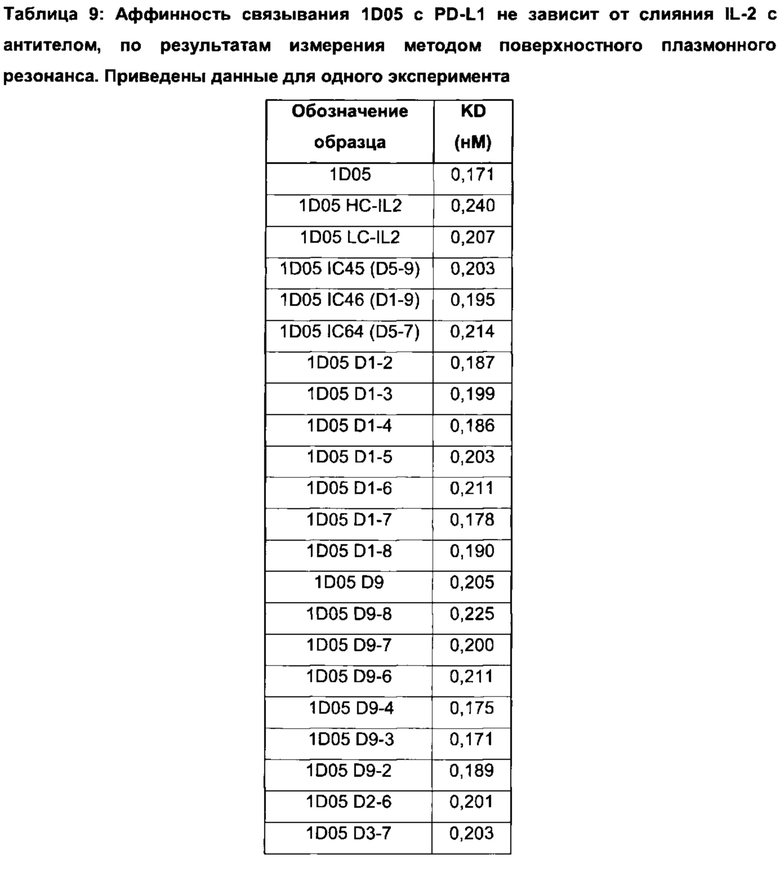
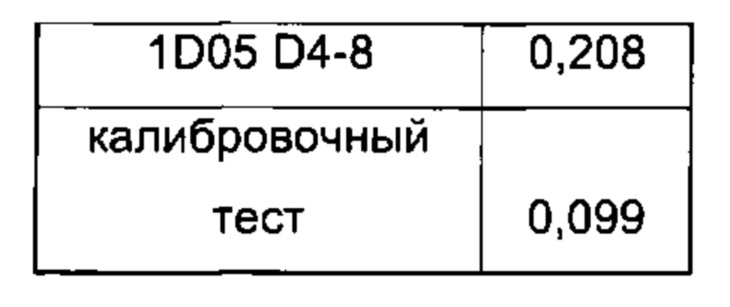
Материалы и методы
Анализ иммуноцитокинов методом поверхностного плазмонного резонанса
Анализ методом поверхностного плазмонного резонанса (SPR) без использования меток проводили на приборе SPR с матрицей ProteOn XPR36 (BioRad). Поверхность захвата антитела против человеческого IgG была создана на чипе биосенсора GLC с использованием реакции аминового сочетания антитела против IgG человека фирмы GE Healthcare. Тестируемые антитела захватывали на этой поверхности, а человеческий PD-L1 (собственного приготовления) использовали в качестве аналита с концентрациями 64 нМ, 16 нМ, 4 нМ, 1 нМ и 0,25 нМ. Анализ проводили при 25°С с использованием HBS-EP (Teknova Н8022). В качестве эталона для сенсограмм связывания использовался один лишь буфер. Данные были проанализированы с использованием модели 1:1, встроенной в программу анализа данных ProteOn XPR36.
Пример 15 - Оценка способности иммуноцитокинов нейтрализовать взаимодействие PD-L1 и PD-1/CD80
Для обеспечения того, чтобы слияние молекулы IL-2 с антителом не нарушало его нейтрализующую способность, прошедшие предварительный отбор иммуноцитокины тестировали методом ИФА нейтрализации. Исследуемые иммуноцитокины, прошедшие предварительный отбор, не отличались от антител дикого типа по их способности нейтрализовать взаимодействия между PD-L1 и PD-1, и между PD-L1 и CD80. Результаты приведены на Фигуре 13 и в Таблице 10. Значения в таблице представляют собой среднее для трех независимых экспериментов.
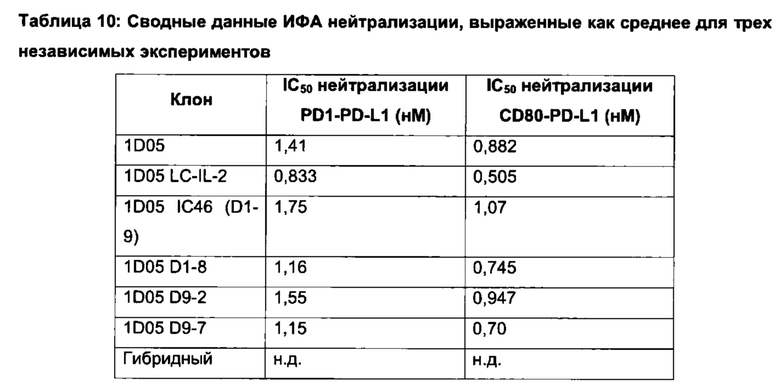

Материалы и методы
а) ИФА нейтрализации PD-L1/PD-1 или PD-L1/CD80
CD80 (R&D Systems) или PD-1 (собственного приготовления), разбавленные до 2,5 мкг/мл, адсорбировали на 96-луночных планшетах с низкой аутофлуоресценцией и высоким связыванием белка (Costar) в течение ночи при 4°С. Избыточный белок удаляли промыванием PBS-Tween (0,1% об./об.), и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего планшеты промывали, как описано выше. 60 мкл титрования (трехкратные разведения из 100 нМ) антитела добавляли к 96-луночному несвязывающему планшету, разведенной в буфере для анализа ИФА (PBS + 0,1% BSA). К планшету добавляли 60 мкл биотинилированного PD-L1 (собственного приготовления, меченый с помощью набора Lightning Link Biotinylation) при рабочей концентрации 16 нМ (FAC 8 нМ), за исключением контрольных лунок, в которые добавляли 60 мкл буфера для анализа ИФА. Планшет инкубировали в течение 30 мин перед переносом 50 мкл на планшеты с нанесенным покрытием.
Планшеты с покрытием инкубировали в течение 1 часа при комнатной температуре. Избыток белка удаляли промыванием PBS-Tween (0,1% об./об.). Связывание PD-L1 детектировали с использованием меченого стрептавидином европия (streptavidin labelled Europium) (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный трисом физиологический раствор)-Твин (0,1% об./об.) и добавляли к планшету 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм планшет-ридером Envision (PerkinElmer). Процент специфического связывания рассчитывали по Уравнению 3.
Значения IC50 определяли с использованием прикладной программы GraphPad Prism путем аппроксимации кривой процента специфического связывания (Уравнение 3) с использованием четырехпараметрического логистического уравнения (Уравнение 4).
Пример 16 - Деиммунизация антител против PD-L1
Чтобы уменьшить вероятность неблагоприятных иммунологических реакций, связанных с анти-PD-L1 иммуноцитокином, был создан ряд мутантов 1D05-антител (SEQ ID NOs: 47-51) с предполагаемым более низким потенциалом иммуногенности, по результатам определения с помощью прикладной программы для анализа эпитопа Т-клеток. Мутации могут быть одиночными или комбинированными. Мутанты оценивали на их способность связывать PD-L1 с такой же аффинностью, как и молекула дикого типа, методом SPR, как описано в Примере 14, с добавлением человеческого PD-L1-аналита с концентрацией 256 нМ. Исследуемые мутации включены как SEQ ID NOs: 47-51, и обозначены подчеркиванием и жирным шрифтом. Каркасные мутации VH (SEQ ID NOs: 47 и 48) не оказывают никакого отрицательного влияния на связывание. Мутация с заменой V на А в CDRH2 (SEQ ID NO: 50) ухудшала связывание, и поэтому будет проанализирована альтернативная мутация (V-Y, SEQ ID NO: 298). Результаты приведены в Таблице 11.
Пример 17 - Ингибирование роста опухоли анти-PD-L1-антителом у NOD/SCID: модель ксенотрансплантата Т-клеток
Ингибирование роста опухоли меланомы оптимизированным прототипом антитела 1D05 в формате hlgG1 LAGA (SEQ ID NO: 205) было продемонстрировано в модели NOD/SCID (нетучные диабетические мыши с тяжелым комбинированным иммунодефицитом):ксенотрансплантат Т-клеток. Т-клетки размножали в присутствии А375, клеточной линии меланомы, в течение 20 дней в присутствии IL-2 и IL-7. Т-клетки имплантировали подкожно совместно со свежими клетками А375, затем через 1 час вводили внутрибрюшинно антитело. Наблюдали за размером опухоли и выживаемостью животных. Опухоли у мышей, получавших лечение антителом 1D05, были меньше, чем у животных, получавших изотипический контроль. Также увеличилось время выживания у мышей, получавших лечение 1D05.
Материалы и методы
Исследования эффективности проводились с использованием модели Т-клеток/ксенотрансплантата на мышах NOD/SCID в соответствии с уточненным методом, описанным Stewart R et al. (Cancer Immunol. Res., 2015 Sep, 3 (9): 1052-62). Камеры системы лейкоредукции были получены от NHSBT (департамент крови и трансплантации Государственной службы здравоохранения Великобритании). HLA-А2-положительные доноры были выбраны по окрашиванию нефракционированной крови с использованием РЕ-меченого анти-человеческого HLA-A2 (Biolegend, Clone:
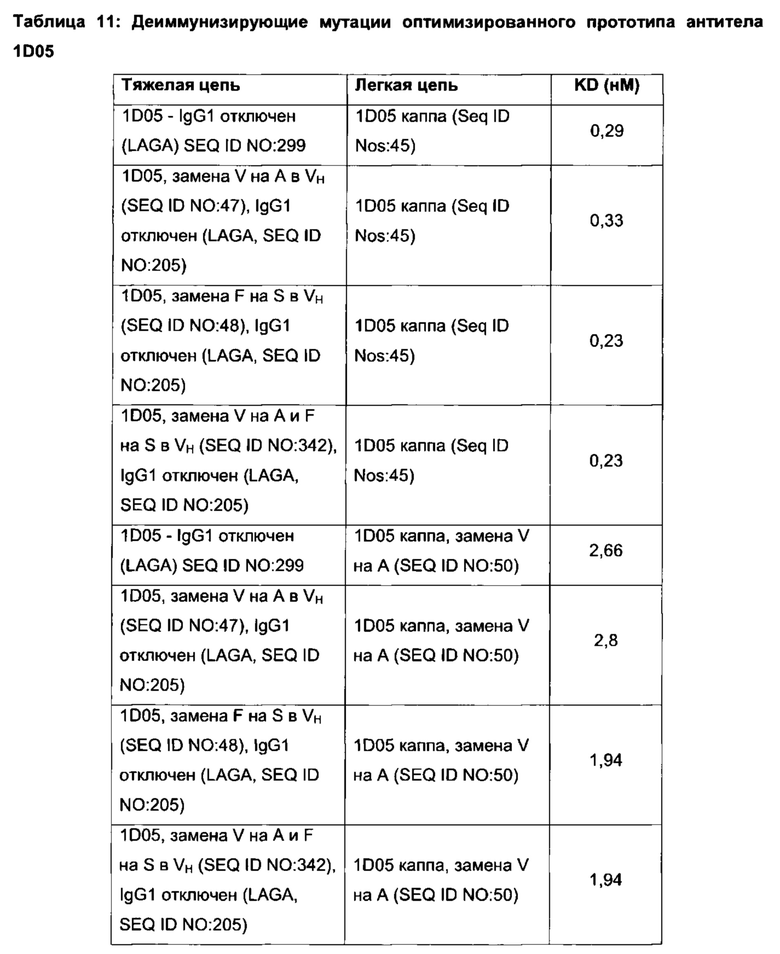
ВВ7.2), красные кровяные клетки затем лизировали, а после этого фиксировали с помощью 4% параформальдегида (PFA) перед сбором данных на проточном цитометре Attune. РВМС выделяли центрифугированием в градиенте плотности над Ficoll. Первичные человеческие CD4+ и CD8+ Т-клетки затем выделяли с использованием набора EasySep для обогащения CD4+ и CD8+ Т-клеток человека (Stemcell Technologies, №№ кат. 19052 и 19053). CD4+ и CD8+ Т-клетки затем культивировали отдельно в течение 20 дней на монослое клеток А375, обработанных митомицином С (на 10-й день Т-клетки пересевали на свежий монослой А375) в присутствии рекомбинантных IL-2 и IL-7 человека (Peprotech). На 20-й день клетки замораживали в 90% hiFBS/10% ДМСО при -80°С в «Mr Frosty» (Nalgene) и хранили в жидком азоте до момента использования. За день до начала in vivo эксперимента клетки оттаивали и помещали в культуру.
В день имплантации подсчитывали CD4+ и CD8+ Т-клетки и смешивали их в соотношении 1:1. Затем смесь CD4+/CD8+ добавляли к опухолевым клеткам А375 и вводили подкожно мышам в заднюю часть правого бока. Экспериментальные группы получали свою первую дозу антитела или изотипический контроль (все вводили внутрибрюшинно в количестве 10 мг/кг) через 1 час после имплантации клеток. Животные получали дополнительные дозы через 3, 6, 8 и 10 дней после имплантации. Развитие опухоли контролировали три раза в неделю с помощью штангенциркуля с цифровой индикацией, с проведением измерений в двух направлениях до конца исследования. Объемы опухолей (мм3) оценивали по стандартной формуле (L × W2)/2 (где L обозначает больший диаметр, а W - меньший диаметр опухоли). Исследования на мышах продолжали проводить до тех пор, пока их опухоли не развивались до среднего диаметра 12 мм, или до достижения ими одной из конечных точек умерщвления из соображений гуманности, описанных в протоколе исследования. Статистику выживания до конечных точек умерщвления из соображений гуманности рассчитывали с использованием метода Каплана-Мейера в программе Prism. Этот подход был использован для определения того, было ли лечение PD-L1 связано с улучшенной выживаемостью.
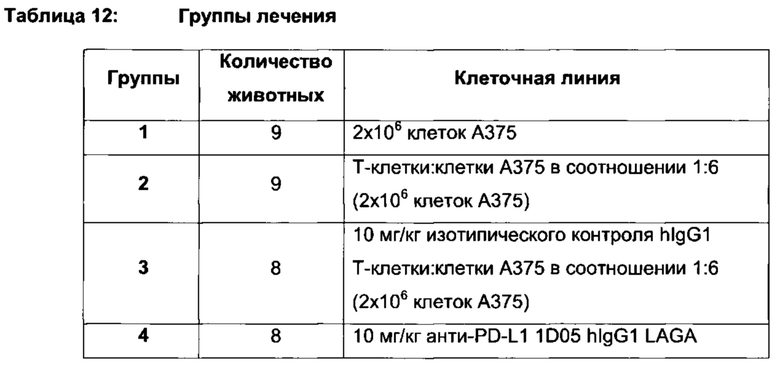

Лечение с использованием изотипического контроля не влияло на развитие опухоли по сравнению с группой, которой вводили CD4+/8+ Т-клетки совместно с опухолевыми клетками. В то же время, лечение анти-PDL1-антителом 1D05 задерживало развитие опухоли по сравнению с изотипическим контролем. Это показано на Фигуре 14.
Все группы, в которых совместно с опухолями вводили Т-клетки, показали увеличение времени участия в исследовании по сравнению с группой, которой вводили только опухоль. Лечение с использованием изотипического контроля не влияло на время участия в исследовании, тогда как лечение анти-PDL1-антителом 1D05 увеличивало время участия в исследовании по сравнению со всеми другими группами, включая группы изотипического контроля. Результаты приведены на Фигуре 15.
Пример 18: Исследования с введением однократной дозы иммуноцитокинов яванским макакам
Чтобы оценить параметры фармакодинамики и фармакокинетики (ФК) в наиболее релевантной животной модели, самцам яванского макака вводили однократно иммуноцитокин (ICK) в дозе 1 мг/кг. Животных наблюдали для выявления клинических проявлений токсичности, и образцы крови брали в течение 7 дней для анализа ФК, продуцирования цитокинов и определения характеристик субпопуляций лейкоцитов. Фазу прижизненных исследований и гематологию, проточную цитометрию и анализ цитокинов проводила фирма Envigo UK (номер исследований GF13YC). Фармакокинетический анализ проводился собственными силами.
Материалы и методы
Для исследования использовали самцов яванского макака в возрасте не менее 2 лет, вес тела регистрировали за 7 дней и 4 дня до начала исследования. Композиции конструктов иммуноцитокинов готовили в 50 мМ ацетате натрия, рН 5,5, с концентрацией 1 мг/мл, и разбавляли до 0,2 мг/мл в физиологическом растворе для внутривенной инфузии со скоростью 5 мл/кг/час. Кровяное давление и температуру тела контролировали перед началом эксперимента и через 1 час и 4 часа после окончания введения дозы. Животных осматривали два раза в день для выявления признаков ухудшения состояния здоровья. Исследование проводилось в двух фазах: начальные дозы 1D05 НС IL-2 ICK и 1D05 LC D9-7 ICK для обеспечения уровня дозы и моментов времени проведения измерений ФК параметров, при необходимости, затем дозу 1D05 LC D9-7 ICK повторяли вместе с четырьмя дополнительными конструктами (см. Таблицу 1). Фаза 2 дозирования 1D05 LC D9-7 ICK обозначена с помощью (2) рядом с названием конструкта.
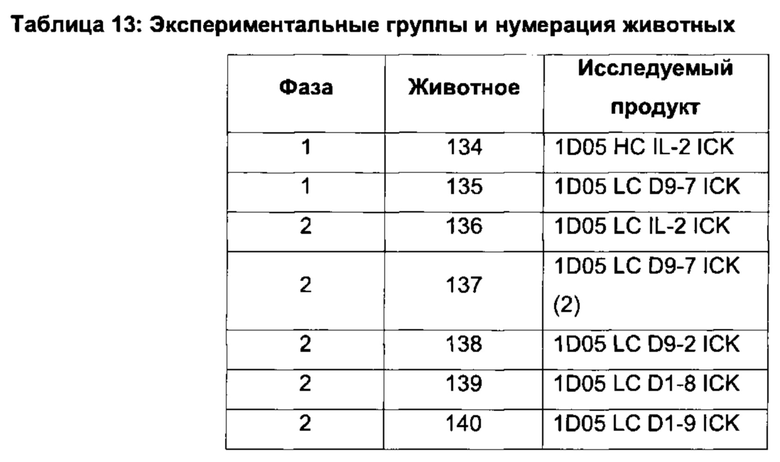
Для гематологического анализа образцы крови натощак брали в предварительно обработанные ЭДТА пробирки до начала эксперимента и через 2, 5 и 7 дней после введения препарата. Измерения основных гематологических параметров проводили с использованием Bayer Advia 120. Результаты показаны на Фиг. 16 и 17.
Для анализа цитокинов и растворимого CD25 образцы крови брали в предварительно обработанную ЭДТА пробирку до начала эксперимента и через 3 дня после введения препарата, а плазму выделяли центрифугированием при 2000 g в течение 10 минут. Образцы замораживали до момента проведения анализа методами мультиплексного MSD (цитокины) или коммерческого ИФА (растворимый CD25). Результаты показаны на Фиг. 18 и 19.
Для иммунофенотипирования образцы крови брали в предварительно обработанные ЭДТА пробирки до начала эксперимента и через 5 дней после введения препарата. Образцы крови окрашивали коктейлями с напрямую конъюгированными моноклональными антителами, затем эритроциты лизировали и образцы фиксировали повторным суспендированием в забуференном фосфатом физиологическом растворе, содержащем 1% формальдегида, перед проведением анализа. Результаты приведены на Фигуре 20.
Для ФК-анализа, образцы крови брали в необработанные пробирки до начала эксперимента, после завершения инфузии (EOI), через 2, 4, 8, 16, 24, 32, 40 и 48 часов после завершения инфузии, с дополнительными измерениями через 72 часа и 96 часов для фазы 2) и сыворотку готовили путем естественного свертывания крови с последующим центрифугированием при 2000 g в течение 10 мин. Образцы сыворотки замораживали на сухом льду для отправки в Kymab. Результаты приведены на Фигуре 21.
Фармакокинетический анализ образцов сыворотки
a) ФК-анализ для детектирования антител против PD-L1
50 мкл/лунку человеческого PD-L1 Flag His (№ID: 505, собственного приготовления), разведенного до 2 мкг/мл в PBS (Sigma, Р3813-10PAK), адсорбировали на 96-луночных флуоресцентных планшетах с высоким связыванием белка (Greiner) в течение ночи при 4°С. Избыток белка удаляли промыванием 3×300 мкл/лунку PBS-Tween (0,1% об./об.) и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего планшеты промывали, как описано выше. Антитела разводили от 10000 нг/мл до 9,77 нг/мл (разведения в соотношении 1/2) в пуле сыворотки яванского макака (Seralab, CYNSRM) для получения 12 стандартов, включая холостой опыт. Стандарты, образцы для контроля качества и пробы разбавляли с минимальным требуемым разбавлением (MRD) 1 к 50 в буфере для анализа ИФА (PBS + 0,1% BSA) и добавляли в 96-луночные планшеты с высоким связыванием с нанесенным покрытием в количестве 50 мкл/лунку. Планшет инкубировали в течение 1 часа при комнатной температуре, после чего планшеты промывали 3× PBS-Tween. Добавляли в планшет 50 мкл биотинилированного козьего анти-человеческого IgG (Southern Biotech) в концентрации 1 мкг/мл. Планшет инкубировали в течение 1 часа при комнатной температуре, после чего планшеты промывали 3× PBS-Tween. Связывание PD-L1 детектировали с использованием меченого стрептавидином европия (streptavidin labelled Europium) (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный Tris физиологический раствор)-Tween (0,1% об./об.) и 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Концентрации определяли с использованием прикладной программы GraphPad Prism путем интерполяции по калибровочной кривой, аппроксимированной с использованием четырехпараметрического логистического уравнения (Уравнение 4). Результаты показаны на фиг. 21а и 21b.
b) ФК-анализ для детектирования интактного иммуноцитокина (антитела, слитого с IL-2)
50 мкл/лунку человеческого PD-L1 Flag His (Seq ID No: 505, собственного приготовления), разведенного до 3 мкг/мл в PBS (Sigma, Р3813-10PAK), адсорбировали на 96-луночном планшете с низкой аутофлуоресценцией и с высоким связыванием белка (Costar) в течение ночи при 4°С. Избыток белка удаляли промыванием 3× 300 мкл/лунку PBS-Tween (0,1% об./об.) и лунки блокировали 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре, после чего планшеты промывали 3× PBS-Tween. Антитела разводили от 50000 нг/мл до 617,3 нг/мл в пуле сыворотки яванского макака (Seralab, CYNSRM) для получения 10 стандартов, включая холостой опыт. Стандарты, образцы для контроля качества и пробы разбавляли с минимальным требуемым разбавлением (MRD) 1 к 20 в буфере для анализа ИФА (PBS + 0,1% BSA) и добавляли в 96-луночные планшеты высокого связывания с нанесенным покрытием в количестве 50 мкл/лунку. Планшет инкубировали в течение 1 часа при комнатной температуре, после чего планшеты промывали 3× PBS-Tween. В планшет добавляли 50 мкл биотинилированного анти-человеческого IL-2 (Peprotech) в количестве 2 мкг/мл. Планшет инкубировали в течение 1 часа при комнатной температуре, после чего планшеты промывали, как описано выше. Связывание детектировали с использованием стрептавидина, меченого европием (streptavidin labelled Europium) (Perkin Elmer), разбавленного 1/1000 в буфере для анализа DELFIA (Perkin Elmer). Планшеты промывали TBS (забуференный Tris физиологический раствор)-Tween (0,1% об./об.) и 50 мкл/лунку раствора DELFIA Enhancement (Perkin Elmer). Флуоресценцию с временным разрешением измеряли при 615 нм на планшет-ридере Envision (PerkinElmer). Концентрации определяли с использованием прикладной программы GraphPad Prism путем интерполяции по калибровочной кривой, аппроксимированной с использованием четырехпараметрического логистического уравнения. Результаты показаны на Фиг. 21с и 21d.
Краткое изложение результатов
После введения дозы не наблюдалось признаков явной опосредованной IL-2 токсичности (лихорадка, сосудистая утечка, диарея). Число лимфоцитов увеличивалось на протяжении исследования для разных конструктов иммуноцитокинов. Конструкты с наиболее укороченными последовательностями (greatest truncations) давали самые низкие уровни пролиферации лимфоцитов; небольшое увеличение наблюдалось для 1D05 LC D1-9 ICK или 1D05 LC D1-8 ICK на протяжении семидневного периода, тогда как 1D05 LC D9-7 ICK и полноразмерный IL-2 вызывали значительную пролиферацию. Лимфопения, наблюдаемая на 2-й день для некоторых конструктов, указывает на маргинацию лимфоцитов из кровообращения (скопление лейкоцитов по краю участка воспаления). За ней следует реактивный лимфоцитоз, который наблюдается в день 5 (Фиг. 16).
Введение конструктов иммуноцитокинов не вызывало значительной анемии (Фиг. 17). Снижение примерно на 20% уровней гемоглобина, гематокрита и эритроцитов наблюдалось в день 7 для наиболее активных конструктов (1D05 НС IL-2 ICK, 1D05 LC IL2 ICK и 1D05 LC D9-7 ICK), и снижение на примерно 10% - для других конструктов. Это согласуется с отдельными результатами исследований иммуноцитокинов тяжелой цепи IL-2. Тромбоцитопения (снижение количества тромбоцитов) не наблюдалась.
IL-2 был сильно увеличен через 3 дня после введения дозы, что указывает на его продуцирование активированными Т-клетками. Однако, существует вероятность того, что анализ является перекрестно-реактивным к человеческому IL-2 и поэтому также может детектировать иммуноцитокин. Не наблюдалось никакой четко выраженной повышающей или понижающей регуляции любого из других цитокинов после введения дозы, хотя имелась тенденция к снижению уровня IL-8 (Фиг. 18). Уровни растворимого CD25, который является биомаркером активации Т-клеток, были сильно увеличены через 3 дня после введения иммуноцитокинов (Фиг. 19). Уровни растворимого CD25 коррелировали с in vitro стимулирующей активностью иммуноцитокинов, описанной в Примере 13.
Введение доз иммуноцитокинов увеличивает количество активированных Т-клеток в крови (Фиг. 20). При введении дозы 1D05 LC IL-2 ICK, количество CD4+ и CD8+ клеток увеличивается, но субпопуляции CD69+ (ранняя активация) и CD25+ (более поздняя активация) значительно увеличиваются по сравнению с уровнями до введения препарата. Увеличение числа клеток является менее заметным для укороченных конструктов. Никаких существенных изменений в количестве B-клеток, NK-клеток и нейтрофилов не наблюдалось, при умеренном увеличении числа моноцитов. Данные для животного, получившего дозу 1D05 LC D9-7 ICK, отсутствуют из-за свертывания образца.
Продукты слияния легкой цепи (LC) имеют более длительный период полувыведения, чем продукты слияния тяжелой цепи (НС), что согласуется с предыдущими данными, полученными для мышей (Gillies SD, Protein Engineering, Design and Selection, 26:10: 561-569, 2013), Период полувыведения 1D05 LC IL-2 ICK составлял около 8 часов, а период полувыведения укороченных конструктов IL-2 был примерно в два раза длиннее (Фигуры 21a и 21b). Увеличение периода полувыведения иммуноцитокинов с укороченным IL-2 по сравнению с полноразмерным IL-2 может отражать уменьшенное связывание с рецепторами IL-2.
Для детектирования интактного иммуноцитокина, т.е. антитела, слитого с IL-2, использовали модифицированный метод анализа (Фигуры 21c и 21d). Этот результат показывает, что часть молекулы IL-2 остается слитой in vivo и не расщепляется.
Пример 19 - Продленное исследование с однократным введением дозы препарата яванским макакам
Для определения продолжительности лимфоцитоза и получения более подробного анализа субпопуляций Т-клеток, будет проведено продленное исследование с однократным введением дозы препарата (номер исследования HQ52PV). Самкам яванского макака вводят 1 мг/кг иммуноцитокина в соответствии с Примером 18 и наблюдают на протяжении по меньшей мере 14 дней. Цитокины будут анализировать в дни 1, 3, 7, 10 и 14, и перед введением препарата. Гематологические измерения будут проводить в дни 2, 5, 7, 10 и 14, и перед введением препарата. Детектирование растворимого CD25 будут проводить в дни 3, 7 и 10, и перед введением препарата. CD127 будет добавлен к панели иммунофенотипирования, чтобы обеспечить возможность детектирования регуляторных Т-клеток (CD3+, CD4+, CD25hi, CD127lo), и анализ будут проводить в дни 1, 5, 7, 10 и 14, и перед введением препарата. ФК-анализ будет выполняться так же, как и раньше. Экспериментальные группы приведены в Таблице 14.
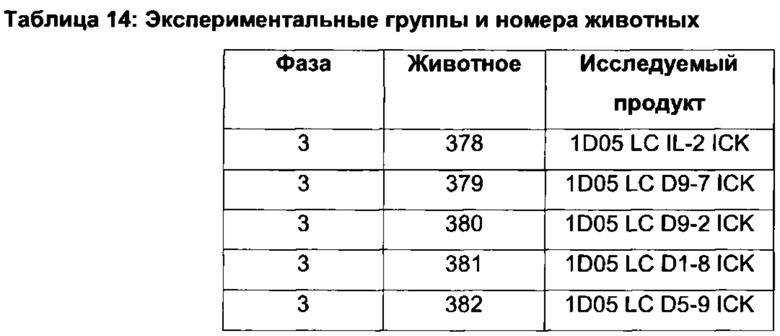
После введения дозы не наблюдалось признаков явной опосредованной IL-2 токсичности (лихорадка, сосудистая утечка, диарея). Количество лимфоцитов достигло пика на 7-й день для всех конструктов иммуноцитокинов. Конструкты с наиболее укороченными последовательностями индуцировали самые низкие уровни пролиферации лимфоцитов; наименьшая пролиферация наблюдалась для 1D05 LC D1-8 ICK, тогда как 1D05 LC D9-7 ICK и полноразмерный IL-2 индуцировали наибольшую пролиферацию. Лимфопения, наблюдаемая на 2-й день для некоторых конструктов, указывает на маргинацию лимфоцитов из кровообращения (скопление лейкоцитов по краю участка воспаления). Следом за этим наблюдался реактивный лимфоцитоз (Фиг. 28). Уровни растворимого CD25, который является биомаркером активации Т-клеток, достигали пика через 3 дня после введения дозы иммуноцитокинов (Фиг. 29). Уровни растворимого CD25 коррелировали с in vitro стимулирующей активностью иммуноцитокинов, описанной в Примере 13.
Введение иммуноцитокиновых конструктов не вызывало значительной анемии (Фиг. 30). Для конструктов иммуноцитокинов наблюдалось снижение уровней гемоглобина, гематокрита и эритроцитов на 10-20%. Уровни гемоглобина оставались пониженными на протяжении всего периода времени у животного, получившего дозу 1D05 LC D1-8 ICK. Слабая тромбоцитопения наблюдалась для двух наиболее активных конструктов в день 5, но после этого уровни восстанавливались. IL-2 был сильно повышен через 3 дня после введения дозы, что указывает на его продуцирование активированными Т-клетками. Однако, существует вероятность того, что анализ является перекрестно-реактивным по отношению к человеческому IL-2, и потому эти уровни отражают присутствие иммуноцитокина. Не наблюдалось четко выраженной повышающей или понижающей регуляции любого из других цитокинов после введения дозы (Фиг. 31).
Как отмечалось ранее в Примере 18, период полувыведения 1D05 LC IL-2 ICK составлял около 8 часов, а период полувыведения укороченных конструктов IL-2 коррелировал с размером удаляемой части последовательности (Фиг. 32). Конструкт иммуноцитокина с самым большим размером удаляемой части последовательности, D1-8, имел самый длинный период полувыведения, приблизительно 24 часа. Увеличение периода полувыведения иммуноцитокинов с укороченным IL-2 по сравнению с полноразмерным IL-2 может отражать уменьшенное связывание с рецепторами IL-2.
Пролиферация CD4+ и CD8+ Т-клеток показана на Фигуре 33. Как было определено при автоматизированном подсчете клеток, степень пролиферации хорошо коррелирует с размером удаляемой части последовательности IL-2, причем наибольшая пролиферация обоих субпопуляций Т-клеток наблюдалась у животного, получивших дозу 1D05 LC ICK D9-7.
Пример 20. Связывание с эндогенно экспрессируемым клеткой hPD-L1 и нейтрализация связывания hPD-L1 с PD-1 и CD80
Оптимизированные прототипы антитела тестируют на способность связываться с клетками ES2, эндогенно экспрессирующими hPD-L1, а также нейтрализацию взаимодействия PD-L1/PD-1 и взаимодействия PD-L1/CD80. Клетки ES2, эндогенно экспрессирующие hPD-L1 (АТСС), разводят в буфере FACS (PBS, 1% BSA, 0,1% азида натрия) и распределяют по трем 96-луночным планшетам с V-образным дном (Greiner) с плотностью 0,5-1×105 клеток на лунку. Клетки промывают 150 мкл PBS и центрифугируют при 300 g в течение 3 минут. Супернатант удаляют аспирацией и добавляют 150 мкл PBS. Эту стадию промывки повторяют.
В планшете 1 (связывание PD-L1) к промытым клеткам добавляют 25 мкл оптимизированного прототипа антитела, эталонного антитела или контрольного антитела, разведенных в буфере FACS. Добавляют 25 мкл буфера FACS и клетки инкубируют при 4°С в течение 60 минут. Добавляют 150 мкл буфера FACS и клетки промывают, как описано выше. Для детектирования связывания антител против PD-L1, анти-человеческий РЕ (Jackson ImmunoResearch) разбавляют 1/500 в буфере FACS и 50 мкл этой смеси добавляют к клеткам. Клетки инкубируют при 4°С в течение 60 минут. Клетки дважды промывают 150 мкл буфера FACS, центрифугируют при 300 g в течение 3 минут после каждой стадии промывки и аспирации супернатанта. Клетки фиксируют добавлением 50 мкл 4% параформальдегида и инкубацией в течение ночи при 4°С. Клетки промывают один раз, как описано выше, и ресуспендируют в буфере FACS для анализа. Интенсивность сигнала РЕ (среднее геометрическое) измеряют методом проточной цитометрии с использованием прибора Beckman Coulter Cytoflex. Строят графики зависимостей для средних геометрических значений без дополнительных расчетов.
В планшете 2 (нейтрализация PD-1) к промытым клеткам добавляют 25 мкл оптимизированного прототипа антитела, эталонного антитела или контрольного антитела, разведенных в буфере FACS. Добавляют 25 мкл биотинилированного PD-1 человека (собственного приготовления, меченый Fc, SEQ ID NO: 6) и клетки инкубируют при 4°С в течение 60 минут. Биотинилирование проводили самостоятельно с использованием набора для конъюгации Lightning Link (Innova Biosciences) в соответствии с инструкциями производителя. Добавляют 150 мкл буфера FACS и клетки промывают, как описано выше. Для детектирования биотинилированного PD-1, стрептавидин-Alexa Fluor 647 (AF647, Jackson ImmunoResearch) разбавляют 1/500 в буфере FACS и добавляют 50 мкл этой смеси к клеткам. Клетки инкубируют при 4°С в течение 60 минут. Клетки дважды промывают 150 мкл буфера FACS, центрифугируют при 300 g в течение 3 минут после каждой стадии промывки и аспирации супернатанта. Клетки фиксируют, промывают и ресуспендируют для анализа, как описано выше. Интенсивность сигнала АРС (среднее геометрическое) измеряют методом проточной цитометрии. Строят графики зависимостей для средних геометрических значений без дополнительных расчетов.
В планшете 3 (нейтрализация CD80) добавляют к промытым клеткам 25 мкл оптимизированного прототипа антитела, эталонного антитела или контрольного антитело, разведенных в буфере FACS. Добавляют 25 мкл биотинилированного человеческого CD80 (меченого Fc, R&D Systems, 140-В1) и клетки инкубируют при 4°С в течение 60 минут. Все остальные стадии выполняют так же, как для планшета 2.
Альтернативно, для одновременного детектирования связывания и нейтрализации, клетки ES2, экспрессирующие hPD-L1, разводят в буфере FACS и распределяют по двум 96-луночным планшетам с V-образным дном (Greiner) с плотностью 0,5-1×105 клеток на лунку. Клетки промывают 150 мкл PBS и центрифугируют при 300 g в течение 3 минут. Супернатант удаляют аспирацией и добавляют 150 мкл PBS. Эту стадию промывки повторяют.
К промытым клеткам добавляют 25 мкл оптимизированного прототипа антитела, эталонного антитела или контрольного антитела, разведенных в буфере FACS. Добавляют 25 мкл биотинилированного человеческого PD-1 (R&D Systems, 8986-PD-100, меченого his) или CD80 (R&D Systems, 9050-В1-100, меченого his) и клетки инкубируют при 4°C в течение 60 минут. Добавляют 150 мкл буфера FACS и клетки промывают, как описано выше. Для детектирования связывания биотинилированного PD-1 или CD80 и анти-PD-L1 антитела, стрептавидин-AF647 и анти-человеческий РЕ разводят каждый 1:500 в буфере FACS и 50 мкл этой смеси добавляют к клеткам. Клетки инкубируют при 4°C в течение 60 минут. Клетки дважды промывают 150 мкл буфера FACS, центрифугируют при 300 g в течение 3 минут после каждой стадии промывки и аспирации супернатанта. Клетки фиксируют, промывают и ресуспендируют для анализа, как описано выше. Интенсивность сигналов РЕ и АРС (среднее геометрическое) измеряют методом проточной цитометрии. Строят графики зависимостей для средних геометрических значений без дополнительных расчетов. Альтернативно, антитело против метки his, конъюгированное с АРС (R&D Systems), может использоваться для детектирования PD-1 или CD80, или PD-1 и CD80 могут быть непосредственно помечены AF647.
Пример 21 - Тестирование оптимизированных прототипов анти-PD-L1 антител в биоанализе репортерных клеток
Способность анти-PDL1-антител нейтрализовать взаимодействие PD-L1/PD-1 на клетках будет определена с использованием анализа на основе биолюминесценции клеток (Promega®). Клетки PD-L1 аАРС/СНО-K1, трансфицированные PD-L1 и белком клеточной поверхности, предназначенным для промотирования активации TCR, культивируют совместно с клетками Jurkat, экспрессирующими PD-1. Эти клетки также презентируют индуцируемый NFAT чувствительный к люциферазе элемент. Совместная культура двух типов клеток в присутствии антитела, способного блокировать взаимодействие PD-1-PD-L1, активирует сигнализацию TCR и опосредуемую NFAT активность люциферазы.
Анализ проводят в соответствии с рекомендациями производителя. Вкратце, клетки PD-L1 аАРС/СНО-K1 культивируют в течение ночи в среде Hams F12 с добавкой 10% hiFBS. На следующий день среду удаляют, добавляют в аналитические планшеты эффекторные клетки PD-1 Jurkat и антитела против PD-L1 на 6 часов при 37°С в RPMI 1640 с добавкой 1% hiFBS. Планшеты считывают после 10 минут инкубации с Bio-Glo™ с помощью планшет-ридера Envision, используя настройки для измерения люминесценции. Активность люциферазы, индуцируемая антителом, представлена в виде кратности индукции по сравнению с сигналом лунок, соответствующих фоновым уровням ответа, в соответствии с Уравнением 8. Значения EC50 рассчитывают с использованием 4-параметрической логистической аппроксимации (уравнение 4).
Уравнение 8

Пример 22 - Фармакокинетические исследования оптимизированных прототипов антител у мышей, экспрессирующих hPD-L1
Оптимизированные прототипы антител в формате человеческого IgG1 с функциональным эффектором (т.е. имеющие константную область IgG1 дикого типа, SEQ ID NO: 341), вводят внутрибрюшинно в дозе 10 мг/кг мышам, экспрессирующим человеческий PD-L1, по восемь мышей на антитело. Образцы крови берут до введения препарата и в моменты времени 2, 4, 8, 12, 24, 48, 72, 96, 192, 336, 508 и 672 часа. Готовят сыворотку и образцы замораживают до проведения анализа. Образцы будут анализироваться в соответствии со способом, описанным для детектирования антитела в Примере 18, со следующим отличием: сыворотку мышей C57BL/6 будут использовать в качестве носителя при построении калибровочных кривых и в холостых опытах. Минимальное требуемое разведение будет отличаться от Примера 18 из-за большего размера вводимой дозы; этот показатель будет определяться эмпирически.
Пример 23 - Фармакокинетическое исследование оптимизированных прототипов антител у не являющихся человеком приматов
Оптимизированные прототипы антител, в формате человеческого IgG1 с функциональным эффектором (т.е. имеющего константную область IgG1 дикого типа, SEQ ID NO: 341), вводят внутривенно 10 мг/кг самцам яванского макака, по три животных на антитело. Образцы крови берут до введения препарата и в моменты времени 2, 4, 8, 12, 24, 48, 72, 96, 192, 336, 508 и 672 часа. Готовят сыворотку и образцы замораживают до проведения анализа. Образцы будут анализировать в соответствии со способом, описанным для детектирования антитела в Примере 18. Минимальное требуемое разведение будет отличаться от Примера 18 из-за большего размера вводимой дозы; этот показатель будет определяться эмпирически.
Пример 24: Активность оптимизированного прототипа антитела в анализе мышиной гибридомы B-клеток : Т-клеток.
Антитела тестировали в анализе совместного культивирования мышиной гибридомы B-клеток : Т-клеток для оценки индукции IL-2. Гибридомные клетки В-лимфоцитов мышей LK35.2 (АТСС), трансфицированные 50 мкл человеческого PD-L1 (SEQ ID NO: 1), приготовленные в среде DMEM (Gibco), дополненной 1% фетальной бычьей сыворотки (Gibco), обрабатывали 10 мкМ пептида овальбумин323-329 (Ovalbumin323-329, Thermo Scientific) и распределяли с плотностью 2×104 клеток/лунку в обработанном 96-луночном планшете для культур тканей (Costar). Затем клетки, нагруженные пептидом овальбумина, смешивали с 50 мкл серийных разведений 1:3 анти-PD-L1 антител или анти-ICOS/PD-L1 биспецифических антител в формате mAb2 ™ от 30 нМ с 9 точками концентраций в DMEM с добавкой 1% фетальной бычьей сыворотки.
После инкубации в течение 1 ч при 37°C, 5% CO2, 100 мкл гибридомной клеточной линии мышиных Т-хелперов DO-11-10 (National Jewish Health), культивированной в течение ночи в DMEM (Gibco), дополненной 1% фетальной бычьей сыворотки (Gibco) добавляли в аналитический планшет в количестве 2×104 клеток/лунку. Совместную культуру LK35.2/DO-11-10 инкубировали в течение ночи при 37°C, 5% CO2 после чего супернатант собирали для оценки продуцирования мышиного IL-2. Клетки, обработанные 1 или 0,1× рабочим маточным раствором коктейля для стимуляции клеток (eBioscience), использовали в качестве положительного контроля для продуцирования мышиного IL-2.
Количественное определение мышиного IL-2 проводили с использованием набора ИФА для определения мышиного IL-2 Duoset (R&D Systems) в соответствии с протоколом производителя, модифицированном путем включения стрептавидина-европия в качестве реагента для детектирования (DELFIA®). Вкратце, аналитические планшеты покрывали в течение ночи при 4°C предоставленным антителом захвата, приготовленном в PBS в концентрации 1 мкг/мл. Планшеты трижды промывали PBS-Tween (0,1% об./об.) перед добавлением 200 мкл 1% мас./об. бычьего сывороточного альбумина (BSA, Sigma) в PBS в течение 1 часа при комнатной температуре. После стадии промывки, выполняемой, как описано выше, добавляли в планшеты для анализа 50 мкл клеточных супернатантов. После инкубации в течение 1 часа добавляли 50 мкл детектирующего антитела с кконцентрацией 200 мкг/мл, приготовленного в 0,1% мас./об. BSA в PBS, и планшеты инкубировали в течение еще одного часа. Планшеты промывали, как описано выше, и добавляли во все лунки на 1 час 50 мкл DELFIA® Eu-N1 стрептавидина, разбавленного 1:500 из маточного раствора в буфере для анализа DELFIA® (Perkin Elmer). Дополнительную стадию промывки проводили с использованием буфера для промывки DELFIA (0,5 М Tris HCl (Gibco), 1% об./об. Tween (Sigma)) перед добавлением 50 мкл раствора DELFIA® Enhancement Solution (Perkin Elmer). Планшет инкубировали в течение 5 минут при комнатной температуре, защищенным от света, и считывали при 615 нм, используя соответствующие настройки DELFIA® для флуоресценции с временным разрешением на планшет-ридере Envision (Perkin Elmer). Концентрацию мышиного IL-2 интерполировали по калибровочной кривой, которую строили параллельно с исследуемыми образцами. Конечные используемые для построения графика значения рассчитывали с использованием Уравнения 9, в котором фоновый сигнал рассчитывали с использованием сигнала, полученного при анализе клеток совместной культуры, обработанных 50 мкл одной лишь среды. Результаты приведены на Фигуре 23. Все антитела сильно повышают продуцирование IL-2 в данной системе совместного культивирования.

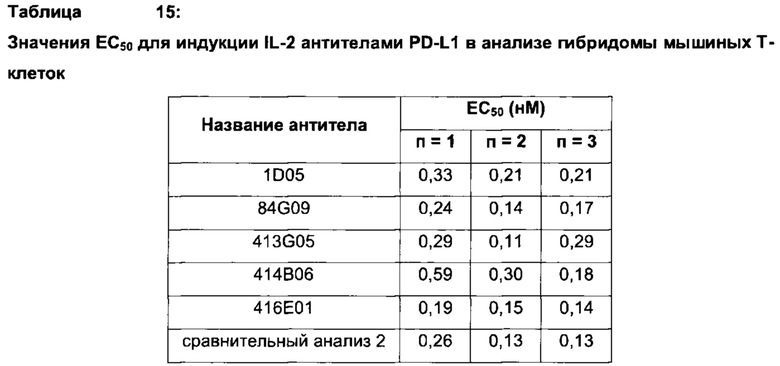
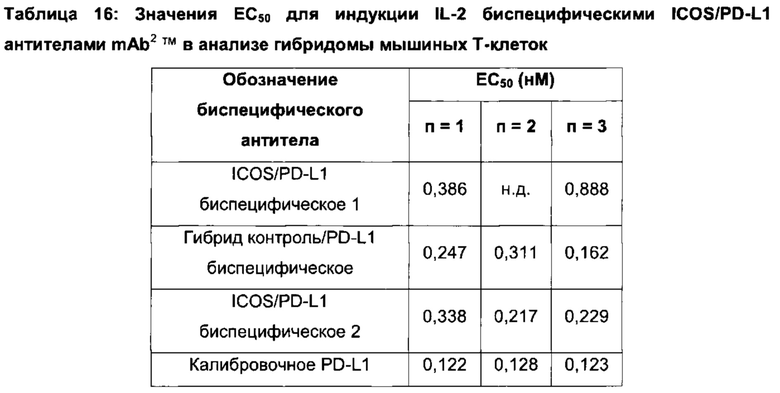
Пример 25 - Тестирование оптимизированных прототипов антитела в реакции смешанных лимфоцитов с использованием активированных дендритных клеток (DC)-Т-клеток
Моноциты были выделены из криоконсервированных РВМС путем отрицательной селекции с использованием набора для выделения моноцитов (Monocyte Isolation Kit) и системы магнитной сепарации MACS™ (Miltenyi Biotec). Моноциты ресуспендировали в среде RPMI 1640, содержащей 10% hiFBS и 100 нг/мл GM-CSF и IL-4 (оба Peprotech). Клетки культивировали в течение 5 дней в не обработанных ТС 6-луночных планшетах (Greiner), чтобы вызвать дифференцировку DC, перед добавлением 100 нг/мл липополисахарида Е. coli O55:В5 (Sigma) для активации DC. Клетки собирали после 24 часов активации и промывали один раз PBS для удаления липополисахарида (LPS) и ресуспендировали при 106/мл в RPMI 10% hiFBS. Аллогенные CD3+ Т-клетки выделяли из криоконсервированных РВМС с использованием набора для выделения суммарных Т-лимфоцитов (Pan T-Cell Isolation) и системы MACS, как указано выше, и ресуспендировали при 2×106/мл в RPMI 10% hiFBS. Последовательные разведения выбранных антител (1:3) из 10 нМ были приготовлены в RPMI 10% hiFBS и добавлены по 50 мкл в 96-луночные плоскодонные планшеты для тканевых культур (ТС) в трех повторностях. DC (100 мкл) и Т-клетки (50 мкл) добавляли в планшеты и инкубировали при 37°C, 5% CO2, в течение пяти дней. Супернатанты удаляли через три дня для измерения IL-2, и через 5 дней для измерения IFNγ. Супернатанты хранили при -20°C до использования. Продуцирование цитокинов измеряли методом DuoSet® ИФА с использованием человеческого IFNγ и IL-2 (R&D Systems), с детектированием с помощью Eu-N1-стрептавидина DELFIA®. Результаты приведены на Фигуре 24.
Пример 26 - Многодозовое исследование иммуноцитокинов на яванских макаках
Фармакология и токсичность двух иммуноцитокинов, 1D05 D9-7 ICK и 1D05 D1-8 ICK (как описано в Примере 14), будут оцениваться в многодозовом исследовании на яванских макаках. Молодым самцам обезьян вводят дозы 1 мг/кг/дозу в соответствии с двумя разными схемами: Схема 1 - животным вводят дозы в день 0 и день 14; схема 2 - животным вводят дозы в дни 0, 2, 14 и 16. В каждой группе дозирования будет по два животных, с наблюдением в течение 28 дней. Группы лечения указаны в таблице 17.


Частота сердечных сокращений, температура тела, частота дыхания и артериальное давление будут измеряться через 1 час и 4 часа после введения дозы. Вес тела будет контролироваться ежедневно. Анализ цитокинов будет проводиться в дни 2, 5, 7, 10, 14, 16, 19, 21, 24 и 28, и перед введением препарата. Гематологические измерения будут проводиться в дни 2, 5, 7, 10, 14, 16, 19, 21, 24 и 28, и перед введением препарата. Детектирование растворимого CD25 будет проводиться в дни 3, 7 и 10, 17, 21, 24, и перед введением препарата. Иммунофенотипирование будет проводиться в дни 7, 10, 14, 24 и 28, и перед введением препарата в соответствии с панелью, описанной в Примере 19. Образцы для фармакокинетического (ФК) анализа будут взяты в следующие моменты времени при каждой инфузии: перед введением препарата, в конце инфузии и через 8, 16, 24, 32, 40, 48, 72 и 96 часов.
Пример 27: Исследование эффективности иммуноцитокина в модели сингенной опухоли
Исследование эффективности будет проводиться с использованием мышиной модели опухоли СТ-26, для сравнения активности суррогатного иммуноцитокина с немодифицированным антителом, и для оценки роли эффекторной функции. В день имплантации мышам BALB/c вводят подкожными инъекциями в заднюю часть правого бока 1×105 клеток СТ-26/животное. Группы лечения получат свою первую дозу антитела или соответствующий контроль (все - внутрибрюшинно по 10 мг/кг) через 6 дней после имплантации опухолевых клеток и дозы будут вводиться три раза в неделю в течение двух недель. Развитие опухоли будет контролироваться три раза в неделю с использованием штангенциркуля с цифровой индикацией, с измерениями в двух направлениях, до конца исследований. Объемы опухолей (мм3) будут оцениваться по стандартной формуле (L×W2)/2 (где L обозначает больший диаметр, и W - меньший диаметр опухоли). Мыши будут участвовать в исследованиях, пока их опухоли не вырастут до среднего диаметра 12 мм, или до достижения ими одной из конечных точек умерщвления из соображений гуманности, описанных в протоколе исследования. Статистика конечных точек умерщвления из соображений гуманности будет рассчитываться с использованием метода Каплана-Мейера в прикладной программе Prism.

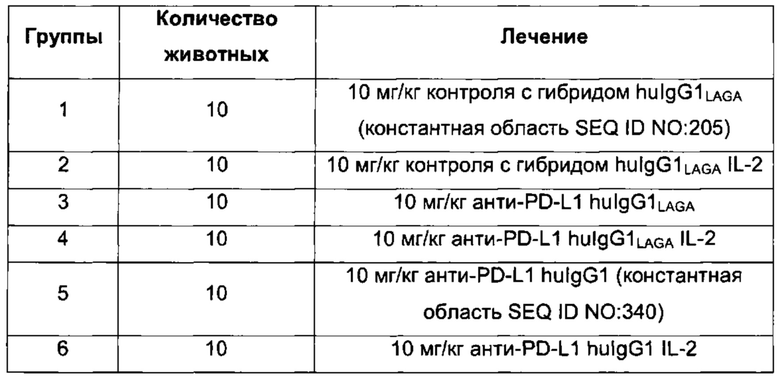
Пример 28: Исследования эффективности иммуноцитокина в модели ксенотрансплантата Т-клеток : клеточной линии меланомы
Исследования эффективности будут проведены с использованием модели ксенотрансплантата Т-клеток : клеточной линии А375 у мышей NOD/SCID с использованием уточненных методов, описанных R. Stewart et al. Вкратце, положительных по HLA-A2 доноров селектируют окрашиванием цельной крови с использованием меченого РЕ антитела против человеческого HLA-A2 (Biolegend), с последующим лизисом эритроцитов и анализом методом проточной цитометрии. Затем будут выделены первичные человеческие CD4+ и CD8+ Т-клетки с использованием набора EasySep для обогащения CD4+ или CD8+ Т-клеток человека (Stemcell Technologies, № кат. 19052/3). Затем клетки CD4+ и CD8+ культивируют отдельно в течение 20 дней на монослое клеток А375, обработанных митомицином С, в присутствии IL-2 и IL-7. Т-клетки наносят на свежий питающий подслой А375 на 10-й день. На 20-й день клетки криоконсервируют и хранят в жидком азоте до момента использования. За день до имплантации Т-клетки оттаивают и культивируют в среде плюс цитокины в течение ночи. В день имплантации CD4+ и CD8+ клетки подсчитывают и смешивают вместе в соотношении 1:1. Т-клетки смешивают со свежими опухолевыми клетками А375 в соотношении 1:6 и вводят мышам подкожно в заднюю часть правого бока. Экспериментальным группам будут введены дозы антитела, иммуноцитокина или соответствующего контроля (все - внутрибрюшинно в дозе 10 мг/кг) через час после имплантации Т-клеток и опухолевых клеток. Развитие опухоли будет контролироваться три раза в неделю с использованием штангенциркуля с цифровой индикацией, с измерениями в двух направлениях, до конца исследований. Объемы опухолей (мм3) будут оцениваться по стандартной формуле (L×W2)/2 (где L обозначает больший диаметр, а W - меньший диаметр опухоли). Мыши будут участвовать в исследованиях, пока их опухоли не вырастут до среднего диаметра 12 мм, или до достижения ими одной из конечных точек умерщвления из соображений гуманности, описанных в протоколе исследования. Статистика конечных точек умерщвления из соображений гуманности будет рассчитываться с использованием метода Каплана-Мейера в прикладной программе Prism. Этот подход будет использоваться для определения того, какое лечение связано с улучшенной выживаемостью. Последующие исследования будут сравнивать конструкты иммуноцитокина с различными активностями IL-2.
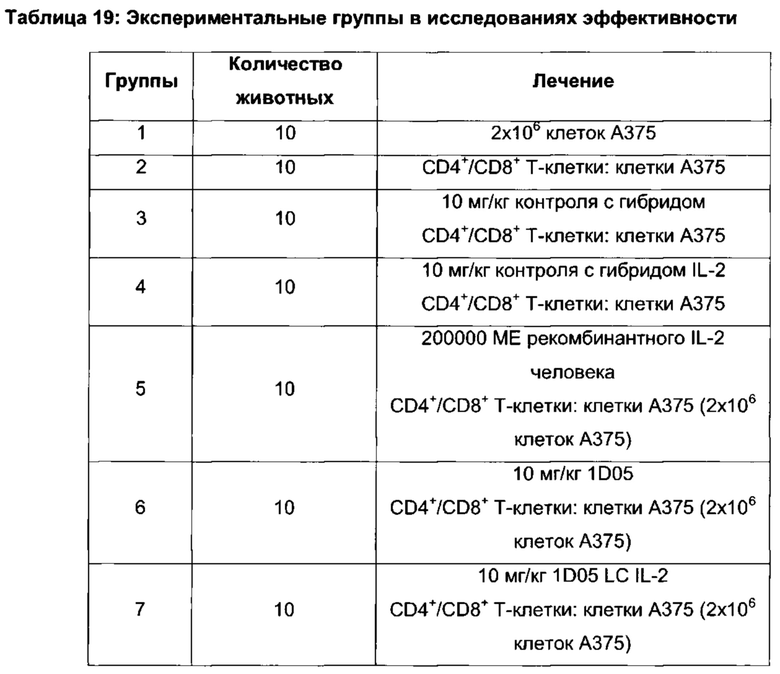
Пример 29: Активность оптимизированных прототипов антитела в репортерном анализе эффекторной функции
Активность антителозависимой клеточно-опосредованной цитотоксичности (ADCC) отобранных антител оценивали с использованием ADCC Reporter Bioassay. Клетки ES2 (АТСС CRL-1978), эндогенно экспрессирующие PD-L1 человека, инкубировали совместно с эффекторными клетками (генетически модифицированные клетки Jurkat, стабильно экспрессирующие рецептор FcγRIIIa человека - V158, Promega), которые продуцируют люциферазу зависимым от концентрации образом в присутствии задействованного в ADCC (ADCC-enabled) антитела. Активность растворимой люциферазы оценивают путем измерения люминесценции, продуцируемой при превращении люциферазой люминогенного субстрата в люминесцентный продукт.
Непосредственно перед анализом клетки-мишени (ES2) центрифугировали и ресуспендировали в RPMI 1640+10% Ultra low IgG FBS (фетальная бычья сыворотка с ультранизким содержанием IgG) (Thermo Fisher Scientific) и высевали по 30000 клеток/лунку (10 мкл/лунку) в 384-луночные планшеты с белым дном. Репортерные (эффекторные) клетки Jurkat NFAT люциферазы ресуспендировали в RPMI 1640+10% Ultra low IgG FBS и добавляли к клеткам-мишеням в количестве 10000 клеток на лунку (10 мкл/лунку). Готовили одиннадцать трехкратных серийных разведений антител из 2,2 нМ в RPMI 1640+10% Ultra low IgG FBS и добавляли к клеткам-мишеням (10 мкл/лунку). Планшеты инкубировали в течение ночи при 37°C, 5% CO2, после чего люминогенный субстрат BioGlo добавляли непосредственно в лунки (30 мкл/лунку) и люминесценцию измеряли количественно на планшет-ридере Envision (Perkin Elmer).
Значения относительных световых единиц (ОЕЛ) из исходных данных (показания Envision) были нормированы по «Кратности индукции» с использованием следующего уравнения:
Уравнение 10:

Данные наносились на график в программе GraphPad Prism с использованием 4-параметрической логистической аппроксимации, а репрезентативный эксперимент показан на Фигуре 34. Результаты приведены в Таблице 20. Все тестируемые антитела индуцировали люминесценцию, что позволяет предположить, что всех они способны индуцировать уничтожение клеток-мишеней по механизму ADCC. Хотя EC50 обычно имеют схожие значения, 416Е01 индуцирует наибольший максимальный уровень люминесценции.
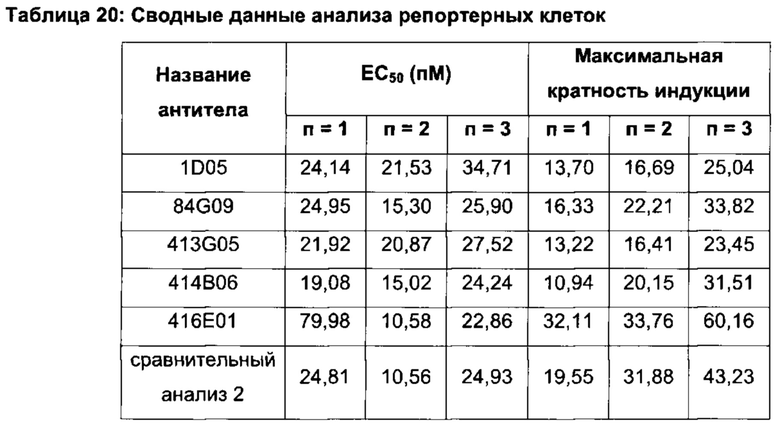
Пример 30: Связывание оптимизированных прототипов антитела с клеточно экспрессируемым PD-L1 яванского макака
Клетки CHO-S, трансфицированные PD-L1 яванского макака, разводили в буфере FACS (PBS + 1% мас./об. BSA + 0,1% мас./об. азида натрия) и распределяли на 96-луночном планшете с V-образными лунками (Greiner) при плотности 1×105 клеток на лунку. Готовили титрования антител из рабочей концентрации 133 нМ в виде серийных разбавлений в соотношении 1/3 в буфере FACS. Планшеты центрифугировали при 300×g в течение 3 минут и супернатант удаляли аспирацией. Добавляли к клеткам 50 мкл на лунку титрованных антител и инкубировали при 4°C в течение 1 часа. Клетки промывали 150 мкл PBS и центрифугировали при 300 g в течение 3 минут. Супернатант удаляли аспирацией и добавляли 150 мкл PBS на лунку. Эта стадия промывки повторялась. Присутствие связанного антитела детектировали путем добавления 50 мкл на лунку анти-человеческого IgG AlexAFIuor 647 (Jackson ImmunoResearch), разбавленного 1/500 в буфере FACS. Клетки инкубировали в течение 1 часа при 4°C в темноте. Клетки промывали, как описано выше. Для фиксации клеток добавляли 50 мкл на лунку 4% об./об. параформальдегида и клетки инкубировали в течение 20 минут при 4°С, осадок клеток собирали центрифугированием при 300×g и планшеты ресуспендировали в 75 мкл PBS. Геометрическое среднее измеряли методом проточной цитометрии с использованием прибора Beckman Coulter CytoFLEX. Alexa Fluor 647 возбуждали лазером с длиной волны 637 нм и детектировали в канале Red (красном) с полосовым фильтром 660/20. Данные были проанализированы с использованием программного обеспечения FlowJo и показаны на Фигуре 35. Все антитела связываются с PD-L1 яванского макака, экспрессируемым на клетках.
Пример 31: Связывание с экспрессируемым СНО hPD-L1 и нейтрализация связывания hPD-L1 с PD-1 и CD80
Клетки СНО, не трансфицированные (обозначаемые как WT (дикий тип)) или трансфицированные hPD-L1, экспрессирующие рекомбинантный PD-L1 человека, разводили в буфере FACS (PBS, 1% BSA, 0,1% азида натрия) и распределяли на трех 96-луночных планшетах с V-образными лунками (Greiner) при плотности 1×105 клеток на лунку. Клетки промывают 150 мкл PBS и центрифугируют при 300 g в течение 3 минут. Супернатант удаляют аспирацией и добавляют 150 мкл PBS. Эту стадию промывки повторяют.
Для планшета 1 (связывание PD-L1), титрованные оптимизированный прототип антитела, эталонное антитело или контрольное антитело готовили из рабочей концентрации 150 нМ в виде серийных разбавлений 1/3 в буфере FACS. 50 мкл антитела, разведенного в буфере FACS, добавляют к промытым клеткам и инкубируют при 4°C в течение 60 минут. Добавляют 150 мкл буфера FACS и клетки промывают, как описано выше. Для детектирования связывания антител против PD-L1, анти-человеческий РЕ (Jackson ImmunoResearch) разбавляют 1/500 в буфере FACS и 50 мкл этой смеси добавляют к клеткам. Клетки инкубируют при 4°C в течение 60 минут. Клетки дважды промывают 150 мкл буфера FACS, центрифугируют при 300 g в течение 3 минут после каждой стадии промывки и аспирации супернатанта. Клетки фиксируют добавлением 100 мкл 4% параформальдегида и инкубацией в течение 30 мин при 4°C. Клетки промывают один раз, как описано выше, и ресуспендируют в 100 мкл буфера FACS для анализа. Интенсивность сигнала PE (среднее геометрическое) измеряют методом проточной цитометрии с использованием прибора Beckman Coulter Cytoflex. Строят графики зависимостей для средних геометрических значений без дополнительных расчетов.
Для планшета 2 (нейтрализация PD-1) биотинилированный PD-1-Fc человека (внутренний экспрессированный, SEQ ID NO: 6) готовили путем титрования из конечной аналитической концентрации 1 мкМ (FAC) в виде серийных разведений 1/2 в буфере FACS. Титрованные образцы оптимизированного прототипа антитела, эталонного антитела или контрольного антитела готовили из рабочей концентрации 300 нМ, 150 нМ FAC, в виде серийных разбавлений 1/3 в буфере FACS. Биотинилированный PD-1 разводили в буфере FACS до рабочей концентрации 60 нМ, 30 нМ FAC. 25 мкл PD-1 и 25 мкл раствора антитела (или 50 мкл титрованного PD1) добавляли к клеткам и инкубировали при 4°C в течение 1 часа. Биотинилирование проводили самостоятельно с использованием набора для конъюгации Lightning Link (Innova Biosciences) в соответствии с инструкциями производителя. Добавляют 150 мкл буфера FACS и клетки промывают, как описано выше. Для детектирования биотинилированного PD-1, стрептавидин-Alexa Fluor 647 (AF647, Jackson ImmunoResearch) разбавляют 1/500 в буфере FACS и добавляют 50 мкл этой смеси к клеткам. Клетки инкубируют при 4°C в течение 60 минут. Клетки дважды промывают 150 мкл буфера FACS, центрифугируют при 300 g в течение 3 минут после каждой стадии промывки и аспирации супернатанта. Клетки фиксируют, промывают и ресуспендируют для анализа, как описано выше. Интенсивность сигнала АРС (среднее геометрическое) измеряют методом проточной цитометрии с использованием прибора Beckman Coulter CYTOFLEX. Для построения графиков данные выражают в процентах связывания рецептора.
Для планшета 3 (нейтрализация CD80) биотинилированный человеческий CD80 (меченый Fc, R&D Systems, 140-В1) готовят титрованием из конечной концентрации анализа 1 мкМ (FAC), серийными разведениями 1/2 в буфере FACS. Титрованные образцы оптимизированного прототипа антитела, эталонного антитела или контрольного антитела готовили из рабочей концентрации 300 нМ, 150 нМ FAC, в виде серийных разбавлений 1/3 в буфере FACS. Биотинилированный CD80 разбавляли в буфере FACS до рабочей концентрации 60 нМ, 30 нМ FAC. К клеткам добавляли 25 мкл CD80 и 25 мкл раствора антитела (или 50 мкл титрованного CD80) и инкубировали при 4°C в течение 1 часа. Все остальные стадии выполняют так же, как для планшета 2.
Уравнение 11: Процент связывания рецептора (проточная цитометрия)
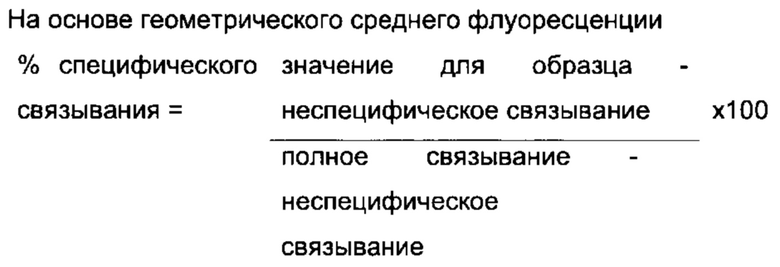
Полное связывание = только биотинилированный PD-1 или CD80 (контроль с гибридом при 150 нм FAC)
Неспецифическое связывание = отсутствие связывания PDL1 (калибровочное значение 2 при 150 нм FAC)
Результаты приведены на Фигуре 36 и в Таблице 21. Все оптимизированные прототипы антител нейтрализуют взаимодействия PD-L1 как с PD-1, так и с CD80.
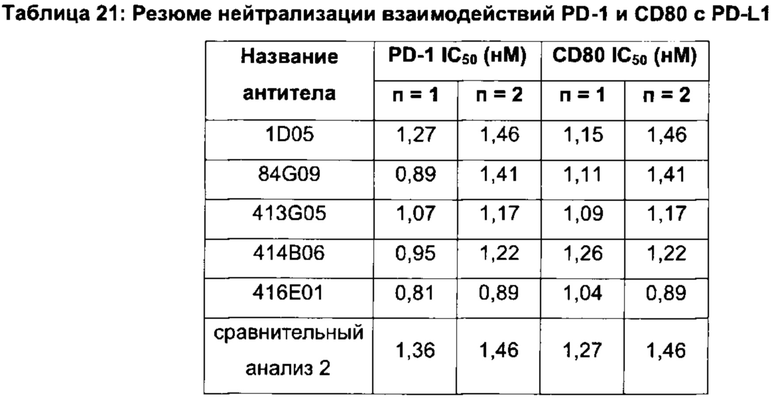
Пример 32: Эффекторная функция оптимизированных прототипов антитела в анализе ADCC первичных NK-клеток
Активность антител по уничтожению клеток-мишеней PD-L1 через ADCC (антителозависимую клеточно-опосредованную цитотоксичность) измеряется с помощью анализа ДНК цитотоксичности DELFIA (Perkin Elmer) с использованием первичных NK-клеток человека в качестве эффекторов и ES2 в качестве клеток-мишеней PD-L1+.
Этот метод основан на загрузке клеток-мишеней ацетоксиметиловым эфиром лиганда, усиливающего флуоресценцию (BATDA), который быстро проникает через клеточную мембрану. Внутри клетки сложноэфирные связи гидролизуются с образованием гидрофильного лиганда (TDA), который уже не проходит через мембрану. После цитолиза лиганд высвобождается и может детектироваться путем добавления европия, который образует с BATDA высокофлуоресцентный и стабильный хелат (EuTDA). Измеренный сигнал напрямую коррелирует со степенью клеточного лизиса.
Клетки ES2 ресуспендируют при 106/мл в среде для анализа (RPMI + 10% FBS с ультранизким содержанием IgG (Gibco)) и нагружают 5 мкл/мл реагента BATDA (Perkin Elmer) в течение 30 мин при 37°C. Клетки затем промывают 3 раза 50 мл PBS (300×g в течение 5 мин) и ресуспендируют при 8×105/мл в среде для анализа, дополненной 2 мМ пробенецида (Life technologies), чтобы уменьшить спонтанное высвобождение BATDA клетками. Супернатант клеток ES2 немедленно после последнего ресуспендирования в среде для анализа используют в качестве фонового контроля.
Готовят семь серийных трехкратных разведений антител PD-L1 и изотипического контроля в среде для анализа + 2 мМ пробенецида из 4 мкг/мл (4× конечная концентрация). NK-клетки выделяют методом отрицательной селекции из свежих МКПК с использованием набора для выделения NK-клеток человека (Human NK Cell Isolation Kit, Miltenyi Biotec) в соответствии с инструкциями производителя и ресуспендируют при 4×106/мл в среде для анализа + 2 мМ пробенецида. В каждую лунку добавляют 50 мкл разбавленного антитела (Ab), 50 мкл клеток-мишеней, нагруженных BATDA, 50 мкл NK-клеток и 50 мкл среды для анализа + 2 мМ пробенецида (конечный объем 200 мкл/лунку), для получения соотношения эффектор : мишень 5:1. Лунки, содержащие только клетки ES или клетки ES2 + буфер для лизиса DELFIA (Perkin Elmer), используются для определения спонтанного и максимального высвобождения, соответственно.
Клетки инкубируют при 37°C, 5% CO2, в течение 4 часов перед центрифугированием планшетов в течение 5 мин при 500×g и переносе 50 мкл бесклеточного супернатанта в микротитровальные планшеты DELFIA (Perkin Elmer). К супернатантам добавляют 200 мкл раствора европия DELFIA Europium (Perkin Elmer) и инкубируют в течение 15 мин при комнатной температуре. Затем флуоресцентный сигнал определяют количественно с помощью планшет-ридера EnVision (PerkinElmer).
Фоновые значения вычитают из всех экспериментальных значений. Удельное высвобождение рассчитываются по следующему уравнению:
Уравнение 12:

Включение посредством ссылок
Все источники, упоминаемые в данном документе, включая патенты, патентные заявки, статьи, руководства и т.п., а также приведенные в них ссылки, включены в данный документ посредством ссылок в той мере, в которой они еще не были включены, в полном объеме.
Эквиваленты
Вышеприведенное письменное описание изобретения считается достаточным для того, чтобы позволить специалисту в данной области техники реализовать изобретение. В приведенном выше описании и Примерах подробно описаны некоторые предпочтительные варианты реализации изобретения. Следует принимать во внимание, однако, что изобретение может быть осуществлено на практике многими способами, и изобретение должно толковаться в соответствии с прилагаемой формулой изобретения и любыми ее эквивалентами.
Следует понимать, что конкретные конфигурации, аспекты, примеры, положения и варианты реализации, раскрытые в данном документе, приведены в качестве иллюстрации, а не как ограничения изобретения. Любая часть данного описания может быть скомбинирована с любой другой частью описания, если иное не следует из контекста.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
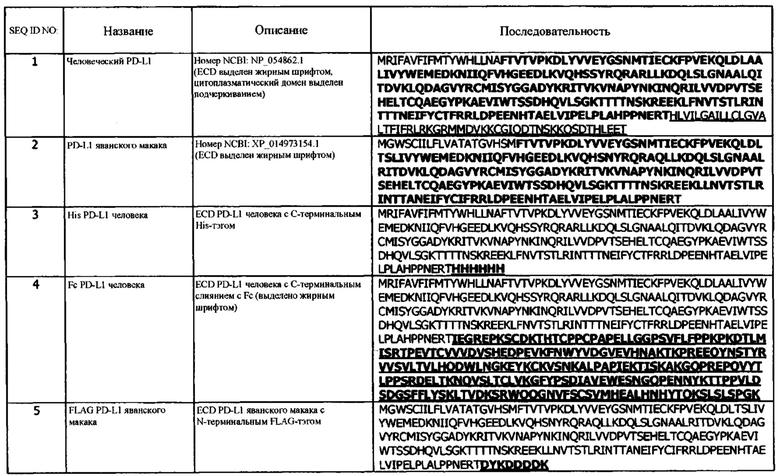
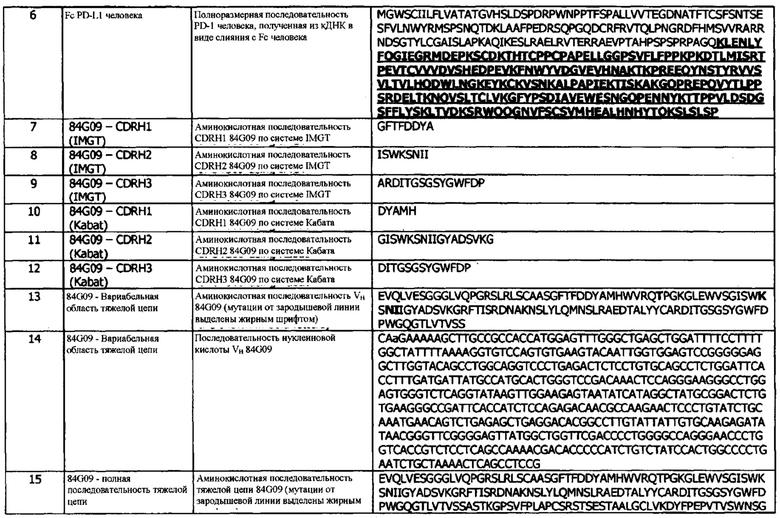
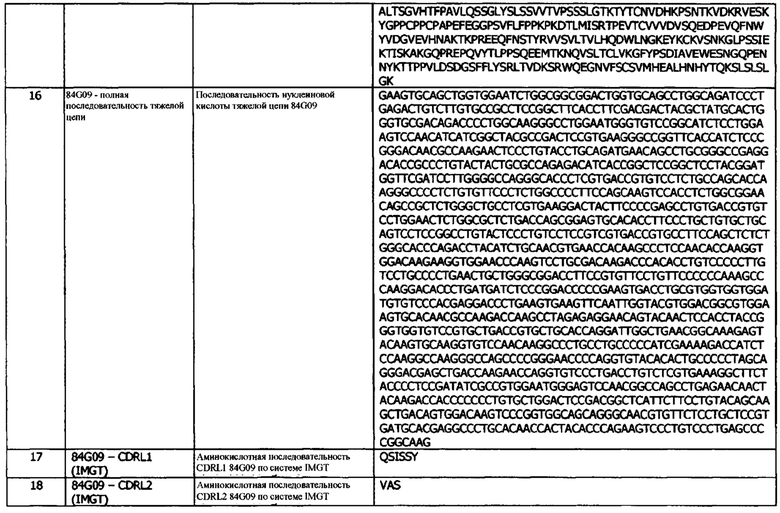
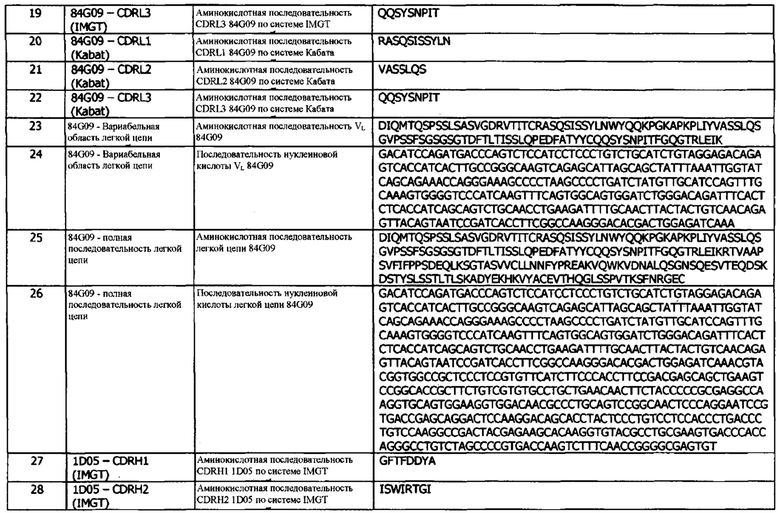
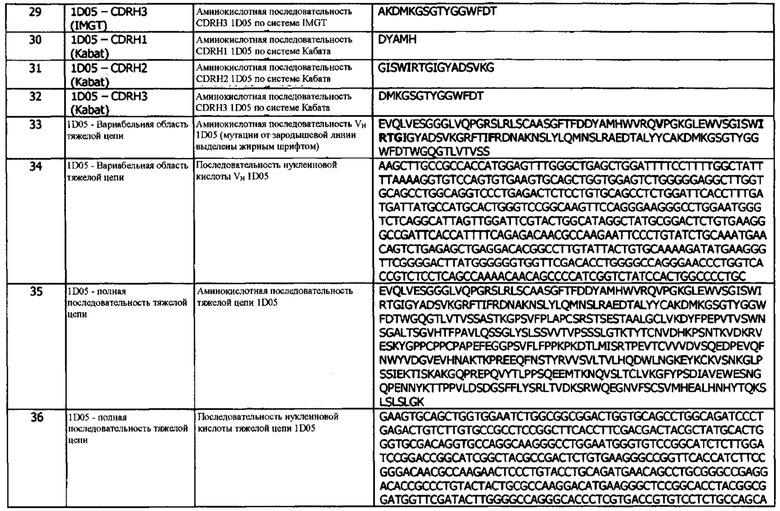
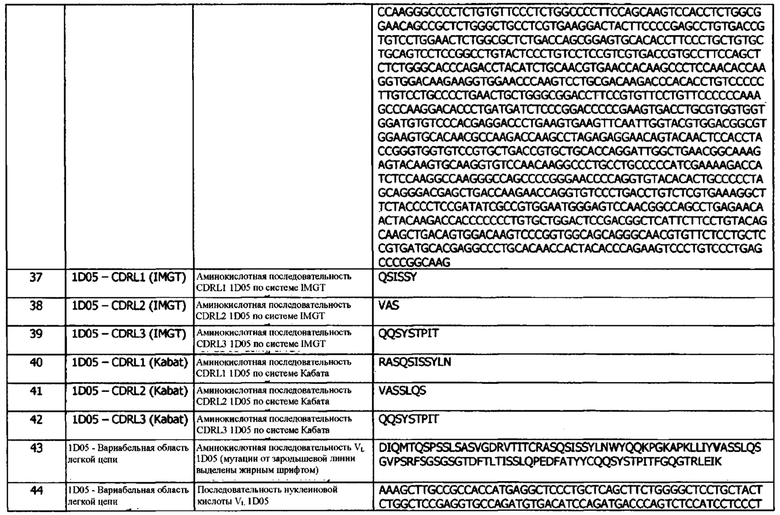
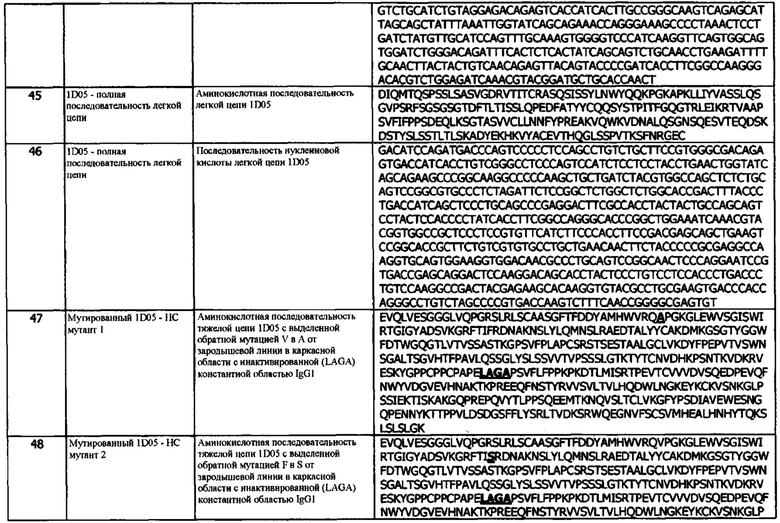
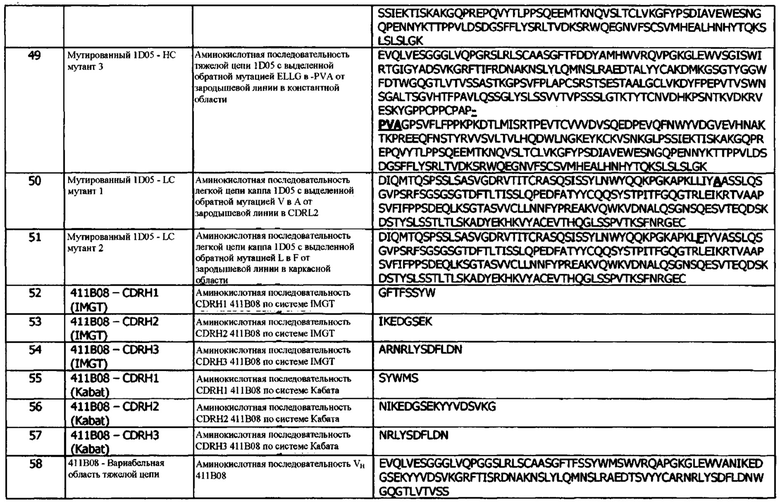
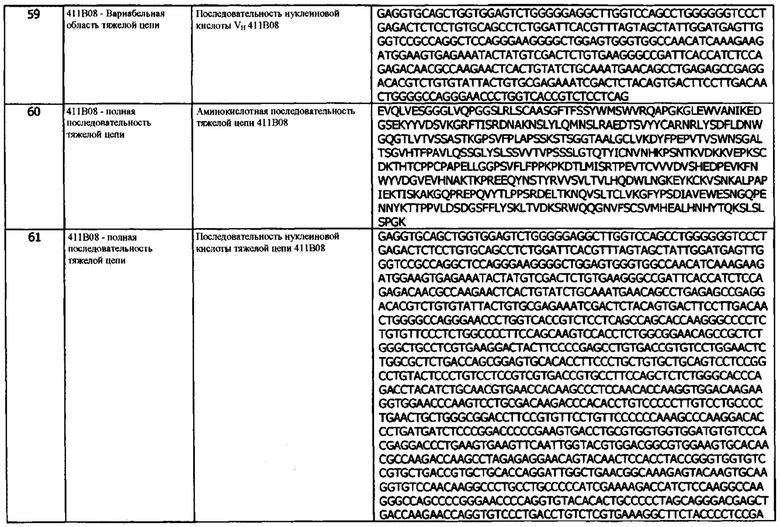
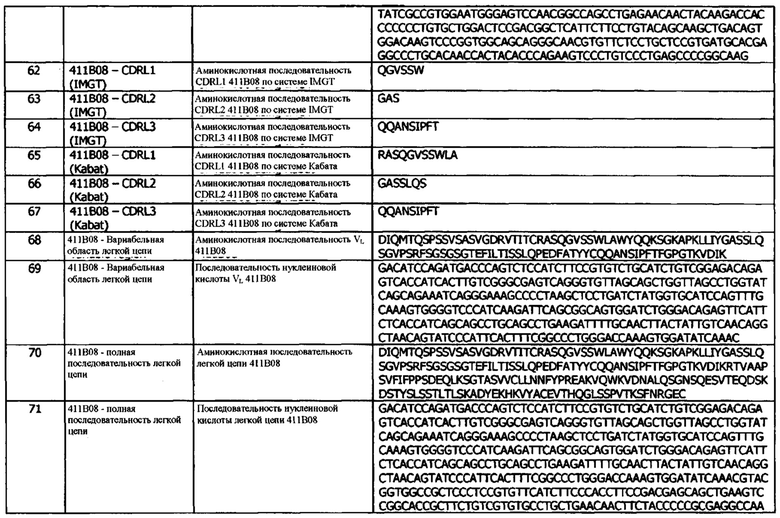
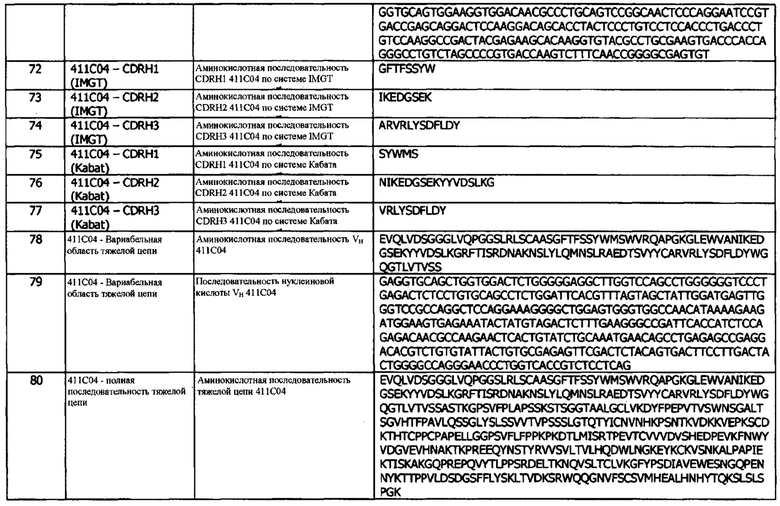

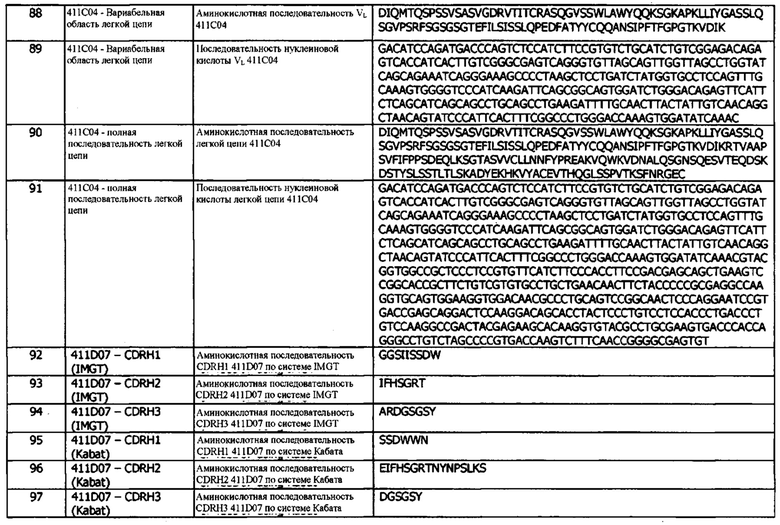
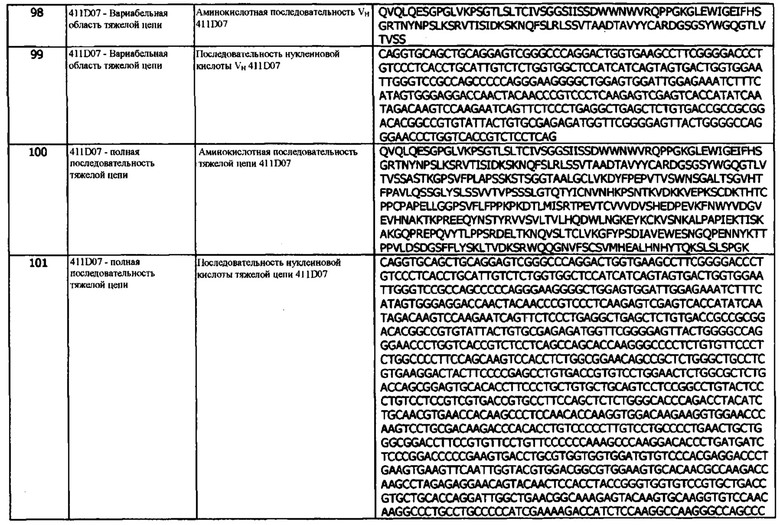
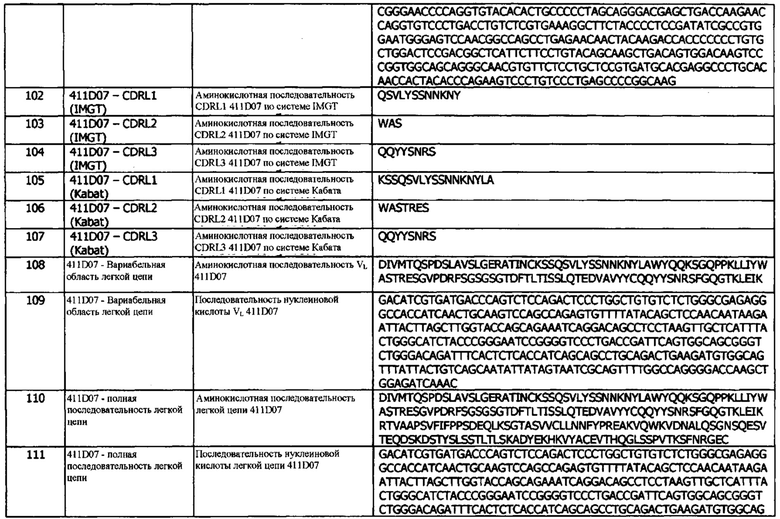
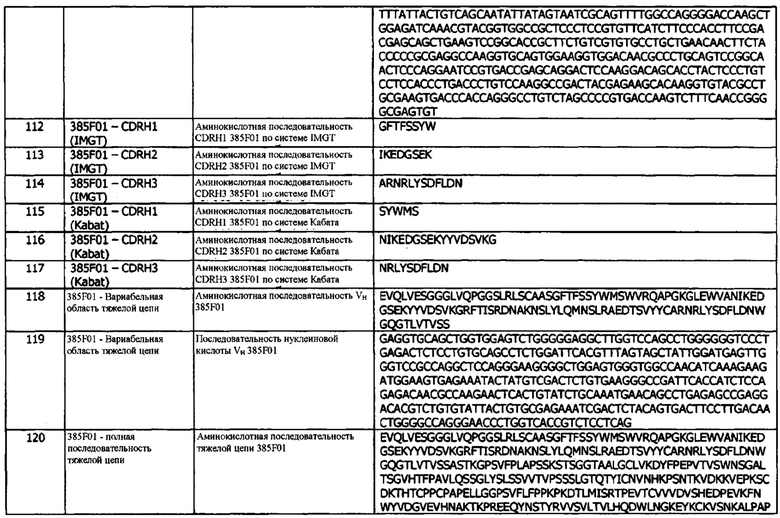
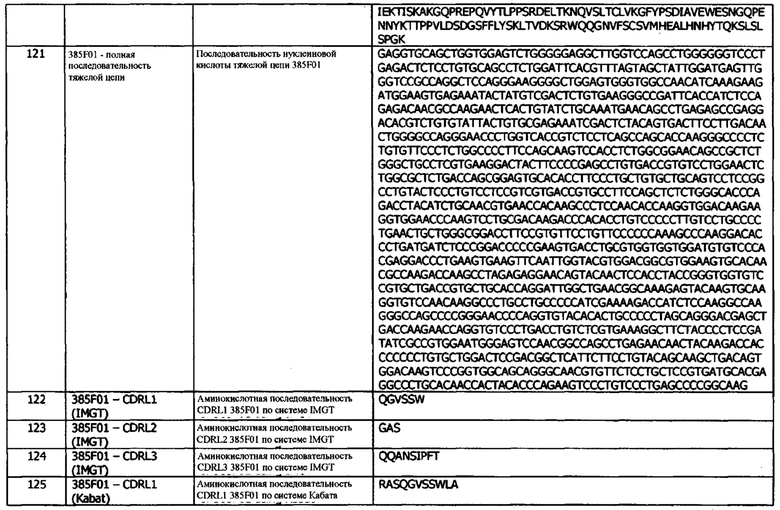
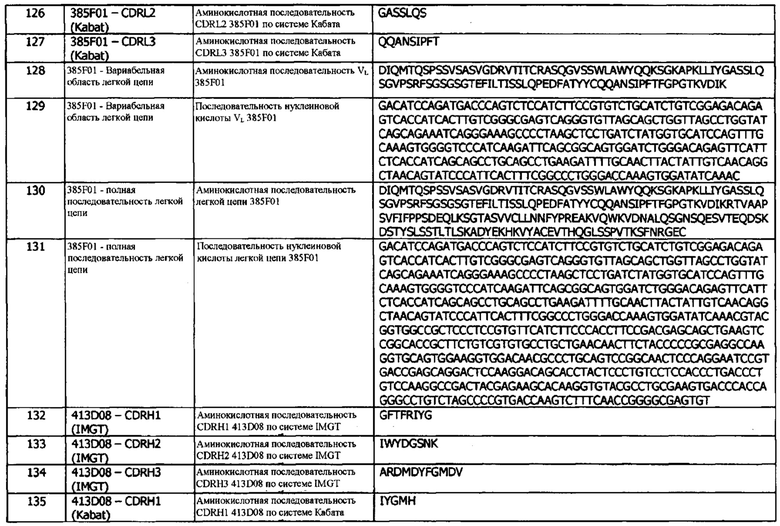
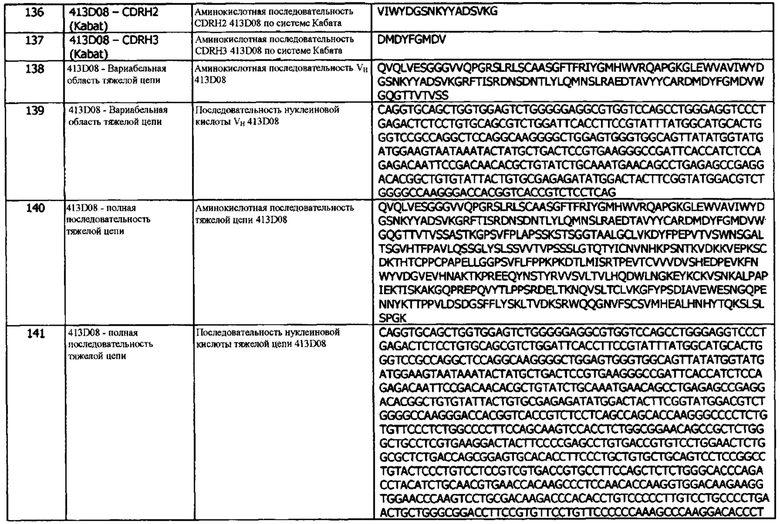
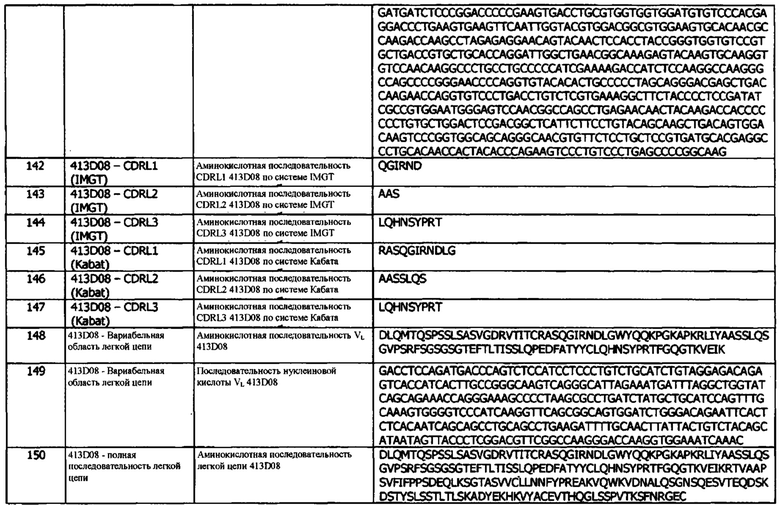
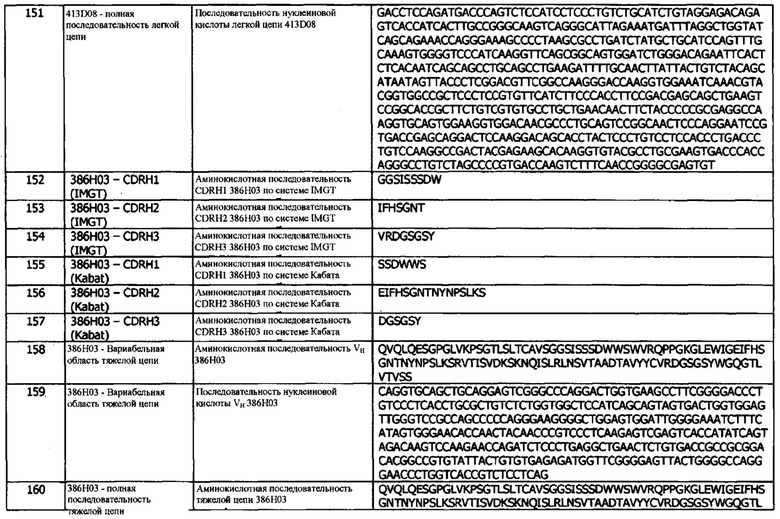
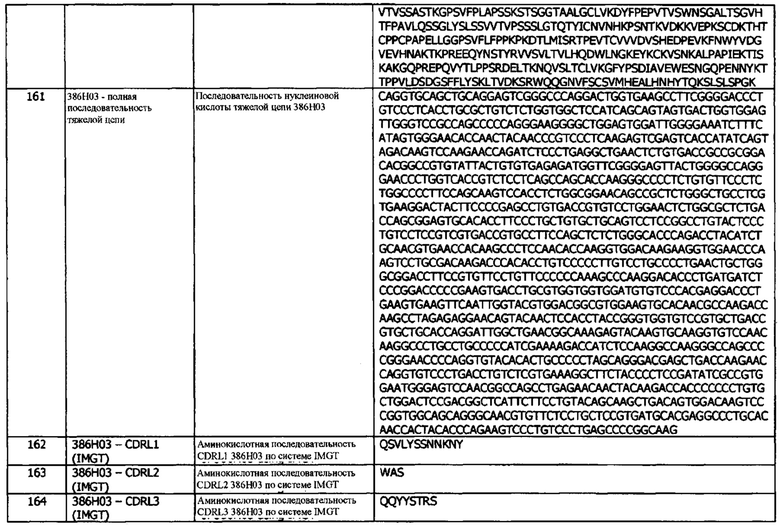
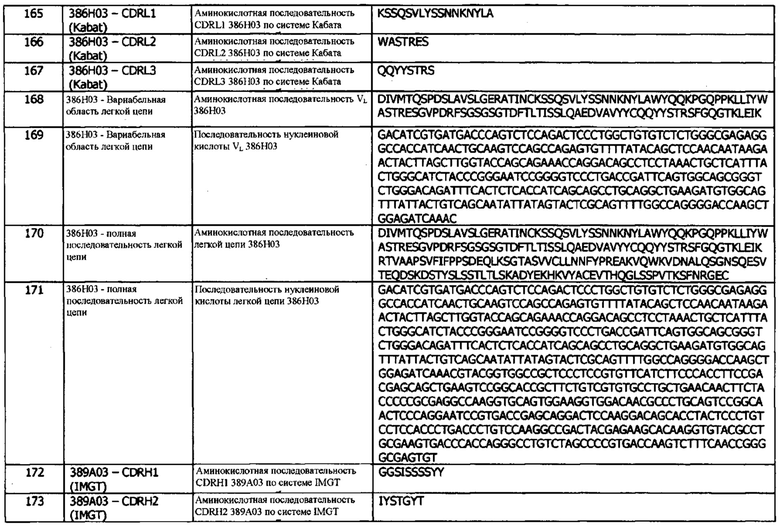
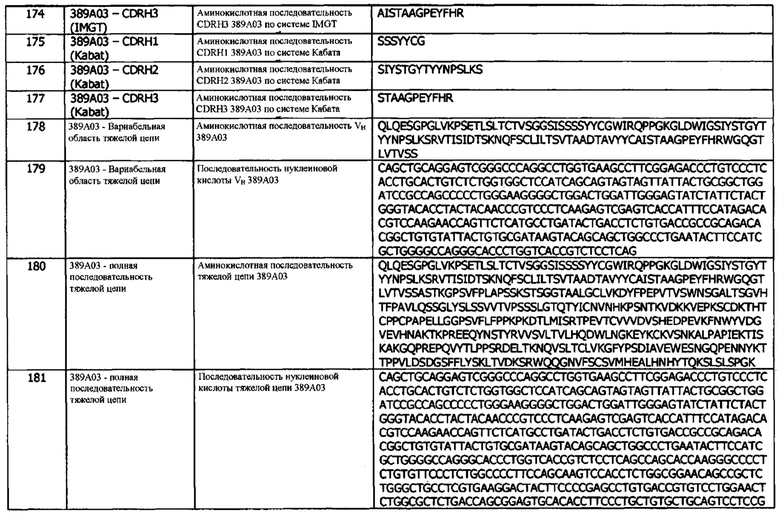
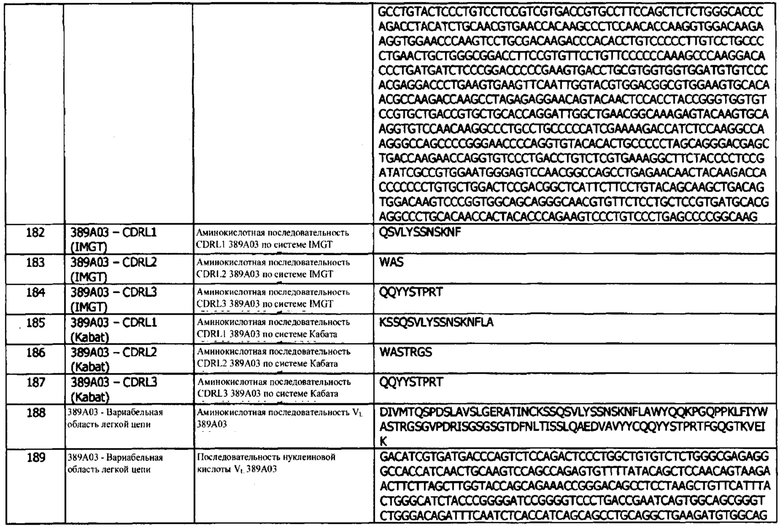
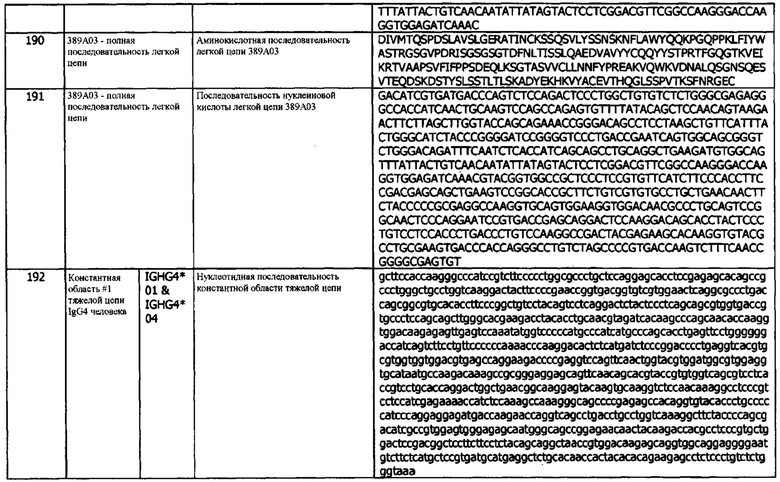
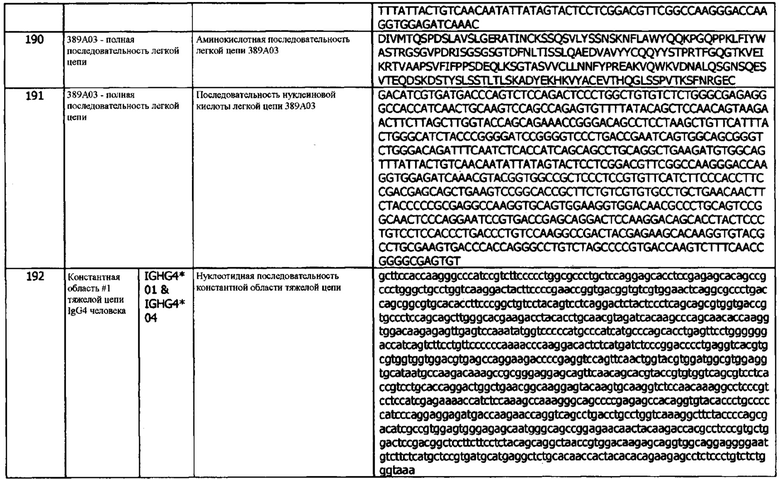
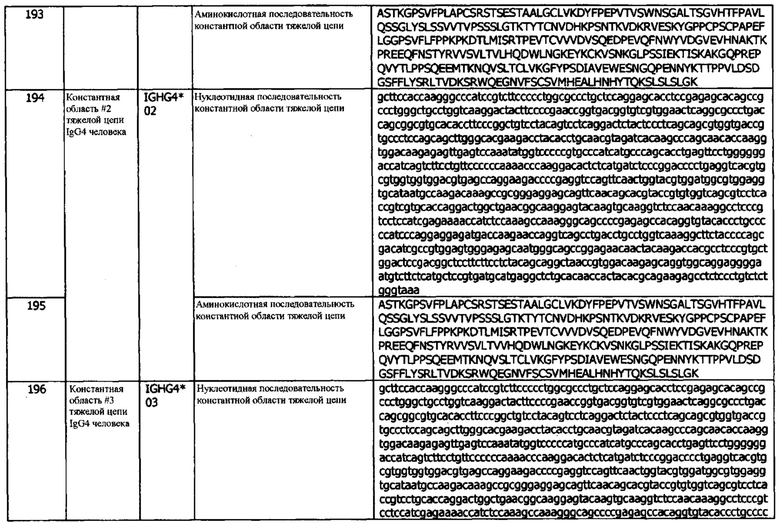
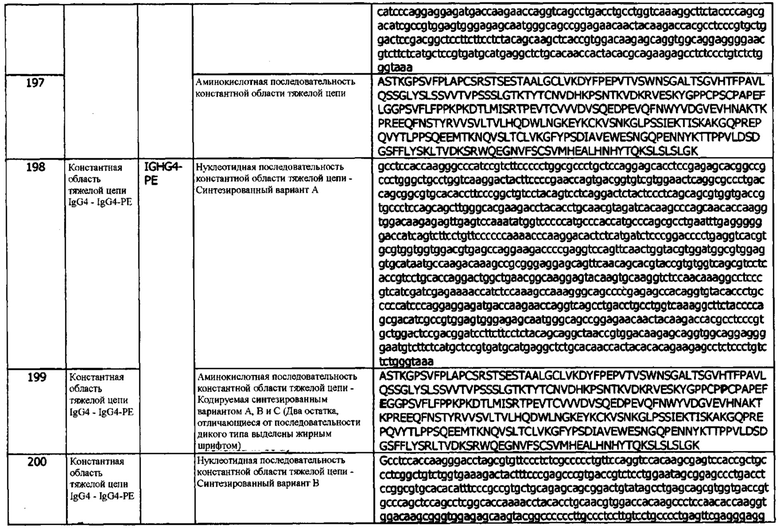
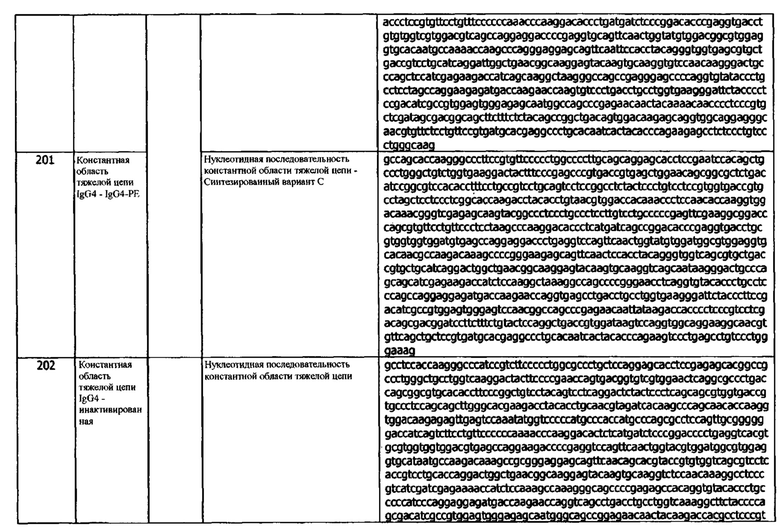
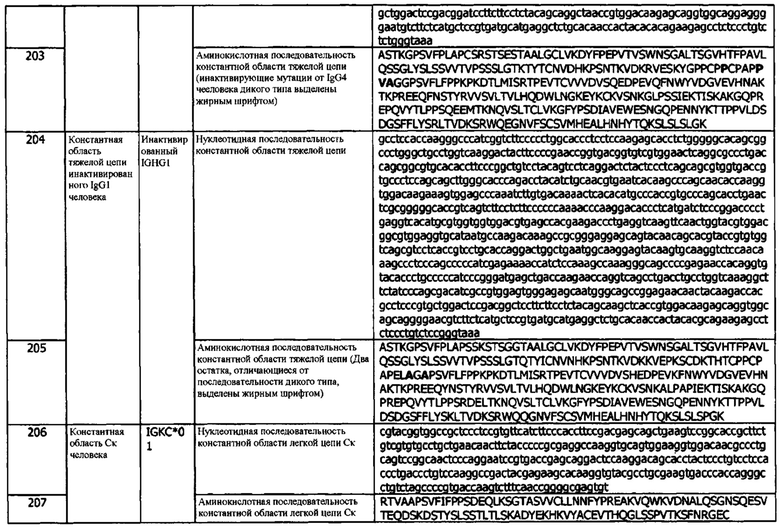
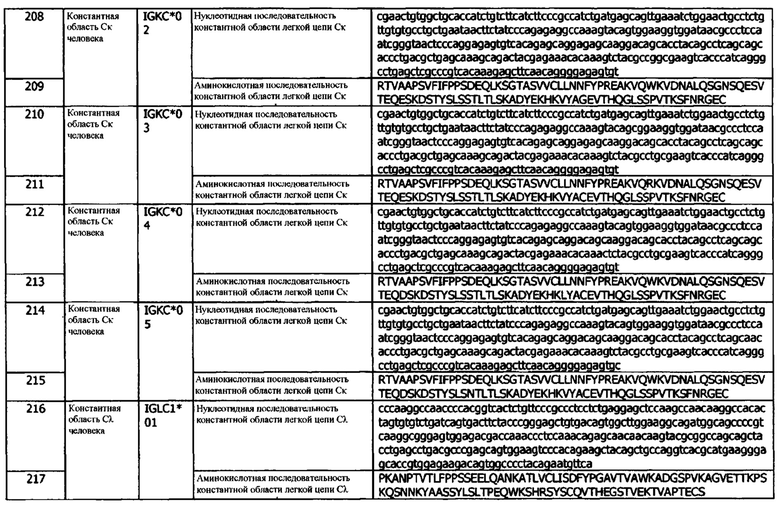
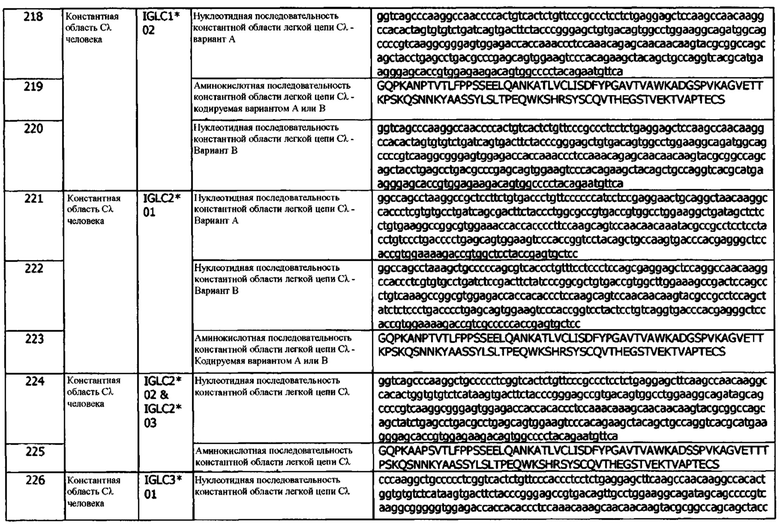

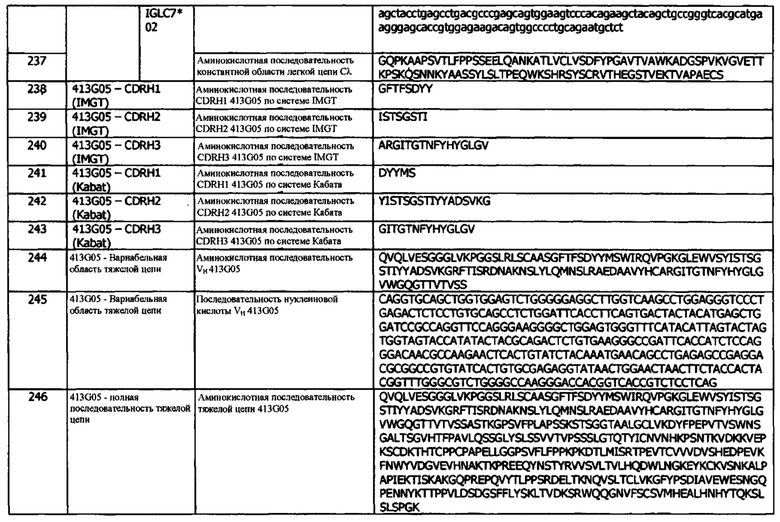

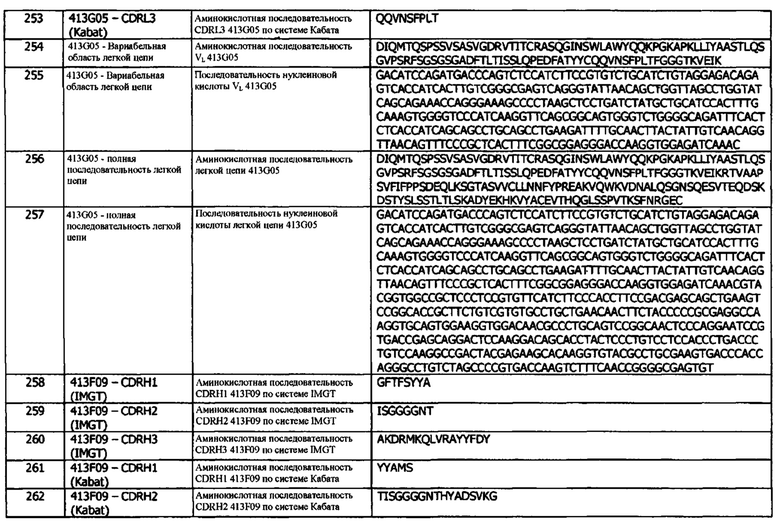
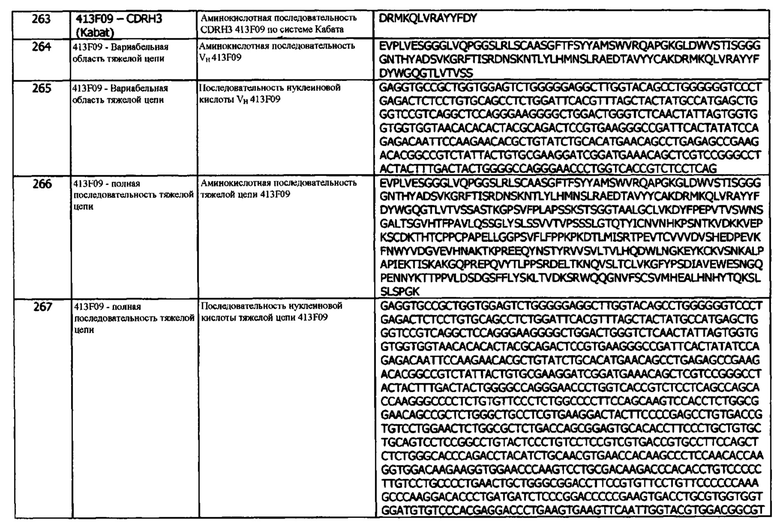
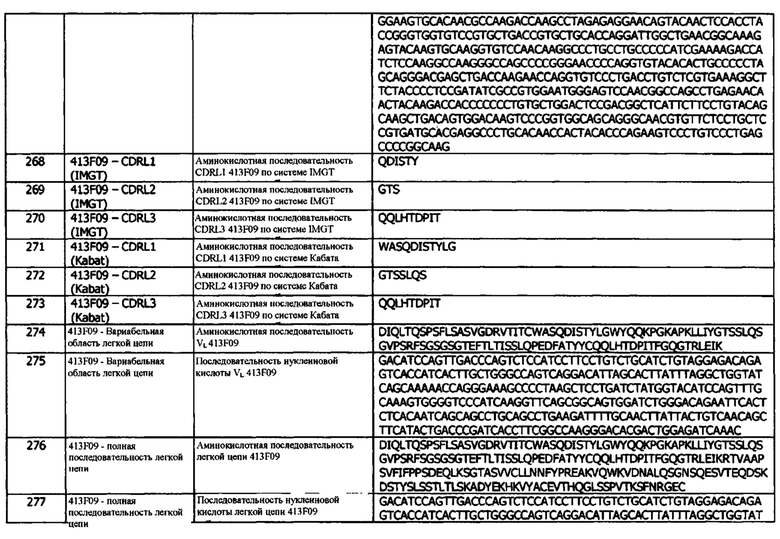
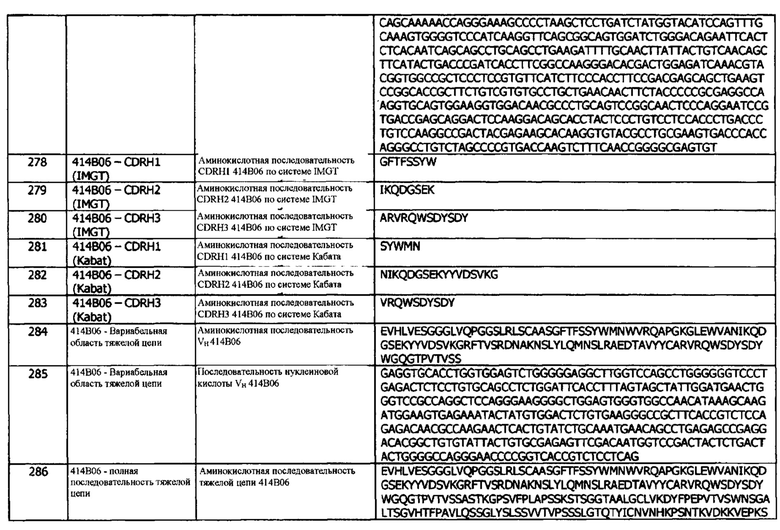
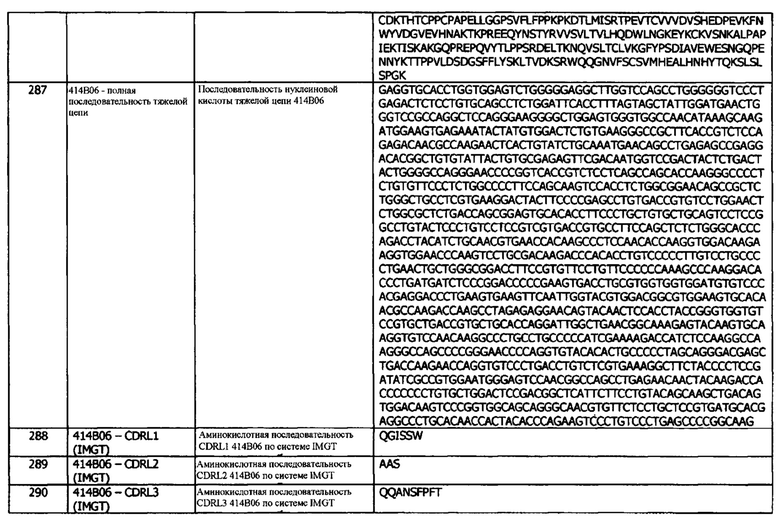
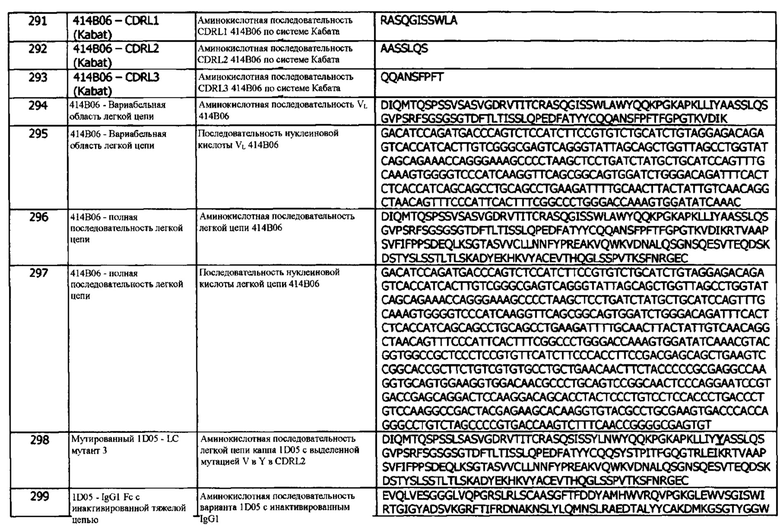
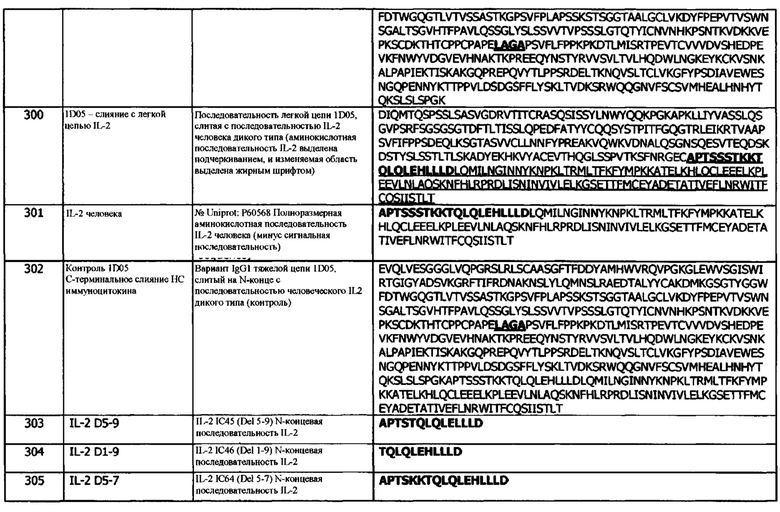
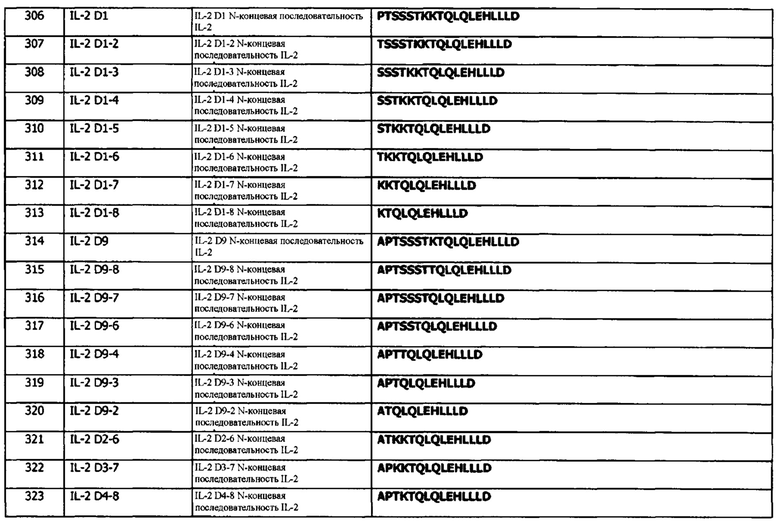
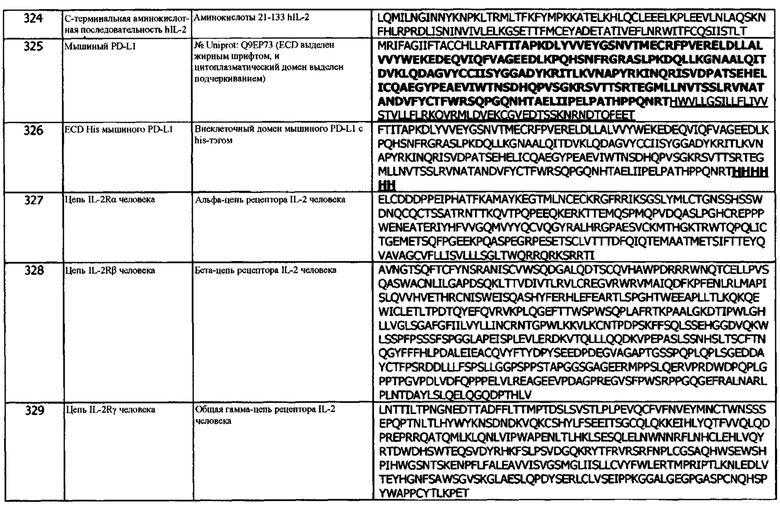
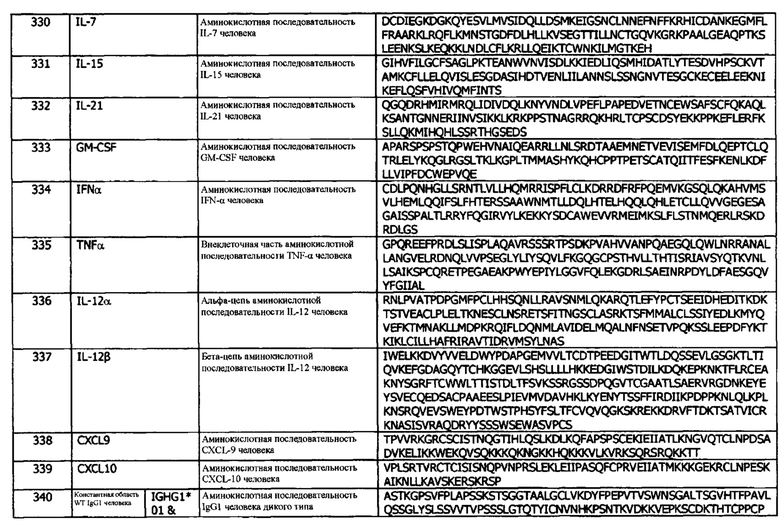

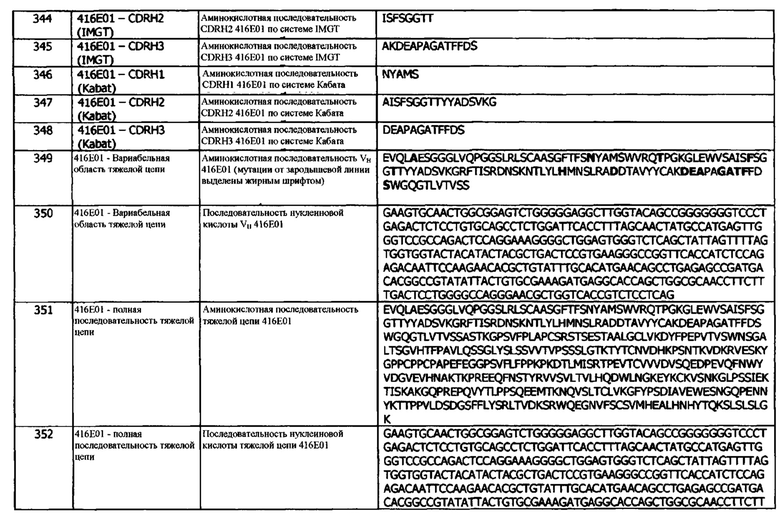

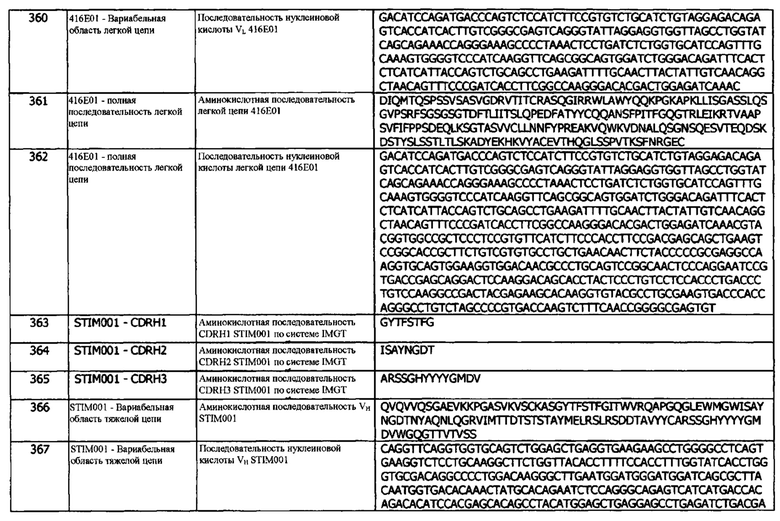

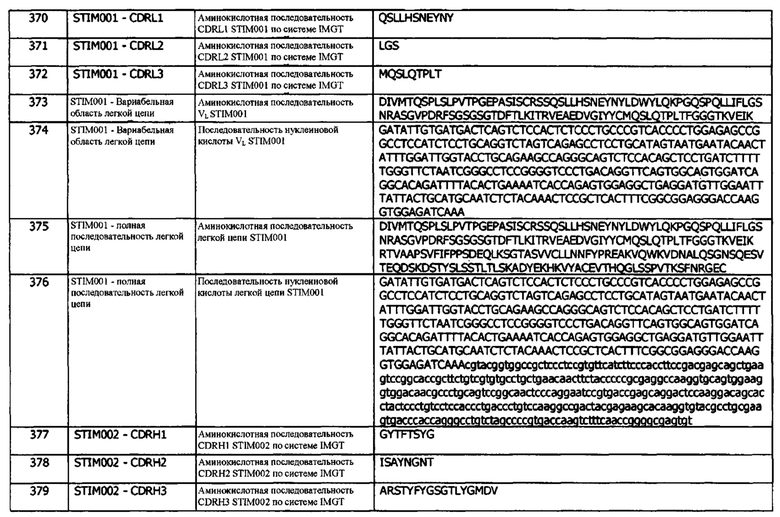
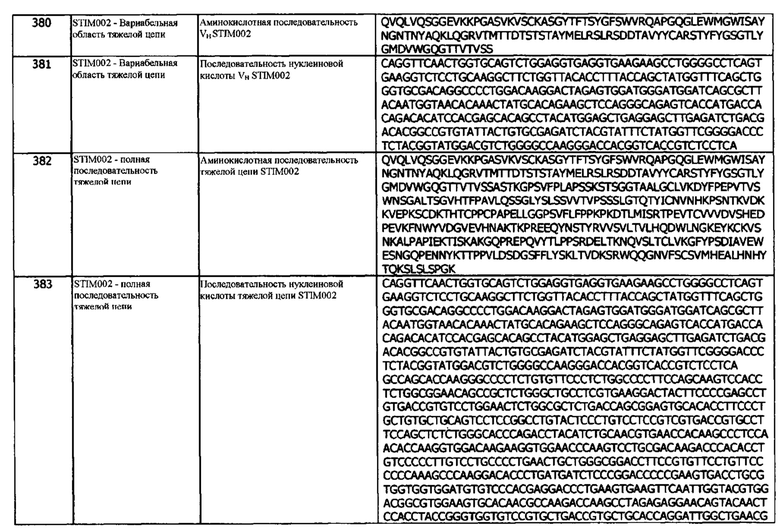
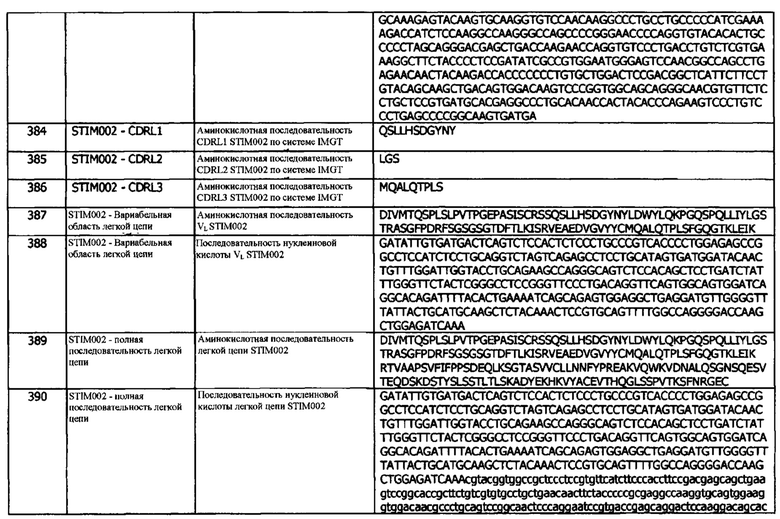
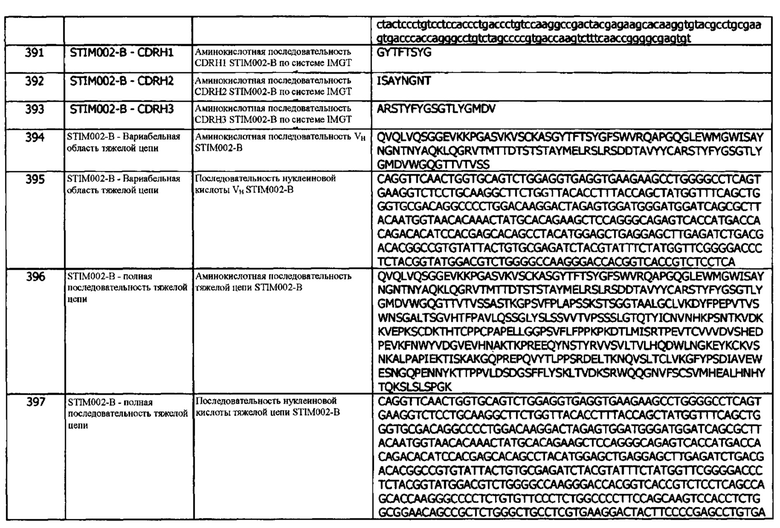
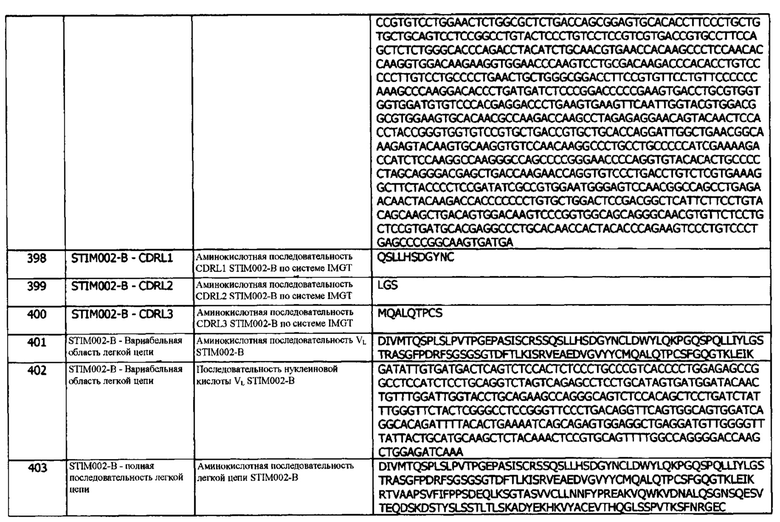
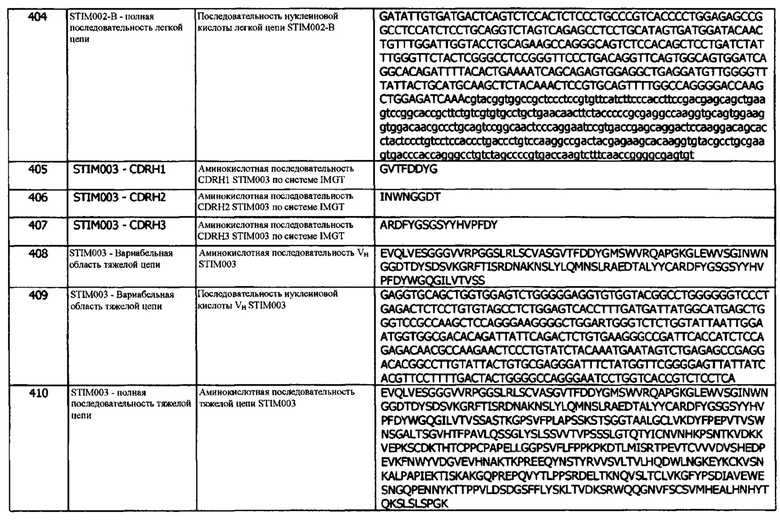
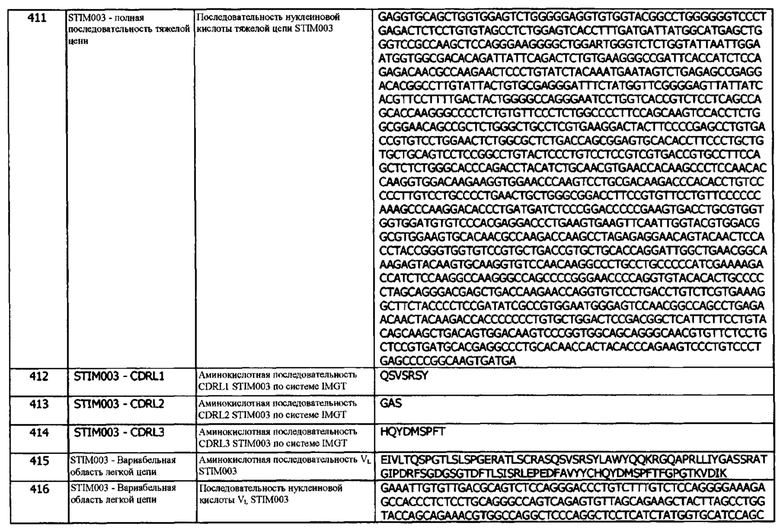
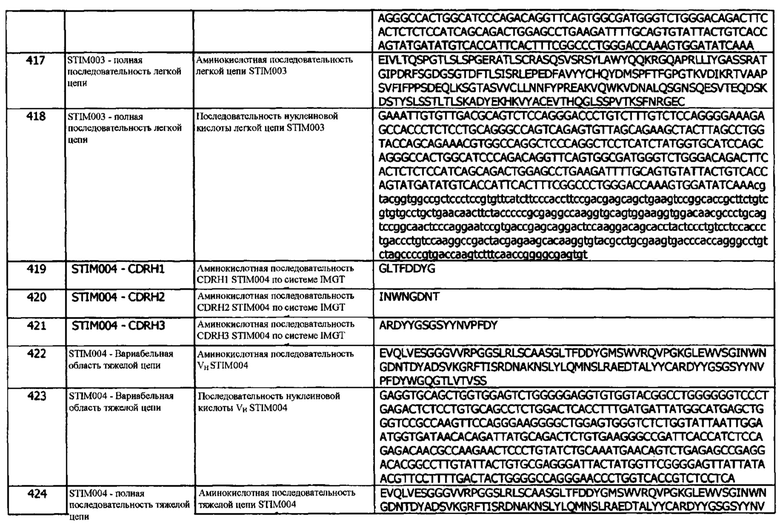

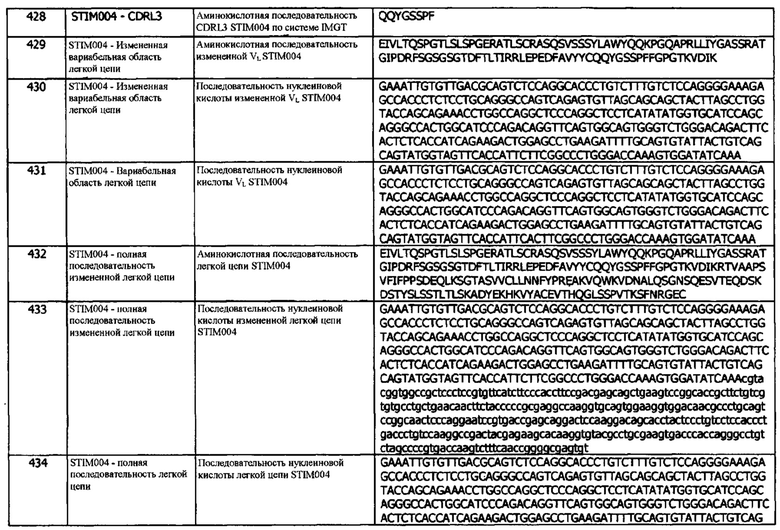
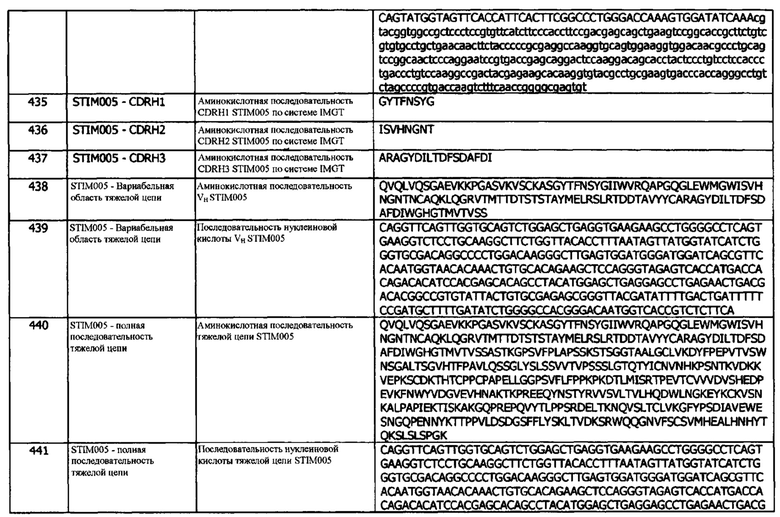
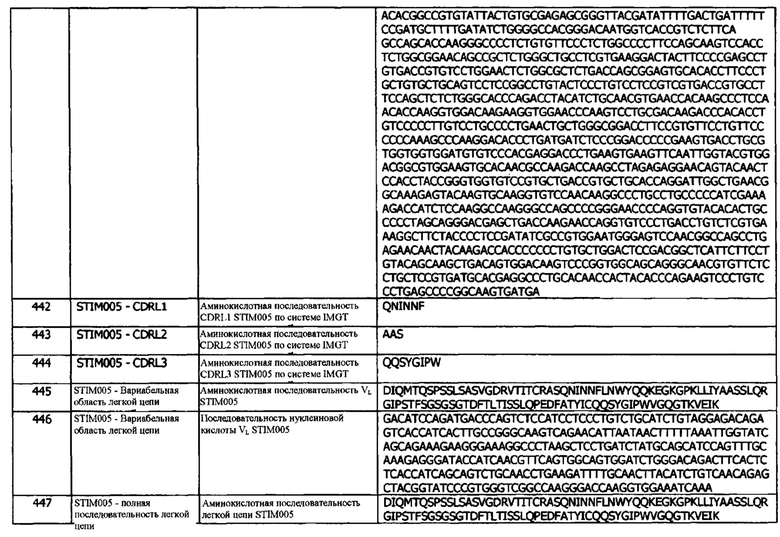
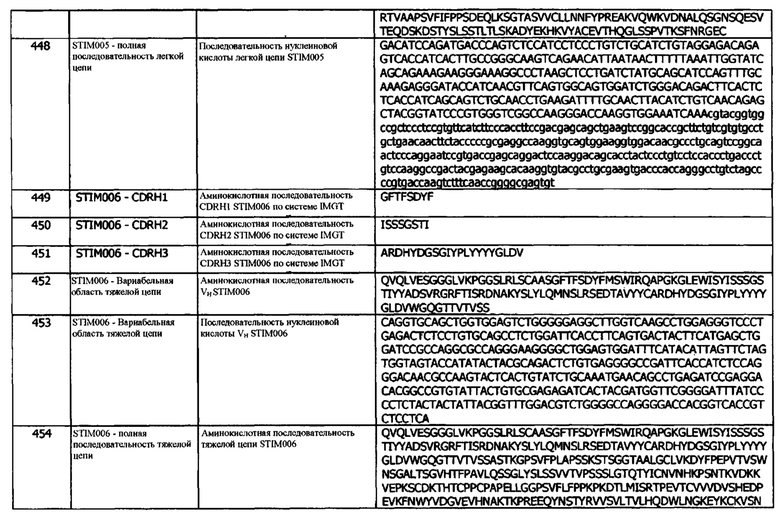

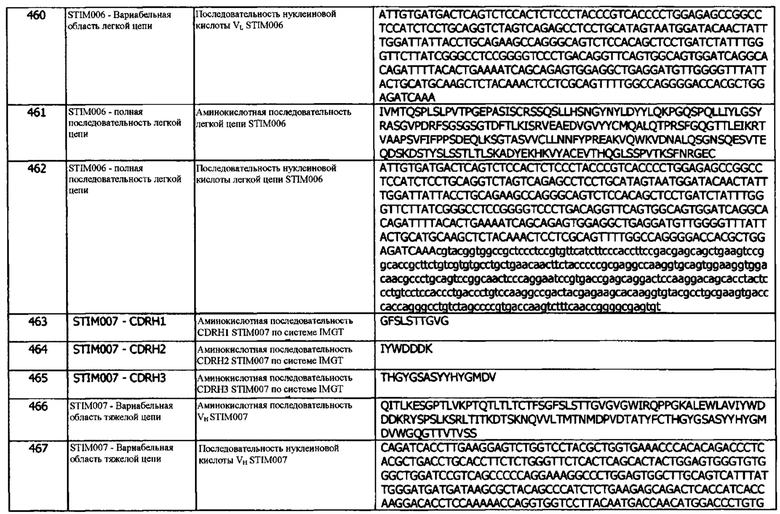
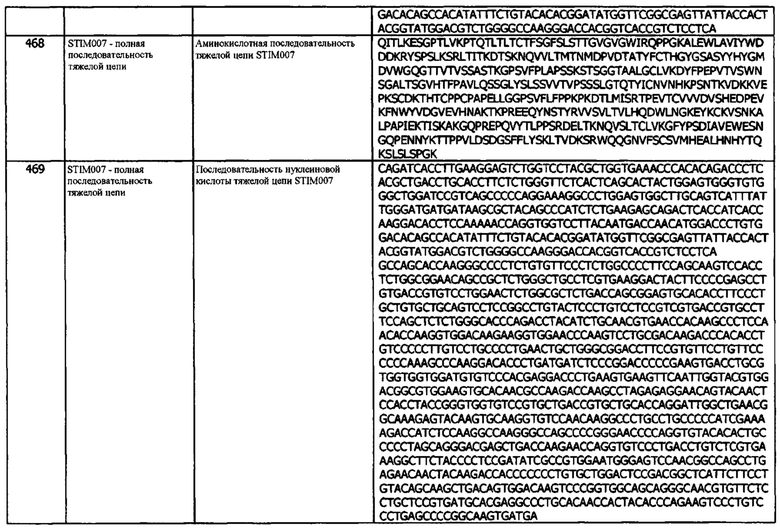
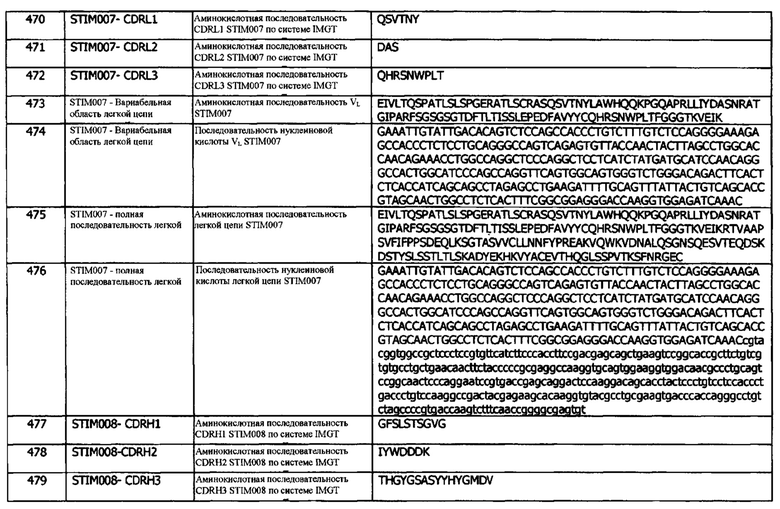
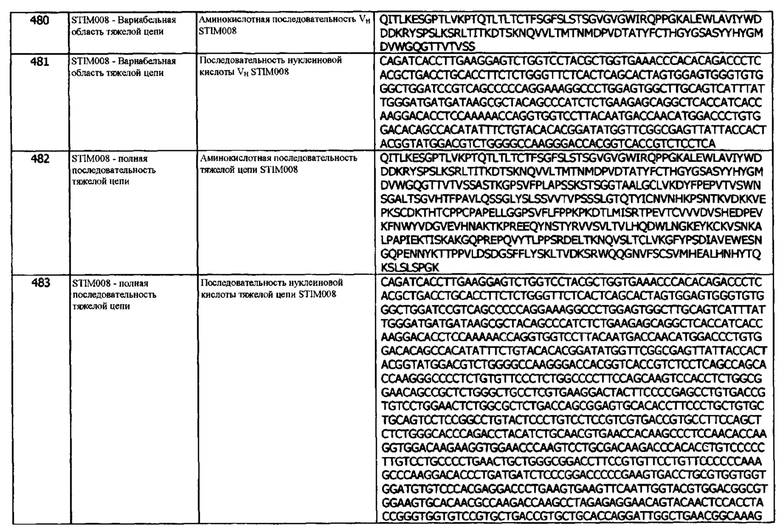
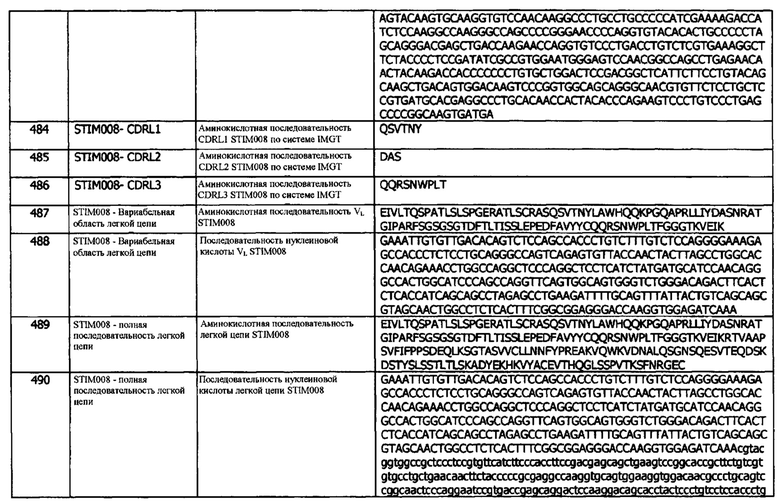
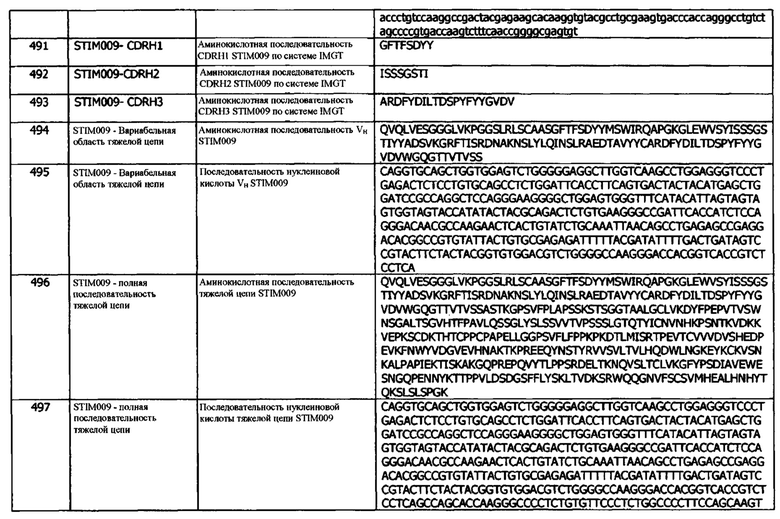
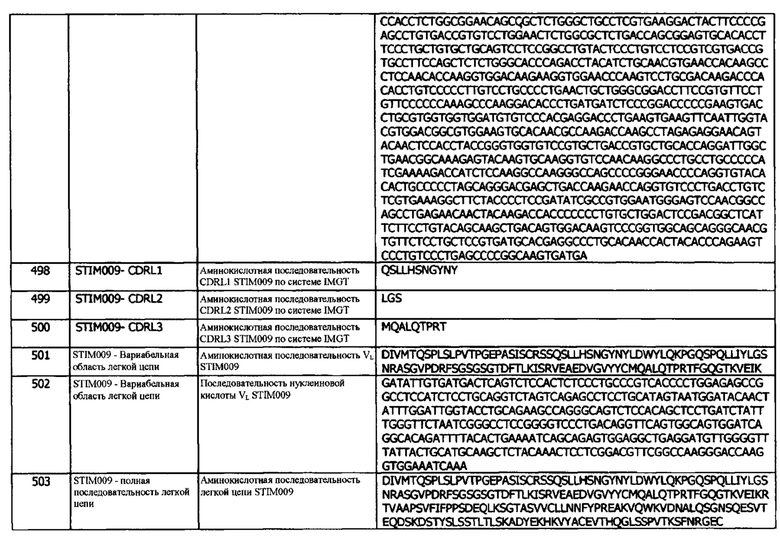
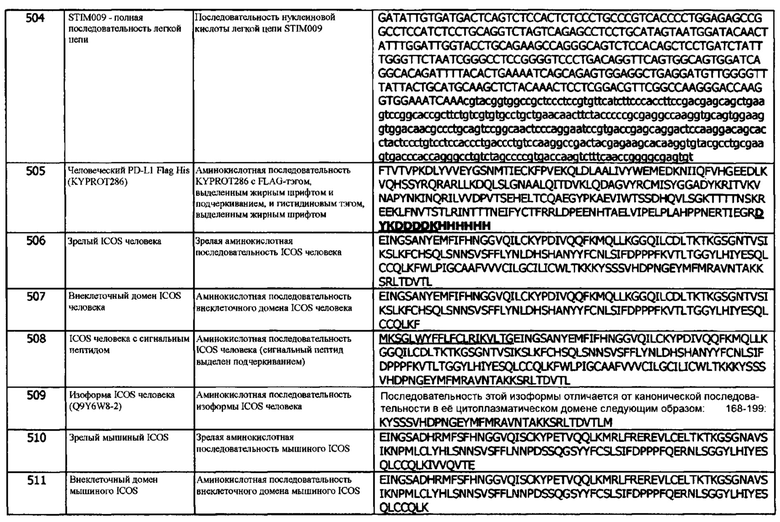




--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Kymab Limited
<120> Immunocytokines
<130> K00035-1 WO
<150> US62/352,291
<151> 2016-06-20
<150> US15/211,504
<151> 2016-07-15
<150> GB1613683.0
<151> 2016-08-09
<150> GB1615224.1
<151> 2016-09-07
<150> GB1615335.5
<151> 2016-09-09
<150> US15/354,971
<151> 2016-11-17
<150> GB1620414.1
<151> 2016-12-01
<150> GB1621782.0
<151> 2016-12-20
<150> GB1702338.3
<151> 2017-02-13
<150> GB1702339.1
<151> 2017-02-13
<150> GB1703071.9
<151> 2017-02-24
<150> US15/480,525
<151> 2017-04-06
<160> 539
<170> PatentIn version 3.5
<210> 1
<211> 290
<212> PRT
<213> Homo Sapien
<400> 1
Met Arg Ile Phe Ala Val Phe Ile Phe Met Thr Tyr Trp His Leu Leu
1 5 10 15
Asn Ala Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr
20 25 30
Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu
35 40 45
Asp Leu Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile
50 55 60
Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser
65 70 75 80
Tyr Arg Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn
85 90 95
Ala Ala Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr
100 105 110
Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val
115 120 125
Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val
130 135 140
Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr
145 150 155 160
Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser
165 170 175
Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn
180 185 190
Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr
195 200 205
Cys Thr Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu
210 215 220
Val Ile Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr His
225 230 235 240
Leu Val Ile Leu Gly Ala Ile Leu Leu Cys Leu Gly Val Ala Leu Thr
245 250 255
Phe Ile Phe Arg Leu Arg Lys Gly Arg Met Met Asp Val Lys Lys Cys
260 265 270
Gly Ile Gln Asp Thr Asn Ser Lys Lys Gln Ser Asp Thr His Leu Glu
275 280 285
Glu Thr
290
<210> 2
<211> 241
<212> PRT
<213> Cynomologus
<400> 2
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Met Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val
20 25 30
Glu Tyr Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys
35 40 45
Gln Leu Asp Leu Thr Ser Leu Ile Val Tyr Trp Glu Met Glu Asp Lys
50 55 60
Asn Ile Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His
65 70 75 80
Ser Asn Tyr Arg Gln Arg Ala Gln Leu Leu Lys Asp Gln Leu Ser Leu
85 90 95
Gly Asn Ala Ala Leu Arg Ile Thr Asp Val Lys Leu Gln Asp Ala Gly
100 105 110
Val Tyr Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile
115 120 125
Thr Val Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu
130 135 140
Val Val Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu
145 150 155 160
Gly Tyr Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val
165 170 175
Leu Ser Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu
180 185 190
Leu Asn Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Ala Asn Glu Ile
195 200 205
Phe Tyr Cys Ile Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala
210 215 220
Glu Leu Val Ile Pro Glu Leu Pro Leu Ala Leu Pro Pro Asn Glu Arg
225 230 235 240
Thr
<210> 3
<211> 245
<212> PRT
<213> Homo Sapien
<400> 3
Met Arg Ile Phe Ala Val Phe Ile Phe Met Thr Tyr Trp His Leu Leu
1 5 10 15
Asn Ala Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr
20 25 30
Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu
35 40 45
Asp Leu Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile
50 55 60
Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser
65 70 75 80
Tyr Arg Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn
85 90 95
Ala Ala Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr
100 105 110
Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val
115 120 125
Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val
130 135 140
Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr
145 150 155 160
Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser
165 170 175
Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn
180 185 190
Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr
195 200 205
Cys Thr Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu
210 215 220
Val Ile Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr His
225 230 235 240
His His His His His
245
<210> 4
<211> 475
<212> PRT
<213> Homo Sapien
<400> 4
Met Arg Ile Phe Ala Val Phe Ile Phe Met Thr Tyr Trp His Leu Leu
1 5 10 15
Asn Ala Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr
20 25 30
Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu
35 40 45
Asp Leu Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile
50 55 60
Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser
65 70 75 80
Tyr Arg Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn
85 90 95
Ala Ala Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr
100 105 110
Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val
115 120 125
Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val
130 135 140
Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr
145 150 155 160
Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser
165 170 175
Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn
180 185 190
Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr
195 200 205
Cys Thr Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu
210 215 220
Val Ile Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr Ile
225 230 235 240
Glu Gly Arg Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
245 250 255
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
260 265 270
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
275 280 285
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
290 295 300
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
305 310 315 320
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
325 330 335
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
340 345 350
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
355 360 365
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
370 375 380
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
385 390 395 400
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
405 410 415
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
420 425 430
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
435 440 445
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470 475
<210> 5
<211> 249
<212> PRT
<213> Cynomologus
<400> 5
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Met Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val
20 25 30
Glu Tyr Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys
35 40 45
Gln Leu Asp Leu Thr Ser Leu Ile Val Tyr Trp Glu Met Glu Asp Lys
50 55 60
Asn Ile Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His
65 70 75 80
Ser Asn Tyr Arg Gln Arg Ala Gln Leu Leu Lys Asp Gln Leu Ser Leu
85 90 95
Gly Asn Ala Ala Leu Arg Ile Thr Asp Val Lys Leu Gln Asp Ala Gly
100 105 110
Val Tyr Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile
115 120 125
Thr Val Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu
130 135 140
Val Val Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu
145 150 155 160
Gly Tyr Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val
165 170 175
Leu Ser Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu
180 185 190
Leu Asn Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Ala Asn Glu Ile
195 200 205
Phe Tyr Cys Ile Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala
210 215 220
Glu Leu Val Ile Pro Glu Leu Pro Leu Ala Leu Pro Pro Asn Glu Arg
225 230 235 240
Thr Asp Tyr Lys Asp Asp Asp Asp Lys
245
<210> 6
<211> 405
<212> PRT
<213> Homo Sapien
<400> 6
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr Phe
20 25 30
Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe Thr
35 40 45
Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr Arg
50 55 60
Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu Asp
65 70 75 80
Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu Pro
85 90 95
Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn Asp
100 105 110
Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala Gln
115 120 125
Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg Ala
130 135 140
Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly Gln
145 150 155 160
Lys Leu Glu Asn Leu Tyr Phe Gln Gly Ile Glu Gly Arg Met Asp Glu
165 170 175
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
180 185 190
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
195 200 205
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
210 215 220
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
225 230 235 240
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
245 250 255
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
260 265 270
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
275 280 285
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
290 295 300
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
305 310 315 320
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
325 330 335
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
340 345 350
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
355 360 365
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
370 375 380
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
385 390 395 400
Leu Ser Leu Ser Pro
405
<210> 7
<211> 8
<212> PRT
<213> Homo Sapien
<400> 7
Gly Phe Thr Phe Asp Asp Tyr Ala
1 5
<210> 8
<211> 8
<212> PRT
<213> Homo Sapien
<400> 8
Ile Ser Trp Lys Ser Asn Ile Ile
1 5
<210> 9
<211> 15
<212> PRT
<213> Homo Sapien
<400> 9
Ala Arg Asp Ile Thr Gly Ser Gly Ser Tyr Gly Trp Phe Asp Pro
1 5 10 15
<210> 10
<211> 5
<212> PRT
<213> Homo Sapien
<400> 10
Asp Tyr Ala Met His
1 5
<210> 11
<211> 17
<212> PRT
<213> Homo Sapien
<400> 11
Gly Ile Ser Trp Lys Ser Asn Ile Ile Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 12
<211> 13
<212> PRT
<213> Homo Sapien
<400> 12
Asp Ile Thr Gly Ser Gly Ser Tyr Gly Trp Phe Asp Pro
1 5 10
<210> 13
<211> 122
<212> PRT
<213> Homo Sapien
<400> 13
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Ser Asn Ile Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Ile Thr Gly Ser Gly Ser Tyr Gly Trp Phe Asp Pro Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 14
<211> 508
<212> DNA
<213> Homo Sapien
<400> 14
caagaaaaag cttgccgcca ccatggagtt tgggctgagc tggattttcc ttttggctat 60
tttaaaaggt gtccagtgtg aagtacaatt ggtggagtcc gggggaggct tggtacagcc 120
tggcaggtcc ctgagactct cctgtgcagc ctctggattc acctttgatg attatgccat 180
gcactgggtc cgacaaactc cagggaaggg cctggagtgg gtctcaggta taagttggaa 240
gagtaatatc ataggctatg cggactctgt gaagggccga ttcaccatct ccagagacaa 300
cgccaagaac tccctgtatc tgcaaatgaa cagtctgaga gctgaggaca cggccttgta 360
ttattgtgca agagatataa cgggttcggg gagttatggc tggttcgacc cctggggcca 420
gggaaccctg gtcaccgtct cctcagccaa aacgacaccc ccatctgtct atccactggc 480
ccctgaatct gctaaaactc agcctccg 508
<210> 15
<211> 449
<212> PRT
<213> Homo Sapien
<400> 15
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Lys Ser Asn Ile Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Ile Thr Gly Ser Gly Ser Tyr Gly Trp Phe Asp Pro Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
Lys
<210> 16
<211> 1356
<212> DNA
<213> Homo Sapien
<400> 16
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcagatc cctgagactg 60
tcttgtgccg cctccggctt caccttcgac gactacgcta tgcactgggt gcgacagacc 120
cctggcaagg gcctggaatg ggtgtccggc atctcctgga agtccaacat catcggctac 180
gccgactccg tgaagggccg gttcaccatc tcccgggaca acgccaagaa ctccctgtac 240
ctgcagatga acagcctgcg ggccgaggac accgccctgt actactgcgc cagagacatc 300
accggctccg gctcctacgg atggttcgat ccttggggcc agggcaccct cgtgaccgtg 360
tcctctgcca gcaccaaggg cccctctgtg ttccctctgg ccccttccag caagtccacc 420
tctggcggaa cagccgctct gggctgcctc gtgaaggact acttccccga gcctgtgacc 480
gtgtcctgga actctggcgc tctgaccagc ggagtgcaca ccttccctgc tgtgctgcag 540
tcctccggcc tgtactccct gtcctccgtc gtgaccgtgc cttccagctc tctgggcacc 600
cagacctaca tctgcaacgt gaaccacaag ccctccaaca ccaaggtgga caagaaggtg 660
gaacccaagt cctgcgacaa gacccacacc tgtccccctt gtcctgcccc tgaactgctg 720
ggcggacctt ccgtgttcct gttcccccca aagcccaagg acaccctgat gatctcccgg 780
acccccgaag tgacctgcgt ggtggtggat gtgtcccacg aggaccctga agtgaagttc 840
aattggtacg tggacggcgt ggaagtgcac aacgccaaga ccaagcctag agaggaacag 900
tacaactcca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ttggctgaac 960
ggcaaagagt acaagtgcaa ggtgtccaac aaggccctgc ctgcccccat cgaaaagacc 1020
atctccaagg ccaagggcca gccccgggaa ccccaggtgt acacactgcc ccctagcagg 1080
gacgagctga ccaagaacca ggtgtccctg acctgtctcg tgaaaggctt ctacccctcc 1140
gatatcgccg tggaatggga gtccaacggc cagcctgaga acaactacaa gaccaccccc 1200
cctgtgctgg actccgacgg ctcattcttc ctgtacagca agctgacagt ggacaagtcc 1260
cggtggcagc agggcaacgt gttctcctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agtccctgtc cctgagcccc ggcaag 1356
<210> 17
<211> 6
<212> PRT
<213> Homo Sapien
<400> 17
Gln Ser Ile Ser Ser Tyr
1 5
<210> 18
<211> 3
<212> PRT
<213> Homo Sapien
<400> 18
Val Ala Ser
1
<210> 19
<211> 9
<212> PRT
<213> Homo Sapien
<400> 19
Gln Gln Ser Tyr Ser Asn Pro Ile Thr
1 5
<210> 20
<211> 11
<212> PRT
<213> Homo Sapien
<400> 20
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 21
<211> 7
<212> PRT
<213> Homo Sapien
<400> 21
Val Ala Ser Ser Leu Gln Ser
1 5
<210> 22
<211> 9
<212> PRT
<213> Homo Sapien
<400> 22
Gln Gln Ser Tyr Ser Asn Pro Ile Thr
1 5
<210> 23
<211> 107
<212> PRT
<213> Homo Sapien
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Ser Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Asn Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 24
<211> 321
<212> DNA
<213> Homo Sapien
<400> 24
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagcccct gatctatgtt gcatccagtt tgcaaagtgg ggtcccatca 180
agtttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta atccgatcac cttcggccaa 300
gggacacgac tggagatcaa a 321
<210> 25
<211> 214
<212> PRT
<213> Homo Sapien
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Ser Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Asn Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 26
<211> 642
<212> DNA
<213> Homo Sapien
<400> 26
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagcccct gatctatgtt gcatccagtt tgcaaagtgg ggtcccatca 180
agtttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta atccgatcac cttcggccaa 300
gggacacgac tggagatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 27
<211> 8
<212> PRT
<213> Homo Sapien
<400> 27
Gly Phe Thr Phe Asp Asp Tyr Ala
1 5
<210> 28
<211> 8
<212> PRT
<213> Homo Sapien
<400> 28
Ile Ser Trp Ile Arg Thr Gly Ile
1 5
<210> 29
<211> 16
<212> PRT
<213> Homo Sapien
<400> 29
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
1 5 10 15
<210> 30
<211> 5
<212> PRT
<213> Homo Sapien
<400> 30
Asp Tyr Ala Met His
1 5
<210> 31
<211> 17
<212> PRT
<213> Homo Sapien
<400> 31
Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 32
<211> 14
<212> PRT
<213> Homo Sapien
<400> 32
Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
1 5 10
<210> 33
<211> 123
<212> PRT
<213> Homo Sapien
<400> 33
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 34
<211> 482
<212> DNA
<213> Homo Sapien
<400> 34
aagcttgccg ccaccatgga gtttgggctg agctggattt tccttttggc tattttaaaa 60
ggtgtccagt gtgaagtgca gctggtggag tctgggggag gcttggtgca gcctggcagg 120
tccctgagac tctcctgtgc agcctctgga ttcacctttg atgattatgc catgcactgg 180
gtccggcaag ttccagggaa gggcctggaa tgggtctcag gcattagttg gattcgtact 240
ggcataggct atgcggactc tgtgaagggc cgattcacca ttttcagaga caacgccaag 300
aattccctgt atctgcaaat gaacagtctg agagctgagg acacggcctt gtattactgt 360
gcaaaagata tgaagggttc ggggacttat ggggggtggt tcgacacctg gggccaggga 420
accctggtca ccgtctcctc agccaaaaca acagccccat cggtctatcc actggcccct 480
gc 482
<210> 35
<211> 450
<212> PRT
<213> Homo Sapien
<400> 35
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
195 200 205
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
210 215 220
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
435 440 445
Gly Lys
450
<210> 36
<211> 1359
<212> DNA
<213> Homo Sapien
<400> 36
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcagatc cctgagactg 60
tcttgtgccg cctccggctt caccttcgac gactacgcta tgcactgggt gcgacaggtg 120
ccaggcaagg gcctggaatg ggtgtccggc atctcttgga tccggaccgg catcggctac 180
gccgactctg tgaagggccg gttcaccatc ttccgggaca acgccaagaa ctccctgtac 240
ctgcagatga acagcctgcg ggccgaggac accgccctgt actactgcgc caaggacatg 300
aagggctccg gcacctacgg cggatggttc gatacttggg gccagggcac cctcgtgacc 360
gtgtcctctg ccagcaccaa gggcccctct gtgttccctc tggccccttc cagcaagtcc 420
acctctggcg gaacagccgc tctgggctgc ctcgtgaagg actacttccc cgagcctgtg 480
accgtgtcct ggaactctgg cgctctgacc agcggagtgc acaccttccc tgctgtgctg 540
cagtcctccg gcctgtactc cctgtcctcc gtcgtgaccg tgccttccag ctctctgggc 600
acccagacct acatctgcaa cgtgaaccac aagccctcca acaccaaggt ggacaagaag 660
gtggaaccca agtcctgcga caagacccac acctgtcccc cttgtcctgc ccctgaactg 720
ctgggcggac cttccgtgtt cctgttcccc ccaaagccca aggacaccct gatgatctcc 780
cggacccccg aagtgacctg cgtggtggtg gatgtgtccc acgaggaccc tgaagtgaag 840
ttcaattggt acgtggacgg cgtggaagtg cacaacgcca agaccaagcc tagagaggaa 900
cagtacaact ccacctaccg ggtggtgtcc gtgctgaccg tgctgcacca ggattggctg 960
aacggcaaag agtacaagtg caaggtgtcc aacaaggccc tgcctgcccc catcgaaaag 1020
accatctcca aggccaaggg ccagccccgg gaaccccagg tgtacacact gccccctagc 1080
agggacgagc tgaccaagaa ccaggtgtcc ctgacctgtc tcgtgaaagg cttctacccc 1140
tccgatatcg ccgtggaatg ggagtccaac ggccagcctg agaacaacta caagaccacc 1200
ccccctgtgc tggactccga cggctcattc ttcctgtaca gcaagctgac agtggacaag 1260
tcccggtggc agcagggcaa cgtgttctcc tgctccgtga tgcacgaggc cctgcacaac 1320
cactacaccc agaagtccct gtccctgagc cccggcaag 1359
<210> 37
<211> 6
<212> PRT
<213> Homo Sapien
<400> 37
Gln Ser Ile Ser Ser Tyr
1 5
<210> 38
<211> 3
<212> PRT
<213> Homo Sapien
<400> 38
Val Ala Ser
1
<210> 39
<211> 9
<212> PRT
<213> Homo Sapien
<400> 39
Gln Gln Ser Tyr Ser Thr Pro Ile Thr
1 5
<210> 40
<211> 11
<212> PRT
<213> Homo Sapien
<400> 40
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 41
<211> 7
<212> PRT
<213> Homo Sapien
<400> 41
Val Ala Ser Ser Leu Gln Ser
1 5
<210> 42
<211> 9
<212> PRT
<213> Homo Sapien
<400> 42
Gln Gln Ser Tyr Ser Thr Pro Ile Thr
1 5
<210> 43
<211> 107
<212> PRT
<213> Homo Sapien
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 44
<211> 418
<212> DNA
<213> Homo Sapien
<400> 44
aaagcttgcc gccaccatga ggctccctgc tcagcttctg gggctcctgc tactctggct 60
ccgaggtgcc agatgtgaca tccagatgac ccagtctcca tcctccctgt ctgcatctgt 120
aggagacaga gtcaccatca cttgccgggc aagtcagagc attagcagct atttaaattg 180
gtatcagcag aaaccaggga aagcccctaa actcctgatc tatgttgcat ccagtttgca 240
aagtggggtc ccatcaaggt tcagtggcag tggatctggg acagatttca ctctcactat 300
cagcagtctg caacctgaag attttgcaac ttactactgt caacagagtt acagtacccc 360
gatcaccttc ggccaaggga cacgtctgga gatcaaacgt acggatgctg caccaact 418
<210> 45
<211> 214
<212> PRT
<213> Homo Sapien
<400> 45
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 46
<211> 642
<212> DNA
<213> Homo Sapien
<400> 46
gacatccaga tgacccagtc cccctccagc ctgtctgctt ccgtgggcga cagagtgacc 60
atcacctgtc gggcctccca gtccatctcc tcctacctga actggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctacgtg gccagctctc tgcagtccgg cgtgccctct 180
agattctccg gctctggctc tggcaccgac tttaccctga ccatcagctc cctgcagccc 240
gaggacttcg ccacctacta ctgccagcag tcctactcca cccctatcac cttcggccag 300
ggcacccggc tggaaatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 47
<211> 450
<212> PRT
<213> Homo Sapien
<400> 47
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
195 200 205
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
210 215 220
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Leu Ala Gly Ala
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
435 440 445
Gly Lys
450
<210> 48
<211> 450
<212> PRT
<213> Homo Sapien
<400> 48
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
195 200 205
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
210 215 220
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Leu Ala Gly Ala
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
435 440 445
Gly Lys
450
<210> 49
<211> 448
<212> PRT
<213> Homo Sapien
<400> 49
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
195 200 205
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
210 215 220
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Val Ala Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 50
<211> 214
<212> PRT
<213> Homo Sapien
<400> 50
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 51
<211> 214
<212> PRT
<213> Homo Sapien
<400> 51
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Phe Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 52
<211> 8
<212> PRT
<213> Homo Sapien
<400> 52
Gly Phe Thr Phe Ser Ser Tyr Trp
1 5
<210> 53
<211> 8
<212> PRT
<213> Homo Sapien
<400> 53
Ile Lys Glu Asp Gly Ser Glu Lys
1 5
<210> 54
<211> 12
<212> PRT
<213> Homo Sapien
<400> 54
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn
1 5 10
<210> 55
<211> 5
<212> PRT
<213> Homo Sapien
<400> 55
Ser Tyr Trp Met Ser
1 5
<210> 56
<211> 17
<212> PRT
<213> Homo Sapien
<400> 56
Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 57
<211> 10
<212> PRT
<213> Homo Sapien
<400> 57
Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn
1 5 10
<210> 58
<211> 119
<212> PRT
<213> Homo Sapien
<400> 58
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 59
<211> 358
<212> DNA
<213> Homo Sapien
<400> 59
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac atcaaagaag atggaagtga gaaatactat 180
gtcgactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagaaatcga 300
ctctacagtg acttccttga caactggggc cagggaaccc tggtcaccgt ctcctcag 358
<210> 60
<211> 449
<212> PRT
<213> Homo Sapien
<400> 60
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 61
<211> 1347
<212> DNA
<213> Homo Sapien
<400> 61
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac atcaaagaag atggaagtga gaaatactat 180
gtcgactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagaaatcga 300
ctctacagtg acttccttga caactggggc cagggaaccc tggtcaccgt ctcctcagcc 360
agcaccaagg gcccctctgt gttccctctg gccccttcca gcaagtccac ctctggcgga 420
acagccgctc tgggctgcct cgtgaaggac tacttccccg agcctgtgac cgtgtcctgg 480
aactctggcg ctctgaccag cggagtgcac accttccctg ctgtgctgca gtcctccggc 540
ctgtactccc tgtcctccgt cgtgaccgtg ccttccagct ctctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gccctccaac accaaggtgg acaagaaggt ggaacccaag 660
tcctgcgaca agacccacac ctgtccccct tgtcctgccc ctgaactgct gggcggacct 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatctcccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccac gaggaccctg aagtgaagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccta gagaggaaca gtacaactcc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg attggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caaggccctg cctgccccca tcgaaaagac catctccaag 1020
gccaagggcc agccccggga accccaggtg tacacactgc cccctagcag ggacgagctg 1080
accaagaacc aggtgtccct gacctgtctc gtgaaaggct tctacccctc cgatatcgcc 1140
gtggaatggg agtccaacgg ccagcctgag aacaactaca agaccacccc ccctgtgctg 1200
gactccgacg gctcattctt cctgtacagc aagctgacag tggacaagtc ccggtggcag 1260
cagggcaacg tgttctcctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ccctgagccc cggcaag 1347
<210> 62
<211> 6
<212> PRT
<213> Homo Sapien
<400> 62
Gln Gly Val Ser Ser Trp
1 5
<210> 63
<211> 3
<212> PRT
<213> Homo Sapien
<400> 63
Gly Ala Ser
1
<210> 64
<211> 9
<212> PRT
<213> Homo Sapien
<400> 64
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 65
<211> 11
<212> PRT
<213> Homo Sapien
<400> 65
Arg Ala Ser Gln Gly Val Ser Ser Trp Leu Ala
1 5 10
<210> 66
<211> 7
<212> PRT
<213> Homo Sapien
<400> 66
Gly Ala Ser Ser Leu Gln Ser
1 5
<210> 67
<211> 9
<212> PRT
<213> Homo Sapien
<400> 67
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 68
<211> 107
<212> PRT
<213> Homo Sapien
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 69
<211> 322
<212> DNA
<213> Homo Sapien
<400> 69
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agctggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcatccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa ac 322
<210> 70
<211> 214
<212> PRT
<213> Homo Sapien
<400> 70
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 71
<211> 642
<212> DNA
<213> Homo Sapien
<400> 71
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agctggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcatccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 72
<211> 8
<212> PRT
<213> Homo Sapien
<400> 72
Gly Phe Thr Phe Ser Ser Tyr Trp
1 5
<210> 73
<211> 8
<212> PRT
<213> Homo Sapien
<400> 73
Ile Lys Glu Asp Gly Ser Glu Lys
1 5
<210> 74
<211> 12
<212> PRT
<213> Homo Sapien
<400> 74
Ala Arg Val Arg Leu Tyr Ser Asp Phe Leu Asp Tyr
1 5 10
<210> 75
<211> 5
<212> PRT
<213> Homo Sapien
<400> 75
Ser Tyr Trp Met Ser
1 5
<210> 76
<211> 17
<212> PRT
<213> Homo Sapien
<400> 76
Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Leu Lys
1 5 10 15
Gly
<210> 77
<211> 10
<212> PRT
<213> Homo Sapien
<400> 77
Val Arg Leu Tyr Ser Asp Phe Leu Asp Tyr
1 5 10
<210> 78
<211> 119
<212> PRT
<213> Homo Sapien
<400> 78
Glu Val Gln Leu Val Asp Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Val Arg Leu Tyr Ser Asp Phe Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 79
<211> 358
<212> DNA
<213> Homo Sapien
<400> 79
gaggtgcagc tggtggactc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccaggaaagg ggctggagtg ggtggccaac ataaaagaag atggaagtga gaaatactat 180
gtagactctt tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagagttcga 300
ctctacagtg acttccttga ctactggggc cagggaaccc tggtcaccgt ctcctcag 358
<210> 80
<211> 449
<212> PRT
<213> Homo Sapien
<400> 80
Glu Val Gln Leu Val Asp Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Val Arg Leu Tyr Ser Asp Phe Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 81
<211> 1347
<212> DNA
<213> Homo Sapien
<400> 81
gaggtgcagc tggtggactc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccaggaaagg ggctggagtg ggtggccaac ataaaagaag atggaagtga gaaatactat 180
gtagactctt tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagagttcga 300
ctctacagtg acttccttga ctactggggc cagggaaccc tggtcaccgt ctcctcagcc 360
agcaccaagg gcccctctgt gttccctctg gccccttcca gcaagtccac ctctggcgga 420
acagccgctc tgggctgcct cgtgaaggac tacttccccg agcctgtgac cgtgtcctgg 480
aactctggcg ctctgaccag cggagtgcac accttccctg ctgtgctgca gtcctccggc 540
ctgtactccc tgtcctccgt cgtgaccgtg ccttccagct ctctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gccctccaac accaaggtgg acaagaaggt ggaacccaag 660
tcctgcgaca agacccacac ctgtccccct tgtcctgccc ctgaactgct gggcggacct 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatctcccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccac gaggaccctg aagtgaagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccta gagaggaaca gtacaactcc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg attggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caaggccctg cctgccccca tcgaaaagac catctccaag 1020
gccaagggcc agccccggga accccaggtg tacacactgc cccctagcag ggacgagctg 1080
accaagaacc aggtgtccct gacctgtctc gtgaaaggct tctacccctc cgatatcgcc 1140
gtggaatggg agtccaacgg ccagcctgag aacaactaca agaccacccc ccctgtgctg 1200
gactccgacg gctcattctt cctgtacagc aagctgacag tggacaagtc ccggtggcag 1260
cagggcaacg tgttctcctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ccctgagccc cggcaag 1347
<210> 82
<211> 6
<212> PRT
<213> Homo Sapien
<400> 82
Gln Gly Val Ser Ser Trp
1 5
<210> 83
<211> 3
<212> PRT
<213> Homo Sapien
<400> 83
Gly Ala Ser
1
<210> 84
<211> 9
<212> PRT
<213> Homo Sapien
<400> 84
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 85
<211> 11
<212> PRT
<213> Homo Sapien
<400> 85
Arg Ala Ser Gln Gly Val Ser Ser Trp Leu Ala
1 5 10
<210> 86
<211> 7
<212> PRT
<213> Homo Sapien
<400> 86
Gly Ala Ser Ser Leu Gln Ser
1 5
<210> 87
<211> 9
<212> PRT
<213> Homo Sapien
<400> 87
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 88
<211> 107
<212> PRT
<213> Homo Sapien
<400> 88
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Ser Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 89
<211> 322
<212> DNA
<213> Homo Sapien
<400> 89
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agttggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcctccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca gcatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa ac 322
<210> 90
<211> 214
<212> PRT
<213> Homo Sapien
<400> 90
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Ser Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 91
<211> 642
<212> DNA
<213> Homo Sapien
<400> 91
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agttggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcctccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca gcatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 92
<211> 9
<212> PRT
<213> Homo Sapien
<400> 92
Gly Gly Ser Ile Ile Ser Ser Asp Trp
1 5
<210> 93
<211> 7
<212> PRT
<213> Homo Sapien
<400> 93
Ile Phe His Ser Gly Arg Thr
1 5
<210> 94
<211> 8
<212> PRT
<213> Homo Sapien
<400> 94
Ala Arg Asp Gly Ser Gly Ser Tyr
1 5
<210> 95
<211> 6
<212> PRT
<213> Homo Sapien
<400> 95
Ser Ser Asp Trp Trp Asn
1 5
<210> 96
<211> 16
<212> PRT
<213> Homo Sapien
<400> 96
Glu Ile Phe His Ser Gly Arg Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 97
<211> 6
<212> PRT
<213> Homo Sapien
<400> 97
Asp Gly Ser Gly Ser Tyr
1 5
<210> 98
<211> 115
<212> PRT
<213> Homo Sapien
<400> 98
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ile Val Ser Gly Gly Ser Ile Ile Ser Ser
20 25 30
Asp Trp Trp Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Ile Phe His Ser Gly Arg Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Ile Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Gly Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 99
<211> 346
<212> DNA
<213> Homo Sapien
<400> 99
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcattg tctctggtgg ctccatcatc agtagtgact ggtggaattg ggtccgccag 120
cccccaggga aggggctgga gtggattgga gaaatctttc atagtgggag gaccaactac 180
aacccgtccc tcaagagtcg agtcaccata tcaatagaca agtccaagaa tcagttctcc 240
ctgaggctga gctctgtgac cgccgcggac acggccgtgt attactgtgc gagagatggt 300
tcggggagtt actggggcca gggaaccctg gtcaccgtct cctcag 346
<210> 100
<211> 445
<212> PRT
<213> Homo Sapien
<400> 100
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ile Val Ser Gly Gly Ser Ile Ile Ser Ser
20 25 30
Asp Trp Trp Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Ile Phe His Ser Gly Arg Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Ile Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Gly Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 101
<211> 1335
<212> DNA
<213> Homo Sapien
<400> 101
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcattg tctctggtgg ctccatcatc agtagtgact ggtggaattg ggtccgccag 120
cccccaggga aggggctgga gtggattgga gaaatctttc atagtgggag gaccaactac 180
aacccgtccc tcaagagtcg agtcaccata tcaatagaca agtccaagaa tcagttctcc 240
ctgaggctga gctctgtgac cgccgcggac acggccgtgt attactgtgc gagagatggt 300
tcggggagtt actggggcca gggaaccctg gtcaccgtct cctcagccag caccaagggc 360
ccctctgtgt tccctctggc cccttccagc aagtccacct ctggcggaac agccgctctg 420
ggctgcctcg tgaaggacta cttccccgag cctgtgaccg tgtcctggaa ctctggcgct 480
ctgaccagcg gagtgcacac cttccctgct gtgctgcagt cctccggcct gtactccctg 540
tcctccgtcg tgaccgtgcc ttccagctct ctgggcaccc agacctacat ctgcaacgtg 600
aaccacaagc cctccaacac caaggtggac aagaaggtgg aacccaagtc ctgcgacaag 660
acccacacct gtcccccttg tcctgcccct gaactgctgg gcggaccttc cgtgttcctg 720
ttccccccaa agcccaagga caccctgatg atctcccgga cccccgaagt gacctgcgtg 780
gtggtggatg tgtcccacga ggaccctgaa gtgaagttca attggtacgt ggacggcgtg 840
gaagtgcaca acgccaagac caagcctaga gaggaacagt acaactccac ctaccgggtg 900
gtgtccgtgc tgaccgtgct gcaccaggat tggctgaacg gcaaagagta caagtgcaag 960
gtgtccaaca aggccctgcc tgcccccatc gaaaagacca tctccaaggc caagggccag 1020
ccccgggaac cccaggtgta cacactgccc cctagcaggg acgagctgac caagaaccag 1080
gtgtccctga cctgtctcgt gaaaggcttc tacccctccg atatcgccgt ggaatgggag 1140
tccaacggcc agcctgagaa caactacaag accacccccc ctgtgctgga ctccgacggc 1200
tcattcttcc tgtacagcaa gctgacagtg gacaagtccc ggtggcagca gggcaacgtg 1260
ttctcctgct ccgtgatgca cgaggccctg cacaaccact acacccagaa gtccctgtcc 1320
ctgagccccg gcaag 1335
<210> 102
<211> 12
<212> PRT
<213> Homo Sapien
<400> 102
Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr
1 5 10
<210> 103
<211> 3
<212> PRT
<213> Homo Sapien
<400> 103
Trp Ala Ser
1
<210> 104
<211> 8
<212> PRT
<213> Homo Sapien
<400> 104
Gln Gln Tyr Tyr Ser Asn Arg Ser
1 5
<210> 105
<211> 17
<212> PRT
<213> Homo Sapien
<400> 105
Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 106
<211> 7
<212> PRT
<213> Homo Sapien
<400> 106
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 107
<211> 8
<212> PRT
<213> Homo Sapien
<400> 107
Gln Gln Tyr Tyr Ser Asn Arg Ser
1 5
<210> 108
<211> 112
<212> PRT
<213> Homo Sapien
<400> 108
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Ser Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Thr Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Asn Arg Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 109
<211> 337
<212> DNA
<213> Homo Sapien
<400> 109
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acaataagaa ttacttagct 120
tggtaccagc agaaatcagg acagcctcct aagttgctca tttactgggc atctacccgg 180
gaatccgggg tccctgaccg attcagtggc agcgggtctg ggacagattt cactctcacc 240
atcagcagcc tgcagactga agatgtggca gtttattact gtcagcaata ttatagtaat 300
cgcagttttg gccaggggac caagctggag atcaaac 337
<210> 110
<211> 219
<212> PRT
<213> Homo Sapien
<400> 110
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Ser Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Thr Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Asn Arg Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 111
<211> 657
<212> DNA
<213> Homo Sapien
<400> 111
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acaataagaa ttacttagct 120
tggtaccagc agaaatcagg acagcctcct aagttgctca tttactgggc atctacccgg 180
gaatccgggg tccctgaccg attcagtggc agcgggtctg ggacagattt cactctcacc 240
atcagcagcc tgcagactga agatgtggca gtttattact gtcagcaata ttatagtaat 300
cgcagttttg gccaggggac caagctggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 112
<211> 8
<212> PRT
<213> Homo Sapien
<400> 112
Gly Phe Thr Phe Ser Ser Tyr Trp
1 5
<210> 113
<211> 8
<212> PRT
<213> Homo Sapien
<400> 113
Ile Lys Glu Asp Gly Ser Glu Lys
1 5
<210> 114
<211> 12
<212> PRT
<213> Homo Sapien
<400> 114
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn
1 5 10
<210> 115
<211> 5
<212> PRT
<213> Homo Sapien
<400> 115
Ser Tyr Trp Met Ser
1 5
<210> 116
<211> 17
<212> PRT
<213> Homo Sapien
<400> 116
Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 117
<211> 10
<212> PRT
<213> Homo Sapien
<400> 117
Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn
1 5 10
<210> 118
<211> 119
<212> PRT
<213> Homo Sapien
<400> 118
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 119
<211> 358
<212> DNA
<213> Homo Sapien
<400> 119
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac atcaaagaag atggaagtga gaaatactat 180
gtcgactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagaaatcga 300
ctctacagtg acttccttga caactggggc cagggaaccc tggtcaccgt ctcctcag 358
<210> 120
<211> 449
<212> PRT
<213> Homo Sapien
<400> 120
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Glu Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Leu Tyr Ser Asp Phe Leu Asp Asn Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 121
<211> 1347
<212> DNA
<213> Homo Sapien
<400> 121
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagt agctattgga tgagttgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac atcaaagaag atggaagtga gaaatactat 180
gtcgactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acgtctgtgt attactgtgc gagaaatcga 300
ctctacagtg acttccttga caactggggc cagggaaccc tggtcaccgt ctcctcagcc 360
agcaccaagg gcccctctgt gttccctctg gccccttcca gcaagtccac ctctggcgga 420
acagccgctc tgggctgcct cgtgaaggac tacttccccg agcctgtgac cgtgtcctgg 480
aactctggcg ctctgaccag cggagtgcac accttccctg ctgtgctgca gtcctccggc 540
ctgtactccc tgtcctccgt cgtgaccgtg ccttccagct ctctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gccctccaac accaaggtgg acaagaaggt ggaacccaag 660
tcctgcgaca agacccacac ctgtccccct tgtcctgccc ctgaactgct gggcggacct 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatctcccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccac gaggaccctg aagtgaagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccta gagaggaaca gtacaactcc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg attggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caaggccctg cctgccccca tcgaaaagac catctccaag 1020
gccaagggcc agccccggga accccaggtg tacacactgc cccctagcag ggacgagctg 1080
accaagaacc aggtgtccct gacctgtctc gtgaaaggct tctacccctc cgatatcgcc 1140
gtggaatggg agtccaacgg ccagcctgag aacaactaca agaccacccc ccctgtgctg 1200
gactccgacg gctcattctt cctgtacagc aagctgacag tggacaagtc ccggtggcag 1260
cagggcaacg tgttctcctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ccctgagccc cggcaag 1347
<210> 122
<211> 6
<212> PRT
<213> Homo Sapien
<400> 122
Gln Gly Val Ser Ser Trp
1 5
<210> 123
<211> 3
<212> PRT
<213> Homo Sapien
<400> 123
Gly Ala Ser
1
<210> 124
<211> 9
<212> PRT
<213> Homo Sapien
<400> 124
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 125
<211> 11
<212> PRT
<213> Homo Sapien
<400> 125
Arg Ala Ser Gln Gly Val Ser Ser Trp Leu Ala
1 5 10
<210> 126
<211> 7
<212> PRT
<213> Homo Sapien
<400> 126
Gly Ala Ser Ser Leu Gln Ser
1 5
<210> 127
<211> 9
<212> PRT
<213> Homo Sapien
<400> 127
Gln Gln Ala Asn Ser Ile Pro Phe Thr
1 5
<210> 128
<211> 107
<212> PRT
<213> Homo Sapien
<400> 128
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 129
<211> 322
<212> DNA
<213> Homo Sapien
<400> 129
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agctggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcatccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa ac 322
<210> 130
<211> 214
<212> PRT
<213> Homo Sapien
<400> 130
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Ile Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 131
<211> 642
<212> DNA
<213> Homo Sapien
<400> 131
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtcggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtgttagc agctggttag cctggtatca gcagaaatca 120
gggaaagccc ctaagctcct gatctatggt gcatccagtt tgcaaagtgg ggtcccatca 180
agattcagcg gcagtggatc tgggacagag ttcattctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagta tcccattcac tttcggccct 300
gggaccaaag tggatatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 132
<211> 8
<212> PRT
<213> Homo Sapien
<400> 132
Gly Phe Thr Phe Arg Ile Tyr Gly
1 5
<210> 133
<211> 8
<212> PRT
<213> Homo Sapien
<400> 133
Ile Trp Tyr Asp Gly Ser Asn Lys
1 5
<210> 134
<211> 11
<212> PRT
<213> Homo Sapien
<400> 134
Ala Arg Asp Met Asp Tyr Phe Gly Met Asp Val
1 5 10
<210> 135
<211> 5
<212> PRT
<213> Homo Sapien
<400> 135
Ile Tyr Gly Met His
1 5
<210> 136
<211> 17
<212> PRT
<213> Homo Sapien
<400> 136
Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 137
<211> 9
<212> PRT
<213> Homo Sapien
<400> 137
Asp Met Asp Tyr Phe Gly Met Asp Val
1 5
<210> 138
<211> 118
<212> PRT
<213> Homo Sapien
<400> 138
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ile Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Asp Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asp Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 139
<211> 355
<212> DNA
<213> Homo Sapien
<400> 139
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag cgtctggatt caccttccgt atttatggca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcagtt atatggtatg atggaagtaa taaatactat 180
gctgactccg tgaagggccg attcaccatc tccagagaca attccgacaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggctgtgt attactgtgc gagagatatg 300
gactacttcg gtatggacgt ctggggccaa gggaccacgg tcaccgtctc ctcag 355
<210> 140
<211> 448
<212> PRT
<213> Homo Sapien
<400> 140
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ile Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Asp Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asp Tyr Phe Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 141
<211> 1344
<212> DNA
<213> Homo Sapien
<400> 141
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag cgtctggatt caccttccgt atttatggca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcagtt atatggtatg atggaagtaa taaatactat 180
gctgactccg tgaagggccg attcaccatc tccagagaca attccgacaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggctgtgt attactgtgc gagagatatg 300
gactacttcg gtatggacgt ctggggccaa gggaccacgg tcaccgtctc ctcagccagc 360
accaagggcc cctctgtgtt ccctctggcc ccttccagca agtccacctc tggcggaaca 420
gccgctctgg gctgcctcgt gaaggactac ttccccgagc ctgtgaccgt gtcctggaac 480
tctggcgctc tgaccagcgg agtgcacacc ttccctgctg tgctgcagtc ctccggcctg 540
tactccctgt cctccgtcgt gaccgtgcct tccagctctc tgggcaccca gacctacatc 600
tgcaacgtga accacaagcc ctccaacacc aaggtggaca agaaggtgga acccaagtcc 660
tgcgacaaga cccacacctg tcccccttgt cctgcccctg aactgctggg cggaccttcc 720
gtgttcctgt tccccccaaa gcccaaggac accctgatga tctcccggac ccccgaagtg 780
acctgcgtgg tggtggatgt gtcccacgag gaccctgaag tgaagttcaa ttggtacgtg 840
gacggcgtgg aagtgcacaa cgccaagacc aagcctagag aggaacagta caactccacc 900
taccgggtgg tgtccgtgct gaccgtgctg caccaggatt ggctgaacgg caaagagtac 960
aagtgcaagg tgtccaacaa ggccctgcct gcccccatcg aaaagaccat ctccaaggcc 1020
aagggccagc cccgggaacc ccaggtgtac acactgcccc ctagcaggga cgagctgacc 1080
aagaaccagg tgtccctgac ctgtctcgtg aaaggcttct acccctccga tatcgccgtg 1140
gaatgggagt ccaacggcca gcctgagaac aactacaaga ccaccccccc tgtgctggac 1200
tccgacggct cattcttcct gtacagcaag ctgacagtgg acaagtcccg gtggcagcag 1260
ggcaacgtgt tctcctgctc cgtgatgcac gaggccctgc acaaccacta cacccagaag 1320
tccctgtccc tgagccccgg caag 1344
<210> 142
<211> 6
<212> PRT
<213> Homo Sapien
<400> 142
Gln Gly Ile Arg Asn Asp
1 5
<210> 143
<211> 3
<212> PRT
<213> Homo Sapien
<400> 143
Ala Ala Ser
1
<210> 144
<211> 9
<212> PRT
<213> Homo Sapien
<400> 144
Leu Gln His Asn Ser Tyr Pro Arg Thr
1 5
<210> 145
<211> 11
<212> PRT
<213> Homo Sapien
<400> 145
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1 5 10
<210> 146
<211> 7
<212> PRT
<213> Homo Sapien
<400> 146
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 147
<211> 9
<212> PRT
<213> Homo Sapien
<400> 147
Leu Gln His Asn Ser Tyr Pro Arg Thr
1 5
<210> 148
<211> 107
<212> PRT
<213> Homo Sapien
<400> 148
Asp Leu Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 149
<211> 322
<212> DNA
<213> Homo Sapien
<400> 149
gacctccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gggcattaga aatgatttag gctggtatca gcagaaacca 120
gggaaagccc ctaagcgcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagaa ttcactctca caatcagcag cctgcagcct 240
gaagattttg caacttatta ctgtctacag cataatagtt accctcggac gttcggccaa 300
gggaccaagg tggaaatcaa ac 322
<210> 150
<211> 214
<212> PRT
<213> Homo Sapien
<400> 150
Asp Leu Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 151
<211> 642
<212> DNA
<213> Homo Sapien
<400> 151
gacctccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gggcattaga aatgatttag gctggtatca gcagaaacca 120
gggaaagccc ctaagcgcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagaa ttcactctca caatcagcag cctgcagcct 240
gaagattttg caacttatta ctgtctacag cataatagtt accctcggac gttcggccaa 300
gggaccaagg tggaaatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 152
<211> 9
<212> PRT
<213> Homo Sapien
<400> 152
Gly Gly Ser Ile Ser Ser Ser Asp Trp
1 5
<210> 153
<211> 7
<212> PRT
<213> Homo Sapien
<400> 153
Ile Phe His Ser Gly Asn Thr
1 5
<210> 154
<211> 8
<212> PRT
<213> Homo Sapien
<400> 154
Val Arg Asp Gly Ser Gly Ser Tyr
1 5
<210> 155
<211> 6
<212> PRT
<213> Homo Sapien
<400> 155
Ser Ser Asp Trp Trp Ser
1 5
<210> 156
<211> 16
<212> PRT
<213> Homo Sapien
<400> 156
Glu Ile Phe His Ser Gly Asn Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 157
<211> 6
<212> PRT
<213> Homo Sapien
<400> 157
Asp Gly Ser Gly Ser Tyr
1 5
<210> 158
<211> 115
<212> PRT
<213> Homo Sapien
<400> 158
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Asp Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Ile Phe His Ser Gly Asn Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Ile Ser
65 70 75 80
Leu Arg Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Gly Ser Gly Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 159
<211> 346
<212> DNA
<213> Homo Sapien
<400> 159
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcgctg tctctggtgg ctccatcagc agtagtgact ggtggagttg ggtccgccag 120
cccccaggga aggggctgga gtggattggg gaaatctttc atagtgggaa caccaactac 180
aacccgtccc tcaagagtcg agtcaccata tcagtagaca agtccaagaa ccagatctcc 240
ctgaggctga actctgtgac cgccgcggac acggccgtgt attactgtgt gagagatggt 300
tcggggagtt actggggcca gggaaccctg gtcaccgtct cctcag 346
<210> 160
<211> 445
<212> PRT
<213> Homo Sapien
<400> 160
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Asp Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Ile Phe His Ser Gly Asn Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Ile Ser
65 70 75 80
Leu Arg Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Gly Ser Gly Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 161
<211> 1335
<212> DNA
<213> Homo Sapien
<400> 161
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcgctg tctctggtgg ctccatcagc agtagtgact ggtggagttg ggtccgccag 120
cccccaggga aggggctgga gtggattggg gaaatctttc atagtgggaa caccaactac 180
aacccgtccc tcaagagtcg agtcaccata tcagtagaca agtccaagaa ccagatctcc 240
ctgaggctga actctgtgac cgccgcggac acggccgtgt attactgtgt gagagatggt 300
tcggggagtt actggggcca gggaaccctg gtcaccgtct cctcagccag caccaagggc 360
ccctctgtgt tccctctggc cccttccagc aagtccacct ctggcggaac agccgctctg 420
ggctgcctcg tgaaggacta cttccccgag cctgtgaccg tgtcctggaa ctctggcgct 480
ctgaccagcg gagtgcacac cttccctgct gtgctgcagt cctccggcct gtactccctg 540
tcctccgtcg tgaccgtgcc ttccagctct ctgggcaccc agacctacat ctgcaacgtg 600
aaccacaagc cctccaacac caaggtggac aagaaggtgg aacccaagtc ctgcgacaag 660
acccacacct gtcccccttg tcctgcccct gaactgctgg gcggaccttc cgtgttcctg 720
ttccccccaa agcccaagga caccctgatg atctcccgga cccccgaagt gacctgcgtg 780
gtggtggatg tgtcccacga ggaccctgaa gtgaagttca attggtacgt ggacggcgtg 840
gaagtgcaca acgccaagac caagcctaga gaggaacagt acaactccac ctaccgggtg 900
gtgtccgtgc tgaccgtgct gcaccaggat tggctgaacg gcaaagagta caagtgcaag 960
gtgtccaaca aggccctgcc tgcccccatc gaaaagacca tctccaaggc caagggccag 1020
ccccgggaac cccaggtgta cacactgccc cctagcaggg acgagctgac caagaaccag 1080
gtgtccctga cctgtctcgt gaaaggcttc tacccctccg atatcgccgt ggaatgggag 1140
tccaacggcc agcctgagaa caactacaag accacccccc ctgtgctgga ctccgacggc 1200
tcattcttcc tgtacagcaa gctgacagtg gacaagtccc ggtggcagca gggcaacgtg 1260
ttctcctgct ccgtgatgca cgaggccctg cacaaccact acacccagaa gtccctgtcc 1320
ctgagccccg gcaag 1335
<210> 162
<211> 12
<212> PRT
<213> Homo Sapien
<400> 162
Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr
1 5 10
<210> 163
<211> 3
<212> PRT
<213> Homo Sapien
<400> 163
Trp Ala Ser
1
<210> 164
<211> 8
<212> PRT
<213> Homo Sapien
<400> 164
Gln Gln Tyr Tyr Ser Thr Arg Ser
1 5
<210> 165
<211> 17
<212> PRT
<213> Homo Sapien
<400> 165
Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 166
<211> 7
<212> PRT
<213> Homo Sapien
<400> 166
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 167
<211> 8
<212> PRT
<213> Homo Sapien
<400> 167
Gln Gln Tyr Tyr Ser Thr Arg Ser
1 5
<210> 168
<211> 112
<212> PRT
<213> Homo Sapien
<400> 168
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Arg Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 169
<211> 337
<212> DNA
<213> Homo Sapien
<400> 169
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acaataagaa ctacttagct 120
tggtaccagc agaaaccagg acagcctcct aaactgctca tttactgggc atctacccgg 180
gaatccgggg tccctgaccg attcagtggc agcgggtctg ggacagattt cactctcacc 240
atcagcagcc tgcaggctga agatgtggca gtttattact gtcagcaata ttatagtact 300
cgcagttttg gccaggggac caagctggag atcaaac 337
<210> 170
<211> 219
<212> PRT
<213> Homo Sapien
<400> 170
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Arg Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 171
<211> 657
<212> DNA
<213> Homo Sapien
<400> 171
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acaataagaa ctacttagct 120
tggtaccagc agaaaccagg acagcctcct aaactgctca tttactgggc atctacccgg 180
gaatccgggg tccctgaccg attcagtggc agcgggtctg ggacagattt cactctcacc 240
atcagcagcc tgcaggctga agatgtggca gtttattact gtcagcaata ttatagtact 300
cgcagttttg gccaggggac caagctggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 172
<211> 10
<212> PRT
<213> Homo Sapien
<400> 172
Gly Gly Ser Ile Ser Ser Ser Ser Tyr Tyr
1 5 10
<210> 173
<211> 7
<212> PRT
<213> Homo Sapien
<400> 173
Ile Tyr Ser Thr Gly Tyr Thr
1 5
<210> 174
<211> 13
<212> PRT
<213> Homo Sapien
<400> 174
Ala Ile Ser Thr Ala Ala Gly Pro Glu Tyr Phe His Arg
1 5 10
<210> 175
<211> 7
<212> PRT
<213> Homo Sapien
<400> 175
Ser Ser Ser Tyr Tyr Cys Gly
1 5
<210> 176
<211> 16
<212> PRT
<213> Homo Sapien
<400> 176
Ser Ile Tyr Ser Thr Gly Tyr Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 177
<211> 11
<212> PRT
<213> Homo Sapien
<400> 177
Ser Thr Ala Ala Gly Pro Glu Tyr Phe His Arg
1 5 10
<210> 178
<211> 120
<212> PRT
<213> Homo Sapien
<400> 178
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
1 5 10 15
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr
20 25 30
Tyr Cys Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Ser Ile Tyr Ser Thr Gly Tyr Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Gln Phe Ser Cys
65 70 75 80
Leu Ile Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ile Ser Thr Ala Ala Gly Pro Glu Tyr Phe His Arg Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 179
<211> 361
<212> DNA
<213> Homo Sapien
<400> 179
cagctgcagg agtcgggccc aggcctggtg aagccttcgg agaccctgtc cctcacctgc 60
actgtctctg gtggctccat cagcagtagt agttattact gcggctggat ccgccagccc 120
cctgggaagg ggctggactg gattgggagt atctattcta ctgggtacac ctactacaac 180
ccgtccctca agagtcgagt caccatttcc atagacacgt ccaagaacca gttctcatgc 240
ctgatactga cctctgtgac cgccgcagac acggctgtgt attactgtgc gataagtaca 300
gcagctggcc ctgaatactt ccatcgctgg ggccagggca ccctggtcac cgtctcctca 360
g 361
<210> 180
<211> 450
<212> PRT
<213> Homo Sapien
<400> 180
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
1 5 10 15
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr
20 25 30
Tyr Cys Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Ser Ile Tyr Ser Thr Gly Tyr Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Gln Phe Ser Cys
65 70 75 80
Leu Ile Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ile Ser Thr Ala Ala Gly Pro Glu Tyr Phe His Arg Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 181
<211> 1350
<212> DNA
<213> Homo Sapien
<400> 181
cagctgcagg agtcgggccc aggcctggtg aagccttcgg agaccctgtc cctcacctgc 60
actgtctctg gtggctccat cagcagtagt agttattact gcggctggat ccgccagccc 120
cctgggaagg ggctggactg gattgggagt atctattcta ctgggtacac ctactacaac 180
ccgtccctca agagtcgagt caccatttcc atagacacgt ccaagaacca gttctcatgc 240
ctgatactga cctctgtgac cgccgcagac acggctgtgt attactgtgc gataagtaca 300
gcagctggcc ctgaatactt ccatcgctgg ggccagggca ccctggtcac cgtctcctca 360
gccagcacca agggcccctc tgtgttccct ctggcccctt ccagcaagtc cacctctggc 420
ggaacagccg ctctgggctg cctcgtgaag gactacttcc ccgagcctgt gaccgtgtcc 480
tggaactctg gcgctctgac cagcggagtg cacaccttcc ctgctgtgct gcagtcctcc 540
ggcctgtact ccctgtcctc cgtcgtgacc gtgccttcca gctctctggg cacccagacc 600
tacatctgca acgtgaacca caagccctcc aacaccaagg tggacaagaa ggtggaaccc 660
aagtcctgcg acaagaccca cacctgtccc ccttgtcctg cccctgaact gctgggcgga 720
ccttccgtgt tcctgttccc cccaaagccc aaggacaccc tgatgatctc ccggaccccc 780
gaagtgacct gcgtggtggt ggatgtgtcc cacgaggacc ctgaagtgaa gttcaattgg 840
tacgtggacg gcgtggaagt gcacaacgcc aagaccaagc ctagagagga acagtacaac 900
tccacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggattggct gaacggcaaa 960
gagtacaagt gcaaggtgtc caacaaggcc ctgcctgccc ccatcgaaaa gaccatctcc 1020
aaggccaagg gccagccccg ggaaccccag gtgtacacac tgccccctag cagggacgag 1080
ctgaccaaga accaggtgtc cctgacctgt ctcgtgaaag gcttctaccc ctccgatatc 1140
gccgtggaat gggagtccaa cggccagcct gagaacaact acaagaccac cccccctgtg 1200
ctggactccg acggctcatt cttcctgtac agcaagctga cagtggacaa gtcccggtgg 1260
cagcagggca acgtgttctc ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 1320
cagaagtccc tgtccctgag ccccggcaag 1350
<210> 182
<211> 12
<212> PRT
<213> Homo Sapien
<400> 182
Gln Ser Val Leu Tyr Ser Ser Asn Ser Lys Asn Phe
1 5 10
<210> 183
<211> 3
<212> PRT
<213> Homo Sapien
<400> 183
Trp Ala Ser
1
<210> 184
<211> 9
<212> PRT
<213> Homo Sapien
<400> 184
Gln Gln Tyr Tyr Ser Thr Pro Arg Thr
1 5
<210> 185
<211> 17
<212> PRT
<213> Homo Sapien
<400> 185
Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser Asn Ser Lys Asn Phe Leu
1 5 10 15
Ala
<210> 186
<211> 7
<212> PRT
<213> Homo Sapien
<400> 186
Trp Ala Ser Thr Arg Gly Ser
1 5
<210> 187
<211> 9
<212> PRT
<213> Homo Sapien
<400> 187
Gln Gln Tyr Tyr Ser Thr Pro Arg Thr
1 5
<210> 188
<211> 113
<212> PRT
<213> Homo Sapien
<400> 188
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Ser Lys Asn Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Phe Ile Tyr Trp Ala Ser Thr Arg Gly Ser Gly Val
50 55 60
Pro Asp Arg Ile Ser Gly Ser Gly Ser Gly Thr Asp Phe Asn Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 189
<211> 340
<212> DNA
<213> Homo Sapien
<400> 189
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acagtaagaa cttcttagct 120
tggtaccagc agaaaccggg acagcctcct aagctgttca tttactgggc atctacccgg 180
ggatccgggg tccctgaccg aatcagtggc agcgggtctg ggacagattt caatctcacc 240
atcagcagcc tgcaggctga agatgtggca gtttattact gtcaacaata ttatagtact 300
cctcggacgt tcggccaagg gaccaaggtg gagatcaaac 340
<210> 190
<211> 220
<212> PRT
<213> Homo Sapien
<400> 190
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Ser Lys Asn Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Phe Ile Tyr Trp Ala Ser Thr Arg Gly Ser Gly Val
50 55 60
Pro Asp Arg Ile Ser Gly Ser Gly Ser Gly Thr Asp Phe Asn Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 191
<211> 660
<212> DNA
<213> Homo Sapien
<400> 191
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc 60
atcaactgca agtccagcca gagtgtttta tacagctcca acagtaagaa cttcttagct 120
tggtaccagc agaaaccggg acagcctcct aagctgttca tttactgggc atctacccgg 180
ggatccgggg tccctgaccg aatcagtggc agcgggtctg ggacagattt caatctcacc 240
atcagcagcc tgcaggctga agatgtggca gtttattact gtcaacaata ttatagtact 300
cctcggacgt tcggccaagg gaccaaggtg gagatcaaac gtacggtggc cgctccctcc 360
gtgttcatct tcccaccttc cgacgagcag ctgaagtccg gcaccgcttc tgtcgtgtgc 420
ctgctgaaca acttctaccc ccgcgaggcc aaggtgcagt ggaaggtgga caacgccctg 480
cagtccggca actcccagga atccgtgacc gagcaggact ccaaggacag cacctactcc 540
ctgtcctcca ccctgaccct gtccaaggcc gactacgaga agcacaaggt gtacgcctgc 600
gaagtgaccc accagggcct gtctagcccc gtgaccaagt ctttcaaccg gggcgagtgt 660
<210> 192
<211> 981
<212> DNA
<213> Homo Sapien
<400> 192
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 193
<211> 327
<212> PRT
<213> Homo Sapien
<400> 193
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 194
<211> 981
<212> DNA
<213> Homo Sapien
<400> 194
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccgtgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcgtgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 195
<211> 327
<212> PRT
<213> Homo Sapien
<400> 195
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Val His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 196
<211> 981
<212> DNA
<213> Homo Sapien
<400> 196
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaagctc accgtggaca agagcaggtg gcaggagggg 900
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 197
<211> 327
<212> PRT
<213> Homo Sapien
<400> 197
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 198
<211> 981
<212> DNA
<213> Homo Sapien
<400> 198
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctgaat ttgagggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 199
<211> 327
<212> PRT
<213> Homo Sapien
<400> 199
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 200
<211> 981
<212> DNA
<213> Homo Sapien
<400> 200
gcctccacca agggacctag cgtgttccct ctcgccccct gttccaggtc cacaagcgag 60
tccaccgctg ccctcggctg tctggtgaaa gactactttc ccgagcccgt gaccgtctcc 120
tggaatagcg gagccctgac ctccggcgtg cacacatttc ccgccgtgct gcagagcagc 180
ggactgtata gcctgagcag cgtggtgacc gtgcccagct ccagcctcgg caccaaaacc 240
tacacctgca acgtggacca caagccctcc aacaccaagg tggacaagcg ggtggagagc 300
aagtacggcc ccccttgccc tccttgtcct gcccctgagt tcgagggagg accctccgtg 360
ttcctgtttc cccccaaacc caaggacacc ctgatgatct cccggacacc cgaggtgacc 420
tgtgtggtcg tggacgtcag ccaggaggac cccgaggtgc agttcaactg gtatgtggac 480
ggcgtggagg tgcacaatgc caaaaccaag cccagggagg agcagttcaa ttccacctac 540
agggtggtga gcgtgctgac cgtcctgcat caggattggc tgaacggcaa ggagtacaag 600
tgcaaggtgt ccaacaaggg actgcccagc tccatcgaga agaccatcag caaggctaag 660
ggccagccga gggagcccca ggtgtatacc ctgcctccta gccaggaaga gatgaccaag 720
aaccaagtgt ccctgacctg cctggtgaag ggattctacc cctccgacat cgccgtggag 780
tgggagagca atggccagcc cgagaacaac tacaaaacaa cccctcccgt gctcgatagc 840
gacggcagct tctttctcta cagccggctg acagtggaca agagcaggtg gcaggagggc 900
aacgtgttct cctgttccgt gatgcacgag gccctgcaca atcactacac ccagaagagc 960
ctctccctgt ccctgggcaa g 981
<210> 201
<211> 981
<212> DNA
<213> Homo Sapien
<400> 201
gccagcacca agggcccttc cgtgttcccc ctggcccctt gcagcaggag cacctccgaa 60
tccacagctg ccctgggctg tctggtgaag gactactttc ccgagcccgt gaccgtgagc 120
tggaacagcg gcgctctgac atccggcgtc cacacctttc ctgccgtcct gcagtcctcc 180
ggcctctact ccctgtcctc cgtggtgacc gtgcctagct cctccctcgg caccaagacc 240
tacacctgta acgtggacca caaaccctcc aacaccaagg tggacaaacg ggtcgagagc 300
aagtacggcc ctccctgccc tccttgtcct gcccccgagt tcgaaggcgg acccagcgtg 360
ttcctgttcc ctcctaagcc caaggacacc ctcatgatca gccggacacc cgaggtgacc 420
tgcgtggtgg tggatgtgag ccaggaggac cctgaggtcc agttcaactg gtatgtggat 480
ggcgtggagg tgcacaacgc caagacaaag ccccgggaag agcagttcaa ctccacctac 540
agggtggtca gcgtgctgac cgtgctgcat caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtca gcaataaggg actgcccagc agcatcgaga agaccatctc caaggctaaa 660
ggccagcccc gggaacctca ggtgtacacc ctgcctccca gccaggagga gatgaccaag 720
aaccaggtga gcctgacctg cctggtgaag ggattctacc cttccgacat cgccgtggag 780
tgggagtcca acggccagcc cgagaacaat tataagacca cccctcccgt cctcgacagc 840
gacggatcct tctttctgta ctccaggctg accgtggata agtccaggtg gcaggaaggc 900
aacgtgttca gctgctccgt gatgcacgag gccctgcaca atcactacac ccagaagtcc 960
ctgagcctgt ccctgggaaa g 981
<210> 202
<211> 981
<212> DNA
<213> Homo Sapien
<400> 202
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctccag ttgcgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 203
<211> 327
<212> PRT
<213> Homo Sapien
<400> 203
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 204
<211> 990
<212> DNA
<213> Homo Sapien
<400> 204
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agtggagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cgcgggggca 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 205
<211> 330
<212> PRT
<213> Homo Sapien
<400> 205
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Ala Gly Ala Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 206
<211> 321
<212> DNA
<213> Homo Sapien
<400> 206
cgtacggtgg ccgctccctc cgtgttcatc ttcccacctt ccgacgagca gctgaagtcc 60
ggcaccgctt ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaggtgcag 120
tggaaggtgg acaacgccct gcagtccggc aactcccagg aatccgtgac cgagcaggac 180
tccaaggaca gcacctactc cctgtcctcc accctgaccc tgtccaaggc cgactacgag 240
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 300
tctttcaacc ggggcgagtg t 321
<210> 207
<211> 107
<212> PRT
<213> Homo Sapien
<400> 207
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 208
<211> 321
<212> DNA
<213> Homo Sapien
<400> 208
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgccgg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 209
<211> 107
<212> PRT
<213> Homo Sapien
<400> 209
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Gly Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 210
<211> 321
<212> DNA
<213> Homo Sapien
<400> 210
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
cggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 211
<211> 107
<212> PRT
<213> Homo Sapien
<400> 211
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Arg Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 212
<211> 321
<212> DNA
<213> Homo Sapien
<400> 212
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaac tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 213
<211> 107
<212> PRT
<213> Homo Sapien
<400> 213
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Leu Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 214
<211> 321
<212> DNA
<213> Homo Sapien
<400> 214
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcaac accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg c 321
<210> 215
<211> 107
<212> PRT
<213> Homo Sapien
<400> 215
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Asn Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 216
<211> 312
<212> DNA
<213> Homo Sapien
<400> 216
cccaaggcca accccacggt cactctgttc ccgccctcct ctgaggagct ccaagccaac 60
aaggccacac tagtgtgtct gatcagtgac ttctacccgg gagctgtgac agtggcttgg 120
aaggcagatg gcagccccgt caaggcggga gtggagacga ccaaaccctc caaacagagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ccgagcagtg gaagtcccac 240
agaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agtggcccct 300
acagaatgtt ca 312
<210> 217
<211> 104
<212> PRT
<213> Homo Sapien
<400> 217
Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 218
<211> 318
<212> DNA
<213> Homo Sapien
<400> 218
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 219
<211> 106
<212> PRT
<213> Homo Sapien
<400> 219
Gly Gln Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 220
<211> 318
<212> DNA
<213> Homo Sapien
<400> 220
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 221
<211> 318
<212> DNA
<213> Homo Sapien
<400> 221
ggccagccta aggccgctcc ttctgtgacc ctgttccccc catcctccga ggaactgcag 60
gctaacaagg ccaccctcgt gtgcctgatc agcgacttct accctggcgc cgtgaccgtg 120
gcctggaagg ctgatagctc tcctgtgaag gccggcgtgg aaaccaccac cccttccaag 180
cagtccaaca acaaatacgc cgcctcctcc tacctgtccc tgacccctga gcagtggaag 240
tcccaccggt cctacagctg ccaagtgacc cacgagggct ccaccgtgga aaagaccgtg 300
gctcctaccg agtgctcc 318
<210> 222
<211> 318
<212> DNA
<213> Homo Sapien
<400> 222
ggccagccta aagctgcccc cagcgtcacc ctgtttcctc cctccagcga ggagctccag 60
gccaacaagg ccaccctcgt gtgcctgatc tccgacttct atcccggcgc tgtgaccgtg 120
gcttggaaag ccgactccag ccctgtcaaa gccggcgtgg agaccaccac accctccaag 180
cagtccaaca acaagtacgc cgcctccagc tatctctccc tgacccctga gcagtggaag 240
tcccaccggt cctactcctg tcaggtgacc cacgagggct ccaccgtgga aaagaccgtc 300
gcccccaccg agtgctcc 318
<210> 223
<211> 106
<212> PRT
<213> Homo Sapien
<400> 223
Gly Gln Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 224
<211> 318
<212> DNA
<213> Homo Sapien
<400> 224
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tatctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 225
<211> 106
<212> PRT
<213> Homo Sapien
<400> 225
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 226
<211> 312
<212> DNA
<213> Homo Sapien
<400> 226
cccaaggctg ccccctcggt cactctgttc ccaccctcct ctgaggagct tcaagccaac 60
aaggccacac tggtgtgtct cataagtgac ttctacccgg gagccgtgac agttgcctgg 120
aaggcagata gcagccccgt caaggcgggg gtggagacca ccacaccctc caaacaaagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ctgagcagtg gaagtcccac 240
aaaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agttgcccct 300
acggaatgtt ca 312
<210> 227
<211> 104
<212> PRT
<213> Homo Sapien
<400> 227
Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 228
<211> 318
<212> DNA
<213> Homo Sapien
<400> 228
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccggggcc agtgacagtt 120
gcctggaagg cagatagcag ccccgtcaag gcgggggtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacgg aatgttca 318
<210> 229
<211> 106
<212> PRT
<213> Homo Sapien
<400> 229
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Pro Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 230
<211> 318
<212> DNA
<213> Homo Sapien
<400> 230
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 231
<211> 106
<212> PRT
<213> Homo Sapien
<400> 231
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 232
<211> 318
<212> DNA
<213> Homo Sapien
<400> 232
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 233
<211> 106
<212> PRT
<213> Homo Sapien
<400> 233
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 234
<211> 318
<212> DNA
<213> Homo Sapien
<400> 234
ggtcagccca aggctgcccc atcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgcctgatc agtgacttct acccgggagc tgtgaaagtg 120
gcctggaagg cagatggcag ccccgtcaac acgggagtgg agaccaccac accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgttca 318
<210> 235
<211> 106
<212> PRT
<213> Homo Sapien
<400> 235
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Asn Thr Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 236
<211> 318
<212> DNA
<213> Homo Sapien
<400> 236
ggtcagccca aggctgcccc atcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcgta agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gtgggagtgg agaccaccaa accctccaaa 180
caaagcaaca acaagtatgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccgggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgctct 318
<210> 237
<211> 106
<212> PRT
<213> Homo Sapien
<400> 237
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Val Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Val Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Arg Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 238
<211> 8
<212> PRT
<213> Homo Sapien
<400> 238
Gly Phe Thr Phe Ser Asp Tyr Tyr
1 5
<210> 239
<211> 8
<212> PRT
<213> Homo Sapien
<400> 239
Ile Ser Thr Ser Gly Ser Thr Ile
1 5
<210> 240
<211> 16
<212> PRT
<213> Homo Sapien
<400> 240
Ala Arg Gly Ile Thr Gly Thr Asn Phe Tyr His Tyr Gly Leu Gly Val
1 5 10 15
<210> 241
<211> 5
<212> PRT
<213> Homo Sapien
<400> 241
Asp Tyr Tyr Met Ser
1 5
<210> 242
<211> 17
<212> PRT
<213> Homo Sapien
<400> 242
Tyr Ile Ser Thr Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 243
<211> 14
<212> PRT
<213> Homo Sapien
<400> 243
Gly Ile Thr Gly Thr Asn Phe Tyr His Tyr Gly Leu Gly Val
1 5 10
<210> 244
<211> 123
<212> PRT
<213> Homo Sapien
<400> 244
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Thr Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Ala Ala Val Tyr His Cys
85 90 95
Ala Arg Gly Ile Thr Gly Thr Asn Phe Tyr His Tyr Gly Leu Gly Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 245
<211> 370
<212> DNA
<213> Homo Sapien
<400> 245
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactactaca tgagctggat ccgccaggtt 120
ccagggaagg ggctggagtg ggtttcatac attagtacta gtggtagtac catatactac 180
gcagactctg tgaagggccg attcaccatc tccagggaca acgccaagaa ctcactgtat 240
ctacaaatga acagcctgag agccgaggac gcggccgtgt atcactgtgc gagaggtata 300
actggaacta acttctacca ctacggtttg ggcgtctggg gccaagggac cacggtcacc 360
gtctcctcag 370
<210> 246
<211> 453
<212> PRT
<213> Homo Sapien
<400> 246
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Thr Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Ala Ala Val Tyr His Cys
85 90 95
Ala Arg Gly Ile Thr Gly Thr Asn Phe Tyr His Tyr Gly Leu Gly Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly Lys
450
<210> 247
<211> 1359
<212> DNA
<213> Homo Sapien
<400> 247
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactactaca tgagctggat ccgccaggtt 120
ccagggaagg ggctggagtg ggtttcatac attagtacta gtggtagtac catatactac 180
gcagactctg tgaagggccg attcaccatc tccagggaca acgccaagaa ctcactgtat 240
ctacaaatga acagcctgag agccgaggac gcggccgtgt atcactgtgc gagaggtata 300
actggaacta acttctacca ctacggtttg ggcgtctggg gccaagggac cacggtcacc 360
gtctcctcag ccagcaccaa gggcccctct gtgttccctc tggccccttc cagcaagtcc 420
acctctggcg gaacagccgc tctgggctgc ctcgtgaagg actacttccc cgagcctgtg 480
accgtgtcct ggaactctgg cgctctgacc agcggagtgc acaccttccc tgctgtgctg 540
cagtcctccg gcctgtactc cctgtcctcc gtcgtgaccg tgccttccag ctctctgggc 600
acccagacct acatctgcaa cgtgaaccac aagccctcca acaccaaggt ggacaagaag 660
gtggaaccca agtcctgcga caagacccac acctgtcccc cttgtcctgc ccctgaactg 720
ctgggcggac cttccgtgtt cctgttcccc ccaaagccca aggacaccct gatgatctcc 780
cggacccccg aagtgacctg cgtggtggtg gatgtgtccc acgaggaccc tgaagtgaag 840
ttcaattggt acgtggacgg cgtggaagtg cacaacgcca agaccaagcc tagagaggaa 900
cagtacaact ccacctaccg ggtggtgtcc gtgctgaccg tgctgcacca ggattggctg 960
aacggcaaag agtacaagtg caaggtgtcc aacaaggccc tgcctgcccc catcgaaaag 1020
accatctcca aggccaaggg ccagccccgg gaaccccagg tgtacacact gccccctagc 1080
agggacgagc tgaccaagaa ccaggtgtcc ctgacctgtc tcgtgaaagg cttctacccc 1140
tccgatatcg ccgtggaatg ggagtccaac ggccagcctg agaacaacta caagaccacc 1200
ccccctgtgc tggactccga cggctcattc ttcctgtaca gcaagctgac agtggacaag 1260
tcccggtggc agcagggcaa cgtgttctcc tgctccgtga tgcacgaggc cctgcacaac 1320
cactacaccc agaagtccct gtccctgagc cccggcaag 1359
<210> 248
<211> 6
<212> PRT
<213> Homo Sapien
<400> 248
Gln Gly Ile Asn Ser Trp
1 5
<210> 249
<211> 3
<212> PRT
<213> Homo Sapien
<400> 249
Ala Ala Ser
1
<210> 250
<211> 9
<212> PRT
<213> Homo Sapien
<400> 250
Gln Gln Val Asn Ser Phe Pro Leu Thr
1 5
<210> 251
<211> 11
<212> PRT
<213> Homo Sapien
<400> 251
Arg Ala Ser Gln Gly Ile Asn Ser Trp Leu Ala
1 5 10
<210> 252
<211> 7
<212> PRT
<213> Homo Sapien
<400> 252
Ala Ala Ser Thr Leu Gln Ser
1 5
<210> 253
<211> 9
<212> PRT
<213> Homo Sapien
<400> 253
Gln Gln Val Asn Ser Phe Pro Leu Thr
1 5
<210> 254
<211> 107
<212> PRT
<213> Homo Sapien
<400> 254
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Val Asn Ser Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 255
<211> 322
<212> DNA
<213> Homo Sapien
<400> 255
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattaac agctggttag cctggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccactt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtgggtc tggggcagat ttcactctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gttaacagtt tcccgctcac tttcggcgga 300
gggaccaagg tggagatcaa ac 322
<210> 256
<211> 214
<212> PRT
<213> Homo Sapien
<400> 256
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Val Asn Ser Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 257
<211> 642
<212> DNA
<213> Homo Sapien
<400> 257
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattaac agctggttag cctggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccactt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtgggtc tggggcagat ttcactctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gttaacagtt tcccgctcac tttcggcgga 300
gggaccaagg tggagatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 258
<211> 8
<212> PRT
<213> Homo Sapien
<400> 258
Gly Phe Thr Phe Ser Tyr Tyr Ala
1 5
<210> 259
<211> 8
<212> PRT
<213> Homo Sapien
<400> 259
Ile Ser Gly Gly Gly Gly Asn Thr
1 5
<210> 260
<211> 16
<212> PRT
<213> Homo Sapien
<400> 260
Ala Lys Asp Arg Met Lys Gln Leu Val Arg Ala Tyr Tyr Phe Asp Tyr
1 5 10 15
<210> 261
<211> 5
<212> PRT
<213> Homo Sapien
<400> 261
Tyr Tyr Ala Met Ser
1 5
<210> 262
<211> 17
<212> PRT
<213> Homo Sapien
<400> 262
Thr Ile Ser Gly Gly Gly Gly Asn Thr His Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 263
<211> 14
<212> PRT
<213> Homo Sapien
<400> 263
Asp Arg Met Lys Gln Leu Val Arg Ala Tyr Tyr Phe Asp Tyr
1 5 10
<210> 264
<211> 123
<212> PRT
<213> Homo Sapien
<400> 264
Glu Val Pro Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Tyr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Asp Trp Val
35 40 45
Ser Thr Ile Ser Gly Gly Gly Gly Asn Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Met Lys Gln Leu Val Arg Ala Tyr Tyr Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 265
<211> 370
<212> DNA
<213> Homo Sapien
<400> 265
gaggtgccgc tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagc tactatgcca tgagctgggt ccgtcaggct 120
ccagggaagg ggctggactg ggtctcaact attagtggtg gtggtggtaa cacacactac 180
gcagactccg tgaagggccg attcactata tccagagaca attccaagaa cacgctgtat 240
ctgcacatga acagcctgag agccgaagac acggccgtct attactgtgc gaaggatcgg 300
atgaaacagc tcgtccgggc ctactacttt gactactggg gccagggaac cctggtcacc 360
gtctcctcag 370
<210> 266
<211> 453
<212> PRT
<213> Homo Sapien
<400> 266
Glu Val Pro Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Tyr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Asp Trp Val
35 40 45
Ser Thr Ile Ser Gly Gly Gly Gly Asn Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Met Lys Gln Leu Val Arg Ala Tyr Tyr Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly Lys
450
<210> 267
<211> 1359
<212> DNA
<213> Homo Sapien
<400> 267
gaggtgccgc tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacgtttagc tactatgcca tgagctgggt ccgtcaggct 120
ccagggaagg ggctggactg ggtctcaact attagtggtg gtggtggtaa cacacactac 180
gcagactccg tgaagggccg attcactata tccagagaca attccaagaa cacgctgtat 240
ctgcacatga acagcctgag agccgaagac acggccgtct attactgtgc gaaggatcgg 300
atgaaacagc tcgtccgggc ctactacttt gactactggg gccagggaac cctggtcacc 360
gtctcctcag ccagcaccaa gggcccctct gtgttccctc tggccccttc cagcaagtcc 420
acctctggcg gaacagccgc tctgggctgc ctcgtgaagg actacttccc cgagcctgtg 480
accgtgtcct ggaactctgg cgctctgacc agcggagtgc acaccttccc tgctgtgctg 540
cagtcctccg gcctgtactc cctgtcctcc gtcgtgaccg tgccttccag ctctctgggc 600
acccagacct acatctgcaa cgtgaaccac aagccctcca acaccaaggt ggacaagaag 660
gtggaaccca agtcctgcga caagacccac acctgtcccc cttgtcctgc ccctgaactg 720
ctgggcggac cttccgtgtt cctgttcccc ccaaagccca aggacaccct gatgatctcc 780
cggacccccg aagtgacctg cgtggtggtg gatgtgtccc acgaggaccc tgaagtgaag 840
ttcaattggt acgtggacgg cgtggaagtg cacaacgcca agaccaagcc tagagaggaa 900
cagtacaact ccacctaccg ggtggtgtcc gtgctgaccg tgctgcacca ggattggctg 960
aacggcaaag agtacaagtg caaggtgtcc aacaaggccc tgcctgcccc catcgaaaag 1020
accatctcca aggccaaggg ccagccccgg gaaccccagg tgtacacact gccccctagc 1080
agggacgagc tgaccaagaa ccaggtgtcc ctgacctgtc tcgtgaaagg cttctacccc 1140
tccgatatcg ccgtggaatg ggagtccaac ggccagcctg agaacaacta caagaccacc 1200
ccccctgtgc tggactccga cggctcattc ttcctgtaca gcaagctgac agtggacaag 1260
tcccggtggc agcagggcaa cgtgttctcc tgctccgtga tgcacgaggc cctgcacaac 1320
cactacaccc agaagtccct gtccctgagc cccggcaag 1359
<210> 268
<211> 6
<212> PRT
<213> Homo Sapien
<400> 268
Gln Asp Ile Ser Thr Tyr
1 5
<210> 269
<211> 3
<212> PRT
<213> Homo Sapien
<400> 269
Gly Thr Ser
1
<210> 270
<211> 9
<212> PRT
<213> Homo Sapien
<400> 270
Gln Gln Leu His Thr Asp Pro Ile Thr
1 5
<210> 271
<211> 11
<212> PRT
<213> Homo Sapien
<400> 271
Trp Ala Ser Gln Asp Ile Ser Thr Tyr Leu Gly
1 5 10
<210> 272
<211> 7
<212> PRT
<213> Homo Sapien
<400> 272
Gly Thr Ser Ser Leu Gln Ser
1 5
<210> 273
<211> 9
<212> PRT
<213> Homo Sapien
<400> 273
Gln Gln Leu His Thr Asp Pro Ile Thr
1 5
<210> 274
<211> 107
<212> PRT
<213> Homo Sapien
<400> 274
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Trp Ala Ser Gln Asp Ile Ser Thr Tyr
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Thr Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu His Thr Asp Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 275
<211> 322
<212> DNA
<213> Homo Sapien
<400> 275
gacatccagt tgacccagtc tccatccttc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgct gggccagtca ggacattagc acttatttag gctggtatca gcaaaaacca 120
gggaaagccc ctaagctcct gatctatggt acatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagaa ttcactctca caatcagcag cctgcagcct 240
gaagattttg caacttatta ctgtcaacag cttcatactg acccgatcac cttcggccaa 300
gggacacgac tggagatcaa ac 322
<210> 276
<211> 214
<212> PRT
<213> Homo Sapien
<400> 276
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Trp Ala Ser Gln Asp Ile Ser Thr Tyr
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Thr Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu His Thr Asp Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 277
<211> 642
<212> DNA
<213> Homo Sapien
<400> 277
gacatccagt tgacccagtc tccatccttc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgct gggccagtca ggacattagc acttatttag gctggtatca gcaaaaacca 120
gggaaagccc ctaagctcct gatctatggt acatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagaa ttcactctca caatcagcag cctgcagcct 240
gaagattttg caacttatta ctgtcaacag cttcatactg acccgatcac cttcggccaa 300
gggacacgac tggagatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 278
<211> 8
<212> PRT
<213> Homo Sapien
<400> 278
Gly Phe Thr Phe Ser Ser Tyr Trp
1 5
<210> 279
<211> 8
<212> PRT
<213> Homo Sapien
<400> 279
Ile Lys Gln Asp Gly Ser Glu Lys
1 5
<210> 280
<211> 12
<212> PRT
<213> Homo Sapien
<400> 280
Ala Arg Val Arg Gln Trp Ser Asp Tyr Ser Asp Tyr
1 5 10
<210> 281
<211> 5
<212> PRT
<213> Homo Sapien
<400> 281
Ser Tyr Trp Met Asn
1 5
<210> 282
<211> 17
<212> PRT
<213> Homo Sapien
<400> 282
Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 283
<211> 10
<212> PRT
<213> Homo Sapien
<400> 283
Val Arg Gln Trp Ser Asp Tyr Ser Asp Tyr
1 5 10
<210> 284
<211> 119
<212> PRT
<213> Homo Sapien
<400> 284
Glu Val His Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Arg Gln Trp Ser Asp Tyr Ser Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 285
<211> 358
<212> DNA
<213> Homo Sapien
<400> 285
gaggtgcacc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagt agctattgga tgaactgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac ataaagcaag atggaagtga gaaatactat 180
gtggactctg tgaagggccg cttcaccgtc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acggctgtgt attactgtgc gagagttcga 300
caatggtccg actactctga ctactggggc cagggaaccc cggtcaccgt ctcctcag 358
<210> 286
<211> 449
<212> PRT
<213> Homo Sapien
<400> 286
Glu Val His Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Arg Gln Trp Ser Asp Tyr Ser Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 287
<211> 1347
<212> DNA
<213> Homo Sapien
<400> 287
gaggtgcacc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagt agctattgga tgaactgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtggccaac ataaagcaag atggaagtga gaaatactat 180
gtggactctg tgaagggccg cttcaccgtc tccagagaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acggctgtgt attactgtgc gagagttcga 300
caatggtccg actactctga ctactggggc cagggaaccc cggtcaccgt ctcctcagcc 360
agcaccaagg gcccctctgt gttccctctg gccccttcca gcaagtccac ctctggcgga 420
acagccgctc tgggctgcct cgtgaaggac tacttccccg agcctgtgac cgtgtcctgg 480
aactctggcg ctctgaccag cggagtgcac accttccctg ctgtgctgca gtcctccggc 540
ctgtactccc tgtcctccgt cgtgaccgtg ccttccagct ctctgggcac ccagacctac 600
atctgcaacg tgaaccacaa gccctccaac accaaggtgg acaagaaggt ggaacccaag 660
tcctgcgaca agacccacac ctgtccccct tgtcctgccc ctgaactgct gggcggacct 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatctcccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccac gaggaccctg aagtgaagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccta gagaggaaca gtacaactcc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg attggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caaggccctg cctgccccca tcgaaaagac catctccaag 1020
gccaagggcc agccccggga accccaggtg tacacactgc cccctagcag ggacgagctg 1080
accaagaacc aggtgtccct gacctgtctc gtgaaaggct tctacccctc cgatatcgcc 1140
gtggaatggg agtccaacgg ccagcctgag aacaactaca agaccacccc ccctgtgctg 1200
gactccgacg gctcattctt cctgtacagc aagctgacag tggacaagtc ccggtggcag 1260
cagggcaacg tgttctcctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ccctgagccc cggcaag 1347
<210> 288
<211> 6
<212> PRT
<213> Homo Sapien
<400> 288
Gln Gly Ile Ser Ser Trp
1 5
<210> 289
<211> 3
<212> PRT
<213> Homo Sapien
<400> 289
Ala Ala Ser
1
<210> 290
<211> 9
<212> PRT
<213> Homo Sapien
<400> 290
Gln Gln Ala Asn Ser Phe Pro Phe Thr
1 5
<210> 291
<211> 11
<212> PRT
<213> Homo Sapien
<400> 291
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 292
<211> 7
<212> PRT
<213> Homo Sapien
<400> 292
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 293
<211> 9
<212> PRT
<213> Homo Sapien
<400> 293
Gln Gln Ala Asn Ser Phe Pro Phe Thr
1 5
<210> 294
<211> 107
<212> PRT
<213> Homo Sapien
<400> 294
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 295
<211> 322
<212> DNA
<213> Homo Sapien
<400> 295
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattagc agctggttag cctggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagat ttcactctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagtt tcccattcac tttcggccct 300
gggaccaaag tggatatcaa ac 322
<210> 296
<211> 214
<212> PRT
<213> Homo Sapien
<400> 296
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 297
<211> 642
<212> DNA
<213> Homo Sapien
<400> 297
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattagc agctggttag cctggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagat ttcactctca ccatcagcag cctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagtt tcccattcac tttcggccct 300
gggaccaaag tggatatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 298
<211> 214
<212> PRT
<213> Homo Sapien
<400> 298
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 299
<211> 453
<212> PRT
<213> Homo Sapien
<400> 299
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Ala Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly Lys
450
<210> 300
<211> 347
<212> PRT
<213> Homo Sapien
<400> 300
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
210 215 220
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
225 230 235 240
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
245 250 255
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
260 265 270
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
275 280 285
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
290 295 300
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
305 310 315 320
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
325 330 335
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr
340 345
<210> 301
<211> 133
<212> PRT
<213> Homo Sapien
<400> 301
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 302
<211> 586
<212> PRT
<213> Homo Sapien
<400> 302
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Phe Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Ala Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly Lys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln
450 455 460
Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly
465 470 475 480
Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys
485 490 495
Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu
500 505 510
Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser
515 520 525
Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val
530 535 540
Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr
545 550 555 560
Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr
565 570 575
Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr
580 585
<210> 303
<211> 14
<212> PRT
<213> Homo Sapien
<400> 303
Ala Pro Thr Ser Thr Gln Leu Gln Leu Glu Leu Leu Leu Asp
1 5 10
<210> 304
<211> 11
<212> PRT
<213> Homo Sapien
<400> 304
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 305
<211> 17
<212> PRT
<213> Homo Sapien
<400> 305
Ala Pro Thr Ser Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu
1 5 10 15
Asp
<210> 306
<211> 19
<212> PRT
<213> Homo Sapien
<400> 306
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp
<210> 307
<211> 18
<212> PRT
<213> Homo Sapien
<400> 307
Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu
1 5 10 15
Leu Asp
<210> 308
<211> 17
<212> PRT
<213> Homo Sapien
<400> 308
Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu
1 5 10 15
Asp
<210> 309
<211> 16
<212> PRT
<213> Homo Sapien
<400> 309
Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 310
<211> 15
<212> PRT
<213> Homo Sapien
<400> 310
Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 311
<211> 14
<212> PRT
<213> Homo Sapien
<400> 311
Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 312
<211> 13
<212> PRT
<213> Homo Sapien
<400> 312
Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 313
<211> 12
<212> PRT
<213> Homo Sapien
<400> 313
Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 314
<211> 19
<212> PRT
<213> Homo Sapien
<400> 314
Ala Pro Thr Ser Ser Ser Thr Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp
<210> 315
<211> 18
<212> PRT
<213> Homo Sapien
<400> 315
Ala Pro Thr Ser Ser Ser Thr Thr Gln Leu Gln Leu Glu His Leu Leu
1 5 10 15
Leu Asp
<210> 316
<211> 17
<212> PRT
<213> Homo Sapien
<400> 316
Ala Pro Thr Ser Ser Ser Thr Gln Leu Gln Leu Glu His Leu Leu Leu
1 5 10 15
Asp
<210> 317
<211> 16
<212> PRT
<213> Homo Sapien
<400> 317
Ala Pro Thr Ser Ser Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 318
<211> 14
<212> PRT
<213> Homo Sapien
<400> 318
Ala Pro Thr Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 319
<211> 13
<212> PRT
<213> Homo Sapien
<400> 319
Ala Pro Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 320
<211> 12
<212> PRT
<213> Homo Sapien
<400> 320
Ala Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10
<210> 321
<211> 15
<212> PRT
<213> Homo Sapien
<400> 321
Ala Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 322
<211> 15
<212> PRT
<213> Homo Sapien
<400> 322
Ala Pro Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 323
<211> 15
<212> PRT
<213> Homo Sapien
<400> 323
Ala Pro Thr Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
1 5 10 15
<210> 324
<211> 113
<212> PRT
<213> Homo Sapien
<400> 324
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
1 5 10 15
Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu
20 25 30
Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu
35 40 45
Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp
50 55 60
Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu
65 70 75 80
Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu
85 90 95
Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu
100 105 110
Thr
<210> 325
<211> 290
<212> PRT
<213> Mus Musculus
<400> 325
Met Arg Ile Phe Ala Gly Ile Ile Phe Thr Ala Cys Cys His Leu Leu
1 5 10 15
Arg Ala Phe Thr Ile Thr Ala Pro Lys Asp Leu Tyr Val Val Glu Tyr
20 25 30
Gly Ser Asn Val Thr Met Glu Cys Arg Phe Pro Val Glu Arg Glu Leu
35 40 45
Asp Leu Leu Ala Leu Val Val Tyr Trp Glu Lys Glu Asp Glu Gln Val
50 55 60
Ile Gln Phe Val Ala Gly Glu Glu Asp Leu Lys Pro Gln His Ser Asn
65 70 75 80
Phe Arg Gly Arg Ala Ser Leu Pro Lys Asp Gln Leu Leu Lys Gly Asn
85 90 95
Ala Ala Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr
100 105 110
Cys Cys Ile Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Leu
115 120 125
Lys Val Asn Ala Pro Tyr Arg Lys Ile Asn Gln Arg Ile Ser Val Asp
130 135 140
Pro Ala Thr Ser Glu His Glu Leu Ile Cys Gln Ala Glu Gly Tyr Pro
145 150 155 160
Glu Ala Glu Val Ile Trp Thr Asn Ser Asp His Gln Pro Val Ser Gly
165 170 175
Lys Arg Ser Val Thr Thr Ser Arg Thr Glu Gly Met Leu Leu Asn Val
180 185 190
Thr Ser Ser Leu Arg Val Asn Ala Thr Ala Asn Asp Val Phe Tyr Cys
195 200 205
Thr Phe Trp Arg Ser Gln Pro Gly Gln Asn His Thr Ala Glu Leu Ile
210 215 220
Ile Pro Glu Leu Pro Ala Thr His Pro Pro Gln Asn Arg Thr His Trp
225 230 235 240
Val Leu Leu Gly Ser Ile Leu Leu Phe Leu Ile Val Val Ser Thr Val
245 250 255
Leu Leu Phe Leu Arg Lys Gln Val Arg Met Leu Asp Val Glu Lys Cys
260 265 270
Gly Val Glu Asp Thr Ser Ser Lys Asn Arg Asn Asp Thr Gln Phe Glu
275 280 285
Glu Thr
290
<210> 326
<211> 226
<212> PRT
<213> Mus Musculus
<400> 326
Phe Thr Ile Thr Ala Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Val Thr Met Glu Cys Arg Phe Pro Val Glu Arg Glu Leu Asp Leu
20 25 30
Leu Ala Leu Val Val Tyr Trp Glu Lys Glu Asp Glu Gln Val Ile Gln
35 40 45
Phe Val Ala Gly Glu Glu Asp Leu Lys Pro Gln His Ser Asn Phe Arg
50 55 60
Gly Arg Ala Ser Leu Pro Lys Asp Gln Leu Leu Lys Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Cys Cys
85 90 95
Ile Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Leu Lys Val
100 105 110
Asn Ala Pro Tyr Arg Lys Ile Asn Gln Arg Ile Ser Val Asp Pro Ala
115 120 125
Thr Ser Glu His Glu Leu Ile Cys Gln Ala Glu Gly Tyr Pro Glu Ala
130 135 140
Glu Val Ile Trp Thr Asn Ser Asp His Gln Pro Val Ser Gly Lys Arg
145 150 155 160
Ser Val Thr Thr Ser Arg Thr Glu Gly Met Leu Leu Asn Val Thr Ser
165 170 175
Ser Leu Arg Val Asn Ala Thr Ala Asn Asp Val Phe Tyr Cys Thr Phe
180 185 190
Trp Arg Ser Gln Pro Gly Gln Asn His Thr Ala Glu Leu Ile Ile Pro
195 200 205
Glu Leu Pro Ala Thr His Pro Pro Gln Asn Arg Thr His His His His
210 215 220
His His
225
<210> 327
<211> 251
<212> PRT
<213> Homo Sapien
<400> 327
Glu Leu Cys Asp Asp Asp Pro Pro Glu Ile Pro His Ala Thr Phe Lys
1 5 10 15
Ala Met Ala Tyr Lys Glu Gly Thr Met Leu Asn Cys Glu Cys Lys Arg
20 25 30
Gly Phe Arg Arg Ile Lys Ser Gly Ser Leu Tyr Met Leu Cys Thr Gly
35 40 45
Asn Ser Ser His Ser Ser Trp Asp Asn Gln Cys Gln Cys Thr Ser Ser
50 55 60
Ala Thr Arg Asn Thr Thr Lys Gln Val Thr Pro Gln Pro Glu Glu Gln
65 70 75 80
Lys Glu Arg Lys Thr Thr Glu Met Gln Ser Pro Met Gln Pro Val Asp
85 90 95
Gln Ala Ser Leu Pro Gly His Cys Arg Glu Pro Pro Pro Trp Glu Asn
100 105 110
Glu Ala Thr Glu Arg Ile Tyr His Phe Val Val Gly Gln Met Val Tyr
115 120 125
Tyr Gln Cys Val Gln Gly Tyr Arg Ala Leu His Arg Gly Pro Ala Glu
130 135 140
Ser Val Cys Lys Met Thr His Gly Lys Thr Arg Trp Thr Gln Pro Gln
145 150 155 160
Leu Ile Cys Thr Gly Glu Met Glu Thr Ser Gln Phe Pro Gly Glu Glu
165 170 175
Lys Pro Gln Ala Ser Pro Glu Gly Arg Pro Glu Ser Glu Thr Ser Cys
180 185 190
Leu Val Thr Thr Thr Asp Phe Gln Ile Gln Thr Glu Met Ala Ala Thr
195 200 205
Met Glu Thr Ser Ile Phe Thr Thr Glu Tyr Gln Val Ala Val Ala Gly
210 215 220
Cys Val Phe Leu Leu Ile Ser Val Leu Leu Leu Ser Gly Leu Thr Trp
225 230 235 240
Gln Arg Arg Gln Arg Lys Ser Arg Arg Thr Ile
245 250
<210> 328
<211> 525
<212> PRT
<213> Homo Sapien
<400> 328
Ala Val Asn Gly Thr Ser Gln Phe Thr Cys Phe Tyr Asn Ser Arg Ala
1 5 10 15
Asn Ile Ser Cys Val Trp Ser Gln Asp Gly Ala Leu Gln Asp Thr Ser
20 25 30
Cys Gln Val His Ala Trp Pro Asp Arg Arg Arg Trp Asn Gln Thr Cys
35 40 45
Glu Leu Leu Pro Val Ser Gln Ala Ser Trp Ala Cys Asn Leu Ile Leu
50 55 60
Gly Ala Pro Asp Ser Gln Lys Leu Thr Thr Val Asp Ile Val Thr Leu
65 70 75 80
Arg Val Leu Cys Arg Glu Gly Val Arg Trp Arg Val Met Ala Ile Gln
85 90 95
Asp Phe Lys Pro Phe Glu Asn Leu Arg Leu Met Ala Pro Ile Ser Leu
100 105 110
Gln Val Val His Val Glu Thr His Arg Cys Asn Ile Ser Trp Glu Ile
115 120 125
Ser Gln Ala Ser His Tyr Phe Glu Arg His Leu Glu Phe Glu Ala Arg
130 135 140
Thr Leu Ser Pro Gly His Thr Trp Glu Glu Ala Pro Leu Leu Thr Leu
145 150 155 160
Lys Gln Lys Gln Glu Trp Ile Cys Leu Glu Thr Leu Thr Pro Asp Thr
165 170 175
Gln Tyr Glu Phe Gln Val Arg Val Lys Pro Leu Gln Gly Glu Phe Thr
180 185 190
Thr Trp Ser Pro Trp Ser Gln Pro Leu Ala Phe Arg Thr Lys Pro Ala
195 200 205
Ala Leu Gly Lys Asp Thr Ile Pro Trp Leu Gly His Leu Leu Val Gly
210 215 220
Leu Ser Gly Ala Phe Gly Phe Ile Ile Leu Val Tyr Leu Leu Ile Asn
225 230 235 240
Cys Arg Asn Thr Gly Pro Trp Leu Lys Lys Val Leu Lys Cys Asn Thr
245 250 255
Pro Asp Pro Ser Lys Phe Phe Ser Gln Leu Ser Ser Glu His Gly Gly
260 265 270
Asp Val Gln Lys Trp Leu Ser Ser Pro Phe Pro Ser Ser Ser Phe Ser
275 280 285
Pro Gly Gly Leu Ala Pro Glu Ile Ser Pro Leu Glu Val Leu Glu Arg
290 295 300
Asp Lys Val Thr Gln Leu Leu Leu Gln Gln Asp Lys Val Pro Glu Pro
305 310 315 320
Ala Ser Leu Ser Ser Asn His Ser Leu Thr Ser Cys Phe Thr Asn Gln
325 330 335
Gly Tyr Phe Phe Phe His Leu Pro Asp Ala Leu Glu Ile Glu Ala Cys
340 345 350
Gln Val Tyr Phe Thr Tyr Asp Pro Tyr Ser Glu Glu Asp Pro Asp Glu
355 360 365
Gly Val Ala Gly Ala Pro Thr Gly Ser Ser Pro Gln Pro Leu Gln Pro
370 375 380
Leu Ser Gly Glu Asp Asp Ala Tyr Cys Thr Phe Pro Ser Arg Asp Asp
385 390 395 400
Leu Leu Leu Phe Ser Pro Ser Leu Leu Gly Gly Pro Ser Pro Pro Ser
405 410 415
Thr Ala Pro Gly Gly Ser Gly Ala Gly Glu Glu Arg Met Pro Pro Ser
420 425 430
Leu Gln Glu Arg Val Pro Arg Asp Trp Asp Pro Gln Pro Leu Gly Pro
435 440 445
Pro Thr Pro Gly Val Pro Asp Leu Val Asp Phe Gln Pro Pro Pro Glu
450 455 460
Leu Val Leu Arg Glu Ala Gly Glu Glu Val Pro Asp Ala Gly Pro Arg
465 470 475 480
Glu Gly Val Ser Phe Pro Trp Ser Arg Pro Pro Gly Gln Gly Glu Phe
485 490 495
Arg Ala Leu Asn Ala Arg Leu Pro Leu Asn Thr Asp Ala Tyr Leu Ser
500 505 510
Leu Gln Glu Leu Gln Gly Gln Asp Pro Thr His Leu Val
515 520 525
<210> 329
<211> 347
<212> PRT
<213> Homo Sapien
<400> 329
Leu Asn Thr Thr Ile Leu Thr Pro Asn Gly Asn Glu Asp Thr Thr Ala
1 5 10 15
Asp Phe Phe Leu Thr Thr Met Pro Thr Asp Ser Leu Ser Val Ser Thr
20 25 30
Leu Pro Leu Pro Glu Val Gln Cys Phe Val Phe Asn Val Glu Tyr Met
35 40 45
Asn Cys Thr Trp Asn Ser Ser Ser Glu Pro Gln Pro Thr Asn Leu Thr
50 55 60
Leu His Tyr Trp Tyr Lys Asn Ser Asp Asn Asp Lys Val Gln Lys Cys
65 70 75 80
Ser His Tyr Leu Phe Ser Glu Glu Ile Thr Ser Gly Cys Gln Leu Gln
85 90 95
Lys Lys Glu Ile His Leu Tyr Gln Thr Phe Val Val Gln Leu Gln Asp
100 105 110
Pro Arg Glu Pro Arg Arg Gln Ala Thr Gln Met Leu Lys Leu Gln Asn
115 120 125
Leu Val Ile Pro Trp Ala Pro Glu Asn Leu Thr Leu His Lys Leu Ser
130 135 140
Glu Ser Gln Leu Glu Leu Asn Trp Asn Asn Arg Phe Leu Asn His Cys
145 150 155 160
Leu Glu His Leu Val Gln Tyr Arg Thr Asp Trp Asp His Ser Trp Thr
165 170 175
Glu Gln Ser Val Asp Tyr Arg His Lys Phe Ser Leu Pro Ser Val Asp
180 185 190
Gly Gln Lys Arg Tyr Thr Phe Arg Val Arg Ser Arg Phe Asn Pro Leu
195 200 205
Cys Gly Ser Ala Gln His Trp Ser Glu Trp Ser His Pro Ile His Trp
210 215 220
Gly Ser Asn Thr Ser Lys Glu Asn Pro Phe Leu Phe Ala Leu Glu Ala
225 230 235 240
Val Val Ile Ser Val Gly Ser Met Gly Leu Ile Ile Ser Leu Leu Cys
245 250 255
Val Tyr Phe Trp Leu Glu Arg Thr Met Pro Arg Ile Pro Thr Leu Lys
260 265 270
Asn Leu Glu Asp Leu Val Thr Glu Tyr His Gly Asn Phe Ser Ala Trp
275 280 285
Ser Gly Val Ser Lys Gly Leu Ala Glu Ser Leu Gln Pro Asp Tyr Ser
290 295 300
Glu Arg Leu Cys Leu Val Ser Glu Ile Pro Pro Lys Gly Gly Ala Leu
305 310 315 320
Gly Glu Gly Pro Gly Ala Ser Pro Cys Asn Gln His Ser Pro Tyr Trp
325 330 335
Ala Pro Pro Cys Tyr Thr Leu Lys Pro Glu Thr
340 345
<210> 330
<211> 152
<212> PRT
<213> Homo Sapien
<400> 330
Asp Cys Asp Ile Glu Gly Lys Asp Gly Lys Gln Tyr Glu Ser Val Leu
1 5 10 15
Met Val Ser Ile Asp Gln Leu Leu Asp Ser Met Lys Glu Ile Gly Ser
20 25 30
Asn Cys Leu Asn Asn Glu Phe Asn Phe Phe Lys Arg His Ile Cys Asp
35 40 45
Ala Asn Lys Glu Gly Met Phe Leu Phe Arg Ala Ala Arg Lys Leu Arg
50 55 60
Gln Phe Leu Lys Met Asn Ser Thr Gly Asp Phe Asp Leu His Leu Leu
65 70 75 80
Lys Val Ser Glu Gly Thr Thr Ile Leu Leu Asn Cys Thr Gly Gln Val
85 90 95
Lys Gly Arg Lys Pro Ala Ala Leu Gly Glu Ala Gln Pro Thr Lys Ser
100 105 110
Leu Glu Glu Asn Lys Ser Leu Lys Glu Gln Lys Lys Leu Asn Asp Leu
115 120 125
Cys Phe Leu Lys Arg Leu Leu Gln Glu Ile Lys Thr Cys Trp Asn Lys
130 135 140
Ile Leu Met Gly Thr Lys Glu His
145 150
<210> 331
<211> 133
<212> PRT
<213> Homo Sapien
<400> 331
Gly Ile His Val Phe Ile Leu Gly Cys Phe Ser Ala Gly Leu Pro Lys
1 5 10 15
Thr Glu Ala Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu
20 25 30
Asp Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser
35 40 45
Asp Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu
50 55 60
Glu Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp
65 70 75 80
Thr Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn
85 90 95
Gly Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu
100 105 110
Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met
115 120 125
Phe Ile Asn Thr Ser
130
<210> 332
<211> 133
<212> PRT
<213> Homo Sapien
<400> 332
Gln Gly Gln Asp Arg His Met Ile Arg Met Arg Gln Leu Ile Asp Ile
1 5 10 15
Val Asp Gln Leu Lys Asn Tyr Val Asn Asp Leu Val Pro Glu Phe Leu
20 25 30
Pro Ala Pro Glu Asp Val Glu Thr Asn Cys Glu Trp Ser Ala Phe Ser
35 40 45
Cys Phe Gln Lys Ala Gln Leu Lys Ser Ala Asn Thr Gly Asn Asn Glu
50 55 60
Arg Ile Ile Asn Val Ser Ile Lys Lys Leu Lys Arg Lys Pro Pro Ser
65 70 75 80
Thr Asn Ala Gly Arg Arg Gln Lys His Arg Leu Thr Cys Pro Ser Cys
85 90 95
Asp Ser Tyr Glu Lys Lys Pro Pro Lys Glu Phe Leu Glu Arg Phe Lys
100 105 110
Ser Leu Leu Gln Lys Met Ile His Gln His Leu Ser Ser Arg Thr His
115 120 125
Gly Ser Glu Asp Ser
130
<210> 333
<211> 127
<212> PRT
<213> Homo Sapien
<400> 333
Ala Pro Ala Arg Ser Pro Ser Pro Ser Thr Gln Pro Trp Glu His Val
1 5 10 15
Asn Ala Ile Gln Glu Ala Arg Arg Leu Leu Asn Leu Ser Arg Asp Thr
20 25 30
Ala Ala Glu Met Asn Glu Thr Val Glu Val Ile Ser Glu Met Phe Asp
35 40 45
Leu Gln Glu Pro Thr Cys Leu Gln Thr Arg Leu Glu Leu Tyr Lys Gln
50 55 60
Gly Leu Arg Gly Ser Leu Thr Lys Leu Lys Gly Pro Leu Thr Met Met
65 70 75 80
Ala Ser His Tyr Lys Gln His Cys Pro Pro Thr Pro Glu Thr Ser Cys
85 90 95
Ala Thr Gln Ile Ile Thr Phe Glu Ser Phe Lys Glu Asn Leu Lys Asp
100 105 110
Phe Leu Leu Val Ile Pro Phe Asp Cys Trp Glu Pro Val Gln Glu
115 120 125
<210> 334
<211> 171
<212> PRT
<213> Homo Sapien
<400> 334
Cys Asp Leu Pro Gln Asn His Gly Leu Leu Ser Arg Asn Thr Leu Val
1 5 10 15
Leu Leu His Gln Met Arg Arg Ile Ser Pro Phe Leu Cys Leu Lys Asp
20 25 30
Arg Arg Asp Phe Arg Phe Pro Gln Glu Met Val Lys Gly Ser Gln Leu
35 40 45
Gln Lys Ala His Val Met Ser Val Leu His Glu Met Leu Gln Gln Ile
50 55 60
Phe Ser Leu Phe His Thr Glu Arg Ser Ser Ala Ala Trp Asn Met Thr
65 70 75 80
Leu Leu Asp Gln Leu His Thr Glu Leu His Gln Gln Leu Gln His Leu
85 90 95
Glu Thr Cys Leu Leu Gln Val Val Gly Glu Gly Glu Ser Ala Gly Ala
100 105 110
Ile Ser Ser Pro Ala Leu Thr Leu Arg Arg Tyr Phe Gln Gly Ile Arg
115 120 125
Val Tyr Leu Lys Glu Lys Lys Tyr Ser Asp Cys Ala Trp Glu Val Val
130 135 140
Arg Met Glu Ile Met Lys Ser Leu Phe Leu Ser Thr Asn Met Gln Glu
145 150 155 160
Arg Leu Arg Ser Lys Asp Arg Asp Leu Gly Ser
165 170
<210> 335
<211> 177
<212> PRT
<213> Homo Sapien
<400> 335
Gly Pro Gln Arg Glu Glu Phe Pro Arg Asp Leu Ser Leu Ile Ser Pro
1 5 10 15
Leu Ala Gln Ala Val Arg Ser Ser Ser Arg Thr Pro Ser Asp Lys Pro
20 25 30
Val Ala His Val Val Ala Asn Pro Gln Ala Glu Gly Gln Leu Gln Trp
35 40 45
Leu Asn Arg Arg Ala Asn Ala Leu Leu Ala Asn Gly Val Glu Leu Arg
50 55 60
Asp Asn Gln Leu Val Val Pro Ser Glu Gly Leu Tyr Leu Ile Tyr Ser
65 70 75 80
Gln Val Leu Phe Lys Gly Gln Gly Cys Pro Ser Thr His Val Leu Leu
85 90 95
Thr His Thr Ile Ser Arg Ile Ala Val Ser Tyr Gln Thr Lys Val Asn
100 105 110
Leu Leu Ser Ala Ile Lys Ser Pro Cys Gln Arg Glu Thr Pro Glu Gly
115 120 125
Ala Glu Ala Lys Pro Trp Tyr Glu Pro Ile Tyr Leu Gly Gly Val Phe
130 135 140
Gln Leu Glu Lys Gly Asp Arg Leu Ser Ala Glu Ile Asn Arg Pro Asp
145 150 155 160
Tyr Leu Asp Phe Ala Glu Ser Gly Gln Val Tyr Phe Gly Ile Ile Ala
165 170 175
Leu
<210> 336
<211> 197
<212> PRT
<213> Homo Sapien
<400> 336
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 337
<211> 306
<212> PRT
<213> Homo Sapien
<400> 337
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 338
<211> 103
<212> PRT
<213> Homo Sapien
<400> 338
Thr Pro Val Val Arg Lys Gly Arg Cys Ser Cys Ile Ser Thr Asn Gln
1 5 10 15
Gly Thr Ile His Leu Gln Ser Leu Lys Asp Leu Lys Gln Phe Ala Pro
20 25 30
Ser Pro Ser Cys Glu Lys Ile Glu Ile Ile Ala Thr Leu Lys Asn Gly
35 40 45
Val Gln Thr Cys Leu Asn Pro Asp Ser Ala Asp Val Lys Glu Leu Ile
50 55 60
Lys Lys Trp Glu Lys Gln Val Ser Gln Lys Lys Lys Gln Lys Asn Gly
65 70 75 80
Lys Lys His Gln Lys Lys Lys Val Leu Lys Val Arg Lys Ser Gln Arg
85 90 95
Ser Arg Gln Lys Lys Thr Thr
100
<210> 339
<211> 77
<212> PRT
<213> Homo Sapien
<400> 339
Val Pro Leu Ser Arg Thr Val Arg Cys Thr Cys Ile Ser Ile Ser Asn
1 5 10 15
Gln Pro Val Asn Pro Arg Ser Leu Glu Lys Leu Glu Ile Ile Pro Ala
20 25 30
Ser Gln Phe Cys Pro Arg Val Glu Ile Ile Ala Thr Met Lys Lys Lys
35 40 45
Gly Glu Lys Arg Cys Leu Asn Pro Glu Ser Lys Ala Ile Lys Asn Leu
50 55 60
Leu Lys Ala Val Ser Lys Glu Arg Ser Lys Arg Ser Pro
65 70 75
<210> 340
<211> 330
<212> PRT
<213> Homo Sapien
<400> 340
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 341
<211> 996
<212> DNA
<213> Homo Sapien
<400> 341
gccagcacca agggcccctc tgtgttccct ctggcccctt ccagcaagtc cacctctggc 60
ggaacagccg ctctgggctg cctcgtgaag gactacttcc ccgagcctgt gaccgtgtcc 120
tggaactctg gcgctctgac cagcggagtg cacaccttcc ctgctgtgct gcagtcctcc 180
ggcctgtact ccctgtcctc cgtcgtgacc gtgccttcca gctctctggg cacccagacc 240
tacatctgca acgtgaacca caagccctcc aacaccaagg tggacaagaa ggtggaaccc 300
aagtcctgcg acaagaccca cacctgtccc ccttgtcctg cccctgaact gctgggcgga 360
ccttccgtgt tcctgttccc cccaaagccc aaggacaccc tgatgatctc ccggaccccc 420
gaagtgacct gcgtggtggt ggatgtgtcc cacgaggacc ctgaagtgaa gttcaattgg 480
tacgtggacg gcgtggaagt gcacaacgcc aagaccaagc ctagagagga acagtacaac 540
tccacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggattggct gaacggcaaa 600
gagtacaagt gcaaggtgtc caacaaggcc ctgcctgccc ccatcgaaaa gaccatctcc 660
aaggccaagg gccagccccg ggaaccccag gtgtacacac tgccccctag cagggacgag 720
ctgaccaaga accaggtgtc cctgacctgt ctcgtgaaag gcttctaccc ctccgatatc 780
gccgtggaat gggagtccaa cggccagcct gagaacaact acaagaccac cccccctgtg 840
ctggactccg acggctcatt cttcctgtac agcaagctga cagtggacaa gtcccggtgg 900
cagcagggca acgtgttctc ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 960
cagaagtccc tgtccctgag ccccggcaag tgatga 996
<210> 342
<211> 450
<212> PRT
<213> Homo Sapien
<400> 342
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Ile Arg Thr Gly Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Met Lys Gly Ser Gly Thr Tyr Gly Gly Trp Phe Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
195 200 205
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
210 215 220
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Leu Ala Gly Ala
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
435 440 445
Gly Lys
450
<210> 343
<211> 8
<212> PRT
<213> Homo Sapien
<400> 343
Gly Phe Thr Phe Ser Asn Tyr Ala
1 5
<210> 344
<211> 8
<212> PRT
<213> Homo Sapien
<400> 344
Ile Ser Phe Ser Gly Gly Thr Thr
1 5
<210> 345
<211> 14
<212> PRT
<213> Homo Sapien
<400> 345
Ala Lys Asp Glu Ala Pro Ala Gly Ala Thr Phe Phe Asp Ser
1 5 10
<210> 346
<211> 5
<212> PRT
<213> Homo Sapien
<400> 346
Asn Tyr Ala Met Ser
1 5
<210> 347
<211> 17
<212> PRT
<213> Homo Sapien
<400> 347
Ala Ile Ser Phe Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 348
<211> 12
<212> PRT
<213> Homo Sapien
<400> 348
Asp Glu Ala Pro Ala Gly Ala Thr Phe Phe Asp Ser
1 5 10
<210> 349
<211> 121
<212> PRT
<213> Homo Sapien
<400> 349
Glu Val Gln Leu Ala Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Phe Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Glu Ala Pro Ala Gly Ala Thr Phe Phe Asp Ser Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 350
<211> 364
<212> DNA
<213> Homo Sapien
<400> 350
gaagtgcaac tggcggagtc tgggggaggc ttggtacagc cgggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagc aactatgcca tgagttgggt ccgccagact 120
ccaggaaagg ggctggagtg ggtctcagct attagtttta gtggtggtac tacatactac 180
gctgactccg tgaagggccg gttcaccatc tccagagaca attccaagaa cacgctgtat 240
ttgcacatga acagcctgag agccgatgac acggccgtat attactgtgc gaaagatgag 300
gcaccagctg gcgcaacctt ctttgactcc tggggccagg gaacgctggt caccgtctcc 360
tcag 364
<210> 351
<211> 448
<212> PRT
<213> Homo Sapien
<400> 351
Glu Val Gln Leu Ala Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Phe Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Glu Ala Pro Ala Gly Ala Thr Phe Phe Asp Ser Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
210 215 220
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 352
<211> 1344
<212> DNA
<213> Homo Sapien
<400> 352
gaagtgcaac tggcggagtc tgggggaggc ttggtacagc cgggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagc aactatgcca tgagttgggt ccgccagact 120
ccaggaaagg ggctggagtg ggtctcagct attagtttta gtggtggtac tacatactac 180
gctgactccg tgaagggccg gttcaccatc tccagagaca attccaagaa cacgctgtat 240
ttgcacatga acagcctgag agccgatgac acggccgtat attactgtgc gaaagatgag 300
gcaccagctg gcgcaacctt ctttgactcc tggggccagg gaacgctggt caccgtctcc 360
tcagccagca ccaagggccc ttccgtgttc cccctggccc cttgcagcag gagcacctcc 420
gaatccacag ctgccctggg ctgtctggtg aaggactact ttcccgagcc cgtgaccgtg 480
agctggaaca gcggcgctct gacatccggc gtccacacct ttcctgccgt cctgcagtcc 540
tccggcctct actccctgtc ctccgtggtg accgtgccta gctcctccct cggcaccaag 600
acctacacct gtaacgtgga ccacaaaccc tccaacacca aggtggacaa acgggtcgag 660
agcaagtacg gccctccctg ccctccttgt cctgcccccg agttcgaagg cggacccagc 720
gtgttcctgt tccctcctaa gcccaaggac accctcatga tcagccggac acccgaggtg 780
acctgcgtgg tggtggatgt gagccaggag gaccctgagg tccagttcaa ctggtatgtg 840
gatggcgtgg aggtgcacaa cgccaagaca aagccccggg aagagcagtt caactccacc 900
tacagggtgg tcagcgtgct gaccgtgctg catcaggact ggctgaacgg caaggagtac 960
aagtgcaagg tcagcaataa gggactgccc agcagcatcg agaagaccat ctccaaggct 1020
aaaggccagc cccgggaacc tcaggtgtac accctgcctc ccagccagga ggagatgacc 1080
aagaaccagg tgagcctgac ctgcctggtg aagggattct acccttccga catcgccgtg 1140
gagtgggagt ccaacggcca gcccgagaac aattataaga ccacccctcc cgtcctcgac 1200
agcgacggat ccttctttct gtactccagg ctgaccgtgg ataagtccag gtggcaggaa 1260
ggcaacgtgt tcagctgctc cgtgatgcac gaggccctgc acaatcacta cacccagaag 1320
tccctgagcc tgtccctggg aaag 1344
<210> 353
<211> 6
<212> PRT
<213> Homo Sapien
<400> 353
Gln Gly Ile Arg Arg Trp
1 5
<210> 354
<211> 3
<212> PRT
<213> Homo Sapien
<400> 354
Gly Ala Ser
1
<210> 355
<211> 9
<212> PRT
<213> Homo Sapien
<400> 355
Gln Gln Ala Asn Ser Phe Pro Ile Thr
1 5
<210> 356
<211> 11
<212> PRT
<213> Homo Sapien
<400> 356
Arg Ala Ser Gln Gly Ile Arg Arg Trp Leu Ala
1 5 10
<210> 357
<211> 7
<212> PRT
<213> Homo Sapien
<400> 357
Gly Ala Ser Ser Leu Gln Ser
1 5
<210> 358
<211> 9
<212> PRT
<213> Homo Sapien
<400> 358
Gln Gln Ala Asn Ser Phe Pro Ile Thr
1 5
<210> 359
<211> 107
<212> PRT
<213> Homo Sapien
<400> 359
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Arg Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ile Ile Thr Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 360
<211> 322
<212> DNA
<213> Homo Sapien
<400> 360
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattagg aggtggttag cctggtatca gcagaaacca 120
gggaaagccc ctaaactcct gatctctggt gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagat ttcactctca tcattaccag tctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagtt tcccgatcac cttcggccaa 300
gggacacgac tggagatcaa ac 322
<210> 361
<211> 214
<212> PRT
<213> Homo Sapien
<400> 361
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Arg Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ile Ile Thr Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 362
<211> 642
<212> DNA
<213> Homo Sapien
<400> 362
gacatccaga tgacccagtc tccatcttcc gtgtctgcat ctgtaggaga cagagtcacc 60
atcacttgtc gggcgagtca gggtattagg aggtggttag cctggtatca gcagaaacca 120
gggaaagccc ctaaactcct gatctctggt gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagat ttcactctca tcattaccag tctgcagcct 240
gaagattttg caacttacta ttgtcaacag gctaacagtt tcccgatcac cttcggccaa 300
gggacacgac tggagatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 363
<211> 8
<212> PRT
<213> Homo Sapien
<400> 363
Gly Tyr Thr Phe Ser Thr Phe Gly
1 5
<210> 364
<211> 8
<212> PRT
<213> Homo Sapien
<400> 364
Ile Ser Ala Tyr Asn Gly Asp Thr
1 5
<210> 365
<211> 14
<212> PRT
<213> Homo Sapien
<400> 365
Ala Arg Ser Ser Gly His Tyr Tyr Tyr Tyr Gly Met Asp Val
1 5 10
<210> 366
<211> 121
<212> PRT
<213> Homo Sapien
<400> 366
Gln Val Gln Val Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Thr Phe
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asp Thr Asn Tyr Ala Gln Asn Leu
50 55 60
Gln Gly Arg Val Ile Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Ser Gly His Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 367
<211> 363
<212> DNA
<213> Homo Sapien
<400> 367
caggttcagg tggtgcagtc tggagctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta caccttttcc acctttggta tcacctgggt gcgacaggcc 120
cctggacaag ggcttgaatg gatgggatgg atcagcgctt acaatggtga cacaaactat 180
gcacagaatc tccagggcag agtcatcatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcctgag atctgacgac acggccgttt attactgtgc gaggagcagt 300
ggccactact actactacgg tatggacgtc tggggccaag ggaccacggt caccgtctcc 360
tca 363
<210> 368
<211> 451
<212> PRT
<213> Homo Sapien
<400> 368
Gln Val Gln Val Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Thr Phe
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asp Thr Asn Tyr Ala Gln Asn Leu
50 55 60
Gln Gly Arg Val Ile Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Ser Gly His Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 369
<211> 1359
<212> DNA
<213> Homo Sapien
<400> 369
caggttcagg tggtgcagtc tggagctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta caccttttcc acctttggta tcacctgggt gcgacaggcc 120
cctggacaag ggcttgaatg gatgggatgg atcagcgctt acaatggtga cacaaactat 180
gcacagaatc tccagggcag agtcatcatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcctgag atctgacgac acggccgttt attactgtgc gaggagcagt 300
ggccactact actactacgg tatggacgtc tggggccaag ggaccacggt caccgtctcc 360
tcagccagca ccaagggccc ctctgtgttc cctctggccc cttccagcaa gtccacctct 420
ggcggaacag ccgctctggg ctgcctcgtg aaggactact tccccgagcc tgtgaccgtg 480
tcctggaact ctggcgctct gaccagcgga gtgcacacct tccctgctgt gctgcagtcc 540
tccggcctgt actccctgtc ctccgtcgtg accgtgcctt ccagctctct gggcacccag 600
acctacatct gcaacgtgaa ccacaagccc tccaacacca aggtggacaa gaaggtggaa 660
cccaagtcct gcgacaagac ccacacctgt cccccttgtc ctgcccctga actgctgggc 720
ggaccttccg tgttcctgtt ccccccaaag cccaaggaca ccctgatgat ctcccggacc 780
cccgaagtga cctgcgtggt ggtggatgtg tcccacgagg accctgaagt gaagttcaat 840
tggtacgtgg acggcgtgga agtgcacaac gccaagacca agcctagaga ggaacagtac 900
aactccacct accgggtggt gtccgtgctg accgtgctgc accaggattg gctgaacggc 960
aaagagtaca agtgcaaggt gtccaacaag gccctgcctg cccccatcga aaagaccatc 1020
tccaaggcca agggccagcc ccgggaaccc caggtgtaca cactgccccc tagcagggac 1080
gagctgacca agaaccaggt gtccctgacc tgtctcgtga aaggcttcta cccctccgat 1140
atcgccgtgg aatgggagtc caacggccag cctgagaaca actacaagac caccccccct 1200
gtgctggact ccgacggctc attcttcctg tacagcaagc tgacagtgga caagtcccgg 1260
tggcagcagg gcaacgtgtt ctcctgctcc gtgatgcacg aggccctgca caaccactac 1320
acccagaagt ccctgtccct gagccccggc aagtgatga 1359
<210> 370
<211> 11
<212> PRT
<213> Homo Sapien
<400> 370
Gln Ser Leu Leu His Ser Asn Glu Tyr Asn Tyr
1 5 10
<210> 371
<211> 3
<212> PRT
<213> Homo Sapien
<400> 371
Leu Gly Ser
1
<210> 372
<211> 9
<212> PRT
<213> Homo Sapien
<400> 372
Met Gln Ser Leu Gln Thr Pro Leu Thr
1 5
<210> 373
<211> 112
<212> PRT
<213> Homo Sapien
<400> 373
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Glu Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Phe Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Thr Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Ser
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 374
<211> 336
<212> DNA
<213> Homo Sapien
<400> 374
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg aatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct ttttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
accagagtgg aggctgagga tgttggaatt tattactgca tgcaatctct acaaactccg 300
ctcactttcg gcggagggac caaggtggag atcaaa 336
<210> 375
<211> 219
<212> PRT
<213> Homo Sapien
<400> 375
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Glu Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Phe Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Thr Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Ser
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 376
<211> 657
<212> DNA
<213> Homo Sapien
<400> 376
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg aatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct ttttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
accagagtgg aggctgagga tgttggaatt tattactgca tgcaatctct acaaactccg 300
ctcactttcg gcggagggac caaggtggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 377
<211> 8
<212> PRT
<213> Homo Sapien
<400> 377
Gly Tyr Thr Phe Thr Ser Tyr Gly
1 5
<210> 378
<211> 8
<212> PRT
<213> Homo Sapien
<400> 378
Ile Ser Ala Tyr Asn Gly Asn Thr
1 5
<210> 379
<211> 17
<212> PRT
<213> Homo Sapien
<400> 379
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
1 5 10 15
Val
<210> 380
<211> 124
<212> PRT
<213> Homo Sapien
<400> 380
Gln Val Gln Leu Val Gln Ser Gly Gly Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 381
<211> 372
<212> DNA
<213> Homo Sapien
<400> 381
caggttcaac tggtgcagtc tggaggtgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttacc agctatggtt tcagctgggt gcgacaggcc 120
cctggacaag gactagagtg gatgggatgg atcagcgctt acaatggtaa cacaaactat 180
gcacagaagc tccagggcag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcttgag atctgacgac acggccgtgt attactgtgc gagatctacg 300
tatttctatg gttcggggac cctctacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 382
<211> 454
<212> PRT
<213> Homo Sapien
<400> 382
Gln Val Gln Leu Val Gln Ser Gly Gly Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 383
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 383
caggttcaac tggtgcagtc tggaggtgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttacc agctatggtt tcagctgggt gcgacaggcc 120
cctggacaag gactagagtg gatgggatgg atcagcgctt acaatggtaa cacaaactat 180
gcacagaagc tccagggcag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcttgag atctgacgac acggccgtgt attactgtgc gagatctacg 300
tatttctatg gttcggggac cctctacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 384
<211> 11
<212> PRT
<213> Homo Sapien
<400> 384
Gln Ser Leu Leu His Ser Asp Gly Tyr Asn Tyr
1 5 10
<210> 385
<211> 3
<212> PRT
<213> Homo Sapien
<400> 385
Leu Gly Ser
1
<210> 386
<211> 9
<212> PRT
<213> Homo Sapien
<400> 386
Met Gln Ala Leu Gln Thr Pro Leu Ser
1 5
<210> 387
<211> 112
<212> PRT
<213> Homo Sapien
<400> 387
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asp Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Thr Arg Ala Ser Gly Phe Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 388
<211> 336
<212> DNA
<213> Homo Sapien
<400> 388
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaactg tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
tgcagttttg gccaggggac caagctggag atcaaa 336
<210> 389
<211> 219
<212> PRT
<213> Homo Sapien
<400> 389
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asp Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Thr Arg Ala Ser Gly Phe Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 390
<211> 657
<212> DNA
<213> Homo Sapien
<400> 390
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaactg tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
tgcagttttg gccaggggac caagctggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 391
<211> 8
<212> PRT
<213> Homo Sapien
<400> 391
Gly Tyr Thr Phe Thr Ser Tyr Gly
1 5
<210> 392
<211> 8
<212> PRT
<213> Homo Sapien
<400> 392
Ile Ser Ala Tyr Asn Gly Asn Thr
1 5
<210> 393
<211> 17
<212> PRT
<213> Homo Sapien
<400> 393
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
1 5 10 15
Val
<210> 394
<211> 124
<212> PRT
<213> Homo Sapien
<400> 394
Gln Val Gln Leu Val Gln Ser Gly Gly Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 395
<211> 372
<212> DNA
<213> Homo Sapien
<400> 395
caggttcaac tggtgcagtc tggaggtgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttacc agctatggtt tcagctgggt gcgacaggcc 120
cctggacaag gactagagtg gatgggatgg atcagcgctt acaatggtaa cacaaactat 180
gcacagaagc tccagggcag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcttgag atctgacgac acggccgtgt attactgtgc gagatctacg 300
tatttctatg gttcggggac cctctacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 396
<211> 454
<212> PRT
<213> Homo Sapien
<400> 396
Gln Val Gln Leu Val Gln Ser Gly Gly Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Tyr Phe Tyr Gly Ser Gly Thr Leu Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 397
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 397
caggttcaac tggtgcagtc tggaggtgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttacc agctatggtt tcagctgggt gcgacaggcc 120
cctggacaag gactagagtg gatgggatgg atcagcgctt acaatggtaa cacaaactat 180
gcacagaagc tccagggcag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcttgag atctgacgac acggccgtgt attactgtgc gagatctacg 300
tatttctatg gttcggggac cctctacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 398
<211> 11
<212> PRT
<213> Homo Sapien
<400> 398
Gln Ser Leu Leu His Ser Asp Gly Tyr Asn Cys
1 5 10
<210> 399
<211> 3
<212> PRT
<213> Homo Sapien
<400> 399
Leu Gly Ser
1
<210> 400
<211> 9
<212> PRT
<213> Homo Sapien
<400> 400
Met Gln Ala Leu Gln Thr Pro Cys Ser
1 5
<210> 401
<211> 112
<212> PRT
<213> Homo Sapien
<400> 401
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asp Gly Tyr Asn Cys Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Thr Arg Ala Ser Gly Phe Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Cys Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 402
<211> 336
<212> DNA
<213> Homo Sapien
<400> 402
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaactg tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
tgcagttttg gccaggggac caagctggag atcaaa 336
<210> 403
<211> 219
<212> PRT
<213> Homo Sapien
<400> 403
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asp Gly Tyr Asn Cys Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Thr Arg Ala Ser Gly Phe Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Cys Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 404
<211> 657
<212> DNA
<213> Homo Sapien
<400> 404
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaactg tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
tgcagttttg gccaggggac caagctggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 405
<211> 8
<212> PRT
<213> Homo Sapien
<400> 405
Gly Val Thr Phe Asp Asp Tyr Gly
1 5
<210> 406
<211> 8
<212> PRT
<213> Homo Sapien
<400> 406
Ile Asn Trp Asn Gly Gly Asp Thr
1 5
<210> 407
<211> 17
<212> PRT
<213> Homo Sapien
<400> 407
Ala Arg Asp Phe Tyr Gly Ser Gly Ser Tyr Tyr His Val Pro Phe Asp
1 5 10 15
Tyr
<210> 408
<211> 124
<212> PRT
<213> Homo Sapien
<400> 408
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Val Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Asn Gly Gly Asp Thr Asp Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Tyr Gly Ser Gly Ser Tyr Tyr His Val Pro Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser
115 120
<210> 409
<211> 372
<212> DNA
<213> Homo Sapien
<400> 409
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgtag cctctggagt cacctttgat gattatggca tgagctgggt ccgccaagct 120
ccagggaagg ggctggartg ggtctctggt attaattgga atggtggcga cacagattat 180
tcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctacaaatga atagtctgag agccgaggac acggccttgt attactgtgc gagggatttc 300
tatggttcgg ggagttatta tcacgttcct tttgactact ggggccaggg aatcctggtc 360
accgtctcct ca 372
<210> 410
<211> 454
<212> PRT
<213> Homo Sapien
<400> 410
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Val Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Asn Gly Gly Asp Thr Asp Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Tyr Gly Ser Gly Ser Tyr Tyr His Val Pro Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 411
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 411
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgtag cctctggagt cacctttgat gattatggca tgagctgggt ccgccaagct 120
ccagggaagg ggctggartg ggtctctggt attaattgga atggtggcga cacagattat 180
tcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctacaaatga atagtctgag agccgaggac acggccttgt attactgtgc gagggatttc 300
tatggttcgg ggagttatta tcacgttcct tttgactact ggggccaggg aatcctggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 412
<211> 7
<212> PRT
<213> Homo Sapien
<400> 412
Gln Ser Val Ser Arg Ser Tyr
1 5
<210> 413
<211> 3
<212> PRT
<213> Homo Sapien
<400> 413
Gly Ala Ser
1
<210> 414
<211> 9
<212> PRT
<213> Homo Sapien
<400> 414
His Gln Tyr Asp Met Ser Pro Phe Thr
1 5
<210> 415
<211> 108
<212> PRT
<213> Homo Sapien
<400> 415
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Arg Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Asp Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Tyr Asp Met Ser Pro
85 90 95
Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 416
<211> 324
<212> DNA
<213> Homo Sapien
<400> 416
gaaattgtgt tgacgcagtc tccagggacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agaagctact tagcctggta ccagcagaaa 120
cgtggccagg ctcccaggct cctcatctat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcgatgg gtctgggaca gacttcactc tctccatcag cagactggag 240
cctgaagatt ttgcagtgta ttactgtcac cagtatgata tgtcaccatt cactttcggc 300
cctgggacca aagtggatat caaa 324
<210> 417
<211> 215
<212> PRT
<213> Homo Sapien
<400> 417
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Arg Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Asp Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Tyr Asp Met Ser Pro
85 90 95
Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 418
<211> 645
<212> DNA
<213> Homo Sapien
<400> 418
gaaattgtgt tgacgcagtc tccagggacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agaagctact tagcctggta ccagcagaaa 120
cgtggccagg ctcccaggct cctcatctat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcgatgg gtctgggaca gacttcactc tctccatcag cagactggag 240
cctgaagatt ttgcagtgta ttactgtcac cagtatgata tgtcaccatt cactttcggc 300
cctgggacca aagtggatat caaacgtacg gtggccgctc cctccgtgtt catcttccca 360
ccttccgacg agcagctgaa gtccggcacc gcttctgtcg tgtgcctgct gaacaacttc 420
tacccccgcg aggccaaggt gcagtggaag gtggacaacg ccctgcagtc cggcaactcc 480
caggaatccg tgaccgagca ggactccaag gacagcacct actccctgtc ctccaccctg 540
accctgtcca aggccgacta cgagaagcac aaggtgtacg cctgcgaagt gacccaccag 600
ggcctgtcta gccccgtgac caagtctttc aaccggggcg agtgt 645
<210> 419
<211> 8
<212> PRT
<213> Homo Sapien
<400> 419
Gly Leu Thr Phe Asp Asp Tyr Gly
1 5
<210> 420
<211> 8
<212> PRT
<213> Homo Sapien
<400> 420
Ile Asn Trp Asn Gly Asp Asn Thr
1 5
<210> 421
<211> 17
<212> PRT
<213> Homo Sapien
<400> 421
Ala Arg Asp Tyr Tyr Gly Ser Gly Ser Tyr Tyr Asn Val Pro Phe Asp
1 5 10 15
Tyr
<210> 422
<211> 124
<212> PRT
<213> Homo Sapien
<400> 422
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Asn Gly Asp Asn Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Tyr Gly Ser Gly Ser Tyr Tyr Asn Val Pro Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 423
<211> 372
<212> DNA
<213> Homo Sapien
<400> 423
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgcag cctctggact cacctttgat gattatggca tgagctgggt ccgccaagtt 120
ccagggaagg ggctggagtg ggtctctggt attaattgga atggtgataa cacagattat 180
gcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctgcaaatga acagtctgag agccgaggac acggccttgt attactgtgc gagggattac 300
tatggttcgg ggagttatta taacgttcct tttgactact ggggccaggg aaccctggtc 360
accgtctcct ca 372
<210> 424
<211> 454
<212> PRT
<213> Homo Sapien
<400> 424
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Arg Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Asp Asp Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Asn Trp Asn Gly Asp Asn Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Tyr Gly Ser Gly Ser Tyr Tyr Asn Val Pro Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 425
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 425
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgcag cctctggact cacctttgat gattatggca tgagctgggt ccgccaagtt 120
ccagggaagg ggctggagtg ggtctctggt attaattgga atggtgataa cacagattat 180
gcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctgcaaatga acagtctgag agccgaggac acggccttgt attactgtgc gagggattac 300
tatggttcgg ggagttatta taacgttcct tttgactact ggggccaggg aaccctggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 426
<211> 7
<212> PRT
<213> Homo Sapien
<400> 426
Gln Ser Val Ser Ser Ser Tyr
1 5
<210> 427
<211> 3
<212> PRT
<213> Homo Sapien
<400> 427
Gly Ala Ser
1
<210> 428
<211> 8
<212> PRT
<213> Homo Sapien
<400> 428
Gln Gln Tyr Gly Ser Ser Pro Phe
1 5
<210> 429
<211> 107
<212> PRT
<213> Homo Sapien
<400> 429
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Phe Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 430
<211> 321
<212> DNA
<213> Homo Sapien
<400> 430
gaaattgtgt tgacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agcagctact tagcctggta ccagcagaaa 120
cctggccagg ctcccaggct cctcatatat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcagtgg gtctgggaca gacttcactc tcaccatcag aagactggag 240
cctgaagatt ttgcagtgta ttactgtcag cagtatggta gttcaccatt cttcggccct 300
gggaccaaag tggatatcaa a 321
<210> 431
<211> 323
<212> DNA
<213> Homo Sapien
<400> 431
gaaattgtgt tgacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agcagctact tagcctggta ccagcagaaa 120
cctggccagg ctcccaggct cctcatatat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcagtgg gtctgggaca gacttcactc tcaccatcag aagactggag 240
cctgaagatt ttgcagtgta ttactgtcag cagtatggta gttcaccatt cacttcggcc 300
ctgggaccaa agtggatatc aaa 323
<210> 432
<211> 214
<212> PRT
<213> Homo Sapien
<400> 432
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Phe Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 433
<211> 642
<212> DNA
<213> Homo Sapien
<400> 433
gaaattgtgt tgacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agcagctact tagcctggta ccagcagaaa 120
cctggccagg ctcccaggct cctcatatat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcagtgg gtctgggaca gacttcactc tcaccatcag aagactggag 240
cctgaagatt ttgcagtgta ttactgtcag cagtatggta gttcaccatt cttcggccct 300
gggaccaaag tggatatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 434
<211> 644
<212> DNA
<213> Homo Sapien
<400> 434
gaaattgtgt tgacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttagc agcagctact tagcctggta ccagcagaaa 120
cctggccagg ctcccaggct cctcatatat ggtgcatcca gcagggccac tggcatccca 180
gacaggttca gtggcagtgg gtctgggaca gacttcactc tcaccatcag aagactggag 240
cctgaagatt ttgcagtgta ttactgtcag cagtatggta gttcaccatt cacttcggcc 300
ctgggaccaa agtggatatc aaacgtacgg tggccgctcc ctccgtgttc atcttcccac 360
cttccgacga gcagctgaag tccggcaccg cttctgtcgt gtgcctgctg aacaacttct 420
acccccgcga ggccaaggtg cagtggaagg tggacaacgc cctgcagtcc ggcaactccc 480
aggaatccgt gaccgagcag gactccaagg acagcaccta ctccctgtcc tccaccctga 540
ccctgtccaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg 600
gcctgtctag ccccgtgacc aagtctttca accggggcga gtgt 644
<210> 435
<211> 8
<212> PRT
<213> Homo Sapien
<400> 435
Gly Tyr Thr Phe Asn Ser Tyr Gly
1 5
<210> 436
<211> 8
<212> PRT
<213> Homo Sapien
<400> 436
Ile Ser Val His Asn Gly Asn Thr
1 5
<210> 437
<211> 17
<212> PRT
<213> Homo Sapien
<400> 437
Ala Arg Ala Gly Tyr Asp Ile Leu Thr Asp Phe Ser Asp Ala Phe Asp
1 5 10 15
Ile
<210> 438
<211> 124
<212> PRT
<213> Homo Sapien
<400> 438
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ser Tyr
20 25 30
Gly Ile Ile Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Val His Asn Gly Asn Thr Asn Cys Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Thr Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Tyr Asp Ile Leu Thr Asp Phe Ser Asp Ala Phe Asp
100 105 110
Ile Trp Gly His Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 439
<211> 372
<212> DNA
<213> Homo Sapien
<400> 439
caggttcagt tggtgcagtc tggagctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttaat agttatggta tcatctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggatgg atcagcgttc acaatggtaa cacaaactgt 180
gcacagaagc tccagggtag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcctgag aactgacgac acggccgtgt attactgtgc gagagcgggt 300
tacgatattt tgactgattt ttccgatgct tttgatatct ggggccacgg gacaatggtc 360
accgtctctt ca 372
<210> 440
<211> 454
<212> PRT
<213> Homo Sapien
<400> 440
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ser Tyr
20 25 30
Gly Ile Ile Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Val His Asn Gly Asn Thr Asn Cys Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Thr Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Tyr Asp Ile Leu Thr Asp Phe Ser Asp Ala Phe Asp
100 105 110
Ile Trp Gly His Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 441
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 441
caggttcagt tggtgcagtc tggagctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggtta cacctttaat agttatggta tcatctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggatgg atcagcgttc acaatggtaa cacaaactgt 180
gcacagaagc tccagggtag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcctgag aactgacgac acggccgtgt attactgtgc gagagcgggt 300
tacgatattt tgactgattt ttccgatgct tttgatatct ggggccacgg gacaatggtc 360
accgtctctt cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 442
<211> 6
<212> PRT
<213> Homo Sapien
<400> 442
Gln Asn Ile Asn Asn Phe
1 5
<210> 443
<211> 3
<212> PRT
<213> Homo Sapien
<400> 443
Ala Ala Ser
1
<210> 444
<211> 8
<212> PRT
<213> Homo Sapien
<400> 444
Gln Gln Ser Tyr Gly Ile Pro Trp
1 5
<210> 445
<211> 106
<212> PRT
<213> Homo Sapien
<400> 445
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asn Ile Asn Asn Phe
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Glu Gly Lys Gly Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Arg Gly Ile Pro Ser Thr Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Ile Cys Gln Gln Ser Tyr Gly Ile Pro Trp
85 90 95
Val Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 446
<211> 318
<212> DNA
<213> Homo Sapien
<400> 446
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gaacattaat aactttttaa attggtatca gcagaaagaa 120
gggaaaggcc ctaagctcct gatctatgca gcatccagtt tgcaaagagg gataccatca 180
acgttcagtg gcagtggatc tgggacagac ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacat ctgtcaacag agctacggta tcccgtgggt cggccaaggg 300
accaaggtgg aaatcaaa 318
<210> 447
<211> 213
<212> PRT
<213> Homo Sapien
<400> 447
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asn Ile Asn Asn Phe
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Glu Gly Lys Gly Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Arg Gly Ile Pro Ser Thr Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Ile Cys Gln Gln Ser Tyr Gly Ile Pro Trp
85 90 95
Val Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 448
<211> 639
<212> DNA
<213> Homo Sapien
<400> 448
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gaacattaat aactttttaa attggtatca gcagaaagaa 120
gggaaaggcc ctaagctcct gatctatgca gcatccagtt tgcaaagagg gataccatca 180
acgttcagtg gcagtggatc tgggacagac ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacat ctgtcaacag agctacggta tcccgtgggt cggccaaggg 300
accaaggtgg aaatcaaacg tacggtggcc gctccctccg tgttcatctt cccaccttcc 360
gacgagcagc tgaagtccgg caccgcttct gtcgtgtgcc tgctgaacaa cttctacccc 420
cgcgaggcca aggtgcagtg gaaggtggac aacgccctgc agtccggcaa ctcccaggaa 480
tccgtgaccg agcaggactc caaggacagc acctactccc tgtcctccac cctgaccctg 540
tccaaggccg actacgagaa gcacaaggtg tacgcctgcg aagtgaccca ccagggcctg 600
tctagccccg tgaccaagtc tttcaaccgg ggcgagtgt 639
<210> 449
<211> 8
<212> PRT
<213> Homo Sapien
<400> 449
Gly Phe Thr Phe Ser Asp Tyr Phe
1 5
<210> 450
<211> 8
<212> PRT
<213> Homo Sapien
<400> 450
Ile Ser Ser Ser Gly Ser Thr Ile
1 5
<210> 451
<211> 21
<212> PRT
<213> Homo Sapien
<400> 451
Ala Arg Asp His Tyr Asp Gly Ser Gly Ile Tyr Pro Leu Tyr Tyr Tyr
1 5 10 15
Tyr Gly Leu Asp Val
20
<210> 452
<211> 128
<212> PRT
<213> Homo Sapien
<400> 452
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Phe Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Tyr Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Asp Gly Ser Gly Ile Tyr Pro Leu Tyr Tyr Tyr
100 105 110
Tyr Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 453
<211> 384
<212> DNA
<213> Homo Sapien
<400> 453
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactacttca tgagctggat ccgccaggcg 120
ccagggaagg ggctggagtg gatttcatac attagttcta gtggtagtac catatactac 180
gcagactctg tgaggggccg attcaccatc tccagggaca acgccaagta ctcactgtat 240
ctgcaaatga acagcctgag atccgaggac acggccgtgt attactgtgc gagagatcac 300
tacgatggtt cggggattta tcccctctac tactattacg gtttggacgt ctggggccag 360
gggaccacgg tcaccgtctc ctca 384
<210> 454
<211> 458
<212> PRT
<213> Homo Sapien
<400> 454
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Phe Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Tyr Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Asp Gly Ser Gly Ile Tyr Pro Leu Tyr Tyr Tyr
100 105 110
Tyr Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
130 135 140
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
145 150 155 160
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
165 170 175
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
180 185 190
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
195 200 205
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
210 215 220
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
225 230 235 240
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
245 250 255
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
260 265 270
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
275 280 285
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
290 295 300
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
305 310 315 320
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
325 330 335
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
340 345 350
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
355 360 365
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
370 375 380
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
385 390 395 400
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
405 410 415
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
420 425 430
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
435 440 445
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 455
<211> 1380
<212> DNA
<213> Homo Sapien
<400> 455
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactacttca tgagctggat ccgccaggcg 120
ccagggaagg ggctggagtg gatttcatac attagttcta gtggtagtac catatactac 180
gcagactctg tgaggggccg attcaccatc tccagggaca acgccaagta ctcactgtat 240
ctgcaaatga acagcctgag atccgaggac acggccgtgt attactgtgc gagagatcac 300
tacgatggtt cggggattta tcccctctac tactattacg gtttggacgt ctggggccag 360
gggaccacgg tcaccgtctc ctcagccagc accaagggcc cctctgtgtt ccctctggcc 420
ccttccagca agtccacctc tggcggaaca gccgctctgg gctgcctcgt gaaggactac 480
ttccccgagc ctgtgaccgt gtcctggaac tctggcgctc tgaccagcgg agtgcacacc 540
ttccctgctg tgctgcagtc ctccggcctg tactccctgt cctccgtcgt gaccgtgcct 600
tccagctctc tgggcaccca gacctacatc tgcaacgtga accacaagcc ctccaacacc 660
aaggtggaca agaaggtgga acccaagtcc tgcgacaaga cccacacctg tcccccttgt 720
cctgcccctg aactgctggg cggaccttcc gtgttcctgt tccccccaaa gcccaaggac 780
accctgatga tctcccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccacgag 840
gaccctgaag tgaagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 900
aagcctagag aggaacagta caactccacc taccgggtgg tgtccgtgct gaccgtgctg 960
caccaggatt ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa ggccctgcct 1020
gcccccatcg aaaagaccat ctccaaggcc aagggccagc cccgggaacc ccaggtgtac 1080
acactgcccc ctagcaggga cgagctgacc aagaaccagg tgtccctgac ctgtctcgtg 1140
aaaggcttct acccctccga tatcgccgtg gaatgggagt ccaacggcca gcctgagaac 1200
aactacaaga ccaccccccc tgtgctggac tccgacggct cattcttcct gtacagcaag 1260
ctgacagtgg acaagtcccg gtggcagcag ggcaacgtgt tctcctgctc cgtgatgcac 1320
gaggccctgc acaaccacta cacccagaag tccctgtccc tgagccccgg caagtgatga 1380
<210> 456
<211> 11
<212> PRT
<213> Homo Sapien
<400> 456
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 457
<211> 3
<212> PRT
<213> Homo Sapien
<400> 457
Leu Gly Ser
1
<210> 458
<211> 9
<212> PRT
<213> Homo Sapien
<400> 458
Met Gln Ala Leu Gln Thr Pro Arg Ser
1 5
<210> 459
<211> 111
<212> PRT
<213> Homo Sapien
<400> 459
Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu
1 5 10 15
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn
20 25 30
Gly Tyr Asn Tyr Leu Asp Tyr Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Gly Ser Tyr Arg Ala Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu
85 90 95
Gln Thr Pro Arg Ser Phe Gly Gln Gly Thr Thr Leu Glu Ile Lys
100 105 110
<210> 460
<211> 333
<212> DNA
<213> Homo Sapien
<400> 460
attgtgatga ctcagtctcc actctcccta cccgtcaccc ctggagagcc ggcctccatc 60
tcctgcaggt ctagtcagag cctcctgcat agtaatggat acaactattt ggattattac 120
ctgcagaagc cagggcagtc tccacagctc ctgatctatt tgggttctta tcgggcctcc 180
ggggtccctg acaggttcag tggcagtgga tcaggcacag attttacact gaaaatcagc 240
agagtggagg ctgaggatgt tggggtttat tactgcatgc aagctctaca aactcctcgc 300
agttttggcc aggggaccac gctggagatc aaa 333
<210> 461
<211> 218
<212> PRT
<213> Homo Sapien
<400> 461
Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu
1 5 10 15
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn
20 25 30
Gly Tyr Asn Tyr Leu Asp Tyr Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Gly Ser Tyr Arg Ala Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu
85 90 95
Gln Thr Pro Arg Ser Phe Gly Gln Gly Thr Thr Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 462
<211> 654
<212> DNA
<213> Homo Sapien
<400> 462
attgtgatga ctcagtctcc actctcccta cccgtcaccc ctggagagcc ggcctccatc 60
tcctgcaggt ctagtcagag cctcctgcat agtaatggat acaactattt ggattattac 120
ctgcagaagc cagggcagtc tccacagctc ctgatctatt tgggttctta tcgggcctcc 180
ggggtccctg acaggttcag tggcagtgga tcaggcacag attttacact gaaaatcagc 240
agagtggagg ctgaggatgt tggggtttat tactgcatgc aagctctaca aactcctcgc 300
agttttggcc aggggaccac gctggagatc aaacgtacgg tggccgctcc ctccgtgttc 360
atcttcccac cttccgacga gcagctgaag tccggcaccg cttctgtcgt gtgcctgctg 420
aacaacttct acccccgcga ggccaaggtg cagtggaagg tggacaacgc cctgcagtcc 480
ggcaactccc aggaatccgt gaccgagcag gactccaagg acagcaccta ctccctgtcc 540
tccaccctga ccctgtccaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 600
acccaccagg gcctgtctag ccccgtgacc aagtctttca accggggcga gtgt 654
<210> 463
<211> 10
<212> PRT
<213> Homo Sapien
<400> 463
Gly Phe Ser Leu Ser Thr Thr Gly Val Gly
1 5 10
<210> 464
<211> 7
<212> PRT
<213> Homo Sapien
<400> 464
Ile Tyr Trp Asp Asp Asp Lys
1 5
<210> 465
<211> 16
<212> PRT
<213> Homo Sapien
<400> 465
Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp Val
1 5 10 15
<210> 466
<211> 124
<212> PRT
<213> Homo Sapien
<400> 466
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Thr
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Val Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 467
<211> 372
<212> DNA
<213> Homo Sapien
<400> 467
cagatcacct tgaaggagtc tggtcctacg ctggtgaaac ccacacagac cctcacgctg 60
acctgcacct tctctgggtt ctcactcagc actactggag tgggtgtggg ctggatccgt 120
cagcccccag gaaaggccct ggagtggctt gcagtcattt attgggatga tgataagcgc 180
tacagcccat ctctgaagag cagactcacc atcaccaagg acacctccaa aaaccaggtg 240
gtccttacaa tgaccaacat ggaccctgtg gacacagcca catatttctg tacacacgga 300
tatggttcgg cgagttatta ccactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 468
<211> 454
<212> PRT
<213> Homo Sapien
<400> 468
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Thr
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Val Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 469
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 469
cagatcacct tgaaggagtc tggtcctacg ctggtgaaac ccacacagac cctcacgctg 60
acctgcacct tctctgggtt ctcactcagc actactggag tgggtgtggg ctggatccgt 120
cagcccccag gaaaggccct ggagtggctt gcagtcattt attgggatga tgataagcgc 180
tacagcccat ctctgaagag cagactcacc atcaccaagg acacctccaa aaaccaggtg 240
gtccttacaa tgaccaacat ggaccctgtg gacacagcca catatttctg tacacacgga 300
tatggttcgg cgagttatta ccactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 470
<211> 6
<212> PRT
<213> Homo Sapien
<400> 470
Gln Ser Val Thr Asn Tyr
1 5
<210> 471
<211> 3
<212> PRT
<213> Homo Sapien
<400> 471
Asp Ala Ser
1
<210> 472
<211> 9
<212> PRT
<213> Homo Sapien
<400> 472
Gln His Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 473
<211> 107
<212> PRT
<213> Homo Sapien
<400> 473
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Asn Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 474
<211> 322
<212> DNA
<213> Homo Sapien
<400> 474
gaaattgtat tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttacc aactacttag cctggcacca acagaaacct 120
ggccaggctc ccaggctcct catctatgat gcatccaaca gggccactgg catcccagcc 180
aggttcagtg gcagtgggtc tgggacagac ttcactctca ccatcagcag cctagagcct 240
gaagattttg cagtttatta ctgtcagcac cgtagcaact ggcctctcac tttcggcgga 300
gggaccaagg tggagatcaa ac 322
<210> 475
<211> 214
<212> PRT
<213> Homo Sapien
<400> 475
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Asn Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 476
<211> 643
<212> DNA
<213> Homo Sapien
<400> 476
gaaattgtat tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttacc aactacttag cctggcacca acagaaacct 120
ggccaggctc ccaggctcct catctatgat gcatccaaca gggccactgg catcccagcc 180
aggttcagtg gcagtgggtc tgggacagac ttcactctca ccatcagcag cctagagcct 240
gaagattttg cagtttatta ctgtcagcac cgtagcaact ggcctctcac tttcggcgga 300
gggaccaagg tggagatcaa accgtacggt ggccgctccc tccgtgttca tcttcccacc 360
ttccgacgag cagctgaagt ccggcaccgc ttctgtcgtg tgcctgctga acaacttcta 420
cccccgcgag gccaaggtgc agtggaaggt ggacaacgcc ctgcagtccg gcaactccca 480
ggaatccgtg accgagcagg actccaagga cagcacctac tccctgtcct ccaccctgac 540
cctgtccaag gccgactacg agaagcacaa ggtgtacgcc tgcgaagtga cccaccaggg 600
cctgtctagc cccgtgacca agtctttcaa ccggggcgag tgt 643
<210> 477
<211> 10
<212> PRT
<213> Homo Sapien
<400> 477
Gly Phe Ser Leu Ser Thr Ser Gly Val Gly
1 5 10
<210> 478
<211> 7
<212> PRT
<213> Homo Sapien
<400> 478
Ile Tyr Trp Asp Asp Asp Lys
1 5
<210> 479
<211> 16
<212> PRT
<213> Homo Sapien
<400> 479
Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp Val
1 5 10 15
<210> 480
<211> 124
<212> PRT
<213> Homo Sapien
<400> 480
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Val Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 481
<211> 372
<212> DNA
<213> Homo Sapien
<400> 481
cagatcacct tgaaggagtc tggtcctacg ctggtgaaac ccacacagac cctcacgctg 60
acctgcacct tctctgggtt ctcactcagc actagtggag tgggtgtggg ctggatccgt 120
cagcccccag gaaaggccct ggagtggctt gcagtcattt attgggatga tgataagcgc 180
tacagcccat ctctgaagag caggctcacc atcaccaagg acacctccaa aaaccaggtg 240
gtccttacaa tgaccaacat ggaccctgtg gacacagcca catatttctg tacacacgga 300
tatggttcgg cgagttatta ccactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 482
<211> 454
<212> PRT
<213> Homo Sapien
<400> 482
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Val Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Phe
85 90 95
Cys Thr His Gly Tyr Gly Ser Ala Ser Tyr Tyr His Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 483
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 483
cagatcacct tgaaggagtc tggtcctacg ctggtgaaac ccacacagac cctcacgctg 60
acctgcacct tctctgggtt ctcactcagc actagtggag tgggtgtggg ctggatccgt 120
cagcccccag gaaaggccct ggagtggctt gcagtcattt attgggatga tgataagcgc 180
tacagcccat ctctgaagag caggctcacc atcaccaagg acacctccaa aaaccaggtg 240
gtccttacaa tgaccaacat ggaccctgtg gacacagcca catatttctg tacacacgga 300
tatggttcgg cgagttatta ccactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 484
<211> 6
<212> PRT
<213> Homo Sapien
<400> 484
Gln Ser Val Thr Asn Tyr
1 5
<210> 485
<211> 3
<212> PRT
<213> Homo Sapien
<400> 485
Asp Ala Ser
1
<210> 486
<211> 9
<212> PRT
<213> Homo Sapien
<400> 486
Gln Gln Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 487
<211> 107
<212> PRT
<213> Homo Sapien
<400> 487
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Asn Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 488
<211> 321
<212> DNA
<213> Homo Sapien
<400> 488
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttacc aactacttag cctggcacca acagaaacct 120
ggccaggctc ccaggctcct catctatgat gcatccaaca gggccactgg catcccagcc 180
aggttcagtg gcagtgggtc tgggacagac ttcactctca ccatcagcag cctagagcct 240
gaagattttg cagtttatta ctgtcagcag cgtagcaact ggcctctcac tttcggcgga 300
gggaccaagg tggagatcaa a 321
<210> 489
<211> 214
<212> PRT
<213> Homo Sapien
<400> 489
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Asn Tyr
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 490
<211> 642
<212> DNA
<213> Homo Sapien
<400> 490
gaaattgtgt tgacacagtc tccagccacc ctgtctttgt ctccagggga aagagccacc 60
ctctcctgca gggccagtca gagtgttacc aactacttag cctggcacca acagaaacct 120
ggccaggctc ccaggctcct catctatgat gcatccaaca gggccactgg catcccagcc 180
aggttcagtg gcagtgggtc tgggacagac ttcactctca ccatcagcag cctagagcct 240
gaagattttg cagtttatta ctgtcagcag cgtagcaact ggcctctcac tttcggcgga 300
gggaccaagg tggagatcaa acgtacggtg gccgctccct ccgtgttcat cttcccacct 360
tccgacgagc agctgaagtc cggcaccgct tctgtcgtgt gcctgctgaa caacttctac 420
ccccgcgagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg caactcccag 480
gaatccgtga ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaag gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtctagcc ccgtgaccaa gtctttcaac cggggcgagt gt 642
<210> 491
<211> 8
<212> PRT
<213> Homo Sapien
<400> 491
Gly Phe Thr Phe Ser Asp Tyr Tyr
1 5
<210> 492
<211> 8
<212> PRT
<213> Homo Sapien
<400> 492
Ile Ser Ser Ser Gly Ser Thr Ile
1 5
<210> 493
<211> 20
<212> PRT
<213> Homo Sapien
<400> 493
Ala Arg Asp Phe Tyr Asp Ile Leu Thr Asp Ser Pro Tyr Phe Tyr Tyr
1 5 10 15
Gly Val Asp Val
20
<210> 494
<211> 127
<212> PRT
<213> Homo Sapien
<400> 494
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Ile Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Tyr Asp Ile Leu Thr Asp Ser Pro Tyr Phe Tyr Tyr
100 105 110
Gly Val Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 495
<211> 381
<212> DNA
<213> Homo Sapien
<400> 495
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactactaca tgagctggat ccgccaggct 120
ccagggaagg ggctggagtg ggtttcatac attagtagta gtggtagtac catatactac 180
gcagactctg tgaagggccg attcaccatc tccagggaca acgccaagaa ctcactgtat 240
ctgcaaatta acagcctgag agccgaggac acggccgtgt attactgtgc gagagatttt 300
tacgatattt tgactgatag tccgtacttc tactacggtg tggacgtctg gggccaaggg 360
accacggtca ccgtctcctc a 381
<210> 496
<211> 457
<212> PRT
<213> Homo Sapien
<400> 496
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Ile Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Tyr Asp Ile Leu Thr Asp Ser Pro Tyr Phe Tyr Tyr
100 105 110
Gly Val Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
210 215 220
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 497
<211> 1377
<212> DNA
<213> Homo Sapien
<400> 497
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt caccttcagt gactactaca tgagctggat ccgccaggct 120
ccagggaagg ggctggagtg ggtttcatac attagtagta gtggtagtac catatactac 180
gcagactctg tgaagggccg attcaccatc tccagggaca acgccaagaa ctcactgtat 240
ctgcaaatta acagcctgag agccgaggac acggccgtgt attactgtgc gagagatttt 300
tacgatattt tgactgatag tccgtacttc tactacggtg tggacgtctg gggccaaggg 360
accacggtca ccgtctcctc agccagcacc aagggcccct ctgtgttccc tctggcccct 420
tccagcaagt ccacctctgg cggaacagcc gctctgggct gcctcgtgaa ggactacttc 480
cccgagcctg tgaccgtgtc ctggaactct ggcgctctga ccagcggagt gcacaccttc 540
cctgctgtgc tgcagtcctc cggcctgtac tccctgtcct ccgtcgtgac cgtgccttcc 600
agctctctgg gcacccagac ctacatctgc aacgtgaacc acaagccctc caacaccaag 660
gtggacaaga aggtggaacc caagtcctgc gacaagaccc acacctgtcc cccttgtcct 720
gcccctgaac tgctgggcgg accttccgtg ttcctgttcc ccccaaagcc caaggacacc 780
ctgatgatct cccggacccc cgaagtgacc tgcgtggtgg tggatgtgtc ccacgaggac 840
cctgaagtga agttcaattg gtacgtggac ggcgtggaag tgcacaacgc caagaccaag 900
cctagagagg aacagtacaa ctccacctac cgggtggtgt ccgtgctgac cgtgctgcac 960
caggattggc tgaacggcaa agagtacaag tgcaaggtgt ccaacaaggc cctgcctgcc 1020
cccatcgaaa agaccatctc caaggccaag ggccagcccc gggaacccca ggtgtacaca 1080
ctgcccccta gcagggacga gctgaccaag aaccaggtgt ccctgacctg tctcgtgaaa 1140
ggcttctacc cctccgatat cgccgtggaa tgggagtcca acggccagcc tgagaacaac 1200
tacaagacca ccccccctgt gctggactcc gacggctcat tcttcctgta cagcaagctg 1260
acagtggaca agtcccggtg gcagcagggc aacgtgttct cctgctccgt gatgcacgag 1320
gccctgcaca accactacac ccagaagtcc ctgtccctga gccccggcaa gtgatga 1377
<210> 498
<211> 11
<212> PRT
<213> Homo Sapien
<400> 498
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 499
<211> 3
<212> PRT
<213> Homo Sapien
<400> 499
Leu Gly Ser
1
<210> 500
<211> 9
<212> PRT
<213> Homo Sapien
<400> 500
Met Gln Ala Leu Gln Thr Pro Arg Thr
1 5
<210> 501
<211> 112
<212> PRT
<213> Homo Sapien
<400> 501
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 502
<211> 336
<212> DNA
<213> Homo Sapien
<400> 502
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
cggacgttcg gccaagggac caaggtggaa atcaaa 336
<210> 503
<211> 219
<212> PRT
<213> Homo Sapien
<400> 503
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 504
<211> 657
<212> DNA
<213> Homo Sapien
<400> 504
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
cggacgttcg gccaagggac caaggtggaa atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 505
<211> 239
<212> PRT
<213> Homo Sapien
<400> 505
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr Ile Glu Gly
210 215 220
Arg Asp Tyr Lys Asp Asp Asp Asp Lys His His His His His His
225 230 235
<210> 506
<211> 179
<212> PRT
<213> Homo Sapien
<400> 506
Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile Phe His Asn Gly
1 5 10 15
Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val Gln Gln Phe Lys
20 25 30
Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp Leu Thr Lys Thr
35 40 45
Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu Lys Phe Cys His
50 55 60
Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Tyr Asn Leu Asp
65 70 75 80
His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser Ile Phe Asp Pro
85 90 95
Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu His Ile Tyr Glu
100 105 110
Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro Ile Gly Cys Ala
115 120 125
Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile Leu Ile Cys Trp Leu
130 135 140
Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro Asn Gly Glu Tyr
145 150 155 160
Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser Arg Leu Thr Asp
165 170 175
Val Thr Leu
<210> 507
<211> 121
<212> PRT
<213> Homo Sapien
<400> 507
Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile Phe His Asn Gly
1 5 10 15
Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val Gln Gln Phe Lys
20 25 30
Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp Leu Thr Lys Thr
35 40 45
Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu Lys Phe Cys His
50 55 60
Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Tyr Asn Leu Asp
65 70 75 80
His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser Ile Phe Asp Pro
85 90 95
Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu His Ile Tyr Glu
100 105 110
Ser Gln Leu Cys Cys Gln Leu Lys Phe
115 120
<210> 508
<211> 199
<212> PRT
<213> Homo Sapien
<400> 508
Met Lys Ser Gly Leu Trp Tyr Phe Phe Leu Phe Cys Leu Arg Ile Lys
1 5 10 15
Val Leu Thr Gly Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile
20 25 30
Phe His Asn Gly Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val
35 40 45
Gln Gln Phe Lys Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp
50 55 60
Leu Thr Lys Thr Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu
65 70 75 80
Lys Phe Cys His Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu
85 90 95
Tyr Asn Leu Asp His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser
100 105 110
Ile Phe Asp Pro Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro
130 135 140
Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile Leu
145 150 155 160
Ile Cys Trp Leu Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro
165 170 175
Asn Gly Glu Tyr Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser
180 185 190
Arg Leu Thr Asp Val Thr Leu
195
<210> 509
<211> 33
<212> PRT
<213> Homo Sapien
<400> 509
Lys Tyr Ser Ser Ser Val His Asp Pro Asn Gly Glu Tyr Met Phe Met
1 5 10 15
Arg Ala Val Asn Thr Ala Lys Lys Ser Arg Leu Thr Asp Val Thr Leu
20 25 30
Met
<210> 510
<211> 128
<212> PRT
<213> Mus Musculus
<400> 510
Glu Ile Asn Gly Ser Ala Asp His Arg Met Phe Ser Phe His Asn Gly
1 5 10 15
Gly Val Gln Ile Ser Cys Lys Tyr Pro Glu Thr Val Gln Gln Leu Lys
20 25 30
Met Arg Leu Phe Arg Glu Arg Glu Val Leu Cys Glu Leu Thr Lys Thr
35 40 45
Lys Gly Ser Gly Asn Ala Val Ser Ile Lys Asn Pro Met Leu Cys Leu
50 55 60
Tyr His Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Asn Asn Pro Asp
65 70 75 80
Ser Ser Gln Gly Ser Tyr Tyr Phe Cys Ser Leu Ser Ile Phe Asp Pro
85 90 95
Pro Pro Phe Gln Glu Arg Asn Leu Ser Gly Gly Tyr Leu His Ile Tyr
100 105 110
Glu Ser Gln Leu Cys Cys Gln Leu Lys Ile Val Val Gln Val Thr Glu
115 120 125
<210> 511
<211> 121
<212> PRT
<213> Mus Musculus
<400> 511
Glu Ile Asn Gly Ser Ala Asp His Arg Met Phe Ser Phe His Asn Gly
1 5 10 15
Gly Val Gln Ile Ser Cys Lys Tyr Pro Glu Thr Val Gln Gln Leu Lys
20 25 30
Met Arg Leu Phe Arg Glu Arg Glu Val Leu Cys Glu Leu Thr Lys Thr
35 40 45
Lys Gly Ser Gly Asn Ala Val Ser Ile Lys Asn Pro Met Leu Cys Leu
50 55 60
Tyr His Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Asn Asn Pro Asp
65 70 75 80
Ser Ser Gln Gly Ser Tyr Tyr Phe Cys Ser Leu Ser Ile Phe Asp Pro
85 90 95
Pro Pro Phe Gln Glu Arg Asn Leu Ser Gly Gly Tyr Leu His Ile Tyr
100 105 110
Glu Ser Gln Leu Cys Cys Gln Leu Lys
115 120
<210> 512
<211> 147
<212> PRT
<213> Mus Musculus
<400> 512
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Glu Ile Asn Gly Ser Ala Asp His Arg Met Phe Ser Phe
20 25 30
His Asn Gly Gly Val Gln Ile Ser Cys Lys Tyr Pro Glu Thr Val Gln
35 40 45
Gln Leu Lys Met Arg Leu Phe Arg Glu Arg Glu Val Leu Cys Glu Leu
50 55 60
Thr Lys Thr Lys Gly Ser Gly Asn Ala Val Ser Ile Lys Asn Pro Met
65 70 75 80
Leu Cys Leu Tyr His Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Asn
85 90 95
Asn Pro Asp Ser Ser Gln Gly Ser Tyr Tyr Phe Cys Ser Leu Ser Ile
100 105 110
Phe Asp Pro Pro Pro Phe Gln Glu Arg Asn Leu Ser Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Ile Val Val Gln
130 135 140
Val Thr Glu
145
<210> 513
<211> 199
<212> PRT
<213> Cynomologus
<400> 513
Met Lys Ser Gly Leu Trp Tyr Phe Phe Leu Phe Cys Leu His Met Lys
1 5 10 15
Val Leu Thr Gly Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile
20 25 30
Phe His Asn Gly Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val
35 40 45
Gln Gln Phe Lys Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp
50 55 60
Leu Thr Lys Thr Lys Gly Ser Gly Asn Lys Val Ser Ile Lys Ser Leu
65 70 75 80
Lys Phe Cys His Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu
85 90 95
Tyr Asn Leu Asp Arg Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser
100 105 110
Ile Phe Asp Pro Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro
130 135 140
Ile Gly Cys Ala Thr Phe Val Val Val Cys Ile Phe Gly Cys Ile Leu
145 150 155 160
Ile Cys Trp Leu Thr Lys Lys Lys Tyr Ser Ser Thr Val His Asp Pro
165 170 175
Asn Gly Glu Tyr Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser
180 185 190
Arg Leu Thr Gly Thr Thr Pro
195
<210> 514
<211> 120
<212> PRT
<213> Cynomologus
<400> 514
Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile Phe His Asn Gly
1 5 10 15
Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val Gln Gln Phe Lys
20 25 30
Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp Leu Thr Lys Thr
35 40 45
Lys Gly Ser Gly Asn Lys Val Ser Ile Lys Ser Leu Lys Phe Cys His
50 55 60
Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu Tyr Asn Leu Asp
65 70 75 80
Arg Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser Ile Phe Asp Pro
85 90 95
Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu His Ile Tyr Glu
100 105 110
Ser Gln Leu Cys Cys Gln Leu Lys
115 120
<210> 515
<211> 240
<212> PRT
<213> Homo Sapien
<400> 515
Asp Thr Gln Glu Lys Glu Val Arg Ala Met Val Gly Ser Asp Val Glu
1 5 10 15
Leu Ser Cys Ala Cys Pro Glu Gly Ser Arg Phe Asp Leu Asn Asp Val
20 25 30
Tyr Val Tyr Trp Gln Thr Ser Glu Ser Lys Thr Val Val Thr Tyr His
35 40 45
Ile Pro Gln Asn Ser Ser Leu Glu Asn Val Asp Ser Arg Tyr Arg Asn
50 55 60
Arg Ala Leu Met Ser Pro Ala Gly Met Leu Arg Gly Asp Phe Ser Leu
65 70 75 80
Arg Leu Phe Asn Val Thr Pro Gln Asp Glu Gln Lys Phe His Cys Leu
85 90 95
Val Leu Ser Gln Ser Leu Gly Phe Gln Glu Val Leu Ser Val Glu Val
100 105 110
Thr Leu His Val Ala Ala Asn Phe Ser Val Pro Val Val Ser Ala Pro
115 120 125
His Ser Pro Ser Gln Asp Glu Leu Thr Phe Thr Cys Thr Ser Ile Asn
130 135 140
Gly Tyr Pro Arg Pro Asn Val Tyr Trp Ile Asn Lys Thr Asp Asn Ser
145 150 155 160
Leu Leu Asp Gln Ala Leu Gln Asn Asp Thr Val Phe Leu Asn Met Arg
165 170 175
Gly Leu Tyr Asp Val Val Ser Val Leu Arg Ile Ala Arg Thr Pro Ser
180 185 190
Val Asn Ile Gly Cys Cys Ile Glu Asn Val Leu Leu Gln Gln Asn Leu
195 200 205
Thr Val Gly Ser Gln Thr Gly Asn Asp Ile Gly Glu Arg Asp Lys Ile
210 215 220
Thr Glu Asn Pro Val Ser Thr Gly Glu Lys Asn Ala Ala Thr Trp Ser
225 230 235 240
<210> 516
<211> 302
<212> PRT
<213> Homo Sapien
<400> 516
Met Arg Leu Gly Ser Pro Gly Leu Leu Phe Leu Leu Phe Ser Ser Leu
1 5 10 15
Arg Ala Asp Thr Gln Glu Lys Glu Val Arg Ala Met Val Gly Ser Asp
20 25 30
Val Glu Leu Ser Cys Ala Cys Pro Glu Gly Ser Arg Phe Asp Leu Asn
35 40 45
Asp Val Tyr Val Tyr Trp Gln Thr Ser Glu Ser Lys Thr Val Val Thr
50 55 60
Tyr His Ile Pro Gln Asn Ser Ser Leu Glu Asn Val Asp Ser Arg Tyr
65 70 75 80
Arg Asn Arg Ala Leu Met Ser Pro Ala Gly Met Leu Arg Gly Asp Phe
85 90 95
Ser Leu Arg Leu Phe Asn Val Thr Pro Gln Asp Glu Gln Lys Phe His
100 105 110
Cys Leu Val Leu Ser Gln Ser Leu Gly Phe Gln Glu Val Leu Ser Val
115 120 125
Glu Val Thr Leu His Val Ala Ala Asn Phe Ser Val Pro Val Val Ser
130 135 140
Ala Pro His Ser Pro Ser Gln Asp Glu Leu Thr Phe Thr Cys Thr Ser
145 150 155 160
Ile Asn Gly Tyr Pro Arg Pro Asn Val Tyr Trp Ile Asn Lys Thr Asp
165 170 175
Asn Ser Leu Leu Asp Gln Ala Leu Gln Asn Asp Thr Val Phe Leu Asn
180 185 190
Met Arg Gly Leu Tyr Asp Val Val Ser Val Leu Arg Ile Ala Arg Thr
195 200 205
Pro Ser Val Asn Ile Gly Cys Cys Ile Glu Asn Val Leu Leu Gln Gln
210 215 220
Asn Leu Thr Val Gly Ser Gln Thr Gly Asn Asp Ile Gly Glu Arg Asp
225 230 235 240
Lys Ile Thr Glu Asn Pro Val Ser Thr Gly Glu Lys Asn Ala Ala Thr
245 250 255
Trp Ser Ile Leu Ala Val Leu Cys Leu Leu Val Val Val Ala Val Ala
260 265 270
Ile Gly Trp Val Cys Arg Asp Arg Cys Leu Gln His Ser Tyr Ala Gly
275 280 285
Ala Trp Ala Val Ser Pro Glu Thr Glu Leu Thr Gly His Val
290 295 300
<210> 517
<211> 113
<212> PRT
<213> Homo Sapien
<400> 517
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
1 5 10 15
Thr Ala Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu
20 25 30
Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu
35 40 45
Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp
50 55 60
Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu
65 70 75 80
Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu
85 90 95
Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu
100 105 110
Thr
<210> 518
<211> 113
<212> PRT
<213> Homo Sapien
<400> 518
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
1 5 10 15
Thr Gln Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu
20 25 30
Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu
35 40 45
Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp
50 55 60
Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu
65 70 75 80
Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu
85 90 95
Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu
100 105 110
Thr
<210> 519
<211> 336
<212> DNA
<213> Homo Sapien
<400> 519
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
ctcagttttg gccaggggac caagctggag atcaaa 336
<210> 520
<211> 657
<212> DNA
<213> Homo Sapien
<400> 520
gatattgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtgatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc tactcgggcc 180
tccgggttcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactccg 300
ctcagttttg gccaggggac caagctggag atcaaacgta cggtggccgc tccctccgtg 360
ttcatcttcc caccttccga cgagcagctg aagtccggca ccgcttctgt cgtgtgcctg 420
ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa cgccctgcag 480
tccggcaact cccaggaatc cgtgaccgag caggactcca aggacagcac ctactccctg 540
tcctccaccc tgaccctgtc caaggccgac tacgagaagc acaaggtgta cgcctgcgaa 600
gtgacccacc agggcctgtc tagccccgtg accaagtctt tcaaccgggg cgagtgt 657
<210> 521
<211> 372
<212> DNA
<213> Homo Sapien
<400> 521
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgtag cctctggagt cacctttgat gattatggca tgagctgggt ccgccaagct 120
ccagggaagg ggctggagtg ggtctctggt attaattgga atggtggcga cacagattat 180
tcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctacaaatga atagtctgag agccgaggac acggccttgt attactgtgc gagggatttc 300
tatggttcgg ggagttatta tcacgttcct tttgactact ggggccaggg aatcctggtc 360
accgtctcct ca 372
<210> 522
<211> 1368
<212> DNA
<213> Homo Sapien
<400> 522
gaggtgcagc tggtggagtc tgggggaggt gtggtacggc ctggggggtc cctgagactc 60
tcctgtgtag cctctggagt cacctttgat gattatggca tgagctgggt ccgccaagct 120
ccagggaagg ggctggagtg ggtctctggt attaattgga atggtggcga cacagattat 180
tcagactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctacaaatga atagtctgag agccgaggac acggccttgt attactgtgc gagggatttc 300
tatggttcgg ggagttatta tcacgttcct tttgactact ggggccaggg aatcctggtc 360
accgtctcct cagccagcac caagggcccc tctgtgttcc ctctggcccc ttccagcaag 420
tccacctctg gcggaacagc cgctctgggc tgcctcgtga aggactactt ccccgagcct 480
gtgaccgtgt cctggaactc tggcgctctg accagcggag tgcacacctt ccctgctgtg 540
ctgcagtcct ccggcctgta ctccctgtcc tccgtcgtga ccgtgccttc cagctctctg 600
ggcacccaga cctacatctg caacgtgaac cacaagccct ccaacaccaa ggtggacaag 660
aaggtggaac ccaagtcctg cgacaagacc cacacctgtc ccccttgtcc tgcccctgaa 720
ctgctgggcg gaccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 780
tcccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 840
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gcctagagag 900
gaacagtaca actccaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggattgg 960
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgaa 1020
aagaccatct ccaaggccaa gggccagccc cgggaacccc aggtgtacac actgccccct 1080
agcagggacg agctgaccaa gaaccaggtg tccctgacct gtctcgtgaa aggcttctac 1140
ccctccgata tcgccgtgga atgggagtcc aacggccagc ctgagaacaa ctacaagacc 1200
accccccctg tgctggactc cgacggctca ttcttcctgt acagcaagct gacagtggac 1260
aagtcccggt ggcagcaggg caacgtgttc tcctgctccg tgatgcacga ggccctgcac 1320
aaccactaca cccagaagtc cctgtccctg agccccggca agtgatga 1368
<210> 523
<211> 990
<212> DNA
<213> Homo Sapien
<400> 523
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 720
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctat agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc cccgggtaaa 990
<210> 524
<211> 330
<212> PRT
<213> Homo Sapien
<400> 524
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 525
<211> 990
<212> DNA
<213> Homo Sapien
<400> 525
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acatcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 526
<211> 330
<212> PRT
<213> Homo Sapien
<400> 526
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Ile Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 527
<211> 978
<212> DNA
<213> Homo Sapien
<400> 527
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cagctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt tgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacgca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 528
<211> 326
<212> PRT
<213> Homo Sapien
<400> 528
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 529
<211> 978
<212> DNA
<213> Homo Sapien
<400> 529
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgacctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
atggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt cgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacaca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 530
<211> 326
<212> PRT
<213> Homo Sapien
<400> 530
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Thr Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Met Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 531
<211> 978
<212> DNA
<213> Homo Sapien
<400> 531
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cagctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt tgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatcgc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacgca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 532
<211> 326
<212> PRT
<213> Homo Sapien
<400> 532
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 533
<211> 978
<212> DNA
<213> Homo Sapien
<400> 533
gcctccacca agggcccatc ggtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgctctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcaacttcgg cacccagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagac agttgagcgc 300
aaatgttgtg tcgagtgccc accgtgccca gcaccacctg tggcaggacc gtcagtcttc 360
ctcttccccc caaaacccaa ggacaccctc atgatctccc ggacccctga ggtcacgtgc 420
gtggtggtgg acgtgagcca cgaagacccc gaggtccagt tcaactggta cgtggacggc 480
gtggaggtgc ataatgccaa gacaaagcca cgggaggagc agttcaacag cacgttccgt 540
gtggtcagcg tcctcaccgt cgtgcaccag gactggctga acggcaagga gtacaagtgc 600
aaggtctcca acaaaggcct cccagccccc atcgagaaaa ccatctccaa aaccaaaggg 660
cagccccgag aaccacaggt gtacaccctg cccccatccc gggaggagat gaccaagaac 720
caggtcagcc tgacctgcct ggtcaaaggc ttctacccca gcgacatctc cgtggagtgg 780
gagagcaatg ggcagccgga gaacaactac aagaccacac ctcccatgct ggactccgac 840
ggctccttct tcctctacag caagctcacc gtggacaaga gcaggtggca gcaggggaac 900
gtcttctcat gctccgtgat gcatgaggct ctgcacaacc actacacaca gaagagcctc 960
tccctgtctc cgggtaaa 978
<210> 534
<211> 326
<212> PRT
<213> Homo Sapien
<400> 534
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ser Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 535
<211> 318
<212> DNA
<213> Homo Sapien
<400> 535
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcgta agtgacttca acccgggagc cgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gtgggagtgg agaccaccaa accctccaaa 180
caaagcaaca acaagtatgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccgggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgctct 318
<210> 536
<211> 106
<212> PRT
<213> Homo Sapien
<400> 536
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Val Ser Asp
20 25 30
Phe Asn Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Val Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Arg Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 537
<211> 990
<212> DNA
<213> Homo Sapien
<400> 537
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agttgagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gggtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 538
<211> 106
<212> PRT
<213> Homo Sapien
<400> 538
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 539
<211> 157
<212> PRT
<213> Homo Sapien
<400> 539
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Met Met Thr Gly Thr Ile Glu Thr Thr Gly Asn Ile Ser
20 25 30
Ala Glu Lys Gly Gly Ser Ile Ile Leu Gln Cys His Leu Ser Ser Thr
35 40 45
Thr Ala Gln Val Thr Gln Val Asn Trp Glu Gln Gln Asp Gln Leu Leu
50 55 60
Ala Ile Cys Asn Ala Asp Leu Gly Trp His Ile Ser Pro Ser Phe Lys
65 70 75 80
Asp Arg Val Ala Pro Gly Pro Gly Leu Gly Leu Thr Leu Gln Ser Leu
85 90 95
Thr Val Asn Asp Thr Gly Glu Tyr Phe Cys Ile Tyr His Thr Tyr Pro
100 105 110
Asp Gly Thr Tyr Thr Gly Arg Ile Phe Leu Glu Val Leu Glu Ser Ser
115 120 125
Val Ala Glu His Gly Ala Arg Phe Gln Ile Pro Ile Glu Gly Arg Asp
130 135 140
Tyr Lys Asp Asp Asp Asp Lys His His His His His His
145 150 155
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| PD-L1 специфические антитела | 2017 |
|
RU2756236C2 |
| АНТАГОНИСТЫ | 2019 |
|
RU2839429C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕСЯ С 4-1ВВ | 2011 |
|
RU2551963C2 |
| КОНСТРУКЦИИ СЛИТОГО БЕЛКА ДЛЯ ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С КОМПЛЕМЕНТОМ | 2019 |
|
RU2824402C2 |
| Т-КЛЕТКИ С КОСТИМУЛИРУЮЩИМ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ, НАЦЕЛЕННЫЕ НА IL13Rα2 | 2015 |
|
RU2749922C2 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ММР9 | 2015 |
|
RU2714043C2 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1, ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗА AL | 2018 |
|
RU2774895C2 |
| АНТИТЕЛА К PD-1 И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2761640C2 |
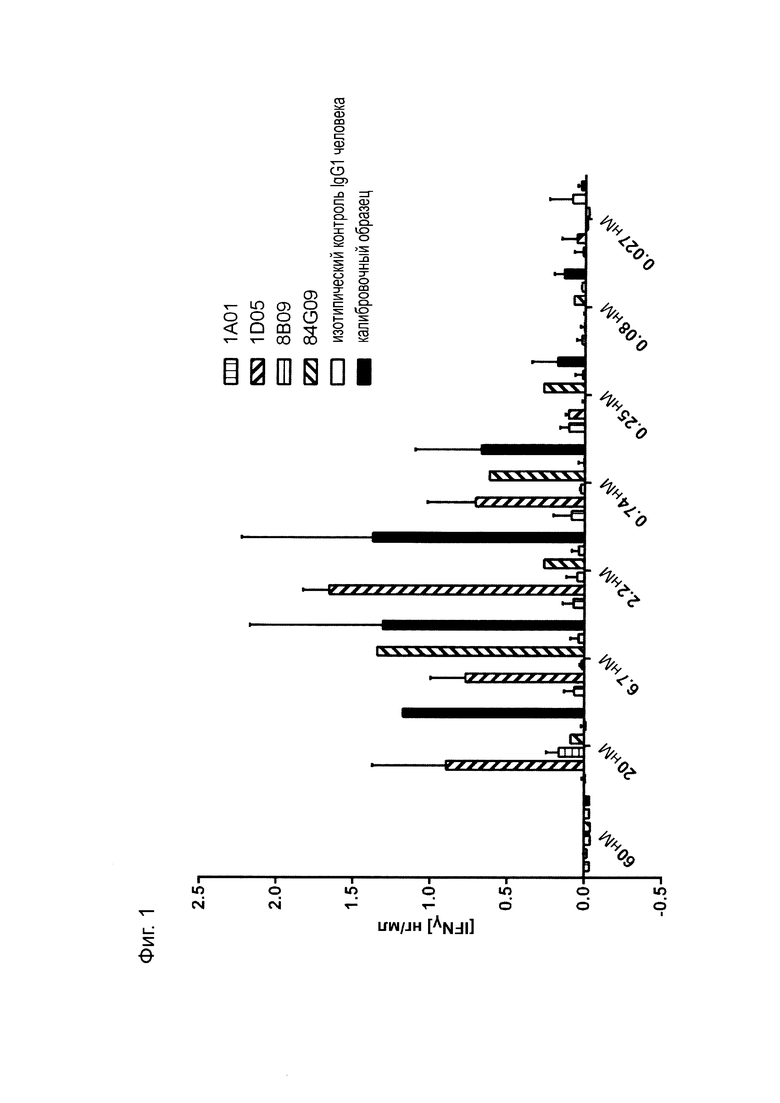
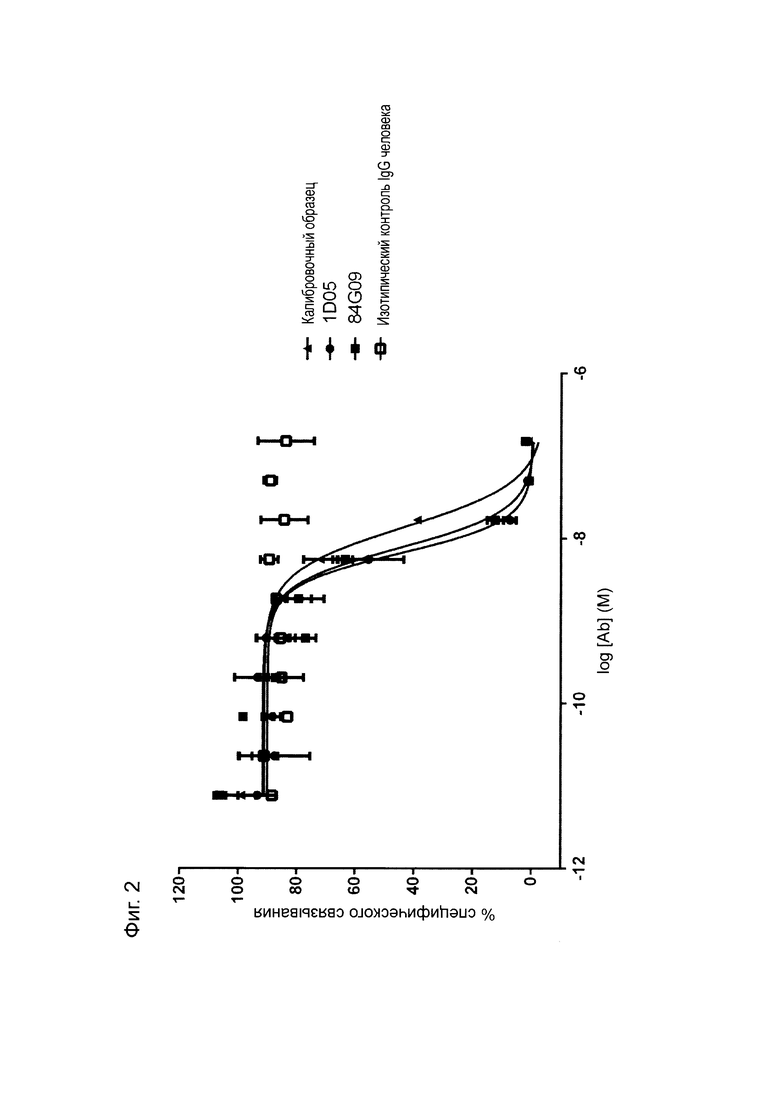
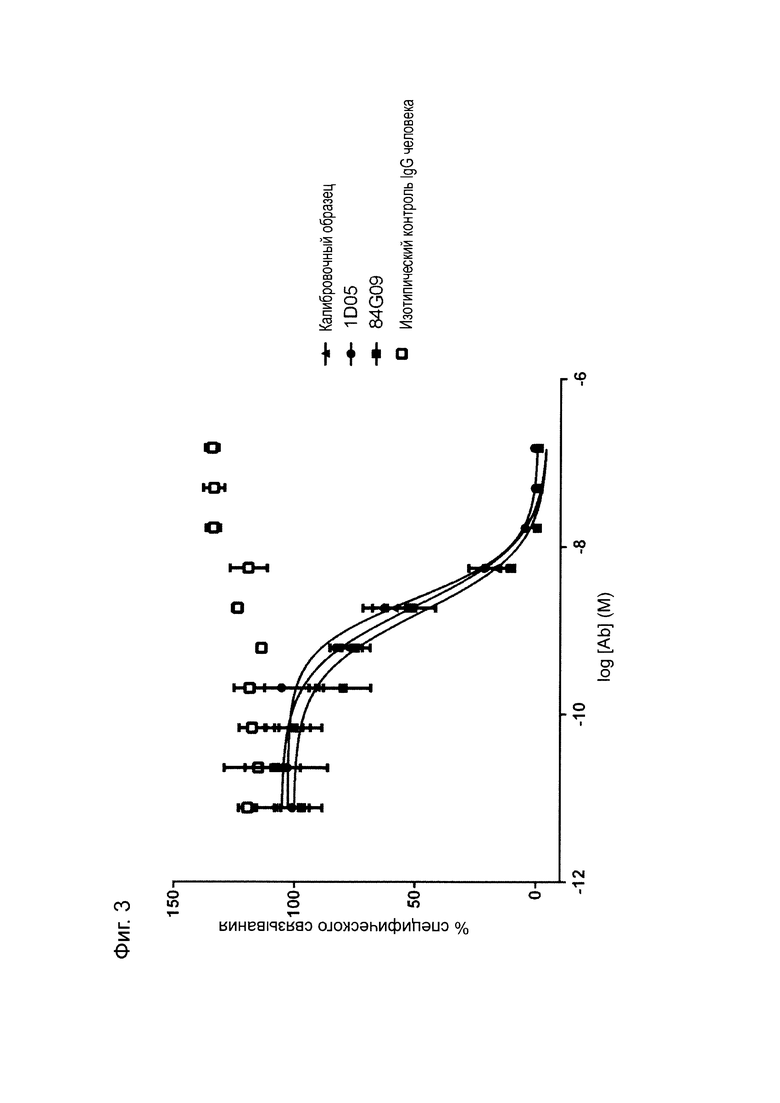
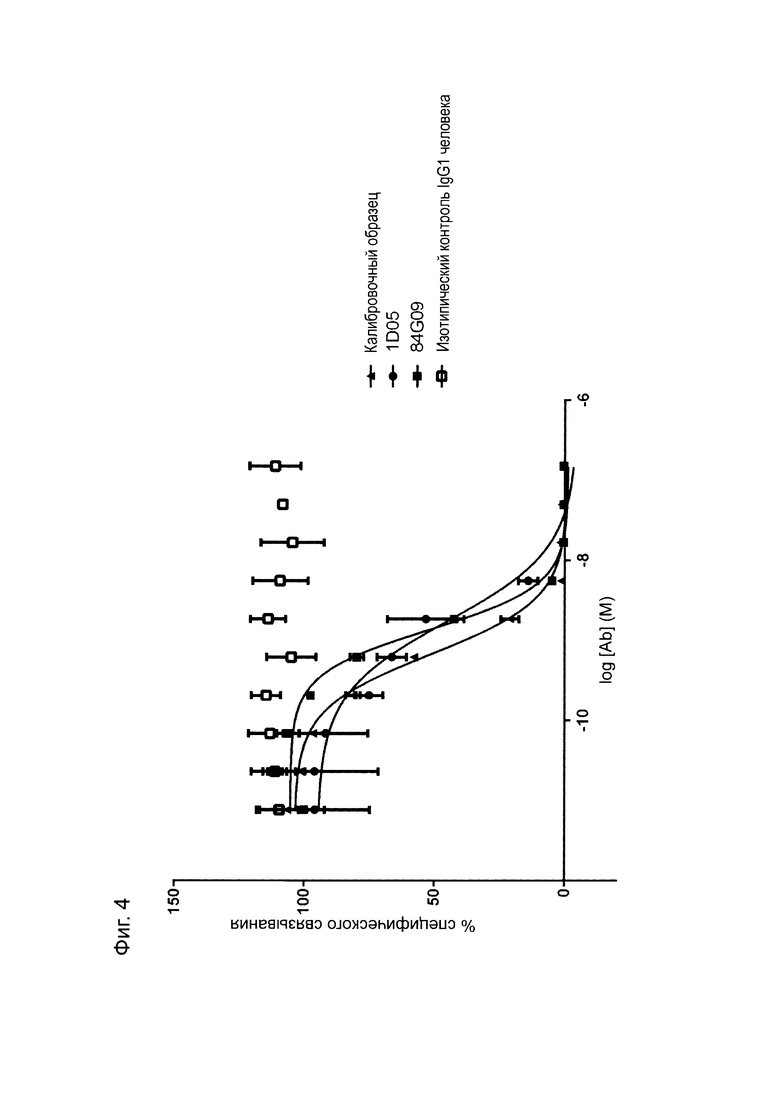
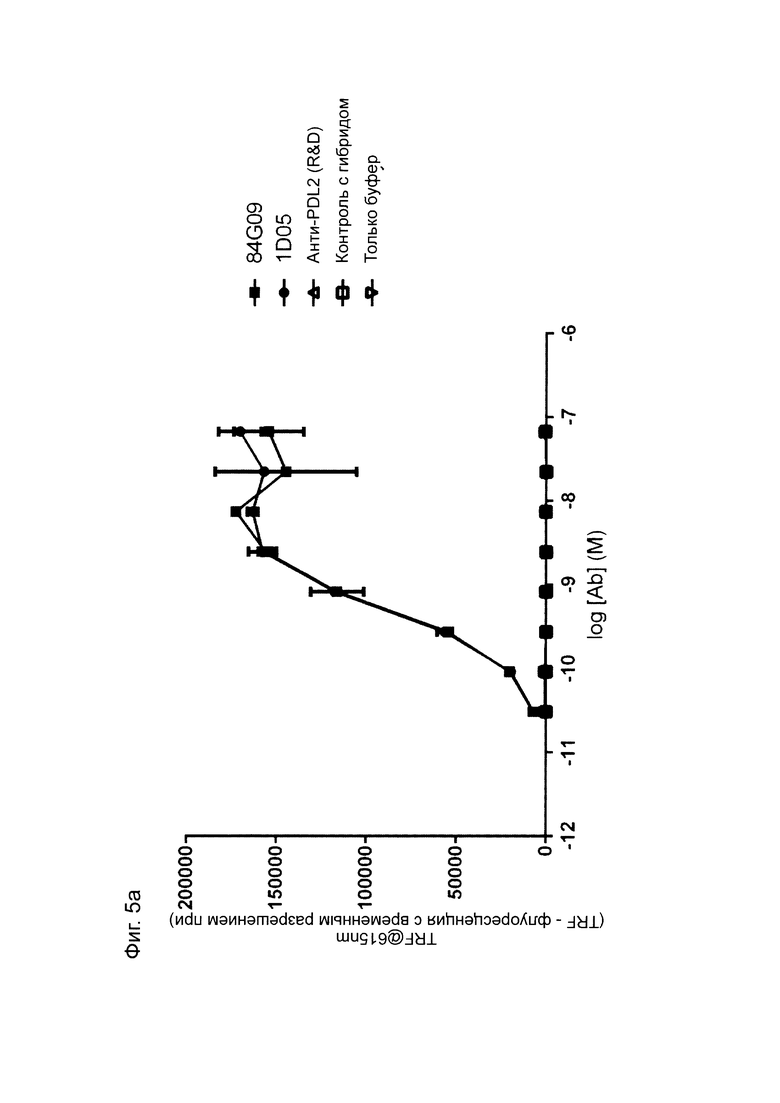
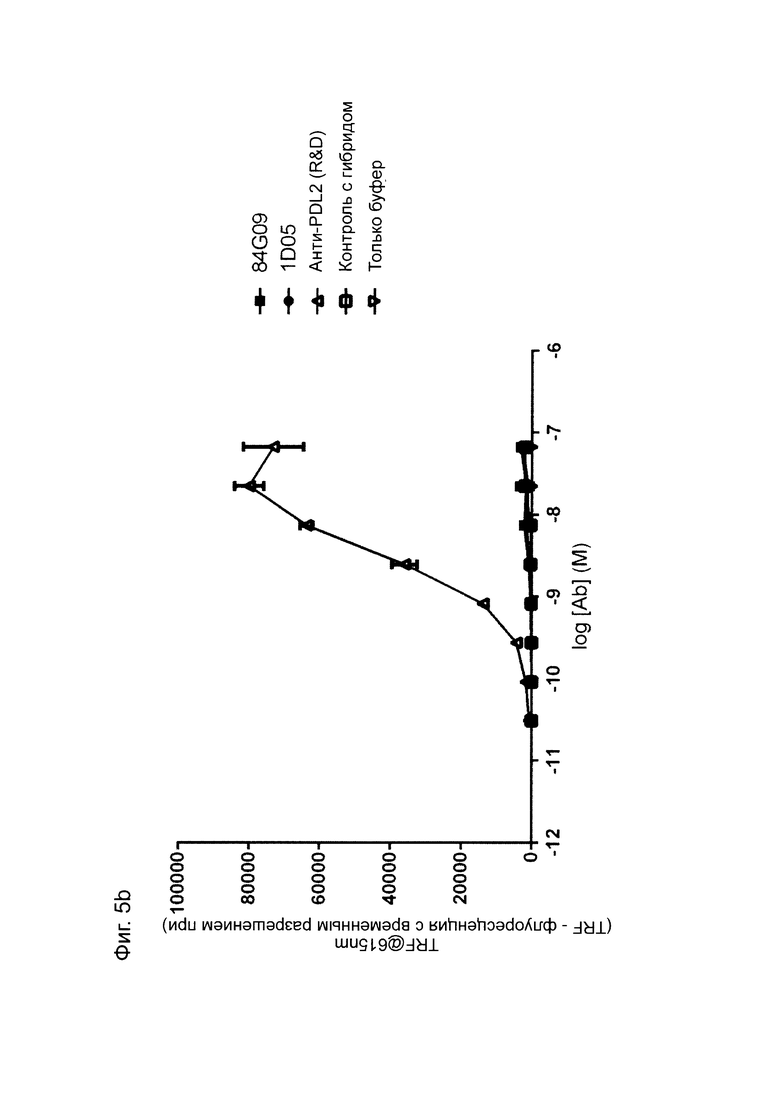
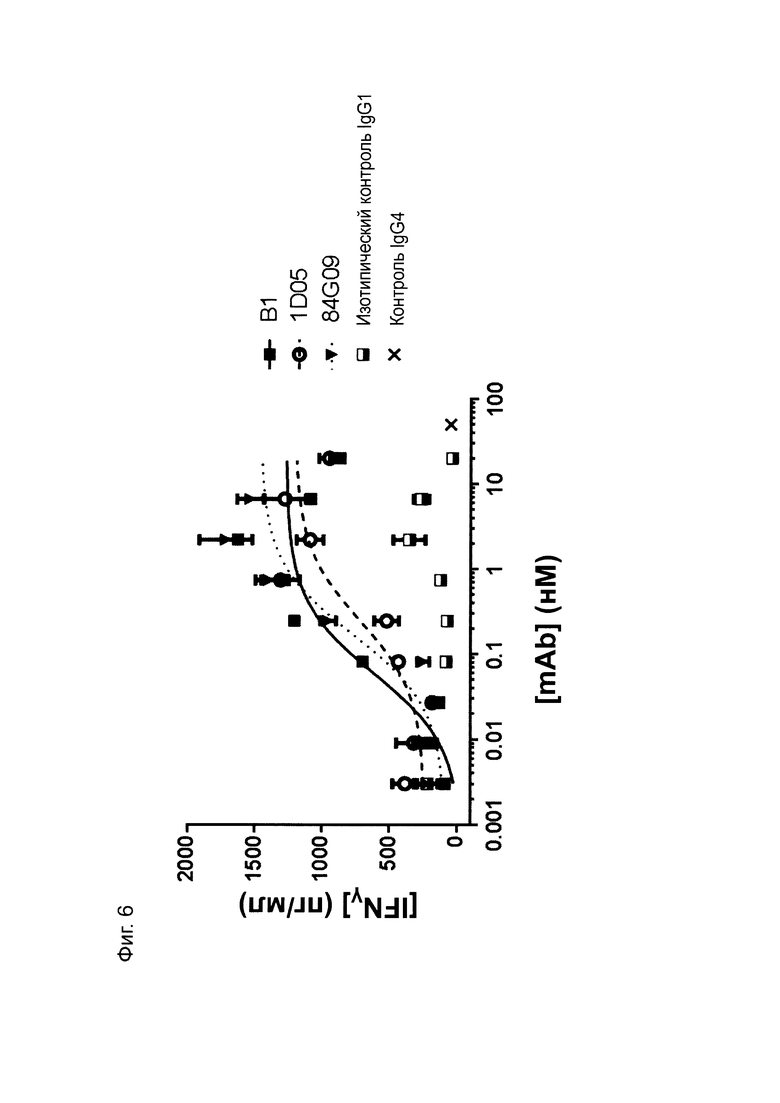
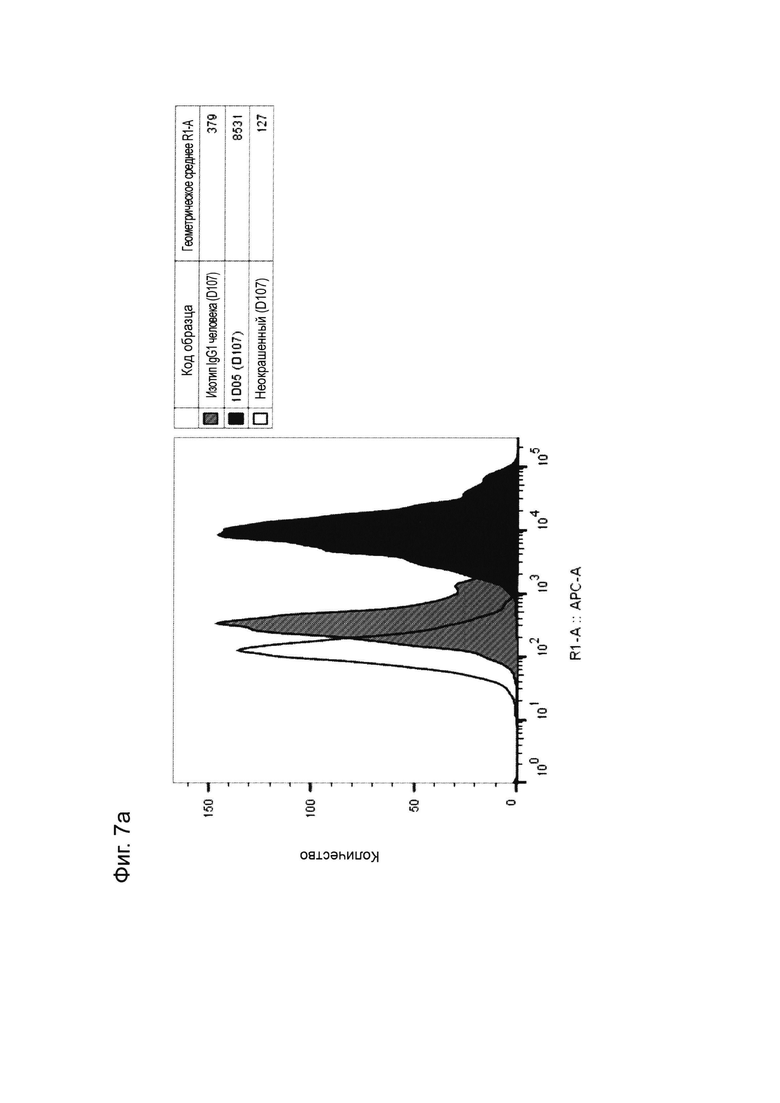
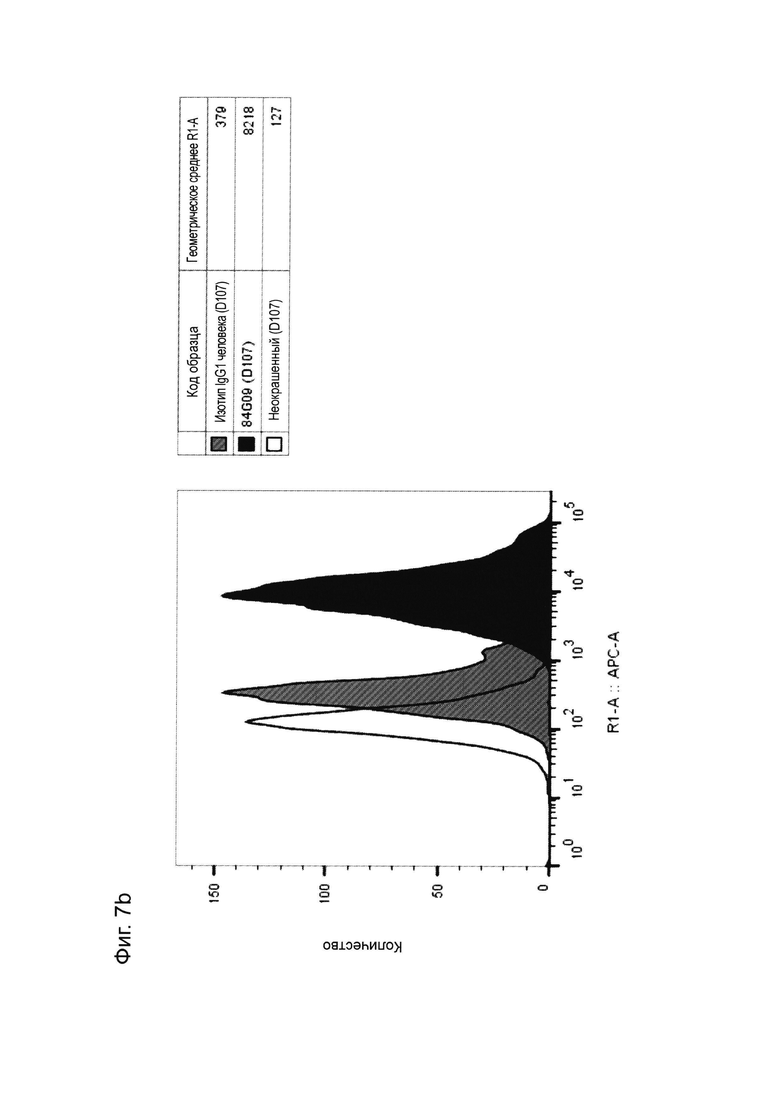
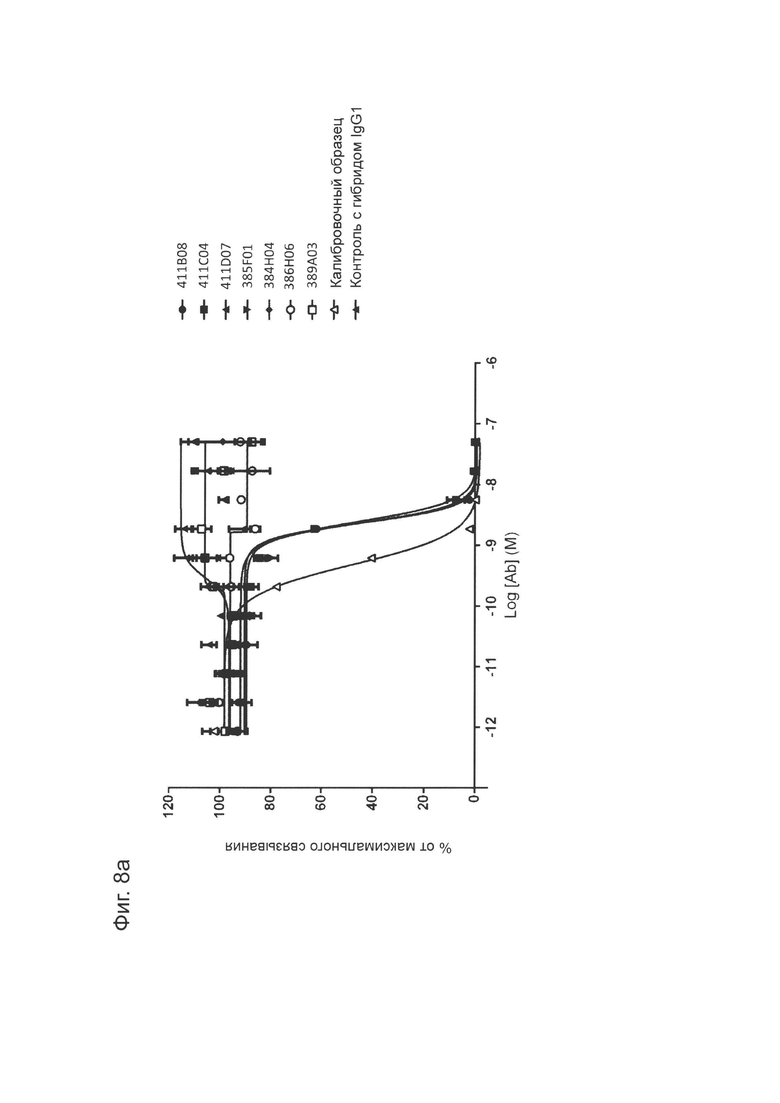
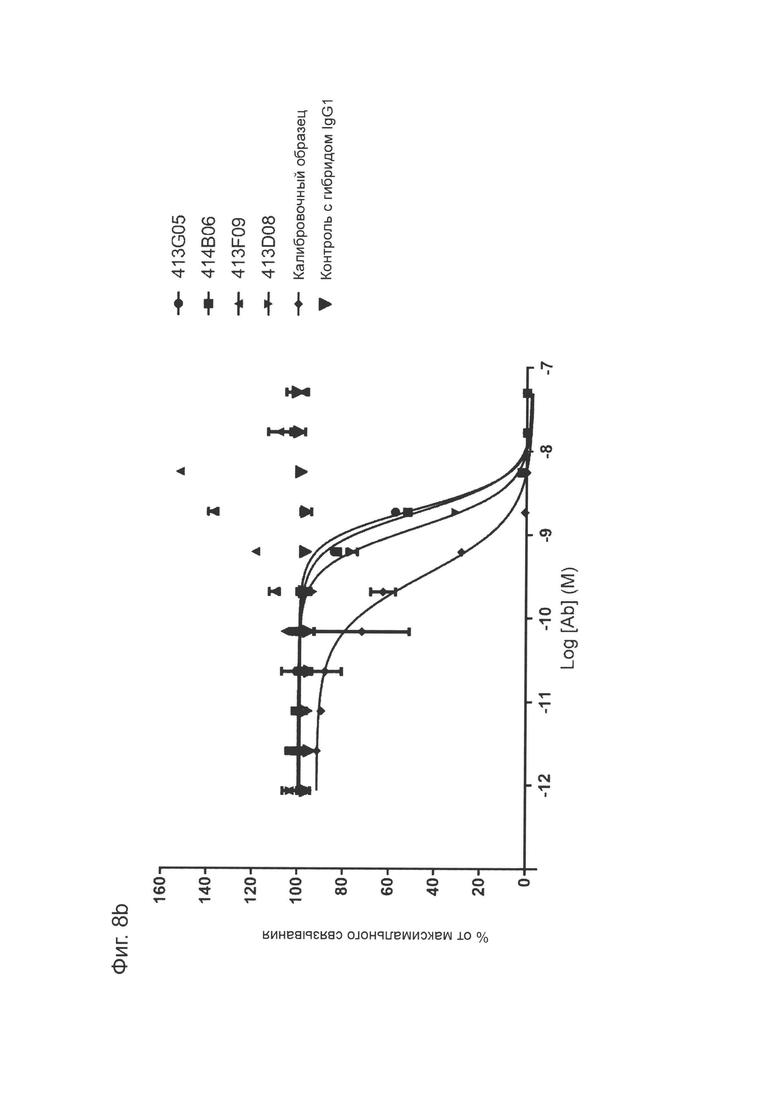
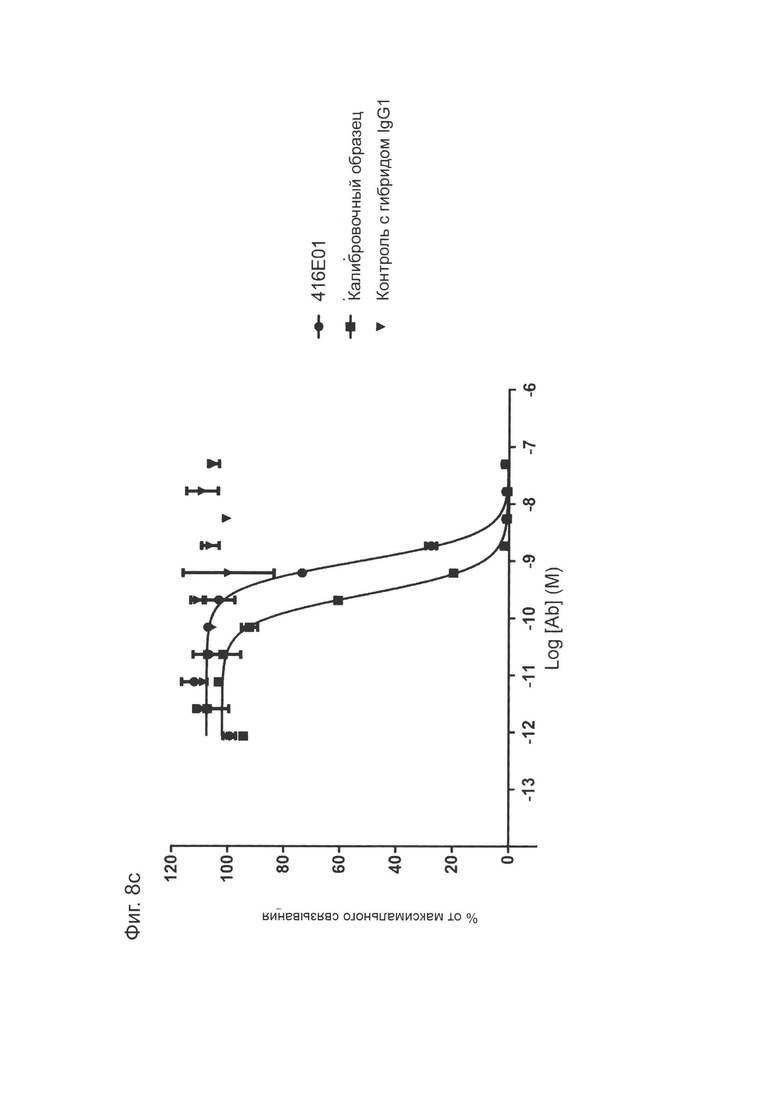
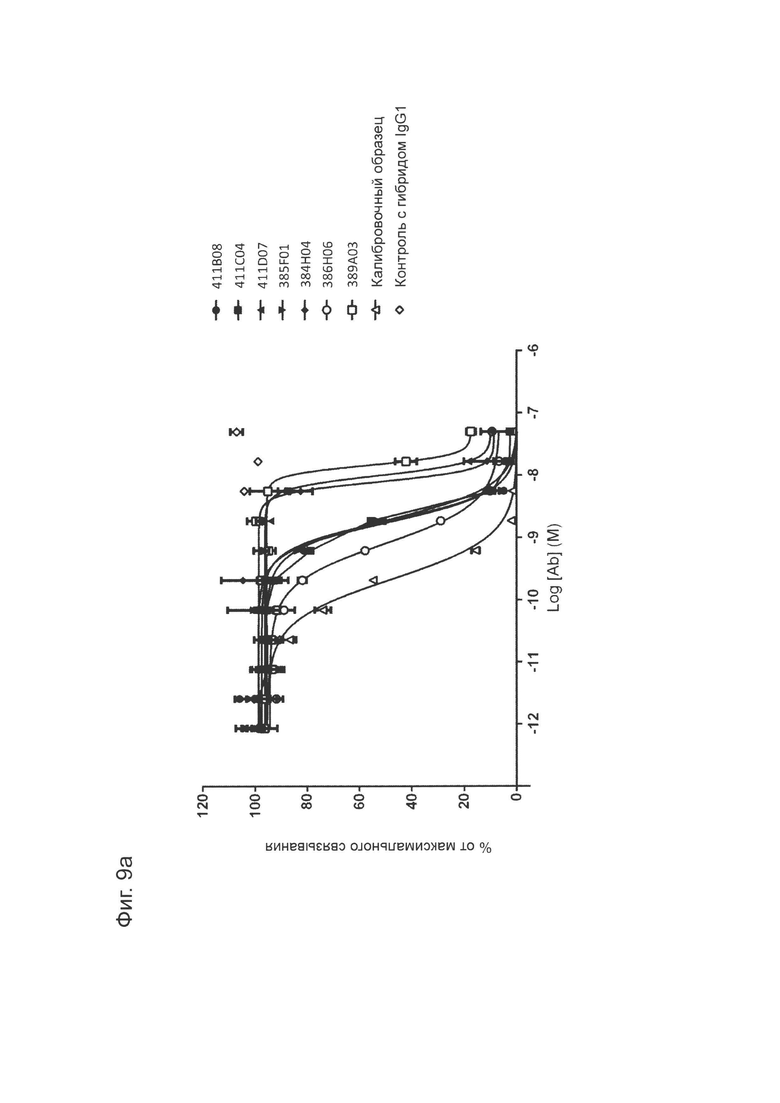
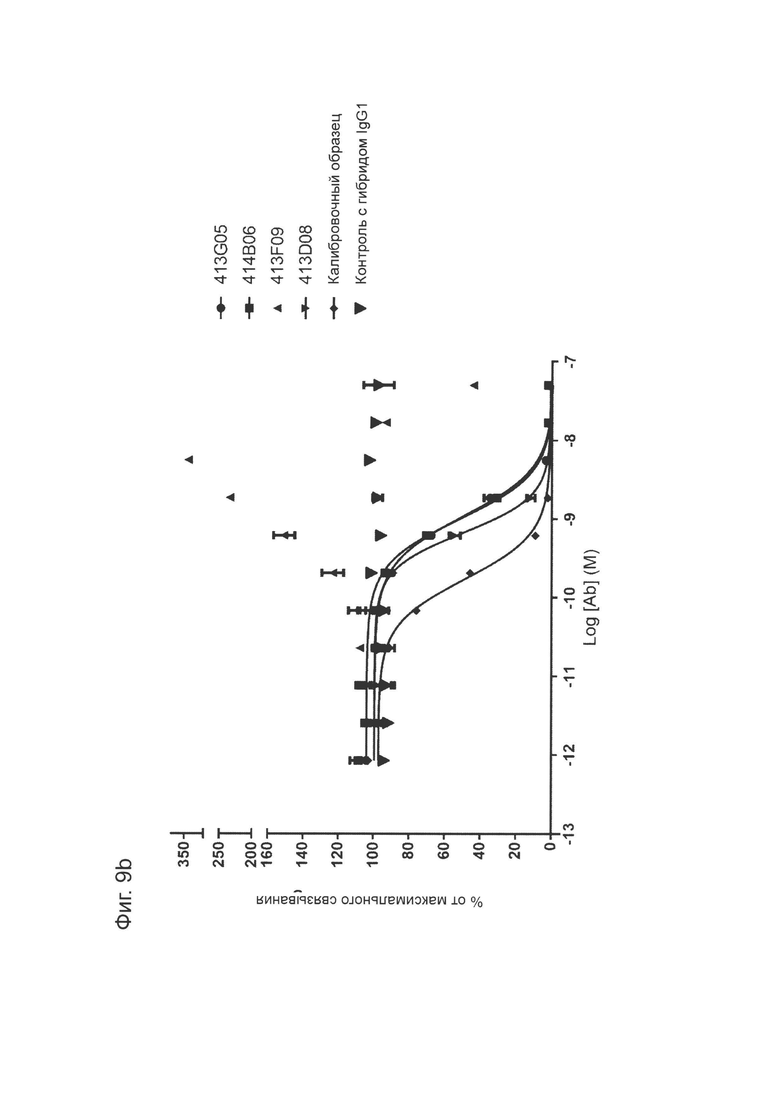
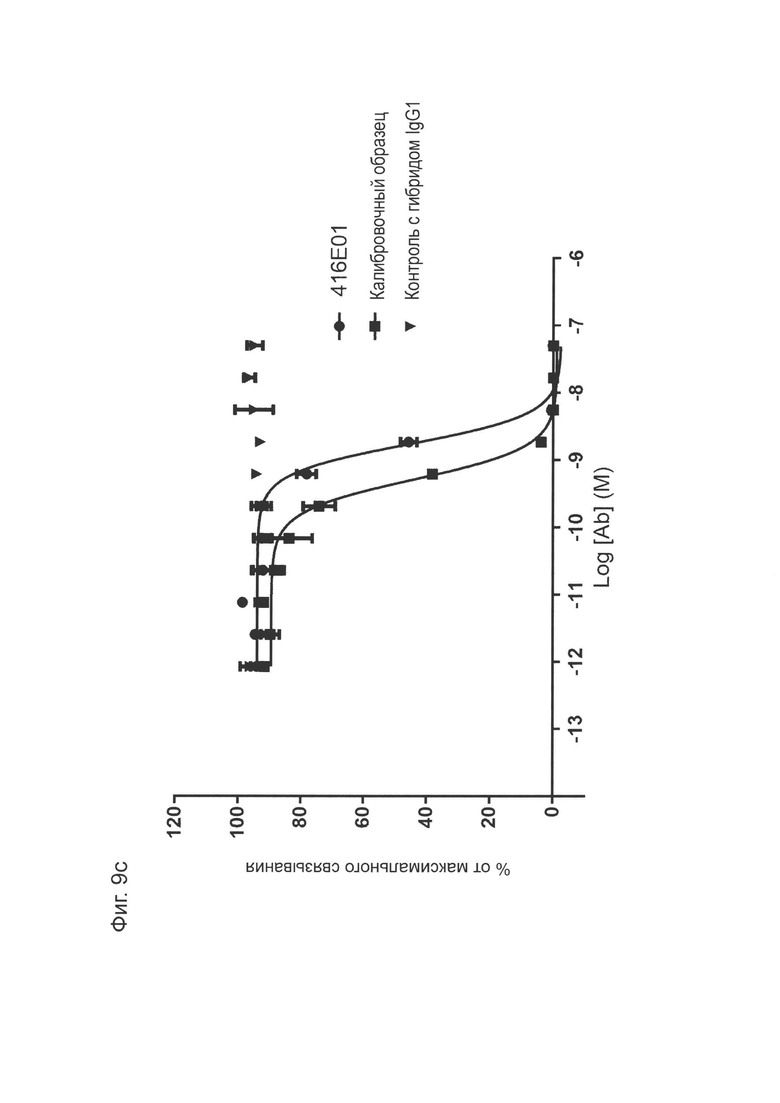
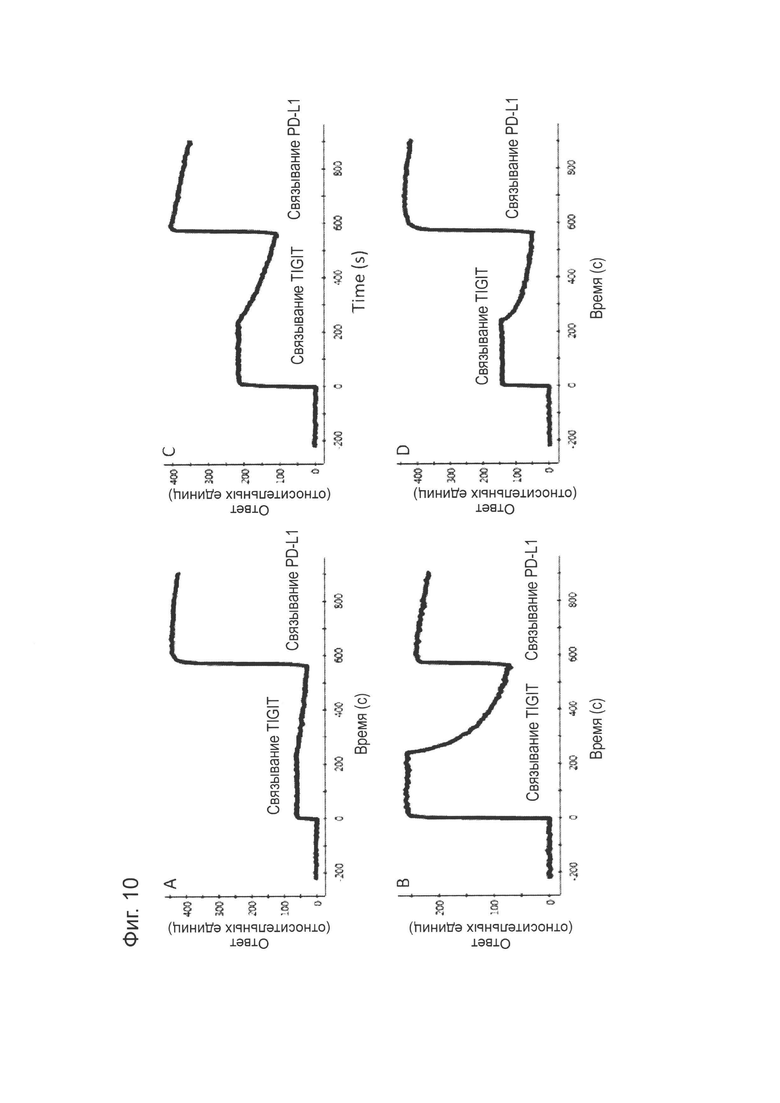
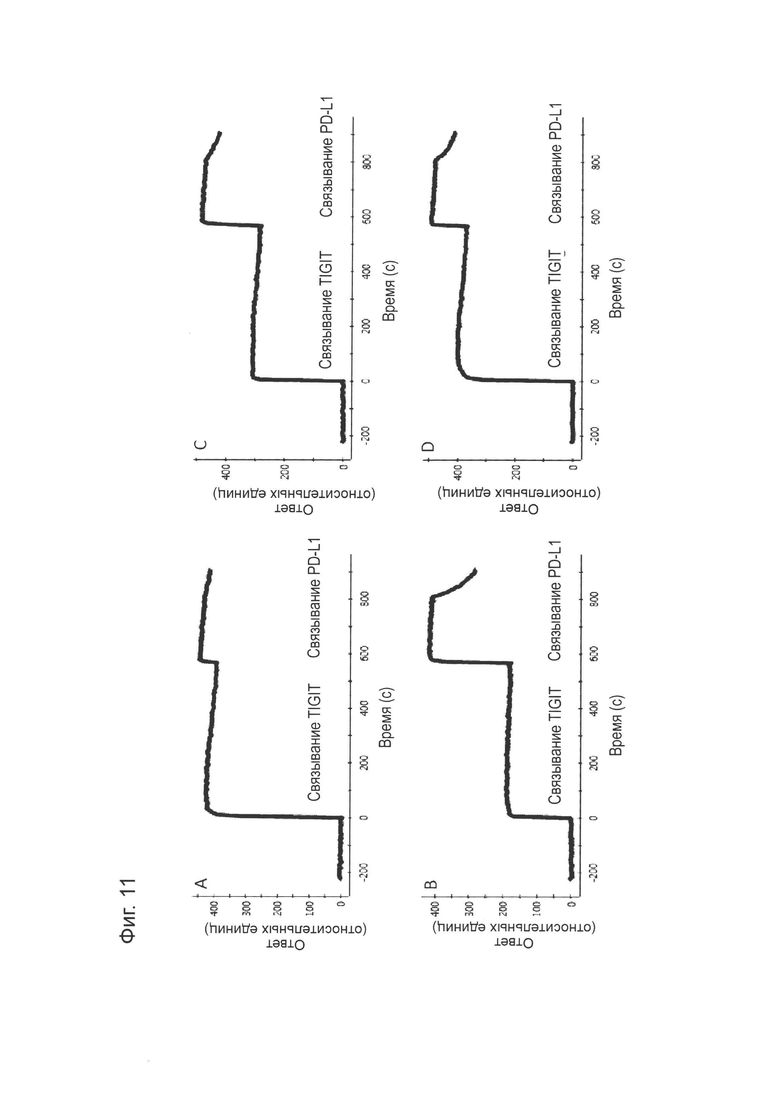
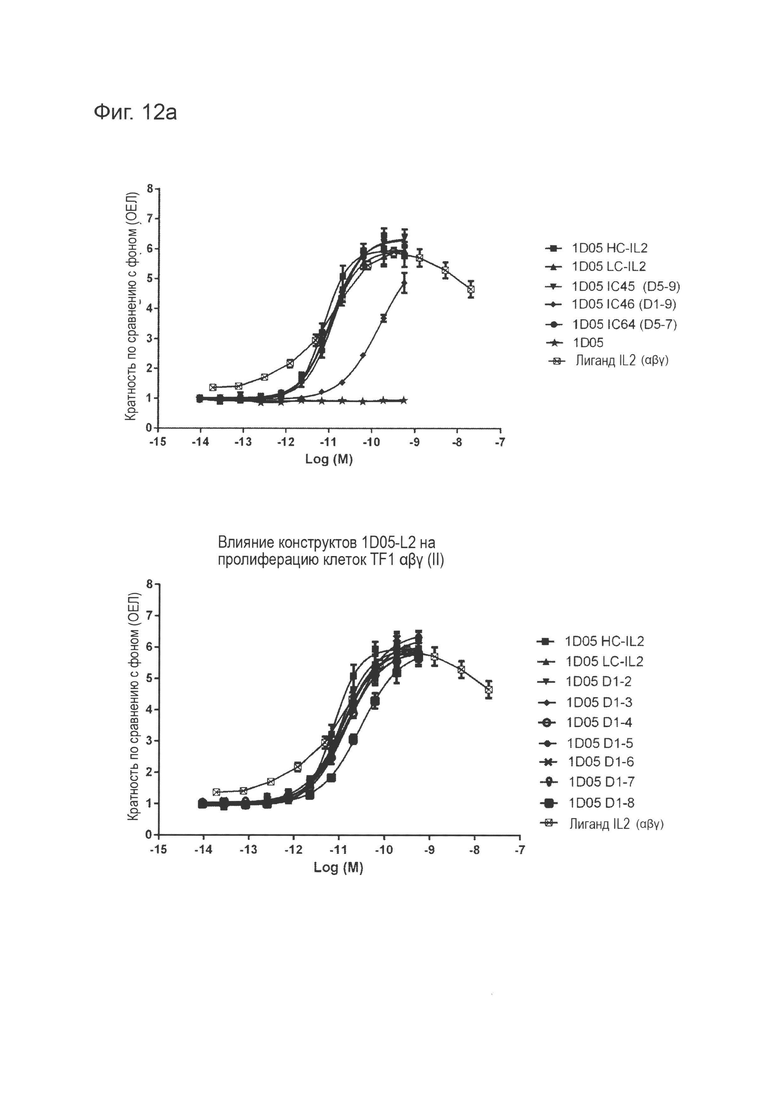
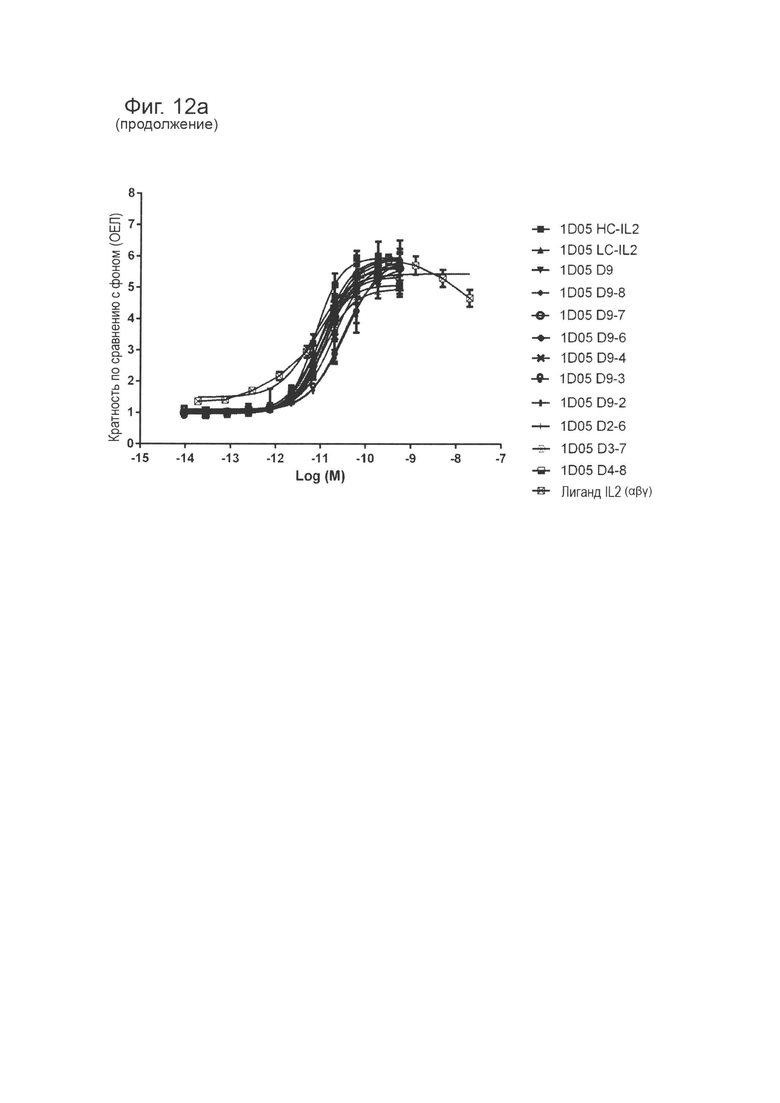
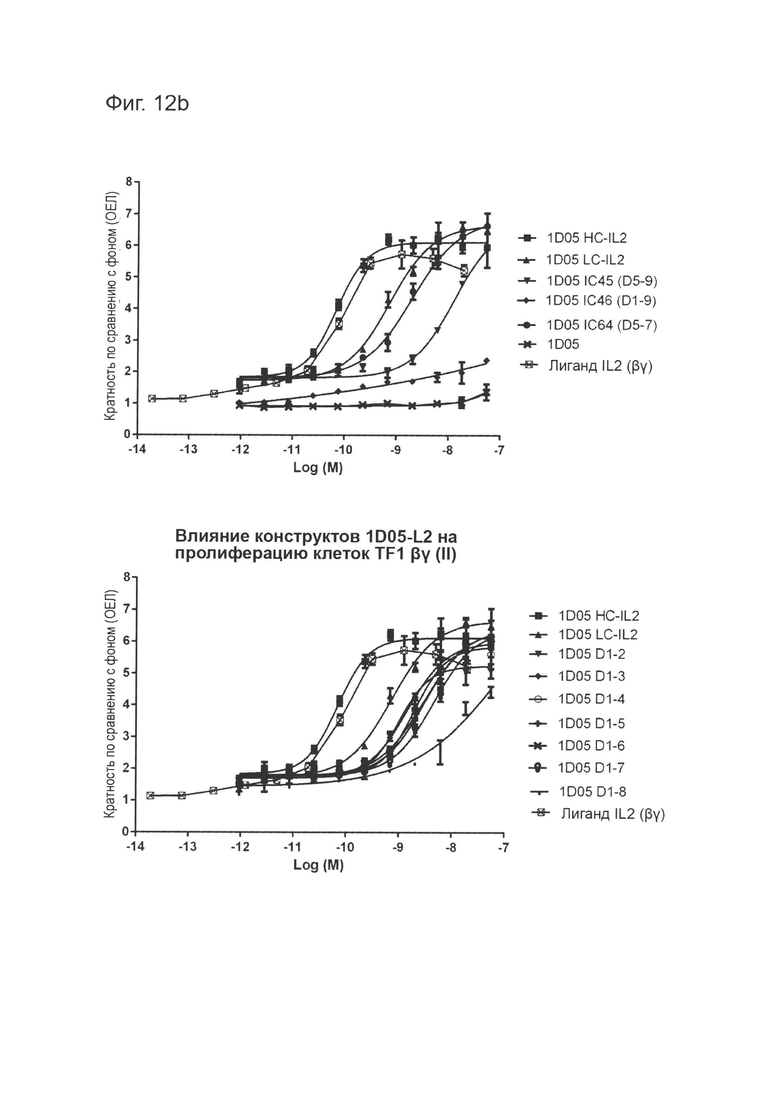
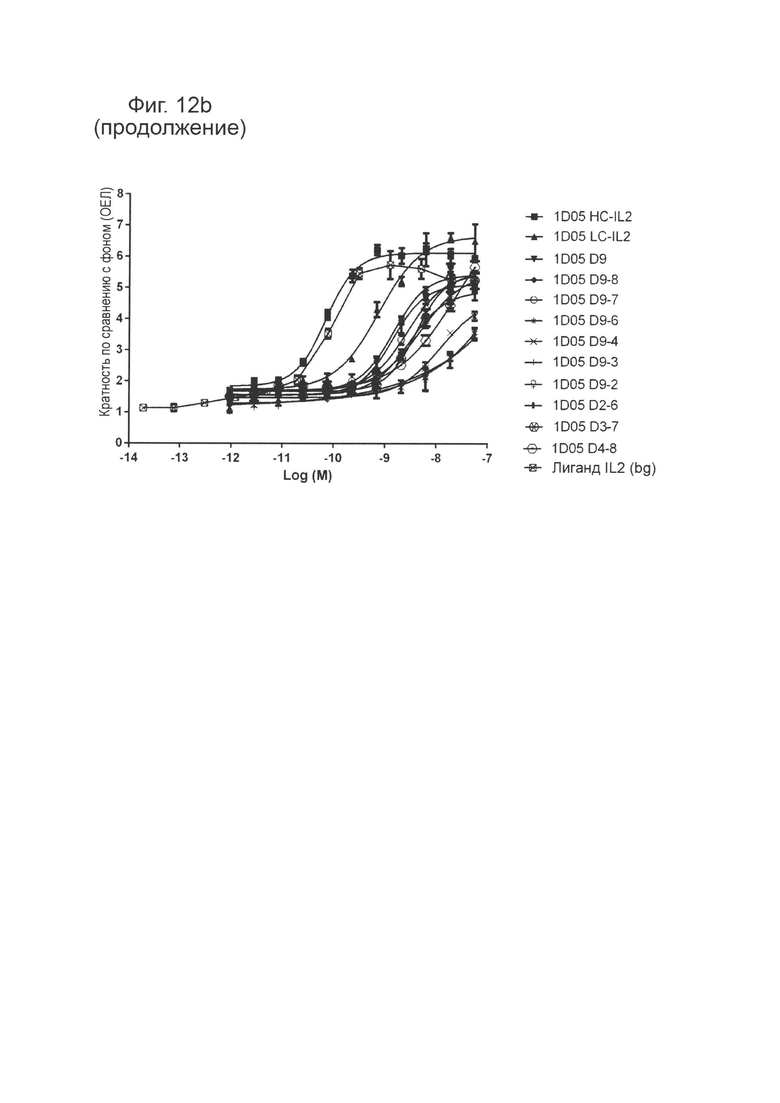
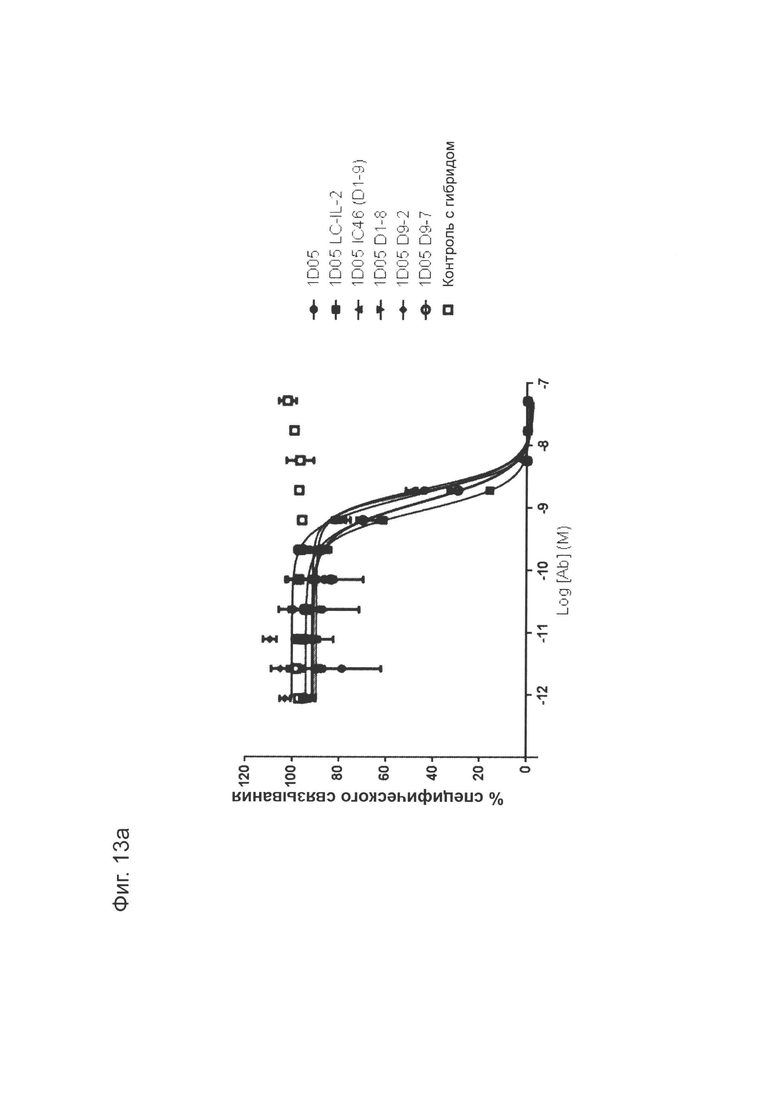
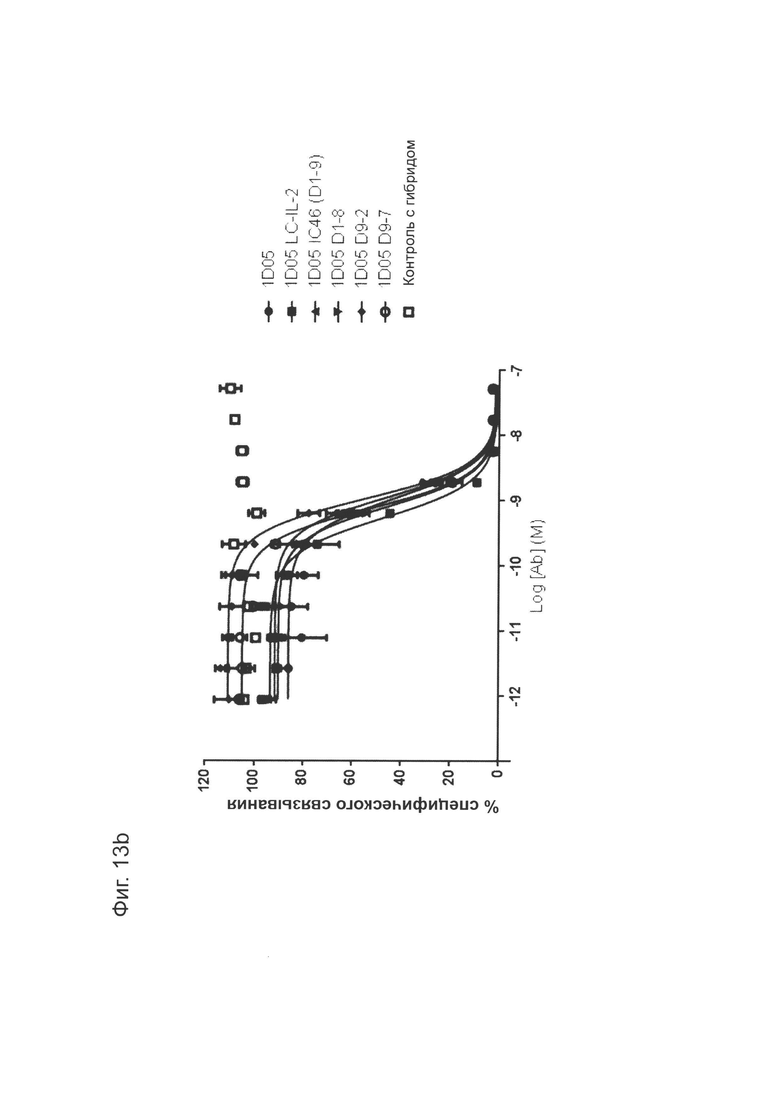
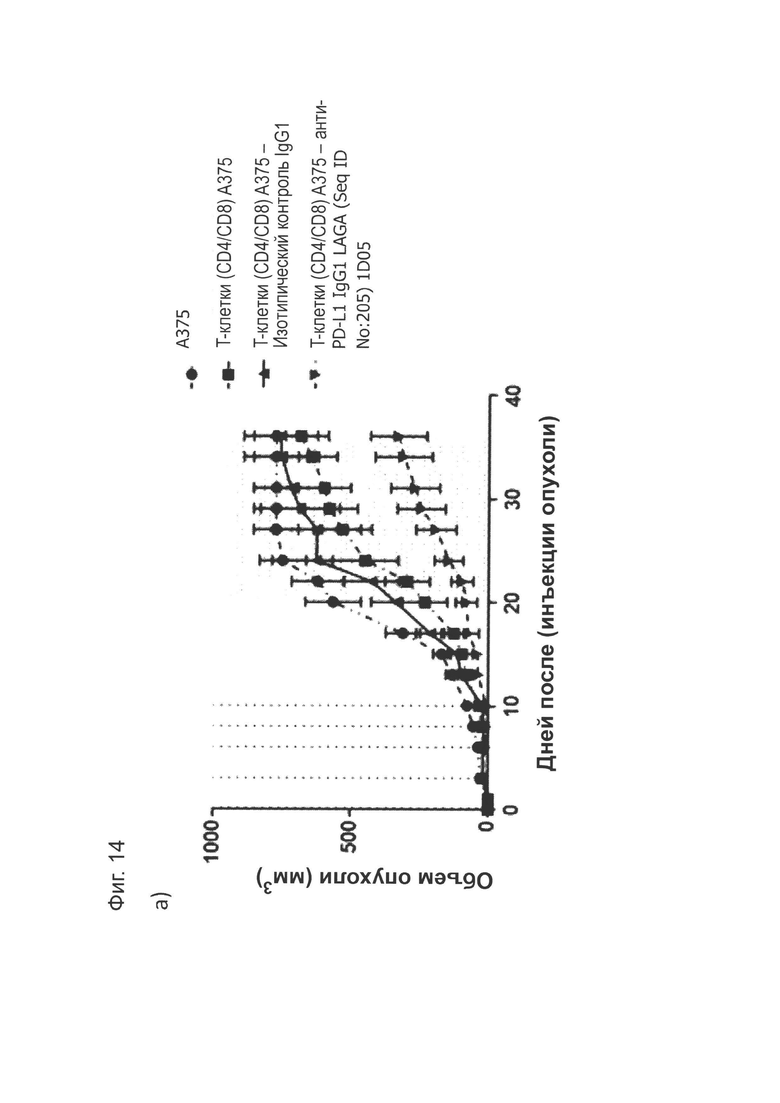
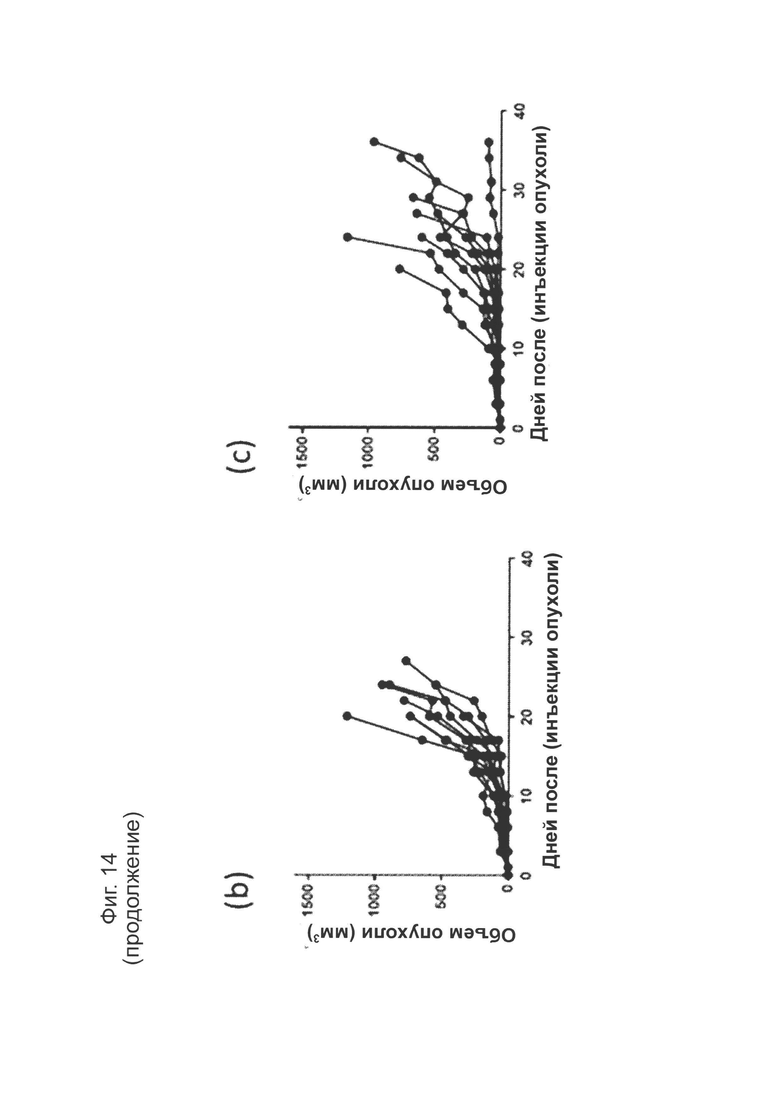
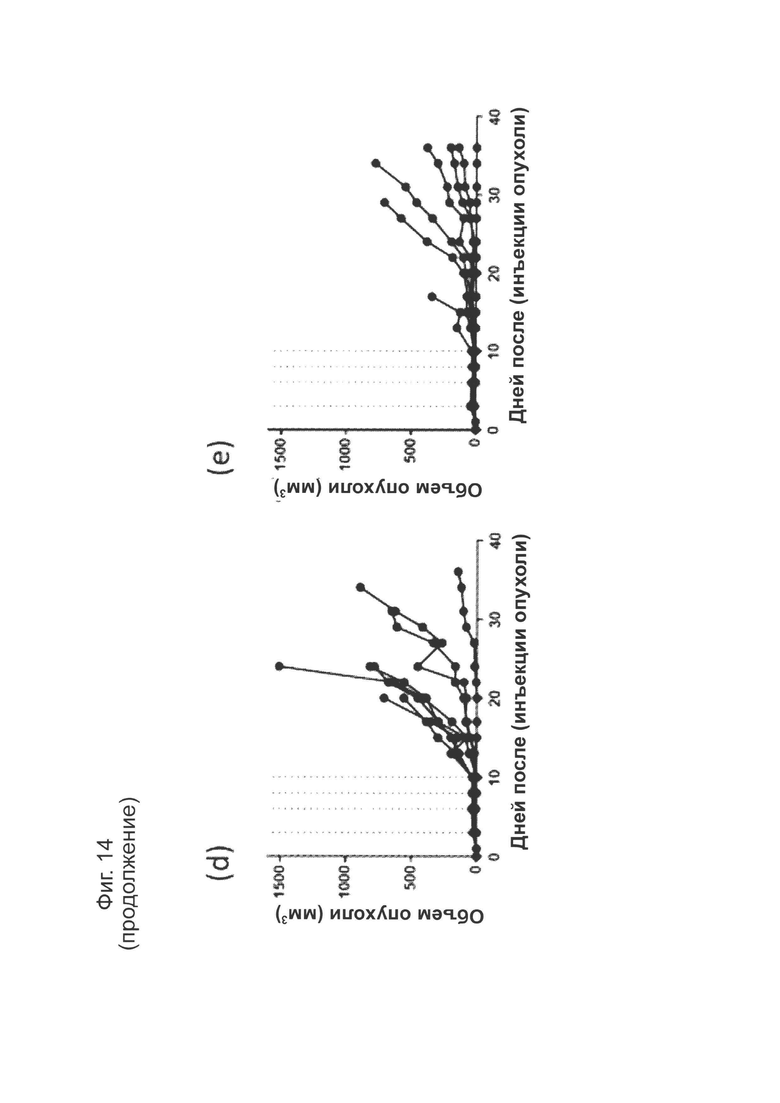
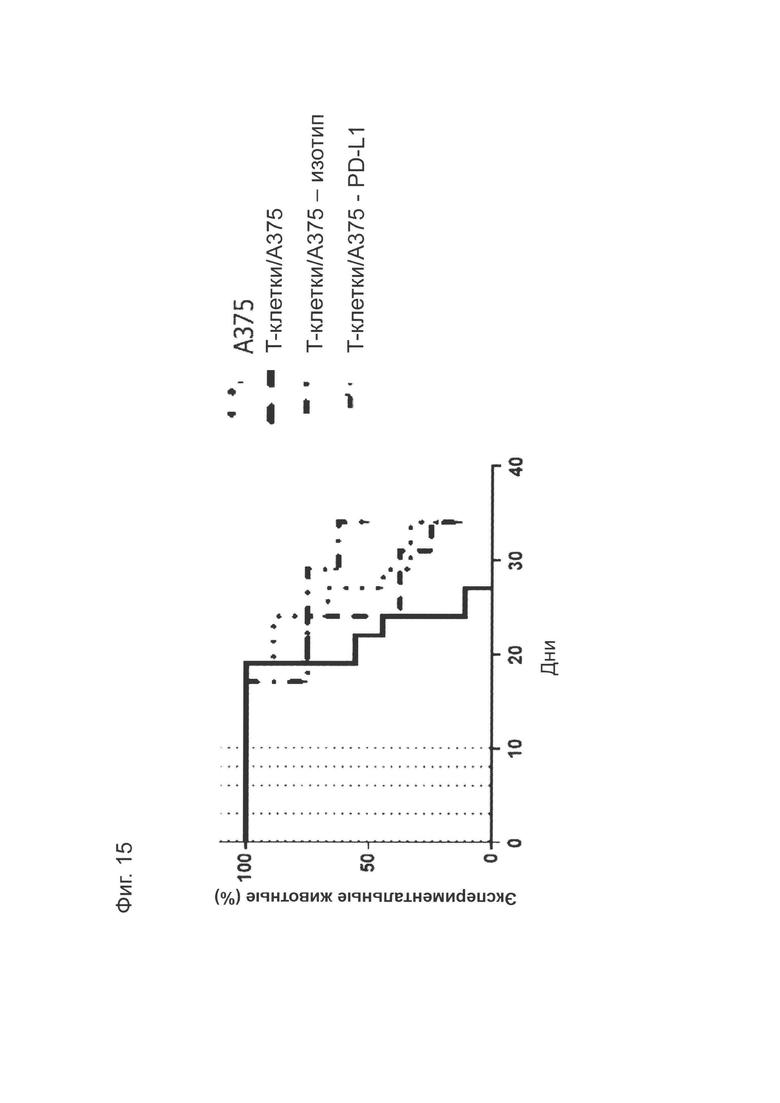
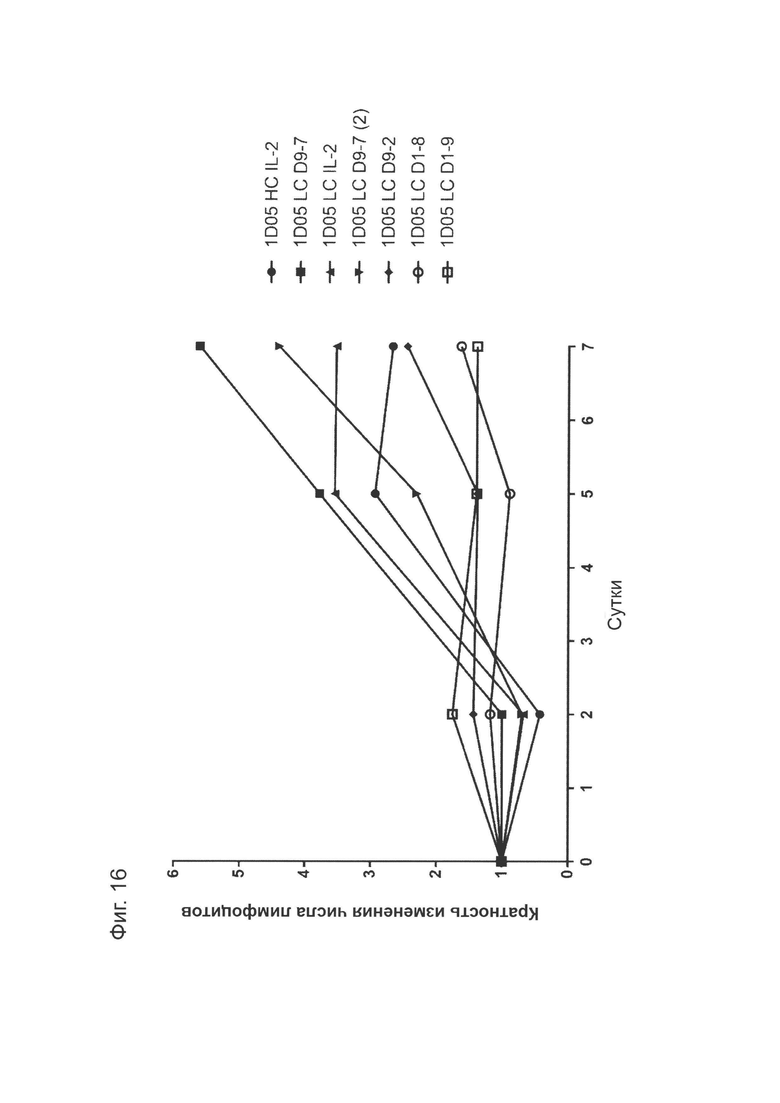
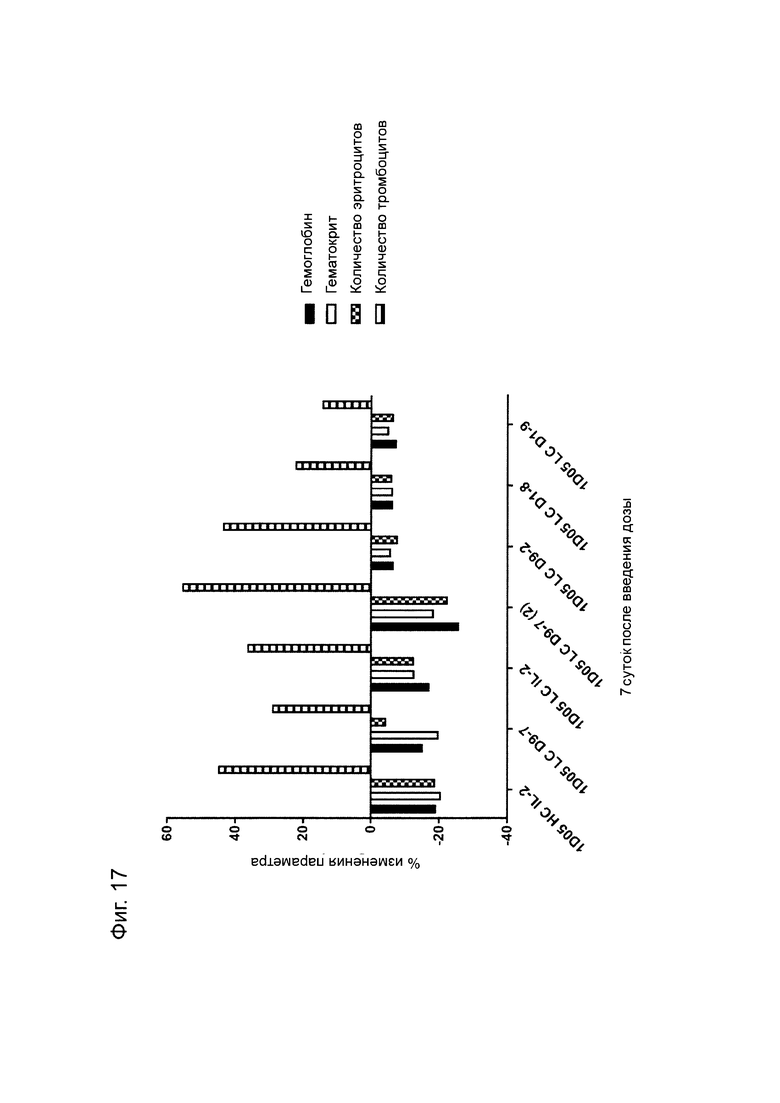
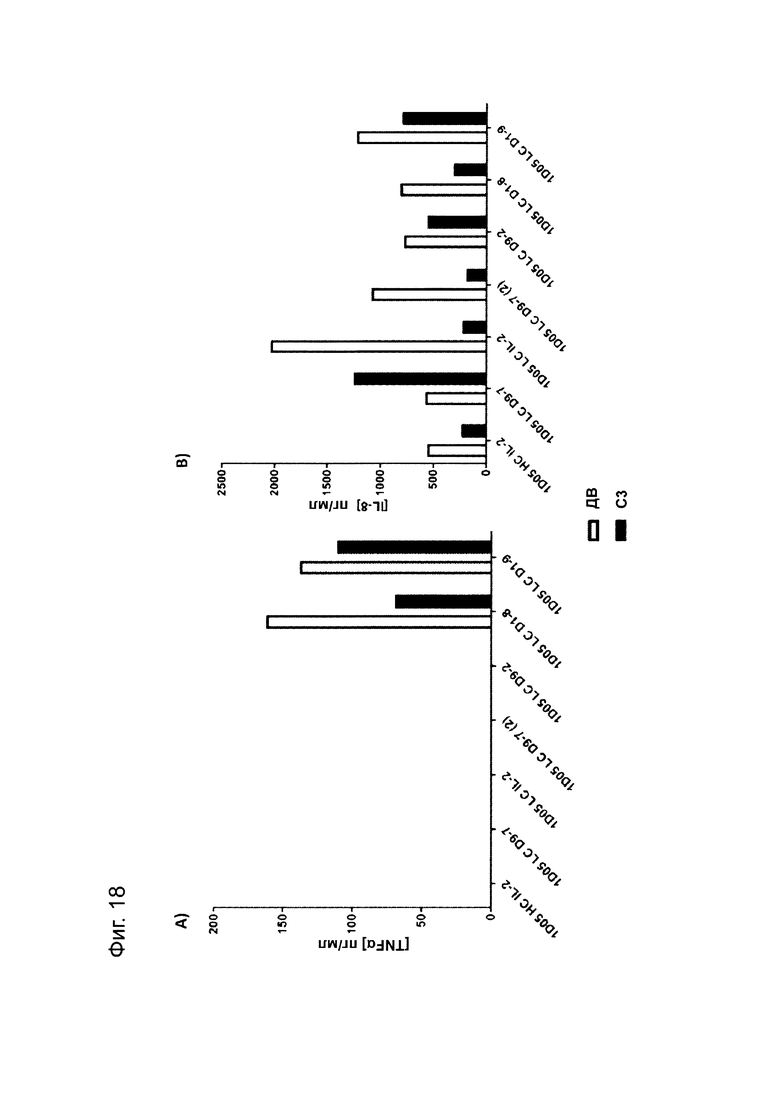
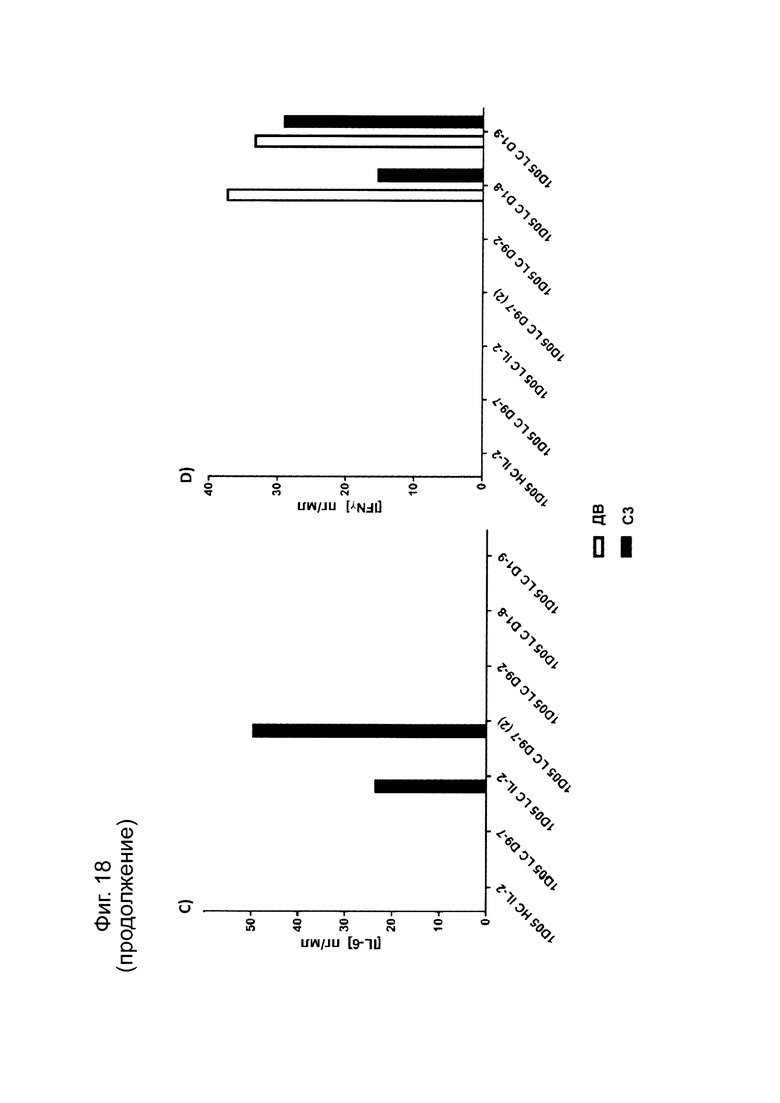
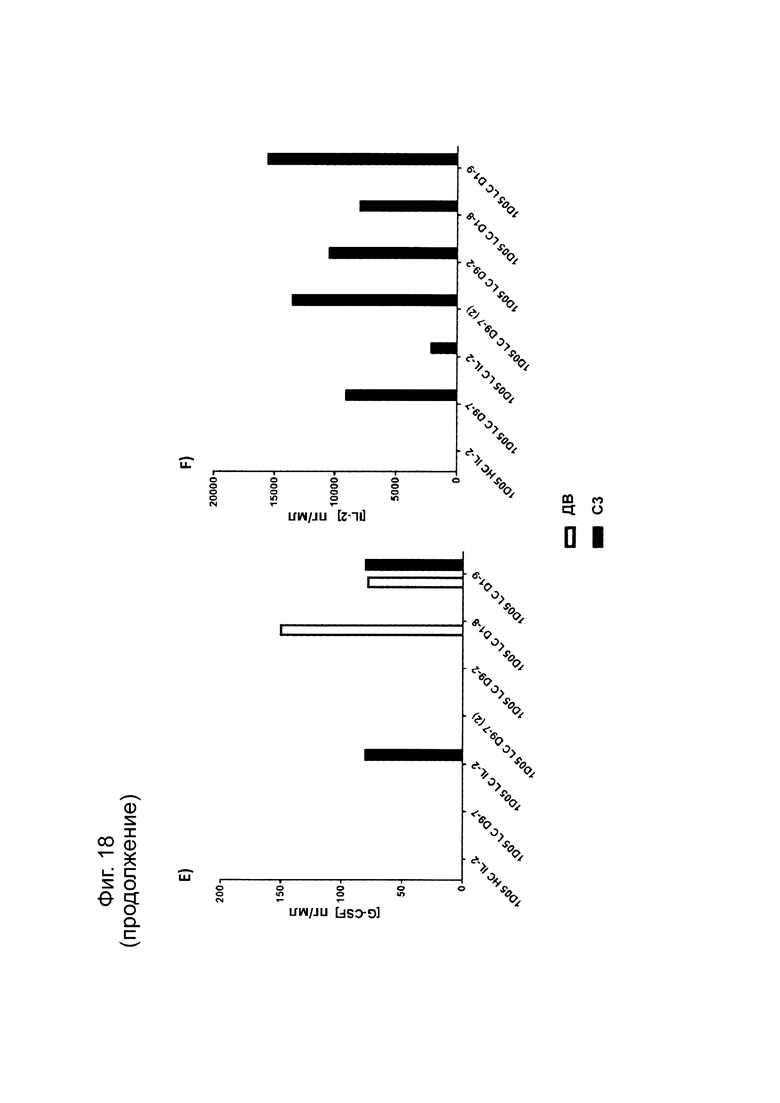
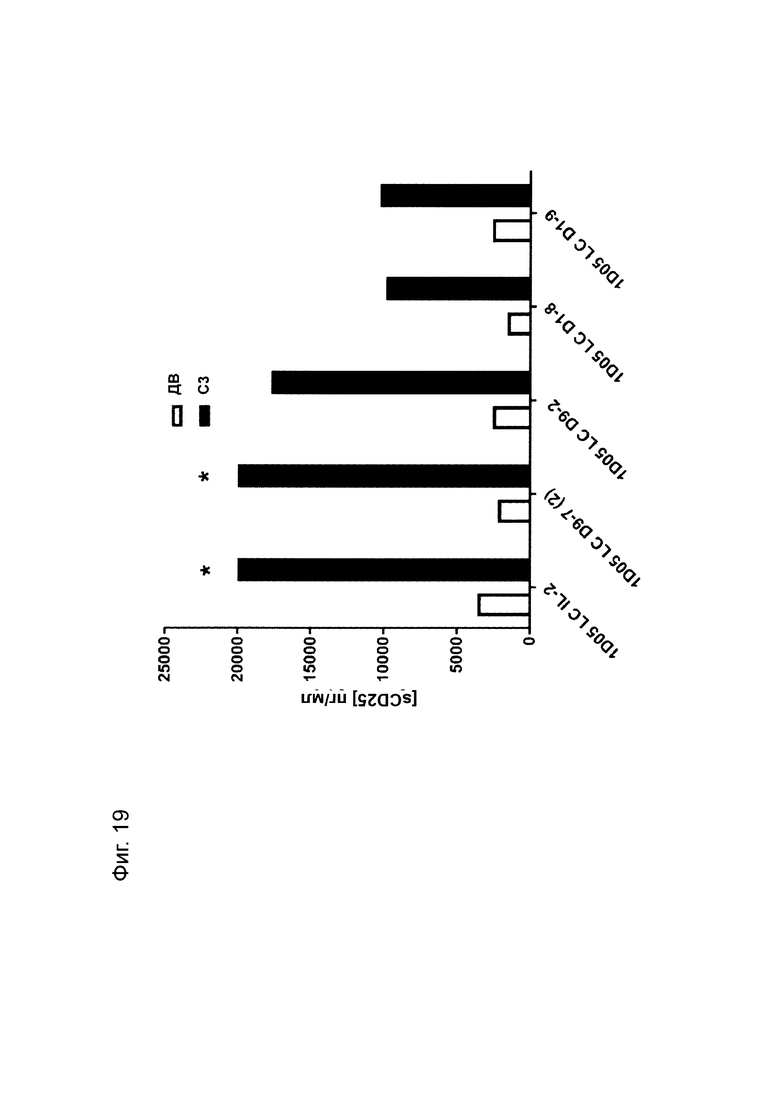

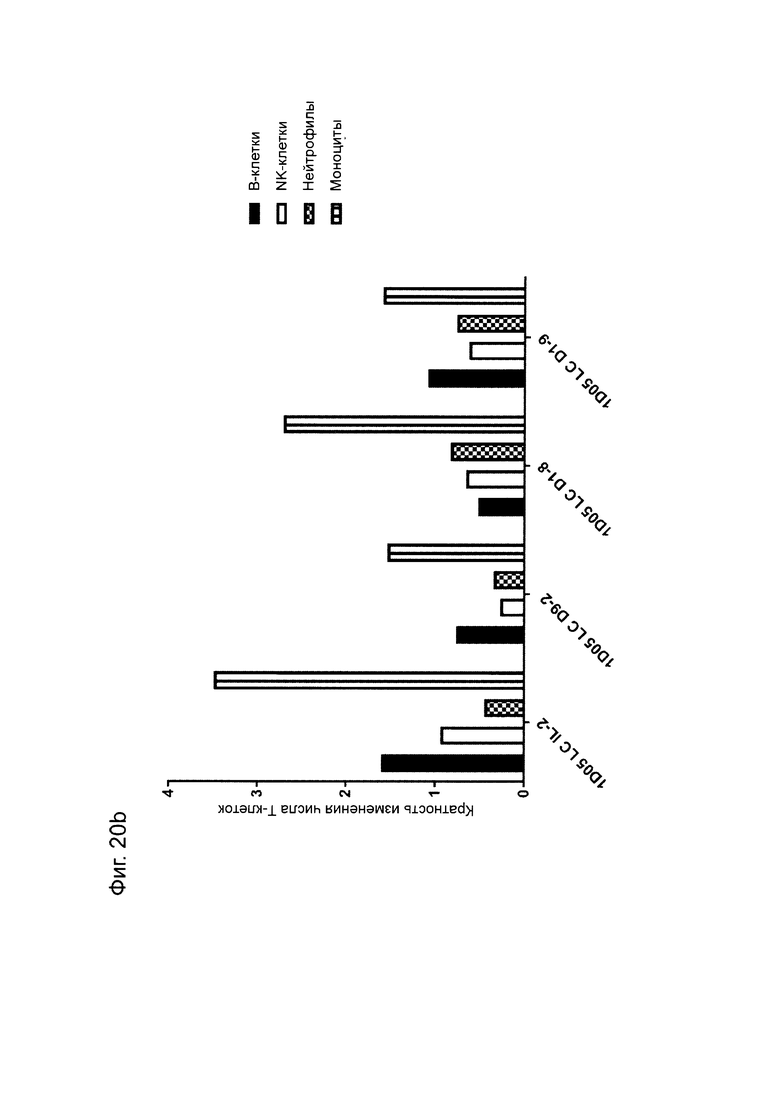
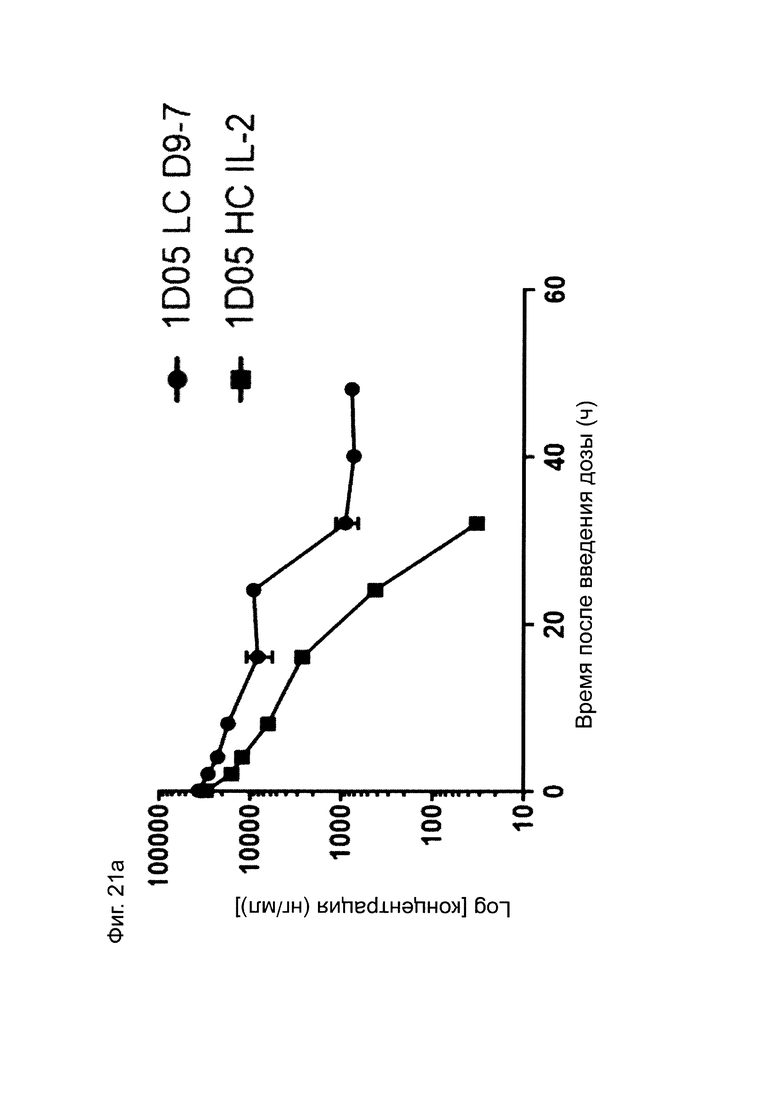
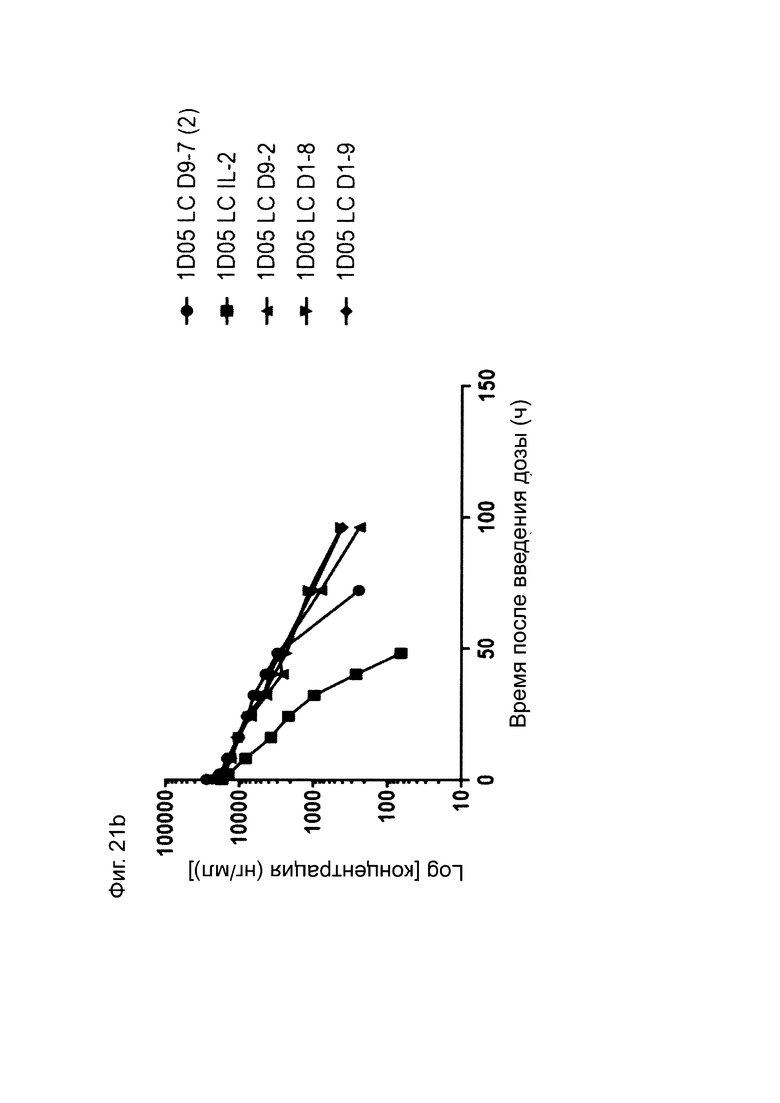
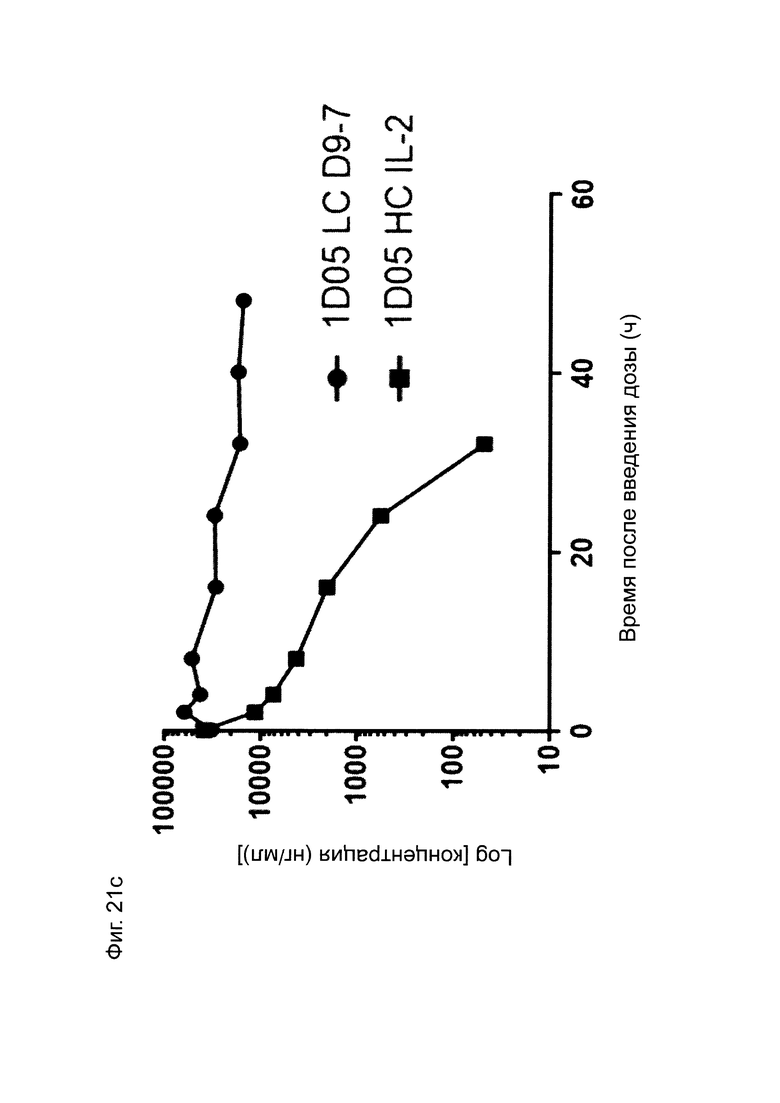
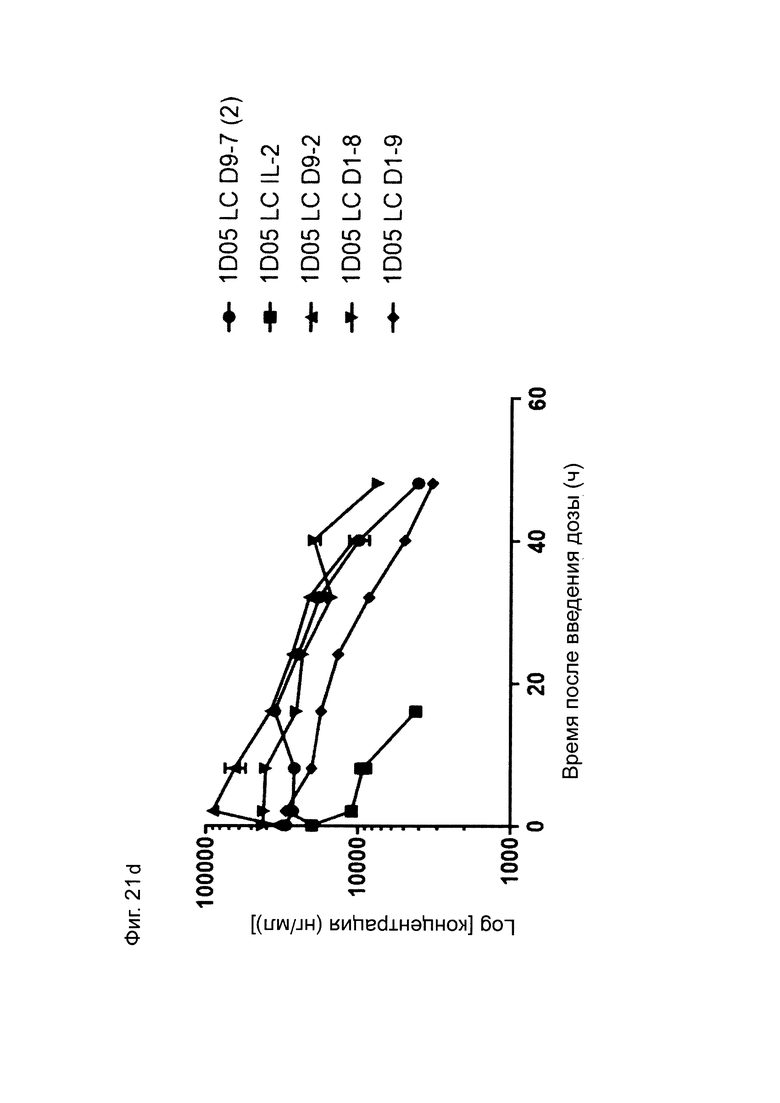
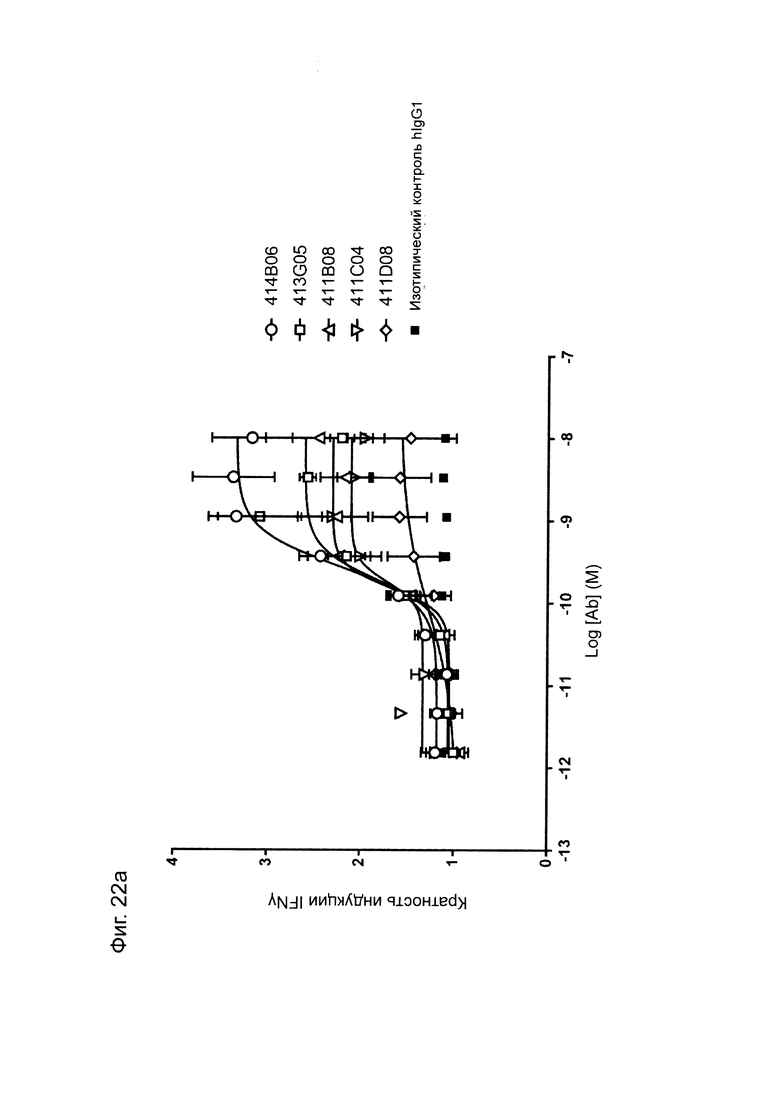
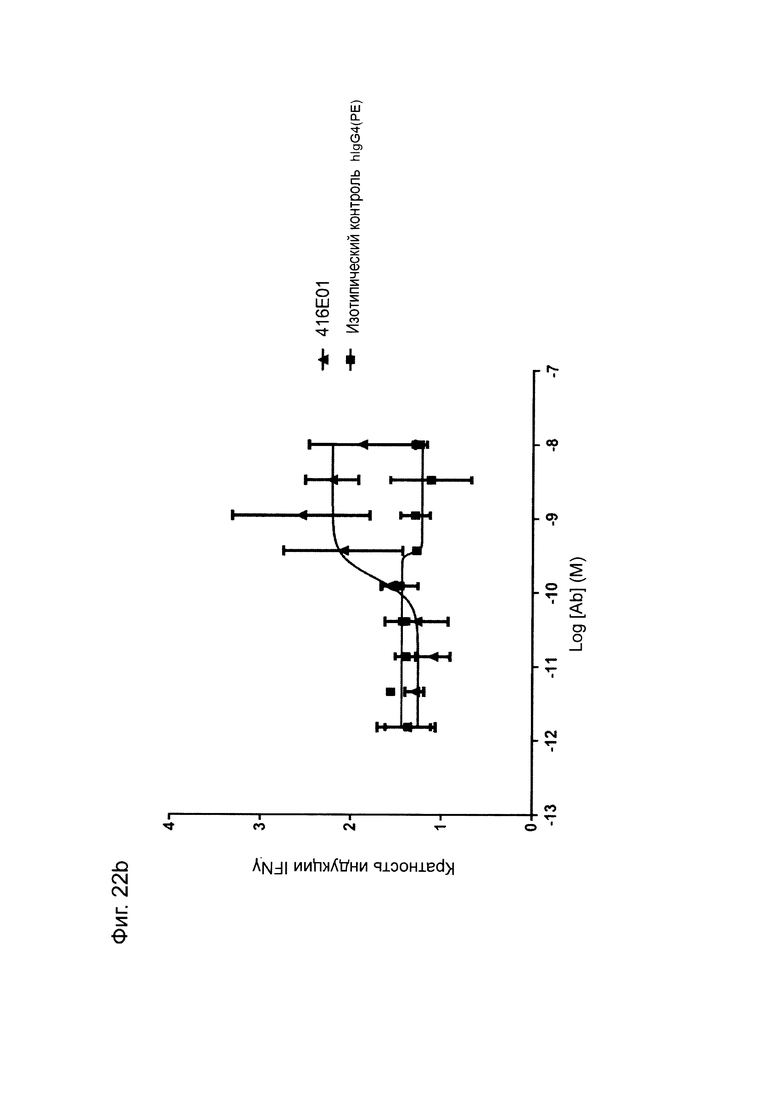
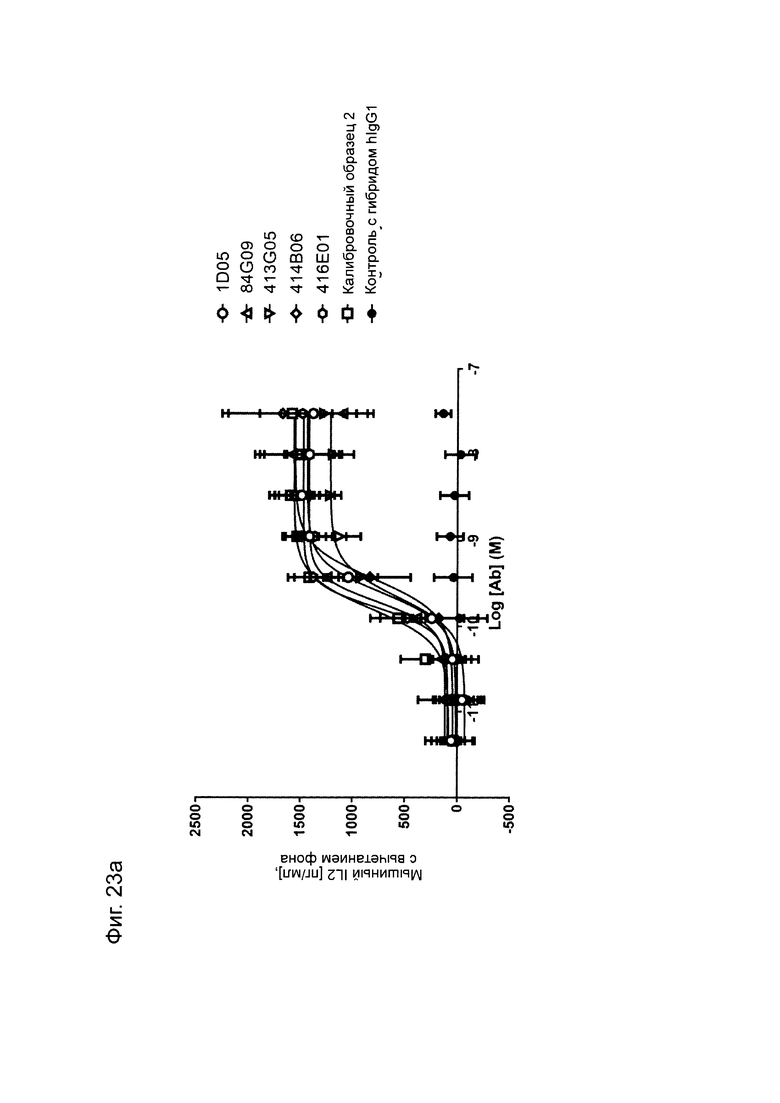
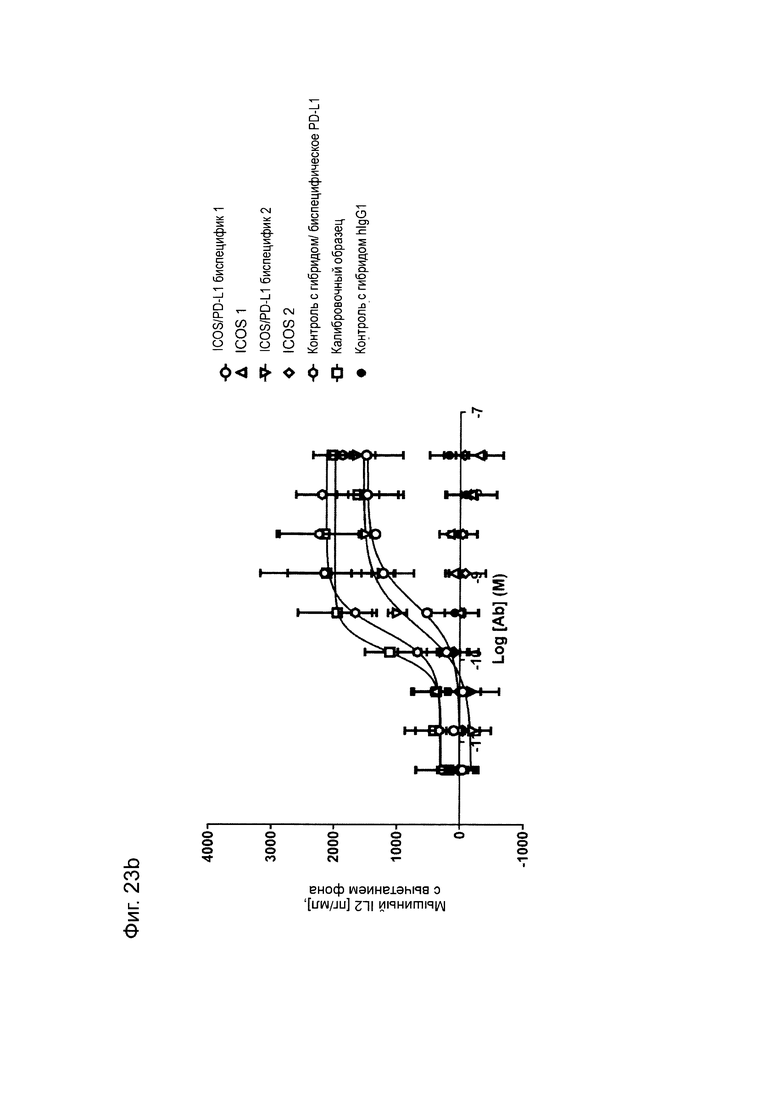
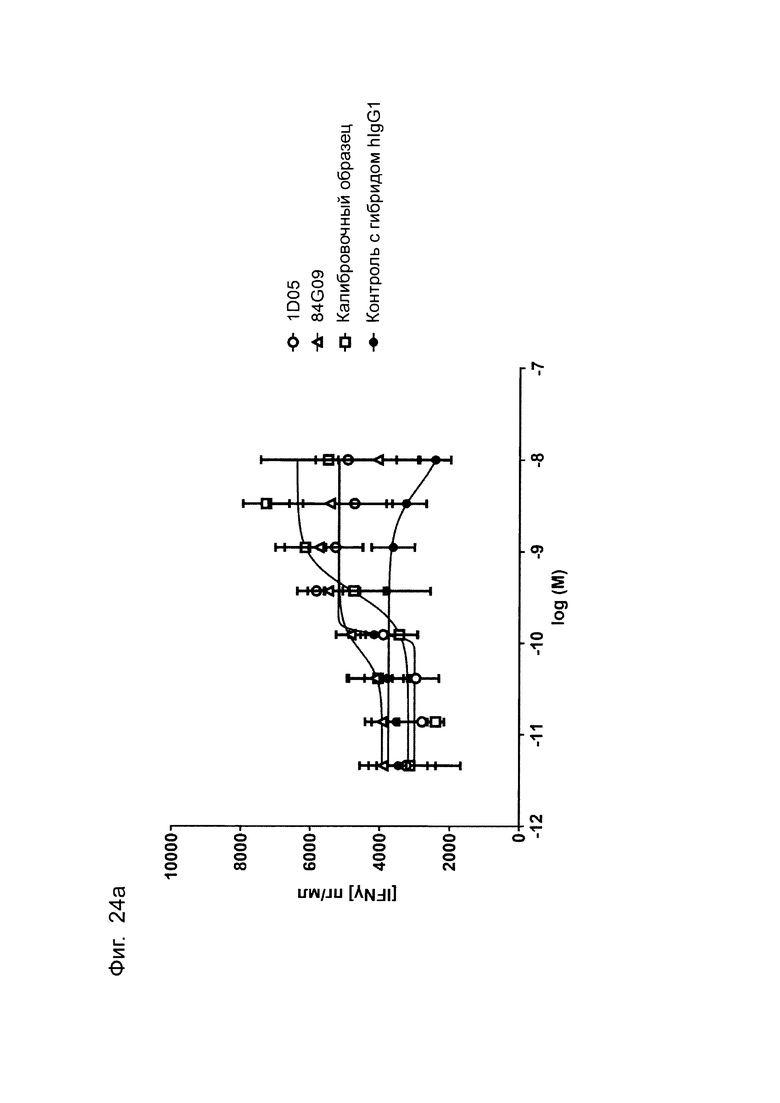
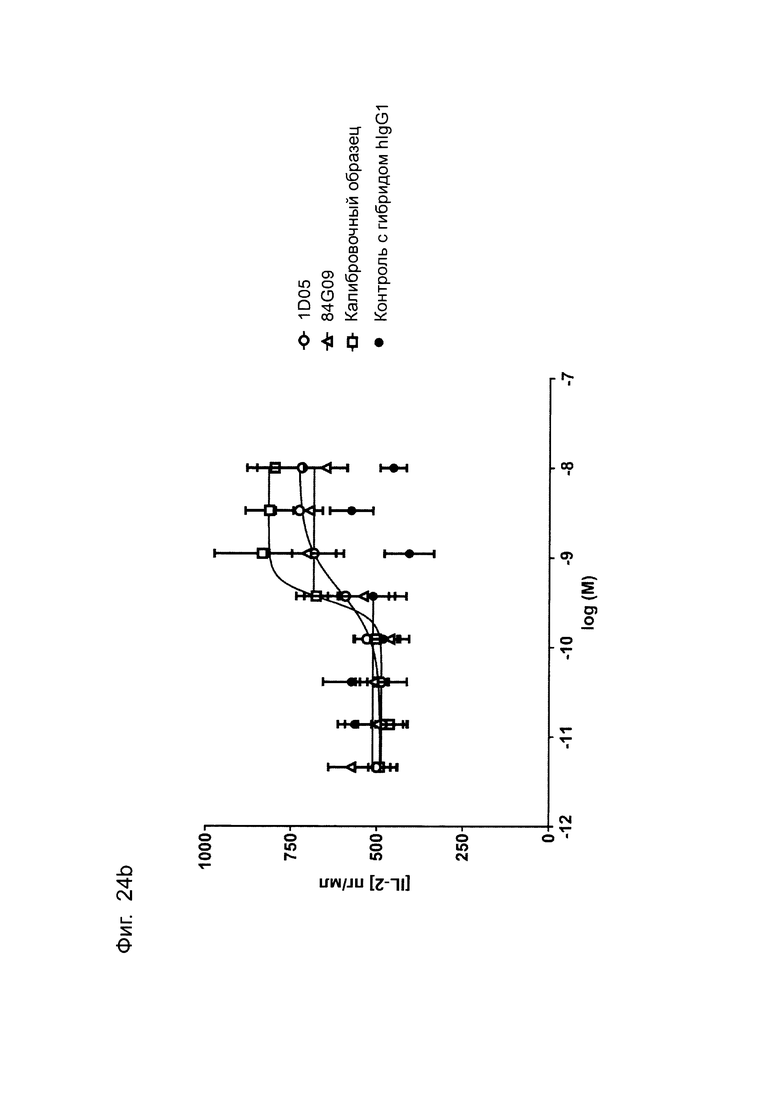
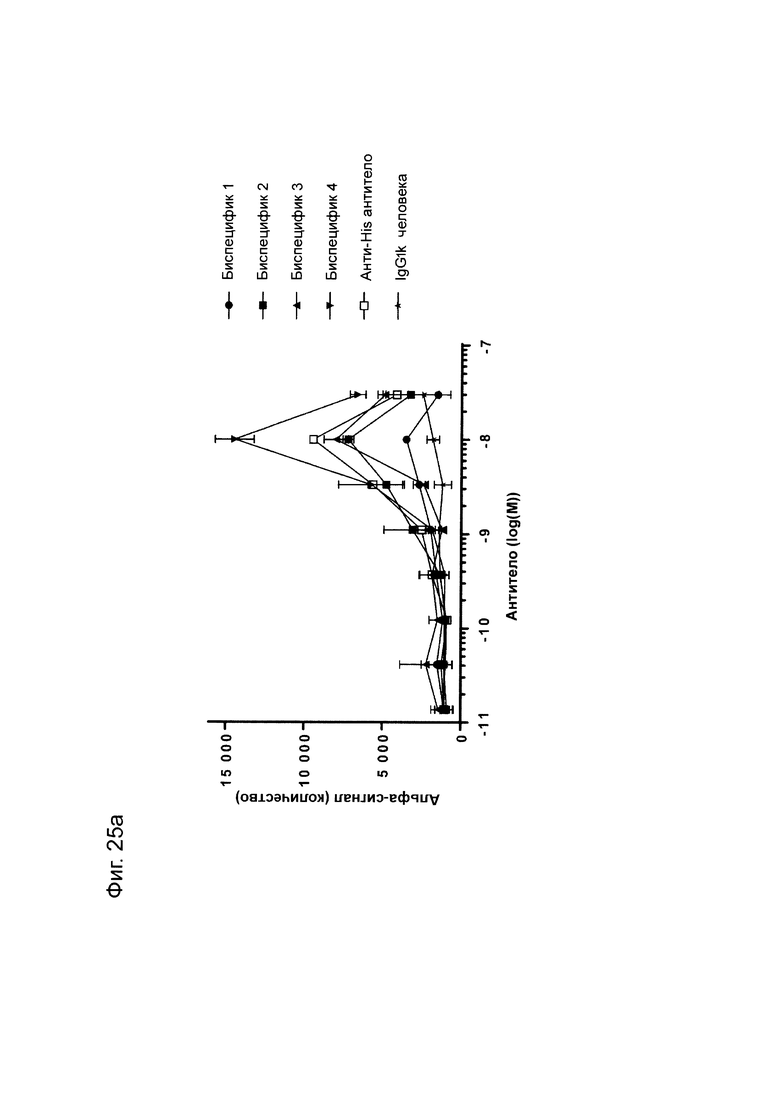
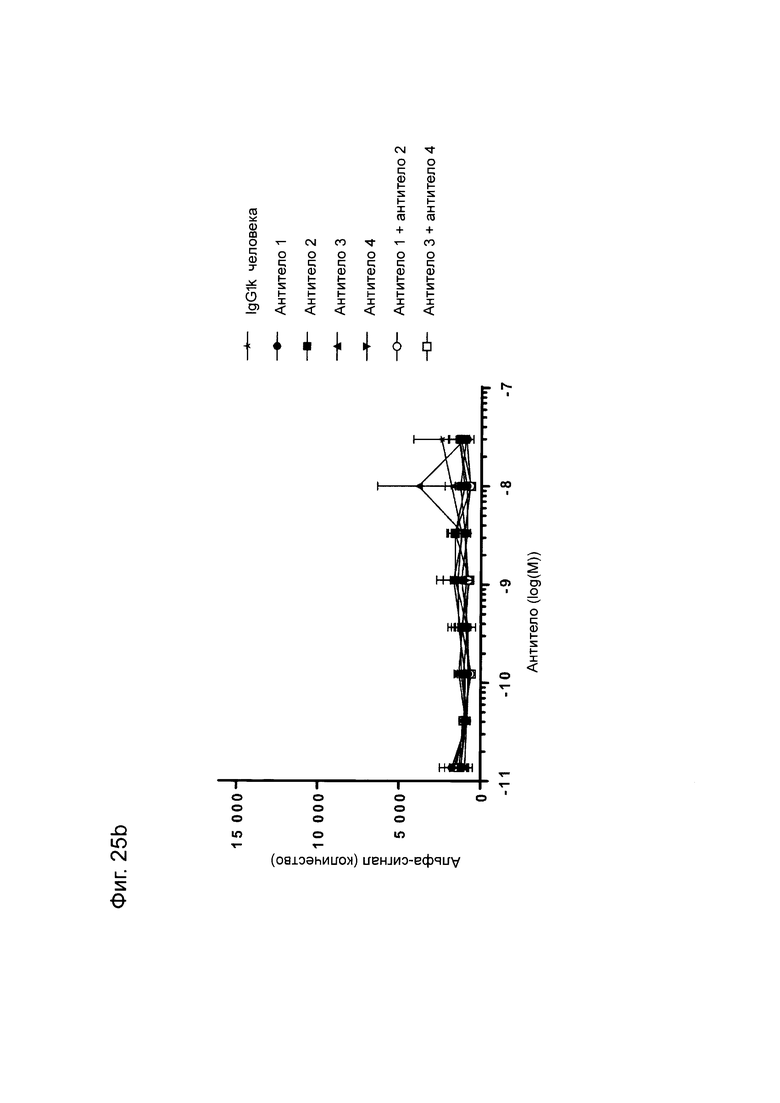
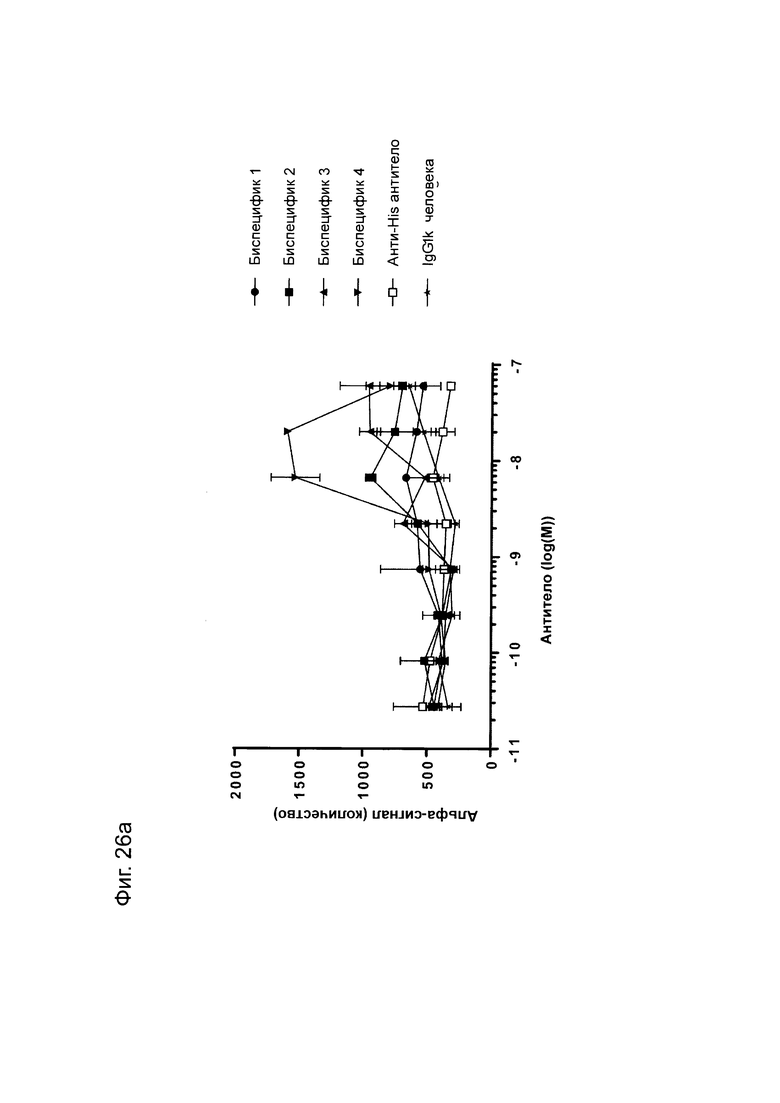
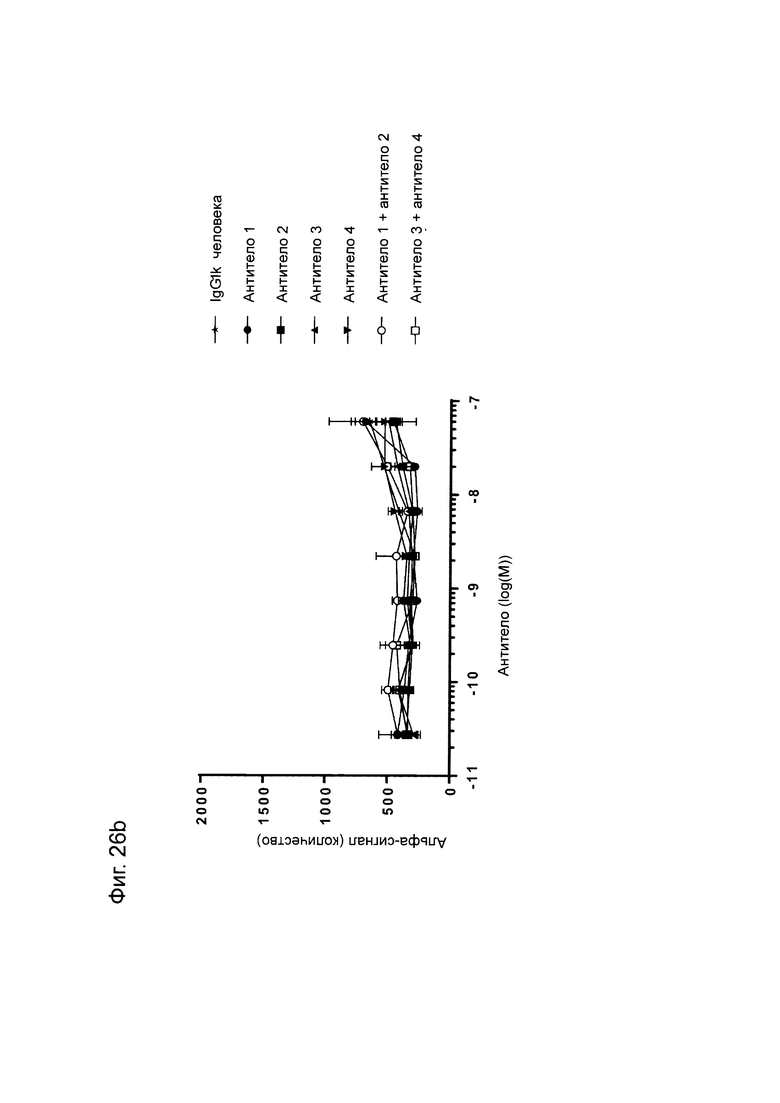
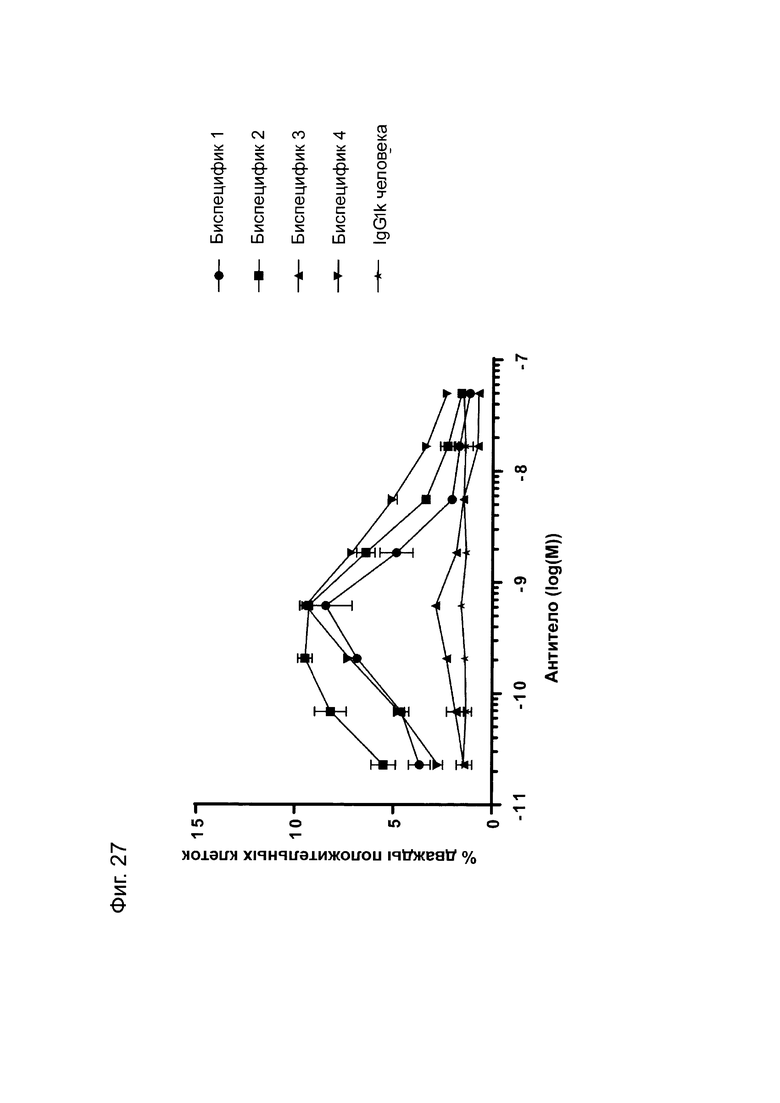
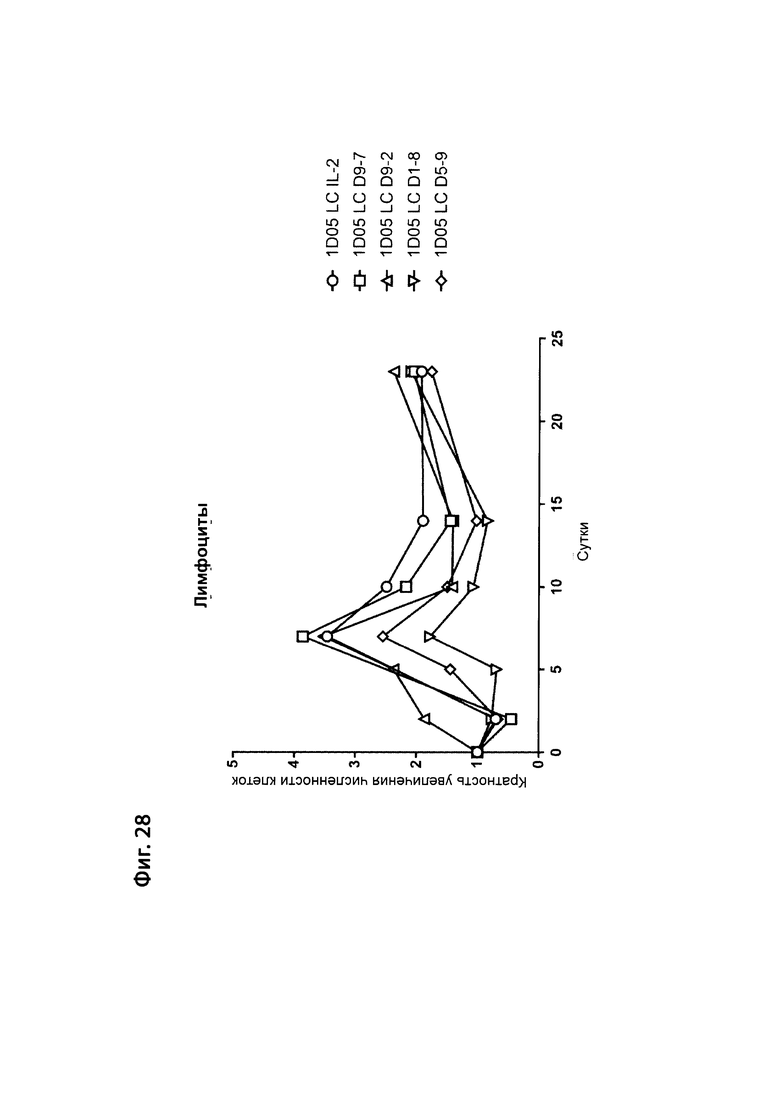
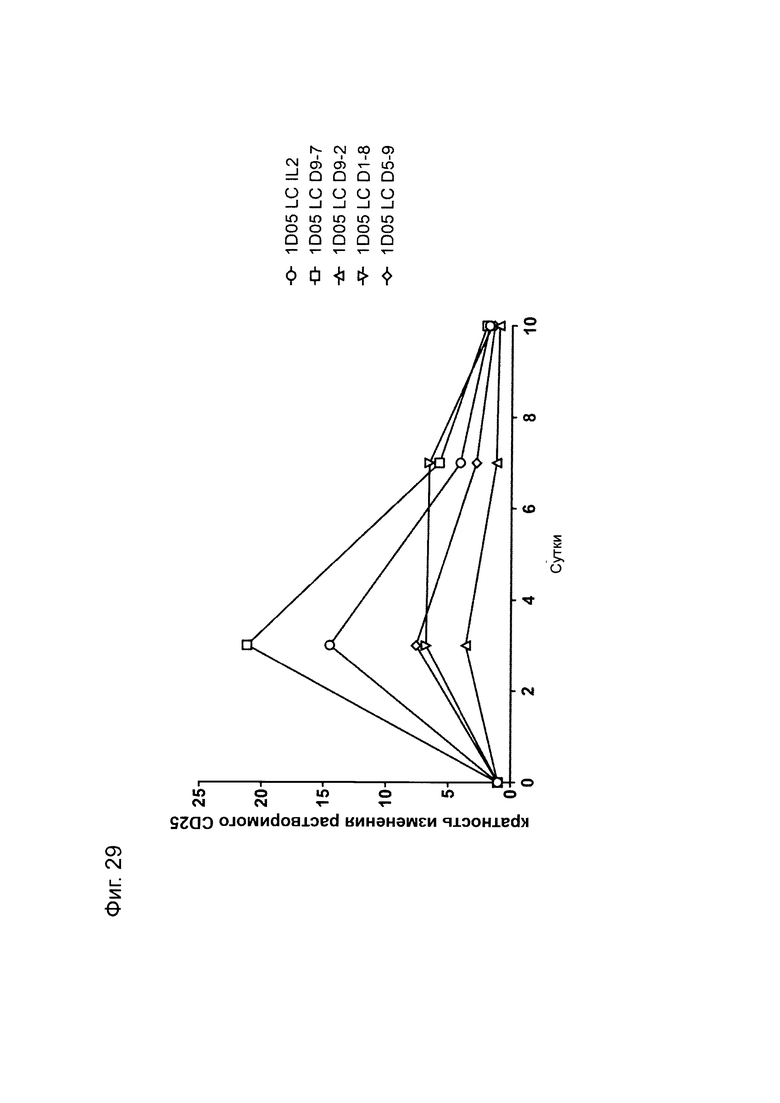
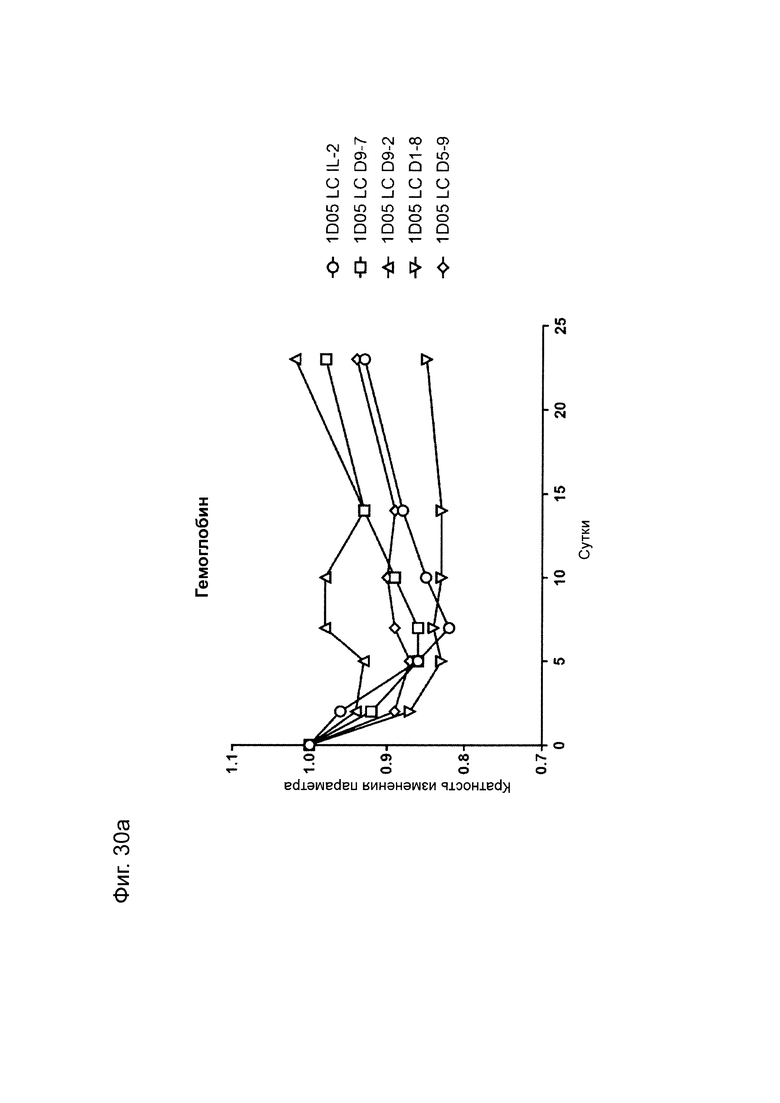
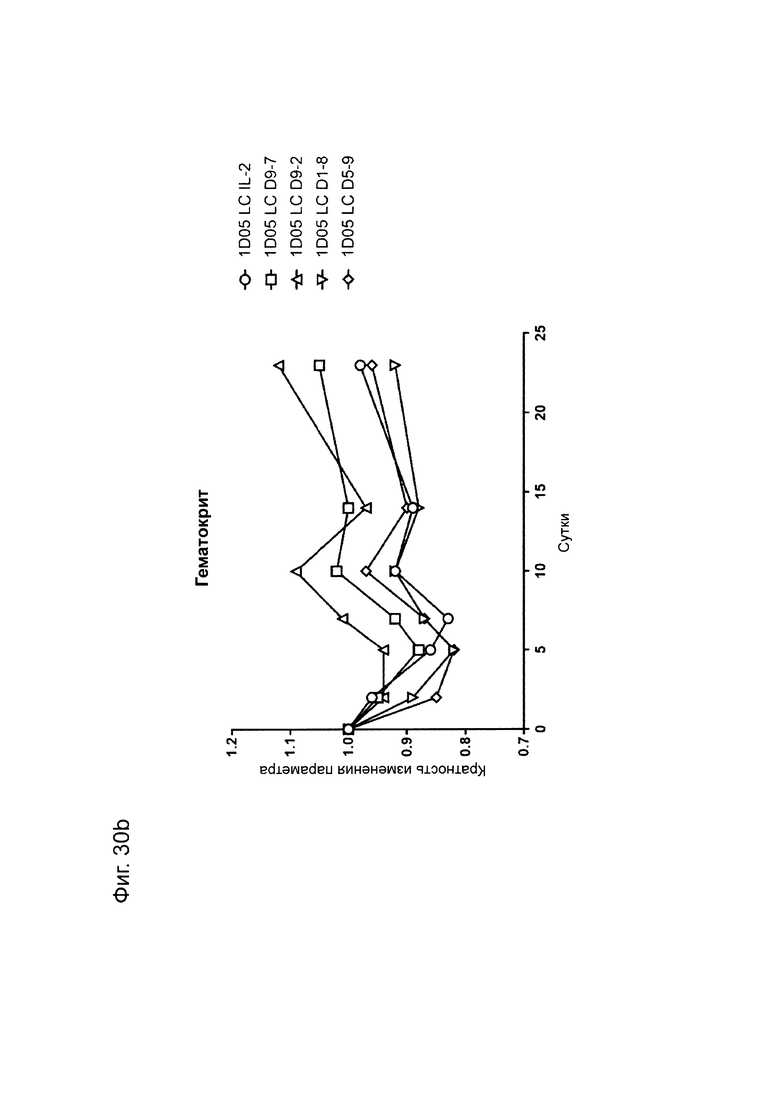
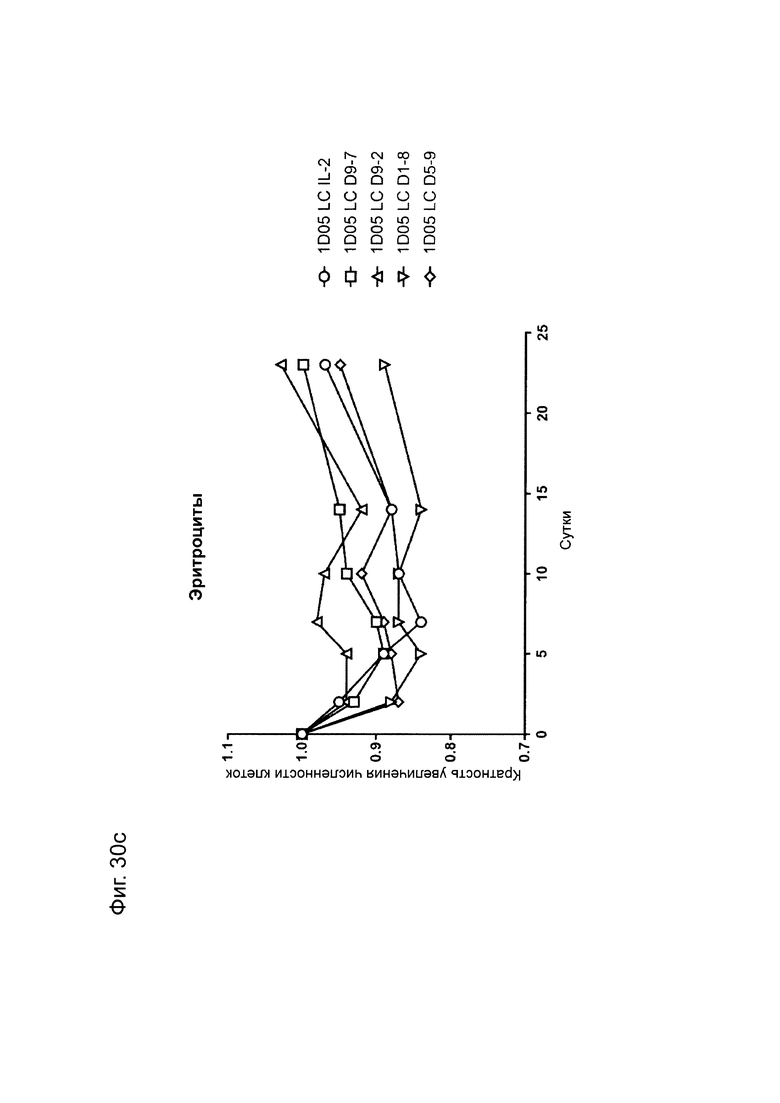
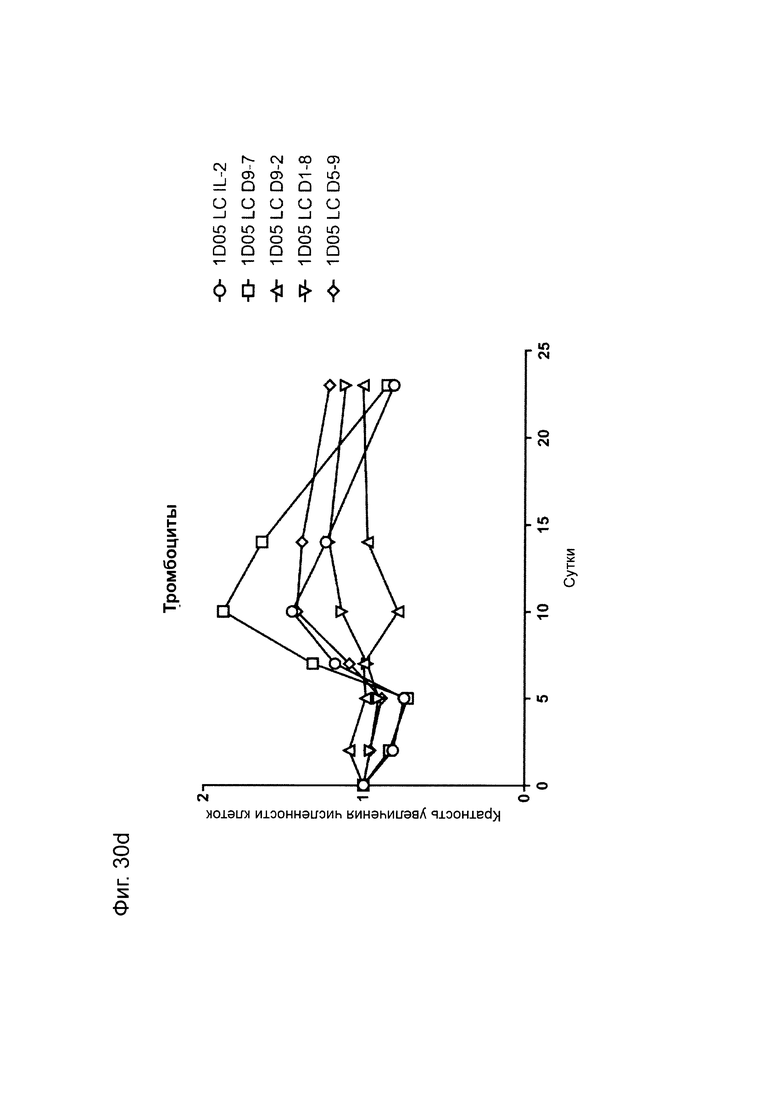
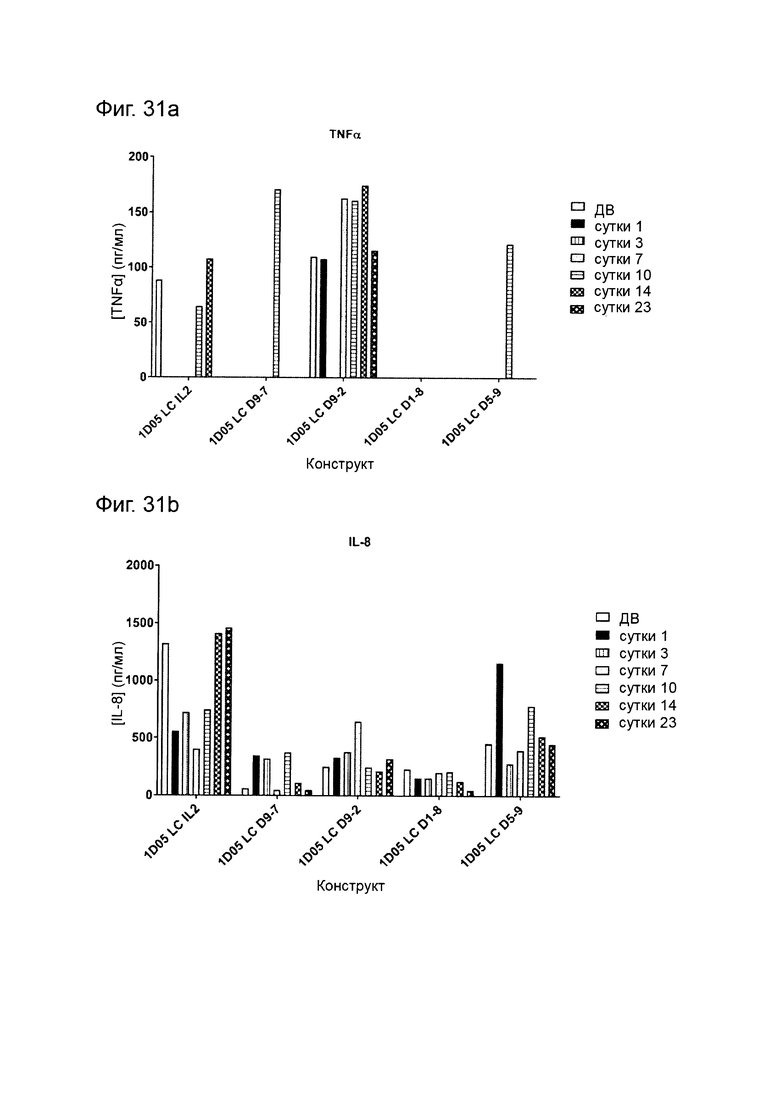
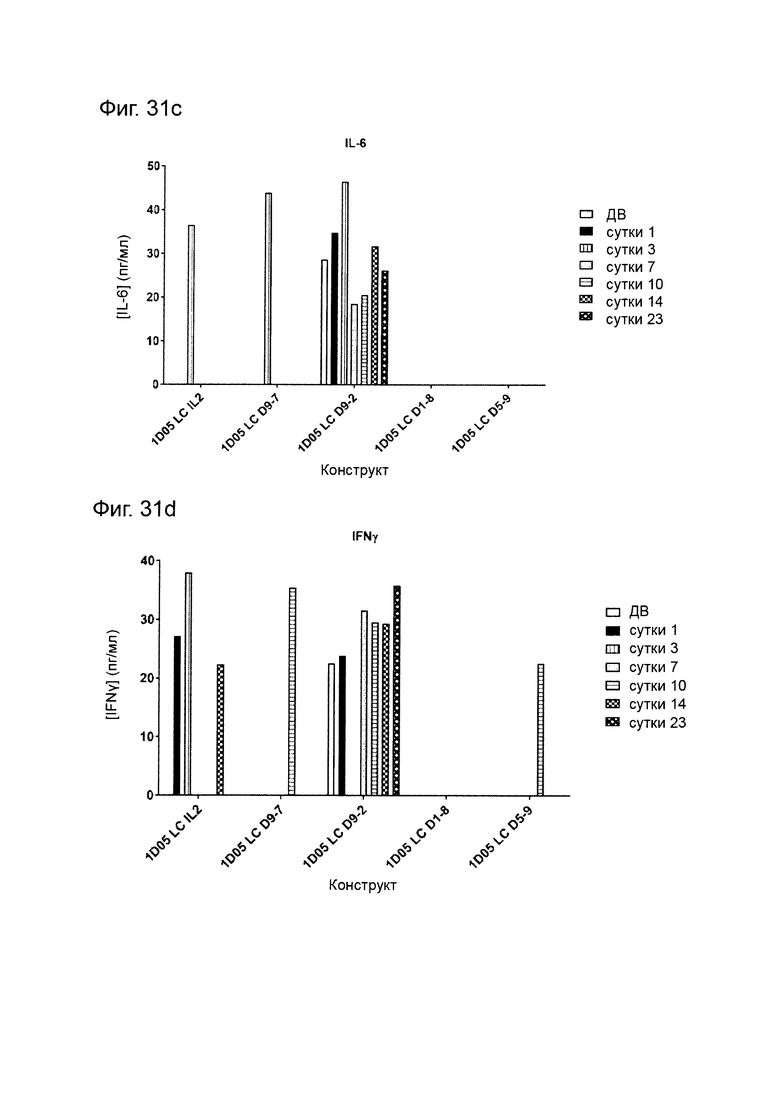
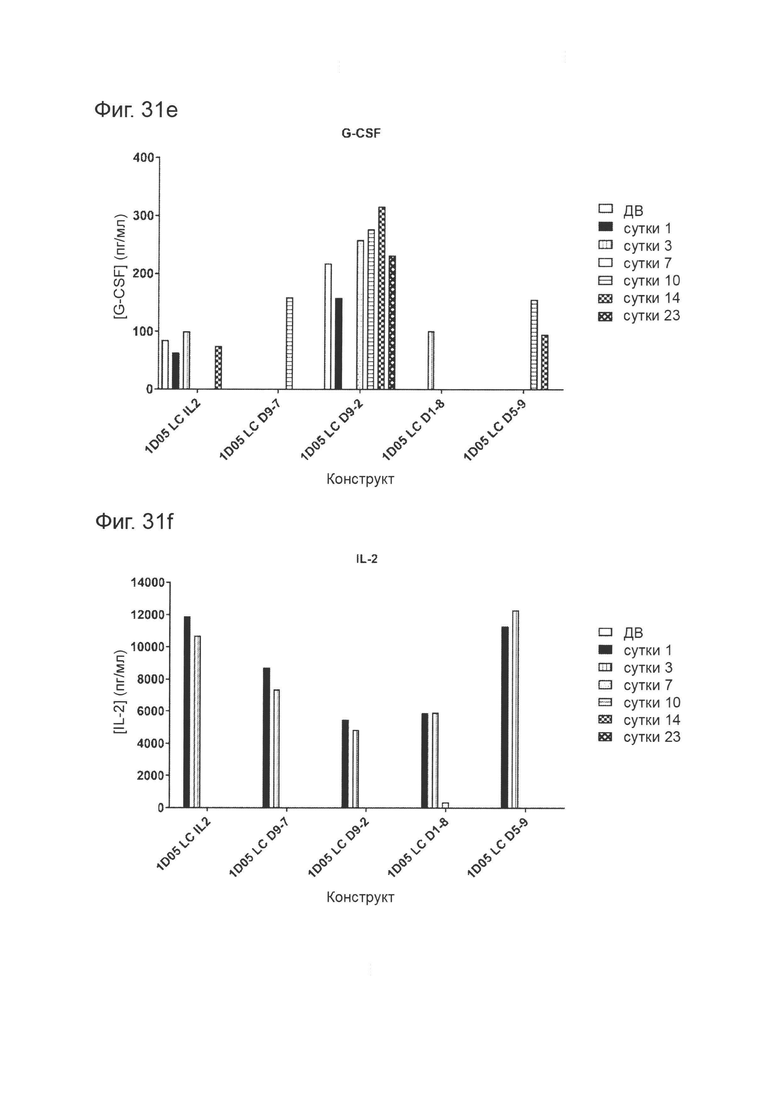
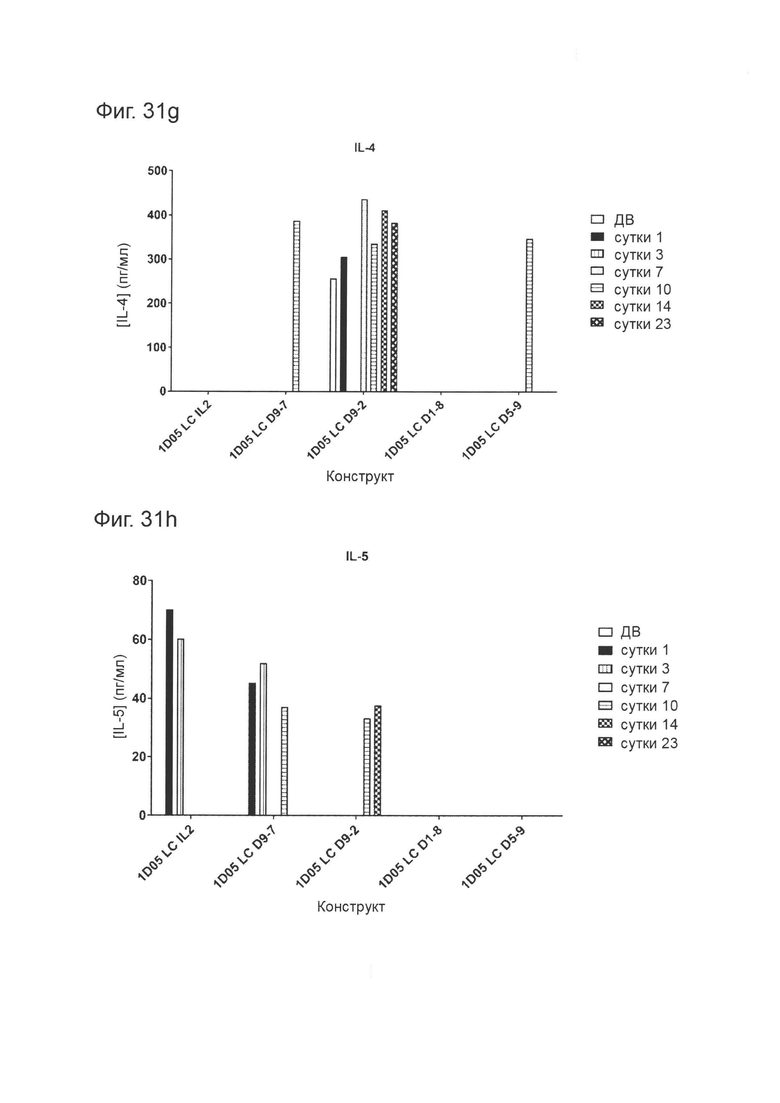
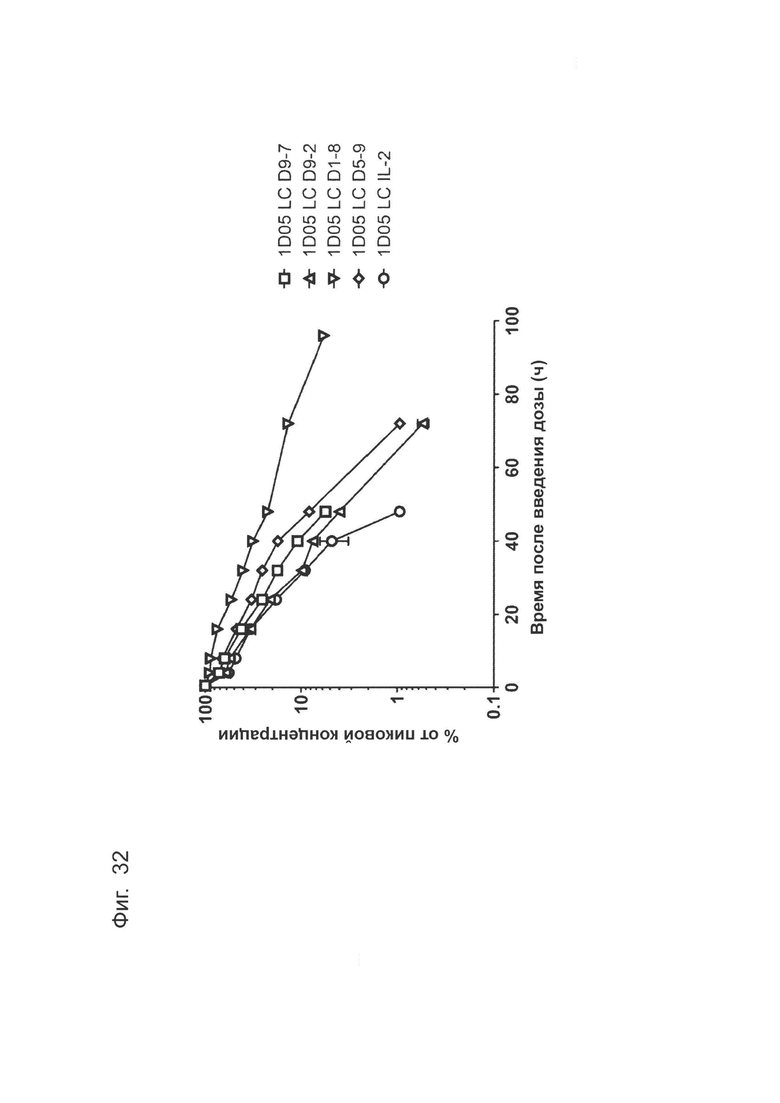
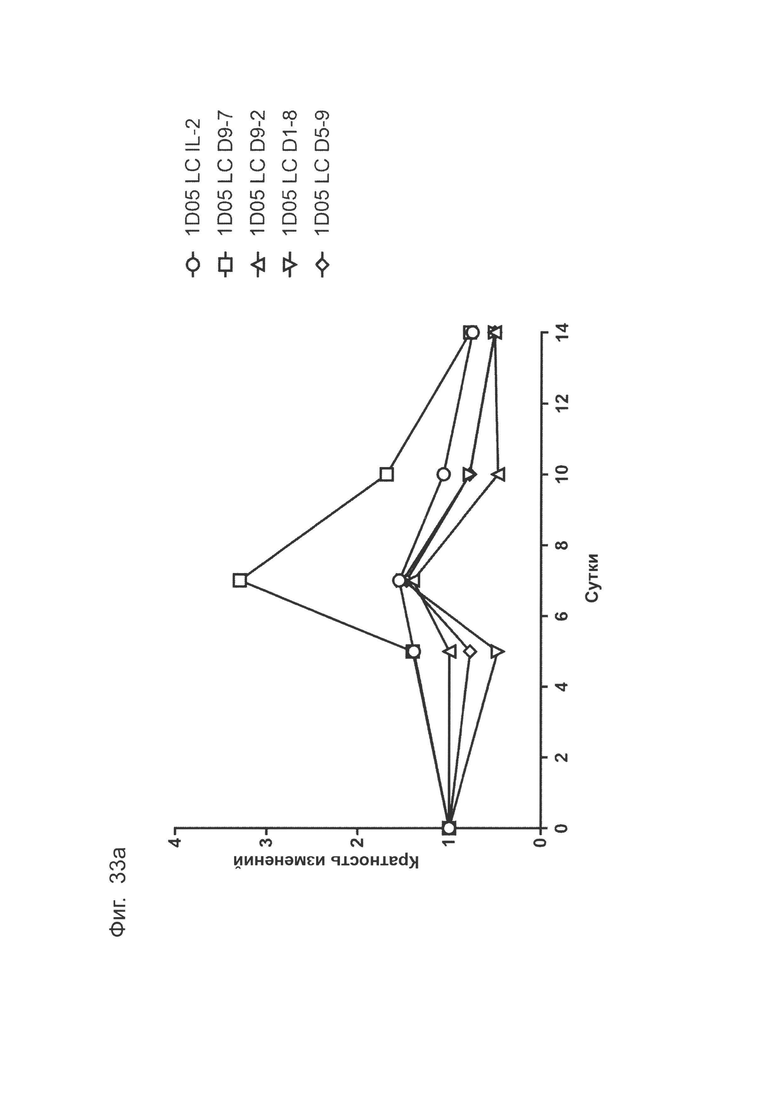
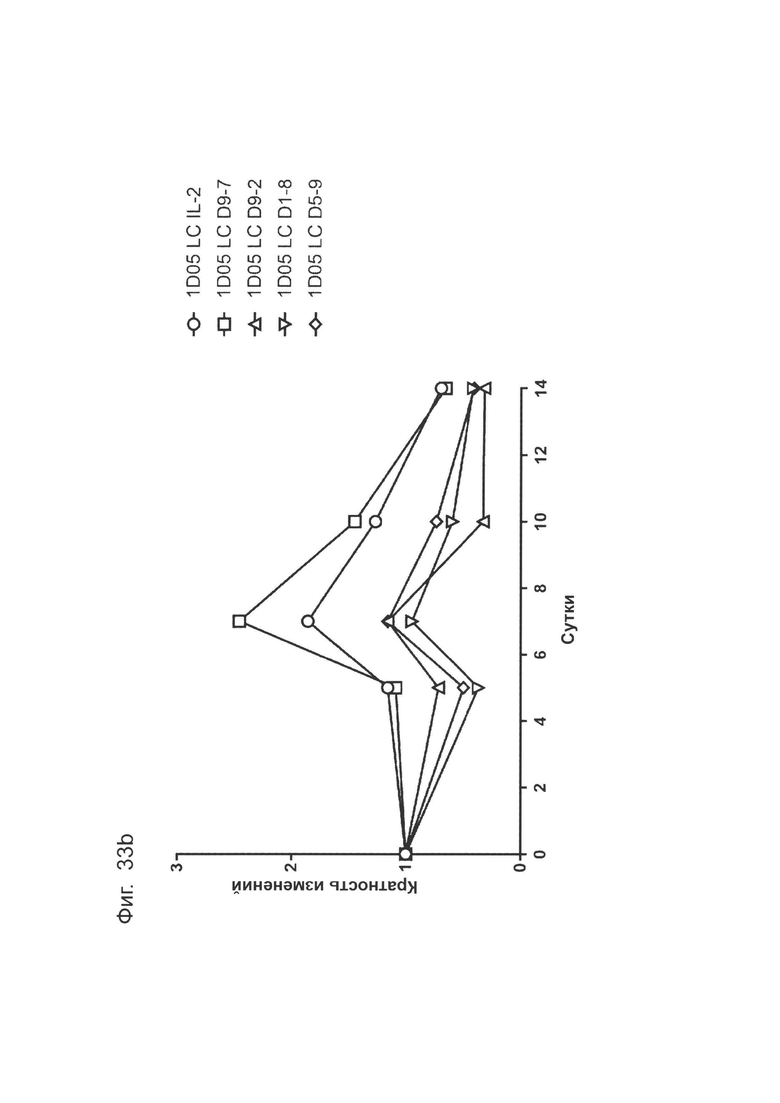
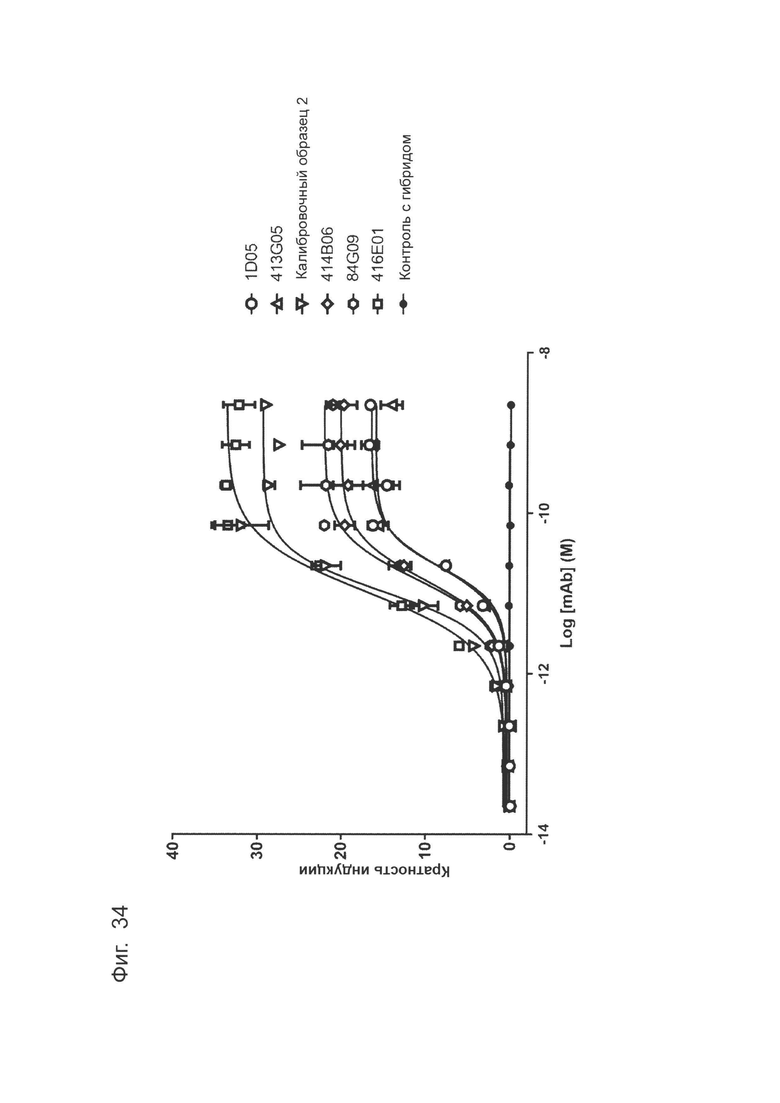
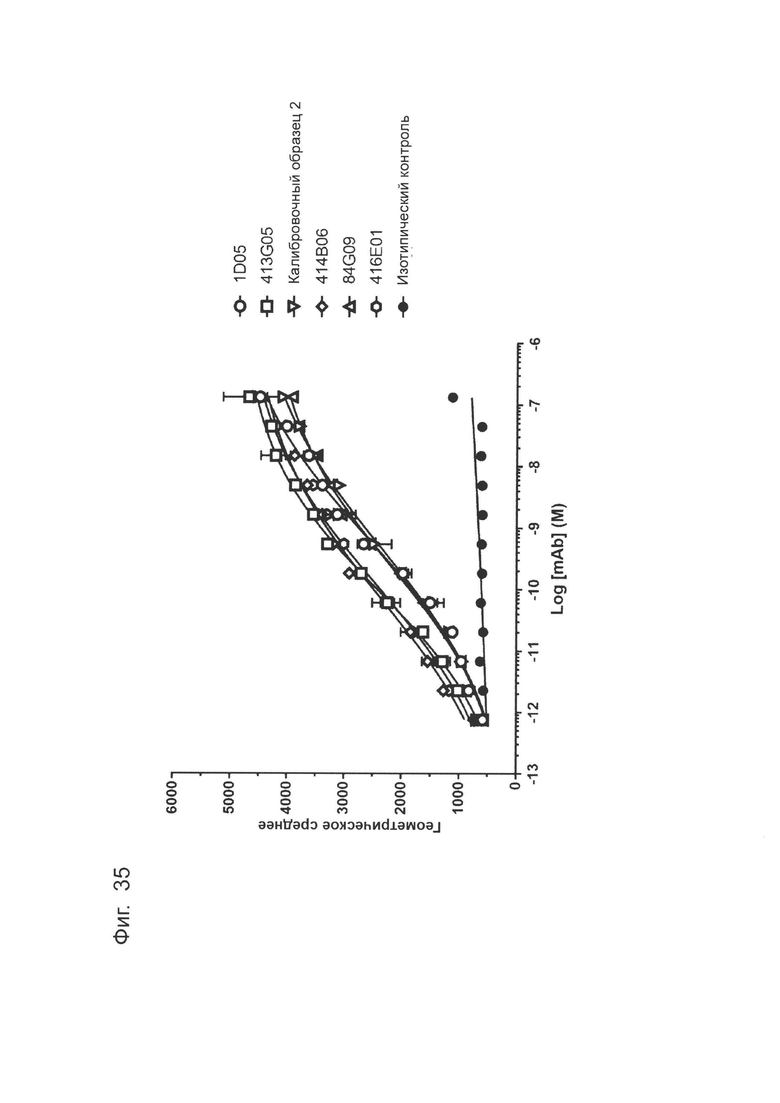
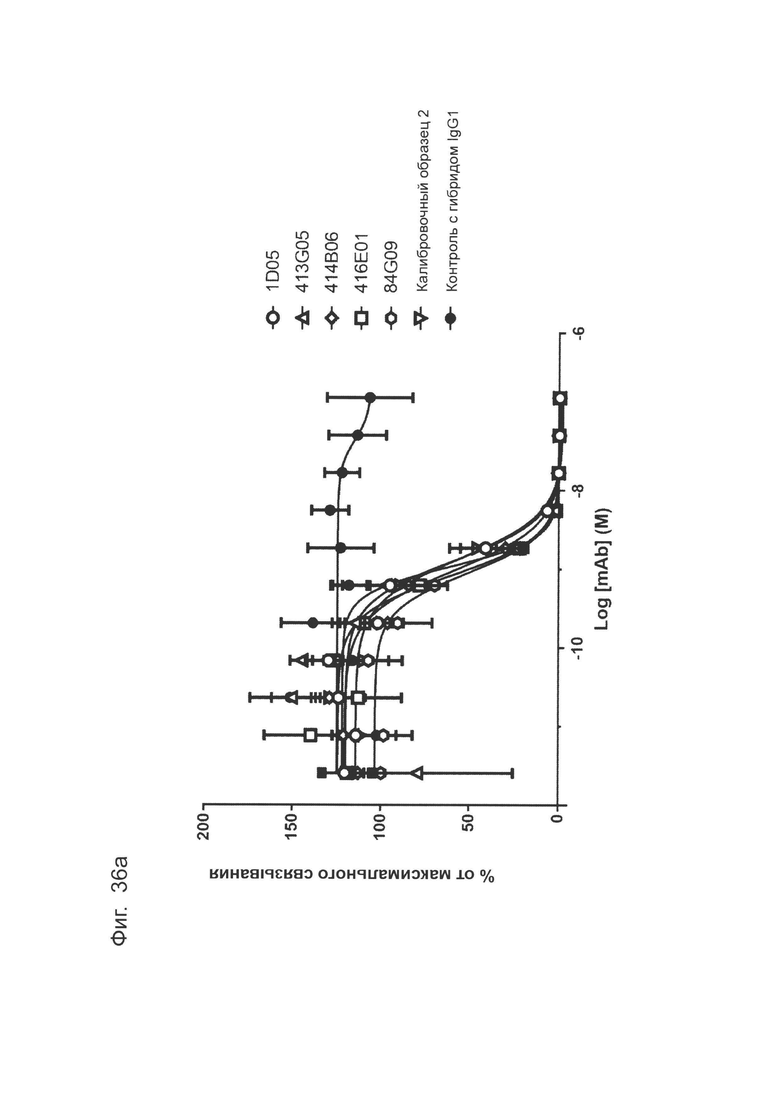
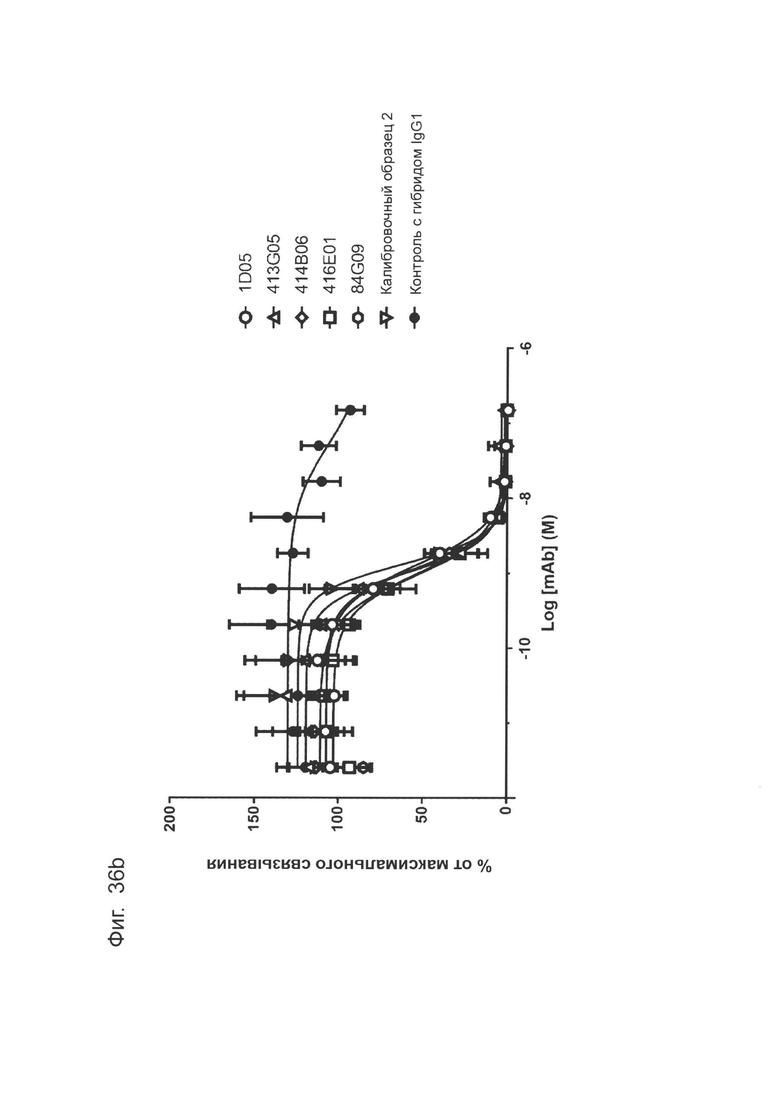
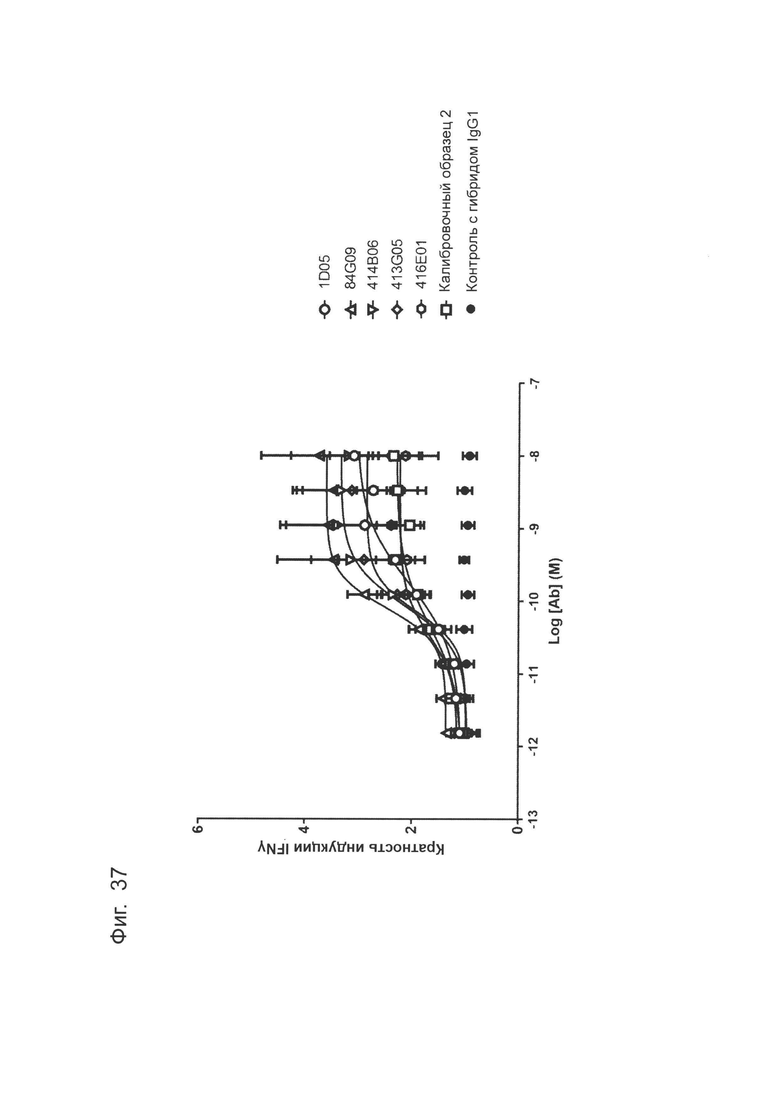
Изобретение относится к области биотехнологии, конкретно к получению иммуноцитокина, способного к специфическому связыванию с антигеном PD-L1 человека и ингибированию связывания PD-L1 с PD-1. Полученный иммуноцитокин содержит человеческий цитокин IL-2, а также тяжелую и лёгкую цепи иммуноглобулина, где тяжелая цепь содержит CDRH1 с SEQ ID NO: 27 или SEQ ID NO: 30, CDRH2 с SEQ ID NO: 28 или SEQ ID NO: 31 и CDRH3 с SEQ ID NO: 29 или SEQ ID NO: 32, а легкая содержит CDRL1 c SEQ ID NO: 37 или SEQ ID NO: 40; CDRL2 с SEQ ID NO: 38, SEQ ID NO: 41 или SEQ ID NO: 50; и CDRL3 с SEQ ID NO: 39 или SEQ ID NO: 42. Полученный иммуноцитокин может быть использован для эффективного лечения опосредованного hPD-L1 заболевания. 10 н. и 26 з.п. ф-лы, 37 ил., 22 табл., 31 пр.
1. Иммуноцитокин, способный к специфическому связыванию с антигеном PD-L1 человека и ингибированию связывания PD-L1 с PD-1, содержащий тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина, причем тяжелая цепь содержит, в направлении от N- к С-концу:
a) домен VH, содержащий CDRH1 c аминокислотной последовательностью SEQ ID NO: 27 или SEQ ID NO: 30; CDRH2 с аминокислотной последовательностью SEQ ID NO: 28 или SEQ ID NO: 31; и CDRH3 с аминокислотной последовательностью SEQ ID NO: 29 или SEQ ID NO: 32; и
b) константную область тяжелой цепи иммуноглобулина;
и причем легкая цепь содержит, в направлении от N- к С-концу:
c) домен VL, содержащий CDRL1 c аминокислотной последовательностью SEQ ID NO: 37 или SEQ ID NO: 40; CDRL2 с аминокислотной последовательностью SEQ ID NO: 38, SEQ ID NO: 41 или SEQ ID NO: 50; и CDRL3 с аминокислотной последовательностью SEQ ID NO: 39 или SEQ ID NO: 42;
d) константную область легкой цепи каппа или лямбда (CL); и
e) человеческий цитокин IL-2;
причем домен VH и домен VL состоят из антигенсвязывающего сайта, который специфически связывается с hPD-L1, представленным в SEQ ID NO: 1.
2. Иммуноцитокин по п. 1, дополнительно содержащий между (d) и (е) пептидный линкер длиной от 1 до 10 аминокислот.
3. Иммуноцитокин по п. 1 или 2, отличающийся тем, что домен VH содержит аминокислотную последовательность, представленную SEQ ID NO: 33, или аминокислотную последовательность вариабельного домена тяжелой цепи, по меньшей мере на 90% идентичную SEQ ID NO: 33, в частности последовательности домена VH в любой из последовательностей тяжелой цепи, представленных SEQ ID NO: 47-49.
4. Иммуноцитокин по любому из предшествующих пунктов, содержащий домен VL, который содержит аминокислотную последовательность, представленную SEQ ID NO: 43, или аминокислотную последовательность вариабельного домена легкой цепи, по меньшей мере на 90% идентичную SEQ ID NO: 43, в частности последовательности домена VL в последовательности легкой цепи, представленной SEQ ID NO: 50 или 51.
5. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что специфически связывается с PD-L1 яванского макака, определенным SEQ ID NO: 2.
6. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что константная область представляет собой константную область человека.
7. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что константная область представляет собой константную область IgG1.
8. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что константная область представляет собой инактивированный IgG1, определенный в SEQ ID NO: 205.
9. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что:
A) домен VH содержит аминокислотную последовательность SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность SEQ ID NO: 43;
B) домен VH содержит аминокислотную последовательность, которая по меньшей мере на 90% идентична SEQ ID NO: 33, а домен VL содержит аминокислотную последовательность, которая по меньшей мере на 90% идентична SEQ ID NO: 43;
C) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность, представленную SEQ ID NO: 43;
D) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность, представленную SEQ ID NO: 43;
E) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность, представленную SEQ ID NO: 43;
F) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность, представленную SEQ ID NO: 43;
G) домен VH содержит аминокислотную последовательность SEQ ID NO:33, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
H) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 47, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
I) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 48, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
J) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 49, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51;
K) домен VH содержит аминокислотную последовательность домена VH, представленную SEQ ID NO: 342, а домен VL содержит аминокислотную последовательность домена VL, представленную SEQ ID NO: 51.
10. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что:
A) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 299, и VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 45;
B) VH и константная область содержат аминокислотную последовательность, которая по меньшей мере на 90% идентична SEQ ID NO: 299, а VL и CL содержат аминокислотную последовательность, которая по меньшей мере на 90% идентична SEQ ID NO: 45;
C) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 47, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 45;
D) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 48, а VL и CL, содержат аминокислотную последовательность, представленную SEQ ID NO: 45;
E) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 49, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 45;
F) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 342, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 45;
G) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 299, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 51;
H) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 47, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 51;
I) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 48, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 51;
J) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 49, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 51;
K) VH и константная область содержат аминокислотную последовательность, представленную SEQ ID NO: 342, а VL и CL содержат аминокислотную последовательность, представленную SEQ ID NO: 51.
11. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что цитокин IL-2 представляет собой человеческий IL-2 (hIL-2) или его вариант, и причем, необязательно, hIL-2 содержит или состоит из аминокислотной последовательности SEQ ID NO: 301 и, также необязательно, hIL-2 содержит вариант IL-2, который содержит модификацию на N-конце, необязательно, делецию от 1 до 10 аминокислот.
12. Иммуноцитокин по п. 11, отличающийся тем, что hIL-2 содержит вариант IL-2, содержащий N-концевую последовательность, выбранную из SEQ ID NO: 303-323.
13. Иммуноцитокин по п. 11 или 12, отличающийся тем, что вариант hIL-2 содержит одну или несколько, в частности от 1 до 5, предпочтительно одну или две, мутаций, независимо выбранных из следующих:
1) D20, в частности D20T;
2) R38, в частности R38W, R38A или R38Q;
3) F42, в частности F42A или F42K;
4) Y45, в частности Y45A;
5) E62, в частности E62A;
6) N88, в частности N88R;
7) C125, в частности C125S;
8) Q126, в частности Q126W; и
9) R38 и F42, в частности R38W и F42K или R38A и F42A;
причем нумерация остатка определена по отношению к последовательности IL-2 дикого типа человека, SEQ ID NO: 301.
14. Иммуноцитокин по п. 11, отличающийся тем, что hIL-2 содержит вариант IL-2, который состоит из N-концевой последовательности, выбранной из SEQ ID NO: 242-262, слитой с аминокислотной последовательностью SEQ ID NO: 324.
15. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что цитокин IL-2 связывается с высокоаффинным (αβγ) рецептором IL-2 с эффективностью, меньшей чем у свободного IL-2, в частности, со значением ЕС50 более 20 пМ, более 50 пМ или более 100 пМ, при измерении путем клеточного пролиферативного анализа.
16. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что IL-2 связывается с рецептором IL-2 промежуточной аффинности (βγ) с эффективностью, меньшей чем у свободного IL-2, в частности, со значением EC50 более 1 нМ, более 5 нМ или более 10 нМ, при измерении путем клеточного пролиферативного анализа.
17. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что IL-2 предпочтительно связывается с высокоаффинным (αβγ) рецептором IL-2, а при сравнении с рецептором IL-2 промежуточной аффинности (βγ), необязательно где соотношение эффективности (potency) IL-2 против высокоаффинного (αβγ) рецептора IL-2 и рецептора IL-2 промежуточной аффинности (βγ) составляет по меньшей мере 2:1.
18. Иммуноцитокин по любому из предшествующих пунктов, отличающийся тем, что антигенсвязывающий сайт связывается с hPD-L1 с аффинностью менее 500 пМ, в частности менее 300 пМ или менее 200 пМ, причем, необязательно, иммуноцитокин обеспечивает соотношение эффективности цитокина IL-2 против высокоаффинного (αβγ) рецептора и аффинности антигенсвязывающего сайта анти-PD-L1 против hPD-L1, равное по меньшей мере 2:1.
19. Применение иммуноцитокина по любому из пп. 1-18 при изготовлении лекарственного средства для введения человеку с целью лечения или профилактики опосредованного hPD-L1 заболевания у человека.
20. Применение по п. 19, где опосредованное hPD-L1 заболевание выбрано из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, в частности меланомы, рака молочной железы, рака яичников, карциномы клеток Меркеля, плоскоклеточного и неплоскоклеточного немелкоклеточного рака легкого, почечно-клеточного рака, рака мочевого пузыря, колоректального рака без микросателлитной нестабильности (MSI), плоскоклеточного рака головы и шеи, мезотелиомы, вирусно-индуцированных раковых заболеваний, в частности рака шейки матки и рака носоглотки, сарком мягких тканей, гематологических злокачественных новобразований, в частности болезни Ходжкина и неходжкинской лимфомы, диффузной крупноклеточной В-клеточной лимфомы.
21. Способ лечения или профилактики опосредованного hPD-L1 заболевания у человека, включающий введение указанному человеку терапевтически эффективного количества иммуноцитокина по любому из пп. 1-18, посредством чего осуществляется лечение или профилактика опосредованного hPD-L1 заболевания.
22. Способ по п. 21, где опосредованное hPD-L1 заболевание выбрано из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, в частности меланомы, рака молочной железы, рака яичников, карциномы клеток Меркеля, плоскоклеточного и неплоскоклеточного немелкоклеточного рака легкого, почечно-клеточного рака, рака мочевого пузыря, колоректального рака без микросателлитной нестабильности (MSI), плоскоклеточного рака головы и шеи, мезотелиомы, вирусно-индуцированных раковых заболеваний, в частности рака шейки матки и рака носоглотки, сарком мягких тканей, гематологических злокачественных новобразований, в частности болезни Ходжкина и неходжкинской лимфомы, диффузной крупноклеточной В-клеточной лимфомы.
23. Применение по п. 19, отличающееся тем, что опосредованное hPD-L1 заболевание является раком, необязательно где рак выбирают из меланомы, рака клеток Меркеля, немелкоклеточного рака легкого, рака мочевого пузыря, неходжкинских лимфом, колоректального рака с микросателлитной нестабильностью (MSI) или рака, выбранного из рака молочной железы, рака яичников, колоректального рака без MSI, в частности меланомы и почечно-клеточного рака.
24. Способ по п. 21, отличающийся тем, что опосредованное hPD-L1 заболевание является раком, необязательно где рак выбирают из меланомы, рака клеток Меркеля, немелкоклеточного рака легкого, рака мочевого пузыря, неходжкинских лимфом, колоректального рака с микросателлитной нестабильностью (MSI) или рака, выбранного из рака молочной железы, рака яичников, колоректального рака без MSI, в частности меланомы и почечно-клеточного рака.
25. Способ по п. 21 или 24, дополнительно включающий проведение для человека дополнительной терапии.
26. Фармацевтическая композиция для лечения или профилактики опосредованного hPD-L1 заболевания, содержащая эффективное количество иммуноцитокина по любому из пп. 1-18 и фармацевтически приемлемый эксципиент, разбавитель или носитель.
27. Фармацевтическая композиция по п. 26, где указанное заболевание выбрано из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, в частности меланомы, плоскоклеточного и неплоскоклеточного немелкоклеточного рака легкого, почечно-клеточного рака, рака мочевого пузыря, плоскоклеточного рака головы и шеи, мезотелиомы, вирусно-индуцированных раковых заболеваний, в частности рака шейки матки и рака носоглотки, саркомы мягких тканей, гематологических злокачественных новообразований, в частности болезни Ходжкина и неходжкинской лимфомы, диффузной крупноклеточной В-клеточной лимфомы.
28. Набор для лечения или профилактики опосредованного hPD-L1 заболевания, включающий фармацевтическую композицию по п. 26 и этикетку или инструкции по применению для лечения или профилактики указанного заболевания у человека.
29. Набор по п. 28, где указанное заболевание выбрано из неопластического или не связанного с новообразованиями заболевания, хронических вирусных инфекций и злокачественных опухолей, в частности меланомы, плоскоклеточного и неплоскоклеточного немелкоклеточного рака легкого, почечно-клеточного рака, рака мочевого пузыря, плоскоклеточного рака головы и шеи, мезотелиомы, вирусно-индуцированных раковых заболеваний, в частности рака шейки матки и рака носоглотки, саркомы мягких тканей, гематологических злокачественных новообразований, в частности болезни Ходжкина и неходжкинской лимфомы, диффузной крупноклеточной В-клеточной лимфомы; причем, необязательно, этикетка или инструкции содержат номер регистрационного удостоверения лекарственного средства.
30. Набор по п. 29, включающий устройство для внутривенного (IV) введения или инъекционное устройство, содержащее иммуноцитокин.
31. Способ лечения пролиферативного заболевания у человека, включающий введение указанному пациенту эффективного количества иммуноцитокина, как определено в любом из пп. 1-18.
32. Нуклеиновая кислота, кодирующая легкую цепь иммуноцитокина, как определено в любом из пп. 1-18.
33. Нуклеиновая кислота, кодирующая тяжелую цепь и легкую цепь иммуноцитокина, как определено в любом из пп. 1-18.
34. Экспрессионный вектор, содержащий нуклеиновую кислоту по п. 33.
35. Вектор по п. 34, который предназначен для экспрессии в клетках CHO или HEK293.
36. Клетка-хозяин для экспрессии иммуноцитокина, способного к специфическому связыванию с антигеном PD-L1 человека и ингибированию связывания PD-L1 с PD-1, содержащая вектор по п. 34 или 35.
| NERI D | |||
| et al., Immunocytokines for cancer treatment: past, present and future, Current opinion in immunology, 2016, V | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| WEST E | |||
| E | |||
| et al., PD-L1 blockade synergizes with IL-2 therapy in reinvigorating exhausted T cells, The Journal of clinical investigation, 2013, V | |||
| Устройство для разметки подлежащих сортированию и резанию лесных материалов | 1922 |
|
SU123A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| ДЕЕВ С | |||
| М | |||
| и др., Современные технологии | |||
Авторы
Даты
2022-03-30—Публикация
2017-06-20—Подача