Область техники
Настоящее изобретение относится к биотехнологии и медицине, в частности к наноразмерным системам комбинированной доставки лекарственных препаратов, по меньшей мере один из которых является таргетным рецептор-специфичным веществом пептидной природы, путем инкапсуляции в ядро и конъюгации на поверхности мицеллярных наночастиц из амфифильного полимера N-винилпирролидона, и может быть использовано для лечения злокачественных новообразований.
Уровень техники
В настоящее время активно разрабатываются различные виды наноносителей для лечения солидных опухолей. Полимерные наночастицы представляют большой интерес благодаря высокой стабильности, настраиваемым свойствам и возможности комбинированной доставки нескольких лекарственных препаратов. Универсальность и уникальные свойства биосовместимого амфифильного полимера N-винилпирролидона обусловили его широкое применение для различных целей. Амфифильные полимеры на основе N-винилпирролидона способны самоагрегироватся в водных растворах с образованием мицеллярных наноразмерных структур и иммобилизовать терапевтические молекулы в мягких условиях. Таким образом, мицеллярные наночастицы на основе поли-N-винилпирролидона перспективны для доставки низкомолекулярных и гидрофобных лекарственных препаратов, а также хорошо подходят для биоконъюгации.
Ближайшим аналогом изобретения может служить техническое решение, известное из RU2580649C1, где раскрывается наноразмерный носитель, который представляет собой мицеллы, состоящие из амфифильных сополимеров, имеющих гидрофильный и гидрофобный полимерные блоки, для доставки биологически активных веществ. Недостатком указанного известного наноразмерного носителя на основе мицелл из амфифильных сополимеров является отсутствие таргетного рецептор-специфического действия лекарственных препаратов в опухоли, что может приводить к неспецифическому действию и недостаточному противоопухолевому эффекту. Также, известно решение (Yagolovich A, Kuskov A, Kulikov P, Kurbanova L, Bagrov D, Artykov A, Gasparian M, Sizova S, Oleinikov V, Gileva A, Kirpichnikov M, Dolgikh D, Markvicheva E. Pharmaceutics. 2021; 13(9):1413), где раскрывается наноразмерный носитель, который представляет собой мицеллы, состоящие из амфифильных сополимеров, имеющих гидрофильный и гидрофобный полимерные блоки, для доставки таргетного рецептор-специфического противоопухолевого белка, конъюгированного с поверхностью мицелл. Данное решение направлено на то, чтобы использовать индукцию апоптоза с помошью рецептор-специфичного варианта TRAIL DR5-B в виде конъюгата с мицеллярными наночастицами для лечения рака. Недостатком указанного решения является потенциально недостаточный противоопухолевый эффект для клинического применения из-за использования только одного лекарственного препарата. Кроме того, известно решение, в котором полимерные наночастицы на основе поли(ε-капролактона) в качестве гидрофобного сегмента и полиэтиленгликоля в качестве гидрофильного сегмента были загружены куркумином и покрыты цитокином TRAIL путем электростатических взаимодействий (Xi Yang, Zhaojun Li, Qinjie Wu, Shouchun Chen, Cheng Yi, Changyang Gong. Drug Delivery, 2017, 24:1, 1526-1536). Указанное решение имело повышенный противоопухолевый эффект за счет синергичного действия куркумина и TRAIL. Однако, конъюгация таргетного рецептор-специфичного белка с поверхностью наночастиц путем электростатического взаимодействия, в отличие от ковалентной конъюгации, не позволяет добиться высокой стабильности комбинированных наночастиц, а также правильной стерической ориентации всех белковых молекул, необходимой для кластеризации рецепторов и максимального усиления сигнала апоптоза при взаимодействии с рецепторами. Кроме того, использование цитокина TRAIL дикого типа не позволяет избежать рецептор-зависимой резистентности опухолей, поскольку TRAIL способен специфически связываться с пятью рецепторами, из которых три являются рецепторами-«ловушками», не передающими сигнал клеточной гибели. В данному случае использование рецептор-специфичного варианта TRAIL DR5-B, было бы более эффективным, поскольку он преодолевает рецептор-зависимую резистентность опухолевых клеток к TRAIL (RU2620165C2, RU2727059C1) благодаря селективному связыванию лишь с одним из пяти рецепторов TRAIL, рецептором смерти DR5 (Gasparian ME, Chernyak BV, Dolgikh DA, Yagolovich AV et al. Apoptosis, 2009, 14:778-787), играющим ключевую роль в передаче сигнала TRAIL-индуцированного апоптоза.
Задачей настоящего изобретения является создание комбинированных наночастиц с повышенным противоопухолевым действием за счет содержания как минимум двух лекарственных противоопухолевых препаратов различной природы, которые позволяют указанным комбинированным наночастицам обладать синергичным эффектом и специфичностью к рецепторам, гиперэкспрессированным в опухолях. Также задачей изобретения является расширения спектра средств таргетной наноразмерной доставки противоопухолевых препаратов с усиленным действием, улучшенными фармакокинетическими характеристиками и повышенной безопасностью.
Указанные задачи решаются путем создания биосовместимых, биоразлагаемых комбинированных мицеллярных наночастиц, состоящих из амфифильных полимеров на основе N-винилпирролидона, содержащих по меньшей мере два лекарственных противоопухолевых препарата, один из которых находится в ядре, а другой является таргетным рецептор-специфичным веществом пептидной природы, ковалентно конъюгированным с поверхностью наночастиц.
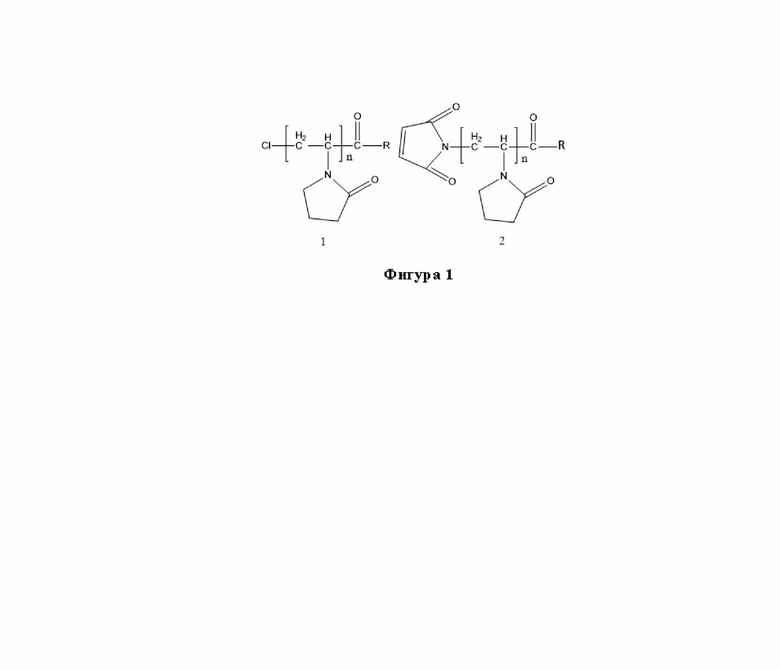
В предпочтительном варианте изобретения комбинированные наночастицы представляют собой мицеллы, состоящие из амфифильных полимеров молекулярной массой от 1 до 30 кДа общей формулы C4H2NO2-(--М--)-(CO)-R и Cl-(--М--)-(CO)-R, в которой (--М--) является гидрофильной частью, состоящей из мономеров N-винилпирролидона, R является гидрофобной частью со структурой -(С8-19-алкил)-СН3, которые содержат в гидрофобном ядре низкомолекулярный противоопухолевый препарат, а таргетное рецептор-специфичное вещество пептидной природы представляет собой рецептор-специфичный вариант цитокина TRAIL DR5-B c последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO 1, при этом содержит замены аминокислотных остатков, способствующие повышению специфичности связывания с рецептором DR5.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является бортезомиб.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является куркумин.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является карфилзомиб.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является паклитаксел.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является доцетаксел.
В других вариантах изобретения противоопухолевым препаратом в ядре комбинированных наночастиц является цисплатин.
В других вариантах таргетное рецептор-специфичное вещество пептидной природы представляет собой рецептор-специфичный вариант цитокина TRAIL DR5-B-iRGD c последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO 2.
При осуществлении изобретения достигается следующий технический результат: созданы новые комбинированные мицеллярные наночастицы, одновременно содержащие в ядре инкапсулированный противоопухолевый препарат, например, бортезомиб, либо куркумин, либо карфилзомиб, либо паклитаксел, либо доцетаксел, либо цисплатин, либо фулвестрант, либо иксабепилон, и конъюгированные на поверхности с DR5-селективным вариантом цитокина TRAIL DR5-B (SEQ ID NO 1) либо TRAIL DR5-B-iRGD (SEQ ID NO 2), что позволяет с повышенной эффективностью уничтожать опухолевые клетки благодаря селективному нацеливанию DR5-B на опухолевые клетки с гиперэкспрессией рецептора DR5, а также синергичному эффекту c противоопухолевым препаратом в гидрофобном ядре наночастиц. Кроме того, технический результат изобретения заключается в стабилизации противоопухолевых препаратов при включении в наночастицы, направленном накоплении в опухолях, контролируемом высвобождении препаратов из гидрофобного ядра, улучшенных фармакокинетических показателях и повышенном терапевтическом эффекте.
Описание чертежей
Фиг. 1. Общая формула полимеров C4H2NO2-(--М--)-(CO)-R и Cl-(--М--)-(CO)-R.
Фиг. 2. Экспрессия и очистка DR5-селективного варианта цитокина TRAIL DR5-B (М =19,6 кДа) в штамме E.coli SHuffle B T7. Электрофорез в 15% полиакриламидном геле. Дорожки: 1 - маркеры молекулярных масс; 2 - 20 мкл ночных культур клеток; 3 - растворимая клеточная фракция; 4 - фракция белков, не связавшихся с Ni-NTA агарозой; 5, 6 - фракции отмывки Ni-NTA агарозы 20 мМ имидазола; 7 - фракция элюции с Ni-NTA агарозы; 8 - фракция после диализа против 150 мМ NaCl; 9 - очищенный белок DR5-B.
Фиг. 3. Экспрессия и очистка DR5-селективного варианта цитокина TRAIL DR5-B-iRGD (М =21,3 кДа) в штамме E.coli SHuffle B T7. Электрофорез в 15% полиакриламидном геле. Дорожки: 1 - маркеры молекулярных масс; 2 - 20 мкл ночных культур клеток; 3 - растворимая клеточная фракция; 4 - фракция белков, не связавшихся с Ni-NTA агарозой; 5, 6 - фракции отмывки Ni-NTA агарозы 20 мМ имидазола; 7 - фракция элюции с Ni-NTA агарозы; 8 - фракция после диализа против 150 мМ NaCl; 9,10 - очищенный белок DR5-B-iRGD.
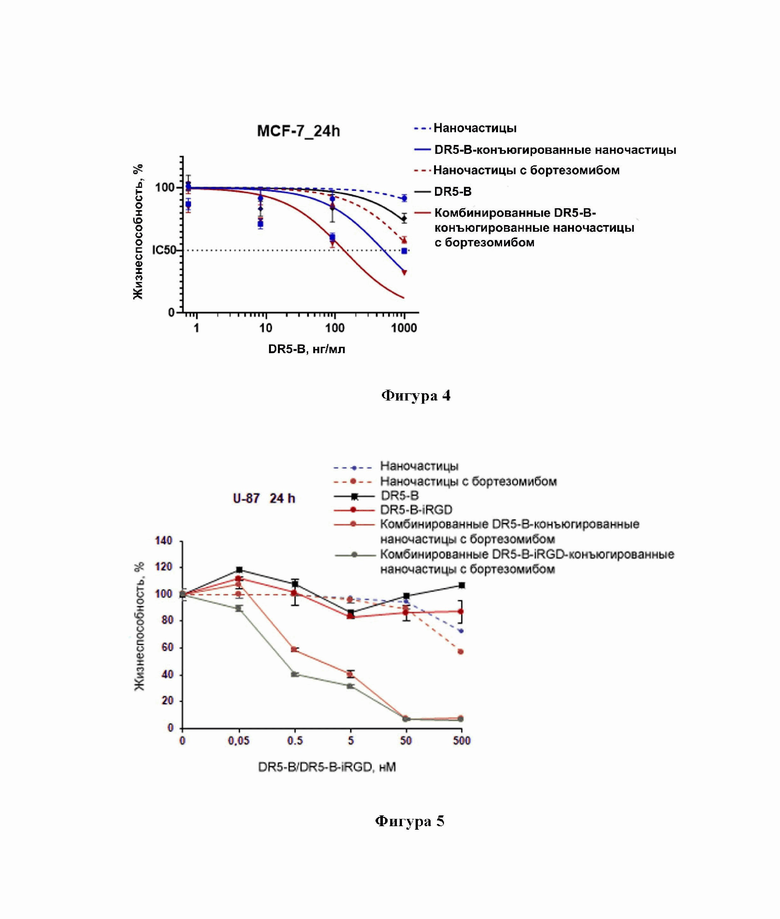
Фиг. 4. Оценка жизнеспособности мультиклеточных 3D-сфероидов из линии клеток MCF-7 под действием свободного белка DR5-B, наночастиц с инкапсулированным бортезомибом, DR5-B-конъюгированных наночастиц без бортезомиба и комбинированных наночастиц.
Фиг. 5. Оценка жизнеспособности клеточной линии U87 под действием свободных белков DR5-B и DR5-B-iRGD, наночастиц с инкапсулированным бортезомибом, и комбинированных DR5-B- либо DR5-B-iRGD-конъюгированных наночастиц с бортезомибом.
Определения и термины
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения.
Термин «амфифильный полимер» означает, что полимер состоит из водорастворимого полимерного и неполимерного алифатического гидрофобного фрагмента.
Рецептором DR5 в настоящем описании называется рецептор смерти, также именуемый TRAIL-R2 либо TNFRSF10B, обозначаемый как O14763-TR10B_HUMAN в базе данных UniProt (https://www.uniprot.org/).
Амфифильный полимер на основе поли-N-винилпирролидона может быть получен путем радикальной полимеризации мономеров в органическом растворителе в присутствии инициатора радикальной полимеризации и регулятора роста длины цепи, при этом в качестве регулятора роста длины цепи применяют длинноцепочечные алифатические хлорангидриды, позволяющие в процессе радикальной гомополимеризации или сополимеризации получить биосовместимый амфифильный гомополимер в одну стадию синтеза, т.е. без дополнительной модификации, что существенно упрощает аппаратурное оформление, сокращает время получения готового амфифильного гомополимера, а также позволяет регулировать среднечисловую молекулярную массу амфифильного гомополимера или сополимера непосредственно в процессе синтеза и получать готовый продукт с высоким выходом.
Модифицированный остатком малеимида (C4H2NO2) амфифильный полимер на основе поли-N-винилпирролидона может быть получен путем взаимодействия малеимид-натрия (C4H2NO2Na) с амфифильным полимером на основе поли-N-винилпирролидона, согласно изобретению, в органическом растворителе (предпочтительно, диоксан или диметилформамид).
Мицеллярные наночастицы из амфифильных полимеров, согласно изобретению, представляют собой наноразмерные частицы, получаемые методом самоассоциации дифильных веществ в водных средах при критической концентрации их мицелообразования (ККМ) или критической концентрации агрегации (ККА) в водных средах с образованием частиц в виде сферических частиц, имеющих размер от 50 до 1500 нм. При этом векторы гидрофобных фрагментов амфифильных молекул полимера обращены внутрь частиц, образуя внутреннее ядро.
Полимерные мицеллярные наночастицы с инкапсулированным в ядре биологически активным веществом бортезомибом, либо куркумином, либо карфилзомибом, либо паклитакселом, либо доцетакселом, либо цисплатином, могут быть получены путем из амфифильных полимеров методом прямого растворения (диспергирования) с последующим диализом и эмульсионным методом (нанопреципитация). Для всех методов амфифильный полимер берут в таких количествах, чтобы в конечном растворе его концентрация была больше критической концентрации агрегации. Включение лекарственного вещества происходит при добавлении в процессе получения наночастиц необходимого количества бортезомиба, либо куркумина, либо карфилзомиба, либо паклитаксела, либо доцетаксела, либо цисплатина. Количество включаемого лекарственного вещества, варьируется от 0.1 до 50 масс. %.
Рецептор-специфичный лиганд пептидной природы, к примеру, DR5-специфичный вариант цитокина TRAIL DR5-B или DR5-B-iRGD iRGD c последовательностями, гомологичными по меньшей мере на 90% последовательностям SEQ ID NO 1 и SEQ ID NO 2, соответственно, может быть получен с использованием векторов для рекомбинантной экспрессии и экспрессирующих клеток-продуцентов, известных специалистам. Выбор промоторов и других регуляторных элементов, а также клеток-продуцентов и экспрессионных штаммов может варьироваться. Возможный вариант воплощения изобретения путем экспрессии рекомбинантного белка DR5-B или DR5-B-iRGD в клетках E.coli описан в патенте №RU2687435C1. Подходящий генетический вектор для экспрессии рекомбинантного рецептор-специфичного белка трансформируется в клетки бактериальных штаммов либо эукариотических линий, предназначенных для экспрессии рекомбинантных белков. Очистка экспрессированного целевого белка осуществляется (но не ограничивается) с помощью стандартных методик, к примеру, аффинной и ионобменной хроматографии.
Конъюгация полимерных мицеллярных наночастиц, содержащих инкапсулированное в ядре биологически активное вещество, например, бортезомиб, либо куркумин, либо карфилзомиб, либо паклитаксел, либо доцетаксел, либо цисплатин, с рецептор-специфичным лигандом пептидной природы, например, DR5-специфичным вариантом цитокина TRAIL DR5-B или DR5-B-iRGD, осуществляется путем клик-химии, а именно с помощью ковалентного связывания аминокислотного остатка цистеина с малеимидными группами на гидрофильных концах молекул полимера в водном растворе.
Биологическая активность комбинированных мицеллярных наночастиц исследуется на моделях опухолей in vitro и in vivo, в частности на мультиклеточных 3D-моделях сфероидов, полученных из опухолевых клеточных линий. В частном случае реализации изобретения описывается способ индукции гибели опухолевых клеток MCF-7, а также U87 с помощью комбинированных наночастиц с инкапсулированным бортезомибом, и конъюгированных с DR5-специфичным вариантом цитокина TRAIL DR5-B либо DR5-B-iRGD, которые демонстрируют повышенный цитотоксический эффект по сравнению со неконъюгированными наночастицами и свободным DR5-В либо DR5-B-iRGD.
Нижеследующие примеры приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Способ синтеза полимера на основе поли-N-винилпирролидона. Амфифильный гомополимер на основе N-винил-2-пирролидона синтезируют в присутствии инициатора радикальной полимеризации азобисизобутилонитрила с использованием хлорангидрида стеариновой кислоты (ПВП-Хаск) в качестве передатчика и одновременно регулятора роста цепи. Смесь мономера ВП, 0,5 % мольн. ХАСК (от ВП), 1 % масс. ДАК и диоксан с соотношением N-винил-2-пирролидона к диоксану 1:2 по объему инкубируют при 70°С в течение 3 часов, после чего содержимое пробирки растворяют в трехкратном объеме дистиллированной воды и диализуют против воды на системе ультрафильтрации Sartorius SARTOFLOW®, Германия. Диализат концентрируют на ротационном испарителе ("Heidilph Hei-Vap Value Digital", Германия) и лиофильно высушивают. Для синтеза малеимид-калия смесь диметоксиэтана, полимера, малеимида и третбутилата калия (с мольным избытком 1,2) перемешивают на магнитной мешалке при температуре 0°С в течение 1 суток, после чего образовавшийся малеимид-калий осаждают в диметиловый эфир. Затем к синтезированному гомополимеру пришивают малеимидную группу путем взаимодействия амфифильного гополимера N-винил-2-пирролидона, содержащего хлор на конце гидрофильной цепи, с малеимид-калием. Синтез полимера, содержащего малеимидную активную группу, проводят на основе диоксана: сухой диоксан, навеску полимера ПВП-ХАСК (0,2033 г) и малеимид-калий (0,005 г) перемешивают на магнитной мешалке при комнатной температуре в течение 1 часа, после чего разбавляют дистиллированной водой в 2 раза и диализуют против воды в течение 3-х суток. Диализат лиофильно высушивают.
Пример 2. Способ инкапсуляции биологически активного вещества в ядро мицеллярных полимерных наночастиц.
Мицеллярные наночастицы получают из смеси 1:1 либо 1:3 модифицированного малеимидом (молекулярной массой 11 кДа) и немодифицированного полимера (молекулярной массой 6 кДа) эмульсионным методом путем совместной гомогенизации под воздействием ультразвука раствора бортезомиба, либо куркумина, либо карфилзомиба, либо паклитаксела, либо доцетаксела, либо цисплатина в хлороформе или дихлорметане и раствора амфифильных полимеров в воде. По окончании гомогенизации хлороформ или дихлорметан удаляют на роторном испарителе. Полученную суспензию мицеллярных частиц с включенным в них бортезомибом, либо куркумином, либо карфилзомибом, либо паклитакселом, либо доцетакселом, либо цисплатином лиофильно высушивают.
Пример 3. Способ получения рекомбинантного DR5-селективного варианта цитокина TRAIL DR5-B c последовательностью, гомологичной по меньшей мере на 90% последовательностям SEQ ID NO 1.
Для последующей ковалентной конъюгации рекомбинантного DR5-специфичного варианта TRAIL DR5-B с мицеллярными наночастицами вводят аминокислотную замену V114С на N-конце полипептидной цепи путем сайт-специфического мутагенеза и получают плазмидный вектор pET32a/dr5-b-v114c. Затем для экспрессии белка плазмидным вектором pET32a/dr5-b-v114c трансформируют компетентные клетки штамма E. coli SHuffle B. Экспрессию белка проводят в среде TB в присутствии 100 мкг/мл ампициллина. Максимальная экспрессия наблюдается при индукции с помощью 0.05 мМ ИПТГ при 28°С в течение 18-20 часов при ротации платформы инкубатора 180 об/мин. Клетки собирают центрифугированием при 5000 g в течение 10 минут при 4°С, отмывают буфером, содержащим 50 мМ фосфата натрия, 300 мМ хлорида натрия (рН 8.0) и хранят при - 80°С. Экспрессию белка в клеточном лизате оценивают с помощью ДСН-ПААГ-электрофореза в 15% геле с окрашиванием краской кумасси бриллиантовый синий R-250. В данном примере уровень экспрессии DR5-селективного варианта цитокина TRAIL DR5-B в 1 литре культуры клеток составляет 340 мг.
Пример 4. Способ очистки рекомбинантного DR5-селективного варианта цитокина TRAIL DR5-B либо DR5-B-iRGD c последовательностями, гомологичными по меньшей мере на 90% последовательностям SEQ ID NO 1 и SEQ ID NO 2, соответственно.
Клетки ресуспендируют в лизис-буфере, содержащем 50 мМ фосфата натрия и 300 мМ хлорида натрия (pH 8.0), и разрушают с помощью установки «French press» (Spectronic Instruments, Inc., США) под давлением 1700 бар. Клеточный лизат центрифугируют при 75000 g при 4°С в течение 40 минут. В вышеописанном примере белок экспрессируется в растворимой форме, что позволяет проводить очистку из цитоплазматической фракции. На первом этапе очистку проводят путем металл-аффинной хроматографии на сорбенте Ni-NTA агарозе. Затем белки диализуют и проводят дополнительную очистку на ионообменном сорбенте SP сефарозе. После очистки белок диализуют против раствора 150 мМ NaCl и стерилизуют через шприцевой фильтр с порами 0,22 мкм с мембраной PVDF. Чистоту полученного рекомбинантного белка анализируют с помощью ДСН-ПААГ-электрофореза в 15% геле с окрашиванием краской кумасси бриллиантовый синий R-250. Чистота препарата в данном примере составляет не менее 98%, Концентрацию белка в очищенном препарате определяют спектрофотометрически при длине волны 280 нм с учетом молярного коэффициента экстинкции 19616 М-1 см-1, определенного по аминокислотной последовательности с помощью программы ProtParam на сервере ExPASy (www.expasy.org). При очистке вышеописанным способом выход очищенного белка составляет 20 мг из 200 мл культуры клеток, при этом препарат проявляет высокую стабильность: при хранении белкового раствора в течение как минимум 6 месяцев не наблюдается ни деградации, ни потери биологической активности.
Пример 5. Способ конъюгации мицеллярных наночастиц, содержащих в ядре инкапсулированный препарат бортезомиб, либо куркумин, либо карфилзомиб, либо паклитаксел, либо доцетаксел, либо цисплатин с рекомбинантным белком DR5-B либо DR5-B-iRGD c последовательностями, гомологичными по меньшей мере на 90% последовательностям SEQ ID NO 1 и SEQ ID NO 2, соответственно.
Конъюгация осуществляется путем клик-химии, а именно с помощью ковалентного связывания аминокислотного остатка цистеина на N-конце полипептидной цепи белка с малеимидными группами на гидрофильных концах молекул полимера в водном растворе. Лиофилизованные наночастицы разводят в растворе 150 мМ NaCl, рН 7.5 в концентрации 5 мг/мл и инкубиуют при комнатной температуре на ночь с раствором белка DR5-B, содержащего аминокислотную замену V114C. Затем реакционную смесь центрифугируют 5 минут при 5000 g и осадок ресуспендируют в растворе 150 мМ NaCl, рН 7.5.
Пример 6. Анализ противоопухолевой активности комбинированных наночастиц, содержащих в ядре инкапсулированный препарат бортезомиб, и ковалентно конъюгированных с рекомбинантным белком DR5-B на поверхности.
Противоопухолевая активность гибридных полимерных мицелл исследуется методом WST-1 теста на мультиклеточных 3D-сфероидах, полученных из линии опухолевых клеток MCF-7. Клеточные сфероиды культивируют в питательной среде DMEM с добавлением 10% фетальной бычьей сыворотки. Далее в культуральную среду добавляют по 10 мкл среды с разведениями исходного DR5-селективного варианта цитокина TRAIL DR5-B, и комбинированных наночастиц в диапазоне от 1 до 1000 нг/мл. После 24 ч инкубации в каждую лунку добавляют по 10 мкл реагента WST-1 и планшеты выдерживают в течение 2 ч при 37°C. Оптическую плотность измеряют с помощью планшетного спектрофотометра при длине волны 450 нм с вычитанием фона при 655 нм. В результате получают значения IC50 2746 нг/мл для свободного белка DR5-B, 1304 нг/мл для наночастиц с инкапсулированным бортезомибом, 75 нг/мл для DR5-B-конъюгированных наночастиц без бортезомиба и 36 нг/мл для комбинированных наночастиц, соответственно, что свидетельствует о повышенной противоопухолевой активности комбинированных наночастиц.
Пример 7. Анализ противоопухолевой активности комбинированных наночастиц, содержащих в ядре инкапсулированный препарат бортезомиб, и ковалентно конъюгированных с рекомбинантным белком DR5-B либо DR5-B-iRGD c последовательностями, гомологичными по меньшей мере на 90% последовательностям SEQ ID NO 1 и SEQ ID NO 2, соответственно, на поверхности.
Противоопухолевая активность гибридных полимерных мицелл исследуется методом WST-1 теста на линии опухолевых клеток глиобластомы человека U87. Клетки культивируют в питательной среде DMEM с добавлением 10% фетальной бычьей сыворотки. Далее в культуральную среду добавляют по 10 мкл среды с разведениями исходного DR5-селективного варианта цитокина TRAIL DR5-B либо DR5-B-iRGD, и комбинированных наночастиц в диапазоне от 0.05 до 500 нМ. После 24 ч инкубации в каждую лунку добавляют по 10 мкл реагента WST-1 и планшеты выдерживают в течение 2 ч при 37°C. Оптическую плотность измеряют с помощью планшетного спектрофотометра при длине волны 450 нм с вычитанием фона при 655 нм. В результате получают значения клеточной гибели до 40% для наночастиц с инкапсулированным бортезомибом, и до 95% для комбинированных DR5-B- либо DR5-B-iRGD-конъюгированных наночастиц c бортезомибом, соответственно, что свидетельствует о повышенной противоопухолевой активности комбинированных наночастиц.
Конкретные подробно описанные примеры экспериментов приведены для иллюстрации настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Указанные комбинированные наночастицы могут использовать в качестве лекарственной формы, предназначенной для лечения солидных онкологических заболеваний, характеризующихся экспрессией рецептора DR5 на поверхности опухолевых клеток. Изобретение позволяет обеспечить повышенный уровень эффективности за счет опухоле-специфичности и усиленному накоплению в опухолевых тканях по сравнению с DR5-специфичным мутантным вариантом противоопухолевого цитокина TRAIL.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="Перечень
последовательностей.xml" softwareName="WIPO Sequence"
softwareVersion="2.1.1" productionDate="2023-07-16">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2023110182/20(021691)</ApplicationNumberText>
<FilingDate>2023-04-20</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>https://www1.fips.ru/registers-doc-view/fips_
servlet </ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2023 110 182</ApplicationNumberText>
<FilingDate>2023-04-20</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">РћРћРћ
"Манебио"</ApplicantName>
<ApplicantNameLatin>LLC Manebio</ApplicantNameLatin>
<InventionTitle languageCode="ru">Комбинированные наночастицы на
основе амфифильных сополимеров N-винилпирролидона для совместной
таргетной доставки лекарственных препаратов </InventionTitle>
<SequenceTotalQuantity>2</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>168</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..168</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Human</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>VRERGPQRVAAHITGTRGRSNTLSSPNSKNEKALGRKINSWESSRSGHS
FLSNLHLRNGELVIHEKGFYYIYSQTNFKFREEIKENTKNDKQMVQYIYKYTSYPDPILLMKSARNSCWS
KDAEYGLYSIYQGGIFELKENDRIFVSVTNERLLDMHHEASFFGAFLVG</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>192</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..192</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q3">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Human</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>VRERGPQRVAAHITGTRGRSNTLSSPNSKNEKALGRKINSWESSRSGHS
FLSNLHLRNGELVIHEKGFYYIYSQTNFKFREEIKENTKNDKQMVQYIYKYTSYPDPILLMKSARNSCWS
KDAEYGLYSIYQGGIFELKENDRIFVSVTNERLLDMHHEASFFGAFLVGGGGGSGGGGSGGGGSCRGDKG
PDC</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Многофункциональные гибридные рекомбинантные белковые препараты для терапии опухолевых заболеваний | 2022 |
|
RU2801367C1 |
| Белковая конструкция на основе рецептор-специфичного мутантного варианта противоопухолевого цитокина TRAIL в виде гибридного белка с пептидом, специфичным к интегрину αvβ3, для терапии солидных опухолей | 2022 |
|
RU2802488C1 |
| СПОСОБ ПОЛУЧЕНИЯ МУТАНТНОГО БЕЛКА TRAIL ЧЕЛОВЕКА | 2009 |
|
RU2405038C1 |
| ВЕКТОРИЗОВАННЫЕ ВОДОСОВМЕСТИМЫЕ ПОЛИМЕРНЫЕ МИЦЕЛЛЯРНЫЕ ЧАСТИЦЫ ДЛЯ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР | 2020 |
|
RU2752177C1 |
| СПОСОБ ИНДУКЦИИ ГИБЕЛИ ОПУХОЛЕВЫХ КЛЕТОК | 2015 |
|
RU2620165C2 |
| Способ получения рекомбинантного противоопухолевого модифицированного белка DR5-B человека | 2018 |
|
RU2687435C1 |
| Способ подавления роста опухолей генно-модифицированным вариантом цитокина TRAIL | 2019 |
|
RU2727059C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИСТЕМЫ ДОСТАВКИ ВОДОНЕРАСТВОРИМЫХ И ПЛОХОРАСТВОРИМЫХ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ И ЛЕКАРСТВЕННАЯ ФОРМА НА ЕЕ ОСНОВЕ | 2006 |
|
RU2325151C2 |
| ВОДОСОВМЕСТИМЫЕ ПОЛИМЕРНЫЕ КОМПОЗИЦИИ ДЛЯ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 2015 |
|
RU2580649C1 |
| КОМБИНАЦИИ АНТИТЕЛ, ОБЛАДАЮЩИХ СЕЛЕКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РЕЦЕПТОРУ ЛИГАНДА, ИНДУЦИРУЮЩЕМУ АПОПТОЗ, АССОЦИИРОВАННЫЙ С ФАКТОРОМ НЕКРОЗА ОПУХОЛИ, И ДРУГИХ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2002 |
|
RU2313368C2 |

Изобретение относится к химии, биотехнологии и фармацевтике, а именно к наночастице для доставки противоопухолевых препаратов. Предложенная наночастица представляет собой мицеллу, состоящую из амфифильных полимеров со среднечисловой молекулярной массой 1-30 кДа общей формулы C4H2NO2-(--М--)-(CO)-R и Cl-(--М--)-(CO)-R, где (--М--) – гидрофильная часть из мономеров N-винилпирролидона, а R – гидрофобная часть со структурой -(С8-19-алкил)-СН3, при этом один из противоопухолевых препаратов является низкомолекулярным и находится в ядре наночастицы, а другой противоопухолевый препарат конъюгирован с поверхностью наночастицы и представляет собой таргетное рецептор-специфичное вещество пептидной природы, которое является вариантом цитокина TRAIL, выбранным из DR5-B c аминокислотной последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO: 1, и DR5-B-iRGD c аминокислотной последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO: 2. Изобретение обеспечивает новые комбинированные мицеллярные наночастицы, характеризующиеся улучшенными фармакокинетическими показателями, повышенным терапевтическим эффектом и контролируемым высвобождением препарата из гидрофобного ядра. 6 з.п. ф-лы, 5 ил., 7 пр.
1. Наночастица для доставки противоопухолевых препаратов, представляющая собой мицеллу, состоящую из амфифильных полимеров, отличающаяся тем, что мицелла состоит из амфифильных полимеров со среднечисловой молекулярной массой 1-30 кДа общей формулы C4H2NO2-(--М--)-(CO)-R и Cl-(--М--)-(CO)-R, в которой (--М--) является гидрофильной частью, состоящей из мономеров N-винилпирролидона, R является гидрофобной частью со структурой -(С8-19-алкил)-СН3, при этом один из противоопухолевых препаратов представляет собой низкомолекулярный противоопухолевый препарат и находится в ядре наночастицы, а другой противоопухолевый препарат конъюгирован с поверхностью наночастицы и представляет собой таргетное рецептор-специфичное вещество пептидной природы, которое является вариантом цитокина TRAIL, выбранным из DR5-B c аминокислотной последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO: 1, и DR5-B-iRGD c аминокислотной последовательностью, гомологичной по меньшей мере на 90% последовательности SEQ ID NO: 2.
2. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является куркумином.
3. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является бортезомибом.
4. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является карфилзомибом.
5. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является цисплатином.
6. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является паклитакселом.
7. Наночастица по п. 1, где низкомолекулярный противоопухолевый препарат, который находится в ядре наночастицы, является доцетакселом.
| ВОДОСОВМЕСТИМЫЕ ПОЛИМЕРНЫЕ КОМПОЗИЦИИ ДЛЯ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 2015 |
|
RU2580649C1 |
| Anne Yagolovich et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Насос | 1917 |
|
SU13A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Коловратный двигатель | 1921 |
|
SU1413A1 |
| Qi Shuai et al | |||
| Cell-Penetrating Peptide Modified PEG-PLA Micelles for Efficient PTX Delivery / | |||
Авторы
Даты
2024-11-22—Публикация
2023-04-20—Подача