Область техники
Настоящее изобретение относится к биологии, химии и биотехнологии, а именно к биолюминесцентной системе червей рода Henlea (H. petushkovi, H. rodionovae).
Уровень техники
Биолюминесценция - процесс излучения света живыми организмами в ходе биохимической реакции, в которой химическая энергия превращается в световую. Способность к биолюминесценции определяется наличием специфического белка люциферазы или фотопротеина. Люциферазы - это ферменты, которые катализируют окисление низкомолекулярных соединений - люциферинов, превращая их в оксилюциферины. Окисление сопровождается выделением света и высвобождением оксилюциферина. Описано несколько типов биолюминесцентных систем.
Например, у ряда морских кишечнополостных описаны системы, включающие белки семейства экворина (Prasher, et al., Biochem. 1987, 26, 1326-1332; Tsuji et al., Photochem Photobiol, 1995, 62(4), 657-661). Семейство экворина (aequorin) включает также обелин (obelin), халистаурин или митрокомин (halistaurin = mitrocomin), фиалидин или клитин (phiallidin = clytin) и т.д. Это фотопротеины, содержащие ковалентно связанный с ними люциферин, который в присутствии ионов Са2+ подвергается химическим превращениям с образованием продукта в возбужденном электронном состоянии.
Для светящихся Henlea sp. недавно были установлены два близкородственных вида: Henlea petushkovi встречаются в окрестностях Красноярска, а Henlea rodionovae обитают в Иркутской области. Эти энхитреиды различаются рядом морфологических и анатомических особенностей (Rota E., et al. Org. Divers. Evol. 2018, 18 (3), 291–312) и имеют биолюминесцентную систему, включающую четыре основных компонента: люциферазу, люциферин, ион кальция и кислород (Петушков ВН, и др. ДАН, 2002, 385 (3), 416-418). Ещё два низкомолекулярных компонента, обладающих флуоресцентными свойствами и способных активировать люминесценцию реакционной смеси in vitro. Предполагается, что именно они, а не люциферин являются эмиттерами в люминесцентной реакции этих червей (Петушков ВН, Родионова НС ДАН, 2018, 481 (4), 451-454).
Компоненты биолюминесцентных систем (люциферазы, фотопротеины, люциферины и т.д.) - широко используемые реагенты для множества анализов, включая диагностические системы, системы контроля качества и т.д. Например, белки семейства экворина широко используются для исследований высвобождения и связывания Са2+ в биологических системах, например, во время мышечного сокращения. Использование биолюминесцентных систем в подробностях описано, например, в Cormier, М.L. et al., Photochem. & Photobiol. 49/4, 509-512 (1989), Smith, D.F. et al. in ′′Bioluminescence and Chemiluminescence: Current Status (P. Stanley & L. Krick, eds.), John Wiley and Sons, Chichester, U.K. 1991, 529-532.
Несмотря на большое количество биолюминесцентных систем, используемых на сегодняшний день, сохраняется потребность в расширении линейки люциферин-люциферазных пар, обладающих новыми свойствами. Расшифровка новых компонентов биолюминесцентных систем позволяет расширить спектр доступных анализов и приложений для использования.
Раскрытие изобретения
Задачей настоящего изобретения является установление компонентов биолюминесцентной системы червей Henlea sp., в частности идентификация молекул кофакторов (активаторов) биолюминесцентной реакции, а также разработка способа выявления биолюминесценции в биологическом образце с помощью компонентов биолюминесцентной системы червей Henlea sp., в частности, кофакторов биолюминесцентной реакции червя Henlea sp.
Технический результат состоит в расширении арсенала технических средств в области применения биолюминесцентных систем и достигается за счет идентификации молекул кофакторов (активаторов) биолюминесцентной реакции Henlea sp. и их применения в качестве компонентов биолюминесцентной реакции, введение которых в люциферин-люциферазную реакцию сопровождается увеличением интенсивности испускаемого света и как результат обеспечивает снижение порога детектируемости люциферазы и биолюминесценции в биологическом образце. Указанные компоненты биолюминесцентной системы червей Henlea sp. являются перспективными для применения в качестве реагентов для множества анализов, включая диагностические системы, системы контроля качества, системы тестирования лекарственных препаратов и т.д.
Настоящее изобретение обеспечивает молекулы, являющиеся компонентами биолюминесцентной реакции Henlea sp, а именно 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат или его таутомера, стереоизомера или энантиомера, фармацевтически приемлемой соли, сольвата или гидрата, характеризующиеся следующей общей формулой I:
 формула I,
формула I,
где R представляет собой водород или сульфогруппу.
Указанный технический результат достигается путем применения соединения 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона и/или его сульфатированного аналога (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата или его таутомера, стереоизомера или энантиомера, фармацевтически приемлемой соли, сольвата или гидрата, характеризующегося следующей общей формулой I:
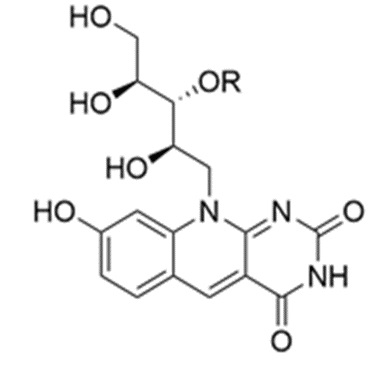 формула I, где R представляет собой водород или сульфогруппу,
формула I, где R представляет собой водород или сульфогруппу,
в качестве в качестве компонента биолюминесцентной реакции, в частности, биолюминесцентной реакции Henlea sp., причем введение которых в люциферин-люциферазную реакцию сопровождается увеличением интенсивности испускаемого света.
Настоящее изобретение также включает набор для детекции люциферазы в биологическом образце, включающий соединение общей формулой I по изобретению в качестве компонента биолюминесцентной реакции.
В частных вариантах воплощения изобретения набор дополнительно включает буфер, детергент, восстановительный агент и/или глицерин.
В частных вариантах воплощения изобретения указанные компоненты набора содержатся в допустимых количествах.
Настоящее изобретение также включает биолюминесцентную композицию, включающую люциферазу, люциферини, по меньшей мере, одно соединение общей формулой I по настоящему изобретению в качестве компонента биолюминесцентной реакции. В частных вариантах воплощения изобретения люцифераза является рекомбинантной. В частных вариантах воплощения изобретения люцифераза представляет собой люциферазу червя Henlea sp. В более конкретных вариантах воплощения изобретения червь представляет собой вид Henlea petushkovi и/или Henlea rodionovae.
Кроме того, настоящее изобретение также обеспечивает способ выявления (детекции) люциферазы в биологическом образце, включающем люциферазу, люциферин и, по меньшей мере, одно соединение по изобретению в качестве компонента биолюминесцентной реакции. В частных вариантах воплощения изобретения люцифераза представляет собой люциферазу червей Henlea sp. В частных вариантах воплощения изобретения люцифераза представляет собой рекомбинантную люциферазу. В частных вариантах воплощения изобретения биологический образец представляет собой ткань и/или клетку. В частных вариантах воплощения изобретения биологический образец характеризуется значением рН в диапазоне от 7 до 8.
В частных вариантах воплощения изобретения способ выявления люциферазы включает следующие этапы:
а) добавление соединения по изобретению к биологическому образцу для получения реакционной смеси;
б) инкубирование реакционной смеси в условиях, подходящих для возникновения биолюминесценции;
в) детектирование биолюминесценции в реакционной смеси.
В частных вариантах воплощения изобретения концентрация соединения общей формулой I по изобретению составляет 0.03-300 мкМ.
Кроме того, обеспечивается способ детекции биолюминесценции в биологическом образце, включающем люциферазу и, по меньше мере, одно соединение по изобретению в качестве компонента биолюминесцентной реакции. В частных вариантах воплощения изобретения люцифераза представляет собой рекомбинантную люциферазу. В частных вариантах воплощения изобретения люцифераза представляет собой люциферазу червя Henlea sp. В более конкретных вариантах воплощения изобретения червь представляет собой вид Henlea petushkovi и/или Henlea rodionovae. В частных вариантах воплощения изобретения биологический образец представляет собой ткань и/или клетку. В частных вариантах воплощения изобретения биологически образец характеризуется значением рН в диапазоне от 7 до 8.
В частных вариантах воплощения изобретения способ детекции биолюминесценции включает следующие этапы:
а) экспрессию гена люциферазы в биологическом образце;
б) добавление люциферина;
в) добавление соединения по изобретению к биологическому образцу;
г) детектирование биолюминесценции.
В частных вариантах воплощения изобретения концентрация соединения по изобретению составляет 0.03-300 мкМ.
Также настоящее изобретение обеспечивает реактивы и наборы реактивов для реализации методов настоящего изобретения.
Настоящее изобретение также включает получение соединений по изобретению.
Для более полного раскрытия вышеперечисленных характеристик настоящего изобретения ниже предлагается детальное описание изобретения, кратко сформулированного выше, в виде ссылок на воплощения, некоторые из которых проиллюстрированы дополнительными фигурами. При этом следует отметить, что прилагаемые фигуры иллюстрируют лишь типичные воплощения настоящего изобретения и, следовательно, не должны быть восприняты в качестве ограничения объема изобретения, которое может допускать другие, в равной степени эффективные, воплощения.
Подробное раскрытие изобретения
Краткое описание чертежей
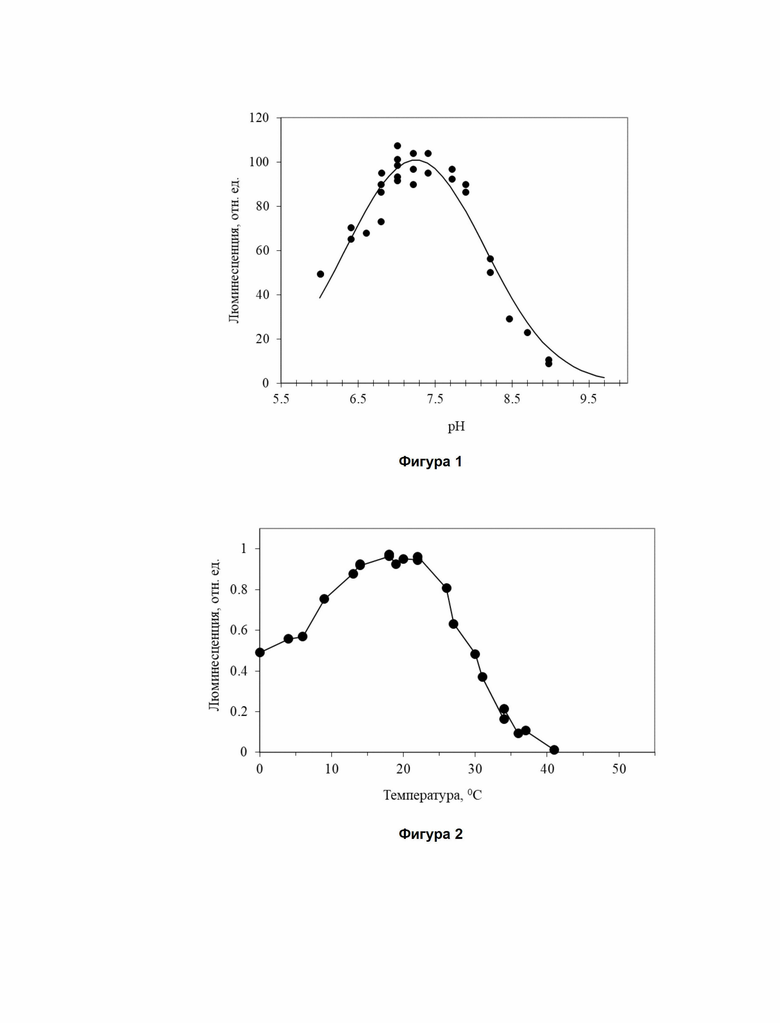
Фиг. 1. pH-зависимость интенсивности биолюминесцентной реакции энхитреид Henlea sp. in vitro. Реакционная смесь 20мМ бис-трис-пропанового буфера, 10 мкл препарата люциферазы, 2 мкл препарата люциферина, 4мкл 0.1М Са2+.
Фиг. 2. Температурная зависимость интенсивности биолюминесцентной реакции энхитреид Henlea sp. in vitro. Реакционная смесь 180 мкл 20мМ трис-HCl буфера pH 7.25, 10 мкл препарата люциферазы, 2 мкл препарата люциферина, 4мкл 0.1М Са2+.
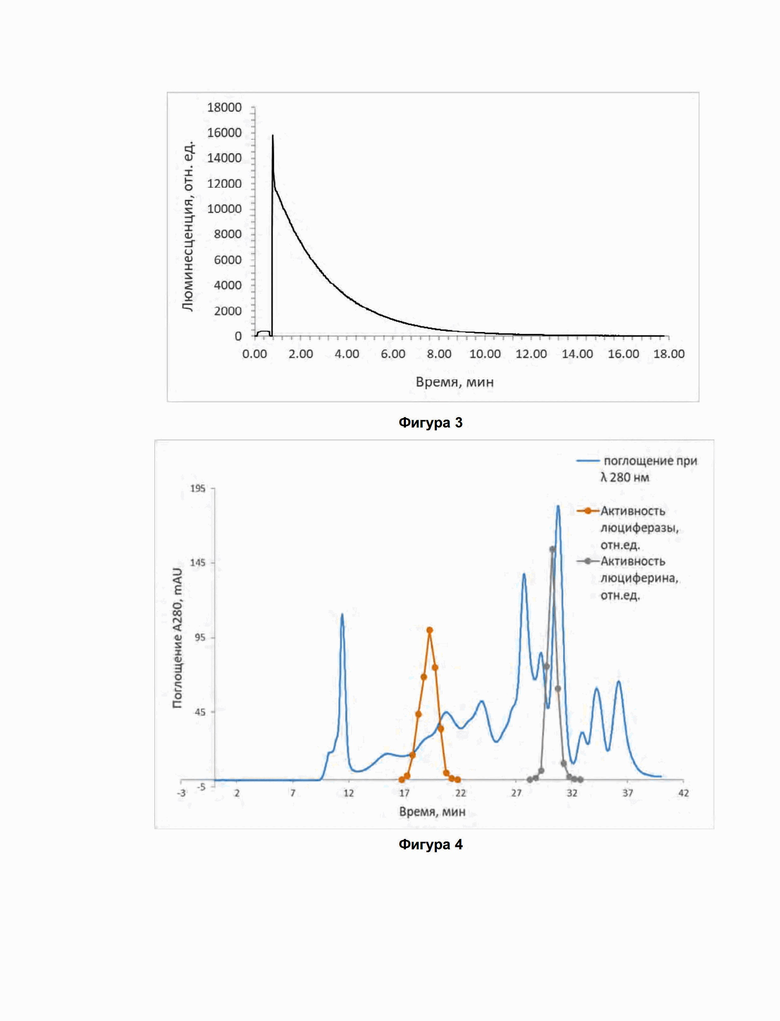
Фиг. 3. Результат измерения биолюминесценции червей Henlea sp. во времени.
Фиг. 4. Хроматографический профиль бесклеточного экстракта червей H. petushkovi и H. rodionovae на основании результатов гель-фильтрации на колонке Superdex 200 10/300 GL (“GE HealthCare”, США). Сплошная линия - сигнал поглощения при длине волны 280 нм. Профили активности люциферазы и люциферина червей H. petushkovi и H. rodionovae в отн. ед. люминесценции.
Фиг. 5. УФ-спектры поглощения пиков компонентов (активаторов по изобретению) биолюминесцентной реакции, схожих с люциферином Henlea по спектральным и хроматографическим свойствам.
Фиг. 6. Флуоресценция компонента ActH.
Фиг. 7. Спектры возбуждения компонента ActH (а), его эмиссии (б) и биолюминесценции Henlea sp. in vivo (в).
Фиг. 8. Структуры компонентов биолюминесцентной системы червей Henlea sp., выделенных из биомассы, установленные с использованием методов ЯМР-спектроскопии и ВЭЖХ-МС.
Фиг. 9. Типичный результат выявления люциферазы в биологических образцах. Динаминка люминесценции реакционной смеси 100 мкл 16мМ МОПС (pH 7.0) и 1 мМ CaCl2, содержащей 2 мкл термоактивированного люциферина и 5 мкл белкового препарата (люциферазная фракция). Наблюдаемая вспышка в ответ на добавление 1 мкл 0.1мМ ActH (30 сек).
Фиг. 10. Зависимость интенсивности биолюминесценции от количества 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона.
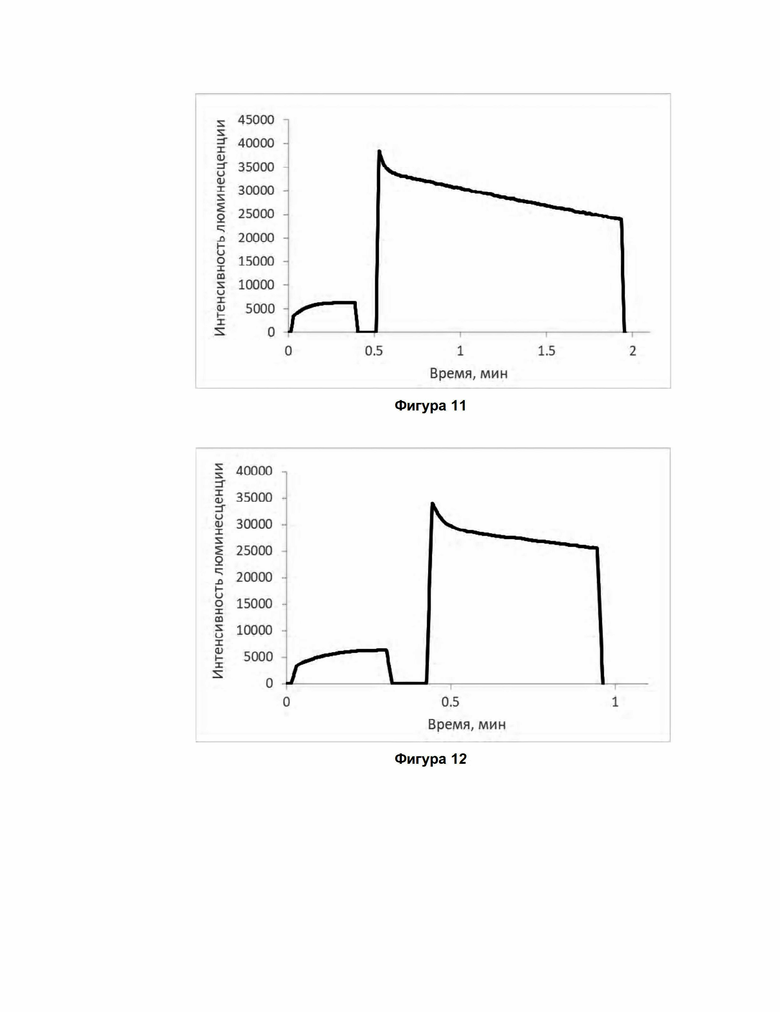
Фиг. 11. Типичный результат детекции биолюминесценции в биологических образцах. Динаминка люминесценции реакционной смеси 100 мкл 16мМ МОПС (pH 7.0) и 1 мМ CaCl2, содержащей 2 мкл высокоочищенного люциферина Henlea sp. и 2 мкл бесклеточного экстракта (люциферазная фракция). Наблюдаемая вспышка в ответ на добавление 1 мкл 0.1мМ ActH (31 сек).
Фиг. 12. Типичный результат выявления люциферазы в биологических образцах. Динаминка люминесценции реакционной смеси 100 мкл 16мМ МОПС (pH 7.0) и 1 мМ CaCl2, содержащей 2 мкл термоактивированного люциферина и 5 мкл белкового препарата (люциферазная фракция). Наблюдаемая вспышка в ответ на добавление 1 мкл 0.1мМ ActS (27 сек).
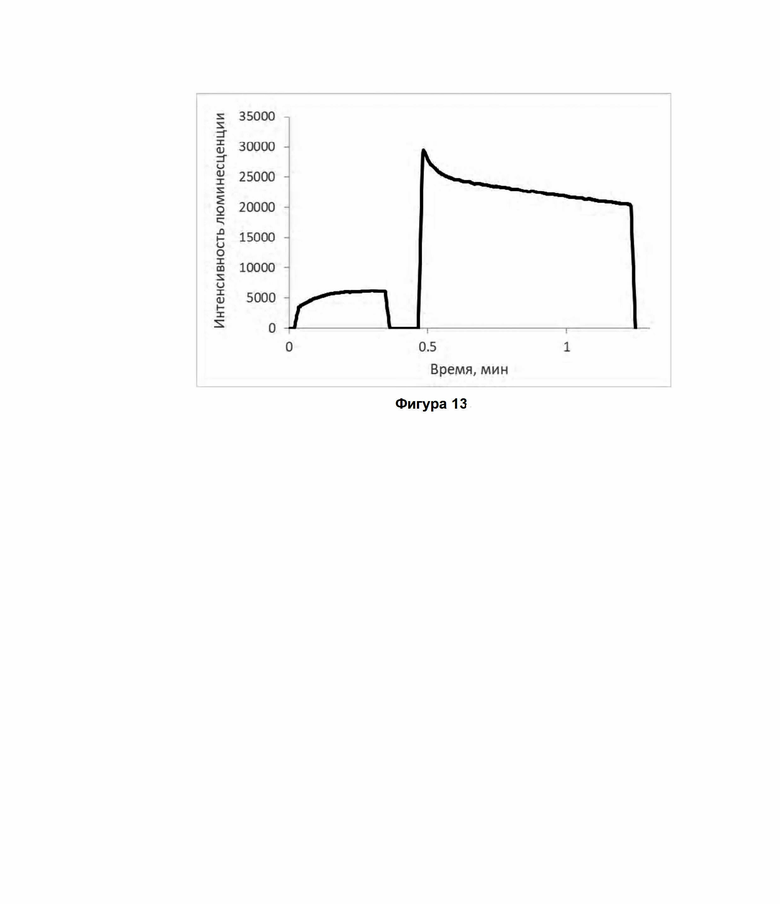
Фиг. 13. Типичный результат детекции биолюминесценции в биологических образцах. Динаминка люминесценции реакционной смеси 100 мкл 16мМ МОПС (pH 7.0) и 1 мМ CaCl2, содержащей 2 мкл высокоочищенного люциферина Henlea sp. и 2 мкл бесклеточного экстракта (люциферазная фракция). Наблюдаемая вспышка в ответ на добавление 1 мкл 0.1мМ ActS (28 сек).
Определения и термины
Различные термины, относящиеся к объектам настоящего изобретения, используются выше и также в описании и в формуле изобретения. Если иное не оговаривается, все технические и научные термины, используемые в данной заявке, имеют то же самое значение, которое понятно для специалистов в данной области. Ссылки на методики, используемые при описании данного изобретения, относятся к хорошо известным методам, включая изменения этих методов и замену их эквивалентными методами, известными специалистам.
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Термин «биолюминесценция» или «люминесценция» в настоящем документе означает процесс излучения света, получаемый в результате реакции между ферментом и субстратом, который генерирует свет.
Термин «предшественник люциферина (предлюциферин)» в настоящем документе означает соединение, способное превращаться в люциферин самопроизвольно или под действием ферментов.
Термин «люциферин» в настоящем документе означает соединение, являющееся субстратом для ферментов люцифераз.
Как здесь используется, термин «люцифераза» означает белок, который обладает способностью к окислению люциферина, где реакция окисления сопровождается выделением света (люминесценцией) и происходит освобождение окисленного люциферина.
«Реакционная смесь люциферазы» содержит фермент люциферазу и материалы, которые позволят ферменту люциферазе генерировать световой сигнал. Необходимые материалы и конкретные концентрации и/или количества материалов, необходимых для генерации люминесцентного сигнала, варьируются в зависимости от используемого фермента люциферазы, а также от типа выполняемого анализа на основе люциферазы. Как правило, для люциферазы червя Henlea sp., эти материалы могут включать: буфер для поддержания реакции при правильном pH, фермент люцифераза червя Henlea sp. или рекомбинантную люциферазу, и люциферин. Часто к раствору могут добавляться другие материалы, в том числе: бычий сывороточный альбумин (BSA), чтобы поддерживать активность люциферазы, восстановители, детергенты, соли, глицерин, аминокислоты, например D-цистеин и др. Типичная реакционная смесь люциферазы может содержать люциферазу червя Henlea sp., 50 мМ MOPS буфер рН 7.0, 5% глицерин.
«Смесь для обнаружения люциферазы» содержит материалы, которые позволят обнаружить фермент люциферазу. Необходимые материалы и конкретные концентрации и/или количества материалов, необходимых для генерации люминесцентного сигнала, могут варьируются в зависимости от используемого фермента люциферазы, а также от типа выполняемого анализа на основе люциферазы. В общем, для люциферазы червя Henlea sp. или рекомбинантной люциферазы эти материалы могут включать в себя: восстановители, детергенты, соли, в частности, хлорид натрия, ацетат натрия, цитрат натрия, глицерин, аминокислоты, субстрат люциферазы - люциферин. Часто к раствору могут добавляться другие материалы, в том числе: буфер для поддержания реакции при правильном pH, бычий сывороточный альбумин (BSA), чтобы поддерживать активность люциферазы, восстановители, детергенты, соли, глицерин, аминокислоты, например D-цистеин и т. д. Типичная смесь для обнаружения люциферазы может содержать субстрат люциферазы - люциферин червя Henlea sp., 50 мМ MOPS буфер рН 7.0.
Как здесь используется, термин "выделенный" означает молекулу или клетку, которые находятся в среде, отличной от среды, в которой молекула или клетка находятся в естественных условиях. Например, указанные компоненты могут находиться по существу в очищенной форме. По существу, очищенная форма означает, что белки являются, по меньшей мере, приблизительно на 20% чистыми, часто, по меньшей мере, на 30% чистыми, обычно на 50% чистыми, или, по меньшей мере, на 90% чистыми.
Для выделения белков могут быть использованы любые общеизвестные и общепринятые методики очистки белка, описанные, например, в Guide to Protein Purification, (Deuthser ed.) (Academic Press, 1990). Например, из исходного источника может быть приготовлен лизат или холодный экстракт и очищен с использованием ВЭЖХ, эксклюзионной хроматографии, гель-электрофореза, аффинной хроматографии и т.п. Белковые препараты могут быть протестированы на наличие активной люциферазы или комплекса люциферазы и люциферина с помощью методов настоящего изобретения.
Как здесь используется, термин "мутант" или "производное" относятся к белку (в частности, к люциферазе), раскрытому в настоящем изобретении, в котором одна или более аминокислот добавлены и/или замещены и/или удалены (делетированы) и/или вставлены (инсертированы) в N-конец и/или С-конец, и/или в пределах нативных аминокислотных последовательностей белков настоящего изобретения. Как здесь используется, термин "мутант" относится к молекуле нуклеиновой кислоты, которая кодирует мутантный белок. Кроме того, термин "мутант" здесь относится к любому варианту, который короче или длиннее белка или нуклеиновой кислоты.
Модификации, а также добавки или делеции могут быть встроены любым методом, известным в данной области (см., например, Gustin et al., Biotechniques (1992) 14: 22; Barany, Gene (1985) 37: 11-123; и Colicelli et al., Mol. Gen. Genet. (1985) 199:537-539), Sambrook et al., Molecular Cloning: A Laboratory Manual, (1989), CSH Press, pp. 15.3-15.108), включая ошибочно-направленную ПЦР, перестановку, сайт-направленный мутагенез с использованием олигонуклеотидов, мутагенез с использованием ПЦР на основе спаренных молекул, мутагенез in vivo, кассетный мутагенез, рекурсивный согласованный мутагенез, экспоненциальный согласованный мутагенез, сайт-направленный мутагенез, случайный мутагенез, генную повторную сборку, генный сайт-насыщенный мутагенез (GSSM), повторную сборку при проведении синтеза лигированием (SLR), или их сочетание. Указанные модификации, добавления или делеции могут быть также встроены способом, включающим рекомбинацию, рекурсивную рекомбинацию последовательности, мутагенез ДНК путем фосфотиоатной модификации, мутагенез на основе включения матрицы, содержащей урацил, мутагенез на основе дуплекса, содержащего бреши, репарационный мутагенез с точечными ошибочными спариваниями, мутагенез с использованием штамма-хозяина, дефицитного по репарации, химический мутагенез, радиогенный мутагенез, делеционный мутагенез, мутагенез с использованием ограничения по селекции, мутагенез с использованием ограничения по очистке, искусственный синтез гена, согласованный мутагенез, создание химерного мультимера нуклеиновой кислоты или их сочетание.
Как здесь используется, термин "функциональный" означает, что нуклеотидная или аминокислотная последовательность может функционировать для указанного испытания или задачи. Термин "функциональный", используемый для описания люцифераз, означает, что белок обладает способностью производить сопровождающуюся люминесценцией реакцию окисления люциферина.
Как здесь используется, термин «кофактор» («активатор») означает органическое или неорганическое низкомолекулярное соединение непептидной природы, которое необходимо для проявления или модулирования активности фермента.
Биологические образцы
Реализация методов настоящего изобретения обеспечивает возникновение люминесценции реакционной смеси, содержащей биологический образец, если указанный образец содержит люциферазу, использующую в качестве субстрата люциферин и в качестве компонента биолюминесцентной реакции соединение 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат. Такую люциферазу содержат, например, способные к биолюминесценции морские энхитреиды Henlea sp.
Биологические образцы могут быть получены с помощью различных технологий, известных в биологии, и включают образцы тканей, клеток, экстракты, гомогенаты, белковые смеси различной степени очистки и т.д. Например, биологические образцы могут быть получены из энхитреид Henlea sp.
Биологические образцы могут также содержать выделенные компоненты (люциферазу или люциферазу и люциферин или предлюциферин) биолюмнесцентных систем энхитреид Henlea sp.
Биологические образцы могут также экспрессировать рекомбинантную люциферазу или её функциональные мутанты. Последовательности нуклеиновых кислот для экспрессии указанных белков могут быть получены из природных источников (например, из энхитреид Henlea sp.) или синтезированы. В настоящее время известно множество методов для клонирования генов, кодирующих белки, обладающие известной активностью. Частично такие методы описаны в Maniatis, T., et al. (Molecular Cloning--A Laboratory Manual Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y. 1982) и Newman и Campagnoni (Neuromethods, v. 16, 1990, pp. 13-48). Например, может быть приготовлена экспрессионная библиотека в подходящих клетках-хозяевах и протестирована на активность люциферазы. Или может быть осуществлено выделение белка из холодного экстракта, определена его частичная аминокислотная последовательность и осуществлено клонирование соответствующей кДНК из образца кДНК из энхитреид Henlea sp. Последовательности нуклеиновых кислот должны быть встроены в кассету экспрессии. Кассета экспрессии может существовать как внехромосомный элемент или может быть включена в геном клетки в результате введения указанной кассеты экспрессии в клетку. В кассете экспрессии нуклеиновая кислота, кодирующая белок, является функционально связанной с регуляторной последовательностью, которая может включить промоторы, энхансеры, терминаторы, операторы, репрессоры и индукторы. После введения кассеты экспрессии в клетку в ней может образовываться функциональный белок. Системы экспрессии включают, например, бактериальные системы, дрожжевые клетки, насекомых, рыб, земноводных или клетки млекопитающих. Методы изготовления кассет экспрессии или систем для экспрессии желаемого продукта известны специалистам, квалифицированным в данной области. Клеточные линии, которые устойчиво экспрессируют люциферазу могут быть выбраны способами, известными в данной области (например, ко-трансфекция с селектируемым маркером, таким как dhfr, gpt, неомицин, гигромицин, что делает возможным выявление и выделение трансфицированных клеток, которые содержат ген, включенный в геном). Вышеописанные системы экспрессии могут использоваться в прокариотических или эукариотических хозяевах. Для получения белка могут использоваться клетки-хозяева, такие как Е. coli, В. subtilis, S. cerevisiae, клетки насекомого в комбинации с бакуловирусными векторами, или клетки высшего организма, такого как позвоночные, например, COS 7 клетки, НЕК 293, СНО, ооциты Xenopus и т.д.
Могут быть также экспрессированы функциональные мутанты природных белков. Как используется в настоящем описании, термин «функциональный» по отношению к люциферазе означает, что указанный белок способен использовать люциферин Henlea sp. в качестве субстрата биолюминесцентной реакции и 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат в качестве кофакторов реакции биолюминесценции.
Реактивы для детекции биолюминесценции
Методы настоящего изобретения основаны на применении 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона и/или его сульфатированного аналога (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата или его таутомера, стереоизомера или энантиомера, фармацевтически приемлемой соли, сольвата или гидрата в качестве компонента биолюминесцентной реакции, в частности для детекции биолюминесценции в биологических образцах.
Как используется в настоящем описании, 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат или его таутомер, стереоизомер или энантиомер, фармацевтически приемлемая соль, сольват или гидрат, имеющие следующую структурную формулу:
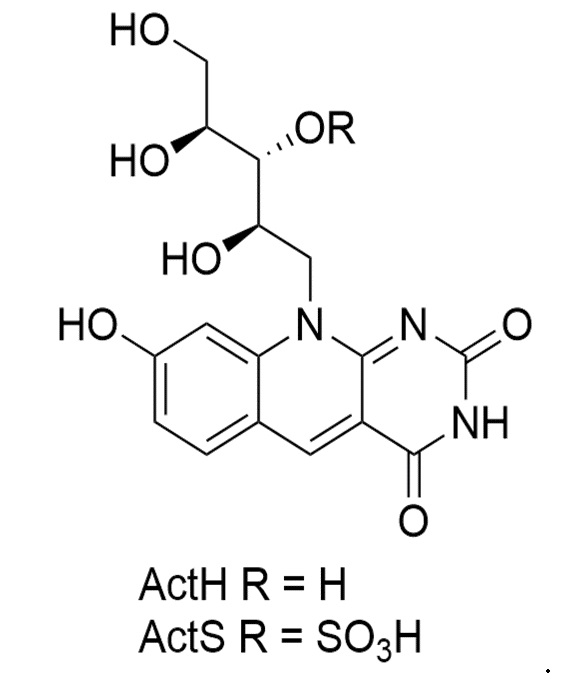
Основу молекулы кофакторов биолюминесцентной реакции червя Henlea sp. составляет конденсированный гетероцикл - 5-деазафлавин, состоящий из двух шестичленных азотсодержащих циклов и одного бензольного цикла. Анализ спектров поглощения активатора H (ActH) и исследование литературных данных показало, что ActH является 5-деаза-8-гидрокси аналогом рибофлавина, называемого кофермент FO. Кофактор FO участвует в окислительно-восстановительных реакциях у продуцентов метана и в депротонированной форме является коферментом ДНК-фотолиаз, найденных у прокариот, некоторых эукариот и архей (Glasa A. F. et al. PNAS, 2009, 106 (28), 11540-11545). Лиофильно высушенные активаторы по изобретению хранятся при -20°С без снижения активности не менее 30 дней, чаще не менее 60 дней, обычно не менее года.
Состав условий для развития биолюминесцентного сигнала
Формирование биолюминесценции зависит от количества и сохранности люциферазы в биологических образцах. Также следует отметить воздействие светового излучения, особенно УФ части спектра, на люциферин, приводящее к его деградации и утрате функциональности, что было подтверждено экспериментально.
Изменение скорости реакции люциферазы Henlea sp. от pH и температуры в каждом случае выражается колоколообразной кривой с одним максимумом (фиг. 1 и 2). Сделана аппроксимация экспериментальных зависимостей нормальных распределений с параметрами pHопт и стандартным отклонением распределения σ. pH варьировали 20мМ бис-трис-пропановым буфером при постоянных количествах люциферазы, люциферина и других компонентов в оптимальных концентрациях. pHопт для Henlea sp. - 7.25 при σ = 0.9. Интервал значений pH для оптимальной скорости реакции Henlea sp. достаточно широк.
Температурный оптимум Henlea sp. равен 20°С. При этом стоит отметить, что, хотя люцифераза Henlea sp. чувствительна к повышению температуры после оптимума, инактивация фермента является полностью обратимой при кратковременном нагревании. Например, при снижении люминесценции на 90% при 37°С быстрый возврат к Tопт восстанавливает люминесценцию до максимального уровня.
Для обеспечения рН могут быть использованы любые стандартные буферные растворы для данного диапазона рН, включая MOPS, HEPES, Трис-HCl, Бис-Трис-пропан. В преимущественных воплощениях молярность буферного раствора не превышает 2, например, не превышает 1, чаще находится в диапазоне от 0.05 до 0.4, обычно от 0.1 до 0.2.
Реакционные смеси для нужд настоящего изобретения могут также содержать компоненты, стабилизирующие и защищающие ферменты биолюминесцентной системы от ингибирующего воздействия следовых количеств ионов тяжелых металлов и от деградации протеазами.
Например, реакционная смесь может содержать дитиотреитол (далее - ДТТ) в концентрации не более 20 мМ, чаще в концентрации от 0.1 до 8 мМ, преимущественно в концентрации 0.1-4 мМ.
Реакционная смесь может также содержать бета-меркаптоэтанол и/или этилендиаминтетрауксусную кислоту (далее – ЭДТА) в конечной концентрации от 0 до 1 мМ.
Например, реакционная смесь может содержать 0.1-2 мМ ДТТ и 0.1-1 мМ ЭДТА.
Также реакционная смесь может содержать ингибиторы протеаз, например, фенилуксусную кислоту или щавелевую кислоту в стандартно используемых концентрациях.
Для нужд настоящего изобретения 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат добавляют к биологическому образцу до конечной концентрации 0.03-300 мкМ, чаще 1-5 мкМ.
В некоторых вариантах воплощения изобретения к образцу добавляют смесь реагентов, включающих буферный раствор, компоненты, стабилизирующие и защищающие ферменты биолюминесцентной системы от ингибирующего воздействия следовых количеств ионов тяжелых металлов и от деградации протеазами, люциферин. В других воплощениях к биологическому образцу сперва добавляют буферный раствор, компоненты, стабилизирующие и защищающие ферменты биолюминесцентной системы от ингибирующего воздействия следовых количеств ионов тяжелых металлов и от деградации протеазами, люциферин, а затем раствор 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона и/или его сульфатированного аналога (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата.
В зависимости от растворителя, использованного для приготовления раствора кофактора (активатора) по изобретению, реакционная смесь может содержать небольшие количества использованных растворителей.
Также реакционная смесь может содержать детергенты, такие как Triton X100 или нонилфеноксиполиэтоксиэтанол. В некоторых вариантах воплощения изобретения концентрация детергентов в реакционной смеси не превышает 0,2%, чаще не превышает 0,1%, оптимально не превышает 0,06%.
Также реакционная смесь может содержать бычий сывороточный альбумин (БСА) или другие белки в концентрации, не превышающей 2%, чаще не превышающей 1%, оптимально не превышающей 0,5%. БСА используется, когда концентрация биологического образца крайне мала, тогда БСА играет роль стабилизатора белков.
Развитие биолюминесцентного сигнала происходит в широком диапазоне температур - от 4 до 40°С, оптимально при 20°С.
Формирование люминесцентного сигнала начинается сразу после инициации реакции при добавлении ключевых реактивов для выявления активности люциферазы, указанных выше.
Максимальная интенсивность люминесценции наблюдается в момент инициации реакции. Далее идет спад, скорость которого определяется активностью ферментов и начальными концентрациями субстратов. При определенных условиях (субстратов много, активность ферментов мала, температура реакции снижена) реакция может наблюдаться в течение одного и более часов (фиг. 3).
Детекция биолюминесценции
Методы настоящего изобретения включают детекцию биолюминесценции, возникающей в биологическом образце, содержащем люциферазу и люциферин при появлении в нем активаторов по изобретению.
Биолюминесценция может быть обнаружена с помощью методов, известных специалистам в данной области, в частности, с помощью визуального скрининга или с использованием люминометра, фотометра, флуориметра, цифровой фотокамеры, с помощью светочувствительной фотопленки. В качестве количественной характеристики может быть использована максимальная интенсивность люминесценции, которая достигается через 5-30 мин после инициации биолюминесцентной реакции или скорость нарастания люминесценции в интервале до 30 мин после инициации биолюминесцентной реакции, например, в течение 1, 2, 5, 10, 20 мин после инициации реакции или дольше.
В преимущественных воплощениях измеряемая люминесценция представляет собой длительное свечение, скорее, чем световые вспышки. В преимущественных воплощениях интенсивность люминесценции зависит от активности ферментов биолюминесцентной системы, присутствующих в образце, начальных концентраций субстратов и температуры реакционной смеси и обычно колеблется в пределах от 10 кв/сек до 10 млн кв/сек, чаще 100 - 100000 кв/сек.
Реакция длится не менее 5 мин после инициации, чаще 10-15 мин, иногда (в зависимости от условий) 30 и более минут.
Испускаемый при окислении люциферина, при участии по меньшей мере, одного соединения согласно настоящему изобретению и/или его функционального аналога свет находится в диапазоне от 430 до 500 нм, чаще в диапазоне от 450 до 475 нм, с максимумом эмиссии при 464 нм.
Способы применения
Методы и реактивы настоящего изобретения могут быть использованы в широком спектре биолюминесцентных анализов in vivo и in vitro.
В частности, методы и реактивы настоящего изобретения могут быть использованы для выявления активных компонентов биолюминесцентных системы энхитреид Henlea sp. в процессе их очистки.
Также методы и реактивы настоящего изобретения могут быть использованы для выявления функциональных аналогов ферментов биолюминесцентной системы энхитреид Henlea sp. в биологических образцах.
Также методы и реактивы настоящего изобретения могут быть использованы для выявления активности рекомбинантной люциферазы в клетках-хозяевах.
В некоторых вариантах воплощения изобретения для осуществления применения должна быть получена нуклеиновая кислота, кодирующая люциферазу. Полученная нуклеиновая кислота должна быть встроена в кассету экспрессии, обеспечивающую временную или постоянную экспрессию этой нуклеиновой кислоты в клетках-хозяевах, например под интересующими исследователя промоторами. Кассета экспрессии может содержать элементы, обеспечивающие адресную доставку конструкции в интересующие клетки или клеточные компартменты, или находится в составе частиц, обеспечивающих адресную доставку. После трансфекции клеток кассетой экспрессии (например, в составе экспрессионного вектора) и по истечении времени, необходимого для наработки в клетках продукта экспрессии, может быть осуществлено выявление активности люциферазы внутри клеток или в клеточном лизате.
Наборы
Также обеспечиваются в соответствии с настоящим изобретением наборы для использования при осуществлении вышеописанных применений.
В некоторых воплощениях наборы обычно включают. По меньшей мере, одно соединение по изобретению, предпочтительно с буферным раствором для растворения указанного соединения и/или его добавления к биологическим образцам. Соединения по изобретению могут присутствовать в растворенном виде в соответствующей среде для хранения, такой как водный или буферный раствор с детергентом, обычно в соответствующей емкости. Альтернативно, соединения по изобретению могут присутствовать в наборе в лиофилизованном виде.
В дополнение к описанным выше компонентам, заявленные наборы могут дополнительно включать инструкции для осуществления заявленных способов. Эти инструкции могут присутствовать в заявленных наборах в различных формах (например, в печатном варианте или на электронном носителе в виде текстового и/или графического файла) в количестве одна или более.
Биолюминисцентные композиции
Также обеспечиваются в соответствии с настоящим изобретением биолюминисцентные композиции для использования при осуществлении вышеописанных применений.
В некоторых воплощениях композиции обычно включают, по меньшей мере, одно соединение по изоретению, предпочтительно с буферным раствором для растворения указанного соединения и/или его добавления к биологическим образцам. Соединения по изобретению могут присутствовать в растворенном виде в соответствующей среде для хранения, такой как водный или буферный раствор с детергентом. Альтернативно, соединения по изобретению могут присутствовать в композиции в лиофилизованном виде.
В некоторых воплощениях композиции обычно включают 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат, предпочтительно с буферным раствором для растворения указанного соединения и/или его добавления к биологическим образцам. 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат может присутствовать в растворенном виде в соответствующей среде для хранения, такой как водный или буферный раствор с детергентом. Альтернативно, 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион и/или его сульфатированный аналог (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат может присутствовать в композиции в лиофилизованном виде.
В дополнение к описанным выше компонентам, заявленные композиции могут дополнительно включать вспомогательные вещества, в частности, адъюванты, растворители и/или наполнители, такие, которые совместимы с соединениями, составляющими суть данного изобретения, и которые не разрушают биологической активности этих соединений.
Следующие примеры предлагаются в качестве иллюстративных, но не ограничивающих.
Примеры
Получение бесклеточных экстрактов червей Henlea sp.
Выбранных из почвы червей H. petushkovi и H. rodionovae промывали и замораживали, накапливая порциями по 1000 особей для экспериментов. Для приготовления бесклеточных экстрактов использовали водные гомогенаты замороженных червей (1 г/5 мл, H2O, 0°C). Клетки дополнительно разрушали ультразвуком в течение 10 мин на ледяной бане, применяя дезинтегратор Sonics Vibra-Cell (“Sonics & Materials, Inc.”, США, диаметр зонда 13 мм, амплитуда 60 мкм). Полученные лизаты центрифугировали при 4°C (центрифуга XPN‑100 с угловым ротором Ti 50.2, “Beckman Coulter”, США, 140 000 g, 5 мин). Супернатант отделяли и использовали для дальнейшего хроматографирования.
Пробу 1-40 мкл супернатанта помещали в кювету люменометра, доводили до 200 мкл 20мМ Трис-HCl pH 7.0. Люминесцентную реакцию инициировали добавлением фракции люциферина 1-4 мкл. Полученный бесклеточный супернатант изначально содержал все компоненты люминесцентной системы Henlea sp. и светился в течение 20–60 мин, постепенно угасая. Полагая, что при этом происходит полное ферментативное “выжигание” люциферина, для воспроизведения люминесцентного сигнала in vitro добавляли свежий люцифериновый экстракт.
Очистка проб образцов нативной люциферазы
На колонку Superdex 200 10/300 GL (“GE HealthCare”, США) в каждом случае наносили 100 мкл супернатанта. Гель-фильтрацию проводили в 10 мМ фосфатном буфере (pH 7.0), содержащем 100 мМ NaCl, со скоростью 0.7 мл/мин при комнатной температуре. Колонку калибровали, используя вещества с известной молекулярной массой: ферритин, альдолаза, каталаза, бычий сывороточный альбумин, овальбумин, миоглобин, рибонуклеаза, цитохром c, рибофлавин. Для определения пиков с люциферазной активностью полученные фракции тестировали в реакциях с высокоочищенным препаратом нативного люциферина энхитреид Henlea sp. Для тестирования активности люциферазы брали по 5 мкл фракции и по 2 мкл люциферина (фиг. 4).
Порядок экстракции люциферина
Люциферин получали из гомогената червей с помощью органических растворителей, таких как ацетон, спирт, этилацетат (при этом люцифераза вместе с другими белками выпадала в осадок). 0.5 мл охлажденного ацетона добавляли к 5-10 замороженным червям, гомогенизировали, выдерживали в течение 60 минут при 0°С, затем центрифугировали (16000 g, 3 мин). Полученный супернатант не обладает люминесцентной активностью, однако добавление его к белковому препарату приводило к испусканию света. Люциферин-содержащую фракцию хранят в темноте при -20°С во избежание инактивации. Вспышку света при добавлении действительно наблюдали, однако раз от раза эффект стимуляции снижался по причине быстрого инактивирования люциферина в такой смеси.
После многочисленных экспериментов было установлено, что свечение погасшего супернатанта можно восстановить добавкой порции этого же экстракта после кратковременного нагрева до 100°C. Таким образом, кажущееся исчезновение люциферина в действительности оказалось его переходом в неактивное, но обратимое состояние. Выяснилось, что люциферин в неактивном состоянии достаточно стабилен, выдерживает концентрирование под вакуумом на роторном испарителе, последующую лиофилизацию и долгие хроматографические процедуры при комнатной температуре. Найденный приём термоактивации люциферина Henlea sp. далее применялся для его тестирования в пробах на всех этапах очистки. Тестирование проводили в 16 мМ буфере MOPS с рН 7,0, содержащем 1 мМ CaCl2, а в качестве люциферазы использовали первичный бесклеточный супернатант Henlea sp. Такой грубый препарат кроме люциферазы содержал неактивный люциферин и различные примеси.
Экстракция, разделение и очистка люциферина и низкомолекулярных компонентов
Замороженных червей гомогенизировали в воде при 0°C и центрифугировали (16000 g, 3 мин). Проводили денатурацию белков супернатанта добавлением соляной кислоты до конечной концентрации 0,3 мМ. Выпавший осадок удаляли центрифугированием (10 000 g, 20 мин). Супернатант, содержащий люциферин, при УФ-облучении ярко флуоресцировал.
Для концентрирования и отделения люцифериновой фракции методом твёрдофазной экстракции супернатант наносили на колонку С16 объёмом 1 мл. После промывки колонки 0,1% муравьиной кислотой целевую фракцию элюировали 3 мл 75% ацетонитрила в воде и доводили её до минимального объёма на роторном испарителе. Далее проводили многоэтапную очистку люциферина на высокоэффективном жидкостном хроматографе Agilent 1260 Infinity (“Agilent Technology”, США) с детектором DAD, используя разные колонки (“Agilent Technology”): обратнофазная ZORBAX Eclipse XDB-C18 (9,4 Å ~ 250 мм) с градиентом ацетонитрила в воде от 5 до 40% в течение 24 мин со скоростью 3 мл/мин; ZORBAX Eclipse XDB-C18 (3 Å ~ 150 мм) с градиентом ацетонитрила в 0,1% формиата от 1 до 40% в течение 10 мин со скоростью 1 мл/мин; анионообменная ZORBAX SAX (4,6 Å ~ 150 мм) с элюированием целевых фракций 0,1 М раствором KH2PO4 (pH 4,6) со скоростью 1 мл/мин. Финальную гель-фильтрацию проводили на колонке Superdex Peptide 10/300 GL (“GE Health Care Life Sciences”, США) с элюированием фракций 50 мМ формиата аммония (рН 4,6) со скоростью 0,8 мл/мин.
В процессе хроматографической очистки люциферина было зарегистрировано неоправданно резкое снижение его суммарной активности. Предположив, что происходит потеря некоего компонента, необходимого для люминесцентной реакции, авторы настоящего изобретения стали отслеживать распределение не только самого люциферина, но и тех фракций, которые при перекрестном тестировании повышали его активность.
Таким образом, на первом хроматографическом этапе авторы настоящего изобретения выявили два пика, способных многократно усиливать биолюминесценцию реакционной смеси. Эти низкомолекулярные компоненты, названные “Активатор H” и “Активатор S”, фракционировали и далее рехроматографировали отдельно. В табл. 1 приведены значения времени удерживания на колонках всех трёх целевых низкомолекулярных компонентов биолюминесцентной системы Henlea sp.
Таблица 1. Хроматографические параметры высокоочищенных компонентов на разных хроматографических колонках.
Анализ низкомолекулярных компонентов биолюминесцентной системы Henlea sp.
УФ-спектры компонентов биолюминесцентной реакции, проявляющих активирующую испускание света активность, а именно фракций 31,1 и 38,6 мин (табл. 1), нормированные при максимуме 395 нм, практически совпадают (фиг. 5). Активаторы флуоресцируют голубым светом с максимумом флуоресценции 464 нм (фиг. 6), который совпадает с максимумом биолюминесценции Henlea sp. in vivo (фиг. 7). Интересно, что спектр возбуждения (фиг. 7) хорошо коррелирует со спектром поглощения (фиг. 5) активаторов. Значительный стоксов сдвиг (70 нм) объясняется переносом энергии возбуждённого состояния люминофора, находящегося в сильно полярной среде (вода). При этом длина волны возбуждения не влияла на спектр испускания.
Структурные исследования активатора люциферина Henlea
В результате многоэтапной хроматографической очистки получено 0.3 оптические единицы Активатора H для снятия MS/MSn и ЯМР спектров. Чистота образца по ЯМР>95%.
Анализ очищенного из биомассы червя природного Активатора H выявил ион [M-H]– с m/z = 362.0986, что соответствует брутто-формуле C16H16N3O7–. Характерные паттерны фрагментации показали, что молекула состоит из двух фрагментов, один из которых углеводный, что было подтверждено ЯМР-спектроскопией. Анализ очищенного природного Активатора S выявил молекулярный ион [M-H]– с m/z = 442.0589, что соответствует формуле C16H16N3O10S–. Как видно, из брутто-формулы, молекула ActS отличается от молекулы ActH на фрагмент SO3. Паттерны фрагментации масс-спектра показали, что первым отцепляется от молекулы именно этот фрагмент, после чего полностью повторяется фрагментация ActH. Это дало основание полагать, что молекулы двух активаторов практически идентичны, с той разницей, что у ActS вместо одной из гидроксильных групп – сульфоэфирная.
Спектры ЯМР компонентов ActH зарегистрированы в двух растворителях: D2O и MeОD. Спектры ActH в D2O (рН 3.46, 10°C) сняты на ЯМР-спектрометре Bruker Avance III 600MHz, оборудованном криодатчиком CPTXI 1H/13C/15N Z-Grad. Были сняты следующие спектры ЯМР: 1H 1D (37 минут на спектр, 8 спектров в целях контроля стабильности образца), 13C-HSQC (21 час), DQF COSY (8.5 часов), ROESY (21 час), 13С-HMBC (22 часа 50 минут, 5 спектров с последующим суммированием для увеличения соотношения сигнал/шум). Разрешение по непрямому направлению составляло 1024 действительные точки (COSY, ROESY) и 2048 точек (HSQC, HMBC).
После регистрации спектров в D2O образец компонента ActH был высушен, растворен в d4-MeOD. Спектры ActS в D2O (рН 2.60, 10°C) и b и ActH в MeOD (10°C) зарегистрированы на ЯМР спектрометре Bruker Avance III 800 MHz, оборудованном криогенно-охлажденным датчиком CPTCI 1H/13C/15N Z-Grad. Сняты следующие спектры: 1H 1D (45 минут на спектр, 6 спектров в целях контроля стабильности образца), 13C-HSQC (21 час, 3 спектра с последующим суммированием в целях улучшения соотношения сигнал/шум), DQF COSY (20,5 часов), TOCSY (27 часов). Структуры компонентов ActH и ActS и химические сдвиги ЯМР показаны на фиг. 8 и в табл. 2.
Наибольший слабопольный сдвиг 0.748 м.д. в спектре 1H-ЯМР ActS наблюдался для протона H-13 (С-3' фрагмента рибозы), что позволило однозначно установить положение сульфоэфирной группы при третьем атоме углерода рибозы.
Таблица 2. Значения химических сдвигов в спектрах ЯМР компонентов биолюминесценцентной системы Henlea sp. ActH и ActS. Значения химических сдвигов углерода взяты из спектров HSQC и/или HMBC.
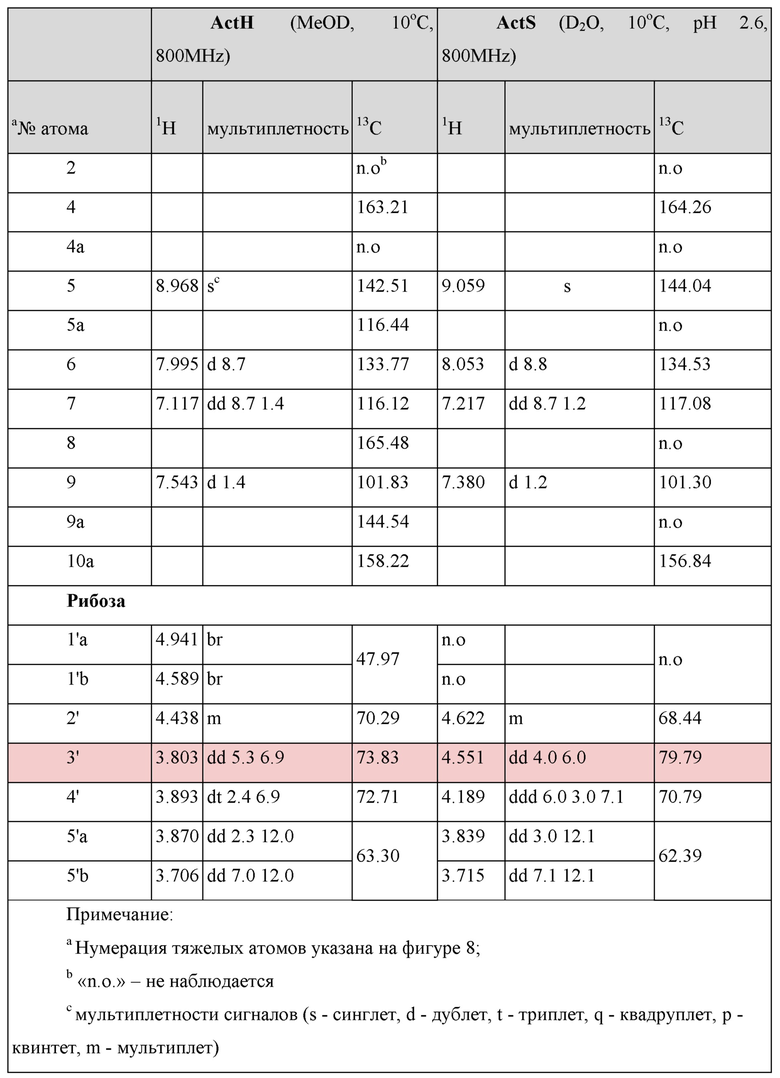
Литературный поиск среди известных природных соединений позволяет найти хромофор FO (McCormick, Morton, JACS 1982, 104, 4014–4015; Kuo et al. J Antibiot (Tokyo) 1989, 42, 475–478; Hossain et al. Org Biomol Chem 2015, 13, 5082–5085; Bender et al. Beilstein J Org Chem 2016, 12, 912–917) в качестве возможной химической структуры Активатора H. Приведенные в литературе данные ЯМР не противоречат такому предположению.
Синтез компонента биолюминесцентной системы Henlea sp. Активатора H по изобретению
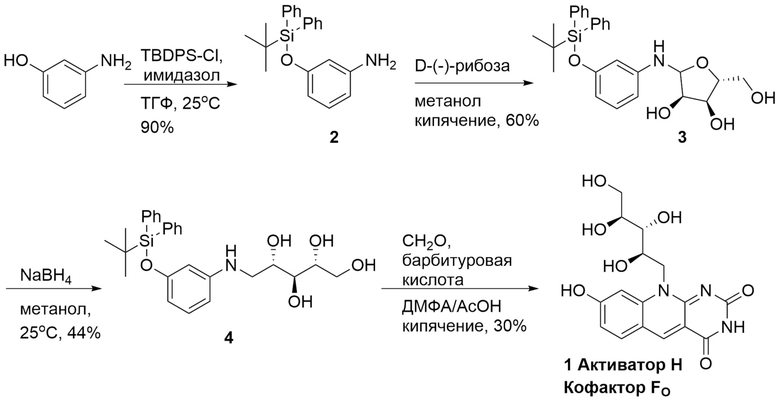
3-((т-бутилдифенилсилил)окси)анилин (2):
Навески имидазола (2.50 г, 36.65 ммоль) и 3-аминофенола 2 (2.00 г, 18.33 ммоль) растворили в абсолютном тетрагидрофуране (далее - ТГФ). Перемешивали при комнатной температуре 30 мин. Далее по каплям добавили дифенил-т-бутилхлорсилан (7.56 г, 27.49 ммоль). Выпал мелкий осадок. Перемешивали при комнатной температуре в инертной атмосфере в течение ночи. При достижении полной конверсии реакционную массу разбавили 100 мл воды, экстагировали эфиром (4×100 мл). За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.8). Продукт был выделен методом колоночной хроматографии (Hex/EtOAc=70:30). Получено светло-жёлтое масло 2 (5.50 г, 86%).
1H NMR (700 MHz, Chloroform-d) δ 7.92-7.79 (m, 4H), 7.56-7.49 (m, 2H), 7.48-7.37 (m, 4H), 6.94 (t, J = 8.0 Hz, 1H), 6.29 (ddd, J = 7.9, 2.2, 0.9 Hz, 1H), 6.27 (ddd, J = 8.1, 2.3, 0.9 Hz, 1H), 6.25 (t, J = 2.2 Hz, 1H), 1.19 (s, 9H).
2-((3-((трет-бутилдифенилсилил)окси)фенил)амино)тетрагидро-2H-пиран-3,4,5-триол (3):
Навески соединения 2 (2.66 г, 7.57 ммоль) и d-(-)-рибозы (1.24 г, 8.17 ммоль) растворили в 26 мл MeOH. Раствор нагрели до кипения в инертной атмосфере. Перемешивали до полного прохождения реакции. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.25). Растворитель отогнали в вакууме, после чего остаток перерастворили в 26 мл дихлорметана. Раствор промывали насыщенным раствором хлорида натрия (5х20 мл). Раствор сушили над безводным сульфатом натрия, после чего дихлорметан отогнали в вакууме. Получили 2,42 г (67%) белого стекловидного вещества (3).
1H NMR (700 MHz, Chloroform-d) δ 7.80 (ddd, J = 8.1, 4.6, 1.4 Hz, 4H), 7.62-7.46 (m, 2H), 7.46-7.36 (m, 4H), 7.33 (s, 1H), 6.98 (t, J = 8.1 Hz, 1H), 6.46-6.30 (m, 2H), 6.25 (t, J = 2.3 Hz, 1H), 5.11 (d, J = 10.1 Hz, 1H), 4.40 (d, J = 9.9 Hz, 1H), 3.94 (dd, J = 12.9, 2.5 Hz, 1H), 3.91-3.84 (m, 2H), 3.64 (dd, J = 7.5, 3.9 Hz, 0H), 3.35 (dd, J = 12.9, 1.4 Hz, 1H), 3.26 (dd, J = 21.6, 8.5 Hz, 2H), 2.94 (d, J = 5.9 Hz, 1H), 1.16 (s, 9H).
2-((3-((трет-бутилдифенилсилил)окси)фенил)амино)пентан-1,2,3,4-тетраол (4):
Тетрагидроборат натрия (1.53 г, 39.96 ммоль) порционно присыпали к раствору соединения 3 (2.42 г, 4.99 ммоль) в сухом метаноле (26 мл), охлаждённому на ледяной бане. После добавления, смесь нагрели до 50оС и перемешивали 16 ч. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.2). После реакционную смесь смешали с 150 мл насыщенного раствора хлористого аммония, после чего её промыли дихлорметаном (далее - ДХМ) (5х50 мл). Органические слои были объединены, растворитель был отогнан в вакууме, а осадок был очищен методом колоночной хроматографии (ДХМ/метанол=90:10). Было получено белое стеклообразное вещество (4) (1.07 г, 44%).
1H NMR (700 MHz, Chloroform-d) δ 7.79 (m, 4H), 7.61-7.38 (m, 2H), 6.94 (t, J = 8.0 Hz, 1H), 6.26 (m, 3H), 3.96-3.57 (m, 3H), 3.23 (m, 2H), 1.16 (s, 9H).
8-гидрокси-10-(2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]-хинолин-2,4(3H, 10H)дион (1):
Навески соединения 4 (0.1 г, 0.21 ммоль), параформальдегида (0.006 г, 0.21 ммоль) и барбитуровой кислоты (0.03 г, 0.21 ммоль) растворили в 2 мл смеси N,N-Диметилформамид (далее – ДМФА)/уксусная кислота (1:1). Раствор нагрели до кипения в инертной атмосфере и перемешивали 40 минут. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 7:3, Rf 0.4). После этого уксусную кислота была отогнана в вакууме, продукт был выделен методом колоночной хроматографии (HCCl3/EtOH=90:10 => EtOH). Было получено 0.02 г (31%) тёмно-жёлтого порошка 1.
1H NMR (700 MHz, DMSO-d6) δ 8.74 (s, 1H), 7.91 (d, J = 8.8 Hz, 1H), 7.20 (s, 1H), 6.91 (d, J = 8.8 Hz, 1H), 4.21 (br, 1H), 3.72 – 3.63 (m, 2H), 3.59 (t, J = 5.7 Hz, 1H), 3.47 (dd, J = 10.9, 6.0 Hz, 2H).
Синтез компонента биолюминесцентной системы Henlea sp. Активатора S по изобретению
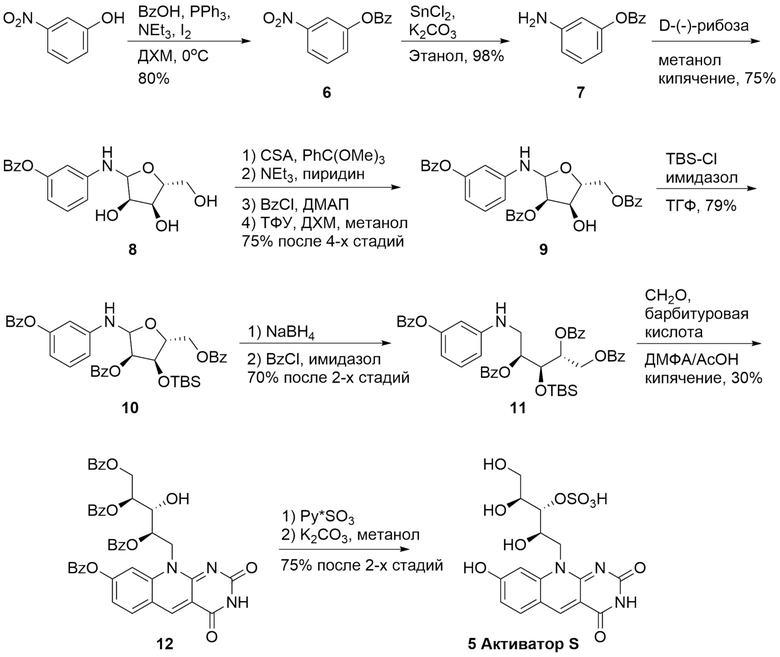
3-нитрофенилбензоат (6)
Трифенилфосфин (5.53 г, 21.1 ммоль) и иод (5.36 г, 21.1 ммоль) растворили в 75 мл ДХМ на ледяной бане. К раствору добавили бензойную кислоту (1.71 г, 14,0 ммоль) и 3-нитрофенол (2.13 г, 15,3 ммоль). Реакцию нагрели до комнатной температуры, после чего перемешивали 20 минут. Продукт был выделен методом колоночной хроматографии (силикагель, EtOAc/Hex (30:70)). Получено 3.02 г соединения 6 (81%).
1H NMR (300 MHz, DMSO-d6) δ 7.69-7.59 (m, 1H), 7.56 (t, J = 7.5 Hz, 1H), 7.53-7.45 (m, 2H), 7.42 (dt, J = 7.5, 1.5 Hz, 1H).
3-аминофенилбензоат (7)
3-нитрофенилбензоат (2.71 г, 11.14 ммоль) и дигидрат дихлорида олова (12.56 г, 55.72 ммоль) растворили в 60 мл EtOH и перемешивали при 100°C в течение часа. Реакционную массу остудили до комнатной температуры и оттитровали насыщенным раствором карбоната калия до pH~8. Раствор был промыт ДХМ (3Х50 мл), после чего органические слои были объединены и просушены над Na2SO4, после чего растворитель был отогнан в вакууме. В результате было получено 2.33 г соединения 7 с выходом, близким к количественному.
1H-NMR (CDCl3, 400 MHz): 8.1 (dd, 2H), 7.63 (td, 1H), 7.50 (t, 2H), 7.18 (t, 1H), 6.59 (m, 3H), 3.45 (s, 2H)
13C-NMR (CDCl3, 100 MHz): 165.15, 151.95, 147.56, 133.47, 130.12, 139.69, 128.51, 112.75, 111.59, 108.48
3-(((3R,4S,5R)-3,4-дигидрокси-5-(гидроксиметил)тетрагидрофуран-2-ил)амино)фенилбензоат (8)
Навески 3-аминофенилбензоата 7 (3,34 г, 15,7 ммоль) и d-(-)-рибозы (2,57 г, 17,1 ммоль) были растворены в 60 мл сухого метанола, после чего смесь нагрели до кипения и перемешивали 6 часов в атмосфере аргона. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.3). После прохождения реакции метанол был отогнан в вакууме и жёлтый порошок был подвергнут очистке методом колоночной хроматографии (ДХМ/MeOH=9:1). В результате был получен светло-жёлтый порошок 8 (4,12 г, 76%).
1H NMR (700 MHz, CD3OD) δ 8.14 – 7.99 (m, 1H), 7.63 (ddt, J = 8.0, 6.8, 1.5 Hz, 1H), 7.56 – 7.44 (m, 1H) 7.00 (td, J = 8.0, 3.7 Hz, 1H), 6.40 (d, J = 8.0 Hz, 1H), 6.31 (dt, J = 13.1, 2.0 Hz, 1H), 6.23 (d, J = 7.8 Hz, 1H), 4.83 (d, J = 7.9 Hz, 1H), 4.11 (br, 1H), 3.95 – 3.44 (m, 5H)
((2R,3R,4R)-4-(бензоилокси)-5-((3-(бензоилокси)фенил)амино)-3-гидрокситетрагидрофуран-2-ил)метилбензоат (9)
К раствору соединения 8 (1.1 г, 4.58 ммоль) и триметилортобензоата (1.25 мл, 6.87 ммоль) в 20 мл ДХМ добавили камфоросульфокислоту (50 мг). Смесь перемешивали при 20°С в течение 10 минут, добавили триэтиламин (0.1 мл), упаривали досуха в вакууме и остаток растворяли в пиридине (7 мл). К полученному раствору прибавляли бензоил хлорид (0.8 мл, 6.87 ммоль) и диметиламинопиридин (10 мг) и смесь перемешивали при 40°С в течение 30 минут. Смесь разлагали добавлением метанола (0.5 мл), соупаривали в вакууме с толуолом и остаток растворяли в хлористом метилене (10 мл). К полученному раствору прибавляли 90% водный раствор трифторуксусной кислоты (1 мл), и смесь перемешивали при 20°С в течение 30 минут, разбавляли хлористым метиленом (30 мл) и промывали насыщенным водным раствором NaHCO3 (3х10 мл). Органическую фазу пропускали через слой силикагеля (EtOAc/толуол 1:5). Сырой продукт растворяли в толуоле (50 мл), добавляли триэтиламин (0.1 мл) и смесь оставляли кристаллизоваться при 4°С на 12 часов. Выпавшие кристаллы отфильтровывали, промывали смесью толуол/гексан (1:1, 30 мл), высушивали в вакууме и получали 1.56 г (76%) кристаллы дибензоата 9.
((2R,3R,4R)-4-(бензоилокси)-5-((3-(бензоилокси)фенил)амино)-3-((трет-бутилдиметилсилил)окси)тетрагидрофуран-2-ил)метилбензоат (10)
Навески имидазола (0.25 г, 3.61 ммоль) и соединения 9 (1.00 г, 1.81 ммоль) растворили в сухом ТГФ. Перемешивали при комнатной температуре 30 мин. Далее порционно добавили диметил-т-бутилхлорсилан (0,41 г, 2,7 ммоль). Выпал мелкий осадок. Перемешивали при комнатной температуре в инертной атмосфере в течение ночи. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.85). При достижении полной конверсии реакционную массу разбавили 100 мл воды, проэкстагировали эфиром (4×100 мл). Продукт был выделен методом колоночной хроматографии (Hex/EtOAc=70:30). Получено светло-жёлтое стекловидное вещество 10 (0,95 г, 79%).
1H NMR (300 MHz, DMSO-d6) δ 8.16 – 8.07 (m, 1H), 8.07-7.94 (m, 2H), 7.64-7.51 (m, 2H), 7.50 – 7.38 (m, 3H), 7.25 (t, J = 7.5 Hz, 0H), 7.15 (d, J = 10.1 Hz, 0H), 6.96 (dt, J = 7.5, 1.5 Hz, 0H), 6.77 (dt, J = 7.5, 1.5 Hz, 0H), 6.53 (t, J = 1.5 Hz, 0H), 5.27 (dd, J = 10.0, 7.0 Hz, 0H), 4.79 (td, J = 7.0, 0.9 Hz, 0H), 4.54 – 4.31 (m, 2H), 4.25 (qd, J = 6.9, 0.8 Hz, 1H), 0.85 (s, 5H), 0.02 (s, 3H).
(2R,3S,4S)-5-((3-(бензоилокси)фенил)амино)-3-((трет-бутилдиметилсилил)окси)пентан-1,2,4-триилтрибензоат (11)
Тетрагидроборат натрия (0.215 г, 5.69 ммоль) порционно присыпали к раствору соединения 10 (0.95 г, 1.42 ммоль) в сухом метаноле (6 мл), охлаждённому на ледяной бане. После добавления, смесь нагрели до комнатной температуры и перемешивали 16 ч. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 9:1, Rf 0.2). После реакционную смесь смешали с 150 мл насыщенного раствора хлористого аммония, после чего её промыли ДХМ (5х50 мл). Органические слои были объединены и посушены над сульфатом натрия, растворитель был отогнан в вакууме, а осадок был перерастворён в 6 мл ТГФ. К полученному раствору добавили имидазол (0.096 г, 1.42 ммоль), перемешивали при комнатной температуре полчаса. После этого к реакционной смеси по каплям добавили бензоилхлорид (0.096 г, 161 мкл, 1.39 ммоль). Реакционную смесь перемешивали при комнатной температуре до полной конверсии (за ходом реакции следили по ТСХ: силикагель, хлороформ-этанол 9:1). Продукт был очищен методом колоночной хроматографии (ДХМ/метанол=90:10). Было получено белое стеклообразное вещество 11 (0.779 г, 71%).
1H NMR (300 MHz, DMSO-d6) δ 8.19 – 8.09 (m, 1H), 8.07-7.96 (m, 3H), 7.68-7.55 (m, 2H), 7.54-7.41 (m, 4H), 7.21 (t, J = 7.5 Hz, 0H), 7.10 (t, J = 7.1 Hz, 0H), 6.91 (d, J = 7.0 Hz, 0H), 6.87 (dt, J = 7.5, 1.4 Hz, 0H), 6.65 (dt, J = 7.5, 1.5 Hz, 0H), 6.41 (t, J = 1.5 Hz, 1H), 4.83 (q, J = 6.9 Hz, 1H), 4.71 (t, J = 7.0 Hz, 0H), 3.86 – 3.53 (m, 1H), 0.84 (s, 5H), 0.01 (s, 3H).
(2S,3R,4R)-5-(8-(бензоилокси)-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)-3-гидроксипентан-1,2,4-триилтрибензоат (12)
Навески соединения 11 (0.75 г, 0.97 ммоль), параформальдегида (0.029 г, 0.97 ммоль) и барбитуровой кислоты (0.124 г, 0.97 ммоль) растворили в 9 мл смеси ДМФА/уксусная кислота (1:1). Раствор нагрели до кипения в инертной атмосфере и перемешивали 40 минут. За ходом реакции следили по ТСХ (силикагель, хлороформ-этанол 8:2, Rf 0.7). После этого уксусную кислота была отогнана в вакууме, продукт был выделен методом колоночной хроматографии (HCCl3/EtOH=90:10 => EtOH). Было получено 0.217 г (29%) тёмно-жёлтого порошка 12.
1H NMR (700 MHz, DMSO-d6) δ 8.17-8.08 (m, 2H), 8.74 (s, 1H), 8.01 (ddt, J = 7.6, 2.9, 1.4 Hz, 6H), 7.91 (d, J = 8.8 Hz, 1H), 7.54-7.42 (m, 8H), 7.20 (s, 1H), 6.91 (d, J = 8.8 Hz, 1H), 4.89-4.67 (m, 4H), 4.61-4.44 (m, 2H), 4.33 (dddd, J = 8.5, 7.0, 6.2, 0.7 Hz, 1H), 4.20 (dd, J = 12.3, 7.0 Hz, 1H).
(2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат (5)
К раствору соединения 12 (217 мг, 0.28 ммоль) в 1 мл ДМФА по каплям добавили раствор комплекса пиридин-триоксида серы (44 мг, 0.27 ммоль) в 1 мл ДМФА, после чего перемешивали при комнатной температуры 3 часа. После этого, к раствору добавили 5 мл, диэтилового эфира, выпавший жёлтый осадок отфильтровали и перерастворили в 1 мл метанола. К реакционной массе добавили 0.5 мл водного раствора карбоната калия (153 мг, 1.11 ммоль), реакционную массу перемешивали при комнатной температуре в течение ночи. Продукт был выделен методом препаративной обращённо-фазной хроматографии (MeCN-H2O C18). Было получено 573 мг (75 %) жёлтого порошка 5.
1H NMR (800 MHz, D2O) δ 9.1 (s, 1H), 8.12 (d, J = 8.8 Hz, 1H), 7.3 (s, 1H), 7.17 (d, J = 8.8 Hz, 1H), 4.69 (m, J = 8.2 Hz, 1H), 4.59 (dd, J = 6.2, 3.9 Hz, 1H), 4.23 (t, J = 5.1 Hz, 1H), 3.81 (dd, J = 12.1, 3.3 Hz, 1H), 3.72 (dd, J = 12.2, 11.8, 6.8 Hz, 1H).
Использование 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона для выявления люциферазы в биологических образцах
Термоактивированный люциферин был получен, как описано выше в разделе «Порядок экстракции люциферина». В качестве образцов использовали хроматографически очищенный на колонкe Superdex 200 белковый препарат из биомассы червей Henlea sp, полученный как описано выше в разделе «Очистка проб образцов нативной люциферазы». 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион был получен, как описано выше в разделе «Синтез компонента биолюминесцентной системы Henlea sp. Активатора H» 2 мкл высокоочищенного люциферина Henlea sp. в 100 мкл 16 мМ MOPS (pH 7.0), содержащем 1мМ CaCl2 помещали в кипящую воду на 1 мин, переносили в термостат на 1 мин при 20°C. Добавляли 5 мкл белкового препарата, добавляли 1 мкл 0.1мМ 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона.
В ходе эксперимента в каждом случае сначала измеряли фоновую люминесценцию экстракта люциферазы, а затем добавляли аликвоты раствора 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона (фиг. 9).
Во всех случаях была выявлена люминесценция биологических образцов.
Измерение зависимости интенсивности биолюминесценции от количества компонента 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона
Термоактивированный люциферин был получен, как описано выше в разделе «Порядок экстракции люциферина». В качестве образцов использовали первичный бесклеточный супернатант из биомассы червей Henlea sp, полученный как описано выше в разделе «Получение образцов нативной люциферазы». 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион был получен, как описано выше в разделе «Синтез компонента биолюминесцентной системы Henlea sp. Активатора H» 2 мкл высокоочищенного люциферина Henlea sp. в 100 мкл 16 мМ MOPS (pH 7.0), содержащем 1мМ CaCl2 помещали в кипящую воду на 1 мин, переносили в термостат на 1 мин при 20°C. Добавляли 2мкл частично очищенной люциферазы.
Биолюминесцентную реакцию активировали добавлением различных количеств раствора 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона. Зависимость люминесценции от концентрации НАДФН показана на фиг. 10. Оптимальная концентрация раствора 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона в реакционной смеси, при которой наблюдалась максимальная биолюминесценция, составила 2.3 мкМ .
Использование 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона для детекции биолюминесценции в биологических образцах
Термоактивированный люциферин был получен, как описано выше в разделе «Порядок экстракции люциферина». В качестве биологических образцов использовали экстракты червей Henlea sp, полученный как описано выше в разделе «Получение бесклеточных экстрактов червей Henlea sp.». 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-дион был получен, как описано выше в разделе «Синтез компонента биолюминесцентной системы Henlea sp. Активатора H» 2 мкл высокоочищенного люциферина Henlea sp. в 100 мкл 16 мМ MOPS (pH 7.0), содержащем 1мМ CaCl2 помещали в кипящую воду на 1 мин, переносили в термостат на 1 мин при 20°C. Добавляли 2 мкл бесклеточного экстракта, добавляли 1 мкл 0.1мМ 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона.
В ходе эксперимента в каждом случае сначала измеряли фоновую люминесценцию экстракта биомассы, а затем добавляли аликвоты раствора 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона (фиг 11).
Во всех случаях была выявлена люминесценция биологических образцов.
Использование (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата для выявления люциферазы в биологических образцах
Термоактивированный люциферин был получен, как описано выше в разделе «Порядок экстракции люциферина». В качестве образцов использовали хроматографически очищенный на колонкe Superdex 200 белковый препарат из биомассы червей Henlea sp, полученный как описано выше в разделе «Очистка проб образцов нативной люциферазы». (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат был получен, как описано выше в разделе «Синтез компонента биолюминесцентной системы Henlea sp. Активатора S» 2 мкл высокоочищенного люциферина Henlea sp. в 100 мкл 16 мМ MOPS (pH 7.0), содержащем 1мМ CaCl2 помещали в кипящую воду на 1 мин, переносили в термостат на 1 мин при 20°C. Добавляли 5 мкл белкового препарата, добавляли 1 мкл 0.1мМ (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата.
В ходе эксперимента в каждом случае сначала измеряли фоновую люминесценцию экстракта люциферазы, а затем добавляли аликвоты раствора (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата (фиг. 12).
Во всех случаях была выявлена люминесценция биологических образцов.
Использование (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата для детекции биолюминесценции в биологических образцах
Термоактивированный люциферин был получен, как описано выше в разделе «Порядок экстракции люциферина». В качестве биологических образцов использовали экстракты червей Henlea sp, полученный как описано выше в разделе «Получение бесклеточных экстрактов червей Henlea sp.». (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфат был получен, как описано выше в разделе «Синтез компонента биолюминесцентной системы Henlea sp. Активатора S» 2 мкл высокоочищенного люциферина Henlea sp. в 100 мкл 16 мМ MOPS (pH 7.0), содержащем 1мМ CaCl2 помещали в кипящую воду на 1 мин, переносили в термостат на 1 мин при 20°C. Добавляли 2 мкл бесклеточного экстракта, затем добавляли 1 мкл 0.1мМ (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата.
В ходе эксперимента в каждом случае сначала измеряли фоновую люминесценцию экстракта биомассы, а затем добавляли аликвоты раствора (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата (фиг. 13).
Во всех случаях была выявлена люминесценция биологических образцов.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Метод и реактивы для детекции активности люциферазы | 2020 |
|
RU2826202C2 |
| Метод и реактивы для детекции активности люциферазы | 2019 |
|
RU2744869C2 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2678327C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОСЕНСИБИЛИЗАТОРА ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2023 |
|
RU2807293C1 |
| ЛЕКАРСТВЕННЫЕ СОЕДИНЕНИЯ | 2014 |
|
RU2691105C1 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2667060C2 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ ОПУХОЛЕВЫХ КЛЕТОК | 2023 |
|
RU2805148C1 |
| МЕТОД И РЕАКТИВЫ ДЛЯ ДЕТЕКЦИИ АКТИВНОСТИ ЛЮЦИФЕРАЗЫ | 2015 |
|
RU2596398C1 |
| Пролекарство ингибитора NS5B HCV полимеразы, способ его получения и применения | 2017 |
|
RU2644156C1 |
| Противовирусная композиция и способ ее применения | 2017 |
|
RU2650610C1 |



Изобретение относится к биологии, химии и биотехнологии. Предложено применение соединения 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона и/или его сульфатированного аналога (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата или его фармацевтически приемлемой соли в качестве компонента биолюминесцентной реакции в биологическом образце, также содержащем люциферазу или нуклеиновую кислоту, кодирующую люциферазу, и люциферин червя Henlea sp. Технический результат состоит в расширении арсенала технических средств в области применения биолюминесцентных систем. 5 з.п. ф-лы, 13 ил., 2 табл.
1. Применение соединения 8-гидрокси-10-((2R,3R,4S)-2,3,4,5-тетрагидроксипентил)пиримидо[4,5-b]хинолин-2,4(3Н,10Н)-диона и/или его сульфатированного аналога (2S,3R,4R)-1,2,4-тригидрокси-5-(8-гидрокси-2,4-диоксо-3,4-дигидропиримидо[4,5-b]хинолин-10(2H)-ил)пентан-3-илгидросульфата или его фармацевтически приемлемой соли, характеризующегося следующей общей формулой I:
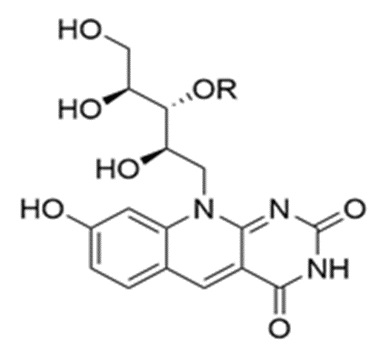 формула I,
формула I,
где R представляет собой водород Н или сульфогруппу -SO3Н,
в качестве компонента биолюминесцентной реакции в биологическом образце, причем биологический образец дополнительно содержит люциферазу или нуклеиновую кислоту, кодирующую люциферазу, и люциферин червя Henlea sp.
2. Применение по п.1, в котором биологически образец представляет собой ткань клетку, экстракт, гомогенат и/или белковую смесь.
3. Применение по п.1, в котором биологический образец характеризуется значением рН в диапазоне от 7 до 8.
4. Применение по п.1, в котором люцифераза является рекомбинантной.
5. Применение по п.1, в котором червь представляет собой вид Henlea petushkovi и/или Henlea rodionovae.
6. Применение по п.1, в котором биолюминесцентная реакция сопровождается увеличением интенсивности испускаемого света.
| МЕТОД И РЕАКТИВЫ ДЛЯ ДЕТЕКЦИИ АКТИВНОСТИ ЛЮЦИФЕРАЗЫ | 2015 |
|
RU2596398C1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| BENDER, M | |||
| et al | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Beilstein Journal of Organic Chemistry, 2016, v | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Клиновая передача | 1923 |
|
SU912A1 |
| PETUSHKOV, V.N | |||
| & RODIONOVA, N.S | |||
| New types of luminescent systems of soil enchytraeids (Annelida: Clitellata: Oligochaeta: Enchytraeidae) | |||
Авторы
Даты
2024-11-25—Публикация
2020-07-08—Подача