Область техники
[0001] Настоящее изобретение относится к искусственному меху и к способу его изготовления.
Предпосылки создания изобретения
[0002] Известные искусственные меха используются в качестве альтернативы натуральным мехам. Так, например, в патентном документе 1 раскрывается искусственный мех, включающий синтетическое волокно, такое как акриловое волокно.
Список цитируемой литературы
Патентная литература
[0003] Патентный документ 1: JP 63-6133 A
Сущность изобретения
Техническая проблема
[0004] В отличие от натурального меха, поставки которого ограничены, искусственный мех может производиться искусственно в большом масштабе. В последние годы, искусственный мех получил широкое распространение, например, в изготовлении одежды, аксессуаров (таких как сумки), ковров и чучел животных. Большинство искусственных мехов, используемых в данной области, изготавливают из акриловых волокон, которые являются легкими и теплыми, подобно пушистой шерсти.
[0005] Однако, обычно искусственный мех включает синтетические волокна и имеет плохие влагопоглощающие свойства. Кроме того, стандартные искусственные меха получают из нефти и во время их изготовления потребляется большое количество энергии.
[0006] Для решения или хотя бы частичного решения этих проблем, искусственный мех можно, например, получать из белкового волокна. Однако, некоторые белковые волокна сжимаются при контактировании с водой. В искусственных мехах, включающих такие белковые волокна, контактирование с водой может приводить к значительному изменению размеров.
[0007] Кроме того, искусственный мех из акриловых волокон, которые часто используется для изготовления искусственного меха, не только создает большую нагрузку на окружающую среду, но и чувствителен к влажности и к воде. В частности, акриловые волокна удлиняются при мойке или т.п.
[0008] Настоящее изобретение было сделано с учетом вышеуказанных обстоятельств. Первой целью настоящего изобретения является изготовление искусственного меха, который обладал бы достаточными влагопоглощающими свойствами и требовал бы меньшее количество энергии, необходимой для его изготовления, а также способ производства искусственного меха.
[0009] Второй целью настоящего изобретения является изготовление искусственного меха, который обладал бы достаточными влагопоглощающими свойствами, требовал бы меньшее количество энергии, необходимой для его изготовления и предотвращал, насколько это возможно, изменение размеров при контактировании с водой.
[0010] Третьей целью настоящего изобретения является изготовление искусственного меха с превосходными функциональными свойствами, такими как водостойкость.
[0011] Четвертой целью настоящего изобретения является изготовление искусственного меха с превосходной водостойкостью.
[0012] Пятой целью настоящего изобретения является разработка подходящего способа изготовления искусственного меха, который обладал бы достаточной влагопоглощающей способностью и требовал бы меньшее количество энергии, необходимой для его изготовления.
[0013] Шестой целью настоящего изобретения является разработка подходящего способа изготовления искусственного меха, который обладал бы достаточной влагопоглощающей способностью, требовал бы меньшее количество энергии, необходимой для его изготовления, и предотвращал, насколько это возможно, изменение размеров при контактировании с водой.
Решение проблемы
[0014] В своем первом аспекте, настоящее изобретение относится к достижению первой цели, например, к нижеследующим объектам изобретения, таким как:
[0015] [1-1] Искусственный мех, включающий искусственное белковое волокно.
[0016] [1-2] Искусственный мех в соответствии с [1-1], где искусственное белковое волокно включает искусственное структурное белковое волокно.
[0017] [1-3] Искусственный мех в соответствии с [1-2], где искусственное структурное белковое волокно включает модифицированное фиброиновое волокно.
[0018] [1-4] Искусственный мех в соответствии с [1-3], где модифицированное фиброиновое волокно включает модифицированное фиброиновое волокно шелка паука.
[0019] [1-5] Искусственный мех в соответствии с любым из [1-1] - [1-4], имеющий предельный кислородный индекс (LOI) 26,0 или более.
[0020] [1-6] Искусственный мех в соответствии с любым из [1-1] - [1-5], имеющий максимальный уровень влагопоглощения и выделения тепла более 0,025°C/г, определенный по следующей формуле A:
Формула A: максимальный уровень влагопоглощения и выделения тепла = {(максимальная температура образца после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г) [В формуле A, среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%].
[0021] [1-7] Искусственный мех в соответствии с [1-6], где максимальный уровень влагопоглощения и выделения тепла составляет 0,031°С/г или более.
[0022] [1-8] Искусственный мех в соответствии с любым из [1-1]-[1-7], имеющий индекс удерживания тепла более 0,18, определенный по следующей формуле B:
Формула B: индекс удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
[В формуле B, степень удерживания тепла (%) измеряют методом сухого контакта (температура: 30°C, скорость ветра: 30 см/сек) и вычисляют по формуле (1 - a/b)×100, где «a» означает количество тепла, рассеиваемого через тестируемый образец, а «b» означает количество тепла, рассеиваемого без тестируемого образца].
[1-9] Искусственный мех в соответствии с [1-8], где индекс удерживания тепла составляет 0,22 или более.
[0023] В своем втором аспекте, настоящее изобретение относится к достижению второй цели, например, к нижеследующим объектам изобретения, таким как:
[0024] [2-1] Искусственный мех, включающий безусадочное белковое волокно.
[0025] [2-2] Искусственный мех в соответствии с [2-1], где белковое волокно во влажном состоянии имеет степень усадки 2% или более, определяемую по следующей формуле I:
степень усадки во влажном состоянии = {1 - (длина белкового волокна во влажном состоянии после контакта с водой/длина белкового волокна после прядения, но до контакта с водой)}×100 (%) … (Формула I).
[0026] [2-3] Искусственный мех в соответствии с [2-1] или [2-2], где белковое волокно в сухом состоянии имеет степень усадки более 7%, определяемую по следующей формуле II:
степень усадки в сухом состоянии = {1 - (длина белкового волокна в сухом состоянии/длина белкового волокна после прядения, но до контакта с водой)}×100 (%) … (Формула II).
[0027] [2-4] Искусственный мех в соответствии с [2-1] - [2-3], где белковое волокно включает модифицированный фиброин.
[0028] [2-5] Искусственный мех в соответствии с [2-4], где модифицированный фиброин представляет собой модифицированный фиброин шелка паука.
[0029] [2-6] Искусственный мех в соответствии с любым из [2-1]-[2-5], имеющий предельный кислородный индекс (LOI) 26,0 или более.
[0030] [2-7] Искусственный мех в соответствии с любым из [2-1]-[2-6], имеющий максимальный уровень влагопоглощения и выделения тепла более 0,025°C/г, определенный по следующей формуле A:
Формула A: максимальный уровень влагопоглощения и выделения тепла = {(максимальная температура образца после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г) [В формуле A, среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%].
[0031] [2-8] Искусственный мех в соответствии с [2-7], где максимальный уровень влагопоглощения и выделения тепла составляет 0,031°С/г или более.
[0032] [2-9] Искусственный мех в соответствии с любым из [2-1]-[2-8], имеющий индекс удерживания тепла более 0,18, определенный по следующей формуле B:
Формула B: индекс удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
[В формуле B, степень удерживания тепла (%) измеряют методом сухого контакта (температура: 30°C, скорость ветра: 30 см/сек.) и вычисляют по формуле (1 - a/b)×100, где «a» означает количество тепла, рассеиваемого через тестируемый образец, а «b» означает количество тепла, рассеиваемого без тестируемого образца].
[2-10] Искусственный мех в соответствии с [2-9], где индекс удерживания тепла составляет 0,22 и более.
[0033] В своем третьем аспекте, настоящее изобретение относится к достижению третьей цели, например, к нижеследующим объектам изобретения, таким как:
[0034] [3-1] Искусственный мех, включающий волокно и обладающий функциональными свойствами.
[0035] [3-2] Искусственный мех в соответствии с [3-1], где волокно включает белковое волокно.
[0036] [3-3] Искусственный мех в соответствии с [3-2], где белковое волокно включает модифицированный фиброин.
[0037] [3-4] Искусственный мех в соответствии с [3-3], где модифицированный фиброин представляет собой модифицированный фиброин шелка паука.
[0038] [3-5] Искусственный мех в соответствии с любым из [3-1]-[3-4], включающий остов, перекрестно связывающийся с белком,
где остов, перекрестно связывающийся с белком, включает: множество полипептидных остовов; множество первых остатков или остатков первого реагента, имеющего по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком; и множество вторых остатков или остатков второго реагента, имеющего одну вторую реакционноспособную группу, способную образовывать связь посредством реакции с первой реакционноспособной группой,
по меньшей мере один из первых остатков перекрестно связывается с полипептидным остовом, и
по меньшей мере один из первых остатков связан с полипептидным остовом на одном конце и со вторым остатком на другом конце.
[0039] [3-6] Искусственный мех в соответствии с любым из [3-1]-[3-5], включающий модифицированный полимер, содержащий гидроксильную группу, где реакционноспособная функциональная группа связана с полимером, содержащим гидроксильную группу.
[0040] [3-7] Искусственный мех в соответствии с любым из [3-1]-[3-6], имеющий предельный кислородный индекс (LOI) 26,0 или более.
[0041] [3-8] Искусственный мех в соответствии с любым из [3-1]-[3-7], имеющий максимальный уровень влагопоглощения и выделения тепла более 0,025°C/г, определенный по следующей формуле A:
Формула A: максимальный уровень влагопоглощения и выделения тепла
= {(максимальная температура образца после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г) [В формуле A, среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%].
[0042] [3-9] Искусственный мех в соответствии с [3-8], где максимальный уровень влагопоглощения и выделения тепла составляет 0,031°С/г или более.
[0043] [3-10] Искусственный мех в соответствии с любым из [3-1]-[3-9], имеющий индекс удерживания тепла более 0,18, определенный по следующей формуле B:
Формула B: индекс удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
[В формуле B, степень удерживания тепла (%) измеряют методом сухого контакта (температура: 30°C, скорость ветра: 30 см/сек) и вычисляют по формуле (1 - a/b)×100, где «a» означает количество тепла, рассеиваемого через тестируемый образец, а «b» означает количество тепла, рассеиваемого без тестируемого образца].
[3-11] Искусственный мех в соответствии с [3-10], где индекс удерживания тепла составляет 0,22 и более.
[0044] В своем четвертом аспекте, настоящее изобретение относится к достижению четвертой цели, например, к нижеследующим объектам изобретения, таким как:
[0045] [4-1] Искусственный мех, включающий волокно и вещество, придающее водостойкость.
[0046] [4-2] Искусственный мех в соответствии с [4-1], где волокно включает белковое волокно.
[0047] [4-3] Искусственный мех в соответствии с [4-2], где белковое волокно включает модифицированный фиброин.
[0048] [4-4] Искусственный мех в соответствии с [4-3], где модифицированный фиброин представляет собой модифицированный фиброин шелка паука.
[0049] [4-5] Искусственный мех в соответствии с любым из [4-2]-[4-4], где модифицированный фиброин и вещество, придающее водостойкость, связаны ковалентной связью.
[0050] [4-6] Искусственный мех в соответствии с любым из [4-1]-[4-5], где вещество, придающее водостойкость, представляет собой по меньшей мере одно вещество, выбранное из группы, состоящей из полимера на основе силикона и полимера на основе фтора.
[0051] [4-7] Искусственный мех в соответствии с любым из [4-1]-[4-6], имеющий предельный кислородный индекс (LOI) 26,0 или более.
[0052] [4-8] Искусственный мех в соответствии с любым из [4-1]-[4-7], имеющий максимальный уровень влагопоглощения и выделения тепла более 0,025°C/г, определенный по следующей формуле A:
Формула A: максимальный уровень влагопоглощения и выделения тепла = {(максимальная температура образца после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г) [В формуле A, среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%].
[0053] [4-9] Искусственный мех в соответствии с [4-8], где максимальный уровень влагопоглощения и выделения тепла составляет 0,031°С/г или более.
[0054] [4-10] Искусственный мех в соответствии с любым из [4-1]-[4-9], имеющий индекс удерживания тепла более 0,18, определенный по следующей формуле B:
Формула B: индекс удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
[В формуле B, степень удерживания тепла (%) измеряют методом сухого контакта (температура: 30°C, скорость ветра: 30 см/сек) и вычисляют по формуле (1 - a/b)×100, где «a» означает количество тепла, рассеиваемого через тестируемый образец, а «b» означает количество тепла, рассеиваемого без тестируемого образца].
[4-11] Искусственный мех в соответствии с [4-10], где индекс удерживания тепла составляет 0,22 и более.
[0055] В своем пятом аспекте, настоящее изобретение относится к достижению пятой цели, например, к нижеследующим объектам изобретения, таким как:
[0056] [5-1] Способ изготовления искусственного меха, включающий применение волокна, содержащего искусственное белковое волокно, для получения ворсовой ткани, имеющей ворс, выступающий на одной или обеих поверхностях ткани; и разрезание петли ворса с образованием разрезного ворса.
[0057] В своем шестом аспекте, настоящее изобретение относится к достижению шестой цели, например, к нижеследующим объектам изобретения, таким как:
[0058] [6-1] Способ изготовления искусственного меха, включающий применение безусадочного белкового волокна, для получения ворсовой ткани, имеющей ворс, выступающий на одной или обеих поверхностях ткани; и разрезание петли ворса с образованием разрезного ворса.
[0059] [6-2] Способ изготовления искусственного меха, включающий применение волокна, содержащего белковое волокно, для получения ворсовой ткани, имеющей ворс, выступающий на одной или обеих поверхностях ткани; разрезание петли ворса с образованием разрезного ворса; и защиту ворса от усадки.
Преимущественные эффекты изобретения
[0060] В соответствии со своим первым аспектом, настоящее изобретение относится к изготовлению искусственного меха, который обладал бы достаточными влагопоглощающими свойствами и требовал бы меньшее количество энергии, необходимой для его изготовления.
[0061] В соответствии со своим вторым аспектом, настоящее изобретение относится к изготовлению искусственного меха, который обладал бы достаточными влагопоглощающими свойствами, требовал бы меньшее количество энергии, необходимой для его изготовления и предотвращал, насколько это возможно, изменение размеров при контактировании с водой.
[0062] В соответствии со своим третьим аспектом, настоящее изобретение относится к изготовлению искусственного меха с превосходными функциональными свойствами, такими как водостойкость.
[0063] В соответствии со своим четвертым аспектом, настоящее изобретение относится к изготовлению искусственного меха с превосходной водостойкостью.
[0064] В соответствии со своим пятым аспектом, настоящее изобретение относится к предпочтительному способу изготовления искусственного меха, который обладал бы достаточной влагопоглощающей способностью и требовал бы меньшее количество энергии, необходимой для его изготовления.
[0065] В соответствии со своим шестым аспектом, настоящее изобретение относится к предпочтительному способу изготовления искусственного меха, который обладал бы достаточной влагопоглощающей способностью, требовал бы меньшее количество энергии, необходимой для его изготовления, и предотвращал, насколько это возможно, изменение размеров при контактировании с водой.
Краткое описание чертежей
[0066] На фиг. 1 схематически проиллюстрирован пример последовательности домена модифицированного фиброина.
На фиг. 2 проиллюстрировано распределение значений z/w (%) в фиброине природного происхождения.
На фиг. 3 проиллюстрировано распределение значений x/y (%) в фиброине природного происхождения.
На фиг. 4 схематически проиллюстрирован пример последовательности домена модифицированного фиброина.
На фиг. 5 схематически проиллюстрирован пример последовательности домена модифицированного фиброина.
На фиг. 6 схематически представлен поясняющий пример прядильного устройства для производства белкового волокна (нитей).
На фиг. 7 представлен график, иллюстрирующий результаты оценки степени усадки изготовленного белкового волокна под действием воды.
На фиг. 8 представлен график, иллюстрирующий пример результатов испытаний для оценки влагопоглощающих свойств и степени выделения тепла.
На фиг. 9 представлена фотография, иллюстрирующая поверхность искусственного меха, изготовленного как описано в примере испытания 13.
На фиг. 10 представлена фотография, иллюстрирующая боковую поверхность искусственного меха, изготовленного, как описано в примере испытания 13.
Описание вариантов осуществления изобретения
[0067] Далее будут подробно описаны варианты осуществления настоящего изобретения. Однако, настоящее изобретение не ограничивается нижеследующими вариантами его осуществления.
[0068] <Первый вариант>
Искусственный мех согласно первому варианту первого аспекта изобретения включает искусственное белковое волокно.
[0069] Искусственное белковое волокно представляет собой штапельное волокно, изготовленное с применением белка в качестве основного исходного сырья. Примерами белков являются природные белки и рекомбинантные белки (искусственные белки). Рекомбинантные белки могут представлять собой любой белок, который может быть получен в промышленных масштабах, например, белки, используемые в промышленных целях, белки, используемые в медицинских целях, и структурные белки. Конкретными примерами белков, используемых в промышленных или в медицинских целях, являются ферменты, регуляторные белки, рецепторы, пептидные гормоны, цитокины, мембранные или транспортные белки, антигены, используемые для вакцинации, вакцины, антигенсвязывающие белки, иммуностимулирующие белки, аллергены, полноразмерные антитела, фрагменты антител и производные антител. Конкретными примерами структурных белков являются шелк паука, шелк тутового шелкопряда, кератин, коллаген, эластин, резилин и происходящие от них белки. Используемый здесь белок предпочтительно представляет собой модифицированный фиброин, а более предпочтительно, модифицированный фиброин шелка паука с точки зрения его превосходной способности удерживать тепло, влагопоглощающих и тепловыделяющих свойств и/или огнестойкости. В соответствии с этим вариантом осуществления изобретения, применение модифицированного фиброина (предпочтительно модифицированного фиброина шелка паука) в качестве белка позволяет придавать искусственному меху такие свойства, как способность удерживать тепло, влагопоглощающие свойства и способность выделять тепло и/или огнестойкость, что тем самым повышает ценность искусственного меха.
[0070] В настоящей заявке, волокна, полученные путем прядения структурного белка, модифицированного фиброина и модифицированного фиброина шелка паука, называются «искусственным структурным белковым волокном», «модифицированным фиброиновым волокном» и «модифицированным волокном фиброина шелка паука», соответственно.
[0071] Модифицированный фиброин согласно этому варианту осуществления изобретения представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n. К любому N-концу и C-концу или к обоим этим концам последовательности домена модифицированного фиброина может быть присоединена другая аминокислотная последовательность (N-концевая последовательность и C-концевая последовательность). N-концевая последовательность и С-концевая последовательность обычно представляют собой, но не ограничиваются ими, области без повторов аминокислотных мотивов, специфичных для фиброина, и каждая такая последовательность имеет приблизительно 100 аминокислотных остатков.
[0072] Используемый здесь термин «модифицированный фиброин» означает фиброин, полученный антропогенным путем (искусственный фиброин). Последовательность домена модифицированного фиброина может отличаться от аминокислотной последовательности фиброина природного происхождения или может быть такой же, как аминокислотная последовательность природного фиброина. Используемый здесь термин «Фиброин природного происхождения» в также означает белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n.
[0073] «Модифицированный фиброин» может представлять собой фиброин, имеющий аминокислотную последовательность природного фиброина как такового; фиброин, имеющий аминокислотную последовательность, модифицированную на основе аминокислотной последовательности природного фиброина (например, фиброин, имеющий аминокислотную последовательность, модифицированную путем модификации клонированной последовательности гена природного фиброина), или фиброин, искусственно созданный и синтезированный независимо от природного фиброина (например, фиброин, имеющий желаемую аминокислотную последовательность и полученный путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность).
[0074] Используемый здесь термин «последовательность домена» означает специфичную для фиброина аминокислотную последовательность, которая дает кристаллическую область (обычно соответствующую мотиву (A)n аминокислотной последовательности) и аморфную область (обычно соответствующую REP аминокислотной последовательности), представленную Формулой 1: [мотив (A)n-REP]m или Формулой 2: [мотив (A)n-REP]m-мотив (A)n. Используемый здесь термин «мотив (A)n» означает аминокислотную последовательность, которая в основном включает аланиновые остатки и имеет от 2 до 27 аминокислотных остатков. Количество аминокислотных остатков в мотиве (A)n может представлять собой целое число от 2 до 20, от 4 до 27, от 4 до 20, от 8 до 20, от 10 до 20, от 4 до 16, от 8 до 16 или от 10 до 16. Кроме того, доля остатков аланина в общем количестве аминокислотных остатков в мотиве (A)n может составлять 40% или более, или также может составлять 60% или более, 70% или более, 80% или более, 83% или более, 85% или более, 86% или более, 90% или более, 95% или более или 100% (то есть, в данном случае, мотив (A)n состоит из аланиновых остатков). Во множестве мотивов (A)n в последовательности домена, по меньшей мере семь мотивов (A)n могут состоять из аланиновых остатков. REP представляет собой аминокислотную последовательность, содержащую от 2 до 200 аминокислотных остатков. REP может представлять собой аминокислотную последовательность, содержащую от 10 до 200 аминокислотных остатков. Символ «m» означает целое число от 2 до 300 и может представлять собой целое число от 10 до 300. Множество мотивов (A)n могут иметь одинаковые или различные аминокислотные последовательности. Во множестве REP, REP могут представлять собой одинаковые или различные аминокислотные последовательности.
[0075] Модифицированный фиброин согласно этому варианту осуществления изобретения может быть получен, например, путем модификации аминокислотной последовательности, которая соответствует клонированной последовательности гена природного фиброина, имеющего по меньшей мере один замененный, делетированный, встроенный и/или добавленный аминокислотный остаток. Замена, делеция, инсерция и/или добавление аминокислотных остатков могут быть осуществлены известными методами, такими как сайт-направленный мутагенез. В частности, это может быть осуществлено методами, описанными в литературе, например, Nucleic Acid Res.10, 6487 (1982) и Methods in Enzymology, 100, 448 (1983).
[0076] «Фиброин природного происхождения» представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n, и их конкретный пример включает последовательности, которые продуцируются насекомыми или паукообразными.
[0077] Примеры фиброина, продуцируемого насекомыми, включают белки шелка, продуцируемые шелкопрядами (такими как Bombyx mori, Bombyx mandarina, Antheraea yamamai, Anteraea pernyi, Eriogyna pyretorum, Pilosamia Cynthia ricini, Samia cynthia, Caligura japonica, Antheraea mylitta и Antheraea assama) и белки шелка шершня, секретируемые личинками Vespa simillima xanthoptera.
[0078] Более конкретные примеры фиброина, продуцируемого насекомыми, включают L-цепь фиброина тутового шелкопряда (номер доступа в GenBank M76430 (нуклеотидная последовательность) и номер доступа AAA27840.1 (аминокислотная последовательность)).
[0079] Примерами фиброина, продуцируемого паукообразными, являются белки шелка паука, продуцируемые пауками, принадлежащими к Araneae. Конкретные примеры белков шелка паука включают белки, продуцируемые пауками, принадлежащими к роду Araneus, такими как Araneus ventricosus, Araneus diadematus, Araneus pinguis, Araneus pentagrammicus и Araneus nojimai, пауками, принадлежащими к роду Neoscona, такими как Neoscona scylla, Neoscona nautica, Neoscona adianta и Neoscona scylloides; пауками, принадлежащими к роду Pronus, такими как Pronous minutus; пауками, принадлежащими к роду Cyrtarachne такими как Cyrtarachne bufo и Cyrtarachne inaequalis; пауками, принадлежащими к роду Gasteracantha, такими как Gasteracantha kuhlii и Gasteracantha mammosa; пауками, принадлежащими к роду Ordgarius, такими как Ordgarius hobsoni и Ordgarius sexspinosus; пауками, принадлежащими к роду Argiope, такими как Argiope amoena, Argiope minuta и Argiope bruennichi; пауками, принадлежащими к роду Arachnura, такими как Arachnura logio; пауками, принадлежащими к роду Acusilas, такими как Acusilas coccineus, пауками, принадлежащими к роду Cytophora, такими как Cyrtophora moluccensis, Cyrtophora exanthematica и Cyrtophora unicolor; пауками, принадлежащими к роду Poltys, такими как Poltys illepidus; пауками, принадлежащими к роду Cyclosa, такими как Cyclosa octotuberculata, Cyclosa sedeculata, Cyclosa vallata и Cyclosa atrata; и пауками, принадлежащими к роду Chorizopes, такими как Chorizopes nipponicus. Кроме того, конкретные примеры белков шелка паука включают белки, продуцируемые пауками семейства Tetragnathidae, то есть, пауками, принадлежащими к роду Tetragnatha, такими как Tetragnatha praedonia, Tetragnatha maxillosa, Tetragnatha extensa и Tetragnatha squamata; пауками, принадлежащими к роду Leucauge, такими как Leucauge magnifica, Leucauge blanda и Leucauge subblanda; пауками, принадлежащими к роду Nephila, такими как Nephila clavata и Nephila pilipes; пауками, принадлежащими к роду Menosira, такими как Menosira ornata, пауками, принадлежащими к роду Dyschiriognatha, такими как Dyschiriognatha tenera; пауками, принадлежащими к роду Latrodectus, такими как Latrodectus mactans, Latrodectus hasseltii, Latrodectus geometricus и Latrodectus tredecimguttatus; и пауками, принадлежащими к роду Euprosthenops. Примерами белков шелка пауков являются белки шелка пауков-шелкопрядов, такие, как MaSp (MaSp1 и MaSp2) и ADF (ADF3 и ADF4), MiSp (MiSp1 и MiSp2), AcSp, PySp и Flag.
[0080] Конкретные примеры белка шелка пауков, продуцируемого паукообразными, включают фиброин-3 (adf-3) [полученный из Araneus diadematus] (номер доступа в GenBank AAC47010 (аминокислотная последовательность), U47855 (нуклеотидная последовательность)), фиброин-4 (adf-4) [полученный из Araneus diadematus] (номер доступа в GenBank AAC47011 (аминокислотная последовательность), U47856 (нуклеотидная последовательность)), белок спидроин 1 шелка паука-шелкопряда [полученный из Nephila clavipes] (номер доступа в GenBank AAC04504 (аминокислотная последовательность), U37520 (нуклеотидная последовательность)), спидроин 1 большого круглого паука [полученный из Latrodectus hesperus] (номер доступа в GenBank ABR68856 (аминокислотная последовательность), EF595246 (нуклеотидная последовательность)), белок спидроин 2 шелка паука-шелкопряда [полученный из Nephila clavata] (доступ в GenBank № AAL32472 (аминокислотная последовательность), AF441245 (нуклеотидная последовательность)), спидроин 1 большого круглого паука [полученный из Euprosthenops australis] (номер доступа в GenBank CAJ00428 (аминокислотная последовательность), AJ973155 (нуклеотидная последовательность)), спидроин 2 большого круглого паука [Eupros thenops Australis] (GenBank, No. CAM32249.1 (аминокислотная последовательность), AM490169 (нуклеотидная последовательность)), белок 1 шелка небольшого круглого паука [Nephila clavipes] (GenBank, No. AAC14589.1 (аминокислотная последовательность)), белок 2 шелка небольшого круглого паука [Nephila clavipes] (номер доступа в GenBank AAC14591.1 (аминокислотная последовательность)) и белок, подобный спидроину небольшого круглого паука [Nephilengys cruentata] (номер доступа в GenBank ABR37278.1 (аминокислотная последовательность).
[0081] Более конкретные примеры фиброина природного происхождения включают фиброин, информация о последовательности которого хранится в NCBI GenBank. Эти примеры можно найти в базе данных NCBI GenBank, где имеется информация о последовательностях. Так, например, из последовательностей, описанных как «INV» в «DIVISION», могут быть взяты последовательности с такими ключевыми словами, как «спидроин», «белок круглого паука», «фиброин», «шелк и полипептид» и «шелк и белок» в разделе «ОПРЕДЕЛЕНИЯ», или последовательности, содержащие цепочки символов определенного продукта в «CDS» и определенные цепочки символов в разделе «ИСТОЧНИК» для «ТИП ТКАНИ».
[0082] Модифицированный фиброин согласно этому варианту осуществления изобретения может представлять собой модифицированный фиброин шелка (или модифицированную аминокислотную последовательность белка шелка, продуцируемого шелкопрядом), или он может представлять собой модифицированный фиброин шелка паука (или модифицированную аминокислотную последовательность белка шелка паука, продуцируемую паукообразными).
[0083] Конкретные примеры модифицированного фиброина включают белок, происходящий от белка шелка, продуцируемого большим круглым пауком-шелкопрядом в железе паука, ответственной за продуцирование шелка (первый модифицированный фиброин); белок, имеющий последовательность домена с пониженным содержанием глициновых остатков (второй модифицированный фиброин); белок, имеющий последовательность домена с пониженным содержанием мотива (A)n (третий модифицированный фиброин); белок, имеющий пониженное содержание глициновых остатков и мотива (A)n (четвертый модифицированный фиброин); белок, имеющий последовательность домена, включающую область, определенный участок которой имеет высокий гидропатический индекс (пятый модифицированный фиброин); и белок, имеющий последовательность домена с пониженным содержанием глутаминовых остатков (шестой модифицированный фиброин).
[0084] Пример первого модифицированного фиброина включает белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. В первом модифицированном фиброине, количество аминокислотных остатков в мотиве (A)n предпочтительно составляет целое число от 3 до 20, более предпочтительно, целое число от 4 до 20, еще более предпочтительно, целое число от 8 до 20, еще более предпочтительно, целое число от 10 до 20, еще более предпочтительно, целое число от 4 до 16, особенно предпочтительно, целое число от 8 до 16, а наиболее предпочтительно, целое число от 10 до 16. В первом модифицированном фиброине, количество аминокислотных остатков, присутствующих в REP в Формуле 1, предпочтительно составляет от 10 до 200, более предпочтительно, от 10 до 150, еще более предпочтительно, от 20 до 100 и еще более предпочтительно, от 20 до 75. В первом модифицированном фиброине, общее количество глициновых остатков, сериновых остатков и аланиновых остатков, включенных в аминокислотную последовательность, представленную формулой 1: [мотив (A)n-REP]m, предпочтительно составляет 40% или более, более предпочтительно, 60% или более, а еще более предпочтительно, 70% или более по отношению к общему количеству аминокислотных остатков.
[0085] Первый модифицированный фиброин может представлять собой полипептид, имеющий звено аминокислотной последовательности, представленной формулой 1: [мотив (A)n-REP]m, и имеющий С-концевую последовательность, соответствующую аминокислотной последовательности любой из SEQ ID NO: 1 - SEQ ID NO: 3 или соответствующую аминокислотной последовательности, которая на 90% или более гомологична аминокислотной последовательности любой из SEQ ID NO: 1 - SEQ ID NO: 3.
[0086] Аминокислотная последовательность SEQ ID NO: 1 идентична аминокислотной последовательности, содержащей 50 аминокислотных остатков, включенных в С-конец аминокислотной последовательности ADF3 (GI: 1263287, NCBI). Аминокислотная последовательность SEQ ID NO: 2 идентична аминокислотной последовательности SEQ ID NO: 1, за исключением того, что у С-конца были удалены 20 аминокислотных остатков. Аминокислотная последовательность SEQ ID NO: 3 идентична аминокислотной последовательности SEQ ID NO: 1, за исключением того, что у С-конца были удалены 29 аминокислотных остатков.
[0087] Более конкретные примеры первого модифицированного фиброина включают (1-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 4 (рекомбинантный белок шелка паука ADF3KaiLargeNRSH1) и (1-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 4. При этом, предпочтительно, чтобы идентичность последовательностей составляла 95% или более.
[0088] Аминокислотная последовательность SEQ ID NO: 4 была получена с помощью нижеследующей мутации. То есть, в аминокислотной последовательности ADF3, имеющей N-конец, к которому была присоединена аминокислотная последовательность, включающая старт-кодон, метку His 10 и сайт распознавания протеазы HRV3C (протеазы риновируса 3C человека) (SEQ ID NO: 5), области повторов с первого по тринадцатый приблизительно удваиваются, и трансляция заканчивается на 1154-м аминокислотном остатке. С-концевая аминокислотная последовательность в аминокислотной последовательности SEQ ID NO: 4 идентична аминокислотной последовательности SEQ ID NO: 3.
[0089] Модифицированный фиброин (1-i) может иметь аминокислотную последовательность SEQ ID NO: 4.
[0090] Последовательность домена второго модифицированного фиброина имеет аминокислотную последовательность природного фиброина, за исключением того, что содержание остатков глицина было снижено. Другими словами, второй модифицированный фиброин имеет аминокислотную последовательность природного фиброина, за исключением того, что по меньшей мере один глициновый остаток в REP был заменен другим аминокислотным остатком.
[0091] Последовательность домена второго модифицированного фиброина может иметь аминокислотную последовательность природного фиброина, за исключением того, что один глициновый остаток по меньшей мере в одной последовательности мотива, выбранной из GGX и GPGXX, в REP был заменен другим аминокислотным остатком (где G представляет собой глициновый остаток, P представляет собой пролиновый остаток, а X представляет собой аминокислотный остаток, не являющийся глицином).
[0092] Во втором модифицированном фиброине, доля последовательностей мотивов, в которых глициновый остаток заменен другим аминокислотным остатком, может составлять 10% или более от всей последовательности мотива.
[0093] Второй модифицированный фиброин может иметь последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, и может иметь аминокислотную последовательность, в которой z/w составляет 30% или более, 40% или более, 50% или более, или 50,9% или более, где «z» представляет собой общее число аминокислотных остатков в аминокислотной последовательности, имеющей XGX (X представляет собой аминокислотный остаток, не являющийся глицином) и включенной во все REP последовательности домена, за исключением интервала от мотива (A)n, расположенного поблизости от C-конца последовательности домена, до С-конца, а «w» представляет собой общее количество аминокислотных остатков, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от C-конца последовательности домена, до С-конца. Отношение аланиновых остатков к общему числу аминокислотных остатков в мотиве (A)n составляет 83% или более, предпочтительно 86% или более, более предпочтительно 90% или более, еще более предпочтительно 95% или более, а наиболее предпочтительно 100% (то есть, в этом случае, мотив (A)n состоит из аланиновых остатков).
[0094] Во втором модифицированном фиброине, доля аминокислотных последовательностей, содержащих XGX, предпочтительно может быть увеличена путем замены одного глицинового остатка в мотиве GGX другим аминокислотным остатком. Во втором модифицированном фиброине, доля аминокислотных последовательностей, содержащих GGX в последовательности домена, предпочтительно составляет 30% или менее, более предпочтительно 20% или менее, еще более предпочтительно 10% или менее, еще более предпочтительно 6% или менее, а еще более предпочтительно 4% или менее, а особенно предпочтительно 2% или менее. Доля аминокислотных последовательностей, содержащих GGX, в последовательности домена, может быть вычислена методом, аналогичным нижеследующему методу вычисления доли аминокислотных последовательностей, имеющих XGX (z/w).
[0095] Метод вычисления z/w будет более подробно описан ниже. Сначала, в фиброине (модифицированном фиброине или природном фиброине), имеющем последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, аминокислотную последовательность, имеющую XGX, извлекают из всех REP последовательности домена, за исключением интервала от мотива (A)n, расположенного поблизости от C-конца последовательности домена, до С-конца. Общее число аминокислотных остатков, включенных в XGX, представлено буквой «z». Так, например, после удаления 50 аминокислотных последовательностей, имеющих XGX (не перекрывающихся), «z» составляет 50×3=150. Так, например, в аминокислотной последовательности, имеющей XGXGX, один X (X в центре) включают в два XGX, и перекрывающуюся часть вычитают для вычисления «z» (то есть, в XGXGX имеется 5 аминокислотных остатков). Символ «w» представляет собой общее количество аминокислотных остатков, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от C-конца последовательности домена, до С-конца, Так, например, в последовательности доменов, представленной на фиг. 1, «w» равно 4+50+4+100+4+10+4+20+4+30=230 (за исключением мотива (A)n, расположенного поблизости от C-конца). Затем «z» делят на «w» и вычисляют z/w (%).
[0096] Далее будет описано z/w в фиброине природного происхождения. Во-первых, при изучении информации об аминокислотных последовательностях, депонированных в NCBI GenBank вышеупомянутым способом, были обнаружены фиброины 663 типов (415 типов фиброина происходят от паукообразных). Среди всех экстрагированных фиброинов, z/w вычисляют вышеупомянутым методом вычисления на основе аминокислотной последовательности природного фиброина, имеющего последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, где доля аминокислотных последовательностей, имеющих GGX, составляет 6% или менее. На фиг. 2 показаны результаты. На фиг. 2, по оси абсцисс отложено z/w (%), а по оси ординат - частота. Как видно на фиг. 2, все значения z/w в природном фиброине составляют менее, чем 50,9% (наибольшее значение составляет 50,86%).
[0097] Во втором модифицированном фиброине, z/w предпочтительно составляет 50,9% или более, более предпочтительно 56,1% или более, еще более предпочтительно 58,7% или более, еще более предпочтительно 70% или более, а еще более предпочтительно 80% или более. Верхний предел z/w не имеет конкретных ограничений, и может составлять, например, 95% или менее.
[0098] Второй модифицированный фиброин может быть получен, например, путем модификации клонированной генной последовательности природного фиброина так, чтобы по меньшей мере часть нуклеотидной последовательности, кодирующей глициновый остаток, была заменена так, чтобы она кодировала другой аминокислотный остаток. В этом случае, в качестве модифицируемого глицинового остатка может быть выбран один глициновый остаток в мотиве GGX или в мотиве GPGXX, либо он может быть заменен так, чтобы z/w составляло 50,9% или более. Альтернативно, второй модифицированный фиброин может быть получен, например, путем конструирования аминокислотной последовательности, удовлетворяющей каждому из вышеперечисленных аспектов, из аминокислотной последовательности природного фиброина и путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность. В любом случае, аминокислотная последовательность природного фиброина может быть модифицирована не только путем замены глицинового остатка в REP аминокислотной последовательности другим аминокислотным остатком, но также путем замены, делеции, инсерции и/или добавления по меньшей мере одного аминокислотного остатка.
[0099] Другой аминокислотный остаток не имеет конкретных ограничений при условии, что он представляет собой аминокислотный остаток, отличающийся от глицинового остатка, но предпочтительно, представляет собой гидрофобный аминокислотный остаток, такой как остаток валина (V), остаток лейцина (L), остаток изолейцина (I), остаток метионина (M), остаток пролина (P), остаток фенилаланина (F) и остаток триптофана (W) или остаток гидрофильной аминокислоты, такой как остаток глутамина (Q), остаток аспарагина (N), остаток серина (S), остаток лизина (K) или остаток глутаминовой кислоты (E). Из этих примеров, более предпочтительным является остаток валина (V), остаток лейцина (L), остаток изолейцина (I), остаток фенилаланина (F) и остаток глутамина (Q), а особенно предпочтительно, остаток глутамина (Q).
[0100] Более конкретные примеры второго модифицированного фиброина включают (2-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 6 (Met-PRT380), SEQ ID NO: 7 (Met-PRT410), SEQ ID NO: 8 (Met-PRT525) или SEQ ID NO: 9 (Met-PRT799), и (2-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9.
[0101] Далее будет описан модифицированный фиброин (2-i). Аминокислотная последовательность SEQ ID NO: 6 является такой же, как аминокислотная последовательность SEQ ID NO: 10 (Met-PRT313), соответствующая фиброину природного происхождения, за исключением того, что все GGX в REP были заменены на GQX. Аминокислотная последовательность SEQ ID NO: 7 является такой же, как аминокислотная последовательность SEQ ID NO: 6, за исключением того, что каждые два мотива (A)n удалены от N-конца до C-конца, а один [мотив (A)n-REP]m встроен перед С-концевой последовательностью. Аминокислотная последовательность SEQ ID NO: 8 является такой же, как аминокислотная последовательность SEQ ID NO: 7, за исключением того, что два аланиновых остатка были встроены в боковую цепь каждого мотива (A)n поблизости от С-конца, а некоторые глутаминовые остатки (Q) были заменены сериновым остатком (S), и что некоторые аминокислоты, расположенные поблизости от C-конца, были делетированы так, чтобы они были по существу равны по молекулярной массе аминокислотной последовательности SEQ ID NO: 7. В аминокислотной последовательности SEQ ID NO: 9, предварительно определенная шарнирная последовательность и последовательность His-метки были присоединены к С-концу последовательности, полученной путем повторного 4-кратного введения области 20-доменной последовательности, присутствующей в аминокислотной последовательности SEQ ID. NO: 7 (где было заменено несколько аминокислотных остатков, расположенных поблизости от C-конца области).
[0102] Значение z/w в аминокислотной последовательности SEQ ID NO: 10 (соответствующей фиброину природного происхождения) составляет 46,8%. Значения z/w в аминокислотных последовательностях SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9 составляют 58,7%, 70,1%, 66,1% и 70,0%, соответственно. Кроме того, в случае соотношения Гизы (которое будет описано), составляющего от 1:1,8 до 11,3, значения x/y в аминокислотных последовательностях SEQ ID NO: 10, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9 составляют 15,0%, 15,0%, 93,4%, 92,7% и 89,8%, соответственно.
[0103] Модифицированный фиброин (2-i) может иметь аминокислотную последовательность SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9.
[0104] Модифицированный фиброин (2-ii) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9. Модифицированный фиброин (2-ii) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0105] Модифицированный фиброин (2-ii) предпочтительно имеет последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9 и имеет аминокислотную последовательность, в которой z/w составляет 50,9% или более, где «z» представляет собой общее количество аминокислотных остатков в аминокислотной последовательности, содержащей XGX (X представляет собой аминокислотный остаток, не являющийся глицином) и включенной в REP, а «w» означает общее количество аминокислотных остатков в REP в последовательности домена.
[0106] Второй модифицированный фиброин может включать последовательность метки на N-конце или на C-конце или на обоих концах. Это обеспечивает выделение, иммобилизацию, обнаружение и визуализацию модифицированного фиброина.
[0107] Последовательность метки может представлять собой, например, аффинную метку, обладающую специфической аффинностью к другой молекуле (способностью связываться с этой молекулой). Конкретный пример аффинной метки включает гистидиновую метку (His-метку). His-метка представляет собой короткий пептид, который имеет приблизительно от 4 до 10 последовательно расположенных гистидиновых остатков и специфически связывается с ионом металла, такого как никель. Соответственно, His-метка может быть использована для выделения модифицированного фиброина с помощью хроматографии на металле, образующем хелатный комплекс. Конкретный пример последовательности метки включает аминокислотную последовательность SEQ ID NO: 11 (аминокислотную последовательность, имеющую последовательность His-метки и шарнирную последовательность).
[0108] Кроме того, может быть использована последовательность метки, такая как глутатион-S-трансфераза (GST), которая специфически связывается с глутатионом или белком, связывающимся с мальтозой (MBP), который специфически связывается с мальтозой.
[0109] Также может быть использована «эпитопная метка», которая участвует в реакции антиген-антитело. Добавление пептида (эпитопа), обладающего антигенностью, в качестве последовательности метки, позволяет антителу связываться с эпитопом. Примеры эпитопной метки включают метку НА (пептидную последовательность гемагглютинина вируса гриппа), метку myc и метку FLAG. С помощью эпитопной метки, модифицированный фиброин может быть легко очищен с высокой специфичностью.
[0110] Кроме того, может быть использована последовательность метки, которая может быть расщеплена специфической протеазой. Модифицированный фиброин, отщепленный от такой последовательности метки, может быть восстановлен путем обработки белка, адсорбированного на последовательности метки, протеазой.
[0111] Более конкретные примеры модифицированного фиброина, имеющего последовательность метки, включают (2-iii) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 12 (PRT380), SEQ ID NO: 13 (PRT410), SEQ ID NO: 14 (PRT525) или SEQ ID NO: 15 (PRT799) и (2-iv) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15.
[0112] Аминокислотные последовательности SEQ ID NO: 16 (PRT313), SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 и SEQ ID NO: 15 получают путем присоединения аминокислотной последовательности SEQ ID NO: 11 (имеющей последовательность His-метки и шарнирную последовательность) к N-концам аминокислотных последовательностей SEQ ID NO: 10, SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9, соответственно.
[0113] Модифицированный фиброин (2-iii) может иметь аминокислотную последовательность SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15.
[0114] Модифицированный фиброин (2-iv) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15. Модифицированный фиброин (2-iv) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0115] Модифицированный фиброин (2-iv) предпочтительно имеет последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15 и имеет аминокислотную последовательность, где z/w составляет 50,9% или более, где «z» означает общее число аминокислотных остатков в аминокислотной последовательности, содержащей XGX (X представляет собой аминокислотный остаток, не являющийся глицином) и включенной в REP, а «w» означает общее число аминокислотных остатков в REP в последовательности домена.
[0116] Второй модифицированный фиброин может включать секреторный сигнал для высвобождения белка, продуцируемого в системе продуцирования рекомбинантного белка, за пределы организма хозяина. Последовательность секреторного сигнала может быть сконструирована соответствующим образом в зависимости от типа хозяина.
[0117] Последовательность домена третьего модифицированного фиброина имеет аминокислотную последовательность природного фиброина, за исключением того, что содержание мотива (A)n является сниженным. Другими словами, последовательность домена третьего модифицированного фиброина имеет аминокислотную последовательность природного фиброина, за исключением того, что по меньшей мере один мотив (A)n был делетирован.
[0118] Третий модифицированный фиброин может иметь аминокислотную последовательность природного фиброина, за исключением того, что от 10 до 40% мотивов (A)n были делетированы.
[0119] Последовательность домена третьего модифицированного фиброина может иметь аминокислотную последовательность природного фиброина, за исключением того, что по меньшей мере один мотив (A)n был удален из последовательности, состоящей из 1-3 мотивов (A)n от N-конца до C-конца.
[0120] Последовательность домена третьего модифицированного фиброина может иметь аминокислотную последовательность природного фиброина, за исключением того, что делеция по меньшей мере двух последовательных мотивов (A)n и делеция одного мотива (A)n повторялись в указанном порядке от N-конца до C-конца.
[0121] Последовательность домена третьего модифицированного фиброина может иметь аминокислотную последовательность, в которой по меньшей мере каждые два мотива (A)n были удалены от N-конца до C-конца.
[0122] Третий модифицированный фиброин имеет последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, и может иметь аминокислотную последовательность, в которой x/y составляет 20% или более, 30% или более, 40% или более, или 50% или более, и если сравнивать количества аминокислотных остатков в REP двух соседних звеньев [мотив (A)n-REP]m последовательно от N-конца к C-концу, то «x» означает максимальное общее число аминокислотных остатков в двух соседних звеньях [мотив (A)n-REP]m, в которых отношение аминокислотных остатков в одном REP к аминокислотным остаткам в другом REP (имеющем меньшее число аминокислотных остатков и определенном как 1) составляет от 1,8 до 11,3, а «y» означает общее число аминокислотных остатков в последовательности домена. Доля аланиновых остатков от общего количества аминокислотных остатков в мотиве (A)n составляет 83% или более, предпочтительно 86% или более, более предпочтительно 90% или более, еще более предпочтительно 95% или более, а наиболее предпочтительно 100% (то есть, в этом случае, мотив (A)n состоит из аланиновых остатков).
[0123] Способ вычисления x/y будет описан более подробно со ссылкой на фиг. 1. На фиг. 1 проиллюстрирована последовательность домена, за исключением N-концевой последовательности и C-концевой последовательности модифицированного фиброина. Эта последовательность домена имеет последовательность «мотив (A)n - первый REP (50 аминокислотных остатков)-мотив (A)n - второй REP (100 аминокислотных остатков)- мотив (A)n-третий REP (10 аминокислотных остатков)-мотив (A)n-четвертый REP (20 аминокислотных остатков)-мотив (A)n-пятый REP (30 аминокислотных остатков)-мотив (A)n» в указанном порядке от N-конца (левая сторона).
[0124] Два смежных звена [мотив (A)n-REP] последовательно выбирают от N-конца до C-конца без перекрывания. В то же время, могут присутствовать неотобранные звенья [мотив (A)n-REP]. На фиг. 1 показан паттерн 1 (сравнение первого REP и второго REP и сравнение третьего REP и четвертого REP), паттерн 2 (сравнение первого REP и второго REP и сравнение четвертого REP и пятого REP), паттерн 3 (сравнение второго REP и третьего REP и сравнение четвертого REP и пятого REP) и паттерн 4 (сравнение первого REP и второго REP). Следует отметить, что звенья [мотив (A)n-REP] могут быть выбраны другими способами.
[0125] Затем, для каждого паттерна, количество аминокислотных остатков сравнивают для REP выбранных двух соседних звеньев [мотив (A)n-REP]. Эти звенья сравнивают путем определения одного REP, имеющего меньшее количество аминокислотных остатков, как 1, и определения отношения аминокислотных остатков в другом REP к аминокислотным остаткам в одном REP, имеющем меньшее число аминокислотных остатков. Так, например, при сравнении первого REP (50 аминокислотных остатков) и второго REP (100 аминокислотных остатков), число аминокислотных остатков во втором REP составляет 100/50=2, где первый REP, имеющий меньшее количество аминокислотных остатков, определяют как 1. Аналогичным образом, при сравнении четвертого REP (20 аминокислотных остатков) и пятого REP (30 аминокислотных остатков), число аминокислотных остатков в пятом REP составляет 30/20=1,5, где четвертый REP, имеющий меньшее количество аминокислотных остатков, определяют как 1.
[0126] На фиг. 1, сплошными линиями обозначены серии звеньев [мотив (A)n-REP], в которых отношение аминокислотных остатков в одном REP к аминокислотным остаткам в другом REP, имеющем меньшее количество аминокислотных остатков (определено как 1), составляет 1,8:11,3. В данном случае, это отношение называется «коэффициентом Гизы». Пунктирными линиями обозначены серии звеньев [мотив (A)n-REP], в которых отношение аминокислотных остатков в одном REP к аминокислотным остаткам в другом REP, имеющем меньшее количество аминокислотных остатков (определено как 1), составляет менее 1,8 или более 11,3.
[0127] В каждом паттерне, все аминокислотные остатки в двух соседних звеньях [мотив (A)n-REP], обозначенные сплошными линиями, суммируют (включая не только количество аминокислотных остатков в REP, но также и количество аминокислотных остатков в мотивах (A)n). Затем сравнивают общие значения для паттернов, и один из них, имеющий наивысшее значение (максимальное общее значение), определяют как «x». В примере, показанном на фиг. 1, общее значение для паттерна 1 является максимальным.
[0128] Затем «x» делят на общее количество аминокислотных остатков «y» последовательности домена для вычисления x/y (%).
[0129] В третьем модифицированном фиброине, x/y предпочтительно составляет 50% или более, более предпочтительно 60% или более, еще более предпочтительно 65% или более, еще более предпочтительно 70% или более, еще более предпочтительно 75% или более, а особенно предпочтительно 80% или более. Верхний предел x/y не имеет конкретных ограничений, но может составлять, например, 100% или менее. Если отношение Гизы составляет от 1:1,9 до 11,3, то x/y предпочтительно составляет 89,6% или более. Если отношение Гизы составляет от 1:1,8 до 3,4, то x/y предпочтительно составляет 77,1% или более. Если отношение Гизы составляет от 1:1,9 до 8,4, то x/y предпочтительно составляет 75,9% или более. Если отношение Гизы составляет от 1:1,9 до 4,1, то x/y предпочтительно составляет 64,2% или более.
[0130] В случае, если третий модифицированный фиброин представляет собой модифицированный фиброин, в котором по меньшей мере семь из множества мотивов (A)n в последовательности домена состоят из аланининовых остатков, то x/y предпочтительно составляет 46,4% или более, более предпочтительно 50% или более, еще более предпочтительно 55% или более, еще более предпочтительно 60% или более, еще более предпочтительно 70% или более, а наиболее предпочтительно 80% или более. Верхний предел x/y не имеет конкретных ограничений, при условии, что он будет составлять 100% или менее.
[0131] В настоящей заявке будет описано x/y в фиброине природного происхождения. Во-первых, при изучении информации об аминокислотных последовательностях, депонированных в NCBI GenBank вышеупомянутым способом, было обнаружено 663 типа фиброина (415 типов фиброина происходят от паукообразных). Для всех экстрагированных фиброинов, х/у вычисляют вышеупомянутым методом вычисления на основе аминокислотной последовательности природного фиброина, имеющего последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Результаты для отношения Гизы от 1:1,9 до 4,1 показаны на фиг. 3.
[0132] На фиг. 3, на оси абсцисс отложены x/y (%), а на оси ординат - частота. Как видно на фиг. 3, все значения x/y в природном фиброине составляют менее 64,2% (наибольшее значение составляет 64,14%).
[0133] Третий модифицированный фиброин может быть получен, например, путем делеции по меньшей мере одной последовательности, кодирующей мотив (A)n, из клонированной генной последовательности природного фиброина, так, чтобы x/y составляло 64,2% или более. Кроме того, третий модифицированный фиброин может быть получен, например, путем конструирования аминокислотной последовательности природного фиброина, за исключением того, что по меньшей мере один мотив (A)n был делетирован так, чтобы x/y составляло 64,2% или более, или путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность. В любом случае, аминокислотная последовательность природного фиброина может быть модифицирована не только путем удаления мотива (A)n из аминокислотной последовательности, но также путем замены, делеции, инсерции и/или добавления по меньшей мере одного аминокислотного остатка.
[0134] Более конкретные примеры третьего модифицированного фиброина включают (3-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 17 (Met-PRT399), SEQ ID NO: 7 (Met-PRT410), SEQ ID NO: 8 (Met-PRT525) или SEQ ID NO: 9 (Met-PRT799) и (3-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9.
[0135] Далее будет описан модифицированный фиброин (3-i). Аминокислотная последовательность SEQ ID NO: 17 была получена путем удаления каждых двух мотивов (A)n от N-конца до C-конца из аминокислотной последовательности SEQ ID NO: 10 (Met-PRT313), соответствующей природному фиброину и путем встраивания одного звена [мотив (A)n-REP]m перед С-концевой последовательностью. Аминокислотная последовательность SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9 является такой, как она описана для второго модифицированного фиброина.
[0136] Если отношение Гизы составляет от 1:1,8 до 11,3, то значение x/y в аминокислотной последовательности SEQ ID NO: 10 (соответствующей фиброину природного происхождения) составляет 15,0%. Оба значения x/y в аминокислотных последовательностях SEQ ID NO: 17 и SEQ ID NO: 7 составляют 93,4%. В аминокислотной последовательности SEQ ID NO: 8, значение x/y составляет 92,7%. В аминокислотной последовательности SEQ ID NO: 9, значение x/y составляет 89,8%. В аминокислотных последовательностях SEQ ID NO: 10, SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9, значения z/w составляют 46,8%, 56,2%, 70,1%, 66,1% и 70,0%, соответственно.
[0137] Модифицированный фиброин (3-i) может иметь аминокислотную последовательность SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9.
[0138] Модифицированный фиброин (3-ii) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9. Модифицированный фиброин (3-II) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0139] Модифицированный фиброин (3-ii) предпочтительно имеет последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, и имеет аминокислотную последовательность, в которой x/y составляет 64,2% или более, где если сравнивать количества аминокислотных остатков в REP двух смежных звеньев [мотив (A)n-REP], последовательно расположенных от N-конца до C-конца, то «x» означает максимальное общее количество аминокислотных остатков в двух смежных звеньях [мотив (A)n-REP]m, где отношение аминокислотных остатков в одном REP к аминокислотным остаткам в другом REP (имеющем меньшее количество аминокислотных остатков и определенное как 1) составляет от 1,8 до 11,3 (отношение Гизы от 1:1,8 до 11,3), а «y» означает общее количество аминокислотных остатков в последовательности домена.
[0140] Третий модифицированный фиброин может включать вышеупомянутую последовательность метки на N-конце и C-конце или на том и другом конце.
[0141] Более конкретные примеры модифицированного фиброина, имеющего последовательность метки, включают (3-iii) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 18 (PRT399), SEQ ID NO: 13 (PRT410), SEQ ID NO: 14 (PRT525) или SEQ ID NO: 15 (PRT799) и (3-iv) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 18, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15.
[0142] Аминокислотные последовательности SEQ ID NO: 18, SEQ ID NO: 13, SEQ ID NO: 14 и SEQ ID NO: 15 получают путем присоединения аминокислотной последовательности SEQ ID NO: 11 (имеющей последовательность His-метки и шарнирную последовательность) к N-концам аминокислотных последовательностей SEQ ID NO: 17, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9, соответственно.
[0143] Модифицированный фиброин (3-iii) может иметь аминокислотную последовательность SEQ ID NO: 18, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15.
[0144] Модифицированный фиброин (3-iv) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 18, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15. Модифицированный фиброин (3-iv) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0145] Модифицированный фиброин (3-iv) предпочтительно на 90% или более идентичен аминокислотной последовательности SEQ ID NO: 18, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15 и имеет аминокислотную последовательность, в которой x/y составляет 64,2% или более, где если сравнивать количества аминокислотных остатков в REP двух смежных звеньев [мотив (A)n-REP], последовательно расположенных от N-конца до C-конца, то «x» означает максимальное общее количество аминокислотных остатков в двух смежных звеньях [мотив (A)n-REP], в которых отношение аминокислотных остатков в одном REP к аминокислотным остаткам в другом REP (имеющем меньшее число аминокислотных остатков и определенном как 1) составляет от 1,8 до 11,3, а «y» представляет собой общее количество аминокислотных остатков в последовательности домена.
[0146] Третий модифицированный фиброин может включать секреторный сигнал для высвобождения белка, продуцируемого в системе продуцирования рекомбинантного белка, за пределы организма хозяина. Последовательность секреторного сигнала может быть сконструирована соответствующим образом в зависимости от типа хозяина.
[0147] Последовательность домена четвертого модифицированного фиброина имеет аминокислотную последовательность природного фиброина, за исключением того, что содержание мотива (A)n и число глициновых остатков является сниженным. Другими словами, четвертый модифицированный фиброин имеет последовательность домена, имеющую аминокислотную последовательность природного фиброина, за исключением того, что по меньшей мере один мотив (A)n был не только был делетирован, но
также и один остаток глицина по меньшей мере в REP был заменен другим аминокислотным остатком. То есть, четвертый модифицированный фиброин представляет собой модифицированный фиброин, обладающий свойствами второго модифицированного фиброина и третьего модифицированного фиброина. Конкретные аспекты четвертого модифицированного фиброина являются такими же, как в описаниях второго модифицированного фиброина и третьего модифицированного фиброина.
[0148] Более конкретные примеры четвертого модифицированного фиброина включают (4-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 7 (Met-PRT410), SEQ ID NO: 8 (Met-PRT525), SEQ ID NO: 9 (Met-PRT799), SEQ ID NO: 13 (PRT410), SEQ ID NO: 14 (PRT525) или SEQ ID NO: 15 (PRT799) и (4-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 13, SEQ ID NO: 14, или SEQ ID NO: 15. Конкретные аспекты модифицированного фиброина, имеющего аминокислотную последовательность SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 13, SEQ ID NO: 14 или SEQ ID NO: 15, описаны ниже.
[0149] Последовательность домена пятого модифицированного фиброина может иметь аминокислотную последовательность, включающую область, имеющую, в определенном участке, высокий гидропатический индекс, который соответствует аминокислотной последовательности природного фиброина, за исключением того, что по меньшей мере один аминокислотный остаток в REP был заменен на аминокислотный остаток, имеющий высокий гидропатический индекс, и/или по меньшей мере один аминокислотный остаток, имеющий высокий гидропатический индекс, был встроен в REP.
[0150] Область, имеющая, в определенном участке, высокий гидропатический индекс, предпочтительно включает от двух до четырех последовательно расположенных аминокислотных остатков.
[0151] Аминокислотный остаток, имеющий высокий гидропатический индекс, более предпочтительно представляет собой аминокислотный остаток, выбранный из изолейцина (I), валина (V), лейцина (L), фенилаланина (F), цистеина (C), метионина (M) и аланина (А).
[0152] Пятый модифицированный фиброин может быть модифицирован не только путем замены по меньшей мере одного аминокислотного остатка в REP аминокислотной последовательности природного фиброина другим аминокислотным остатком, имеющим высокий гидропатический индекс, и/или путем встраивания по меньшей мере одного аминокислотного остатка, имеющего высокий гидропатический индекс, в REP, но также и путем замены, делеции, встраивания и/или добавления по меньшей мере одного аминокислотного остатка.
[0153] Пятый модифицированный фиброин может быть получен, например, путем замены по меньшей мере одного гидрофильного аминокислотного остатка в REP (например, аминокислотного остатка с отрицательным гидропатическим индексом) гидрофобным аминокислотным остатком (например, аминокислотным остатком, имеющим положительный гидропатический индекс) в клонированной генной последовательности природного фиброина, и/или путем встраивания по меньшей мере одного гидрофобного аминокислотного остатка в REP. Кроме того, пятый модифицированный фиброин может быть получен, например, путем конструирования аминокислотной последовательности природного фиброина, за исключением того, что по меньшей мере один гидрофильный аминокислотный остаток в REP заменяют гидрофобным аминокислотным остатком и/или по меньшей мере один гидрофобный аминокислотный остаток встраивают в REP, и путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность. В любом случае, аминокислотная последовательность природного фиброина может быть модифицирована не только путем замены по меньшей мере одного гидрофильного аминокислотного остатка гидрофобным аминокислотным остатком в REP аминокислотной последовательности и/или путем встраивания по меньшей мере одного гидрофобного аминокислотного остатка в REP аминокислотной последовательности, но также и путем замены, делеции, встраивания и/или добавления по меньшей мере одного аминокислотного остатка.
[0154] Пятый модифицированный фиброин может иметь последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, и может иметь аминокислотную последовательность, в которой p/q составляет 6,2% или более, где «p» представляет общее количество аминокислотных остатков, включенных в область, где четыре последовательно расположенных аминокислотных остатка имеют средний гидропатический индекс 2,6 или более во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена до С-конца, а «q» представляет собой общее количество аминокислотных остатков, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена до С-конца.
[0155] В настоящем изобретении, в качестве гидропатического индекса аминокислотного остатка используется известный индекс (Hydropathy index: Kyte J, & Doolittle R (1982) «A simple method for displaying the hydropathic character of a protein», J. Mol. Biol., 157, pp. 105-132). В частности, в нижеследующей таблице 1 представлен гидропатический индекс (далее также называемый «HI») каждой аминокислоты.
[0156]
[0157] Метод вычисления p/q будет более подробно описан ниже. В вычислениях используют последовательность домена, представленную формулой 1: [мотив (A)n-REP]m, за исключением интервала от мотива (A)n, расположенного поблизости от C-конца последовательности домена, до C-конца (далее также называемого «последовательностью A»). Сначала, для всех REP, включенных в последовательность A, вычисляют средний гидропатический индекс четырех последовательных аминокислотных остатков. Средний гидропатический индекс определяют путем деления суммы HI каждого аминокислотного остатка в четырех последовательных аминокислотных остатках на 4 (количество аминокислотных остатков). Средний гидропатический индекс определяют для всех четырех последовательных аминокислотных остатков (для вычисления, каждый аминокислотный остаток используют в среднем от одного до четырех раз). Затем определяют область, в которой четыре последовательных аминокислотных остатка имеют средний гидропатический индекс 2,6 или более. Даже когда определенный аминокислотный остаток соответствует множеству «четырех последовательных аминокислотных остатков, имеющих средний гидропатический индекс 2,6 или более», то считается, что эта область включает один аминокислотный остаток. Общее количество аминокислотных остатков, включенных в область, равно «p». Общее количество аминокислотных остатков, включенных в последовательность A, равно «q».
[0158] Так, например, в случае, когда «четыре последовательных аминокислотных остатка со средним гидропатическим индексом 2,6 или более» удаляют из 20 участков (без перекрывания), то имеется 20 серий из четырех последовательно расположенных аминокислотных остатков (без перекрывания) в области, где четыре последовательно расположенных аминокислотных остатка имеют средний гидропатический индекс 2,6 или более, и, таким образом, «p» составляет 20×4=80. Кроме того, например, в случае, если один аминокислотный остаток перекрывается в двух сериях из «четырех последовательно расположенных аминокислотных остатков, имеющих средний гидропатический индекс 2,6 или более», то область, где четыре последовательно расположенных аминокислотных остатка имеют средний гидропатический индекс 2,6 или более, рассматривается как включающая семь аминокислотных остатков (p=2×4-1=7). Перекрывающийся аминокислотный остаток вычитается, то есть, он обозначается «-1»). Так, например, последовательность домена, представленная на фиг. 4, включает семь серий «четырех последовательно расположенных аминокислотных остатков, имеющих средний гидропатический индекс 2,6 или более» без перекрывания, и, таким образом, «p» составляет 7×4=28. Кроме того, например, в последовательности доменов, представленной на фиг. 4, «q» равно 4+50+4+40+4+10+4+20+4+30=170 (исключая мотив (A)n в конце C-конца). Затем «p» делят на «q» и вычисляют p/q (%). В примере, проиллюстрированном на фиг. 4, 28/170=16,47%.
[0159] В пятом модифицированном фиброине, p/q предпочтительно составляет 6,2% или более, более предпочтительно 7% или более, еще более предпочтительно 10% или более, еще более предпочтительно 20% или более, а наиболее предпочтительно 30% или более. Верхний предел p/q не имеет конкретных ограничений, но он может составлять, например, 45% или менее.
[0160] Пятый модифицированный фиброин может быть получен, например, путем модификации клонированной аминокислотной последовательности природного фиброина с получением аминокислотной последовательности, включающей область, имеющую в определенном участке высокий гидропатический индекс, следующим образом. То есть, по меньшей мере один гидрофильный аминокислотный остаток в REP (например, аминокислотный остаток с отрицательным гидропатическим индексом) заменяют гидрофобным аминокислотным остатком (например, аминокислотным остатком с положительным гидропатическим индексом) и/или по меньшей мере один гидрофобный аминокислотный остаток встраивают в REP так, чтобы удовлетворялось вышеупомянутое условие p/q. Альтернативно, пятый модифицированный фиброин может быть получен, например, путем конструирования аминокислотной последовательности, удовлетворяющей условию p/q, из аминокислотной последовательности природного фиброина и путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность. В любом случае, аминокислотная последовательность природного фиброина может быть модифицирована не только путем замены по меньшей мере одного аминокислотного остатка в REP аминокислотной последовательности другим аминокислотным остатком, имеющим высокий гидропатический индекс, и/или путем встраивания по меньшей мере одного аминокислотного остатка, имеющего высокий гидропатический индекс, в REP аминокислотной последовательности, но также и путем замены, делеции, встраивания и/или добавления по меньшей мере одного аминокислотного остатка.
[0161] Аминокислотный остаток с высоким гидропатическим индексом не имеет конкретных ограничений, но предпочтительно представляет собой изолейцин (I), валин (V), лейцин (L), фенилаланин (F), цистеин (C), метионин (M) и аланин (A). Из этих примеров, более предпочтительными являются валин (V), лейцин (L) и изолейцин (I).
[0162] Более конкретные примеры пятого модифицированного фиброина включают (5-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 19 (Met-PRT720), SEQ ID NO: 20 (Met-PRT665) или SEQ ID NO: 21 (Met-PRT666), и (5-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 19, SEQ ID NO: 20 или SEQ ID NO: 21.
[0163] Далее будет описан модифицированный фиброин (5-i). Аминокислотную последовательность SEQ ID NO: 19 получают путем встраивания двух сайтов аминокислотной последовательности, имеющей три аминокислотных остатка (VLI), в каждый второй REP аминокислотной последовательности SEQ ID NO: 7 (Met-PRT410), за исключением последовательности домена на конце С-конца, а затем путем замены части глутаминовых остатков (Q) остатками серина (S) и удаления части аминокислот на С-конце. Аминокислотную последовательность SEQ ID NO: 20 получают путем встраивания одного сайта аминокислотной последовательности, имеющей три аминокислотных остатка (VLI), в каждый второй REP аминокислотной последовательности SEQ ID NO: 8 (Met-PRT525). Аминокислотную последовательность SEQ ID NO: 21 получают путем встраивания двух сайтов аминокислотной последовательности, имеющей три аминокислотных остатка (VLI), в каждый второй REP аминокислотной последовательности SEQ ID NO: 8.
[0164] Модифицированный фиброин (5-i) может иметь аминокислотную последовательность SEQ ID NO: 19, SEQ ID NO: 20 или SEQ ID NO: 21.
[0165] Модифицированный фиброин (5-ii) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 19, SEQ ID NO: 20 или SEQ ID NO: 21. Модифицированный фиброин (5-ii) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0166] Модифицированный фиброин (5-ii) предпочтительно имеет последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 19, SEQ ID NO: 20 или SEQ ID NO: 21, и имеет аминокислотную последовательность, в которой p/q составляет 6,2% или более, где «p» представляет собой общее количество аминокислотных остатков, включенных в область, где четыре последовательно расположенных аминокислотных остатков имеют средний гидропатический индекс 2,6 или более во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца, а «q» означает общее количество аминокислотных остатков, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца.
[0167] Пятый модифицированный фиброин может включать последовательность метки на N-конце или на C-конце или на том и другом конце.
[0168] Более конкретные примеры модифицированного фиброина, имеющего последовательность метки, включают (5-iii) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 22 (PRT720), SEQ ID NO: 23 (PRT665) или SEQ ID NO: 24 (PRT666), и (5-iv) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24.
[0169] Аминокислотные последовательности SEQ ID NO: 22, SEQ ID NO: 23 и SEQ ID NO: 24 получают путем присоединения аминокислотной последовательности SEQ ID NO: 11 (имеющей последовательность His-метки и шарнирную последовательность) к N-концам аминокислотных последовательностей SEQ ID NO: 19, SEQ ID NO: 20 и SEQ ID NO: 21, соответственно.
[0170] Модифицированный фиброин (5-iii) может иметь аминокислотную последовательность SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24.
[0171] Модифицированный фиброин (5-iv) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24. Модифицированный фиброин (5-iv) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m. Идентичность последовательностей предпочтительно составляет 95% или более.
[0172] Модифицированный фиброин (5-iv) предпочтительно имеет последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 22, SEQ ID NO: 23 или SEQ ID NO: 24 и имеет аминокислотную последовательность, в которой p/q составляет 6,2% или более, где «p» означает общее количество аминокислотных остатков, включенных в область, где четыре последовательно расположенных аминокислотных остатка имеют средний гидропатический индекс 2,6 или более во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца, а «q» означает общее количество аминокислотных остатков, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца.
[0173] Пятый модифицированный фиброин может включать секреторный сигнал для высвобождения белка, продуцируемого в системе продуцирования рекомбинантного белка, за пределы организма хозяина. Последовательность секреторного сигнала может быть сконструирована соответствующим образом в зависимости от типа хозяина.
[0174] Шестой модифицированный фиброин имеет аминокислотную последовательность природного фиброина, за исключением того, что он имеет пониженное содержание глутаминовых остатков.
[0175] В шестом модифицированном фиброине, по меньшей мере один мотив, выбранный из мотива GGX и мотива GPGXX, предпочтительно включен в аминокислотную последовательность REP.
[0176] В случае, если шестой модифицированный фиброин включает мотив GPGXX в REP, то содержание мотивов GPGXX обычно составляет 1% или более, а также оно может составлять 5% или более, а предпочтительно 10% или более. Содержание мотивов GPGXX не имеет конкретных ограничений по верхнему значению и может составлять 50% или менее, либо 30% или менее.
[0177] Используемый здесь термин «содержание мотивов GPGXX» означает величину, вычисленную с применением нижеследующего метода.
В фиброине, имеющем последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n (в модифицированном фиброине или природном фиброине), содержание мотивов GPGXX вычисляют как s/t, где «s» означает число, полученное путем утроения общего количества мотивов GPGXX во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца (то есть, общее количество G и P в мотивах GPGXX), а «t» означает общее количество аминокислотных остатков во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца, а также за исключением мотивов (A)n.
[0178] При вычислении содержания мотивов GPGXX, «последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца», используют для исключения негативного влияния на результаты вычисления содержания мотивов GPGXX, если «m» мало (то есть, если последовательность домена является короткой). Это связано с тем, что «интервал от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца» (последовательности, соответствующей REP) может включать последовательность, которая имеет низкую корреляцию со специфической последовательностью фиброина. В случае, если «мотив GPGXX» расположен на С-конце REP, и даже если «XX» представляет собой, например, «AA», то он рассматривается как «мотив GPGXX».
[0179] На фиг. 5 схематически показана последовательность домена модифицированного фиброина. Метод вычисления содержания мотивов GPGXX будет конкретно описан со ссылкой на фиг. 5. Сначала, в последовательности домена модифицированного фиброина, представленной на фиг. 5 (типа «[мотив (A)n-REP]m-мотив (A)n»), все REP включены в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца» (показано как «область А» на фиг. 5). Количество мотивов GPGXX для вычисления «s» равно 7, а «s» равно 7×3=21. Аналогичным образом, поскольку все REP включены в «последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца» (показано как «область A» на фиг. 5), то общее количество «t» аминокислотных остатков во всех REP, если мотивы (A)n дополнительно исключены из последовательности, составляет 50+40+10+20+30=150. Затем «s» делят на «t» для вычисления s/t (%). В модифицированном фиброине, показанном на фиг. 5, s/t составляет 21/150=14,0%.
[0180] В шестом модифицированном фиброине, содержание глутаминовых остатков предпочтительно составляет 9% или менее, более предпочтительно 7% или менее, еще более предпочтительно 4% или менее, а особенно предпочтительно 0%.
[0181] «Содержание глутаминовых остатков» означает здесь величину, вычисленную нижеследующим методом.
В фиброине, имеющем последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m- мотив (A)n (в модифицированном фиброине или в природном фиброине), содержание глутаминовых остатков вычисляют как u/t, где «u» означает общее количество глутаминовых остатков во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца (соответствующей «области А» на фиг. 5), а «t» означает общее количество аминокислотных остатков во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца и, кроме того, за исключением мотивов (A)n. При вычислении содержания глутаминовых остатков, «последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца» используется по причине, описанной выше.
[0182] Последовательность домена шестого модифицированного фиброина может иметь аминокислотную последовательность природного фиброина, за исключением того, что по меньшей мере один глутаминовый остаток в REP удаляют или по меньшей мере один глутаминовый остаток заменяют другим аминокислотным остатком.
[0183] «Другой аминокислотный остаток» может представлять собой аминокислотный остаток, не являющийся глутаминовым остатком, а предпочтительно он представляет собой аминокислотный остаток, имеющий более высокий гидропатический индекс, чем у глутаминового остатка. Гидропатический индекс каждого аминокислотного остатка показан в таблице 1.
[0184] Как показано в таблице 1, пример аминокислотного остатка, имеющего более высокий гидропатический индекс, чем у глутаминового остатка, включает остаток, выбранный из изолейцина (I), валина (V), лейцина (L), фенилаланина (F), цистеина (C), метионина (M), аланина (A), глицина (G), треонина (T), серина (S), триптофана (W), тирозина (Y), пролина (P) и гистидина (H). Из этих примеров, аминокислотный остаток более предпочтительно выбран из изолейцина (I), валина (V), лейцина (L), фенилаланина (F), цистеина (C), метионина (M) и аланина (A), а еще более предпочтительно из изолейцина (I), валина (V), лейцина (L) и фенилаланина (F).
[0185] В шестом модифицированном фиброине, каждый REP предпочтительно имеет уровень гидропатии -0,8 или более, более предпочтительно -0,7 или более, еще более предпочтительно 0 или более, еще более предпочтительно 0,3 или более, а особенно предпочтительно 0,4 или более. Верхний предел уровня гидропатии каждого REP не имеет конкретных ограничений, но может составлять 1,0 или менее или 0,7 или менее.
[0186] Используемый здесь термин «уровень гидропатии каждого REP» означает величину, вычисленную нижеследующим методом.
В фиброине, имеющем последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n (в модифицированном фиброине или в природном фиброине), уровень гидропатии каждого REP вычисляют как v/t, где «v» означает сумму гидропатических индексов для всех аминокислотных остатков во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца (соответствующей «области А» на фиг. 5), а «t» означает общее количество аминокислотных остатков во всех REP, включенных в последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца и, кроме того, за исключением мотивов (A)n. При вычислении уровня гидропатии каждого REP, «последовательность домена, за исключением интервала от мотива (A)n, расположенного поблизости от С-конца последовательности домена, до С-конца» используется по причине, описанной выше.
[0187] Последовательность домена шестого модифицированного фиброина может быть изменена не только путем удаления по меньшей мере одного глутаминового остатка в REP аминокислотной последовательности природного фиброина и/или путем замены по меньшей мере одного глутаминового остатка в REP другим аминокислотным остатком, но также и путем замены, делеции, встраивания и/или добавления по меньшей мере одного аминокислотного остатка.
[0188] Шестой модифицированный фиброин может быть получен, например, путем делеции по меньшей мере одного глутаминового остатка в REP из клонированной генной последовательности природного фиброина и/или путем замены по меньшей мере одного глутаминового остатка в REP другим аминокислотным остатком. Кроме того, шестой модифицированный фиброин может быть получен, например, путем конструирования аминокислотной последовательности природного фиброина, за исключением того, что по меньшей мере один глутаминовый остаток в REP был удален и/или по меньшей мере один глутаминовый остаток в REP заменен другим аминокислотным остатком, и путем химического синтеза нуклеиновой кислоты, кодирующей сконструированную аминокислотную последовательность.
[0189] Более конкретные примеры шестого модифицированного фиброина включают (6-i) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 25 (Met-PRT888), SEQ ID NO: 26 (Met-PRT965), SEQ ID NO: 27 (Met-PRT889), SEQ ID NO: 28 (Met-PRT916), SEQ ID NO: 29 (Met-PRT918), SEQ ID NO: 30 (Met-PRT699), SEQ ID NO: 31 (Met-PRT698), SEQ ID NO: 32 (Met-PRT966), SEQ ID NO: 41 (Met-PRT917) или SEQ ID NO: 42 (Met-PRT1028), и (6-ii) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательностью SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 41 или SEQ ID NO: 42.
[0190] Далее будет описан модифицированный фиброин (6-i). Аминокислотную последовательность SEQ ID NO: 25 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 (Met-PRT410) на VL. Аминокислотную последовательность SEQ ID NO: 26 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на TS и замены оставшегося Q на A. Аминокислотную последовательность SEQ ID NO: 27 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на VL и замены оставшегося Q на I. Аминокислотную последовательность SEQ ID NO: 28 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на VI и замены оставшегося Q на L. Аминокислотную последовательность SEQ ID NO: 29 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на VF и путем замены оставшегося Q на I.
[0191] Аминокислотную последовательность SEQ ID NO: 30 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 8 (Met-PRT525) на VL. Аминокислотную последовательность SEQ ID NO: 31 получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 8 на VL и замены оставшегося Q на I.
[0192] Аминокислотную последовательность SEQ ID NO: 32 получают путем замены всех QQ на VF в последовательности, полученной путем 2-кратного введения повторов области 20-доменной последовательности, присутствующей в аминокислотной последовательности SEQ ID NO: 7 (Met-PRT410), а затем замены оставшегося Q на I.
[0193] Аминокислотную последовательность SEQ ID NO: 41 (Met-PRT917) получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на LI и замены оставшегося Q на V. Аминокислотную последовательность SEQ ID NO: 42 (Met-PRT1028) получают путем замены всех QQ в аминокислотной последовательности SEQ ID NO: 7 на IF и путем замены оставшегося Q на T.
[0194] Каждая из аминокислотных последовательностей SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 41 и SEQ ID NO: 42 имеет содержание глутаминовых остатков 9% или менее (таблица 2).
[0195]
[0196] Модифицированный фиброин (6-i) может иметь аминокислотную последовательность SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 41 или SEQ ID NO: 42.
[0197] Модифицированный фиброин (6-ii) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 41 или SEQ ID NO: 42. Модифицированный фиброин (6-ii) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n. Идентичность последовательностей предпочтительно составляет 95% или более.
[0198] В модифицированном фиброине (6-ii), содержание глутаминовых остатков предпочтительно составляет 9% или менее. В модифицированном фиброине (6-ii), содержание мотивов GPGXX предпочтительно составляет 10% или более.
[0199] Шестой модифицированный фиброин может включать последовательность метки на N-конце или C-конце или на том и другом конце. Это позволяет осуществлять выделение, иммобилизацию, обнаружение и визуализацию модифицированного фиброина.
[0200] Более конкретные примеры модифицированного фиброина, имеющего последовательность метки, включают (6-iii) модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 33 (PRT888), SEQ ID NO: 34 (PRT965), SEQ ID NO: 35 (PRT889), SEQ ID NO: 36 (PRT916), SEQ ID NO: 37 (PRT918), SEQ ID NO: 38 (PRT699), SEQ ID NO: 39 (PRT698), SEQ ID NO: 40 (PRT966), SEQ ID NO: 43 (PRT917) или SEQ ID NO: 44 (PRT1028), и (6-iv) модифицированный фиброин, имеющий аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 43 или SEQ ID NO: 44.
[0201] Аминокислотные последовательности SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 43 и SEQ ID NO: 44 получают путем присоединения аминокислотной последовательности SEQ ID NO: 11 (имеющей последовательность His-метки и шарнирную последовательность) к N-концам аминокислотных последовательностей SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 41 и SEQ ID NO: 42, соответственно. К каждому N-концу добавляют только последовательность метки, которая не изменяет содержание глутаминовых остатков. Соответственно, все аминокислотные последовательности SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 43 и SEQ ID NO: 44 имеют содержание глутаминовых остатков 9% или менее (таблица 3).
[0202]
[0203] Модифицированный фиброин (6-iii) может иметь аминокислотную последовательность SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 43 или SEQ ID NO: 44.
[0204] Модифицированный фиброин (6-iv) имеет аминокислотную последовательность, которая на 90% или более идентична аминокислотной последовательности SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 43 или SEQ ID NO: 44. Модифицированный фиброин (6-iv) также представляет собой белок, имеющий последовательность домена, представленную формулой 1: [мотив (A)n-REP]m или формулой 2: [мотив (A)n-REP]m-мотив (A)n. Идентичность последовательностей предпочтительно составляет 95% или более.
[0205] В модифицированном фиброине (6-iv), содержание глутаминовых остатков предпочтительно составляет 9% или менее. В модифицированном фиброине (6-iv), содержание мотивов GPGXX предпочтительно составляет 10% или более.
[0206] Шестой модифицированный фиброин может включать секреторный сигнал для высвобождения белка, продуцируемого в системе продуцирования рекомбинантного белка, за пределы организма хозяина. Последовательность секреторного сигнала может быть сконструирована соответствующим образом в зависимости от типа хозяина.
[0207] Модифицированный фиброин может также представлять собой модифицированный фиброин, обладающий по меньшей мере двумя или более свойствами, которыми обладают первый модифицированный фиброин, второй модифицированный фиброин, третий модифицированный фиброин, четвертый модифицированный фиброин, пятый модифицированный фиброин и шестой модифицированный фиброин.
[0208] Модифицированный фиброин может представлять собой гидрофильный модифицированный фиброин или гидрофобный модифицированный фиброин. Используемый здесь «гидрофильный модифицированный фиброин» имеет средний гидропатический индекс (HI), равный нулю или менее, который вычисляют следующим образом. То есть, сначала вычисляют сумму HI для всех аминокислотных остатков, включенных в модифицированный фиброин, а затем эту сумму делят на общее количество аминокислотных остатков, и получают средний HI. Гидропатический индекс представлен в таблице 1. Кроме того, «гидрофобный модифицированный фиброин» имеет средний HI более нуля. Гидрофильный модифицированный фиброин обладает превосходной огнестойкостью. Гидрофобный модифицированный фиброин, в частности, обладает превосходными влагопоглощающими свойствами и способностью выделять тепло, и способностью удерживать тепло.
[0209] Примеры гидрофильного модифицированного фиброина включают модифицированные фиброины, имеющие аминокислотную последовательность SEQ ID NO: 4, аминокислотную последовательность SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, аминокислотную последовательность SEQ ID NO: 13, SEQ ID NO: 11, SEQ ID NO: 14 или SEQ ID NO: 15, аминокислотную последовательность SEQ ID NO: 18, SEQ ID NO: 7, SEQ ID NO: 8 или SEQ ID NO: 9, аминокислотную последовательность SEQ ID NO: 17, SEQ ID NO: 11, SEQ ID NO: 14 или SEQ ID NO: 15 и аминокислотную последовательность SEQ ID NO: 19, SEQ ID NO: 20 или SEQ ID NO: 21.
[0210] Примеры гидрофобного модифицированного фиброина включают модифицированные фиброины, имеющие аминокислотную последовательность SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33 или SEQ ID NO: 43 и аминокислотную последовательность SEQ ID NO: 35, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 39, SEQ ID NO: 40, SEQ ID NO: 41 или SEQ ID NO: 44.
[0211] Модифицированный фиброин согласно этому варианту осуществления изобретения может быть получен с применением стандартной технологии с применением нуклеиновой кислоты, кодирующей модифицированный фиброин. Нуклеиновая кислота, кодирующая модифицированный фиброин, может быть химически синтезирована на основе информации о нуклеотидной последовательности, или она может быть синтезирована, например, с помощью ПЦР.
[0212] Так, например, белок растворяют в растворителе, растворяющем белок, для приготовления прядильного раствора, и этот прядильный раствор формуют с применением известного метода прядения волокна, такого как мокрое прядение, сухое прядение, сухое-мокрое прядение и прядение из расплава, в результате чего получают искусственное белковое волокно. Примеры растворителя, растворяющего белок, включают диметилсульфоксид (ДМСО), N, N-диметилформамид (ДМФ), муравьиную кислоту и гексафторизопропанол (HFIP). Неорганическая соль может быть добавлена к растворителю в качестве стимулятора растворения.
[0213] (Искусственный мех)
Искусственный мех согласно этому варианту осуществления изобретения может включать волокно, отличающееся от искусственного белкового волокна, при условии, что это не будет негативно влиять на эффекты настоящего изобретения. Примеры других волокон включают синтетическое волокно, такое как найлон, полиамид, полиэфир, полиакрилонитрил, полиолефин, поливиниловый спирт, полиэтилентерефталат, политетрафторэтилен и акриловую смолу, регенерированное волокно, такое как купра, искусственный шелк и лиоцелл, и натуральное волокно, такое как хлопок, хлопчатобумажная ткань, шелк, шерсть и кашемир.
[0214] Искусственный мех согласно этому варианту осуществления изобретения может дополнительно включать компоненты, не являющиеся волокном. Примеры других компонентов включают красители, лубриканты, антиоксиданты, поглотители ультрафиолетового излучения, красители, наполнители, сшивающие агенты, матирующие агенты и выравнивающие агенты.
[0215] Согласно этому варианту осуществления изобретения, искусственный мех может иметь максимальный уровень влагопоглощения и выделения тепла более 0,025°C/г, определяемый в соответствии со следующей формулой A:
Формула A: максимальный уровень влагопоглощения и выделения тепла = {(максимальная температура образца, достигнутая после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г).
Следует отметить, что в соответствии с формулой A, среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%.
[0216] Искусственный мех согласно этому варианту осуществления изобретения может иметь максимальный уровень влагопоглощения и выделения тепла 0,026°C/г или более, 0,027°C/г или более, 0,028°C/г или более, 0,029°C/г или более, 0,030°C/г или более, 0,031°C/г или более, 0,035°C/г или более или 0,040°C/г или более. Верхний предел максимального уровня влагопоглощения и выделения тепла не имеет конкретных ограничений, но обычно он составляет 0,060°C/г или менее.
[0217] Искусственный мех согласно этому варианту осуществления изобретения может иметь предельный кислородный индекс (LOI) 18,0 или более, 20,0 или более, 22,0 или более, 24,0 или более, 26,0 или более, 28,0 или более, 29,0 или более и 30,0 или более. В настоящем описании, LOI представляет собой значение, измеренное с применением метода испытаний для гранулированных материалов или синтетической смолы, имеющей низкую температуру плавления, как предписано в Уведомлении № 50, выданном 31 мая 1995 г. начальником Агентства по безопасности при работе с опасными продуктами, по борьбе с пожарами и стихийными бедствиями.
[0218] Искусственный мех согласно этому варианту осуществления изобретения может иметь индекс удерживания тепла более 0,18, определенный в соответствии со следующей формулой B.
Формула B: индекс удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
В настоящем изобретении, степень удерживания тепла измеряют методом сухого контакта с применением Thermo Labo II (при скорости ветра 30 см/сек) и методом, описанным в Примерах.
[0219] Искусственный мех согласно этому варианту осуществления изобретения может иметь индекс удерживания тепла, например, 0,20 или более, 0,22 или более, 0,24 или более, 0,26 или более, 0,28 или более, 0,30 или более или 0,32 или более. Верхний предел индекса удерживания тепла не имеет конкретных ограничений и может составлять, например, 0,60 или менее или 0,40 или менее.
[0220] (Способ изготовления искусственного меха)
Искусственный мех согласно этому варианту осуществления изобретения может быть изготовлен, например, способом, включающим: изготовление ворсовой ткани, где вышеупомянутое волокно (волокно, включающее искусственное белковое волокно) используют для получения ворсовой ткани, имеющей большое число ворсинок, выступающих на одной поверхности или на обеих поверхностях ткани; фрагментацию для разрезания (среза) петли каждой ворсинки с получением разрезного ворса; и, при необходимости, расчесывание расческой разрезного ворса и/или мойку для промывки тканого полотна, на котором был образован разрезной ворс.
[0221] Изготовление ворсовой ткани может быть осуществлено, например, путем ворсового плетения и ворсового вязания, которые известны как способы изготовления ворсового тканого полотна или ворсового трикотажного полотна. При производстве ворсового тканого полотна, ворс могут быть образован при изготовлении основной пряжи (изготовлении основного ворса) или уточной пряжи (изготовлении уточного ворса). Размер каждой ворсинки (ворсовой петли) может быть соответствующим образом установлен в соответствии с применением искусственного меха и может составлять, например, 5 мм или более или 50 мм или менее.
[0222] Разрезание может быть осуществлено, например, в соответствии с общепринятой техникой изготовления разрезного ворса.
[0223] Следует отметить, что волокно, используемое для изготовления искусственной кожи согласно этому варианту осуществления изобретения, может включать искусственное белковое волокно, и вид волокна как пряжи не имеет конкретных ограничений. Другими словами, пряжа может представлять собой, например, пучок нитей, крученую пряжу, полученную путем скручивания такого пучка нитей, или штапельную пряжу, включая штапельное волокно. Штапельная пряжа может представлять собой крученую пряжу при условии, что она может быть изготовлена путем прядения. Пряжу такого типа изготавливают известным способом. Так, например, штапельная пряжа может быть получена способом, включающим: прядение волокна для формования волокнистого исходного сырья в соответствии с обычно применяемой техникой изготовления волокна; гофрирование для обжатия полученного волокна по мере необходимости; резку для разрезания волокна в целях получения штапельного полотна (короткоштапельного волокна); обработку водой для промывки штапельного волокна водой, если это необходимо; отбивку для разводки и/или дефибрации штапельного полотна, если это необходимо; и прядение штапельного полотна.
[0224] Прядение волокна может быть выполнено в соответствии с общепринятой техникой. Метод прядения волокна может представлять собой любой метод, такой, как мокрое прядение, сухое прядение, сухое-мокрое прядение и прядение из расплава.
[0225] Обжатие может быть осуществлено по мере необходимости, например, путем механического обжима, такого как прессование, или путем контактирования штапельного полотна с водной средой (далее называемого «обжатие водой»).
[0226] Водная среда представляет собой жидкую или газообразную (паровую) среду, содержащую воду (включая водяной пар). Водная среда может представлять собой воду или жидкую смесь воды и гидрофильного растворителя. Примеры гидрофильного растворителя включают летучие растворители, такие как этанол и метанол или пар из этих растворителей. Водная среда может представлять собой жидкую смесь воды и летучего растворителя, такого как этанол и метанол, и предпочтительно представляет собой воду или жидкую смесь воды и этанола. Применение водной среды, содержащей летучий растворитель или его пар, увеличивает скорость сушки после обжатия водой, что может придать извитому штапельному волокну ощущение мягкости. Соотношение между водой и летучим растворителем или его паром не имеет конкретных ограничений. Так, например, массовое соотношение вода:летучий растворитель или его пар может составлять от 10:90 до 90:10. Доля воды предпочтительно составляет 30 масс.% или более и может составлять 40 масс.% или 50 масс.% или более.
[0227] Водная среда предпочтительно представляет собой жидкость или газ при температуре от 10 до 230°C, включая воду (или водяной пар). Водная среда может иметь температуру 10°C или выше, 25°C или выше, 40°C или выше, 60°C или выше, или 100°C или выше, и может иметь температуру 230°C или ниже, 120°C или ниже, или 100°C или ниже.
[0228] Время контактирования с водной средой не имеет конкретных ограничений и может составлять 30 секунд или более, одну минуту или более или две минуты или более. С точки зрения производительности, время предпочтительно составляет 10 минут или менее. Контактирование с водной средой может осуществляться при нормальном давлении или при пониженном давлении (например, в вакууме).
[0229] В способе контактирования штапельного волокна с водной средой, это штапельное волокно может быть погружено в водную среду, или водная среда может быть распылена на это волокно. Альтернативно, штапельное волокно может быть подвергнуто воздействию окружающей среды, заполненной паром водной среды. В случае, если водной средой является пар, то водную среду подвергают контактированию со штапельным волокном с помощью обычного устройства для парообразования. Конкретные примеры устройства для парообразования включают устройство для парообразования типа FMSA (поставляемое Fukushin Kougyo. Co., Ltd.) и EPS-400 (поставляемое Tsujii Senki Kogyo). В конкретном способе обжима штапельного волокна с применением пара водной среды, например, штапельное волокно хранят в заранее подготовленной камере для хранения, а пар водной среды вводят в эту камеру для контактирования со штапельным волокном, а температуру внутри камеры для хранения доводят до заданной температуры (например, от 100°C до 230°C).
[0230] Штапельное волокно, контактирующее с водной средой, может быть высушено. Способ сушки не имеет конкретных ограничений и может представлять собой естественную сушку или сушку горячим воздухом или горячим валиком. Температура сушки не имеет конкретных ограничений и может составлять, например, от 20 до 150°C, предпочтительно от 40 до 120°C, а более предпочтительно от 60 до 100°C.
[0231] Резка может быть проведена на любом устройстве, подходящем для резки волокна. Пример такого устройства включает настольную машину для резки волокна (s/NO. IT-160201-NP-300). Длина штапельного волокна не имеет конкретных ограничений и может составлять, например, 20 мм или более. Штапельное волокно может иметь длину от 20 до 140 мм, от 70 до 140 мм или от 20 до 70 мм.
[0232] Обработка водой может быть осуществлена при необходимости способом, аналогичным способу обжатия водой или т.п.
[0233] Отбивка может быть осуществлена по мере необходимости и может быть проведена, например, путем вскрытия или дефибрации штапельного волокна на машине для отбивки (на разбивателе) или на дефибрирующей машине (на прочесывателе).
[0234] Прядение может быть осуществлено известным методом. Примеры метода прядения включают прядение хлопка, камвольное прядение и шерстопрядение. Эти примеры способа прядения не имеют конкретных ограничений по устройству, и этот способ может быть осуществлен с применением стандартного устройства. Штапельная пряжа может представлять собой однониточную пряжу или пряжу из смешанного волокна, такую как двухниточная пряжа (например, пряжа из смешанного волокна, состоящая из искусственного белкового волокна и другого вышеупомянутого волокна).
[0235] <Второй вариант>
Искусственный мех согласно второму варианту осуществления второго аспекта изобретения включает безусадочное белковое волокно.
[0236] Белковое волокно представляет собой штапельное волокно, полученное с применением белка в качестве основного сырья. Так, например, белок растворяют в растворителе для приготовления прядильного раствора, и этот прядильный раствор формуют с применением известного метода прядения волокна, такого как мокрое прядение, сухое прядение, сухое-мокрое прядение и прядение из расплава, в результате чего получают белковое волокно. Примеры растворителя, растворяющего белок, включают диметилсульфоксид (ДМСО), N, N-диметилформамид (ДМФ), муравьиную кислоту и гексафторизопропанол (HFIP). Неорганическая соль может быть добавлена к растворителю в качестве стимулятора растворения.
[0237] На фиг. 6 представлен схематически поясняющий пример прядильного устройства для изготовления белкового волокна. Прядильное устройство 1000, показанное на фиг. 6, представляет собой пример прядильного устройства для сухого-мокрого прядения, включающего экструдер 101, устройство 102 для производства невытянутой пряжи, устройство 103 для мокрого теплового вытягивания и сушильное устройство 104.
[0238] Далее будет описан способ прядения волокна с применением прядильного устройства 1000. Сначала раствор для прядения 106, хранящийся в резервуаре 107, вытягивают из фильеры 109 с помощью шестереночного насоса 108. В лаборатории, раствор для прядения может быть загружен в цилиндр, а затем его экструдируют из сопла с помощью шприцевого насоса. Затем, экструдированный раствор для прядения 106 подают в коагулирующую жидкость 111 в резервуаре для коагулирующей жидкости 120 через воздушный зазор 119 для удаления растворителя и коагуляции белка с получением волокнистого коагулята. Затем волокнистый коагулят подают в теплую воду 112 в ванне для вытяжки 121 и вытягивают. Степень удлинения определяют по отношению скоростей между выходным прижимным роликом 113 и приемным прижимным роликом 114. После этого, вытянутый волокнистый коагулят подают в сушильное устройство 104 и сушат в канале для пряжи 122 с получением белкового волокна 136 с последующей намоткой белкового волокна 136 для получения намотанной пряжи 105. Обозначения с 118а по 118g относятся к нитеводителям.
[0239] (Противоусадочная обработка)
Примеры метода предотвращения усадки белкового волокна включают: метод водной усадки, где белковое волокно после прядения, но до контакта с водой, подвергают контактированию с водой для необратимой усадки, и метод сухой термоусадки, где белковое волокно после прядения, но до контакта с водой, нагревают, а затем подвергают релаксации для необратимой усадки. Метод водной усадки и метод сухой термоусадки могут быть осуществлены на белковом волокне перед изготовлением искусственного меха, или они могут быть осуществлены на уже изготовленном искусственном мехе (до или после разрезания петли каждой ворсинки).
[0240] Считается, что необратимая усадка белкового волокна происходит, например, по следующим причинам. Одной из возможных причин является вторичная структура или третичная структура белкового волокна, а другой возможной причиной является снятие остаточного напряжения в белковом волокне, например, путем его вытягивания в процессе производства.
[0241] Метод водной усадки включает усадку, при которой белковое волокно после прядения, но до контакта с водой, подвергают контактированию с водой для необратимой усадки. При усадке, белковое волокно сжимается при контактировании с водой независимо от внешней силы. Вода, которую необходимо приводить в контакт, может представлять собой воду в жидком или газообразном состоянии. Способ осуществления контактирования белкового волокна с водой не имеет конкретных ограничений. Так, например, белковое волокно может быть погружено в воду, или вода при нормальной температуре, или вода в нагретом состоянии, например пар, может быть распылена на белковое волокно. Альтернативно, белковое волокно может подвергаться воздействию окружающей среды с высокой влажностью, наполненной водяным паром. Из этих примеров, предпочтительным является способ погружения белкового волокна в воду, поскольку он позволяет эффективно сократить время усадки и упростить технологическое оборудование. В конкретном способе погружения белкового волокна в воду, белковое волокно (или искусственный мех) помещают в контейнер, наполненный водой при заданной температуре, и приводят в контакт с водой.
[0242] Температура воды, которая должна контактировать с белковым волокном, не имеет конкретных ограничений, но предпочтительно, она составляет, например, температуру ниже точки кипения. Такая температура улучшает обрабатываемость и удобоукладываемость при усадке. Верхний предел температуры воды предпочтительно составляет 90°C или ниже, а более предпочтительно 80°C или ниже. Нижний предел температуры воды составляет предпочтительно 10°C или выше, более предпочтительно 40°C или выше и еще более предпочтительно 70°C или выше. Температуру воды, которую необходимо приводить в контакт с белковым волокном, можно регулировать в соответствии с волокном, включенным в белковое волокно. Кроме того, пока белковое волокно контактирует с влагой, температура воды может быть постоянной или она может быть изменена для достижения заданной температуры.
[0243] Время контактирования белкового волокна с водой не имеет конкретных ограничений и может составлять, например, одну минуту или более. Время может составлять 10 минут или более, 20 минут или более или 30 минут или более. Верхний предел времени не имеет конкретных ограничений, но может составлять, например, 120 минут или менее, 90 минут или менее или 60 минут или менее с точки зрения сокращения времени производственного процесса и исключения возможности гидролиза белкового волокна.
[0244] После усадки, метод водной усадки может дополнительно включать сушку белкового волокна после контактирования с водой.
[0245] Способ сушки не имеет конкретных ограничений и может включать, например, естественную сушку или принудительную сушку с применением сушильного оборудования. Температура сушки не имеет конкретных ограничений при условии, что она будет ниже температуры, при которой происходит термическое разрушение белка. Обычно, температура сушки составляет в пределах от 20 до 150°C, предпочтительно в пределах от 40 до 120°C, а более предпочтительно в пределах от 60 до 100°C. В этих температурных пределах можно быстро и эффективно высушить белковое волокно, не вызывая, при этом, термического разрушения или подобного повреждения белка. Время сушки выбирают соответствующим образом в соответствии с температурой сушки и т.п.
Так, например, время сушки может быть установлено таким образом, чтобы исключить влияние на качество, физические свойства и т.п. трикотажного или тканого материала из-за чрезмерного высыхания белкового волокна.
[0246] Метод сухой термоусадки включает нагревание белкового волокна после прядения, но до контакта с водой; и релаксацию и сжатие для ослабления и необратимой усадки нагретого белкового волокна.
[0247] При нагревании, температура нагрева предпочтительно равна или выше температуры размягчения белка, используемого в белковом волокне. В данном случае, температура размягчения белка представляет собой температуру, при которой начинается усадка из-за релаксации напряжения белкового волокна. При расслаблении и усадке путем нагревания при температуре, равной температуре размягчения белка или выше, волокно сжимается до такой степени, что оно не может быть получено только путем простого удаления влаги из волокна. Соответственно, полученное белковое волокно в достаточной степени защищено от усадки или изменения размеров из-за контакта с водой. Температура нагревания предпочтительно составляет 80°C или выше, более предпочтительно от 180 до 280°C, еще более предпочтительно от 200 до 240°C, а еще более предпочтительно от 220 до 240°C.
[0248] Время нагревания составляет предпочтительно 60 секунд или менее, более предпочтительно 30 секунд или менее, а еще более предпочтительно 5 секунд или менее с точки зрения удлинения волокна после термообработки. Считается, что продолжительность нагревания не оказывает существенного влияния на напряжение.
[0249] При релаксации и усадке, скорость релаксации предпочтительно превышена более чем в 1 раз, более предпочтительно в 1,4 раза или более, еще более предпочтительно в 1,7 раза или более, а особенно предпочтительно в 2 раза или более. Под скоростью релаксации понимается, например, отношение скорости подачи к скорости намотки белкового волокна.
[0250] (Белковое волокно и белок)
В искусственном мехе согласно второму варианту осуществления изобретения, усадку белкового волокна предотвращают путем обработки, предотвращающей усадку и тем самым изменение размеров из-за контакта с водой. Следовательно, белковое волокно (и белок), используемое для изготовления искусственного меха, может представлять собой белковое волокно, размер которого по своей природе может изменяться (значительно) из-за контакта с водой.
[0251] Так, например, белковое волокно во влажном состоянии может иметь степень усадки 2% или более. Степень усадки во влажном состоянии может составлять 4% или более, 6% или более, 8% или более, 10% или более, 15% или более, 20% или более, 25% или более или 30% или более. Верхний предел степени усадки во влажном состоянии обычно составляет 80% или менее. Степень усадки во влажном состоянии определяют по следующей формуле I:
Степень усадки во влажном состоянии = {1 - (длина белкового волокна во влажном состоянии после контакта с водой/длина белкового волокна после прядения, но до контакта с водой)}×100 (%) … (Формула I).
[0252] Кроме того, белковое волокно в сухом состоянии может иметь, например, степень усадки более 7%. Степень усадки в сухом состоянии может составлять 15% или более, 25% или более, 32% или более, 40% или более, 48% или более, 56% или более, 64% или более или 72% или более. Верхний предел степени усадки в сухом состоянии обычно составляет 80% или менее. Степень усадки в сухом состоянии определяют по следующей формуле II:
Степень усадки в сухом состоянии = {1 - (длина белкового волокна в сухом состоянии/длина белкового волокна после прядения, но до контакта с водой)}×100 (%) … (Формула II).
[0253] Белок, используемый в качестве исходного материала для получения белкового волокна, не имеет конкретных ограничений и может представлять собой любой белок. Примеры белка включают природные белки и рекомбинантные белки (искусственные белки). Рекомбинантные белки могут представлять собой любой белок, который может быть получен в промышленных масштабах, например белки, используемые в промышленных целях, белки, используемые в медицинских целях, и структурные белки. Конкретные примеры белков, используемых в промышленных или медицинских целях, включают ферменты, регуляторные белки, рецепторы, пептидные гормоны, цитокины, мембранные или транспортные белки, антигены, используемые для вакцинации, вакцины, антигенсвязывающие белки, иммуностимулирующие белки, аллергены, полноразмерные антитела, фрагменты антител и производные антител. Конкретные примеры структурных белков включают шелк паука, шелк шелкопряда, кератин, коллаген, эластин, резилин и белки, полученные из этих белков. Используемый здесь белок предпочтительно представляет собой модифицированный фиброин, а более предпочтительно, модифицированный фиброин шелка паука с точки зрения его превосходной способности удерживать тепло, влагопоглощающих и тепловыделяющих свойств и/или огнестойкости. Применение модифицированного фиброина (предпочтительно, модифицированного фиброина шелка паука) в качестве белка позволяет сообщать искусственному меху согласно этому варианту изобретения такие свойства, как способность удерживать тепло, влагопоглощающие и тепловыделяющие свойства и/или огнестойкость, что тем самым будет повышать ценность искусственного меха.
[0254] При изготовлении искусственного меха согласно этому варианту осуществления изобретения (второму варианту изобретения) может быть использован модифицированный фиброин, аналогичный модифицированному фиброину, используемому при изготовлении искусственного меха согласно первому варианту осуществления изобретения.
[0255] (Искусственный мех)
Искусственный мех согласно этому варианту осуществления изобретения может включать волокно, отличающееся от белкового волокна, при условии, что это не будет негативно влиять на эффекты изобретения. Примеры других волокон включают волокна, подобные волокну, включенному в искусственный мех согласно первому варианту осуществления изобретения.
[0256] Искусственный мех согласно этому варианту осуществления может дополнительно включать компоненты, отличающиеся от волокон. Примеры других компонентов включают компоненты, подобные другим компонентам, включенным в искусственный мех согласно первому варианту осуществления изобретения.
[0257] Искусственный мех согласно этому варианту осуществления изобретения может также иметь максимальный уровень влагопоглощения и выделения тепла, предельный кислородный индекс (LOI) и индекс удерживания тепла, аналогичные этим показателям для искусственного меха согласно первому варианту осуществления изобретения.
[0258] (Способ изготовления искусственного меха)
Искусственный мех согласно этому варианту осуществления изобретения может быть изготовлен, например, способом, включающим: изготовление ворсовой ткани, где вышеупомянутое волокно (волокно, включающее белковое волокно) используют для получения ворсовой ткани, имеющей ворсинки, выступающие на одной поверхности или на обеих поверхностях ткани; фрагментацию для разрезания (среза) петли каждой ворсинки с получением разрезного ворса; противоусадочную обработку для предотвращения усадки и, при необходимости, расчесывание расческой разрезного ворса и/или мойку для промывки тканого полотна, на котором был образован разрезной ворс. Внешний вид волокна, используемого при производстве ворсовой ткани, не имеет конкретных ограничений при условии, что такое волокно будет включать белковое волокно. Другими словами, при производстве ворсовой ткани можно использовать, например, крученую пряжу, полученную путем скручивания пучка нитей, или штапельную пряжу, включая штапельное волокно.
[0259] В частности, например, способ производства волокна согласно одному варианту осуществления изобретения включает защиту белкового волокна от усадки. В данном случае, белковое волокно может быть подвергнуто обработке для предотвращения усадки перед связыванием пряжи, перед скручиванием или перед прядением (в виде нитей или в виде штапельного волокна), либо оно может быть подвергнуто обработке для предотвращения усадки после связывания пряжи, после скручивания или после прядения. Кроме того, способ согласно этому варианту осуществления изобретения включает: изготовление ворсовой ткани, где безусадочное белковое волокно используют для изготовления ворсовой ткани, имеющей ворс, выступающий на одной или обеих поверхностях ткани; и разрезание (фрагментацию) петли ворса с образованием разрезного ворса. Этот способ может дополнительно включать расчесывание и/или промывку по мере необходимости.
[0260] Так, например, способ производства согласно другому варианту осуществления изобретения включает: изготовление ворсовой ткани, где волокно, включающее белковое волокно, используют для изготовления ворсовой ткани, имеющей ворс, выступающий на одной или на обеих поверхностях ткани, путем ворсового плетения или ворсового вязания; разрезание петли ворса с образованием разрезного ворса; и обработку ворсовой ткани для предотвращения усадки. Этот способ может дополнительно включать расчесывание и/или промывку по мере необходимости. Защита от усадки может быть проведена до или после разрезания.
[0261] Обработка против усадки, описанная в соответствии с этим аспектом, может быть применена для защиты от усадки.
[0262] Изготовление ворсовой ткани и разрезание могут быть аналогичны, например, изготовлению ворсовой ткани и разрезанию, применяемым при изготовлении искусственной кожи согласно первому варианту осуществления изобретения.
[0263] Штапельная пряжа может представлять собой крученую пряжу при условии, что она может быть изготовлена путем прядения. Пряжа такого типа может быть изготовлена известным способом, например, способом, включающим: прядение волокна для формования волокнистого исходного сырья в соответствии с обычно применяемой техникой изготовления волокна; гофрирование для обжатия полученного волокна по мере необходимости; резку для разрезания волокна в целях получения штапельного полотна (короткоштапельного волокна); отбивку для разводки и/или дефибрации штапельного полотна, если это необходимо; и прядение штапельного полотна.
[0264] Прядение волокна может быть осуществлено в соответствии с общепринятой техникой. Метод прядения волокна может представлять собой любой метод, такой, как мокрое прядение, сухое прядение, сухое-мокрое прядение и прядение из расплава.
[0265] Обжатие может быть осуществлено по мере необходимости, например, путем механического обжима, такого как прессование.
[0266] Стадии разрезания, отбивки и прядения также, например, аналогичны стадиям разрезания, отбивки и прядения, проводимым при изготовлении искусственной кожи согласно первому варианту осуществления изобретения. Длина штапельного волокна, изготовленного путем разрезания, не имеет конкретных ограничений и составляет, например, 20 мм или более, либо она может составлять от 20 до 140 мм, от 70 до 140 мм или от 20 до 70 мм.
[0267] <Третий вариант>
Искусственный мех согласно третьему варианту осуществления третьего аспекта изобретения включает волокно, обладающее функциональными свойствами.
[0268] Примеры волокна, включенного в искусственную кожу согласно этому варианту осуществления изобретения (третьему варианту изобретения), включают синтетическое волокно, такое как найлон, полиамид, полиэфир, полиакрилонитрил, полиолефин, поливиниловый спирт, полиэтилентерефталат, политетрафторэтилен и акриловую смолу, регенерированное волокно, такое как купра, искусственный шелк и лиоцелл, натуральное волокно, такое как хлопок, хлопчатобумажная ткань, шелк, шерсть и кашемир, искусственное волокно, такое как белковое волокно и их композиции.
[0269] Волокно предпочтительно включает модифицированный фиброин, а более предпочтительно модифицированный фиброин шелка паука. Присутствие модифицированного фиброина (предпочтительно модифицированного фиброина шелка паука) придает искусственному меху такие функциональные свойства, как способность удерживать тепло, влагопоглощающие и тепловыделяющие свойства и/или огнестойкость. Модифицированный фиброин может быть включен в искусственный мех в виде модифицированного фиброинового волокна (белкового волокна) или конъюгата, состоящего из модифицированного фиброинового волокна и другого волокна. Волокно, которое входит в состав искусственного меха согласно этому варианту осуществления изобретения (третьему варианту осуществления изобретения), может включать модифицированный фиброин, аналогичный фиброину, который предпочтительно используется в искусственном мехе согласно первому и второму вариантам осуществления изобретения.
[0270] Искусственный мех в соответствии с этим вариантом осуществления изобретения может обладать функциональными свойствами, поскольку он содержит вещество, придающее функциональные свойства (например, предварительно определенное вещество, перекрестно связывающееся с белком и модифицированный полимер, содержащий гидроксильную группу, во втором способе и в третьем способе, которые будут описаны ниже) в дополнение к нормальному волокну, или он может обладать функциональными свойствами, поскольку он содержит волокно, обладающее функциональными свойствами (например, модифицированное фиброин-содержащее волокно в первом методе, описанном ниже, и волокно, содержащее предварительно определенное вещество, перекрестно связывающееся с белком, и модифицированный полимер, содержащий гидроксильную группу, во втором способе и в третьем способе, которые будут описаны ниже).
[0271] Примерами способов придания искусственному меху функциональных свойств являются включение в искусственный мех модифицированного фиброина (первый способ), включение в искусственный мех предварительно определенного вещества, перекрестно связывающегося с белком (второй способ) или включение в искусственный мех модифицированного полимера, содержащего гидроксильную группу, где реакционноспособная функциональная группа связана с полимером, содержащим гидроксильную группу (третий способ).
[0272] (Первый способ)
В первом способе используют, например, модифицированное фиброин-содержащее волокно (белковое волокно или конъюгированное волокно) в качестве сырья для изготовления искусственного меха, обладающего функциональными свойствами. Модифицированное фиброин-содержащее волокно может быть получено путем прядения исходного материала, содержащего модифицированный фиброин, в соответствии с обычно применяемой технологией. Включение в волокно модифицированного фиброина будет сообщать этому волокну функциональные свойства, такие как способность удерживать тепло, влагопоглощающие и тепловыделяющие свойства и/или огнестойкость, и тем самым, сообщать искусственному меху согласно этому варианту осуществления изобретения функциональные свойства (способность удерживать тепло, влагопоглощающие и тепловыделяющие свойства и/или огнестойкость). Модифицированный фиброин предпочтительно представляет собой модифицированный фиброин шелка паука, поскольку он обладает преимущественными вышеуказанными функциональными свойствами. Подробное описание модифицированного фиброина приводится выше.
[0273] (Второй способ)
Во втором способе, предварительно определенное вещество, перекрестно связывающееся с белком, включает множество полипептидных остовов, множество первых остатков и множество вторых остатков. Первые остатки представляют собой остатки первого реагента, имеющего по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком. Вторые остатки представляют собой остатки второго реагента, имеющего одну вторую реакционноспособную группу, способную образовывать связь посредством реакции с первой реакционноспособной группой. По меньшей мере один из первых остатков перекрестно связывается с полипептидным остовом, и по меньшей мере один из первых остатков связан с полипептидным остовом на одном конце и со вторым остатком на другом конце.
[0274] Во втором способе используют, например, волокно, содержащее предварительно определенное вещество, перекрестно связывающееся с белком, в качестве исходного материала для изготовления искусственного меха, обладающего функциональными свойствами. Волокно, содержащее предварительно определенное вещество, перекрестно связывающееся с белком, может быть получено, например, путем прядения исходного материала, содержащего предварительно определенное вещество, перекрестно связывающееся с белком, в соответствии с обычно применяемой методикой. Волокно, содержащее предварительно определенное вещество, перекрестно связывающееся с белком, также может быть получено путем прядения исходного материала, содержащего белок, в соответствии с обычно применяемой технологией для получения белкового исходного волокна или композиционного исходного волокна (предшественника), а затем путем взаимодействия исходного волокна (предшественника) с первым реагентом и вторым реагентом для перекрестного сшивания белка в исходном волокне. Кроме того, во втором способе, например, с применением смеси нормального волокна и предварительно определенного вещества, перекрестно связывающегося с белком, в качестве исходного вещества, можно получить искусственный мех, обладающий функциональными свойствами.
[0275] Более конкретно, второй способ включает: первую стадию, в которой вещество-предшественник, содержащий белок, подвергают реакции с первым реагентом, имеющим по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком с образованием промежуточного соединения; и вторую стадию, в которой промежуточное соединение подвергают реакции взаимодействия со вторым реагентом, имеющим одну вторую реакционноспособную группу, способную образовывать связь посредством реакции с первой реакционноспособной группой, с образованием вещества. Примеры «вещества» в этом способе включают само предварительно определенное вещество, перекрестно связывающееся с белком (предшественником является сам белок) и белковое волокно или многокомпонентное волокно, содержащее белок (вещество-предшественник представляет собой белковую нить или композиционную нить, содержащую белок).
[0276] Первой стадией является взаимодействие вещества-предшественника, содержащего белок, с первым реагентом. Первый реагент представляет собой полифункциональный реагент, имеющий по меньшей мере две первые реакционноспособные группы, способные образовывать связь в результате реакции с белком. В первой стадии, белок может быть перекрестно связан с первым реагентом.
[0277] Белок имеет по меньшей мере одну реакционноспособную функциональную группу, выбранную из группы, состоящей из амидной группы, гидроксильной группы, фенольной гидроксильной группы, аминогруппы, карбоксильной группы, тиоловой группы, селенольной группы, имидазолильной группы, индолильной группы и гуанидиногруппы. Первые реакционноспособные группы первого реагента могут представлять собой группы, которые реагируют с реакционноспособной функциональной группой с образованием связи.
[0278] Первые реакционноспособные группы предпочтительно представляют собой электрофильные группы. В случае, когда первые реакционноспособные группы являются электрофильными группами, то связь легко образуется посредством реакции присоединения с реакционноспособной функциональной группой белка.
[0279] Предпочтительные примеры первых реакционноспособных групп или электрофильных групп включают группы, представленные следующими формулами (A-1), (A-2), (A-3), (A-4), (A-5), и (А-6). Волнистая линия в каждой формуле представляет связь каждой группы.
[0280] [Формула 1]
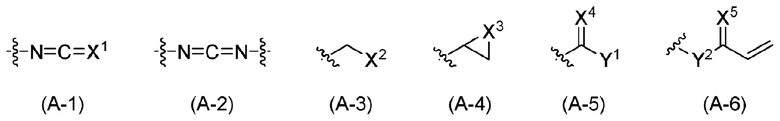
[0281] В формуле (A-1), X1 представляет собой атом кислорода (O) или атом серы (S). Более предпочтительно, X1 представляет собой атом кислорода.
[0282] В Формуле (A-3), X2 представляет собой уходящую группу. Уходящая группа не имеет конкретных ограничений при условии, что она дает возможность осуществлять реакцию нуклеофильного замещения реакционноспособной функциональной группой белка. Примеры уходящей группы включают атом галогена (атом фтора (F), атом хлора (Cl), атом брома (Br) и атом йода (I)), группу сложного эфира сульфоновой кислоты (-OSO2R1), группу сложного эфира карбоновой кислоты (-OCOR2) и четвертичную аммониевую группу (-NR33). R1 может представлять собой, например, атом фтора, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. R2 может представлять собой, например, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. R3 может представлять собой, например, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. R1, R2 и R3 могут иметь заместитель. Примеры заместителя включают алкильную группу, алкенильную группу, арильную группу и атом галогена.
[0283] Более предпочтительные примеры X2 включают атом хлора, атом брома, атом йода, сложноэфирную группу и сложноэфирную группу сульфоновой кислоты. Из этих примеров, более предпочтительными являются атом брома, атом йода и группа сложного эфира сульфоновой кислоты. Более предпочтительные примеры R1 включают атом фтора, алкильную группу (в частности, метильную группу, этильную группу, бензильную группу и аллильную группу), перфторалкильную группу (в частности, трифторметильную группу и пентафторэтильную группу) и арильную группу (в частности, фенильную группу, толильную группу, нафтильную группу и фторфенильную группу). Более предпочтительные примеры R2 включают алкильную группу (в частности, метильную группу, этильную группу, бензильную группу и аллильную группу), перфторалкильную группу (в частности, трифторметильную группу и пентафторэтильную группу) и арильную группу (в частности, фенильную группу, толильную группу, нафтильную группу и фторфенильную группу). Более предпочтительные примеры R3 включают алкильную группу (в частности, метильную группу, этильную группу, бензильную группу и аллильную группу) и арильную группу (в частности, фенильную группу, толильную группу, нафтильную группу и фторфенильную группу).
[0284] В формуле (A-4), Х3 представляет собой атом кислорода (O), атом серы (S), группу, представленную -NR4-, или группу, представленную -C(R5)2-. R4 может представлять собой, например, атом водорода, алкильную группу, арильную группу, галогенированную алкильную группу, галогенированную арильную группу, арилсульфонильную группу, алкилсульфонильную группу, ацильную группу или карбаматную группу. R5 представляет собой электроноакцепторную группу. Примеры электроноакцепторной группы включают карбонильную группу, цианогруппу, арильную группу, алкенильную группу и алкинильную группу. Две R5 могут быть одинаковыми или различными. R4 и R5 могут иметь заместитель. Примеры заместителя включают алкильную группу, алкенильную группу, арильную группу и атом галогена.
[0285] Более предпочтительно, Х3 представляет собой атом кислорода. Более предпочтительные примеры R4 включают арилсульфонильную группу, алкилсульфонильную группу, ацильную группу и карбаматную группу.
[0286] В формуле (A-5), Х4 представляет собой атом кислорода (O) или атом серы (S), а Y1 представляет собой атом галогена, гидроксильную группу, группу, представленную -R6, группу, представленную -OR6 или группу, представленную -OCOR6. R6 может представлять собой, например, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. R6 может иметь заместитель. Примеры заместителя включают алкильную группу, алкенильную группу, арильную группу и атом галогена.
[0287] Х4 более предпочтительно представляет собой атом кислорода. Y1 более предпочтительно представляет собой атом галогена, группу, представленную -OR6, группу, представленную -OCOR6 или т.п. Более предпочтительные примеры R6 включают алкильную группу и арильную группу.
[0288] В формуле (A-6), Х5 представляет собой атом кислорода (О) или атом серы (S), а Y2 представляет собой атом кислорода (O), атом серы (S) или группу, представленную NR7. R7 может представлять собой, например, алкилсульфонильную группу, арилсульфонильную группу, ацильную группу, карбаматную группу, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. R7 может иметь заместитель. Примеры заместителя включают алкильную группу, алкенильную группу, арильную группу и атом галогена.
[0289] Более предпочтительно, Х5 представляет собой атом кислорода. Еще более предпочтительно, Y2 представляет собой атом кислорода. Более предпочтительные примеры R7 включают алкилсульфонильную группу, арилсульфонильную группу, ацильную группу и карбаматную группу.
[0290] Первый реагент может представлять собой соединение, имеющее две или более первых реакционноспособных групп. Количество первых реакционноспособных групп первого реагента не имеет конкретных ограничений и может составлять, например, от 2 до 10000, а предпочтительно, от 2 до 1000.
[0291] Первая стадия может быть осуществлена, например, путем контактирования первого реакционного раствора, содержащего первый реагент, с веществом-предшественником и путем нагревания вещества-предшественника.
[0292] Первый реакционный раствор может не содержать растворителя или может дополнительно содержать растворитель. Растворитель первого реакционного раствора не имеет конкретных ограничений, при условии, что он может растворять первый реагент и не ингибирует реакцию между реакционноспособной функциональной группой белка и первой реакционноспособной группой. В случае, если первые реакционноспособные группы являются электрофильными группами, то предпочтительные примеры растворителя первого реакционного раствора включают N, N-диметилацетамид, N, N-диметилформамид, N-метилпирролидон, бензол, толуол, ксилол, мезитилен, тетрагидрофуран, диметилсульфоксид, этилацетат, бутилацетат и ацетат монометилового эфира пропиленгликоля.
[0293] Условия проведения реакции на первой стадии не имеют конкретных ограничений, при условии, что реакционноспособная функциональная группа белка будет реагировать с первой реакционноспособной группой.
[0294] В первой стадии, предпочтительно, чтобы по меньшей мере часть первого реагента перекрестно связывалась с белком, и по меньшей мере часть первых реакционноспособных групп оставалась в промежуточном продукте. То есть, в первой стадии предпочтительно получить промежуточное соединение, которое включает белок, перекрестно связанный с первым реагентом, и имеет первые реакционноспособные группы.
[0295] Так, например, в случае, если первый реагент представляет собой соединение, имеющее две первые реакционноспособные группы, то часть первого реагента может перекрестно связываться с белком (то есть обе первые реакционноспособные группы могут реагировать с белком). Кроме того, в другой части первых реакционноспособных групп, только одна из первых реакционноспособных групп может реагировать с белком, в то время как другая первая реакционноспособная группа может оставаться непрореагировавшей в промежуточном продукте.
[0296] Альтернативно, например, в случае, если первый реагент представляет собой соединение, имеющее три или более первых реакционноспособных групп, в части первого реагента, все первые реакционноспособные группы могут перекрестно связываться с белком (то есть, все первые реакционноспособные группы могут реагировать с белком), а в другой части первого реагента, часть первых реакционноспособных групп может реагировать с белком, а другая часть или другие части первых реакционноспособных групп могут оставаться непрореагировавшими в промежуточном продукте.
[0297] Реакция в первой стадии может также называться реакцией образования боковых цепей, имеющих первые реакционноспособные группы или структуры, перекрестно связанные с первым реагентом, если принять во внимание то, что реакционноспособная функциональная группа белка служит в качестве исходной точки. Количество перекрестно связанных структур и боковых цепей может быть скорректировано в зависимости от количества первого реагента, используемого в реакции. Уменьшение количества используемого первого реагента имеет тенденцию к образованию небольшого количества боковых цепей и большого количества перекрестно связанных структур, а увеличение количества используемого первого реагента имеет тенденцию к образованию небольшого количества перекрестно связанных структур и большого количества боковых цепей.
[0298] Количество перекрестно связанных структур и боковых цепей также может быть скорректировано, например, путем проведения предварительной стадии, а затем первой стадии, где часть первых реакционноспособных групп первого реагента реагирует со второй реакционноспособной группой второго реагента. Количество первых реакционноспособных групп, которые не прореагировали со второй реакционноспособной группой в предварительной стадии, может быть скорректировано соответствующим образом путем регуляции, например, количества второго реагента по сравнению с первым реагентом, используемым в предварительной стадии. Соответственно, в первой стадии, количество связей между первыми реакционноспособными группами и белком можно быть легко скорректировано, что позволяет легко регулировать количество перекрестно связанных структур и боковых цепей белка.
[0299] Другими словами, перед проведением первой стадии, второй способ может дополнительно включать: предварительную стадию, в которой часть первого реагента подвергают реакции с частью второго реагента так, чтобы часть первых реакционноспособных групп первого реагента реагировала с частью второй реакционноспособной группы второго реагента.
[0300] Образование множества перекрестно связанных структур имеет тенденцию к повышению, например, водостойкости (например, способности регулировать величину усадки из-за контакта с влагой и способности регулировать величину усадки во время сушки после контакта с влагой), механической прочности и термостойкости материала. Кроме того, образование множества боковых цепей имеет тенденцию улучшать функциональные свойства (например, описанную здесь структуру), сообщаемые этому материалу. Во втором способе, доля перекрестно связанных структур и боковых цепей может быть соответствующим образом отрегулирована в соответствии с желаемыми свойствами.
[0301] В первой стадии получают промежуточный продукт, содержащий реагирующее вещество, содержащее белок, и первый реагент. В реагирующем веществе, белок перекрестно связывается с первым реагентом, и при этом, может остаться непрореагировавшая первая реакционноспособная группа. Другими словами, реагирующее вещество может содержать полипептидный остов, происходящий от белка; перекрестно связанную часть, которая связывает полипептидный остов; и боковую цепь, которая связана с полипептидным остовом и имеет первую реакционноспособную группу на конце.
[0302] Вторая стадия представляет собой реакцию взаимодействия промежуточного продукта, полученного в первой стадии, со вторым реагентом. Второй реагент имеет одну вторую реакционноспособную группу, способную образовывать связь посредством взаимодействия с первой реакционноспособной группой. Вторая стадия может также представлять собой стадию взаимодействия первой реакционноспособной группы, оставщейся в промежуточном продукте, со вторым реагентом.
[0303] Вторая реакционноспособная группа второго реагента не имеет конкретных ограничений и может быть соответствующим образом заменена в зависимости от типа первых реакционноспособных групп. Так, например, если первые реакционноспособные группы являются электрофильными группами, то вторая реакционноспособная группа предпочтительно представляет собой нуклеофильную группу.
[0304] Примеры второй реакционноспособной группы или нуклеофильной группы включают гидроксильную группу, тиоловую группу, аминогруппу и группу, представленную следующей формулой (B-1).
[0305][Формула 2]
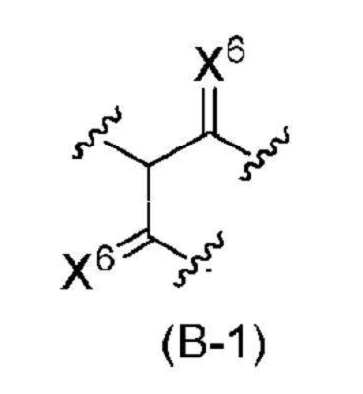
[0306] В формуле (B-1), Х6 представляет собой атом кислорода (O) или атом серы (S).
[0307] Примеры группы, представленной формулой (B-1), включают группу, представленную следующей формулой (B-1-1).
[0308][Формула 3]
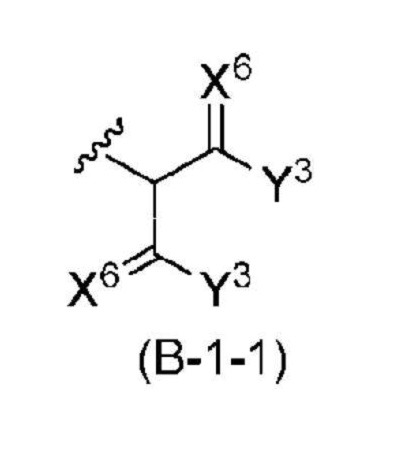
[0309] В формуле (B-1-1), Y3 представляет собой одновалентную группу. Примеры Y3 включают алкильную группу, алкенильную группу, алкинильную группу, арильную группу, алкоксигруппу, алкилсульфидную группу, арилсульфидную группу, монозамещенную аминогруппу и дизамещенную аминогруппу. Из этих примеров предпочтительными являются алкильная группа, арильная группа, алкоксигруппа и монозамещенная аминогруппа. Y3 может иметь заместитель. Примеры заместителя включают алкильную группу, алкенильную группу, арильную группу и атом галогена.
[0310] Второй реагент может представлять собой соединение, имеющее одну вторую реакционноспособную группу, и может дополнительно иметь реакционноспособную группу, которая является инертной по отношению к реакции во второй стадии (реакция между первой реакционноспособной группой и второй реакционноспособной группой). При реакции с таким вторым реагентом, функциональная группа может быть легко введена в материал, начиная с непрореагировавшей первой реакционноспособной группы в промежуточном продукте.
[0311] Функциональная группа не имеет конкретных ограничений и может представлять собой группу, которая непосредственно сообщает исходному веществу функциональные свойства, или может представлять собой группу, которая сообщает этому веществу способность реагировать с другим реагентом.
[0312] Примеры функциональной группы включают углеводородные группы, такие как алкильная группа, алкенильная группа и алкинильная группа; группы, имеющие кольцевую структуру, такие как арильная группа и гетероциклическая группа; реакционноспособные группы, защищенные защитной группой (такой как гидроксильная группа, аминогруппа и тиоловая группа); группы, имеющие карбонильную группу (-C(=O)-) или имеющие такую структуру, как эфирная связь (-O-), амидная связь (>NC(=O)-), уретановая связь (>NC(=O)O-), карбамидная связь (>N(C=O)N<) и карбонатная связь (-OC(=O)O-). Примеры функциональной группы также включают алкоксисилильную группу, сульфонильную группу (-S(=O)-, карбоксильную группу (-C(=O)OH), группу сульфоновой кислоты (-S(=O)2OH) и четвертичную аммониевую группу.
[0313] Так, например, если реакционноспособная группа представляет собой алкильную группу, то структура продукта улучшается. Следовательно, например, в случае, когда продукт является волокнистым, то второй реагент, имеющий алкильную группу в качестве функциональной группы, позволяет получить материал, имеющий превосходную структуру и хорошее качество на ощупь.
[0314] Что касается известного белкового продукта, то хотя перекрестное связывание повышает водостойкость и прочность материала, однако, его структура ухудшается, что может вызывать проблемы в том случае, когда белковый материал непосредственно касается кожи человека. Однако, согласно второму способу, с применением функциональной группы могут быть достигнуты отличная структура и превосходное качество на ощупь при сохранении водостойкости и механической прочности за счет перекрестного связывания. Соответственно, можно получить материал, который может быть предпочтительно использован для изготовления изделий, которые непосредственно соприкасаются с кожей человека.
[0315] Вторая стадия может быть осуществлена, например, путем контактирования второго реакционного раствора, содержащего второй реагент, с промежуточным продуктом и путем нагревания этого промежуточного продукта.
[0316] Второй реакционный раствор может не содержать растворителя и может дополнительно содержать растворитель. Растворитель второго реакционного раствора не имеет конкретных ограничений и может представлять собой, например, любой растворитель, который может растворять второй реагент и не ингибирует реакцию между первой реакционноспособной группой и второй реакционноспособной группой. Если первые реакционноспособные группы представляют собой электрофильные группы, а вторая реакционноспособная группа представляет собой нуклеофильную группу, то предпочтительные примеры растворителя второго реакционноспособного раствора включают N, N-диметилацетамид, N, N-диметилформамид, N-метилпирролидон, бензол, толуол, ксилол, мезитилен, тетрагидрофуран, диметилсульфоксид, этилацетат, бутилацетат и ацетат монометилового эфира пропиленгликоля.
[0317] Во второй стадии, количество используемого второго реагента не имеет конкретных ограничений. Так, например, количество используемого второго реагента может превышать количество первых реакционноспособных групп в промежуточном продукте.
[0318] Во второй стадии, часть или все первые реакционноспособные группы в промежуточном продукте утилизуются за счет реакции со второй реакционноспособной группой. Желательно, чтобы первые реакционноспособные группы не оставались в продукте на максимально возможном уровне. Соответственно, во втором способе предпочтительно, чтобы все первые реакционноспособные группы утилизовались в результате реакции со второй реакционноспособной группой или в результате другой побочной реакции.
[0319] Во второй стадии получают продукт, содержащий вещество, перекрестно связывающееся с белком.
[0320] Во втором способе, первый остаток указывает на структуру первого реагента, за исключением первых реакционноспособных групп. Кроме того, второй остаток указывает на структуру второго реагента, за исключением второй реакционноспособной группы.
[0321] Полипептидный остов и первый остаток связаны связью (карбамидной связью, если реакционноспособная функциональная группа является аминогруппой, а первые реакционноспособные группы являются изоцианатными группами), образованной посредством реакции реакционноспособной функциональной группы белка и первой реакционноспособной группы. Первый остаток и второй остаток связаны связью (уретановой связью в случае, когда, например, первые реакционноспособные группы являются изоцианатными группами, а вторая реакционноспособная группа представляет собой гидроксильную группу), образованной посредством реакции между первой реакционноспособной группой и второй реакционноспособной группой.
[0322] Во втором способе, белок перекрестно связывается посредством первого реагента, что сообщает продукту превосходную водостойкость, механическую прочность и термостойкость. Во втором способе, поскольку функциональная группа может быть введена посредством второго реагента, начиная с первой реакционноспособной группы, оставшейся в промежуточном продукте, то можно легко получить продукт с различными функциями.
[0323](Третий способ)
В третьем способе, модифицированный полимер, содержащий гидроксильную группу, представляет собой полимер, в котором реакционноспособная функциональная группа связана с полимером, содержащим гидроксильную группу. Модифицированный полимер, содержащий гидроксильную группу, может быть получен, например, посредством реакции полимера, содержащего гидроксильную группу, с реагентом, имеющим реакционноспособную функциональную группу.
[0324] Полимер, содержащий гидроксильную группу, может быть использован без каких-либо конкретных ограничений, при условии, что он будет представлять собой полимерное соединение, имеющее гидроксильную группу. Конкретные примеры полимера, содержащего гидроксильную группу, включают полисахарид, такой как крахмал, гликоген, целлюлоза, хитин, агароза, гиалуроновая кислота, хондроитинсульфат, пектин и каррагенан; и синтетический полимер, такой как поливиниловый спирт (ПВС) и фенольная смола.
[0325] С точки зрения биоразлагаемости, полимер, содержащий гидроксильную группу, предпочтительно представляет собой полисахарид. Кроме того, с точки зрения высокой растворимости в дополнение к способности к биологическому разложению, полимер, содержащий гидроксильную группу, предпочтительно представляет собой крахмал.
[0326] Реакционноспособная функциональная группа представляет собой функциональную группу, обладающую свойством (таким как гидрофобное свойство и гидрофильное свойство), соответствующим передаваемым функциональным свойствам (например, водостойкости, гидрофильности, липофильности и маслостойкости), и эту группу выбирают в соответствии с функциональными свойствами, которые она сообщает.
[0327] Так, например, для повышения водостойкости, в качестве реакционноспособной функциональной группы может быть использована алкильная группа, такая как метильная группа, этильная группа, н-пропильная группа и изопропильная группа, ароматическая группа, такая как фенильная группа и нафтильная группа и гидрофобная функциональная группа или ацильная группа, такая как ацетильная группа, пропаноильная группа и бензоильная группа.
[0328] Реагент, имеющий реакционноспособную функциональную группу, представляет собой соединение, имеющее функциональную группу и дополнительно имеющее связывающую функциональную группу, связанную с полимером, содержащим гидроксильную группу. Связывающая функциональная группа может представлять собой функциональную группу, которая может быть связана с полимером, содержащим гидроксильную группу, водородной связью или ковалентной связью, но предпочтительно, она представляет собой функциональную группу, которая может быть ковалентно связана с полимером, содержащим гидроксильную группу, а более предпочтительно, она представляет собой функциональную группу, которая может быть ковалентно связана с гидроксильной группой в полимере, содержащем гидроксильную группу.
[0329] Примеры реагента, имеющего реакционноспособную функциональную группу, включают изоцианаты, имеющие реакционноспособную функциональную группу (RN=C=O, где R представляет собой реакционноспособную функциональную группу), ангидриды кислот (RC(=O)-OC(=O)-R, где R представляет собой функциональную группу), эпоксиды, азиридины и алкилгалогениды. Предпочтительные примеры реагента, имеющего реакционноспособную функциональную группу, включают изоцианат, имеющий реакционноспособную функциональную группу, и ангидрид уксусной кислоты, поскольку эти реагенты могут быть ковалентно связаны с гидроксильной группой в полимере, содержащем гидроксильную группу. Изоцианат, имеющий реакционноспособную функциональную группу, является более предпочтительным, поскольку в него может быть введена любая функциональная группа.
[0330] В третьем способе используют, например, волокно, содержащее модифицированный полимер, содержащий гидроксильную группу, в качестве сырья для изготовления искусственного меха, обладающего функциональными свойствами. Волокно, содержащее модифицированный полимер, включающий гидроксильную группу, может быть получено, например, путем прядения исходного материала, смешанного с модифицированным полимером, содержащим гидроксильную группу, в соответствии с обычно применяемой технологией. Кроме того, в третьем способе, например, с применением смеси обычного волокна и модифицированного полимера, содержащего гидроксильную группу, в качестве исходного материала, можно получить искусственный мех, обладающий функциональными свойствами.
[0331] Содержание модифицированного полимера, включающего гидроксильную группу, в исходном материале не имеет конкретных ограничений и может быть соответствующим образом установлено в зависимости от сообщаемых функциональных свойств и т.п. Содержание модифицированного полимера, включающего гидроксильную группу, может составлять, например, от 0,001 до 70 масс.%, от 0,01 до 65 масс.% или от 0,1 до 60 масс.% от общей массы искусственного меха.
[0332] Модифицированный полимер, содержащий гидроксильную группу, предпочтительно связан с волокном водородной связью. Это еще больше улучшает функциональные свойства. Водородная связь может образовываться, например, между функциональной группой в модифицированном полимере, содержащем гидроксильную группу (например, функциональная группа может быть гидроксильной группой, функциональной реакционноспособной группой или связывающей функциональной группой), и функциональной группой в волокне (например, аминогруппой и карбоксильной группой в белковом волокне).
[0333] В третьем способе, искусственный мех может дополнительно включать полимер, содержащий гидроксильную группу. Полимер, содержащий гидроксильную группу, предпочтительно представляет собой полимер такого же типа, как и полимер, содержащий гидроксильную группу, который является исходным материалом для модифицированного полимера, содержащего гидроксильную группу. Если искусственный мех включает полимер, содержащий гидроксильную группу, то содержание полимера, содержащего гидроксильную группу, может составлять 50 масс.% или более, 60 масс.% или более, 70 масс.% или более или 80 масс.% или более по отношению к 100 масс.% от общего количества модифицированного полимера, содержащего гидроксильную группу, и полимера, содержащего гидроксильную группу. Верхний предел может составлять 90 масс.% или менее.
[0334] Искусственный мех, полученный вторым или третьим способом, может содержать, а может и не содержать модифицированный фиброин.
[0335] Искусственный мех согласно этому варианту осуществления изобретения может дополнительно включать компоненты, отличающиеся от волокна. Примеры других компонентов включают красители, лубриканты, антиоксиданты, поглотители ультрафиолетового излучения, красители, наполнители, сшивающие агенты, матирующие агенты и выравнивающие агенты в дополнение к заранее определенному веществу, перекрестно связывающемуся с белком, и модифицированному полимеру, содержащему гидроксильные группы.
[0336] Даже в искусственном мехе согласно этому варианту осуществления изобретения, если используется модифицированное фиброин-содержащее волокно, то искусственный мех может иметь максимальный уровень влагопоглощения и выделения тепла, предельный кислородный индекс (LOI) и индекс удерживания тепла, аналогичные параметрам искусственного меха согласно первому варианту осуществления изобретения.
[0337] (Способ изготовления искусственного меха)
С применением вышеупомянутого волокна (волокна, содержащего искусственное белковое волокно), искусственный мех согласно этому варианту осуществления изобретения может быть изготовлен способом, например, аналогичным способу изготовления искусственного меха согласно первому варианту осуществления изобретения.
[0338] <Четвертый пример>
Искусственный мех согласно четвертому варианту четвертого аспекта изобретения включает волокно и вещество, придающее водостойкость.
[0339] Примеры волокна, включенного в искусственную кожу согласно этому варианту осуществления изобретения (четвертому варианту), включают синтетическое волокно, такое как найлон, полиамид, полиэфир, полиакрилонитрил, полиолефин, поливиниловый спирт, полиэтилентерефталат, политетрафторэтилен и акриловую смолу, регенерированное волокно, такое как купра, искусственный шелк и лиоцелл, натуральное волокно, такое как хлопок, хлопчатобумажная ткань, шелк, шерсть и кашемир, искусственное волокно, такое как белковое волокно, и их композиции.
[0340] Волокно предпочтительно включает модифицированный фиброин, а более предпочтительно модифицированный фиброин шелка паука. Присутствие модифицированного фиброина (предпочтительно модифицированного фиброина шелка паука) придает искусственному меху такие функциональные свойства, как способность удерживать тепло, влагопоглощающие и тепловыделяющие свойства и/или огнестойкость. Модифицированный фиброин может быть включен в искусственный мех в виде модифицированного фиброинового волокна (белкового волокна) или конъюгата, состоящего из модифицированного фиброинового волокна и другого волокна. Волокно, которое входит в состав искусственного меха согласно этому варианту осуществления изобретения (четвертому варианту осуществления изобретения), может включать модифицированный фиброин, аналогичный фиброину, который предпочтительно используется в искусственном мехе согласно первому, второму и третьему вариантам осуществления изобретения.
[0341] Так, например, белок растворяют в растворяющем растворителе для приготовления прядильного раствора, и прядильный раствор формуют с применением известного метода прядения волокон, такого как мокрое прядение, сухое прядение, сухое-мокрое прядение и прядение из расплава с получением белкового волокна. Примеры растворителя, растворяющего белок, включают диметилсульфоксид (ДМСО), N, N-диметилформамид (ДМФ), муравьиную кислоту и гексафторизопропанол (HFIP). Неорганическая соль может быть добавлена к растворителю в качестве стимулятора растворения.
[0342] Белковое волокно, содержащее модифицированный фиброин, может содержать другой белок, отличающийся от модифицированного фиброина. Другой белок не имеет конкретных ограничений и может быть любым белком.
[0343] (Вещество, придающее водостойкость)
Вещество, придающее водостойкость, представляет собой вещество, способное повышать водостойкость искусственного меха. Благодаря веществу, придающему водостойкость, искусственный мех приобретает улучшенные водоотталкивающие свойства и безусадочные свойства при его контакте с водой. Соответственно, искусственный мех также имеет улучшенные водонепроницаемые свойства. Искусственный мех может содержать вещество одного вида, придающее водостойкость, или он может содержать такое вещество двух или более видов.
[0344] Конкретные примеры вещества, придающего водостойкость, включают гидрофобный полимер, такой как полимер на основе фтора и полимер на основе силикона, а также модифицированный полимер, содержащий гидроксильную группу, где гидрофобная функциональная группа связана с полимером, содержащим гидроксильную группу. Если искусственный мех включает белок, то конкретные примеры вещества, придающего водостойкость, также включают вещество, связывающееся с белком, такое как полифункциональный реагент, имеющий по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком (первый реагент), и реагент, имеющий по меньшей мере одну первую реакционноспособную группу, способную образовывать связь посредством реакции с белком, и имеющий функциональную группу.
[0345] Полимер на основе фтора не имеет конкретных ограничений, при условии, что он представляет собой полимер, содержащий фтор. Полимер на основе фтора может, например, представлять собой полимер, полученный посредством полимеризации олефина, содержащего фтор. Примеры полимера на основе фтора включают политетрафторэтилен, политрифторэтилен, полихлортрифторэтилен, поливинилфторид, поливинилиденфторид, полиперфторалкилвиниловый эфир, полиперфторпропилен, сополимер политетрафторэтилена и перфторпропилена, сополимер тетрафторэтилена и этилена и сополимер поливинилфторида и этилена. Полимер на основе фтора может представлять собой сополимер (статистический сополимер, блок-сополимер или чередующийся сополимер), полученный посредством полимеризации двух или более мономеров, включенных в вышеупомянутые полимеры.
[0346] Полимер на основе силикона не имеет конкретных ограничений, при условии, что он представляет собой полимер, имеющий полисилоксановую структуру в основной цепи. Полимер на основе силикона может представлять собой, например, гомополимер или сополимер (статистический сополимер, блок-сополимер или чередующийся сополимер), полученный посредством полимеризации мономеров одного или по меньшей мере двух видов, имеющих силоксановое структурное звено. Полимер на основе силикона может представлять собой сополимер (статистический сополимер, блок-сополимер или чередующийся сополимер), полученный посредством полимеризации мономеров одного или по меньшей мере двух видов, имеющих силоксановое структурное звено и мономеров одного или по меньшей мере двух видов, не имеющих силоксанового структурного звена.
[0347] Модифицированный полимер, содержащий гидроксильную группу, представляет собой полимер, в котором гидрофобная функциональная группа связана с полимером, содержащим гидроксильную группу. Модифицированный полимер, содержащий гидроксильную группу, может быть получен, например, посредством реакции взаимодействия полимера, содержащего гидроксильную группу, с реагентом, имеющим гидрофобную функциональную группу.
[0348] Полимер, содержащий гидроксильную группу, может быть использован без конкретных ограничений, при условии, что он представляет собой полимерное соединение, имеющее гидроксильную группу. Конкретные примеры полимера, содержащего гидроксильную группу, включают полисахарид, такой как крахмал, гликоген, целлюлоза, хитин, агароза, гиалуроновая кислота, хондроитинсульфат, пектин и каррагенан; и синтетический полимер, такой как поливиниловый спирт (ПВС) и фенольная смола. С точки зрения биоразлагаемости, полимер, содержащий гидроксильную группу, предпочтительно представляет собой полисахарид. Кроме того, с точки зрения высокой растворимости в дополнение к способности к биологическому разложению, полимер, содержащий гидроксильную группу, предпочтительно представляет собой крахмал.
[0349] Реагент, имеющий гидрофобную функциональную группу, представляет собой соединение, имеющее гидрофобную функциональную группу и дополнительно имеющее связывающую функциональную группу, связанную с полимером, содержащим гидроксильную группу. Связывающая функциональная группа может представлять собой функциональную группу, которая может быть связана с полимером, содержащим гидроксильную группу, посредством водородной связи или ковалентной связи, но предпочтительно, она представляет собой функциональную группу, которая может быть ковалентно связана с полимером, содержащим гидроксильную группу, а более предпочтительно, функциональную группу, которая может быть ковалентно связана с гидроксильной группой в полимере, содержащем гидроксильную группу. Примеры гидрофобной функциональной группы включают алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа и изопропильная группа; ароматические группы, такие как фенильная группа и нафтильная группа; и ацильные группы, такие как ацетильная группа, пропаноильная группа и бензоильная группа. Примеры реагента, имеющего гидрофобную функциональную группу, включают изоцианаты, имеющие гидрофобную функциональную группу (RN=C=O, где R представляет собой гидрофобную функциональную группу), ангидриды кислот (RC(=O)-OC(=O)-R, где R представляет собой гидрофобную функциональную группу), эпоксиды, азиридины и алкилгалогениды.
[0350] Содержание гидрофобного полимера в искусственном мехе согласно этому варианту осуществления изобретения может составлять от 0,001 до 70 масс.%, от 0,01 до 65 масс.%, от 0,1 до 60 масс.%, от 1 до 50 масс.%, от 1 до 40 масс.%, от 1 до 30 масс.%, от 1 до 20 масс.%, от 1 до 10 масс.% или от 1 до 5 масс.% от общей массы искусственного меха.
[0351] Примеры вещества, связующегося с белком, включают полифункциональный реагент, имеющий по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком (первый реагент), и реагент, имеющий по меньшей мере одну первую реакционноспособную группу, способную образовывать связь посредством реакции с белком, и функциональную группу (функциональный реагент).
[0352] Первый реагент имеет первые реакционноспособные группы, способные образовывать связь посредством реакции взаимодействия по меньшей мере с одной реакционноспособной функциональной группой, выбранной из группы, состоящей из амидной группы, гидроксильной группы, фенольной гидроксильной группы, аминогруппы, карбоксильной группы, тиоловой группы, селенольной группы, имидазолильной группы, индолильной группы и гуанидиногруппы, включенных в белок.
[0353] Примеры первых реакционноспособных групп включают группы, представленные следующими формулами (A-1), (A-2), (A-3), (A-4), (A-5) и (A-6). Волнистая линия в каждой формуле представляет связь каждой группы.
[Формула 1]
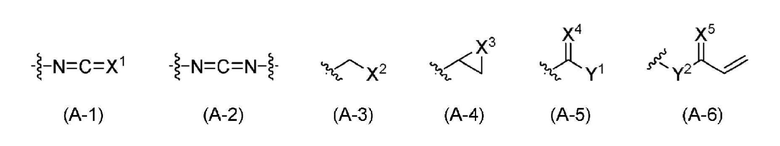
[0354] В формуле (A-1), X1 представляет собой атом кислорода (O) или атом серы (S). В Формуле (A-3), X2 представляет собой уходящую группу. В формуле (A-4), Х3 представляет собой атом кислорода (O), атом серы (S), группу, представленную -NR4-, или группу, представленную -C(R5)2-. R4 может представлять собой, например, атом водорода, алкильную группу, арильную группу, галогенированную алкильную группу, галогенированную арильную группу, арилсульфонильную группу, алкилсульфонильную группу, ацильную группу или карбаматную группу. R5 представляет собой электроноакцепторную группу. В формуле (A-5), Х4 представляет собой атом кислорода (O) или атом серы (S), а Y1 представляет собой атом галогена, гидроксильную группу, группу, представленную -R6, группу, представленную -OR6 или группу, представленную -OCOR6. R6 может представлять собой, например, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу. В формуле (A-6), Х5 представляет собой атом кислорода (О) или атом серы (S), а Y2 представляет собой атом кислорода (O), атом серы (S) или группу, представленную NR7. R7 может представлять собой, например, алкилсульфонильную группу, арилсульфонильную группу, ацильную группу, карбаматную группу, алкильную группу, арильную группу, галогенированную алкильную группу или галогенированную арильную группу.
[0355] Функциональный реагент может быть получен посредством реакции взаимодействия первого реагента с реагентом (вторым реагентом), который имеет (одну) вторую реакционноспособную группу, способную образовывать связь посредством реакции с первой реакционноспособной группой, и имеет функциональную группу.
[0356] Примеры второй реакционноспособной группы включают гидроксильную группу, тиоловую группу, аминогруппу и группу, представленную следующей формулой (B-1).
[Формула 2]
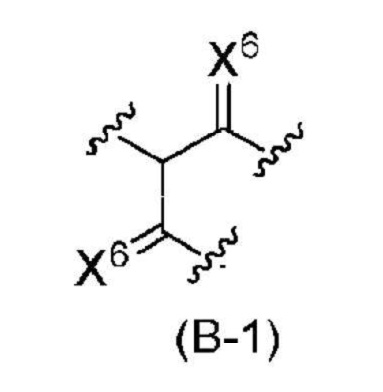
[0357] В формуле (B-1), X6 представляет собой атом кислорода (O) или атом серы (S).
[0358] Примеры функциональной группы включают углеводородные группы, такие как алкильная группа, алкенильная группа и алкинильная группа; группы, имеющие кольцевую структуру, такие как арильная группа и гетероциклическая группа; реакционноспособные группы, защищенные защитной группой (такой как гидроксильная группа, аминогруппа и тиоловая группа); группы, имеющие карбонильную группу (-C(=O)-) или имеющие такую структуру, как эфирная связь (-O-), амидная связь (>NC(=O)-), уретановая связь (> NC (=O)O-), карбамидная связь (>N(C=O)N<) и карбонатная связь (-OC(=O)O-). Примеры функциональной группы также включают алкоксисилильную группу, сульфонильную группу (-S(=O)-, карбоксильную группу (-C(=O)OH), группу сульфоновой кислоты (-S(=O)2OH) и четвертичную аммониевую группу.
[0359] Конкретные примеры первого реагента включают гександиизоцианат (HDI). Конкретные примеры второго реагента включают бутанол (BuOH).
[0360] Вещество, придающее водостойкость, предпочтительно представляет собой полимер на основе фтора или полимер на основе силикона с точки зрения улучшения водоотталкивающих свойств искусственного меха и предотвращения его усадки при контакте с водой.
[0361] Примеры способа добавления вещества, придающего водостойкость искусственному меху, включают: способ согласно первому варианту осуществления изобретения, в котором искусственный мех изготавливают в соответствии с обычно применяемой технологией с применением волокна, содержащего вещество, придающее водостойкость (например, волокна, смешанного с веществом, придающим водостойкость, или волокна, связанного с веществом, придающим водостойкость); способ согласно второму варианту осуществления изобретения, в котором вещество, придающее водостойкость, смешивают с искусственным мехом, изготовленным из волокна, не содержащего вещества, придающего водостойкость; и способ согласно третьему варианту осуществления изобретения, в котором вещество, придающее водостойкость, связывают с искусственным мехом, изготовленным из волокна, которое не содержит вещества, придающего водостойкость. В способе согласно второму варианту осуществления изобретения, искусственный мех и вещество, придающее водостойкость, необязательно должны быть связаны друг с другом.
[0362] Способ согласно третьему варианту осуществления изобретения включает связывание вещества, придающего водостойкость, с искусственным мехом. Таке связывание может быть осуществлено, например, с применением таких методов, как покрытие или погружение вещества, придающего водостойкость, для его контактирования с искусственным мехом; нагревание или облучения плазмой, если это необходимо, и тем самым связывание искусственного меха и вещества, придающего водостойкость. Если вещество, придающее водостойкость, представляет собой, например, гидрофобный полимер, такой как полимер на основе силикона и полимер на основе фтора, то связывание может представлять собой стадию ковалентного связывания искусственного меха и вещества, придающего водостойкость, например, посредством облучения искусственного меха плазмой при контактировании искусственного меха с веществом, придающим водостойкость, или с предшественником (мономером) вещества, придающего водостойкость. Даже если используется предшественник (мономер) вещества, придающего водостойкость, то этот предшественник (мономер) вещества, придающего водостойкость, полимеризуют посредством облучения плазмой с образованием вещества, придающего водостойкость (гидрофобного полимера, такого как полимер на основе силикона и полимер на основе на основе фтора). Соответственно, может быть получен искусственный мех, содержащий вещество, придающее водостойкость. Способ согласно третьему варианту осуществления изобретения может быть осуществлен не только на искусственном мехе, но и на ворсовой ткани перед стрижкой.
[0363] Плазма, используемая для облучения, может быть соответствующим образом выбрана в зависимости, например, от типа искусственного меха (используемого волокна) и вещества, придающего водостойкость (или его предшественника). Нагнетаемый газ может течь со скоростью, например, от 0,1 л/мин или более до 10 л/мин или менее. Плотность генерируемой плазмы может составлять, например, в пределах от 1×1013 см-3 или более до 1×1015 см-3 или менее. Нагнетаемый газ может представлять собой, например, инертный газ, такой как гелий, неон и аргон, либо он может представлять собой кислород или азот. В качестве нагнетаемого газа можно также использовать воздух.
[0364] Облучение плазмой может быть осуществлено с помощью известного устройства для плазменного облучения. Пример устройства для плазменного облучения включает оборудование для плазменной обработки, поставляемое от Europlasma.
[0365] (Искусственный мех)
Искусственный мех согласно этому варианту осуществления изобретения может дополнительно содержать компоненты, отличающиеся от волокна и вещества, придающего водостойкость. Примеры других компонентов включают красители, лубриканты, антиоксиданты, поглотители ультрафиолетового излучения, красители, наполнители, перекрестносшивающие агенты, матирующие агенты и выравнивающие агенты.
[0366] Даже в искусственном мехе согласно этому варианту осуществления изобретения, если используется модифицированное фиброин-содержащее волокно, то искусственный мех может иметь максимальный уровень влагопоглощения и выделения тепла, предельный кислородный индекс (LOI) и индекс удерживания тепла, аналогичные параметрам искусственного меха согласно первому варианту осуществления изобретения.
[0367] (Способ изготовления искусственного меха)
С применением вышеупомянутого волокна (волокна, содержащего искусственное белковое волокно), искусственный мех согласно этому варианту осуществления изобретения может быть изготовлен способом, например, аналогичным способу изготовления искусственного меха согласно первому варианту изобретения.
[0368] (Применение искусственного меха)
Искусственный мех согласно этому варианту осуществления изобретения (с первого по четвертый варианты осуществления изобретения) может быть использован в любых целях, для достижения которых используется известный искусственный мех (искусственный мех, изготовленный с применением синтетического волокна) (например, для пошива одежды, для изготовления таких аксессуаров, как сумки, ковры, и для изготовления чучел животных).
Примеры
[0369] Настоящее изобретение будет более подробно описано ниже в примерах испытаний. Однако, настоящее изобретение не ограничивается этими примерами испытаний.
[0370] [Пример испытания 1: Получение модифицированного фиброина]
Были получены модифицированный фиброин шелка паука, имеющий аминокислотную последовательность SEQ ID NO: 18 (PRT399), модифицированный фиброин шелка паука, имеющий аминокислотную последовательность SEQ ID NO: 12 (PRT380), модифицированный фиброин шелка паука, имеющий аминокислотную последовательность кислотная последовательность SEQ ID NO: 13 (PRT410), модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 37 (PRT918), модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 40 (PRT966), и модифицированный фиброин, имеющий аминокислотную последовательность SEQ ID NO: 15 (PRT799). Были синтезированы нуклеиновые кислоты, кодирующие сконструированные модифицированные фиброины. К 5'-концу каждой нуклеиновой кислоты добавляли сайт NdeI, а сайт EcoRI помещали ниже стоп-кодона. Нуклеиновые кислоты клонировали в векторы для клонирования (pUC118). После этого, нуклеиновые кислоты подвергали фрагментации рестриктирующим ферментом с применением NdeI и EcoRI, а затем подвергали рекомбинации и превращали в векторы для экспрессии белка pET-22b(+), с получением экспрессионных векторов.
[0371] Полученные экспрессионные векторы использовали для трансформации Escherichia coli BLR (DE3). Трансформированные Escherichia coli культивировали в течение 15 часов в 2 мл культуральной среды LB, содержащей ампициллин. Бульон добавляли к 100 мл посевной культуральной среды, содержащей ампициллин (таблица 4), так, чтобы OD600 достигала 0,005. Бульон выдерживали при температуре 30°C и подвергали культивированию в колбе (в течение приблизительно 15 часов) до тех пор, пока OD600 не достигала 5, с получением посевного бульона.
[0372]
Среда для посевной культуры
[0373] 500 мл среды для культивирования (таблица 5) добавляли в ферментер, и в этот ферментер добавляли посевной бульон так, чтобы OD600 составляла 0,05. Бульон культивировали и постоянно поддерживали при температуре 37°C и pH 6,9. Кроме того, бульон поддерживали так, чтобы концентрация растворенного кислорода составляла 20% от концентрации насыщенного растворенного кислорода.
[0374]
Среда для культивирования
[0375] Сразу после того, как глюкоза в среде для культивирования была полностью израсходована, добавляли питательный раствор (455 г/л глюкозы, 120 г/л дрожжевого экстракта) со скоростью 1 мл/мин. Бульон культивировали и постоянно поддерживали при температуре 37°C и pH 6,9. Кроме того, бульон культивировали в течение 20 часов, и поддерживали так, чтобы концентрация растворенного кислорода составляла 20% от концентрации насыщенного растворенного кислорода. После этого, в бульон добавляли 1 М изопропил-β-тиогалактопиранозида (IPTG) до конечной концентрации 1 мМ для индуцирования экспрессии модифицированных фиброинов. Через двадцать часов после добавления IPTG, бульон центрифугировали для выделения бактериальных клеток. Затем проводили электрофорез в ДСН-ПААГ с применением бактериальных клеток, полученных из бульона перед добавлением IPTG и из бульона после добавления IPTG. Из-за появления полосы, имеющей размер целевого модифицированного фиброина в зависимости от добавления IPTG, определяли экспрессию целевого модифицированного фиброина.
[0376] Бактериальные клетки, выделенные через два часа после добавления IPTG, промывали 20 мМ буферного раствора трис-HCl (pH 7,4). Промытые бактериальные клетки суспендировали в 20 мМ трис-HCl-буфера (pH 7,4), содержащего приблизительно 1 мМ PMSF, и клетки разрушали с помощью гомогенизатора высокого давления (поставляемого от GEA Niro Soavi). Разрушенные клетки центрифугировали с получением осадка. Полученный осадок промывали 20 мМ Трис-HCl-буфера (pH 7,4) до тех пор, пока осадок не достигал высокого уровня чистоты. Промытый осадок суспендировали в 8М гуанидинового буфера (8М гидрохлорида гуанидина, 10 мМ дигидрофосфата натрия, 20 мМ NaCl, 1 мМ Трис-HCl, pH 7,0) в концентрации 100 мг/мл, а затем растворяли путем перемешивания мешалкой при 60°C в течение 30 минут. После растворения, полученный продукт диализовали водой с применением диализной трубки (целлюлозной трубки 36/32, поставляемой от Sanko Junyaku Co., Ltd.). Белые агрегированные белки, полученные после диализа, собирали центрифугированием с последующим удалением влаги на лиофилизаторе и сбором лиофилизованных порошков с получением модифицированных фиброинов (PRT399, PRT380, PRT410, PRT918, PRT966 и PRT799).
[0377] PRT918 и PRT966 представляют собой гидрофобные модифицированные фиброины, имеющие средний HI больше нуля. PRT410, PRT399 и PRT799 представляют собой гидрофильные модифицированные фиброины, имеющие средний HI, равный нулю или менее.
[0378] [Пример испытания 2: Получение модифицированного фиброинового волокна и оценка его усадки (1)]
LiCl растворяли в диметилсульфоксиде (ДМСО) в концентрации 4,0 масс.% для приготовления растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина (PRT399, PRT380, PRT410 или PRT799) в концентрации 18 масс.% или 24 масс.% с последующим растворением смеси в течение трех часов с помощью шейкера. После этого удаляли нерастворившиеся вещества и пену с получением модифицированного раствора фиброина.
[0379] Полученный раствор модифицированного фиброина использовали в качестве прядильного раствора (прядильного раствора полимера) для изготовления модифицированного волокна из фиброина шелка паука, пряденного и вытянутого методом сухого-мокрого прядения с помощью прядильного устройства 1000, показанного на фиг. 6. Прядильное устройство, используемое в этом примере, является таким же, как и прядильное устройство 1000, показанное на фиг. 6, за исключением того, что это прядильное устройство включает второе устройство для производства невытянутой пряжи (вторая ванна), расположенное между устройством 102 для изготовления невытянутой пряжи (первая ванна) и устройством для мокрого вытягивания посредством нагревания 103 (третья ванна). Сухое-мокрое прядение проводили в следующих условиях.
Диаметр сопла экструдера: 0,2 мм.
Температура коагуляционной ванны: от 2 до 15°C.
Общий коэффициент удлинения: 1-4 раза.
Температура сушки: 60°C.
[0380] (Оценка усадки)
Оценивали степень усадки каждого из полученных модифицированных фиброиновых волокон (примеры изготовления 1-19). Другими словами, усадку оценивали после контактирования каждого модифицированного фиброинового волокна (волокна после прядения, но до контакта с водой) с водой так, чтобы оно находилось во влажном состоянии (стадия контактирования), и последующей сушки смоченного волокна (стадия сушки), в результате чего получали величину степени усадки каждого модифицированного фиброинового волокна во влажном состоянии и степени усадки каждого модифицированного фиброинового волокна в сухом состоянии после смачивания.
[0381] <Стадия контактирования>
Из рулона пряжи каждого из модифицированных волокон фиброина вырезали множество модифицированных волокон фиброина (длиной 30 см) для тестирования. Множество модифицированных фиброиновых волокон объединяли в пучки для получения пучков модифицированных фиброиновых волокон, имеющих весовой номер 150 денье. К каждому пучку модифицированных фиброиновых волокон прикрепляли свинцовый груз (0,8 грамма), и каждый пучок модифицированных фиброиновых волокон погружали в воду на 10 минут при температуре, указанной в таблицах 6-9. После этого определяли длину каждого пучка модифицированных фиброиновых волокон в воде. Измерение осуществляли после того как свинцовый груз (0,8 грамма) был прикреплен к каждому пучку модифицированных фиброиновых волокон, так, чтобы пучки модифицированных фиброиновых волокон не давали усадку. Затем была вычислена степень усадки модифицированных фиброиновых волокон во влажном состоянии в соответствии со следующей формулой V. В формуле V, L0 означает длину (30 см) каждого пучка модифицированных фиброиновых волокон перед погружением в воду, а Lw означает длину каждого пучка модифицированных фиброиновых волокон во влажном состоянии после погружения в воду.
Степень усадки во влажном состоянии (%) = {1 - (Lw/L0)}×100 (Формула V).
[0382] <Стадия сушки>
После стадии контактирования, пучки модифицированных фиброиновых волокон удаляли из воды. Пучки модифицированных фиброиновых волокон, извлеченные из воды, оставляли для сушки при комнатной температуре в течение двух часов с прикрепленным к ним 0,8-граммовым свинцовым грузом. После сушки измеряли длину каждого пучка модифицированных фиброиновых волокон. Затем в соответствии с нижеследующей формулой VI вычисляли степень усадки модифицированных фиброиновых волокон, высушенных после их пребывания во влажном состоянии (степень усадки в сухом состоянии). В формуле VI, L0 означает длину (30 см) каждого пучка модифицированных фиброиновых волокон перед погружением в воду, а Lwd означает длину каждого пучка модифицированных фиброиновых волокон в сухом состоянии после погружения в воду.
Степень усадки в сухом состоянии (%) = {1- (Lwd/L0)}×100 (%) (Формула VI).
[0383] Результаты представлены в таблицах 6-9. В таблицах 6-9, величины «общего коэффициента удлинения» представляют собой значения, полученные во процессе прядения волокна.
[0384]
[0385]
[0386]
[0387]
[0388] Как во влажном, так и в сухом состоянии, модифицированные фиброиновые волокна имели высокую степень усадки. С другой стороны, модифицированные фиброиновые волокна, оцениваемые на усадку (подвергнутые усадке), имели значительно меньшую степень усадки, если модифицированные фиброиновые волокна снова были подвергнуты контактированию с водой. Возможная причина этого факта заключается в том, что усадка ослабляла остаточное напряжение, вызываемое вытягиванием во время прядения и т.п.
[0389] [Пример испытания 3: Получение модифицированного фиброинового волокна и оценка усадки (2)]
Модифицированный фиброин (PRT799) добавляли к муравьиной кислоте в концентрации 24 масс.%. Затем смесь растворяли при перемешивании при комнатной температуре в течение одного часа. После этого удаляли нерастворимые вещества и пену с получением модифицированного раствора фиброина.
[0390] Полученный модифицированный раствор фиброина использовали в качестве прядильного раствора (прядильного раствора полимера) с получением модифицированного фиброинового волокна посредством сухого-мокрого прядения на прядильном устройстве 1000, показанном на фиг. 6. Сухое-мокрое прядение проводили в следующих условиях.
Температура коагулирующей жидкости (метанола): 5-10°C.
Общий коэффициент удлинения: в 6 раз.
Температура сушки: 80°C.
[0391] Полученное модифицированное фиброиновое волокно использовали для термоусадки в свободном состоянии. Модифицированное фиброиновое волокно подвергали контактированию с пластиной для сухого нагрева, нагретой до заданной температуры, и пропускали над пластиной для сухого нагрева. Скорость подачи была увеличена относительно линейной скорости намотки для релаксации модифицированного фиброинового волокна. Для проведения процедуры сухой релаксации, провисание уменьшали путем нагревания. Величина, полученная путем деления скорости подачи на скорость намотки, рассматривалась как «степень релаксации». В этом испытании, степень релаксации была отрегулирована так, чтобы провисание модифицированного фиброинового волокна, вызванное чрезмерной подачей, давало максимальную степень усадки, которая может быть компенсирована релаксацией. Степень релаксации корректировали путем регуляции по меньшей мере одного подающего валика и приемного валика.
[0392] Оценку усадки после обработки водой проводили по следующей методике. Волокно после термоусадки в свободном состоянии разрезали на куски по 300 мм (образец для испытаний) и погружали в воду при 40°C на 10 минут без нагрузки. Сразу после этого была измерена длина тестируемого образца (длина во влажном состоянии), и тестируемый образец сушили при комнатной температуре в течение двух часов. После этого измеряли длину тестируемого образца (длину волокна после сушки) для определения степени усадки под действием воды. Степень усадки под действием воды представляет собой численное значение, вычисляемое по следующей формуле (1):
Степень усадки под действием воды = (1 - длина волокна после сушки/длина волокна до погружения)×100 … (1)
[0393] (Пример испытания 3-1)
Была исследована связь между температурой нагревания и степенью релаксации. В примере испытания 3-1, процедуры, проводимые в примерах испытания 3-1-1-3-1-7, осуществляли в различных условиях, за исключением того, что длина до погружения в воду была установлена на 300 мм. В частности, испытания проводили при различных температурах нагревания, с различными степенями релаксации и различными периодами выдерживания. В таблице 10 показаны температура и условия релаксации, а также результаты измерения степени усадки. Как показано в таблице 10, чем выше температура нагревания и чем выше степень релаксации, тем ниже степень усадки под действием воды. Как показали результаты примеры испытания 3-1-3-3-1-5, нагревание при температуре 220°C или выше обеспечивает степень усадки под действием воды 4% или менее. Следует отметить, что в примере 5, где использовалась температура нагревания 280°C, волокно было окрашено. Как показали результаты испытаний, оптимальная температура нагревания составляла 240°C.
[0394]
[0395] (Пример испытания 3-2)
Затем была исследована связь между степенью релаксации и степенью усадки под действием воды. В примере испытания 3-2, процедуры, проводимые в примерах испытания 3-2-1-3-2-6, осуществляли в различных условиях, за исключением того, что длина до погружения в воду была установлена на 300 мм, температура нагревания была установлена на 240°C, а время выдерживания было установлено на одну минуту (60 секунд). В частности, испытания проводили при различных степенях релаксации (с различными скоростями подачи). В таблице 11 показаны условия релаксации и результаты измерения степени усадки. Как показано в таблице 11, чем ниже степень усадки под действием воды, тем выше степень релаксации. Как показали результаты, представленные в примерах испытания 3-2-3-3-2-5, увеличение степени релаксации в 1,4-2,0 раза дает степень усадки под действием воды 16% или менее.
[0396]
[0397] (Пример испытания 3-3)
Была исследована взаимосвязь между степенью усадки под действием воды и различными температурами нагревания, временем нагревания и степенью релаксации. В примере испытания 3-3, процедуры, проводимые в примерах испытания 3-3-1-3-3-10, осуществляли в различных условиях, за исключением того, что длина до погружения в воду была установлена на 300 мм. В частности, испытания проводили при различных температурах нагревания, времени нагревания (времени выдерживания) и степенями релаксации (скоростью подачи/скоростью намотки). В таблице 12 показаны температура и условия релаксации, а также результаты измерения степени усадки. В примере испытания 3-3-10, тестируемый образец погружали в воду и сушили, но не подвергали релаксации и не нагревали. Как показали результаты примеров испытания 3-3-4-3-3-9, нагревание при температуре 200°C или выше обеспечивает степень усадки под действием воды менее 15%. Установка температуры нагревания на 220°C или выше снижает степень усадки под действием воды до низкого уровня, такого как 4% или менее. Что касается времени выдерживания, то для усадки достаточно пяти секунд. Увеличение времени выдерживания почти не влияло на степень усадки.
[0398]
[0399] [Пример испытания 4: Обработка для предотвращения усадки и оценка трикотажного или тканого материала с применением модифицированного фиброинового волокна]
[Изготовление, обработка для предотвращения усадки и оценка трикотажного полотна]
(Пример испытания 4-1)
Трикотажное полотно было изготовлено путем кругового вязания на бесшовной кругловязальной машине с применением модифицированного фиброинового волокна, полученного как описано в Примере испытания 2, за исключением того, что общий коэффициент удлинения во время прядения волокна был увеличен в 4,55 раза. В данном случае, пряжа модифицированного фиброинового волокна имела номер 58,1 Nm, а бесшовная вязальная машина имела калибр 18.
[0400] Полученное трикотажное полотно было помечено квадратом, имеющим длину стороны 1 см как в направлении петельного столбика, так и в направлении петельного ряда. После этого, трикотажное полотно погружали в воду при 20°C на 10 минут. После погружения в воду, трикотажное полотно подвергали противоусадочной обработке путем сушки.
[0401] <Оценка степени изменения размеров>
Степень изменения размеров (%) как в направлении петельного столбика, так и в направлении петельного ряда трикотажного полотна, подвергнутого обработке для предотвращения усадки, вычисляли по нижеследующей формуле. В этой формуле, L0f означает длину одной стороны квадрата, отмеченного на трикотажном полотне до контактирования с водой, а Lwf означает длину одной стороны квадрата, отмеченного на трикотажном полотне после обработки для предотвращения усадки. Результаты представлены в таблице 13.
Формула: Степень изменения размеров = {(Lwf/L0f) - 1}×100 (%).
[0402] <Измерение степени увеличения числа петель>
Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, было подсчитано количество петель на 1 см как в направлении петельного столбика, так и в направлении петельного ряда, а затем вычисляли степень увеличения количества петель по следующей формуле. В этой формуле, N0 означает число петель трикотажного полотна до контактирования с водой, а Nw означает число петель трикотажного полотна после обработки для предотвращения усадки. Результаты представлены в таблице 13.
Формула: Степень увеличения числа петель = {(Nw/N0)-1}×100 (%).
[0403] <Измерение степени увеличения плотности вязания>
Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, было подсчитано число петель на 1 см2, а затем вычисляли степень увеличения плотности трикотажного полотна по нижеследующей формуле. В этой формуле, М0 означает плотность трикотажного полотна до контактирования с водой, а Мw означает плотность трикотажного полотна после обработки для предотвращения усадки. Результаты представлены в таблице 13.
Формула: Степень увеличения плотности трикотажного полотна = {(Мw/М0) - 1}×100 (%).
[0404] <Измерение степени увеличения прочности на разрыв>
Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, то прочность на разрыв измеряли в соответствии с методом, описанным в JIS L 1096B, а затем вычисляли степень увеличения прочности на разрыв по нижеследующей формуле. В этой формуле, R0 означает прочность на разрыв трикотажного полотна до контактирования с водой, а Rw означает прочность на разрыв трикотажного полотна после обработки для предотвращения усадки. Результаты представлены в таблице 13.
Формула: Степень увеличения прочности на разрыв = {(Rw/R0) - 1}×100 (%).
[0405] (Пример испытания 4-2)
Трикотажное полотно было изготовлено методом уточного вязания на бесшовной вязальной машине с применением фиброинового волокна из натурального шелка (пряжи из натурального шелка) вместо модифицированного фиброинового волокна. Фиброиновое волокно из натурального шелка согласно изобретению было получено путем связывания двух нитей (номер пряжи 29 Nm). Бесшовная вязальная машина имела калибр 18. Полученное трикотажное полотно подвергали обработке для предотвращения усадки как описано в примере испытания 4-1. Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, то были вычислены степень изменения размеров, степень увеличения числа петель и степень увеличения плотности трикотажного полотна. Результаты представлены в таблице 13.
[0406] (Пример испытания 4-3)
Трикотажное полотно получали как описано в Примере испытания 4-1, за исключением того, что вместо модифицированного фиброинового волокна использовали волокно из полиэтилентерефталата (ПЭТ). Полученное трикотажное полотно подвергали обработке для предотвращения усадки в условиях, аналогичных условиям, описанным в Примере испытания 4-1. Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, то были вычислены степень изменения размеров, степень увеличения числа петель, степень увеличения плотности трикотажного полотна и прочность на разрыв. Результаты представлены в таблице 13.
[0407] (Пример испытания 4-4)
Трикотажное полотно получали как описано в Примере испытания 4-1, за исключением того, что вместо модифицированного фиброинового волокна использовали волокно из полиэтилентерефталата (ПЭТ), и что вместо кругового вязания использовали плоское вязание. Полученное трикотажное полотно подвергали обработке для предотвращения усадки в условиях, аналогичных условиям, описанным в Примере испытания 4-1. Что касается полученного трикотажного полотна и трикотажного полотна, подвергнутого обработке для предотвращения усадки, то были вычислены степень изменения размеров, степень увеличения числа петель, степень увеличения плотности трикотажного полотна и прочность на разрыв. Результаты представлены в таблице 13.
[0408]
r
[0409] [Изготовление, обработка для предотвращения усадки и оценка тканого полотна]
С применением крученой пряжи, включающей модифицированное фиброиновое волокно, было изготовлено тканое полотно четырех типов, имеющих разную плотность переплетения, как показано в нижеследующей таблице 14, путем простого переплетения на рапирном ткацком станке (поставляемом от Evergreen Automatic Sampling Loom: CCI) (Примеры испытания 4-5-4-8). В данном случае, крученая пряжа, включающая модифицированное фиброиновое волокно, имела номер 190d, а число кручений на метр составляло 450 Т/m.
[0410] Каждое полученное тканое полотно четырех типов погружали в воду при 40°C на 10 минут и подвергали обработке для предотвращения усадки путем сушки. После этого оценивали плотность тканых материалов как описано в Примерах испытаний 4-5-4-8. Результаты показаны в нижеследующей таблице 14. В таблице 14, плотность плетения показана как «плотность основы, умноженная на плотность утка». Так, например, плотность плетения «26×26» означает «плотность основы 26 (пряжа/дюйм) и плотность утка 26 (пряжа/дюйм)».
[0411] Четыре типа тканых материалов, имеющих различную плотность, как показано ниже в Таблице 14, представляли собой тканый материал, полученный способом, аналогичным вышеупомянутому способу, за исключением того, что вместо крученой пряжи, включающей модифицированное фиброиновое волокно (Пример испытания 4-9-4-12), использовали крученую пряжу, включающую полиамидное волокно. В данном случае, крученая пряжа, включающая полиамидное волокно, имела номер 150d, а число кручений на метр составляло 150 Т/m.
[0412] Тканый материал, полученный, как описано в Примерах испытаний 4-9-4-12, был подвергнут обработке для предотвращения усадки способом, аналогичным вышеупомянутому способу. После этого оценивали плотность тканых материалов, полученных, как описано в Примерах испытаний 4-9-4-12. Результаты также показаны в таблице 14.
[0413]
[0414] [Пример испытания 5: Получение и оценка белкового волокна, обладающего функциональными свойствами]
(Пример испытания 5-1)
<Получение прядильного полимера (прядильного раствора)>
В 11400 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 200 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и 400 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и изоцианатная группа фенилизоцианата были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0415] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 300 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора. Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0416] <Получение белкового волокна>
Полученный прядильный раствор нагревали до 60°C и фильтровали через металлический фильтр с размером отверстий 5 мкм. После этого, фильтрат оставляли в шприце из нержавеющей стали объемом 30 мл для удаления пены. Полученный продукт выгружали из встроенного сопла, имеющего диаметр иглы 0,2 мм, в 100 масс.% коагуляционную ванну с метанолом, с применением газообразного азота. Температура выгрузки составляла 60°C, а давление выгрузки составляло 0,3 МПа. После коагуляции, полученную исходную пряжу наматывали со скоростью намотки 3,00 м/мин и сушили естественным путем с получением белкового волокна (модифицированного фиброинового волокна).
[0417] <Испытание на усадку под действием воды>
Полученное белковое волокно разрезали на длину приблизительно 10 см, и перед погружением в воду измеряли длину (см) пряжи. Затем пряжу погружали на одну минуту в водяную баню при 40°C. После этого, пряжу вынимали из водяной бани, сушили в вакууме при комнатной температуре в течение 15 минут с последующим измерением длины высушенной пряжи. Степень усадки белкового волокна под действием воды вычисляли по следующей формуле:
Степень усадки под действием воды (%) = {(длина до погружения/длина после погружения и сушки) - 1}×100.
[0418] (Пример испытания 5-2)
<Получение прядильного раствора (прядильного раствора полимера)>
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 253 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 147 мг ангидрида уксусной кислоты (поставляемого Wako Pure Chemical Industries, Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и ангидрид уксусной кислоты были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), с которым была связана ацетильная группа (реакционноспособная функциональная группа). После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0419] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора. Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0420] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0421] (Пример испытания 5-3)
<Получение прядильного раствора (прядильного раствора полимера)>
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 215 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 185 мг ангидрида уксусной кислоты (поставляемого Wako Pure Chemical Industries, Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и ангидрид уксусной кислоты были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), с которым была связана ацетильная группа (реакционноспособная функциональная группа). После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 50% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0422] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора. Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0423] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0424] (Пример испытания 5-4)
<Получение прядильного раствора (прядильного раствора полимера)>
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 128 мг поливинилового спирта (ПВС) (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 272 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа ПВС и фенилизоцианат были подвергнуты реакции взаимодействия с получением модифицированного ПВС (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный ПВС был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0425] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора. Содержание модифицированного ПВС в прядильном растворе составляло 17 масс.% от общего количества модифицированного ПВС и ПВС.
[0426] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0427] (Пример испытания 5-5)
<Получение прядильного раствора (прядильного раствора полимера)>
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 193 мг поливинилового спирта (ПВС) (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 207 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа ПВС и фенилизоцианат были подвергнуты реакции взаимодействия с получением модифицированного ПВС (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный ПВС был модифицирован на 50% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0428] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора. Содержание модифицированного ПВС в прядильном растворе составляло 17 масс.% от общего количества модифицированного ПВС и ПВС.
[0429] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0430] (Пример испытания 5-6)
<Получение прядильного раствора (прядильного раствора полимера)>
К растворителю (диметилсульфоксиду (ДМСО), содержащему 4 масс.% LiCl) добавляли 1200 мг порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора.
[0431] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0432] (Пример испытания 5-7)
<Получение прядильного раствора (прядильного раствора полимера)>
К растворителю (диметилсульфоксиду (ДМСО), содержащему 4 масс.% LiCl) добавляли 3000 мг порошка модифицированного фиброина (PRT799) и 600 мг крахмала (доступного от Wako Pure Chemical Industries, Ltd.), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора.
[0433] <Получение белкового волокна и испытание на усадку под действием воды>
С применением полученного прядильного раствора было изготовлено белковое волокно и было проведено испытание на усадку под действием воды как описано в Примере испытания 5-1.
[0434] Результаты представлены на фиг. 7 и в таблице 15. В таблице 15, в Примере испытания 3-1 показан Пример испытания 5-1, в Примере испытания 3-2 показан Пример испытания 5-2, в Примере испытания 3-3 показан Пример испытания 5-3, в Примере испытания 3-4 показан Пример испытания 5-4, в Примере испытания 3-5 показан Пример испытания 5-5, в Примере испытания 3-6 показан Пример испытания 5-6, а в Примере испытания 3-7 показан Пример испытания 5-7.
*1 (Содержание модифицированного полимера, содержащего гидроксильную группу/общее количество модифицированного полимера, содержащего гидроксильную группу, и полимера, содержащего гидроксильную группу)×100.
[0435] Из прядильного раствора, содержащего модифицированный полимер, содержащий гидроксильную группу (модифицированный крахмал или модифицированный ПВС), с которым гидрофобная функциональная группа (фенильная группа или ацетильная группа) была связана в качестве реакционноспособной функциональной группы, и содержащий белок (модифицированный фиброин)) (Примеры испытаний 5-1-5-5 (Примеры испытаний 3-1-3-5 в таблице 15) было получено белковое волокно, имеющее водостойкость и пониженную степень усадки под действием воды по сравнению с прядильным раствором, изготовленным только из белка (Пример испытания 5-6 (Пример испытания 3-6 в таблице 15)) и прядильным раствором, изготовленным из белка и немодифицированного полимера, содержащего гидроксильную группу (Пример испытания 5-7 (Пример испытания 3-7 в таблице 15)). Изготовление трикотажного или тканого полотна из такого белкового волокна придает трикотажному или тканому материалу функциональные свойства (водостойкость).
[0436] [Пример испытания 6: Получение и оценка функционального белкового волокна]
(Пример изготовления 1)
К диметилсульфоксиду (ДМСО) добавляли вышеупомянутый белок фиброин шелка паука (PRT799) в концентрации 24 масс.%. К этой смеси добавляли LiCl в качестве стимулятора растворения в концентрации 4,0 масс.%. Затем, фиброин шелка паука растворяли в течение трех часов на шейкере для получения раствора в ДМСО. Пыль и пузырьки в полученном растворе ДМСО были удалены для приготовления прядильного раствора. Прядильный раствор имел вязкость 5000 сП (сантипуаз) при 90°C.
[0437] Сухое-мокрое прядение осуществляли с применением прядильного раствора, полученного, как описано выше, и известного прядильного устройства с получением мононити, включающей фиброин шелка паука. Следует отметить, что в данном случае, сухое-мокрое прядение осуществляли при следующих условиях.
Температура коагулирующей жидкости (метанол): 5-10°C.
Общий коэффициент удлинения: 6-кратный.
Температура сушки: 80°C.
[0438] Штапельную пряжу изготавливали известным способом из модифицированного фиброинового волокна шелка паука, полученного вышеупомянутым способом. С применением штапельной пряжи, включающей модифицированное фиброиновое волокно шелка паука, квадратную трикотажную ткань размером 5 см (трикотажное или тканое полотно) связывали путем уточного вязания на стандартной вязальной машине. Штапельная пряжа, включающая модифицированное фиброиновое волокно шелка паука, имела номер 58,1 Nm, а вязальная машина имела калибр 18.
[0439] (Пример испытания 6-1)
Трикотажное или тканое полотно (квадратное трикотажное полотно размером 5 см), полученное как описано в Примере изготовления 1, погружали в 20 мл гександиизоцианата (HDI). Затем, трикотажное или тканое полотно, пропитанное HDI, помещали между алюминиевой фольгой и нагревали при 130°C в течение 30 минут. Затем, нагретое трикотажное или тканое полотно вынимали, погружали в 20 мл бутанола (BuOH) и проводили реакции взаимодействия при 100°C в течение 240 минут. После реакции, тестируемый образец промывали ТГФ и получали трикотажное или тканое полотно с функциональными свойствами (с которым были связаны вещества, придающие водостойкость (первый реагент и второй реагент)).
[0440] (Пример испытания 6-2)
Трикотажное или тканое полотно, полученное как описано в Примере изготовления 1, оценивали как трикотажное или тканое полотно Примера испытания 6-2.
[0441] (Пример испытания 6-3)
Трикотажное или тканое полотно, полученное как описано в Примере изготовления 1, погружали в 20 мл гександиизоцианата (HDI, первого реагента). Затем, трикотажное или тканое полотно, пропитанное HDI, помещали между алюминиевой фольгой и нагревали при 130°C в течение 30 минут. Затем, трикотажное или тканое полотно промывали ТГФ с получением трикотажного или тканого полотна, которое было описано в Примере испытания 6-3, и с которым был связан только первый реагент.
[0442] Что касается трикотажных или тканых материалов, описанных в Примерах испытания 6-1-6-3, водостойкость (усадка) и структура были оценены с применением нижеследующего метода испытаний.
[0443] <Оценка водостойкости (усадки)>
Каждое трикотажное или тканое полотно было помечено карандашом как квадрат размером 3 см и было использовано в качестве образца для оценки. Образцы для оценки промывали в режиме мойки «чистка Учи (профессиональная чистка на дому)» в стиральной машине (Na-VG 1100L), поставляемой от Panasonic Corporation. Затем образцы дегидратировали в течение 15 минут в той же самой стиральной машине и сушили естественным путем в течение 120 минут. Затем измеряли продольную и поперечную длины каждого квадрата до и после стирки, в результате чего была определена степень усадки в продольном и поперечном направлениях. Один и тот же тест был проведен трижды, и в качестве результата оценки использовали среднее значение для трех испытаний. Каждый результат показан в таблице 16. В таблице 16, Пример испытания 4-1 представляет Пример испытания 6-1, Пример испытания 4-2 представляет Пример испытания 6-2, а Пример испытания 4-3 представляет Пример испытания 6-3.
[0444] <Оценка структуры>
Структуру каждого трикотажного или тканого материала оценивали в три стадии. Что касается структуры трикотажного или тканого материала в Примере испытаний 6-2, используемого в качестве стандарта (B), то ткань с лучшим качеством на ощупь была оценена как «А», а ткань с грубой структурой и плохим качеством на ощупь была оценена как «C». Каждый результат показан в таблице 16.
[0445]
[0446] [Пример испытания 7: Получение и оценка тканого материала с применением модифицированного фиброинового волокна]
(1) Получение прядильного раствора (прядильного раствора полимера)
Хлорид лития растворяли в ДМСО в концентрации 4 масс.% для получения растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина (PRT799) в концентрации 24 масс.%. Полученный продукт растворяли в алюминиевом нагревательном блоке при 90°C в течение одного часа с последующим удалением нерастворимых веществ и пузырьков, с получением прядильного раствора (прядильного раствора полимера).
[0447] (2) Прядение
Прядильный раствор загружали в резервный резервуар и выгружали в ванну со 100 масс.% метанолом для коагуляции через сопло с одним отверстием, имеющим диаметр 0,1 или 0,2 мм, с применением шестеренного насоса. Объем выгрузки был доведен до 0,01-0,08 мл/мин. После коагуляции проводили промывку и вытяжку в промывочной ванне со 100 масс.% метанолом. После мойки и вытяжки проводили сушку с применением плиты для сухого нагрева, и полученную исходную пряжу (модифицированное фиброиновое волокно) наматывали.
[0448] (3) Получение тканых материалов
Из полученного модифицированного фиброинового волокна получали шелковую основу. Шелковая основа была изготовлена путем полотняного переплетения с получением тканого полотна.
[0449] (4) Связывание вещества, сообщающего тканому полотну водостойкость
На полученный тканый материал наносили мономеры для покрытия на основе фтора, и проводили плазменную обработку с помощью устройства для плазменной обработки (поставляемого от Europlasma). Плазменную обработку проводили для получения тканого материала, имеющего ковалентно связанные полимеры на основе фтора, в которых были полимеризованы мономеры для покрытия на основе фтора (вещество, придающее водостойкость). Nanofics 110 (Пример испытания 7-2) и Nanofics 120 (Пример испытания 7-3) (оба поставляются от Europlasma) были использованы в качестве мономеров для покрытия на основе фтора.
[0450] (5) Оценка водоотталкивающих свойств
Испытание на водоотталкивающие свойства (испытание распылением) проводили на тканом полотне, обработанном плазмой (Пример испытания 7-2 и Пример испытания 7-3), и на тканых материалах, не подвергнутых плазменной обработке (Пример испытания 7-1). Испытание на водоотталкивающие свойства (испытание распылением) проводили в соответствии с ISO 4920: 2012. Образцы для испытаний оценивали визуально в соответствии со следующей 6-балльной оценкой (по шкале от 0 до 5).
Балл 5: Сухая поверхность без капель воды.
Балл 4: Сухая поверхность с небольшими каплями воды.
Балл 3: Слегка влажная поверхность.
Балл 2: Влажная поверхность с перемежающимися влажными участками, соединенными друг с другом.
Балл 1: Деталь, контактирующая с водой, полностью смачивается.
Оценка 0: Полностью влажная поверхность.
[0451] Результаты представлены в таблице 17. Тканый материал, не подвергнутый плазменной обработке (Пример испытания 7-1), получил оценку 0, в то время как тканые материалы, подвергнутые плазменной обработке (Пример испытания 7-2 и Пример испытания 7-3), получили оценку 4, что указывает на водостойкость (водоотталкивающие свойства). В таблицах 17, 18 и 19 в Примере испытания 2-1 показан Пример испытания 7-1, в Примере испытания 2-2 показан Пример испытания 7-2, а в Примере испытания 2-3 показан Пример испытания 7-3.
[0452]
[0453] (6) Оценка структуры и усадки
Из каждого тканого материала вырезали 5 см2-образец для испытаний, как описано в Примерах испытаний 7-1-7-3. На одной поверхности каждого тестируемого образца карандашом были отмечены вершины (четыре точки) 30 мм-квадрата. Каждый образец для испытаний погружали в воду при 40°C на 10 минут и сушили в вакууме при комнатной температуре. Эту процедуру повторяли пять раз. Вакуумную сушку осуществляли с помощью вакуумного сушильного шкафа (VOS-310C, поставляемого от Tokyo Rikakikai Co., Ltd.) под давлением 0,1 МПа в течение 30 минут. В конце каждого цикла, структуру оценивали на ощупь и измеряли расстояния между отмеченными четырьмя точками для оценки степени усадки.
[0454] Структуру определяли по следующим критериям. Результаты показаны в таблице 18. Обработанные плазмой тканые материалы Примера испытания 7-2 и Примера испытания 7-3 были защищены от разрушения структуры по сравнению с тканым материалом Примера испытания 7-1, который не подвергался плазменной обработке.
Балл 5: Хороший как оригинал.
Балл 4: Хороший, но немного уступает оригиналу.
Балл 3: Удовлетворительный, но немного грубоватый.
Балл 2: Плохой и грубоватый, но сгибаемый.
Балл 1: Очень плохой, грубоватый и не поддается изгибу.
[0455]
[0456] Степень усадки вычисляли по нижеследующей формуле. Следует отметить, что «средняя длина всех сторон» представляет собой величину, полученную путем деления общей длины всех сторон квадрата (отмеченных четырьмя точками) на 4.
Степень усадки (%) = {1-(средняя длина всех сторон (мм)/30 мм)}×100.
Результаты представлены в таблице 19. Обработанные плазмой тканые материалы Примера испытания 2-2 и Примера испытания 7-3 имели меньшую степень усадки, чем тканый материал Примера испытания 7-1, который не подвергался плазменной обработке.
[0457]
[0458] [Пример испытания 8: Получение и оценка трикотажного полотна с применением модифицированного фиброинового волокна]
(1) Получение прядильного раствора (прядильного раствора полимера)
Хлорид лития растворяли в ДМСО в концентрации 4 масс.% для получения растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина (PRT918) в концентрации 24 масс.%. Полученный продукт растворяли в алюминиевом нагревательном блоке при 90°C в течение одного часа с последующим удалением нерастворимых веществ и пузырьков с получением прядильного раствора (прядильного раствора полимера).
[0459] (2) Прядение
Прядильный раствор загружали в резервный резервуар и выгружали в ванну со 100 масс.% метанолом для коагуляции через сопло с одним отверстием, имеющим диаметр 0,1 или 0,2 мм, с применением шестеренного насоса. Объем выгрузки был доведен до 0,01-0,08 мл/мин. После коагуляции проводили промывку и вытяжку в промывочной ванне со 100 масс.% метанолом. После мойки и вытяжки проводили сушку с применением плиты для сухого нагрева, и полученную исходную пряжу (модифицированное фиброиновое волокно) наматывали.
[0460] (3) Получение трикотажного полотна для оценки
Полученное модифицированное фиброиновое волокно разрезали для получения модифицированного фиброинового штапельного волокна. Полученное модифицированное фиброиновое штапельное волокно отбивали и подвергали прядению на стандартном прядильном устройстве для получения пряжи. Полученная штапельная пряжа была связана на вязальной машине для изготовления всех предметов одежды (MACH2XS, доступной от Shima Seiki MFG., Ltd.) с получением трикотажного полотна.
[0461] (4) Связывание вещества, придающего трикотажному полотну водостойкость
На полученный трикотажный материал наносили мономеры для покрытия на основе фтора, и проводили плазменную обработку с помощью устройства для плазменной обработки (поставляемого от Europlasma). Плазменную обработку проводили для получения трикотажного материала, имеющего ковалентно связанные полимеры на основе фтора, в которых были полимеризованы мономеры для покрытия на основе фтора (вещество, придающее водостойкость) (Пример испытания 3-2). Nanofics 120 (поставляемый от Europlasma) использовали в качестве мономеров для покрытия на основе фтора.
[0462] (5) Оценка водоотталкивающих свойств
Испытание на водоотталкивающие свойства (испытание распылением) проводили как описано в Примере испытания 7 на трикотажном полотне, обработанном плазмой (Пример испытания 8-2), и на трикотажном полотне, не подвергнутом плазменной обработке (Пример испытания 8-1). Результаты представлены в таблице 20. Трикотажное полотно, не подвергшееся плазменной обработке (Пример испытания 8-1), было оценено как 0, а трикотажное полотно, подвергшееся плазменной обработке (Пример испытания 8-2), было оценено как 5, что указывает на водостойкость (водоотталкивающие свойства). В нижеприведенных таблицах 20, 21 и 22, в Примере испытания 3-1 показан Пример испытания 8-1, а в Примере испытания 3-2 показан Пример испытания 8-2.
[0463] (6) Оценка структуры и усадки
Из каждого тканого материала вырезали 5 см2-образец для испытаний, как описано в Примерах испытаний 8-1 и 8-2. На одной поверхности каждого тестируемого образца карандашом были отмечены вершины (четыре точки) 30 мм2-квадрата. В качестве предварительной обработки, каждый образец для испытаний погружали в воду при 40°C на 10 минут и сушили в вакууме при комнатной температуре. Эту процедуру повторяли пять раз. Вакуумную сушку осуществляли в вакуумном сушильном шкафу (VOS-310C, поставляемого от Tokyo Rikakikai Co., Ltd.) под давлением 0,1 МПа в течение 30 минут.
[0464] Далее, промывку, сушку, погружение и высушивание повторяли в указанном порядке пять раз для каждого тестируемого образца, подвергнутого предварительной обработке. При промывке, тестируемый образец промывали в течение пяти минут в стиральной машине (NA-VG 1100L), поставляемой от Panasonic Corporation, с применением моющего средства (универсальной очищающей жидкости), поставляемого корпорацией Lion, и промывали дважды, а затем, дегидратировали в течение одной минуты. При сушке, тестируемый образец сушили при комнатной температуре и при заданном давлении 0,1 МПа в течение 30 минут с применением вакуумной сушилки при постоянной температуре (VOS-310C, поставляемого от Tokyo Rikakikai Co., Ltd.). При погружении, тестируемый образец был погружен в воду на 10 минут при температуре 40°C. В конце каждого цикла, структура была оценена на ощупь в соответствии с критериями, аналогичными критериям Примера испытания 7, и расстояние между отмеченными четырьмя точками было измерено для оценки степени усадки.
[0465] Результаты оценки структуры на ощупь показаны в таблице 21. «Начало» означает результат оценки после предварительной обработки и до начала цикла. Трикотажное полотно Примера испытания 8-2 (в таблице 21, Примера испытания 2-2), подвергнутое плазменной обработке, было защищено от разрушения структуры, по сравнению с трикотажным полотном Примера испытания 8-1 (в таблице 21, Примера испытания 2-1), не подвергнутым плазменной обработке.
[0466] Результаты оценки степени усадки показаны в таблице 22. Трикотажное полотно Примера испытания 8-2 (в таблице 22 Примера испытания 2-2), подвергнутое плазменной обработке, имело меньшую степень усадки, чем трикотажное полотно Примера испытания 8-1 (в таблице 22 Примера испытания 2-1), не подвергнутое плазменной обработке.
[0467] [Пример испытания 9: Получение и оценка модифицированного фиброинового волокна]
<Пример испытания 9-1>
(1) Получение прядильного раствора (прядильного раствора полимера)
В 11400 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 200 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и 400 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и изоцианатная группа фенилизоцианата были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0468] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 300 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера). Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0469] (2) Получение волокна, содержащего модифицированный фиброин и вещество, сообщающее водостойкость
Полученный прядильный раствор нагревали до 60°C и фильтровали через металлический фильтр с размером отверстий 5 мкм. После этого, фильтрат оставляли в шприце из нержавеющей стали объемом 30 мл для удаления пены. Полученный продукт выгружали из встроенного сопла, имеющего диаметр иглы 0,2 мм, в коагуляционную ванну с 100 масс.% метанолом с применением газообразного азота. Температура выгрузки составляла 60°C, а давление выгрузки составляло 0,3 МПа. После коагуляции, полученную исходную пряжу наматывали со скоростью намотки 3,00 м/мин и сушили естественным путем с получением волокна, содержащего модифицированный фиброин и вещество, сообщающее водостойкость (модифицированный крахмал).
[0470] Оценка усадки
Полученное волокно разрезали на длину приблизительно 10 см, и перед погружением в воду измеряли длину (см) пряжи. Затем пряжу погружали на одну минуту в водяную баню при 40°C. После этого, пряжу вынимали из водяной бани, сушили в вакууме при комнатной температуре в течение 15 минут с последующим измерением длины высушенной пряжи. Степень усадки волокна вычисляли по нижеследующей формуле. Результаты представлены в таблице 23.
Степень усадки (%) = {(длина до погружения/длина после погружения и сушки) - 1}×100.
В таблице 23, в Примере испытания 5-1 показан Пример испытания 9-1, в Примере испытания 5-2 показан Пример испытания 9-2, описанный ниже, в Примере испытания 5-3 показан Пример испытания 9-3, описанный ниже, в Примере испытания 5-4 показан Пример испытания 9-4, описанный ниже, в Примере испытания 5-5 показан Пример испытания 9-5, описанный ниже, в Примере испытания 5-6 показан Пример испытания 9-6, описанный ниже, и в Примере испытания 5-7 показан Пример испытания 9-7, описанный ниже.
[0471] <Пример испытания 9-2>
(1) Получение прядильного раствора (прядильного раствора полимера)
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 253 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 147 мг ангидрида уксусной кислоты (поставляемого Wako Pure Chemical Industries, Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и ангидрид уксусной кислоты были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), с которым была связана ацетильная группа (реакционноспособная функциональная группа). После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0472] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера). Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0473] (2) Получение волокна, содержащего модифицированный фиброин и вещество, придающее водостойкость
С применением полученного прядильного раствора было изготовлено волокно, содержащее модифицированный фиброин и вещество, придающее водостойкость (модифицированный крахмал), как описано в Примере 9-1.
[0474] (3) Оценка усадки
Усадку полученного волокна оценивали как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0475] <Примере испытания 9-3>
(1) Получение прядильного раствора (прядильного раствора полимера)
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 215 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 185 мг ангидрида уксусной кислоты (поставляемого Wako Pure Chemical Industries, Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа крахмала и ангидрид уксусной кислоты были подвергнуты реакции взаимодействия с получением модифицированного крахмала (модифицированного полимера, содержащего гидроксильную группу), с которым была связана ацетильная группа (реакционноспособная функциональная группа). После вычисления соотношений загруженных веществ, модифицированный крахмал был модифицирован на 50% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0476] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера). Содержание модифицированного крахмала в прядильном растворе составляло 17 масс.% от общего количества модифицированного крахмала и крахмала.
[0477] (2) Получение волокна, содержащего модифицированный фиброин и вещество, придающее водостойкость
С применением полученного прядильного раствора было изготовлено волокно, содержащее модифицированный фиброин и вещество, придающее водостойкость (модифицированный крахмал), как описано в Примере испытания 5-1.
[0478] (3) Оценка усадки
Усадку полученного волокна оценивали как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0479] <Пример испытания 9-4>
(1) Получение прядильного раствора (прядильного раствора полимера)
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 128 мг поливинилового спирта (ПВС) (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 272 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа ПВС и фенилизоцианат были подвергнуты реакции взаимодействия с получением модифицированного ПВС (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный ПВС был модифицирован на 100% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0480] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера). Содержание модифицированного ПВС в прядильном растворе составляло 17 масс.% от общего количества модифицированного ПВС и ПВС.
[0481] (2) Получение волокна, содержащего модифицированный фиброин и вещество, придающее водостойкость
С применением полученного прядильного раствора было изготовлено волокно, содержащее модифицированный фиброин и вещество, придающее водостойкость (модифицированный ПВС), как описано в Примере испытания 9-1.
[0482] (3) Оценка усадки
Усадку полученного волокна оценивали как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0483] <Пример испытания 9-5>
(1) Получение прядильного раствора (прядильного раствора полимера)
В 7600 мг растворителя (диметилсульфоксида (ДМСО), содержащего 4 масс.% LiCl) растворяли 193 мг поливинилового спирта (ПВС) (поставляемого Wako Pure Chemical Industries, Ltd.) и добавляли 207 мг фенилизоцианата (поставляемого Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием смеси при 90°C в течение четырех часов для реакции взаимодействия материалов. Соответственно, гидроксильная группа ПВС и фенилизоцианат были подвергнуты реакции взаимодействия с получением модифицированного ПВС (модифицированного полимера, содержащего гидроксильную группу), в котором фенильная группа (реакционноспособная функциональная группа) была связана посредством уретановой связи. После вычисления соотношений загруженных веществ, модифицированный ПВС был модифицирован на 50% (процент, при котором гидроксильная группа была превращена в реакционноспособную функциональную группу).
[0484] После охлаждения реакционного раствора до комнатной температуры, к реакционному раствору добавляли 2000 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера). Содержание модифицированного ПВС в прядильном растворе составляло 17 масс.% от общего количества модифицированного ПВС и ПВС.
[0485] (2) Получение волокна, содержащего модифицированный фиброин и вещество, придающее водостойкость
С применением полученного прядильного раствора было изготовлено волокно, содержащее модифицированный фиброин и вещество, придающее водостойкость (модифицированный ПВС), как описано в Примере испытания 9-1.
[0486] (3) Оценка усадки
Усадку полученного волокна оценивали как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0487] <Пример испытания 9-6>
(1) Получение прядильного раствора (прядильного раствора полимера)
К растворителю (диметилсульфоксиду (ДМСО), содержащему 4 масс.% LiCl) добавляли 1200 мг лиофилизованного порошка модифицированного фиброина (PRT799), и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера).
[0488] (2) Получение волокна
С применением полученного прядильного раствора было изготовлено волокно, как описано в Примере испытания 9-1.
[0489](3) Оценка усадки
Усадку полученного волокна оценивали, как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0490] <Пример испытания 9-7>
(1) Получение прядильного раствора (прядильного раствора полимера)
К растворителю (диметилсульфоксиду (ДМСО), содержащему 4 масс.% LiCl) добавляли 3000 мг лиофилизованного порошка модифицированного фиброина (PRT799) и 600 мг крахмала (поставляемого Wako Pure Chemical Industries, Ltd.) и смесь перемешивали при 90°C в течение 12 часов для растворения с получением прозрачного прядильного раствора (прядильного раствора полимера).
[0491](2) Получение волокна
С применением полученного прядильного раствора было изготовлено волокно как описано в Примере испытания 9-1.
[0492](3) Оценка усадки
Усадку полученного волокна оценивали как описано в Примере испытания 9-1. Результаты представлены в таблице 23.
[0493]
*1 (Содержание модифицированного полимера, содержащего гидроксильную группу/общее количество модифицированного полимера, содержащего гидроксильную группу, и полимера, содержащего гидроксильную группу)×100.
[0494] Волокно, содержащее модифицированный фиброин и вещество, придающее водостойкость (полимер, содержащий гидроксильную группу (модифицированный крахмал или модифицированный ПВС)), имело пониженную степень усадки по сравнению с волокном, не содержащим вещества, придающего водостойкость.
[0495] [Пример испытания 10: Оценка огнестойкости модифицированного фиброинового волокна]
LiCl растворяли в диметилсульфоксиде (ДМСО) в концентрации 4,0 масс.% для приготовления растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина (PRT799) в концентрации 24 масс.% с последующим растворением смеси в течение трех часов на шейкере. После этого нерастворимые вещества и пену удаляли с получением модифицированного раствора фиброина (прядильного раствора).
[0496] Полученный прядильный раствор нагревали до 90°C и фильтровали через металлический фильтр с размером отверстий 5 мкм. После этого, фильтрат оставляли в шприце из нержавеющей стали объемом 30 мл для удаления пены. Полученный продукт выгружали из встроенного сопла, имеющего диаметр иглы 0,2 мм, в коагуляционную ванну с 100 масс.% метанолом. Температура выгрузки составляла 90°C. После коагуляции, полученную исходную пряжу наматывали и сушили естественным путем с получением модифицированного фиброинового волокна (исходного волокна).
[0497] С применением полученного фиброинового модифицированного волокна (скрученной пряжи) было получено трикотажное полотно для оценки, которое было изготовлено путем кругового вязания на кругловязальной машине. Трикотажное полотно имело толщину 180 денье и калибр 18. Для получения тестируемого образца отрезали 20 граммов полученного трикотажного полотна.
[0498] Испытание на воспламеняемость проводили в соответствии с методом испытаний для гранулированных материалов или синтетической смолы с низкой температурой плавления, как предписано в Уведомлении № 50, выданном 31 мая 1995 г. начальником Агентства по безопасности при работе с опасными продуктами, по борьбе с пожарами и стихийными бедствиями. Испытание проводили при температуре 22°C, относительной влажности 45% и атмосферном давлении 1021 гПа. В таблице 24 показаны результаты оценки (концентрация кислорода (%), скорость горения (%) и преобразованная скорость горения (%)).
[0499]
[0500] Как показали результаты испытания на огнестойкость, предельный кислородный индекс (LOI) модифицированных фиброиновых (PRT799) волокон составлял 27,2. Обычно, если ткань имеет LOI 26 или более, то она считается огнестойкой. Результат показал, что модифицированное фиброиновое волокно обладает превосходной огнестойкостью.
[0501] [Пример испытания 11: Оценка влагопоглощающих и тепловыделяющих свойств модифицированного фиброинового волокна]
LiCl растворяли в диметилсульфоксиде (ДМСО) в концентрации 4,0 масс.% для приготовления растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина в концентрации 24 масс.% с последующим растворением смеси в течение трех часов на шейкере. После этого, нерастворимые вещества и пену удаляли с получением модифицированного раствора фиброина (прядильного раствора).
[0502] Полученный прядильный раствор нагревали до 60°C и фильтровали через металлический фильтр с размером отверстий 5 мкм. После этого, фильтрат оставляли в шприце из нержавеющей стали объемом 30 мл для удаления пены. Полученный продукт выгружали из встроенного сопла, имеющего диаметр иглы 0,2 мм, в коагуляционную ванну с 100 масс.% метанолом. Температура выгрузки составляла 60°C. После коагуляции, полученную исходную пряжу наматывали и сушили естественным путем с получением модифицированного фиброинового волокна (исходного волокна).
[0503] Для сравнения было получено коммерчески доступное шерстяное волокно, хлопковое волокно, тенацелевое волокно, искусственное волокно и полиэфирное волокно.
[0504] С применением каждого из этих волокон было изготовлено трикотажное полотно для оценки, которое было получено путем уточного вязания на уточной вязальной машине. Трикотажное полотно, содержащее модифицированное фиброиновое волокно (PRT 918), имело толщину 1/30 N (номер однослойной пряжи), а калибр был установлен на 18. Трикотажное полотно, содержащее модифицированное фиброиновое волокно (PRT799), имело толщину 1/30 N (номер однослойной пряжи), а калибр был установлен на 16. Толщина и калибр трикотажного полотна, изготовленного с применением других волокон, были отрегулированы так, чтобы коэффициент покрытия был почти такой же как у трикотажного полотна, изготовленного с применением волокна PRT918 и волокна PRT799. Подробное описание представлено ниже.
Толщина шерсти: 2/30 N (двухслойная пряжа), калибр: 14.
Толщина хлопчатобумажной ткани: 2/34 N (двуслойная пряжа), калибр: 14.
Толщина тенацелевой ткани: 2/30 N (двухслойная пряжа), калибр: 15.
Толщина искусственной ткани: 1/38 N (однослойная пряжа), калибр: 14.
Толщина полиэфирного волокна: 1/60 N (однослойная пряжа), калибр: 14.
[0505] Два вырезанных куска трикотажного полотна размером 10 см × 10 см объединяли, и четыре стороны объединенного полотна сшивали с получением ткани для испытаний (образца). Образец для испытаний выдерживали в среде с низкой влажностью (температура: 20±2°C, относительная влажность: 40±5%) в течение четырех часов или более, а затем переносили в среду с высокой влажностью (температура: 20°C±2°C, относительная влажность: 90±5%). Температуру образца для испытаний измеряли в течение 30 минут с интервалом в одну минуту с применением датчика температуры, прикрепленного к центру внутренней части тестируемого образца.
[0506] Исходя из результатов измерений был определен максимальный уровень влагопоглощения и выделения тепла в соответствии со следующей формулой А.
Формула A: максимальный уровень влагопоглощения и выделения тепла = {(максимальная температура образца, определенная после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия)} (°C)/массу образца (г).
[0507] На фиг. 8 представлен график, где показан пример результатов испытаний на поглощение влаги и выделение тепла. На графике, ноль означает момент времени, когда образец переносится из среды с низкой влажностью в среду с высокой влажностью, а время (мин.) выдерживания образца в среде с высокой влажностью отложено на оси абсцисс. Температура, измеренная датчиком температуры (температура образца), отложена на оси ординат. На графике, представленном на фиг. 8, точка, обозначаемая «М», соответствует максимальной температуре образца. В таблице 25 показаны результаты оценки максимального уровня влагопоглощения и выделения тепла.
[0508]
[0509] В таблице 25 показано, что модифицированные фиброиновые волокна (волокно PRT918 и волокно PRT799) имеют максимально высокие уровни влагопоглощения и выделения тепла, а также обладают превосходными влагопоглощающими и тепловыделяющими свойствами по сравнению со стандартными волокнами.
[0510] [Пример испытания 12: Оценка термостойкости модифицированного фиброинового волокна]
LiCl растворяли в диметилсульфоксиде (ДМСО) в концентрации 4,0 масс.% для приготовления растворителя. К растворителю добавляли лиофилизованный порошок модифицированного фиброина в концентрации 24 масс.% с последующим растворением смеси в течение трех часов на шейкере. После этого, нерастворимые вещества и пену удаляли с получением модифицированного раствора фиброина (прядильного раствора).
[0511] Полученный прядильный раствор нагревали до 60°C и фильтровали через металлический фильтр с размером отверстий 5 мкм. После этого, фильтрат оставляли в шприце из нержавеющей стали объемом 30 мл для удаления пены. Полученный продукт выгружали из встроенного сопла, имеющего диаметр иглы 0,2 мм, в коагуляционную ванну с 100 масс.% метанолом. Температура выгрузки составляла 60°C. После коагуляции, полученную исходную пряжу наматывали и сушили естественным путем с получением модифицированного фиброинового волокна (исходного волокна).
[0512] Для сравнения было получено коммерчески доступное шерстяное волокно, шелковое волокно, хлопчатобумажное волокно, искусственное волокно и полиэфирное волокно.
[0513] С применением каждого из этих волокон было изготовлено трикотажное полотно для оценки, которое было получено путем уточного вязания на уточной вязальной машине. Трикотажное полотно, содержащее модифицированное фиброиновое волокно (PRT966), имело номер пряжи 30 Nm, число кручений 1, калибр 18 и удельный вес 90,1 г/м2. Трикотажное полотно, содержащее модифицированное фиброиновое волокно (PRT799), имело номер пряжи 30 Nm, число кручений 1, калибр 16 и удельный вес 111,0 г/м2. Толщина и калибр трикотажного полотна, изготовленного с применением других волокон, были отрегулированы так, чтобы коэффициент покрытия был почти такой же, как у трикотажного полотна, изготовленного с применением волокна PRT966 и волокна PRT799. Подробное описание представлено ниже.
Номер шерстяной пряжи: 30 Nm, число кручений 2, калибр 14, удельный вес: 242,6 г/м2.
Номер шелковой пряжи: 60 Nm, число кручений 2, калибр: 14, удельный вес: 225,2 г/м2.
Номер хлопчатобумажной пряжи: 34 Nm, число кручений 2, калибр 14, удельный вес: 194,1 г/м2.
Номер искусственной пряжи: 30 Nm, число кручений 1, калибр 14, удельный вес: 181,8 г/м2.
Номер пряжи из полиэфирного волокна: 30 Nm, число кручений 1, калибр 14, удельный вес: 184,7 г/м2.
[0514] Термостойкость оценивали с применением устройства KES-F7 Thermo Labo II, поставляемого от Kato Tech Co., Ltd., с применением метода сухого контакта (метода, основанного на предположении, что кожа и одежда находятся в прямом контакте друг с другом в сухом состоянии). В качестве ткани для испытаний (образца) использовали трикотажное полотно размером 20 см × 20 см. Тестируемый образец помещали на горячую пластину, установленную на заданную температуру (30°C), и количество тепла, рассеиваемого через тестируемый образец (а), измеряли при скорости ветра 30 см/сек. в аэродинамической трубе. Количество тепла, рассеиваемого без установки тестируемого образца (b), было определено в условии, аналогичных условиям, приведенным выше, в результате чего была вычислена степень удерживания тепла (%) в соответствии со следующей формулой:
Степень удерживания тепла (%) = (1 - a/b)×100.
[0515] Исходя из результатов измерения определяли коэффициент удерживания тепла по формуле B.
Формула B: коэффициент удерживания тепла = степень удерживания тепла (%)/удельный вес образца (г/м2).
[0516] Результат вычисления коэффициента удерживания тепла показан в таблице 26. Материалы с более высоким коэффициентом удерживания тепла оцениваются как превосходные по своей способности удерживать тепло.
[0517]
[0518] В таблице 26 показано, что модифицированные фиброиновые волокна (волокно PRT966 и волокно PRT799) имеют высокий коэффициент удерживания тепла и превосходную термостойкость по сравнению со стандартным волокном.
[0519] [Пример испытания 13: Изготовление искусственного меха]
Лиофилизованный порошок модифицированного фиброина (PRT 966) добавляли к муравьиной кислоте в концентрации 30 масс.% с последующим растворением смеси в течение 1,5 часа с применением резервуара для растворения, снабженного лопастями для перемешивания. После этого, нерастворимые вещества и пену удаляли с получением модифицированного раствора фиброина (прядильного раствора). Полученный модифицированный раствор фиброина шелка паука использовали в качестве прядильного раствора (прядильного раствора полимера), а модифицированное фиброиновое волокно шелка паука (нити) было изготовлено сухим-мокрым способом прядения с применением известного устройства для сухого-мокрого прядения. Затем, полученное модифицированное фиброиновое волокно механически обжимали с помощью известного устройства для придания извитости, а затем, нарезали на образцы длиной от 110 до 150 мм с получением штапельного волокна. Штапельную пряжу получали с применением штапельного волокна стандартным методом. Затем, полученную штапельную пряжу использовали для изготовления ворсового трикотажного полотна, имеющего ворсинки, выступающие на одной поверхности, путем ворсового вязания. После этого, петлю каждой ворсинки разрезали, и ворсинки расчесывали. Соответственно, был изготовлен искусственный мех, включающий модифицированное фиброиновое волокно. Фотографии полученного искусственного меха показаны на фиг. 9 и 10.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Spiber Inc.
<120> Искусственный мех и способ его изготовления
<130> 19PS032WO1
<160> 44
<170> PatentIn version 3.5
<210> 1
<211> 50
<212> PRT
<213> Araneus diadematus
<400> 1
Ser Gly Cys Asp Val Leu Val Gln Ala Leu Leu Glu Val Val Ser Ala
1 5 10 15
Leu Val Ser Ile Leu Gly Ser Ser Ser Ile Gly Gln Ile Asn Tyr Gly
20 25 30
Ala Ser Ala Gln Tyr Thr Gln Met Val Gly Gln Ser Val Ala Gln Ala
35 40 45
Leu Ala
50
<210> 2
<211> 30
<212> PRT
<213> Araneus diadematus
<400> 2
Ser Gly Cys Asp Val Leu Val Gln Ala Leu Leu Glu Val Val Ser Ala
1 5 10 15
Leu Val Ser Ile Leu Gly Ser Ser Ser Ile Gly Gln Ile Asn
20 25 30
<210> 3
<211> 21
<212> PRT
<213> Araneus diadematus
<400> 3
Ser Gly Cys Asp Val Leu Val Gln Ala Leu Leu Glu Val Val Ser Ala
1 5 10 15
Leu Val Ser Ile Leu
20
<210> 4
<211> 1154
<212> PRT
<213> Искусственная последовательность
<220>
<223> рекомбинантный белок шелка паука ADF3KaiLargeNRSH1
<400> 4
Met His His His His His His His His His His Ser Ser Gly Ser Ser
1 5 10 15
Leu Glu Val Leu Phe Gln Gly Pro Ala Arg Ala Gly Ser Gly Gln Gln
20 25 30
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
35 40 45
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr
50 55 60
Gly Pro Gly Ser Gly Gln Gln Gly Pro Ser Gln Gln Gly Pro Gly Gln
65 70 75 80
Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
85 90 95
Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro
100 105 110
Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
115 120 125
Ala Gly Gly Asn Gly Pro Gly Ser Gly Gln Gln Gly Ala Gly Gln Gln
130 135 140
Gly Pro Gly Gln Gln Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala
145 150 155 160
Gly Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly
165 170 175
Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
180 185 190
Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly Gln Gly Pro Gly Gln Gln
195 200 205
Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
210 215 220
Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
225 230 235 240
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly
245 250 255
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly
260 265 270
Tyr Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro
275 280 285
Tyr Gly Pro Gly Ala Ser Ala Ala Ser Ala Ala Ser Gly Gly Tyr Gly
290 295 300
Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln
305 310 315 320
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly
325 330 335
Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
340 345 350
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly
355 360 365
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly
370 375 380
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
385 390 395 400
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
405 410 415
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly
420 425 430
Gln Gly Ala Tyr Gly Pro Gly Ala Ser Ala Ala Ala Gly Ala Ala Gly
435 440 445
Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
450 455 460
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
465 470 475 480
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly
485 490 495
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly
500 505 510
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
515 520 525
Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ala Ser Ala Ala Val Ser
530 535 540
Val Ser Arg Ala Arg Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln
545 550 555 560
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
565 570 575
Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly
580 585 590
Gln Gln Gly Pro Ser Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly
595 600 605
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly
610 615 620
Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro
625 630 635 640
Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Gly Gly Asn Gly
645 650 655
Pro Gly Ser Gly Gln Gln Gly Ala Gly Gln Gln Gly Pro Gly Gln Gln
660 665 670
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro
675 680 685
Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly
690 695 700
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr
705 710 715 720
Gly Pro Gly Ser Gly Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln
725 730 735
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly
740 745 750
Tyr Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
755 760 765
Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
770 775 780
Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Tyr Gly Gln Gln Gly
785 790 795 800
Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala
805 810 815
Ser Ala Ala Ser Ala Ala Ser Gly Gly Tyr Gly Pro Gly Ser Gly Gln
820 825 830
Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro
835 840 845
Gly Ala Ser Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser
850 855 860
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
865 870 875 880
Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
885 890 895
Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly Gln Gln Gly
900 905 910
Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
915 920 925
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
930 935 940
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly Gln Gly Ala Tyr Gly
945 950 955 960
Pro Gly Ala Ser Ala Ala Ala Gly Ala Ala Gly Gly Tyr Gly Pro Gly
965 970 975
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
980 985 990
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
995 1000 1005
Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser
1010 1015 1020
Ala Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Ser Gly Gln
1025 1030 1035
Gln Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Gly
1040 1045 1050
Gln Gly Pro Tyr Gly Pro Gly Ala Ala Ser Ala Ala Val Ser Val
1055 1060 1065
Gly Gly Tyr Gly Pro Gln Ser Ser Ser Val Pro Val Ala Ser Ala
1070 1075 1080
Val Ala Ser Arg Leu Ser Ser Pro Ala Ala Ser Ser Arg Val Ser
1085 1090 1095
Ser Ala Val Ser Ser Leu Val Ser Ser Gly Pro Thr Lys His Ala
1100 1105 1110
Ala Leu Ser Asn Thr Ile Ser Ser Val Val Ser Gln Val Ser Ala
1115 1120 1125
Ser Asn Pro Gly Leu Ser Gly Cys Asp Val Leu Val Gln Ala Leu
1130 1135 1140
Leu Glu Val Val Ser Ala Leu Val Ser Ile Leu
1145 1150
<210> 5
<211> 24
<212> PRT
<213> Искусственная последовательность
<220>
<223> His-метка и старт-кодон
<400> 5
Met His His His His His His His His His His Ser Ser Gly Ser Ser
1 5 10 15
Leu Glu Val Leu Phe Gln Gly Pro
20
<210> 6
<211> 597
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT380
<400> 6
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly
35 40 45
Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro
50 55 60
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala
65 70 75 80
Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Ala Ala
85 90 95
Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln
100 105 110
Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly
115 120 125
Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
145 150 155 160
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
165 170 175
Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly
180 185 190
Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
195 200 205
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala
210 215 220
Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
225 230 235 240
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly
245 250 255
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro
260 265 270
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
275 280 285
Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly
290 295 300
Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro
305 310 315 320
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro
325 330 335
Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Ala Ala Ala
340 345 350
Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
355 360 365
Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly
370 375 380
Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro
385 390 395 400
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
405 410 415
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
420 425 430
Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala
435 440 445
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr
450 455 460
Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly
465 470 475 480
Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
485 490 495
Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
500 505 510
Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly
515 520 525
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser
530 535 540
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala
545 550 555 560
Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly
565 570 575
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln
580 585 590
Gly Pro Gly Ala Ser
595
<210> 7
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT410
<400> 7
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro
50 55 60
Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln
85 90 95
Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro
165 170 175
Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
180 185 190
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly
195 200 205
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
260 265 270
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
340 345 350
Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln
355 360 365
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro
450 455 460
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
485 490 495
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser
500 505 510
Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
530 535 540
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser
545 550 555 560
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
580 585 590
<210> 8
<211> 565
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT525
<400> 8
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Ala Ala Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly
20 25 30
Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
35 40 45
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
50 55 60
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala
65 70 75 80
Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly
85 90 95
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
100 105 110
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly
115 120 125
Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly
145 150 155 160
Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
165 170 175
Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly
180 185 190
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser
195 200 205
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly
210 215 220
Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala
225 230 235 240
Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser
245 250 255
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Gln
260 265 270
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser
275 280 285
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala
290 295 300
Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
305 310 315 320
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln
325 330 335
Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly
340 345 350
Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser
355 360 365
Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala
370 375 380
Ala Ala Ala Ala Ala Gly Ser Tyr Gln Gln Gly Pro Gly Gln Gln Gly
385 390 395 400
Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly
405 410 415
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr
420 425 430
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
435 440 445
Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro
450 455 460
Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly
465 470 475 480
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro
485 490 495
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
500 505 510
Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln
515 520 525
Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly
530 535 540
Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln
545 550 555 560
Gly Pro Gly Ala Ser
565
<210> 9
<211> 2364
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT799
<400> 9
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro
50 55 60
Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln
85 90 95
Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro
165 170 175
Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
180 185 190
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly
195 200 205
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
260 265 270
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
340 345 350
Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln
355 360 365
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro
450 455 460
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
485 490 495
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser
500 505 510
Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
530 535 540
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser
545 550 555 560
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln
580 585 590
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
595 600 605
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr
610 615 620
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
625 630 635 640
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
645 650 655
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
660 665 670
Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
675 680 685
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
690 695 700
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
705 710 715 720
Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
725 730 735
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
740 745 750
Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro
755 760 765
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly
770 775 780
Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly
785 790 795 800
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
805 810 815
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
820 825 830
Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
835 840 845
Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln
850 855 860
Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln
865 870 875 880
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
885 890 895
Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly
900 905 910
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
915 920 925
Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
930 935 940
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln
945 950 955 960
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr
965 970 975
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly
980 985 990
Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln
995 1000 1005
Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln
1010 1015 1020
Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro
1025 1030 1035
Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln
1040 1045 1050
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly
1055 1060 1065
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
1070 1075 1080
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
1085 1090 1095
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln
1100 1105 1110
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
1115 1120 1125
Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
1130 1135 1140
Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
1145 1150 1155
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
1160 1165 1170
Pro Gly Ala Ser Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser
1175 1180 1185
Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln
1190 1195 1200
Gly Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
1205 1210 1215
Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro
1220 1225 1230
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
1235 1240 1245
Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
1250 1255 1260
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro
1265 1270 1275
Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro
1280 1285 1290
Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro
1295 1300 1305
Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
1310 1315 1320
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser
1325 1330 1335
Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr
1340 1345 1350
Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
1355 1360 1365
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser
1370 1375 1380
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
1385 1390 1395
Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser
1400 1405 1410
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln
1415 1420 1425
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly
1430 1435 1440
Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala
1445 1450 1455
Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
1460 1465 1470
Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln
1475 1480 1485
Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln
1490 1495 1500
Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln
1505 1510 1515
Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala
1520 1525 1530
Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly
1535 1540 1545
Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr
1550 1555 1560
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr
1565 1570 1575
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala
1580 1585 1590
Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro
1595 1600 1605
Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr
1610 1615 1620
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro
1625 1630 1635
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala
1640 1645 1650
Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln
1655 1660 1665
Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
1670 1675 1680
Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro
1685 1690 1695
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
1700 1705 1710
Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly
1715 1720 1725
Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly
1730 1735 1740
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln
1745 1750 1755
Gln Gly Pro Gly Ala Ser Gly Gln Gln Gly Pro Tyr Gly Pro Gly
1760 1765 1770
Ala Ser Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly
1775 1780 1785
Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln
1790 1795 1800
Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
1805 1810 1815
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser
1820 1825 1830
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
1835 1840 1845
Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln
1850 1855 1860
Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
1865 1870 1875
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala
1880 1885 1890
Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly
1895 1900 1905
Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser
1910 1915 1920
Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly
1925 1930 1935
Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
1940 1945 1950
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser
1955 1960 1965
Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser
1970 1975 1980
Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
1985 1990 1995
Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro
2000 2005 2010
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
2015 2020 2025
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
2030 2035 2040
Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly
2045 2050 2055
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly
2060 2065 2070
Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly
2075 2080 2085
Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
2090 2095 2100
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
2105 2110 2115
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln
2120 2125 2130
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly
2135 2140 2145
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
2150 2155 2160
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala
2165 2170 2175
Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr
2180 2185 2190
Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly
2195 2200 2205
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
2210 2215 2220
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala
2225 2230 2235
Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser
2240 2245 2250
Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln
2255 2260 2265
Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln
2270 2275 2280
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
2285 2290 2295
Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro
2300 2305 2310
Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln
2315 2320 2325
Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser
2330 2335 2340
Gly Gln Gln Gly Ser Ser Val Asp Lys Leu Ala Ala Ala Leu Glu
2345 2350 2355
His His His His His His
2360
<210> 10
<211> 597
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT313
<400> 10
Met Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gly Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gly Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gly Gln Gly
35 40 45
Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro
50 55 60
Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala Ala
65 70 75 80
Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Ala Ala
85 90 95
Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gln Gln
100 105 110
Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly
115 120 125
Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Gly Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
145 150 155 160
Ala Ala Ala Ala Gly Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro
165 170 175
Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly
180 185 190
Gly Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly
195 200 205
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Ala Ala
210 215 220
Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
225 230 235 240
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Gln Gly Pro Tyr Gly
245 250 255
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Tyr Gly Pro
260 265 270
Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
275 280 285
Gly Gly Asn Gly Pro Gly Ser Gly Gly Tyr Gly Pro Gly Gln Gln Gly
290 295 300
Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Gln Gly Pro
305 310 315 320
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro
325 330 335
Gly Gly Gln Gly Pro Gly Gly Tyr Gly Pro Gly Ser Ser Ala Ala Ala
340 345 350
Ala Ala Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
355 360 365
Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly
370 375 380
Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gln Gln Gly Pro
385 390 395 400
Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
405 410 415
Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
420 425 430
Ala Ala Gly Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala
435 440 445
Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gly Tyr
450 455 460
Gly Pro Tyr Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly
465 470 475 480
Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
485 490 495
Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
500 505 510
Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gly Tyr Gly
515 520 525
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Asn Gly Pro Gly Ser
530 535 540
Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gly Ser Ala Ala Ala
545 550 555 560
Ala Ala Gly Gly Tyr Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly
565 570 575
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln
580 585 590
Gly Pro Gly Ala Ser
595
<210> 11
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> His-метка
<400> 11
Met His His His His His His Ser Ser Gly Ser Ser
1 5 10
<210> 12
<211> 608
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT380
<400> 12
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala
35 40 45
Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
50 55 60
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro
65 70 75 80
Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
85 90 95
Ser Gly Gln Gln Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
100 105 110
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser
115 120 125
Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly
130 135 140
Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr
145 150 155 160
Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
165 170 175
Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
180 185 190
Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Tyr
195 200 205
Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln
210 215 220
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Ser
225 230 235 240
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala
245 250 255
Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
260 265 270
Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro
275 280 285
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro
290 295 300
Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala
305 310 315 320
Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
325 330 335
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
340 345 350
Gly Gln Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly
355 360 365
Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
370 375 380
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala
385 390 395 400
Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro
405 410 415
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln
420 425 430
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
435 440 445
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala
450 455 460
Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro
465 470 475 480
Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
485 490 495
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
500 505 510
Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala
515 520 525
Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Ala
530 535 540
Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro
545 550 555 560
Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr
565 570 575
Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
580 585 590
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
595 600 605
<210> 13
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT410
<400> 13
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr
35 40 45
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
85 90 95
Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
100 105 110
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
115 120 125
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly
195 200 205
Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly
210 215 220
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln
275 280 285
Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
305 310 315 320
Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
355 360 365
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly
405 410 415
Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln
420 425 430
Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser
435 440 445
Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
465 470 475 480
Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
500 505 510
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
515 520 525
Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln
545 550 555 560
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro
565 570 575
Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Gln Gln Gly Pro Gly Ala Ser
595 600
<210> 14
<211> 576
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT525
<400> 14
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
20 25 30
Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly
35 40 45
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
50 55 60
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly
65 70 75 80
Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
85 90 95
Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly
100 105 110
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala
115 120 125
Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr
130 135 140
Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr
145 150 155 160
Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly
165 170 175
Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala
180 185 190
Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Tyr Ala Ser Ala
195 200 205
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Gln
210 215 220
Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly
225 230 235 240
Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
245 250 255
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
260 265 270
Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly
275 280 285
Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro
290 295 300
Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly
305 310 315 320
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
325 330 335
Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr
340 345 350
Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
355 360 365
Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln
370 375 380
Gln Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala
385 390 395 400
Gly Ser Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
405 410 415
Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
420 425 430
Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln
435 440 445
Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly
450 455 460
Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro
465 470 475 480
Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
485 490 495
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly Pro
500 505 510
Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
515 520 525
Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser
530 535 540
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala
545 550 555 560
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
565 570 575
<210> 15
<211> 2375
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT799
<400> 15
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr
35 40 45
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
85 90 95
Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
100 105 110
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
115 120 125
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly
195 200 205
Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly
210 215 220
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln
275 280 285
Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
305 310 315 320
Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
355 360 365
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly
405 410 415
Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln
420 425 430
Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser
435 440 445
Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
465 470 475 480
Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
500 505 510
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
515 520 525
Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln
545 550 555 560
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro
565 570 575
Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Gln Gly Pro Tyr Gly
595 600 605
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser
610 615 620
Gly Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln
625 630 635 640
Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
645 650 655
Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
660 665 670
Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly
675 680 685
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
690 695 700
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln
705 710 715 720
Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln
725 730 735
Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr
740 745 750
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly
755 760 765
Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala
770 775 780
Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr
785 790 795 800
Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly
805 810 815
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro
820 825 830
Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr
835 840 845
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn
850 855 860
Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
865 870 875 880
Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
885 890 895
Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln
900 905 910
Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly
915 920 925
Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
930 935 940
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala
945 950 955 960
Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
965 970 975
Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser
980 985 990
Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly
995 1000 1005
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly
1010 1015 1020
Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly
1025 1030 1035
Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
1040 1045 1050
Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Tyr
1055 1060 1065
Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
1070 1075 1080
Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly
1085 1090 1095
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala
1100 1105 1110
Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
1115 1120 1125
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
1130 1135 1140
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser
1145 1150 1155
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
1160 1165 1170
Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
1175 1180 1185
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
1190 1195 1200
Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln
1205 1210 1215
Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
1220 1225 1230
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly
1235 1240 1245
Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly
1250 1255 1260
Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr Gly
1265 1270 1275
Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
1280 1285 1290
Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly
1295 1300 1305
Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln
1310 1315 1320
Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln
1325 1330 1335
Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala
1340 1345 1350
Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Tyr Ala
1355 1360 1365
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln
1370 1375 1380
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly
1385 1390 1395
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly
1400 1405 1410
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala
1415 1420 1425
Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr
1430 1435 1440
Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr
1445 1450 1455
Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
1460 1465 1470
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1475 1480 1485
Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
1490 1495 1500
Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly
1505 1510 1515
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly
1520 1525 1530
Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
1535 1540 1545
Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
1550 1555 1560
Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
1565 1570 1575
Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Gln
1580 1585 1590
Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
1595 1600 1605
Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly
1610 1615 1620
Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala
1625 1630 1635
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly
1640 1645 1650
Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly
1655 1660 1665
Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly
1670 1675 1680
Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala
1685 1690 1695
Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly
1700 1705 1710
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
1715 1720 1725
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser
1730 1735 1740
Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser
1745 1750 1755
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
1760 1765 1770
Ala Ser Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1775 1780 1785
Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro
1790 1795 1800
Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
1805 1810 1815
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln
1820 1825 1830
Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala
1835 1840 1845
Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln
1850 1855 1860
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
1865 1870 1875
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln
1880 1885 1890
Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser
1895 1900 1905
Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro
1910 1915 1920
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala
1925 1930 1935
Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro
1940 1945 1950
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro
1955 1960 1965
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln
1970 1975 1980
Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala
1985 1990 1995
Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
2000 2005 2010
Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly Gln Gln Gly
2015 2020 2025
Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly
2030 2035 2040
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala
2045 2050 2055
Ala Ala Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser
2060 2065 2070
Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
2075 2080 2085
Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro
2090 2095 2100
Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly
2105 2110 2115
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala
2120 2125 2130
Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
2135 2140 2145
Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
2150 2155 2160
Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro
2165 2170 2175
Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln
2180 2185 2190
Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln
2195 2200 2205
Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro
2210 2215 2220
Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Gln
2225 2230 2235
Gln Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly
2240 2245 2250
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
2255 2260 2265
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
2270 2275 2280
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly Pro Gly Gln
2285 2290 2295
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
2300 2305 2310
Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly
2315 2320 2325
Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr
2330 2335 2340
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
2345 2350 2355
Ser Ser Val Asp Lys Leu Ala Ala Ala Leu Glu His His His His
2360 2365 2370
His His
2375
<210> 16
<211> 608
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT313
<400> 16
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gly
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gly Ser Ala Ala Ala
35 40 45
Ala Ala Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gln Gln Gly
50 55 60
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Tyr Gly Pro
65 70 75 80
Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
85 90 95
Ser Gly Gln Gln Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly
100 105 110
Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser
115 120 125
Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gln Gln Gly
130 135 140
Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gly Tyr
145 150 155 160
Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
165 170 175
Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala
180 185 190
Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gly Tyr Gly Pro Tyr
195 200 205
Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gln
210 215 220
Gln Gly Pro Tyr Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Ser
225 230 235 240
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala
245 250 255
Ala Ala Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
260 265 270
Ala Ala Ala Ala Gly Gly Tyr Gly Tyr Gly Pro Gly Gly Gln Gly Pro
275 280 285
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Asn Gly Pro
290 295 300
Gly Ser Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gly Ser Ala
305 310 315 320
Ala Ala Ala Ala Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala
325 330 335
Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro
340 345 350
Gly Gly Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly
355 360 365
Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
370 375 380
Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Ala
385 390 395 400
Ala Ala Ala Ala Gly Gly Tyr Gln Gln Gly Pro Gly Gly Gln Gly Pro
405 410 415
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Gln
420 425 430
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
435 440 445
Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala
450 455 460
Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gly Tyr Gly Pro Tyr Gly Pro
465 470 475 480
Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
485 490 495
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly
500 505 510
Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Ala Ala
515 520 525
Ala Ala Ala Gly Pro Gly Ser Gly Gly Tyr Gly Pro Gly Ala Ser Ala
530 535 540
Ala Ala Ala Ala Gly Gly Asn Gly Pro Gly Ser Gly Gly Tyr Gly Pro
545 550 555 560
Gly Gln Gln Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Gly Tyr
565 570 575
Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
580 585 590
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
595 600 605
<210> 17
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT399
<400> 17
Met Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gly Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gly Ser Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gln Gln Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Tyr Gly Pro
50 55 60
Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gly Tyr Gly Pro Gly Gly
85 90 95
Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Gly Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gly Tyr Gly Gln Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro
165 170 175
Gly Gly Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr
180 185 190
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Gly
195 200 205
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Gly Tyr Gly Tyr Gly Pro Gly Gly Gln Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Gly Asn Gly Pro Gly Ser Gly Gly
260 265 270
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gly Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro
340 345 350
Tyr Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gln Gln
355 360 365
Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gly Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Gly Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro
450 455 460
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Gly Tyr Gly Pro Gly Ala Ser Gly Gly Asn Gly
485 490 495
Pro Gly Ser Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gly Ser
500 505 510
Ala Ala Ala Ala Ala Gly Gly Tyr Gln Gln Gly Pro Gly Gly Gln Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly
530 535 540
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Gly Ser
545 550 555 560
Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
580 585 590
<210> 18
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT399
<400> 18
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gly
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gly Ser Gly Gly Tyr
35 40 45
Gly Pro Gly Gly Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly
85 90 95
Pro Gly Ala Ser Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Gly Gln
100 105 110
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser
115 120 125
Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Gly Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Gly Tyr Gly Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Gln Gln Gly Pro Gly Gly Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly
195 200 205
Gln Gln Gly Pro Tyr Gly Pro Gly Gly Ser Gly Ser Gly Gln Gln Gly
210 215 220
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Gly Tyr Gly Tyr Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Gly Asn Gly Pro Gly Ser Gly Gly Tyr Gly Pro Gly Gln
275 280 285
Gln Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Gln
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr
305 310 315 320
Gly Pro Gly Gly Gln Gly Pro Gly Gly Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gly
355 360 365
Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gln Gln Gly Pro Gly Gly Gln
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gly Gln Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gly Tyr Gly
405 410 415
Pro Gly Gly Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gly
420 425 430
Tyr Gly Ser Gly Pro Gly Gly Tyr Gly Pro Tyr Gly Pro Gly Gly Ser
435 440 445
Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Pro Gly Gln Gln Gly Pro
465 470 475 480
Tyr Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Gly Tyr Gly Pro Gly Ala Ser Gly Gly Asn Gly Pro Gly Ser Gly Gly
500 505 510
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gly Ser Ala Ala Ala Ala Ala
515 520 525
Gly Gly Tyr Gln Gln Gly Pro Gly Gly Gln Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Gly Tyr Gly Ser Gly Pro Gly Gln
545 550 555 560
Gln Gly Pro Tyr Gly Pro Gly Gly Ser Gly Ser Gly Gln Gln Gly Pro
565 570 575
Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Gln Gln Gly Pro Gly Ala Ser
595 600
<210> 19
<211> 612
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT720
<400> 19
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
20 25 30
Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu
50 55 60
Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Ser Ala Ser Ala Ala
65 70 75 80
Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly
85 90 95
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
100 105 110
Ser Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Val Leu Ile Gly Pro
115 120 125
Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala
130 135 140
Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala
145 150 155 160
Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser
165 170 175
Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Val Leu Ile Gly Pro Gly
180 185 190
Gln Tyr Val Leu Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly
195 200 205
Gln Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
210 215 220
Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr
245 250 255
Val Leu Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr
260 265 270
Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly
275 280 285
Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro
290 295 300
Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile
305 310 315 320
Gly Pro Tyr Val Leu Ile Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
325 330 335
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly
340 345 350
Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala
355 360 365
Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile Gly
370 375 380
Pro Tyr Val Leu Ile Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Gln Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
405 410 415
Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
420 425 430
Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln
435 440 445
Val Leu Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
450 455 460
Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly
465 470 475 480
Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
485 490 495
Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile
500 505 510
Gly Pro Tyr Val Leu Ile Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
515 520 525
Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
530 535 540
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser
545 550 555 560
Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Val Leu Ile Gly Pro Gly
565 570 575
Gln Gln Gly Pro Tyr Val Leu Ile Gly Pro Gly Ala Ser Ala Ala Ala
580 585 590
Ala Ala Gly Pro Gly Ser Gly Gln Gln Val Leu Ile Gly Pro Gly Ala
595 600 605
Ser Val Leu Ile
610
<210> 20
<211> 592
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT665
<400> 20
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Ala Ala Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly
20 25 30
Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
35 40 45
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
50 55 60
Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
65 70 75 80
Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly
85 90 95
Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly
100 105 110
Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser
115 120 125
Val Leu Ile Gly Pro Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala
130 135 140
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr
145 150 155 160
Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly
165 170 175
Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln
180 185 190
Val Leu Ile Gly Pro Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala
195 200 205
Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro
210 215 220
Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln
225 230 235 240
Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln
245 250 255
Gln Val Leu Ile Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
260 265 270
Ala Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr
275 280 285
Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly
290 295 300
Pro Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala
305 310 315 320
Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser
325 330 335
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly
340 345 350
Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro
355 360 365
Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr
370 375 380
Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Pro Gly Pro Ser
385 390 395 400
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gln Gln Gly Pro Gly Gln
405 410 415
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro
420 425 430
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
435 440 445
Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
450 455 460
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Tyr
465 470 475 480
Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly
485 490 495
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
500 505 510
Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Pro
515 520 525
Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln
530 535 540
Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr
545 550 555 560
Gly Pro Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala
565 570 575
Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Val Leu Ile
580 585 590
<210> 21
<211> 619
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT666
<400> 21
Met Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Ala Ala Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly
20 25 30
Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln
35 40 45
Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
50 55 60
Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Ser
65 70 75 80
Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln
85 90 95
Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly
100 105 110
Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser
115 120 125
Tyr Gly Ser Val Leu Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro
130 135 140
Tyr Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln
145 150 155 160
Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr
165 170 175
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
180 185 190
Ala Gly Ser Gly Gln Gln Val Leu Ile Gly Pro Gly Gln Tyr Val Leu
195 200 205
Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr
210 215 220
Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly
225 230 235 240
Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala
245 250 255
Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr
260 265 270
Val Leu Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly
275 280 285
Ser Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
290 295 300
Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln
305 310 315 320
Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln
325 330 335
Gln Val Leu Ile Gly Pro Tyr Val Leu Ile Gly Pro Gly Ala Ser Ala
340 345 350
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly Pro
355 360 365
Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr
370 375 380
Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly
385 390 395 400
Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu Ile Gly Pro Gly
405 410 415
Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gln Gln Gly Pro
420 425 430
Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln
435 440 445
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly
450 455 460
Pro Gly Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln Val Leu Ile Gly
465 470 475 480
Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser
485 490 495
Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly
500 505 510
Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
515 520 525
Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile
530 535 540
Gly Pro Tyr Val Leu Ile Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
545 550 555 560
Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln
565 570 575
Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly
580 585 590
Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln
595 600 605
Val Leu Ile Gly Pro Gly Ala Ser Val Leu Ile
610 615
<210> 22
<211> 623
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT720
<400> 22
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
20 25 30
Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly Gln Tyr
35 40 45
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu Ile Gly Pro Gly Gln
65 70 75 80
Gln Val Leu Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro
85 90 95
Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly
100 105 110
Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala Ala Ala Ala
115 120 125
Ala Gly Ser Tyr Gly Ser Val Leu Ile Gly Pro Gly Gln Gln Val Leu
130 135 140
Ile Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
145 150 155 160
Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln
165 170 175
Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala
180 185 190
Gly Ser Gly Gln Gln Val Leu Ile Gly Pro Gly Gln Tyr Val Leu Ile
195 200 205
Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly
210 215 220
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln
225 230 235 240
Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala
245 250 255
Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu Ile Gly Pro
260 265 270
Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly
275 280 285
Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly
290 295 300
Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala
305 310 315 320
Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu
325 330 335
Ile Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro
340 345 350
Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly
355 360 365
Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
370 375 380
Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu Ile
385 390 395 400
Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gln Gln Gly
405 410 415
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln
420 425 430
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro
435 440 445
Gly Gln Tyr Val Leu Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro
450 455 460
Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly
465 470 475 480
Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln
485 490 495
Gln Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
500 505 510
Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu
515 520 525
Ile Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
530 535 540
Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
545 550 555 560
Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
565 570 575
Gly Gln Tyr Gln Gln Val Leu Ile Gly Pro Gly Gln Gln Gly Pro Tyr
580 585 590
Val Leu Ile Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
595 600 605
Ser Gly Gln Gln Val Leu Ile Gly Pro Gly Ala Ser Val Leu Ile
610 615 620
<210> 23
<211> 603
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT665
<400> 23
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
20 25 30
Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly
35 40 45
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
50 55 60
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu Ile
65 70 75 80
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
85 90 95
Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser Gly Gln Tyr
100 105 110
Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser Ser Ala
115 120 125
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Val Leu Ile Gly Pro
130 135 140
Gly Gln Gln Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly
145 150 155 160
Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
165 170 175
Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala
180 185 190
Ala Ala Ala Ala Ala Ala Gly Ser Gly Gln Gln Val Leu Ile Gly Pro
195 200 205
Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly
210 215 220
Ser Tyr Gly Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Gln
225 230 235 240
Ser Gly Ser Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Ala Ser
245 250 255
Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile Gly
260 265 270
Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser
275 280 285
Tyr Gly Tyr Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser
290 295 300
Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly
305 310 315 320
Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln
325 330 335
Val Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
340 345 350
Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly
355 360 365
Pro Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser
370 375 380
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln
385 390 395 400
Val Leu Ile Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
405 410 415
Ala Ala Gly Ser Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro Tyr Gly
420 425 430
Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala
435 440 445
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu Ile
450 455 460
Gly Pro Gly Gln Gln Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
465 470 475 480
Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro
485 490 495
Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly Gln Gly Pro Tyr Gly
500 505 510
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro
515 520 525
Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala
530 535 540
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala
545 550 555 560
Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln
565 570 575
Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser
580 585 590
Gly Gln Gln Gly Pro Gly Ala Ser Val Leu Ile
595 600
<210> 24
<211> 630
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT666
<400> 24
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Gln
1 5 10 15
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
20 25 30
Gly Ser Asn Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Gln Ser Gly
35 40 45
Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly Ser
50 55 60
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val Leu Ile
65 70 75 80
Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Ser Ala Ser Ala Ala Ala
85 90 95
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Gly Pro Gly Ala Ser
100 105 110
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Gln Gly Pro Gly
115 120 125
Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Val Leu
130 135 140
Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Gly Ser Ala Ala
145 150 155 160
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro
165 170 175
Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly Gln Gln
180 185 190
Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Gly Gln
195 200 205
Gln Val Leu Ile Gly Pro Gly Gln Tyr Val Leu Ile Gly Pro Tyr Ala
210 215 220
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly
225 230 235 240
Gln Gln Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Gln Gln Gly
245 250 255
Pro Gly Gln Gln Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala
260 265 270
Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu Ile Gly Pro
275 280 285
Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Tyr Gly
290 295 300
Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly
305 310 315 320
Pro Gly Ser Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Pro Ser
325 330 335
Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Gln Val Leu Ile Gly
340 345 350
Pro Tyr Val Leu Ile Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala
355 360 365
Ala Gly Ser Tyr Gly Pro Gly Gln Gln Gly Pro Gly Gln Tyr Gly Pro
370 375 380
Gly Ser Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro Gly Ser Ser
385 390 395 400
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Gln Gln Val
405 410 415
Leu Ile Gly Pro Tyr Val Leu Ile Gly Pro Gly Pro Ser Ala Ala Ala
420 425 430
Ala Ala Ala Ala Gly Ser Tyr Gln Gln Gly Pro Gly Gln Gln Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Gln Gly Pro Tyr Gly Pro
450 455 460
Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Val
465 470 475 480
Leu Ile Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Ser Ala Ser Ala
485 490 495
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Tyr
500 505 510
Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Gln Gln Gly
515 520 525
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
530 535 540
Gly Ser Tyr Gly Pro Gly Gln Gln Val Leu Ile Gly Pro Tyr Val Leu
545 550 555 560
Ile Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
565 570 575
Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser
580 585 590
Gly Gln Tyr Gly Pro Gly Gln Gln Gly Pro Gly Pro Ser Ala Ala Ala
595 600 605
Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Gln Val Leu Ile Gly Pro
610 615 620
Gly Ala Ser Val Leu Ile
625 630
<210> 25
<211> 593
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT888
<400> 25
Met Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala
1 5 10 15
Ser Ala Ala Ala Ala Ala Gly Gln Asn Gly Pro Gly Ser Gly Val Leu
20 25 30
Gly Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly
35 40 45
Val Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln
50 55 60
Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala
65 70 75 80
Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly Gln Tyr Gly
85 90 95
Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala Ala
100 105 110
Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr
115 120 125
Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Gln
130 135 140
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly Pro Gly
145 150 155 160
Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Val
165 170 175
Leu Gly Pro Gly Gln Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala
180 185 190
Gly Gln Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
195 200 205
Gln Ser Gly Ser Gly Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala
210 215 220
Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro
225 230 235 240
Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Tyr Gly Pro Gly
245 250 255
Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly
260 265 270
Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Gln Ser Ala Ala
275 280 285
Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser
290 295 300
Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly
305 310 315 320
Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly
325 330 335
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Val
340 345 350
Leu Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln
355 360 365
Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser
370 375 380
Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
385 390 395 400
Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala
405 410 415
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Gln Tyr
420 425 430
Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro Gly Ser Gly Val Leu Gly
435 440 445
Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
450 455 460
Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Gln Ser Ala Ala
465 470 475 480
Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly
485 490 495
Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro
500 505 510
Gly Gln Ser Ala Ala Ala Ala Ala Gly Gln Tyr Val Leu Gly Pro Gly
515 520 525
Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
530 535 540
Gln Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Gln
545 550 555 560
Ser Gly Ser Gly Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala Ser
565 570 575
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala
580 585 590
Ser
<210> 26
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT965
<400> 26
Met Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Ala Asn Gly Pro Gly Ser Gly Thr Ser Gly Pro Gly
20 25 30
Ala Ser Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Gly Thr Ser Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Ala Tyr Gly Pro
50 55 60
Gly Thr Ser Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Thr Ser Gly Pro Gly Ala Ser Gly Ala Tyr Gly Pro Gly Thr
85 90 95
Ser Gly Pro Gly Thr Ser Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Ala Tyr Gly Ser Gly Pro Gly Thr Ser Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Ala Tyr Gly Ala Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Ala Tyr Gly Pro Gly Thr Ser Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Thr Ser Gly Pro
165 170 175
Gly Ala Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr
180 185 190
Gly Ser Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Gly
195 200 205
Ser Gly Thr Ser Gly Pro Gly Thr Ser Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Ala Tyr Gly Tyr Gly Pro Gly Thr Ser Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Ala Asn Gly Pro Gly Ser Gly Ala
260 265 270
Tyr Gly Pro Gly Thr Ser Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Gly Ala Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro
340 345 350
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr Thr Ser
355 360 365
Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Ala Tyr Gly Ser Gly Pro Gly Ala Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Ala Ser Gly Pro Gly Ser Gly Thr Ser Gly Ala Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Pro
450 455 460
Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Ala Tyr Gly Pro Gly Ala Ser Gly Ala Asn Gly
485 490 495
Pro Gly Ser Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Gly Ala Ser
500 505 510
Ala Ala Ala Ala Ala Gly Ala Tyr Thr Ser Gly Pro Gly Thr Ser Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly
530 535 540
Ser Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Gly Ser
545 550 555 560
Gly Thr Ser Gly Pro Gly Thr Ser Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Thr Ser Gly Pro Gly Ala Ser
580 585 590
<210> 27
<211> 593
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT889
<400> 27
Met Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala
1 5 10 15
Ser Ala Ala Ala Ala Ala Gly Ile Asn Gly Pro Gly Ser Gly Val Leu
20 25 30
Gly Pro Gly Ile Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly
35 40 45
Val Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile
50 55 60
Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala
65 70 75 80
Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly Ile Tyr Gly
85 90 95
Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala Ala
100 105 110
Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr
115 120 125
Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile Tyr Gly Ile
130 135 140
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Ile Tyr Gly Pro Gly
145 150 155 160
Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Val
165 170 175
Leu Gly Pro Gly Ile Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala
180 185 190
Gly Ile Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
195 200 205
Ile Ser Gly Ser Gly Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala
210 215 220
Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro
225 230 235 240
Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Tyr Gly Pro Gly
245 250 255
Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly
260 265 270
Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Ile Ser Ala Ala
275 280 285
Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser
290 295 300
Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly
305 310 315 320
Ile Tyr Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly
325 330 335
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val
340 345 350
Leu Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile
355 360 365
Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser
370 375 380
Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
385 390 395 400
Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala
405 410 415
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Ile Tyr
420 425 430
Gly Pro Tyr Gly Pro Gly Ile Ser Gly Pro Gly Ser Gly Val Leu Gly
435 440 445
Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile
450 455 460
Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala
465 470 475 480
Ala Ala Ala Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly
485 490 495
Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro
500 505 510
Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Leu Gly Pro Gly
515 520 525
Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
530 535 540
Ile Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ile
545 550 555 560
Ser Gly Ser Gly Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala Ser
565 570 575
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala
580 585 590
Ser
<210> 28
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT916
<400> 28
Met Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Leu Asn Gly Pro Gly Ser Gly Val Ile Gly Pro Gly
20 25 30
Leu Ser Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Gly Val Ile Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Leu Tyr Gly Pro
50 55 60
Gly Val Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Val Ile Gly Pro Gly Ala Ser Gly Leu Tyr Gly Pro Gly Val
85 90 95
Ile Gly Pro Gly Val Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Leu Tyr Gly Ser Gly Pro Gly Val Ile Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Leu Tyr Gly Leu Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Leu Tyr Gly Pro Gly Val Ile Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Val Ile Gly Pro
165 170 175
Gly Leu Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr
180 185 190
Gly Ser Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Leu Ser Gly
195 200 205
Ser Gly Val Ile Gly Pro Gly Val Ile Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Leu Tyr Gly Tyr Gly Pro Gly Val Ile Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Leu Asn Gly Pro Gly Ser Gly Leu
260 265 270
Tyr Gly Pro Gly Val Ile Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Gly Leu Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro
340 345 350
Tyr Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala Gly Leu Tyr Val Ile
355 360 365
Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Val Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Leu Tyr Gly Ser Gly Pro Gly Leu Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Leu Ser Gly Pro Gly Ser Gly Val Ile Gly Leu Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Pro
450 455 460
Gly Val Ile Gly Pro Tyr Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Leu Tyr Gly Pro Gly Ala Ser Gly Leu Asn Gly
485 490 495
Pro Gly Ser Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Gly Leu Ser
500 505 510
Ala Ala Ala Ala Ala Gly Leu Tyr Val Ile Gly Pro Gly Val Ile Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly
530 535 540
Ser Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Leu Ser Gly Ser
545 550 555 560
Gly Val Ile Gly Pro Gly Val Ile Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Val Ile Gly Pro Gly Ala Ser
580 585 590
<210> 29
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT918
<400> 29
Met Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Ile Asn Gly Pro Gly Ser Gly Val Phe Gly Pro Gly
20 25 30
Ile Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro
50 55 60
Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Val Phe Gly Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val
85 90 95
Phe Gly Pro Gly Val Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Ile Tyr Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Val Phe Gly Pro
165 170 175
Gly Ile Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
180 185 190
Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly
195 200 205
Ser Gly Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Ile Tyr Gly Tyr Gly Pro Gly Val Phe Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile
260 265 270
Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
340 345 350
Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe
355 360 365
Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Ile Ser Gly Pro Gly Ser Gly Val Phe Gly Ile Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro
450 455 460
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly
485 490 495
Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser
500 505 510
Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly
530 535 540
Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser
545 550 555 560
Gly Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ala Ser
580 585 590
<210> 30
<211> 565
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT699
<400> 30
Met Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Ala Ala Gly Ser Asn Gly Pro Gly Ser Gly Val Leu Gly
20 25 30
Pro Gly Gln Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Val
35 40 45
Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
50 55 60
Gln Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala
65 70 75 80
Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly
85 90 95
Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser
100 105 110
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly
115 120 125
Val Leu Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly
145 150 155 160
Pro Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala
165 170 175
Ala Ala Ala Ala Ala Gly Ser Gly Val Leu Gly Pro Gly Gln Tyr Gly
180 185 190
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser
195 200 205
Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly
210 215 220
Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala
225 230 235 240
Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser
245 250 255
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Val
260 265 270
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser
275 280 285
Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala
290 295 300
Ala Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala
305 310 315 320
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu
325 330 335
Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly
340 345 350
Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser
355 360 365
Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala
370 375 380
Ala Ala Ala Ala Ala Gly Ser Tyr Val Leu Gly Pro Gly Val Leu Gly
385 390 395 400
Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly
405 410 415
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr
420 425 430
Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
435 440 445
Ala Gly Ser Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro
450 455 460
Gly Gln Ser Gly Pro Gly Ser Gly Val Leu Gly Gln Gly Pro Tyr Gly
465 470 475 480
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro
485 490 495
Gly Val Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
500 505 510
Ala Ala Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln
515 520 525
Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly
530 535 540
Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu
545 550 555 560
Gly Pro Gly Ala Ser
565
<210> 31
<211> 565
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT698
<400> 31
Met Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Ala Ala Gly Ser Asn Gly Pro Gly Ser Gly Val Leu Gly
20 25 30
Pro Gly Ile Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Val
35 40 45
Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
50 55 60
Ile Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala
65 70 75 80
Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly
85 90 95
Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser
100 105 110
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly
115 120 125
Val Leu Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser Gly
145 150 155 160
Pro Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala
165 170 175
Ala Ala Ala Ala Ala Gly Ser Gly Val Leu Gly Pro Gly Ile Tyr Gly
180 185 190
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser
195 200 205
Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly
210 215 220
Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala
225 230 235 240
Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser
245 250 255
Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Val
260 265 270
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser
275 280 285
Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala
290 295 300
Ala Ala Ala Ala Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala
305 310 315 320
Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu
325 330 335
Gly Pro Gly Ile Tyr Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly
340 345 350
Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser
355 360 365
Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala
370 375 380
Ala Ala Ala Ala Ala Gly Ser Tyr Val Leu Gly Pro Gly Val Leu Gly
385 390 395 400
Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly
405 410 415
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr
420 425 430
Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala
435 440 445
Ala Gly Ser Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro
450 455 460
Gly Ile Ser Gly Pro Gly Ser Gly Val Leu Gly Ile Gly Pro Tyr Gly
465 470 475 480
Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro
485 490 495
Gly Val Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala
500 505 510
Ala Ala Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile
515 520 525
Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly
530 535 540
Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu
545 550 555 560
Gly Pro Gly Ala Ser
565
<210> 32
<211> 1179
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT966
<400> 32
Met Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Ile Asn Gly Pro Gly Ser Gly Val Phe Gly Pro Gly
20 25 30
Ile Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro
50 55 60
Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Val Phe Gly Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val
85 90 95
Phe Gly Pro Gly Val Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Ile Tyr Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Val Phe Gly Pro
165 170 175
Gly Ile Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
180 185 190
Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly
195 200 205
Ser Gly Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Ile Tyr Gly Tyr Gly Pro Gly Val Phe Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile
260 265 270
Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
340 345 350
Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe
355 360 365
Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Ile Ser Gly Pro Gly Ser Gly Val Phe Gly Ile Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro
450 455 460
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly
485 490 495
Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser
500 505 510
Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly
530 535 540
Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser
545 550 555 560
Gly Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ala Ser Gly Pro
580 585 590
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
595 600 605
Gly Ile Asn Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ile Ser Gly
610 615 620
Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly Pro Gly Ser
625 630 635 640
Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe
645 650 655
Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val
660 665 670
Phe Gly Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
675 680 685
Gly Val Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr
690 695 700
Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Ser Ala Ala Ala Ala
705 710 715 720
Ala Gly Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly
725 730 735
Ala Ser Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala
740 745 750
Ser Ala Ala Ala Ala Ala Gly Ser Gly Val Phe Gly Pro Gly Ile Tyr
755 760 765
Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly
770 775 780
Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val
785 790 795 800
Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala
805 810 815
Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala
820 825 830
Ala Ala Gly Ile Tyr Gly Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly
835 840 845
Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro
850 855 860
Gly Val Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly
865 870 875 880
Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
885 890 895
Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro Gly Ser
900 905 910
Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala
915 920 925
Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro
930 935 940
Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly
945 950 955 960
Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Phe Gly
965 970 975
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile
980 985 990
Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala
995 1000 1005
Gly Ile Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro
1010 1015 1020
Gly Ile Ser Gly Pro Gly Ser Gly Val Phe Gly Ile Gly Pro Tyr
1025 1030 1035
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro
1040 1045 1050
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala
1055 1060 1065
Ala Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile
1070 1075 1080
Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
1085 1090 1095
Gly Ile Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro
1100 1105 1110
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
1115 1120 1125
Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly
1130 1135 1140
Pro Gly Ile Ser Gly Ser Gly Val Phe Gly Pro Gly Val Phe Gly
1145 1150 1155
Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val
1160 1165 1170
Phe Gly Pro Gly Ala Ser
1175
<210> 33
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT888
<400> 33
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln
20 25 30
Asn Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Gln Ser Gly Gln Tyr
35 40 45
Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly
85 90 95
Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Val
100 105 110
Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser
115 120 125
Gly Pro Gly Val Leu Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Gln Tyr Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Val Leu Gly Pro Gly Gln Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly
195 200 205
Val Leu Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Val Leu Gly
210 215 220
Pro Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Gln Tyr Gly Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro Gly Val
275 280 285
Leu Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Leu
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr
305 310 315 320
Gly Pro Gly Val Leu Gly Pro Gly Gln Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Gln
355 360 365
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Val Leu Gly Pro Gly Val Leu
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly
405 410 415
Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Gln
420 425 430
Tyr Gly Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser
435 440 445
Gly Pro Gly Ser Gly Val Leu Gly Gln Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro
465 470 475 480
Tyr Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln
500 505 510
Tyr Gly Pro Gly Val Leu Gly Pro Gly Gln Ser Ala Ala Ala Ala Ala
515 520 525
Gly Gln Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Gln Tyr Gly Ser Gly Pro Gly Val
545 550 555 560
Leu Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Val Leu Gly Pro
565 570 575
Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Val Leu Gly Pro Gly Ala Ser
595 600
<210> 34
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT965
<400> 34
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Thr
1 5 10 15
Ser Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ala
20 25 30
Asn Gly Pro Gly Ser Gly Thr Ser Gly Pro Gly Ala Ser Gly Ala Tyr
35 40 45
Gly Pro Gly Thr Ser Gly Pro Gly Thr Ser Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Thr Ser Gly
85 90 95
Pro Gly Ala Ser Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Gly Thr
100 105 110
Ser Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Ser
115 120 125
Gly Pro Gly Thr Ser Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Ala Tyr Gly Ala Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Thr Ser Gly Pro Gly Ala Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Ser Gly Pro Gly
195 200 205
Thr Ser Gly Pro Tyr Gly Pro Gly Ala Ser Gly Ser Gly Thr Ser Gly
210 215 220
Pro Gly Thr Ser Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Ala Tyr Gly Tyr Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Ala Asn Gly Pro Gly Ser Gly Ala Tyr Gly Pro Gly Thr
275 280 285
Ser Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Thr Ser
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr
305 310 315 320
Gly Pro Gly Thr Ser Gly Pro Gly Ala Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly Ala
355 360 365
Ser Ala Ala Ala Ala Ala Gly Ala Tyr Thr Ser Gly Pro Gly Thr Ser
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Thr Ser Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ala Tyr Gly
405 410 415
Pro Gly Thr Ser Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ala
420 425 430
Tyr Gly Ser Gly Pro Gly Ala Tyr Gly Pro Tyr Gly Pro Gly Ala Ser
435 440 445
Gly Pro Gly Ser Gly Thr Ser Gly Ala Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Pro Gly Thr Ser Gly Pro
465 470 475 480
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Ala Tyr Gly Pro Gly Ala Ser Gly Ala Asn Gly Pro Gly Ser Gly Ala
500 505 510
Tyr Gly Pro Gly Thr Ser Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
515 520 525
Gly Ala Tyr Thr Ser Gly Pro Gly Thr Ser Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Ala Tyr Gly Ser Gly Pro Gly Thr
545 550 555 560
Ser Gly Pro Tyr Gly Pro Gly Ala Ser Gly Ser Gly Thr Ser Gly Pro
565 570 575
Gly Thr Ser Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Thr Ser Gly Pro Gly Ala Ser
595 600
<210> 35
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT889
<400> 35
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile
20 25 30
Asn Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ile Ser Gly Ile Tyr
35 40 45
Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly
85 90 95
Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Val
100 105 110
Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser
115 120 125
Gly Pro Gly Val Leu Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Val Leu Gly Pro Gly Ile Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly
195 200 205
Val Leu Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Leu Gly
210 215 220
Pro Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Ile Tyr Gly Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val
275 280 285
Leu Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Leu
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
305 310 315 320
Gly Pro Gly Val Leu Gly Pro Gly Ile Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ile
355 360 365
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Leu Gly Pro Gly Val Leu
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly
405 410 415
Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ile
420 425 430
Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro Gly Ile Ser
435 440 445
Gly Pro Gly Ser Gly Val Leu Gly Ile Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro
465 470 475 480
Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile
500 505 510
Tyr Gly Pro Gly Val Leu Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
515 520 525
Gly Ile Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val
545 550 555 560
Leu Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Leu Gly Pro
565 570 575
Gly Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Val Leu Gly Pro Gly Ala Ser
595 600
<210> 36
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT916
<400> 36
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Leu
20 25 30
Asn Gly Pro Gly Ser Gly Val Ile Gly Pro Gly Leu Ser Gly Leu Tyr
35 40 45
Gly Pro Gly Val Ile Gly Pro Gly Val Ile Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Ile Gly
85 90 95
Pro Gly Ala Ser Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Gly Val
100 105 110
Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Ser
115 120 125
Gly Pro Gly Val Ile Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Leu Tyr Gly Leu Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Val Ile Gly Pro Gly Leu Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Ser Gly Pro Gly
195 200 205
Val Ile Gly Pro Tyr Gly Pro Gly Leu Ser Gly Ser Gly Val Ile Gly
210 215 220
Pro Gly Val Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Val Ile Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Leu Tyr Gly Tyr Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Leu Asn Gly Pro Gly Ser Gly Leu Tyr Gly Pro Gly Val
275 280 285
Ile Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Ile
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr
305 310 315 320
Gly Pro Gly Val Ile Gly Pro Gly Leu Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly Leu
355 360 365
Ser Ala Ala Ala Ala Ala Gly Leu Tyr Val Ile Gly Pro Gly Val Ile
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Ile Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Leu Tyr Gly
405 410 415
Pro Gly Val Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Leu
420 425 430
Tyr Gly Ser Gly Pro Gly Leu Tyr Gly Pro Tyr Gly Pro Gly Leu Ser
435 440 445
Gly Pro Gly Ser Gly Val Ile Gly Leu Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Pro Gly Val Ile Gly Pro
465 470 475 480
Tyr Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Leu Tyr Gly Pro Gly Ala Ser Gly Leu Asn Gly Pro Gly Ser Gly Leu
500 505 510
Tyr Gly Pro Gly Val Ile Gly Pro Gly Leu Ser Ala Ala Ala Ala Ala
515 520 525
Gly Leu Tyr Val Ile Gly Pro Gly Val Ile Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Leu Tyr Gly Ser Gly Pro Gly Val
545 550 555 560
Ile Gly Pro Tyr Gly Pro Gly Leu Ser Gly Ser Gly Val Ile Gly Pro
565 570 575
Gly Val Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Val Ile Gly Pro Gly Ala Ser
595 600
<210> 37
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT918
<400> 37
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile
20 25 30
Asn Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ile Ser Gly Ile Tyr
35 40 45
Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Phe Gly
85 90 95
Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val
100 105 110
Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser
115 120 125
Gly Pro Gly Val Phe Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly
195 200 205
Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Phe Gly
210 215 220
Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Ile Tyr Gly Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val
275 280 285
Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Phe
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
305 310 315 320
Gly Pro Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile
355 360 365
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Phe Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly
405 410 415
Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ile
420 425 430
Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro Gly Ile Ser
435 440 445
Gly Pro Gly Ser Gly Val Phe Gly Ile Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
465 470 475 480
Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile
500 505 510
Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
515 520 525
Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val
545 550 555 560
Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Phe Gly Pro
565 570 575
Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Val Phe Gly Pro Gly Ala Ser
595 600
<210> 38
<211> 576
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT699
<400> 38
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
20 25 30
Gly Ser Asn Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Gln Ser Gly
35 40 45
Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser
50 55 60
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly
65 70 75 80
Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
85 90 95
Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly Gln Tyr Gly Pro Gly
100 105 110
Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala
115 120 125
Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr
130 135 140
Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Gln Tyr
145 150 155 160
Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Gln Tyr Gly
165 170 175
Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala
180 185 190
Gly Ser Gly Val Leu Gly Pro Gly Gln Tyr Gly Pro Tyr Ala Ser Ala
195 200 205
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Val Leu
210 215 220
Gly Pro Tyr Gly Pro Gly Gln Ser Gly Ser Gly Val Leu Gly Pro Gly
225 230 235 240
Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
245 250 255
Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
260 265 270
Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly
275 280 285
Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser Gly Gln Tyr Gly Pro
290 295 300
Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly
305 310 315 320
Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
325 330 335
Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu Gly Pro Gly Gln Tyr
340 345 350
Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
355 360 365
Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val
370 375 380
Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala
385 390 395 400
Gly Ser Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
405 410 415
Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala
420 425 430
Ala Ala Ala Ala Ala Ala Gly Pro Gly Gln Tyr Gly Pro Gly Val Leu
435 440 445
Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly
450 455 460
Ser Gly Pro Gly Gln Tyr Gly Pro Tyr Gly Pro Gly Gln Ser Gly Pro
465 470 475 480
Gly Ser Gly Val Leu Gly Gln Gly Pro Tyr Gly Pro Gly Ala Ser Ala
485 490 495
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu Gly Pro
500 505 510
Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
515 520 525
Ser Gly Gln Tyr Gly Pro Gly Ala Ser Gly Gln Asn Gly Pro Gly Ser
530 535 540
Gly Gln Tyr Gly Pro Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala
545 550 555 560
Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser
565 570 575
<210> 39
<211> 576
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT698
<400> 39
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Ala Ala
20 25 30
Gly Ser Asn Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ile Ser Gly
35 40 45
Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser
50 55 60
Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly
65 70 75 80
Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
85 90 95
Gly Ser Gly Val Leu Gly Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly
100 105 110
Val Leu Gly Pro Gly Val Leu Gly Pro Gly Ser Ser Ala Ala Ala Ala
115 120 125
Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Val Leu Gly Pro Tyr
130 135 140
Gly Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile Tyr
145 150 155 160
Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Ile Tyr Gly
165 170 175
Pro Gly Val Leu Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala
180 185 190
Gly Ser Gly Val Leu Gly Pro Gly Ile Tyr Gly Pro Tyr Ala Ser Ala
195 200 205
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Ser Gly Pro Gly Val Leu
210 215 220
Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Leu Gly Pro Gly
225 230 235 240
Val Leu Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro
245 250 255
Gly Val Leu Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
260 265 270
Ala Ala Gly Ser Tyr Gly Tyr Gly Pro Gly Val Leu Gly Pro Tyr Gly
275 280 285
Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro
290 295 300
Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly
305 310 315 320
Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala
325 330 335
Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu Gly Pro Gly Ile Tyr
340 345 350
Gly Pro Gly Ser Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
355 360 365
Ser Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val
370 375 380
Leu Gly Pro Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala
385 390 395 400
Gly Ser Tyr Val Leu Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly
405 410 415
Ala Ser Gly Pro Gly Val Leu Gly Pro Tyr Gly Pro Gly Ala Ser Ala
420 425 430
Ala Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Leu
435 440 445
Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly
450 455 460
Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro Gly Ile Ser Gly Pro
465 470 475 480
Gly Ser Gly Val Leu Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala
485 490 495
Ala Ala Ala Ala Ala Ala Gly Ser Tyr Gly Pro Gly Val Leu Gly Pro
500 505 510
Tyr Gly Pro Gly Pro Ser Ala Ala Ala Ala Ala Ala Ala Gly Pro Gly
515 520 525
Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser
530 535 540
Gly Ile Tyr Gly Pro Gly Val Leu Gly Pro Gly Pro Ser Ala Ala Ala
545 550 555 560
Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Leu Gly Pro Gly Ala Ser
565 570 575
<210> 40
<211> 1190
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT966
<400> 40
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Val
1 5 10 15
Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile
20 25 30
Asn Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ile Ser Gly Ile Tyr
35 40 45
Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Phe Gly
85 90 95
Pro Gly Ala Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val
100 105 110
Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser
115 120 125
Gly Pro Gly Val Phe Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly
195 200 205
Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Phe Gly
210 215 220
Pro Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Ile Tyr Gly Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val
275 280 285
Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Phe
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
305 310 315 320
Gly Pro Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile
355 360 365
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Val Phe Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly
405 410 415
Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ile
420 425 430
Tyr Gly Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro Gly Ile Ser
435 440 445
Gly Pro Gly Ser Gly Val Phe Gly Ile Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
465 470 475 480
Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly Ser Gly Ile
500 505 510
Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala
515 520 525
Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val
545 550 555 560
Phe Gly Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Phe Gly Pro
565 570 575
Gly Val Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Val Phe Gly Pro Gly Ala Ser Gly Pro Gly Val Phe Gly Pro
595 600 605
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Asn Gly Pro
610 615 620
Gly Ser Gly Val Phe Gly Pro Gly Ile Ser Gly Ile Tyr Gly Pro Gly
625 630 635 640
Val Phe Gly Pro Gly Val Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala
645 650 655
Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser
660 665 670
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Phe Gly Pro Gly Ala
675 680 685
Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Val Phe Gly Pro
690 695 700
Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly
705 710 715 720
Val Phe Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser
725 730 735
Gly Ile Tyr Gly Ile Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
740 745 750
Ile Tyr Gly Pro Gly Val Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala
755 760 765
Ala Gly Ser Gly Val Phe Gly Pro Gly Ile Tyr Gly Pro Tyr Ala Ser
770 775 780
Ala Ala Ala Ala Ala Gly Ile Tyr Gly Ser Gly Pro Gly Val Phe Gly
785 790 795 800
Pro Tyr Gly Pro Gly Ile Ser Gly Ser Gly Val Phe Gly Pro Gly Val
805 810 815
Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Phe
820 825 830
Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile Tyr
835 840 845
Gly Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ala Ser Gly
850 855 860
Ile Asn Gly Pro Gly Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro
865 870 875 880
Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Phe Gly Pro Tyr
885 890 895
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly
900 905 910
Val Phe Gly Pro Gly Ile Tyr Gly Pro Gly Ser Ser Gly Pro Gly Val
915 920 925
Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Ile
930 935 940
Tyr Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser Ala Ala
945 950 955 960
Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly Pro Tyr
965 970 975
Gly Pro Gly Ala Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly
980 985 990
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Tyr Gly Pro Gly Val
995 1000 1005
Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly
1010 1015 1020
Ser Gly Pro Gly Ile Tyr Gly Pro Tyr Gly Pro Gly Ile Ser Gly
1025 1030 1035
Pro Gly Ser Gly Val Phe Gly Ile Gly Pro Tyr Gly Pro Gly Ala
1040 1045 1050
Ser Ala Ala Ala Ala Ala Gly Ile Tyr Gly Pro Gly Val Phe Gly
1055 1060 1065
Pro Tyr Gly Pro Gly Ile Ser Ala Ala Ala Ala Ala Gly Pro Gly
1070 1075 1080
Ser Gly Ile Tyr Gly Pro Gly Ala Ser Gly Ile Asn Gly Pro Gly
1085 1090 1095
Ser Gly Ile Tyr Gly Pro Gly Val Phe Gly Pro Gly Ile Ser Ala
1100 1105 1110
Ala Ala Ala Ala Gly Ile Tyr Val Phe Gly Pro Gly Val Phe Gly
1115 1120 1125
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Ile Tyr
1130 1135 1140
Gly Ser Gly Pro Gly Val Phe Gly Pro Tyr Gly Pro Gly Ile Ser
1145 1150 1155
Gly Ser Gly Val Phe Gly Pro Gly Val Phe Gly Pro Tyr Ala Ser
1160 1165 1170
Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Phe Gly Pro Gly
1175 1180 1185
Ala Ser
1190
<210> 41
<211> 590
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT917
<400> 41
Met Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Val Asn Gly Pro Gly Ser Gly Leu Ile Gly Pro Gly
20 25 30
Val Ser Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Gly Leu Ile Gly
35 40 45
Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Tyr Gly Pro
50 55 60
Gly Leu Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
65 70 75 80
Ser Gly Leu Ile Gly Pro Gly Ala Ser Gly Val Tyr Gly Pro Gly Leu
85 90 95
Ile Gly Pro Gly Leu Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
100 105 110
Gly Val Tyr Gly Ser Gly Pro Gly Leu Ile Gly Pro Tyr Gly Ser Ala
115 120 125
Ala Ala Ala Ala Gly Pro Gly Ser Gly Val Tyr Gly Val Gly Pro Tyr
130 135 140
Gly Pro Gly Ala Ser Gly Pro Gly Val Tyr Gly Pro Gly Leu Ile Gly
145 150 155 160
Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Leu Ile Gly Pro
165 170 175
Gly Val Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr
180 185 190
Gly Ser Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Val Ser Gly
195 200 205
Ser Gly Leu Ile Gly Pro Gly Leu Ile Gly Pro Tyr Ala Ser Ala Ala
210 215 220
Ala Ala Ala Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ser Ser
225 230 235 240
Ala Ala Ala Ala Ala Gly Val Tyr Gly Tyr Gly Pro Gly Leu Ile Gly
245 250 255
Pro Tyr Gly Pro Gly Ala Ser Gly Val Asn Gly Pro Gly Ser Gly Val
260 265 270
Tyr Gly Pro Gly Leu Ile Gly Pro Gly Val Ser Ala Ala Ala Ala Ala
275 280 285
Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala
290 295 300
Ala Ala Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Gly Val Tyr Gly
305 310 315 320
Pro Gly Ser Ser Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ser
325 330 335
Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro
340 345 350
Tyr Gly Pro Gly Val Ser Ala Ala Ala Ala Ala Gly Val Tyr Leu Ile
355 360 365
Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly
370 375 380
Leu Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly
385 390 395 400
Pro Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Ser Ala Ser Ala Ala
405 410 415
Ala Ala Ala Gly Val Tyr Gly Ser Gly Pro Gly Val Tyr Gly Pro Tyr
420 425 430
Gly Pro Gly Val Ser Gly Pro Gly Ser Gly Leu Ile Gly Val Gly Pro
435 440 445
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Pro
450 455 460
Gly Leu Ile Gly Pro Tyr Gly Pro Gly Val Ser Ala Ala Ala Ala Ala
465 470 475 480
Gly Pro Gly Ser Gly Val Tyr Gly Pro Gly Ala Ser Gly Val Asn Gly
485 490 495
Pro Gly Ser Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Gly Val Ser
500 505 510
Ala Ala Ala Ala Ala Gly Val Tyr Leu Ile Gly Pro Gly Leu Ile Gly
515 520 525
Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly
530 535 540
Ser Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Val Ser Gly Ser
545 550 555 560
Gly Leu Ile Gly Pro Gly Leu Ile Gly Pro Tyr Ala Ser Ala Ala Ala
565 570 575
Ala Ala Gly Pro Gly Ser Gly Leu Ile Gly Pro Gly Ala Ser
580 585 590
<210> 42
<211> 587
<212> PRT
<213> Искусственная последовательность
<220>
<223> Met-PRT1028
<400> 42
Met Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala
1 5 10 15
Ala Ala Ala Gly Thr Gly Pro Gly Ser Gly Ile Phe Gly Pro Gly Thr
20 25 30
Ser Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Gly Ile Phe Gly Pro
35 40 45
Gly Ser Ser Ala Ala Ala Ala Ala Gly Pro Gly Thr Tyr Gly Pro Gly
50 55 60
Ile Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser
65 70 75 80
Gly Ile Phe Gly Pro Gly Ala Ser Gly Thr Tyr Gly Pro Gly Ile Phe
85 90 95
Gly Pro Gly Ile Phe Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
100 105 110
Thr Tyr Gly Ser Gly Pro Gly Ile Phe Gly Pro Tyr Gly Ser Ala Ala
115 120 125
Ala Ala Ala Gly Pro Gly Ser Gly Thr Tyr Gly Thr Gly Pro Tyr Gly
130 135 140
Pro Gly Ala Ser Gly Pro Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro
145 150 155 160
Ser Ala Ser Ala Ala Ala Ala Ala Gly Ser Gly Ile Phe Gly Pro Gly
165 170 175
Thr Tyr Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly
180 185 190
Ser Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Thr Ser Gly Ser
195 200 205
Gly Ile Phe Gly Pro Gly Ile Phe Gly Pro Tyr Ala Ser Ala Ala Ala
210 215 220
Ala Ala Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala
225 230 235 240
Ala Ala Ala Ala Gly Thr Tyr Gly Tyr Gly Pro Gly Ile Phe Gly Pro
245 250 255
Tyr Gly Pro Gly Ala Ser Gly Thr Gly Pro Gly Ser Gly Thr Tyr Gly
260 265 270
Pro Gly Ile Phe Gly Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Pro
275 280 285
Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala
290 295 300
Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Gly Thr Tyr Gly Pro Gly
305 310 315 320
Ser Ser Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala
325 330 335
Ala Ala Ala Ala Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Tyr Gly
340 345 350
Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Thr Tyr Ile Phe Gly Pro
355 360 365
Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Ile Phe
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
385 390 395 400
Thr Tyr Gly Pro Gly Ile Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala
405 410 415
Ala Gly Thr Tyr Gly Ser Gly Pro Gly Thr Tyr Gly Pro Tyr Gly Pro
420 425 430
Gly Thr Ser Gly Pro Gly Ser Gly Ile Phe Gly Thr Gly Pro Tyr Gly
435 440 445
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly Pro Gly Ile
450 455 460
Phe Gly Pro Tyr Gly Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Pro
465 470 475 480
Gly Ser Gly Thr Tyr Gly Pro Gly Ala Ser Gly Thr Gly Pro Gly Ser
485 490 495
Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Gly Thr Ser Ala Ala Ala
500 505 510
Ala Ala Gly Thr Tyr Ile Phe Gly Pro Gly Ile Phe Gly Pro Tyr Gly
515 520 525
Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly Ser Gly Pro
530 535 540
Gly Ile Phe Gly Pro Tyr Gly Pro Gly Thr Ser Gly Ser Gly Ile Phe
545 550 555 560
Gly Pro Gly Ile Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly
565 570 575
Pro Gly Ser Gly Ile Phe Gly Pro Gly Ala Ser
580 585
<210> 43
<211> 601
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT917
<400> 43
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Leu
1 5 10 15
Ile Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Val
20 25 30
Asn Gly Pro Gly Ser Gly Leu Ile Gly Pro Gly Val Ser Gly Val Tyr
35 40 45
Gly Pro Gly Leu Ile Gly Pro Gly Leu Ile Gly Pro Gly Ser Ser Ala
50 55 60
Ala Ala Ala Ala Gly Pro Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro
65 70 75 80
Ser Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Leu Ile Gly
85 90 95
Pro Gly Ala Ser Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Gly Leu
100 105 110
Ile Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Ser
115 120 125
Gly Pro Gly Leu Ile Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly
130 135 140
Pro Gly Ser Gly Val Tyr Gly Val Gly Pro Tyr Gly Pro Gly Ala Ser
145 150 155 160
Gly Pro Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Ser Ala Ser Ala
165 170 175
Ala Ala Ala Ala Gly Ser Gly Leu Ile Gly Pro Gly Val Tyr Gly Pro
180 185 190
Tyr Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Ser Gly Pro Gly
195 200 205
Leu Ile Gly Pro Tyr Gly Pro Gly Val Ser Gly Ser Gly Leu Ile Gly
210 215 220
Pro Gly Leu Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro
225 230 235 240
Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala
245 250 255
Gly Val Tyr Gly Tyr Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly
260 265 270
Ala Ser Gly Val Asn Gly Pro Gly Ser Gly Val Tyr Gly Pro Gly Leu
275 280 285
Ile Gly Pro Gly Val Ser Ala Ala Ala Ala Ala Gly Pro Gly Leu Ile
290 295 300
Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr
305 310 315 320
Gly Pro Gly Leu Ile Gly Pro Gly Val Tyr Gly Pro Gly Ser Ser Gly
325 330 335
Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala
340 345 350
Ala Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly Val
355 360 365
Ser Ala Ala Ala Ala Ala Gly Val Tyr Leu Ile Gly Pro Gly Leu Ile
370 375 380
Gly Pro Tyr Gly Pro Gly Ala Ser Gly Pro Gly Leu Ile Gly Pro Tyr
385 390 395 400
Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Val Tyr Gly
405 410 415
Pro Gly Leu Ile Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Val
420 425 430
Tyr Gly Ser Gly Pro Gly Val Tyr Gly Pro Tyr Gly Pro Gly Val Ser
435 440 445
Gly Pro Gly Ser Gly Leu Ile Gly Val Gly Pro Tyr Gly Pro Gly Ala
450 455 460
Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Pro Gly Leu Ile Gly Pro
465 470 475 480
Tyr Gly Pro Gly Val Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly
485 490 495
Val Tyr Gly Pro Gly Ala Ser Gly Val Asn Gly Pro Gly Ser Gly Val
500 505 510
Tyr Gly Pro Gly Leu Ile Gly Pro Gly Val Ser Ala Ala Ala Ala Ala
515 520 525
Gly Val Tyr Leu Ile Gly Pro Gly Leu Ile Gly Pro Tyr Gly Pro Gly
530 535 540
Ala Ser Ala Ala Ala Ala Ala Gly Val Tyr Gly Ser Gly Pro Gly Leu
545 550 555 560
Ile Gly Pro Tyr Gly Pro Gly Val Ser Gly Ser Gly Leu Ile Gly Pro
565 570 575
Gly Leu Ile Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
580 585 590
Ser Gly Leu Ile Gly Pro Gly Ala Ser
595 600
<210> 44
<211> 598
<212> PRT
<213> Искусственная последовательность
<220>
<223> PRT1028
<400> 44
Met His His His His His His Ser Ser Gly Ser Ser Gly Pro Gly Ile
1 5 10 15
Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Thr
20 25 30
Gly Pro Gly Ser Gly Ile Phe Gly Pro Gly Thr Ser Gly Thr Tyr Gly
35 40 45
Pro Gly Ile Phe Gly Pro Gly Ile Phe Gly Pro Gly Ser Ser Ala Ala
50 55 60
Ala Ala Ala Gly Pro Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Ser
65 70 75 80
Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile Phe Gly Pro
85 90 95
Gly Ala Ser Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Gly Ile Phe
100 105 110
Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly Ser Gly
115 120 125
Pro Gly Ile Phe Gly Pro Tyr Gly Ser Ala Ala Ala Ala Ala Gly Pro
130 135 140
Gly Ser Gly Thr Tyr Gly Thr Gly Pro Tyr Gly Pro Gly Ala Ser Gly
145 150 155 160
Pro Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Ser Ala Ser Ala Ala
165 170 175
Ala Ala Ala Gly Ser Gly Ile Phe Gly Pro Gly Thr Tyr Gly Pro Tyr
180 185 190
Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly Ser Gly Pro Gly Ile
195 200 205
Phe Gly Pro Tyr Gly Pro Gly Thr Ser Gly Ser Gly Ile Phe Gly Pro
210 215 220
Gly Ile Phe Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly
225 230 235 240
Ile Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
245 250 255
Thr Tyr Gly Tyr Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ala
260 265 270
Ser Gly Thr Gly Pro Gly Ser Gly Thr Tyr Gly Pro Gly Ile Phe Gly
275 280 285
Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Pro Gly Ile Phe Gly Pro
290 295 300
Tyr Gly Pro Gly Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly Pro
305 310 315 320
Gly Ile Phe Gly Pro Gly Thr Tyr Gly Pro Gly Ser Ser Gly Pro Gly
325 330 335
Ile Phe Gly Pro Tyr Gly Pro Gly Ser Ser Ala Ala Ala Ala Ala Gly
340 345 350
Thr Tyr Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Thr Ser Ala
355 360 365
Ala Ala Ala Ala Gly Thr Tyr Ile Phe Gly Pro Gly Ile Phe Gly Pro
370 375 380
Tyr Gly Pro Gly Ala Ser Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro
385 390 395 400
Gly Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Thr Tyr Gly Pro Gly
405 410 415
Ile Phe Gly Pro Ser Ala Ser Ala Ala Ala Ala Ala Gly Thr Tyr Gly
420 425 430
Ser Gly Pro Gly Thr Tyr Gly Pro Tyr Gly Pro Gly Thr Ser Gly Pro
435 440 445
Gly Ser Gly Ile Phe Gly Thr Gly Pro Tyr Gly Pro Gly Ala Ser Ala
450 455 460
Ala Ala Ala Ala Gly Thr Tyr Gly Pro Gly Ile Phe Gly Pro Tyr Gly
465 470 475 480
Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Thr Tyr
485 490 495
Gly Pro Gly Ala Ser Gly Thr Gly Pro Gly Ser Gly Thr Tyr Gly Pro
500 505 510
Gly Ile Phe Gly Pro Gly Thr Ser Ala Ala Ala Ala Ala Gly Thr Tyr
515 520 525
Ile Phe Gly Pro Gly Ile Phe Gly Pro Tyr Gly Pro Gly Ala Ser Ala
530 535 540
Ala Ala Ala Ala Gly Thr Tyr Gly Ser Gly Pro Gly Ile Phe Gly Pro
545 550 555 560
Tyr Gly Pro Gly Thr Ser Gly Ser Gly Ile Phe Gly Pro Gly Ile Phe
565 570 575
Gly Pro Tyr Ala Ser Ala Ala Ala Ala Ala Gly Pro Gly Ser Gly Ile
580 585 590
Phe Gly Pro Gly Ala Ser
595
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| В ВЫСОКОЙ СТЕПЕНИ СЖАТОЕ СИНТЕТИЧЕСКОЕ ФИБРОИНОВОЕ ВОЛОКНО, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ СЖАТИЯ СИНТЕТИЧЕСКОГО ФИБРОИНОВОГО ВОЛОКНА | 2018 |
|
RU2757909C2 |
| Выделенный модифицированный белок VPI капсида аденоассоциированного вируса 9 серотипа (AAV9), капсид и вектор на его основе | 2021 |
|
RU2825667C2 |
| МОДУЛЯЦИЯ АКТИВНОСТИ REP БЕЛКА ПРИ ПОЛУЧЕНИИ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (ЗКДНК) | 2020 |
|
RU2812850C2 |
| Выделенный модифицированный белок VP1 капсида аденоассоциированного вируса 5 серотипа (AAV5), капсид и вектор на его основе | 2019 |
|
RU2751592C2 |
| АДЕНОВИРУСЫ И СПОСОБЫ ПРИМЕНЕНИЯ АДЕНОВИРУСОВ | 2019 |
|
RU2782528C1 |
| Вакцина на основе AAV5 для индукции специфического иммунитета к вирусу SARS-CoV-2 и/или профилактики коронавирусной инфекции, вызванной SARS-CoV-2 | 2020 |
|
RU2760301C1 |
| REP белок в качестве белкового антигена для диагностических анализов | 2017 |
|
RU2769568C2 |
| Кодон-оптимизированная нуклеиновая кислота, которая кодирует белок фактора свёртывания крови IX, и ее применение | 2021 |
|
RU2831751C2 |
| АНТИ-CEACAM1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2754876C2 |
| АНТИТЕЛА ПРОТИВ СОБАЧЬЕГО CTLA-4 | 2020 |
|
RU2818586C2 |
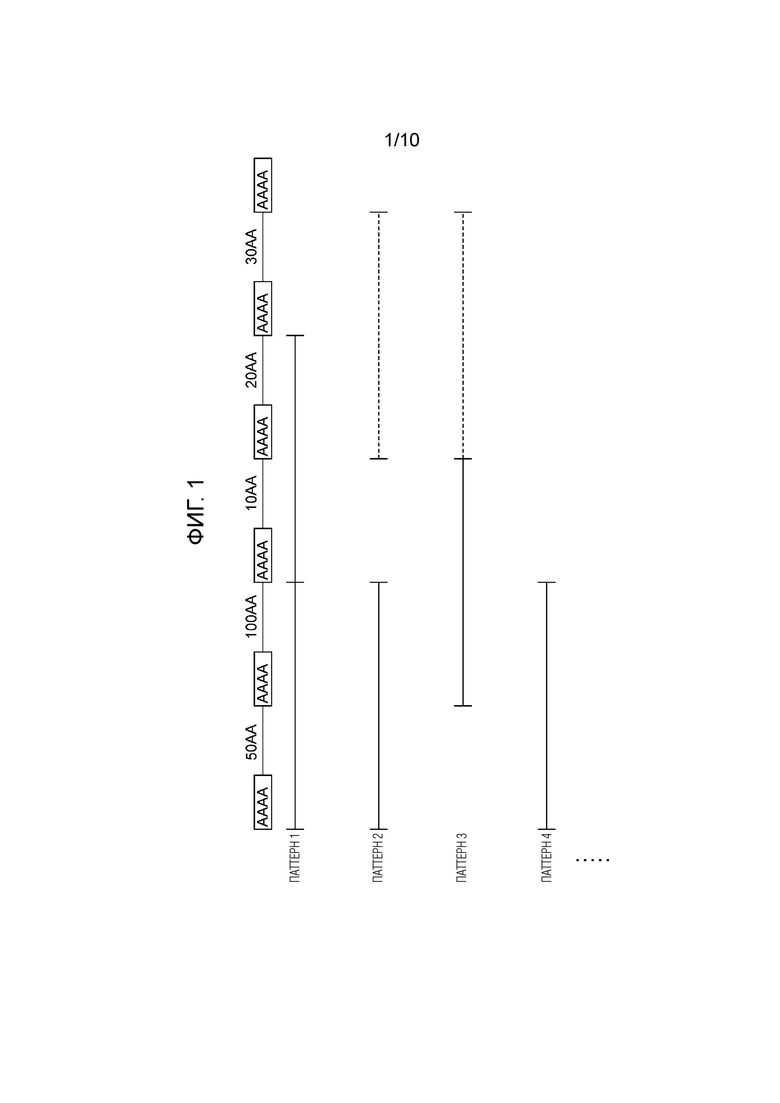
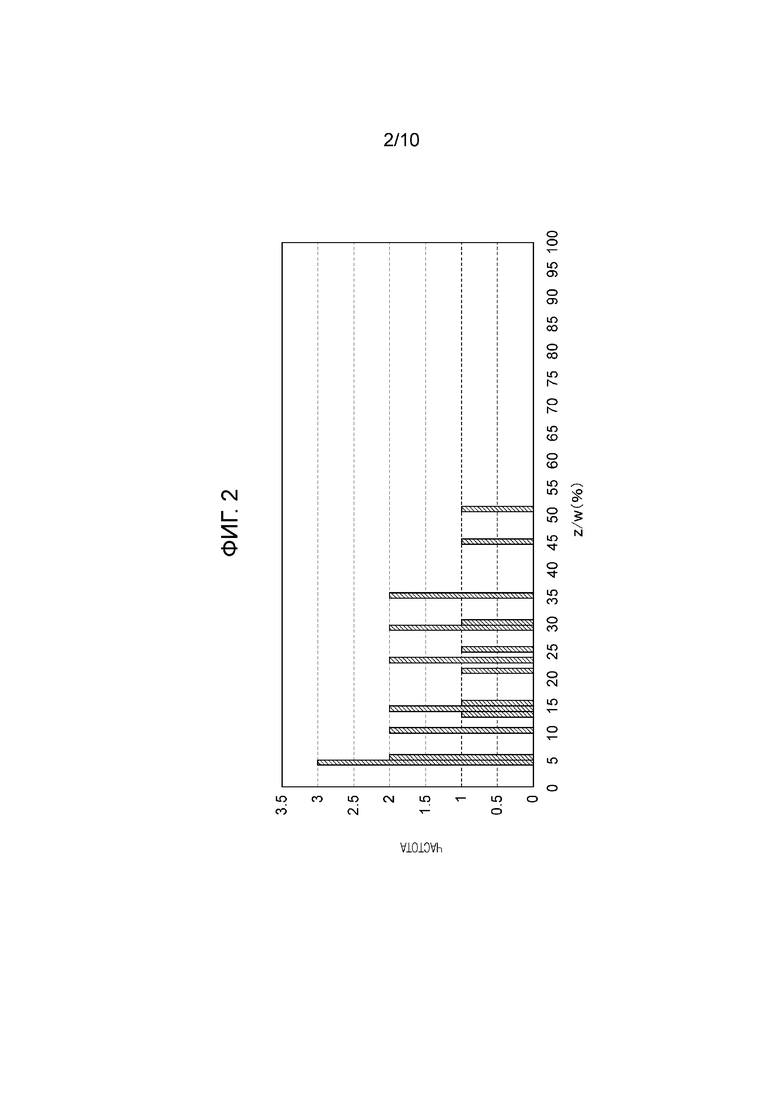
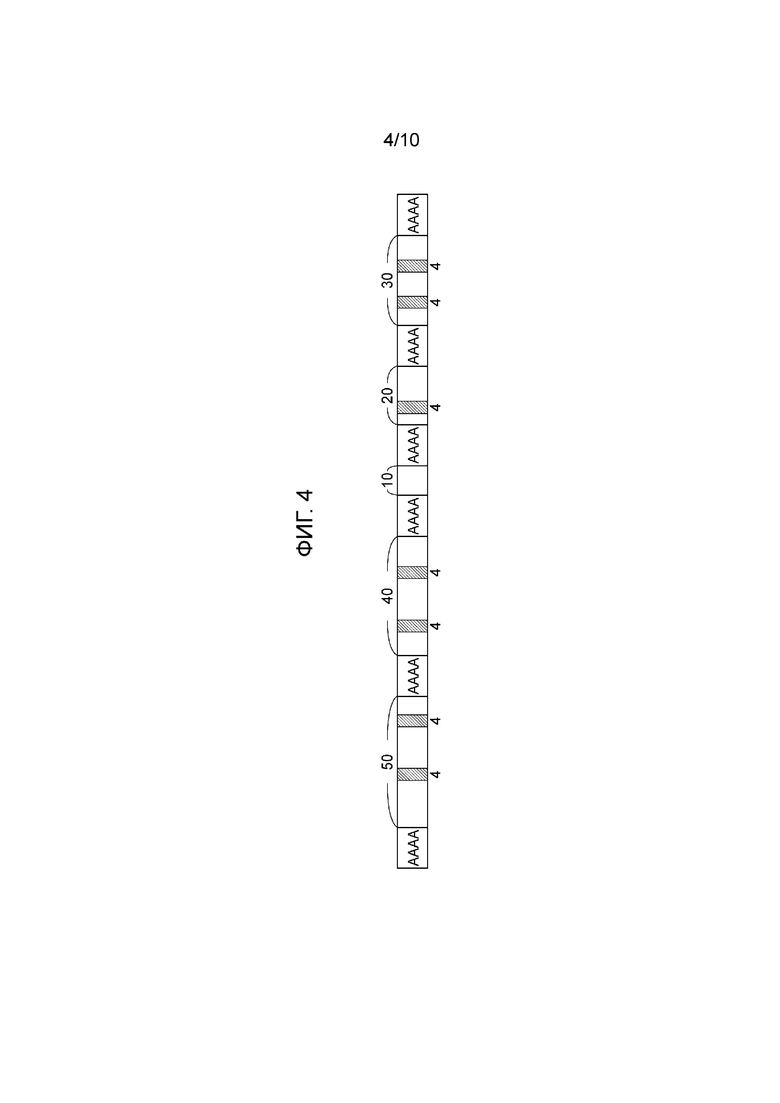
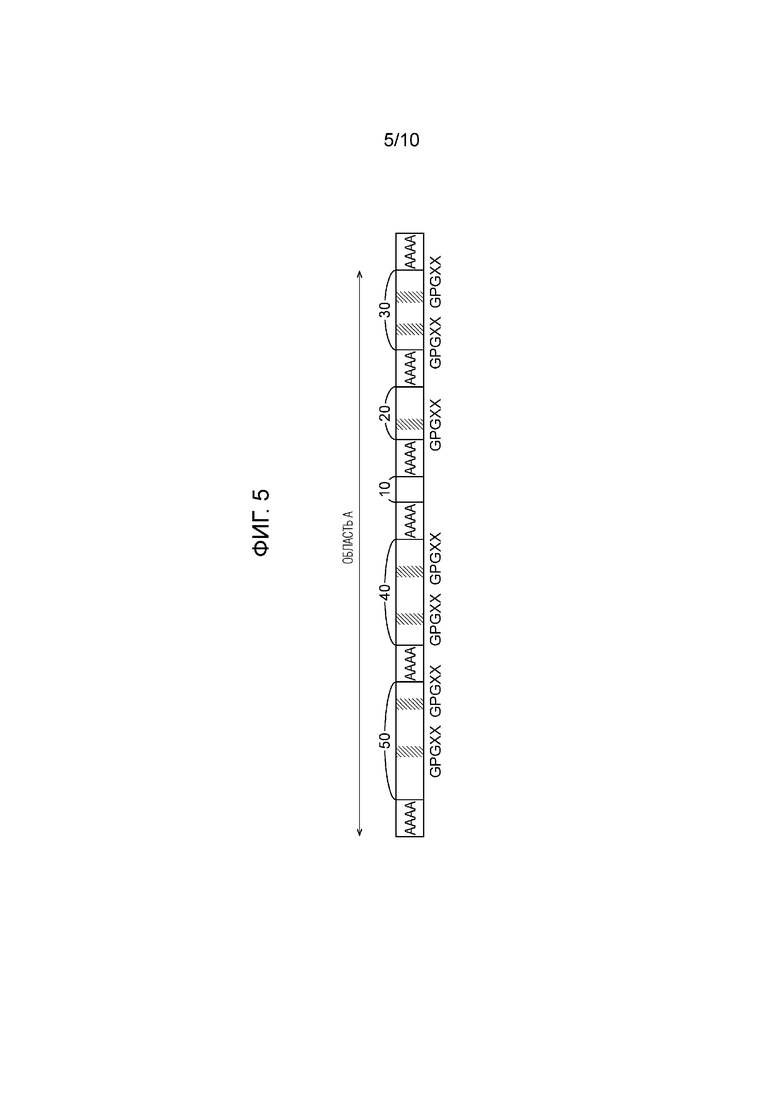
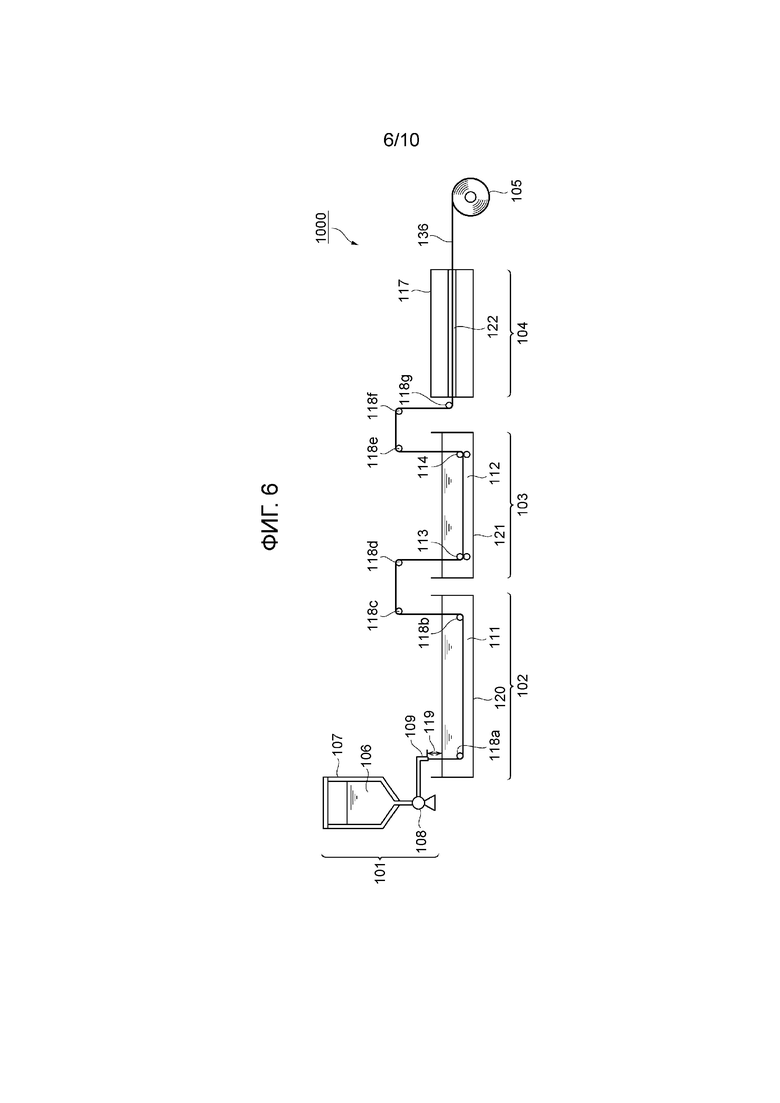
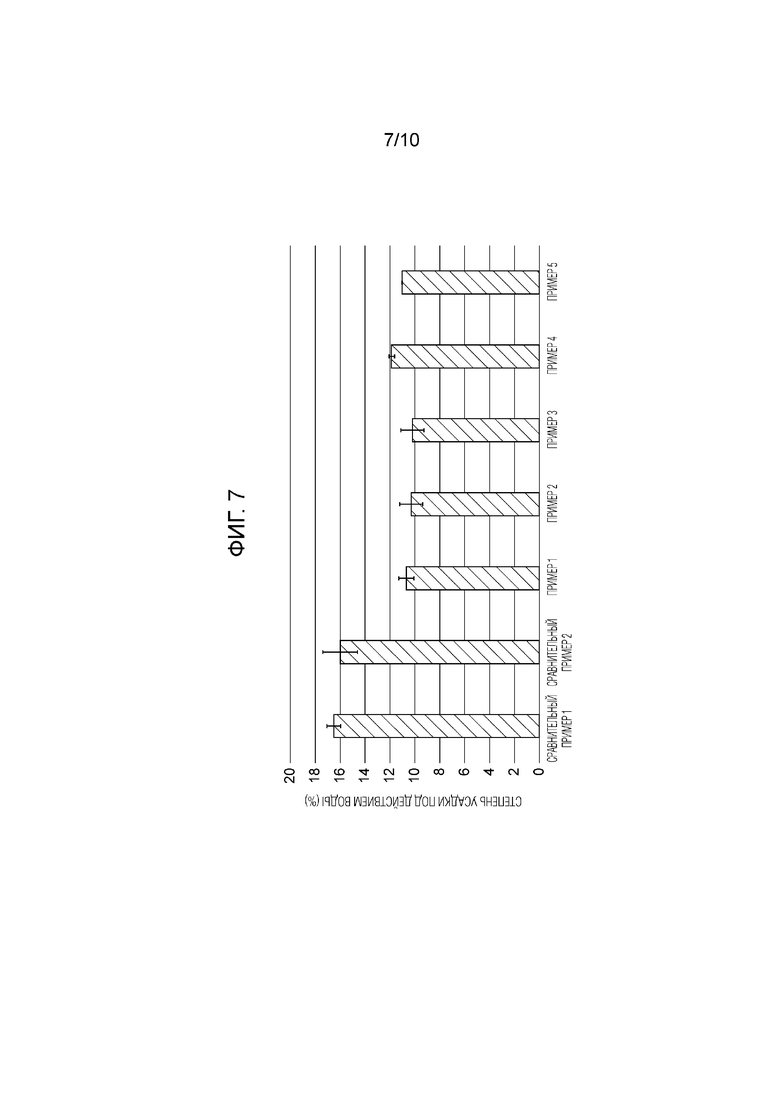
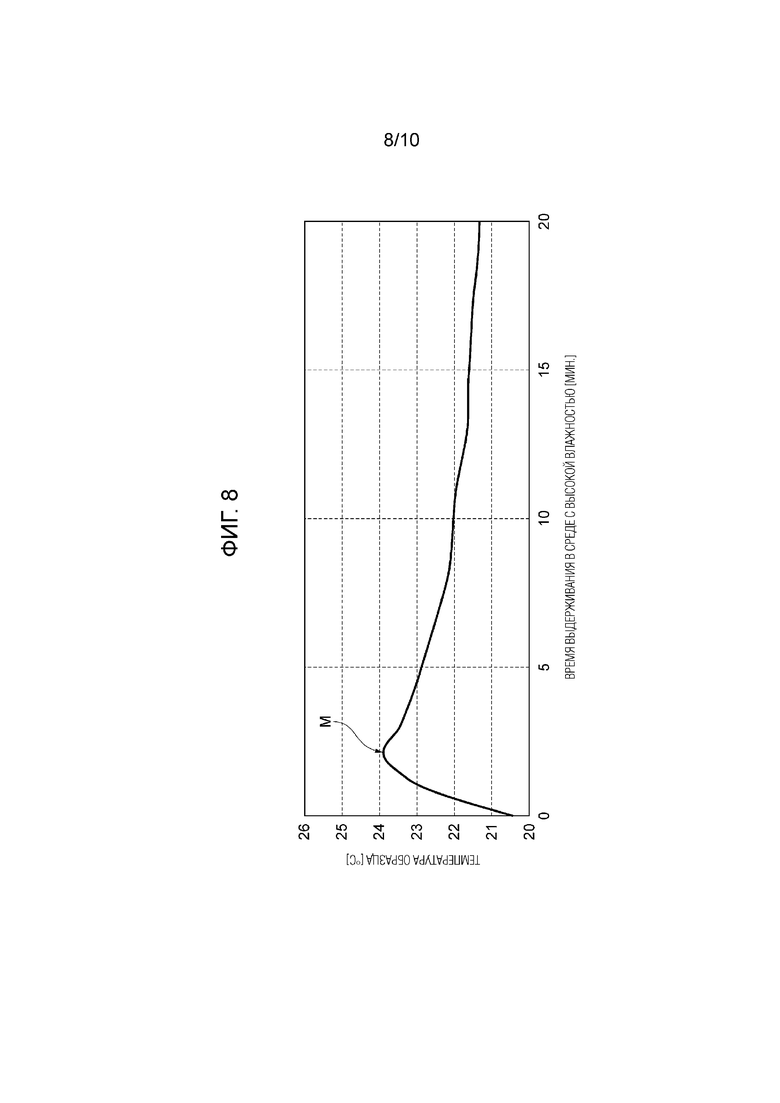

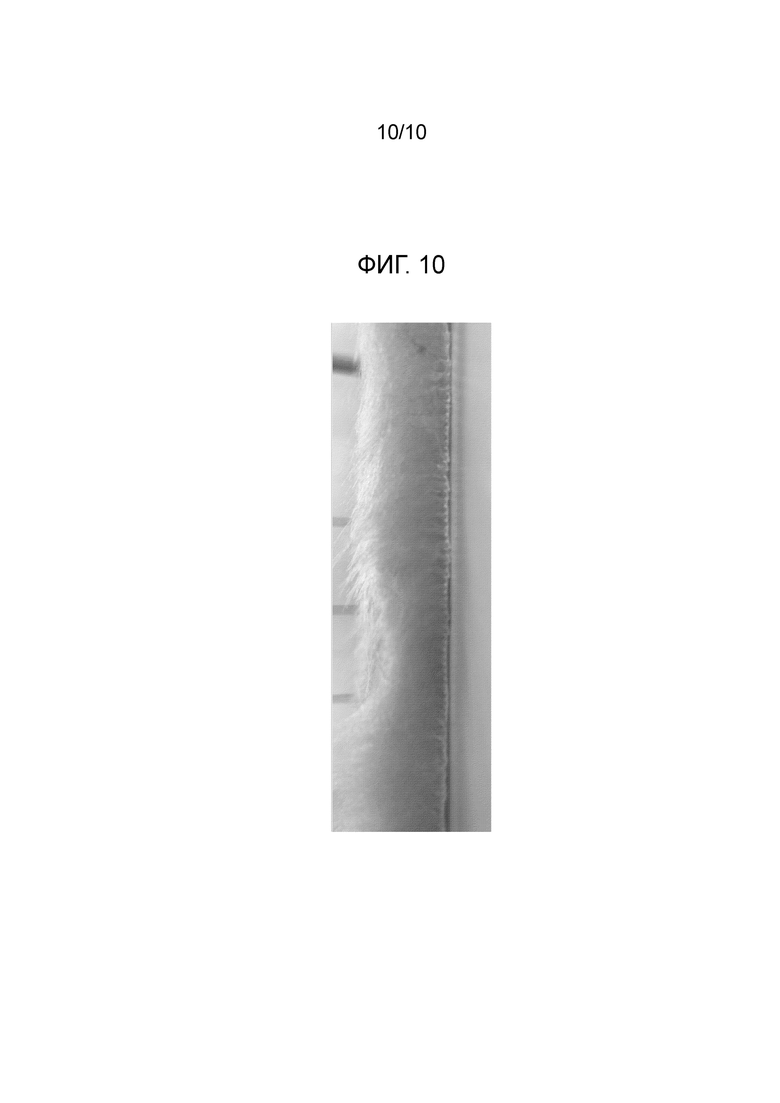
Заявлен искусственный мех, включающий искусственное белковое волокно. При этом искусственный мех обладает достаточными влагопоглощающими свойствами и на производство которого требуется меньше энергии. 2 н. и 11 з.п. ф-лы, 10 ил., 26 табл.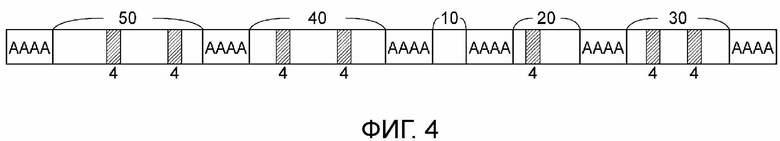
1. Искусственный мех, содержащий искусственное структурное белковое волокно, включающее модифицированное фиброиновое волокно.
2. Мех по п. 1, где модифицированное фиброиновое волокно включает модифицированное фибриновое волокно шелка паука.
3. Мех по п. 1 или 2, где белковое волокно во влажном состоянии имеет степень усадки 2% или более, определяемую как
(1 - длина белкового волокна во влажном состоянии после контакта с водой/длина белкового волокна после прядения, до контакта с водой)×100%.
4. Мех по п. 3, где белковое волокно в сухом состоянии имеет степень усадки более 7%, определяемую как
(1 - длина белкового волокна в сухом состоянии/длина белкового волокна после прядения, до контакта с водой)×100%.
5. Мех по любому из пп. 1-4, где мех содержит вещество, перекрестно связывающееся с белком,
где вещество, перекрестно связывающееся с белком, включает: множество полипептидных остовов; множество первых остатков или остатков первого реагента, имеющего по меньшей мере две первые реакционноспособные группы, способные образовывать связь посредством реакции с белком; и множество вторых остатков или остатков второго реагента, имеющего одну вторую реакционноспособную группу, способную образовывать связь посредством реакции с первой реакционноспособной группой,
по меньшей мере один из первых остатков перекрестно связывается с полипептидным остовом, и
по меньшей мере один из первых остатков связан с полипептидным остовом на одном конце и со вторым остатком на другом конце.
6. Мех по п. 5, содержащий модифицированный полимер, содержащий гидроксильную группу, где реакционноспособная функциональная группа связана с полимером, содержащим гидроксильную группу.
7. Мех по любому из пп. 1-6, содержащий вещество, придающее водостойкость.
8. Мех по п. 7, где модифицированный фиброин и вещество, придающее водостойкость, являются ковалентно связанными.
9. Мех по п. 7 или 8, где вещество, придающее водостойкость, представляет собой по меньшей мере одно вещество, выбранное из полимера на основе силикона и полимера на основе фтора.
10. Мех по любому из пп. 1-9, имеющий предельный кислородный индекс (LOI) 26,0 или более.
11. Мех по любому из пп. 1-10, имеющий максимальный уровень поглощения влаги и выделения тепла более 0,025°C/г, определенный как
(максимальная температура образца, полученная после переноса образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия, °C) - (температура образца при переносе образца в среду с высокой влажностью из среды с низкой влажностью до тех пор, пока температура образца не достигнет равновесия, °C)/массу образца, г,
где среда с низкой влажностью означает среду с температурой 20°C и относительной влажностью 40%, а среда с высокой влажностью означает среду с температурой 20°C и относительной влажностью 90%.
12. Мех по любому из пп. 1-11, имеющий коэффициент удерживания тепла более 0,18, определенный как
степень удерживания тепла, %/удельный вес образца, г/м2,
где степень удерживания тепла в % определяют по формуле (1 - a/b)×100,
где a означает количество тепла, рассеиваемого через тестируемый образец, а b означает количество тепла, рассеиваемого без тестируемого образца, причем данные параметры a и b измеряют методом сухого контакта при температуре 30°C, скорости ветра 30 см/сек.
13. Способ изготовления искусственного меха, включающий:
применение волокна, содержащего искусственное структурное белковое волокно, включающее модифицированное фиброиновое волокно, для получения ворсовой ткани, имеющей ворсинки, выступающие на одной или обеих поверхностях ткани; и
разрезание петли ворса с получением разрезного ворса.
| WO 2017159565 A1, 21.09.2017 | |||
| JP 63282379 A, 18.11.1988 | |||
| JPS 5865036 A, 18.04.1983 | |||
| Способ контроля эффективности магнитной обработки водного потока | 1989 |
|
SU1773875A1 |
| US 2019135880 A1, 09.05.2019 | |||
| WO 2018164020 A1, 13.09.2018. | |||
Авторы
Даты
2024-12-02—Публикация
2020-06-24—Подача