Изобретение относится к санитарии и медицине, в частности к дезинфицирующим средствам.
Новые молекулы обладают выраженным биоцидным эффектом в отношении болезнетворных бактерий, грибков, микобактерий туберкулеза и вирусов.
Необходимость дезинфекции существует во многих отраслях промышленности: в медицине, ветеринарии, сельском хозяйстве. Дезинфекция подразумевает уничтожение условно-патогенных и патогенных микроорганизмов.
Дезинфицирующие средства повсеместно используются в медицинской практике, в быту и многих других областях человеческой деятельности. Особенно важна роль мероприятий по дезинфекции в условиях эпидемий или при угрозе распространения опасных инфекций, в связи с чем обеспечение медицинских организаций и населения эффективными антисептическими средствами относится к задачам государственной важности.
Общими требованиями, предъявляемыми к таким средствам, являются эффективность подавления всех типов патогенной микрофлоры, включая возбудителей микробных, грибковых и вирусных инфекций, а также безопасность для человека и окружающей среды. Существующие препараты лишь частично удовлетворяют этим требованиям, и поэтому разработка новых антисептических средств остается актуальной.
Большинство дезинфицирующих средств нельзя использовать долго, а именно, более четырех месяцев, поскольку возникает привыкание. Практически все дезинфицирующие средства содержат поверхностно активные вещества (ПАВ), отдушки, четвертичные аминные соединения (ЧАС), относятся к 3 классу токсичности (опасности), не обладают длительным действием, требуют смывания водой.
Дезинфицирующие средства повсеместно используются в медицинской практике, в быту и многих других областях человеческой деятельности. Особенно важна роль мероприятий по дезинфекции в условиях эпидемий или при угрозе распространения опасных инфекций, в связи с чем обеспечение медицинских организаций и населения эффективными антисептическими средствами относится к задачам государственной важности. Общими требованиями, предъявляемыми к таким средствам, являются эффективность подавления всех типов патогенной микрофлоры, включая возбудителей микробных, грибковых и вирусных инфекций, а также безопасность для человека и окружающей среды. Существующие препараты лишь частично удовлетворяют этим требованиям, и поэтому разработка новых антисептических средств остается актуальной.
Одним из наиболее широко применяемых местных антисептиков в разных областях медицины является хлоргексидин. Его используют в клинической практике уже более 60 лет, однако некоторые новые данные требуют большей осторожности в применении хлоргексидина.
Хлоргексидин уже более полувека успешно применяется в качестве антисептика (для обработки операционного поля и рук хирурга, дезинфекции хирургического инструментария, при гнойно-септических процессах и т.д.). Он был открыт в 1950 году, и уже в 1954 году на рынке появился первый коммерческий продукт на его основе. В 1970-1980-е гг. применение хлоргексидина во многих странах стало рутинной практикой, при этом целый ряд клинических исследований показал его высокую антибактериальную активность. Позже хлоргексидин стали применять не только в виде дезинфицирующих растворов, но и для импрегнации центральных катетеров, имплантатов, одежды для пациентов, в качестве антибактериального компонента в лубрикантах, применяемых в урологической практике, и др. История применения хлоргексидина оставалась практически безоблачной достаточно долго, но полученные в последние годы данные вызывают определенные опасения относительно безопасности его использования.
Молекула хлоргексидина состоит из двух симметричных хлорфенилзамещенных бигуанидовых групп, соединённых гидрофобной гексаметиленовой цепочкой, при физиологическом значении рН существует в виде бикатиона. Механизм антимикробного действия хлоргексидина, как и у большинства катионных антисептиков, реализуется на уровне клеточной мембраны. Бикатион хлоргексидина прочно адсорбируется на микробной стенке, связывая анионные центры (сульфатные, фосфатные и карбоксильные группы) мембранообразующих протеинов, фосфолипидов и полисахаридов. Тем самым хлоргексидин устанавливает «мост» между парами соседних фосфолипидов, вытесняя при этом двухвалентные катионы, такие как Mg2+ и Ca2+. В низких концентрациях это вызывает обратимый бактериостатический эффект, а при более высоких концентрациях происходит кристаллизация клеточной мембраны, что приводит к нарушению её структуры, и в конечном итоге ведёт к гибели бактериальных клеток.
Долгое время считалось, что хлоргексидин не вызывает развития резистентности у микроорганизмов. Однако ряд исследователей указывают на то, что такой риск существует. Так, еще в 2002 году S.E. Brooks и соавт. обнаружили контаминацию поверхности диспенсеров мыла с 2% хлоргексидином панрезистентными штаммами Acinetobacter и Klebsiella, полирезистентными Pseudomonas и метициллин-резистентными Staphylococcus aureus (MRSA). И если рост выделенных с диспенсеров штаммов MRSA ингибировался in vitro хлоргексидином в концентрации до 0,0019%, то грамотрицательные изоляты продолжали размножаться в присутствии 1% хлоргексидина.
Группа ученых из Великобритании (L.J. Bock et al., 2016) оценили активность нескольких хлоргексидин-содержащих дезинфицирующих средств в отношении 14 клинических штаммов Klebsiella pneumoniae, выделенных до и после начала широкого применения этого антисептика в клинической практике («музейные» и «клинические»). Они установили, что не все препараты хлоргексидина убивают K. pneumoniae после рекомендованной экспозиции. Ожидаемо, что более устойчивыми оказались те штаммы, которые были выделены уже после начала рутинного применения данного антисептика. Активность препаратов зависела не только от концентрации хлоргексидина и времени экспозиции, но и от вспомогательных компонентов, которые могли повышать и в некоторых случаях даже снижать активность хлоргексидина. Также было установлено, что для шести штаммов после воздействия сублетальными концентрациями хлоргексидина минимальная подавляющая концентрация возросла в несколько раз, что подтвердило способность K. pneumoniae адаптироваться к этому антисептику.
Но еще большая опасность кроется в том, что хлоргексидин может вызывать у бактерий устойчивость к другим антибиотикам, в том числе у проблемных мультирезистентных патогенов из так называемой группы ESKAPE. Появление и быстрое распространение штаммов Enterobacteriacae, продуцирующих карбапенемазу, сделало практически незаменимым в лечении вызванных ими инфекций такой новый антибиотик, как колистин. В свою очередь, Matthew E. Wand с коллегами (Великобритания) показали способность хлоргексидина провоцировать формирование устойчивости Klebsiella pneumoniae к колистину.
Результаты этого исследования были опубликованы в октябре 2016 года в журнале Antimicrobial Agents and Chemotherapy, который выпускается Американским обществом микробиологии. Авторы еще раз подтвердили гипотезу о том, что K. pneumoniae может выжить при повышенной концентрации хлоргексидина, а также проверили предположение о том, что такое воздействие может вызывать резистентность к другим антибиотикам. И действительно, у пяти из шести штаммов, развивших устойчивость к хлоргексидину, также была обнаружена резистентность к колистину. Исследователи идентифицировали генные мутации, которые обеспечивали микроорганизмам устойчивость к обоим соединениям (рис. 1). Однако интересно, что адаптация K. pneumoniae к колистину не приводила к увеличению устойчивости к хлоргексидину, несмотря на наличие соответствующих мутаций. Введение плазмиды, содержащей мутировавший ген из штаммов, адаптированных к хлоргексидину, в штамм K. pneumoniae дикого типа приводило к повышению устойчивости к колистину, но не к хлоргексидину. По мнению исследователей, такой механизм устойчивости к хлоргексидину и колистину может приобретать не только K. pneumoniae, но и другие грамотрицательные патогены. В целом авторы этой работы считают, что потенциальный риск развития резистентности к колистину в результате воздействия хлоргексидина имеет важные клинические последствия и что полученные ими данные являются первым сигналом о необходимости пересмотра современных схем профилактики инфекционных осложнений.
В своей публикации в The Journal of Hospital Infection (ноябрь 2016 года) G. Kampf отмечает, что устойчивость к хлоргексидину редко демонстрируют такие микроорганизмы, как Escherichia coli, Salmonella spp., S. aureus и коагулазонегативные стафилококки. В то же время достаточно часто обнаруживают устойчивые к хлоргексидину штаммы Enterobacter spp., Pseudomonas spp., Proteus spp., Providencia spp., Enterococcus spp. По мнению автора, устойчивость к хлоргексидину является причиной многочисленных вспышек госпитальных инфекций и может ассоциироваться с развитием резистентности к другим антибиотикам. G. Kampf считает, что с целью минимизации риска селекции устойчивых штаммов нозокомиальных патогенов необходимо определить более четкие показания для профилактического применения хлоргексидина и ограничить его чрезмерно широкое применение.
При этом следует помнить о том, что хлоргексидин является веществом с высоким аллергенным потенциалом. По данным C. Abdallah (2015), частота гиперчувствительности к хлоргексидину при проведении аллергологических тестов составляет примерно 2%, а у лиц с атопическим дерматитом может достигать 5%. Основная ответственность за развитие аллергических реакций на хлоргексидин возлагается сегодня на гексаметиленовую группу в его молекуле (G.F. Calogiuri et al., 2013).
В последние годы отмечено существенное увеличение частоты серьезных аллергических реакций (тяжелой крапивницы, отека Квинке, анафилактического шока) при использовании хлоргексидина, о чем в феврале 2017 года сообщило Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA). Так, в период с января 1969 по июнь 2015 года в FDA поступило 43 сообщения о случаях анафилаксии при применении хлоргексидина, при этом более половины из них были зарегистрированы после 2010 года. В двух случаях тяжелая аллергическая реакция на хлоргексидин закончилась летальным исходом. Эксперты FDA предполагают, что, вероятно, были и другие случаи, о которых им неизвестно.
С учетом вышеизложенных данных FDA рекомендует производителям безрецептурных продуктов, в состав которых входит этот антисептик, добавить в инструкцию и на упаковку предупреждение о возможности развития серьезных аллергических реакций. Рецептурные препараты и средства с хлоргексидином, продающиеся в США, уже содержат соответствующие предупредительные надписи. Также FDA рекомендует специалистам здравоохранения перед назначением или использованием продуктов, содержащих хлоргексидин, тщательно собрать аллергологический анамнез. При подозрении или наличии аллергической реакции на хлоргексидин в анамнезе следует использовать альтернативные антисептики. Необходимо инструктировать пациентов о немедленном прекращении использования хлоргексидина и обращении к врачу при появлении аллергической реакции.
Особую проблему представляет аллергия на хлоргексидин в периоперационном периоде, поскольку анестезия и само вмешательство повышают риск развития и тяжесть анафилактических реакций. По данным E. Moka и соавт. (2015), примерно треть всех случаев анафилаксии, связанных с хлоргексидином, приходится именно на периоперационный период. Ситуация в данном случае существенно усугубляется тем, что пациент находится под простыней и, как правило, в бессознательном или седированном состоянии, что не дает возможности распознать ранние признаки анафилаксии и оказать своевременную помощь.
Важно подчеркнуть, что тщательно собранный анамнез перед операцией и выбор альтернативного антисептика во многих случаях позволил бы избежать развития тяжелой анафилаксии. Так, L.H. Garvey и соавт. представили описание четырех случаев развития тяжелых аллергических реакций на хлоргексидин во время проведения хирургических вмешательств, при которых понадобилось введение адреналина. Аллергия на антисептик подтвердилась кожным тестом. Последующий опрос пациентов показал, что у каждого из них уже отмечались незначительные симптомы аллергии, такие как сыпь, при проводившихся ранее процедурах или операциях. В другом докладе, в котором представлены шесть случаев анафилактических реакций на хлоргексидин во время операции (A. Nakonechna et al., 2014), у пяти из шести пациентов при детальном опросе можно было бы заранее заподозрить аллергическую предрасположенность. Следует отметить, что аллергическую реакцию в периоперационном периоде многие врачи склонны относить на счет анестезии, забывая о том, что ее причиной могут быть и другие средства, в том числе хлоргексидин. Так, ретроспективный анализ историй болезней пациентов с подозрением на аллергическую реакцию, связанную с общей анестезией, показал, что причинными факторами IgE-опосредованных реакций в 61,8% случаев были миорелаксанты, в 14,5% - антибиотики, в 9,2% - латекс, в 5,2% - хлоргексидин (J. Antunes et al., 2014). По данным M. S. Opstrup и соавт., хлоргексидин был причиной 9,6% случаев периоперационных аллергических реакций. Но поскольку врачи редко подозревают хлоргексидин в качестве причины анафилаксии, у одного пациента может произойти несколько эпизодов, прежде чем аллерген будет идентифицирован. Исходя из этого, аллергологическое тестирование пациентов с периоперационными анафилактическими реакциями является обязательным и должно включать не только анестетики и миорелаксанты, но также латекс и хлоргексидин. V. Nagendran и соавт. (2009) сообщают о четырех случаях аллергии на хлоргексидин у медицинских работников, что также заслуживает определенного внимания.
Таким образом, сразу два фактора - возможность индукции резистентности к антибиотикам резерва и высокий риск серьезных аллергических реакций - требуют от клиницистов более осторожного отношения к такому широко используемому местному антисептику, как хлоргексидин, большего внимания заслуживают альтернативные дезинфицирующие средства.
Задачей настоящего изобретения является разработка эффективного антисептического и дезинфицирующего средства пролонгированного действия.
Техническим результатом настоящего изобретения является высокая эффективность дезинфицирующего и антисептического средства при наличии выраженного бактерицидного, туберкулоцидного, фунгицидного, вирулицидного и противогельминтного действия, а также его безопасность.
Изобретение представляет собой антисептическое и дезинфицирующее средство, содержащее в качестве действующего вещества одно из следующих соединений:
А)
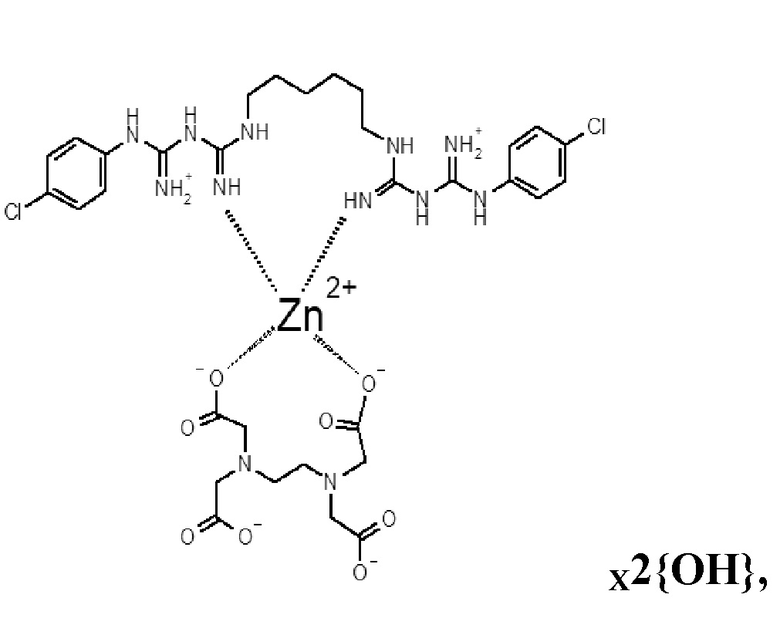
Б)
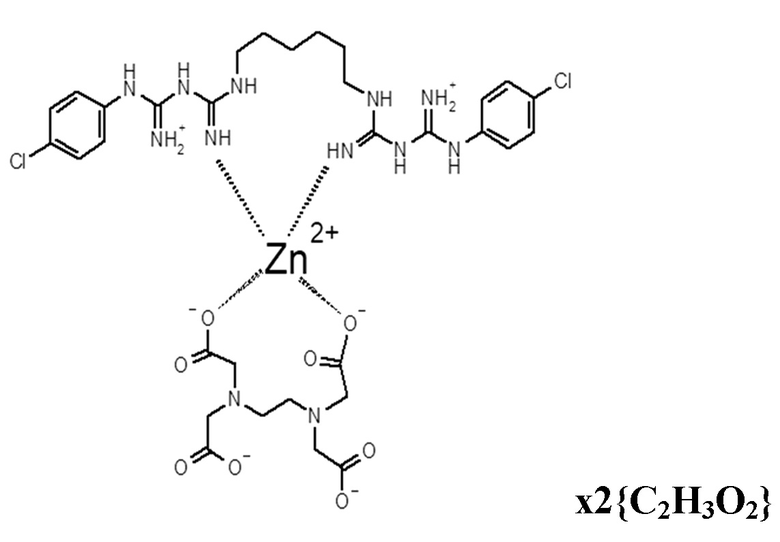
В)
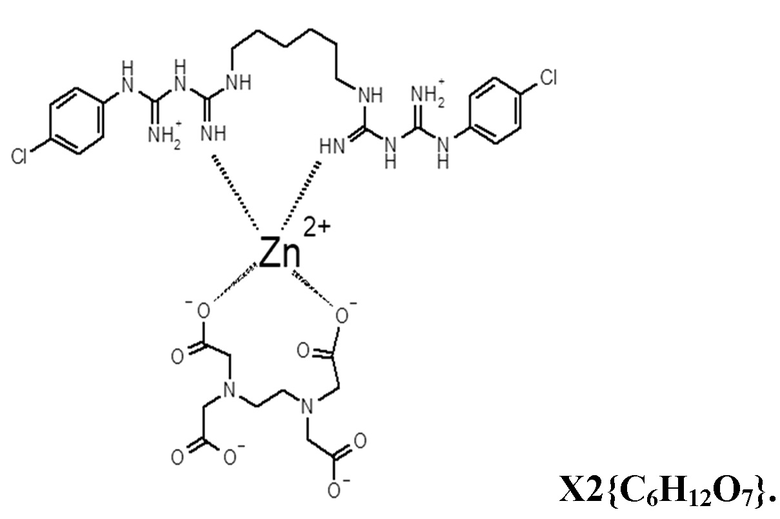
Изобретение касается также применения такого средства в качестве безопасного средства, обладающего бактерицидным, туберкулоцидным, фунгицидным, вирулицидным и противогельминтным действием.
Рис. 1. Мутации, обеспечивающие устойчивость Klebsiella pneumoniae к хлоргексидину, ассоциируется с мутациями, приводящими к резистентности этого микроорганизма к колистину.
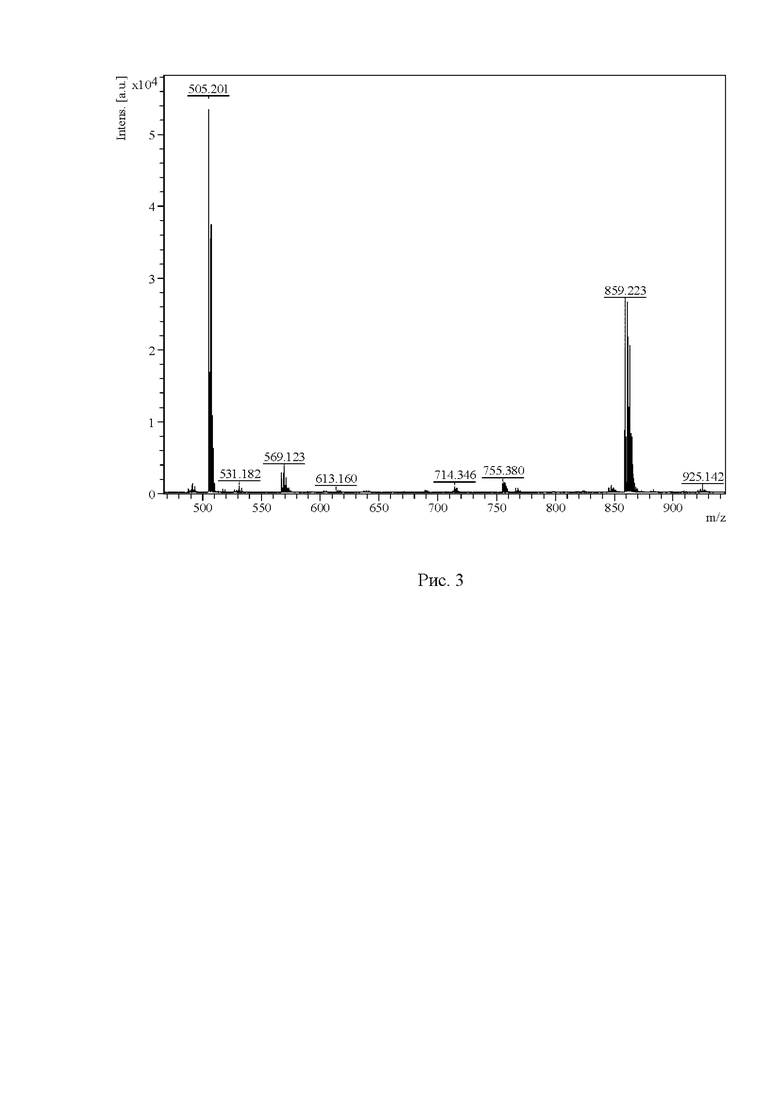
Рис. 2 Спектр МАЛДИ-МС ТРИГЕКСИЛОН-основание m/z 500-900.
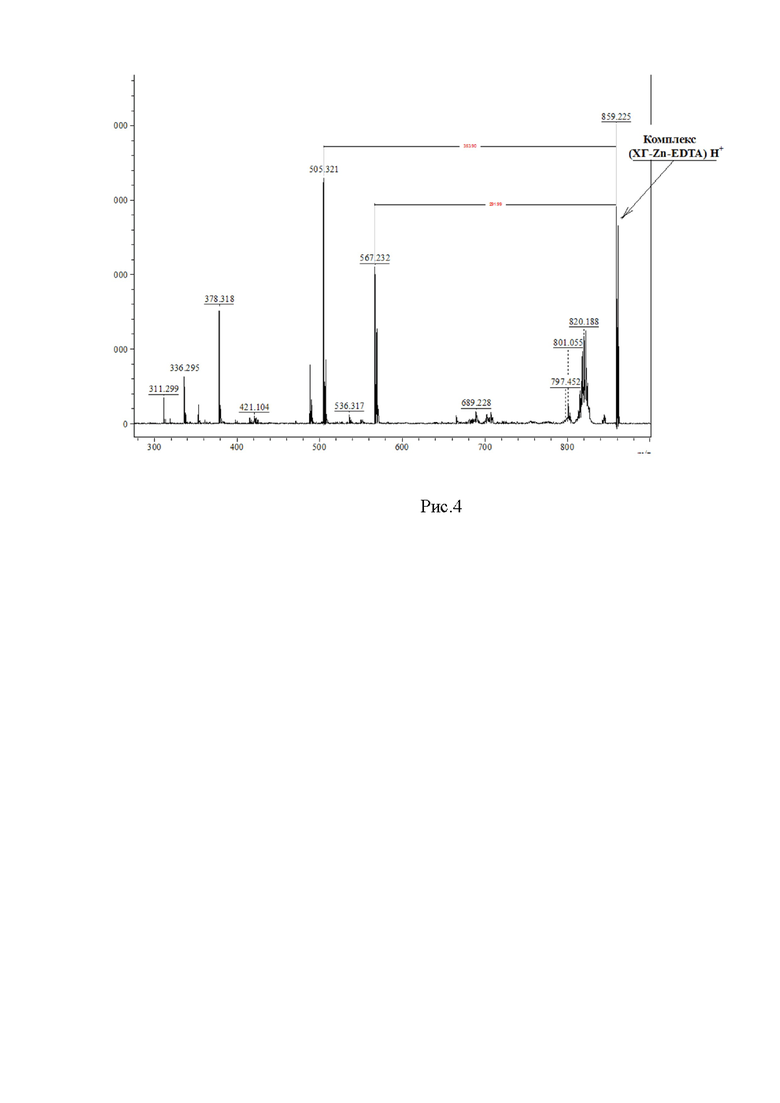
Рис. 3 Спектр МАЛДИ-МС ТРИГЕКСИЛОН-биацетат m/z 500-900.
Рис. 4 Спектр МАЛДИ-МС ТРИГЕКСИЛОН-биглюконат.
Изобретение осуществляется следующим образом.
Нами получен ряд производных средства ТРИГЕКСИЛОН (1,6-ди-[бис-(4-хлорфенилбигуанидо]гексана-цинка тилендиаминтетраацетат), отличающиеся тем, что молекула содержит разные формы хлоргексидина, представленные в образцах 1-6. Соединения, приведенные в образцах 1-6 являются новыми - хелатными производными хлоргексидин-ЭДТА-цинкового комплекса, что подтверждено спектральными анализами.
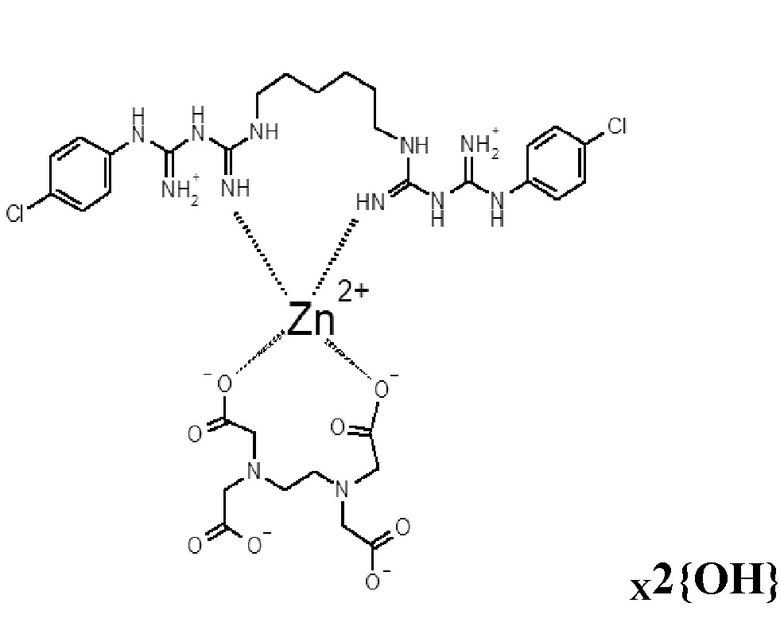
Структурная формула хлоргексидин-ЭДТА-цинкового комплекса антисептика «ТРИГЕКСИЛОН» выглядит следующим образом:
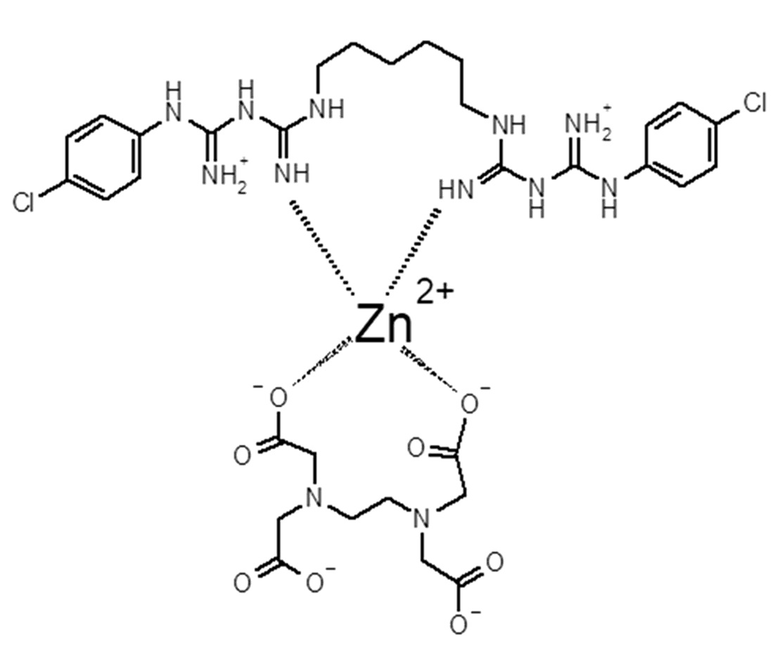
Образцы №1 и №2 содержат одинаковые компоненты, но в разной концентрации. Так как вносится хлоргексидин основание, то синтезируется ТРИГЕКСИЛОН-основание.
Образец №1. В мерной колбе вместимостью 100 мл растворяют трилон В 0,3 г , ZnCI2 0,12 г и хлоргексидин основание 0,2 г и перемешивают, после чего доводят объем до метки водой.
Образец №2. В мерной колбе вместимостью 100 мл растворяют трилон В 0,6 г , ZnCI2 0,24 г и хлоргексидин основание 0,4 г и перемешивают, после чего доводят объем до метки.
Таким образом получается ТРИГЕКСИЛОН-основание.
Спектр МАЛДИ-МС ТРИГЕКСИЛОН-основания m/z 500-900.
Масс-спектрометрическое исследование. Анализ осуществляли методом матрично-активированной лазерной десорбции/ионизации - масс-спектрометрии (МАЛДИ-МС). Исследуемое средство разбавляли водой в 100 раз. На ячейку МАЛДИ мишени наносили 0,5 мкл полученного раствора, добавляли 0,5 мкл раствора матрицы 5 мг/мл и высушивали. В качестве матрицы использовали α-циано-4-гидроксикоричную кислоту, которую растворяли в 70% ацетонитриле с добавкой 0,1% трифторуксусной кислоты (ТФУ). После высушивания МАЛДИ мишени анализировали с помощью масс-спектрометра UltrafleXtreme.
Масс-спектры были получены в режиме рефлектрон при регистрации положительных ионов с помощью тандемного времяпролетного масс-спектрометра UltrafleXtreme (Bruker Daltonics) на базе Научного парка СПбГУ.
Элементный состав комплекса хлоргексидин-ЭДТА-Zn устанавливали стандартным методом (CHN анализ), а количественное содержание цинка определяли методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой с использованием спектрометра Optima 2100DV (Perkin Elmer). Для выделения индивидуального комплекса из раствора, средство концентрировали упариванием в вакууме до 1/10 от исходного объема, выделившийся кристаллический продукт отделяли, промывали водой и сушили на воздухе при 40°С до постоянного веса. Полученный комплекс представляет собой бесцветный мелкокристаллический порошок ограниченно растворимый в воде.
В структуре данного комплекса содержится центральный четырехкоординированный двухзарядный катион цинка, двухзарядный катион хлоргексидиния и четырехзарядный анион полностью депротонированной молекулы ЭДТА. Судя по относительной интенсивности массового иона m/z МН+ 859.22 в масс-спектрах МАЛДИ, а также по характеру фрагментации этого иона, получаемый комплекс отличается высокой стабильностью, сопоставимой с устойчивостью бинарного комплекса ЭДТА-Zn. Стабильность бихелатного хлоргексидин-ЭДТА-Zn комплекса можно объяснить внутримолекулярным хелатообразованием, в результате чего катионные и анионные фрагменты в данной системе стехиометрически уравновешивают друг друга, образуя в сумме электронейтральную молекулу. Спектр МАЛДИ-МС ТРИГЕКСИЛОН основания m/z 500-900, подтверждает, что он содержится во всех приведенных ниже образцах № 1-2.
Данные масс-спектров (рис. 2) доказывают включение хлоргексидина в состав прочного тройного комплекса с участием ЭДТА и цинка, что позволяет объяснить повышенную биоцидную активность антисептика «ТРИГЕКСИЛОН». Молекула «ТРИГЕКСИЛОН» обладает бактерицидным, туберкулоцидным, фунгицидным и вирулицидным действием. В высокой концентрации присутствует бихелатный тройной комплекс Хлоргексидин-ЭДТА-цинк, зарегистрированный в виде протонированного иона МН+ 859.22 Да.
Образцы №3 и №4 содержат одинаковые компоненты, но в разной концентрации.
Так как вносится хлоргексидин биацетат, то синтезируется ТРИГЕКСИЛОН-биацетат.
Образец № 3. В мерной колбе вместимостью 100 мл растворяют 2,5 г основания хлоргексидина, добавляют 40,0 мл воды очищенной и 1,0 мл ледяной уксусной кислоты. Смесь перемешивают до полного растворения, после чего добавляют 3.1 г TWEEN-80 и продолжают перемешивать до получения однородного раствора. Параллельно растворяют 3.2 г ацетата цинка дигидрата и 1,5 г ЭДТА в 300 мл воды и перемешивают. После полного растворения всех ингредиентов приливают раствор ЭДТА-цинкового комплекса, после чего доводят объем до метки водой.
Образец № 4. В мерной колбе вместимостью 100 мл растворяют 4 г основания хлоргексидина, добавляют 40,0 мл воды очищенной и 3.6 мл ледяной уксусной кислоты. Смесь перемешивают до полного растворения и продолжают перемешивать до получения однородного раствора. Параллельно растворяют 12.6 г ацетата цинка дигидрата и 6.0 г ЭДТА в 300 мл воды. После полного растворения всех ингредиентов приливают раствор ЭДТА-цинкового комплекса после чего доводят объем до метки.
Таким образом получается ТРИГЕКСИЛОН-биацетат

Аналогичным образом проводилась матрично-ассоциированная лазерно индуцированная десорбция-ионизация с масс-спектрометрией (МАЛДИ-МС). Матрица - 3,4-дигидроксиацетофенон.
Режим анализа: рефлектрон, регистрация положительных ионов.
Данные масс-спектров приведены на рис. 3.
На спектре ТРИГЕКСИЛОН-биацетата присутствует бихелатный трехкомпонентный комплекс Хлоргексидин-ЭДТА-цинк, зарегистрированный в виде протонированного иона МН+ 859.22 Да.
Образцы №5 и №6 содержат одинаковые компоненты, но в разной концентрации.
Образец №5. В мерной колбе вместимостью 100 мл растворяют трилон В 0,5 г, ZnCI2, 0,22 г и хлоргексидин биглюконат 0,4г. и перемешивают, после чего доводят объем до метки водой.
Образец №6. В мерной колбе вместимостью 100 мл растворяют трилон В 0,5 г, ZnCI2 , 0,22г и хлоргексидин биглюконат 0,4г. и перемешивают, после чего доводят объем до метки водой.
Так как вносится хлоргексидин биглюконат, то синтезируется ТРИГЕКСИЛОН биглюконат.
Таким образом получается ТРИГЕКСИЛОН-биацетат следующей формулы

Указанным выше образом проводилась матрично-ассоциированная лазерно-индуцированная десорбция-ионизация с масс-спектрометрией (МАЛДИ-МС). Матрица - СНСА (альфа-цианкоричная кислота).
Режим анализа: рефлектрон, регистрация положительных ионов.
Данные масс-спектров приведены на рис. 4.
Комплексное соединение было зарегистрировано методом МАЛДИ-МС в виде протонированного иона МН+ 859.22 Да.
Новые молекулы представляют бихелатные трехкомпонентные хлоргексидин-ЭДТА-Zn комплексы, содержащие «ТРИГЕКСИЛОН», обладают выраженным биоцидным эффектом в отношении болезнетворных бактерий, грибков, микобактерий туберкулеза и вирусов. По уровню биоцидной активности и широте спектра действия они значительно превосходят хлоргексидин.
Пример 1
Определение антимикробной активности
Сравнительное изучение активности полученных комплексов in vitro на серии стандартных микроорганизмов, показало, что они обладают более высокой антимикробной активностью, чем индивидуальный биглюконат хлоргексидина в такой же концентрации.
В таблице 1 показано, как растворы различных форм средства ТРИГЕКСИЛОН ингибируют рост перечисленных бактерий и дрожжей и грибов
tropicalis
(Трилон Б-; хлорид цинка; хлоргексидин основание)
(Трилон Б, хлорид цинка, хлоргексидин ацетат)
(Трилон Б, хлорид цинка хлоргексидин биглюканат).
Биологическое действие средства определяли по диаметру роста культур в см.
В представленной таблице показано ингибирующее действие.
При этом активность полученных комплексов намного выше, чем активность биглюконатхлоргиксидина.
Пример 2
Вирулицидная активность полученных комплексов.
Тест-вирус, используемый при испытаниях:
Вирус полиомиелита, вакцинный штамм, тип 1, получен из ГУ НИИ полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН. Титр вируса 6,5 1дТЦИД5о.
Аденовирус человека, тип 5, получен из Государственной коллекции вирусов Института вирусологии им. Д.И. Ивановского» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России. Титр вируса 5,5 lg ТЦИД50 Клетки. Для работы с вирусом полиомиелита использовали перевиваемую культуру клеток почки зеленых мартышек Vero, для работы с аденовирусом - перевиваемую линию клеток НЕр-2.
Результаты испытаний представлены в таблицах 2-5 ниже. Исследование вирулицидного действия средства показало, что при времени обработки от 1,0 до 5,0 минут методом «протирание» средство инактивирует полиовирус на 4,0-5,0 lg ТЦИД50 (табл.2). Режимы дезинфекции объектов, контаминированных полиовирусом, средством представлены в таблице 3. Аденовирус на контаминированных объектах ингибировался на 4,0-4,5 lg ТЦИД50 при времени обработки в течение 3 минут (табл. 4), что позволяет рекомендовать режимы дезинфекции, представленные в таблице 5.
Исследование вирулицидной активности средства при обработке тест-объектов, контаминированных вирусом полиомиелита.
1 - ТРИГЕКСИЛОН-основание.
2 - ТРИГЕКСИЛОН-биацетат.
3 - ТРИГЕКСИЛОН-биглюконат.
1/2/3
Режимы дезинфекции средством объектов, контаминированных полиовирусом
Исследование вирулицидной активности средства при обработке тест- объектов, контаминированных аденовирусом
lg|дтцид50
1/2/3
вирус:средство1:9
Режимы дезинфекции средством объектов, контаминированных аденовирусом
Пример 3
Исследование безопасности полученных комплексов.
Условия моделирования исследований: для определения острой токсичности на лабораторных животных при внутрижелудочном введении, при нанесении на кожу, ингаляционной опасности методом статической ингаляционной затравки, использовали представленный образец в нативном виде. Испытания проводили на теплокровных половозрелых животных - белых крысах массой 210-220 г, белых мышах массой 22-24 г в опытных и контрольных группах.
Результаты исследований безопасности средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат
показатели
измерения
исследований
при введении в желудок, DL50 (белые крысы)
при нанесении на кожу, DL50 (белые крысы)
методом статической ингаляционной затравки
(белые мыши)
-однократно -10 аппликаций
(белые крысы)
0
Полученные данные свидетельствуют о низкой острой токсичности средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат. Летучие компоненты средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат не раздражают слизистые оболочки глаз и верхние дыхательные пути. Гибели животных не отмечено. Местно-раздражающее действие на кожу отсутствует.
Представленные данные показывают, что средства ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРЕГЕКСИЛОН-биглюконат по параметрам острой токсичности по ГОСТ 12.1.007-76 относятся к 4 классу малоопасных веществ при нанесении на кожу, к 4 классу малоопасных веществ при введении в желудок, при ингаляционном воздействии в виде паров по степени летучести (С20) средство малоопасно. Средства относятся к 4 классу малотоксичных веществ при введении в брюшину согласно классификации К.К. Сидорова. Рабочие растворы средства не оказывают сенсибилизирующего и раздражающего действия на кожу. В виде аэрозоля рабочие растворы не обладают раздражающим эффектом на слизистых оболочках глаз и дыхательных путей.
Пример 4
Влияние средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат на возбудителя туберкулеза М. terrae.
показатели
поверхности
(количество
тест-объектов-3)
%
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
обеззараживания
Экспозиция 5 минут.
резиновых
перчатках
Эксперименты в таблице №7 показывают, что полученные средства проводят обеззараживание полностью, т.е. обладают туберкулоцидным действием.
Пример 5
Также проводилась проверка влияния средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРЕГЕКСИЛОН-биглюконат на Общую, Грамположительную и Грамотрицательную микрофлору при гигиенической обработке рук, кожи предплечья и операционного поля.
показатели
обсемененности
%
обработки
обработки
Дезинфицирующее средство ТРИГЕКСИЛОН-основание/ ТРИГЕКСИЛОН-биацетат /
ТРЕГЕКСИЛОН-биглюконат
10
Двукратное протирание кожи раздельными стерильными тампонами, обильно
смоченными средством.
Экспозиция 2 минуты.
Пример 6
Противогельминтное действие средств ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат.
Исследования показывают высокую степень контаминации внешней среды яйцами гельминтов плотоядных от 33,98 до 40,9%. Преобладающим видом гельминта является Toxocaracanis.
Суммарно яйца гельминтов данного подотряда выявлялись в 40,54% - 54,28% положительных проб почвы. Из группы биогельминтов в почве чаще всего выявляются яйца представителей семейства Taeniidae.
Яйца всех этих групп гельминтов являются потенциально опасными для человека.
ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат при экспозиции в течение 24 часов приводили к разрушению наружной оболочки у 66,8%-67,0% яиц токсакар (Toxocaracanis) и 97,8-98,23% яиц тениид (Taeniahydatigena), что повышало их чувствительность к воздействию факторов внешней среды и приводило к 100% гибели спустя 1 час при повышении или понижении температуры внешней среды.
При этом необходимо отметить, что в яйцах токсакар (Toxocaracanis) визуально сохранивших целостность оболочек, увеличилась ее проницаемость, внесении раствора метиленового синего во взвесь яиц привело к прокрашиванию оболочки у всех не разрушившихся яиц. Инкубирование яиц токсакар подвергавшихся воздействию раствора ТРИГЕКСИЛОН-основание, ТРИГЕКСИЛОН-биацетат и ТРИГЕКСИЛОН-биглюконат не привило к развитию личиночной стадии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АНТИСЕПТИЧЕСКОГО И ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА | 2022 |
|
RU2801796C1 |
| АНТИСЕПТИЧЕСКОЕ ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2020 |
|
RU2724581C1 |
| ЖИДКАЯ ДЕЗИНФИЦИРУЮЩАЯ И АНТИСЕПТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ И ВЕТЕРИНАРИИ | 2020 |
|
RU2725991C1 |
| КОЖНОЕ АНТИСЕПТИЧЕСКОЕ СРЕДСТВО "СЕПТУСТИН-АНТИСЕПТ" | 2006 |
|
RU2317110C1 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2020 |
|
RU2726364C1 |
| СПОСОБ ОБРАБОТКИ РУК МЕДИЦИНСКОГО ПЕРСОНАЛА, ГНОЙНЫХ РАН, ИНЪЕКЦИОННЫХ И ОПЕРАЦИОННЫХ ПОЛЕЙ И СТЕРИЛИЗАЦИИ МЕДИЦИНСКОГО ИНСТРУМЕНТАРИЯ | 1997 |
|
RU2122865C1 |
| СРЕДСТВО ДЛЯ ДЕЗИНФИЦИРУЮЩЕЙ ОБРАБОТКИ КОЖНОГО ПОКРОВА | 2013 |
|
RU2521323C1 |
| СОЛЮБИЛИЗАЦИЯ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2017 |
|
RU2696259C2 |
| ЛИОТРОПНЫЙ ЖИДКИЙ КРИСТАЛЛ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2021 |
|
RU2750598C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ | 2000 |
|
RU2161961C1 |
Изобретение относится к области санитарии и медицины. Предложено антисептическое и дезинфицирующее средство, полученное смешиванием следующих компонентов: А) трилон В - 0,3 г, ZnCl2 - 0,12 г, хлоргексидин основание - 0,2 г, вода - до 100 мл; или Б) хлоргексидин основание - 2,5 г, ледяная уксусная кислота - 1,0 мл, TWEEN-80 - 3,1 г, ацетат цинка дигидрат - 3,2 г, ЭДТА- 1,5 г, вода - до 100 мл; или В) трилон В - 0,5 г, ZnCl2 - 0,22 г, хлоргексидин биглюконат - 0,4 г, вода - до 100 мл. При этом образуется одно из следующих соединений: ТРИГЕКСИЛОН-основание (А), ТРИГЕКСИЛОН-биацетат (Б) или ТРИГЕКСИЛОН-биглюконат (В). Предложено также применение указанного средства в качестве безопасного комплексного средства, обладающего бактерицидным, туберкулоцидным, фунгицидным и противогельминтным действием. Изобретение обеспечивает высокую эффективность дезинфицирующего и антисептического средства при наличии выраженного бактерицидного, туберкулоцидного, фунгицидного, вирулицидного и противогельминтного действия, а также его безопасность. 2 н.п. ф-лы, 4 ил., 8 табл., 6 пр.
1. Антисептическое и дезинфицирующее средство, полученное смешиванием следующих компонентов:
А) трилон В - 0,3 г, ZnCI2 - 0,12 г, хлоргексидин основание - 0,2 г, вода - до 100 мл, с образованием комплекса со структурной формулой
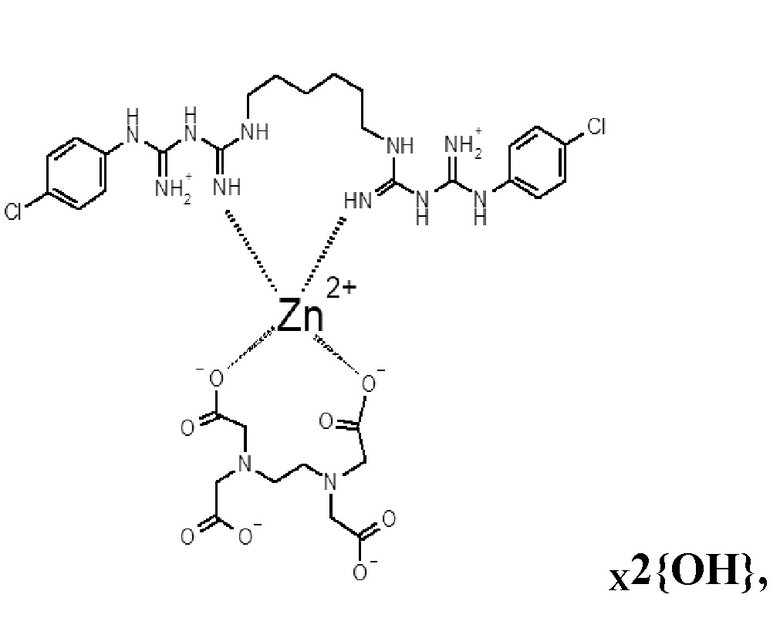
или
Б) хлоргексидин основание - 2,5 г, ледяная уксусная кислота - 1,0 мл, TWEEN-80 - 3.1 г, ацетат цинка дигидрат - 3.2 г, ЭДТА - 1,5 г, вода до 100 мл, с образованием комплекса со структурной формулой
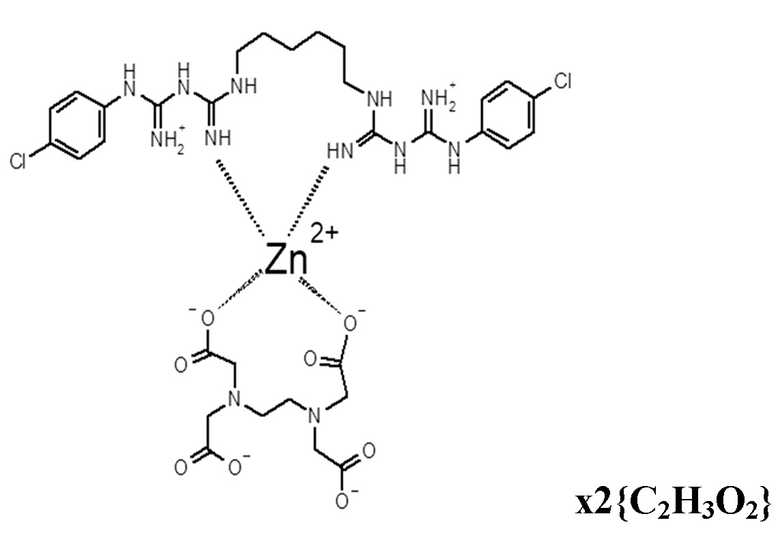
или
В) трилон В - 0,5 г , ZnCI2 - 0,22 г, хлоргексидин биглюконат - 0,4 г, вода - до 100 мл, с образованием комплекса со структурной формулой
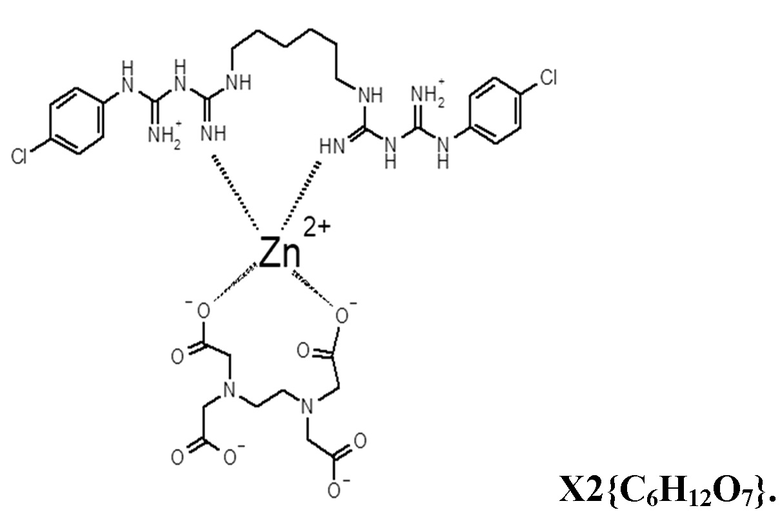
2. Применение средства по п.1 в качестве безопасного комплексного средства, обладающего бактерицидным, туберкулоцидным, фунгицидным и противогельминтным действием.
| ЖИДКАЯ ДЕЗИНФИЦИРУЮЩАЯ И АНТИСЕПТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ И ВЕТЕРИНАРИИ | 2020 |
|
RU2725991C1 |
| В.А | |||
| ГАЛЫНКИН Антимикробная и вирулицидная активность трехкомпонентного комплекса хлоргексидин-ЭДТА-цинк | |||
| Медицина экстремальных ситуаций, т | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| Опубл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| КОНОПСКАЯ В.А | |||
| и др | |||
| Инсектицидная эффективность некоторых | |||
Авторы
Даты
2024-12-02—Публикация
2023-04-01—Подача