1. Область техники
Настоящее изобретение относится к варианту АТФ(аденозинтрифосфат)-зависимой протеазы и способу получения L-аминокислот с ее применением.
2. Описание уровня техники
L-аминокислоты являются основными структурными блоками белков и имеют различные важные области применения, такие как фармацевтическое сырье и пищевые добавки, корма для животных, питательные вещества, пестициды, бактерицидные агенты и так далее. В частности, аминокислоты с разветвленной цепью (ВСАА) в совокупности включают L-валин, L-лейцин и L-изолейцин, которые являются незаменимыми аминокислотами, а также известно, что аминокислоты с разветвленной цепью обладают антиоксидантным эффектом и эффектом прямого стимулирования синтеза белка в мышечных клетках.
Вместе с тем, получение аминокислот с разветвленной цепью с помощью микроорганизмов в основном осуществляют с применением микроорганизмов рода Escherichia или микроорганизмов рода Corynebacterium, а также известно, что аминокислоты с разветвленной цепью получают путем биосинтеза из пировиноградной кислоты в несколько стадий с применением 2-кетоизокапроата в качестве предшественника (патент США №9885093, патент США №10351859, патент США №8465962). Однако в получении аминокислот с разветвленной цепью с помощью микроорганизмов имеется проблема, заключающаяся в том, что промышленное крупномасштабное получение затруднено.
Тем не менее, с возрастанием потребности в аминокислотах с разветвленной цепью сохраняется необходимость в поиске возможности эффективного получения аминокислот с разветвленной цепью.
Авторы настоящего изобретения предприняли значительные усилия для увеличения возможностей получения аминокислот с разветвленной цепью, и в результате они разработали способ получения аминокислот с разветвленной цепью в высоких концентрациях с применением варианта АТФ-зависимой протеазы, который стал основой настоящего изобретения.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Задачей настоящего изобретения является обеспечение микроорганизма рода Corynebacterium, в котором активность АТФ-зависимой протеазы ослаблена по сравнению с немодифицированным микроорганизмом, предпочтительно микроорганизма рода Corynebacterium, обладающего способностью продуцировать аминокислоты с разветвленной цепью.
Другой задачей настоящего изобретения является обеспечение варианта ClpC, в котором удалена аминокислотная последовательность, соответствующая положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5.
Еще одной задачей настоящего изобретения является обеспечение полинуклеотида, кодирующего вариант ClpC согласно настоящему изобретению.
Еще одной задачей настоящего изобретения является обеспечение способа получения аминокислот с разветвленной цепью, включающего стадию культивирования в среде микроорганизма рода Corynebacterium согласно настоящему изобретению или микроорганизма рода Corynebacterium, содержащего любой один или более из вариантов ClpC согласно настоящему изобретению, или полинуклеотид согласно настоящему изобретению, и содержащий его вектор.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВОПЛОЩЕНИЙ
Настоящее изобретение будет подробно описано далее. При этом каждое описание и воплощение, раскрытые в настоящем изобретении, также могут быть применены к другим описаниям и воплощениям. То есть все комбинации различных элементов, раскрытых в настоящем изобретении, входят в объем настоящего изобретения. Кроме того, объем настоящего изобретения не ограничивается конкретным описанием, представленным ниже. Также специалисты в данной области техники узнают или смогут выявить с помощью не более чем рутинной экспериментальной работы множество эквивалентов конкретных воплощений настоящего изобретения, описанных в настоящем документе. В свою очередь, эти эквиваленты следует рассматривать как входящие в объем настоящего изобретения.
В одном из аспектов настоящего изобретения предложен микроорганизм рода Corynebacterium, в котором активность АТФ-зависимой протеазы ослаблена по сравнению с немодифицированным микроорганизмом.
В настоящем документе термин «АТФ-зависимая протеаза (ЕС 3.4.21.92)» относится к ферменту, который осуществляет гидролиз белка с получением небольших пептидов в присутствии АТФ и Mg2+. Термин «АТФ-зависимая протеаза» согласно настоящему изобретению может использоваться взаимозаменяемо с терминами Clp-эндопептидаза, АТФ-зависимая Clp-протеаза, ClpP или Clp-протеаза.
Ослабление АТФ-зависимой протеазы согласно настоящему изобретению может представлять собой ослабление активности АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы.
Термин «АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы» может использоваться взаимозаменяемо с термином «АТФаза семейства ААА» или «ClpC». В настоящем изобретении последовательность АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы может быть получена из GenBank NCBI, который является известной базой данных. В частности, указанная субъединица может представлять собой полипептид, обладающий активностью АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы, кодируемый clpC, но без ограничения этим.
АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы согласно настоящему изобретению может иметь происхождение из рода Corynebacterium. Например, АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы согласно настоящему изобретению может иметь происхождение из Corynebacterium glutamicum.
АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы согласно настоящему изобретению может включать полипептид, представленный SEQ ID NO: 5 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней.
Например, аминокислотная последовательность, имеющая 90% или более идентичности аминокислотной последовательности SEQ ID NO: 5 согласно настоящему изобретению, может представлять собой аминокислотную последовательность, имеющую по меньшей мере 91% или более, 92% или более, 93% или более, 94% или более, 95% или более, 96% или более, 96,26% или более, 97% или более, 97,5% или более, 97,7% или более, 97,8% или более, 98% или более, 98,5% или более, 98,7% или более, 98,8% или более, 99% или более, 99,5% или более, 99,7% или более, 99,8% или более, или менее 100% гомологии или идентичности аминокислотной последовательности SEQ ID NO: 5 согласно настоящему изобретению. Кроме того, очевидно, что белки, имеющие аминокислотные последовательности, в которых некоторые последовательности удалены, модифицированы, заменены или добавлены, также включены в объем подлежащего ослаблению белка в настоящем изобретении при условии, что указанные аминокислотные последовательности имеют указанную гомологию или идентичность и проявляют активность, идентичную или соответствующую активности АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы.
При этом АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы согласно настоящему изобретению может иметь полипептид, представленный аминокислотной последовательностью SEQ ID NO: 5 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней, или может состоять или по существу состоять из указанного полипептида. АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы согласно настоящему изобретению может включать субъединицы, имеющие добавление незначимой последовательности до или после SEQ ID NO: 5 или аминокислотной последовательности, имеющей 90% или более идентичности с ней (то есть добавление последовательности, которая не изменяет функцию белка, с N-конца и/или С-конца аминокислотной последовательности), или природную мутацию, молчащую мутацию или консервативную замену.
«Консервативная замена» означает замену одной аминокислоты на другую аминокислоту, имеющую близкие структурные и/или химические свойства. Такая аминокислотная замена обычно может происходить на основании сходства полярности, заряда, растворимости, гидрофобности, гидрофильности и/или амфипатического характера остатков. Обычно консервативная замена может по существу не влиять или не влиять на активность белков или полипептидов.
Микроорганизм согласно настоящему изобретению может содержать полипептид, имеющий делецию аминокислот, соответствующих положениям 431-433 на основании последовательности, представленной SEQ ID NO: 5, или полинуклеотид, имеющий делецию нуклеотидов, соответствующих положениям 1291-1299 на основании последовательности, представленной SEQ ID NO: 6.
В настоящем документе термин «соответствующий» относится к аминокислотным остаткам или нуклеотидным остаткам в положениях, обозначенных в полипептиде или полинуклеотиде, или аминокислотным остаткам или нуклеотидным остаткам, которые аналогичны, идентичны или гомологичны остаткам, обозначенным в полипептиде или полинуклеотиде. Идентификация аминокислоты или нуклеотида в соответствующем положении может представлять собой определение конкретной аминокислоты или нуклеотида в последовательности, которая отнесена к конкретной последовательности. В настоящем документе термин «соответствующая область» обычно относится к подобному или соответствующему положению в родственном белке или эталонном белке.
Например, произвольную аминокислотную последовательность выравнивают с SEQ ID NO: 5 или SEQ ID NO: 6, и на основании этого каждый аминокислотный остаток указанной аминокислотной последовательности может быть пронумерован относительно аминокислотного остатка, соответствующего аминокислотному остатку SEQ ID NO: 6, или обозначенного номером положения нуклеотидного остатка, соответствующего нуклеотидному остатку SEQ ID NO: 6. Например, алгоритм выравнивания последовательностей, описанный в настоящем изобретении, может определять положение аминокислоты или положение, в котором происходит модификация, такая как замена, вставка или делеция, посредством сравнения с положением в запрашиваемой последовательности (также называемой «эталонной последовательностью»).
Для таких выравниваний может быть применен, например, алгоритм Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453), программа Needleman из пакета EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000), Trends Genet. 16: 276-277) и тому подобное, но без ограничения этим, а также могут быть надлежащим образом применены программа для выравнивания последовательностей, алгоритм попарного сравнения последовательностей и так далее, известные в данной области техники.
В настоящем документе термин «ослабление» активности полипептида представляет собой понятие, включающее как случай, когда активность снижена по сравнению с эндогенной активностью, так и случай, когда активность отсутствует. Термин «ослабление» может использоваться взаимозаменяемо с такими терминами, как инактивация, недостаточность, понижающая регуляция, снижение, уменьшение, аттенуация и так далее.
Ослабление может также включать случай, когда активность полипептида как таковая снижена или устранена вследствие вариации полинуклеотида, кодирующего указанный полипептид, и так далее, по сравнению с активностью указанного полипептида, изначально присущей микроорганизму, случай, когда общий уровень активности полипептида и/или концентрация (уровень экспрессии) в клетке являются низкими вследствие ингибирования экспрессии гена полинуклеотида, кодирующего полипептид, или вследствие ингибирования трансляции в полипептид, по сравнению с таковыми у природного штамма, случай, когда полинуклеотид совсем не экспрессируется, и/или случай, когда активность полипептида отсутствует, даже если полинуклеотид экспрессируется. «Эндогенная активность» означает активность конкретного полипептида, изначально присущую родительскому штамму до изменения признака, или микроорганизму дикого типа, или немодифицированному микроорганизму, в случае, когда признак изменяется в результате генетической изменчивости, вызванной природными или искусственными факторами. Термин «эндогенная активность» может использоваться взаимозаменяемо с термином «активность до модификации». Тот факт, что активность полипептида «инактивирована, недостаточна, снижена, подвергается понижающей регуляции, уменьшена или аттенуирована» по сравнению с эндогенной активностью, означает, что активность полипептида является более низкой по сравнению с активностью конкретного полипептида, изначально присущей родительскому штамму до изменения признака или немодифицированному микроорганизму.
Такое ослабление активности полипептида может быть осуществлено любым способом, известным в данной области техники, но способ без ограничения этим, и ослабление может быть достигнуто путем применения различных способов, хорошо известных в данной области техники (например, Nakashima N et al., Bacterial cellular engineering by genome editing and gene silencing. Int J Mol Sci. 2014;15(2):2773-2793, Sambrook et al. Molecular Cloning 2012 и так далее).
В частности, ослабление активности полипептида согласно настоящему изобретению может представлять собой:
1) полную или частичную делецию гена, кодирующего полипептид;
2) модификацию регулирующей экспрессию области (или регулирующей экспрессию последовательности) для снижения экспрессии гена, кодирующего полипептид;
3) модификацию аминокислотной последовательности, составляющей полипептид, для устранения или ослабления активности полипептида (например, делецию/замену/добавление одной или более аминокислот в аминокислотной последовательности);
4) модификацию последовательности гена, кодирующего полипептид, для устранения или ослабления активности полипептида (например, делецию/замену/добавление одного или более оснований нуклеиновой кислоты в последовательности оснований нуклеиновой кислоты гена полипептида для кодирования полипептида, который был модифицирован для устранения или ослабления активности полипептида);
5) модификацию инициирующего кодона транскрипта гена, кодирующего полипептид, или последовательности оснований, кодирующей область 5'-UTR (5'-UTR);
6) введение антисмыслового олигонуклеотида (например, антисмысловой РНК), который комплементарно связывается с транскриптом гена, кодирующего полипептид;
7) добавление последовательности, комплементарной последовательности Шайна-Дальгарно, перед последовательностью Шайна-Дальгарно гена, кодирующего полипептид, для образования вторичной структуры, к которой не может быть присоединена рибосома;
8) добавление транскрибируемого в обратном направлении промотора к 3'-концу открытой рамки считывания (ORF) последовательности гена, кодирующей полипептид (конструирование на основе обратной транскрипции (RTE)); или
9) комбинацию двух или более подходов, выбранных из 1) - 8), но без конкретного ограничения этим. Например,
1) частичная или полная делеция гена, кодирующего полипептид, может представлять собой полное удаление полинуклеотида, кодирующего интересующий исходный полипептид в хромосоме, замену на полинуклеотид, в котором удалены некоторые нуклеотиды, или замену на маркерный ген.
Кроме того, 2) модификация регулирующей экспрессию области (или регулирующей экспрессию последовательности) может представлять собой делецию, вставку, неконсервативную или консервативную замену или появление вариации в регулирующей экспрессию области (или регулирующей экспрессию последовательности) вследствие их комбинации, или замену на последовательность, проявляющую более слабую активность. Регулирующая экспрессию область содержит промотор, операторную последовательность, последовательность, кодирующую сайт связывания рибосомы, и последовательность, регулирующую терминацию транскрипции и трансляции, но без ограничения этим.
Также 3) и 4) модификация аминокислотной последовательности или полинуклеотидной последовательности может представлять собой делецию, вставку или неконсервативную или консервативную замену в аминокислотной последовательности полипептида или полинуклеотидной последовательности, кодирующей полипептид, или появление вариации в последовательности вследствие их комбинации, или замену на аминокислотную последовательность или полинуклеотидную последовательность, модифицированную с обеспечением проявления более слабой активности, или на аминокислотную последовательность или полинуклеотидную последовательность, модифицированную с обеспечением отсутствия активности, вследствие чего активность полипептида ослаблена, но без ограничения этим. Например, экспрессия гена может быть ингибирована или ослаблена путем введения вариации в полинуклеотидную последовательность и образования стоп-кодона, но без ограничения этим.
Также 5) модификация инициирующего кодона транскрипта гена, кодирующего полипептид, или последовательности оснований, кодирующей область 5'-UTR, может представлять собой, например, замену на последовательность оснований, кодирующую другой инициирующий кодон, обеспечивающий более низкую скорость экспрессии полипептида по сравнению с исходным инициирующим кодоном, но без ограничения этим.
Также в отношении 6) введения антисмыслового олигонуклеотида (например, антисмысловой РНК), который комплементарно связывается с транскриптом гена, кодирующего полипептид, может быть сделана ссылка на документы, например, [Weintraub, Н. et al., Antisense-RNA as a molecular tool for genetic analysis, Reviews -Trends in Genetics, Vol. 1(1) 1986].
Также 7) добавление последовательности, комплементарной последовательности Шайна-Дальгарно, перед последовательностью Шайна-Дальгарно гена, кодирующего полипептид, для образования вторичной структуры, к которой не может быть присоединена рибосома, может быть для того, чтобы сделать трансляцию мРНК (матричная РНК) невозможной или замедлить скорость трансляции мРНК.
Также 8) добавление транскрибируемого в обратном направлении промотора к 3'-концу открытой рамки считывания (ORF) последовательности гена, кодирующей полипептид (конструирование на основе обратной транскрипции (RTE)) может быть для ослабления активности за счет создания антисмыслового нуклеотида, комплементарного транскрипту гена, кодирующего полипептид.
Микроорганизм согласно настоящему изобретению может обладать способностью продуцировать аминокислоту с разветвленной цепью. В частности, аминокислота с разветвленной цепью согласно настоящему изобретению может представлять собой L-валин или L-изолейцин.
В настоящем документе термин «микроорганизм (или штамм)» включает все микроорганизмы дикого типа или генетически модифицированные природным или искусственным образом микроорганизмы, и он может представлять собой микроорганизм, в котором конкретный механизм ослаблен или усилен вследствие вставки чужеродного гена, или усиления активности, или инактивации эндогенного гена, и он может представлять собой микроорганизм, включающий генетическую модификацию для продуцирования интересующего полипептида, белка или продукта.
В частности, штамм согласно настоящему изобретению может представлять собой микроорганизм, для получения которого родительскому штамму, не обладающему способностью продуцировать аминокислоты с разветвленной цепью, придают способность продуцировать аминокислоты с разветвленной цепью, или микроорганизм, для получения которого в микроорганизм, обладающий способностью продуцировать аминокислоты с разветвленной цепью, вводят ослабленную АТФ-зависимую протеазу согласно настоящему изобретению или кодирующий ее полинуклеотид (или вектор, содержащий такой полинуклеотид) вместо природной АТФ-зависимой протеазы, или природную АТФ-зависимую протеазу модифицируют с получением ослабленной АТФ-зависимой протеазы согласно настоящему изобретению, но без ограничения этим.
В настоящем изобретении микроорганизм, в котором экспрессируется вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы и продуцируется аминокислота с разветвленной цепью, может представлять собой микроорганизм, отличающийся тем, что в него включен полинуклеотид согласно настоящему изобретению и в нем экспрессируется вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы, и, таким образом, увеличивается его способность продуцировать аминокислоту с разветвленной цепью. В частности, в настоящем изобретении микроорганизм, в котором экспрессируется вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы и продуцируется аминокислота с разветвленной цепью, или микроорганизм, обладающий способностью экспрессировать вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы и способностью продуцировать аминокислоту с разветвленной цепью, может представлять собой микроорганизм, в котором активность АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы ослаблена, и некоторые гены пути биосинтеза аминокислот с разветвленной цепью усилены или ослаблены, или активность АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы ослаблена, и некоторые гены пути деградации аминокислот с разветвленной цепью усилены или ослаблены.
Микроорганизм рода Corynebacterium согласно настоящему изобретению может представлять собой микроорганизм, дополнительно, в котором усилена активность малой субъединицы изофермента 1 ацетолактатсинтазы, усилена активность аспартокиназы, ослаблена активность гомосериндегидрогеназы и/или усилена активность биосинтетической IlvA L-треониндегидратазы.
В настоящем документе термин «усиление» активности полипептида означает, что активность полипептида повышена по сравнению с его исходной активностью. Термин «усиление» может использоваться взаимозаменяемо с такими терминами, как активация, повышающая регуляция, сверхэкспрессия, повышение и так далее. В настоящем документе активация, усиление, повышающая регуляция, сверхэкспрессия и повышение могут включать как проявление активности, которой изначально не было, так и проявление улучшенной активности по сравнению с исходной активностью или активностью до модификации. Термин «исходная активность» означает активность конкретного полипептида, изначально присущую родительскому штамму до изменения признака или немодифицированному микроорганизму, в случае, когда признак изменяется посредством генетической вариации за счет природных или искусственных факторов. Он может использоваться взаимозаменяемо с термином «активность до модификации». Тот факт, что активность полипептида «усилена», «подвергается повышающей регуляции», «сверхэкспрессирована» или «повышена» по сравнению с исходной активностью, означает, что активность полипептида является улучшенной по сравнению с активностью и/или концентрацией (уровнем экспрессии) конкретного полипептида, изначально присущими родительскому штамму до изменения признака или немодифицированному микроорганизму.
Усиление может быть достигнуто путем введения чужеродного полипептида или усиления исходной активности и/или концентрации (уровня экспрессии) полипептида. Усиление активности полипептида может быть подтверждено повышением степени активности и уровня экспрессии соответствующего полипептида или количества продукта, полученного посредством соответствующего полипептида.
Для усиления активности полипептида могут быть применены различные способы, хорошо известные в данной области техники, и способ не ограничен при условии, что активность интересующего полипептида может быть усилена по сравнению с активностью у микроорганизма до модификации. В частности, могут быть применены хорошо известные специалистам в данной области техники методы генной инженерии и/или белковой инженерии, которые представляют собой рутинные методы молекулярной биологии, но способ не ограничивается ими (например, Sitnicka et al. Functional Analysis of Genes. Advances in Cell Biology. 2010, vol. 2. 1-16, Sambrook et al. Molecular Cloning 2012 и так далее).
В частности, усиление активности полипептида согласно настоящему изобретению может представлять собой:
1) увеличение числа внутриклеточных копий полинуклеотида, кодирующего полипептид;
2) замену области регуляции экспрессии гена в хромосоме, кодирующей полипептид, последовательностью, проявляющей сильную активность;
3) модификацию инициирующего кодона транскрипта гена, кодирующего полипептид, или последовательности оснований, кодирующей 5'-UTR;
4) модификацию аминокислотной последовательности для усиления активности полипептида;
5) модификацию полинуклеотидной последовательности, кодирующей полипептид, для усиления активности полипептида (например, модификацию полинуклеотидной последовательности гена полипептида для кодирования полипептида, который был модифицирован для усиления активности полипептида);
6) введение чужеродного полипептида, проявляющего активность указанного полипептида, или чужеродного полинуклеотида, кодирующего указанный полипептид;
7) оптимизацию кодонов полинуклеотида, кодирующего полипептид;
8) анализ третичной структуры полипептида для выбора подлежащего воздействию сайта и для выполнения модификации или химической модификации подлежащего воздействию сайта; или
9) комбинацию двух или более подходов, выбранных из 1) - 8), но без конкретного ограничения этим.
Такое усиление активности полипептида может представлять собой повышение активности или концентрации уровня экспрессии соответствующего полипептида относительно активности или концентрации полипептида, экспрессируемого в штамме микроорганизма дикого типа или штамме микроорганизма до модификации, или увеличение количества продукта, полученного посредством соответствующего полипептида, но без ограничения этим.
В микроорганизме согласно настоящему изобретению частичная или полная модификация полинуклеотида может быть вызвана посредством (а) гомологичной рекомбинации с использованием вектора для вставки в хромосому в микроорганизме или редактированием генома с использованием сконструированной нуклеазы (например, CRISPR-Cas9) и/или (б) обработки излучением, например ультрафиолетовым излучением и радиоактивным излучением, и/или химическими веществами, но без ограничения этим. Способ частичной или полной модификации гена может включать способ с использованием технологии рекомбинации ДНК. Например, путем введения в микроорганизм нуклеотидной последовательности или вектора, содержащего нуклеотидную последовательность, гомологичную интересующему гену, что вызывает гомологичную рекомбинацию, ген может быть частично или полностью удален. Введенная нуклеотидная последовательность или вектор могут включать доминантный селективный маркер, но без ограничения этим.
Микроорганизм рода Corynebacterium согласно настоящему изобретению может представлять собой Corynebacterium glutamicum, Corynebacterium crudilactis, Corynebacterium deserti, Corynebacterium efficiens, Corynebacterium callunae, Corynebacterium stationis, Corynebacterium singulare, Corynebacterium halotolerans, Corynebacterium striatum, Corynebacterium ammoniagenes, Corynebacterium pollutisoli, Corynebacterium imitans, Corynebacterium testudinoris или Corynebacterium flavescens.
В другом аспекте настоящего изобретения предложен вариант ClpC, в котором удалена аминокислотная последовательность, соответствующая положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5.
Вариант ClpC может представлять собой вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы. «ClpC» или «АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы» является такой, как описано выше.
Например, вариант ClpC согласно настоящему изобретению может включать полипептид, представленный аминокислотной последовательностью SEQ ID NO: 1 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней.
Вариант ClpC согласно настоящему изобретению может иметь полипептид, представленный аминокислотной последовательностью SEQ ID NO: 1 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней, как описано выше, или может состоять или по существу состоять из указанного полипептида. В частности, вариант ClpC согласно настоящему изобретению может включать аминокислотную последовательность, имеющую 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 99,5%, 99,7% или 99,9% или более гомологии или идентичности с аминокислотной последовательностью, представленной SEQ ID NO: 1. Кроме того, очевидно, что варианты, имеющие аминокислотные последовательности, в которых некоторые последовательности удалены, модифицированы, заменены, консервативно заменены или добавлены, также включены в объем настоящего изобретения при условии, что указанные аминокислотные последовательности имеют указанную гомологию или идентичность и проявляют эффективность, соответствующую эффективности варианта ClpC согласно настоящему изобретению.
В настоящем документе термин «вариант» относится к полипептиду, который имеет аминокислотную последовательность, отличную от аминокислотной последовательности варианта до модификации путем консервативной замены и/или модификации одной или более аминокислот, но при этом его сохраняет функции или свойства. Такой вариант обычно может быть идентифицирован путем модификации одной или более аминокислот в аминокислотной последовательности полипептида и оценки свойств модифицированного полипептида. Другими словами, способность варианта может быть увеличена, может остаться неизменной или быть уменьшена по сравнению со способностью полипептида до вариации. Некоторые варианты могут включать варианты, в которых удалены одна или более частей, таких как N-концевая лидерная последовательность или трансмембранный домен. Другие варианты могут включать варианты, в которых часть N-конца и/или С-конца удалена из зрелого белка. Термин «вариант» может использоваться взаимозаменяемо с такими терминами, как модификация, модифицированный полипептид, модифицированный белок, мутант, мутеин и дивергент, и не ограничивается ими при условии, что этот термин используется в значении видоизменения.
Кроме того, вариант может включать делеции или добавления аминокислот, которые оказывают минимальное влияние на свойства и вторичную структуру полипептида. Например, сигнальная (или лидерная) последовательность, котрансляционно или посттрансляционно участвующая в транслокации белка, может быть конъюгирована с N-концом варианта. Вариант может быть конъюгирован с другими последовательностями или линкерами таким образом, чтобы его идентифицировать, очистить или синтезировать.
В настоящем документе термин «гомология» или «идентичность» означает степень сходства между двумя заданными последовательностями аминокислот или последовательностями оснований и может быть выражена в процентах. Термины «гомология» и «идентичность» часто могут использоваться взаимозаменяемо.
Гомология последовательности или идентичность консервативного полинуклеотида или полипептида определяется стандартными алгоритмами выравнивания, и совместно может использоваться штраф за пропуск по умолчанию, установленный используемой программой. По существу, гомологичные или идентичные последовательности, как правило, способны гибридизоваться с полной последовательностью или ее частью в умеренно строгих или очень строгих условиях. Очевидно, что гибридизация также включает гибридизацию полинуклеотида с полинуклеотидом, содержащим общий кодон или кодон с учетом вырожденности кодонов.
Имеют ли какие-либо две полинуклеотидные или полипептидные последовательности гомологию, сходство или идентичность, можно определить с использованием известных компьютерных алгоритмов, таких как программное обеспечение «FASTA», например с использованием параметров по умолчанию, как описано в источнике Pearson et al (1988) [Proc. Natl. Acad. Sci. USA 85]: 2444. В качестве альтернативы, гомология, сходство или идентичность могут быть определены с помощью алгоритма Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453), выполняемого в программе Needleman из пакета EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277) (версия 5.0.0 или более поздняя) (включая пакет программного обеспечения GCG (Devereux, J. et al. Nucleic Acids Research 12: 387(1984)), BLASTP, BLASTN, FASTA (Atschul, [S.] [F.,] [ET AL., J MOLEC BIOL 215]: 403 (1990); Guide to Huge Computers, Martin J. Bishop, [ED.,] Academic Press, San Diego, 1994, и [CARILLO ETA/.](1988) SIAM J Applied Math 48: 1073). Например, для определения гомологии, сходства или идентичности можно использовать программное обеспечение BLAST Национального центра биотехнологической информации или ClustalW.
Гомологию, сходство или идентичность полинуклеотидов или полипептидов можно определить путем сравнения информации о последовательности с использованием, например, компьютерной программы GAP, как описано в Needleman et al. (1970), J Mol Biol. 48:443, о чем сообщалось, например, в источнике Smith and Waterman, Adv. Appl. Math(1981) 2:482. Вкратце, программа GAP может быть определена как значение, полученное путем деления количества выровненных одинаковым образом символов (а именно, нуклеотидов или аминокислот) на общее количество символов в более короткой из двух последовательностей. Параметры по умолчанию для программы GAP могут включать (1) матрицу бинарных сравнений (включая значения 1 для идентичности и 0 для неидентичности) и матрицу взвешенных сравнений Gribskov et al (1986) Nucl. Acids Res. 14: 6745 (или матрицу замен EDNAFULL (NCBI NUC4.4 версии EMBOSS)), как описано в источнике Schwartz and Dayhoff, eds., Atlas Of Protein Sequence And Structure, National Biomedical Research Foundation, pp.353-358(1979); (2) штраф 3,0 за каждый пропуск и дополнительный штраф 0,10 за каждый символ в каждом пропуске (или штраф 10 за открытие пропуска, штраф 0,5 за продолжение пропуска) и (3) отсутствие штрафа за концевые пропуски.
В качестве одного из примеров настоящего изобретения вариант согласно настоящему изобретению может обладать активностью АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы. Кроме того, вариант согласно настоящему изобретению может обладать активностью, повышающей продукцию аминокислот с разветвленной цепью по сравнению с полипептидом дикого типа, обладающим активностью АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы.
В еще одном аспекте настоящего изобретения предложен полинуклеотид, кодирующий вариант ClpC согласно настоящему изобретению.
«Вариант ClpC» и «вариант АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы» являются такими, как описано выше.
В настоящем документе термин «полинуклеотид» представляет собой цепь ДНК или РНК, имеющую заданную или большую длину, представляющую собой полимер нуклеотидов, в котором нуклеотидные мономеры соединены в длинную цепь ковалентными связями, и, более конкретно, он означает полинуклеотидный фрагмент, кодирующий указанный вариант.
Полинуклеотид, кодирующий вариант ClpC согласно настоящему изобретению, может включать последовательность оснований, кодирующую полипептид, представленный аминокислотной последовательностью SEQ ID NO: 1 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней. В качестве примера настоящего изобретения полинуклеотид согласно настоящему изобретению может содержать или включать полинуклеотид, представленный нуклеотидной последовательностью SEQ ID NO: 2 или нуклеотидной последовательностью, имеющей 90% или более идентичности с ней. Кроме того, полинуклеотид согласно настоящему изобретению может состоять или по существу состоять из полинуклеотида, представленного нуклеотидной последовательностью SEQ ID NO: 2.
В полинуклеотиде согласно настоящему изобретению в кодирующей области могут быть выполнены различные модификации при условии, что аминокислотная последовательность варианта согласно настоящему изобретению не изменяется, принимая во внимание вырожденность кодонов или предпочтительные кодоны в организмах, предназначенных для экспрессии варианта согласно настоящему изобретению.
Кроме того, полинуклеотид согласно настоящему изобретению может включать зонд, который может быть получен из известной последовательности гена, например последовательности без ограничений при условии, что она представляет собой последовательность, которая может гибридизоваться с комплементарной последовательностью полностью или с частью полинуклеотидной последовательности согласно настоящему изобретению в строгих условиях. «Строгие условия» означают условия, обеспечивающие специфичную гибридизацию между полинуклеотидами. Эти условия подробно описаны в документах (см. J. Sambrook et al., Molecular Cloning, A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory press, Cold Spring Harbor, New York, 1989; F.M. Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc., New York, 9.50-9.51, 11.7-11.8). Их примеры включают условия, при которых полинуклеотиды, имеющие более высокую гомологию или идентичность, а именно полинуклеотиды, имеющие 70% или более, 75% или более, 80% или более, 85% или более, 90% или более, 95% или более, 96% или более, 97% или более, 98% или более или 99% или более гомологии или идентичности, гибридизуются друг с другом, в то время как полинуклеотиды, имеющие более низкую гомологию или идентичность, не гибридизуются друг с другом, или условия промывки для обычной Саузерн-гибридизации, при которых промывку выполняют однократно, конкретно от двух до трех раз при концентрации соли и температуре, эквивалентных 60°С, 1X SSC, 0,1% SDS, конкретно 60°С, ОДХ SSC, 0,1% SDS, более конкретно 68°С, 0,1Х SSC, 0,1% SDS.
Для гибридизации необходимо, чтобы две нуклеиновые кислоты имели комплементарные последовательности, хотя допускаются несоответствия между основаниями в зависимости от строгости гибридизации. Термин «комплементарный» используется для описания соответствия между нуклеотидными основаниями, способными гибридизоваться друг с другом. Например, применительно к ДНК, аденин комплементарен тимину, а цитозин комплементарен гуанину. Следовательно, полинуклеотид согласно настоящему изобретению может также включать по существу схожие последовательности нуклеиновых кислот, а также выделенные фрагменты нуклеиновых кислот, которые комплементарны полной последовательности.
В частности, полинуклеотид, имеющий гомологию или идентичность с полинуклеотидом согласно настоящему изобретению, может быть обнаружен с применением условий гибридизации, включающих стадию гибридизации при значении Tm 55°С и описанные выше условия. Значение Tm может составлять 60°С, 63°С или 65°С, но без ограничения этим, и может быть соответствующим образом подобрано специалистами в данной области техники в соответствии с задачей.
Надлежащая строгость гибридизации полинуклеотида зависит от длины и степени комплементарности полинуклеотида, и эти переменные хорошо известны в данной области техники (например, J. Sambrook et al., см. выше).
В еще одном аспекте настоящего изобретения предложен вектор, содержащий полинуклеотид согласно настоящему изобретению.
Указанный вектор может представлять собой экспрессионный вектор для обеспечения экспрессии полинуклеотида в клетках-хозяевах, но без ограничения этим.
Вектор согласно настоящему изобретению относится к конструкции ДНК, содержащей интересующую полинуклеотидную последовательность, функционально связанную с подходящей регуляторной последовательностью таким образом, что интересующий ген может быть введен в подходящего хозяина. Регуляторная последовательность может содержать промотор, способный инициировать транскрипцию, любую операторную последовательность для регуляции транскрипции, последовательность, кодирующую подходящий сайт связывания с рибосомой в мРНК, и последовательность, регулирующую терминацию транскрипции и трансляции. Вектор может быть трансформирован в подходящую клетку-хозяина и затем реплицирован или функционировать независимо от генома хозяина, либо может быть встроен в сам геном. Например, интересующий полинуклеотид в хромосоме может быть заменен на модифицированный полинуклеотид с помощью вектора для внутриклеточной вставки в хромосому. Вставка полинуклеотида в хромосому может быть осуществлена любым способом, известным в данной области техники, например путем гомологичной рекомбинации, но без ограничения этим.
Вектор, применяемый в настоящем изобретении, не имеет конкретных ограничений, может быть применен любой вектор, известный в данной области техники. Примеры обычно применяемых векторов могут включать природные или рекомбинантные плазмиды, космиды, вирусы и бактериофаги. Например, в качестве фагового вектора или космидного вектора могут быть применены pWE15, М13, MBL3, MBL4, IXII, ASHII, APII, t10, t11, Charon4A, Charon21A или тому подобное. В качестве плазмидного вектора могут быть применены система pDZ, система pBR, система pUC, система pBluescript II, система pGEM, система pTZ, система pCL, система рЕТ или тому подобное. В частности, могут быть применены векторы pDZ, pDC, pDCM2, pACYC177, pACYC184, pCL, pECCG117, pUC19, pBR322, pMW118, pCC1BAC или тому подобное.
Например, полинуклеотид, кодирующий интересующий полипептид, может быть вставлен в хромосому с помощью вектора для внутриклеточной вставки в хромосому. Вставка полинуклеотида в хромосому может быть осуществлена любым способом, известным в данной области техники, например путем гомологичной рекомбинации, но без ограничения этим. Вектор может дополнительно содержать селективный маркер для выявления вставки в хромосому. Селективный маркер предназначен для отбора клеток, трансформированных векторами, то есть для выявления вставки интересующей молекулы нуклеиновой кислоты, и могут быть применены маркеры, которые обеспечивают селектируемые фенотипы, такие как устойчивость к лекарственным средствам, ауксотрофия, устойчивость к цитотоксическим агентам или экспрессия поверхностных полипептидов. В среде, обработанной селектирующим агентом, выживают или проявляют другие фенотипические признаки только клетки, экспрессирующие селективный маркер, и, таким образом, могут быть отобраны трансформированные клетки.
В настоящем документе термин «трансформация» означает, что вектор, содержащий полинуклеотид, кодирующий интересующий белок, вводят в клетку-хозяина таким образом, чтобы белок, кодируемый полинуклеотидом, мог быть экспрессирован в клетке-хозяине. Трансформированный полинуклеотид может быть локализован путем вставки в хромосому клетки-хозяина или локализован вне хромосомы при условии, что он может быть экспрессирован в клетке-хозяине. При этом полинуклеотид включает ДНК и РНК, кодирующие интересующий белок. Полинуклеотид может быть введен в любой форме при условии, что он может быть введен в клетку-хозяина и затем экспрессирован. Например, полинуклеотид может быть введен в клетку-хозяина в виде экспрессионной кассеты, которая представляет собой генетическую конструкцию, содержащую все компоненты, необходимые для самостоятельной экспрессии. Экспрессионная кассета обычно может содержать промотор, функционально связанный с полинуклеотидом, сигнал терминации транскрипции, сайт связывания рибосомы и сигнал терминации трансляции. Экспрессионная кассета может быть представлена в форме экспрессионного вектора, способного к саморепликации. Кроме того, полинуклеотид может быть введен в клетку-хозяина в его собственной форме и функционально связан с последовательностью, необходимой для экспрессии в клетке-хозяине, но без ограничения этим.
Способ трансформации вектора согласно настоящему изобретению включает любой способ введения нуклеиновой кислоты в клетку и может быть осуществлен путем выбора соответствующей стандартной методики, известной в данной области техники, в зависимости от клетки-хозяина. Например, указанный способ может включать электропорацию, осаждение фосфатом кальция (CaPO4), осаждение хлоридом кальция (CaCl2), микроинъекцию, метод с применением полиэтиленгликоля (PEG), метод с применением DEAE-декстрана, метод с применением катионных липосом и метод с применением ацетата лития-DMSO и так далее, но без ограничения этим.
При этом в настоящем документе термин «функционально связанный» означает, что полинуклеотидная последовательность с функциональной точки зрения связана с промоторной последовательностью, которая инициирует и опосредует транскрипцию полинуклеотида, кодирующего интересующий белок согласно настоящему изобретению.
В еще одном аспекте настоящего изобретения предложен штамм рода Corynebacterium, содержащий любой один или более из вариантов согласно настоящему изобретению, полинуклеотид согласно настоящему изобретению или вектор согласно настоящему изобретению.
Штамм согласно настоящему изобретению может представлять собой штамм, содержащий любой один или более из вариантов согласно настоящему изобретению, полинуклеотид согласно настоящему изобретению и вектор, содержащий полинуклеотид согласно настоящему изобретению; штамм, модифицированный для экспрессии варианта согласно настоящему изобретению или полинуклеотида согласно настоящему изобретению; штамм (например, рекомбинантный штамм), экспрессирующий вариант согласно настоящему изобретению или полинуклеотид согласно настоящему изобретению; или штамм (например, рекомбинантный штамм), обладающий активностью варианта согласно настоящему изобретению, но без ограничения этим.
Например, штамм согласно настоящему изобретению представляет собой клетку или микроорганизм, трансформированные вектором, содержащим полинуклеотид согласно настоящему изобретению или полинуклеотид, кодирующий вариант ClpC согласно настоящему изобретению, и экспрессирует вариант ClpC согласно настоящему изобретению. Применительно к задачам настоящего изобретения штамм согласно настоящему изобретению может включать все микроорганизмы, обладающие способностью продуцировать аминокислоты с разветвленной цепью вследствие включения варианта ClpC согласно настоящему изобретению. Например, штамм согласно настоящему изобретению может представлять собой рекомбинантный штамм, для получения которого полинуклеотид, кодирующий вариант ClpC согласно настоящему изобретению, вводят в микроорганизм, продуцирующий аминокислоты с разветвленной цепью, с обеспечением экспрессии варианта ClpC, и тем самым усиливают способность продуцировать аминокислоты с разветвленной цепью. Рекомбинантный штамм, обладающий усиленной способностью продуцировать аминокислоты с разветвленной цепью, может представлять собой микроорганизм, обладающий усиленной способностью продуцировать аминокислоты с разветвленной цепью по сравнению с природным микроорганизмом дикого типа или микроорганизмом без модификации ClpC (то есть микроорганизмом, экспрессирующим альдегиддегидрогеназу дикого типа (SEQ ID NO: 5) или микроорганизмом, который не экспрессирует модифицированный белок (SEQ ID NO: 1)), но без ограничения этим. Например, микроорганизм без модификации ClpC, который является целевым штаммом при сравнении увеличения способности продуцировать аминокислоты с разветвленной цепью, может представлять собой штамм СА08-0072 (KCCM11201P, US 8465962 В2) или KCJI-38 (KCCM11248P, патент Кореи №10-1335789), но без ограничения этим.
В настоящем документе термин «немодифицированный микроорганизм» не исключает штаммы, содержащие мутации, которые могут естественным образом встречаться в микроорганизмах, и может обозначать штамм дикого типа или природный штамм как таковой, или может обозначать штамм до изменения признака в результате генетической вариации вследствие действия природных или искусственных факторов. Например, немодифицированный микроорганизм может представлять собой штамм, в который не введен или еще не был введен вариант ClpC, описанный в настоящем документе. Термин «немодифицированный микроорганизм» может использоваться взаимозаменяемо с терминами «штамм до модификации», «микроорганизм до модификации», «неизмененный штамм», «немодифицированный штамм», «неизмененный микроорганизм» или «эталонный микроорганизм».
В еще одном аспекте настоящего изобретения предложен способ получения аминокислот с разветвленной цепью, включающий стадию культивирования в среде микроорганизма рода Corynebacterium, в котором активность АТФ-зависимой протеазы согласно настоящему изобретению ослаблена по сравнению с немодифицированным микроорганизмом, или микроорганизма рода Corynebacterium, содержащего вариант ClpC согласно настоящему изобретению, полинуклеотид, кодирующий вариант ClpC согласно настоящему изобретению, или вектор согласно настоящему изобретению.
В настоящем документе термин «культивирование» означает выращивание микроорганизма рода Corynebacterium согласно настоящему изобретению в надлежащим образом регулируемых условиях среды. Процесс культивирования согласно настоящему изобретению может быть осуществлен с применением подходящей среды и условий культивирования, известных в данной области техники. Такой процесс культивирования может быть легко отрегулирован и применен специалистами в данной области в зависимости от выбранного штамма. В частности, культивирование может представлять собой культивирование периодического типа, непрерывного типа и/или культивирование периодического типа с подпиткой, но без ограничения этим.
В настоящем документе термин «среда» означает смесь веществ, содержащую питательные вещества, необходимые для культивирования микроорганизма рода Corynebacterium согласно настоящему изобретению, в качестве основного компонента, а также среда обеспечивает питательные вещества и факторы роста, включая воду, которые необходимы для выживания и развития. В частности, в качестве среды и других условий культивирования, применяемых для культивирования микроорганизма рода Corynebacterium согласно настоящему изобретению, может быть применена любая среда без конкретных ограничений, при условии, что она представляет собой среду, применяемую для обычного культивирования микроорганизмов. Микроорганизм рода Corynebacterium согласно настоящему изобретению можно культивировать в обычной среде, содержащей надлежащие источники углерода, источники азота, источники фосфора, неорганические соединения, аминокислоты и/или витамины и так далее, при контроле температуры, рН и так далее, в аэробных условиях.
В частности, культуральная среда для штамма рода Corynebacterium описана в документе [«Manual of Methods for General Bacteriology», American Society for Bacteriology (Washington D.C., USA, 1981)].
В настоящем изобретении источники углерода включают углеводы, такие как глюкоза, сахароза, лактоза, фруктоза, сахароза, мальтоза и так далее; сахарные спирты, такие как маннит, сорбит и так далее, органические кислоты, такие как пировиноградная кислота, молочная кислота, лимонная кислота и так далее; аминокислоты, такие как глутаминовая кислота, метионин, лизин и так далее; и тому подобное. Могут быть применены органические питательные вещества природного происхождения, такие как гидролизат крахмала, меласса, сырая меласса, рисовые отруби, маниока, остатки сахарного тростника и кукурузный экстракт. В частности, могут быть применены углеводы, такие как глюкоза и стерилизованная предварительно обработанная меласса (то есть меласса, превращенная в восстанавливающий сахар), а также могут быть применены подходящие количества других источников углерода различными способами без ограничений. Эти источники углерода могут быть использованы в отдельности или в комбинации двух или более из них, но без ограничения этим.
В качестве источников азота могут быть применены неорганические источники азота, такие как аммиак, сульфат аммония, хлорид аммония, ацетат аммония, фосфат аммония, карбонат аммония, нитрат аммония и так далее; а также органические источники азота, такие как аминокислоты, такие как глутаминовая кислота, метионин, глутамин и так далее, пептон, NZ-amine, мясной экстракт, дрожжевой экстракт, экстракт солода, кукурузный экстракт, гидролизат казеина, рыба или продукты ее разложения, а также обезжиренный соевый жмых или продукты его разложения и так далее. Эти источники азота могут быть использованы в отдельности или в комбинации двух или более из них, но без ограничения этим.
Источники фосфора могут включать однозамещенный фосфат калия, двузамещенный фосфат калия или соответствующие им натрийсодержащие соли. В качестве неорганических соединений могут быть применены хлорид натрия, хлорид кальция, хлорид железа, сульфат магния, сульфат железа, сульфат марганца, карбонат кальция и так далее. В дополнение к этим соединениям могут быть включены аминокислоты, витамины и/или подходящие предшественники и так далее. Эти компоненты или предшественники можно добавлять в среду периодически или непрерывно, но без ограничения этим.
Также во время культивирования микроорганизма рода Corynebacterium согласно настоящему изобретению рН среды можно регулировать путем добавления в среду соединений, таких как гидроксид аммония, гидроксид калия, аммиак, фосфорная кислота или серная кислота, надлежащим образом. Во время культивирования пенообразование можно подавлять с помощью противовспенивающего агента, такого как полигликолевый сложный эфир жирной кислоты. В среду может подаваться кислород или кислородсодержащий газ для поддержания аэробного состояния среды, или газ может не подаваться, или может подаваться азот, водород или газообразный диоксид углерода для поддержания анаэробных и микроаэробных условий, но без ограничения этим.
При культивировании согласно настоящему изобретению температура культуры может поддерживаться на уровне 20°С-45°С, в частности 25°С-40°С, и штамм можно культивировать в течение от приблизительно 10 часов до приблизительно 160 часов, но без ограничения этим.
Аминокислоты с разветвленной цепью, продуцируемые при культивировании согласно настоящему изобретению, могут секретироваться в среду или могут оставаться в клетках.
Способ получения аминокислот с разветвленной цепью согласно настоящему изобретению может дополнительно включать стадию получения микроорганизма рода Corynebacterium согласно настоящему изобретению, стадию приготовления среды для культивирования указанного микроорганизма или комбинацию этих стадий (в любом порядке), например, до стадии культивирования.
Способ получения аминокислот с разветвленной цепью согласно настоящему изобретению может дополнительно включать стадию выделения аминокислот с разветвленной цепью из среды в зависимости от культуры (среды, подвергнутой культивированию) или из микроорганизма рода Corynebacterium согласно настоящему изобретению. После стадии культивирования может быть дополнительно включена стадия выделения.
Выделение может представлять собой сбор интересующих аминокислот с разветвленной цепью посредством подходящего способа, известного в данной области техники, в зависимости от способа культивирования микроорганизма согласно настоящему изобретению, например, способа периодического культивирования, непрерывного культивирования или периодического культивирования с подпиткой. Например, могут быть использованы центрифугирование, фильтрование, обработка осадителем для кристаллизации белка (высаливание), экстракция, ультразвуковая дезинтеграция, ультрафильтрация, диализ, различные виды хроматографии, такие как хроматография на молекулярных ситах (гель-фильтрация), адсорбционная хроматография, ионообменная хроматография аффинная хроматография, ВЭЖХ (высокоэффективная жидкостная хроматография), или их комбинация. Интересующие аминокислоты с разветвленной цепью могут быть выделены из среды или из микроорганизма посредством подходящего способа, известного в данной области техники.
Кроме того, способ получения аминокислот с разветвленной цепью согласно настоящему изобретению может дополнительно включать стадию очистки. Очистка может быть выполнена посредством подходящего способа, известного в данной области техники. Например, в случае, когда способ получения аминокислот с разветвленной цепью согласно настоящему изобретению включает как стадию выделения, так и стадию очистки, стадия выделения и стадия очистки могут быть выполнены с перерывами (или непрерывно) независимо от их порядка, или они могут быть выполнены одновременно или путем объединения в одну стадию, но без ограничения этим.
В способе согласно настоящему изобретению вариант, полинуклеотид, вектор, микроорганизм и аминокислота с разветвленной цепью и тому подобное являются такими, как описано в других аспектах.
В еще одном аспекте настоящего изобретения предложена композиция для получения аминокислот с разветвленной цепью, содержащая вариант согласно настоящему изобретению, полинуклеотид, кодирующий указанный вариант, вектор, содержащий указанный полинуклеотид, или микроорганизм согласно настоящему изобретению; среду, в которой культивировали микроорганизм согласно настоящему изобретению; или комбинацию двух или более из указанного.
Композиция согласно настоящему изобретению может дополнительно содержать произвольно выбранные подходящие эксципиенты, обычно используемые в композициях для получения аминокислот с разветвленной цепью. Такие эксципиенты могут представлять собой, например, консервант, смачивающий агент, диспергирующий агент, суспендирующий агент, забуферивающий агент, стабилизатор или изотонический агент, но без ограничения этим.
В композиции согласно настоящему изобретению вариант, полинуклеотид, вектор, штамм, среда, аминокислоты с разветвленной цепью и тому подобное являются такими, как описано в других аспектах.
В еще одном аспекте настоящего изобретения предложено применение микроорганизма рода Corynebacterium, в котором активность АТФ-зависимой протеазы ослаблена по сравнению с немодифицированным микроорганизмом, для получения аминокислот с разветвленной цепью.
В еще одном аспекте настоящего изобретения предложено применение варианта ClpC, в котором удалена аминокислотная последовательность, соответствующая положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5, или полинуклеотида, кодирующего указанный вариант ClpC, для получения аминокислот с разветвленной цепью.
Далее настоящее изобретение будет более подробно описано со ссылкой на иллюстративные воплощения. Однако следующие иллюстративные воплощения являются лишь предпочтительными воплощениями для целей иллюстрации настоящего изобретения и, таким образом, не предназначены для ограничения ими объема настоящего изобретения. При этом технические аспекты, не описанные в настоящем документе, могут быть в достаточной степени поняты и легко воплощены специалистами в области техники, к которой относится настоящее изобретение, или близких областях техники.
Пример 1. Отбор вариантов с усиленной способностью продуцировать L-валин методом искусственной мутации
1-1. Искусственный мутагенез с помощью UV (ультрафиолетового) облучения
Для отбора вариантного штамма, имеющего усиленную способность продуцировать L-валин, Corynebacterium glutamicum СА08-0072 (KCCM11201P, US 8465962 В2), который является продуцирующим L-валин NTG-штаммом, наносили на содержащую агар питательную среду и культивировали при 30°С в течение 36 часов.
Сотни полученных таким образом колоний подвергали UV-облучению при комнатной температуре для индуцирования случайных мутаций в геноме штамма.
Состав питательной среды является следующим.
<Питательная среда (рН 7,2)>
10 г глюкозы, 5 г мясного экстракта, 10 г полипептона, 2,5 г хлорида натрия, 5 г дрожжевого экстракта, 20 г агара, 2 г мочевины (в расчете на 1 л дистиллированной воды).
1-2. Определение титра продукта ферментации штамма, полученного путем мутагенеза, и отбор штамма
Для отбора вариантных штаммов с усиленной способностью продуцировать L-валин по сравнению с Corynebacterium glutamicum СА08-0072, который использовали в качестве родительского штамма в Примере 1-1, осуществляли определение титра продукта ферментации для штаммов с индуцированными случайными мутациями.
В частности, каждую колонию пересевали в питательную среду и каждый штамм высевали в колбу объемом 250 мл с угловыми перегородками, содержащую 25 мл среды для продуцирования, и культивировали при 30°С в течение 72 часов при встряхивании со скоростью 200 об/мин. Составы питательной среды и среды для продуцирования, соответственно, являются следующими.
<Питательная среда (рН 7,2)>
10 г глюкозы, 5 г мясного экстракта, 10 г полипептона, 2,5 г хлорида натрия, 5 г дрожжевого экстракта, 20 г агара, 2 г мочевины (в расчете на 1 л дистиллированной воды).
<Среда для продуцирования (рН 7,0)>
100 г глюкозы, 40 г сульфата аммония, 2,5 г соевого белка, 5 г кукурузного экстракта, 3 г мочевины, 1 г двузамещенного фосфата калия, 0,5 г гептагидрата сульфата магния, 100 мкг биотина, 1 мг тиамин-НСl, 2 мг пантотената кальция, 3 мг никотинамида, 30 г карбоната кальция (в расчете на 1 л дистиллированной воды).
После этого анализировали концентрации L-валина посредством ВЭЖХ, и определенные при анализе концентрации L-валина показаны в таблице 1 ниже.

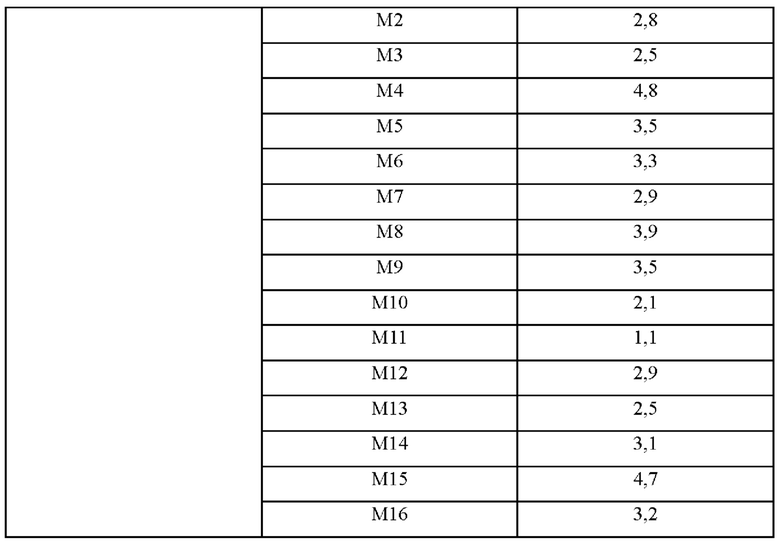
С учетом данных таблицы 1 был выбран штамм М4, который демонстрирует наибольшее увеличение продукции L-валина по сравнению с контрольным штаммом СА08-0072.
Пример 2. Идентификация вариации посредством секвенирования генов
Основные гены штамма М4, продемонстрировавшего усиленную способность продуцировать L-валин в Примере 1, секвенировали и сравнивали с генами штамма СА08-0072 и штамма Corynebacterium glutamicum дикого типа АТСС14067. В результате было подтверждено, что штамм М4 содержит вариацию в определенном положении открытой рамки считывания (ORF) clpC, которая является одной из гексамерных обладающих АТФазной активностью шаперонных субъединиц, составляющих АТФ-зависимую протеазу. В частности, было подтверждено, что штамм М4 имел делецию нуклеотидов в положениях 1291-1299 (SEQ ID NO: 4) в последовательности, представленной SEQ ID NO: 6. Последовательность, представленная SEQ ID NO: 6, представляет собой последовательность, обычно включенную в ORF clpC Corynebacterium glutamicum дикого типа (АТСС14067, АТСС13032 и АТСС13869).
В следующих примерах была предпринята попытка подтвердить влияние указанной вариации на продукцию аминокислот микроорганизмами рода Corynebacterium.
Пример 3. Получение штамма с введенной вариацией и исследование способности продуцировать L-валин
3-1. Получение штамма путем введения вариации в Corynebacterium glutamicum СА08-0072 и оценка способности продуцировать L-валин
Конструировали вектор для введения нуклеотидной последовательности (SEQ ID NO: 2), в которой нуклеотиды в положениях 1291-1299 (SEQ ID NO: 4) в последовательности, представленной SEQ ID NO: 6, были удалены, в продуцирующий L-валин NTG-штамм Corynebacterium glutamicum СА08-0072. В частности, геномную ДНК штамма Corynebacterium glutamicum дикого типа АТСС14067 выделяли с использованием мини-набора для выделения ДНК G-Spin Total DNA Extraction Mini Kit (Intron, Cat. No 17045) в соответствии с протоколом, представленным в наборе. Осуществляли ПЦР (полимеразная цепная реакция) с использованием каждой геномной ДНК в качестве матрицы и праймеров SEQ ID NO: 7 и 8, а также праймеров SEQ ID NO: 9 и 10 с получением фрагментов ДНК (А и В), соответственно. Используемые в этом случае последовательности праймеров представлены в таблице 2 ниже.
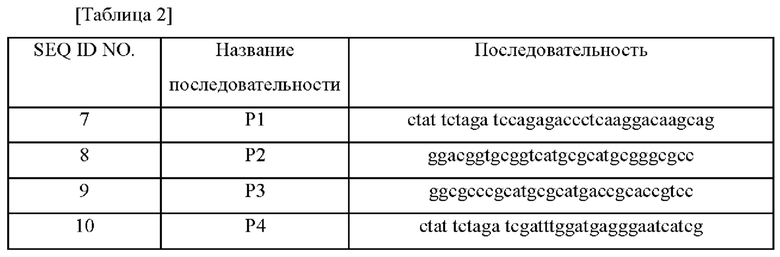
Осуществляли ПЦР с перекрывающимися праймерами с использованием двух указанных фрагментов в качестве матриц и праймеров SEQ ID NO: 7 и 10 с получением продукта ПЦР длиной 1040 п.н. (пар нуклеотидов) (далее в настоящем документе называемого «фрагмент с введенной вариацией»). ПЦР осуществляли следующим образом: денатурация при 94°С в течение 5 минут; 25 циклов денатурации при 94°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 60 секунд; и полимеризация при 72°С в течение 7 минут. Фрагменты с введенной вариацией обрабатывали ферментом рестрикции XbaI (New England Biolabs, Beverly, MA), а затем лигировали с вектором pDZ (патент США №9109242 и международная публикация патента №2008-033001), не способным к репликации в Corynebacterium glutamicum, который был обработан тем же ферментом рестрикции, с использованием лигазы Т4 (New England Biolabs, Beverly, MA). Полученный ген трансформировали в Е. coli DH5α и осуществляли отбор в среде LB, содержащей 25 мг/л канамицина, и получали ДНК с использованием набора для очистки плазмидной ДНК DNA-spin plasmid DNA purification kit (Intron) для конструирования рекомбинантной плазмиды pDZ-clpC_M4.
Полученную описанным выше образом рекомбинантную плазмиду pDZ-clpC_М4 трансформировали в продуцирующий L-валин штамм Corynebacterium glutamicum СА08-0072 путем гомологичной рекомбинации в хромосоме (van der Rest et al., Appl Microbiol Biotechnol 52:541-545, 1999). Штамм, в котором вектор был встроен в хромосому путем гомологичной рекомбинации, отбирали в среде, содержащей 25 мг/л канамицина. Затем осуществляли ПЦР для трансформанта Corynebacterium glutamicum, в котором был завершен вторичный кроссинговер, с использованием праймеров SEQ ID NO: 7 и 10 с получением штамма, в котором была введена вариация в ORF clpC на хромосоме. Рекомбинантный штамм был назван Corynebacterium glutamicum СА08-0072-clpC_М4.
Для сравнения способности продуцировать L-валин между полученным продуцирующим L-валин штаммом Corynebacterium glutamicum СА08-0072 и СА08-0072-clpC_М4 осуществляли определение титра продукта ферментации.
В частности, каждый штамм пересевали в питательную среду и высевали в колбу объемом 250 мл с угловыми перегородками, содержащую 25 мл среды для продуцирования, и культивировали при 30°С в течение 72 часов при встряхивании со скоростью 200 об/мин. Составы питательной среды и среды для продуцирования, соответственно, являются следующими.
<Питательная среда (рН 7,2)>
10 г глюкозы, 5 г мясного экстракта, 10 г полипептона, 2,5 г хлорида натрия, 5 г дрожжевого экстракта, 20 г агара, 2 г мочевины (в расчете на 1 л дистиллированной воды).
<Среда для продуцирования (рН 7,0)>
100 г глюкозы, 40 г сульфата аммония, 2,5 г соевого белка, 5 г кукурузного экстракта, 3 г мочевины, 1 г двузамещенного фосфата калия, 0,5 г гептагидрата сульфата магния, 100 мкг биотина, 1 мг тиамин-НС1, 2 мг пантотената кальция, 3 мг никотинамида, 30 г карбоната кальция (в расчете на 1 л дистиллированной воды).
После этого анализировали концентрации L-валина посредством ВЭЖХ, и определенные при анализе концентрации L-валина показаны в таблице 3 ниже.
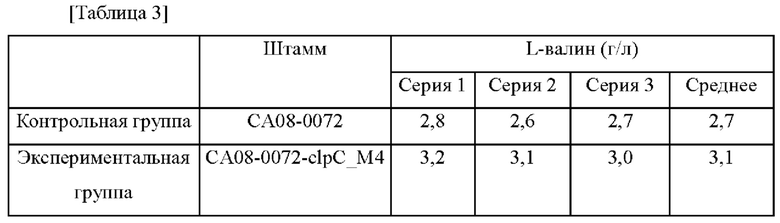
Как показывают результаты, представленные в таблице 3, было подтверждено, что способность штамма CA08-0072-clpC_М4 продуцировать L-валин возрастала на 14% по сравнению с контрольной группой. В результате было подтверждено, что способность продуцировать L-валин может быть улучшена за счет вариации ORF clpC.
CA08-0072-clpC_M4 был назван СА08-1542 и депонирован в Корейском центре культур микроорганизмов в соответствии с Будапештским договором 2 июля 2020 г. под регистрационным номером KCCM12755R
3-2. Получение штамма путем введения вариации в Corynebacterium glutamicum CJ7V и оценка способности продуцировать L-валин
Для проверки того, наблюдается ли такой же эффект у других продуцирующих L-валин штаммов, принадлежащих к виду Corynebacterium glutamicum, один из типов вариации [ilvN(A42V); Biotechnology and Bioprocess Engineering, June 2014, Volume 19, Issue 3, pp 456-467] вводили в штамм Corynebacterium glutamicum дикого типа ATCC14067 с получением штамма с улучшенной способностью продуцировать L-валин.
В частности, геномную ДНК штамма Corynebacterium glutamicum дикого типа АТСС14067 выделяли с помощью мини-набора для выделения ДНК G-Spin Total DNA Extraction Mini Kit. Для конструирования вектора для введения вариации A42V в ген ilvN осуществляли ПЦР с использованием геномной ДНК в качестве матрицы и праймеров SEQ ID NO: 11 и 12, а также праймеров SEQ ID NO: 13 и 14 с получением фрагментов ДНК (А и В), соответственно. Используемые в этом случае последовательности праймеров представлены в таблице 4 ниже.
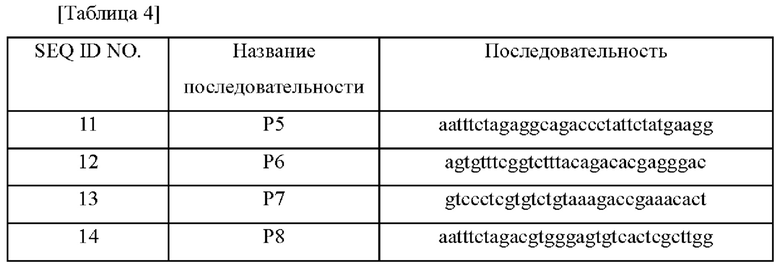
Осуществляли ПЦР с перекрывающимися праймерами с использованием двух указанных фрагментов в качестве матриц и праймеров SEQ ID NO: 11 и 14 с получением продукта ПЦР длиной 1044 п.н. (далее в настоящем документе называемого «фрагмент с введенной вариацией»). ПЦР осуществляли следующим образом: денатурация при 94°С в течение 5 минут; 25 циклов денатурации при 94°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 60 секунд; и полимеризация при 72°С в течение 7 минут. В результате были получены полинуклеотиды длиной 537 п.н. как для фрагмента А, так и для фрагмента В. Полученные таким образом фрагменты с введенной вариацией обрабатывали ферментом рестрикции Xbal, а затем лигировали с вектором pDZ, обработанным тем же ферментом рестрикции, с использованием лигазы Т4. Полученный ген трансформировали в Е. coli DH5α и осуществляли отбор в среде LB, содержащей 25 мг/л канамицина, и получали ДНК с использованием набора для очистки плазмидной ДНК DNA-spin plasmid DNA purification kit. Вектор, предназначенный для введения вариации A42V в ген ilvN, был назван pDZ-ilvN(A42V).
Затем полученную описанным выше образом рекомбинантную плазмиду pDZ-ilvN(A42V) трансформировали в Corynebacterium glutamicum АТСС14067 дикого типа путем гомологичной рекомбинации в хромосоме. Штамм, в котором вектор был встроен в хромосому путем гомологичной рекомбинации, отбирали в среде, содержащей 25 мг/л канамицина. Затем осуществляли ПЦР для трансформанта Corynebacterium glutamicum, в котором был завершен вторичный кроссинговер, с использованием праймеров SEQ ID NO: 11 и 14 для амплификации фрагмента гена, а затем идентифицировали штамм с введенной вариацией путем анализа секвенирования гена. Рекомбинантный штамм, в который была введена вариация, был назван Corynebacterium glutamicum CJ7V.
Corynebacterium glutamicum CJ7V трансформировали посредством pDZ-clpC_M4 таким же образом, как в Примере 3-1, с получением штамма, в котором была введена вариация в ORF clpC, и полученный штамм был назван CJ7V-clpC_M4.
Для сравнения способности полученного штамма продуцировать L-валин указанный штамм культивировали таким же образом, как в Примере 3-1, и анализировали концентрацию L-валина, и определенная при анализе концентрация L-валина приведена в таблице 5 ниже.
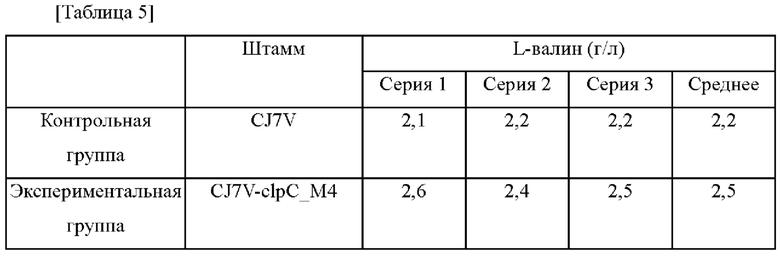
Как показывают результаты, представленные в таблице 5, было подтверждено, что способность штамма CJ7V-clpC_М4 продуцировать L-валин возрастала на 14% по сравнению с контрольной группой. Другими словами, было также подтверждено, что способность микроорганизма рода Corynebacterium продуцировать L-валин может быть улучшена за счет вариации ORF гена clpC.
3-3. Получение штамма путем введения вариации в Corynebacterium glutamicum CJ8V и оценка способности продуцировать L-валин
Для проверки того, наблюдается ли такой же эффект у других продуцирующих L-валин штаммов, принадлежащих виду Corynebacterium glutamicum, один из типов вариации [ilvN(A42V)] вводили в штамм Corynebacterium glutamicum дикого типа АТСС13869 таким же образом, как в Примере 3-2, с получением вариантного штамма, обладающего способностью продуцировать L-валин. Рекомбинантный штамм был назван Corynebacterium glutamicum CJ8V.
Для получения штамма, в котором вариация clpC была введена в Corynebacterium glutamicum CJ8V, рекомбинантный вектор pDZ-clpC_М4, полученный в Примере 3-1, трансформировали в CJ8V. Штамм, в котором вектор был встроен в хромосому путем гомологичной рекомбинации, отбирали в среде, содержащей 25 мг/л канамицина. Затем трансформант Corynebacterium glutamicum, в котором был завершен вторичный кроссинговер, исследовали с использованием праймеров SEQ ID NO: 7 и 10 и идентифицировали штамм с введенной вариацией clpC. Рекомбинантный штамм, идентифицированный описанным выше образом, был назван Corynebacterium glutamicum CJ8V-clpC_М4.
Для сравнения способности полученного штамма продуцировать L-валин указанный штамм культивировали таким же образом, как в Примере 3-1, и анализировали концентрацию L-валина, и определенная при анализе концентрация L-валина приведена в таблице 6 ниже.
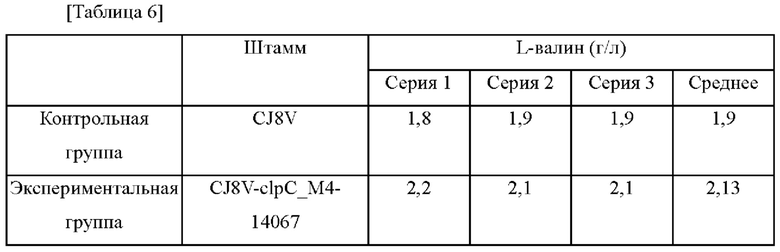
Как показывают результаты, представленные в таблице 6, было подтверждено, что способность штамма CJ8V-clpC_М4 продуцировать L-валин возрастала на 12% по сравнению с контрольной группой. Другими словами, было также подтверждено, что способность микроорганизма рода Corynebacterium продуцировать L-валин может быть улучшена за счет вариации ORF гена clpC.
Пример 4. Получение продуцирующего изолейцин штамма и оценка способности к продуцированию
4-1. Получение штамма путем введения вариации ORF clpC в продуцирующий L-изолейцин штамм Corynebacterium glutamicum KCCM11248P и его оценка
Получали штамм, для получения которого рекомбинантная плазмида pDZ-clpC_М4, полученная в Примере 3-1, была введена в продуцирующий L-изолейцин штамм Corynebacterium glutamicum KCJI-38 (КССМ11248Р, патент США №9885093) таким же образом, как в Примере 3, путем гомологичной рекомбинации в хромосоме, и полученный штамм был назван KCJI-38-clpC_М4. Полученный штамм культивировали описанным ниже способом и осуществляли сравнение его способности продуцировать изолейцин.
В частности, каждый штамм высевали в колбу объемом 250 мл с угловыми перегородками, содержащую 25 мл среды для посева, и культивировали при 30°С в течение 20 часов при встряхивании со скоростью 200 об/мин. Затем 1 мл посевной культуры высевали в колбу объемом 250 мл с угловыми перегородками, содержащую 24 мл среды для продуцирования, и культивировали при 30°С в течение 48 часов при встряхивании со скоростью 200 об/мин. Составы среды для посева и среды для продуцирования, соответственно, являются следующими.
<Среда для посева (рН 7,0)>
20 г глюкозы, 10 г пептона, 5 г дрожжевого экстракта, 1,5 г мочевины, 4 г KH2PO4, 8 г K2HPO4, 0,5 г MgSO47H2O, 100 мкг биотина, 1000 мкг тиамин-HCl, 2000 мкг пантотената кальция, 2000 мкг никотинамида (в расчете на 1 л дистиллированной воды).
<Среда для продуцирования (рН 7,0)>
50 г глюкозы, 12,5 г (NH4)2SO4, 2,5 г соевого белка, 5 г кукурузного экстракта, 3 г мочевины, 1 г KH2PO4, 0,5 г MgSO47H2O, 100 мкг биотина, 1000 мкг тиамин-HCl, 2000 мкг пантотената кальция, 3000 мкг никотинамида, 30 г СаСО3 (в расчете на 1 л дистиллированной воды).
После завершения культивирования определяли способность продуцировать L-изолейцин посредством ВЭЖХ. Концентрации L-изолейцина в культуре каждого исследуемого штамма приведены в таблице 7 ниже.
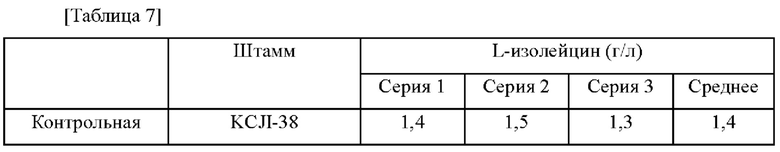

Как показано в таблице 7, было подтверждено, что концентрация L-изолейцина в KCJI-38-clpC_М4, в который был введен вариант clpC, возрастала приблизительно на 55% по сравнению с продуцирующим L-изолейцин штаммом KCJI-38. Это подтвердило, что способность продуцировать L-изолейцин может быть улучшена путем изменения гена clpC. Приведенные выше результаты показывают, что введение вариации ORF clpC в продуцирующий L-изолейцин штамм рода Corynebacterium является эффективным в отношении продукции L-изолейцина.
KCJI-38-с1рС_М4 был назван СА10-3123 и депонирован в Корейском центре культур микроорганизмов в соответствии с Будапештским договором 1 декабря 2020 г. под регистрационным номером KCCM12858R
4-2. Получение продуцирующего L-изолейцин штамма путем введения вариации ORF clpC в штамм Corynebacterium glutamicum дикого типа АТСС13032 и оценка способности продуцировать L-изолейцин
Для оценки влияния введения вариации clpC-M4 на способность продуцировать L-изолейцин получали штаммы путем введения в штамм Corynebacterium glutamicum АТСС13032 (далее называемый WT (дикий тип)) известного варианта аспартокиназы (lysC(L377K)) (US 10662450 В2), варианта гомосериндегидрогеназы (hom(R407H)) (Appl. Microbiol. Biotechnol. 45, 612-620 (1996)) или варианта L-треониндегидратазы (ilvA(V323A)) (Appl. Enviro. Microbiol., Dec. 1996, p.4345-4351) и сравнивали их способность продуцировать L-изолейцин.
В частности, ПЦР осуществляли с использованием хромосомы WT в качестве матрицы и праймеров SEQ ID NO: 15 и 16 или SEQ ID NO: 17 и 18. Используемые в этом случае последовательности праймеров представлены в таблице 8 ниже.
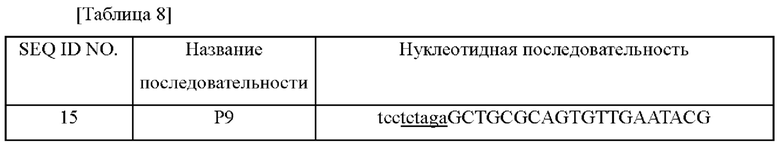
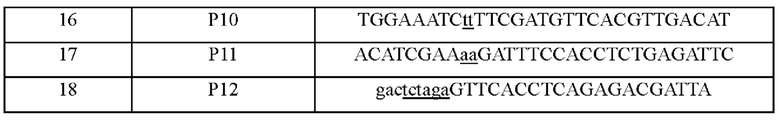
ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 30 секунд; и полимеризация при 72°С в течение 7 минут. В результате были получены, соответственно, вышележащий фрагмент ДНК длиной 509 п.н. с 5'-конца и нижележащий фрагмент ДНК длиной 520 п.н. с 3'-конца гена, к центру относительно которых расположена вариация гена lysC. Осуществляли ПЦР с использованием двух указанных амплифицированных фрагментов ДНК в качестве матриц и праймеров SEQ ID NO: 15 и 18. ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 30 секунд; и полимеризация при 72°С в течение 7 минут. В результате был амплифицирован фрагмент ДНК длиной 1011 п.н., содержащий вариацию гена lysC (L377K), кодирующий вариант аспартокиназы, в котором лейцин в положении 377 заменен на лизин. Вектор pDZ и амплифицированный фрагмент ДНК длиной 1011 п.н. обрабатывали ферментом рестрикции XbaI, лигировали с использованием ДНК-лигазы и затем клонировали с получением плазмиды, названной pDZ-lysC (L377K).
Полученный описанным выше образом вектор pDZ-lysC (L377K) вводили в штамм WT методом, включающим применение электрических импульсов (Appl. Microbiol. Biothcenol. (1999, 52:541-545)), и затем получали трансформированный штамм в селективной среде, содержащей 25 мг/л канамицина. Был получен штамм WT::lysC (L377K), в котором нуклеотидная вариация была введена в ген lysC с помощью фрагмента ДНК, встроенного в хромосому в процессе вторичной рекомбинации.
Кроме того, для получения вектора для введения horn (R407H) осуществляли ПЦР с использованием геномной ДНК дикого типа в качестве матрицы и праймеров SEQ ID NO: 19 и 20, а также SEQ ID NO: 21 и 22. Используемые в этом случае последовательности праймеров представлены в таблице 9 ниже.

ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 30 секунд; и полимеризация при 72°С в течение 7 минут. В результате были получены, соответственно, вышележащий фрагмент ДНК длиной 220 п.н. с 5'-конца и нижележащий фрагмент ДНК длиной 220 п.н. с 3'-конца гена, к центру относительно которых расположена вариация гена hom. Осуществляли ПЦР с использованием двух указанных амплифицированных фрагментов ДНК в качестве матриц и праймеров SEQ ID NO: 19 и 20. ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 30 секунд; и полимеризация при 72°С в течение 7 минут. В результате был амплифицирован фрагмент ДНК длиной 440 п.н., содержащий вариацию гена hom. Применяемый описанным выше образом вектор pDZ и амплифицированный фрагмент ДНК длиной 440 п.н. обрабатывали ферментом рестрикции XbaI, лигировали с использованием ДНК-лигазы и затем клонировали с получением плазмиды, названной pDZ-hom(R407H).
Полученный описанным выше образом вектор pDZ-hom(R407H) вводили в штамм WT::lysC(L377K) методом, включающим применение электрических импульсов, и затем получали трансформированный штамм в селективной среде, содержащей 25 мг/л канамицина. Был получен штамм WT::lysC(L377K)-hom(R407H), в котором нуклеотидная вариация была введена в ген hom с помощью фрагмента ДНК, встроенного в хромосому в процессе вторичной рекомбинации.
Таким же образом, как в приведенном выше Примере, получали штамм путем введения рекомбинантной плазмиды pDZ-clpC_M4, полученной в Примере 3-1, в штамм WT::lysC(L377K)-hom(R407H) путем гомологичной рекомбинации в хромосоме, и полученный штамм был назван WT::lysC(L377K)-hom(R407H)-clpC М4.
При этом для получения вектора, в котором известная вариация ilvA(V323A) (S. Morbach et al., Appl. Enviro. Microbiol., 62(12): 4345-4351, 1996) была введена в ген ilvA, конструировали пару праймеров (SEQ ID NO: 23 и 24) для амплификации вышележащего фрагмента с 5'-конца и пару праймеров (SEQ ID NO: 25 и 26) для амплификации нижележащего фрагмента с 3'-конца, соответственно, к центру относительно которых расположена вариация. В праймеры SEQ ID NO: 23 и 26 был введен сайт рестрикции BamHI (подчеркнут) на каждом конце. В праймерах SEQ ID NO: 24 и 25 вариацию с нуклеотидной заменой (подчеркнута) помещали в сайт, который был сконструирован так, чтобы указанные области пересекались друг с другом. Сконструированные в этом случае последовательности праймеров представлены в таблице 10 ниже.
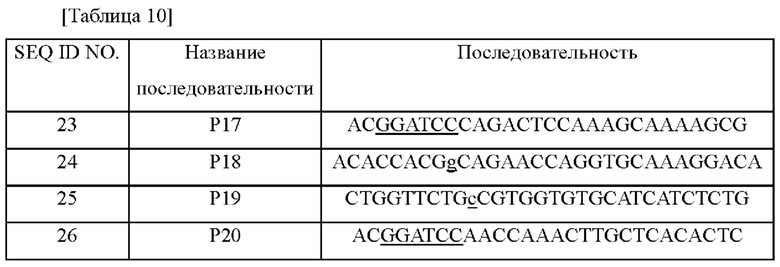
ПЦР осуществляли с использованием хромосомы WT в качестве матрицы и праймеров SEQ ID NO: 23 и SEQ ID NO: 24, SEQ ID NO: 25 и SEQ ID NO: 26. ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 30 секунд; и полимеризация при 72°С в течение 7 минут. В результате были получены, соответственно, вышележащий фрагмент ДНК длиной 627 п.н. с 5'-конца и нижележащий фрагмент ДНК длиной 608 п.н. с 3'-конца гена, к центру относительно которых расположена вариация гена ilvA. Осуществляли ПЦР с использованием двух указанных амплифицированных фрагментов ДНК в качестве матриц и праймеров SEQ ID NO: 23 и 26. ПЦР осуществляли следующим образом: денатурация при 95°С в течение 5 минут; 30 циклов денатурации при 95°С в течение 30 секунд, отжига при 55°С в течение 30 секунд и полимеризации при 72°С в течение 60 секунд; и полимеризация при 72°С в течение 7 минут. В результате был амплифицирован фрагмент ДНК размером 1217 п.н., содержащий вариацию гена ilvA, кодирующий вариант IlvA, в котором L-валин в положении 323 заменен на аланин. Вектор pECCG117 (патент Кореи №10-0057684) и фрагмент ДНК длиной 1217 п.н. обрабатывали рестрикционным ферментом BamHI, лигировали с использованием ДНК-лигазы и клонировали с получением плазмиды, названной pECCG117-ilvA (V323A).
Штамм ATCC13032::hom(R407H)-lysC(L377K)-clpC/pECCG117-ilvA(V323A) получали путем введения вектора pECCG117-ilvA(V323A) в ATCC13032::hom(R407H)-lysC(L377K)-clpC_М4 согласно приведенному выше Примеру. Также в качестве контроля получали штамм путем введения только вариации ilvA(V323A) в ATCC13032::-hom(R407H)-lysC(L377K).
Полученные штаммы культивировали таким же образом, как и в методе культивирования в колбах в Примере 4-1, и определяли концентрации L-изолейцина в культурах. Результаты определения концентрации L-изолейцина в культурах штаммов приведены в таблице 11 ниже.
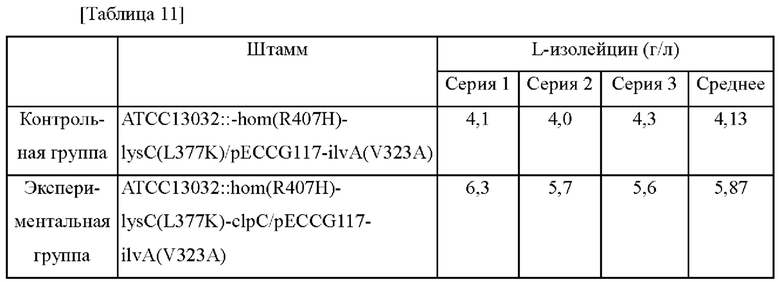
Как показано в таблице 11, было подтверждено, что по сравнению с ATCC13032::-hom(R407H)-lysC(L377K)/pECCG117-ilvA(V323A), для получения которого в ATCC13032::-hom(R407H)-lysC(L377K) была введена только вариация ilvA(V323A), АТСС13032::hom(R407H)-lysC(L377K)-clpC_M4/pECCG117-ilvA(V323A), в который была дополнительно введена вариация clpC_М4, продемонстрировал увеличение концентрации L-изолейцина приблизительно на 42%. Приведенные выше результаты показывают, что введение вариации clpC в продуцирующий L-изолейцин штамм рода Corynebacterium является эффективным в отношении продукции L-изолейцина.
На основании приведенного выше описания специалистам в данной области техники будет понятно, что настоящее изобретение может быть воплощено в другой конкретной форме без изменения его технической сущности или основных характеристик. В связи с этим следует понимать, что приведенное выше воплощение является не ограничивающим, а иллюстративным во всех аспектах. Объем настоящего изобретения определяется прилагаемой формулой изобретения, а не предшествующим ей описанием, и, следовательно, все изменения и модификации, находящиеся в рамках формулы изобретения, или эквиваленты таких пределов должны рассматриваться как охватываемые формулой изобретения.
Эффект изобретения
Микроорганизм согласно настоящему изобретению может с высокой эффективностью продуцировать аминокислоты с разветвленной цепью. Кроме того, полученные аминокислоты с разветвленной цепью могут быть применены в различных продуктах, таких как фармацевтическое сырье и пищевые добавки, корма для животных, питательные вещества, пестициды, бактерицидные агенты и так далее.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CJ CheilJedang Corporation
<120> Мутантная АТФ-зависимая протеаза и
способ получения L-аминокислоты с ее
применением
<130> OPA21217
<150> KR 10-2020-0173802
<151> 2020-12-11
<160> 26
<170> KoPatentIn 3.0
<210> 1
<211> 922
<212> PRT
<213> Artificial Sequence
<220>
<223> Вариант ClpC ORF AA
<400> 1
Met Phe Glu Arg Phe Thr Asp Arg Ala Arg Arg Val Ile Val Leu Ala
1 5 10 15
Gln Glu Glu Ala Arg Met Leu Asn His Asn Tyr Ile Gly Thr Glu His
20 25 30
Ile Leu Leu Gly Leu Ile His Glu Gly Glu Gly Val Ala Ala Lys Ala
35 40 45
Leu Glu Ser Met Gly Ile Ser Leu Asp Ala Val Arg Gln Glu Val Glu
50 55 60
Glu Ile Ile Gly Gln Gly Ser Gln Pro Thr Thr Gly His Ile Pro Phe
65 70 75 80
Thr Pro Arg Ala Lys Lys Val Leu Glu Leu Ser Leu Arg Glu Gly Leu
85 90 95
Gln Met Gly His Lys Tyr Ile Gly Thr Glu Phe Leu Leu Leu Gly Leu
100 105 110
Ile Arg Glu Gly Glu Gly Val Ala Ala Gln Val Leu Val Lys Leu Gly
115 120 125
Ala Asp Leu Pro Arg Val Arg Gln Gln Val Ile Gln Leu Leu Ser Gly
130 135 140
Tyr Glu Gly Gly Gln Gly Gly Ser Pro Glu Gly Gly Gln Gly Ala Pro
145 150 155 160
Thr Gly Gly Asp Ala Val Gly Ala Gly Ala Ala Pro Gly Gly Arg Pro
165 170 175
Ser Ser Gly Gly Pro Gly Glu Arg Ser Thr Ser Leu Val Leu Asp Gln
180 185 190
Phe Gly Arg Asn Leu Thr Gln Ala Ala Lys Asp Gly Lys Leu Asp Pro
195 200 205
Val Val Gly Arg Asp Lys Glu Ile Glu Arg Ile Met Gln Val Leu Ser
210 215 220
Arg Arg Thr Lys Asn Asn Pro Val Leu Ile Gly Glu Pro Gly Val Gly
225 230 235 240
Lys Thr Ala Val Val Glu Gly Leu Ala Leu Asp Ile Val Asn Gly Lys
245 250 255
Val Pro Glu Thr Leu Lys Asp Lys Gln Val Tyr Ser Leu Asp Leu Gly
260 265 270
Ser Leu Val Ala Gly Ser Arg Tyr Arg Gly Asp Phe Glu Glu Arg Leu
275 280 285
Lys Lys Val Leu Lys Glu Ile Asn Gln Arg Gly Asp Ile Ile Leu Phe
290 295 300
Ile Asp Glu Ile His Thr Leu Val Gly Ala Gly Ala Ala Glu Gly Ala
305 310 315 320
Ile Asp Ala Ala Ser Leu Leu Lys Pro Lys Leu Ala Arg Gly Glu Leu
325 330 335
Gln Thr Ile Gly Ala Thr Thr Leu Asp Glu Tyr Arg Lys His Ile Glu
340 345 350
Lys Asp Ala Ala Leu Glu Arg Arg Phe Gln Pro Val Gln Val Pro Glu
355 360 365
Pro Ser Val Asp Leu Thr Val Glu Ile Leu Lys Gly Leu Arg Asp Arg
370 375 380
Tyr Glu Ala His His Arg Val Ser Ile Thr Asp Gly Ala Leu Thr Ala
385 390 395 400
Ala Ala Gln Leu Ala Asp Arg Tyr Ile Asn Asp Arg Phe Leu Pro Asp
405 410 415
Lys Ala Val Asp Leu Ile Asp Glu Ala Gly Ala Arg Met Arg Met Thr
420 425 430
Ala Pro Ser Ser Leu Arg Glu Val Asp Glu Arg Ile Ala Asp Val Arg
435 440 445
Arg Glu Lys Glu Ala Ala Ile Asp Ala Gln Asp Phe Glu Lys Ala Ala
450 455 460
Gly Leu Arg Asp Lys Glu Arg Lys Leu Gly Glu Glu Arg Ser Glu Lys
465 470 475 480
Glu Lys Gln Trp Arg Ser Gly Asp Leu Glu Asp Ile Ala Glu Val Gly
485 490 495
Glu Glu Gln Ile Ala Glu Val Leu Ala Asn Trp Thr Gly Ile Pro Val
500 505 510
Phe Lys Leu Thr Glu Ala Glu Ser Ser Arg Leu Leu Asn Met Glu Glu
515 520 525
Glu Leu His Lys Arg Ile Ile Gly Gln Asp Glu Ala Val Lys Ala Val
530 535 540
Ser Arg Ala Ile Arg Arg Thr Arg Ala Gly Leu Lys Asp Pro Lys Arg
545 550 555 560
Pro Ser Gly Ser Phe Ile Phe Ala Gly Pro Ser Gly Val Gly Lys Thr
565 570 575
Glu Leu Ser Lys Ala Leu Ala Gly Phe Leu Phe Gly Asp Asp Asp Ser
580 585 590
Leu Ile Gln Ile Asp Met Gly Glu Phe His Asp Arg Phe Thr Ala Ser
595 600 605
Arg Leu Phe Gly Ala Pro Pro Gly Tyr Val Gly Tyr Glu Glu Gly Gly
610 615 620
Gln Leu Thr Glu Lys Val Arg Arg Lys Pro Phe Ser Val Val Leu Phe
625 630 635 640
Asp Glu Ile Glu Lys Ala His Lys Glu Ile Tyr Asn Thr Leu Leu Gln
645 650 655
Val Leu Glu Asp Gly Arg Leu Thr Asp Gly Gln Gly Arg Ile Val Asp
660 665 670
Phe Lys Asn Thr Val Leu Ile Phe Thr Ser Asn Leu Gly Thr Ser Asp
675 680 685
Ile Ser Lys Ala Val Gly Leu Gly Phe Ser Gly Ser Ser Glu Thr Asp
690 695 700
Ser Asp Ala Gln Tyr Asp Arg Met Lys Asn Lys Val His Asp Glu Leu
705 710 715 720
Lys Lys His Phe Arg Pro Glu Phe Leu Asn Arg Ile Asp Glu Ile Val
725 730 735
Val Phe His Gln Leu Thr Lys Asp Gln Ile Val Gln Met Val Asp Leu
740 745 750
Leu Ile Gly Arg Val Ser Asn Ala Leu Ala Glu Lys Asp Met Ser Ile
755 760 765
Glu Leu Thr Glu Lys Ala Lys Asp Leu Leu Ala Ser Arg Gly Phe Asp
770 775 780
Pro Val Leu Gly Ala Arg Pro Leu Arg Arg Thr Ile Gln Arg Glu Ile
785 790 795 800
Glu Asp Gln Met Ser Glu Lys Ile Leu Phe Gly Glu Ile Gly Ala Gly
805 810 815
Glu Ile Val Thr Val Asp Val Glu Gly Trp Asp Gly Glu Ser Lys Asp
820 825 830
Thr Asp Arg Ala Lys Phe Thr Phe Thr Pro Arg Pro Lys Pro Met Pro
835 840 845
Glu Gly Lys Phe Ser Glu Ile Ser Val Gln Ala Ala Glu Ala Ile Gln
850 855 860
Asp Val Asp Ser Ala Ala Asp Gly Asp Val Pro Glu Thr Asp Ser Leu
865 870 875 880
Ser Asp Ile Asp Leu Glu Thr Leu Glu Lys Phe Glu Glu Asp Val Glu
885 890 895
Asn Gly Thr Asp Ile Asp Gln Val Ser Gly Asp Tyr Tyr Gly Thr Asp
900 905 910
Asp Gln Gly Gly Thr Ala Pro Ser Lys Glu
915 920
<210> 2
<211> 2769
<212> DNA
<213> Artificial Sequence
<220>
<223> Вариант clpC ORF NT
<400> 2
atgttcgaga ggtttaccga tcgtgcacgc cgcgtgattg tgctcgcgca ggaagaggcg 60
cgcatgctca accacaatta catcggcacg gagcacattc tcctcggcct cattcacgag 120
ggcgagggcg ttgcagccaa ggctttggaa tccatgggaa tttccctgga cgccgtccgc 180
caggaagtcg aagagattat cggccagggc tcccagccca ccaccggcca cattcctttt 240
actccacgtg ccaagaaggt cctggagctc agcctccgcg agggactaca gatgggacac 300
aagtacatcg gtactgagtt cctgcttctc ggtttgatcc gtgagggcga gggcgttgct 360
gcccaggtcc tggtcaagct tggtgctgat ctgccacgcg tgcgtcagca agttattcag 420
cttctctccg gctacgaagg tggccagggc ggatccccag agggcggtca gggcgcccct 480
actggcggtg acgctgttgg tgcaggagct gctcctggcg gtcgtccatc ttcgggcggc 540
ccaggcgagc gttctacctc tttggttctt gaccagttcg gccgcaacct cacccaggcc 600
gcaaaggacg gcaagctgga cccagttgtt ggtcgtgata aggaaatcga gcgcatcatg 660
caggtgctct cccgtcgtac caagaacaac ccagttctta ttggtgagcc aggtgttggt 720
aagaccgcag ttgttgaagg tcttgcacta gacattgtta acggcaaggt tccagagacc 780
ctcaaggaca agcaggttta ctcccttgac ttaggttcac tggttgcagg ttcccgttac 840
cgcggtgact tcgaagagcg cctgaagaag gtcctcaagg agattaacca gcgcggcgac 900
atcatcctgt ttatcgatga gatccacacc ctcgtgggtg caggtgcagc agaaggcgca 960
atcgacgccg cctccctgct taagccaaag cttgcccgcg gtgaactgca gaccattggt 1020
gcaaccacct tggacgagta ccgtaagcac attgaaaagg acgcagctct tgagcgtcgt 1080
ttccagccag tgcaggttcc agagccttcg gttgatctca ccgttgagat cttgaagggt 1140
ctgcgcgacc gctacgaagc tcaccaccgc gtatccatca ccgatggtgc tcttaccgca 1200
gcagctcagc ttgctgatcg ctacattaac gaccgcttct tgccagataa ggccgttgac 1260
ctcatcgatg aggctggcgc ccgcatgcgc atgaccgcac cgtcctccct ccgcgaggtt 1320
gatgagcgca tcgctgatgt tcgccgtgag aaggaagcag cgatcgatgc tcaggacttt 1380
gagaaggcag caggtcttcg cgataaggag cgcaagctcg gcgaagagcg ttcagagaag 1440
gaaaagcagt ggcgctccgg cgacctcgag gacattgctg aggttggcga agagcagatc 1500
gcagaagtac tggccaactg gactggtatt cctgtcttca agctcaccga agctgagtct 1560
tcccgcctgc tcaacatgga agaagagttg cacaagcgca tcatcggaca ggatgaagct 1620
gtcaaggctg tctcccgtgc gatccgtcgt acccgtgcag gtctgaagga tcctaagcgt 1680
ccttccggct ccttcatctt cgctggtcca tccggtgttg gtaagaccga gctgtccaag 1740
gcacttgctg gattcctctt cggtgacgat gattccctca tccaaatcga catgggtgaa 1800
ttccacgacc gcttcaccgc gtcccgactc ttcggtgccc ctccgggata cgttggctac 1860
gaagaaggtg gccagctgac cgagaaggtt cgccgtaagc cattctccgt tgtgcttttc 1920
gacgagatcg agaaggccca caaggagatc tacaacacct tgctgcaggt gttggaagat 1980
ggtcgcctta ccgatggtca gggtcgcatt gtggacttca agaacaccgt cctgatcttc 2040
acctccaacc tgggcacctc tgacatctcc aaggctgttg gcctgggctt ctccggatcc 2100
tctgagactg acagcgatgc tcagtacgac cgcatgaaga acaaggtcca cgacgagctg 2160
aagaagcact tccgccctga gttcctgaac cgtattgatg agatcgtggt cttccaccag 2220
ctcaccaagg atcagatcgt tcagatggtc gaccttctta ttggccgcgt gtccaacgca 2280
ctggctgaga aggacatgag catcgaactg actgagaagg ctaaggatct ccttgccagc 2340
cgcggcttcg atccagttct gggtgcacga ccattgcgtc gcaccattca gcgcgaaatc 2400
gaagaccaga tgtccgagaa gatcctcttc ggagaaatcg gtgctggcga gatcgtcacc 2460
gtcgacgtcg aaggctggga cggcgagtcc aaggacaccg accgtgcgaa gttcaccttc 2520
acaccacgtc caaagccaat gccagaaggt aagttctctg agatctccgt acaggctgca 2580
gaagcaatcc aagatgtaga ttccgcagct gacggcgatg tcccagaaac cgattcactt 2640
tccgacattg accttgaaac ccttgagaag ttcgaggaag atgtagaaaa cggcaccgac 2700
attgatcagg tatccggtga ctactacggc accgatgatc agggaggcac tgctccaagc 2760
aaggagtag 2769
<210> 3
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> 431~433 AA
<400> 3
Ile Lys Arg
1
<210> 4
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> 1291~1299 NT
<400> 4
atcaagcgc 9
<210> 5
<211> 925
<212> PRT
<213> Unknown
<220>
<223> ORF WT AA ClpC
<400> 5
Met Phe Glu Arg Phe Thr Asp Arg Ala Arg Arg Val Ile Val Leu Ala
1 5 10 15
Gln Glu Glu Ala Arg Met Leu Asn His Asn Tyr Ile Gly Thr Glu His
20 25 30
Ile Leu Leu Gly Leu Ile His Glu Gly Glu Gly Val Ala Ala Lys Ala
35 40 45
Leu Glu Ser Met Gly Ile Ser Leu Asp Ala Val Arg Gln Glu Val Glu
50 55 60
Glu Ile Ile Gly Gln Gly Ser Gln Pro Thr Thr Gly His Ile Pro Phe
65 70 75 80
Thr Pro Arg Ala Lys Lys Val Leu Glu Leu Ser Leu Arg Glu Gly Leu
85 90 95
Gln Met Gly His Lys Tyr Ile Gly Thr Glu Phe Leu Leu Leu Gly Leu
100 105 110
Ile Arg Glu Gly Glu Gly Val Ala Ala Gln Val Leu Val Lys Leu Gly
115 120 125
Ala Asp Leu Pro Arg Val Arg Gln Gln Val Ile Gln Leu Leu Ser Gly
130 135 140
Tyr Glu Gly Gly Gln Gly Gly Ser Pro Glu Gly Gly Gln Gly Ala Pro
145 150 155 160
Thr Gly Gly Asp Ala Val Gly Ala Gly Ala Ala Pro Gly Gly Arg Pro
165 170 175
Ser Ser Gly Gly Pro Gly Glu Arg Ser Thr Ser Leu Val Leu Asp Gln
180 185 190
Phe Gly Arg Asn Leu Thr Gln Ala Ala Lys Asp Gly Lys Leu Asp Pro
195 200 205
Val Val Gly Arg Asp Lys Glu Ile Glu Arg Ile Met Gln Val Leu Ser
210 215 220
Arg Arg Thr Lys Asn Asn Pro Val Leu Ile Gly Glu Pro Gly Val Gly
225 230 235 240
Lys Thr Ala Val Val Glu Gly Leu Ala Leu Asp Ile Val Asn Gly Lys
245 250 255
Val Pro Glu Thr Leu Lys Asp Lys Gln Val Tyr Ser Leu Asp Leu Gly
260 265 270
Ser Leu Val Ala Gly Ser Arg Tyr Arg Gly Asp Phe Glu Glu Arg Leu
275 280 285
Lys Lys Val Leu Lys Glu Ile Asn Gln Arg Gly Asp Ile Ile Leu Phe
290 295 300
Ile Asp Glu Ile His Thr Leu Val Gly Ala Gly Ala Ala Glu Gly Ala
305 310 315 320
Ile Asp Ala Ala Ser Leu Leu Lys Pro Lys Leu Ala Arg Gly Glu Leu
325 330 335
Gln Thr Ile Gly Ala Thr Thr Leu Asp Glu Tyr Arg Lys His Ile Glu
340 345 350
Lys Asp Ala Ala Leu Glu Arg Arg Phe Gln Pro Val Gln Val Pro Glu
355 360 365
Pro Ser Val Asp Leu Thr Val Glu Ile Leu Lys Gly Leu Arg Asp Arg
370 375 380
Tyr Glu Ala His His Arg Val Ser Ile Thr Asp Gly Ala Leu Thr Ala
385 390 395 400
Ala Ala Gln Leu Ala Asp Arg Tyr Ile Asn Asp Arg Phe Leu Pro Asp
405 410 415
Lys Ala Val Asp Leu Ile Asp Glu Ala Gly Ala Arg Met Arg Ile Lys
420 425 430
Arg Met Thr Ala Pro Ser Ser Leu Arg Glu Val Asp Glu Arg Ile Ala
435 440 445
Asp Val Arg Arg Glu Lys Glu Ala Ala Ile Asp Ala Gln Asp Phe Glu
450 455 460
Lys Ala Ala Gly Leu Arg Asp Lys Glu Arg Lys Leu Gly Glu Glu Arg
465 470 475 480
Ser Glu Lys Glu Lys Gln Trp Arg Ser Gly Asp Leu Glu Asp Ile Ala
485 490 495
Glu Val Gly Glu Glu Gln Ile Ala Glu Val Leu Ala Asn Trp Thr Gly
500 505 510
Ile Pro Val Phe Lys Leu Thr Glu Ala Glu Ser Ser Arg Leu Leu Asn
515 520 525
Met Glu Glu Glu Leu His Lys Arg Ile Ile Gly Gln Asp Glu Ala Val
530 535 540
Lys Ala Val Ser Arg Ala Ile Arg Arg Thr Arg Ala Gly Leu Lys Asp
545 550 555 560
Pro Lys Arg Pro Ser Gly Ser Phe Ile Phe Ala Gly Pro Ser Gly Val
565 570 575
Gly Lys Thr Glu Leu Ser Lys Ala Leu Ala Gly Phe Leu Phe Gly Asp
580 585 590
Asp Asp Ser Leu Ile Gln Ile Asp Met Gly Glu Phe His Asp Arg Phe
595 600 605
Thr Ala Ser Arg Leu Phe Gly Ala Pro Pro Gly Tyr Val Gly Tyr Glu
610 615 620
Glu Gly Gly Gln Leu Thr Glu Lys Val Arg Arg Lys Pro Phe Ser Val
625 630 635 640
Val Leu Phe Asp Glu Ile Glu Lys Ala His Lys Glu Ile Tyr Asn Thr
645 650 655
Leu Leu Gln Val Leu Glu Asp Gly Arg Leu Thr Asp Gly Gln Gly Arg
660 665 670
Ile Val Asp Phe Lys Asn Thr Val Leu Ile Phe Thr Ser Asn Leu Gly
675 680 685
Thr Ser Asp Ile Ser Lys Ala Val Gly Leu Gly Phe Ser Gly Ser Ser
690 695 700
Glu Thr Asp Ser Asp Ala Gln Tyr Asp Arg Met Lys Asn Lys Val His
705 710 715 720
Asp Glu Leu Lys Lys His Phe Arg Pro Glu Phe Leu Asn Arg Ile Asp
725 730 735
Glu Ile Val Val Phe His Gln Leu Thr Lys Asp Gln Ile Val Gln Met
740 745 750
Val Asp Leu Leu Ile Gly Arg Val Ser Asn Ala Leu Ala Glu Lys Asp
755 760 765
Met Ser Ile Glu Leu Thr Glu Lys Ala Lys Asp Leu Leu Ala Ser Arg
770 775 780
Gly Phe Asp Pro Val Leu Gly Ala Arg Pro Leu Arg Arg Thr Ile Gln
785 790 795 800
Arg Glu Ile Glu Asp Gln Met Ser Glu Lys Ile Leu Phe Gly Glu Ile
805 810 815
Gly Ala Gly Glu Ile Val Thr Val Asp Val Glu Gly Trp Asp Gly Glu
820 825 830
Ser Lys Asp Thr Asp Arg Ala Lys Phe Thr Phe Thr Pro Arg Pro Lys
835 840 845
Pro Met Pro Glu Gly Lys Phe Ser Glu Ile Ser Val Gln Ala Ala Glu
850 855 860
Ala Ile Gln Asp Val Asp Ser Ala Ala Asp Gly Asp Val Pro Glu Thr
865 870 875 880
Asp Ser Leu Ser Asp Ile Asp Leu Glu Thr Leu Glu Lys Phe Glu Glu
885 890 895
Asp Val Glu Asn Gly Thr Asp Ile Asp Gln Val Ser Gly Asp Tyr Tyr
900 905 910
Gly Thr Asp Asp Gln Gly Gly Thr Ala Pro Ser Lys Glu
915 920 925
<210> 6
<211> 2778
<212> DNA
<213> Unknown
<220>
<223> ORF WT NT clpC
<400> 6
atgttcgaga ggtttaccga tcgtgcacgc cgcgtgattg tgctcgcgca ggaagaggcg 60
cgcatgctca accacaatta catcggcacg gagcacattc tcctcggcct cattcacgag 120
ggcgagggcg ttgcagccaa ggctttggaa tccatgggaa tttccctgga cgccgtccgc 180
caggaagtcg aagagattat cggccagggc tcccagccca ccaccggcca cattcctttt 240
actccacgtg ccaagaaggt cctggagctc agcctccgcg agggactaca gatgggacac 300
aagtacatcg gtactgagtt cctgcttctc ggtttgatcc gtgagggcga gggcgttgct 360
gcccaggtcc tggtcaagct tggtgctgat ctgccacgcg tgcgtcagca agttattcag 420
cttctctccg gctacgaagg tggccagggc ggatccccag agggcggtca gggcgcccct 480
actggcggtg acgctgttgg tgcaggagct gctcctggcg gtcgtccatc ttcgggcggc 540
ccaggcgagc gttctacctc tttggttctt gaccagttcg gccgcaacct cacccaggcc 600
gcaaaggacg gcaagctgga cccagttgtt ggtcgtgata aggaaatcga gcgcatcatg 660
caggtgctct cccgtcgtac caagaacaac ccagttctta ttggtgagcc aggtgttggt 720
aagaccgcag ttgttgaagg tcttgcacta gacattgtta acggcaaggt tccagagacc 780
ctcaaggaca agcaggttta ctcccttgac ttaggttcac tggttgcagg ttcccgttac 840
cgcggtgact tcgaagagcg cctgaagaag gtcctcaagg agattaacca gcgcggcgac 900
atcatcctgt ttatcgatga gatccacacc ctcgtgggtg caggtgcagc agaaggcgca 960
atcgacgccg cctccctgct taagccaaag cttgcccgcg gtgaactgca gaccattggt 1020
gcaaccacct tggacgagta ccgtaagcac attgaaaagg acgcagctct tgagcgtcgt 1080
ttccagccag tgcaggttcc agagccttcg gttgatctca ccgttgagat cttgaagggt 1140
ctgcgcgacc gctacgaagc tcaccaccgc gtatccatca ccgatggtgc tcttaccgca 1200
gcagctcagc ttgctgatcg ctacattaac gaccgcttct tgccagataa ggccgttgac 1260
ctcatcgatg aggctggcgc ccgcatgcgc atcaagcgca tgaccgcacc gtcctccctc 1320
cgcgaggttg atgagcgcat cgctgatgtt cgccgtgaga aggaagcagc gatcgatgct 1380
caggactttg agaaggcagc aggtcttcgc gataaggagc gcaagctcgg cgaagagcgt 1440
tcagagaagg aaaagcagtg gcgctccggc gacctcgagg acattgctga ggttggcgaa 1500
gagcagatcg cagaagtact ggccaactgg actggtattc ctgtcttcaa gctcaccgaa 1560
gctgagtctt cccgcctgct caacatggaa gaagagttgc acaagcgcat catcggacag 1620
gatgaagctg tcaaggctgt ctcccgtgcg atccgtcgta cccgtgcagg tctgaaggat 1680
cctaagcgtc cttccggctc cttcatcttc gctggtccat ccggtgttgg taagaccgag 1740
ctgtccaagg cacttgctgg attcctcttc ggtgacgatg attccctcat ccaaatcgac 1800
atgggtgaat tccacgaccg cttcaccgcg tcccgactct tcggtgcccc tccgggatac 1860
gttggctacg aagaaggtgg ccagctgacc gagaaggttc gccgtaagcc attctccgtt 1920
gtgcttttcg acgagatcga gaaggcccac aaggagatct acaacacctt gctgcaggtg 1980
ttggaagatg gtcgccttac cgatggtcag ggtcgcattg tggacttcaa gaacaccgtc 2040
ctgatcttca cctccaacct gggcacctct gacatctcca aggctgttgg cctgggcttc 2100
tccggatcct ctgagactga cagcgatgct cagtacgacc gcatgaagaa caaggtccac 2160
gacgagctga agaagcactt ccgccctgag ttcctgaacc gtattgatga gatcgtggtc 2220
ttccaccagc tcaccaagga tcagatcgtt cagatggtcg accttcttat tggccgcgtg 2280
tccaacgcac tggctgagaa ggacatgagc atcgaactga ctgagaaggc taaggatctc 2340
cttgccagcc gcggcttcga tccagttctg ggtgcacgac cattgcgtcg caccattcag 2400
cgcgaaatcg aagaccagat gtccgagaag atcctcttcg gagaaatcgg tgctggcgag 2460
atcgtcaccg tcgacgtcga aggctgggac ggcgagtcca aggacaccga ccgtgcgaag 2520
ttcaccttca caccacgtcc aaagccaatg ccagaaggta agttctctga gatctccgta 2580
caggctgcag aagcaatcca agatgtagat tccgcagctg acggcgatgt cccagaaacc 2640
gattcacttt ccgacattga ccttgaaacc cttgagaagt tcgaggaaga tgtagaaaac 2700
ggcaccgaca ttgatcaggt atccggtgac tactacggca ccgatgatca gggaggcact 2760
gctccaagca aggagtag 2778
<210> 7
<211> 35
<212> DNA
<213> Artificial Sequence
<220>
<223> P1
<400> 7
ctattctaga tccagagacc ctcaaggaca agcag 35
<210> 8
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P2
<400> 8
ggacggtgcg gtcatgcgca tgcgggcgcc 30
<210> 9
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P3
<400> 9
ggcgcccgca tgcgcatgac cgcaccgtcc 30
<210> 10
<211> 34
<212> DNA
<213> Artificial Sequence
<220>
<223> P4
<400> 10
ctattctaga tcgatttgga tgagggaatc atcg 34
<210> 11
<211> 32
<212> DNA
<213> Artificial Sequence
<220>
<223> P5
<400> 11
aatttctaga ggcagaccct attctatgaa gg 32
<210> 12
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P6
<400> 12
agtgtttcgg tctttacaga cacgagggac 30
<210> 13
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P7
<400> 13
gtccctcgtg tctgtaaaga ccgaaacact 30
<210> 14
<211> 32
<212> DNA
<213> Artificial Sequence
<220>
<223> P8
<400> 14
aatttctaga cgtgggagtg tcactcgctt gg 32
<210> 15
<211> 29
<212> DNA
<213> Artificial Sequence
<220>
<223> P9
<400> 15
tcctctagag ctgcgcagtg ttgaatacg 29
<210> 16
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P10
<400> 16
tggaaatctt ttcgatgttc acgttgacat 30
<210> 17
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P11
<400> 17
acatcgaaaa gatttccacc tctgagattc 30
<210> 18
<211> 29
<212> DNA
<213> Artificial Sequence
<220>
<223> P12
<400> 18
gactctagag ttcacctcag agacgatta 29
<210> 19
<211> 29
<212> DNA
<213> Artificial Sequence
<220>
<223> P13
<400> 19
tcctctagac tggtcgcctg atgttctac 29
<210> 20
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> P14
<400> 20
cacgatcaga tgtgcatcat cat 23
<210> 21
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> P15
<400> 21
atgatgatgc acatctgatc gtg 23
<210> 22
<211> 29
<212> DNA
<213> Artificial Sequence
<220>
<223> P16
<400> 22
gactctagat tagtcccttt cgaggcgga 29
<210> 23
<211> 28
<212> DNA
<213> Artificial Sequence
<220>
<223> P17
<400> 23
acggatccca gactccaaag caaaagcg 28
<210> 24
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P18
<400> 24
acaccacggc agaaccaggt gcaaaggaca 30
<210> 25
<211> 30
<212> DNA
<213> Artificial Sequence
<220>
<223> P19
<400> 25
ctggttctgc cgtggtgtgc atcatctctg 30
<210> 26
<211> 28
<212> DNA
<213> Artificial Sequence
<220>
<223> P20
<400> 26
acggatccaa ccaaacttgc tcacactc 28
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Новый вариант цитратсинтазы и способ получения L-аминокислот c его применением | 2022 |
|
RU2836733C1 |
| Микроорганизмы, продуцирующие L-валин, и способ получения L-валина с их использованием | 2021 |
|
RU2822660C1 |
| НОВЫЙ ВАРИАНТ ЦИТРАТСИНТАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-ВАЛИНА C ЕГО ПРИМЕНЕНИЕМ | 2022 |
|
RU2835063C1 |
| Новый вариант пролиндегидрогеназы и способ получения L-валина с его применением | 2021 |
|
RU2795067C1 |
| Новый вариант аспарагинсинтазы и способ получения L-валина с его применением | 2021 |
|
RU2793442C1 |
| НОВЫЙ ВАРИАНТ АТФ-ФОСФОРИБОЗИЛТРАНСФЕРАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-ВАЛИНА С ЕГО ПРИМЕНЕНИЕМ | 2021 |
|
RU2793399C1 |
| Новый вариант белка и способ получения L-лизина с его применением | 2021 |
|
RU2793405C1 |
| Новый вариант аспартокиназы и способ получения L-аминокислоты с использованием этого варианта | 2018 |
|
RU2730025C1 |
| НОВЫЙ ВАРИАНТ МИКОТИОНРЕДУКТАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-ЛИЗИНА С ЕГО ПРИМЕНЕНИЕМ | 2021 |
|
RU2793438C1 |
| Новый вариант L-тирозин-экспортирующего белка и способ получения L-тирозина с его использованием | 2021 |
|
RU2808831C1 |
Изобретение относится к биотехнологии. Предложен полипептид, участвующий в получении аминокислоты с разветвленной цепью, содержащий делецию аминокислот, соответствующих положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин. Также предложен микроорганизм рода Corynebacterium для получения указанных аминокислот с разветвленной цепью, в котором активность АТФ(аденозинтрифосфат)-зависимой протеазы ослаблена по сравнению с немодифицированным микроорганизмом, где указанный микроорганизм содержит вышеуказанный полипептид или полинуклеотид, имеющий делецию нуклеотидов, соответствующих положениям 1291-1299 на основании последовательности, представленной SEQ ID NO: 6. Также предложены способ получения указанных аминокислот с разветвленной цепью с использованием указанного микроорганизма, а также применение микроорганизма или полипептида для получения указанных аминокислот с разветвленной цепью. Изобретение обеспечивает получение L-валина или L-изолейцина с высоким выходом. 5 н. и 6 з.п. ф-лы, 11 табл., 4 пр.
1. Микроорганизм рода Corynebacterium для получения аминокислоты с разветвленной цепью, в котором активность АТФ(аденозинтрифосфат)-зависимой протеазы ослаблена по сравнению с немодифицированным микроорганизмом, где указанный микроорганизм содержит полипептид, имеющий делецию аминокислот, соответствующих положениям 431-433 на основании последовательности, представленной SEQ ID NO: 5, или полинуклеотид, имеющий делецию нуклеотидов, соответствующих положениям 1291-1299 на основании последовательности, представленной SEQ ID NO: 6, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин.
2. Микроорганизм рода Corynebacterium по п. 1, где ослабление представляет собой ослабление активности АТФ-связывающей субъединицы АТФ-зависимой Clp-протеазы.
3. Микроорганизм рода Corynebacterium по п. 2, где АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы имеет происхождение из рода Corynebacterium.
4. Микроорганизм рода Corynebacterium по п. 2, где АТФ-связывающая субъединица АТФ-зависимой Clp-протеазы включает полипептид, представленный SEQ ID NO: 5 или аминокислотной последовательностью, имеющей 90% или более идентичности с ней.
5. Микроорганизм рода Corynebacterium по п. 1, где указанный микроорганизм рода Corynebacterium представляет собой Corynebacterium glutamicum.
6. Полипептид, участвующий в получении аминокислоты с разветвленной цепью, содержащий делецию аминокислот, соответствующих положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин.
7. Полипептид по п. 6, где указанный полипептид состоит из аминокислотной последовательности SEQ ID NO: 1 или аминокислотной последовательности, имеющей 90% или более идентичности с ней.
8. Способ получения аминокислоты с разветвленной цепью, включающий стадию культивирования в среде микроорганизма рода Corynebacterium по п. 1, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин.
9. Способ по п. 8, дополнительно включающий стадию выделения аминокислоты с разветвленной цепью из среды или из микроорганизма после стадии культивирования.
10. Применение микроорганизма рода Corynebacterium по п. 1 для получения аминокислоты с разветвленной цепью, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин.
11. Применение полипептида, содержащего делецию аминокислот, соответствующих положениям 431-433 на основании аминокислотной последовательности, представленной SEQ ID NO: 5, для получения аминокислоты с разветвленной цепью, где аминокислота с разветвленной цепью представляет собой L-валин или L-изолейцин.
| WO 2002020574 A1, 14.03.2002 | |||
| CN 108085287 A, 29.05.2018 | |||
| ENGELS S | |||
| et al., clpC and clpP1P2 gene expression in Corynebacterium glutamicum is controlled by a regulatory network involving the transcriptional regulators ClgR and HspR as well as the ECF sigma factor sigmaH | |||
| Mol Microbiol | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| doi: | |||
Авторы
Даты
2024-12-06—Публикация
2021-07-12—Подача