Изобретение относится к получению алюмосиликатных сорбционных материалов заданного состава, с определенной дисперсностью, содержащих щелочные металлы, а именно, к синтезу обладающего высокими функциональными свойствами наноструктурированного рентгеноаморфного алюмосиликата лития и может найти применение при очистке технологических вод атомного энергетического цикла по производству электроэнергии и других водных сред, загрязненных долгоживущими радионуклидами цезия, а также в химико-металлургической промышленности при очистке жидких радиоактивных отходов и сточных вод от долгоживущих радионуклидов цезия.
Известен (а.с. RU 1731726, опубл. 1992.05.07) способ получения крупнопористого цеолита ZSM-3 путем смешения растворов алюмината натрия, силиката натрия и гидроксида лития при молярных соотношениях компонентов в пересчете на оксиды: Li2O+Na2O=0,3-0,6; (Li2O+Na2O)/SiO2=2,16-6,25; SiO2/Al2O3=4,9-5,1; H2O/(Li2O+Na2O)=30,87 дисперсностью-57,00. При этом предварительно путем сливания растворов силиката натрия и гидроксида лития готовят раствор (Na, Li)-силиката, который после охлаждения до 0°С приливают к раствору алюмината натрия и интенсивно перемешивают до получения реакционной смеси в виде однородного геля. Путем термостатирования последнего при 65-90°С в течение 3 суток осуществляют его гидротермальную кристаллизацию с выделением чистой фазы ZSM-3. Полученный продукт находит применение в качестве сорбента, ионообменника и катализатора, однако данные по его сорбционным свойствам в отношении радионуклидов цезия отсутствуют. Кроме того, недостатками известного способа являются сложность и продолжительность используемых технологических процедур (охлаждение, термостатирование), а также присутствие в ряде случаев примеси филлипсита (минерала сложного химического состава из группы цеолитов), причем в различном количестве, что влечет за собой необходимость подбора и варьирования условий синтеза.
Известен описанный в патенте RU 2214858, опубл. 2003.10.27, способ получения сорбента для очистки жидких радиоактивных отходов (ЖРО) от радионуклидов, в том числе, от радионуклидов цезия, а также от ионов цветных и тяжелых металлов, включающий синтез аналога природного алюмосиликата с использованием в качестве алюмо-кремнийсодержащего исходного сырья полых алюмосиликатных микросфер (ценосфер), представляющих собой стеклокристаллические компоненты в виде сферических гранул плотностью менее 1,0 г/см3 и размером 50-400 мкм, выделяемых из полученных от сжигания каменного угля летучих зол тепловых электростанций. Ценосферы смешивают с 1-3 М водным раствором NaOH и выдерживают при температуре 80-100°С в течение 32-72 часов. К недостаткам известного способа относится значительная длительность этапа подготовки сырья, обусловленная многооперационностью (состав ценосфер стабилизируют путем их «сортировки» по размеру, плотности и магнитным свойствам). Поскольку химический состав сырья, полученного при сжигании углей разных бассейнов, варьирует в широком диапазоне, его подготовка является сложной, процесс получения сорбционного материала получается продолжительным, при этом характеристики получаемого материала отличаются нестабильностью. Его сорбционная емкость достигает примерно 2 мг-экв/г, а с учетом того, что ценосферы составляют не более 1,5% от объема летучей золы, которая к тому же является их единственным источником, их нельзя рассматривать как серьезное сырье для получении сорбента.
Наиболее близким к предлагаемому является способ получения наноструктурированного рентгеноаморфного алюмосиликата - сорбента цезия (RU 2510292, опубл. 2014.03.27), заключающийся в том, что смешивают мелкодисперсный кремнезем с 1-3 М водным раствором гидроксида калия, полученную реакционную смесь подвергают гидротермальной обработке при температуре не менее 120°С в течение 2-3 ч, отфильтровывают образовавшийся примесной осадок, к фильтрату добавляют раствор соли алюминия с анионом кислоты более сильной, чем поликремневая, перемешивают полученную реакционную смесь в течение 10-180 мин до установления нейтрального значения рН=7, отделяют образовавшийся осадок целевого продукта, промывают его и обезвоживают с применением центрифугирования и/или сушки при 95-105°С, при этом исходные компоненты берут в массовом соотношении, обеспечивающем получение алюмосиликата калия с формулой KAlSi3O8, значение сорбционной емкости которого при извлечении радионуклидов Cs+ из раствора его солей в дистилляте равно 3,6 ммоль/г.
Однако степень сорбционной очистки водных сред, загрязненных долгоживущими радионуклидами цезия, а также сорбционной очистки ЖРО с помощью полученного известным способом сорбента в ряде случаев является недостаточной. Выполненная очистка не обеспечивает успешного решения (на 100%) экологических проблем, связанных с загрязнением указанными нуклидами.
Задача изобретения - создание способа получения наноструктурированного рентгеноаморфного алюмосиликатного сорбента, обеспечивающего эффективную сорбционную очистку технологических вод и природных водных сред, а также ЖРО от долгоживущих радионуклидов цезия.
Технический результат предлагаемого способа заключается в увеличении сорбционной емкости получаемого с его помощью сорбционного материала по отношению к долгоживущим радионуклидам цезия и соответствующем повышении эффективности очистки водных сред и жидких радиоактивных отходов от указанных радионуклидов, в первую очередь, за счет использования щелочного металла с более высоким сродством к ионам цезия, а также за счет получения сорбционного материала со слоистой структурой и высокой удельной поверхностью, при этом практически не загрязненного балластными примесями.
Указанный технический результат достигают способом получения наноструктурированного рентгеноаморфного сорбента цезия, согласно которому мелкодисперсный кремнезем смешивают с водным раствором гидроксида щелочного металла, полученную суспензию подвергают гидротермальной обработке при температуре не менее 120° в течение 2-3 часов, отфильтровывают выпавший осадок балластных примесей, к очищенному составу добавляют раствор соли алюминия с анионом кислоты более сильной, чем поликремневая, выдерживают полученную реакционную смесь при перемешивании до достижения нейтрального значения pH=7 с получением осадка целевого продукта, который отделяют фильтрованием, промывают и обезвоживают, при этом, в отличие от известного способа, в качестве гидроксида щелочного металла используют гидроксид лития LiOH, в качестве соли алюминия - хлористый алюминий AlCl3, исходные компоненты берут в расчетных количествах, обеспечивающих массовое соотношение Si : А1=3:1.
В преимущественном варианте осуществления способа растворимые компоненты используют в виде раствора в прокипяченной дистиллированной воде.
Предлагаемый способ осуществляют следующим образом.
Силикат лития получают согласно общей формуле:
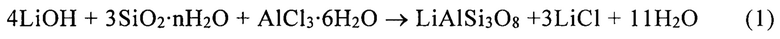
в два этапа.
Сначала проводят синтез жидкого литиевого стекла с силикатным модулем 1,5:

Для этого мелкодисперсный кремнезем смешивают с раствором гидроксида лития в прокипяченной дистиллированной воде, которую обрабатывают таким образом для удаления СО2 во избежание образования карбоната лития Li2CO3, способного загрязнить получаемый сорбент и ухудшить его сорбционные свойства.
Полученную суспензию подвергают гидротермальной обработке при температуре 120-150° в течение 2,0-2,5 часов. Отфильтровывают выпавший осадок балластных примесей, в основном, внесенных с кремнеземом.
Затем в очищенный раствор жидкого стекла при постоянном перемешивании добавляют в расчетном количестве, согласно уравнению (1), хлористый алюминий AlCl3, который перед введением в реакционную смесь растворяют в предварительно прокипяченной дистиллированной воде для удаления растворенного в воде СО2.
Дальнейший синтез ведут, выдерживая реакционную смесь при комнатной температуре с перемешиванием до установления нейтрального значения рН=7,0. По окончанию процесса синтеза с получением осадка алюмосиликата лития LiAlSi3O8 в качестве целевого продукта - последний отфильтровывают от раствора, промывают дистиллированной водой до отрицательной реакции на хлор-ионы и обезвоживают путем нагрева при температуре 95-105°С, преимущественно выше 100°С, но не допуская перегрева.
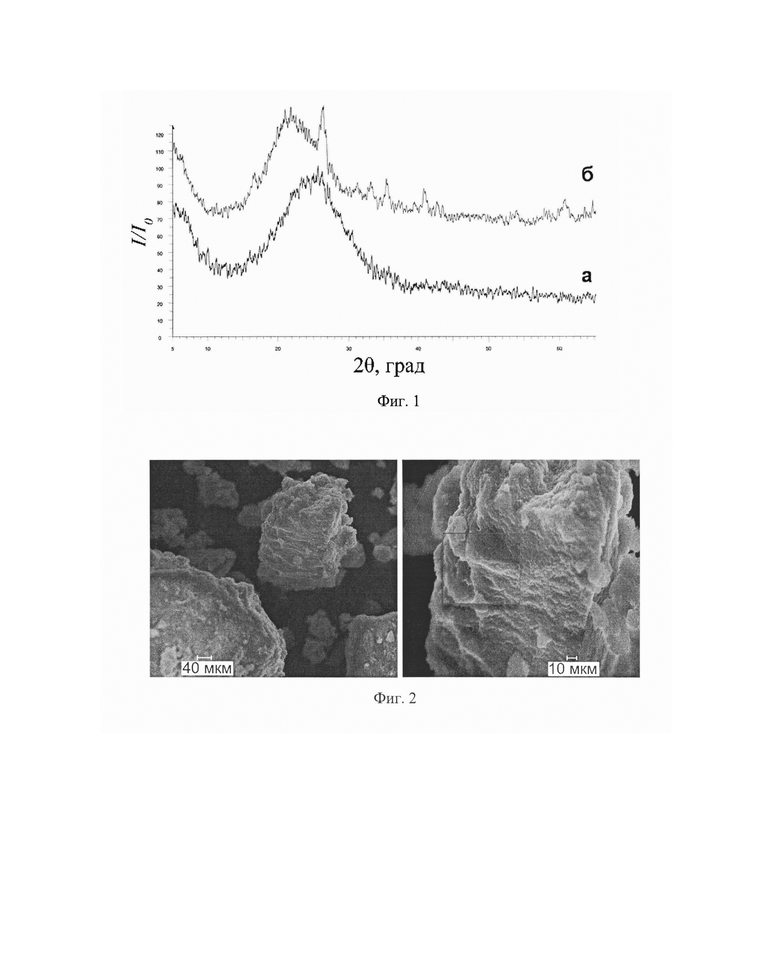
Рентгенофазовый анализ показывает, что синтезированный алюмосиликат лития является рентгеноаморфным, о чем свидетельствует размытый пик, характерный для аморфных веществ в диапазоне углов 15-35° (как показано на фиг. 1а). При нагреве образца до 1000° вследствие частичной кристаллизации на рентгенограмме появляются пики (фиг. 1б), которые, однако, не удается отнести к конкретной кристаллической фазе.
Полученный материал обладает удельной поверхностью 120-135 м2/г и плотностью 2,5 г/см3, имеет рыхлую слоистую структуру, характерную для глин и глинистых минералов типа каолинит, монтмориллонит, вермикулит и др.
Дисперсность полученного алюмосиликата лития находится в пределах 10-40 нм и зависит от температуры гидротермальной обработки на первом этапе. На фиг. 2 приведено СЭМ изображение образца алюмосиликата лития, содержащего частицы разной дисперсности.
Эксперименты по сорбции ионов Cs+ в статических условиях показывают, что по величине максимальной сорбционной емкости синтезированный предлагаемым способом сорбент заметно превосходит прототип (4,7 ммоль/г в сравнении с 3,6 ммоль/г у прототипа), а также многие известные природные и синтетические алюмосиликаты.
Достигнутое значение максимальной сорбционной емкости алюмосиликата лития по отношению к ионам Cs+ определяется высоким химическим сродством цезия и лития (в частности, превышающим величину химического сродства цезия и калия), а также его морфологией. Рыхлая слоистая структура полученного алюмосиликата лития, обычная для глин и глинистых минералов, с межслойными пустотами, занимающими значительный объем, характеризует высокое значение его удельной поверхности и свидетельствует о его способности «поглотить» значительное количество сорбированного вещества, в частности, радиоактивного цезия.
Примеры конкретного осуществления способа
Для синтеза были использованы следующие реактивы: гидроксид лития ГОСТ 8595-83, мелкодисперсный кремнезем (микрокремнезем конденсированный ТУ 5743-048-02495332-96) марки МКУ-85 и алюминий хлористый 6-водный марки хч (ТУ СТП КОМП 2-191-10).
Гидроксид лития перед введением в реакционную смесь растворяли в предварительно прокипяченной дистиллированной воде, чтобы удалить растворенный СО2. На первом этапе было получено жидкое литиевое стекло с силикатным модулем, равным 1,5. Затем после удаления осадка балластной примеси в очищенное жидкое стекло при постоянном перемешивании добавляли раствор хлорида алюминия в прокипяченной дистиллированной воде.
Полученный осадок целевого продукта - алюмосиликата лития отделяли от раствора с помощью фильтра «синяя лента», промывали дистиллированной водой, контролируя наличие хлор-ионов до их полного удаления, и обезвоживали нагреванием при температуре в интервале 95-105°С, избегая перегрева.
По данным рентгенофлуоресцентного анализа, содержание Si в полученном материале составляет 74,9 масс. %, а Al - 24,8 масс. %, т.е. фактическое соотношение Si/Al равно 3:1, что соответствует исходному соотношению, заданному при синтезе (содержание кремния 2,7 моля, алюминия - 0,9 моля).
Для количественного определения элементного состава синтезированных алюмосиликатов был применен энергодисперсионный рентгенофлуоресцентный метод с использованием спектрометра Shimadzu EDX 800 HS (Япония), при этом относительная погрешность определения не превышала ±10%.
Рентгенограммы образцов снимали на автоматическом дифрактометре D8 ADVANCE (Германия) с вращением образца в CuKα-излучении. Рентгенофазовый анализ (РФА) проводили с использованием программы поиска EVA с банком порошковых данных PDF-2.
На фиг. 1 приведена дифрактограмма образца полученного алюмосиликата лития: (1а - исходный образец после сушки при температуре 105°С, 1б - образец после обжига при 1000°С), которая свидетельствует о его рентгеноаморфности. Пик, появившийся в результате кристаллизации после отжига, оказалось невозможно идентифицировать.
Изучение морфологии образцов проводили на сканирующем электронном микроскопе (СЭМ) высокого разрешения HitachiS5500 (Япония). Перед съемкой образцы покрывали проводящим слоем платины. Съемку проводили при ускоряющем напряжении 7 кВ и вакууме 10-5 мм ртутного столба.
Значение удельной поверхности образцов определяли методом низкотемпературной адсорбции азота с использованием прибора «Сорбтомер-М» (Россия).
Эксперименты по сорбции ионов Cs+ проводили в статических условиях при соотношении твердой (сорбент) и жидкой (раствор, содержащий радионуклиды Cs+) фаз, равном 1:400, и температуре 20°С из водных растворов хлорида цезия без солевого фона с различными начальными концентрациями ионов Cs+ от 0.5 до 106.8 ммоль⋅л-1.
В несколько пробирок помещали по 0,05 г сорбента, в каждую пробирку добавляли по 20 мл водного раствора хлорида цезия CsCl с разными начальными концентрациями ионов Cs+, полученными разбавлением раствора CsCl с концентрацией ионов Cs+15 г⋅л-1, приготовленного из его точной навески.
После непрерывного перемешивания на магнитной мешалке RT 15 power (IKA WERKE, Германия) в течение 3 часов растворы отфильтровывали от сорбента с помощью бумажного фильтра «белая лента» и определяли в фильтратах концентрацию ионов Cs+.
Определение концентрации ионов лития Li+ и цезия Cs+ в анализируемых растворах выполняли методом ИСП-МС на спектрометре Agilent 8800 (Agilent Technologies, USA, 2013) с относительной погрешностью не более 10%. Перед выполнением измерений растворы разбавляли в 100 раз. Для анализа были выбраны аналитические изотопы 7Li и 133Cs.
Сорбционную емкость Ас, (ммоль⋅г-1) образцов полученного алюмосиликата лития рассчитывали по формуле:

где Сисх - исходная концентрация ионов Cs+ в растворе, ммоль⋅л-1; Ср - равновесная концентрация ионов Cs+ в растворе, ммоль⋅л-1; V - объем раствора, л; m - масса сорбента, г.
Степень извлечения ионов Cs+ α (%) рассчитывали по формуле:

Коэффициент межфазного распределения Kd (мл⋅г-1) определяли следующим образом:

где Сисх - исходная концентрация ионов Cs+ в растворе (ммоль⋅л-1); Ср - равновесная концентрация Cs+ (ммоль⋅л-1); V - объем раствора (л); m - масса сорбента, г.
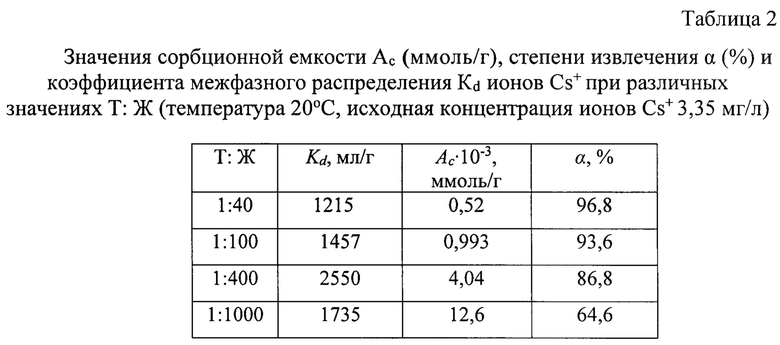
В таблице 1 приведены исходные и равновесные концентрации цезия в водных растворах при заданных условиях: Т : Ж=1:400; Т - твердая фаза, содержащая сорбент; Ж - жидкая фаза, содержащая ионы Cs+; температура Т=20°С, масса сорбента 0,05 г и объем 0,02 л.
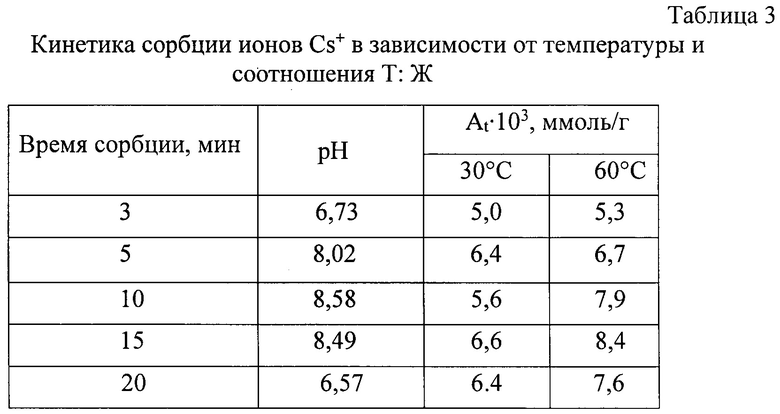
Значения сорбционной емкости Ас, (ммоль/г) синтезированного сорбента, степени извлечения ионов цезия а (%) и коэффициента межфазного распределения Kd в зависимости от соотношения Т : Ж при температуре 20°С и исходной концентрации ионов Cs+ 3,35 мг/л (25,2 мкмоль/л) приведены в таблице 2. В таблице 3 приведены данные по кинетике сорбции полученным сорбционным материалом ионов цезия Cs+ из водных растворов при разных температурах.
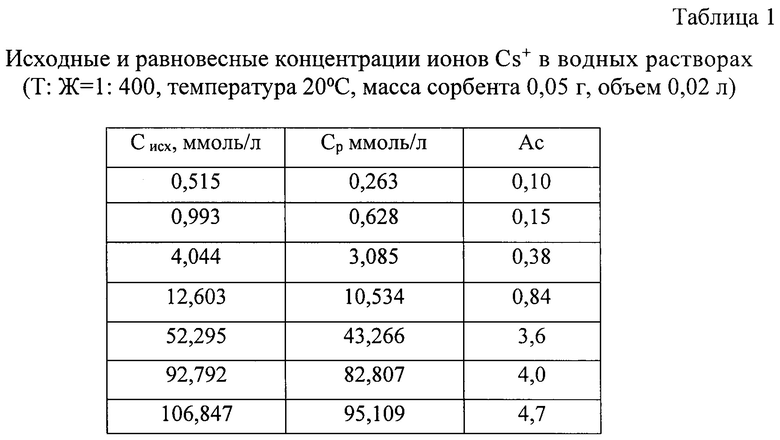
Зависимость коэффициента межфазного распределения цезия на алюмосиликате лития и степени извлечения ионов Cs+ от соотношения твердой и жидкой фаз приведена в таблице 2.
Из полученных данных следует, что при Т : Ж=1:40 степень извлечения ионов Cs+ достигает 97%. В этом случае большой расход сорбента оправдан необходимостью быстрого снижения содержания радионуклидов и соответствующего радиоактивного излучения до минимальных значений и приведения их в соответствие с санитарными нормами.
Пример 1
В пластиковый реакционный сосуд вносили навеску 9,6 г гидроксида лития, 20,5 г микрокремнезема и добавляли 100 мл дистиллированной воды. После гидротермальной обработки (120°С, 3 часа) в полученный раствор жидкого литиевого стекла при перемешивании добавляли 30 граммов алюминия хлористого 6-водного марки «хч». Синтез проводили в закрытом сосуде при 20°С в течение 3 часов. Образовавшийся продукт реакции промывали дистиллированной водой до отрицательной реакции на хлор-ионы и сушили при 105°С.
Полученный рентгеноаморфный алюмосиликат лития с удельной поверхностью 120 м2/г использовали для извлечения ионов Cs+ (условия сорбции: сорбат - CsCl «чда», соотношение твердой и жидкой фаз Т : Ж=1:2000, температура 20°С, время сорбции 3 часа). Сорбционная емкость сорбента при указанных условиях по отношению к ионам цезия составляет 0,05 ммоль⋅г-1, степень извлечения достигает 80%, а значение коэффициента межфазного распределения Kd составляет 7339 мл/г, при этом является одним из наибольших и представляет особый интерес для случаев захоронения радиоактивных отходов.
Пример 2
Кинетические свойства алюмосиликата лития, полученного в примере 1, были исследованы в ходе сорбции ионов цезия. Опыты по кинетике сорбции ионов Cs+ проводили в статических условиях при соотношении твердой и жидкой фаз, равном 1:400, температуре 30 и 60°С из водных растворов хлорида цезия CsCl без солевого фона с начальной концентрацией ионов Cs+ 3,35 мг⋅л-1 в течение от 3 до 20 минут.
Полученные результаты приведены в таблице 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ЦЕЗИЯ | 2012 |
|
RU2516639C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ЦЕЗИЯ | 2012 |
|
RU2510292C1 |
| Способ получения барийсодержащего алюмосиликатного сорбента с использованием растительного сырья | 2022 |
|
RU2787778C1 |
| Сорбционный материал для селективного извлечения радионуклидов стронция из сложных по ионному составу растворов и способ извлечения радионуклидов стронция с его помощью | 2018 |
|
RU2680964C1 |
| Способ получения магнитного композиционного сорбента | 2022 |
|
RU2826365C2 |
| СПОСОБ ИММОБИЛИЗАЦИИ РАДИОАКТИВНЫХ ОТХОДОВ В МИНЕРАЛОПОДОБНОЙ МАТРИЦЕ | 2010 |
|
RU2439726C1 |
| Способ получения алюмосиликатного сорбента | 2022 |
|
RU2825254C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА НА ОСНОВЕ МИКРОСФЕР ЗОЛ-УНОСА ДЛЯ ОЧИСТКИ ЖИДКИХ РАДИОАКТИВНЫХ ОТХОДОВ (ВАРИАНТЫ) | 2012 |
|
RU2501603C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РАДИОНУКЛИДОВ ИЗ ВОДНЫХ РАСТВОРОВ | 2006 |
|
RU2330340C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТОНКОСЛОЙНОГО СОРБЕНТА | 2007 |
|
RU2356619C1 |
Изобретение относится к получению алюмосиликатных сорбционных материалов и может найти применение при очистке технологических вод атомного энергетического цикла по производству электроэнергии, а также в химико-металлургической промышленности при очистке жидких радиоактивных отходов и сточных вод от долгоживущих радионуклидов цезия. Для получения наноструктурированного рентгеноаморфного сорбента цезия мелкодисперсный кремнезём смешивают с водным раствором гидроксида лития LiOH. Полученную суспензию подвергают гидротермальной обработке при температуре не менее 120°С в течение 2,0-3,0 ч, отфильтровывают выпавший осадок балластных примесей. К очищенному составу добавляют раствор хлористого алюминия AlCl3, выдерживают полученную реакционную смесь при перемешивании до достижения нейтрального значения рН=7 с получением осадка целевого продукта, который отделяют фильтрованием, промывают и обезвоживают. Исходные компоненты берут в расчетных количествах, обеспечивающих массовое соотношение Si:Al=3:1. Растворимые компоненты используют в виде раствора в прокипяченной дистиллированной воде. Изобретение позволяет увеличить сорбционную емкость сорбента по отношению к долгоживущим радионуклидам цезия, повысить эффективность сорбционной очистки водных сред и жидких радиоактивных отходов от указанных радионуклидов. 2 ил., 3 табл., 2 пр.
Способ получения наноструктурированного рентгеноаморфного сорбента цезия, согласно которому мелкодисперсный кремнезём смешивают с водным раствором гидроксида щелочного металла, полученную суспензию подвергают гидротермальной обработке при температуре не менее 120°С в течение 2,0-3,0 ч, отфильтровывают выпавший осадок балластных примесей, к очищенному составу добавляют раствор соли алюминия с анионом кислоты более сильной, чем поликремневая, выдерживают полученную реакционную смесь при перемешивании до достижения нейтрального значения рН=7 с получением осадка целевого продукта, который отделяют фильтрованием, промывают и обезвоживают, отличающийся тем, что в качестве гидроксида щелочного металла используют гидроксид лития LiOH, в качестве соли алюминия – хлористый алюминий AlCl3, при этом исходные компоненты берут в расчетных количествах, обеспечивающих массовое соотношение Si:Al=3:1, и растворяют в предварительно прокипяченной дистиллированной воде.
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ЦЕЗИЯ | 2012 |
|
RU2510292C1 |
| ГОРДИЕНКО П | |||
| С | |||
| и др., Синтез и сорбционные свойства наноструктурированного алюмосиликата лития, Актуальные физикохимические проблемы адсорбции и синтеза нанопористых материалов: Всероссийский симпозиум с международным участием, посвященный памяти чл.-корр | |||
| РАН В.А | |||
| Авраменко, Москва, 17-21 октября 2022 года, | |||
Авторы
Даты
2024-12-09—Публикация
2023-10-09—Подача