УРОВЕНЬ ТЕХНИКИ
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретение относится к соединению, антагонисту эндотелинового рецептора A и фармацевтической композиции.
ОПИСАНИЕ РОДСТВЕННОГО УРОВНЯ ТЕХНИКИ
[0002]
Эндотелин (ET) является пептидом, образующихся в клетках эндотелия сосудов и обладает сосудосуживающим действием. Эндотелиновый рецептор A (ETA) и эндотелиновый рецептор B (ETB) известны, как рецепторы эндотелина. Рецептор ETA участвует в сужении кровеносных сосудов, центральной активации симпатической нервной системы, стимулировании секреции альдостерона и т.п. Рецептор ETB участвует в расширении сосудов, клиренсе эндотелина и т.п.
[0003]
Сообщали, что рецептор ETA связан с разными заболеваниями. Например, имеются сообщения о связи рецептора ETA с легочной гипертензией (например, The New England Journal of Medicine, 2002, 346, pp 896-903; и International Heart Journal, 2020, 61, pp 799-805), фокально-сегментарным гломерулосклерозом (например, Journal of the American society of Nephrology, 2018, 29, pp 2745-2754), IgA нефропатией (например, Nephron, 1996, 72, pp 454-460), хроническим заболеванием почек (включая диабетическую нефропатию) (например, The Lancet, 2019, 393, pp 1937-1947; и Hypertension, 2011, 57, pp 772-779), поражением почек, связанным с синдромом серповидных эритроцитов (например, Journal of the American society of Nephrology, 2017, 28, pp 2443-2458), острым поражением почек (например, Transplantation, 2001, 71, pp 211-216), гипертензией (например, Hypertension, 2008, 52, pp 452-459), неалкогольным стеатогепатитом (NASH) (например, Drug Research, 2015, 65, pp 272-280; World Journal of Hepatology, 2016, 8, pp 933-941; и Digestive Diseases and Sciences, 2007, 52, pp 2622-2628), раком (например, Nature reviews cancer, 2013, 13, pp 637-651), болью, связанной с эндометриозом (например, European Journal of Pain, 2018, 22, pp 501-510; и Fertility and Sterility, 1994, 61, pp 1083- 1087), осложнениями, связанными со склеродермией (например, Inflammation & Allergy - Drug Targets, 2011, 10, pp 19-26; и Annals of the Rheumatic Diseases, 2011, 70, pp 32-38), спазмом мозговых сосудов (например, Molecular medicine reports, 2018, 18, pp 5229-5236) и гипертрофической кардиомиопатией (например, Journal of the American Heart Association, 2014, 3, e00126).
[0004]
Описаны разные соединения, оказывающие антагонистическое воздействие на рецептор ETA (например, U.S. Patent Nos. 5514696 и 5612359, и International Publication Nos. WO 1996/40681, WO 1996/31492, WO 1998/49162, WO 1998/13366, WO 1998/33780, WO 1998/33781, WO 2001/49685, WO 2004/35057 и WO 2013/115162). В частности, известно, что ситаксентан, оказывающий антагонистическое воздействие на рецептор ETA, селективно ингибирует рецептор ETA в отличие от рецептора ETB и сообщали, что он обладает значительной лекарственной эффективностью при клинических исследованиях легочной гипертензии, связанной с заболевание соединительной ткани (European Heart Journal, 2008, 29, pp 1936-1948), не увеличивая концентрации эндотелина в крови (Pharmacological Reviews, 2016, 68, pp. 357-418) и не вызывая периферический отек (Annual Review of Pharmacology and Toxicology, 2007, 47, pp 731-759).
Литература родственного уровня техники
[0005]
Патентная литература 1: U.S. Patent No. 5514696
Патентная литература 2: U.S. Patent No. 5612359
Патентная литература 3: WO 1996/40681
Патентная литература 4: WO 1996/31492
Патентная литература 5: WO 1998/49162
Патентная литература 6: WO 1998/13366
Патентная литература 7: WO 1998/33780
Патентная литература 8: WO 1998/33781
Патентная литература 9: WO 2001/49685
Патентная литература 10: WO 2004/35057
Патентная литература 11: WO 2013/115162
[0006]
Непатентная литература 1: The New England Journal of Medicine, 2002, 346, pp 896-903
Непатентная литература 2: International Heart Journal, 2020, 61, pp 799-805
Непатентная литература 3: Journal of the American society of Nephrology, 2018, 29, pp 2745-2754
Непатентная литература 4: Nephron, 1996, 72, pp 454-460
Непатентная литература 5: The Lancet, 2019, 393, pp 1937-1947
Непатентная литература 6: Hypertension, 2011, 57, pp 772-779
Непатентная литература 7: Journal of the American society of Nephrology, 2017, 28, pp 2443-2458
Непатентная литература 8: Transplantation, 2001, 71, pp 211-216
Непатентная литература 9: Hypertension, 2008, 52, pp 452-459
Непатентная литература 10: Drug Research, 2015, 65, pp 272-280
Непатентная литература 11: World Journal of Hepatology, 2016, 8, pp 933-941
Непатентная литература 12: Digestive Diseases and Sciences, 2007, 52, pp 2622-2628
Непатентная литература 13: Nature reviews cancer, 2013, 13, pp 637-651
Непатентная литература 14: European Journal of Pain, 2018, 22, pp 501-510
Непатентная литература 15: Fertility and Sterility, 1994, 61, pp 1083- 1087
Непатентная литература 16: Inflammation & Allergy - Drug Targets, 2011, 10, pp 19-26
Непатентная литература 17: Annals of the Rheumatic Diseases, 2011, 70, pp 32-38
Непатентная литература 18: Molecular medicine reports, 2018, 18, pp 5229-5236
Непатентная литература 19: Journal of the American Heart Association, 2014, 3, e00126
Непатентная литература 20: European Heart Journal, 2008, 29, pp 1936-1948
Непатентная литература 21: Pharmacological Reviews, 2016, 68, pp. 357-418
Непатентная литература 22: Annual Review of Pharmacology and Toxicology, 2007, 47, pp 731-759
[0007]
Объектом настоящего изобретения является соединение, оказывающее антагонистическое воздействие на рецептор ETA, и антагонист рецептора ETA или фармацевтическая композиция, содержащая соединение.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008]
Авторы настоящего изобретения провели тщательные исследования и в результате завершили настоящее изобретение путем установления того, что соединение, обладающее особой структурой, оказывает антагонистическое воздействие на рецептор ETA.
[0009]
Настоящее изобретение включает следующие варианты осуществления.
[1]
Соединение, описывающееся следующей формулой (1):
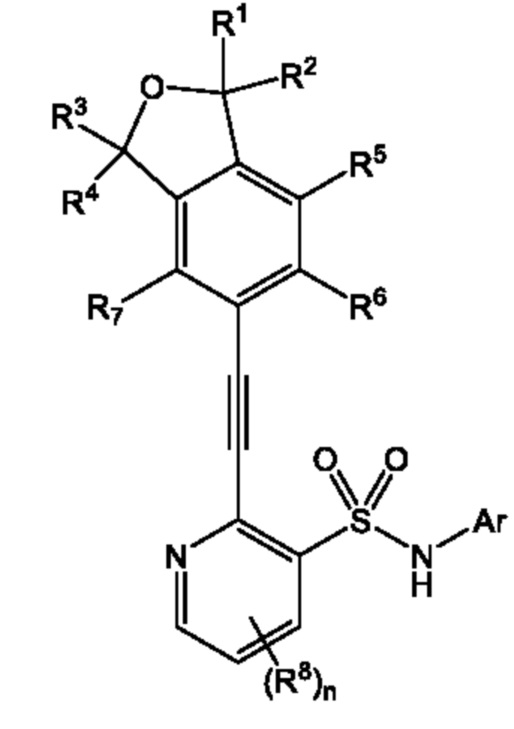 (1)
(1)
где
R1 и R2 все независимо означают водород или алкил,
R3 и R4 все независимо означают водород или алкил, или
R3 и R4 вместе образуют оксогруппу,
R5 - R7 все независимо означают водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу,
каждый R8 независимо означает алкил, галогеналкил или галоген,
n является целым числом, равным от 0 до 3, и
Ar описывается следующей формулой (Ar1) или (Ar2):
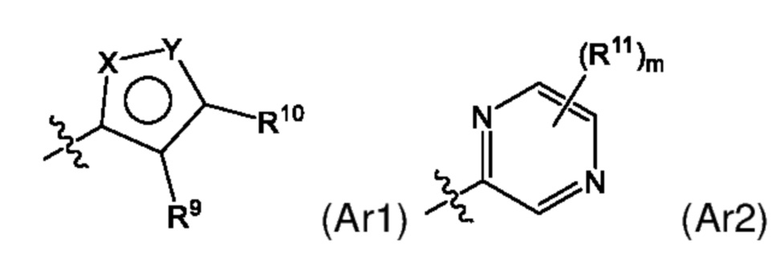
где
X и Y означают азот и кислород соответственно или кислород и азот соответственно,
R9 и R10 все независимо означают водород, алкил, галогеналкил или галоген,
каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу и
m является целым числом, равным от 0 до 3,
или его фармацевтически приемлемая соль.
[2]
Соединение или его фармацевтически приемлемая соль по параграфу [1], где каждый из R1 и R2 означает водород.
[3]
Соединение или его фармацевтически приемлемая соль по параграфу [1] или [2], где каждый из R5 и R7 означает водород и R6 означает алкил.
[4]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [3], где n равно 0.
[5]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [4], где Ar описывается формулой (Ar1).
[6]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [5], где каждый из R9 и R10 означает алкил.
[7]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [6], где X и Y означают азот и кислород соответственно.
[8]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [6], где X и Y означают кислород и азот соответственно.
[9]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [4], где Ar описывается формулой (Ar2).
[10]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [4] и [9], где каждый R11 независимо означает алкил или алкоксигруппу.
[11]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [4], [9] и [10, где m равно 2.
[12]
Соединение или его фармацевтически приемлемая соль по параграфу [1], где соединение выбрано из группы, состоящей из следующих соединений:
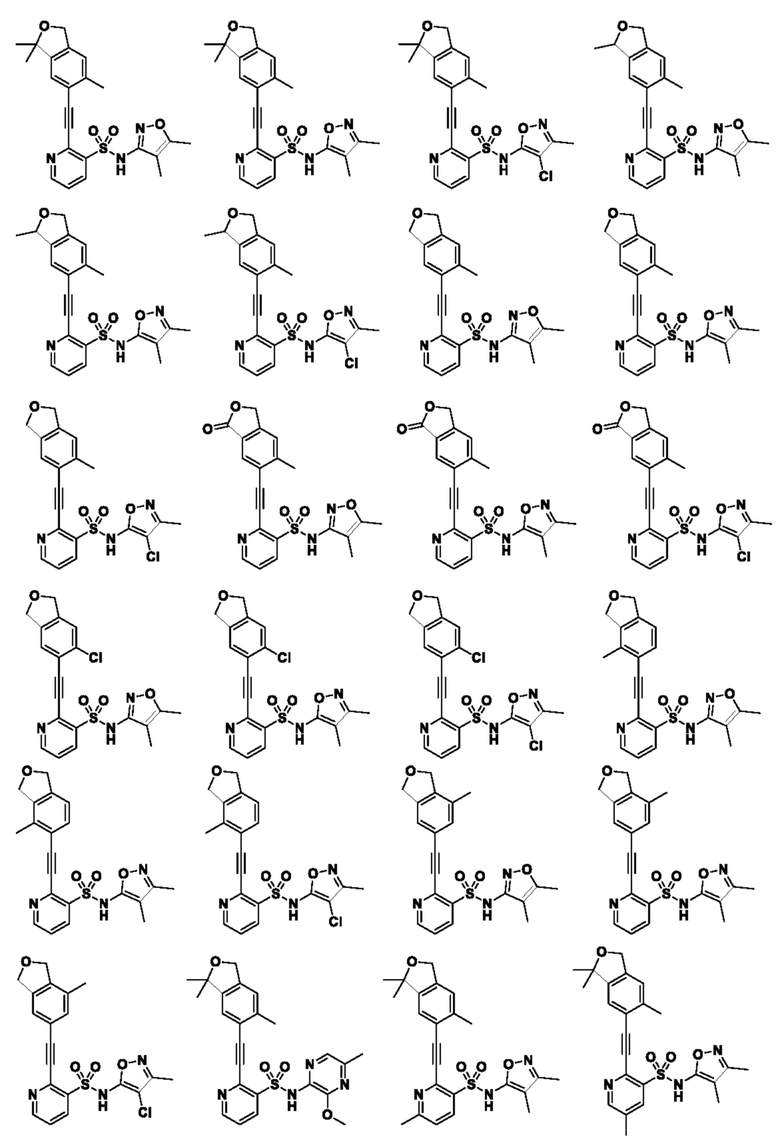
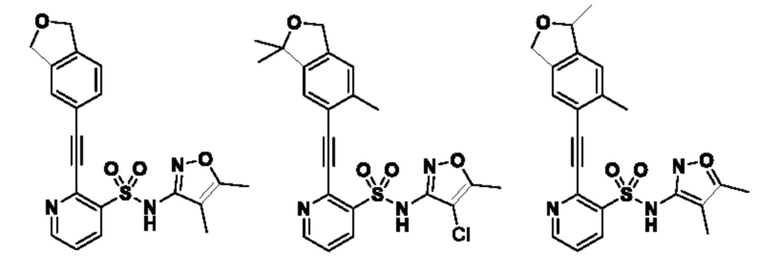
[13]
Антагонист эндотелинового рецептора A, включающий соединение или его фармацевтически приемлемую соль по любому из параграфов [1] - [12].
[14]
Антагонист эндотелинового рецептора A по параграфу [13], где антагонист эндотелинового рецептора A селективно ингибирует эндотелиновый рецептор A в отличие от эндотелинового рецептора B.
[15]
Фармацевтическая композиция, включающая соединение или его фармацевтически приемлемую соль по любому из параграфов [1] - [12].
[16]
Фармацевтическая композиция по параграфу [15] для предупреждения или лечения заболевания, выбранного из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
[0010]
Настоящее изобретение также включает следующие варианты осуществления.
[A1]
Способ ингибирования эндотелинового рецептора A, включающий введение эффективного количества соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] нуждающемуся в нем пациенту.
[A2]
Способ по параграфу [A1], где способ обеспечивает селективное ингибирование эндотелинового рецептора A в отличие от эндотелинового рецептора B.
[A3]
Способ предупреждения или лечения заболевания, включающий введение эффективного количества соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] нуждающемуся в нем пациенту.
[A4]
Способ по параграфу [A3], где заболевание выбрано из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
[0011]
[B1]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [12] для применения для ингибирования эндотелинового рецептора A.
[B2]
Соединение или его фармацевтически приемлемая соль по параграфу [B1], где его применение обеспечивает селективное ингибирование эндотелинового рецептора A в отличие от эндотелинового рецептора B.
[B3]
Соединение или его фармацевтически приемлемая соль по любому из параграфов [1] - [12] для применения для предупреждения или лечения заболевания.
[B4]
Соединение или его фармацевтически приемлемая соль по параграфу [B3], где заболевание выбрано из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
[0012]
[C1]
Применение соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] для ингибирования эндотелинового рецептора A.
[C2]
Применение по параграфу [C1], где применение обеспечивает селективное ингибирование эндотелинового рецептора A в отличие от эндотелинового рецептора B.
[C3]
Применение соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] для предупреждения или лечения заболевания.
[C4]
Применение по параграфу [C3], где заболевание выбрано из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
[0013]
[D1]
Применение соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] для получения антагониста эндотелинового рецептора A.
[D2]
Применение по параграфу [D1], где антагонист эндотелинового рецептора A селективно ингибирует эндотелиновый рецептор A в отличие от эндотелинового рецептора B.
[D3]
Применение соединения или его фармацевтически приемлемой соли по любому из параграфов [1] - [12] для получения фармацевтической композиции для предупреждения или лечения заболевания.
[D4]
Применение по параграфу [D3], где заболевание выбрано из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
[0014]
Настоящее изобретение может дать соединение, оказывающее антагонистическое воздействие на рецептор ETA, и антагонист рецептора ETA или фармацевтическую композицию, содержащую соединение.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0015]
Ниже в настоящем изобретении специально описаны варианты осуществления настоящего изобретения. Однако настоящее изобретение не ограничиваются ими и без отклонения от сущности настоящего изобретения в него можно внести различные изменения или модификации.
[0016]
<Соединение>
В одном варианте осуществления настоящее изобретение относится к соединению, описывающемуся следующей формулой (1):
 (1)
(1)
где
R1 и R2 все независимо означают водород или алкил,
R3 и R4 все независимо означают водород или алкил, или
R3 и R4 вместе образуют оксогруппу,
R5 - R7 все независимо означают водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу,
каждый R8 независимо означает алкил, галогеналкил или галоген,
n является целым числом, равным от 0 до 3, и
Ar описывается следующей формулой (Ar1) или (Ar2):

где
X и Y означают азот и кислород соответственно или кислород и азот соответственно,
R9 и R10 все независимо означают водород, алкил, галогеналкил или галоген,
каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу и
m является целым числом, равным от 0 до 3,
или его фармацевтически приемлемой соли.
[0017]
Алкил (включая алкил в галогеналкиле; это же применимо ниже в настоящем изобретении), использующийся в настоящем изобретении, может быть линейным, может быть разветвленным или может быть циклическим.
Алкильный фрагмент в алкоксигруппе (включая алкоксигруппу в галогеналкоксигруппе; это же применимо ниже в настоящем изобретении), использующийся в настоящем изобретении, может быть линейным, может быть разветвленным или может быть циклическим.
Алкил и алкоксигруппа, использующаяся в настоящем изобретении, могут быть замещенными заместителем или могут быть незамещенными. Примеры заместителя включают галоген, а также гидроксигруппу, алкоксигруппу, аминогруппу, карбоксил и карбонил.
[0018]
В формуле (1) R1 и R2 все независимо означают водород или алкил, предпочтительно водород.
Алкил, обозначенный с помощью каждого R1 и R2, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
[0019]
В формуле (1) R3 и R4 все независимо означают водород или алкил, или R3 и R4 вместе образуют оксогруппу (=O). Предпочтительно, если R3 и R4 все независимо означают водород или алкил.
Алкил, обозначенный с помощью каждого R3 и R4, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
[0020]
В формуле (1) R5 означает водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, предпочтительно водород.
Алкил, обозначенный с помощью R5, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Алкоксигруппа, обозначенная с помощью R5, предпочтительно представляет собой алкоксигруппу, содержащую от 1 до 6 атомов углерода, более предпочтительно алкоксигруппу, содержащую от 1 до 3 атомов углерода, еще более предпочтительно метоксигруппу.
Галоген в галогеналкиле и галогеналкоксигруппе, обозначенной с помощью R5, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0021]
В формуле (1) R6 означает водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, предпочтительно алкил.
Алкил, обозначенный с помощью R6, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Алкоксигруппа, обозначенная с помощью R6, предпочтительно представляет собой алкоксигруппу, содержащую от 1 до 6 атомов углерода, более предпочтительно алкоксигруппу, содержащую от 1 до 3 атомов углерода, еще более предпочтительно метоксигруппу.
Галоген в галогеналкиле и галогеналкоксигруппе, обозначенной с помощью R6, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0022]
В формуле (1) R7 означает водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, предпочтительно водород.
Алкил, обозначенный с помощью R7, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Алкоксигруппа, обозначенная с помощью R7, предпочтительно представляет собой алкоксигруппу, содержащую от 1 до 6 атомов углерода, более предпочтительно алкоксигруппу, содержащую от 1 до 3 атомов углерода, еще более предпочтительно метоксигруппу.
Галоген в галогеналкиле и галогеналкоксигруппе, обозначенной с помощью R7, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0023]
В формуле (1) каждый R8 независимо означает алкил, галогеналкил или галоген, предпочтительно алкил или галоген.
Алкил, обозначенный с помощью R8, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Галоген в галогеналкиле, обозначенном с помощью R8, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0024]
В формуле (1) n является целым числом, равным от 0 до 3, предпочтительно 0 или 1, более предпочтительно 0.
[0025]
В формуле (1) Ar описывается формулой (Ar1) или (Ar2).
[0026]
В формуле (Ar1) X и Y означают азот и кислород соответственно или кислород и азот соответственно.
[0027]
В формуле (Ar1) R9 означает водород, алкил, галогеналкил или галоген, предпочтительно алкил.
Алкил, обозначенный с помощью R9, предпочтительно означает алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Галоген в галогеналкиле, обозначенном с помощью R9, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0028]
В формуле (Ar1) R10 означает водород, алкил, галогеналкил или галоген, предпочтительно алкил.
Алкил, обозначенный с помощью R10, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Галоген в галогеналкиле, обозначенном с помощью R10, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0029]
В формуле (Ar2) каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, предпочтительно алкил или алкоксигруппу, более предпочтительно алкил и алкоксигруппу.
Алкил, обозначенный с помощью R11, предпочтительно представляет собой алкил, содержащий от 1 до 6 атомов углерода, более предпочтительно алкил, содержащий от 1 до 3 атомов углерода, еще более предпочтительно метил.
Алкоксигруппа, обозначенная с помощью R11, предпочтительно представляет собой алкоксигруппу, содержащую от 1 до 6 атомов углерода, более предпочтительно алкоксигруппу, содержащую от 1 до 3 атомов углерода, еще более предпочтительно метоксигруппу.
Галоген в галогеналкиле и галогеналкоксигруппе, обозначенной с помощью R11, предпочтительно представляет собой фтор, хлор, бром или йод, более предпочтительно фтор или хлор.
[0030]
В формуле (Ar2) m является целым числом, равным от 0 до 3, предпочтительно 2.
[0031]
На соединение, описывающееся следующей формулой (1), не налагаются особые ограничения и им предпочтительно является любое из следующих соединений.
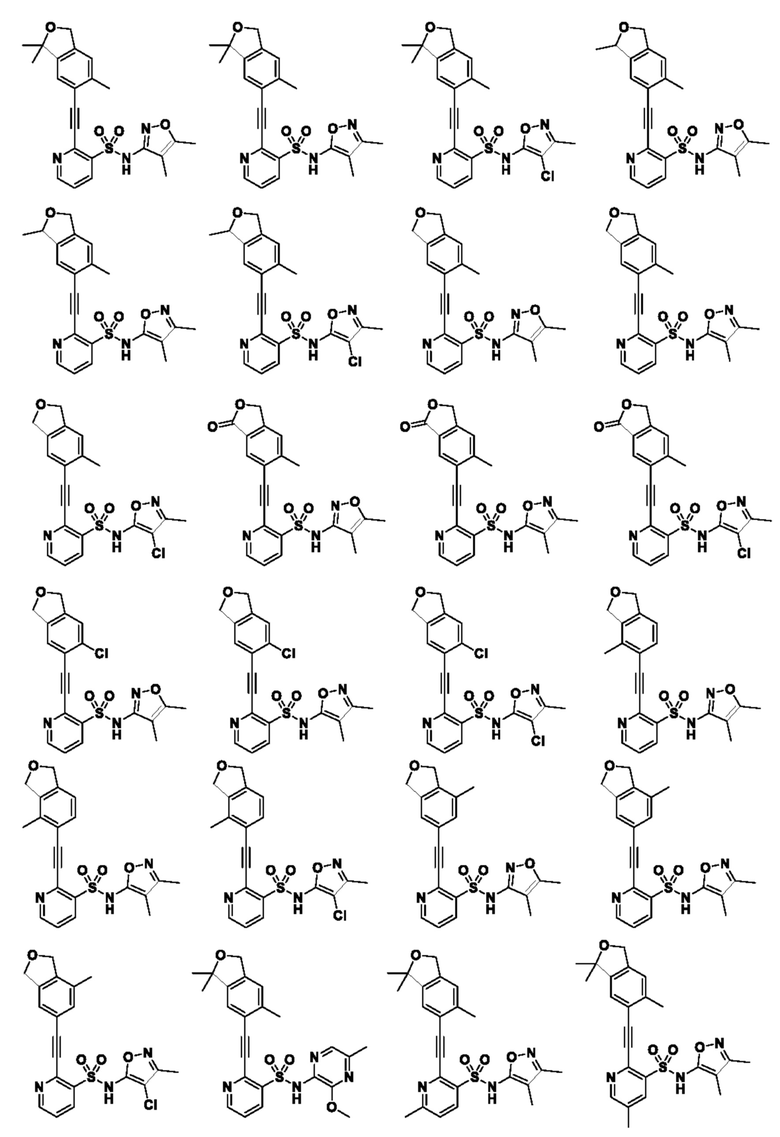
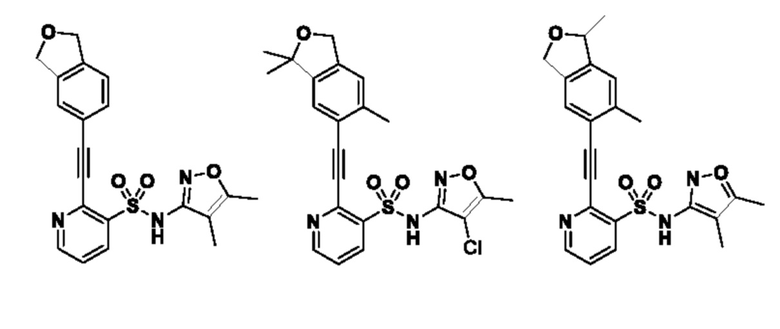
[0032]
На фармацевтически приемлемую соль соединения, описывающегося формулой (1), не налагаются особые ограничения, если соль можно использовать в качестве лекарственного средства. Ее примеры могут включать: соли неорганической кислоты, такие как гидрохлорид, сульфат, нитрат, фосфат и гидробромид; соли органической кислоты, такие как фумарат, малеат, малат, тартрат, сукцинат, цитрат, метансульфонат, п-толуолсульфонат, ацетат, лактат и пальмитат; соли щелочных металлов и соли щелочноземельных металлов.
[0033]
Соединение, описывающееся следующей формулой (1), или его фармацевтически приемлемая соль может образовывать сольват, такой как гидрат. Сольват, использующийся в настоящем изобретении, входит в число соединений, описывающихся формулой (1), или их фармацевтически приемлемых солей.
[0034]
Если соединение, описывающееся формулой (1), или его фармацевтически приемлемая соль обладает стереоизомерами (например, энантиомерами и диастереоизомерами), отдельные стереоизомеры и их смесь (например, рацемат) входят в число соединений, описывающихся формулой (1), или их фармацевтически приемлемых солей.
[0035]
На форму соединения описывающегося формулой (1), или его фармацевтически приемлемой соли не налагаются особые ограничения. Соединение, описывающееся формулой (1), или его фармацевтически приемлемая соль может находиться в форме кристаллов или может находиться в аморфной форме. Если соединение, описывающееся формулой (1), или его фармацевтически приемлемая соль обладает кристаллическими полиморфами, соединение, описывающееся формулой (1), или его фармацевтически приемлемая соль может находиться в любой кристаллической форме.
[0036]
<Антагонист эндотелинового рецептора A>
В одном варианте осуществления настоящее изобретение относится к антагонисту рецептора ETA, содержащему соединение, описывающееся формулой (1), или его фармацевтически приемлемую соль. Рецептор ETA и рецептор ETB являются известными рецепторами эндотелина. Ингибирование рецептора ETB может привести к затруднениям, таким как повышение уровней эндотелина в крови или возникновение периферического отека. Предпочтительно, если антагонист рецептора ETA этого варианта осуществления может селективное ингибировать эндотелиновый рецептор A в отличие от эндотелинового рецептора B.
[0037]
В частности, отношение (обеспечивающая ингибирование рецептора ETB концентрация (IC50))/(обеспечивающая ингибирование рецептора ETA концентрация (IC50)) предпочтительно равно 2000 или более, более предпочтительно 4000 или более, еще более предпочтительно 6000 или более, еще более предпочтительно 8000 или более, особенно предпочтительно 10000 или более. На верхнее предельное значение отношения (обеспечивающая ингибирование рецептора ETB концентрация (IC50))/(обеспечивающая ингибирование рецептора ETA концентрация (IC50)) не налагаются особые ограничения и оно может равняться, например, 100000, 80000, 60000 или 40000. Обеспечивающую ингибирование рецептора ETB концентрацию и обеспечивающую ингибирование рецептора ETA концентрацию можно измерить по методике, описанной в примерах.
[0038]
Обеспечивающая ингибирование рецептора ETA концентрация (IC50) антагониста рецептора ETA этого варианта осуществления предпочтительно равна 10 нМ или менее, более предпочтительно 8,0 нМ или менее, еще более предпочтительно 6,0 нМ или менее, еще более предпочтительно 4,0 нМ или менее, особенно предпочтительно 2,0 нМ или менее. На нижнее предельное значение обеспечивающей ингибирование рецептора ETA концентрации (IC50) не налагаются особые ограничения и она может равняться, например, 0,005 нМ, 0,01 нМ или 0,05 нМ.
[0039]
Обеспечивающая ингибирование рецептора ETB концентрация (IC50) антагониста рецептора ETA этого варианта осуществления предпочтительно равна 1000 нМ или более, более предпочтительно 2000 нМ или более, еще более предпочтительно 3000 нМ или более, еще более предпочтительно 4000 нМ или более, особенно предпочтительно 5000 нМ или более. На верхнее предельное значение обеспечивающей ингибирование рецептора ETB концентрации (IC50) не налагаются особые ограничения и она может равняться, например, 10000 нМ, 15000 нМ или 20000 нМ.
[0040]
Применение антагониста рецептора ETA этого варианта осуществления может лечить и/или предупреждать заболевание, связанное с (опосредуемого с помощью) рецептором ETA.
[0041]
<Фармацевтическая композиция>
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение, описывающееся формулой (1), или его фармацевтически приемлемую соль.
[0042]
Примеры заболевания, на которое направлена фармацевтическая композиция этого варианта осуществления могут включать легочную гипертензию, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
Примеры нефропатии могут включать фокально-сегментарный гломерулосклероз, IgA нефропатию, хроническое заболевание почек (включая диабетическую нефропатию) и поражение почек, связанное с синдромом серповидных эритроцитов.
Примеры гепатита могут включать неалкогольный стеатогепатит (NASH) и алкогольный гепатит.
Примеры рака могут включать рак предстательной железы, плоскоклеточный рак, немелкоклеточный рак легких и меланома.
Примеры боли могут включать боль, связанную с эндометриозом, хроническую боль, невропатическую боль, боль при раке и воспалительную боль.
Примеры осложнений, связанных с аутоиммунным заболеванием, могут включать осложнения, связанные со склеродермией, и осложнения, связанные с васкулитом.
Примеры сердечной недостаточности могут включать недостаточность правых отделов сердца, сердечную недостаточность левых отделов сердца, сердечную недостаточность, связанную с гипертрофическая кардиомиопатия, сердечную недостаточность, связанную с дилатационная кардиомиопатия, сердечная недостаточность с сохраненной фракцией выброса и сердечную недостаточность со сниженной фракцией выброса.
Примеры спазма сосудов могут включать спазм мозговых сосудов и вазоспастическую стенокардию.
[0043]
Фармацевтическую композицию этого варианта осуществления можно вводить перорально или парентерально. Примеры дозированной формы для перорального введения включают таблетки, пилюли, гранулы, порошки, капсулы, сиропы, эмульсии и суспензии. Примеры дозированной формы для парентерального введения включают средства для инъекции, вливания, капли, глазные капли и суппозитории.
[0044]
Фармацевтическая композиция этого варианта осуществления необязательно может содержать инертный наполнитель, связующее, смазывающее вещество, разрыхлитель, подсластитель, поверхностно-активное вещество, суспендирующий агент, эмульгирующий агент, окрашивающее вещество, консервант, отдушку, модификатор лекарственных веществ, стабилизатор, загуститель и т. п.
[0045]
Доза фармацевтической композиции этого варианта осуществления меняется в зависимости от состояния или массы тела пациента, типа соединения, типа заболевания, пути введения и т. п. и надлежащее количество может определить врач.
[0046]
<Методика получения соединения>
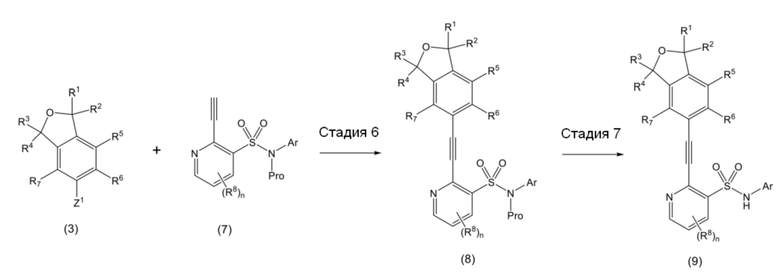
Соединение, описывающееся формулой (1), или его фармацевтически приемлемую соль можно синтезировать путем соответствующего применения методики, известной в данной области техники. Примеры методики синтеза могут включать следующие схемы A - C:
<Схема A>
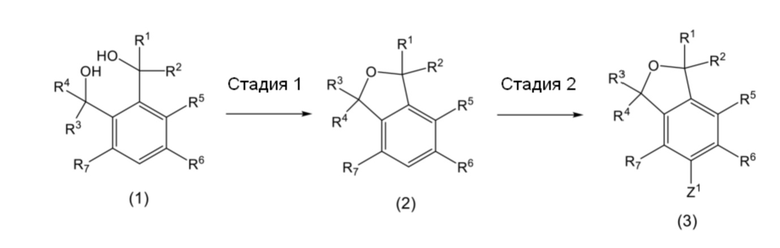
<Схема B>
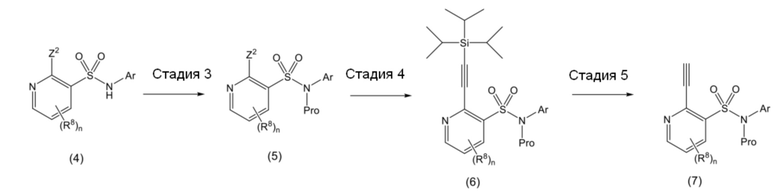
<Схема C>
[0047]
На схемах A - C, R1 - R8, n и Ar являются такими, как определено выше, Z1 и Z2 каждый означает галоген и Pro означает защитную группу.
[0048]
На схеме A соединение (1) вводят в реакцию, например, с гидридом натрия и получают соединение (2) (стадия 1). Соединение (2) вводят в реакцию с галогеном (например, йодом) и получают соединение (3) (стадия 2).
[0049]
На схеме B аминогруппу соединения (4) защищают защитной группой (например, метоксиметильной группой) и получают соединение (5) (стадия 3). Соединение (5) вводят в реакцию с триизопропилсилилацетиленом и получают соединение (6) (стадия 4). Соединение (6) вводят в реакцию, например, с тетрабутиламмонийфторидом и получают соединение (7) (стадия 5).
[0050]
На схеме C соединение (3) вводят в реакцию с соединением (7) и получают соединение (8) (стадия 6). Из соединения (8) удаляют защитную группу и получают соединение (9) (стадия 7).
[0051]
Если соединение, описывающееся формулой (1), или его фармацевтически приемлемая соль обладает стереоизомерами, изомеры можно разделить по методике, известной в данной области техники. Примеры методики, известной в данной области техники, могут включать хроматографию, ферментные методики и методики кристаллизации.
[Примеры]
[0052]
Ниже настоящее изобретение описано подробнее со ссылкой на примеры и сравнительные примеры. Однако технический объем настоящего изобретения не ограничивается только ими.
[0053]
[Пример получения 1-1]
6-Бром-5-метилизобензофуран-1(3H)-он
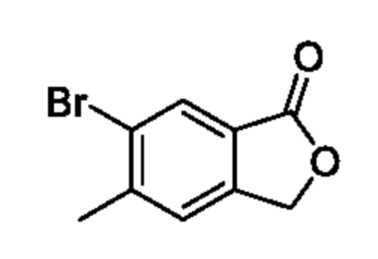
К смеси 3-бром-4-метилбензойной кислоты (1,5 г, 7,01 ммоля) и 1,1-дибромметана (20 мл) добавляли гидрофосфат калия (3,6 г, 21,0 ммоля) и ацетат палладия(II) (157 мг, 0,70 ммоля) при комнатной температуре и реакционную смесь перемешивали при 140°C в течение 48 ч. Температуру реакционной смеси возвращали к комнатной и фильтровали через целит, и промывали этилацетатом. Растворитель из фильтрата отгоняли при пониженном давлении и остаток растирали с этанолом и получали искомое соединение (1,3 г).
1H NMR (400 MHz, CDCl3): δ 8,09 (s, 1H), 7,37 (s, 1H), 5,23 (s, 2H), 2,53 (s, 3H).
[0054]
[Пример получения 1-2]
6-Бром-1,1,5-триметил-1,3-дигидроизобензофуран
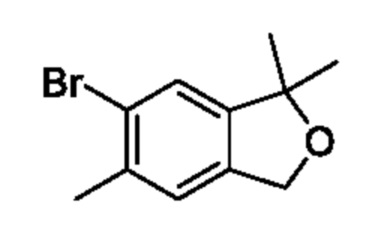
К смеси 6-бром-5-метилизобензофуран-1(3H)-она (1,00 г, 4,41 ммоля) и тетрагидрофурана (10 мл) добавляли метилмагниййодид (3,0 M раствор в диэтиловом эфире, 4,5 мл, 13,5 ммоля) при -15°C и смесь перемешивали при такой же температуре, как выше, в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (615 мг).
1H NMR (400 MHz, CDCl3): δ 7,45 (d, J=5,2 Hz, 1H), 7,20 (d, J=5,2 Hz, 1H), 4,77 (d, J=5,2 Hz, 2H), 2,37 (d, J=5,2 Hz, 3H), 1,68 (d, J=5,2 Hz, 6H).
[0055]
[Пример получения 1-3]
2-Хлор-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамид
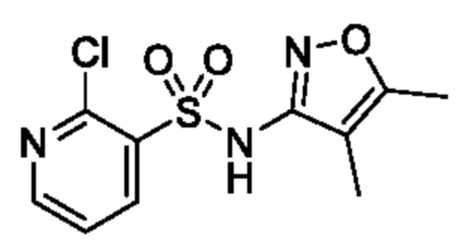
К смеси 4,5-диметилизоксазол-3-амина (1,0 г, 8,92 ммоля) и пиридина (20,0 мл) постепенно добавляли 4-диметиламинопиридин (109 мг, 0,892 ммоля) и 2-хлорпиридин-3-сульфонилхлорид (2,84 г, 13,4 ммоля) при 0°C и реакционную смесь перемешивали при 50°C в течение 16 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия. Растворитель отгоняли при пониженном давлении и получали искомое соединение (1,50 г) в неочищенном виде. Это соединение использовали в следующей реакции без дополнительной очистки.
ESI-MS: m/z 288,0 [M+1]+
[0056]
[Пример получения 1-4]
2-Хлор-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
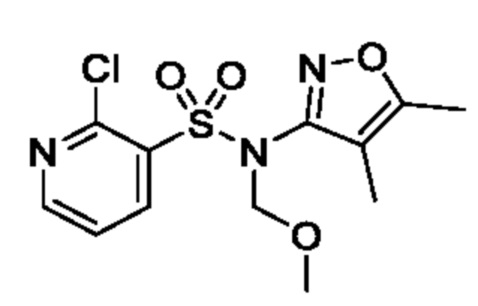
К смеси 2-хлор-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамида (1,80 г, 6,26 ммоля) и DMF (30,0 мл) постепенно добавляли 60% гидрид натрия (695 мг, 17,4 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли хлорметилметиловый эфир (1,06 мл, 13,9 ммоля) и смесь перемешивали при комнатной температуре в течение 3 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,20 г).
ESI-MS: m/z 332,07 [M+1]+
[0057]
[Пример получения 1-5]
N-(4,5-Диметилизоксазол-3-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамид
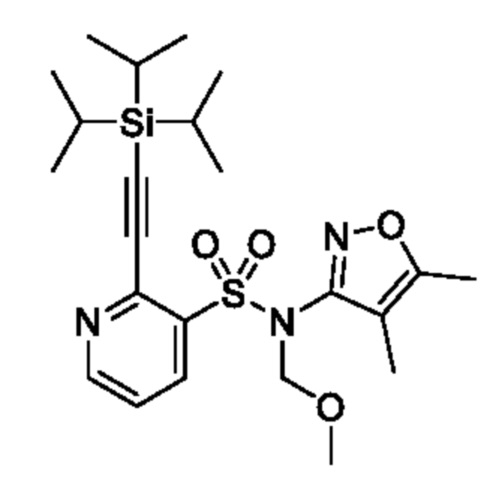
В атмосфере аргона к смеси 2-хлор-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (400 мг, 1,21 ммоля), триэтиламина (0,50 мл, 3,62 ммоля), триизопропилсилилацетилена (440 мг, 2,41 ммоля) и THF (5,00 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (84,6 мг, 0,121 ммоля) и йодид меди(I) (11,5 мг, 0,0362 ммоля) и реакционную смесь перемешивали при 55°C в течение 6 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,150 г).
1H NMR (400 MHz, DMSO-d6) δ 8,82 (d, 1H, J=4,8 Hz), 8,21 (d, 1H, J=8 Hz), 7,63-7,60 (m, 1H), 5,16 (s, 2H), 3,34 (s, 3H), 2,32 (s, 3H), 1,85 (s, 3H), 1,14 (bs, 21H).
[0058]
[Пример получения 1-6]
N-(4,5-Диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамид
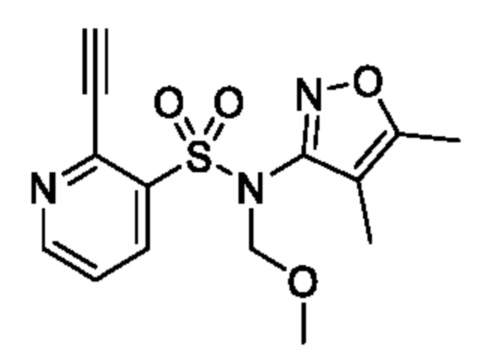
К смеси N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамида (150 мг, 4,3 ммоля) и THF (3,00 мл) постепенно добавляли тетрабутиламмонийфторид (1 моль/л раствор в тетрагидрофуране, 0,942 мл, 12,9 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,060 г).
ESI-MS: m/z 322,19 [M+1]+
[0059]
[Пример получения 1-7]
N-(4,5-Диметилизоксазол-3-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
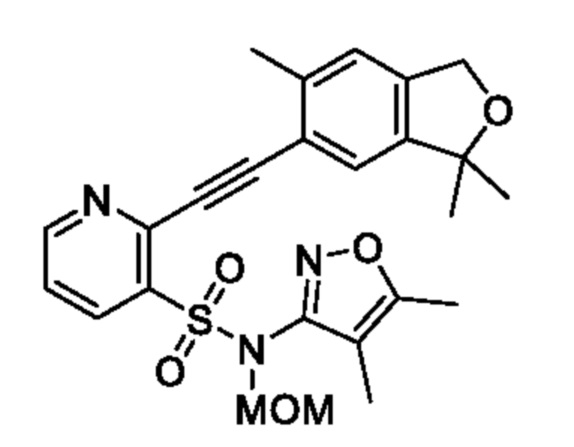
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (0,4 г, 1,25 ммоля) и N,N-диметилформамида (5 мл) добавляли 6-бром-1,1,5-триметил-1,3-дигидроизобензофуран (0,36 г, 1,49 ммоля), сульфат меди(II) (7,8 мг, 0,04 ммоля), триэтиламин (1,04 мл, 7,48 ммоля), аскорбат натрия (24 мг, 0,12 ммоля) и тетракис(трифенилфосфин)палладий(0) (28 мг, 0,02 ммоля) и реакционную смесь перемешивали при 80°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Kinetex F5, (250×50 мм) 5 мкм, смешанный раствор 0,1% водный раствор трифторуксусной кислоты/ацетонитрил-метанол (1:1)) и получали искомое соединение (615 мг).
ESI-MS: m/z 482,29 [M+1]+
[0060]
[Пример 1]
N-(4,5-Диметилизоксазол-3-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
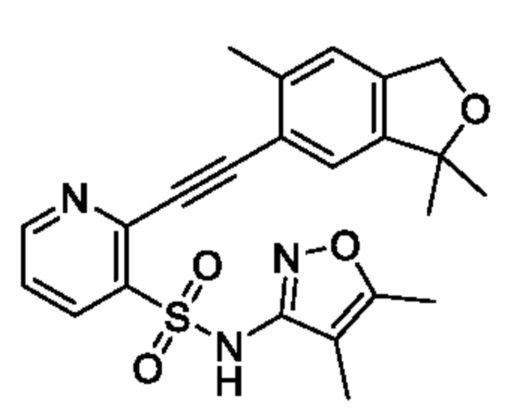
К смеси N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (90 мг, 0,18 ммоля) и метанола (5 мл) добавляли 6 моль/л хлористоводородную кислоту (1 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Omega Ps C18 (250×21,2 мм) 5 мкм, смешанный раствор 0,1% водный раствор трифторуксусной кислоты/ацетонитрил-метанол (1:1)) и получали искомое соединение (30 мг).
ESI-MS: m/z 438,24 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,06 (s, 1H), 8,83 (d, J=4,8 Hz, 2H), 8,35 (d, J=8 Hz, 1H), 7,66-7,63 (m, 1H), 7,48 (s, 1H), 7,24 (s, 1H), 4,96 (s, 2H), 2,46 (s, 3H), 2,07 (s, 3H), 1,81 (s, 3H), 1,43 (s, 6H).
[0061]
[Пример получения 2-1]
(E)-N'-(2-Гидрокси-5-метилбензилиден)ацетогидразид
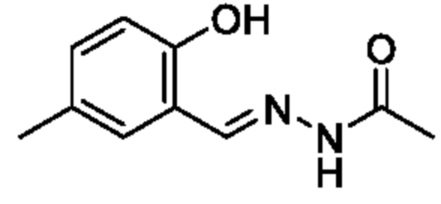
К смеси 2-гидрокси-5-метилбензальдегида (10 г, 73,5 ммоля) и этанола (50 мл) постепенно добавляли ацетогидразид (5,44 г, 73,5 ммоля) при комнатной температуре и реакционную смесь перемешивали при 90°C в течение 16 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и остаток промывали гексаном и получали искомое соединение (10 г) в неочищенном виде. Это соединение использовали в следующей реакции без дополнительной очистки.
[0062]
[Пример получения 2-2]
2-Ацетил-5-метилбензальдегид
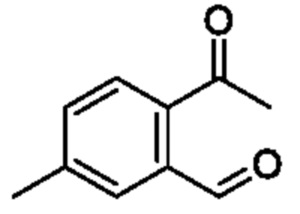
К смеси (E)-N'-(2-гидрокси-5-метилбензилиден)ацетогидразида (6 г, 31,3 ммоля) и тетрагидрофурана (90 мл) добавляли ацетат свинца(IV) (15,1 г, 34,4 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь фильтровали через целит, и промывали этилацетатом. Фильтрат промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,3 г).
ESI-MS: m/z 163,1 [M+1]+
[0063]
[Пример получения 2-3]
1-(2-(Гидроксиметил)-4-метилфенил)этан-1-ол
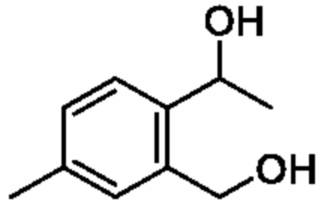
К смеси 2-ацетил-5-метилбензальдегид (2,5 г, 15,4 ммоля), тетрагидрофуран (10 мл) и этанол (30 мл), борогидрид натрия (2,9 г, 77,2 ммоля) добавляли при 0°C и реакционную смесь перемешивали при 70°C в течение 2 ч. Температуру реакционной смеси возвращали к комнатной и к реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,8 г).
1H NMR (400 MHz, CDCl3): δ 7,38-7,35 (m, 1H), 7,16 (d, J=2,4 Hz, 2H), 5,19-5,14 (m, 1H), 4,81 (t, J=8 Hz, 1H), 4,63 (d, J=12 Hz, 2H), 2,68 (s, 2H), 2,35 (d, J=4,8 Hz, 3H), 2,45 (d, J=5,2 Hz, 2H).
[0064]
[Пример получения 2-4]
1,5-Диметил-1,3-дигидроизобензофуран
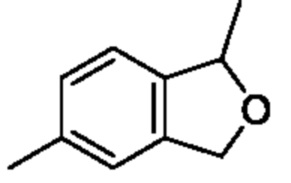
К смеси 1-(2-(гидроксиметил)-4-метилфенил)этан-1-ола (1,6 г, 9,64 ммоля) и тетрагидрофурана (16 мл) постепенно добавляли 60% гидрид натрия (1,07 г, 11,2 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси добавляли триметилфосфат (3,5 г, 24,1 ммоля) при комнатной температуре и смесь перемешивали при такой же температуре, как выше, в течение 16 ч. К реакционной смеси добавляли воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,0 г).
1H NMR (400 MHz, CDCl3): δ 7,12-7,06 (m, 3H), 5,31 (d, J=6,4 Hz, 1H), 5,14-5,01 (m, 2H), 2,39 (s, 3H), 1,50 (d, J=6,4 Hz, 3H).
[0065]
[Пример получения 2-5]
6-Бром-1,5-диметил-1,3-дигидроизобензофуран
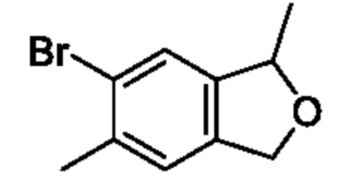
К смеси 1,5-диметил-1,3-дигидроизобензофурана (700 мг, 4,73 ммоля) и дихлорметана (7 мл) добавляли N-бромсукцинимид (842 мг, 4,73 ммоля) и трифторметансульфоновую кислоту (700 мг, 4,73 ммоля) при 0°C и смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,7 г).
1H NMR (400 MHz, CDCl3): δ 7,32 (dd, J=8,4 Hz, J=9,2 Hz, 1H), 7,09 (d, J=8 Hz, 1H), 5,29-5,24 (m, 1H), 5,07-5,02 (m, 1H), 4,95 (t, J=7,6 Hz, 1H), 2,41 (d, J=8,4 Hz, 3H), 1,49-1,46 (m, 3H).
[0066]
[Пример получения 2-6]
2-((3,6-Диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
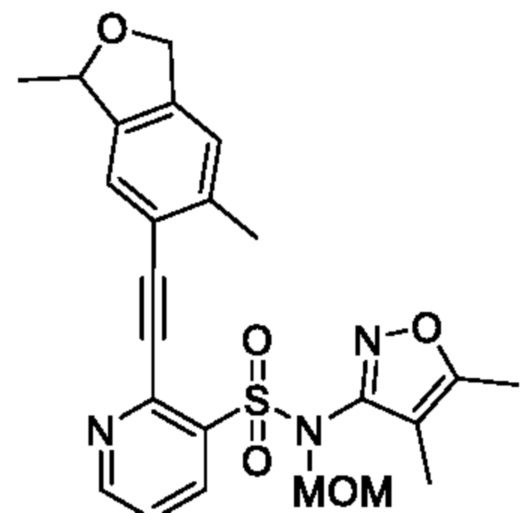
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (0,7 г, 2,18 ммоля) и N,N-диметилформамида (5 мл) добавляли 6-бром-1,5-диметил-1,3-дигидроизобензофуран (0,54 г, 2,40 ммоля), йодид меди(I) (83 мг, 0,436 ммоля), триэтиламин (0,6 мл, 4,36 ммоля) и тетракис(трифенилфосфин)палладий(0) (250 мг, 0,218 ммоля) и реакционную смесь перемешивали при 80°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C8 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (50 мг).
ESI-MS: m/z 468,27 [M+1]+
[0067]
[Пример 2]
2-((3,6-Диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамид
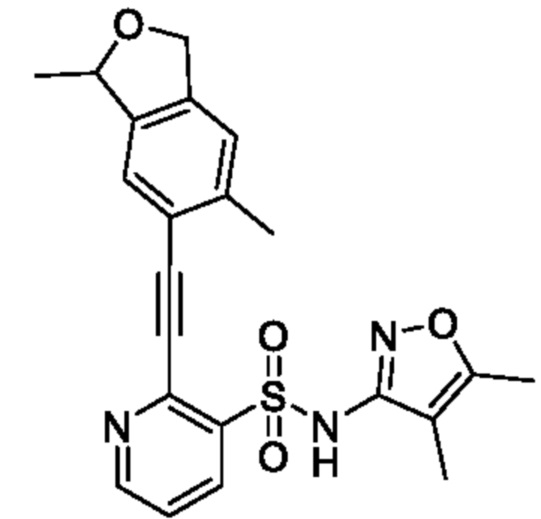
К смеси 2-((3,6-диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (50 мг, 0,107 ммоля) и метанола (5 мл) добавляли 6 моль/л хлористоводородную кислоту (1 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C8 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (22 мг).
ESI-MS: m/z 424,31 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,06 (s, 1H), 8,82 (d, J=4 Hz, 1H), 8,34 (t, J=6,8 Hz, 1H), 7,66-7,62 (m, 1H), 7,47 (d, J=5,2 Hz, 1H), 7,27 (d, J=5,2 Hz, 1H), 5,22 (d, J=9,6 Hz, 1H), 5,05-5,00 (m,1H), 4,95-4,90 (m, 1H), 2,47 (s, 3H), 2,09 (d, J=4,8 Hz, 3H), 1,81 (d, J=4,8 Hz, 3H), 1,42 (t, J=5,2 Hz, 3H).
[0068]
[Пример получения 3-1]
(4-Метил-1,2-фенилен)диметанол
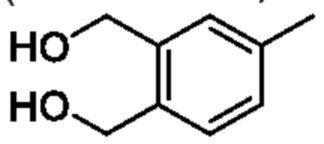
К смеси 5-метилизобензофуран-1,3-диона (100 г, 617 ммоля) и THF (1000 мл) постепенно добавляли комплекс борана с диметилсульфидом (156 мл, 1,85 моля) при 0°C и реакционную смесь перемешивали при 80°C в течение 16 ч. Температуру реакционной смеси возвращали к комнатной и к реакционной смеси добавляли метанол. Растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (40,0 г).
1H NMR (400 MHz, DMSO-d6) δ 7,23 (d, 1H, J=8,0 Hz), 7,18 (br s, 1H), 7,02 (d, 1H, J=7,6 Hz), 5,02 (t, 1H, J=5,6 Hz), 4,98 (t, 1H, J=5,2 Hz), 4,49 (dd, 4H, J=8,4, 14 Hz), 2,27 (s, 3H).
[0069]
[Пример получения 3-2]
5-Метил-1,3-дигидроизобензофуран
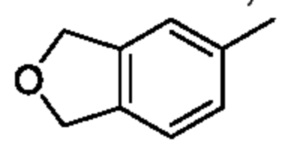
К смеси (4-метил-1,2-фенилен)диметанола (40,0 г, 263 ммоля) и DMF (200 мл) постепенно добавляли 50% гидрид натрия (15,8 г, 657 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли триметилфосфат (92,0 г, 657 ммоля) и смесь перемешивали при комнатной температуре в течение 3 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (20,50 г).
1H NMR (400 MHz, CDCl3) δ 7,12 (d, 1H, J=7,6 Hz), 7,08 (br s, 1H), 7,06 (d, 1H, J=4,8 Hz), 5,08 (s, 4H), 2,37 (s, 3H).
[0070]
[Пример получения 3-3]
5-Йод-6-метил-1,3-дигидроизобензофуран
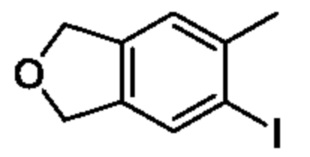
К смеси 5-метил-1,3-дигидроизобензофурана (1,00 г, 7,45 ммоля), метанола (5,00 мл) и этанола (5,00 мл) постепенно добавляли сульфат серебра (4,65 г, 14,9 ммоля) и йод (1,89 г, 14,9 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 1 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,60 г).
1H NMR (400 MHz, CDCl3) δ 7,68 (s, 1H), 7,11 (s, 1H), 5,03 (d, 4H, J=5,2 Hz), 2,44 (s, 3H).
[0071]
[Пример получения 3-4]
N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)-2-((6-метил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
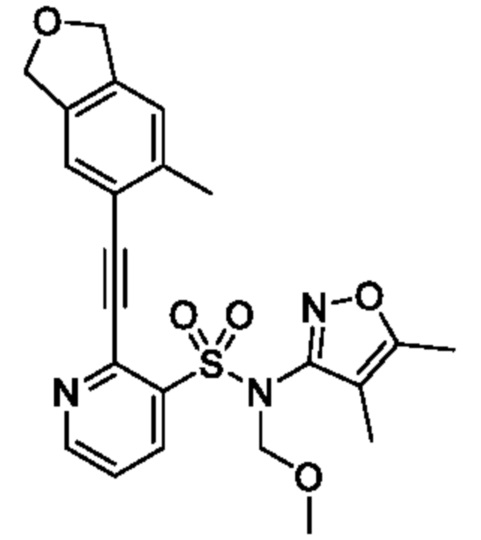
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (2,50 г, 7,78 ммоля), 5-йод-6-метил-1,3-дигидроизобензофурана (2,23 г, 8,56 ммоля), триэтиламина (2,19 мл, 15,6 ммоля) и толуола (30,0 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (899 мг, 0,778 ммоля) и йодид меди(I) (148 мг, 0,778 ммоля) и реакционную смесь перемешивали при 65°C в течение 6 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,60 г).
ESI-MS: m/z 454,27 [M+1]+
[0072]
[Пример 3]
N-(4,5-Диметилизоксазол-3-ил)-2-((6-метил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
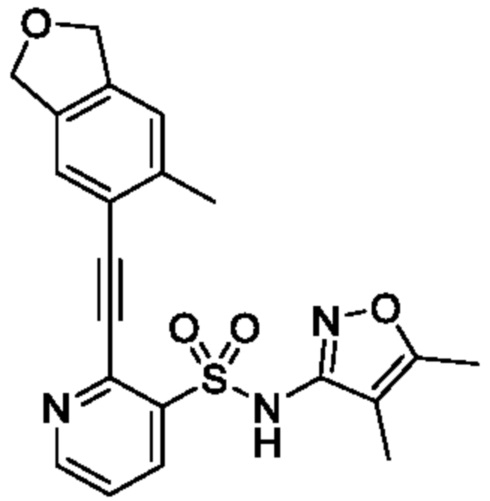
К смеси N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)-2-((6-метил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (1,00 г, 2,21 ммоля) и метанола (10,0 мл) добавляли 6 моль/л хлористоводородную кислоту (5,0 мл) при комнатной температуре и реакционную смесь перемешивали при 60°C в течение 16 ч. Температуру реакционной смеси возвращали к комнатной, и растворитель отгоняли при пониженном давлении. К остатку добавляли этилацетат. Органический слой промывали водой и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,110 г).
1H NMR (400 MHz, DMSO-d6) δ 11,03 (s, 1H), 8,82 (dd, 1H, J=4,8, 1,6 Hz), 8,33 (dd, 1H, J=8,4, 1,6 Hz), 7,63-7,60 (m, 1H), 7,50 (bs, 1H), 7,29 (bs, 1H), 5,00 (s, 4H), 2,50 (s, 3H), 2,10 (s, 3H), 1,80 (s, 3H).
[0073]
[Пример получения 4-1]
N-(4,5-Диметилизоксазол-3-ил)-N-(метоксиметил)-2-((6-метил-3-оксо-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
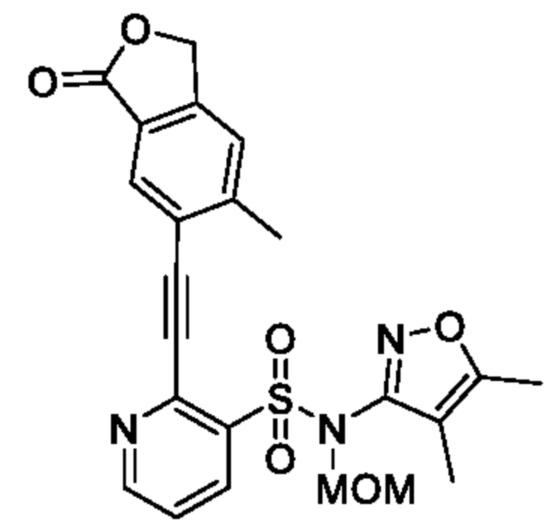
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (0,4 г, 1,24 ммоля) и N,N-диметилформамида (5 мл) добавляли 6-бром-5-метилизобензофуран-1(3H)-он (0,366 г, 1,61 ммоля), йодид меди(I) (47 мг, 0,24 ммоля), триэтиламин (0,35 мл, 2,48 ммоля) и тетракис(трифенилфосфин)палладий(0) (143 мг, 0,12 ммоля) и реакционную смесь перемешивали при 80°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C8 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (50 мг).
ESI-MS: m/z 468,24 [M+1]+
[0074]
[Пример 4]
N-(4,5-Диметилизоксазол-3-ил)-2-((6-метил-3-оксо-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
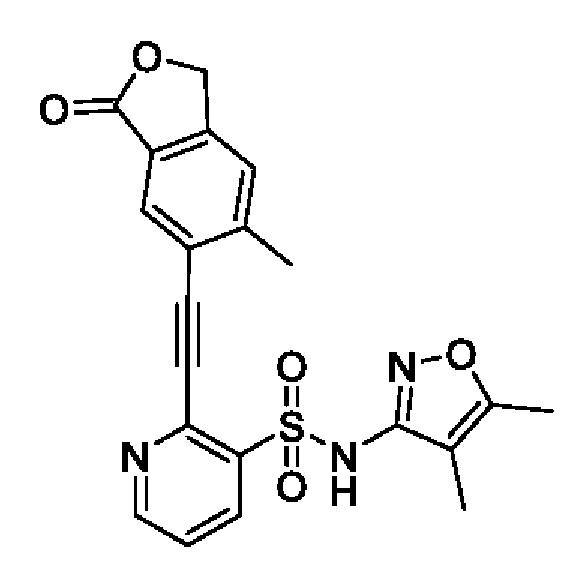
К смеси N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)-2-((6-метил-3-оксо-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (50 мг, 0,10 ммоля) и метанола (5 мл) добавляли 6 моль/л хлористоводородную кислоту (1 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (12 мг).
ESI-MS: m/z 424,18 [M+1]+
1H NMR (400 MHz, DMSO-d6) δ 11,21 (s, 1H), 8,86 (t, J=5,2 Hz, 1H), 8,37 (t, J=5,2 Hz, 1H), 8,08 (d, J=4,8 Hz, 1H), 7,67 (t, J=4,8 Hz, 2H), 5,45 (d, J=5,2 Hz, 2H), 2,61 (d, J=5,2 Hz, 3H), 2,11 (d, J=5,2 Hz, 3H), 1,81 (d, J=5,2 Hz, 3H).
[0075]
[Пример получения 5-1]
2-((1,3-Дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
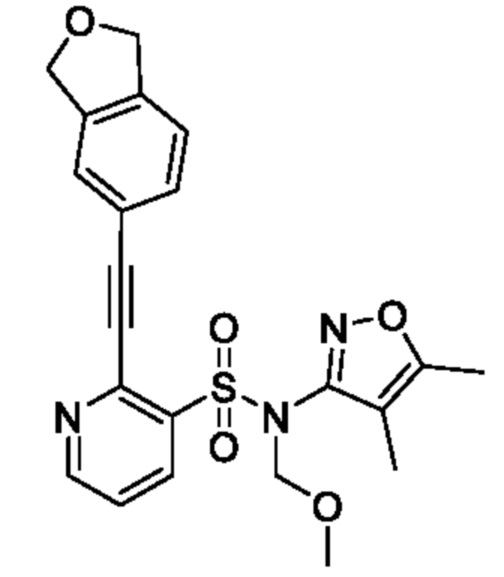
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (250 мг, 0,778 ммоля) и толуола (10 мл) добавляли 5-бром-1,3-дигидроизобензофуран (170 мг, 0,856 ммоля), йодид меди(I) (15 мг, 0,077 ммоля), триэтиламин (0,22 мл, 1,56 ммоля) и тетракис(трифенилфосфин)палладий(0) (90 мг, 0,077 ммоля) и реакционную смесь перемешивали при 80°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (50 мг).
ESI-MS: m/z 440,27 [M+1]+
[0076]
[Пример 5]
2-((1,3-Дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамид
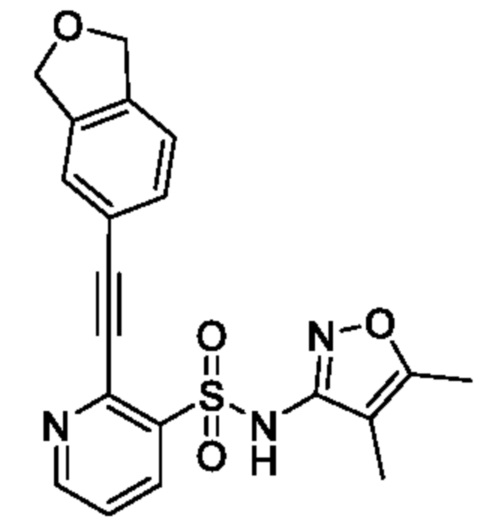
К смеси 2-((1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (100 мг, 0,227 ммоля) и метанола (5 мл) добавляли 6 моль/л хлористоводородную кислоту (1 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 8 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (16 мг).
ESI-MS: m/z 396,23 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,10 (s, 1H), 8,80 (s, 1H), 8,34 (t, J=6,4 Hz, 1H), 7,63 (t, J=13,2 Hz, 1H), 7,57-7,53 (m, 2H), 7,44 (t, J=6,4 Hz, 1H), 5,05 (d, J=8 Hz, 1H), 3,33 (s, 3H), 2,09 (s, 3H), 1,80 (s, 3H).
[0077]
[Пример получения 6-1]
5-Хлор-6-йодизобензофуран-1(3H)-он
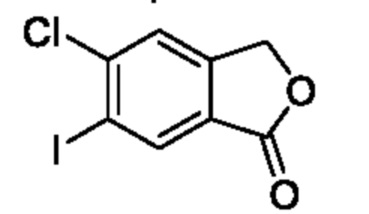
В атмосфере аргона к смеси 4-хлор-3-йодбензойной кислоты (1,0 г, 3,5 ммоля), 1,1-дибромметана (15 мл) и гидрофосфата калия (2,25 г, 10,6 ммоля) добавляли ацетат палладия(II) (80 мг, 0,35 ммоля) и реакционную смесь перемешивали при 140°C в течение 16 ч. Температуру реакционной смеси возвращали к комнатной и фильтровали через целит, и промывали этилацетатом. Фильтрат промывали водой и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,4 г).
1H NMR (400 MHz, DMSO-d6): δ 8,35 (s, 1H), 7,97 (s, 1H), 5,34 (s, 2H).
[0078]
[Пример получения 6-2]
5-Хлор-6-йод-1,3-дигидроизобензофуран-1-ол
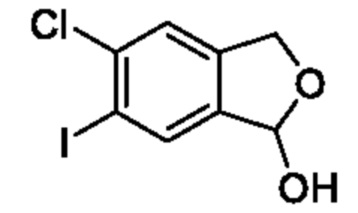
К смеси 5-хлор-6-йодизобензофуран-1(3H)-она (200 мг, 0,680 ммоля) и дихлорметана (30 мл) добавляли диизобутилалюминийгидрид (20% раствор в толуоле, 1,7 мл, 2,0 ммоля) при -78°C и смесь перемешивали при такой же температуре, как выше, в течение 2 ч. насыщенный водный раствор хлорида аммония к реакционной смеси добавляли, и фильтровали через целит, и промывали этилацетатом. Фильтрат промывали водой и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (70 мг).
1H NMR (400 MHz, DMSO-d6): δ 7,89 (s, 1H), 7,61 (s,1H),6,89 (d, J=7,6 Hz, 1H), 6,75 (dd, J=7,6, 8,0 Hz, 1H),4,99 (d, J=13,6 Hz, 1H), 4,84 (d, J=12,8 Hz, 1H), 4,83 (d, J=13,6 Hz, 1H).
[0079]
[Пример получения 6-3]
5-Хлор-6-йод-1,3-дигидроизобензофуран
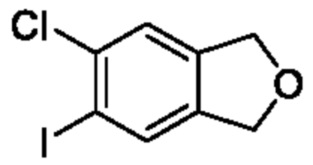
К смеси 5-хлор-6-йод-1,3-дигидроизобензофуран-1-ола (300 мг, 1,01 ммоля) и дихлорметана (26 мл) добавляли трифторуксусную кислоту (0,11 мл, 1,5 ммоля) и триэтилсилан (0,4 мл, 2,6 ммоля) при комнатной температуре и смесь перемешивали при такой же температуре, как выше, в течение 4 ч. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали дихлорметаном. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (200 мг).
1H NMR (400 MHz, DMSO-d6): δ 7,90 (s, 1H), 7,56 (s, 1H), 4,94 (s, 4H).
[0080]
[Пример получения 6-4]
2-((6-Хлор-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
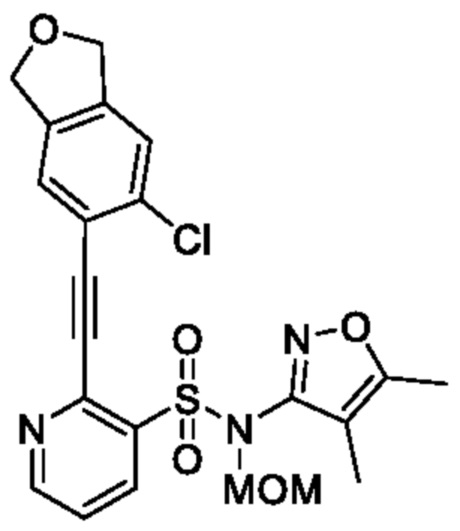
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (120 мг, 0,373 ммоля) и N,N-диметилформамида (5 мл) добавляли 5-хлор-6-йод-1,3-дигидроизобензофуран (126 мг, 0,448 ммоля), йодид меди(I) (7,08 мг, 0,037 ммоля), триэтиламин (0,16 мл, 1,12 ммоля) и тетракис(трифенилфосфин)палладий(0) (43 мг, 0,037 ммоля) и реакционную смесь перемешивали при 60°C в течение 2 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (95 мг).
ESI-MS: m/z 473,9 [M+1]+
[0081]
[Пример 6]
2-((6-Хлор-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамид
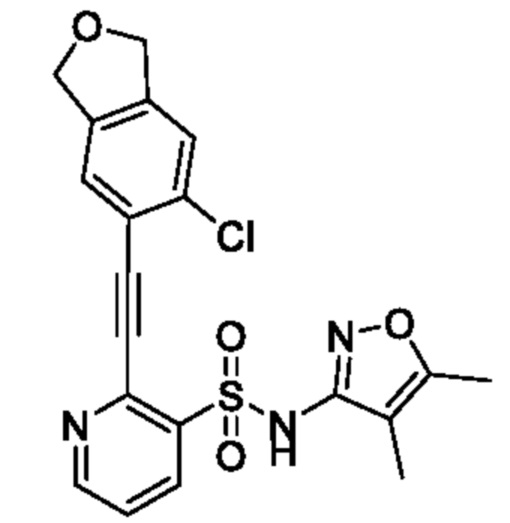
К смеси 2-((6-хлор-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (120 мг, 0,253 ммоля), метанола (5 мл) и ацетонитрила (1 мл) добавляли 50% серную кислоту (1,2 мл) при 0°C и реакционную смесь перемешивали при 60°C в течение 2 ч. Температуру реакционной смеси возвращали к комнатной, к ней добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Kinetex penta C18 (250×50 мм) 5 мкм, 0,1% водный раствор трифторуксусной кислоты/ацетонитрил) и получали искомое соединение (40 мг).
ESI-MS: m/z 430,01 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,08 (s, 1H), 8,84 (d, J=4,0 Hz, 1H), 8,34 (d, J= 8,4 Hz, 1H), 7,69-7,65 (m, 1H), 7,64 (s,1H),7,61 (s,1H), 4,14 (s, 4H), 2,11 (s, 3H), 1,79 (s,3H).
[0082]
[Пример получения 7-1]
2-(2-(Гидроксиметил)-4-метилфенил)пропан-2-ол
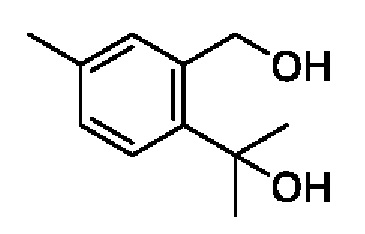
К смеси 5-метилизобензофуран-1(3H)-она (2,40 г, 16,2 ммоля) и тетрагидрофурана (30 мл) добавляли метилмагнийбромид (3,0 M раствор в эфире, 16,2 мл, 48,6 ммоля) при 0°C и смесь перемешивали при комнатной температуре в течение 3 ч. К реакционной смеси добавляли насыщенный водный раствор хлорида аммония, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,30 г).
1H NMR (400Hz, DMSO-d6) δ 7,30 (s, 1H), 7,19 (d, J=8,0 Hz, 1H), 6,95 (d, J=8,0 Hz, 1H), 5,09 (s, 1H), 4,98 (t, J=5,6 Hz, 1H), 4,75 (d, J=5,6 Hz, 2H), 2,25 (s, 3H), 1,46 (s, 6H).
[0083]
[Пример получения 7-2]
1,1,5-Триметил-1,3-дигидроизобензофуран
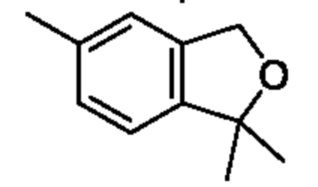
К смеси 2-(2-(гидроксиметил)-4-метилфенил)пропан-2-ола (1,30 г, 7,22 ммоля) и тетрагидрофурана (20 мл) постепенно добавляли 50% гидрид натрия (0,69 г, 14,4 ммоля) при 0°C и смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси постепенно добавляли триметилфосфат (2,01 г, 14,4 ммоля) при комнатной температуре и смесь перемешивали при такой же температуре, как выше, в течение 4 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,60 г).
1H NMR (400Hz, DMSO-d6) δ 7,11 (d, J=7,6 Hz, 1H), 7,04 (t, J=4,8 Hz, 2H), 4,89 (s, 2H), 2,29 (s, 3H), 1,37 (s, 6H).
[0084]
[Пример получения 7-3]
6-Йод-1,1,5-триметил-1,3-дигидроизобензофуран
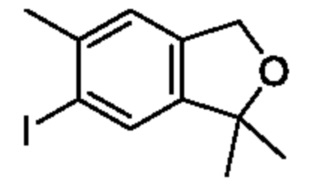
К смеси 1,1,5-триметил-1,3-дигидроизобензофурана (0,60 г, 3,7 ммоля) и дихлорметана (10 мл) постепенно добавляли N-йодсукцинимид (1,60 г, 7,40 ммоля) и трифторметансульфоновую кислоту (1,10 г, 7,40 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 2 ч. К реакционной смеси добавляли 10% водный раствор тиосульфата натрия к, затем экстрагировали дихлорметаном. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,30 г).
1H NMR (400Hz, DMSO-d6) δ 7,71 (s, 1H), 7,22 (s, 1H), 4,86 (s, 2H), 2,35 (s, 3H), 1,38 (s, 6H).
[0085]
[Пример получения 7-4]
2-Хлор-N-(4-хлор-5-метилизоксазол-3-ил)пиридин-3-сульфонамид
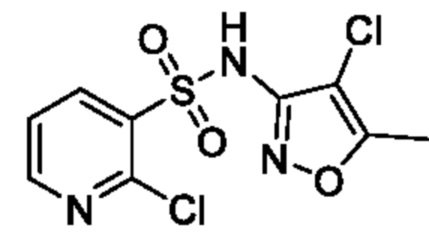
К смеси 4-хлор-5-метилизоксазол-3-амина (2,98 г, 22,6 ммоля) и пиридина (50 мл) постепенно добавляли 4-диметиламинопиридин (0,69 г, 5,66 ммоля) и 2-хлорпиридин-3-сульфонилхлорид (4,0 г, 18,8 ммоля) при 0°C и реакционную смесь перемешивали при 55°C в течение 16 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали с помощью 2 н. хлористоводородной кислоты и насыщенным рассолом и сушили над сульфатом натрия. Растворитель отгоняли при пониженном давлении и получали искомое соединение (1,90 г) в неочищенном виде. Это соединение использовали в следующей реакции без дополнительной очистки.
ESI-MS: m/z 307,98 [M+1]+
[0086]
[Пример получения 7-5]
2-Хлор-N-(4-хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
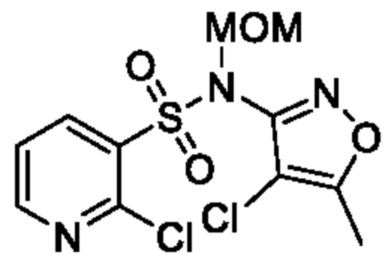
К смеси 2-хлор-N-(4-хлор-5-метилизоксазол-3-ил)пиридин-3-сульфонамида (1,90 г, 6,98 ммоля) и N,N-диметилформамида (20,0 мл) постепенно добавляли 50% гидрид натрия (594 мг, 12,3 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли хлорметилметиловый эфир (0,69 мл, 9,28 ммоля) и смесь перемешивали при комнатной температуре в течение 3 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,0 г).
1H NMR (400Hz, DMSO-d6) δ 8,71 (d, J=4,4 Hz, 1H), 8,39 (d, J=8,0 Hz, 1H), 7,66 (dd, J=7,6 Hz, 4,8 Hz, 1H), 5,20 (s, 2H), 3,39 (s, 3H), 2,43 (s, 3H).
[0087]
[Пример получения 7-6]
N-(4-Хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамид
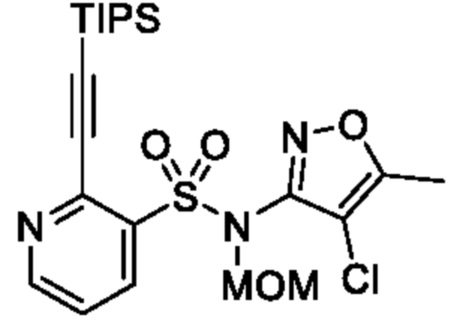
В атмосфере аргона к смеси 2-хлор-N-(4-хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (1,20 г, 3,41 ммоля), триэтиламина (1,44 мл, 10,2 ммоля), триизопропилсилилацетилена (1,24 г, 6,83 ммоля) и тетрагидрофурана (15 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (239 мг, 0,34 ммоля) и йодид меди(I) (20 мг, 0,10 ммоля) и реакционную смесь перемешивали при 55°C в течение 6 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,70 г).
1H NMR (400Hz, DMSO-d6) δ 8,83 (d, J=3,6 Hz, 1H), 8,28 (t, J=7,2 Hz, 1H), 7,62-7,66 (m, 1H), 5,19 (s, 2H), 3,33 (d, J=6,0 Hz, 3H), 2,43 (s, 3H), 1,10 (d, J=3,6 Hz, 21H).
[0088]
[Пример получения 7-7]
N-(4-Хлор-5-метилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамид
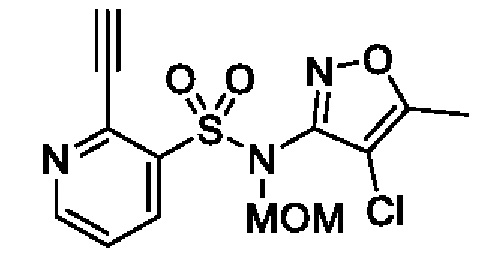
К смеси N-(4-хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамида (0,70 г, 1,4 ммоля) и тетрагидрофурана (10 мл) постепенно добавляли тетрабутиламмонийфторид (1 моль/л раствор в тетрагидрофуране, 2,81 мл, 2,81 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,38 г).
ESI-MS: m/z 342,15 [M+1]+
[0089]
[Пример получения 7-8]
N-(4-Хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
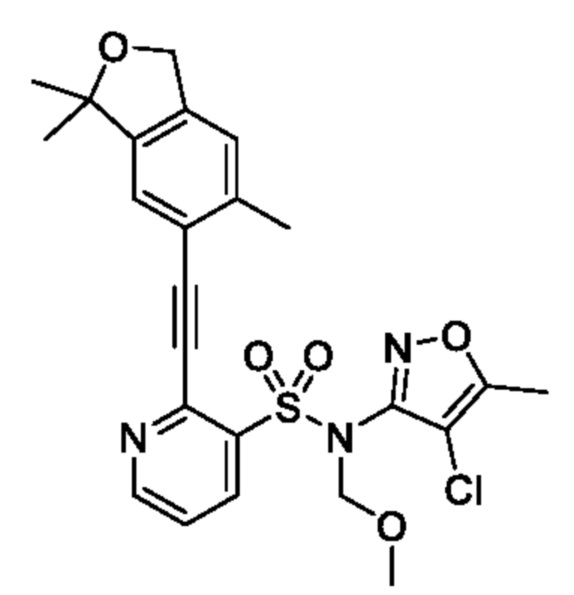
В атмосфере аргона к смеси N-(4-хлор-5-метилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (0,38 г, 1,11 ммоля) и толуола (5 мл) добавляли 6-йод-1,1,5-триметил-1,3-дигидроизобензофуран (0,32 г, 1,11 ммоля), йодид меди(I) (6,35 мг, 0,03 ммоля), триэтиламин (0,46 мл, 3,34 ммоля) и тетракис(трифенилфосфин)палладий(0) (128 мг, 0,11 ммоля) и реакционную смесь перемешивали при 65°C в течение 6 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,25 г).
ESI-MS: m/z 502,10 [M+1]+
[0090]
[Пример 7]
N-(4-Хлор-5-метилизоксазол-3-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
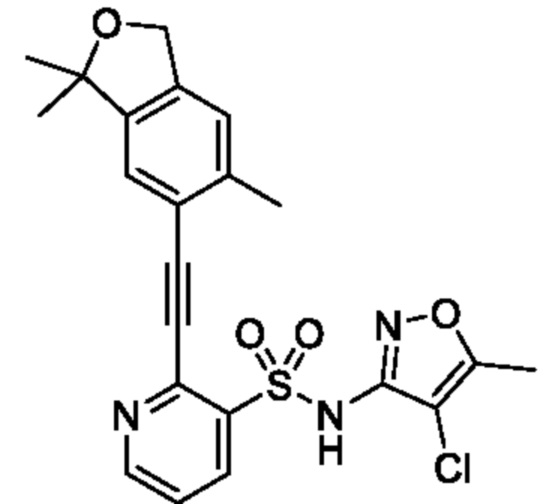
К смеси N-(4-хлор-5-метилизоксазол-3-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (0,25 г, 0,49 ммоля) и метанола (3 мл) добавляли 6 моль/л хлористоводородную кислоту (3 мл) при 0°C и реакционную смесь перемешивали при 60°C в течение 16 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (35 мг).
ESI-MS: m/z 458,08 [M+1]+
1H-NMR (400Hz, DMSO-d6) δ 8,52 (d, J=3,6 Hz, 1H), 8,19 (d, J=8,0, 1H), 7,46 (s, 1H), 7,39 (dd, J=8,0, 4,8 Hz, 1H), 7,18 (s, 1H), 4,94 (s, 2H), 2,54 (s, 3H), 2,11 (s, 3H), 1,42 (s, 6H).
[0091]
[Пример получения 8-1]
2-Хлор-N-(3,4-диметилизоксазол-5-ил)пиридин-3-сульфонамид
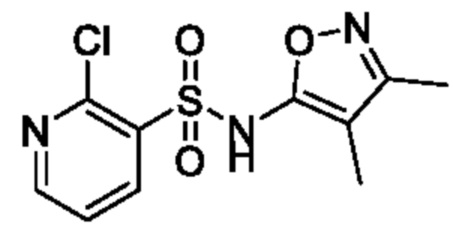
К смеси 3,4-диметилизоксазол-5-амина (1,0 г, 8,9 ммоля) и пиридина (10 мл) постепенно добавляли 4-диметиламинопиридин (108 мг, 0,89 ммоля) и 2-хлорпиридин-3-сульфонилхлорид (2,8 г, 13,2 ммоля) при комнатной температуре и реакционную смесь перемешивали при 50°C в течение 16 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали с помощью 2 н. хлористоводородной кислоты и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (2,0 г).
ESI-MS: m/z 287,9 [M+1]+
[0092]
[Пример получения 8-2]
2-Хлор-N-(3,4-диметилизоксазол-5-ил)-N-(метоксиметил)пиридин-3-сульфонамид
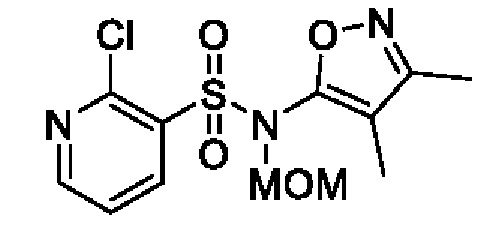
К смеси 2-хлор-N-(3,4-диметилизоксазол-5-ил)пиридин-3-сульфонамида (2,0 г, 7,0 ммоля) и N,N-диметилформамида (10 мл) постепенно добавляли 60% гидрид натрия (334 мг, 13,9 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли хлорметилметиловый эфир (0,83 г, 10,5 ммоля) и смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (2,0 г).
ESI-MS: m/z 332,18 [M+1]+
[0093]
[Пример получения 8-3]
N-(3,4-Диметилизоксазол-5-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамид
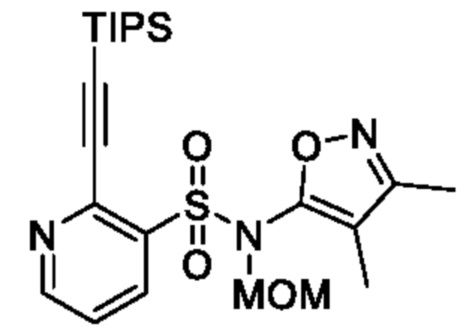
В атмосфере аргона к смеси 2-хлор-N-(3,4-диметилизоксазол-5-ил)-N-(метоксиметил)пиридин-3-сульфонамида (2,0 г, 6,0 ммоля), триэтиламина (1,8 г, 18 ммоля), триизопропилсилилацетилена (1,65 г, 9,06 ммоля) и N,N-диметилформамида (10 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (150 мг, 0,604 ммоля) и йодид меди(I) (114 мг, 0,604 ммоля) и реакционную смесь перемешивали при 100°C в течение 16 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,5 г).
ESI-MS: m/z 478,1 [M+1]+
[0094]
[Пример получения 8-4]
N-(3,4-Диметилизоксазол-5-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамид
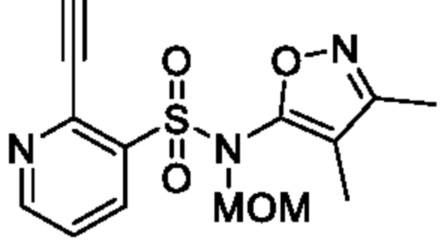
К смеси N-(3,4-диметилизоксазол-5-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамида (1,0 г, 2,1 ммоля) и тетрагидрофурана (10 мл) постепенно добавляли тетрабутиламмонийфторид (1 моль/л раствор в тетрагидрофуране, 3,1 мл, 3,1 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли воду, затем экстрагировали этилацетатом. Органический слой сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (350 мг).
ESI-MS: m/z 322,0 [M+1]+
[0095]
[Пример получения 8-5]
N-(3,4-Диметилизоксазол-5-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
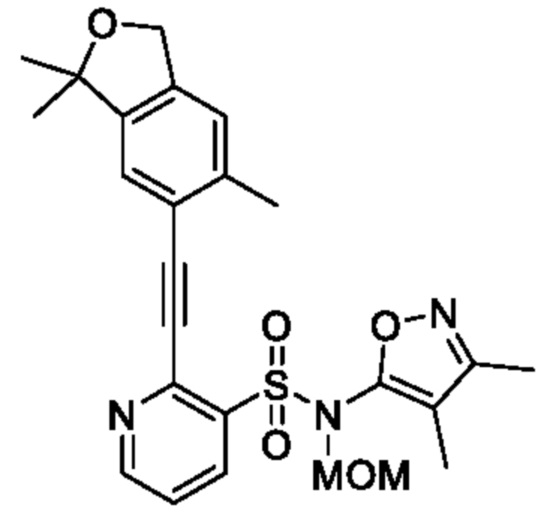
В атмосфере аргона к смеси N-(3,4-диметилизоксазол-5-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (300 мг, 0,93 ммоля) и N,N-диметилформамида (3 мл), 6-йод-1,1,5-триметил-1,3-дигидроизобензофуран (296 мг, 1,02 ммоля) добавляли йодид меди(I) (17 мг, 0,09 ммоля), триэтиламин (282 мг, 2,79 ммоля) и тетракис(трифенилфосфин)палладий(0) (103 мг, 0,09 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (250 мг).
ESI-MS: m/z 482,39 [M+1]+
[0096]
[Пример 8]
N-(3,4-Диметилизоксазол-5-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
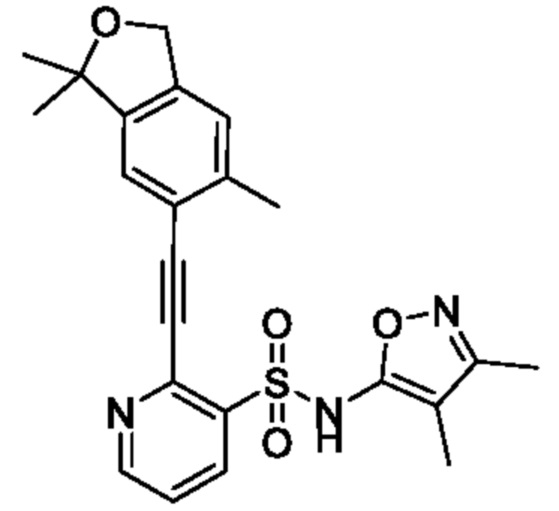
К смеси N-(3,4-диметилизоксазол-5-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (200 мг, 0,415 ммоля) и метанола (4 мл) добавляли 50% серную кислоту (4 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 1 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (60 мг).
ESI-MS: m/z 438,31 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,25 (s, 1H), 8,79 (s, 1H), 8,30 (d, J= 7,2 Hz, 1H), 7,609 (s, 1H), 7,390 (s, 1H), 7,224 (s, 1H), 4,95 (s, 2H), 2,46 (s, 3H),1,82 (s, 3H), 1,66 (s, 3H), 1,43 (s, 6H).
[0097]
[Пример получения 9-1]
2-Хлор-N-(4-хлор-3-метилизоксазол-5-ил)пиридин-3-сульфонамид
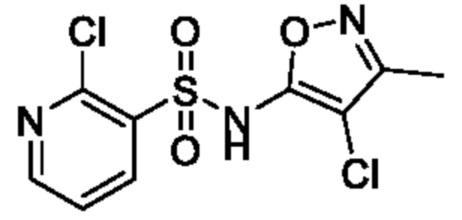
К смеси 4-хлор-3-метилизоксазол-5-амина (1,5 г, 11,4 ммоля) и тетрагидрофурана (15 мл) постепенно добавляли 60% гидрид натрия (909 мг, 22,7 ммоля) и 2-хлорпиридин-3-сульфонилхлорид (2,89 г, 13,6 ммоля) при 0°C и смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (2,5 г).
ESI-MS: m/z 307,9 [M+1]+
[0098]
[Пример получения 9-2]
2-Хлор-N-(4-хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)пиридин-3-сульфонамид
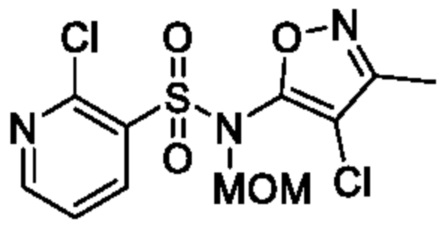
К смеси 2-хлор-N-(4-хлор-3-метилизоксазол-5-ил)пиридин-3-сульфонамида (1,8 г, 5,8 ммоля) и N,N-диметилформамида (20 мл) постепенно добавляли 60% гидрид натрия (467 мг, 11,7 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли хлорметилметиловый эфир (0,54 мл, 8,8 ммоля) и смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (1,3 г).
ESI-MS: m/z 352,27 [M+1]+
[0099]
[Пример получения 9-3]
N-(4-Хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамид
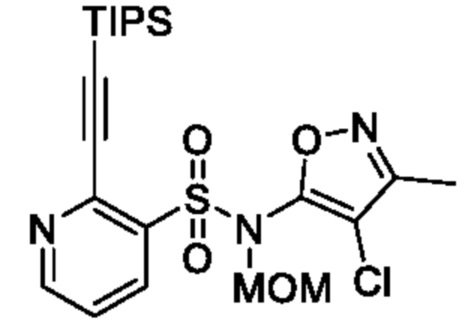
В атмосфере аргона к смеси 2-хлор-N-(4-хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)пиридин-3-сульфонамида (1,3 г, 3,7 ммоля), триэтиламина (1,46 мл, 11,1 ммоля), триизопропилсилилацетилена (0,8 г, 4,4 ммоля) и N,N-диметилформамида (6,5 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (134 мг, 0,184 ммоля) и йодид меди(I) (140 мг, 0,738 ммоля) и реакционную смесь перемешивали при 100°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и фильтровали через целит, и промывали этилацетатом. Фильтрат промывали водой и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (600 мг).
ESI-MS: m/z 498,51 [M+1]+
[0100]
[Пример получения 9-4]
N-(4-Хлор-3-метилизоксазол-5-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамид
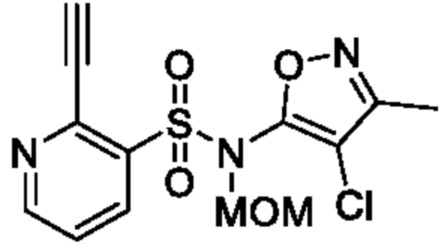
К смеси N-(4-хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)-2-((триизопропилсилил)этинил)пиридин-3-сульфонамида (600 мг, 1,20 ммоля) и тетрагидрофурана (10 мл) постепенно добавляли тетрабутиламмонийфторид (1 моль/л раствор в тетрагидрофуране, 1,2 мл, 1,2 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли воду, затем экстрагировали этилацетатом. Органический слой сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (220 мг).
ESI-MS: m/z 342,0 [M+1]+
[0101]
[Пример получения 9-5]
N-(4-Хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
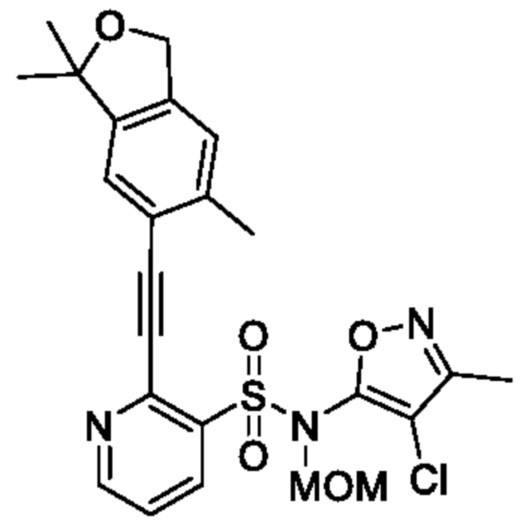
В атмосфере аргона к смеси N-(4-хлор-3-метилизоксазол-5-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (250 мг, 0,73 ммоля) и N,N-диметилформамида (5 мл) добавляли 6-йод-1,1,5-триметил-1,3-дигидроизобензофуран (232 мг, 0,81 ммоля), йодид меди(I) (27 мг, 0,15 ммоля), триэтиламин (0,48 мл, 3,66 ммоля) и тетракис(трифенилфосфин)палладий(0) (84 мг, 0,073 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (200 мг).
ESI-MS: m/z 502,56 [M+1]+
[0102]
[Пример 9]
N-(4-Хлор-3-метилизоксазол-5-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
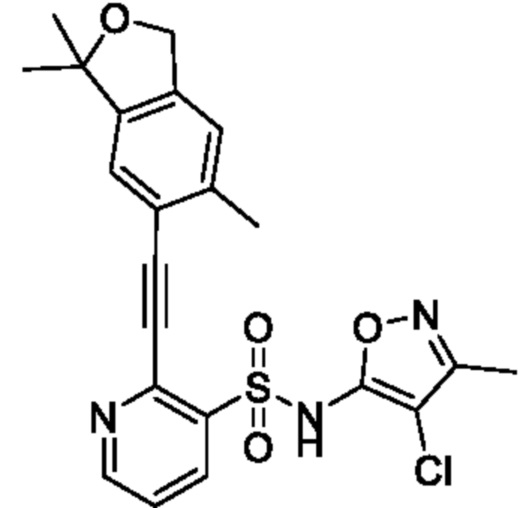
К смеси N-(4-хлор-3-метилизоксазол-5-ил)-N-(метоксиметил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамида (200 мг, 0,39 ммоля) и метанола (2 мл) добавляли 50% серную кислоту (2 мл) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток перекристаллизовывали из диэтилового эфира и получали искомое соединение (35 мг).
ESI-MS: m/z 458,36 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 8,69 (d, J=3,6 Hz, 1H), 8,30 (dd, J=8,0 Hz, 1,2 Hz, 1H), 7,55-7,52 (m, 1H), 7,49 (s, 1H), 7,07 (s, 1H), 4,94 (s, 2H), 2,49 (s, 3H), 1,89 (s, 3H), 1,42 (s, 6H).
[0103]
[Пример получения 10-1]
2-Хлор-N-(3-метокси-5-метилпиразин-2-ил)пиридин-3-сульфонамид
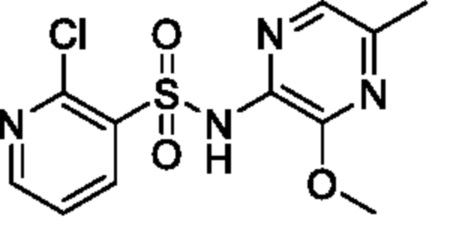
К смеси 3-метокси-5-метилпиразин-2-амина (0,2 г, 1,4 ммоля) и пиридина (5 мл) постепенно добавляли 4-диметиламинопиридин (17,5 мг, 0,143 ммоля) и 2-хлорпиридин-3-сульфонилхлорид (366 мг, 1,73 ммоля) при комнатной температуре и реакционную смесь перемешивали при 70°C в течение 16 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали с помощью 6 н. хлористоводородной кислоты и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,16 г).
ESI-MS: m/z 315,0 [M+1]+
[0104]
[Пример получения 10-2]
2-Хлор-N-(3-метокси-5-метилпиразин-2-ил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамид
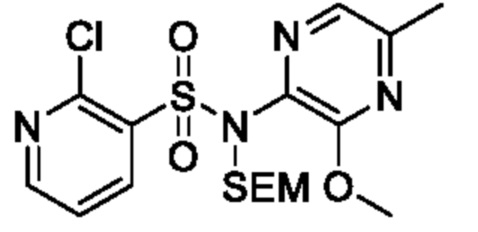
К смеси 2-хлор-N-(3-метокси-5-метилпиразин-2-ил)пиридин-3-сульфонамида (50 мг, 0,16 ммоля) и N,N-диметилформамида (2 мл) постепенно добавляли карбонат калия (44 мг, 0,32 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси постепенно добавляли 2-(триметилсилил)этоксиметилхлорид (0,1 мл, 0,24 ммоля) и смесь перемешивали при комнатной температуре в течение 30 мин. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (40 мг).
ESI-MS: m/z 445,0 [M+1]+
[0105]
[Пример получения 10-3]
N-(3-Метокси-5-метилпиразин-2-ил)-2-((триизопропилсилил)этинил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамид
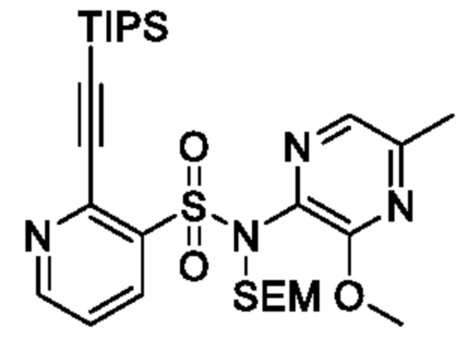
В атмосфере аргона к смеси 2-хлор-N-(3-метокси-5-метилпиразин-2-ил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамида (0,4 г, 0,9 ммоля), триэтиламин (0,4 мл, 2,7 ммоля), триизопропилсилилацетилена (0,3 мл, 1,3 ммоля) и N,N-диметилформамида (5 мл) добавляли бис(трифенилфосфин)палладий(II)дихлорид (63 мг, 0,089 ммоля) и йодид меди(I) (34,2 мг, 0,179 ммоля) и реакционную смесь перемешивали при 100°C в течение 5 ч. Температуру реакционной смеси возвращали к комнатной и фильтровали через целит, и промывали этилацетатом. Фильтрат промывали водой и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (160 мг).
ESI-MS: m/z 591,55 [M+1]+
[0106]
[Пример получения 10-4]
2-Этинил-N-(3-метокси-5-метилпиразин-2-ил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамид
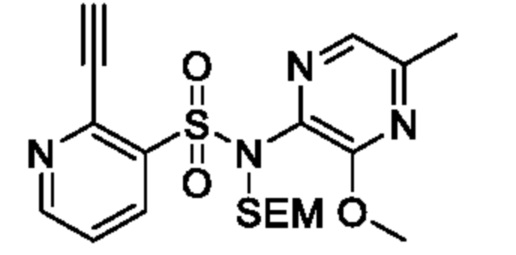
К смеси N-(3-метокси-5-метилпиразин-2-ил)-2-((триизопропилсилил)этинил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамида (0,16 г, 0,27 ммоля) и тетрагидрофурана (5 мл) постепенно добавляли тетрабутиламмонийфторид (1 моль/л раствор в тетрагидрофуране, 0,27 мл, 0,27 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли воду, затем экстрагировали этилацетатом. Органический слой сушили над сульфатом натрия и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (80 мг).
ESI-MS: m/z 435,2 [M+1]+
[0107]
[Пример получения 10-5]
N-(3-Метокси-5-метилпиразин-2-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамид
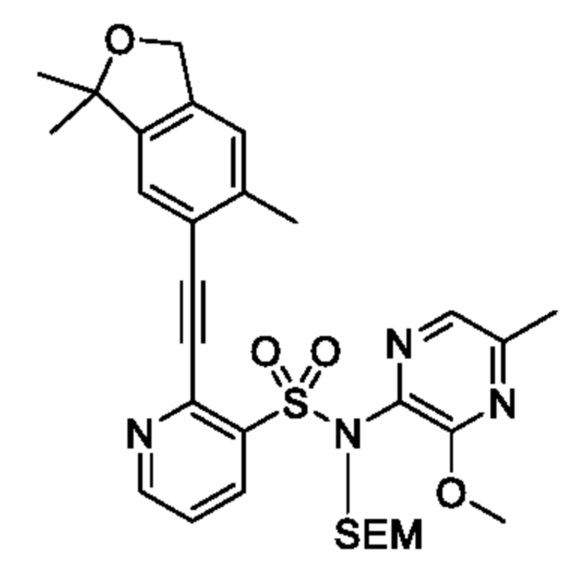
В атмосфере аргона к смеси 2-этинил-N-(3-метокси-5-метилпиразин-2-ил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамида (200 мг, 0,460 ммоля) и N,N-диметилформамида (5 мл) добавляли 6-йод-1,1,5-триметил-1,3-дигидроизобензофуран (146 мг, 0,506 ммоля), йодид меди(I) (9 мг, 0,046 ммоля), триэтиламин (0,2 мл, 1,38 ммоля) и тетракис(трифенилфосфин)палладий(0) (53 мг, 0,046 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (170 мг).
ESI-MS: m/z 595,4 [M+1]+
[0108]
[Пример 10]
N-(3-Метокси-5-метилпиразин-2-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)пиридин-3-сульфонамид
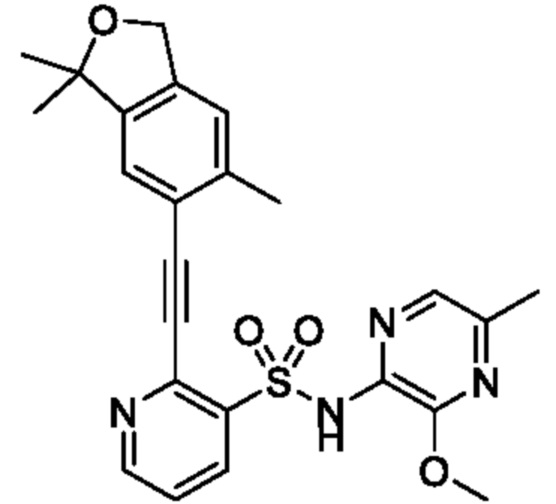
К смеси N-(3-метокси-5-метилпиразин-2-ил)-2-((3,3,6-триметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-((2-(триметилсилил)этокси)метил)пиридин-3-сульфонамида (200 мг, 0,336 ммоля) и метанола (5 мл) добавляли 50% серную кислоту (3 мл) при 0°C и реакционную смесь перемешивали при 60°C в течение 1 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор бикарбоната натрия, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (35 мг).
ESI-MS: m/z 465,35 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 10,98 (s, 1H), 8,79 (d, J=4,0 Hz, 1H), 8,36 (dd, J=1,6, 8,0 Hz, 1H), 7,62 (dd, J=4,8,8,4 Hz, 1H) 7,51 (s, 1H), 7,22 (s,1H), 4,95 (s, 2H), 3,80 (s, 3H), 2,44 (s, 3H), 2,22 (s, 3H), 1,44 (s, 6H).
[0109]
[Пример получения 11-1]
(E)-N'-(2-Гидрокси-4-метилбензилиден)ацетогидразид
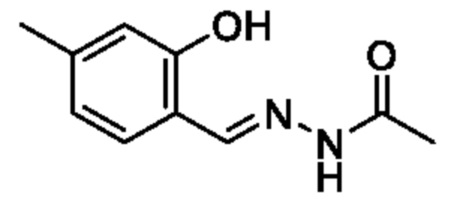
К смеси 2-гидрокси-4-метилбензальдегида (3,0 г, 22 ммоля) и этанола (40 мл) добавляли ацетогидразид (1,64 г, 22,1 ммоля) при комнатной температуре и реакционную смесь перемешивали при 90°C в течение 16 ч. Растворитель из реакционной смеси отгоняли при пониженном давлении и остаток промывали гексаном и получали искомое соединение (3,0 г) в неочищенном виде. Это соединение использовали в следующей реакции без дополнительной очистки.
[0110]
[Пример получения 11-2]
2-Ацетил-4-метилбензальдегид
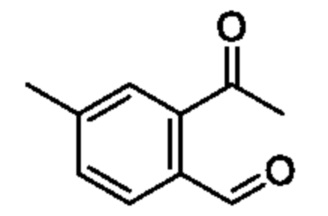
К смеси (E)-N'-(2-гидрокси-4-метилбензилиден)ацетогидразида (4,6 г, 24 ммоля) и тетрагидрофурана (50 мл) добавляли ацетат свинца(IV) (11,7 г, 26,3 ммоля) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь фильтровали через целит и промывали этилацетатом. Фильтрат промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (2,0 г).
1H NMR (400 MHz, CDCl3): δ 10,19 (d, J=4 Hz, 1H), 7,84-7,81 (m, 1H), 7,46 (t, J=6,8 Hz, 2H), 2,65 (d, J=4 Hz, 3H), 2,50 (d, J=3,6 Hz, 3H)
[0111]
[Пример получения 11-3]
1-(2-(Гидроксиметил)-5-метилфенил)этан-1-ол
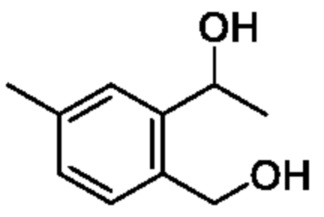
К смеси 2-ацетил-4-метилбензальдегида (1,4 г, 8,0 ммоля), тетрагидрофурана (3,8 мл) и этанола (11,2 мл) добавляли борогидрид натрия (1,5 г, 40 ммоля) при 0°C и реакционную смесь перемешивали при 70°C в течение 2 ч. Температуру реакционной смеси возвращали к комнатной и к реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,85 г).
1H NMR (400 MHz, CDCl3): δ 7,27 (s, 1H), 7,20 (d, J=7,6 Hz, 1H), 6,83(d, J=7,2 Hz, 1H), 5,01-4,91 (m, 3H), 4,53-4,46 (m, 2H), 2,27 (s, 3H), 1,28 (d, J=6,4 Hz, 3H).
[0112]
[Пример получения 11-4]
1,6-Диметил-1,3-дигидроизобензофуран
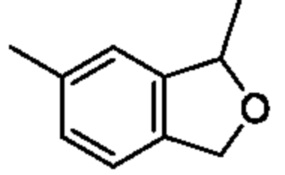
К смеси 1-(2-(гидроксиметил)-5-метилфенил)этан-1-ола (0,90 г, 5,4 ммоля) и тетрагидрофурана (10 мл) постепенно добавляли 60% гидрид натрия (0,52 г, 13,6 ммоля) при 0°C и смесь перемешивали при такой же температуре, как выше, в течение 30 мин. К реакционной смеси добавляли триметилфосфат (1,5 мл, 13,6 ммоля) при комнатной температуре и смесь перемешивали при такой же температуре, как выше, в течение 16 ч. К реакционной смеси добавляли воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,6 г).
1H NMR (400 MHz, CDCl3): δ 7,12-7,07 (m, 2H), 6,98 (d, J=5,2 Hz, 1H), 5,31-5,28 (m, 1H), 5,13-5,00 (m, 2H), 2,39 (d, J=5,2 Hz, 3H), 1,52-1,48 (m, 3H).
[0113]
[Пример получения 11-5]
5-Бром-1,6-диметил-1,3-дигидроизобензофуран
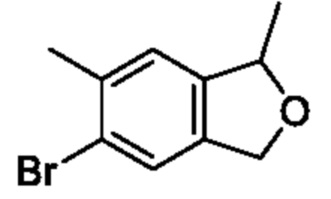
К смеси 1,6-диметил-1,3-дигидроизобензофурана (600 мг, 4,05 ммоля) и дихлорметана (10 мл) добавляли N-бромсукцинимид (721 мг, 4,05 ммоля) и трифторметансульфоновую кислоту (1,8 г, 12,2 ммоля) при 0°C и смесь перемешивали при комнатной температуре в течение 2 ч. К реакционной смеси добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле(гексан/этилацетат) и получали искомое соединение (0,3 г).
1H NMR (400 MHz, CDCl3): δ 7,51 (d, J=5,2Hz, 1H), 7,26 (d, J=5,2 Hz, 1H), 5,17-5,12 (m, 1H), 4,96 (d, J=12,8 Hz, 1H), 4,88-4,84 (m, 1H), 2,35 (d, J=5,2 Hz, 3H), 1,37 (t, J=6 Hz, 3H).
[0114]
[Пример получения 11-6]
2-((1,6-Диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамид
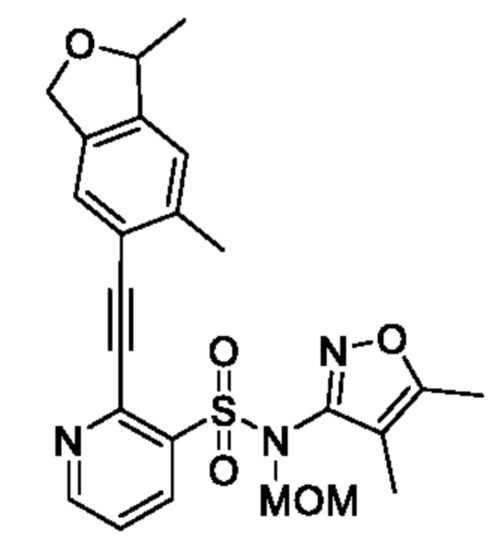
В атмосфере аргона к смеси N-(4,5-диметилизоксазол-3-ил)-2-этинил-N-(метоксиметил)пиридин-3-сульфонамида (0,40 г, 1,24 ммоля) и N,N-диметилформамида (5 мл) добавляли 5-бром-1,6-диметил-1,3-дигидроизобензофуран (0,337 г, 1,49 ммоля), йодид меди(I) (47 мг, 0,249 ммоля), триэтиламин (0,36 мл, 2,49 ммоля) и тетракис(трифенилфосфин)палладий(0) (143 мг, 0,124 ммоля) и реакционную смесь перемешивали при 80°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (25 мг).
ESI-MS: m/z 468,23 [M+1]+
[0115]
[Пример 11]
2-((1,6-Диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)пиридин-3-сульфонамид
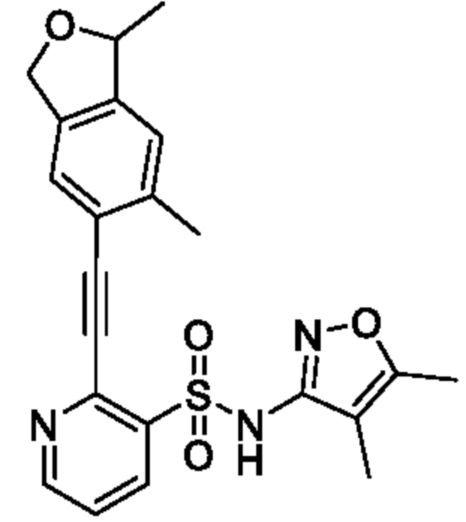
К смеси 2-((1,6-диметил-1,3-дигидроизобензофуран-5-ил)этинил)-N-(4,5-диметилизоксазол-3-ил)-N-(метоксиметил)пиридин-3-сульфонамида (30 мг, 0,064 ммоля) и метанола (5 мл) добавляли 6 моль/л хлористоводородную кислоту (0,5 мл) при 0°C и реакционную смесь перемешивали при 50°C в течение 4 ч. Температуру реакционной смеси возвращали к комнатной и к ней добавляли охлажденную льдом воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным рассолом и сушили над сульфатом натрия, и растворитель отгоняли при пониженном давлении. Остаток очищали с помощью высокоэффективной жидкостной хроматографии (Luna C18 (250×50 мм) 10 мкм, 0,1% водный раствор муравьиной кислоты/ацетонитрил) и получали искомое соединение (5 мг).
ESI-MS: m/z 424,0 [M+1]+
1H NMR (400 MHz, DMSO-d6): δ 11,02 (s, 1H), 8,81 (d, J=5,2 Hz, 1H), 8,34 (t, J=8 Hz, 1H), 7,63 (t, J=4,4 Hz, 1H), 7,48 (d, J=5,6 Hz, 1H), 7,26 (d, J=5,6 Hz, 1H), 5,22(d, J=5,6 Hz, 1H), 5,05-5,00 (m,1H), 4,92 (t, J=6,4 Hz, 1H), 2,48 (d, J=8,8 Hz, 3H), 2,09 (d, J=6,4 Hz, 3H), 1,81 (d, J=6,4 Hz, 3H), 1,41 (t, J=6 Hz, 3H).
[0116]
[Сравнительный пример 1]
В сравнительном примере 1 использовали ситаксентан, описывающийся следующей формулой.
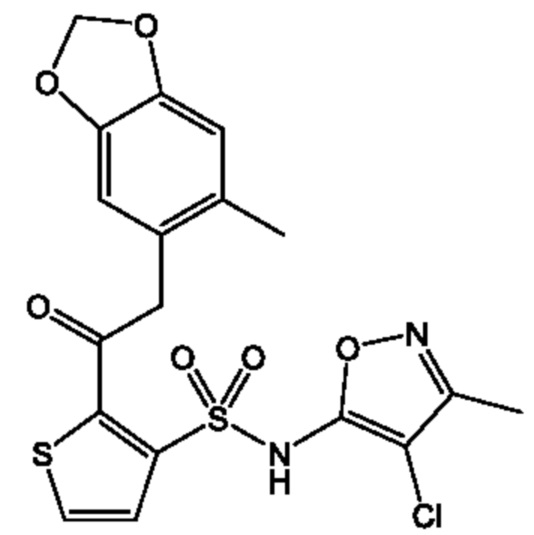
[0117]
[Сравнительный пример 2]
В сравнительном примере 2 использовали соединение, описывающееся следующей формулой. Это соединение является соединением, описанным в примере 1 в Международной публикации № WO 2013/115162.
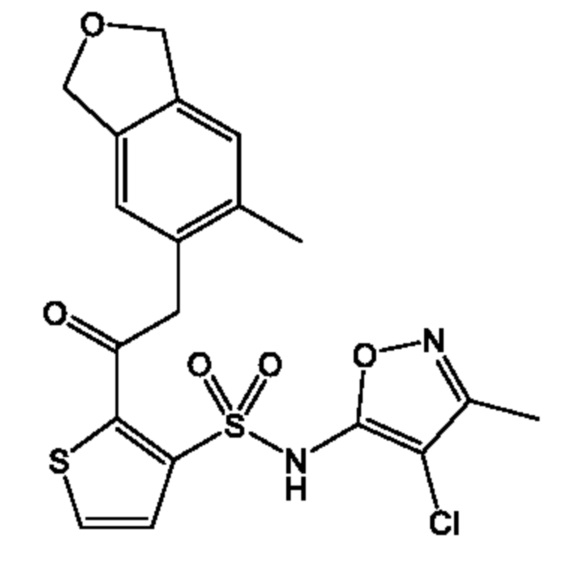
[0118]
[Пример исследования 1-1: Ингибирующее воздействие на эндотелиновый рецептор A]
Ингибирующее воздействие на эндотелиновый рецептор A изучали по следующей методике.
Клетки CHO-K1-mt aequorin, которым придана способность экспрессировать эндотелиновый рецептор A человека (Accession Number NP_001948.1), выращивали в среде без антибиотика в течение 18 ч, затем обрабатывали с помощью PBS-EDTA (5 мМ EDTA), центрифугировали (2 мин, 405×г, комнатная температура) и затем суспендировали в буфере для анализа (DMEM/HAM's F12 с HEPES+0,1% BSA, не содержащего протеазы).
[0119]
Клетки при содержании1×106 клеток/мл инкубировали при комнатной температуре в течение 4 ч в присутствии коэлентеразина h (Molecular Probes, Inc.) (конечная концентрация: 5 мкМ). Агонистическую реакцию на основе эндотелина использовали для определения концентрации эндотелина, соответствующей EC80.
[0120]
Затем, 50 мкл (10000 клеток/лунка) суспензии клеток обрабатывали с помощью коэлентеразина h и 50 мкл буфера для анализа, содержащего исследуемое вещество (конечная концентрация: 0,5% в DMSO) добавляли в каждую лунку 96-луночного планшета. через 15 мин добавляли эндотелин, так чтобы конечная концентрация являлась концентрацией, соответствующей EC80 . Активность по отношению к рецептору измеряли по испускаемому световому излучению в FDSS6000 (Hamamatsu Photonics K.K.). Значения IC50 рассчитывали с помощью программного обеспечения XLfit (ID Business Solutions Ltd. (IDBS)).
[0121]
Образец, обладающий значением IC50, равным 1,0 нМ или менее, или оказывал ингибирующее воздействие, составляющее 50% или более при 1,0 нМ, обозначали, как "A"; образец, обладающий значением IC50, равным более 10 нМ, или оказывал ингибирующее воздействие, составляющее менее 50% при 10 нМ, обозначали, как "C"; образец с характеристиками, промежуточными между характеристиками "A" и "C", обозначали, как "B". Результаты приведены в таблице 1-1.
[Таблица 1-1]
Таблица 1-1: Ингибирующее воздействие на рецептор ETA
[0122]
[Пример исследования 1-2: Ингибирующее воздействие на эндотелиновый рецептор B]
Ингибирующее воздействие на эндотелиновый рецептор B изучали по следующей методике.
Клетки CHO-K1-mt aequorin, которым придана способность экспрессировать эндотелиновый рецептор B человека (Accession Number NP_000106.1), выращивали в среде без антибиотика в течение 18 ч, затем обрабатывали с помощью PBS-EDTA (5 мМ EDTA), центрифугировали (2 мин, 405×г, комнатная температура) и затем суспендировали в буфере для анализа (DMEM/HAM's F12 с HEPES+0,1% BSA, не содержащего протеазы).
[0123]
Клетки при содержании 1×106 клеток/мл инкубировали при комнатной температуре в течение 4 ч в присутствии коэлентеразина h (Molecular Probes, Inc.) (конечная концентрация: 5 мкМ). Агонистическую реакцию на основе эндотелина использовали для определения концентрации эндотелина, соответствующей EC80.
[0124]
Затем 50 мкл (10000 клеток/лунка) суспензии клеток обрабатывали с помощью коэлентеразина h и 50 мкл буфера для анализа, содержащего исследуемое вещество (конечная концентрация: 0,5% в DMSO) добавляли в каждую лунку 96-луночного планшета. через 15 мин добавляли эндотелин, так чтобы конечная концентрация являлась концентрацией, соответствующей EC80 . Активность по отношению к рецептору измеряли по испускаемому световому излучению в FDSS6000 (Hamamatsu Photonics K.K.).
[0125]
Образец, обладающий значением IC50, равным 1000 нМ или менее, или оказывал ингибирующее воздействие, составляющее 50% или более при 1000 нМ, обозначали, как "A"; образец, обладающий значением IC50, равным более 5000 нМ, или оказывал ингибирующее воздействие, составляющее менее 50% при 5000 нМ, обозначали, как "C"; образец с характеристиками, промежуточными между характеристиками "A" и "C", обозначали, как "B". Результаты приведены в таблице 1-2.
[Таблица 1-2]
Таблица 1-2: Ингибирующее воздействие на рецептор ETB
[0126]
Как в случае селективности по отношению к ETA, образец, который удовлетворял любому из следующих критериев, обозначали, как "++".
1. Отношение значение ETB IC50/значение ETA IC50 больше 5000
2. Оказывающий ингибирующее воздействие на ETA, составляющее 50% или более при 1,0 нМ, и ингибирующее воздействие на ETB, составляющее менее 50% при 5000 нМ
Образец, который обладал отношением ETB IC50/значение ETA IC50, равным более 1000 и 5000 или менее, обозначали, как "+".
Результаты приведены в таблице 1-3.
[Таблица 1-3]
Таблица 1-3: Селективность по отношению к ETA (ETB/ETA)
[0127]
[Пример исследования 2: Ингибирующее воздействие CYP2C9]
Ингибирующее воздействие CYP2C9 изучали по следующей методике.
(1) Замороженную фракцию микросом печени размораживали на льду и разводили буфером на основе фосфата калия (част./млрд) до конечной концентрации, равной 0,5 мг/мл.
(2) К ней добавляли субстрат для исследования (диклофенак: D6899 фирмы Sigma-Aldrich Co. LLC), так чтобы ее конечная концентрация равнялась 2,5 мкМ.
(3) Смесь медленно перемешивали и инкубировали при 37±1°C в течение 5 мин и получали раствор реакционной смеси.
(4) 801 мкл Раствора реакционной смеси помещали в каждую пробирку и исследуемое соединение серийно разводили с помощью 0,9 мкл добавляемого к ней DMSO, так чтобы ее конечная концентрация равнялась от 9,1 до 20000 нМ (разведения 1/3 при 8 концентрациях). В этом контексте 0,9 мкл DMSO добавляли в случае отрицательной контрольной группы и 0,9 мкл сульфафеназола (S0758 фирмы Sigma-Aldrich Co. LLC) с установлением конечной концентрации, равной 1 мкМ, с помощью DMSO, добавляли в случае положительной контрольной группы.
(5) После перемешивания аликвоты по 270 мкл переносили в каждую из двух чистых пробирок и инкубировали на водяной бане со встряхиванием при 37±1°C в течение 5 мин.
(6) Реакцию инициировали путем добавления 30 мкл 10 мМ NADPH и пробирки инкубировали при 37°C±1°C в течение 10 мин.
(7) Пробирки извлекали из водяной бани со встряхиванием и реакцию останавливали путем добавления 300 мкл раствора для остановки реакции. После перемешивания пробирки центрифугировали при 1021×g при 4°C в течение 20 мин.
(8) Количество субстрата для исследования метаболизма определяли с помощью LC-MS/MS для расчета степени ингибирования при каждой концентрации исследуемого соединения.
(9) Значения IC50 рассчитывали с помощью программного обеспечения GraphPad Prism5. Образец, обладающий значением IC50, равным 1 мкМ или менее, обозначали, как "++"; образец, обладающий значением IC50 в диапазоне от более 1 мкМ до 10 мкМ или менее, обозначали, как "+"; и образец, обладающий значением IC50, равным более 10 мкМ, обозначали, как "-". Результаты приведены в таблице 2.
[0128]
[Таблица 2]
Таблица 2
[0129]
[Пример исследования 3: Метаболическая стабильность в микросомах печени человека и мыши]
Метаболическую стабильность в микросомах печени человека изучали по следующей методике.
1. Материалы
(1) Микросомы печени человека: 20 мг/мл
(2) Исследуемые соединение: 1,1 мМ раствор в DMSO
(3) Буферный раствор на основе фосфата калия: 66,7 мМ (pH 7,4)
(4) Раствор NADPH: 10 мМ в буферном растворе на основе фосфата калия
(5) Останавливающий раствор: 0,5% раствор муравьиной кислоты в ацетонитриле, содержащий варфарин в качестве внутреннего стандарта
[0130]
2. Методика
971,5 мкл Буферного раствора на основе фосфата калия и 27,5 мкл микросом печени человека помещали в полиэтиленовую пробирку и суспендировали. К нему добавляли 1 мкл исследуемого соединения и аликвоту в 180 мкл этой смеси переносили в чистую пробирку. Смесь предварительно инкубировали при 37°C в течение 5 мин. Затем к ней добавляли 20 мкл раствора NADPH (для времени инкубирования, равного 30 мин) или 20 мкл буферного раствора на основе фосфата калия (для времени инкубирования, равного 0 мин). После инкубирования реакцию останавливали путем добавления 200 мкл останавливающего раствора. Затем, пробирку центрифугировали при 3220×g в течение 20 мин и концентрацию неизмененной формы исследуемого соединения в 200 мкл надосадочной жидкости измеряли с помощью LC-MS/MS. На основании площади полученного пика для неизмененой формы остаточное содержание (%) неизмененой формы рассчитывали с использованием содержания при времени инкубирования, равном 0 мин, равного 100%.
[0131]
Метаболическую стабильность в микросомах печени мыши исследовали по такой же методике, как приведенная выше, с тем отличием, что микросомы печени мыши использовали вместо микросом печени человека. Остаточные содержания (%)неизмененой формы через 30 мин приведены в таблице 3.
[Таблица 3]
Таблица 3
[0132]
[Пример исследования 4: Исследование проницаемости мембраны PAMPA]
Исследование проницаемости мембраны проводили с использованием PAMPA. Конкретная методика является следующей.
(1) Лецитин при концентрации 2% (мас./об.) добавляли в раствор додекана и полностью растворяли.
(2) 5 мкл Раствора лецитин/додекан добавляли в каждую лунку донорного планшета. Для этого конец пипетки располагали так, чтобы он не касался мембраны.
(3) Сразу после этого 150 мкл раствора донора (5% DMSO-PBS), содержащего исследуемое соединение (10 мкМ) добавляли в каждую лунку донорного планшета и 300 мкл водного буфера добавляли к в каждую лунку акцепторного планшета из PTFE.
(4) Донорный планшет, заполненный раствором донора, содержащим исследуемое соединение, медленно помещали на акцепторный планшет и нижнюю поверхность мембраны приводили в соприкосновение с буфером во всех лунках.
(5) После закрывания аппарат инкубировали при комнатной температуре в течение 16 ч.
(6) После инкубирования 100 мкл раствора отбирали с каждой верхней поверхности и нижней поверхности мембраны в акцепторном планшете и к ним добавляли ацетонитрил, содержащий такое же количество внутреннего стандарта.
(7) Концентрацию исследуемого соединения измеряли для расчета скорости проникновения.
Результаты приведены в таблице 4. Образец, обладающий значением скорости проникновения, равным 1×10-8 см/с или менее, обозначали, как "C"; образец, обладающий значением в диапазоне от более 1×10-8 см/с до 10×10-8 см/с или менее, обозначали, как "B"; и образец, обладающий значением, равным более 10×10-8 см/с, обозначали, как "A".
[0133]
[Таблица 4]
Таблица 4
[0134]
[Пример исследования 5: Исследование вызванного BigET-1 артериального давления]
У каждого самца крысы Wistar в возрасте от 8 до 20 недель трахею исследовали катетером для обработки дыхательных путей, в сонную артерию вводили катетер для измерения артериального давления, в бедренную вену вводили катетер для введения BigET-1 и в двенадцатиперстную кишку вводили катетер для введения для введения исследуемого вещества при обработке анальгетиком и анестезии уретаном. После подтверждения того, что артериальное давление и частота сердечных сокращения стали стабильными, в двенадцатиперстную кишку вводили разбавитель (0,5% раствор метилцеллюлозы 400) или 30 мг/кг (5 мл/кг) исследуемого вещества с доведением до объема разбавителем. Через 1 ч в нее вводили BigET-1 (20 мкг/кг) и проводили мониторинг давления и в течение 60 мин после введения BigET-1. Исследование проводили с использованием n=6 крыс в группе. При исследовании систолическое артериальное давление и диастолическое артериальное давление определяли в течение 20 каждые 5 мин, начиная от 5 мин до введения BigET-1 и продолжая до 60 мин после введения BigET-1 и AUC0-60 мин (мм рт.ст.×мин) в течение 60 мин после введения BigET-1 рассчитывали с использованием изменения по сравнению со значением, полученным за 5 мин до введения BigET-1. Для сопоставления AUC для группы животных, которым вводили разбавитель, и группы животных, которым вводили исследуемое вещество, использовали критерий t Стьюдента.
[Таблица 5]
Таблица 5
Среднее значение ±SD, N=6, #: p <0,01 по сравнению с группой животных, которым вводили разбавитель
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ, ОБЛАДАЮЩЕЕ ЦИКЛИЧЕСКОЙ СТРУКТУРОЙ | 2018 |
|
RU2795119C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2'-ФТОР-2'-АЛКИЛЗАМЕЩЕННЫХ ИЛИ ДРУГИХ ЗАМЕЩЕННЫХ РИБОФУРАНОЗИЛПИРИМИДИНОВ И ПУРИНОВ И ИХ ПРОИЗВОДНЫХ | 2005 |
|
RU2433124C2 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА И ПИРАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2686117C1 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРА КАЗЕИНКИНАЗЫ 1δ И/ИЛИ АКТИВИН-РЕЦЕПТОР-ПОДОБНОЙ КИНАЗЫ 5 | 2021 |
|
RU2810065C1 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ЦИАНОЕНОНА КАК МОДУЛЯТОРЫ KEAP1 | 2021 |
|
RU2822828C1 |
| СУЛЬФОНАМИДЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ ЭНДОТЕЛИН-ЗАВИСИМЫХ ЗАБОЛЕВАНИЙ, СПОСОБ ИНГИБИРОВАНИЯ СВЯЗЫВАНИЯ ЭНДОТЕЛИНОВОГО ПЕПТИДА С ЭНДОТЕЛИН -(ЕТ) ИЛИ -(ЕТ) РЕЦЕПТОРАМИ, СПОСОБ ИЗМЕНЕНИЯ ВЫЗЫВАЕМОЙ ЭНДОТЕЛИНОВЫМИ РЕЦЕПТОРАМИ АКТИВНОСТИ. | 1994 |
|
RU2151144C1 |
| N-(1H-ИМИДАЗОЛ-2-ИЛ)БЕНЗАМИД И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2020 |
|
RU2806754C1 |
| СОЕДИНЕНИЯ, ИНГИБИРУЮЩИЕ (БЛОКИРУЮЩИЕ) ГОРЬКИЙ ВКУС, СПОСОБЫ ИХ ПРИМЕНЕНИЯ И ПОЛУЧЕНИЯ | 2008 |
|
RU2522456C2 |
| БИАРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ И КОСМЕТИЧЕСКАЯ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1998 |
|
RU2185373C2 |
| ПРОИЗВОДНОЕ ТИОФЕНА И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2781643C2 |
Изобретение относится к соединению формулы (1), антагонисту эндотелинового рецептора А, а также фармацевтической композиции на его основе. Технический результат: получены новые соединения, которые могут быть применимы для профилактики или лечения заболевания, связанного с рецептором эндотелина А. 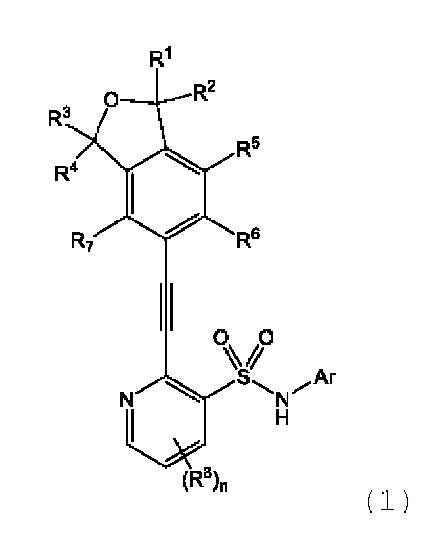 Где R1 и R2 все независимо означают водород или алкил, R3 и R4 все независимо означают водород или алкил, или R3 и R4 вместе образуют оксогруппу, R5-R7 все независимо означают водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, каждый R8 независимо означает алкил, галогеналкил или галоген, n является целым числом, равным от 0 до 3, и Ar описывается следующей формулой (Ar1) или (Ar2):
Где R1 и R2 все независимо означают водород или алкил, R3 и R4 все независимо означают водород или алкил, или R3 и R4 вместе образуют оксогруппу, R5-R7 все независимо означают водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу, каждый R8 независимо означает алкил, галогеналкил или галоген, n является целым числом, равным от 0 до 3, и Ar описывается следующей формулой (Ar1) или (Ar2): 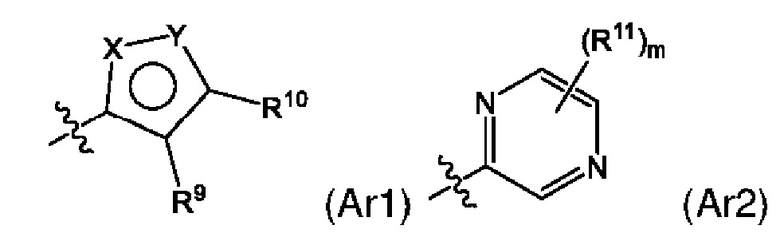 где X и Y означают азот и кислород соответственно или кислород и азот соответственно, R9 и R10 все независимо означают водород, алкил, галогеналкил или галоген, каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу и m является целым числом, равным от 0 до 3, где: алкил, представленный каждым из R1, R2, R3, R4, R5-R7, R8, R9, R10 и R11, представляет собой алкил, имеющий от 1 до 6 атомов углерода, где галогеналкил, представленный каждым из R5-R7, R8, R9, R10 и R11, представляет собой галогеналкил, имеющий от 1 до 6 атомов углерода, где алкокси, представленный каждым из R5-R7 и R11, представляет собой алкокси, имеющий от 1 до 6 атомов углерода, где галогеналкокси, представленный каждым из R5-R7 и R11, представляет собой галогеналкокси, имеющий от 1 до 6 атомов углерода или его фармацевтически приемлемая соль. 3 н. и 12 з.п. ф-лы, 7 табл., 13 пр.
где X и Y означают азот и кислород соответственно или кислород и азот соответственно, R9 и R10 все независимо означают водород, алкил, галогеналкил или галоген, каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу и m является целым числом, равным от 0 до 3, где: алкил, представленный каждым из R1, R2, R3, R4, R5-R7, R8, R9, R10 и R11, представляет собой алкил, имеющий от 1 до 6 атомов углерода, где галогеналкил, представленный каждым из R5-R7, R8, R9, R10 и R11, представляет собой галогеналкил, имеющий от 1 до 6 атомов углерода, где алкокси, представленный каждым из R5-R7 и R11, представляет собой алкокси, имеющий от 1 до 6 атомов углерода, где галогеналкокси, представленный каждым из R5-R7 и R11, представляет собой галогеналкокси, имеющий от 1 до 6 атомов углерода или его фармацевтически приемлемая соль. 3 н. и 12 з.п. ф-лы, 7 табл., 13 пр.
1. Соединение, описывающееся следующей формулой (1):
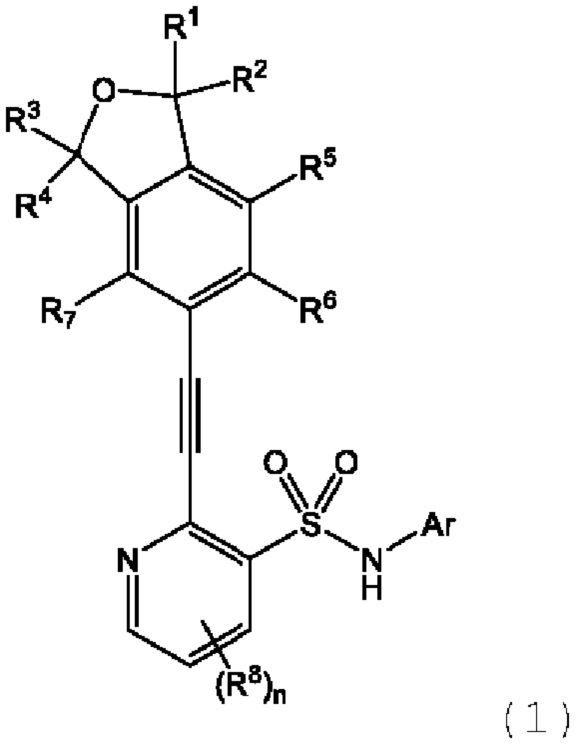
где
R1 и R2 все независимо означают водород или алкил,
R3 и R4 все независимо означают водород или алкил, или
R3 и R4 вместе образуют оксогруппу,
R5-R7 все независимо означают водород, алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу,
каждый R8 независимо означает алкил, галогеналкил или галоген,
n является целым числом, равным от 0 до 3, и
Ar описывается следующей формулой (Ar1) или (Ar2):
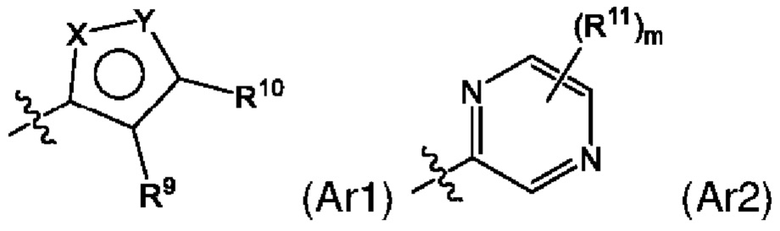
где
X и Y означают азот и кислород соответственно или кислород и азот соответственно,
R9 и R10 все независимо означают водород, алкил, галогеналкил или галоген,
каждый R11 независимо означает алкил, галогеналкил, галоген, алкоксигруппу или галогеналкоксигруппу и
m является целым числом, равным от 0 до 3,
где:
алкил, представленный каждым из R1, R2, R3, R4, R5-R7, R8, R9, R10 и R11, представляет собой алкил, имеющий от 1 до 6 атомов углерода,
где галогеналкил, представленный каждым из R5-R7, R8, R9, R10 и R11, представляет собой галогеналкил, имеющий от 1 до 6 атомов углерода,
где алкокси, представленный каждым из R5-R7 и R11, представляет собой алкокси, имеющий от 1 до 6 атомов углерода,
где галогеналкокси, представленный каждым из R5-R7 и R11, представляет собой галогеналкокси, имеющий от 1 до 6 атомов углерода
или его фармацевтически приемлемая соль.
2. Соединение или его фармацевтически приемлемая соль по п. 1, где каждый из R1 и R2 означает водород.
3. Соединение или его фармацевтически приемлемая соль по п. 1 или 2, где каждый из R5 и R7 означает водород и R6 означает алкил, имеющий от 1 до 6 атомов углерода.
4. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-3, где n равно 0.
5. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-4, где Ar описывается формулой (Ar1).
6. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-5, где каждый из R9 и R10 означает алкил, имеющий от 1 до 6 атомов углерода.
7. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-6, где X и Y означают азот и кислород соответственно.
8. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-6, где X и Y означают кислород и азот соответственно.
9. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-4, где Ar описывается формулой (Ar2).
10. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-4 и 9, где каждый R11 независимо означает алкил, имеющий от 1 до 6 атомов углерода, или алкоксигруппу, имеющую от 1 до 6 атомов углерода.
11. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-4, 9 и 10, где m равно 2.
12. Соединение или его фармацевтически приемлемая соль по п. 1, где соединение выбрано из группы, состоящей из следующих соединений:
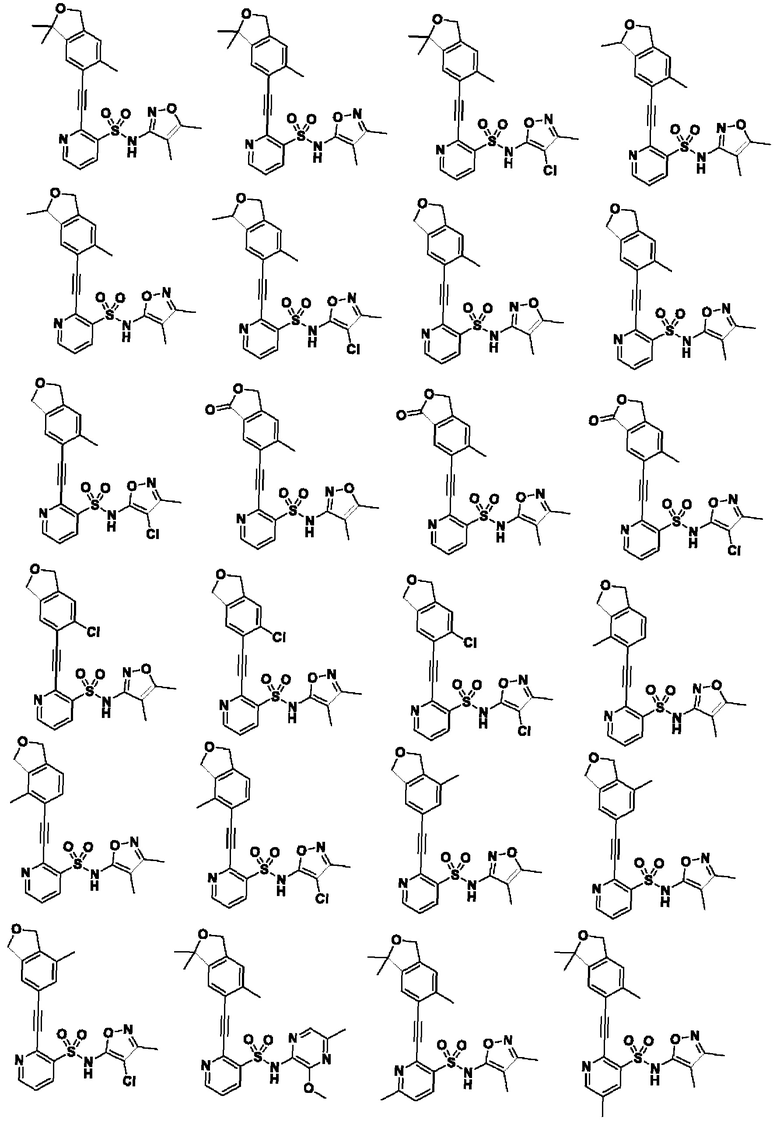
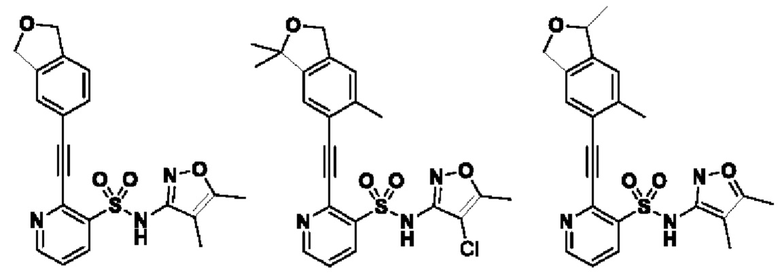
13. Антагонист эндотелинового рецептора А для профилактики или лечения заболевания, связанного с рецептором эндотелина А, содержащий эффективное количество соединения или его фармацевтически приемлемой соли по любому из пп. 1-12.
14. Антагонист эндотелинового рецептора А по п. 13, где антагонист эндотелинового рецептора А селективно ингибирует эндотелиновый рецептор А в отличие от эндотелинового рецептора В.
15. Фармацевтическая композиция для профилактики или лечения заболевания, связанного с рецептором эндотелина А, содержащая эффективное количество соединения или его фармацевтически приемлемой соли по любому из пп. 1-12, где заболевание, связанное с рецептором эндотелина А, выбрано из группы, состоящей из следующих: легочная гипертензия, нефропатия, гипертензия, гепатит, рак, боль, осложнения, связанные с аутоиммунным заболеванием, сердечная недостаточность и спазм сосудов.
| ПРОИЗВОДНОЕ СИТАКСЕНТАНА | 2013 |
|
RU2622386C2 |
| WO 2013127729 A1, 06.09.2013 | |||
| ПРОИЗВОДНЫЕ N-ГЕТЕРОАРИЛ-ПИРИДИНСУЛЬФОНАМИДА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОТИВОДЕЙСТВИЯ ОДНОМУ ИЛИ БОЛЕЕ ВОЗДЕЙСТВИЯМ ЭНДОТЕЛИНА | 1996 |
|
RU2172738C2 |
| Электроизоляционная лента и способ ее изготовления | 1976 |
|
SU649046A1 |
| Электрическая сварочная машина | 1931 |
|
SU32075A1 |
Авторы
Даты
2024-12-09—Публикация
2022-06-21—Подача