Область техники
Изобретение относится к фармакологии и медицине, более конкретно к фармацевтической композиции, содержащей метансульфонат (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона и модифицированный циклодекстрин и характеризующейся высокой противогрибковой активностью, которые, в частности, могут использоваться для профилактики и лечения инфекционных заболеваний у субъекта, в частности заболеваний, вызванных кандидозными и филоментозными патогенами.
Уровень техники
Недостаточная эффективность современной противомикробной терапии обусловлена в значительной степени развитием резистентности у возбудителей к имеющимся лекарственным препаратам. Именно поэтому во всем мире проводится интенсивный поиск и разработка новых эффективных лекарственных соединений. Несмотря на все усилия, современный арсенал медицинских средств недостаточен и не позволяет проводить эффективное лечение многих заболеваний, в том числе грибковых инфекций. Имеющиеся в настоящее время противогрибковые препараты - полиены и азолы, влияющие на главный компонент мембраны грибов - эргостерол, не обеспечивают должной избирательности действия. Они весьма токсичны, более того, многие штаммы возбудителей приобретают резистентность к препаратам группы азолов.
Более того, зачастую эффективные противогрибковые агенты слаборастворимы в воде и характеризуются низкой биодоступностью. При этом, важнейшим фармацевтическим свойством, оказывающим влияние на достижение лекарственным веществом системного кровотока, является водная растворимость. Улучшение растворимости лекарственного или биоактивного соединения направлено на повышение его биодоступности и терапевтической эффективности.
Из уровня техники известно новое противогрибковое соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион [RU 2703997], характеризующееся высокой противогрибковой активностью. Однако, данное соединение является плохо растворимым в воде соединением. Также, указанное соединение плохо растворимо в буферных растворах и гексане, и чуть лучше растворимо в спиртах [Tatyana V. Volkova et al. New antifungal compound: Solubility thermodynamics and partitioning processes in biologically relevant solvents. Journal of Molecular Liquids 2020, 310, 113148].
Разработка новых лекарственных форм, обеспечивающих целевую доставку фармацевтической субстанции к определенным органам или тканям, является важнейшей нетривиальной задачей при разработке лекарственного средства и требует значительных усилий.
Раскрытие изобретения
Технической задачей данного изобретение является разработка и создание композиции, включающей противогрибковое соединение и характеризующейся высокой растворимостью, стабильностью и эффективностью, которая подходит, в частности, как для перорального, так и для парентерального применения.
Поставленная задача решается посредством разработки и создания твердой фармацевтической композиции для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта, включающей:
- терапевтически или профилактически эффективное количество метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона;
- модифициронный β-циклодекстрин, который представляет собой 2-гидроксипропил-β-циклодекстрин или сульфобутиловый эфир-β-циклодекстрина;
причем мольное соотношение метансульфоната соединения и модифицированного β-циклодекстрина составляет 1:2 - 1:5.
В частных вариантах воплощения изобретения композиция дополнительно содержит, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество.
В частных вариантах воплощения изобретения вспомогательное вещество представляет собой наполнитель.
В частных вариантах воплощения изобретения заболевание вызвано грибковой инфекцией.
Изобретение также включает применение вышеуказанной композиции для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта. В частных вариантах воплощения изобретения заболевание вызвано грибковой инфекцией. Более конкретно, заболевание микробной этиологии вызвано грибом рода Candida spp., Aspergillus spp., Microsporum spp., Trichophyton spp. и/или Epidermophyton spp. В некоторых частных вариантах воплощения изобретения заболевание микробной этиологии вызвано грибом вида Candida albicans, C. non albicans, C.auris, Aspergillus fumigatus. Aspergillus niger, Rhizopus spp., Microsporum canis или Trichophyton rubrum.
В частных вариантах воплощения изобретения заболевание представляет собой заболевание глаз, кожи, ногтей и/или внутренних органов. В некоторых конкретных вариантах воплощения изобретения заболевание представляет собой дерматофитию, поверхностный микоз, кандидоз кожи и/или ногтей, вагинальный кандидоз, кандидозный стоматит, эндокардит, системный кандидоз или аспергилез.
Предметом настоящего изобретения также является фармацевтическая композиция для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта, включающая:
- терапевтически или профилактически эффективное количество метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона;
- модифицированный β-циклодекстрин, который представляет собой 2-гидроксипропил-β-циклодекстрин или сульфобутиловый эфир-β-циклодекстрина;
- растворитель;
причем мольное соотношение метансульфоната соединения и модифицированного β-циклодекстрина составляет 1:2 - 1:5.
В частных вариантах воплощения изобретения растворитель представляет собой воду.
В частных вариантах воплощения изобретения вода представляет собой воду очищенную.
В частных вариантах воплощения изобретения вода представляет собой деионизованную воду, воду для инъекций.
Изобретение также включает применение вышеуказанной композиции для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта.
В частных вариантах воплощения изобретения композицию вводят субъекту парентерально. Более конкретно, композицию вводят посредством инфузии или внутримышечной инъекции.
В частных вариантах воплощения изобретения композицию вводят субъекту перорально. Более конкретно, композицию вводят в виде раствора для приема внутрь.
В частных вариантах воплощения изобретения композицию применяют местно.
В частных вариантах воплощения изобретения заболевание вызвано грибковой инфекцией. Более конкретно, заболевание микробной этиологии вызвано грибом рода Candida spp., Aspergillus spp., Microsporum spp., Trichophyton spp. и/или Epidermophyton spp. В некоторых частных вариантах воплощения изобретения заболевание микробной этиологии вызвано грибом вида Candida albicans, C. non albicans, C. auris, Aspergillus fumigatus. Aspergillus niger, Rhizopus spp., Microsporum canis или Trichophyton rubrum.
В частных вариантах воплощения изобретения заболевание представляет собой заболевание глаз, кожи, ногтей и/или внутренних органов. В некоторых конкретных вариантах воплощения изобретения заболевание представляет собой дерматофитию, поверхностный микоз, кандидоз кожи и/или ногтей, вагинальный кандидоз, кандидозный стоматит, эндокардит, системный кандидоз или аспергилез.
Настоящее изобретение также включает способ получения вышеуказанной фармацевтической композиции, включающий растворение твердой фармацевтической композиции по изобретению в растворителе.
В частных вариантах воплощения изобретения растворитель представляет собой воду. Более конкретно, вода представляет собой воду очищенную. В некоторых частных вариантах воплощения изобретения вода представляет собой деионизованную воду, воду для инъекций.
Настоящее изобретение также включает способ лечения и/или профилактики инфекционного заболевания микробной этиологии у субъекта, включающий введение субъекту любой композиции по изобретение. В частных вариантах воплощения изобретения композицию вводят субъекту перорально или парентерально. В частных вариантах воплощения изобретения композицию применяют местно.
Настоящее изобретение также включает получение любой композиции по изобретению.
В результате осуществления изобретения достигаются следующие технические результаты:
- разработка твердой фармацевтической композиции на основе метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион и модифицированного β-циклодекстрина, характеризующаяся высокой растворимостью и стабильностью, причем указанная композиция может быть растворена в одном или нескольких растворителях незадолго до введения пациенту, для обеспечения композиции, подходящей для перорального или парентерального введения;
- твердая композиция по изобретению имеет приемлемое время растворения в растворителях и может применяться в виде раствора для приема внутрь, в виде таблеток, внутримышечных инъекций, глазных капель или в виде инфузий, и, следовательно, предоставляя возможность легкого применения для приготовления фармацевтической композиции, которая будет доставляться, в частности, перорально или парентерально;
- наряду с этим твердая композиция по изобретению может применяться в виде таблеток;
- разработка стабильной и эффективной фармацевтической композиции на основе метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион и модифицированного β-циклодекстрина, растворителя, подходящей, в частности, для перорального, более конкретно такое введение осуществляют путем приема раствора внутрь, или парентерального введения пациентам, более конкретно такое введение осуществляют путем инфузии или внутримышечной инъекции;
- разработка способа получения фармацевтической композиции, подходящей, в частности, для перорального или парентерального введения пациентам, включающий растворение твердой фармацевтической композиции по изобретению в растворителе;
- в целом, изобретение обеспечивает возможность эффективного введения соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион субъектам, несмотря на сложные физико-химические характеристики указанного соединения.
Краткое описание чертежей.
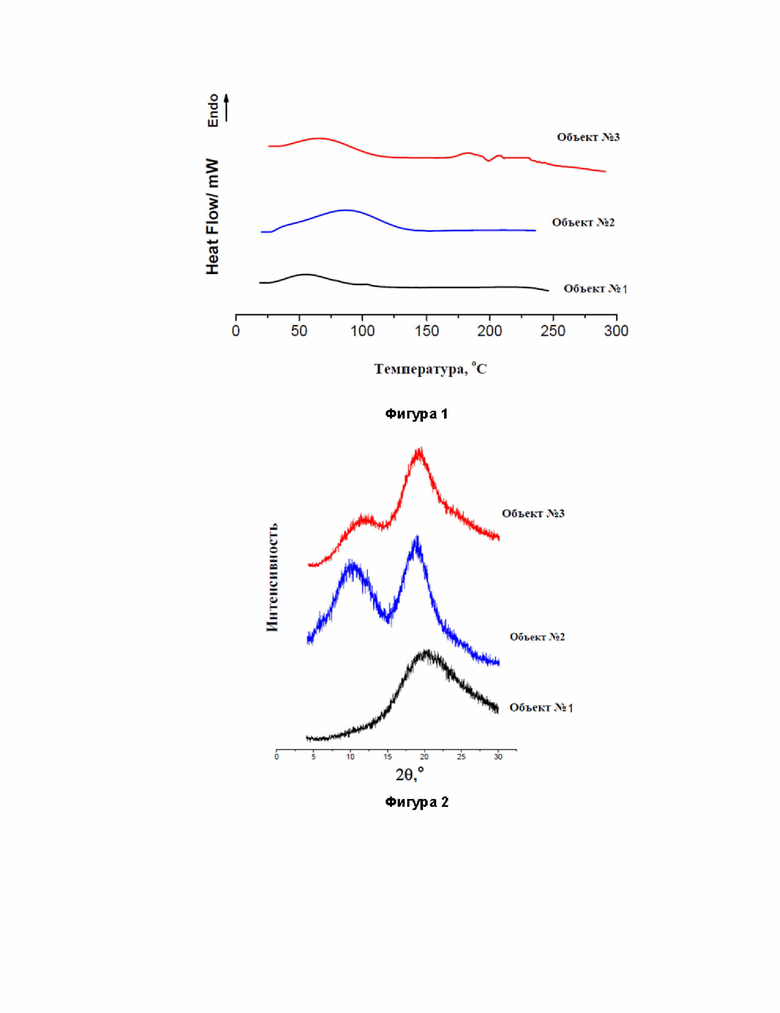
Фигура 1. ДСК кривые Объектов №1, 2 и 3.
Фигура 2. Результаты РСА Объектов №1, 2 и 3.
Фигура 3. ИК спектры Объектов №1, 2 и 3.
Фигура 4. Профили растворения Объекта №1 и 3 в дистиллированной воде (рН 6.8) при 25.0 °С.
Фигура 5. Дифрактограммы объекта №3: исходный образец (a) и образец после 3 месяцев хранения при 25.0 °С (б).
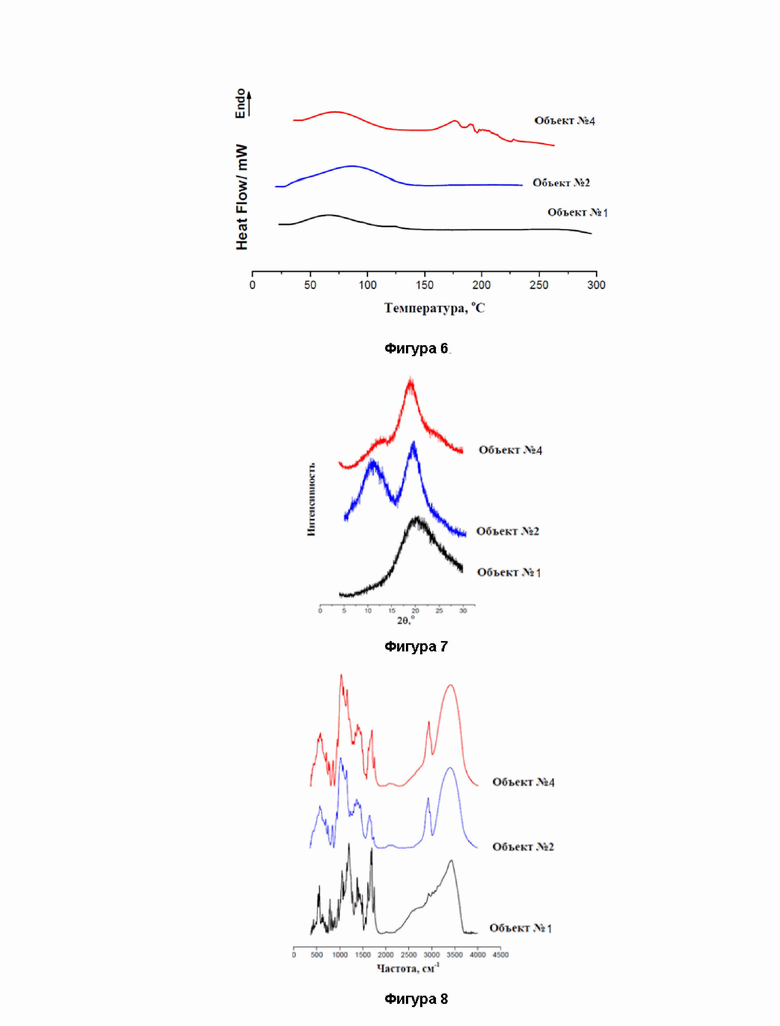
Фигура 6. ДСК кривые Объектов №1, 2 и 4.
Фигура 7. Результаты РСА Объектов №1, 2 и 4.
Фигура 8. ИК спектры Объектов №, 2 и 4.
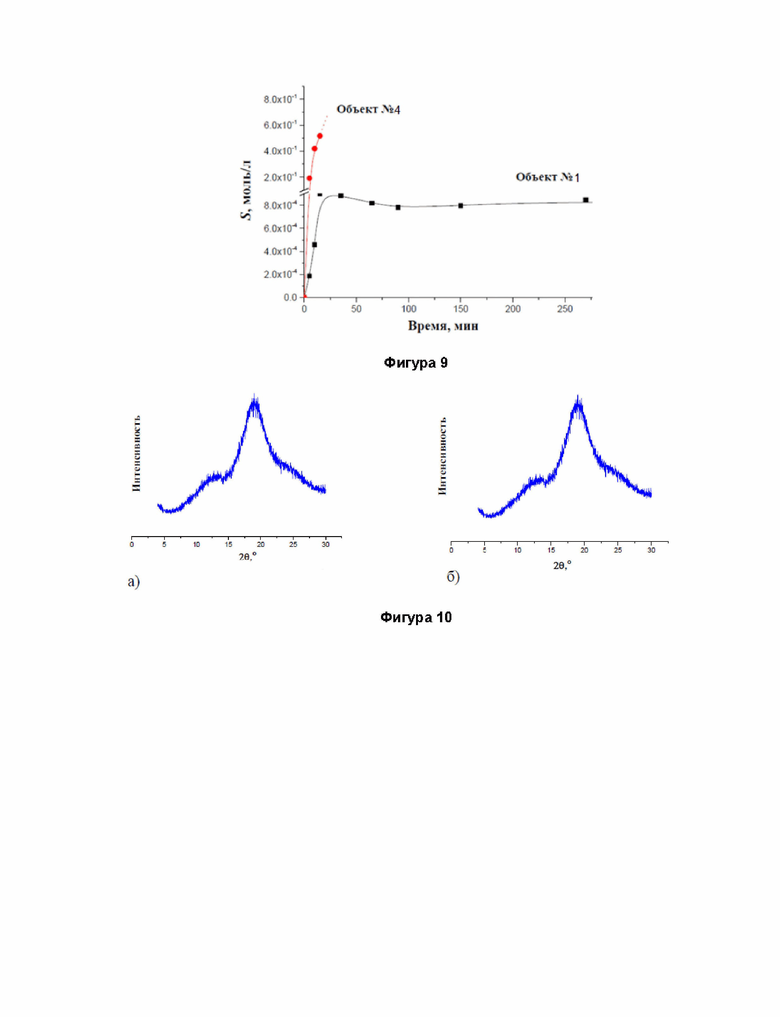
Фигура 9. Профили растворения Объекта №1 и 4 в дистиллированной воде (рН 6.8) при 25.0 °С.
Фигура 10. Дифрактограммы объекта №4: исходный образец (a) и образец после 3 месяцев хранения при 25.0 °С (б).
Подробное раскрытие изобретения
Определение и термины
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения. Следующие определения применяются в данном документе, если иное не указано явно.
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «иметь», «включать» и «содержать» или их вариации, например такие как «имеет», «имеющий», «включает», «включающий», «содержит» или «содержащий», следует понимать, как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых. Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Термин «и/или» означает один, несколько или все перечисленные элементы.
Также здесь перечисление числовых диапазонов по конечным точкам включает все числа, входящие в этот диапазон.
Термин «необязательный» или «необязательно» или «опциональный» или «опционально», используемый в данном документе, означает, что описываемое впоследствии событие или обстоятельство может, но не обязательно, произойти, и что описание включает случаи, когда событие или обстоятельство происходит, и случаи, в которых оно не происходит.
Термин «модифицированный циклодекстрин» в настоящем документе относится к производным β-циклодекстрина. Производные в настоящей заявке обозначают β-циклодекстрины, имеющие различные заместители, включая (2-гидроксипропил)-β- циклодекстрин, сульфобутиловый эфир β-циклодекстрина. «HP-β-циклодекстрин» также называется «гидроксипропил-β-циклодекстрин» или «2-гидроксипропил-β-циклодекстрин» или «гидроксипропилбетадекс».
Соединение L-173 представляет собой (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион, характеризуется следующей структурной формулой:
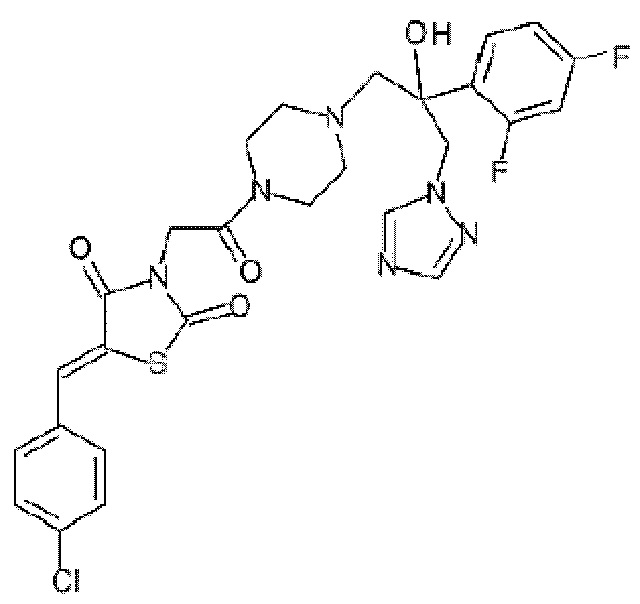
Термин «мезилат» (или «метансульфонат») относится к соли металсульфонофой кислоты. Мезилат-ион имеет структуру:
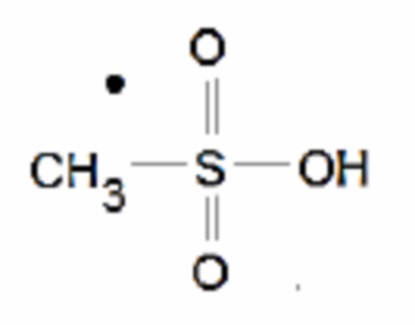
Термин «свободное основание» относится к Соединению L-173, когда оно не находится в форме соли.
Фармацевтическая композиция, описанная в настоящей заявке, в особенности представляет собой фармацевтическую композицию на основе циклодекстрина. «Фармацевтическая композиция на основе циклодекстрина» обозначает композицию, содержащую циклодекстрин, которая является подходящей для фармацевтического введения.
Как используется в настоящей заявке, термин "растворитель" представляет собой растворитель, используемый для растворения фармацевтической композиции, подходящей для, в частности, парентерального введения, используя в качестве исходной твердую фармацевтическую композицию. Твердая фармацевтическая композиция предпочтительно представляет собой порошок или таблетку, в предпочтительном варианте, растворитель представляет собой воду. В частных вариантах воплощения изобретения вода представляет собой воду очищенную. Более конкретно, вода представляет собой деионизованную воду, воду для инъекций.
Осуществление изобретения
Как уже было отмечено выше соединение (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-дион (соединение L-173) является плохо растворимым в воде соединением. Для обеспечения безопасного и эффективного введения соединение L-173, и для проявления необходимых терапевтических эффектов, соединение L-173 должно быть растворено при более высокой концентрации. Известным средством повышения растворимости лекарственных препаратов является использование циклодекстринов в качестве солюбилизирующих агентов. Однако использование такого подхода не привело к ожидаемым результатам.
Было проведено исследование, в ходе которого оценивалась растворимость потенциального противогрибкового соединения L-173 с добавлением модифицированного β-циклодекстрина (β-ЦД), а именно 2-гидроксипропил-β-циклодекстрина (HP-β-ЦД) или гептакис(2,6-ди-O-метил)-β-циклодекстрина (DM-β-ЦД), в водном растворе (pH 2.0 и pH 7.4) при 298,15-313,15 К.
В результате проведенного исследования показана недостаточность растворения комплексов соединения L-173 с модифицированным циклодекстрином для создания лекарственного средства, в частности, для применения в качестве средства для инфузий или внутримышечных инъекций (таблица 1).
Таблица 1. Растворимость комплексов соединения L-173 с циклодекстрином при рН 2.0 и 7.4.
Вышеуказанные результаты показывают, что хотя циклодекстрины хорошо известны в качестве солюбилизирующих агентов, однако их применение ограничено, поскольку они не являются эффективными растворителями для всех соединений.
Однако, автором настоящего изобретения неожиданно было обнаружено, что при получении комплексов на основе циклодекстринов не просто со свободным основанием активного соединения L-173, а с солью метансульфоновой кислоты соединения L-173, такие комплексы показали превосходную растворимость и могут быть перспективными для получение лекарственного средства. В результате применения комплексов мезилата соединения L-173 с модифицированным циклодекстрином, а именно с 2-гидроксипропил-β-циклодекстрином, в частности, в соотношении 1:2 - 1:5, в некоторых конкретных вариантах в соотношении 1:2 - 1:3, получены величины растворимости в сотни раз превышающие значения, полученных с применением свободного основания соединения L-173 (таблица 2).
Таблица 2. Растворимость комплексов на основе модифицированного циклодекстрина и мезилата соединения L-173 по изобретению.
>412.7 (EV)
(EV**) получен с использованием испарения до постоянной массы.
β-ЦД - 2-гидроксипропил-β-циклодекстрина.
Таким образом, создание комплекса мезилата соединения L-173 в сочетании с модифицированным β-циклодекстрином, в частности, с 2-гидроксипрпил-β-циклодекстрином, позволяет получать водорастворимые лекарственные составы которые могут найти применение в виде различных форм введения, а именно в виде таблеток, растворов для местного применения (глазные капли, ротоглотка), внутримышечных и внутрижелудочных растворов или иньекционных лекарственных препаратов.
Получение соединения L-173
Методика получения данного соединения подробно описана в документе RU 2703997.
Получение соли метансульфоновой кислоты и соединения L-173
Получают из основного L-173 и метансульфоновой кислоты в сухом этилацетате, количество кислоты берут в пропорции: 1 моль L-173 на 2 моль кислоты. После прибавления кислоты к раствору основания в этилацетате образуется суспензия, которую фильтруют и промывают этилацетатом и сушат при комнатной температуре в вакууме.
Растворители, использованные в процессе, готовят специально. Этилацетат промывают водным раствором натрия гидрокарбоната, насыщенным водным раствором натрия хлорида, сушат над безводным натрия сульфатом и перегоняют при атмосферном давлении.
Методы анализа
Объекты исследования
Объект №1 - метансульфонат соединения L-173;
Объект №2 - 2-гидроксипропил-β-циклодекстрина;
Объект №3 (объект №1+объект №2) - твердая композиция, включающая 2-гидроксипропил-β-циклодекстрина и метансульфоната соединения L-173, полученная с использованием механохимической обработки;
Объект №4 (объект №1+объект №2) - твердая композиция, включающая 2-гидроксипропил-β-циклодекстрина и метансульфоната соединения L-173, полученная с использованием испарения до постоянной массы.
Дифференциальная сканирующая калориметрия
Все эксперименты проводились с использованием дифференциального сканирующего калориметра (ДСК) теплового потока DSC Perkin Elmer DSC 4000. Калибровка прибора осуществлялась по температурам и энтальпиям фазовых переходов двух стандартных соединений (цинк и индий).
Рентгеноструктурный анализ
Данные РСА были получены на дифрактометре Bruker D8 Advance (CuKα1 - излучение, λ = 1.5406 Å) в интервале углов 4-50 2θ и шагом 0.02 2θ.
Инфракрасная спектроскопия
ИК-спектры объектов №1-4 были получены с использованием инфракрасного спектрометра с преобразованием Фурье, модель Vertex 80v (Bruker Optik GmbH, Германия). Спектральный диапазон составлял 400-4600 см-1 при 128 сканированиях и разрешении 2 см-1. Образцы исследуемых соединений и композиций были растерты в ступке с кристаллическим KBr и для проведения измерений запрессованы в таблетки.
Кинетическая растворимость
Для каждой системы получение профиля растворения кристаллической формы проводилось согласно следующей методике. Избыточное количество исследуемого объекта добавлялась к 60 мл растворителя (дистиллированная вода, рН 6.8), предварительно термостатированного при 25.0 ± 0.1 °С. Полученная суспензия встряхивалась в воздушном термостате при данной температуре. Отбор проб проводился через установленные промежутки времени. После каждого отбора образца убыль растворителя компенсировалась чистым растворителем до постоянного объема. Аликвота объемом 1 мл фильтровалась через стерильные шприцевые фильтры с мембраной из политетрофторэтилена и диаметром пор 0.22 мкм. Определение концентрации вещества в исследуемом растворе проводилось спектофотометрически на приборе Carry 50 (США) в ультрафиолетовой области спектра. Точность спектрофотометрических измерений составляла 2 %. Детектирование исследуемых соединений проводилось при характеристическом значении длины волны максимума поглощения соединения (334 нм).
Релиз
Скорость высвобождения объекта №1 из твердой композиции (объект №3 или объект №4) была определена с помощью тестера растворимости Electrolab EDT-08LX (Индия). Таблетку массой 200 мг, выполненную из твердой композиции на основе соединения L-173 и производного циклодекстрина, готовили прямым прессованием с помощью гидравлического пресса (диаметр 8 мм). Далее держатель с образцом погружался в 400 мл дистиллированной воды и вращался с постоянной скоростью 125 об/мин и температуре 25±0.1 °С. Отбор проб производился при 10 реперных точках в течение 80 мин с начала эксперимента. После каждого отбора пробы объем среды растворения возмещался тем же количеством воды. Содержание объекта исследования в отобранных аликвотах измеряли спектрофотометрически. Анализ таблеток после эксперимента методом ДСК показал, что комплекс соединения с производным циклодекстрином оставался стабильным в течение времени эксперимента.
Получение твердой композиции - объект №3 - с использованием механохимической обработки
Получение твердой композиции проводилось при молярном соотношении компонентов 1:2. Соотношение компонентов составляло 300 мг метансульфоната соединения L-173 (Объект №1) и 1200 мг 2-гидроксипропил-β-циклодекстрина (Объект №2). Для оптимизации процесса комплексообразования был использован метод механоактивации смеси с помощью планетарной мельницы. Данный подход наиболее часто применяется на практике и зарекомендовал себя как эффективный. Выбор оптимальных условий проведения эксперимента определялся путем варьирования скорости и времени перемола.
Физическую смесь Объекта №1 и Объекта №2 помещали в агатовую ячейку планетарной микромельницы Pulverisette 7 (Fritsch, Германия) вместе с 10 агатовыми шариками диаметром 3 мм. Процесс механоактивации (перемола) продолжали в течение 1 часа со скоростью 600 об/мин. Полученный порошок измельчали и просеивали через сито с размером отверстий 0.4 мм. С целью предотвращения сорбции атмосферной влаги образцы хранили в закупоренных стеклянных флаконах.
ДСК анализ Объекта №3
На кривой ДСК Объекта №3 наблюдается широкий эндотермический пик в интервале 40 - 120 °С, связанный с удалением воды из полости циклодекстрина (Фиг. 1). Аналогичный пик зафиксирован у использованного циклодекстрина, который объясняется тем же процессом испарения воды. Небольшие тепловые пики на кривой ДСК Объекта №3 при температуре около 200 °С, возможно, обусловлены изменением подвижности концевых групп компонентов системы или диффузионными эффектами. Процесс удаления незначительного количества воды из образца также обнаружен у индивидуального производного (Объект №1) при его нагревании до 100 °С.
Отсутствие острых пиков на кривых ДСК Объекта №1, Объект №2 и Объекта №3 свидетельствуют об аморфной природе индивидуальных составляющих и образованного механохимическим методом комплекса.
Исследование Объекта №3 методом рентгеноструктурного анализа
Дифрактограммы Объекта №1, Объекта №2 и Объекта №3 характеризуются аморфными гало, которые свидетельствуют о неупорядоченной структуре компонентов и композиции (Фиг. 2).
Следует отметить, что положение пиков комплекса отражает дифракционную картину составляющих его веществ. Полученные результаты позволяют сделать заключение об аморфной природе комплекса Объекта №3, что согласуется с данными ДСК.
Исследование Объекта №3 методом инфракрасной спектроскопии
На Фиг. 3 представлены ИК-спектры индивидуальных компонентов комплекса, а именно Объекта №1 и Объект №2, а также полученного механохимическим методом комплекса Объекта №3.
Для ИК-спектра Объекта №1 характерно наличие острых интенсивных пиков, которые отсутствуют в спектре объекта №3. Данный факт указывает на то, что Объект №1 вошел в полость использованного циклодекстрина и, в связи с этим его присутствие не регистрируется в спектре комплекса.
Полученные данные согласуются с результатами ДСК и РСА.
Получение кинетических зависимостей растворения Объекта №3 в воде при 25 °С
Как было установлено, исследуемый Объект №3 имеет высокую растворимость в воде и, в связи с этим добавление его в раствор проводилось небольшими порциями. При этом визуальное наблюдение показало, что по мере повышения содержания объекта №3 плотность и вязкость раствора возрастает, но донная фаза не образуется. Эксперимент был прекращен, когда вязкость раствора стала настолько большой, что корректно отобрать пробу для измерений стало невозможно. При этом концентрация изученного Объект №1 достигла значения 0.490 моль/л. (Фиг. 4). Использование Объекта №1 в составе композиции объекта №3 показало увеличение растворимости в 644 раза по сравнению с использованием просто Объекта №1.
Получение зависимости высвобождения (релиза) из таблетки твердого Объекта №3
Эксперимент по высвобождению Объект №1 из таблетки твердой композиции Объекта №3 предусматривает регистрацию концентрации активного вещества через определенные промежутки времени. В связи с большим объемом растворителя и высокой растворимостью твердой композиции в воде измерить время релиза не представлялось возможным. Время полного растворения таблетки в воде (рН 6.8) составило 3 минуты.
Изучение термодинамической стабильности Объекта №3
Анализ дифратограмм образца твердой композиции Объекта №3, полученных в первый, второй и третий месяц хранения при температуре 25 °С и атмосферном давлении, не выявил никаких изменений в интенсивности и положении пиков. На Фиг. 5 в качестве сравнения представлена дифратограмма исходного образца комплекса и того же образца после трех месяцев хранения. Полученные результаты позволяют сделать заключение о высокой стабильности твердого комплекса в течение длительного времени.
Получение Объекта №4 с использованием испарения до постоянной массы
Получение объекта №4 проводилось при молярном соотношении компонентов 1:2. Соотношение компонентов составляло 300 мг Объекта №1 и 1200 мг Объекта №2. Для оптимизации процесса комплексообразования был использовано соиспарение смеси при нагревании. Такой подход хорошо зарекомендовал себя при получении твердых дисперсий биоактивных соединений. Выбор оптимальных условий проведения эксперимента определялся путем варьирования природы растворителя, температуры и времени перемешивания.
Физическую смесь Объекта №1 и Объекта №2 помещали в круглодонную колбу и приливали 100 мл этилового спирта. При перемешивании получали истинный раствор, который продолжали перемешивать при температуре 40 °С в течение 12 часов. Далее раствор упаривали на роторном испарителе в вакууме при температуре бани 45 °С до постоянной массы. Полученный порошок измельчали и просеивали через сито с размером отверстий 0.4 мм. С целью предотвращения сорбции атмосферной влаги образцы хранили в закупоренных стеклянных флаконах.
Получение ДСК кривых для Объекта №4
На Фиг. 6 представлены ДСК кривые индивидуального производного (Объект №1), использованного 2-гидроксипропил-β-циклодекстрина (Объект №2) и Объекта №4, полученного методом соиспарения. Во всех трех изученных объектах обнаружен широкий эндотермический пик в интервале температур 25-120°С, связанный с удалением воды. Отсутствие острых пиков, характеризующих фазовые переходы, свидетельствует о неупорядоченной структуре чистых компонентов и комплекса на их основе.
Исследование Объекта №4 методом рентгеноструктурного анализа
Дифратограммы исходных составляющих (Объект №1 и Объект №2) и полученного Объекта №4 показаны на Фиг. 7. Широкие пики или аморфные гало, наблюдаемые на всех трех образцах, свидетельствуют о неупорядоченной структуре Объектов изучения. Полученные данные являются подтверждением аморфного состояния объекта №4 и согласуются с результатами ДСК.
Исследование Объекта №4 методом инфракрасной спектроскопии
Сравнение спектров индивидуального производного (Объект №1), 2-гидроксипропил-β-циклодекстрина (Объект №2) и Объекта №4, полученного методом соиспарения, показало образование комплекса включения (Фиг. 8). При этом в спектре комплекса присутствуют пики связей, характерные для индивидуального циклодекстрина, а также пики связей, зафиксированные для Объекта №1. Представленные данные указывают на вхождение Объекта №1 в полость 2-гидроксипропил-β-циклодекстрина при получении комплекса включения методом соиспарения.
Получение кинетической зависимости растворения Объекта №4 в воде при 25 °С
Эксперимент получения кинетической зависимости растворения выполнялся путем добавления Объекта №4 в воду с целью образования раствора с донной фазой. Однако, в связи с высокой растворимостью Объекта №4 процесс растворения происходил достаточно быстро, но при этом донная фаза не формировалась. Значения концентрации Объекта №1 в растворе, определенные за 15 минут от начала эксперимента приведены на Фиг. 9. По истечении этого времени вязкость раствора стала настолько большой, что это не позволило отбирать пробу для анализа с удовлетворительной точностью. Измерения были остановлены при достижении концентрации Объекта №1 в растворе - 0.517 моль/литр.
Высвобождение Объекта №4 из таблетки в воде при 25°С
Установлено, что процесс растворения таблетки комплекса Объекта №4 в достаточно большом объеме растворителя (400 мл) происходит с высокой скоростью и через 5 минут таблетка была полностью растворена. По этой причине оказалось невозможно за это ограниченное время получить зависимость высвобождения Объекта №1 из таблетки от времени.
Изучение термодинамической стабильности Объекта №4
Для исследования стабильности твердого Объекта №4 был использован метод рентгеноструктурного анализа от порошка. Дифрактограммы образца Объекта №4 были получены в указанной планом последовательности. В течение трех месяцев хранения при комнатной температуре и атмосферном давлении никаких изменений в положении и интенсивности пиков на дифрактограммах Объекта №4 обнаружено не было, что указывает на его высокую стабильность.
Изучение термодинамической стабильности растворов при комнатной температуре
На основе полученных экспериментальных данных можно сделать заключение, что Объект №3 и Объект №4 имеют превосходные характеристики растворения. Растворимость Объекта №1 в составе данных композиций увеличилась в 644 раза по сравнению с индивидуальным соединением. Показателем термодинамической стабильности Объекта №3 и Объекта №4 служило постоянство концентрации Объекта №1 в водных растворах указанных объектов. Начальная концентрация Объекта №1 в приготовленных растворах была равна 6.3⋅10-4 моль/литр (0.5 г/литр). Измерения концентрации Объекта №1 проводились в течение 2-х недель. За это время отклонения в величине исходной концентрации Объекта №1 не превышали экспериментальных ошибок измерения растворимости (2-4%), что указывает на высокую стабильность растворов объектов №3 и №4.
Исследование долгосрочной стабильности композиций по изобретению
Исследованию долгосрочной стабильности было повергнуты 2 серии образцов из одной партии: твердая композиция, включающая в составе мезилатную соль соединения L-173 и 2-гироксипропил-β-циклодекстрина в соотношении 1:2, а также раствор указанной твердой композиции в воде (дейтертрованной), что было сделано для удобства контроля метод ЯМР спектроскопии через разные промежутки времени. Твердый образец при хранении в холодильнике при 8°С в течение 2 лет не претерпел никаких деструкций и все химические сдвиги соответствовали структуре и начальному образцу (контроль через 12 месяцев после начала хранения и через 24 месяца). В водном растворе через 1 месяц стояния раствора при комнатной температуре наблюдалось появление дополнительной примеси (до 5%) которая увеличилась за 6 месяцев до 12 процентов. Полученные результаты свидетельствуют в пользу долгосрочного хранения в виде твердой лекарственной формы с растворением непосредственно перед введением препарата.
Характеристика биологической активности
Для подтверждения эффективности водорастворимых форм проведено исследование на модели выживаемости при диссеминированной кандидозной инфекции у крыс. В эксперименте животные, инфицированные грибом Candida albicans, в течении 2-х недель получали терапию по следующей схеме:
1. Композиция, включающая мезилатную соль L-173 и 2-гидроксипропил-β-циклодекстрин, в дозе 10 мг/кг 2 раза в день;
2. Композиция, включающая мезилатную соль L-173 и 2-гидроксипропил-β-циклодекстрин, в дозе 30 мг/кг 1 раза в день;
3. Препарат сравнения Флуконазол в дозе 15 мг/кг 1 раз в день.
Доза в 20 мг/кг определена в экспериментах, проведенных на основании данных по элиминации кандидозных гифов при однократном внутрижелудочном введении соединения L-173 [RU2703997].
Таблица 3.
Контрольная группа с заражением
Как видно из таблицы 3 водорастворимые формы в составе комплекса с 2-гидроксипропил- β-циклодекстрином в дозах от 20 мг/кг при 2-х кратном приеме (группа 1) или 30 мг/кг при однократном приеме (группа 3) обеспечивают 100% выживаемость инфицированных животных.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Новые потенциальные противогрибковые средства на основе тиазолидин-2,4-диона и триазола | 2023 |
|
RU2814730C1 |
| Гибридные амиды на основе триазола и тиазолидина, обладающие антимикробной активностью | 2018 |
|
RU2703997C1 |
| Соль гликопептидного антибиотика и фармацевтические композиции на ее основе | 2023 |
|
RU2827992C1 |
| 3,5-Замещенные производные тиазолидин-2,4-диона, обладающие противомикробной активностью | 2018 |
|
RU2690161C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ ЛИЗИНА, ПРОЛИНА И ТРИТЕРПЕНОВОЙ КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ РНК И ДНК-СОДЕРЖАЩИМИ ВИРУСАМИ, ТАКИМИ КАК: ГРИПП, ГЕРПЕС, ОПОЯСЫВАЮЩИЙ ЛИШАЙ, ПАПИЛЛОМА ЧЕЛОВЕКА, АДЕНОНОВИРУСЫ, А ТАКЖЕ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ ГРАМ-ПОЛОЖИТЕЛЬНЫМИ И ГРАМ-ОТРИЦАТЕЛЬНЫМИ МИКРООРГАНИЗМАМИ | 2013 |
|
RU2535052C1 |
| ГИБРИДНЫЕ ЭФИРЫ НА ОСНОВЕ ПРОИЗВОДНЫХ ТИАЗОЛИДИН-2,4-ДИОНА И АЗОЛОВ (1Н-1,3-ИМИДАЗОЛА И 1Н-1,3,4-ТРИАЗОЛА) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2662153C1 |
| КОМПЛЕКСЫ ВКЛЮЧЕНИЯ ПЕРИНДОПРИЛА | 2005 |
|
RU2372353C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2004 |
|
RU2358729C2 |
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ ГРАМИЦИДИНА С, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2800287C1 |
| ПЕРОРАЛЬНЫЕ ПРОТИВОГРИБКОВЫЕ КОМПОЗИЦИИ | 1994 |
|
RU2118899C1 |
Группа изобретений относится к химии и фармацевтике, а именно к вариантам фармацевтической композиции для профилактики и/или лечения инфекционного заболевания микробной этиологии, к применению одной из композиций для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта и к способу ее получения. Предложенные композиции включают терапевтически или профилактически эффективное количество метансульфоната (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3-(1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона и модифицированный β-циклодекстрин при их мольном соотношении 1:2-1:5, где модифицированный β-циклодекстрин представляет собой 2-гидроксипропил-β-циклодекстрин или сульфобутиловый эфир-β-циклодекстрина. Группа изобретений обеспечивает создание композиций, характеризующихся высокой растворимостью, стабильностью и эффективностью, подходящих для перорального и парентерального введения. 4 н. и 23 з.п. ф-лы, 10 ил., 3 табл.
1. Фармацевтическая композиция для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта, включающая:
- терапевтически или профилактически эффективное количество метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3- (1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона;
- модифицированный β-циклодекстрин, который представляет собой 2-гидроксипропил-β-циклодекстрина или сульфобутиловый эфир-β-циклодекстрина;
причем мольное соотношение метансульфоната соединения и модифицированного β-циклодекстрина составляет 1:2-1:5, при этом композиция выполнена в твердой форме.
2. Фармацевтическая композиция по п.1, которая дополнительно содержит, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество.
3. Фармацевтическая композиция по п.2, в которой вспомогательное вещество представляет собой наполнитель.
4. Фармацевтическая композиция по п.1, в которой заболевание вызвано грибковой инфекцией.
5. Фармацевтическая композиция по п.4, в котором заболевание микробной этиологии вызвано грибом рода Candida spp., Aspergillus spp., Rhizopus spp., Microsporum spp., Trichophyton spp. и/или Epidermophyton spp.
6. Фармацевтическая композиция по п.4, характеризующееся тем, что заболевание микробной этиологии вызвано грибом вида Candida albicans, C. non albicans, C. auris, Aspergillus fumigatus, Aspergillus niger, Rhizopus spp., Microsporum canis или Trichophyton rubrum.
7. Фармацевтическая композиция по п.1, характеризующееся тем, что заболевание представляет собой заболевание глаз, кожи, ногтей и/или внутренних органов.
8. Фармацевтическая композиция по п.7, в котором заболевание представляет собой дерматофитию, поверхностный микоз, кандидоз кожи и/или ногтей, вагинальный кандидоз, кандидозный стоматит, эндокардит, системный кандидоз или аспергилез.
9. Фармацевтическая композиция для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта, включающая:
- терапевтически или профилактически эффективное количество метансульфоната соединения (5Z)-5-[(4-хлорфенил)метилиден]-3-(2-{4-[2-(2,4-дифторфенил)-2-гидрокси-3- (1,2,4-триазол-1-ил)пропил]пиперазин-1-ил}-2-оксоэтил)-1,3-тиазолидин-2,4-диона;
- модифицированный β-циклодекстрин, который представляет собой 2-гидроксипропил-β-циклодекстрина или сульфобутиловый эфир-β-циклодекстрина;
- растворитель;
причем мольное соотношение метансульфоната соединения и модифицированного β-циклодекстрина составляет 1:2-1:5.
10. Фармацевтическая композиция по п.9, в которой растворитель представляет собой воду.
11. Фармацевтическая композиция по п.10, в которой вода представляет собой воду очищенную.
12. Фармацевтическая композиция по п.11, в которой вода представляет собой деионизованную воду, воду для инъекций.
13. Фармацевтическая композиция по п.9, в которой заболевание вызвано грибковой инфекцией.
14. Применение композиции по любому из пп.9-13 для профилактики и/или лечения инфекционного заболевания микробной этиологии у субъекта.
15. Применение по п.14, в котором композицию вводят субъекту парентерально.
16. Применение по п.15, в котором композицию вводят посредством инфузии или внутримышечной инъекции.
17. Применение по п.14, в котором композицию вводят перорально.
18. Применение по п.17, в котором композицию вводят в виде раствора для приема внутрь.
19. Применение по п.14, в котором заболевание вызвано грибковой инфекцией.
20. Применение по п.14, в котором заболевание микробной этиологии вызвано грибом рода Candida spp., Aspergillus spp., Rhizopus spp., Microsporum spp., Trichophyton spp. и/или Epidermophyton spp.
21. Применение по п.14, характеризующееся тем, что заболевание микробной этиологии вызвано грибом вида Candida albicans, C. non albicans, C. auris, Aspergillus fumigatus, Aspergillus niger, Rhizopus spp., Microsporum canis или Trichophyton rubrum.
22. Применение по п.14, характеризующееся тем, что заболевание представляет собой заболевание глаз, кожи, ногтей и/или внутренних органов.
23. Применение по п.22, в котором заболевание представляет собой дерматофитию, поверхностный микоз, кандидоз кожи и/или ногтей, вагинальный кандидоз, кандидозный стоматит, эндокардит, системный кандидоз или аспергилез.
24. Способ получения фармацевтической композиции по п.9, включающий растворение фармацевтической композиции по любому из пп.1-8 в растворителе.
25. Способ по п.24, в котором растворитель представляет собой воду.
26. Способ по п.25, в которой вода представляет собой воду очищенную.
27. Способ по п.26, в которой вода представляет собой деионизованную воду, воду для инъекций.
| Volkova T.V | |||
| et al | |||
| Comparative analysis of solubilization and complexation characteristics for new antifungal compound with cyclodextrins | |||
| Impact of cyclodextrins on distribution process / European Journal of Pharmaceutical Sciences, 2020, v | |||
| Способ приготовления кирпичей для футеровки печей, служащих для получения сернистого натрия из серно-натриевой соли | 1921 |
|
SU154A1 |
| Способ изготовления завитков искусственного каракуля | 1956 |
|
SU105531A1 |
| Гибридные амиды на основе триазола и тиазолидина, обладающие антимикробной активностью | 2018 |
|
RU2703997C1 |
| Volkova T.V | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2024-12-09—Публикация
2023-10-10—Подача