ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Настоящая заявка испрашивает преимущество приоритета по предварительной заявке на патент США №63/013098, поданной 21 апреля 2020 года, содержание которой включено в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТИ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[2] Настоящее изобретение относится к аналитическим способам и системам, основанным на измерении флуоресценции, и в частности к способам осуществления валидации для оценки достоверности и воспроизводимости результатов измерений, полученных с помощью аналитического прибора, основанного на измерении флуоресценции.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[3] Системы клеточного анализа, основанные на измерении флуоресценции, такие как проточная цитометрия и сортировка флуоресцентно-активированных клеток (FACS), являются мощными инструментами для измерения количества различных клеточных элементов в тестируемом образце, таких как рецепторы клеточной поверхности и внутриклеточные компоненты. В методах FACS для окрашивания образцов используют конъюгированные с антителами флуорохромы (флуоресцентные красители) и таким образом получают сигнал о наличии и количестве таких элементов, как клеточные рецепторы или другие клеточные маркеры, пептиды и нуклеиновые кислоты. Разработка нескольких различных флуорохромов, каждый из которых характеризуется уникальным идентифицируемым спектром испускания, позволяет одновременно использовать более одного флуорохрома. Вследствие их объединенной мощности и универсальности проточную цитометрию и FACS обычно применяют в процессе разработки лекарственных средств, например, для иммунофенотипирования, анализа экспрессии или занятости рецепторов и других функциональных анализов.
[4] Несмотря на свою мощность, способы проточной цитометрии и FACS обычно более сложны в отношении валидации, чем другие аналитические способы, по целому ряду причин. Среди этих причин отсутствие стандартизации протоколов, отсутствие стандартизированных эталонных материалов и применение сложных и чувствительных инструментов. Моноклональные и поликлональные антитела, обычно используемые для окрашивания, не стандартизированы и могут существенно различаться по качеству и эффективности. Таким образом, исследователь должен тщательно оценивать, работают ли используемые реагенты надлежащим образом. Тем не менее, у исследователя мало руководств по проведению валидации данного способа и прибора. Согласно FDA США, например, валидация определяется просто как оценка пригодности способа для предполагаемых путей использования, и рекомендуется, что процесс валидационного тестирования должен гарантировать, что анализ соответствует предварительно определенным стандартам, надежно работает и является подходящим для его предполагаемого применения. В руководствах FDA признается, что универсального регулирования валидации не существует, и они не содержат конкретного руководства по валидационным анализам. Отсутствие стандартных или общепринятых нормативных руководств и справочных материалов для валидации является проблемой, которая, к сожалению, недостаточно описана в литературе. Проблема валидации способа является еще более сложной, если считается, что клетка-или маркер-мишень, представляющие интерес, присутствуют в образце в очень низких концентрациях. Существует потребность в улучшенных способах осуществления валидации для осуществления валидации эффективности аналитических методов и систем, основанных на измерении флуоресценции.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[5] Среди различных аспектов настоящего изобретения представлен способ осуществления валидации измерений с помощью аналитического прибора, основанного на измерении флуоресценции, в отношении популяции окрашенных клеток-мишеней в тестируемом образце, при этом способ включает: (а) отрицательное окрашивание или наличие отрицательно окрашенных клеток в первой части эталонного образца, содержащего клетки-мишени, экспрессирующие маркер клеток-мишеней; (b) положительное окрашивание или наличие положительно окрашенных клеток-мишеней во второй части эталонного образца; (с) осуществление анализа первой части эталонного образца с помощью прибора с получением результата измерения флуоресценции, указывающего на концентрацию клеток-мишеней в первой части эталонного образца, и осуществление анализа второй части эталонного образца с помощью прибора с получением результата измерения флуоресценции, указывающего на концентрацию клеток-мишеней во второй части эталонного образца; (d) на основании результатов измерений флуоресценции, полученных в (с), получение серии разбавлений, включающей множество разбавленных образцов, при этом каждый разбавленный образец характеризуется номинальной концентрацией клеток-мишеней, каждая номинальная концентрация клеток превышает концентрацию клеток-мишеней, на которую указывал результат измерения флуоресценции отрицательно окрашенной первой части в (а), где номинальная концентрация в каждом разбавленном образце отличается от номинальной концентрации в каждом из остальных разбавленных образцов; (е) осуществление анализа серии разбавленных образцов из (d) с помощью прибора с получением серии результатов измерений флуоресценции, предусматривающих измерение флуоресценции каждого разбавленного образца, и (f) сравнение номинальной концентрации клеток из (d) для каждого разбавленного образца и результата измерения флуоресценции из (е) для осуществления количественной оценки эффективности способа окрашивания с помощью прибора. Прибор может представлять собой, например, проточный цитометр.
[6] В другом аспекте настоящее изобретение предусматривает способ осуществления валидации измерений с помощью проточного цитометра в отношении популяции окрашенных клеток-мишеней в тестируемом образце, при этом способ включает: (а) отрицательное окрашивание или наличие отрицательно окрашенных клеток в первой части эталонного образца, содержащего клетки-мишени, экспрессирующие маркер клеток-мишеней; (b) положительное окрашивание или наличие положительно окрашенных клеток-мишеней во второй части эталонного образца; (с) осуществление анализа обеих из первой части и второй части эталонного образца с помощью проточного цитометра с получением результатов измерений флуоресценции, указывающих на концентрацию клеток-мишеней в каждой из первой части эталонного образца и второй части эталонного образца; (d) на основании результатов измерений флуоресценции, полученных в (с), получение серии разбавленных образцов, каждый из которых характеризуется номинальной концентрацией клеток-мишеней, систематически варьирующейся в серии разбавлений, где номинальная концентрация клеток в по меньшей мере одном разбавленном образце превышает концентрацию клеток-мишеней, на которую указывал результат измерения флуоресценции отрицательно окрашенной первой части в (а); (е) осуществление анализа серии разбавленных образцов из (d) с помощью проточного цитометра с получением серии результатов измерений флуоресценции, предусматривающих измерение флуоресценции каждого разбавленного образца, и (f) сравнение номинальной концентрации клеток из (d) для каждого разбавленного образца и результата измерения флуоресценции из (е) для осуществления количественной оценки эффективности способа окрашивания с помощью проточного цитометра.
[7] Любой из раскрытых способов может включать один или несколько любых из следующих признаков. Сравнение в (f) может предусматривать, например, выполнение статистического расчета разницы между номинальной концентрацией клеток и измерением флуоресценции для каждого разбавленного образца с определением по меньшей мере одного из линейности, диапазона, точности, прецизионности, предела выявления (LOD) и нижнего предела количественного определения (LLOQ) для прибора и способа окрашивания. Определение LLOQ может предусматривать, например, осуществление идентификации концентрации клеток-мишеней, ассоциированное с предварительно определенным критерием прецизионности и предварительно определенным критерием точности. Отрицательное окрашивание клеток-мишеней в первой части эталонного образца в (а) может предусматривать введение в первую часть эталонного образца (i) флуоресцентного красителя для исключения мертвых клеток, (ii) неспецифического антитела, конъюгированного с флуорохромом, например, антитела изотипического контроля, и (ill) специфического антитела, способного специфически связывать маркер-мишень (антиген) на клетке-мишени, неконъюгированного с флуорохромом.
Неспецифическое антитело, которое конъюгировано с флуорохромом для отрицательного окрашивания, может предусматривать антитело, не обладающее способностью специфически связываться с клеточным антигеном, такое как, например, IgD, IgG, IgA, IgM или IgE. Отрицательно окрашенную первую часть можно получать в отсутствие стадии деплеции клеток. Положительное окрашивание клеток-мишеней во второй части эталонного образца в (b) может предусматривать введение во вторую часть эталонного образца (i) флуоресцентного красителя для исключения мертвых клеток (того же красителя, который использовался для отрицательного окрашивания) и (ii) того же самого специфического антитела, которое использовалось для отрицательного окрашивания, но не неконъюгированного с флуорохромом, а скорее конъюгированного с тем же флуорохромом, который использовался для отрицательного окрашивания (при котором флуорохром конъюгирован с неспецифическим антителом). В любом из способов флуоресцентный краситель для исключения мертвых клеток, используемый для окрашивания, может быть выбран из красителя, связывающего нуклеиновые кислоты, йодида пропидия, DAPI, DRAQ7, 7-AAD, T0-PR0-3 и красителя, реагирующего с аминогруппами. Используемый флуорохром может быть выбран из известных флуорохромов, например без ограничения из аллофикоцианина (АРС), АРС С750, АРС AF700, бриллиантового фиолетового (BV)421, BV510, хилита 7 (Н7) BV605, BV650, РЕ CF594, флуоресцеинизотиоцианата (FITC), R-фикоэритрина (РЕ или R-PE), РЕ-Су7 (РЕ, связанного с цианиновым красителем Су7), АРС-Су7 (АРС, связанного с цианиновым красителем Су7), АРС-Н7 (АРС, связанного с хилитом 7, представляющим собой аналог Су (Н7)). Маркер клеток-мишеней может быть выбран, например, из CD3, CD4 и CD8 в качестве маркера Т-клеток, CD19 в качестве маркера В-клеток, CD235a в качестве маркера эритроцитов, CD56 в качестве маркера естественных клеток-киллеров (NK), CD14 в качестве маркера моноцитов и CD66b в качестве маркера гранулоцитов. В одном аспекте популяция клеток-мишеней представляет собой популяцию Т-клеток, и маркер клеток-мишеней представляет собой CD3.
[8] Способ может дополнительно предусматривать мультиплексирование посредством отрицательного окрашивания и положительного окрашивания двух или более различных маркеров-мишеней клеток-мишеней или потенциально окрашивание двух или более различных маркеров-мишеней двух или более клеток-мишеней. Отрицательное окрашивание может дополнительно предусматривать введение в первую часть эталонного образца двух или более специфических антител, при этом каждое специфическое антитело способно специфически связывать один из двух или более маркеров-мишеней и не конъюгировано с флуорохромом. Положительное окрашивание может дополнительно предусматривать введение во вторую часть эталонного образца двух или более специфических антител, каждое из которых конъюгировано с флуорохромом.
[9] Расчет в (f) можно выполнять с помощью процессора, соединенного с прибором или проточным цитометром. Тестируемый образец может содержать клетку-мишень, присутствующую в концентрации, составляющей не более чем 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%. Серия разбавлений может предусматривать разбавленный образец, характеризующийся самой высокой концентрацией клеток-мишеней, где самая высокая концентрация составляет 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%. В любом из способов серия разбавленных образцов может содержать по меньшей мере два, три, четыре, пять, шесть, семь, восемь, девять или десять разбавленных образцов.
[10] В другом аспекте настоящее изобретение предусматривает энергонезависимый машиночитаемый носитель, содержащий инструкции для компьютерного процессора для выполнения сравнения на стадии (f) любого из раскрытых способов или для выполнения любых статистических расчетов для определения любого одного или нескольких из линейности, диапазона, точности, прецизионности, предела выявления (LOD) и самого нижнего предела количественного определения (LLOQ) для прибора и способа окрашивания.
[11] В еще одном аспекте настоящее изобретение предусматривает систему для валидации результатов измерений флуоресценции в тестируемом образце, полученных с помощью прибора, основанного на измерении флуоресценции, содержащую прибор, основанный на измерении флуоресценции, и компьютер, соединенный с прибором, основанным на измерении флуоресценции, и содержащий машиночитаемый носитель, содержащий инструкции для компьютерного процессора, описанного выше. В системе прибор, основанный на измерении флуоресценции, может представлять собой проточный цитометр.
[12] В еще одном аспекте настоящее изобретение предусматривает набор, содержащий реагенты для окрашивания клеток в эталонном образце, для осуществления валидации аналитического способа, основанного на измерении флуоресценции, для осуществления анализа клеток-мишеней в тестируемом образце, при этом набор содержит: (i) реагенты для отрицательного окрашивания, предусматривающие: (а) флуоресцентный краситель для исключения мертвых клеток, (b) неспецифическое антитело, конъюгированное с флуорохромом, и (с) неконъюгированное специфическое антитело, способное специфически связывать маркер-мишень (антиген) на клетках-мишенях; (11) реагенты для положительного окрашивания, предусматривающие: (а) флуоресцентный краситель для исключения мертвых клеток и (b) специфическое антитело, конъюгированное с флуорохромом, и инструкции по (а) отрицательному окрашиванию первой части эталонного образца, (b) положительному окрашиванию второй части эталонного образца и (с) получению серии разбавлений, включающей множество разбавленных образцов, каждый из которых характеризуется номинальной концентрацией клеток-мишеней, систематически варьирующейся в серии разбавлений, где номинальная концентрация клеток в по меньшей мере одном разбавленном образце больше, чем концентрация клеток-мишеней, на которую указывал результат измерения флуоресценции отрицательно окрашенной первой части.
[13] Другие аспекты и признаки настоящего изобретения подробно описаны ниже.
ССЫЛКА НА ЦВЕТНЫЕ ГРАФИЧЕСКИЕ МАТЕРИАЛЫ
[14] Файл заявки содержит по меньшей мере одну фотографию, выполненную в цвете. Копии данной публикации патентной заявки с цветными фотографиями будут предоставлены патентным ведомством по запросу и после уплаты необходимой пошлины.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[15] На фиг. 1 представлено схематическое изображение способа согласно настоящему изобретению, в котором предложен альтернативный способ применения клеточного сортера, решающий техническую проблему получения препарата клеток, характеризующегося концентрацией клеток, близкой к 0,00%.
[16] Фиг. 2 представляет собой график FACS, демонстрирующий типичные результаты, полученные с отрицательно окрашенным образцом. Показанные события были гейтированы по жизнеспособным клеткам на основании прямого и бокового светорассеяния и PI (для исключения мертвых клеток).
[17] Фиг. 3 представляет собой график FACS, демонстрирующий типичные результаты, полученные с положительно окрашенным образцом. Показанные события были гейтированы по жизнеспособным клеткам на основании прямого и бокового светорассеяния и PI (для исключения мертвых клеток).
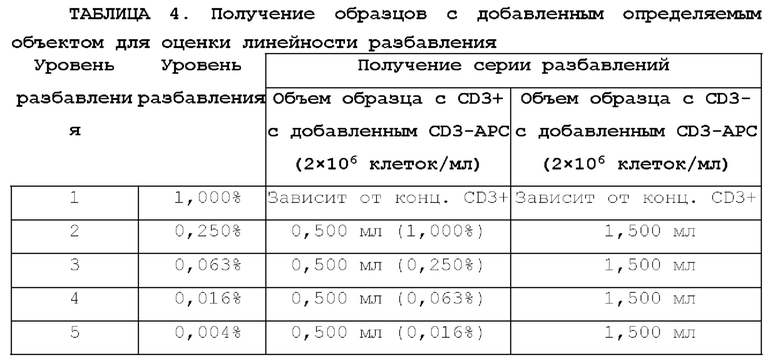
[18] На фиг. 4 изображена последовательность процедур для получения образцов для оценки линейности.
[19] На фиг. 5 изображена последовательность процедур для получения серии разбавлений.
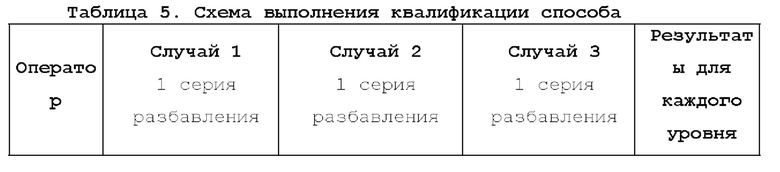
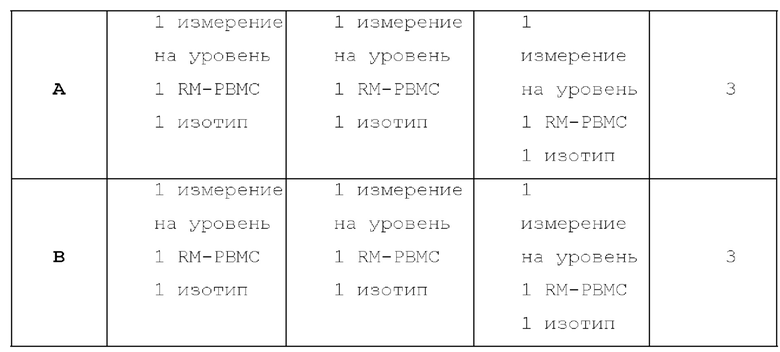
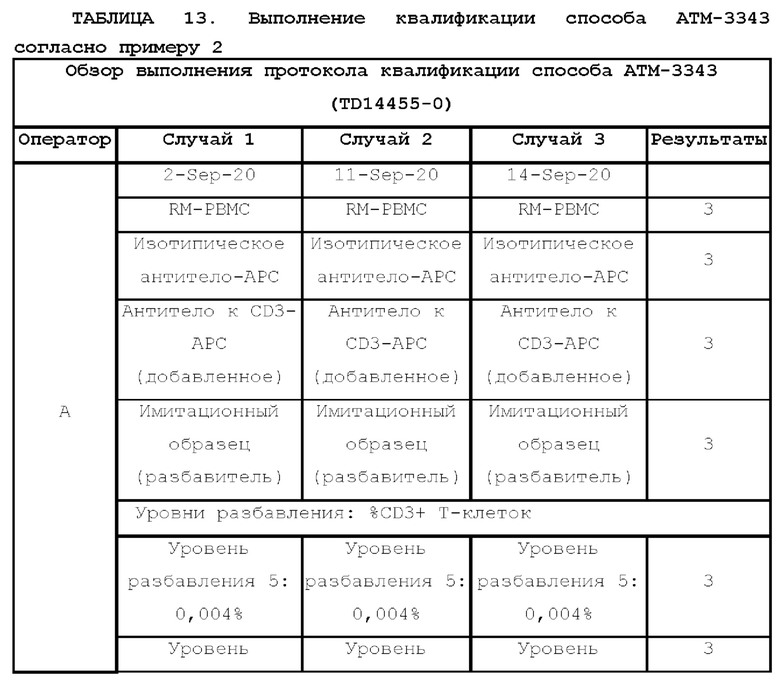
[20] На фиг. 6 изображено выполнение квалификации способа двумя операторами в трех различных случаях, указанных в примере 2.
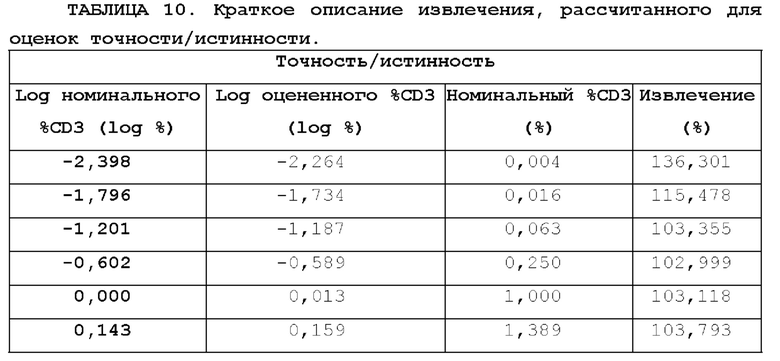
[21] Фиг. 7 представляет собой график остатков для непреобразованного номинального %CD3 и расчетного %CD3 (результат) для а) непреобразованных данных и b)-f) различных логарифмически преобразованных данных.
[22] На фиг. 8 изображен процент (%) расчетного %CD3 по сравнению с номинальным %CD3. Пунктирные линии указывают на 100+30% восстановление.
[23] На фиг. 9 изображен регрессионный анализ образцов с оцененной линейностью.
ПОДРОБНОЕ ОПИСАНИЕ
[24] Валидация аналитического способа имеет решающее значение для оценки достоверности и воспроизводимости аналитических измерений, основанных на измерении флуоресценции. Чтобы такие измерения были ценными, они должны быть воспроизводимыми. Например, сортировка флуоресцентно-активированных клеток (FACS) представляет собой специализированный тип анализа, основанного на измерении флуоресценции, и представляет собой мощный способ сортировки смеси биологических клеток на отдельные популяции на основании флуоресцентных сигналов каждой клетки. В отличие от проточной цитометрии, выполняемой для простого подсчета и сортировки клеток, FACS обеспечивает как качественный, так и количественный анализ с применением данных, полученных посредством проточной цитометрии. Важно чтобы аналитические измерения, основанные на измерении флуоресценции, такие как измерения, выполняемые с применением FACS, были должным образом валидированы вследствие различий в качестве и эффективности антител, используемых в таких аналитических методиках.
[25] Один из подходов к валидации основан на получении серии разбавлений из нескольких разбавлений или образцов с добавленным определяемым объектом, каждый из которых характеризуется известной или номинальной концентрацией клетки-мишени или маркера-мишени. Например, серийные разбавления выполняют посредством добавления известных количеств клетки-мишени с получением нескольких образцов с известными (номинальными) концентрациями клеток, систематически варьирующимися от более высокой концентрации, например, 50%, до более низкой концентрации, например, 1% клеток. Образцы с добавленным определяемым объектом анализируют с помощью цитометра, и для каждого образца с добавленным определяемым объектом получают результаты измерений флуоресценции. Образцы с добавленным определяемым объектом сравнивают с измеренными значениями, полученными с помощью цитометра. Точность прибора и способа окрашивания определяют посредством статистических расчетов, например, посредством расчета корреляции номинальных и измеренных значений, определения крутизны зависимости, определения R-sq и т.п. Как известно, предел выявления (LOD) FACS и/или предел количественного определения (LOQ) можно рассчитать посредством окрашивания и получения повторного образца(образцов) с добавленным определяемым объектом и его анализа с помощью цитометра с получением результатов измерений положительных событий. Затем можно использовать валидированные анализы для выявления и количественного определения концентрации клеток в образце.
[26] Для точного получения серии образцов с добавленным определяемым объектом требуется по меньшей мере два образца: один или несколько образцов, каждый из которых характеризуется известной (номинальной) концентрацией клетки-мишени или маркера-мишени, и образец, который практически не содержит клетки-мишени или маркера-мишени (концентрация составляет приблизительно 0). Обычно используют более одного образца с добавленным определяемым объектом. Например, валидация прибора и способа окрашивания с применением пяти (5) уровней предусматривает получение серии образцов с добавленным определяемым объектом, содержащих пять различных номинальных концентраций клетки-мишени или маркера-мишени (например, 2%, 4%, 6%, 8% и 10%), плюс один образец, содержащий 0%. Для получения серии образцов с добавленным определяемым объектом эталонный материал, содержащий известную относительно более высокую концентрацию клетки-мишени или маркера-мишени, представляющих интерес, последовательно и систематически разбавляют с получением серии образцов с добавленным определяемым объектом, характеризующихся более низкими концентрациями. Тем не менее, во многих случаях получение образцов с добавленным определяемым объектом затруднено вследствие отсутствия готового исходного эталонного материала. Например, если представляющим интерес аналитом является клетка, такая как CD3+ клетка (Т-клетка), такого стандартного эталонного материала не существует. Другими словами, нельзя просто приобрести стандартный эталонный материал, характеризующийся известной концентрацией, такой как 10% или 0% CD3+ клеток, который можно разбавить с получением образцов с добавленным определяемым объектом, характеризующихся более низкими концентрациями, составляющими 8, 6, 4 и 2%. Теоретически для получения серии образцов с добавленным определяемым объектом с последовательно более низкими концентрациями можно использовать коммерчески доступные клеточные сортеры. Однако при низких расчетных концентрациях клетки-мишени или маркера-мишени, составляющих, например, приблизительно 0,1% или ниже, вплоть до приблизительно 0,01%, такой подход является дорогостоящим и времязатратным.
[27] Настоящее изобретение решает техническую проблему обеспечения отрицательных эталонных образцов и образцов с добавленным определяемым объектом для ситуации, когда не существует стандартного эталонного материала, и обеспечения получения образцов с добавленным определяемым объектом в концентрации ниже 0,1%, что является полезным для валидации, если клетка-мишень или маркер-мишень присутствует в концентрации ниже 0,1%. Например, в зависимости от используемого прибора и окрашивания LLOQ может быть ниже 0,01%. Соответственно, настоящее изобретение относится к способам и системам для валидации результатов измерений, полученных с помощью аналитического прибора, основанного на измерении флуоресценции, такого как проточный цитометр, окрашенной популяции клеток-мишеней в тестируемом образце.
Аналитические приборы, основанные на измерении флуоресценции
[28] Аналитический прибор, основанный на измерении флуоресценции, предусматривает любой аналитический прибор, способный измерять флуоресцентный сигнал в качестве индикатора присутствия аналита-мишени или типа клеток-мишеней в образце. В зависимости от используемого оборудования и способов прибор может быть способен к количественному определению аналита-мишени или типа клеток-мишеней в тестируемом образце на основании интенсивности флуоресцентного сигнала. Одним из примеров аналитического прибора, основанного на измерении флуоресценции, является проточный цитометр. FACS (сортировка флуоресцентно-активированных клеток) представляет собой другую, но родственную методику, основанную на проточной цитометрии. Проточная цитометрия представляет собой способ, при котором используют проточный цитометр для исследования и определения экспрессии молекул как внутри, так и снаружи клетки, а также для определения и характеризации отдельных типов клеток. Проточную цитометрию также можно использовать для определения других параметров, таких как размер клеток, объем и чистота образца выделенных клеток. FACS представляет собой методику проточной цитометрии, при которой применяют специфические антитела, меченные флуорохромами, для получения данных по экспрессии и сортировки образцов клеток по ряду переменных.
[29] FACS можно проводить с применением любого из ряда типов проточных цитометров, включая традиционные проточные цитометры, акустические фокусирующие цитометры, клеточные сортеры или визуализирующие проточные цитометры. В наиболее распространенных традиционных цитометрах используется обжимающая жидкость для фокусирования потока образца и обычные лазеры, такие как лазеры с длиной волны 488 нм (синий), 405 нм (фиолетовый), 532 нм (зеленый), 552 нм (зеленый), 561 нм (зелено-желтый), 640 нм (красный) и 355 нм (ультрафиолетовый). В акустических фокусирующих цитометрах для фокусирования клеток для анализа используются ультразвуковые волны, что предотвращает засорение образца и позволяет вводить большее количество образца. Клеточные сортеры представляют собой тип традиционных проточных цитометров, позволяющий пользователю собирать образцы после обработки. Клетки, которые являются положительными по требуемому параметру, можно отделить от клеток, которые являются отрицательными по данным параметрам. Визуализирующие цитометры представляют собой традиционные цитометры в сочетании с флуоресцентной микроскопией и все они предназначены для быстрого анализа образца в отношении морфологии и многопараметрической флуоресценции как на уровне отдельной клетки, так и на уровне популяции. Проточные цитометры обычно соединяют с компьютером, содержащим процессор, который контролирует функционирование прибора. Способы и системы, описанные в данном документе, можно применять для использования любого проточного цитометра, описанного в данном документе.
Способы
[30] Способы, описанные в данном документе, решают техническую проблему обеспечения отрицательного эталона и образцов с низким уровнем добавленного определяемого объекта, когда не существует стандартного эталонного материала, что таким образом позволяет осуществлять надежную валидацию результатов измерений, основанных на измерении флуоресценции, например, с помощью проточного цитометра (FACS), в ситуациях, где клетка-мишень или маркер-мишень присутствуют в образце в концентрации ниже 0,1% или даже меньше.
[31] Фиг. 1 представляет собой схематическую иллюстрацию способа. Положительно и отрицательно окрашенные эталонные образцы получают с применением антитела, способного специфически связывать маркер клеток-мишеней (специфического антитела), и "изотипического антитела" (неспецифического антитела), и флуорохрома, конъюгированного со специфическим антителом или с неспецифическим антителом, в зависимости от того, выполняют отрицательное или положительное окрашивание. Более конкретно, эталонный образец получают и делят на две части. Первую часть эталонного образца отрицательно окрашивают с помощью (а) флуоресцентного красителя для исключения мертвых клеток, (11) неспецифического антитела, конъюгированного с флуорохромом, например, антитела изотипического контроля, и (III) специфического антитела, способного специфически связывать маркер-мишень (антиген) на клетке-мишени. Для отрицательного окрашивания специфическое антитело не конъюгируют с флуорохромом. Неспецифическое антитело, конъюгированное с флуорохромом для отрицательного окрашивания, представляет собой антитело, способное связываться с клеткой, которая не содержит эпитопа, специфического в отношении данного антитела, т.е. связывается с клеткой, но не посредством специфического связывания, как при связывании антитела со специфическим эпитопом на клетке, и таким образом неспецифическое антитело также характеризуется высокой константой диссоциации (Kd) в отношении маркера, как более подробно описано ниже. В качестве неспецифического антитела можно использовать любой из неспецифических иммуноглобулинов IgD, IgG, IgA, IgM или IgE.
[32] Вторую часть эталонного образца положительно окрашивают с помощью флуоресцентного красителя для исключения мертвых клеток (того же красителя, который использовался на стадии отрицательного окрашивания) и того же специфического антитела, которое использовалось для отрицательного окрашивания, но не неконъюгированного, а скорее конъюгированного с тем же флуорохромом, который использовался для отрицательного окрашивания (в котором флуорохром конъюгирован с неспецифическим антителом).
[33] Маркером клетки-мишени может быть любой клеточный маркер, такой как любой известный маркер Т-клетки, В-клетки, NK-клетки, эритроцита, гранулоцита или моноцита. Маркеры Т-клеток, например, включают без ограничения CD3, CD4, CD8, CD69, CD71 и CD25. Маркеры В-клеток включают без ограничения IL-б, CD19, CD25, CD30, CD27, CD38, CD78, CD138 и CD319. В одном аспекте, например, маркер-мишень может быть выбран из CD3 в качестве маркера Т-клеток, CD19 в качестве маркера В-клеток, CD235a в качестве маркера эритроцитов, CD56 в качестве маркера естественных клеток-киллеров (NK), CD14 в качестве маркера моноцитов и CD66b в качестве маркера гранулоцитов. Следует понимать, что валидацию в отношении более чем одного маркера популяции клеток можно легко выполнить посредством применения способа к нескольким образцам из одного эталонного материала с применением в каждом случае подходящего специфического антитела. В качестве неограничивающего примера для валидации двух разных протоколов окрашивания для двух разных маркеров популяции Т-клеток способ можно осуществлять в первый раз с применением антитела, которое специфически связывает CD3, и во второй раз осуществлять с применением антитела, которое специфически связывается с CD4.
[34] Следует понимать, что выбор маркера-мишени определяет выбор специфического для окрашивания. Специфическое связывание антитела с маркером-мишенью относится к способности антитела распознавать эпитоп(эпитопы) маркера таким образом, что выбранное антитело проявляет высокую аффинность связывания в отношении маркера и предпочтительно низкую аффинность связывания в отношении других перекрестно-реагирующих разновидностей. Как правило, аффинность связывания молекулы описывают с применением константы диссоциации (или равновесия) (Кd). Чем ниже константа диссоциации, тем выше аффинность связывания или степень связывания антитела А с аналитом (маркером) В. Таким образом, антитело, специфическое в отношении маркера, демонстрирует низкую константу диссоциации (Kd) в отношении маркера. Способы определения Kd данного антитела очень хорошо описаны в литературе, что дополнительно отмечено ниже. Антитела, которые генерируют плохой сигнал при низких концентрациях, будут характеризоваться высокой вариабельностью (шумом), и поэтому их будет трудно отличить от антител с более высокой измеренной перекрестной реактивностью. Используемый в данном документе термин "специфическое антитело" относится к антителу, характеризующемуся Кd в отношении маркера-мишени, составляющей не более 10 нМ или ниже, не более 7 нМ или ниже, не более 5 нМ или ниже, не более 1 нМ или ниже, не более 0,5 нМ или ниже, не более 0,15 нМ или не более 0,1 нМ или ниже 0,1 нМ. В качестве неограничивающего примера можно выбрать специфическое антитело, которое характеризуется специфическим связыванием с маркером-мишенью с Kd 5 нМ или ниже, например, 2 нМ или ниже, предпочтительно 1 нМ или ниже и более предпочтительно 0,7 нМ или ниже. Значение Kd, описывающее аффинность связывания антитела, считающегося специфическим в отношении маркера-мишени, предоставляется коммерческими поставщиками коммерчески доступных антител или может быть определено посредством хорошо известных способов, включая без ограничения флуоресцентное титрование, конкурентный ELISA, калориметрические способы, такие как изотермическая титрационная калориметрия (ITC), проточный цитометрический анализ с титрованием (FACS-титрование) и поверхностный плазмонный резонанс (BIAcore). Такие способы хорошо описаны в литературе. (См., например, Goodrich & Kugel, 2007, Binding and Kinetics for Molecular Biologists, Cold Spring Harbour Laboratory Press, Cold Spring Harbour, N.Y.; De Jong, L. A. A. et al., J. Chromatogr. В 829(1-2):1-25 (2005); Heinrich, L. et al. J. Immunol. Methods 352 (1-2):13-22 (2010); Williams, M. A. & Daviter, T. (Eds.) 2013, Protein-Ligand Interactions, Methods and Applications, Springer, New York, N.Y.).
[35] Соответственно, специфическое антитело в настоящем изобретении представляет собой любое антитело, характеризующееся Kd не более 1 нМ, не более 0,5 нМ, не более 0,15 нМ или не более 0,1 нМ в отношении любого из маркеров клеток-мишеней, включая без ограничения любой из маркеров клеток, описанных в данном документе: CD3, CD4, CD8, CD69, CD71 и CD25, IL-6, CD19, CD25, CD30, CD27, CD38, CD78, CD138 и CD319. CD235a, CD56, CD14 и CD66b. Специфические антитела могут представлять собой поликлональные, моноклональные, химерные, гуманизированные или полностью человеческие антитела. Они могут быть представлять собой одноцепочечные или многоцепочечные антитела. Хотя подходящие специфические антитела могут быть приобретены и обычно приобретаются у коммерческих поставщиков, моноклональные антитела также можно получать из гибридом или в клетках-хозяевах, содержащих векторы, содержащие последовательности нуклеиновой кислоты, кодирующие антитела, которые затем экспрессируются клетками. Таким образом, описанные в данном документе специфические антитела можно получать посредством трансформации клетки-хозяина по меньшей мере одной молекулой нуклеиновой кислоты, кодирующей специфическое антитело; экспрессии молекулы нуклеиновой кислоты в клетке-хозяине и выделения специфического антитела, при этом все данные стадии можно осуществлять с применением материалов и методик, хорошо известных из уровня техники. Коммерческие поставщики специфических антител к широкому спектру маркеров клеток среди прочих включают без ограничения BD Biosciences, Takara Bio USA (например, предлагает моноклональное антитело к CD3 (ОКТЗ)); BioX Cell (Лебанон, Нью-Гэмпшир; например, предлагает моноклональное антитело к CD19 человека); Thermo-Fisher Scientific Inc.; BioLegend Inc.; Bio-Rad Antibodies.
[36] Флуоресцентный краситель для исключения мертвых клеток, используемый как на стадиях отрицательного окрашивания, так и на стадиях положительного окрашивания, может представлять собой любой краситель, который позволяет отличать жизнеспособные клетки от мертвых или погибающих клеток, и данные красители также известны как красители для определения жизнеспособности. Например, красители для определения жизнеспособности предусматривают красители, которые не являются мембранопроницаемыми, не проходят через клеточные мембраны. Например, красители, связывающие нуклеиновые кислоты, которые не проникают через клеточные мембраны, будут избирательно окрашивать доступную нуклеиновую кислоту (например, ДНК) мертвых и погибающих клеток и не будут окрашивать недоступную нуклеиновую кислоту внутри жизнеспособных клеток с интактными мембранами. В качестве альтернативы, краситель для исключения мертвых клеток или краситель для определения жизнеспособности может представлять собой краситель, связывающий белок (краситель, реагирующий с аминогруппами), а не краситель, связывающий нуклеиновые кислоты. Красители, связывающие белки, связываются как с живыми, так и с мертвыми клетками, но мертвые и погибающие клетки с разрушенными мембранами более интенсивно окрашиваются красителем, который имеет доступ к большему количеству внутриклеточного белка, и таким образом мертвые и погибающие клетки демонстрируют более высокую интенсивность флуоресценции. Таким образом, с применением либо красителя, связывающего нуклеиновые кислоты, либо красителя, реагирующего с аминогруппами, мертвые клетки можно исключить посредством гейтирования по менее интенсивно окрашенной популяции, которая содержит живые клетки. Красители для исключения мертвых клеток предусматривают многочисленные и коммерчески доступные красители, связывающие нуклеиновые кислоты, красители, реагирующие с аминогруппами, такие как без ограничения йодид пропидия, DAPI, DRAQ7, 7-AAD, T0-PR0-3, красители, фиксирующие живые/мертвые клетки, фиксирующие красители eFluor, красители Horizon, красители Biolegend Zombie и красители Ghost. Краситель, реагирующий с аминогруппами, предусматривает М1420МР, М1410, D6105, Р130, Р6114, А10168, М10165, D10161, D374, D126, D1421, В30250, Н185, Н1428, Н1193, Р30253, А30000, А30100, С10164, Р10163, S6110, D2184, D2183, D3834 и другие.
[37] Флуорохром может представлять собой любо флуорохром, который имеет характеристический спектр испускания в видимой области, такой как без ограничения любой из многих известных флуорохромов, коммерчески доступных в настоящее время, таких как аллофикоцианин (АРС), АРС С750, АРС AF700, бриллиантовый фиолетовый (BV)421, BV510, хилит 7 (Н7) BV605, BV650, РЕ CF594, флуоресцеинизотиоцианат (FITC), R-фикоэритрин (РЕ или R-PE), РЕ-Су7 (РЕ, связанный с цианиновым красителем Су7), АРС-Су7 (АРС, связанный с цианиновым красителем Су7), АРС-Н7 (АРС связанный с хилитом 7, представляющим собой аналог Су (Н7)).
[38] Сайты связывания маркера-мишени в отрицательно окрашенном образце (образце, окрашенном с помощью изотипического антитела) блокируются с применением неконъюгированного варианта специфического антитела, т.е. специфического антитела, с которым флуорохром не конъюгирован или не связан ковалентно. Положительно окрашенный образец затем используют для получения по меньшей мере двух или обычно более двух образцов с добавленным определяемым объектом посредством добавления определяемого объекта к номинальным концентрациям клеток мишеней с применением отрицательно окрашенных клеток. Затем серию образцов с добавленным определяемым объектом анализируют в проточном цитометре с определением с помощью инструмента измеренной концентрации каждого образца с добавленным определяемым объектом. Данные (номинальную и измеренную концентрацию каждого образца с добавленным определяемым объектом) наносят на график и статистически анализируют в отношении корреляции и для расчета параметров валидации, таких как линейность, точность, прецизионность, LOD и/или LLOQ. Следует понимать, что в любом из способов анализ сравнения данных по номинальной и измеренной концентрации клеток для количественной оценки эффективности способа окрашивания в приборе можно проводить с помощью компьютерного процессора, соединенного с прибором, такого как процессор, настроенный согласно инструкциям для выполнения одного или нескольких стандартных статистических тестов в отношении различий между каждой номинальной концентрацией клеток и результатом измерения флуоресценции для каждого разбавленного образца, для определения по меньшей мере одного из линейности, диапазона, точности, прецизионности, LOD и LLOQ для прибора и способа окрашивания. Определение LLOQ может предусматривать, например, осуществление идентификации концентрации клеток-мишеней, ассоциированное с предварительно определенным критерием прецизионности и предварительно определенным критерием точности.
[39] В примере 1 ниже проиллюстрированы способы, используемые для определения концентрации жизнеспособных Т-клеток в образце клеточного продукта с применением йодида пропидия в качестве красителя для исключения мертвых клеток, антитела к CD3, IgG в качестве неспецифического антитела и аллофикоцианина в качестве флуорохрома. Однако следует понимать, что любое из красителя для исключения мертвых клеток, пары маркера клеток (CD3) и специфического антитела (антитела к CD3), неспецифического антитела (IgG) и/или флуорохрома (АРС) в примере может быть заменено как описано в данном документе. После отрицательного и положительного окрашивания положительно окрашенный образец разбавляют до планируемого самого высокого требуемого уровня добавленного определяемого объекта (самой высокой номинальной концентрации клеток-мишеней) с применением отрицательно окрашенных клеток и затем получают серийные разбавления с получением разбавленных образцов с систематически варьирующимися номинальными концентрациями клеток. Серия разбавлений может предусматривать любое кратное число. Теоретически можно использовать даже два разбавленных образца, однако на практике получают по меньшей мере три разбавленных образца, номинальная концентрация каждого из которых варьируется, предпочтительно для систематического облегчения анализа. Серия разбавлений может предусматривать три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать или больше разбавленных (с добавленным определяемым объектом) образцов. В качестве неограничивающего примера номинальная концентрация каждого разбавленного (с добавленным определяемым объектом) образца может варьироваться от 0,1% до 0,003%, но следует понимать, что выбор номинальных значений будет варьироваться в зависимости от ряда факторов, таких как ожидаемая концентрация клетки-мишени или маркера-мишени в образце, количество используемых образцов с добавленным определяемым объектом, приборы, используемый протокол окрашивания и т.п.
[40] Кроме того, следует понимать, что способы и системы по настоящему изобретению решают проблему получения образца для отрицательного контроля для тестируемого образца, который может содержать клетку-мишень, присутствующую в концентрации, составляющей не более 2%, 1,5%, 1%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,25%, 0,2%, 0,15%, 0,1%, 0,05%, 0,02% или не более 0,01%. Для сравнения, серия разбавлений может предусматривать разбавленный образец, характеризующийся самой высокой концентрацией клеток-мишеней, где самая высокая концентрация составляет 2%, 1,5%, 1%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,25%, 0,2%, 0,15%, 0,1%, 0,05%, 0,02% или 0,01%. Например, способы, предусмотренные в данном документе, можно использовать для определения клетки-мишени или маркера-мишени, считающихся остатком или примесью в образце. Например, в составе естественных клеток-киллеров CD3+ клетки или Т-клетки могут считаться остатком или примесью. Способ по настоящему изобретению может позволить определение остатка или примеси при очень низком уровне, например, менее 2%, 1,5%, 1%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,25%, 0,2%, 0,15%, 0,1%, 0,05%, 0,02% или 0,01%.
Системы
[41] Настоящее изобретение также предусматривает системы и устройства, включающие любые один или несколько приборов, основанных на измерении флуоресценции, и соответствующие системные компоненты для реализации раскрытых способов и их различных аспектов и признаков. Системы могут предусматривать, например, один или несколько приборов, основанных на измерении флуоресценции, один или несколько компьютерных процессоров, соединенных с прибором(приборами), и необязательно предусматривать один или несколько образцов любых клеток, красителей, флуорохромов, маркеров клеток, антител или любую их комбинацию. Например, настоящее изобретение предусматривает энергонезависимый машиночитаемый носитель, содержащий исполняемые процессором инструкции для выполнения процессором любого анализа данных или статистических расчетов с применением данных, сгенерированных прибором, как описано в данном документе. Система для валидации результатов измерений флуоресценции, полученных с помощью прибора, основанного на измерении флуоресценции, может предусматривать прибор, основанный на измерении флуоресценции, соединенный с ним компьютер и машиночитаемый носитель, содержимое которого можно прочитать на данном компьютере, содержащий исполняемые процессором инструкции. Как подробно описано в данном документе выше, прибор может представлять собой проточный цитометр, который можно использовать для проведения FACS.
Наборы
[42] Настоящее изобретение также предусматривает наборы и устройства, содержащие любые один или несколько образцов клеток, красителей, флуорохромов, маркеров клеток, специфических и/или неспецифических антител, буферов, разбавителей или любую их комбинацию для выполнения любого из способов валидации, описанных в данном документе. Набор может содержать, например, любые один или несколько реагентов в количествах, необходимых для отрицательного и/или положительного окрашивания клеток в эталонном образце для валидации аналитического способа, основанного на измерении флуоресценции, для анализа клеток-мишеней в тестируемом образце. Набор может содержать компоненты, необходимые для отрицательного окрашивания, включая любые одно или несколько из флуоресцентного красителя для исключения мертвых клеток, неспецифического антитела, конъюгированного с флуорохромом, и неконъюгированного специфического антитела, описанного в данном документе, которое способно специфически связывать маркер-мишень (антиген) на клетках-мишенях. Набор может содержать компоненты, необходимые для положительного окрашивания, включая любые один или несколько из флуоресцентных красителей для исключения мертвых клеток и специфического антитела, конъюгированного с флуорохромом, описанного в данном документе.
[43] Следует понимать, что специфическое антитело как для отрицательного окрашивания, так и для положительного окрашивания будет одним и тем же, что обусловлено выбранным маркером клеток-мишеней. Сходным образом, флуорохром в наборе как для отрицательного окрашивания, так и для положительного окрашивания является одним и тем же. Набор может содержать письменные инструкции в печатном или электронном формате по отрицательному и положительному окрашиванию эталонного образца и по получению серии разбавлений, описанной в данном документе выше. Инструкции могут дополнительно предусматривать любые одну или несколько инструкций по применению набора для осуществления любого из способов валидации, описанных в данном документе; получению эталонного образца и/или чтению, анализу и интерпретации результатов способа валидации. Набор может для удобства содержать один или несколько контейнеров для получения и/или хранения любого из реагентов и компоненты для их маркировки.
ОПРЕДЕЛЕНИЯ
[44] Поскольку в вышеописанные аппарат, наборы и способы могут быть внесены различные изменения без отступления от объема настоящего изобретения, то подразумевается, что все материалы, содержащиеся в приведенном выше описании и в примерах, приведенных ниже, следует интерпретировать как иллюстративные, а не в ограничительном смысле.
[45] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют значение, обычно понятное специалисту в области техники, к которой принадлежит настоящее изобретение. Следующие справочные материалы
предоставляют специалисту общее определение многих терминов, используемых в настоящем изобретении: The Cambridge Dictionary of Science and Technology (Walker ed., 1988); The Glossary of Genetics, 5th Ed., R. Rieger et al. (eds.), Springer Verlag (1991), и Hale & Marham, The Harper Collins Dictionary of Biology (1991). Следующие термины, используемые в данном документе, имеют приписанные им значения, если не указано иное.
[46] При представлении элементов настоящего изобретения или его предпочтительных аспектов подразумевается, что формы единственного числа, формы множественного числа и "указанный" означают наличие одного или нескольких элементов. Термины "содержащий", "предусматривающий" и "имеющий" предназначены для включения и означают, что могут присутствовать дополнительные элементы, отличные от перечисленных элементов.
[47] Термин "содержащий" означает "включающий, но не обязательно с ограничением"; это конкретно указывает на открытое включение в описанную таким образом комбинацию, группу, серию и т.п., или принадлежность в ней. Используемые в данном документе термины "содержащий" и "включающий" являются включительными и/или открытыми и не исключают дополнительные неуказанные элементы или процессы способа. Термин "состоящий в значительной степени из" является более ограничивающим, чем "содержащий", но не таким ограничительным, как "состоящий из". В частности, термин "состоящий в значительной степени из" ограничивает принадлежность указанных материалов или стадий к материалам или стадиям, которые существенно не влияют на важные характеристики заявленного изобретения.
ПРИМЕРЫ
[48] Любые публикации, обсуждаемые в данном документе, предоставлены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в данном документе не следует истолковывать как признание того, что настоящее изобретение не имеет оснований для противопоставления такому раскрытию на основании более раннего изобретения.
[49] Следующие примеры включены для демонстрации настоящего изобретения. Специалистам в данной области техники должно быть понятно, что методики, раскрытые в следующих примерах, представляют собой методики, разработанные авторами настоящего изобретения для надлежащего осуществления настоящего изобретения на практике. Однако специалистам в данной области техники в свете настоящего изобретения следует понимать, что в настоящее изобретение могут быть внесены многие изменения с получением при этом сходного или аналогичного результата без отступления от сущности и объема настоящего изобретения, поэтому все изложенные материалы следует интерпретировать как иллюстративные, а не в ограничительном смысле.
Пример 1. Получение образцов с добавленным определяемым объектом для валидации анализа посредством проточной цитометрии
[50] В данном примере получали образцы с добавленным определяемым объектом для валидации анализа посредством проточной цитометрии "мишени, представляющей собой редкое событие" для определения LLOQ (самого низкого уровня количественного определения) остатка или примеси, присутствующих в образце.
Способ
[51] Фиг. 1 представляет собой схематическую иллюстрацию способа. Положительные и отрицательно окрашенные образцы клеток получали с применением "маркера-мишени, конъюгированного с флуорохромом" (специфического антитела) и "изотипического антитела" (неспецифического антитела) соответственно. Сайты связывания маркера-мишени в отрицательно окрашенном образце (образце, окрашенном с помощью изотипического антитела) блокировали с применением неконъюгированного варианта специфического антитела, т.е. антитела, с которым не был ковалентно связан флуорохром. Затем положительно окрашенный образец добавляли к целевым клеткам с номинальным процентным содержанием с применением отрицательно окрашенных клеток. Образцы с добавленным определяемым объектом анализировали в проточном цитометре с получением измеренных значений процентного содержания. Затем данные (номинальные и измеренные значения процентного содержания образцов с добавленным определяемым объектом) использовали для статистического анализа для расчета параметров валидации, таких как линейность, точность, прецизионность и LLOQ.
Процедуры получения образцов
[52] В данном примере описана валидация процентного содержания жизнеспособных Т-клеток в клеточном продукте с применением следующей панели для окрашивания:

РI=йодид пропидия, и АРС=аллофикоцианин
Жизнеспособные Т-клетки идентифицируют как PI-CD3+.
а) Получение отрицательно окрашенного образца
[53] Клеточный тестируемый образец делили на две части. Одну часть окрашивали в соответствии с протоколами производителя с применением разработанной панели для окрашивания: комбинация антитела, конъюгированного с флуорохромом, и красителя для исключения мертвых клеток, необходимая для гейтирования по популяции жизнеспособных клеток, представляющей интерес. В случае популяции клеток-мишеней в смеси для окрашивания использовали изотипический контроль. В данном примере использовали следующую смесь для окрашивания:

РI=йодид пропидия, IqG=иммуноглобулин G, и
АРС=аллофикоцианин
[54] После окрашивания к конечному раствору клеток добавляли неконъюгированное антитело к целевому маркеру. В данном примере неконъюгированное антитело представляло собой очищенное антитело к CD3. Как показано на фиг. 2, на графике FACS показан результат, полученный с отрицательно окрашенным образцом. События, показанные в данном примере, гейтировали по жизнеспособным клеткам на основании прямого и бокового светорассеяния и PI (для исключения мертвых клеток).
b) Получение положительно окрашенного образца
[55] Из клеточного тестируемого образца на стадии 1 другую часть клеток в соответствии с протоколом производителя окрашивали с применением разработанной панели для окрашивания:

[56] Как показано на фиг. 3, на графике FACS показан результат, полученный с положительно окрашенным образцом. События, показанные в данном примере, гейтировали по жизнеспособным клеткам на основании прямого и бокового светорассеяния и PI (для исключения мертвых клеток).
c) Получение образцов с низким уровнем добавленных Т-клеток Положительно окрашенный образец разбавляли до планируемого самого высокого уровня добавленного определяемого объекта (номинальной концентрации клеток-мишеней) с применением отрицательно окрашенных клеток из стадии 1 и затем получали серийные разбавления с получением разбавленных образцов с систематически варьирующимися номинальными значениями процентного содержания Т-клеток.
Анализ образцов
[57] Образцы с добавленным определяемым объектом получали как описано выше и использовали для получения результатов измерений флуоресценции с помощью проточного цитометра, при этом каждое измерение соответствует номинальной концентрации CD3+ клеток в образце с добавленным определяемым объектом. Каждую номинальную концентрацию и соответствующий результат измерения флуоресценции с помощью проточного цитометра подвергали рутинным статистическим рутинным анализам, как описано в другом месте данного документа, для оценки точности и надежности измерений.
[58] В данном примере описан новый препарат отрицательно окрашенных клеток с применением изотипического антитела, конъюгированного с флуорохромом, и неконъюгированного антитела. Обычно клетки, деплетированные по популяции клеток мишеней, полученные с помощью магнитных шариков или клеточного сортера, используют для получения популяции для отрицательного контроля для получения образцов с добавленным определяемым объектом. Однако данные процедуры деплеции редко позволяют деплетировать до 99,9% целевой популяции. Как следствие, популяция для отрицательного контроля будет вносить вклад в фон, составляющий не менее 0,1%, поэтому получение образцов с добавленным определяемым объектом в количестве ниже 0,1% является невозможным. Валидация аналитического способа, основанного на измерении флуоресценции, такого как FACS, с LLOQ ниже 0,1% является сложной задачей. Данный пример демонстрирует эффективное получение популяции для отрицательного контроля, характеризующейся концентрацией клеток-мишеней ниже 0,1%, и обеспечивает получение образцов с добавленным определяемым объектом в количестве ниже 0,1% для валидации. В зависимости от используемых приборов и панели для окрашивания способы по настоящему изобретению способны обеспечивать LLOQ ниже 0,01%.
Пример 2. Протокол квалификации способа количественного определения Т-клеток в лекарственном продукте на основе K-NK
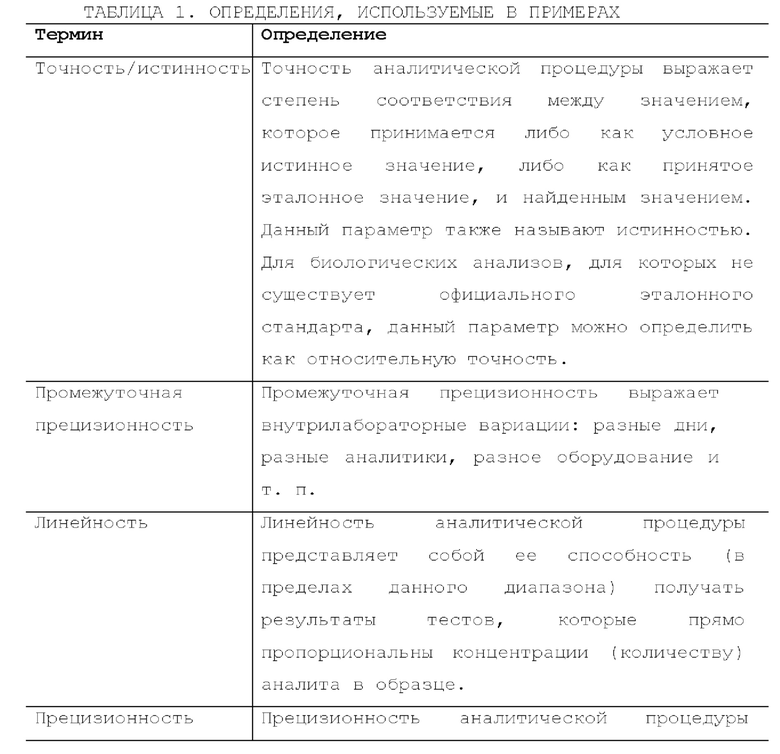
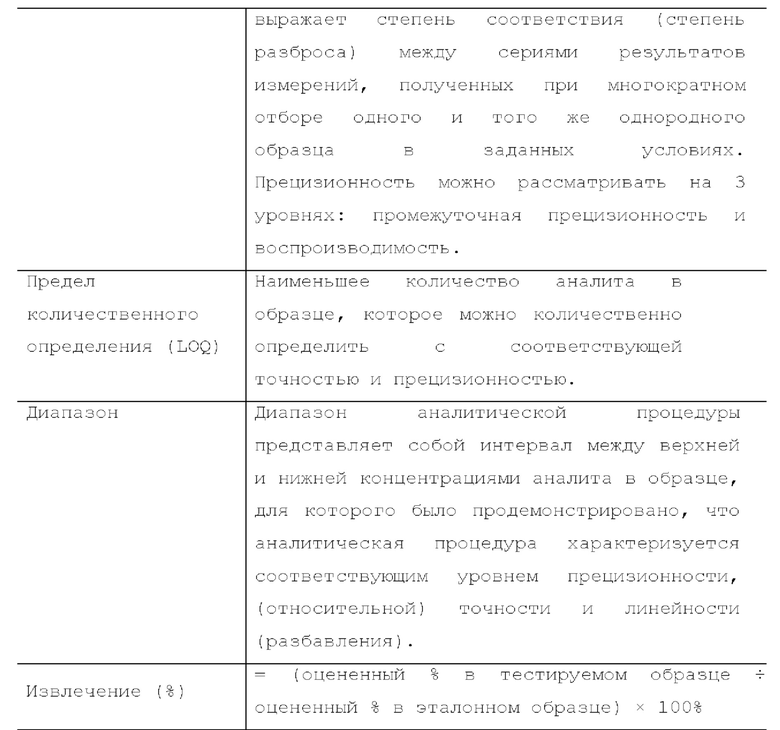
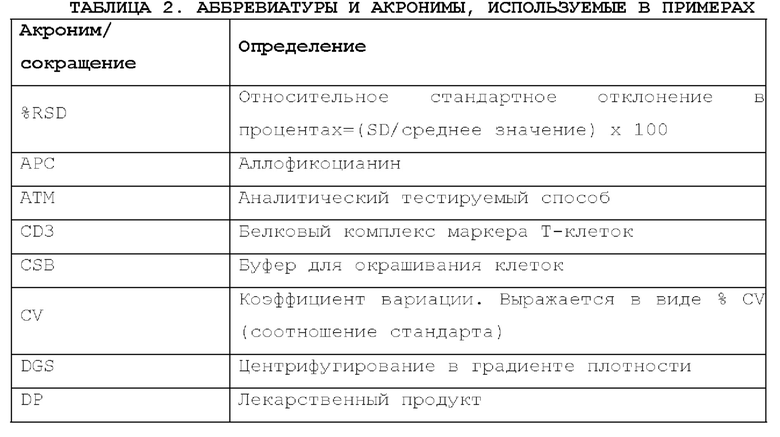
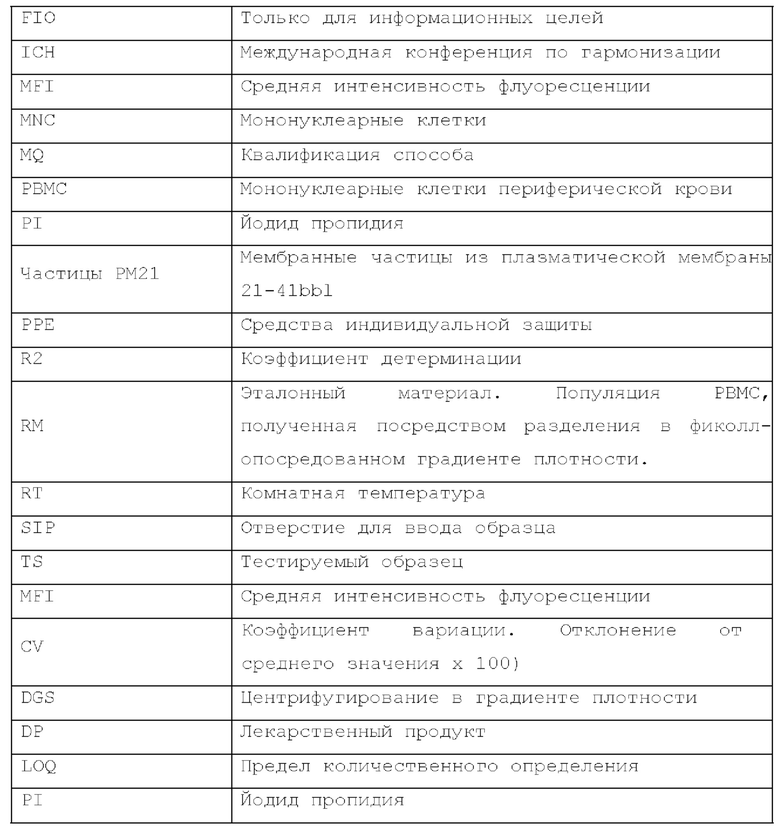
[59] Данный протокол квалификации способа обеспечивает процедуру квалификации способа количественного определения Т-клеток (ссылка на протокол: АТМ-3343) для количественного определения клеток, экспрессирующих CD3+, в композиции на основе размноженных естественных клеток-киллеров (лекарственный продукт (DP) на основе K-NK), такой как композиции, раскрытые в РСТ-публикации WO 2018160673 A1, раскрытие которой включено в данный документ посредством ссылки во всей своей полноте. DP на основе K-NK представлял собой препарат на основе деплетированных по CD3+ лимфоцитов донора, NK-клетки из которого размножали до больших количеств и плотности in vitro с применением мембранных частиц, полученных из плазматической мембраны 21-41bbl (РМ21), таких как частицы, описанные в WO 2018160673 A1. Первичной примесью в DP на основе K-NK были остаточные клетки, экспрессирующие CD3+, которые способны вызывать реакцию "трансплантат против хозяина" при введении пациентам сверх клинически релевантного предела. Для выявления и обеспечения количественного определения в DP на основе K-NK остаточных клеток, экспрессирующих CD3+, с низкой концентрацией, был разработан способ на основе FACS, описанный в данном документе, для выявления и/или количественного определения содержания исключительно жизнеспособных CD3+ клеток. Определения, представленные в таблице 1 и таблице 2, используются на протяжении следующих примеров.
[60] РВМС здорового донора (RM-PBMC 225398) применяли в качестве "образцов для положительного контроля" для проверки окрашивания CD3+ и установки гейта по CD3+ для анализа посредством проточной цитометрии. Эти РВМС получали посредством процедур центрифугирования в градиенте плотности. Данный положительный контроль не имел ассоциированных критериев приемлемости, но использовался для настройки гейта и проверки добавления и реактивности антител к CD3-APC.
[61] Тестируемый образец, применяемый для данной квалификации, представлял собой криоконсервированный образец NK-клеток "20035 d14". Образцы 20035 d14 получали посредством дальнейшей обработки NK-клеток, размноженных с применением платформы на основе частиц РМ21, и они были получены после дня 7 и были репрезентативными в отношении продукта на основе K-NK. После приобретения эти клетки культивировали в лаборатории в течение семи дней и подвергали криоконсервации при 5×107 клеток на флакон в день 14. Этот материал составляли в криоконсервированном виде в CS10, и хотя он не содержал плазмалит или HSA, образцы промывали в буфере для окрашивания клеток (CSB) и ресуспендировали в CSB перед окрашиванием посредством аналитической процедуры. Таким образом, матрицу всех тестируемых образцов стандартизировали перед аналитической процедурой, независимо от исходного состава. Посредством тестирования эффективности в ходе разработки способа определяли относительное среднее содержание жизнеспособных CD3+ клеток, составляющее 1,4% (n=8), для образца 20035 d14.
[62] Используемое оборудование представляло собой классический акустический фокусирующий проточный цитометр AttuneTM, и программное обеспечение, используемое для сбора и обработки данных, представляло собой Attune Cytometric Software v2.1 и JMP v14.
[63] Аналитический способ и процедуру разрабатывали для выявления и количественного определения клеток, экспрессирующих CD3+, в низких концентрациях. Вкратце, образец с высокой концентрацией клеток несколько раз промывали в буфере для окрашивания для FACS и затем окрашивали с помощью антитела к CD3-APC для выявления клеток, экспрессирующих CD3+, и йодида пропидия (PI) для выявления мертвых клеток. Затем образец ресуспендировали до фиксированной концентрации и получали с помощью проточного цитометра Attune. Данные проточной цитометрии обрабатывали с применением Attune Cytometric Software v2.1. Чтобы получить разрешение с прецизионным и точным количественным определением при содержании клеток, составляющем 0,01%, получали 1×106 жизнеспособных MNC. Стратегию гейтирования в ходе проточной цитометрии для АТМ-3343 определяли как МNС-*отдельные клетки-*жизнеспособные МNС-*жизнеспособные CD3+.
Квалификацию разрабатывали для демонстрации пригодности способа для выявления и количественного определения процентного состава клеток, экспрессирующих CD3+. Зарегистрированные параметры включают % жизнеспособных CD3+ клеток.
[64] Получение тестируемых образцов. Для анализа линейности, точности/истинности и прецизионности криоконсервированный тестируемый образец 20035 d14 разделяли на два препарата. Одну аликвоту (1×108 клеток) окрашивали с помощью IgG-APC и немеченого антитела к CD3 с получением имитационного образца CD3, а вторую аликвоту (2×107 клеток) окрашивали с помощью антитела к CD3-APC. Образец, окрашенный с помощью изотипического антитела (IgG-APC), служил в качестве разбавителя и матричного образца для добавления к полностью окрашенному образцу для оценки линейности и относительной точности способа. Для блокирования сайтов связывания CD3 вследствие какого-либо переноса антитела к CD3-APC из добавляемого образца применяли немеченое антитело к CD3. Перед получением плотность клеток корректировали с достижением частоты событий, составляющей 1000 событий/ сек, в соответствии с АТМ-3343-0. Концентрацию исходного положительно окрашенного образца с добавленным CD3+ и отрицательно окрашенного образца, окрашенного с помощью IgG-APC, применяли для получения схемы разбавления. Образцы, окрашенные с помощью антитела к CD3-APC, разделяли на два образца; 1) для определения %CD3+ и 2) для использования в качестве образца с добавленным определяемым объектом. Сходным образом, одну аликвоту (одну десятую часть препарата) образца, окрашенного с помощью IgG-APC, применяли для определения % CD3+, а остальную часть образца применяли в качестве разбавителя в схеме оценки линейности.
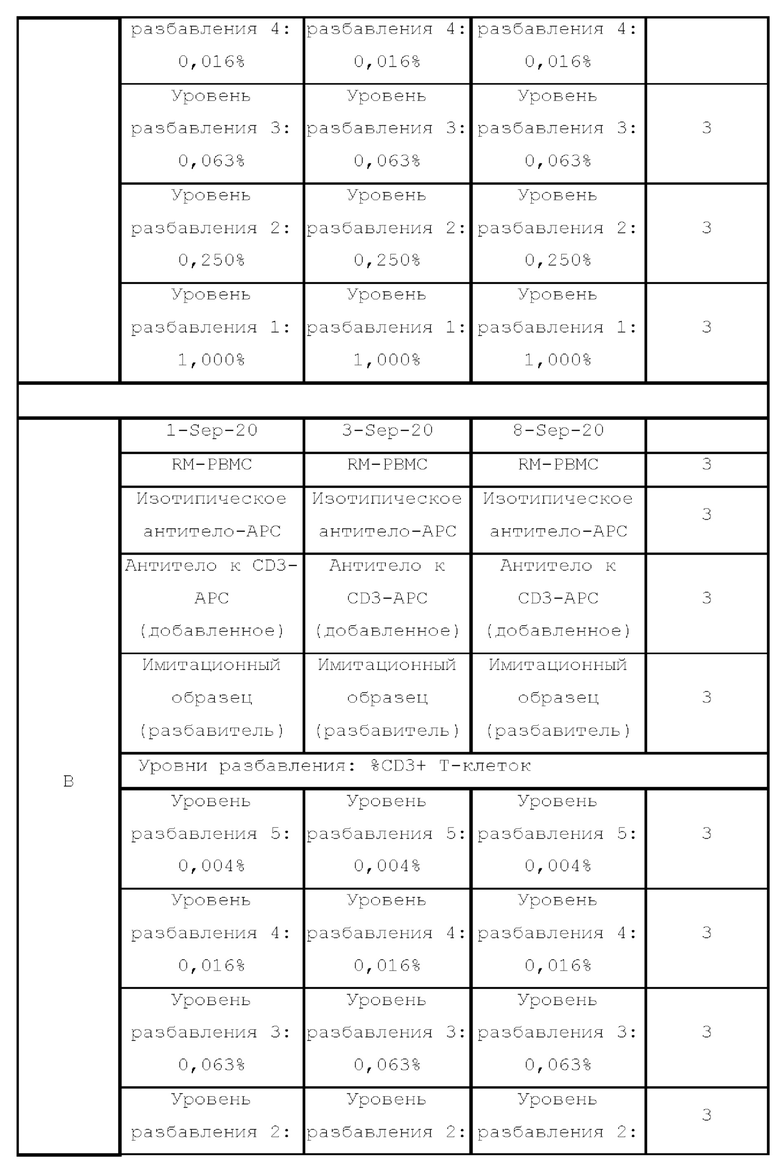
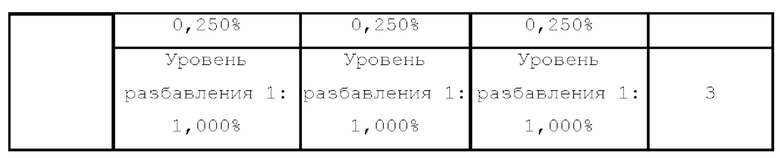
[65] Получение образцов. Образцы получали в соответствии с АТМ-3343 и масштабировали, как описано в таблице 3, включая окрашивание образцов для положительного контроля, образцов, окрашенных с помощью IgG-APC, и образцов, окрашенных с помощью антитела к CD3-APC. Поскольку 1×108 клеток окрашивали с помощью IgG-APC, количество применяемых реагентов повышали в 10 раз. Кроме того, для блокирования сайтов связывания CD3 добавляли молярные эквиваленты немеченого антитела к CD3. Окрашивание с помощью антитела к CD3-APC проводили с применением 2×107 клеток, поэтому количество реагентов, применяемых согласно АТМ-3343, было удвоено. Дополнительные резервные пробирки не применяли. Каждый образец серийного разбавления характеризовался одинаковой концентрацией клеток, составляющей 2×106/мл (минимальный объем 2 мл). Процедурный поток для получения как образцов для оценки линейности, так и серии разбавлений, проиллюстрирован на фиг. 4 и фиг. 5 соответственно. Получали серию 4-кратных разбавлений до пяти уровней и она включала диапазон разбавления от 1,00% до 0,004%. Образцы с добавленным определяемым объектом получали в соответствии с таблицей 4. Для каждого случая получали и применяли один образец для положительного контроля, один образец, окрашенный с помощью IgG-APC, и один образец, окрашенный с помощью антитела к CD3-APC.







[66] Набор данных для оценки квалификационных параметров, а именно линейности, точности/истинности, прецизионности и специфичности, получали из 3 случаев, выполненных 2 операторами, как показано на фиг. 6. Один тестируемый образец для каждого случая обрабатывали в соответствии с приведенной выше схемой разбавления и квалификацию проводили в соответствии со схемой, проиллюстрированной в таблице 5 ниже. Образцы обрабатывали в соответствии с АТМ-3343 (серийное разбавление было эквивалентно тестируемым образцам). Сначала получали уровень разбавления 5, затем уровень разбавления 4 и последовательно до первого уровня разбавления. Создавали одну точку сбора данных на уровень для каждого случая. Для этого квалификационного тестирования на каждом уровне осуществляли три измерения для каждого оператора для всего шести точек сбора данных на уровень разбавления.
[67] Относительная точность/истинность. Относительную точность или истинность оценивали с применением среднего значения, полученного для тестируемого материала, по отношению к соответствующему номинальному относительному проценту CD3+ на уровень разбавления. Промежуточную прецизионность определяли для случая и аналитика в зависимости от уровня разбавления.
[68] Диапазон процедуры определяли посредством тестирования линейности разбавления. Нижний предел количественного определения определяли посредством тестирования линейности как наименьшее разбавление, которое характеризовалось подходящим уровнем прецизионности и относительной точности.
[69] Антитела и краситель для определения жизнеспособности, применяемые для АТМ-3343, перечислены в таблице б. Для сравнения использовали среднее значение из 6 измерений (по одному на случай для каждого оператора) для каждого типа образца.

[70] Диапазон процедуры определяли посредством тестирования линейности разбавления. Нижний предел количественного определения определяли посредством тестирования линейности как наименьшее разбавление, которое характеризовалось подходящим уровнем прецизионности и относительной точности.
[71] Линейность. Проводили линейный регрессионный анализ для определения значения R2 посредством аппроксимации измеренного относительного процента из всех анализов к номинальному относительному проценту в качестве фиксированного эффекта в линейной смешанной модели с применением JMP.
Извлечение для каждого уровня тестируемого образца из оценки линейности сравнивали с номинальными относительными процентными значениями в линейной смешанной модели с взаимодействием случая и оператора, заданных в качестве случайных эффектов, с применением JMP.
[72] Прецизионность (вариация между анализами). Оценку вариации промежуточной прецизионности рассчитывали посредством аппроксимации относительного процента в линейном смешанном режиме в JMP, где случай и оператор установлены в качестве случайных эффектов, и номинальный относительный процент установлен в качестве фиксированного эффекта.
[73] Диапазон аналитической процедуры определяли посредством анализа точности и прецизионности с применением линейной смешанной модели, созданной с применением JMP. Нижний предел количественного определения определяли посредством анализа точности и прецизионности с применением линейной смешанной модели, созданной с применением JMP. LOQ определяли как наименьшую концентрацию образца, которая соответствовала условиям соответствующей точности и прецизионности.
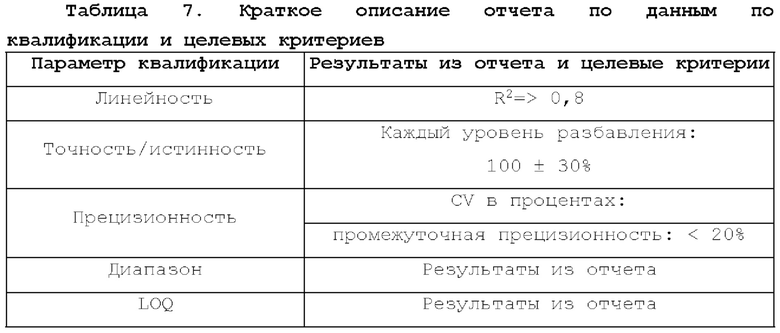
[74] Для квалификации способа не устанавливали критерии приемлемости, но целевые критерии перечислены в таблице 7.
Пример 3. Количественный анализ CD3+ Т-клеток в лекарственном продукте на основе K-NK
[75] Цель. В данном примере представлены результаты квалификации способа АТМ-3343, где были протестированы точность, прецизионность, линейность, предел количественного определения и диапазон. Параметры и процедуры квалификации были изложены в примере 2. Эти процедуры были разработаны для оценки чувствительных аналитических результатов, полученных посредством способа АТМ-3343, и определения предела количественного определения % остаточной примеси CD3+ Т-клеток в DP на основе К-NK. В данном примере также обобщены данные по квалификации способа, полученные двумя операторами в трех случаях, как это задано в примере 2. Результаты регрессионного анализа для сравнения наблюдаемых и прогнозируемых целевых результатов измерений применяют для определения результатов определения квалификационных параметров для примера 2.
[76] Материалы и реагенты. Материалы и реагенты, описанные в АТМ-3343, применяли для выполнения протокола квалификации, как подробно описано в примере 2. Используемые материалы и реагенты перечислены в таблице 8.
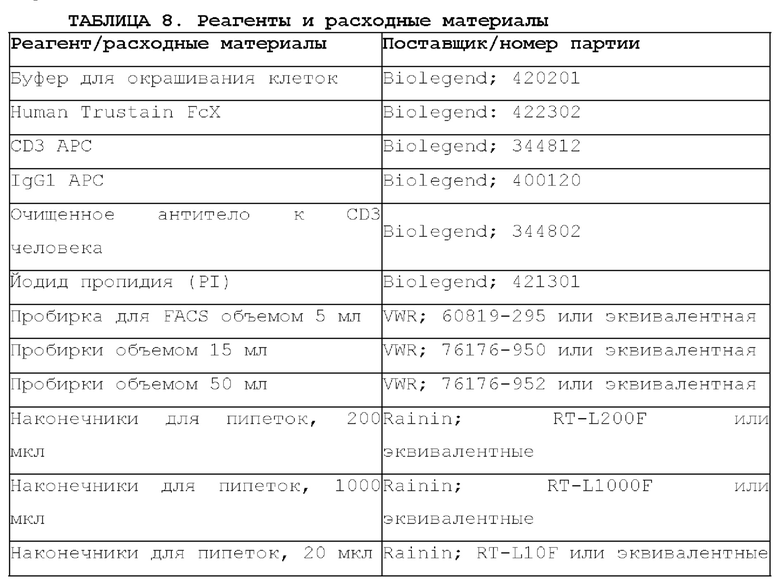
[77] Используемое оборудование предусматривало классический акустический фокусирующий цитометр AttuneTM и центрифугу (Thermo Scientific) (. Используемое программное обеспечение представляло собой Attune Cytometric Software v2.1 и JMP v. 14.3.0.
[78] Криоконсервированные образцы PBMC-225398 применяли в качестве положительного контроля для проверки гейтирования по CD3+ и установки гейта по CD3+ для анализа посредством проточной цитометрии. Получение РВМС-225398 описано в примере 2.
[79] Материал испытуемых образцов. Криоконсервированные NK-клетки из партии 20035 dl4 применяли в качестве тестируемых образцов для квалификации данного способа. Получение клеток 20035 d14 для квалификации данного способа описано в примере 2. Клетки 20035 d14 размножали с применением частиц РМ21 после деплеции по CD3+ и применяли в стандартизированной матрице образцов в данном анализе, следовательно, эти клетки являются репрезентативными для DP на основе K-NK. Партия 20035 d14 характеризуется средним % содержанием CD3+, составляющим 1,389%, что было определено в качестве части тестирования эффективности способа с применением черновой версии АТМ-3343 (тестируемый образец анализировали в 2 случаях, с 2 флаконами с образцами и 2 повторами для n=8). 1, 38 9% CD3+ представляет собой ожидаемое (номинальное) значение для испытуемого образца.
[80] Стрелками от верхнего к нижнему разделу таблицы) и впоследствии включены в сопутствующий статистический анализ.
[81] Процедура. Квалификация способа для тестирования линейности, точности/истинности и прецизионности описана в примере 2. Вкратце, восстановленные после криоконсервации образцы NK 20035 d14 окрашивали с помощью изотипического антитела-АРС и антитела к CD3-APC в соответствии с АТМ-3343. Клетки, окрашенные с помощью изотипического антитела, также окрашивали в целях имитации для получения матрицы образцов в качестве разбавителя для добавления CD3+Т-клеток. Эти клетки, окрашенные в целях имитации, обрабатывали немеченым очищенным антителом к CD3 для блокирования любого связывания CD3-APC вследствие любого переноса раствора антитела в ходе добавления CD3+ Т-клеток. Таким образом, серийные разбавления для оценки линейности определения CD3+ Т-клеток получали в матрице образцов DP на основе K-NK и в соответствии с требованиями, установленными в примере 2 (фигура 6). Анализ данных проводили в программном обеспечении для статистического анализа JMP V14.3.0. Номинальные (прогнозируемые) и оцененные (результаты) значения %CD3+ сопоставляли из отчетов двух аналитиков с тремя случаями для каждого. Для тестируемого образца, используемого для добавления, требовался анализ посредством АТМ-3343 для определения содержания CD3+ в препаратах с добавленным определяемым объектом с окрашиванием в целях имитации, и измерение проводили для каждого случая. Поэтому проводили 6 измерений в соответствии со способом тестирования, эти точки сбора данных включали в анализ данных по квалификации способа в качестве дополнительного уровня (уровня 0), используемого для оценки линейности, точности, прецизионности и диапазона. Для выбора регрессионной модели (фигура 7) изучали графики остатков непреобразованного и логарифмически (Log10, Log, логистическая регрессия, логит-регрессия в процентах и логит-регрессия) преобразованного номинального %CD3 и оцененного %CD3. При анализе графика остатков непреобразованные данные демонстрировали тенденцию к разбросу данных с небольшим разбросом на более низком уровне и более широким разбросом на более высоком уровне. Поэтому данные подвергали преобразованию для дальнейшего анализа. Log10-преобразование было самым простым преобразованием, которое приводит к улучшенному распределению данных на графике остатков. Поэтому для дальнейшего анализа были отобраны "номинальные" и "оцененные" данные с Log10-преобразованием %CD3 с тремя знаками после запятой. Результаты, показанные в таблицах, представлены с точностью до трех знаков после запятой.
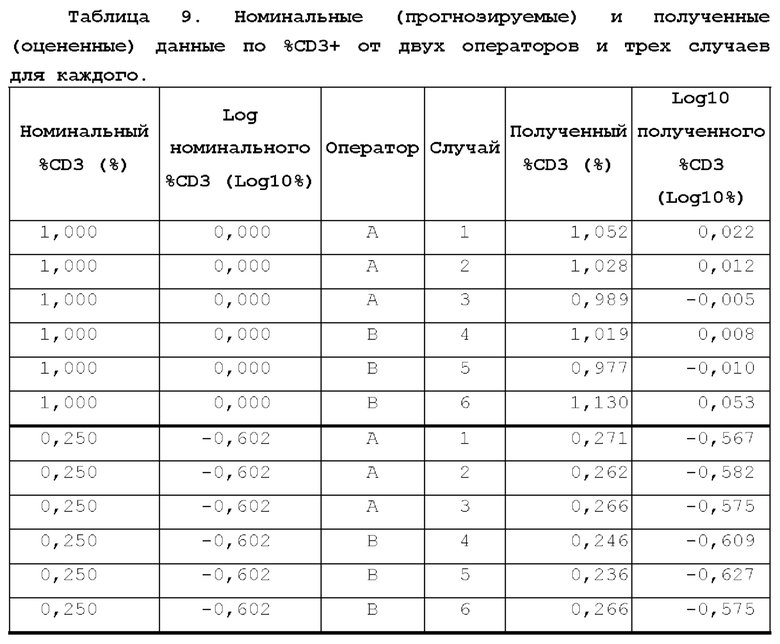
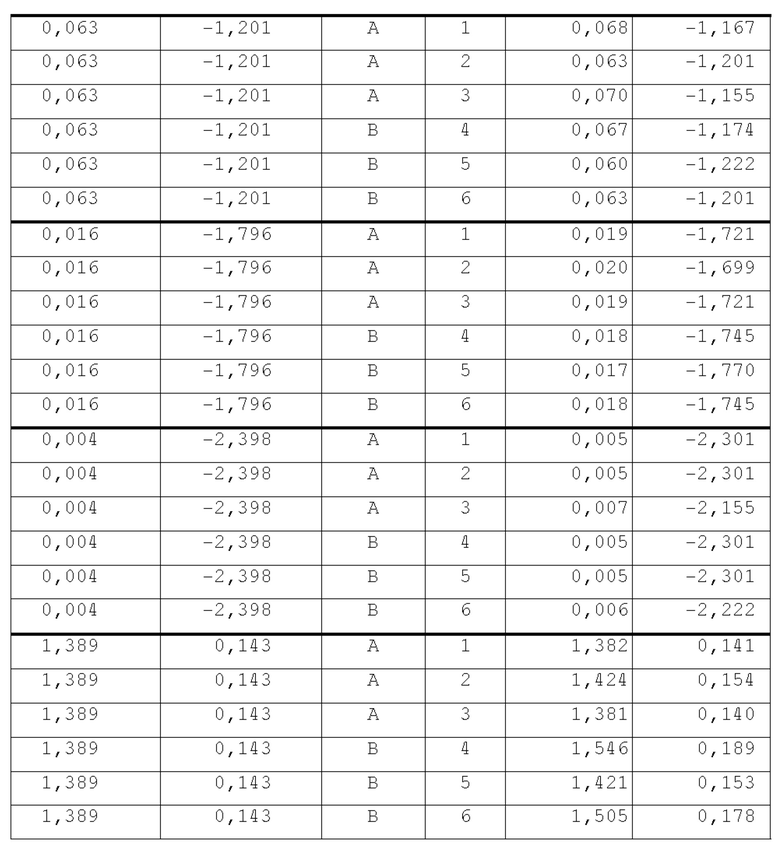
[82] Результаты. Точность анализировали с применением линейной смешанной модели с применением "оператора" и "случая" в качестве случайных факторов. Извлечение рассчитывали по приведенному ниже уравнению:
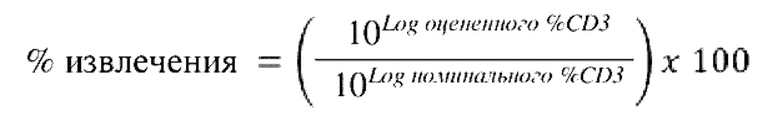
[83] Целевые критерии приемлемости для относительной точности, изложенные в примере 2, составляли 10 0+30%. Значения % извлечения для уровней разбавления с номинальным %CD3, 0,016-1, 389%, находились в пределах 10 0+30% критериев приемлемости.
Номинальный %CD3 при уровне CD3+ Т-клеток, составляющем 0,004%, не соответствовал критериям приемлемости для точности (таблица 10 и фигура 8).
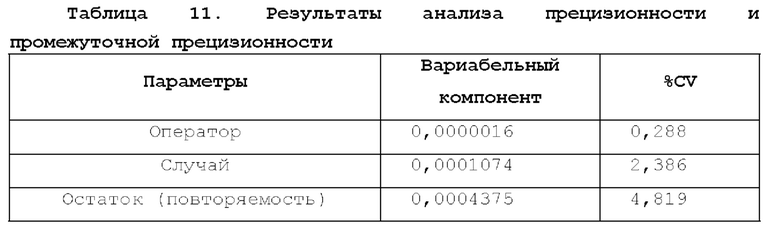
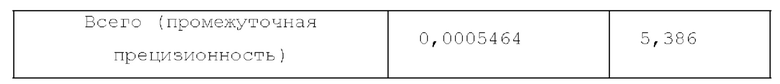
[84] Прецизионность. Прецизионность анализировали с применением линейной смешанной модели в JMP V14.3.0 с применением "оператора" и "случая" в качестве случайных факторов. Как задано в примере 2, вследствие ограничений по времени последовательные повторные измерения в отношении одних и тех же образцов не проводили. Поскольку на уровне 5 (номинальное значение уровня CD3+ Т-клеток составляет 0,004%) не были достигнуты критерии приемлемости для точности/истинности, номинальные и оцененные данные, полученные на этом уровне, были исключены из анализа прецизионности. Критерии приемлемости, изложенные в примере 2, заключались в том, чтобы указать %CV для прецизионности и <20% CV для промежуточной точности. Результаты определения %CV для "оператора", "случая", "остатка" и промежуточной точности составляли 0,288, 2,386, 4,819 и 5,386% соответственно (таблица 11). Таким образом, уровни 0-4 (1, 389-0,016% CD3+ Т-клеток) соответствовали критериям приемлемости для анализа прецизионности.
[85] Линейность. Для определения линейности количественного определения CD3+ клетки, окрашенные с помощью антитела к CD3-АРС, добавляли и серийно разбавляли в матрице образцов DP на основе K-NK, как показано на фигуре 5, для прогнозирования пяти уровней оценки %CD3+ Т-клеток (уровни 1-5 или 1,000-0,004% CD3+ Т-клеток). Матрица образцов состояла из имитационных клеток, обработанных изотипическим антителом-АРС и очищенным немеченым антителом к CD3 человека (отрицательное окрашивание). Немеченое (неконъюгированное) антитело к CD3 включали для блокирования любого окрашивания CD3 вследствие переноса антитела к CD3-APC из образца с добавленным определяемым объектом в разбавитель матрицы образцов. Данные по неразбавленным тестируемым образцам, полученные в случае добавления определяемого объекта, включали в качестве дополнительного уровня (уровня 0) для оценки линейности; таким образом, линейность оценивали от 1,389% до 0,004% CD3+ Т-клеток. Поскольку оцененные результаты на номинальном уровне 5 (0,004% CD3+ Т-клеток) не соответствовали критериям приемлемости для точности, данный уровень был исключен из анализа линейности в регрессионной модели. График регрессии и остаток по прогнозируемому графику показаны на (фигуре 9). Целевые критерии для линейности, изложенные в примере 2, соответствовали R2>0,8. Значение R2, наблюдаемое при регрессионном анализе, составляло 0,999 (таблица 12). Таким образом, линейность для уровней 0-4, 1,389-0,016% CD3+ Т-клеток, соответствовала целевым критериям приемлемости.

[86] Диапазон. Диапазон количественного определения %CD3+ Т-клеток определяли посредством анализа точности и прецизионности с применением линейной смешанной модели, созданной в JMP V14.3.0. Точность анализировали для пяти уровней разбавления (1-5) с ожидаемым содержанием CD3+ Т-клеток, составляющим 1,000-0,004%, согласно схеме четырехкратного разбавления в пределах матрицы образцов DP на основе K-NK. Включение неразбавленного тестируемого образца привело к добавлению дополнительного уровня с повышением верхнего диапазона до 1,389% CD3+ Т-клеток. Результат прогнозируемого количественного определения %CD3+Т-клеток для уровней (0-4), 1,389-0,016% CD3+ Т-клеток, соответствовал критериям приемлемости для точности (100%+30%). Уровень 5 (0, 004% CD3+ Т-клеток) не соответствовал критериям приемлемости для точности. Таким образом, диапазон для данного способа определяли как составляющий от 1,389% до 0,016% при количественном определении CD3+ Т-клеток. %CD3+ Т-клеток ниже этого диапазона количественного определения следует указывать как BLOQ (нижний предел количественного определения), в то время как %CD3+ Т-клеток выше этого диапазона количественного определения следует указывать как выше ULOQ (верхний предел количественного определения). Критерии достоверности анализа при получении 1×106 жизнеспособных отдельных клеток должны быть соблюдены, чтобы указать в отчете результаты в пределах этого диапазона количественного определения.
[87] DP на основе K-NK состоял из NK-клеток, которые были размножены до высоких значений плотности in vitro из деплетированной по CD3+ Т-клеткам популяции РВМС с применением частиц РМ21. Примесь в DP на основе K-NK может представлять собой остаточные CD3+ Т-клетки после деплеции, которые могут сохраняться на уровнях ниже определенных пределов определения, характерных для ранее проведенных аналитических анализов. Таким образом, для выявления низких (<0,3% CD3+ Т-клеток) уровней остаточных CD3+ Т-клеток как потенциальной примеси в DP на основе K-NK был разработан способ АТМ-3343 на основе проточной цитометрии. В АТМ-3343 сочетаются стадии блокирования и промывки для специфического окрашивания и получения CD3+ Т-клеток. В данном способе применяли реагенты, представляющие собой human TruStain FcX, CD3-APC и изотипическое антитело-АРС, для специфического выявления и количественного определения %CD3+ Т-клеток в DP на основе K-NK. в качестве положительного контроля применяли эталонную популяцию РВМС. Учитывая требования для количественного определения низких уровней CD3+согласно АТМ-3343 было задано получение 1×106 жизнеспособных отдельных клеток из образцов DP на основе K-NK для удовлетворения статистических ожиданий.
[88] Данные по параметрам квалификации, включая точность, прецизионность, линейность и диапазон, получали с двумя операторами по три случая на каждого. В каждом случае получали эталонный материал и клетки, окрашенные с помощью изотипического антитела-АРС или антитела к CD3-APC в дополнение к получению пяти уровней предварительно определенных значений % концентрации CD3+клеток (таблица 8). В каждом случае эти уровни разбавления получали посредством добавления CD3+ Т-клеток в матрицу имитационных (обработанных изотипическим антителом и немеченым антителом к CD3) образцов клеток из DP на основе K-NK. Параметры сбора данных проточной цитометрии устанавливали для получения 1×106 жизнеспособных отдельных клеток из каждого образца на основании стратегии последовательного гейтирования (всего событий> MNC> одиночные клетки> жизнеспособные клетки> CD3+), изложенной в АТМ-3343 и примере 2.
[89] Краткое описание. Квалификацию данного способа проводили в соответствии с процедурами, описанными в примере 2, "Протокол квалификации способа количественного анализа Т-клеток посредством АТМ-3343". Лекарственный продукт (DP) на основе K-NK состоял из NK-клеток, размноженных до высоких значений плотности in vitro из деплетированной по CD3+ Т-клеткам популяции РВМС, полученных от донора. АТМ-3343 был разработан для выявления и количественного определения низкой частоты остаточных CD3+ Т-клеток в пределах популяции из 1×106 жизнеспособных отдельных клеток посредством проточной цитометрии. Данные, оцененные в данном отчете по квалификации способа, были получены двумя аналитиками с тремя случаями для каждого. Оценка параметров точности, прецизионности и линейности, изложенная в примере 2, демонстрирует пригодность АТМ-3343 для его предполагаемого применения для выявления и количественного определения остаточных CD3+ Т-клеток в DP на основе K-NK. АТМ-3343 был точным и прецизионным при измерении различных уровней в диапазоне от 0,016% до 1,389% примеси CD3+ Т-клеток в DP на основе K-NK (таблица 14). Значение R2, составляющее 0, 999, для количественного определения %CD3+ в данном диапазоне соответствовало критериям приемлемости для линейности матрицы образцов DP на основе K-NK. Таким образом, посредством данного способа установлено выявление 0,016% CD3+ Т-клеток в качестве предела количественного определения (LOQ). Выявление CD3+ Т-клеток посредством АТМ-3343 является специфическим и позволяет надежно отличать положительные события от фонового шума при окрашивании с помощью изотипического антитела. Посредством АТМ-3343 необходимо получить 1×106 жизнеспособных отдельных клеток из DP на основе K-NK для соответствия критериям достоверности. В целом, используемый протокол является подходящим для определения примеси CD3+ Т-клеток в DP на основе K-NK. % CD3+ Т-клеток ниже или выше диапазона количественного определения от 0,016% до 1,38 9% следует указывать как BLOQ (нижний предел количественного определения) или выше ULOQ (верхний предел количественного определения) соответственно. Этот диапазон количественного определения, полученный при получении 1×106 жизнеспособных отдельных клеток, определенный в данной квалификации, может быть установлен в качестве критериев достоверности и пригодности системы.
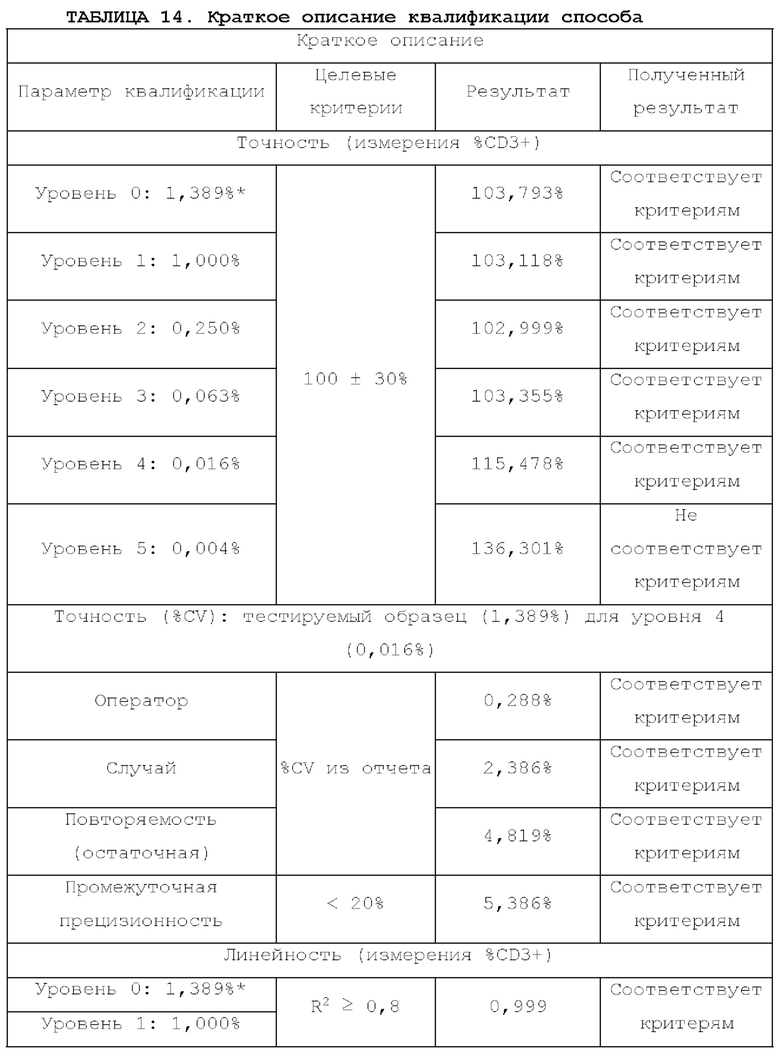
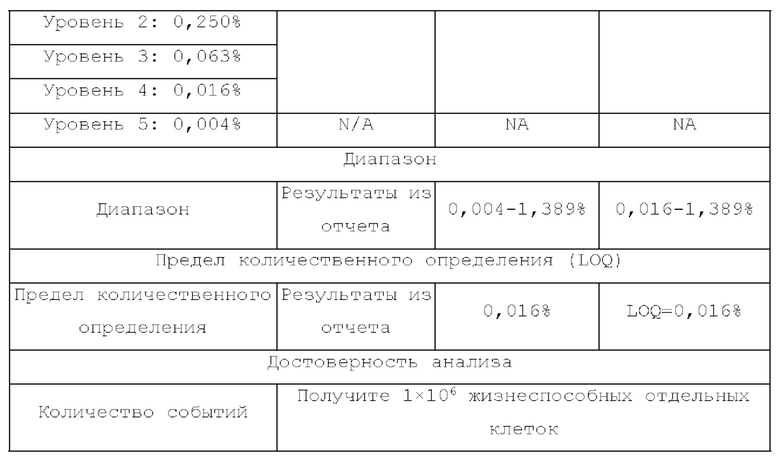
*Уровень 0: Неразбавленный тестируемый образец из партии 20035 d14, также называемый как CD3-APC (с добавленным определяемым объектом) в таблице 5.
[90] Заключение. АТМ-3343 был квалифицирован для количественного определения низкого (>0,016%) %CD3+ Т-клеток в DP на основе K-NK. Точность, прецизионность и линейность количественного определения %CD3 +Т-клеток в диапазоне от 0,016% до 1,38 9% были определены как приемлемые в соответствии с параметрами квалификации. Для надежного измерения уровня примесей CD3+ Т-клеток в DP на основе K-NK требовалось определить достоверность анализа АТМ-3343 и критерии пригодности системы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧАСТОТЫ МУТАНТНЫХ ПО Т-КЛЕТОЧНОМУ РЕЦЕПТОРУ ЛИМФОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ЧЕЛОВЕКА | 2006 |
|
RU2316766C1 |
| СПОСОБ ДИСКРИМИНАЦИИ ПО МЕНЬШЕЙ МЕРЕ ДВУХ КЛЕТОЧНЫХ ПОПУЛЯЦИЙ И ЕГО ПРИМЕНЕНИЕ | 2006 |
|
RU2397494C2 |
| Способ обнаружения внутриклеточных возбудителей инфекции в клетках спермы | 2013 |
|
RU2664734C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ТЕРАПЕВТИЧЕСКОЙ КЛЕТОЧНОЙ КОМПОЗИЦИИ | 2018 |
|
RU2775967C2 |
| Способ молекулярной количественной детекции локальной распространенности немелкоклеточного рака легкого методом двойного иммунофлуоресцентного окрашивания нормальной и опухолевой ткани органа | 2020 |
|
RU2732973C1 |
| СПОСОБЫ И СРЕДСТВА ДЛЯ МОНИТОРИНГА НАРУШЕНИЯ ТКАНЕВОГО ГОМЕОСТАЗА В ОРГАНИЗМЕ | 2012 |
|
RU2635767C2 |
| СПОСОБ ПРИМЕНЕНИЯ ZOT ИЛИ ЗОНУЛИНА ДЛЯ ИНГИБИРОВАНИЯ АНТИГЕН-СПЕЦИФИЧЕСКОЙ ПРОЛИФЕРАЦИИ ЛИМФОЦИТОВ | 1999 |
|
RU2214271C2 |
| Способ определения клеточного состава атеросклеротических бляшек | 2015 |
|
RU2616243C1 |
| ПРОБИОТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2763311C2 |
| FC-ОПТИМИЗИРОВАННЫЕ АНТИТЕЛА К CD25 ДЛЯ ИСТОЩЕНИЯ ОПУХОЛЕСПЕЦИФИЧЕСКИХ КЛЕТОК | 2018 |
|
RU2839380C1 |
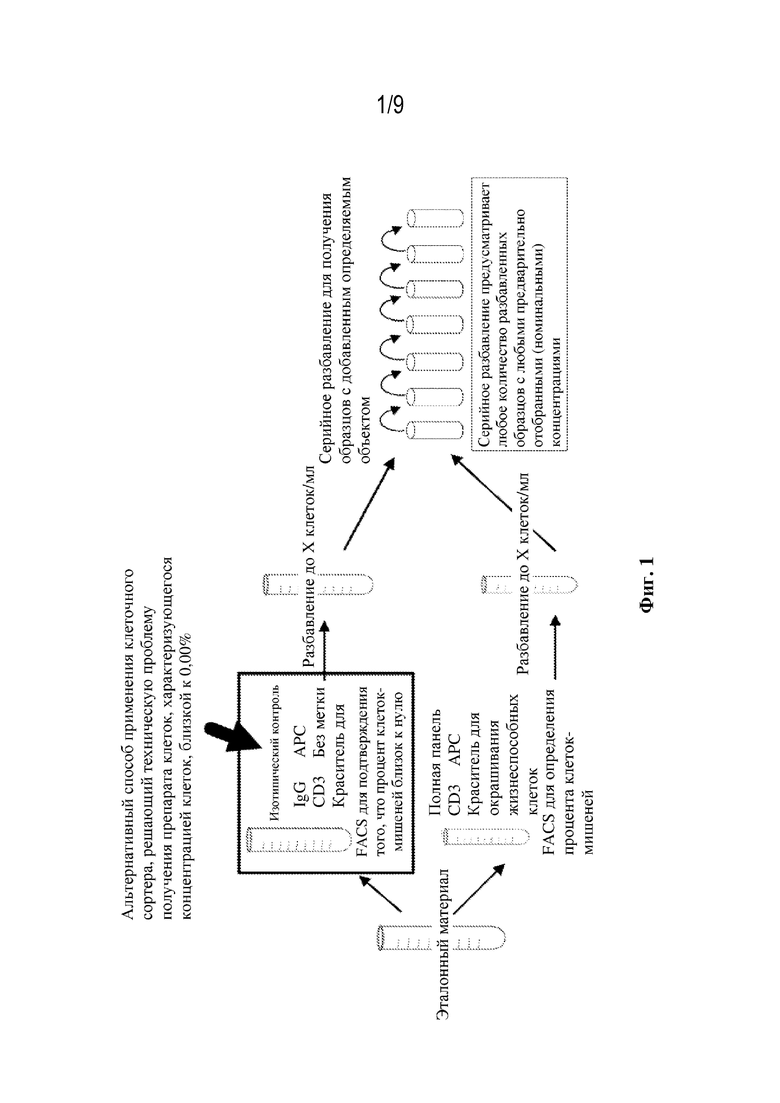
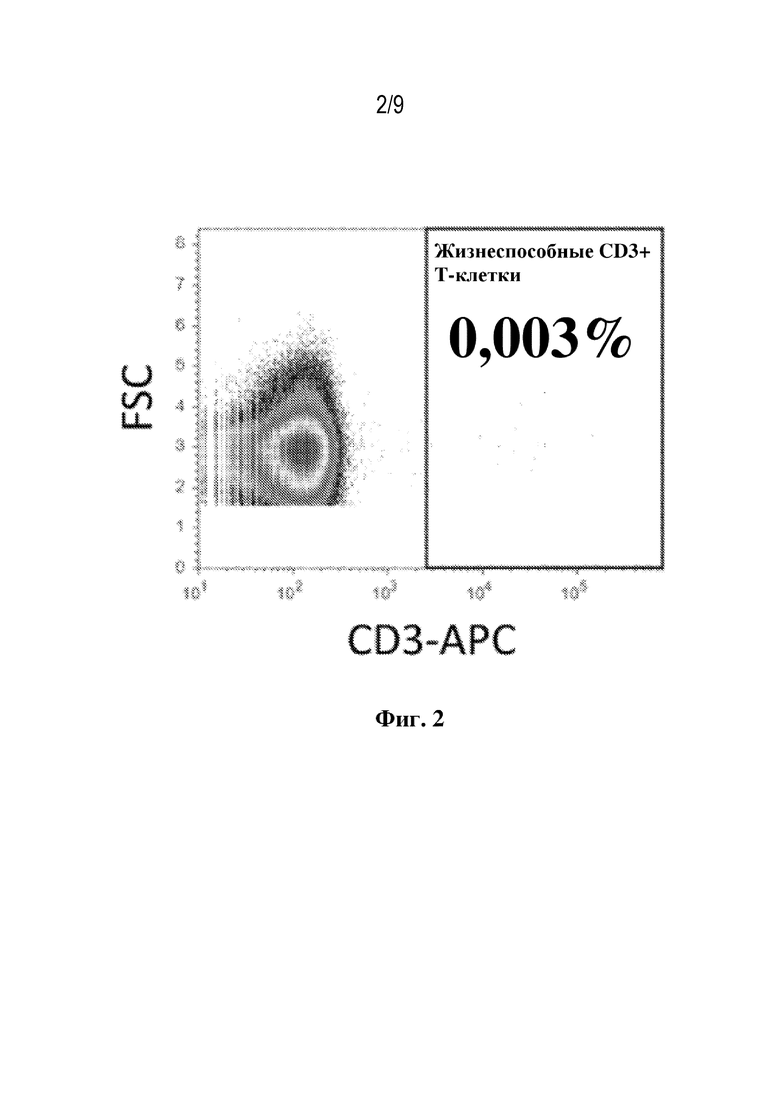
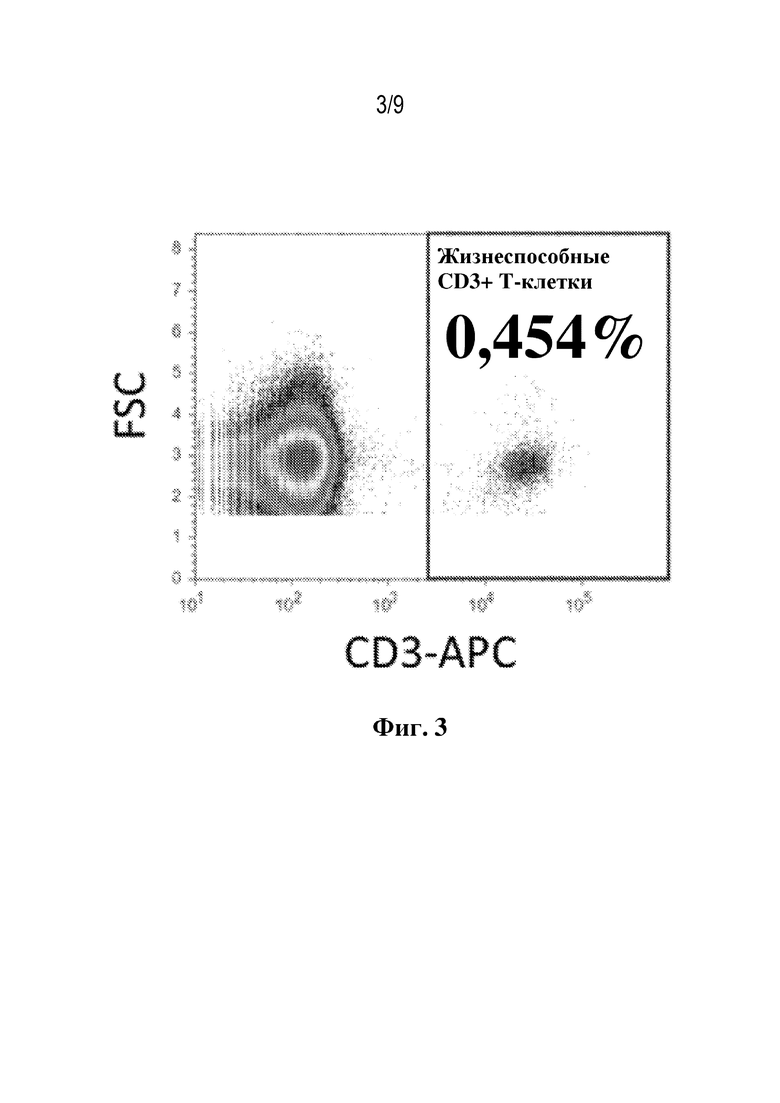
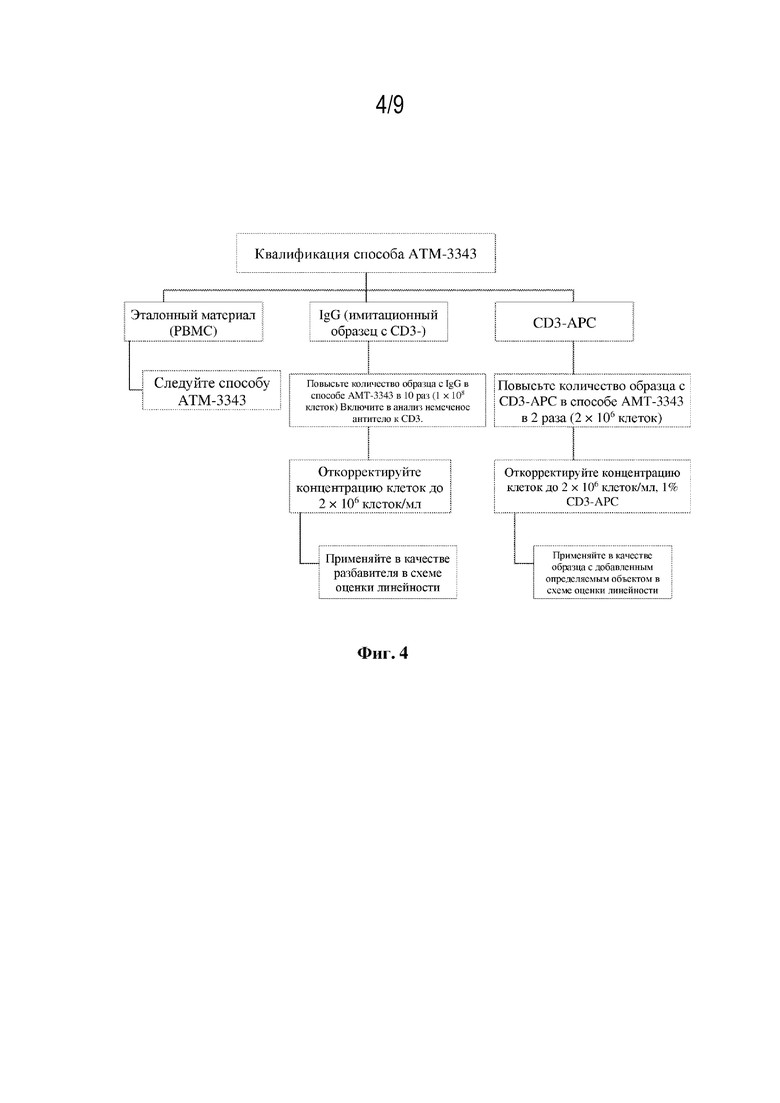
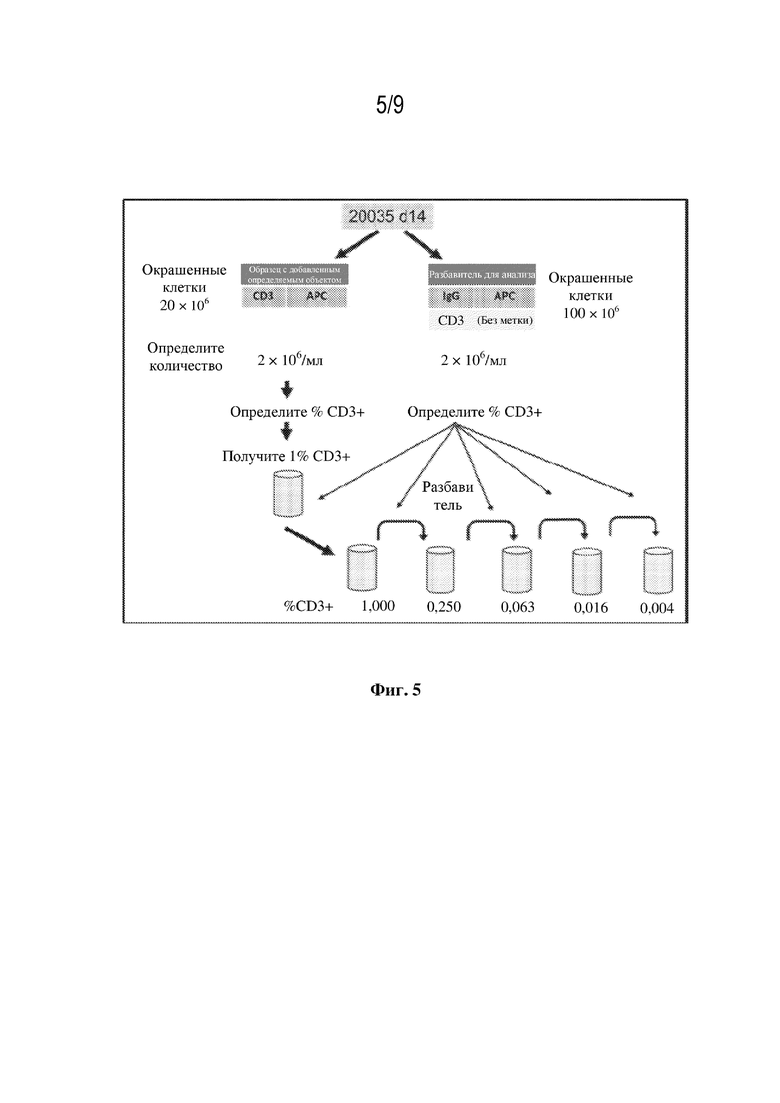
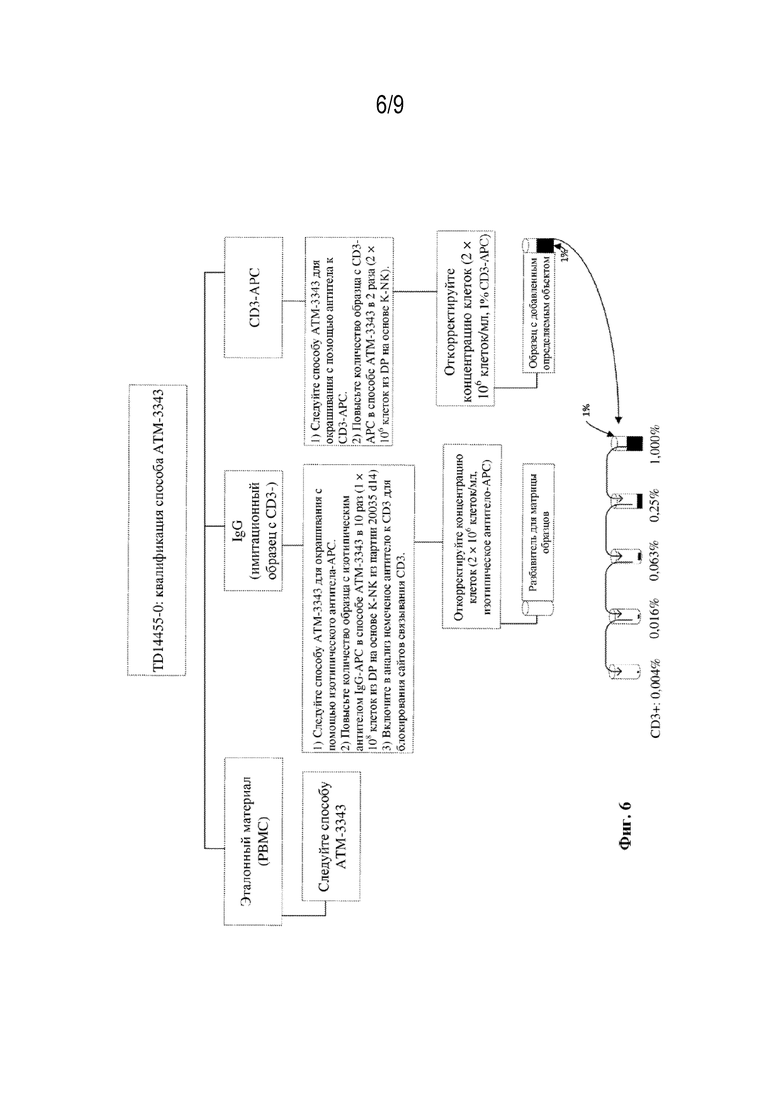

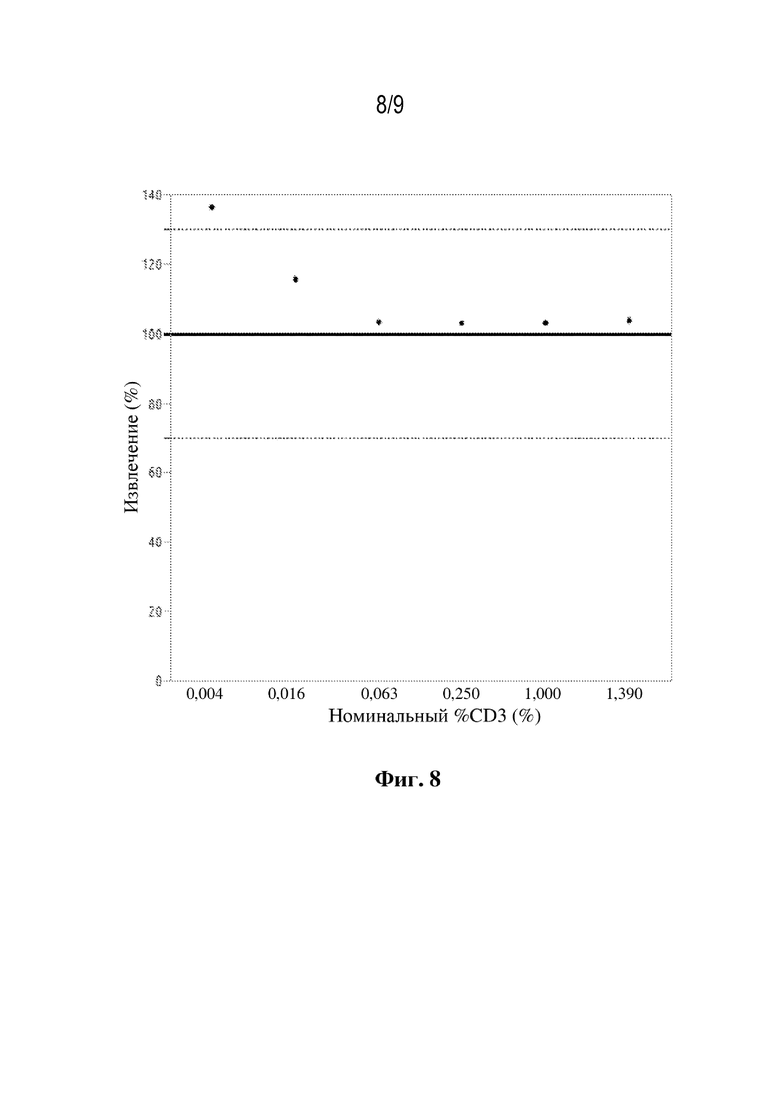
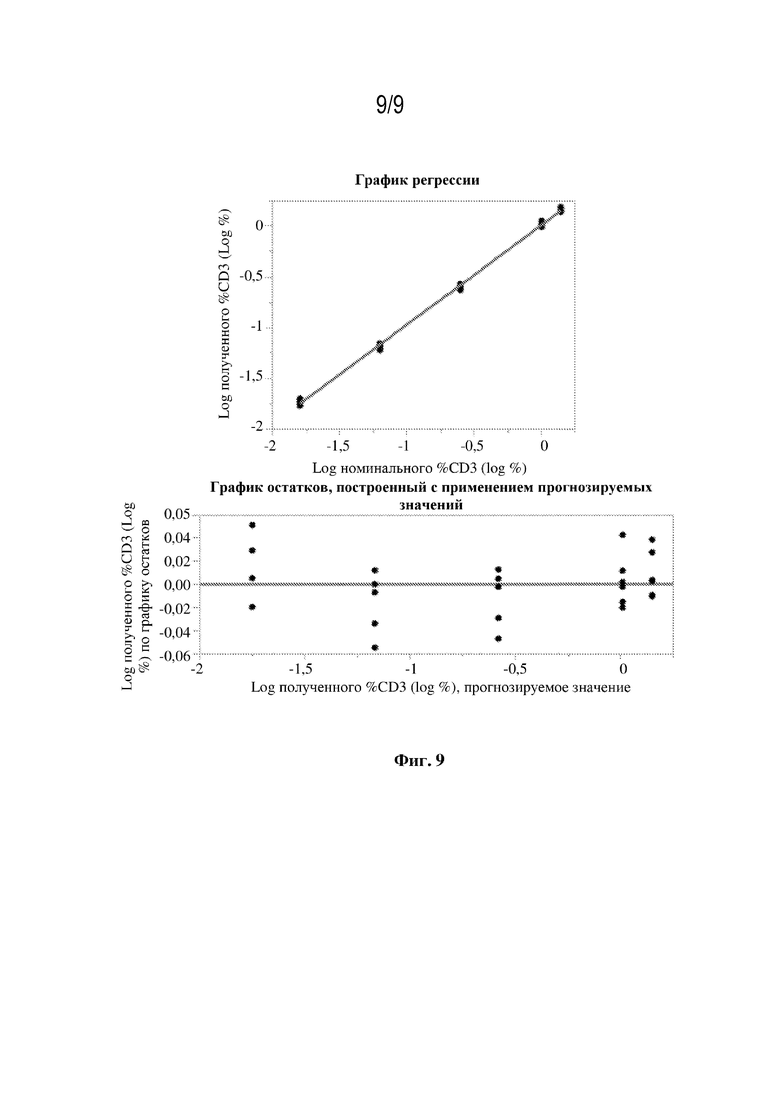
Изобретение относится к способам осуществления валидации для оценки достоверности и воспроизводимости результатов измерений. Способ осуществления валидации измерений с помощью аналитического прибора, основанного на измерении флуоресценции, в отношении популяции окрашенных клеток-мишеней в тестируемом образце включает: (a) негативное окрашивание в первой части эталонного образца, содержащего клетки-мишени, экспрессирующие маркер клеток-мишеней, где негативное окрашивание предусматривает введение в первую часть эталонного образца флуоресцентного красителя для исключения мертвых клеток, неспецифического антитела, конъюгированного с флуорохромом, и специфического антитела, способного специфически связывать маркер-мишень на клетке-мишени; (b) позитивное окрашивание во второй части эталонного образца, где позитивное окрашивание во второй части эталонного образца в (b) включает введение во вторую часть эталонного образца флуоресцентного красителя, исключающего мертвые клетки, и специфического антитела, конъюгированного с флуорохромом; (c) осуществление анализа первой части и второй части эталонного образца с помощью прибора с получением результата измерения флуоресценции, указывающего на концентрацию клеток-мишеней; (d) на основании результатов, полученных в (с), разведение позитивно окрашенных клеток-мишеней во второй части эталонного образца с негативно окрашенными клетками-мишенями в первой части эталонного образца для получения разбавленного образца, имеющего самую высокую концентрацию клеток-мишеней, из которого получают серии разбавлений, где каждый разбавленный образец характеризуется номинальной концентрацией клеток-мишеней, каждая номинальная концентрация клеток превышает концентрацию клеток-мишеней, на которую указывал результат измерения флуоресценции негативно окрашенной первой части в (а), где номинальная концентрация в каждом разбавленном образце отличается от номинальной концентрации в каждом из остальных разбавленных образцов, и где самая высокая концентрация клеток-мишеней в образце разведения составляет 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%; (e) анализ серий разбавленных образцов из (d) с помощью прибора с получением серии результатов измерений флуоресценции; (f) сравнение номинальной концентрации клеток из (d) и измерение флуоресценции из (е) для каждого разбавленного образца для осуществления количественной оценки эффективности способа окрашивания с помощью прибора, где сравнение в (f) предусматривает выполнение статистического расчета разницы между номинальной концентрацией клеток и измерением флуоресценции для каждого разбавленного образца с определением по меньшей мере одного из линейности, диапазона, точности, прецизионности, предела выявления (LOD) и нижнего предела количественного определения (LLOQ) для прибора и способа окрашивания, и где определение LLOQ предусматривает осуществление идентификации концентрации клеток-мишеней, ассоциированное с предварительно определенным критерием прецизионности и предварительно определенным критерием точности. Техническим результатом является улучшение способов осуществления валидации аналитических методов и систем. 5 н. и 12 з.п. ф-лы, 9 ил., 14 табл.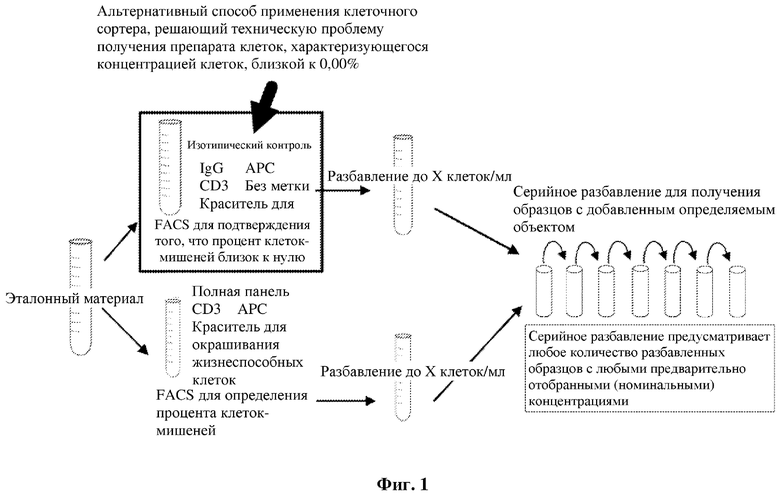
1. Способ осуществления валидации измерений с помощью аналитического прибора, основанного на измерении флуоресценции, в отношении популяции окрашенных клеток-мишеней в тестируемом образце, при этом способ включает:
(a) негативное окрашивание или наличие негативно окрашенных клеток-мишеней в первой части эталонного образца, содержащего клетки-мишени, экспрессирующие маркер клеток-мишеней, где негативное окрашивание клеток-мишеней в первой части эталонного образца в (а) предусматривает введение в первую часть эталонного образца (i) флуоресцентного красителя для исключения мертвых клеток, (ii) неспецифического антитела, конъюгированного с флуорохромом, и (iii) специфического антитела, способного специфически связывать маркер-мишень на клетке-мишени;
(b) позитивное окрашивание или наличие позитивно окрашенных клеток-мишеней во второй части эталонного образца, где позитивное окрашивание клеток-мишеней во второй части эталонного образца в (b) включает введение во вторую часть эталонного образца (i) флуоресцентного красителя, исключающего мертвые клетки, и (ii) специфического антитела, конъюгированного с флуорохромом;
(c) осуществление анализа первой части эталонного образца с помощью прибора с получением результата измерения флуоресценции, указывающего на концентрацию клеток-мишеней в первой части эталонного образца, и осуществление анализа второй части эталонного образца с помощью прибора с получением результата измерения флуоресценции, указывающего на концентрацию клеток-мишеней во второй части эталонного образца;
(d) на основании результатов измерений флуоресценции, полученных в (с), разведение позитивно окрашенных клеток-мишеней во второй части эталонного образца с негативно окрашенными клетками-мишенями в первой части эталонного образца для получения разбавленного образца, имеющего самую высокую концентрацию клеток-мишеней, из которого получают серии разбавлений, включающей множество разбавленных образцов, при этом каждый разбавленный образец характеризуется номинальной концентрацией клеток-мишеней, каждая номинальная концентрация клеток превышает концентрацию клеток-мишеней, на которую указывал результат измерения флуоресценции негативно окрашенной первой части в (а), где номинальная концентрация в каждом разбавленном образце отличается от номинальной концентрации в каждом из остальных разбавленных образцов, и где самая высокая концентрация клеток-мишеней в образце разведения, имеющем самую высокую концентрацию клеток-мишеней в серии разведений, составляет 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%;
(e) анализ серий разбавленных образцов из (d) с помощью прибора с получением серии результатов измерений флуоресценции, предусматривающих измерение флуоресценции каждого разбавленного образца;
(f) сравнение номинальной концентрации клеток из (d) и измерение флуоресценции из (е) для каждого разбавленного образца для осуществления количественной оценки эффективности способа окрашивания с помощью прибора, где сравнение в (f) предусматривает выполнение статистического расчета разницы между номинальной концентрацией клеток и измерением флуоресценции для каждого разбавленного образца с определением по меньшей мере одного из линейности, диапазона, точности, прецизионности, предела выявления (LOD) и нижнего предела количественного определения (LLOQ) для прибора и способа окрашивания, и где определение LLOQ предусматривает осуществление идентификации концентрации клеток-мишеней, ассоциированное с предварительно определенным критерием прецизионности и предварительно определенным критерием точности.
2. Способ по п. 1, где флуоресцентный краситель для исключения мертвых клеток выбран из красителя, связывающего нуклеиновые кислоты, йодида пропидия, DAPI, DRAQ7, 7-AAD, ТО-PRO-3 и красителя, реагирующего с аминогруппами.
3. Способ по п. 1, где неспецифическое антитело, конъюгированное с флуорохромом, включает антитело, не обладающее способностью специфически связываться с клеточным антигеном.
4. Способ по п. 3, где неспецифическое антитело, конъюгированное с флуорохромом, включает любой из IgD, IgG, IgA, IgM или IgE, конъюгированный с флуорохромом.
5. Способ по п. 1, где флуорохром выбран из аллофикоцианина (АРС), АРС С750, АРС AF700, бриллиантового фиолетового (BV)421, BV510, хилита 7 (Н7) BV605, BV650, РЕ CF594, флуоресцеинизотиоцианата (FITC), R-фикоэритрина (РЕ или R-PE), РЕ-Су7 (РЕ, связанного с цианиновым красителем Су7), АРС-Су7 (АРС, связанного с цианиновым красителем Су7), АРС-Н7 (АРС, связанного с хилитом 7, представляющим собой аналог Су (Н7)).
6. Способ по п. 1, где маркер клеток-мишеней выбран из CD3 в качестве маркера Т-клеток, CD19 в качестве маркера В-клеток, CD235a в качестве маркера эритроцитов, CD56 в качестве маркера естественных клеток-киллеров (NK), CD14 в качестве маркера моноцитов и CD66b в качестве маркера гранулоцитов.
7. Способ по п. 1, где популяция клеток-мишеней представляет собой популяцию Т-клеток, а маркер клеток-мишеней представляет собой CD3.
8. Способ по п. 1, где тестируемый образец содержит клетку-мишень, присутствующую в концентрации, составляющей не более 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%.
9. Способ по п. 1, где негативно окрашенную первую часть тестируемого образца получают в отсутствие стадии деплеции клеток.
10. Способ по п. 1, где прибор, основанный на измерении флуоресценции, представляет собой проточный цитометр.
11. Способ осуществления валидации измерений с помощью проточного цитометра в отношении популяции окрашенных клеток-мишеней в тестируемом образце, при этом способ включает:
(a) негативное окрашивание или наличие негативно окрашенных клеток-мишеней в первой части эталонного образца, содержащего клетки-мишени, экспрессирующие маркер клеток-мишеней, где негативное окрашивание клеток-мишеней в первой части эталонного образца в (а) предусматривает введение в первую часть эталонного образца (i) флуоресцентного красителя для исключения мертвых клеток, (ii) неспецифического антитела, конъюгированного с флуорохромом, и (iii) специфического антитела, способного специфически связывать маркер-мишень на клетке-мишени;
(b) позитивное окрашивание или наличие позитивно окрашенных клеток-мишеней во второй части эталонного образца, где позитивное окрашивание клеток-мишеней во второй части эталонного образца в (b) включает введение во вторую часть эталонного образца (i) флуоресцентного красителя, исключающего мертвые клетки, и (ii) специфического антитела, конъюгированного с флуорохромом;
(c) осуществление анализа обеих из первой части и второй части эталонного образца с помощью проточного цитометра с получением результатов измерении флуоресценции, указывающих на концентрацию клеток-мишеней в каждой из первой части эталонного образца и второй части эталонного образца;
(d) на основании результатов измерений флуоресценции, полученных в (с), разведение позитивно окрашенных клеток-мишеней во второй части эталонного образца с негативно окрашенными клетками-мишенями в первой части эталонного образца для получения разбавленного образца, имеющего самую высокую концентрацию клеток-мишеней, из которого получают серии разбавленных образцов, каждый из которых характеризуется номинальной концентрацией клеток-мишеней, систематически варьирующейся в серии разбавлений, где номинальная концентрация клеток в по меньшей мере одном разбавленном образце больше, чем концентрация клеток-мишеней, на которую указывал результат измерения флуоресценции негативно окрашенной первой части в (а), и где самая высокая концентрация клеток-мишеней в образце разведения, имеющем самую высокую концентрацию клеток-мишеней в серии разведений, составляет 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%;
(e) анализ серий разбавленных образцов из (d) с помощью проточного цитометра с получением серии результатов измерений флуоресценции, предусматривающих измерение флуоресценции каждого разбавленного образца;
(f) сравнение номинальной концентрации клеток из (d) и измерение флуоресценции из (е) для каждого разбавленного образца для осуществления количественной оценки эффективности способа окрашивания с помощью проточного цитометра, где сравнение в (f) предусматривает выполнение статистического расчета разницы между номинальной концентрацией клеток и измерением флуоресценции для каждого разбавленного образца с определением по меньшей мере одного из линейности, диапазона, точности, прецизионности, предела выявления (LOD) и нижнего предела количественного определения (LLOQ) для прибора и способа окрашивания, и где определение LLOQ предусматривает осуществление идентификации концентрации клеток-мишеней, ассоциированное с предварительно определенным критерием прецизионности и предварительно определенным критерием точности.
12. Способ по п. 11, где маркер клеток-мишеней выбран из CD3 в качестве маркера Т-клеток, CD19 в качестве маркера В-клеток, CD235a в качестве маркера эритроцитов, CD56 в качестве маркера естественных клеток-киллеров (NK), CD14 в качестве маркера моноцитов и CD66b в качестве маркера гранулоцитов.
13. Способ по п. 11, где тестируемый образец содержит клетку-мишень, присутствующую в концентрации, составляющей не более 2%, 1%, 0,5%, 0,2%, 0,1%, 0,05% или 0,02%.
14. Способ по п. 1 или 11, где серия разбавленных образцов содержит по меньшей мере два, три, четыре, пять, шесть, семь, восемь, девять или десять разбавленных образцов.
15. Энергонезависимый машиночитаемый носитель, содержащий инструкции для компьютерного процессора для выполнения стадии сравнения (f) в п. 1 или 11.
16. Система для осуществления валидации результатов измерений флуоресценции в тестируемом образце, полученных с помощью прибора, основанного на измерении флуоресценции, содержащая прибор, основанный на измерении флуоресценции, и компьютер, соединенный с прибором, основанным на измерении флуоресценции, и содержащий машиночитаемый носитель по п. 15, где прибор, основанный на измерении флуоресценции, представляет собой проточный цитометр.
17. Набор, содержащий реагенты для окрашивания клеток в эталонном образце, для осуществления валидации аналитического способа, основанного на измерении флуоресценции, для осуществления анализа клеток-мишеней в тестируемом образце, при этом набор содержит:
реагенты для негативного окрашивания, предусматривающие: (а) флуоресцентный краситель для исключения мертвых клеток, (b) неспецифическое антитело, конъюгированное с флуорохромом, и (с) специфическое антитело, способное специфически связывать маркер-мишень на клетках-мишенях, не конъюгированное с флуорохромом;
реагенты для позитивного окрашивания, предусматривающие: (а) флуоресцентный краситель для исключения мертвых клеток и (b) специфическое антитело, конъюгированное с флуорохромом, и
инструкции по (а) негативному окрашиванию первой части эталонного образца, (b) позитивному окрашиванию второй части эталонного образца и (с) получению серии разбавлений, включающей множество разбавленных образцов, каждый из которых характеризуется номинальной концентрацией клеток-мишеней, варьирующейся в серии разбавлений, где номинальная концентрация клеток в по меньшей мере одном разбавленном образце больше, чем концентрация клеток-мишеней, на которую указывал результат измерения флуоресценции негативно окрашенной первой части.
| WOOD, B | |||
| ET AL | |||
| "VALIDATION OF CELL-BASED FLUORESCENCE ASSAYS: PRACTICE GUIDELINES FROM THE ICSH AND ICCS - PART V - ASSAY PERFORMANCE CRITERIA", CYTOMETRY PART B: CLINICAL CYTOMETRY, V | |||
| Способ приготовления сернистого красителя защитного цвета | 1921 |
|
SU84A1 |
| Способ очищения амида ортотолуолсульфокислоты | 1921 |
|
SU315A1 |
| WATSON JV, WALPORT MJ "MOLECULAR CALIBRATION IN FLOW CYTOMETRY WITH SUB-ATTOGRAM DETECTION LIMIT", J IMMUNOL METHODS, V | |||
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
Авторы
Даты
2024-12-13—Публикация
2021-04-21—Подача