Область техники, к которой относится изобретения
Настоящее изобретение относится к новым химическим соединениям и к способам их применения в терапии и препаратах. В частности, изобретение относится к определенным замещенным гетероциклическим пиразольным соединениям и к способам их применения при ингибировании, регуляции и/или модуляции рецепторных тирозинкиназ типа III, таких как FLT3, PDGFR, c-KIT и/или CSF-1R, и связанных с ними путей трансдукции сигнала.
Уровень техники
Протеинкиназы (ПК) играют важную роль в путях трансдукции клеточных сигналов, которые регулируют различные функции клеток, такие как дифференциация, пролиферация, миграция, выживаемость и апоптоз. Эти ферменты катализируют перенос фосфатной группы из АТФ в остаток тирозина, серина или треонина на белковом субстрате. Фосфорилирование киназой и дефосфорилирование фосфатазой вовлечены в бесчисленные клеточные процессы, которые реагируют на различные внутриклеточные или внеклеточные сигналы, регуляцию клеточных функций и активацию или деактивацию клеточных операций. Рецепторные тирозинкиназы (РТК) представляют собой подсемейство протеинкиназ, и класс RTK, известный как семейство рецепторных тирозинкиназ типа III, в состав которого входят FLT3, PDGFR, c-KIT и CSF-1R, связан с различными пролиферативными и воспалительными заболеваниями.
Низкомолекулярные ингибиторы рецепторных тирозинкиназ типа III обеспечивают рациональный подход к новым терапиям для лечения аутоиммунных заболеваний и, в частности, к блокировке хронического разрушения тканей, опосредованного врожденной иммунной системой. Более того, ингибирование рецепторных тирозинкиназ типа III также обеспечивает рациональный подход к новым терапиям для лечения рака, особенно для лечения инвазивности рака, ангиогенеза или васкулогенеза рака, метастаза рака, и иммунотолерантности к раку.
FLT3 (Fms-подобная тирозинкиназа 3, также называемая Flk2) и ее лиганд (FL) представляет собой один из регуляторов нормального кроветворения, и при ОМЛ часто встречается активирование мутации или сверхэкспрессии FLT3. Разрабатывается более дюжины известных ингибиторов FLT3, некоторые из них продемонстрировали многообещающие клинические эффекты и получили одобрение для лечения FLT3 мутант-положительного ОМЛ. Рецептор FLT3 также экспрессируется в значительной части предшественников дендритных клеток, и стимуляция рецептора FLT3 вызывает пролиферацию и дифференциацию этих предшественников на дендритные клетки (DC). Поскольку дендритные клетки являются главными инициаторами T-клеточных иммунных ответов, в том числе аутореактивных иммунных ответов, ингибирование FLT3 обеспечивает механизм для регуляции в сторону уменьшения DC-опосредованных воспалительных или аутоиммунных ответов. Одно исследование показывает, что FLT3-ингибитор CEP-701 эффективен в снижении потери миелина при экспериментальном аутоиммунном энцефаломиелите (EAE), мышиной модели рассеянного склероза. В сыворотке крови пациентов с лангергансоклеточным гистиоцитозом и системной красной волчанкой обнаруживаются высокие уровни лиганда FLT3. Данное наблюдение дополнительно указывает на активацию сигнального пути FLT3 при дисрегуляции предшественников дендритных клеток при этих аутоиммунных заболеваниях.
PDGFR (рецептор тромбоцитарного фактора роста) и его лиганд (PDGF) регулируют клеточную пролиферацию, выживание, дифференциацию и миграцию клеток, прежде всего, мезенхимального происхождения. Аномалии пути PDGF, в том числе сверхэкспрессия или усиление рецепторов PDGF (PDGFR), усиление мутаций функциональных точек или активирование хромосомных транслокаций, наблюдались при широком спектре патологических состояний, таких как рак, фиброз, неврологические состояния и атеросклероз, что делает их потенциальными мишенями для лечения заболеваний.
c-KIT (также известный как рецептор фактора роста стволовых клеток, SCFR) и его лиганд (SCF) индуцируют пролиферацию, дифференциацию или миграцию клеток в пределах кроветворных, гематогенных и меланогенных линий дифференцировки на различных стадиях развития. Присутствие мутаций c-KIT представляет собой ключевой диагностический маркер желудочно-кишечной стромальной опухоли (GIST). Gleevec (иматиниба мезилат или STI571), первый одобренный FDA ингибитор рецепторной тирозинкиназы (РТК), первоначально одобренный для лечения c-Abl-опосредованного хронического миелоидного лейкоза, получил одобрение FDA для c-KIT-опосредованного GIST в 2002 году и подтвердил молекулярный подход к ингибированию c-KIT для лечения GIST. Мутации с приобретением функции в c-KIT также связаны с тучно-клеточным/миелоидным лейкозом и семиномами/дисгерминомами. Мутации c-KIT также были выявлены в некоторых меланомах и признаны потенциальной терапевтической мишенью для меланомы.
CSF1R (также известный как рецептор мокрофагального колониестимулирующего фактора (M-CSFR) или Fms) представляет собой рецептор для макрофагального колониестимулирующего фактора (M-CSF или CSF-1). CSF-1/CSF-1R является первичным фактором роста, регулирующим выживание, пролиферацию и дифференциацию клеток мононуклеарной фагоцитарной линии дифференцировки. Множество исследований продемонстрировало, что CSF-1/CSF-1R играет определенную роль в тканях опухоли. Повышенная экспрессия или активация CSF-1R и/или его лиганда обнаружена при различных видах рака, и повышенные уровни M-CSF связаны с неблагоприятным прогнозом при раке некоторых видов. M-CSF представляет собой один из нескольких цитокинов, участвующих в выборе опухоль-ассоциированных макрофагов (ОАМ), которые способствуют ангиогенезу опухоли и прогрессированию опухоли до метастазов. Активация CSF-1R также ведет к пролиферации и дифференциации предшественников остеокластов, тем самым, опосредуя процесс резорбции кости. Следовательно, ингибирование CSF-1R обеспечивает лечение рака, особенно инвазии, ангиогенеза, метастазирования рака, иммунотолерантности к раку и метастазов в кость. Благодаря своей роли в биологии остеокластов, CSF-1R также является важной терапевтической мишенью для остеопороза, воспалительного артрита и других воспалительных эрозий костей.
Хотя показано, что различные ингибиторы тирозинкиназы являются полезными терапевтическими средствами, все равно существует потребность в ингибиторах киназы типа III.
Раскрытие изобретения
Данное изобретение имеет отношение к новым ингибиторам, которые ингибируют киназы, особенно РТК класса III, такие как киназы FLT3, PDGFRα, c-KIT и/или CSF-1R, для лечения заболеваний или нарушений, опосредованных такими киназами. Ингибиторы данного изобретения также находят применение при лечении других заболеваний млекопитающих, в том числе заболеваний человека, опосредованных киназами FLT3, PDGFR, c-KIT или CSF-1R. В число таких заболеваний, без ограничения, входят рак, аутоиммунные заболевания и резорбтивные заболевания костей.
Варианты осуществления изобретения основаны на неожиданных выводах о том, что определенные гетероциклические пиразольные соединения могут ингибировать активность членов семейства рецепторных тирозинкиназ типа III (например, FLT3, PDGFR, c-KIT и CSF-1R). Соединения полезны в терапевтических способах лечения, фармацевтических композициях и способах модулирования активности киназ FLT3, PDGFR, c-KIT и/или CSF-1R, в том числе диких и/или мутированных форм киназ FLT3, PDGFR, c-KIT и/или CSF-1R. Эти свойства позволяют использовать эти гетероциклические пиразольные компоненты при лечении заболеваний и/или состояний, связанных с протеин-тирозин киназой.
В соответствии с вариантами осуществления данного изобретения соединение может иметь общую Формулу I:
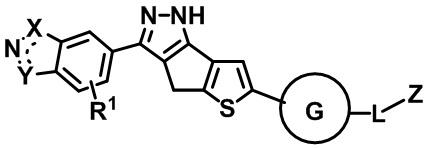
Формула (I)
или стереоизомер, таутомер, фармацевтически приемлемая соль, связующее ее протеолиз-таргетированной химеры (PROTAC), в которых
X выбран из группы, состоящей из CR2 и NR3;
Y выбран из группы, состоящей из CR2 и NR3;
G выбран из группы, состоящей из необязательно замещенного арила, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, алкинила и прямой связи;
L выбран из группы, состоящей из -CH=, -CHR4-, -(CH2)q-, -NR5-, -O-, -O(CH2)q-, -C(O)-, -C(O)(CH2)q-, -C(O)NH-, -SO2-, и прямой связи, в которой q представляет собой индивидуально или независимо целое число от 1 до 4;
Z выбран из группы, состоящей из водорода, C1-C4 алкила, C1-C4 алкиламина, C1-C4 диалкиламина и необязательно замещенного гетероциклила и гетероциклического спиро-соединения;
R1 выбран из группы, состоящей из водорода, дейтерия, галогена, гидроксила, амино, циано, трифторметила, трифторметокси, нитро, C1-C6 алкила, C1-C6 алкокси, C1-C6 алкиламино и C1-C6 диалкиламино;
R2 выбран из группы, состоящей из водорода, дейтерия, галогена, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, C5-C6 циклоалкенила, C1-C6 алкиламино, C1-C6 диалкиламино, C3-C6 циклоалкиламино, C1-C6 алкокси, C3-C6 циклоалкокси, арила, 3-6-членного гетероциклила и 5-6-членного гетероарила, в которой алкиламино, диалкиламино, алкокси, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкиламино, циклоалкокси, гетероциклил, арил и гетероарил необязательно замещаются галогеном, амино, гидроксилом, циано, нитро, акрилом, ацилокси, C1-C4 алкилом, C1-C4 гидроксил алкилом, C1-C4 алкокски алкилом, C1-C4 ацилокси алкилом, C1-C4 алкокси, C1-C4 диалкиламино, C3-C6 циклоалклом, 3-6-членным гетероциклилом, арилом и 5-6-членным гетероарилом;
R3 выбран из группы, состоящей из водорода, дейтерия, C1-C6 алкила, C1-C6 алкил карбонила, C2-C6 алкенил карбонила, C1-C6 алкокси карбонила, амино карбонила, C1-C6 алкиламино карбонила и C1-C6 диалкиламино карбонила; и
R4 выбран из группы, состоящей из водорода, дейтерия и C1-C6 алкила; и
R5 выбран из группы, состоящей из водорода и C1-C6 алкила.
В другом аспекте варианты осуществления изобретения обеспечивают фармацевтические композиции, каждая из которых содержит соединение Формулы I, стереоизомер, таутомер, сольват, пролекарство или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель, разбавитель или наполнитель.
В другом аспекте варианты осуществления изобретения обеспечивают способы ингибирования рецепторных тирозинкиназ типа III, например, киназ FLT3, PDGFR, c-KIT и/или CSF-1R у млекопитающего. Способ изобретения включает: введение указанному млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения Формулы I.
В другом аспекте изобретения варианты осуществления изобретения обеспечивают связующее протеолиз-таргетированной химеры (PROTAC) для деградации рецепторных тирозинкиназ типа III, например, киназ FLT3, PDGFR, c-KIT и/или CSF-1R у млекопитающих по убиквитиновому пути. Протеолиз-таргетированная химера (PROTAC), один из видов двухосновных молекул, возможно удаление ненужных белков, индуцируемых внутриклеточной протеолитической селективностью. PROTAC состоит из двух белок-связывающих частей, одна для убиквитин-лигазы E3 и другая для белков-мишеней (связующее, описанное в настоящем документе). Связывая два белка, PROTAC привносит белок-мишень в лигазу E3, что приводит в результате к маркировке (например, к убиквитинированию) белка-мишени для последующей деградации протеасомой. Известно, что многие молекулы связывают различные убиквитин-лигазы E3, такие как нутлин, метил-бестатин, лиганд VHL, талидомид, помалидомид и леналидомид, как описано в WO 2019/140003 A1, раскрытие которого включено посредством ссылки. Любой из этих связующих лигазы E3 может быть объединен с соединением изобретения. Между двумя связующими фрагментами может быть использован линкер для обеспечения интервала между реакциями присоединения и легкости их осуществления. Некоторые примеры линкеров можно найти в WO 2019/140003. Кроме того, Бурслем и соавторы были вдохновлены пригодностью рецепторных тирозинкиназ для деградации белков-мишеней посредством протеолиз-таргетированных химер (PROTAC) при низких наномолярных концентрациях. Они использовали известный ингибитор FLT3, квизартиниб, в качестве рекрутингового элемента и установили лиганд Гиппеля-Линдау (VHL) с помощью оптимизированного линкера для развития FLT3 PROTAC. Это соединение эффективно индуцировало деградацию белка FLT3-ITD в клетках MOLM-14 и клетках MV4-11 при низких наномолярных концентрациях (Журнал Американского химического общества 2018 г.; 140: 16428-16432).
В другом аспекте варианты осуществления изобретения обеспечивают способы лечения заболевания или нарушения, выбранного из фиброза, заболевания, связанного с костями, рака, аутоиммунного нарушения, воспалительного заболевания, и сердечно-сосудистого заболевания у млекопитающего. Способ изобретения включает: введение указанному млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения Формулы I или его фармацевтически приемлемой соли. Предложен способ лечения заболевания или нарушения, опосредованного киназами FLT3 и/или PDGFR киназами или опосредованного мутантной киназой киназ FLT3 и/или PDGFR киназами, включающий: введение субъекту, нуждающемуся в этом, терапевтически эффективного количества фармацевтической композиции, содержащей вышеуказанное соединение, его стереоизомер или его фармацевтически приемлемую соль, и фармацевтически приемлемый разбавитель или носитель, или модуль нацеливания на белок.
В другом аспекте варианты осуществления изобретения обеспечивают применение соединения Формулы I при производстве лекарственного средства для лечения заболевания или нарушения, выбранного из фиброза, заболевания, связанного с костями, рака, аутоиммунного нарушения, воспалительного заболевания, и сердечно-сосудистого заболевания у млекопитающего.
В другом аспекте варианты осуществления изобретения обеспечивают применение соединения Формулы I при лечении заболевания или нарушения, выбранного из фиброза, заболевания, связанного с костями, рака, аутоиммунного нарушения, воспалительного заболевания, и сердечно-сосудистого заболевания у млекопитающего.
В другом аспекте варианты осуществления изобретения обеспечивают промежуточные продукты для приготовления соединений Формулы I. В одном варианте осуществления определенные соединения Формулы I можно использовать в качестве промежуточных продуктов для приготовления других соединений Формулы I.
В другом аспекте варианты осуществления изобретения обеспечивают процессы для приготовления, способы разделения и способы очистки соединений, описанных в настоящем документе.
Другие аспекты и преимущества изобретения станут очевидными из следующего описания и прилагаемых формул изобретения.
Осуществление изобретения
Определение
Теперь будет сделана подробная ссылка на некоторые варианты осуществления, примеры которых проиллюстрированы в прилагаемых структурах и формулах. Несмотря на то, что будут описаны перечисленные варианты осуществления, следует понимать, что они не предназначены для ограничения изобретения этими вариантами осуществления. Напротив, изобретение предназначено для охвата всех альтернатив, модификаций и эквивалентов, которые могут быть включены в объем настоящего изобретения, как определено в пунктах формулы изобретения. Специалист в данной области техники распознал бы множество способов и материалов, аналогичных или эквивалентных способам и материалам, описанным здесь, которые могли бы быть использованы на практике в соответствии с настоящим изобретением. Настоящее изобретение ни коим образом не ограничивается способами и материалами, описанными в настоящем документе. В случае, если один или несколько включенных литературных источников и аналогичных материалов отличаются от этой заявки или противоречат ей, включая, без ограничения, определенные термины, использование терминов, описанные техники или нечто подобное, эта заявка имеет преимущественную силу.
Термин “алкил” означает прямолинейный или разветвленный одновалентный насыщенный углеводород, содержащий, если не заявлено иное, 1-20 атомов углерода. Числовые диапазоны в этом описании предназначены для включения любого (любых) числа (чисел) в определенный диапазон, как если бы отдельные числа были раскрыты отдельно. Например, алкильная группа из 1-20 углеродов включала бы C1, C2, …C20, а также C1-C20, C1-C15, C1-C10, C1-C6, C1-C4 и т. д. В число примеров алкилов входят, без ограничения, метил, этил, н-пропил, и-пропил, н-бутил, и-бутил и т-бутил.
Термин «алкенил» означает прямолинейный или разветвленный одновалентный углеводород, содержащий 2-20 атомов углевода (например, C2-C10) и одну или несколько двойных связей. В число примеров алкенилов входят, без ограничения, этенил, пропенил, аллил и 1,4-бутадиенил.
Термин «алкинил» означает прямолинейный или разветвленный одновалентный углеводород, содержащий 2-20 атомов углевода (например, C2-C10) и одну или несколько тройных связей. В число примеров алкинилов входят, без ограничения, этинил, 1-пропинил, 1- и 2-бутинил и 1-метил-2-бутинил.
Термин «алокси» означает -O-алкил радикал, в котором алкиловая часть такая, как определено выше. В число примеров алкокси входят, без ограничения, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изо-бутокси, втор-бутокси и трет-бутокси.
Термин «ацилокси» означает -O-C(O)-R радикал, в котором R может представлять собой H, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил или гетероарил.
Термин «амино» означает NH2. Термин «алкиламино» означает -N(R)-алкил радикал, в котором R может представлять собой H, алкил, алкенил, алкинил, циклоалкил, цклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил или гетероарил.
Термин «циклоалкил» означает систему колец одновалентных насыщенных углеводородов, имеющую в своем составе от 3 до 30 атомов углерода (например, C3-C6 или C3-C12). В число примеров циклоалкила входят, без ограничения, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и адамантанил.
Термин «циклоалкенил» означает систему колец одновалентных неароматических углеводородов, имеющую в своем составе от 3 до 30 атомов углерода (например, C3-C6 или C3-C12) и одну или несколько двойных связей. В число примеров входят циклопентенил, циклогексенил и циклогептенил.
Термин «гетероциклоалкил» означает ароматическую 5-8-членную моноциклическую, 8-12-членную бициклическую или 11-14-членную трициклическую кольцевую систему, имеющую в своем составе один или несколько гетероатомов (таких как O, N, S или Se). В число примеров гетероциалоалкильных групп входят, без ограничения, пиперазинил, пирролидинил, пиперидинил, диоксанил, морфолинил и тетрагидрофуранил.
Термин «гетероциклоалкенил» означает ароматическую 5-8-членную моноциклическую, 8-12-членную бициклическую или 11-14-членную трициклическую кольцевую систему, имеющую в своем составе один или несколько гетероатомов (таких как O, N, S или Se) и одну или несколько двойных связей.
Термин «арил» означает одновалентную 6-углеродную моноциклическую, 10-углеродную бициклическую или 14-углеродную трициклическую ароматическую кольцевую систему. В число примеров арильных групп входят, без ограничения, фенил, нафтил и антраценил.
Термин «арилоксил» означает -O-арил. Термин «ариламино» означает -N(R)-арил, в котором R может представлять собой H, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил или гетероарил. Термин «гетероарил» относится к ароматической 5-8-членной моноциклической, 8-12-членной бициклической или 11-14-членной трициклической кольцевой системе, имеющей один или несколько гетероатомов (таких как O, N, S или Se). В число примеров гетероарильных групп входят, без ограничения, пиридил, фурил, имидазолил, бензимидазолил, пиримидинил, тиенил, хинолинил, индолил, тиазолил, пирролил, изохинолинил, пуринил, оксазолил, пиразолил и карбазолил. Во всех этих терминах «арильная» часть такая, как определено выше.
Термин «галоген» означает F, Cl, Br или I. Предпочтительно, это - F, Cl или Br.
Описанные выше алкил, алкенил, алкинил, циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, амино, алкиламино, ариламино, алкокси, арилокси, арил и гетероарил могут быть замещенными или незамещенными фрагментами. В число возможных заместителей амино, алкиламино, ариламино, алкокси, арилокси, циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил и гетероарил входят, без ограничения, C1-C10 алкил, C2-C10 алкенил, C2-C10 алкинил, C3-C20 циклоалкил, C3-C20 циклоалкенил, C1-C20 гетероциклоалкил, C1-C20 гетероциклоалкенил, C1-C10 алкокси, арил, арилокси, гетероарил, гетероарилокси, амино, C1-C10 алкиламино, ариламино, гидрокси, гало, оксо (O=), тиоксо (S=), тио, C1-C10 алкилтио, арилтио, C1-C10 алкилсульфонил, арилсульфонил, ациламино, аминоацил, аминотиоацил, амидино, меркапто, амидо, тиоуреидо, тиоцианато, сульфонамидо, гуанидин, уреидо, циано, нитро, ацил, тиоацил, ацилокси, карбамидо, карбамил (-C(O)NH2), карбоксильный (-COOH) и карбоновый эфир. С другой стороны, в число возможных заменителей алкила, алкенила или алкинила входят все вышеперечисленные заменители, за исключением C1-C10 алкила. Циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил и гетероарил могут также быть слиты друг с другом.
Здесь представлены соединения и их фармацевтические композиции, которые полезны при лечении или профилактике заболеваний, состояний и/или нарушений, модулируемых/опосредуемых (или связанных с) рецепторными тирозинкиназами типа III, такими как киназы FLT3, PDGFR, c-KIT и/или CSF-1R.
В некоторых вариантах осуществления изобретения предусмотрены соединения формулы I:

Формула (1)
или стереоизомер, таутомер, фармацевтически приемлемая соль, связующее ее протеолиз-таргетированной химеры (PROTAC), в которых
X выбран из группы, состоящей из CR2 и NR3;
Y выбран из группы, состоящей из CR2 и NR3;
G выбран из группы, состоящей из необязательно замещенного арила, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, алкинила и прямой связи;
L выбран из группы, состоящей из -CHR4-, -(CH2)q-, -NR5-, -O-, -O(CH2)q-, -C(O) -, -C(O)(CH2)q-, -C(O)NH-, -SO2-, и прямой связи, в которых каждый q является индивидуально и независимо целым числом от 1 до 4;
Z выбран из группы, состоящей из водорода, C1-C4 алкила, C1-C4 алкиламина, C1-C4 диалкиламина, необязательно замещенного четырех-, пяти- и шестичленного циклического амина и необязательно замещенного гетероциклила и гетероциклического спиро соединения;;
R1 выбрано из группы, состоящей из водорода, дейтерия, галогена, гидроксила, амино, циано, трифторометила, трифторометокси, нитро, C1-C6 алкила, C1-C6 алкокси, C1-C6 алкиламино и C1-C6 диалкиламино;
R2 выбран из группы, состоящей из водорода, дейтерия, галогена, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C6 циклоалкила, C5-C6 циклоалкенила, C1-C6 алкиламино, C1-C6 диалкиламино, C3-C6 циклоалкиламино, C1-C6 алкокси, C3-C6 циклоалкокси, арила, 3-6-членного гетероциклила и 5-6-членного гетероарила, в которой алкиламино, диалкиламино, алкокси, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкиламино, циклоалкокси, гетероциклил, арил и гетероарил необязательно замещаются галогеном, амино, гидроксилом, циано, нитро, акрилом, ацилокси, C1-C4 алкилом, C1-C4 гидроксил алкилом, C1-C4 алкокски алкилом, C1-C4 ацилокси алкилом, C1-C4 алкокси, C1-C4 диалкиламино, C3-C6 циклоалклом, 3-6-членным гетероциклилом, арилом и 5-6-членным гетероарилом;
R3 выбран из группы, состоящей из водорода, дейтерия, C1-C6 алкила, C1-C6 алкилкарбонила, C2-C6 алкенилкарбонила, C1-C6 алкоксикарбонила, аминокарбонила, C1-C6 алкиламинокарбонила и C1-C6 диалкиламинокарбонила;
R4 выбран из группы, состоящей из водорода, дейтерия, C1-C6 алкила; и
R5 выбран из группы, состоящей из водорода и C1-C6 алкила.
Специалист в данной области должен понимать, что в приведенной выше формуле (I) все возможные комбинации или пермутации различных заместителей находятся в пределах объема изобретения. Эти соединения могут быть приготовлены с использованием легкодоступных материалов/реагентов и известных химических реакций. Основываясь на общих знаниях в данной области и учении по этому раскрытию, специалист в данной области должен быть в состоянии приготавливать и использовать эти соединения без ненужных экспериментов.
На следующих схемах реакций, со Схемы 1 по Схему 6, представлены типовые процедуры, которые можно использовать для приготовления соединений Формулы (I). Тем не менее, специалист в данной области должен понимать, что эти примеры представлены только для иллюстрации и что модификации или вариации возможны без отклонения от объема изобретения. Гетероциклическое пиразольное соединение, синтезированное в соответствии с вариантами осуществления изобретения, можно очистить посредством любых известных методов, таких как колоночная флэш-хроматография, высокоэффективная жидкостная хроматография, кристаллизация или любые другие подходящие методы.
Путь синтезирования I
Схема 1
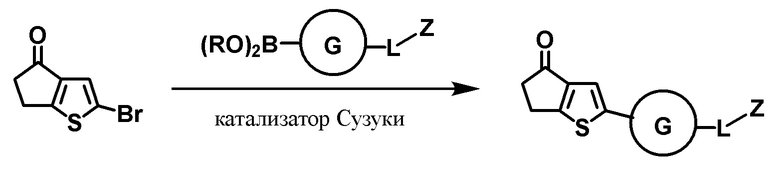
Борная кислота или боронат (1.2 экв.) была добавлена в раствор 2-Вромо-5,6-дигидро-4Н-циклопента[b]тиофен-4-один (1,0 экв.) в 1,4-диоксане/воде (5:1). В раствор добавили K2CO3 (2 экв.) и катализатор Сузуки с сочетанием Pd(II) или Pd(0) (5~8 мол. %) (например, Pd(dppf)Cl2, Pd(PPh3)4, или Pd(OAc)2, и т. д.). Получившаяся в результате смесь была нагрета с обратным холодильником. После завершения реакции была добавлена вода, и раствор был экстрагирован этилацетатом. Органические слои были высушены поверх MgSO4 и испарены в вакууме. Окончательное соединение было получено после очистки методом хроматографии.
Схема 2
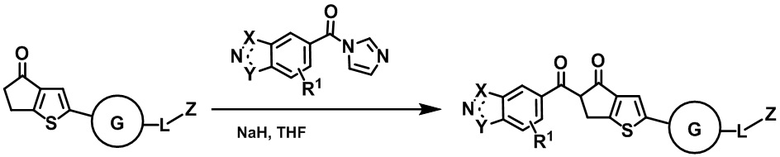
60% гидрид натрия (NAH, 1,3 экв.) был добавлен в суспензию активного эфира имидазола (1,1 экв.) и д игидроциклопента[b]тиофен-4-один производного (1,0 экв.) в тетрагидрофуране (THF, 0,2 М) в атмосфере азота. Реакция затем нагревалась с обратным холодильником в течение 4 часов. После завершения реакции реакция была погашена уксусной кислотой (HOAc, 1,5 экв.) при температуре 0°C. Получившийся в результате желтый осадок был затем отфильтрован и промыт водой и холодным метанолом. Затем твердое вещество было высушено в вакууме с получением желаемого соединения 1,3-дикетона.
Схема 3
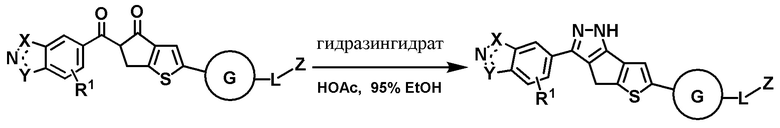
Гидразингидрат (3 экв.) был добавлен в суспензию дикетона (1 экв.) и уксусной кислоты (HOAc, 5 экв.) в этаноле (EtOH, 0,2 М). Реакция затем нагревалась с обратным холодильником в течение 6 часов. После завершения реакции, получившийся в результате желтый осадок был затем отфильтрован и промыт водой и холодным метанолом. Затем твердое вещество было высушено в вакууме с получением желаемого пиразольного соединения.
Путь синтезирования II
Схема 4
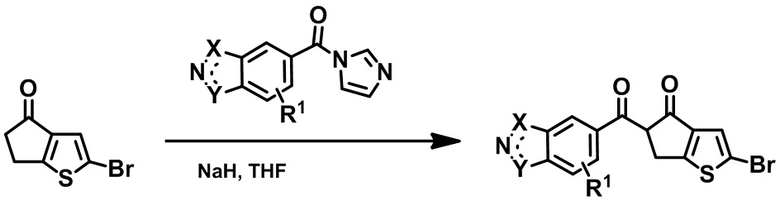
60% гидрид натрия (NAH, 1,3 экв.) был добавлен в суспензию активного эфира имидазола (1,1 экв.) и д игидроциклопента[b]тиофен-4-один производного (1,0 экв.) в тетрагидрофуране (ТГФ, 0,2 М) в атмосфере азота. Реакция затем нагревалась с обратным холодильником в течение 4 часов. После завершения реакции, реакция была погашена уксусной кислотой (AcOH, 1,5 экв.) при температуре 0°C. Получившийся в результате осадок был затем отфильтрован и промыт водой и холодным метанолом. Затем твердое вещество было высушено в вакууме с получением желаемого соединения 1,3-дикетона.
Схема 5
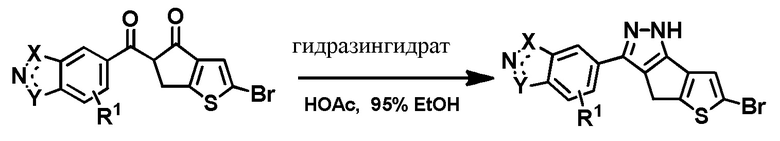
Гидразингидрат (3 экв.) был добавлен в суспензию дикетона (1 экв.) и уксусной кислоты (HOAc, 5 экв.) в этаноле (EtOH ,0,2 М). Реакция затем нагревалась собратным холодильником в течение 6 часов. После завершения реакции, получившийся в результате осадок был затем отфильтрован и промыт водой и холодным метанолом. Затем твердое вещество было высушено в вакууме с получением желаемого пиразольного соединения.
Схема 6
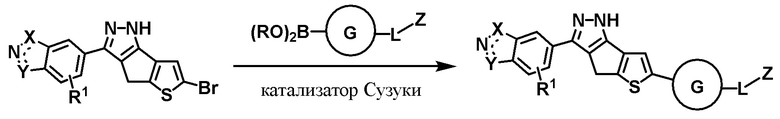
Борная кислота или боронат (1.2 экв.) была добавлена в раствор производного пиразола (1.0 экв.) в 1,4-диоксане/воде (5:1). В раствор были добавлены карбонат калия (K2CO3, 2 экв.) и обычный катализатор Сузуки с сочетанием Pd(II) или Pd(0) (5~8 мол. %) (например, Pd(dppf)Cl2, Pd(PPh3)4, или Pd(OAc)2, etc.). Получившаяся в результате смесь была нагрета с обратным холодильником. После завершения реакции была добавлена вода, и раствор был экстрагирован этилацетатом. Органические слои были высушены поверх MgSO4 и испарены в вакууме. Окончательное соединение было получено после очистки методом хроматографии.
На указанных выше схемах реакций проиллюстрировано, как можно приготовить гетероциклические пиразольные соединения. Специалист в данной области должен понимать, что предусмотренные реакции и реагенты, используемые в этих реакциях, известны в данной области. Следовательно, исходя из вышеуказанных учений и общих знаний в данной области, гетероциклические пиразольные соединения с различными заместителями в том виде, в котором они определены в настоящем документе, могут быть приготовлены специалистом в данной области без изобретательских усилий.
Соединения Формулы I представляют собой новые мощные ингибиторы рецепторных тирозинкиназ типа III, например, киназ FLT3, PDGFR, c-KIT и/или CSF-1R, и могут быть полезны при профилактике и лечении нарушений, возникающих в результате действия этих киназ.
Соединения Формулы I могут иметь терапевтическую ценность при лечении заболеваний или нарушений, выбранных из фиброза, заболеваний, связанных с костями, рака, аутоиммунных нарушений, воспалительных заболеваний, и сердечно-сосудистых заболеваний.
В соответствии с некоторыми вариантами осуществления изобретения, соединения Формулы I полезны для лечения фиброзирующих заболеваний. В число примеров фиброза входят идиопатический легочный фиброз (IPF), нефрогенный генный системный фиброз (NSF), цирроз печени, вызванная диабетом нефропатия, фиброз сердца (например, эндомиокардиальный фиброз), средостенный фиброз, миелофиброз, забрюшинный фиброз, болезнь Крона, келоидное образование, склеродермию и системный склероз. К дополнительным примерам фиброзных заболеваний относятся фокально-сегментарный гломерулосклероз (FSGS), интерстициальное легочное заболевание при системном склерозе (SSC-ILD), первичный билиарный цирроз, этаноловый цирроз, интерстициальный фиброз и атрофия канальцев (CAD), пролиферативная витреоретинопатия и рубцевание (гипертрофическое и келоидное).
В соответствии с некоторыми вариантами осуществления изобретения соединения Формулы I полезны для лечения заболеваний, связанных с костями, в том числе метастатического заболевания костей, обусловленной лечением потери костной массы, остеопороза, ревматоидного артрита, анкилозирующего спондилоартрита, болезни Паджета и заболевания пародонта. Остеопороз может быть связан с (1) менопаузой у женщин, (2) старением у мужчин или женщин, (3) неоптимальным ростом костей в детском и подростковом возрасте, который привел к неспособности достичь пиковой костной массы, и/ или (4) потерей костной массы на фоне других заболеваний, расстройств пищевого поведения, приема лекарственных средств и/или терапевтических способов лечения (например, в результате лечения глюкокортикоидами, терапии ингибирования ароматазы или антиандрогенной терапии).
Другие остеолитические заболевания, которые можно лечить в соответствии с вариантами осуществления настоящего изобретения, являются более локализованными. Конкретным примером является обусловленный опухолью остеолиз. В данном состоянии рак кости или метастазы в костях обуславливают локализованный остеолиз, который вызывает боль, слабость или переломы костей. Такой локализованный остеолиз также позволяет опухолям увеличиваться в размерах, создавая для них большее пространство в кости и высвобождая факторы роста из костного матрикса. В настоящее время известно, что в число видов рака, вызывающих остеолиз, обусловленный опухолью, входят гематологические злокачественные новообразования (например, миелома и лимфома) и плотные опухоли (например, молочной железы, предстательной железы, легких, почек и щитовидной железы), лечение всех этих видов рака предусматривается посредством настоящего изобретения.
В соответствии с некоторыми вариантами осуществления изобретения, соединения Формулы I полезны для лечения рака и пролиферативных нарушений. В число примеров входят множественная миелома, острый миелоидный лейкоз (ОМЛ), хронический миелоидный лейкоз (ХМЛ), рак предстательной железы, рак молочной железы, рак яичников, меланома, мультиформная глиобластома, гигантоклеточная опухоль кости (также известная под названием остеокластома), гигантоклеточная опухоль сухожильного влагалища (также известная под названием теносиновиальная гигантоклеточная опухоль или TGCT), метастазирование опухолей в другие ткани, другие хронические миелопролиферативные заболевания, например, миелофиброз и пигментный виллезонодулярный синовит (PVNS).
В соответствии с некоторыми вариантами осуществления изобретения соединения Формулы I полезны для лечения аутоиммунных нарушений и воспалительных заболеваний, в том числе, без ограничения, ревматоидного артрита, остеоартрита, псориатического артрита, анкилозирующего спондилоартрита, болезни Стилла у взрослых, гломерулонефрита, остеопороза, синдрома Шегрена, воспалительного заболевания кишечника, язвенного колита, болезни Крона, гистиоцитоза клеток Лангерганса, гемофагоцитарного синдрома, мультицентрического ретикулогистиоцитоза и болезни Педжета. К дополнительным примерам аутоиммунных заболеваний и нарушений относятся первичный склерозирующий холангит и отторжение трансплантатов (в том числе печеночных, почечных и сердечных/легочных трансплантатов).
В соответствии с некоторыми вариантами осуществления изобретения соединения Формулы I полезны для лечения сердечно-сосудистых заболеваний. В число примеров сердечно-сосудистых заболеваний входят атеросклероз, заболевание периферических сосудов, заболевание коронарной артерии, ишемия/реперфузия, гипертонию, рестеноз, легочная артериальная гипертензия и артериальное воспаление. К дополнительным примерам сердечно-сосудистых заболеваний относятся острый респираторный дистресс-синдром (ARDS), проходимость артериовенозных (AV) свищей и веноокклюзионная болезнь (после HSC/BMT).
Гетероциклические пиразольные соединения, описанные в настоящем документе, могут содержать не ароматическую двойную связь и один или несколько асимметричных центров, например, в заместителях, присоединенных к основным ароматическим кольцам. Следовательно, эти соединения могут возникать в виде рацематов и рацемических смесей, одиночных энантиомеров, индивидуальных диастереомеров, диастереомерных смесей и цис- или транс- изомерных форм. Все такие изомерные формы находятся в пределах объема изобретения. Гетероциклические пиразольные соединения изобретения могут иметь кислотные или основные функциональные группы (например, на замещающих группах), которые могут образовывать соли, в частности, фармацевтически приемлемые соли. Образование таких солей представляет собой рутинную практику в фармацевтической отрасли. В число примеров солей, которые можно использовать с гетероциклическими пиразольными соединениями изобретения, входят хлорид, сульфат, мезилат, безилат, тозилат, формиат, ацетат, малат, сукцинат и т.д. для основных функциональных групп. Такие гетероциклические пиразольные соли находятся в пределах объема изобретения. Подобным образом, кислотные или основные группы могут быть функционализированы, например, в эфиры. Такие функционализированные производные будут гидролизированы in vivo. Следовательно, такие производные могут функционировать в качестве пролекарств из гетероциклических пиразольных соединений изобретения. Образование пролекарств предполагает только рутинные навыки, и специалист в данной области должен знать, как приготавливать и использовать такие пролекарства без ненужных экспериментов.
Также в объем данного изобретения входят (1) фармацевтическая композиция, которая содержит эффективное количество, как минимум, одного из гетероциклических пиразольных соединений изобретения и фармацевтически приемлемый носитель, (2) способ лечения заболевания, связанного с протеинкиназой (например, рака), путем введения субъекту, нуждающемуся в таком лечении, эффективного количестваа такого гетероциклического пиразольного соединения, и (3) способ снижения активности, как минимум, одной протеинкиназы путем контакта, как минимум, одной протеинкиназы, как минимум, с одним из гетероциклических пиразольных соединений данного изобретения.
Используемый здесь термин «заболевание/нарушение, связанное с протеинкиназой», или «заболевание/нарушение, связанное с протеинкиназой», или «заболевание/нарушение, модулируемое протеинкиназой», относится к заболеванию или состоянию, которое характеризуется аномальной активностью протеинкиназы (ПК), или к заболеванию или состоянию, которое можно лечить посредством изменений активности, как минимум, одного ПК. Аномальная активность ПК может возникать в результате повышенного уровня экспрессии ПК или в присутствии экспрессии ПК, которая не возникает в нормальных условиях. В число связанных с ПК заболеваний/нарушений, описанных в настоящем документе, входят, без ограничения, рак, диабет, нарушение гиперпролиферации, гиперпролиферативные нарушения почек, заболевание почек, болезнь фон Гиппеля-Линдау, рестеноз, фиброз, псориаз, остеоартрит, ревматоидный артрит, воспалительное заболевание, иммунологические нарушения, такие как аутоиммунные заболевания (например, СПИД, волчанка и т.д.), сердечно-сосудистые нарушения (например, атеросклероз) и пролиферативные нарушения кровеносных сосудов, например, аномальный васкулогенез.
Термин «лечение» означает введение гетероциклического пиразольного соединения изобретения субъекту, у которого есть заболевание/нарушение, связанное с протеинкиназой, или имеются его симптомы или предрасположенность к нему, с целью лечения, заживления, частичного снятия симптомов, облегчения, изменения, устранения, улучшения состояния, купирования, воздействия или уменьшения риска нарушения, симптомов нарушения или предрасположенности к нему. Например, лечение рака означает лечение, ведущее в результате к ингибированию роста рака или роста раковых клеток, к регрессии роста рака (т.е. оно уменьшает размер обнаруживаемого рака) или к исчезновению рака.
Термин «эффективное количество» означает количество/объем активного вещества, который требуется для оказания предусмотренного терапевтического воздействия у субъекта. Эффективные количества могут варьировать, как признается специалистами в данной области, в зависимости от путей введения в организм, вариантов использования наполнителей и возможности использования вместе с другими веществами. Определение эффективного количества требует только рутинных навыков, и специалист в данной области должен быть в состоянии определять такие эффективные количества для предусмотренного применения без проведения ненужных экспериментов. Субъект, нуждающийся в лечении, должен относиться к млекопитающим. Термин «млекопитающее» означает человека или не человекоподобное млекопитающее, например, собак, кошек, свиней, коров, овец, ослов, лошадей, крыс или мышей.
Для осуществления способа настоящего изобретения любую из описанных выше фармацевтических композиций можно вводить перорально, парентерально, с помощью ингаляционного спрея, местно, ректально, назально, буккально, вагинально или через имплантированный резервуар. Термин «парентеральный», используемый в настоящем документе, включает подкожные, внутрикожные, внутривенные, внутримышечные, внутрисуставные, внутриартериальные, внутрисиновиальные, внутристернальные, междустенные, внутриочаговые и внутричерепные инъекцтионные или инфузионные методы. В соответствии с некоторыми вариантами осуществления изобретения гетероциклическое пиразольное соединение данного изобретения можно вводить внутривенно, в число подходящих носителей могут входить, без ограничения, физиологический солевой или натрий-фосфатный буферный раствор (PBS) и растворы с содержанием загущающих и солюбилизирующих компонентов, например, глюкозы, полиэтиленгликоля и полипропиленгликоля и их смесей.
Стерильная инъекционная композиция, например, стерильная инъекционная водная или маслянистая суспензия, может быть приготовлена по известным в данной области технологиям с использованием подходящих диспергирующих или смачивающих агентов (например, TWEEN 80) и суспендирующих агентов. Стерильный инъекционный препарат может также представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, которые могут быть использованы, - маннитол, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используются стерильные жирные масла (например, синтетические моно- или диглицериды). Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, пригодны для приготовления инъекционных препаратов, так же как и натуральные фармацевтически приемлемые масла, например, оливковое масло или касторовое масло, особенно в их полиоксиэтилированный версиях. Эти масляные растворы или суспензии могут также содержать спиртовой разбавитель или дисперсант с длинной цепью, либо карбоксиметилцеллюлозу или аналогичные диспергаторы. Для целей приготовления лекарственной формы также можно использовать другие широко применяемые поверхностно-активные вещества, например, Tweens или Spans или иные аналогичные эмульгирующие вещества или усилители биодоступности, которые обычно используются при производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм.
Композиция для перорального введения может представлять собой любую приемлемую для перорального приема лекарственную форму, включая, без ограничения, капсулы, таблетки, эмульсии и водные суспензии, дисперсии и растворы. В случае с таблетками для перорального использования, в число носителей, которые широко применяются, входят лактоза и кукурузный крахмал. Также обычно добавляются смазывающие вещества, например, стеарат магния. Для перорального введения в капсульной форме в число применяемых разбавителей входят лактоза и сушеный кукурузный крахмал. При пероральном введении водных суспензий или эмульсий активный ингредиент может быть суспендирован или растворен в масляной фазе в сочетании с эмульгирующими или суспендирующими веществами. При желании можно добавлять определенные подслащающие, ароматизирующие или красящие вещества. Назальный аэрозольная или ингаляционная композиция может быть приготовлена в соответствии с методами, хорошо известными в области фармацевтического производства. Композицию с содержанием гетероциклического пиразольного соединения можно также вводить в форме суппозиториев для ректального введения.
Носитель в фармацевтической композиции должен быть «приемлемым» в смысле совместимости с активным ингредиентом лекарственной формы (и предпочтительно, способным стабилизировать его) и не причинения вреда субъекту, которого предполагается лечить. Один или несколько солюбилизирующих компонентов (например, циклодекстрин), которые образуют более растворимые комплексы с активными гетероциклическими пиразольными компонентами, можно использовать в качестве фармацевтических носителей для доставки активных компонентов. В число примеров других носителей входят коллоидный диоксид кремния, стеарат магния и лаурилсульфат натрия.
На указанных выше схемах реакций проиллюстрировано, как можно приготовить гетероциклические пиразольные соединения. Специалист в данной области должен понимать, что предусмотренные реакции и реагенты, используемые в этих реакциях, известны в данной области. Следовательно, исходя из вышеуказанных учений и общих знаний в данной области, гетероциклические пиразольные соединения с различными заместителями в том виде, в котором они определены в настоящем документе, могут быть приготовлены специалистом в данной области без изобретательских усилий.
Считается, что приведенное выше описание адекватно позволило реализовать настоящее изобретение без дальнейшей проработки. Следовательно, следующие примеры следует толковать как просто иллюстративные и никоим образом не ограничивающие остальную часть раскрытия.
ПРИМЕР 1: Синтез соединений формулы (I)
Приводимые в качестве примеров гетероциклические пиразольные соединения перечислены в таблице 1. Их 1H ЯМР и массовые данные представлены в таблице 2.
Таблица 1. Гетероциклические пиразольные соединения
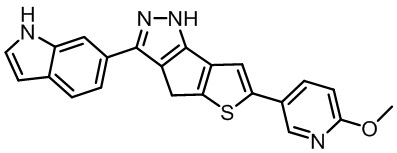
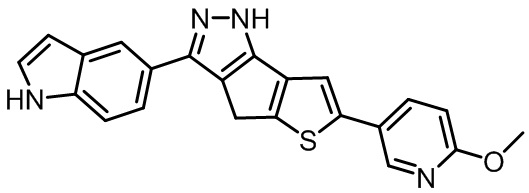
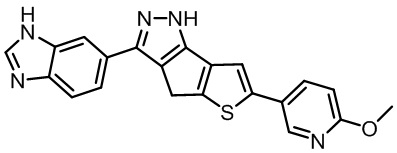
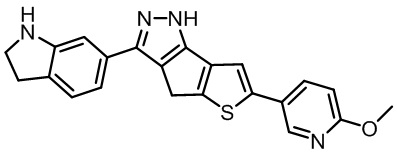
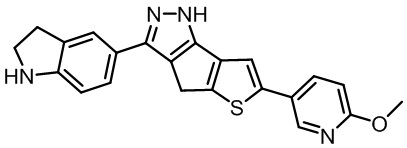
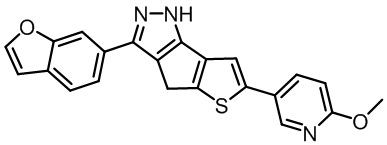
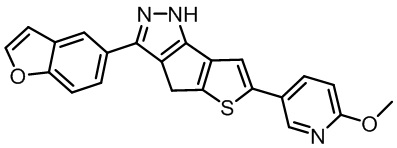
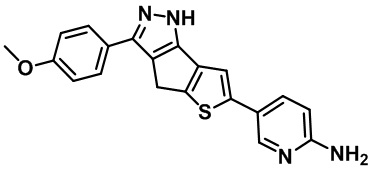
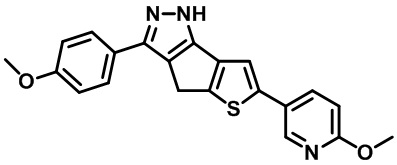
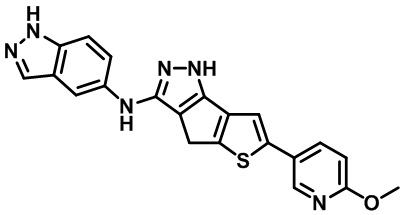
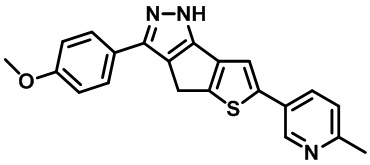
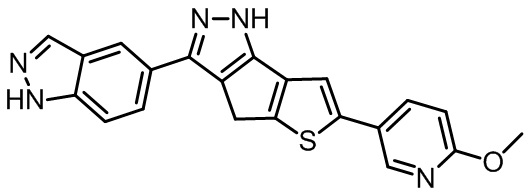
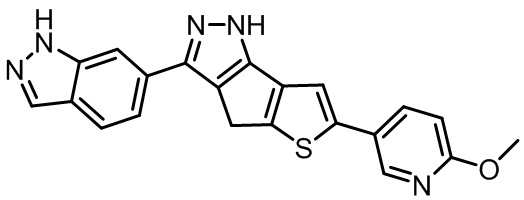
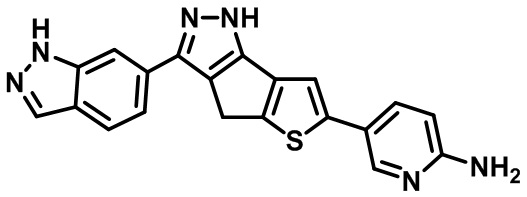
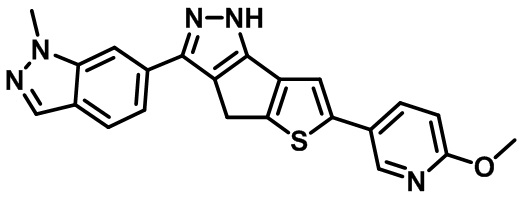
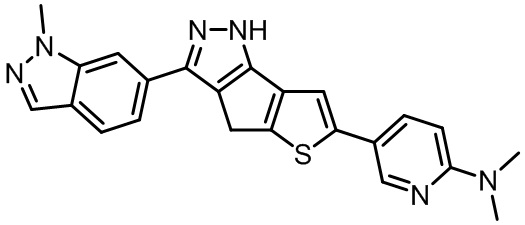
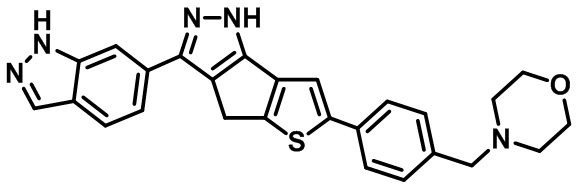
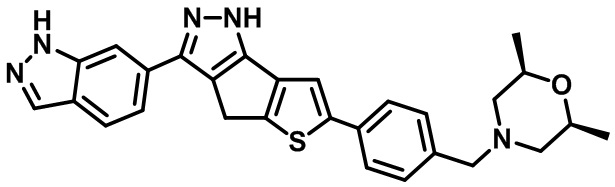
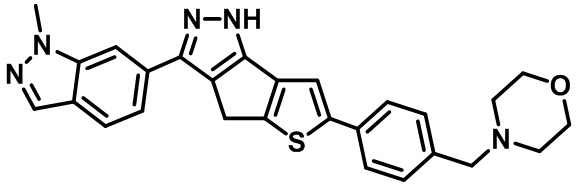
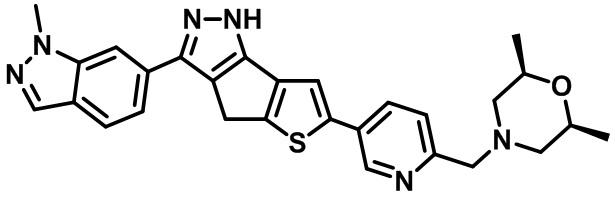
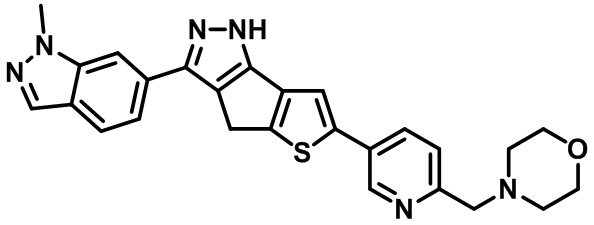
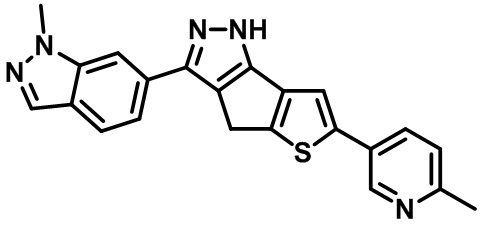
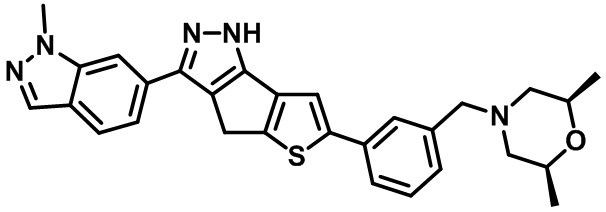
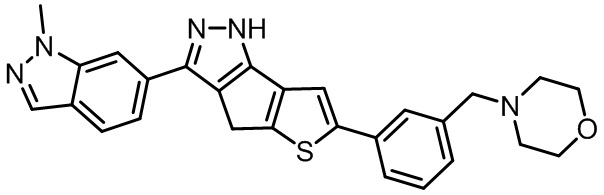
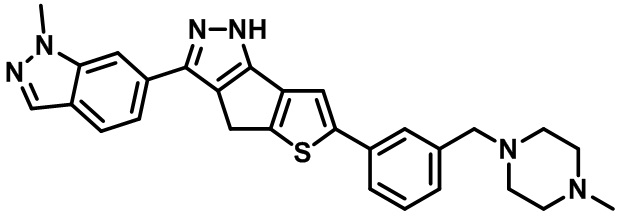
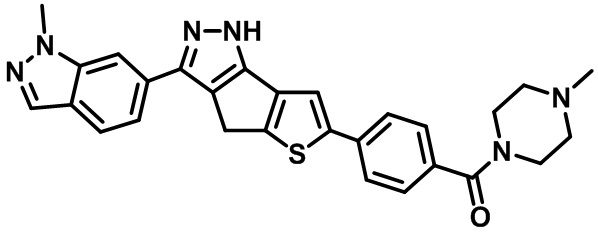
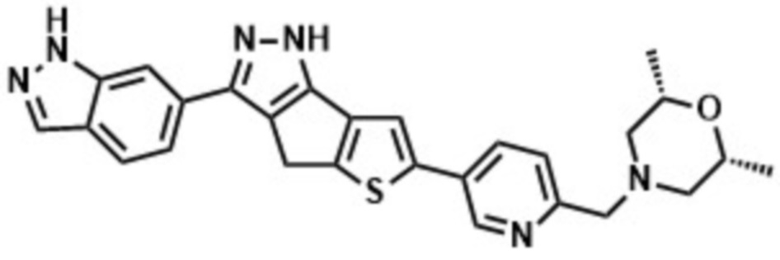
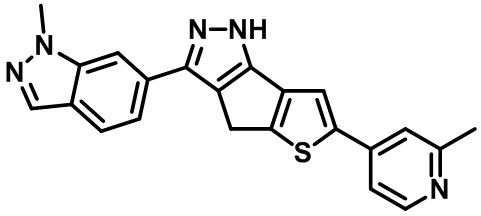
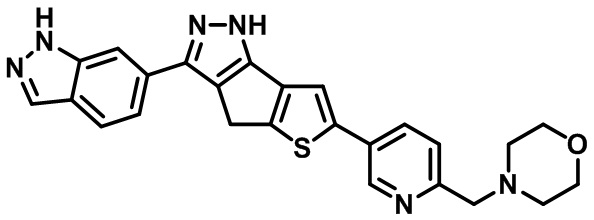
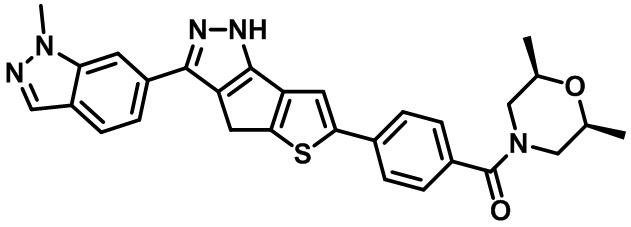
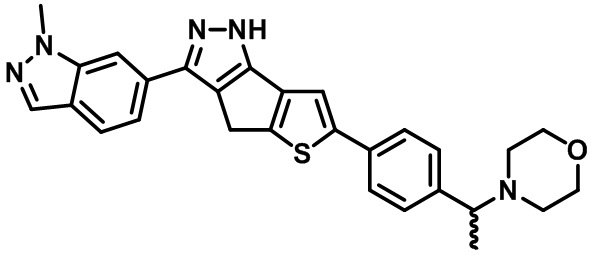
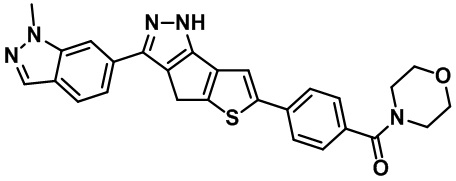
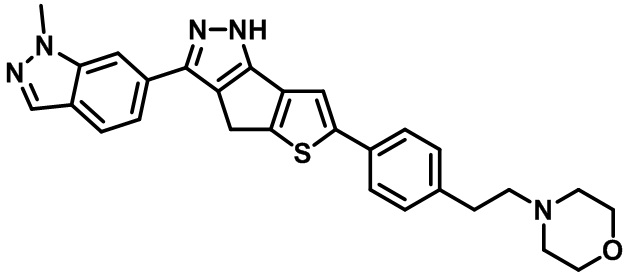
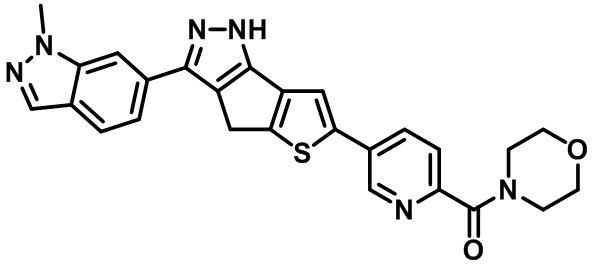
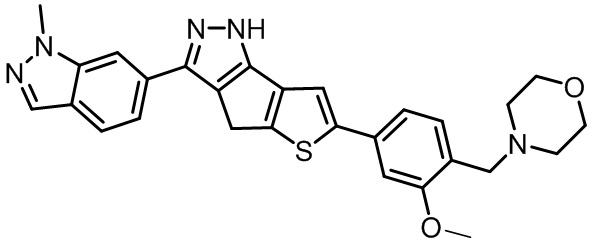
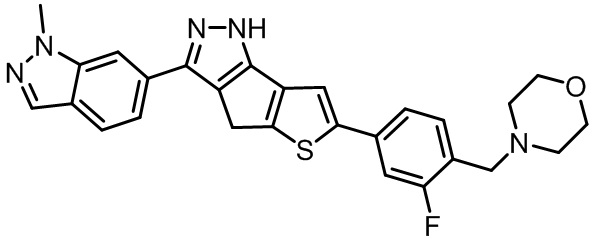
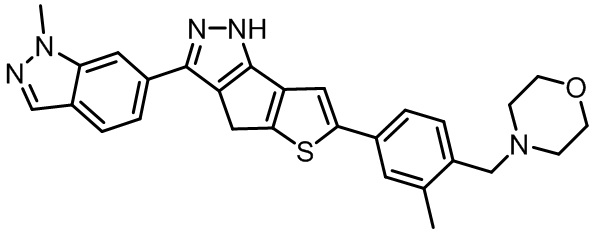
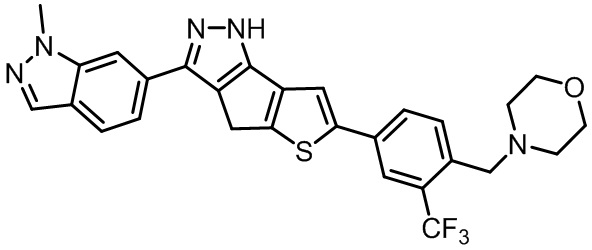
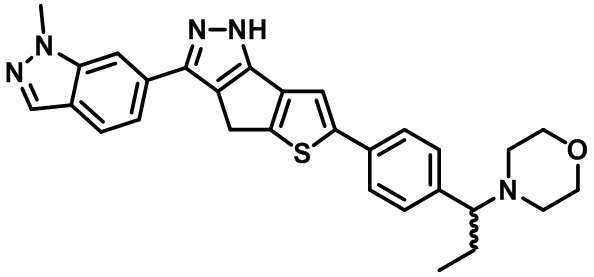
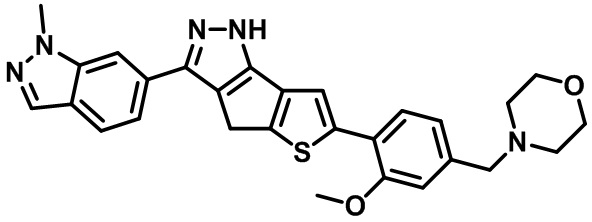
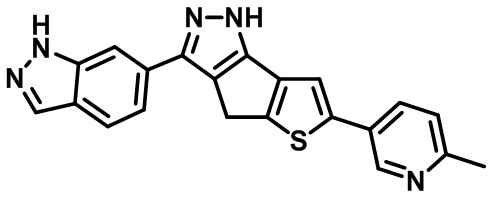
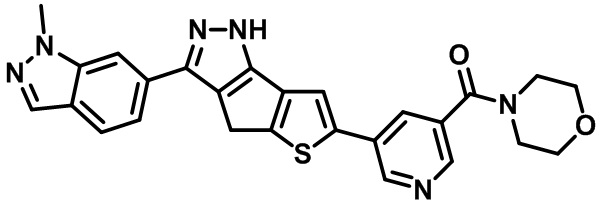
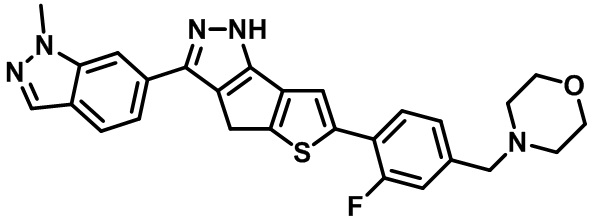
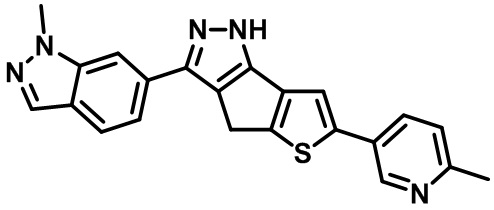
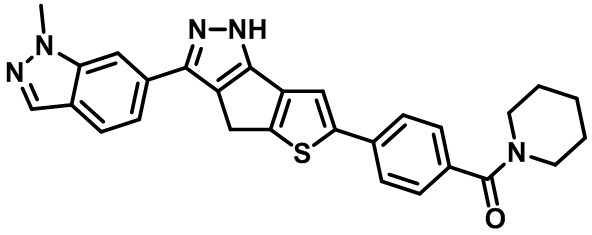
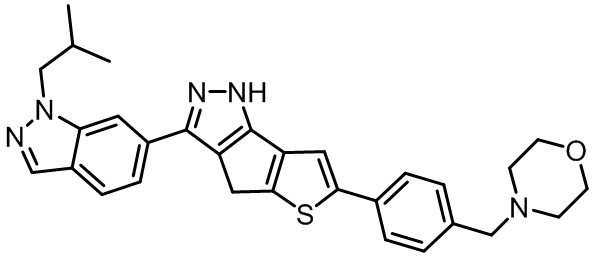
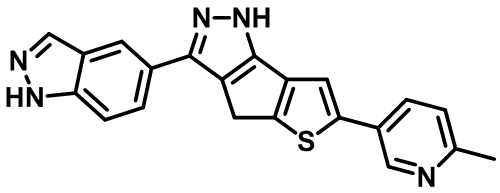
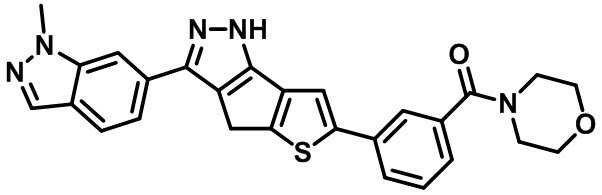
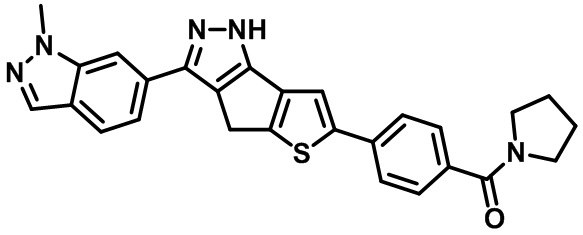
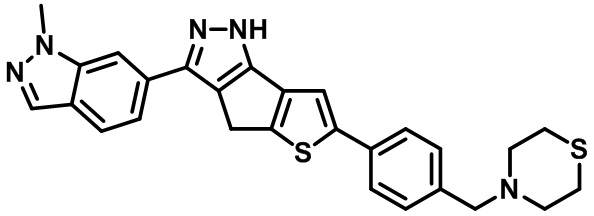
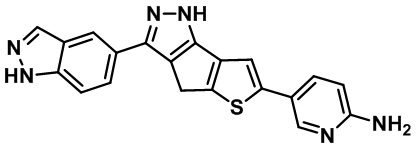
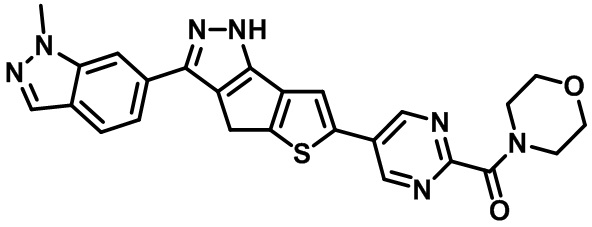
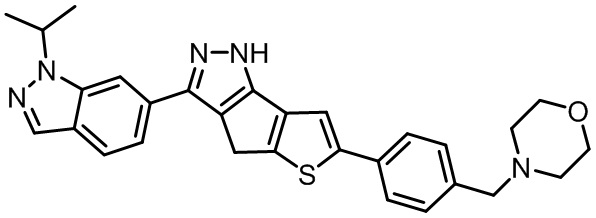
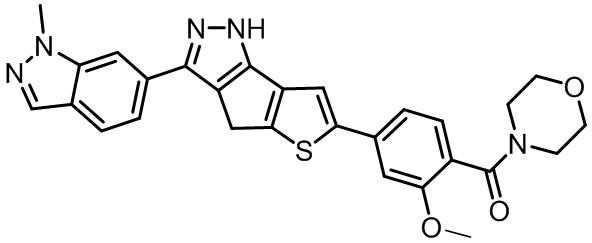
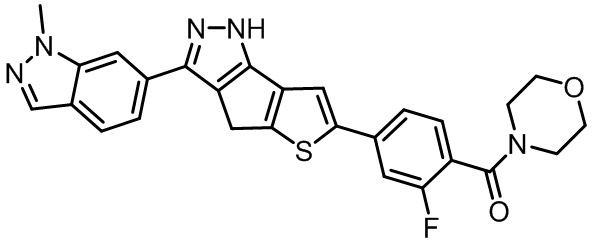
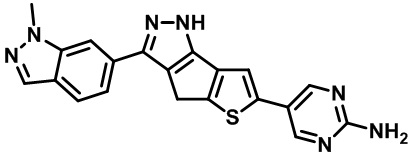
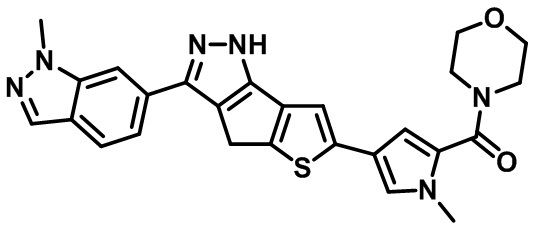
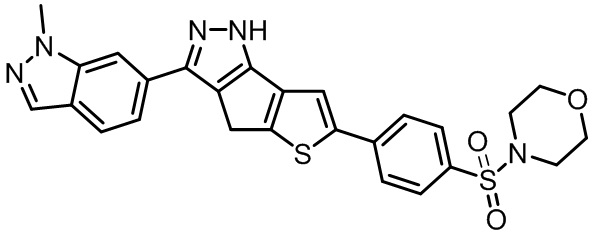
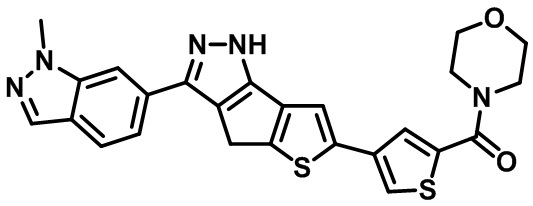
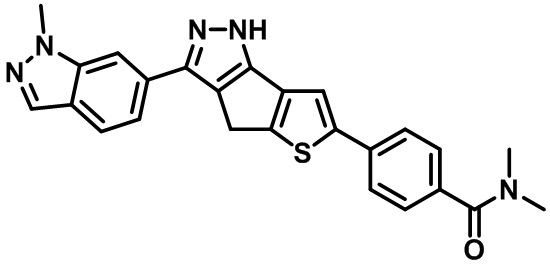
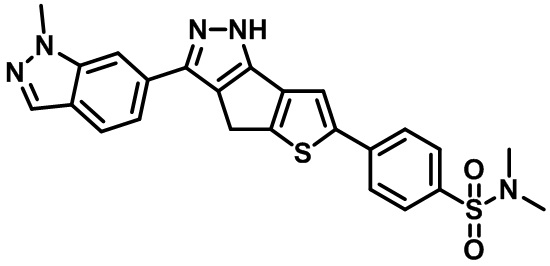
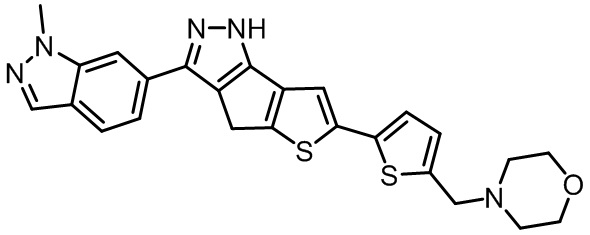
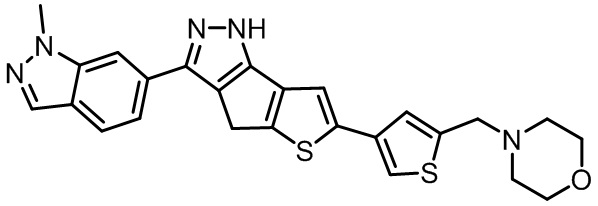
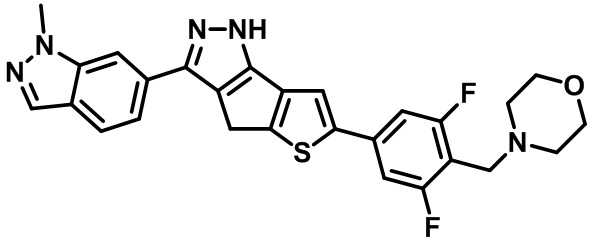
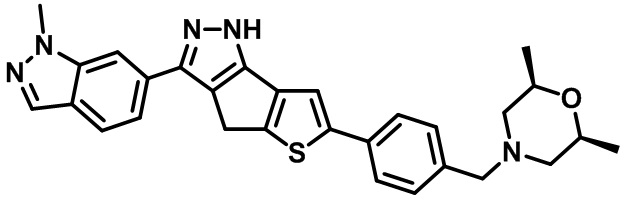
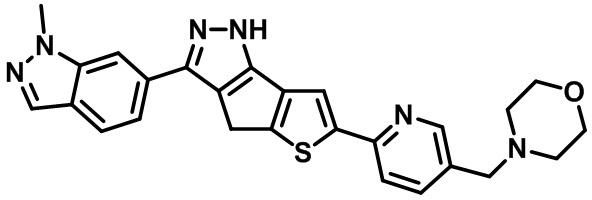
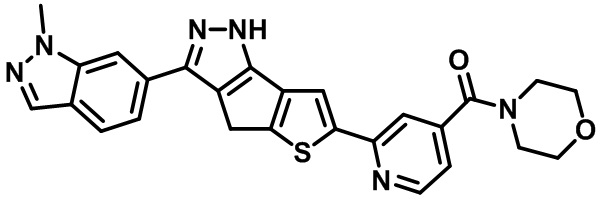
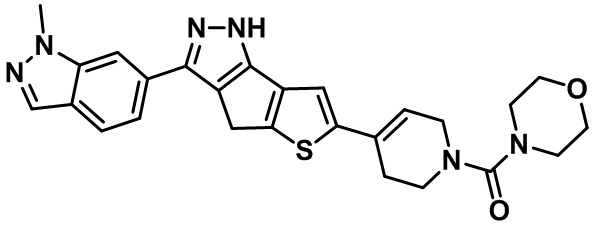
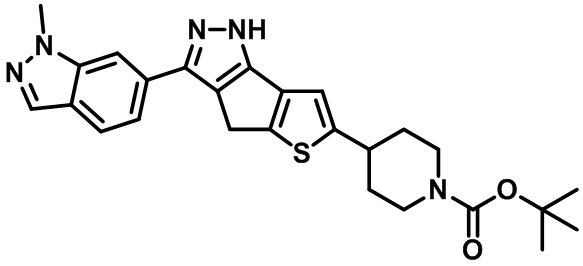
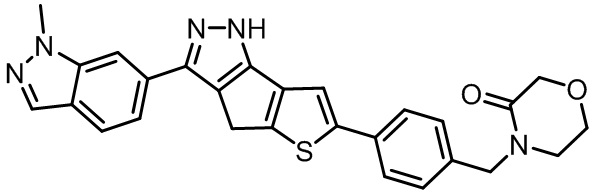
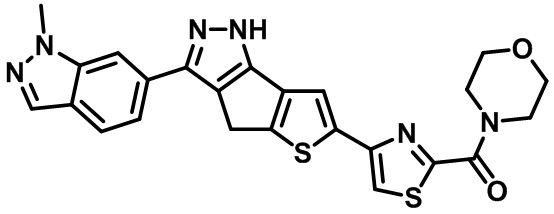
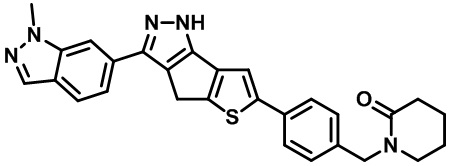
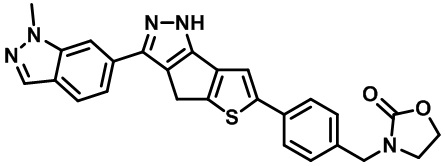
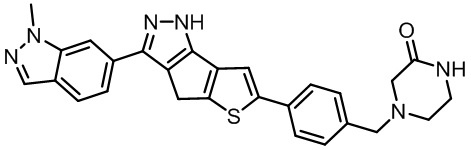
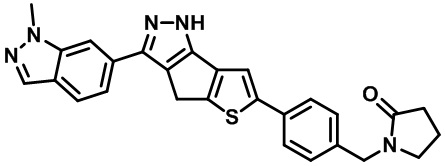
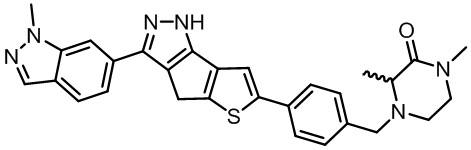
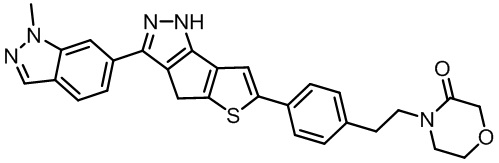
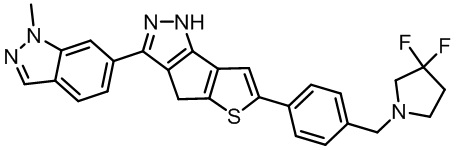
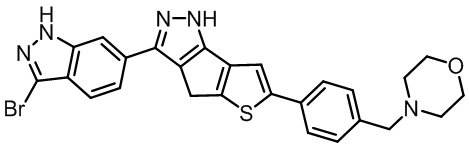
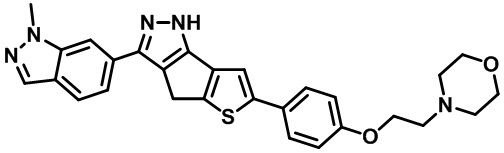
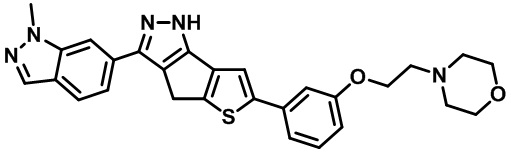
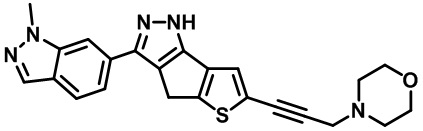
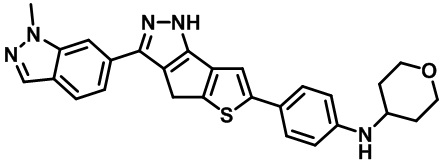
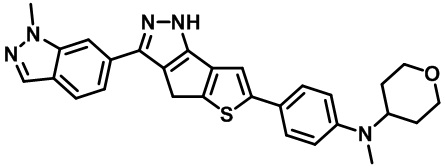
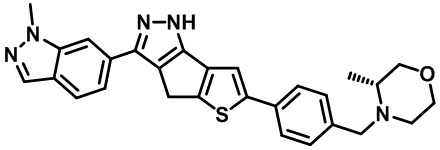
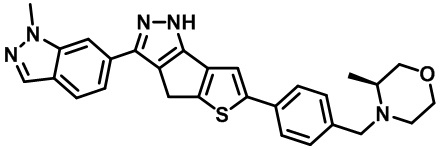
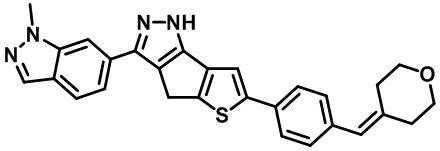
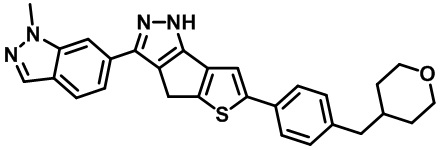
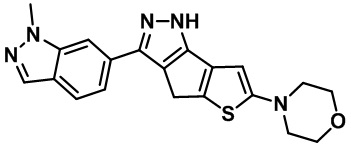
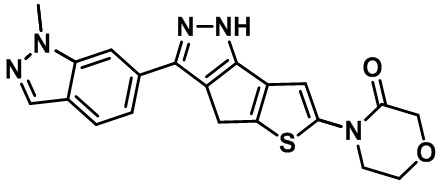
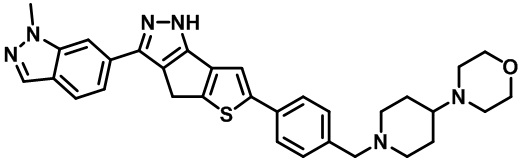
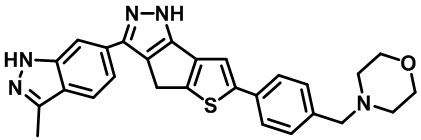
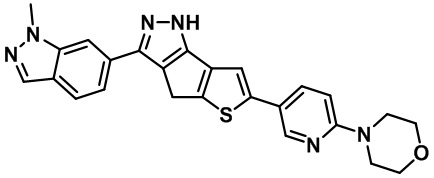
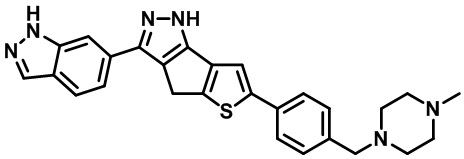
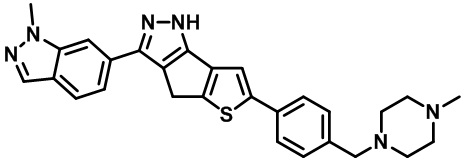
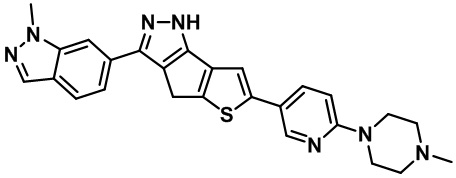
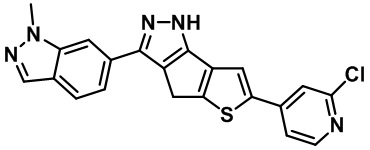
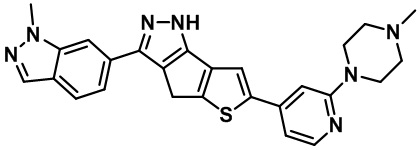
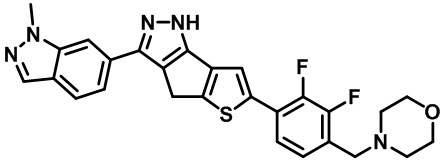
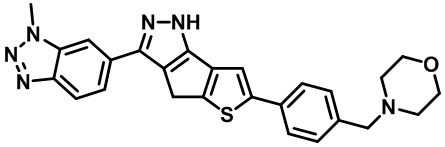
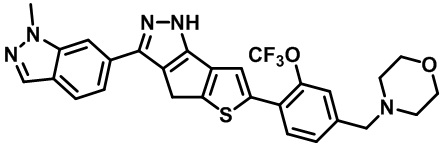
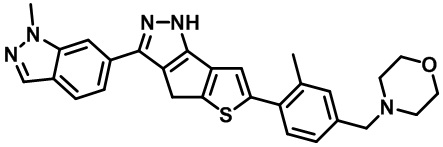
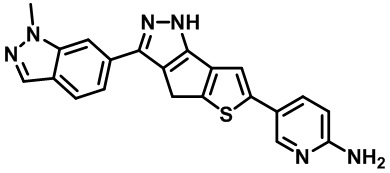
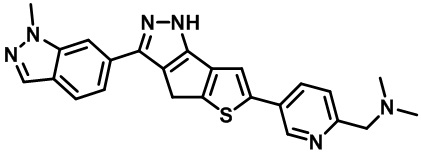
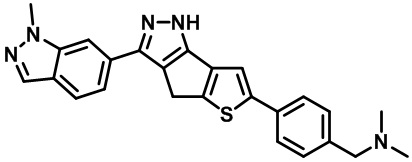
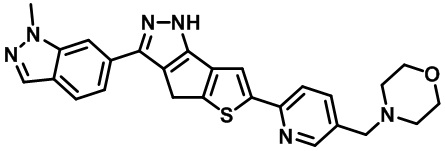
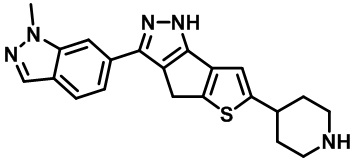
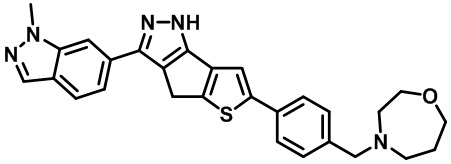
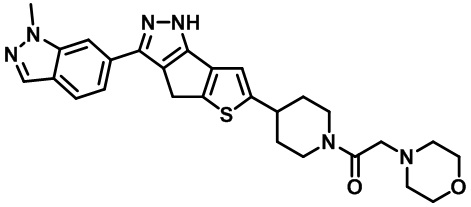
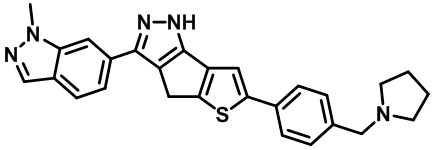
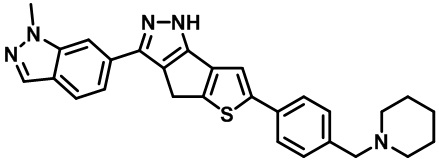
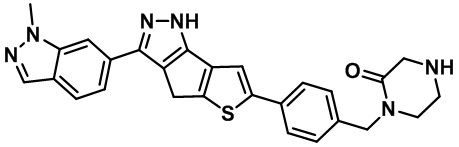
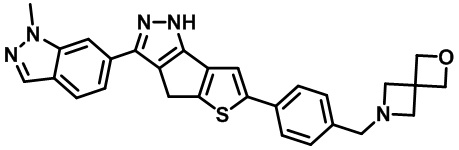
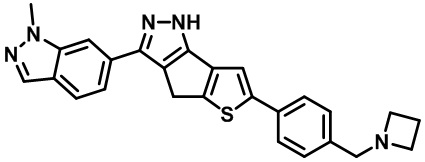
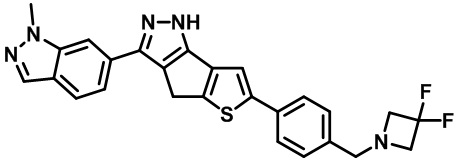
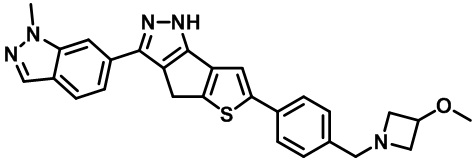
Таблица 2. 1H ЯМР и массовые данные
ПРИМЕР 2: Оценка ингибирующей активности соединений формулы (I) в ходе биохимических анализов in vitro
Различные соединения Формулы I были проверены на их ингибирующую активность в отношении целого ряда рецепторных тирозин киназ. Краткие описания различных анализов представлены ниже.
Анализ киназы FLT3
Ингибирование активности киназы FLT3 тестовым соединением, раскрытом в настоящем документе, было оценено методом AlphaScreen (PerkinElmer, Akron, Огайо, США). Стандартными условиями проведения анализа являлись 1,5 мкг рекомбинантной киназы FLT3 (SignalChem, Ричмонд, Британская Колумбия) с 6 мкг биотин-конъюгированного Poly-(Glu 4: Tyr 1) (Cisbio, Бедфорд, Массачусетс, США) в аналитическом буфере (10 μM АТФ, 10 мМ хлористый калий, pH7.0, 0,21 мМ ЭДТА, 0,5% глицерин, 1 мг/мл БСА, 0,01% 2-меркаптоэтанол, 0,001% Brij35, 10 мМ MgCl2) в окончательном объеме 25 μл. Реакции инкубировались при температуре 30 °C в течение 30 минут, и инкубирование было прекращено путем добавления 5 мкл 50 мМ ЭДТА. Анализ получившегося в результате продукта проводился с использованием комплекта AlphaScreen, и подсчет выполнялся с помощью Enspire Alpha (PerkinElmer, Уолтем, Массачусетс, США). Показания контрольной реакции (полная реакционная смесь) были обозначены как 0% ингибирование, а показания для реакции без фермента - как 100% ингибирование. Значения IC50 ингибиторов были определены после проведения анализов с каждым соединением в последовательно разбавленных концентрациях в дупликации. Анализ результатов проводился с использованием программного обеспечения линейной регрессии (GraphPad Prism 5; GraphPad Software Inc.)
Анализ мутантной киназы FLT3-D835Y
Оценка ингибирования активности мутантной киназы FLT3-D835Y тестовым соединением, раскрытым в настоящем документе, проводилась с помощью AlphaScreen (PerkinElmer). Стандартными условиями проведения анализа были 1 мкг рекомбинантной мутантной киназы FLT3-D835Y (SignalChem) с 6 мкг биотин-конъюгированного Poly-(Glu 4: Tyr 1) (Cisbio) в аналитическом буфере (10 μM АТФ, 10 мМ хлористый калий, pH7.0, 0,21 мМ ЭДТА, 0,5% глицерин, 1 мг/мл БСА, 0,01% 2-меркаптоэтанол, 0,001% Brij35, 10 мМ MgCl2) в окончательном объеме 25 μл. Реакции инкубировались при температуре 30°C в течение 30 минут, и инкубирование было прекращено путем добавления 5 мкл 50 мМ ЭДТА. Анализ получившегося в результате продукта проводился с использованием комплекта AlphaScreen, и подсчет выполнялся с помощью Enspire Alpha (PerkinElmer). Показания контрольной реакции (полная реакционная смесь) были обозначены как 0% ингибирование, а показания для реакции без фермента - как 100% ингибирование. Значения IC50 ингибиторов были определены после проведения анализов с каждым соединением в последовательно разбавленных концентрациях в дупбикации. Анализ результатов проводился с использованием программного обеспечения линейной регрессии (GraphPad Prism 5; GraphPad Software Inc.)
Анализ киназы αPDGFR
Оценка ингибирования активности киназы PDGFRα тестовым соединением, раскрытым в настоящем документе, проводилась с использованием AlphaScreen (PerkinElmer). Стандартным условиями проведения анализа были 1,5 мкг рекомбинантной киназы PDGFRα (SignalChem) с 6 мкг биотин-конъюгированным Poly-(Glu 4: Tyr 1) (Cisbio) в аналитическом буфере (10 μM АТФ, 10 мМ хлористый калий, pH 7.0, 0,21 мМ ЭДТА, 0,5% глицерин, 1 мг/мл БСА, 0,01% 2-меркаптоэтанол, 0,001% Brij35, 10 мМ MgCl2) в окончательном объеме 25 μл. Реакции инкубировались при температуре 30°C в течение 30 минут, и инкубирование было прекращено путем добавления 5 мкл 50 мМ ЭДТА. Анализ получившегося в результате продукта проводился с использованием комплекта AlphaScreen, и подсчет выполнялся с помощью Enspire Alpha (PerkinElmer). Показания контрольной реакции (полная реакционная смесь) были обозначены как 0% ингибирование, а показания для реакции без фермента - как 100% ингибирование. Значения IC50 ингибиторов были определены после проведения анализов с каждым соединением в последовательно разбавленных концентрациях в дупбикации. Анализ результатов проводился с использованием программного обеспечения линейной регрессии (GraphPad Prism 5; GraphPad Software Inc.)
Анализ киназы MET
Соединения, раскрытые в настоящем документе, были протестированы при ингибировании активности киназы MET, оцененной с использованием AlphaScreen (PerkinElmer) в виде обратного скрининга (сравнения) для демонстрации их избирательной активности ингибирования киназы в отношении рецепторных тирозинкиназ класса III. Поскольку киназа MET принадлежала к семейству рецепторных тирозинкиназ класса VIII, она имеет одну трансмембранную αцепь, связанную с одной внеклеточнойβ цепью, которая отличается от семейства РТК класса III с 5-ю иммуноглобулин-подобными внеклеточными доменами. Стандартными условиями проведения анализа являлись 1 мкг рекомбинантной киназы MET (SignalChem) с 3-мя мкг биотин-конъюгированного Poly-(Glu 4: Tyr 1) (Cisbio) в аналитическом буфере (10 μM АТФ, 10 мМ хлористый кальций, pH 7.0, 0,21 мМ ЭДТА, 0,5% глицерин, 1 мг/мл БСА, 0,01% 2-меркаптоэтанол, 0,001% Brij35, 10 мМ MgCl2) в окончательном объеме 25 μл. Реакции инкубировались при температуре 30°C в течение 45 минут, и ингибирование было прекращено путем добавления 5 мкл 50 мМ ЭДТА. Анализ получившегося в результате продукта проводился с использованием комплекта AlphaScreen, и подсчет выполнялся с помощью Enspire Alpha (PerkinElmer). Показания контрольной реакции (полная реакционная смесь) были обозначены как 0% ингибирование, а показания для реакции без фермента - как 100% ингибирование. Значения IC50 ингибиторов были определены после проведения анализов с каждым соединением в последовательно разбавленных концентрациях в дупликации. Анализ результатов проводился с использованием программного обеспечения линейной регрессии (GraphPad Prism 5; GraphPad Software Inc.)
Результаты
В сравнении с активностью ингибирования киназы MET, соединения изобретения были признаны обладающими неожиданной и избирательной ингибирующей активностью в отношении РТК класса III. Более конкретно, все соединения изобретения показывают значения IC50 ниже 10 нМ для киназы FLT3, а также для мутантной киназы FLT3-D835Y, и 57 из 105 соединений изобретения показывают значение IC50 ниже 10 нМ для киназы PDGFR, что демонстрирует высокую удельную активность соединений изобретения в отношении РТК класса III. Значения IC50 для соединений изобретения в отношении мутантных киназ FLT3, FLT3-D835Y, киназы PDGFRα и киназы Met подытожены в таблице 3. В таблице символ «A+» означает, что IC50 составляет менее 1 нМ, «A» означает, что IC50 составляет в пределах 1 -10 нМ, «B» означает, что IC50 составляет в пределах10-30 Нм, «C» означает, что IC50 составляет от 30 до 100 нМ, «D» означает, что IC50 составляет от 100 до 300 нМ, «E» означает, что IC50 составляет от 300 до1000 нМ и «F» означает, что IC50 составляет больше 1000 нМ.
Таблица 3. Ранжирование значений IC50 для отдельных рецепторных тирозинкиназ
№
D835Y
ПРИМЕР 3: Оценка анти-пролиферативной активности соединений формулы (I) в отношении панели линии раковых клеток человека с различной сигнальной зависимостью
Как отмечено выше, соединения изобретения можно использовать для лечения заболеваний или нарушений, связанных с протеинкиназой. Заболеваниями, связанными с протеинкиназой, могут быть рак, аутоиммунное заболевание или пролиферативное нарушение кровеносных сосудов. Рак может быть раком легких, раком толстой кишки, колоректальным раком, раком молочной железы, раком предстательной железы, раком печени, раком поджелудочной железы, раком мочевого пузыря, раком желудка, раком почек, раком слюнных желез, раком яичников, раком тела матки, раком шейки матки, раком полости рта, раком кожи, раком головного мозга, лимфомой или лейкемией.
Ингибирование роста клеток соединениями было измерено с использованием анализа CellTiterTM-96. Цитотоксичность соединений изобретения оценивали на панелях клеточных линий с различными зависимостями сигнального пути, включая клетку острого миелоидного лейкоза человека MV4-11 с мутацией FLT3-ITD, клетку острого миелоидного лейкоза человека Molm-14 с мутацией FLT3-ITD, клетку острого моноцитарного лейкоза человека THP-1 с мутацией NRAS G12D, клетку меланомы A375 с мутацией BRAF V600E и клетку HCC827 NSCLC с мутацией делеции экзона 19 EGFR.
Клеточная культура MV4-11
Соединения, раскрытые в настоящем документе, были протестированы в ходе анализа пролиферации клеток MV4-11 для определения их удельной клеточной активности в отношении роста клеток, зависимого от пути сигнальной системы FLT3. Клетки MV4-11 представляют собой клетки острого миелоидного лейкоза человека (ОМЛ), содержащие лиганд-независимую FLT3-ITD-активирующую мутацию, которая делает аномальную пролиферацию клеток ОМЛ зависимой от пути сигнальной системы FLT3. Ингибирование активности киназы FLT3 будет иметь результатом сниженный рост и/или гибель клеток. Клетки MV4-11 (каталожный № CRL-9591) были получены из Американской коллекции типовых культур (ATCC, Манассас, Виргиния). Вкратце, клетки выращивали в среде IMDM, дополненной 10% инактивированной теплом фетальной бычьей сывороткой, и инкубировали при температуре 37°C в атмосфере 5% CO2. Клеткам давали возможность расширяться до достижения насыщения, после чего их подвергали суб-культивированию или собирали для использования в анализе.
Клеточная культура Molm-14
Соединения, раскрытые в настоящем документе, были протестированы в ходе анализа пролиферации клеток Molm-14 для определения их удельной клеточной активности в отношении роста клеток, зависимого от пути сигнальной системы FLT3. Клетки Molm-14 представляют собой клетки острого миелоидного лейкоза человека (ОМЛ), содержащие лиганд-независимую FLT3-ITD-активирующую мутацию, которая делает аномальную пролиферацию клеток ОМЛ зависимой от пути сигнальной системы FLT3. Ингибирование активности киназы FLT3 будет иметь результатом сниженный рост и/или гибель клеток. Клетки Molm-14 (каталожный № ACC-777) были получены из Немецкой коллекции микроорганизмов и клеточных культур (DSMZ, Брауншвейг, Германия). Вкратце, клетки выращивали в среде RPMI 1640, дополненной 10% инактивированной теплом фетальной бычьей сывороткой, и инкубировали при температуре 37°C в атмосфере 5% CO2. Клеткам давали возможность расширяться до достижения насыщения, после чего их подвергали суб-культивированию или собирали для использования в анализе.
Клеточная культура THP-1
Соединения, раскрытые в настоящем документе, были протестированы в ходе анализа пролиферации клеток THP-1 в виде обратного скрининга (сравнения) для демонстрации их избирательной анти-пролиферативной активности по отношению к росту клеток, который всецело зависит от сигнальной системы РТК класса III. Клетки THP-1 представляют собой клетки острого моноцитарного лейкоза человека с мутацией NRAS G12D, которая делает рост клеток независимым от сигнальной системы РТК класса III. Клетки THP-1 (каталожный № TIB-202) были получены из ATCC. Вкратце, клетки выращивали в среде RPMI 1640, дополненной 10% инактивированной теплом фетальной бычьей сывороткой и 0,05 мМ 2-меркаптоэтанолом, и инкубировали при температуре 37°C в атмосфере 5% CO2. Клеткам давали возможность расширяться до достижения насыщения, после чего их подвергали суб-культивированию или собирали для использования в анализе.
Клеточная культура A375
Соединения, раскрытые в настоящем документе, были протестированы в ходе анализа пролиферации клеток A375 в виде обратного скрининга для демонстрации их избирательной анти-пролиферативной активности по отношению к росту клеток, который всецело зависит от сигнальной системы РТК класса III. Клетки A375 представляют собой клетки меланомы, кодирующие мутацию BRFA V600E, которая делает рост клеток зависимым от сигнальной системы BRAF вместо сигнальной системы РТК класса III. Клетки A375 (каталожный № CRL-1619) были получены из ATCC. Вкратце, клетки культивировали в DMEM с содержанием 10% ФБС, и инкубировали при температуре 37°C в атмосфере 5% CO2. Клеткам давали возможность расширяться до достижения насыщения, после чего их подвергали суб-культивированию или собирали для использования в анализе.
Клеточная культура HCC827
Соединения, раскрытые в настоящем документе, были протестированы в ходе анализа пролиферации клеток HCC827 в виде обратного скрининга для демонстрации их избирательной анти-пролиферативной активности по отношению к росту клеток, который всецело зависит от сигнальной системы РТК класса III. Клетки HCC827 представляют собой клетки немелкоклеточной карциномы легких (NSCLC), кодирующие мутацию делеции экзона 19 EGFR, которая делает рост клеток зависимым от сигнальной системы EGFR вместо сигнальной системы РТК класса III. Клетки HCC827 (каталожный № CRL-2868) были получены из ATCC. Вкратце, клетки культивировали в среде RPMI 1640, дополненной 10% ФБС, и инкубировали при температуре 37°C в атмосфере 5% CO2. Клеткам давали возможность расширяться до достижения насыщения, после чего их подвергали суб-культивированию или собирали для использования в анализе.
Клетки MV4-11, Molm-14, THP-1, A375 и HCC827 высевали в 96-луночные планшеты при 6500, 25000, 5000, 2000 и 8000 клеток/лунка, соответственно, и инкубировали при температуре 37°C в атмосфере 5% CO2 в течение ночи. Затем эти посеянные клетки обрабатывали увеличивающимися концентрациями тестируемых соединений и инкубировали еще 72 часа. В конце инкубации был добавлен реактив CellTiter96® AQueous One Solution (Promega, Сан-Луис-Обиспо, Калифорния, США), и его инкубировали в течение дополнительных 2-4 часов. Жизнеспособность клеток определялась путем измерения оптической плотности при 490 нм с использованием считывающего устройства для микропланшетов EMax® (Molecular Devices, Сан-Хосе, Калифорния, США).
Результаты
В сравнении с анти-пролиферативной активностью в клетках THP-1, A375 или HCC827, соединения изобретения проявляли неожиданную и избирательную цитотоксичность по отношению к росту клеток, который всецело зависит от сигнальной системы РТК класса III. Более конкретно, 68 соединений изобретения показывают значения IC50, составляющие ниже 30 нМ, для роста лейкозных клеток с зависимостью от сигнальной системы FLT3, что демонстрирует высокую удельную клеточную активность соединений изобретения.
Значения 50% ингибирующей концентрации (IC50) были рассчитаны путем построения графиков процентных соотношений ингибирования роста и концентраций соединения с использованием программного обеспечения GraphPad Prism 5 для подгонки кривой. Анти-пролиферативная активность соединений изобретения подытожена в таблице 4. В таблице символ «A» обозначает, что IC50 составляет менее 0,03 μM, «B» означает, что IC50 составляет от 0,03 до 0,1 μM, «C» означает, что IC50 составляет от 0,1 до 0,3 μM, «D» означает, что IC50 составляет от 0,3 до 1 μM, «E» означает, что IC50 составляет от 1 до 10 μM, а «F» означает, что IC50 превышает 10 μМ.
Таблица 4. Ранжирование анти-пролиферативной активности в отношении панели клеточной линии
№
(FLT3-ITD)
(FLT3-ITD)
NRASN12D
BRAFV600E
EGFRExon19_del
Данные в таблице 4 четко указывают на то, что соединения изобретения обладают неожиданной и избирательной анти-пролиферационной активностью в отношении роста раковых клеток, который всецело зависит от пути сигнальной системы РТК класса III. Следовательно, эти соединения можно использовать при лечении заболеваний, связанных с протеинкиназой, например, заболеваний или расстройств, опосредованных киназами FLT3, PDGFR, c-KIT и/или CSF-1R или опосредованных мутантными киназами FLT3, PDGFR, c-KIT и/или киназой CSF-1R. Способ в соответствии с одним вариантом осуществления изобретения предполагает введение пациенту, нуждающемуся в нем, эффективного количества соединения изобретения.
ПРИМЕР 4: Индентификация конъюгированных гетероциклическими пиразольными производными 6,5-слитых двуциклических гетероарилов в положении 5 или 6 с положением 2 в виде атома озота (Формула I) с демонстрацией неожиданной и превосходной удельной активности в отношении киназы FLT3, а также его мутанта.

Формула (I)
Как показано в таблице 5, Соединение 1 и Соединение 2 являются почти идентичными по структуре Примерам от A до G, соответственно, за исключением того, что 6,5-слитые бициклические гетероарильные кольца в Соединении 1 и Соединении 2 содержат по 2 атома азота в 2-х положениях, в отличие от Примеров от A до G.
Таблица 5. Сравнение удельной активности in vitro обладающих признаками изобретения соединений формулы (I) с аналогичными соединениями
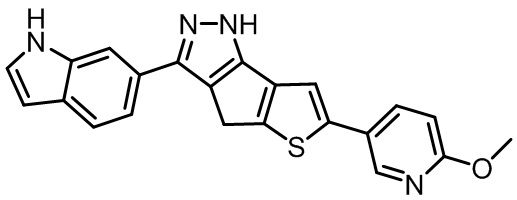

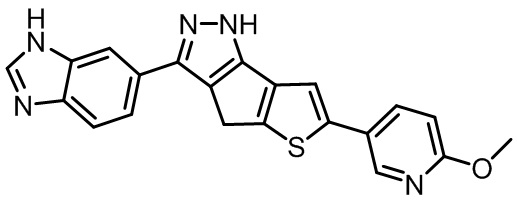
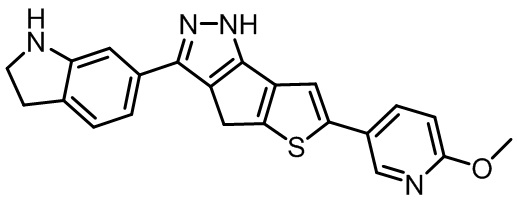
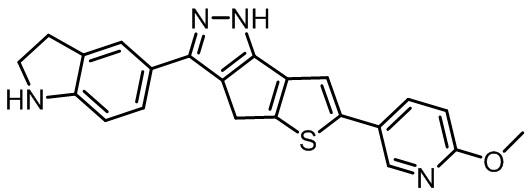



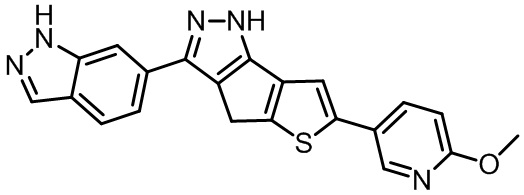
Неожиданно было замечено, что Соединение 1 и Соединение 2 обладают превосходящей удельной активностью по сравнению с удельной активностью Примеров от A до G при ингибировании киназы FLT3 , а также мутанта FLT3-D835Y с приблизительно в 5 или более раз лучшей удельной активностью. Исходя из представленных выше результатов, неожиданно обнаруживается, что 6,5-слитый бициклический гетероарил, содержащий 2 атома азота в 2-х положениях, демонстрирует крайне эффективную ингибирующую активность в отношении киназы FLT3 и ее мутантов.
ПРИМЕР 5: Сравнение удельной активности соединения формулы (I) с удельной активностью структурно близких соединений в ограничительной части формулы изобретения
Соединения из Примеров от H до K были найдены или предусмотрены в ограничительной части формулы изобретения (US 8853207 B2). Соединение 40 и Соединение 3 были выбраны для сравнения их удельной активности in vitro с удельной активностью соединений Примера H. Соединение 1 и Соединение 2 были выбраны для сравнения их удельной активности in vitro с удельной активностью Примеров I и J. Соединение 36 и Соединение 30 были выбраны для сравнения их удельной активности in vitro с удельной активностью Примера K.
Как показано в таблице 6, Соединение 40, Соединение 3, Соединение 1, Соединение 2, Соединение 36 и Соединение 30 почти идентичны по структуре соединениям из Примеров от H до K, соответственно, за исключением того, что соединения изобретения имеют по одному замещенному индазольному фрагменту, присоединенному непосредственно к пиразолу, в отличие от соединений ограниченой части формулы изобретения из Примеров от H до K.
Таблица 6. Сравнение удельной активности in vitro соединений, обладающих признаками изобретения, с соединениями, предусмотренными в ограничительной части формулы изобретения
(Ex-78 в US8853207B2)
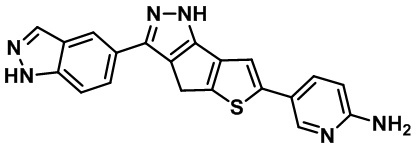

(Ex-76 в US8853207B2)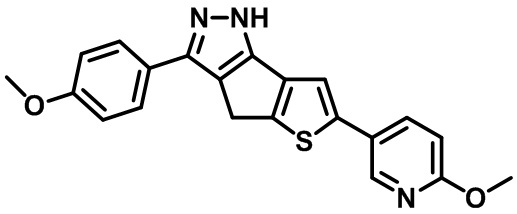
[Формула (I) в US 8853207 B2)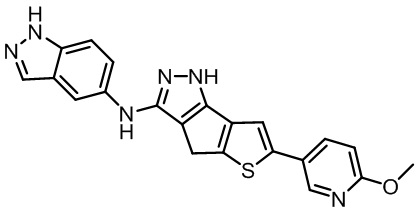
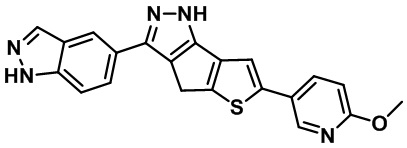
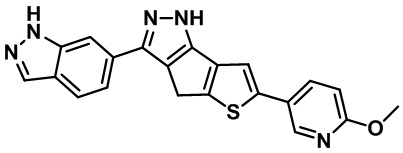
[Формула (I) в US 8853207 B2)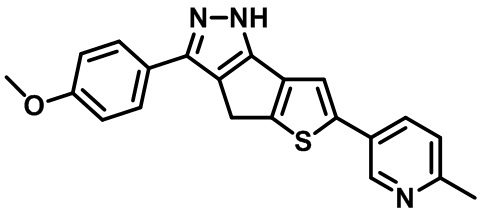


Неожиданно, в отличие от соединений ограничительной части формулы изобретения из Примеров от H до K, соединения изобретения продемонстрировали превосходящую удельную активность при ингибировании киназы FLT3 и ее мутанта с приблизительно в 10 или более раз большей удельной активностью.
ПРИМЕР 6: Оценка клеточной удельной активности соединений формулы (I) в отношении фосфорилирования FLT3 и его нижележащего эффектора STAT5 в линии лейкозных клеток MV4-11 с конститутивной активацией сигнала FLT3.
FLT3 экспрессируется в клетках ОМЛ у большинства пациентов, и FLT3 мутирует приблизительно в 30% клеток ОМЛ. В число мутаций входят внутренние тандемные дупликации (ВТД), имеющиеся в клетках ОМЛ приблизительно у 25% пациентов, и точечные мутации в тирозинкиназном домене (ТКД), имеющиеся приблизительно у 5% пациентов. Как ВТД, так и ОМЛ мутации активируются, вызывая лиганд-независимую или конститутивную активацию сигнальной системы рецепторов FLT3, способствуя, тем самым, цитокин-независимому выживанию и пролиферации клеток ОМЛ (Кровь 2002; 100:1532-42). Как FLT3-ITD, так и FLT3 TKD мутации ведут в результате к конститутивной активации сигнальной системы FLT3, которая предусматривает путь киназы FLT3 и ее нисходящие пролиферативные пути активации сигнальной системы, в том числе путь киназы Ras/MAPK (MEK)/внеклеточной сигнал-регулируемой киназы (ERK) и путь PI3K/Akt. Кроме того, в отличие от сигнальной системы FLT3 дикого типа, FLT3-ITD эффективно активирует путь STAT5. STAT5 индуцирует ее гены-мишени, такие как циклин D1, c-myc и анти-апоптотический ген p21, которые важны для роста клеток. Эти эффекты могут указывать на роль FLT3-ITD в аберрантном росте лейкозных клеток. Конститутивная активация FLT3-ITD STAT5 может ускорить рост клеток ОМЛ (J Гематология/Онкология. 2011; 4: 13.).
Эффективные соединения формулы (I) в ПРИМЕРЕ 2 были оценены методом вестерн-блоттинг анализа для не регулярной клеточной удельной активности в отношении фосфорилирования FLT3 и его нижележащего эффектора STAT5 в линии лейкозных клеток MV4-11 с конститутивной активацией сигнальной системы FLT3. Для вестерн-блоттинг экспериментов, клетки MV4-11 культивировались в среде IMDM с содержанием 0,1% ФБС в течение ночи. В день проведения анализа обрабатывались три миллиона клеток с соединением или без него в течение 3-х часов в пробирках объемом 15 мл. Затем, цельноклеточные лизаты были собраны вскоре после экстракции путем добавления 2× буферов для образца ДСР и кипячения на нагревательной плитке при температуре 105°C в течение 15 минут. Получившиеся в результате клеточные лизаты были разделены методом ДСР-ПААГ-электрофореза и перенесены в ПВДФ-мембрану. Экспрессия белка была обнаружена при использовании иммуноблота с соответствующими первичным антителом и вторичным антителом с соблюдением стандартных процедур. Антитела к p-FLT3 (Tyr-591), анти-кроличьи IgG HRP-связанные вторичные антитела и анти-мышиные IgG HRP-связанные вторичные антитела, были приобретены у компании Cell Signaling Technology. Антитела к p-STAT5 (Tyr-694) были приобретены у компании BD biosciences. Антитела к актину были приобретены у компании R&D system. Иммуноблоты были выявлены методом хемилюминесценции (субстрат максимальной чувствительности SuperSignal™ West Femto, Thermo) и обнаружены с помощью системы визуализации ChemiDoc™ MP (Bio-Rad). Интенсивность полос вестерн-блота также определялась количественно с помощью системы визуализации ChemiDoc™ MP. Значения относительной интенсивности полос, соответствующие вариантам медикаментозного лечения при разовой концентрации (30 нМ), были сравнены с контрольной группой ДМСО. Процент (%) ингибирования при каждой концентрации лекарственного средства были вычислен с использованием формулы:
Процент (%) ингибирования = (1 - Относительная интенсивность) × 100.
Выбранные соединения формулы I, демонстрирующие ингибирование более 50% в отношении фосфорилирования FLT3 и ее нижележащего эффектора STAT5 при медикаментозном лечении при 30 нМ, были перечислены в следующей таблице 7.
Таблица 7. Ингибирование фосфорилирования FLT3 и ее нисходящего эффектора STAT5 в FLT3-ITD-положительных лейкозных клетках MV4-11
(при обработке 30 нМ)
Некоторые варианты осуществления изобретения относятся к способам лечения заболевания, связанного с протеинкиназой. Способ в соответствии с одним вариантом осуществления изобретения предполагает введение пациенту, нуждающемуся в нем, эффективного количества соединения изобретения.
Хотя изобретение было описано в отношении ограниченного числа вариантов осуществления, специалисты в данной области, обладающие преимуществами этого раскрытия, оценят, что могут быть разработаны другие варианты осуществления, которые не выходят за рамки изобретения в том виде, в котором оно раскрыто в настоящем документе. Соответственно, объем изобретения должен быть ограничен только прилагаемыми пунктами формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДАЗОЛИЛИЗОКСАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ТАКИХ КАК ЗЛОКАЧЕСТВЕННОЕ НОВООБРАЗОВАНИЕ | 2020 |
|
RU2836662C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2716136C2 |
| ПИРАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ FSHR И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2663898C2 |
| ИНГИБИТОРЫ РЕПЛИКАЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2019 |
|
RU2812128C2 |
| ПРОИЗВОДНЫЕ ТИЕНО[2,3-с]ХИНОЛИНА-4-ОНА, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РВК-ЗАВИСИМОГО ЗАБОЛЕВАНИЯ | 2011 |
|
RU2574398C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗОПИРИДИНИЛ-АМИНОПИРИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РАКА | 2010 |
|
RU2619463C2 |
| СОЕДИНЕНИЯ ГЕТЕРОАРИЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ТКБ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2742122C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| АМИНОТРИАЗОЛОПИРИДИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2009 |
|
RU2552642C2 |
| 5-ЗАМЕЩЕННЫЕ ИНДАЗОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ | 2008 |
|
RU2487873C2 |
Изобретение относится соединению формулы (II), (III), (IV) или (V), или его стереоизомеру, или его фармацевтически приемлемой соли. В указанных формулах значения переменных следующие: G выбран из группы, состоящей из необязательно замещенного C6-арила, необязательно замещенного 5-6-членного гетероарила, имеющего один или несколько гетероатомов, выбранных из N и S, необязательно замещенного 5-8-членного гетероциклила, имеющего один или несколько гетероатомов, выбранных из O и N, С2-С10-алкинила и прямой связи; L выбран из группы, состоящей из –CH=, -CHR4-, -(CH2)q-, -NR5-, -O-, -O(CH2)q-, -C(O)-, -C(O)(CH2)q-, -SO2- и прямой связи, в которых каждый q является индивидуально и независимо целым числом от 1 до 4; Z выбран из группы, состоящей из водорода, дейтерия, галогена, C1-C4 алкила, C1-C4 алкиламина, C1-C4 диалкиламина и необязательно замещенного 4-7-членного гетероциклила или гетероциклического спиро-соединения; R1 выбран из группы, состоящей из водорода и дейтерия; R2 выбран из группы, состоящей из водорода, дейтерия, галогена и C1-C6 алкила; R3 выбран из группы, состоящей из водорода, дейтерия и C1-C6 алкила; R4 выбран из группы, состоящей из группы, состоящей из дейтерия и C1-C6 алкила; и R5 выбран из группы, состоящей из водорода и C1-C6 алкила. Также предложены фармацевтическая композиция, содержащая указанное соединение, и способ лечения с использованием указанного соединения. Предложенные соединения ингибируют киназы РТК класса III, такие как киназы FLT3, PDGFR, и могут применяться для лечения заболеваний или нарушений, опосредованных такими киназами, в частности, рака. 3 н. и 7 з.п. ф-лы, 7 табл., 6 пр.
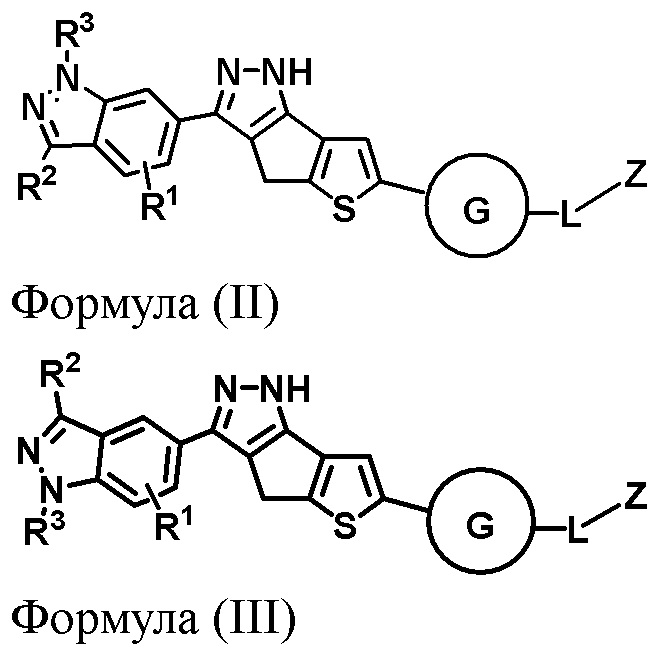
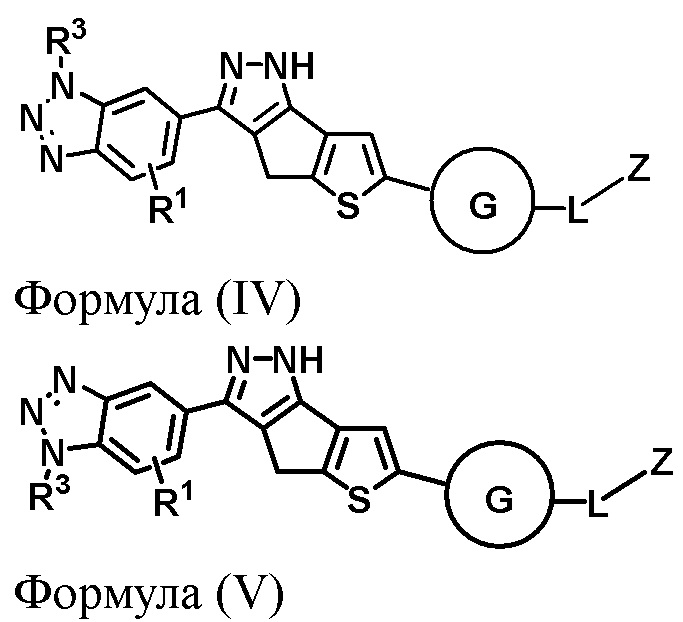
1. Соединение формулы (II), (III), (IV) или (V):
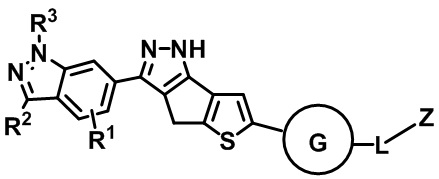
Формула (II)
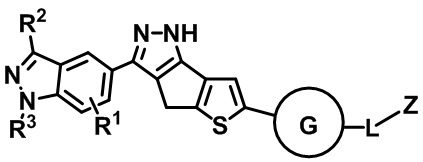
Формула (III)
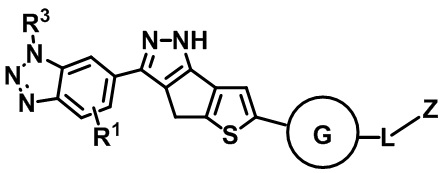
Формула (IV)
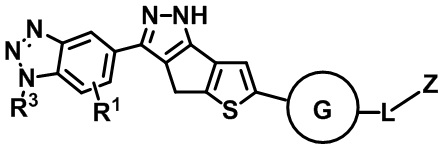
Формула (V)
или стереоизомер, фармацевтически приемлемая соль, в котором
G выбран из группы, состоящей из необязательно замещенного C6-арила, необязательно замещенного 5-6-членного гетероарила, имеющего один или несколько гетероатомов, выбранных из N и S, необязательно замещенного 5-8-членного гетероциклила, имеющего один или несколько гетероатомов, выбранных из O и N, С2-С10-алкинила и прямой связи;
L выбран из группы, состоящей из -CH=, -CHR4-, -(CH2)q-, -NR5-, -O-, -O(CH2)q-, -C(O)-, -C(O)(CH2)q-, -SO2- и прямой связи, в которых каждый q является индивидуально и независимо целым числом от 1 до 4;
Z выбран из группы, состоящей из водорода, дейтерия, галогена, C1-C4 алкила, C1-C4 алкиламина, C1-C4 диалкиламина и необязательно замещенного 4-7-членного гетероциклила или гетероциклического спиро-соединения;
R1 выбран из группы, состоящей из водорода и дейтерия;
R2 выбран из группы, состоящей из водорода, дейтерия, галогена и C1-C6 алкила;
R3 выбран из группы, состоящей из водорода, дейтерия и C1-C6 алкила;
R4 выбран из группы, состоящей из группы, состоящей из дейтерия и C1-C6 алкила; и
R5 выбран из группы, состоящей из водорода и C1-C6 алкила.
2. Соединение по п. 1, в котором кольцо G представляет собой необязательно замещенный C6-арил, необязательно замещенный 5-6-членный гетероарил, имеющий один или несколько гетероатомов, выбранных из N и S, необязательно замещенный 5-8-членный гетероциклил, имеющий один или несколько гетероатомов, выбранных из O и N или C2-C10-алкинил.
3. Соединение по п. 2, в котором кольцо G выбирается из группы, состоящей из:
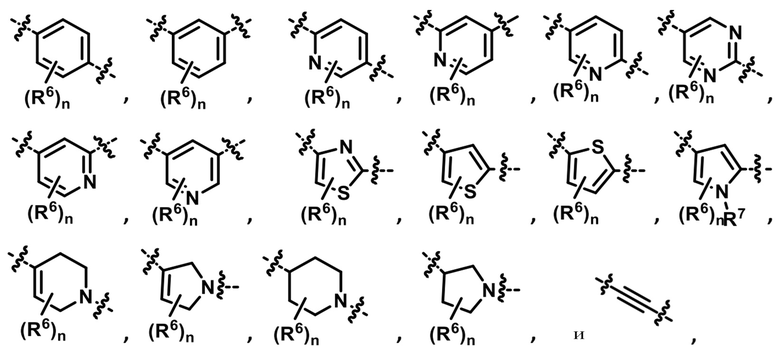
в котором
R6 выбран из группы, состоящей из водорода, дейтерия, галогена, нитро, циано, трифторметила, трифторметокси, C1-C6 алкила и C1-C6 алкокси;
каждый n является индивидуально и независимо целым числом от 0 до 4; и
R7 является водородом.
4. Соединение по п. 3, в котором Z представляет собой фторид, хлорид, бромид, диметиламино или необязательно замещенное четырех-, пяти- или шестичленное или семичленное гетероциклил или гетероциклическое спиро-соединение.
5. Соединение по п. 4, в котором Z выбирается из группы, состоящей из:
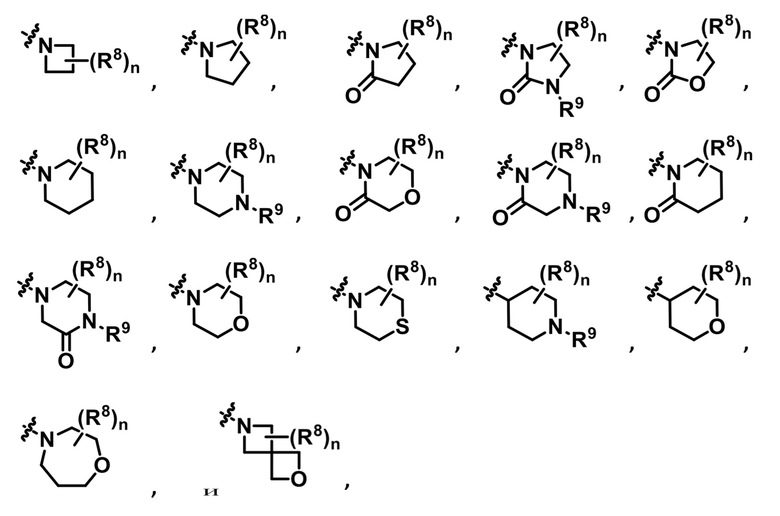
в котором
R8 выбран из группы, состоящей из водорода, дейтерия, галогена, нитро, циано, трифторметила, трифторметокси, 4-морфолинила, C1-C6 алкила и C1-C6 алкокси;
каждый n является индивидуально и независимо целым числом от 0 до 4; и
R9 выбран из группы, состоящей из водорода, дейтерия и C1-C6 алкила.
6. Соединение по п. 1, представляющее собой:
3-(1H-индазол-5-ил)-6-(6-метоксипиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1H-индазол-6-ил)-6-(6-метоксипиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
5-(3-(1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-амин,
6-(6-метоксипиридин-3-ил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
N,N-диметил-5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-амин,
4-(4-(3-(1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
(2S,6R)-4-(4-(3-(1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)-2,6-диметилморфолин,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
(2S,6R)-2,6-диметил-4-((5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)метил)морфолин,
4-((5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)метил)морфолин,
3-(1-метил-1H-индазол-6-ил)-6-(6-метилпиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
(2S,6R)-2,6-диметил-4-(3-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(3-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
3-(1-метил-1H-индазол-6-ил)-6-(3-((4-метилпиперазин-1-ил)метил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(4-метилпиперазин-1-ил)метанон,
(2R,6S)-4-((5-(3-(1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)метил)-2,6-диметилморфолин,
3-(1-метил-1H-индазол-6-ил)-6-(2-метилпиридин-4-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
4-((5-(3-(1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)метил)морфолин,
((2S,6R)-2,6-диметилморфолино)(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)метанон,
4-(1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)этил)морфолин,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(морфолино)метанон,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенетил)морфолин,
(5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)(морфолино)метанон,
4-(2-метокси-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(2-фтор-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(2-метил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)-2-(трифторометил)бензил)морфолин,
4-(1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)пропил)морфолин,
4-(3-метокси-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
3-(1H-индазол-6-ил)-6-(6-метилпиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
(5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-3-ил)(морфолино)метанон,
4-(3-фтор-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
3-(1-метил-1H-индазол-6-ил)-6-(6-метилпиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(пиперидин-1-ил)метанон,
4-(4-(3-(1-изобутил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
3-(1H-индазол-5-ил)-6-(6-метилпиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
(3-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(морфолино)метанон,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(пирролидин-1-ил)метанон,
3-(1-метил-1H-индазол-6-ил)-6-(4-(тиоморфолинометил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
5-(3-(1H-индазол-5-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-амин,
(5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиримидин-2-ил)(морфолино)метанон,
4-(4-(3-(1-изопропил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
(2-метокси-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(морфолино)метанон,
(2-фтор-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)(морфолино)метанон,
5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиримидин-2-амин,
метил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]амразол-6-ил)-1H-пиррол-2-ил)(морфолино)метанон,
4-((4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)сульфонил)морфолин,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопентал[1,2-c]пиразол-6-ил)тиофен-2-ил)(морфолино)метанон,
N,N-диметил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензамид,
N,N-диметил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензолсульфонамид,
4-((5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)тиофен-2-ил)метил)морфолин,
4-((4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)тиофен-2-ил)метил)морфолин,
4-(2,6-дифтор-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
(2S,6R)-2,6-диметил-4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-((6-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-3-ил)метил)морфолин,
(2-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-4-ил)(морфолино)метанон,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопентал[1,2-c]пиразол-6-ил)-3,6-дигидропиридин-1(2H)-ил)(морфолино)метанон,
трет-бутил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента [1,2-c]пиразол-6-ил)пиперидин-1-карбоксилат,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин-3-он,
(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)тиазол-2-ил)(морфолино)метанон,
1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пиперидин-2-он,
3-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)оксазолидин-2-он,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пиперазин-2-он,
1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пирролидин-2-он,
1,3-диметил-4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пиперазин-2-он,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенетил)морфолин-3-он,
6-(4-((3,3-дифторпирролидин-1-ил)метил)фенил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
4-(4-(3-(3-бром-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(2-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенокси)этил)морфолин,
4-(2-(3-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенокси)этил)морфолин,
4-(3-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)проп-2-ин-1-ил)морфолин,
N-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)тетрагидро-2H-пиран-4-амин,
N-метил-N-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)тетрагидро-2H-пиран-4-амин,
(R)-3-метил-4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
(S)-3-метил-4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
3-(1-метил-1H-индазол-6-ил)-6-(4-((тетрагидро-4H-пиран-4-илиден)метил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1-метил-1H-индазол-6-ил)-6-(4-((тетрагидро-2H-пиран-4-ил)метил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)морфолин,
4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)морфолин-3-он,
4-(1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пиперидин-4-ил)морфолин,
4-(4-(3-(3-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)морфолин,
3-(1H-индазол-6-ил)-6-(4-((4-метилпиперазин-1-ил)метил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1-метил-1H-индазол-6-ил)-6-(4-((4-метилпиперазин-1-ил)метил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1-метил-1H-индазол-6-ил)-6-(6-(4-метилпиперазин-1-ил)пиридин-3-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
6-(2-хлорпиридин-4-ил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1-метил-1H-индазол-6-ил)-6-(2-(4-метилпиперазин-1-ил)пиридин-4-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
4-(2,3-дифтор-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(4-(3-(1-метил-1H-бензо[д][1,2,3]триазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)-3-(трифторметокси)бензил)морфолин,
4-(3-метил-4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)морфолин,
5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-амин,
N,N-диметил-1-(5-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-2-ил)метанамин,
N,N-диметил-1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)фенил)метанамин,
4-((6-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пиридин-3-ил)метил)морфолин,
3-(1-метил-1H-индазол-6-ил)-6-(пиперидин-4-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
4-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)-1,4-оксазепан,
1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)пипередин-1-ил)-2-морфолиноэтан-1-он,
3-(1-метил-1H-индазол-6-ил)-6-(4-(пирролидин-1-илметил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
3-(1-метил-1H-индазол-6-ил)-6-(4-(пиперидин-1-илметил)фенил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
1-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)пиперазин-2-он,
6-(4-(3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол-6-ил)бензил)-2-окса-6-азаспиро[3.3]гептан,
6-(4-(азетидин-1-илметил)фенил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол,
6-(4-((3,3-дифторазетидин-1-ил)метил)фенил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол, или
6-(4-((3-метоксиазетидин-1-ил)метил)фенил)-3-(1-метил-1H-индазол-6-ил)-1,4-дигидротиено[2',3':4,5]циклопента[1,2-c]пиразол.
7. Фармацевтическая композиция для лечения заболевания или расстройства, опосредованного FLT3 и/или PDGFR киназами или опосредованного мутантной киназой FTL3 и/или PDGFR киназами, содержащая соединение по любому из пп. 1-6, его стереоизомер или его фармацевтически приемлемую соль и фармацевтически приемлемый разбавитель или носитель.
8. Способ лечения заболевания или нарушения, опосредованного киназами FLT3 и/или PDGFR киназами или опосредованного мутантной киназой киназ FLT3 и/или PDGFR киназами, включающий: введение субъекту, нуждающемуся в этом, терапевтически эффективного количества фармацевтической композиции, содержащей соединение по любому из пп. 1-6, его стереоизомер или его фармацевтически приемлемую соль и фармацевтически приемлемый разбавитель, или носитель, или модуль нацеливания на белок.
9. Способ по п. 8, в котором заболеванием или нарушением является рак.
10. Способ по п. 9, в котором рак выбирается из группы, состоящей из множественной миеломы, острого миелоидного лейкоза (ОМЛ), хронического миелоидного лейкоза (ХМЛ), рака предстательной железы, рака молочной железы, рака яичников, меланомы, мультиформной глиобластомы, гигантоклеточной опухоли кости, немелкоклеточного рака легких, гигантоклеточной опухоли сухожильной оболочки, метастазирования опухолей в другие ткани, миелофиброза, пигментированного виллонодулярного синовита или желудочно-кишечной стромальной опухоли.
| US 20130274255 A1, 17.10.2013 | |||
| US 20130072457 A1, 21.03.2013 | |||
| US 20080287475 A1, 20.11.2008 | |||
| СОЕДИНЕНИЯ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В ФАРМАЦЕВТИКЕ | 2006 |
|
RU2425677C2 |
| ЗАМЕЩЕННЫЕ N-(1H-ИНДАЗОЛ-4-ИЛ) ИМИДАЗОЛ [1,2-А]ПИРИДИН-3- КАРБОКСАМИДНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕЦЕПТОРНОЙ ТИРОЗИНКИНАЗЫ III ТИПА | 2011 |
|
RU2591195C2 |
Авторы
Даты
2025-01-13—Публикация
2020-08-22—Подача