ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретение относится к соли 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (ниже в настоящем изобретении она может сокращенно обозначаться, как соединение I), ее кристаллическим формам и т. п.
УРОВЕНЬ ТЕХНИКИ
[0002]
Было предположено, что сфингозин-1-фосфат [(2S,3R,4E)-2-амино-3-гидроксиоктадека-4-енил-1-фосфорной кислоты; ниже в настоящем изобретении он может сокращенно обозначаться, как S1P] является липидом, синтезируемым внутриклеточным метаболизмом сфинголипидов или воздействием секретированной сфингозинкиназы за пределами клеток, и действует, как межклеточный медиатор и внутриклеточный вторичный медиатор.
[0003]
Известно, что из числа рецепторов S1P рецептор S1P5 (EDG-8) значительно экспрессируется в олигодендроцитах и клетках-предшественниках олигодендроцитов и показано, что при активации рецептора S1P5 промотируется индукция дифференциации клеток-предшественников олигодендроцитов в олигодендроциты (см. непатентную литературу 1 и 2). Олигодендроциты являются типом глиальных клеток, которые связываются с аксонами нервных клеток с образованием миелиновых оболочек (миелина). Поэтому соединение, обладающее агонистической активностью по отношению к рецептору S1P5, считается применимым для лечения демиелинизирующих заболеваний, таких как рассеянный склероз и нейродегенеративные заболевания, поскольку оно промотирует регенерацию миелина, который исчез (демиелинизация) из нервных клеток.
[0004]
Кроме того, известно, что рецептор S1P5 значительно экспрессируется также в природных клетках-киллерах (NK) и установлено, что миграция клеток NK индуцируется активацией рецептора S1P5 (см. непатентную литературу 3).
[0005]
Кроме того, поскольку рецептор S1P5 значительно экспрессируется в патрулирующих моноцитах, для которых известно, что они участвуют в опухолевом иммунитете, активация рецептора S1P5 может вызвать иммунную активацию опухоли (см. непатентную литературу 4 и 5).
[0006]
С другой стороны, рецептор S1P1 рецептор экспрессируется в сердечно-сосудистой системе или лимфоцитах. Известно, что соединение, обладающее агонистической активностью по отношению к рецептору S1P1, может оказывать уменьшающее количество лимфоцитов воздействие и снижать частоту сердечных сокращений.
[0007]
При этом известно, что в качестве дигидронафталина, способного связываться с рецептором S1P, соединение, описывающееся общей формулой (a):
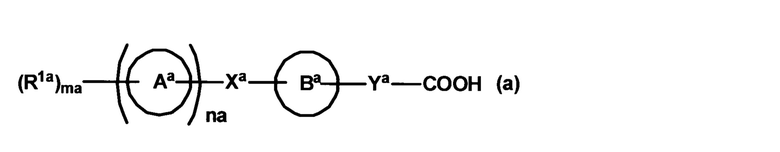
где кольцо Aa представляет собой циклическую группу, кольцо Ba представляет собой циклическую группу, необязательно дополнительно содержащую заместитель, Xa означает связь или мостик, содержащий от 1 до 8 атомов в основной цепи, Ya означает связь или мостик, содержащий от 1 до 10 атомов в основной цепи, na равно 0 или 1, если na равно 0, ma равно 1 и R1a означает атом водорода или заместитель, если na равно 1, ma означает целое число, равное 0 или от 1 до 7, и R1a означает заместитель (если ma равно 2 или более, множество R1a могут быть одинаковыми или разными) (при условии, что использовали определение каждой группы)), особенно специфически связывается с рецепторами EDG-1 (S1P1) и EDG-6 (S1P4) (см. патентную литературу 1).
[0008]
Кроме того, известно, что в качестве дигидронафталина, обладающего способностью связываться с рецептором S1P, соединение, описывающееся общей формулой (b):
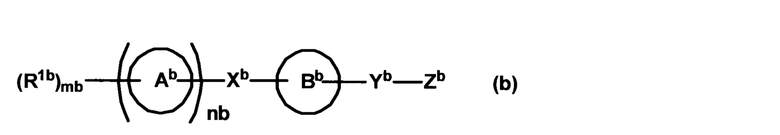
где кольцо Ab представляет собой циклическую группу, кольцо Bb представляет собой циклическую группу, необязательно дополнительно содержащую заместитель, Xb означает связь или мостик, содержащий от 1 до 8 атомов в основной цепи, Yb означает связь или мостик, содержащий от 1 до 10 атомов в основной цепи, Zb означает кислотную группу, необязательно защищенную, nb равно 0 или 1, если nb равно 0, mb равно 1 и R1b означает атом водорода или заместитель, если nb равно 1, mb означает целое число, равное 0 или от 1 до 7, и R1b означает заместитель (если mb равно 2 или более, множество R1b могут быть одинаковыми или разными) (при условии, что использовали определение каждой группы)), специфически связывается с рецепторами EDG-1 (S1P1), EDG-6 (S1P4) и/или EDG-8 (S1P5) (см. патентную литературу 2).
[0009]
Кроме того, в WO 2019/163917 A (ниже в настоящем изобретении может сокращенно обозначаться, как патентная литература 3) описано соединение I в качестве соединения, обладающего агонистической активностью по отношению к рецептору S1P5.
[0010]
Однако соль соединения I и ее кристаллические формы, раскрытые в настоящем изобретении не описаны ни в одном из документов предшествующего уровня техники.
ЛИТЕРАТУРА
Патентная литература
[0011]
Патентная литература 1: WO 2005/020882 A
Патентная литература 2: WO 2006/064757 A
Патентная литература 3: WO 2019/163917 A
Непатентная литература
[0012]
Непатентная литература 1: The Journal of Neuroscience, vol. 25, no. 6, pp. 1459-1469, 2005
Непатентная литература 2: The FASEB Journal, vol. 21, pp. 1503-1514, 2007
Непатентная литература 3: Nature Immunology, vol. 8, no. 12, pp. 1337-1344, 2007
Непатентная литература 4: European Journal of Immunology, vol. 43, pp. 1667-1675, 2013
Непатентная литература 5: Science, vol. 350, no. 6263, pp. 985-990, 2015
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКИЕ ЗАДАЧИ
[0013]
Целью настоящего изобретения является предоставление соединения, обладающего улучшенным балансом агонистической активности по отношению к рецептору S1P5 и активности по отношению к рецептору S1P1, и формы, пригодной для использования в качестве лекарственных веществ для фармацевтических препаратов.
РЕШЕНИЯ ЗАДАЧ
[0014]
В результате обширных исследований для решения указанных выше задач авторы настоящего изобретения установили, что существуют кристаллические формы соединения I, соль соединения I и кристаллические формы его солей, которые являются пригодными для использования в качестве лекарственных веществ для фармацевтических препаратов (их можно совместно обозначать, как соединение, предлагаемое в настоящем изобретении).
[0015]
Таким образом, настоящее изобретение относится, например, к следующим вариантам осуществления
[1] соль 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
[2] соль согласно [1], которая находится в кристаллической форме,
[3] кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
и т. п.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[0016]
Соединение I обладает высокой селективной по рецептору S1P5 агонистической активностью по отношению к рецептору S1P1 и поэтому применимо для лечения опосредуемых S1P5 заболеваний, например, нейродегенеративных заболеваний, аутоиммунных заболеваний, инфекционных заболеваний или рака. Кроме того, кристаллические формы соединения I, соль соединения I и кристаллические формы его солей, раскрытые в настоящем изобретении, превосходны по химической стабильности и поэтому применимы в качестве лекарственных веществ для фармацевтических препаратов.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0017]
На фиг. 1 приведена порошковая рентгенограмма кристалла D соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0018]
На фиг. 2 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла D соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0019]
На фиг. 3 приведена порошковая рентгенограмма кристалла B гидрата соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0020]
На фиг. 4 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла B гидрата соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0021]
На фиг. 5 приведена порошковая рентгенограмма кристалла A монобензоата соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0022]
На фиг. 6 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла A монобензоата соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0023]
На фиг. 7 приведена порошковая рентгенограмма кристалла A моно(4-гидроксибензоата) соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0024]
На фиг. 8 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла A моно(4-гидроксибензоата) соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0025]
На фиг. 9 приведена порошковая рентгенограмма кристалла B моно(4-гидроксибензоата) соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0026]
На фиг. 10 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла B моно(4-гидроксибензоата) соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0027]
На фиг. 11 приведена порошковая рентгенограмма кристалла C гидрата моно(4-гидроксибензоата) соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0028]
На фиг. 12 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла C гидрата моно(4-гидроксибензоата) соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0029]
На фиг. 13 приведена порошковая рентгенограмма кристалла B гемисульфата соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0030]
На фиг. 14 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла B гемисульфата соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0031]
На фиг. 15 приведена порошковая рентгенограмма кристалла A моно-триптофаната соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0032]
На фиг. 16 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла A моно-триптофаната соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0033]
На фиг. 17 приведена порошковая рентгенограмма кристалла A гемисукцината соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0034]
На фиг. 18 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла A гемисукцината соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0035]
На фиг. 19 приведена порошковая рентгенограмма кристалла B гемиадипата соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0036]
На фиг. 20 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла B гемиадипата соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0037]
На фиг. 21 приведена термограмма термогравиметрии (TG) кристалла B гидрата соединения I (по вертикальной оси отложена масса (%) и по горизонтальной оси отложена температура (°C)).
[0038]
На фиг. 22 приведена термограмма термогравиметрии (TG) кристалла C гидрата моно(4-гидроксибензоата) соединения I (по вертикальной оси отложена масса (%) и по горизонтальной оси отложена температура (°C)).
[0039]
На фиг. 23 приведена порошковая рентгенограмма кристалла A соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0040]
На фиг. 24 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла A соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0041]
На фиг. 25 приведена порошковая рентгенограмма кристалла D геми(4-гидроксибензоата) соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0042]
На фиг. 26 приведена порошковая рентгенограмма кристалла E моно(4-гидроксибензоата) соединения I (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0043]
На фиг. 27 приведена термограмма дифференциальной сканирующей калориметрии (DSC) кристалла E моно(4-гидроксибензоата) соединения I (по вертикальной оси отложен тепловой поток (Вт/г) и по горизонтальной оси отложена температура (°C)).
[0044]
На фиг. 28 приведена рассчитанная порошковая рентгенограмма (условия 1) гидрата совместного кристалла соединения I и 4-гидроксибензойной кислоты (кристалл I) (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
[0045]
На фиг. 29 приведена рассчитанная порошковая рентгенограмма (условия 2) гидрата совместного кристалла соединения I и 4-гидроксибензойной кислоты (кристалл I) (по вертикальной оси отложена интенсивность (импульсы) и по горизонтальной оси отложены 2θ (градусы)).
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0046]
Ниже настоящее изобретение описано подробно.
В настоящем изобретении 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновая кислота (соединение I) означает соединение, описывающееся следующей структурной формулой:
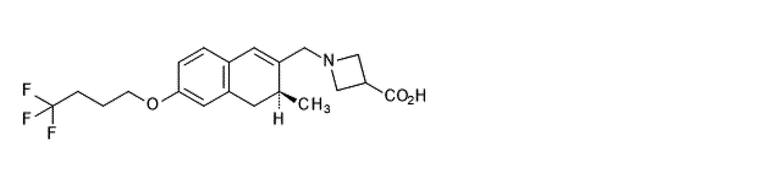
где символ

показывает, что образуется связь с обратной стороны поверхности бумаги (т. е. α-конфигурацию) и символ

показывает, что образуется связь с передней стороны поверхности бумаги (т. е. β-конфигурацию).
[0047]
В настоящем изобретении соединением, предлагаемым в настоящем изобретении, предпочтительно является:
кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
моно(4-гидроксибензоат) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
моно(4-гидроксибензоат) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
моно-триптофанат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
моно-триптофанат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
гемисукцинат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, или
гемисукцинат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
более предпочтительно,
кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
моно(4-гидроксибензоат) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
моно-триптофанат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
или
гемисукцинат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме,
более предпочтительно,
кристалл D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
кристалл A моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
кристалл B моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
кристалл A моно-триптофаната 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
или
кристалл A гемисукцината 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты и
особенно предпочтительно,
кристалл A моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты.
[0048]
В настоящем изобретении в качестве соединения, предлагаемого в настоящем изобретении,
кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным и
кристалл D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты является более предпочтительным.
[0049]
В настоящем изобретении в качестве соединения, предлагаемого в настоящем изобретении,
моно(4-гидроксибензоат) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным,
моно(4-гидроксибензоат) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме является более предпочтительным,
кристалл A моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты или
кристалл B моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным и
кристалл A моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты является особенно предпочтительным.
[0050]
В настоящем изобретении в качестве соединения, предлагаемого в настоящем изобретении,
моно-триптофанат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным,
моно-триптофанат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме является более предпочтительным и
кристалл A моно-триптофаната 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным.
[0051]
В настоящем изобретении в качестве соединения, предлагаемого в настоящем изобретении,
гемисукцинат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным,
гемисукцинат 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты в кристаллической форме является более предпочтительным и
кристалл A гемисукцината 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты также является предпочтительным.
[0052]
В настоящем изобретении соединением, предлагаемым в настоящем изобретении, предпочтительно является превосходное по химической стабильности. Соединением более предпочтительно является соединение, обладающее остаточным содержанием (%), равным 95% или более, более предпочтительно соединение, обладающее остаточным содержанием (%), равным 99% или более и особенно предпочтительно соединение, обладающее остаточным содержанием (%), равным 99% или более при условиях 1 или условиях 2, определенным по методике, описанной в исследовании химической стабильности, представленном ниже.
[0053]
В настоящем изобретении различия в кристаллической форме устанавливаются с помощью порошковой рентгенограммы, дифференциальной сканирующей калориметрии (DSC), кристаллографических данных и/или позиционных параметров (парциальных атомных координат).
[0054]
Кристалл D соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (a) и (b). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (a) и (b).
[0055]
(a) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 1, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 1, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 1, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 1, (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 11,6, примерно 15,2, примерно 17,0, примерно 18,8, примерно 21,1, примерно 22,8, примерно 23,3 и примерно 24,9 градуса, или (vi) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 6,5, примерно 7,8, примерно 8,6, примерно 11,6, примерно 15,2, примерно 17,0, примерно 18,8, примерно 21,1, примерно 22,8, примерно 23,3 и примерно 24,9 градуса.
[0056]
(b) Обладает термограммой DSC, приведенной на фиг. 2, или эндотермическим пиком с температурой начала, равной примерно 128°C, или температурой пика, равной примерно 133°C, на термограмме DSC.
[0057]
Кристалл B гидрата соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (c) и (d). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (c) и (d).
[0058]
(c) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 3, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 3, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 2, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 2, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 10,3, примерно 14,9, примерно 17,9, примерно 18,1, примерно 18,6, примерно 22,6, примерно 23,4 и примерно 24,4 градуса.
[0059]
(d) Обладает термограммой DSC, приведенной на фиг. 4, или (i) эндотермическим пиком с температурой начала, равной примерно 80°C, или температурой пика, равной примерно 97°C, и/или (ii) эндотермическим пиком с температурой начала, равной примерно 110°C, или температурой пика, равной примерно 112°C, на термограмме DSC.
[0060]
Кристалл A монобензоата соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (e) и (f). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (e) и (f).
[0061]
(e) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 5, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 5, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 3, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 3, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 11,5, примерно 17,1, примерно 18,0, примерно 18,4, примерно 19,3, примерно 20,4, примерно 21,9, примерно 22,1 и примерно 24,1 градуса.
[0062]
(f) Обладает термограммой DSC, приведенной на фиг. 6, или эндотермическим пиком с температурой начала, равной примерно 137°C, или температурой пика, равной примерно 139°C, на термограмме DSC.
[0063]
Кристалл A моно(4-гидроксибензоата) соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (g) и (h). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (g) и (h).
[0064]
(g) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 7, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 7, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 4, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 4, (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 5,4, примерно 6,9, примерно 13,9, примерно 18,1, примерно 19,4, примерно 19,8, примерно 20,9 и примерно 24,7 градуса, или (vi) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 5,4, примерно 6,9, примерно 12,8, примерно 13,9, примерно 18,1, примерно 19,4, примерно 19,8, примерно 20,9 и примерно 24,7 градуса.
[0065]
(h) Обладает термограммой DSC, приведенной на фиг. 8, или эндотермическим пиком с температурой начала, равной примерно 150°C, или температурой пика, равной примерно 153°C, на термограмме DSC.
[0066]
Кристалл B моно(4-гидроксибензоата) соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (k) и (l). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (k) и (l).
[0067]
(k) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 9, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 9, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 5, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 5, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 5,6, примерно 11,3, примерно 13,2, примерно 15,9, примерно 16,9, примерно 18,8, примерно 22,7 и примерно 24,2 градуса.
[0068]
(l) Обладает термограммой DSC, приведенной на фиг. 10, или эндотермическим пиком с температурой начала, равной примерно 154°C, или температурой пика, равной примерно 158°C, на термограмме DSC.
[0069]
Кристалл C гидрата моно(4-гидроксибензоата) соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (m) и (n). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (m) и (n).
[0070]
(m) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 11, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 11, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 6, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 6, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 12,3, примерно 14,4, примерно 15,0, примерно 16,0, примерно 16,7, примерно 20,3, примерно 23,9 и примерно 24,8 градуса.
[0071]
(n) Обладает термограммой DSC, приведенной на фиг. 12, или (i) эндотермическим пиком с температурой начала, равной примерно 78°C, или температурой пика, равной примерно 93°C, (ii) эндотермическим пиком с температурой начала, равной примерно 105°C, или температурой пика, равной примерно 114°C, (iii) эндотермическим пиком с температурой начала, равной примерно 152°C, или температурой пика, равной примерно 155°C, (iv) экзотермическим пиком с температурой начала, равной примерно 114°C, или температурой пика, равной примерно 120°C, и/или (v) экзотермическим пиком с температурой начала, равной примерно 159°C, или температурой пика, равной примерно 165°C, на термограмме DSC.
[0072]
Кристалл B гемисульфата соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (o) и (p). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (o) и (p).
[0073]
(o) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 13, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 13, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 7, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 7, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 5,7, примерно 15,1, примерно 16,7, примерно 17,3, примерно 18,9, примерно 21,0, примерно 21,5 и примерно 23,1 градуса.
[0074]
(p) Обладает термограммой DSC, приведенной на фиг. 14, или эндотермическим пиком с температурой начала, равной примерно 161°C, или температурой пика, равной примерно 166°C, на термограмме DSC.
[0075]
Кристалл A моно-триптофаната соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (q) и (r). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (q) и (r).
[0076]
(q) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 15, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 15, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 8, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 8, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 8,0, примерно 9,7, примерно 16,0, примерно 17,0, примерно 18,9, примерно 19,1, примерно 22,2 и примерно 24,6 градуса.
[0077]
(r) Обладает термограммой DSC, приведенной на фиг. 16, или (i) эндотермическим пиком с температурой начала, равной примерно 178°C, или температурой пика, равной примерно 183°C и/или (ii) экзотермическим пиком с температурой начала, равной примерно 185°C, или температурой пика, равной примерно 187°C, на термограмме DSC.
[0078]
Кристалл A гемисукцината соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (s) и (t). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (s) и (t).
[0079]
(s) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 17, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 17, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 9, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 9, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 6,4, примерно 6,9, примерно 12,9, примерно 13,8, примерно 17,2, примерно 18,1, примерно 19,3, примерно 23,9 и примерно 24,3 градуса.
[0080]
(t) Обладает термограммой DSC, приведенной на фиг. 18, или (i) эндотермическим пиком с температурой начала, равной примерно 111°C, или температурой пика, равной примерно 114°C, и/или (ii) эндотермическим пиком с температурой начала, равной примерно 137°C, или температурой пика, равной примерно 140°C, на термограмме DSC.
[0081]
Кристалл B гемиадипата соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (u) и (w). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (u) и (w).
[0082]
(u) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 19, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 19, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 10, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 10, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 7,0, примерно 8,6, примерно 10,8, примерно 15,9, примерно 17,4, примерно 18,6 и примерно 24,2 градуса.
[0083]
(w) Обладает термограммой DSC, приведенной на фиг. 20, или эндотермическим пиком с температурой начала, равной примерно 123°C, или температурой пика, равной примерно 125°C, на термограмме DSC.
[0084]
Кристалл A соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (aa) и (bb). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (aa) и (bb).
[0085]
(aa) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 23, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 23, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 14, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 14, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 15,9, примерно 17,0, примерно 19,3, примерно 20,1, примерно 20,6, примерно 22,8 и примерно 28,4 градуса.
[0086]
(bb) Обладает термограммой DSC, приведенной на фиг. 24, или (i) широким эндотермическим пиком от температуры начала, равной примерно 53°C, до температуры конца, равной примерно 87°C и/или (ii) эндотермическим пиком с температурой начала, равной примерно 108°C, или температурой пика, равной примерно 111°C, на термограмме DSC.
[0087]
Кристалл D геми(4-гидроксибензоата) соединения I характеризуется физико-химическими характеристиками следующего (cc).
[0088]
(cc) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 25, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 25, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 15, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 15, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 8,1, примерно 10,8, примерно 13,5, примерно 16,1, примерно 19,8, примерно 22,5, примерно 23,5 и примерно 25,6 градуса.
[0089]
Кристалл E моно(4-гидроксибензоата) соединения I характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (dd) и (ee). Предпочтительно, характеризуется физико-химическими характеристиками обоих следующих пунктов (dd) и (ee).
[0090]
(dd) Обладает (i) порошковой рентгенограммой, приведенной на фиг. 26, (ii) углом дифракции (2θ) на порошковой рентгенограмме, приведенным на фиг. 26, (iii) порошковой рентгенограммой, обладающей углом дифракции (2θ) в основном таким, как угол дифракции (2θ), приведенный в таблице 16, (iv) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из в основном такого же угла дифракции (2θ), как угол дифракции (2θ), приведенный в таблице 16, или (v) порошковой рентгенограммой, содержащей по меньшей мере один, два, три, четыре, пять или более пяти пиков при угле дифракции (2θ), выбранном из следующих: примерно 8,9, примерно 12,5, примерно 15,3, примерно 16,5, примерно 17,5, примерно 20,4 и примерно 22,1 градуса.
[0091]
(ee) Обладает термограммой DSC, приведенной на фиг. 27, или (i) эндотермическим пиком с температурой начала, равной примерно 104°C, или температурой пика, равной примерно 113°C, (ii) эндотермическим пиком с температурой начала, равной примерно 147°C, или температурой пика, равной примерно 153°C, на термограмме DSC и/или (iii) экзотермическим пиком с температурой начала, равной примерно 117°C, или температурой пика, равной примерно 121°C, на термограмме DSC.
[0092]
Гидрат совместного кристалла соединения I и 4-гидроксибензойной кислоты (кристалл I) характеризуется физико-химическими характеристиками по меньшей мере одного из следующих пунктов (ff), (gg), (hh), (kk), (мм) и (nn). Предпочтительно, характеризуется по меньшей мере двумя физико-химическими характеристиками из следующих пунктов (ff), (gg), (hh), (kk), (мм) и (nn).
[0093]
(ff) Обладает (i) рассчитанной порошковой рентгенограммой, приведенной на фиг. 28 и (ii) углом дифракции (2θ) на рассчитанной порошковой рентгенограмме, приведенным на фиг. 28.
[0094]
(gg) Обладает (i) рассчитанной порошковой рентгенограммой, приведенной на фиг. 29 и (ii) углом дифракции (2θ) на рассчитанной порошковой рентгенограмме, приведенным на фиг. 29.
[0095]
(hh) Обладает кристаллографическими характеристиками, эквивалентными следующим.
Постоянная решетки: a=6,1374 (2) Å
b=12,8245 (3) Å
c=17,8596 (5) Å
α=72,297 (2)°
β=85,002 (3)°
γ=79,591 (3)°
V=1316,35 (7)Å3
Пространственная группа: P1 (#1)
Фактор R: 0,0475
Значение параметра Флэка: -0,04 (7)
[0096]
(kk) Обладает кристаллографическими характеристиками, эквивалентными следующим.
Постоянная решетки: a=6,1599 (2) Å
b=12,9850 (6) Å
c=18,1997 (10) Å
α=71,547 (5)°
β=86,306 (4)°
γ=80,124 (4)°
V=1360,33 (12) Å3
Пространственная группа: P1 (#1)
Фактор R: 0,0760
Значение параметра Флэка: 0,09 (14)
[0097]
(мм) Обладает позиционными параметрами (парциальными атомными координатами), приведенными в таблице 17.
[0098]
(nn) Обладает позиционными параметрами (парциальными атомными координатами), приведенными в таблице 18.
[0099]
В настоящем изобретении каждая кристаллическая форма соединения I обладает физико-химическими характеристиками, описанными в настоящем описании, но все спектральные характеристики могут немного меняться вследствие своей природы, так что их невозможно точно понять. Например, в данных порошковой рентгенограммы вследствие их природы угол дифракции (2θ) и общий вид важны для определения идентичности кристалла и относительная интенсивность может немного меняться в зависимости от направления роста кристалла, размера частицы и условий измерения. Кроме того, для данных DSC общий вид важен для определения идентичности кристалла и он может немного меняться в зависимости от условий измерения. Поэтому в число соединений, предлагаемых в настоящем изобретении, включено соединение, обладающее в целом сходной картиной порошковой рентгенограммы или диаграммой DSC.
[0100]
В настоящем изобретении описание угла дифракции (2θ (градусы)) на порошковой рентгенограмме и температуры начала (°C) и температуры пика (°C) эндотермического пика при анализе DSC означает, что означает, что включен диапазон погрешностей, обычно допустимый в методике измерения значений, и учтен в приближенном значении угла дифракции и температуры начала, и температуры пика эндотермического пика. Например, "примерно" для угла дифракции (2θ (градусы)) на порошковой рентгенограмме означает ± 0,2 градуса в одном варианте осуществления и ± 0,1 градуса в еще одном варианте осуществления. "Примерно" для температуры начала (°C) или температуры пика (°C) эндотермического пика при анализе DSC означает ± 2°C в одном варианте осуществления и ± 1°C в еще одном варианте осуществления.
[0101]
В одном варианте осуществления настоящего изобретения каждая кристаллическая форма соединения I является в основном чистой. Указание, что она является "в основном чистой" означает, что конкретная кристаллическая форма составляет по меньшей мере 50% содержащегося соединения I. Кроме того, в другом варианте осуществления каждая кристаллическая форма составляет по меньшей мере 75%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или примерно от 94% до 98% содержащегося соединения I.
[0102]
В одном варианте осуществления настоящего изобретения кристаллом соединения I является кристалл свободной формы соединения I.
В настоящем изобретении кристаллом свободной формы является кристалл, состоящий из одного компонента.
[0103]
В настоящем изобретении примеры кристалла гидрата соединения I и/или кристалла гидрата моно(4-гидроксибензоата) соединения I включают от 0,5 гидрата до 5 гидрата. В одном варианте осуществления настоящего изобретения гидрат представляет собой 0,5 гидрат, 1 гидрат, 1,5 гидрата, 2 гидрата или 2,5 гидрата. В одном варианте осуществления настоящего изобретения гидрат представляет собой от 0,5 гидрата до 1,0 гидрата и в некоторых вариантах осуществления гидрат представляет собой 0,5, 0,6, 0,7, 0,8, 0,9 или 1 гидрат.
[0104]
В настоящем изобретении на гидрат не налагаются особые ограничения, если он является кристаллом, который стабильно удерживает существенное количество воды в условиях окружающей среды (температура, относительная влажность и т. п.), в которых обычно хранят и используют лекарственное средство. Например, в настоящем изобретении моногидрат является кристаллом, который стабильно удерживает 1 экв. воды в условиях окружающей среды (температура, относительная влажность и т. п.), в которых обычно хранят и используют лекарственное средство.
[0105]
В обозначении названия соединения дефис (-) между соединением I и 4-гидроксибензойной кислотой может обозначаться длинным тире или двойным дефисом (--).
[0106]
В настоящем изобретении соединение, предлагаемое в настоящем изобретении, можно получить, например, по следующей методике, по эквивалентной ей методике или по методике, описанной в примерах. При перекристаллизации можно использовать или не использовать затравочный кристалл.
[0107]
В настоящем изобретении то, что описано, как соль может представлять собой совместный кристалл.
[0108]
[Токсичность]
Соединение, предлагаемое в настоящем изобретении, обладает достаточно никой токсичностью и его можно безопасно использовать в качестве лекарственного средства.
[0109]
[Применение для фармацевтических препаратов]
Соединение, предлагаемое в настоящем изобретении, применимо для лечения и/или предупреждения опосредуемых S1P5 заболеваний.
[0110]
Соединение, предлагаемое в настоящем изобретении, можно использовать для лечения и/или предупреждения опосредуемых S1P5 заболеваний. Примеры таких заболеваний включают нейродегенеративное заболевание, аутоиммунное заболевание, инфекцию, рак и т. п.
[0111]
Примеры нейродегенеративного заболевания включают связанные с состоянием тревоги заболевания (например, состояние социальной тревоги, невроз тревоги, обсессивно-компульсивное нарушение, посттравматическое стрессовое нарушение (PTSD) и т. п.), полиглутаминовую болезнь, пигментную дегенерацию сетчатки, невроз, судороги, паническое расстройство, нарушение сна, депрессию, реактивную депрессию, эпилепсию, болезнь Паркинсона, синдром паркинсонизма, синдром Дауна, шизофрению, аутономную атаксию, болезнь Гентингтона, слабоумие типа Альцгеймера, аффективное расстройство (включая депрессивное или биполярное расстройство), нарушения познавательной способности, мигрень, головную боль напряжения, сильную приступообразную головную боль с периодическими рецидивами, диссоциативное расстройство, боковой амиотрофический склероз, нейромиелит зрительного нерва, неврит зрительного нерва, острый рассеянный энцефаломиелит, алларгический энцефаломиелит, болезнь Маркиафавы-Микели, болезнь Бинсвангера, погрессирующую мультифокальную лейкоэнцефалопатию, постинфекцонный энцефалит, центральный понтинный миелинолиз, адренолейкодистрофию, мультисистемную атрофию, болезнь Краббе, метахроматическую лейкодистрофую, болезнь Александера, болезнь Канавана, синдром Коккейна, болезнь Пелицеуса-Мерцбахера, синдром Гурлер, синдром Хантера, болезнь Помпе, болезнь Фабри, болезнь Фарбера, ганглиозидоз типа I, синдром Лоу, повреждение спинного мозга, поперечный миелит, спиноцеребеллярную дегенерацию, хроническую воспалительную демиелинизирующую полирадикулоневропатию (CIDP), синдром Гийена-Барре, фенилкетонурию, болезнь Рефсума, болезнь Шарко-Мари-Тута, болезнь Гоше, болезнь Ниманна-Пика, болезнь Тея-Сакса, болезнь Сандхоффа, рассеянный склероз, синдром ломкой X-хромосомы, аутизм, инсомнию, нервный кашель, психогенный судорожный приступ, психогенный синкопальный приступ, писчий спазм, спастическую кривошею, невропатию, нейродегенерацию с накоплением железа в головном мозге, слабоумие с тельцами Леви и т. п.
[0112]
Примеры аутоиммунного заболевания включают воспалительную болезнь кишечника, артрит, волчанку, ревматизм, псориатический артрит, остеоартрит, болезнь Стилла, ювенильный артрит, сахарный диабет типа 1, злокачественную миастению, тиреоидит Хашимото, тиреоидит при недостатке йода, базедову болезнь, синдром Шегрена, болезнь Аддисона, синдром опсоклонус-миоклонус, анкилозирующий спондилит, антифосфолипидный синдром, апластическую анемию, аутоиммунный гепатит, целиакию, синдром Гудпасчера, идиопатическую тромбоцитопеническую пурпуру, склеродермию, первичный билиарный цирроз, болезнь Рейтера, синдром Такаясу, височный артериит, тепловую аутоиммунную гемолитическую анемию, гранулематоз Вегенера, псориаз, генерализованную алопецию, болезнь Бехчета, синдром хронической усталости, автономную невропатию, эндометриоз, интерстициальный цистит, миотонию, вульводинию, системную красную волчанку и т. п.
[0113]
Примеры инфекции включают смптомы, которые развиваются при инфекции нормальной клетки in vivo одним или большим количеством типов патогенных микроорганизмов, примерами которых являются вирусы, бактерии, грибы и т. п. и пролиферацию патогенных микроорганизмов и т. п. Описанные выше патогенные микроорганизмы также включают Rickettsia, Chlamydia, простейшие, паразиты и т. п.
[0114]
Примеры вирусов, которые вызывают инфекции, включают вирусы гепатита человека (например, вирус гепатита B, вирус гепатита C, вирус гепатита A и вирус гепатита E и т. п.), ретровирусы человека, вирусы иммунодефицита человека (например, HIV1 и HIV2 и т. п.), вирусы T-клеточного лейкоза человека или Т-лимфотропные вирусы человека (например, HTLV1 и HTLV2 и т. п.), вирус простого герпеса типа 1 или типа 2, вирус Эпштейна-Барра (EB), цитомегаловирус, вирус ветряной оспы, вирусы герпеса человека (например, вирус герпеса человека 6 и т. п.), полиовирус, вирус кори, вирус краснухи, вирус японского энцефалита, вирус свинки, вирус гриппа, вирусы простуды (например, аденовирус, энтеровирус, риновирус и т. п.), вирус, который вызывает тяжелый острый респираторный синдром (SARS), вирус Эбола, вирус Западного Нила, флавивирус, ЕСНО-вирус, вирус коксаки, коронавирус, респираторно-синцитиальный вирус, ротавирус, норовирус, саповирус, парвовирус, вирус вакцины, вирус HTL, вирус денге, вирус папилломы, вирус контагиозного моллюска, вирус бешенства, вирус JC, арбовирус, вирус энцефалита, хантавирус, вирус Эбола и т. п.
[0115]
Примеры бактерий, которые вызывают инфекцию, включают Vibrio cholerae, Salmonella enterica, Escherichia coli, Legionella, Bacillus anthracis, Helicobacter pylori, Listeria monocytogenes, Mycobacterium tuberculosis, нетуберкулезные микобактерии, Staphylococcus, Streptococcus, Streptococcus pneumoniae, Neisseria meningitidis, Klebsiella pneumoniae, Serratia, Corynebacterium diphtheriae, Brucella, Bartonella henselae, Erysipelothrix rhusiopathiae, Actinomyces, Borrelia burgdorferi, Clostridium perfringens, Shigella dysenteriae, Yersinia pestis, Clostridium tetani, Enterobacter и т. п.
[0116]
Примеры грибов, которые вызывают инфекцию, включают Candida, Aspergillus, Cryptococcus, Blastomyces, Coccidioides, Histoplasma, Paracoccidioides, Sporothrix и т. п.
[0117]
Примеры постейших, которые вызывают инфекцию, включают Plasmodium, Toxoplasma gondii и т. п.
[0118]
Примеры паразитов, которые вызывают инфекцию, включают Entamoeba histolytica, Ascaris lumbricoides, Babesia, Cryptosporidium, Giardia lamblia, Ancylostoma, Enterobius vermicularis, Schistosoma, Cestoda, Trichinella spiralis, Trichuris trichiura и т. п.
[0119]
Примеры других микроорганизмов, которые вызывают инфекцию, включают Mycoplasma, Spirochaeta и т. п.
Рак включает все злокачественные опухоли и их примеры включают раковые заболевания, связанные с черепно-мозговым нервом (например, педиатрические опухоли головного мозга (например, нейробластома, медуллобластома, астроцитома (ювенильная пилоцитарная астроцитома), эпендимому, краниофарингиому, герминомы, глиому зрительного нерва, папиллому хориоидного сплетения и глиому ствола головного мозга), опухоли головного мозга взрослых (например, астроцитома взрослых, злокачественная астроцитома взрослых, глиобластома взрослых, эпендимома взрослых, злокачественная эпендимома взрослых, злокачественная олигодендроглиома взрослых, медуллобластома взрослых, менингиома взрослых и злокачественная менингиома взрослых), глиому (например, астроцитома, олигодендроглиома, эпендимома и глиома ствола головного мозга), аденому гипофиза, шванному слухового нерва, ретинобластома, увеальную злокачественную меланому и т. п.), раковые заболевания дыхательных путей (например, раковые заболевания глотки (например, рак носоглотки, ротоглоточный рак и гипофарингеальный рак), рак гортани, рак придаточной полости носа, раковые заболевания легких (например, мелкоклеточный рак и немелкоклеточный рак), тимома, мезотелиома и т. п.), желудочно-кишечные раковые заболевания (например, рак пищевода, рак желудка, дуоденальный рак, колоректальные раковые заболевания (например, рак толстой кишки, рак прямой кишки и рак анального канала) и т. п.), раковые заболевания полости рта (например, рак десны, рак языка, рак слюнной железы и т. п.), раковые заболевания мочевой системы (например, рак пениса, рак почечной лоханки, почечноклеточный рак, тестикулярная опухоль, рак предстательной железы, рак мочевого пузыря и т. п.), раковые заболевания, которые поражают женщин (рак вульвы, раковые заболевания матки (например, рак шейки матки и рак эндометрия), саркома матки, трофобластные заболевания (например, хорионаденома, хориокарцинома, трофобластическая болезнь плацентарной площадки и стойкая трофобластическая болезнь), рак влагалища, рак молочной железы, саркома молочной железы, рак яичников, герминома яичников и т. п.), раковые заболевания кожи (например, меланома (злокачественная меланома) (например, злокачественная лентигиозная меланома, меланома с поверхностным распространением, нодулярная меланома, акральная лентигиозная меланома и эрозивная меланома), грибовидный микоз, плоскоклеточная карцинома, базально-клеточная карцинома, продромальные признаки рака кожи, внутриэпидермальная карцинома (например, актиничный кератоз, болезнь Боуэна и болезнь Педжета), лимфоматоидный папулез, кожная CD30 положительная анапластическая крупноклеточная лимфома, синдром Сезари, кожная B-клеточная лимфома и т. п.), раковые заболевания кости и мышц (например, остеосаркома, саркома мягкой ткани, рабдомиосаркома, синовиальная саркома, липосаркома и т. п.), рак щитовидной железы, карциноид, рак печени (гепатома), гептобластома, рак желчных протоков, рак желчного пузыря, рак поджелудочной железы, эндокринные опухоли поджелудочной железы (например, инсулинома, гастринома, VIPomar и т. п.), карцинома неизвестной первичной локализации, наследственные опухоли семейные опухоли (например, наследственный неполипозный колоректальный рак, семейный аденоматозный полипоз, наследственный рак молочной железы, синдром рака яичников, синдром Ли-Фраумени, наследственная меланома, опухоль Вильмса, наследственная папиллярная почечноклеточная карцинома, синдром фон Гиппеля-Линдау, полиэндокринная неоплазия и т. п.), лейкоз (например, острый миелолейкоз, острый лимфобластный лейкоз, миелодиспластический синдром, хронический миелолейкоз·хроническое миелопролиферативное нарушение, T-клеточный лейкоз взрослых-лимфома, хронический лимфолейкоз, В-клеточная лимфома и т. п.), множественная миелома, первичная макроглобулинемия, злокачественная лимфома (например, ходжкинская лимфома, неходжкинская лимфома (промежуточные и высокодифференцированные лимфомы, лимфома Беркитта, лимфобластная лимфома, фолликулярная лимфома, лимфома из клеток мантии, MALT (лимфоидная ткань, связанная со слизистой оболочкой) лимфома, NK (природный киллер) лимфома и т. п.)) и т. п.
[0120]
Соединение, предлагаемой в настоящем изобретении, предпочтительно применимо для лечения и/или предупреждения нейродегенеративных заболеваний.
[0121]
Соединение, предлагаемое в настоящем изобретении, более предпочтительно применимо для лечения и/или предупреждения мультисистемной атрофии или болезни Паркинсона.
[0122]
Соединение, предлагаемое в настоящем изобретении, можно вводить в виде объединенного лекарственного средства в комбинации с другим лекарственным средством для:
1) дополнения и/или усиления профилактического и/или терапевтического эффекта соединения,
2) улучшения динамики и всасывания соединения, снижения дозы и/или
3) уменьшения побочных эффектов соединения.
[0123]
Объединенное лекарственное средство из соединения, предлагаемого в настоящем изобретении, и другого лекарственного средства можно вводить в виде объединенного средства, содержащего оба компонента в одном препарате, или можно вводить в виде отдельных препаратов. При введении в виде отдельных препаратов включены одновременное введение и поочередное введение. Кроме того, при поочередном введении соединение, предлагаемое в настоящем изобретении, можно вводить первым и другое лекарственное средство можно вводить позже или другое лекарственное средство можно вводить первым и соединение, предлагаемое в настоящем изобретении, можно вводить позже. Методики введения могут быть одинаковыми или разными.
[0124]
На заболевание, на которое оказывает профилактическое и/или терапевтическое воздействие объединенное лекарственное средство, не налагаются особые ограничения и можно лечить любое заболевание, на которое соединение, предлагаемое в настоящем изобретении, оказывает дополнительное и/или усиленное профилактическое и/или терапевтическое воздействие.
[0125]
Кроме того, объединенное лекарственное средство, объединенное с соединением, предлагаемым в настоящем изобретении, включает не только обнаруженные ранее средства, но и те средства, которые будут обнаружены в будущем.
[0126]
Примеры другого лекарственного средства для дополнения и/или усиления профилактического и/или терапевтического воздействия соединения, предлагаемого в настоящем изобретении, на нейродегенеративное заболевание включают ингибиторы ацетилхолинэстеразы, модуляторы никотинового рецептора, супрессоры выработки, секреции, накопления, агглютинации и/или осаждения β-амилоидного белка (например, ингибитор β-секретазы, ингибитор γ-секретазы, лекарственное средство, оказывающее ингибирующее воздействие на агглютинацию β-амилоидного белка, β-амилоидная вакцина, фермент, разрушающий β-амилоид и т. п.), активаторы функции головного мозга (например, активатор метаболизма головного мозга, лекарственное средство, улучшающее мозговое кровообращение и т. п.), агонисты допаминового рецептора (стимуляторы допаминового рецептора), лекарственные средства, ускоряющие высвобождения допамина (лекарственные средства, ускоряющие секрецию допамина или лекарственные средства, ускоряющие высвобождения допамина), ингибиторы потребления допамина, агонисты допамина, антагонисты допамина, карбонат лития, серотонинергические агонисты, антагонисты серотонина (например, антагонист 5-HT2A, антагонист 5-HT3, антагонист 5-HT4, антагонист 5-HT7 и т. п.), ингибиторы моноаминоксидазы (MAO), ингибиторы декарбоксилазы ароматической L-аминокислоты (DCI), добавки норэпинефрина (норадреналина), антихолинергические лекарственные средства, ингибиторы пирокатехин-O-метилтрансферазы (COMT), трапевтические лекарственные средства для бокового амиотрофическиого склероза, трапевтические лекарственные средства для гиперлипидемии, ингибиторы апоптоза, лекарственные средства, ускоряющие дифференциацию регенерации нервов, гипотензивные лекарственные средства, трапевтические лекарственные средства для диабета, трапевтические лекарственные средства для осложнения при диабете, антидепрессанты (например, трициклический антидепрессант, тетрациклический антидепрессант и т. п.), лекарственные средства для борьбы с состоянием тревоги, противоэпилептические лекарственные средства, противосудорожные лекарственные средства, антиспазматические лекарственные средства, нестероизные противовоспалительные лекарственные средства, противоцитокиновые лекарственные средства (например, ингибитор TNF, ингибитор MAP киназы и т. п.), стероиды, пловые гормоны или их производные (например, прогестерон, эстрадиол, эстрадиол бензоат и т. п.), тиреоидные гормоны, паратиреоидные гормоны (например, PTH и т. п.), блокаторы кальциевых каналов (антагонисты кальция), антагонисты кальциевого рецептора, агонисты опиоидного рецептора, антагонисты N-метил-D-2-амино-5-D-аспартатного (NMDA) рецептора, агонисты VR-1 рецептора, лекарственные средства, блокирующие нервно-мышечное соединение, агонисты каннабиноидного-2 рецептора, модуляторы GABAA рецептора (например, агонист GABAA рецептора и т. п.), модуляторы GABAB рецептора, простагландины, антагонисты холецистокинина, ингибиторы синтазы оксида азота (NOS), местные анестетики, нейротрофические факторы (например, нейротрофин, надсемейство TGF-β, семейство нейрокина, фактор роста и т. п.), симпатомиметические лекарственные средства, парасимпатомиметические лекарственные средства, симпатолитические лекарственные средства, антагонисты простагландинового рецептора, агонисты простагландинового рецептора, ингибиторы карбоангидразы, гиперосмотические лекарственные средства, сосудорасширяющие лекарственные средства, метаболические активаторы, диуретические лекарственные средства (например, тиазидное диуретические лекарственное средство, петлевое диуретическое лекарственное средство, калийсберегающие диуретическое лекарственное средство и т. п.), лекарственные средства, улучшающе периферический кровоток, иммуносупрессорные лекарственные средства (например, диметилфумарат, глатирамерацетат, интерферон бета-1a, интерферон бета-1b, финголимод), иммуноглобулины, антагонисты рецептора α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты (AMPA)/каиновой кислоты, ингибиторы Rho-киназы, витамины (например, витамин B6, витамин B12 и т. п.), ингибиторы циклооксигеназы (COX)-2, лекарственные средства против головокружения, трапевтические лекарственные средства для анемии, трапевтические лекарственные средства для отравления тяжелым металлом, агонисты мускаринового рецептора, ингибиторы альдозоредуктазы, лекарственные средства, ускоряющие регенерацию нервов, ингибиторы протеинкиназы C (PKC), ингибиторы конечного продукта гликирования (AGE), поглотители реакционноспособных кислородсожержащих соединений, мышечные релаксанты и т. п.
[0127]
Дозу другого лекарственного средства можно соответствующим образом выбрать на основании клинически используемой дозы. Кроме того, соотношение объединения соединения I и другого средства можно соответствующим образом выбрать в соответствии с возрастом и массой тела субъекта, которому вводят, методики введения, длительности введения, целевого заболевания, симптома, комбинации и т. п. Например, можно использовать от 0,01 до 100 мас. част. другого средства в пересчете на 1 мас. част. соединения I. Любые два или большее количество других средств можно вводить в комбинации в подходящем соотношении.
[0128]
Для использования соединения, предлагаемого в настоящем изобретении, или объединенного средства из соединения, предлагаемого в настоящем изобретении, и другого средства для указанной выше цели его обычно готовят в виде соответствующей фармацевтической композиции вместе с фармацевтически приемлемым носителем и затем вводят системно или местно в пероральной или парентеральной форме.
[0129]
Соединение, предлагаемое в настоящем изобретении, вводят млекопитающему (предпочтительно человеку, более предпочтительно пациенту) в фармацевтически эффективном количестве.
[0130]
Доза соединения, предлагаемого в настоящем изобретении, меняется в зависимости от возраста, массы тела, симптома, терапевтического эффекта, методики введения, времени лечения и т. п. Однако соединение, предлагаемое в настоящем изобретении, или сопутствующее лекарственное средство для соединения, предлагаемого в настоящем изобретении, и другое лекарственное средство вводят перорально, обычно, в диапазоне от 1 нг до 1000 мг за один раз одному взрослому, от одного до нескольких раз в сутки, или вводят парентерально, в диапазоне от 0,1 нг до 10 мг за один раз одному взрослому, от одного до нескольких раз в сутки, или непрерывно вводят внутривенно в диапазоне от 1 до 24 ч в сутки. Как указано выше, поскольку доза меняется в зависимости от разных условий, может быть достаточной доза, меньшая указанной выше, или может быть необходимым введение за пределами диапазона.
[0131]
Если вводят соединение, предлагаемое в настоящем изобретении, или объединенное средство из соединения, предлагаемого в настоящем изобретении, и другого средства, его используют в виде твердого препарата для внутреннего введения или в виде жидкого препарата для перорального введения, препарата пролонгированного высвобождения или препарата регулируемого высвобождения для перорального введения, средства для инъекции, наружного препарата, средства для ингаляции или суппозитория для парентерального введения и т. п.
[0132]
Соединение, предлагаемое в настоящем изобретении, используют в качестве лекарственного вещества для указанных выше фармацевтических препаратов.
[0133]
Настоящее изобретение относится, например, к следующим вариантам осуществления.
[1] Соль 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты;
[2] соединение по пункту [1], приведенному выше, где солью является моно(4-гидроксибензоат);
[3] соединение по пункту [2], приведенному выше, которое находится в кристаллической форме;
[4] кристалл по пункту [3], приведенному выше, содержащий на порошковой рентгенограмме по меньшей мере два или большее количество дифракционных пиков при углах дифракции (2θ), выбранных из числа следующих: примерно 5,4, примерно 6,9, примерно 12,8, примерно 13,9, примерно 18,1, примерно 19,4, примерно 19,8, примерно 20,9 и примерно 24,7 градуса;
[5] кристалл по пункту [3] или [4], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 6,9, примерно 12,8, примерно 13,9 и примерно 24,7 градуса;
[6] кристалл по любому из пунктов [3] - [5], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 5,4, примерно 6,9, примерно 13,9, примерно 18,1, примерно 19,4, примерно 19,8, примерно 20,9 и примерно 24,7 градуса;
[7] кристалл по любому из пунктов [4] - [6], приведенному выше, не содержащий на порошковой рентгенограмме дифракционный пик при углах дифракции (2θ), равных примерно 11,3 и примерно 14,4 градуса;
[8] кристалл по любому из пунктов [4] - [7], приведенному выше, не содержащий на порошковой рентгенограмме дифракционный пик при углах дифракции (2θ), равных примерно 7,5, примерно 8,1 и примерно 8,9 градуса;
[9] кристалл по любому из пунктов [3] - [8], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных примерно 5,4, примерно 6,9, примерно 10,3, примерно 12,8, примерно 13,9, примерно 15,0, примерно 15,3, примерно 15,9, примерно 16,6, примерно 16,8, примерно 18,1, примерно 19,4, примерно 19,8, примерно 20,9, примерно 21,8, примерно 22,7, примерно 23,6, примерно 24,7, примерно 25,4, примерно 25,8, примерно 26,3, примерно 26,7, примерно 27,6, примерно 27,8, примерно 30,3, примерно 33,4 и примерно 34,2 градуса;
[10] кристалл по любому из пунктов [3] - [9], приведенному выше, характеризующийся порошковой рентгенограммой, приведенной на фиг. 7;
[11] кристалл по любому из пунктов [3] - [10], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 150°C, или температурой пика, равной примерно 153°C по данным дифференциальной сканирующей калориметрии;
[12] кристалл по любому из пунктов [3] - [11], приведенному выше, характеризующийся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг. 8;
[13] кристалл по пункту [3], приведенному выше, содержащий на порошковой рентгенограмме дифракционный пик при угле дифракции (2θ), равном по меньшей мере примерно 11,3 градуса;
[14] кристалл по пункту [3], приведенному выше, содержащий на порошковой рентгенограмме по меньшей мере два или большее количество дифракционных пиков при углах дифракции (2θ), выбранных из числа следующих: примерно 5,6, примерно 11,3, примерно 13,2, примерно 15,9, примерно 16,9, примерно 18,8, примерно 22,7 и примерно 24,2 градуса;
[15] кристалл по любому из пунктов [3], [13] или [14], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 5,6, примерно 11,3, примерно 13,2, примерно 15,9, примерно 16,9, примерно 18,8, примерно 22,7 и примерно 24,2 градуса;
[16] кристалл по любому из пунктов [3] или [13] - [15], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных примерно 5,6, примерно 7,0, примерно 7,9, примерно 11,3, примерно 12,3, примерно 13,2, примерно 13,9, примерно 15,9, примерно 16,9, примерно 17,4, примерно 17,9, примерно 18,4, примерно 18,8, примерно 19,4, примерно 19,9, примерно 20,4, примерно 21,0, примерно 21,2, примерно 21,9, примерно 22,7, примерно 23,2, примерно 23,4, примерно 24,2, примерно 25,2, примерно 26,5, примерно 27,5, примерно 29,1, примерно 29,8, примерно 30,5 и примерно 34,1 градуса;
[17] кристалл по любому из пунктов [3] или [13] - [16], приведенному выше, характеризующийся порошковой рентгенограммой, приведенной на фиг. 9;
[18] кристалл по любому из пунктов [3] или [13] - [17], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 154°C, или температурой пика, равной примерно 158°C по данным дифференциальной сканирующей калориметрии;
[19] кристалл по любому из пунктов [3] или [13] - [18], приведенному выше, характеризующийся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг. 10;
[20] соединение по пункту [1], приведенному выше, где солью является моно-триптофанат;
[21] соединение по пункту [20], приведенному выше, которое находится в кристаллической форме;
[22] кристалл по пункту [21], приведенному выше, содержащий на порошковой рентгенограмме по меньшей мере два или большее количество дифракционных пиков при углах дифракции (2θ), выбранных из числа следующих: примерно 8,0, примерно 9,7, примерно 16,0, примерно 17,0, примерно 18,9, примерно 19,1, примерно 22,2 и примерно 24,6 градуса;
[23] кристалл по пункту [21] или [22], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 8,0, примерно 9,7, примерно 16,0, примерно 17,0, примерно 18,9, примерно 19,1, примерно 22,2 и примерно 24,6 градуса;
[24] кристалл по любому из пунктов [21] - [23], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных примерно 8,0, примерно 9,7, примерно 12,8, примерно 15,6, примерно 16,0, примерно 16,6, примерно 17,0, примерно 17,3, примерно 17,6, примерно 18,2, примерно 18,6, примерно 18,9, примерно 19,1, примерно 19,6, примерно 20,9, примерно 21,3, примерно 21,7, примерно 21,9, примерно 22,2, примерно 22,6, примерно 23,4, примерно 23,8, примерно 24,6, примерно 25,3, примерно 25,7, примерно 26,2, примерно 26,6, примерно 27,1, примерно 27,4, примерно 27,9, примерно 28,2, примерно 28,7, примерно 29,1, примерно 29,9, примерно 30,2, примерно 30,9, примерно 32,0, примерно 32,2, примерно 32,5, примерно 33,1, примерно 34,1, примерно 34,5 и примерно 34,8 градуса;
[25] кристалл по любому из пунктов [21] - [24], приведенному выше, характеризующийся порошковой рентгенограммой, приведенной на фиг. 15;
[26] кристалл по любому из пунктов [21] - [25], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 178°C, или температурой пика, равной примерно 183°C по данным дифференциальной сканирующей калориметрии;
[27] кристалл по любому из пунктов [21] - [26], приведенному выше, обладающий экзотермическим пиком с температурой начала, равной примерно 185°C, или температурой пика, равной примерно 187°C по данным дифференциальной сканирующей калориметрии;
[28] кристалл по любому из пунктов [21] - [27], приведенному выше, характеризующийся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг. 16;
[29] соединение по пункту [1], приведенному выше, где солью является гемисукцинат;
[30] соединение по пункту [29], приведенному выше, которое находится в кристаллической форме;
[31] кристалл по пункту [30], приведенному выше, содержащий на порошковой рентгенограмме по меньшей мере два или большее количество дифракционных пиков при углах дифракции (2θ), выбранных из числа следующих: примерно 6,4, примерно 6,9, примерно 12,9, примерно 13,8, примерно 17,2, примерно 18,1, примерно 19,3, примерно 23,9 и примерно 24,3 градуса;
[32] кристалл по пункту [30] или [31], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 6,4, примерно 6,9, примерно 12,9, примерно 13,8, примерно 17,2, примерно 18,1, примерно 19,3, примерно 23,9 и примерно 24,3 градуса;
[33] кристалл по любому из пунктов [30] - [32], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных примерно 6,1, примерно 6,4, примерно 6,9, примерно 12,9, примерно 13,8, примерно 16,6, примерно 17,2, примерно 18,1, примерно 18,3, примерно 18,7, примерно 19,3, примерно 19,9, примерно 20,5, примерно 20,7, примерно 21,0, примерно 21,4, примерно 21,9, примерно 22,1, примерно 22,7, примерно 23,0, примерно 23,6, примерно 23,9, примерно 24,3, примерно 24,6, примерно 25,2, примерно 25,8, примерно 26,0, примерно 27,4, примерно 27,5, примерно 27,8, примерно 28,7, примерно 29,5, примерно 30,2, примерно 30,5, примерно 30,8, примерно 31,3, примерно 31,7, примерно 32,3, примерно 32,5, примерно 33,8, примерно 34,1, примерно 34,5 и примерно 34,9 градуса;
[34] кристалл по любому из пунктов [30] - [33], приведенному выше, характеризующийся порошковой рентгенограммой, приведенной на фиг. 17;
[35] кристалл по любому из пунктов [30] - [34], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 111°C, или температурой пика, равной примерно 114°C по данным дифференциальной сканирующей калориметрии;
[36] кристалл по любому из пунктов [30] - [35], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 137°C, или температурой пика, равной примерно 140°C по данным дифференциальной сканирующей калориметрии;
[37] кристалл по любому из пунктов [30] - [36], приведенному выше, характеризующийся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг. 18;
[38] кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты,
[39] кристалл по пункту [38], приведенному выше, содержащий на порошковой рентгенограмме по меньшей мере два или большее количество дифракционных пиков при углах дифракции (2θ), выбранных из числа следующих: примерно 6,5, примерно 7,8, примерно 8,6, примерно 11,6, примерно 15,2, примерно 17,0, примерно 18,8, примерно 21,1, примерно 22,8, примерно 23,3 и примерно 24,9 градуса;
[40] кристалл по пункту [38] или [39], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 6,5, примерно 7,8, примерно 8,6 и примерно 11,6 градуса;
[41] кристалл по любому из пунктов [38] - [40], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере примерно 11,6, примерно 15,2, примерно 17,0, примерно 18,8, примерно 21,1, примерно 22,8, примерно 23,3 и примерно 24,9 градуса;
[42] кристалл по любому из пунктов [39] - [41], приведенному выше, не содержащий на порошковой рентгенограмме дифракционный пик при углах дифракции (2θ), равных примерно 5,8 градуса и примерно 19,9 градуса;
[43] кристалл по любому из пунктов [38] - [42], приведенному выше, содержащий на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных примерно 6,5, примерно 7,8, примерно 8,6, примерно 11,6, примерно 13,0, примерно 13,1, примерно 15,2, примерно 15,8, примерно 17,0, примерно 17,3, примерно 18,8, примерно 18,9, примерно 19,3, примерно 20,9, примерно 21,1, примерно 21,3, примерно 22,8, примерно 23,3, примерно 23,6, примерно 23,8, примерно 24,0, примерно 24,9, примерно 25,8, примерно 26,4, примерно 27,1, примерно 27,9, примерно 29,8, примерно 30,4, примерно 30,7, примерно 31,6, примерно 32,0 и примерно 34,0 градуса;
[44] кристалл по любому из пунктов [38] - [43], приведенному выше, характеризующийся порошковой рентгенограммой, приведенной на фиг. 1;
[45] кристалл по любому из пунктов [38] - [44], приведенному выше, обладающий эндотермическим пиком с температурой начала, равной примерно 128°C, или температурой пика, равной примерно 133°C по данным дифференциальной сканирующей калориметрии;
[46] кристалл по любому из пунктов [38] - [45], приведенному выше, характеризующийся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг. 2;
[47] фармацевтическая композиция, содержащая соединение по любому из пунктов [1] - [46], приведенному выше, и фармацевтически приемлемый носитель;
[48] фармацевтическая композиция по пункту [47], приведенному выше, которая является профилактическим и/или терапевтическим средством для опосредуемого S1P5 заболевания;
[49] фармацевтическая композиция по пункту [48], приведенному выше, где опосредуемым S1P5 заболеванием является нейродегенеративное заболевание;
[50] фармацевтическая композиция по пункту [49], приведенному выше, где нейродегенеративным заболеванием является мультисистемная атрофия или болезнь Паркинсона;
[51] профилактическое и/или терапевтическое средство для опосредуемого S1P5 заболевания, содержащее соединение по любому из пунктов [1] - [46], приведенному выше;
[52] способ предупреждения и/или лечения опосредуемого S1P5 заболевания, включающий введение млекопитающему эффективного количества соединения по любому из пунктов [1] - [46], приведенному выше;
[53] соединение по любому из пунктов [1] - [46], приведенному выше, для применения для лечения и/или предупреждения опосредуемых S1P5 заболеваний; и
[54] применение соединения по любому из пунктов [1] - [46], приведенному выше, для приготовления профилактического и/или терапевтического средства для опосредуемого S1P5 заболевания.
ПРИМЕРЫ
[0134]
Ниже настоящее изобретение описано подробно со ссылкой на примеры, но настоящее изобретение не ограничивается только ими.
[0135]
Растворители, указанные в скобках в разделе о разделении с помощью хроматографии и TLC, являются растворителями для элюирования или растворителями для проявления и отношения являются объемными.
[0136]
Растворители, указанные в скобках в разделе о NMR, являются растворителями, использующимися для измерений.
[0137]
Названия соединении, использующихся в настоящем описании, обычно получены с использованием компьютерной программы ACD/Name (зарегистрированная торговая марка) of Advanced Chemistry Development, Lexichem Toolkit 1.4.2 of OpenEye Scientific Software, или ChemDraw (зарегистрированная торговая марка) Ultra of PerkinElmer, которые образуют названия в соответствии с праивлами IUPAC или в соответствии с номенклатурой IUPAC.
[0138]
LCMS проводили с использованием системы Waters i-class при следующих условиях.
[0139]
Колонка: YMC Triart C18 2,0 мм×30 мм, 1,9 мкм;
Скорость потока: 1,0 мл/мин;
Температура: 30°C;
Подвижная фаза A: 0,1% водный раствор трифоруксусной кислоты (TFA);
Подвижная фаза B: 0,1% раствор TFA - ацетонитрил:
Градиентный режим (указано отношение количества подвижной фазы (A) к количеству подвижной фазы (B)):
от 0 до 0,10 мин: (95% : 5%); от 0,10 до 1,20 мин: от (95% : 5%) до (5% : 95%); от 1,20 до 1,50 мин: (5% : 95%).
[0140]
Порошковую рентгенограмму снимали при любых из следующих условий.
[0141]
Условия 1
Устройство: SmartLab производства фирмы Rigaku Corporation
Мишень: Cu
Напряжение: 45 кВ
Ток: 200 мА
Скорость сканирования: 30 градусов/мин
[0142]
Условия 2
Устройство: SmartLab производства фирмы Rigaku Corporation
Мишень: Cu
Напряжение: 45 кВ
Ток: 200 мА
Скорость сканирования: 10 градусов/мин
[0143]
Дифференциальную сканирующую калориметрию (DSC) проводили при любых из следующих условий.
[0144]
Условия 1
Устройство: Discovery DSC производства фирмы TA Instruments
Ячейка для образца: алюминиевая чашка
Скорость потока азота: 40 мл/мин
[0145]
Условия 2
Устройство: TGA/DSC 3+ производства фирмы Mettler Toledo
Ячейка для образца: алюминиевая чашка
Скорость потока азота: 40 мл/мин
[0146]
Условия 3
Устройство: DSC822e производства фирмы Mettler Toledo
Ячейка для образца: алюминиевая чашка
Скорость потока азота: 40 мл/мин
[0147]
Рентгенограмму монокристалла снимали при следующих условиях.
[0148]
Условия 1
Устройство: SuperNova производства фирмы Rigaku Corporation
Мишень: CuKα (λ=1,54184 Å)
Напряжение: 50 кВ
Ток: 0,8 мА
Шаг сканирования: 1°
Температура: 100 K
[0149]
Условия 2
Устройство: SuperNova производства фирмы Rigaku Corporation
Мишень: CuKα (λ=1,54184 Å)
Напряжение: 50 кВ
Ток: 0,8 мА
Шаг сканирования: 1°
Температура: 297 K
[0150]
Пример 1: 6-Метокси-3-метил-3,4-дигидронафталин-2-карбальдегид
К раствору 6-метокси-3-метил-3,4-дигидронафталин-1(2H)-она (регистрационный номер CAS: 5563-21-3) (1 г) в метаноле (100 мл) добавляли борогидрид натрия (398 мг) при 0°C. Раствор реакционной смеси нагревали до комнатной температуры и перемешивали в течение 2 ч, затем к нему добавляли водный раствор хлорида аммония и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным рассолом и сушили над безводным сульфатом натрия, и затем растворитель отгоняли. Полученный остаток предварительно очищали с помощью колоночной хроматографии на силикагеле (гексан : этилацетат=10 : 1) и без обработки использовали в следующей реакции. Оксихлорид фосфора (2,2 г) добавляли к раствору в N,N-диметилформамиде (DMF) (100 мл) полученного предварительно очищенного продукта. Раствор реакционной смеси нагревали до 60°C и перемешивали в течение 8 ч. Затем раствор реакционной смеси выливали в смесь воды со льдом и перемешивали в течение 5 мин и затем органический слой отделяли. Органический слой промывали насыщенным рассолом и сушили над безводным сульфатом натрия и растворитель отгоняли. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (гексан : этилацетат=10 : 1 → 5 : 1) и получали искомое соединение (299 мг), обладающее следующими значениями физической характеристики.
1H-NMR (CDCl3): δ 9,57, 7,30-7,24, 6,82-6,78, 3,85, 3,08, 2,65, 0,92.
[0151]
Пример 2: 6-Гидрокси-3-метил-3,4-дигидронафталин-2-карбальдегид
К раствору соединения (299 мг), полученного в примере 1, в дихлорметане (DCM) (100 мл), по каплям добавляли трибромид бора (815 мг) при 0°C. После перемешивания смеси при 0°C в течение 3 ч раствор реакционной смеси выливали в смесь воды со льдом и перемешивали в течение 5 мин и затем органический слой отделяли. Органический слой промывали насыщенным рассолом и сушили над безводным сульфатом натрия и растворитель отгоняли. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (гексан : этилацетат=5 : 1) и получали искомое соединение (200 мг), обладающее следующими значениями физической характеристики.
1H-NMR (CDCl3): δ 9,57, 7,18, 6,72, 3,08, 2,60, 0,94.
[0152]
Пример 3: (R)-6-Гидрокси-3-метил-3,4-дигидронафталин-2-карбальдегид
Соединение, полученное в примере 2, подвергали оптическому разделению с помощью HPLC (использованная колонка: Daicel Corporation CHIRALCEL OJ-H (4,6 мм I.D.×250 мм L), подвижная фаза: н-гексан : 2-пропанол=80 : 20, скорость потока: 1 мл/мин, температура: 40°C, длина волны: 245 нм) и искомое соединение получали в виде первого пика (время удерживания: примерно 6,9 мин).
[0153]
Пример 3(1): (S)-6-Гидрокси-3-метил-3,4-дигидронафталин-2-карбальдегид
С помощью оптического разделения в примере 3 искомое соединение получали в виде второго пика (время удерживания: примерно 8,1 мин).
[0154]
Пример 4: (S)-Метил-1-((6-гидрокси-3-метил-3,4-дигидронафталин-2-ил)метил)азетидин-3-карбоксилат
К раствору соединения (5,00 г), полученного в примере 3(1), в DCM (265 мл), добавляли гидрохлорид метилазетидин-3-карбоксилата (5,24 г) (регистрационный номер CAS: 100202-39-9) и диизопропилэтиламин (6,00 мл) и смесь перемешивали при комнатной температуре в течение 30 мин. После охлаждения льдом к жидкой реакционной смеси добавляли триацетоксиборогидрид натрия (7,32 г) и смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную жидкость концентрировали при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле (аминосиликагель, гексан : этилацетат=50 : 50 → 0 : 100) и получали искомое соединение (6,00 г), обладающее следующими значениями физической характеристики.
1H-NMR (CDCl3): δ 6,88, 6,63-6,56, 6,21, 3,71, 3,64-3,51, 3,42-3,22, 3,03, 2,94, 2,49, 2,37, 0,92;
LCMS: время удерживания 0,61 мин.
[0155]
Пример 5: Метил-1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоксилат
К раствору в тетрагидрофуране (THF) (5,0 мл) соединения (511 мг), полученного в примере 4, добавляли раствор в толуоле (0,97 мл) 4,4,4-трифторбутанола (273 мг), трифенилфосфин (559 мг) и 2,2 моль/л диэтилазодикарбоксилат и смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную жидкость концентрировали, и полученный остаток очищали с помощью колоночной хроматографии на силикагеле (аминосиликагель, гексан : этилацетат=90 : 10 → 80 : 20) и получали искомое соединение (312 мг), обладающее следующими значениями физической характеристики.
1H-NMR (CDCl3): δ 6,93, 6,69-6,61, 6,22, 3,99, 3,71, 3,65-3,50, 3,42-3,21, 3,02, 2,96, 2,52, 2,44-2,21, 2,10-1,96, 0,92;
LCMS: время удерживания 0,90 мин.
[0156]
Пример 6: 1-[[(3S)-3-Метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновая кислота
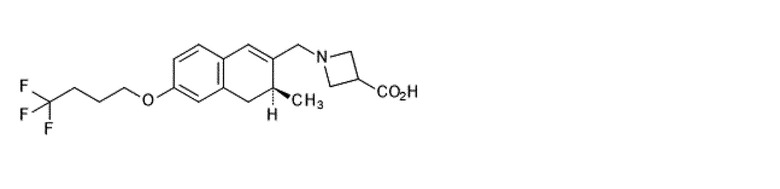
[0157]
2 н. Водный раствор гидроксида натрия (4,5 мл) добавляли к раствору в метаноле (3,0 мл) соединения (1,20 г), полученного в примере 5, и реакционную жидкость перемешивали при комнатной температуре в течение 16 ч. К нему добавляли 1 н. водный раствор хлористоводородной кислоты (9,0 мл) и смесь концентрировали при пониженном давлении, затем полученный остаток очищали с помощью колоночной хроматографии на силикагеле (диолсиликагель, DCM : MeOH=10 : 0 → 5 : 5) и дополнительно очищали с помощью колоночной хроматографии на силикагеле (ODS, H2O : CH3CN=10 : 0 → 50 : 50) и получали искомое соединение (846 мг), обладающее следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 6,95, 6,71, 6,68, 6,20, 3,98, 3,46-3,36, 3,24-3,12, 2,96, 2,82, 2,49, 2,39, 2,31, 1,89, 0,83;
LCMS: время удерживания 0,85 мин.
[0158]
В частности, соединение примера 6 в настоящем изобретении является таким же, как соединение примера 15 (34) в патентной литературе 3 и соединение примера 6 в настоящем изобретении, полученное способом, описанным в патентной литературе 3, или способом, описанным в примерах 1-6 в настоящем изобретении является аморфным.
[0159]
Пример 7: Кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл D)
Соединение (250 мг), полученное в примере 6, растворяли путем добавления метанола при комнатной температуре и объем доводили до постоянного значения, равного 5 мл. 200 мкл Этого раствора отмеряли в пробирку и концентрировали при пониженном давлении при 35°C, затем к нему добавляли ацетон (50 мкл), и смесь перемешивали при комнатной температуре в течение 2 недель. Осадок в пробирке сушили при пониженном давлении при комнатной температуре в течение 1 ч и получали искомое соединение в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0160]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 1 и фиг. 2 соответственно.
[0161]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 1.
[Таблица 1]
[0162]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 1,2 мг
Скорость нагревания: 10°C/мин (от 20 до 180°C)
Эндотермический пик: температура начала равна примерно 128°C, температура пика равна примерно 133°C
[0163]
Пример 8: Кристалл гидрата 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл B)
Соединение (250 мг), полученное в примере 6, растворяли путем добавления метанола при комнатной температуре и объем доводили до постоянного значения, равного 5 мл. 200 мкл этого раствора отмеряли в пробирку и концентрировали при пониженном давлении при 35°C, затем к нему добавляли 97% водный раствор ацетона (20 мкл), и смесь перемешивали при комнатной температуре в течение 1 дня. Осадок в пробирке сушили при пониженном давлении при комнатной температуре в течение 1 ч и получали искомое соединение в виде белого кристаллического твердого вещества, обладающее следующими значениями физической характеристики.
Порошковая рентгенограмма, термограмма DSC и термограмма термогравиметрии (TG) кристалла, полученные при следующих условиях, приведены на фиг. 3, фиг. 4 и фиг. 21 соответственно.
[0164]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 2.
[Таблица 2]
[0165]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 1,0 мг
Скорость нагревания: 10°C/мин (от 20 до 180°C)
Первый эндотермический пик: температура начала равна примерно 80°C, температура пика равна примерно 97°C
Второй эндотермический пик: температура начала равна примерно 110°C, температура пика равна примерно 112°C
[0166]
(3) Термогравиметрия (TG)
Устройство: TGA/DSC 3+ производства фирмы Mettler Toledo
Количество образца: 2,1 мг
Ячейка для образца: алюминиевая чашка
Скорость потока азота: 40 мл/мин
Скорость нагревания: 10°C/мин (от 25 до 180°C)
Потеря массы, равная примерно 3,1%, была обнаружена в диапазоне от примерно комнатной температуры до примерно 100°C.
[0167]
Пример 9: Кристалл монобензоата 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл A)
[0168]
Смесь соединения (1,5 г), полученного в примере 7, и бензойной кислоты (0,48 г) растворяли путем добавления метанола (7,5 мл) при комнатной температуре и затем смесь концентрировали при пониженном давлении при 35°C. К ней добавляли ацетонитрил (3,0 мл) и смесь перемешивали при комнатной температуре в течение 1 ч. Суспендированые кристаллы собирали фильтрованием и сушили при 40°C при пониженном давлении в течение ночи и получали 1,86 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 7,95, 7,62, 7,50, 6,97, 6,73-6,67, 6,21, 4,00, 3,44-3,37, 3,25-3,12, 2,95, 2,84, 2,45-2,31, 1,95-1,88, 0,85.
[0169]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 5 и фиг. 6 соответственно.
[0170]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 3.
[Таблица 3]
[0171]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 2
Количество образца: 1,8 мг
Скорость нагревания: 10°C/мин (от 25 до 180°C)
Эндотермический пик: температура начала равна примерно 137°C, температура пика равна примерно 139°C
[0172]
Пример 10: Кристалл моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл A)
Ацетонитрил (30 мл) добавляли к смеси соединения (3,0 г), полученного в примере 7, и 4-гидроксибензойной кислоты (1,08 г) при комнатной температуре и смесь перемешивали в течение ночи. Затем суспендированые кристаллы собирали фильтрованием и сушили при 50°C при пониженном давлении в течение 3 ч и получали 4,0 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 12,76-12,01, 10,46-10,00, 7,78, 6,97, 6,81, 6,75-6,65, 6,21, 4,04-3,95, 3,45-3,33, 3,25-3,09, 2,94, 2,84, 2,48-2,27, 1,96-1,85, 0,84.
[0173]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 7 и фиг. 8 соответственно.
[0174]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 4.
[Таблица 4]
[0175]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 2
Количество образца: 2,1 мг
Скорость нагревания: 10°C/мин (от 25 до 180°C)
Эндотермический пик: температура начала равна примерно 150°C, температура пика равна примерно 153°C
[0176]
Пример 11: Кристалл моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл B)
Метанол (300 мкл) и дистиллированную воду (30 мкл) добавляли к смеси соединения (150 мг), полученного в примере 7, и 4-гидроксибензойной кислоты (54 мг) при комнатной температуре и смесь перемешивали в течение ночи. Затем суспензию концентрировали и сушили при пониженном давлении и получали 204 мг искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0177]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 9 и фиг. 10 соответственно.
[0178]
(1) Порошковая рентгенограмма
Условия измерений: условия 2
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 5.
[Таблица 5]
[0179]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 2
Количество образца: 3,0 мг
Скорость нагревания: 10°C/мин (от 25 до 180°C)
Эндотермический пик: температура начала равна примерно 154°C, температура пика равна примерно 158°C
[0180]
Пример 12: Кристалл гидрата моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл C)
Дистиллированную воду (30 мл) добавляли к смеси соединения (3,0 г), полученного в примере 7, и 4-гидроксибензойной кислоты (1,08 г) при комнатной температуре и смесь перемешивали в течение ночи. Затем суспендированые кристаллы собирали фильтрованием и сушили при комнатной температуре при пониженном давлении в течение 3 ч и получали 4,14 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0181]
Порошковая рентгенограмма, термограмма DSC и термограмма TG кристалла, полученные при следующих условиях, приведены на фиг. 11, фиг. 12 и фиг. 22 соответственно.
[0182]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 6.
[Таблица 6]
[0183]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 2
Количество образца: 2,2 мг
Скорость нагревания: 10°C/мин (от 25 до 200°C)
Первый эндотермический пик: температура начала равна примерно 78°C, температура пика равна примерно 93°C
Второй эндотермический пик: температура начала равна примерно 105°C, температура пика равна примерно 114°C
Третий эндотермический пик: температура начала равна примерно 152°C, температура пика равна примерно 155°C
Первый экзотермический пик: температура начала равна примерно 114°C, температура пика равна примерно 120°C
Второй экзотермический пик: температура начала равна примерно 159°C, температура пика равна примерно 165°C
[0184]
(3) Термогравиметрия (TG)
Устройство: TGA/DSC 3+ производства фирмы Mettler Toledo
Количество образца: 2,2 мг
Ячейка для образца: алюминиевая чашка
Скорость потока азота: 40 мл/мин
Скорость нагревания: 10°C/мин (от 25 до 200°C)
Потеря массы, равная примерно 3,1%была обнаружена в диапазоне от примерно комнатной температуры до примерно 100°C.
[0185]
Пример 13: Кристалл гемисульфата 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл B)
1 мл метанола добавляли к соединению (150 мг), полученному в примере 6 и смесь перемешивали. В бане со льдом 0,39 мл 0,5 моль/л водного раствора серной кислоты понемногу по каплям добавляли к этому раствору и смесь перемешивали в течение 5 мин. Растворитель отгоняли при пониженном давлении и сушили при пониженном давлении при комнатной температуре в течение 15 мин. К ней добавляли 1,5 мл ацетонитрила и смесь обрабатывали ультразвуком и затем перемешивали при комнатной температуре в течение 21 ч. К ней добавляли 1,0 мл ацетонитрила и смесь перемешивали при комнатной температуре в течение ночи. Твердое вещество собирали фильтрованием и сушили при комнатной температуре при пониженном давлении и получали 114 мг искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 13,38-12,76, 11,03-10,33, 7,06, 6,81-6,73, 6,53, 4,42-4,23, 4,22-4,11, 4,11-3,92, 3,91-3,78, 3,75-3,57, 2,92, 2,61-2,34, 1,98-1,87, 0,84.
[0186]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 13 и фиг. 14 соответственно.
[0187]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 7.
[Таблица 7]
[0188]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 1,0 мг
Скорость нагревания: 10°C/мин (от 25 до 180°C)
Эндотермический пик: температура начала равна примерно 161°C, температура пика равна примерно 166°C
[0189]
Пример 14: Кристалл моно-триптофаната 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл A)
Смешанный растворитель из метанола (1,5 мл) и ацетонитрила (8,5 мл) добавляли к смеси соединения (0,99 г), полученного в примере 7, и триптофана (0,53 г) и смесь перемешивали при 55°C в течение 3 дней. К ней дополнительно добавляли метанол (0,75 мл), ацетонитрил (4,25 мл) и дистиллированную воду (1 мл) и смесь перемешивали при 25°C в течение 15 мин. Суспендированые кристаллы собирали фильтрованием и сушили при пониженном давлении при комнатной температуре в течение ночи. Дистиллированную воду (7 мл) добавляли к кристаллам и смесь перемешивали при 25°C в течение 1 дня. Суспендированые кристаллы собирали фильтрованием и сушили при пониженном давлении при комнатной температуре в течение 4 дней и получали 1,40 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 10,87, 7,55, 7,34, 7,19, 7,09-7,05, 7,00-6,96, 6,73-6,67, 6,21, 4,00, 3,43-3,11, 2,97-2,91, 2,87-2,81, 2,44-2,32, 1,95-1,88, 0,85.
[0190]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 15 и фиг. 16 соответственно.
[0191]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 8.
[Таблица 8]
[0192]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 0,8 мг
Скорость нагревания: 10°C/мин (от 20 до 200°C)
Эндотермический пик: температура начала равна примерно 178°C, температура пика равна примерно 183°C
Экзотермический пик: температура начала равна примерно 185°C, температура пика равна примерно 187°C
[0193]
Пример 15: Кристалл гемисукцината 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл A)
Смесь соединения (1,0 г), полученного в примере 7, и янтарной кислоты (0,32 г) растворяли в изопропаноле (7 мл) при 70°C. Смесь охлаждали до 25°C и перемешивали в течение 3 дней. Осадившиеся кристаллы собирали фильтрованием и сушили при комнатной температуре на воздухе в течение 40 мин и получали 1,0 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 12,25, 6,97, 6,73-6,68, 6,22, 4,00, 3,44-3,39, 3,24-3,14, 2,97, 2,87-2,82, 2,44-2,32, 1,93-1,89, 0,85.
[0194]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 17 и фиг. 18 соответственно.
[0195]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 9.
[Таблица 9]
[0196]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 0,8 мг
Скорость нагревания: 10°C/мин (от 20 до 180°C)
Первый эндотермический пик: температура начала равна примерно 111°C, температура пика равна примерно 114°C
Второй эндотермический пик: температура начала равна примерно 137°C, температура пика равна примерно 140°C
[0197]
Пример 16: Кристалл гемиадипата 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл B)
Смесь соединения (1,0 г), полученного в примере 7, и адипиновой кислоты (0,20 г) растворяли в этанол (7 мл) при 45°C. Смесь охлаждали до 25°C, к ней добавляли диэтиловый эфир (60 мл), смесь перемешивали в течение 2 дней и суспендированые кристаллы собирали фильтрованием и сушили при пониженном давлении при комнатной температуре в течение ночи. К кристаллам дополнительно добавляли адипиновую кислоту (0,084 г) и ацетон (8 мл) и смесь перемешивали в течение 6 дней. Суспендированые кристаллы собирали фильтрованием и сушили при пониженном давлении при комнатной температуре в течение ночи и получали 0,87 г искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (DMSO-d6): δ 12,16, 6,97, 6,73-6,67, 6,21, 4,00, 3,44-3,37, 3,24-3,12, 2,95, 2,87-2,82, 2,47-2,31, 2,23-2,18, 1,95-1,88, 1,54-1,46, 0,85.
[0198]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 19 и фиг. 20 соответственно.
[0199]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 10.
[Таблица 10]
[0200]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 1
Количество образца: 0,6 мг
Скорость нагревания: 10°C/мин (от 20 до 180°C)
Эндотермический пик: температура начала равна примерно 123°C, температура пика равна примерно 125°C
[0201]
Пример 17: Кристалл 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл A)
Часть соединения, полученного в примере 6, очищали с помощью колоночной хроматографии на силикагеле (ODS, H2O : CH3CN=90 : 10 → 0 : 10). Затем смесь концентрировали и сушили при 40°C и получали 113 мг искомого соединения в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0202]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 23 и фиг. 24 соответственно.
[0203]
(1) Порошковая рентгенограмма
Условия измерений: условия 2
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 14.
[Таблица 14]
[0204]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 3
Количество образца: 1,29 мг
Скорость нагревания: 10°C/мин (от 5 до 120°C)
Первый эндотермический пик: широкий пик от примерно 50°C до примерно 90°C
Второй эндотермический пик: температура начала равна примерно 108°C, температура пика равна примерно 111°C
[0205]
Пример 18: Кристалл геми(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл D)
К 20 мг соединения, полученного в примере 11, добавляли 88 мкл DMSO и 112 мл воды. Смесь перемешивали при 40°C в течение 1 недели и кристаллы собирали фильтрованием и получали искомое соединение в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
1H-NMR (метанол-d4): δ 7,81-7,74, 6,99-6,93, 6,75-6,62, 6,44, 4,24-4,04, 3,99-3,86, 3,82-3,73, 3,41-3,28, 2,93, 2,58-2,52, 2,36-2,19, 1,97-1,87, 0,85.
[0206]
Порошковая рентгенограмма кристалла, полученная при следующих условиях, приведена на фиг. 25.
[0207]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 15.
[Таблица 15]
[0208]
Пример 19: Кристалл моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты (кристалл E)
Соединение,, полученное в примере 12, сушили при пониженном давлении при 90°C в течение 2 ч и получали искомое соединение в виде белого кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0209]
Порошковая рентгенограмма и термограмма DSC кристалла, полученные при следующих условиях, приведены на фиг. 26 и фиг. 27 соответственно.
[0210]
(1) Порошковая рентгенограмма
Условия измерений: условия 1
Результаты для углов дифракции (2θ) (градусы) и относительных интенсивностей (%), полученные с помощью порошковой рентгенографии с использованием излучения Cu-Kα, приведены в таблице 16.
[Таблица 16]
[0211]
(2) Дифференциальная сканирующая калориметрия (DSC)
Условия измерений: условия 2
Количество образца: 2,05 мг
Скорость нагревания: 10°C/мин (от 35 до 185°C)
Первый эндотермический пик: температура начала равна примерно 104°C, температура пика равна примерно 113°C
Второй эндотермический пик: температура начала равна примерно 147°C, температура пика равна примерно 153°C
Первый экзотермический пик: температура начала равна примерно 117°C, температура пика равна примерно 121°C
[0212]
Пример 20: Кристалл моногидрата 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты-4-гидроксибензойной кислоты (1 : 1) (кристалл I)
(Моногидрат совместного кристалла соединения I и 4-гидроксибензойной кислоты (1 : 1) (кристалл I))
20 мг соединения, полученного в примере 10. растворяли в 800 мкл изопропанола. Раствор делили на аликвоты по 100 мкл (раствор A) и 150 мкл (раствор B) и концентрировали на воздухе в течение 1 дня. Затравочные кристаллы, полученные из раствора, полученного концентрированием раствора A, добавляли к раствору, полученному концентрированием раствора B, и выдерживали в течение нескольких часов и получали искомое соединение в виде кристаллического твердого вещества, обладающего следующими значениями физической характеристики.
[0213]
Результаты рентгенографии монокристалла кристаллов приведены ниже.
[0214]
(1) Кристаллографические данные
Условия измерений: условия 1
Постоянная решетки: a=6,1374 (2)Å
b=12,8245 (3)Å
c=17,8596 (5)Å
α=72,297 (2)°
β=85,002 (3)°
γ=79,591 (3)°
V=1316,35 (7)Å3
Пространственная группа: P1 (#1)
Фактор R: 0,0475
Значение параметра Флэка: -0,04 (7)
[0215]
(2) Позиционные параметры (парциальные атомные координаты)
Условия измерений: условия 1
Результаты для позиционных параметров (парциальных атомных координат), полученные с помощью рентгенографии монокристалла с использованием излучения Cu-Kα, приведены в таблице 17 (×104). Следует отметить, что номера атомов в таблице 17 не согласуются с номерами атомов в таблице 18.
[Таблица 17-1]
[Таблица 17-2]
[0216]
(3) Рассчитанная порошковая рентгенограмма
Порошковая рентгенограмма, рассчитанная по позиционным параметрам (парциальным атомным координатам), измеренным при условиях 1, приведена на фиг. 28.
[0217]
(4) Кристаллографические данные
Условия измерений: условия 2
Постоянная решетки: a=6,1599 (2)Å
b=12,9850 (6)Å
c=18,1997 (10)Å
α=71,547 (5)°
β=86,306 (4)°
γ=80,124 (4)°
V=1360,33 (12)Å3
Пространственная группа: P1 (#1)
Фактор R: 0,0760
Значение параметра Флэка: 0,09 (14)
[0218]
(5) Позиционные параметры (парциальные атомные координаты)
Условия измерений: условия 2
Результаты для позиционных параметров (парциальных атомных координат), полученные с помощью рентгенографии монокристалла с использованием излучения Cu-Kα, приведены в таблице 18 (×104). Следует отметить, что номера атомов в таблице 18 не согласуются с номерами атомов в таблице 17.
[Таблица 18]
[0219]
(6) Рассчитанная порошковая рентгенограмма
Порошковая рентгенограмма, рассчитанная по позиционным параметрам (парциальным атомным координатам), измеренным при условиях 2, приведена на фиг. 29.
[0220]
Сравнительный пример: (S)-3-Фтор-1-[(6-метокси-3-метил-3,4-дигидронафталин-2-ил)метил]азетидин-3-карбоновая кислота
1H-NMR (DMSO-d6): δ 6,99, 6,71, 6,68, 6,27, 3,82-3,64, 3,63-3,35, 3,30-3,15, 2,86, 2,52, 2,36, 0,85;
LCMS: время удерживания 0,65 мин.
[0221]
Воздействие соединения I можно продемонстрировать с помощью следующих экспериментов, но не ограничивается только ими.
[0222]
(1) Биологический экспериментальный пример 1: Исследование агонистической активности по отношению к рецептору S1P соединений, предлагаемых в настоящем изобретении, путем мониторинга внутриклеточной концентрации кальция
Клетки яичника китайского хомячка (CHO), в которых сверхэкспрессировали гены человеческого S1P1 (EDG-1) или человеческого S1P5 (EDG-8), выращивали в среде Нэма F-12, содержащей 10% FBS (фетальная бычья сыворотка), пенициллин/стрептомицин и генетицин (0,25 мг/мл). Среду заменяли за один день до проведения анализа кальция и в день анализа. Через 4 ч после замены среды среду удаляли и один раз промывали забуференным фосфатом физиологическим раствором. К ней добавляли 0,05% трипсин.EDTA для отслаивания клеток и затем добавляли среду для выделения клеток. Собранную суспензию клеток суспензия центрифугировали для удаления надосадочной жидкости и суспендировали в забуференном фосфатом физиологическом растворе для подсчета количества клеток. Клетки суспендировали в растворе Нэнкса, содержащем Calcium 6 Assay Reagent (выпускает фирма Molecular Devices), 20 мМ HEPES и 2,5 мМ пробенецида, так что получали концентрацию, равную 1,1×106 клеток/мл и инкубировали при 37°C в течение примерно 1 ч. Затем надосадочную жидкость удаляли центрифугированием и клетки суспендировали в растворе Нэнкса, содержащем 20 мМ HEPES, 2,5 мМ пробенецида и 0,1% BSA, так что получали концентрацию, равную 2,2×106 клеток/мл. Суспензию высевали в 96-луночный планшет по 80 мкл/лунка. Планшет помещали в систему скрининга флуоресценции лекарственных средств (FDSS6000), соединение I или сравнительное соединение и S1P последовательно добавляли и увеличение внутриклеточной концентрации кальция до и после добавления измеряли при длине волны возбуждения, равной 480 нм, и длине волны флуоресценции, равной 540 нм. Увеличение внутриклеточной концентрации кальция рассчитывали по интенсивности сигнала при длине волны флуоресценции и агонистическую активность каждого соединения рассчитывали по интенсивности сигнала при добавлении S1P вместо соединения, принятой равной 100% активности.
[0223]
[Результаты]
Агонистические активности (значения EC50) для соединения I и сравнительных соединений по отношению к рецептору S1P1 или рецептору S1P5 приведены в таблице 11.
В качестве сравнительных соединений в дополнение к сравнительному примеру, описанному в настоящем изобретении, гидрохлорид 1-{[1-метил-6-(октилокси)-3,4-дигидро-2-нафталинил]метил}-3-азетидинкарбоновой кислоты, описанный в примере 31 (58) в патентной литературе 1, использовали в качестве сравнительного соединения A и 1-({6-[(2-метокси-4-пропилбензил)окси]-1-метил-3,4-дигидро-2-нафталинил}метил)-3-азетидинкарбоновую кислоту, описанную в примере 37 в патентной литературе 2, использовали в качестве сравнительного соединения B.
[0224]
Соединения сравнительных примеров не обладают агонистической активностью по отношению к рецептору S1P1 и S1P5. Сравнительное соединение A и сравнительное соединение B обладало агонистической активностью по отношению к рецептору S1P1 и S1P5, причем агонистическая активность по отношению к рецептору S1P1 была сильнее, чем агонистическая активность по отношению к рецептору S1P5.
[0225]
В отличие от этого, установлено, что соединение I обладало селективной агонистической активностью по отношению к рецептору S1P5 и улучшился баланс агонистической активности по отношению к рецептору S1P5 и активности по отношению к рецептору S1P1.
[0226]
[Таблица 11]
[0227]
(2) Биологический экспериментальный пример 2: Измерение клиренса для крыс
Раствор соединения I вводили в хвостовую вену самцам крыс SD натощак. После введения крыс фиксировали вручную и через регулярные промежутки времени брали кровь из яремной вены с использованием гепарин-натрия. Кровь центрифугировали при 10000 g, 3 мин, 4°C и получали плазму. Концентрацию соединения I в плазме измеряли с помощью LC/MS/MS. Клиренс рассчитывали по изменению концентрации в плазме с использованием программного обеспечения для фармакокинетического анализа Phoenix WinNonlin (Certara USA, Inc.).
[0228]
[Результаты]
Поскольку соединение I обладало низким клиренсом, можно было ожидать высокую биодоступность.
[0229]
(3) Биологический экспериментальный пример 3: Измерение ингибирующего воздействия сравнительного соединения C на связывание [33P]S1P с S1P5 (EDG-8)
С использованием фракции мембран клеток яичника китайского хомячка (CHO), в которой сверхэкспрессировали гены человека S1P1 (EDG-1) или человека S1P5, реакцию проводили в 96-луночном планшете для анализа с использованием фракции мембран, содержащей 60 мкг белка/мл. В каждую лунку помещали 100 мкл раствора разбавителя (DMSO), разведенного связывающим буфером (50 ммоль/л, Tris pH 7,5, 5 ммоль/л, MgCl2, 0,5% BSA, Complete EDTA free (1 таблетка/50 мл)) или раствора соединения в двойной концентрации и добавляли 50 мкл 0,16 нмоль/л [33P]-S1P (выпускает фирма American Radiolabeled Chemicals), разведенного связывающим буфером, затем к нему добавляли раствор фракции мембран (50 мкл) и реакцию смеси проводили при комнатной температуре в течение 60 мин. После завершения реакции смесь фильтровали с отсасыванием с использованием 96-луночного UNIFILTER, промывали промывочным буфером (50 ммоль/л, Tris pH 7,5, 0,5% BSA) (150 мл) и затем сушили при температуре от 50 до 60°C в течение от 30 до 60 мин. К нему добавляли MicroScint (торговое название) 20 (50 мкл/лунка) и планшет закрывали с помощью TopSeal-A, затем радиоактивность измеряли с помощью TopCount (выпускает фирма Perkin Elmer).
[0230]
[Исследование]
Концентрацию соединения, при которой 50% специфического связывания [33P]-S1P с S1P1 человека и S1P5 человека заменено (значение IC50), использовали в качестве объекта исследования. Степень специфического связывания определяли путем вычитания степени неспецифического связывания [33P]-S1P (cpm - импульсы в минуту) из среднего значения (cpm) степени полного связывания [33P]-S1P (cpm) и степени связывания [33P]-S1P (cpm) при лечении разбавителем или соединением. Степень специфического связывания [33P]-S1P принимали за 100% и рассчитывали относительное значение (%) степени специфического связывания при каждой концентрации соединения. Из значений, использованных при лечении концентрации разбавителя или соединения, характеризующихся относительным значением (%)от 25 до 75%, выбирали концентрацию при лечении при которой проявлялось относительное значение, близкое к 50%, и значение IC50 рассчитывали путем замены относительного значения (%) и концентрации при лечении на Y и X соответственно, в следующей формуле.
Y=100 / (1+10X-logIC50)
[0231]
[Результаты]
В качестве сравнительного соединения C использовали гидрохлорид 3-({[6-(3-циклогексилпропокси)-1-метил-3,4-дигидро-2-нафталинил]метил}амино)пропановой кислоты, описанный в примере 31 (45) в патентной литературе 1. Сравнительное соединение C обладало ингибирующей активностью (значение IC50), равной 1,0 нмоль/л или 8,5 нмоль/л для связывания [33P]-S1P с S1P1 или S1P5 соответственно.
[0232]
(4) Биологический экспериментальный пример 4: Эффективность в модели экспериментального аутоиммунного энцефаломиелита на мышах
Использовали самок мышей C57BL/J (Charles River Laboratories Japan, Inc., возраст в начале эксперимента: 7 или 8 недель). Миелиновый олигодендроцитовый гликопротеин [последовательность 35-55 MEVGWYRSPFSRVVHLYRNGK (AnaSpec, Inc., ниже в настоящем изобретении MOG35-55)] растворяли в физиологическом растворе (Otsuka Pharmaceutical Factory, Inc.) и получали раствор концентрации 2 мг/мл. Раствор концентрации 2 мг/мл MOG35-55 и такое же количество FCA H37Ra (Difco Laboratories) смешивали и получали эмульсию и эмульсию использовали в качестве индуцирующего агента. Иммунизацию проводили путем подкожного введения 0,2 мл индуцирующего агента в бок мыши с помощью стеклянного шприца с иглой для инъекции 26G. День иммунизации определяли, как день 0 иммунизации и 0,2 мл раствора концентрации 1 мкг/мл токсина Pertussis (List Biological Laboratories) внутривенно вводили в хвостовую вену в день 0 и день 2 иммунизации (см. Cell Mol Immunol, Vol. 2, pp. 439-448, 2005).
[0233]
В день перед иммунизацией определяли массу тела и мышей равномерно разделяли на группы, так чтобы не наблюдалась значимое различие средних значений массы тела в каждой группе. После разделения на группы введение исследуемого соединения (соединение I), соединения для положительного контроля (FTY720; финголимод) или разбавителя (вода для инъекции) начинали в один и тот же день и каждое исследуемое соединение повторяющимся образом перорально вводили один раз в сутки в течение 30 дней от дня перед иммунизацией до дня 28 иммунизации. Количество вводимого раствора рассчитывали на основании индивидуальной массы тела в день введения.
[0234]
При исследовании неврологического симптома степень паралича описывали показателем, который использовали в качестве показателя неврологического симптома (0: нормальный, 1: обвислый хвост, 2: парез задних конечностей, 3: паралич задних конечностей, 4: паралич четырех конечностей, 5: состояние. близкое к смерти). Период наблюдения определен от дня перед иммунизацией и каждый день от дня 5 до дня 29 иммунизации и наблюдения проводили до введения исследуемого соединения и т. п. (см. Proc. Natl. Acad. Sci. USA, Vol. 103, pp. 13451-13456, 2006).
[0235]
[Результаты]
Соединение I показало эффективность в этой модели.
[0236]
(5) Исследование химической стабильности
Стабильность солей и/или кристаллических форм, предлагаемых в настоящем изобретении, исследовали при хранении в условиях 1 или условиях 2. После хранения остаточное содержание (%) хранимого образца при всех условиях рассчитывали с помощью HPLC на основе выраженной в процентах площади для образца, хранившегося при -20°C.
[0237]
<Условия и времена хранения>
Условия 1. 60°C: 1 месяц: измельченный
Условия 2. 80°C: 1 неделя: неизмельченный
Сравнительный вариант каждого образца хранили при -20°C.
[0238]
[Результаты]
Остаточные содержания (%) соединений, предлагаемых в настоящем изобретении, после хранения при условиях 1 приведены в таблице 12 и остаточные содержания (%) соединений, предлагаемых в настоящем изобретении, после хранения при условиях 2 приведены в таблице 13.
[Таблица 12]
[0239]
[Таблица 13]
Установлено, что соединение, предлагаемое в настоящем изобретении, превосходно по химической стабильности. Соединение, обладающее остаточным содержанием, равным 99% или более, после хранения при условиях 1 и/или условиях 2 является особенно предпочтительным для использования в качестве лекарственного вещества для фармацевтического препарата.
[0240]
[Примеры получения]
Пример получения 1
Путем смешивания следующих компонентов обычным образом и последующего таблетирования получали примерно 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента.
Кристалл D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты... 100 г
Кальциевая соль карбоксиметилцеллюлозы (разрыхлитель)... 20 г
Стеарат магния (смазывающее вещество)... 10 г
Микрокристаллическая целлюлоза... 870 г
[0241]
Пример получения 2
Следующие компоненты смешивали обычным образом и затем фильтровали через фильтр для улавливания пыли и аликвоты по 5 мл помещали в ампулы и ампулы термически стерилизовали в автоклаве и получали примерно 10000 ампул, каждая из которых содержит 20 мг активного ингредиента.
Кристалл D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты... 200 г
Маннит... 20 г
Дистиллированная вода... 50 л
ПРОМЫШЛЕННОЕ ПРИМЕНЕНИЕ
[0242]
Соединение I обладает селективной агонистической активностью по отношению к рецептору S1P5 и поэтому применимо для лечения опосредуемых S1P5 заболеваний, например, нейродегенеративных заболеваний и т. п. Кроме того, соли и/или кристаллические формы, предлагаемые в настоящем изобретении, применимы в качестве лекарственных веществ для фармацевтических препаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ АГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РЕЦЕПТОРУ S1P5 | 2019 |
|
RU2781541C2 |
| СРЕДСТВА, СТИМУЛИРУЮЩИЕ РОСТ ВОЛОС | 2005 |
|
RU2342384C2 |
| КРИСТАЛЛ 3-(ДИФТОРМЕТИЛ)-1-МЕТИЛ-N-(1,1,3-ТРИМЕТИЛ-2,3-ДИГИДРО-1H-ИНДЕН-4-ИЛ)-1H-ПИРАЗОЛ-4-КАРБОКСАМИДА | 2020 |
|
RU2834648C1 |
| ПОЛИМОРФНЫЕ И АМОРФНЫЕ ФОРМЫ {2-ФТОР-5-[3-((Е)-2-ПИРИДИН-2-ИЛВИНИЛ)-1Н-ИНДАЗОЛ-6-ИЛАМИНО]ФЕНИЛ}АМИДА 2,5-ДИМЕТИЛ-2Н-ПИРАЗОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2005 |
|
RU2324692C1 |
| КРИСТАЛЛЫ 3,5-ДИЗАМЕЩЕННОГО БЕНЗОЛАЛКИНИЛЬНОГО СОЕДИНЕНИЯ | 2016 |
|
RU2672563C1 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 1-(5'-(5-(3,5-ДИХЛОРО-4-ФТОРФЕНИЛ)-5-(ТРИФТОРМЕТИЛ)-4,5-ДИГИДРОИЗОКСАЗОЛ-3-ИЛ)-3'Н-СПИРО[АЗЕТИДИН-3,1'-ИЗОБЕНЗОФУРАН]-1-ИЛ)-2-(МЕТИЛСУЛЬФОНИЛ)ЭТАНОНА | 2013 |
|
RU2614978C2 |
| ПОЛИМОРФНЫЕ МОДИФИКАЦИИ N-[(3-ФТОР-4-МЕТОКСИПИРИДИН-2-ИЛ)МЕТИЛ]-3-(МЕТОКСИМЕТИЛ)-1-({ 4-[(2-ОКСОПИРИДИН-1-ИЛ)МЕТИЛ]ФЕНИЛ} МЕТИЛ)ПИРАЗОЛ-4-КАРБОКСАМИДА И ИХ СОЛИ | 2017 |
|
RU2756273C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА TLR7/TLR8 | 2019 |
|
RU2792005C2 |
| СОЛИ И ТВЕРДЫЕ ФОРМЫ МОНОБАКТАМНОГО АНТИБИОТИКА | 2016 |
|
RU2754180C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОИЗВОДНЫХ ДИГИДРОПИРИМИДИНА | 2013 |
|
RU2646599C2 |
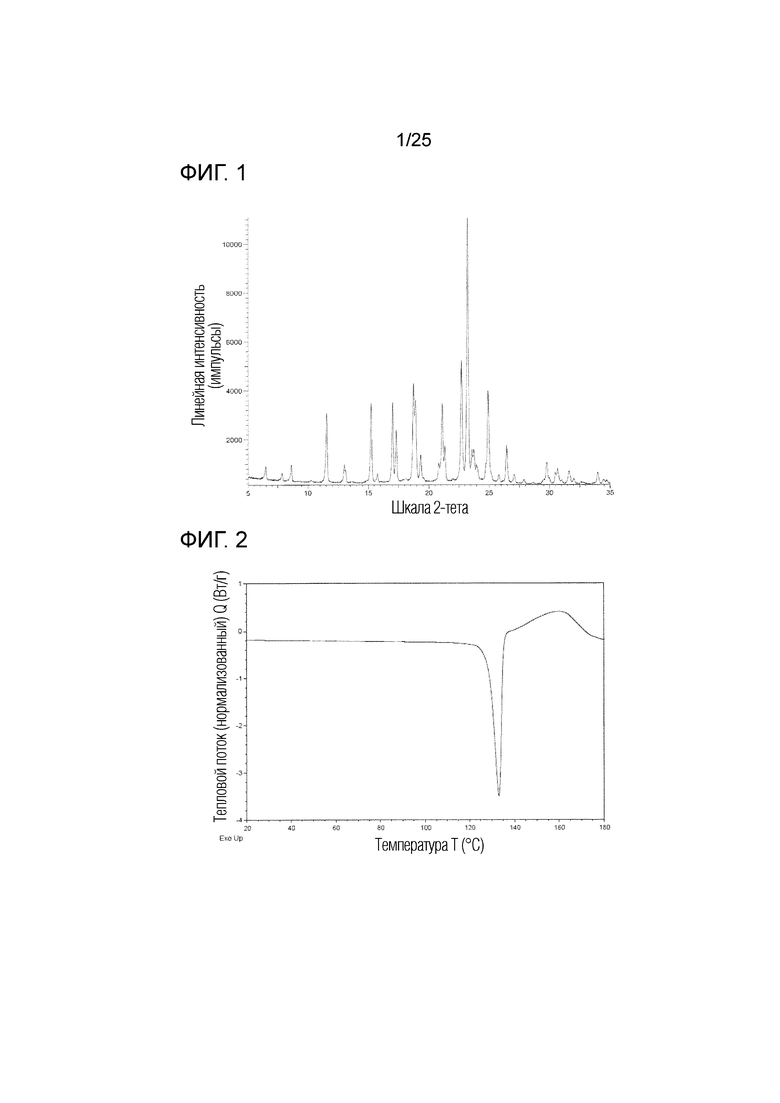
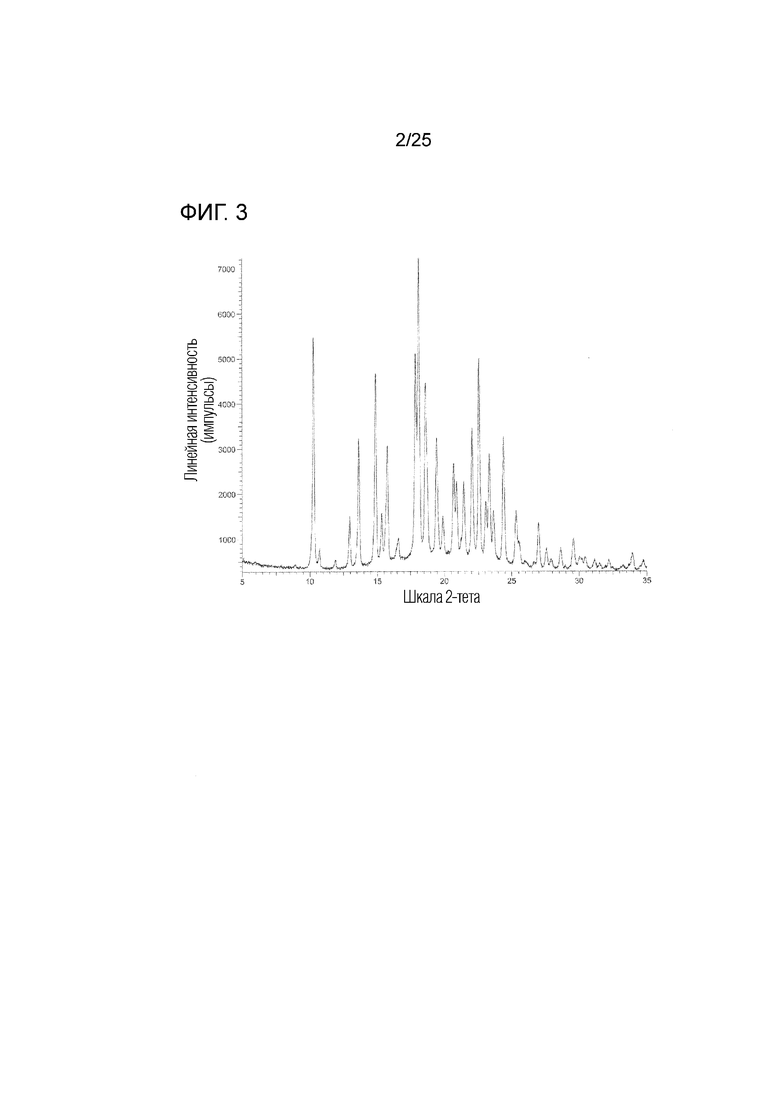
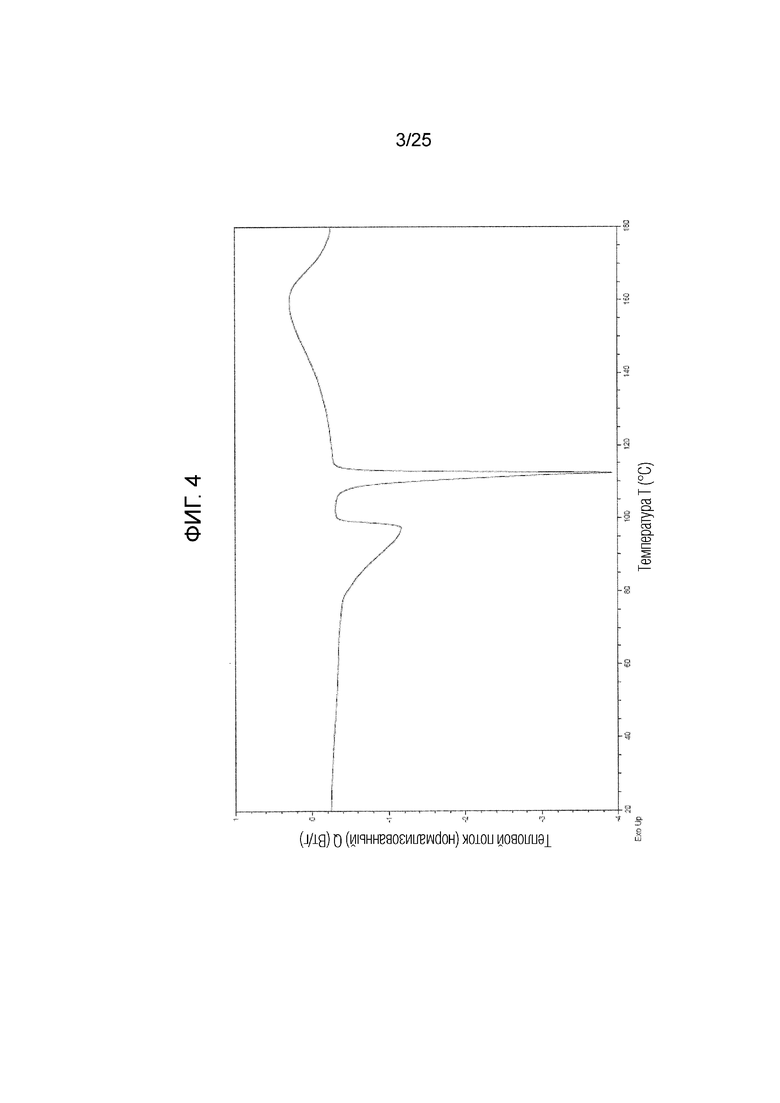
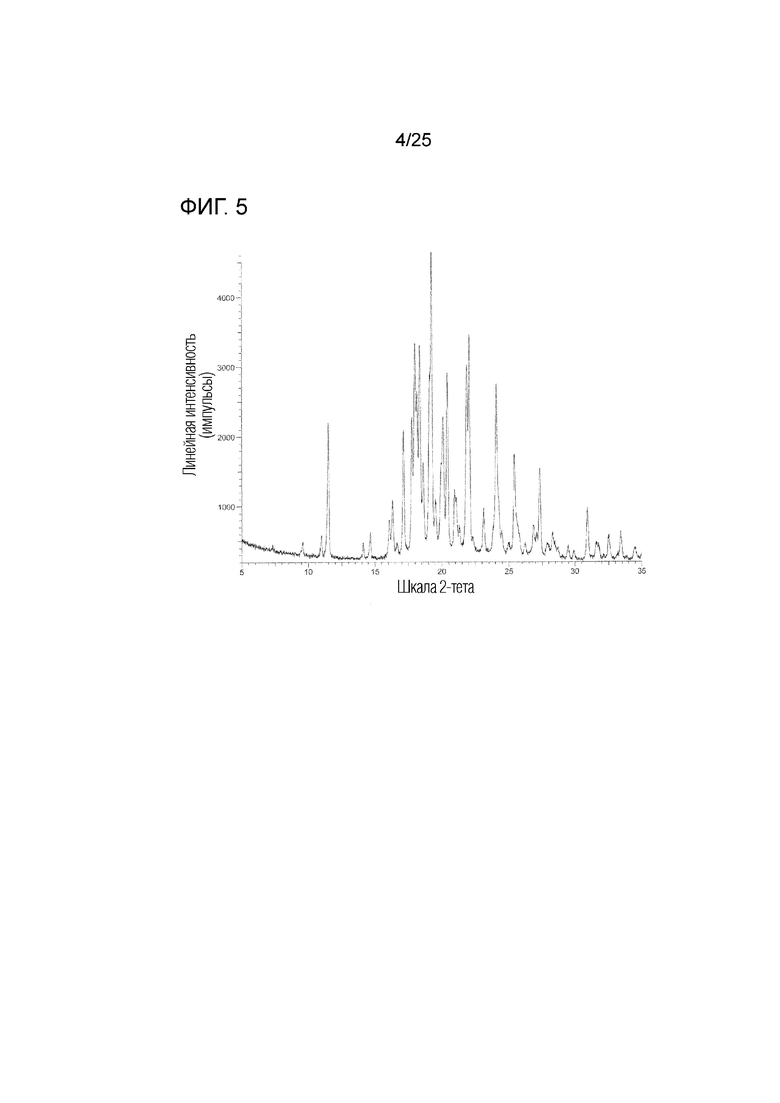
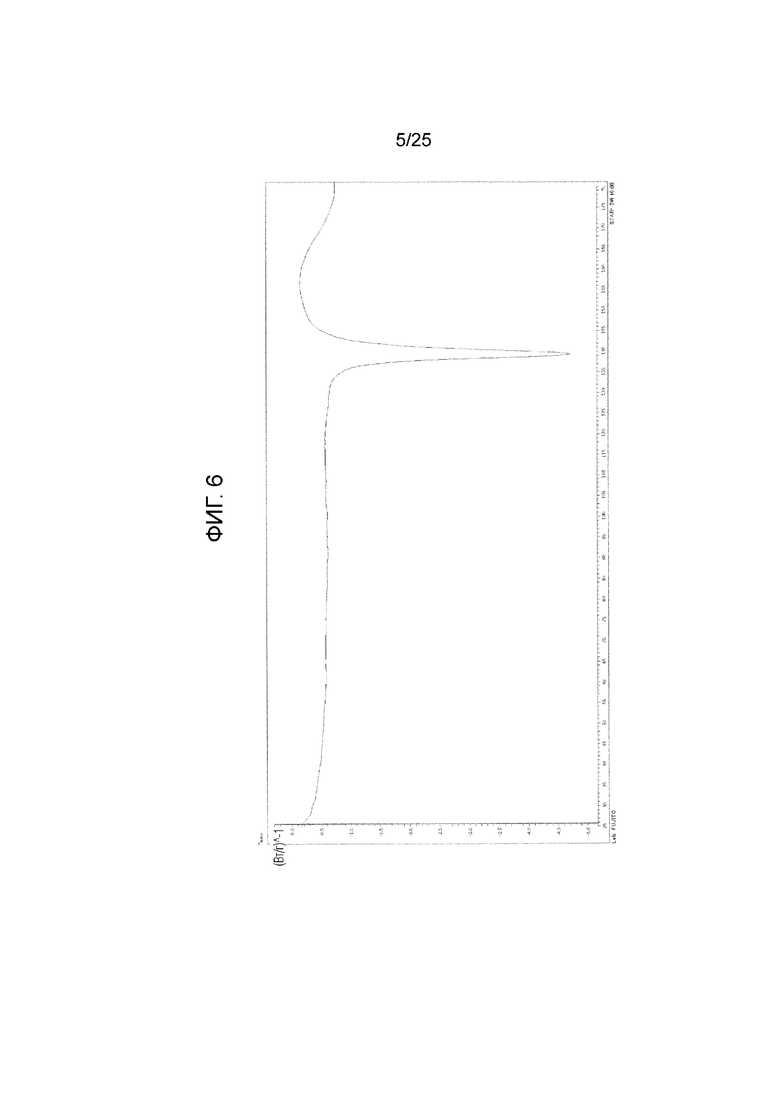
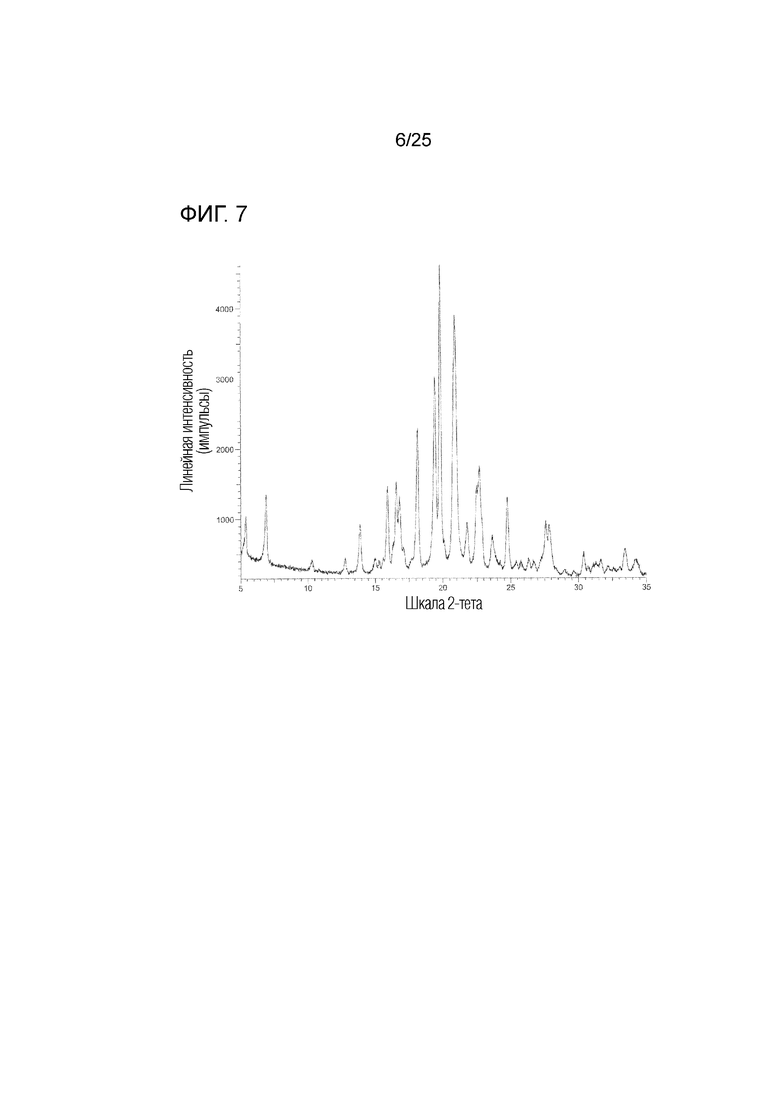
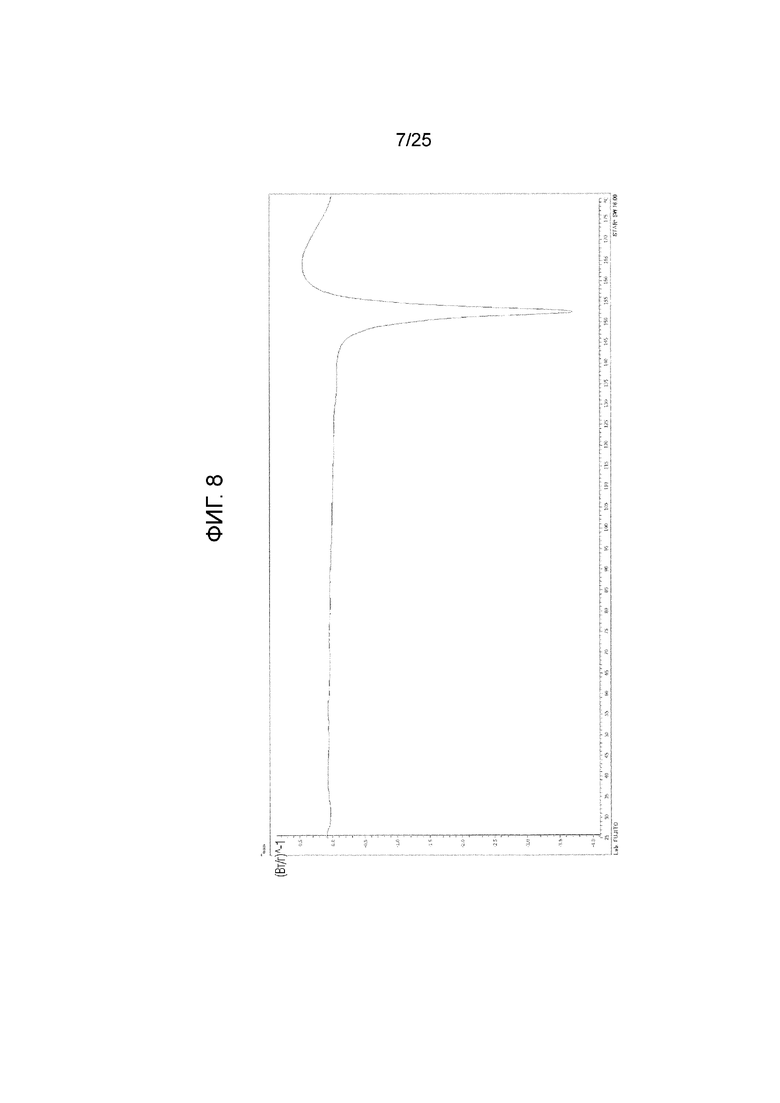
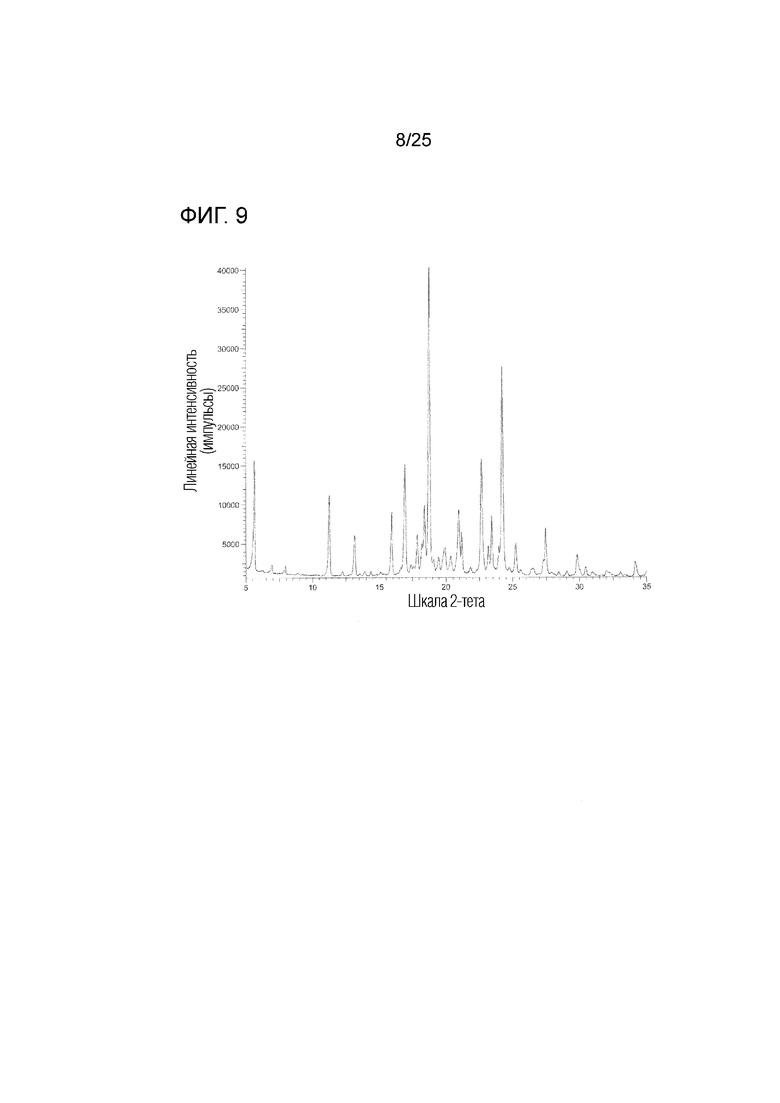
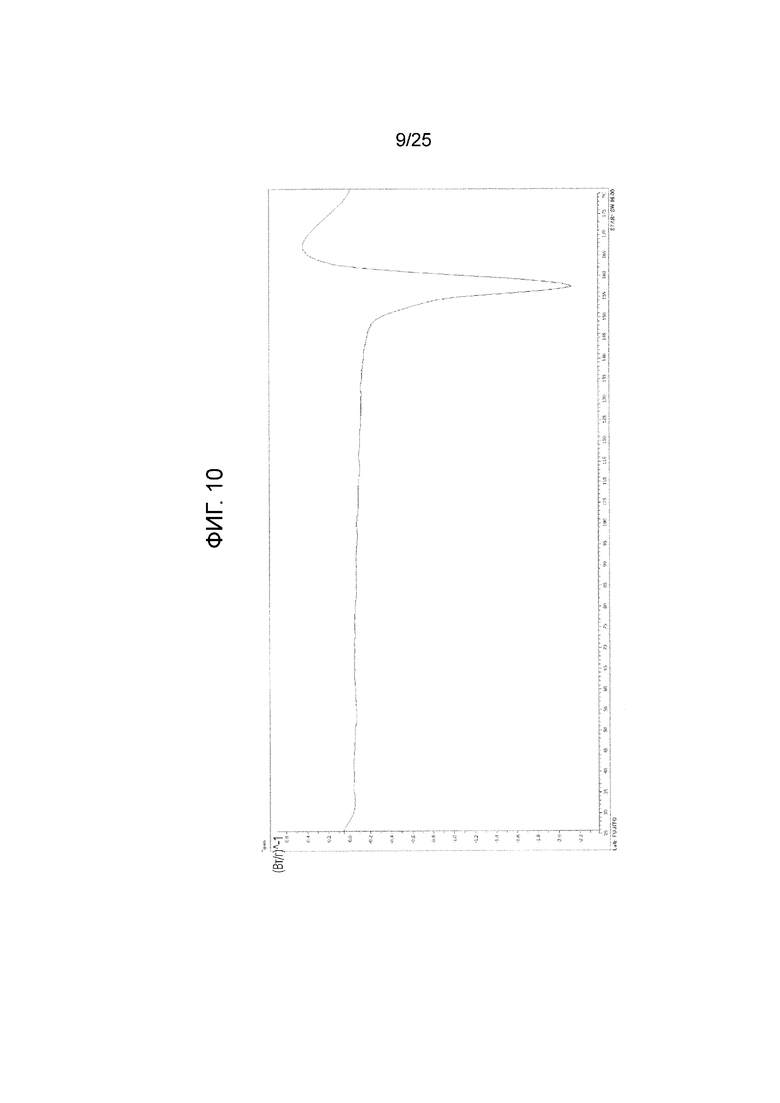
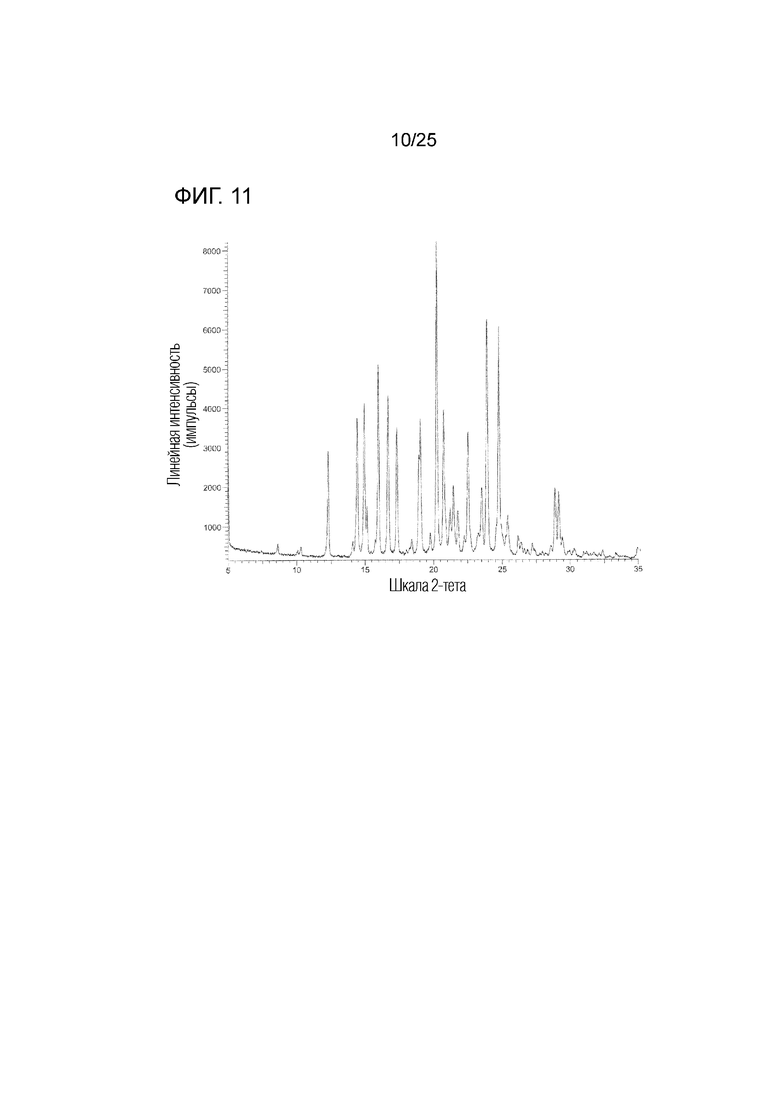
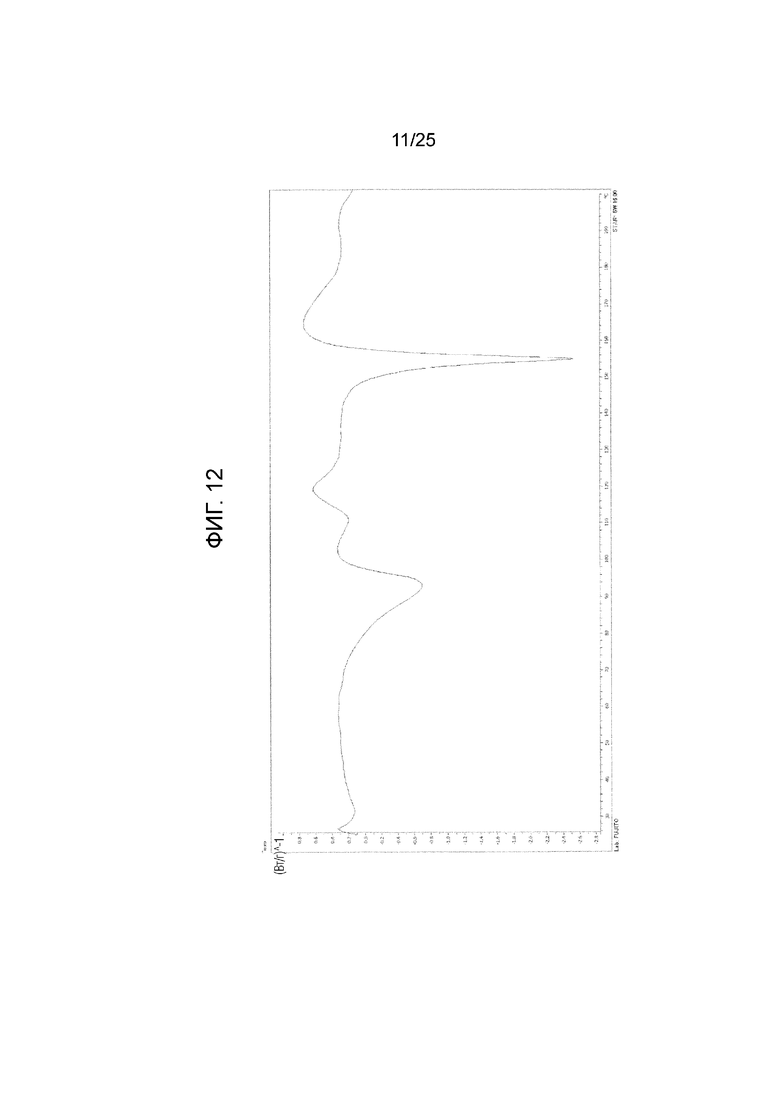
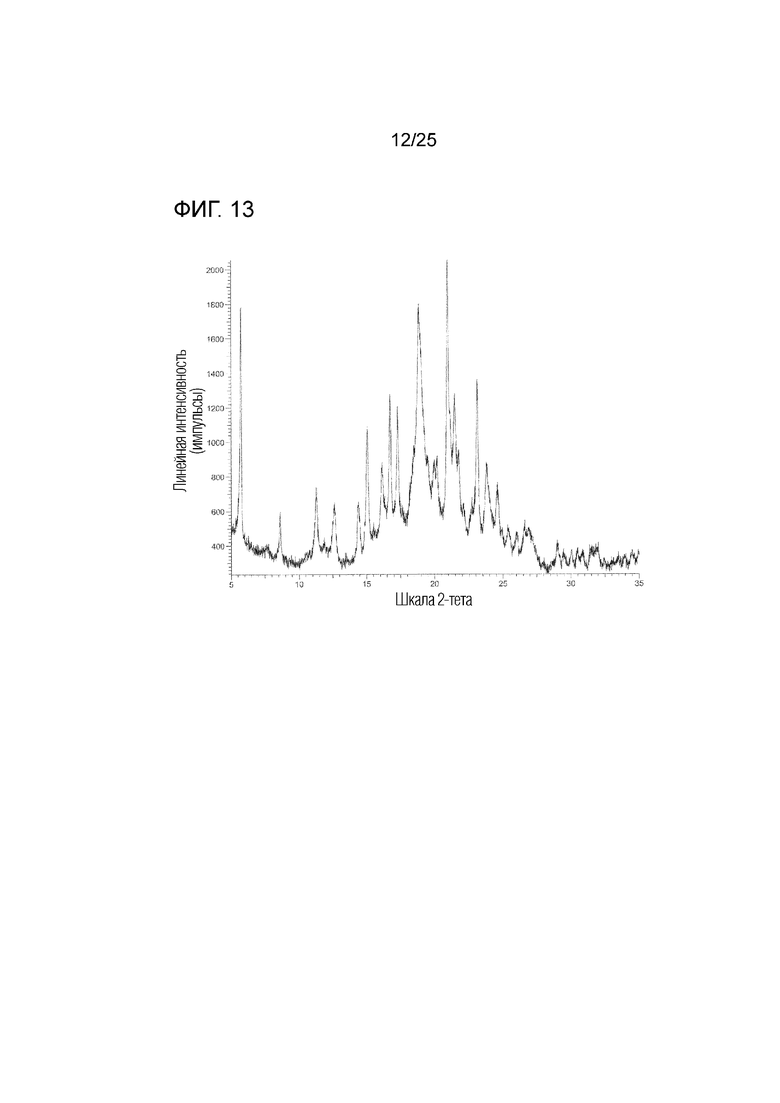
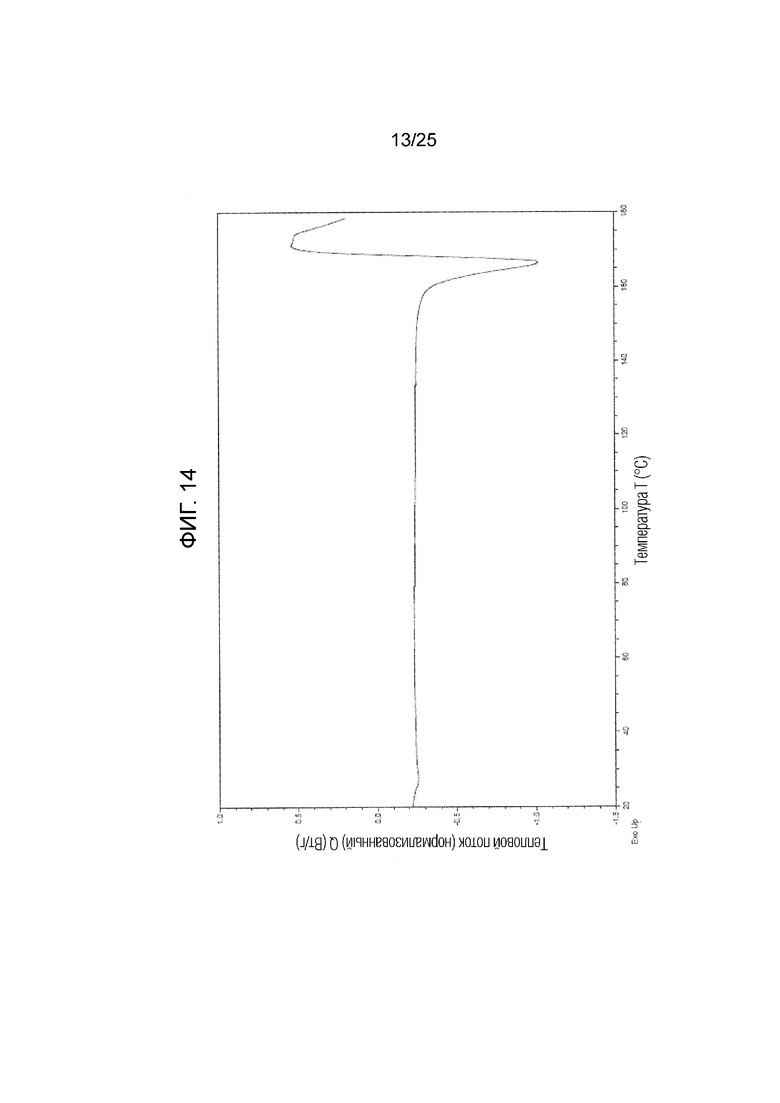
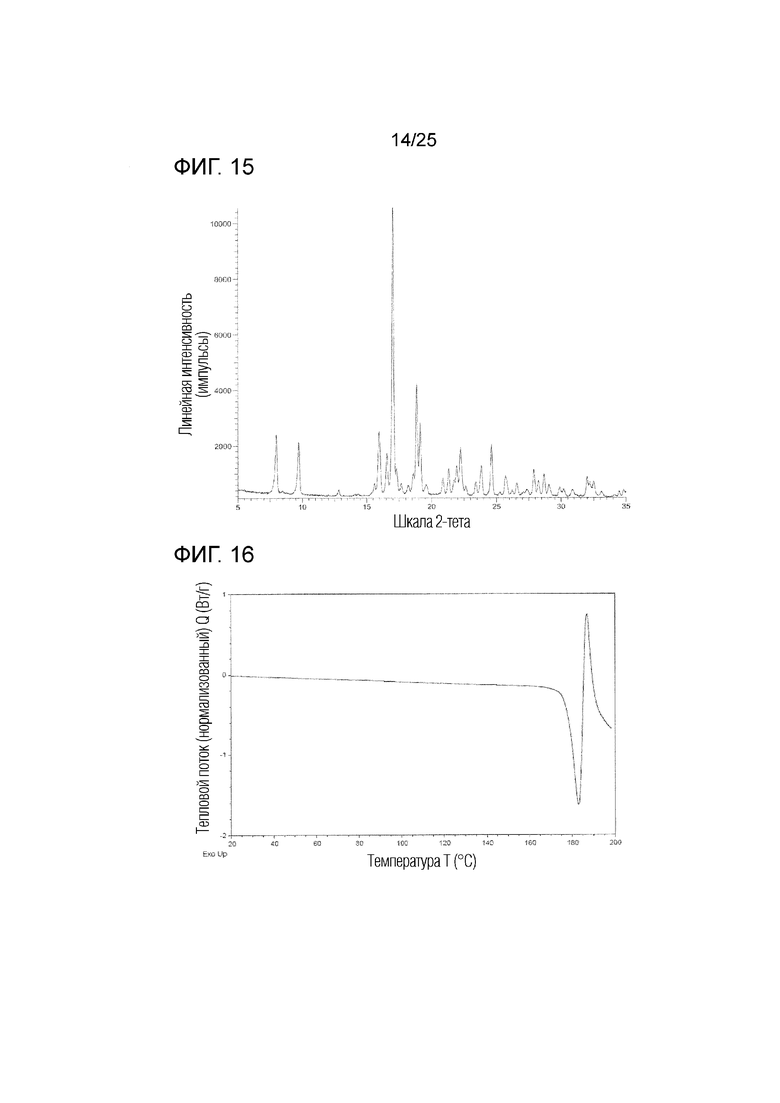
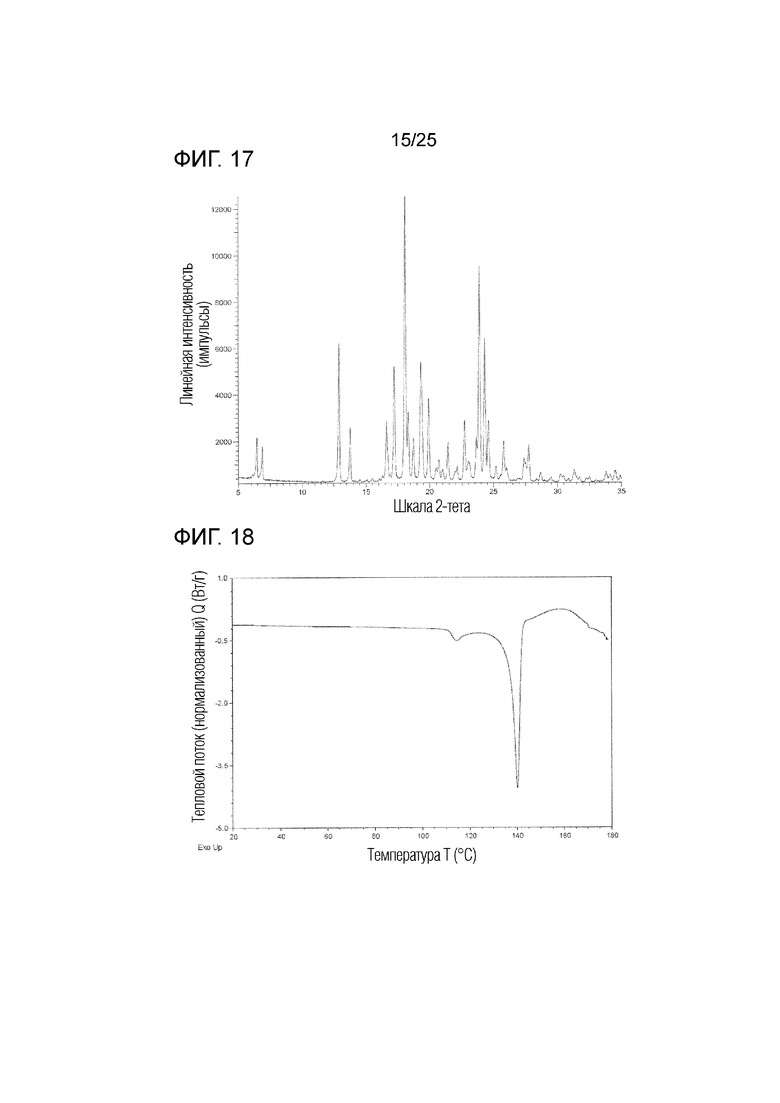
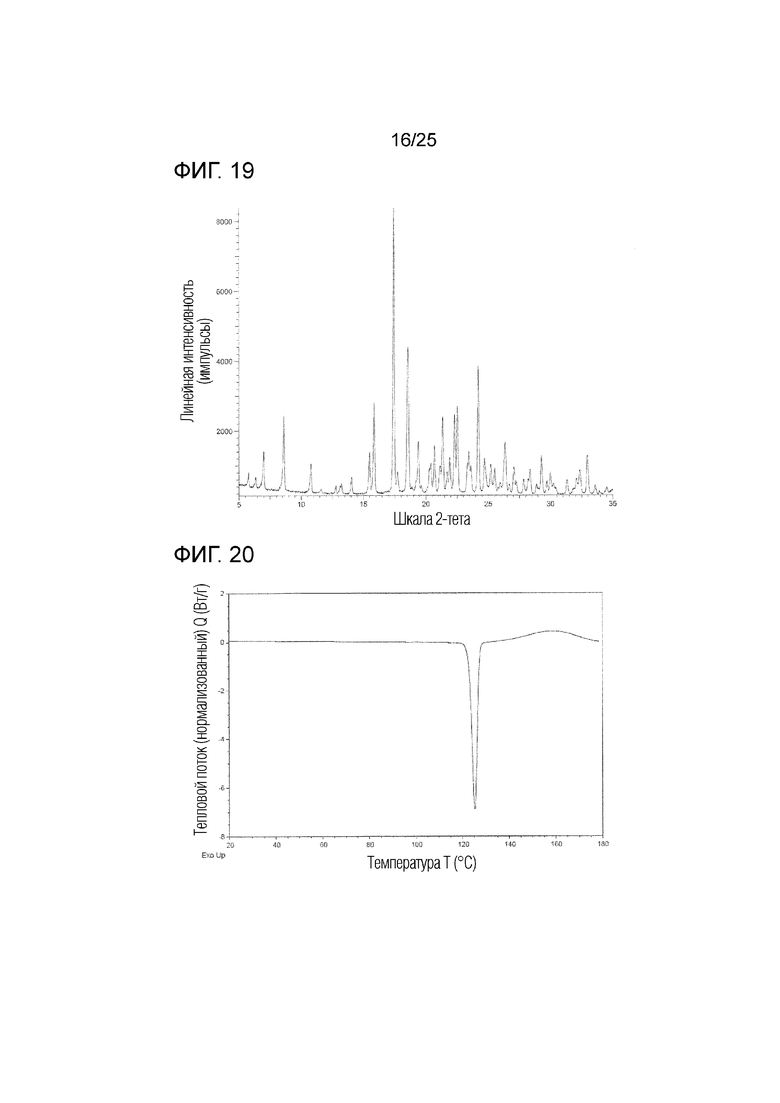
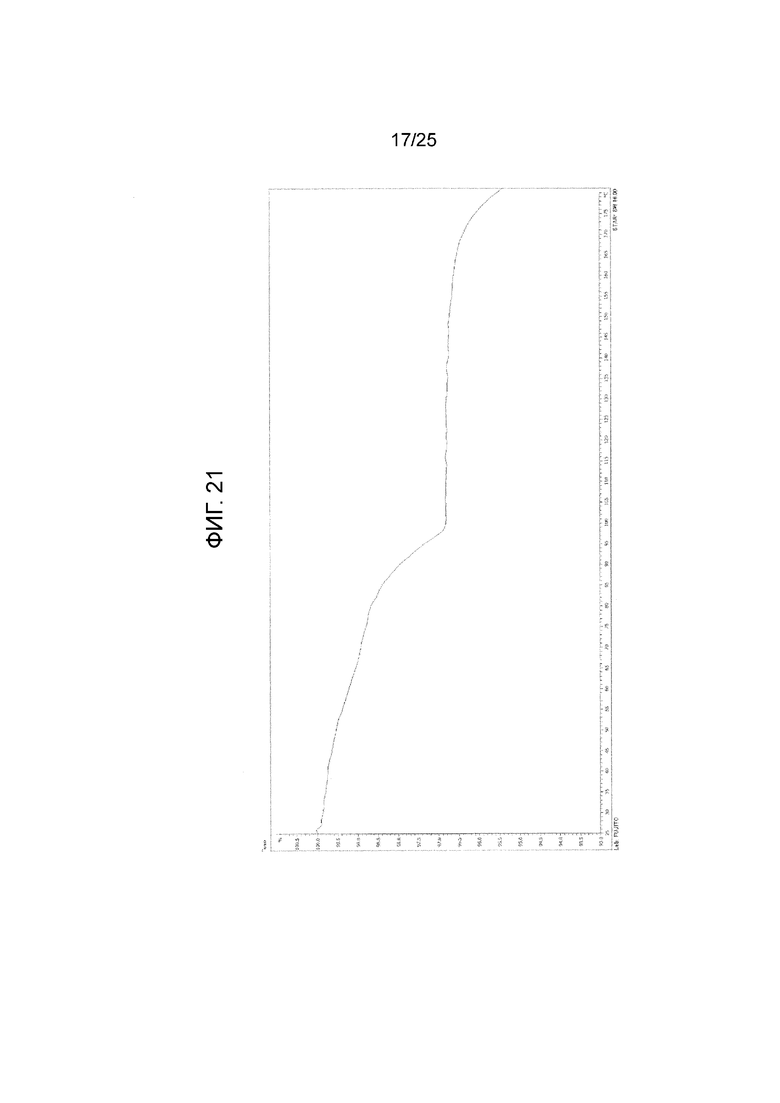
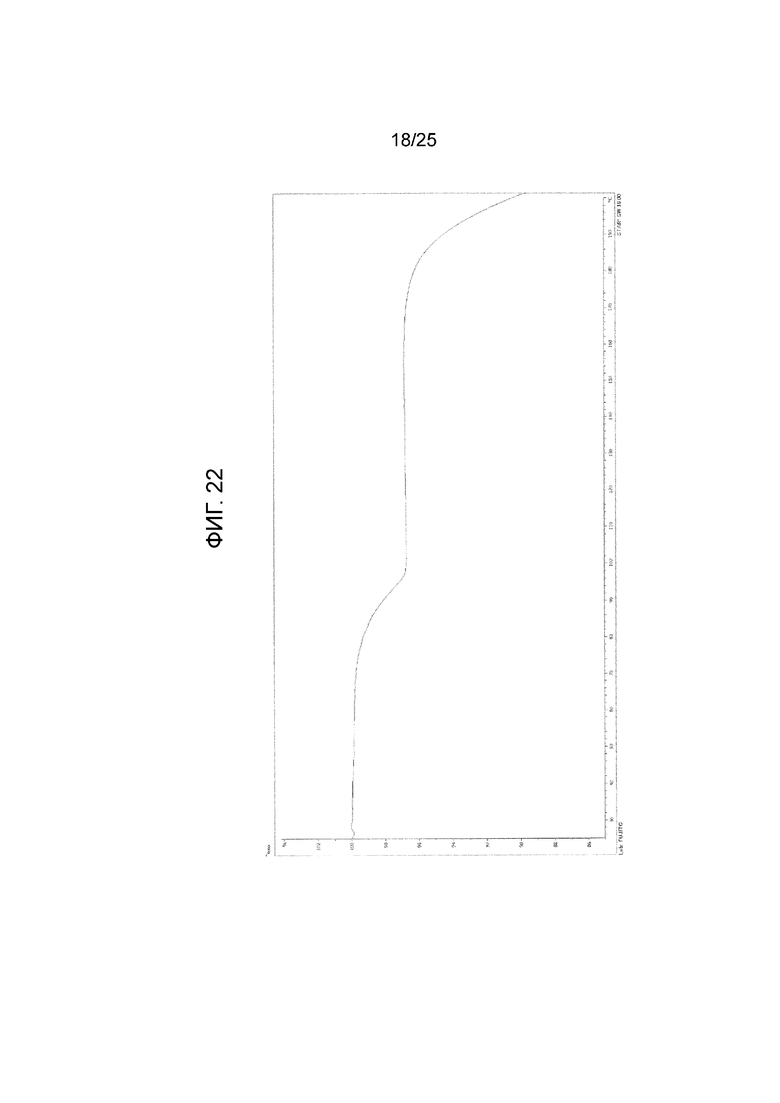
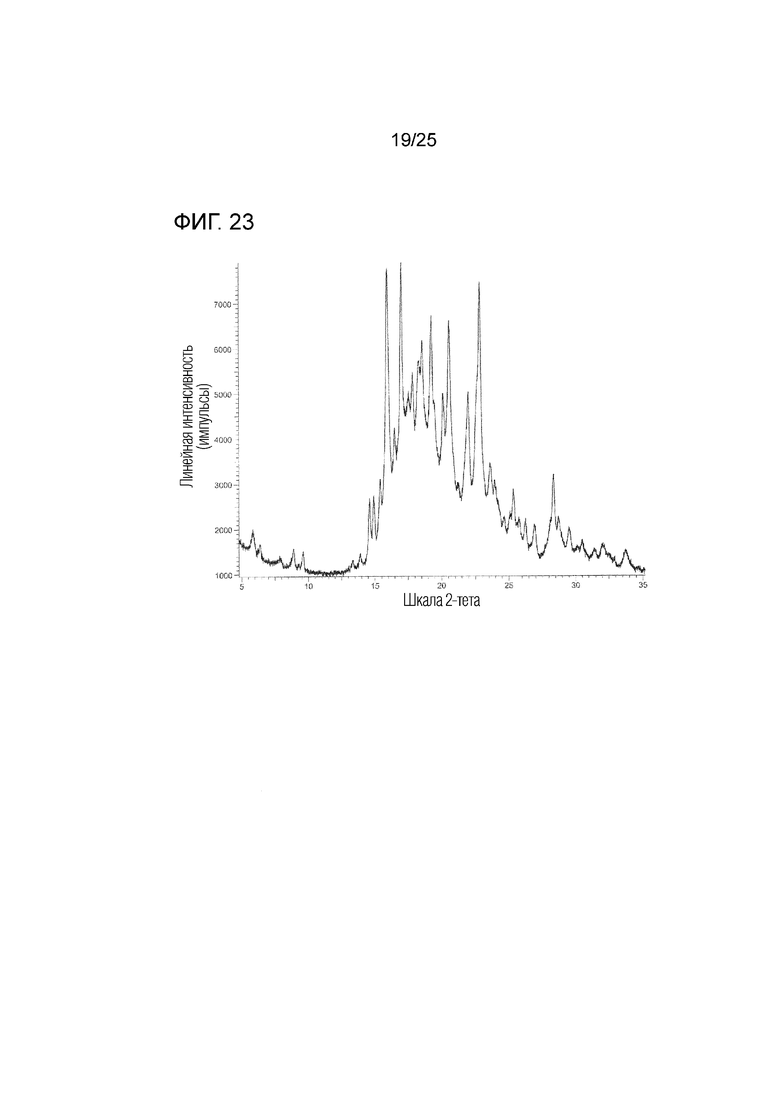
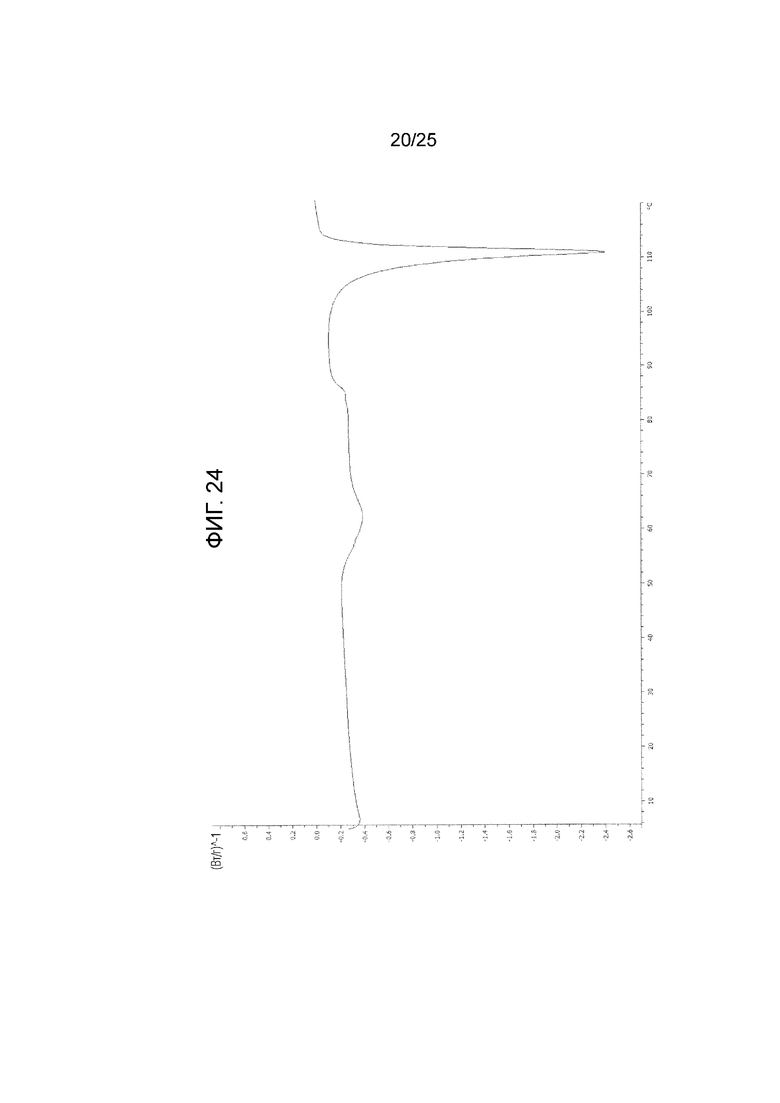
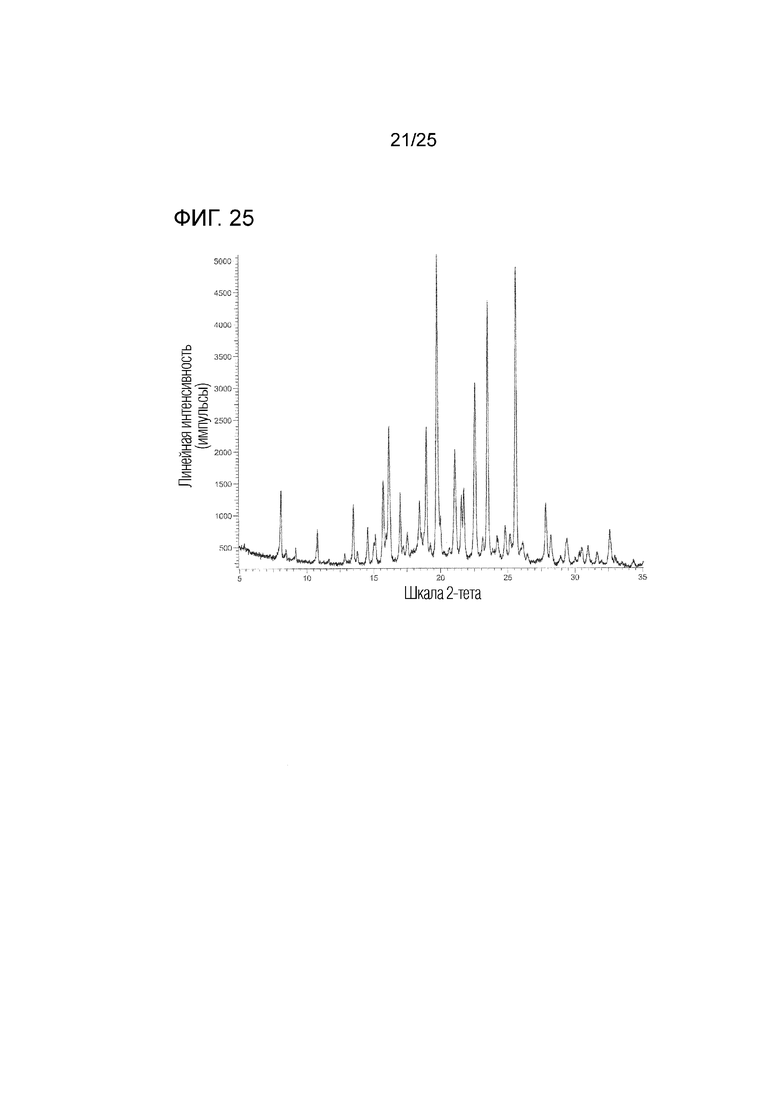
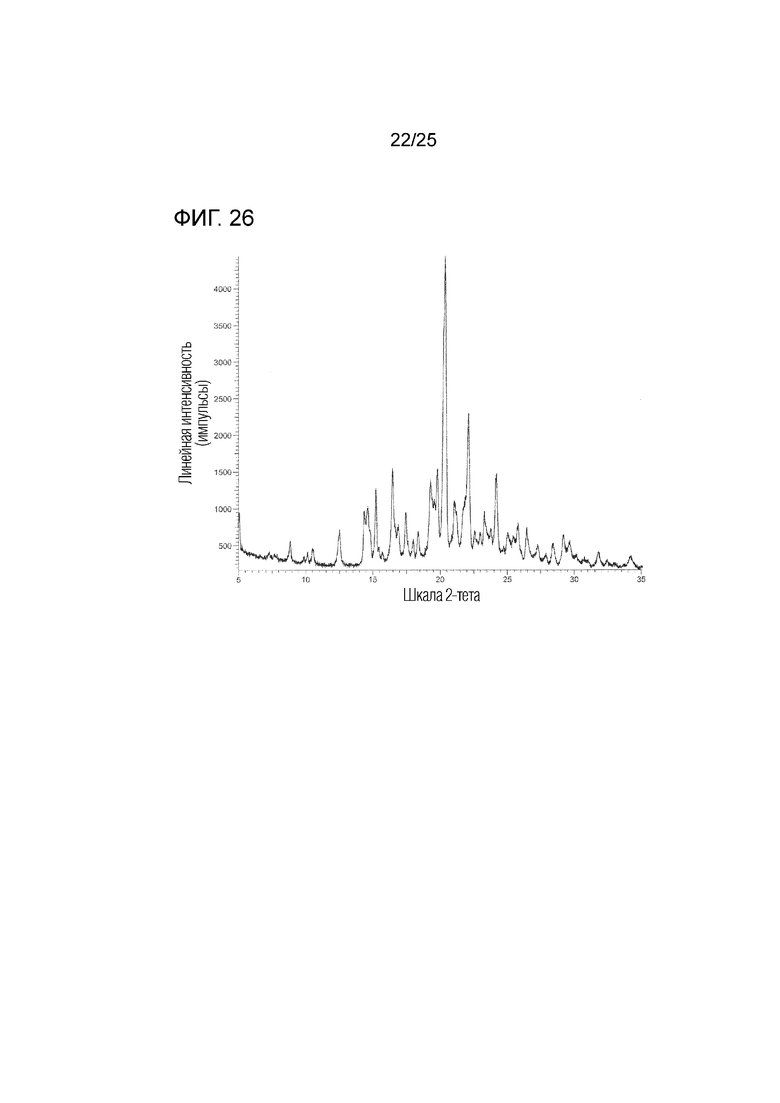
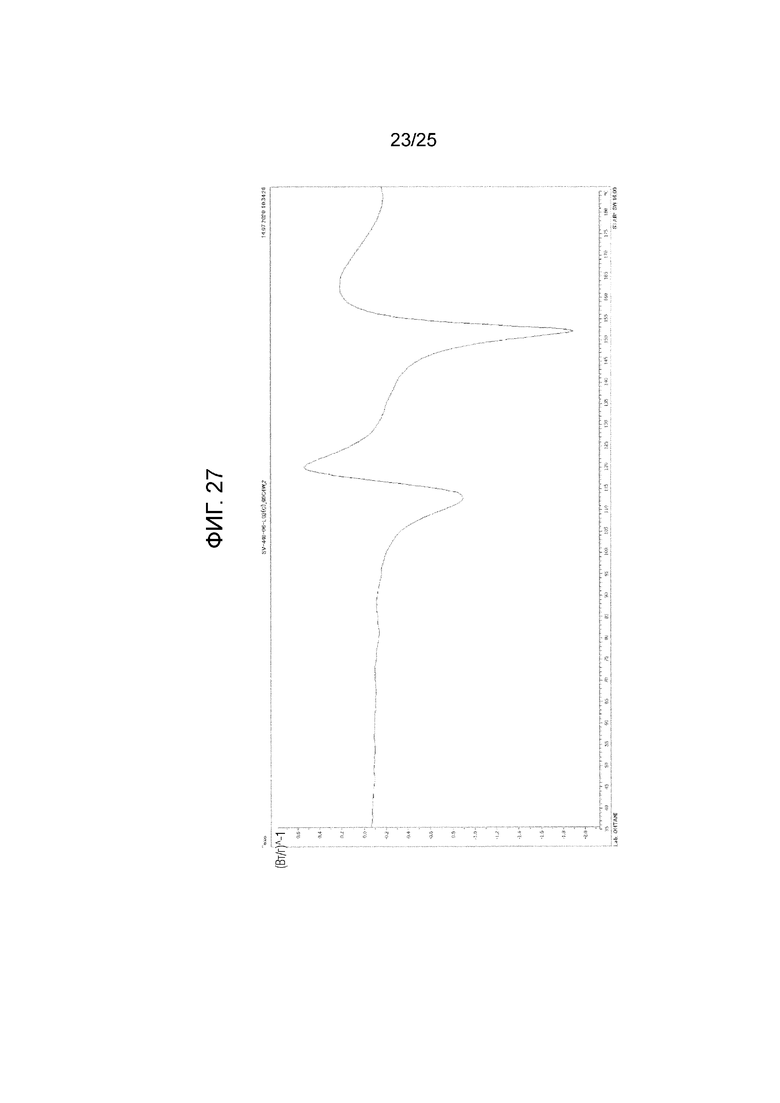
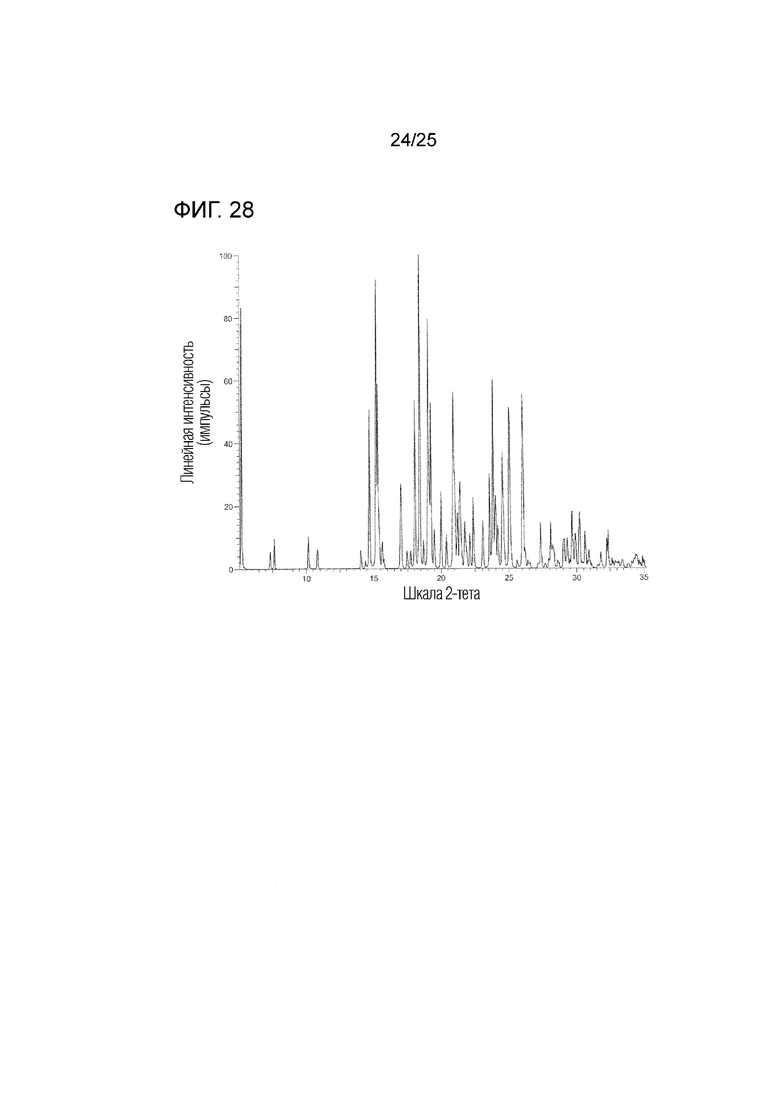
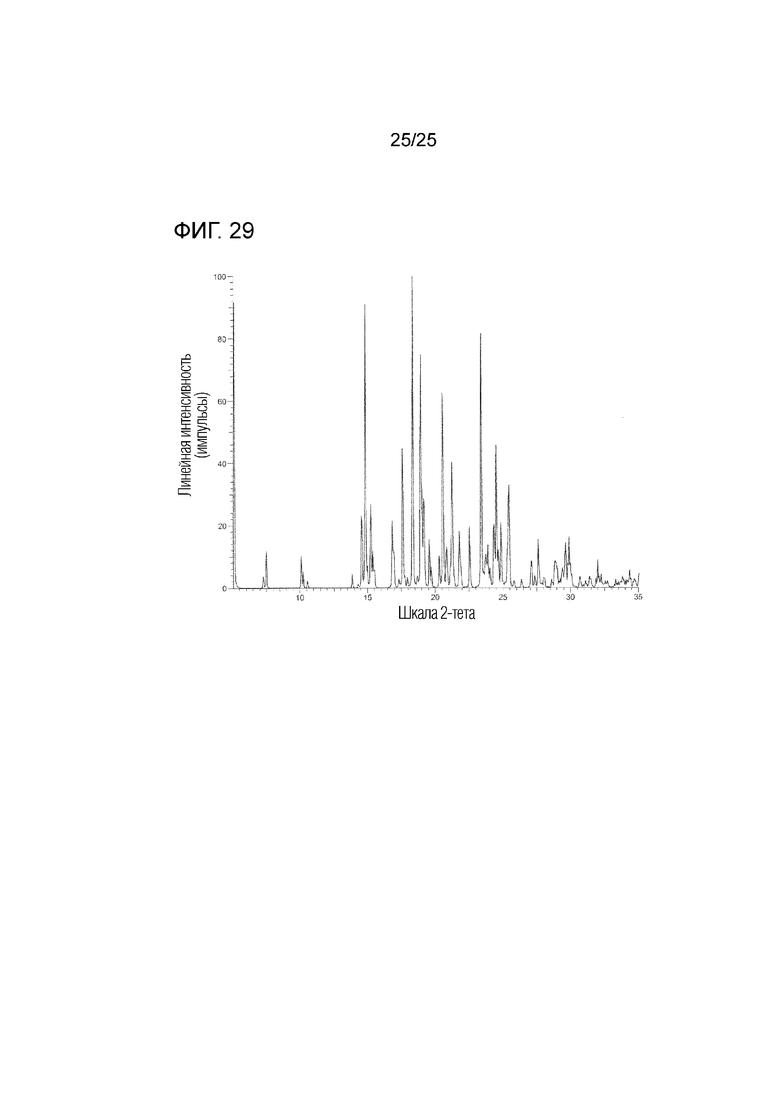
Изобретение относится к соли 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, где солью является моно(4-гидроксибензоат). Изобретение относится к кристаллической форме А моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, содержащей на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере 6,9±0,2 градуса, 12,8±0,2 градуса, 13,9±0,2 градуса и 2 4,7±0,2 градуса. Также изобретение относится к фармацевтической композиции, обладающей агонистической активностью по отношению к рецептору S1P5, содержащей фармацевтически эффективное количество соединения по изобретению и фармацевтически приемлемый носитель. Способ получения кристаллической формы А моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты по изобретению включаюет стадии смешивания кристалла D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, содержащего на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ) (приведены в формуле изобретения), и 4-гидроксибензойной кислоты; добавления ацетонитрила к полученной смеси при комнатной температуре; перемешивания полученной смеси в течение ночи; фильтрования суспендированых кристаллов и сушки кристаллов при 50°С при пониженном давлении в течение 3 ч. Технический результат - моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты для применения для предупреждения и/или лечения опосредуемого S1P5 заболевания. 7 н. и 10 з.п. ф-лы, 29 ил., 18 табл., 25 пр.
1. Соль 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, где солью является моно(4-гидроксибензоат).
2. Кристаллическая форма А моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, содержащая на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере 6,9±0,2 градуса, 12,8±0,2 градуса, 13,9±0,2 градуса и 2 4,7±0,2 градуса.
3. Кристаллическая форма по п. 2, содержащая на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере 5,4±0,2 градуса, 6,9±0,2 градуса, 13,9±0,2 градуса, 18,1±0,2 градуса, 19,4±0,2 градуса, 19,8±0,2 градуса, 20,9±0,2 градуса и 24,7±0,2 градуса.
4. Кристаллическая форма по п. 2 или 3, не содержащая на порошковой рентгенограмме дифракционный пик при углах дифракции (2θ), равных 11,3±0,2 градуса и 14,4±0,2 градуса.
5. Кристаллическая форма по любому из пп. 2-4, содержащая на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных 5,4±0,2 градуса, 6,9±0,2 градуса, 10,3±0,2 градуса, 12,8±0,2 градуса, 13,9±0,2 градуса, 15,0±0,2 градуса, 15,3±0,2 градуса, 15,9±0,2 градуса, 16,6±0,2 градуса, 16,8±0,2 градуса, 18,1±0,2 градуса, 19,4±0,2 градуса, 19,8±0,2 градуса, 20,9±0,2 градуса, 21,8±0,2 градуса, 22,7±0,2 градуса, 23,6±0,2 градуса, 24,7±0,2 градуса, 25,4±0,2 градуса, 25,8±0,2 градуса, 26,3±0,2 градуса, 26,7±0,2 градуса, 27,6±0,2 градуса, 27,8±0,2 градуса, 30,3±0,2 градуса, 33,4±0,2 градуса и 34,2±0,2 градуса.
6. Кристаллическая форма по любому из пп. 2-5, характеризующаяся порошковой рентгенограммой, приведенной на фиг. 7.
7. Кристаллическая форма по любому из пп. 2-6, обладающая эндотермическим пиком с температурой начала, равной 150°С±2°С, или температурой пика, равной 153°С±2°С, по данным дифференциальной сканирующей калориметрии.
8. Кристаллическая форма по любому из пп. 2-7, характеризующаяся термограммой дифференциальной сканирующей калориметрии, приведенной на фиг.8.
9. Фармацевтическая композиция, обладающая агонистической активностью по отношению к рецептору S1P5, содержащая фармацевтически эффективное количество соединения по любому из пп. 1-8 и фармацевтически приемлемый носитель.
10. Фармацевтическая композиция по п. 9, которая является профилактическим и/или терапевтическим средством для опосредуемого S1P5 заболевания.
11. Фармацевтическая композиция по п. 10, где опосредуемым S1P5 заболеванием является нейродегенеративное заболевание.
12. Фармацевтическая композиция по п. 11, где нейродегенеративным заболеванием является мультисистемная атрофия или болезнь Паркинсона.
13. Профилактическое и/или терапевтическое средство для опосредуемого S1P5 заболевания, содержащее соединение по любому из пп. 1-8.
14. Способ предупреждения и/или лечения опосредуемого S1P5 заболевания, включающий введение млекопитающему эффективного количества соединения по любому из пп. 1-8.
15. Соединение по любому из пп. 1-8 для применения для предупреждения и/или лечения опосредуемого S1P5 заболевания.
16. Применение соединения по любому из пп. 1-8 для приготовления профилактического и/или терапевтического средства для опосредуемого S1P5 заболевания.
17. Способ получения кристаллической формы А моно(4-гидроксибензоата) 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, содержащей на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), равных по меньшей мере 6,9±0,2 градуса, 12,8±0,2 градуса, 13,9±0,2 градуса и 24,7±0,2 градуса,
включающий стадии:
смешивания кристалла D 1-[[(3S)-3-метил-6-(4,4,4-трифторбутокси)-3,4-дигидронафталин-2-ил]метил]азетидин-3-карбоновой кислоты, содержащего на порошковой рентгенограмме дифракционные пики при углах дифракции (2θ), представленные в Таблице:
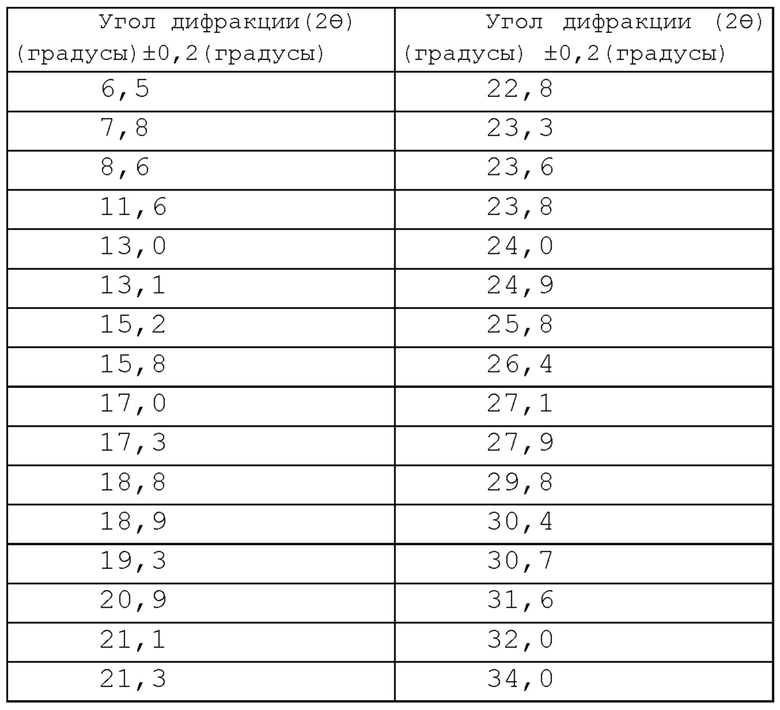
и 4-гидроксибензойной кислоты;
добавления ацетонитрила к полученной смеси при комнатной температуре;
перемешивания полученной смеси в течение ночи;
фильтрования суспендированых кристаллов и
сушки кристаллов при 50°С при пониженном давлении в течение 3 ч.
| ПРОИЗВОДНОЕ АМИНОКАРБОНОВОЙ КИСЛОТЫ И ПРИМЕНЕНИЕ УКАЗАННОГО ВЕЩЕСТВА В МЕДИЦИНСКИХ ЦЕЛЯХ | 2005 |
|
RU2433121C2 |
| EP 1826197 B1, 18.01.2012 | |||
| WO 2016088834 A1, 09.06.2016 | |||
| СОЕДИНЕНИЕ, СПОСОБНОЕ К СВЯЗЫВАНИЮ С РЕЦЕПТОРОМ S1P, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2390519C2 |
| Richard J.Bastin et al.: "Salt selection and Optimisation Procedures for Pharmaceutical New Chemical Entities", ORGANIC PROCESS RESEARCH & DEVELOPMENT, 2000, vol.4, p.427-435 | |||
| Sarma B | |||
| et al | |||
| Solid formation of pharmaceuticals: | |||
Авторы
Даты
2025-01-20—Публикация
2020-08-19—Подача