Заявленное изобретение относится к области биологии, а в частности к медицине, ветеринарии, биохимии, и может быть применимо для удовлетворения потребностей человека.
Описание проблемы
Болезни, травмы, врожденные пороки развития неизбежно сопровождают человека на протяжении всего исторического процесса и закономерно, что их присутствие в жизни людей порождает бесконечный поиск возможностей преодоления преград на пути к здоровью. Среди прочих идея об одном способе исцеления живет в сознании человечества еще со времен древнегреческих мифов о Прометее. Восстановление утраченных тканей и их функций в древности считалось подлинным волшебством, но развитие науки и техники сегодня позволяет приблизить чудо к реальности. С середины 1980-х годов регенеративная медицина из теоретического понятия превратилась в обширное поле для научной деятельности. Первый раз официально термин «тканевая инженерия» озвучен профессором Y. Fung в 1987 г. (Университет Калифорнии, Сан-Диего, США), несколько позднее появился термин «регенеративная медицина». Для некоторых ученых регенеративная медицина ассоциирована с использованием стволовых клеток, для других - это более широкое понятие, а тканевая инженерия составляет только часть этой области, третьи же считают термины «регенеративная медицина» и «тканевая инженерия» взаимозаменяемыми. Основными предпосылками развития регенеративной медицины стали глобальные проблемы трансплантологии и реконструктивной хирургии, среди которых перманентный недостаток донорских тканей и органов и высокая смертность пациентов в ожидании донора, необходимость пожизненной иммуносупрессивной терапии, нехватка аутотканей и их биологические изменения в новой локации, невозможность полной биологической интеграции искусственных протезов. Кожа, костная ткань, хрящи, сосуды - это лишь некоторые примеры органов и тканей, которые возможно создать в лаборатории благодаря регенеративной медицине; каждый день данный список неизменно расширяется. На данный момент сложно найти область медицины, где бы разработки тканевой инженерии и клеточной терапии не были востребованы.
Согласно общепринятым понятиям, регенеративная медицина определяется как область исследований, в которой поврежденные ткани и органы восстанавливаются под действием искусственно контролируемой регенерации, витального биологического процесса, индуцирующего клеточную дифференцировку и рост. Глобально для исследователей в регенеративной медицине существует 3 области интереса: изучение клеток, возможность использования нативных и синтезируемых биокаркасов (скаффолдов), применение различных рекомбинантных факторов роста и других клеточных мишеней.
Многочисленные исследования в регенеративной медицине направлены на изучение клеток как основного «регенераторного» материала. Они образуют основу всех тканей, поэтому представить процесс регенерации без их участия невозможно. В ряде случаев организму хватает собственных клеточных ресурсов для восстановления в месте повреждения. Однако при прогнозе недостаточности ресурсов внутренней среды для адекватного завершения регенеративных процессов и реституции ткани альтернативой могут являться клетки из внешнего источника. Наиболее перспективными для этих целей на данный момент представляются прогениторные (стволовые) клетки, основной особенностью которых является способность к пролиферации и дифференцировке. Стволовые клетки обнаруживаются практически в любой ткани организма, однако для целей регенеративной медицины наиболее часто выделяют следующие категории: мезенхимные (МСК) - мультипотентные клетки, источником которых является жир, костный мозг и другие ткани. При использовании данного вида клеток отсутствует риск опухолевой трансформации, так как при имплантации в поврежденную область их регенераторный эффект более реализуется через секрецию широкого спектра противовоспалительных медиаторов и цитокинов, нежели пролиферацию. Существуют отработанные протоколы их накопления и получения;
эмбриональные - плюрипотентные. Клетки, обладающие наибольшим регенераторным потенциалом. При использовании сохраняется риск опухолевой трансформации (развития тератомы);
индуцированные - способные к пролиферации и дифференцировке клетки, полученные с помощью генетического перепрограммирования.
In vivo клетки окружены сложной структурой, называемой межклеточным веществом или экстрацеллюлярным матриксом. Находясь в матриксе, клетки получают возможность поддерживать морфологическую структуру ткани и органа. При повреждении ткани неизбежно нарушается и структура матрикса. Еще одной стратегией регенеративной медицины является использование специальных клеточных носителей - скаффолдов, которые создают благоприятное микроокружение для клеток. За счет этого увеличивается продолжительность жизни клеток, обеспечивается их миграция, облегчается ангиогенез и тем самым усиливаются регенераторные эффекты. При разработке учитывается тот факт, что скаффолд должен обладать следующими свойствами:
- иметь высокий индекс гистосовместимости и не вызывать иммунологическое отторжение;
- иметь пористую структуру для облегчения проникновения клеток и обеспечения ткани кислородом;
- поддерживать форму в течение определенного периода времени для предотвращения инвазии окружающей ткани и сохранения пространства для клеточной регенерации;
- подвергаться биодеградации, когда процессы регенерации завершены.
Современные скаффолды изготавливаются на основе биополимеров, синтетических полимеров и неорганических комплексов. Наиболее распространенными составляющими являются коллаген, желатин, гиалуроновая кислота и глюкозамингликан - среди биополимеров; полигликолевая кислота, полимолочная кислота - среди синтетических полимеров; а также гидроксиапатит, фосфаты и карбонаты кальция - среди неорганических комплексов. При изготовлении скаффолдов используются методики децеллюляризации, электроспиннинга, 3D-принтинга.
В процессе регенерации факторы регуляции и цитокины управляют ростом клеток и их дифференцировкой. Они обладают различными функциями, включая потенциацию и ингибирование роста клеток, их деления и перехода в апоптоз. Во время восстановления тканей факторы не работают самостоятельно, эффект наблюдается лишь при функционировании целых групп факторов. Самая крупная группа факторов регуляции получила название «факторы роста». На сегодняшний день большинство исследований в области регенеративной медицины находится в одной из описанных выше областей или на их пересечении. По всему миру не прекращаются поиски оптимальной модели скаффолда или комбинации регуляторных факторов, изучается возможность применения различных типов стволовых клеток. Регенеративные технологии востребованы практически во всех областях медицины, в том числе и в оториноларингологии.
Возможности регенеративной медицины в области оториноларингологии крайне широки, что объясняется большой вариативностью ЛОР-патологий. За последнее время опубликовано более 100 научных статей, включая фундаментальные, доклинические и идущие клинические исследования.
Исследование возможностей регенеративной медицины ведутся в отношении восстановления повреждений тканей наружного, среднего и внутреннего уха.
Японские ученые S. Kanemaru и соавт. (2014 г.) в эксперименте с участием 65 пациентов показали восстановление мягких тканей наружного слухового прохода с помощью введения желатиновой губки, инфильтрированной bFGF, и последующим закрытием наружного слухового прохода фибриновым клеем. По истечении 3 мес поврежденные ткани полностью восстановились в 90% случаев. Аналогичным способом 3 годами ранее исследователи S. Kanemaru и соавт. (2011 г.) из Японии уже получили значимые результаты и в лечении стойких перфораций барабанной перепонки. Полное закрытие стойких перфораций наблюдалось в 98% случаев по результатам 3-недельного контроля. Данная методика позволила сократить до минимума объем оперативных вмешательств у пациентов с обширными перфорациями барабанной перепонки.
В области доклинических исследований значительных успехов достигли эксперименты N. Hakuba и соавт. (2014 г.), где продемонстрированы преимущества использования для пластики перфорации барабанной перепонки комплекса рекомбинантного фактора роста фибробластов и желатинового геля, положительный результат достигнут у 100% животных, в то время как в контрольной группе, где использовался только желатиновый гель, полноценное закрытие дефекта наблюдалось у 61%. Особый интерес представляют результаты пилотных клинических исследований. При прямой аппликации фактора роста фибробластов на края подострой перфорации барабанной перепонки у 11 из 12 пациентов произошло полное закрытие дефекта, в группе контроля спонтанное закрытие отмечено лишь у 9 из 17 пациентов.
Также для лечения пациентов с хроническим средним отитом при помощи методов тканевой инженерии созданы аналоги воздушных клеток сосцевидного отростка.
Состоящие из гидроксиапатита искусственные воздушные клетки, вживленные пациентам с хроническим средним отитом, восстанавливали функционирование системы газообмена в полости среднего уха, чем существенно улучшали результаты лечения. Трифосфат кальция, в свою очередь, показал наилучшие результаты среди других синтетических материалов, по своим особенностям он оказался практически идентичен нативным костным структурам.
Также интересными на сегодняшний день являются исследования регенеративной медицины в отоневрологии, а именно в лечении сенсоневральной тугоухости. Группа ученых М. Perny и соавт. (2017 г.) из Швейцарии в эксперименте на мышах представили регенеративную стратегию, в которой описывается технология стимуляции дифференцировки эндогенных клеток в новые волосковые клетки или возможности имплантации экзогенных стволовых клеток для замещения волосковых клеток. В результате эксперимента были получены положительные результаты на животных моделях, однако процесс контроля дифференцировки по-прежнему остается проблематичным.
Без использования реконструктивных технологий невозможно представить и ринологию. В коррекции деформаций наружного носа используют хрящевую ткань пациента, из которой выращивают необходимые хрящи для реконструкций. Так, исследователи из Швейцарии представили результаты реконструкции крыла носа у пациентов после удаления опухоли с помощью хряща, полученного из хондроцитов перегородки носа. Через 6 мес после имплантации хряща в 85% случаев вживленные ткани обладали свойствами нативных структур; через 12 мес все пациенты были довольны эстетическими результатами.
В работе G. Sándor и соавт. (2014 г.) продемонстрирована техника закрытия перфорации перегородки носа у 2 пациентов с помощью жировых МСК и скаффолда на основе b-трифосфата кальция. В этой же работе показана успешная облитерация лобной пазухи аналогичным материалом у 3 пациентов с рецидивирующим фронтитом.
Еще одной актуальной областью научного поиска в ринологии являются расстройства ольфакторной функции. Данная патология крайне сложно поддается лечению, но возможным терапевтическим методом в будущем может стать введение стволовых клеток в носовую полость. По результатам доклинических исследований, проведенных в Южной Корее, интраназальное введение нейрональных стволовых клеток из обонятельной луковицы животным с аносмией, вызванной интраперитонеальной инъекцией 3-метилиндола, существенно ускоряет восстановление обонятельной функции в эксперименте.
Исследование X. Xu и соавт. (2015 г.) показало положительный эффект имплантации жировых МСК вместе с аутологичной жировой тканью в нижние носовые раковины при синдроме пустого носа. Группе итальянских ученых удалось получить статистически значимые результаты в терапии пациентов с синдромом пустого носа после инъекций жировой ткани в сочетании с плазмой, богатой тромбоцитами. Среди 22 пациентов положительный эффект лечения наблюдался у 20. Данное исследование позволяет снизить число инвазивных реконструктивных операций на носовых раковинах и ускорить процесс восстановления пациентов.
Среди многочисленных поражений гортани и трахеи, в терапии которых применимы подходы регенеративной медицины, особый интерес для исследователей представляют парезы и параличи гортанных нервов и рубцовые повреждения. С 2014 г. проводятся эксперименты по терапии пареза возвратного гортанного нерва; в ряде доклинических исследований внутривенное введение МСК при острой травме возвратного гортанного нерва демонстрировало тенденцию к более выраженному восстановлению подвижности складок. Однако статистически значимых результатов достичь пока так и не удалось.
Подскладковые стенозы гортани и трахеи стабильно удерживают лидирующие позиции среди нерешенных задач ларингологии. В течение последних лет ведутся исследования, основанные на модели использования децеллюляризованных основ донорской трахеи или биосинтетических скаффолдов с последующим нанесением на них различных клеток. По результатам экспериментального исследования F. Gray и соавт. (2012 г.) при трансплантации тканеинженерного комплекса децеллюляризованной трахеи и амниотических стволовых клеток эмбрионам овец наблюдается полная эпителизация трансплантата и статистически значимое увеличение просвета трахеи. В работе Т. Go и соват.(2010 г.) на свиньях наилучший результат и стойкий просвет трахеи получены в группе, где использовался каркас донорской трахеи с нанесенными снаружи хондроцитами, дифференцированными из МСК, и эпителиальными клетками дыхательных путей, распределенными по внутренней поверхности импланта. Еще одним наиболее востребованным направлением научных исследований в ларингологии является изучение рубцовых поражений голосовых складок. На данный момент, несмотря на разнообразие существующих методов лечения, их функциональный результат существенно ограничен, так как они не способны восстановить структуру собственной пластинки голосовой складки, обеспечивающую вибрацию последней за счет уникальной архитектоники и состава белков межклеточного матрикса. Использование методов регенеративной медицины в решении данной проблемы выглядит многообещающе. Более чем в 20 экспериментальных работах на животных продемонстрированы антифибротические эффекты жировых, костномозговых МСК, а также клеток из других источников при их имплантации в повреждения голосовых складок изолированно или в комплексе со скаффолдами. Общими гистологическими находками в складках с введенными стволовыми клетками были снижение количества коллагеновых депозитов в рубцах, уменьшение толщины слизистой оболочки, а также увеличение содержания гиалуроновой кислоты. Не менее интересными являются результаты анализа механических свойств голосовых складок. В работах В. Svensson и соавт. (2010 г.) и K. Young-Mo и соавт. (2013 г.) методом параллельной сдвиговой реометрии показано, что регенерация повреждений в голосовых складках в присутствии аллогенных костномозговых стволовых клеток приближает их механические свойства, такие как динамическая вязкость и эластический модуль, к их значениям в интактной слизистой оболочке. В настоящее время в открытых источниках имеется информация о 2-х клинических исследованиях по терапии рубцовых повреждений голосовых складок с использованием клеточных продуктов.
В последнее время в мировой оториноларингологии возрос интерес к достижениям регенеративной медицины. За последние несколько лет в большом количестве экспериментальных исследований продемонстрирована эффективность подобных подходов. В то же время, несмотря на, казалось бы, обширную доказательную базу, количество проводимых клинических исследований остается сравнительно небольшим. С одной стороны, это может свидетельствовать о несовершенстве нормативноправового регулирования в области регенеративной медицины, с другой - о несоответствии качества доклинических исследований требованиям этических комитетов или аналогичных организаций. В некоторых странах существуют механизмы приоритетного рассмотрения препаратов для клеточной терапии с целью вывода на рынок, например процедуры ускоренного рассмотрения, ускоренного утверждения, условной регистрации. Биомедицинские клеточные продукты в России являются отдельным классом медицинских средств, отличным от биологических лекарственных препаратов, и регулируются Федеральным законом от 23.06.2016 №180-ФЗ «О биомедицинских клеточных продуктах». На сегодняшний день остаются открытыми также многие вопросы в подходах к реализации требований по проведению доклинических исследований, однако перспективность продолжения последних в данном направлении очевидна. Оториноларингология ежедневно сталкивается с множеством патологий, при которых не обойтись без регенеративных технологий. Восстановление тканей и их функций в этой области методами регенеративной медицины позволит решить задачи, которые раньше казались невыполнимыми [1].
Задачи изобретения
Вышецитированные исследования и примеры показывают чрезвычайную сложность и высокую стоимость имеющихся на данном этапе развития медицинской и биологической науки технологий по хотя-бы частичному восстановлению тканей биологических объектов и применяются при серьезных патологиях и травмах. В заявленном изобретении поставлена задача обеспечить регенерацию эпителия и дермальных структур человека, домашних и сельскохозяйственных животных при бытовых травмах доступными, физиологически безопасными в допустимых к применению дозах (Д<100 от ЛД 50) и дешевыми химическими реагентами. В фармакопее известны из уровня техники регенеративные препараты актовегин /депротеинизироаанный экстракт из крови телят/, метилурацил, эмплан, эмалан, мазь спасатель на основе этилпарабенов/ F/, адгелон, гекспантель, пантесепт, рекреол, хондроитин, экстракт сабура по Филатову /биостимулятор из сырья алоэ/ и др., представляющие разные классы химических веществ и действующих, как стимуляторы регенерации тканей. Заявленных в изобретении ингредиентов смеси среди них нет.
Однако из истории фармакологии ясно, что зачастую многие химические вещества давно известные в применении обладают дополнительными свойствами, ранее наблюдаемыми, но недостаточно изученными и не внедренными в массовое широкое применение. Так, сульфаниламиды в истории медицины были первыми химиотерапевтическими (системными) антибактериальными средствами, которые нашли широкое применение в практической медицине для лечения инфекционных болезней и осложнений после травм и оперативных вмешательств. С появлением пенициллина и других антибиотиков, а в последнее время фторхинолонов, их использование сократилось, однако значения препараты этой группы не потеряли и в ряде случаев успешно назначаются при инфекционных заболеваниях, вызванных чувствительными к ним микроорганизмами. Сульфаниламиды подавляют рост грамположительных и грамотрицательных бактерий, некоторых простейших (возбудители малярии, токсоплазмоза), хламидий (при трахоме, паратрахоме). Их действие связано главным образом с нарушением образования необходимых для развития микроорганизмов фолата и дигидрофолата, в молекулу которых входит пара-аминобензойная кислота: сульфаниламиды близки по химическому строению к пара-аминобензойной кислоте, они захватываются микробной клеткой вместо пара-аминобензойной кислоты и тем самым нарушают течение в ней обменных процессов. Делятся 4 группы: а) короткого действия (сульфаниламид, сульфатиазол, сульфаэтидол, сульфадимидин и др.); б) среднего действия (сульфадиазин и др.); в) длительного действия (сульфаметоксипиридазин, сульфамонометоксин, сульфадиметоксин и др.); г) сверхдлительного действия (сульфален и др.). Более чем 80-летний период применения обусловил появление большого количества микробных штаммов, устойчивых к сульфаниламидам. Преодолеть резистентность микрофлоры удается, сочетая сульфаниламиды с триметопримом. Используются Ко-тримоксазол (сульфаметоксазол + триметоприм) - бисептол, гросептол Мафенид Месульфамид (стрептоцид растворимый) Сульфагуанидин (сульгин) Сульфадимидин (сульфадимезин) Сульфадиметоксин Сульфален Сульфаметоксазол Сульфаметрол + Триметоприм (лидаприм) Сульфаниламид (ранавексим, стрептоцид белый) Сульфасалазин Сульфатиазол серебра (аргосульфан) Сульфацетамид (сульфацил натрия) Сульфаэтидол (этазол натрия) Фталсульфатиазол (фталазол) [2].
Уровень техники, сущность изобретения
Целю изобретения является создание простой и эффективной фармкомпозиции для усиления репарации, регенерации кожных покровов человека и животных после полученных травм при терапии вне стационара, в т.ч. в военно-полевых условиях. Известны российские патенты на изобретения, например обзором:
- RU 2211031 С1, 20.06.2002, Е.Б. Иванова, где заявлено лекарственное средства стимуляции регенерации и репарации тканей в виде клатрата карбамида и дидецилдиметилдиаммоний бромида, однако данное средство имеет узкий фармакологический спектр действия;
- RU 2715719 С1, 02.08.2019, Гаджиева А.А, Лосьон для восст. кожи лица, где заявлена камфора и левомицетин /косметология/, что также неприемлемо в травматологии;
- RU 2693228 C2, 08.02.2017, Варфаломеев В.Н., Староверов И.В., Композиция для ускорения заживления ран, где применяется лецитин, серебро, карбопол, триэтаноламин. Данный препарат не бактериостатичени не обладает антисептическим эффектом на широкие штаммы микрофлоры;
- RU 2177314 С2, 22.03.2000, Кривошеин Ю.С., Рудько А.П., Состав с репаративными и болеутоляющими свойствами, для применения в медицине и ветеринарии, где используется пантенол, тримекаин, мирамистин. Известно, что аммонийные соединения не обладают должной антибактериальной активностью на многие штаммы микрофлоры. Более близким к заявленному изобретению из уровня техники можно считать прототип по сульфаниламиду - изобретение с патентом RU 2103993 С1, 05.06.1996, в котором используется в виде линимента 5%, ТВИН 80, глицерин, жир кашалота, вода. Однако концентрация действующего вещества низка и подходит состав более на слизистые. Также отчасти прототипом является советское изобретение Исаака Постовского 1944 г. - «паста Постовского» из стрептоцида и бентонитовой глины - для лечения ран и ожогов. В заявленном средстве больше компонентов, они действуют дополняя терапевтический эффект друг друга своими индивидуальными уникальными физико-химическими характеристиками.
Из истории отечественной и зарубежной науки известно, что при применении пронтозила, белого сульфаниламида (фиг. 1) еще в конце 30-х годов прошлого века учеными были замечены на практике их дополнительные регенеративные, репаративные свойства при заживлении раневых поверхностей. Так, в Казанском медицинском журнале в 40-х гг. прошлого века публиковались работы Лаишевского А.А. «Наблюдение над лечением гнойных ран белым стрептоцидом», Л.С. Персианинова «Современное состояние вопроса о стрептоциде», Зулкарнеева Р.Х. «Сульфидинотерапия пневмонии в годы ВОВ», где «побочным» эффектом антимикробной терапии зачастую описывались также наблюдаемые процессы быстрого восстановления поверхностных тканей, слизистой [3].
Из уровня техники известно, что для построения структур соединительной ткани (матрикс, промежуточные филаменты) у позвоночных животных помимо коллагена и эластина участвуют специфические гликопротеины - нидоген, энтактин, ламинин, фибронектин, виментин, декорин, тубулин и пр. (фиг. 2), причем гликозоаминогликаны, образующие межклеточное вещество, как и все формулы сульфаниламидов содержат атомы S. Серосодержащие аминокислоты цистеин Cys C3H7NO2S, цистин C6H12N2O4S2, метионин Met C5H11NO2S имеют крайне важное значение в формировании кожи, шерсти, ногтей, волос, костей, в посттрансляционной модификации белков млекопитающих и при недостатке серы в организме, связанной, например, с интенсивным восстановлением соединительной ретикулофиброзной ткани, восполнение данного элемента на локальном уровне может происходить по-видимому при наружном применении серосодержащих препаратов в месте регенерации. Серы в организме человека содержится около 0,16% от общей массы, в виде органических соединений и она входит в состав молекул биологически активных агентов - инсулина, гепарина, таурина, глутатиона, регулирующих ряд жизненно важных биохимических процессов в организме. Так, трипептид глутатион GSH, регулируемый глутаматцистеинлигазой, содержится в цитоплазме в значительных количествах /5 мМ/, синтезируется с участием серосодержащего цистеина, глицина, глутаминовой кислоты и является основным клеточным антиоксидантом, участвует в каскаде биохимических реакций лейкотриенов, белков теплового шока, выделяемых на клеточный стресс, в том числе при травмах, он восстанавливает любую дисульфидную связь, ингибирует окислительный стресс. Известно, что внешнее воздействие в виде раневого фактора /альтерация/ вызывает на патоанатомическом уровне разрыв мембран клеточных органелл, выброс медиаторов инфламмации гистамина, серотонина, активацию калликреин - кининовой системы с выбросом брадикинина, ацидоз, что приводит и к образованию большого количества свободнорадикальных групп, в т.ч. супероксид иона, пероксинитрита, гидроксила [10]. Локально в месте травмы меняется гемодинамика, лимфоток, процессы экскудации - пролиферации. Задачей лечения травмы является устранение инфекционных агентов и недопущение их вторичной инвазии, удаление продуктов имбибиции, аутолиза, лимфоцитоза /гной/, восстановление рН и окислительно-восстановительного равновесия.
Компоненты
Белый сульфаниламид /стрептоцид/ C6H802N2S применяется в официальной фармакопее для лечения рожистого воспаления, ангины, гонореи, эпидемического цереброспинального менингита, т.к. является заместителем парааминобензойной кислоты в дегидроптеоратсинтазе микроорганизмами /бактерии/ при процессе биосинтеза фолиевой кислоты, что нарушает работу нуклеиновых кислот, действуя бактериостатически [4].
Неорганическая сера /кристаллическая, осажденная/ используется в ветеринарии перкутанно и перорально для улучшения состояния копыт, когтей, шерсти животных, используется и в нутрициологии, преимущественно в виде сульфона-метилсульфонилметана (CH3)2SO2 [5].
Шунгит - природный минерал, содержащий уникальные углеродистые структуры - фуллерены, в виде порошка широко используется как мощный антиоксидант, содержит 26 компонентов, в т.ч. оксиды железа, калия, алюминия, магния, марганца, титана, фосфора, элементы барий, медь, молибден, мышьяк, хром, цинк, стронций, ваннадий и пр. [6]. Болотный мох сфагнум (фиг. 3), содержащий фенольные и тритерпеновые соединения, обладающие бактерицидной активностью, использовался ранее как антисептическое, гигроскопическое средство в хирургии, комбустиологии [7].
Тальк /тетрасиликат магния/ [8], крахмал картофельный [9] также обладают гигроскопическими свойствами, что позволяет их использовать в качестве наполнителей в фармакологических субстанциях, присыпках.
Таким образом, автором изобретения было установлено эксперементально, что применение в заявленной смеси/ композиции в установленной формулой концентрациях/ соотношениях белого сульфаниламида, тетрасиликата магния, крахмала картофельного, неорганической серы, шунгита в порошке и измельченного сырья мха сфагнума позволяет добиться хороших результатов репаративно регенеративного восстановления дермы, эпидермиса при травмах кожи, на 50% ускоряя время заживления, первичным натяжением, без серьезных медицинских/ветеринарных процедур в домашних условиях. Компоненты средства усиливают действие основного вещества - стрептоцида /бактериостатика, репаратора и регенератора/, т.к. действуют керотолитически, гигроскопически /сфагнум/, антиоксидантно /шунгит/, восполняют недостаток сульфидов, образуют пентатионовую кислоту, действующую бактерицидно /сера/, а порошок крахмала обладает склеивающими рану свойствами.
Осуществление изобретения
Репаративно-регенеративное средство по А.С. Кудрину на основе смеси белого сульфаниламида, мелкодисперсной неорганической серы, картофельного крахмала, тетрасиликата магния, сухого сырья Sphagnum palustre, шунгитного порошка применяемое в медицинской и ветеринарной травматологии, представляющее собой сухую субстанцию, где 50% массы составляет белый сульфаниламид, 20% массы составляет крахмал картофельный, 5% мелкодисперсная неорганическая сера, 10% порошок тетрасиликата магния, 10% порошок измельченного сухого сырья сфагнума болотного, 5% шунгитный порошок, применяется при травмах эпидермального, дермального слоев кожи человека и животных после первичной хирургической обработки раневой поверхности для дезинфекции, регенерации, репарации не менее 2-х раз в сутки в течении минимум 7 суток.
Примеры реализации изобретения
На человеке. Пациент 1. 2022 г. Травма зигзагообразной формы резаная кисти левой руки, между digitus minimum и соседним пальцем глубокая, хирургическая /стеклом/. Зияет, кровотечение, сильный болевой синдром. Место травмы промыто под струей воды, применена томпонада и обработка 6% пергидроля для остановки кровотечения, с последующей засыпкой в раневые полости представленной фармкомпозиции, составлением лоскутов кожи краями для склеивания и тугой фиксацией. Перевязки каждые сутки с заменой порошковой композиции поверхностно. Наблюдались повторные кровотечения, боли нет через 5 суток. На 7 сутки наблюдается схватывание краев раны, без образования вторичного рубца, через 14 суток - полное заживление (фигура 4).
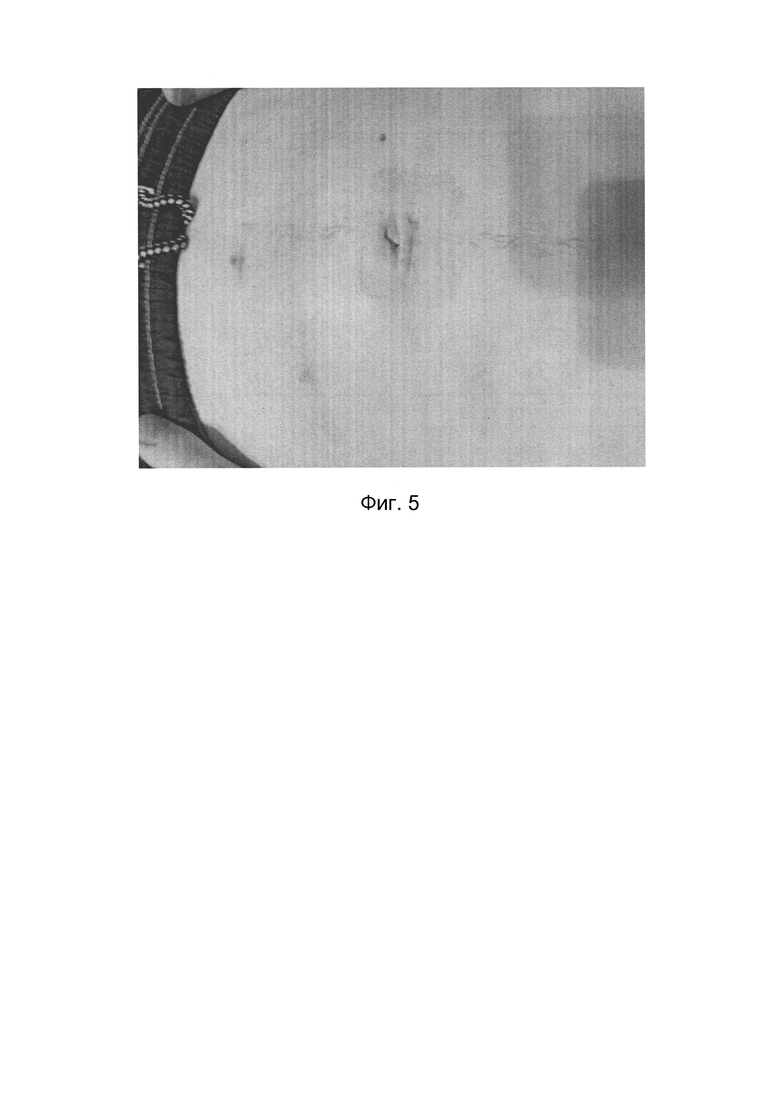
Пациент 2. 2022 г. Состояние после лапараскопической аппендектомии. Применяется на ушитые хирургической лигатурой проколы в брюшной полости после троакара порошок аптечного препарата "Ранавексим" /стрептоцид/. Заживление произошло быстро, отмечается безболезненность. Через 14 дней остатки шовного материала извлечены хирургическим зажимом, раны зарубцевались полностью через 25 суток, без осложнений, с образованием Рубцовых /грануляционная ткань/ изменений на коже (фигура 5).
Пациент 3. 2022 г. Контроль. Бытовая колотая травма pes dexter, с образованием рассеченной кожи 2 см., глубина 0,5 см., кровотечение. ПХО спиртовый раствор калия йодида, асептическая повязка, рекомендовано профилактическое введение анатоксина и перевязки с пропиткой нераздражающими антисептиками /Йодинол/. При повторных осмотрах полное заживление кожи наблюдалось через 30 дней, с образованием рубца из келоидной ткани.
Массовое тестирование. 2022 г. Группой добровольцев в 25 человек нанесены на обработанную 96% этиловым спиртом кожу бедра стерильнымии скарификаторами по 3 неглубокие царапины «а,б,с» до легкой кровоточивости. Царапины «а» не обрабатывались, на царапинах «б» применено заявленное средство путем ежедневного втирания, царапины «с» обработаны 3 раза по 1 разу в сутки штатным антисептиком хлоргексидином. Наблюдением установлено время заживления ран. Статистика: необработанные царапины «а» среднее время заживления 12 суток; обрабатываемые средством царапины «б» 7 суток, обработанные в виде ПХО хлоргексидином царапины «с» 9 суток. Результат статистически достоверен, t критерий <0,05.
На животных. 2023 г. Кошка безродная /самец/, возраст около 5 лет, две свежие поверхностные рваные раны кожи в области головы и шеи, загрязнены, после первичной хирургической обработки из которых одна обрабатывалась 7 суток стандартно /бриллиантовый зеленый/, вторая засыпалась заявленной смесью на основе белого сульфаниламида /стрептоцида/, без наложения пластыря. Рана, леченная стандартно, зарубцевалась через 15 суток, келоид, рана леченная с применением заявленной смеси схватилась через 7 суток поверхностным натяжением. В дальнейшем наблюдении через 2 месяца именно на ее месте отмечен нормальный рост шерсти, в отличие от стандартно леченной, где шерсть отсутствует, а наличествует гиперпластическая васкуляризированная ткань.
Заявленное изобретение проверено автором на наличие мировой новизны, при патентном иске в открытых базах данных не было обнаружено аналогичного запрашиваемому патента. Изобретение легко реализуемо, промышленно применимо, экспериментально подтверждено, имеет должный технический уровень и может неограниченно применятся по назначению.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ ИНФОРМАЦИИ:
1. Возможности регенеративной медицины. В.М. Свистушкин, Старостина С.В. и др., Москва. Первый госмосмедуниверситет Сеченова. 2019. Открытый источник в сети Интернет https://doi.org/10.26442/20751753.2019.11.190641 (Время обращения 13.06.23).
2. Сульфаниламидные препараты. Открытый источник в сети Интернет http://www.cnshb.ru/AKDiL/0048/base/Rs/330001.shtm (Время обращения 16.06.23).
3. Казанский медицинский журнал. ISSN 0368-4814. Лаишевский В.В. Наблюдение над лечением гнойных ран белым стрептоцидом. Том 36, N1, (1940), стр. 18-20. Том 27, N3 (2017) Зулкарнеев. Сульфидинотерапия.
4. Открытый источник в сети Интернет https://vvww.rlsnet.ru/active-substance/sultanilamid-1626 (Время обращения 12.06.23).
5. Сера - биологическая роль. Интернет-источник http://moydietolog.ru/sera (Время обращения 16.06.23).
6. Применение шунгита. Интернет-источник https://www.mineraly.ru/application/16/ (Время обращения 16.06.23).
7. Сфагнум (Sphagnum L.). Интернет-источник https://lektrava.ru/enciclopedia/sfagnum/
8. Тальк медицинский. Интернет-источник https://talksib.ru/talc/products (Время обращения 15.06.23).
9. Применение картофельного крахмала в медицине и быту. Интернет-источник https://agronom.expert (Время обращения 14.06.22).
10. Международный медицинский журнал. УДК 612.015.14:546.21:577.352.38. 2012. д. фармк. н. Сыровая А.О. и др. «Биологическая роль свободных радикалов в развитии патологических состояний». Интернет-источник https://repo.knmu.ua/bistresm/123456789/1891/1/ (Время обращения 17.06.23).


Изобретение относится к области медицины, а именно к репаративно-регенеративному средству при травмах кожи. Репаративно-регенеративное средство при травмах кожи на основе смеси белого сульфаниламида, мелкодисперсной неорганической серы, картофельного крахмала, тетрасиликата магния, сухого сырья Sphagnum palustre, шунгитного порошка, представляющее собой сухую субстанцию, где 50% массы составляет белый сульфаниламид, 20% массы составляет крахмал картофельный, 5% - мелкодисперсная неорганическая сера, 10% - порошок тетрасиликата магния, 10% - порошок измельченного сухого сырья сфагнума болотного, 5% - шунгитный порошок. Указанное изобретение может быть использовано для усиления репарации, регенерации кожных покровов человека и животных после полученных травм при терапии вне стационара. 5 ил.
Репаративно-регенеративное средство при травмах кожи на основе смеси белого сульфаниламида, мелкодисперсной неорганической серы, картофельного крахмала, тетрасиликата магния, сухого сырья Sphagnum palustre, шунгитного порошка, представляющее собой сухую субстанцию, где 50% массы составляет белый сульфаниламид, 20% массы составляет крахмал картофельный, 5% - мелкодисперсная неорганическая сера, 10% - порошок тетрасиликата магния, 10% - порошок измельченного сухого сырья сфагнума болотного, 5% - шунгитный порошок.
| ЛИНИМЕНТ РАСТВОРИМОГО СТРЕПТОЦИДА 5%-НОГО | 1996 |
|
RU2103993C1 |
| ПУДРА-ПРИСЫПКА | 1993 |
|
RU2049462C1 |
| Состав и технология получения присыпки ранозаживляющего действия | 2017 |
|
RU2709102C2 |
| TAFFEL, M | |||
| et al | |||
| Effect of Local Application of Sulfanilamide upon Wound Healing | |||
| Proceedings of the Society for Experimental Biology and Medicine | |||
| Приспособление для выделки кирпичей с замкнутой со всех сторон полостью | 1925 |
|
SU1941A1 |
Авторы
Даты
2025-01-28—Публикация
2023-07-17—Подача