Область техники
Изобретение относится к области химии, фармацевтики и химико-фармацевтической промышленности, а именно к новой кристаллической форме 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината и содержащих ее фармацевтической композиции и лекарственному средству. Изобретение может использоваться в качестве противоаллергического средства.
Уровень техники
В настоящее время на фармацевтическом рынке присутствует большое количество лекарственных препаратов, являющихся производными гетероциклических соединений. Особый интерес вызывают производные пуринового основания - ксантина, к которым относятся такие известные соединения, как теофиллин, теобромин и кофеин. Данные соединения характеризуются широким профилем фармакологической активности и относительной безопасностью.
В уровне техники известны производные ксантина - соединение 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантин и его сукцинатная соль следующей формулы
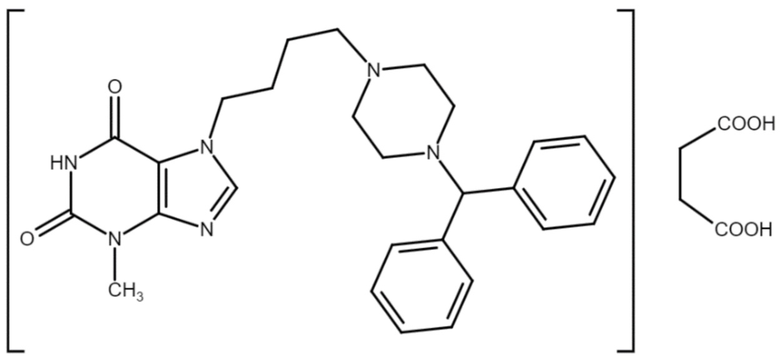
3-Метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцинат
Соединение впервые было раскрыто в патенте RU 2333212 (опубл. 10.09.2008). В примере 4 указанного патента приведены его физико-химические характеристики без сведений о способе получения. Далее в патенте RU 2373207 (опубл. 20.11.2009) сообщается, что 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцинат может быть получен нейтрализацией основания 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина соответствующей органической кислотой.
В работе R.G. GLUSHKOV et al., A new group of 1-and 7-[ω-(benzhydryl-1-alkyl]-3-methylxanthine derivatives with antihistamine activity, PHARMACEUTICAL CHEMISTRY JOURNAL, 2011, V. 45, N. 1, pp. 1-11, были детально исследованы антигистаминовая и противоаллергическая активности сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина (теоритина). Также показано, что соединение не оказывает влияние на артериальное давление и центральную нервную систему, не обладает выраженной обезболивающей активностью. Были испытаны и другие производные 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина (соли, гидраты), однако отмечается, что сукцинатная соль обладает оптимальными фармакотерапевтическими свойствами, среди которых указаны отсутствие гигроскопичности, термическая стабильность, хорошая растворимость в воде и оптимальный рН водного раствора.
В работе С.В. ПУЧНИНА и др., Разработка состава таблеток теоритина, Фармация, 2013, 3, c. 45-47 приведены результаты микроскопического исследования сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина. Сообщается, что кристаллы субстанции имели вытянутую форму с соотношением длина - толщина около 1:3. Такая форма кристаллов, по мнению авторов, объясняет низкую сыпучесть продукта и высокую степень уплотнения порошка при вибрационном воздействии. Дополнительно было проведено сравнение по сыпучести составов таблетируемой массы, содержащих в качестве вспомогательных веществ микрокристаллическую целлюлозу РН 101, 102 и 200, Ludipress, Formax, а также крахмал, натрий карбоксиметилкрахмал и кросповидон. Полученные таблетки впоследствии нашли применение в качестве лекарственного средства, обладающего противоаллергической активностью (Инструкция по медицинскому применению Теоритин® МФ, ЛП-005435, дата регистрации - 29.03.2019).
Техническая проблема, которая не была решена рассмотренными аналогами, заключается в недостаточной терапевтической эффективности и биодоступности лекарственных средств, полученных на основе солей 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината. Само химическое соединение и его лекарственные формы недостаточно исследованы, не проработаны другие области фармацевтического применения.
Раскрытие сущности изобретения
Технический результат
Технические результаты, на достижение которых направлено настоящее изобретение, заключаются в:
- ускорении наступления терапевтического эффекта;
- увеличении терапевтической эффективности;
- расширении арсенала лекарственных средств для симптоматической терапии аллергических заболеваний и состояний;
- отсутствие токсичности, мутагенной активности и сенсибилирующих свойств;
- новые неожиданные свойства по сравнению с прототипом, среди которых антихемокиновое, антимикробное, противоастматическое и жаропонижающее действия.
Каждый из указанных технических результатов относится как к самому веществу (новой кристаллической форме сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина), так и к содержащим его фармацевтической композиции и лекарственному средству.
Далее приведено разъяснение понятий и терминов, указанных в технических результатах.
Под терапевтической эффективностью понимается способность лекарственного средства обеспечивать фармакологическое действие. Терапевтическая эффективность любого конкретного лекарственного средства может быть определена путем оценки ответа пациента или животного после введения ему лекарственного средства; при этом лекарственное средство с высокой терапевтической эффективностью будет обеспечивать большее ослабление симптомов и/или их исчезновение, чем лекарственное средство с низкой терапевтической эффективностью.
Под мутагенной активностью понимается способность химического вещества вызывать мутации.
Под сенсибилирующими свойствами понимается способность химического вещества воздействовать как аллерген.
Под антихемокиновым действием понимается способность действующего вещества подавлять избыточное выделение воспалительных хемокинов (например, интерлейкин, фактор некроза опухоли α (TNF-α) и т.д.).
Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина
Настоящая техническая проблема решается, а указанные технические результаты достигаются благодаря кристаллической форме сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина. Сукцинат 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина представляет собой химическое соединение следующей структурной формулы:

Альтернативные структуры:
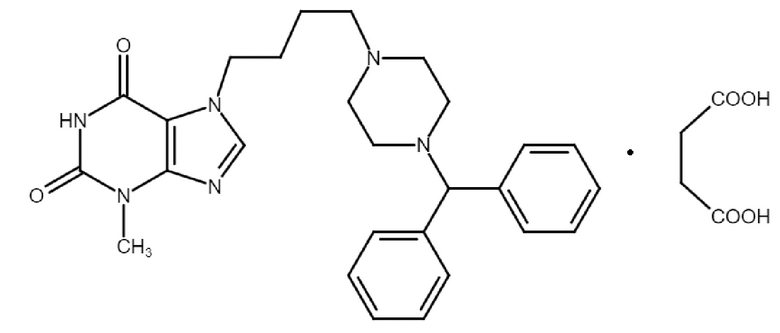
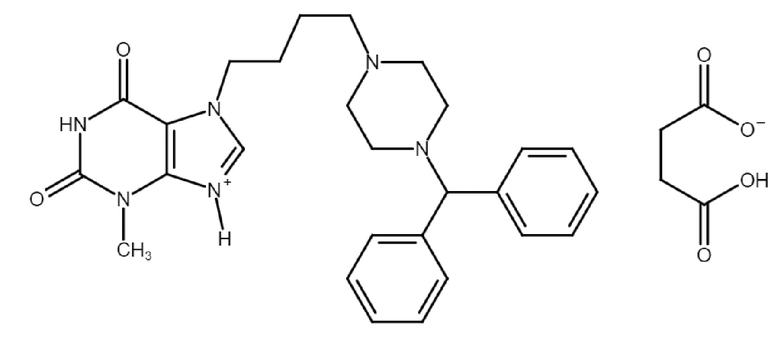
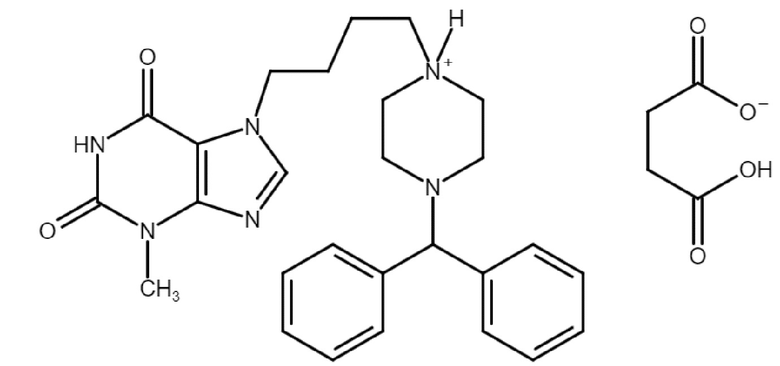
Указанное соединение представляет собой соль или аддукт янтарной кислоты (бутандиовой) и 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина.
Рациональное название - бензгидрилпиперазинилбутилметилксантина сукцинат.
Другие названия: сукцинат 7-{4-[4-(дифенилметил)пиперазин-1-ил]бутил}-3-метил-2,3,6,7-тетрагидро-1Н-пурин-2,6-диона, сукцинат 7-[4-(4-бензгидрилпиперазинил-1)бутил]-3-метилксантина.
Указанное соединение представляет собой фармацевтически приемлемую соль. Понятие «фармацевтически приемлемые соли» в контексте настоящего изобретения означает относительно нетоксичные соли кислот и оснований. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания и подходящей органической или неорганической кислоты.
Понятие «кристаллическая форма» в контексте настоящего изобретения относится к веществу в твердой форме, в которой молекулы занимают упорядоченное положение в пространстве и образуют кристаллическую решетку. Упорядоченное положение молекул в кристаллической решетке называется дальним порядком. Для исследования кристаллических форм обычно применяют метод порошковой рентгеновской дифракции.
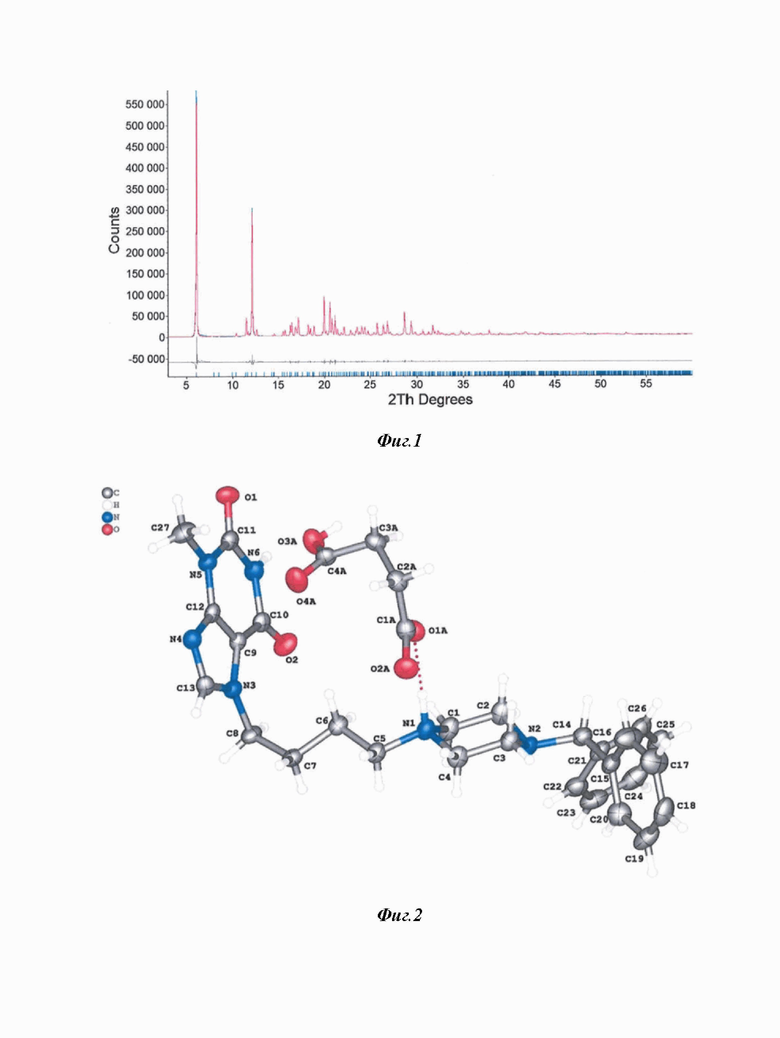
Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина согласно настоящему изобретению может быть охарактеризована положениями пиков в порошковой рентгенограмме, полученной с использованием Cu(Kα)-излучения, 2θ, град: 6.1±0.2 и 12.2±0.2. В предпочтительном варианте кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина согласно настоящему изобретению может быть охарактеризована положениями пиков в порошковой рентгенограмме, полученной с использованием Cu(Kα)-излучения, 2θ, град: 6.1±0.2, 12.2±0.2, 20.0±0.2, 20.7±0.2 и 28.7±0.2. В еще более предпочтительном варианте кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина согласно настоящему изобретению может быть охарактеризована порошковой рентгенограммой, представленной на Фиг.1.
В другом варианте кристаллическая форма 1-[2-(1-метилимидазол-4-ил)этил]пергидроазин-2,6-диона согласно настоящему изобретению может быть охарактеризована сингонией кристаллической решетки и параметрами элементарной кристаллической ячейки. Кристаллическая ячейка представляет собой параллелепипед, построенный на узлах кристаллической решетки, параллельные переносы (трансляции) которого в трех измерениях позволяют построить всю кристаллическую решетку. Параметрами кристаллической решетки являются величины ребер (a, b и c) и величины углов между ними (α, β и γ). В предпочтительном варианте сингонией кристаллической решетки кристаллической формы 1-[2-(1-метилимидазол-4-ил)этил]пергидроазин-2,6-диона согласно настоящему изобретению является моноклинная сингония. В моноклинной сингонии кристалл построен из параллелепипедов, в которых α и γ = 90°, β ≠ 90°. Параметрами кристаллической решетки моноклинной сингонии являются величины ребер и величина непрямого угла. В кристаллической форме сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина согласно настоящему изобретению величины ребер составляют 11.43±0.50 Å, 29.10±0.50 Å и 9.17±0.50 Å; и величина угла составляет (град): 104.71°±5.00°. Следует учитывать, что наблюдаемые параметры кристаллической ячейки могут зависеть от температуры измерений. В предпочтительном варианты величины ребер составляют (Å, ангстрем) 11.4312(13) Å, 29.103(4) Å и 9.1768(13) Å, и величина угла составляет (град) 104.713(6)° при температуре 140 К.
Метод порошковой рентгеновской дифрактометрии позволяет идентифицировать даже небольшие изменения в состоянии атомной решетки кристалла, не детектируемые другими методами. Рентгенография поликристаллических образцов позволяет определять состояния твердого тела (кристаллическое, разные его формы, аморфное, или их комбинации). Значение структурных исследований весьма велико. Определение связи между атомной структурой и свойствами вещества позволяет устанавливать рациональный контроль за технологическими процессами, раскрывать причины изменения этих свойств под действием того или иного фактора, дает возможность более сознательно управлять технологическим процессом создания фармацевтических субстанций и изменять его в нужном направлении.
Метод порошковой рентгеновской дифракции основан на получении и последующем анализе дифракционной картины, возникающей в результате дифракции рентгеновских лучей на порошке или поликристаллическом образце исследуемого материала. В общем случае кристалл можно представить серией плоскостей, на которые под углом θ направляется луч рентгеновского излучения. Дифрагированные лучи фиксируются при помощи детектора или фотопленки. Для получения дифрактограммы от кристаллического порошка проводят измерение интенсивностей рассеянного излучения в зависимости от угла 2θ между образцом и первичным пучком. По формуле Вульфа-Брегга nλ = 2dsinθ можно рассчитать межплоскостные расстояния в кристалле. Полученные данные для каждого вещества строго индивидуальны, поэтому рентгенограмма однозначно характеризует исследуемое вещество (см. ОФС.1.2.1.1.0011.15 Рентгеновская порошковая дифрактометрия).
Фармацевтическая композиция
Настоящая техническая проблема решается, а указанные технические результаты достигаются также благодаря фармацевтической композиций, обладающей противоаллергической активностью, включающей кристаллическую сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина настоящего изобретения и по меньшей мере один фармацевтически приемлемый эксципиент.
Под фармацевтической композицией понимается пригодная для использования для людей или животных композиция (смесь, состав и т.д.), включающая активную фармацевтическую субстанцию. Активная фармацевтическая субстанция в фармацевтической композиции включает действующее вещество - кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина настоящего изобретения. Специалисту в данной области будет понятно, что к фармацевтической композиции настоящего изобретения будут относиться также композиции, содержащие одно или несколько других активных фармацевтических субстанций, например, другие антигистаминные и противоаллергические субстанции.
Понятия «включает» и «содержит» в контексте настоящего изобретения означает, что указанные фармацевтические композиции (лекарственные средства, группы компонентов и т.д.) включают перечисленные далее компоненты/ингредиенты, но не исключают включение других компонентов/ингредиентов.
В предпочтительном варианте фармацевтическая композиция представляет собой состав в виде твердой формы. Примерами твердых лекарственных форм являются порошки, гранулы, брикеты, капсулы, таблетки, драже и т.д. Специалисту в данной области будет понятно, что фармацевтическая композиция настоящего изобретения может иметь любую другую форму, обеспечивающую сохранность положительных свойств активной фармацевтической субстанции. В наиболее предпочтительном варианте твердая форма представляет собой порошок, гранулу, капсулу или таблетку. Порошком является твердая недозированная лекарственная форма, состоящая из твердых отдельных сухих частиц различной дисперсности, обладающая свойством сыпучести. Капсулой является твердая дозированная или недозированная лекарственная форма, включающая твердую (как правило, желатиновую) оболочку, внутри которой заключен инкапсулят, содержащий одно или более действующих веществ с добавлением или без вспомогательных веществ. Гранулой является твердая дозированная лекарственная форма в виде крупинок (агрегатов частиц порошка) круглой, цилиндрической или неправильной формы, содержащая одно или несколько действующих веществ с добавлением вспомогательных веществ. Таблеткой является твердая дозированная лекарственная форма, чаще всего получаемая прессованием порошков или гранул, содержащих одно или более действующих веществ с добавлением или без вспомогательных веществ.
Количественное содержание кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина в фармацевтической композиции выбирается из диапазона от 0.01 до 100 мас. %, в предпочтительном варианте от 1.00 до 80.00 мас. %, в более предпочтительном от 1.00 до 20.00 мас. %, например, 1.00 мас. %, 2.00 мас. %, 2.50 мас. %, 3.00 мас. %, 3.50 мас. %, 4.00 мас. %, 4.50 мас. %, 5.00 мас. %, 5.50 мас. %, 6.00 мас. %, 6.50 мас. %, 7.00 мас. %, 8.00 мас. %, 9.00 мас. %, 10.00 мас. %, 12.00 мас. %, 14.00 мас. %, 16.00 мас. %, 18.00 мас. %, 20.00 мас. %; от 1.00 мас. % до 10.00 мас. %, от 1.00 мас. % до 5.00 мас. %, от 1.00 мас. % до 3.00 мас. %, от 1.00 мас. % до 2.00 мас. %, от 2.00 мас. % до 3.00 мас. %, от 3.00 мас. % до 7.00 мас. %, включая все промежуточные значения. Например, значение 2.50 мас. % входит в качестве одного из значений в диапазон от 1.00 мас. % до 20.00 мас. %.
В другом предпочтительном варианте фармацевтическая композиция включает кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина настоящего изобретения в эффективном количестве.
Понятие «эффективное количество» в контексте настоящего изобретения относится к количеству фармацевтической композиции или лекарственного средства, которое при введении субъекту является достаточным для воздействия такого лечения на заболевание, нарушение или симптом. «Эффективное количество» может изменяться, например, в зависимости от того, в какой форме находится вещество, от природы заболевания, нарушения и/или симптомов заболевания или нарушения, от тяжести заболевания, нарушения и/или симптомов заболевания или нарушения, от возраста субъекта, подлежащего лечению, и/или от веса субъекта, подлежащего лечению. Надлежащее количество в каждом конкретном случае будет очевидно специалисту в данной области или может быть определено путем стандартных экспериментов.
В предпочтительном варианте кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина содержится в фармацевтической композиции или лекарственном средстве и используется в определенной дозировке. Дозировка кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина согласно настоящему изобретению, может находиться в диапазоне от 1 мг до 100 мг в сутки, предпочтительно от 1 мг до 10 мг, наиболее предпочтительно от 2 мг до 5 мг в сутки, например, 2 мг или 4 мг в сутки. Указанная дозировка может быть введена как одной дозой, так и разделена на несколько приемов в течение суток. Предпочтительный режим дозирования составляет от 4 мг один раз в сутки или 2 мг 2 раза в сутки. В предпочтительном варианте в твердой форме фармацевтической композиции или лекарственного средства кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина находится в количестве, соответствующем рекомендуемой дозировке.
Понятие «дозировка», используемое здесь, характеризует содержание одного или нескольких действующих веществ в количественном выражении на единицу дозы, или единицу объема, или единицу массы в соответствии с лекарственной формой, либо для некоторых видов лекарственных форм количество высвобождаемого из лекарственной формы действующего вещества за единицу времени.
Фармацевтическая композиция настоящего изобретения включает по меньшей мере один фармацевтически приемлемый эксципиент, являющийся носителем действующих веществ, обеспечивающий требуемый объем/массу и необходимые характеристики лекарственного средства в определенной лекарственной форме. В предпочтительном варианте фармацевтическая композиция включает фармацевтически приемлемый эксципиент, который выбирают из группы, включающей наполнитель, связывающее вещество, смазывающее вещество, разрыхляющее вещество, скользящее вещество, консервант, корригент, краситель.
Наполнители (носители, разбавители) добавляются для получения определенной массы лекарственной формы. Примерами наполнителей являются крахмал, сахара, оксид магния, целлюлоза, микроцеллюлоза (МКЦ), карбонат кальция, декстрин, амилопектин, сорбит, маннит, пектин.
Связывающие вещества добавляются для заполнения межчастичного пространства и для увеличения контактной поверхности частиц, что необходимо для таблетирования твердых лекарственных форм. Примерами связывающих веществ являются альгинат натрия, сахар, желатин, крахмал, поливиниловый спирт, производные целлюлозы, поливинилпирролидон (повидон).
Скользящие вещества добавляются для уменьшения шероховатости твердой лекарственной формы, что облегчает ее высыпание. Примерами скользящих веществ являются крахмал, тальк, полиэтиленоксид-4000, аэросил.
Смазывающие вещества облегчаются выталкивание твердой формы (например, таблетки из матрицы). Примерами смазывающих веществ являются стеариновая кислота и ее соли (стеарат магния), жиры.
Разрыхляющие вещества (дезинтегрант, диспергирующий агент) облегчают растворение фармацевтической композиции и лекарственной формы. Примерами разрыхляющих веществ являются гидрокарбонат натрия, твин-80, альгинат натрия.
Корригенты используются для улучшения вкуса (подсластитель) и запаха (ароматизатор). К ним относятся сахар, какао, ванилин.
Красители (пигменты) используются для улучшения внешнего вида фармацевтической композиции и лекарственной формы. Примерами красителей являются диоксид титана, индигокармин.
Количество, состав и форма фармацевтически приемлемого эксципиента могут быть выбраны специалистом в данной области произвольно при условии полного или частичного сохранения кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина.
Пути введения фармацевтической композиции по настоящему изобретению включают, но не ограничиваются пероральным, местным, трансдермальным, сублингвальным и ректальным путями. В предпочтительном варианте фармацевтическую композицию вводят перорально или сублингвально.
Лекарственное средство
Настоящая техническая проблема решается, а указанные технические результаты достигаются также благодаря лекарственному средству в твердой форме для лечения аллергических заболеваний или расстройств, включающему кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина или фармацевтическую композицию настоящего изобретения. Предпочтительный характер лечения - симптоматический.
Под лекарственным средством (лекарственным препаратом) понимаются пригодные для использования у людей или животных активную фармацевтическую субстанцию или фармацевтическую композицию в виде лекарственной формы.
Настоящее изобретение относится к лекарственному средству в твердой лекарственной форме. Примерами твердых форм являются порошки, гранулы, брикеты, капсулы, пеллеты, таблетки, драже и т.д. Специалисту в данной области будет понятно, что лекарственное средство настоящего изобретения может иметь любую форму, обеспечивающую сохранность положительных свойств активной фармацевтической субстанции. В наиболее предпочтительном варианте твердая форма представляет собой порошок, гранулу, капсулу или таблетку.
В качестве лекарственного средства настоящего изобретения может выступать активная фармацевтическая субстанция и фармацевтическая композиция, включающие кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина. В предпочтительном варианте лекарственное средство также включает по меньшей мере один фармацевтически приемлемый эксципиент, однако его наличие не является обязательным.
Количественное содержание кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина в лекарственном средстве выбирается из диапазона от 0.01 до 100 мас. %, в предпочтительном варианте от 1.00 до 80.00 мас. %, в более предпочтительном от 1.00 до 20.00 мас. %, например, 1.00 мас. %, 2.00 мас. %, 2.50 мас. %, 3.00 мас. %, 3.50 мас. %, 4.00 мас. %, 4.50 мас. %, 5.00 мас. %, 5.50 мас. %, 6.00 мас. %, 6.50 мас. %, 7.00 мас. %, 8.00 мас. %, 9.00 мас. %, 10.00 мас. %, 12.00 мас. %, 14.00 мас. %, 16.00 мас. %, 18.00 мас. %, 20.00 мас. %; от 1.00 мас. % до 10.00 мас. %, от 1.00 мас. % до 5.00 мас. %, от 1.00 мас. % до 3.00 мас. %, от 1.00 мас. % до 2.00 мас. %, от 2.00 мас. % до 3.00 мас. %, от 3.00 мас. % до 7.00 мас. %, включая все промежуточные значения. Например, значение 2.50 мас. % входит в качестве одного из значений в диапазон от 1.00 мас. % до 20.00 мас. %.
Определения фармацевтически приемлемого эксципиента, дозировки и путей введения лекарственного средства аналогичны таковым для фармацевтической композиции настоящего изобретения.
Применение кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина и содержащих ее фармацевтической композиции и лекарственного средства
Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться в качестве противоаллергических средств, то есть для лечения аллергических заболеваний или расстройств.
Под противоаллергическими средствами понимаются лекарственные средства, предназначенные для уменьшения или полного устранения таких симптомов, как, например, покраснения, экземы, сыпь и зуд на любом участке тела (крапивница, кожный дерматит), отек лица, затрудненное дыхание или глотание, насморк, заложенность носа (аллергический ринит), раздраженные глаза (аллергический конъюктивит) и т.д. Симптомы аллергии часто развиваются очень стремительно. Поэтому для эффективного купирования состояния необходимы противоаллергические препараты, которые обеспечивают быстрое наступление терапевтического эффекта.
Механизм антигистаминного действия связан c эффективной, длительной и избирательной блокадой H1-гистаминовых рецепторов.
Также авторами настоящего изобретения было неожиданно обнаружено, что кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, фармацевтическая композиция и лекарственное средство настоящего изобретения могут эффективно препятствовать возникновению острого состояния выработки большого количества медиаторов воспаления - хемокинов. Указанное состояние характеризуется патологическим системным воспалением тканей организма, которое без своевременного лечения может приводить к самым разным осложнениям и даже к летальному исходу.
Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться в качестве противоастматических средств. Противоастматические средства направлены на купирование укорочения дыхания и сужения дыхательных путей, вызванного воспалением дыхательных путей и сжатием окружающих гладких мышц.
Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, фармацевтическая композиция и лекарственное средство настоящего изобретения могут применяться в качестве эффективных жаропонижающих средств. Жаропонижающее (антипиретическое) действие может проявляться в снижении температуры тела при лихорадке.
Если не указано иное, все технические и специальные термины, использованные в данном контексте, имеют общепринятое в данной области техники значение.
Краткое описание чертежей
Фиг.1 - рентгенограмма кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина;
Фиг.2 - пространственное строение, полученное методом рентгеноструктурного анализа;
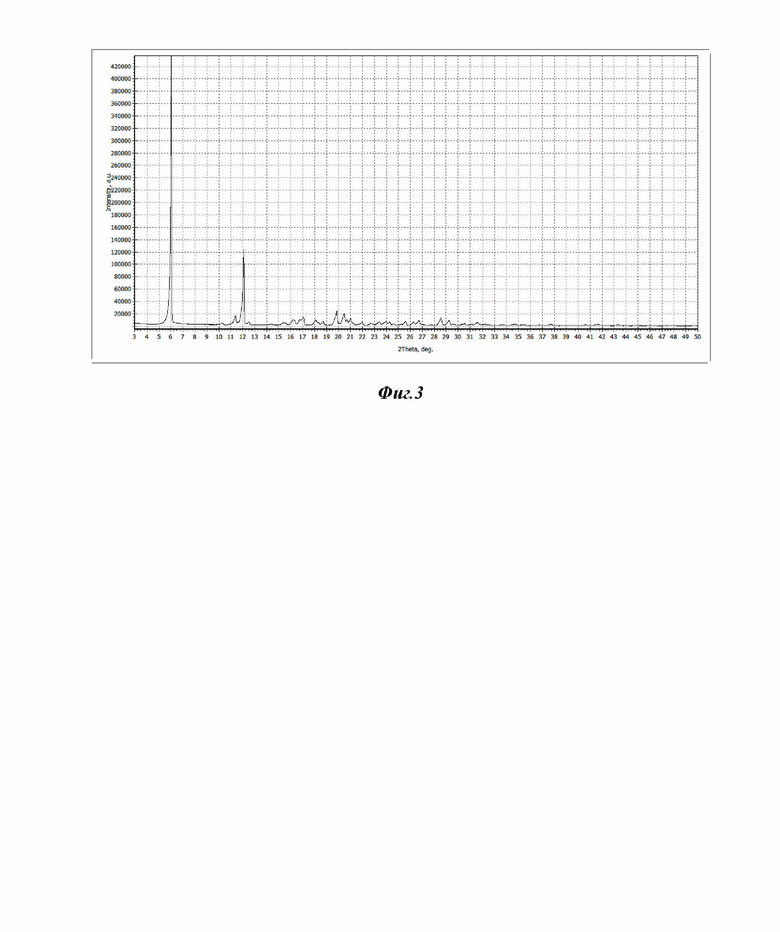
Фиг.3 - рентгенограмма кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина в испытании методом ускоренного старения.
Осуществление изобретения
Для иллюстративных целей далее представлены примеры, которые не ограничивают объем настоящего изобретения.
Пример 1. Получение кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина
3-Метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантин (свободное основание) был получен согласно RU 2333212.
Далее к 3.0 г (6.35 ммоль) 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина в 20 мл этилацетата добавляли 1.5 г (12.70 ммоль) янтарной кислоты. Полученную смесь кипятили в течение 25 минут, после чего давали остыть. К полученному раствору добавляли 15 мл воды в качестве антирастворителя, в результате чего наблюдалось слабое помутнение раствора. Далее смесь охлаждали до +10°C и выдерживали при этой температуре в течение 2 часов. Выпавшие кристаллы отфильтровывали, высушивали сначала при пониженном давлении (60-80 мм рт.ст.), затем в эксикаторе над P2O5 до тех пор, пока масса кристаллов не перестала уменьшаться при дальнейшем высушивании. Получено 3.2 г (85%) кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина.
Форму согласно прототипу (RU 2373207) получали простой перекристаллизацией из 95% этанола.
Полученные кристаллы были исследованы методами рентгеновской дифракции.
Все исследования методом порошковой рентгеновской дифракции выполнены на дифрактометре Bruker D8 Advance, оборудованном системой автоматических щелей для монохроматизации и фокусировки (λ[CuKα]=1.5418 Å), а также позиционно-чувствительным детектором LynxEye, в угловом диапазоне 3-60° с шагом 0.02 по углу 2θ с использованием геометрии на отражение.
На Фиг.1 представлена порошковая рентгенограмма полученной кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина. В табл. 1 перечислены положения углов 2θ и их относительные интенсивности.
Таблица 1. Углы (2θ, град) и их относительные интенсивности (I, %) кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина.
На дифрактограмме кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина наблюдали следующие интенсивные пики (максимумы) при углах дифракции 2θ (± 0,2°): 6.1, 12.2, 20.0, 20.7 и 28.7. Характеристичными пиками являлись: 6.1 и 12.2.
Пример 2. Рентгеноструктурный анализ
Все рентгенодифракционные исследования монокристаллов проведены на дифрактометре Bruker Apex II с использованием координатного детектора Photon-II. Структуры решены с помощью метода двойного пространства и функции минимума суперпозиции Паттерсона (программа SHELXT, см. G.M. SHELDRICK, SHELXT-Integrated space-group and crystal-structure determination, ACTA CRYSTALLOGRAPHICA SECTION A: FOUNDATIONS AND ADVANCES, 2015, V.71, N.1, pp. 3-8). Уточнение структур выполнено в полноматричном анизотропном приближении для всех атомов кроме водородных. Атомы водорода рассчитаны геометрически и включены в уточнение в изотропном приближении с наложением ограничений на длины связей C-H и N-H. Все расчеты по уточнению структур выполнены с использованием программы SHELXL (см. G.M. SHELDRICK, Crystal structure refinement with SHELXL, ACTA CRYSTALLOGRAPHICA SECTION C: STRUCTURAL CHEMISTRY, 2015, V. 71, N. 1, pp. 3-8).
Кристаллографическая информация (для температуры 140 К): моноклинная сингония, пространственная группа P21/n, a = 9.1768(13) Å, b = 29.103(4) Å, c = 11.4312(13) Å, β = 104.713(6)°, Z = 4, T = 140 K. Более подробная информация представлена в табл. 2.
Таблица 2. Кристаллографические данные сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина
Пространственное строение молекулы представлено на Фиг.2.
Пример 3. Исследования противогистаминной активности
Нескольким группам морских свинок (по 2-3 в каждой) вводили в желудок (через зонд) субстанцию (по 5 мг) кристаллической формы 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината настоящего изобретения (активная фармацевтическая субстанция - АФС) и субстанцию 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината согласно прототипу (прототип) за 2 ч, 1.2 и 3 суток до внутривенного в ведения гистамина (10 мкг/кг) уже в условиях наркоза и искусственной вентиляции легких.
Изучение противогистаминной активности осуществляли с помощью модифицированного метода Концетта-Ресслера (H. KONZETT and R. RÖSSLER, Versuchsanordnung zu Untersuchungen an der Bronchialmuskulatur, NAUNYN-SCHMIEDEBERGS ARCHIV FÜR EXPERIMENTELLE PATHOLOGIE UND PHARMAKOLOGIE, 1940, V. 195, N. 1, pp. 71-74), основанного на регистрации тонуса бронхиальной мускулатуры у морских свинок-самцов, наркотизированных внутрибрюшинным введением уретана в дозе 1500 мг/кг. Затем у предварительно наркотизированных животных через сагиттальный разрез мягких тканей в области шеи выделяли трахею и яремную вену, в которую вводили полиэтиленовый катетер диаметром 0,8 мм, который фиксировали лигатурой. В трахею вставляли канюлю, которую через Y-образный стеклянный разветвитель подсоединяли с помощью системы полихлорвиниловых трубочек к датчику бронхоспазма (Ugo Basile Bronchospasm transducer, Mod. 7020), а также к аппарату искусственного дыхания для грызунов (Animal EDCO Rodent Ventilator, Mod. 803). Параметры искусственной вентиляции легких в каждом эксперименте рассчитывали по специальной номограмме, прилагаемой к аппарату искусственного дыхания. Графическую регистрацию тонуса бронхиальных мышц осуществляли в непрерывном динамическом режиме в течение всего опыта с помощью одноканального самописца. Режим записи предусматривал регистрацию фонового уровня тонуса бронхиальной мускулатуры и регистрацию величины его увеличения после введения гистамина (до и после введения исследуемых веществ).
Внутривенное введение гистамина в дозе 10 мкг/кг вызывает бронхоспазм (повышение тонуса бронхиальной мускулатуры), сопровождавшееся сдвигом стрелки самописца на 60,0 ± 5,0 мм вверх от исходной величины.
Установлено, что по активности и длительности противогистаминного действия (3 суток) субстанция настоящего изобретения на 10-12% превосходит субстанцию по прототипу (см. табл. 3).
степень блокады бронхоспазма в %
Таким образом, кристаллическая форма настоящего изобретения может применяться для симптоматического лечения бронхоспазмов, которые при несвоевременной терапии могут привести к развитию бронхиальной астмы.
Пример 4. Фармакокинетические исследования
Эксперимент проводили на крысах линии Вистар, которых рандомизированно делили на две группы, в каждой группе по 5 животных. Животные получали при помощи зонда в дозе 5 мг/кг:
Группа 1: кристаллическая форма 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината согласно предложенному изобретению, полученная в примере 1;
Группа 2: 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцинат, полученный согласно прототипу RU 2373207.
Образцы крови отбирались через катетер в яремной вене через 0.25 ч, 0.5 ч, 1.0 ч, 1.5 ч, 2.0 ч, 4.0 ч, 6.0 ч, 8.0 ч, и 12.0 ч, после чего в плазме крови методом ВЭЖХ определялась концентрация вещества. Условия хроматографирования:
колонка - «Luna С-18(2)» (Phenomenex; 250×4,6 мм; 5 мкм), оснащенная универсальной предколонкой - “SpheroGuard” С18, 4,0×3,0 мм.
подвижная фаза - 0,01 M KH2PO4 : метанол (в соотношении 2:3);
скорость потока - 1.3 мл/мин;
длина волны детектирования - 273 нм.
Хроматографирование проводили при комнатной температуре (20-22°С).
Перед хроматографированием подвижную фазу фильтровали и дегазировали на ультразвуковой бане. В этих условиях время удерживания исследуемого вещества составило 6.1 мин. Результаты исследования представлены в табл. 4.
Группа 1
Содержание действующего вещества в крови животного через 15 минут после введения кристаллической формы настоящего изобретения достоверно выше, чем в случае использования формы вещества согласно прототипу.
Пример 5. Исследование жаропонижающего действия
Для оценки жаропонижающего действия использовали известную методику (см. F.ZHANG et al., Metabolomic study of the fever model induced by baker's yeast and the antipyretic effects of aspirin in rats using nuclear magnetic resonance and gas chromatography-mass spectrometry, JOURNAL OF PHARMACEUTICAL AND BIOMEDICAL ANALYSIS, 2013, V. 81, pp. 168-177). Эксперимент проводили на крысах линии Вистар, которых рандомизированно делили на три группы, в каждой группе по 5 животных. Каждой крысе 1 группы вводили кристаллическую форму по примеру 1 (далее - активная фармацевтическая субстанция или АФС) в дозе 4 мг/кг вводили внутрижелудочно с помощью зонда однократно через 14 ч после введения дрожжей, каждой крысе 2 группы вводили форму согласно прототипу аналогичным образом. Третья группа была контрольной. Ректальную температуру измеряли электротермометром (AT-12R PHYSITEMP, производство Израиль) до введения пирогена и через 12, 24, 48, и 72 ч после него. Результаты в виде прироста температуры по отношению к значениям до введения пирогена представлены в табл. 5.
Группа 1 (АФС)
Группа 2 (прототип)
Группа 3 (контроль)
Из полученных данных следует, что 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантин сукцинат обладает антипиретическим действием. Эффект усиливается в случае применения кристаллической формы настоящего изобретения.
Пример 6. Оценка стабильности
Стабильность кристаллической формы 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината, полученной в примере 1, оценивали методом ускоренного старения согласно ОФС.1.1.0009.15 Сроки годности лекарственных средств, государственной фармакопеи РФ. При повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается.
Срок годности (С) при температуре хранения (txp) связан с экспериментальным сроком годности (СЭ) при повышенной температуре экспериментального хранения (tэ) уравнением Вант-Гоффа:
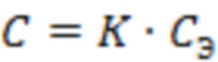 ;
; 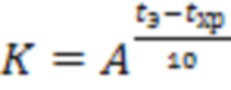 ;
;
где А - температурный коэффициент, который принимается равным 2.5.
Были выбраны условия хранения в эксперименте ускоренного старения: 30 дней при температуре 60°C (соответствует 2 годам при комнатной температуре). Для проведения исследования образец кристаллической формы 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината, полученной в примере 1, оставляли в климатической камере на 30 дней при температуре 60°C. Далее была зарегистрирована рентгенограмма полученного образца. Результаты измерений представлены на фиг.3. На полученной картине отсутствовали дополнительные рефлексы, что свидетельствует о чистоте формы и о сохранении кристаллической структуры. Таким образом, кристаллическая форма 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина сукцината остается стабильной в выбранных условиях хранения.
Пример 7. Исследование токсичности
Исследование острой токсичности при внутрижелудочном введении проводили в соответствии с Руководством по проведению доклинических исследований лекарственных средств. Часть первая, Под ред. А.Н. МИРОНОВА, М.: Гриф и К, 2012, 944 с. Использовали внутрижелудочное (пероральное) введение раствора кристаллической формы по примеру 1 в дозе 1000 мг/кг (в несколько приемов).
Через 14 дней после введения препарата были проведены эвтаназия и патоморфологическое вскрытие животных. При вскрытии крыс никаких изменений внутренних органов не наблюдалось.
Пример 8. Получение фармацевтической композиции и лекарственного средства
Для приготовления фармацевтической композиции и лекарственной формы использовали:
Композиция 1
Композиция 2
Указанные вещества просеивали, взвешивали и смешивали.
Композиции таблетировали на таблеточной машине, состоящей из стальной матрицы с отверстиями и двумя расположенными друг над другом хромированными стержнями - верхними и нижними пуансонами. Нижний пуансон фиксирует пространство в матрице, в которое засыпается фармацевтическая композиция. Далее верхний пуансон спрессовывает композицию. Затем верхний и нижний пуансоны последовательно удаляются из матрицы, выталкивая таблетку.
Изобретение относится к кристаллической форме сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, которая может найти применение в качестве противоаллергического средства средства. Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина характеризуется положениями пиков в порошковой рентгенограмме, полученной с использованием Cu(Kα)-излучения, 2θ, град: 6.1±0.2, 12.2±0.2 и 20.0±0.2. Изобретение также относится к содержащим указанную форму фармацевтической композиции и лекарственному средству, а также к их применению для лечения аллергических заболеваний или расстройств. Технический результат - ускорение наступления терапевтического эффекта, увеличение терапевтической эффективности, наличие свойства жаропонижающего действия. 5 н. и 9 з.п. ф-лы, 3 ил., 5 табл., 8 пр.
1. Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, характеризующаяся положениями пиков в порошковой рентгенограмме, 2θ, град: 6.1±0.2, 12.2±0.2 и 20.0±0.2.
2. Кристаллическая форма по п.1, характеризующаяся положениями пиков в порошковой рентгенограмме, полученной с использованием Cu(Kα)-излучения, 2θ, град: 6.1±0.2, 12.2±0.2, 20.0±0.2, 20.7±0.2 и 28.7±0.2.
3. Кристаллическая форма сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина, характеризующаяся моноклинной сингонией, величинами ребер кристаллической ячейки,  (ангстрем): 9.17±0.50
(ангстрем): 9.17±0.50  , 29.10±0.50
, 29.10±0.50  и 11.43±0.50
и 11.43±0.50  и величиной угла (град) 104.71°±5.00°.
и величиной угла (град) 104.71°±5.00°.
4. Кристаллическая форма по п.3, характеризующаяся величинами ребер,  (ангстрем): 9.1768(13)
(ангстрем): 9.1768(13)  , 29.103(4)
, 29.103(4)  и 11.4312(13)
и 11.4312(13)  и величиной угла (град) 104.713(6)° при температуре 140 К.
и величиной угла (град) 104.713(6)° при температуре 140 К.
5. Фармацевтическая композиция, обладающая противоаллергической активностью, включающая кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина в эффективном количестве по любому из пп.1-4 и по меньшей мере один фармацевтически приемлемый эксципиент.
6. Фармацевтическая композиция по п.5, отличающаяся тем, что указанная композиция представляет собой состав в виде твердой формы.
7. Фармацевтическая композиция по п.6, отличающаяся тем, что твердая форма представляет собой порошок, гранулу, капсулу или таблетку.
8. Фармацевтическая композиция по п.5, отличающаяся тем, что указанная композиция включает кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина по любому из пп.1-4 в эффективном количестве.
9. Фармацевтическая композиция по п.5, отличающаяся тем, что каждый фармацевтически приемлемый эксципиент выбирают из группы, включающей наполнитель, связывающее вещество, смазывающее вещество, разрыхляющее вещество, скользящее вещество, консервант, корригент и краситель.
10. Лекарственное средство в твердой форме для лечения аллергических заболеваний или расстройств, включающее кристаллическую форму сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина по любому из пп.1-4 или фармацевтическую композицию по любому из пп.5-9.
11. Лекарственное средство по п.10, отличающееся тем, что твердая форма представляет собой порошок, гранулу, капсулу или таблетку.
12. Лекарственное средство по п.10, отличающееся тем, что включает по меньшей мере один фармацевтически приемлемый эксципиент.
13. Лекарственное средство по п.12, отличающееся тем, что каждый фармацевтически приемлемый эксципиент выбирают из группы, включающей наполнитель, связывающее вещество, смазывающее вещество, разрыхляющее вещество, скользящее вещество, консервант, корригент и краситель.
14. Применение кристаллической формы сукцината 3-метил-7-[4-(4-бензгидрилпиперазинил-1)бутил]ксантина по любому из пп.1-4 для лечения аллергических заболеваний.
| СПОСОБ ПОЛУЧЕНИЯ 3-МЕТИЛ-7-[4-(БЕНЗГИДРИЛ-4-ПИПЕРАЗИНИЛ-1) БУТИЛ]КСАНТИНА И ЕГО СОЛЕЙ С ОРГАНИЧЕСКИМИ ИЛИ НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ | 2008 |
|
RU2373207C1 |
| 2007 |
|
RU2333212C1 | |
| Р.Г | |||
| Глушков и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Химико-фармацевтический журнал | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| И.С | |||
| Гущин, К.Л | |||
| Крышень, А.Б | |||
| Бондаренко | |||
| Противовоспалительная активность | |||
Авторы
Даты
2025-02-11—Публикация
2022-09-29—Подача