Область изобретения
Настоящее изобретение в целом относится к областям фармакологии и медицины. Более конкретно, настоящее изобретение относится к новым композициям и многоцелевым терапевтическим подходам, способным свести к минимуму местное воспаление и его последствия у субъектов, страдающих иммунными, инфекционными, травматическими или токсическими местными расстройствами. Изобретение также раскрывает новые композиции и способы лечения или предотвращения развития синдрома высвобождения цитокинов.
Предпосылки изобретения
Почти все повреждения кожи и слизистых оболочек, независимо от того, имеют ли они травматическое, аллергическое, токсическое, вирусное или бактериальное происхождение, включают клеточное повреждение, которое вызывает местный воспалительный ответ иммунной системы. Этот иммунный ответ является самым первым защитным и восстановительным ответом, ведущим к системной реакции с высвобождением множества связанных с заболеванием факторов, цитокинов и других белков, которые вызывают местное воспаление, боль и отек в качестве общих симптомов. Для борьбы с патогеном иммунные клетки, особенно лейкоциты, включая В-клетки, Т-клетки, природные клетки-киллеры, макрофаги, дендритные клетки и моноциты, активируются и продуцируют множество специфичных для заболевания цитокинов в месте инфекции или воспаления для подавления патогена в острой фазе. Если инфекция продолжается, в качестве защитного механизма высвобождается все больше и больше провоспалительных цитокинов для поддержания воспаления. Если болезнь не удается излечить и она продолжает прогрессировать, продолжает активироваться все больше и больше иммунных клеток, что может привести к стрессу и нарушению регуляции всего механизма иммунного ответа, приводя к внезапному высвобождению чрезмерно большого количества специфических для многих заболеваний белков и провоспалительных цитокинов в качестве защитного механизма. Это явление известно как синдром выброса цитокинов (CRS) или цитокиновый шторм (CS), который вызывает, например, распространенное тяжелое воспаление (покраснение), приводящее к повреждению тканей, экссудации клеточной жидкости, отеку, боли, жару, внесосудистому давлению, снижению тканевой перфузии, нарушению целостности клеточной мембраны и образованию межклеточных щелей. Время появления симптомов, цитокины, индуцирующие CRS, тяжесть CRS и его последствия зависят от индуцирующего агента, локализации заболевания и степени активации иммунных клеток. CRS приводит к тяжелому местному и системному воспалению, а также генерализованному воспалению с различными симптомами в зависимости от затронутых органов. В случае местных респираторных инфекций системное воспаление может в частности поражать легкие, вызывая утечку из легочных кровеносных сосудов, накопление жидкости в легких, распространенный отек и дыхательную недостаточность, что может привести к смерти при отсутствии лечения. Смертность от всех причин, связанная с CRS, оценивается как около 40%. IL-6 считается основным CRS, индуцирующим провоспалительные цитокины при легочном CRS, но из-за повышенного содержания других цитокинов точная физиопатология CRS еще не установлена. Если CRS не влияет на жизненно важные органы, он может внезапно усугубить патологию без летального исхода.
Настоящее изобретение относится только к местным заболеваниям, вызывающим местное воспаление как начальную физиопатологическую реакцию. Первоначальное местное поражение обычно вызывается патогенным агентом, аллергеном, загрязняющими веществами или любым веществом, нарушающим клеточные функции. Слизистая оболочка носа и дыхательных путей, ротовая полость, поверхность горла, кожа, вагинальные и анальные отверстия, слизистая оболочка желудочно-кишечного тракта и поверхность глаз являются ключевыми органами, где местные клеточные повреждения вызваны внешним воздействием, но они также могут быть вызваны внутренними токсическими раздражителями, такими как вирус герпеса.
Все местные заболевания, включающие воспаление, разрушение клеток и нарушением клеточной целостности в любой части тела, могут привести к CRS. К таким местным заболеваниям относятся, например, вирусные респираторные инфекции, назальная и глазная аллергия, астма, воспалительные респираторные заболевания, воспалительные заболевания глаз, псориаз, экзема, дерматит, геморрой, хронические раны, диабетические язвы и язвы желудка.
CRS обычно наблюдается при вирусных заболеваниях, затрагивающих кожу или слизистые оболочки, таких как заболевания, связанные с гриппом и коронавирусом, которые вызывают разрушение клеток и хроническое воспаление.
Многие вирусы имеют внешний капсид, который содержит на своей поверхности специфические гликопротеины (Gps). Примеры вирусных Gps включают H (гемагглютинин) и N (нейраминидаза) Gps на вирусе гриппа; Gps C (gC) и B (gB) на вирусе герпеса; шиповидный белок S (S1 и S2) Gps на коронавирусах COVID-19, SARS и MERS. Инфекция начинается, когда вирусный гликопротеин присоединяется к своему комплементарному рецептору клетки-хозяина, заражая ее и проникая в клетку для размножения. Многие вирусы не могут разрушить клеточную стенку хозяина и нуждаются в помощи местных доступных протеолитических ферментов (белков), чтобы проникнуть в клетку. Вирус убивает клетки, и на зараженной поверхности высвобождаются миллионы свободных вирусных частиц, которые начинают размножаться в окружающих тканях и заражать новые клетки. Гибель клеток приводит к образованию брешей в естественном клеточном барьере, что делает возможным системное проникновение других патогенов.
В случае вирусных инфекций носа или горла вирус постепенно поражает слизистую оболочку верхних и нижних дыхательных путей и достигает легких. Если распространение вируса не остановить быстро, это приводит к обширному повреждению клеток и воспалению глотки и слизистой оболочки дыхательных путей.
Назальная и глазная аллергия, астма и воспалительные респираторные заболевания в основном вызываются вирусными инфекциями, аллергенами или загрязняющими веществами. Возбудители попадают на слизистую оболочку носа, рта или глаз в результате воздействия окружающей среды и вызывают местное раздражение, воспаление и повреждение клеток, образуя щели в слизистой оболочке, через которые воспалительные белки могут попасть в системный кровоток. Слизистые оболочки этих органов содержат сенсорные TRP-рецепторы (каналы с транзиторным рецепторным потенциалом), стимуляция которых запускает нейрогенный воспалительный каскад путем продуцирования TSLP (тимусного стромального лимфопротеина). Воспалительные и аллергенные каскады активируют дендритные клетки и TH2-лимфоциты, что приводит к высвобождению воспалительных цитокинов (например, IL-4, IL-6, IL-23, IL-33, TNF-α) с последующей активацией B-лимфоцитов и высвобождение антител IgE. Связывание IgE на поверхности тучных клеток вызывает высвобождение гистамина, лейкотриенов, простагландинов и других белков, которые начинают местно накапливаться на поврежденной поверхности. Хотя основная физиопатология воспаления остается идентичной, расположение, тип и концентрация этих белков могут варьироваться от заболевания к заболеванию (белки, специфичные для заболевания), что требует различных подходов к лечению каждого заболевания.
Если местное воспаление не лечить, оно разрушает клетки слизистой оболочки, создавая межклеточные щели из-за утраты межклеточной соединительной ткани. Эти межклеточные щели обеспечивают прямое системное проникновение местных белков, цитокинов, аллергенов и загрязняющих веществ, которые поддерживают воспалительные и иммунные каскады, ведущие к хроническому воспалению, обширной клеточной деструкции, хронической аллергии, дыхательной недостаточности, астме, а затем увеличивают риск начала CRS. Если воздействие патогена не заблокировать, сенсибилизацию каналов TRP и других провоспалительных рецепторов не остановить, концентрацию цитокинов и нежелательных белков поверхности, таких как гистамин, IgE и TSLP, не снизить, а щели между клетками не вылечить, болезнь становится хронической и более вероятно возникновение CRS.
Также было показано, что некоторые лекарственные средства могут провоцировать CRS, например, ритуксимаб, тисагенлеклейсел CD19 CAR-T клеток, TGN1412 или терализумаб и другие биотерапевтические лекарственные средства, модулирующие иммунную систему, такие как муромонаб-CD3 и алемтузумаб. Механизм остается таким же, за исключением того, что эти лекарственные средства могут модулировать и нарушать регуляцию иммунной системы.
Псориаз, экзема и дерматит являются иммунными заболеваниями, при которых нарушение регуляции факторов роста приводит к чрезмерному и неконтролируемому росту клеток, высыханию и шелушению кожи. Плохая адгезия клеток кожи приводит к проникновению бактериальной контаминации в очаг поражения, которые начинают разрушать клетки. Разрушение клеток приводит к высвобождению множества провоспалительных цитокинов на поверхности, и заболевание становится хроническим.
Хронические раны, такие как пролежни и диабетические язвы, чрезвычайно трудно излечить, так как помимо того, что они содержат мертвые клетки, клеточный дебрис и множество протеолитических ферментов, которые препятствуют росту клеток и заживлению ран, эти поражения остаются открытыми для внешней среды и часто загрязняются. По этой причине большинство хронических ран, таких как пролежни, диабетические язвы или венозные язвы на ногах, никогда не заживают, и около 40% пациентов умирают до того, как у них наступает заживление раны. Для заживления требуется рост клеток, что, в свою очередь, требует чистой, свободной от химических веществ и источников воспаления и увлажненной среды. Чтобы очистить повреждение, человеческий организм естественным образом вырабатывает более 27 различных матриксных металлопротеиназ (MMP). Эти протеолитические ферменты направлены на расщепление белкового дебриса на более мелкие частицы, которые могут быть удалены через раневую экссудацию. Однако, в настоящее время хорошо известно, что некоторые из этих MMP (MMP 2, 3, 8, 9 и 13) разрушают не только белковый дебрис, но и белки, составляющие клеточный матрикс, такие как коллаген, эластин, ламинин, а также гиалуроновую кислоту. В отсутствие этого клеточного матрикса клетки не могут прикрепиться, не могут расти, и рана не может зажить.
Геморроидальная шишка представляет собой расширенные и воспаленные кровеносные сосуды со специфическими геморроидальными провоспалительными цитокинами на поверхности.
Все приведенные выше примеры местных заболеваний кожи, слизистых оболочек носа, полости рта, желудка и дыхательных путей или поверхности глаз показывают, что они всегда связаны с разрушением клеток и нарушением клеточной целостности. Очаговая и местная клеточная деструкция приводит к росту бактерий, запуску воспалительной реакции с высвобождением связанных с болезнью специфических провоспалительных цитокинов (например, интерлейкинов) и других белков (например, гистамина, MMP, IgE) на поврежденной поверхности. Кроме того, в зависимости от происхождения заболевания, поражение может также содержать патогены, такие как вирусные частицы, аллергены, загрязняющие вещества, частицы тяжелых металлов, таких как мышьяк, ртуть, кадмий и свинец.
К сожалению, поскольку CRS имеет многофакторное происхождение, в настоящее время не существует эффективного средства профилактики или лечения CRS. Идеальное лечение должно быть многоцелевым, чтобы предотвратить возникновение CRS, и потому оно должно: i) очищать зараженную поверхность, захватывая и/или удаляя токсические соединения (источники бактериальной и прочих видов контаминации), ii) защищать зараженную поверхность против новой инфекции, iii) обеспечивать благоприятную чистую среду для роста клеток и заполнения межклеточных щелей. Но оно также должно iv) останавливать или уменьшать цикл высвобождения разрушительных цитокинов и v) подавлять воспаление, чтобы уменьшить раздражение, боль, зуд и дальнейшее повреждение клеток. Если какой-либо из этих факторов не будет устранен должным образом, выздоровление будет отложено, а в худшем случае может произойти цитокиновый шторм, который может привести к смерти.
Например, легочный цитокиновый синдром, вызванный коронавирусной инфекцией, вызывается внезапным высвобождением большого количества цитокинов, главным образом IL-6, что может вызвать тяжелое воспаление и отек легких. Дыхательная недостаточность может привести к смерти. Другие CRS, которые не поражают легкие, обнаружить трудно, поскольку они усугубляют воспаление и ухудшают течение заболевания, не вызывая повреждения сердца или легких. Для лечения воспаления легких, вызванного коронавирусом, специфические антитела к IL-6 (тоцилизумаб) оказались малоэффективными и до сих пор не одобрены для предотвращения CRS. Другие методы лечения, такие как высокие дозы кортикостероидов, абсорбция цитокинов с помощью экстракорпоральной гемофильтрации, переливание богатой антителами плазмы или лечение хлорохином, оказались малоэффективными.
Другие симптоматические средства для лечения CRS являются моноцелевыми и малоэффективными, поскольку они направлены исключительно против воспаления (противовоспалительные лекарственные средства) или микробной контаминации (антисептики и антибиотики), внутриклеточных вирусов (тамифлю, который действует внутриклеточно, поскольку местные противовирусные лекарственные средства еще не обнаружены), на облегчение боли (анестетики или анальгетики) или блокирование одного специфического цитокина.
На протяжении веков растительные экстракты, богатые таннинами, использовались местно в качестве средств, помогающих заживлению ран, уменьшающих контаминацию или уменьшающих воспаление и боль, но результаты неудовлетворительны, поскольку, вероятно, растительные таннины связываются только с несколькими неселективными белками или цитокинами и, вероятно, также ингибируют полезные белки, которые необходимы для заживления.
Среди видов лечения, посвященных очистке поврежденной поверхности, полоскание горла морской или соленой водой до сих пор считается одним из лучших средств против инфекции или воспаления горла. Эти осмотически активные растворы образуют гипертоническую пленку на слизистой оболочке глотки, а возникающая в результате экссудация гипотонической жидкости наружу помогает уменьшить нагрузку источников контаминации на глотку или раневые поверхности. К сожалению, эта пленка гипертонического раствора в течение нескольких минут разбавляется вытекающей гипотонической жидкостью, что ограничивает эффективность этого лечения. Более того, концентрация NaCl (не более 3,4%) характеризуется низкой осмотической способностью и потому не может оказывать сильное осмотическое действие. Эту концентрацию нельзя увеличить из-за возникающего в результате сильного раздражения, повреждения клеток, жжения слизистой оболочки и химической индуцированной клеточной цитотоксичности.
В документе WO 2014/194966 раскрывается применение гипертонических осмотически активных композиций для местного применения с целью очистки поверхностных повреждений посредством осмотического потока жидкости. Эти композиции содержат глицерин и растительные таннины, которые способны связывать глицерин, чтобы получить композицию, также называемую «пленкообразующий глицерин», с увеличенным временем удерживания на живой биологической поверхности. Такую пленкообразующую композицию глицерина можно использовать в качестве эффективного местного средства для очистки поврежденной поверхности. Осмотическое давление, создаваемое пленкой глицерина, притягивает гипотоническую жидкость из внутренних частей ткани, тем самым отделяя и дренируя источники контаминации поверхности. Сведение к минимуму контакта поврежденной поверхности с поступающими патогенами и снижение концентрации источников контаминации стимулирует рост клеток и формирование неповрежденного клеточного барьера. Однако таннины в пленкообразующем глицерине предназначены для связывания только с глицерином, а не с какими-либо другими специфическими белками или макромолекулами, связанными с заболеванием. Они не оказывают или оказывают лишь незначительное влияние на уменьшение содержания очень низкомолекулярных соединений, таких как цитокины, другие белки, связанные с заболеванием, или цитотоксические макромолекулы, которые играют ключевую роль в поддержании воспаления и замедлении процесса заживления. Поскольку они не могут быть полностью удалены осмотическим потоком жидкости, токсические молекулы, такие как вирусные частицы, воспалительные цитокины, гистамин, IgE, факторы роста и другие малые белки, продолжают оказывать вредное воздействие. Авторы изобретения заметили, что даже если среди миллионов вирусных частиц или цитокинов, высвобождающихся на поврежденной поверхности, 99 % частиц удаляются посредством осмотического потока, оставшегося 1% достаточно для инфицирования новых клеток или поддержания воспалительного каскада. Хотя осмотически активная глицериновая пленка удаляет большое количество свободно плавающих молекул с поверхности, со временем ее эффективность снижается, осмотическое давление и эффективность очистки постепенно уменьшаются. Оставшиеся небольшие токсические молекулы продолжают поддерживать воспалительные, аллергические и иммунные каскады, которые могут вызвать CRS.
Следовательно, существует необходимость в поиске многоцелевого механизма, который, помимо защиты и очистки поврежденной поверхности, может одновременно нейтрализовать специфические для заболевания провоспалительные цитокины, запускающие воспаление TRP-рецепторы, белки, патогены и/или другие токсические молекулы с целью для подавления воспаления и минимизации риска CRS и его последствий.
Такие композиции должны быть полностью безопасными, нецитотоксичными, быстродействующими, применимыми местно, чтобы избежать системной абсорбции.
Краткое описание сущности изобретения
В настоящем изобретении предлагается новый многоцелевой терапевтический подход для профилактики или лечения местного воспаления, воспалительных заболеваний и их последствий, таких как неконтролируемое высвобождение цитокинов, называемое цитокиновым синдромом (CS) или синдромом высвобождения цитокинов (CRS). Изобретение относится к композициям и способам, которые воздействуют на несколько мишеней, вовлеченных в запуск CRS, и которые могут быть использованы у людей или животных.
Настоящее изобретение относится к композиции, содержащей по меньшей мере один полимер двойного действия, связанный с глицерином и способный связываться по меньшей мере с одним провоспалительным соединением, для местного применения при профилактике или лечении местного воспалительного заболевания и его последствий у нуждающегося в этом субъекта.
В соответствии с воплощением композиция предназначена для местного применения при профилактике или лечении синдрома высвобождения цитокинов.
В соответствии с воплощением по меньшей мере одно провоспалительное соединение выбрано из группы, состоящей из матриксных металлопротеаз, гистаминов, цитокинов, клеточных рецепторов, ионов металлов, иммуноглобулинов или вирусных гликопротеинов.
В соответствии с воплощением местное воспалительное заболевание выбрано из группы, состоящей из вирусных инфекций, риносинусита, ран и язв, псориаза, экземы, дерматита, аллергии, астмы, вызванных контаминацией респираторных заболеваний, вызванных контаминацией местных повреждений, желудочно-кишечных язв, геморроя, генитальных инфекций, аллергии глаза, конъюнктивита и воспаления глаз.
В соответствии с предпочтительным воплощением общее количество по меньшей мере одного полимера двойного действия составляет от 0,01 до 5 мас.% от общей массы указанной композиции, предпочтительно от 0,01 до 3,5 мас.% от общей массы указанной композиции.
В соответствии с другим воплощением композиция дополнительно содержит по меньшей мере один ингредиент, выбранный из группы, состоящей из меда, экстракта прополиса, растительной камеди, такой как ксантановая камедь и/или аравийская камедь, и ароматических масел.
В соответствии с другим воплощением композиция дополнительно содержит по меньшей мере одно лекарственное средство, такое как анальгетик, антибиотик, противовоспалительное лекарственное средство, антигистаминное средство, сосудорасширяющее средство, бронхолитическое средство, противоотечное лекарственное средство, соединение, связывающее специфические местные рецепторы, или ароматическое масло.
В соответствии с воплощением композицию наносят местно на поврежденную и/или воспаленную биологическую поверхность, такую как кожа, слизистая оболочка глаза, конъюнктива, роговица, поверхности рта, носа, желудочно-кишечного тракта, дыхательных путей или половых органов.
В соответствии с воплощением композицию наносят в виде жидкости, ингалятора, жидкой повязки, раствора, геля, крема, пасты или мази, и она представлена в виде спреев, тюбиков, ампул, ватных или полимерных повязок, гранул, порошка или мягких желатиновых капсул.
В соответствии с воплощением по меньшей мере один полимер двойного действия является натуральным, полусинтетическим и/или синтетическим.
В соответствии с другим воплощением по меньшей мере один полимер двойного действия представляет собой таннин, полученный из растения или частей растения
В соответствии с другим воплощением ингредиент и/или лекарственное средство захвачены полимерными связями указанной композиции для замедленного высвобождения ингредиента и/или лекарственного средства с целью дальнейшего усиления терапевтических свойств композиции.
Изобретение также относится к способу получения композиции, содержащей по меньшей мере один связанный с глицерином полимер двойного действия, в котором содержится захваченный ингредиент и/или лекарственное средство для замедленного высвобождения, с целью дальнейшего усиления терапевтических свойств композиции. Способ по изобретению содержит следующие этапы:
- смешивание глицерина с ингредиентом и/или лекарственным средством, а затем
- добавление по меньшей мере одного полимера двойного действия для формирования сетки глицерин-полимер двойного действия вокруг ингредиента и/или лекарственного средства.
Краткое описание чертежей
Фигура: (A) Глицерин, содержащий 4 полимера двойного действия: P. ginseng + C. sinensis + C. longa + U. dioica; (B) Профиль GCMS глицерина. Глицерин определяется как одиночный пик между 31-32 минутами с пА 340; (C) только P. ginseng; (D) только C. sinensis; (E) только C. longa; (F) только U. dioica.
Раскрытие изобретения
В контексте изобретения термин «местное воспалительные заболевания» или «воспалительные местные заболевания» обозначает все воспалительные заболевания, при которых патологические симптомы проявляются на поверхности органа или тела, такой как кожа, полость рта, полость носа, включая верхние и нижние дыхательные пути, поверхности глотки и/или глаз, половые органы, анальное отверстие, а также слизистая оболочка желудочно-кишечного тракта (ЖК).
В контексте изобретения термин «многофакторное заболевание» означает, что существует множество факторов, действующих совместно, чтобы вызвать возникновение заболевания. При всех местных заболеваниях, когда воспаление становится хроническим, чрезмерная активация иммунной реакции заполняет пораженный участок большим количеством про- и противовоспалительных цитокинов и других белков, что может вызвать обширную деструкцию тканей. Например, при местной аллергической реакции наблюдается клеточное повреждение, появление большого количества воспалительных цитокинов, TSLP, гистамина, антител IgE и аллергенов на аллергической поверхности, что способствует продолжению аллергической реакции. Примерами местных многофакторных заболеваний, протекающих с участием цитокинов, являются, например, вирусные и бактериальные инфекции горла, риносинусит, кашель, аллергический и вызванный контаминацией ринит, астма, генитальные инфекции, хронические язвы и раны кожи и слизистых оболочек, местные сосудистые патологии, такие как геморрой, и глазные воспалительные заболевания. Связанные с заболеванием цитокины и их концентрация могут варьироваться в зависимости от типа инфекции, места повреждения, типа пораженных клеток и степени повреждения ткани. Таким образом, местные воспалительные заболевания по изобретению можно условно разделить на пять категорий: (1) хронические раны кожи и слизистых оболочек, (2) воспалительные заболевания носа, полости рта, половых органов и кожи, (3) респираторные заболевания, (4) вирусные заболевания, (5) заболевания глаз.
В соответствии с воплощением местное воспалительное заболевание выбрано из группы, состоящей из вирусных инфекций, риносинусита, ран и язв, псориаза, экземы, дерматита, аллергии, астмы, вызванных контаминацией респираторных заболеваний, вызванных контаминацией местных повреждений, желудочно-кишечных язв, геморроя, генитальных инфекций, глазной аллергии, конъюнктивита и воспаления глаз. В контексте изобретения профилактика или лечение CRS означает профилактику или лечение множества факторов, участвующих в местных воспалительных заболеваниях. Все эти триггерные факторы CRS должны быть либо уменьшены, либо заблокированы одновременно, чтобы свести к минимуму воспалительный порог, запускающий CRS. Таким образом, ключевыми факторами являются прекращение контакта с причиной заболевания, восстановление естественных барьерных функций слизистой оболочки путем очистки воспаленной поверхности с целью стимуляции роста клеток и минимизация концентрации провоспалительных триггеров, то есть специфических цитокинов, других белков, рецепторов клеточной поверхности или макромолекул (CPRM) одновременно. В контексте изобретения «провоспалительное соединение» и «CPRM» используются для обозначения белков, рецепторов клеточной поверхности, макромолекул, аллергенов и загрязняющих веществ, таких как ионы металлов и другие соединения, которые связаны с местной воспалительной реакцией.
В контексте изобретения термины «нейтрализация» и «блокировка» обозначают потерю активности молекулы-мишени из-за того, что она либо вытесняется из сайта, либо связывается с другими молекулами таким образом, что не может выполнять свою функцию.
Задача настоящего изобретения относится к композициям, содержащим по меньшей мере один полимер двойного действия, связанный с глицерином, с одной стороны, и способный связываться с одним или более CPRM для местного применения с целью минимизации местного воспаления и вероятности начала CRS у нуждающегося в этом субъекта. Полимеры двойного действия способны связываться с глицерином, а также с одним или несколькими провоспалительными соединениями, рецепторами или токсичными молекулами.
Глицерол или глицерин представляет собой кипящий при высокой температуре, вязкий, бесцветный, гигроскопичный и сладкий раствор без запаха. Он характеризуется высокой осмотичностью и способностью притягивать гипотоническую жидкость через полупроницаемую мембрану. Это молекула тригидроксисахарного спирта с тремя основными цепями каркаса из трех атомов углерода, каждая из которых ковалентно связана с гидроксильной группой.
Наличие нескольких свободных гидроксильных групп и атомов углерода делает его органическим полиоловым соединением с названием по IUPAC 1,2,3-пропантриол. Три гидроксильные группы глицерина дают ему возможность реагировать со многими органическими кислотами с образованием сложных эфиров и с полимерными веществами с образованием макромолекул.
Глицерин не является сильным раздражителем, но высокие концентрации могут раздражать чувствительные ткани. Таким образом, концентрация глицерина в композициях может быть выбрана, исходя из необходимости гидратирующих и очищающих свойств, необходимых для лечения конкретной местной патологии, и чувствительности биологической ткани, на которую будет наноситься композиция. Например, фарингит часто сопровождается тяжелой бактериальной инфекцией, при которой микроорганизмы прочно прилипают к поверхности горла, что требует высокой осмотической силы для отделения и дренирования загрязняющих веществ. Поскольку поверхность горла менее чувствительна к раздражению, концентрация глицерина в пленкообразующем глицерине была высокой (более 50%). Для лечения риносинусита, поскольку слизистая оболочка носа является наиболее чувствительным органом в организме, концентрацию глицерина поддерживали на низком уровне (менее 30%). Композиции, содержащие более высокую концентрацию глицерина и связывающих глицерин таннинов или полимеров с низким содержанием вспомогательных веществ (воды), образуют тонкую пленку, устойчивую к механическим воздействиям, по сравнению с низкой концентрацией глицерина. Для местных повреждений, требующих высокой очищающей активности, концентрация глицерина была высокой (до 99%), в то время как низкие концентрации использовались для чувствительных поврежденных поверхностей и тех, которые требуют более низкой осмотической очистки.
Согласно изобретению композиции для местного применения также содержат полимеры двойного действия. Все полимеры, будь то природные или синтетические, обладают сильной способностью связываться со специфическими белками (такими как цитокины, гистамин, IgE), а также с различными другими органическими соединениями, включая макромолекулы, аллергены, частицы тяжелых металлов, ионы металлов, аминокислоты и алкалоиды. Связывание полимер-белок или полимер-макромолекула является специфичным, поскольку все полимеры не могут связываться со всеми молекулами, но они могут связываться более чем с одной молекулой одновременно из-за их большого размера. «Полимеры двойного действия» по изобретению представляют собой полимеры, которые обладают способностью связываться с молекулами глицерина и одновременно, в дополнение, с одним или несколькими специфическими CPRM, т.е. специфическими цитокинами, такими как IL-6, другими белками, такими как IgE, рецептором клеточной поверхности, таким как рецептор TRP, или ионами металлов, такими как As, Pb, Hg. Этот конкретный признак важен, потому что, если полимер или ассоциация полимеров, способных блокировать определенные CPRM или ионы металлов, наносят непосредственно на рану, они быстро удаляются осмотическим потоком жидкости, так как не прикреплены к молекулам глицерина и не находятся в составе пленкообразующего глицерина. Таким образом, двойную активность могут проявлять только такие природные, полусинтетические или синтетические полимеры, которые обладают способностью связываться не только с молекулами глицерина, но также с одним или несколькими провоспалительными CPRM, связанными с заболеванием. Если на поврежденную поверхность наносят только полимеры, связывающие CPRM, это может блокировать некоторые белки, но защитный и очищающий эффект глицерина будет отсутствовать. В этом случае клетки не будут расти, патогены продолжат поступать в организм и воспаление сохранится.
Несколько примеров предпочтительных провоспалительных соединений (CPRM) раскрыты в табл. 1 ниже.
Таблица 1
В соответствии с предпочтительным воплощением полимеры двойного действия по изобретению способны связываться по меньшей мере с одним соединением, выбранным из группы, состоящей из матриксных металлопротеаз, гистаминов, цитокинов, рецепторов TRP, ионов металлов, иммуноглобулинов и вирусных гликопротеинов.
В соответствии с воплощением полимеры двойного действия способны связываться по меньшей мере с одним цитокином, выбранным из группы, состоящей из хемокинов, интерферонов, интерлейкинов, лимфокинов, факторов некроза опухоли, стромального лимфопоэтина тимуса (TSLP) и факторов роста.
Источники контаминации - это вещества, попавшие в окружающую среду, которые оказывают нежелательное воздействие или негативно влияют на полезность ресурса, например, такие вещества как выхлопные газы транспортных средств, содержащие цитотоксические молекулы, такие как частицы тяжелых металлов (As, Cd, Hg и Pb), или макромолекулы. Следовательно, в соответствии с воплощением, полимеры двойного действия способны связываться по меньшей мере с одним ионом металла, выбранным из мышьяка, кадмия, свинца и/или ртути.
Матриксные металлопротеазы (MMP), также называемые матриксными металлопротеиназами или матриксинами, представляют собой протеолитические ферменты, которые участвуют в очистке повреждений посредством протеолиза, в модуляции роста клеток, а также в деградации всех видов белков внеклеточного матрикса. Они также участвуют в процессинге нескольких биоактивных молекул, взаимодействии с рецепторами клеточной поверхности, высвобождении апоптотических лигандов, инактивации хемокинов/цитокинов, миграции клеток (адгезии/дисперсии), дифференцировке, ангиогенезе, апоптозе и защите хозяина.
В соответствии с воплощением полимеры двойного действия способны связываться по меньшей мере с одной матриксной металлопротеазой (MMP), выбранной из MMP-1, MMP-2, MMP-3, MMP-8, MMP-9, MMP-13.
В соответствии с другим воплощением полимеры двойного действия способны связываться по меньшей мере с одним рецептором клеточной поверхности, предпочтительно с рецептором каналов с транзиторным рецепторным потенциалом (TRP), таким как высвобождающие TSLP TRP-рецепторы.
Концентрация полимеров двойного действия, природных, синтетических или полусинтетических, в композиции должна быть как можно ниже и не должна превышать тех уровней, которые препятствуют образованию пленки и их потенциалу связывания CPRM. Таким образом, в соответствии с воплощением, общее содержание полимеров двойного действия варьируется от около 0,01 до около 5 мас.% от общей массы композиции, предпочтительно от около 0,01% до около 3,5 мас.% от общей массы композиции. В соответствии с конкретным воплощением общее содержание полимеров двойного действия составляет менее 2,0 мас.% от общей массы композиции. Такие концентрации позволяют сохранить осмотическую активность пленкообразующего глицерина. Более того, полимеры, используемые в композициях, не должны быть цитотоксичными в используемых концентрациях.
Качество, количество и ассоциация полимеров двойного действия могут быть изменены в зависимости от участка местного применения и состояния поврежденной поверхности.
Примерами синтетических полимеров являются полиэтилен, синтетический каучук, поливинилхлорид (ПВХ), поли[имино(1,6-диоксогексаметилен)иминогексаметилен] (торговая марка Nylon-66), политетрафторэтилен (торговая марка Teflon), акриловое волокно (например, торговая марка Orlon), карбоксиметилцеллюлоза в составе натриевой соли (CMCNa, также называемая кармеллоза), поли(виниловый спирт) (PVOH), полиакриламид (PCM), полиакрилат натрия (SPA), полиэтиленгликоль (PEG), плюроник F-127 (PL127), Klucel - Гидроксипропилцеллюлоза (HPC) и (или_ Solagum (ассоциация камеди акации и ксантановой камеди). Поскольку полимеры представляют собой очень большие молекулы и не могут всасываться в организме, даже синтетические полимеры можно использовать для местного применения.
Природные полимеры, такие как таннины, представляют собой полимерные фенольные соединения, содержащиеся в растительных веществах, с молярной массой от 300 до 3000 Да и даже до 30 000 Да. В соответствии с воплощением, природные полимеры двойного действия получают из любого растения или части растения, богатого таннинами. Методы экстракции природного полимера из растения или части растения хорошо известны в данной области техники, например это может быть технология экстракция путем замачивания, использования аппарата Сокслета или процеживания, как указано в работе Dang Xuan Cuong и соавт. (2019).
Синтетические или полусинтетические полимеры двойного действия получают химическим путем или химически модифицируют из природных полимеров.
Синтетические, полусинтетические или природные полимеры двойного действия по изобретению можно использовать совместно в соответствии с провоспалительными CPRM, связанными с конкретным заболеванием, которые необходимо блокировать.
Для получения полимеров двойного действия по изобретению сначала выбирают нецитотоксический полимер, а затем проверяют его способность связываться с глицерином и с одним или несколькими провоспалительными соединениями (CPRM). Сначала можно проверить, способен ли полимер связываться с глицерином, и, если полимер связывается с глицерином, дополнительно проверить, связывается ли он с одним или несколькими специфическими для заболевания CPRM, или наоборот. В данной области техники существует несколько способов проверки способности полимера связываться с глицерином и с одним или несколькими CPRM.
Примером способа проверки способности полимера связываться с глицерином является получение первого профиля ГХ/ВЭЖХ одного полимера и сравнение его со вторым профилем ГХ/ВЭЖХ комбинации полимера с глицерином. Профили ГХ или ВЭЖХ могут быть получены способами, хорошо известными в данной области. Если первый профиль отличается от второго профиля, это означает, что полимер связался с молекулой глицерина. Минимальную концентрацию полимера, способного связываться со 100% молекулами глицерина, выбирают для оценки связывания CPRM.
Методику оценки связывания CPRM, специфичного для заболевания, выбирают в соответствии с типом CPRM. Например, иммуноферментный анализ ELISA хорошо приспособлен для оценки связывания полимера с цитокинами или белковым рецептором. Связывание ионов металлов можно оценить путем инкубации полимеров с 50% цитотоксической концентрацией одного или более ионов металлов, таких как мышьяк или кадмий, с последующим сравнением разницы цитотоксичности до и после инкубации в конкретных клеточных культурах. Если токсичность снижается, можно предположить, что CPRM связался с полимером. Чтобы оценить нейтрализацию вируса полимерами, полимеры можно инкубировать с известной цитотоксической концентрацией определенного вируса (например, вируса гриппа, герпеса, коронавируса) с последующим воздействием комплекса полимер-вирус на чувствительные к вирусу клетки in vitro. Снижение цитотоксичности смеси, инкубированной с полимером, по сравнению с контролем вируса, инкубируемого без полимера, демонстрирует нейтрализацию вируса. Концентрация полимеров, необходимая для нейтрализации 100% вируса, может быть определена количественно. Если эксперименты in vitro или иммунологические эксперименты невозможны (например, для летучих металлов, таких как Hg), CPRM можно вводить перорально или местно на чувствительных моделях животных (например, крысах, мышах, морских свинках), и характеризующие различия токсичности параметры потребляемого и не потребляемого полимера могут быть определены количественно. Снижение токсичности, связанной с CPRM-полимерами, по сравнению с одним CPRM должно указывать на нейтрализацию CPRM из-за связывания полимера. Эффективность составов, нейтрализующих CPRM, можно проверить на животных моделях или в клинических исследованиях с участием людей.
Таким образом, в зависимости от воспалительного местного заболевания, которое необходимо вылечить, и, следовательно, от вовлеченных CPRM, можно выбрать из тысяч существующих природных, полусинтетических или синтетических полимеров те, которые имеют двойное действие и которые подходят для настоящего изобретения.
Дополнительно в композиции по изобретению могут быть включены загустители и гелеобразующие агенты с целью увеличения толщины и абсорбирующей способности пленки, в частности, при местных патологиях, когда источники контаминации из окружающей среды (например, аллергены - пыльца, ионы металлов, источники контаминации) продолжают воздействовать на биологическую поверхность (например, слизистую оболочку носа). Композиции могут также содержать консерванты. В соответствии с воплощением композиции по изобретению дополнительно содержат по меньшей мере один загуститель/гелеобразующий ингредиент, выбранный из группы, состоящей из меда, экстракта прополиса, растительной камеди, такой как ксантановая камедь и/или гуммиарабик, и ароматических масел или стабилизатора, выбранного из группы консервантов, таких как сорбат калия, бензоат натрия и лимонная кислота.
При создании среды для роста клеток также важно использовать только безопасные для клеток концентрации веществ, которые не являются цитотоксическими.
В соответствии с воплощением композиции по изобретению дополнительно содержат по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
В соответствии с воплощением композиции по изобретению дополнительно содержат по меньшей мере одно лекарственное средство, такое как анальгетик, антибиотик, противовоспалительное средство, антигистаминное средство, противовирусное средство, сосудорасширяющее средство, бронхолитическое средство, противоотечное лекарство, специфический полимер, связывающий местный рецептор, и ароматические масла.
Примерами подходящих анальгетиков являются салициловая кислота, парацетамол, морфин, ингибиторы CGRP или Cox-2, ацетаминофен, NSAID или триптаны.
Примерами подходящих антибиотиков являются бета-лактамы, аминогликозиды, тетрациклины, глицилциклины, макролиды, азалиды, кетолиды, синергистины, линкозаниды, фторхинолоны, фениколы, рифамицины, сульфамиды, триметоприм, гликопептиды, оксазолидиноны, нитромидазолы и липопептиды.
Примерами подходящего противовоспалительного лекарственного средства являются салицилат и его соли, целекоксиб, диклофенак, дифлунизал, этодолак, фенопрофен, флурбипрофен, ибупрофен, индометацин, кетопрофен, меклофенамат, мефенамовая кислота, мелоксикам, набуметон, напроксен, оксапрозин, пироксикам, рофекоксиб салсалат, сулиндак, толметин, вальдекоксиб, преднизолон, преднизолон, метилпреднизолон, метилпреднизолон кортизол, кортизон, гидрокортизон, кортикостерон, тиксокортол, циклесонид, предникарбат, триамцинолон ацетонид, триамцинолоновый спирт, мометазон, амцинонид, будесонид, дезонид, флуоцинонид, флуоцинолон ацетонид, галцинонид, гидрокортизон-17-валерат, галометазон, алкарбазон-бетазон, преданикометазон, бета-метазон 17-бутират, клобетазол-17-пропионат, флуокортолон, флуокортолон, флупредниденацетат, дексаметазон.
Примерами подходящих антигистаминных лекарственных средств являются цетиризин, бромфенирамин, хлорфенирамин, клемастин, фексофенадин, лоратадин.
Примерами подходящих сосудорасширяющих средств являются беназеприл, каптоприл, эналаприл, лизиноприл, моэксиприл, хинаприл, периндоприл.
Примерами подходящих бронхолитиков являются агонисты бета-2, антихолинергические средства и теофиллин.
Примерами подходящих противоотечных лекарственных средств являются диуретики, такие как фуросемид, и местные противовоспалительные лекарственные средства.
Примерами подходящего лекарственного средства, связывающего специфические местные рецепторы, являются розиглитазон, капсаицин, хлорид дифениленйодония, линопидин и подобные агонисты и антагонисты.
Примерами подходящего ароматического масла являются ароматическое масло Mentha piperita, ароматическое масло Eucalyptus globulus, ароматическое масло Rosmarinus officinalis, ароматическое масло Thymus satureioides, масло Linum usitatissimum, ароматическое масло Citrus limonum и их комбинации.
Композиции по изобретению можно получить путем смешивания глицерина по меньшей мере с одним полимером двойного действия. В соответствии с воплощением, с целью дополнительного усиления терапевтического потенциала композиций по изобретению полимеры двойного действия также можно смешивать для дополнительного связывания или захвата ингредиента или лекарственного средства с целью медленного высвобождения или повышения эффективности.
В соответствии с другим воплощением по меньшей мере один ингредиент и/или лекарственное средство не связывается с полимером двойного действия, но остается захваченным между полимерными связями композиции для пролонгированного высвобождения, чтобы еще больше усилить терапевтические свойства композиции. Предпочтительно по меньшей мере один указанный ингредиент и/или лекарственное средство представляет собой по меньшей мере одно ароматическое масло.
Изобретение также относится к способу получения такой композиции, причем указанный способ содержит 1) стадию смешивания глицерина с ингредиентом и/или лекарственным средством и затем 2) стадию добавления по меньшей мере одного полимера двойного действия.
В соответствии с предпочтительным воплощением способ содержит 1) смешивание глицерина по меньшей мере с одним ароматическим маслом и затем 2) добавление по меньшей мере одного полимера двойного действия.
Композиции для местного применения по изобретению представляют собой жидкие или полужидкие композиции. Эти жидкие или полужидкие продукты можно наносить местно в виде жидкости, ингалятора, повязки, раствора, геля, крема, пасты или мази, они представляют собой спреи, тюбики, ампулы, ватные или полимерные повязки с жидким покрытием или мягкие желатиновые капсулы, обеспечивающие покрытие целевой поверхности пленкой продукта. Пленка должна оставаться в контакте с пораженной поверхностью, чтобы оказывать осмотическое воздействие и продолжать защищать, увлажнять и очищать поверхность, а также нейтрализовать избранные CPRM посредством полимеров двойного действия.
Пероральные составы можно применять в виде жидкости, содержащей мягкие желатиновые капсулы, или в виде полутвердого порошка или гранул, содержащих глицерин и полимерную ассоциацию в приемлемой основе. Затем, в соответствии с конкретным воплощением, композиции по изобретению готовят в виде жидких или полужидких лекарственных форм, содержащих порошок или гранулы, для однократного или многократного введения субъекту. В соответствии с другим воплощением композиции по изобретению вводят в виде жидкости, ингалятора, повязки, раствора, геля, крема, пасты или мази, они представляют собой спреи, тюбики, ампулы, жидкие включенные ватные или полимерные повязки, гранулы, порошок или мягкие желатиновые капсулы. Чтобы травмированная поверхность насыщалась кислородом, повязка, защищающая рану, должна быть воздухопроницаемой.
Чаще всего эти фармацевтические лекарственные средства назначают пациенту в «упаковках для пациентов», содержащих несколько дозированных единиц или другие средства для введения отмеренных стандартных доз, такие как спреи, аэрозольные флаконы, саше или капсулы, для использования в течение определенного периода лечения в одноразовой упаковке, обычно в виде спрея или тюбика с вязким раствором. Изобретение также включает фармацевтический состав, как описано выше, в сочетании с упаковочным материалом, подходящим для указанных составов.
Композицию по настоящему изобретению можно наносить местно на поврежденную и/или воспаленную биологическую поверхность, такую как кожа, слизистая оболочка глаз, полости рта, носа, желудочно-кишечного тракта, дыхательных путей или половых органов, для профилактики или лечения местного воспалительного заболевания и его последствий.
Таким образом, изобретение относится к способу профилактики или лечения местного воспалительного заболевания и его последствий. Предпочтительным последствием является CRS. Следовательно, изобретение относится к способу профилактики или лечения CRS.
Способ профилактики или лечения местного воспалительного заболевания по настоящему изобретению содержит местное введение нуждающемуся субъекту композиции, содержащей по меньшей мере один полимер двойного действия, связанный с глицерином и способный связываться по меньшей мере с одним провоспалительным соединением, нуждающемуся в этом субъекту.
Терапию по изобретению можно проводить в сочетании с любой другой терапией. Она может быть предоставлена дома, в кабинете врача, в клинике, амбулаторном отделении больницы или в стационаре, чтобы врач мог внимательно наблюдать за последствиями терапии и вносить любые необходимые коррективы.
Длительность терапии зависит от стадии подлежащего лечению заболевания, возраста и состояния пациента.
Дозировка, частота и способ введения зависят от стадии и локализации подлежащего лечению заболевания, возраста и состояния больного, а также чувствительности поверхности, на которой находится очаг поражения.
Примеры
Пример 1. Выбор природного полимера двойного действия
Для оценки связывающих свойств полимеров с провоспалительными соединениями и цитокинами, специфичными для заболевания, и/или другими белками, и/или рецепторами клеточной поверхности, и/или макромолекулами (CPRM) были выбраны только такие полимеры, которые способны связываться с глицерином. Дополнительно их оценили на цитотоксический потенциал, чтобы убедиться, что концентрация связывания CPRM является нецитотоксической и может использоваться в приемлемых фармацевтических формах. В соответствии с местными концентрациями цитокинов, специфических для конкретного заболевания, другими специфическими белками, макромолекулами или ионами металлов, которые необходимо нейтрализовать, природные полимеры изучили на предмет взаимодействия с каждой молекулой-мишенью (анализ ELISA для каждого белка, анализы нейтрализации вируса клеточной культуры для нейтрализации белка капсиды вируса, инкубация полимера с ионом металла in vitro с последующим измерением цитотоксичности in vitro или определением концентрации ионов металлов в крови in vivo, а также анализ влияния каждой ММР на клеточный матрикс с последующим ростом клеток in vitro при заживлении ран). Минимальные концентрации каждого полимера, связывающего глицерин, или наилучшее сочетание полимеров, способных в равной степени связывать и нейтрализовать максимальное количество CPRM, связанных с заболеванием, затем связывали с глицерином для придания глицериновому пленкообразующему веществу длительной стабильности при местном применении.
А - Получение природных полимеров (таннинов)
81 богатая танинами часть растения в форме целого растения (WP), листьев (L), цветов (Fl), плодов (F), семян (S), коры (B) или корня (R) использовали для приготовления экстрактов, обогащенных таннином, применяя технологии замачивания (M), метода Сокслета (S) или процеживание (P) для сбора обогащенных таннином фракций, которые либо использовали в виде жидкого экстракта, либо дополнительно сушили и использовали в виде порошков. Процессы экстракции известны специалистам в данной области. Вкратце, для извлечения богатых таннином фракций методом Сокслета высушенные образцы (2,5 г) упаковывали в целлюлозную вставку (33×80 мм) (Whatman, GE Healthcare, Великобритания) с помощью аппарата Сокслета (MS-EAM M-TOP, Индонезия), и экстрагировали 250 мл этанола в течение 10 ч (один цикл в час) при 80°С. Замачивание проводили, помещая 0,2 г порошка высушенных листьев в плотно закрытую стеклянную пробирку вместимостью 50 мл, содержащую 20 мл этанола, затем встряхивая при 150 об/мин в течение 24 ч при комнатной температуре (30 ± 5°C). Аналогично формировали перколяционную колонку в одноразовом шприце (диаметр 0,5 см, высота 10 см) (NIPRO, Япония). Набор представлял собой 0,1 г порошка листьев, упакованных в шприц для получения объема слоя 0,2 мл. Эффлюент загрузки 10 мл собирали в виде фракции со скоростью потока, регулируемой на уровне 0,1-0,2 мл/мин с помощью вакуумного коллектора (12-Port Teknokrama, Испания). Все жидкие экстракты фильтровали через ватман № 4 и доводили объем для компенсации испарения. Экстракты затем выпаривали и сушили при 60°С, получая высушенный порошок. Все образцы хранили в отдельных флаконах темного стекла с плотными пробками при 4°С до проведения анализа.
С целью идентификации растений растворимые или частично растворимые цельные экстракты анализировали для количественного определения активного ингредиента, специфичного для растений. Эти экстракты затем использовали для приготовления композиций, а также для дальнейшей фармакологической, аналитической, клинической оценки и оценки безопасности готовых композиций.
B - Выбор синтетических или полусинтетических полимеров
Синтетические полимеры могут быть синтезированы из природного таннинового основания, как описано Maria-Fraga и соавт. (2020) или могут быть синтезированы химически в соответствии с желаемым профилем связывания. Синтетические таннины можно приобрести у коммерческих поставщиков, таких как Sigma Aldrich. Ниже показаны восемь ключевых полимерных структур двойного действия, содержащих глицерин и демонстрирующих сродство связывания с одним из CPR или M (табл. 2). Их использовали в различных композициях в соответствии со специфичностью связывания в нецитотоксических концентрациях от 0,01% до 5,0% (мас/мас). 8 синтетических полимеров перечислены в табл. 2 ниже.
Таблица 2
В композициях использовались только те синтетические полимеры, которые обладают двойным действием, не всасываются в организме и действуют исключительно местно, либо сами по себе, либо в сочетании с другими природными или полусинтетическими полимерами.
C - Испытание цитотоксичности
Максимальную нецитотоксическую концентрацию каждого синтетического или природного полимера оценивали in vitro на 3 различных клеточных культурах (клеточная линия MDBK, клеточная линия MDCK, клеточная линия Chang Liver), приобретенных в коллекции клеточных культур ATCC. Кратко, клетки выращивали в 96-луночных культуральных планшетах (90 мкл MEM + 10% фетальной телячьей сыворотки) для получения 100% монослоя клеток. Культуральную среду отбрасывали и заменяли бессывороточной MEM, содержащей 0,1%, 0,3%, 1,0%, 2,0% и 5,0% (мас./мас.) концентрации каждого изучаемого полимера. Гибель клеток оценивали после 72-часового воздействия путем подсчета количества живых клеток. Максимальная концентрация исследуемого продукта, демонстрирующая отсутствие клеточных эффектов, считалась нецитотоксической. Только те образцы, которые не демонстрировали цитотоксичности при концентрации 2,0% или выше, были оставлены для оценки активности глицерина и специфического связывания CPRM.
D - Выбор концентрации полимера/таннина в готовой композиции
Авторы заметили, что большинство порошкообразных полимеров/таннинов могут быть включены в конечную композицию в концентрации менее 5,0% мас./мас. Более высокие концентрации делают композицию полутвердой, твердой или непрозрачной, что не позволяет наносить ее местно в виде осмотической пленки. Поэтому все испытуемые продукты тестировали при концентрациях 0,01, 0,03, 0,10%, 0,20%, 0,30%, 1,0%, 2,0% и 3,0%.
Антибелковую активность оценивали для следующих CPRM, специфичных для воспалительных и местных заболеваний: гистамин, IgE, TRP, TSLP, TNF-альфа, IFN-гамма, TGF-бета, IL-1бета, IL-2, IL-4, IL-5, IL-6, IL-8, IL-10, IL-12, IL-13, IL-23, IL-25 IL-33, MMP-1, MMP-2, MMP-3, MMP-8, MMP-9 и MMP-13.
В композициях можно использовать любой природный или синтетический полимер двойного действия, обладающий способностью связываться с одним или несколькими специфическими для заболевания провоспалительными соединениями (CPRM). Около 15% изученных полимеров показали связывание с одним или несколькими CPRM. Например, среди широко используемых пищевых экстрактов растений только следующие 14 из 81 природного полимера показали селективную активность против CPRM: экстракт плодов Vaccinium macrocarpon (Vma) (F), полученный методом замачивания (M), сокращенно Vma-F-M; листья Camellia sinensis (Cs-L-M); семена Vitis vinifera (Vv-S-P); плоды бузины черной (Sn-F-M); листья Hedera helix (Hh-L-M); плоды Ribes nigrum (Rn-F-M); корневища куркумы длинной (Cl-R-P); корни женьшеня обыкновенного (Pg-R-M); Семена Glycine max (Gm-S-M); цельное растение Urtica dioica (Ud-WP-M); Artemisia annua, (Aa), Calendula officinalis (Cao-Fl-M); цельное растение Salix alba (Sa-WP-M); и цветы Tanacetum parthenium (Tp-Fl-M). Их использовали очищенными, не очищенными в виде жидкого или порошкообразного экстракта, в фармацевтически приемлемых и нецитотоксических концентрациях.
Пример 2. Выбор таннинов, связывающих глицерин
Глицерин не удается обнаружить с помощью ВЭЖХ. Поэтому его идентифицировали с помощью ГХ-МС (газовой хроматографии в сочетании с масс-спектрометрией). Глицерин может быть обнаружен как одиночный пик между 31-32 минутами с пА 340 (фиг. 1-B).
Для проверки связывания глицерина с полимером профили ВЭЖХ и/или ГХ-МС индивидуального полимера сравнивали с профилем глицерин + полимер (фиг. 1). Два полученных хроматографических профиля не демонстрируют пики полимера и/или глицерина, но представляют собой совершенно другую хроматограмму, показывающую, что все полимеры, включенные в композицию, полностью связываются с глицерином.
Затем полимеры/таннины, связывающие глицерин, оценили для определения их специфических свойств связывания CPRPM.
A - Оценка свойств связывания цитокинов и других белков со стороны полимеров/таннинов
Антибелковую активность 81 экстракта, богатого нецитотоксичными полимерами/таннинами, оценивали с использованием ELISA (твердофазный иммуноферментный анализ) для каждого белка. Кратко, анализ ELISA представляет собой метод анализа на планшетах, предназначенный для обнаружения и количественного определения пептидов, белков, антител, факторов роста и гормонов. Сэндвич-ELISA количественно определяет антигены между двумя слоями антител (т.е. антител захвата и детектирования). Измеряемый антиген должен содержать не менее двух антигенных эпитопов, способных связываться с антителом, поскольку в сэндвиче функционирует не менее двух антител. Детектирующее антитело связано с ферментом, и детектирование осуществляется путем оценки активности конъюгированного фермента посредством инкубации с субстратом с получением измеряемого продукта.
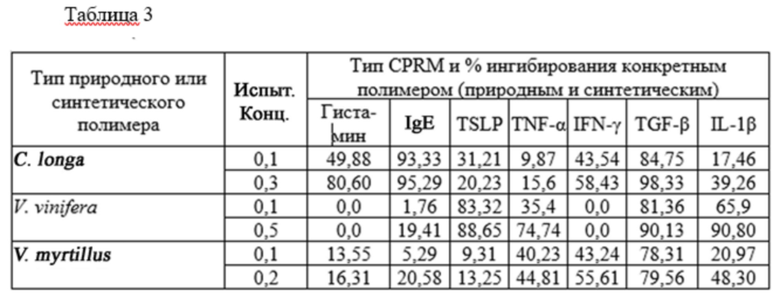
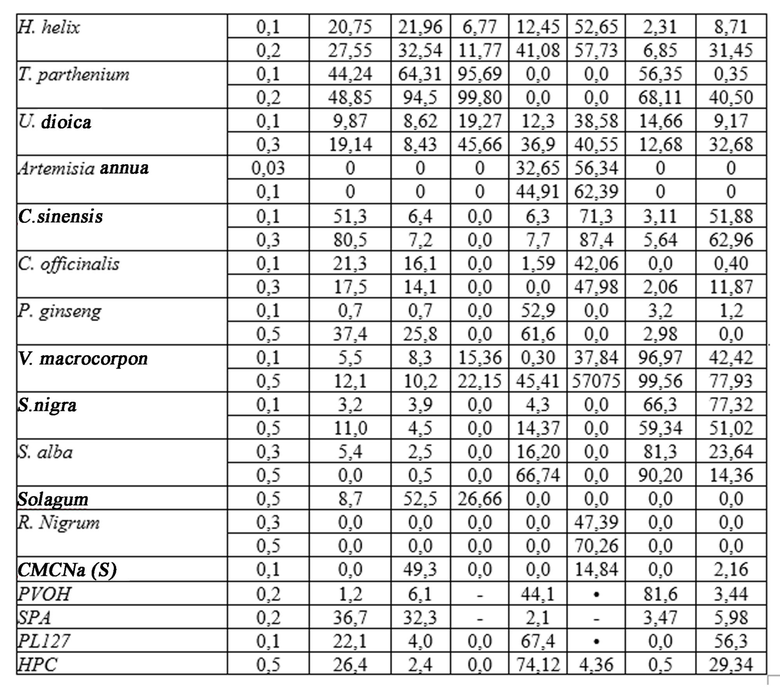
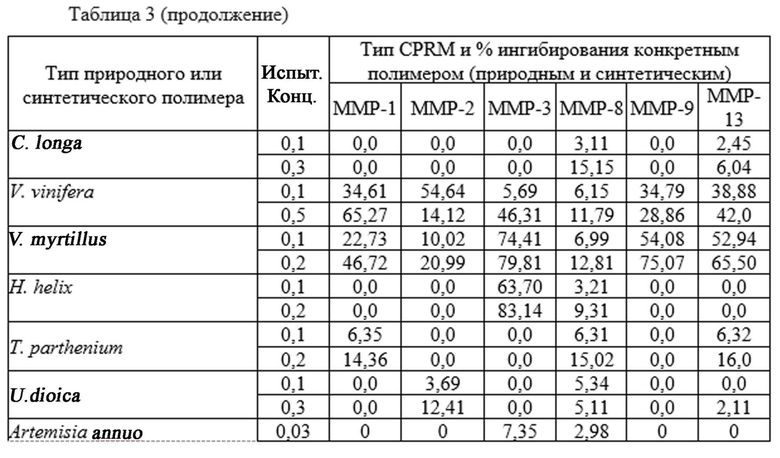
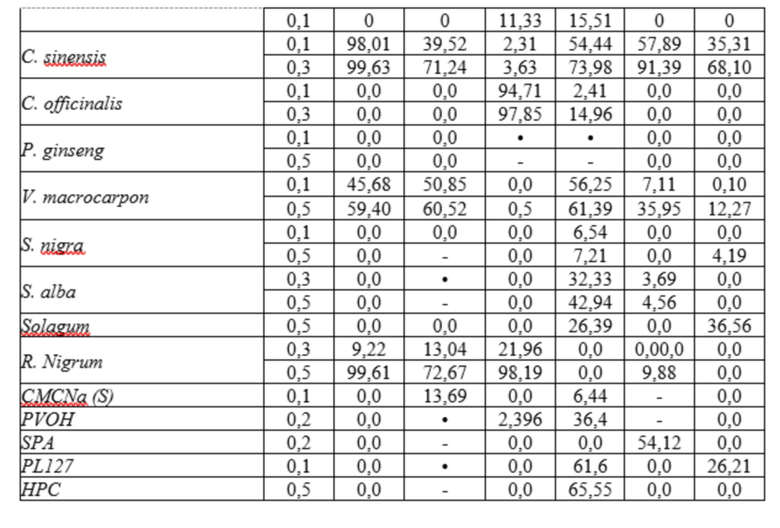
Результаты показаны в табл. 3 ниже. В этой таблице описаны свойства связывания относящихся к заболеванию белков, макромолекул и/или ионов металлов (% ингибирования по сравнению с контролями) с полимерами, связанными с глицерином в фармакологически приемлемых концентрациях. Конц. = испытанная концентрация полимера, S = синтетический таннин, EGF = эпителиальный фактор роста, FGF = фактор роста фибробластов, MMP = матриксные металлопротеазы, - = не проводили.
Средние значения свойства связывания с полимерами относящихся к заболеванию белков для глицерин-связанных полимеров. Результаты представляют собой среднее значение для 3 анализов при 2 наиболее активных и нецитотоксических концентрациях.
Средние значения свойства связывания с полимерами относящихся к заболеванию белков для глицерин-связанных таннинов, с использованием анализа ELISA.
Каждый исследуемый продукт в связывающей глицерин концентрации был включен в 30% раствор глицерина для анализа. Результаты указывают на отсутствие или наличие свойств двойного связывания каждого анализируемого продукта. Результаты представляют собой среднее значение 3 анализов в 2 наиболее активных и нецитотоксических концентрациях для 81 природного или синтетического полимера. Ниже представлены только результаты для полимеров двойного действия (глицерин + одно из провоспалительных соединений, связанных с заболеванием (CPRM)).
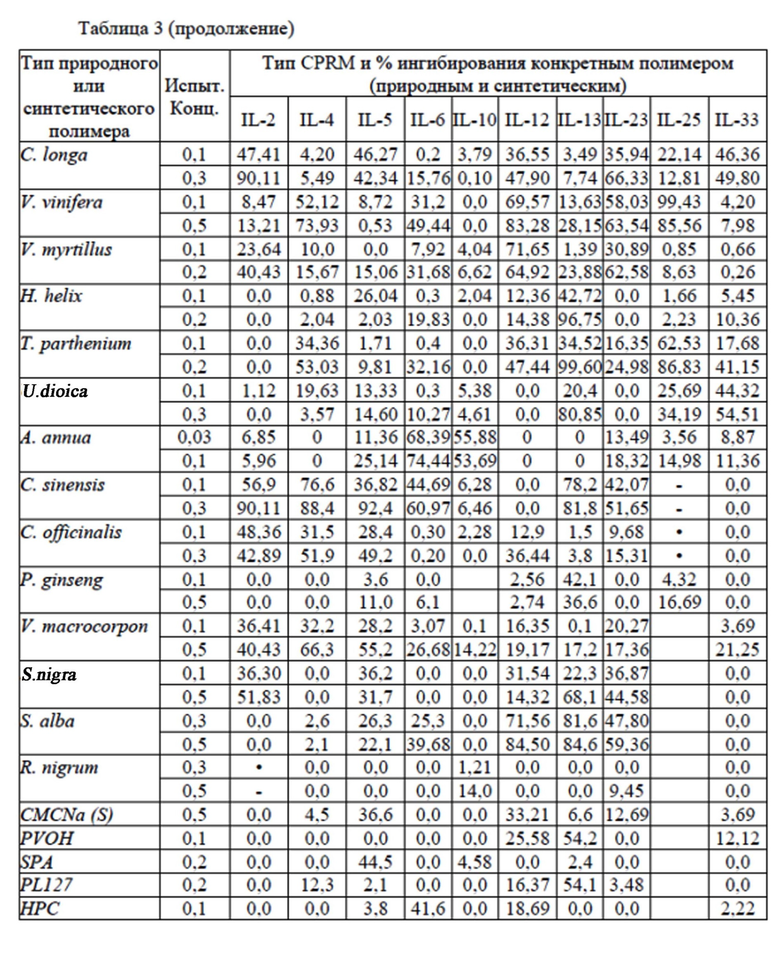
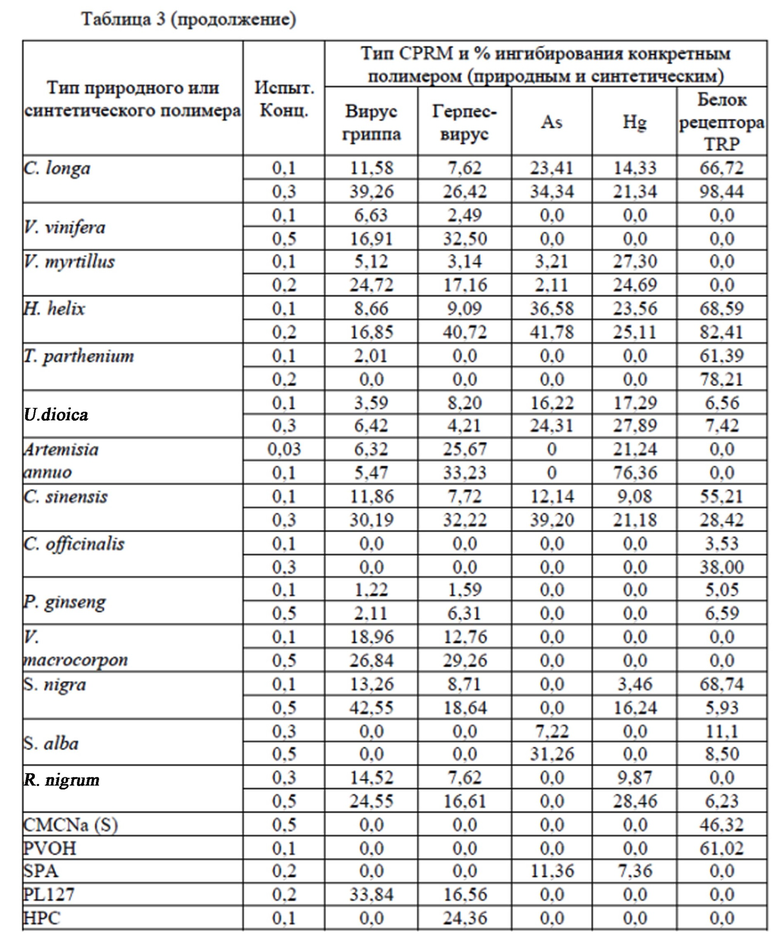
Примечание: по причине агглютинации полимеров в некоторых случаях более высокие концентрации (конц.) может быть менее эффективными. Все остальные полимеры продемонстрировали ингибирование менее чем 20% для ключевых белков, макромолекул или ионов металлов, связанных с заболеванием.
Вывод: свойства связывания белков, макромолекул или ионов металлов для 81 выбранного природного или синтетического связывающего глицерин полимера оценили с помощью ELISA при различных концентрациях. Результаты представлены для концентраций ниже 0,5%, которые используются для приготовления композиций. Среди 81 анализируемого продукта 15 натуральных и 5 синтетических образцов показали ингибирование более 20% для одного или более белков, макромолекул или ионов металлов. Результаты показывают, что (1) связывание полимера двойного действия с белком, макромолекулой или ионом металла является высокоспецифичным, поскольку не все полимеры связываются со всеми молекулами. (2) Один полимер двойного действия может связываться более чем с одним белком. (3) В зависимости от конкретного связанного с заболеванием белка, макромолекулы или иона металла, которые необходимо нейтрализовать, полимеры двойного действия были связаны в фармакологически приемлемых концентрациях, чтобы максимально увеличить антагонистические эффекты.
B - Оценка свойств связывания таннинов с вирусными гликопротеинами
Противовирусную активность ключевых природных или синтетических полимеров определяли в культурах клеток in vitro путем количественного определения гибели клеток, вызванной вирусом. Клетки Vero для вируса герпеса и культуры клеток-хозяев MDCK для вируса гриппа выращивали в 96-луночных планшетах для тканевых культур (37°C - 5% CO2). Минимальные концентрации вируса, способные вызвать 100% гибель клеток (инфицирующая доза для тканевой культуры: TCID100) за 72 часа определяли окрашиванием живых клеток МТТ с измерением оптической плотности при 560 нм. Двадцать семь нецитотоксичных связывающих глицерин полимеров в концентрации от 0,10% до 0,30% инкубировали по отдельности с 0,9% раствором NaCl или с 30% пленкообразующим глицерином в течение 1 часа и подвергали воздействию культур клеток-хозяев в течение 72 часов, после чего измеряли вызванную вирусом гибель клеток. Снижение гибели клеток было обусловлено связыванием полимера и капсидного белка вируса и, как следствие, нейтрализацией вируса. Полимеры, демонстрирующие противовирусную активность, затем связывали друг с другом (по 0,10% каждый) и эксперименты повторяли (n=3; 16 лунок на эксперимент). Результаты выражены в виде % увеличения (+) или уменьшения (-) роста вируса по сравнению с (TCID100) необработанными контрольными вирусами.
Результаты представлены в табл. 4 ниже (Vma = Vaccinium macrocarpon, Vmy: Vaccinium myrtillus, Vv = семена Vitis vinifera, Sn = Sambucus nigra, Hh = Hedera helix, Rn = Ribes nigrum, Cl = Curcuma longa, Co = Calendula officinalis, Ud = Urtica dioica, Cs = Camellia sinensis, CMCNa = натриевая соль карбоксиметилцеллюлозы, PL127 = Pluronic F-127, HPC = гидроксипропилцеллюлоза).
Снижение роста (-) пропорционально ингибированию вируса в %.
Таблица 4. Снижение роста вируса (%) для связывающего глицерин полимера (0,10%) в физиологическом растворе (контроль) или в глицерине
После первоначальных экспериментов 12 из 32 полимеров и их ассоциаций продемонстрировали противовирусную активность от умеренной до сильной в отношении вирусов гриппа (H1N1) или герпеса. Полимерами двойного действия были Vma, Vmy, Vv, Sn, Hh, Rn, Cl, Co, Ud, Cs, CMCNa, PL127 и HPC.
Результаты показывают, что: (1) только 12 из 32 полимеров нейтрализуют более 5% вируса, (2) Противовирусная активность специфична, так как некоторые полимеры, нейтрализующие вирус герпеса, не были эффективны против вируса гриппа, (3) Ассоциации некоторых конкретных полимеров более эффективны, чем отдельные полимеры, (4) Противовирусная активность значительно сильнее, если противовирусные полимеры были предварительно инкубированы с пленкообразующим глицерином, а также (5) пленкообразующий глицерин усиливает противовирусную активность, вероятно, за счет презентации сайтов связывания полимер-вирус в лучшей конфигурации.
C - Оценка свойств связывания ионов металлов
Цель этих исследований заключалась в оценке связывания и нейтрализации ионов металлов мышьяка (As) и кадмия (Cd) с предварительной инкубацией или без нее, с природными или синтетическими таннинами в 2 разных концентрациях на 3 разных клеточных линиях in vitro. Клеточные линии представляли собой MDBK (Madin-Darby Bovine Kidney): эпителиальную клеточную линию почек крупного рогатого скота, CHANG LIVER: линию клеток печени человека и HeLa (линию иммортализованных клеток рака шейки матки человека).
Кадмий (CdCl2) и мышьяк (NaAs02) были приобретены в компании Sigma (Великобритания). Металлы смешивали в культуральной среде (MEM) в различных концентрациях от 10-4 до 10-7 относительно концентрации маточного раствора. Затем десять мкл этого раствора прибавляли к 90 мкл культуральной среды с целью получения конечной концентрации для анализа. В соответствии с наблюдаемыми результатами оценки клеточной токсичности концентрации дополнительно уточнили, чтобы определить концентрацию, которая вызывает почти 50% гибель клеток (± 4,0%). Как только были определены вызывающие 50% гибель клеток концентрации As и Cd, (концентрации CT50), эти концентрации использовали для дальнейших экспериментов (для смешивания с полимерами или в качестве положительных контролей).
D – Связывание иона металла и полимера
Различные концентрации каждого полимера в композиции, содержащей глицерин, инкубировали с CT50 концентрацией ионов металла в течение 1 часа при 37°C и воздействовали ими на клеточные линии. Если металлы связываются полимерами, они не могут проявлять цитотоксичность. Определяли снижение цитотоксичности (n=3, минимум 8 лунок на концентрацию). % Снижения пропорционален % нейтрализации иона металла.
Обнаружено, что семь полимерных композиций (Cl, Vmy, CMCNa, HPC, Hh, Ud и Cs) нейтрализуют до 60% ионов металлов. Приготовили различные полимерные ассоциации, блокирующие до 90% металлов. Эти полимеры использовали в композициях для местного применения, требующих нейтрализации тяжелых металлов.
Ртуть (Hg) является летучим металлом, связывание ртути с полимером определяли на крысах. Проанализировали все ключевые полимеры и их ассоциации. Группе крыс (6+6/группа) давали с пищей 1 мг/кг Hg, второй группе 4 мг/кг, третьей группе 4 мг/Hg и 300 мг/кг полимеров двойного действия, а четвертую группу кормили так же, как и третью группу, за исключением того, что ассоциацию «полимеры двойного действия-Hg» предварительно инкубировали в течение 1 часа при комнатной температуре. Животных умертвляли через 14 дней многократного введения и измеряли количество паров ртути в крови. В случае одной из полимерных ассоциаций (Cl + Hh) у животных 3-й группы содержание Hg в крови было на 31,26% меньше, а у животных 4-й группы - на 94,30% меньше, по сравнению с контролем ртути 2-й группы. Эти результаты показывают, что ртуть также можно нейтрализовать с помощью специфических полимеров и полимерных ассоциаций.
Концепция композиций двойного действия для лечения специфических местных заболеваний
Все композиции содержат глицерин с одним или несколькими полимерами/таннинами двойного действия, т.е. полимером/таннином, способным связываться с глицерином (пленкообразующий глицерин), и с одним или несколькими специфическими для заболевания CPRM.
Спреи для горла находились в алюминиевых контейнерах вместимостью 30 мл для взрослых и алюминиевых контейнерах вместимостью 20 мл для детей, снабженных устройством для распыления для местного применения. Дозировка: 3-4 распыления на поверхность горла 2-3 раза в день в течение максимум 14 дней.
Назальные спреи для лечения ринита, аллергии на загрязнение и синусита были расфасованы в пластиковые контейнеры вместимостью 15 мл для взрослых и детей, снабженные устройством для распыления для местного применения. Дозировка: 3-4 распыления на поверхность носа 2-3 раза в день в течение максимум 14 дней. Лечение аллергии применяли по мере необходимости во время воздействия аллергена (симптоматическое лечение) или за 15 минут до воздействия аллергена (профилактическое лечение).
Лекарственные средства для местного нанесения на кожу, раны, геморрой, герпес и половые органы расфасованы в пластиковые тюбики вместимостью 10 мл или 50 мл. В зависимости от поверхности поражения количество, достаточное для образования тонкой пленки продукта на поврежденной поверхности, наносили 5-6 раз в день непосредственно на поврежденную поверхность.
Для лечения язвы желудка 5 мл раствора продукта вводили перорально 4 раза в день в течение максимум 14 дней.
Для лечения воспаления желудочно-кишечного тракта 10% пленкообразующий глицерин, содержащий 2 полимерных экстракта, смешивали с тегументом семян испагулы в качестве наполнителя, а порошок расфасовывали в пакетики по 5 г. Такая же самая композиция была также приготовлена в виде гранул. 5 г продукта вводили перорально один раз в день в течение 1 месяца и повторяли при необходимости.
Для лечения внутреннего геморроя 1 г вязкого продукта помещали в желатиновые суппозитории и вводили по 1 суппозиторию утром и вечером в течение 6 недель подряд.
Гель для местного применения для лечения кожных инфекций, содержащий пленкообразующий глицерин с ароматическими маслами, также был расфасовали в стеклянные флаконы вместимостью 30 мл, снабженные роликовым аппликатором. Продукт наносили два раза в день в течение максимального периода 1 месяц.
Все композиции содержали природные или синтетические специфические связывающие CPRM полимеры двойного действия для создания пленкообразующего глицерина и одновременного связывания с одним или несколькими специфическими для заболевания CPRM.
В некоторые композиции добавляли очень небольшое количество ароматических масел в качестве вспомогательного вещества для улучшения запаха.
Ниже приведены несколько примеров композиций по изобретению, которые демонстрируют положительный эффект при лечении местных воспалительных заболеваний:
- Глицерин 74,94%, мед 13,57%, вода 10,76%, экстракт Vitis vinifera 0,44%, экстракт Sambucus nigra 0,29%, особенно подходит для лечения инфекции горла.
- Глицерин 74,94%, вода 16,76%, мед 7,57%, CMCNa 0,30%, экстракт Sambucus nigra 0,43, особенно подходит для лечения инфекции горла.
- Глицерин 62%, вода 31,19%, мед 6%, HPC 0,15%, PL127 0,35%, ПЭГ 0,23%, ароматическое масло Mentha piperita 0,02%, ароматическое масло Eucalyptus globulus 0,02%, ароматическое масло Rosmarinus officinalis 0,02%, ароматическое масло Thymus satureioides 0,02%, особенно подходит для лечения боли в горле.
- Глицерин 62%, вода 36,62%, экстракт Hedera helix 0,96%, экстракт Ribes nigrum 0,36%, ароматическое масло Mentha piperita 0,02%, ароматическое масло Rosmarinus officinalis 0,02%, ароматическое масло Thymus satureioides 0,02%, особенно подходит для лечения боли в горле и воспаления.
- Глицерин 49,20%, вода 50,68%, PCM 0,02%, экстракт Curcuma longa 0,08%, ароматическое масло Eucalyptus globulus 0,02%, особенно подходит для лечения влажного кашля.
- Глицерин 40%, вода 50,43%, мед 8%, экстракт Calendula officinalis 0,5%, ароматическое масло Eucalyptus globulus 0,02%, масло Linum usitatissimum 0,05%, экстракт прополиса 1%, особенно подходит для лечения сухого кашля.
- Глицерин 37,37%, вода 62,04%, экстракт Vaccinium macrocarpon 0,13%, экстракт Camellia sinensis 0,23%, экстракт Vaccinium myrtillus 0,13%, экстракт Sambucus nigra 0,1%, особенно подходит для лечения назальных инфекций (риносинусита).
- Глицерин 26,14%, вода 73,2%, HPC 0,5%, ароматическое масло Mentha piperita 0,04%, ароматическое масло Eucalyptus globulus 0,04%, ароматическое масло Rosmarinus officinalis 0,04%, ароматическое масло Thymus satureioides 0,04%, особенно подходит для лечения назальных инфекций (риносинусита).
- Глицерин 26%, вода 73,02%, HPC 0,5%, экстракт Vaccinium macrocarpon 0,07%, экстракт Camellia sinensis 0,13%, экстракт Vaccinium myrtillus 0,07%, SPA 0,21%, особенно подходит для лечения назальных инфекций (риносинусита).
- Глицерин 9,8%, вода 89,317%, Solagum 0,5%, экстракт Ribes nigrum 0,05%, экстракт Curcuma longa 0,08%, ароматическое масло Mentha piperita 0,05%, ароматическое масло Eucalyptus globulus 0,05%, ароматическое масло Rosmarinus officinalis 0,05%, ароматическое масло Thymus satureioides. 0,05%, консерванты 0,053% (сорбат калия 0,025%, бензоат натрия 0,025%, лимонная кислота 0,003%), особенно подходит для лечения назальных инфекций (риносинусита).
- Глицерин 2%, вода 96,9%, Solagum 0,5%, экстракт Camellia sinensis 0,09%, экстракт Curcuma longa 0,08%, экстракт женьшеня Panax 0,06%, экстракт Urtica dioica 0,1%, ароматическое масло Citrus limonum 0,05%, консерванты 0,22% (сорбат калия). 0,1%, бензоат натрия 0,1%, лимонная кислота 0,02%), особенно подходит для лечения аллергического ринита.
- Глицерин 3 %, вода 95,84 %, HPC 0,55 %, экстракт Vaccinium myrtillus 0,1 %, экстракт Hedera helix 0,13 %, экстракт Curcuma longa 0,07 %, ароматическое масло Mentha Piperita 0,08 %, консерванты 0,23 % (сорбат калия 0,1 %, бензоат натрия 0,1 %, лимонная кислота 0,03%), особенно подходит для лечения аллергии, вызванной загрязнением окружающей среды.
- Глицерин 9,8%, вода 89,15%, PL127 0,25%, HPC 0,25%, экстракт Camellia sinensis 0,08%, экстракт Curcuma longa 0,07%, экстракт Urtica dioica 0,08%, экстракт Tanacetum parthenium 0,1%, консерванты 0,22% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,02%), особенно подходит для лечения респираторных симптомов, вызванных загрязнением и аллергенами.
- Глицерин 74,63%, вода 11%, мед 13,58%, экстракт Vitis vinifera 0,44%, экстракт Sambucus nigra 0,29%, экстракт Glycine max 0,06%, особенно подходит для лечения инфекций горла у детей.
- Глицерин 74,63%, мед 6%, вода 18,54%, экстракт Vitis vinifera 0,44%, экстракт Sambucus nigra 0,29%, экстракт Ribes nigrum 0,1%, особенно подходит для лечения инфекций и болей горла у детей.
- Глицерин 53%, вода 41,81%, мед 4,5%, экстракт Ribes nigrum 0,36%, экстракт Curcuma longa 0,08%, ароматическое масло Citrus limonum 0,02%, консерванты 0,23% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,03%), особенно подходит для лечения кашля у детей.
- Глицерин 13 %, вода 85,96 %, HPC 0,5 %, экстракт Vaccinium macrocarpon 0,07 %, экстракт Vaccinium myrtillus 0,07 %, экстракт Sambucus nigra 0,05 %, экстракт Ribes nigrum 0,13 %, консерванты 0,22 % (сорбат калия 0,1 %, бензоат натрия 0,1 %, лимонная кислота 0,02%), особенно подходит для лечения назальных инфекций у детей.
- Глицерин 4%, вода 94,87%, Solagum 0,6%, экстракт Vaccinium macrocarpon 0,1%, PVOH 0,1%, экстракт женьшеня Panax 0,06%, ароматическое масло Thymus satureioides 0,03%, ароматическое масло Citrus limonum 0,02%, консерванты 0,22% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,02%), особенно подходит для лечения аллергического ринита у детей.
- Глицерин 67,04%, вода 1,15%, мед 31,41%, ксантановая камедь 0,08%, экстракт Vaccinium macrocarpon 0,16%, экстракт Vaccinium myrtillus 0,16%, особенно подходит для лечения язв во рту.
- Глицерин 67,04%, вода 1,15%, мед 31,41%, ксантановая камедь 0,08%, экстракт Vaccinium macrocarpon 0,16%, экстракт Vaccinium myrtillus 0,16%, особенно подходит для лечения язвы желудка.
- Глицерин 73,85%, вода 11,94%, мед 13,6%, экстракт Vaccinium macrocarpon 0,28%, экстракт Vaccinium myrtillus 0,33%, особенно подходит для лечения орального мукозита, вызванного химиотерапией.
- Глицерин 66,15%, вода 25,50%, мед 5,85%, экстракт Vaccinium macrocarpon 1,5%, экстракт Vaccinium myrtillus 1,30%, Artemisia annua 0,70%, особенно подходит для лечения травматического инфицированного орального мукозита.
- Глицерин 66,52%, вода 1,54%, мед 31,44%, ксантановая камедь 0,08%, экстракт Camellia sinensis 0,26%, экстракт Vaccinium myrtillus 0,16%, особенно подходит для лечения хронических ран.
- Глицерин 7,70%, вода 91,56%, HPC 0,60%, экстракт Hedera helix 0,04%, экстракт Curcuma longa 0,20%, Tanacetum parthenium 0,08%, особенно подходит для лечения глазной аллергии.
- Глицерин 21,0%, вода 78,20%, Solagum 0,50%, Vaccinium macrocarpon 0,14%, экстракт Vaccinium myrtillus 0,16%, особенно подходит для лечения сухости глаз.
- Глицерин 13,6%, вода 86,0%, PL127 0,25%, экстракт Tanacetum parthenium 0,14%, экстракт камеди Papaya-Folium Eriobotryae 0,01%, особенно подходит для лечения диабетической ретинопатии.
- Глицерин 7,70%, вода 91,97%, HPC 0,20%, экстракт Urtica dioica 0,05%, экстракт семян Vitis vinifera 0,08%, особенно подходит для лечения глазного конъюнктивита.
- Глицерин 16,5%, вода 83,28%, CMCNa 0,12%, экстракт Tanacetum parthenium 0,08%, экстракт корня Curcuma longa 0,01%, ароматическое масло Mentha piperita 0,01%, особенно подходит для лечения вызванных загрязнением красных глаз и увеита.
- Глицерин 97,72%, вода 1,79%, экстракт Vaccinium macrocarpon 0,16%, экстракт Sambucus nigra 0,33%, лимонная кислота qsp pH 4-5, особенно подходит для лечения генитального герпеса.
- Глицерин 74,56%, вода 2,6%, мед 21,97%, ксантановая камедь 0,16%, экстракт Camellia sinensis 0,21%, экстракт Vitis vinifera 0,32%, экстракт Sambucus nigra 0,18%, особенно подходит для лечения лабиального герпеса.
- Глицерин 75,02%, вода 3,12%, мед 20,92%, ксантановая камедь 0,08%, экстракт Vaccinium macrocarpon 0,11%, экстракт Camellia sinensis 0,43%, экстракт Vitis vinifera 0,32%, особенно подходит для лечения псориаза, экземы и дерматита.
- Глицерин 64,70%, вода 34,61%, CMCNa 0,10%, экстракт Vaccinium macrocarpon 0,18%, экстракт Vitis vinifera 0,36%, ароматическое масло Mentha piperita 0,05%, особенно подходит для лечения наружного геморроя.
- Глицерин 97,33%, вода 1,56%, экстракт Vaccinium macrocarpon 0,23%, экстракт Vitis vinifera 0,36%, ароматическое масло Mentha piperita 0,02%, масло Linum usitatissimum 0,5%, особенно подходит для лечения внутреннего геморроя.
- Глицерин 5,5%, вода 83,28%, CMCNa 0,12%, экстракт Tanacetum parthenium 0,04%, экстракт Artemisia annua 1,46%, особенно подходит для лечения инфицированных повреждений глаз.
Все готовые композиции до использования хранили при температуре от 10°С до 40°С в темном месте. Все продукты были произведены во Франции в соответствии с нормами GMP или ISO13485, применимыми к лекарствам или медицинским изделиям. Все композиции были протестированы в соответствии с методами и нормами, предложенными в Европейской фармакопее и применимыми к лекарственным средствам местного применения. Обнаружено, что композиции биосовместимы с материалом контейнеров, стабильны в течение 3 лет, стабильны после вскрытия упаковки в течение 3 месяцев, слегка раздражают глаза в первые 1-2 минуты после нанесения, не раздражает кожу, не обладают мутагенным или канцерогенным действием, не вступают в какие-либо клеточные, метаболические, рецепторные или иммунологические взаимодействия, поскольку они не всасываются в организм, и нетоксичны при пероральном приеме в дозе до 5 мл/кг, не оказывает неблагоприятного воздействия на гематологические, биохимические показатели крови, мочи, массу органов или внутриклеточные гистологические параметры.
Любое многофакторное местное заболевание, включающее разрушение клеток, хроническое воспаление и системную иммунную стимуляцию, может вызывать CRS. Поскольку CRS в настоящее время неизлечим, проводить клинические исследования, индуцируя CRS, затруднительно. Таким образом, клинические исследования были проведены для тех заболеваний, которые связаны с разрушением клеток, хроническим воспалением и системной иммунной стимуляцией, способных привести к развитию CRS, если их не лечить.
Клиническую эффективность композиций, содержащих глицерин и полимеры, которые способны связываться только с глицерином, сравнивали с клинической эффективностью композиций, содержащих глицерин и полимеры двойного действия по изобретению.
Сравнительные исследования клинической эффективности и безопасности проводили у пациентов с различной многофакторной местной патологией. В целом пациентов разделили на 2 группы. Первую группу лечили плацебо «пленкообразующий глицерин» (FG), содержащим только полимеры, связывающие глицерин, в то время как вторую группу лечили композицией, содержащей такую же концентрацию природных и/или синтетических полимеров двойного действия, способных связываться с цитокинами, специфичными для определенных заболеваний, белков или ионов металлов (CPRM) и глицерина (DFG). Более высокая эффективность композиций, содержащих полимеры двойного действия, по сравнению с соответствующей композицией FG, отражает дополнительное подавление CPRM, связанных с заболеванием, позволяющее избежать возникновения CRS.
Композиции, содержащие полимеры двойного действия, были выбраны из 35 композиций, представленных выше. Состав соответствующих FG был идентичен, за исключением того, что полимеры заменили той же концентрацией 1, 2 или 3 растительных полимеров, не обладающих связывающими свойствами ни с одним из CPRM, участвующих в заболевании. Первый полимер заменили экстрактом плодов Rubusfruticosus, богатым гидролизуемыми и конденсированными таннинами, второй (если есть) - экстрактом хвои Pinus sylvestris, третий - экстрактом листьев и коры Mangifera indica, а синтетический полимер (если есть) - порошкообразным HPC.
Все клинические исследования были проведены после одобрения этическим комитетом в соответствии с нормами GCP. Краткое изложение эксперимента и результаты, полученные для каждой композиции, приведены ниже.
* означает статистическое отличие по сравнению с соответствующим плацебо в тот же момент времени p<0,05, T0 означает наблюдение, сделанное непосредственно перед началом лечения, M = мужчины, F = женщины; контроль: композиции, содержащие глицерин и по меньшей мере один полимер, не являющийся полимером «двойного действия», контроль еще называют «пленкообразующим глицериновым контролем» = FG; композиции, содержащие глицерин и по меньшей мере один полимер двойного действия по изобретению, называют «полимером двойного действия, содержащим пленкообразующий глицерин» = DFG.
A - Тестовая композиция № 1: (противовирусное и антибактериальное средство против сильной боли в горле)
Композиция №1: глицерин 74,94%, мед 13,57%, вода 10,76%, экстракт Vitis vinifera 0,44%, экстракт Sambucus nigra 0,29%. Данной композицией заполняли алюминиевые контейнеры вместимостью 30 мл с распылителем, особенно подходящим для лечения инфекции горла.
Целевая патология: сильная боль в горле; Тип исследования: двойное слепое, плацебо-контролируемое, многоцентровое; Продолжительность лечения: 14 дней; Способ применения: 4-5 распылений на поверхность горла 3-4 раза в день; Количество больных: группа 1 (FG) = 20; группа 2 (DFG) = 30.
Параметры: влияние на воспаление горла, боль, затруднение глотания, отек горла, раздражение горла, бактериальные отложения на поверхности горла, а также побочные эффекты при их наличии.
Результаты: Воспаление горла. Средний балл воспаления горла не изменился в группе FG в течение первых 24 часов, но наблюдалось очень небольшое и прогрессирующее снижение до 14-го дня. Средние баллы составили 4,58 и 2,47 на 4-й и 7-й дни (5,36 / 10 в начале) в группе FG в сравнении с 1,83* и 0,22* в группе DFG.
По сравнению со средними баллами для группы FG снижение было на 20-40*-60*-80* и на 90*% выше в группе DFG на 2-3-4-7 и 14-й дни соответственно. Эти результаты ясно показывают заметное положительное влияние DFG на воспаление горла, что указывает на лучшее ингибирование цитокинов и вирусов.
Боль в горле: через 1 ч после первого применения средний балл боли в горле снизился на 4,52% в группе DFG по сравнению с FG. Уменьшение было быстрее со 2-го дня с сильным уменьшением между 3-м и 4-м днями. На 7-й день средний балл боли снизился на 75% в группе DFG по сравнению с 28% в группе FG. На 14-й день интенсивность боли снизилась на 55% в группе FG по сравнению с 93% в группе DFG.
Аналогичное снижение наблюдалось и для всех других параметров, где излечение было в два раза быстрее и полнее в DFG. Ни у одного пациента не было зарегистрировано побочных эффектов. Эти результаты доказывают, что композиция DFG более активна по сравнению с одним только FG.
B - Тестовая композиция № 2 (Противовирусная композиция для лечения инфекции гриппа с тяжелым воспалением, деструкцией слизистой оболочки носа и бактериальной контаминацией)
Композиция № 2: глицерин 74,94%, вода 16,76%, мед 7,57%, CMCNa 0,30%, экстракт Sambucus nigra 0,43%. Данной композицией заполняли алюминиевые контейнеры вместимостью 30 мл с распылителем, особенно подходящим для лечения инфекции горла.
Двойное слепое, плацебо-контролируемое, многоцентровое пилотное исследование по оценке эффективности и безопасности композиции № 2 по сравнению с FG для лечения тяжелого воспаления горла и роста бактерий путем количественного определения концентрации воспалительных цитокинов, вирусных частиц и бактериальной нагрузки в мазках из горла.
Продолжительность лечения: 14 дней; Способ применения: 4-5 распылений на поверхность горла 3-4 раза в день; Количество больных: группа 1 (FG) = 21; группа 2 (DFG) = 40.
Параметры: мазки из горла собирали в день 0 (до лечения), дни 0, 1, 3 и 7. В каждый момент времени один мазок использовали для количественного определения вирусов путем внесения мазка в 5 мл среды для культивирования клеток, а затем фильтрации жидкости через фильтр 0,22 мкм и инфицирования культур клеток, чувствительных к вирусу гриппа MDCK, с целью определения количества вируса в мазке. Второй мазок использовали для определения концентрации бактерий, а третий - для определения количества цитокинов, специфичных для вирусной инфекции (TNF-альфа, IL-4 и IL-6).
Результаты. На 1-й, 3-й и 7-й день (24 часа после заражения) наблюдались следующие результаты:
Средняя гибель клеток в контрольных культурах в день 0 - через 24 часа = 92,2% (группы FG и DFG).
Рост вируса вызывал гибель клеток в FG на 1, 3 и 7-е сутки: 78,6%, 71,2% и 68,4%, тогда как в DFG она составляла 52,3%, 26,1% и 11,3%.
% пациентов с количеством бактерий в мазках 103/мл в день 0 (24 часа): средний контроль = 66,5%.
В дни 1 (48 часов), 3 и 7: в группе FG 29,7%, 21,5% и 19,6%, тогда как в группе DFG - 16,1%, 6,4% и 0,0%.
Количественное определение цитокинов с помощью ELISA, пг/мл. Средняя концентрация до лечения: 811 пг/мл. В дни 1, 3 и 7: группа FG для TNF-альфа: 656 (±78), 542 (±44) и 523 (±46) пг/мл, в то время как в группе DFG было 366 (±48), 123 (±36) и 28 (±9) пг/мл.
Концентрация IL-4 в начале (день 0 инфекции, показания через 24 часа) составляла 89,5 пг/мл. На 1-й (48 ч), 3-й и 7-й дни в группе FG она составляла 94 (±13), 79 (±14) и 71 (±15) пг/мл, а в группе DFG - 40 (±9), 11 (±6) и 2,5 (±0,5) пг/мл.
Концентрация IL-6 в начале (день 0 инфекции, показания через 24 часа) составляла 66,3 пг/мл. На 1-й (48 ч), 3-й и 7-й день в группе FG она составляла: 55,2 (±7,2), 44,2 (±6,3) и 48,9 (±5,5) пг/мл, а в группе DFG - 12,3 (±3,1), 2,6 (±0,7) и 0,0 (±0) пг/мл.
Все остальные симптомы гриппа, включая лихорадку, боль в горле, покалывание в горле и зуд, уменьшились в среднем на 72% в группе DFG по сравнению с 24% в группе FG в течение 3 дней лечения. Ни у одного пациента не было отмечено нежелательных явлений
Эти результаты ясно показывают, что композиция DFG, нейтрализующая белок специфического заболевания, действует одновременно на несколько факторов и способствует более быстрому выздоровлению. Считается, что очень быстрое выздоровление в группе DFG связано со снижением концентрации вируса, заживлением слизистой оболочки носа и сильным снижением уровня цитокинов TNF-альфа, IL-4 и IL-6, участвующих в факторах запуска CRS назальных, синусоидальных, верхних и нижних дыхательных путей.
C - Тестовая композиция № 3 для лечения псориаза, экземы и дерматита
Композиция № 3: глицерин 75,02%, вода 3,12%, мед 20,92%, ксантановая камедь 0,08%, экстракт Vaccinium macrocarpon 0,11%, экстракт Camellia sinensis 0,43%, экстракт Vitis vinifera 0,32%. Данной композицией заполнили пластиковые тюбики вместимостью 50 мл, особенно подходящие для лечения. Тип исследования: Сравнительное 6-недельное одиночное слепое клиническое исследование с композицией № 3 для лечения псориаза, экземы или дерматита (PED) с помощью FG по сравнению с DFG в течение периода 42 дня.
Композиция с тестовым продуктом № 3, тюбики вместимостью 50 мл, содержащие вязкую жидкость (FG или DFG).
Количество пациентов: группа 1 (FG) = 51 (29M + 22F); Группа 2: (DFG) = 56 (33М + 23F).
Способ применения: непосредственно на очаги поражения, местно, 3 раза в день в течение 6 недель.
Результаты. По сравнению с началом лечения (Т0) в группе FG в среднем на 15% уменьшались эритема, зуд, отек, намокание, сухость и шелушение поражений в период со 2 по 6-ю неделю по сравнению со средним снижением тех же параметров на 72% в группе DFG. Статистическая значимость DFG в сравнении с FG = *. Нежелательные явления во всех группах отсутствуют.
Вывод: DFG значительно уменьшает признаки эритемы и зуда, отека очага поражения, выделения из очага поражения, сухости очага поражения, зуда, шелушения, образования корочек и улучшает параметры качества жизни, по оценке исследователей и пациентов, уже со второй недели после начала лечения. Эти результаты показывают, что FG, который просто защищает, очищает и увлажняет очаги поражения, не влияет на индуцированный цитокинами рост клеток, в то время как DFG, который воздействует на множество факторов заболевания (блокирует индуцированный EGF и FGF неконтролируемый рост клеток), почти в 4-5 раз более эффективен при лечении симптомов заболевания.
D - Тестовая композиция № 4 для лечения вирусного риносинусита и дыхательной недостаточности у взрослых
Композиция № 4: глицерин 26%, вода 73,02%, HPC 0,5%, экстракт Vaccinium macrocarpon 0,07%, экстракт Camellia sinensis 0,13%, экстракт Vaccinium myrtillus 0,07%, SPA 0,21%. Данной композицией заполнили пластиковые контейнеры вместимостью 15 мл с распылителем, особенно подходящим для лечения назальной инфекции (риносинусита).
Тип исследования: 21-дневное, одиночное слепое, рандомизированное с FG в сравнении с DFG.
Композиция с тестовым продуктом № 4
Количество пациентов: группа 1 (FG) = 45; Группа 2 (DFG): = 58. Балл оценки тяжести синусита (SSS) > 10 для пациентов, включенных в исследование.
Способ применения: 3-4 распыления за одно применение два раза в день в течение максимального периода 21 день. Изучаемые параметры: ССС, потребность в антибактериальной терапии, развитие тяжелых респираторных симптомов, свидетельствующих о CRS.
Результаты. Несмотря на то, что спреи FG оказались полезными после одной недели лечения (среднее уменьшение симптомов -38%), лечение DFG дало значительно большее, статистически значимое улучшение, чем лечение FG, в отношении скорости и степени уменьшения симптомов, что привело к меньшей потребности в антибиотикотерапии.
Дополнительная эффективность DFG по сравнению с эффективностью FG в дни 1, 3, 7, 14 и 21 для лечения (1) заложенности носа составила -30,55%, -49,54%, -64,13%, -75,14% и -87,09%; (2) насморка составила +58,25%, +25,76%, -65,39%, -48,78% и -52,25%; (3) боли в пазухах составила -62,81%, -76,02%, -66,72%, -48,97% и -55,63%; (4) общее уменьшение симптомов составило -62,1%, -73,09%, -77,46%, -70,05% и -83,21%.
У шести из 45 пациентов в группе FG развились тяжелые респираторные симптомы в период с 9-го по 21-й день, и им потребовалась госпитализация, для сравнения в группе DFG таких пациентов не было. Двадцать два из 45 пациентов в группе FG нуждались в антибактериальной терапии по сравнению с 2 из 58 пациентов в группе DFG. Статистическая значимость DFG в сравнении с FG = * с 3-го дня. Нежелательные явления, связанные с приемом препарата, во всех группах отсутствовали.
Вывод: Вирусный синусит включает присутствие вирусных частиц и провоспалительных цитокинов на слизистой оболочке носа, повреждение слизистой оболочки носа и системный воспалительный каскад, который может привести к тяжелой дыхательной недостаточности и запуску CRS. Было показано, что композиция по изобретению эффективна в уменьшении симптомов риносинусита по сравнению с одним FG без каких-либо нежелательных эффектов и, таким образом, подавляет те факторы, которые могут вызвать CRS.
E - Тестовая композиция № 5 для лечения воспаления носа с инфекцией и дыхательной недостаточностью
Композиция № 5: глицерин 9,8%, вода 89,317%, Solagum 0,5%, экстракт Ribes nigrum 0,05%, экстракт Curcuma longa 0,08%, ароматическое масло Mentha piperita 0,05%, ароматическое масло Eucalyptus globulus 0,05%, ароматическое масло Rosmarinus officinalis 0,05%, ароматическое масло Thymus satureioides 0,05%, консерванты 0,053% (сорбат калия 0,025%, бензоат натрия 0,025%, лимонная кислота 0,003%). Данной композицией заполнили пластиковые контейнеры вместимостью 15 мл с распылителем, особенно подходящим для лечения назальной инфекции (риносинусита).
Тип исследования: 14-дневное, сравнительное, рандомизированное, двойное слепое, в параллельных группах.
Испытуемый продукт: композиция № 5
Пациенты: группа 1 (FG) = 16; группа 2 (DFG) = 38. Балл оценки тяжести синусита (SSS) >10. Включенные в исследование пациенты характеризовались тяжелой дыхательной недостаточностью, сильным воспалением пазух и носа и были госпитализированы для оказания респираторной помощи, чтобы избежать возникновения CRS.
Параметры: изменение тяжести риносинусита и общей оценки симптомов, т.е. суммы показателей ринореи (выделений из носа), постназального затекания, заложенности носа, головной боли, лицевой боли/давления по сравнению с исходным уровнем до 30 минут после начала приема первой дозы в день 1, день 2, день 3, день 6, день 14 или день излечения. Потребность в антибактериальной терапии, респираторной поддержке и общий синоназальный исход (SNOT) оценивается по шкале от 1 до 10.
Способ применения: 2-3 распыления на одно применение, три раза в день в течение максимального периода 14 дней.
Ключевые параметры: улучшение респираторных симптомов на 50% по сравнению с началом лечения (Т0), потребность в антибактериальной терапии, развитие CRS-подобных симптомов, концентрация IL-6 в носовой слизи в 0-й день по сравнению с 7-м днем.
Результаты: DFG оказался значительно более эффективным, чем FG, в отношении симптоматического лечения и почти полного купирования риносинусита и респираторных симптомов у пациентов, госпитализированных с тяжелым воспалением верхних дыхательных путей, синуситом и склонных к CRS. DFG, скорее всего, оказывал значительно более сильное давление на пазухи, тем самым открывая и дренируя заблокированное содержимое пазух в течение первых 3 дней лечения, поскольку большинство клинических признаков (особенно головная и лицевая боль) существенно уменьшились с сильным носовым потоком в течение первых 24 часов. Прогрессирующее улучшение дыхательной недостаточности наблюдалось с 1-го дня лечения, а симптомы SNOT уменьшились на 50% в течение 4 дней у пациентов группы DFG по сравнению с 9 днями в группе FG. Девять из 16 пациентов (56,25%) в группе FG нуждались в антибиотикотерапии и/или противовоспалительной терапии по сравнению с только 7/38 (18,42%) в группе DFG. На 14-й день респираторную поддержку осуществляли у 7/16 (43,75%) пациентов в группе FG по сравнению с 2/58 (3,44%) в группе DFG. Концентрация IL-6 в мазках из носа в дни 0 (до начала лечения) и 7 составляла 78 и 42 пг/мл (-41,66%) в группе FG по сравнению с 79 и 12 пг/мл (-82,61%) в группе DFG. Оба продукта были полностью безопасны и хорошо переносились пациентами, поскольку ни один из пациентов не жаловался на побочные эффекты, и ни один из пациентов не прекратил участие в исследовании.
Вывод: Композиция, содержащая полимеры двойного действия, почти в два раза эффективнее композиции (FG), содержащей только полимеры, связывающие глицерин. Композиции по изобретению можно использовать для подавления тяжелого воспаления носа и предотвращения развития CRS.
F - Тестовая композиция № 6 для лечения тяжелого аллергического ринита, вызванного сенной лихорадкой, у взрослых.
Композиция № 6: глицерин 2%, вода 96,9%, Solagum 0,5%, экстракт Camellia sinensis 0,09%, экстракт Curcuma longa 0,08%, экстракт женьшеня Panax 0,06%, экстракт Urtica dioica 0,1%, ароматическое масло Citrus limonum 0,05%, консерванты 0,22% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,02%). Данной композицией заполнили пластиковые контейнеры вместимостью 15 мл с распылителем, особенно подходящим для лечения аллергического ринита.
Двойное слепое, рандомизированное, плацебо-контролируемое, многоцентровое клиническое исследование было проведено для оценки эффективности и безопасности FG в сравнении с DFG для лечения аллергического ринита.
Это исследование проводили у пациентов, страдающих тяжелым аллергическим ринитом (АР). Тридцать один пациент лечили DFG, содержащим антигистамин, анти-IgE, анти-IL-2, 4, 6 и 23 полимера двойного действия, а 15 пациентов лечили FG в качестве продукта сравнения (CP). Оба продукта (аэрозольные баллончики по 15 мл) наносили местно на слизистую оболочку носа 3-4 раза в день в течение 3 недель. Общие баллы, баллы оценки рефлекторных и мгновенных назальных симптомов ринореи, выделений из носа, чихания и зуда, а также баллы оценки состояния глаза (зуд, слезотечение, покраснение) и баллы оценки использования средств экстренной помощи определяли ежедневно в течение недель от -1 до +3 с использованием от 0 (отсутствие симптомов) до 3 баллов (тяжелые симптомы). Опросники качества жизни при риноконъюнктивите (RQLQ) заполняли в начале и в конце исследования. FG использовали так же, как и DFG. Средние еженедельные результаты в обеих группах сравнивали с баллами в начале лечения (базовый уровень) и между двумя группами.
Результаты. Установлено, что FG лишь незначительно уменьшает симптоматическую выраженность аллергического ринита. Среднее снижение по сравнению с исходным уровнем (T0) в конце 1-й, 2-й и 3-й недель составило соответственно 11,7%, 13,6% и 15,1% в отношении общей оценки назальных симптомов (rTNSS); 9,9%, 14,5% и 15,8% в отношении общей оценки глазных симптомов (rTOSS); и 4,97%, 8,45% и 10,94% в отношении мгновенной общей оценки глазных симптомов перед введением дозы (am-iTOSS, p: Незначимо: NS).
За тот же период, по сравнению с показателями FG, снижение в группе DFG было выше на 37,7%, 58,4% и 73,5% для rTNSS; 38,3%, 54,6% и 64,1% для rTOSS и 29,84%, 48,91% и 59,77% для am-iTOSS (*p<0,05 для всех параметров относительно FG в те же моменты времени). Опрос качества жизни при риноконъюнктивите (RQLQ), проведенный с помощью стандартного установленного опросника, показал улучшение на 50,28% в группе DFG по сравнению с 22,85% в группе FG. В течение периода исследования по меньшей мере одно средство неотложной помощи использовали 80% пациентов в группе FG по сравнению только с 29% в группе DFG. Оба продукта хорошо переносились и не вызывали нежелательных эффектов.
Вывод. В отсутствие благоприятного для клеток, безопасного и многоцелевого лечения аллергического ринита использование механического осмотического барьерного раствора пленкообразователя, содержащего специфические полимеры, ингибирующие CPRM, в пленкообразующем глицерине (DFG), является высокоэффективным и безопасным способом блокирования нового контакта с аллергеном, очистки слизистой оболочки носа от источников контаминации, нейтрализации гистамина и IgE, а также остановки воспалительного каскада для уменьшения вероятности развития CRS.
G - Тестовая композиция № 7 для лечения орального мукозита, вызванного химиотерапией и лучевой терапией (тяжелое воспаление полости рта и/или желудка с обширным повреждением тканей).
Композиция № 7: глицерин 73,85%, вода 11,94%, мед 13,6%, экстракт Vaccinium macrocarpon 0,28%, экстракт Vaccinium myrtillus 0,33%. Данной композицией заполнили алюминиевые контейнеры вместимостью 20 мл с распылителем, особенно подходящим для лечения орального мукозита, вызванного химиотерапией.
Одиночное слепое, рандомизированное, плацебо-контролируемое клиническое исследование для оценки эффективности и безопасности DFG по сравнению с обычно используемыми противовоспалительными и/или антибиотическими средствами для лечения вызванного лучевой и химиотерапией мукозита полости рта, сопровождающегося тяжелым воспалением полости рта и желудка и способным привести к смерти по причине CRS. В исследование было включено 69 пациентов. 48 пациентов получали DFG, а 21 - обычно используемые пероральные местные лекарственные средства в качестве контрольной группы.
Язвы, вызванные оральным мукозитом, лечили 4-5 раз в день в течение 28 дней. Степень общего мукозита, интенсивность боли и ощущения жжения, образование новых язв и влияние на нарушение приема пищи оценивали до лечения, через 30 минут после первого применения продукта и в дни 1, 2, 3, 4, 7, 14, 21 и 28. Симптомы оценивали по шкале от 0 (отсутствие симптомов) до 4 (тяжелые симптомы) или от 0 до 10 для некоторых параметров.
Результаты: по сравнению с группой обычно используемого лечения лекарственными средствами, группа DFG показала значимо более высокое улучшение на 28-й день в отношении орального мукозита (0,83/4 в DFG в сравнении с 2,10/4 в контрольной группе), боли (2,05/10 в сравнении с 5,71/10 в контрольной группе), перорального мукозита и ощущение жжения в желудке (1,92/10 в сравнении с 5,76 в контрольной группе), способности к приему пищи, инфицирования поражений (0,52/4 в сравнении с 1,95 в контрольной группе) и улучшения приема твердой пищи (2,38/4 в сравнении с 1,50/4 в контрольной группе). На скорость образования новых язв это не повлияло. Поскольку лечение мукозита требует комплексного терапевтического подхода, направленного на одновременное устранение источников контаминации и токсичных химических веществ из язвы, а также на создание благоприятной среды для роста здоровых клеток, DFG оказался как минимум в 3-4 раза более эффективным в достижении этих целей по сравнению со стандартными противовоспалительными или антибактериальными средствами.
H - композиция № 8 для лечения тяжелого хронического кашля у взрослых
Композиция № 8: глицерин 40%, вода 50,43%, мед 8%, экстракт Calendula officinalis 0,5%, ароматическое масло Eucalyptus globulus 0,02%, масло Linum usitatissimum 0,05%, экстракт прополиса 1%. Данной композицией заполнили алюминиевые контейнеры вместимостью 30 мл с распылителем, особенно подходящим для лечения сухого кашля.
Тип исследования: 14-дневное рандомизированное плацебо-контролируемое двойное слепое исследование эффективности и безопасности проводили путем применения спрея от кашля (30 мл спрей), 4-5 распылений, 3-4 раза в день в течение 14 дней подряд.
Количество пациентов: 17 в группе FG в сравнении с 37 в группе DFG.
Параметры: Первичный результат определялся как влияние на тяжесть и частоту сухого кашля, а также изменения в раздражении горла, боли в горле, влияние на воспаление горла (отек, покраснение горла) и связанные параметры, которые обобщены в Лейчестерском опроснике по кашлю (LCQ) для качества жизни, связанного с кашлем. Изменения оценивались по шкале от 0 до 10 (0 указывает на отсутствие симптомов) непосредственно перед 1-й обработкой, через 5 минут и 2 часа, а также на 1, 2, 3, 6, 9 и 14 день, причем оценку проводил исследователь (день 0, 1 и 14) или пациенты.
Результаты. По сравнению с лечением FG, лечение DFG вызвало мгновенное и сильное снижение средних показателей тяжести сухого кашля (например, на 9-й день: средний балл составил 5,8/10 для FG в сравнении с 3,6/10 для DFG), частоты кашля (день 9: 5,3/10 для FG в сравнении с 2,2/10 для DFG), раздражения горла (4,8/10 для FG в сравнении с 1,6/10 для DFG), воспаления горла (4,7/10 для FG в сравнении с 0,8/10 для DFG), с заметным улучшением параметров Лейчестерском опросника по кашлю. DFG был по меньшей мере в 2-3 раза более быстрым и эффективным в облегчении симптомов кашля по сравнению с лечением только FG. DFG сильно снижал воспаление и микробную контаминацию благодаря длительному разжижению слизи. Ни у одного из пациентов после прекращения лечения случаев CRS не наблюдалось.
I - композиция № 9 для лечения воспалений и болей в горле у детей.
Композиция № 9: глицерин 74,63%, мед 6%, вода 18,54%, экстракт Vitis vinifera 0,44%, экстракт Sambucus nigra 0,29%, экстракт Ribes nigrum 0,1%. Данной композицией заполняли алюминиевые контейнеры вместимостью 20 мл с распылителем, особенно подходящим для лечения инфекции и болей в горле у детей.
Тип исследования: Клиническая эффективность и безопасность композиции № 9, предназначенной для лечения воспалительных болей в горле у детей в возрасте от 3 до 15 лет.
Презентация продукта: оба продукта в алюминиевых контейнерах вместимостью 20 мл с распылителем. Количество пациентов: группа 1 (FG) = 9; группа 2 (DFG) = 20. Способ применения: 3-4 распыления на поверхность горла за одно применение, 4-5 раз в день в течение максимального периода 14 дней. Параметры: влияние на параметры воспаления горла на 1-й, 3-й, 6-й, 14-15-й день или день выздоровления (в зависимости от того, что раньше).
Результаты: % улучшения (+) или ухудшения (-) клинических симптомов в группе DFG по сравнению с группой FG на 1, 2, 6 и 14 дни в отношении следующих параметров: (1) затруднение при глотании +11,48%; +42,59%, +74,42% и +93,33%; (2) отек горла +5,38%, +30,99%, +52,94% и +91,43%; (3) раздражение горла +2,08%, +22,37%, +60,34% и +97,18%; (4) воспаление горла +5,0%, +40,1%, +72,58 и +97,37%; и (5) бактериальные отложения на поверхности горла: +2,27% (+2 часа), +41,43 на 3-й день, +59,09% на 6-й день и +88,89% на 14-й день.
Наличие микроорганизмов в мазках горла. В начале исследования у 8/9 детей в группе FG и у 15/20 в группе DFG мазок горла был положительный на наличие бактерий. На 6-й день только 2/9 детей в группе FG и 3/20 в группе DFG были положительными. Эти результаты демонстрируют значительно более сильный и быстрый эффект DFG по сравнению с монотерапией FG для подавления воспаления горла у детей без каких-либо дополнительных нежелательных явлений. Отличный противовоспалительный эффект наблюдался уже через 2 дня лечения композицией DFG.
J - композиция №10 для лечения сухого кашля у детей
Композиция № 10: глицерин 53%, вода 41,81%, мед 4,5%, экстракт Ribes nigrum 0,36%, экстракт Curcuma longa 0,08%, ароматическое масло Citrus limonum 0,02%, консерванты 0,23% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,03%). Данной композицией заполняли алюминиевые контейнеры вместимостью 20 мл с распылителем, особенно подходящим для лечения кашля у детей.
Тип исследования: Клиническая эффективность и безопасность двух композиций для лечения сухого кашля: DFG в сравнении с FG для лечения сухого кашля у детей. Количество пациентов: группа 1 (FG) = 9; группа 2 (DFG) = 20 (возраст от 3 до 15 лет). Способ применения: оба продукта были представлены в виде спреев по 15 мл и наносились в виде 3-4 распылений на поверхность горла за одно применение, 4-5 раз в день в течение максимального периода 15 дней. Параметры: выраженность и частота кашля, дискомфорта в груди и першения в горле через 2 ч после первого применения в дни 1, 3, 6 и 15 или до полного выздоровления.
Результаты: % изменения для DFG по сравнению с FG через 2 часа и в дни 3, 6 и 15 в отношении следующего: (1) кашель: 0,0%, -45,79%, -89,71% и -99,0%; (2) дискомфорт в груди: -3,19%; -47,72%, -75,48% и -91,66%; (3) раздражение горла: 0,0%, -66,6%, -88,2% и -98,0%; (4) качество жизни (QOL): средний балл оценки качества жизни был примерно одинаковым в обеих группах в начале исследования. Через 14 дней лечения качество жизни значительно улучшилось в группе DFG (средний балл 41,60) по сравнению с группой FG (23,30); и (5) потребность в антибиотикотерапии: 70% в группе FG по сравнению с 25% в группе DFG.
Вывод: композиция DFG почти в два раза более эффективна в отношении уменьшения симптомов сухого кашля у детей по сравнению с лечением только FG.
К - композиция №11 для лечения хронического воспалительного риносинусита у детей
Композиция № 11: глицерин 13%, вода 85,96%, HPC 0,5%, экстракт Vaccinium macrocarpon 0,07%, экстракт Vaccinium myrtillus 0,07%, экстракт Sambucus nigra 0,05%, экстракт Ribes nigrum 0,13%, консерванты 0,22% (сорбат калия 0,1%, натрия бензоат 0,1%, лимонная кислота 0,02%). Данной композицией заполняли пластиковые контейнеры вместимостью 15 мл с распылителем, особенно подходящим для лечения назальной инфекции у детей.
Тип исследования: 14-дневное сравнительное, рандомизированное, двойное слепое, обсервационное клиническое исследование в параллельных группах для оценки эффективности подавления хронического воспаления под действием FG по сравнению с DFG у детей, страдающих хроническим риносинуситом.
Презентация и применение тестируемого продукта: 15 мл назальных спреев, 2-3 распыления на одно применение, два раза в день в течение максимального периода 14 дней. Количество больных: 1-я группа (FG) = 10; Группа 2 (DFG) =20.
Параметры: балл оценки тяжести риносинусита (RSSS) через 30 минут после начала приема первой дозы в день 1, день 3, день 6, день 14-15 или день выздоровления (в зависимости от того, что раньше), влияние на ринорею или заложенность носа, лихорадку, кашель, отсутствие хорошего сна, боль при надавливании на лицо.
Результаты: % улучшения (+) или ухудшения (-) клинических симптомов с оценкой эффективности FG двойного действия по сравнению с оценкой эффективности FG на 1, 2, 6 и 14 дни в отношении следующего: (1) ринорея: +11,69%; +44,12%, +61,70% и +95,0%; (2) кашель: -2,13%, +35,65%, +52,81% и +93,62%; (3) влияние на сон: 0,0%, +50,40%, +62,89% и +97,18%; (4) влияние на лицевую боль при надавливании: +2,27%, +41,51%, +57,89% и +93,31%; (5) влияние на лихорадку: снижение балла оценки лихорадки на 57% в группе DFG по сравнению с группой FG; и (6) эффективность продукта: 90% пациентов в группе DFG оценили эффективность продукта как отличную по сравнению с 15% в группе FG (65% пациентов в группе FG оценили продукт как удовлетворительный или хороший).
Вывод. Композиция DFG признана более эффективной в отношении подавления симптомов хронического воспалительного риносинусита у детей по сравнению с композицией FG. Обе композиции хорошо переносились детьми. Уменьшение клинических признаков указывает на сильный противовоспалительный эффект DFG, который может быть связан с подавлением провоспалительных цитокинов.
L - композиция № 12 для лечения воспалительного аллергического ринита глаз и носа у детей
Композиция № 12: глицерин 4%, вода 94,87%, Solagum 0,6%, экстракт Vaccinium macrocarpon 0,1%, PVOH 0,1%, экстракт Panax ginseng 0,06%, ароматическое масло Thymus satureioides 0,03%, ароматическое масло Citrus limonum 0,02%, консерванты 0,22% (сорбат калия 0,1%, бензоат натрия 0,1%, лимонная кислота 0,02%). Данной композицией заполняли пластиковые контейнеры вместимостью 15 мл с распылителем, особенно подходящим для лечения аллергического ринита у детей.
Тип исследования: 14-дневное, одиночное слепое, рандомизированное с композицией FG и DFG. Количество пациентов: группа FG = 10; группа 2: группа DFG = 20. Балл оценки тяжести синусита, вызванного аллергеном (SSS)> 10. Способ применения: были предоставлены спреи по 15 мл, которые использовали по 3-4 распыления на одно применение два раза в день в течение максимального периода 14 дней в обеих группах.
Параметры: насморк, TNSS (общая оценка назальных симптомов), покраснение глаз, TOSS (общая оценка глазных симптомов). Концентрацию гистамина определяли в мазках из носа, собранных в 0-й день (до лечения) и в 1-й день (24 часа) у 8 случайных пациентов каждой группы. Мазки промывали 1 мл физиологического раствора и измеряли концентрацию гистамина с использованием набора ELISA на гистамин (ABCAM-ab213975) при 450 нм.
Результаты: Хотя спреи FG оказались полезными, DFG продемонстрировал значительно больший эффект, показав статистически значимое улучшение в отношении скорости и степени уменьшения симптомов, что привело к меньшей потребности в противовоспалительной терапии.
Улучшенная эффективность DFG по сравнению с эффективностью FG на 1, 2, 7 и 14 дни для следующего: (1) насморк: +12,68%; -28,17%, -73,24% и -91,55%; (2) TNSS: -2,59%, -18,75%, -56,66% и -87,50%; (3) слезотечение: 0,0%, -18,57%, -55,71% и -100,0%; (4) зуд глаз: -5,75%, -41,38%, -89,66% и -98,85%; (5) отек глаз: -9,09%, -34,64%, -77,27% и -100,0%; (6) TOSS: -5,30%, -13,73%, -75,60% и -100,0%; (7) гистамин в Т0 и через 24 часа: средние концентрации, обнаруженные в группе FG, составляли 8,35 и 3,60 нмоль по сравнению с 7,80 и 0,20 в группе DFG, что означает сильную местную гистамин-блокирующую активность композиции DGF в сравнении с композицией FG; и (8) QOL в день 7: 52,7% в группе FG в сравнении с 72,61 в группе DFG.
Эти результаты показывают, что тестируемый продукт DFG был значительно более эффективным в снижении симптоматических проявлений аллергического ринита у детей по сравнению с одним только FG из-за его специфических свойств блокирования гистамина и провоспалительных цитокинов. Благоприятный эффект наблюдается через 3-7 дней лечения. Составы DFG были намного лучше и быстрее. Механизм действия этого эффекта может быть связан с более высокими связывающими свойствами CPRM композиции DFG по сравнению с FG.
Выводы по фармакологическим и клиническим данным
Эти результаты доказывают, что клиническая эффективность композиций, содержащих полимеры двойного действия и глицерин (DFG), значительно выше по сравнению с пленкообразующим глицерином (FG) для лечения всех местных воспалительных заболеваний. Почему и когда может возникнуть CRS, пока неясно, но он наблюдался при всех видах хронических воспалительных заболеваний. Интенсивность, тяжесть и последствия CRS варьируются в зависимости от локализации и типа заболевания. CRS, поражающие жизненно важные органы, такие как легкие или сердце, легко обнаружить, поскольку они могут вызывать дыхательную или сердечную недостаточность. Физиопатология хронического местного заболевания обычно включает продолжительное патогенное повреждение, обширное клеточное повреждение, местное и системное присутствие чрезмерно высоких концентраций провоспалительных цитокинов и белков, связанных с множественными заболеваниями, которые поддерживают хронический воспалительный каскад. CRS является следствием цепочки реакций, в которой каждый фактор взаимозависим от другого, и все эти факторы активируются при появлении клинических признаков заболевания. Таким образом, любое эффективное лечение должно быть многоцелевым, чтобы частично или полностью блокировать все причины, вызывающие CRS.
Результаты использования этих композиций для местного применения, содержащих полимеры двойного действия с осмотическим глицерином, доказывают, что указанные композиции можно безопасно использовать для подавления большого количества факторов, участвующих в запуске CRS.
Ссылки
Dang Xuan Cuong et al. Tannin extraction from plants. Глава в книге - Structural properties, Biological properties and current knowledge: Chapter on Tannin extraction. IntechOpen publisher, May 13th 2019. doi: 10.5772/intechopen.86040.
Maria Fraga-Corral et al. Technological application of tannin-based extracts. Molecules 2020, 25(3)614. doi: 10.3390/molecules25030614.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, СОДЕРЖАЩАЯ ГЛИЦЕРИН И ТАНИН | 2013 |
|
RU2640020C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ КИШЕЧНЫХ ПОВРЕЖДЕНИЙ | 2017 |
|
RU2772870C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ Actinidia, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2423139C2 |
| ПРИМЕНЯЕМЫЕ МЕСТНО СТРОНЦИЙСОДЕРЖАЩИЕ КОМПЛЕКСЫ ДЛЯ ЛЕЧЕНИЯ БОЛИ, ЗУДА И ВОСПАЛЕНИЯ | 2013 |
|
RU2605279C2 |
| ПРИМЕНЕНИЕ АНТИ-CD40-АНТИТЕЛ | 2006 |
|
RU2442606C2 |
| Композиция для лечения и профилактики заболеваний верхних дыхательных путей в форме назального спрея | 2024 |
|
RU2839143C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ МОЧЕВЫВОДЯЩИХ ПУТЕЙ | 2016 |
|
RU2637650C2 |
| СОСТАВЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ВЕРХНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2011 |
|
RU2580643C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ AKKERMANSIA MUCINIPHILA И ЭКСТРАКТ ЗЕЛЕНОГО ЧАЯ | 2021 |
|
RU2829638C1 |
| НАЦЕЛЕННЫЕ НА БЕЛКИ СОЕДИНЕНИЯ, ИХ КОМПОЗИЦИИ, СПОСОБЫ И ПРИМЕНЕНИЯ | 2016 |
|
RU2694895C2 |
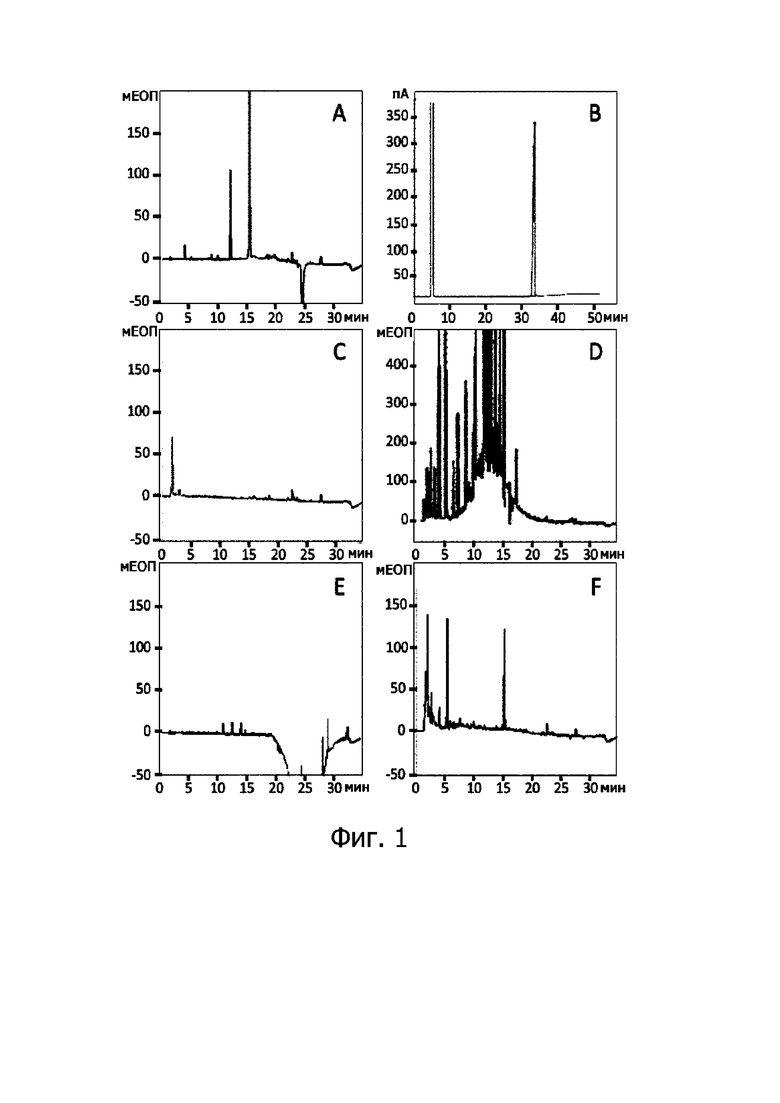
Настоящее изобретение относится к применению композиции, содержащей по меньшей мере один полимер двойного действия в концентрации от 0,01 до 5 мас.% от общей массы композиции, связанный с глицерином и способный связываться по меньшей мере с одним провоспалительным соединением; глицерин и подходящее вспомогательное вещество, для профилактики или лечения местного воспалительного заболевания и синдрома высвобождения цитокинов у нуждающегося в этом субъекта. Настоящее изобретение обеспечивает новый многоцелевой терапевтический подход для профилактики или лечения топического/местного воспаления, воспалительных заболеваний и их последствий, таких как неконтролируемое высвобождение цитокинов, называемое цитокиновым синдромом (CS) или синдромом высвобождения цитокинов (CRS). 10 з.п. ф-лы, 1 ил., 4 табл., 2 пр.
1. Применение композиции, содержащей по меньшей мере один полимер двойного действия в концентрации от 0,01 до 5 мас.% от общей массы композиции, связанный с глицерином и способный связываться по меньшей мере с одним провоспалительным соединением; глицерин и подходящее вспомогательное вещество, для профилактики или лечения местного воспалительного заболевания и синдрома высвобождения цитокинов у нуждающегося в этом субъекта.
2. Применение композиции по п. 1, где по меньшей мере одно провоспалительное соединение выбрано из группы, состоящей из матриксных металлопротеаз, гистаминов, цитокинов, клеточных рецепторов, ионов металлов, иммуноглобулинов или вирусных гликопротеинов.
3. Применение композиции по любому из предыдущих пунктов, где местное воспалительное заболевание выбрано из группы, состоящей из вирусных инфекций, риносинусита, ран и язв, псориаза, экземы, дерматита, аллергии, астмы, вызванных загрязнением окружающей среды респираторных заболеваний, вызванных загрязнением окружающей среды топических повреждений, язв желудочно-кишечного тракта, геморроя, генитальных инфекций, глазной аллергии, конъюнктивита и воспаления глаз.
4. Применение композиция по любому из предыдущих пунктов, где общее количество по меньшей мере одного полимера двойного действия составляет от 0,01 до 3,5 мас.% от общей массы указанной композиции.
5. Применение композиции по любому из предыдущих пунктов, которая дополнительно содержит по меньшей мере один ингредиент, выбранный из группы, состоящей из меда, экстракта прополиса, растительной камеди, такой как ксантановая камедь и (или) аравийская камедь, и ароматических масел.
6. Применение композиции по любому из предыдущих пунктов, которая дополнительно содержит по меньшей мере одно лекарственное средство, такое как анальгетик, антибиотик, противовоспалительное лекарственное средство, антигистаминное средство, сосудорасширяющее средство, бронхолитическое средство, противоотечное лекарственное средство, соединение, связывающее специфические местные рецепторы, или ароматическое масло.
7. Применение композиции по любому из предыдущих пунктов, где указанную композицию наносят местно на поврежденную и (или) воспаленную биологическую поверхность, такую как кожа, слизистая оболочка глаза, конъюнктива, роговица, поверхности рта, носа, желудочно-кишечного тракта, дыхательных путей или половых органов.
8. Применение композиции по любому из предыдущих пунктов, где указанную композицию применяют в виде жидкости, ингалятора, жидкой повязки, раствора, геля, крема, пасты или мази, и она представлена в виде спреев, тюбиков, ампул, ватных или полимерных повязок с жидким покрытием, гранул, порошка или мягких желатиновых капсул.
9. Применение композиции по любому из предыдущих пунктов, где по меньшей мере один полимер двойного действия является природным, полусинтетическим и (или) синтетическим.
10. Применение композиции по п. 9, где по меньшей мере один полимер двойного действия представляет собой таннин, полученный из растения или частей растения.
11. Применение композиции по п. 5 или 6, где ингредиент и (или) лекарственное средство захвачены полимерными связями указанной композиции для замедленного высвобождения ингредиента и (или) лекарственного средства для дальнейшего усиления терапевтических свойств композиции.
| WO 2012065651 A1, 24.05.2012 | |||
| КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, СОДЕРЖАЩАЯ ГЛИЦЕРИН И ТАНИН | 2013 |
|
RU2640020C2 |
| JP 2018109032 A, 12.07.2018 | |||
| Hans-Walter Roth et al., Valuation of carboxymethylcellulose 0.5% / glycerin 0.9% and sodium hyaluronate 0.18% artificial tears in patients with mild to moderate dry eye / Clinical Optometry, 2011, pp | |||
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
| Regina Folster-Holst et al., Synthetic Tannins in | |||
Авторы
Даты
2025-02-12—Публикация
2020-09-08—Подача