Область техники
Изобретение относится к области биотехнологии и медицины, а именно к получению штамма Clostridium sporogenes номер В-14642 в Государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ - Оболенск» ФБУН «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, способного продуцировать коллагеназу для использования в клеточных технологиях.
Предшествующий уровень техники
Клостридиальные коллагеназы характеризуются высокой специфичностью действия на коллагеновые волокна и могут быть отнесены к "истинным" коллагеназам. Они широко используются в биотехнологии, медицине, для лабораторных целей. Так коллагеназа используется для профилактики и лечения рубцовых образований, в том числе контрактуры Дюпюитрена (заболевание кисти, связанное с рубцовым перерождением и укорачиванием ладонных сухожилий), а также в диагностических и лабораторных целях, например, для дезинтеграции тканей in vitro. Среди них наиболее изученными являются коллагеназы, синтезируемые бактерией Clostridium histolyticum, которые характеризуются высокой специфичностью действия на коллагеновые волокна. Однако для культивирования Cl. histolyticum и массовой продукции коллагеназы необходимы сложные меры предосторожности, так как эта бактерия является анаэробным патогеном, вызывающим газовую гангрену и продуцирующим токсины. Для оптимального биосинтеза коллагеназ культурой Cl. histolyticum использовалась сложная питательная среда.
Одним из самых перспективных направлений использования коллагеназ являются клеточные технологии, где они применяются для получения стромально-васкулярной фракции клеток жировой ткани, а также для выделения и культивирования чистых первичных клеток.
От продуктивности штамма, затрат на его культивирование, скорости его роста и накопления целевого продукта, а также себестоимости питательных сред зависит эффективность промышленного производства любых продуктов микробного синтеза.
В патенте ЕР 0468411 29.01.1992 «А mutant of bacterium Clostridium histolyticum, a process for the obtaining thereof, and its use in the production of clostripain-free collagenase» описан мутантный штамм Clostridium histolyticum K26 clo 88, полученный путем обработки исходного дикого штамма мутагенным агентом, и способный к синтезу коллагеназы на среде с протеозопептоном, соевым пептоном, неорганическими солями, витаминами. Недостатком использования мутантного штамма в производственном процессе является его нестабильность.
Описан еще один способ получения коллагеназы путем культивирования С.histolyticum (патент WO 2007/089851), где очистка препарата ведется с использованием ультрафильтрации с размером пор 10 кДа, что позволяет отделить только олигопептиды и небольшие белки, кроме того применяется ионообменная хроматография на колонке с Q-Sepharose HP. Это более дорогой способ очистки препарата.
Известен также способ получения микробной коллагеназы из ультрафильтрата культуральной жидкости Streptomyces lavendulae ИНМИ-36-SV (RU 95104309, 1996). Препарат получают из ультраконцентрата культуральной жидкости штамма Streptomyces lavendulae ИНМИ-36-SV с помощью ионнообменной хроматографии на ДЕАЕ-целлюлозе, гельфильтрации на сефадексе G-100 и лиофилизации. Данный препарат имеет более высокую коллагеназную активность, чем препарат из Clostridium histolyticum, однако способ имеет ряд недостатков, в частности многостадийность и относительно невысокий выход.
Наиболее близкими аналогами заявляемого изобретения является штамм Clostridium histolyticum 468 (RU 2180002 27.02.2002 «Способ получения коллагеназы») и штамм Clostridium histolyticum SK В-8362 (RU 2684220 23.03.2018). Штамм Clostridium histolyticum 468 (RU 2180002) синтезирует коллагеназу при культивировании на среде, содержащей гидролизат казеина и соевого шрота, неорганические соли, витамины. Данный штамм растет на сложной питательной среде, компоненты которой требуют предварительной подготовки. Кроме того, время культивирования штамма достаточно продолжительное (72±1 ч). Штамм Clostridium histolyticum SK В-8362 (RU 2684220) растет на стандартизированных питательных средах, однако время культивирования штамма достаточно продолжительное (44 ч).
Таким образом, в уровне техники существует потребность в новых продуцентах коллагеназы с высокой удельной активностью, коротким сроком культивирования для использования в клеточных технологиях и в медицине.
Раскрытие сущности изобретения
Технической задачей предлагаемого изобретения является расширение арсенала продуцентов коллагеназы с целью использования в клеточных технологиях, а также для использования в медицине.
Техническим результатом является штамм Clostridium sporogenes - продуцент коллагеназы, депонированный в Государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ - Оболенск» ФБУН «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека под центр прикладной микробиологии и биотехнологии» под номером В-14642 от 20 декабря 2023 года, для использования в клеточных технологиях и в медицине. Свидетельство о депонировании №1811 от 20 декабря 2023 года.
Указанный технический результат, достигается тем, что штамм Clostridium sporogenes В-14642 синтезирует коллагеназу от 0,85 до 0,93 мг в миллилитре культурального фильтра при культивировании от 12 до 24 часов в анаэробных условиях при 37°С на среде с триптоном и дрожжевым экстрактом. Также технический результат достигается тем, что предлагаемый штамм является диким штаммом с неизменными свойствами, не относится к IV группе патогенности и адаптирован под лабораторные и промышленные питательные среды и может быть использован в клеточных технологиях и в медицине.
Краткое описание чертежей
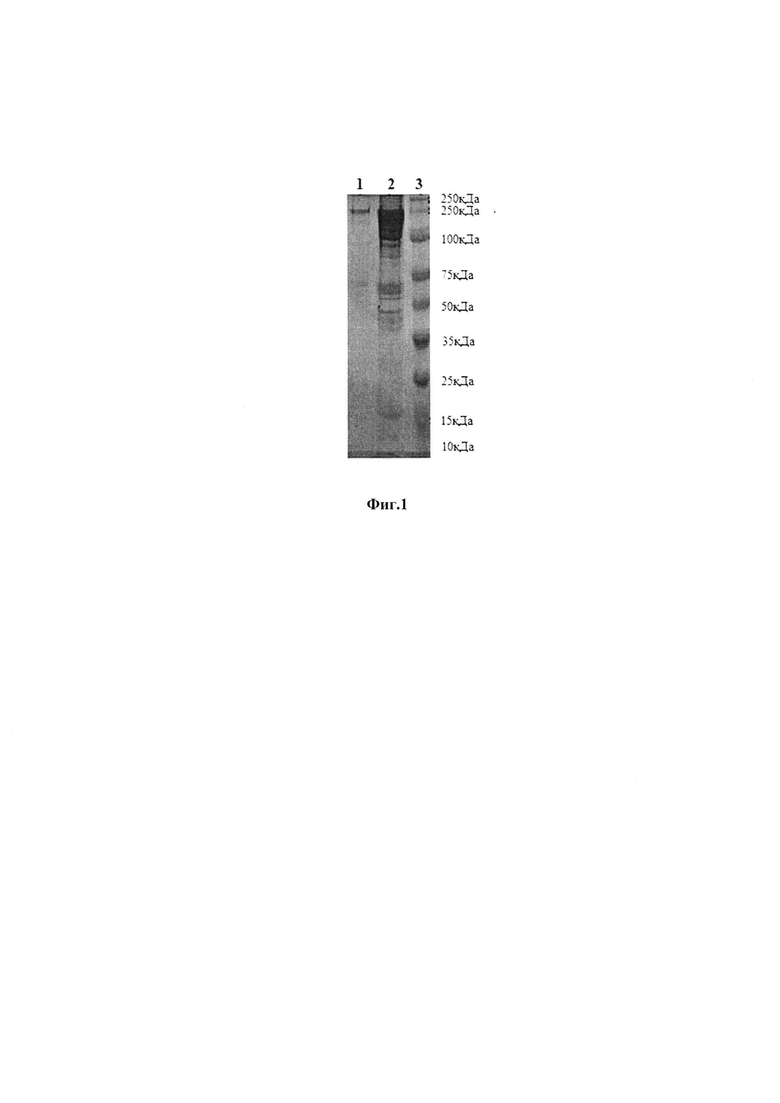
На фигуре представлен молекулярный вес коллагеназы из штамма Cl. sporogenes В-14642.
1. культуральный фильтрат;
2. концентрат;
3. маркеры молекулярного веса.
Реализация изобретения
Штамм Clostridium sporogenes В-14642 выделен ООО "Обл-Био" в г. Оболенске 02 сентября 2023 года. Был первично идентифицирован как продуцент коллагеназы на селективной питательной среде, содержащей коллаген.
Морфологические признаки: подвижные палочки, при окраске по Грамму окрашивались как грамположительные. Споры овальные, располагаются субтерминально. Рост на жидкой среде с глюкозой сопровождался помутнением и энергичным газообразованием. На плотной среде штаммы формировали полупрозрачные, с матовой поверхностью колонии диаметром 4-6 мм. Культуральные особенности: рост на жидкой среде с глюкозой сопровождался помутнением и энергичным газообразованием. На плотной среде штаммы формировали полупрозрачные, с матовой поверхностью колонии диаметром 4-6 мм. Штамм оксидазо- и каталазо - отрицательный, лецитиназная и липазная активность отрицательные, индол не образует, однако наблюдается образование газа, гидролизирует желатин. Продукция антигенов, ферментов, токсинов: продукция в среду при культивировании коллагеназы 140 кДа. Токсичность для лабораторных животных: по результатам биопробы, LD50 - отсутствует при подкожном и внутрибрюшинном введении белым беспородным мышам и морским свинкам в дозе от 1 мг до 10 мг. Не патогенен согласно данным на лабораторных животных: LD50 отсутствует при подкожном и внутрибрюшинном введении белым беспородным мышам и морским свинкам в дозе 5×109 КОЕ. Устойчив к антибактериальным препаратам: канамицин от 100 мкг/мл и выше подавляет рост, устойчив к хлорамфениколу. Генетические характеристики Clostridium sporogenes В-14642. При исследовании первичной нуклеотидной последовательности 16S РНК с помощью Web Nucleotide Blast исследуемая культура была идентифицирована как Clostridium sporogenes с высокой степенью достоверности 98,97% (см. табл.1).


Штамм Clostridium sporogenes В-14642 хранят при температуре 6-8°С в разведенном 1/5 бульоне Рамона в смеси с 80% глицерином (соотношение 1:4) в виде споровой суспензии или в лиофильно высушенном виде на защитной среде с добавлением желатина.
Осуществление изобретения подтверждается следующими примерами
Пример 1
Выращивание посевной культуры Clostridium sporogenes В-14642 в колбах. Приготовление инокулята. В стерильную колбу Эрленмейера объемом 750 мл помещали 250 мл среды 2YT с добавлением 0,9% агар-агара, рН 7,4-7,5. Добавляли в колбу 1 мл стока культуры Clostridium sporogenes № В-14642, выращенного на среде 2YT. Выращивали культуру в CO2 инкубаторе статично при температуре 37°С. Время выращивания - в течение 24 часов до оптической плотности ОП прим. 3,7 при 10× разведении, рН 7,2 при 650 нм. Всего объем посевного материала 250 мл. Состав среды 2YT (расчет составлен на 1 литр): Триптон (микробиологический Диаэм) - 20 гр; Дрож. экстракт (Дао-Фуд WY-30) - 12,8 гр; MgCl2 - 100 мг; NaCl - 5 гр; K2HPO4 - 1 гр; Цистеин - 100 мг и рН=7,4-7,5. Среда стерилизовали в автоклаве при 0,5 атм, 20 мин.
Выращивание культуры в реакторе. Процесс выращивания проводили в реакторе БИОР 0,003, с рабочим заполнением 2 л. Реактор перед приготовлением среды обрабатывали дезинфицирующим раствором и тщательно промывали стерильной водой. Ферментер 3 литровый. Объем среды 2 л. Стерилизовали ферментер без среды при 131°С (2,1 бар), 40 мин. 126°С (0,6 бар), 60 мин. Среду стерилизовали в бутыли с отводом при 126°С (0,6 бар), 60 мин. Среда вводится отдельно через колбу с отводом, аэрация над средой СО2. Целевая культура имеет форму палочек с закруглением на конце. Грамположительные. Расположенные одиночно, некоторые стоят в коротких цепях. В процессе культивирования производили титрование рН 1%-ным раствором NH4OH. Каждые 12 часов отбирали стерильно пробы объемом 2 мл. Пробы центрифугировали при 5000 об/мин в течение 15 мин. Соблюдая условия асептики, отбирали надосадочную жидкость в объеме 0,03 мл и закапывали в лунки на заранее приготовленных чашках Петри (агароза+желатин). Чашки помещали в термостат при 37°С с экспозицией 12 часов.
Активность вещества оценивали по диаметру ареала вокруг лунок на чашке Петри. Продолжительность культивирования свыше 12 часов не влияла на активность целевого вещества, диаметр ареола по истечении 12 и 24 часов составил 23 мм, диаметр контрольного образца составил 23 мм. OD600 при 12 часовом культивировании составила 1.48, при 24 часах культивирования - 2,86.
После культивирования была проведена аналитическая оценка синтеза коллагеназы с помощью коллагена, меченого FITC. В качестве контроля была использована коллагеназа Cl. histolyticum (StemCell Inc.). Синтез коллагеназы составил на 12 часов - 0,85 мг/мл и на 24 часа - 0,93 мг/мл культурального фильтрата.
Таким образом, штамм Clostridium sporogenes В-14642 позволяет получить коллагеназу от 0,85 до 0,93 мг в миллилитре культурального фильтра при культивировании от 12 до 24 часов в анаэробных условиях при 37°С на среде с триптоном и дрожжевым экстрактом для использования в клеточных технологиях и в медицине. При этом используются стандартизированные промышленные и лабораторные питательные среды.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="последовательность
Clostridium sporogenes.xml" softwareName="WIPO Sequence"
softwareVersion="2.1.1" productionDate="2024-07-16">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText></ApplicationNumberText>
<FilingDate>2024-07-05</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1</ApplicantFileReference>
<ApplicantName languageCode="ru">Федеральное государственное
бюджетное научное учреждение "Российский научный центр хирургии
имени академика Б.В. Петровского" </ApplicantName>
<ApplicantNameLatin>Federal State Budgetary Scientific Institution
"Russian Scientific Center of Surgery named after academician
B.V. Petrovsky" </ApplicantNameLatin>
<InventionTitle languageCode="ru">Штамм Clostridium Sporogenes
B-14642 - продуцент коллагеназы</InventionTitle>
<SequenceTotalQuantity>1</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>1363</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1363</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Clostridium
sporogenes</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gcggacgggtgagtaacacgtgggtaacctgcctcaaagtgggggatag
ccttccgaaaggaagattaataccgcataacataagagaatcgcatgattaacttatcaaagatttattg
ctttgagatggacccgcggcgcattagctagttgctaaggtaacggcttaccaaggcaacgatgcgtagc
cgacctgagagggtgatcggccacattggaactgagacacggtccagactcctacgggaggcagcagtgg
ggaatattgcgcaataggggaaaccctgacgcagcaacgccgcgtgggtgatgaaggtcttcggattgta
aagccctgttttctgggacgataatgacggtaccagaggaggaagccacggctaactacgtgccagcagc
cgcggtaatacgtaggaggcgagcgttgtccggatttactgggcgtaaagggtgcgtaggcggatgttta
agtgggatgtgaaatccccgggcttaacctgggggctgcattccaaactggatatctagagtgcaggaga
ggaaagcggaattcctagtgtagcggtgaaatgcgtagagattaggaagaacaccagtggcgaaggcggc
tttctggtctgtaactgacgctgaggcacgaaagcgtgggtagcaaataggattagataccctggtagtc
cacgccgtaaacgatggatactaggtgtagggggtatcaactccccctgtgccgcagttaacacaataag
tatcccgcctggggagtacggtcgcaagattaaaactcaaaggaattgatgggggcccgcacaagcagcg
gagcatgtggtttaattcgaagcaacgcgaagaaccttacctggacttgacatcccttgcatagcctaga
gataggtgaagcccttcggggcaaggagacaggtggtgcatgcttgtcgtcagctcgtgtcgtgagatgt
taggttaagtcctgcaacgagcgcaacccttgttataagttgctaccattaagttgagcactctaatgag
actgcctgggtaaccaggaggaaggtggggatgacgtcaaatcatcatgccccttatgtccagggctaca
cacgtgctacaatgctaggtacaataagacgcaagaccgtgacgtggagcaaaacttataaaacctatct
cagttcggattgcaggctgcaactcgcctacatgaagcaggagttgctagtaatcgcgaatcagaatgtc
gcggtgaatacgttcccgggccttgtacacaccgcccgtcacaccatgagagctggtaacacccgaagtc
cgtgaggtaaccgtaaggagccagcggccgaaggtgggattagtgattggggtg</INSDSeq_sequen
ce>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ CLOSTRIDIUM HISTOLYTICUM - ПРОДУЦЕНТ КОЛЛАГЕНАЗЫ | 2018 |
|
RU2684220C1 |
| ШТАММ HAEMOPHILUS INFLUENZAE SPB ТИП В - ВЫСОКОАКТИВНЫЙ ПРОДУЦЕНТ КАПСУЛЬНОГО ПОЛИСАХАРИДА ПОЛИРИБОЗИЛРИБИТОЛФОСФАТА | 2016 |
|
RU2624014C1 |
| Композиция антибактериальная для продления срока годности охлажденной рыбы и снижения риска возникновения инфекций, передаваемых пищевым путем, штаммы бактериофагов, используемые для ее получения | 2016 |
|
RU2644667C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНАЗЫ | 1999 |
|
RU2180002C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА КОЛЛАЛИЗИН&αχιρχ;, ЛИОФИЛИЗАТА ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРА ДЛЯ МЕСТНОГО И ПАРЕНТЕРАЛЬНОГО ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ФИБРОПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2687973C1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 2F9-ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К ЛИЗОСТАФИНУ И ИНГИБИРУЮЩИХ ЕГО ЛИТИЧЕСКУЮ АКТИВНОСТЬ | 2013 |
|
RU2525663C1 |
| ШТАММ Bacillus lentus - ПРОДУЦЕНТ БАКТЕРИОЦИНОПОДОБНОЙ СУБСТАНЦИИ АНТИМИКРОБНОГО ДЕЙСТВИЯ И СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОЦИНОПОДОБНОЙ СУБСТАНЦИИ | 2013 |
|
RU2530552C1 |
| Штамм Bacillus mojavensis Lhv-97, обладающий фунгицидной и бактерицидной активностью | 2017 |
|
RU2648163C1 |
| ШТАММ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 1G7 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К БОТУЛИНИЧЕСКОМУ ТОКСИНУ ТИПА В | 2014 |
|
RU2571208C1 |
| ШТАММ ENTERОCOCCUS MUNDTII, ПРОДУЦИРУЮЩИЙ СУБСТАНЦИЮ ПЕПТИДНОЙ ПРИРОДЫ С АНТИЛИСТЕРИОЗНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532227C1 |
Изобретение относится к области биотехнологии и представляет собой штамм Clostridium sporogenes В-14642, обладающий способностью синтезировать секретируемую коллагеназу от 0,85 до 0,93 мг/мл культурального фильтра при культивировании от 12 до 24 часов в анаэробных условиях при 37°С на среде с триптоном и дрожжевым экстрактом. Штамм депонирован в Государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ - Оболенск» ФБУН «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Изобретение обеспечивает расширение арсенала штаммов микроорганизмов, обладающих способностью к продуцированию коллагеназы. 1 ил., 1 табл., 1 пр.
Штамм Clostridium sporogenes B-14642, обладающий способностью синтезировать секретируемую коллагеназу от 0,85 до 0,93 мг/мл культурального фильтра при культивировании от 12 до 24 часов в анаэробных условиях при 37°С на среде с триптоном и дрожжевым экстрактом и депонированный в Государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ - Оболенск» ФБУН «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека.
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНАЗЫ | 1999 |
|
RU2180002C2 |
| ШТАММ CLOSTRIDIUM HISTOLYTICUM - ПРОДУЦЕНТ КОЛЛАГЕНАЗЫ | 2018 |
|
RU2684220C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОЙ КОЛЛАГЕНАЗЫ | 2008 |
|
RU2389794C2 |
| US 20120237497 A1, 20.09.2012 | |||
| Способ получения гидропроизводных нафтопиранов | 1973 |
|
SU468411A3 |
| WO 2019052586 A1, 21.03.2019 | |||
| DE 69114935 T2, 30.05.1996. | |||
Авторы
Даты
2025-02-21—Публикация
2024-07-18—Подача