Известен способ получения коллагеназы путем культивирования штамма Clostridium histolyticum 468 в казеиново-соево-пепсиновой среде. Культивирование проводили в ферментере объемом 160 л в течение 72 ч при 37°С в среде следующего состава (г/л): гидролизат казеина и соевого шрота - 969, NaH2PO4 - 1,5, K2НРO4 - 1,5, пиридоксин - 0,0020, рибофлавин - 0,0020, тиамина бромид - 0,0020, фолиевая кислота - 0,0020, пантотенат кальция - 0,0020, никотиновая кислота - 0,0020, липоевая кислота - 0,0020, биотин - 0,0010. Фермент очищали и концентрировали на ультрафильтрационных мембранах с порогом задержания веществ по молекулярной массе 50 кДа, полученный концентрат лиофильно высушивали. Активность 1 мг готового препарата составляла 0,20-0,25 ед. лейцина за 20 мин инкубации в реакционной смеси (патент RU 2180002 опубликован в 2002 г., с 17.05.2011 патент прекратил действие). Недостатком данного способа является сложность использования данной питательной среды в промышленных масштабах, а именно в необходимости предварительной подготовки соевого шрота, а также в использовании дорогостоящих витаминов и необходимости многократной отмывки коллагеназы.
Описан еще один способ получения коллагеназы путем культивирования С. histolyticum (патент WO 2007/089851 А2). В отличии от нашей технологии очистка препарата ведется с использованием ультрафильтрации с размером пор 10 кДа, что позволяет отделить только олигопептиды и небольшие белки. Другим отличием является применение ионообменной хроматографии на колонке с Q-Sepharose HP. Это более дорогой способ, по сравнению с предложенной нами гель-фильтрацией, которая более эффективно разделяет белки по молекулярной массе, что особенно важно при получении высокомолекулярных белков, таких как коллагеназа.
В 2017 году ФГУП СПбНИИВС ФМБА России разработан способ получения Коолализина® в виде высокоочищенного препарата с высокой активностью комплекса коллагеназ, основанный на культивировании Clostridium histolyticum 468 или оригинального продуцента Clostridium histolyticum SK В-8362 на среде Рамона с последующим усовершенсвованием технологии выделения, концентрирования и очистки фракций, содержащих коллагеназы. По сравнению с ранее использованными способами получения препарата коллагеназы путем культивирования продуцента Clostridium histolyticum штамм 468 на бульоне Рамона с добавлением 1% (по объему) глюкозы с последующим осаждением 60% сульфатом аммония и очисткой методом гельфильтрации на колонке, заполненной сефадексом G-100 (Авторское свидетельство 694534, кл. С12D 13/10, 1979) культуральная жидкость подвергается очистке через каскад глубинных фильтров с диаметром пор от 3,0-0,8 до 0,3-0,1 мкм. С целью исключения попадания клеток культуры в нативный раствор введена дополнительная номинальная и абсолютная фильтрация через стерилизующие фильтры 0,2 мкм. Все это в комплексе позволяет получать нативный раствор освобожденный от бактериальной массы с минимальными потерями по коллагеназной активности и исключает риск попадания культуры в нативный раствор. Выделение и концентрирование фермента методом тангенциальной ультрафильтрации нативного раствора исключает стадию высаливания белков сульфатом аммония. Концентрирование проводят в 15 раз от исходного объема с одновременным разделением продукта на мембранах 50 кДа на необходимые фракции белков. Замена стадии высаливания белков на ультрафильтрацию значительно сокращает время основных технологических и вспомогательных операций с 26 часов до 2-3 часов, а также исключает использование в производством процессе аммонийной соли серной кислоты, с необходимостью последующего отделения ее от целевого белка центрифугированием. Использование мембран в 50 кДа позволяет получать продукт с отсечением балластных веществ (липидов, нуклеиновых кислот, низкомолекулярных комплексов), а также значительно осветлять раствор концентрата коллагеназ.
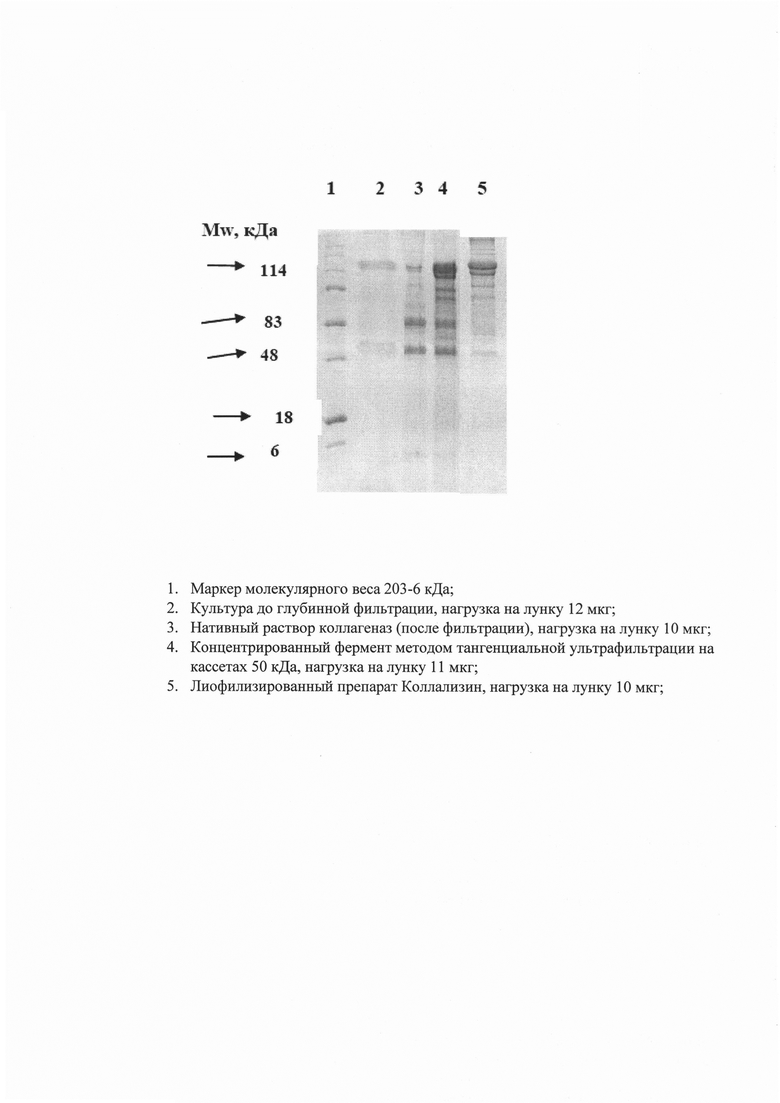
Дополнительная микрофильтрация концентрата через фильтр 0,45 мкм и очистка гель-хроматографией с применением современного сорбента Sephacryl S-100, позволяет получать высокоочищенный препарат, содержащий комплекс коллагеназ с высокой активностью. Включение стадии фильтрации через мембранные фильтры 0,45 мкм значительно снижает биологическую нагрузку на сорбент при хроматографической очистке, а замена геля Sephadex G-100 на современный Sephacryl S-100 позволило увеличить скорость фильтрации в 10 раз. Очищенный концентрат коллагеназ подвергают концентрированию в 10 раз на кассете с отсечением 5 кДа. На рисунке представлены результаты электрофореза белков коллагеназ в промежуточных продуктах на различных стадиях очистки и в лиофилизированном препарате. Как видно из данных, представленных на рисунке 1, все проведенные мероприятия при постадийном подходе к усовершенствованию технологии позволили получить высокоочищенный препарат при сохранении высокой коллагеназной активности.
Пример получения Коллализина®.
Для получения данного препарата культивируют штамм Clostridium histolyticum 468 или оригинальный продуцент Clostridium histolyticum SK В-8362. Запаянную пробирку со штаммом культуры на полужидком агаре вскрывают и ее содержимое пипеткой переносят в 10 пробирок (по 1,0 мл в каждую), содержащих среду Рамона, предварительно прогретой до 60-70°С. Пробирки с культурой выдерживают в термостате при температуре (37±1)°С в течение (24±2) ч. По истечении времени путем визуального контроля и микроскопии отбирают пробирки с наиболее хорошим ростом чистой культуры. Отобранные образцы культуры пересевают на пробирки с 20 мл среды Рамона, предварительно прогретые до 60-70°С из расчета 5 мл культуры на 1 пробирку. Пробирки с внесенной культурой выдерживают в термостате при температуре (37±1)°С в течение (24±2) ч. Полученный посевной материал используют для получения культуральной жидкости. В качестве питательной среды используют бульон Рамона, содержащий пептон Рамона, мясной экстракт 1:1, натрий хлористый, кровь говяжью сухую, воду очищенную.
Стерильный бульон Рамона, содержащей глюкозу в оптимальной для выращивания культуры концентрации, перед посевом подогревают до температуры 60-70°С и засевают посевной материал. Питательную среду с культурой выдерживают при температуре (37±1)°С при оптимальной длительности культивирования, обеспечивающем синтез фермента с максимальной коллагеназной активностью. По окончании процесса биосинтеза фермента производят отбор проб для микроскопии и определения коллагеназной активности качественной реакцией (измеряют оптическую плотность фильтрата лизированного коллагена при длине волны 510 нм).
Нативный раствор получают отделением микробной массы из культуральной жидкости с помощью фильтрации через каскад глубинных фильтров с диаметром пор от 3,0-0,8 до 0,3-0,1 мкм. Попадание клеток культуры в продукт исключает использование капсул для номинальной и абсолютной стерилизации (0,2 мкм).
Полученный фильтрат подают на установку тангенциальной фильтрации с кассетами 50 кДа. К раствору добавляют двукратный объем воды для инъекций, доводят значение рН до 7,18 при помощи 1 М NaOH и концентрируют на ультрафильтрационной установке при помощи мембран с размером пор 50 к Да в 15 раз от исходного объема. В полученном концентрате контролируют содержание белка по методу Лоури и по методу Бредфорда, коллагеназную активность, чистоту целевого белка.
Предварительную очистку проводят методом микрофильтрации на мембранах с размером пор 0,45 мкм.
Полученный концентрат, содержащий смесь коллагеназ, очищают методом гель-фильтрации на хроматографической колонке, размером 108*950 мм заполненной сорбентом на основе Sephacryl S-100. Элюцию проводят фосфатно-буферным раствором (рН 7,2±0,2). Концентрат подают со скоростью 4,0-6,0 л/ч, при температуре (5±3)°С. Начало сбора фракций определяют по результатам измерений оптической плотности элюата при длине волны 280 нм. Сбор осуществляют до начала выхода пигмента. Очищенный препарат, содержащий смесь высокоактивных коллагеназ, подвергают концентрированию на ультрафильтрационной установке при помощи мембран с размером пор 5 кДа в 10 раз от исходного объема, затем стерилизуют с использованием мембранных фильтров с размером пор 0,2 мкм. Разливают в ампулы или флаконы и лиофильно высушивают.
Способ позволяет получить препарат, обладающий коллагеназной активностью равной не менее 10000 КЕ в ампуле или флаконе и сохраняющий стабильность всех показателей качества в течение установленного срока годности (2 года).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООЧИЩЕННОГО КОНЦЕНТРИРОВАННОГО ПРЕПАРАТА С КОЛЛАГЕНАЗНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2781289C1 |
| ШТАММ CLOSTRIDIUM HISTOLYTICUM - ПРОДУЦЕНТ КОЛЛАГЕНАЗЫ | 2018 |
|
RU2684220C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ПРОТЕОЛИТИЧЕСКОГО ФЕРМЕНТА ТЕРРИЛИТИНА | 2015 |
|
RU2584601C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНАЗЫ | 1999 |
|
RU2180002C2 |
| Штамм Clostridium sporogenes B-14642 - продуцент коллагеназы | 2024 |
|
RU2835110C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНОЛИТИЧЕСКОГО ФЕРМЕНТА | 2020 |
|
RU2758788C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА КОЛЛАГЕНАЗЫ | 2003 |
|
RU2265052C2 |
| Способ получения вакцины гемофильной тип b конъюгированной | 2019 |
|
RU2704452C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕОЛИТИЧЕСКОГО ПРЕПАРАТА ДЛЯ ГИДРОЛИЗА СТРУКТУРНЫХ БЕЛКОВ | 2003 |
|
RU2244741C1 |
| ШТАММ Bacillus licheniformis БСТ-1-ПРОДУЦЕНТ ПЕНИЦИЛЛИНАЗЫ И СПОСОБ ПОЛУЧЕНИЯ ПЕНИЦИЛЛИНАЗЫ | 2002 |
|
RU2221041C1 |
Изобретение относится к биотехнологии и медицине, в частности к промышленной технологии получения ферментного препарата Коллализин® для использования в медицинских целях. Способ получения Коллализина® путем культивирования продуцента Clostridium histolyticum в анаэробных условиях на питательной среде Рамона с последующим отделением микробной массы путем фильтрации, при этом для культивирования используют продуцент Clostridium histolyticum 468 или продуцент Clostridium histolyticum SK В-8362, а отделение микробной массы проводят с помощью каскада глубинных фильтров с диаметром пор от 3,0-0,8 до 0,3-0,1 мкм с исключением попадания культуры в нативный раствор, применяя номинальную и абсолютную стерилизующую фильтрацию нативного раствора с дальнейшей ультрафильтрацией, концентрированием и хроматографической очисткой на основе сорбента Sephacryl S-100. Применение Коллализина® для лечения фибропролиферативных заболеваний. Вышеописанный способ получения позволяет получить препарат, обладающий высокой коллагеназной активностью и сохраняющий стабильность всех показателей качества в течение установленного срока годности 2 года. 2 н. и 4 з.п. ф-лы, 1 ил., 1 пр.
1. Способ получения Коллализина® путем культивирования продуцента Clostridium histolyticum в анаэробных условиях на питательной среде Рамона с последующим отделением микробной массы путем фильтрации, отличающийся тем, что для культивирования используют продуцент Clostridium histolyticum 468 или продуцент Clostridium histolyticum SK В-8362, а отделение микробной массы проводят с помощью каскада глубинных фильтров с диаметром пор от 3,0 - 0,8 до 0,3 - 0,1 мкм с исключением попадания культуры в нативный раствор, применяя номинальную и абсолютную стерилизующую фильтрацию нативного раствора с дальнейшей ультрафильтрацией, концентрированием и хроматографической очисткой на основе сорбента Sephacryl S-100.
2. Способ по п. 1, отличающийся тем, что коллагеназу очищают и концентрируют в 15 раз, применяя тангенциальную ультрафильтрацию с кассетами 50 кДа.
3. Способ по п. 1 или п. 2, отличающийся тем, что вводят стадию микрофильтрации с размером пор 0,45 мкм концентрата коллагеназ перед подачей на хроматографическую колонку.
4. Способ по п. 1, отличающийся тем, что использование сорбента Sephacryl S-100 увеличивает скорость фильтрации в 10 раз.
5. Способ по п. 1 или 2, отличающийся тем, что добавляют стадию концентрирования очищенного концентрата коллагеназ в 10 раз на ультрафильтрационной установке с применением кассет 5 кДа.
6. Применение Коллализина®, полученного способом по п.1, для лечения фибропролиферативных заболеваний.
| Способ получения коллагеназы | 1978 |
|
SU694534A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНАЗЫ | 1999 |
|
RU2180002C2 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2019-05-17—Публикация
2018-04-03—Подача