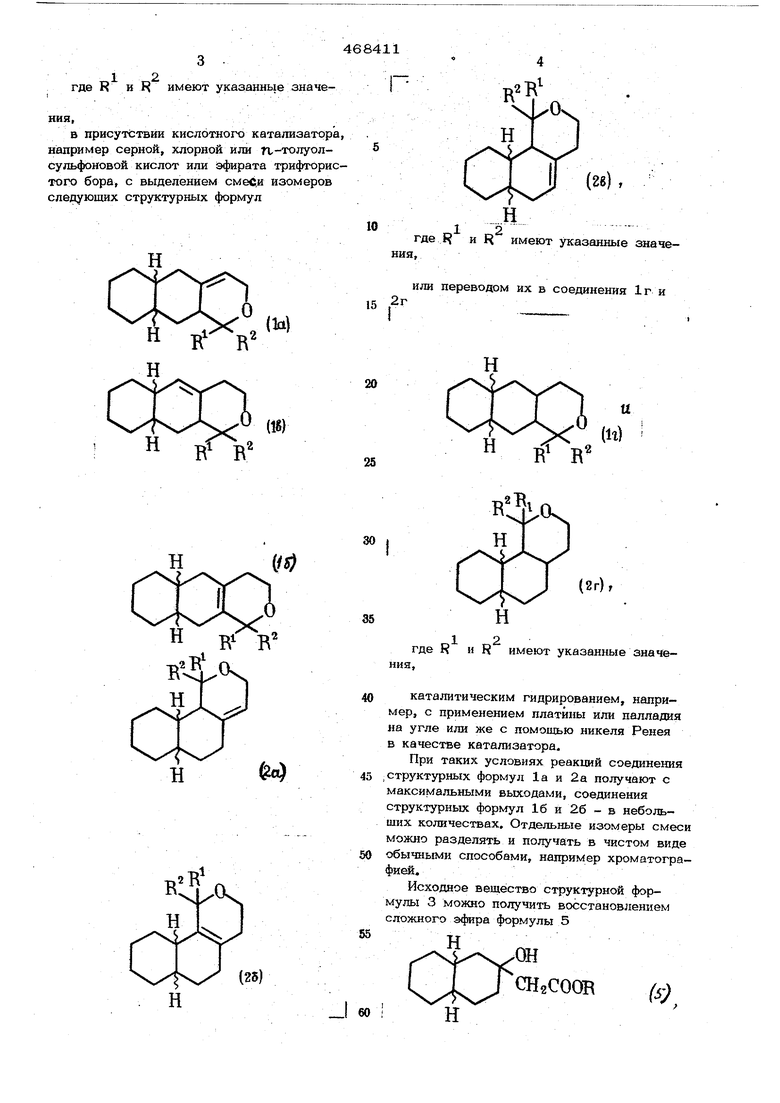
11зоб()етонне относится к способу получения новых соединений - Г1 дропроизводных на4)тони))а)1ов 1 или 2 9 (1) 12 где R и R (каждый) - низшая tinкилъная группа с 1-4 атомами углерода, а 25 нунктярные линии означают факультативную двойную связь, находящуюся у атома углерода 4а. Эти соединения могут найти применение в пщл юмешол промышленности. Снособ основан на известной реакции получения конденсированных ниранов взаимодействием ароматических спиртов с кетонами в присутствии кислотного катали-, затора. Сущность нредлагаемого способа заключается в том, что 2-оксиэтил-2-оксидекалин формулы 3 СН2-СНд,ОН (3) конденсируют с пизгиим диалки/псетоном формулы 4 II г(4) I R-C-R , 46841 12 где R и R имеют указанньш значев присутствии кислотного катализатора, например серной, хлорной или гг-толуол-5 сульфоновой кислот или Эфирата трифтористого бора, с выделением смести изомеров следующих структурных формул
(18)
В R
ния.
или переводом их в соединения 1г и
U
(1г)
1 R 1 2 . де R и R имеют указанные значеН
1 60
12 где R и R имеют указанные значения.
каталитическим гидрированием, например, с применением платины или палладия на угле или же с помощью никеля Ренея в качестве катализатора.
При таких условиях реакций соединения
45 .структурных формул 1а и 2а получают с максимальными выходами, соединения структурных формул 16 и 26 - в небольших количествах. Отдельные изомеры смеси можно разделять и получать в чистом виде
50 обычными способами, нащэимер хроматографией.
Исходное вещество структурной формулы 3 можно получить восстановлением сложного эфира формулы 5
СНгСОШ
.
где i - алкильная группа с 1-6 атомами углерода.
Восстановление осуществляют обычными Способами, в частности обработкой натрием в соответствующем растворителе например безводном этаноле, или диизобутидалюминийгидрйдомГ
Вещество формулы 5 можно получить обработкой смеси цис- и .транс- р -декалонов tf - галогенсложным зефиром формулы 6.
(6),
,
где X - атом галогена, предпочтительн атом брома,
R - алкильная группа с 1-6 атомами углерода, i в присутствии цннка.
I Реакцию можно ускорять добавлением небольщого количества активатора, к ко- торым относятся, например, йод, хлорисг тая и бромистая ртуть или медь. Группа R предпочтительно представляетсобой метиловый или этиловый остатки. .
В примерах описывается получение как целевых продуктов формул 1 и 2, так и исходных продуктов формул 3 и 5.
Пример,, 94 г 2-оксиэтил-2оксидекалина растворяют в 1500 мл ацетона, потом добавляют 30 мл концентрированной серной кислоты, раствор 7 час
выдерживают при комнатной температуре
Затем раствор нейтрализуют ЮЬО мл 9%ного водного раствора бикарбоната натрия, экстрагируют -бензолом и промывают до нейтральной реакции. Образуется 70 г сырого продукта, который после ректифИ кации дает 45 г смеси декагидро-1,1диметил-1Н-нафто()пирана и .деКагидро-1,1 -ДИМ ётил-1 Н-нафтО (1,2-с) пирана структурных формул 1(а-в) к 2 ); ,т.кйп. 88-.90°С/1 мм рт.ст.; П 1,5110 выход--около 4О%.
Исходный продукт можно получить следующим образом,
А. К 112 г электрЪлитнЬто цинкового порошка в бензоле, в который было добавлено несколько кристаллов хлористой ртути, по каплям добавляют несколько миллилитров раствора 228 г Д -декалона, 228 г этилбромацетата и 450 мл безводного бензола. Чтобы вызвать начало реакции, смесь разогревают с обратным холр- дильником, затем добавляют остаток укаванной смеси и еще 2 j4ac HatrpeBaioT.-.c ; обратным холодильником. После охлаждения реакционную смесь ги;чэолизуют 850 мл 10%-ного водного раствора серной кислоты. Смесь-экстрагируют бензолом, бензольную фазу промывают до нейтральной реакции, бензол отгоняю,т и получают 330 г сырого продукта, который после ректификации под давлением 0,5
мм рт.ст. дает 310 г (выход 86%) чистого 2-карб; этоксиметил-2-оксидекалина, Т.КИП7112-115 С/0,5 мм рт.ст,jfi 1,4863;.
В. 86,25 г натрия в виде мелких ку- i очков добавляют в смесь 6О г 2-карбэ- оксиметил-2-оксидекалина и 900 мл безводного этанола. Начинается бурная реакция, вызьюающая нагрев до температуры
ефлегмадаи смеси. .
нагревают с обратным холодальнйком,
охлаждают, добавляют 1 л НО, спирт
.. ,
Отгоняют, остаток растворяют в небольшом ,
количестве теплой воды. После охлаждения
трижды экстрагируют 250 мл диэтиловохх)
эфира. Эфирную фазу промывают до нейтральной реакции и перегоняют. Образуется 4Ог сырого продукта, который после ректификации под давлением 0,5 мм рт.ст.дает 22 г (выход около 42%) 2-оксиэтил-2-оксидекалина, т.кип7138--140 С/0,5 мм рт.ст.В. Раствор 235 г диизобутилалюминийгидрида в 300 мл сухого бензола по каплям добавляют в смесь 12О г 2-карбэт6ксиметил-2-оксидекалина и 120 мл сухого бензола в атмосфере азота. Во время добавления температуру реакционной смеси выдер-
живают при 15-2О С, По окончании добавления еще 2 часа выдерживают при этой температуре, затем охлаждают до и гидролизуют 1500 мл 10%-ного водного раствора серной кислоты. Затем дают нагреться до комнатной температуры, органическую фазу сливают, маточный раствор дважды экстрагируют бензолом по 250 мл. Соединенные бензольные экстракты промывают до нейтральной реакции. После удаления перегонкой растворителя на водяной бане в вакууме .получают сырой продукт, который после ректификации дает 72 г (выход 72%) 2-оксиэтил-2-оксидекалина, т.кип. 147°С/1 мм рт.ст,
Пример 2. 11Ог декагидродиметилнафтопирана (полученного аналогично примеру 1) 8 час гидрируют в 50 мл абсолютного этанола в присутствии 3,3 г 5%-ного
палладия на угле в автоклаве (250 мл) под давлением водорода 80 кг/см при 120°С. После охлаждения и удаления катализатора спирт отгоняют в вакууме и получают 1ОО г сырого продукта, который после ректификации дает 90 г смеси (выход 80%) пергидро-1,1-диметилнафго (2,3-с)пирана и пергищзо-1,1-диметилнафто(1,2-с)пирана, т.кип.-95-96Ос/0,55 мм рт.ст.; П1,5О10.
Предмет изобретения
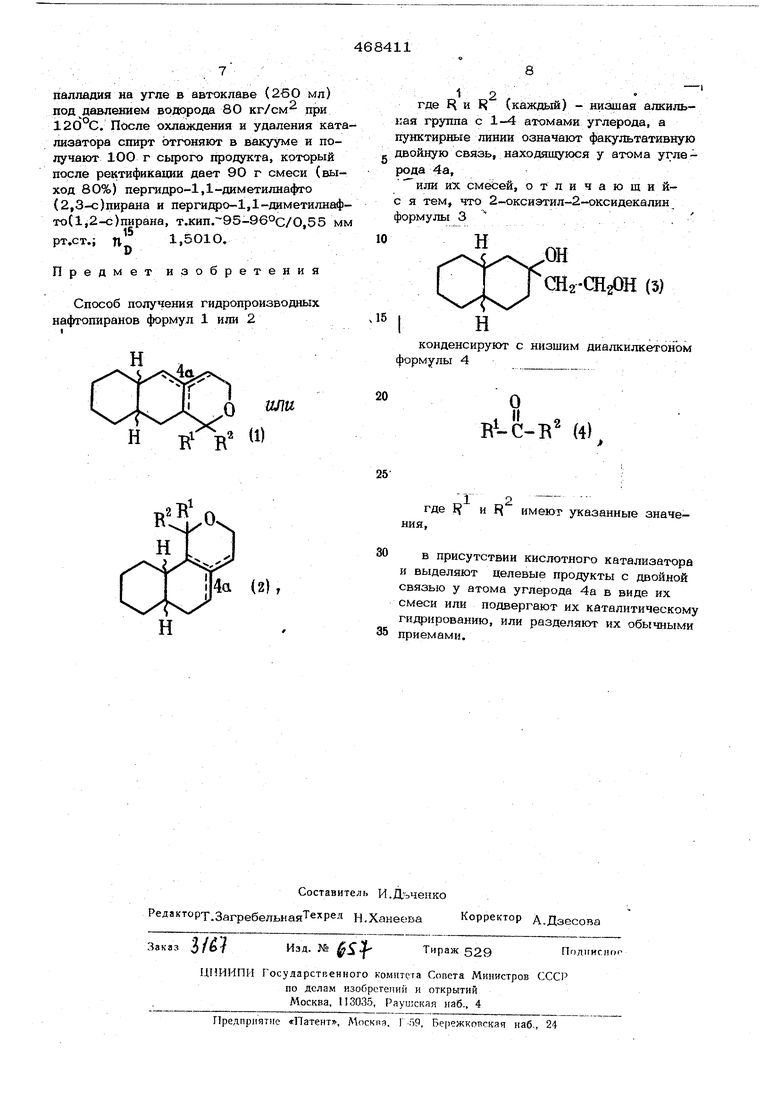
Способ получения гидропроизводных нафюпиранов формул 1 или 2
О или В
1
где R и R (каждый) - низшая алкилькая группа с 1-4 атомами углерода, а пунктирные линии означают факультативную двойную связь, находящуюся у атома угле рода 4а,
или их смесей, отличающийс я тем, что 2-ОКСИЭТИЛ-2-ОКСИ дека ЛИН формулы 3
10Н
I I ГсНг-СНзОН (3)
Н
конденсируют с низшим диалкилкетоном формулы 4
О
1 Н9
(4)

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения транс-5а-арилдекагидро- бЕНзАзЕпиНОВ или иХ СОлЕй | 1977 |
|
SU843743A3 |
| Способ получения производныхциС-4A-фЕНилОКТАгидРО-1H-2-пиРиН-диНА или иХ СОлЕй | 1977 |
|
SU812174A3 |
| Способ получения 4а-арил-цис-декагидроизохинолинов | 1975 |
|
SU682126A3 |
| Способ получения производных 3-алкил-6а,7,8,9,10,10а-гексагидро-6н-дибензо (в,д) пиранов | 1974 |
|
SU524517A3 |
| СЕРУЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МЕВИНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2041205C1 |
| ЦИКЛОПЕНТАДИЕНИЛЬНЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2159758C2 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДИБЕНЗОЦИКЛОГЕПТАДИЕНА | 1972 |
|
SU335824A1 |
| Способ получения производных циклопропана | 1967 |
|
SU691076A3 |
| Способ получения производных 2-окси-3-аминопропана или их -окисей или солей | 1974 |
|
SU659089A3 |

4а (2),
где J и Я имеют указанные значения,
в присутствии кислотного катализатора и выделяют целевые продукты с двойной связью у атома углерода 4а в виде их смеси или подвергают их каталитическому гидрированию, или разделяют их обычными приемами.
Авторы
Даты
1975-04-25—Публикация
1973-02-16—Подача