Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2-амино-4,6-динитрофенола в биологическом материале, и может быть использовано в практике химико-токсикологических, экспертно-криминалистических и клинических лабораторий. Способ относится к числу массовых.
Известен способ определения алкилдинитрофенолов в биологическом материале, который заключается в том что биологический объект обрабатывают при перемешивании трижды по 30 минут порциями ацетона. объём каждой из которых численно в два раза превышает массу биологического объекта, полученные ацетоновые излечение объединяют, испаряют до сухого остатка в токе воздуха при комнатной температуре, остаток растворяют в гексане, полученный раствор трижды экстрагируют щелочным раствором (универсальный буфер с рН 11,98, разбавленный водой в четыре раза) при соотношении объёмов органической и водной фаз 1:1, щелочные экстракты отделяют, объединяют, подкисляют 24%-ным раствором хлороводородной кислоты до рН 2-3, экстрагируют порциями диэтилового эфира трижды при соотношении водной и органической фаз 1,5-2:1 по объёму, эфирные извлечения объединяют, эфир испаряют, сухой остаток растворяют в ацетоне, часть этого раствора наносят на линию старта хроматографической пластины типа Силуфол UV-254, хроматографируют в системе растворителей хлороформ-гексан в соотношении 7:4 по объёму, анализируемое вещество идентифицируют по величине Rf, извлекают из сорбента диметилформамидом и определяют спектрофотометрическим методом по интенсивности светопоглощения элюата, используя уравнение калибровочного графика (А. с. 1786426 SU. G01N31/00 (2006.01); G01N30/90 (2006.01). Способ определения алкилдинитрофенолов в биологическом материале / Шорманов В.К., Нестерова А.В. (SU). – № 4884097/04; заявл. 19.11.1990; опубл. 07.01.1993, Бюл. № 1. – 11 с.).
Способ характеризуется недостаточно высокой чувствительностью.
Известен способ определения 4-нитрофенолов в биологическом материале, состоящий в том, что биологическую ткань измельчают, трижды по полчаса настаивают с порциями уксусного ангидрида, масса каждой из которых численно в два раза превышает массу биоматериала, извлечения отделяют от твёрдых частиц биоматериала, объединяют, испаряют до половины объема, разбавляют водой в объемном соотношении 1:3, экстрагируют диэтиловым эфиром, насыщенным водой, экстрагент испаряют, полученный остаток растворяют в хлороформе, экстрагируют водно-щелочным раствором при pH 9,0-9,5, экстракт отделяют, подкисляют до pH 2-3, повторно экстрагируют диэтиловым эфиром, насыщенным водой, полученный экстракт отделяют, экстрагент испаряют до сухого остатка, который затем растворяют в хлороформе и подвергают хроматографическому определению методом высокоэффективной жидкостной хроматографии в колонке, заполненной силикагелем "Силасорб 600" с размером частиц 5 мкм, с использованием в качестве подвижной фазы системы растворителей, состоящей из гексана и пропанола-2, взятых в объемном соотношении 20:1 (Пат. 2121681 RU. G01N 33/50 (2006.01). Способ определения 4-нитрофенолов в биологическом материале / Шорманов В.К.; заявитель и патентообладатель: Шорманов В.К. (RU). – № 94021200/14; заявл. 07.06.1994; опубл. 10.11.98, Бюл. № 31. – 7 с.).
Способ характеризуется недостаточно высокой чувствительностью.
Наиболее близким является способ определения 2-амино-4,6- динитрофенола в биологическом материале, заключающийся в том, что биологический объект измельчают, двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 1:1 по объёму, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, растворитель из объединенного извлечения испаряют в токе воздуха комнатной температуры, остаток растворяют в ацетоне, ацетоновый раствор наносят на пластину «Сорбфил» ПТСХ-АФ-А с УФ-индикатором, хроматографируют, используя двухкомпонентную подвижную фазу ацетон-хлороформ в отношении 7:3 по объёму, анализируемое вещество извлекают из хроматограммы диметилформамидом и проводят определение физико-химическим методом, которым является спектрофотометрия, по интенсивности светопоглощения элюата, измеряемой в области 489 нм. (Погосян, Н.Г. Исследование сохраняемости 2-амино-4,6-динитрофенола в биологическом материале при хранении в различных температурных режимах // Химия и химическая технология в XXI веке: материалы XXII научно-практической конференции студентов и молодых ученых (Томск, 17-20 мая 2021 г.). – Томск: ФГАОУ ВО НИ ТПУ, 2021. – Т. 1. – С. 323-324.).
Способ характеризуется недостаточно высокой чувствительностью определения.
Техническим результатом настоящего изобретения является повышение чувствительности определения 2-амино-4,6-динитрофенола в образце тканей или органов.
Технический результат достигается тем, что биологический объект измельчают, двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 6:4 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, растворитель из объединенного извлечения испаряют в токе воздуха комнатной температуры, остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, остаток растворяют в смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему, хроматографируют в полупрепаративной колонке с силикагелем «Меrck» 40/63 мкм, используя двухкомпонентную подвижную фазу ацетон-диэтиловый эфир в отношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают уксусном ангидридом в условиях кипячения при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют в токе азота до сухого остатка, остаток растворяют в этилацетате и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия, в капиллярной колонке HP-5MS длиной 30 м и внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) диметилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм, используя газ-носитель гелий, подаваемый со скоростью 1,0 мл/мин, и масс-селективный детектор, работающий в режиме электронного удара, начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола, исходя из площади хроматографического пика его О-ацетильного производного.
Способ осуществляется следующим образом: биологический объект, содержащий 2-амино-4,6-динитрофенол, измельчают, двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 6:4 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта полученные органические извлечения объединяют, растворитель из объединенного извлечения испаряют в токе воздуха комнатной температуры, остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, остаток растворяют в смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему, хроматографируют в полупрепаративной колонке с силикагелем «Меrck» 40/63 мкм, используя двухкомпонентную подвижную фазу ацетон-диэтиловый эфир в отношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают уксусном ангидридом в условиях кипячения при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют в токе азота до сухого остатка, остаток растворяют в этилацетате и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия, в капиллярной колонке HP-5MS длиной 30 м и внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) диметилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм, используя газ-носитель гелий, подаваемый со скоростью 1,0 мл/мин, и масс-селективный детектор, работающий в режиме электронного удара, начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола, исходя из площади хроматографического пика его О-ацетильного производного.
Способ иллюстрируется следующими примерами.
Пример 1
Определение 2-амино-4,6-динитрофенола в ткани печени
К 10 г измельчённой до размеров частиц 0,2-0,5 мм ткани печени прибавляют 10 мг 2-амино-4,6-динитрофенола, тщательно перемешивают биологический объект с веществом и оставляют на 1,5 часа при температуре 18-22оС. По истечении указанного времени биологический объект двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 6:4 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси ацетон-ацетонитрил в отношении 6:4 по объему и выдерживают 30 минут при периодическом перемешивании. Извлечение отделяют от твёрдых частиц биоматериала, операцию настаивания повторяют в указанных условиях.
Полученные органические извлечения объединяют, растворитель из объединённого извлечения испаряют в токе воздуха комнатной температуры, остаток неоднократно (трижды по 3 минуты) обрабатывают порциями ацетона по 15 мл каждая при энергичном перемешивании, извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, остаток растворяют в 4 мл смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему. Полученный раствор вносят в хроматографическую полупрепаративную колонку размерами 490×11 мм, заполненную 10 г силикагеля «Меrck» 40/63 мкм. Хроматографируют, элюируя двухкомпонентной подвижной фазой ацетон-диэтиловый эфир в отношении 6:4 по объему. Элюат собирают отдельными фракциями по 2 мл каждая.
Фракции элюата с 9 по 36 включительно, содержащие анализируемое вещество, объединяют, элюент испаряют в токе воздуха при температуре 18-22оС, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают 5 мл уксусного ангидрида, образующийся раствор количественно переносят в коническую колбу вместимостью 25 мл и кипятят с прямым холодильником при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют из реакционного раствора в токе азота до сухого остатка, остаток растворяют в 10 мл этилацетата (раствор А). 0,5 мл раствора А вносят в мерную колбу вместимостью 25 мл, доводят этилацетатом до метки (раствор Б) и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия.
В процессе определения 4 мкл раствора Б вводят в хромато-масс-спектрометр.
Определение проводят, используя хромато-масс-спектрометр Shimadzu GCMS-QP2010 Ultra.
Хроматографирование осуществляют в капиллярной колонке HP-5MS длиной 30 м, внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) метилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм.
Начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола по площади хроматографического пика его О-ацетильного производного.
В качестве газа-носителя используется гелий. Подача газа-носителя производится со скоростью 1 мл/мин. Режим с делением потока 1:2. Масс-селективный детектор работает в режиме электронного удара (70 эВ). Регистрация масс-спектра проводится по полному ионному току с задержкой 2,9 минуты. Диапазон сканирования составляет 40-600 m/z.
Пик на хроматограмме с временем удерживания 8,07 мин соответствует О-ацетильному производному 2-амино-4,6-динитрофенола. В масс-спектре данного соединения, снятому по полному ионному току, обнаруживаются сигналы ряда характеристических заряженных частиц с массовыми числами 50, 62, 90, 119, 131, 177, 193, 223. Наиболее интенсивной является частица с массовым числом 223, интенсивность которой принимается за 100 %.
2-амино-4,6-динитрофенол идентифицируют по сочетанию времени удерживания соответствующего О-ацетильного производного в неподвижной фазе колонки и специфического набора сигналов характеристических заряженных частиц в его масс-спектре.
Количество 2-амино-4,6-динитрофенола вычисляют, исходя из площади хроматографического пика, соответствующего его О-ацетильному производному и полученного при регистрации интенсивности по полному ионному току, а затем пересчитывают на навеску анализируемого вещества, внесённую в биологический материал.
Построение градуировочного графика
В ряд мерных колб вместимостью 25 мл вносят 0,8, 1,6, 2,4, 5,0 мл 0,125% раствора и 1,0, 2,0, 3,0, 4,0, 6,0, 8,0 и 10,0 мл 1,25% раствора 2-амино-4,6-динитрофенола в этилацетате и доводят объём содержимого каждой колбы до метки этилацетатом. 0,1 мл каждого из растворов вносят в выпарительную чашку и испаряют в токе воздуха при комнатной температуре до сухого остатка.
Остаток обрабатывают 5 мл уксусного ангидрида, образующийся раствор количественно переносят в коническую колбу вместимостью 25 мл и кипятят с прямым холодильником при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют из реакционного раствора в токе азота до сухого остатка, остаток растворяют в 10 мл этилацетата.
4 мкл каждого из полученных растворов вводят в хромато-масс-спектрометр.
Определение проводят, используя хромато-масс-спектрометр Shimadzu GCMS-QP2010 Ultra.
Хроматографирование осуществляют в капиллярной колонке HP-5MS длиной 30 м, внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) метилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм.
Начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола по площади хроматографического пика его О-ацетильного производного.
В качестве газа-носителя используется гелий. Подача газа-носителя производится со скоростью 1 мл/мин. Режим с делением потока 1:2. Масс-селективный детектор работает в режиме электронного удара (70 эВ). Регистрация масс-спектра проводится по полному ионному току с задержкой 2,9 минуты. Диапазон сканирования составляет 40-400 m/z.
По результатам измерений на хромато-масс-спектрометре строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 8,0⋅10-10 – 1,0⋅10-7 г.
Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
S = 1113552⋅C - 25939,
где S – площадь хроматографического пика; C – концентрация определяемого вещества в хроматографируемой пробе, нг.
Результаты количественного определения 2-амино-4,6-динитрофенола в ткани печени представлены в таблице 1.
Пример 2
Определение 2-амино-4,6-динитрофенола в ткани лёгких
К 10 г измельчённой до размеров частиц 0,2-0,5 мм ткани лёгких прибавляют 10 мг 2-амино-4,6-динитрофенола, тщательно перемешивают биологический объект с веществом и оставляют на 1,5 часа при температуре 18-22оС. По истечении указанного времени биологический объект двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 6:4 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси ацетон-ацетонитрил в отношении 6:4 по объему и выдерживают 30 минут при периодическом перемешивании. Извлечение отделяют от твёрдых частиц биоматериала, операцию настаивания повторяют в указанных условиях.
Полученные органические извлечения объединяют, растворитель из объединённого извлечения испаряют в токе воздуха комнатной температуры, остаток неоднократно (трижды по 3 минуты) обрабатывают порциями ацетона по 15 мл каждая при энергичном перемешивании, извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, остаток растворяют в 4 мл смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему. Полученный раствор вносят в хроматографическую полупрепаративную колонку размерами 490×11 мм, заполненную 10 г силикагеля «Меrck» 40/63 мкм. Хроматографируют, элюируя двухкомпонентной подвижной фазой ацетон-диэтиловый эфир в отношении 6:4 по объему. Элюат собирают отдельными фракциями по 2 мл каждая.
Фракции элюата с 9 по 36 включительно, содержащие анализируемое вещество, объединяют, элюент испаряют в токе воздуха при температуре 18-22оС, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают 5 мл уксусного ангидрида, образующийся раствор количественно переносят в коническую колбу вместимостью 25 мл и кипятят с прямым холодильником при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют из реакционного раствора в токе азота до сухого остатка, остаток растворяют в 10 мл этилацетата (раствор А). 0,5 мл раствора А вносят в мерную колбу вместимостью 25 мл, доводят этилацетатом до метки (раствор Б) и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия.
В процессе определения 4 мкл раствора Б вводят в хромато-масс-спектрометр.
Определение проводят, используя хромато-масс-спектрометр Shimadzu GCMS-QP2010 Ultra.
Хроматографирование осуществляют в капиллярной колонке HP-5MS длиной 30 м, внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) метилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм.
Начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола по площади хроматографического пика его О-ацетильного производного.
В качестве газа-носителя используется гелий. Подача газа-носителя производится со скоростью 1 мл/мин. Режим с делением потока 1:2. Масс-селективный детектор работает в режиме электронного удара (70 эВ). Регистрация масс-спектра проводится по полному ионному току с задержкой 2,9 минуты. Диапазон сканирования составляет 40-600 m/z.
Пик на хроматограмме с временем удерживания 8,07 мин соответствует О-ацетильному производному 2-амино-4,6-динитрофенола. В масс-спектре данного соединения, снятому по полному ионному току, обнаруживаются сигналы ряда характеристических заряженных частиц с массовыми числами 50, 62, 90, 119, 131, 177, 193, 223. Наиболее интенсивной является частица с массовым числом 223, интенсивность которой принимается за 100 %.
2-амино-4,6-динитрофенол идентифицируют по сочетанию времени удерживания соответствующего О-ацетильного производного в неподвижной фазе колонки и специфического набора сигналов характеристических заряженных частиц в его масс-спектре.
Количество 2-амино-4,6-динитрофенола вычисляют, исходя из площади хроматографического пика, соответствующего его О-ацетильному производному и полученного при регистрации интенсивности по полному ионному току, а затем пересчитывают на навеску анализируемого вещества, внесённую в биологический материал.
Построение градуировочного графика и его уравнение приводятся выше в примере 1.
Результаты количественного определения 2-амино-4,6-динитрофенола в ткани лёгких представлены в таблице 2.
Пример 3
Определение 2-амино-4,6-динитрофенола в ткани почек
К 10 г измельчённой до размеров частиц 0,2-0,5 мм ткани почек прибавляют 10 мг 2-амино-4,6-динитрофенола, тщательно перемешивают биологический объект с веществом и оставляют на 1,5 часа при температуре 18-22оС. По истечении указанного времени биологический объект двукратно по 30 минут обрабатывают порциями органического изолирующего агента, которым является смесь ацетон-ацетонитрил в отношении 6:4 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси ацетон-ацетонитрил в отношении 6:4 по объему и выдерживают 30 минут при периодическом перемешивании. Извлечение отделяют от твёрдых частиц биоматериала, операцию настаивания повторяют в указанных условиях.
Полученные органические извлечения объединяют, растворитель из объединённого извлечения испаряют в токе воздуха комнатной температуры, остаток неоднократно (трижды по 3 минуты) обрабатывают порциями ацетона по 15 мл каждая при энергичном перемешивании, извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, остаток растворяют в 4 мл смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему. Полученный раствор вносят в хроматографическую полупрепаративную колонку размерами 490×11 мм, заполненную 10 г силикагеля «Меrck» 40/63 мкм. Хроматографируют, элюируя двухкомпонентной подвижной фазой ацетон-диэтиловый эфир в отношении 6:4 по объему. Элюат собирают отдельными фракциями по 2 мл каждая.
Фракции элюата с 9 по 36 включительно, содержащие анализируемое вещество, объединяют, элюент испаряют в токе воздуха при температуре 18-22оС, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают 5 мл уксусного ангидрида, образующийся раствор количественно переносят в коническую колбу вместимостью 25 мл и кипятят с прямым холодильником при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют из реакционного раствора в токе азота до сухого остатка, остаток растворяют в 10 мл этилацетата (раствор А). 0,5 мл раствора А вносят в мерную колбу вместимостью 25 мл, доводят этилацетатом до метки (раствор Б) и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия.
В процессе определения 4 мкл раствора Б вводят в хромато-масс-спектрометр.
Определение проводят, используя хромато-масс-спектрометр Shimadzu GCMS-QP2010 Ultra.
Хроматографирование осуществляют в капиллярной колонке HP-5MS длиной 30 м, внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-фенил) метилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм.
Начальная температура термостата колонки составляет 70оС, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70оС до 200оС со скоростью 40оС в минуту, затем с 200оС до 290оС со скоростью 12,5оС в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250оС, температура квадруполя 150оС, температура интерфейса детектора 290оС, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола по площади хроматографического пика его О-ацетильного производного.
В качестве газа-носителя используется гелий. Подача газа-носителя производится со скоростью 1 мл/мин. Режим с делением потока 1:2. Масс-селективный детектор работает в режиме электронного удара (70 эВ). Регистрация масс-спектра проводится по полному ионному току с задержкой 2,9 минуты. Диапазон сканирования составляет 40-600 m/z.
Пик на хроматограмме с временем удерживания 8,07 мин соответствует О-ацетильному производному 2-амино-4,6-динитрофенола. В масс-спектре данного соединения, снятому по полному ионному току, обнаруживаются сигналы ряда характеристических заряженных частиц с массовыми числами 50, 62, 90, 119, 131, 177, 193, 223. Наиболее интенсивной является частица с массовым числом 223, интенсивность которой принимается за 100 %.
2-амино-4,6-динитрофенол идентифицируют по сочетанию времени удерживания соответствующего О-ацетильного производного в неподвижной фазе колонки и специфического набора сигналов характеристических заряженных частиц в его масс-спектре.
Количество 2-амино-4,6-динитрофенола вычисляют, исходя из площади хроматографического пика, соответствующего его О-ацетильному производному и полученного при регистрации интенсивности по полному ионному току, а затем пересчитывают на навеску анализируемого вещества, внесённую в биологический материал.
Построение градуировочного графика и его уравнение приводятся выше в примере 1.
Результаты количественного определения 2-амино-4,6-динитрофенола в ткани почек представлены в таблице 3.
Предлагаемый способ по сравнению с прототипом в 3 раза повышает чувствительность определения в биологическом материале и в 667 раз в хроматографируемой пробе. Сравнительная характеристика предлагаемого и известного способов представлена в таблице 4.
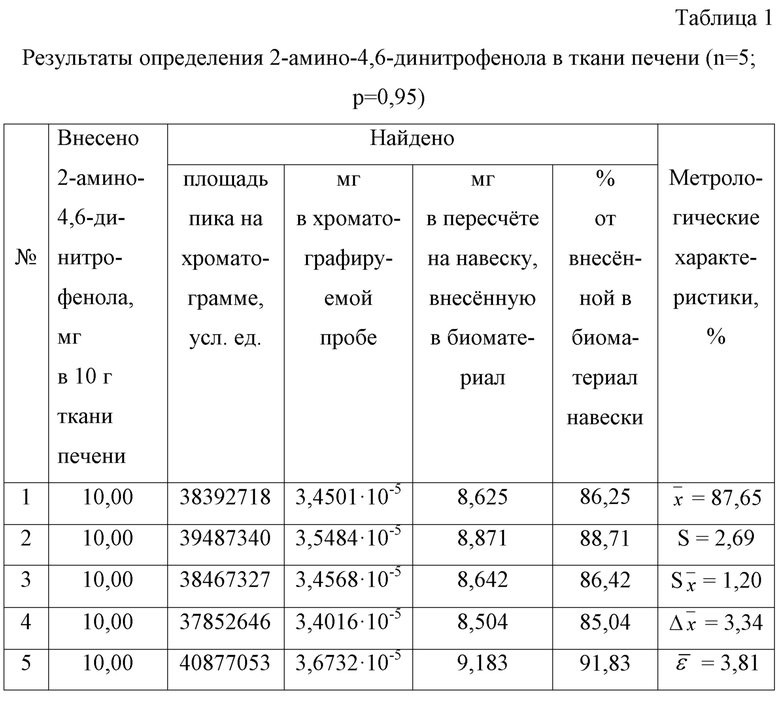
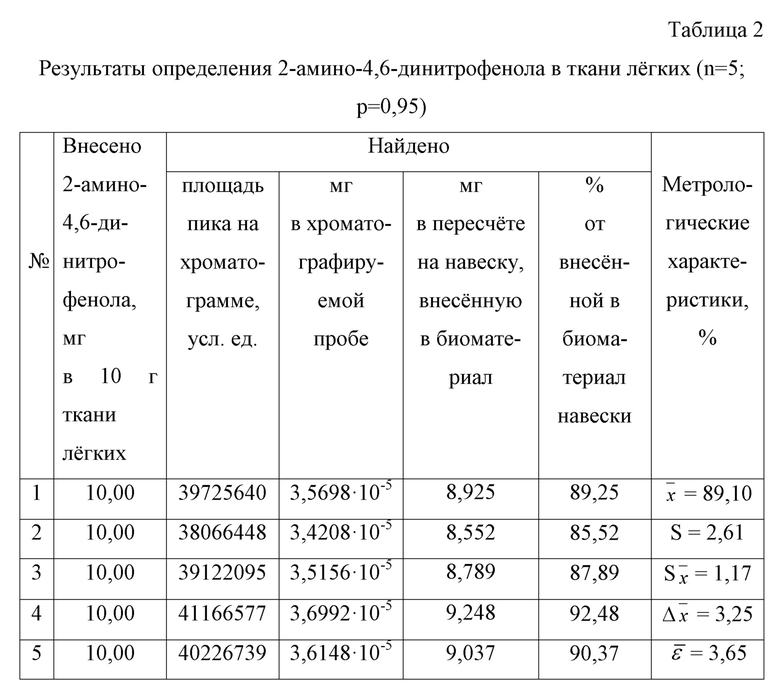
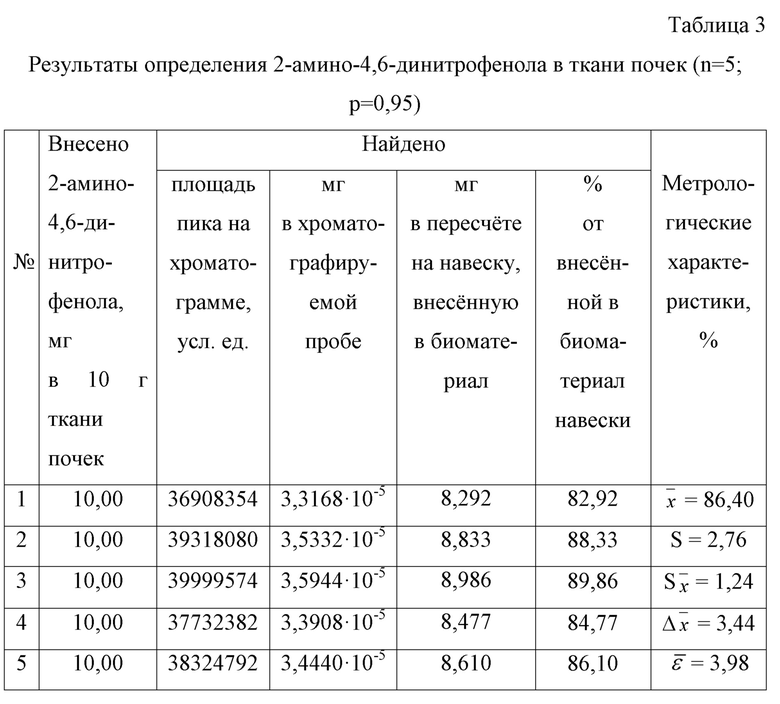
Таблица 4
Сравнительная характеристика предлагаемого и известного способов
(на примере исследования ткани печени)
а) в 100 г биоматериала
б) в детектируемой пробе
6,0⋅10-10 г
4,0⋅10-7 г
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения нифедипина в биологическом материале | 2023 |
|
RU2812598C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-ДИМЕТИЛГИДРОКСИБЕНЗОЛА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2024 |
|
RU2832324C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 3-МЕТОКСИГИДРОКСИБЕНЗОЛА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2013 |
|
RU2546292C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИДРОКСИБЕНЗОЛА И ЕГО МОНОМЕТИЛЬНЫХ ЗАМЕЩЕННЫХ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2014 |
|
RU2550953C1 |
| Способ определения О-(2,3-дигидро-2,2-диметил-7-бензофуранил)-N-метилкарбамата и О-(2,3-дигидро-2,2-диметил-7-бензофуранил)-N-(дибутиламиносульфенил)-N-метилкарбамата в биологическом материале | 2016 |
|
RU2623070C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ N-(4-НИТРО-2-ФЕНОКСИФЕНИЛ)-МЕТАНСУЛЬФОНАМИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2013 |
|
RU2537121C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЛОЖНОГО НИТРОФЕНОЛЬНОГО ПРЕПАРАТА "НИТРАФЕН" В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1999 |
|
RU2153169C1 |
| Способ определения кофеина в биологическом материале | 2016 |
|
RU2638789C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 4-НИТРОАНИЛИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2012 |
|
RU2519048C1 |
| Способ определения 3-метоксигидроксибензола в биологическом материале | 2016 |
|
RU2613310C1 |
Изобретение относится к области биохимии. Описан способ определения 2-амино-4,6-динитрофенола в образце органа или ткани, заключающийся в том, что образец измельчают, двукратно по 30 минут обрабатывают порциями органического изолирующего агента при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу образца. Полученные органические извлечения объединяют, растворитель из объединённого извлечения испаряют в токе воздуха комнатной температуры, остаток растворяют, хроматографируют, используя двухкомпонентную подвижную фазу, и проводят определение физико-химическим методом. Техническим результатом настоящего изобретения является повышение чувствительности определения 2-амино-4,6-динитрофенола в образце тканей или органов. 4 табл., 3 пр.
Способ определения 2-амино-4,6-динитрофенола в образце органа или ткани, заключающийся в том, что образец измельчают, двукратно по 30 минут обрабатывают порциями органического изолирующего агента при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу образца, полученные органические извлечения объединяют, растворитель из объединённого излечения испаряют в токе воздуха комнатной температуры, остаток растворяют, хроматографируют, используя двухкомпонентную подвижную фазу, и проводят определение физико-химическим методом, отличающийся тем, что в качестве органического изолирующего агента используется смесь ацетон-ацетонитрил в отношении 6:4 по объему, после испарения растворителя из объединённого извлечения остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, упаривают в токе воздуха комнатной температуры до полного удаления растворителя, перед хроматографированием остаток растворяют в смеси растворителей ацетон-диэтиловый эфир в отношении 6:4 по объему, хроматографируют в полупрепаративной колонке с силикагелем 40/63 мкм, используя двухкомпонентную подвижную фазу ацетон-диэтиловый эфир в отношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, анализируемое вещество, содержащееся в остатке, переводят в О-ацетильное производное, для чего остаток обрабатывают уксусным ангидридом в условиях кипячения при 139°C в течение 25 минут, после чего уксусный ангидрид удаляют в токе азота до сухого остатка, остаток растворяют в этилацетате и проводят определение физико-химическим методом, которым является хромато-масс-спектрометрия, в капиллярной колонке HP-5MS длиной 30 м и внутренним диаметром 0,25 мм с неподвижной фазой, представляющей собой (5%-ный фенил) диметилполисилоксан, при толщине плёнки неподвижной фазы 0,25 мкм, используя газ-носитель гелий, подаваемый со скоростью 1,0 мл/мин, и масс-селективный детектор, работающий в режиме электронного удара, начальная температура термостата колонки составляет 70°С, данная температура выдерживается в течение 2 минут, в дальнейшем температура повышается от 70°С до 200°С со скоростью 40°С в минуту, затем с 200°С до 290°С со скоростью 12,5°С в минуту, конечная температура колонки выдерживается в течение 2 минут, температура инжектора составляет 250°С, температура квадруполя 150°С, температура интерфейса детектора 290°С, регистрируют интенсивность сигнала, обусловленного заряженными частицами, образующимися при бомбардировке анализируемого вещества, вышедшего из капиллярной колонки и попавшего в источник ионов, ионизирующим пучком электронов с энергией 70 эВ, регистрируют масс-спектр по полному ионному току и вычисляют количество 2-амино-4,6-динитрофенола исходя из площади хроматографического пика его О-ацетильного производного.
| Погосян, Н.Г | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Химия и химическая технология в XXI веке: материалы XXII научно-практической конференции студентов и молодых ученых (Томск, 17-20 мая 2021 г.), Томск: ФГАОУ ВО НИ ТПУ, 2021,Т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Прибор для наглядного представления свойств кривых 2 порядка (механические подвижные чертежи) | 1921 |
|
SU323A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 4-НИТРОФЕНОЛОВ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1994 |
|
RU2121681C1 |
Авторы
Даты
2025-02-24—Публикация
2024-06-03—Подача